| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
Глава XIII. ХИМИКО-ТЕРМИЧЕСКАЯ ОБРАБОТКА СТАЛИ
1. Теория химико-термической обработки
Химико-термическая обработка по сравнению с поверхностной закалкой, например высокочастотной, обладает некоторыми особенностями и преимуществами (уступая поверхностной закалке в производитель ности):
1. Независимость от внешней формы изделия. С одинаковым успехом можно обрабатывать и сложные, и простые по форме изделия, получая по всей поверхности упрочненный слой одинаковой толщины. При поверхностной же закалке внешняя форма изделия имеет большое значение, у многих деталей машин внешняя форма такова, что исключает возможность применения поверхностной закалки.
2. Большее различие между свойствами сердцевины и поверхности, чем при поверхностной закалке. При химико-термической обработке разница в свойствах определяется различием в строении и в составе, а при поверхностной закалке — только различием в строении.
3. Последствия перегрева поверхности могут быть устранены последующей термической обработкой, тогда как при поверхностной закалке перегрев не может быть устранен, так как она является последней операцией.
Обычно при химико-термической обработке деталь помещают в среду, богатую элементом, который диффундирует в металл.
В случае газового окружения (наиболее частный случай) при химико-термической обработке происходят три элементарных процесса.
Первый процесс — диссоциация. Протекает в газовой среде и состоит в распаде молекул и образовании активных атомов диффундирующего элемента. Например

Степень распада молекул газа  называется степенью диссоциации.
называется степенью диссоциации.
Второй процесс — абсорбция. Происходит на границе газ—металл и состоит в поглощении (растворении) поверхностью свободных атомов. Этот процесс возможен только в том случае, если диффундирующий элемент В способен растворяться в основном металле А.
Проникновение насыщающего элемента вглубь — диффузия. Она характеризует третий процесс.
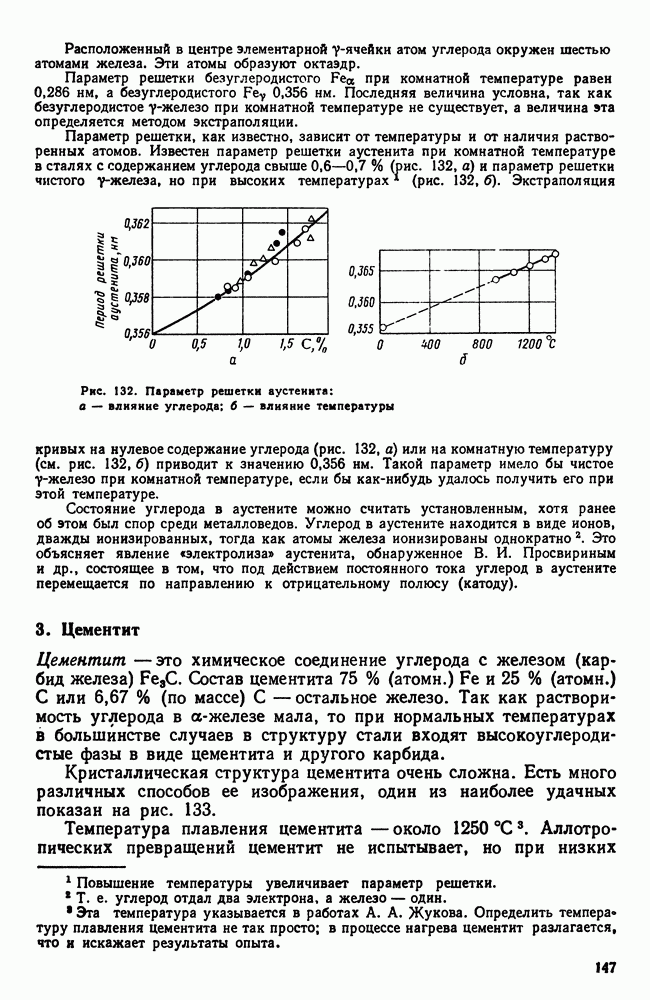
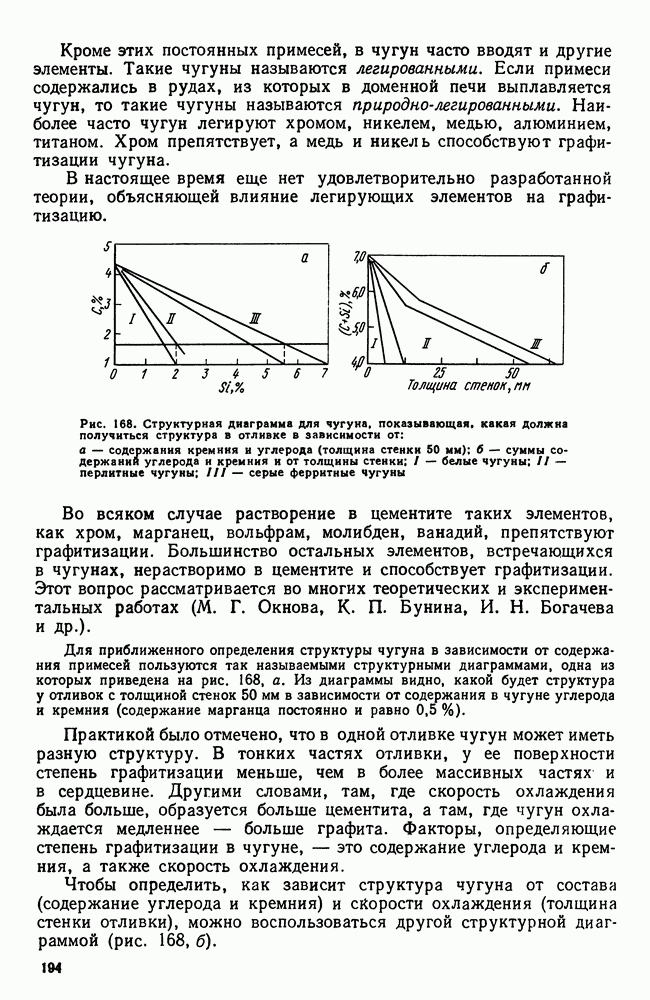
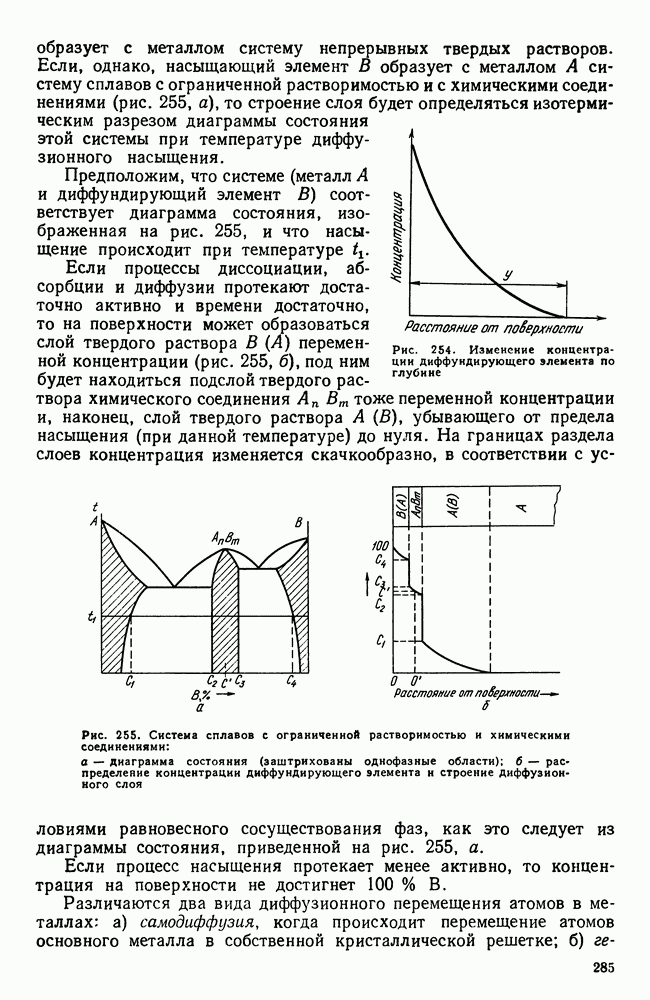
В результате образуется диффузионный слой, на поверхности которого концентрация диффундирующего элемента наибольшая; по мере удаления от поверхности концентрация падает (рис. 254), глубина проникновения (у на рис. 254) будет представлять собой толщину слоя. Так обстоит дело, если диффундирующий элемент
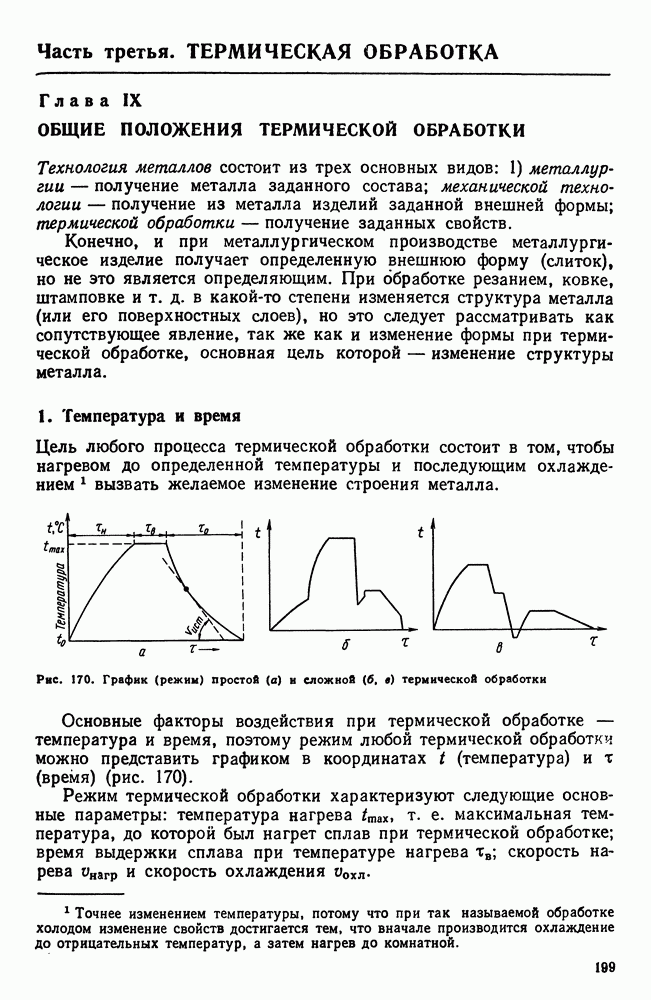
образует с металлом систему непрерывных твердых растворов. Если, однако, насыщающий элемент В образует с металлом А систему сплавов с ограниченной растворимостью и с химическими соединениями (рис. 255, а), то строение слоя будет определяться изотермическим разрезом диаграммы состояния этой системы при температуре диффузионного насыщения.
Предположим, что системе (металл А и диффундирующий элемент В) соответствует диаграмма состояния, изображенная на рис. 255, и что насыщение происходит при температуре 
Если процессы диссоциации, абсорбции и диффузии протекают достаточно активно и времени достаточно, то на поверхности может образоваться слой твердого раствора  переменной концентрации (рис. 255, б), под ним будет находиться подслой твердого раствора химического соединения
переменной концентрации (рис. 255, б), под ним будет находиться подслой твердого раствора химического соединения  тоже переменной концентрации и, наконец, слой твердого раствора
тоже переменной концентрации и, наконец, слой твердого раствора  убывающего от предела насыщения (при данной температуре) до нуля. На границах раздела слоев концентрация изменяется скачкообразно, в соответствии с условиями равновесного сосуществования фаз, как это следует из диаграммы состояния, приведенной на рис. 255, а.
убывающего от предела насыщения (при данной температуре) до нуля. На границах раздела слоев концентрация изменяется скачкообразно, в соответствии с условиями равновесного сосуществования фаз, как это следует из диаграммы состояния, приведенной на рис. 255, а.

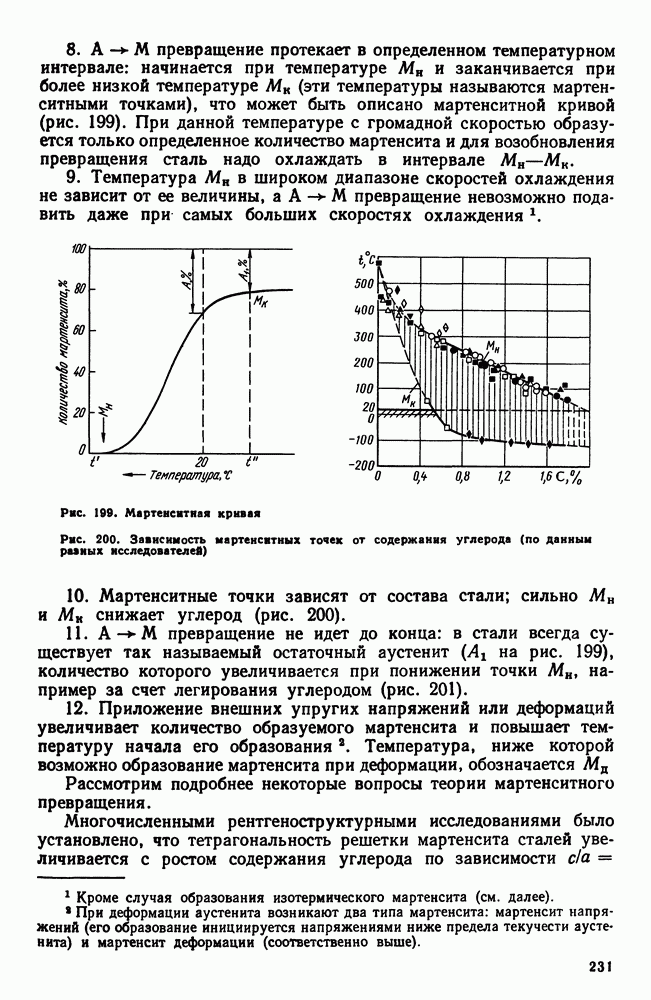
Рис. 254. Изменение концентрации диффундирующего элемента по глубине

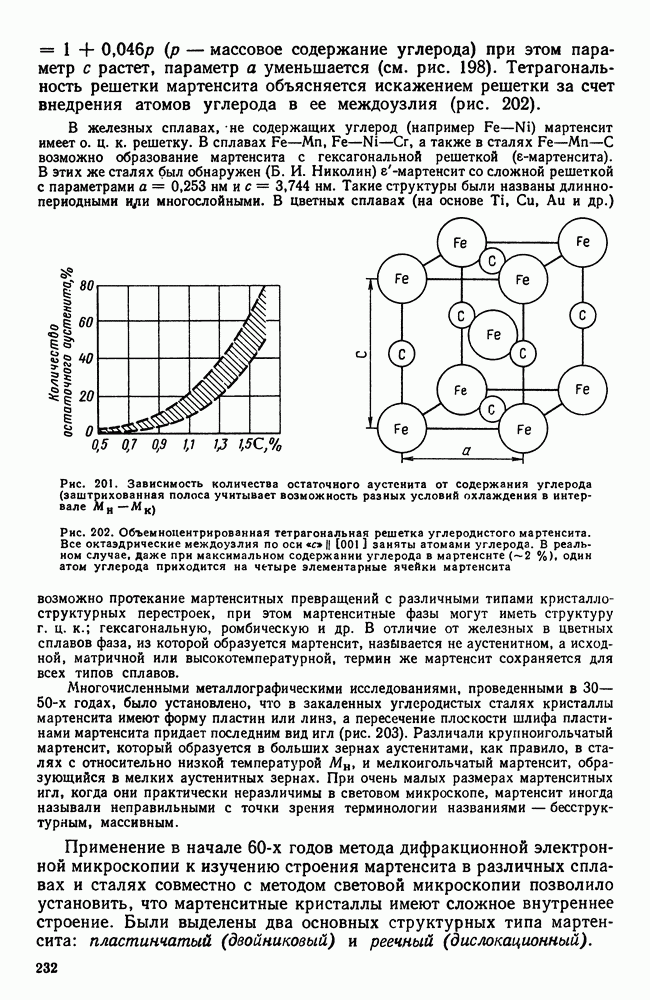
Рис. 255. Система сплавов с ограниченной растворимостью и химическими соединениями: а — диаграмма состояния (заштрихованы однофазные области); б — распределение концентрации диффундирующего элемента и строение диффузионного слоя
Если процесс насыщения протекает менее активно, то концентрация на поверхности не достигнет 
Различаются два вида диффузионного перемещения атомов в металлах: а) самодиффузия, когда происходит перемещение атомов основного металла в собственной кристаллической решетке; б)
гетеродиффузия, когда происходит перемещение инородных (растворенных) атомов в чужой кристаллической решетке.
В первом случае в результате хаотического теплового движения отдельные атомы основного металла время от времени меняют места в своей кристаллической решетке, совершая перескок из одного положения в другое. Этот процесс перемещения однородных атомов происходит непрерывно и хаотически по направлению и не изменяет концентрации.
Во втором случае перемещение инородных атомов происходит в направлении от мест высокой концентрации к местам низкой концентрации. Этот процесс совершается самопроизвольно, так как состояние с неравномерной концентрацией обладает большей свободной энергией, чем состояние с равномерным распределением растворенных атомов.

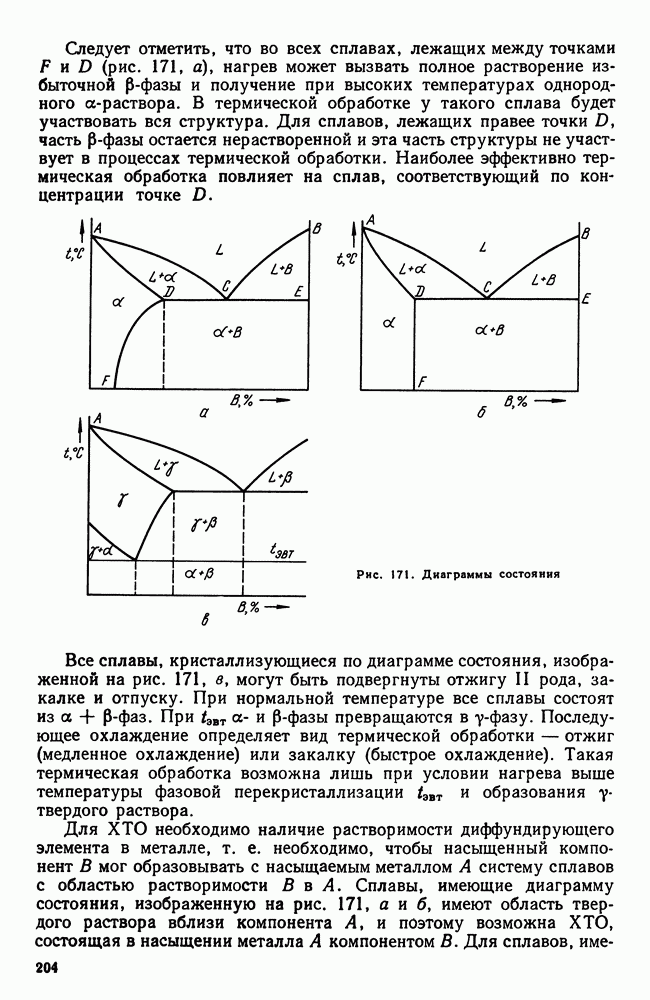
Рис. 256.
Как осуществляется диффузионное перемещение атомов?
Как указывалось ранее (см. гл. I), в любом веществе происходит флуктуация тепловых колебаний, в результате которой отдельные атомы приобретают значительно большую энергию, чем средний уровень энергии атомов, характеризуемый температурой данного тела. Эти атомы могут покидать равновесные положения в узлах решетки и перемещаться в междоузлиях, оставляя места в узлах решетки и перемещаться в междоузлиях, оставляя места в узлах решетки незанятыми.
Атом, расположенный в междоузлии решетки, называется дислоцированным атомом (рис. 256), а узел в кристаллической решетке, не занятый атомом, называется, как уже говорилось в гл. I, вакансией. Для атомов вокруг вакансии или дислоцированного атома нарушается равномерность окружения атомами-соседями по сравнению с бездефектными участками решетки (см. рис. 257). В результате этого вокруг вакансии или вокруг дислоцированного атома возникает поле упругих искажений кристаллической решетки.
Гипотетический механизм гетеродиффузии, который аналогичен механизму самодиффузии, описан Я. И. Френкелем и в настоящее время является общепринятым. Если по соседству с атомом А (см. рис. 256) имеется вакансия (дырка), то он может легко переместиться
со своего места в дырку; на место атома А встанет атом В, на место атома В — атом С и т. д. Одновременно с перемещением атомов происходит как бы перемещение «дырки». Процесс гетеродиффузии удобнее описывать как перемещение инородных атомов, а процесс самодиффузии — как перемещение «дырок».
Для того чтобы атом А перешел из своего исходного положения в соседнюю «дырку», он должен предварительно занять промежуточное положение в междоузлии. Работа, которая требуется для того, чтобы вырвать атом из регулярного положения, называется энергией активации (или теплотой разрыхления) и является важнейшей характеристикой способности атомов к перемещению.
Величина эта не зависит от температуры, а определяется природой вещества.

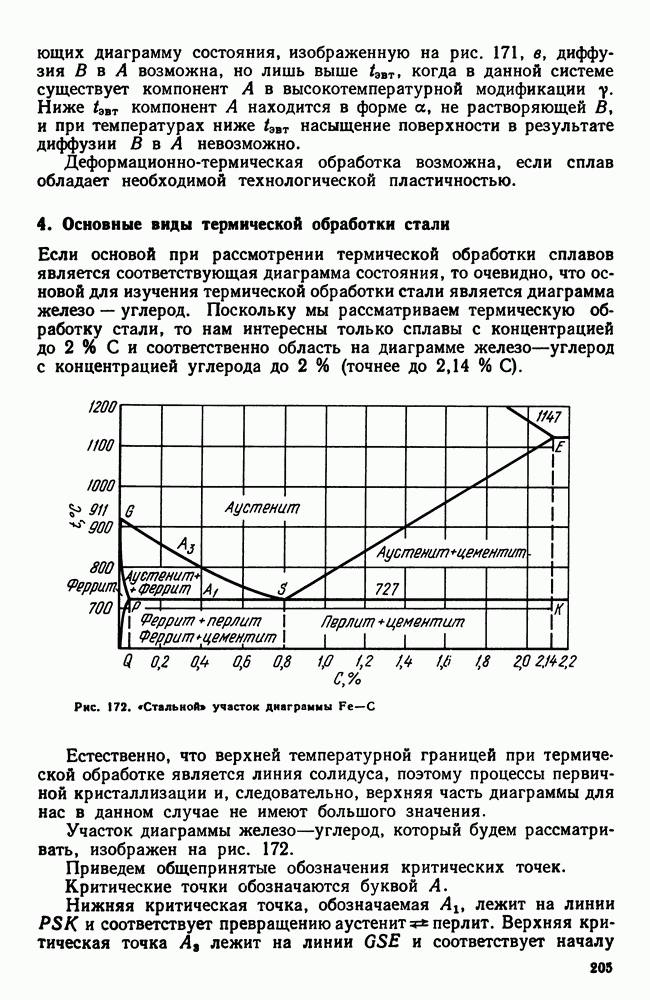
Рис. 257. Зависимость коэффициента диффузии от температуры
Влияние температуры, значительно ускоряющее диффузионные процессы, обусловлено тем, Что с повышением температуры увеличиваются тепловые колебания и благодаря этому увеличивается число «дырок» в решетке.
Количественно процесс диффузии характеризуется так называемым коэффициентом диффузии  который численно равен количеству вещества, продиффундировавшего через площадку в
который численно равен количеству вещества, продиффундировавшего через площадку в  в течение секунды при перепаде концентраций по обе стороны площадки, равном единице (0 и
в течение секунды при перепаде концентраций по обе стороны площадки, равном единице (0 и  вещества В), и имеет размерность квадратный сантиметр на секунду
вещества В), и имеет размерность квадратный сантиметр на секунду 
Зависимость  от температуры выражается уравнением
от температуры выражается уравнением 

где А — коэффициент, зависящий от кристаллической решетки;  — энергия активации;
— энергия активации;  — основание натуральных логарифмов;
— основание натуральных логарифмов;  — газовая постоянная; Т—абсолютная температура.
— газовая постоянная; Т—абсолютная температура.
Так как  и
и  не зависят от температуры, то для данного вещества коэффициент диффузии очень сильно возрастает с повышением температуры (рис. 257, а), а в координатах
не зависят от температуры, то для данного вещества коэффициент диффузии очень сильно возрастает с повышением температуры (рис. 257, а), а в координатах  эта зависимость изобразится прямой линией (рис. 257, б).
эта зависимость изобразится прямой линией (рис. 257, б).
Из уравнения (1) следует, что коэффициент диффузии разных веществ чрезвычайно сильно зависит от уровня энергии активации; чем больше  тем резко меньше
тем резко меньше 
В твердых растворах внедрения процесс диффузии облегчается тем, что не требуется вывода атома (иона) растворителя в иррегулярное положение, и поэтому энергия активации меньше, чем при образовании твердых растворов замещения. Например, при диффузии углерода в ужелезе  . В случае диффузии металлов в ужелезе (растворы замещения)
. В случае диффузии металлов в ужелезе (растворы замещения)  . Коэффициенты диффузии в этих двух случаях различаются в тысячи и десятки тысяч раз. Так, для стали с 0,2 % С при 1100 °С коэффициент
. Коэффициенты диффузии в этих двух случаях различаются в тысячи и десятки тысяч раз. Так, для стали с 0,2 % С при 1100 °С коэффициент  для диффузии углерода и
для диффузии углерода и  для диффузии молибдена.
для диффузии молибдена.

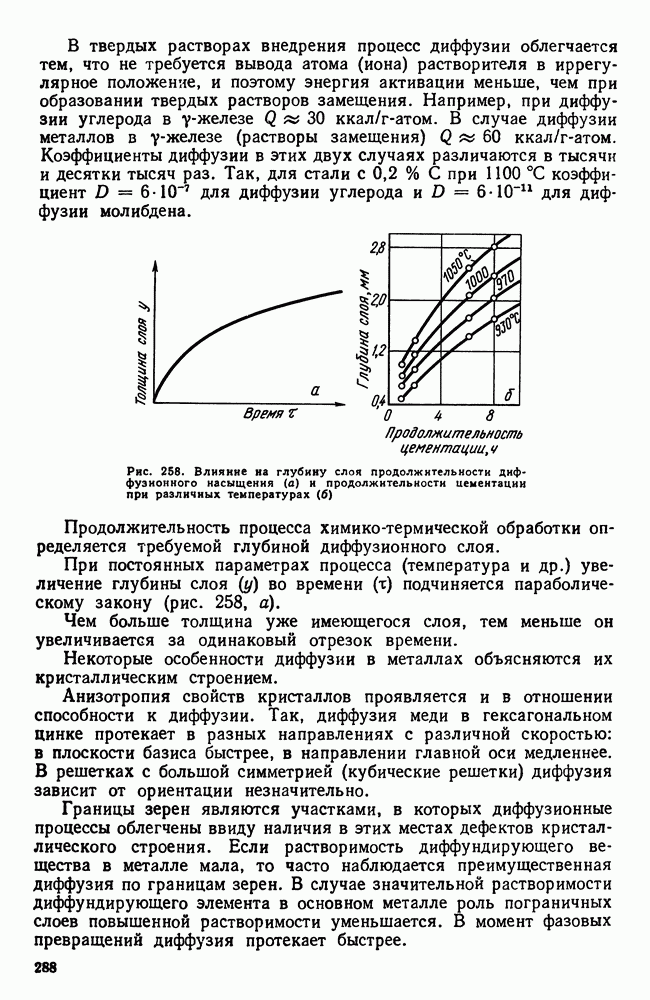
Рис. 258. Влияние на глубину слоя продолжительности диффузионного насыщения (а) и продолжительности цементации при различных температурах (б)
Продолжительность процесса химико-термической обработки определяется требуемой глубиной диффузионного слоя.
При постоянных параметрах процесса (температура и др.) увеличение глубины слоя  во времени
во времени  подчиняется параболическому закону (рис. 258, а).
подчиняется параболическому закону (рис. 258, а).
Чем больше толщина уже имеющегося слоя, тем меньше он увеличивается за одинаковый отрезок времени.
Некоторые особенности диффузии в металлах объясняются их кристаллическим строением.
Анизотропия свойств кристаллов проявляется и в отношении способности к диффузии. Так, диффузия меди в гексагональном цинке протекает в разных направлениях с различной скоростью: в плоскости базиса быстрее, в направлении главной оси медленнее. В решетках с большой симметрией (кубические решетки) диффузия зависит от ориентации незначительно.
Границы зерен являются участками, в которых диффузионные процессы облегчены ввиду наличия в этих местах дефектов кристаллического строения. Если растворимость диффундирующего вещества в металле мала, то часто наблюдается преимущественная диффузия по границам зерен. В случае значительной растворимости диффундирующего элемента в основном металле роль пограничных слоев повышенной растворимости уменьшается. В момент фазовых превращений диффузия протекает быстрее.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- Часть первая. ТЕОРИЯ СПЛАВОВ
- Глава I. КРИСТАЛЛИЧЕСКОЕ СТРОЕНИЕ МЕТАЛЛОВ
- 2. Классификация металлов
- 3. Кристаллическое строение металлов
- 4. Кристаллические решетки металлов
- 5. Реальное строение металлических кристаллов
- 6. Анизотропия свойств кристаллов
- 7. Методы изучения строения металлов
- Глава II. КРИСТАЛЛИЗАЦИЯ
- 1. Три состояния вещества
- 2. Энергетические условия процесса кристаллизации
- 3. Механизм процесса кристаллизации
- 4. Форма кристаллических образований
- 5. Строение слитка
- 6. Превращения в твердом состояние. Полиморфизм
- 7. Магнитные превращения
- 8. Закалка из жидкого состояния. Аморфное состояние
- Глава III. МЕХАНИЧЕСКИЕ СВОЙСТВА. НАКЛЕП И РЕКРИСТАЛЛИЗАЦИЯ
- 2. Упругая и пластическая деформация. Несовершенства решетки и прочность металлов
- 3. Сверхпластичность
- 4. Разрушение
- 5. Методы определения механических свойств
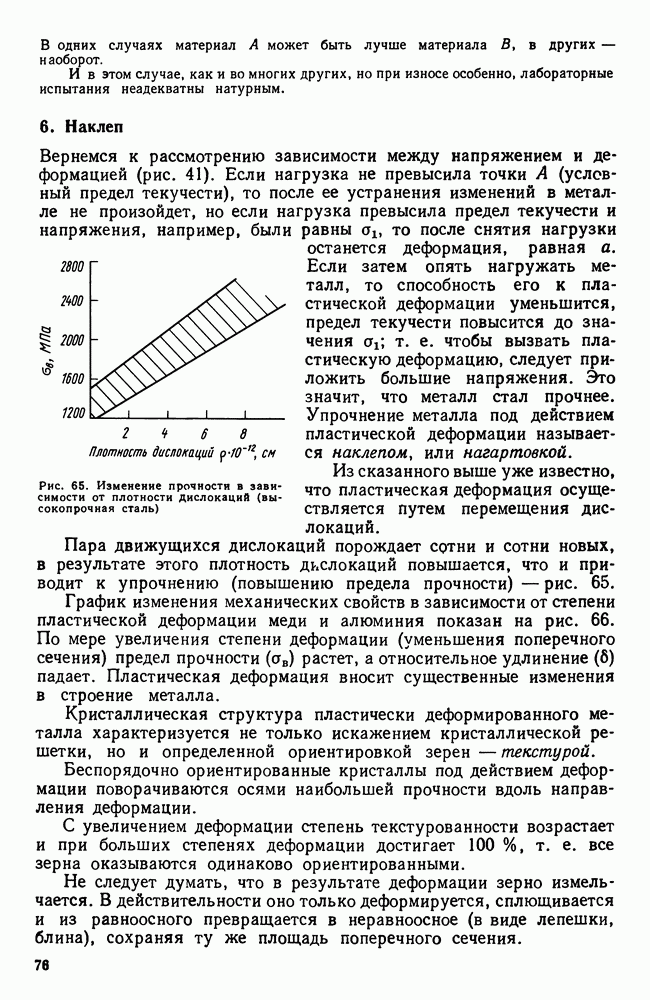
- 6. Наклеп
- 7. Влияние нагрева на строение и свойства деформированного металла (рекристаллизационные процессы)
- Глава IV. СТРОЕНИЕ СПЛАВОВ
- 2. Химическое соединение
- 3. Твердый раствор на основе одного из компонентов сплава
- 4. Твердый раствор на основе химического соединения
- 5. Упорядоченные твердые растворы
- 6. Электронные соединения (фазы Юм-Розери)
- 7. Фазы Лавеса
- 8. Фазы внедрения
- Глава V. ДИАГРАММА СОСТОЯНИЯ
- 2. Общие замечания о построении диаграмм состояния
- 3. Экспериментальное построение диаграмм
- 4. Диаграмма состояния для сплавов, образующих механические смеси из чистых компонентов (I рода)
- 5. Правило отрезков
- 6. Диаграмма состояния для сплавов с неограниченной растворимостью в твердом состоянии (II рода)
- 7. Диаграмма состояния для сплавов с ограниченной растворимостью в твердом состоянии (III рода)
- 8. Диаграмма состояния для сплавов, образующих химические соединения (IV рода)
- 9. Диаграмма состояния для сплавов, испытывающих полиморфные превращения
- 10. Кристаллизация сплавов в неравновесных условиях
- 11. Системы с тремя компонентами
- 12. Упрощенные методы изучения многокомпонентных систем
- 13. Связь между свойствами сплавов и типом диаграммы состояния
- Часть вторая. ЖЕЛЕЗОУГЛЕРОДИСТЫЕ СПЛАВЫ
- Глава VI. ДИАГРАММА ЖЕЛЕЗО—УГЛЕРОД
- 2. Железо
- 3. Цементит
- 4. Диаграмма состояния
- Глава VII. УГЛЕРОДИСТЫЕ СТАЛИ
- 1. Влияние углерода на свойства стали
- 2. Влияние постоянных примесей на свойства стали
- 3. Сталь различных способов производства. Чистая сталь
- 4. Углеродистая сталь общего назначения
- 5. Нагартованная сталь
- 6. Листовая сталь для холодной штамповки
- 7. Обрабатываемость резанием. Автоматные стали
- Глава VIII. ЧУГУН
- 2. Структура чугуна. Формы графита
- 3. Структура и свойства чугуна
- 4. Примеси в чугуне
- 5. Марки серых и высокопрочных чугунов
- 6. Ковкий чугун
- Часть третья. ТЕРМИЧЕСКАЯ ОБРАБОТКА
- Глава IX. ОБЩИЕ ПОЛОЖЕНИЯ ТЕРМИЧЕСКОЙ ОБРАБОТКИ
- 2. Классификация видов термической обработки
- 3. Термическая обработка и диаграмма состояния
- 4 Основные виды термической обработки стали
- 5. Четыре основных превращения в стали
- Глава X. ТЕОРИЯ ТЕРМИЧЕСКОЙ ОБРАБОТКИ СТАЛИ
- 2. Рост аустенитного зерна
- 3. Распад аустенита
- 4. Мартенситное превращение
- 5. Бейнитное превращение
- 6. Превращения при отпуске
- 7. Влияние термической обработки на свойства стали
- 8. Термомеханическая обработка
- Глава XI. ПРАКТИКА ТЕРМИЧЕСКОЙ ОБРАБОТКИ СТАЛИ
- 2. Время нагрева
- 3. Химическое воздействие нагревающей среды
- 4. Закалочные среды
- 5. Прокаливаемость
- 6. Внутренние напряжения
- 7. Способы закалки
- 8. Обработка стали холодом
- 9. Дефекты, возникающие при закалке
- 10. Отжиг и нормализация
- Глава XII. ПОВЕРХНОСТНАЯ ЗАКАЛКА СТАЛИ
- 2. Высокочастотная закалка
- Глава XIII. ХИМИКО-ТЕРМИЧЕСКАЯ ОБРАБОТКА СТАЛИ
- 2. Цементация стали
- 3. Азотирование стали
- 4. Цианирование стали
- 5. Диффузионная металлизация
- Часть четвертая. ЛЕГИРОВАННЫЕ СТАЛИ И СПЛАВЫ
- Глава XIV. ВЛИЯНИЕ ЛЕГИРУЮЩИХ ЭЛЕМЕНТОВ
- 2. Влияние элементов на полиморфизм железа
- 3. Распределение легирующих элементов в стали
- 4. Влияние легирующих элементов на феррит
- 5. Карбидная фаза в легированных сталях
- 6. Влияние легирующих элементов на превращения в стали
- Глава XV. КЛАССИФИКАЦИЯ И МАРКИРОВКА ЛЕГИРОВАННЫХ СТАЛЕЙ
- 2. Маркировка легированных сталей
- Глава XVI. КОНСТРУКЦИОННЫЕ СТАЛИ
- 1. Механические свойства стали, влияние структуры и легирующих элементов
- 2. Термическая обработка конструкционных сталей
- 3. Цементуемые (низкоуглеродистые) стали
- 4. Улучшаемые (среднеуглеродистые) стали
- 5. Высокопрочные стали
- 6. Свариваемость стали
- 7. Строительная сталь
- 8. Арматурная сталь
- 9. Пружинная сталь
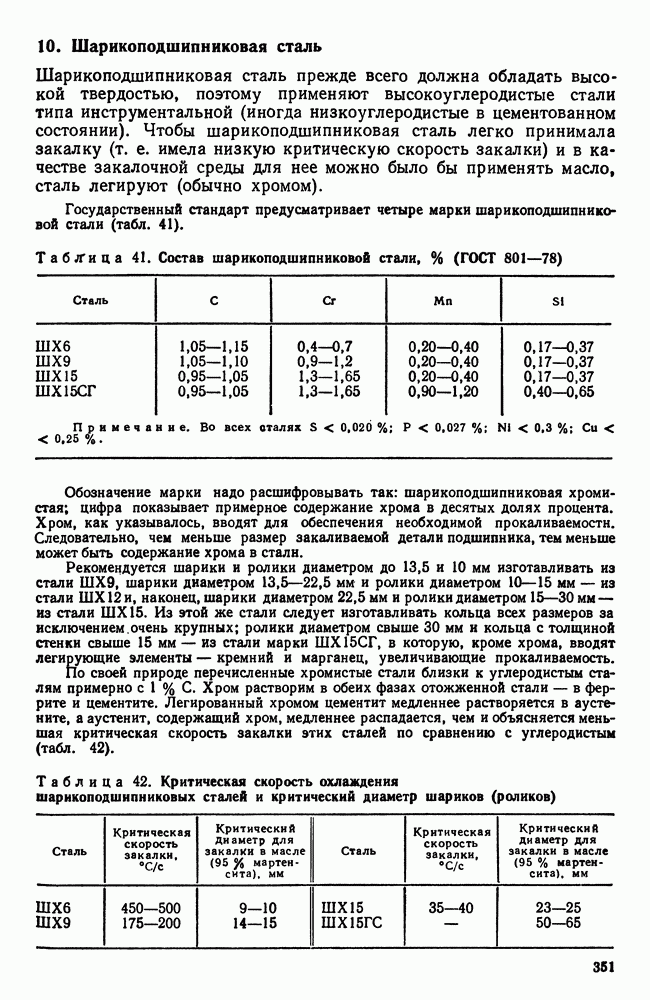
- 10. Шарикоподшипниковая сталь
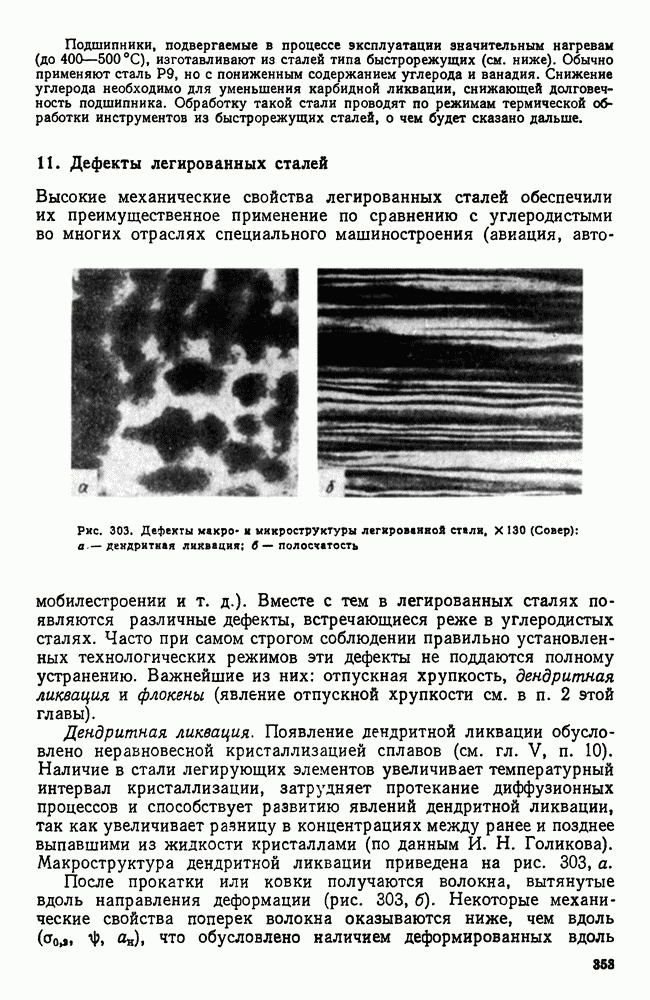
- 11. Дефекты легированных сталей
- Глава XVII. ИНСТРУМЕНТАЛЬНЫЕ СТАЛИ
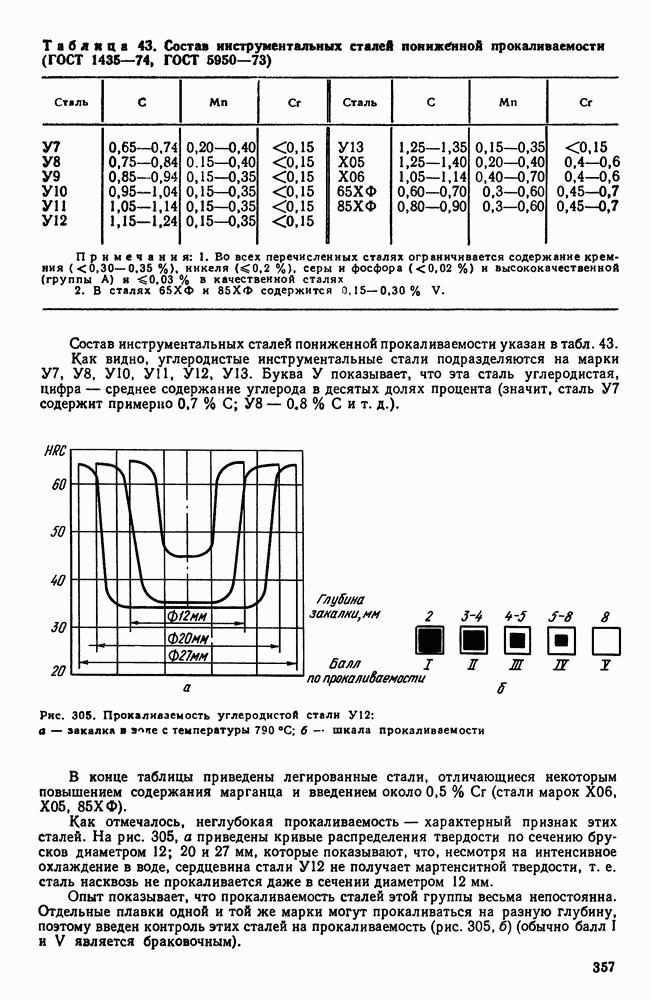
- 2. Инструментальные стали пониженной прокаливаемости
- 3. Инструментальные стали повышенной прокаливаемости (легированные инструментальные стали)
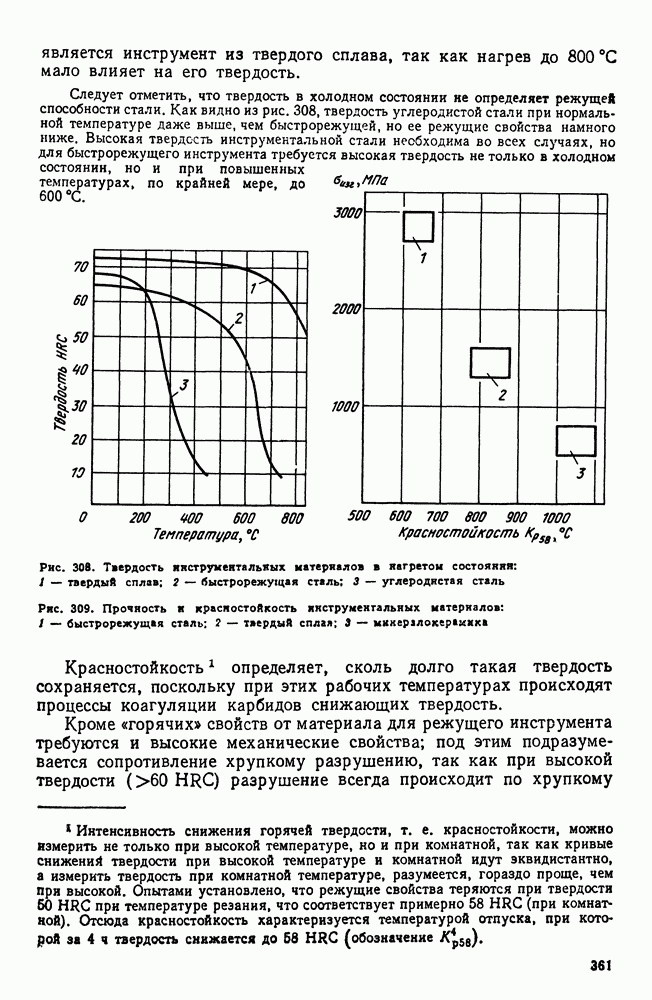
- 4. Быстрорежущие стали
- 5. Штамповые стали
- 6. Твердые сплавы
- Глава XVIII. ЖАРОСТОЙКИЕ И ЖАРОПРОЧНЫЕ СТАЛИ И СПЛАВЫ
- 2. Жаропрочность
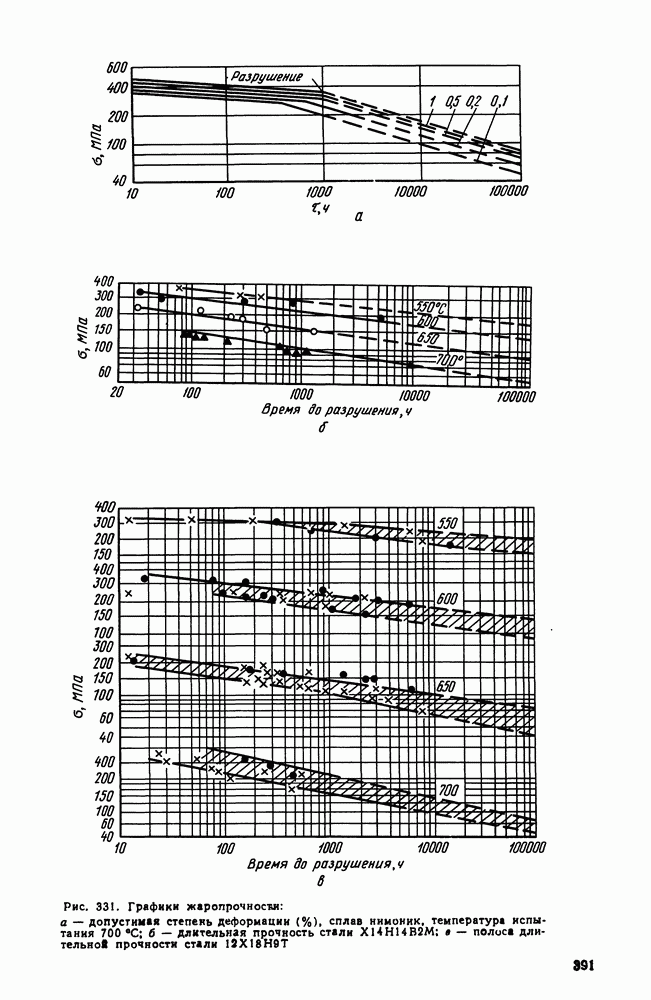
- 3. Оценка жаропрочных свойств
- 4. Влияние структуры и состава на жаропрочность
- 5. Классификация жаропрочных материалов
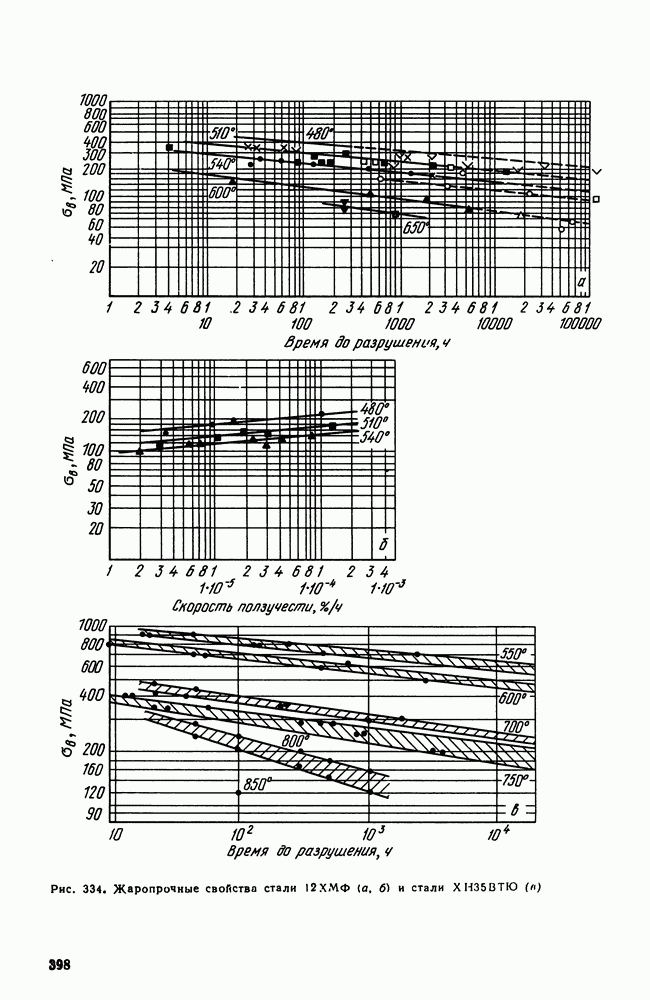
- 6. Перлитные и мартенситные жаропрочные стали
- 7. Аустенитные жаропрочные стали
- 8. Никелевые и кобальтовые жаропрочные сплавы
- Глава XIX. КОРРОЗИОННОСТОЙКИЕ (НЕРЖАВЕЮЩИЕ) СТАЛИ И СПЛАВЫ
- 2. Хромоникелевые нержавеющие стали
- 3. Кислотостойкие стали и сплавы
- 4. Криогенные стали и сплавы
- Глава XX. ИЗНОСОСТОЙКИЕ СТАЛИ И СПЛАВЫ
- 2. Графитизированная сталь
- 3. Высокомарганцовистая сталь
- 4. Наплавочные материалы
- Глава XXI. ТИТАН И ЕГО СПЛАВЫ
- 2. Легирование титана
- 3. Фазовые превращения в титановых сплавах
- 5. Термическая обработка титановых сплавов
- 6. Примеси в титановых сплавах
- 7. Коррозионная стойкость титана
- Глава XXII. ТУГОПЛАВКИЕ МЕТАЛЛЫ
- 2. Взаимодействие тугоплавких металлов с другими элементами и между собой
- 3. Механические свойства и жаропрочность
- 4. Хладноломкость тугоплавких металлов
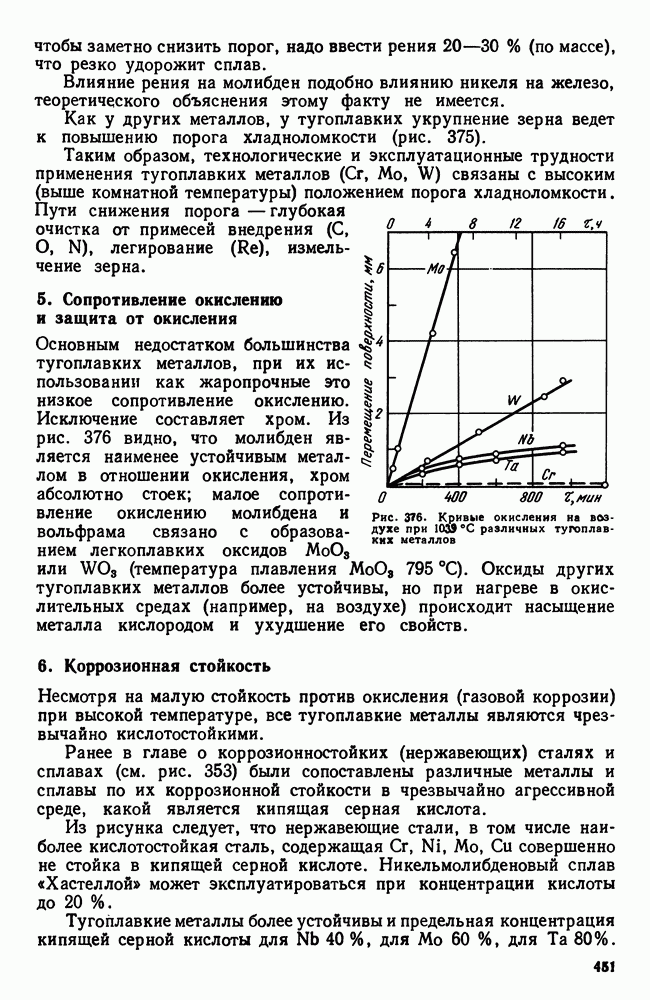
- 5. Сопротивление окислению и защита от окисления
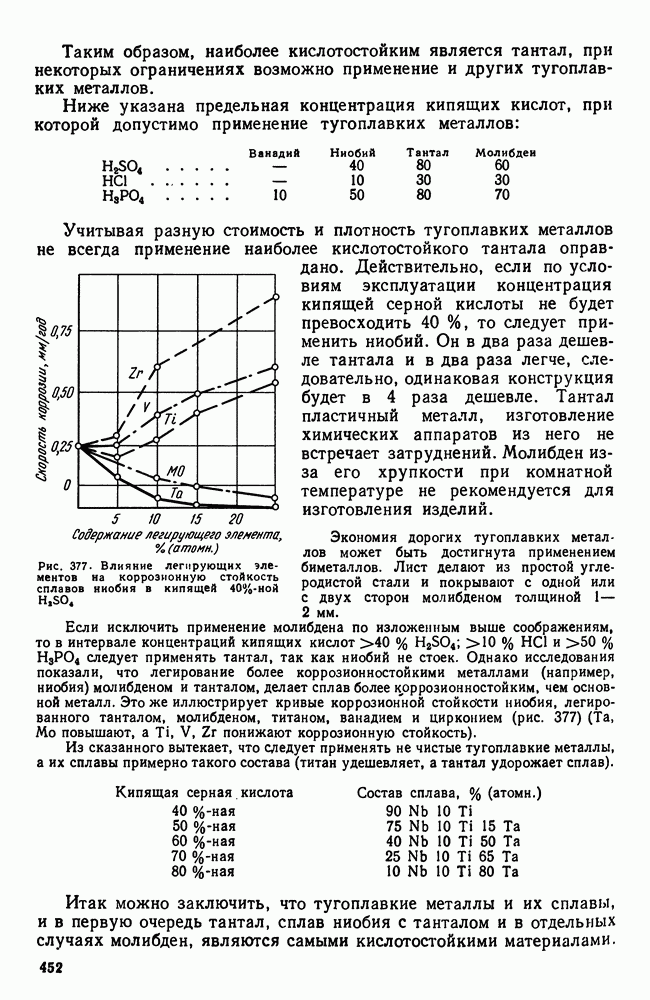
- 6. Коррозионная стойкость
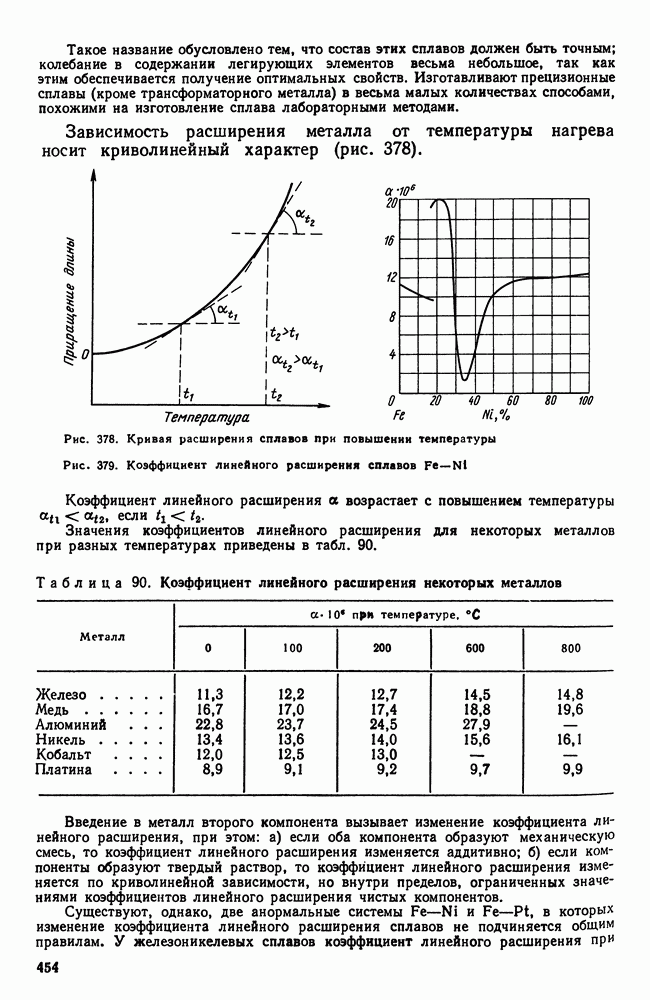
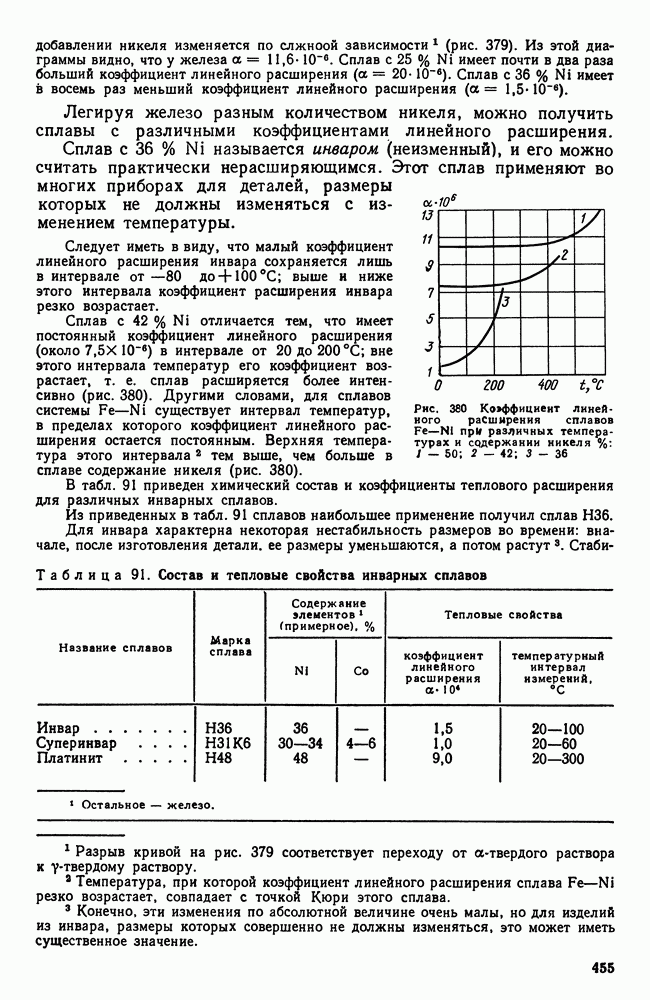
- Глава XXIII. СПЛАВЫ С ОСОБЫМИ ТЕПЛОВЫМИ И УПРУГИМИ СВОЙСТВАМИ
- 2. Сплавы с постоянным модулем упругости
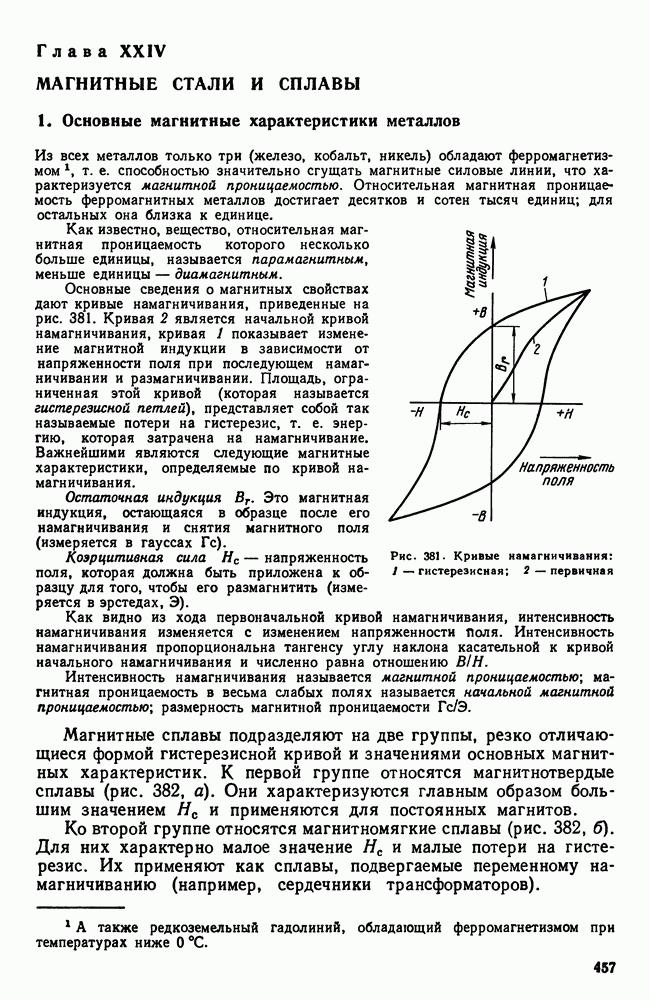
- Глава XXIV. МАГНИТНЫЕ СТАЛИ И СПЛАВЫ
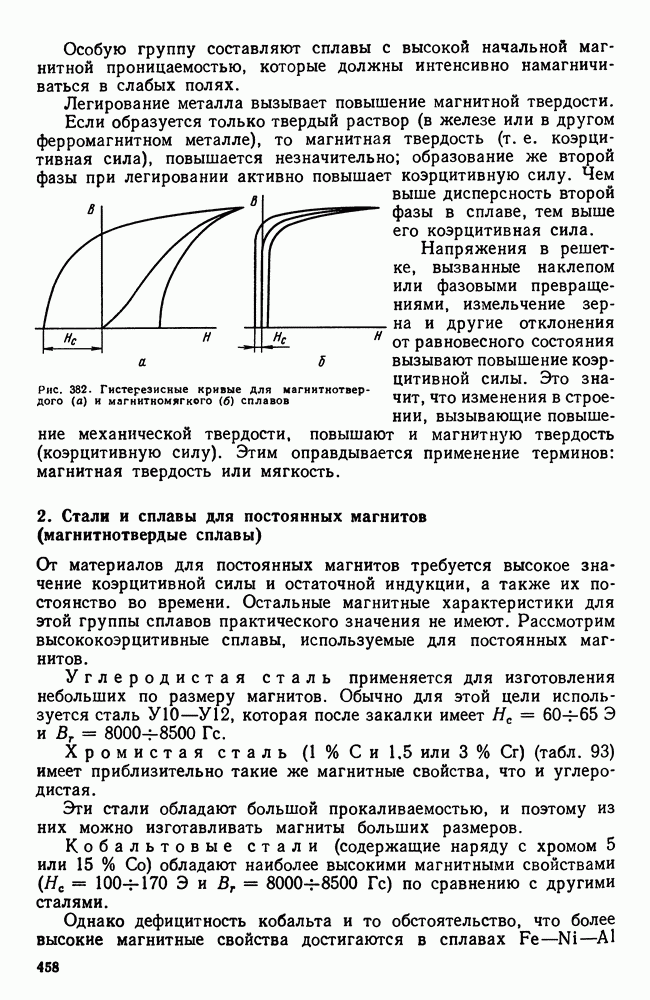
- 2. Стали и сплавы для постоянных магнитов (магнитнотвердые сплавы)
- 3. Магнитномягкие сплавы
- 4. Немагнитные стали
- 5. Электротехнические сплавы
- Глава XXV. СПЛАВЫ АТОМНОЙ ЭНЕРГЕТИКИ
- 2. Конструкционные материалы. Теплоносители
- 3. Ядерное горючее (уран, плутоний, торий)
- Часть пятая. Цветные металлы и сплавы
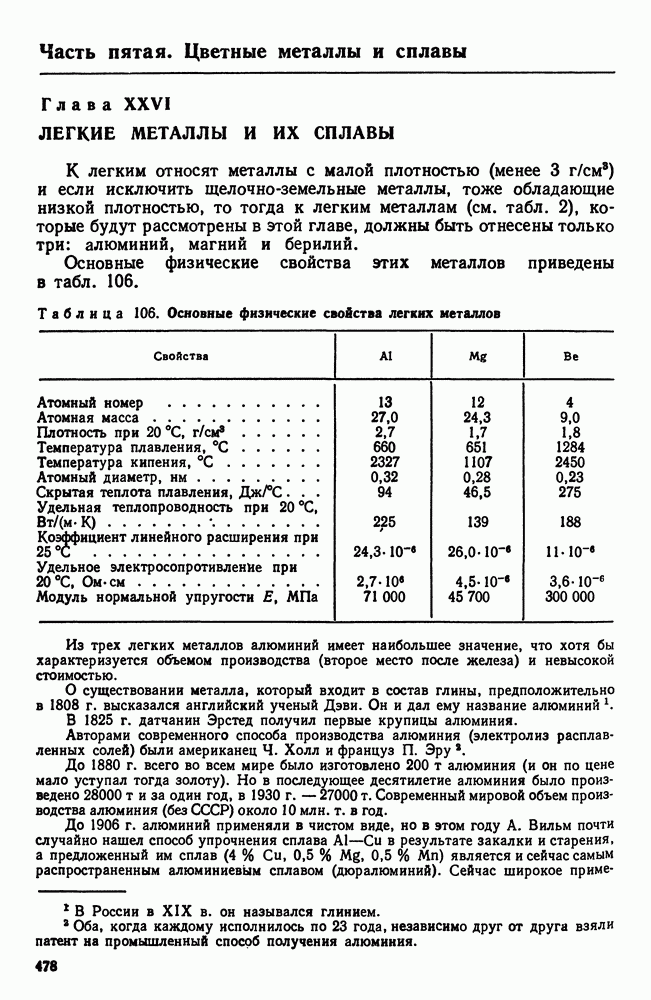
- Глава XXVI. ЛЕГКИЕ МЕТАЛЛЫ И ИХ СПЛАВЫ
- 1. Свойства алюминия
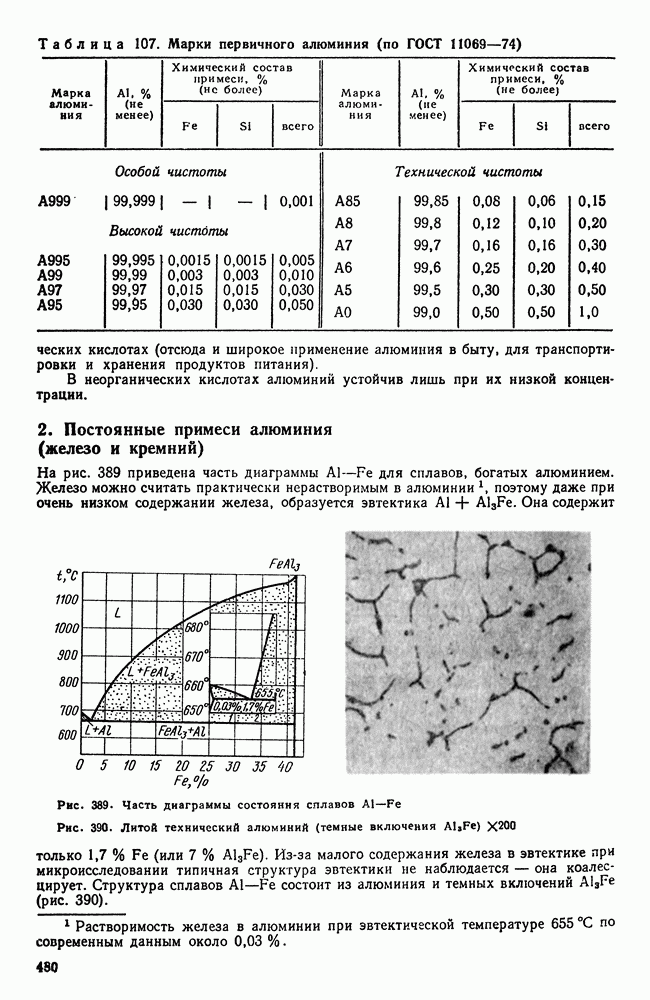
- 2. Постоянные примеси алюминия (железо и кремний)
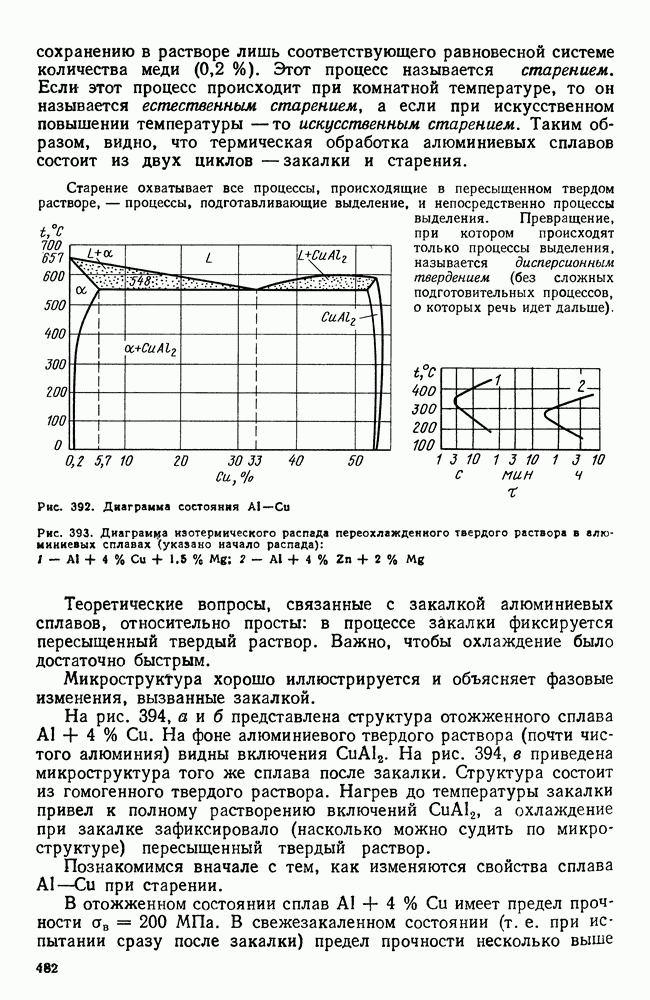
- 3. Термическая обработка сплавов Al-Cu
- 4. Влияние состава алюминиевых сплавов на процессы, происходящие при термической обработке
- 5. Классификация алюминиевых сплавов
- 6. Деформируемые сплавы, не упрочняемые термической обработкой
- 7. Дюралюминий и другие деформируемые сплавы, упрочняемые термической обработкой
- 8. Алюминиевые сплавы для поковок и штамповок
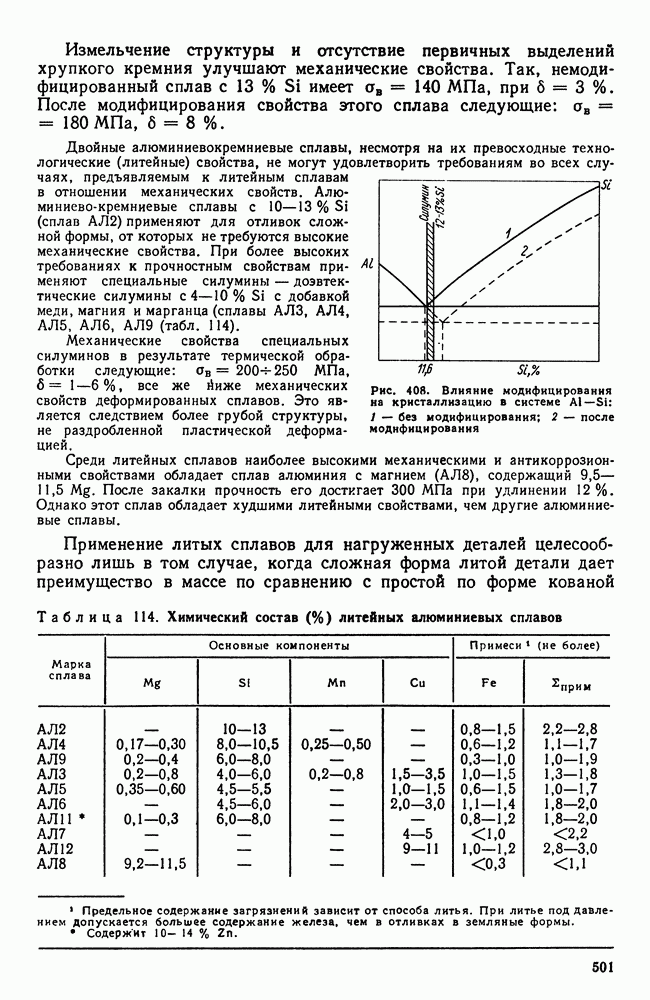
- 9. Силумины и другие алюминиевые сплавы для фасонного литья
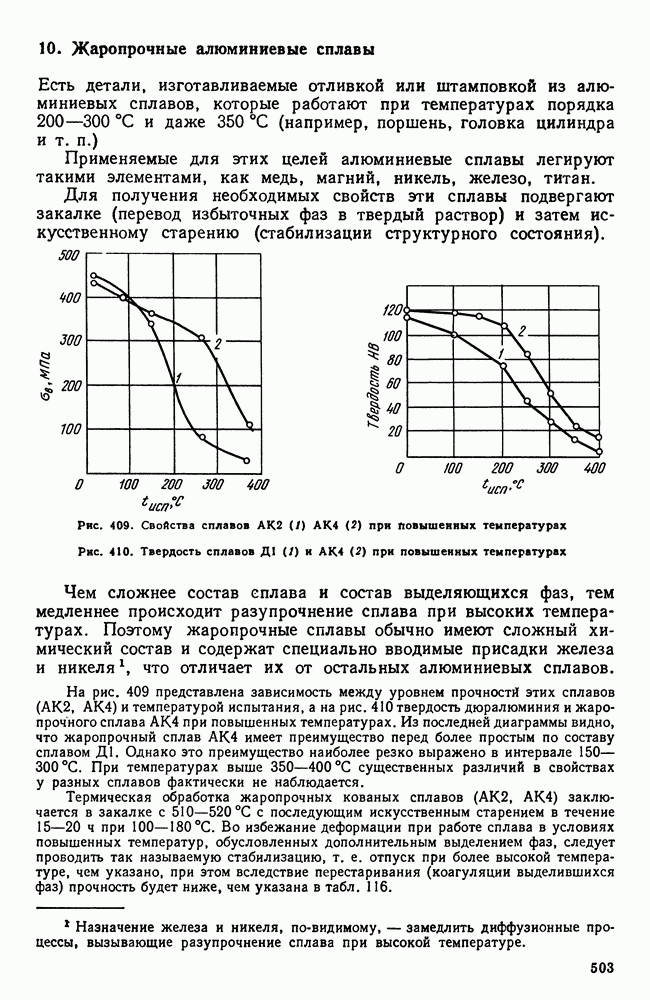
- 10. Жаропрочные алюминиевые сплавы
- 11. Магний
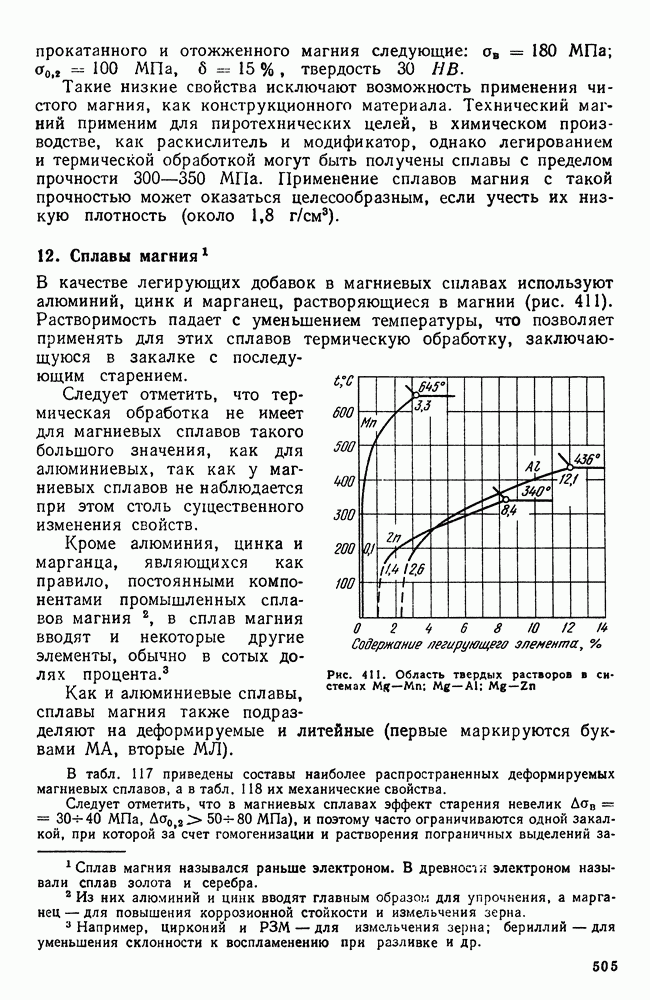
- 12. Сплавы магния
- 13. Бериллий
- 14. Сплавы бериллия
- Глава XXVII. МЕДЬ И ЕЕ СПЛАВЫ
- 2. Сплавы меди с цинком (латуни)
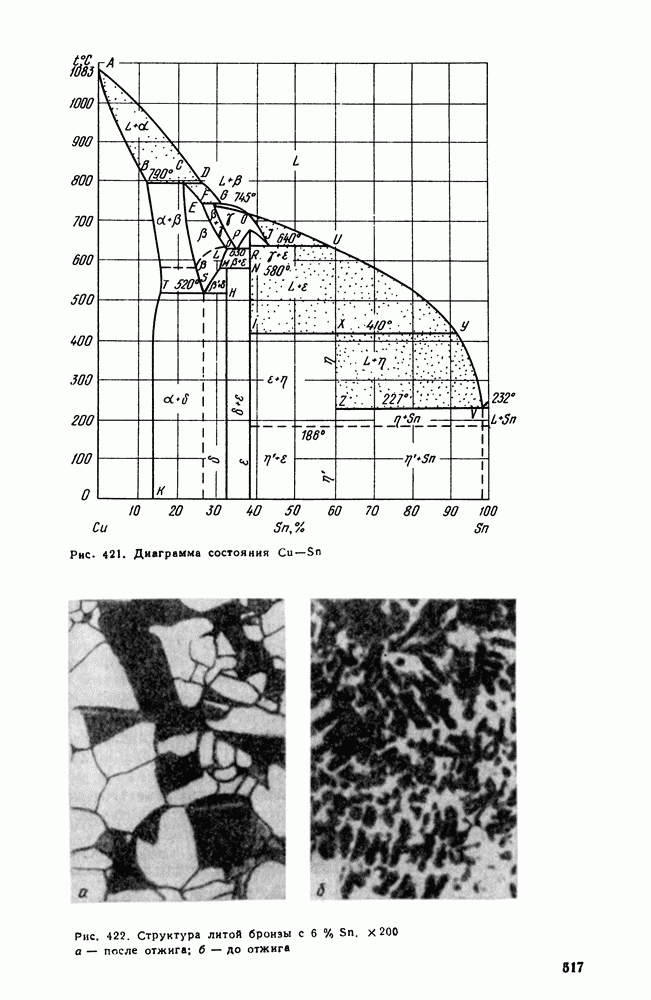
- 3. Сплавы меди с оловом (оловянистые бронзы)
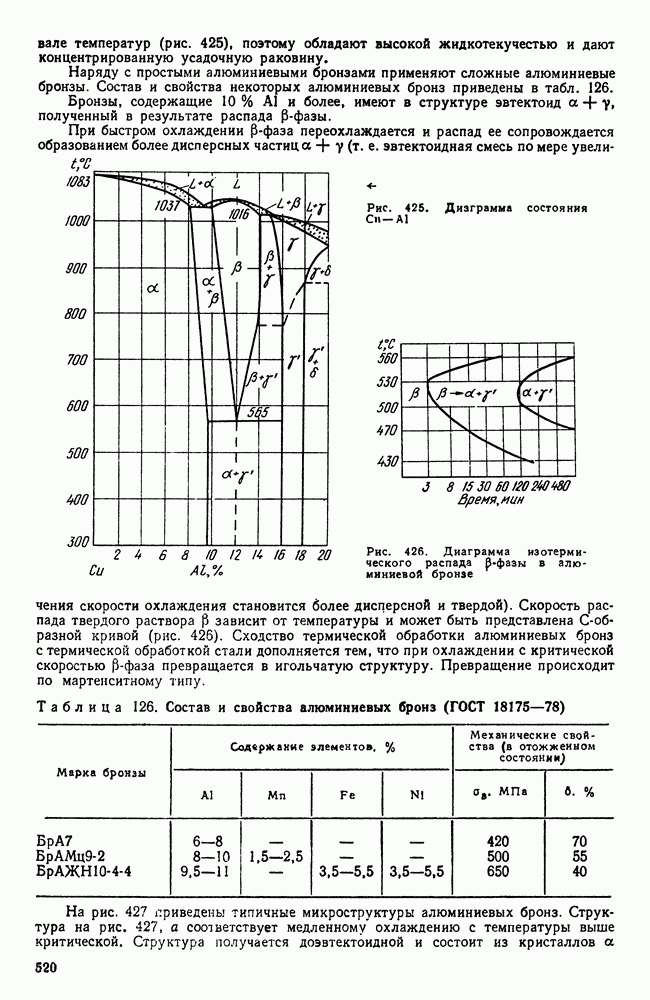
- 4. Сплавы меди с алюминием, кремнием, бериллием и другими элементами
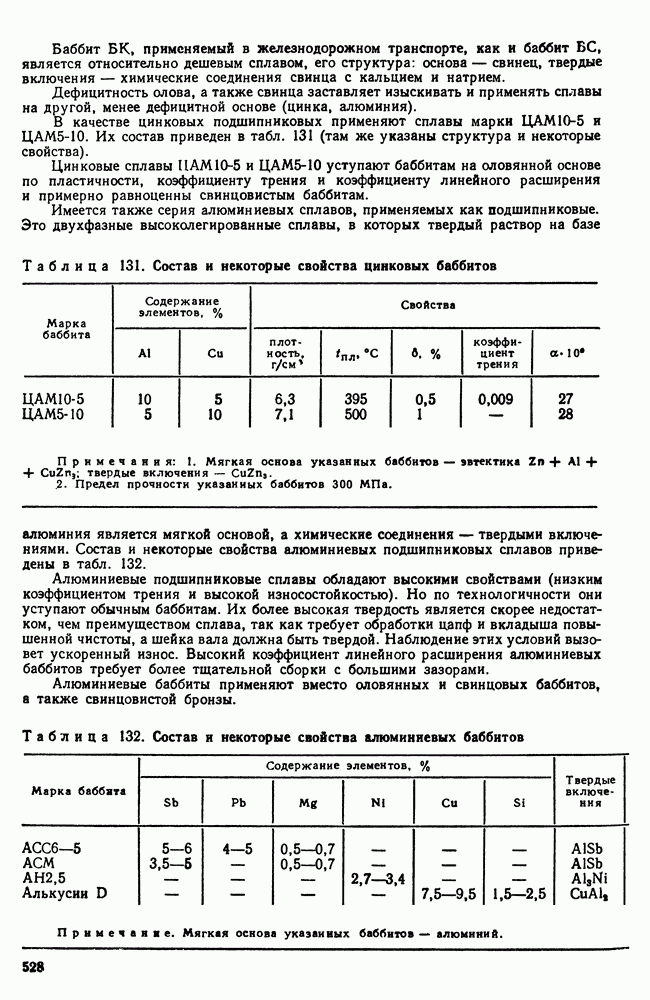
- ГЛАВА XXVIII. ПОДШИПНИКОВЫЕ СПЛАВЫ И ПРИПОИ
- 2. Легкоплавкие подшипниковые сплавы (баббиты)
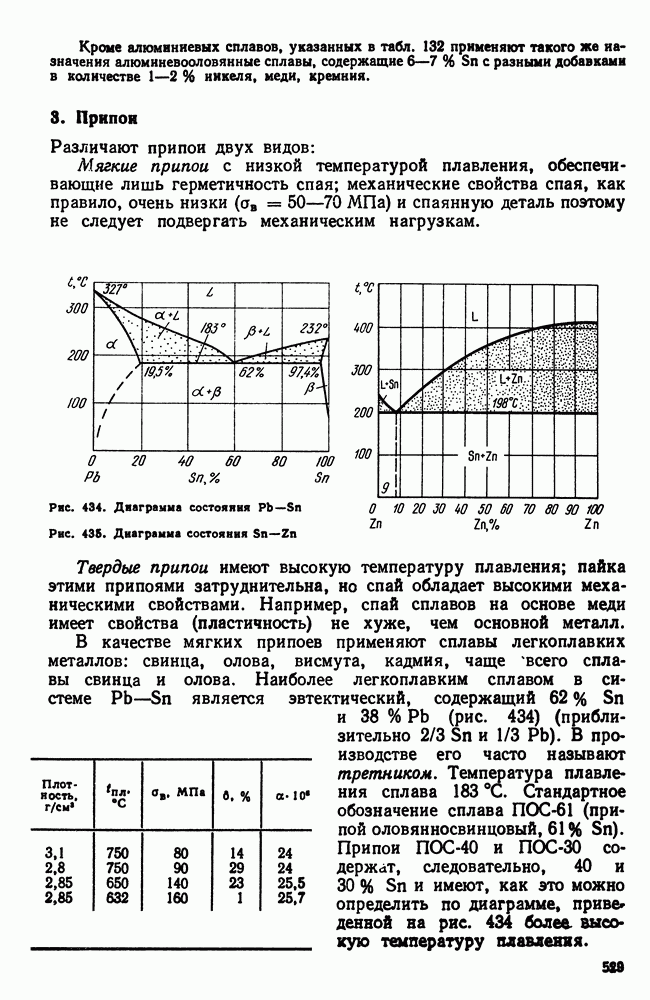
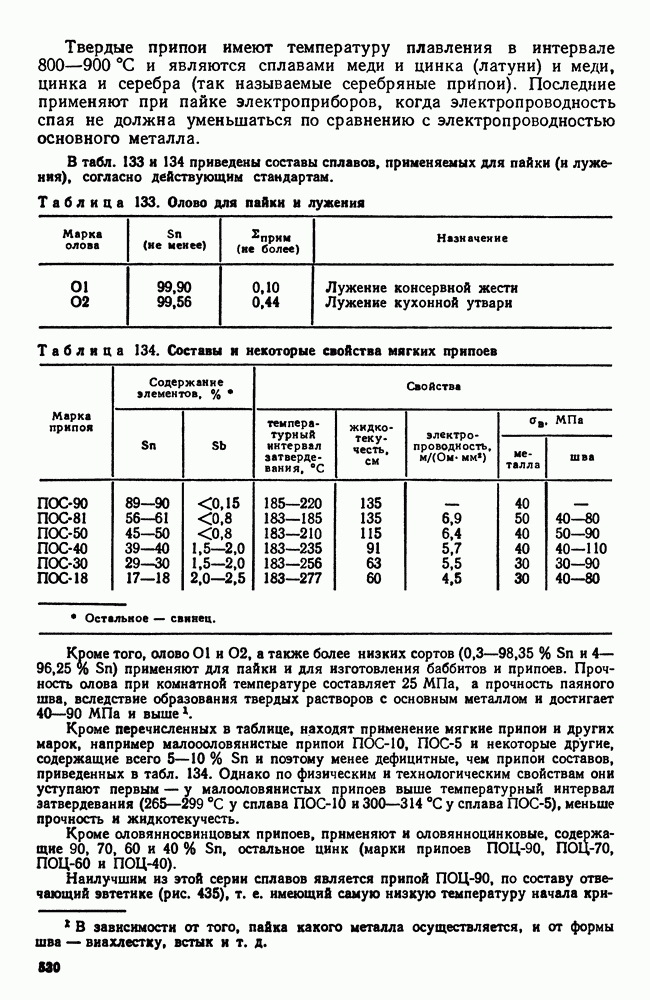
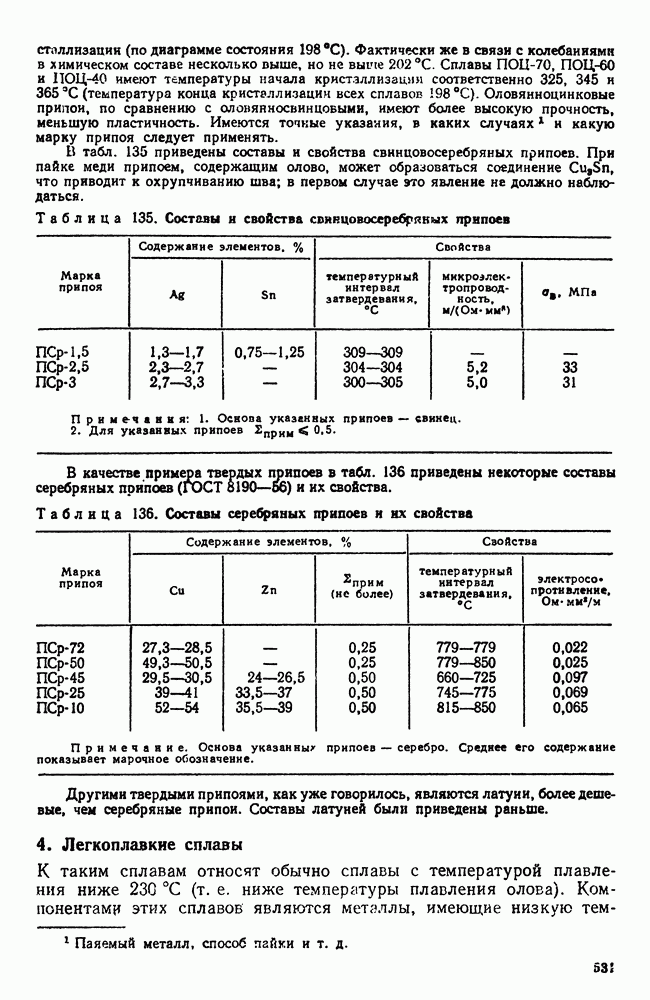
- 3. Припои
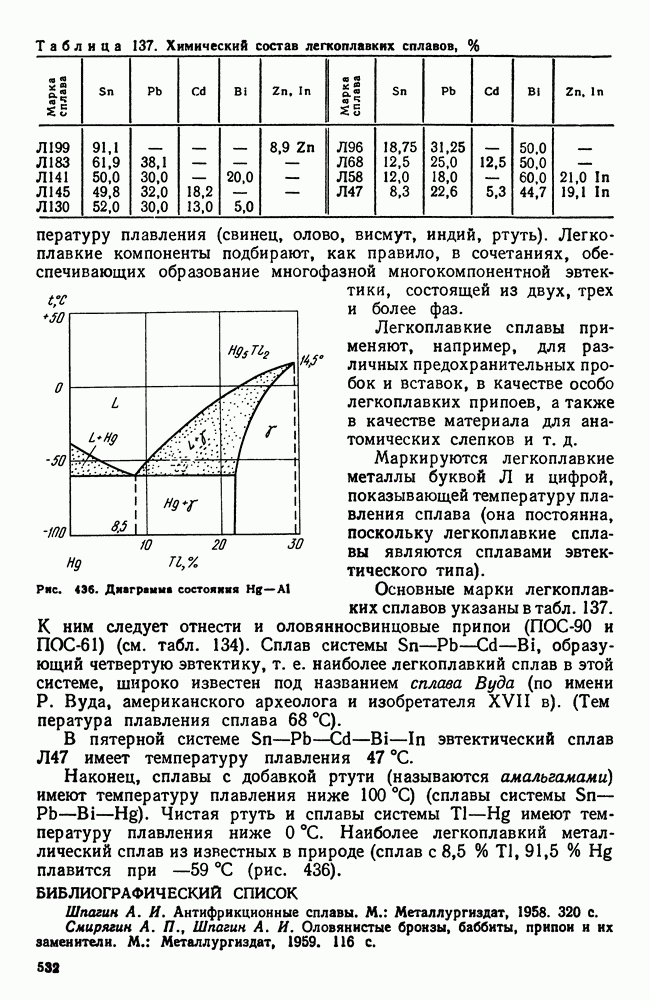
- 4. Легкоплавкие сплавы
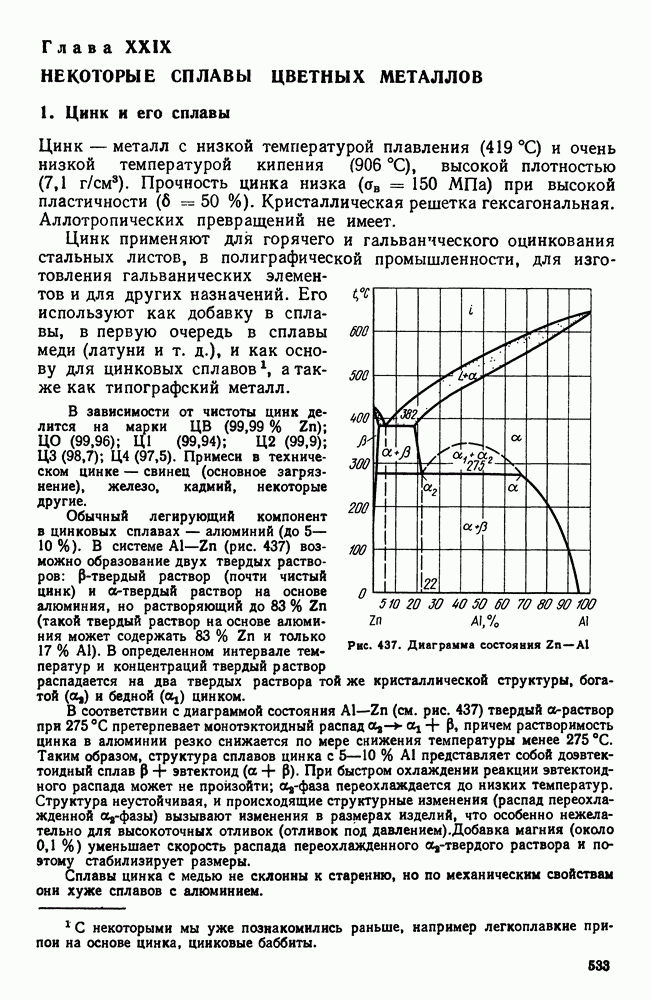
- Глава XXIX. НЕКОТОРЫЕ СПЛАВЫ ЦВЕТНЫХ МЕТАЛЛОВ
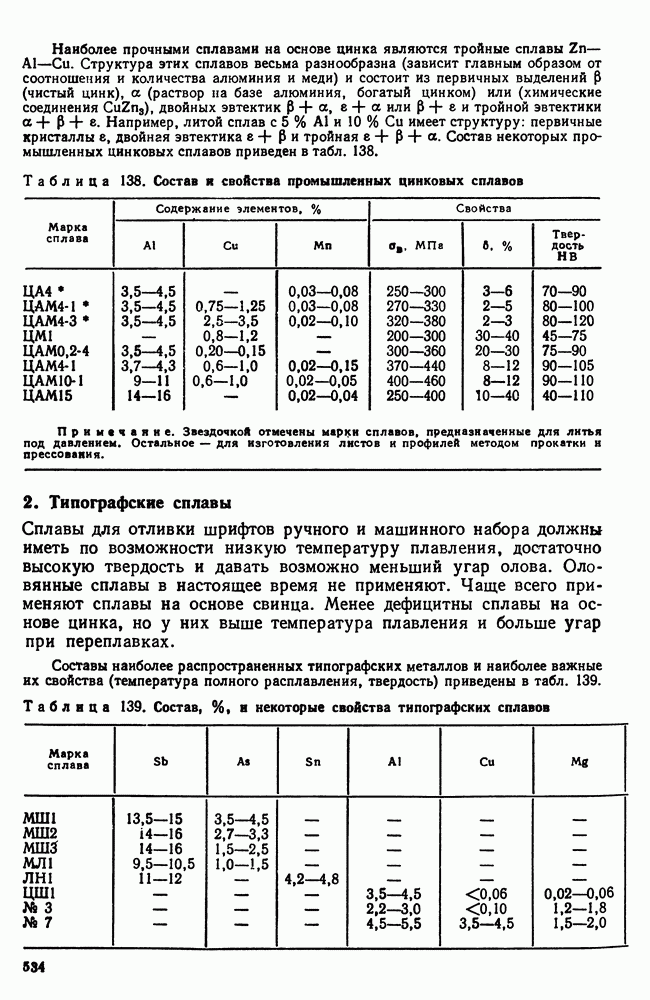
- 2. Типографские сплавы
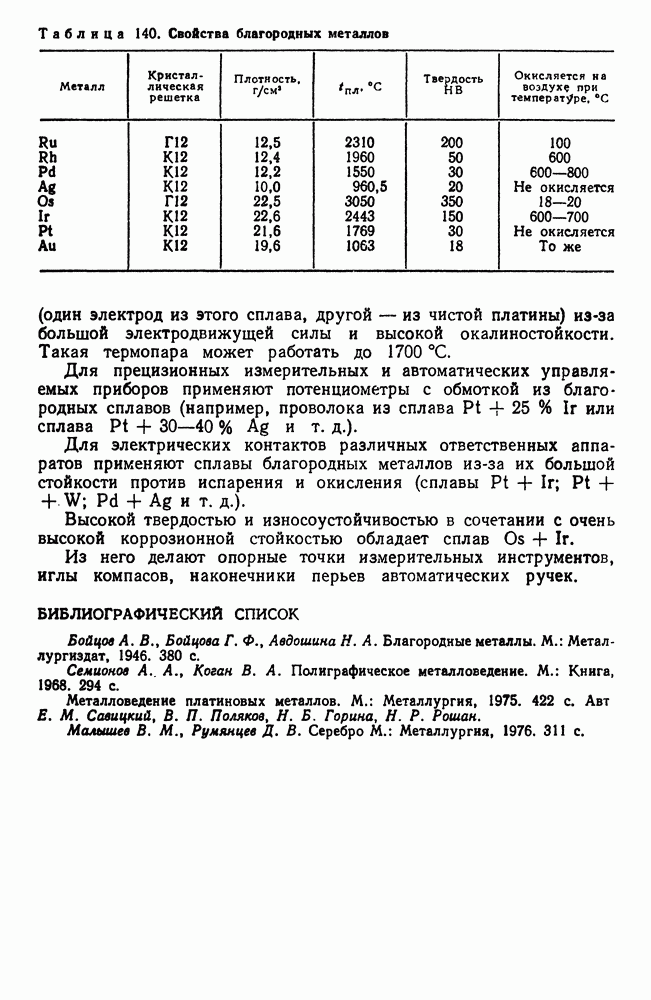
- 3. Благородные металлы