| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ЗАБОЛЕВАНИЯ, СВЯЗАННЫЕ С НАРУШЕНИЕМ МЕТАБОЛИЗМА ПИРИМИДИНОВ (ТАБЛ. 35.3)
Как отмечалось выше, конечными продуктами метаболизма пуринов являются хорошо растворимые в воде соединения, такие, как  аммиак, Р-аланин и пропионат. Вот почему при состояниях, характеризующихся избыточным образованием пиримидинов, клинические симптомы слабо выражены. В случаях гиперурикемии, обусловленной избыточной продукцией ФРПФ, наблюдаются повышенный синтез пиримидиновых нуклеотидов и соответственно увеличенная экскреция конечных продуктов метаболизма, в частности Р-аланина. Поскольку для синтеза тимидилата необходим
аммиак, Р-аланин и пропионат. Вот почему при состояниях, характеризующихся избыточным образованием пиримидинов, клинические симптомы слабо выражены. В случаях гиперурикемии, обусловленной избыточной продукцией ФРПФ, наблюдаются повышенный синтез пиримидиновых нуклеотидов и соответственно увеличенная экскреция конечных продуктов метаболизма, в частности Р-аланина. Поскольку для синтеза тимидилата необходим  нарушения метаболизма фолата и витамина В12 приводят к дефициту ТМР (влияние недостатка витамина В12 реализуется опосредованно).
нарушения метаболизма фолата и витамина В12 приводят к дефициту ТМР (влияние недостатка витамина В12 реализуется опосредованно).
Экскреция с мочой Р-аминоизобутирата—ауто-сомный рецессивный признак. Он распространен главным образом среди жителей Востока. Это нарушение
Таблица 35.3. Наследуемые нарушения метаболизма пиримидинов и связанные с ними изменения активности ферментов

не рассматривается как патологическое состояние (об этом уже шла речь при обсуждении катаболизма пиримидинов).
Описаны два типа первичной наследственной оротовой ацидурии. Более распространенная форма (хотя и встречающаяся весьма редко) связана с утратой во всех тестированных типах клеток функции двух ферментов — оротатфосфорибозилтрансферазы и оротидилат(ОМР)-декарбоксилазы (рис. 35.19). Организм пациентов с этим типом оротовой ацидурии можно считать ауксотрофным по пиримидину. Заболевание легко поддается лечению уридином. В детском возрасте для больных характерны отставание в развитии, мегалобластическая анемия и «оранжевая кристаллоурия» (оротовая кислота). При отсутствии лечения пиримидиновыми нуклеозидами пациенты подвержены инфекциям. Второй тип наследуемой оротовой ацидурии (тип II) связан с недостатком только ОМР-декарбоксилазы (рис. 35.19). У пациентов, страдающих оротовой ацидурией первого типа, основным продуктом экскреции является оротовая кислота. При обследовании больного ацидурией второго типа оказалось, что у него экскрети-руется главным образом оротидин и лишь небольшое количество оротовой кислоты. В эритроцитах пациентов с оротовой ацидурией типа I были значительно повышены удельные активности аспартаттранскарбамоилазы и дигидрооротазы; они, однако, возвратились к норме при пероральном приеме пациентами уридина. Эти наблюдения свидетельствуют о том, что конечные продукты пути биосинтеза пиримидинов регулируют активность рассматриваемых ферментов. В условиях недостатка конечных продуктов происходит дерепрессия, вероятно, координированного характера, по крайней мере этих двух ферментов.
Данные по энзимологии пути биосинтеза пиримидинов позволяют предполагать, что в одной белковой молекуле локализованы активные центры карбамоилфосфатсинтазы, аспартаттранскарбамоилазы и дигидрооротазы, а в другой — активные центры оротат-фосфорибозилтрансферазы и ОМР-декарбоксилазы.
У больных с недостаточностью орнитинтранс-карбамоилазы — митохондриального фермента клеток печени, ответственного за раннюю стадию синтеза мочевины и аргинина, наблюдается увеличение экскреции оротовой кислоты, урацила и уридина. По-видимому, в митохондриях этих пациентов в результате снижения активности орнитинтранскар-бамоилазы накапливается карбамоилфосфат. Митохондриальный карбамоилфосфат диффундирует в цитозоль, где используется как субстрат для синтеза пиримидиновых нуклеотидов de novo. При избыточном образовании оротовой кислоты диагностируется оротовая ацидурия. Обычно она проявляется в легкой форме и не сопровождается образованием кристаллов. Синтез и экскреция оротовой кислоты у таких больных усиливаются при употреблении в пищу продуктов богатых азотом, таких, как мясо.
Оротовую ацидурию могут вызывать по крайней мере два лекарственных препарата. Аллопуринол (4-гидроксипиразолопиримидин) - пуриновый аналог, ингибирующий ксантиноксидазу. Этот препарат широко используется для лечения некоторых форм подагры. Аллопуринол может фосфорибозилироваться оротат-фосфорибозилтрансферазой, конкурентно ингибируя фосфорибозилирование оротовой

Рис. 35.19. А. Ферментные дефекты и их последствия при оротовой ацидурии типа I, которая характеризуется недостаточностью двух ферментов — оротатфосфорибозилтрансферазы и оротидилат-декарбоксилазы. Б. Недостаточность оротидилат-декарбоксилазы, приводящая к оротовой ацидурии типа II. Пунктирные линии со знаком минус показывают пути ингибирования по принципу обратной связи в нормальных условиях. При оротовой ацидурии типа I с мочой экскретируется оротовая кислота. При оротовой ацидурии типа II в роли экскретируемых соединений выступают оротовая кислота и оротидин. Аббревиатуры расшифрованы на рис. 35.15.(Redrawn and reproduced, with permission, from Smith L. H. Ir. Pyrimidine metabolism in man. N. Engl. Med. 1973, 288, p. 764) кислоты. Более того, образующийся необычный нуклеотид подавляет оротидилатдекарбоксилазу, вызывая тем самым оротовую ацидурию и оротидинурию. Однако путь биосинтеза пиримидинов, по крайней мере у человека, «приспосабливается» к такому ингибированию, и «пиримидиновое голодание» имеет место только на ранних стадиях лечения препаратом.
6-Азауридин после превращения в 6-азауридилат функционирует как конкурентный ингибитор ОМР-декарбоксилазы, что приводит к увеличению экскреции оротовой кислоты и оротидина.
При специфическом поражении митохондрий клеток печени (синдром Рейе) имеет место вторичная оротовая ацидурия. Дело в том, что пораженные митохондрии оказываются неспособными утилизировать карбамоилфосфат, который, как и в случае наследуемой недостаточности орнитинтранскарбамоилазы, вызывает избыточное образование оротовой кислоты.
ЛИТЕРАТУРА
Ames В. N. et al. Uric acid provides an antioxidant defense in humans against oxidant- and radical-caused aging and cancer: A hypothesis, Proc. Natl. Acad. Sci. USA, 1981, 78, 6858.
Henderson J. F. Regulation of Purine Biosynthesis, Monograph, No. 170, American Chemical Society, 1972.
Henderson J.F., Paterson A.R.P. Nucleotide Metabolism: An Introduction, Academic Press, 1973.
Jones M. Pyrimidine nucleotide biosynthesis in animal cells, Annu. Rev. Biochem., 1980, 49, 253.
Kempe T. D. et al. Stable mutants of mammalian cells that overproduce the first three enzymes of pyrimidine nucleotide biosynthesis, Cell, 1976, 9, 541.
Martin D. W. Jr., Gelfand E. W. Biochemistry of diseases of im-munodevelopment, Annu. Rev. Biochem., 1981, 50, 845.
Smith L.H. Jr. Pyrimidine metabolism in man, N. Engl. J. Med., 1973, 288, 764.
Stanbury J. B. et al. (eds.) The Metabolic Basis of Inherited Disease, 5th ed., McGraw-Hill, 1983.
Thelander L., Reichard P. Reduction of ribonucleotides, Annu. Rev. Biochem., 1979, 48, 133.
Wyngaarden J. B., Kelley W. N. Gout and Hyperuricemia, Gru-ne and Stratton, 1976.
| << Предыдущий параграф | Следующий параграф >> |
- Раздел IV. Структура, функция и репликация информационных макромолекул
- СТРУКТУРА ПУРИНОВЫХ И ПИРИМИДИНОВЫХ ОСНОВАНИЙ
- ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА ПУРИНОВЫХ И ПИРИМИДИНОВЫХ ОСНОВАНИЙ
- НУКЛЕОЗИДЫ И НУКЛЕОТИДЫ
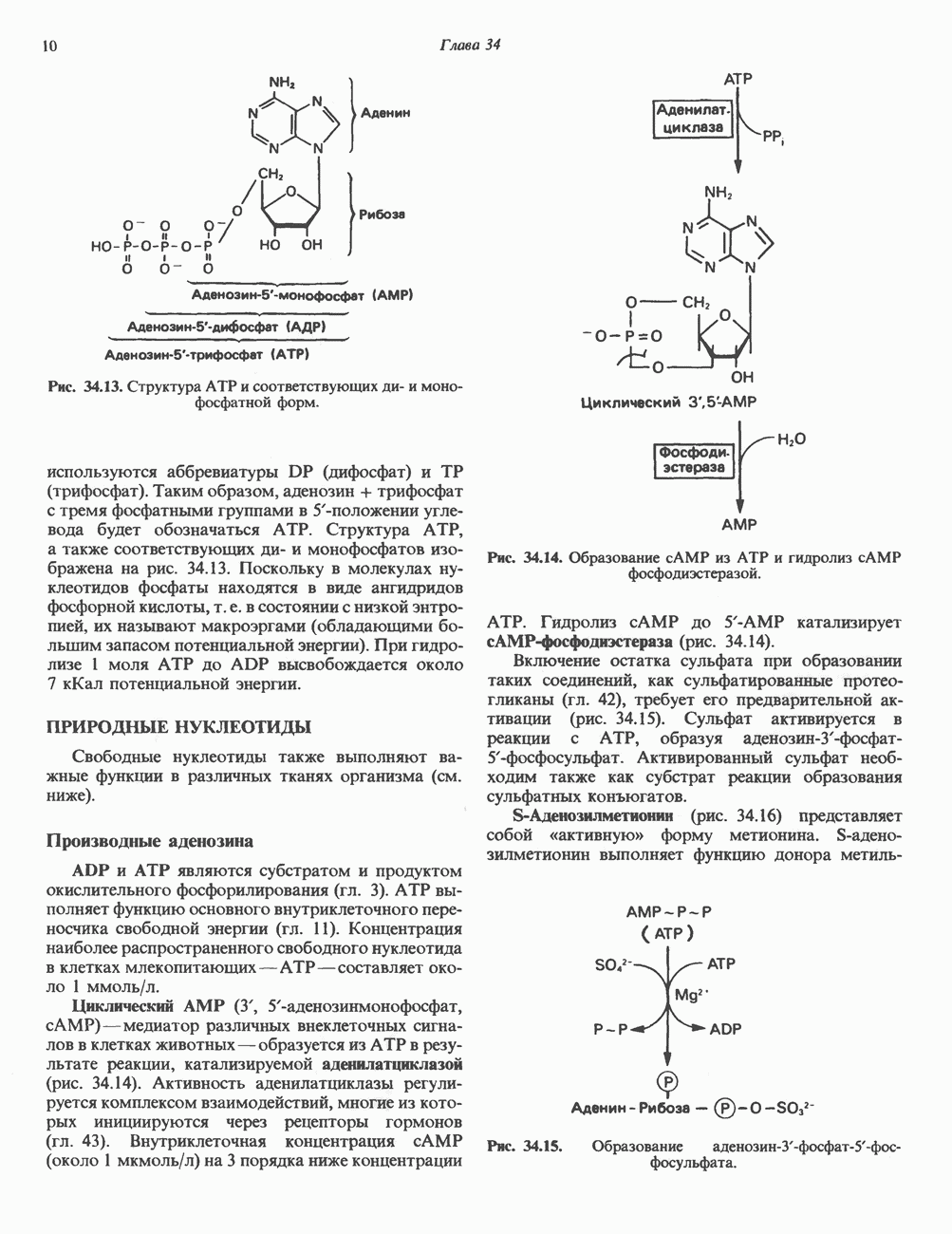
- ПРИРОДНЫЕ НУКЛЕОТИДЫ
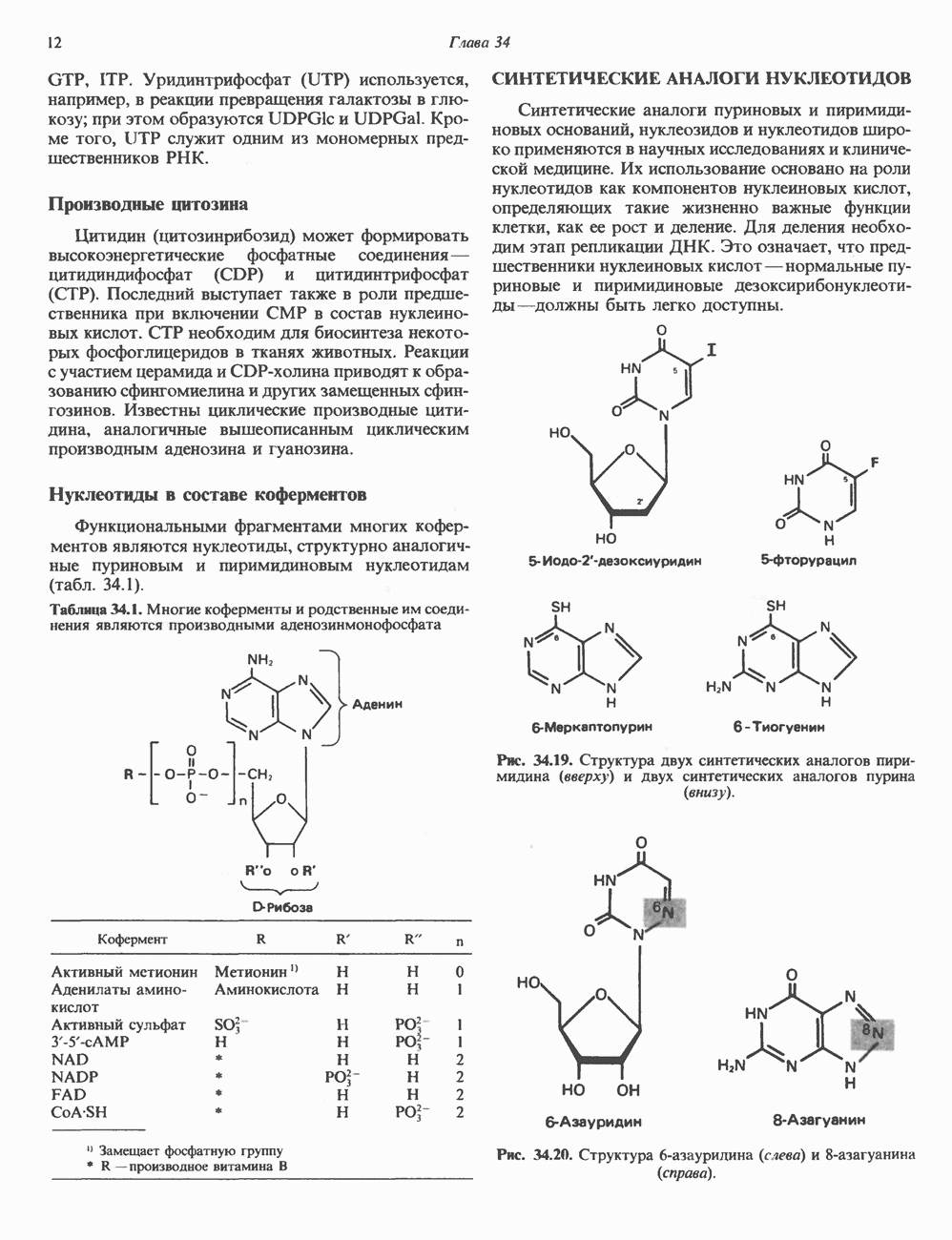
- СИНТЕТИЧЕСКИЕ АНАЛОГИ НУКЛЕОТИДОВ
- Глава 35. Метаболизм пуриновых и пиримидиновых нуклеотидов
- УСВОЕНИЕ
- ПУРИНЫ
- ПИРИМИДИНЫ
- КЛИНИЧЕСКИЕ НАРУШЕНИЯ МЕТАБОЛИЗМА ПУРИНОВ (ТАБЛ. 35.1)
- ЗАБОЛЕВАНИЯ, СВЯЗАННЫЕ С НАРУШЕНИЕМ МЕТАБОЛИЗМА ПИРИМИДИНОВ (ТАБЛ. 35.3)
- Глава 36. Технология рекомбинантных ДНК
- ОСНОВНЫЕ СВОЙСТВА ДНК
- ОСНОВНЫЕ ПОНЯТИЯ ГЕННОЙ ИНЖЕНЕРИИ
- НЕКОТОРЫЕ ПРАКТИЧЕСКИЕ ПРИЛОЖЕНИЯ ТЕХНОЛОГИИ РЕКОМБИНАНТНОЙ ДНК
- ГЕННАЯ ИНЖЕНЕРИЯ И АНАЛИЗ МОЛЕКУЛЯРНОЙ ПРИРОДЫ ЗАБОЛЕВАНИЙ
- СЛОВАРЬ-СПРАВОЧНИК
- ЛИТЕРАТУРА
- Глава 37. Структура и функция нуклеиновых кислот
- ДНК
- РНК
- Глава 38. Организация и репликация ДНК
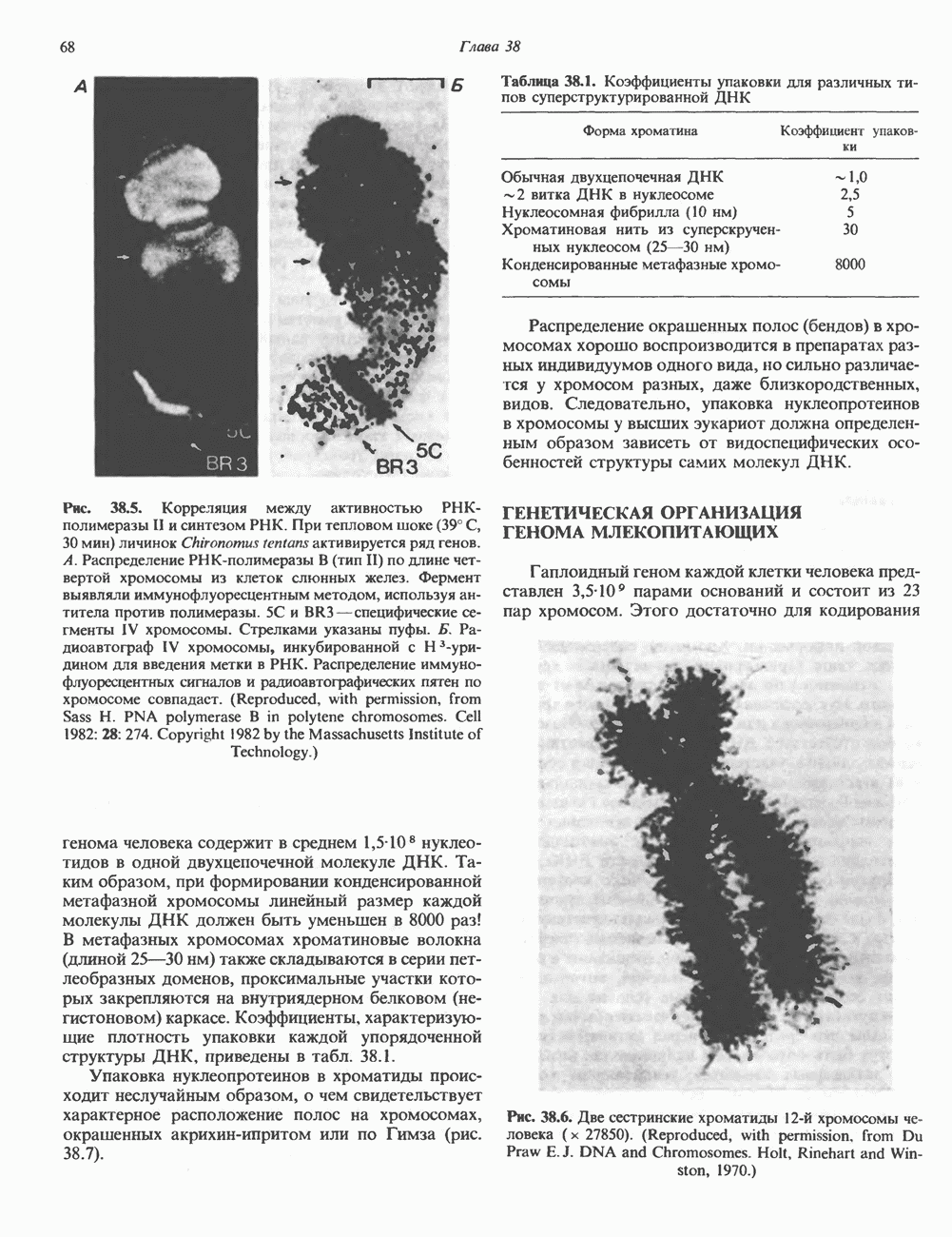
- ХРОМАТИН
- ГИСТОНЫ И НУКЛЕОСОМЫ
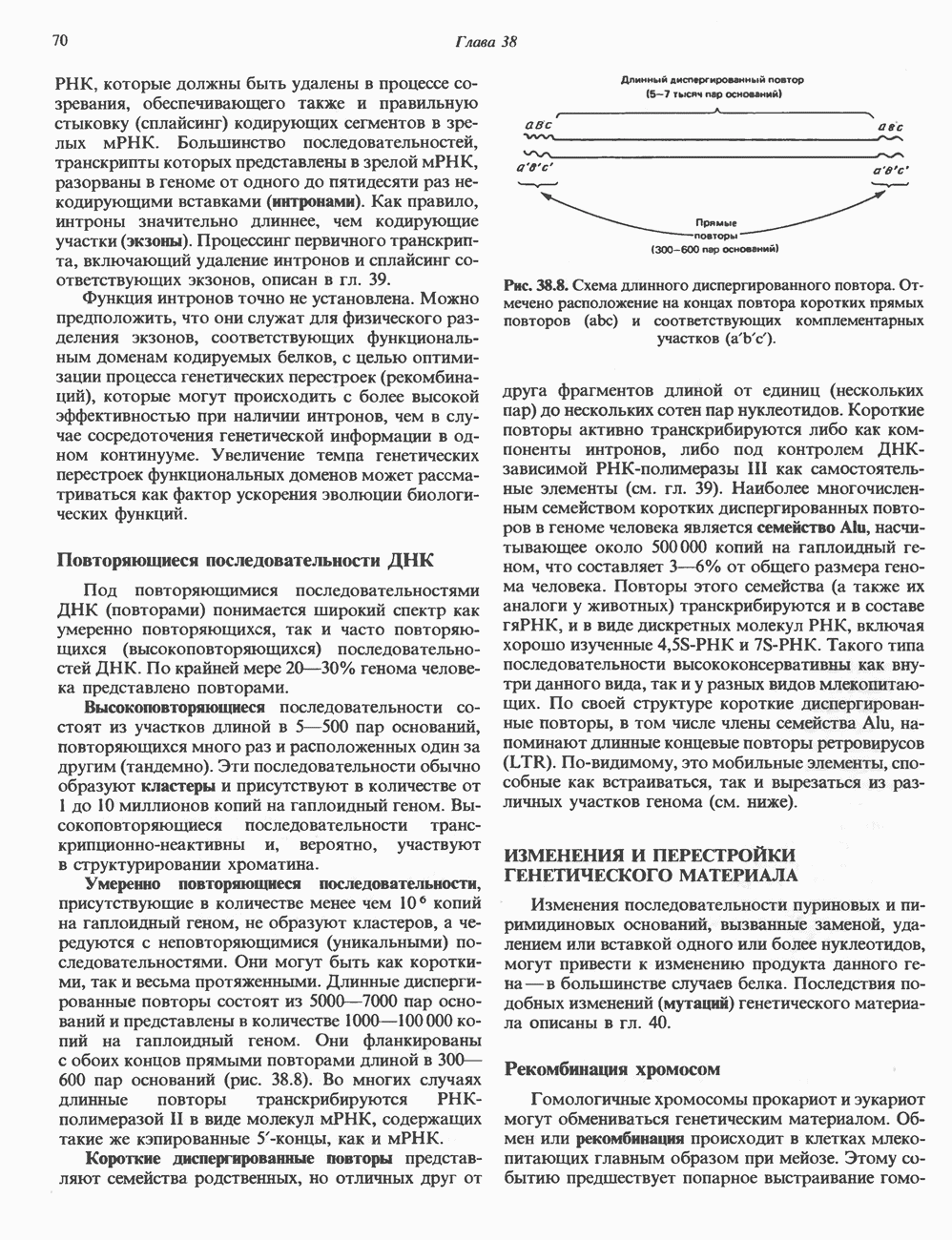
- ГЕНЕТИЧЕСКАЯ ОРГАНИЗАЦИЯ ГЕНОМА МЛЕКОПИТАЮЩИХ
- ИЗМЕНЕНИЯ И ПЕРЕСТРОЙКИ ГЕНЕТИЧЕСКОГО МАТЕРИАЛА
- СИНТЕЗ И РЕПЛИКАЦИЯ ДНК
- Глава 39. Синтез и процессинг РНК
- СИНТЕЗ РНК
- ПРОЦЕССИНГ МОЛЕКУЛ РНК
- НУКЛЕАЗЫ
- Глава 40. Синтез белка и генетический код
- ИНФОРМАЦИОННЫЙ ПОТОК
- КОДОНЫ И СИНТЕЗ БЕЛКА
- ТРАНСПОРТНЫЕ РНК И СИНТЕЗ БЕЛКА
- МУТАЦИИ
- ПРОЦЕСС СИНТЕЗА БЕЛКА
- Глава 41. Регуляция экспрессии генов
- РЕГУЛЯЦИЯ ЭКСПРЕССИИ ГЕНОВ У ПРОКАРИОТ
- РЕГУЛЯЦИЯ ЭКСПРЕССИИ ГЕНОВ У ЭУКАРИОТ
- Раздел V. Биохимия внутри- и межклеточных коммуникаций
- Глава 42. Мембраны: структура, сборка и функции
- ПОДДЕРЖАНИЕ НОРМАЛЬНОГО СОСТАВА СРЕДЫ
- СТРУКТУРА МЕМБРАН
- ОРГАНИЗАЦИЯ МЕМБРАННЫХ ЛИПИДОВ
- МЕМБРАННЫЕ БЕЛКИ
- ИСКУССТВЕННЫЕ МЕМБРАНЫ
- ЖИДКОСТНО-МОЗАИЧНАЯ МОДЕЛЬ МЕМБРАН
- СБОРКА МЕМБРАН
- СПЕЦИАЛИЗИРОВАННЫЕ ФУНКЦИИ МЕМБРАН
- ТРАНСМЕМБРАННЫЙ ПЕРЕНОС МАЛЫХ МОЛЕКУЛ
- ТРАНСМЕМБРАННОЕ ПЕРЕМЕЩЕНИЕ МАКРОМОЛЕКУЛ
- ПЕРЕДАЧА ИНФОРМАЦИИ В КЛЕТКУ
- МЕЖКЛЕТОЧНЫЕ КОНТАКТЫ И КОММУНИКАЦИИ
- Глава 43. Характеристика эндокринной системы
- ОБЩИЕ СВОЙСТВА
- РАЗНООБРАЗИЕ ЭНДОКРИННОЙ СИСТЕМЫ
- КОНЦЕПЦИЯ ЖЕЛЕЗЫ-МИШЕНИ
- КОНЦЕПЦИЯ РЕГУЛЯТОРНОГО МЕХАНИЗМА ОБРАТНОЙ СВЯЗИ
- РЕЦЕПТОРЫ ГОРМОНОВ
- Глава 44. Действие гормонов
- КЛАССИФИКАЦИЯ ГОРМОНОВ
- МЕХАНИЗМ ДЕЙСТВИЯ ГОРМОНОВ I ГРУППЫ
- МЕХАНИЗМ ДЕЙСТВИЯ ГОРМОНОВ II ГРУППЫ (ПЕПТИДНЫХ ГОРМОНОВ)
- 1. сАМР КАК ВТОРОЙ ПОСРЕДНИК
- 2. ДЕЙСТВИЕ ГОРМОНОВ, ОПОСРЕДОВАННОЕ КАЛЬЦИЕМ И ФОСФОИНОЗИТИДАМИ
- 3. ГОРМОНЫ С НЕИЗВЕСТНЫМ ВНУТРИКЛЕТОЧНЫМ ПОСРЕДНИКОМ
- Глава 45. Гормоны гипофиза и гипоталамуса
- ГОРМОНЫ ГИПОТАЛАМУСА
- ГОРМОНЫ ПЕРЕДНЕЙ ДОЛИ ГИПОФИЗА
- I. ГРУППА ГОРМОН РОСТА — ПРОЛАКТИН—ХОРИОНИЧЕСКИЙ СОМАТОМАММОТРОПИН
- 2. ГРУППА ГЛИКОПРОТЕИНОВЫХ ГОРМОНОВ
- 3. СЕМЕЙСТВО ПЕПТИДОВ ПРООПИОМЕЛАНОКОРТИНА (ПОМК)
- ГОРМОНЫ ЗАДНЕЙ ДОЛИ ГИПОФИЗА
- 1. ОКСИТОЦИН
- 2. АНТИДИУРЕТИЧЕСКИЙ ГОРМОН (АДГ; ВАЗОПРЕССИН)
- Глава 46. Гормоны щитовидной железы
- БИОСИНТЕЗ ТИРЕОИДНЫХ ГОРМОНОВ
- 1. МЕТАБОЛИЗМ ТИРЕОГЛОБУЛИНА
- 2. МЕТАБОЛИЗМ ИОДИДА
- ТРАНСПОРТ И МЕТАБОЛИЗМ ГОРМОНОВ ЩИТОВИДНОЙ ЖЕЛЕЗЫ
- РЕГУЛЯЦИЯ СИНТЕЗА И ВЫСВОБОЖДЕНИЯ ГОРМОНОВ ЩИТОВИДНОМ ЖЕЛЕЗЫ
- МЕХАНИЗМ ДЕЙСТВИЯ ТИРЕОИДНЫХ ГОРМОНОВ
- ПАТОФИЗИОЛОГИЯ
- Глава 47. Гормоны, регулирующие метаболизм кальция
- ОБЩИЕ ХАРАКТЕРИСТИКИ
- ГОМЕОСТАЗ КАЛЬЦИЯ
- ГОРМОНЫ, УЧАСТВУЮЩИЕ В ГОМЕОСТАЗЕ КАЛЬЦИЯ
- 2. КАЛЬЦИТРИОЛ
- 3. КАЛЬЦИТОНИН (КТ)
- Глава 48. Гормоны коры надпочечников
- ГОРМОНЫ
- НОМЕНКЛАТУРА И ХИМИЯ СТЕРОИДОВ
- БИОСИНТЕЗ СТЕРОИДНЫХ ГОРМОНОВ НАДПОЧЕЧНИКОВ
- СЕКРЕЦИЯ, ТРАНСПОРТ И МЕТАБОЛИЗМ СТЕРОИДНЫХ ГОРМОНОВ НАДПОЧЕЧНИКОВ
- РЕГУЛЯЦИЯ СИНТЕЗА СТЕРОИДНЫХ ГОРМОНОВ НАДПОЧЕЧНИКОВ
- ВОЗДЕЙСТВИЕ СТЕРОИДНЫХ ГОРМОНОВ НАДПОЧЕЧНИКОВ НА МЕТАБОЛИЗМ
- КЛАССИФИКАЦИЯ И МЕХАНИЗМ ДЕЙСТВИЯ СТЕРОИДНЫХ ГОРМОНОВ
- ПАТОФИЗИОЛОГИЯ КОРЫ НАДПОЧЕЧНИКОВ
- Глава 49. Гормоны мозгового вещества надпочечников
- БИОСИНТЕЗ КАТЕХОЛАМИНОВ
- ЗАПАСАНИЕ И СЕКРЕЦИЯ КАТЕХОЛАМИНОВ
- МЕТАБОЛИЗМ КАТЕХОЛАМИНОВ
- РЕГУЛЯЦИЯ СИНТЕЗА КАТЕХОЛАМИНОВ
- КЛАССИФИКАЦИЯ И МЕХАНИЗМ ДЕЙСТВИЯ КАТЕХОЛАМИНОВ
- ПАТОФИЗИОЛОГИЯ МОЗГОВОГО СЛОЯ НАДПОЧЕЧНИКОВ
- Глава 50. Гормоны половых желез
- ГОРМОНЫ СЕМЕННИКОВ
- РЕГУЛЯЦИЯ ФУНКЦИИ СЕМЕННИКОВ
- ФИЗИОЛОГИЧЕСКИЕ ЭФФЕКТЫ ГОРМОНОВ СЕМЕННИКОВ
- МЕХАНИЗМ ДЕЙСТВИЯ ГОРМОНОВ СЕМЕННИКОВ
- ПАТОФИЗИОЛОГИЯ РЕПРОДУКТИВНОЙ СИСТЕМЫ У МУЖЧИН
- БИОСИНТЕЗ И МЕТАБОЛИЗМ ГОРМОНОВ ЯИЧНИКОВ
- РЕГУЛЯЦИЯ И ФИЗИОЛОГИЧЕСКОЕ ДЕЙСТВИЕ ГОРМОНОВ ЯИЧНИКОВ
- МЕХАНИЗМ ДЕЙСТВИЯ ГОРМОНОВ ЯИЧНИКОВ
- ПАТОФИЗИОЛОГИЯ ЖЕНСКОЙ РЕПРОДУКТИВНОЙ СИСТЕМЫ
- ГОРМОНЫ ПОЛОВЫХ ЖЕЛЕЗ И ПОЛОВАЯ ДИФФЕРЕНЦИРОВКА
- ФЕНОТИПИЧЕСКИЙ ПОЛ
- Глава 51. Гормоны поджелудочной железы
- ИНСУЛИН
- ИНСУЛИНОПОДОБНЫЕ ФАКТОРЫ РОСТА
- ГЛЮКАГОН
- СОМАТОСТАТИН
- ПАНКРЕАТИЧЕСКИЙ ПОЛИПЕПТИД
- Глава 52. Гормоны желудочно-кишечного тракта
- СВОЙСТВА ГОРМОНОВ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА
- СЕМЕЙСТВО СЕКРЕТИНА
- СЕМЕЙСТВО ГАСТРИН—ХОЛЕЦИСТОКИНИН
- ДРУГИЕ ПЕПТИДЫ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА
- Раздел VI. Частные вопросы
- Питание, пищеварение и всасывание
- ПИТАНИЕ
- РАСХОД ЭНЕРГИИ
- АЗОТ АМИНОКИСЛОТ И ПОТРЕБНОСТЬ В СПЕЦИФИЧЕСКИХ АМИНОКИСЛОТАХ
- ПОТРЕБНОСТЬ В УГЛЕВОДАХ
- ПОТРЕБНОСТЬ В ПИЩЕВЫХ ВОЛОКНАХ
- ПОТРЕБНОСТЬ В ЛИПИДАХ
- ПОТРЕБНОСТЬ В ВИТАМИНАХ
- ПОТРЕБНОСТЬ В МИНЕРАЛЬНЫХ ВЕЩЕСТВАХ
- РЕКОМЕНДАЦИИ В ОБЛАСТИ ДИЕТЫ
- ПИЩЕВАРЕНИЕ
- ПИЩЕВАРЕНИЕ В ЖЕЛУДКЕ
- ПАНКРЕАТИЧЕСКОЕ И КИШЕЧНОЕ ПИЩЕВАРЕНИЕ
- ВСАСЫВАНИЕ В ЖЕЛУДОЧНО-КИШЕЧНОМ ТРАКТЕ
- ВСАСЫВАНИЕ ГЛЮКОЗЫ
- ВСАСЫВАНИЕ ЛИПИДОВ
- ВСАСЫВАНИЕ АМИНОКИСЛОТ И БЕЛКА
- ПРОЦЕССЫ ГНИЕНИЯ И БРОЖЕНИЯ В КИШЕЧНИКЕ
- Глава 54. Гликопротеины и протеогликаны
- ГЛИКОПРОТЕИНЫ
- ОПРЕДЕЛЕНИЕ, ОЧИСТКА И СТРУКТУРНЫЙ АНАЛИЗ ГЛИКОПРОТЕИНОВ
- САХАРА, ПРИСУТСТВУЮЩИЕ В ГЛИКОПРОТЕИНАХ
- НУКЛЕОТИДСАХАРА
- ЭКЗОГЛИКОЗИДАЗЫ И ЭНДОГЛИКОЗИДАЗЫ
- ЛЕКТИНЫ
- КЛАССИФИКАЦИЯ ГЛИКОПРОТЕИНОВ
- I-КЛЕТОЧНАЯ БОЛЕЗНЬ
- АНТИГЕНЫ ГРУПП КРОВИ
- ПРОТЕОГЛИКАНЫ И ГЛИКОЗАМИНОГЛИКАНЫ
- ДЕГРАДАЦИЯ ПОЛИСАХАРИДНЫХ КОМПОНЕНТОВ ГЛИКОПРОТЕИНОВ И ПРОТЕОГЛИКАНОВ
- ФУНКЦИИ ГЛИКОЗАМИНОГЛИКАНОВ И ПРОТЕОГЛИКАНОВ
- Глава 55. Плазма крови и процесс свертывания
- ФУНКЦИИ КРОВИ
- БЕЛКИ ПЛАЗМЫ
- СВЕРТЫВАНИЕ КРОВИ
- Глава 56. Сократительные и структурные белки
- МЫШЦЫ
- КЛЕТОЧНАЯ ПОДВИЖНОСТЬ И ЦИТОСКЕЛЕТ
- Глава 57. Рак, онкогены, факторы роста
- БИОХИМИЧЕСКИЕ ЛАБОРАТОРНЫЕ ТЕСТЫ И РАК
- ПРИЧИНЫ ВОЗНИКНОВЕНИЯ РАКОВЫХ ОПУХОЛЕЙ
- ОНКОГЕННЫЕ ВИРУСЫ
- ТРАНСФОРМАЦИЯ
- ОНКОГЕНЫ
- ПОЛИПЕПТИДНЫЕ ФАКТОРЫ РОСТА
- ДЕЙСТВИЕ ФАКТОРОВ РОСТА ПО ЭНДОКРИННОМУ, ПАРАКРИННОМУ ИЛИ АУТОКРИННОМУ ТИПУ
- БИОХИМИЧЕСКИЕ МЕХАНИЗМЫ ДЕЙСТВИЯ ФАКТОРОВ РОСТА
- ФАКТОРЫ РОСТА И ОНКОГЕНЫ
- ПРОГРЕССИЯ ОПУХОЛЕЙ
- МЕТАСТАЗИРОВАНИЕ
- Приложение
- ХИМИЧЕСКИЙ СОСТАВ КРОВИ И ЖИДКИХ СРЕД ОРГАНИЗМА
- СТАНДАРТНЫЕ КЛИНИКО-ЛАБОРАТОРНЫЕ ПОКАЗАТЕЛИ В ТРАДИЦИОННОЙ СИСТЕМЕ И СИСТЕМЕ СИ
- НОРМАЛЬНЫЕ ЛАБОРАТОРНЫЕ ПОКАЗАТЕЛИ
- Список сокращений