| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ГЕННАЯ ИНЖЕНЕРИЯ И АНАЛИЗ МОЛЕКУЛЯРНОЙ ПРИРОДЫ ЗАБОЛЕВАНИЙ
Нормальные генетические варианты
Существуют нормальные варианты последовательностей ДНК человека (полиморфизм). Такие варианты встречаются примерно 1 раз на 500 нуклеотидов или 107 раз на геном. Сюда входят делеции, вставки, а также единичные замены нуклеотидов. У здоровых людей эти изменения либо не затрагивают кодирующих последовательностей, либо происходят в функционально несущественных участках кодирующих областей ДНК. Полиморфизм структуры ДНК может быть прямо связан и с определенными заболеваниями. В последние годы феномен полиморфизма все чаще используется для идентификации соответствующих специфических генов.
Генетические изменения, вызывающие заболевания
На более ранних этапах развития медицинской генетики существовало представление, что большинство наследственных болезней вызвано точковыми мутациями, которые проявляются в функциональном несовершенстве соответствующего измененного белка. Роль точковых мутаций в возникновении наследственных патологий действительно велика, к этому следует добавить только, что генетические заболевания могут быть вызваны нарушениями на любой стадии процесса, представленного на рис. 36.1. Это положение хорошо иллюстрируется исследованиями гена  -глобина, имеющего кластерную организацию и картированного на одиннадцатой хромосоме (рис. 36.7, 36.8). Биосинтез дефектного
-глобина, имеющего кластерную организацию и картированного на одиннадцатой хромосоме (рис. 36.7, 36.8). Биосинтез дефектного  -глобина служит причиной целого ряда заболеваний. Патологические симптомы могут быть связаны с нарушениями как в самом гене, так и в его окружении (табл. 36.6).
-глобина служит причиной целого ряда заболеваний. Патологические симптомы могут быть связаны с нарушениями как в самом гене, так и в его окружении (табл. 36.6).
Точковые мутации
Классический пример заболевания, связанного с точковой мутацией, - серповидноклеточная анемия. Болезнь вызывается заменой всего лишь одного из  оснований, составляющих полный геном человека: в шестом кодоне
оснований, составляющих полный геном человека: в шестом кодоне  -глобинового гена
-глобинового гена

Рис. 36.8. Мутации гена Р-глобина, обусловливающие  -талассемию. Ген представлен в ориентации
-талассемию. Ген представлен в ориентации  . Заштрихованы нетранслируемые 5- и 3-области. При чтении в направлении
. Заштрихованы нетранслируемые 5- и 3-области. При чтении в направлении  затемненные участки—экзоны 1 —3, светлые участки интроны 1 и 2. Мутации, затрагивающие контроль транскрипции
затемненные участки—экзоны 1 —3, светлые участки интроны 1 и 2. Мутации, затрагивающие контроль транскрипции  локализованы в
локализованы в  -фланкирующей области. Идентифицированы отмеченные на рисунке некоторые nonsense-мутации (Д), мутации, влияющие на процессинг (О) и расщепление РНК
-фланкирующей области. Идентифицированы отмеченные на рисунке некоторые nonsense-мутации (Д), мутации, влияющие на процессинг (О) и расщепление РНК  В некоторых областях выявлено большое количество мутаций. Такие участки помечены квадратными скобками.
В некоторых областях выявлено большое количество мутаций. Такие участки помечены квадратными скобками.
Таблица 36.6. Структурные изменения в гене  -глобина
-глобина

аденин заменяется на тнмин. С измененного кодона считывается не глутаминовая кислота, а валин, что приводит к структурным нарушениям молекулы ( -глобина. Некоторые точковые мутации вызывают снижение либо полную остановку синтеза Р-глобина. Результатом таких нарушений является Р-талассемия (талассемии—класс заболеваний, связанных с нарушениями синтеза глобина). На рис. 36.8 представлены позиции точковых мутаций, нарушающих какую-либо из многочисленных стадий процесса образования нормальной Р-глобиновой
-глобина. Некоторые точковые мутации вызывают снижение либо полную остановку синтеза Р-глобина. Результатом таких нарушений является Р-талассемия (талассемии—класс заболеваний, связанных с нарушениями синтеза глобина). На рис. 36.8 представлены позиции точковых мутаций, нарушающих какую-либо из многочисленных стадий процесса образования нормальной Р-глобиновой  и, следовательно, вызывающих Р-талассемию.
и, следовательно, вызывающих Р-талассемию.
Делеции, вставки и перестройки ДНК
Исследования геномов бактерий, вирусов, дрожжей и дрозофилы показывают, что отдельные участки ДНК могут менять свое положение в геноме. Утрата функционально важного участка ДНК, перестановка фрагментов ДНК внутри гена, вставка в его кодирующий или регуляторный участок, как правило, вызывают изменения в уровне экспрессии данного гена, приводящие к заболеванию. Молекулярный анализ Р-талассемии выявляет большое число подобных случаев (особенно делеций). Создается впечатление, что кластеры глобиновых генов весьма подвержены повреждениям. Делеции в а-глобиновом кластере, локализованном в 16-й хромосоме, приводят к а-талассемии. Для большинства таких делеций отмечена четкая взаимосвязь с этническим происхождением. Жители севера Европы, филиппинцы, негроиды и представители средиземно-морских популяций имеют нарушения различного типа, но все они ведут к утрате гемоглобина А и а-талассемии.
Подобный анализ можно провести и для многих других заболеваний. Обычно точковые мутации идентифицируют путем определения нуклеотидной последовательности изучаемого гена, но, если мутация затрагивает сайт рестрикции, для ее выявления достаточно рестрикционного анализа. Делеции и вставки ДНК-фрагментов больших чем 50 пар оснований определяют методом блоттинга по Саузерну.
Анализ родословных
На примере серповидноклеточной анемии можно убедиться в том, насколько эффективен генно-инженерный подход при изучении болезней человека. Замена основания в кодирующей цепи ДНК гена гемоглобина приводит к изменению последовательности, соответствующей шестому кодону:

При этом исчезает сайт рестриктазы  стрелками указаны места расщепления, см. табл. 36.1). Другие Mst II-сайты (рис. 36.9) остаются
стрелками указаны места расщепления, см. табл. 36.1). Другие Mst II-сайты (рис. 36.9) остаются

Рис. 36.9. Анализ родословных в случае серповидноклеточной анемии. В верхней части рисунка (А) показано начало гена 6-глобина с сайтами расщепления рестриктазой Mst II (Т) У нормального (А) и серповидноклеточного (S) В-глобина В результате расщепления ДНК здоровых индивидуумов рестриктазой Mst II образуются специфические фрагменты ДНК размером 1,15 и 0.2 т. п. н. Замена одного основания у больных серповидноклеточной анемией приводит к потере одного из трех  -сайтов в области гена и соответственно к появлению только одного специфического Mst II-фрагмента размером 1,35 т. п. н. Это различие в длине легко обнаруживается методом Саузерн-блоттинга
-сайтов в области гена и соответственно к появлению только одного специфического Mst II-фрагмента размером 1,35 т. п. н. Это различие в длине легко обнаруживается методом Саузерн-блоттинга  . (На данном рисунке положение фрагмента длиной 0,2 т. п. н. не указано.) Анализ родословных демонстрирует три возможных генотипа АА-норма (О), AS-гетерозигота по гену серповидноклеточности (ОП) и SS-гомозигота по гену серповидных эритроцитов
. (На данном рисунке положение фрагмента длиной 0,2 т. п. н. не указано.) Анализ родословных демонстрирует три возможных генотипа АА-норма (О), AS-гетерозигота по гену серповидноклеточности (ОП) и SS-гомозигота по гену серповидных эритроцитов  Этот подход позволяет осуществлять пренатальную диагностику заболевания серповидноклеточной анемией и выявлять гетерозиготных носителей соответствующего гена
Этот подход позволяет осуществлять пренатальную диагностику заболевания серповидноклеточной анемией и выявлять гетерозиготных носителей соответствующего гена 
неизменными и могут быть расщеплены этой рестриктазой. Поэтому Саузерн-блоттинг обработанных ферментом образцов ДНК нормальных (АА), гетерозиготных (AS) и гомозиготных (SS) пациентов дает три типа распределения фрагментов (рис. 36.9). Этот пример показывает, как на уровне ДНК можно провести анализ родословной с использованием описываемых в этой главе принципов и подходов. Такой анализ весьма эффективен при изучении ряда генетических заболеваний, вызванных делениями, вставками и (реже) точковыми мутациями с изменением сайтов рестрикции (как в только что рассмотренном примере).
Пренатальная диагностика
Дородовая диагностика наследственных заболеваний возможна, если известна природа генетического нарушения и имеется соответствующий зонд. Анализу по Саузерну можно подвергнуть ДНК клеток, собранных из 10 мл амниотической жидкости (или полученных с помощью биопсии ворсинок
хориона). Плод с рестрикционным вариантом АА (рис. 36.9) нормален и не является носителем серповидноклеточной анемии. В случае варианта SS можно с уверенностью предсказать развитие болезни. Уже сейчас существуют зонды для подобного анализа многих заболеваний.
Полиморфизм длины рестрикционных фрагментов (ПДРФ)
Изменения в последовательностях ДНК, вызванные описанными выше причинами, могут обусловливать изменения в расположении сайтов рестрикции и поэтому сказываться на длине рестрикционных фрагментов. Устойчивое наследуемое изменение в распределении длин рестрикционных фрагментов (наблюдаемое для более чем 1 % численности популяции) называют полиморфизмом длины рестрикционных фрагментов (ПДРФ). Этот феномен может быть результатом либо точковых замен (серповидноклеточная анемия), либо делеций и вставок (талассемии). В последнее время ПДРФ стали с успехом использовать в диагностических целях. Рестрикционный полиморфизм обнаружен как в последовательностях известных генов, так и в участках ДНК с неизвестной функцией. ПДРФ может нарушать биологическую функцию, а может и не иметь никаких биологических последствий; в любом случае соответствующие измененные локусы наследуются в соответствии с законами Менделя. Основная область использования этого феномена (а известно уже около 350 случаев ПДРФ) — диагностика наследственных заболеваний, функциональная природа которых неизвестна. Вначале с помощью ПДРФ устанавливают группу сцепления, а затем методом последовательной гибридизации определяют локус, ответственный за заболевание. Согласно методу последовательной гибридизации, фрагмент, представляющий один из концов длинной цепи ДНК, используют в качестве зонда для выявления другого фрагмента, который перекрывается с первым и в то же время выходит за его пределы. Применение этого подхода, называемого «прогулка по хромосоме» (рис. 36.10), обеспечивает «передвижение» по цепи ДНК вплоть до интересующей области. Направление передвижения контролируется по рестрикционной карте. «Прогулка по хромосоме» особенно удобна при изучении Х-сцепленных болезней, поскольку в данном случае экспрессируется только один из двух аллелей. 20% выявленных случаев ПДРФ относится именно к Х-хромосоме, и именно для нее составлена практически полная карта. Используя феномен ПДРФ, можно локализовать ген любой  -сцепленной болезни (например, мышечной дистрофии Дюшенна). С помощью ПДРФ удалось установить, что генетический дефект при хорее Гентингтона затрагивает конец короткого плеча хромосомы 4, а ген, вызывающий поликистоз почек, сцеплен с локусом а-глобина на хромосоме 16.
-сцепленной болезни (например, мышечной дистрофии Дюшенна). С помощью ПДРФ удалось установить, что генетический дефект при хорее Гентингтона затрагивает конец короткого плеча хромосомы 4, а ген, вызывающий поликистоз почек, сцеплен с локусом а-глобина на хромосоме 16.
Генная терапия
Заболевания, вызванные функциональной недостаточностью продукта того или иного гена, можно лечить с помощью «заместительной» терапии (табл. 36.5). Стратегия подхода заключается в клонировании гена (например, гена, кодирующего аденозинде-заминазу) в векторе, способном включиться в геном клетки хозяина. Весьма перспективным представляется использование для этого предшественников клеток костного мозга. Можно надеяться, что такие клетки «приживутся» и будут размножаться, синтезируя трансгенный продукт. Конечно, ген, перенесенный в соматические клетки, потомкам не передается.
В последнее время ведутся интенсивные поиски

Рис. 36.10. Метод «прогулка по хромосоме». Пусть необходимо обнаружить ген X в рамках протяженного фрагмента ДНК. Точное положение гена неизвестно, однако имеется первичный зонд  соответствующий некоему участку генома (показан в данном случае на 5-конце исследуемого фрагмента ДНК). Кроме того, имеется библиотека перекрывающихся фрагментов генома. (Для упрощения на рисунке изображены только пять фрагментов.) Первичный зонд гибридизуется только с клонами, содержащими фрагмент 1. Этот фрагмент можно использовать далее в качестве зонда для выявления фрагмента 2. Процедура последовательной гибридизации повторяется вплоть до обнаружения фрагмента 4, который гибридизуется с фрагментом 5, содержащим искомый ген X.
соответствующий некоему участку генома (показан в данном случае на 5-конце исследуемого фрагмента ДНК). Кроме того, имеется библиотека перекрывающихся фрагментов генома. (Для упрощения на рисунке изображены только пять фрагментов.) Первичный зонд гибридизуется только с клонами, содержащими фрагмент 1. Этот фрагмент можно использовать далее в качестве зонда для выявления фрагмента 2. Процедура последовательной гибридизации повторяется вплоть до обнаружения фрагмента 4, который гибридизуется с фрагментом 5, содержащим искомый ген X.
путей генно-инженерного воздействия на половые клетки. Соответствующие эксперименты проводят на лабораторных животных. Гены, инъецированные в оплодотворенные яйцеклетки мыши, в некоторых случаях встраиваются в геном. Полученных трансгенных животных используют для изучения характера экспрессии генов в разных тканях, а также для выявления специфических генов онтогенеза. Трансгенный подход недавно с успехом был использован для коррекции генетического дефекта у мышей. В оплодотворенные яйцеклетки мыши с наследственным гипогонадизмом (гл. 55) инъецировали ДНК, содержащую кодирующую последовательность предшественника гонадолиберина. У части развившихся из таких яйцеклеток мышей этот ген нормально экспрессировался. Фенотипически эти мыши были нормальными во всех отношениях. Их потомство также не проявляло недостаточности по гонадолиберину. Приведенный пример свидетельствует о принципиальной возможности экспрессии трансгенов в соматических клетках и их передачи потомству.
| << Предыдущий параграф | Следующий параграф >> |
- Раздел IV. Структура, функция и репликация информационных макромолекул
- СТРУКТУРА ПУРИНОВЫХ И ПИРИМИДИНОВЫХ ОСНОВАНИЙ
- ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА ПУРИНОВЫХ И ПИРИМИДИНОВЫХ ОСНОВАНИЙ
- НУКЛЕОЗИДЫ И НУКЛЕОТИДЫ
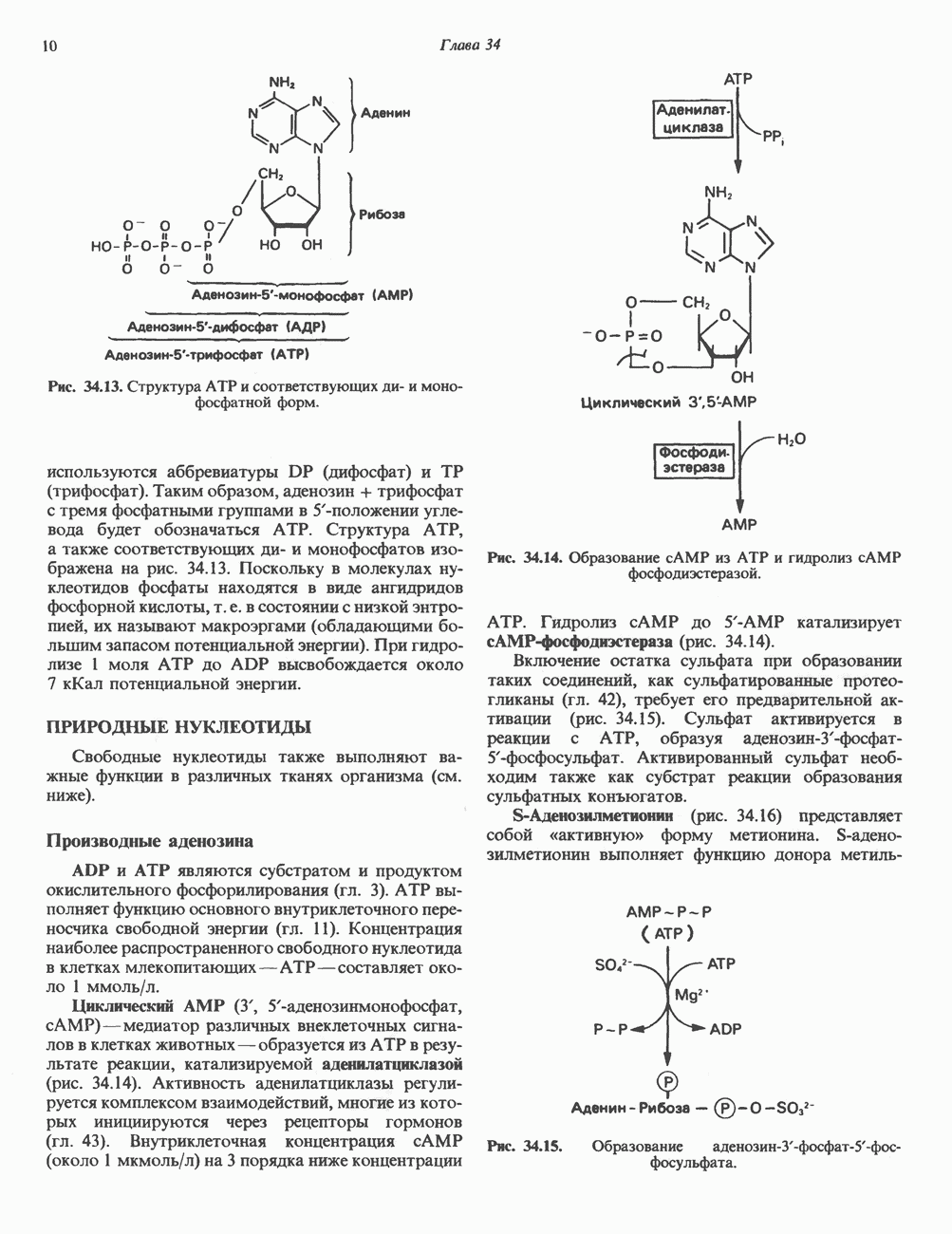
- ПРИРОДНЫЕ НУКЛЕОТИДЫ
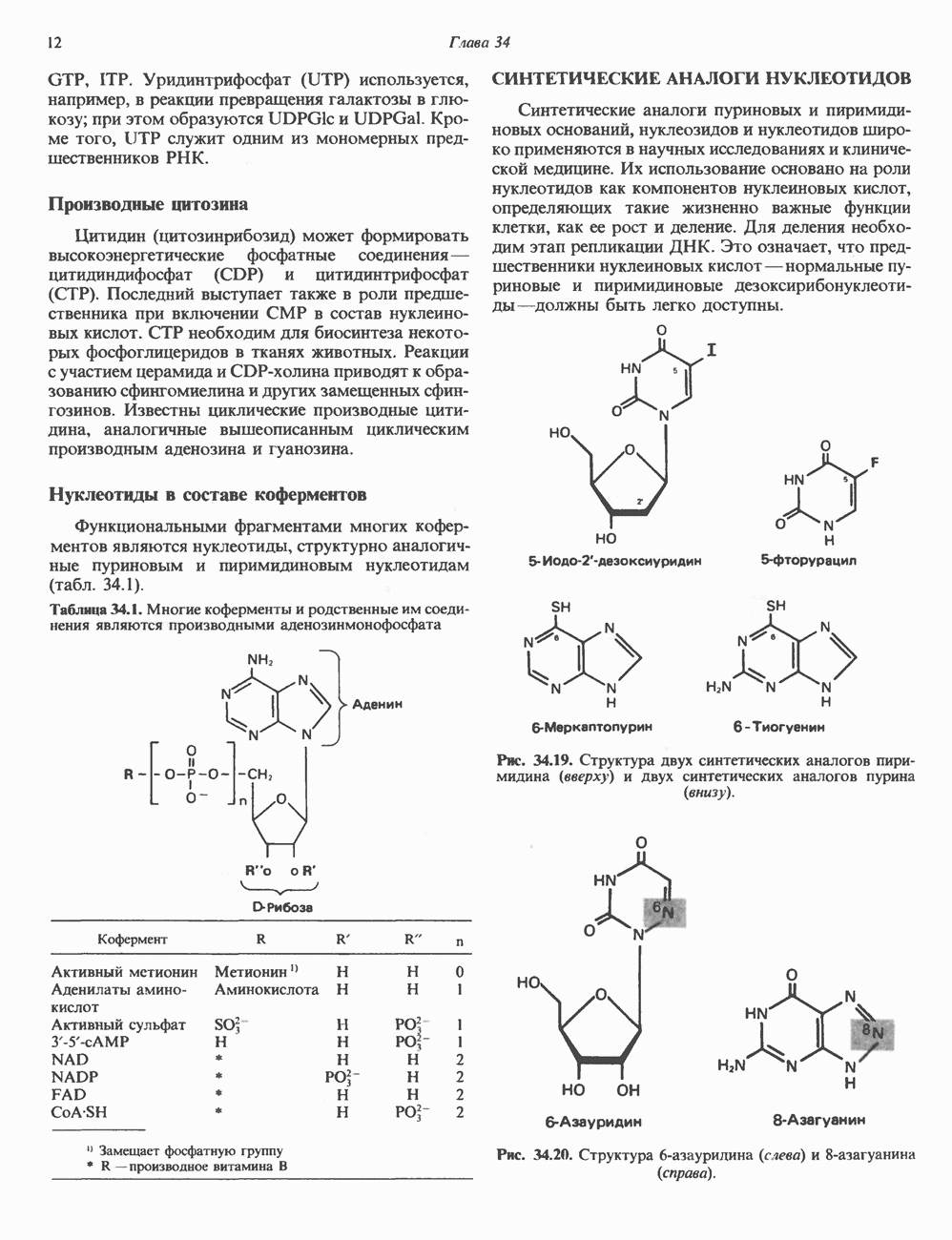
- СИНТЕТИЧЕСКИЕ АНАЛОГИ НУКЛЕОТИДОВ
- Глава 35. Метаболизм пуриновых и пиримидиновых нуклеотидов
- УСВОЕНИЕ
- ПУРИНЫ
- ПИРИМИДИНЫ
- КЛИНИЧЕСКИЕ НАРУШЕНИЯ МЕТАБОЛИЗМА ПУРИНОВ (ТАБЛ. 35.1)
- ЗАБОЛЕВАНИЯ, СВЯЗАННЫЕ С НАРУШЕНИЕМ МЕТАБОЛИЗМА ПИРИМИДИНОВ (ТАБЛ. 35.3)
- Глава 36. Технология рекомбинантных ДНК
- ОСНОВНЫЕ СВОЙСТВА ДНК
- ОСНОВНЫЕ ПОНЯТИЯ ГЕННОЙ ИНЖЕНЕРИИ
- НЕКОТОРЫЕ ПРАКТИЧЕСКИЕ ПРИЛОЖЕНИЯ ТЕХНОЛОГИИ РЕКОМБИНАНТНОЙ ДНК
- ГЕННАЯ ИНЖЕНЕРИЯ И АНАЛИЗ МОЛЕКУЛЯРНОЙ ПРИРОДЫ ЗАБОЛЕВАНИЙ
- СЛОВАРЬ-СПРАВОЧНИК
- ЛИТЕРАТУРА
- Глава 37. Структура и функция нуклеиновых кислот
- ДНК
- РНК
- Глава 38. Организация и репликация ДНК
- ХРОМАТИН
- ГИСТОНЫ И НУКЛЕОСОМЫ
- ГЕНЕТИЧЕСКАЯ ОРГАНИЗАЦИЯ ГЕНОМА МЛЕКОПИТАЮЩИХ
- ИЗМЕНЕНИЯ И ПЕРЕСТРОЙКИ ГЕНЕТИЧЕСКОГО МАТЕРИАЛА
- СИНТЕЗ И РЕПЛИКАЦИЯ ДНК
- Глава 39. Синтез и процессинг РНК
- СИНТЕЗ РНК
- ПРОЦЕССИНГ МОЛЕКУЛ РНК
- НУКЛЕАЗЫ
- Глава 40. Синтез белка и генетический код
- ИНФОРМАЦИОННЫЙ ПОТОК
- КОДОНЫ И СИНТЕЗ БЕЛКА
- ТРАНСПОРТНЫЕ РНК И СИНТЕЗ БЕЛКА
- МУТАЦИИ
- ПРОЦЕСС СИНТЕЗА БЕЛКА
- Глава 41. Регуляция экспрессии генов
- РЕГУЛЯЦИЯ ЭКСПРЕССИИ ГЕНОВ У ПРОКАРИОТ
- РЕГУЛЯЦИЯ ЭКСПРЕССИИ ГЕНОВ У ЭУКАРИОТ
- Раздел V. Биохимия внутри- и межклеточных коммуникаций
- Глава 42. Мембраны: структура, сборка и функции
- ПОДДЕРЖАНИЕ НОРМАЛЬНОГО СОСТАВА СРЕДЫ
- СТРУКТУРА МЕМБРАН
- ОРГАНИЗАЦИЯ МЕМБРАННЫХ ЛИПИДОВ
- МЕМБРАННЫЕ БЕЛКИ
- ИСКУССТВЕННЫЕ МЕМБРАНЫ
- ЖИДКОСТНО-МОЗАИЧНАЯ МОДЕЛЬ МЕМБРАН
- СБОРКА МЕМБРАН
- СПЕЦИАЛИЗИРОВАННЫЕ ФУНКЦИИ МЕМБРАН
- ТРАНСМЕМБРАННЫЙ ПЕРЕНОС МАЛЫХ МОЛЕКУЛ
- ТРАНСМЕМБРАННОЕ ПЕРЕМЕЩЕНИЕ МАКРОМОЛЕКУЛ
- ПЕРЕДАЧА ИНФОРМАЦИИ В КЛЕТКУ
- МЕЖКЛЕТОЧНЫЕ КОНТАКТЫ И КОММУНИКАЦИИ
- Глава 43. Характеристика эндокринной системы
- ОБЩИЕ СВОЙСТВА
- РАЗНООБРАЗИЕ ЭНДОКРИННОЙ СИСТЕМЫ
- КОНЦЕПЦИЯ ЖЕЛЕЗЫ-МИШЕНИ
- КОНЦЕПЦИЯ РЕГУЛЯТОРНОГО МЕХАНИЗМА ОБРАТНОЙ СВЯЗИ
- РЕЦЕПТОРЫ ГОРМОНОВ
- Глава 44. Действие гормонов
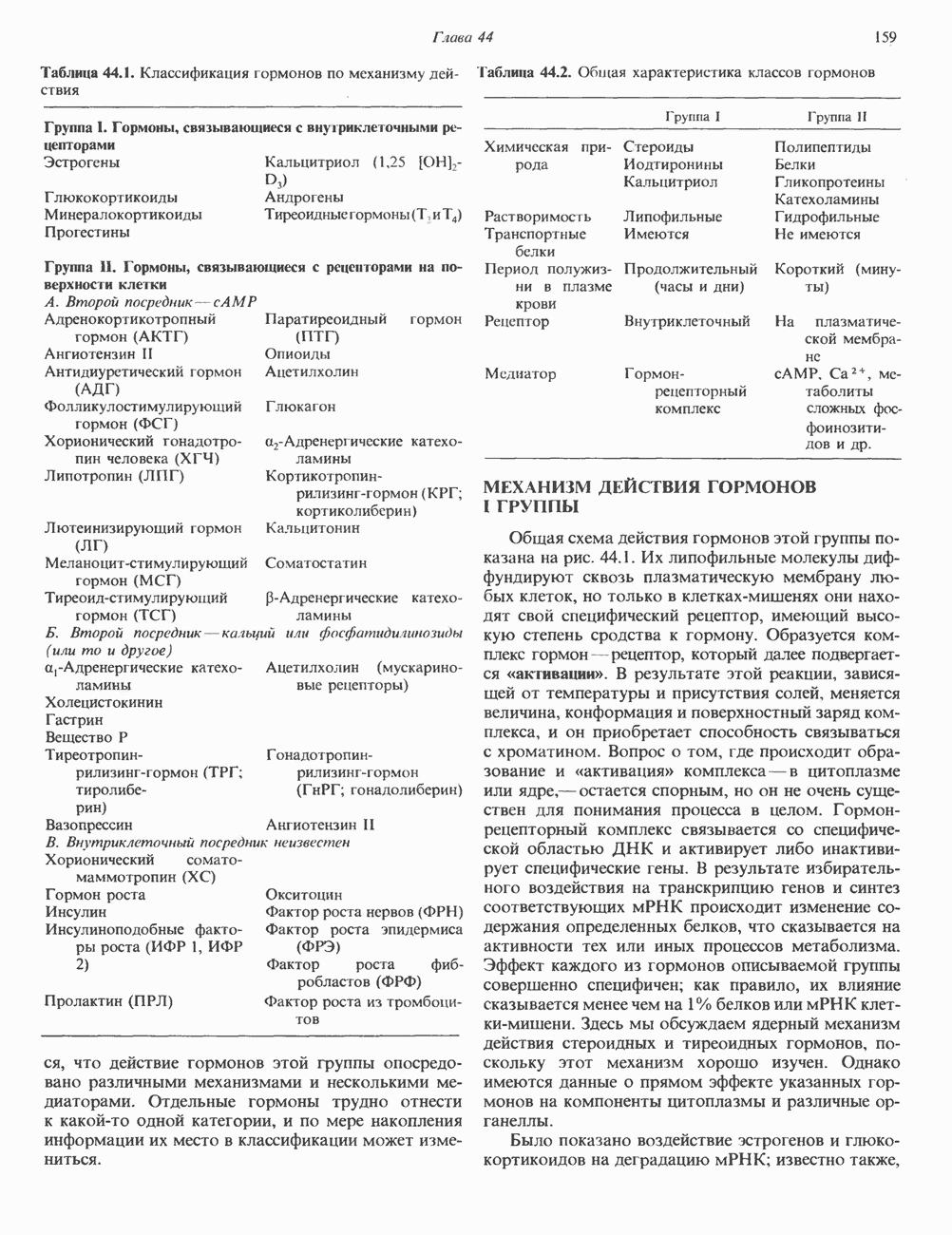
- КЛАССИФИКАЦИЯ ГОРМОНОВ
- МЕХАНИЗМ ДЕЙСТВИЯ ГОРМОНОВ I ГРУППЫ
- МЕХАНИЗМ ДЕЙСТВИЯ ГОРМОНОВ II ГРУППЫ (ПЕПТИДНЫХ ГОРМОНОВ)
- 1. сАМР КАК ВТОРОЙ ПОСРЕДНИК
- 2. ДЕЙСТВИЕ ГОРМОНОВ, ОПОСРЕДОВАННОЕ КАЛЬЦИЕМ И ФОСФОИНОЗИТИДАМИ
- 3. ГОРМОНЫ С НЕИЗВЕСТНЫМ ВНУТРИКЛЕТОЧНЫМ ПОСРЕДНИКОМ
- Глава 45. Гормоны гипофиза и гипоталамуса
- ГОРМОНЫ ГИПОТАЛАМУСА
- ГОРМОНЫ ПЕРЕДНЕЙ ДОЛИ ГИПОФИЗА
- I. ГРУППА ГОРМОН РОСТА — ПРОЛАКТИН—ХОРИОНИЧЕСКИЙ СОМАТОМАММОТРОПИН
- 2. ГРУППА ГЛИКОПРОТЕИНОВЫХ ГОРМОНОВ
- 3. СЕМЕЙСТВО ПЕПТИДОВ ПРООПИОМЕЛАНОКОРТИНА (ПОМК)
- ГОРМОНЫ ЗАДНЕЙ ДОЛИ ГИПОФИЗА
- 1. ОКСИТОЦИН
- 2. АНТИДИУРЕТИЧЕСКИЙ ГОРМОН (АДГ; ВАЗОПРЕССИН)
- Глава 46. Гормоны щитовидной железы
- БИОСИНТЕЗ ТИРЕОИДНЫХ ГОРМОНОВ
- 1. МЕТАБОЛИЗМ ТИРЕОГЛОБУЛИНА
- 2. МЕТАБОЛИЗМ ИОДИДА
- ТРАНСПОРТ И МЕТАБОЛИЗМ ГОРМОНОВ ЩИТОВИДНОЙ ЖЕЛЕЗЫ
- РЕГУЛЯЦИЯ СИНТЕЗА И ВЫСВОБОЖДЕНИЯ ГОРМОНОВ ЩИТОВИДНОМ ЖЕЛЕЗЫ
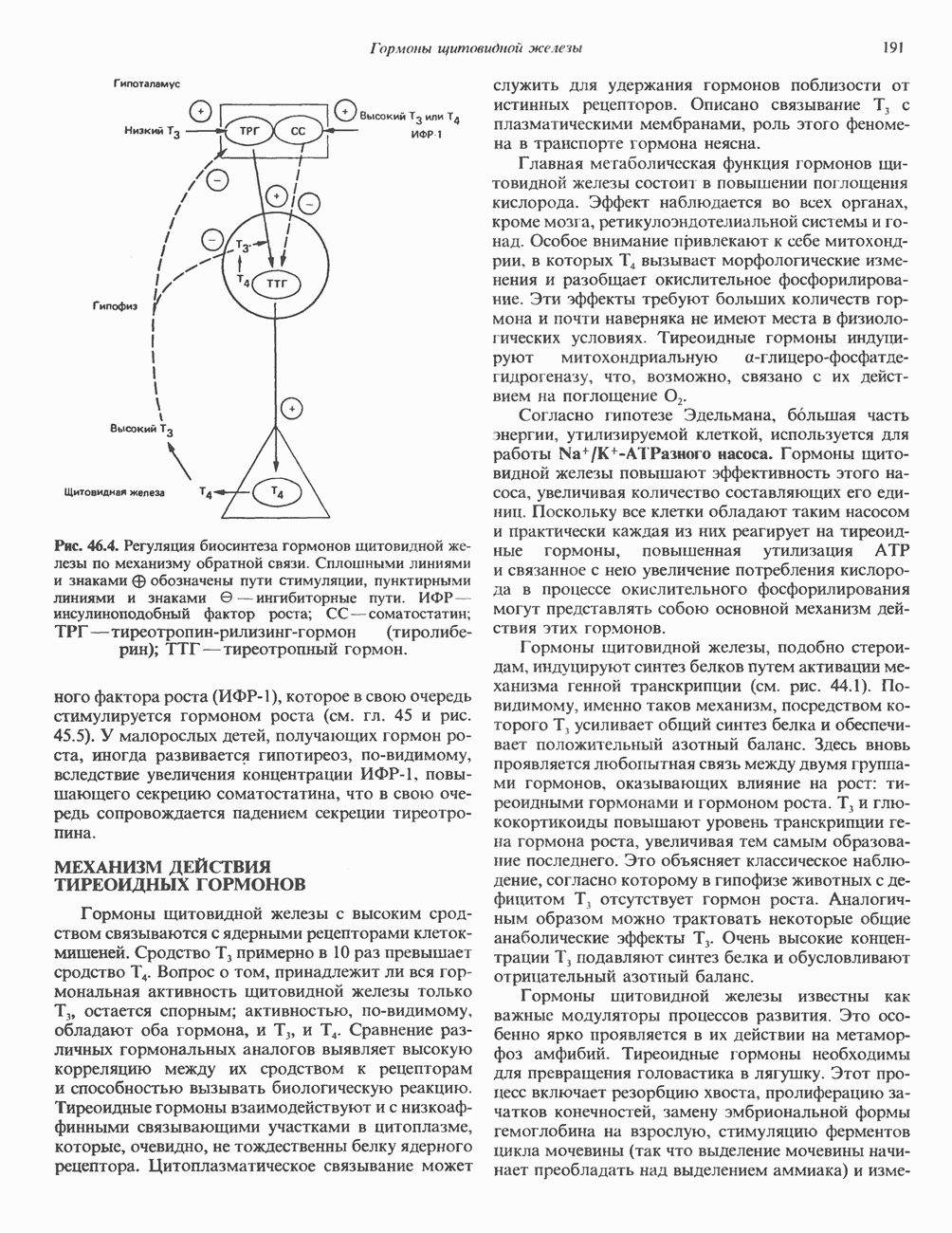
- МЕХАНИЗМ ДЕЙСТВИЯ ТИРЕОИДНЫХ ГОРМОНОВ
- ПАТОФИЗИОЛОГИЯ
- Глава 47. Гормоны, регулирующие метаболизм кальция
- ОБЩИЕ ХАРАКТЕРИСТИКИ
- ГОМЕОСТАЗ КАЛЬЦИЯ
- ГОРМОНЫ, УЧАСТВУЮЩИЕ В ГОМЕОСТАЗЕ КАЛЬЦИЯ
- 2. КАЛЬЦИТРИОЛ
- 3. КАЛЬЦИТОНИН (КТ)
- Глава 48. Гормоны коры надпочечников
- ГОРМОНЫ
- НОМЕНКЛАТУРА И ХИМИЯ СТЕРОИДОВ
- БИОСИНТЕЗ СТЕРОИДНЫХ ГОРМОНОВ НАДПОЧЕЧНИКОВ
- СЕКРЕЦИЯ, ТРАНСПОРТ И МЕТАБОЛИЗМ СТЕРОИДНЫХ ГОРМОНОВ НАДПОЧЕЧНИКОВ
- РЕГУЛЯЦИЯ СИНТЕЗА СТЕРОИДНЫХ ГОРМОНОВ НАДПОЧЕЧНИКОВ
- ВОЗДЕЙСТВИЕ СТЕРОИДНЫХ ГОРМОНОВ НАДПОЧЕЧНИКОВ НА МЕТАБОЛИЗМ
- КЛАССИФИКАЦИЯ И МЕХАНИЗМ ДЕЙСТВИЯ СТЕРОИДНЫХ ГОРМОНОВ
- ПАТОФИЗИОЛОГИЯ КОРЫ НАДПОЧЕЧНИКОВ
- Глава 49. Гормоны мозгового вещества надпочечников
- БИОСИНТЕЗ КАТЕХОЛАМИНОВ
- ЗАПАСАНИЕ И СЕКРЕЦИЯ КАТЕХОЛАМИНОВ
- МЕТАБОЛИЗМ КАТЕХОЛАМИНОВ
- РЕГУЛЯЦИЯ СИНТЕЗА КАТЕХОЛАМИНОВ
- КЛАССИФИКАЦИЯ И МЕХАНИЗМ ДЕЙСТВИЯ КАТЕХОЛАМИНОВ
- ПАТОФИЗИОЛОГИЯ МОЗГОВОГО СЛОЯ НАДПОЧЕЧНИКОВ
- Глава 50. Гормоны половых желез
- ГОРМОНЫ СЕМЕННИКОВ
- РЕГУЛЯЦИЯ ФУНКЦИИ СЕМЕННИКОВ
- ФИЗИОЛОГИЧЕСКИЕ ЭФФЕКТЫ ГОРМОНОВ СЕМЕННИКОВ
- МЕХАНИЗМ ДЕЙСТВИЯ ГОРМОНОВ СЕМЕННИКОВ
- ПАТОФИЗИОЛОГИЯ РЕПРОДУКТИВНОЙ СИСТЕМЫ У МУЖЧИН
- БИОСИНТЕЗ И МЕТАБОЛИЗМ ГОРМОНОВ ЯИЧНИКОВ
- РЕГУЛЯЦИЯ И ФИЗИОЛОГИЧЕСКОЕ ДЕЙСТВИЕ ГОРМОНОВ ЯИЧНИКОВ
- МЕХАНИЗМ ДЕЙСТВИЯ ГОРМОНОВ ЯИЧНИКОВ
- ПАТОФИЗИОЛОГИЯ ЖЕНСКОЙ РЕПРОДУКТИВНОЙ СИСТЕМЫ
- ГОРМОНЫ ПОЛОВЫХ ЖЕЛЕЗ И ПОЛОВАЯ ДИФФЕРЕНЦИРОВКА
- ФЕНОТИПИЧЕСКИЙ ПОЛ
- Глава 51. Гормоны поджелудочной железы
- ИНСУЛИН
- ИНСУЛИНОПОДОБНЫЕ ФАКТОРЫ РОСТА
- ГЛЮКАГОН
- СОМАТОСТАТИН
- ПАНКРЕАТИЧЕСКИЙ ПОЛИПЕПТИД
- Глава 52. Гормоны желудочно-кишечного тракта
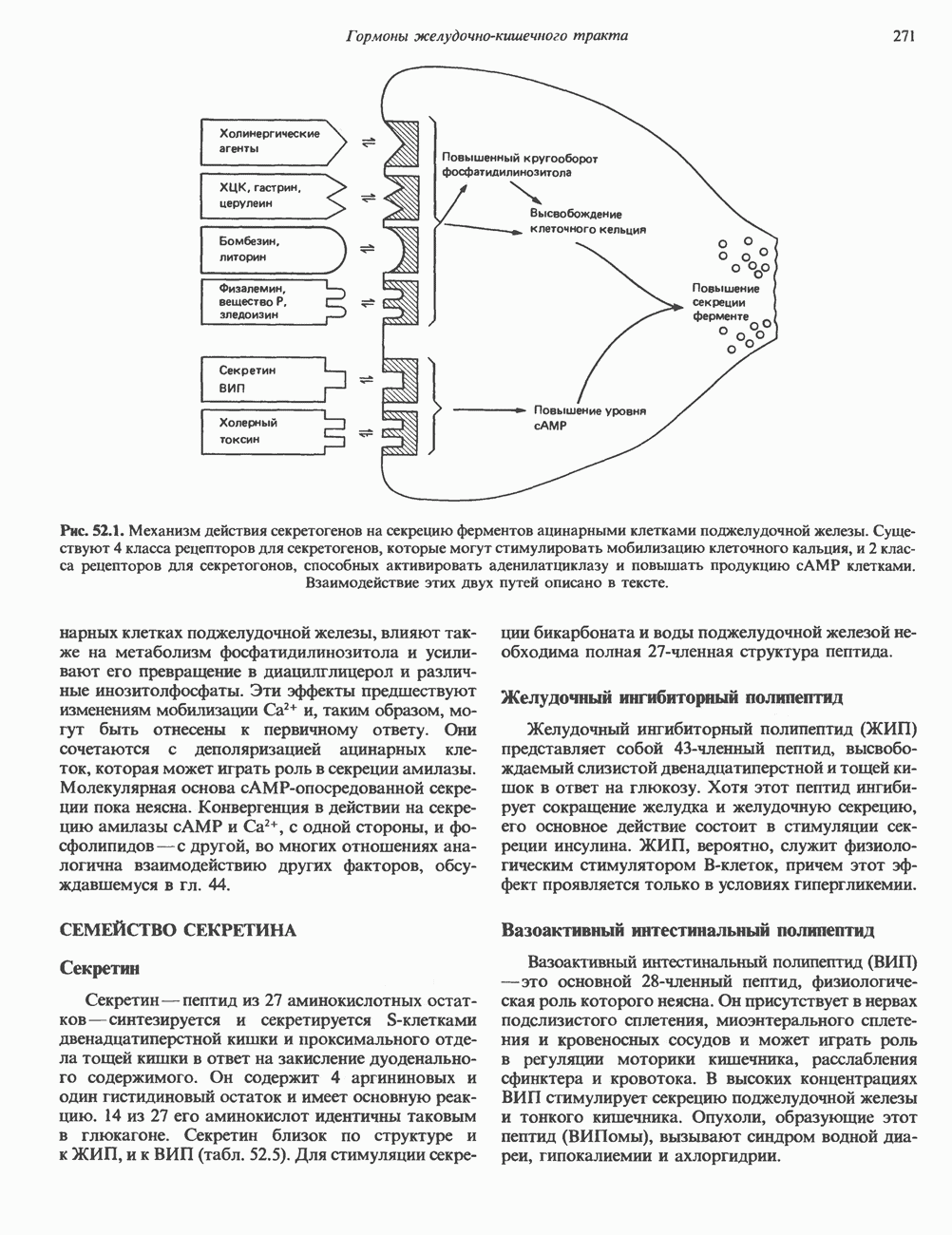
- СВОЙСТВА ГОРМОНОВ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА
- СЕМЕЙСТВО СЕКРЕТИНА
- СЕМЕЙСТВО ГАСТРИН—ХОЛЕЦИСТОКИНИН
- ДРУГИЕ ПЕПТИДЫ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА
- Раздел VI. Частные вопросы
- Питание, пищеварение и всасывание
- ПИТАНИЕ
- РАСХОД ЭНЕРГИИ
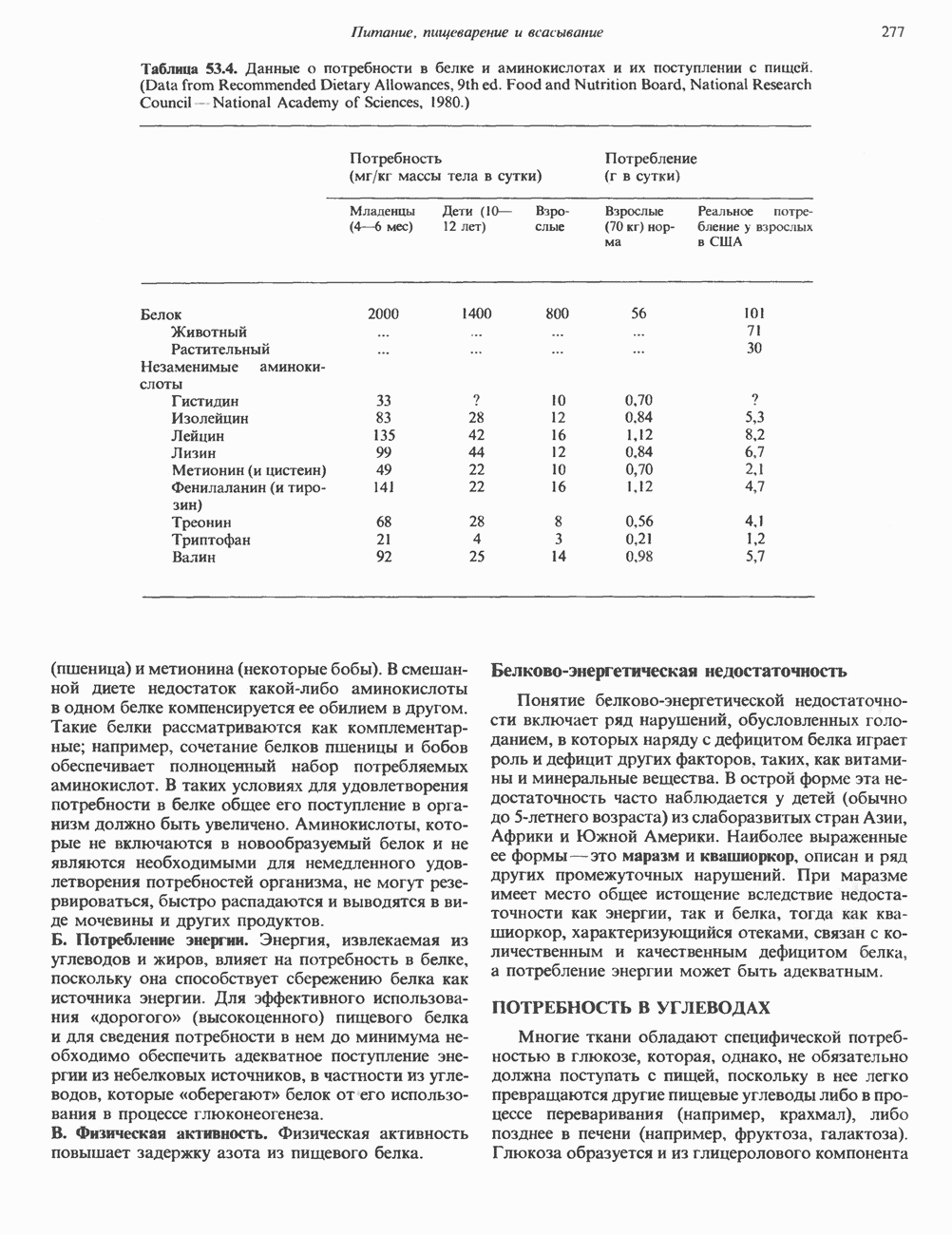
- АЗОТ АМИНОКИСЛОТ И ПОТРЕБНОСТЬ В СПЕЦИФИЧЕСКИХ АМИНОКИСЛОТАХ
- ПОТРЕБНОСТЬ В УГЛЕВОДАХ
- ПОТРЕБНОСТЬ В ПИЩЕВЫХ ВОЛОКНАХ
- ПОТРЕБНОСТЬ В ЛИПИДАХ
- ПОТРЕБНОСТЬ В ВИТАМИНАХ
- ПОТРЕБНОСТЬ В МИНЕРАЛЬНЫХ ВЕЩЕСТВАХ
- РЕКОМЕНДАЦИИ В ОБЛАСТИ ДИЕТЫ
- ПИЩЕВАРЕНИЕ
- ПИЩЕВАРЕНИЕ В ЖЕЛУДКЕ
- ПАНКРЕАТИЧЕСКОЕ И КИШЕЧНОЕ ПИЩЕВАРЕНИЕ
- ВСАСЫВАНИЕ В ЖЕЛУДОЧНО-КИШЕЧНОМ ТРАКТЕ
- ВСАСЫВАНИЕ ГЛЮКОЗЫ
- ВСАСЫВАНИЕ ЛИПИДОВ
- ВСАСЫВАНИЕ АМИНОКИСЛОТ И БЕЛКА
- ПРОЦЕССЫ ГНИЕНИЯ И БРОЖЕНИЯ В КИШЕЧНИКЕ
- Глава 54. Гликопротеины и протеогликаны
- ГЛИКОПРОТЕИНЫ
- ОПРЕДЕЛЕНИЕ, ОЧИСТКА И СТРУКТУРНЫЙ АНАЛИЗ ГЛИКОПРОТЕИНОВ
- САХАРА, ПРИСУТСТВУЮЩИЕ В ГЛИКОПРОТЕИНАХ
- НУКЛЕОТИДСАХАРА
- ЭКЗОГЛИКОЗИДАЗЫ И ЭНДОГЛИКОЗИДАЗЫ
- ЛЕКТИНЫ
- КЛАССИФИКАЦИЯ ГЛИКОПРОТЕИНОВ
- I-КЛЕТОЧНАЯ БОЛЕЗНЬ
- АНТИГЕНЫ ГРУПП КРОВИ
- ПРОТЕОГЛИКАНЫ И ГЛИКОЗАМИНОГЛИКАНЫ
- ДЕГРАДАЦИЯ ПОЛИСАХАРИДНЫХ КОМПОНЕНТОВ ГЛИКОПРОТЕИНОВ И ПРОТЕОГЛИКАНОВ
- ФУНКЦИИ ГЛИКОЗАМИНОГЛИКАНОВ И ПРОТЕОГЛИКАНОВ
- Глава 55. Плазма крови и процесс свертывания
- ФУНКЦИИ КРОВИ
- БЕЛКИ ПЛАЗМЫ
- СВЕРТЫВАНИЕ КРОВИ
- Глава 56. Сократительные и структурные белки
- МЫШЦЫ
- КЛЕТОЧНАЯ ПОДВИЖНОСТЬ И ЦИТОСКЕЛЕТ
- Глава 57. Рак, онкогены, факторы роста
- БИОХИМИЧЕСКИЕ ЛАБОРАТОРНЫЕ ТЕСТЫ И РАК
- ПРИЧИНЫ ВОЗНИКНОВЕНИЯ РАКОВЫХ ОПУХОЛЕЙ
- ОНКОГЕННЫЕ ВИРУСЫ
- ТРАНСФОРМАЦИЯ
- ОНКОГЕНЫ
- ПОЛИПЕПТИДНЫЕ ФАКТОРЫ РОСТА
- ДЕЙСТВИЕ ФАКТОРОВ РОСТА ПО ЭНДОКРИННОМУ, ПАРАКРИННОМУ ИЛИ АУТОКРИННОМУ ТИПУ
- БИОХИМИЧЕСКИЕ МЕХАНИЗМЫ ДЕЙСТВИЯ ФАКТОРОВ РОСТА
- ФАКТОРЫ РОСТА И ОНКОГЕНЫ
- ПРОГРЕССИЯ ОПУХОЛЕЙ
- МЕТАСТАЗИРОВАНИЕ
- Приложение
- ХИМИЧЕСКИЙ СОСТАВ КРОВИ И ЖИДКИХ СРЕД ОРГАНИЗМА
- СТАНДАРТНЫЕ КЛИНИКО-ЛАБОРАТОРНЫЕ ПОКАЗАТЕЛИ В ТРАДИЦИОННОЙ СИСТЕМЕ И СИСТЕМЕ СИ
- НОРМАЛЬНЫЕ ЛАБОРАТОРНЫЕ ПОКАЗАТЕЛИ
- Список сокращений