| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
РЕГУЛЯЦИЯ ЭКСПРЕССИИ ГЕНОВ У ПРОКАРИОТ
Lac-оперон
В 1961 г. Франсуа Жакоб и Жак Моно описали ставшую теперь классической модель оперона. Их концепция в значительной мере была основана на изучении регуляции метаболи:  лактозы у кишечной палочки Е. coli. Молекулярный механизм регуляции генов, участвующих в метаболизме лактозы, на сегодняшний день наиболее изучен. Фермент
лактозы у кишечной палочки Е. coli. Молекулярный механизм регуляции генов, участвующих в метаболизме лактозы, на сегодняшний день наиболее изучен. Фермент  -галактозидаза гидролизует лактозу до галактозы и глюкозы (рис. 41.2). Структурный ген р-галактозидазы (ген
-галактозидаза гидролизует лактозу до галактозы и глюкозы (рис. 41.2). Структурный ген р-галактозидазы (ген  ) локализован в одном кластере с геном, ответственным за синтез галактозид-пермеазы, осуществляющей активный транспорт галактозы в клетку (ген Y) и геном галактозидацетила-зы (ген А), функциональное значение которой неизвестно. Структурные гены трех соответствующих ферментов связаны физически и образуют так называемый Lac-оперон (рис. 41.3). Такая генетическая компоновка структурных и соответствующих регуляторных генов обеспечивает скоординированную экспрессию всех трех ферментов метаболизма лактозы. Все три гена транскрибируются в виде обшей молекулы мРНК, содержащей независимые кодоны начала трансляции (AUG) и стоп-кодоны (UAA) для каждого цистрона. Такой тип мРНК называется полинис ровной
) локализован в одном кластере с геном, ответственным за синтез галактозид-пермеазы, осуществляющей активный транспорт галактозы в клетку (ген Y) и геном галактозидацетила-зы (ген А), функциональное значение которой неизвестно. Структурные гены трех соответствующих ферментов связаны физически и образуют так называемый Lac-оперон (рис. 41.3). Такая генетическая компоновка структурных и соответствующих регуляторных генов обеспечивает скоординированную экспрессию всех трех ферментов метаболизма лактозы. Все три гена транскрибируются в виде обшей молекулы мРНК, содержащей независимые кодоны начала трансляции (AUG) и стоп-кодоны (UAA) для каждого цистрона. Такой тип мРНК называется полинис ровной  Образование полицистронных мРНК характерно главным образом для прокариогических организмов.
Образование полицистронных мРНК характерно главным образом для прокариогических организмов.
Когда в растущую культуру клеток Е. coli добавляют лактозу или некоторые ее аналоги, экспрессия активностей ( -галактозидазы, галактоз и дпермеазы и галактозидацетилазы возрастает в 10—100 раз. Индукция лактозного оперона по вышеприведенной классификации ответов относится к типу А (рис. 41.1). После удаления индуктора (сигнала) интенсивность наработки всех трех ферментов падает. Поскольку сами ферменты в клетках Е. coli не подвергаются существенной деградации, уровень активности
-галактозидазы, галактоз и дпермеазы и галактозидацетилазы возрастает в 10—100 раз. Индукция лактозного оперона по вышеприведенной классификации ответов относится к типу А (рис. 41.1). После удаления индуктора (сигнала) интенсивность наработки всех трех ферментов падает. Поскольку сами ферменты в клетках Е. coli не подвергаются существенной деградации, уровень активности  -галактозидазы и двух других ферментов остается на прежнем уровне и падает лишь в связи с «разбавлением» в результате клеточного деления.
-галактозидазы и двух других ферментов остается на прежнем уровне и падает лишь в связи с «разбавлением» в результате клеточного деления.
Когда клетки Е. coli выращивают в среде, содержащей смесь лактозы и глюкозы, в качестве единственных источников углерода, то в первую очередь метаболизируется глюкоза. После исчерпания глюкозы в среде рост клеток временно приостанавливается, пока не пройдет индукция лактозного оперона, в результате которой достигается уровень экспрессии соответствующих ферментов, достаточный для обеспечения метаболизма лактозы. Несмотря на то, что лактоза присутствует с самого начала, Lac-оперон не

Рис. 41.3. Взаимное расположение структурных и регулярных генов в Lac-опероне.
(см. скан)
Рис. 41.4. Механизм репрессии и дерепрессии Lас-оперона. В отсутствие индуктора (А) репрессор (продукт конститутивно экспрессируемого гена  ), связываясь с оператором, препятствует посадке РНК-полимеразы на локус промотора и соответственно предотвращает транскрипцию структурных генов Z, Y, А. В присутствии индуктора (Б) конститутивно синтезируемый репрессор инактивируется и не можег связаться с оператором. В этом случае при наличии сАМР — САР-комплекса РНК-полимераза транскрибирует структурные гены Z, Y, А. Образующаяся полицистронная цепь мРНК транслируется с образованием белковых молекул
), связываясь с оператором, препятствует посадке РНК-полимеразы на локус промотора и соответственно предотвращает транскрипцию структурных генов Z, Y, А. В присутствии индуктора (Б) конститутивно синтезируемый репрессор инактивируется и не можег связаться с оператором. В этом случае при наличии сАМР — САР-комплекса РНК-полимераза транскрибирует структурные гены Z, Y, А. Образующаяся полицистронная цепь мРНК транслируется с образованием белковых молекул  -гатактозидазы. пермеазы и ацетилазы. обеспечивающих нормальный катаболизм лактозы.
-гатактозидазы. пермеазы и ацетилазы. обеспечивающих нормальный катаболизм лактозы.
индуцируется до полного исчерпания глюкозы. Этот феномен сначала объясняли исходя из предположения о репрессии оперона одним из продуктов катаболизма глюкозы. Поэтому он получил название — «катаболитная репрессия». Сейчас уже известно, что «катаболитная репрессия» в действительности опосредуется действием белка-активатора катаболитных генов — так называемого САР-белка (от англ. catabolite gene activator protein)-совместно с сАМР. Уровень экспрессии многих индуцибельных ферментных систем или оперонов у Е. coli и других прокариот чувствителен к катаболитной репрессии (см. ниже).
Физиология индукции Lас-оперона в настоящее время хорошо изучена (рис. 41.4). Экспрессия нормального гена Lас-оперона конститутивна, она проявляется в наработке с постоянной скоростью субъединиц Lac-penpeccopa. Белковая молекула Lac-репрессора состоит из четырех идентичных субъединиц, каждая из которых имеет мол. массу 38 000. Репрессор — продукт гена  - обладает высоким сродством к соответствующему операторному локусу
- обладает высоким сродством к соответствующему операторному локусу  около
около  Операторный локус — это определенный участок последовательности двухцепочечной ДНК длиной 27 пар оснований. В рамках этого участка последовательность длиной 21 п. о. характеризуется двойной симметрией вращения (показано сплошными линиями, ось симметрии обозначена точками):
Операторный локус — это определенный участок последовательности двухцепочечной ДНК длиной 27 пар оснований. В рамках этого участка последовательность длиной 21 п. о. характеризуется двойной симметрией вращения (показано сплошными линиями, ось симметрии обозначена точками):

Минимальный эффективный размер оператора, с которым может связаться молекула Lac-репрессора, составляет 17 пар оснований (выделены жирным шрифтом). В каждый данный момент времени с оператором связаны две субъединицы репрессора. Внутри последовательности в 17 пар оснований по крайней мере одно основание каждой пары принимает участие в узнавании и связывании репрессора. Связывание происходит в основном в большой бороздке ДНК без нарушения нормальной двухспиральной структуры области оператора. Участок молекулы репрессора, включающий первые 52 аминокислотных остатка, связывается с ДНК, не проявляя, судя по всему, специфичности к какой-то определенной последовательности. Другая область репрессора (остатки с 53 по 58) строго специфично связывается с  -звенным фрагментом операторной области протяженностью 6—7 нм. Аминокислотные остатки в положении 74—75 особенно важны для связывания индуктора с молекулой репрессора. Операторный локус находится между промотором, к которому перед началом транскрипции присоединяется ДНК-зависимая РНК-полимераза, и началом гена Z— структурного гена
-звенным фрагментом операторной области протяженностью 6—7 нм. Аминокислотные остатки в положении 74—75 особенно важны для связывания индуктора с молекулой репрессора. Операторный локус находится между промотором, к которому перед началом транскрипции присоединяется ДНК-зависимая РНК-полимераза, и началом гена Z— структурного гена  -галактозидазы (рис. 41.3). Присоединившись к оператору, репрессор препятствует транскрипции операторного локуса и дистальных структурных генов Z, Y и А. Таким образом, репрессор является негативным регулятором; в его присутствии подавляется экспрессия Z, Y и Л-генов. Обычно на клетку приходится 20—40 тетрамерных молекул репрессора и 1—2 операторных локуса.
-галактозидазы (рис. 41.3). Присоединившись к оператору, репрессор препятствует транскрипции операторного локуса и дистальных структурных генов Z, Y и А. Таким образом, репрессор является негативным регулятором; в его присутствии подавляется экспрессия Z, Y и Л-генов. Обычно на клетку приходится 20—40 тетрамерных молекул репрессора и 1—2 операторных локуса.
Аналог лактозы, способный индуцировать экспрессию Lас-оперона и не являющийся в то же время истинным субстратом  -галактозидазы, можно назвать нерасходуемым индуктором. Добавление лактозы или нерасходуемого индуктора к культуре бактерий, выращиваемой на плохо утилизируемом источнике углерода (например, сукцинате), вызывает незамедлительную индукцию ферментов Lac-оперона. Небольшие количества лактозы или индуктора способны проникать в бактериальную клетку и в отсутствие пермеазы. Молекулы репрессора, как связанные с операторным локусом, так и находящиеся в свободном виде в цитоплазме, обладают сродством к молекулам индуктора. Связывание индуктора с молекулой репрессора, прикрепленной к операторному локусу, вызывает конформационные изменения структуры репрессора и приводит к диссоциации комплекса с ДНК. Если к этому моменту ДНК-зависимая РНК-полимераза уже связана с кодирующей цепью в промоторной области, то начинается транскрипция. Образующаяся при этом полицистронная мРНК имеет на 5-конце последовательность, комплементарную кодирующей цепи оператора. Таким образом, индуктор дерепрессирует Lac-оперон и обеспечивает возможность транскрипции структурных генов (
-галактозидазы, можно назвать нерасходуемым индуктором. Добавление лактозы или нерасходуемого индуктора к культуре бактерий, выращиваемой на плохо утилизируемом источнике углерода (например, сукцинате), вызывает незамедлительную индукцию ферментов Lac-оперона. Небольшие количества лактозы или индуктора способны проникать в бактериальную клетку и в отсутствие пермеазы. Молекулы репрессора, как связанные с операторным локусом, так и находящиеся в свободном виде в цитоплазме, обладают сродством к молекулам индуктора. Связывание индуктора с молекулой репрессора, прикрепленной к операторному локусу, вызывает конформационные изменения структуры репрессора и приводит к диссоциации комплекса с ДНК. Если к этому моменту ДНК-зависимая РНК-полимераза уже связана с кодирующей цепью в промоторной области, то начинается транскрипция. Образующаяся при этом полицистронная мРНК имеет на 5-конце последовательность, комплементарную кодирующей цепи оператора. Таким образом, индуктор дерепрессирует Lac-оперон и обеспечивает возможность транскрипции структурных генов ( -галактозидазы, галактозидпермеазы и галактозидацетилазы. Трансляция полицистронной мРНК может начаться еще до полного завершения транскрипции. Дерепрессия Lac-оперона позволяет клетке синтезировать ферменты, необходимые для катаболизма лактозы как источника энергии.
-галактозидазы, галактозидпермеазы и галактозидацетилазы. Трансляция полицистронной мРНК может начаться еще до полного завершения транскрипции. Дерепрессия Lac-оперона позволяет клетке синтезировать ферменты, необходимые для катаболизма лактозы как источника энергии.
Для связывания РНК-полимеразы с последовательностью промотора необходимо наличие комплекса белка-активатора катаболитных генов (САР) с сАМР. Накопление сАМР происходит независимым образом только при недостатке в питательной среде источника углерода. В присутствии глюкозы или глицерола в концентрациях, обеспечивающих рост, концентрация сАМР в бактерии оказывается недостаточной для образования комплекса с САР и ДНК-зависимая РНК-полимераза не может начать транскрипцию Lас-оперона. Транскрипция начинается только при наличии комплекса САР-сАМР, связанного с промотором. Комплекс САР— сАМР действует как позитивный регулятор, поскольку его присутствие необходимо для обеспечения экспрессии генов. Таким образом, Lac-оперон является объектом как позитивной, так и негативной регуляции.
Если ген  мутирует таким образом, что его продукт — Lac-penpeccop — утрачивает способность связываться с оператором, то экспрессия Lac-оперона становится конститутивной. И наоборот, если мутация приводит к неспособности репрессора связываться с индуктором, то дерепрессии Lac-оперона (необходимым условием которой является именно образование комплекса между индуктором и репрессором, связанным с операторной областью) не наблюдается даже при высоких концентрациях индуктора в среде.
мутирует таким образом, что его продукт — Lac-penpeccop — утрачивает способность связываться с оператором, то экспрессия Lac-оперона становится конститутивной. И наоборот, если мутация приводит к неспособности репрессора связываться с индуктором, то дерепрессии Lac-оперона (необходимым условием которой является именно образование комплекса между индуктором и репрессором, связанным с операторной областью) не наблюдается даже при высоких концентрациях индуктора в среде.
Мутантная бактерия, у которой операторная последовательность изменена так, что нормальный репрессор оказывается неспособным связаться с ней, также приобретает способность к конститутивной экспрессии Lac-onepoнa.
Бактериофаг лямбда
Некоторые бактерии несут вирусы (умеренные бактериофаги), которые либо встроены в хромосому клетки-хозяина и реплицируются вместе с ней, либо существуют в клетке автономно и реплицируются самостоятельно, что в конечном итоге приводит к лизису и гибели бактерий. Один из таких умеренных бактериофагов — бактериофаг лямбда (X). При инфицировании чувствительных бактерий Е. coli он «инъецирует» в бактериальную клетку свой геном, состоящий из линейной двухцепочечной ДНК размером 45000 пар оснований (рис. 41.5). В зависимости от физиологического статуса микроорганизма дальнейшее развитие фага может протекать либо по лизогенному пути, который заключается в интеграции фаговой ДНК с хозяйским геномом и сохранении

Рис. 41.5. Заражение E.coli фагом начинается с адсорбции фаговой частицы на поверхности бактериальной клетки (1). Следующий этап — инъекция фаговой ДНК (темная линия) в клетку (2, 3). Далее события развиваются в одном из двух возможных направлений. При лизогенном пути фаговая ДНК встраивается в бактериальную хромосому (4, 5). В этом случае ДНК фага реплицируется, как интегральная часть хромосомы — пассивно, при клеточном делении. К четки, несущие интегрированный («спящий») вирус, называют лизогенными, а сам интегрированныи фаг профагом. При альтернативном литическом пути развития инфекции фаговая ДНК реплицируется независимо (6) и направляет синтез фаговых белков (7). Образуется около 100 новых фаговых частиц. Размножение фага в конечном итоге приводит к лизису клетки-хозяина (8). Профаг может быть индуцирован при воздействии различных факторов, например при ультрафиолетовом облучении (9). Индуцирующий агент осуществляет переключение в работе двух альтернативных наборов генов. При этом ДНК фага вырезается из хозяйской хромосомы (10) и начинается литиче-ский цикл. (Reproduced, with permission, from Ptashne М., Johnson A. D., Pabo С. О A genetic switch in a bacterial virus. Sci. Am. [Nov.] 1982, 247, 128.)
в скрытой форме вплоть до «активации» (см. ниже), либо по пути лигического развития. При этом происходит серия репликаций ДНК фага и образуется примерно 100 копий фагового генома. Каждый из них пакуется в белковый капсид, зрелые фаговые частицы вызывают лизис хозяйской клетки. Освободившиеся бактериофаги могут вновь инфицировать чувствительные бактериальные клетки.
Будучи интегрированной с геномом клетки-хозяина, ДНК фага X сохраняется в «скрытом» состоянии (в виде профага) до тех пор, пока не будет подвержена активации в результате воздействия на лизогенную клетку тех или иных ДНК-повреждающих агентов. В ответ на такое воздействие профаг «индуцируется» — начинается транскрипция и трансляция фаговых генов, необходимых для вырезания фаговой ДНК из хозяйской хромосомы, ее репликации, упаковки в белковый капсид и клеточного лизиса. Это развитие запускается с помощью механизма, подобного триггерному, что соответствует варианту С на рис. 41.1. Это означает, что после акта индукции профака обратное развитие становится невозможным: процесс протекает вплоть до клеточного лизиса и высвобождения новых фаговых частиц. Переключение пути развития с лизогенного (состояние профага) на литический (вирулентный фаг) прекрасно изучено на молекулярном и генетическом уровнях и будет далее представлено в виде парадигмы.
В переключении пути развития фага участвует область ДНК размером в  пар оснований, называемая «правым оператором»
пар оснований, называемая «правым оператором»  (рис. 41.6. Правый оператор фланкирован слева структурным геном репрессора фага лямбда, а справа — структурным геном другого регуляторного белка, называемого его. Единственным фаговым геном, экспрессирующимся при нахождении фаговой ДНК в составе хозяйской хромосомы, т. е. в состоянии профага, является ген репрессора. При литическом развитии ген репрессора не экспрессируется, но идет активная экспрессия гена его, равно как и многих других фаговых генов. Таким образом, когда ген репрессора включен, ген его — включен, и наоборот, когда ген его включен, ген репрессора — выключен. Как мы увидим далее, эти два гена регулируют друг друга, что в конечном счете и определяет выбор между литическим и лизогенным путями развития фага X.
(рис. 41.6. Правый оператор фланкирован слева структурным геном репрессора фага лямбда, а справа — структурным геном другого регуляторного белка, называемого его. Единственным фаговым геном, экспрессирующимся при нахождении фаговой ДНК в составе хозяйской хромосомы, т. е. в состоянии профага, является ген репрессора. При литическом развитии ген репрессора не экспрессируется, но идет активная экспрессия гена его, равно как и многих других фаговых генов. Таким образом, когда ген репрессора включен, ген его — включен, и наоборот, когда ген его включен, ген репрессора — выключен. Как мы увидим далее, эти два гена регулируют друг друга, что в конечном счете и определяет выбор между литическим и лизогенным путями развития фага X.
Область оператора состоит из трех расположенных друг за другом дискретных похожих, но не идентичных участков последовательности длиной по 17 пар оснований (рис. 41.6, Б). Каждый из этих трех участков  может связывать репрессор или стобелок главным образом за счет контактов между молекулой белка небольшой бороздкой двойной спирали ДНК. Область ДНК между генами репрессора и его также содержит две промоторные
может связывать репрессор или стобелок главным образом за счет контактов между молекулой белка небольшой бороздкой двойной спирали ДНК. Область ДНК между генами репрессора и его также содержит две промоторные

Рис. 41.6. Схематическое изображение правого оператора  фага X. (серия рисунков с последовательным увеличением количества деталей структуры). Область оператора — это участок фаговой ДНК размером около 80 п. о. А. Операторная область фланкируется геном лямбда-репрессора (слева) и геном регуляторного белка его (справа). Б. Область оператора состоит из трех функциональных участков
фага X. (серия рисунков с последовательным увеличением количества деталей структуры). Область оператора — это участок фаговой ДНК размером около 80 п. о. А. Операторная область фланкируется геном лямбда-репрессора (слева) и геном регуляторного белка его (справа). Б. Область оператора состоит из трех функциональных участков  каждый длиной 17 пар оснований. Все три участка узнаются как репрессором, так и белком его. Эти участки перекрываются с последовательностями двух промоторов, т. е. с участками связывания РНК-полимеразы, что необходимо для начала синтеза мРНК (волнистая линия), по которой затем идет синтез соответствующего белка. В. Нуклеотидная последовательность участка Or 1. (Reproduced with permission from Ptashne М., Johnson A. D, Pabo C.O. A genetic switch in a bacterial virus. Sci. Am. [Nov.] 1982, 247, 128.)
каждый длиной 17 пар оснований. Все три участка узнаются как репрессором, так и белком его. Эти участки перекрываются с последовательностями двух промоторов, т. е. с участками связывания РНК-полимеразы, что необходимо для начала синтеза мРНК (волнистая линия), по которой затем идет синтез соответствующего белка. В. Нуклеотидная последовательность участка Or 1. (Reproduced with permission from Ptashne М., Johnson A. D, Pabo C.O. A genetic switch in a bacterial virus. Sci. Am. [Nov.] 1982, 247, 128.)
последовательности, которые определяют связывание РНК-полимеразы в определенной ориентации. Один промотор направляет транскрипцию вправо, и потому с него транскрибируется его и другие дистальные гены. Другой промотор направляет транскрипцию влево, т. е. в направлении транскрипции гена репрессора (рис. 41.6, В).
Продукт гена репрессора, белок-репрессор, состоящий из 236 аминокислот, организован в двухдоменную структуру, в которой N-концевой домен связывается с ДНК операторного участка, а С-концевой домен отвечает за связывание с другой молекулой репрессора с образованием димера. Димерный репрессор связывается с ДНК оператора более прочно, чем мономер (рис. 41.7, А-В).
Продукт гена его, сто-белок, состоящий из 66 аминокислот, обладает однодоменной структурой, но также связывается более прочно с оператором в димерной форме (рис. 47.7, Г). Очевидно, что единственный домен  -белка отвечает как за связывание с ДНК, так и за димеризацию.
-белка отвечает как за связывание с ДНК, так и за димеризацию.
В лизогенной бактерии, содержащей  в состоянии профага, Х-репрессор связывается преимущественно с
в состоянии профага, Х-репрессор связывается преимущественно с  и при этом за счет кооперативных взаимодействий способствует связыванию другой димерной молекулы репрессора с участком
и при этом за счет кооперативных взаимодействий способствует связыванию другой димерной молекулы репрессора с участком  Из трех участков оператора наименьшим сродством к репрессору характеризуется участок
Из трех участков оператора наименьшим сродством к репрессору характеризуется участок  Связывание репрессора с
Связывание репрессора с  приводит к двум основным эффектам. Во-первых, РНК-полимераза не может связаться с правонанравленным промотором, и, следовательно, сго-ген не экспрессируется. Во-вторых, как сказано выше, репрессорный димер, связавшись с
приводит к двум основным эффектам. Во-первых, РНК-полимераза не может связаться с правонанравленным промотором, и, следовательно, сго-ген не экспрессируется. Во-вторых, как сказано выше, репрессорный димер, связавшись с  усиливает связывание другого димера с
усиливает связывание другого димера с  Связывание репрессора с
Связывание репрессора с  дает важный дополнительный эффект, проявляющийся в повышении эффективности связывания РНК-полимеразы с левонаправленным промотором, перекрывающимся с
дает важный дополнительный эффект, проявляющийся в повышении эффективности связывания РНК-полимеразы с левонаправленным промотором, перекрывающимся с  , что приводит к усилению экспрессии гена репрессора. Такое усиление, по-видимому, опосредовано взаимодействием белок— белкового характера между репрессором, связанным с
, что приводит к усилению экспрессии гена репрессора. Такое усиление, по-видимому, опосредовано взаимодействием белок— белкового характера между репрессором, связанным с  и РНК-полимеразой, связанной с промотором. Следовательно, Х-репрессор служит одновременно и негативным регулятором, препятствующим транскрипции гена его, и позитивным регулятором, усиливающим транскрипцию своего собственного гена. Этот двойственный характер действия репрессора обусловливает стабильность состояния профага: репрессор не только подавляет экспрессию генов литического развития, но и усиливает свою собственную экспрессию. И то и другое способствует поддержанию лизогенного статуса клетки (т. е. существование бактеориофага в форме профага). Когда концентрация репрессора достигает очень высоких значений, становится возможным его связывание с
и РНК-полимеразой, связанной с промотором. Следовательно, Х-репрессор служит одновременно и негативным регулятором, препятствующим транскрипции гена его, и позитивным регулятором, усиливающим транскрипцию своего собственного гена. Этот двойственный характер действия репрессора обусловливает стабильность состояния профага: репрессор не только подавляет экспрессию генов литического развития, но и усиливает свою собственную экспрессию. И то и другое способствует поддержанию лизогенного статуса клетки (т. е. существование бактеориофага в форме профага). Когда концентрация репрессора достигает очень высоких значений, становится возможным его связывание с  что в свою очередь понижает эффективность транскрипции гена репрессора с левого промотора. Как следствие этого, концентрация репрессора снижается до таких значений, при которых происходит диссоциация комплекса репрессора с участком
что в свою очередь понижает эффективность транскрипции гена репрессора с левого промотора. Как следствие этого, концентрация репрессора снижается до таких значений, при которых происходит диссоциация комплекса репрессора с участком  .
.
Когда ДНК-повреждающий сигнал, например ультрафиолетовое облучение, оказывает воздействие на лизогенную бактериальную клетку, образующиеся фрагменты одноцепочечной ДНК активируют специфическую бактериальную протеазу, кодируемую геном гесА (рис. 41.8). Активированная  -протеаза расщепляет ту часть молекулы
-протеаза расщепляет ту часть молекулы

Рис. 41.7. Белок лямбда-репрессора представляет собой полипептид длиной 236 аминокислот. Полипептид свертывается в гантелеобразную структуру, в рамках которой можно выделить два домена — N- и С-концевой. Эти два домена соединены между собой участком полипептидной цепи, чувствительным к действию протеаз (А). Единичные молекулы репрессора (мономеры) ассоциируют в димеры (В). Димер способен вновь диссоциировать до мономеров. Мономеры удерживаются в димере в основном за счет взаимодействия С-концевых доменов (область контакта заштрихована). Димеры репрессора способны обратимо связываться с операторным участком, проявляя наибольшее сродство к участку  Контакты с ДНК (заштрихованная область) осуществляются в основном при участии
Контакты с ДНК (заштрихованная область) осуществляются в основном при участии  -концевых доменов. Веток его (Г) однодоменный белок, обладающий сайтами димеризации; в димерной форме этот белок связывается с оператором, предпочтительно с участком
-концевых доменов. Веток его (Г) однодоменный белок, обладающий сайтами димеризации; в димерной форме этот белок связывается с оператором, предпочтительно с участком  . (Reproduced with permission from Ptashne М., Johnson A. D. Pabo C. O. A genetic switch in bacterial virus Sci. Am [Nov.] 1982, 247, 128.)
. (Reproduced with permission from Ptashne М., Johnson A. D. Pabo C. O. A genetic switch in bacterial virus Sci. Am [Nov.] 1982, 247, 128.)
репрессора, которая соединяет его N- и С-концевые домены. Такое расщепление приводит к диссоциации димера репрессора, а затем и его комплекса с  Последствия удаления репрессора с участков
Последствия удаления репрессора с участков  легко предсказуемы. РНК-полимераза немедленно получает доступ к правонаправленному промотору и начинает транскрипцию гена его. Кроме того, утрачивается и усиливающий эффект комплекса репрессор—
легко предсказуемы. РНК-полимераза немедленно получает доступ к правонаправленному промотору и начинает транскрипцию гена его. Кроме того, утрачивается и усиливающий эффект комплекса репрессор— на левостороннюю транскрипцию (рис. 41.8).
на левостороннюю транскрипцию (рис. 41.8).
Белок сто, образующийся при трансляции новообразованного транскрипта, также связывается с операторной областью в димерной форме, но порядок предпочтения операторных участков у сго-белка — обратный по сравнению с белком-репрессором. То есть сто-белок наиболее прочно связывается с  при этом полностью отсутствует какой-либо кооперативный эффект связывания с
при этом полностью отсутствует какой-либо кооперативный эффект связывания с  в отношении связывания другой димерной молекулы с участком
в отношении связывания другой димерной молекулы с участком  При повышении концентрации сго-белок начинает связываться с
При повышении концентрации сго-белок начинает связываться с  а затем и с
а затем и с  .
.
«Посадка» сго-белка на  незамедлительно отключает левостороннюю транскрипцию и, следовательно,
незамедлительно отключает левостороннюю транскрипцию и, следовательно,
Рис. 41.8. Четыре стадии жизненного цикла фага X и схема переключения пути развития. Лизогенный путь (вирус в состоянии профага) избирается при связывании димерного репрессора с  Посадка репрессора на
Посадка репрессора на  способствует связыванию другой молекулы репрессора с
способствует связыванию другой молекулы репрессора с  . В состоянии профага (вверху) димеры репрессора, связавшись с
. В состоянии профага (вверху) димеры репрессора, связавшись с  препятствуют посадке РНК-полимеразы на расположенный справа промотор и таким образом блокируют синтез сго-белка (негативный контроль). При этом одновременно стимулируется связывание полимеразы с расположенным слева промотором (позитивный контроль), что приводит к более активной транскрипции гена репрессора (рспрессорная мРНК изображена волнистой линией) и соответственно к более эффективной наработке бетка-репрессора, обеспечивающего поддержание лизогенного состояния. Профаг может быть индуцирован,
препятствуют посадке РНК-полимеразы на расположенный справа промотор и таким образом блокируют синтез сго-белка (негативный контроль). При этом одновременно стимулируется связывание полимеразы с расположенным слева промотором (позитивный контроль), что приводит к более активной транскрипции гена репрессора (рспрессорная мРНК изображена волнистой линией) и соответственно к более эффективной наработке бетка-репрессора, обеспечивающего поддержание лизогенного состояния. Профаг может быть индуцирован,  да активированная ультрафиолетовым облучением протеаза
да активированная ультрафиолетовым облучением протеаза  А начинает расщеплять мономеры репрессора. Равновесие между свободными молекулами мономеров, димеров и связанных с оператором димеров нарушается, и димеры покидают операторный участок. Ничто более не способствует связыванию РНК-полимеразы с левым промотором, и синтез репрессора прекращается. В процессе индукции высвобождаются все операторные участки, полимераза связывается с правым промотором и начинается наработка сго-белка. На ранних этапах литического цикла единичный димер сго-белка связывается с участком
А начинает расщеплять мономеры репрессора. Равновесие между свободными молекулами мономеров, димеров и связанных с оператором димеров нарушается, и димеры покидают операторный участок. Ничто более не способствует связыванию РНК-полимеразы с левым промотором, и синтез репрессора прекращается. В процессе индукции высвобождаются все операторные участки, полимераза связывается с правым промотором и начинается наработка сго-белка. На ранних этапах литического цикла единичный димер сго-белка связывается с участком  к которому он обладает повышенным сродством. Теперь полимераза не может связаться с левым промотором, а правый промотор остается доступным. Полимераза продолжает связываться с ним. Происходит транскрипция гена его и других ранних литических генов. Устанавливается литический путь развития. (Reproduced with permission from Ptashne М., Johnson A. D., Pabo C. O. A genetic switch in bacterial virus. Sci. Am. [Nov.] 1982, 247, 128.)
к которому он обладает повышенным сродством. Теперь полимераза не может связаться с левым промотором, а правый промотор остается доступным. Полимераза продолжает связываться с ним. Происходит транскрипция гена его и других ранних литических генов. Устанавливается литический путь развития. (Reproduced with permission from Ptashne М., Johnson A. D., Pabo C. O. A genetic switch in bacterial virus. Sci. Am. [Nov.] 1982, 247, 128.)
Рисунок (см. скан)
препятствует дальнейшей экспрессии гена репрессора. Таким образом происходит полное переключение — экспрессируется сго-ген, а ген репрессора выключен. Это событие необратимо, вслед за ним начинается экспрессия остальных фаговых генов, т. е. запускается цикл нормального литичеекого развития фага X. Когда концентрация сго-белка становится достаточно высокой, он связывается с участком  и таким образом снижает уровень экспрессии собственного гена, что существенно для реализации последних стадий цикла литичеекого развития.
и таким образом снижает уровень экспрессии собственного гена, что существенно для реализации последних стадий цикла литичеекого развития.
И для сго-белка, и для белка-репрессора с помощью методов рентгеновской кристаллографии установлена пространственная структура. Предложены и проверены модели связывания данных белков с ДНК, проанализированы и имеющие к этому отношение молекулярные и генетические события. До настоящего времени  остается наиболее изученным и в отношении молекулярного механизма регуляции экспрессии генов.
остается наиболее изученным и в отношении молекулярного механизма регуляции экспрессии генов.
Аттенуация транскрипции
Бактериальные опероны, ответственные за биосинтез аминокислот, часто обладают дополнительной системой контроля экспрессии, основанной на преждевременной терминации транскрипции. Этот процесс, называемый аттенуацией, функционирует независимо от промоторно — операторной системы регуляции экспрессии. Аттенуация используется для регуляции экспрессии в ответ на воздействие различных физиологических факторов. Процесс регуляции на основе аттенуации включает начало трансляции, остановку рибосомы и переключение альтернативных вариантов вторичной структуры РНК, один из которых формирует терминатор транскрипции, а другой — препятствует образованию терминаторной структуры. У Е. соН объектами аттенуации являются опероны триптофана, фенилаланина, гистидина, треонина, лейцина, изолейцина и валина.
Остановимся на аттенуации триптофанового  оперона, как наиболее полно изученной системе. Структура триптофанового
оперона, как наиболее полно изученной системе. Структура триптофанового  оперона представлена на рис. 41.9. Его промоторно—операторная система регуляции аналогична описанной выше для Lас-оперона. Репрессия Тгр-оперона приводит к
оперона представлена на рис. 41.9. Его промоторно—операторная система регуляции аналогична описанной выше для Lас-оперона. Репрессия Тгр-оперона приводит к  -кратному снижению уровня транскрипции, однако мутанты, лишенные функциональной системы репрессии, тем не менее сохраняют способность отвечать на триптофановое голодание 8 10-кратным повышением уровня синтеза Тгр-мРНК. При анализе других типов мутаций в Е.
-кратному снижению уровня транскрипции, однако мутанты, лишенные функциональной системы репрессии, тем не менее сохраняют способность отвечать на триптофановое голодание 8 10-кратным повышением уровня синтеза Тгр-мРНК. При анализе других типов мутаций в Е.  стало ясно, что процесс аттенуации связан скорее с эффективностью трансляции триптофановых кодонов, чем с непосредственным влиянием изменения концентрации свободного триптофана в среде.
стало ясно, что процесс аттенуации связан скорее с эффективностью трансляции триптофановых кодонов, чем с непосредственным влиянием изменения концентрации свободного триптофана в среде.

Рис. 41.9. Регуляторная область и структурные гены Тгр-оперона E.coli Инициация транскрипции контролируется промотором-оператором Терминация транскрипции контролируется аттенуатором в области  -звенной лидернои последовательности
-звенной лидернои последовательности  Вес молекулы полимеразы, осуществляющие транскрипцию оперона, прежде чем двигаться дальше, делают временную остановку на участке аттенуации (Reproduced with permission from Yanofsky С Attenuation in control of expression of bacterial operons. Nature 1981, 289, 751.)
Вес молекулы полимеразы, осуществляющие транскрипцию оперона, прежде чем двигаться дальше, делают временную остановку на участке аттенуации (Reproduced with permission from Yanofsky С Attenuation in control of expression of bacterial operons. Nature 1981, 289, 751.)
Вскоре было установлено, что в  -участке (рис. 41.9) оперона может происходить преждевременная гермипация транскрипции, предотвращающая транскрипцию дистальных генов
-участке (рис. 41.9) оперона может происходить преждевременная гермипация транскрипции, предотвращающая транскрипцию дистальных генов  оперона. Эта преждевременная терминация происходит тогда, когда трансляция триптофановых кодонов в Trpl протекает с нормальной скоростью. В результате такой терминации (аттенуации) образуется так называемый лидерный транскрипт длиной 140 нуклеогидов вместо протяженного полицистронного транскрипта всего оперона, необходимого для образования всех ферментов пути биосинтеза триптофана. С помощью методов генной инженерии удалось получить мутации по аттенуаторному участку и провести анализ соответствующих нуклеотидных последовательностей. Комбинация генетических и генно-инженерных подходов позволила воссоздать следующую динамическую картину процесса аттенуации.
оперона. Эта преждевременная терминация происходит тогда, когда трансляция триптофановых кодонов в Trpl протекает с нормальной скоростью. В результате такой терминации (аттенуации) образуется так называемый лидерный транскрипт длиной 140 нуклеогидов вместо протяженного полицистронного транскрипта всего оперона, необходимого для образования всех ферментов пути биосинтеза триптофана. С помощью методов генной инженерии удалось получить мутации по аттенуаторному участку и провести анализ соответствующих нуклеотидных последовательностей. Комбинация генетических и генно-инженерных подходов позволила воссоздать следующую динамическую картину процесса аттенуации.
На участке  - промотора РНК-полимераза, свободная от контроля со стороны репрессора, начинает транскрипцию оперона и доходит до 90-го нуклеотида (рис. 41.10), где она делает временную остановку. Во время этой паузы к образовавшемуся
- промотора РНК-полимераза, свободная от контроля со стороны репрессора, начинает транскрипцию оперона и доходит до 90-го нуклеотида (рис. 41.10), где она делает временную остановку. Во время этой паузы к образовавшемуся  -концу лидерного транскрипта в области 27—29 стартовою кодона AUG прикрепляется рибосома, происходит трансляция лидерною пептида длиной 14 аминокислот. Начиная с положения 54, в транскрипте последовательно расположены два трипюфановых кодона, поэтому для продолжения трансляции необходимо присутствие тРН
-концу лидерного транскрипта в области 27—29 стартовою кодона AUG прикрепляется рибосома, происходит трансляция лидерною пептида длиной 14 аминокислот. Начиная с положения 54, в транскрипте последовательно расположены два трипюфановых кодона, поэтому для продолжения трансляции необходимо присутствие тРН  . Следует отметить, что триптофан — относительно редкая аминокислота. Еще реже два остатка триптофана располагаются друт за другом в составе полипептидов.
. Следует отметить, что триптофан — относительно редкая аминокислота. Еще реже два остатка триптофана располагаются друт за другом в составе полипептидов.

Рис. 41.10. Нуклеотидная последовательность 5-конца Trp-мРНК. Показан нетерминированный транскрипт. При терминации транскрипции на аттенуаторе образуется  -нуклеотидный транскрипт. Его З-конец обозначен стрелкой. 3-Конец 90-членного транскрипта, образованного при остановке в сайте паузы транскрипции, показан жирной чертой. Два сайта связывания рибосомы с триплетами AUG в центре подчеркнуты. Заключены в квадраты кодоны начала (AUG) и конца (UGA) трансляции. Показаны предполагаемые аминокислотные последовательности лидерного пептида и начала белка Trp Е. (Reproduced with permisson from Yanofsky С. Attenuation in the control of expression of bacterial operons. Nature 1981, 289, 751.)
-нуклеотидный транскрипт. Его З-конец обозначен стрелкой. 3-Конец 90-членного транскрипта, образованного при остановке в сайте паузы транскрипции, показан жирной чертой. Два сайта связывания рибосомы с триплетами AUG в центре подчеркнуты. Заключены в квадраты кодоны начала (AUG) и конца (UGA) трансляции. Показаны предполагаемые аминокислотные последовательности лидерного пептида и начала белка Trp Е. (Reproduced with permisson from Yanofsky С. Attenuation in the control of expression of bacterial operons. Nature 1981, 289, 751.)
поэтому трансляция лидерного пептида является способом «тестирования» уровня  , который в свою очередь зависит от уровня триптофана в клетке. Когда РНК-полимераза возобновляет транскрипцию после сайта остановки (в положении 90), рибосома, транслирующая лидерный пептид, доходит до стоп-кодона (в положении 70) при наличии в достаточных количествах тРНКТгр. При недостатке
, который в свою очередь зависит от уровня триптофана в клетке. Когда РНК-полимераза возобновляет транскрипцию после сайта остановки (в положении 90), рибосома, транслирующая лидерный пептид, доходит до стоп-кодона (в положении 70) при наличии в достаточных количествах тРНКТгр. При недостатке  рибосома останавливается раньше — на участке, содержащем два тандемных триптофановых кодона. Положение рибосомы на лидерном транскрипте определяет выбор одной из двух альтернативных вторичных структур, образуемых РНК-транскриптом.
рибосома останавливается раньше — на участке, содержащем два тандемных триптофановых кодона. Положение рибосомы на лидерном транскрипте определяет выбор одной из двух альтернативных вторичных структур, образуемых РНК-транскриптом.
Нуклеотидная последовательность лидерного транскрипта такова, что между областями, обозначенными цифрами 1 и 2, 3 и 4, возможно формирование шпилечных структур (рис. 41.11) в соответствии с правилами образования комплементарных пар (А: U, G: С). Шпилька между областями 3 и 4 служит сигналом терминации транскрипции. В этом случае транскрипция завершается примерно за 140-м нуклеотидом с образованием преждевременно терминированного транскрипта длиной 140 нуклеотидов.
Области 2 и 3 транскрипта также способны образовать шпильку. Это приводит к образованию альтернативной вторичной структуры, препятствующей формированию терминирующего сигнала шпильки  Когда рибосома временно останавливается на двух
Когда рибосома временно останавливается на двух  -кодонах (рис. 41.11, Б), область 1 оказывается «защищена», а области 2 и 3 образуют шпилечную структуру. Тем самым исключается преждевременная терминация и РНК-полимераза может продолжить транскрипцию за 140-й нуклеотид с образованием полицистронной мРНК, которая кодирует ферменты биосинтеза триптофана.
-кодонах (рис. 41.11, Б), область 1 оказывается «защищена», а области 2 и 3 образуют шпилечную структуру. Тем самым исключается преждевременная терминация и РНК-полимераза может продолжить транскрипцию за 140-й нуклеотид с образованием полицистронной мРНК, которая кодирует ферменты биосинтеза триптофана.
Если в клетке имеется достаточное количество Тгр-тРНКТгр, рибосома проходит  -кодоны в лидерной последовательности и доходит до сигнала остановки трансляции (UGA) в области 2, экранируя таким образом обе области — 1 и 2. При этом сегменты 3 и 4 могут образовать шпильку—сигнал преждевременной терминации транскрипции, далее которого РНК-полимераза не сможет вести транскрипцию оперона. Вместо полицистронной
-кодоны в лидерной последовательности и доходит до сигнала остановки трансляции (UGA) в области 2, экранируя таким образом обе области — 1 и 2. При этом сегменты 3 и 4 могут образовать шпильку—сигнал преждевременной терминации транскрипции, далее которого РНК-полимераза не сможет вести транскрипцию оперона. Вместо полицистронной  кодирующей ферменты триптофанового оперона, образуется преждевременно терминированный транскрипт длиной 140 нуклеотидов. Образование взаимоисключающих вторичных структур (между областями 2 и 3 или 3 и 4) и является внутриклеточным сигналом, информирующим РНК-полимеразу о способности клетки транслировать триптофано-вые кодоны.
кодирующей ферменты триптофанового оперона, образуется преждевременно терминированный транскрипт длиной 140 нуклеотидов. Образование взаимоисключающих вторичных структур (между областями 2 и 3 или 3 и 4) и является внутриклеточным сигналом, информирующим РНК-полимеразу о способности клетки транслировать триптофано-вые кодоны.
На рис. 41.12 представлены аминокислотные последовательности лидерных пептидов, предсказанные по соответствующим нуклеотидным последовательностям, для нескольких других оперонов Е. coli и Salmonella typhimurium. Из рисунка видно, что в лидирующей последовательности существенно превалирует именно та аминокислота, ферменты биосинтеза которой кодируются данным опероном.
Недавно феномен аттенуации был описан и для клеток млекопитающих. Механизм аттенуации для них неизвестен, однако очевидно, что он должен сильно отличаться от вышеописанного, поскольку транскрипция и трансляция у эукариот происходят в разных внутриклеточных компартментах.

Рис. 41.11. Модель процесса аттенуации для Тгр-оперона E.coli. При избытке триптофана рибосома, транслирует ли-дерную РНК, в результате синтезируется полный лидерный пептид. Рибосома маскирует области 1 и 2 цепи мРНК и препятствует таким образом образованию шпилек из последовательностей 1:2 и 2:3. В этих условиях свободно образуется только шпилька 3:4, РНК-полимераза (не показана) транскрибирует лидерный пептид до полной остановки транскрипции. При недостатке триптофана заряженная тРНКТгр будет лимитирующим фактором и рибосома задержится на тандемных триптофановых кодонах лидерно-го пептида. В данном случае рибосома маскирует только область, поэтому может образоваться шпилька 2:3, что исключает возможность образования терминирующей шпильки 3:4. В связи с этим РНК-полимераза продолжает транскрипцию области структурных генов. Когда лидерный транскрипт не транслируется, становится возможным образование шпильки 1:2 непосредственно после синтеза соответствующих участков в ходе транскрипции, что в свою очередь создает благоприятные условия для формирования терминирующей шпильки 3:4. (Reproduced with permission from Oxender D., Zurawski G., Yanofsky C. Atte-nuration of the Escherichia coli tryptophan operon: Role of RNA secondary structure involving trytophan codon region. Proc. Natl. Acad. Sci. USA 1979. 76, 5524.)
| << Предыдущий параграф | Следующий параграф >> |
- Раздел IV. Структура, функция и репликация информационных макромолекул
- СТРУКТУРА ПУРИНОВЫХ И ПИРИМИДИНОВЫХ ОСНОВАНИЙ
- ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА ПУРИНОВЫХ И ПИРИМИДИНОВЫХ ОСНОВАНИЙ
- НУКЛЕОЗИДЫ И НУКЛЕОТИДЫ
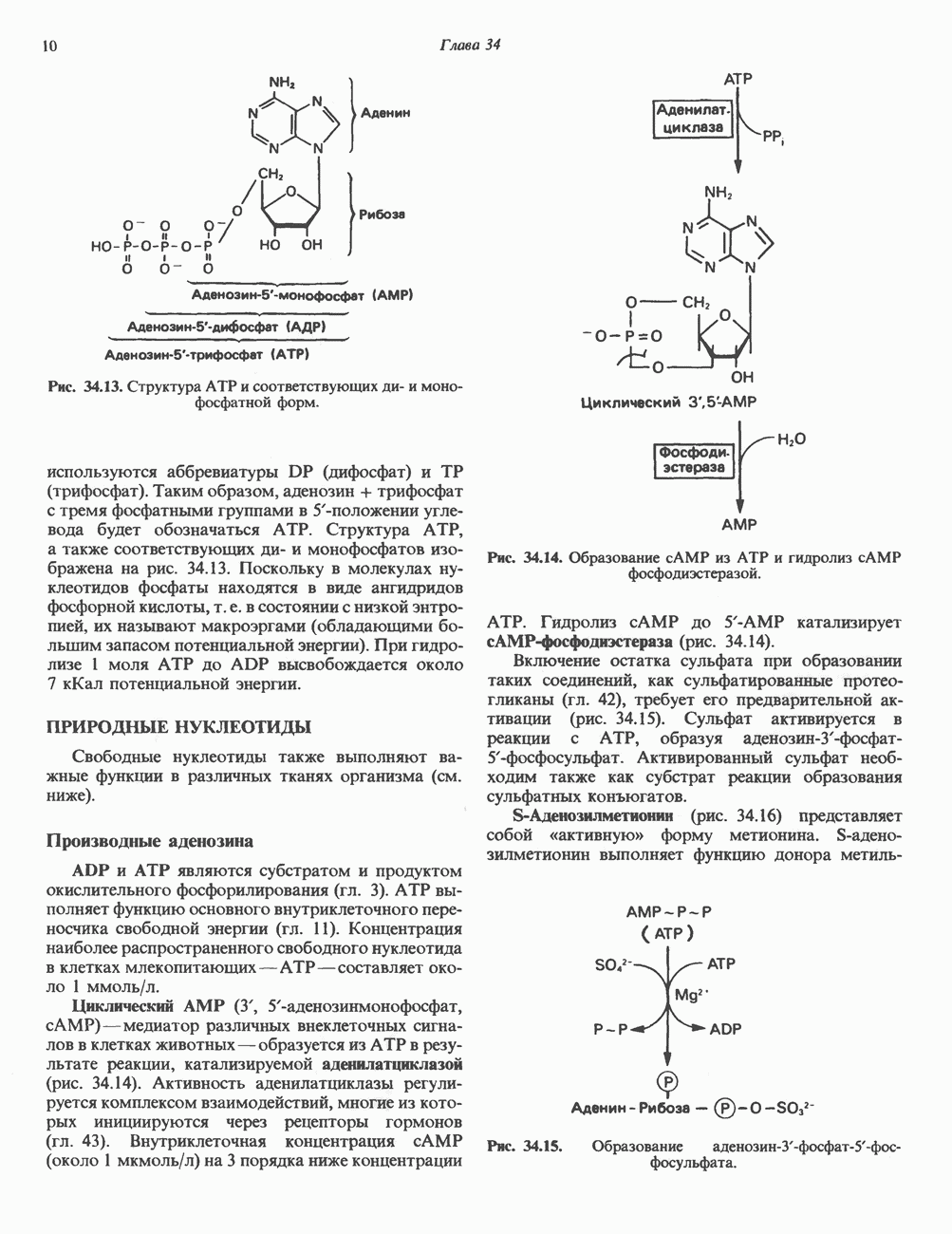
- ПРИРОДНЫЕ НУКЛЕОТИДЫ
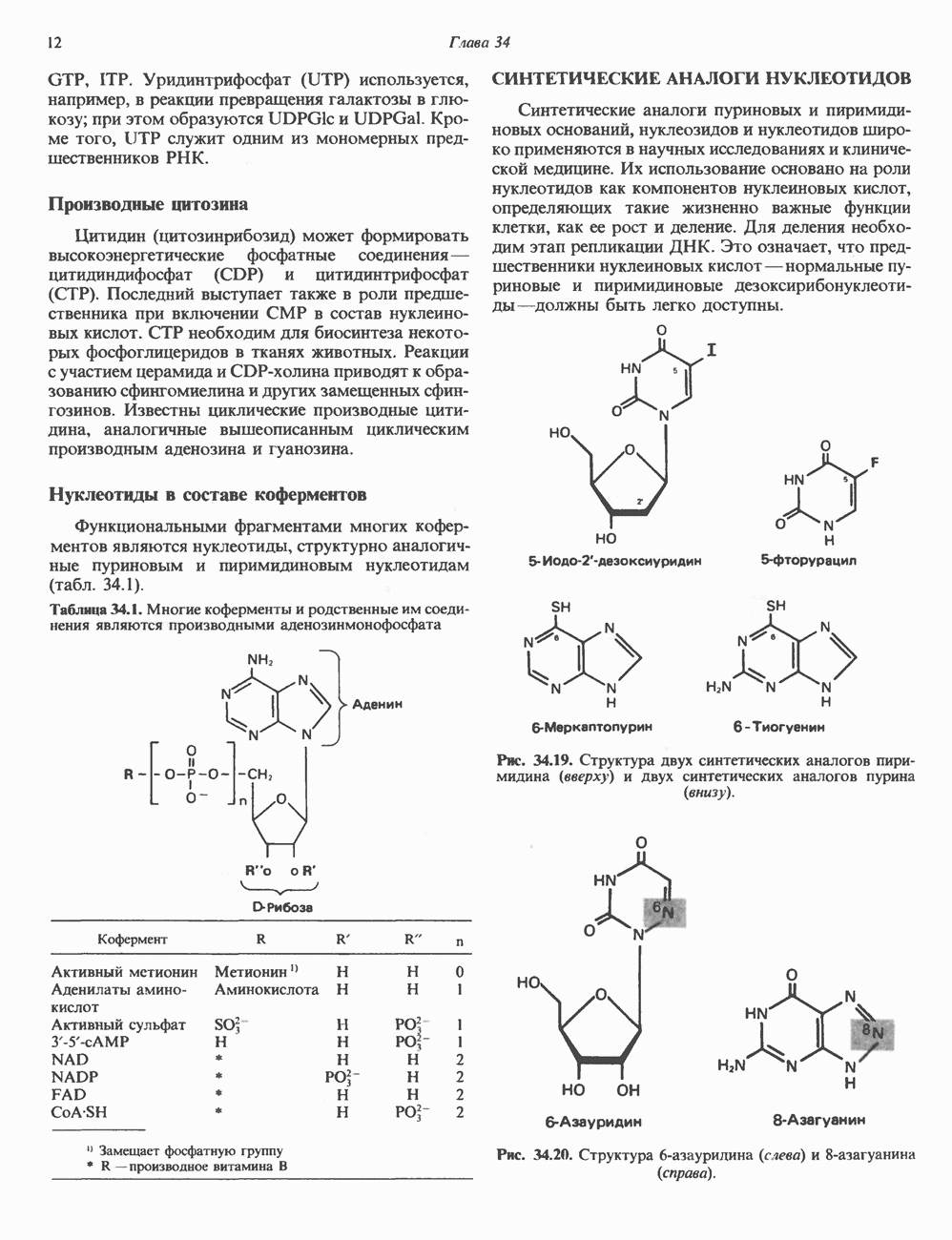
- СИНТЕТИЧЕСКИЕ АНАЛОГИ НУКЛЕОТИДОВ
- Глава 35. Метаболизм пуриновых и пиримидиновых нуклеотидов
- УСВОЕНИЕ
- ПУРИНЫ
- ПИРИМИДИНЫ
- КЛИНИЧЕСКИЕ НАРУШЕНИЯ МЕТАБОЛИЗМА ПУРИНОВ (ТАБЛ. 35.1)
- ЗАБОЛЕВАНИЯ, СВЯЗАННЫЕ С НАРУШЕНИЕМ МЕТАБОЛИЗМА ПИРИМИДИНОВ (ТАБЛ. 35.3)
- Глава 36. Технология рекомбинантных ДНК
- ОСНОВНЫЕ СВОЙСТВА ДНК
- ОСНОВНЫЕ ПОНЯТИЯ ГЕННОЙ ИНЖЕНЕРИИ
- НЕКОТОРЫЕ ПРАКТИЧЕСКИЕ ПРИЛОЖЕНИЯ ТЕХНОЛОГИИ РЕКОМБИНАНТНОЙ ДНК
- ГЕННАЯ ИНЖЕНЕРИЯ И АНАЛИЗ МОЛЕКУЛЯРНОЙ ПРИРОДЫ ЗАБОЛЕВАНИЙ
- СЛОВАРЬ-СПРАВОЧНИК
- ЛИТЕРАТУРА
- Глава 37. Структура и функция нуклеиновых кислот
- ДНК
- РНК
- Глава 38. Организация и репликация ДНК
- ХРОМАТИН
- ГИСТОНЫ И НУКЛЕОСОМЫ
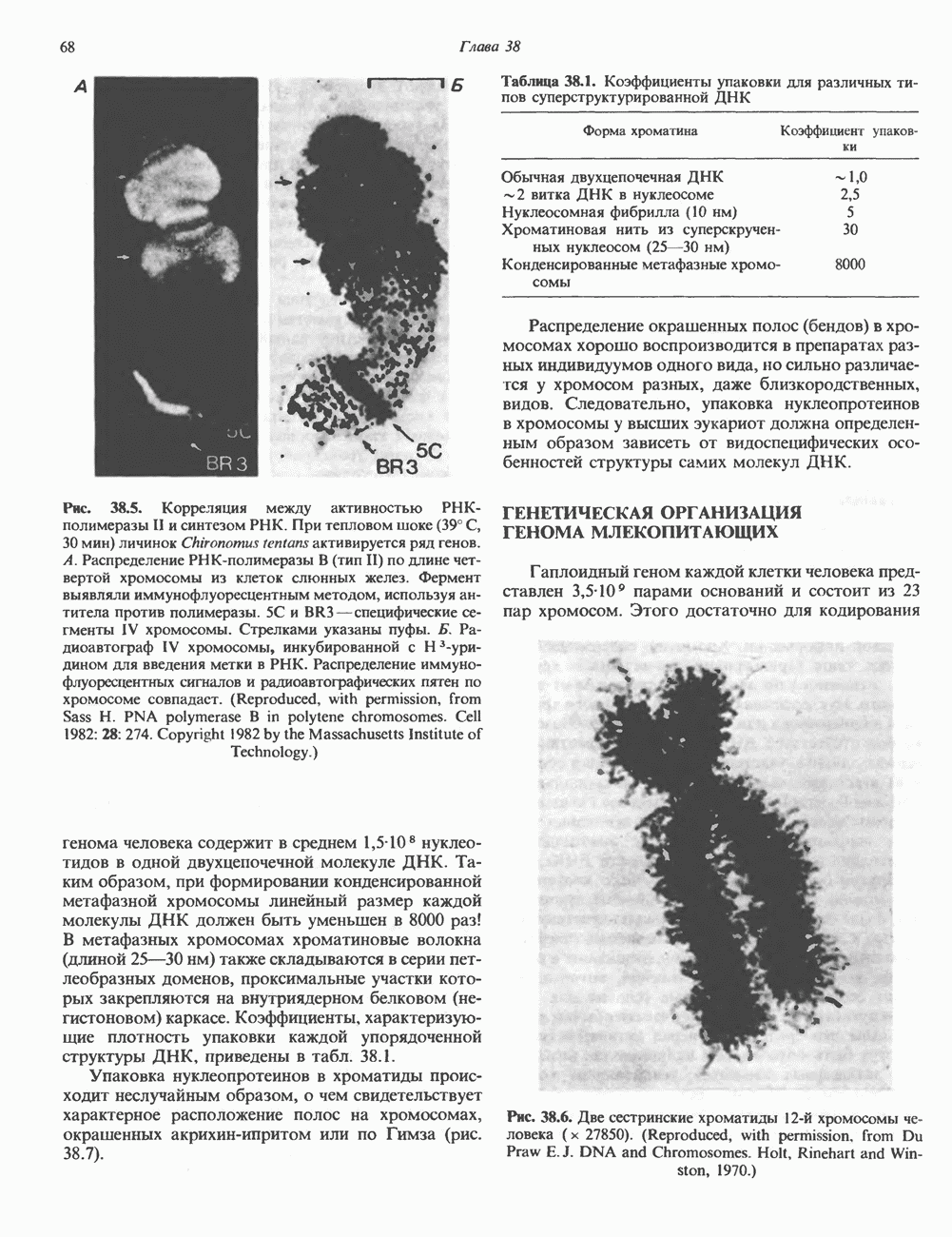
- ГЕНЕТИЧЕСКАЯ ОРГАНИЗАЦИЯ ГЕНОМА МЛЕКОПИТАЮЩИХ
- ИЗМЕНЕНИЯ И ПЕРЕСТРОЙКИ ГЕНЕТИЧЕСКОГО МАТЕРИАЛА
- СИНТЕЗ И РЕПЛИКАЦИЯ ДНК
- Глава 39. Синтез и процессинг РНК
- СИНТЕЗ РНК
- ПРОЦЕССИНГ МОЛЕКУЛ РНК
- НУКЛЕАЗЫ
- Глава 40. Синтез белка и генетический код
- ИНФОРМАЦИОННЫЙ ПОТОК
- КОДОНЫ И СИНТЕЗ БЕЛКА
- ТРАНСПОРТНЫЕ РНК И СИНТЕЗ БЕЛКА
- МУТАЦИИ
- ПРОЦЕСС СИНТЕЗА БЕЛКА
- Глава 41. Регуляция экспрессии генов
- РЕГУЛЯЦИЯ ЭКСПРЕССИИ ГЕНОВ У ПРОКАРИОТ
- РЕГУЛЯЦИЯ ЭКСПРЕССИИ ГЕНОВ У ЭУКАРИОТ
- Раздел V. Биохимия внутри- и межклеточных коммуникаций
- Глава 42. Мембраны: структура, сборка и функции
- ПОДДЕРЖАНИЕ НОРМАЛЬНОГО СОСТАВА СРЕДЫ
- СТРУКТУРА МЕМБРАН
- ОРГАНИЗАЦИЯ МЕМБРАННЫХ ЛИПИДОВ
- МЕМБРАННЫЕ БЕЛКИ
- ИСКУССТВЕННЫЕ МЕМБРАНЫ
- ЖИДКОСТНО-МОЗАИЧНАЯ МОДЕЛЬ МЕМБРАН
- СБОРКА МЕМБРАН
- СПЕЦИАЛИЗИРОВАННЫЕ ФУНКЦИИ МЕМБРАН
- ТРАНСМЕМБРАННЫЙ ПЕРЕНОС МАЛЫХ МОЛЕКУЛ
- ТРАНСМЕМБРАННОЕ ПЕРЕМЕЩЕНИЕ МАКРОМОЛЕКУЛ
- ПЕРЕДАЧА ИНФОРМАЦИИ В КЛЕТКУ
- МЕЖКЛЕТОЧНЫЕ КОНТАКТЫ И КОММУНИКАЦИИ
- Глава 43. Характеристика эндокринной системы
- ОБЩИЕ СВОЙСТВА
- РАЗНООБРАЗИЕ ЭНДОКРИННОЙ СИСТЕМЫ
- КОНЦЕПЦИЯ ЖЕЛЕЗЫ-МИШЕНИ
- КОНЦЕПЦИЯ РЕГУЛЯТОРНОГО МЕХАНИЗМА ОБРАТНОЙ СВЯЗИ
- РЕЦЕПТОРЫ ГОРМОНОВ
- Глава 44. Действие гормонов
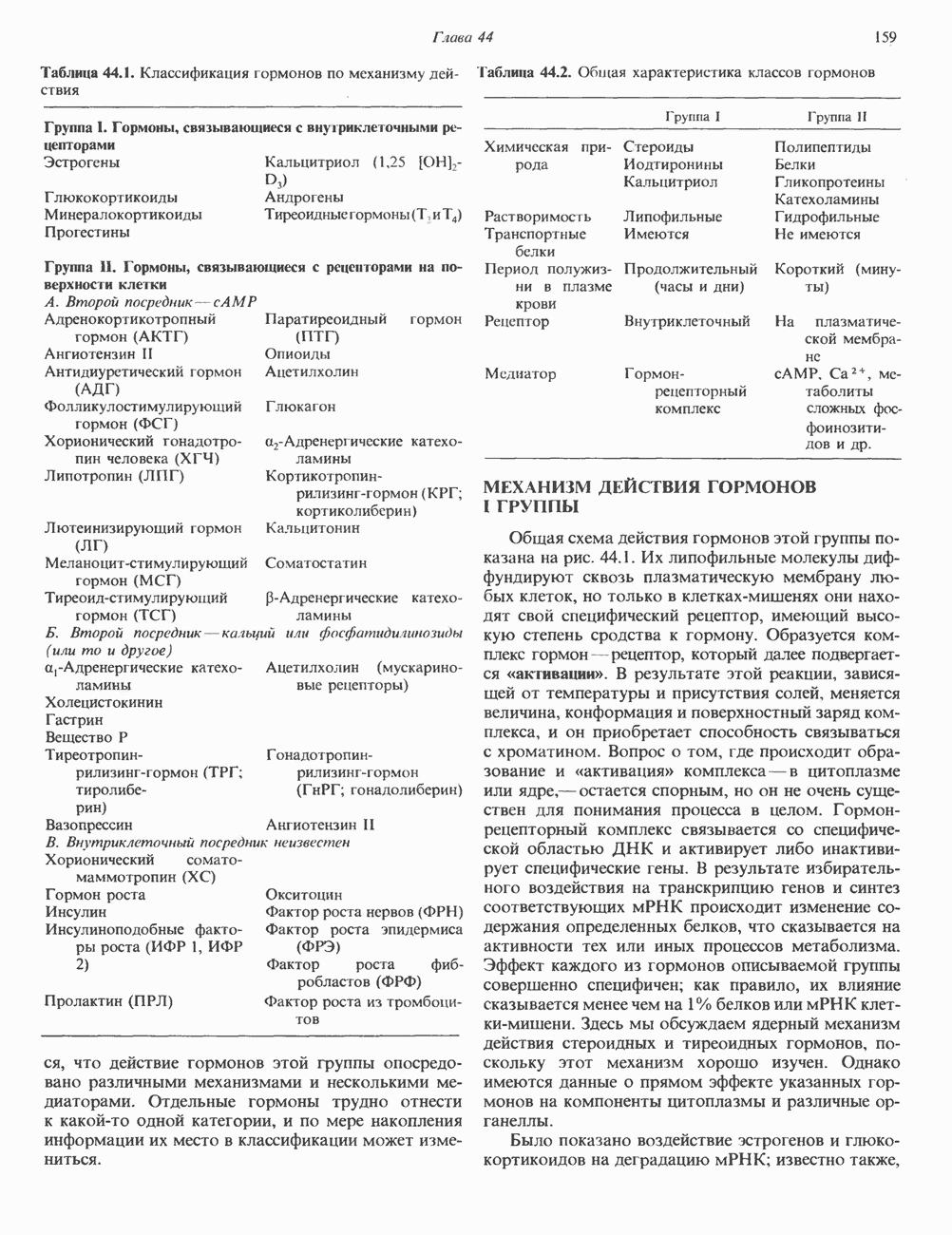
- КЛАССИФИКАЦИЯ ГОРМОНОВ
- МЕХАНИЗМ ДЕЙСТВИЯ ГОРМОНОВ I ГРУППЫ
- МЕХАНИЗМ ДЕЙСТВИЯ ГОРМОНОВ II ГРУППЫ (ПЕПТИДНЫХ ГОРМОНОВ)
- 1. сАМР КАК ВТОРОЙ ПОСРЕДНИК
- 2. ДЕЙСТВИЕ ГОРМОНОВ, ОПОСРЕДОВАННОЕ КАЛЬЦИЕМ И ФОСФОИНОЗИТИДАМИ
- 3. ГОРМОНЫ С НЕИЗВЕСТНЫМ ВНУТРИКЛЕТОЧНЫМ ПОСРЕДНИКОМ
- Глава 45. Гормоны гипофиза и гипоталамуса
- ГОРМОНЫ ГИПОТАЛАМУСА
- ГОРМОНЫ ПЕРЕДНЕЙ ДОЛИ ГИПОФИЗА
- I. ГРУППА ГОРМОН РОСТА — ПРОЛАКТИН—ХОРИОНИЧЕСКИЙ СОМАТОМАММОТРОПИН
- 2. ГРУППА ГЛИКОПРОТЕИНОВЫХ ГОРМОНОВ
- 3. СЕМЕЙСТВО ПЕПТИДОВ ПРООПИОМЕЛАНОКОРТИНА (ПОМК)
- ГОРМОНЫ ЗАДНЕЙ ДОЛИ ГИПОФИЗА
- 1. ОКСИТОЦИН
- 2. АНТИДИУРЕТИЧЕСКИЙ ГОРМОН (АДГ; ВАЗОПРЕССИН)
- Глава 46. Гормоны щитовидной железы
- БИОСИНТЕЗ ТИРЕОИДНЫХ ГОРМОНОВ
- 1. МЕТАБОЛИЗМ ТИРЕОГЛОБУЛИНА
- 2. МЕТАБОЛИЗМ ИОДИДА
- ТРАНСПОРТ И МЕТАБОЛИЗМ ГОРМОНОВ ЩИТОВИДНОЙ ЖЕЛЕЗЫ
- РЕГУЛЯЦИЯ СИНТЕЗА И ВЫСВОБОЖДЕНИЯ ГОРМОНОВ ЩИТОВИДНОМ ЖЕЛЕЗЫ
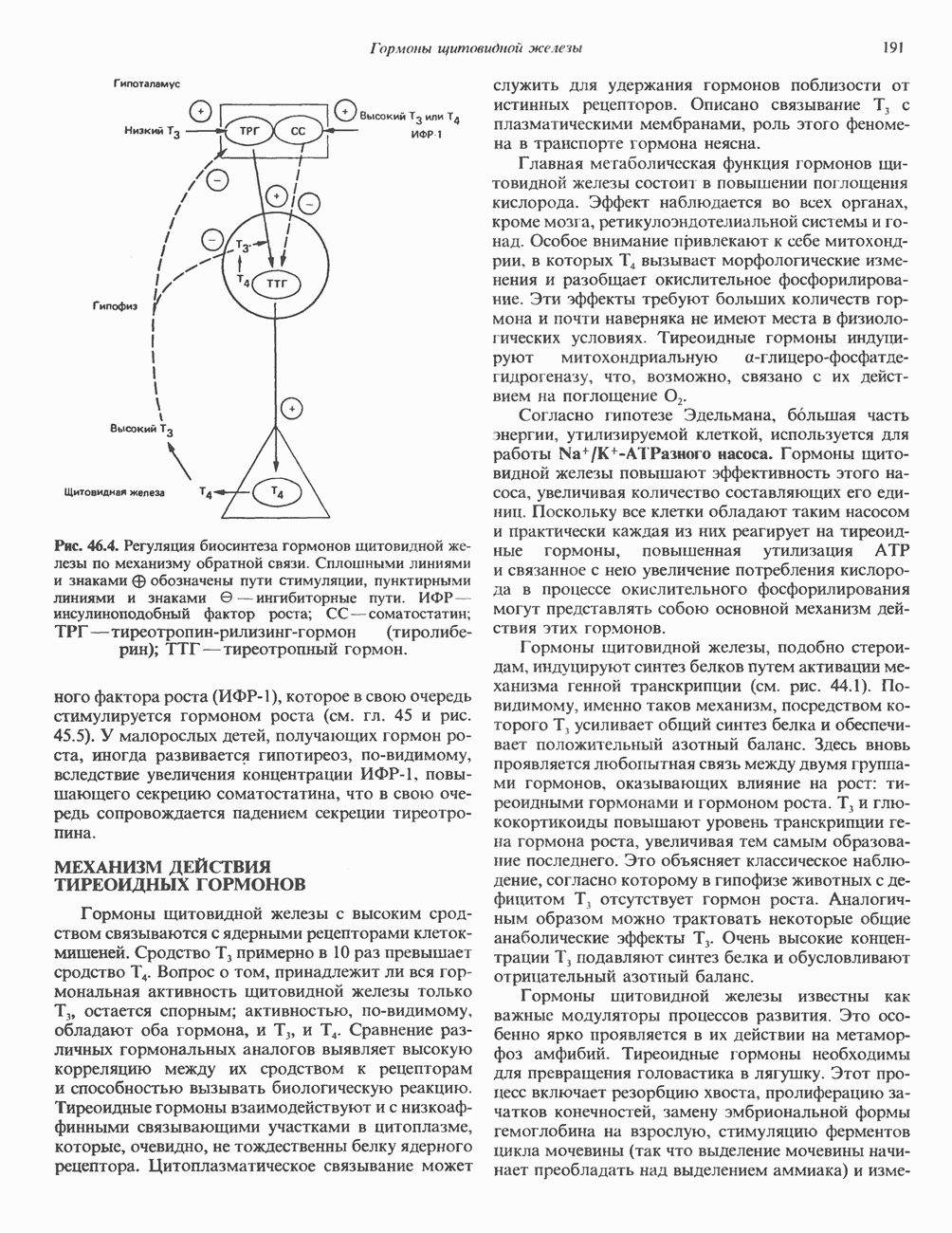
- МЕХАНИЗМ ДЕЙСТВИЯ ТИРЕОИДНЫХ ГОРМОНОВ
- ПАТОФИЗИОЛОГИЯ
- Глава 47. Гормоны, регулирующие метаболизм кальция
- ОБЩИЕ ХАРАКТЕРИСТИКИ
- ГОМЕОСТАЗ КАЛЬЦИЯ
- ГОРМОНЫ, УЧАСТВУЮЩИЕ В ГОМЕОСТАЗЕ КАЛЬЦИЯ
- 2. КАЛЬЦИТРИОЛ
- 3. КАЛЬЦИТОНИН (КТ)
- Глава 48. Гормоны коры надпочечников
- ГОРМОНЫ
- НОМЕНКЛАТУРА И ХИМИЯ СТЕРОИДОВ
- БИОСИНТЕЗ СТЕРОИДНЫХ ГОРМОНОВ НАДПОЧЕЧНИКОВ
- СЕКРЕЦИЯ, ТРАНСПОРТ И МЕТАБОЛИЗМ СТЕРОИДНЫХ ГОРМОНОВ НАДПОЧЕЧНИКОВ
- РЕГУЛЯЦИЯ СИНТЕЗА СТЕРОИДНЫХ ГОРМОНОВ НАДПОЧЕЧНИКОВ
- ВОЗДЕЙСТВИЕ СТЕРОИДНЫХ ГОРМОНОВ НАДПОЧЕЧНИКОВ НА МЕТАБОЛИЗМ
- КЛАССИФИКАЦИЯ И МЕХАНИЗМ ДЕЙСТВИЯ СТЕРОИДНЫХ ГОРМОНОВ
- ПАТОФИЗИОЛОГИЯ КОРЫ НАДПОЧЕЧНИКОВ
- Глава 49. Гормоны мозгового вещества надпочечников
- БИОСИНТЕЗ КАТЕХОЛАМИНОВ
- ЗАПАСАНИЕ И СЕКРЕЦИЯ КАТЕХОЛАМИНОВ
- МЕТАБОЛИЗМ КАТЕХОЛАМИНОВ
- РЕГУЛЯЦИЯ СИНТЕЗА КАТЕХОЛАМИНОВ
- КЛАССИФИКАЦИЯ И МЕХАНИЗМ ДЕЙСТВИЯ КАТЕХОЛАМИНОВ
- ПАТОФИЗИОЛОГИЯ МОЗГОВОГО СЛОЯ НАДПОЧЕЧНИКОВ
- Глава 50. Гормоны половых желез
- ГОРМОНЫ СЕМЕННИКОВ
- РЕГУЛЯЦИЯ ФУНКЦИИ СЕМЕННИКОВ
- ФИЗИОЛОГИЧЕСКИЕ ЭФФЕКТЫ ГОРМОНОВ СЕМЕННИКОВ
- МЕХАНИЗМ ДЕЙСТВИЯ ГОРМОНОВ СЕМЕННИКОВ
- ПАТОФИЗИОЛОГИЯ РЕПРОДУКТИВНОЙ СИСТЕМЫ У МУЖЧИН
- БИОСИНТЕЗ И МЕТАБОЛИЗМ ГОРМОНОВ ЯИЧНИКОВ
- РЕГУЛЯЦИЯ И ФИЗИОЛОГИЧЕСКОЕ ДЕЙСТВИЕ ГОРМОНОВ ЯИЧНИКОВ
- МЕХАНИЗМ ДЕЙСТВИЯ ГОРМОНОВ ЯИЧНИКОВ
- ПАТОФИЗИОЛОГИЯ ЖЕНСКОЙ РЕПРОДУКТИВНОЙ СИСТЕМЫ
- ГОРМОНЫ ПОЛОВЫХ ЖЕЛЕЗ И ПОЛОВАЯ ДИФФЕРЕНЦИРОВКА
- ФЕНОТИПИЧЕСКИЙ ПОЛ
- Глава 51. Гормоны поджелудочной железы
- ИНСУЛИН
- ИНСУЛИНОПОДОБНЫЕ ФАКТОРЫ РОСТА
- ГЛЮКАГОН
- СОМАТОСТАТИН
- ПАНКРЕАТИЧЕСКИЙ ПОЛИПЕПТИД
- Глава 52. Гормоны желудочно-кишечного тракта
- СВОЙСТВА ГОРМОНОВ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА
- СЕМЕЙСТВО СЕКРЕТИНА
- СЕМЕЙСТВО ГАСТРИН—ХОЛЕЦИСТОКИНИН
- ДРУГИЕ ПЕПТИДЫ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА
- Раздел VI. Частные вопросы
- Питание, пищеварение и всасывание
- ПИТАНИЕ
- РАСХОД ЭНЕРГИИ
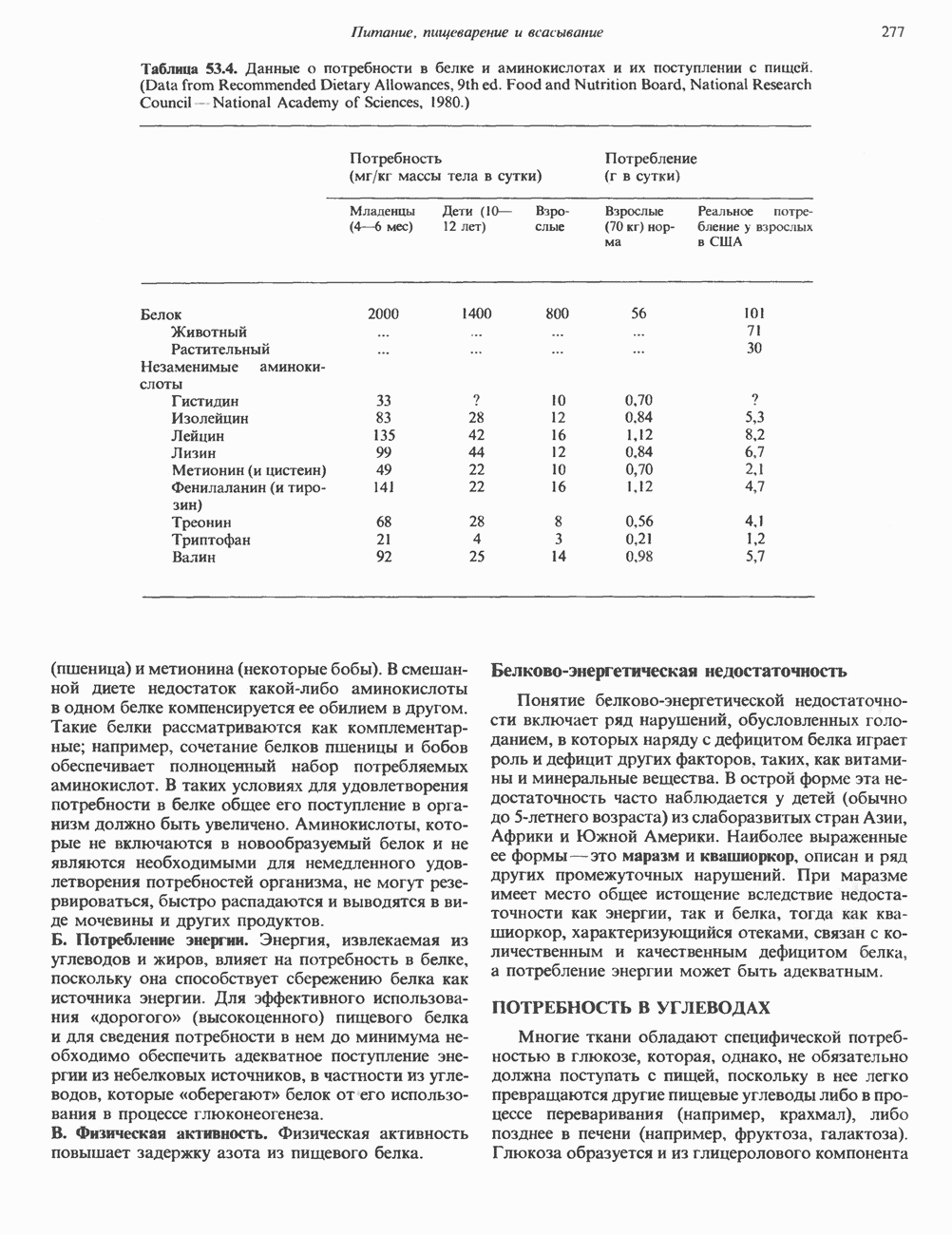
- АЗОТ АМИНОКИСЛОТ И ПОТРЕБНОСТЬ В СПЕЦИФИЧЕСКИХ АМИНОКИСЛОТАХ
- ПОТРЕБНОСТЬ В УГЛЕВОДАХ
- ПОТРЕБНОСТЬ В ПИЩЕВЫХ ВОЛОКНАХ
- ПОТРЕБНОСТЬ В ЛИПИДАХ
- ПОТРЕБНОСТЬ В ВИТАМИНАХ
- ПОТРЕБНОСТЬ В МИНЕРАЛЬНЫХ ВЕЩЕСТВАХ
- РЕКОМЕНДАЦИИ В ОБЛАСТИ ДИЕТЫ
- ПИЩЕВАРЕНИЕ
- ПИЩЕВАРЕНИЕ В ЖЕЛУДКЕ
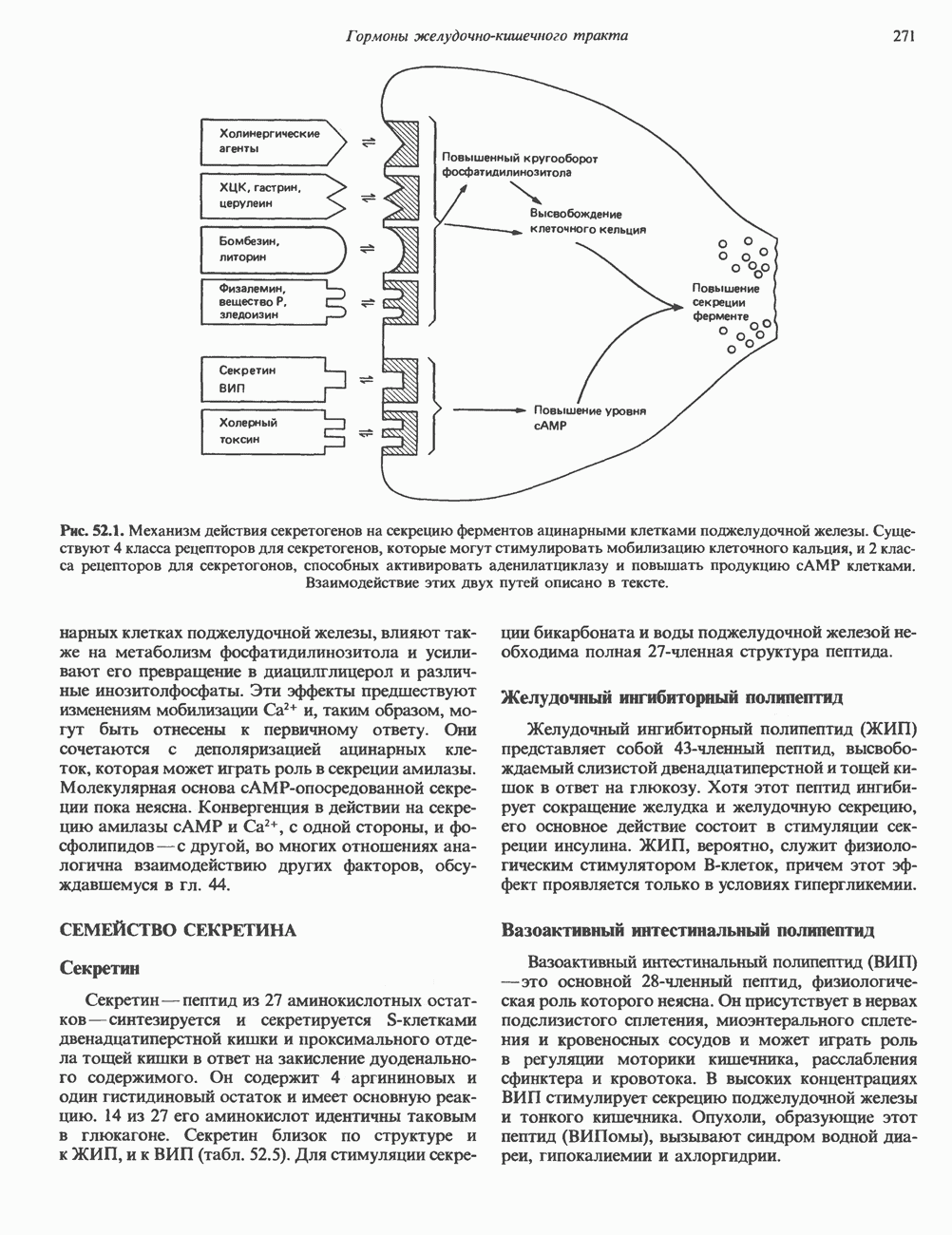
- ПАНКРЕАТИЧЕСКОЕ И КИШЕЧНОЕ ПИЩЕВАРЕНИЕ
- ВСАСЫВАНИЕ В ЖЕЛУДОЧНО-КИШЕЧНОМ ТРАКТЕ
- ВСАСЫВАНИЕ ГЛЮКОЗЫ
- ВСАСЫВАНИЕ ЛИПИДОВ
- ВСАСЫВАНИЕ АМИНОКИСЛОТ И БЕЛКА
- ПРОЦЕССЫ ГНИЕНИЯ И БРОЖЕНИЯ В КИШЕЧНИКЕ
- Глава 54. Гликопротеины и протеогликаны
- ГЛИКОПРОТЕИНЫ
- ОПРЕДЕЛЕНИЕ, ОЧИСТКА И СТРУКТУРНЫЙ АНАЛИЗ ГЛИКОПРОТЕИНОВ
- САХАРА, ПРИСУТСТВУЮЩИЕ В ГЛИКОПРОТЕИНАХ
- НУКЛЕОТИДСАХАРА
- ЭКЗОГЛИКОЗИДАЗЫ И ЭНДОГЛИКОЗИДАЗЫ
- ЛЕКТИНЫ
- КЛАССИФИКАЦИЯ ГЛИКОПРОТЕИНОВ
- I-КЛЕТОЧНАЯ БОЛЕЗНЬ
- АНТИГЕНЫ ГРУПП КРОВИ
- ПРОТЕОГЛИКАНЫ И ГЛИКОЗАМИНОГЛИКАНЫ
- ДЕГРАДАЦИЯ ПОЛИСАХАРИДНЫХ КОМПОНЕНТОВ ГЛИКОПРОТЕИНОВ И ПРОТЕОГЛИКАНОВ
- ФУНКЦИИ ГЛИКОЗАМИНОГЛИКАНОВ И ПРОТЕОГЛИКАНОВ
- Глава 55. Плазма крови и процесс свертывания
- ФУНКЦИИ КРОВИ
- БЕЛКИ ПЛАЗМЫ
- СВЕРТЫВАНИЕ КРОВИ
- Глава 56. Сократительные и структурные белки
- МЫШЦЫ
- КЛЕТОЧНАЯ ПОДВИЖНОСТЬ И ЦИТОСКЕЛЕТ
- Глава 57. Рак, онкогены, факторы роста
- БИОХИМИЧЕСКИЕ ЛАБОРАТОРНЫЕ ТЕСТЫ И РАК
- ПРИЧИНЫ ВОЗНИКНОВЕНИЯ РАКОВЫХ ОПУХОЛЕЙ
- ОНКОГЕННЫЕ ВИРУСЫ
- ТРАНСФОРМАЦИЯ
- ОНКОГЕНЫ
- ПОЛИПЕПТИДНЫЕ ФАКТОРЫ РОСТА
- ДЕЙСТВИЕ ФАКТОРОВ РОСТА ПО ЭНДОКРИННОМУ, ПАРАКРИННОМУ ИЛИ АУТОКРИННОМУ ТИПУ
- БИОХИМИЧЕСКИЕ МЕХАНИЗМЫ ДЕЙСТВИЯ ФАКТОРОВ РОСТА
- ФАКТОРЫ РОСТА И ОНКОГЕНЫ
- ПРОГРЕССИЯ ОПУХОЛЕЙ
- МЕТАСТАЗИРОВАНИЕ
- Приложение
- ХИМИЧЕСКИЙ СОСТАВ КРОВИ И ЖИДКИХ СРЕД ОРГАНИЗМА
- СТАНДАРТНЫЕ КЛИНИКО-ЛАБОРАТОРНЫЕ ПОКАЗАТЕЛИ В ТРАДИЦИОННОЙ СИСТЕМЕ И СИСТЕМЕ СИ
- НОРМАЛЬНЫЕ ЛАБОРАТОРНЫЕ ПОКАЗАТЕЛИ
- Список сокращений