| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ 11. Измерения в атомной физике
Познакомившись с основными представлениями о строении атома, остановимся теперь на тех экспериментальных фактах, которые послужили фундаментом для развития этих представлений.
Опыты Томсона. Удельный заряд частицы, т. е. отношение электрического заряда частицы к ее массе, можно определить, изучая отклонение пучка движущихся частиц поперечными электрическим и магнитным полями. Измерение удельного заряда электрона таким методом было впервые выполнено Дж. Томсоном с помощью катодных лучей. Катодные лучи в действительности представляют собой пучок быстрых электронов в трубке, из которой выкачан воздух.
Если бы все частицы в пучке имели одинаковую скорость, то определить отношение их заряда  к массе
к массе  можно было бы следующим способом. Отклонение
можно было бы следующим способом. Отклонение  пучка частиц, параллельного пластинам конденсатора, электрическим полем напряженности Е (рис. 25), определяется соотношением
пучка частиц, параллельного пластинам конденсатора, электрическим полем напряженности Е (рис. 25), определяется соотношением

Измеряя  можно было бы найти удельный заряд
можно было бы найти удельный заряд  если бы была известна скорость частиц и. Эту скорость можно определить, если кроме электрического создать магнитное поле, перпендикулярное пучку частиц и электрическому полю, и подобрать его индукцию В так, чтобы пучок не отклонялся. Компенсация действия электрической и магнитной сил будет происходить при выполнении условия
если бы была известна скорость частиц и. Эту скорость можно определить, если кроме электрического создать магнитное поле, перпендикулярное пучку частиц и электрическому полю, и подобрать его индукцию В так, чтобы пучок не отклонялся. Компенсация действия электрической и магнитной сил будет происходить при выполнении условия

откуда 
Именно таким путем Дж. Томсон впервые измерил  для катодных лучей в 1897 г. Оказалось, что для катодных лучей при любом составе остаточного газа в трубке и при любом материале электродов отношение
для катодных лучей в 1897 г. Оказалось, что для катодных лучей при любом составе остаточного газа в трубке и при любом материале электродов отношение  имеет одно и то же значение.
имеет одно и то же значение.

Рис. 25. К расчету отклонения пучка электронов в однородном электрическом поле
Установление этого факта и было по существу экспериментальным открытием электрона.
Опыты Буша. Одна из трудностей в этих исследованиях состояла в том, что электроны в пучке катодных лучей обладали большим разбросом скоростей. Для исключения влияния этого разброса Томсон в других модификациях опыта использовал параллельные электрическое и магнитное поля. После прохождения через такие поля частицы с единственным значением  и различными скоростями образуют на фотопластинке след в виде параболы. По форме этой параболы можно было определить
и различными скоростями образуют на фотопластинке след в виде параболы. По форме этой параболы можно было определить  со значительно большей точностью. Применяя такой «метод парабол» к ионным пучкам (анодным лучам), Дж. Томсон в 1912 г. открыл изотопы нерадиоактивных элементов.
со значительно большей точностью. Применяя такой «метод парабол» к ионным пучкам (анодным лучам), Дж. Томсон в 1912 г. открыл изотопы нерадиоактивных элементов.
Определение удельного заряда электрона можно выполнить с использованием только магнитного поля. Такие измерения были впервые выполнены в 20-е годы X. Бушем методом фокусировки пучка электронов в продольном магнитном поле. Продольная фокусировка расходящегося пучка электронов была рассмотрена в § 16 книги 2 курса. Этот метод позволяет выполнить измерения с большей точностью, но предъявляет более жесткие требования к характеристикам электронных пучков.
Опыты Милликена. Из опытов с ионными пучками можно определить не только  но и сам электрический заряд, если из независимых источников получить информацию о массе иона. Однако такими методами не удается получить точного значения элементарного электрического заряда е.
но и сам электрический заряд, если из независимых источников получить информацию о массе иона. Однако такими методами не удается получить точного значения элементарного электрического заряда е.
Точные измерения элементарного заряда были выполнены Р. Милликеном в серии классических опытов 1908-1916 гг.
Эти опыты принесли неопровержимое доказательство дискретности электрических зарядов в природе.
Милликен измерял электрический заряд малых капелек масла, используемого для смазки часовых механизмов. Схема его установки показана на рис. 26. В тщательно изготовленный плоский конденсатор через отверстие в верхней пластине могут попадать мелкие капли масла, полученные с помощью специального распылителя. Чтобы конвекционные потоки воздуха не влияли на поведение капель, конденсатор помещался в защитный кожух, температура и давление внутри которого поддерживались постоянными.

Рис. 26. Схема опытов Милликена
На пластины конденсатора подавалось постоянное напряжение от источника в несколько киловольт. В ходе опыта это напряжение можно было изменять. При распылении масла образующиеся капли, как правило, заряжаются и, попадая в конденсатор, движутся под действием силы тяжести и приложенного электрического поля. Движение отдельной капли можно наблюдать в микроскоп через специальное окошко.
С помощью рентгеновского излучения можно ионизировать воздух между пластинами конденсатора. Тогда заряд капли, а с ним и скорость установившегося движения в воздухе в том же электрическом поле могут скачком измениться. Измеряя скорости устоявшегося движения одной и той же капли в одном и том же электрическом поле, можно сравнить ее прежний и новый заряды  и
и  . Если капля мала, а электричество имеет атомистическое, дискретное строение, то можно ожидать, что заряд капли состоит из небольшого числа элементарных зарядов. В таком случае отношение
. Если капля мала, а электричество имеет атомистическое, дискретное строение, то можно ожидать, что заряд капли состоит из небольшого числа элементарных зарядов. В таком случае отношение  будет отношением небольших целых чисел. Именно это и наблюдалось в опытах Милликена.
будет отношением небольших целых чисел. Именно это и наблюдалось в опытах Милликена.
Дискретность электрического заряда. В результате было надежно установлено, что в природе любые электрические заряды состоят из дискретных порций определенной величины. Такая величина обозначается через  и называется элементарным электрическим зарядом. Его числовое значение равно
и называется элементарным электрическим зарядом. Его числовое значение равно  Кл. Заряд электрона равен —е. Точно таким же положительным зарядом обладает позитрон. Еще более замечательным фактом является равенство по величине заряда электрона и положительного заряда протона. Последнее равенство было проверено в очень тонких экспериментах, которые заключались в исследовании электронейтральности атома водорода и молекулы водорода. Их результаты свидетельствуют, что электрон и протон имеют одинаковые заряды с погрешностью до
Кл. Заряд электрона равен —е. Точно таким же положительным зарядом обладает позитрон. Еще более замечательным фактом является равенство по величине заряда электрона и положительного заряда протона. Последнее равенство было проверено в очень тонких экспериментах, которые заключались в исследовании электронейтральности атома водорода и молекулы водорода. Их результаты свидетельствуют, что электрон и протон имеют одинаковые заряды с погрешностью до 
По современным представлениям электрон и протон — это совершенно разные, очень далекие друг от друга по своим
характеристикам элементарные частицы. Совпадение их электрических зарядов с такой фантастической степенью точности не имеет в современной физике никакого глубокого теоретического обоснования. Квантование электрического заряда и по сей день представляется таинственным универсальным законом природы. Никто не знает, почему электрические заряды всех заряженных элементарных частиц в точности одинаковы.
Опыт показывает также, что электрические заряды всех заряженных элементарных частиц не только одинаковы, но и не зависят от состояния их движения. Электрическая нейтральность установлена на опыте и для атома гелия с почти такой же высокой точностью, как и для молекулы водорода. Атом гелия построен из тех же заряженных «кирпичиков», что и молекула водорода, — двух протонов и двух электронов, — но движутся эти частицы в атоме гелия совершенно иначе, нежели в молекуле водорода.
«Взвешивание» электрона. Опыты Милликена, в которых был измерен элементарный электрический заряд, можно рассматривать и как «взвешивание» электрона, массу которого непосредственно определить невозможно. Измерив заряд электрона, Милликен смог определить его массу, воспользовавшись найденным Томсоном отношением заряда к массе в опытах по отклонению электронных пучков. Ситуация здесь до некоторой степени аналогична «взвешиванию» Земли в опыте Кавендиша по лабораторному измерению гравитационной постоянной: взвесить Землю непосредственно невозможно, но можно определить произведение ее массы на гравитационную постоянную из астрономических наблюдений, т. е. по отклонению движущихся тел гравитационным полем Земли.
Массы атомов и молекул. Наиболее точные методы измерения масс атомов и молекул основаны на фокусировке пучков заряженных частиц — ионов этих атомов или молекул — при помощи

Рис. 27. Схема масс-спектрометра с фокусировкой однородным магнитным полем
различных комбинаций электрических и магнитных полей. Устроенные на таком принципе приборы называются масс-спектрографами (в случае фотографической регистрации) и масс-спектрометрами (при электрической регистрации). Первый масс-спектрограф был изобретен и построен Ф. Астоном.
Существует большое разнообразие конфигураций полей, используемых в этих приборах. В наиболее распространенном масс-спектрографе с однородным магнитным полем ионы, образованные в ионном источнике, вылетают из щели  (рис. 27) в виде расходящегося пучка. Распространяясь в вакууме, этот пучок в магнитном поле разделяется на пучки ионов с разными значениями отношения заряда к массе. Каждый такой пучок, несмотря на разброс скоростей ионов, магнитное поле собирает в своем фокусе, т. е. фокусировка пучков частиц с разными значениями
(рис. 27) в виде расходящегося пучка. Распространяясь в вакууме, этот пучок в магнитном поле разделяется на пучки ионов с разными значениями отношения заряда к массе. Каждый такой пучок, несмотря на разброс скоростей ионов, магнитное поле собирает в своем фокусе, т. е. фокусировка пучков частиц с разными значениями  происходит в разных местах
происходит в разных местах  Сравнивая положения фокусов, можно определить отношения масс ионов в разных пучках.
Сравнивая положения фокусов, можно определить отношения масс ионов в разных пучках.
Принцип действия масс-спектрографа. Поясним принцип фокусировки расходящегося пучка заряженных частиц на примере метода фокусировки поперечным магнитным полем на протяжении половины окружности  радиан).
радиан).
Пусть источник ионов находится в точке  (рис. 28) и пусть все частицы характеризуются одним и тем же значением удельного заряда
(рис. 28) и пусть все частицы характеризуются одним и тем же значением удельного заряда  Будем считать, что все ионы вылетают из источника с одинаковой по модулю скоростью, но с небольшим разбросом по направлению.
Будем считать, что все ионы вылетают из источника с одинаковой по модулю скоростью, но с небольшим разбросом по направлению.
Ион, скорость которого направлена вверх на рис. 28, движется в магнитном поле, перпендикулярном плоскости рисунка, по окружности радиусом


Рис. 28. Фокусировка поперечным однородным магнитным полем
Другой ион, вылетающий под небольшим углом а (рис. 28), в однородном магнитном поле движется по такой же окружности, повернутой как целое вокруг начальной точки  Эта окружность пересечет диаметр
Эта окружность пересечет диаметр  первой окружности в точке В. Легко видеть, что
первой окружности в точке В. Легко видеть, что

Хотя максимальное расхождение траекторий этих двух ионов, как видно из рис. 28, равно  расстояние
расстояние  пропорциональное квадрату малого угла а, значительно меньше. Поэтому, если источником
пропорциональное квадрату малого угла а, значительно меньше. Поэтому, если источником
 служит щель, через которую влетают ионы, то
служит щель, через которую влетают ионы, то  будет «изображением» этой щели в виде сравнительно узкой полоски. Таким образом, поперечное однородное магнитное поле фокусирует расходящийся пучок, действуя подобно цилиндрической линзе.
будет «изображением» этой щели в виде сравнительно узкой полоски. Таким образом, поперечное однородное магнитное поле фокусирует расходящийся пучок, действуя подобно цилиндрической линзе.
Селектор скоростей ионов. Для получения пучка ионов с одинаковыми по модулю скоростями используют фильтры скоростей. Схема самого простого фильтра скоростей показана на рис. 29: пучок заряженных частиц с различающимися скоростями пропускается через скрещенные электрическое  и магнитное
и магнитное  поля. Очевидно, что через малое выходное отверстие смогут пройти только те ионы, скорость которых удовлетворяет условию (2). Ионы с другими скоростями будут задержаны диафрагмой
поля. Очевидно, что через малое выходное отверстие смогут пройти только те ионы, скорость которых удовлетворяет условию (2). Ионы с другими скоростями будут задержаны диафрагмой 
Масс-спектрометр с поперечной фокусировкой. На рис. 30 показана схема масс-спектрометра А. Демпстера с фокусировкой на  радиан.
радиан.

Рис. 29. Схема фильтра скоростей заряженных частиц

Рис. 30. Схема масс-спектрометра Демпстера
Ионы, создаваемые источником А, приобретают одинаковую дополнительную энергию под действием ускоряющей разности потенциалов  приложенной между источником А и выходной щелью С. Через щель
приложенной между источником А и выходной щелью С. Через щель  слегка расходящийся пучок ионов попадает в область, где действует поперечное однородное магнитное поле В. Ионы, обладающие различными значениями
слегка расходящийся пучок ионов попадает в область, где действует поперечное однородное магнитное поле В. Ионы, обладающие различными значениями  в соответствии с (3) фокусируются в разных местах, так как движутся по окружностям разных радиусов. Входящую в (3) скорость
в соответствии с (3) фокусируются в разных местах, так как движутся по окружностям разных радиусов. Входящую в (3) скорость  можно определить из условия
можно определить из условия

в котором пренебрегается первоначальной кинетической энергией теплового движения ионов по сравнению с энергией, приобретаемой ими при разгоне в электрическом поле. С помощью (3) и (5) для квадрата радиуса окружности получаем

Подбирая ускоряющее напряжение  или индукции магнитного поля В так, чтобы при данном
или индукции магнитного поля В так, чтобы при данном  радиус
радиус  приобретал нужное значение, можно выпустить через выходную щель
приобретал нужное значение, можно выпустить через выходную щель  ионы любой массы. При этом можно не только измерять массы ионов, но и количественно исследовать состав исходного вещества: сила тока ионов через коллектор Р служит мерой количества ионов данной массы.
ионы любой массы. При этом можно не только измерять массы ионов, но и количественно исследовать состав исходного вещества: сила тока ионов через коллектор Р служит мерой количества ионов данной массы.
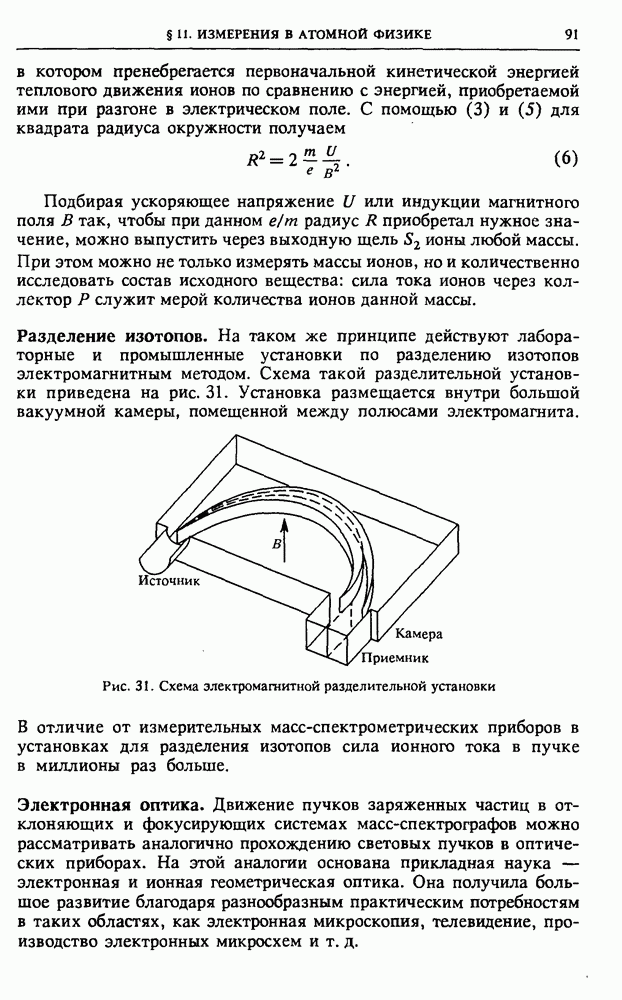
Разделение изотопов. На таком же принципе действуют лабораторные и промышленные установки по разделению изотопов электромагнитным методом. Схема такой разделительной установки приведена на рис. 31. Установка размещается внутри большой вакуумной камеры, помещенной между полюсами электромагнита.

Рис. 31. Схема электромагнитной разделительной установки
В отличие от измерительных масс-спектрометрических приборов в установках для разделения изотопов сила ионного тока в пучке в миллионы раз больше.
Электронная оптика. Движение пучков заряженных частиц в отклоняющих и фокусирующих системах масс-спектрографов можно рассматривать аналогично прохождению световых пучков в оптических приборах. На этой аналогии основана прикладная наука — электронная и ионная геометрическая оптика. Она получила большое развитие благодаря разнообразным практическим потребностям в таких областях, как электронная микроскопия, телевидение, производство электронных микросхем и т. д.
В современных приборах, где используются электронные и ионные пучки, удается добиться совершенной фокусировки пучка частиц с заданным значением  обладающих некоторым разбросом как модуля скорости, так и ее направления.
обладающих некоторым разбросом как модуля скорости, так и ее направления.
Разрешающая способность. Основной характеристикой качества масс-спектроскопической системы является ее разрешающая способность. Это понятие перенесено из теории оптических спектральных приборов. Говорят, что масс-спектрограф обладает разрешающей способностью  если минимальная относительная разность масс А
если минимальная относительная разность масс А  для двух близких по массе частиц, регистрируемых раздельно, определяется равенством
для двух близких по массе частиц, регистрируемых раздельно, определяется равенством

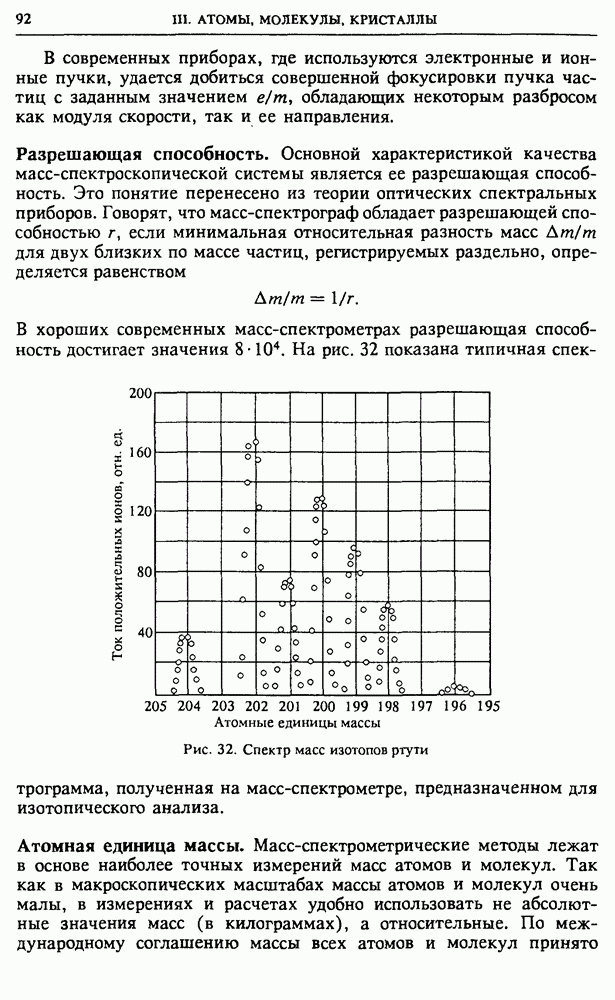
В хороших современных масс-спектрометрах разрешающая способность достигает значения 

Рис. 32. Спектр масс изотопов ртути
На рис. 32 показана типичная спектрограмма, полученная на масс-спектрометре, предназначенном для изотопического анализа.
Атомная единица массы. Масс-спектрометрические методы лежат в основе наиболее точных измерений масс атомов и молекул. Так как в макроскопических масштабах массы атомов и молекул очень малы, в измерениях и расчетах удобно использовать не абсолютные значения масс (в килограммах), а относительные. По международному соглашению массы всех атомов и молекул принято
сравнивать с массой атома углерода, точнее его изотопа  Углерод выбран потому, что он входит в огромное число химических соединений.
Углерод выбран потому, что он входит в огромное число химических соединений.
За атомную единицу массы принимается 1/12 массы изотопа углерода  чтобы в этой шкале массы протона и нейтрона были близки к единице, а масса атома любого химического элемента выражалась числом, близким к целому.
чтобы в этой шкале массы протона и нейтрона были близки к единице, а масса атома любого химического элемента выражалась числом, близким к целому.
Относительной атомной (или молекулярной) массой  вещества называют отношение массы атома (или молекулы)
вещества называют отношение массы атома (или молекулы)  данного вещества к 1/12 массы
данного вещества к 1/12 массы  атома углерода
атома углерода 

Относительные массы всех химических элементов измерены очень точно. Складывая относительные атомные массы элементов, входящих в состав молекулы определенного вещества, можно, зная его химическую формулу, приближенно вычислить относительную молекулярную массу. Например, относительная масса молекулы воды  равна
равна  если эта молекула содержит наиболее распространенные изотопы
если эта молекула содержит наиболее распространенные изотопы 
Точные измерения атомных масс. Для точных определений неизвестной массы какого-либо иона необходимо построить градуировочную кривую масс-спектрометра. Эта кривая сначала строится грубо путем выбора цепочки масс атомных или молекулярных ионов, отличающихся приблизительно на одну единицу массы, например  Если для данной цепочки массы ионов известны с погрешностью, например, 0,1% (что легко достигается химическими методами), то с такой же погрешностью можно построить график зависимости координаты линии в спектре масс на фотопластинке от относительной массы. Затем эту грубую градуировку уточняют. Это можно сделать, например, таким способом. Уменьшим ускоряющее напряжение при неизменном магнитном поле настолько, чтобы на место линии
Если для данной цепочки массы ионов известны с погрешностью, например, 0,1% (что легко достигается химическими методами), то с такой же погрешностью можно построить график зависимости координаты линии в спектре масс на фотопластинке от относительной массы. Затем эту грубую градуировку уточняют. Это можно сделать, например, таким способом. Уменьшим ускоряющее напряжение при неизменном магнитном поле настолько, чтобы на место линии  попала линия
попала линия  Тогда все новые положения массовых линий будут соответствовать значениям масс, изменившимся в отношении 16/15.
Тогда все новые положения массовых линий будут соответствовать значениям масс, изменившимся в отношении 16/15.
После такой градуировки можно измерить очень маленькую разность масс между некоторой неизвестной массой и эталонной. Среди множества углеводородов почти всегда можно подобрать очень близкие по массе соединения. Две близкие массы образуют так называемый дублет в спектре масс. Примером могут служить ионы  (кислород и метан). Если относительная погрешность измерения разности масс
(кислород и метан). Если относительная погрешность измерения разности масс  этих ионов составляет всего 0,1% (что составляет несколько сотых долей от атомной
этих ионов составляет всего 0,1% (что составляет несколько сотых долей от атомной
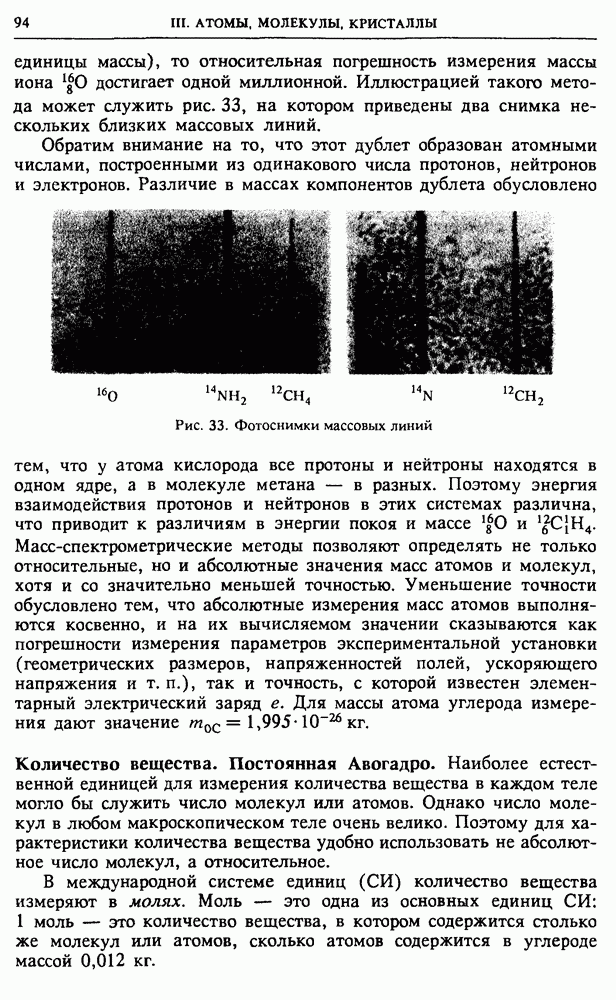
единицы массы), то относительная погрешность измерения массы иона  достигает одной миллионной. Иллюстрацией такого метода может служить рис. 33, на котором приведены два снимка нескольких близких массовых линий.
достигает одной миллионной. Иллюстрацией такого метода может служить рис. 33, на котором приведены два снимка нескольких близких массовых линий.
Обратим внимание на то, что этот дублет образован атомными числами, построенными из одинакового числа протонов, нейтронов и электронов.

Рис. 33. Фотоснимки массовых линий
Различие в массах компонентов дублета обусловлено тем, что у атома кислорода все протоны и нейтроны находятся в одном ядре, а в молекуле метана — в разных. Поэтому энергия взаимодействия протонов и нейтронов в этих системах различна, что приводит к различиям в энергии покоя и массе  Масс-спектрометрические методы позволяют определять не только относительные, но и абсолютные значения масс атомов и молекул, хотя и со значительно меньшей точностью. Уменьшение точности обусловлено тем, что абсолютные измерения масс атомов выполняются косвенно, и на их вычисляемом значении сказываются как погрешности измерения параметров экспериментальной установки (геометрических размеров, напряженностей полей, ускоряющего напряжения и т.
Масс-спектрометрические методы позволяют определять не только относительные, но и абсолютные значения масс атомов и молекул, хотя и со значительно меньшей точностью. Уменьшение точности обусловлено тем, что абсолютные измерения масс атомов выполняются косвенно, и на их вычисляемом значении сказываются как погрешности измерения параметров экспериментальной установки (геометрических размеров, напряженностей полей, ускоряющего напряжения и т.  так и точность, с которой известен элементарный электрический заряд е. Для массы атома углерода измерения дают значение
так и точность, с которой известен элементарный электрический заряд е. Для массы атома углерода измерения дают значение  кг.
кг.
Количество вещества. Постоянная Авогадро. Наиболее естественной единицей для измерения количества вещества в каждом теле могло бы служить число молекул или атомов. Однако число молекул в любом макроскопическом теле очень велико. Поэтому для характеристики количества вещества удобно использовать не абсолютное число молекул, а относительное.
В международной системе единиц (СИ) количество вещества измеряют в молях. Моль — это одна из основных единиц СИ:
1 моль — это количество вещества, в котором содержится столько же молекул или атомов, сколько атомов содержится в углероде массой 0,012 кг.
Моль любого вещества содержит одно и то же число атомов или молекул. Это число обозначается  и называется постоянной Авогадро. Постоянную Авогадро можно найти, если разделить массу одного моля углерода на массу одного атома углерода:
и называется постоянной Авогадро. Постоянную Авогадро можно найти, если разделить массу одного моля углерода на массу одного атома углерода:

Количество вещества  т. е. число молей, равно отношению числа молекул
т. е. число молей, равно отношению числа молекул  в данном теле к постоянной Авогадро
в данном теле к постоянной Авогадро 

Молярная масса. Для характеристики конкретного вещества наряду с относительной молекулярной массой  в физике и химии широко используется молярная масса М. Молярной массой называют массу данного вещества, взятого в количестве одного моля. Молярная масса равна произведению массы
в физике и химии широко используется молярная масса М. Молярной массой называют массу данного вещества, взятого в количестве одного моля. Молярная масса равна произведению массы  одной молекулы данного вещества на постоянную Авогадро
одной молекулы данного вещества на постоянную Авогадро 

Если в формуле (9) числитель и знаменатель домножить на массу одной молекулы  то для количества вещества
то для количества вещества  в теле можно написать
в теле можно написать

где  — масса тела.
— масса тела.
Размеры атомов и молекул. Представление о размерах отдельных атомов и молекул можно получить разными способами. Если предположить, что в конденсированном состоянии (т. е. в жидкой или твердой фазе) атомы или молекулы вещества «соприкасаются» друг с другом, то, определив приходящийся на одну молекулу объем, можно оценить ее размеры. Например,  воды занимает объем
воды занимает объем  и содержит
и содержит  молекул, где
молекул, где  Поэтому приходящийся на одну молекулу объем составляет
Поэтому приходящийся на одну молекулу объем составляет  а ее линейный размер
а ее линейный размер  см.
см.
Согласующуюся с этим значением оценку размеров молекул можно получить без использования постоянной Авогадро, если обратиться к простому опыту по растеканию капли масла на поверхности воды (опыт Ленгмюра). Предположив, что в масляном пятне молекулы располагаются в один слой, можно оценить толщину слоя, а тем самым и линейный размер молекул масла, разделив объем растекшейся капли масла на площадь образовавшегося пятна.
Более надежную информацию о расстояниях между атомами в твердых телах и жидкостях дают опыты по дифракции рентгеновского излучения — рентгено-структурный анализ. Оказывается, что молекулы многих веществ имеют размеры порядка  см.
см.

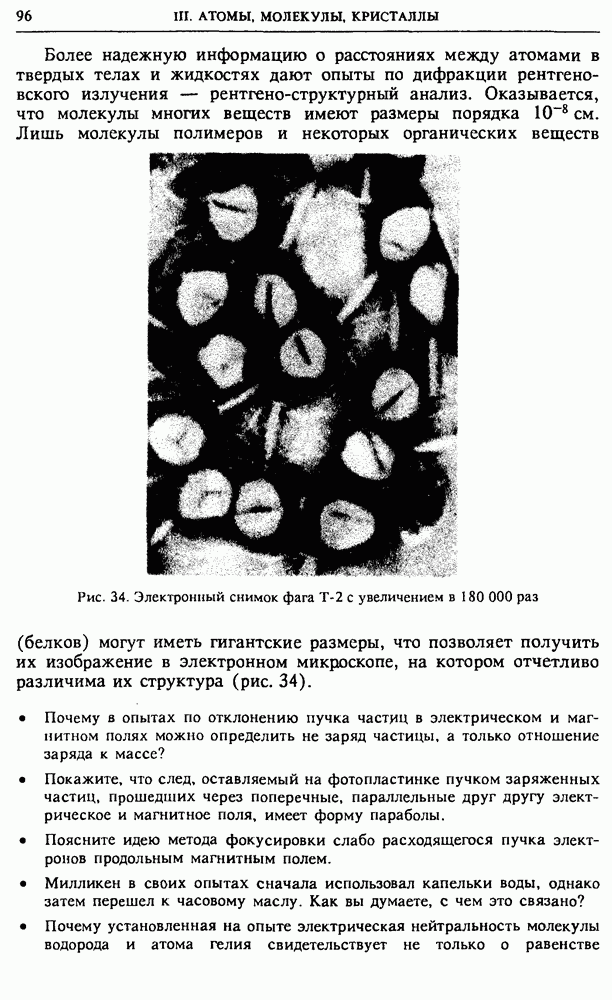
Рис. 34. Электронный снимок фага  с увеличением в
с увеличением в  раз
раз
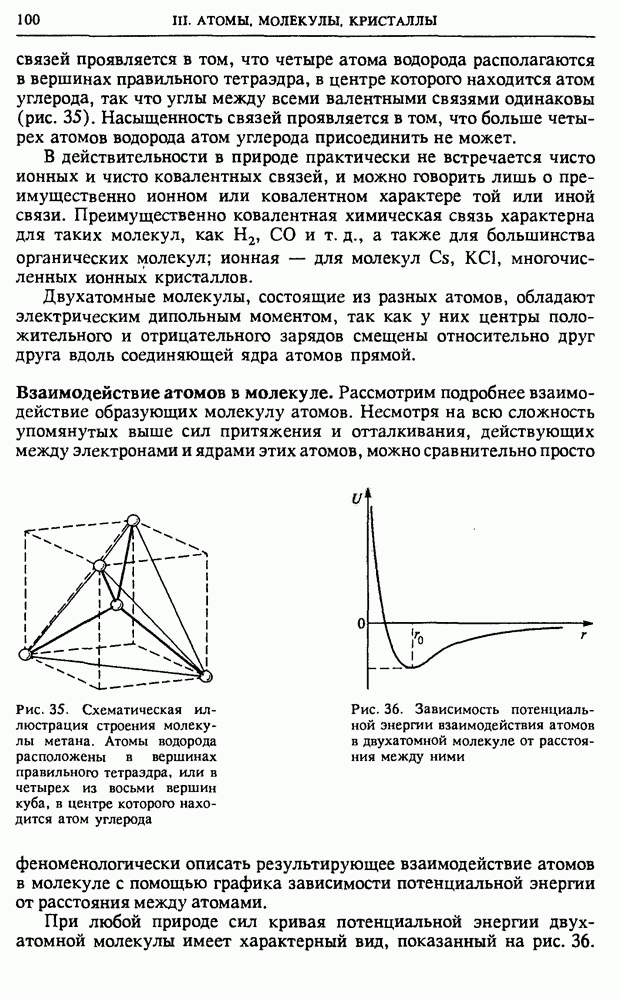
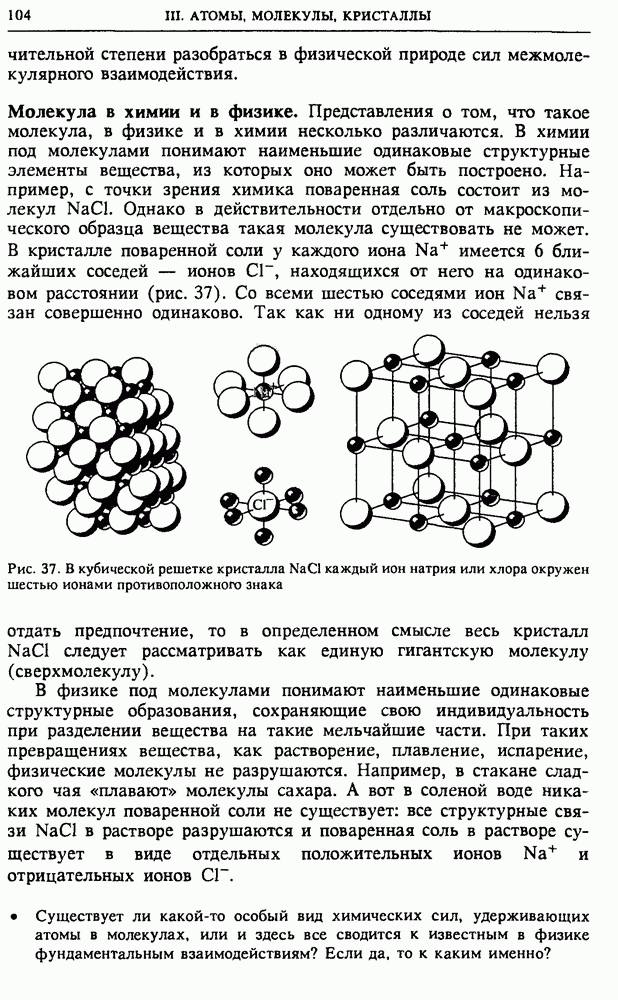
Лишь молекулы полимеров и некоторых органических веществ (белков) могут иметь гигантские размеры, что позволяет получить их изображение в электронном микроскопе, на котором отчетливо различима их структура (рис. 34).
• Почему в опытах по отклонению пучка частиц в электрическом и магнитном полях можно определить не заряд частицы, а только отношение заряда к массе?
• Покажите, что след, оставляемый на фотопластинке пучком заряженных частиц, прошедших через поперечные, параллельные друг другу электрическое и магнитное поля, имеет форму параболы.
• Поясните идею метода фокусировки слабо расходящегося пучка электронов продольным магнитным полем.
• Милликен в своих опытах сначала использовал капельки воды, однако затем перешел к часовому маслу. Как вы думаете, с чем это связано?
• Почему установленная на опыте электрическая нейтральность молекулы водорода и атома гелия свидетельствует не только о равенстве
электрических зарядов электрона и протона, но и о независимости величины заряда каждой частицы от ее движения?
• Проведите подробное сопоставление опыта Милликена по «взвешиванию» электрона и опыта Кавендиша по «взвешиванию» Земли.
• Поясните принцип фокусировки ионов в поперечном магнитном поле.
• Объясните принцип действия масс-спектрометра и его применение для количественного исследования состава вещества.
• Какую величину называют разрешающей способностью масс-спектрометра? Что она характеризует?
• Как вводится атомная единица массы? Почему она основывается на атоме углерода  ?
?
• Что такое относительная атомная или молекулярная масса? Почему при ее вычислении с помощью химической формулы вещества мы получаем приближенные значения?
• Поясните, каким образом достигается относительная точность  при масс-спектрографическом измерении массы изотопа
при масс-спектрографическом измерении массы изотопа  с использованием дублета
с использованием дублета  .
.
• При сгорании углерода  углерода соединились с
углерода соединились с  кислорода. Изменилось ли в результате этой химической реакции количество вещества?
кислорода. Изменилось ли в результате этой химической реакции количество вещества?
• Сколько молекул воды содержится в капле объемом  ?
?
• Как можно оценить размеры отдельных молекул?
| << Предыдущий параграф | Следующий параграф >> |
- I. ТЕОРИЯ ОТНОСИТЕЛЬНОСТИ
- § 2. Релятивистская кинематика
- § 3. Преобразования Лоренца
- § 4. Релятивистская динамика
- § 5. Примеры релятивистского движения частиц
- II. ЗАКОНЫ МИКРОМИРА. ЧАСТИЦЫ И ВОЛНЫ
- § 6. Световые кванты
- § 7. Границы применимости классической физики
- § 8. Свет — частицы или волны?
- § 9. Законы движения в квантовой физике
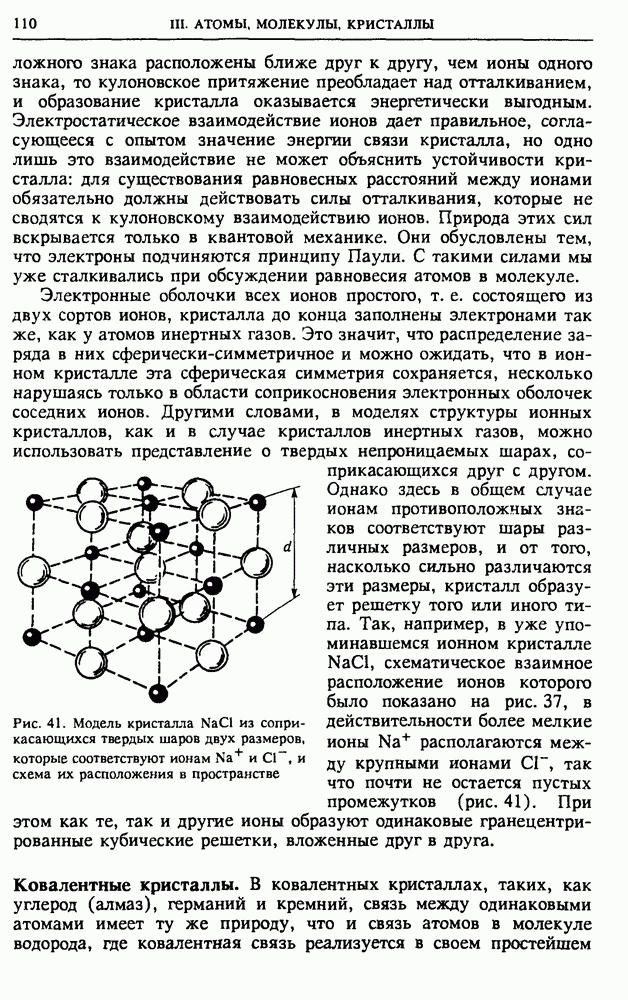
- III. АТОМЫ, МОЛЕКУЛЫ, КРИСТАЛЛЫ
- § 10. Строение атома
- § 11. Измерения в атомной физике
- § 12. Молекулы
- § 13. Кристаллы
- IV. ОСНОВЫ ТЕРМОДИНАМИКИ
- § 14. Основные понятия термодинамики
- § 15. Уравнение состояния газа
- § 16. Первый закон термодинамики
- § 17. Примеры применения первого закона термодинамики
- § 18. Второй закон термодинамики
- § 19. Методы термодинамики и их применения
- V. ОСНОВЫ МОЛЕКУЛЯРНО-КИНЕТИЧЕСКОЙ ТЕОРИИ
- § 20. Экспериментальные основания статистической механики
- § 21. Молекулярно-кинетическая теория идеального газа
- § 22. Статистические распределения
- § 23. Тепловое равновесие в статистической механике
- § 24. Статистическая природа необратимости тепловых процессов
- § 25. Газы, жидкости, фазовые переходы
- § 26. Реальные газы. Уравнение Ван-дер-Ваальса
- § 27. Фазовые переходы
- VI. АТОМЫ И ИЗЛУЧЕНИЕ
- § 28. Излучение света атомами
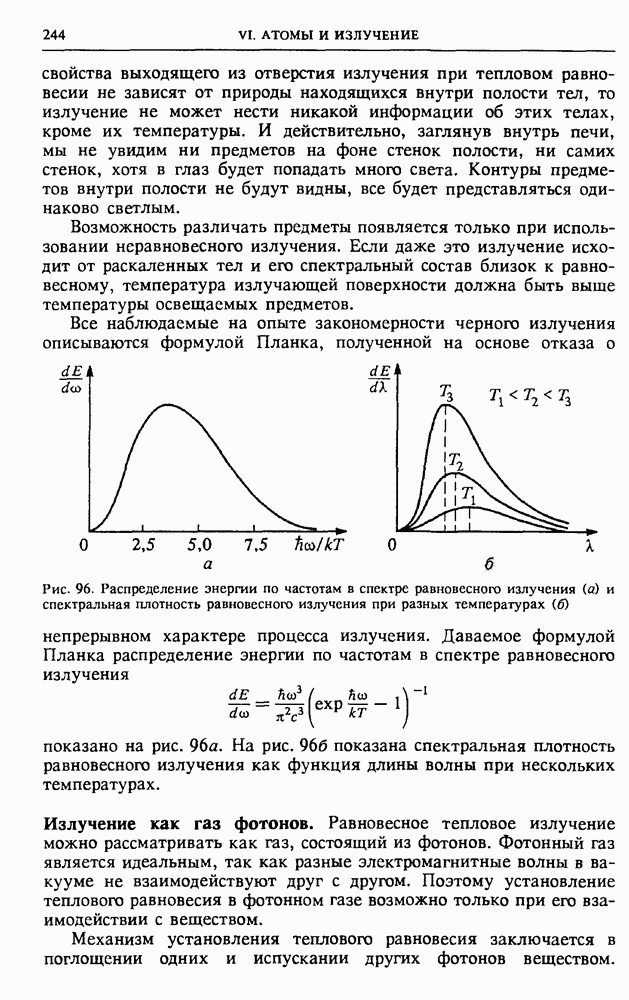
- § 29. Излучение света нагретыми телами
- § 30. Вынужденное излучение. Квантовые усилители и генераторы света
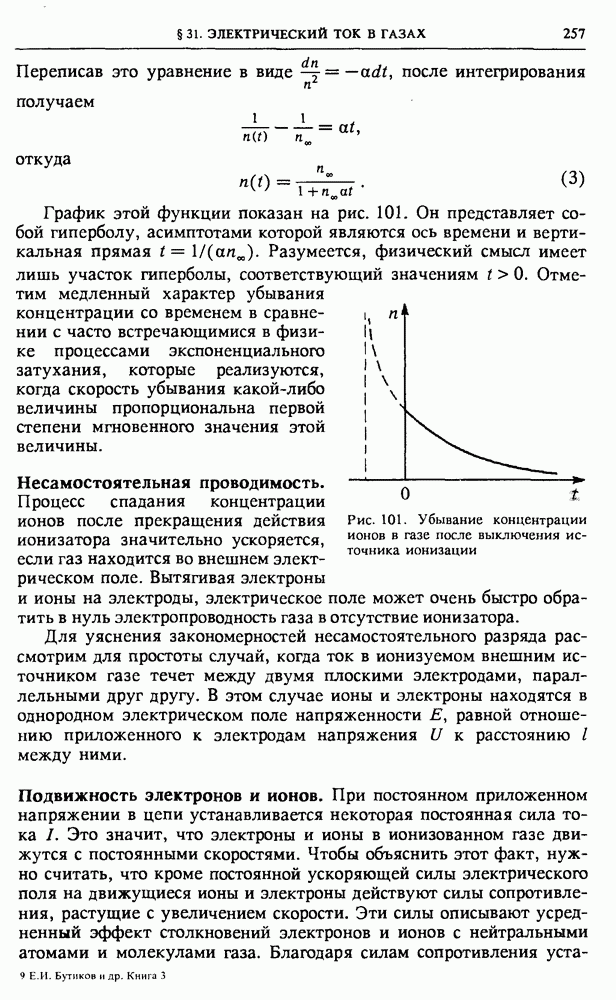
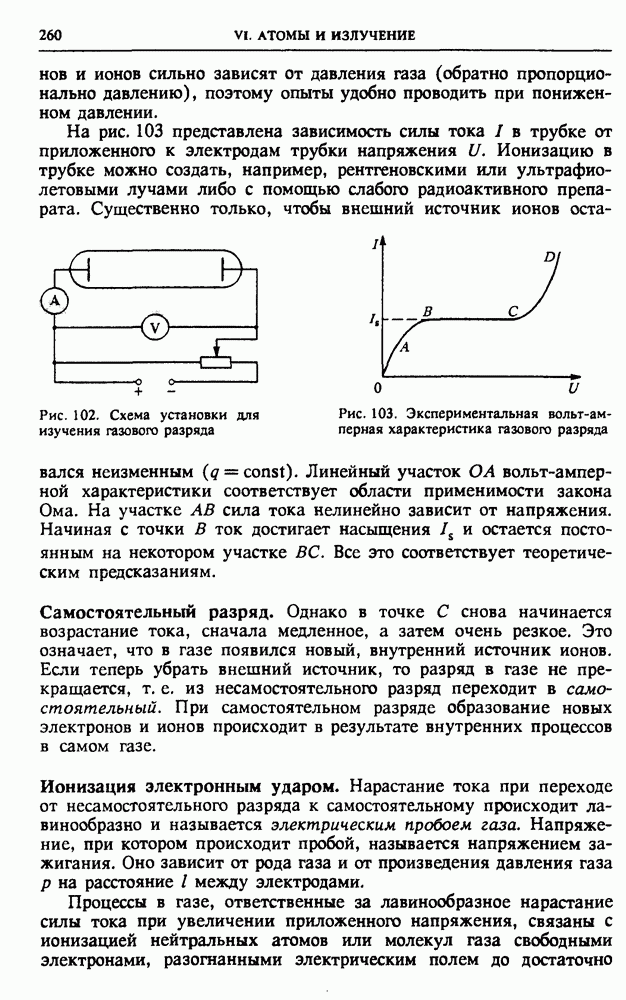
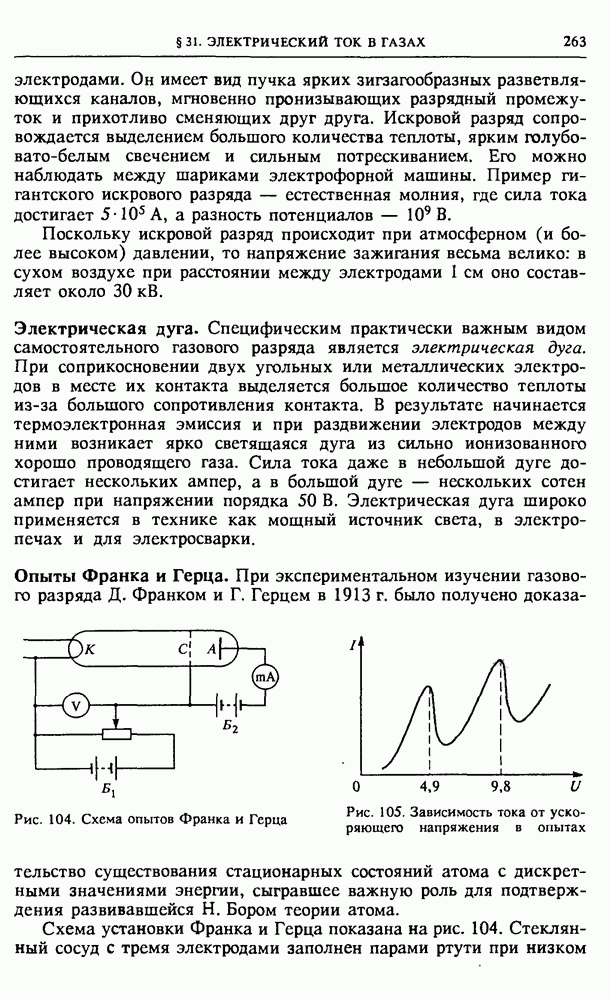
- § 31. Электрический ток в газах
- § 32. Электрический ток в жидкостях
- § 33. Плазма
- VII. ЭЛЕКТРОННЫЕ СВОЙСТВА ТВЕРДЫХ ТЕЛ
- § 34. Электронная структура кристаллов
- § 35. Электронные свойства металлов
- § 36. Электронные свойства полупроводников
- § 37. Полупроводниковые приборы
- VIII. АТОМНОЕ ЯДРО И ЭЛЕМЕНТАРНЫЕ ЧАСТИЦЫ
- § 38. Строение атомного ядра
- § 39. Радиоактивность. Ядерные реакции
- § 40. Элементарные частицы