| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ 26. Реальные газы. Уравнение Ван-дер-Ваальса
Поведение реальных газов в той или иной степени отличается от поведения идеального газа, описываемого уравнением Менделеева-Клапейрона. Отклонения зависят не только от того, с каким
газом — кислородом, азотом и т. д. - мы имеем дело, но и от тех условий, в которых находится газ. Чем более разрежен газ и чем выше его температура, тем менее заметны эти отклонения. Поэтому применимость модели идеального газа к какому-либо реальному газу определяется не только свойствами самого газа, такими, как размеры и масса его молекул и взаимодействия между ними, но и условиями, в которых находится газ.
О моделях реального газа. Взаимодействие между молекулами того или иного реального газа имеет настолько сложный характер, что невозможно получить уравнение состояния, которое количественно правильно описывало бы поведение реального газа во всей области возможных изменений его температуры и плотности. Можно, однако, написать приближенное уравнение состояния реального газа, учитывающее основные качественные особенности межмолекулярного взаимодействия.
В модели идеального газа не учитывалось ни взаимодействие молекул на расстоянии, ни конечный размер самих молекул. Напомним, что силы взаимодействия между молекулами имеют электромагнитную природу, хотя в целом молекулы электрически нейтральны. На больших расстояниях преобладают силы притяжения между молекулами, а на малых — силы отталкивания. Силы притяжения между молекулами быстро убывают с увеличением расстояния между ними, и поэтому при малой плотности газ ведет себя как идеальный. Но тем не менее силы притяжения существенны, так как именно они приводят к конденсации газа в жидкость. Отталкивание молекул на малых расстояниях настолько быстро возрастает при их сближении, что с хорошей точностью молекулы можно считать твердыми взаимно не проникающими телами и говорить об их собственном объеме и эффективном диаметре. Этот объем ставит предел возможному сжатию газа.
Модель твердых шаров. Приведенные соображения позволяют предложить простейшую микроскопическую модель реального газа — модель твердых шаров. В этой модели молекулы рассматриваются как твердые шары радиуса  взаимодействующие только при соприкосновении друг с другом. Кроме радиуса
взаимодействующие только при соприкосновении друг с другом. Кроме радиуса  система характеризуется массой
система характеризуется массой  молекул (шаров), их концентрацией
молекул (шаров), их концентрацией  и средней кинетической энергией теплового движения
и средней кинетической энергией теплового движения 
Чтобы разобраться в свойствах такой модели, найдем соответствующий ей безразмерный параметр  , составленный из
, составленный из  Поскольку время входит только в
Поскольку время входит только в  то
то  в безразмерный параметр
в безразмерный параметр  входить не может. Но тогда не может входить в него и масса
входить не может. Но тогда не может входить в него и масса  . А из оставшихся величин
. А из оставшихся величин  можно составить только один независимый безразмерный параметр
можно составить только один независимый безразмерный параметр  физический смысл которого — отношение собственного объема шара к среднему
физический смысл которого — отношение собственного объема шара к среднему
объему, приходящемуся на одну молекулу в газе. Предельному случаю идеального газа соответствует сильное разрежение, т. е.  когда энергия взаимодействия молекул должна стать пренебрежимо малой по сравнению с энергией теплового движения
когда энергия взаимодействия молекул должна стать пренебрежимо малой по сравнению с энергией теплового движения 
В сильно сжатом газе отношение средней энергии взаимодействия молекул к их кинетической энергии должно зависеть от температуры, поскольку с уменьшением температуры отклонение реального газа от идеального становится все более и более заметным. Однако в модели твердых шаров это отклонение определяется только параметром у и, следовательно, не зависит от температуры. Поэтому последовательная микроскопическая модель реального газа должна учитывать взаимодействие молекул друг с другом и на расстоянии, а не только при непосредственном соприкосновении.
Модель Ван-дер-Ваальса. Приступая к получению приближенного уравнения состояния реального газа, будем считать, что взаимодействие молекул приводит лишь к небольшим поправкам в уравнении состояния идеального газа. При достаточно высоких температурах и малых плотностях газа искомое уравнение должно приводить к тем же результатам, что и уравнение Менделеева—Клапейрона.
Учет размеров молекул. Прежде всего учтем конечные собственные размеры молекул. Фактически это приводит к тому, что предоставленный молекулам газа для движения объем будет меньше объема сосуда V. Поэтому в уравнении состояния одного моля идеального газа заменим объем V на  где
где  — характерная для данного газа положительная постоянная, учитывающая занимаемый молекулами объем:
— характерная для данного газа положительная постоянная, учитывающая занимаемый молекулами объем:

Из этого уравнения видно, что объем газа V не может быть сделан меньше, чем  так как при
так как при  давление газа
давление газа  неограниченно возрастает. Разумеется, не следует ожидать, что при значениях V, близких к
неограниченно возрастает. Разумеется, не следует ожидать, что при значениях V, близких к  уравнение (1) будет правильно описывать поведение газа, ибо по своему смыслу постоянная
уравнение (1) будет правильно описывать поведение газа, ибо по своему смыслу постоянная  является малой поправкой:
является малой поправкой: 
Учет взаимодействия между молекулами. Учтем теперь проявляющееся на больших расстояниях притяжение между молекулами. Притяжение должно приводить к уменьшению оказываемого газом давления на стенки сосуда, так как на каждую находящуюся вблизи стенки молекулу будет действовать со стороны остальных молекул газа сила, направленная внутрь сосуда. Поэтому давление на стенки  будет меньше значения, даваемого выражением (1), на некоторую величину
будет меньше значения, даваемого выражением (1), на некоторую величину 

От чего может зависеть величина  Можно ожидать, что в грубом приближении сила, действующая на каждую молекулу со стороны всех остальных, будет пропорциональна числу окружающих молекул, т. е. плотности газа. Следовательно, и поправка к передаваемому отдельной молекулой импульсу при ударе о стенку пропорциональна плотности газа. Поправка же к передаваемому при ударах о стенку всеми молекулами импульсу (т. е. к давлению) будет пропорциональна квадрату плотности газа или, что то же самое, обратно пропорциональна квадрату объема. Поэтому выражение для
Можно ожидать, что в грубом приближении сила, действующая на каждую молекулу со стороны всех остальных, будет пропорциональна числу окружающих молекул, т. е. плотности газа. Следовательно, и поправка к передаваемому отдельной молекулой импульсу при ударе о стенку пропорциональна плотности газа. Поправка же к передаваемому при ударах о стенку всеми молекулами импульсу (т. е. к давлению) будет пропорциональна квадрату плотности газа или, что то же самое, обратно пропорциональна квадрату объема. Поэтому выражение для  можно записать в виде
можно записать в виде

где а — характерная для данного газа положительная постоянная. Поскольку  как и
как и  является малой поправкой, должно выполняться неравенство
является малой поправкой, должно выполняться неравенство  Подставляя
Подставляя  из формулы (3) в уравнение (2), получим
из формулы (3) в уравнение (2), получим

Уравнение (4) называется уравнением Ван-дер-Ваальса. Оно приближенно учитывает особенности поведения реального газа, обусловленные межмолекулярным взаимодействием и собственными размерами молекул. Постоянные Ван-дер-Ваальса а и  определяются опытным путем: их значения для каждого газа выбираются таким образом, чтобы уравнение (4) наилучшим образом описывало поведение данного газа.
определяются опытным путем: их значения для каждого газа выбираются таким образом, чтобы уравнение (4) наилучшим образом описывало поведение данного газа.
Феноменологический характер уравнения Ван-дер-Ваальса. Не следует рассматривать приведенные выше рассуждения как строгий вывод уравнения состояния реального газа. Они представляют собой пример феноменологического подхода, при котором качественный вид закономерности устанавливается с помощью наводящих соображений, а количественные характеристики — в данном случае постоянные  — находятся из сравнения с экспериментом. Как и всякое феноменологическое соотношение, уравнение Ван-дер-Ваальса в некоторой области — при достаточно высоких температурах и малых плотностях — дает правильное количественное описание свойств реального газа, тогда как во всей области изменения параметров оно дает только качественную картину поведения газа.
— находятся из сравнения с экспериментом. Как и всякое феноменологическое соотношение, уравнение Ван-дер-Ваальса в некоторой области — при достаточно высоких температурах и малых плотностях — дает правильное количественное описание свойств реального газа, тогда как во всей области изменения параметров оно дает только качественную картину поведения газа.
Кроме уравнения Ван-дер-Ваальса было предложено много других эмпирических уравнений состояния реальных газов. Некоторые из них дают лучшее согласие с опытом за счет большего числа входящих в них феноменологических постоянных. Однако при качественном исследовании поведения реальных газов удобно использовать именно уравнение Ван-дер-Ваальса благодаря его простоте и ясному физическому смыслу.
Изотермы Ван-дер-Ваальса. Для исследования поведения газа, подчиняющегося уравнению Ван-дер-Ваальса, рассмотрим определяемые этим уравнением изотермы, т. е. кривые зависимости  от V при заданных значениях температуры Т. С этой целью перепишем уравнение (4) в виде
от V при заданных значениях температуры Т. С этой целью перепишем уравнение (4) в виде

При фиксированных значениях  это уравнение третьей степени относительно V. Уравнение третьей степени имеет либо один, либо три вещественных корня. Поэтому при данных значениях давления и температуры уравнение (5) дает либо одно, либо три значения объема. Это значит, что на
это уравнение третьей степени относительно V. Уравнение третьей степени имеет либо один, либо три вещественных корня. Поэтому при данных значениях давления и температуры уравнение (5) дает либо одно, либо три значения объема. Это значит, что на  -диаграмме изотерма пересекает горизонтальную прямую
-диаграмме изотерма пересекает горизонтальную прямую  либо в одной точке, либо в трех точках.
либо в одной точке, либо в трех точках.
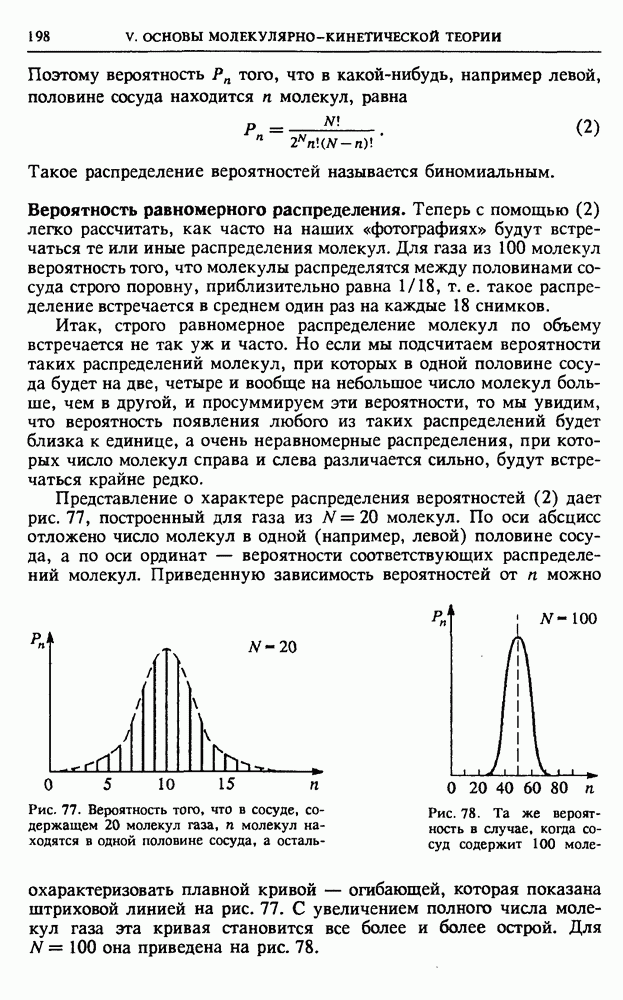
На рис. 85 приведены изотермы, соответствующие различным значениям температуры 

Рис. 85. Изотермы газа Ван-дер-Ваальса на  -диаграмме
-диаграмме
Изотерма, соответствующая достаточно высокой температуре  мало отличается от изотермы идеального газа, и одно из самых существенных отличий заключается в том, что значение объема V ни при каких давлениях не может быть меньше
мало отличается от изотермы идеального газа, и одно из самых существенных отличий заключается в том, что значение объема V ни при каких давлениях не может быть меньше  При достаточно низких температурах
При достаточно низких температурах  изотермы содержат волнообразный участок, так что прямая
изотермы содержат волнообразный участок, так что прямая  трижды пересекает изотерму. Существует некоторая температура Тк, такая, что соответствующая ей изотерма отделяет все монотонные изотермы, лежащие выше нее, от «горбатых», лежащих ниже. Такая температура и соответствующая ей изотерма носят название критических.
трижды пересекает изотерму. Существует некоторая температура Тк, такая, что соответствующая ей изотерма отделяет все монотонные изотермы, лежащие выше нее, от «горбатых», лежащих ниже. Такая температура и соответствующая ей изотерма носят название критических.
Экспериментальные изотермы Эндрюса. Для того чтобы выяснить смысл этой на первый взгляд весьма странной зависимости, следует
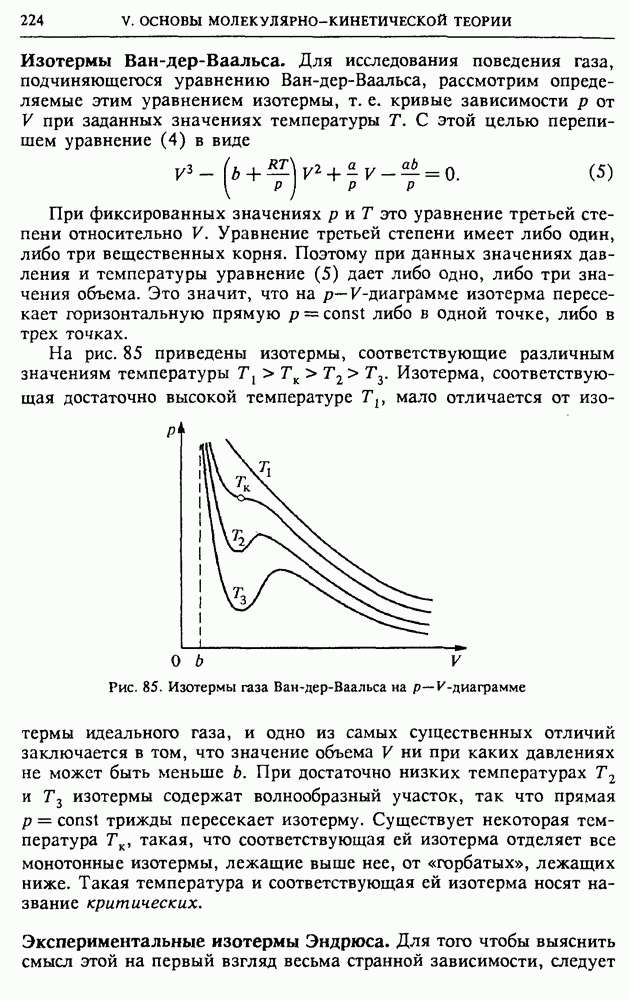
обратиться к опыту. На рис. 86 показаны полученные экспериментально изотермы углекислого газа  При высоких температурах эти изотермы очень похожи на изотермы идеального газа.
При высоких температурах эти изотермы очень похожи на изотермы идеального газа.

Рис. 86. Экспериментальные изотермы углекислого газа
При низких температурах характер изотерм существенно другой: у них имеется горизонтальный участок, на котором давление остается постоянным, несмотря на изменение объема.
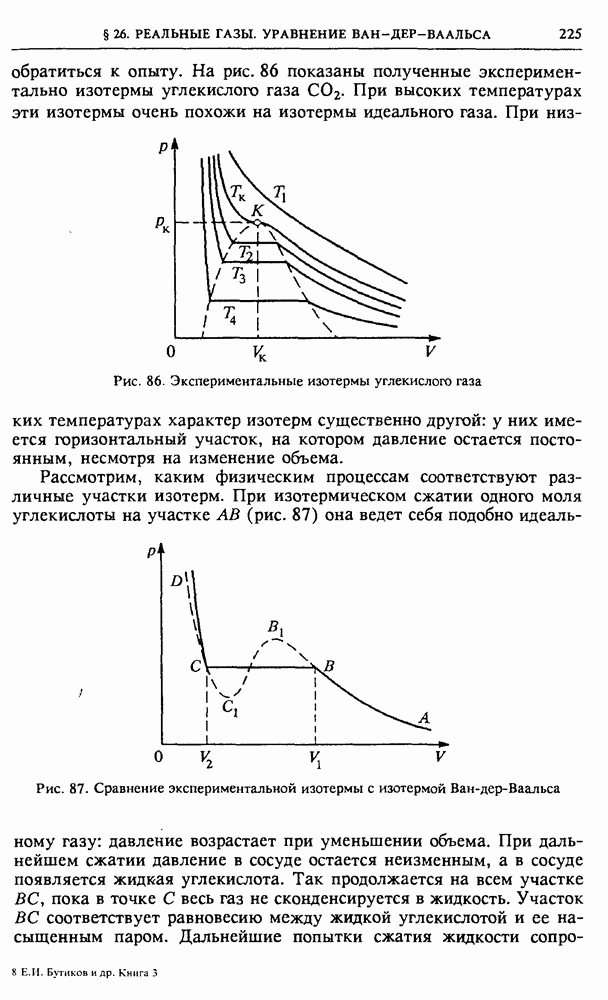
Рассмотрим, каким физическим процессам соответствуют различные участки изотерм. При изотермическом сжатии одного моля углекислоты на участке  (рис. 87) она ведет себя подобно идеальному газу: давление возрастает при уменьшении объема.
(рис. 87) она ведет себя подобно идеальному газу: давление возрастает при уменьшении объема.

Рис. 87. Сравнение экспериментальной изотермы с изотермой Ван-дер-Ваальса
При дальнейшем сжатии давление в сосуде остается неизменным, а в сосуде появляется жидкая углекислота. Так продолжается на всем участке  пока в точке С весь газ не сконденсируется в жидкость. Участок
пока в точке С весь газ не сконденсируется в жидкость. Участок  соответствует равновесию между жидкой углекислотой и ее насыщенным паром. Дальнейшие попытки сжатия жидкости
соответствует равновесию между жидкой углекислотой и ее насыщенным паром. Дальнейшие попытки сжатия жидкости
сопровождаются резким увеличением давления при самом незначительном уменьшении объема.
Наложим на график экспериментально полученной изотермы теоретическую кривую Ван-дер-Ваальса для той же самой температуры. Параметры  можно выбрать так, чтобы на участке
можно выбрать так, чтобы на участке  соответствующем газообразному состоянию, обе кривые практически совпадали. Это значит, что уравнение Ван-дер-Ваальса вполне удовлетворительно описывает свойства паров, далеких от насыщения. Крутой ход теоретической изотермы на участке
соответствующем газообразному состоянию, обе кривые практически совпадали. Это значит, что уравнение Ван-дер-Ваальса вполне удовлетворительно описывает свойства паров, далеких от насыщения. Крутой ход теоретической изотермы на участке  качественно правильно передает малую сжимаемость жидкости, хотя экспериментальная изотерма на этом участке идет еще круче. Но волнообразный участок теоретической изотермы совершенно не похож на соответствующее ему плато экспериментальной кривой.
качественно правильно передает малую сжимаемость жидкости, хотя экспериментальная изотерма на этом участке идет еще круче. Но волнообразный участок теоретической изотермы совершенно не похож на соответствующее ему плато экспериментальной кривой.
Метастабильные состояния. Однако оказывается, что ряд состояний, попадающих в область «горбов», может быть экспериментально осуществлен при соблюдении определенных условий. Так, в свободном от пыли и заряженных частиц пространстве удается при постепенном сжатии получить пары при давлении, большем давления насыщенных паров при данной температуре. Такие пары называются пересыщенными, и их состояния достаточно хорошо описываются участком  теоретической изотермы (см. рис. 87). Эти состояния при появлении центров конденсации — ионов, пылинок, мельчайших капелек — становятся неустойчивыми, и пересыщенный пар мгновенно конденсируется в туман.
теоретической изотермы (см. рис. 87). Эти состояния при появлении центров конденсации — ионов, пылинок, мельчайших капелек — становятся неустойчивыми, и пересыщенный пар мгновенно конденсируется в туман.
Пересыщенный пар можно получить не только при изотермическом сжатии, но и при охлаждении насыщенного пара. Поэтому его иногда называют также переохлажденным. Такой способ получения пересыщенного пара используется в камере Вильсона, нашедшей широкое применение на заре ядерной физики для регистрации заряженных частиц.
Жидкая углекислота при постепенном изотермическом расширении может сохраниться в жидком состоянии и при давлении, меньшем давления насыщенных паров при данной температуре. Такие состояния, как уже отмечалось, называются перегретой жидкостью, и им соответствует участок  теоретической изотермы Ван-дер-Ваальса. Перегретая жидкость может быть получена также нагреванием жидкости при постоянном давлении, если принять меры к тому, чтобы жидкость и стенки сосуда не содержали растворенных газов, которые при нагревании могут выделяться с образованием пузырьков и становиться зародышами новой фазы. При появлении центров кипения перегретая жидкость мгновенно закипает.
теоретической изотермы Ван-дер-Ваальса. Перегретая жидкость может быть получена также нагреванием жидкости при постоянном давлении, если принять меры к тому, чтобы жидкость и стенки сосуда не содержали растворенных газов, которые при нагревании могут выделяться с образованием пузырьков и становиться зародышами новой фазы. При появлении центров кипения перегретая жидкость мгновенно закипает.
Таким образом, участки  и
и  теоретической изотермы соответствует состояниям вещества, которые, хотя и неустойчивы, но могут быть осуществлены экспериментально. Такие состояния называются метастабильными.
теоретической изотермы соответствует состояниям вещества, которые, хотя и неустойчивы, но могут быть осуществлены экспериментально. Такие состояния называются метастабильными.
Абсолютно неустойчивые состояния. Состояния вещества на участке  рис. 87) являются абсолютно неустойчивыми и вообще не могут осуществляться в природе, так как им соответствует уменьшение давления при сжатии. Представим на минуту, что такие состояния возможны. Пусть небольшая часть вещества случайно сжалась в результате флуктуации плотности. Тогда давление в этом месте уменьшится и станет меньше давления окружающей среды. Это приведет к дальнейшему сжатию выделенного вещества и т. д. - система самопроизвольно выходит из такого неустойчивого состояния.
рис. 87) являются абсолютно неустойчивыми и вообще не могут осуществляться в природе, так как им соответствует уменьшение давления при сжатии. Представим на минуту, что такие состояния возможны. Пусть небольшая часть вещества случайно сжалась в результате флуктуации плотности. Тогда давление в этом месте уменьшится и станет меньше давления окружающей среды. Это приведет к дальнейшему сжатию выделенного вещества и т. д. - система самопроизвольно выходит из такого неустойчивого состояния.
Если неустойчивость состояний, соответствующих участкам  и
и  обусловливалась наличием центров конденсации и кипения и потому была в принципе устранимой, то неустойчивость состояний на участке
обусловливалась наличием центров конденсации и кипения и потому была в принципе устранимой, то неустойчивость состояний на участке  связана с неизбежными тепловыми флуктуациями и принципиально неустранима. Поэтому такие состояния теоретической изотермы никогда не осуществляются.
связана с неизбежными тепловыми флуктуациями и принципиально неустранима. Поэтому такие состояния теоретической изотермы никогда не осуществляются.
Наличие неосуществимого участка на изотермах Ван-дер-Ваальса при температурах ниже критической означает, что при постепенном изменении объема вещество не может все время оставаться однородным: в некоторый момент должно произойти расслоение вещества на две фазы — жидкую и газообразную.
В связи с этим интересно отметить, что эмпирическое уравнение Ван-дер-Ваальса, полученное с целью введения малых поправок к уравнению состояния идеального газа, фактически оказалось эффективным в гораздо более широкой области. В самом деле, оно указало на существование критической температуры и на необходимость расслоения вещества на фазы при температурах ниже критической. Оно также отразило возможность существования состояний пересыщенного пара и перегретой жидкости, качественно описало малую сжимаемость жидкостей и т. п.
Критическое состояние вещества.
Проследим, как изменяется по мере повышения температуры область сосуществования двух фаз на  К-диаграмме.
К-диаграмме.

Рис. 88. Границы равновесия различных фаз вещества на  -диаграмме
-диаграмме
Прямолинейный участок экспериментальной изотермы уменьшается с ростом температуры и при критической температуре стягивается в одну точку К на рис. 86. Если соединить между собой точки начала горизонтальных участков на всех изотермах, а также точки концов этих участков, то получим некоторую кривую  (рис. 88). Эта кривая представляет собой границу, отделяющую состояния, в которых вещество существует в двух находящихся в равновесии
(рис. 88). Эта кривая представляет собой границу, отделяющую состояния, в которых вещество существует в двух находящихся в равновесии
фазах, от однофазных состояний. Соответствующие точке К давление и объем получили название критических. Состояние вещества в точке К называется критическим состоянием.
В критической точке сливаются в одну три точки, в которых горизонтальный участок экспериментальной изотермы пересекает изотерму Ван-дер-Ваальса.
В критическом состоянии исчезает различие между жидкостью и газом, нет и никакой границы раздела между ними. При этом теряют смысл такие понятия, как поверхностное натяжение, теплота парообразования.
Сжимаемость вещества при приближении к критическому состоянию неограниченно возрастает: график изотермы в окрестности этой точки идет горизонтально и, следовательно, малое изменение объема вещества не сопровождается изменением давления. Это приводит к существованию больших флуктуаций плотности в критическом состоянии, которые проявляются, например, в явлении критической опалесценции — сильном рассеянии света на случайных неоднородностях.
Границы равновесия разных фаз вещества между собой показаны на диаграмме состояний (рис. 88). Граница  является чисто условной и соответствует историческому делению газообразного состояния на пар и «истинный газ» в зависимости от того, находится ли вещество при температуре ниже или выше критической. В отличие от границы
является чисто условной и соответствует историческому делению газообразного состояния на пар и «истинный газ» в зависимости от того, находится ли вещество при температуре ниже или выше критической. В отличие от границы  на этой диаграмме, при переходе через границу
на этой диаграмме, при переходе через границу  никаких качественных изменений в веществе не происходит.
никаких качественных изменений в веществе не происходит.
• В каких явлениях обнаруживаются отклонения поведения реальных газов от предсказаний модели идеального газа?
• Почему модель твердых шаров не в состоянии объяснить факт усиления отклонения свойств реального газа от идеального при понижении температуры?
• Какой физический смысл имеют параметры а и  , фигурирующие в уравнении Ван-дер-Ваальса? Какова их размерность? Каким образом определяются их значения для реальных газов?
, фигурирующие в уравнении Ван-дер-Ваальса? Какова их размерность? Каким образом определяются их значения для реальных газов?
• В чем заключается феноменологический характер уравнения Ван-дер-Ваальса?
• С чем связан качественно различный вид изотерм Ван-дер-Ваальса при разных температурах?
• Опишите физические процессы при изменении объема системы, соответствующие разным участкам экспериментальной изотермы,
• Как практически можно осуществить метастабильные состояния, соответствующие участкам  теоретической изотермы Ван-дер-Ва-альса (рис. 87)?
теоретической изотермы Ван-дер-Ва-альса (рис. 87)?
• Почему участок  теоретической изотермы (рис. 87) принципиально неосуществим на опыте?
теоретической изотермы (рис. 87) принципиально неосуществим на опыте?
• Поясните, каким образом уравнение Ван-дер-Ваальса указывает на необходимость расслоения вещества на фазы при температурах ниже критической.
• Что такое критическое состояние? Какими свойствами обладает вещество в критическом состоянии?
• Поясните, почему при переходе через границу  на рис. 88, разделяющую газ и пар, никаких качественных изменений в состоянии вещества не происходит.
на рис. 88, разделяющую газ и пар, никаких качественных изменений в состоянии вещества не происходит.
| << Предыдущий параграф | Следующий параграф >> |
- I. ТЕОРИЯ ОТНОСИТЕЛЬНОСТИ
- § 2. Релятивистская кинематика
- § 3. Преобразования Лоренца
- § 4. Релятивистская динамика
- § 5. Примеры релятивистского движения частиц
- II. ЗАКОНЫ МИКРОМИРА. ЧАСТИЦЫ И ВОЛНЫ
- § 6. Световые кванты
- § 7. Границы применимости классической физики
- § 8. Свет — частицы или волны?
- § 9. Законы движения в квантовой физике
- III. АТОМЫ, МОЛЕКУЛЫ, КРИСТАЛЛЫ
- § 10. Строение атома
- § 11. Измерения в атомной физике
- § 12. Молекулы
- § 13. Кристаллы
- IV. ОСНОВЫ ТЕРМОДИНАМИКИ
- § 14. Основные понятия термодинамики
- § 15. Уравнение состояния газа
- § 16. Первый закон термодинамики
- § 17. Примеры применения первого закона термодинамики
- § 18. Второй закон термодинамики
- § 19. Методы термодинамики и их применения
- V. ОСНОВЫ МОЛЕКУЛЯРНО-КИНЕТИЧЕСКОЙ ТЕОРИИ
- § 20. Экспериментальные основания статистической механики
- § 21. Молекулярно-кинетическая теория идеального газа
- § 22. Статистические распределения
- § 23. Тепловое равновесие в статистической механике
- § 24. Статистическая природа необратимости тепловых процессов
- § 25. Газы, жидкости, фазовые переходы
- § 26. Реальные газы. Уравнение Ван-дер-Ваальса
- § 27. Фазовые переходы
- VI. АТОМЫ И ИЗЛУЧЕНИЕ
- § 28. Излучение света атомами
- § 29. Излучение света нагретыми телами
- § 30. Вынужденное излучение. Квантовые усилители и генераторы света
- § 31. Электрический ток в газах
- § 32. Электрический ток в жидкостях
- § 33. Плазма
- VII. ЭЛЕКТРОННЫЕ СВОЙСТВА ТВЕРДЫХ ТЕЛ
- § 34. Электронная структура кристаллов
- § 35. Электронные свойства металлов
- § 36. Электронные свойства полупроводников
- § 37. Полупроводниковые приборы
- VIII. АТОМНОЕ ЯДРО И ЭЛЕМЕНТАРНЫЕ ЧАСТИЦЫ
- § 38. Строение атомного ядра
- § 39. Радиоактивность. Ядерные реакции
- § 40. Элементарные частицы