| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
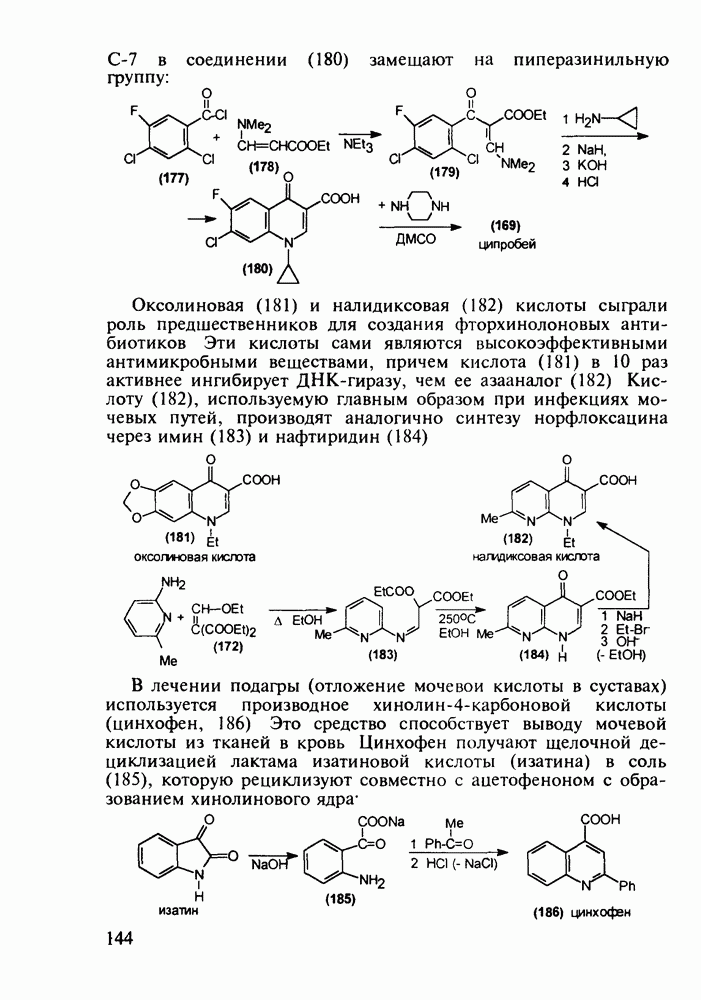
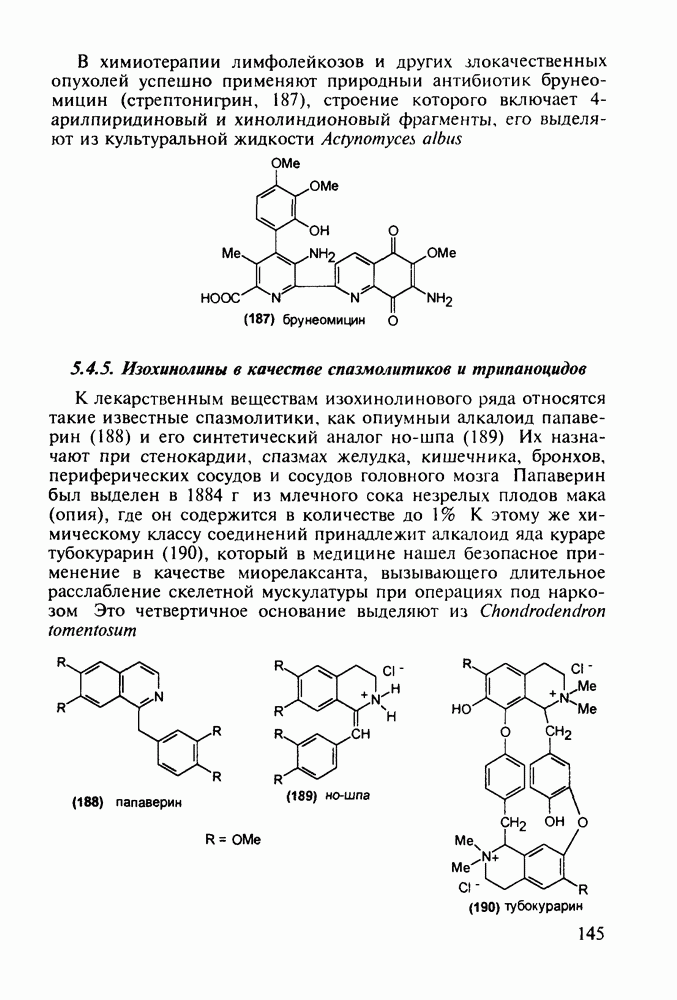
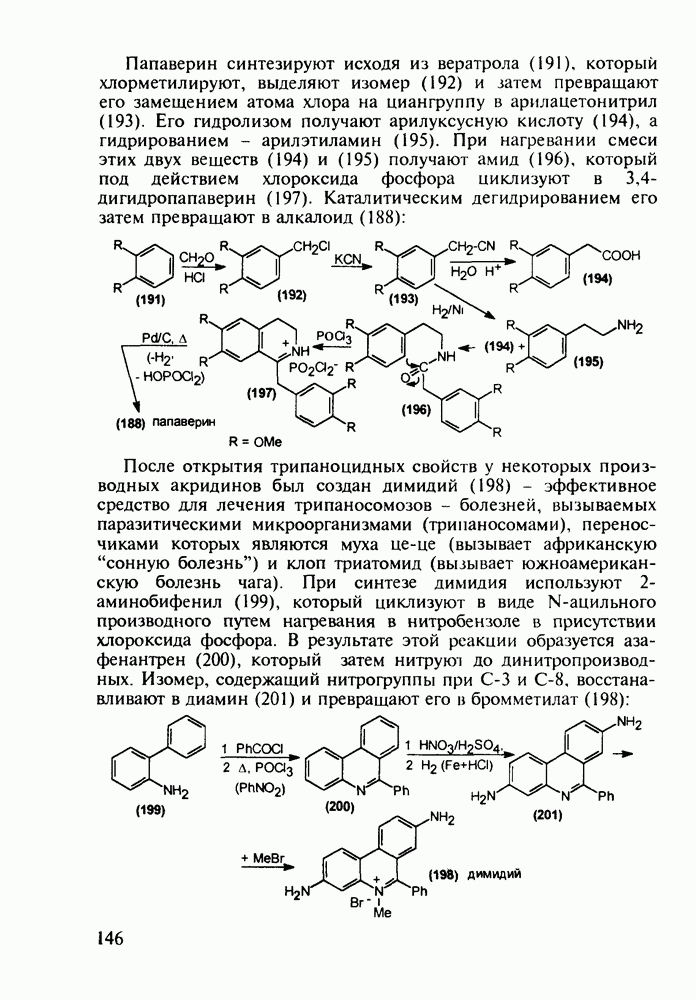
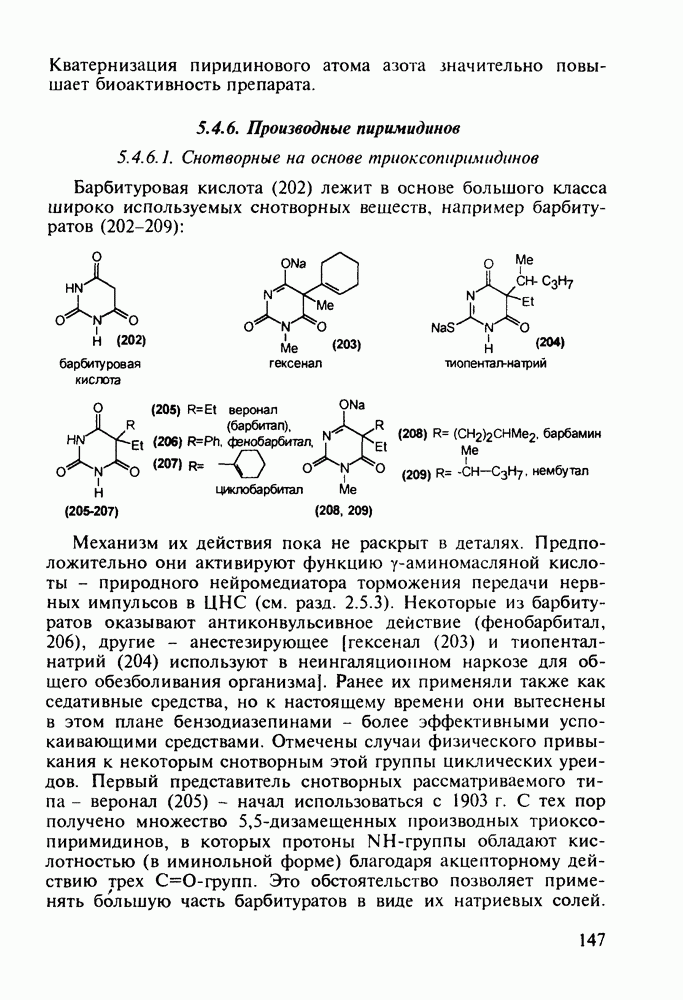
2.5. Аминокислоты
2.5.1. Производные а-аминокислот. Витамин U. Эндогенные олигопептиды
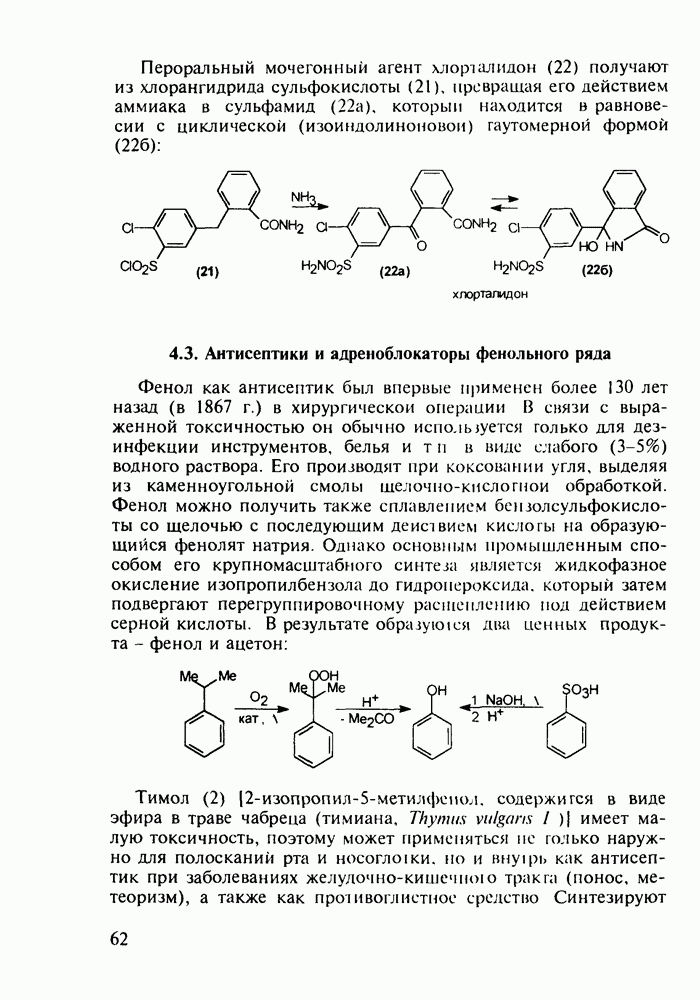
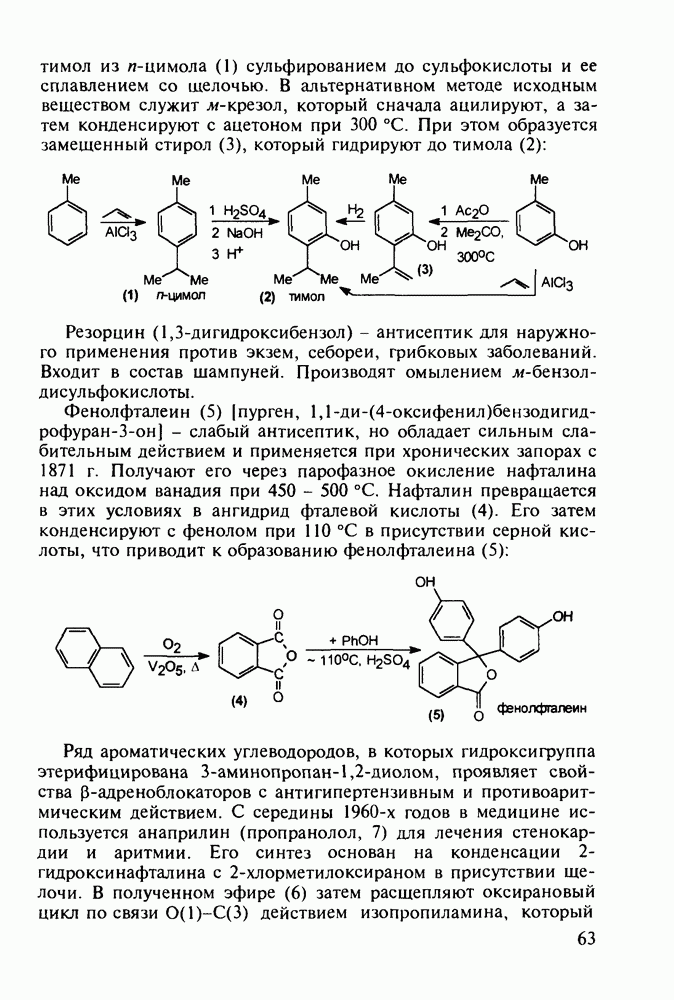
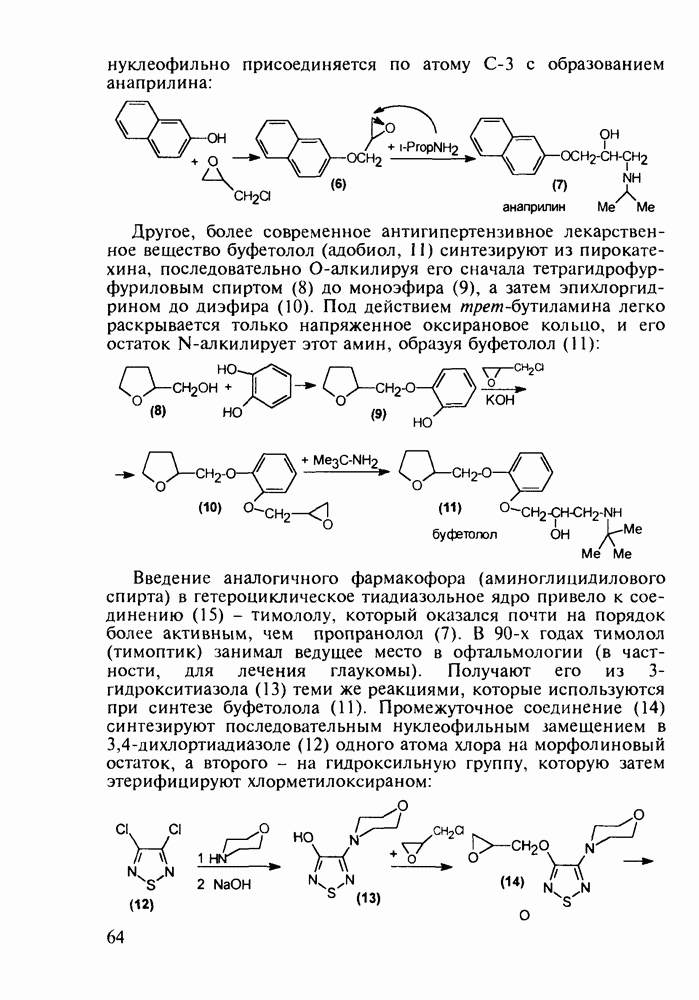
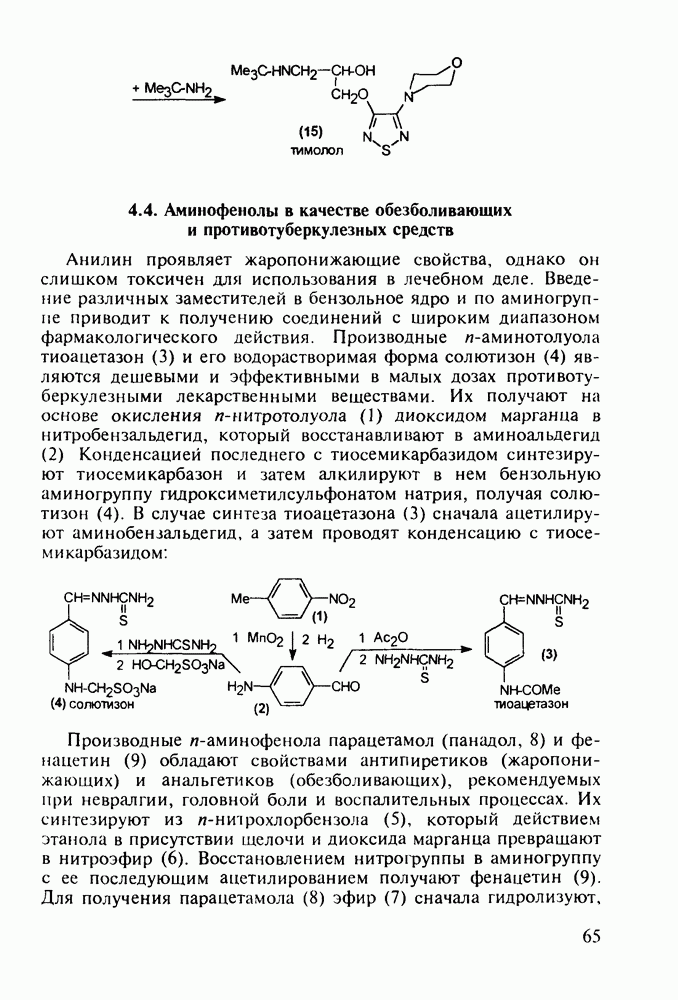
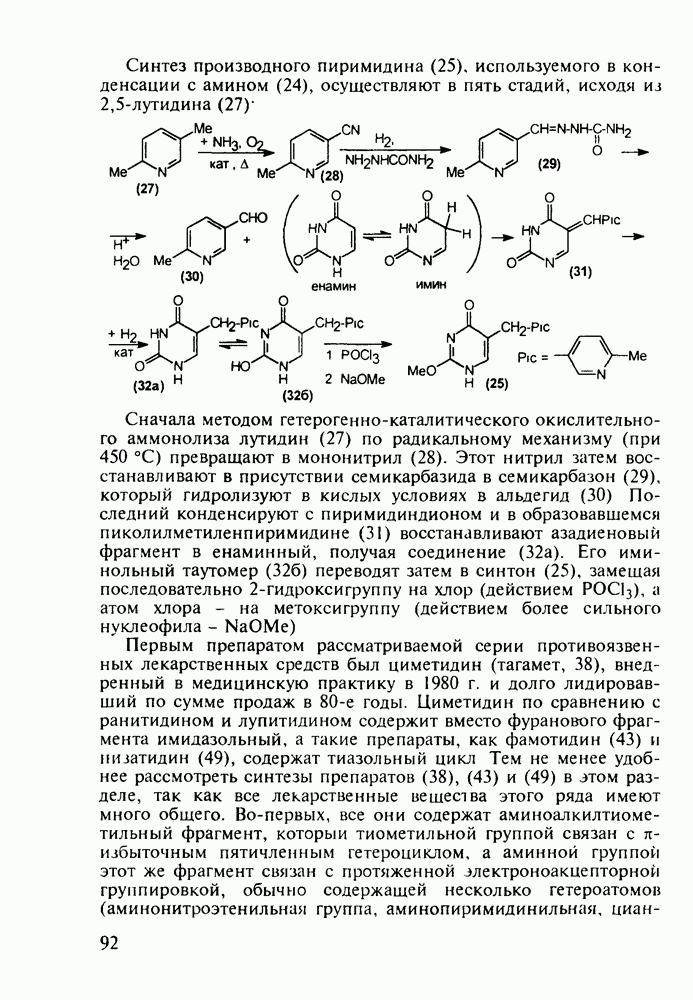
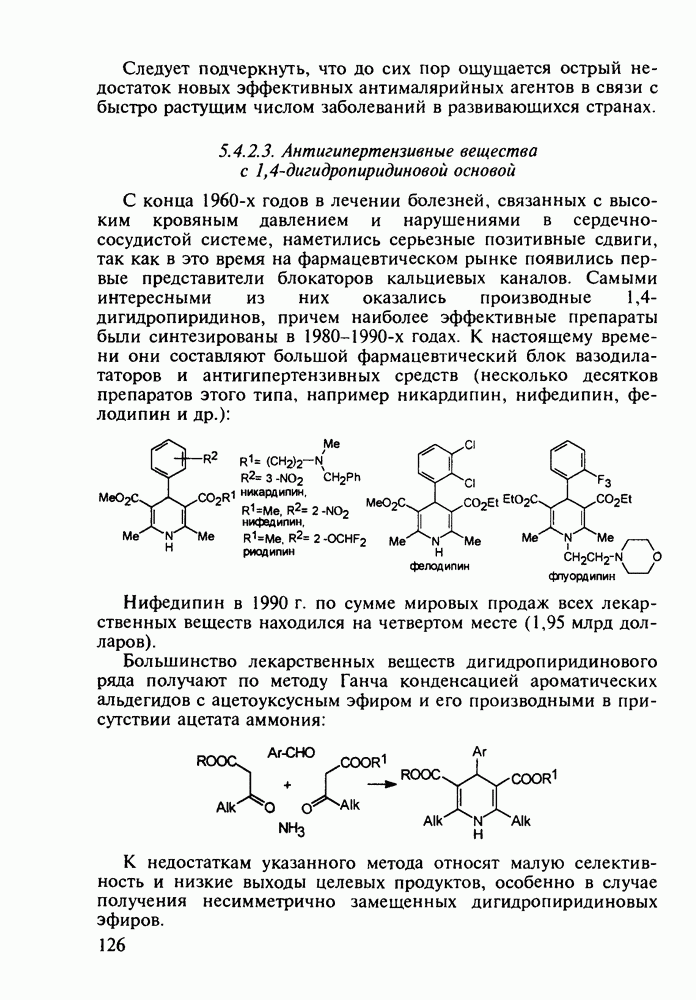
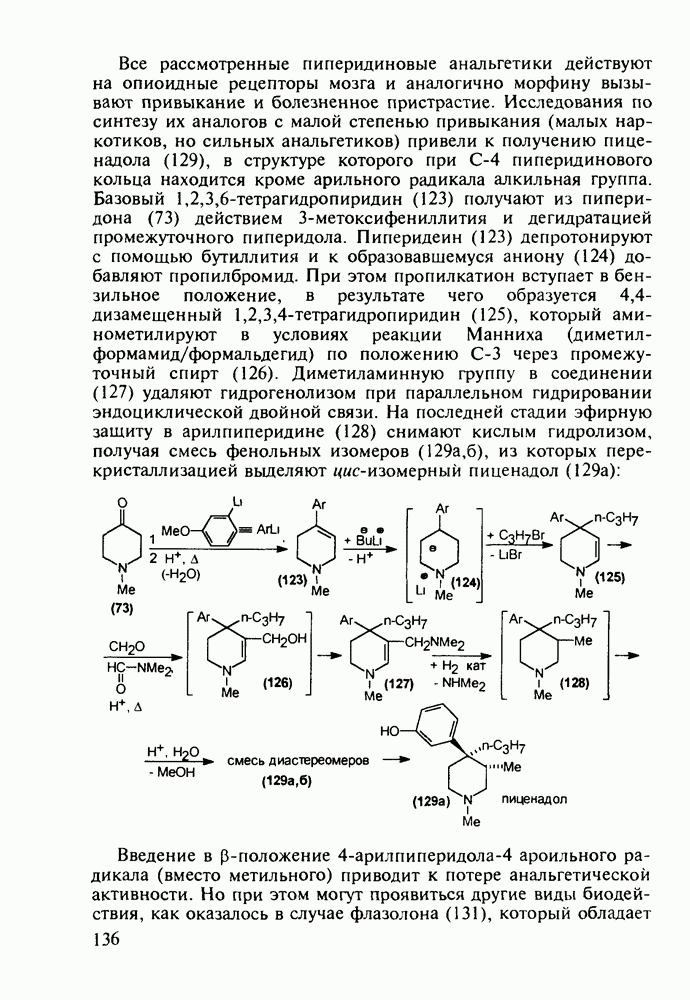
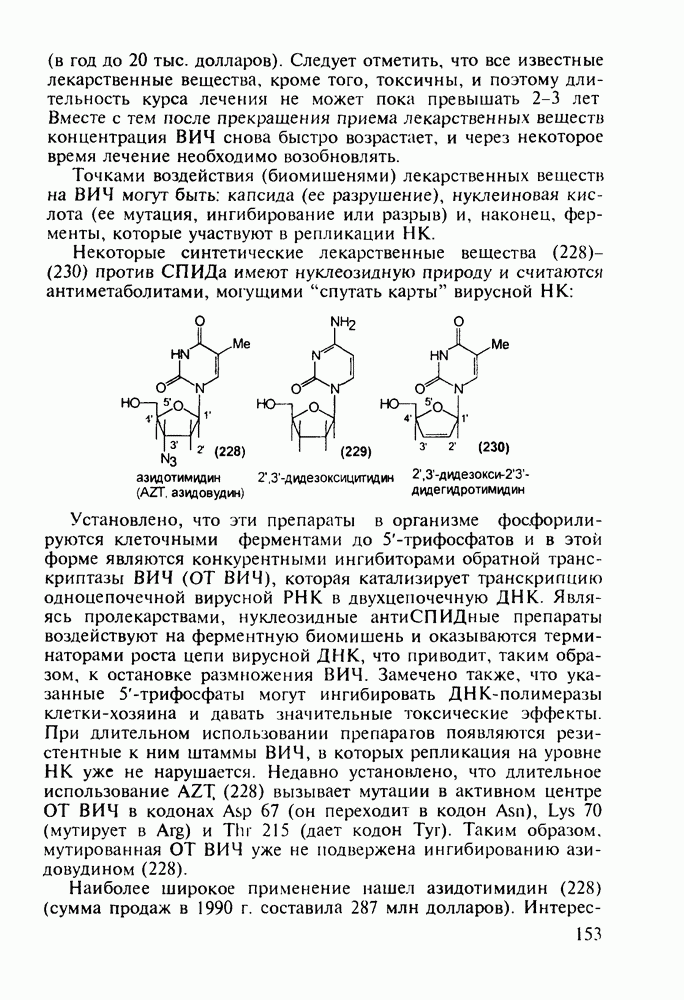
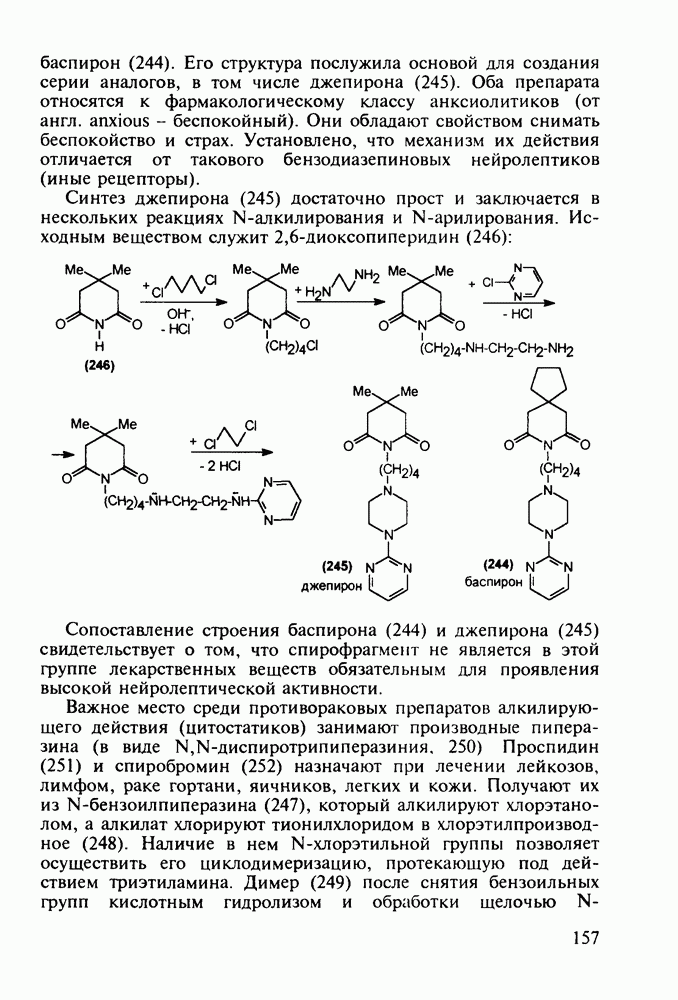
В настоящее время суммарное производство а-аминокислот составляет в мире около полумиллиона тонн в год. Оно стало крупнотоннажным благодаря их широкому применению как в медицине, так и в сельском хозяйстве (ростстимулирующие кормовые добавки) и в пищевой промышленности (вкусовые и консервирующие вещества). О практическом значении индивидуальных аминокислот говорят масштабы их химического и биохимического синтеза: триптофан производят в количестве от 0,2 до 0,3 тыс. т, глицин - 7-10 тыс. т, лизин - около 50 тыс. т, метионин - 150-200 тыс. т и глутаминовую кислоту - более 200 тыс. т в год.
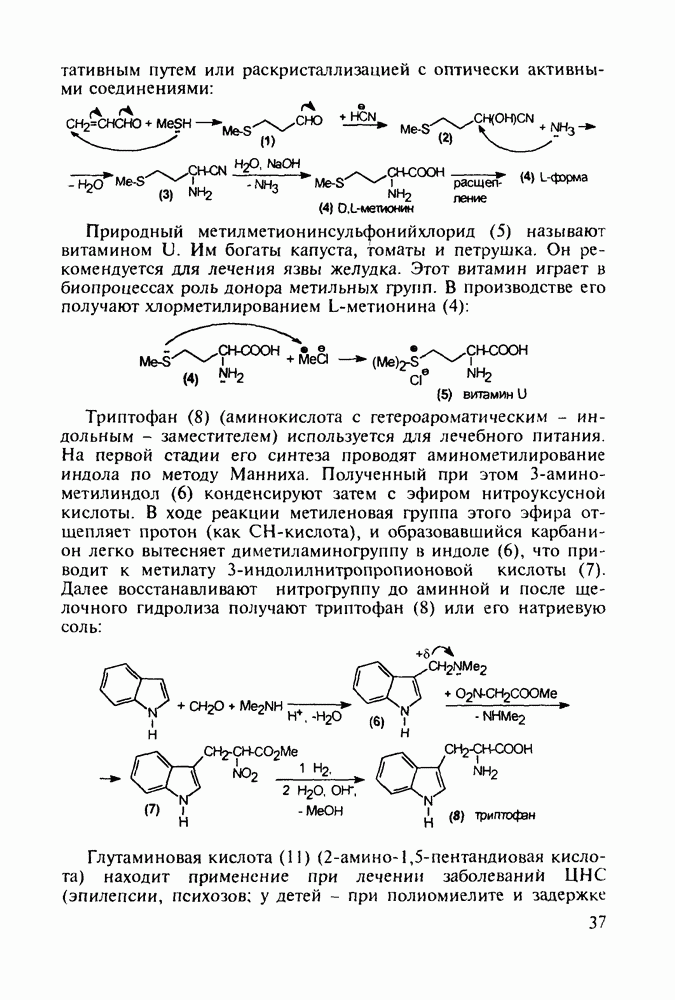
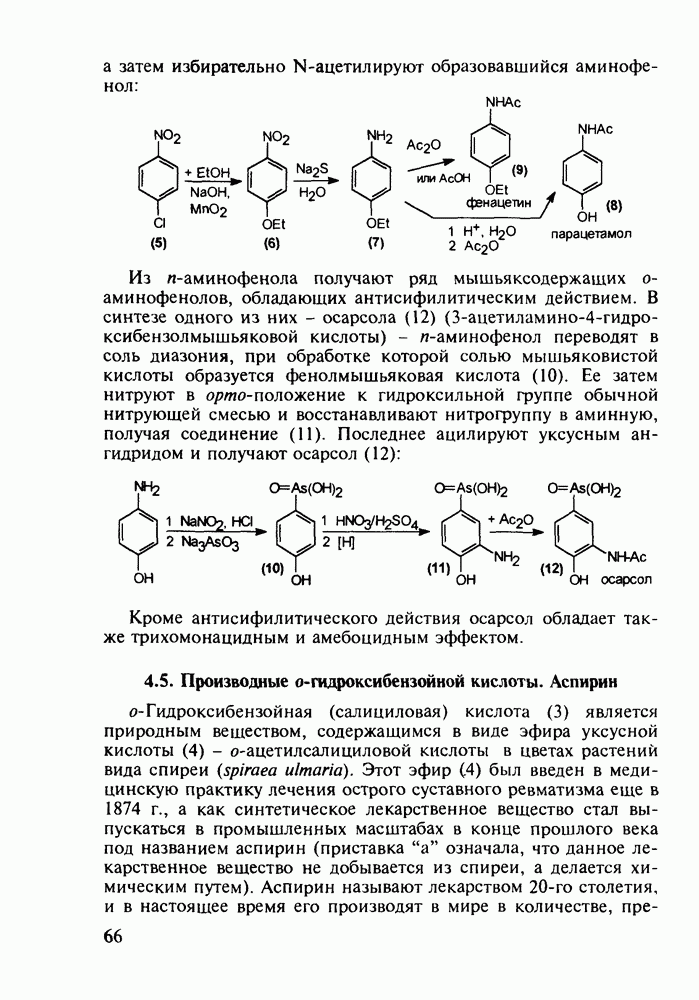
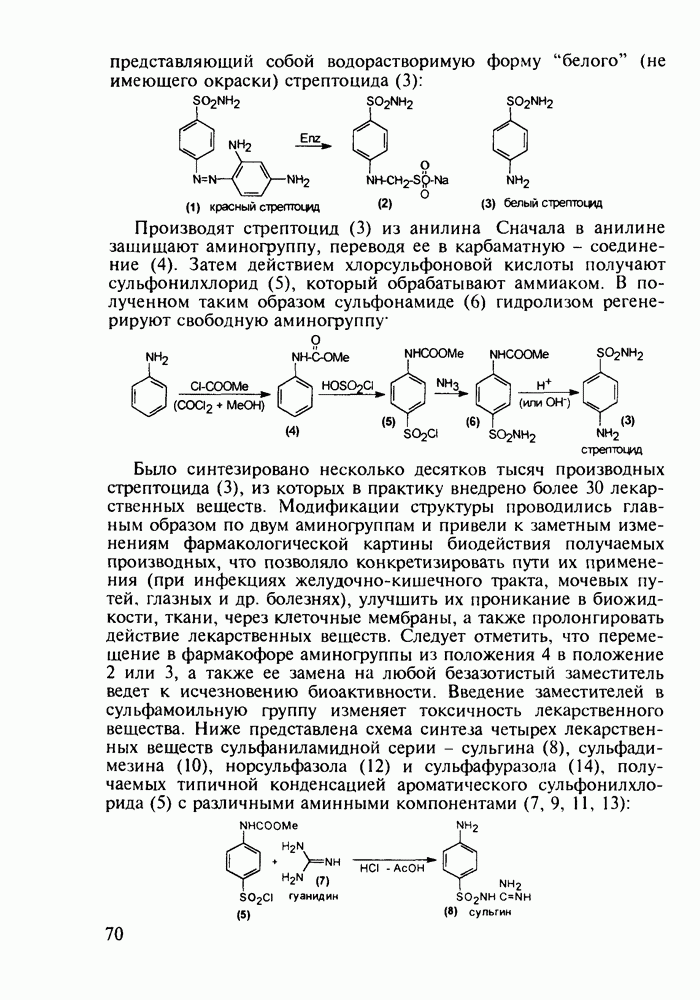
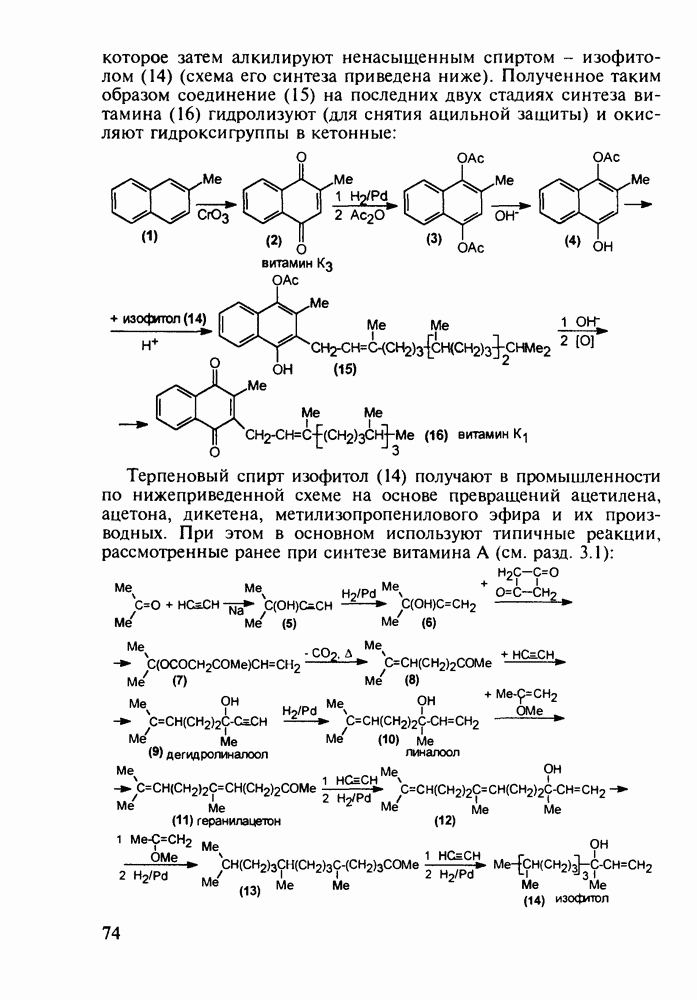
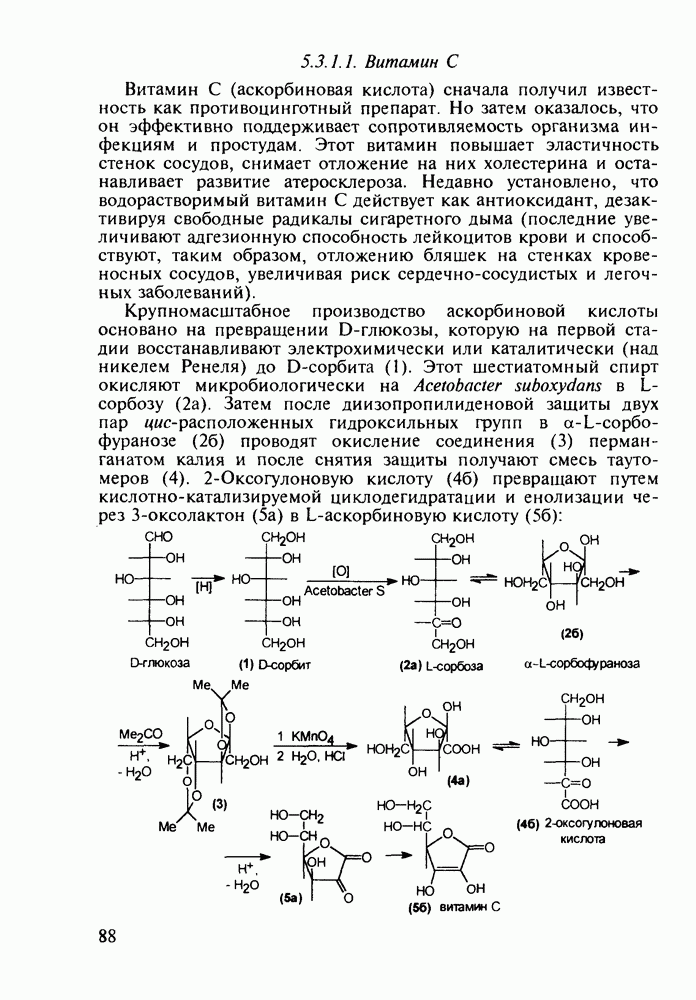
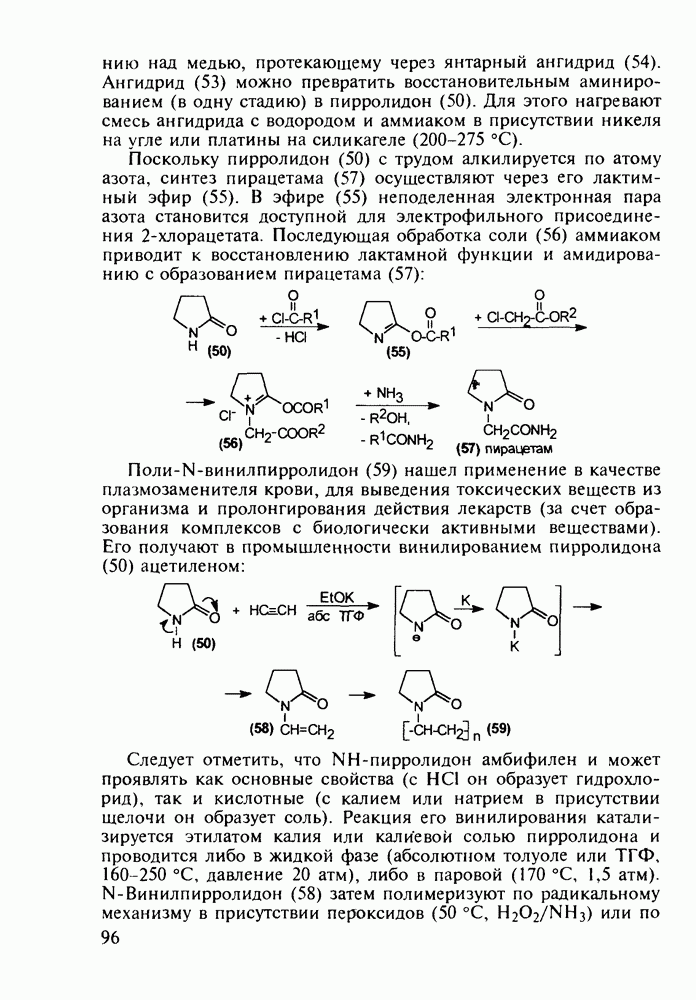
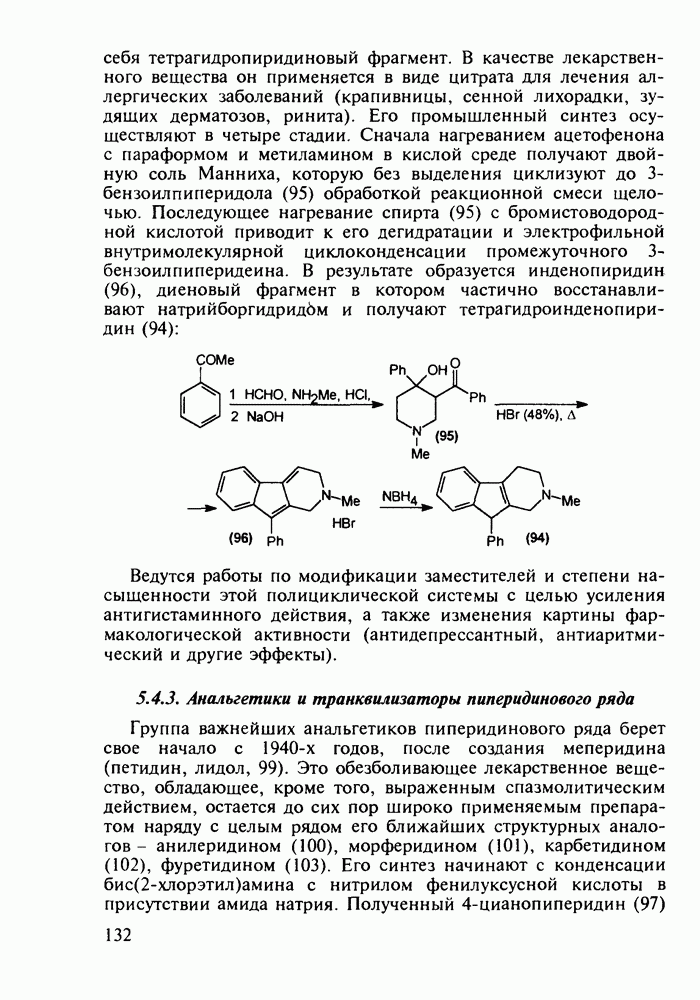
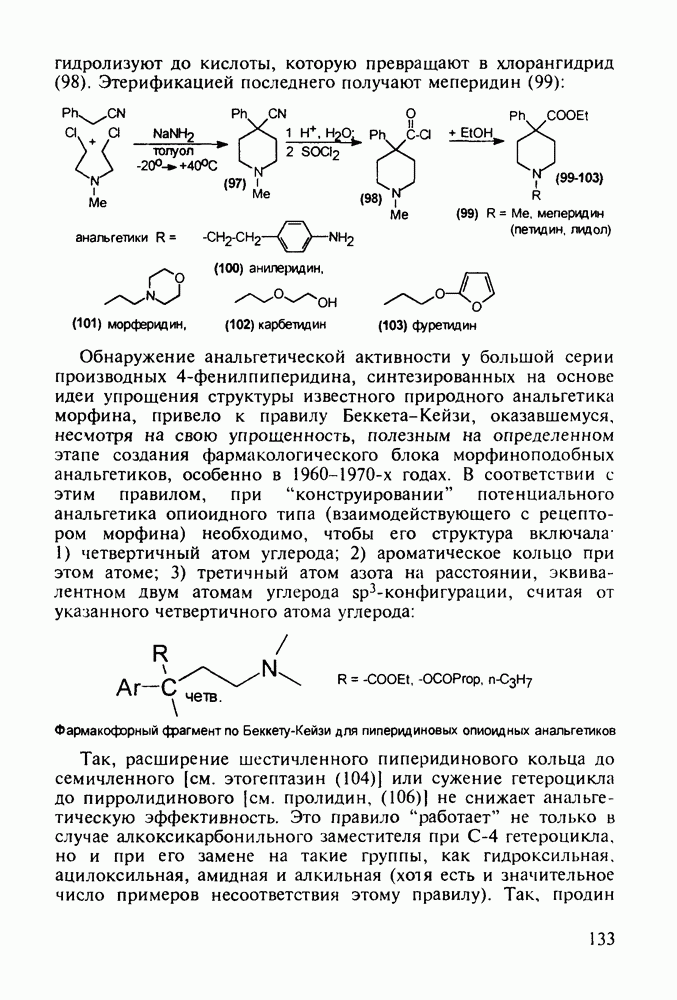
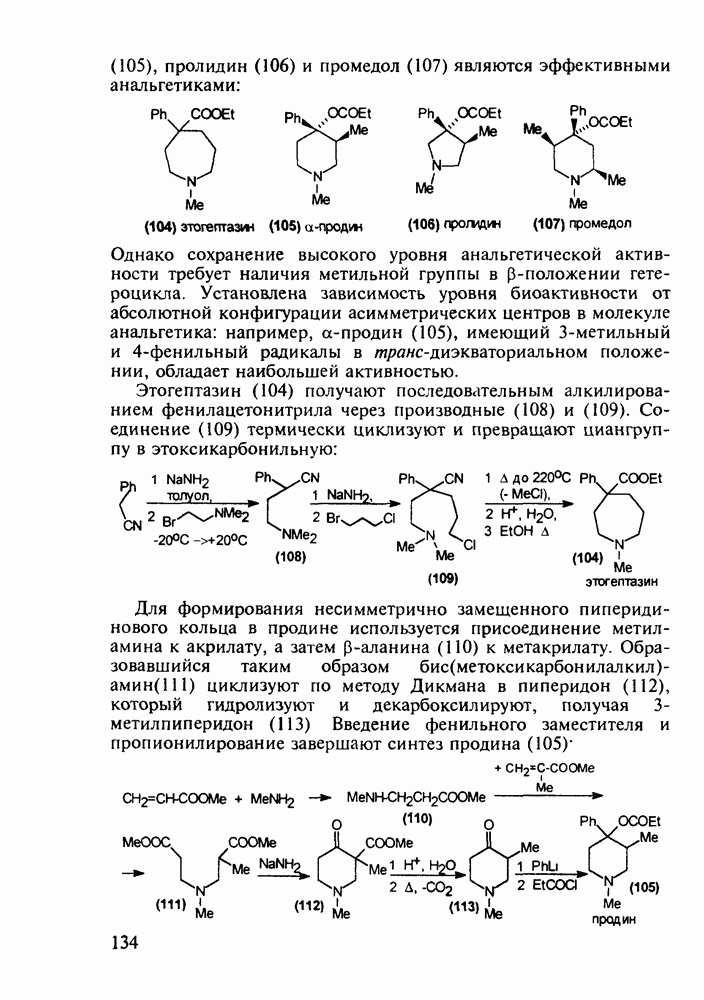
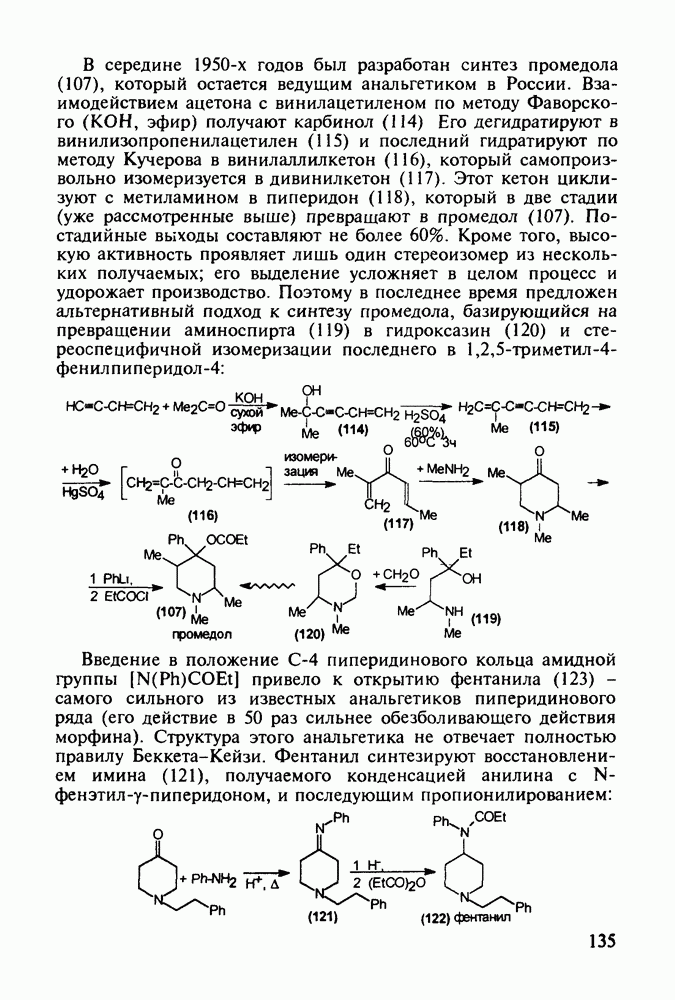
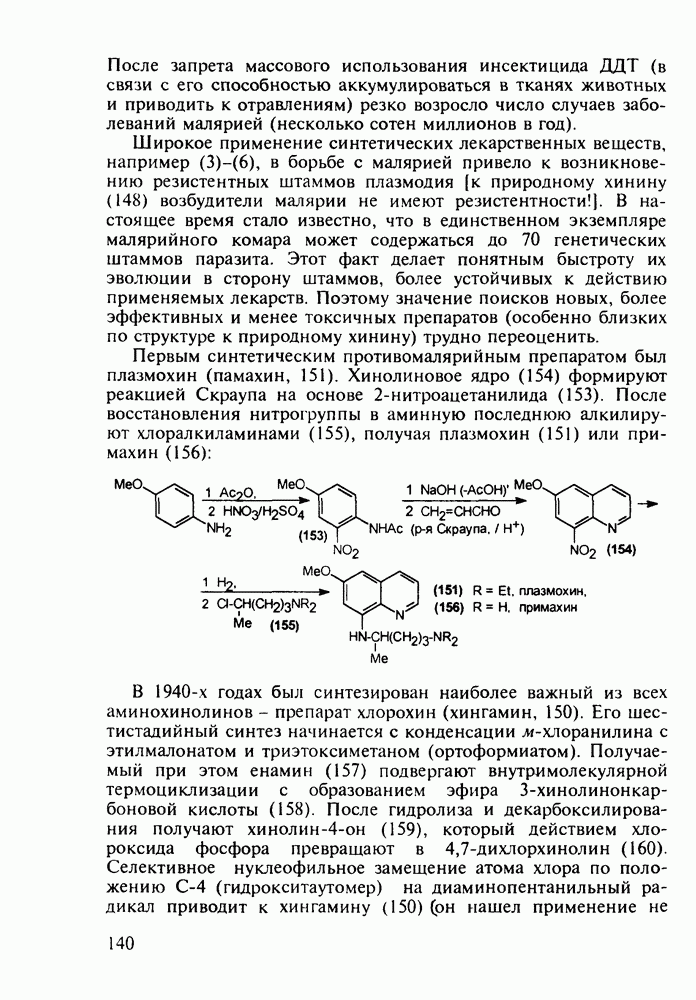
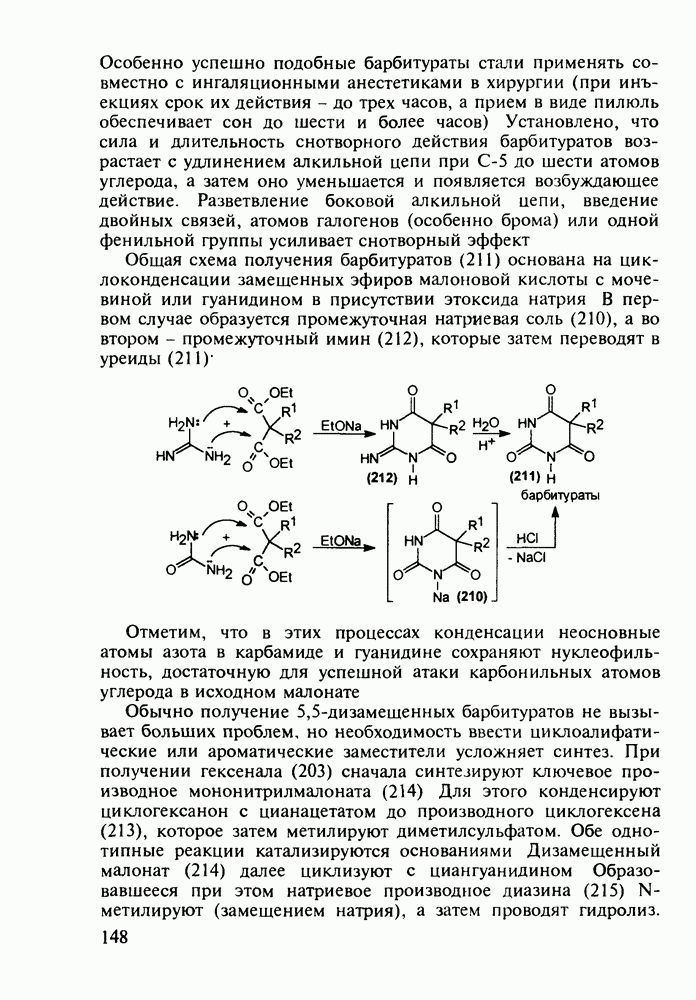
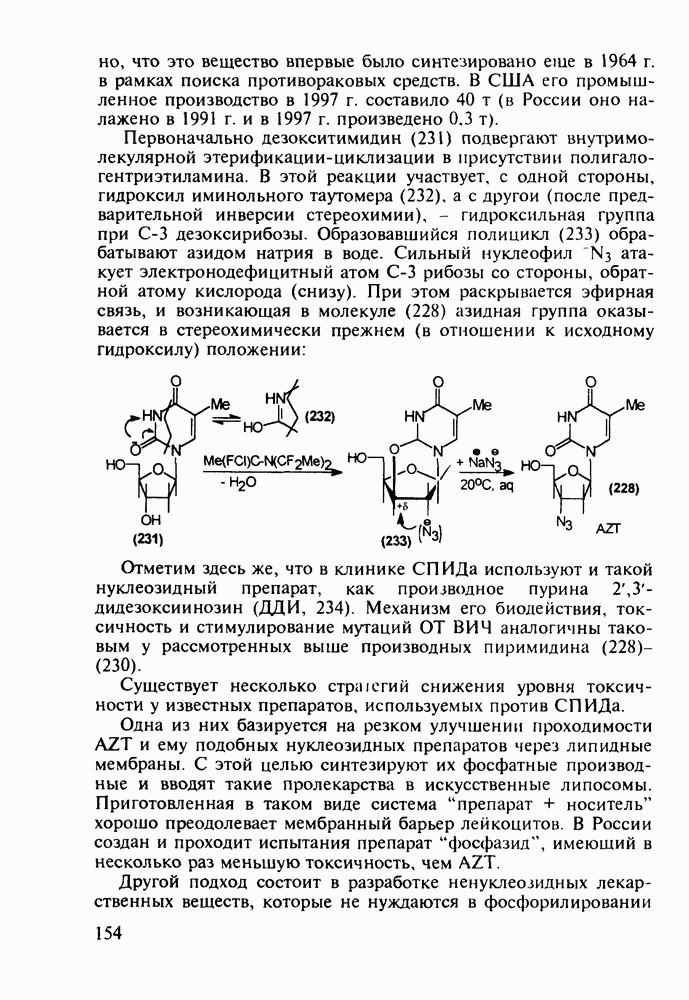
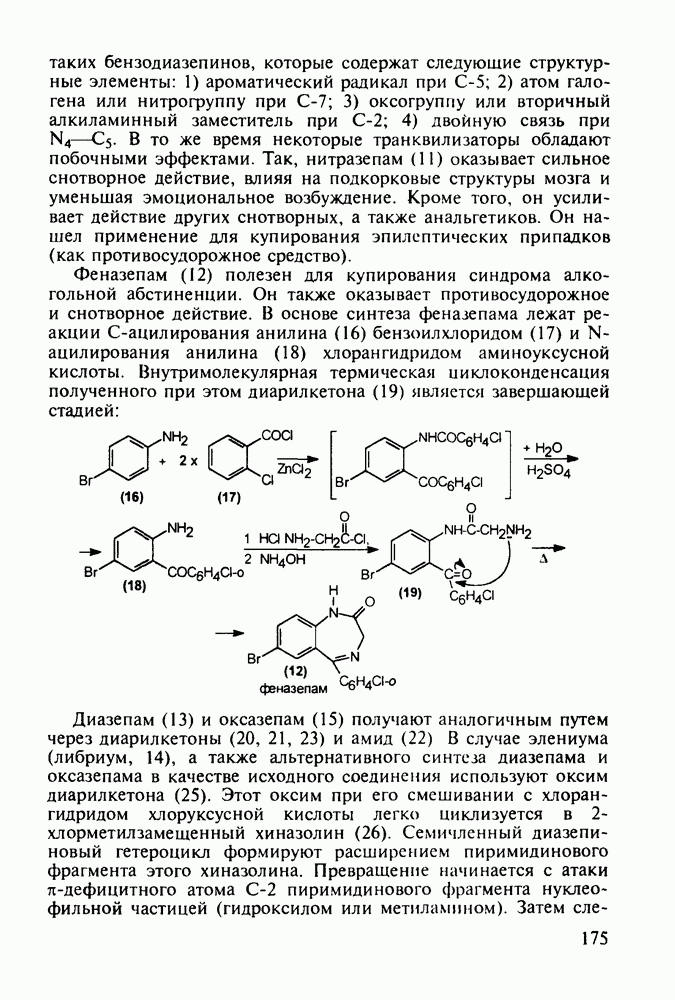
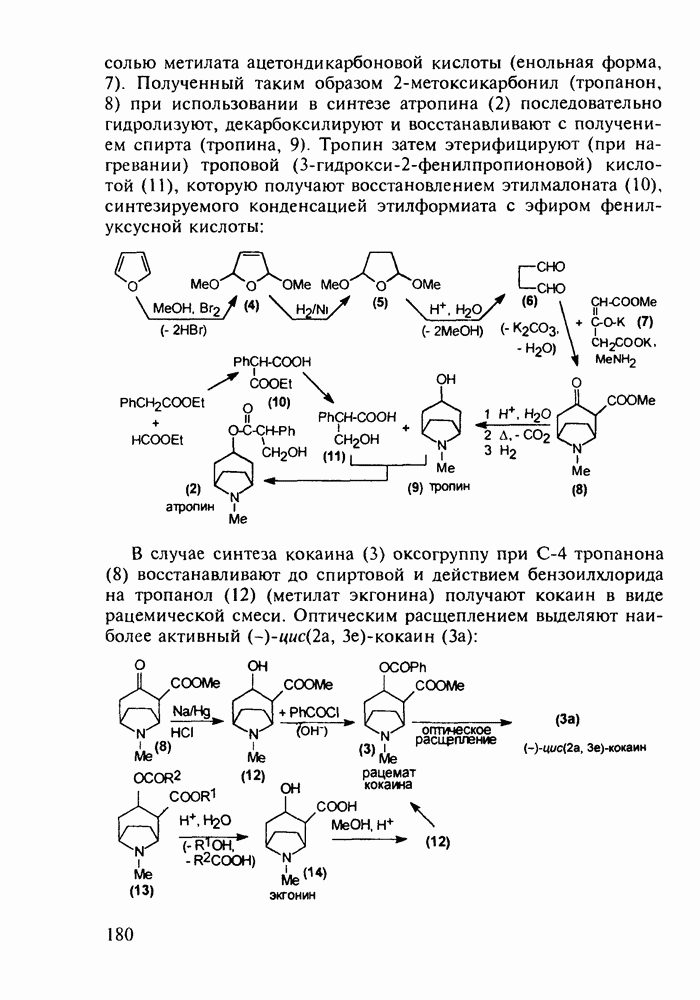
Метионин (4) (2-амино-4-метилтиобутановая кислота) используют в медицине для лечения и профилактики токсических поражений печени и при диабете. Его получают синтетически, исходя из акролеина и тиометанола. Реакция присоединения тиометанола по  -связи акролеина дает метилтиопропаналь (1). Последний по реакции Штреккера легко цианируется по карбонильной группе с образованием циангидрина (2), в котором затем аммиак нуклеофильно замещает ОН-группу. На следующей стадии образовавшийся таким образом геминальный аминонитрил (3) гидролизуют в щелочной среде до рацемического метионина (4). Его активную
-связи акролеина дает метилтиопропаналь (1). Последний по реакции Штреккера легко цианируется по карбонильной группе с образованием циангидрина (2), в котором затем аммиак нуклеофильно замещает ОН-группу. На следующей стадии образовавшийся таким образом геминальный аминонитрил (3) гидролизуют в щелочной среде до рацемического метионина (4). Его активную  -форму выделяют ферментативным
-форму выделяют ферментативным
путем или раскристаллизацией с оптически активными соединениями:

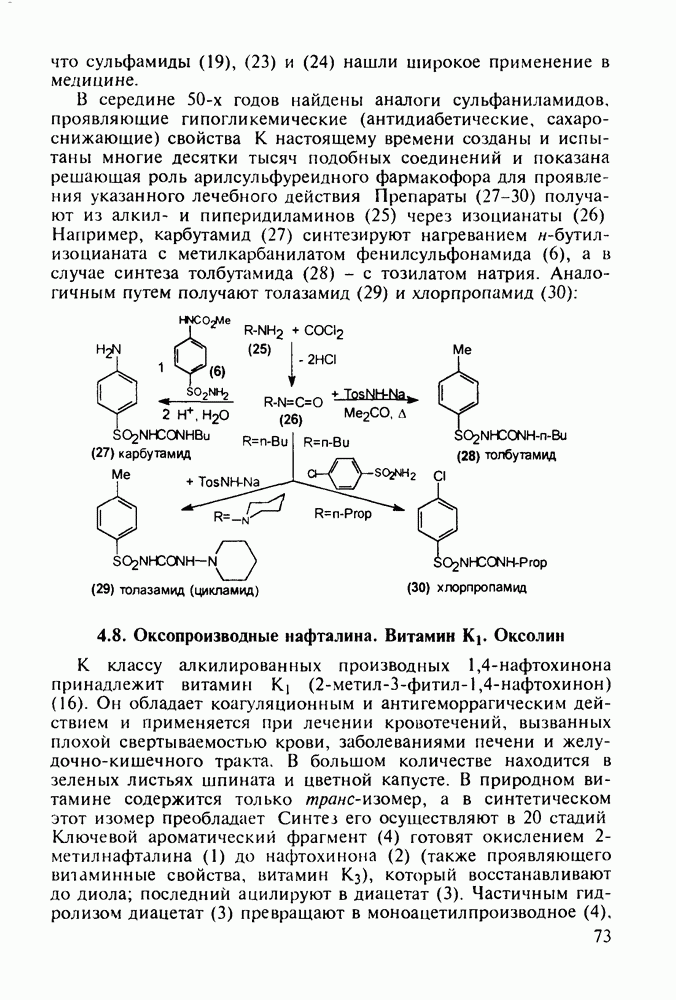
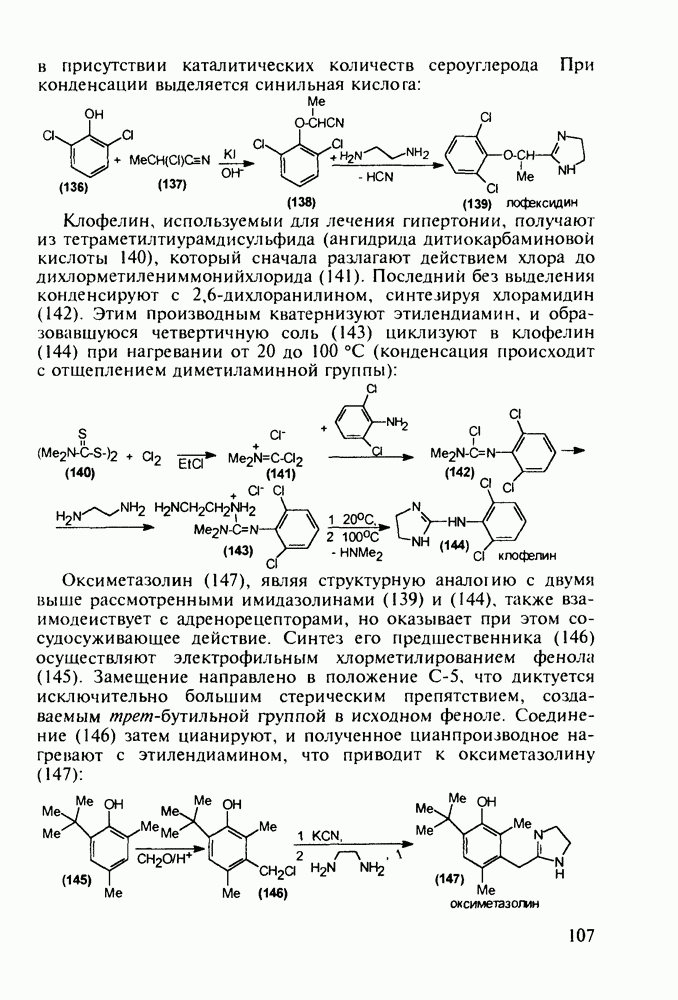
Природный метилметионинсульфонийхлорид (5) называют витамином U. Им богаты капуста, томаты и петрушка. Он рекомендуется для лечения язвы желудка. Этот витамин играет в биопроцессах роль донора метальных групп. В производстве его получают хлорметилированием L-метионина (4):

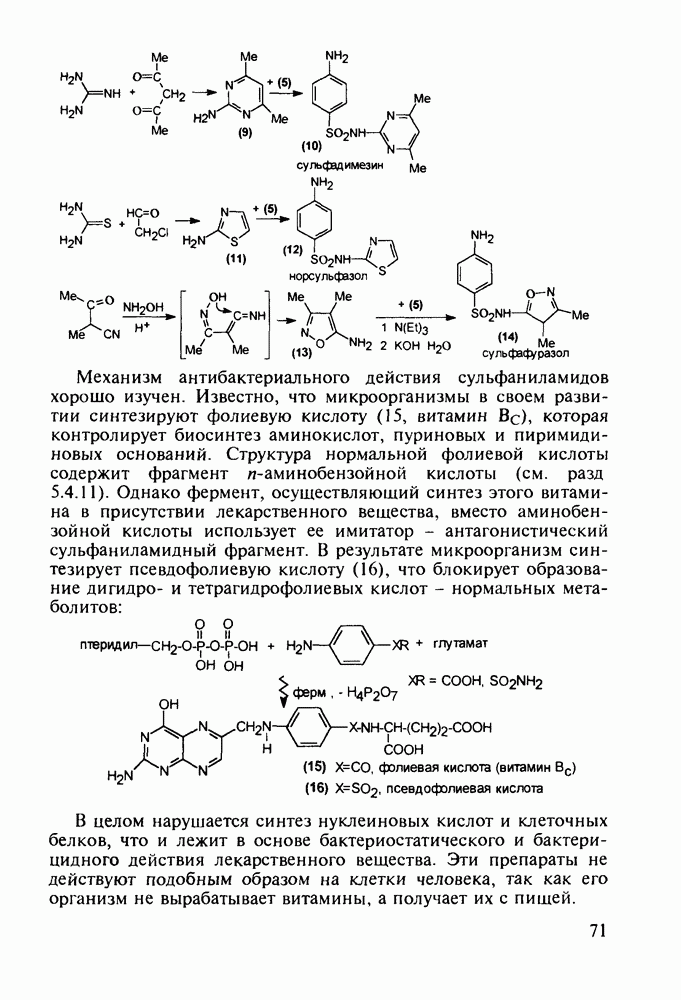
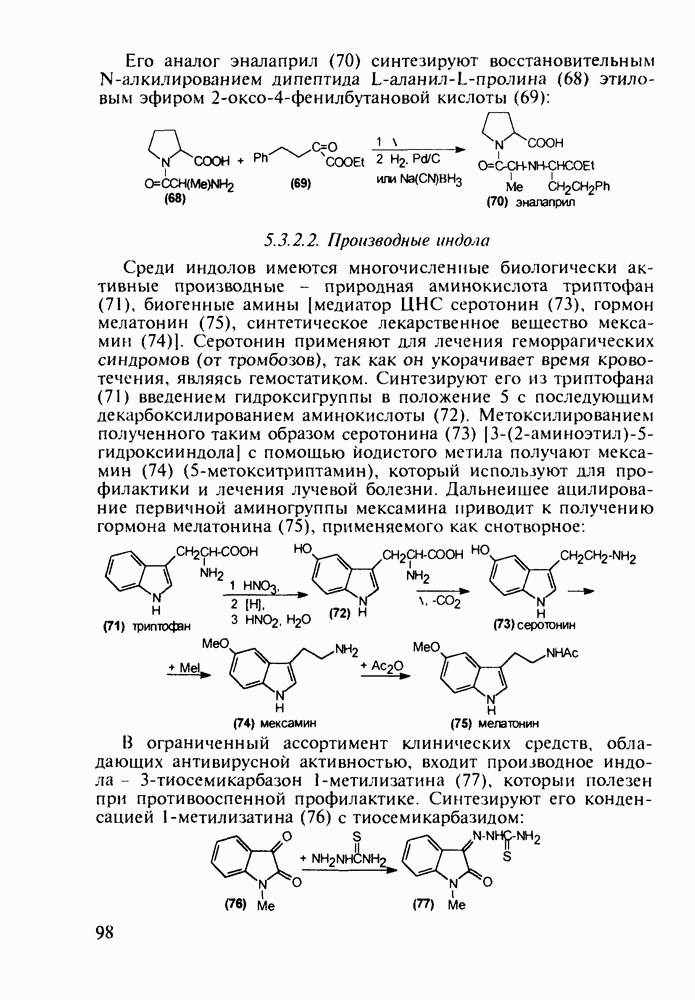
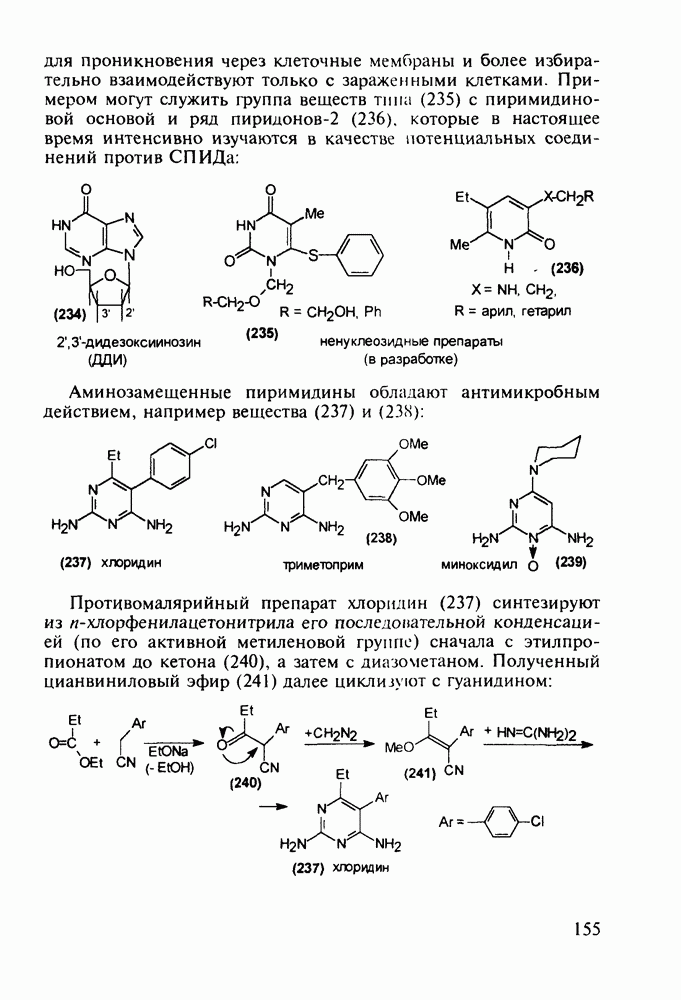
Триптофан (8) (аминокислота с гетероароматическим - индольным - заместителем) используется для лечебного питания. На первой стадии его синтеза проводят аминометилирование индола по методу Манниха. Полученный при этом 3-амино-метилиндол (6) конденсируют затем с эфиром нитроуксусной кислоты. В ходе реакции метиленовая группа этого эфира отщепляет протон (как СН-кислота), и образовавшийся карбанион легко вытесняет диметиламиногруппу в индоле (6), что приводит к метилату 3-индолилнитропропионовой кислоты (7). Далее восстанавливают нитрогруппу до аминной и после щелочного гидролиза получают триптофан (8) или его натриевую соль:

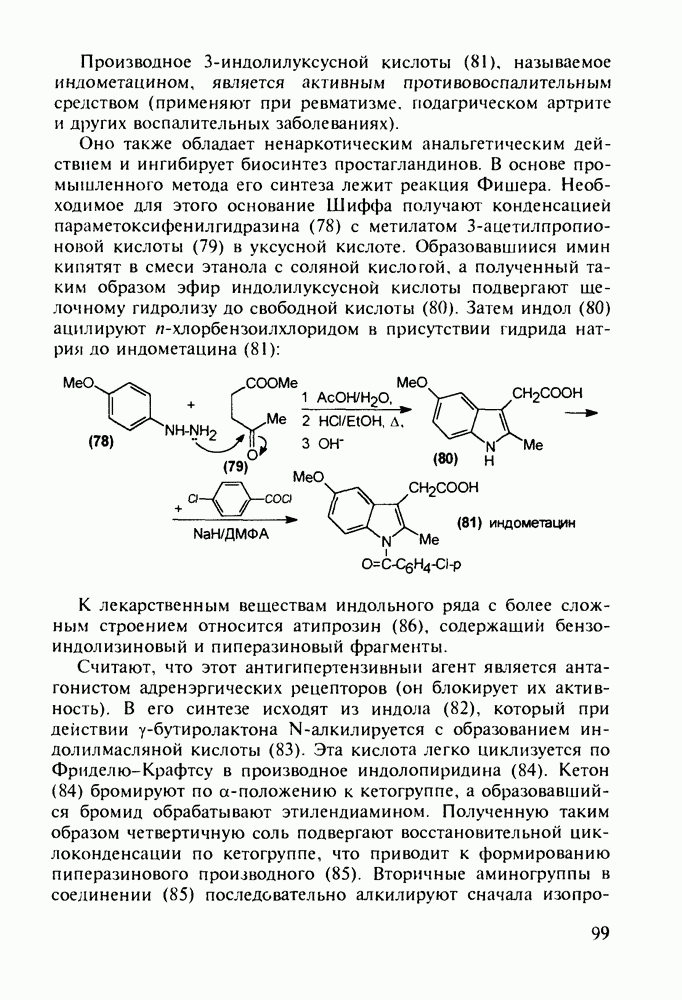
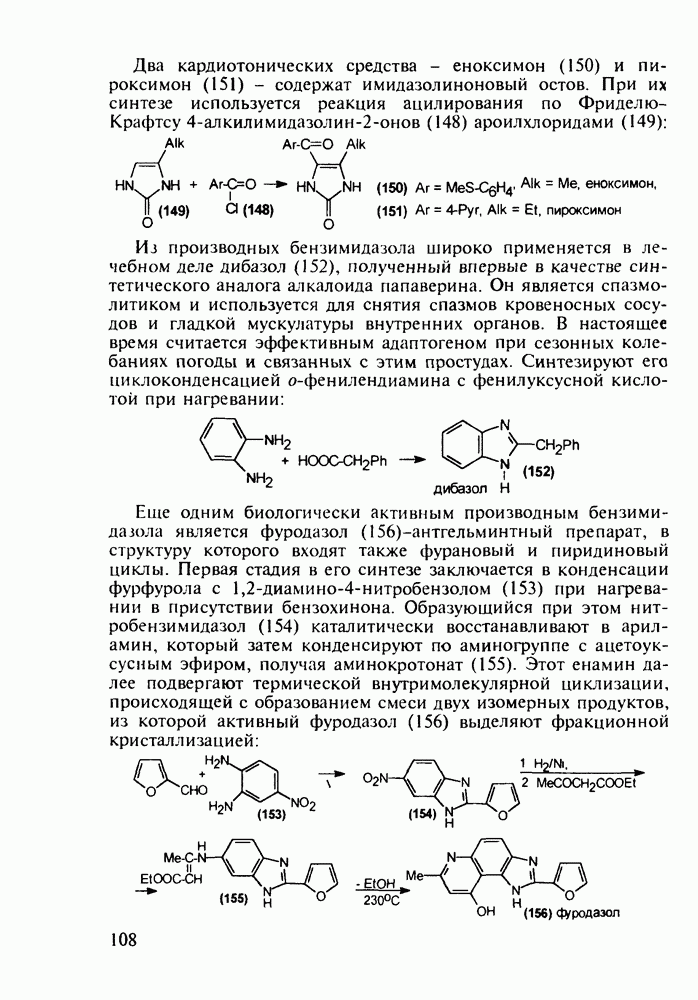
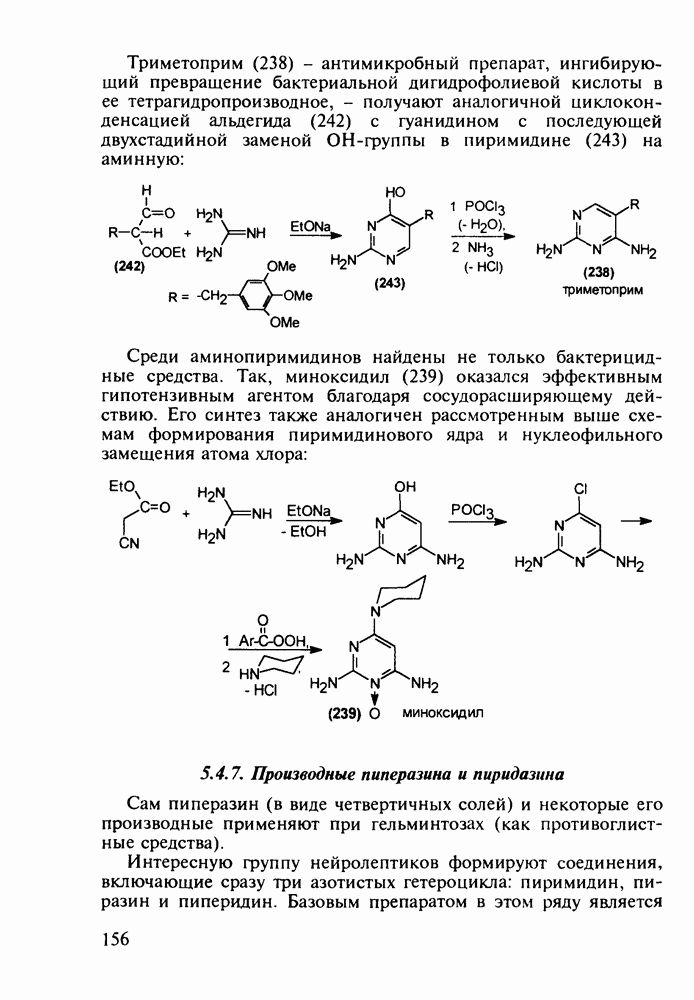
Глутаминовая кислота (11) (2-амино-1,5-пентандиовая кислота) находит применение при лечении заболеваний ЦНС (эпилепсии, психозов; у детей - при полиомиелите и задержке
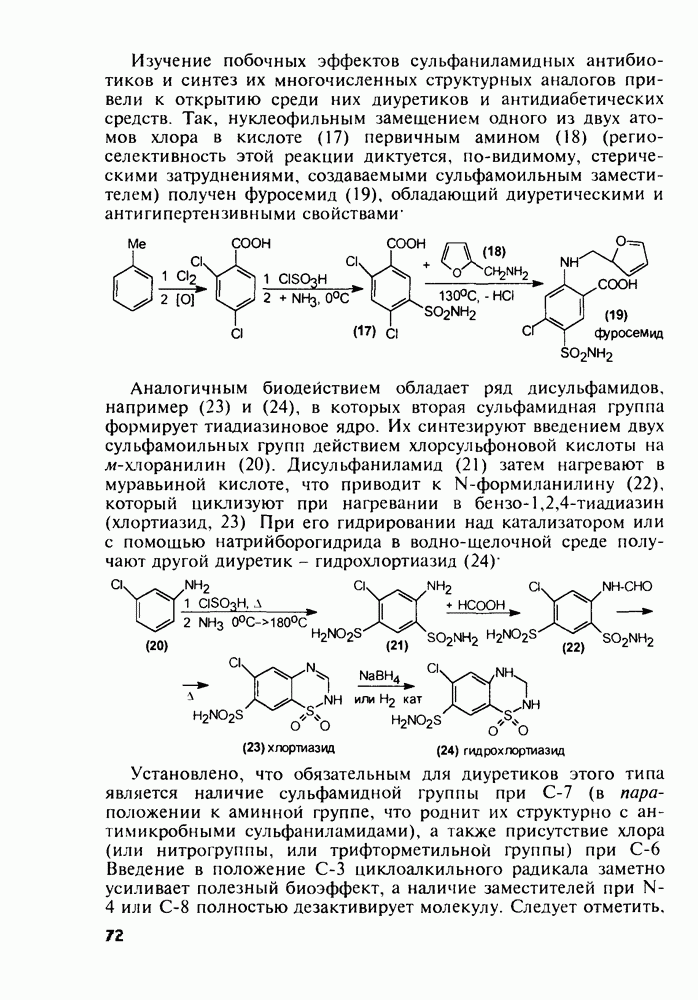
психического развития). Ее натриевая соль используется как вкусовая и консервирующая добавка в пищевые продукты. Глутаминовую кислоту (11) синтезируют на основе акрилонитрила, который гидрокарбонилируют в присутствии катализаторов (триарилфосфинкарбонилы кобальта или рения) до нитрилальдегида (9). Последний превращают по методу Штреккера в аминодинитрил глутаровой кислоты (10), который затем омыляют в присутствии щелочи при 100 °С в  -динатрийглутамат. Расщепление рацемата на индивидуальные энантиомеры осуществляют кристаллизацией его раствора в присутствии
-динатрийглутамат. Расщепление рацемата на индивидуальные энантиомеры осуществляют кристаллизацией его раствора в присутствии  -глутаминовой кислоты (
-глутаминовой кислоты ( -форма соли при этом выпадает в осадок):
-форма соли при этом выпадает в осадок):
 (9)
(9)
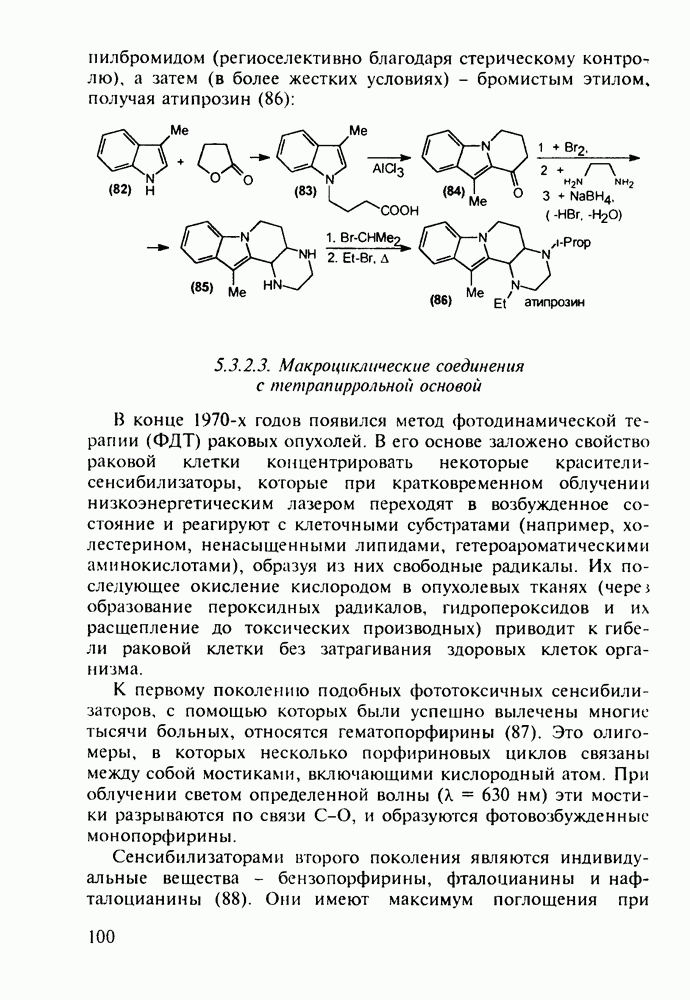
В 1999 г. был открыт необычный нейромедиатор -  -серин,
-серин,  Оказалось, что эта правосторонняя а-аминокислота вырабатывается в организме человека из левосторонних а-аминокислот (из их
Оказалось, что эта правосторонняя а-аминокислота вырабатывается в организме человека из левосторонних а-аминокислот (из их  -форм). Еще одна неожиданность заключалась в том, что биосинтез
-форм). Еще одна неожиданность заключалась в том, что биосинтез  -серина осуществляется не в самих нейронах, а в астроцитах - клетках, покрывающих нейроны. Из астроцита этот нейромедиатор затем диффундирует в нервную клетку и взаимодействует со специальными рецепторами. Начинается разработка лекарственных веществ, регулирующих активность фермента, контролирующего синтез
-серина осуществляется не в самих нейронах, а в астроцитах - клетках, покрывающих нейроны. Из астроцита этот нейромедиатор затем диффундирует в нервную клетку и взаимодействует со специальными рецепторами. Начинается разработка лекарственных веществ, регулирующих активность фермента, контролирующего синтез  -серина. Эти лекарства, как ожидается, могут оказаться полезными при инсультах, гипертонических кризах и помогут защищать нейроны от необратимых повреждений.
-серина. Эти лекарства, как ожидается, могут оказаться полезными при инсультах, гипертонических кризах и помогут защищать нейроны от необратимых повреждений.
Ряд олигомеров а-аминокислот играет значительную роль в жизнедеятельности организма и некоторые из них применяют в медицинской практике. Так, метиловый эфир дипептида  -аспарагил-
-аспарагил- -фенилаланина (аспартат, аспартам) используют при диабете как малокалорийный заменитель сахара (в 150 раз слаще глюкозы). Его производят синтетическим или микробиологическим путем конденсацией аспарагина и метилата фенилаланина:
-фенилаланина (аспартат, аспартам) используют при диабете как малокалорийный заменитель сахара (в 150 раз слаще глюкозы). Его производят синтетическим или микробиологическим путем конденсацией аспарагина и метилата фенилаланина:

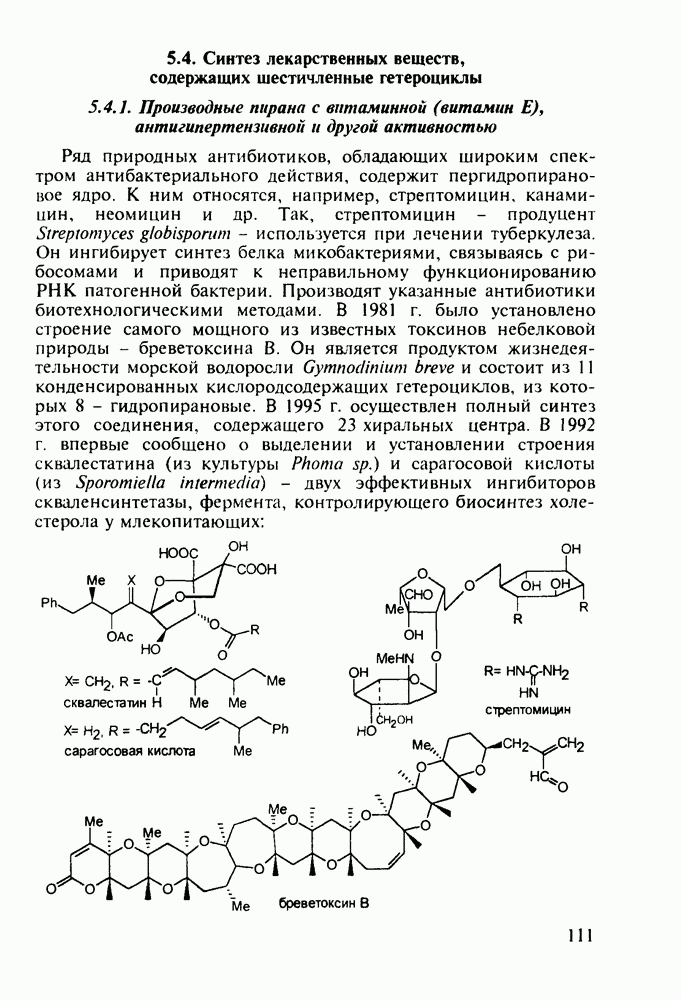
Природный антибиотик грамицидин S, продуцируемый споровой палочкой (Bacillus brevis), представляет собой циклический декапептид: 
Он обладает бактериостатическим и бактерицидным действием и применяется для лечения ран, ожогов, воспалительных заболеваний, а также в качестве противозачаточного средства. Этот антибактериальный пептид интересен также тем, что в его составе фенилаланин имеет  -форму. В последнее время было выделено несколько небольших природных пептидов (из кожи древесных лягушек, ганглий улиток, яда пауков), которые содержат одну или две
-форму. В последнее время было выделено несколько небольших природных пептидов (из кожи древесных лягушек, ганглий улиток, яда пауков), которые содержат одну или две  -аминокислоты. Было подтверждено, что
-аминокислоты. Было подтверждено, что  -форма аминокислотного остатка в такого рода пептидах резко увеличивает их устойчивость к гидролитическому действию экзо- и эндопротеаз. Этот факт учитывается при создании олигопептидных лекарственных веществ пролонгированного действия.
-форма аминокислотного остатка в такого рода пептидах резко увеличивает их устойчивость к гидролитическому действию экзо- и эндопротеаз. Этот факт учитывается при создании олигопептидных лекарственных веществ пролонгированного действия.
За последние 25 лет выделены и охарактеризованы многообразные эндогенные пептиды человеческого организма: пептиды сна, нейропептиды и пептидные гормоны. Так, сон вызывается нонапептидом  . Подобные пептиды оказались очень лабильны и пока их трудно использовать в качестве снотворных лекарственных веществ. Энкефалины и эндорфины являются природными опиоидными пептидами, обладающими мощным агонистическим действием на опиатные рецепторы (нейропептиды):
. Подобные пептиды оказались очень лабильны и пока их трудно использовать в качестве снотворных лекарственных веществ. Энкефалины и эндорфины являются природными опиоидными пептидами, обладающими мощным агонистическим действием на опиатные рецепторы (нейропептиды):

Некоторые пептиды обладают гормональным действием. Эти гормоны синтезируются в разных органах - гипоталамусе, гипофизе, поджелудочной железе, плазме крови. Пептидные гормоны, как и все гормоны, выполняют роль регуляторов активности органов и клеток, служа в основном для изменения скорости синтеза ферментов, биокатализа и проницаемости биомембран. Их синтез железами внутренней секреции и выброс в кровь находится под контролем нервной системы. Инсулин представляет собой димер, в котором унэйкозапептид связан с трикозапептидом двумя дисульфидными мостиками. Он вырабатывается у человека поджелудочной железой и служит регулятором уровня

Рис. 4 Схема образования ангиотензинов и внутриклеточного вторичного сигнала (ц-АМФ) Указаны места возможного действия лнтигипсртензивных лекарственных веществ Обозначения АТГ - ангиотензиноген,  - ангиотензин I, AT-II - ангиотензин II, АТФ - аденозинтрифосфат,
- ангиотензин I, AT-II - ангиотензин II, АТФ - аденозинтрифосфат,  -АМФ - циклоаденозинмонофосфат,
-АМФ - циклоаденозинмонофосфат,  лекарственное иешество
лекарственное иешество
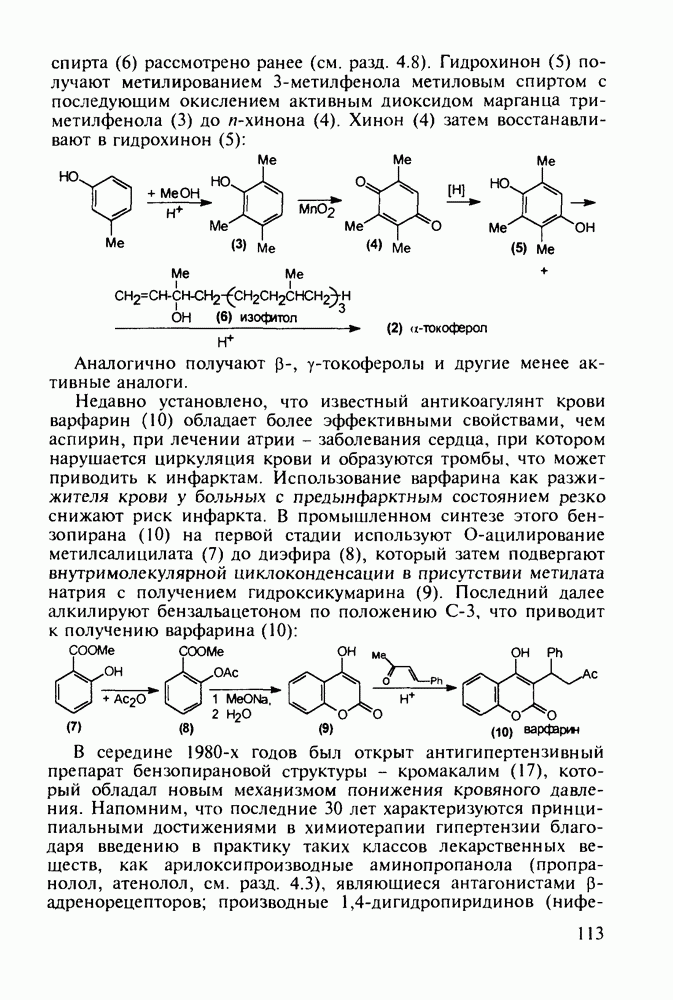
глюкозы в крови. Его применяют против сахарного диабета. Важнейшими регуляторами кровяного давления являются гормональные окта- и декапептиды, названные ангиотензинами II и I (они повышают давление крови):

а также нонапептиды брадикинин (понижает давление) и вазопрессин (повышает давление и является, кроме того, антидиуретиком).
Почки обладают эндокринной функцией и выделяют в кровь протеолитический фермент ренин, который превращает один из белков плазмы крови (ангиотензиноген) в декапептид ангиотензин I (рис. 4). От последнего затем ферментативно удаляется  -концевой дипептид, что приводит к образованию более активного ангиотензина II.
-концевой дипептид, что приводит к образованию более активного ангиотензина II.
Поскольку пептидные гормоны не проникают в клетку, они передают заключенную в них сигнальную информацию внутрь клетки посредством связывания с рецептором (хеморецептором или ионным каналом), представляющим собой совокупность белковых или небелковых молекул.
В данном случае ангиотензин II образует с хеморецептором ( -белок) комплекс, который активирует (через внутриклеточный
-белок) комплекс, который активирует (через внутриклеточный
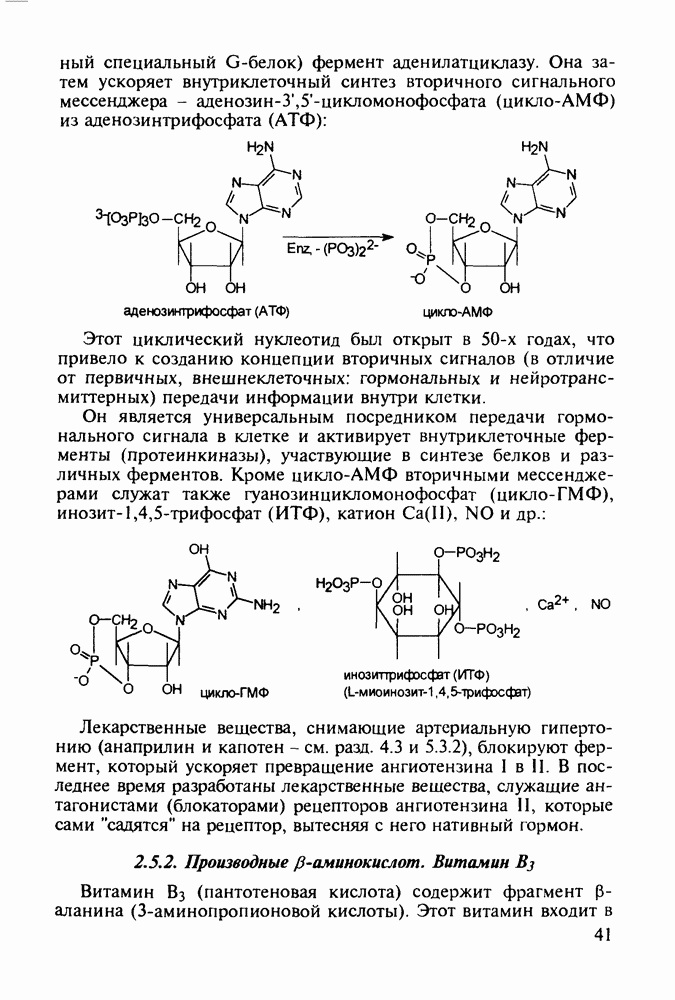
специальный G-белок) фермент аденилатциклазу. Она затем ускоряет внутриклеточный синтез вторичного сигнального мессенджера  из аденозинтрифосфата (АТФ):
из аденозинтрифосфата (АТФ):

Этот циклический нуклеотид был открыт в 50-х годах, что привело к созданию концепции вторичных сигналов (в отличие от первичных, внешнеклеточных: гормональных и нейротранс-миттерных) передачи информации внутри клетки.
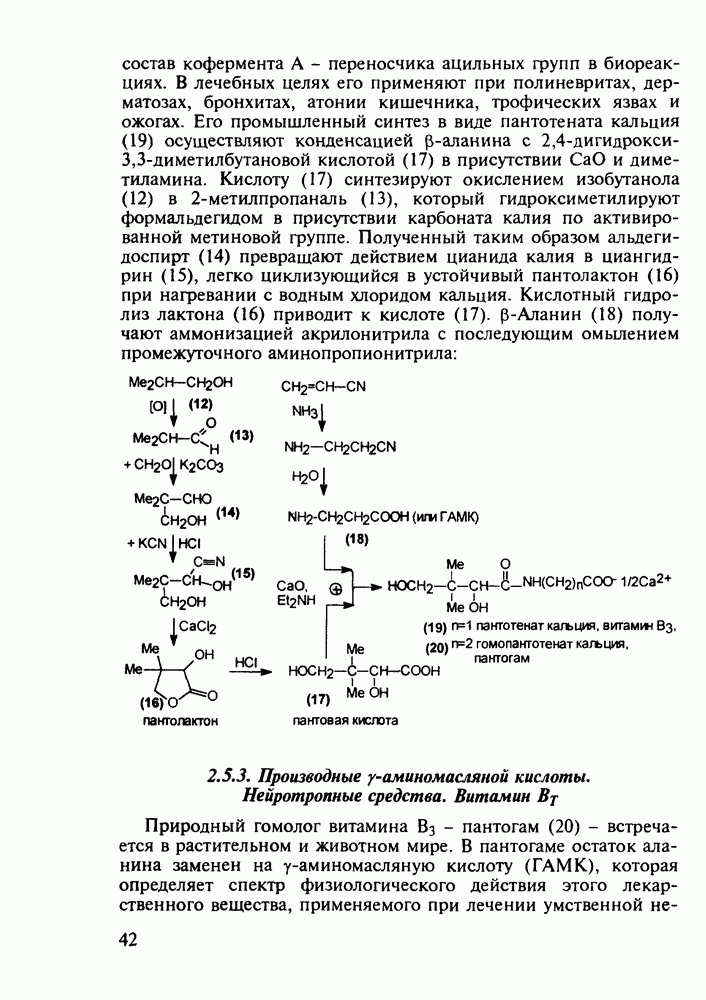
Он является универсальным посредником передачи гормонального сигнала в клетке и активирует внутриклеточные ферменты (протеинкиназы), участвующие в синтезе белков и различных ферментов. Кроме цикло-АМФ вторичными мессенджерами служат также гуанозинцикломонофосфат (цикло-ГМФ), инозит-1,4,5-трифосфат (ИТФ), катион  и др.:
и др.:

Лекарственные вещества, снимающие артериальную гипертонию (анаприлин и капотен - см. разд. 4.3 и 5.3.2), блокируют фермент, который ускоряет превращение ангиотензина I в II. В последнее время разработаны лекарственные вещества, служащие антагонистами (блокаторами) рецепторов ангиотензина II, которые сами "садятся" на рецептор, вытесняя с него нативный гормон.
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие
- 1. ВВЕДЕНИЕ
- 1.1. Эволюция органической химии лекарственных веществ
- 1.2. Современные требования к лекарственным веществам
- 1.3. Стадии биологического изучения лекарственного вещества
- 1.4. Основы стратегии создания новых синтетических лекарственных веществ
- 1.5. Связь структура-биологическая активность
- 1.6. Принципиальная схема разработки нового лекарственного вещества
- 1.7. Классификация лекарственных веществ
- 1.8. Основные болезни человека и ведущие группы лекарственных веществ на современном фармацевтическом рынке
- 2. СИНТЕЗ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ АЛИФАТИЧЕСКОГО РЯДА
- 2.2. Группа противораковых веществ с дихлордиэтиламинным фармакофором
- 2.3. Алканолы, аминоалканолы и их эфиры. Нейромедиатор ацетилхолин и холиномиметики
- 2.4. Альдегиды и кислоты. Витамины F и B15
- 2.5. Аминокислоты
- 2.5.2. Производные b-аминокислот. Витамин B3
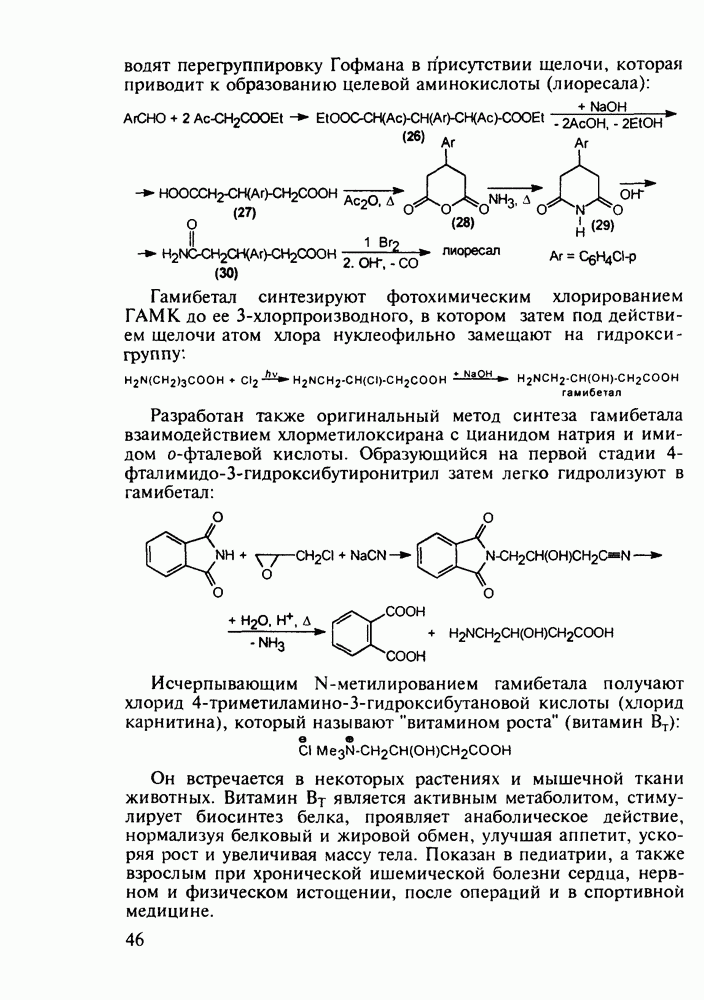
- 2.5.3. Производные у-аминомасляной кислоты. Нейротропные средства. Витамин BT
- 2.5.4. Другие аминокислоты
- 3. ЛЕКАРСТВЕННЫЕ ВЕЩЕСТВА АЛИЦИКЛИЧЕСКОГО РЯДА
- 3.2. Противозачаточные и противовоспалительные вещества на основе циклопентафенантрена. Синтез витамина D
- 3.3. Камфора. Производные адамантана в качестве антивирусных средств
- 4. СИНТЕЗ ПРОИЗВОДНЫХ АРОМАТИЧЕСКОГО РЯДА
- 4.2. Антигистаминные препараты группы диарилметана
- 4.3. Антисептики и адреноблокаторы фенольного ряда
- 4.4. Аминофенолы в качестве обезболивающих и противотуберкулезных средств
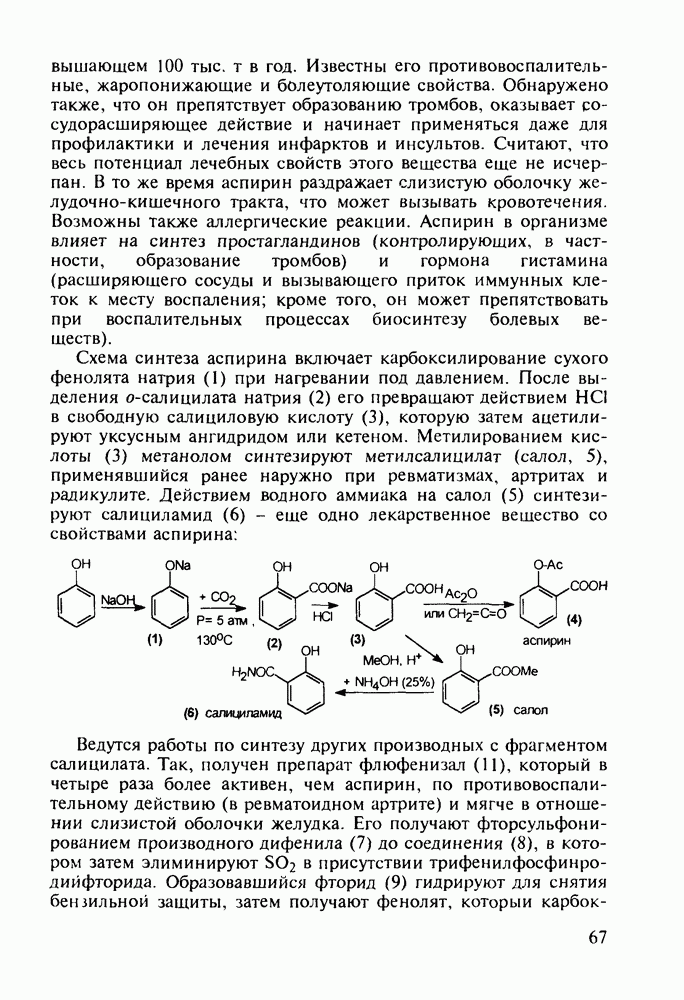
- 4.5. Производные о-гидроксибензойной кислоты. Аспирин
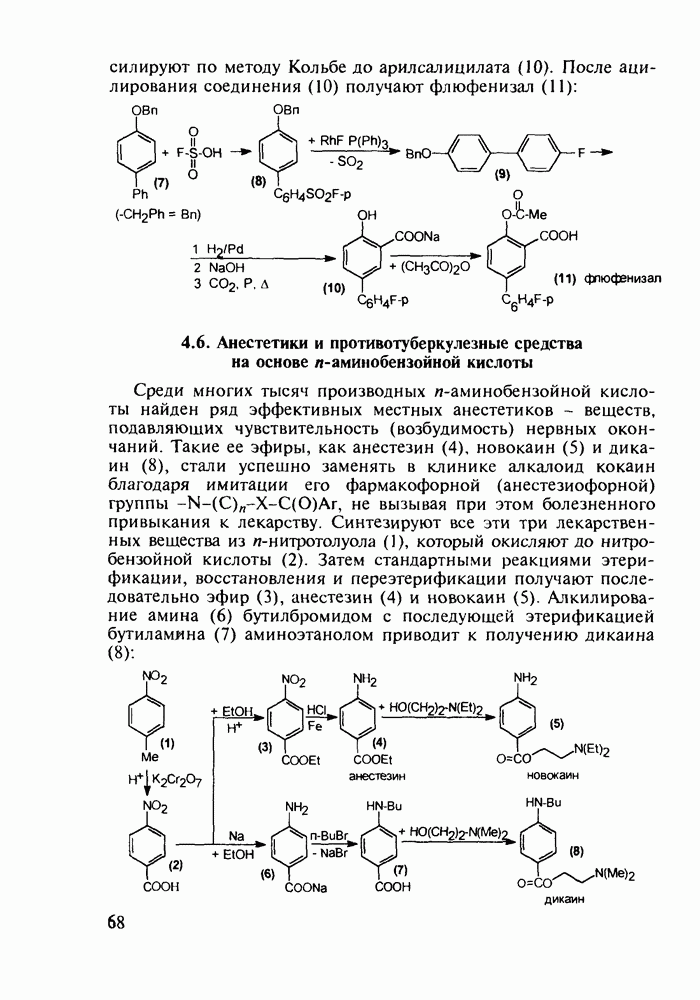
- 4.6. Анестетики и противотуберкулезные средства на основе n-аминобензойной кислоты
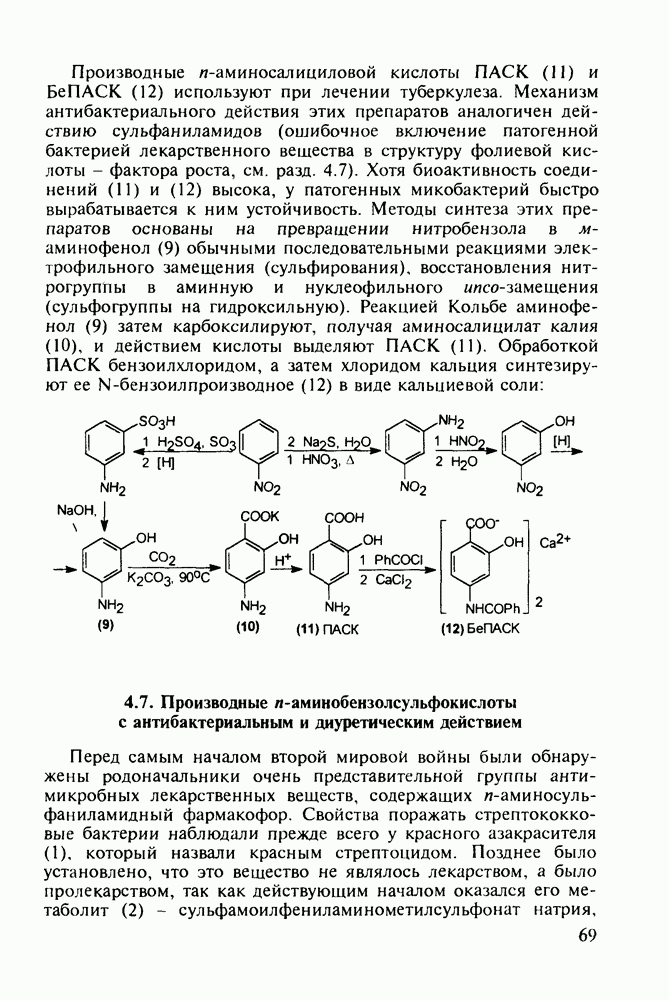
- 4.7. Производные n-аминобензолсульфокислоты с антибактериальным и диуретическим действием
- 4.8. Оксопроизводные нафталина. Витамин К1. Оксолин
- 5. ХИМИЯ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ С БАЗОВЫМ ГЕТЕРОЦИКЛИЧЕСКИМ ФРАГМЕНТОМ
- 5.2. Антибиотики, содержащие четырехчленное азетидиновое ядро
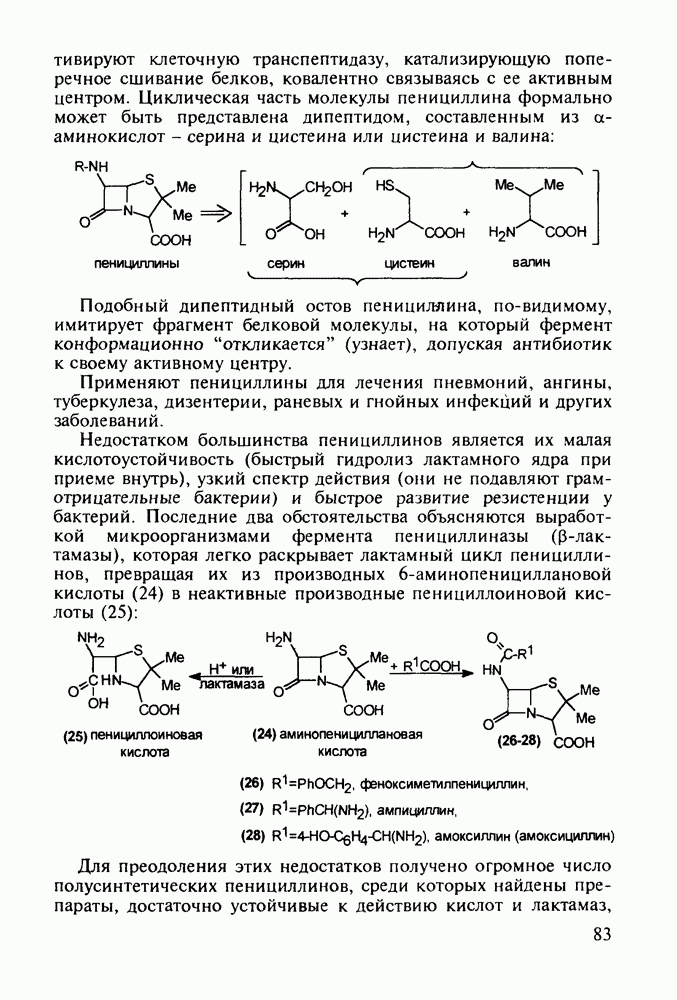
- 5.2.2. Пенициллины. Моксалактам
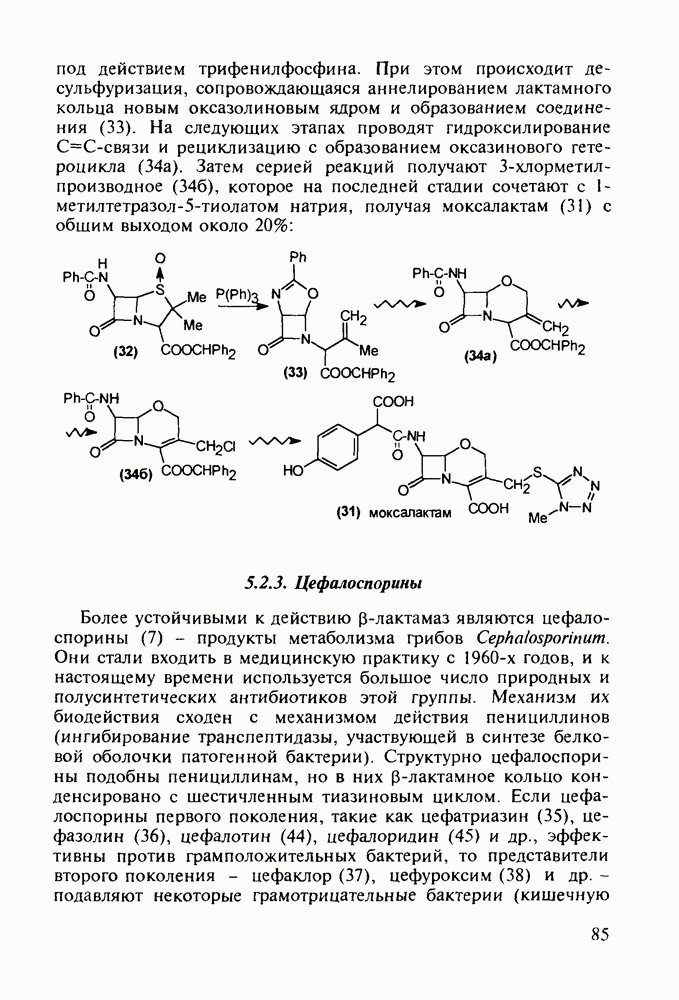
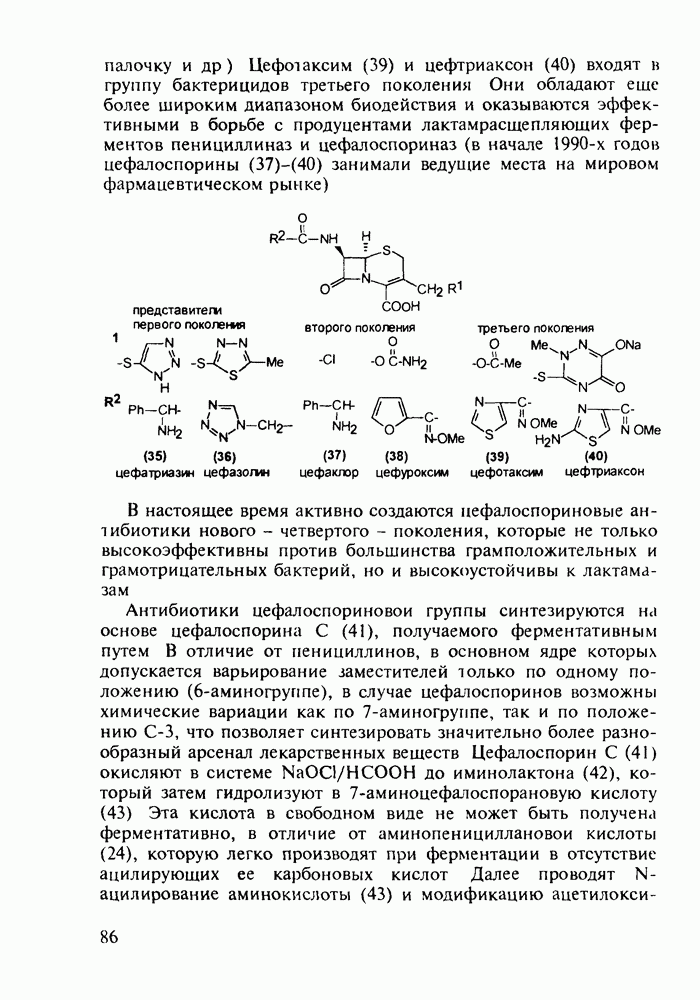
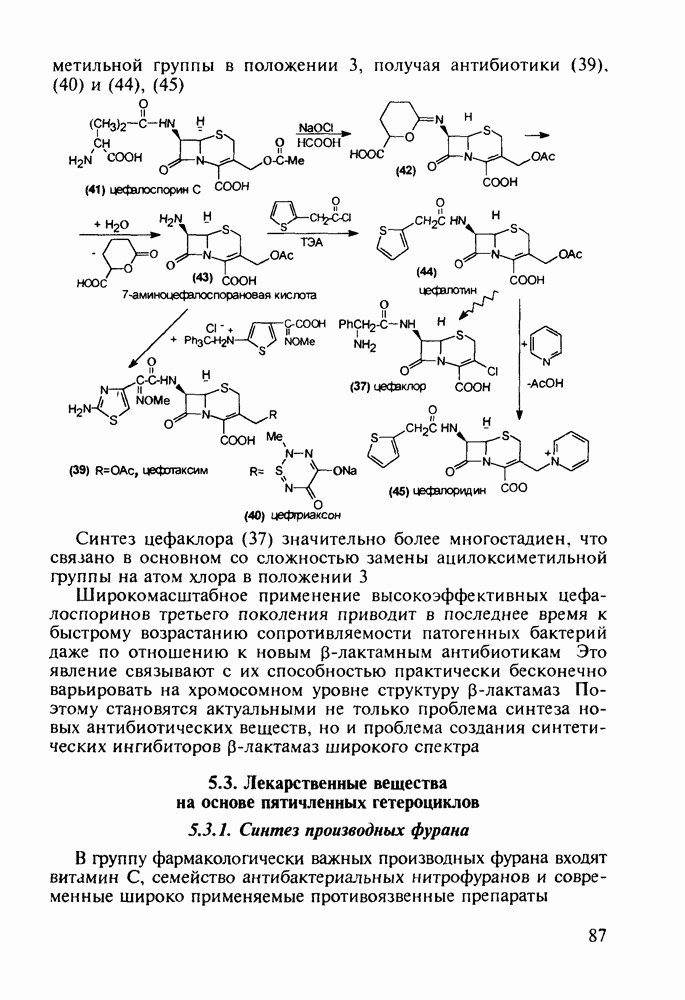
- 5.2.3. Цефалоспорины
- 5.3. Лекарственные вещества на основе пятичленных гетероциклов
- 5.3.2. Синтез производных пиррола
- 5.3.3. Оксазолидины. Антибиотик циклосерин
- 5.3.4. Антипиретики и анальгетики пиразолинового ряда
- 5.3.5. Имидазолы с противопаразитарной, антигипертензивной и другой биоактивностью
- 5.3.6. Производные тиазола. Витамин В1
- 5.3.7. Психостимуляторы с оксадиазольным и тетразольным гетероциклами
- 5.4. Синтез лекарственных веществ, содержащих шестичленные гетероциклы
- 5.4.2. Синтез лекарственных веществ пиридинового ряда
- 5.4.3. Анальгетики и транквилизаторы пиперидинового ряда
- 5.4.4. Производные хинолина с антималярийным и антибактериальным действием
- 5.4.5. Изохинолины в качестве спазмолитиков и трипаноцидов
- 5.4.6. Производные пиримидинов
- 5.4.7. Производные пиперазина и пиридазина
- 5.4.8. Бензотиазины. Нейролептики фенотиазинового ряда
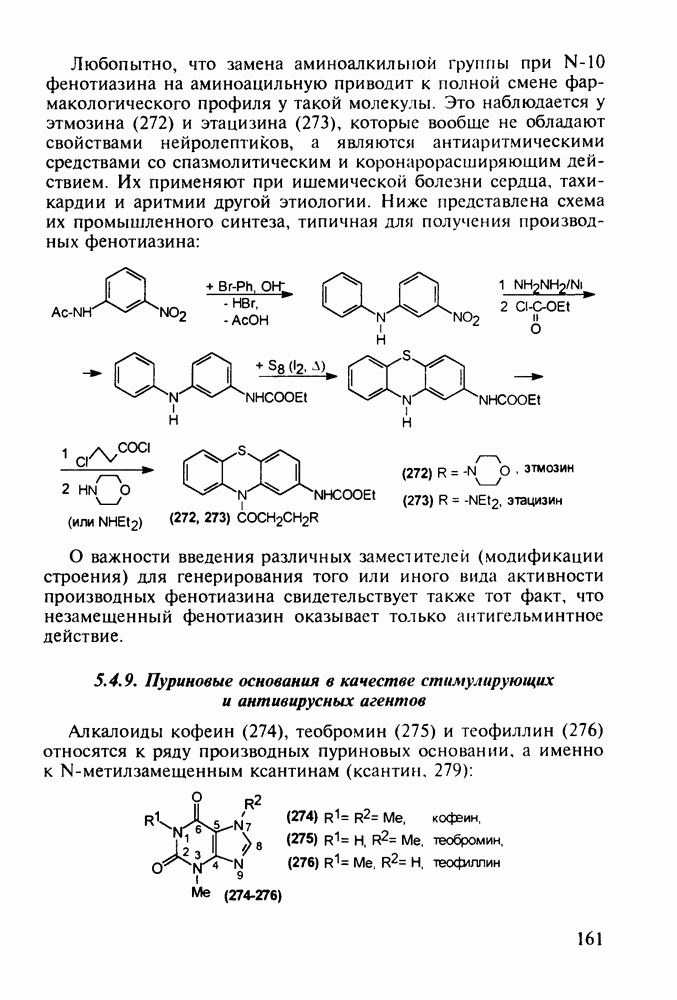
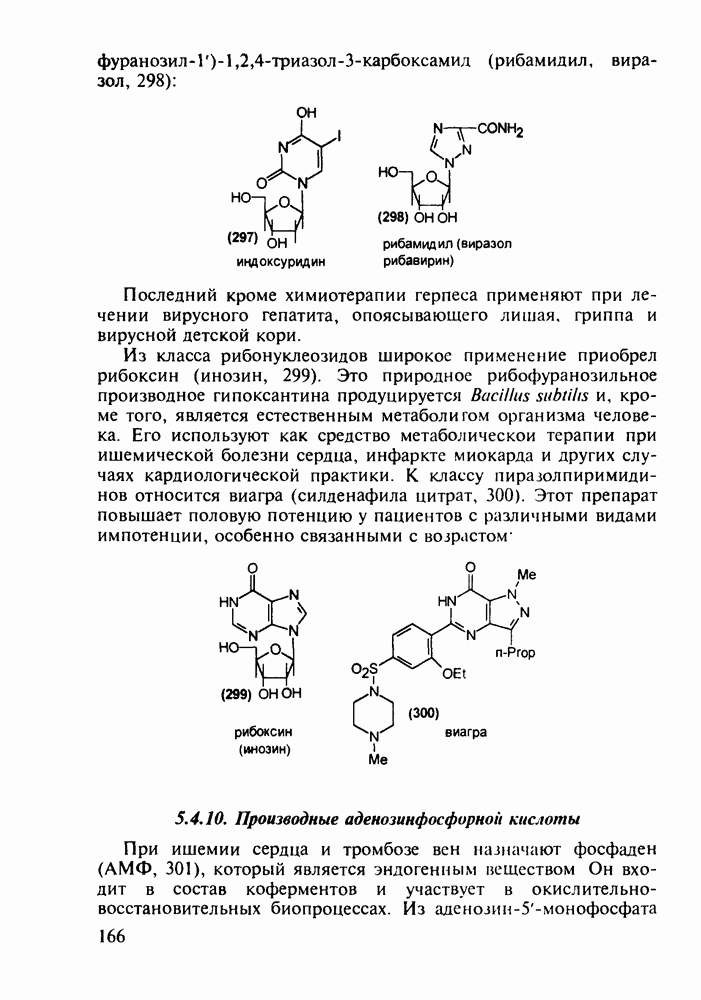
- 5.4.9. Пуриновые основания в качестве стимулирующих и антивирусных агентов
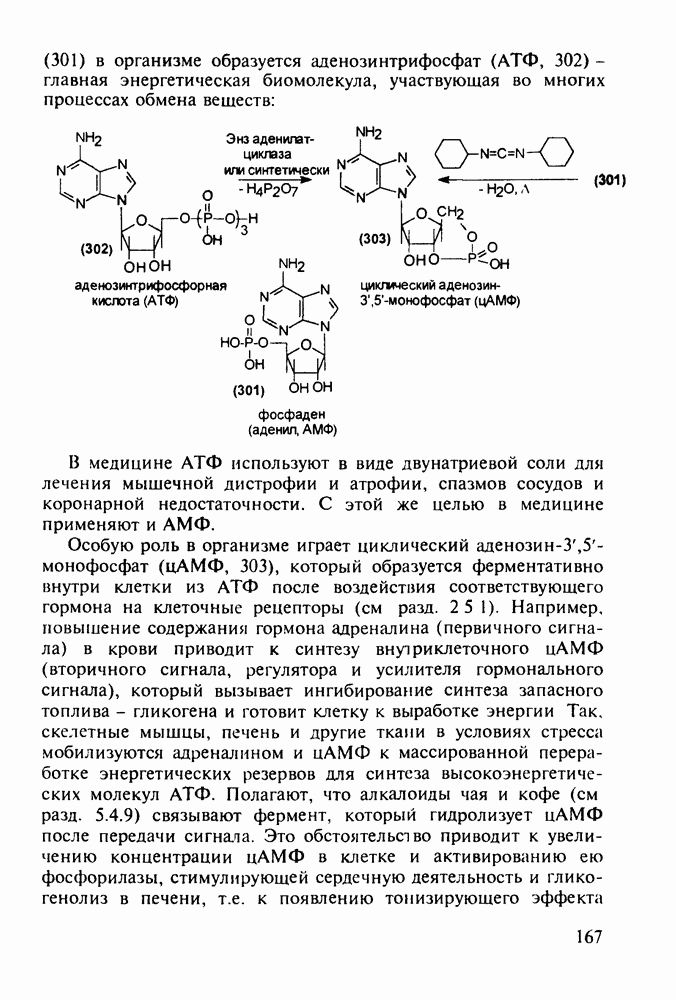
- 5.4.10. Производные аденозинфосфорной кислоты
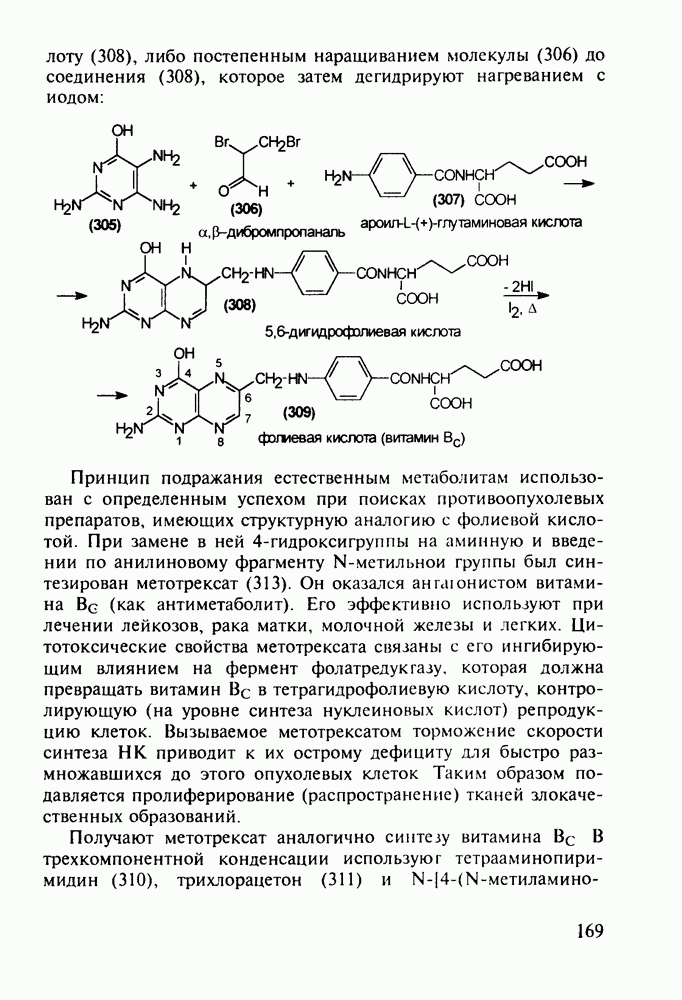
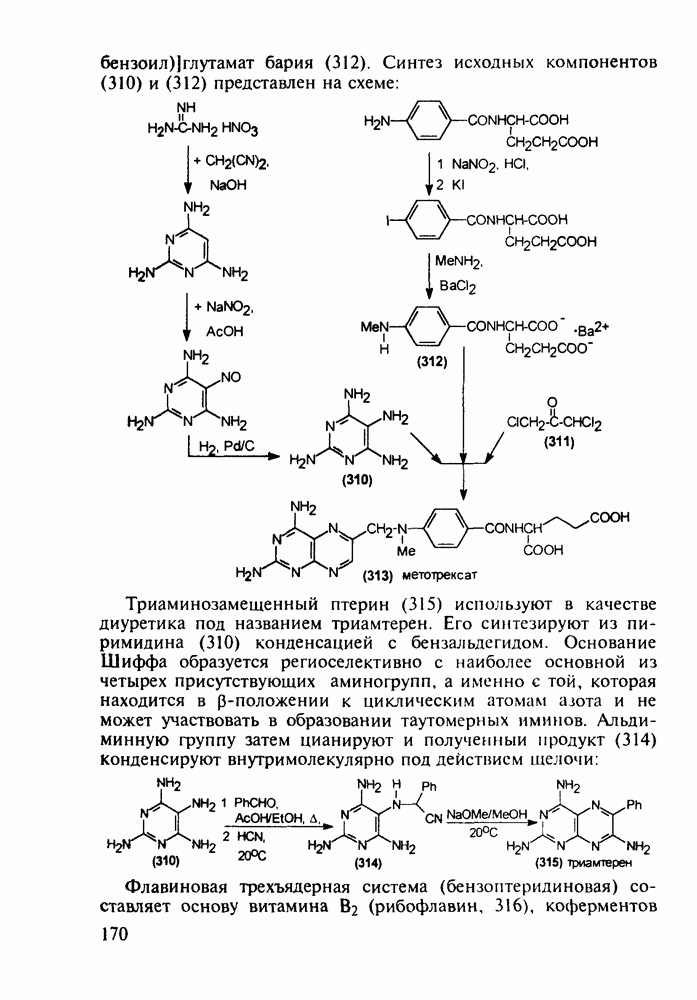
- 5.4.11. Производные птеридина с витаминной (витамины Вс и В2) и противораковой активностью
- 5.5. Лекарственные вещества, содержащие семичленный гетероцикл
- 5.5.2. Транквилизаторы группы 1,4-бензодиазепина
- 5.6. Производные азабициклооктанов в качестве спазмолитиков и анестетиков. Лекарственные препараты на основе хинуклидина
- 5.7. Производные азабициклононанов в качестве анальгетиков
- 5.7.1. Группа пентазоцина
- 5.7.2. Морфин, его агонисты и антагонисты
- РЕКОМЕНДУЕМАЯ ЛИТЕРАТУРА