| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
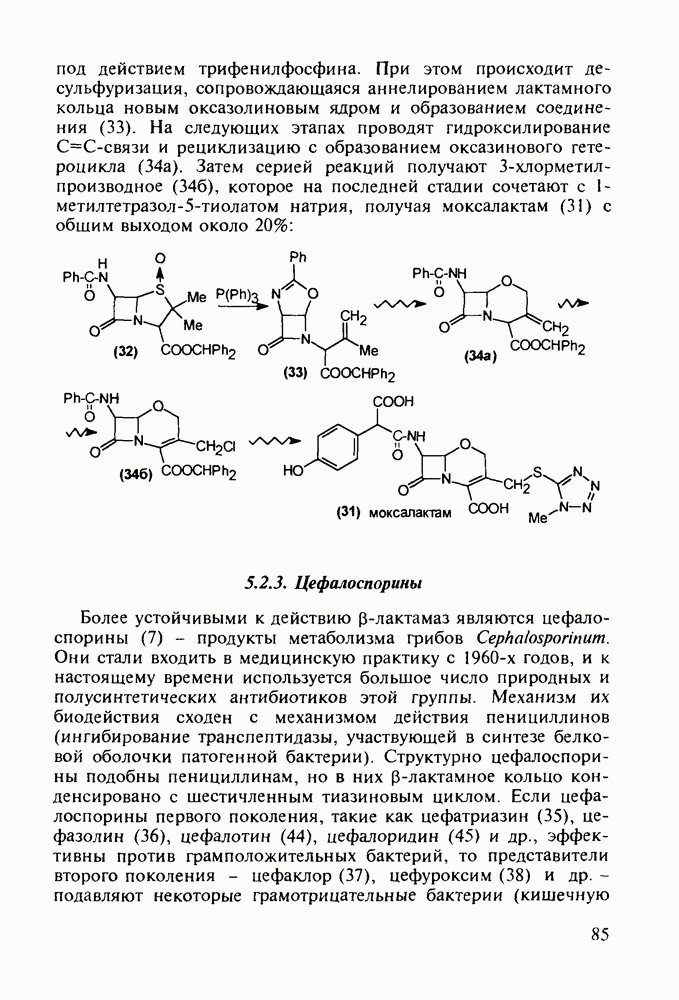
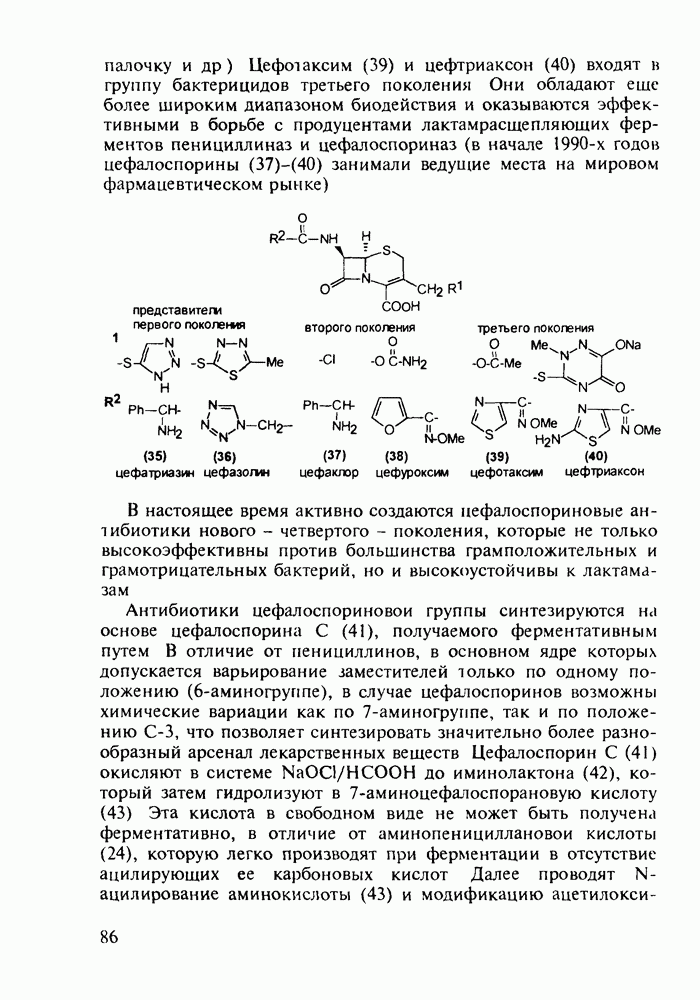
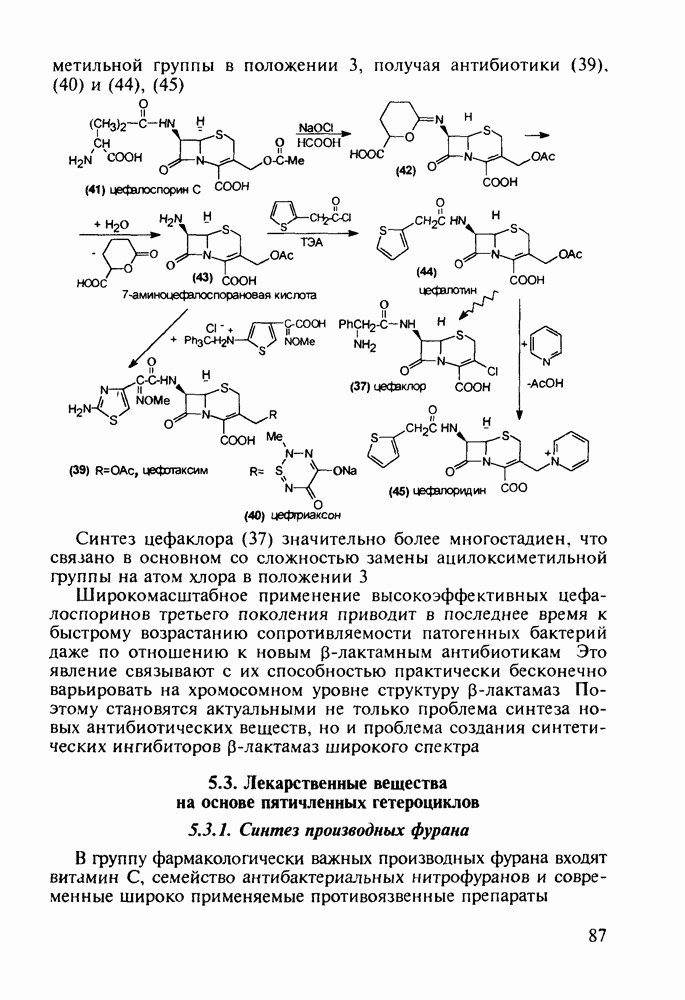
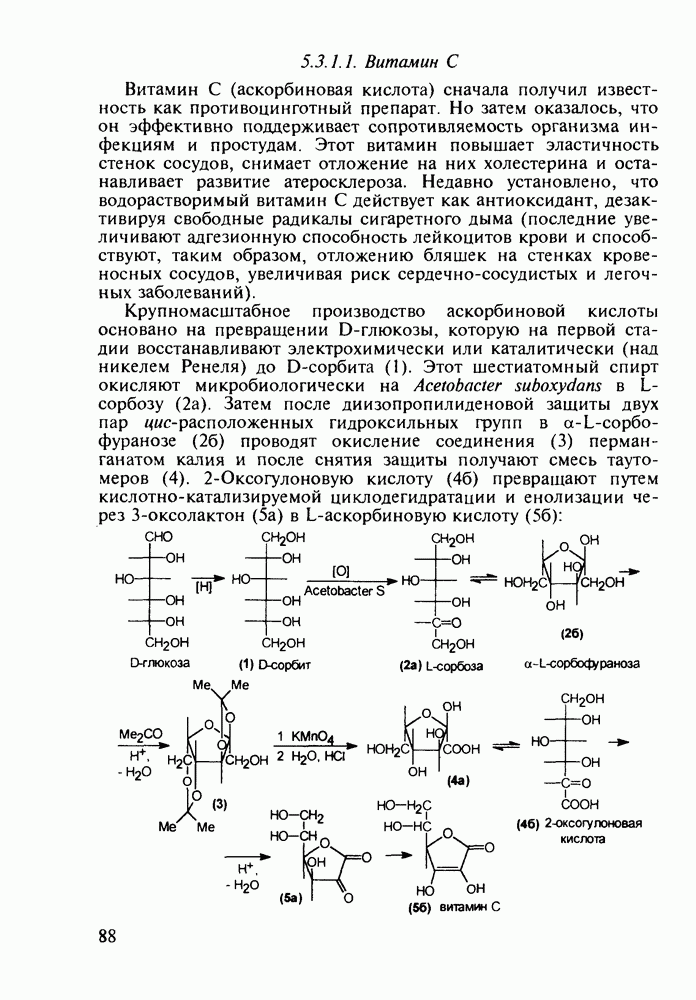
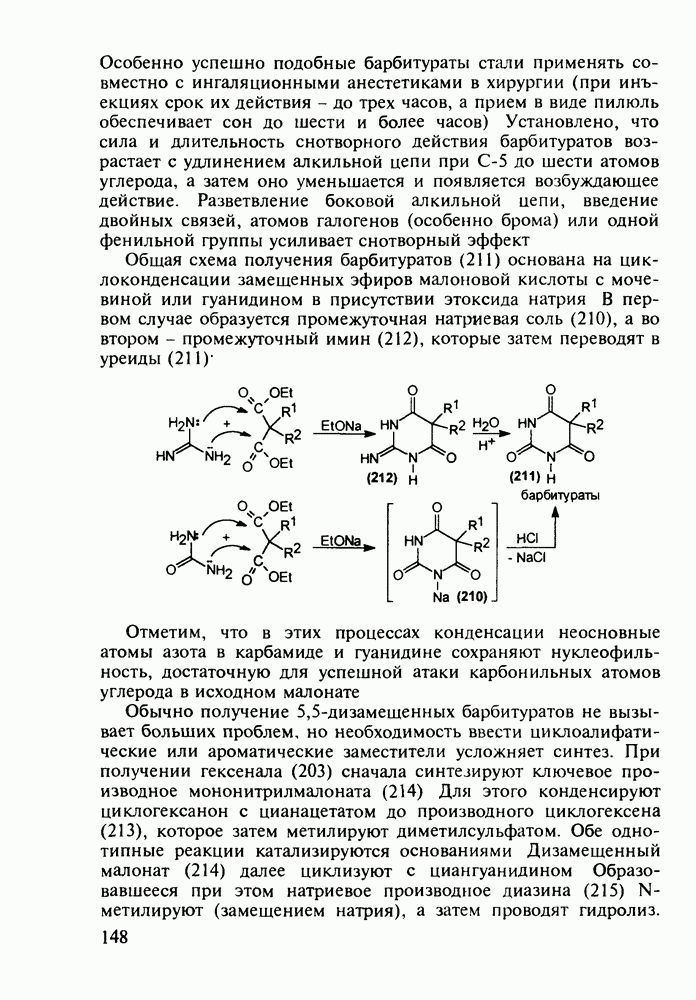
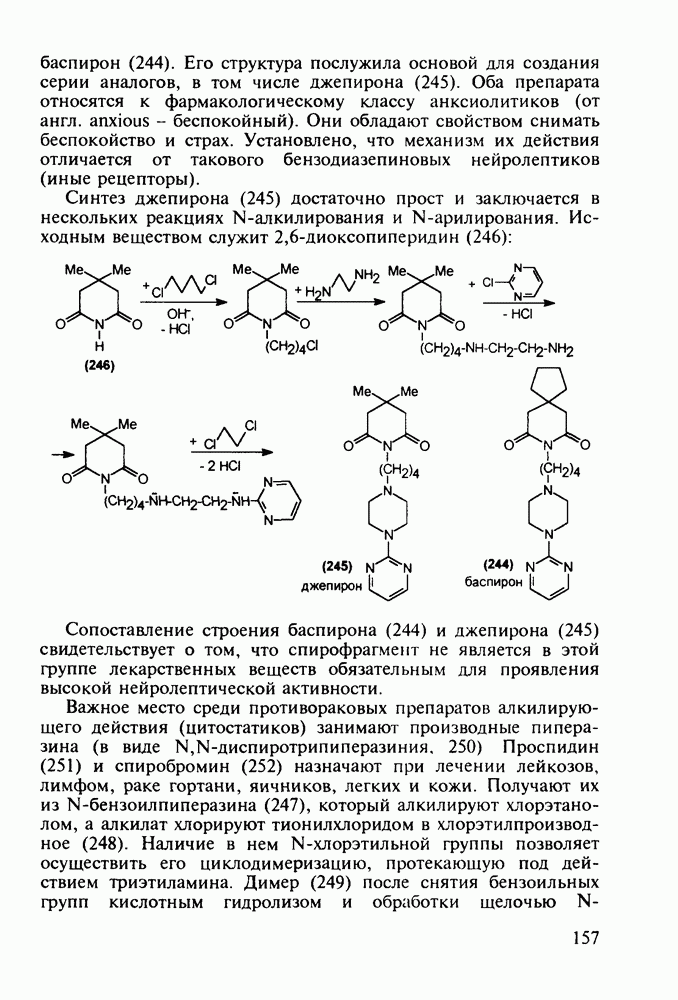
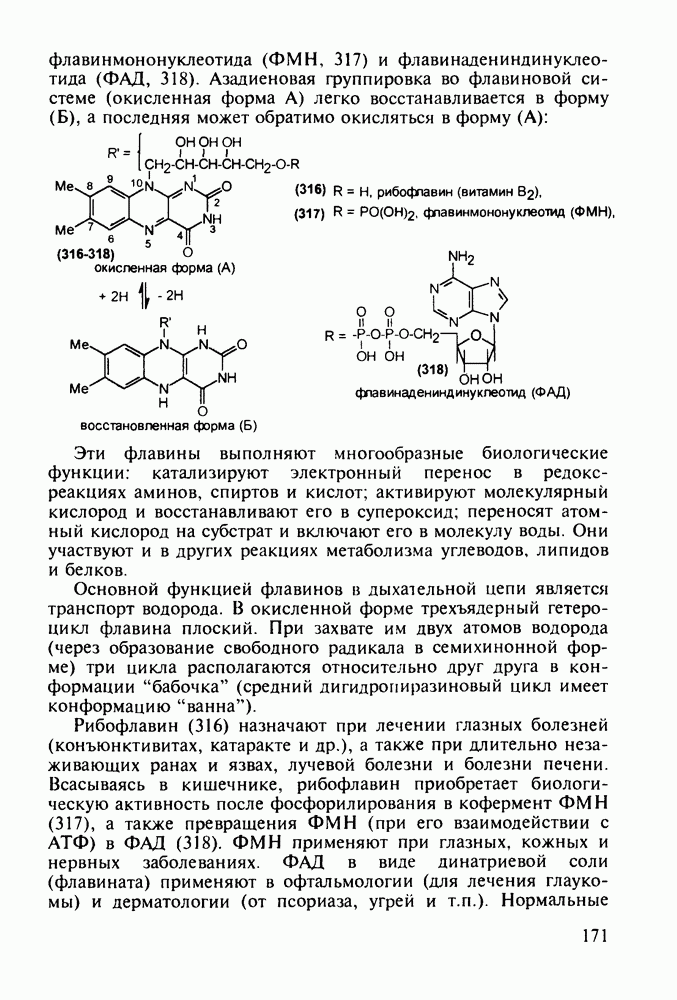
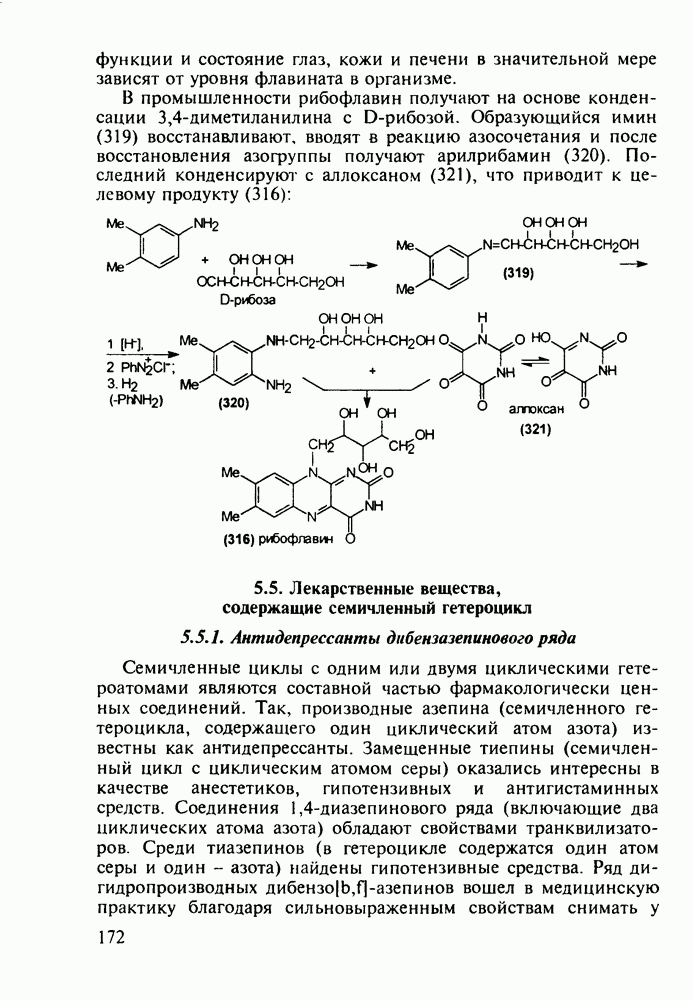
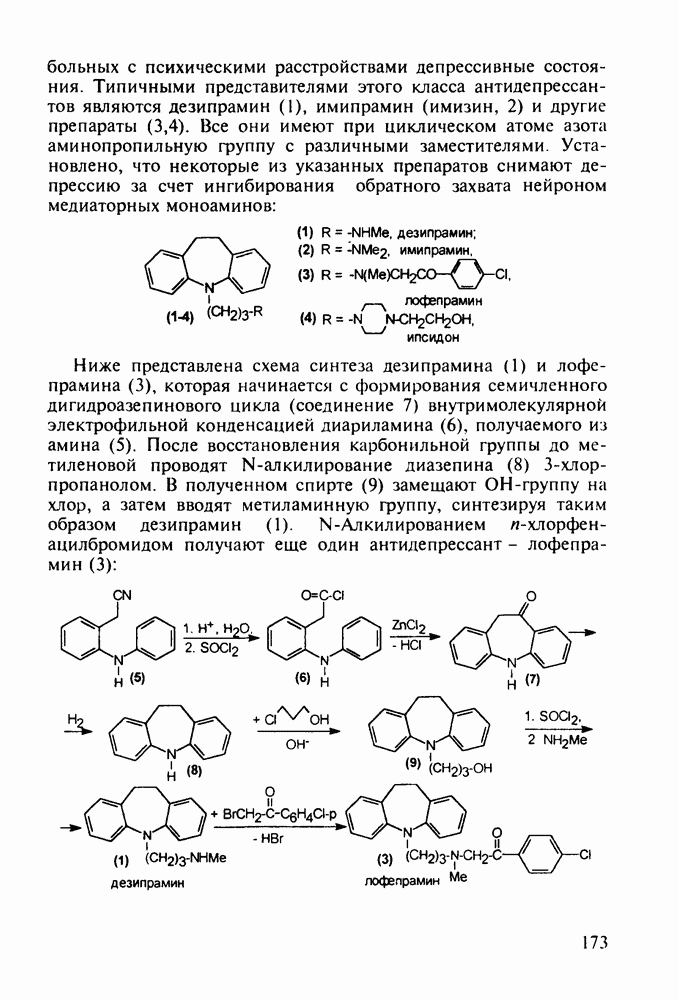
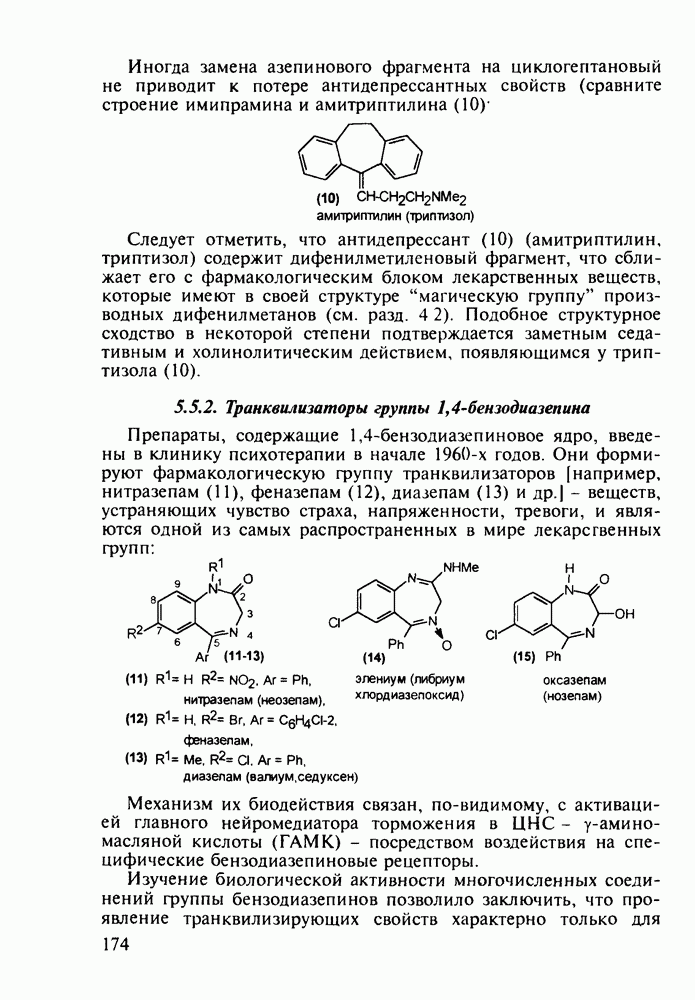
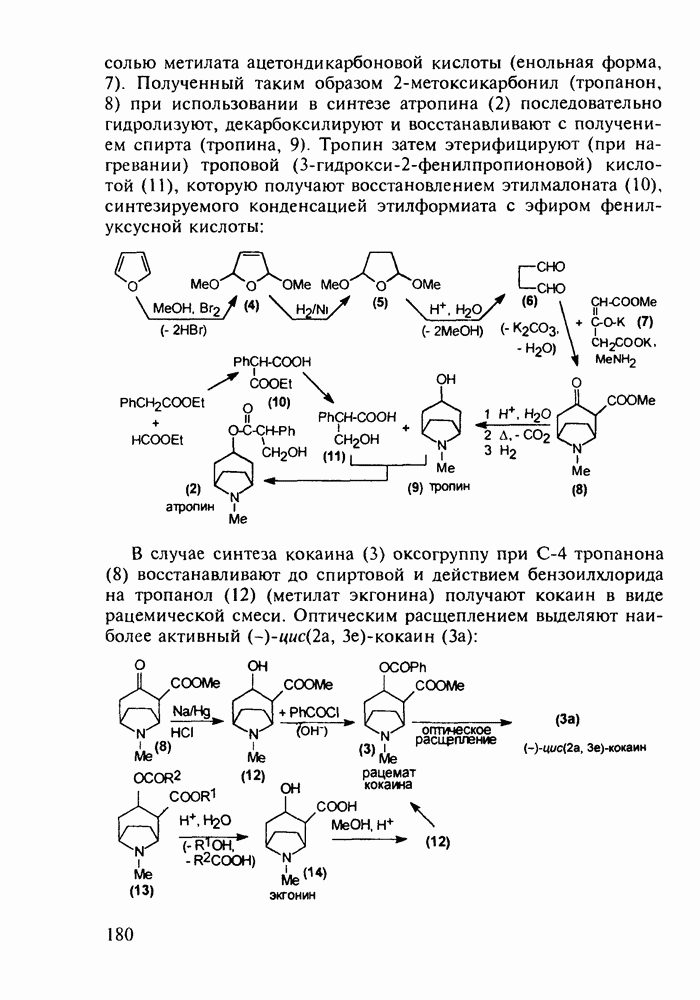
5.5.2. Транквилизаторы группы 1,4-бензодиазепина
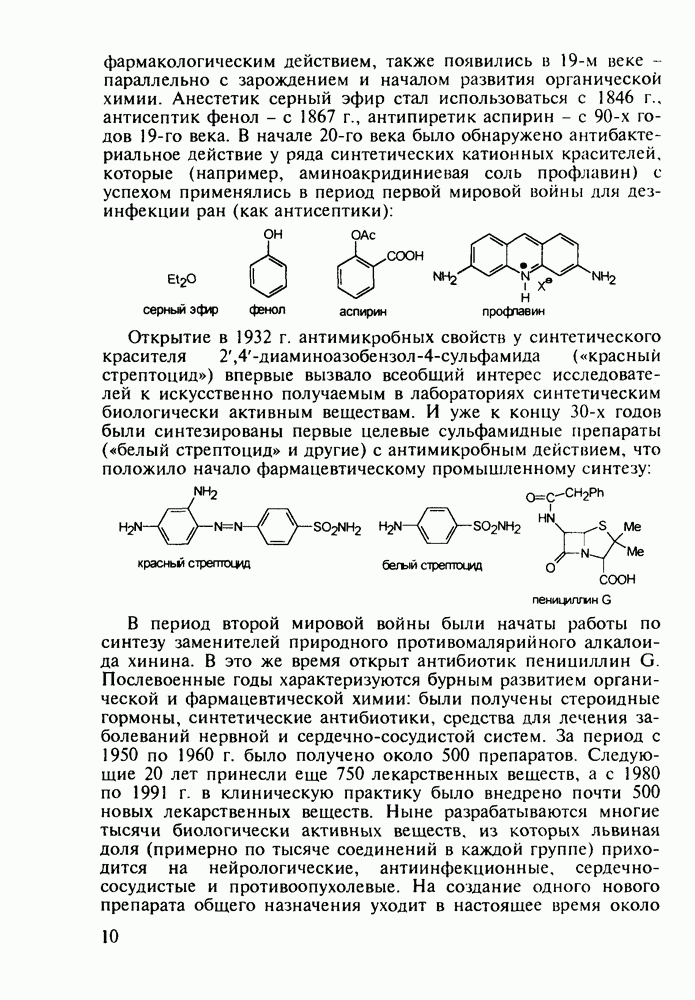
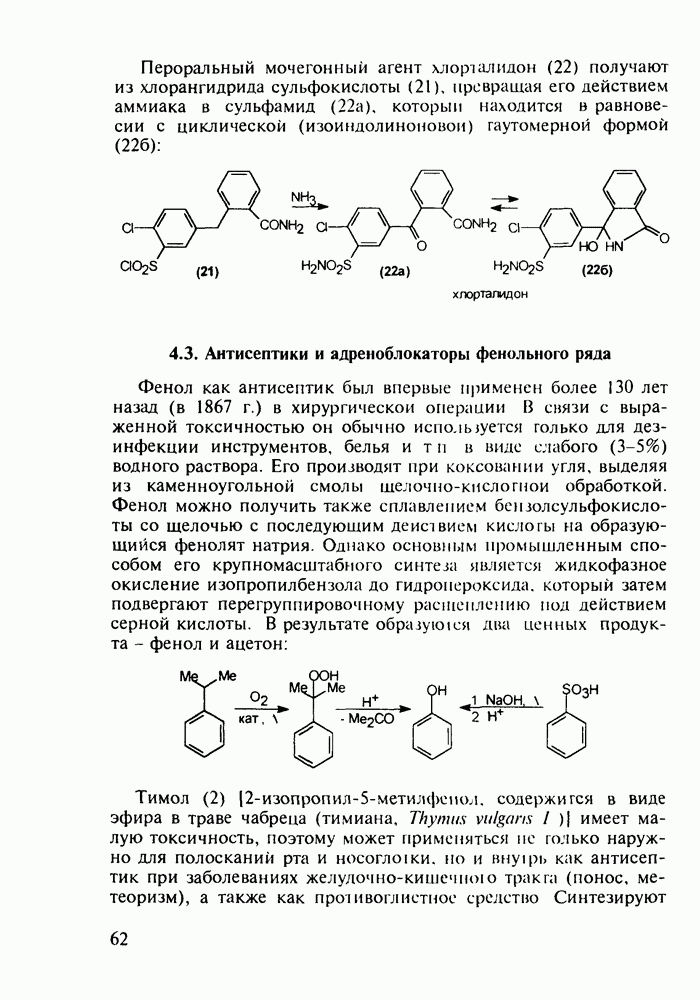
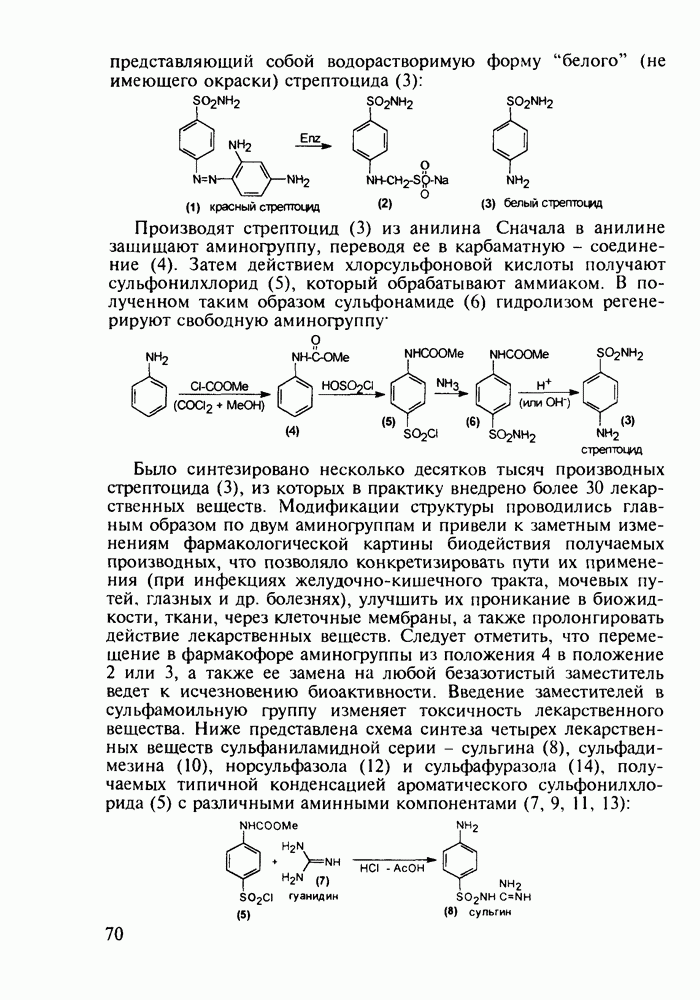
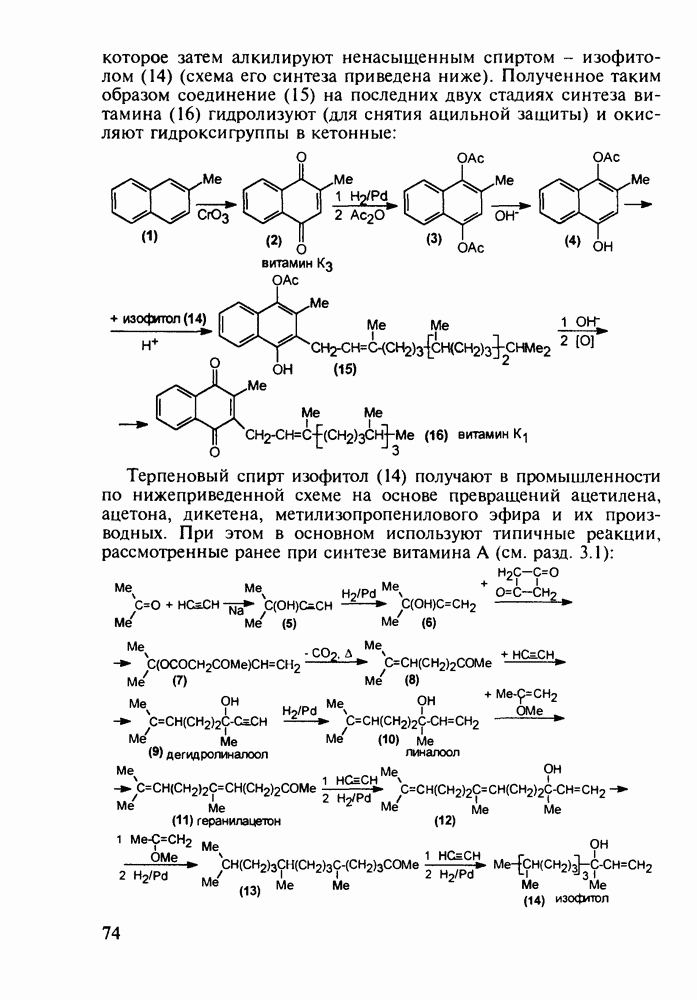
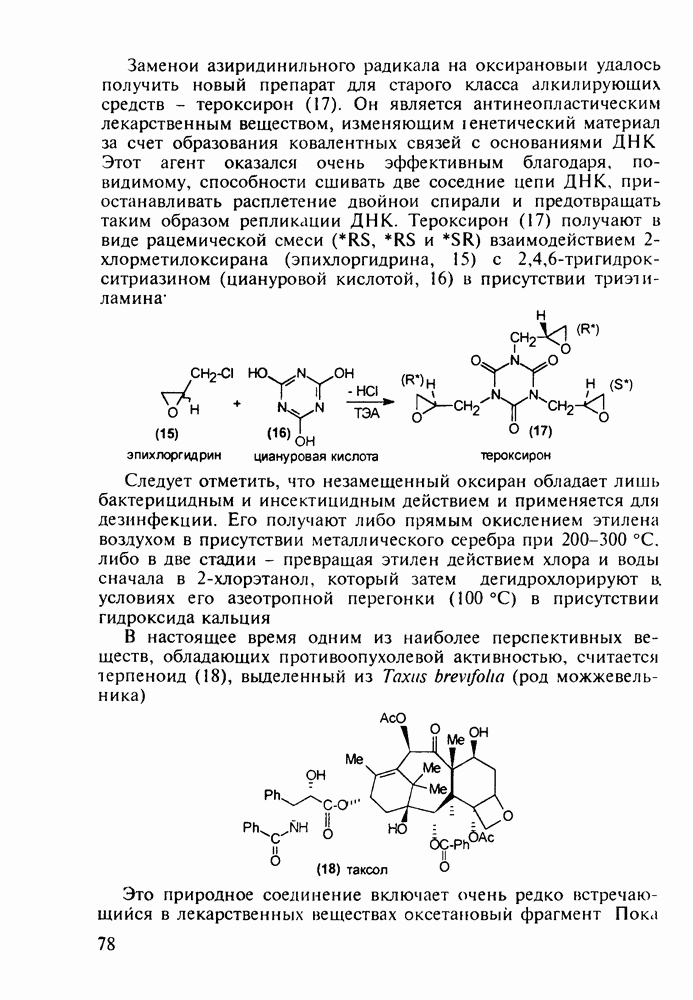
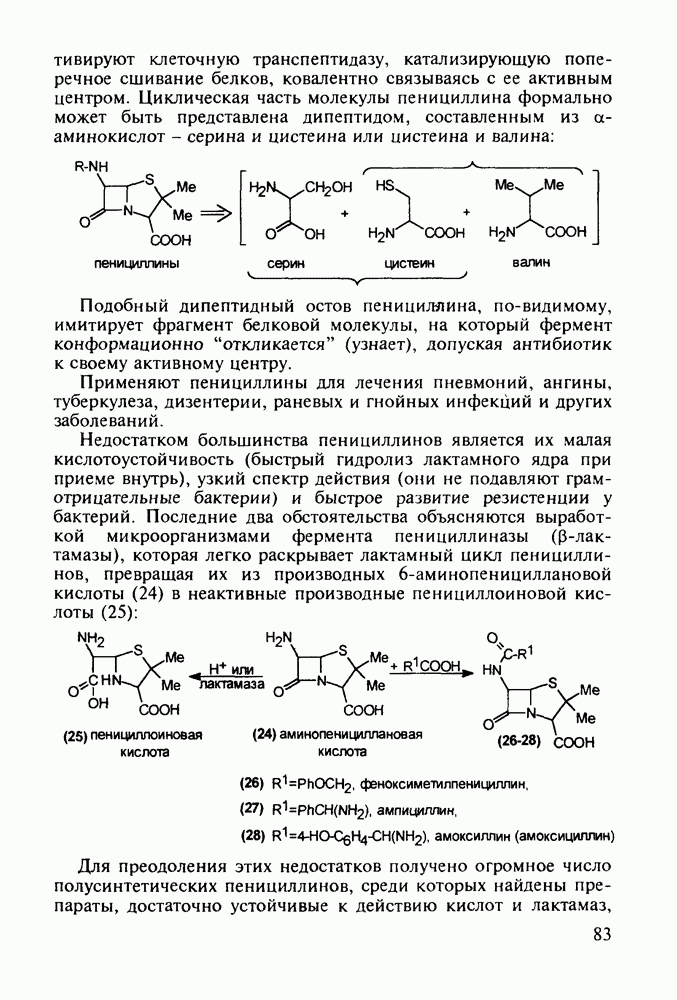
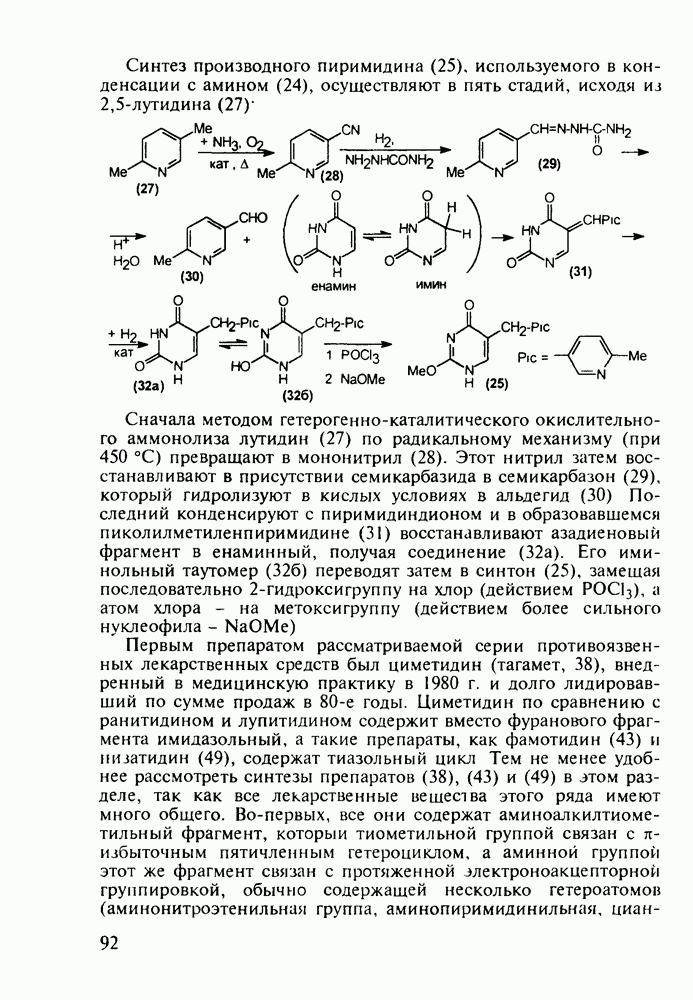
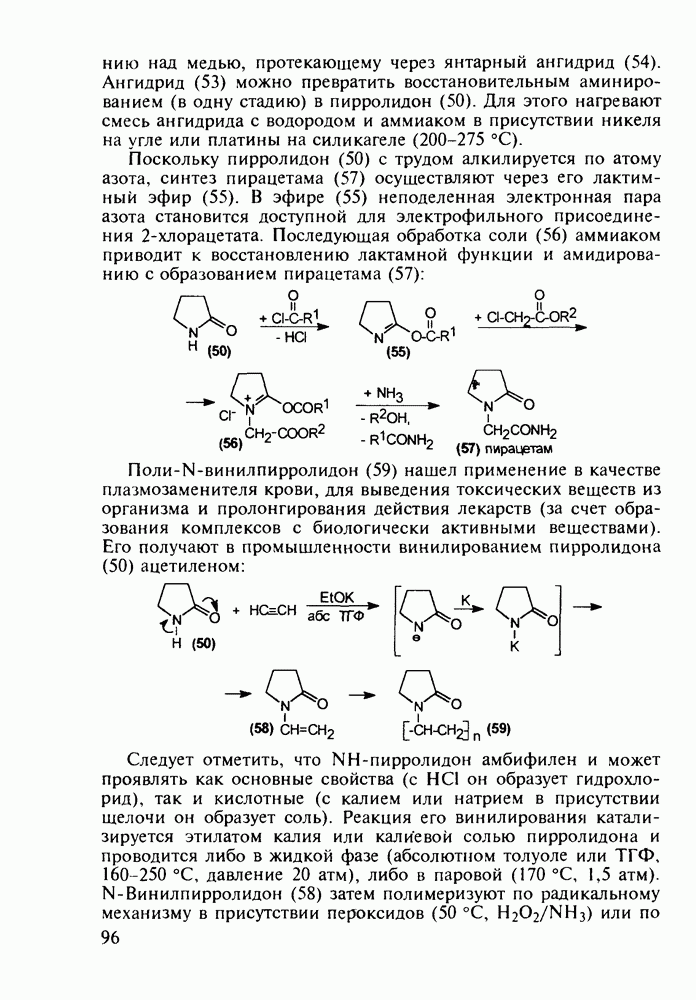
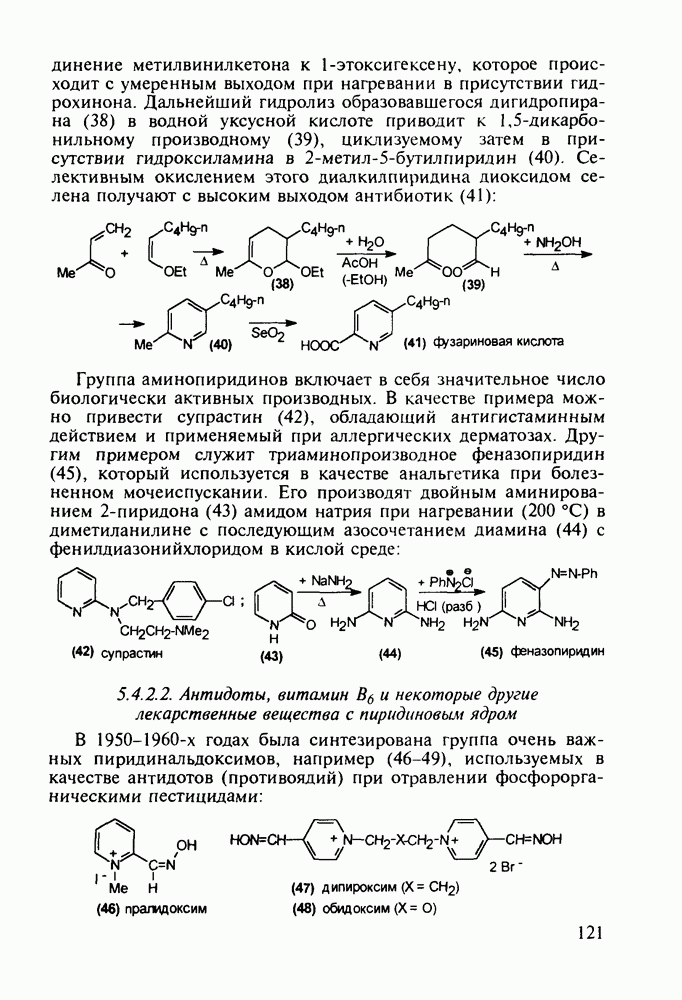
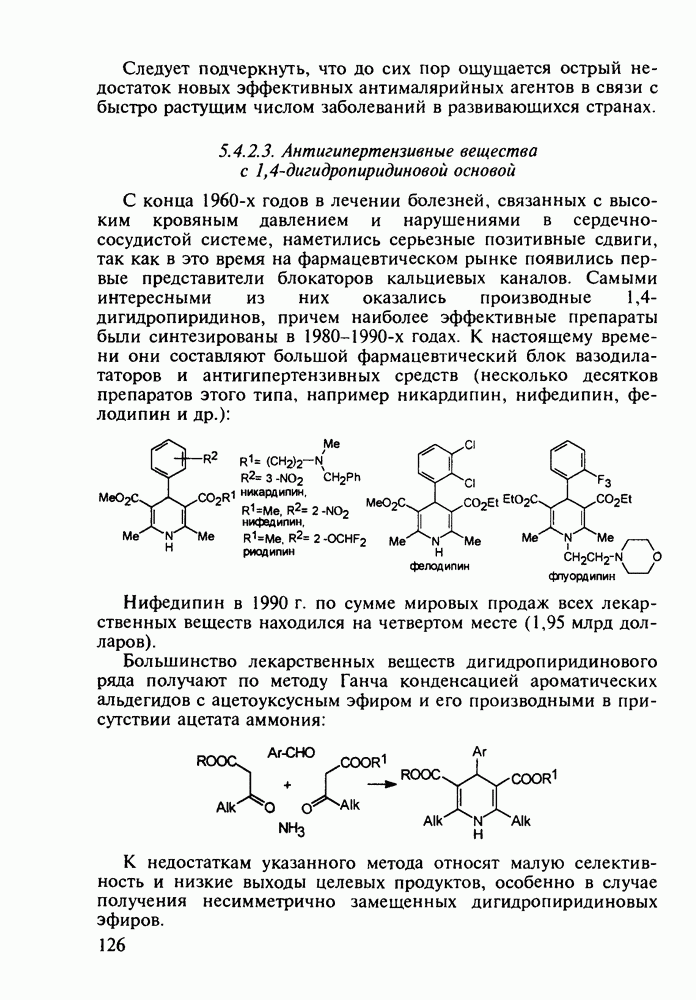
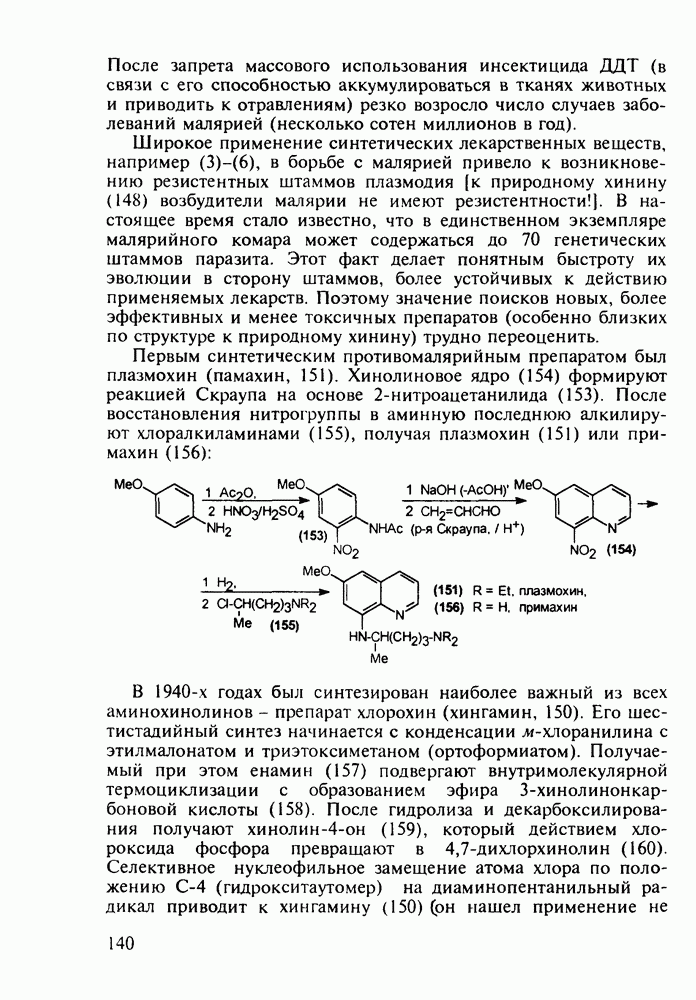
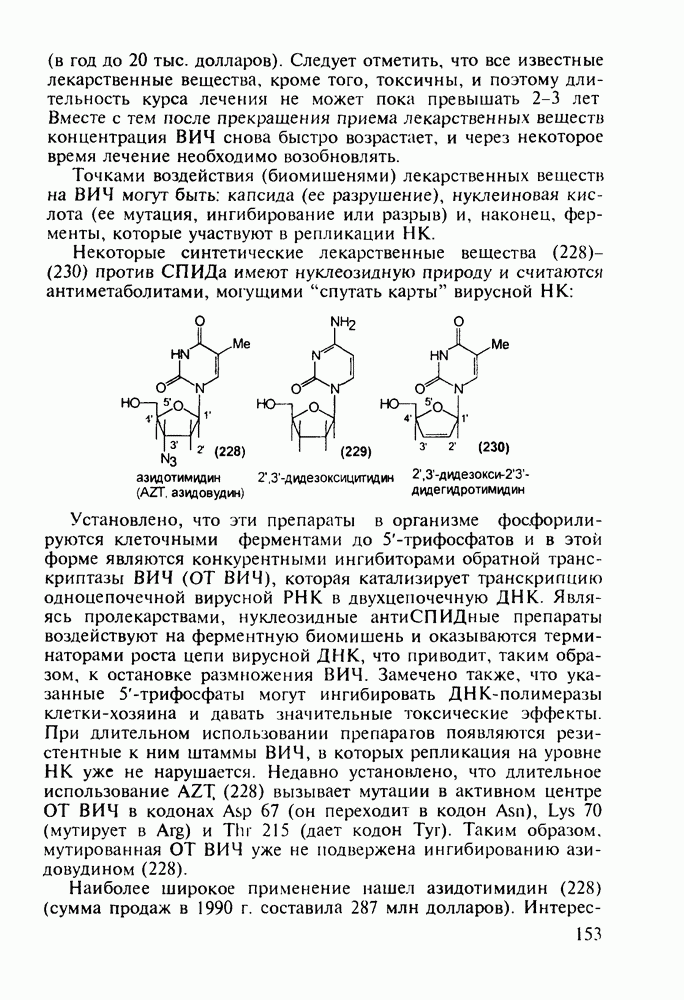
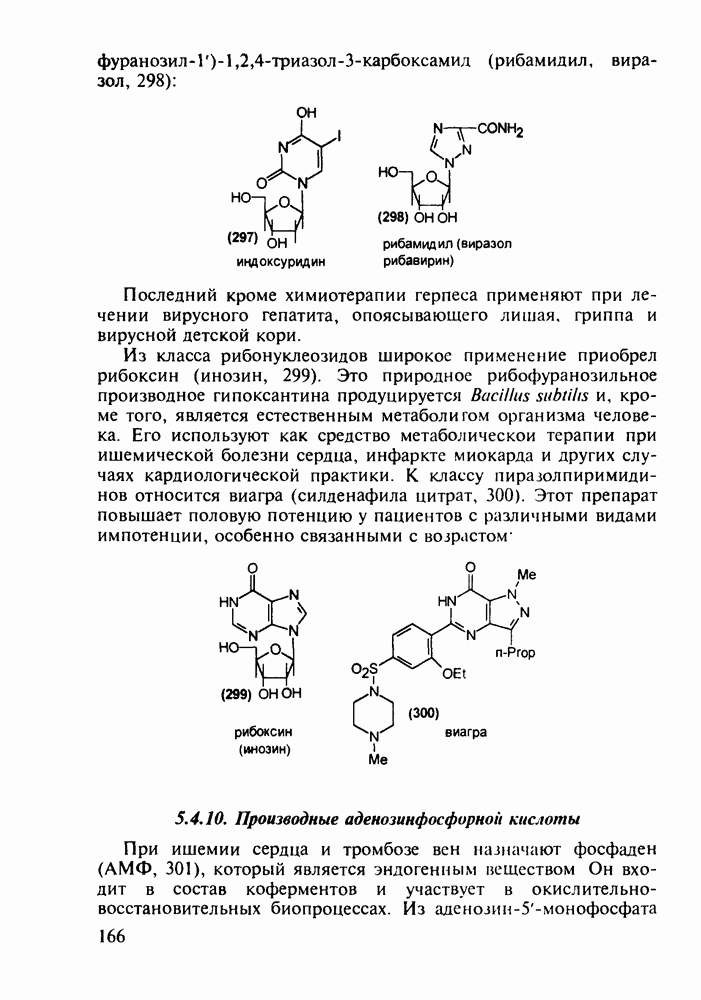
Препараты, содержащие 1,4-бензодиазепиновое ядро, введены в клинику психотерапии в начале 1960-х годов. Они формируют фармакологическую группу транквилизаторов [например, нитразепам (11), феназепам (12), диазепам (13) и др.] - веществ, устраняющих чувство страха, напряженности, тревоги, и являются одной из самых распространенных в мире лекарственных групп:

Механизм их биодействия связан, по-видимому, с активацией главного нейромедиатора торможения в ЦНС - у-аминомасляной кислоты (ГАМК) - посредством воздействия на специфические бензодиазепиновые рецепторы.
Изучение биологической активности многочисленных соединений группы бензодиазепинов позволило заключить, что проявление транквилизирующих свойств характерно только для
таких бензодиазепинов, которые содержат следующие структурные элементы: 1) ароматический радикал при С-5; 2) атом галогена или нитрогруппу при С-7; 3) оксогруппу или вторичный алкиламинный заместитель при С-2; 4) двойную связь при  . В то же время некоторые транквилизаторы обладают побочными эффектами. Так, нитразепам (11) оказывает сильное снотворное действие, влияя на подкорковые структуры мозга и уменьшая эмоциональное возбуждение. Кроме того, он усиливает действие других снотворных, а также анальгетиков. Он нашел применение для купирования эпилептических припадков (как противосудорожное средство).
. В то же время некоторые транквилизаторы обладают побочными эффектами. Так, нитразепам (11) оказывает сильное снотворное действие, влияя на подкорковые структуры мозга и уменьшая эмоциональное возбуждение. Кроме того, он усиливает действие других снотворных, а также анальгетиков. Он нашел применение для купирования эпилептических припадков (как противосудорожное средство).
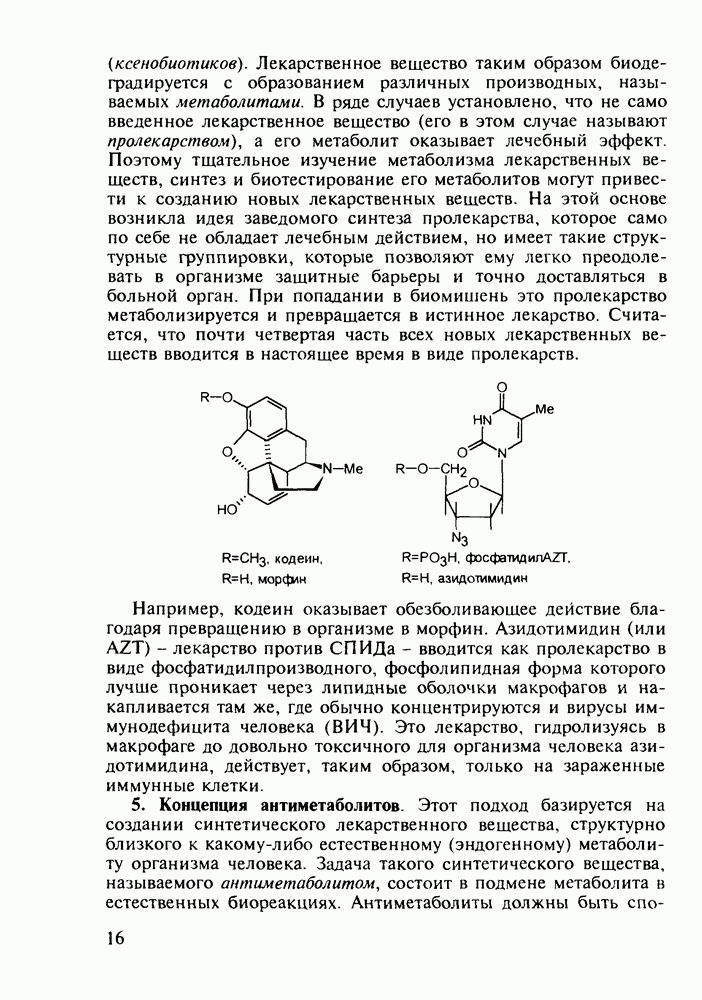
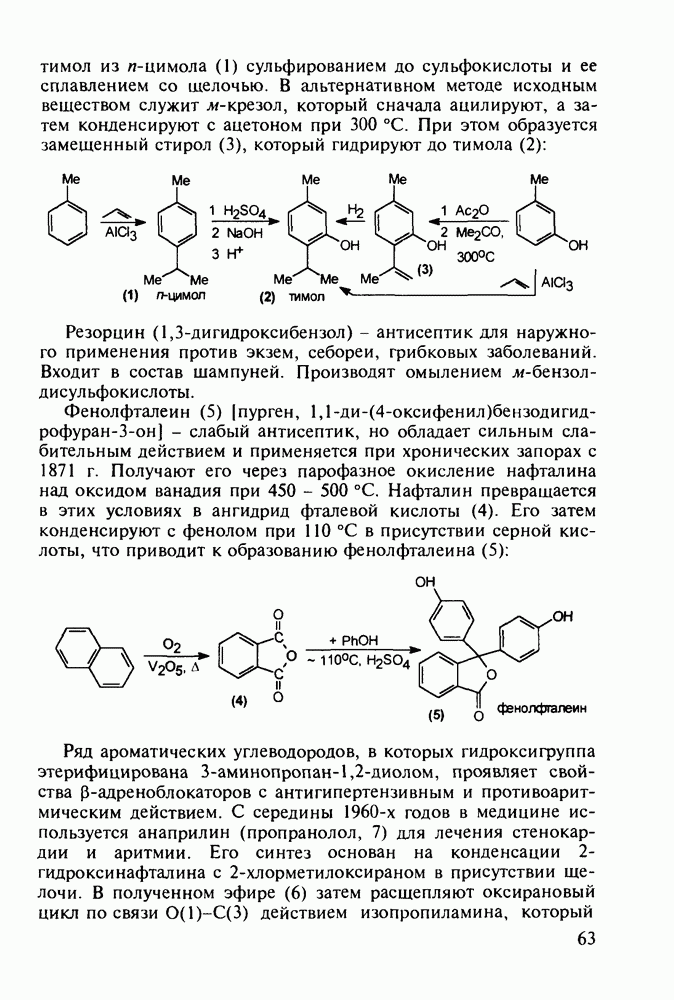
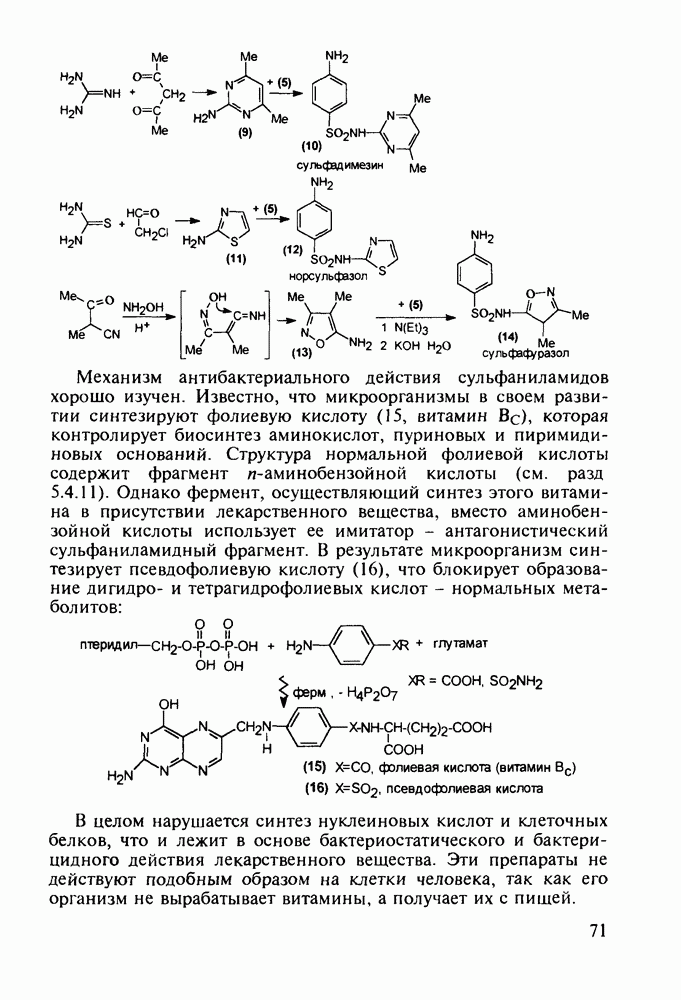
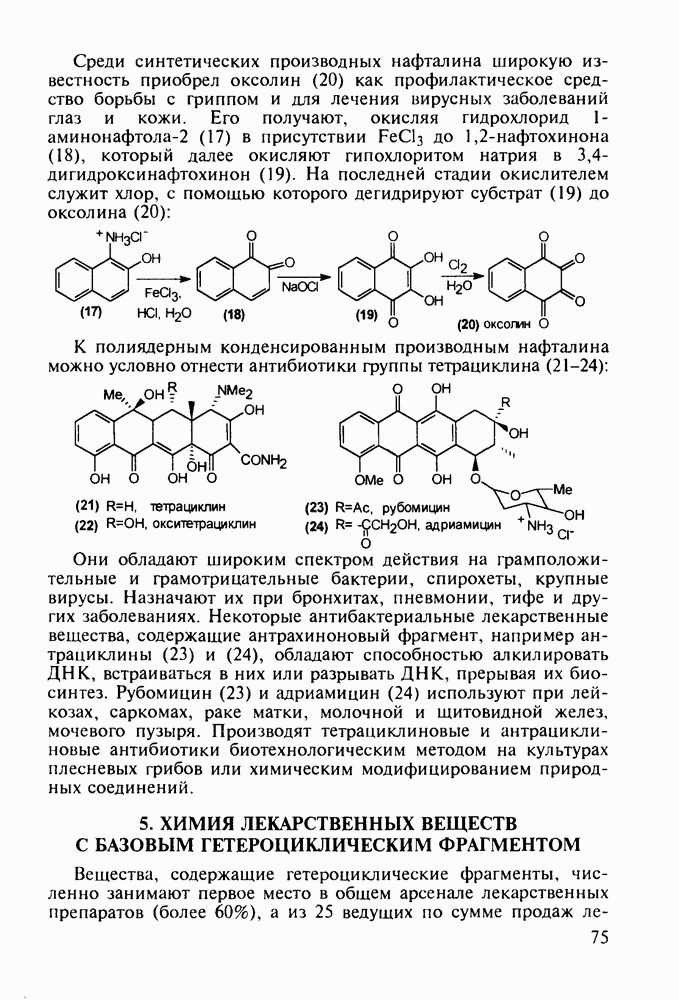
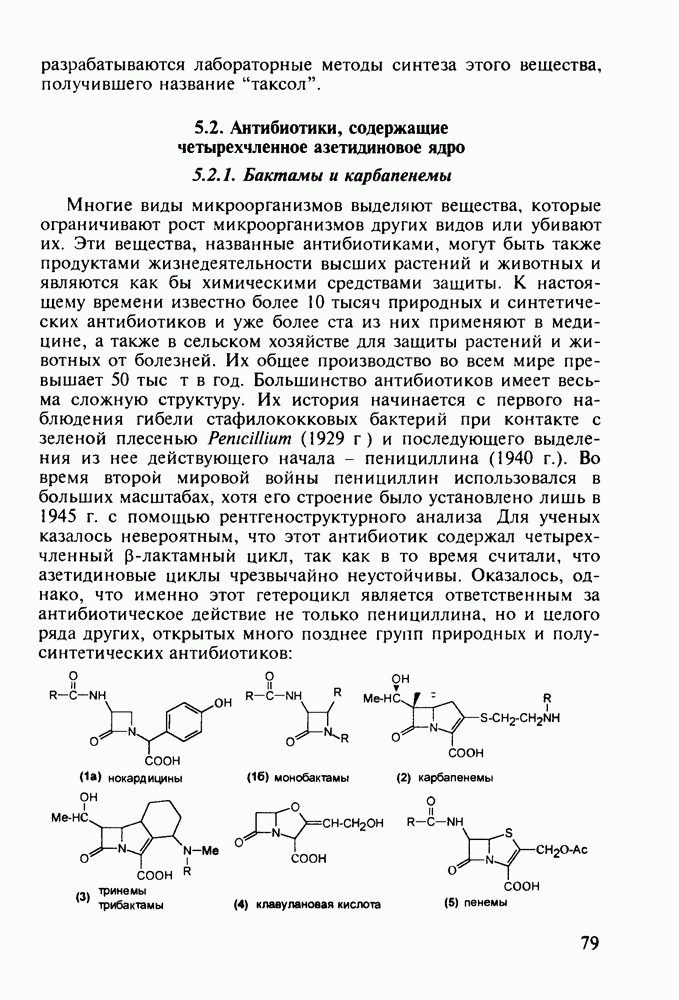
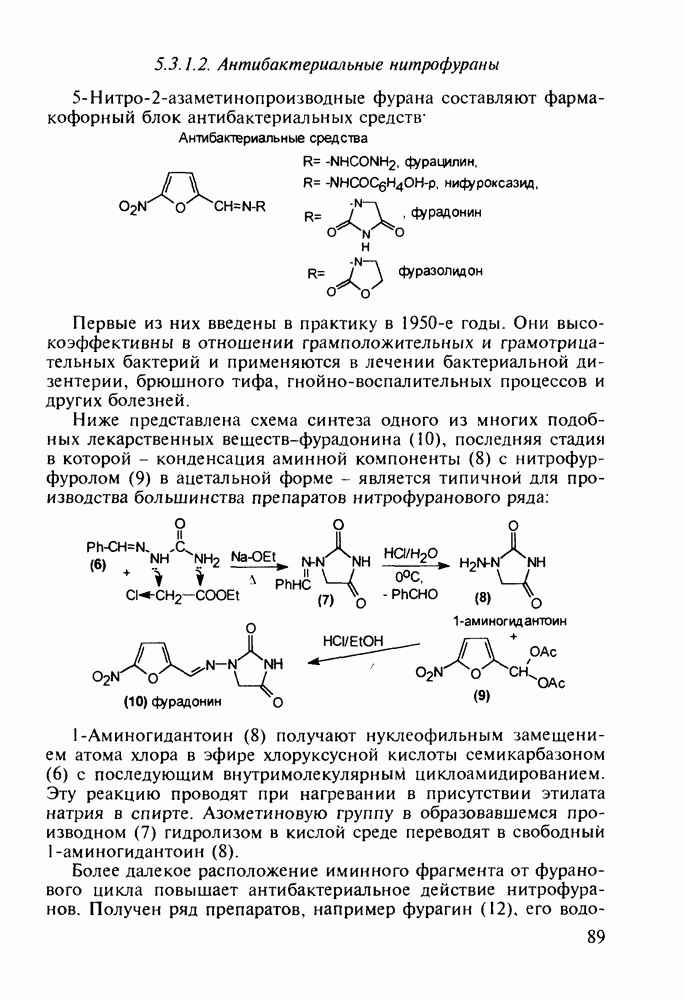
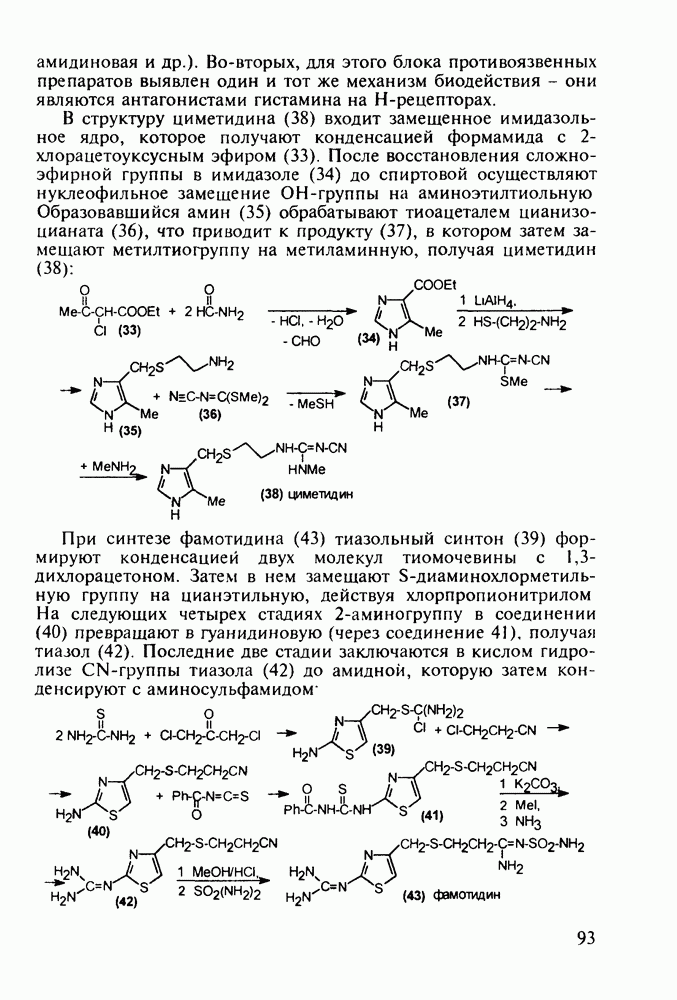
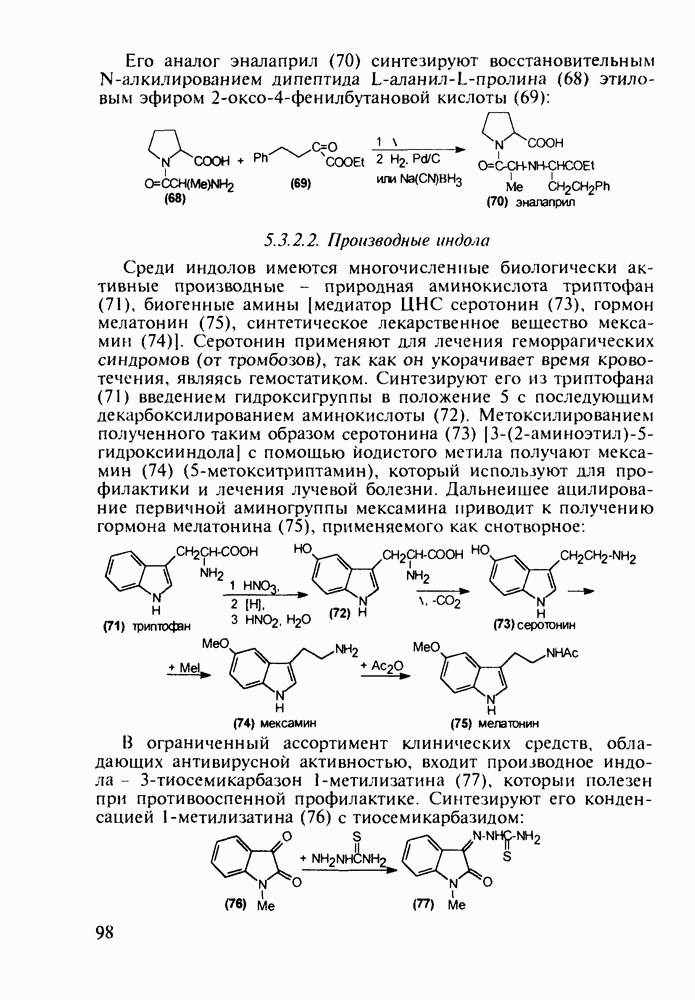
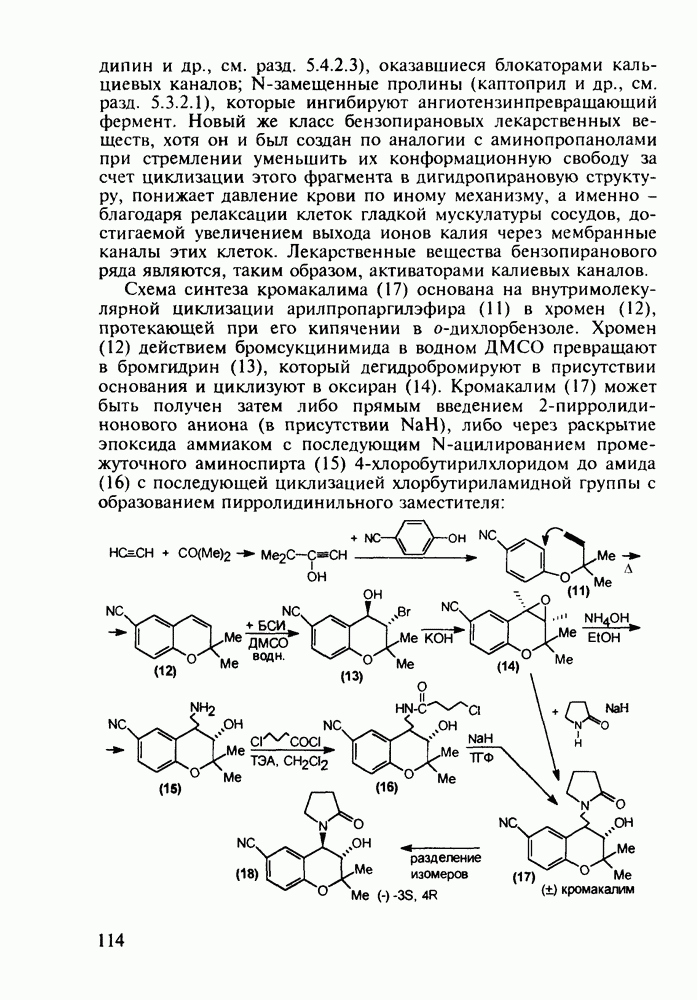
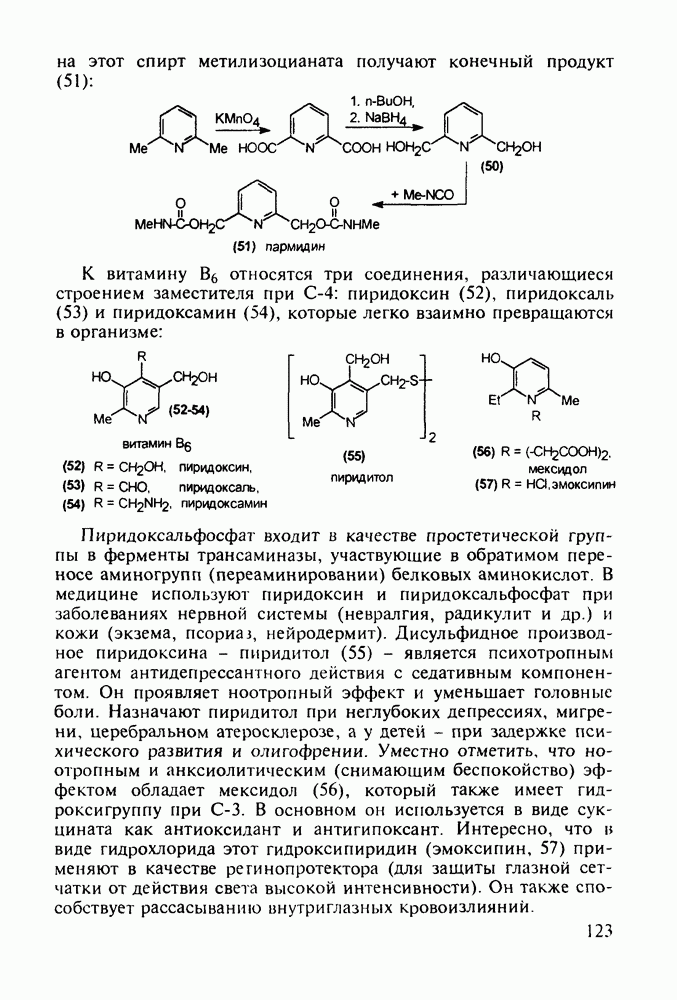
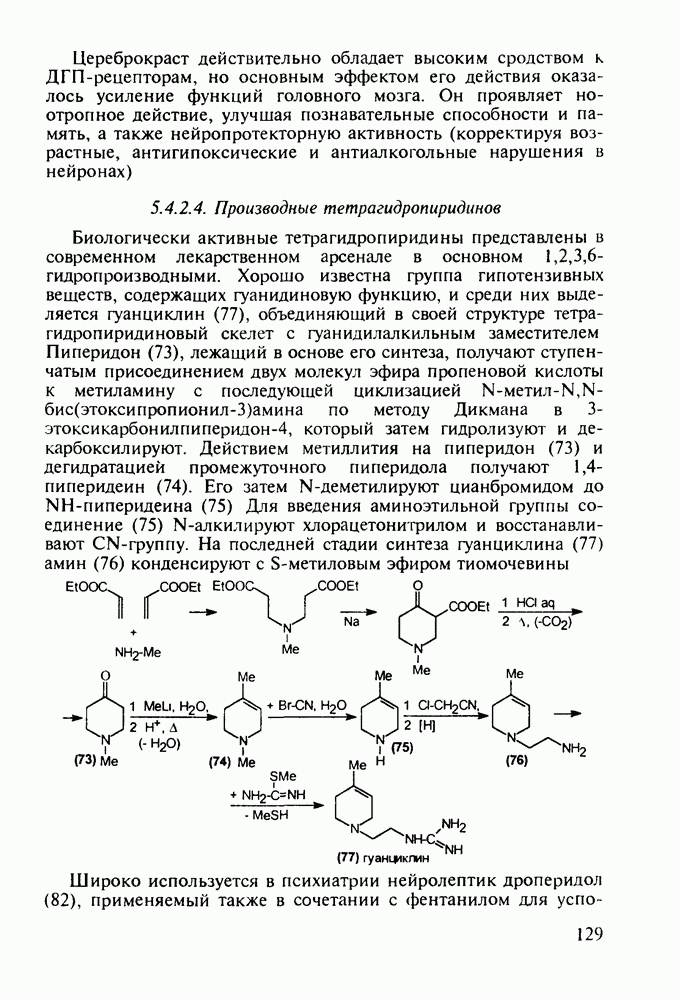
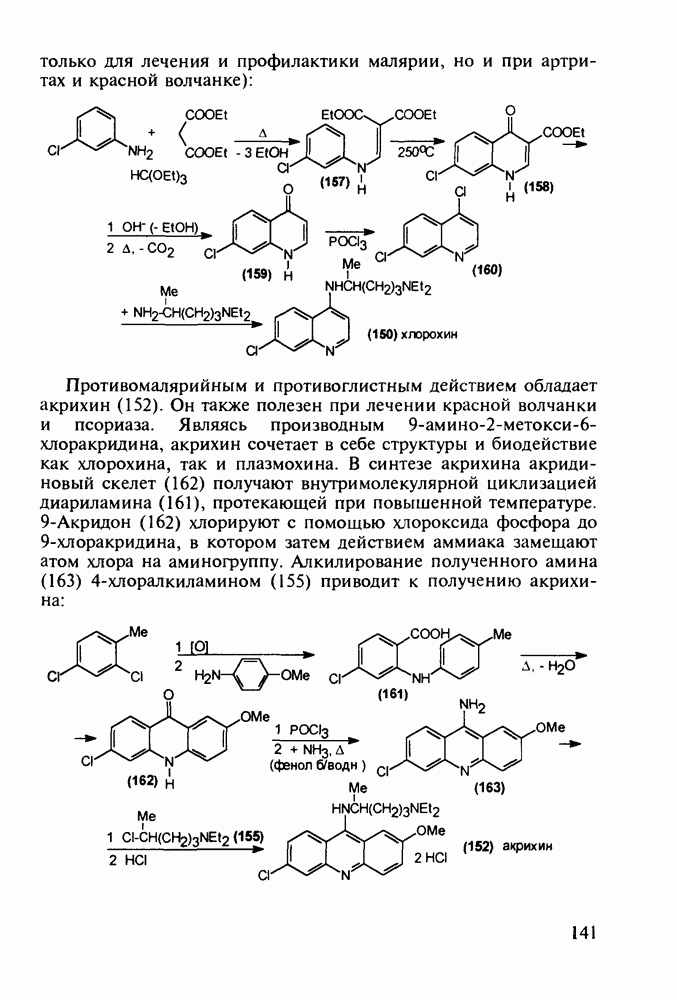
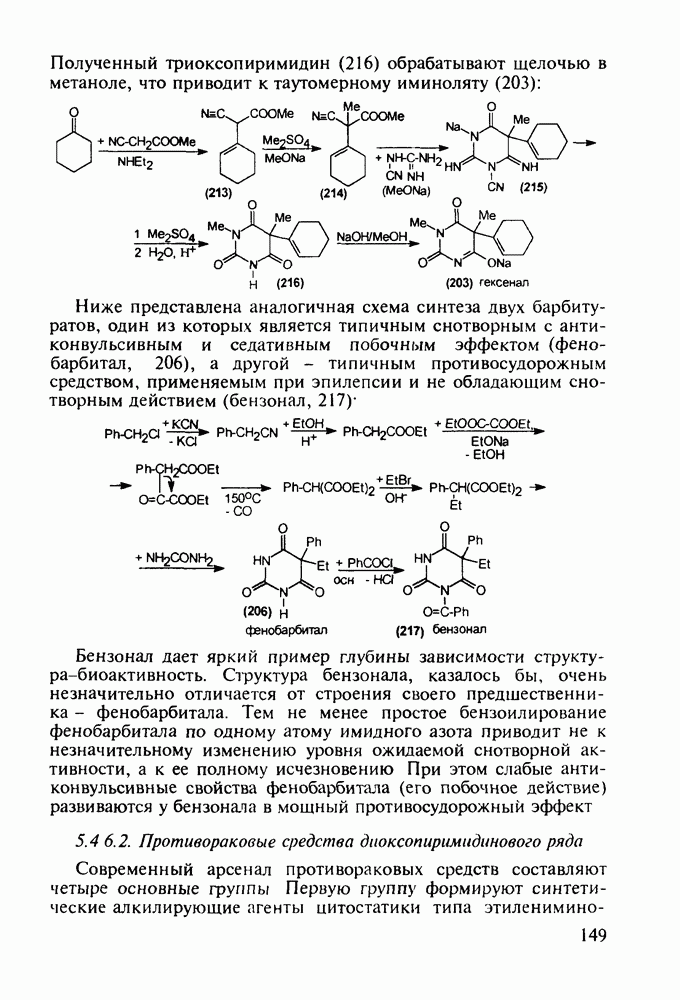
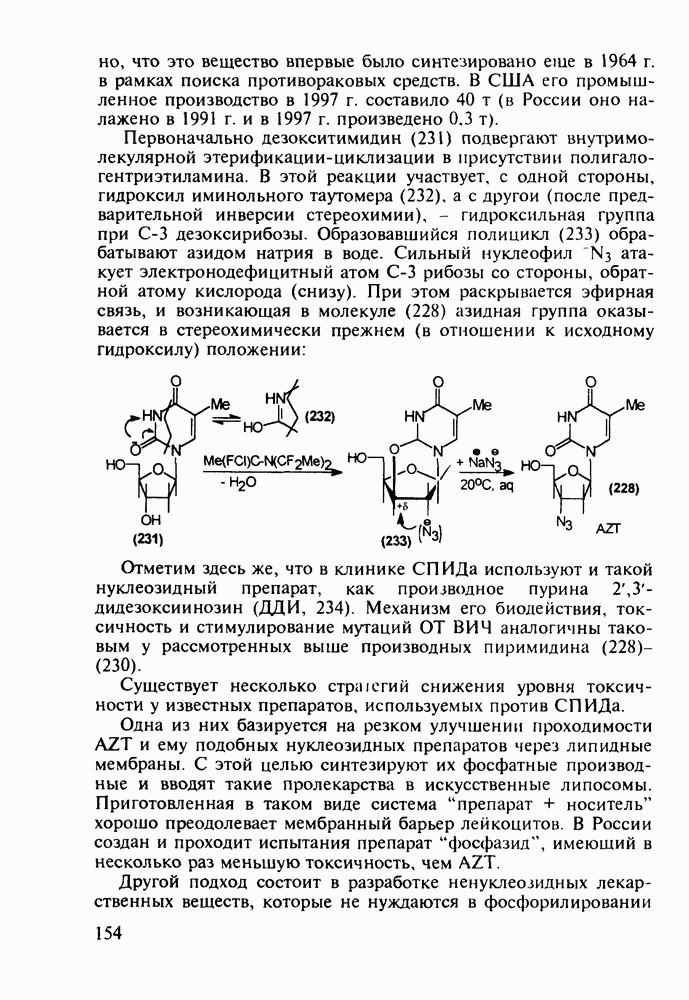
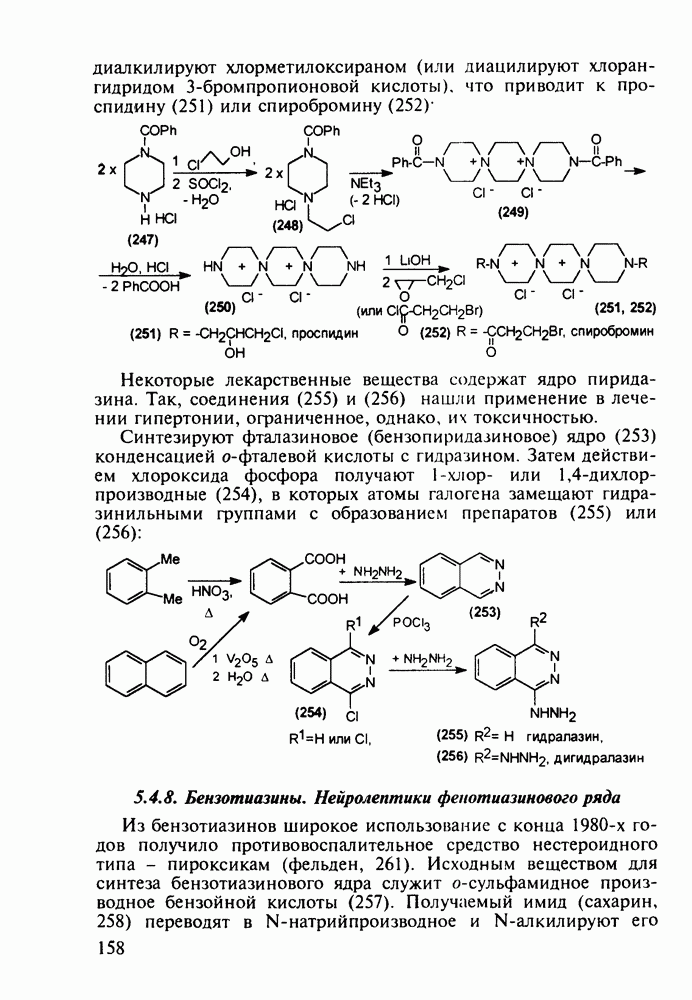
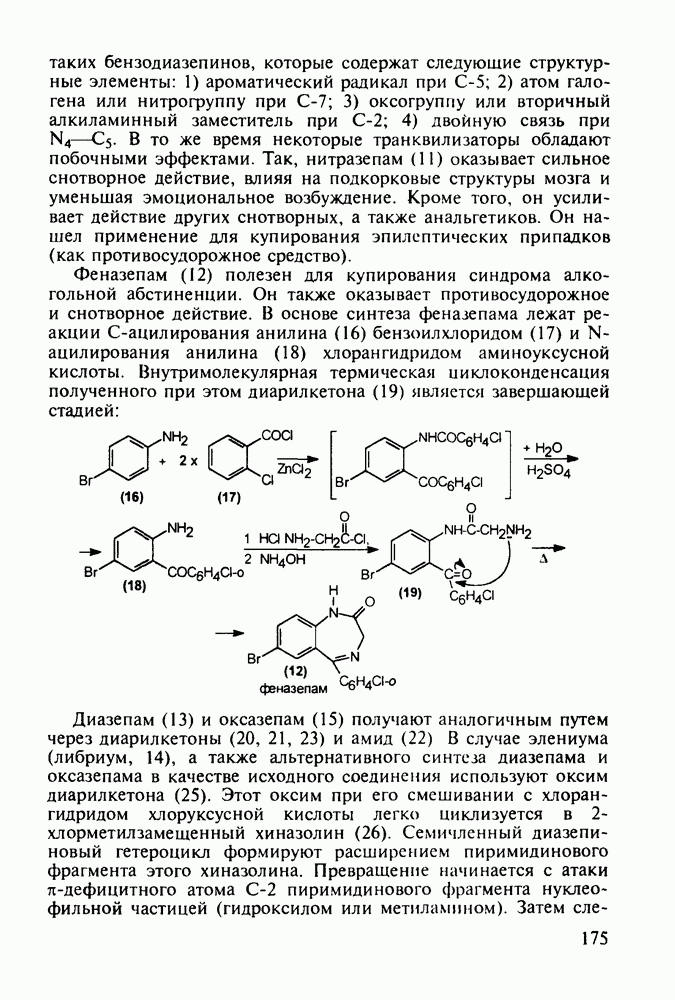
Феназепам (12) полезен для купирования синдрома алкогольной абстиненции. Он также оказывает противосудорожное и снотворное действие. В основе синтеза феназепама лежат реакции С-ацилирования анилина (16) бензоилхлоридом (17) и N-ацилирования анилина (18) хлоран гидридом аминоуксусной кислоты. Внутримолекулярная термическая циклоконденсация полученного при этом диарилкетона (19) является завершающей стадией:

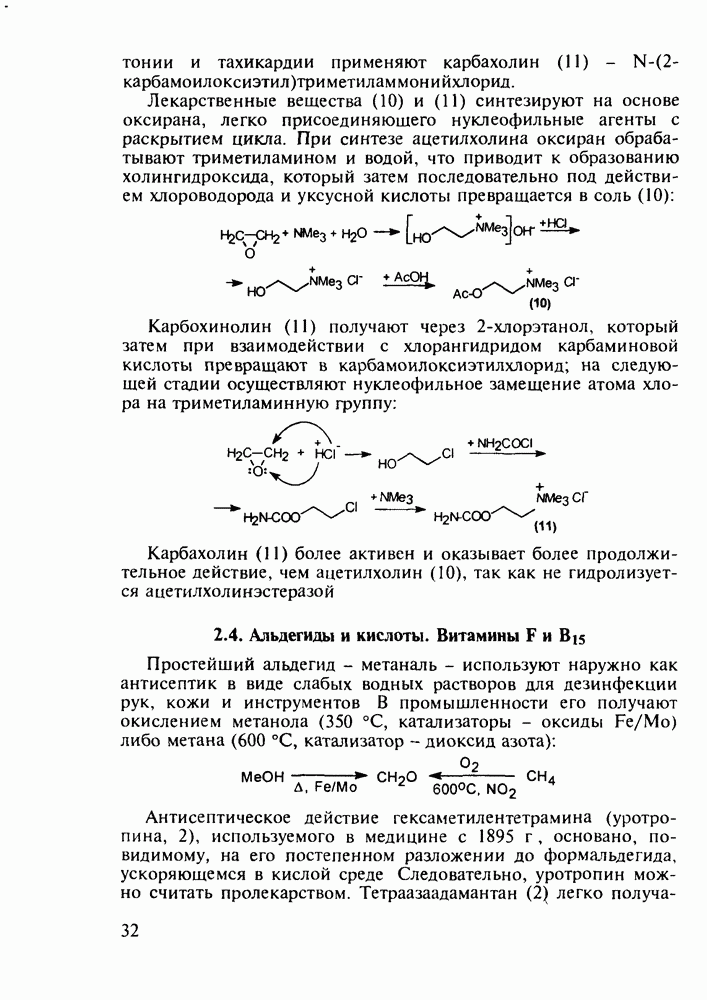
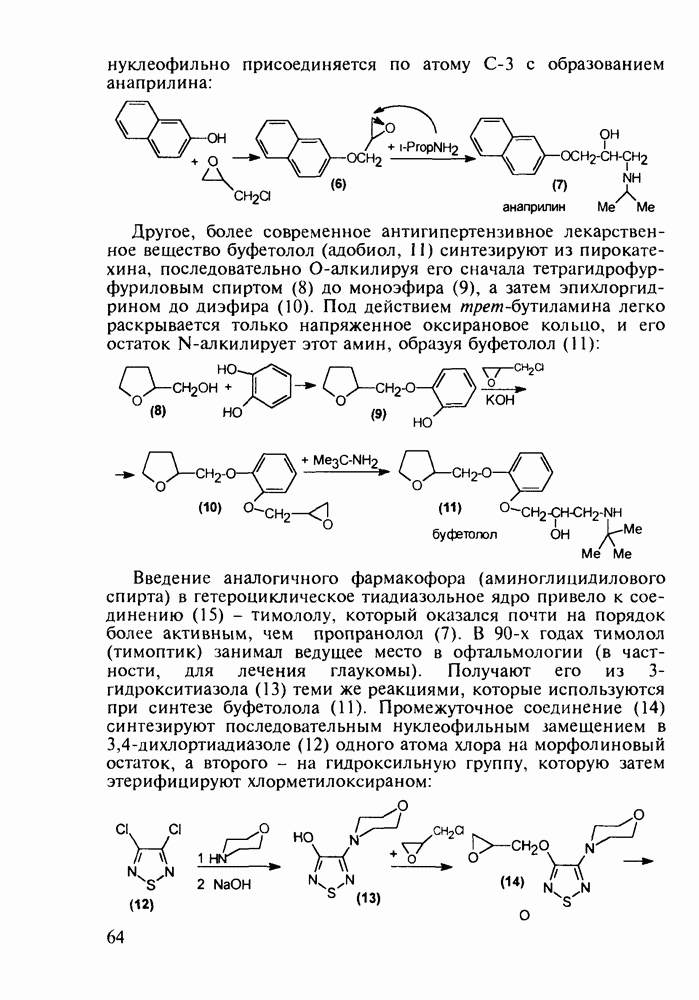
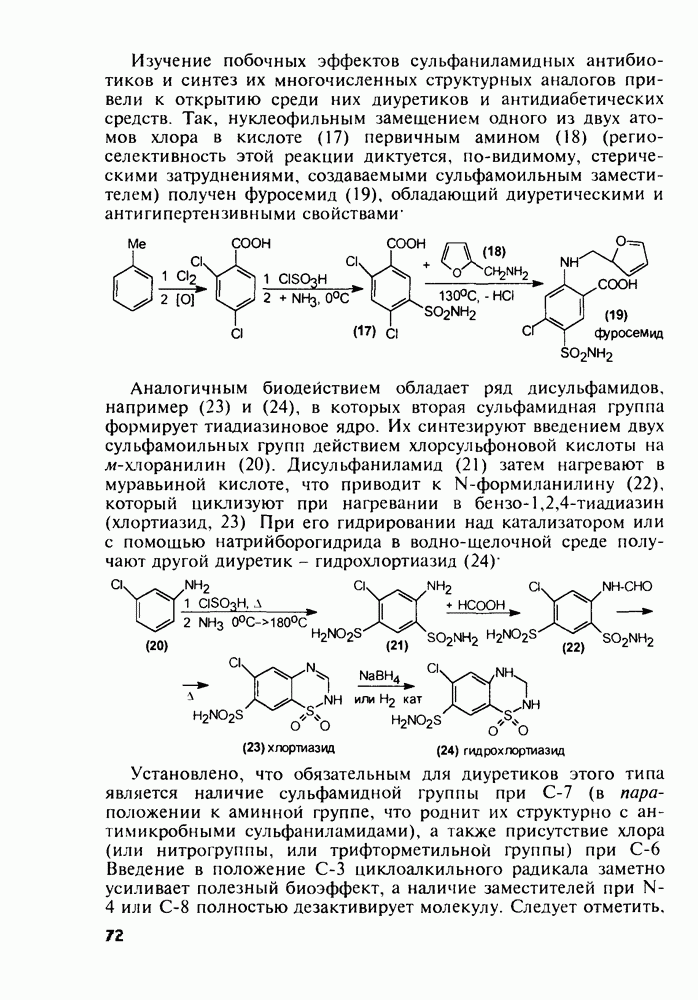
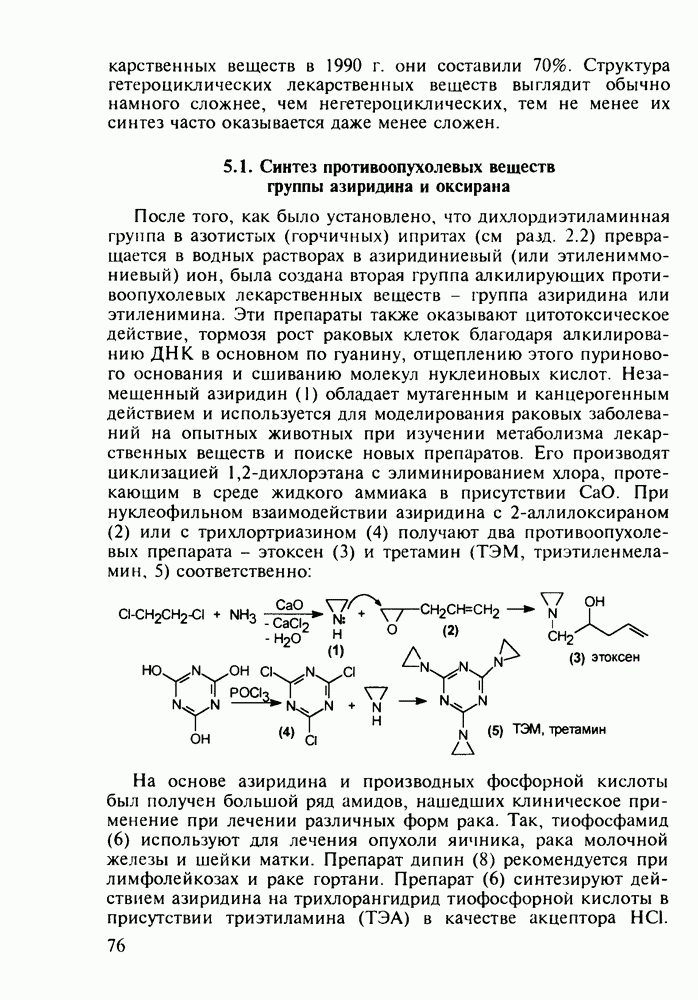
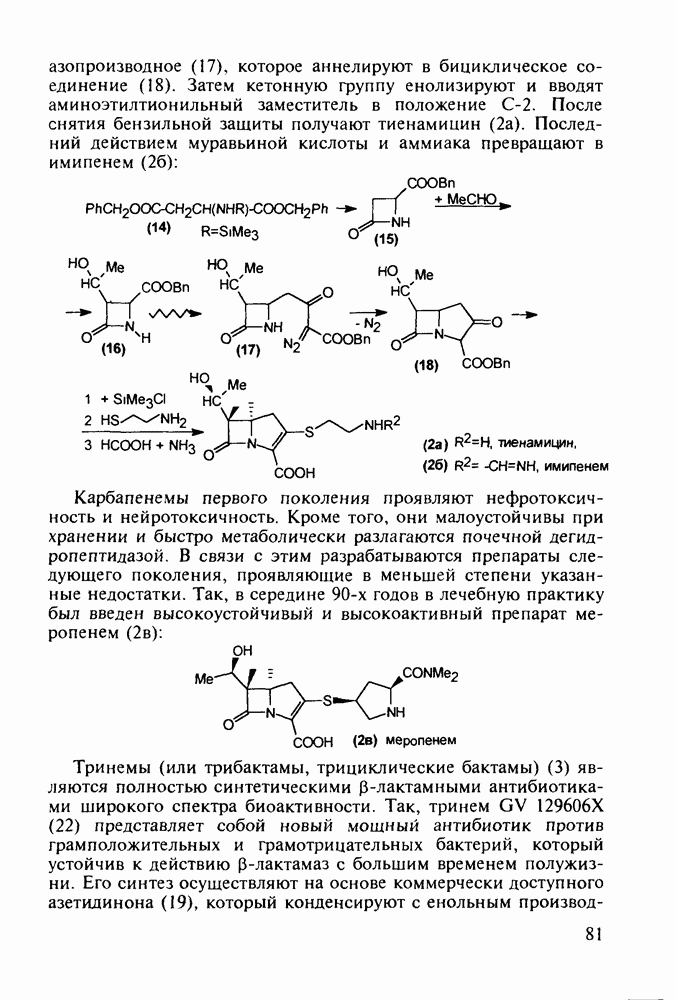
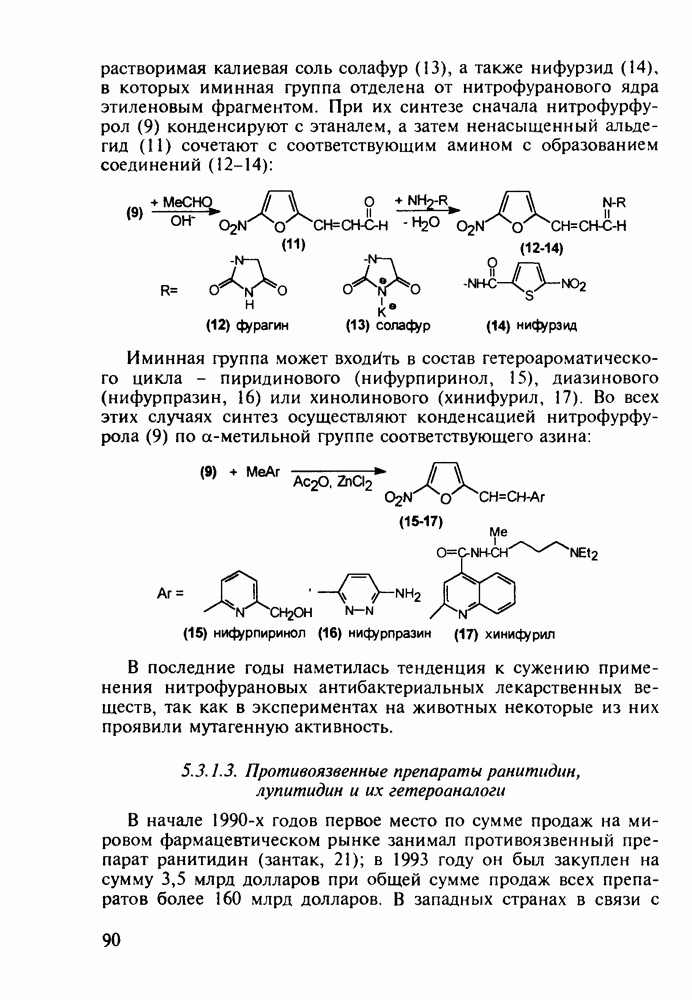
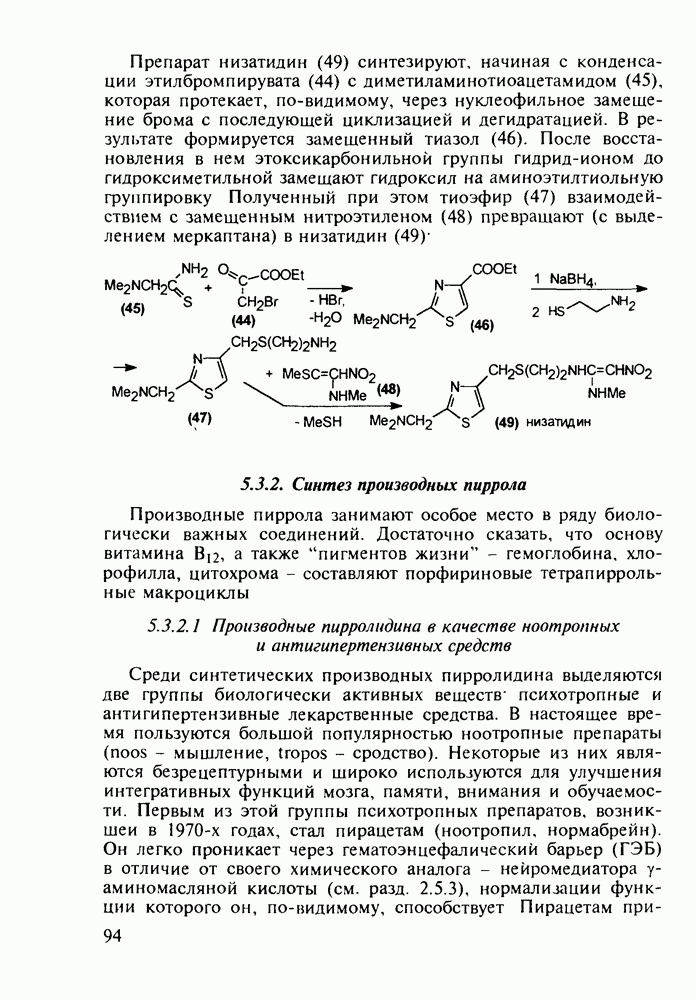
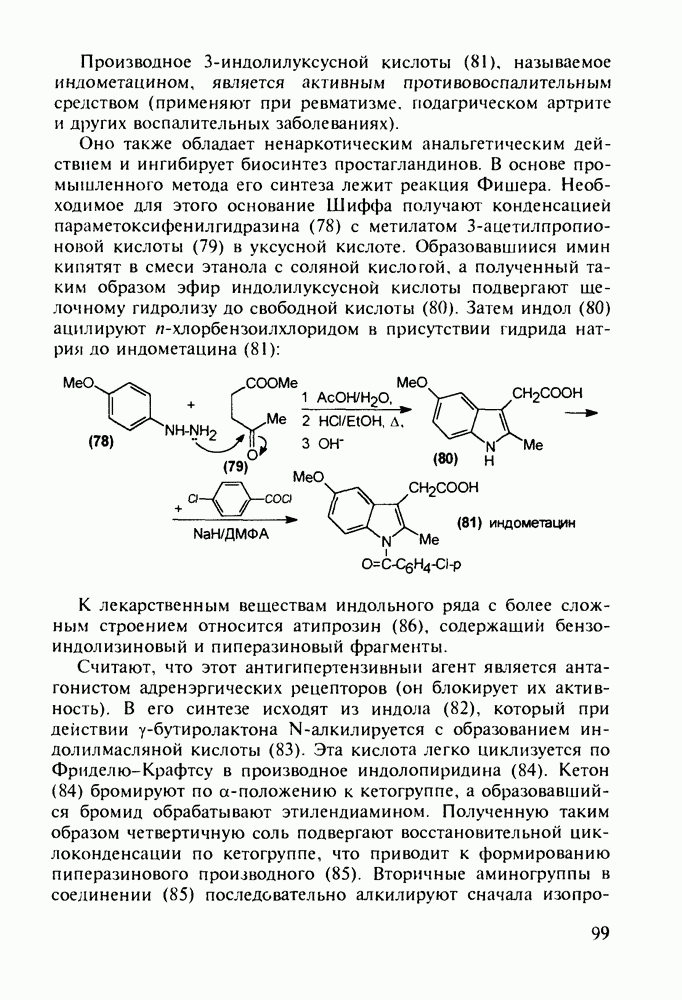
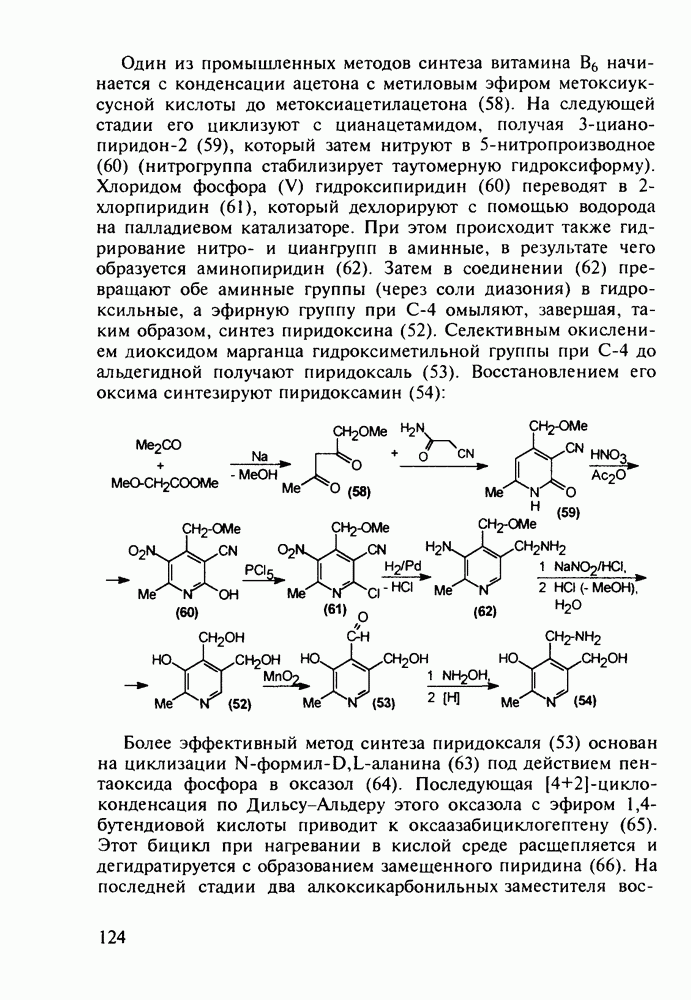
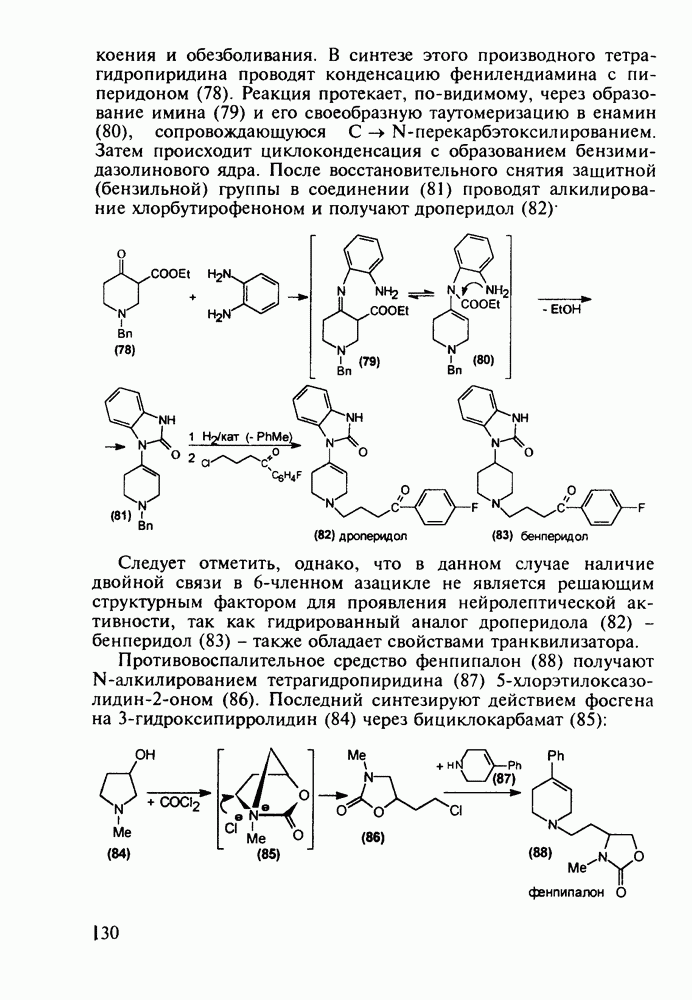
Диазепам (13) и оксазепам (15) получают аналогичным путем через диарилкетоны (20, 21, 23) и амид (22) В случае элениума (либриум, 14), а также альтернативного синтеза диазепама и оксазепама в качестве исходного соединения используют оксим диарилкетона (25). Этот оксим при его смешивании с хлорангидридом хлоруксусной кислоты легко цмклизуется в 2-хлорметилзамещенный хиназолин (26). Семичленный диазепиновый гетероцикл формируют расширением пиримидинового фрагмента этого хиназолина. Превращение начинается с атаки  -дефицитного атома С-2 пиримидинового фрагмента нуклеофильной частицей (гидроксилом или метиламином). Затем следует
-дефицитного атома С-2 пиримидинового фрагмента нуклеофильной частицей (гидроксилом или метиламином). Затем следует
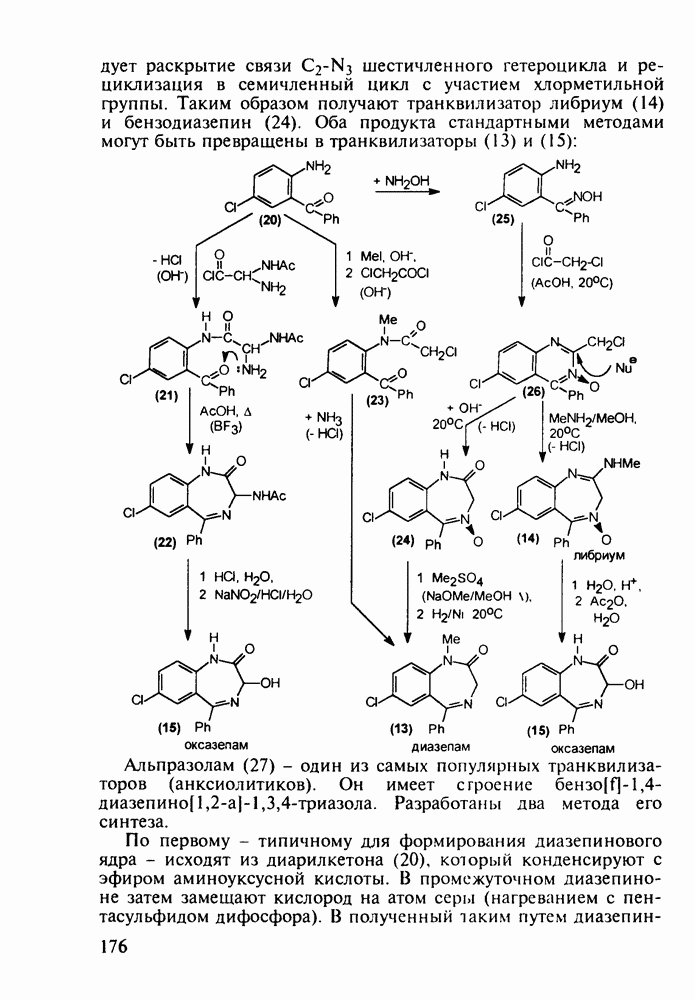
раскрытие связи  шестичленного гетероцикла и рециклизация в семичленный цикл с участием хлорметильной группы. Таким образом получают транквилизатор либриум (14) и бензодиазепин (24). Оба продукта стандартными методами могут быть превращены в транквилизаторы (13) и (15):
шестичленного гетероцикла и рециклизация в семичленный цикл с участием хлорметильной группы. Таким образом получают транквилизатор либриум (14) и бензодиазепин (24). Оба продукта стандартными методами могут быть превращены в транквилизаторы (13) и (15):

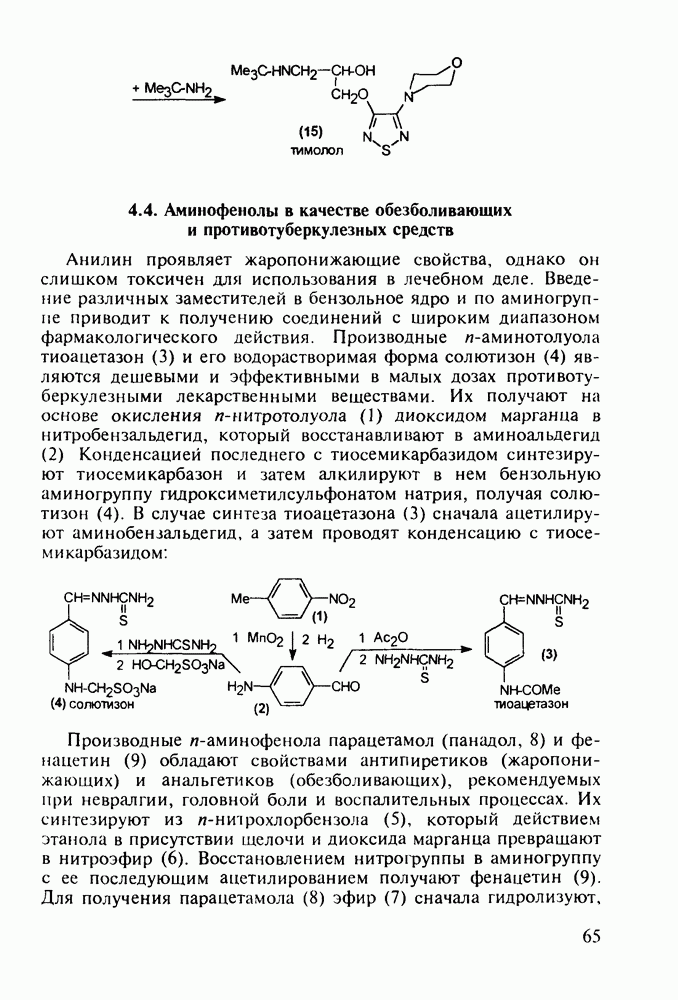
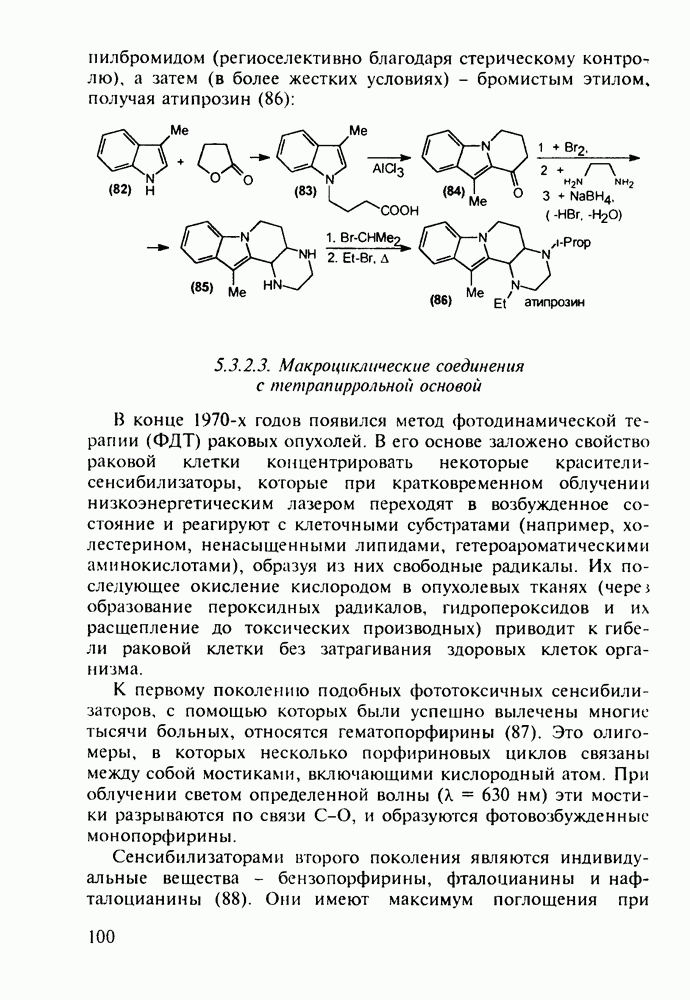
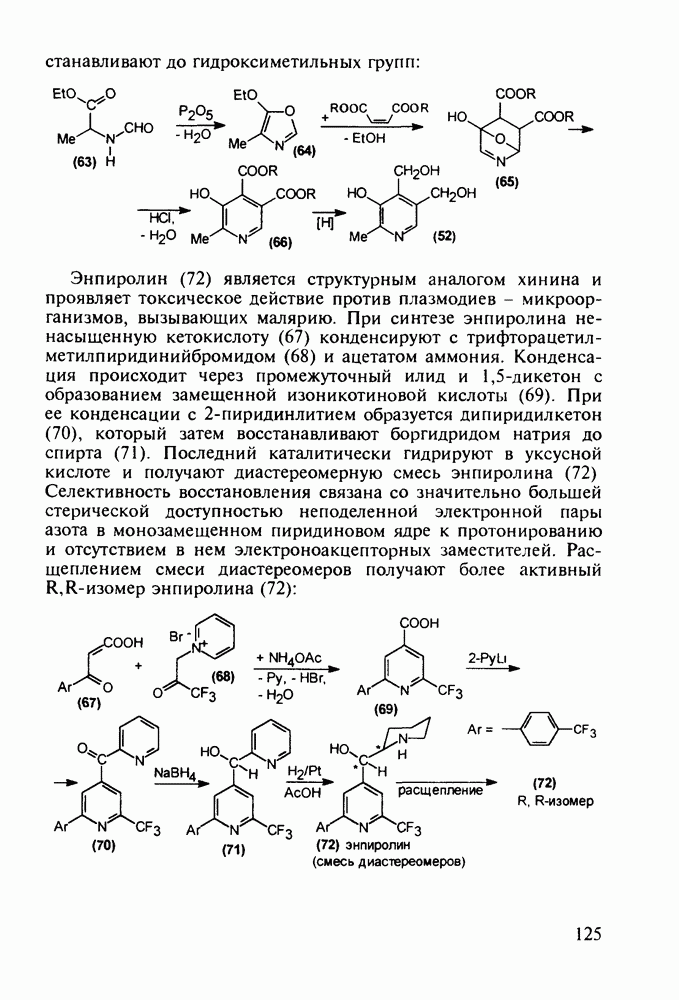
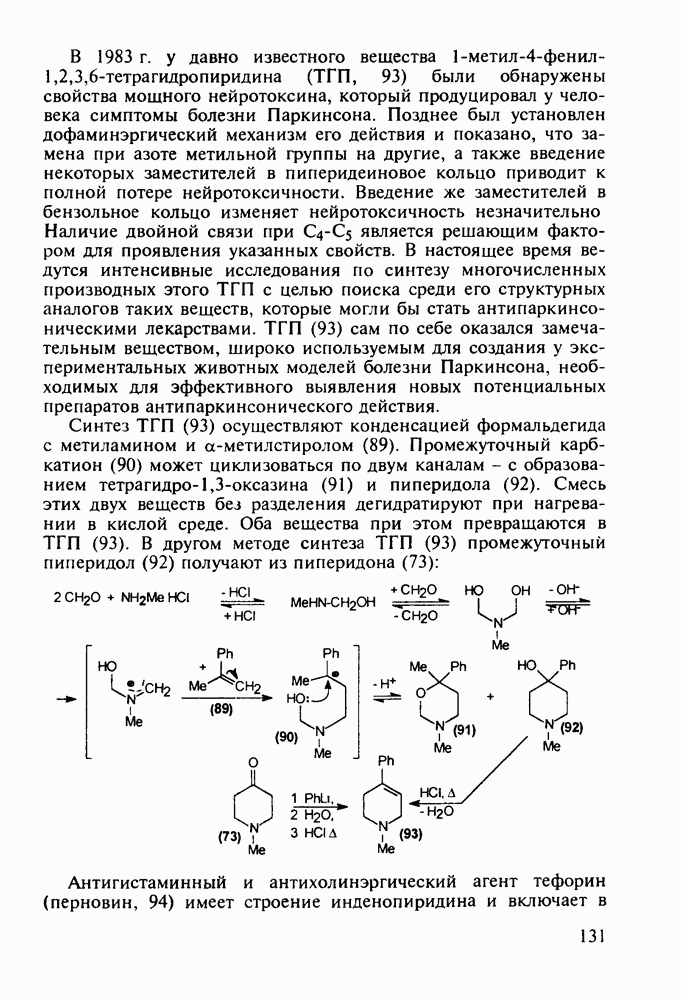
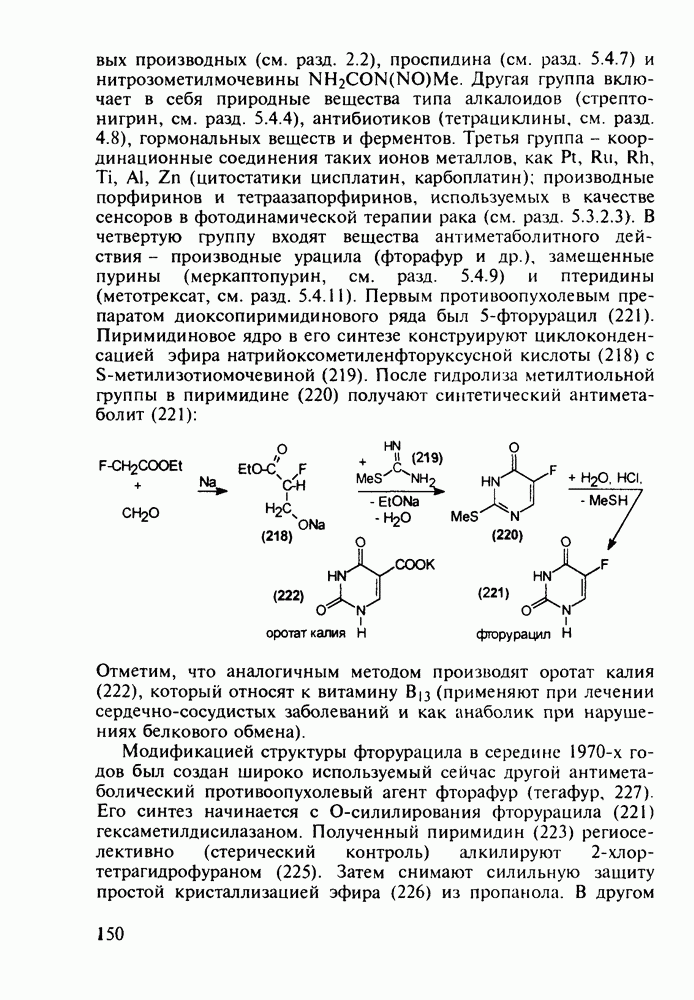
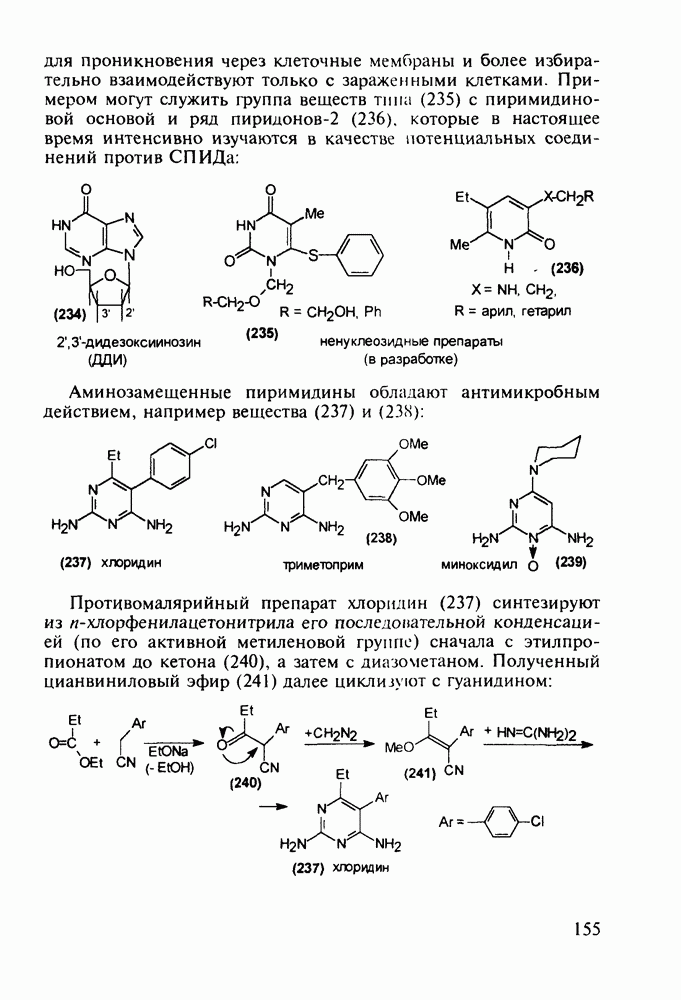
Альпразолам (27) - один из самых популярных транквилизаторов (анксиолитиков). Он имеет строение  Разработаны два метода его синтеза.
Разработаны два метода его синтеза.
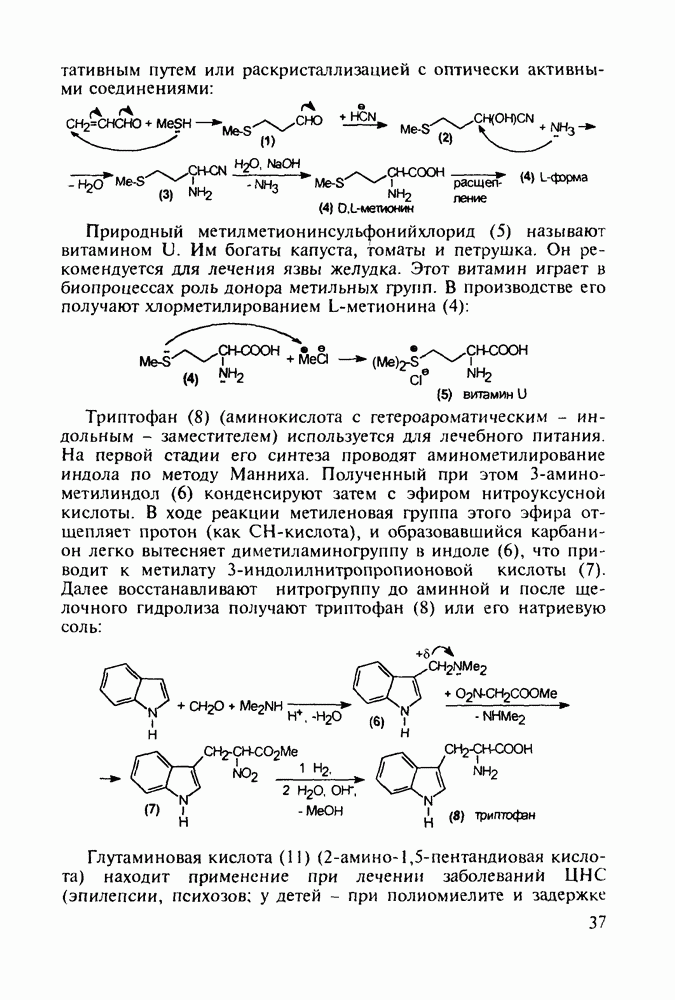
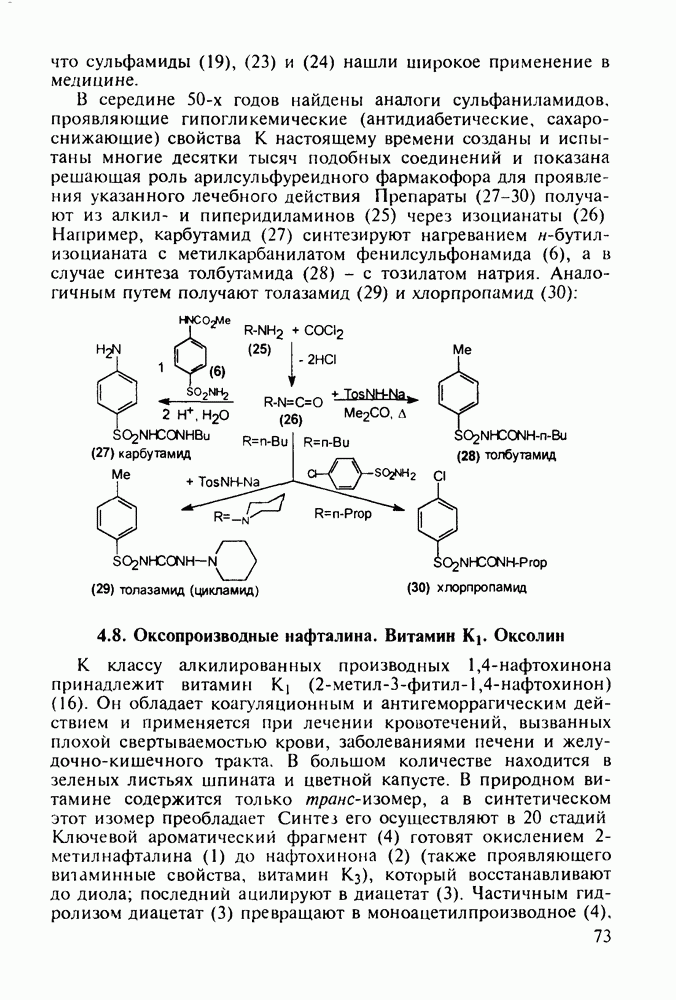
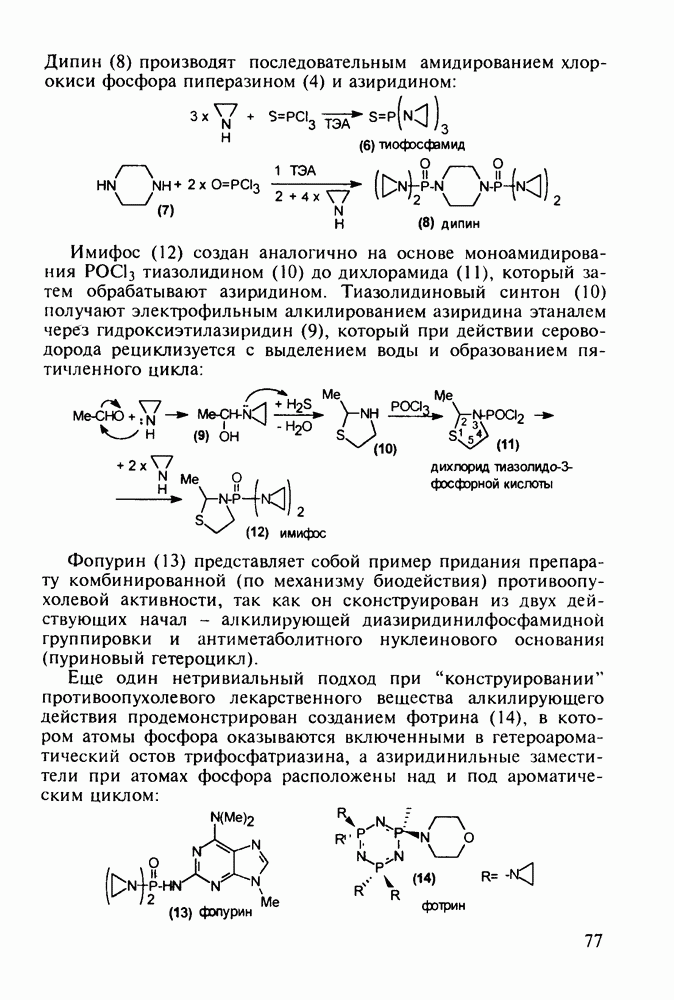
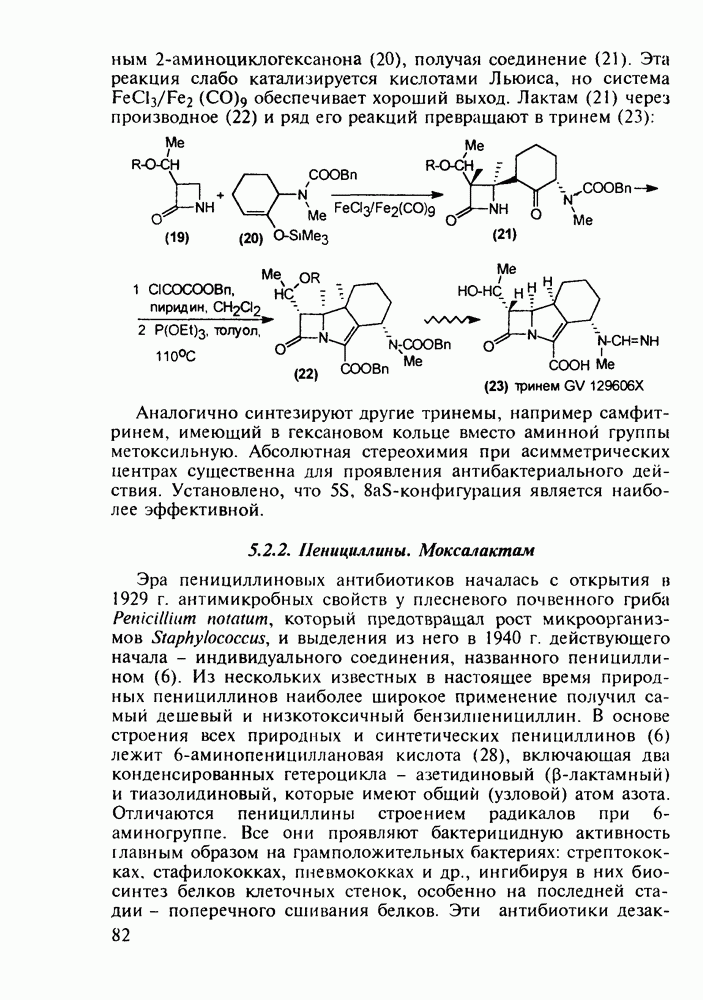
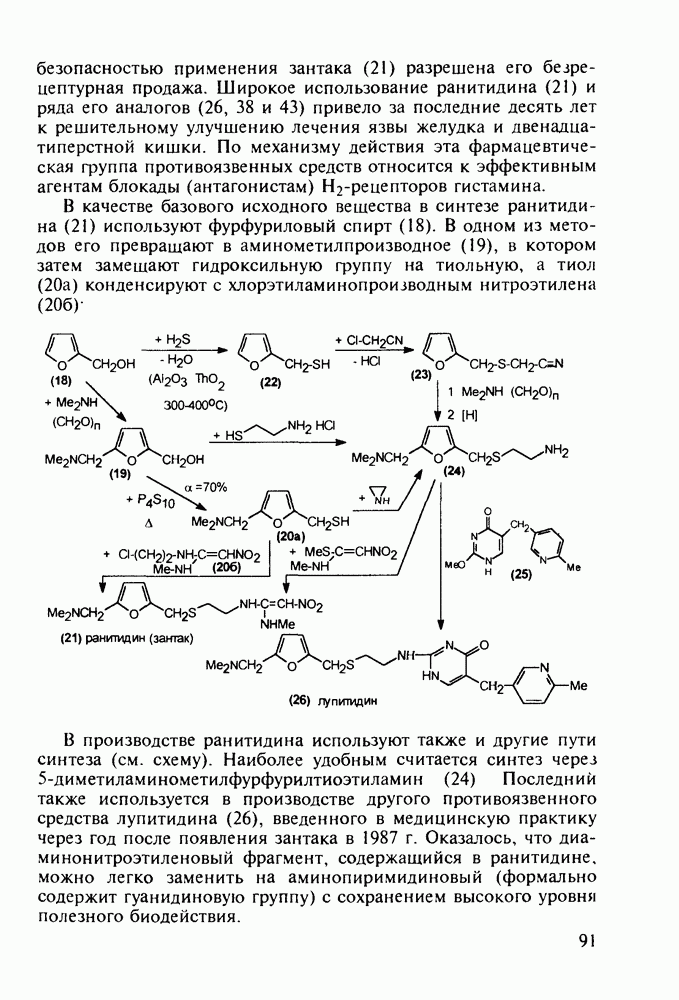
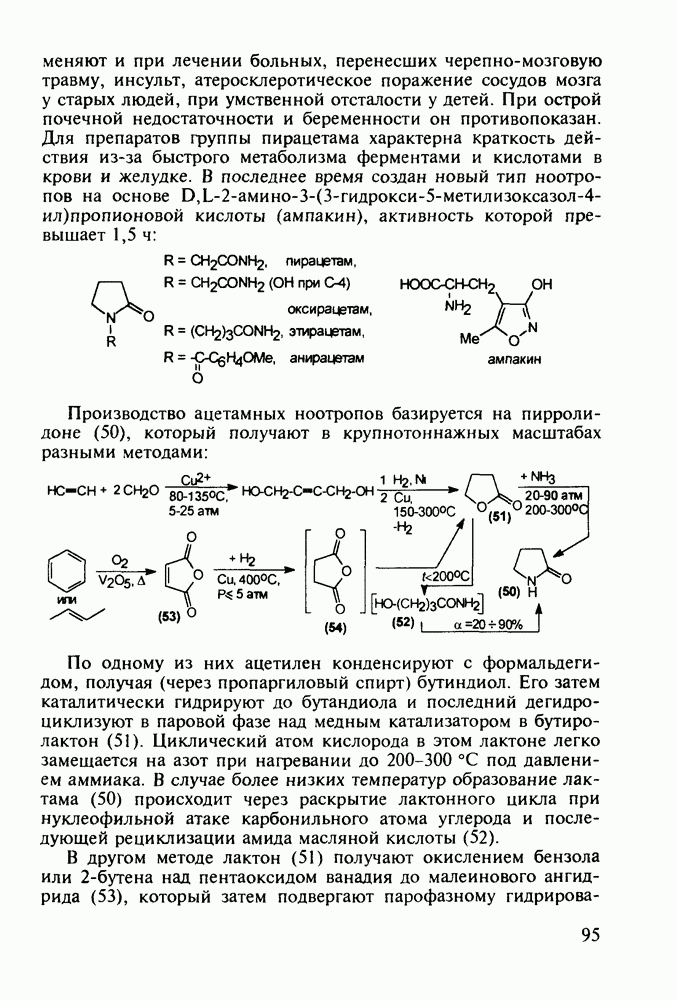
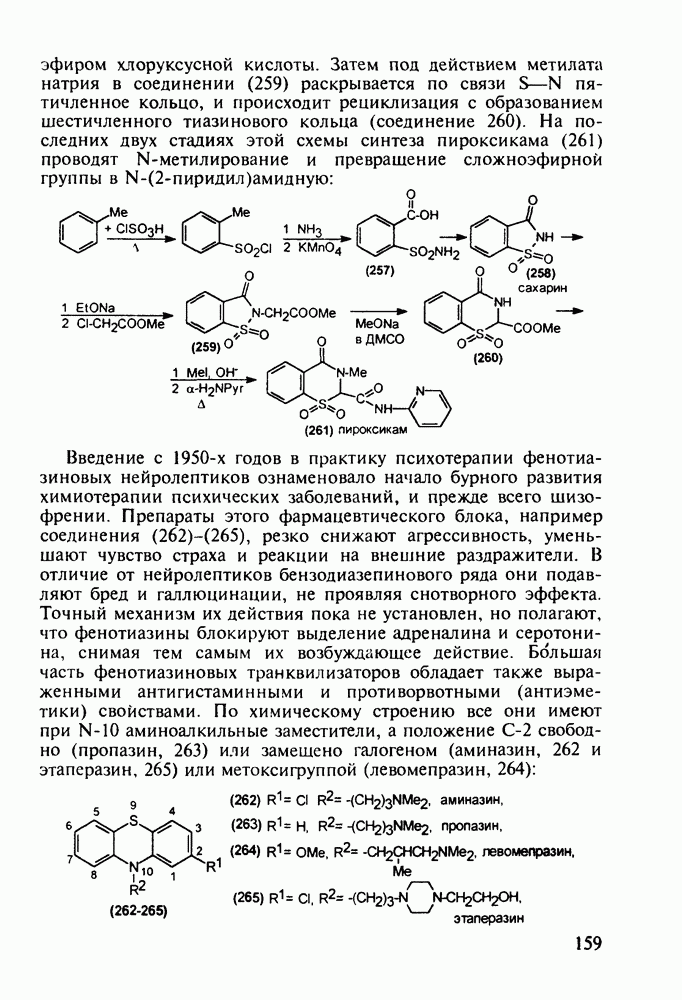
По первому - типичному для формирования диазепинового ядра - исходят из диарилкетона (20), который конденсируют с эфиром аминоуксусной кислоты. В промежуточном диазепиноне затем замещают кислород на атом серы (нагреванием с пентасульфидом дифосфора). В полученный таким путем диазепинтион
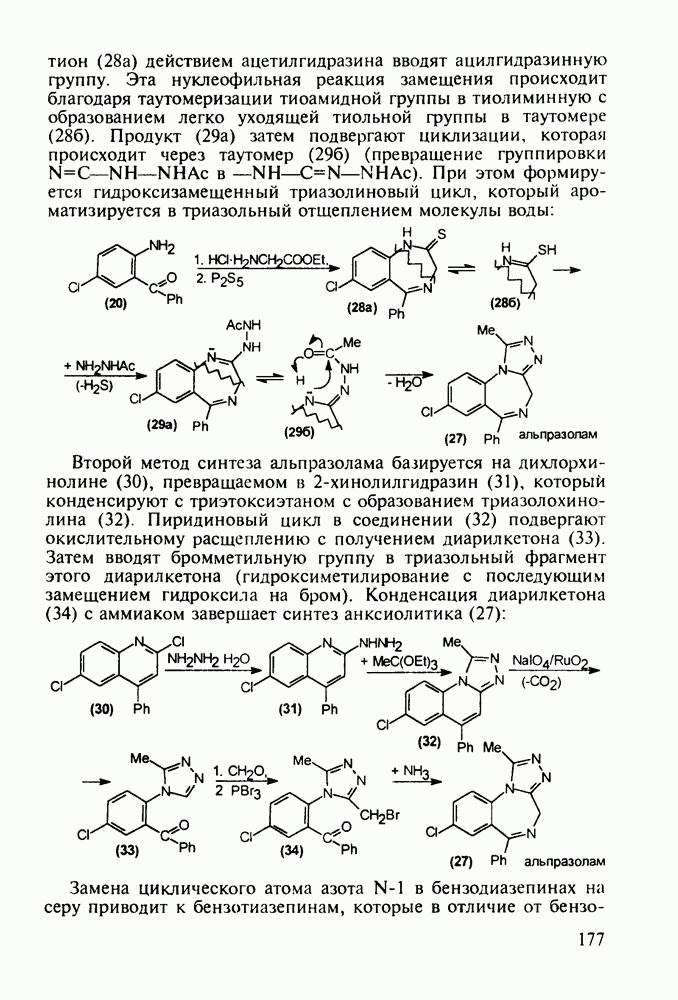
(28а) действием ацетилгидразина вводят ацилгидразинную группу. Эта нуклеофильная реакция замещения происходит благодаря таутомеризации тиоамидной группы в тиолиминную с образованием легко уходящей тиольной группы в таутомере (286). Продукт (29 а) затем подвергают циклизации, которая происходит через таутомер (296) (превращение группировки  . При этом формируется гидроксизамещенный триазолиновый цикл, который ароматизируется в триазольный отщеплением молекулы воды:
. При этом формируется гидроксизамещенный триазолиновый цикл, который ароматизируется в триазольный отщеплением молекулы воды:

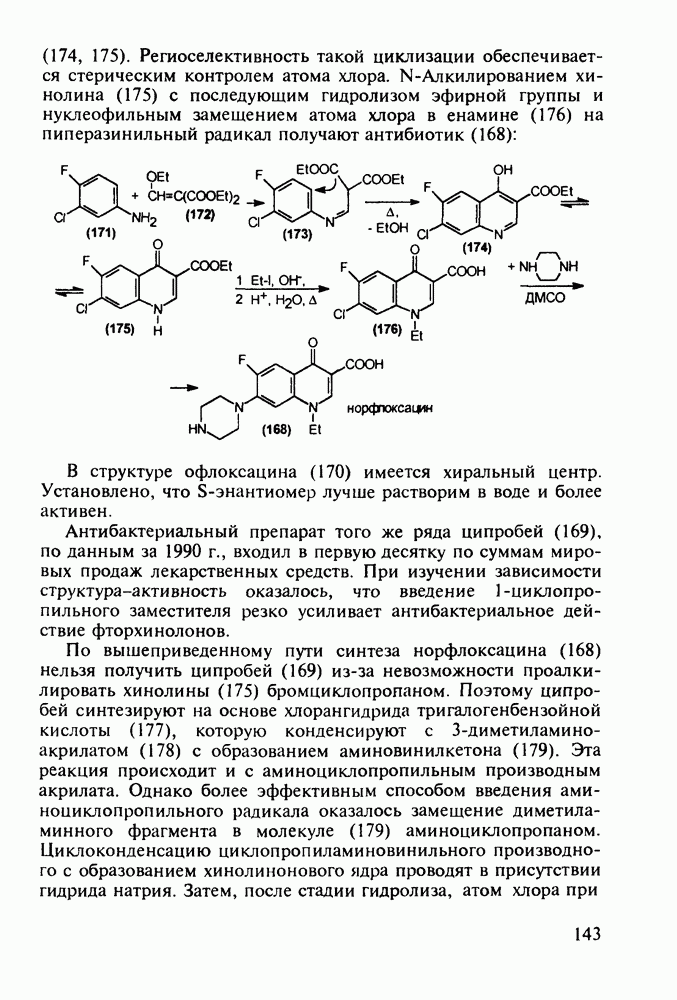
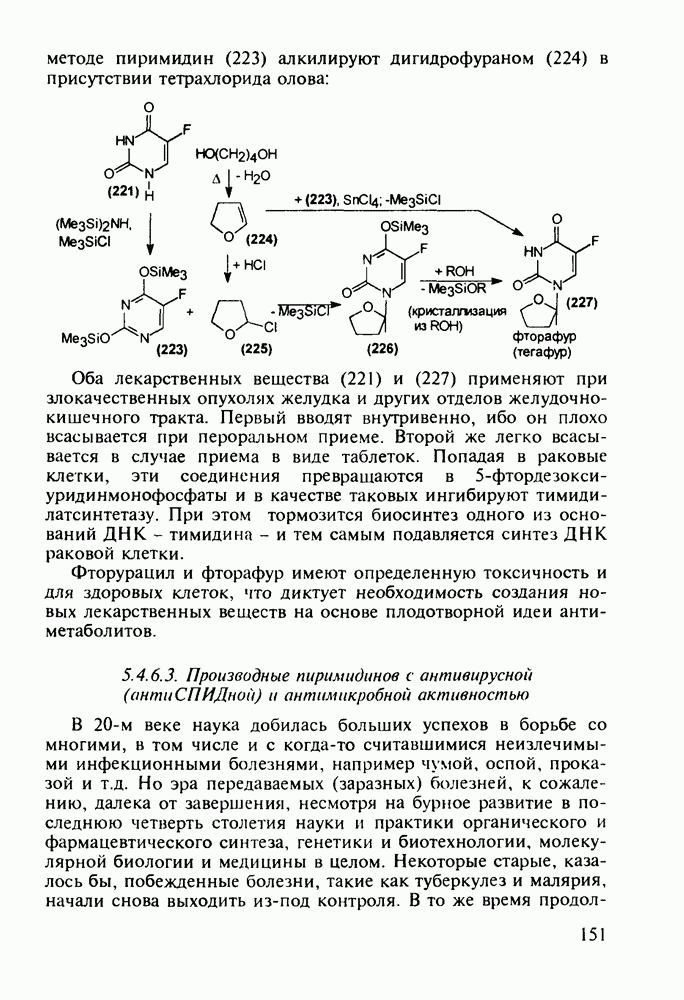
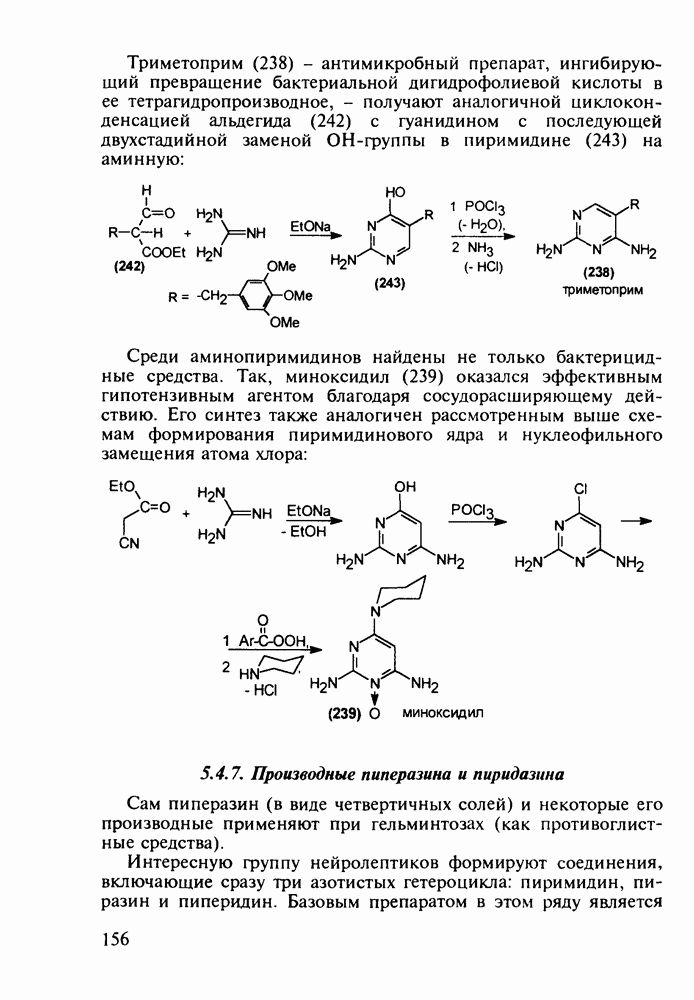
Второй метод синтеза альпразолама базируется на дихлорхинолине (30), превращаемом в 2-хинолилгидразин (31), который конденсируют с триэтоксиэтаном с образованием триазолохинолина (32). Пиридиновый цикл в соединении (32) подвергают окислительному расщеплению с получением диарилкетона (33). Затем вводят бромметильную группу в триазольный фрагмент этого диарилкетона (гидроксиметилирование с последующим замещением гидроксила на бром). Конденсация диарилкетона (34) с аммиаком завершает синтез анксиолитика (27):

Замена циклического атома азота  в бензодиазепинах на серу приводит к бензотиазепинам, которые в отличие от бензодиазепинов
в бензодиазепинах на серу приводит к бензотиазепинам, которые в отличие от бензодиазепинов
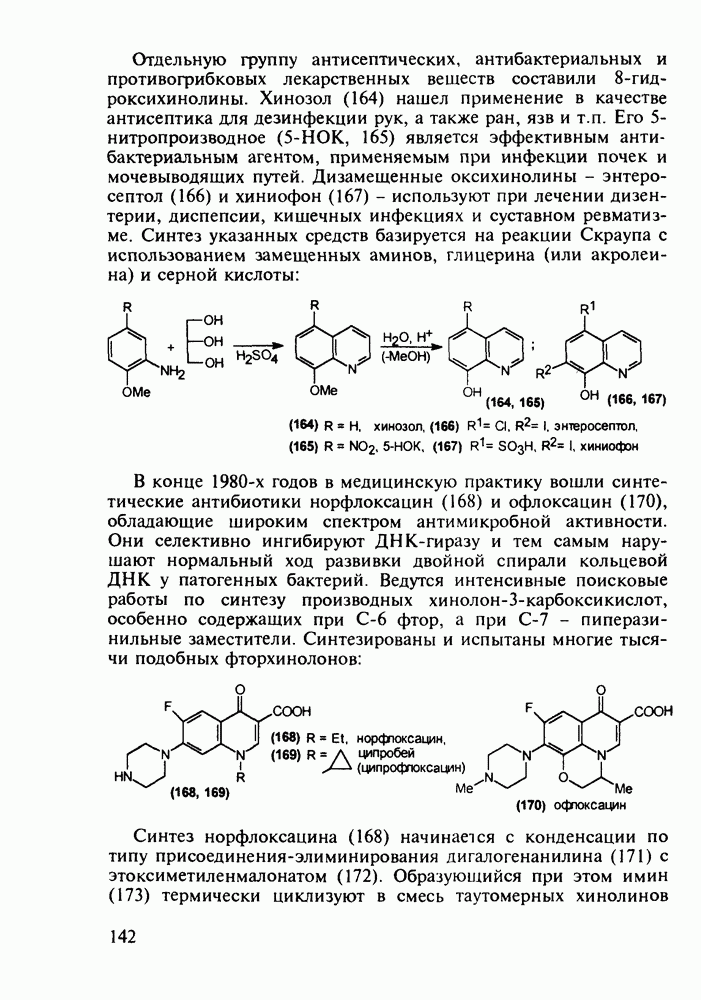
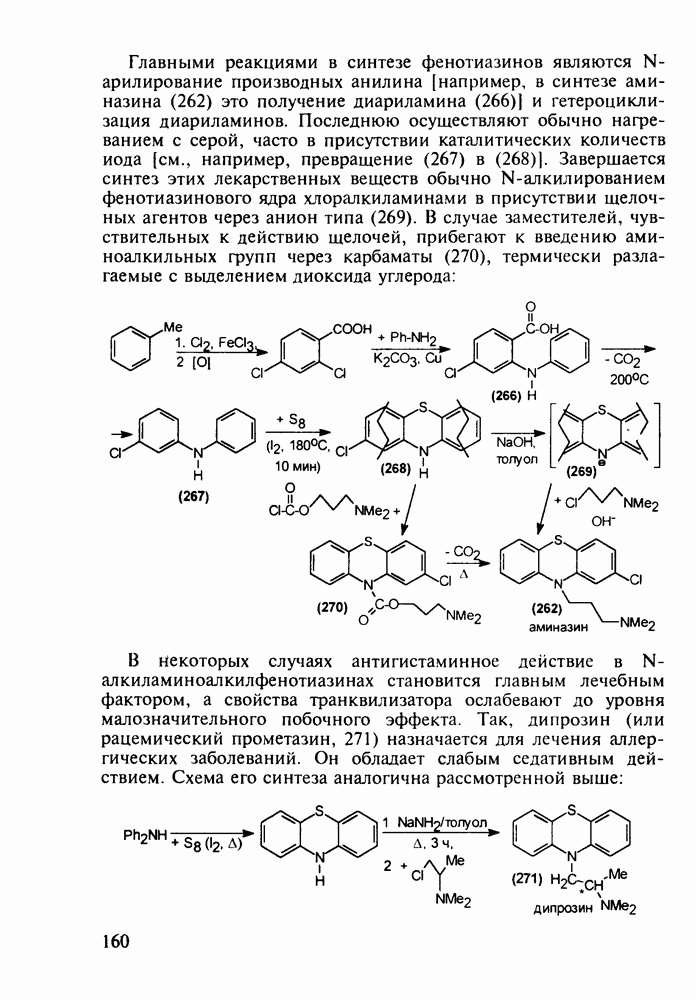
не обладают выраженными седативными свойствами. Среди производных бензотиазепинов найдены антагонисты кальциевых каналов. Лекарственное вещество кардизем (дил-тиазем, 35) широко используют в качестве гипотензивного средства (13-е место по сумме продаж в мире в начале 1990-х годов).
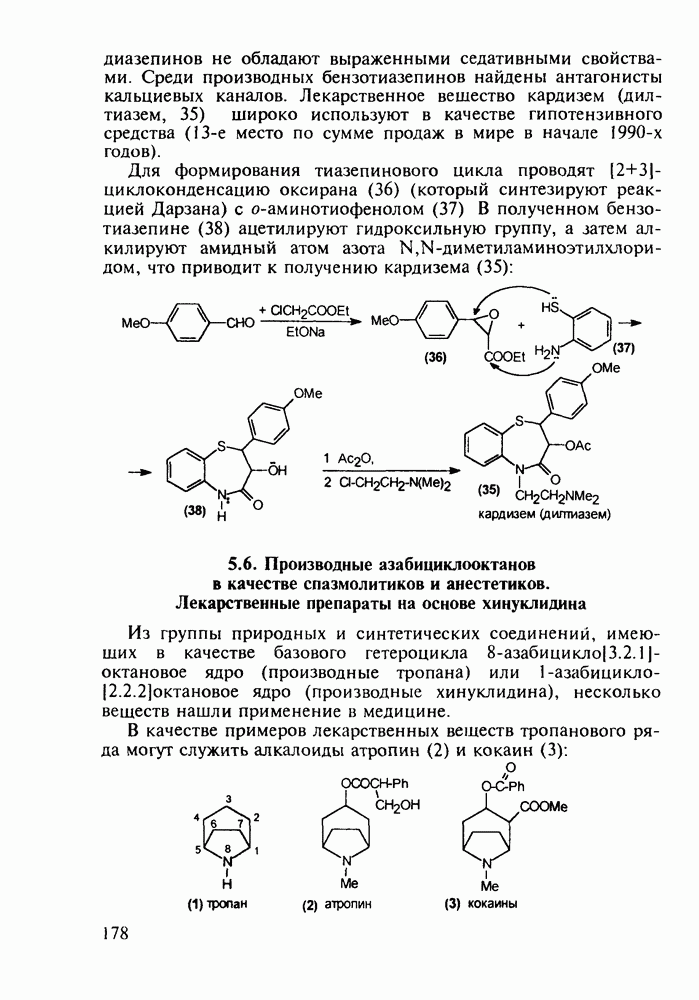
Для формирования тиазепинового цикла проводят [ -циклоконденсацию оксирана (36) (который синтезируют реакцией Дарзана) с
-циклоконденсацию оксирана (36) (который синтезируют реакцией Дарзана) с  -аминотиофенолом (37) В полученном бензотиазепине (38) ацетилируют гидроксильную группу, а затем алкилируют амидный атом азота
-аминотиофенолом (37) В полученном бензотиазепине (38) ацетилируют гидроксильную группу, а затем алкилируют амидный атом азота  -диметиламиноэтилхлоридом, что приводит к получению кардизема (35):
-диметиламиноэтилхлоридом, что приводит к получению кардизема (35):

| << Предыдущий параграф | Следующий параграф >> |
- Предисловие
- 1. ВВЕДЕНИЕ
- 1.1. Эволюция органической химии лекарственных веществ
- 1.2. Современные требования к лекарственным веществам
- 1.3. Стадии биологического изучения лекарственного вещества
- 1.4. Основы стратегии создания новых синтетических лекарственных веществ
- 1.5. Связь структура-биологическая активность
- 1.6. Принципиальная схема разработки нового лекарственного вещества
- 1.7. Классификация лекарственных веществ
- 1.8. Основные болезни человека и ведущие группы лекарственных веществ на современном фармацевтическом рынке
- 2. СИНТЕЗ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ АЛИФАТИЧЕСКОГО РЯДА
- 2.2. Группа противораковых веществ с дихлордиэтиламинным фармакофором
- 2.3. Алканолы, аминоалканолы и их эфиры. Нейромедиатор ацетилхолин и холиномиметики
- 2.4. Альдегиды и кислоты. Витамины F и B15
- 2.5. Аминокислоты
- 2.5.2. Производные b-аминокислот. Витамин B3
- 2.5.3. Производные у-аминомасляной кислоты. Нейротропные средства. Витамин BT
- 2.5.4. Другие аминокислоты
- 3. ЛЕКАРСТВЕННЫЕ ВЕЩЕСТВА АЛИЦИКЛИЧЕСКОГО РЯДА
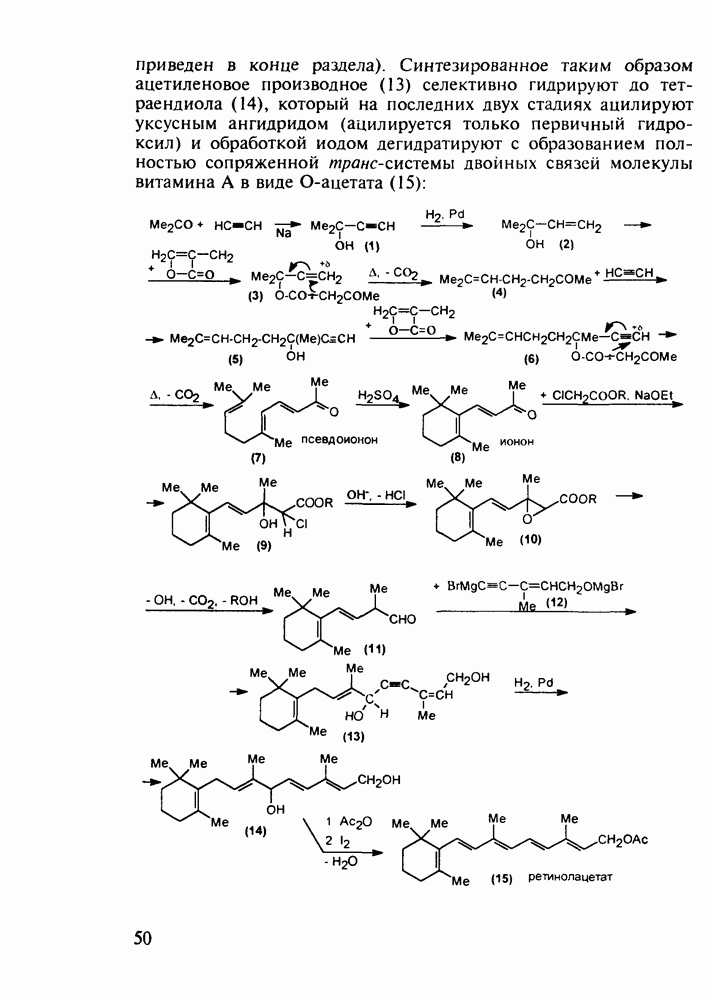
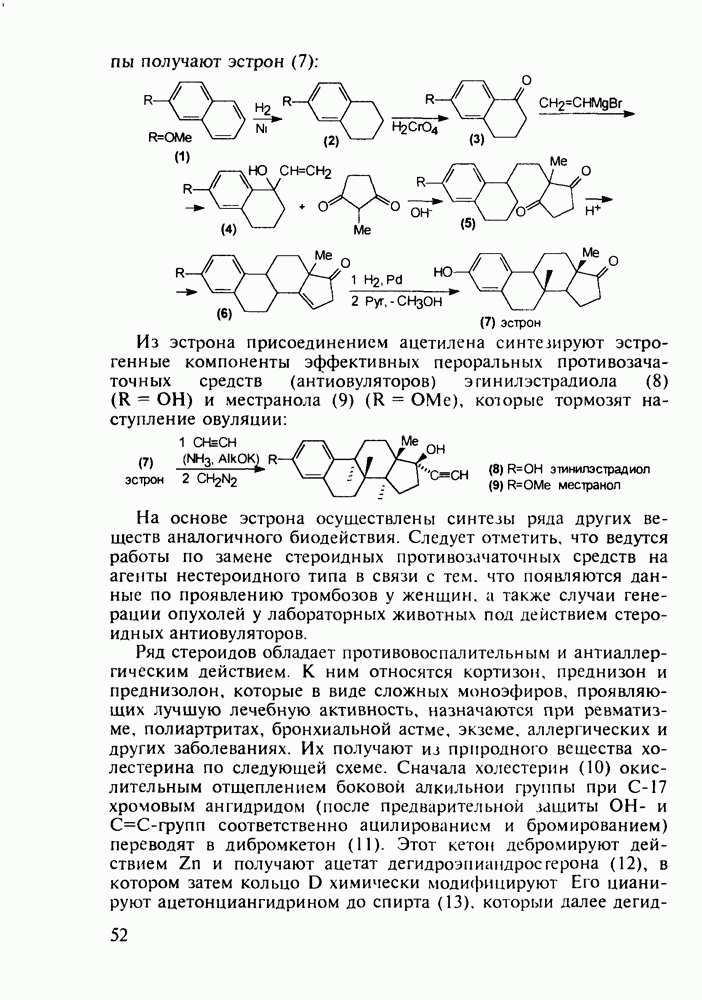
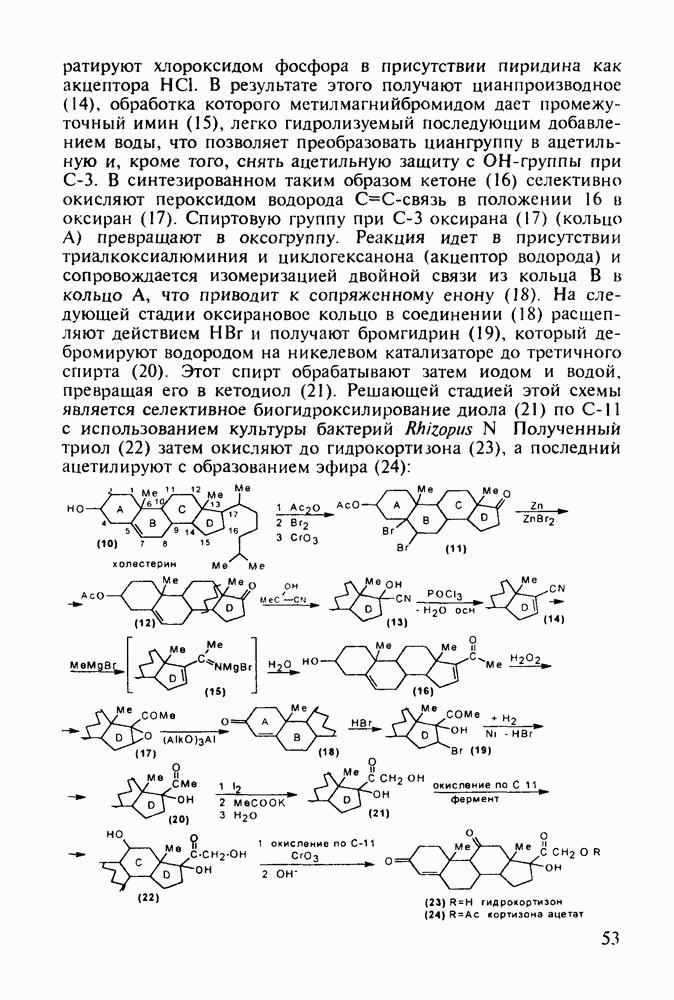
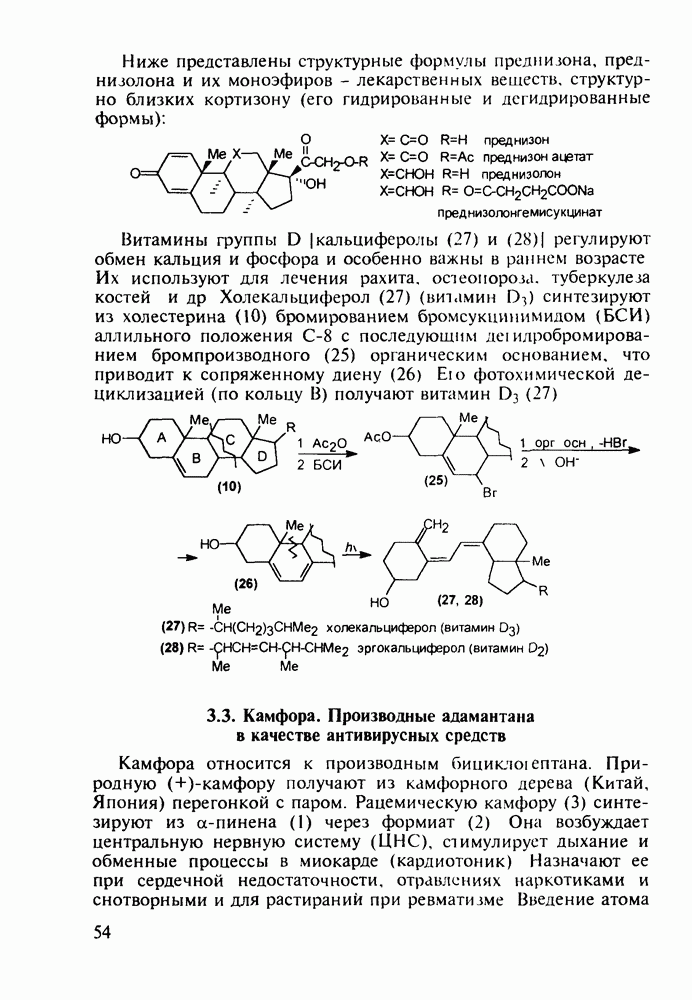
- 3.2. Противозачаточные и противовоспалительные вещества на основе циклопентафенантрена. Синтез витамина D
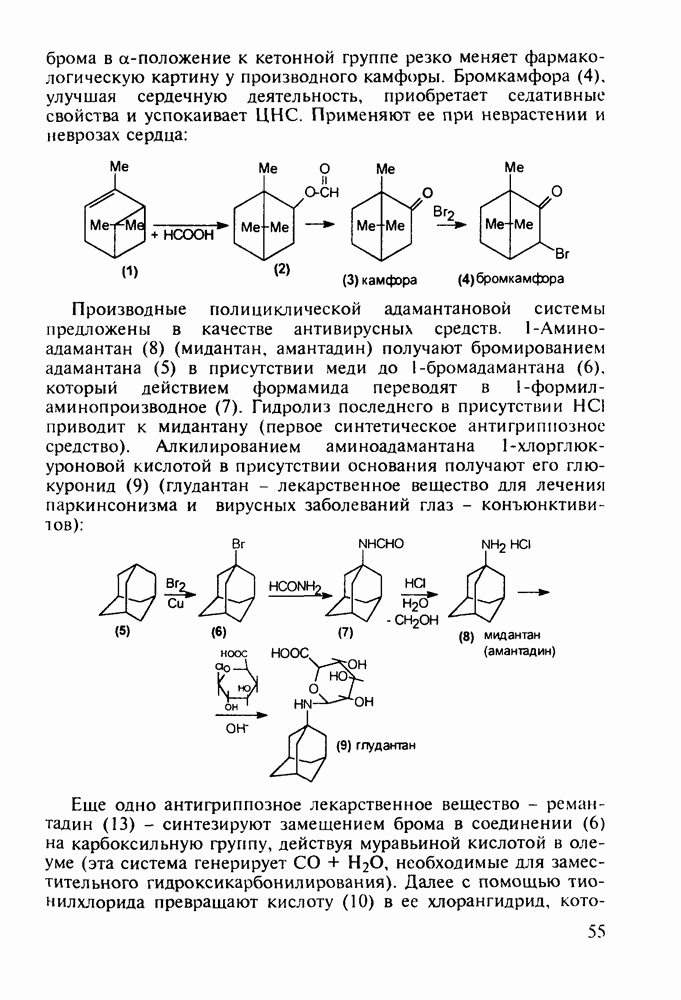
- 3.3. Камфора. Производные адамантана в качестве антивирусных средств
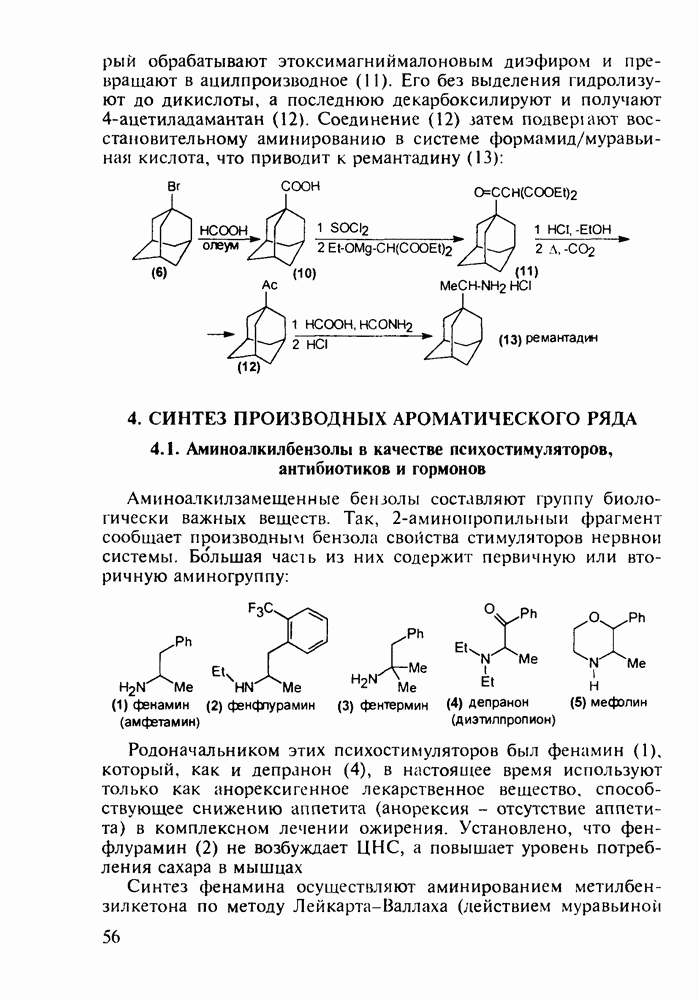
- 4. СИНТЕЗ ПРОИЗВОДНЫХ АРОМАТИЧЕСКОГО РЯДА
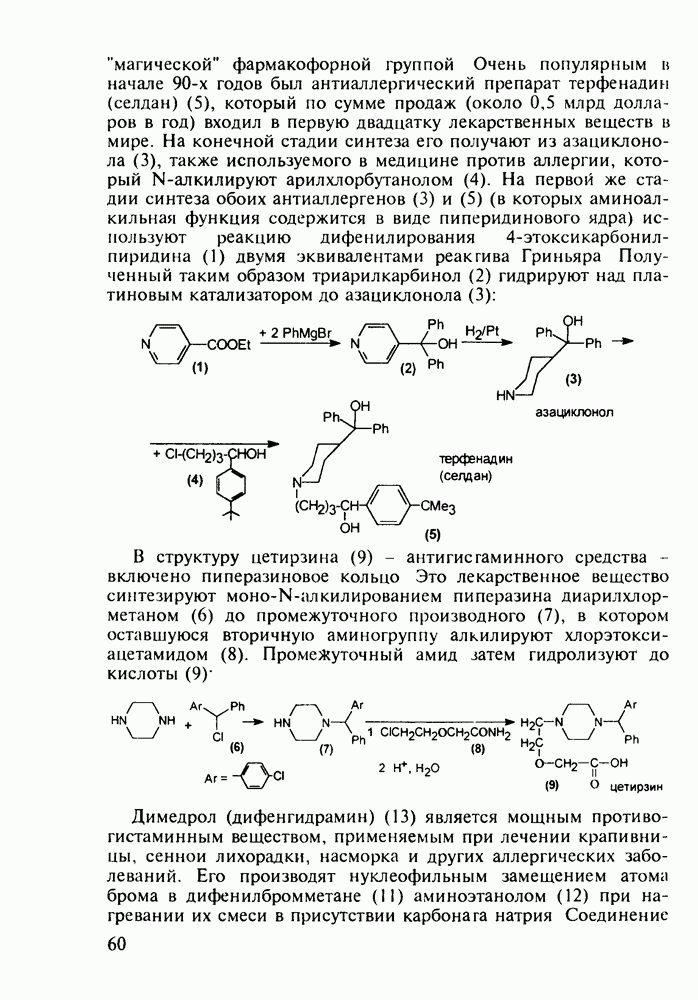
- 4.2. Антигистаминные препараты группы диарилметана
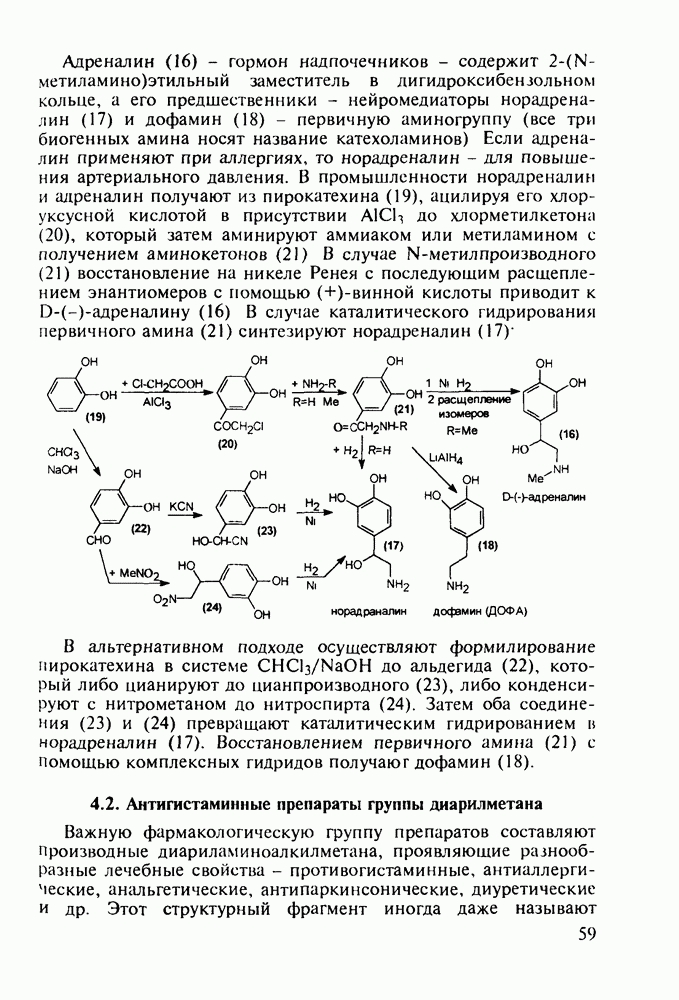
- 4.3. Антисептики и адреноблокаторы фенольного ряда
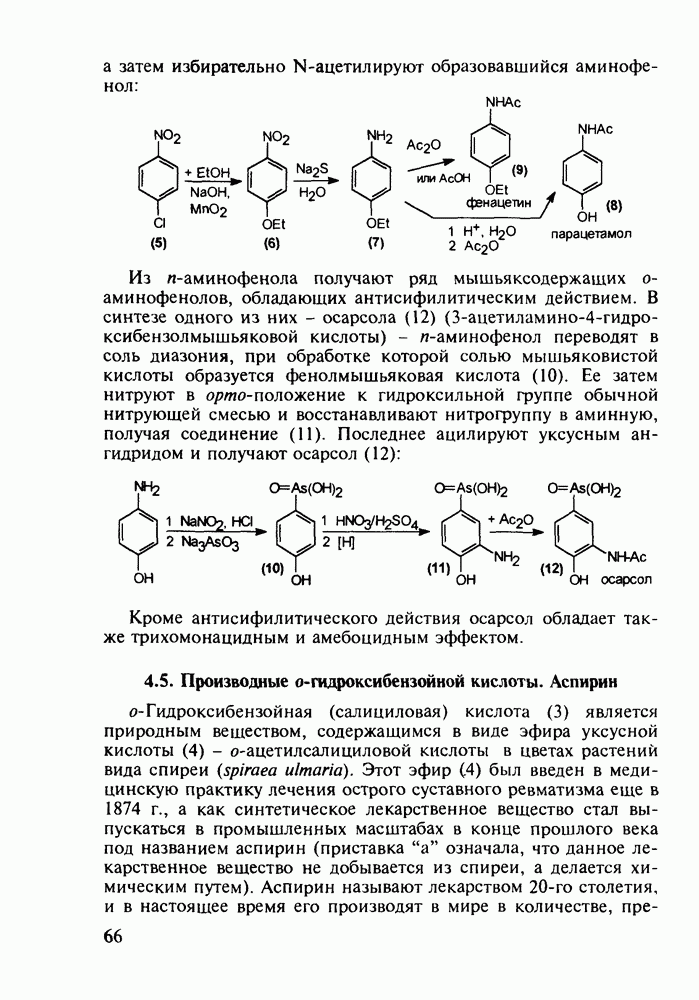
- 4.4. Аминофенолы в качестве обезболивающих и противотуберкулезных средств
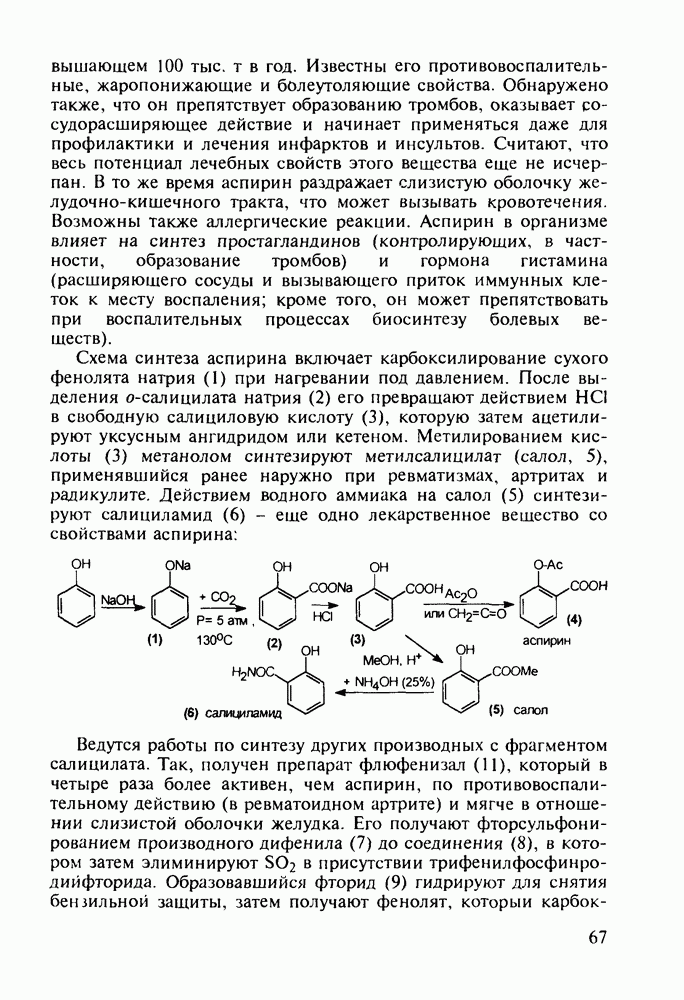
- 4.5. Производные о-гидроксибензойной кислоты. Аспирин
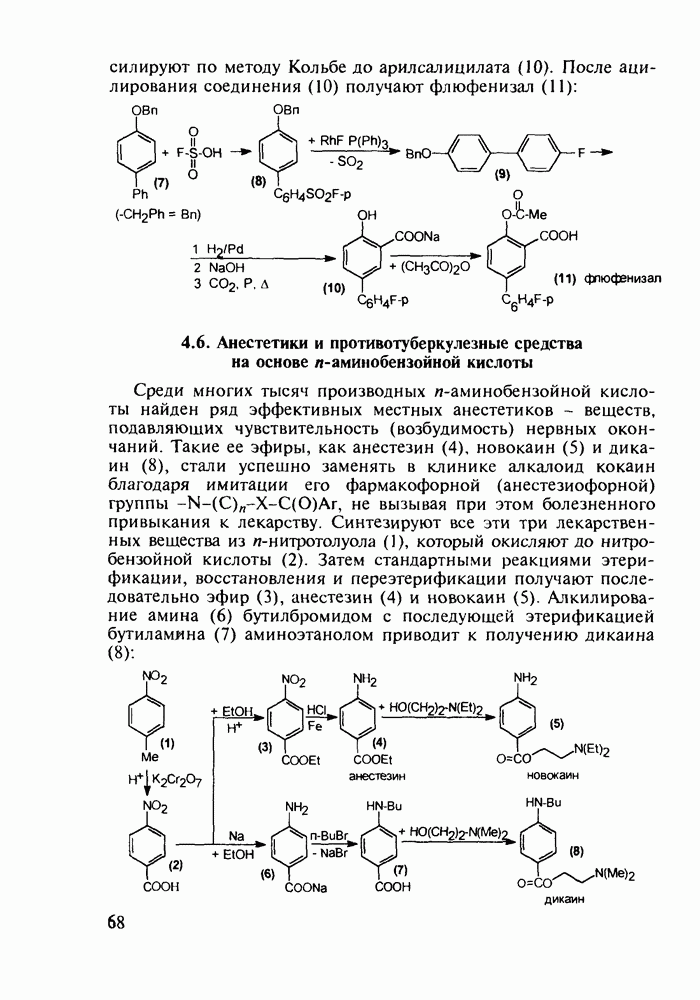
- 4.6. Анестетики и противотуберкулезные средства на основе n-аминобензойной кислоты
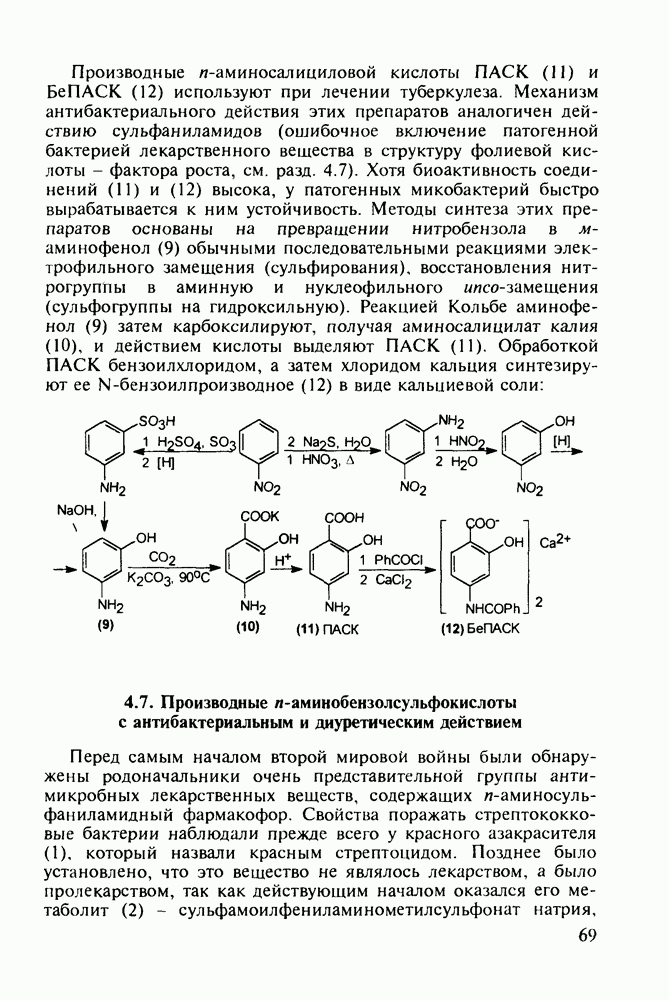
- 4.7. Производные n-аминобензолсульфокислоты с антибактериальным и диуретическим действием
- 4.8. Оксопроизводные нафталина. Витамин К1. Оксолин
- 5. ХИМИЯ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ С БАЗОВЫМ ГЕТЕРОЦИКЛИЧЕСКИМ ФРАГМЕНТОМ
- 5.2. Антибиотики, содержащие четырехчленное азетидиновое ядро
- 5.2.2. Пенициллины. Моксалактам
- 5.2.3. Цефалоспорины
- 5.3. Лекарственные вещества на основе пятичленных гетероциклов
- 5.3.2. Синтез производных пиррола
- 5.3.3. Оксазолидины. Антибиотик циклосерин
- 5.3.4. Антипиретики и анальгетики пиразолинового ряда
- 5.3.5. Имидазолы с противопаразитарной, антигипертензивной и другой биоактивностью
- 5.3.6. Производные тиазола. Витамин В1
- 5.3.7. Психостимуляторы с оксадиазольным и тетразольным гетероциклами
- 5.4. Синтез лекарственных веществ, содержащих шестичленные гетероциклы
- 5.4.2. Синтез лекарственных веществ пиридинового ряда
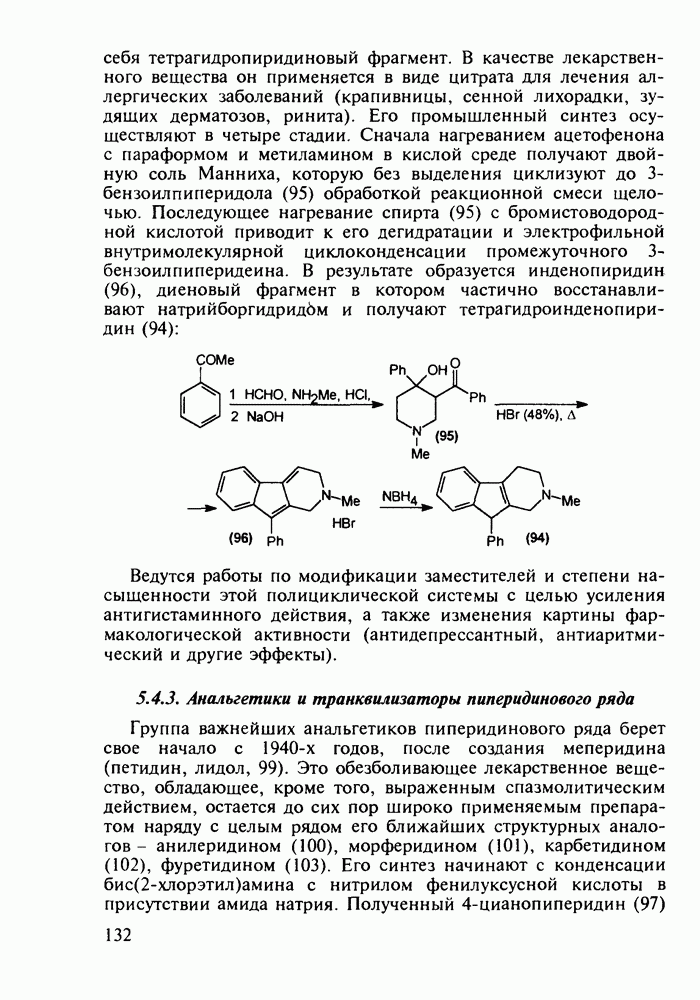
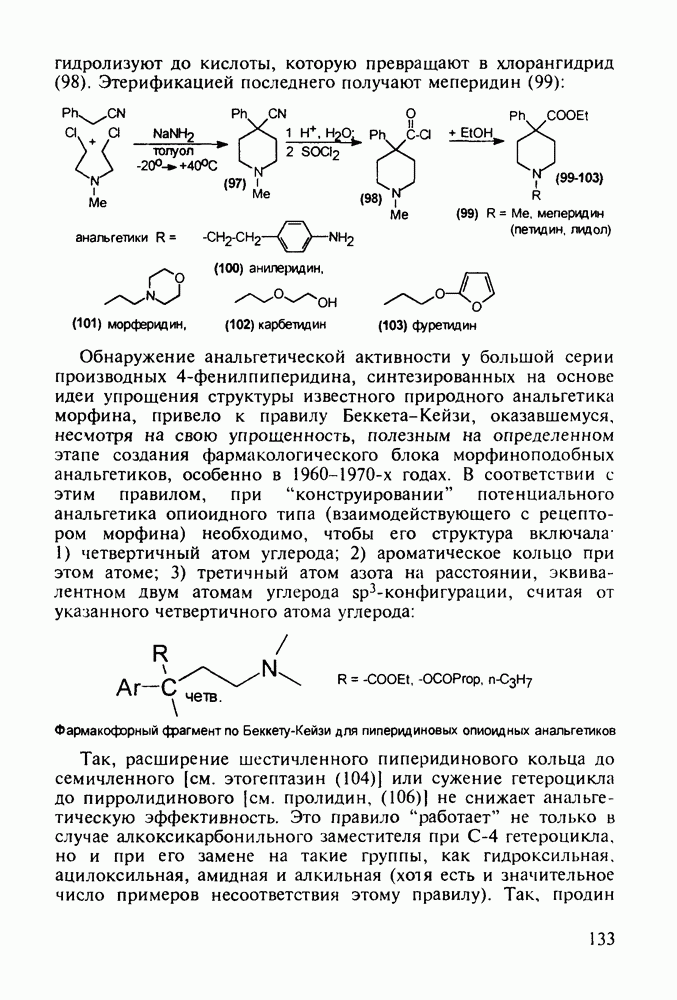
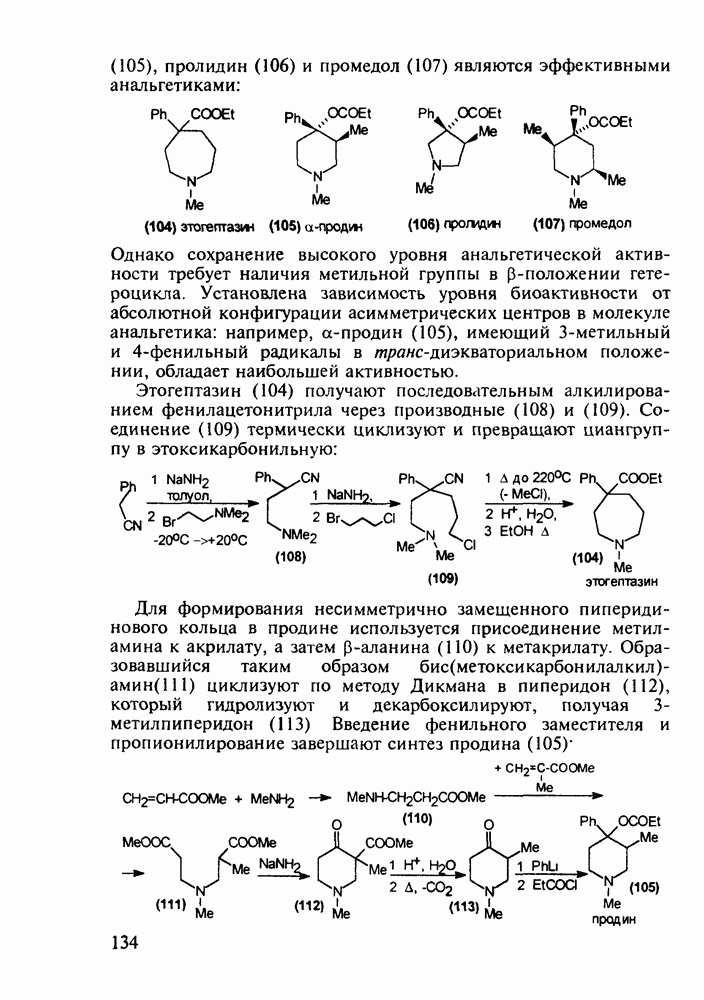
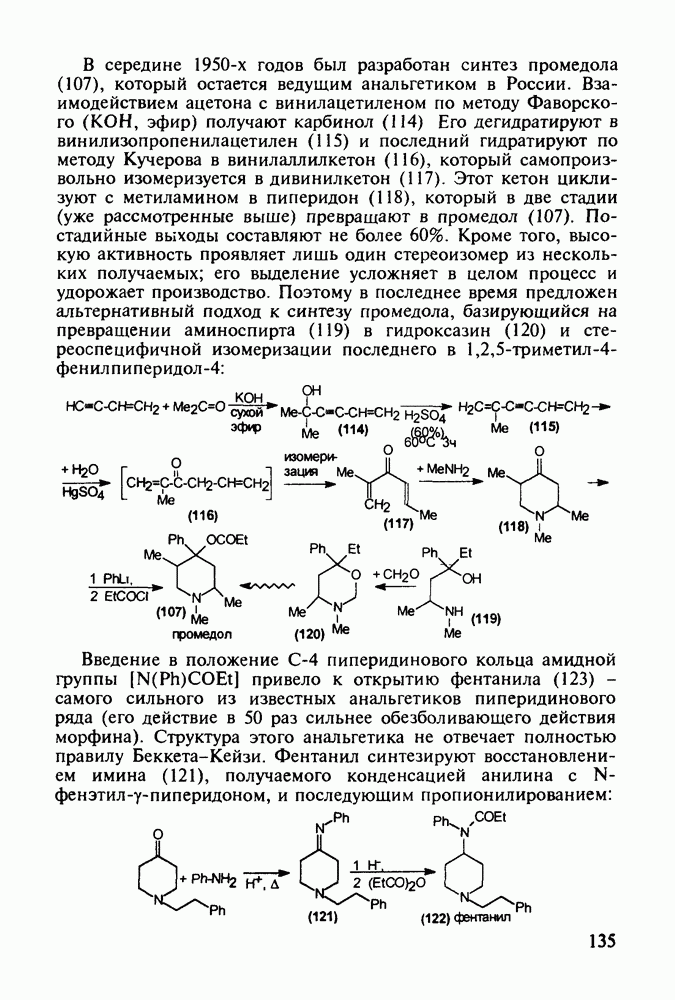
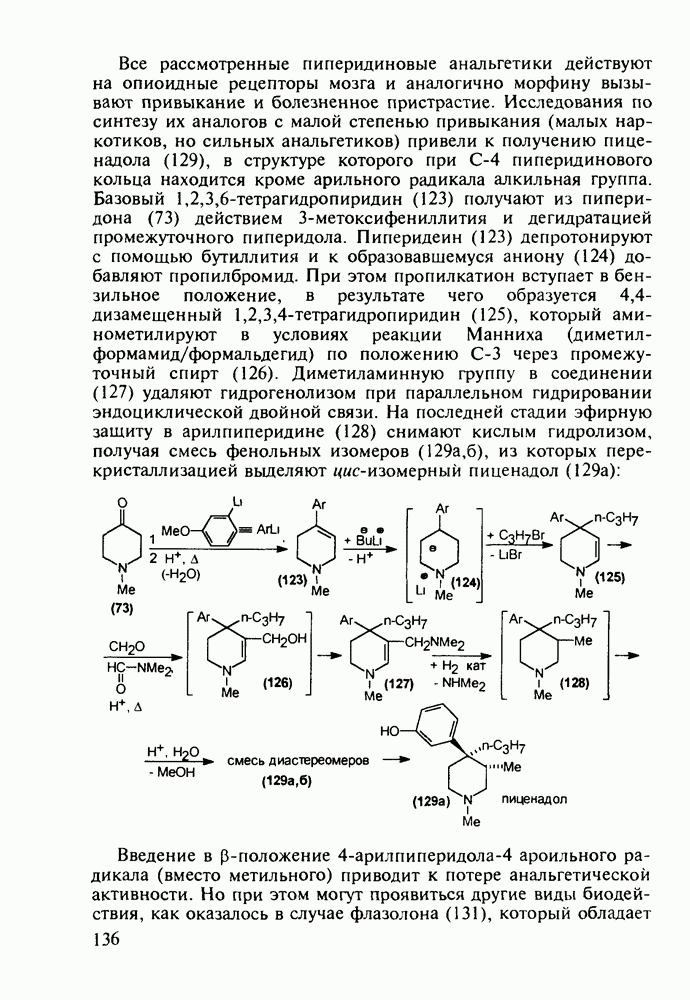
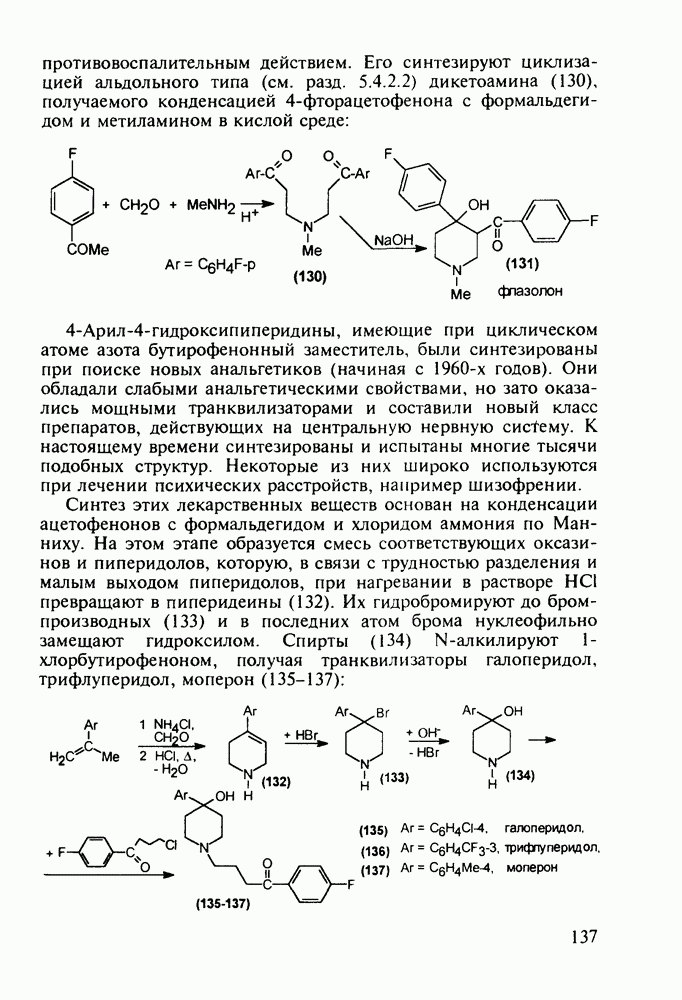
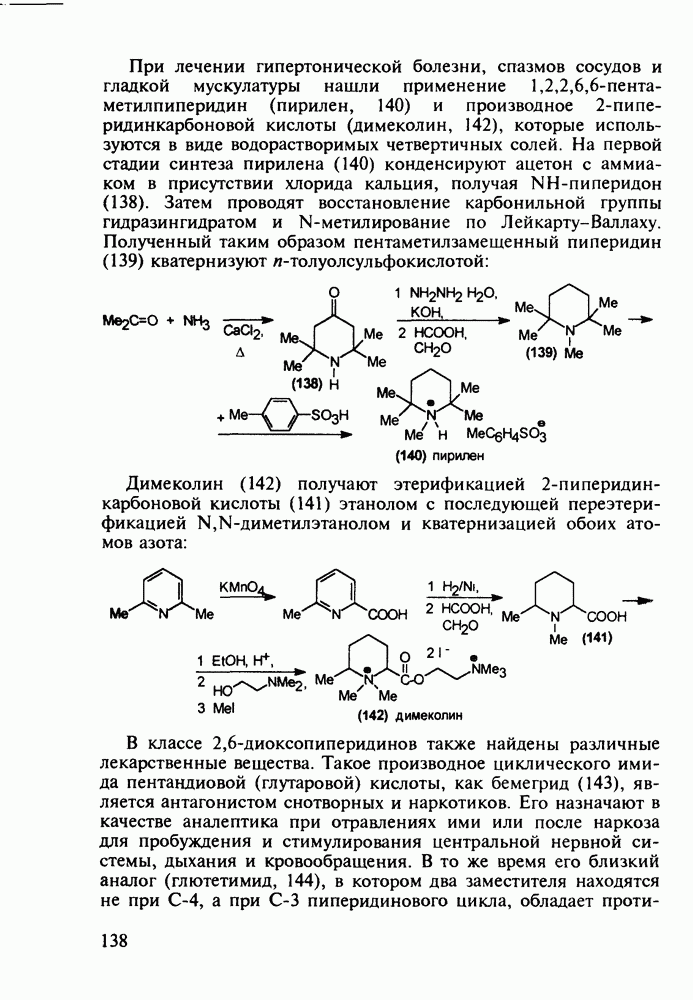
- 5.4.3. Анальгетики и транквилизаторы пиперидинового ряда
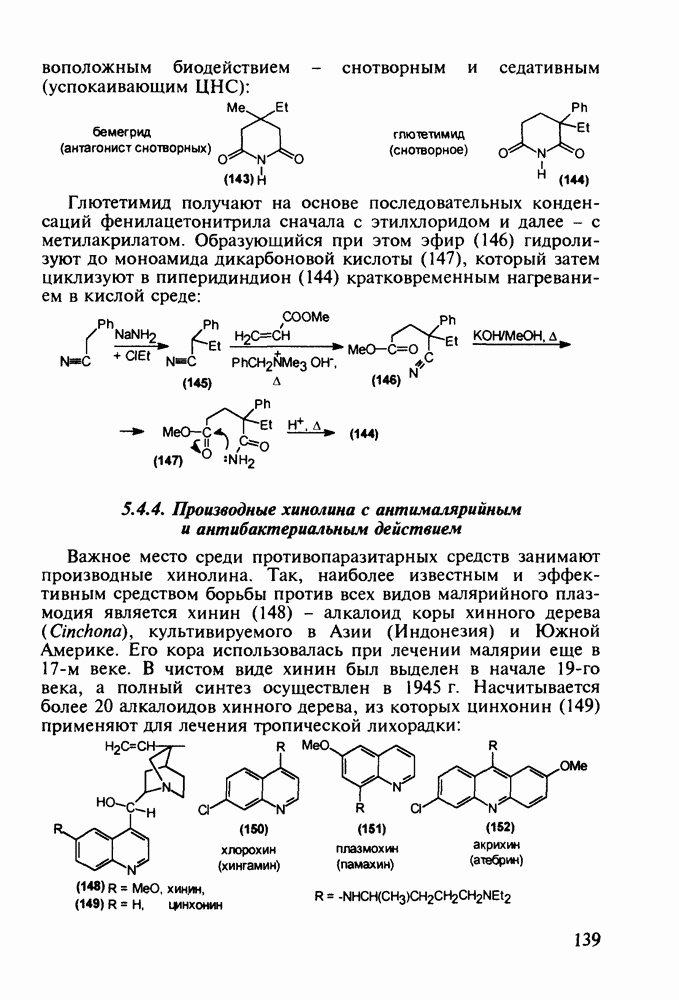
- 5.4.4. Производные хинолина с антималярийным и антибактериальным действием
- 5.4.5. Изохинолины в качестве спазмолитиков и трипаноцидов
- 5.4.6. Производные пиримидинов
- 5.4.7. Производные пиперазина и пиридазина
- 5.4.8. Бензотиазины. Нейролептики фенотиазинового ряда
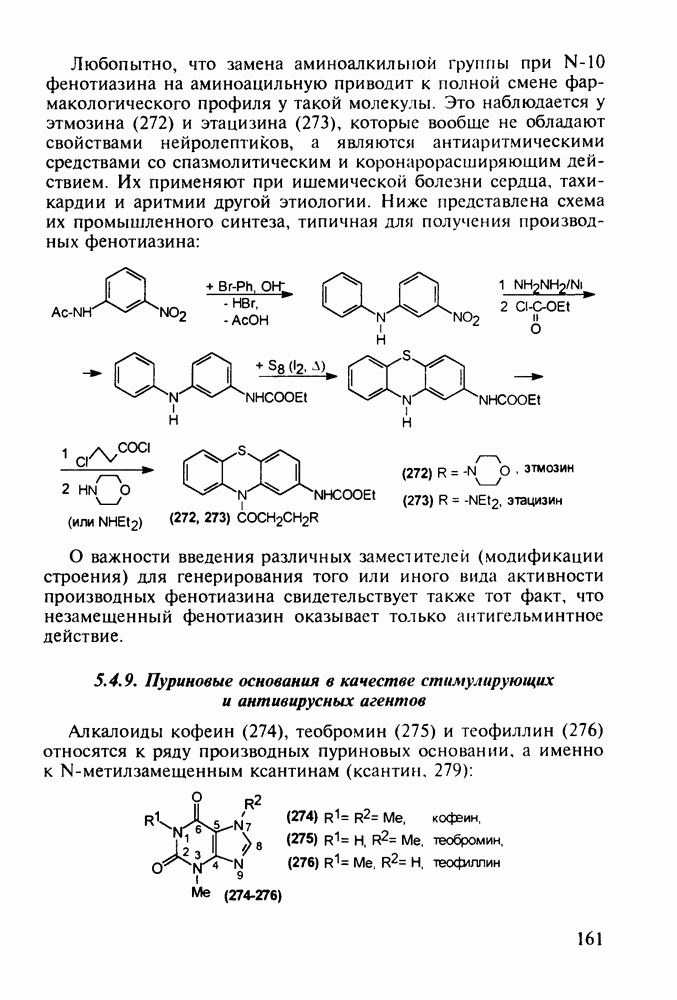
- 5.4.9. Пуриновые основания в качестве стимулирующих и антивирусных агентов
- 5.4.10. Производные аденозинфосфорной кислоты
- 5.4.11. Производные птеридина с витаминной (витамины Вс и В2) и противораковой активностью
- 5.5. Лекарственные вещества, содержащие семичленный гетероцикл
- 5.5.2. Транквилизаторы группы 1,4-бензодиазепина
- 5.6. Производные азабициклооктанов в качестве спазмолитиков и анестетиков. Лекарственные препараты на основе хинуклидина
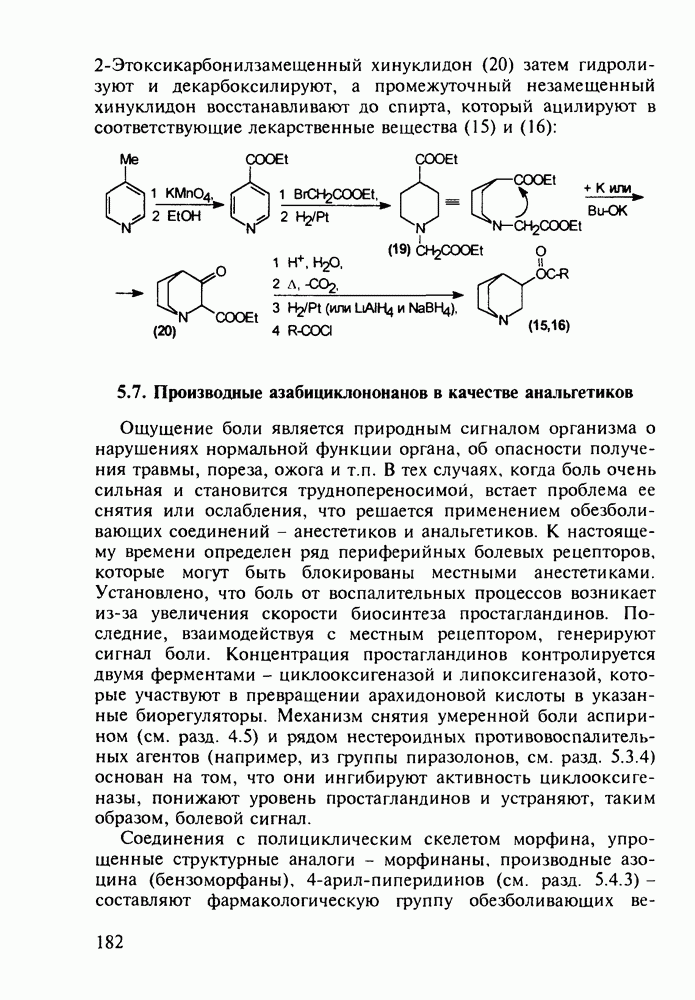
- 5.7. Производные азабициклононанов в качестве анальгетиков
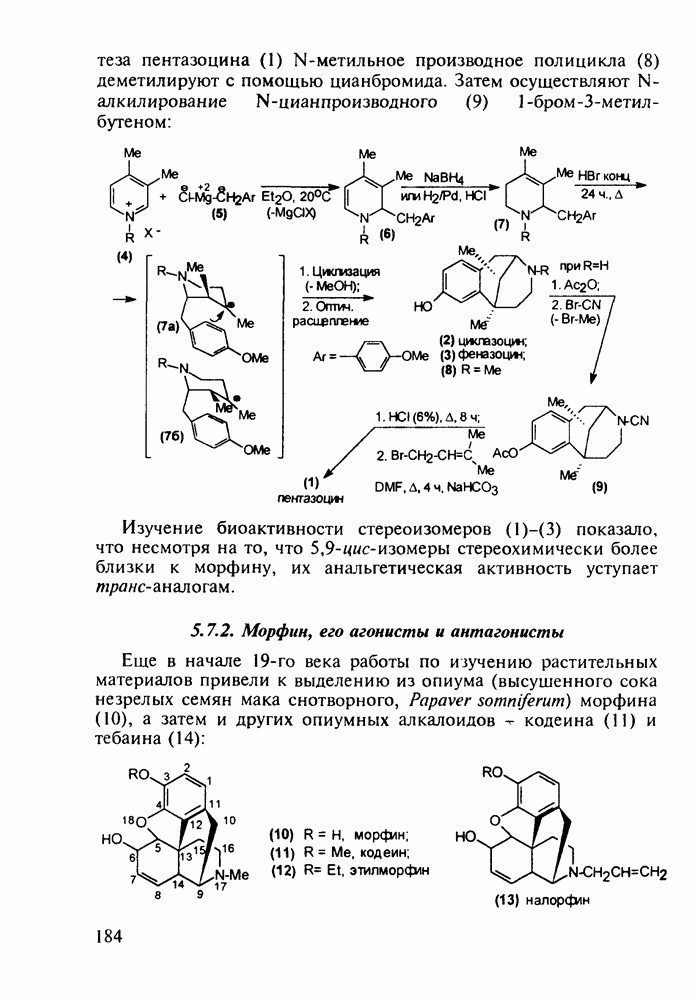
- 5.7.1. Группа пентазоцина
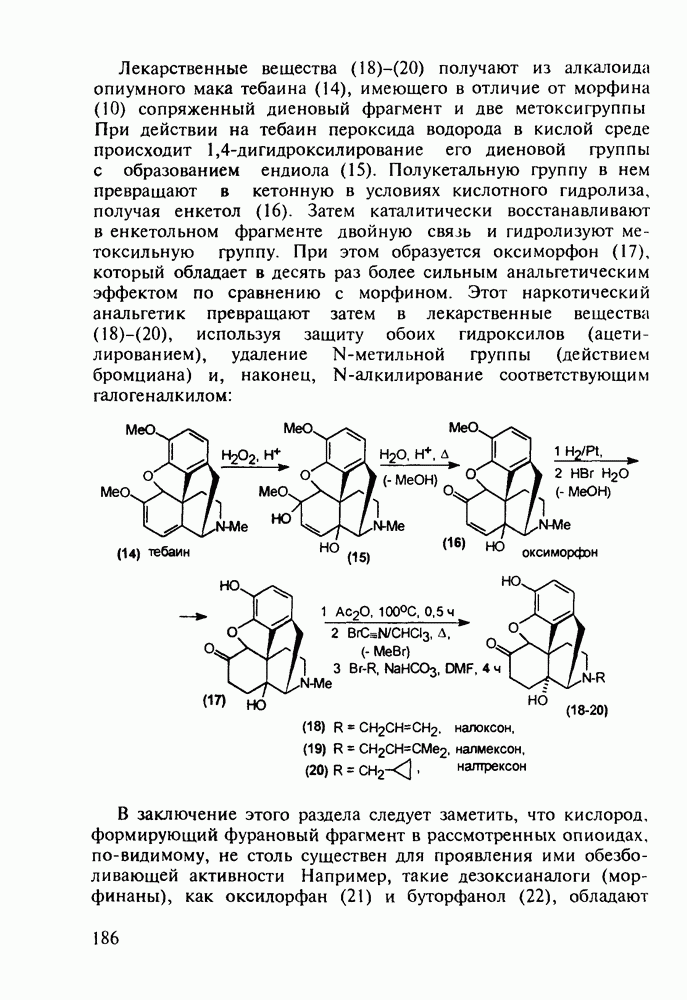
- 5.7.2. Морфин, его агонисты и антагонисты
- РЕКОМЕНДУЕМАЯ ЛИТЕРАТУРА