| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
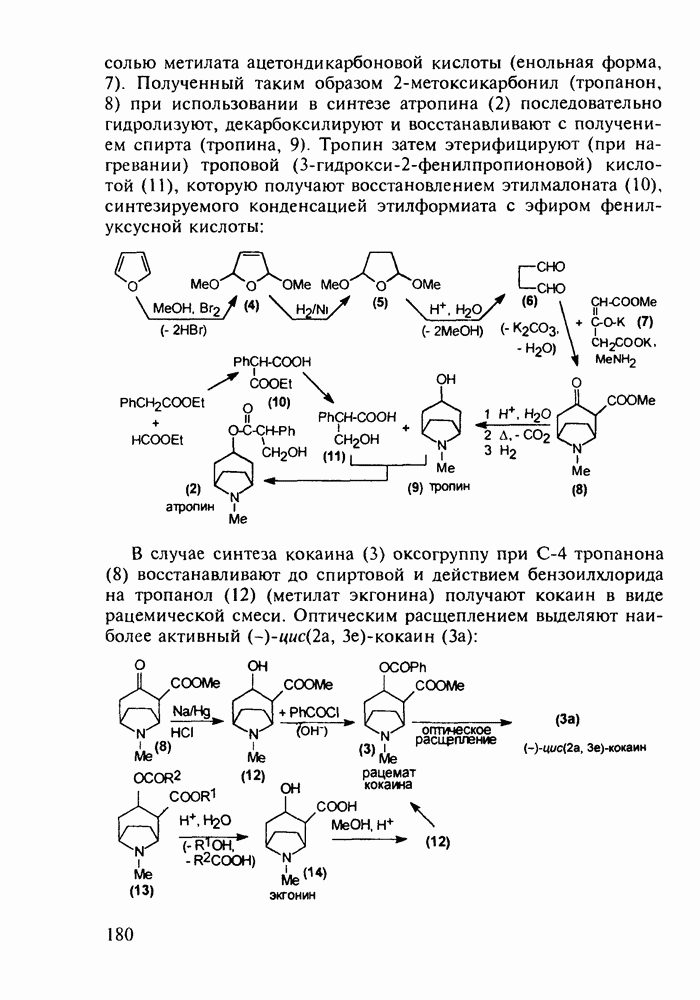
5.4.8. Бензотиазины. Нейролептики фенотиазинового ряда
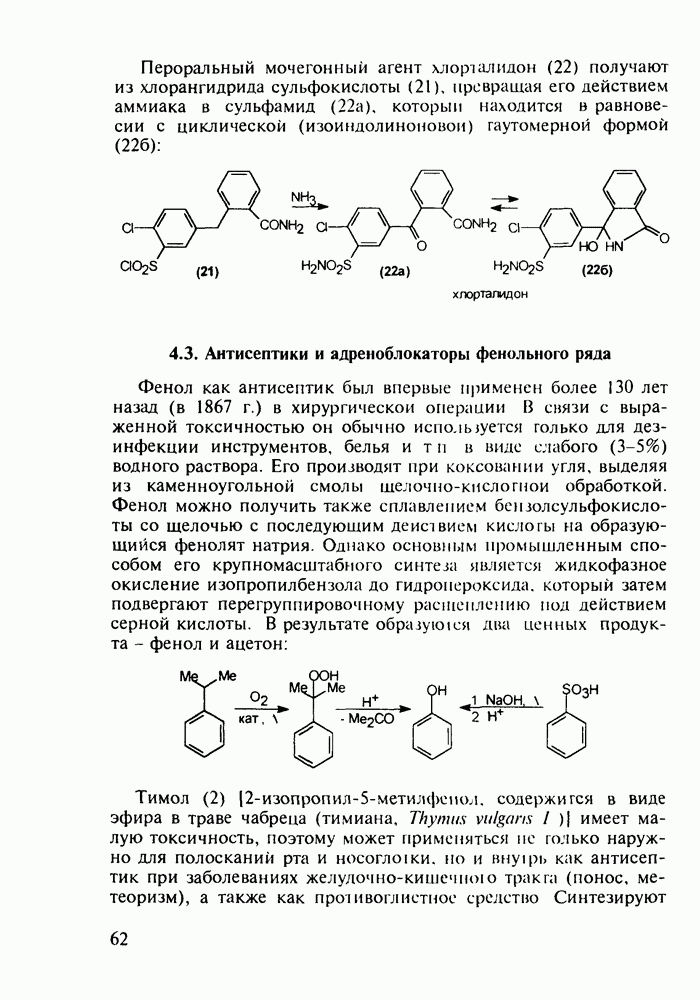
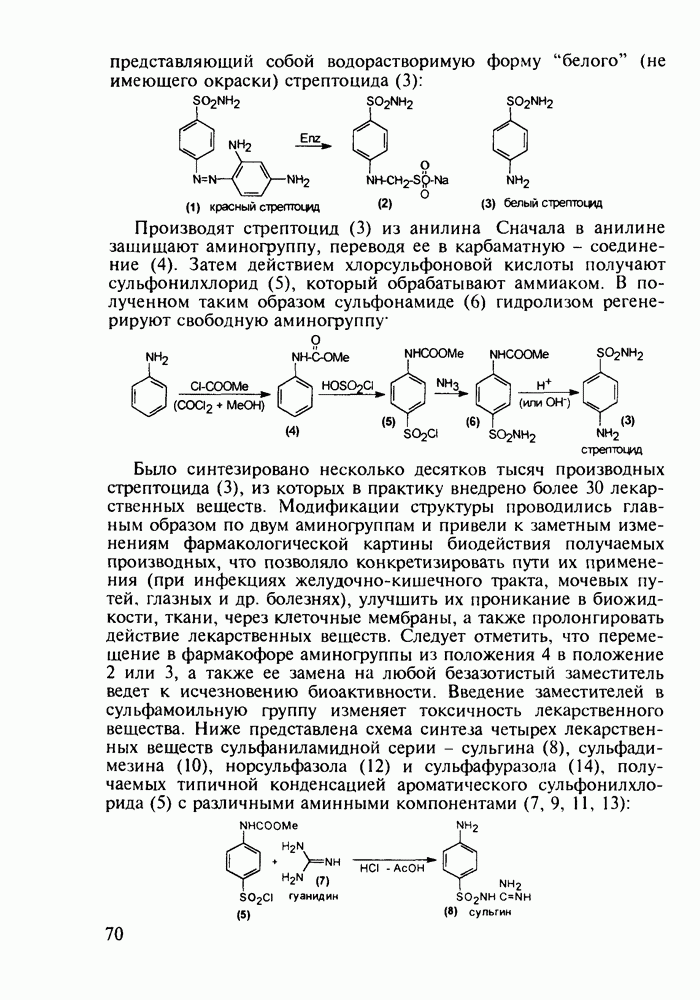
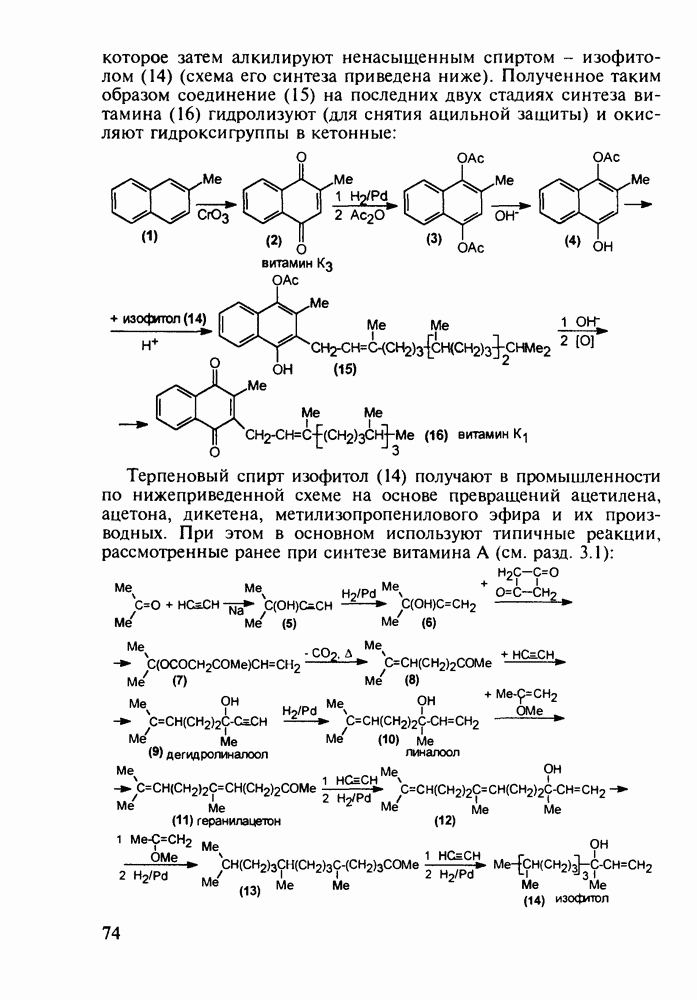
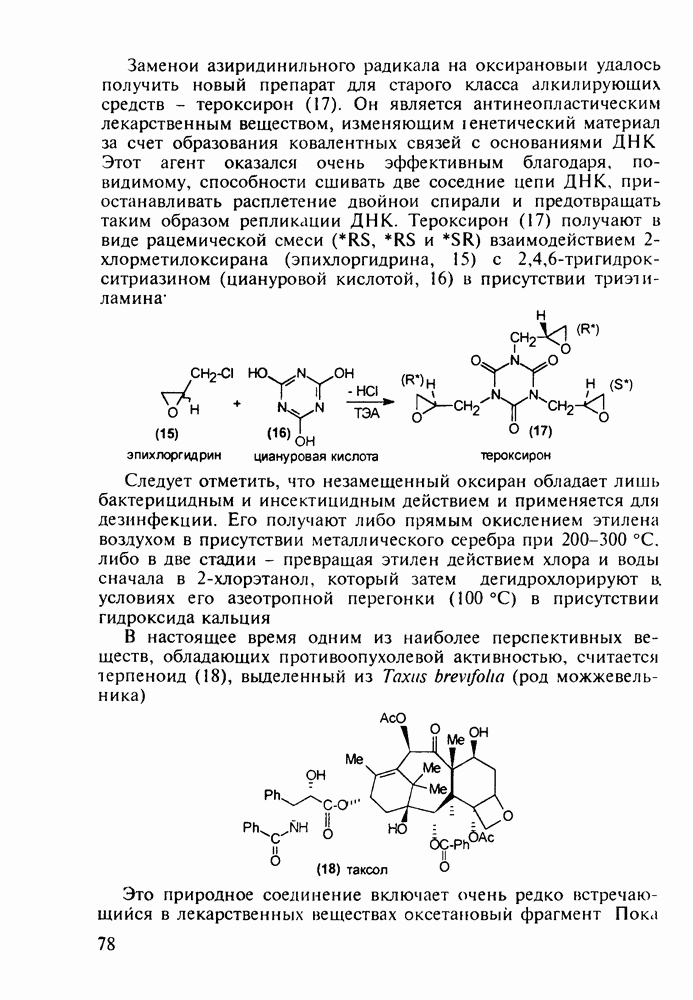
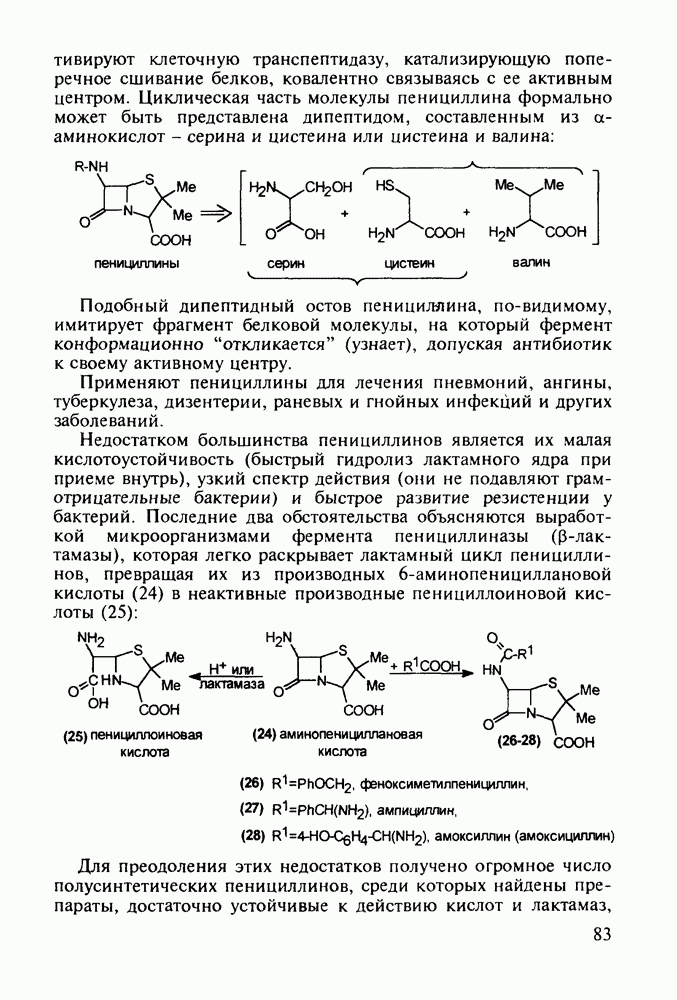
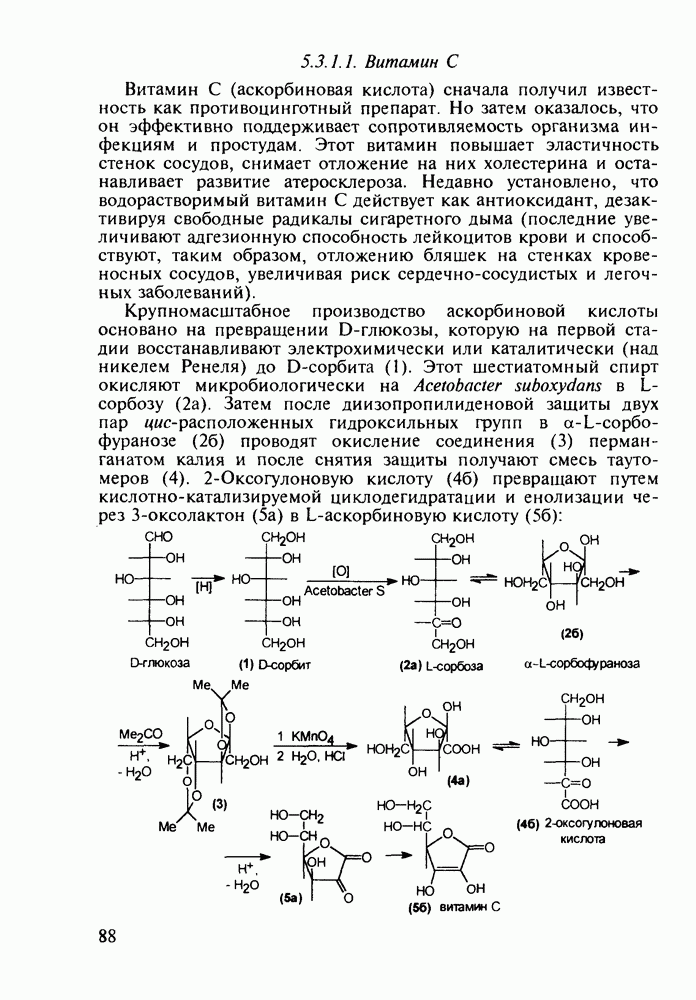
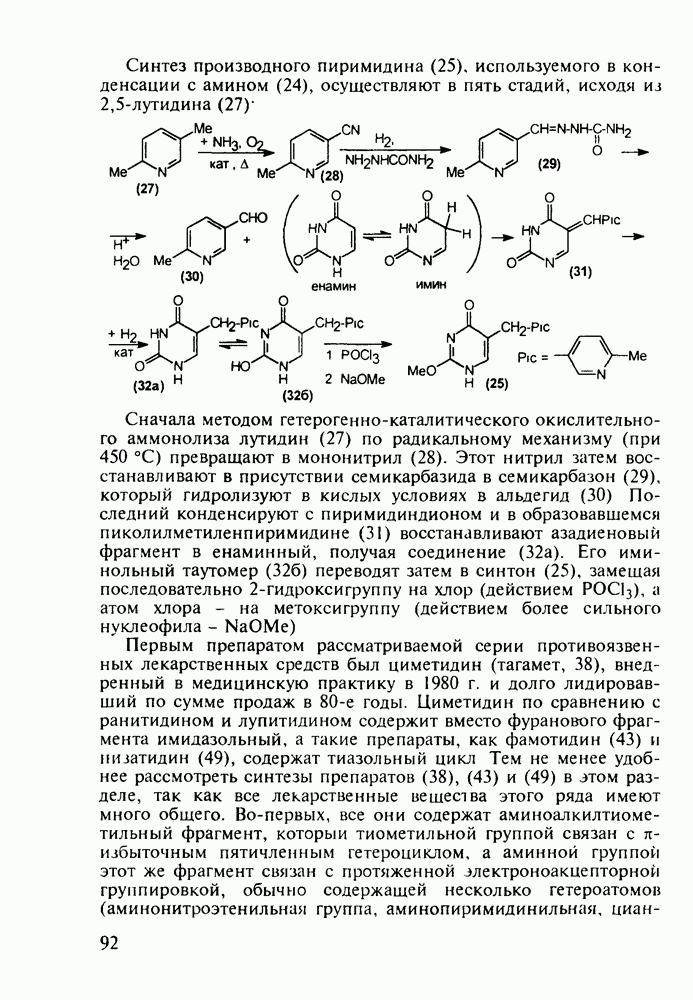
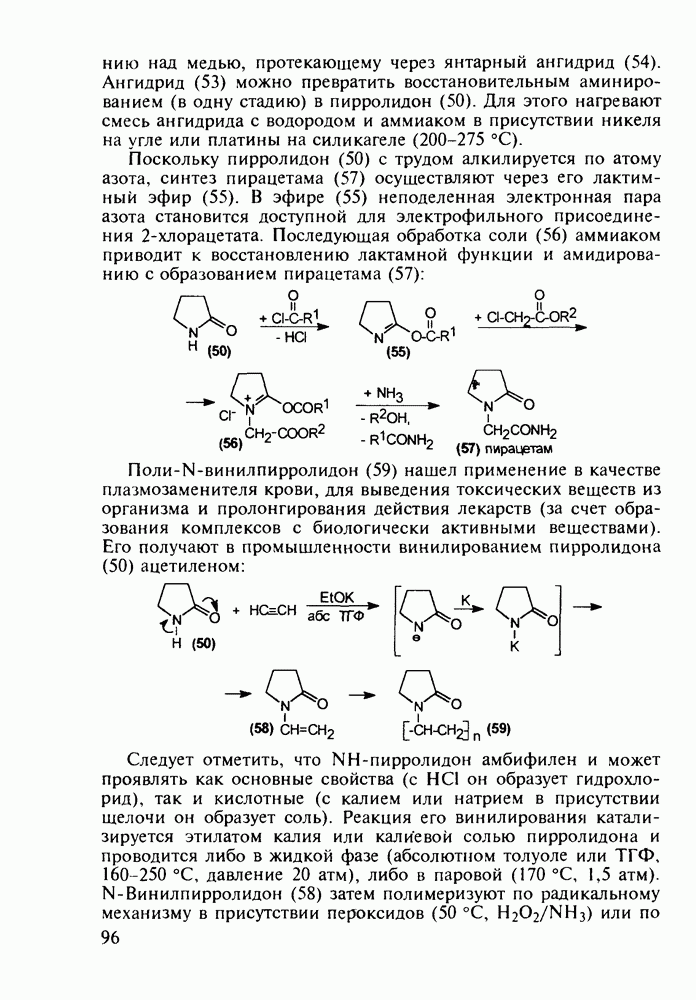
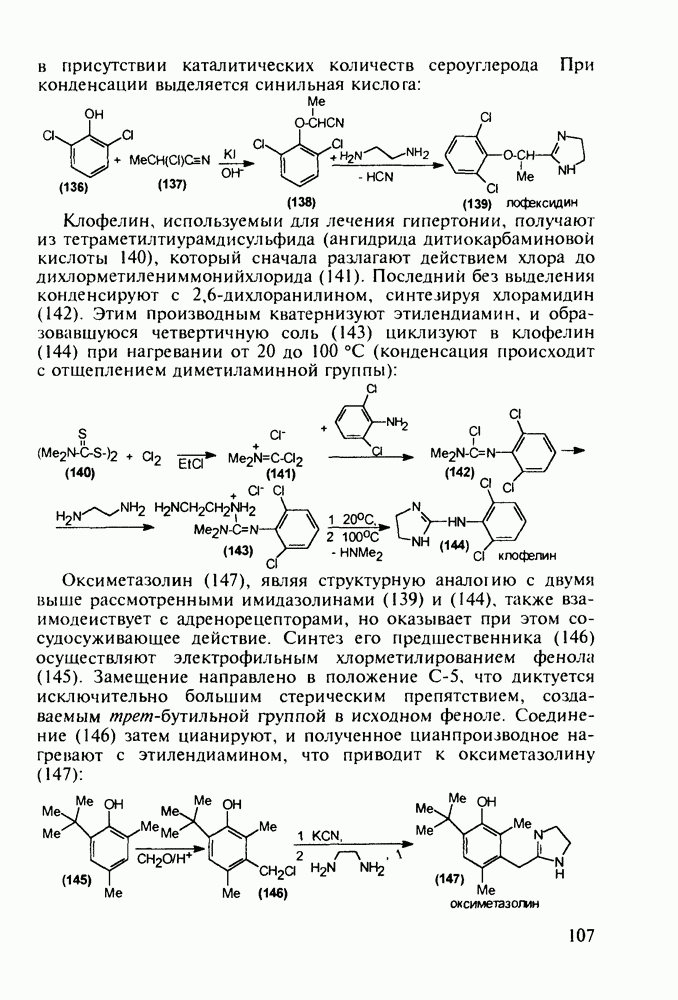
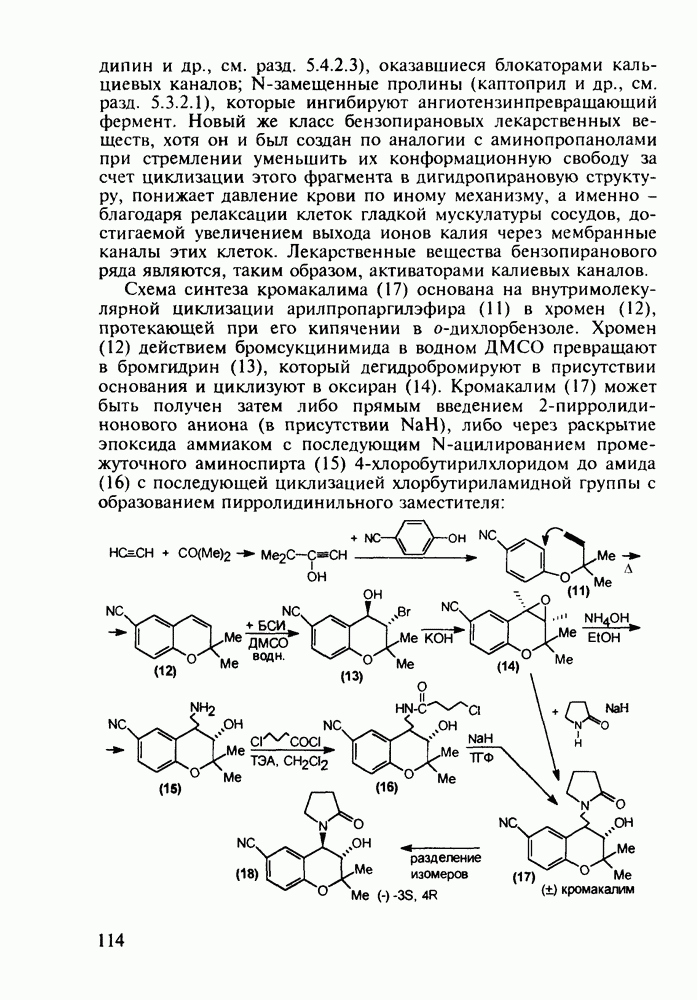
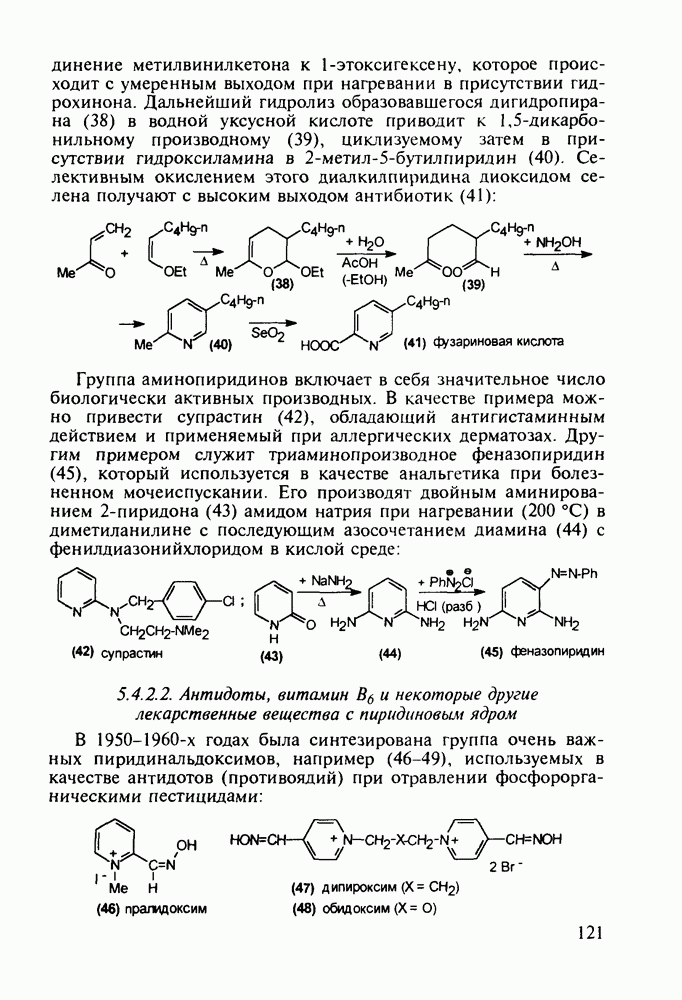
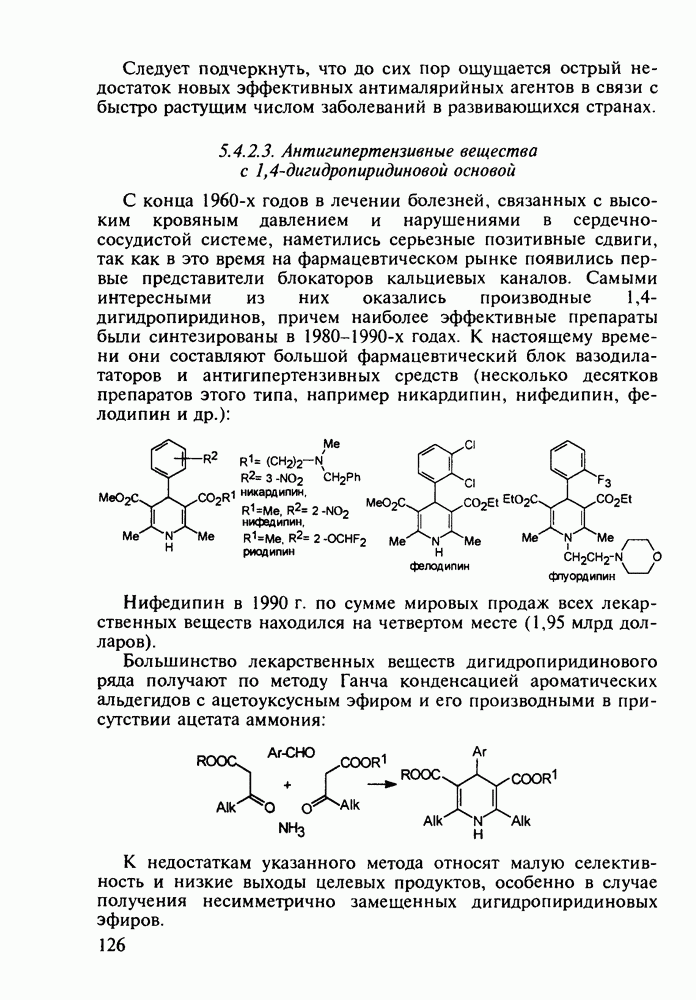
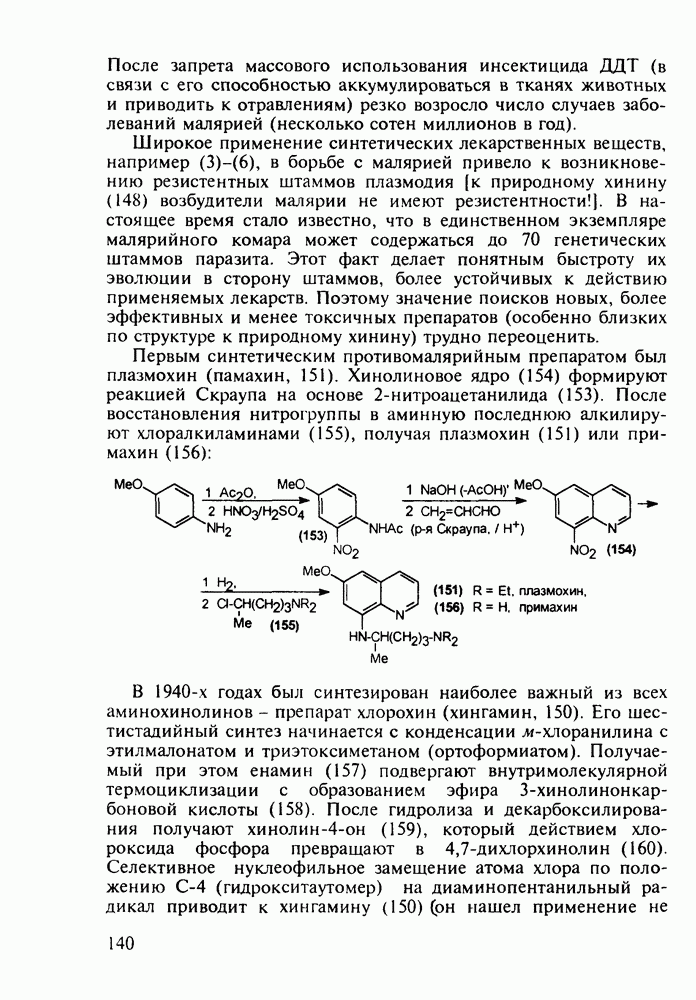
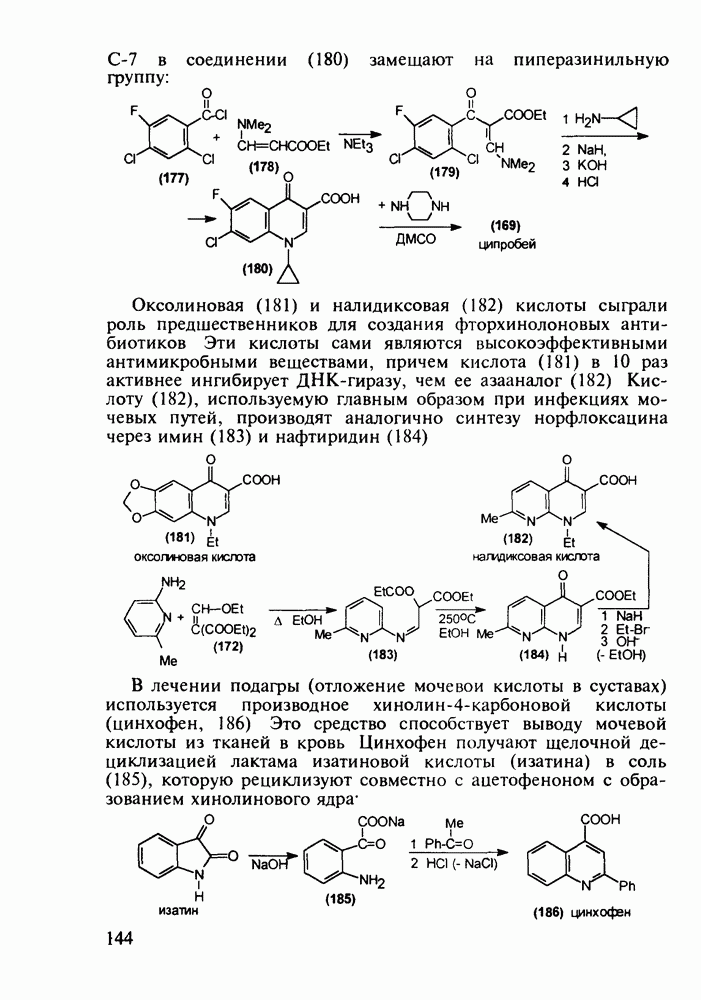
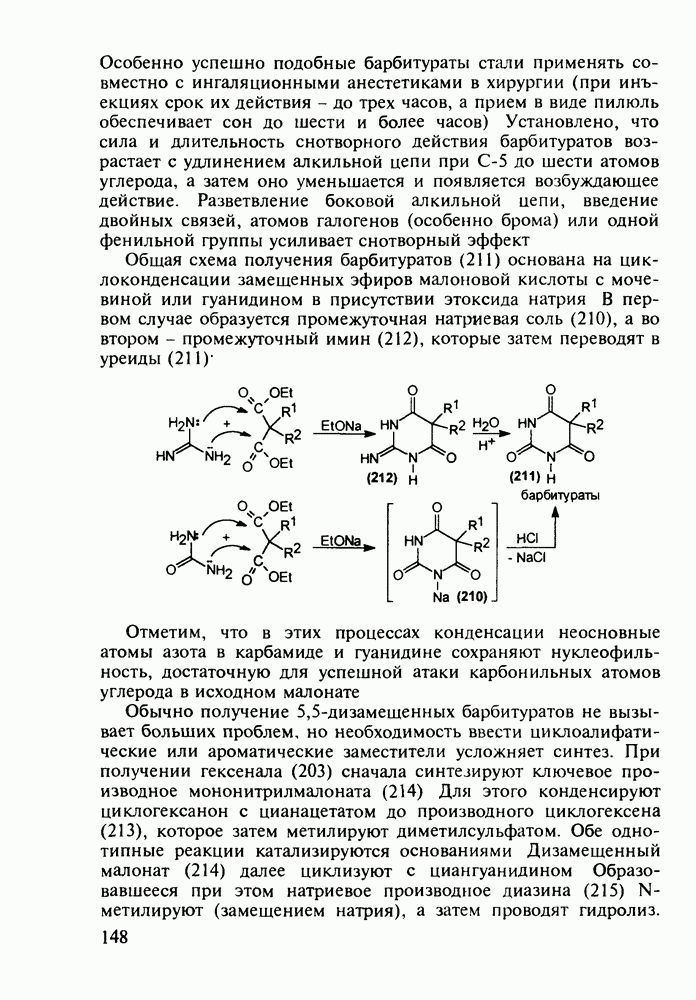
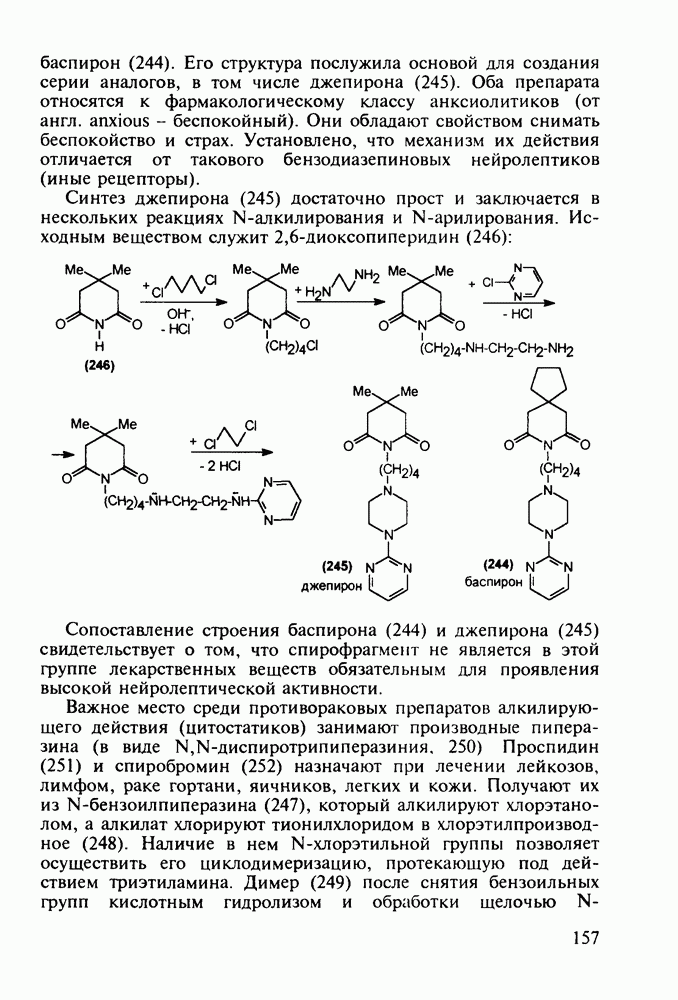
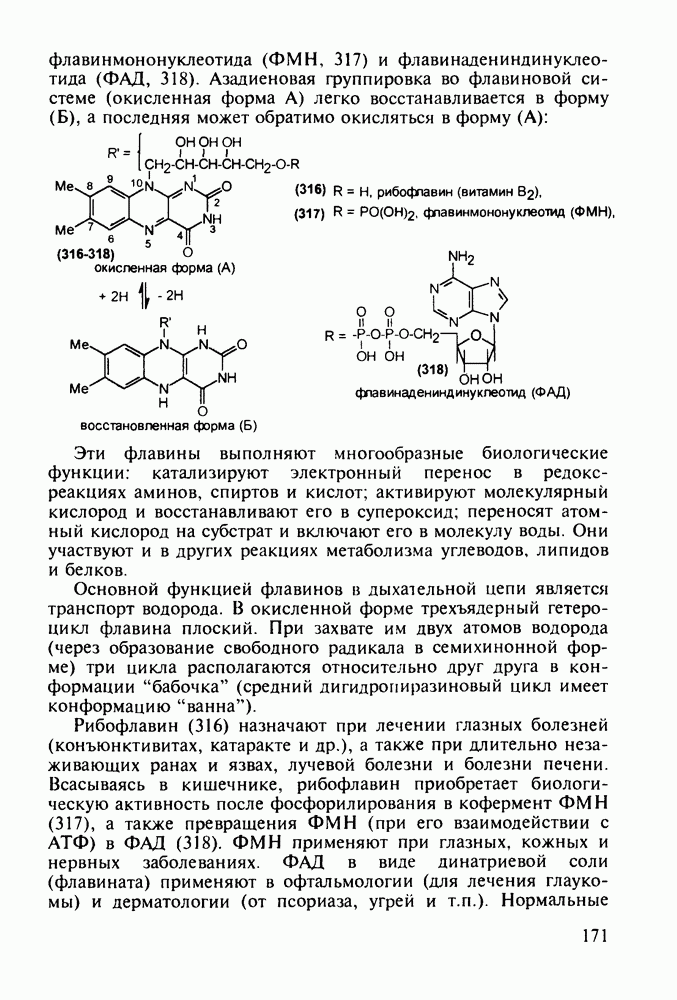
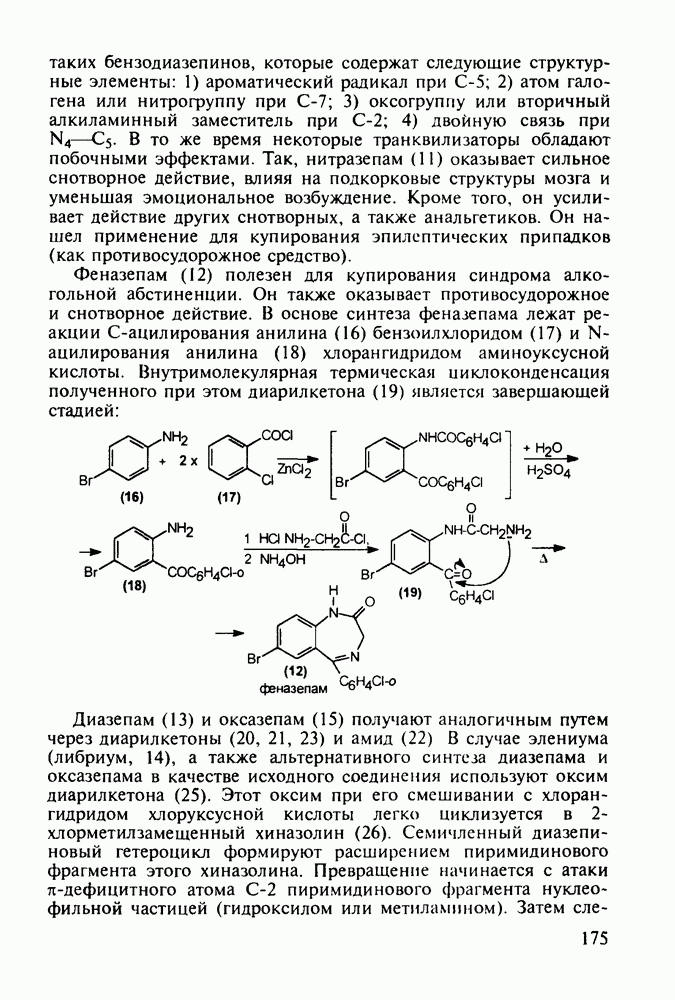
Из бензотиазинов широкое использование с конца 1980-х годов получило противовоспалительное средство нестероидного типа - пироксикам (фельден, 261). Исходным веществом для синтеза бензотиазинового ядра служит  -сульфамидное производное бензойной кислоты (257). Получаемый имид (сахарин, 258) переводят в N-натрийпроизводное и N-алкилируют его
-сульфамидное производное бензойной кислоты (257). Получаемый имид (сахарин, 258) переводят в N-натрийпроизводное и N-алкилируют его
эфиром хлоруксусной кислоты. Затем под действием метилата натрия в соединении (259) раскрывается по связи S—N пятичленное кольцо, и происходит рециклизация с образованием шестичленного тиазинового кольца (соединение 260). На последних двух стадиях этой схемы синтеза пироксикама (261) проводят N-метилирование и превращение сложноэфирной группы в N-(2-пиридил)амидную:

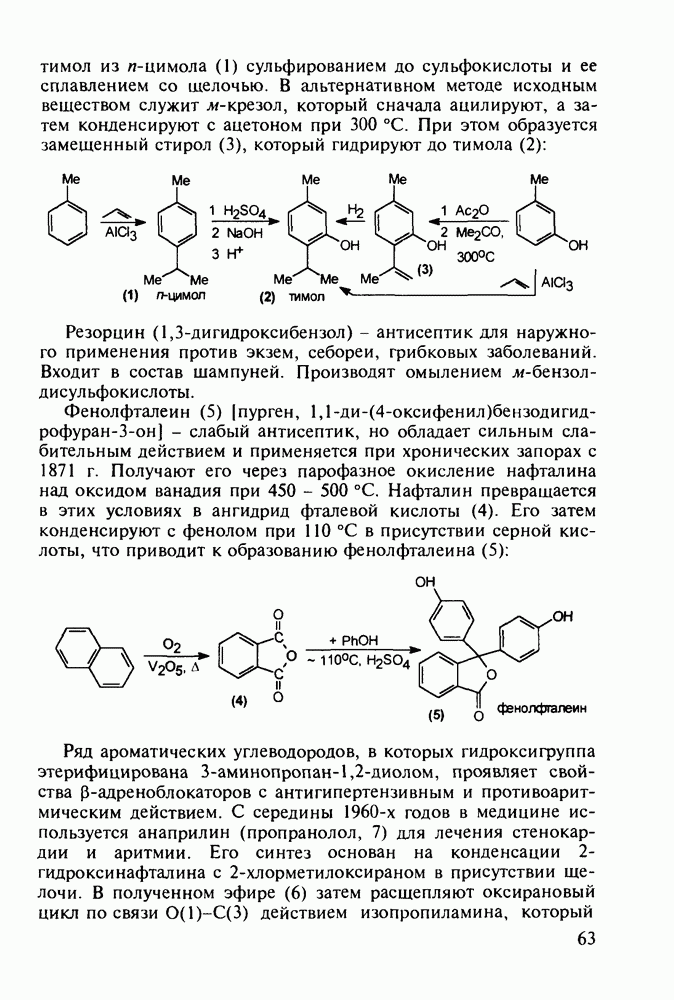
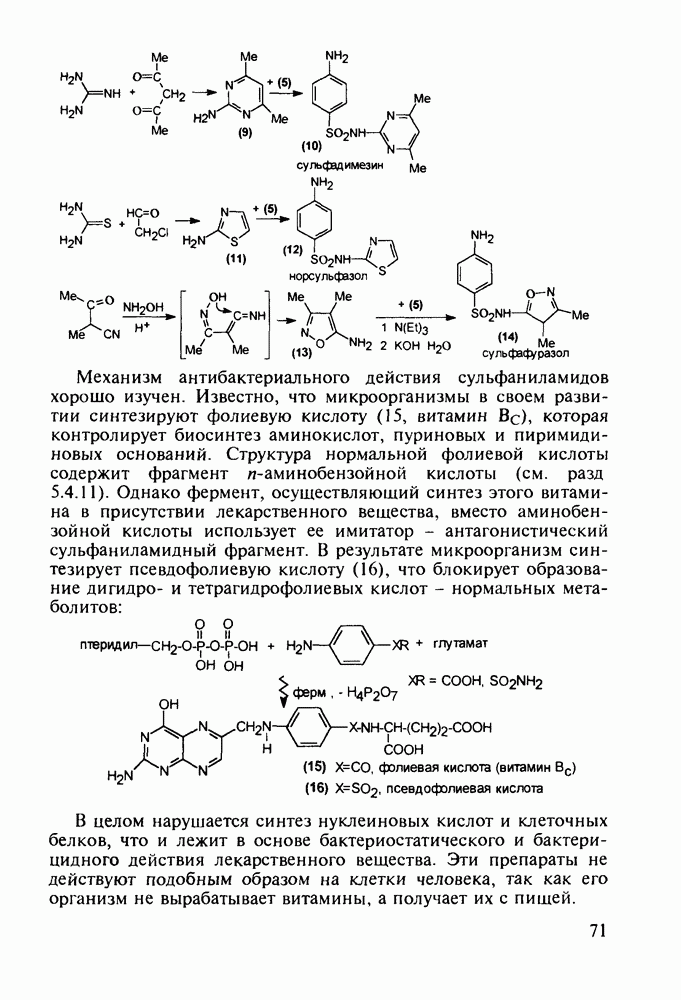
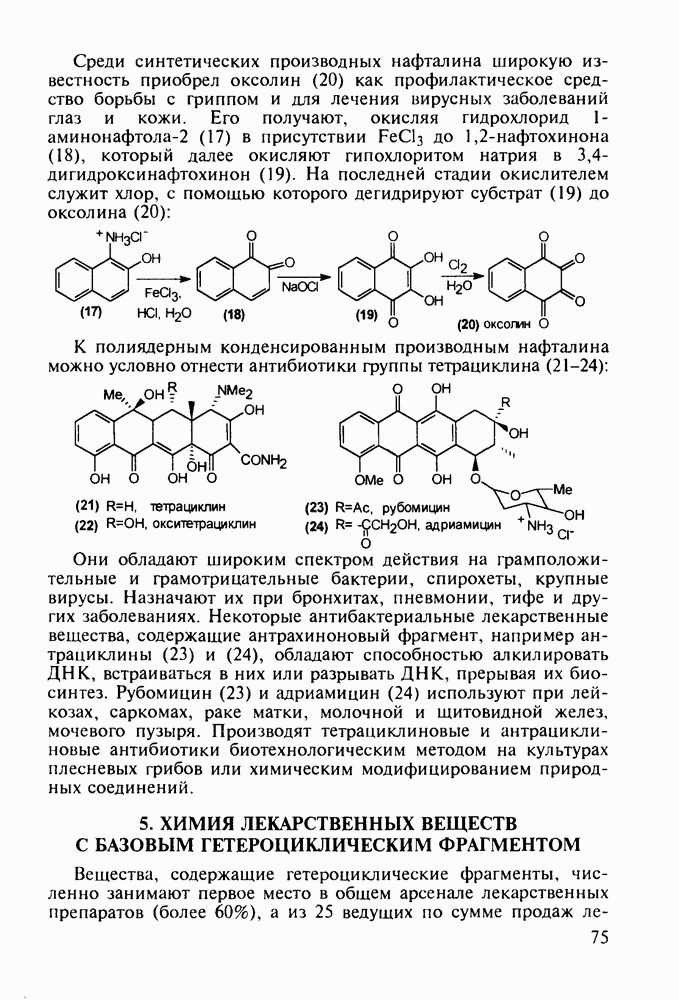
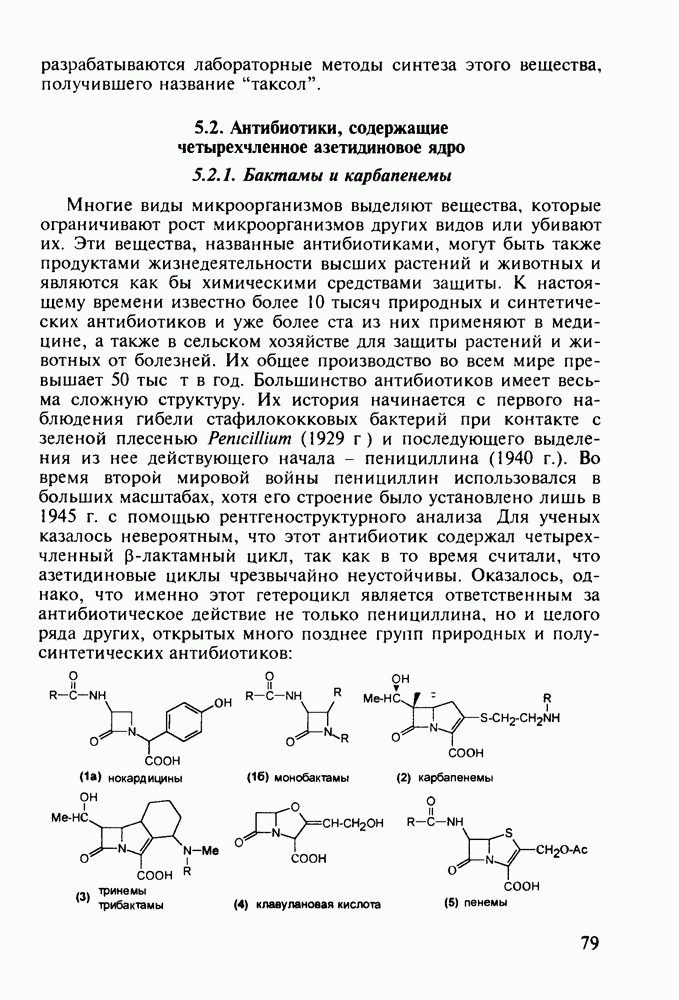
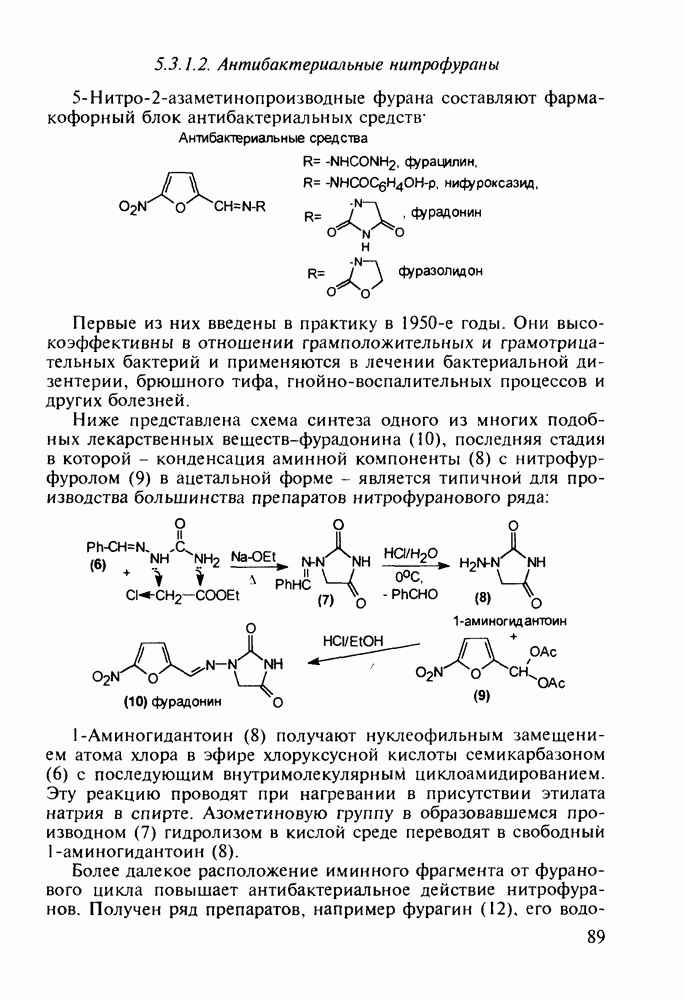
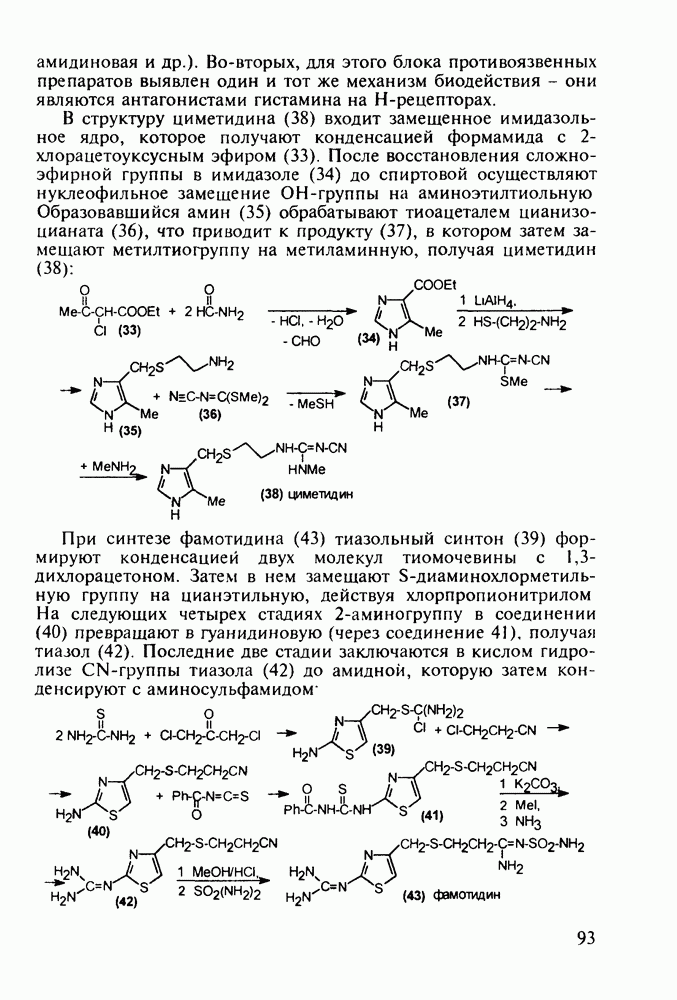
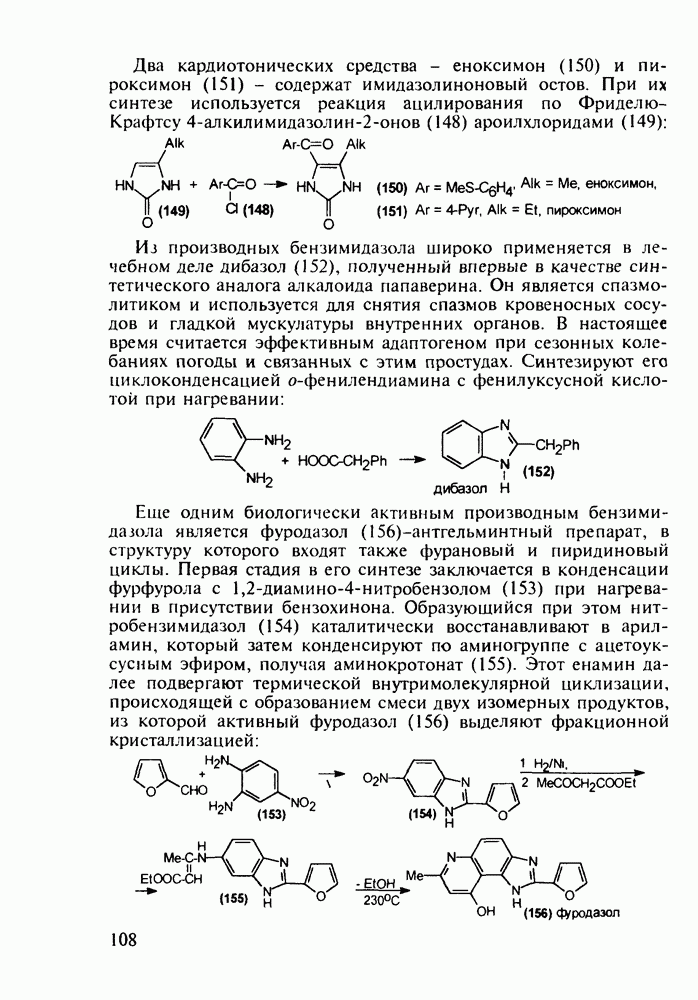
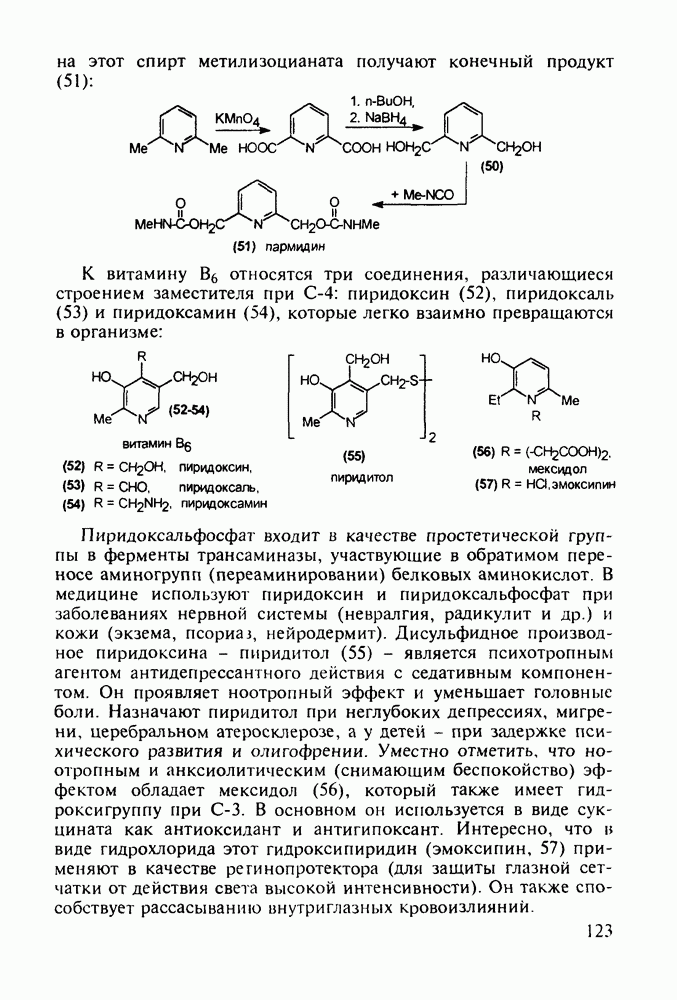
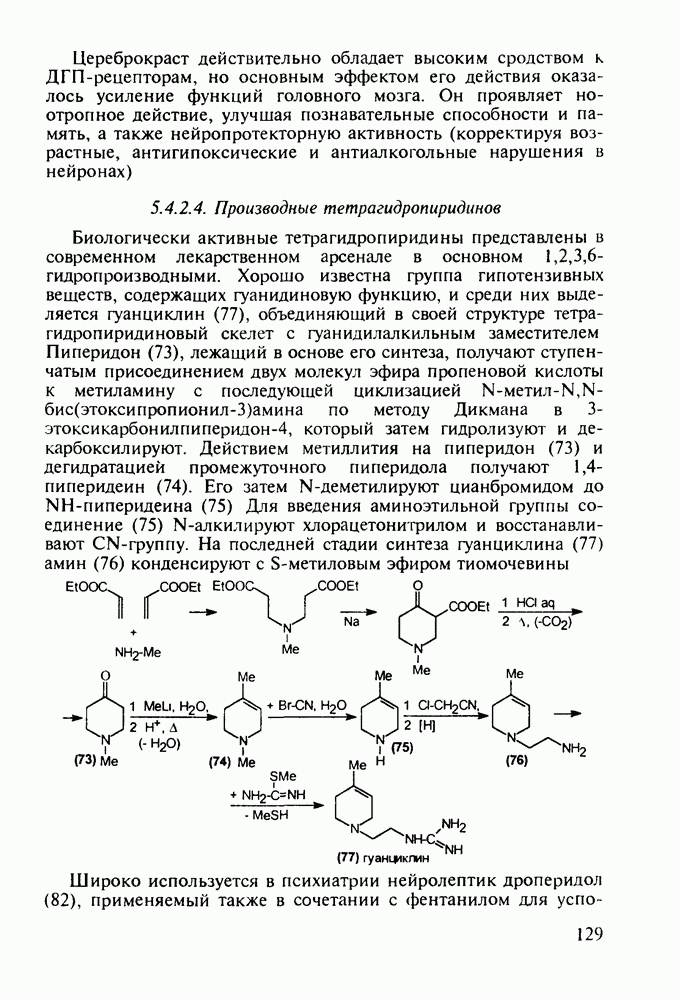
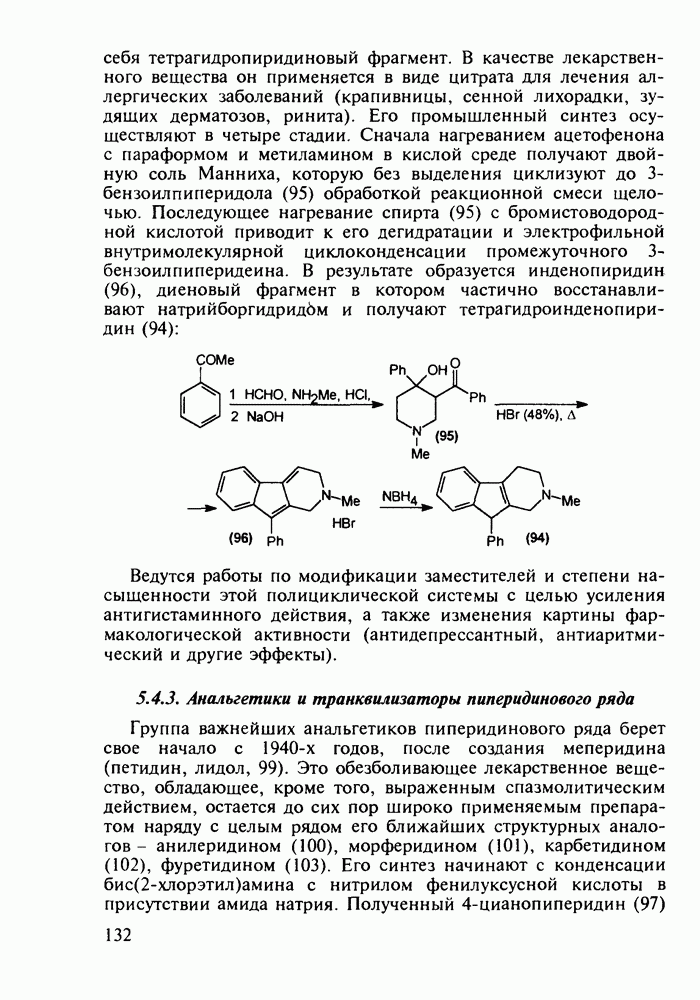
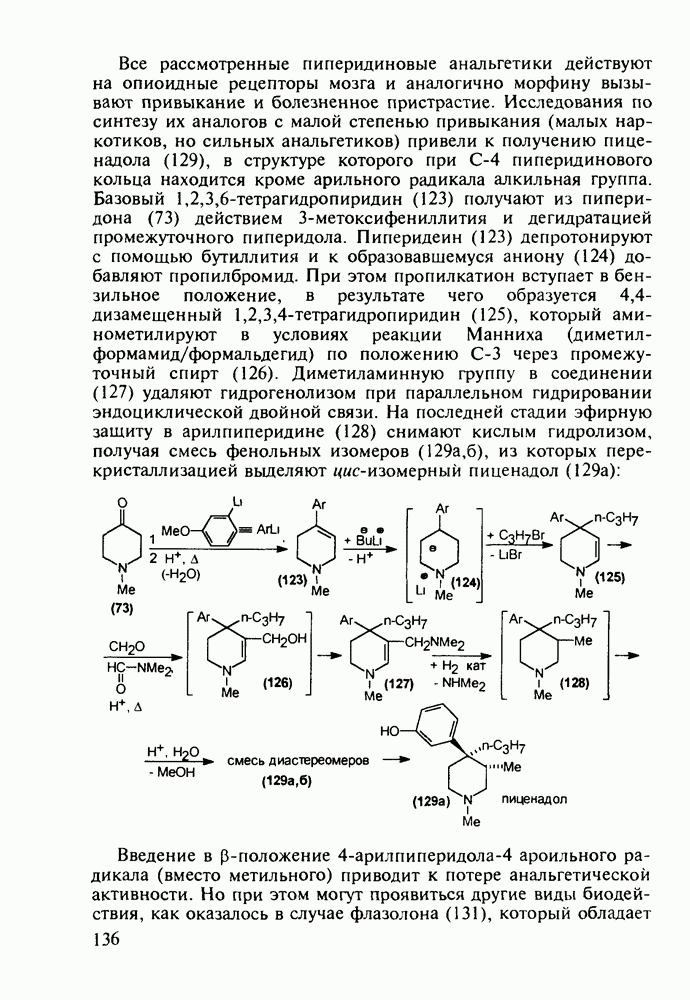
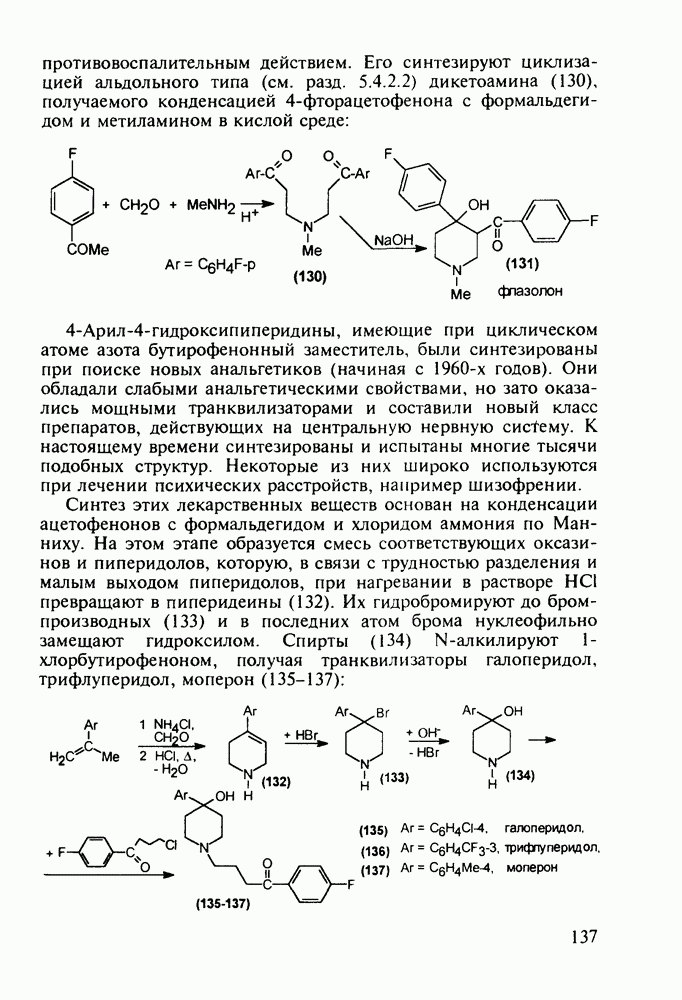
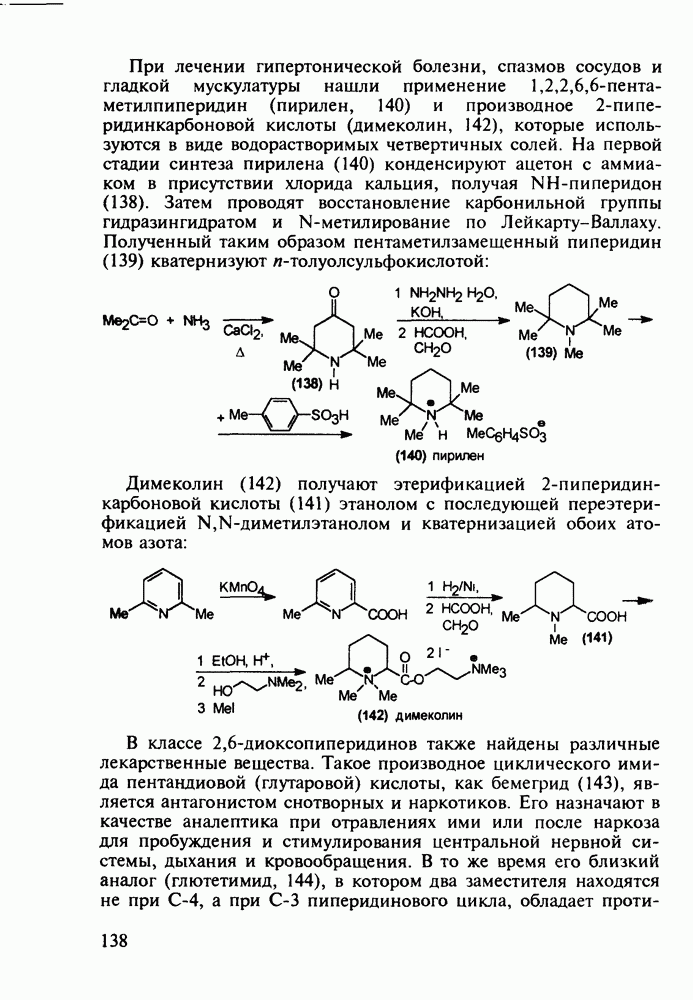
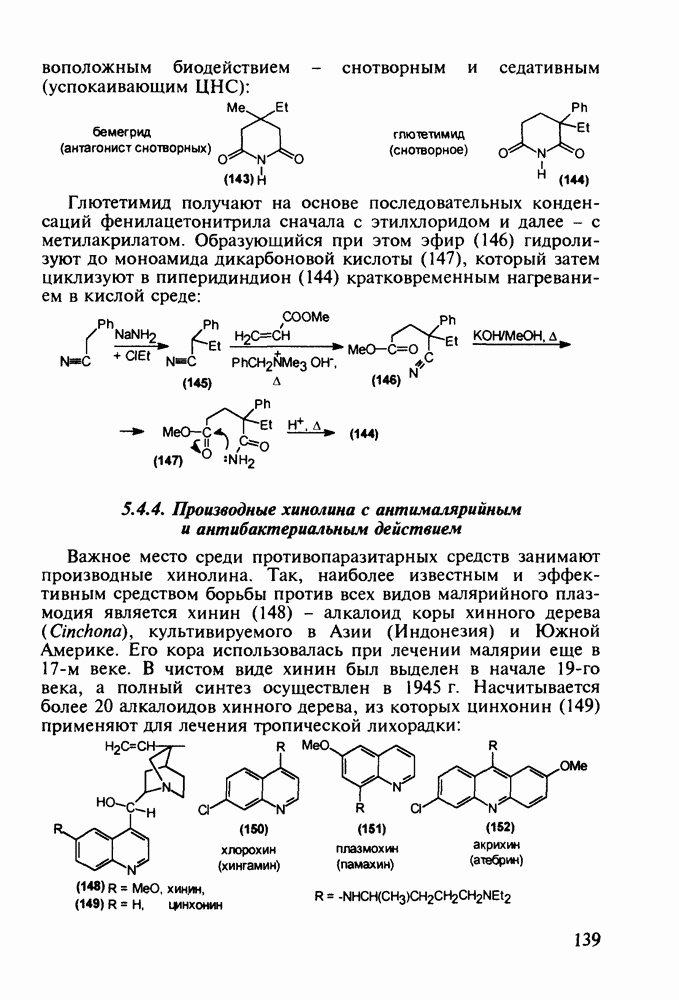
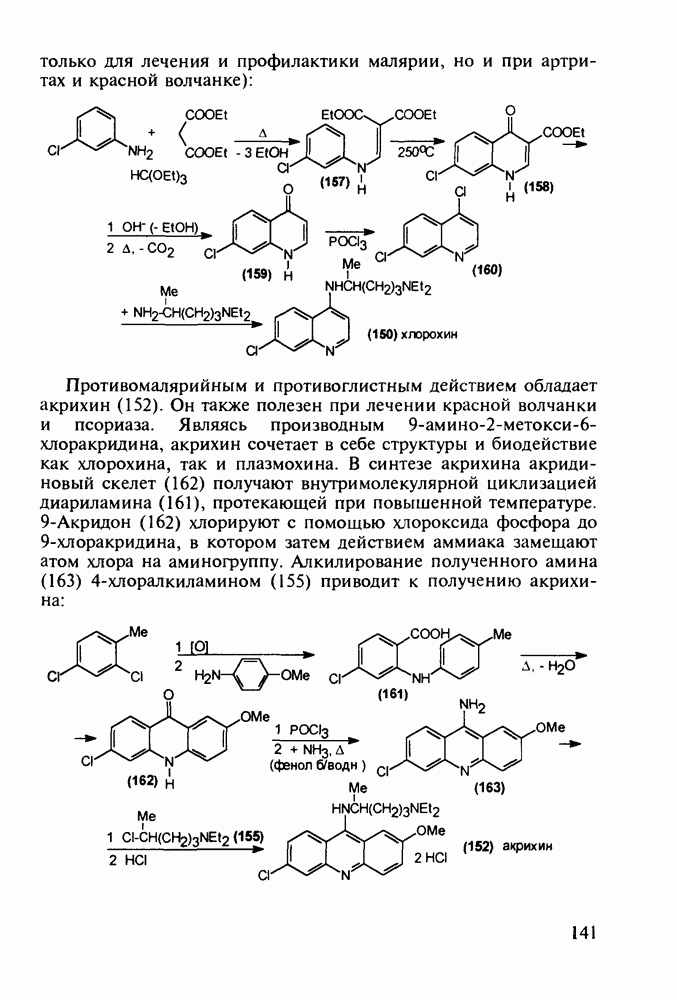
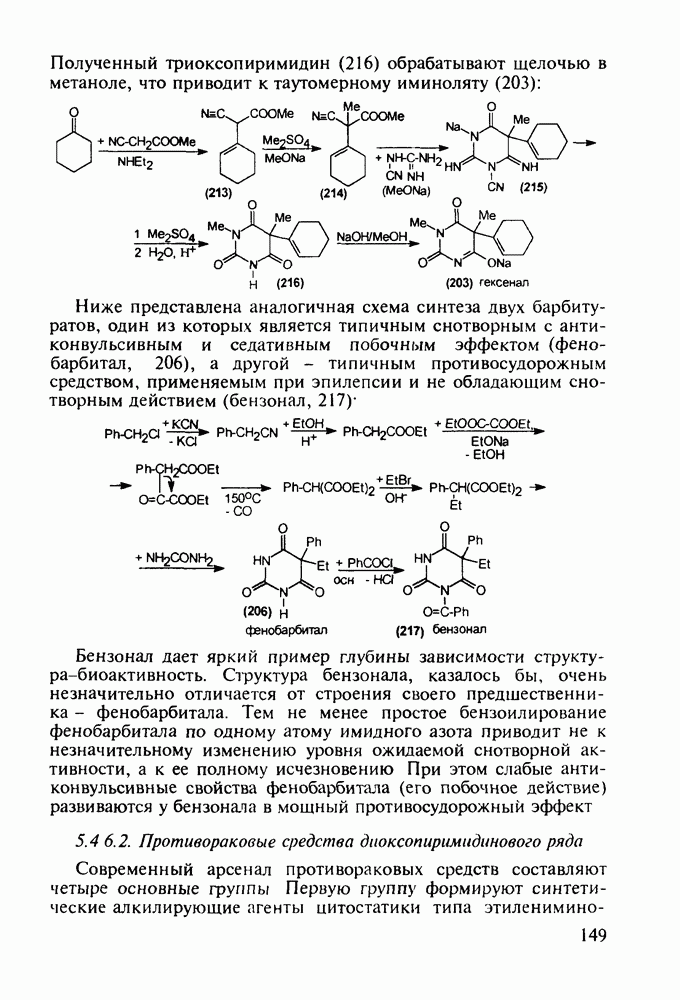
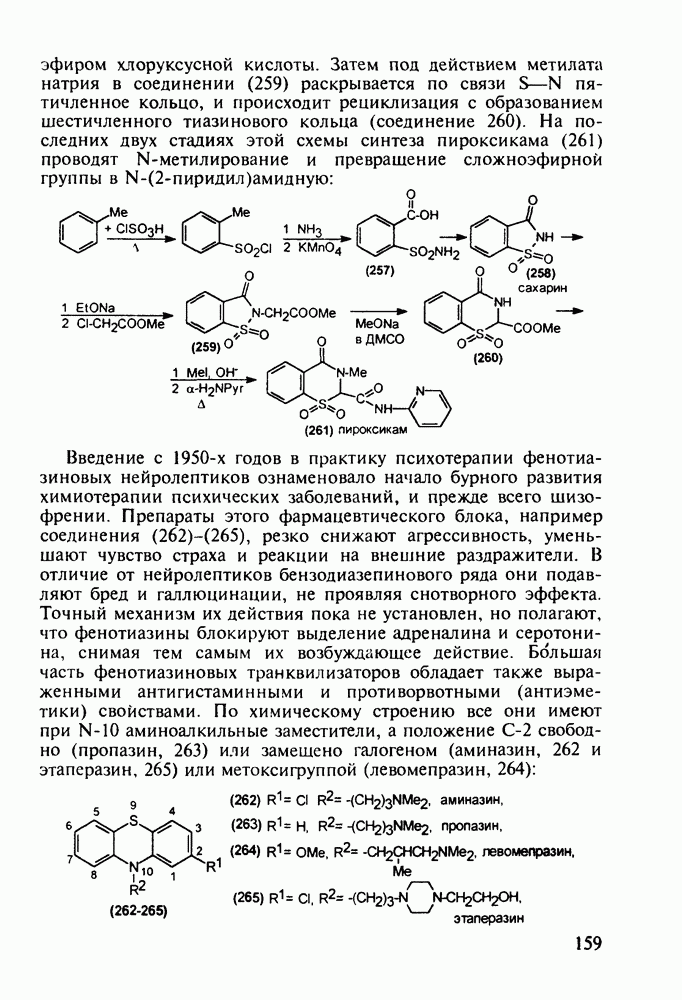
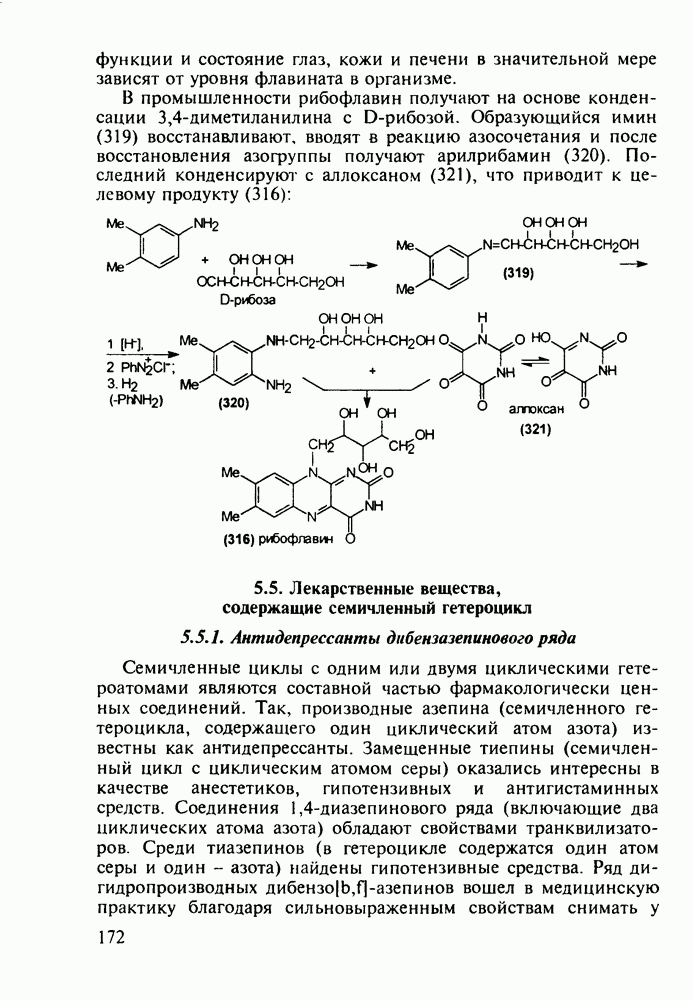
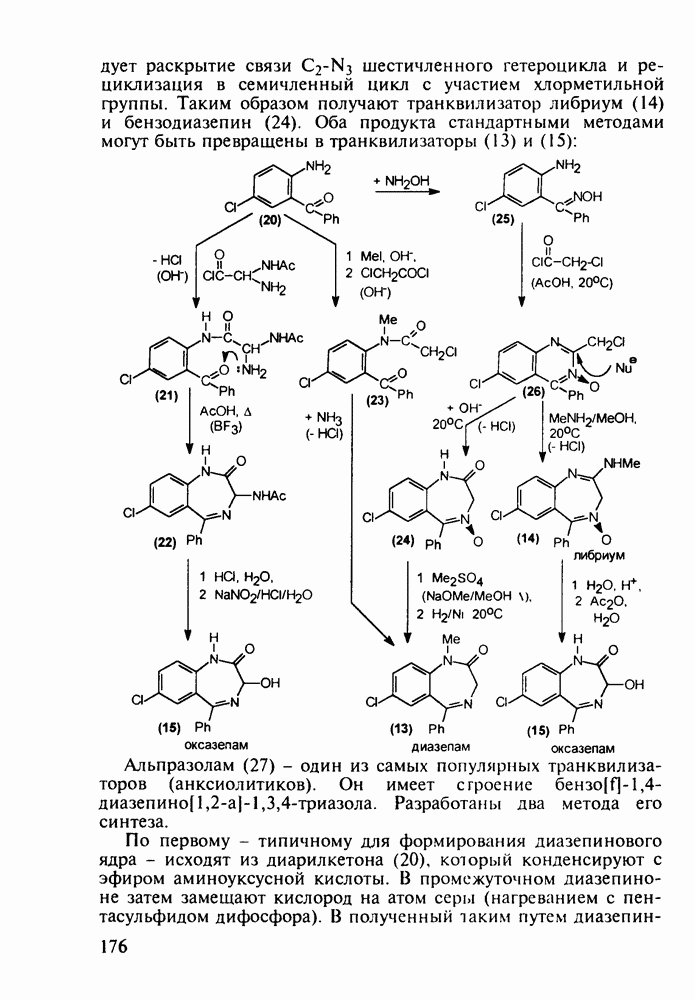
Введение с 1950-х годов в практику психотерапии фенотиазиновых нейролептиков ознаменовало начало бурного развития химиотерапии психических заболеваний, и прежде всего шизофрении. Препараты этого фармацевтического блока, например соединения (262)-(265), резко снижают агрессивность, уменьшают чувство страха и реакции на внешние раздражители. В отличие от нейролептиков бензодиазепинового ряда они подавляют бред и галлюцинации, не проявляя снотворного эффекта. Точный механизм их действия пока не установлен, но полагают, что фенотиазины блокируют выделение адреналина и серотонина, снимая тем самым их возбуждающее действие. Большая часть фенотиазиновых транквилизаторов обладает также выраженными антигистаминными и противорвотными (антиэме-тики) свойствами. По химическому строению все они имеют при N-10 аминоалкильные заместители, а положение С-2 свободно (пропазин, 263) или замешено галогеном (аминазин, 262 и этаперазин, 265) или метоксигруппой (левомепразин, 264):

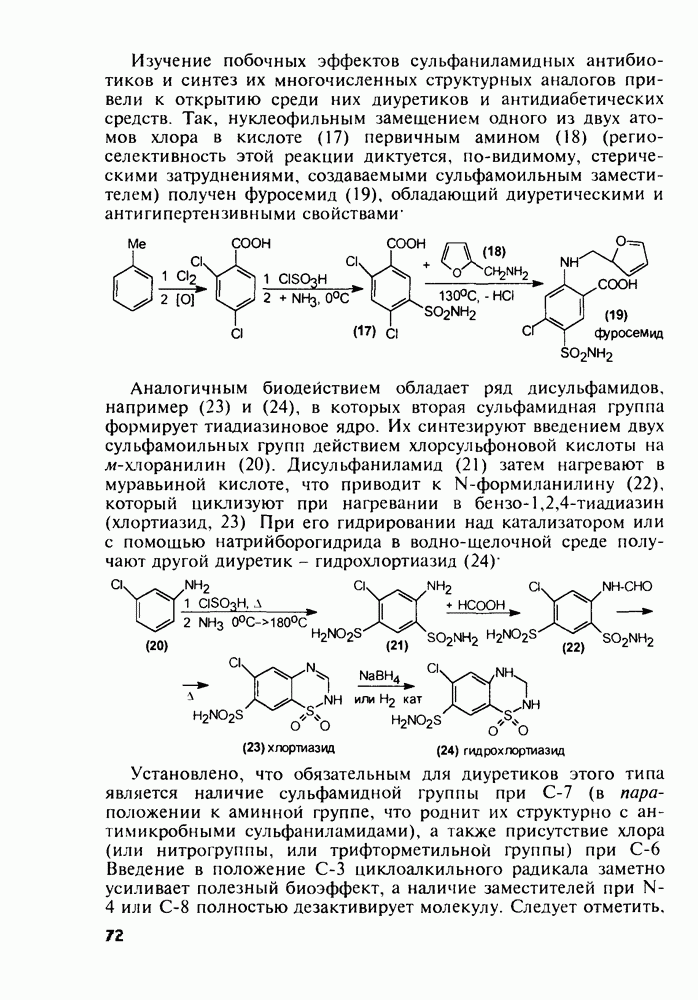
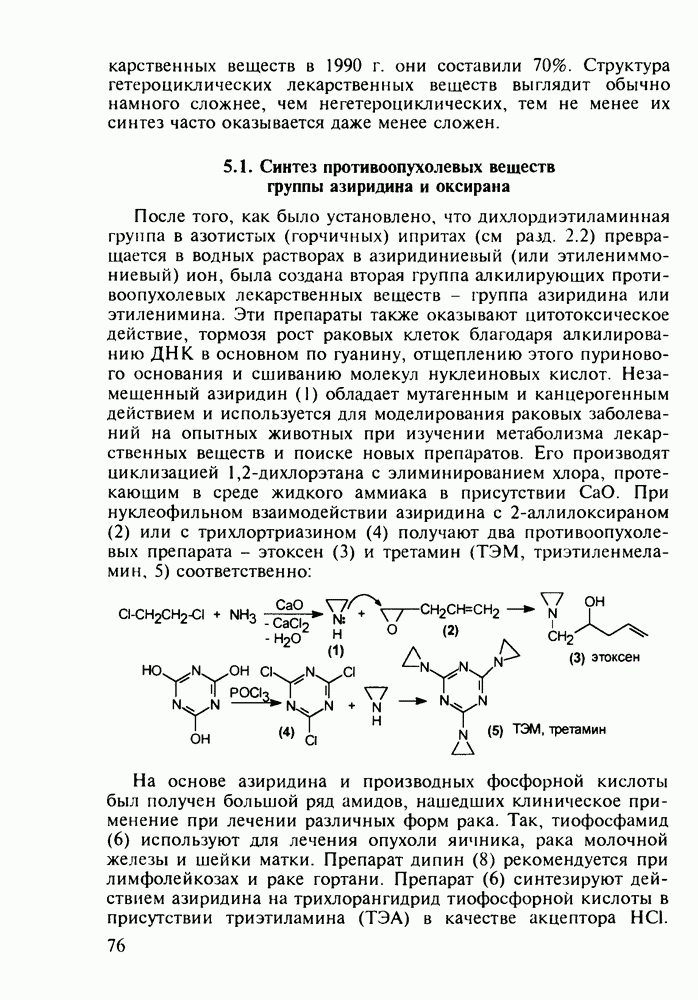
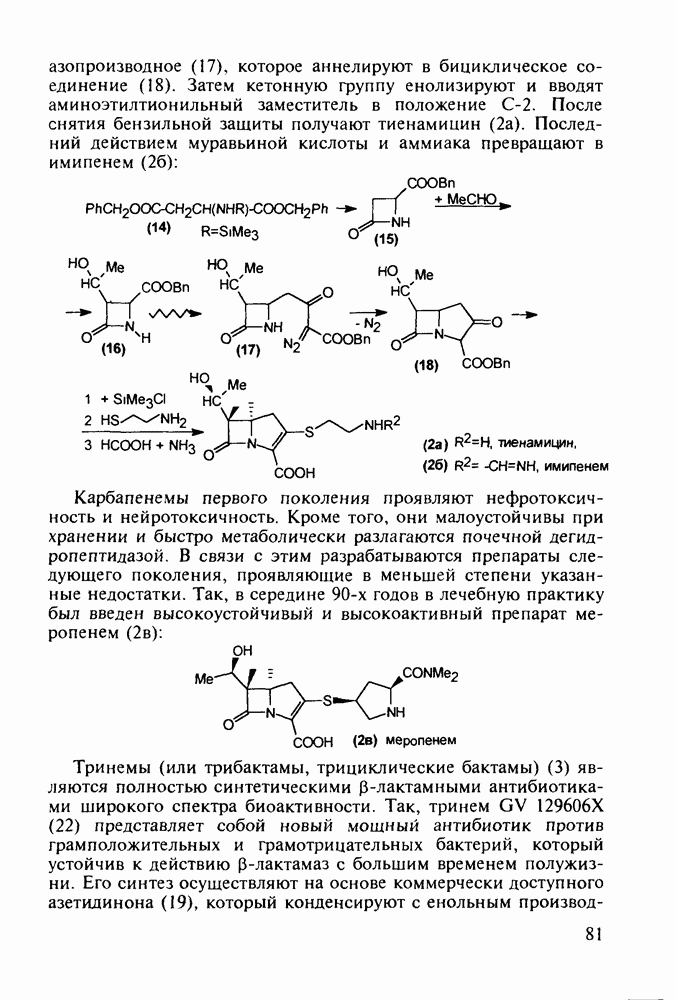
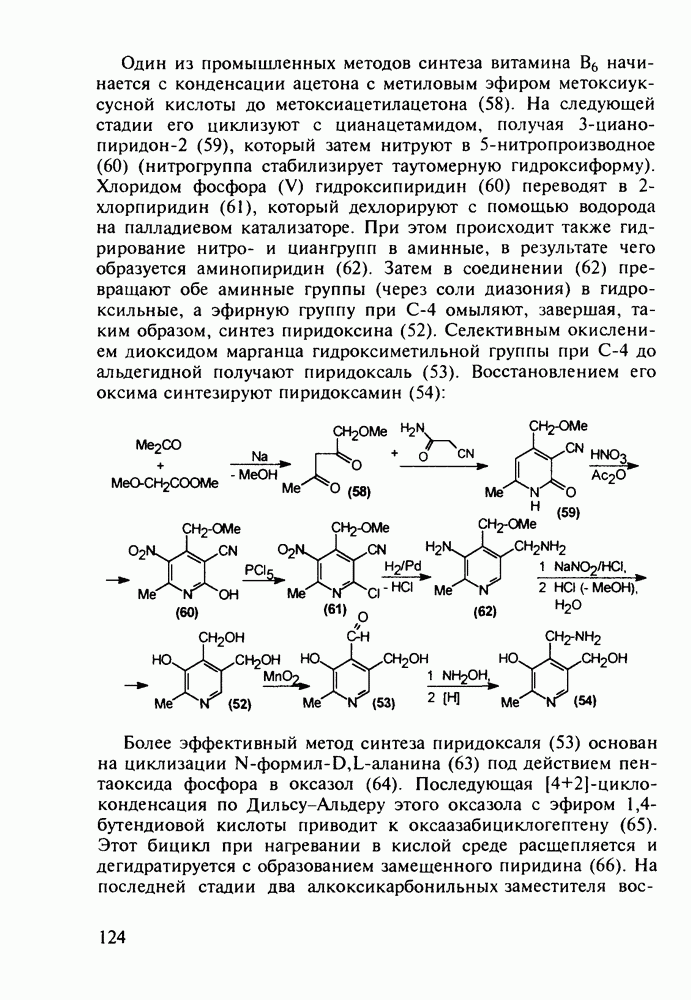
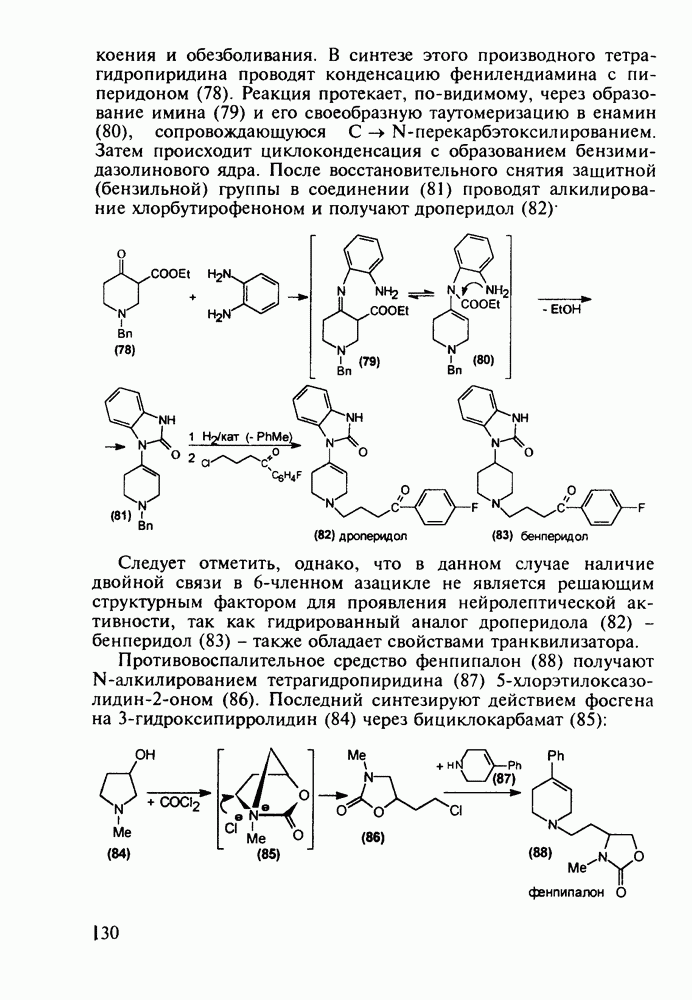
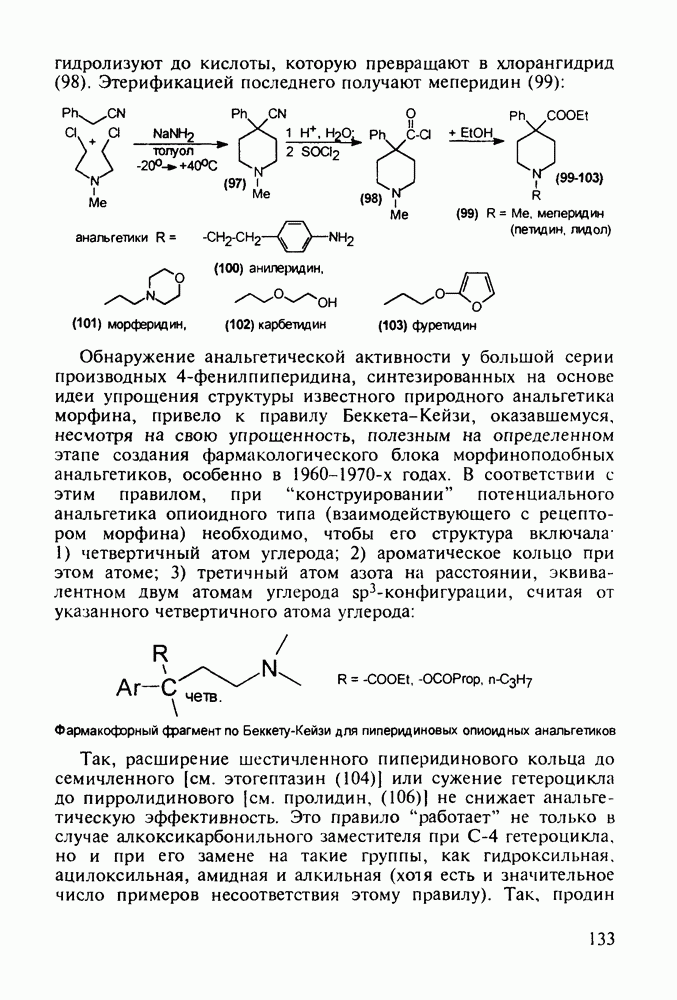
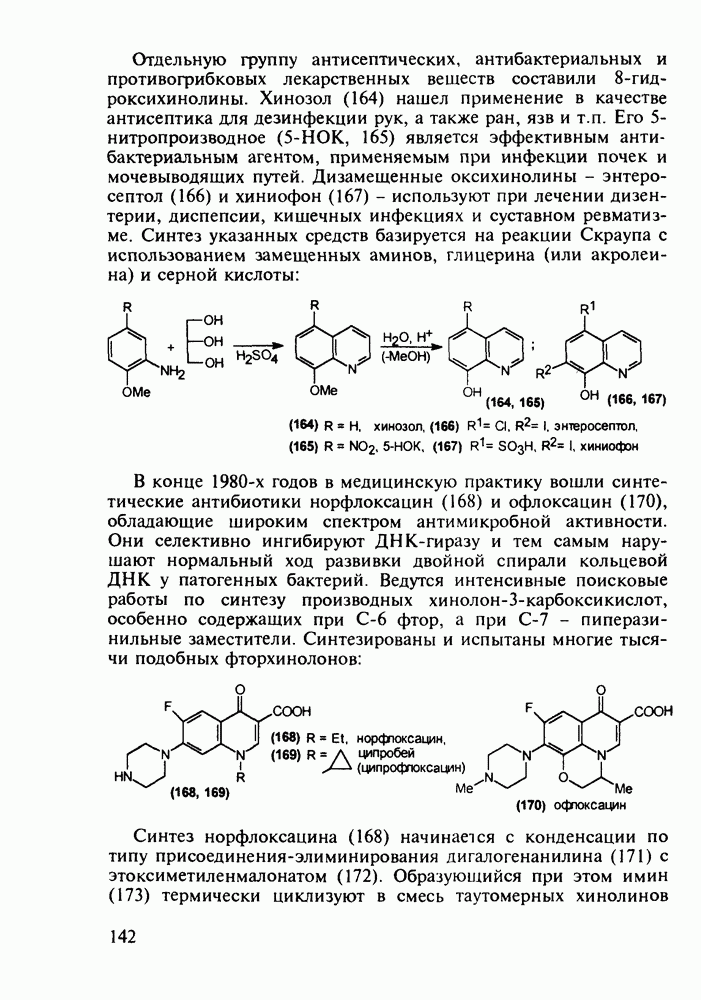
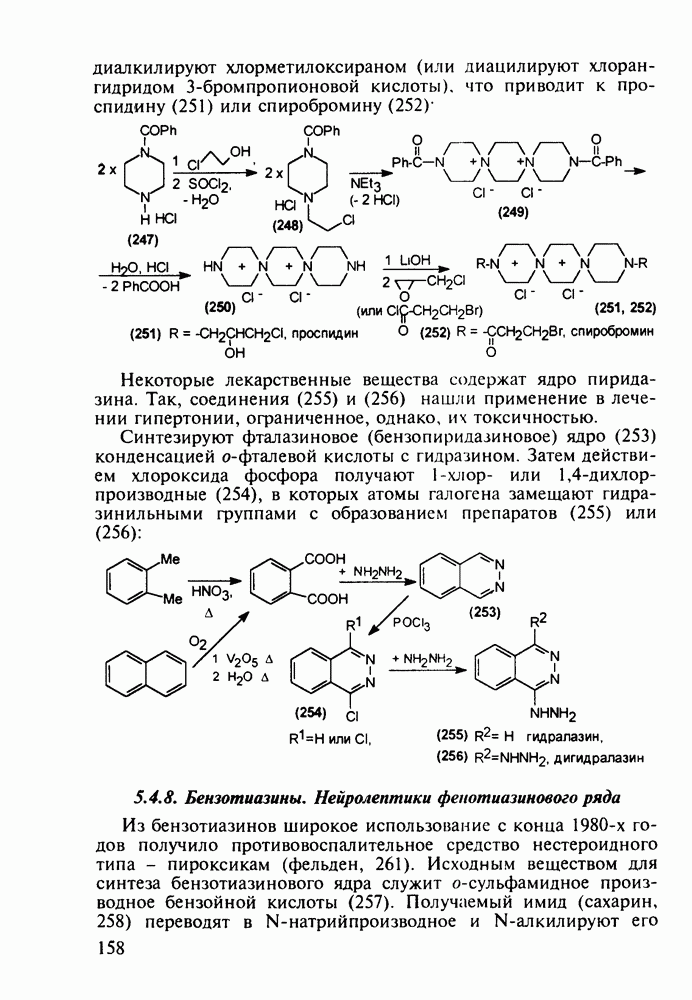
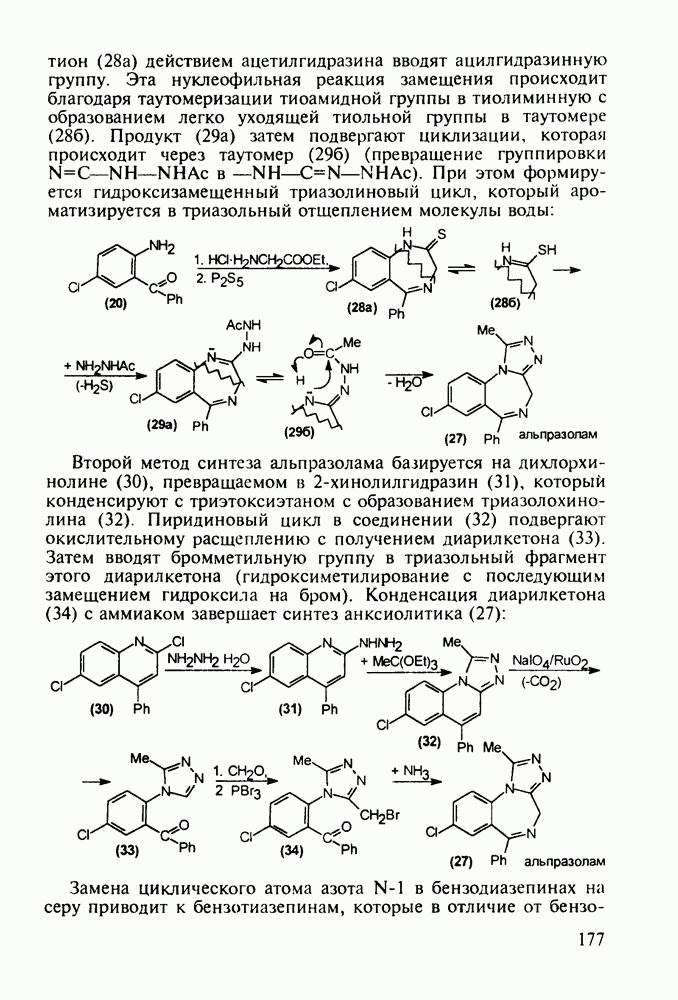
Главными реакциями в синтезе фенотиазинов являются N-арилирование производных анилина [например, в синтезе аминазина (262) это получение диариламина (266)] и гетероциклизация диариламинов. Последнюю осуществляют обычно нагреванием с серой, часто в присутствии каталитических количеств иода [см., например, превращение (267) в (268)]. Завершается синтез этих лекарственных веществ обычно N-алкилированием фенотиазинового ядра хлоралкиламинами в присутствии щелочных агентов через анион типа (269). В случае заместителей, чувствительных к действию щелочей, прибегают к введению аминоалкильных групп через карбаматы (270), термически разлагаемые с выделением диоксида углерода:

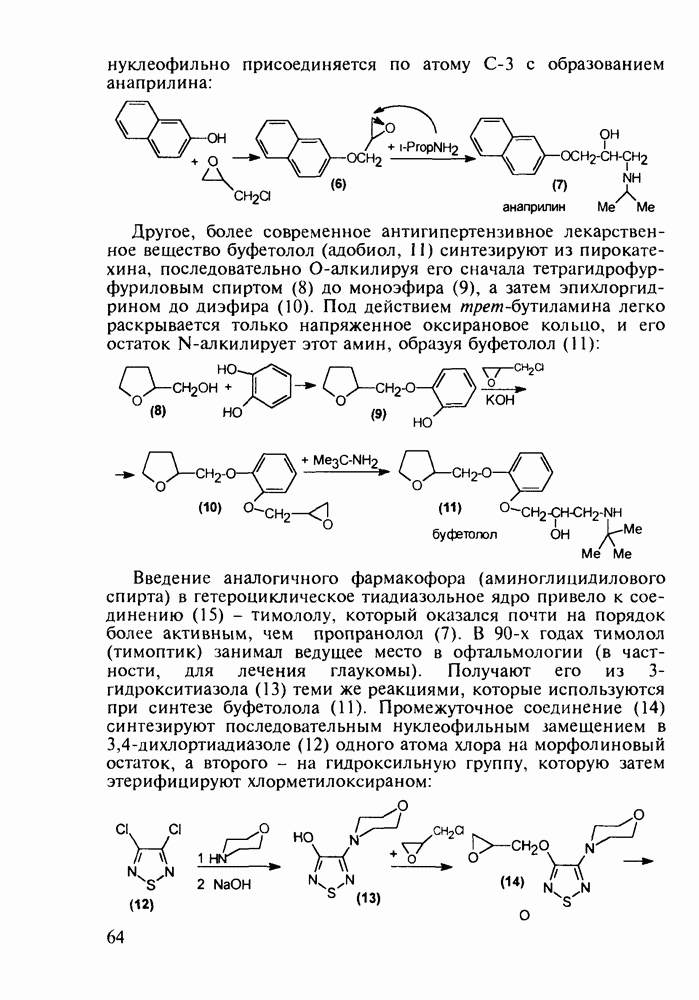
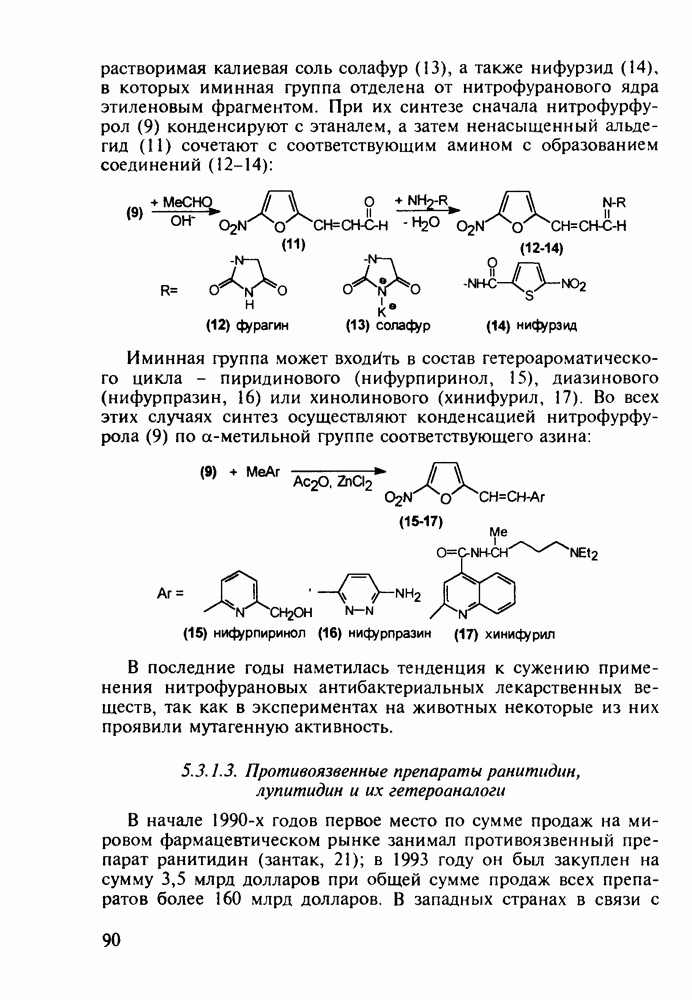
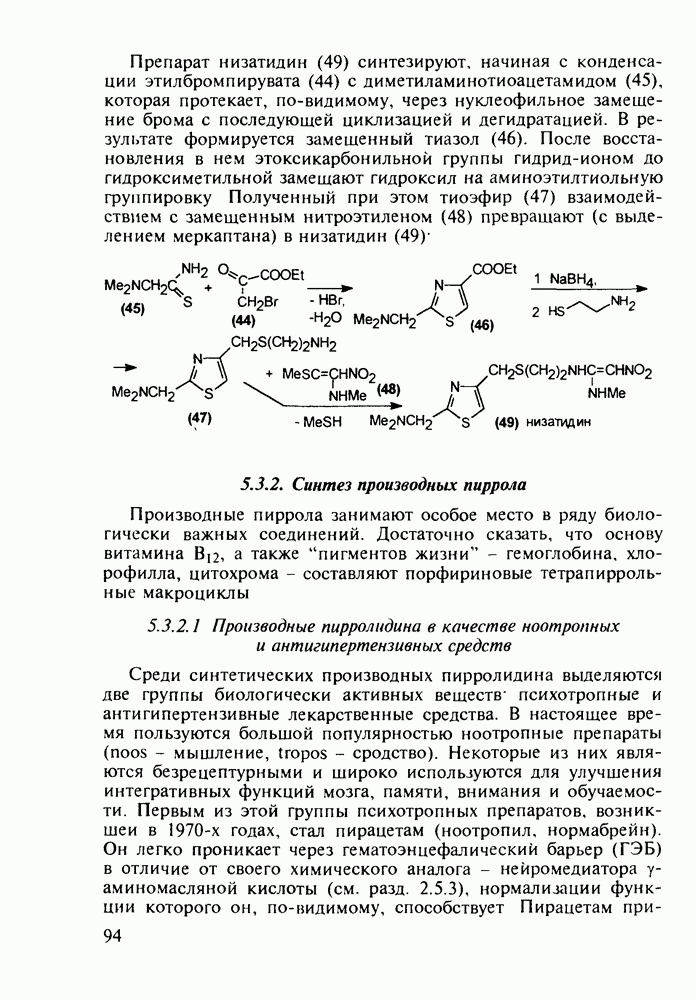
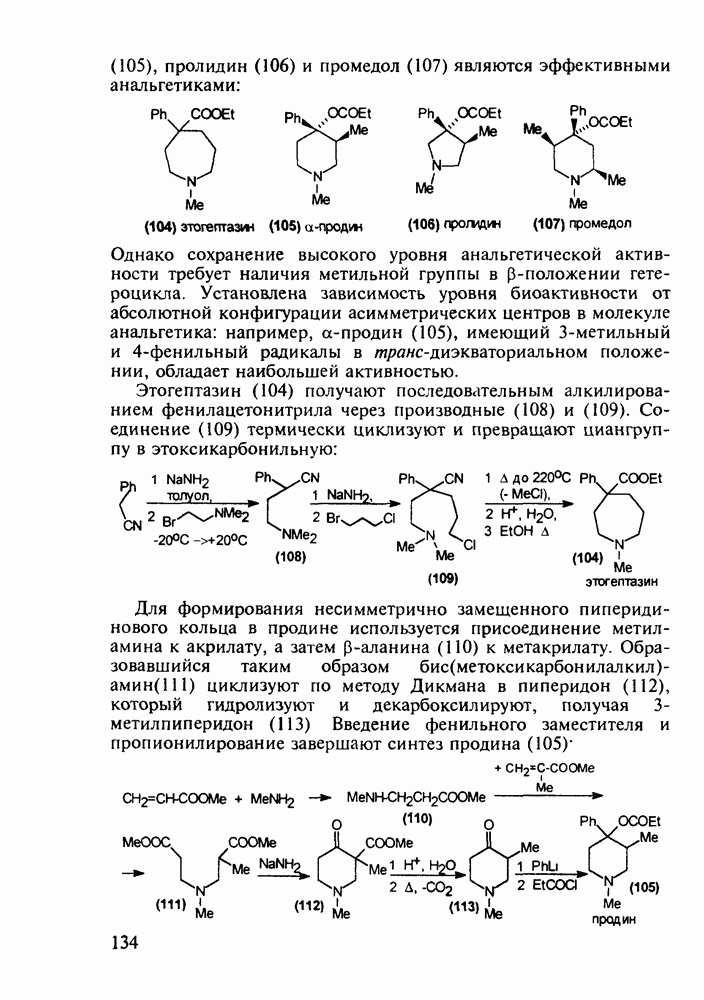
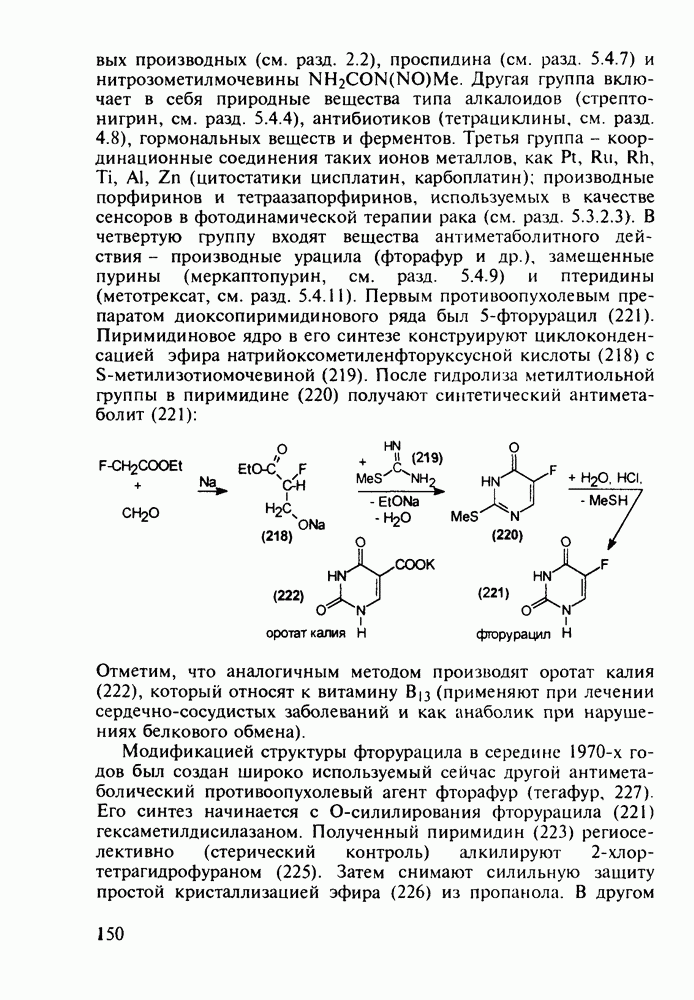
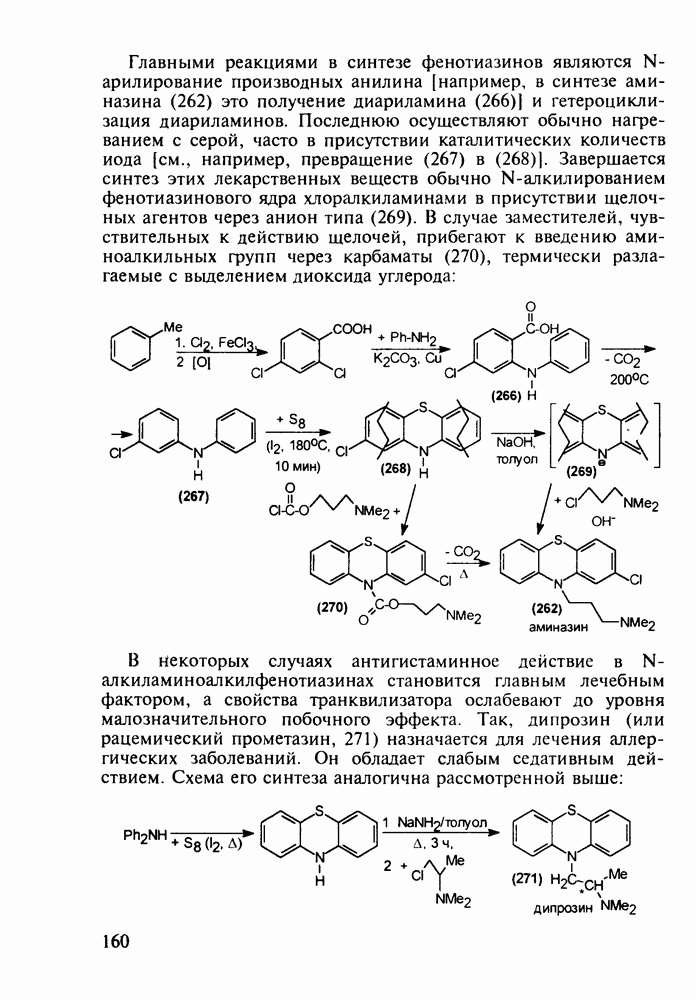
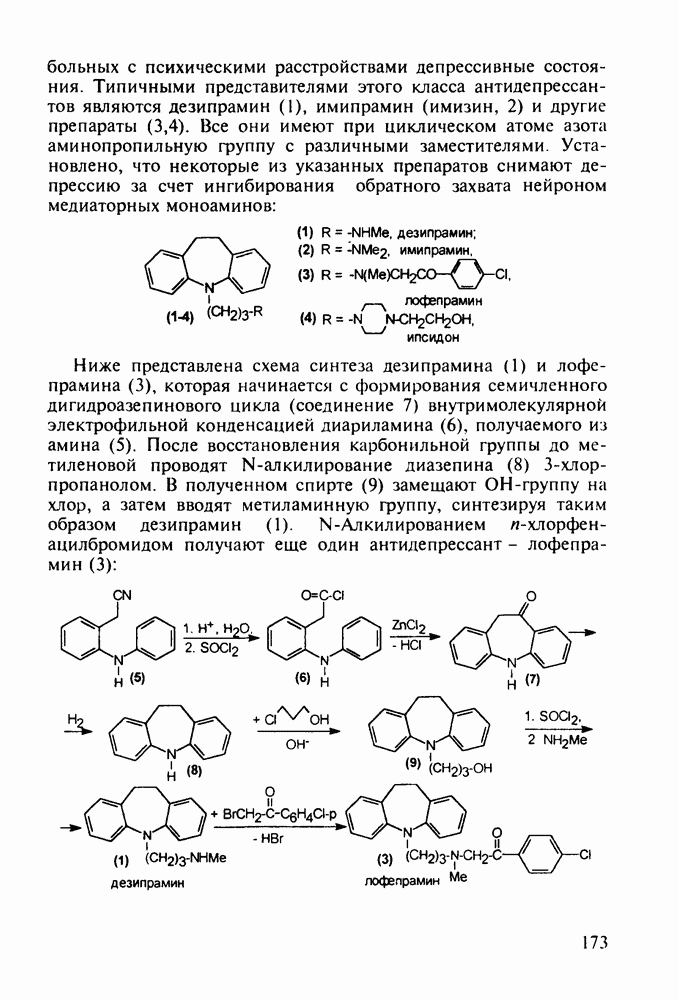
В Некоторых случаях антигистаминное действие в N-алкиламиноалкилфенотиазинах становится главным лечебным фактором, а свойства транквилизатора ослабевают до уровня малозначительного побочного эффекта. Так, дипрозин (или рацемический прометазин, 271) назначается для лечения аллергических заболеваний. Он обладает слабым седативным действием. Схема его синтеза аналогична рассмотренной выше:

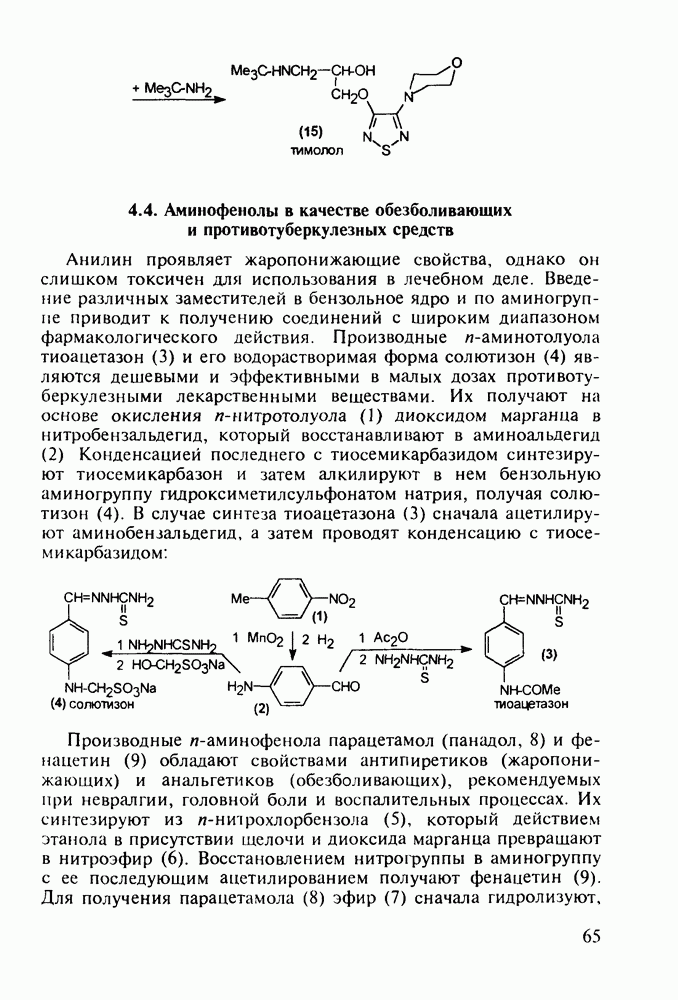
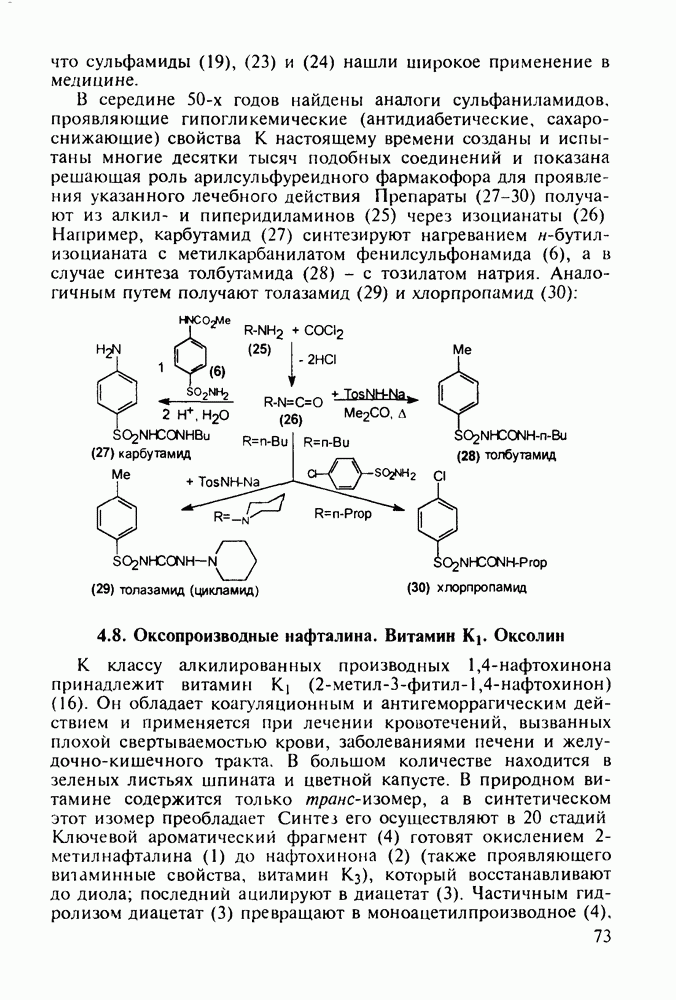
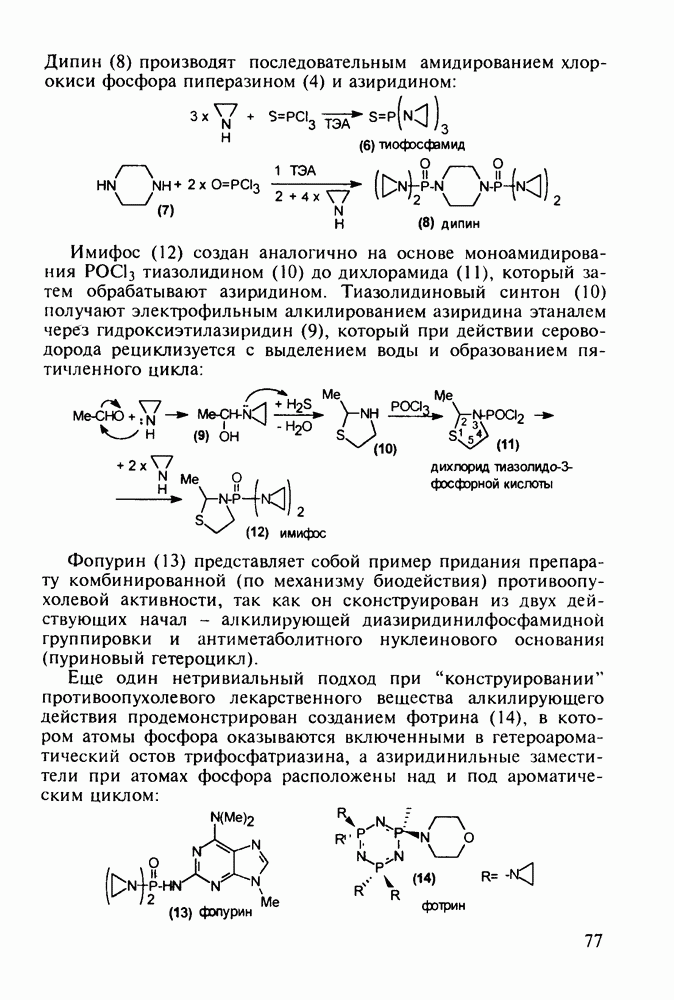
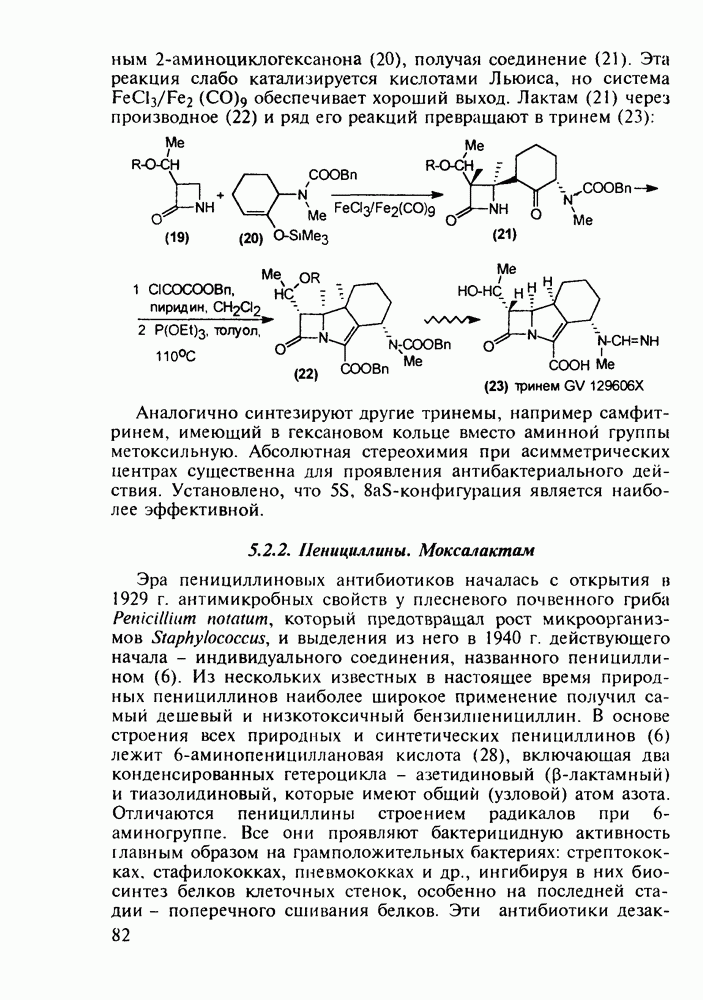
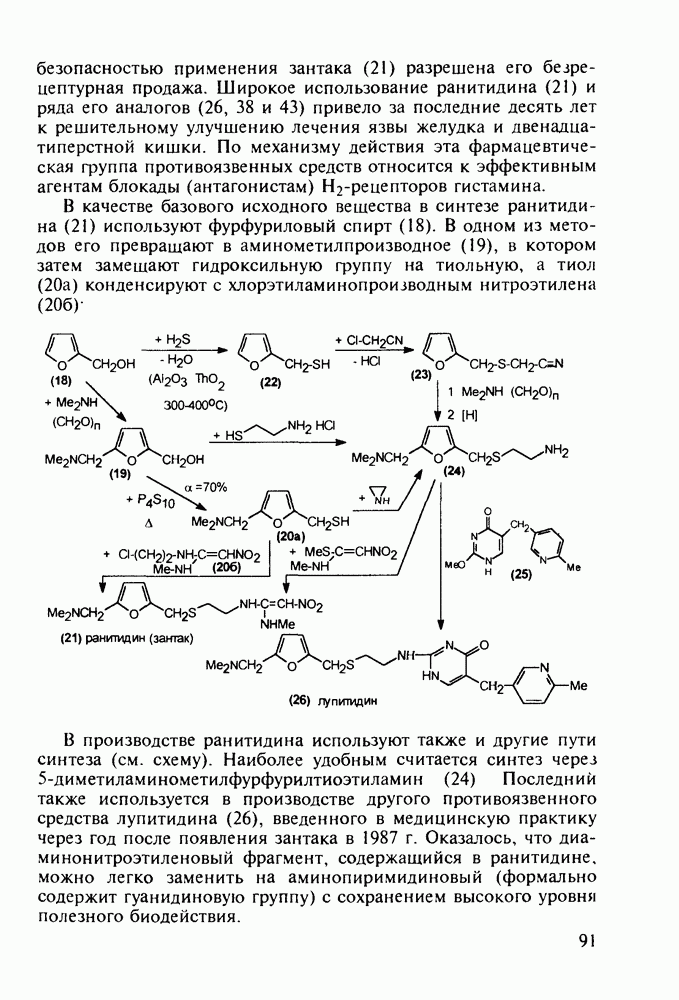
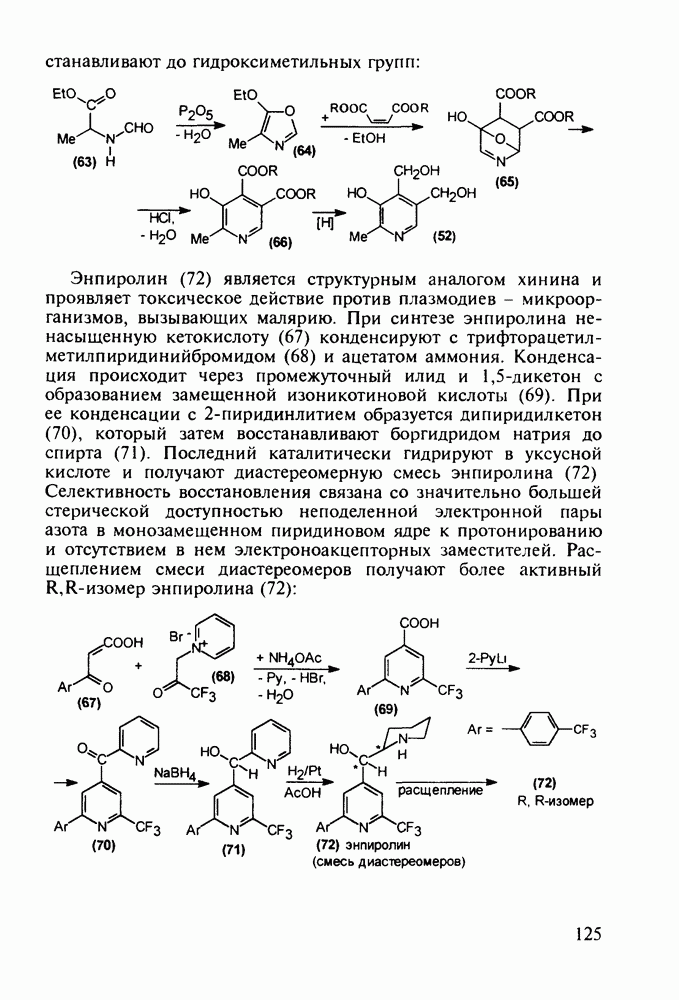
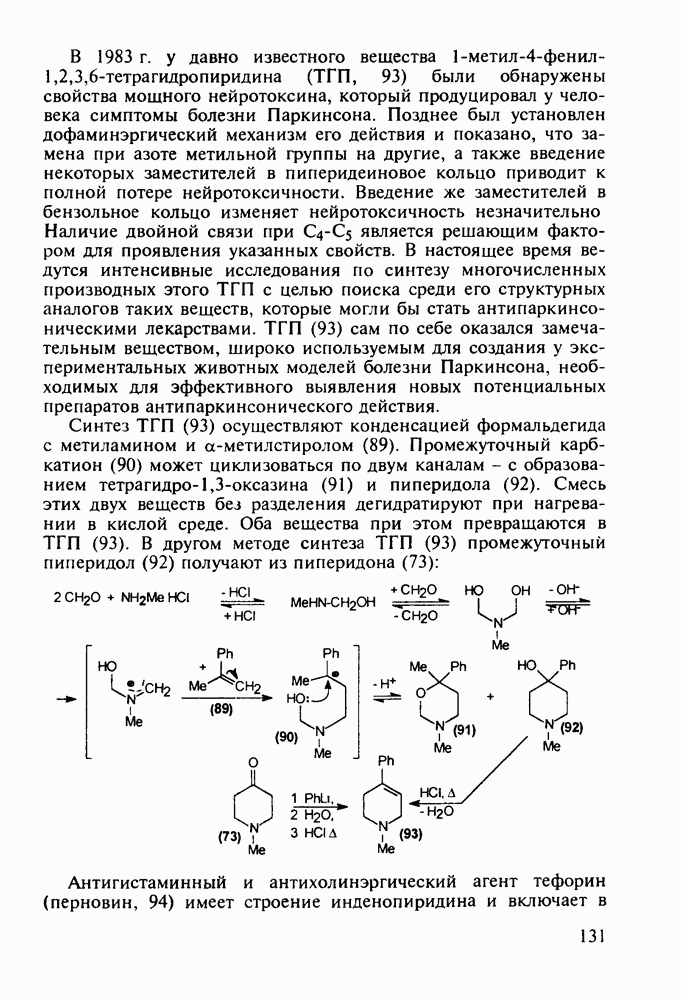
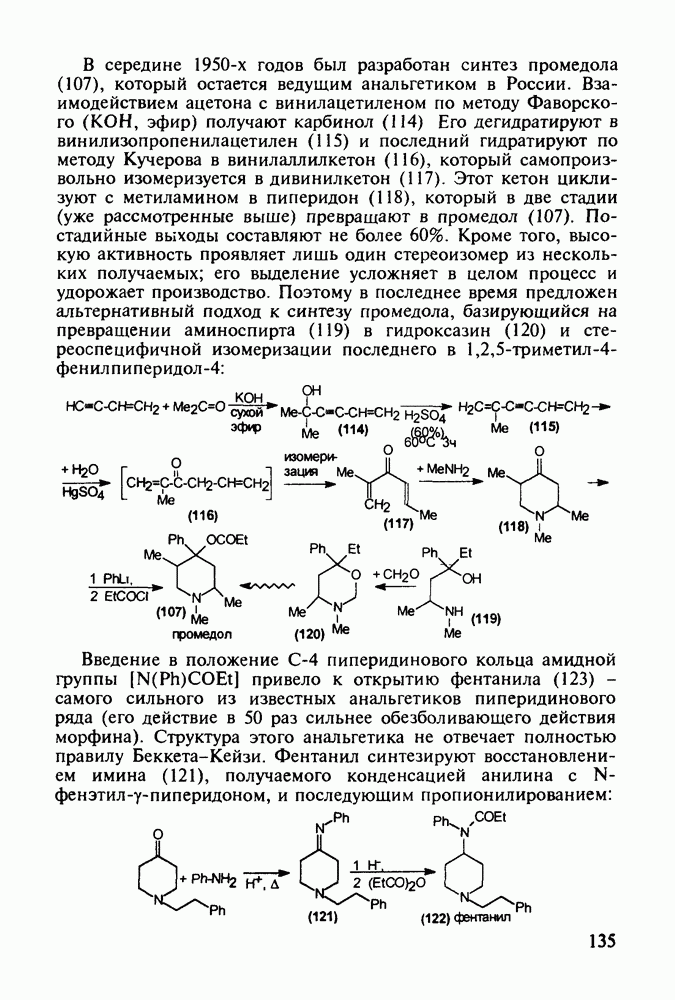
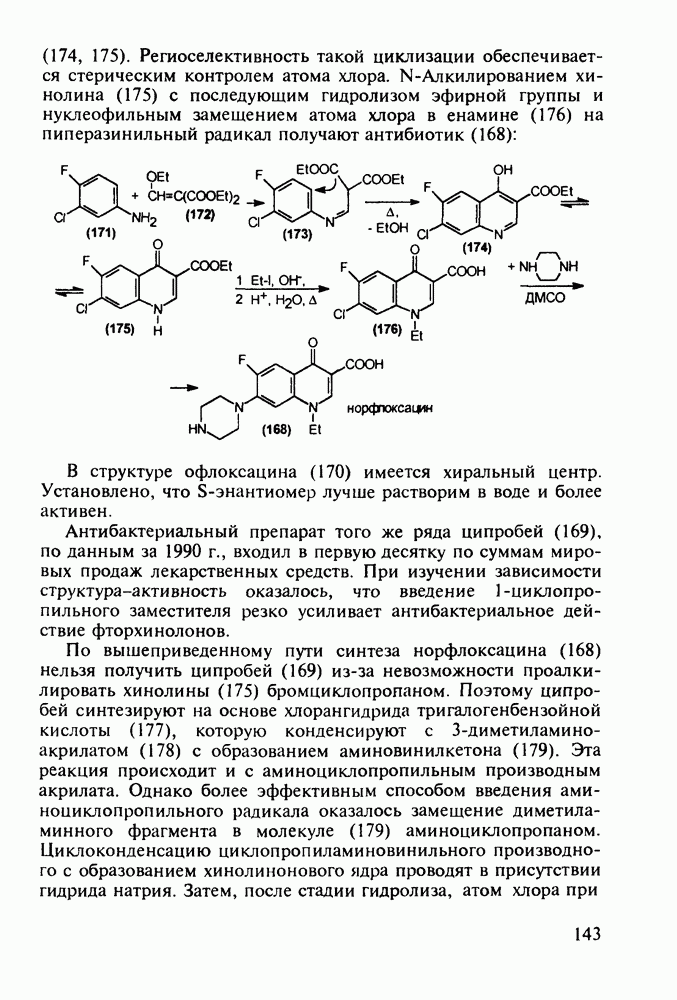
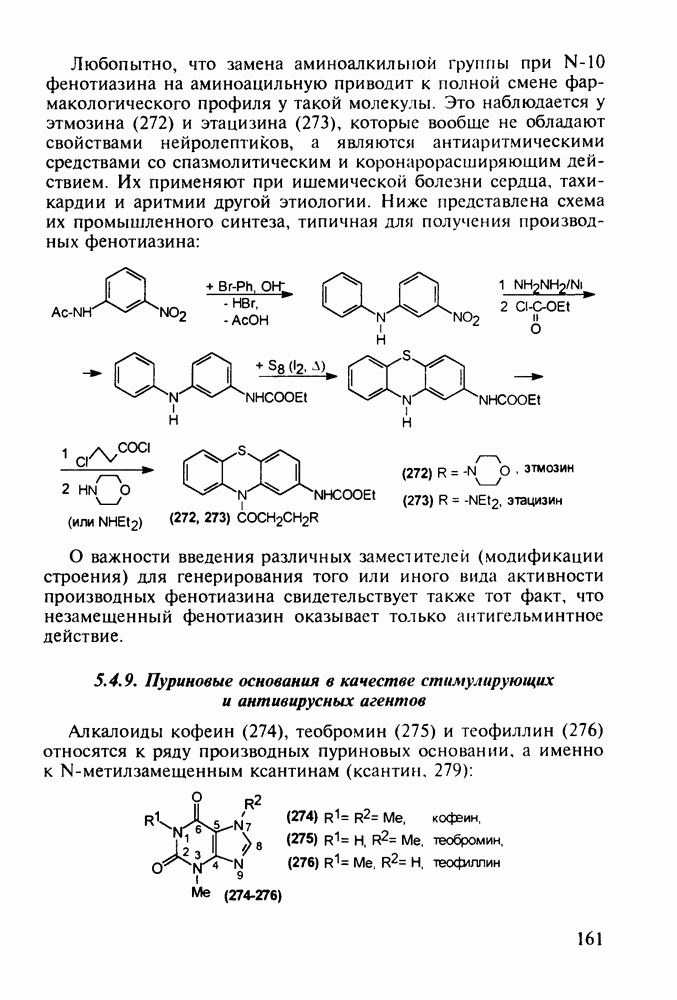
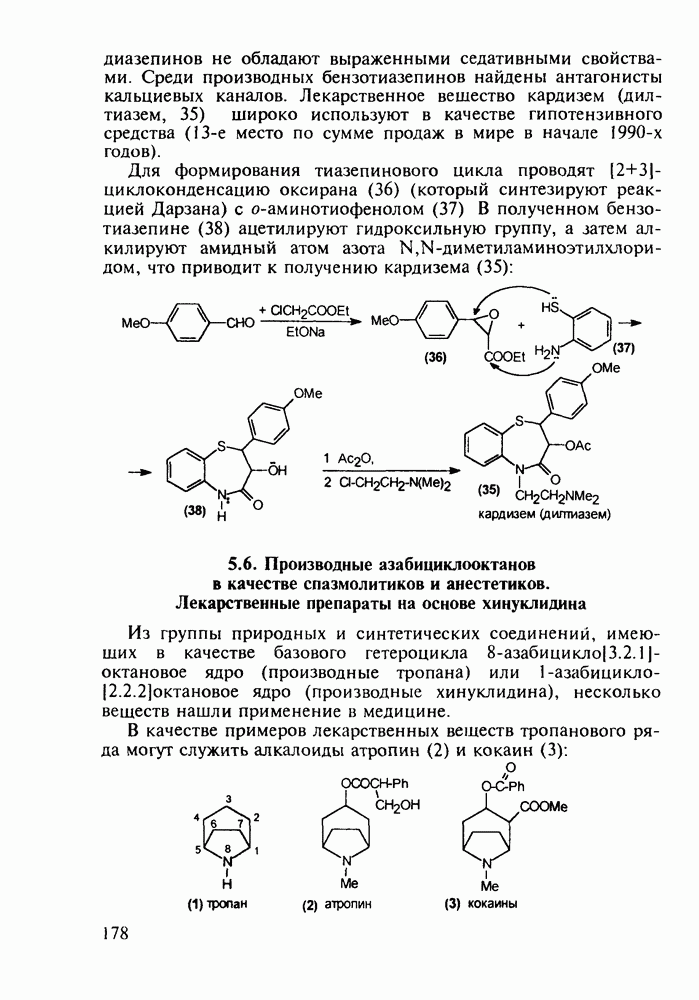
Любопытно, что замена аминоалкильной группы при  фенотиазина на аминоацильную приводит к полной смене фармакологического профиля у такой молекулы. Это наблюдается у этмозина (272) и этацизина (273), которые вообще не обладают свойствами нейролептиков, а являются антиаритмическими средствами со спазмолитическим и коронарорасширяюшим действием. Их применяют при ишемической болезни сердца, тахикардии и аритмии другой этиологии. Ниже представлена схема их промышленного синтеза, типичная для получения производных фенотиазина:
фенотиазина на аминоацильную приводит к полной смене фармакологического профиля у такой молекулы. Это наблюдается у этмозина (272) и этацизина (273), которые вообще не обладают свойствами нейролептиков, а являются антиаритмическими средствами со спазмолитическим и коронарорасширяюшим действием. Их применяют при ишемической болезни сердца, тахикардии и аритмии другой этиологии. Ниже представлена схема их промышленного синтеза, типичная для получения производных фенотиазина:

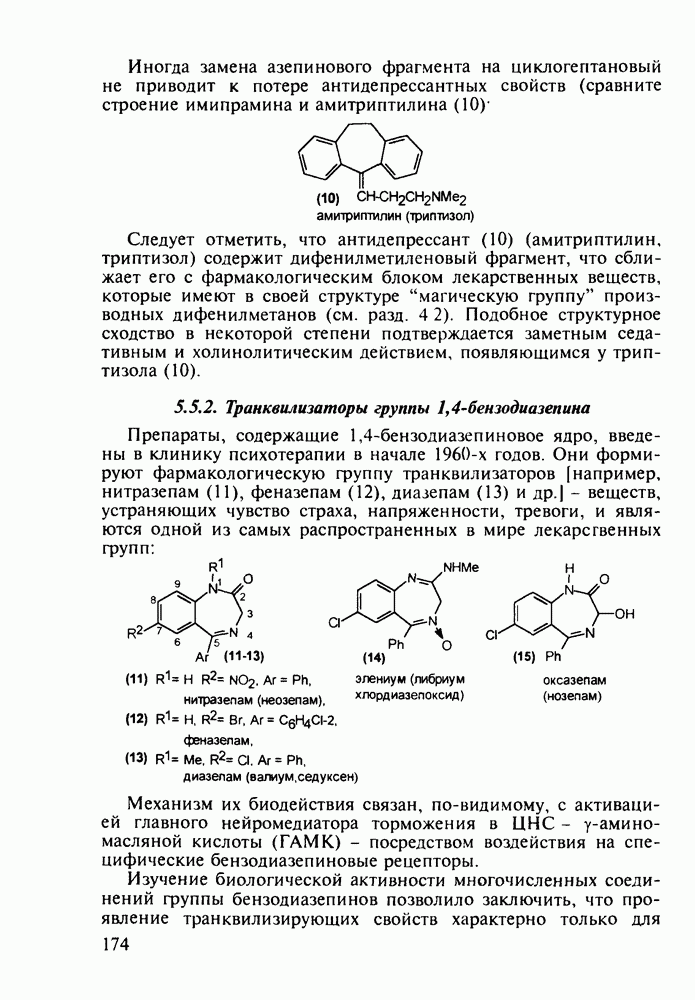
О важности введения различных заместителей (модификации строения) для генерирования того или иного вида активности производных фенотиазина свидетельствует также тот факт, что незамещенный фенотиазин оказывает только антигельминтное действие.
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие
- 1. ВВЕДЕНИЕ
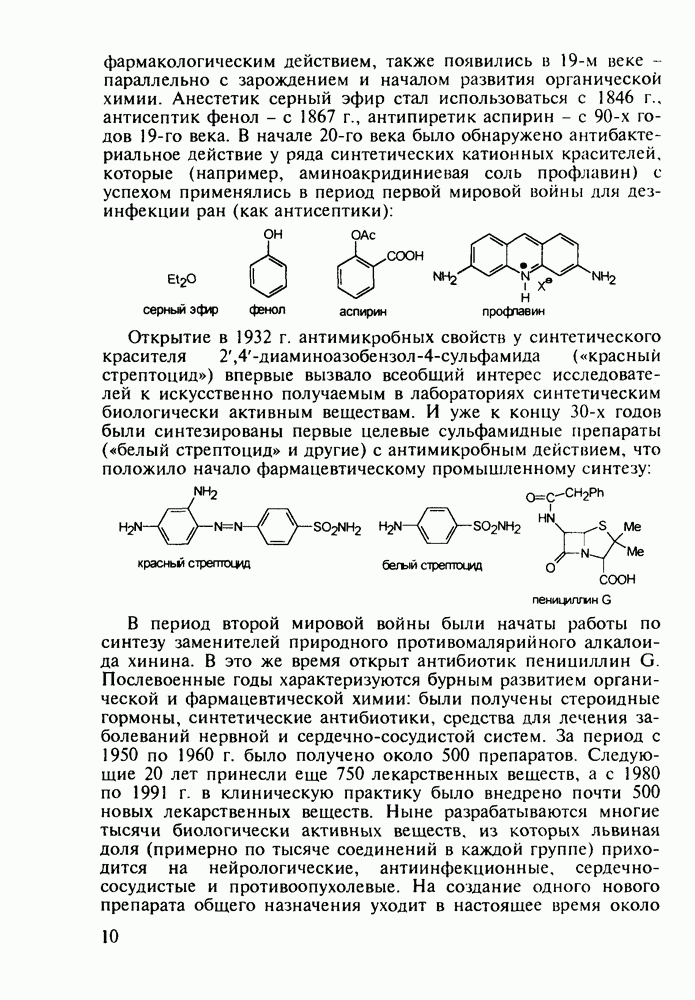
- 1.1. Эволюция органической химии лекарственных веществ
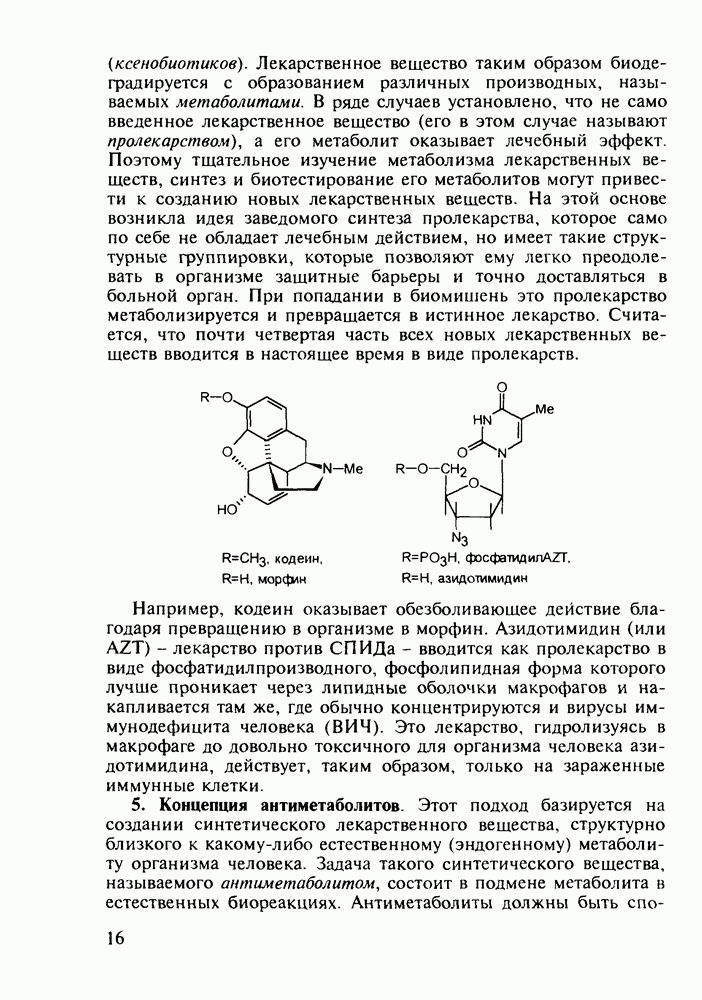
- 1.2. Современные требования к лекарственным веществам
- 1.3. Стадии биологического изучения лекарственного вещества
- 1.4. Основы стратегии создания новых синтетических лекарственных веществ
- 1.5. Связь структура-биологическая активность
- 1.6. Принципиальная схема разработки нового лекарственного вещества
- 1.7. Классификация лекарственных веществ
- 1.8. Основные болезни человека и ведущие группы лекарственных веществ на современном фармацевтическом рынке
- 2. СИНТЕЗ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ АЛИФАТИЧЕСКОГО РЯДА
- 2.2. Группа противораковых веществ с дихлордиэтиламинным фармакофором
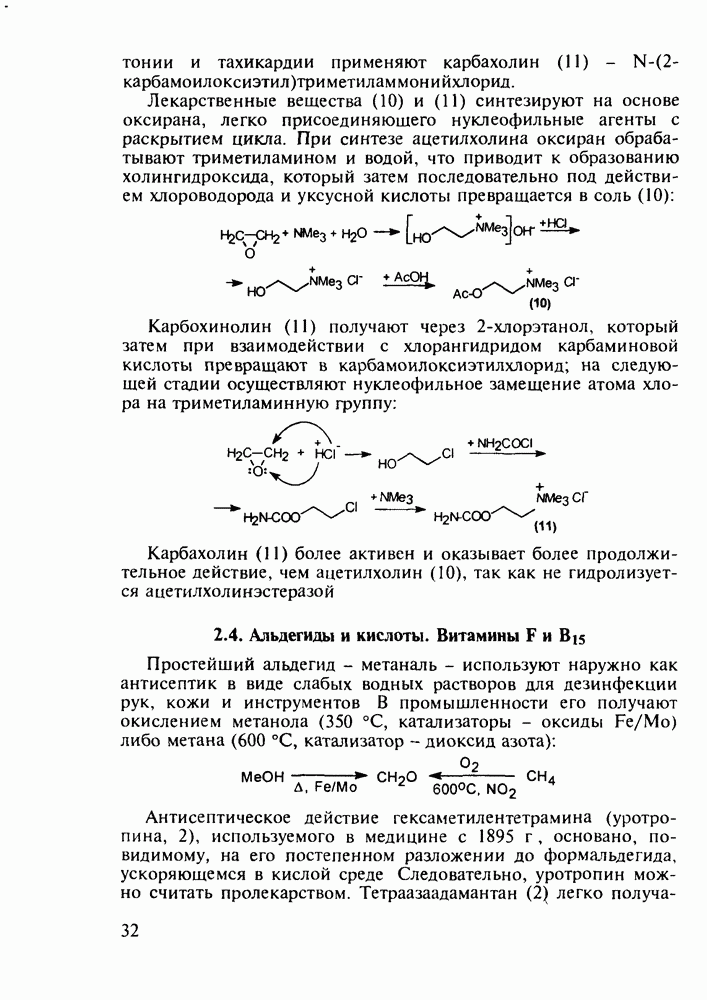
- 2.3. Алканолы, аминоалканолы и их эфиры. Нейромедиатор ацетилхолин и холиномиметики
- 2.4. Альдегиды и кислоты. Витамины F и B15
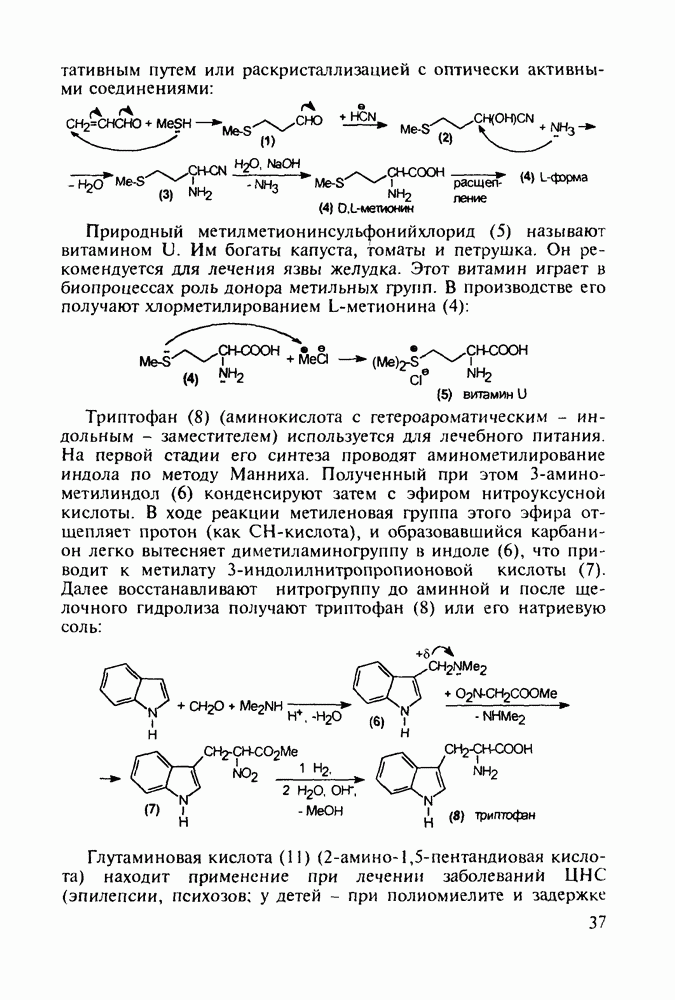
- 2.5. Аминокислоты
- 2.5.2. Производные b-аминокислот. Витамин B3
- 2.5.3. Производные у-аминомасляной кислоты. Нейротропные средства. Витамин BT
- 2.5.4. Другие аминокислоты
- 3. ЛЕКАРСТВЕННЫЕ ВЕЩЕСТВА АЛИЦИКЛИЧЕСКОГО РЯДА
- 3.2. Противозачаточные и противовоспалительные вещества на основе циклопентафенантрена. Синтез витамина D
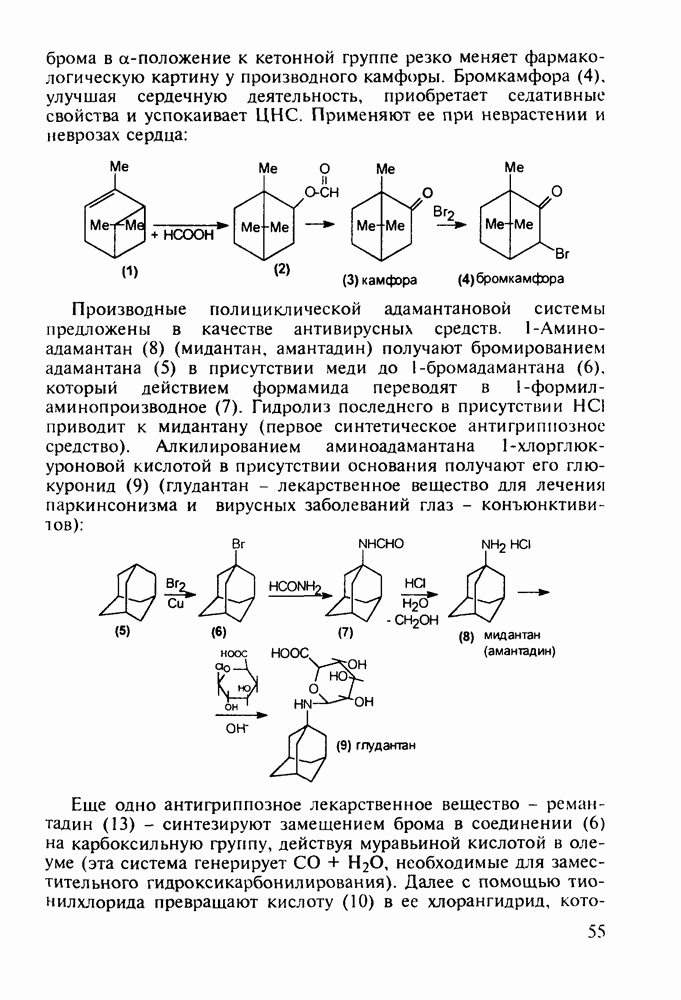
- 3.3. Камфора. Производные адамантана в качестве антивирусных средств
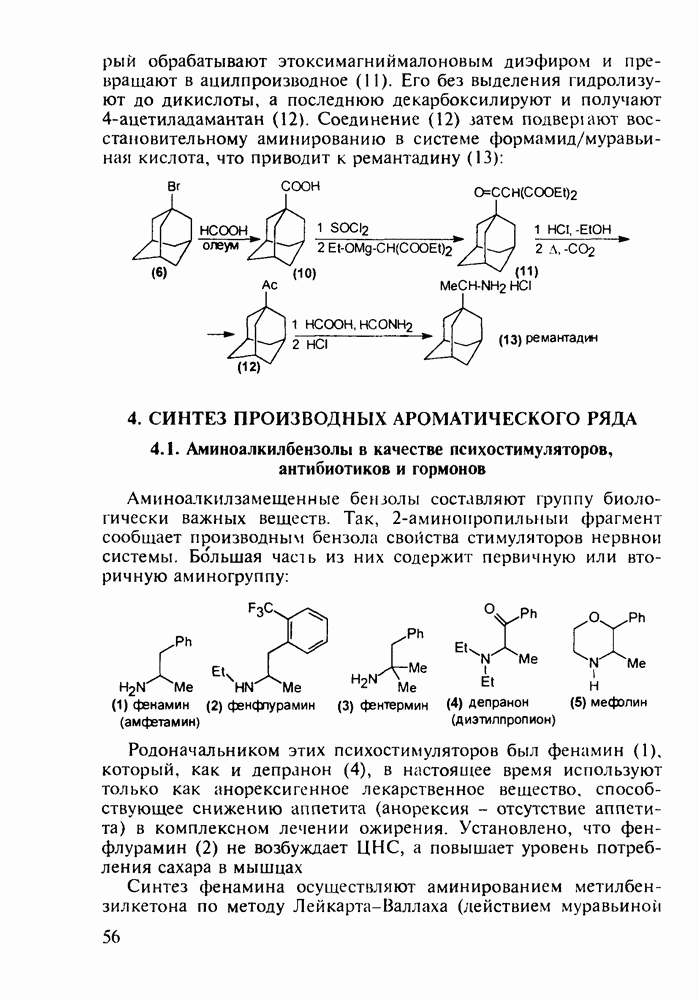
- 4. СИНТЕЗ ПРОИЗВОДНЫХ АРОМАТИЧЕСКОГО РЯДА
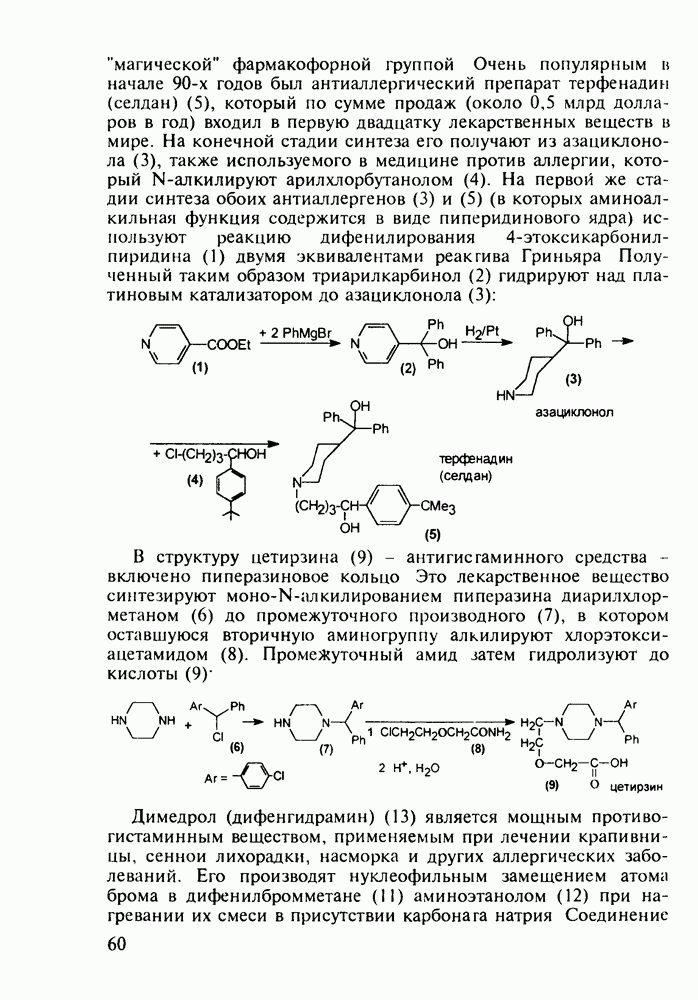
- 4.2. Антигистаминные препараты группы диарилметана
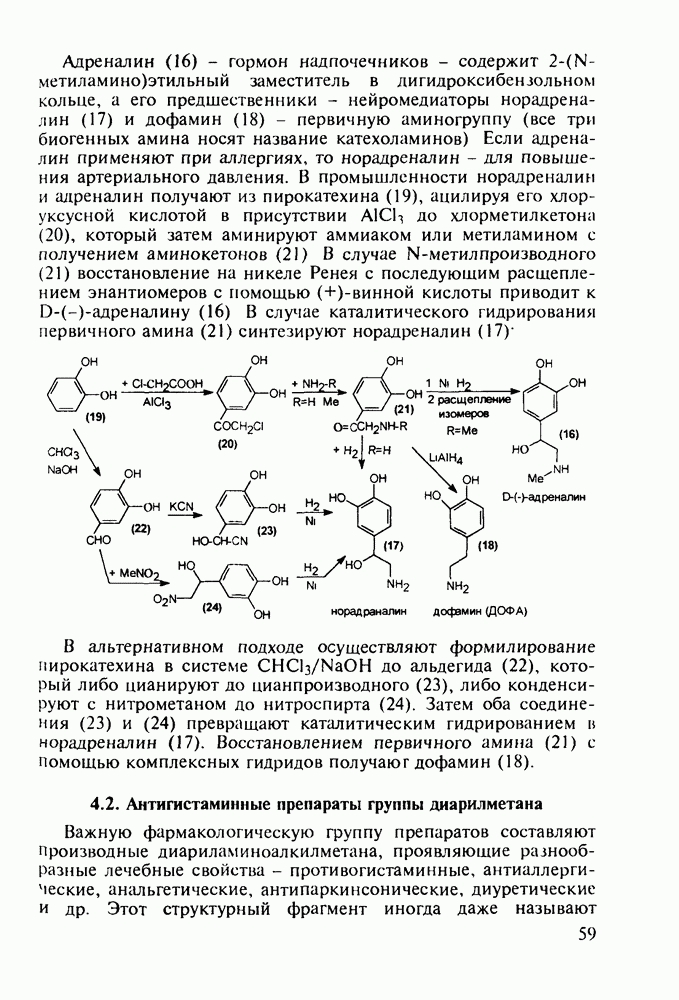
- 4.3. Антисептики и адреноблокаторы фенольного ряда
- 4.4. Аминофенолы в качестве обезболивающих и противотуберкулезных средств
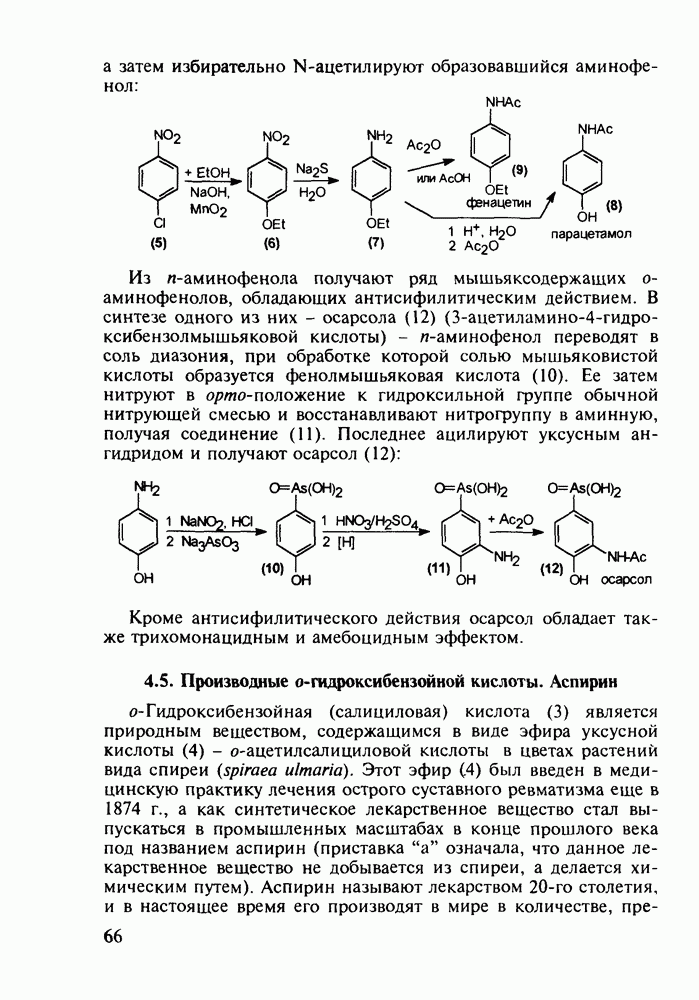
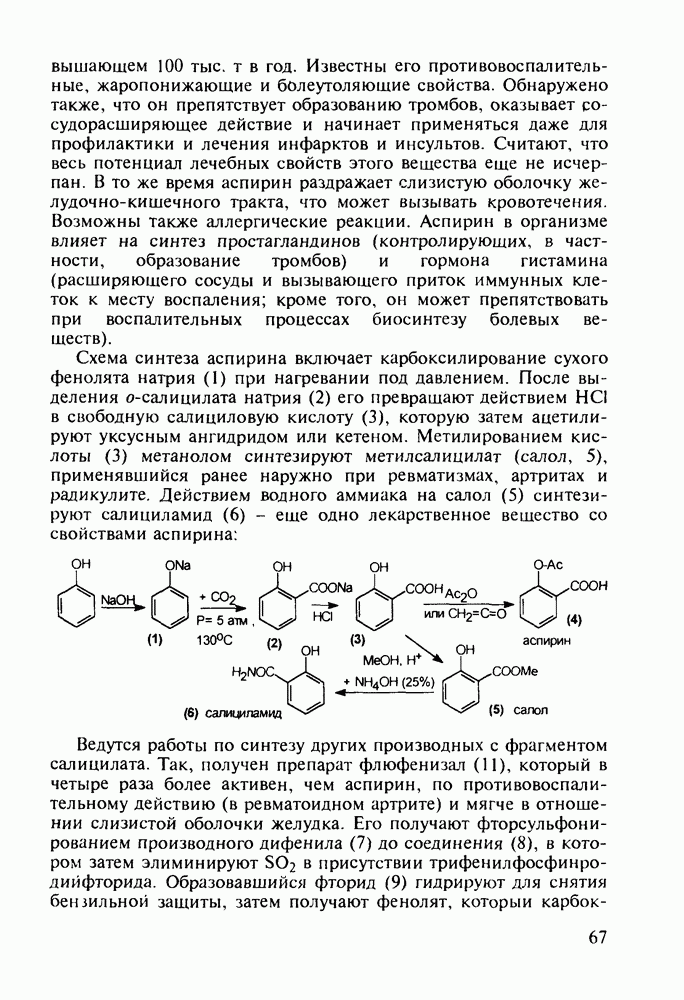
- 4.5. Производные о-гидроксибензойной кислоты. Аспирин
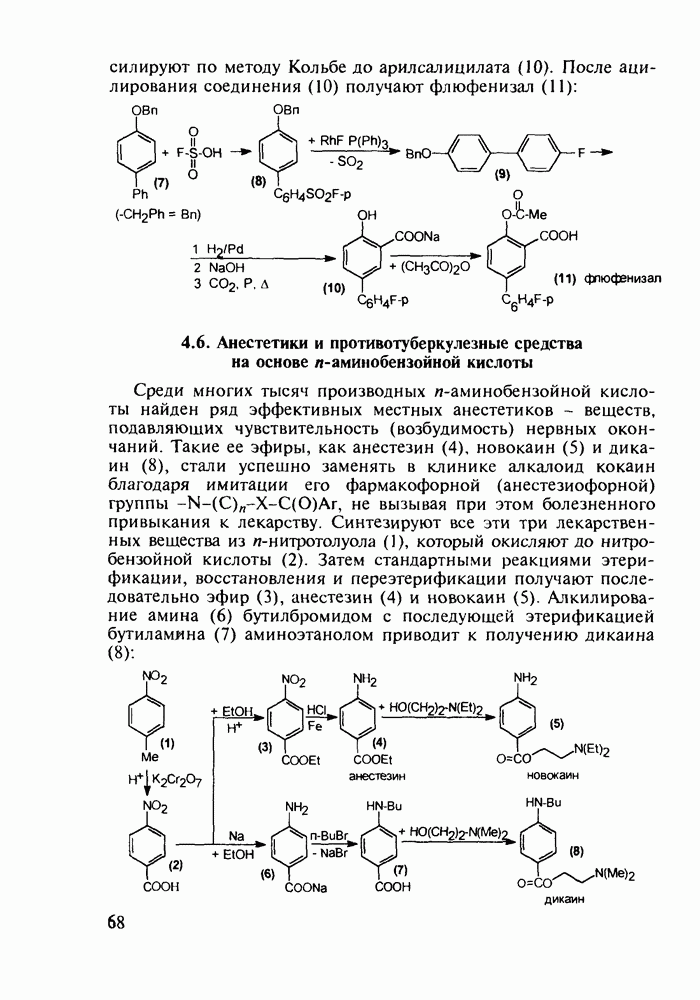
- 4.6. Анестетики и противотуберкулезные средства на основе n-аминобензойной кислоты
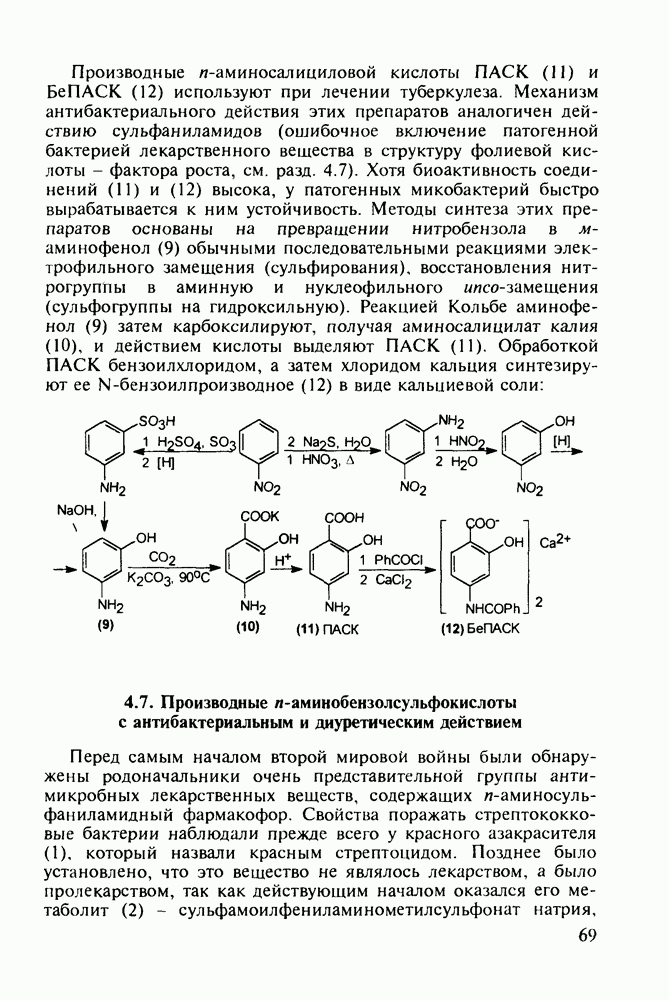
- 4.7. Производные n-аминобензолсульфокислоты с антибактериальным и диуретическим действием
- 4.8. Оксопроизводные нафталина. Витамин К1. Оксолин
- 5. ХИМИЯ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ С БАЗОВЫМ ГЕТЕРОЦИКЛИЧЕСКИМ ФРАГМЕНТОМ
- 5.2. Антибиотики, содержащие четырехчленное азетидиновое ядро
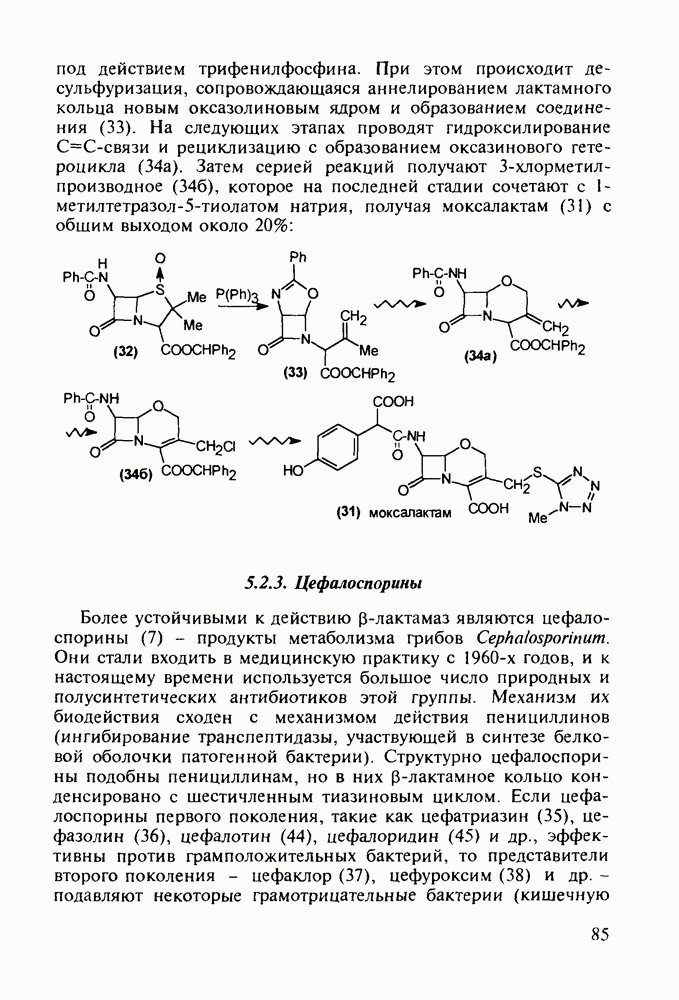
- 5.2.2. Пенициллины. Моксалактам
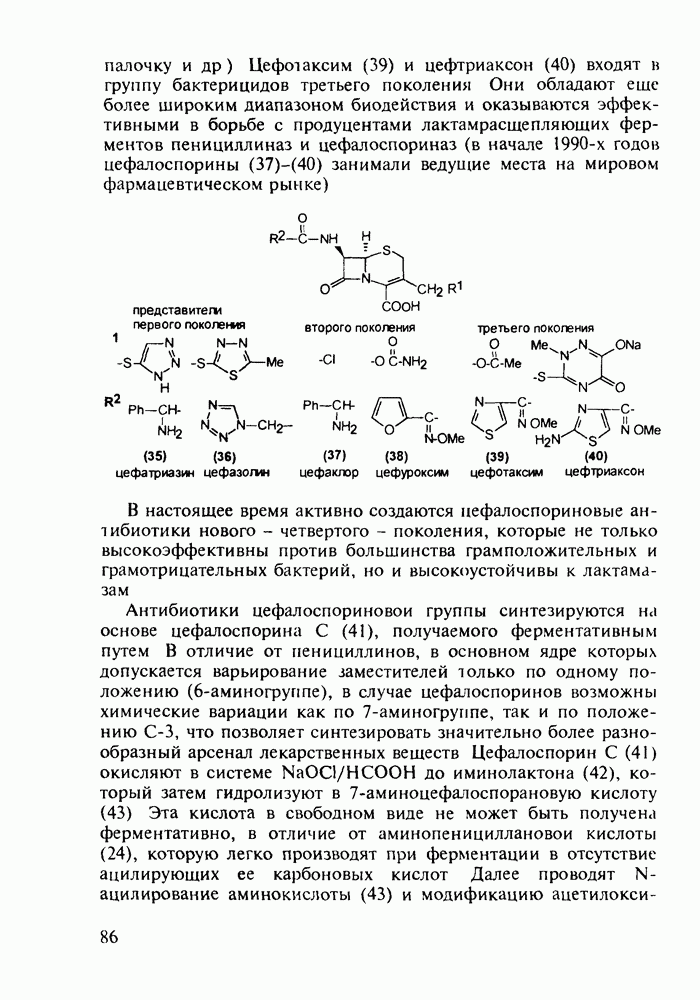
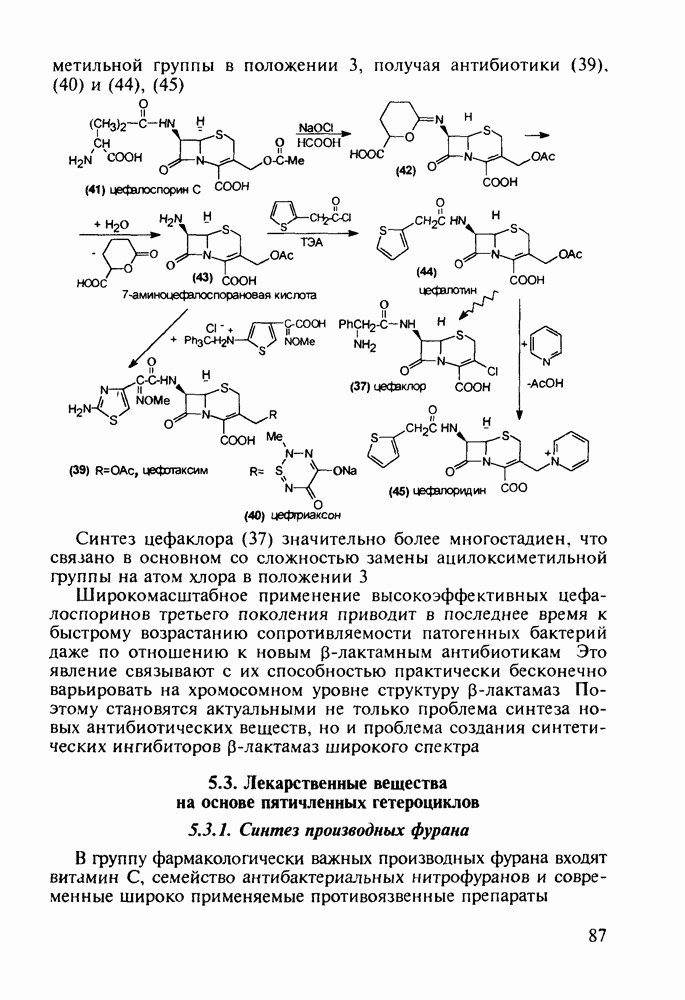
- 5.2.3. Цефалоспорины
- 5.3. Лекарственные вещества на основе пятичленных гетероциклов
- 5.3.2. Синтез производных пиррола
- 5.3.3. Оксазолидины. Антибиотик циклосерин
- 5.3.4. Антипиретики и анальгетики пиразолинового ряда
- 5.3.5. Имидазолы с противопаразитарной, антигипертензивной и другой биоактивностью
- 5.3.6. Производные тиазола. Витамин В1
- 5.3.7. Психостимуляторы с оксадиазольным и тетразольным гетероциклами
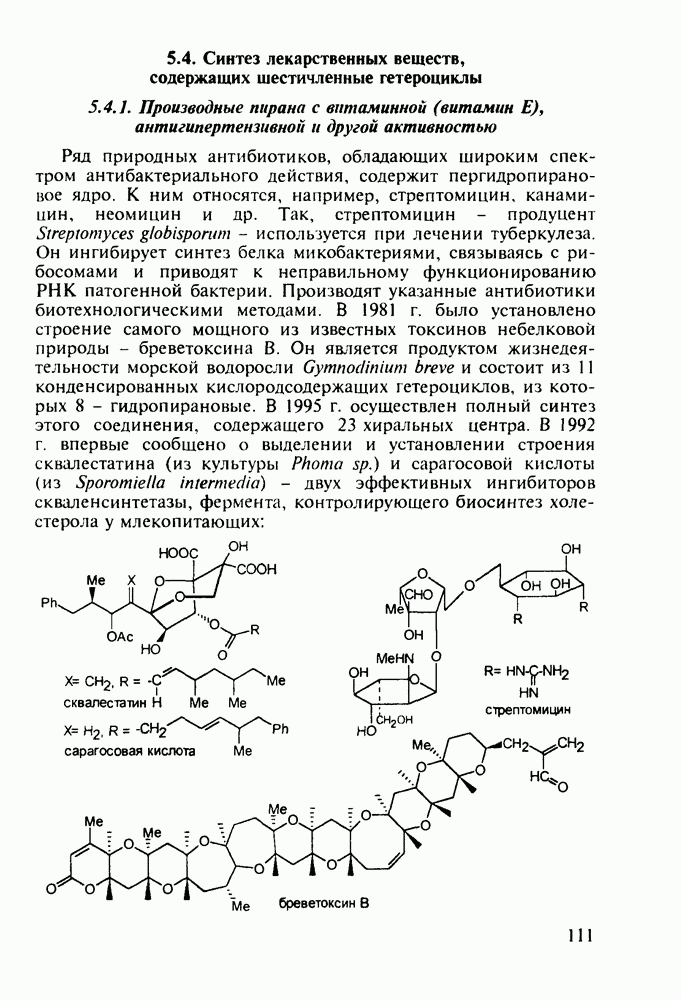
- 5.4. Синтез лекарственных веществ, содержащих шестичленные гетероциклы
- 5.4.2. Синтез лекарственных веществ пиридинового ряда
- 5.4.3. Анальгетики и транквилизаторы пиперидинового ряда
- 5.4.4. Производные хинолина с антималярийным и антибактериальным действием
- 5.4.5. Изохинолины в качестве спазмолитиков и трипаноцидов
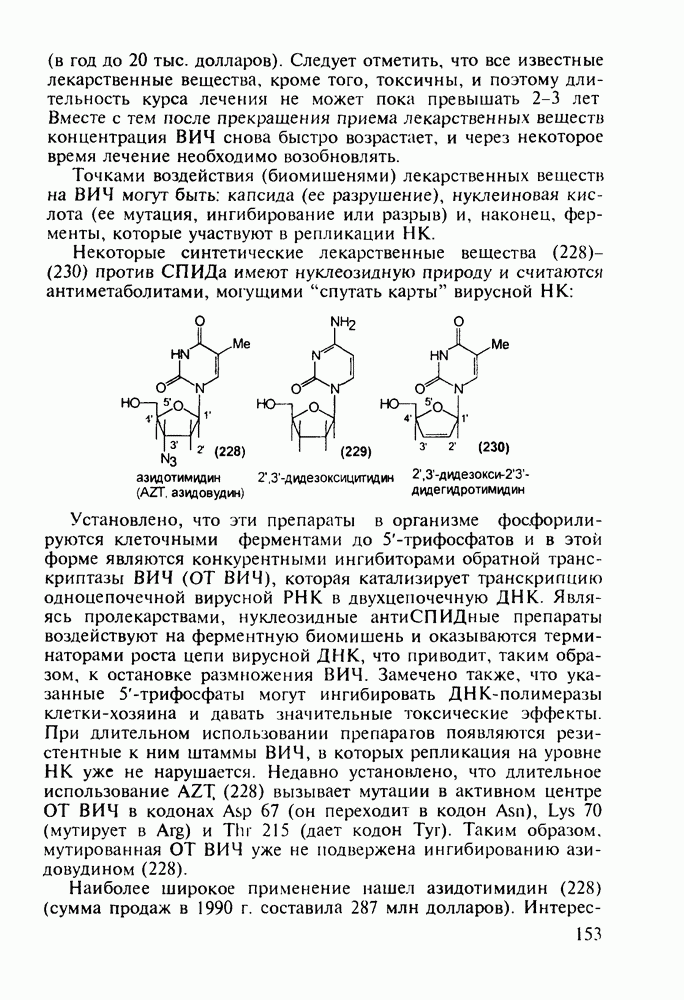
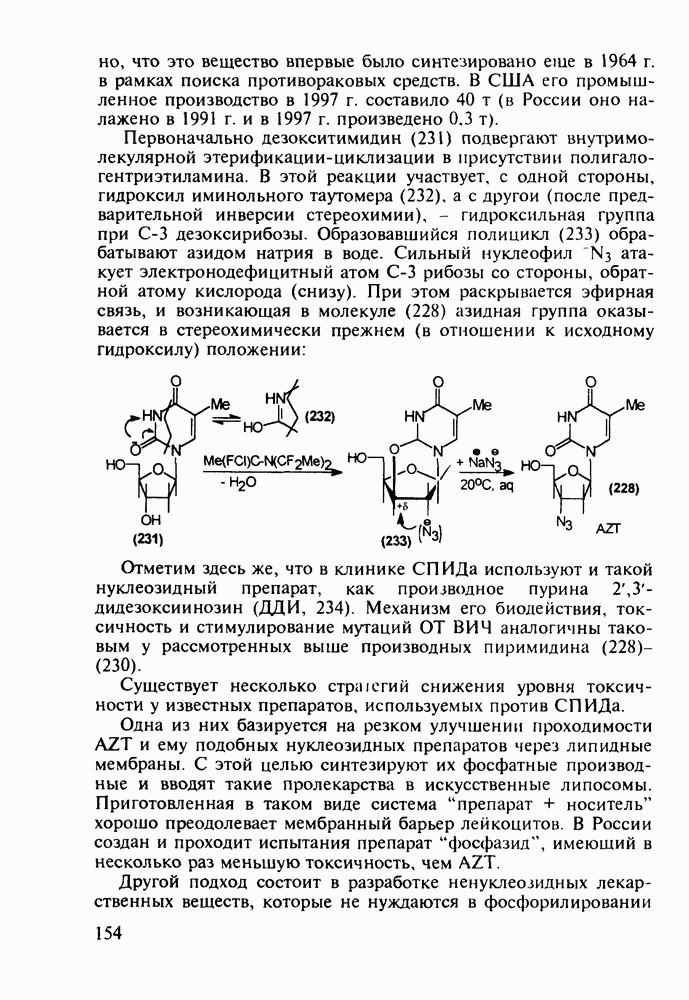
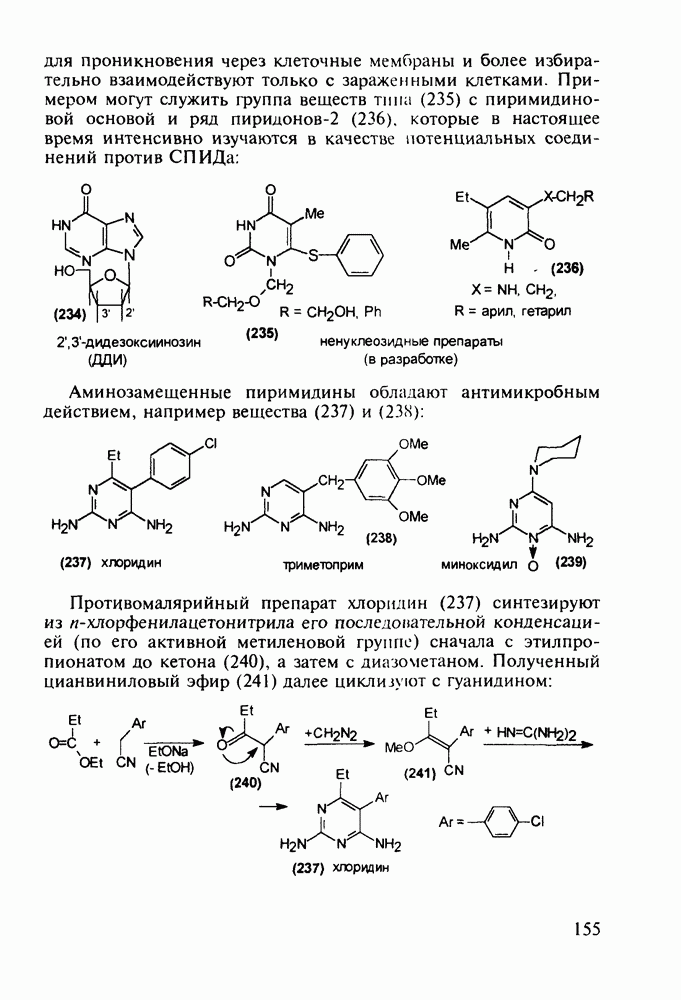
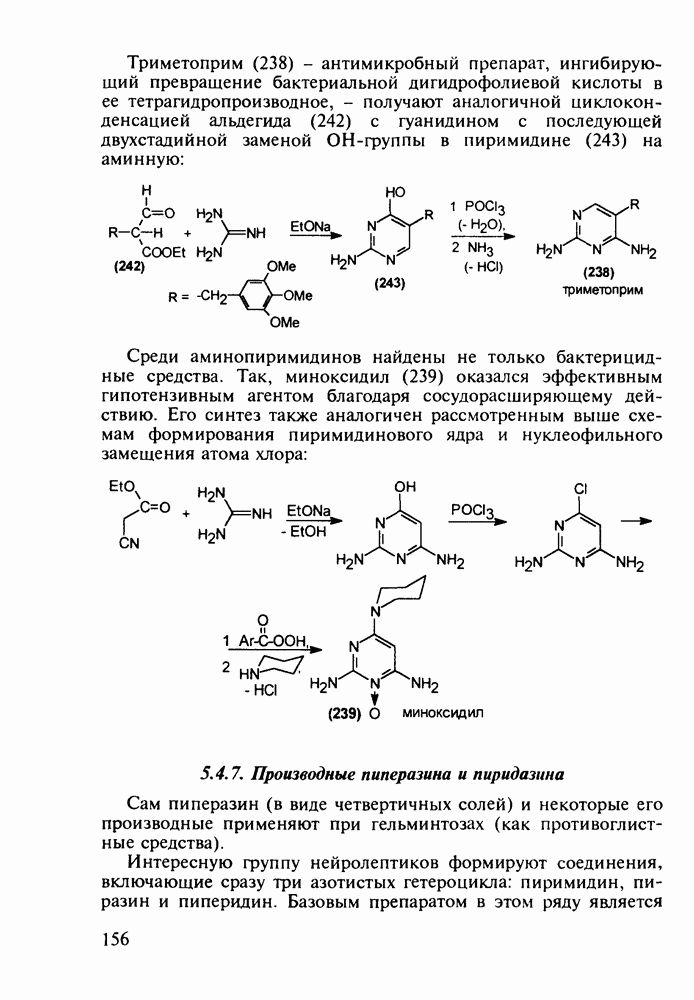
- 5.4.6. Производные пиримидинов
- 5.4.7. Производные пиперазина и пиридазина
- 5.4.8. Бензотиазины. Нейролептики фенотиазинового ряда
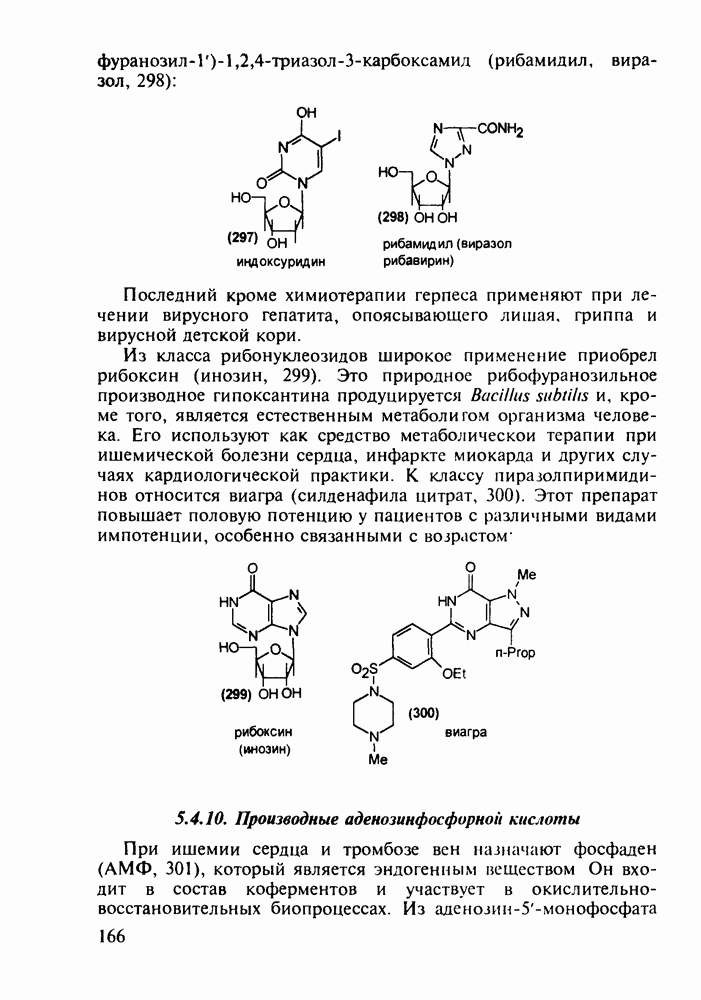
- 5.4.9. Пуриновые основания в качестве стимулирующих и антивирусных агентов
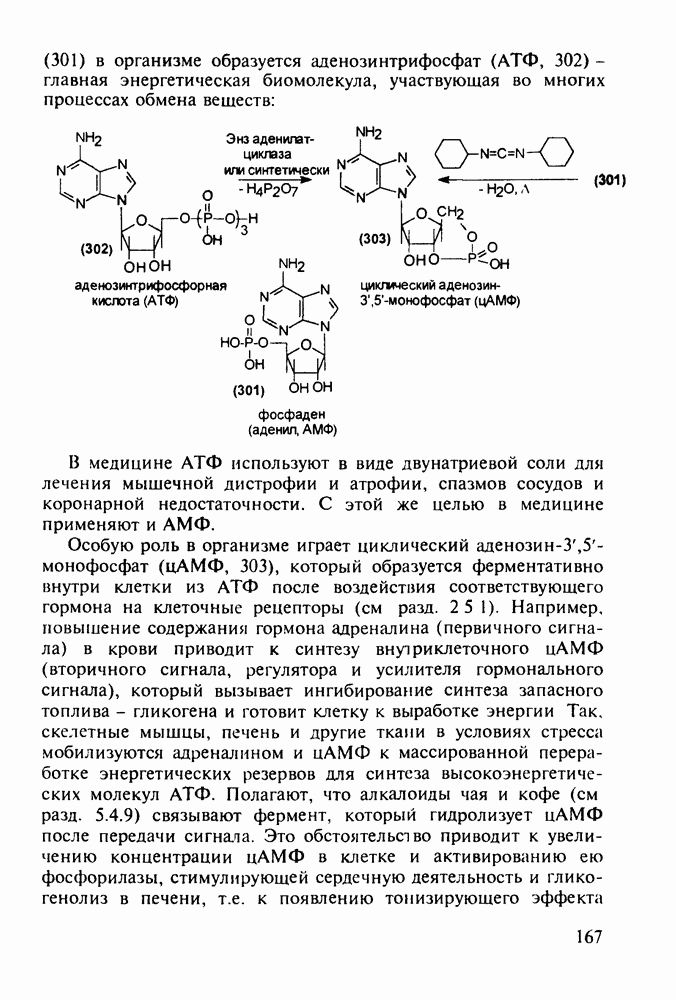
- 5.4.10. Производные аденозинфосфорной кислоты
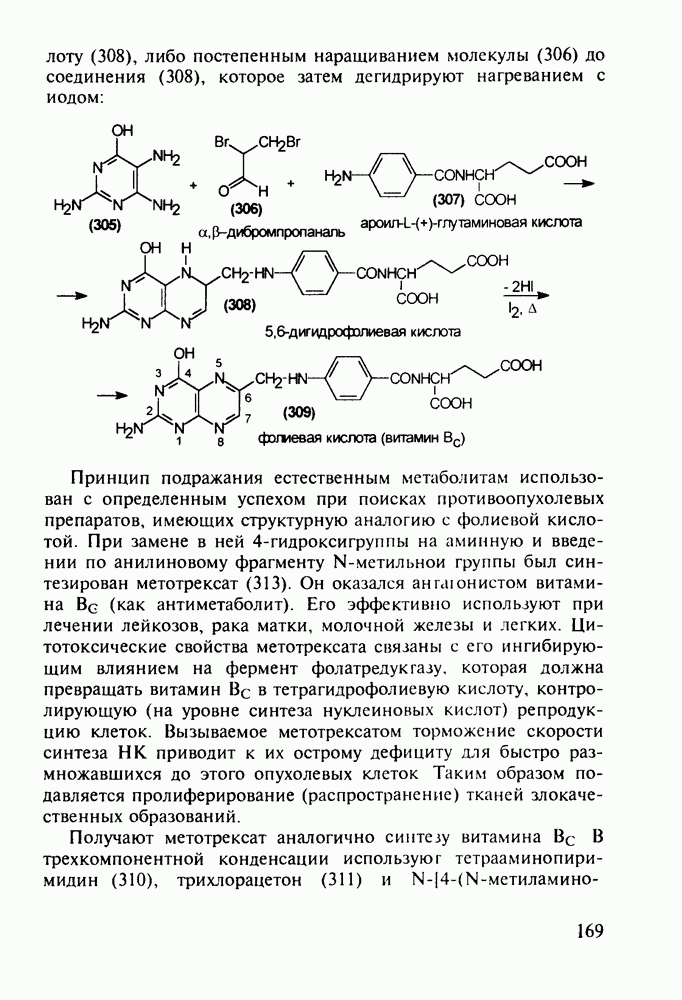
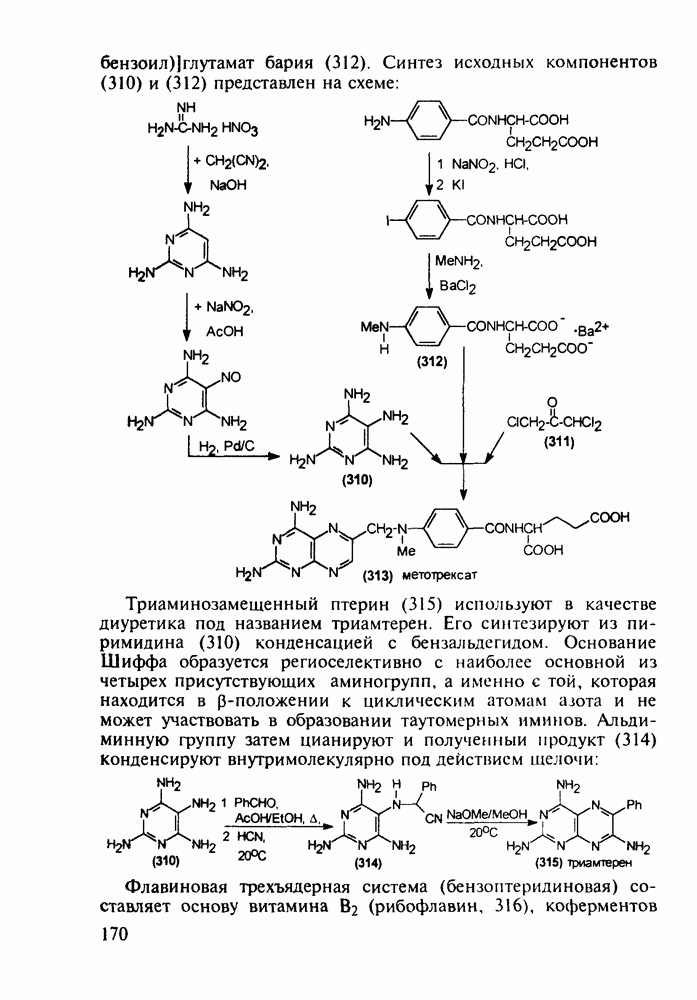
- 5.4.11. Производные птеридина с витаминной (витамины Вс и В2) и противораковой активностью
- 5.5. Лекарственные вещества, содержащие семичленный гетероцикл
- 5.5.2. Транквилизаторы группы 1,4-бензодиазепина
- 5.6. Производные азабициклооктанов в качестве спазмолитиков и анестетиков. Лекарственные препараты на основе хинуклидина
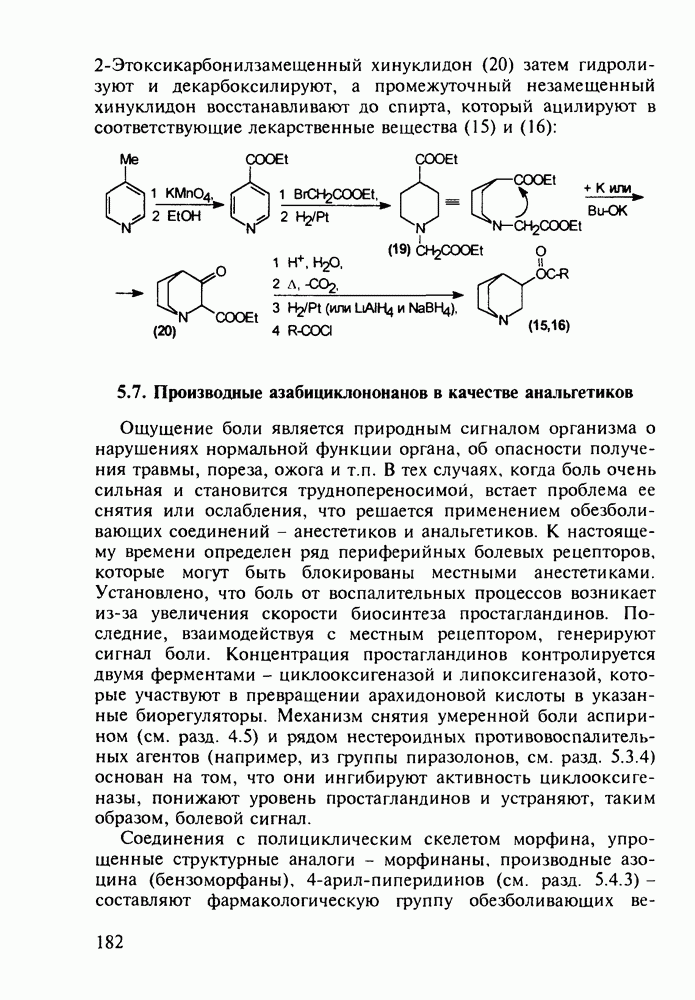
- 5.7. Производные азабициклононанов в качестве анальгетиков
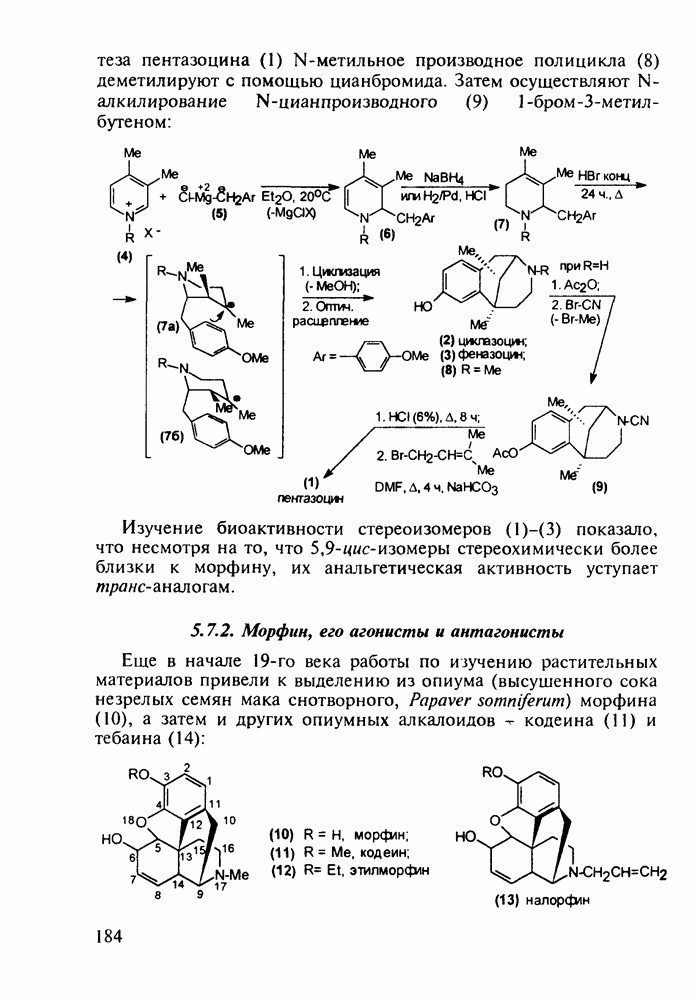
- 5.7.1. Группа пентазоцина
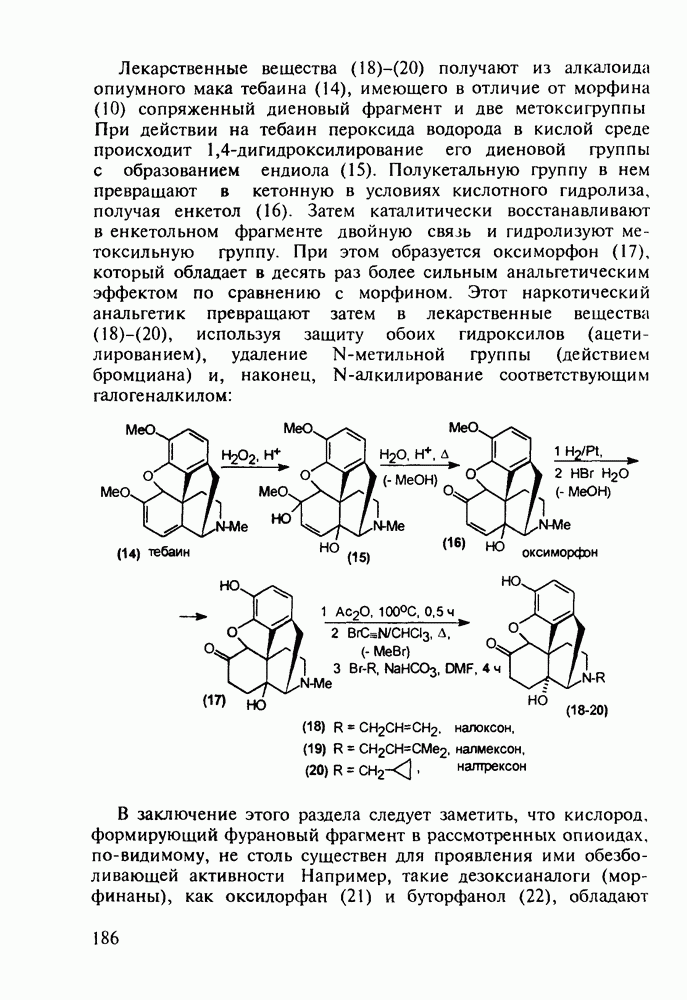
- 5.7.2. Морфин, его агонисты и антагонисты
- РЕКОМЕНДУЕМАЯ ЛИТЕРАТУРА