| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
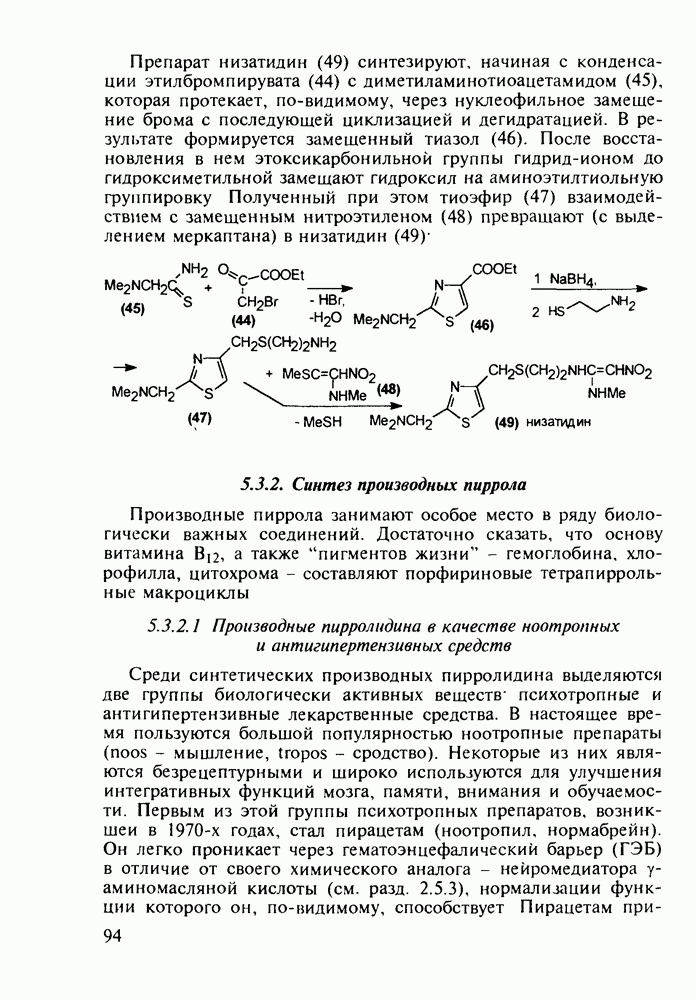
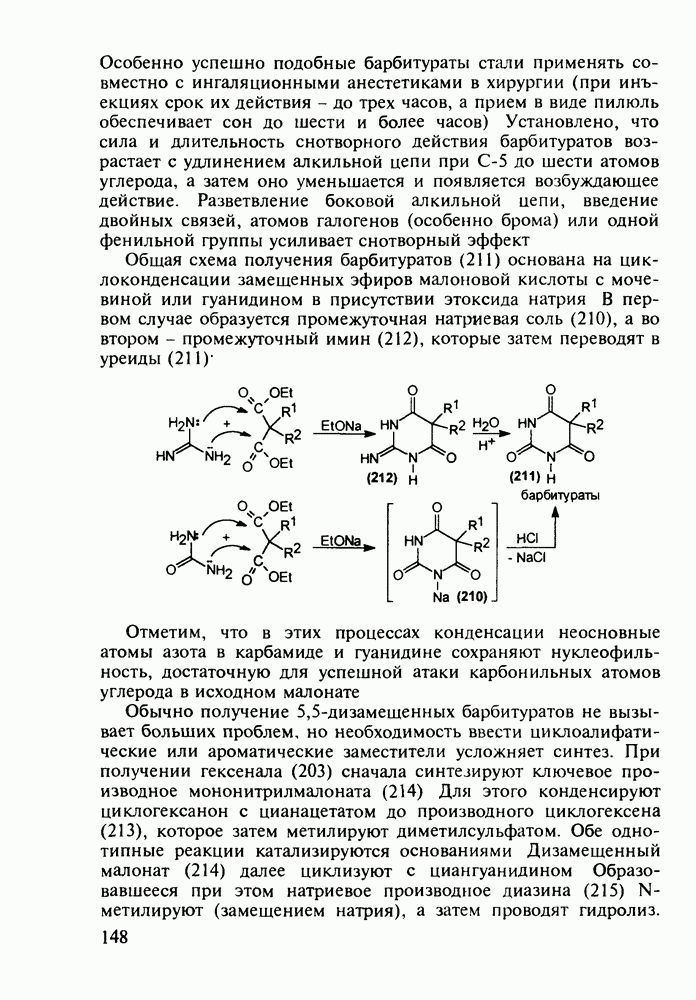
5.3.2. Синтез производных пиррола
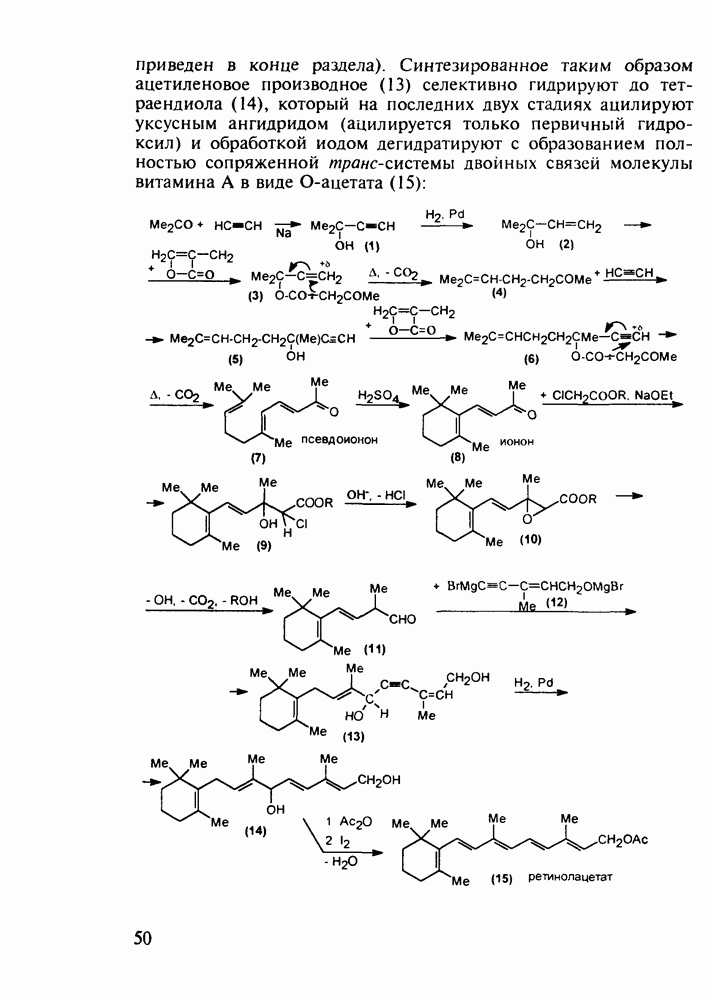
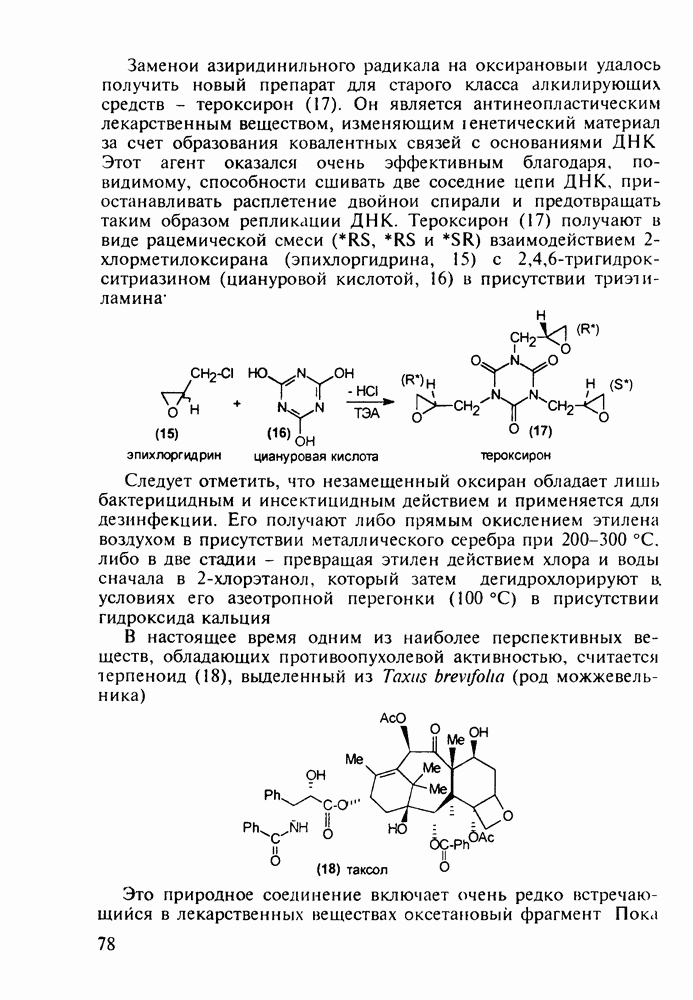
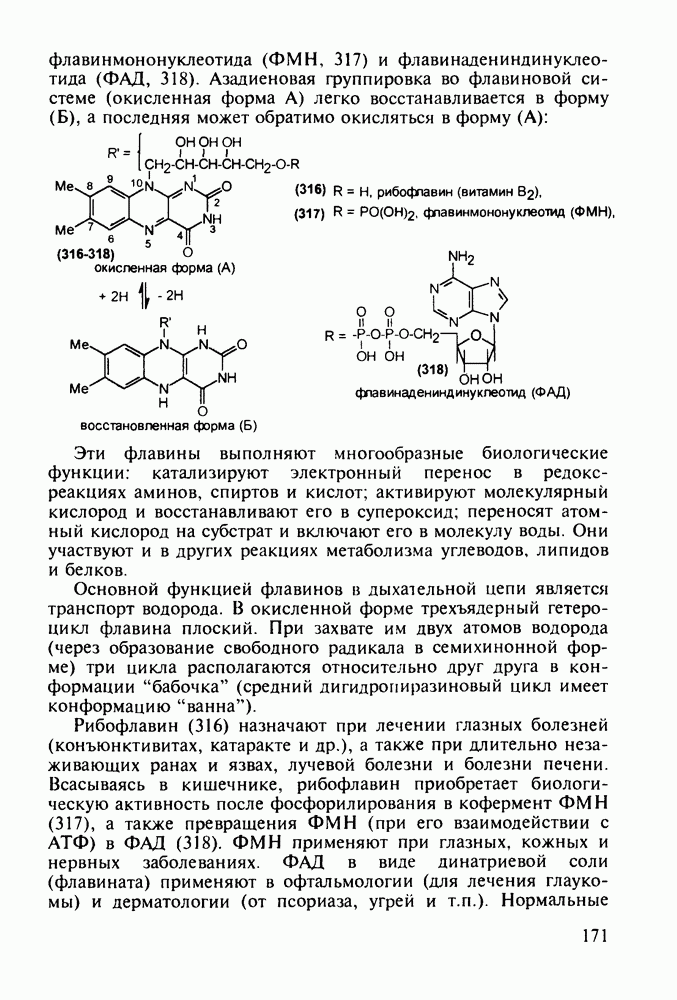
Производные пиррола занимают особое место в ряду биологически важных соединений. Достаточно сказать, что основу витамина  , а также “пигментов жизни” - гемоглобина, хлорофилла, цитохрома - составляют порфириновые тетрапиррольные макроциклы
, а также “пигментов жизни” - гемоглобина, хлорофилла, цитохрома - составляют порфириновые тетрапиррольные макроциклы
5.3.2.1 Производные пирролидина в качестве ноотропных и антигипертензивных средств
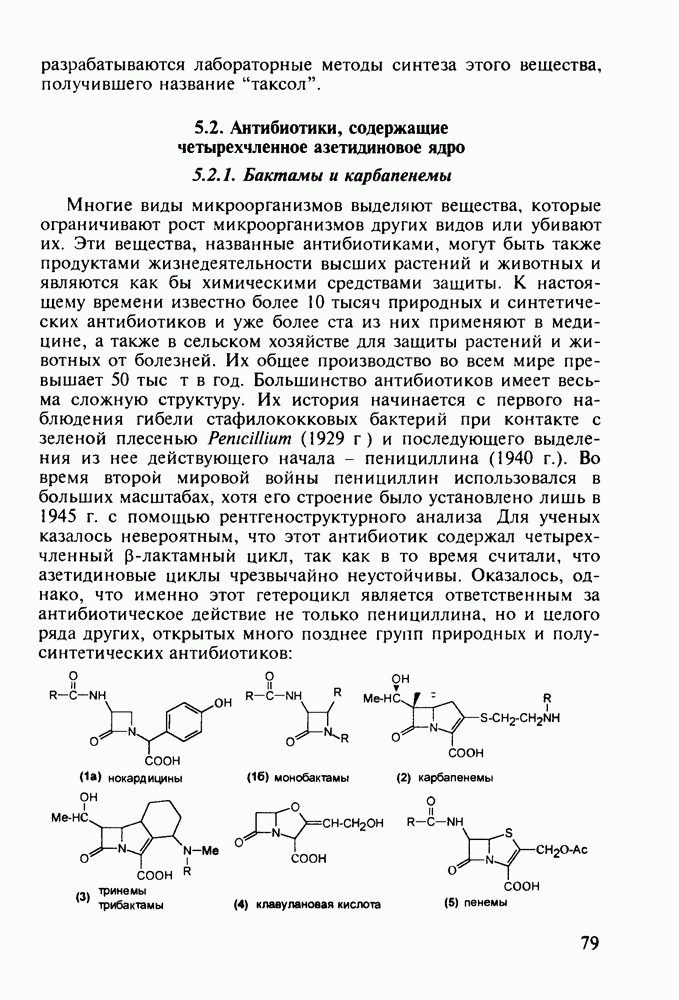
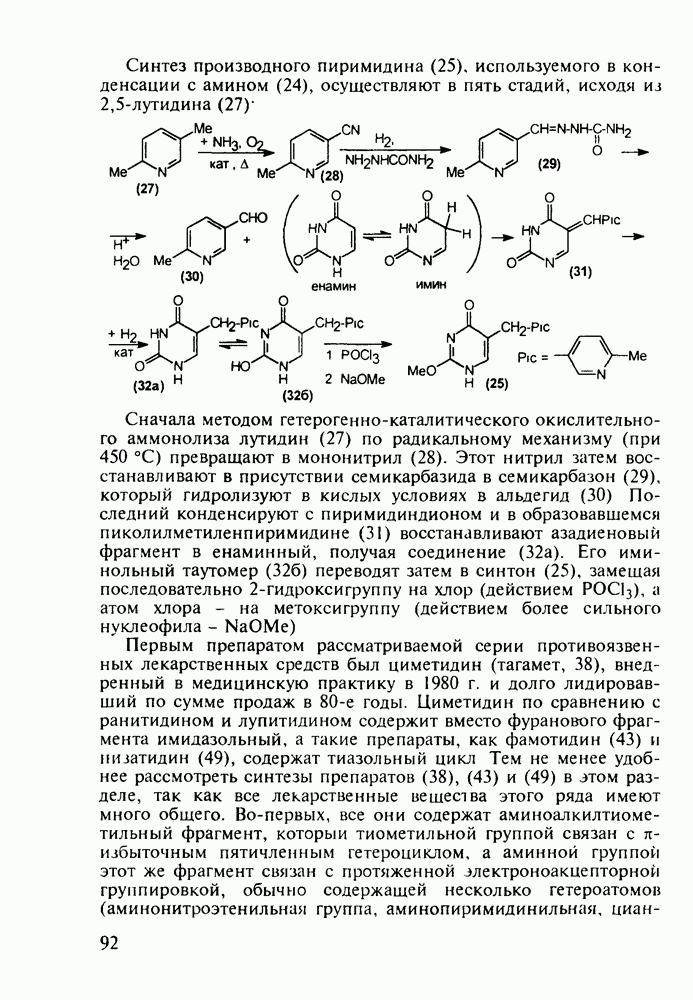
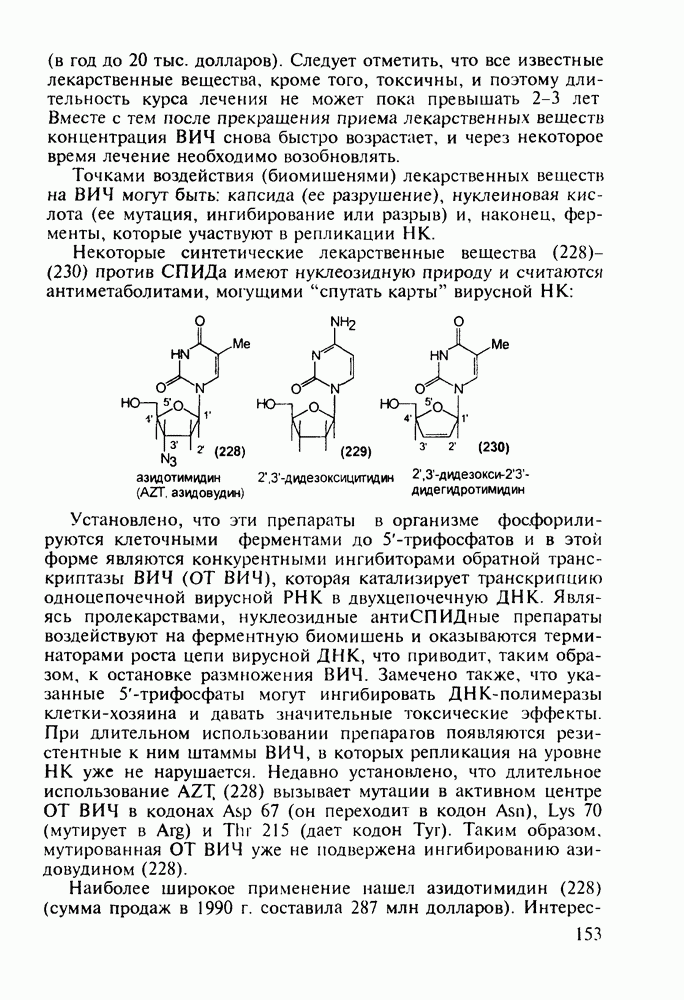
Среди синтетических производных пирролидина выделяются две группы биологически активных веществ- психотропные и антигипертензивные лекарственные средства. В настоящее время пользуются большой популярностью ноотропные препараты (noos - мышление, tropos - сродство). Некоторые из них являются безрецептурными и широко используются для улучшения интегративных функций мозга, памятй, внимания и обучаемости. Первым из этой группы психотропных препаратов, возникшей в 1970-х годах, стал пирацетам (ноотропил, нормабрейн). Он легко проникает через гематоэнцефалический барьер (ГЭБ) в отличие от своего химического аналога - нейромедиатора у-аминомасляной кислоты (см. разд. 2.5.3), нормализации функции которого он, по-видимому, способствует Пирацетам применяют
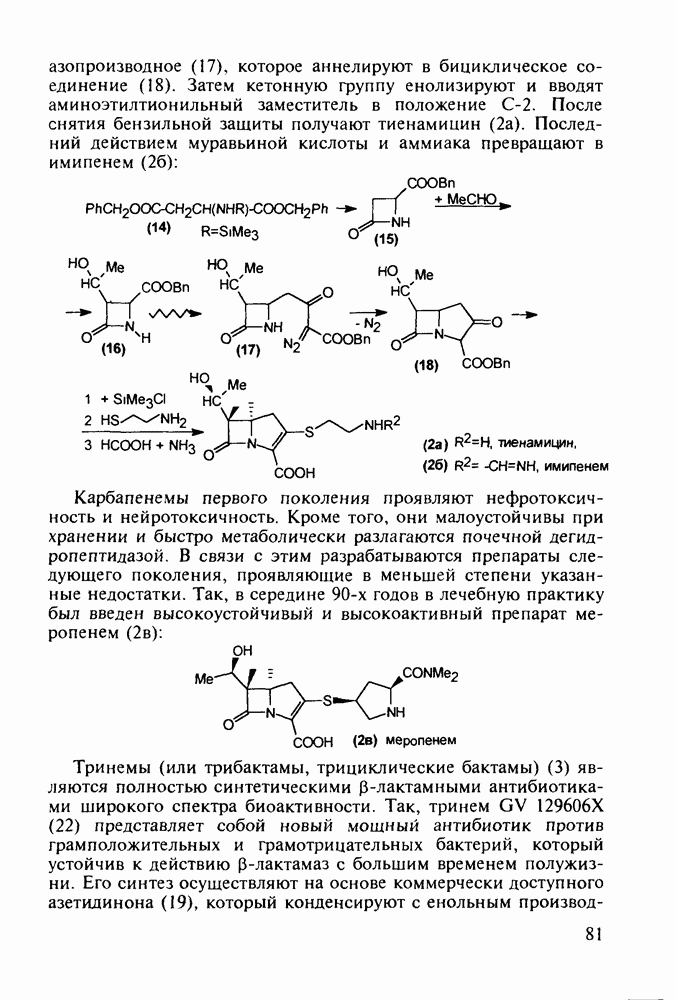
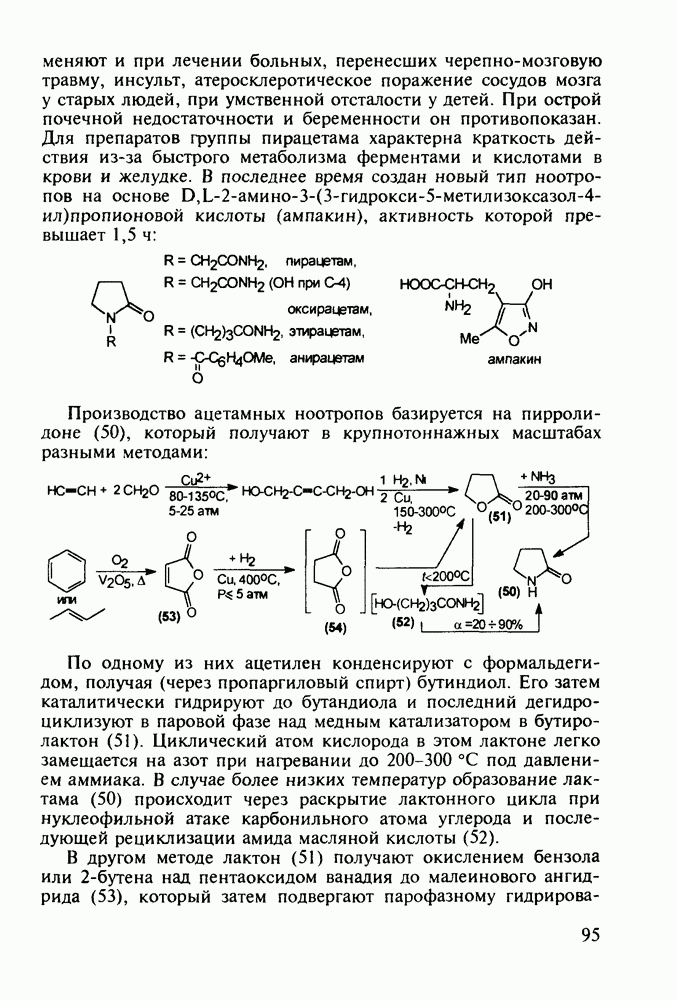
и при лечении больных, перенесших черепно-мозговую травму, инсульт, атеросклеротическое поражение сосудов мозга у старых людей, при умственной отсталости у детей. При острой почечной недостаточности и беременности он противопоказан. Для препаратов группы пирацетама характерна краткость действия из-за быстрого метаболизма ферментами и кислотами в крови и желудке. В последнее время создан новый тип ноотропов на основе  кислоты (ампакин), активность которой превышает
кислоты (ампакин), активность которой превышает 

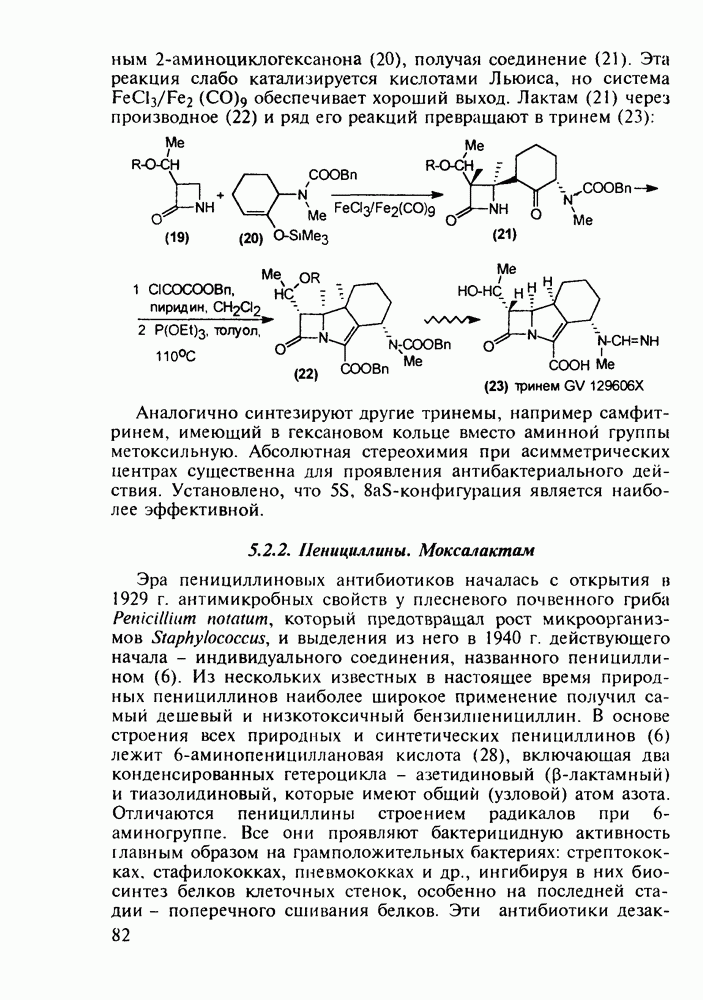
Производство ацетамных ноотропов базируется на пирролидоне (50), который получают в крупнотоннажных масштабах разными методами:

По одному из них ацетилен конденсируют с формальдегидом, получая (через пропаргиловый спирт) бутиндиол. Его затем каталитически гидрируют до бутандиола и последний дегидроциклизуют в паровой фазе над медным катализатором в бутиролактон (51). Циклический атом кислорода в этом лактоне легко замещается на азот при нагревании до 200-300 °С под давлением аммиака. В случае более низких температур образование лактама (50) происходит через раскрытие лактонного цикла при нуклеофильной атаке карбонильного атома углерода и последующей рециклизации амида масляной кислоты (52).
В другом методе лактон (51) получают окислением бензола или 2-бутена над пентаоксидом ванадия до малеинового ангидрида (53), который затем подвергают парофазному гидрированию
над медью, протекающему через янтарный ангидрид (54). Ангидрид (53) можно превратить восстановительным аминиро-ванием (в одну стадию) в пирролидон (50). Для этого нагревают смесь ангидрида с водородом и аммиаком в присутствии никеля на угле или платины на силикагеле (200-275 °С).
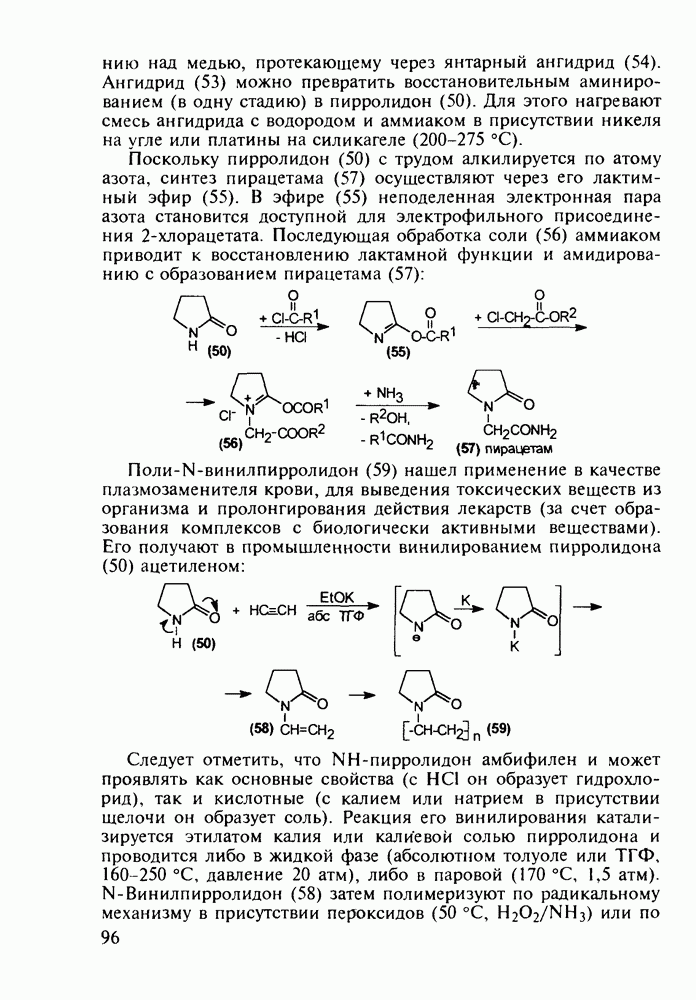
Поскольку пирролидон (50) с трудом алкилируется по атому азота, синтез пирацетама (57) осуществляют через его лактимный эфир (55). В эфире (55) неподеленная электронная пара азота становится доступной для электрофильного присоединения  -хлорацетата. Последующая обработка соли (56) аммиаком приводит к восстановлению лактамной функции и амидированию с образованием пирацетама (57):
-хлорацетата. Последующая обработка соли (56) аммиаком приводит к восстановлению лактамной функции и амидированию с образованием пирацетама (57):

Поли-N-винилпирролидон (59) нашел применение в качестве плазмозаменителя крови, для выведения токсических веществ из организма и пролонгирования действия лекарств (за счет образования комплексов с биологически активными веществами). Его получают в промышленности винилированием пирролидона (50) ацетиленом:

Следует отметить, что  -пирролидон амбифилен и может проявлять как основные свойства (с
-пирролидон амбифилен и может проявлять как основные свойства (с  он образует гидрохлорид), так и кислотные (с калием или натрием в присутствии щелочи он образует соль). Реакция его винилирования катализируется этилатом калия или калиевой солью пирролидона и проводится либо в жидкой фазе (абсолютном толуоле или ТГФ, 160-250 °С, давление 20 атм), либо в паровой (170 °С, 1,5 атм). N-Винилпирролидон (58) затем полимеризуют по радикальному механизму в присутствии пероксидов
он образует гидрохлорид), так и кислотные (с калием или натрием в присутствии щелочи он образует соль). Реакция его винилирования катализируется этилатом калия или калиевой солью пирролидона и проводится либо в жидкой фазе (абсолютном толуоле или ТГФ, 160-250 °С, давление 20 атм), либо в паровой (170 °С, 1,5 атм). N-Винилпирролидон (58) затем полимеризуют по радикальному механизму в присутствии пероксидов  или по
или по
координационно-каталитическому механизму на катализаторах Цикпера-Натта.
На основе тройного сополимера N-винилпирролидона с акриламидом и этилакрилатом (60)

созданы биорастворимые матрицы, несущие в виде комплекса или в виде раствора в полимере то или иное лекарственное вещество. Этот прием позволяет значительно пролонгировать биодействие препаратов, резко повысить эффективность лечения, а также увеличить сроки хранения лекарственных веществ и снизить их расход.
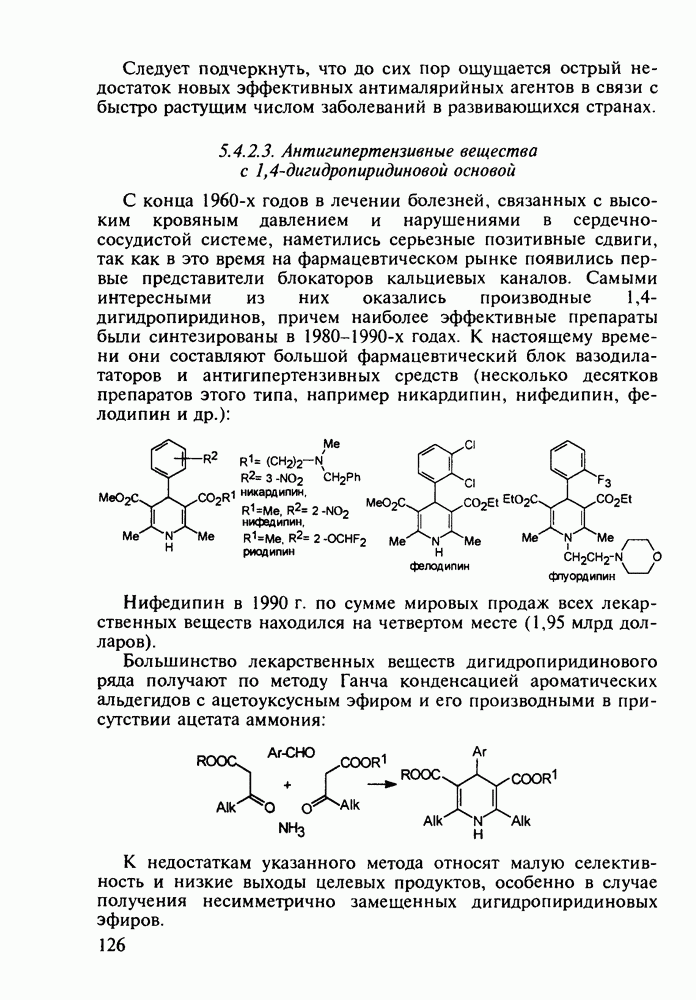
Из производных пирролидина выделяются два лекарственных вещества, вошедших в практику в качестве антигипертензивных (сердечно-сосудистых) средств в 1980-х годах, - это каптоприл (капотен, 67) и эналаприл (вазотек, 70). В 1990-м году они занимали 2-е и 3-е места соответственно по сумме мировых продаж фармацевтических препаратов (по 1,5 млрд долларов каждый). Оба препарата по механизму своего действия ингибируют ангиотензинпревращающий фермент (см. разд. 2.5 1). Полагают, что эналаприл является пролекарством, распадающимся в результате метаболизма с образованием лекарственной молекулы. В настоящее время продолжаются многочисленные синтезы родственных соединений этого класса лекарственных веществ Каптоприл представляет собой  -пролин. На начальной стадии его синтеза осуществляют присоединение тиоуксусной кислоты (62) к метакриловой (61) с последующим превращением полученного тиоэфира (63) в хлорангидрид (64). Последним затем ацилируют L-пролин (65), а образовавшееся N-ацилпроизводное (66) гидролизуют в смеси аммиака с метанолом, получая каптоприл (67):
-пролин. На начальной стадии его синтеза осуществляют присоединение тиоуксусной кислоты (62) к метакриловой (61) с последующим превращением полученного тиоэфира (63) в хлорангидрид (64). Последним затем ацилируют L-пролин (65), а образовавшееся N-ацилпроизводное (66) гидролизуют в смеси аммиака с метанолом, получая каптоприл (67):

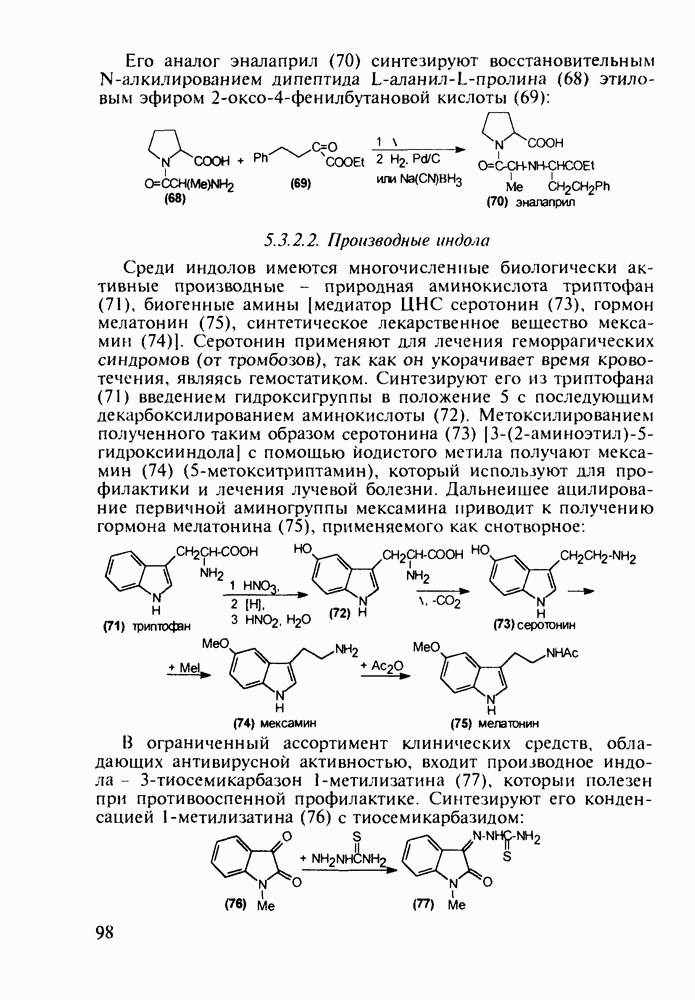
Его аналог эналаприл (70) синтезируют восстановительным N-алкилированием дипептида Ь-аланил-Ь-пролина (68) этиловым эфиром 2-оксо-4-фенилбутановой кислоты (69):

5.3.2.2. Производные индола
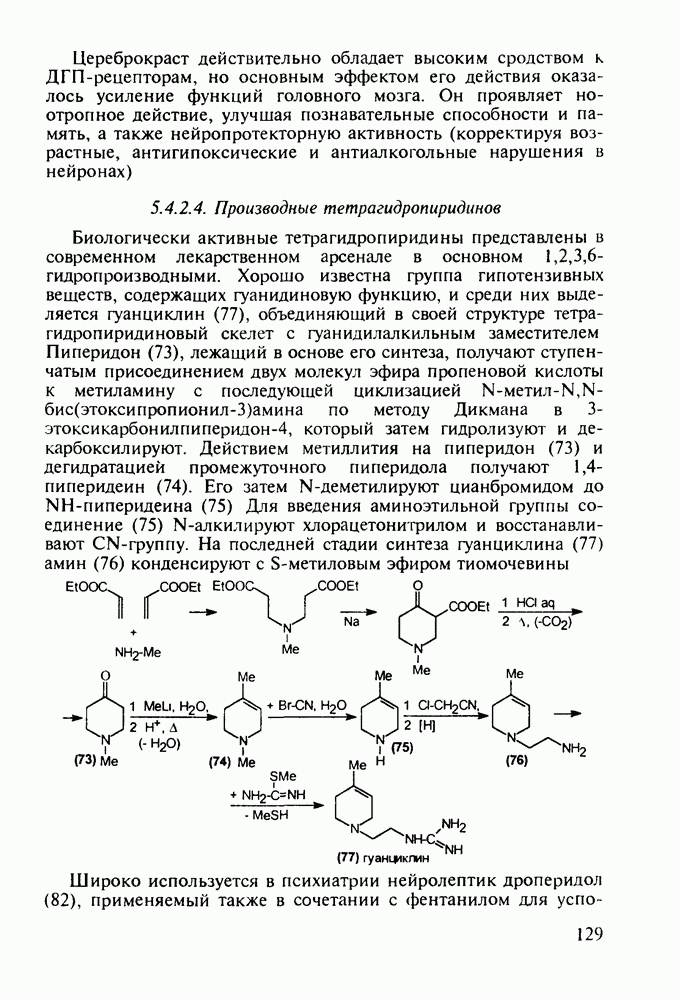
Среди индолов имеются многочисленные биологически активные производные - природная аминокислота триптофан (71), биогенные амины [медиатор ЦНС серотонин (73), гормон мелатонин (75), синтетическое лекарственное вещество мексамин (74)]. Серотонин применяют для лечения геморрагических синдромов (от тромбозов), так как он укорачивает время кровотечения, являясь гемостатиком. Синтезируют его из триптофана (71) введением гидроксигруппы в положение 5 с последующим декарбоксилированием аминокислоты (72). Метоксилированием полученного таким образом серотонина  с помощью йодистого метила получают мексамин (74) (
с помощью йодистого метила получают мексамин (74) ( -метокситриптамин), который используют для профилактики и лечения лучевой болезни. Дальнейшее ацилирование первичной аминогруппы мексамина приводит к получению гормона мелатонина (75), применяемого как снотворное:
-метокситриптамин), который используют для профилактики и лечения лучевой болезни. Дальнейшее ацилирование первичной аминогруппы мексамина приводит к получению гормона мелатонина (75), применяемого как снотворное:

В ограниченный ассортимент клинических средств, обладающих антивирусной активностью, входит производное индола - 3-тиосемикарбазон 1-метилизатина (77), который полезен при противооспенной профилактике. Синтезируют его конденсацией 1-метилизатина (76) с тиосемикарбазидом:

Производное 3-индолилуксусной кислоты (81), называемое индометацином, является активным противовоспалительным средством (применяют при ревматизме, подагрическом артрите и других воспалительных заболеваниях).
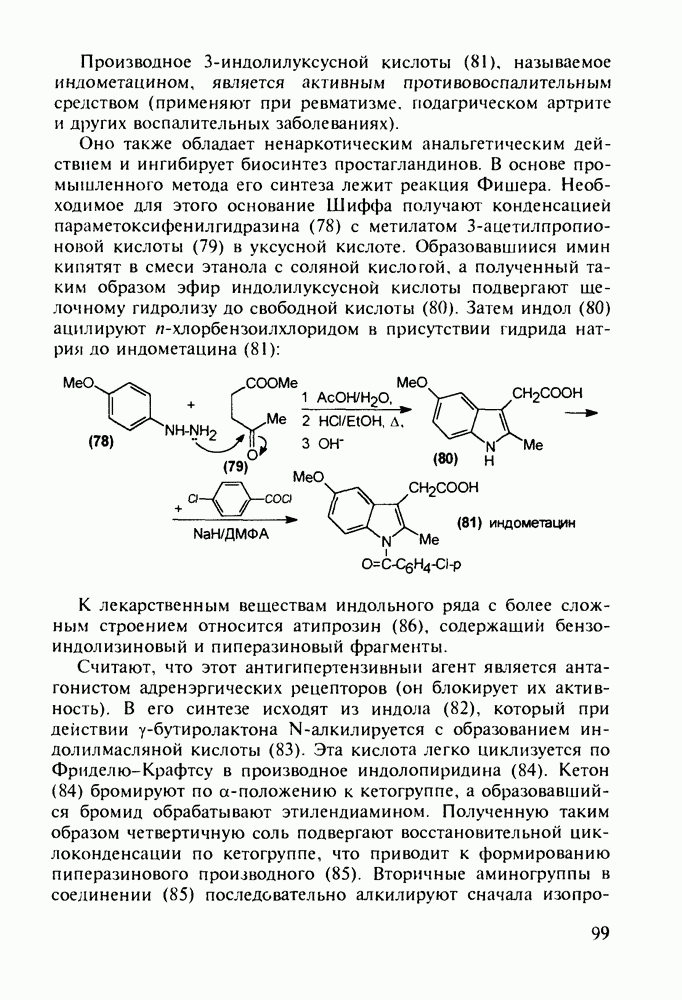
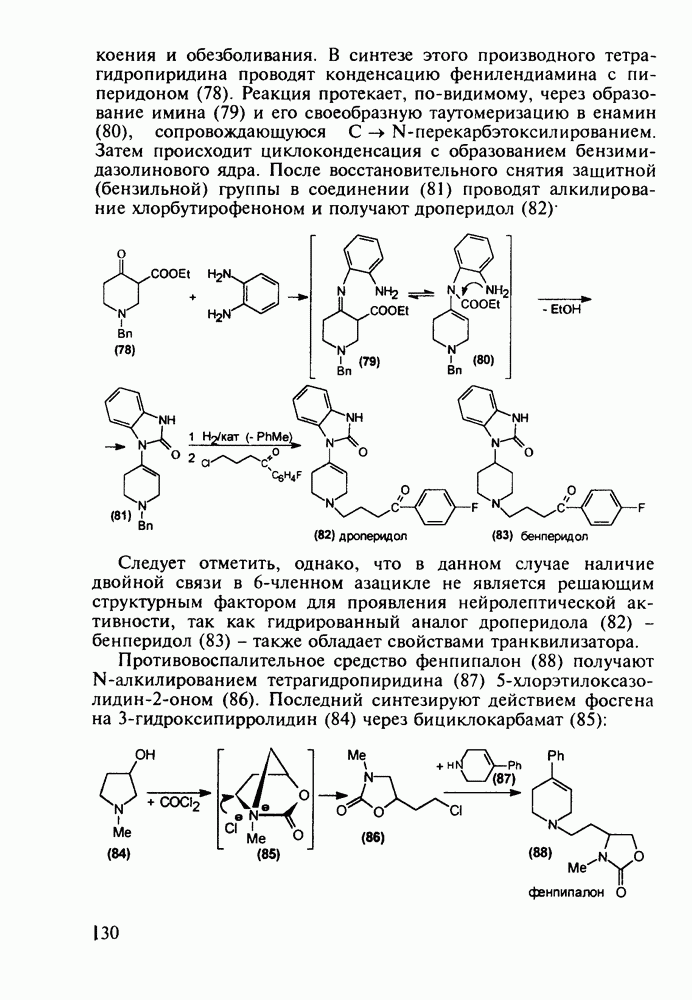
Оно также обладает ненаркотическим анальгетическим действием и ингибирует биосинтез простагландинов. В основе промышленного метода его синтеза лежит реакция Фишера. Необходимое для этого основание Шиффа получают конденсацией параметоксифенилгидразина (78) с метилатом 3-ацетилпропионовой кислоты (79) в уксусной кислоте. Образовавшийся имин кипятят в смеси этанола с соляной кислотой, а полученный таким образом эфир индолилуксусной кислоты подвергают щелочному гидролизу до свободной кислоты (80). Затем индол (80) ацилируют  -хлорбензоилхлоридом в присутствии гидрида натрия до индометацина (81):
-хлорбензоилхлоридом в присутствии гидрида натрия до индометацина (81):

К лекарственным веществам индольного ряда с более сложным строением относится атипрозин (86), содержащий бензо-индолизиновый и пиперазиновый фрагменты.
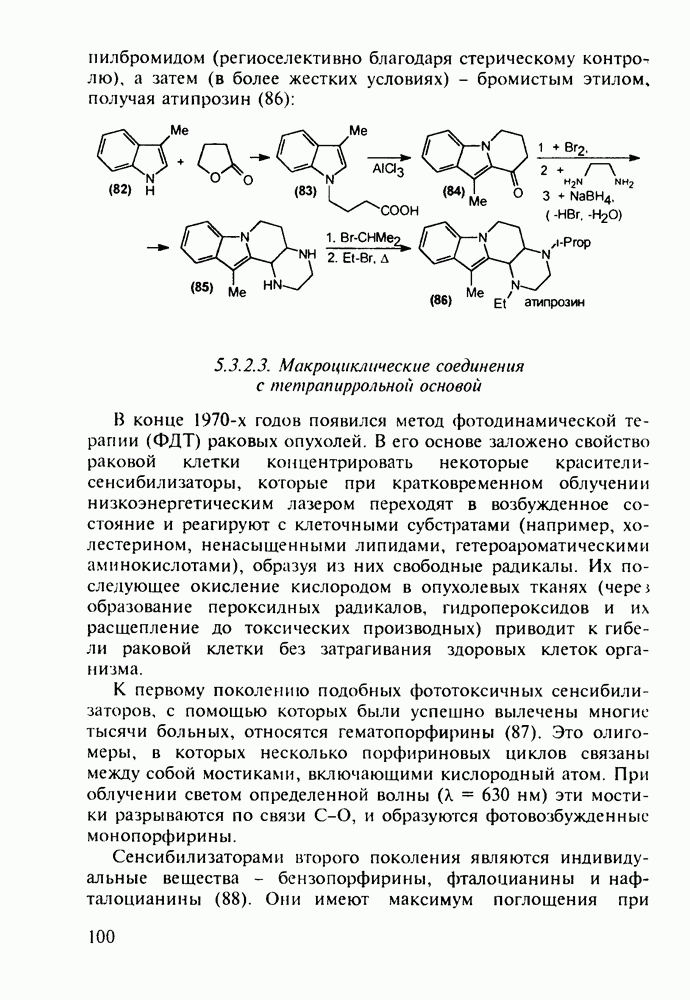
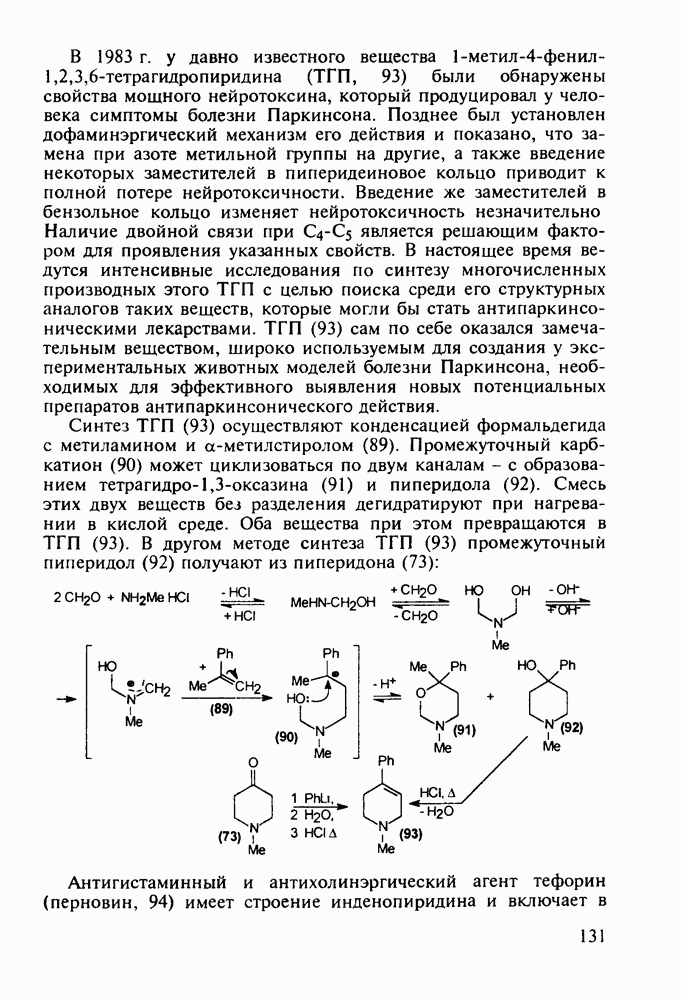
Считают, что этот антигипертензивныи агент является антагонистом адренэргических рецепторов (он блокирует их активность). В его синтезе исходят из индола (82), который при действии у-бутиролактона N-алкилируется с образованием индолилмасляной кислоты (83). Эта кислота легко циклизуется по Фриделю-Крафтсу в производное индолопиридина (84). Кетон (84) бромируют по  -положению к кетогруппе, а образовавшийся бромид обрабатывают этилендиамином. Полученную таким образом четвертичную соль подвергают восстановительной циклоконденсации по кетогруппе, что приводит к формированию пиперазинового производного (85). Вторичные аминогруппы в соединении (85) последовательно алкилируют сначала изопропилбромидом
-положению к кетогруппе, а образовавшийся бромид обрабатывают этилендиамином. Полученную таким образом четвертичную соль подвергают восстановительной циклоконденсации по кетогруппе, что приводит к формированию пиперазинового производного (85). Вторичные аминогруппы в соединении (85) последовательно алкилируют сначала изопропилбромидом
пилбромидом (региоселективно благодаря стерическому контролю), а затем (в более жестких условиях) - бромистым этилом, получая атипрозин (86):

5.3.2.3. Макроциклические соединения с тетрапиррольной основой
В конце 1970-х годов появился метод фотодинамической терапии (ФДТ) раковых опухолей. В его основе заложено свойство раковой клетки концентрировать некоторые красители-сенсибилизаторы, которые при кратковременном облучении низкоэнергетическим лазером переходят в возбужденное состояние и реагируют с клеточными субстратами (например, холестерином, ненасыщенными липидами, гетероароматическими аминокислотами), образуя из них свободные радикалы. Их последующее окисление кислородом в опухолевых тканях (через образование пероксидных радикалов, гидропероксидов и их расщепление до токсических производных) приводит к гибели раковой клетки без затрагивания здоровых клеток организма.
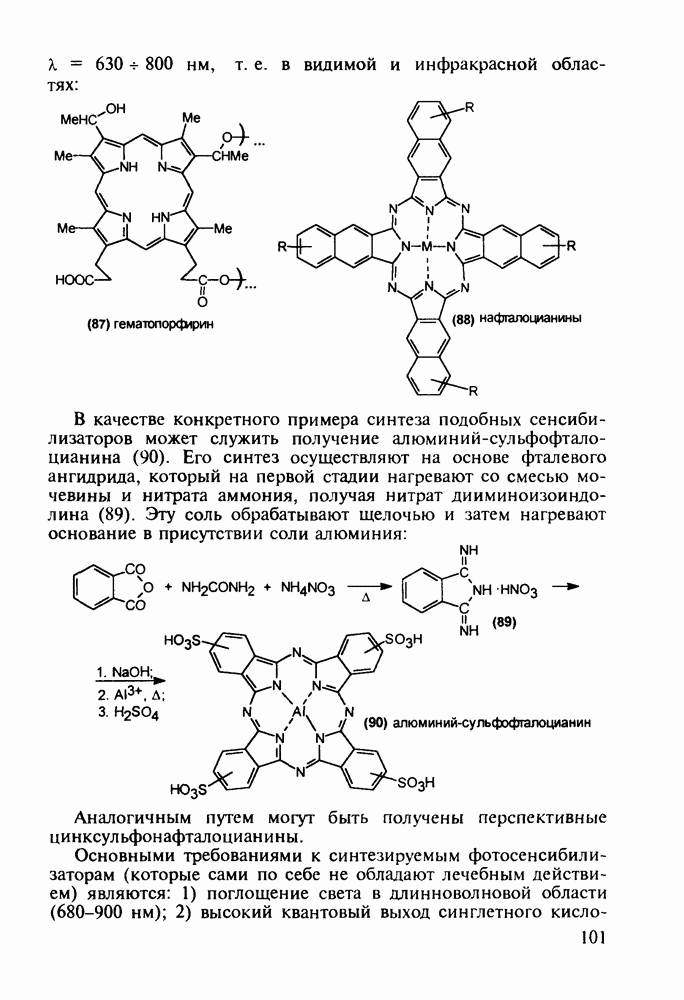
К первому поколению подобных фототоксичных сенсибилизаторов, с помощью которых были успешно вылечены многие тысячи больных, относятся гематопорфирины (87). Это олигомеры, в которых несколько порфириновых циклов связаны между собой мостиками, включающими кислородный атом. При облучении светом определенной волны  эти мостики разрываются по связи
эти мостики разрываются по связи  и образуются фотовозбужденные монопорфирины.
и образуются фотовозбужденные монопорфирины.
Сенсибилизаторами второго поколения являются индивидуальные вещества - бензопорфирины, фталоцианины и нафталоцианины (88). Они имеют максимум поглощения при
 нм, т. е. в видимой и инфракрасной областях:
нм, т. е. в видимой и инфракрасной областях:

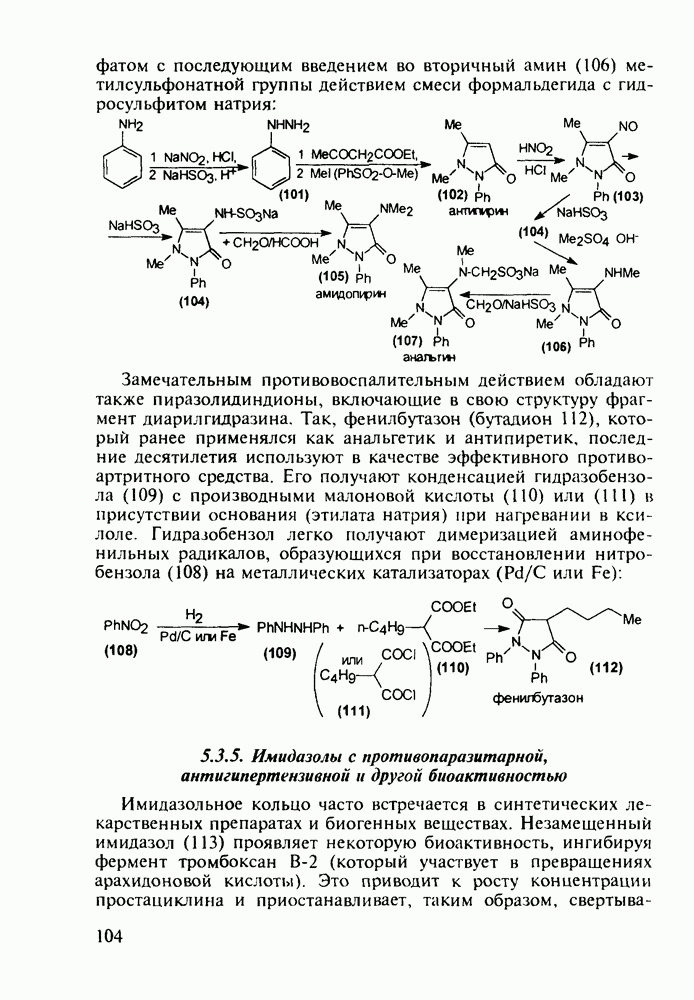
В качестве конкретного примера синтеза подобных сенсибилизаторов может служить получение алюминий-сульфофталоцианина (90). Его синтез осуществляют на основе фталевого ангидрида, который на первой стадии нагревают со смесью мочевины и нитрата аммония, получая нитрат дииминоизоиндолина (89). Эту соль обрабатывают щелочью и затем нагревают основание в присутствии соли алюминия:

Аналогичным путем могут быть получены перспективные цинксульфонафталоцианины.
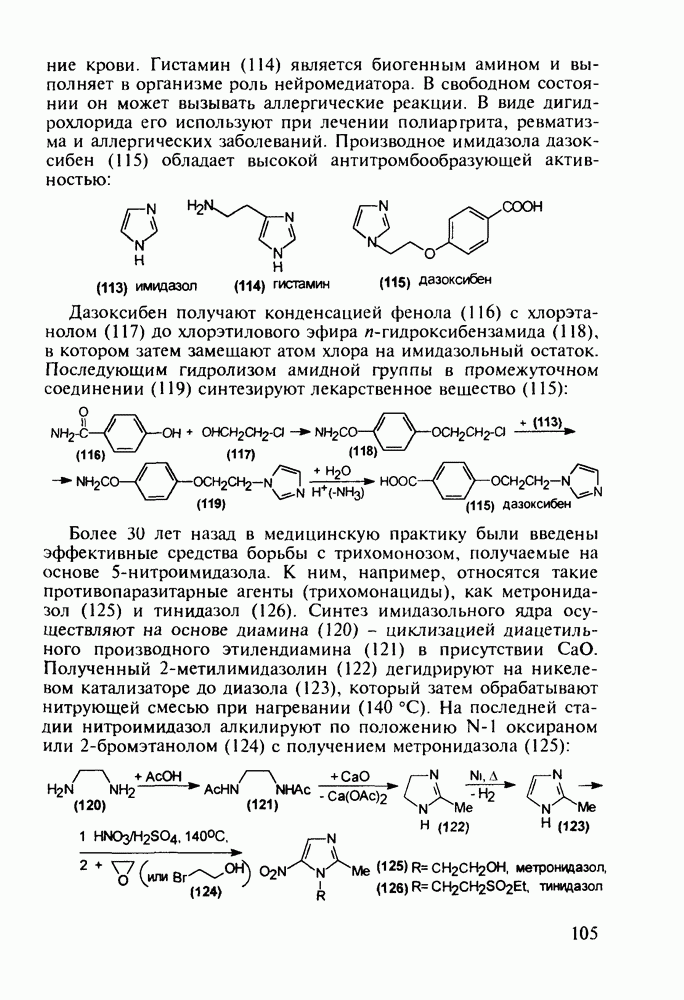
Основными требованиями к синтезируемым фотосенсибилизаторам (которые сами по себе не обладают лечебным действием) являются: 1) поглощение света в длинноволновой области (680-900 нм); 2) высокий квантовый выход синглетного кислорода;
3) низкая фотоокислительная стабильность; 4) селективность транспортировки к опухолям. Эти свойства обеспечивают сдерживание многих раковых заболеваний путем деструкции опухолей (некроза раковой клетки) на ранней и средней стадиях болезни. Фотосенсибилизаторы почти не подвержены метаболизму и выделяются из организма неизмененными.
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие
- 1. ВВЕДЕНИЕ
- 1.1. Эволюция органической химии лекарственных веществ
- 1.2. Современные требования к лекарственным веществам
- 1.3. Стадии биологического изучения лекарственного вещества
- 1.4. Основы стратегии создания новых синтетических лекарственных веществ
- 1.5. Связь структура-биологическая активность
- 1.6. Принципиальная схема разработки нового лекарственного вещества
- 1.7. Классификация лекарственных веществ
- 1.8. Основные болезни человека и ведущие группы лекарственных веществ на современном фармацевтическом рынке
- 2. СИНТЕЗ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ АЛИФАТИЧЕСКОГО РЯДА
- 2.2. Группа противораковых веществ с дихлордиэтиламинным фармакофором
- 2.3. Алканолы, аминоалканолы и их эфиры. Нейромедиатор ацетилхолин и холиномиметики
- 2.4. Альдегиды и кислоты. Витамины F и B15
- 2.5. Аминокислоты
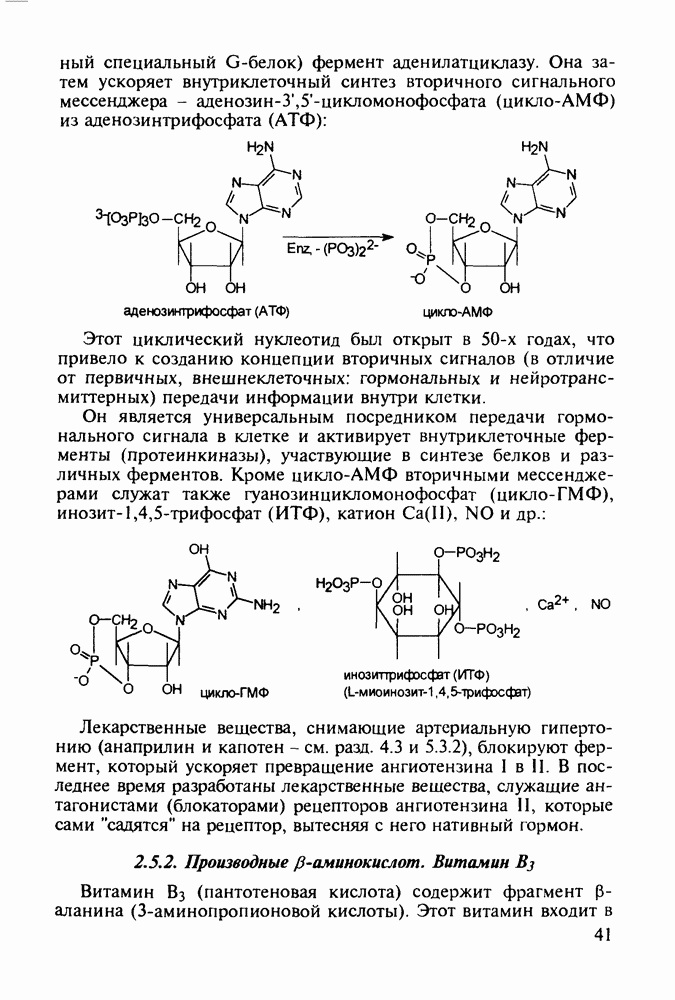
- 2.5.2. Производные b-аминокислот. Витамин B3
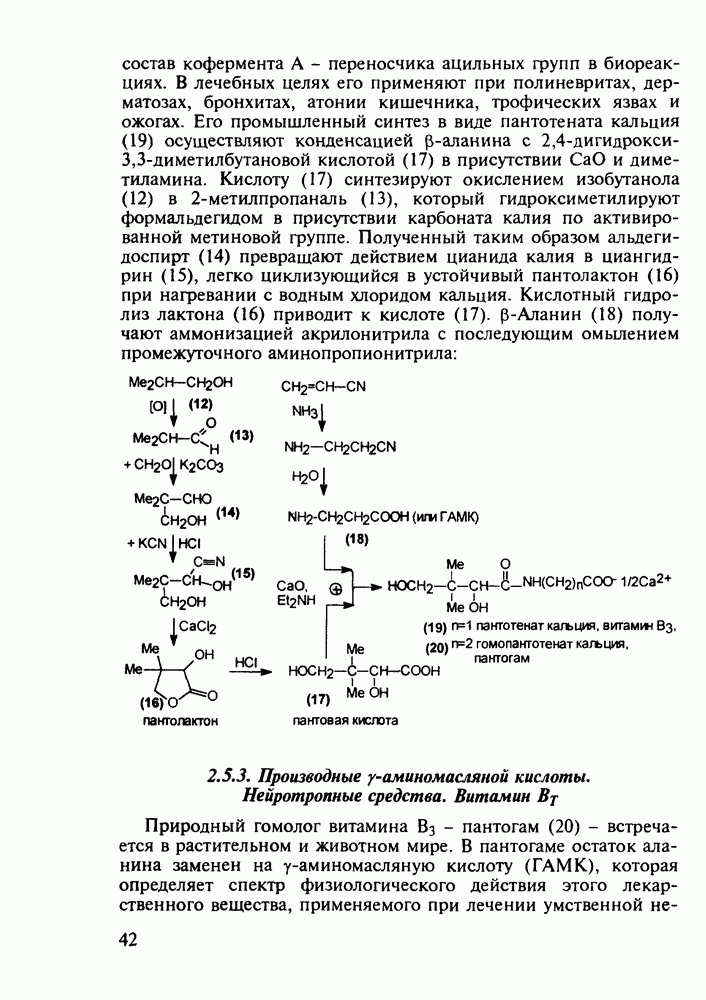
- 2.5.3. Производные у-аминомасляной кислоты. Нейротропные средства. Витамин BT
- 2.5.4. Другие аминокислоты
- 3. ЛЕКАРСТВЕННЫЕ ВЕЩЕСТВА АЛИЦИКЛИЧЕСКОГО РЯДА
- 3.2. Противозачаточные и противовоспалительные вещества на основе циклопентафенантрена. Синтез витамина D
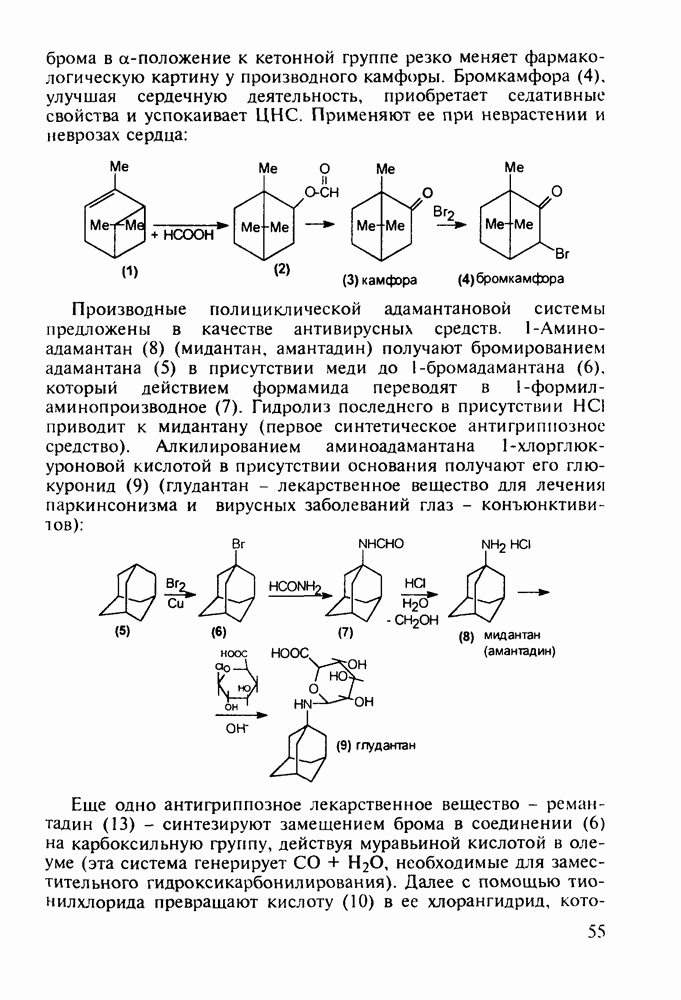
- 3.3. Камфора. Производные адамантана в качестве антивирусных средств
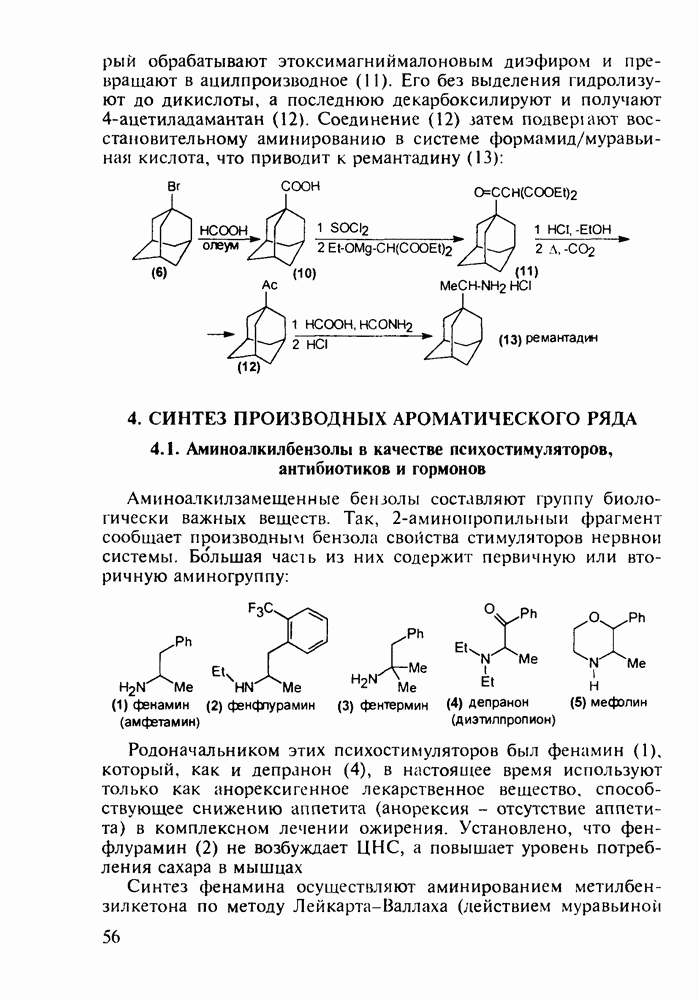
- 4. СИНТЕЗ ПРОИЗВОДНЫХ АРОМАТИЧЕСКОГО РЯДА
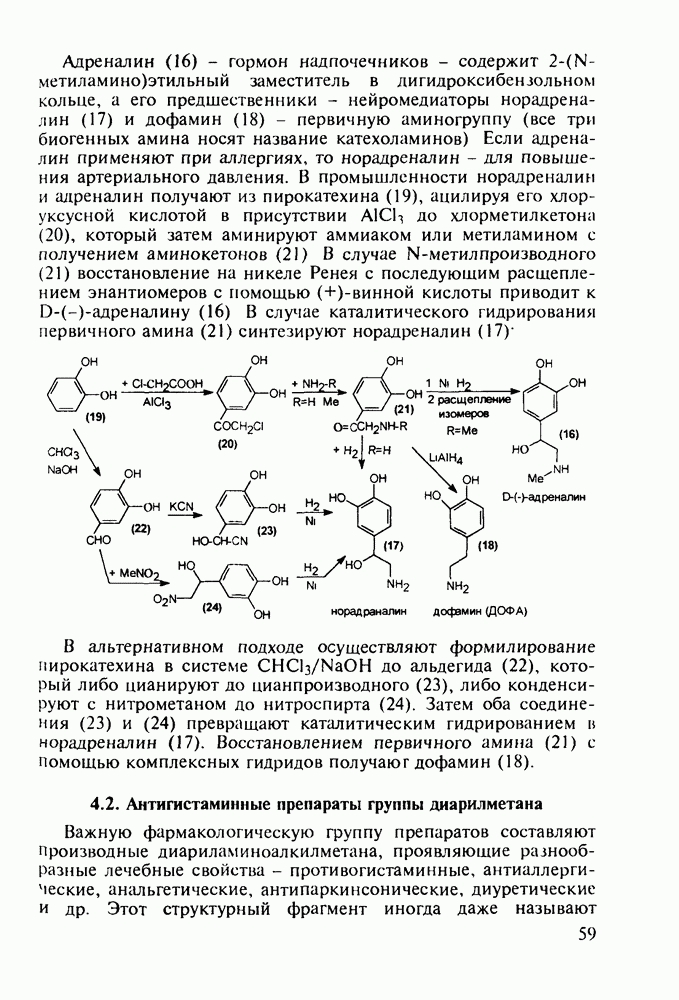
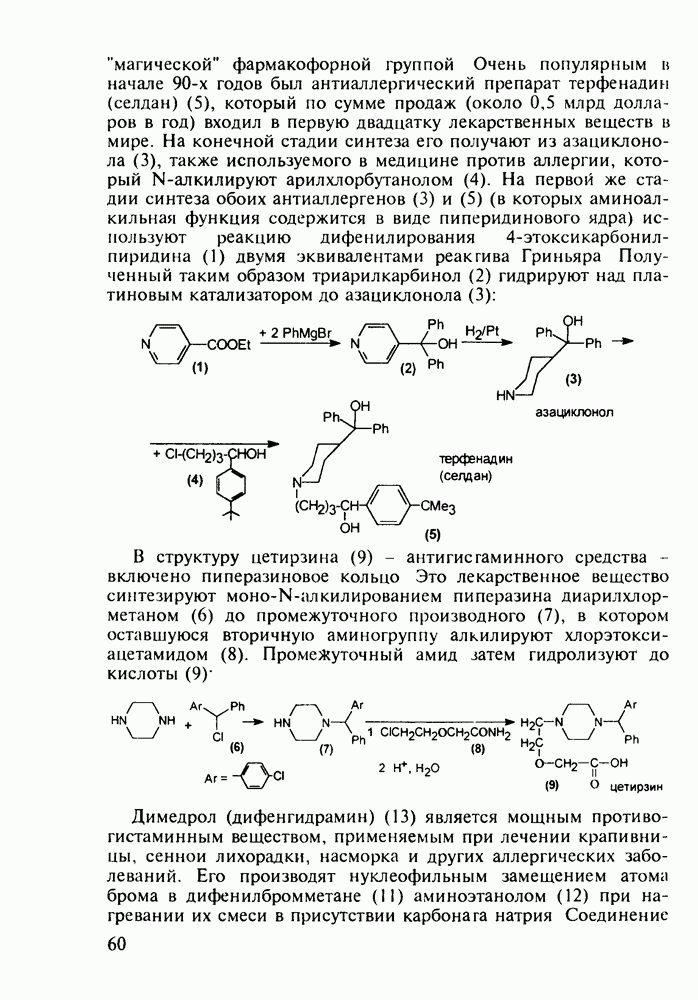
- 4.2. Антигистаминные препараты группы диарилметана
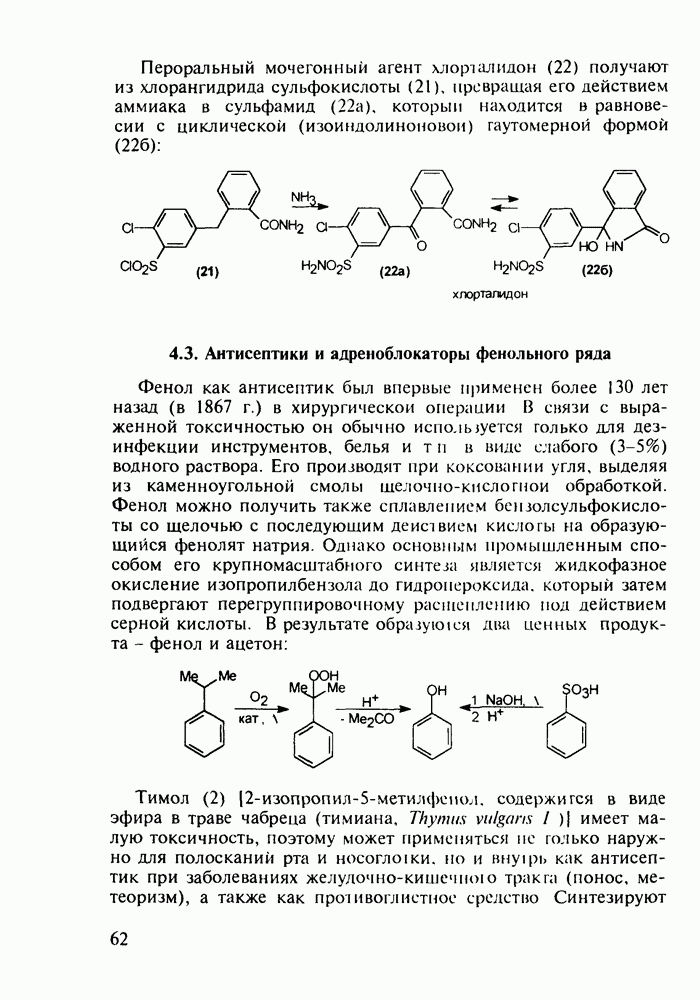
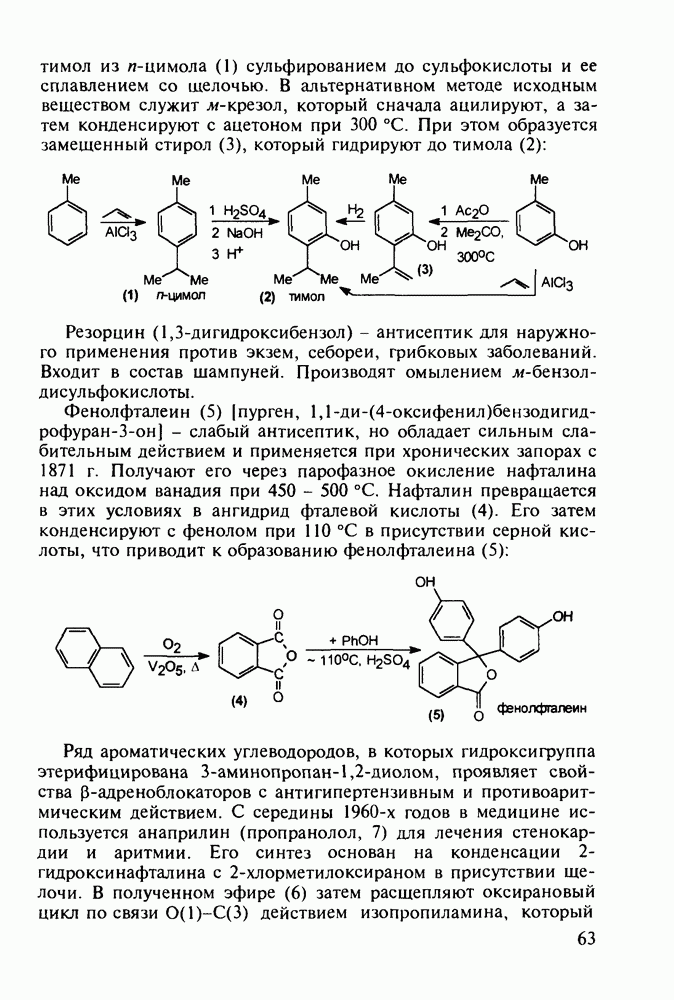
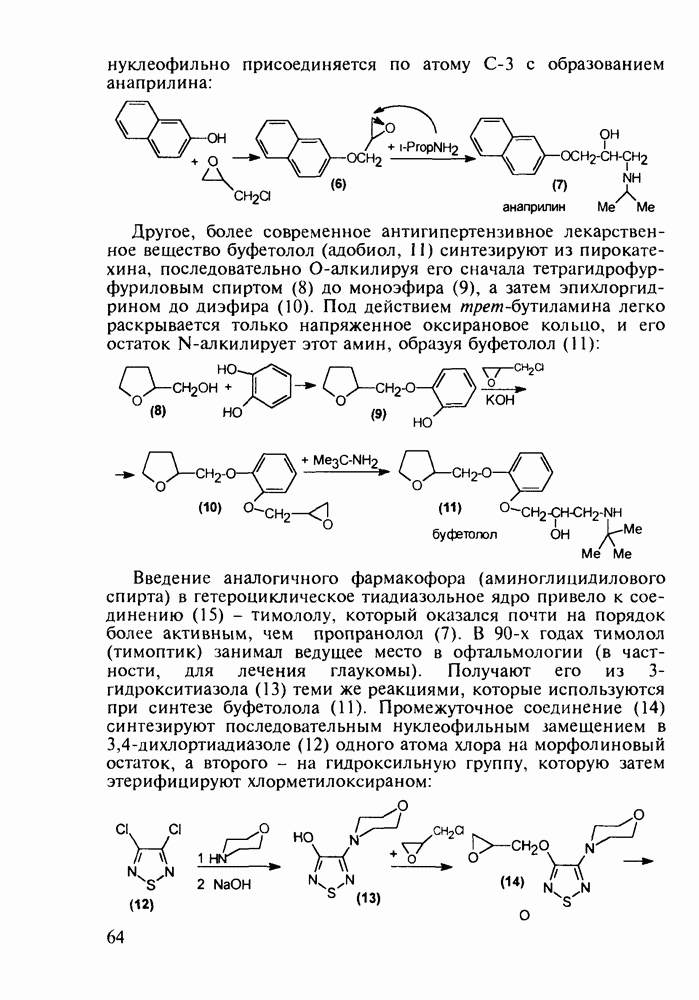
- 4.3. Антисептики и адреноблокаторы фенольного ряда
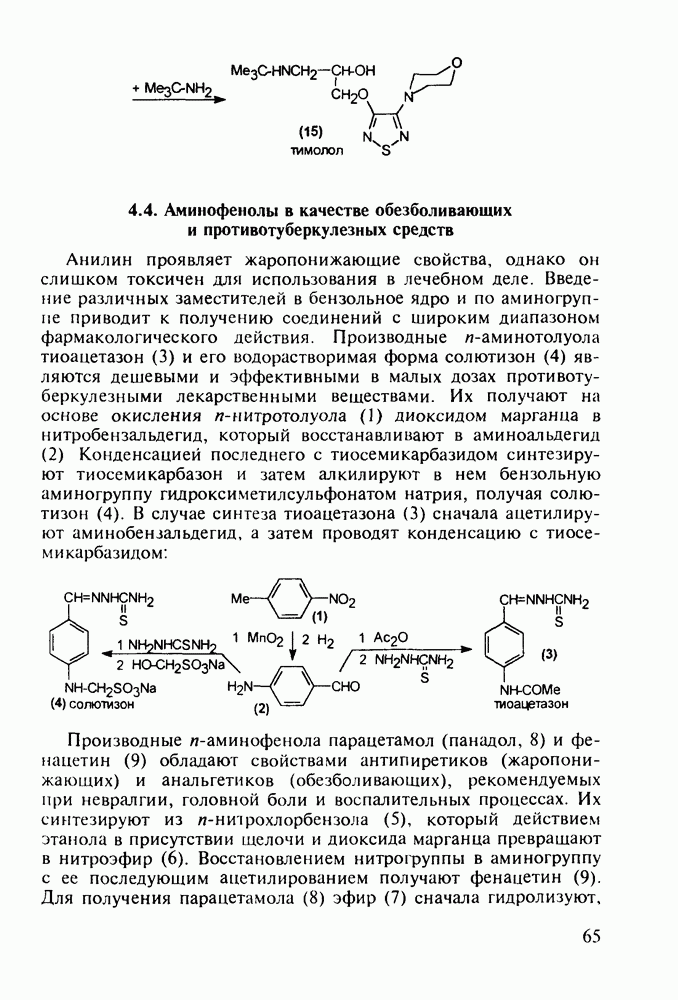
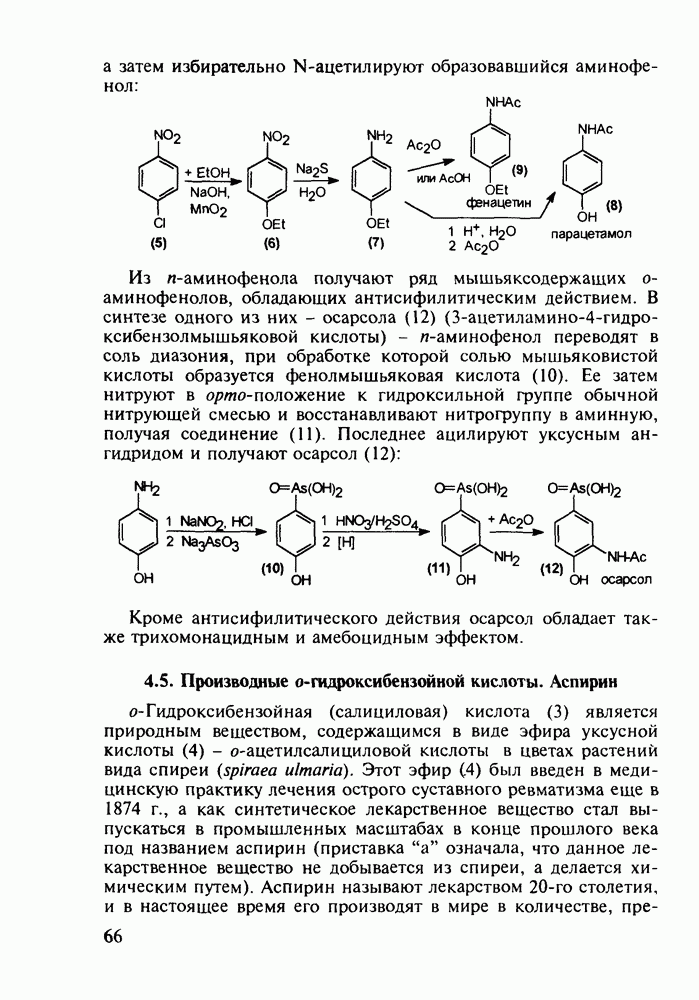
- 4.4. Аминофенолы в качестве обезболивающих и противотуберкулезных средств
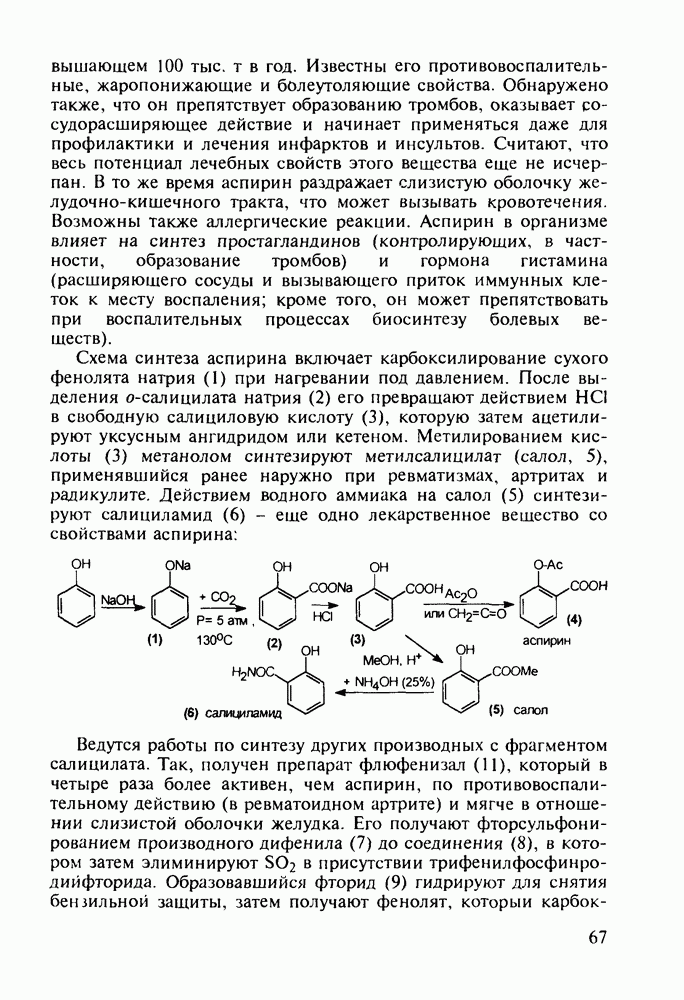
- 4.5. Производные о-гидроксибензойной кислоты. Аспирин
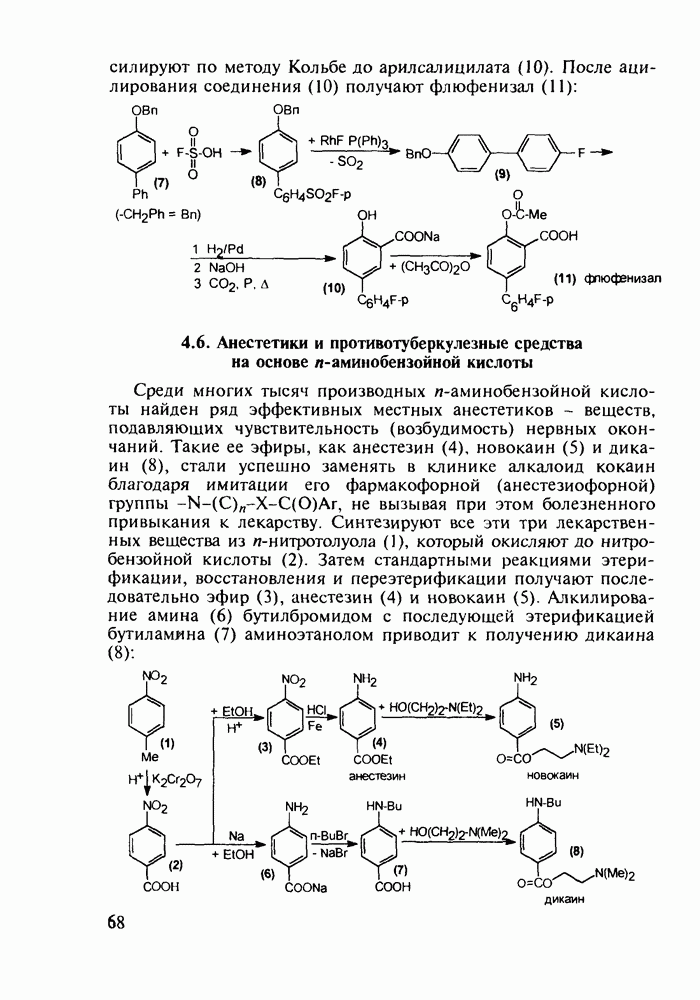
- 4.6. Анестетики и противотуберкулезные средства на основе n-аминобензойной кислоты
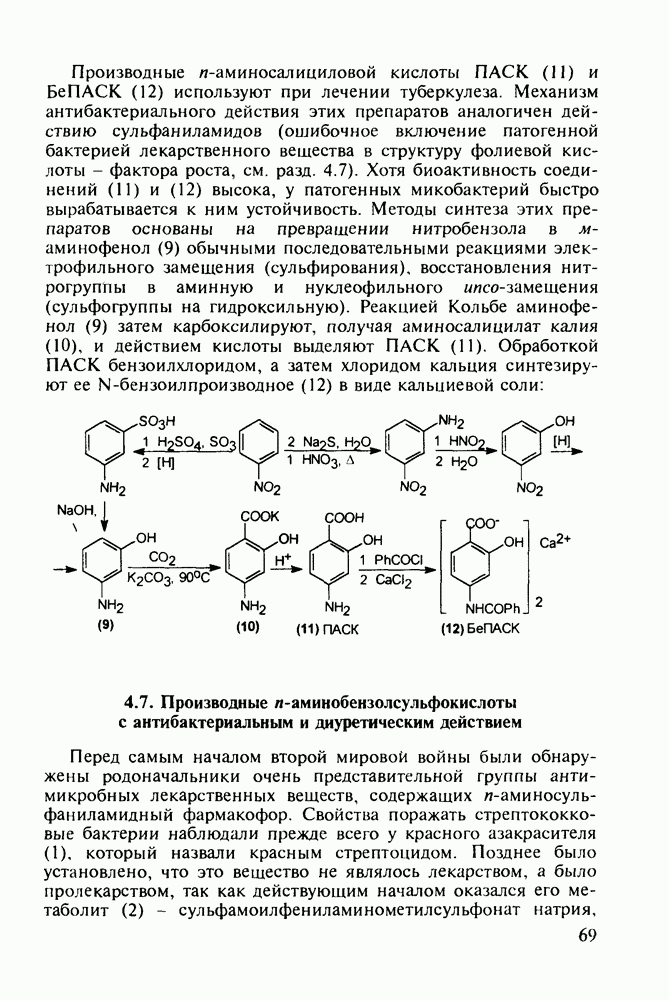
- 4.7. Производные n-аминобензолсульфокислоты с антибактериальным и диуретическим действием
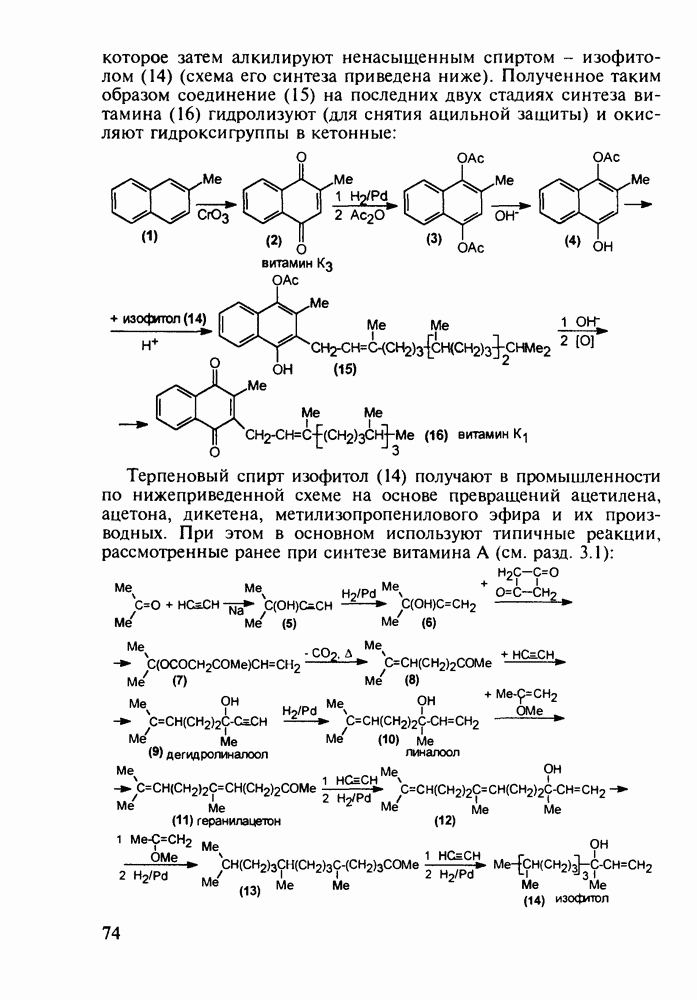
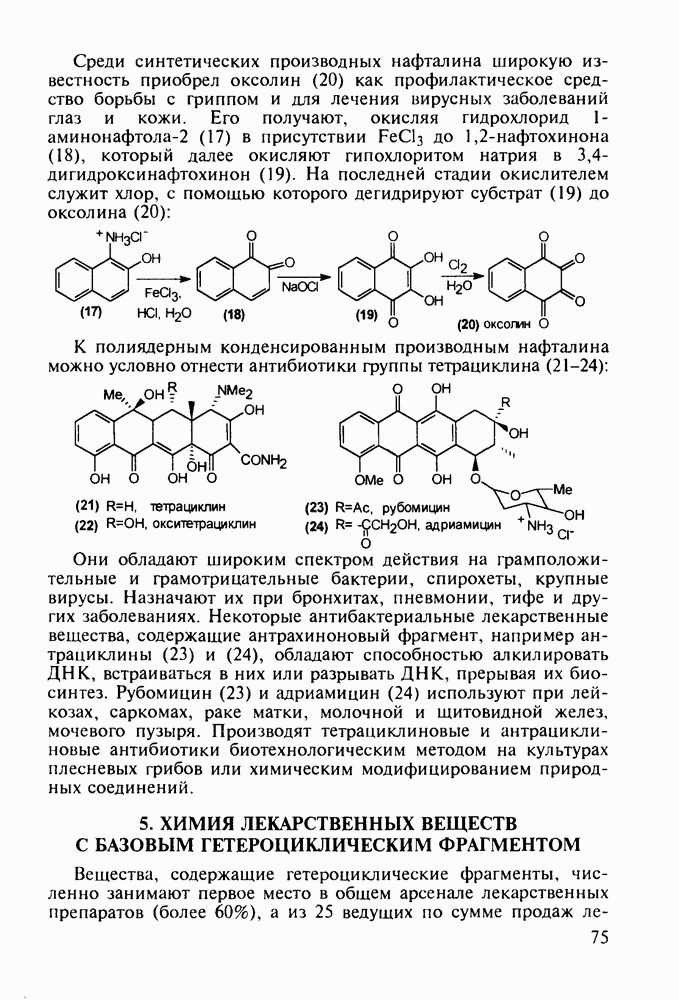
- 4.8. Оксопроизводные нафталина. Витамин К1. Оксолин
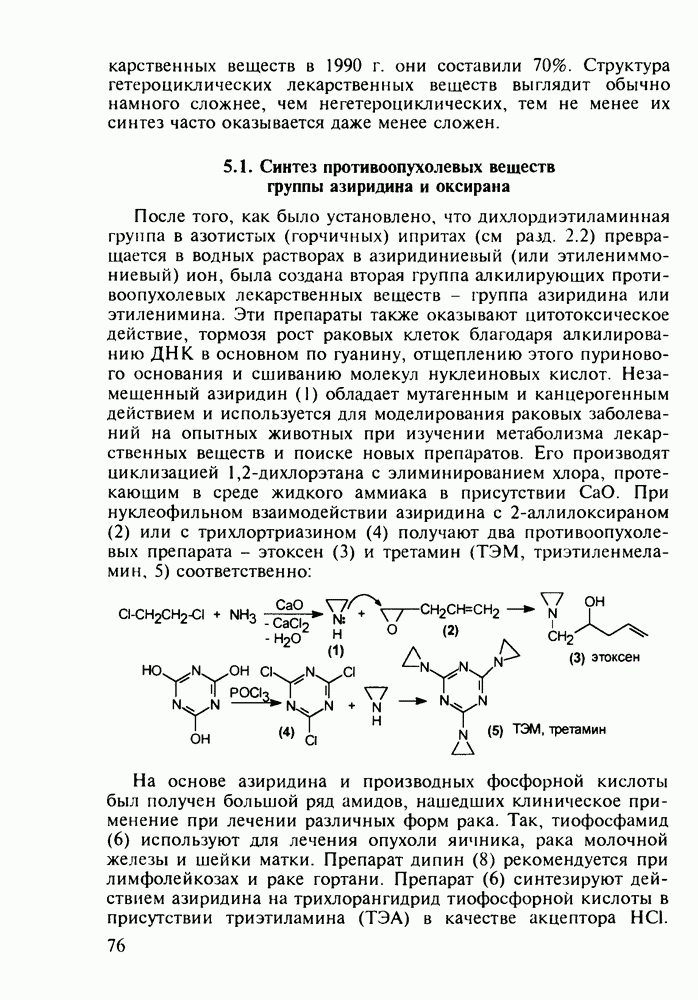
- 5. ХИМИЯ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ С БАЗОВЫМ ГЕТЕРОЦИКЛИЧЕСКИМ ФРАГМЕНТОМ
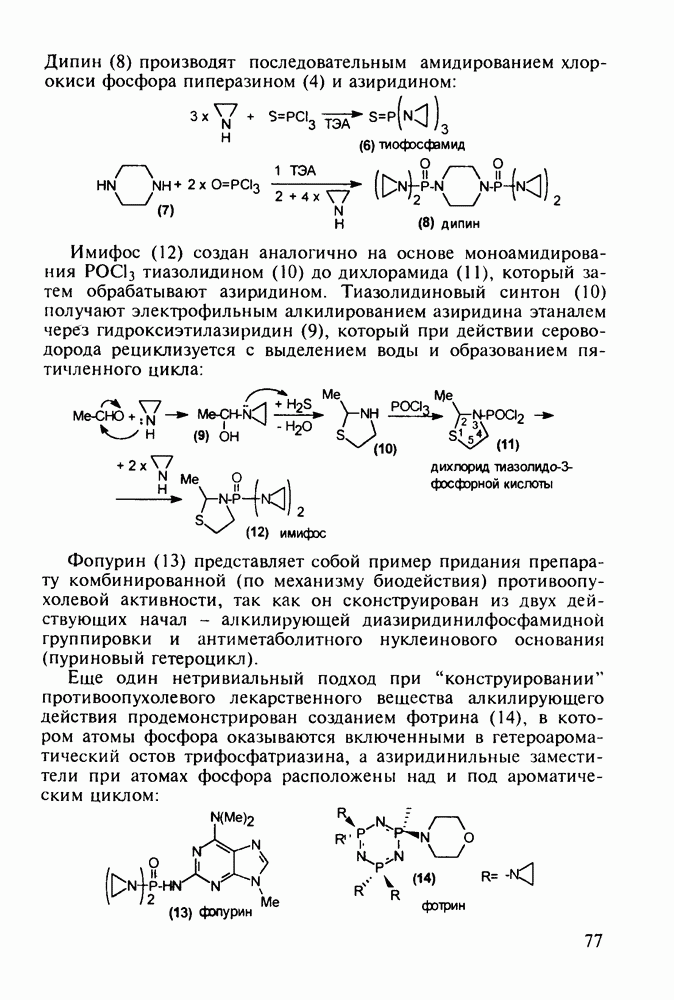
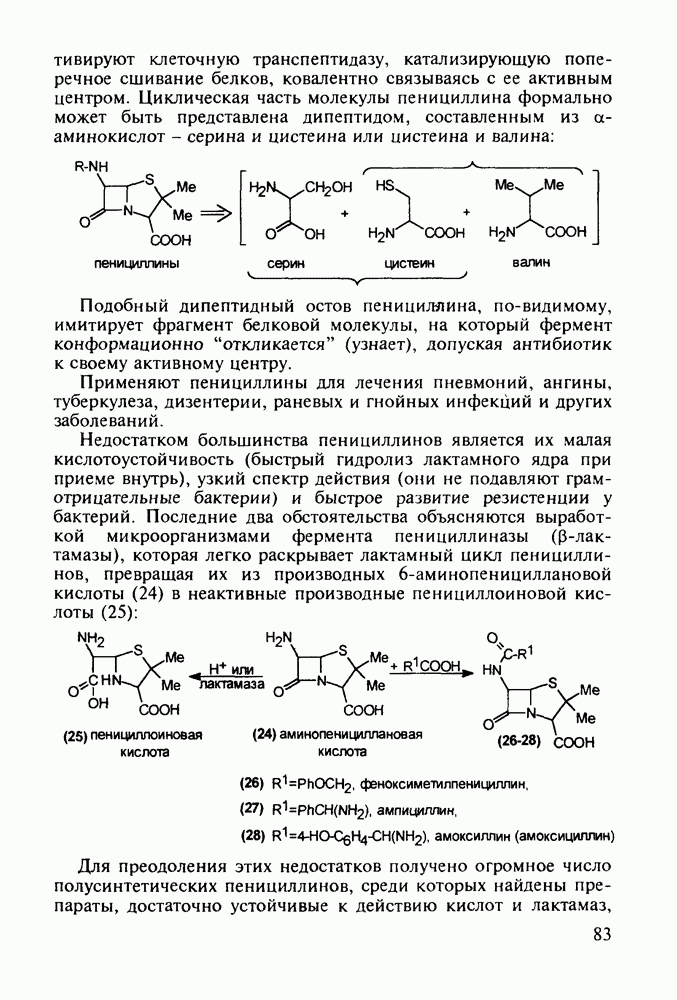
- 5.2. Антибиотики, содержащие четырехчленное азетидиновое ядро
- 5.2.2. Пенициллины. Моксалактам
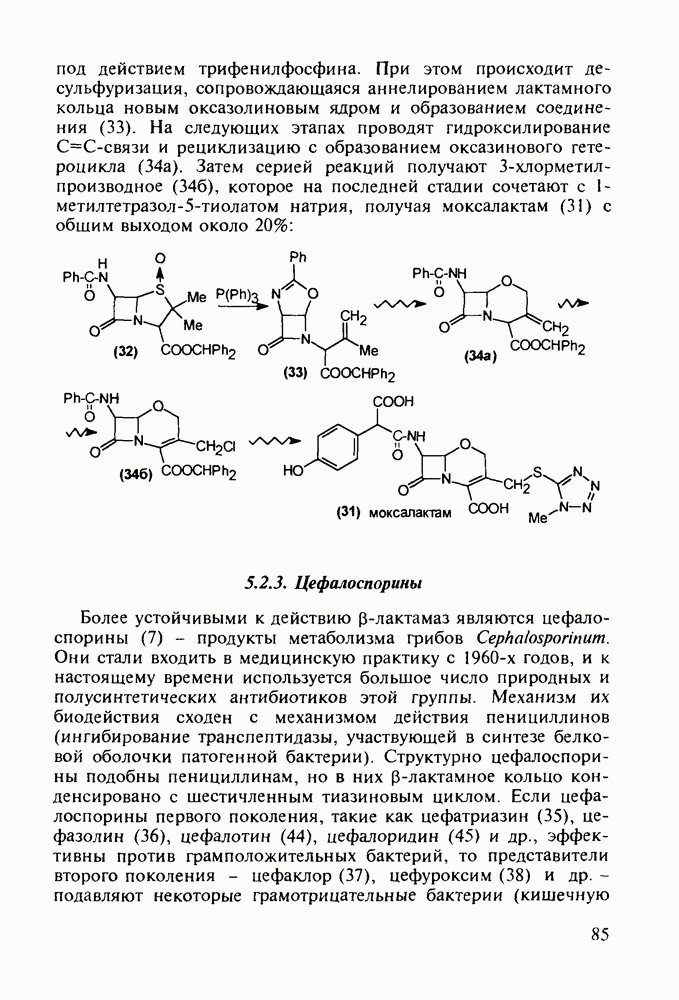
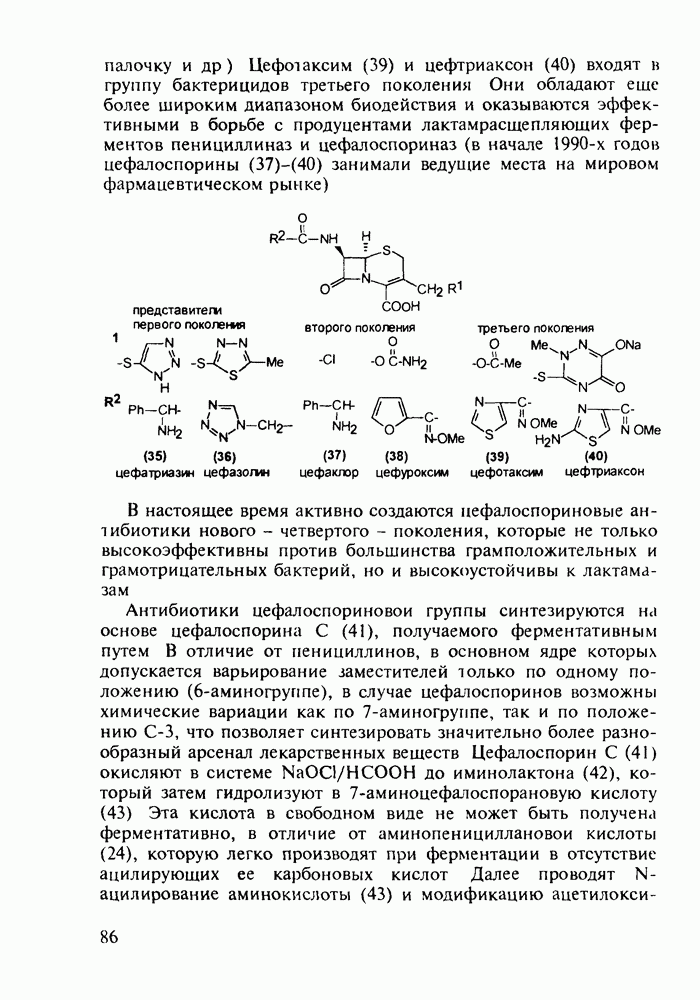
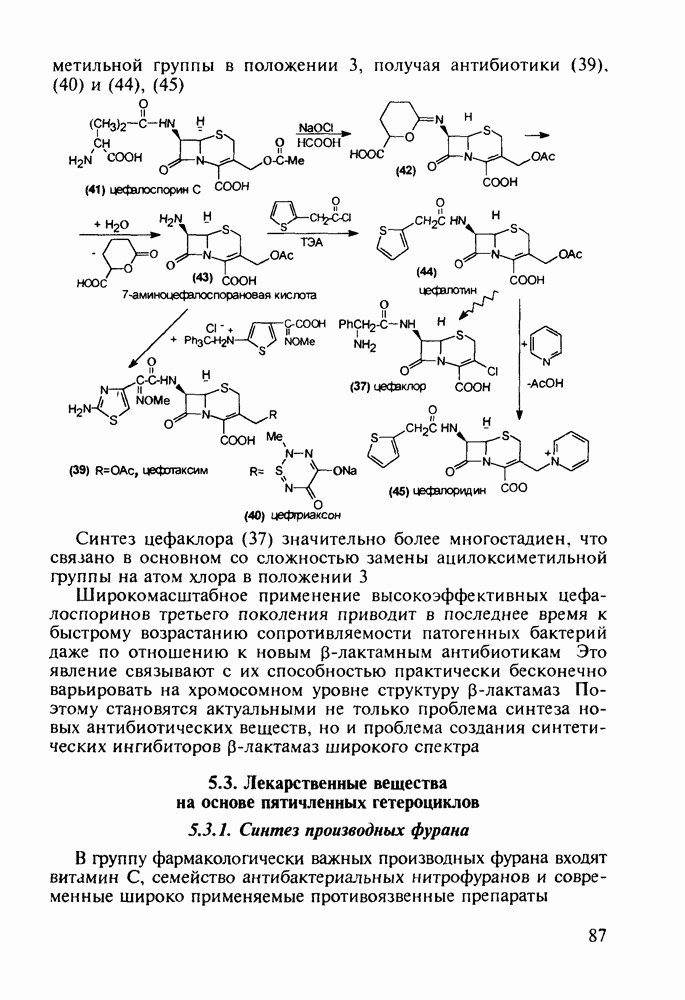
- 5.2.3. Цефалоспорины
- 5.3. Лекарственные вещества на основе пятичленных гетероциклов
- 5.3.2. Синтез производных пиррола
- 5.3.3. Оксазолидины. Антибиотик циклосерин
- 5.3.4. Антипиретики и анальгетики пиразолинового ряда
- 5.3.5. Имидазолы с противопаразитарной, антигипертензивной и другой биоактивностью
- 5.3.6. Производные тиазола. Витамин В1
- 5.3.7. Психостимуляторы с оксадиазольным и тетразольным гетероциклами
- 5.4. Синтез лекарственных веществ, содержащих шестичленные гетероциклы
- 5.4.2. Синтез лекарственных веществ пиридинового ряда
- 5.4.3. Анальгетики и транквилизаторы пиперидинового ряда
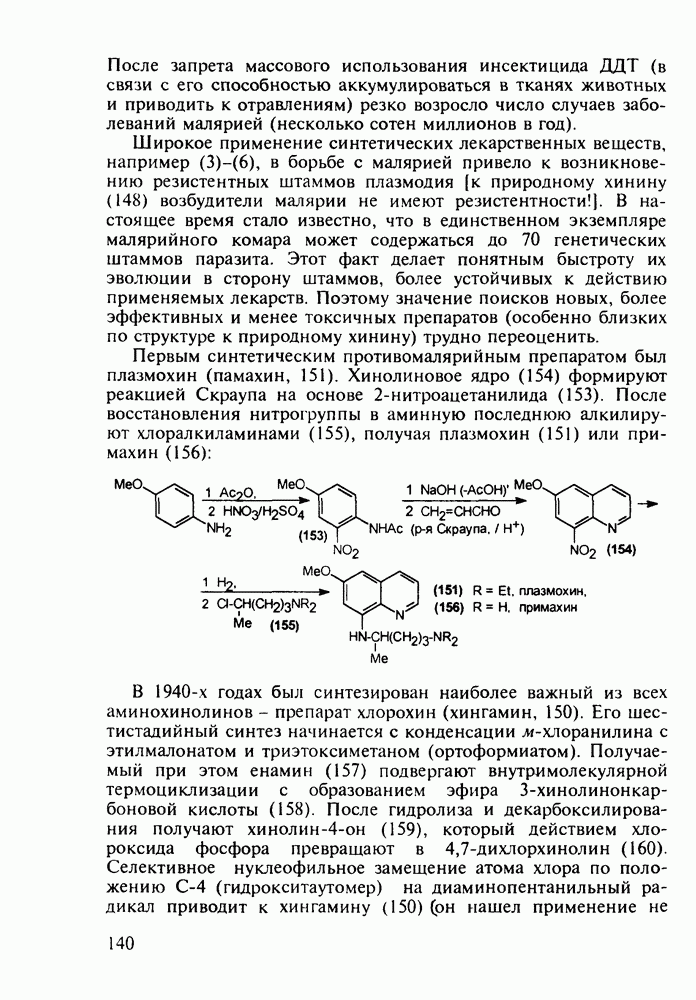
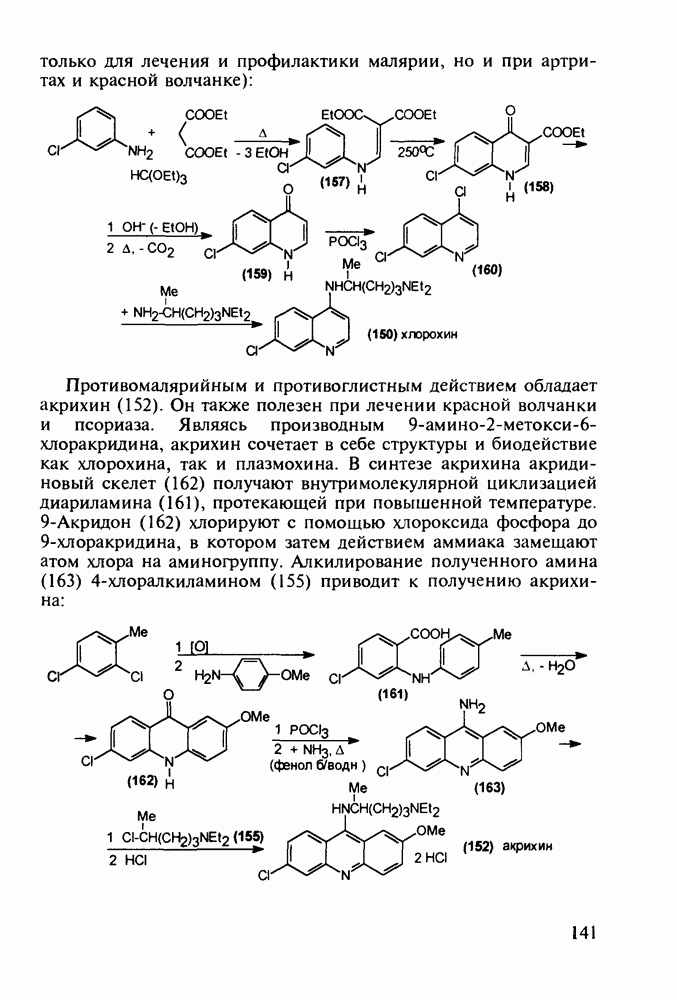
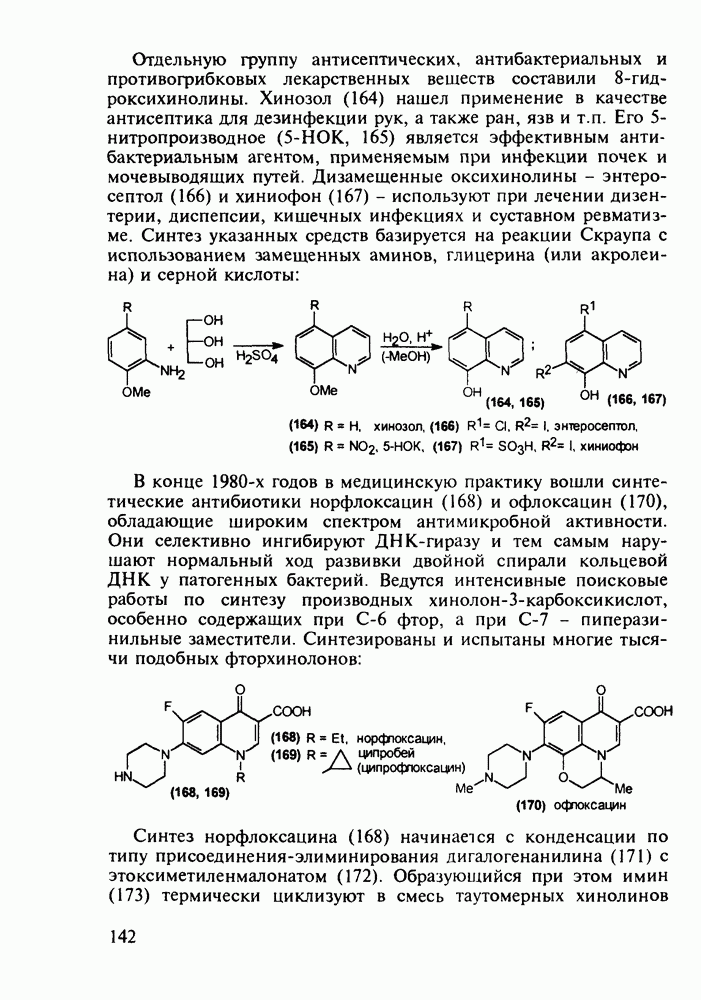
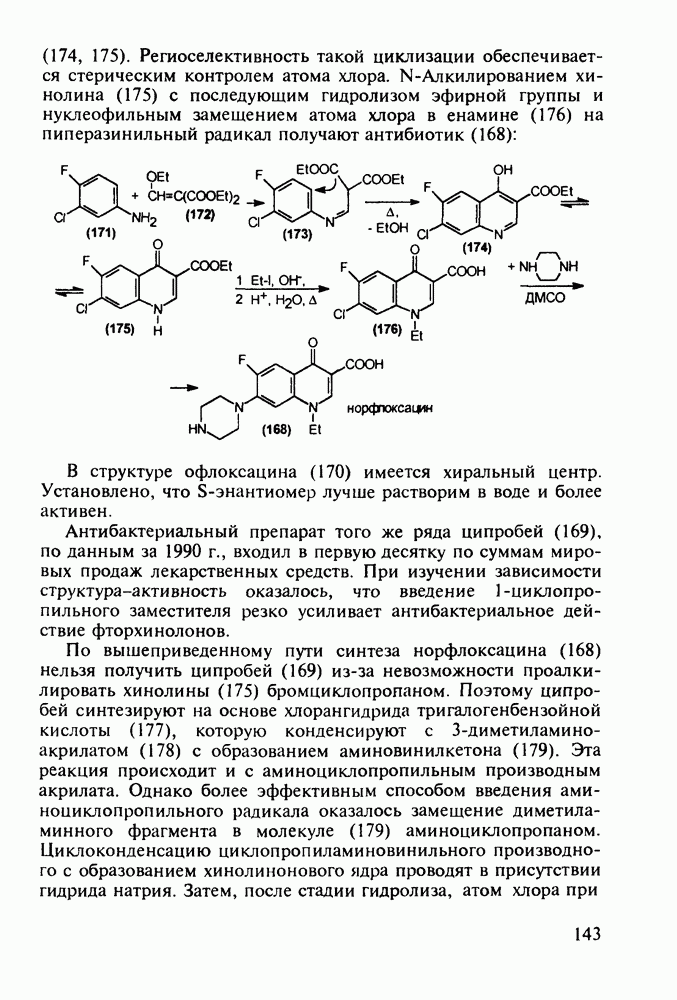
- 5.4.4. Производные хинолина с антималярийным и антибактериальным действием
- 5.4.5. Изохинолины в качестве спазмолитиков и трипаноцидов
- 5.4.6. Производные пиримидинов
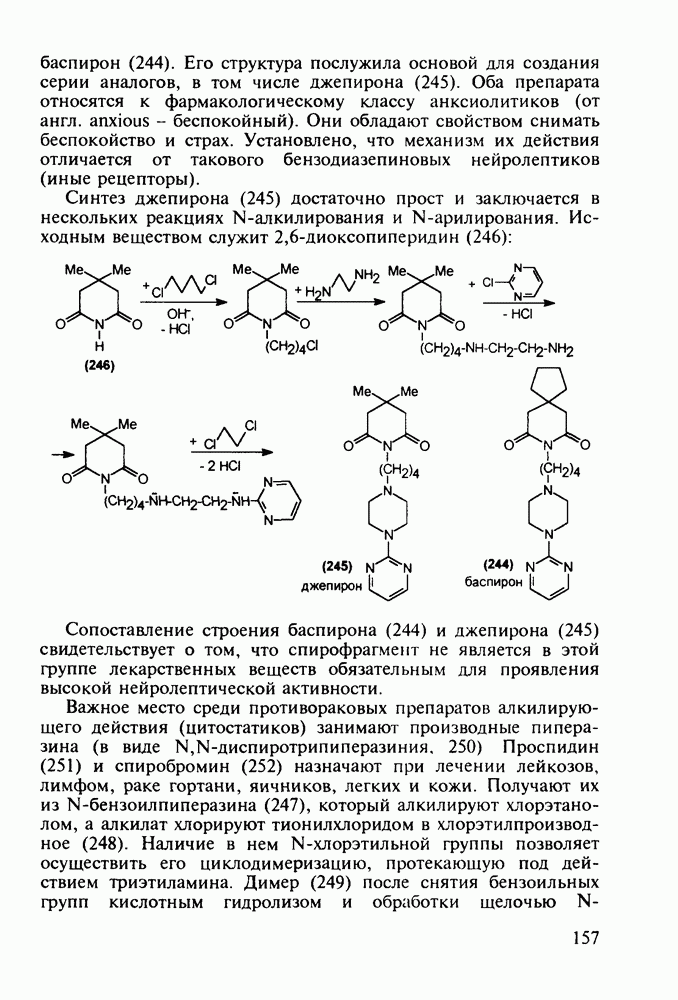
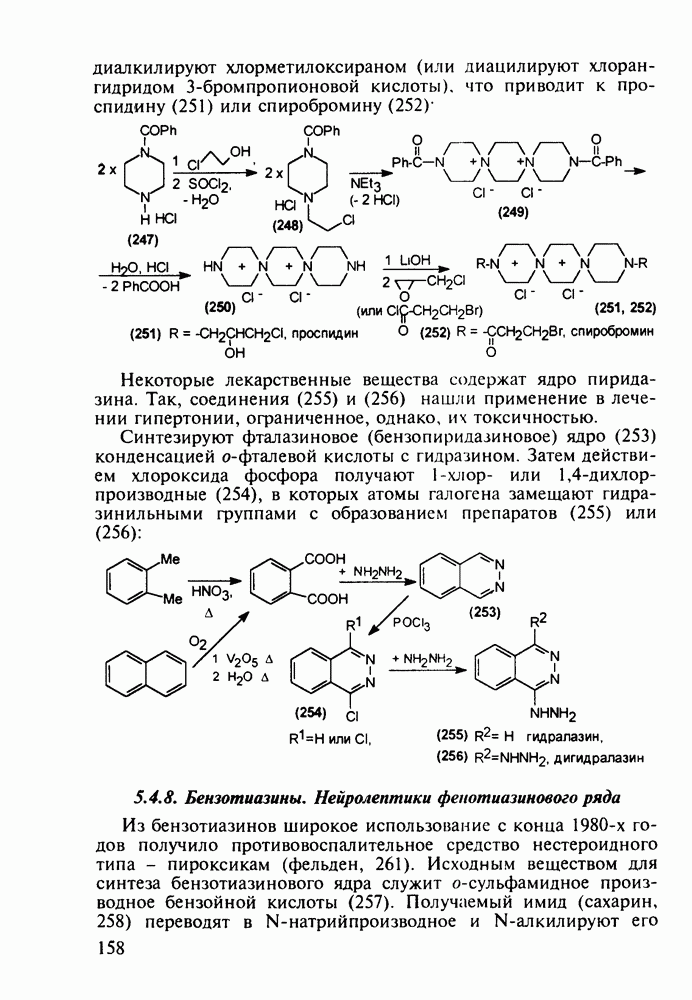
- 5.4.7. Производные пиперазина и пиридазина
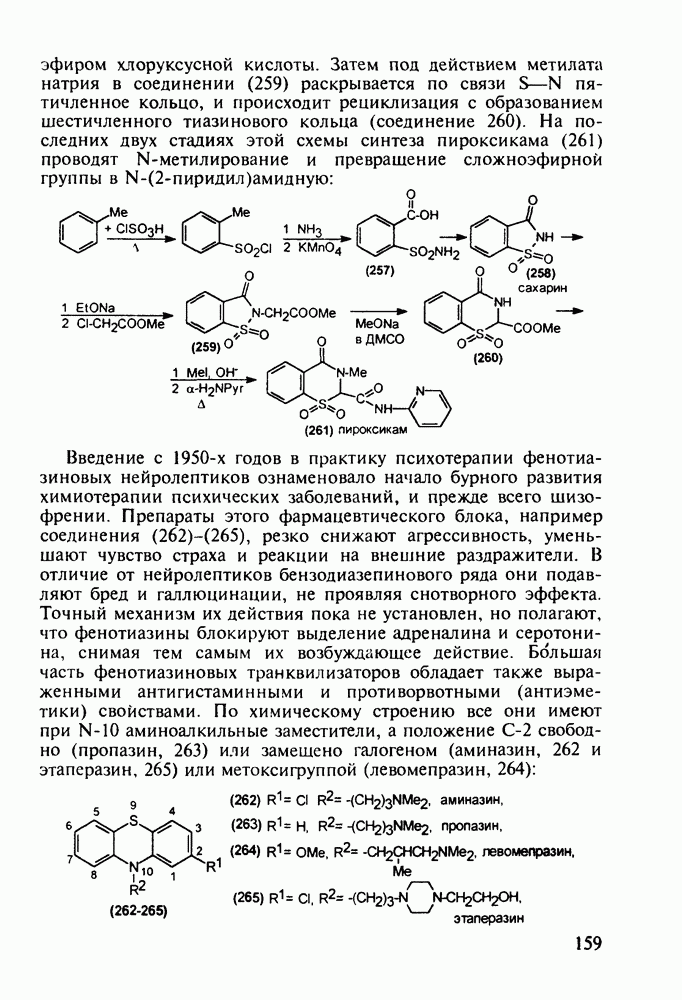
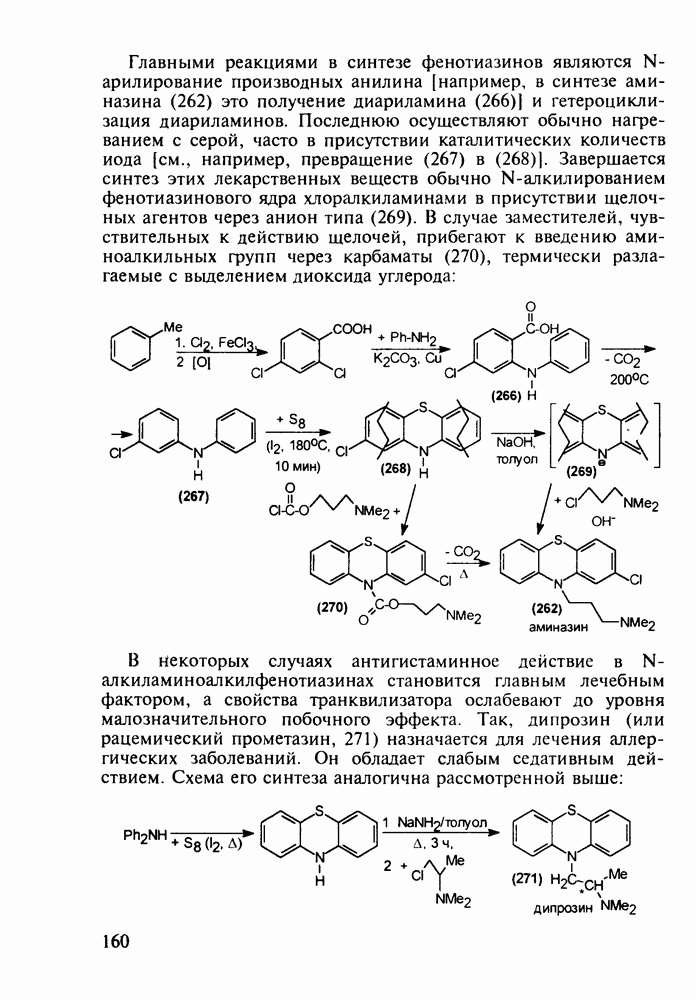
- 5.4.8. Бензотиазины. Нейролептики фенотиазинового ряда
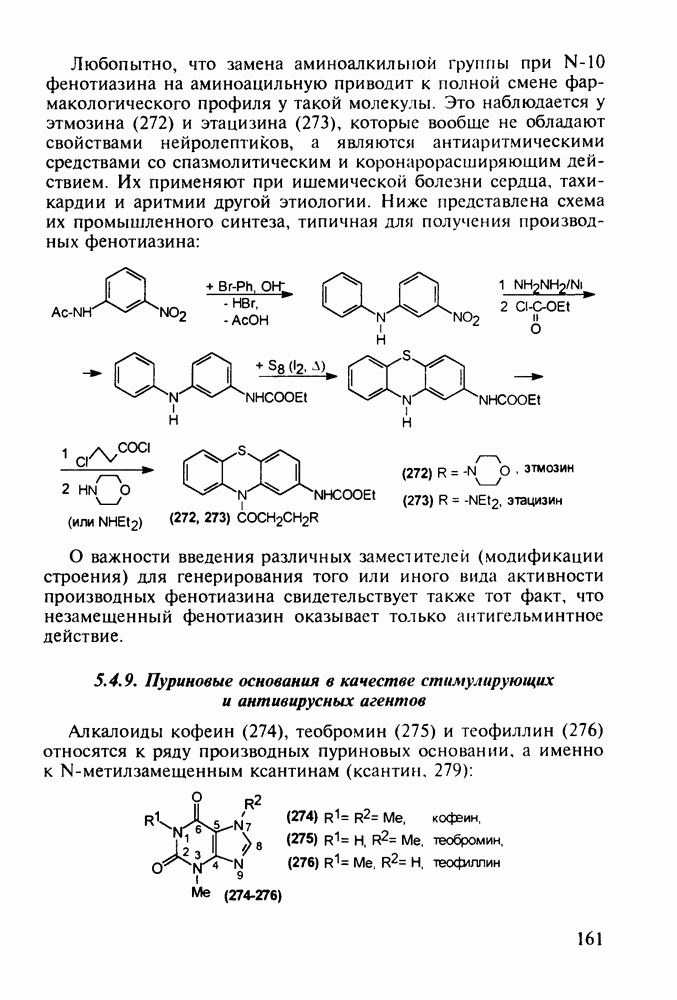
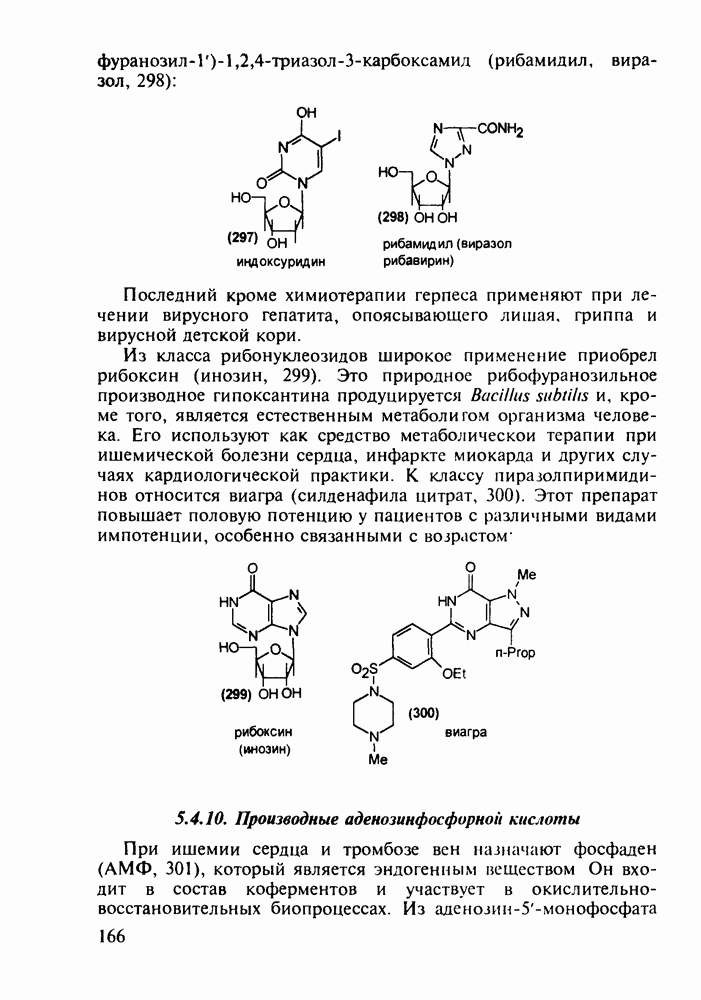
- 5.4.9. Пуриновые основания в качестве стимулирующих и антивирусных агентов
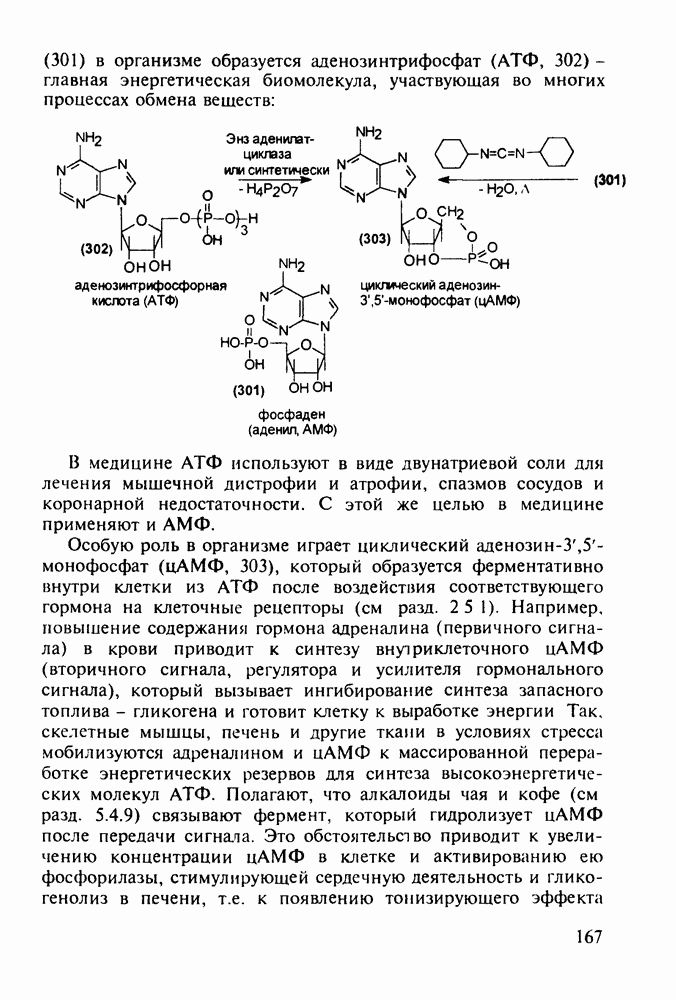
- 5.4.10. Производные аденозинфосфорной кислоты
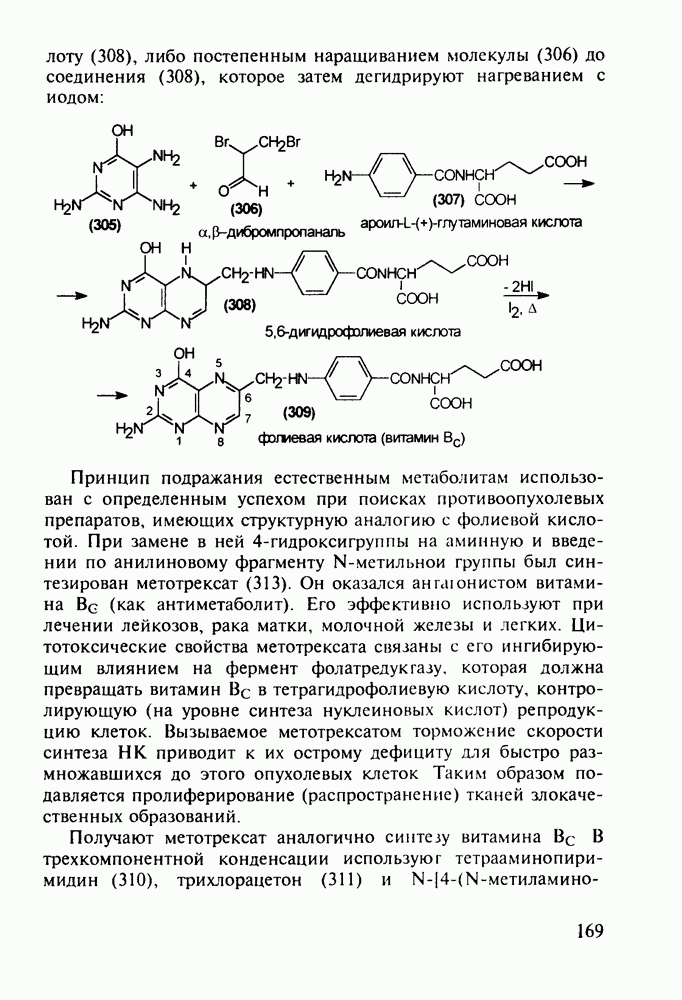
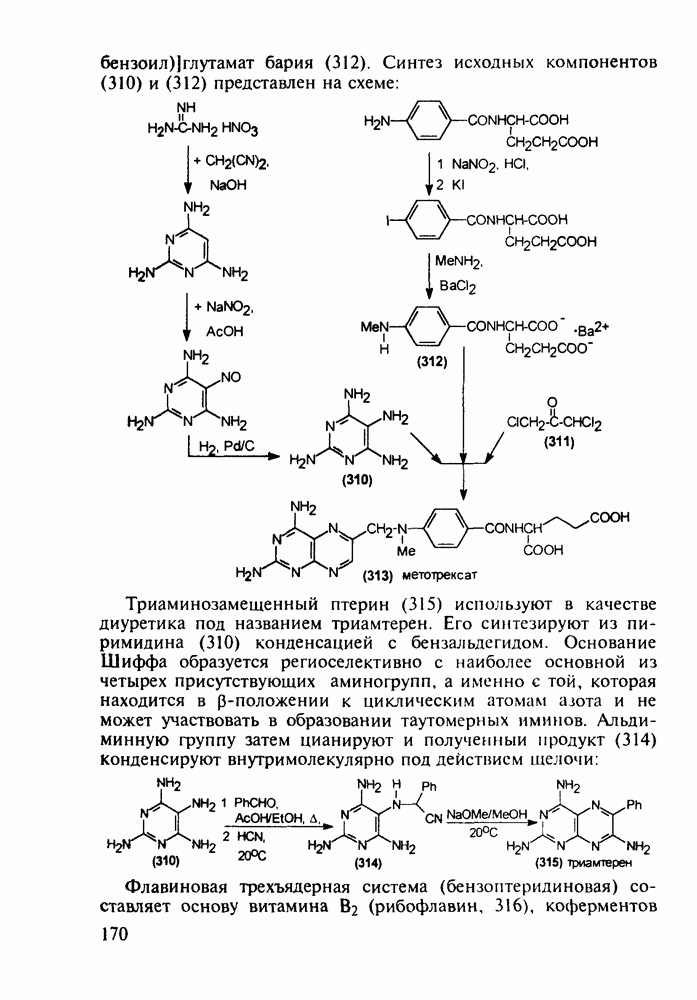
- 5.4.11. Производные птеридина с витаминной (витамины Вс и В2) и противораковой активностью
- 5.5. Лекарственные вещества, содержащие семичленный гетероцикл
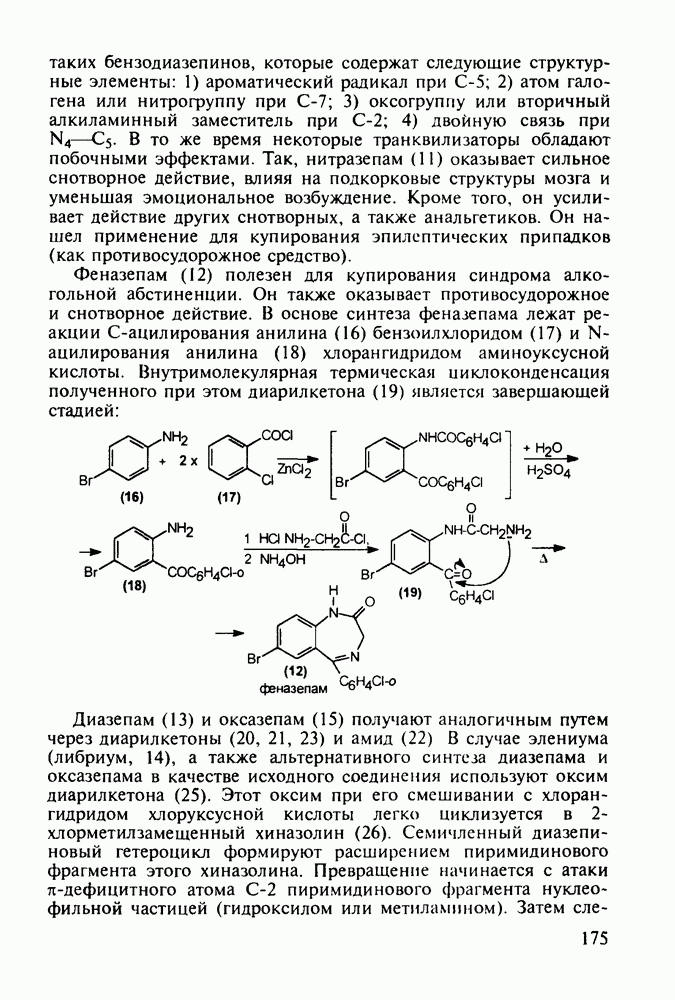
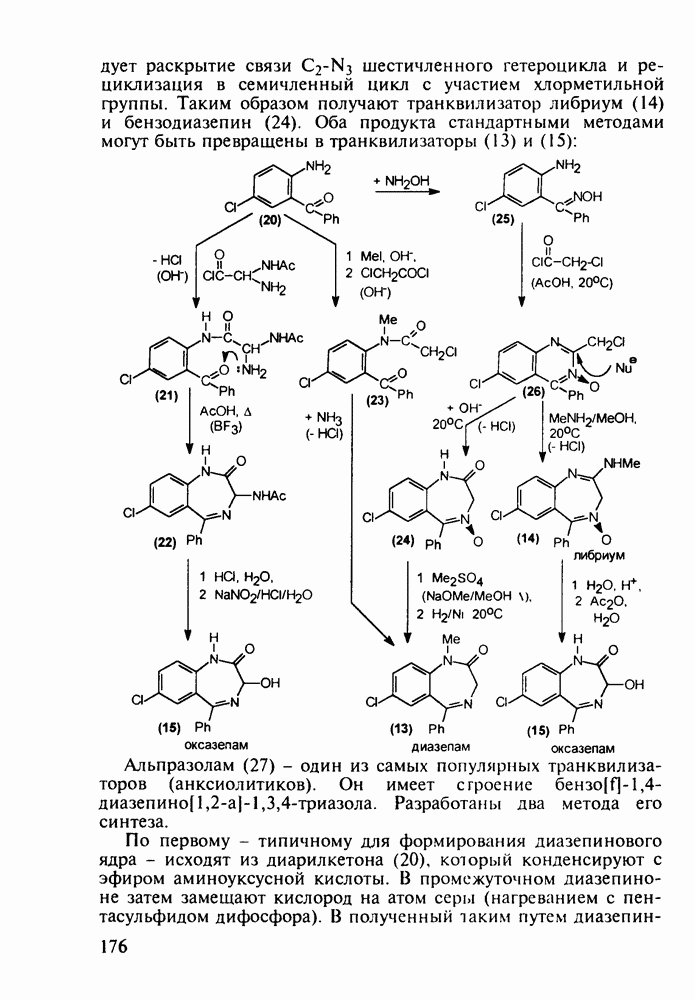
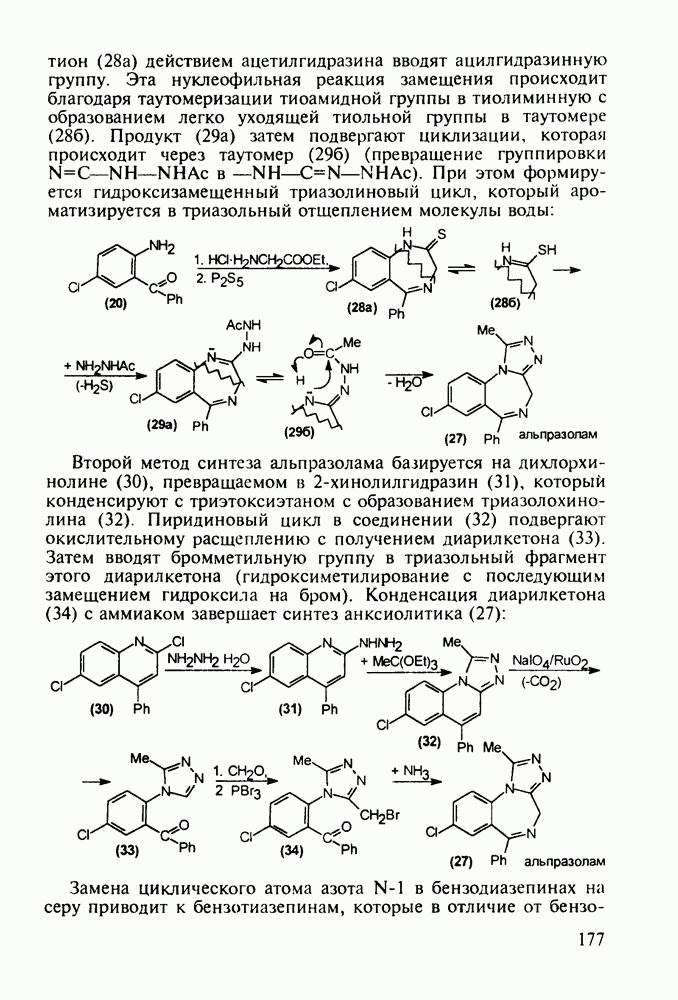
- 5.5.2. Транквилизаторы группы 1,4-бензодиазепина
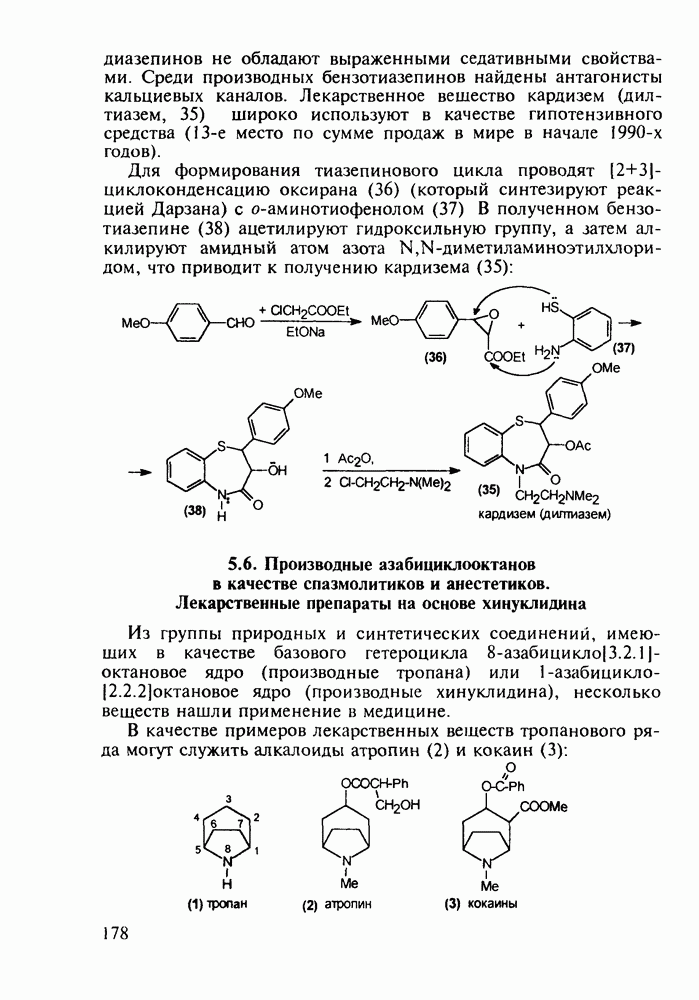
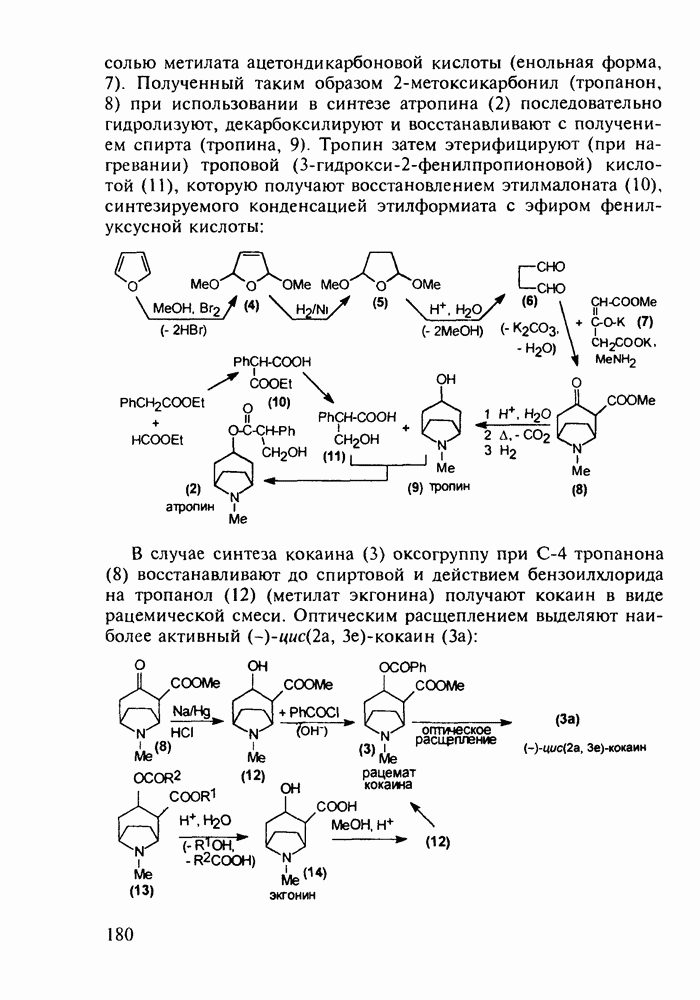
- 5.6. Производные азабициклооктанов в качестве спазмолитиков и анестетиков. Лекарственные препараты на основе хинуклидина
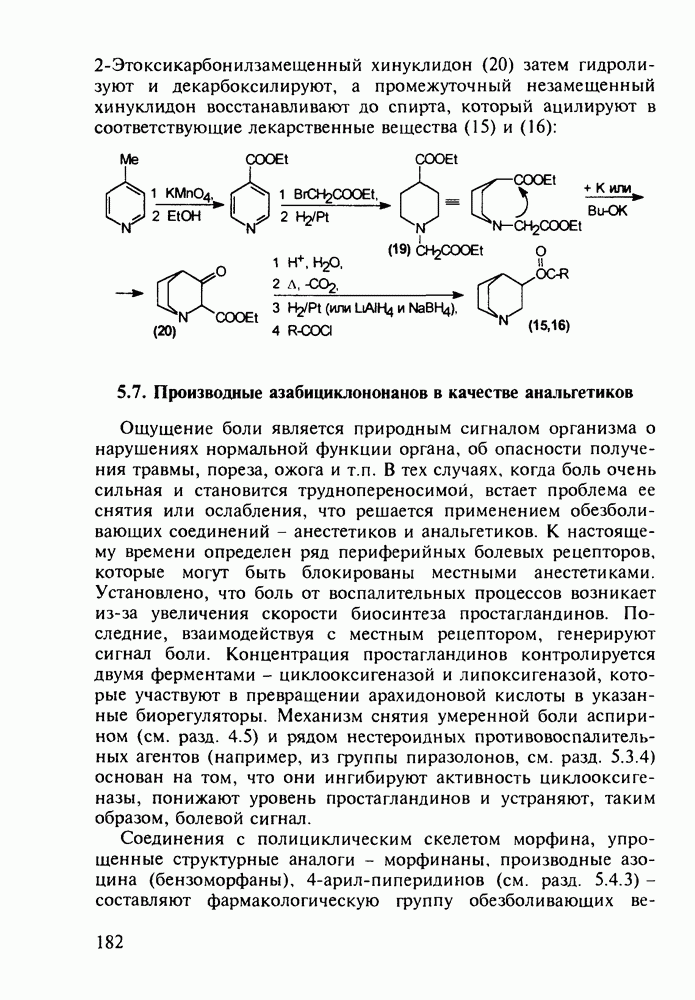
- 5.7. Производные азабициклононанов в качестве анальгетиков
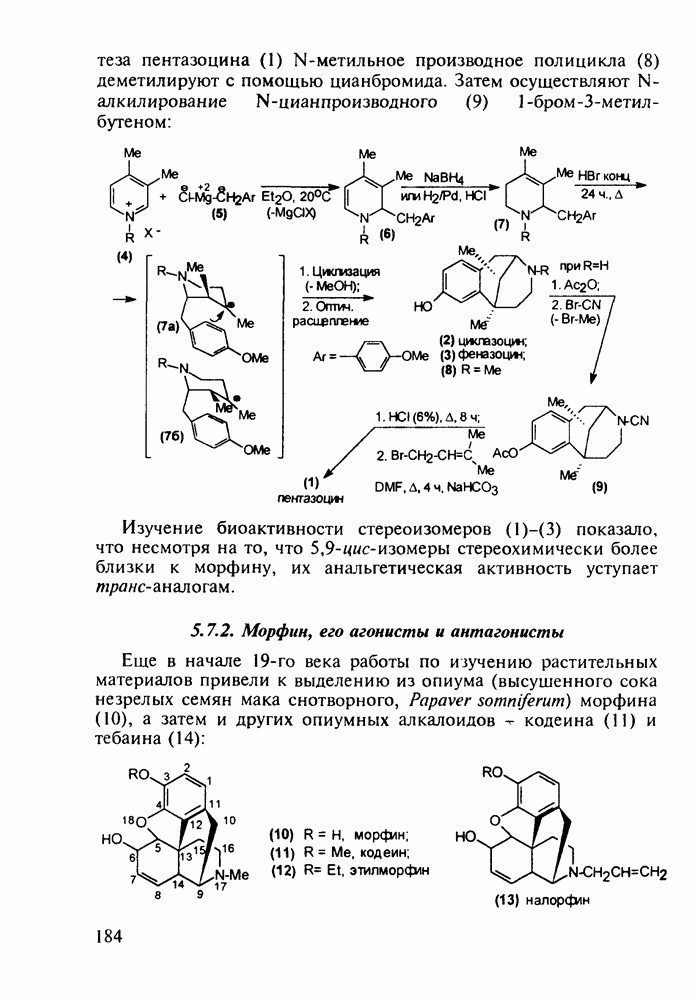
- 5.7.1. Группа пентазоцина
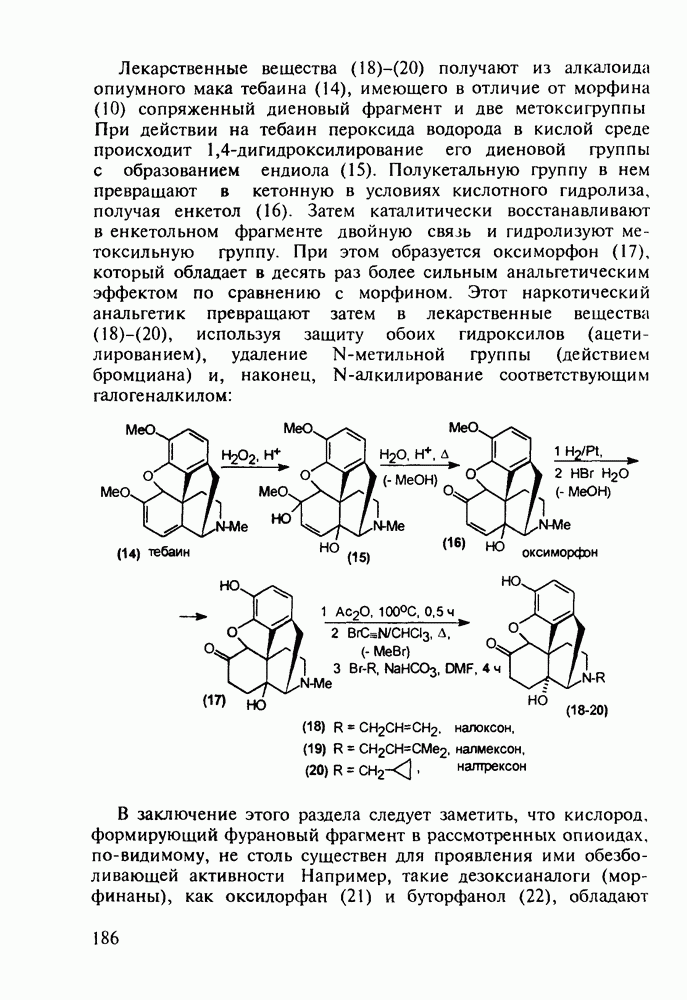
- 5.7.2. Морфин, его агонисты и антагонисты
- РЕКОМЕНДУЕМАЯ ЛИТЕРАТУРА