| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
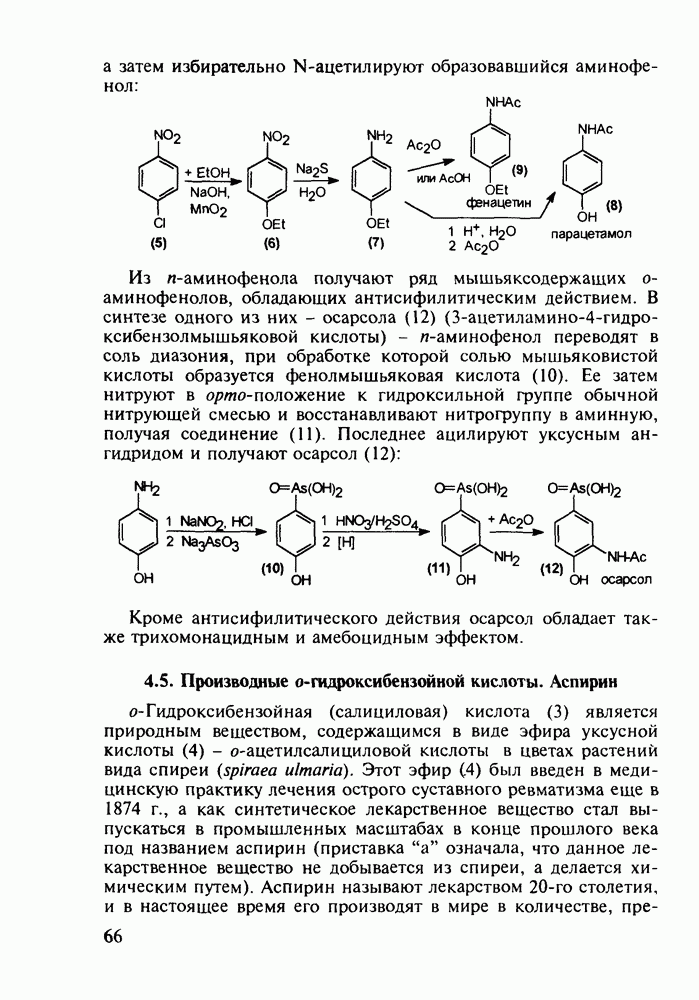
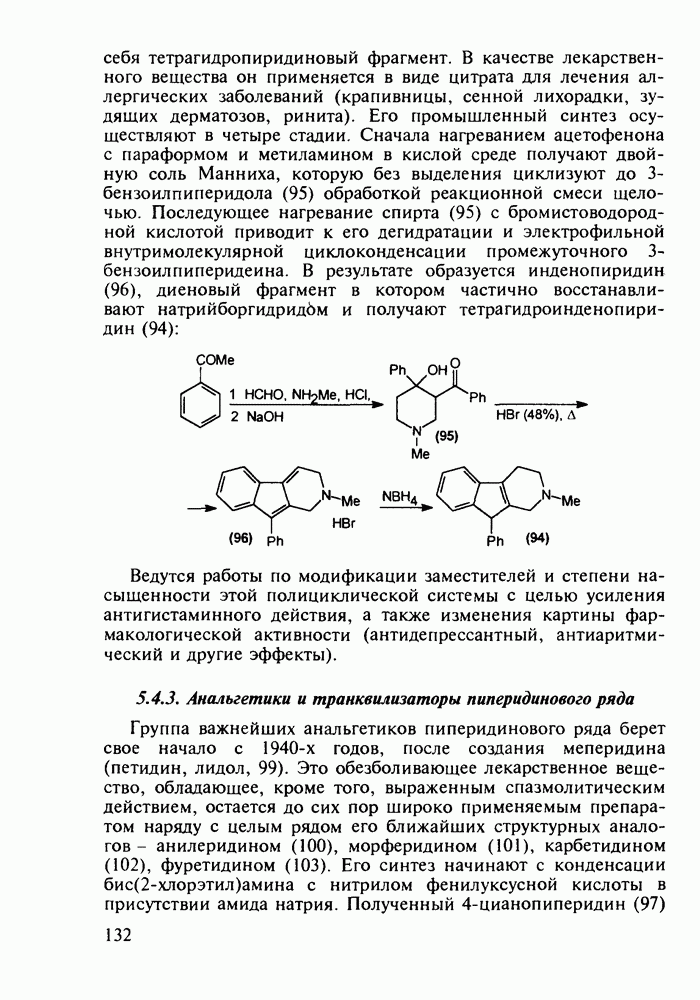
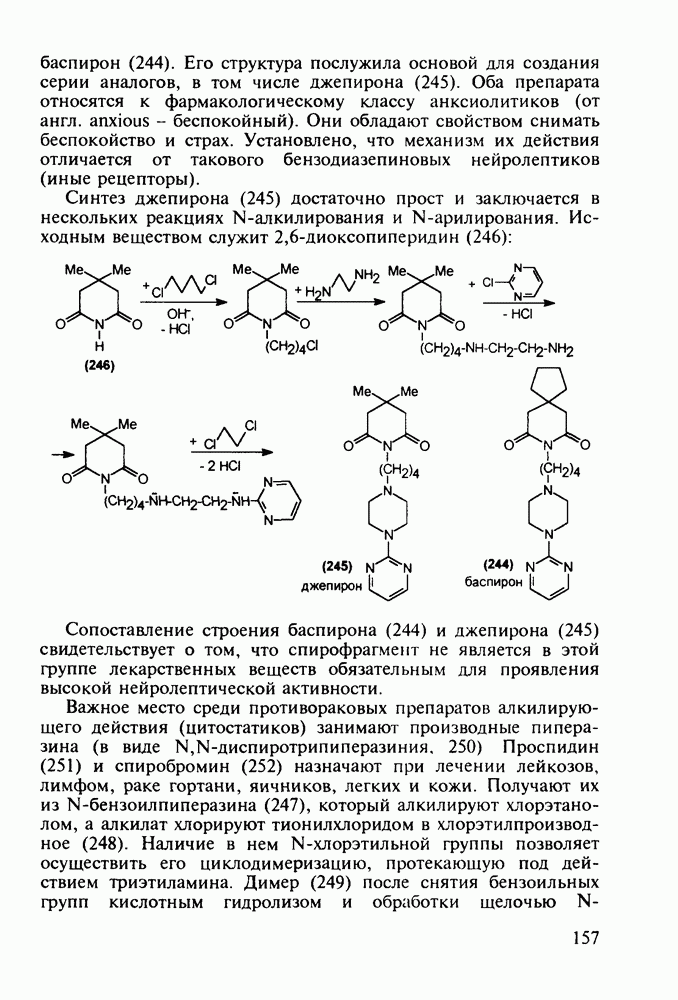
4.5. Производные о-гидроксибензойной кислоты. Аспирин
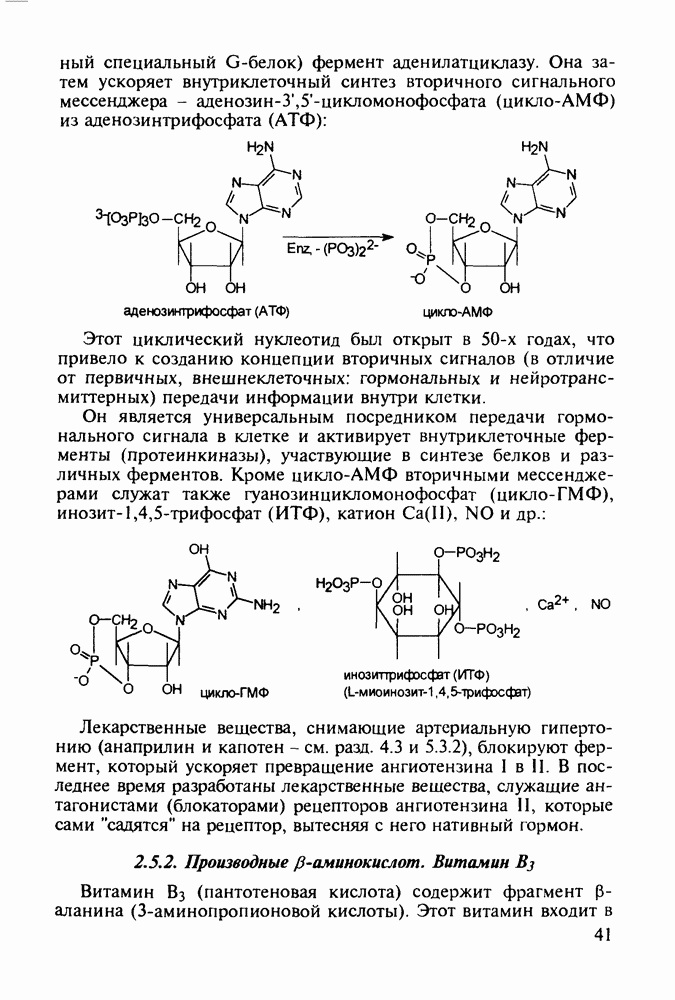
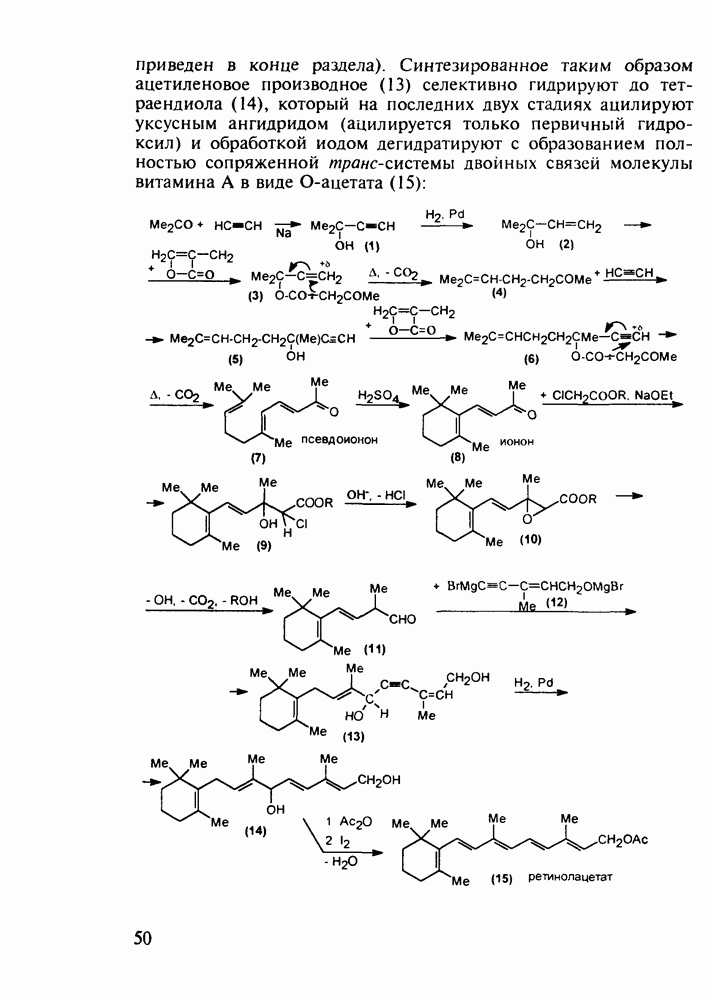
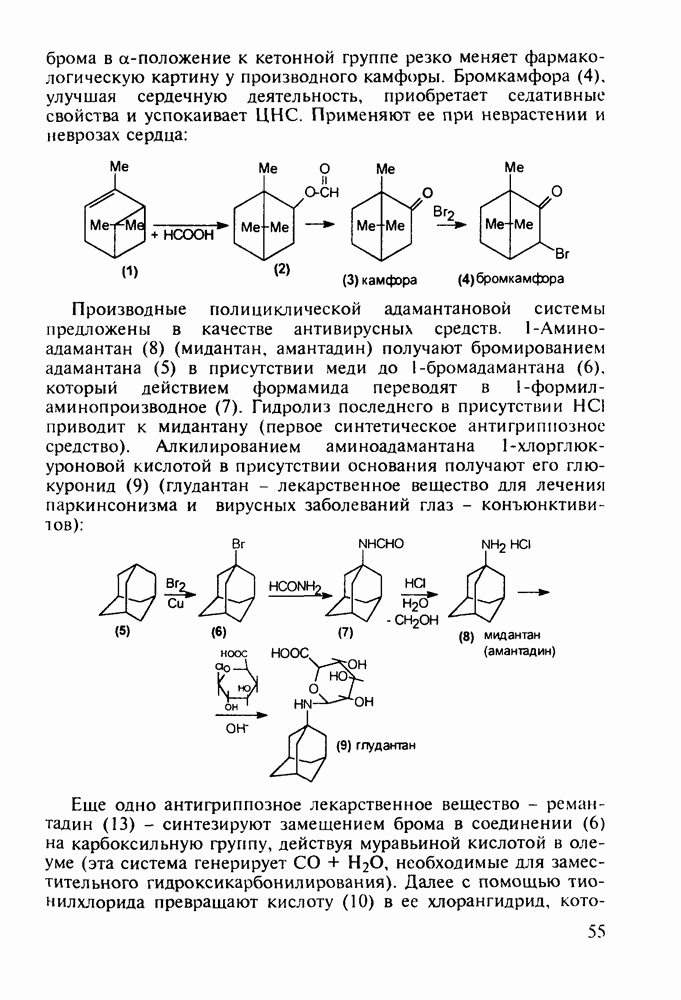
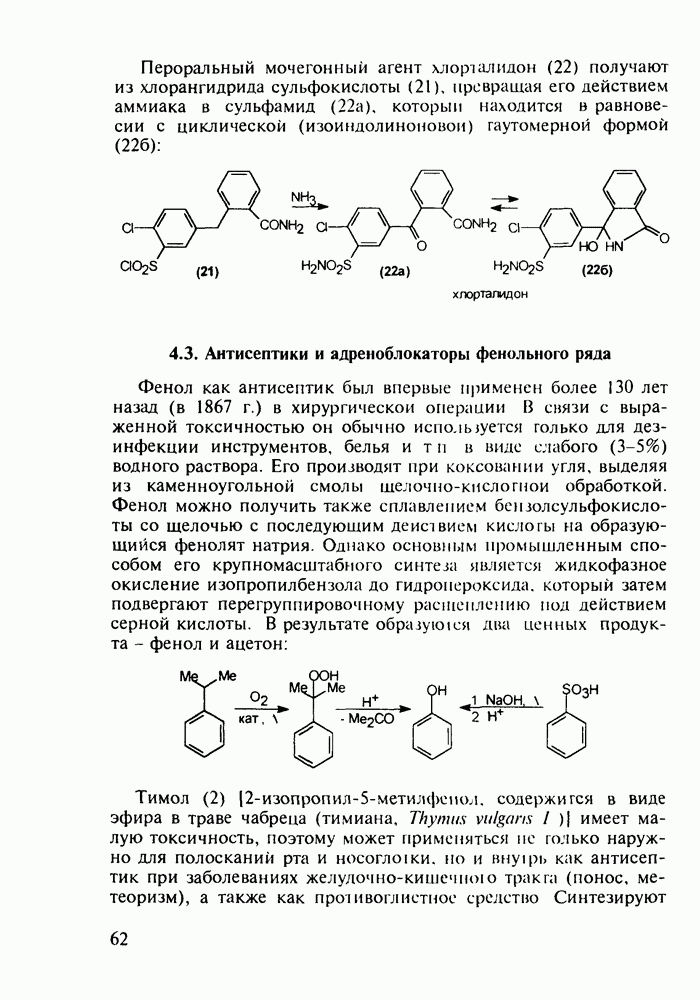
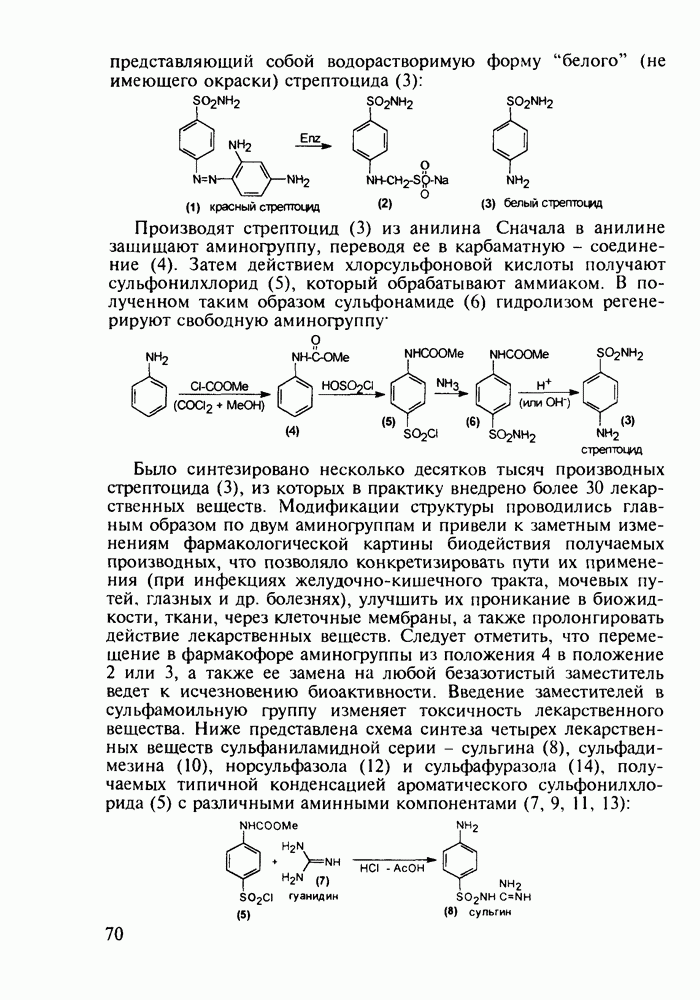
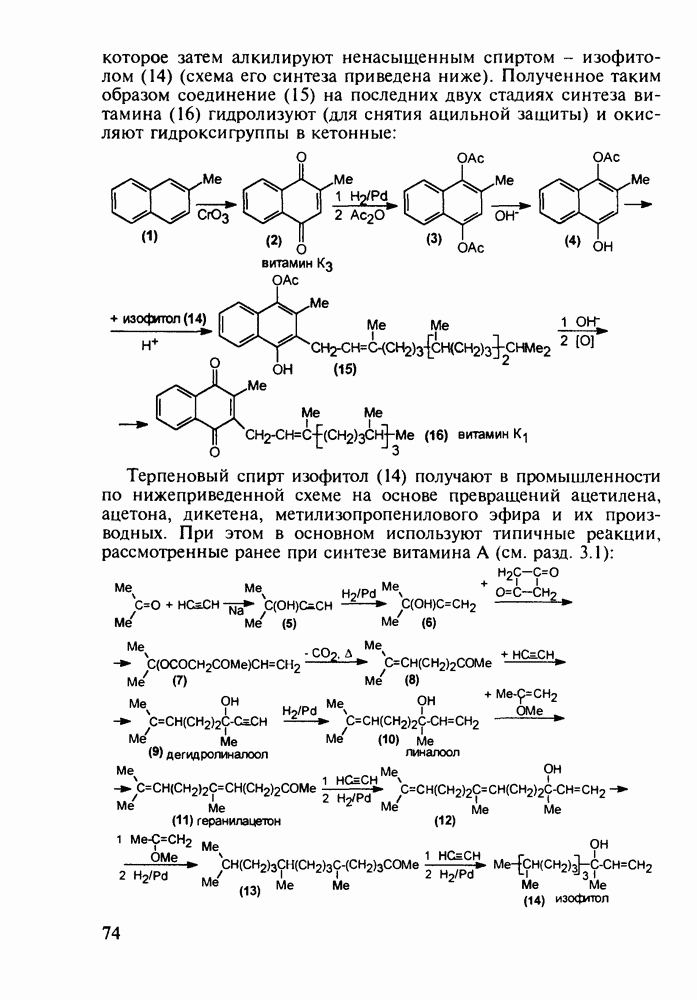
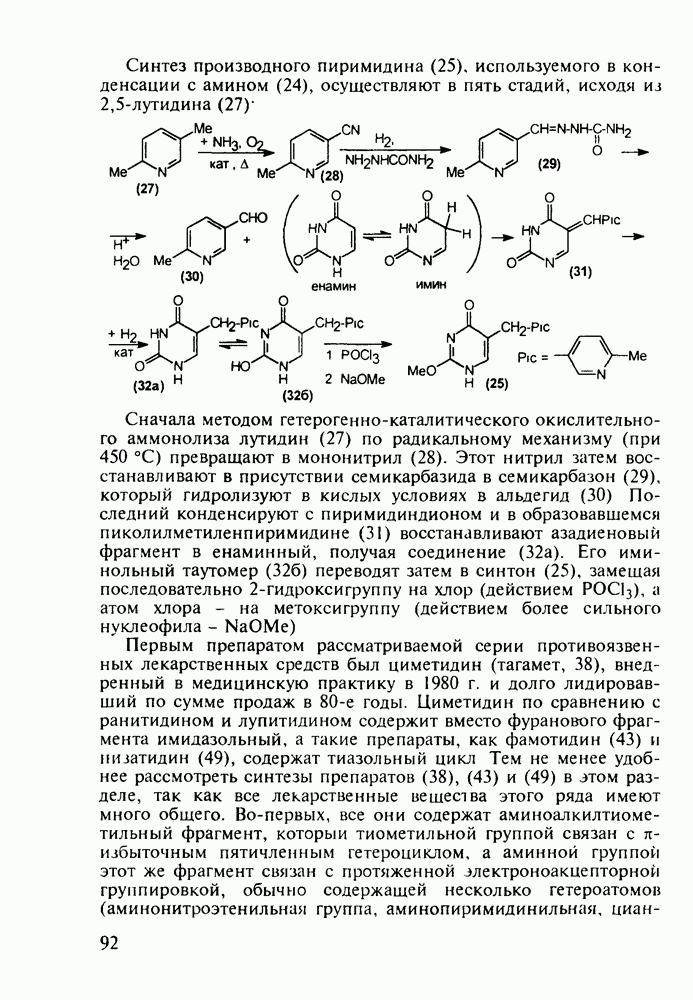
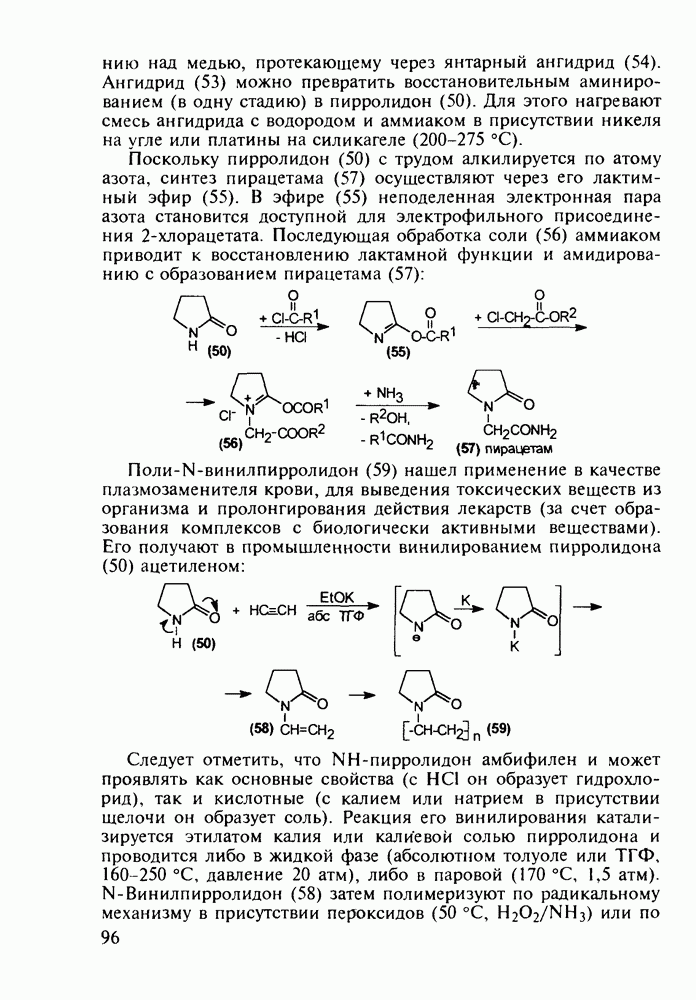
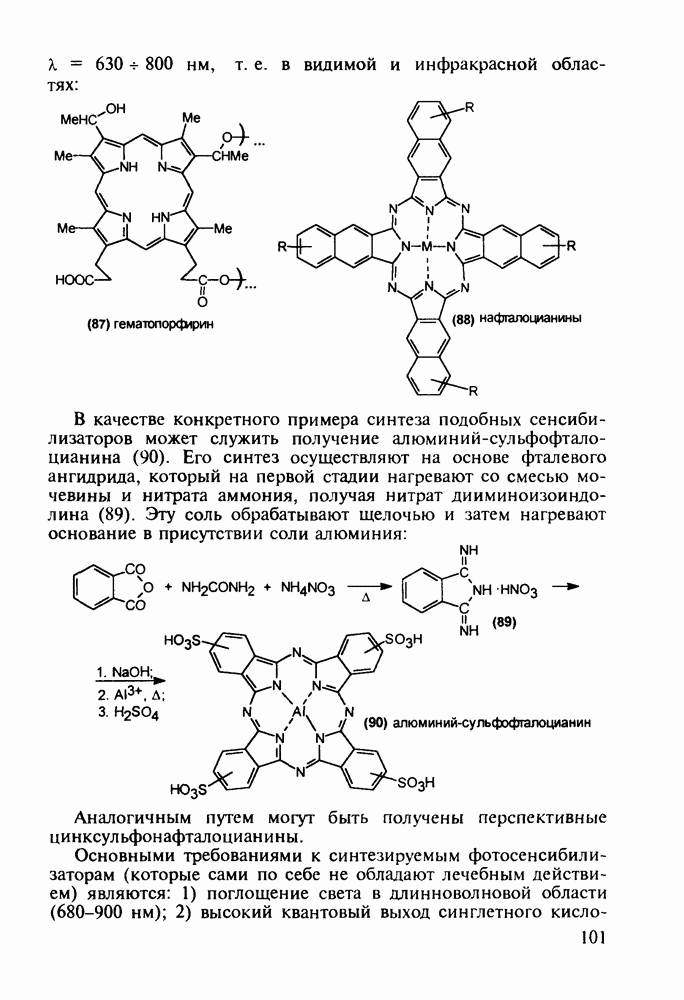
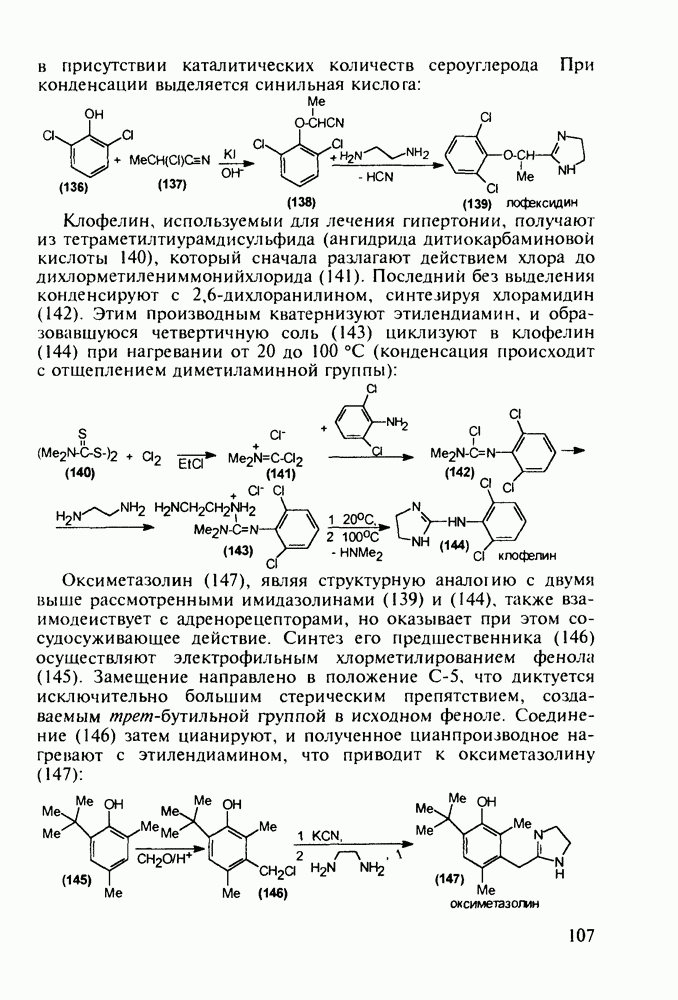
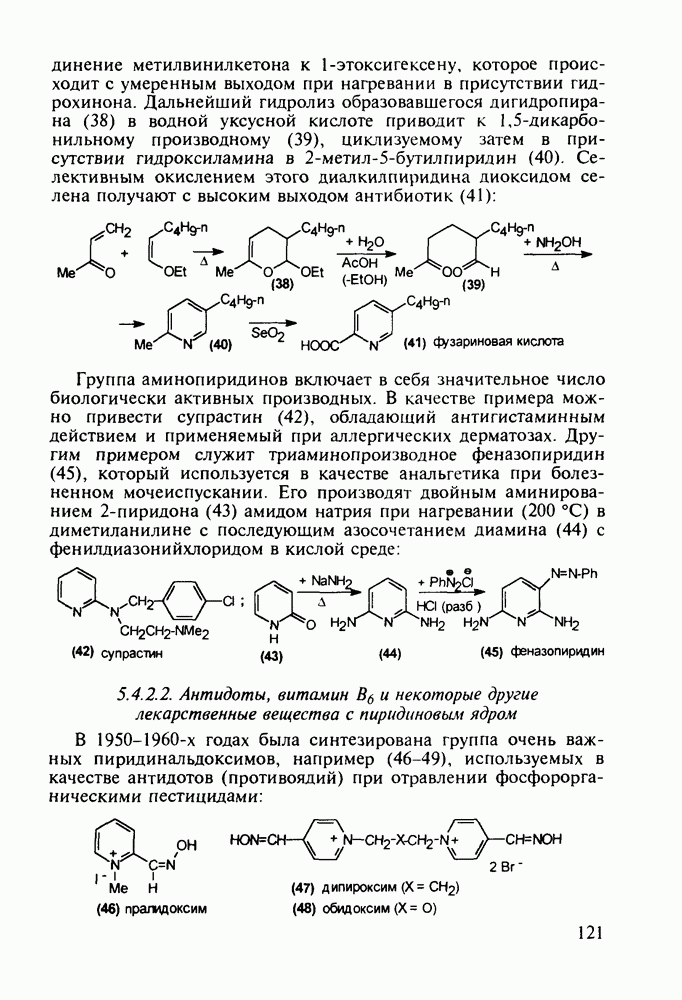
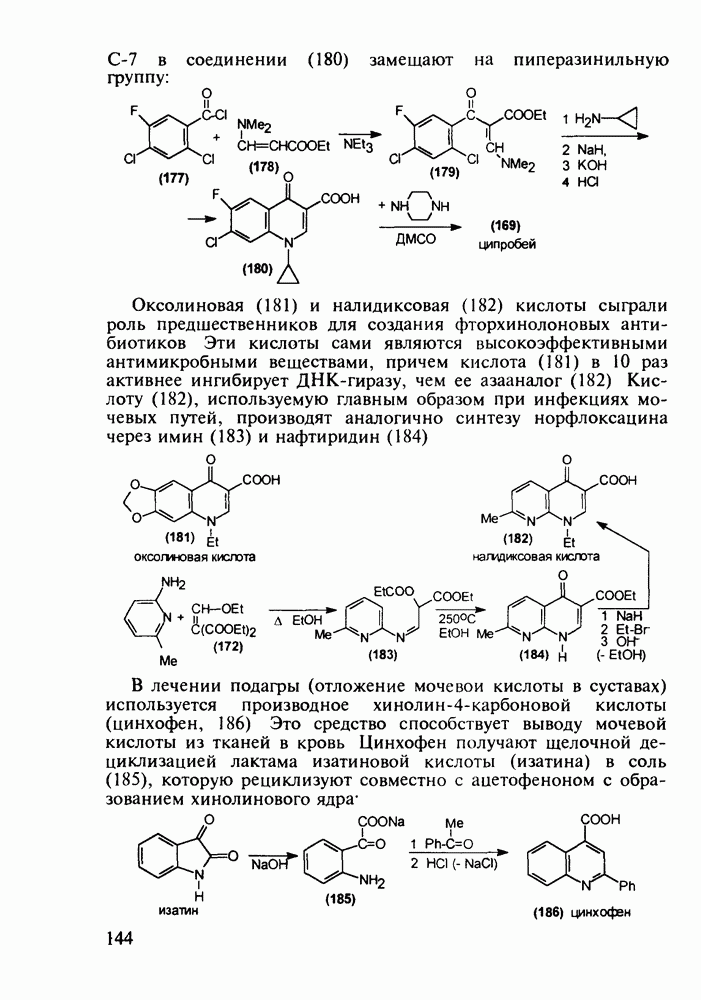
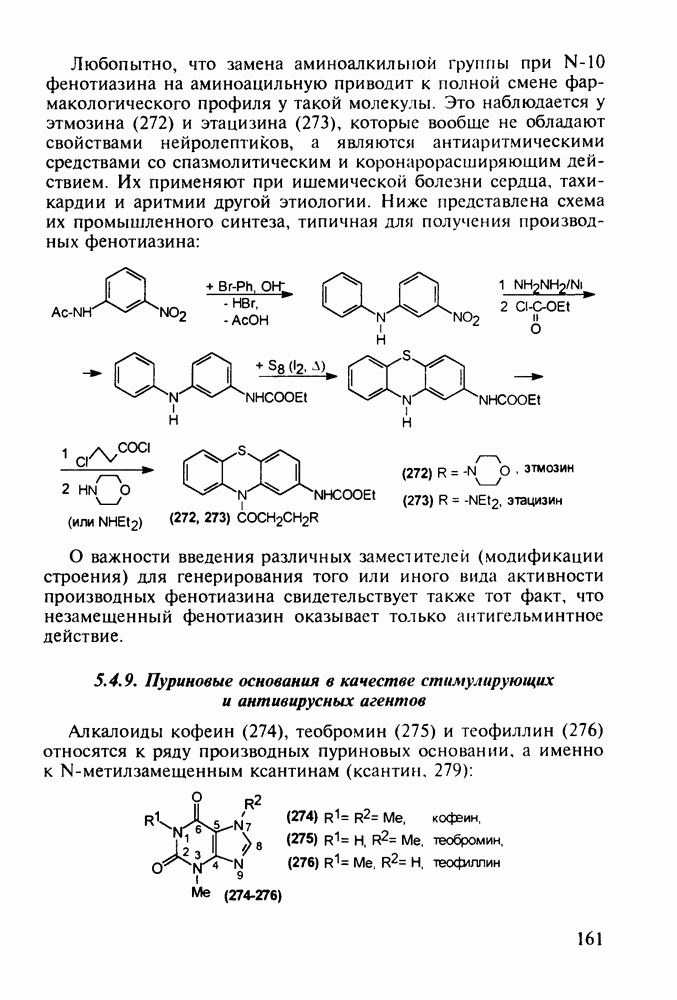
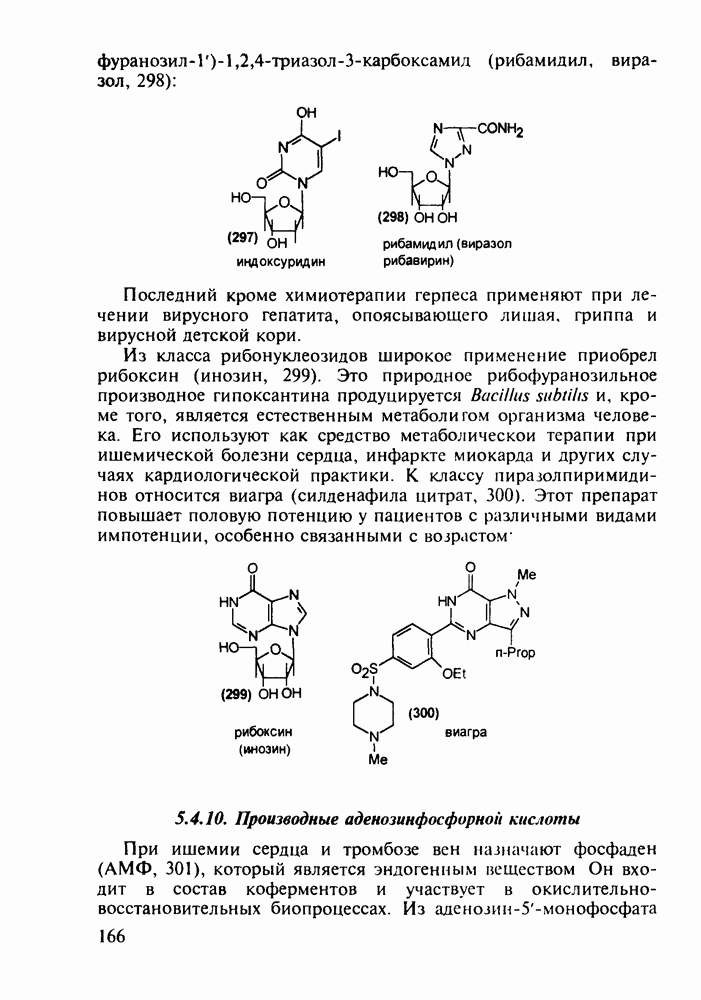
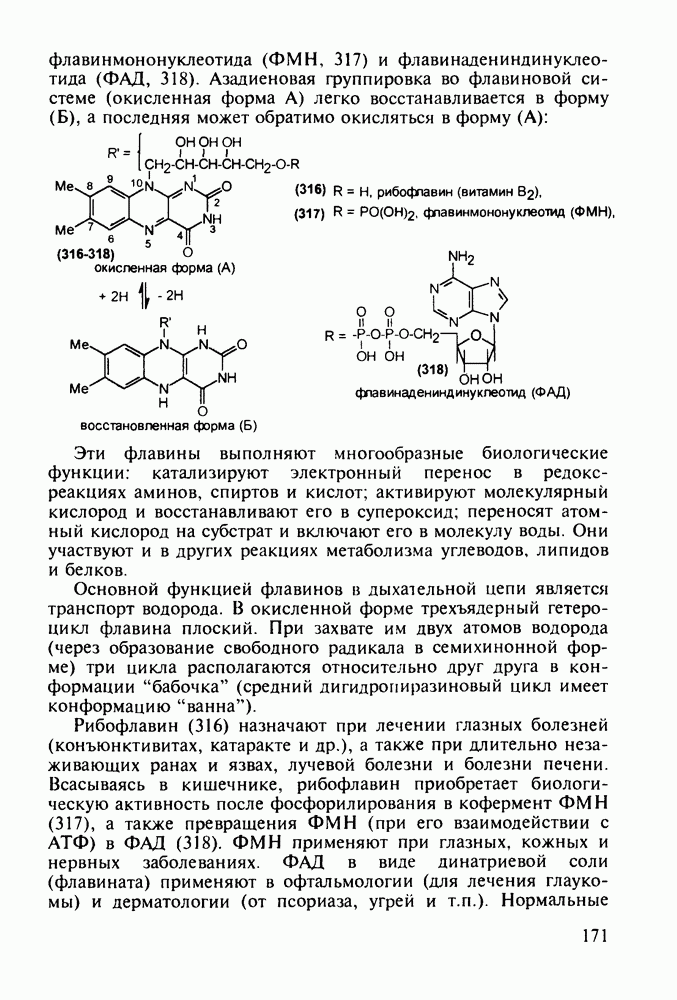
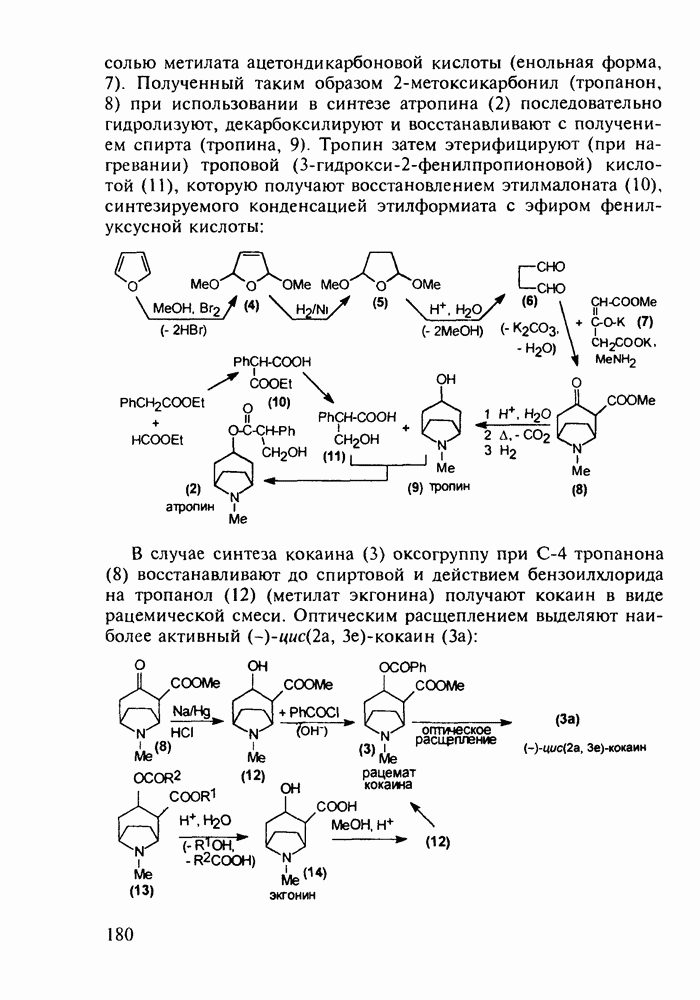
о-Гидроксибензойная (салициловая) кислота (3) является природным веществом, содержащимся в виде эфира уксусной кислоты (4) -  -ацетилсалициловой кислоты в цветах растений вида спиреи (spiraea ulmaria). Этот эфир (4) был введен в медицинскую практику лечения острого суставного ревматизма еще в 1874 г., а как синтетическое лекарственное вещество стал выпускаться в промышленных масштабах в конце прошлого века под названием аспирин (приставка
-ацетилсалициловой кислоты в цветах растений вида спиреи (spiraea ulmaria). Этот эфир (4) был введен в медицинскую практику лечения острого суставного ревматизма еще в 1874 г., а как синтетическое лекарственное вещество стал выпускаться в промышленных масштабах в конце прошлого века под названием аспирин (приставка  означала, что данное лекарственное вещество не добывается из спиреи, а делается химическим путем). Аспирин называют лекарством 20-го столетия, и в настоящее время его производят в мире в количестве, превышающем
означала, что данное лекарственное вещество не добывается из спиреи, а делается химическим путем). Аспирин называют лекарством 20-го столетия, и в настоящее время его производят в мире в количестве, превышающем
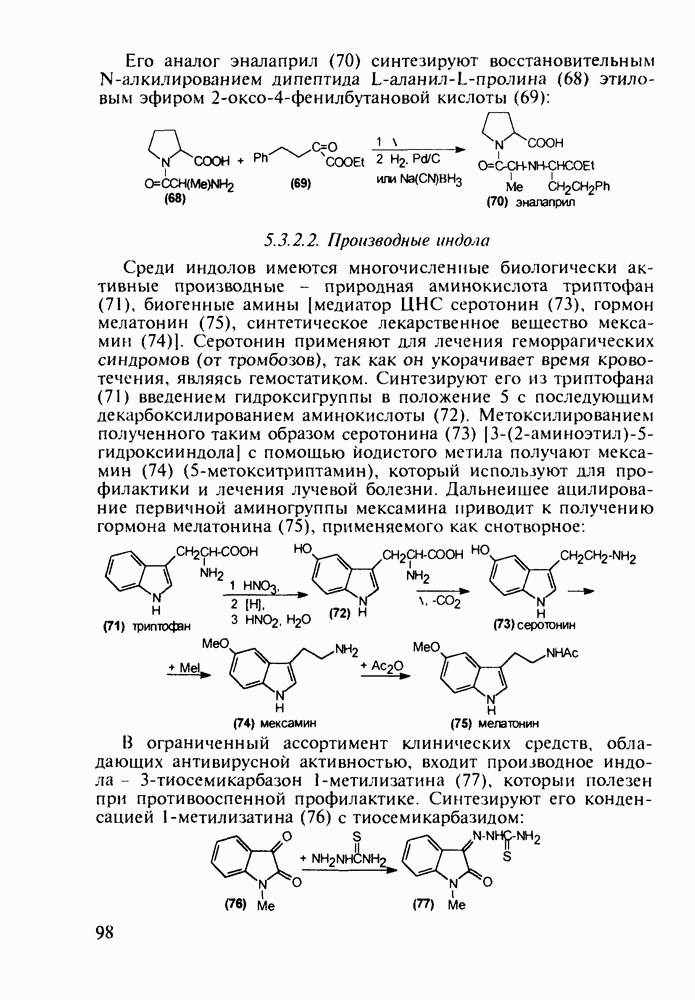
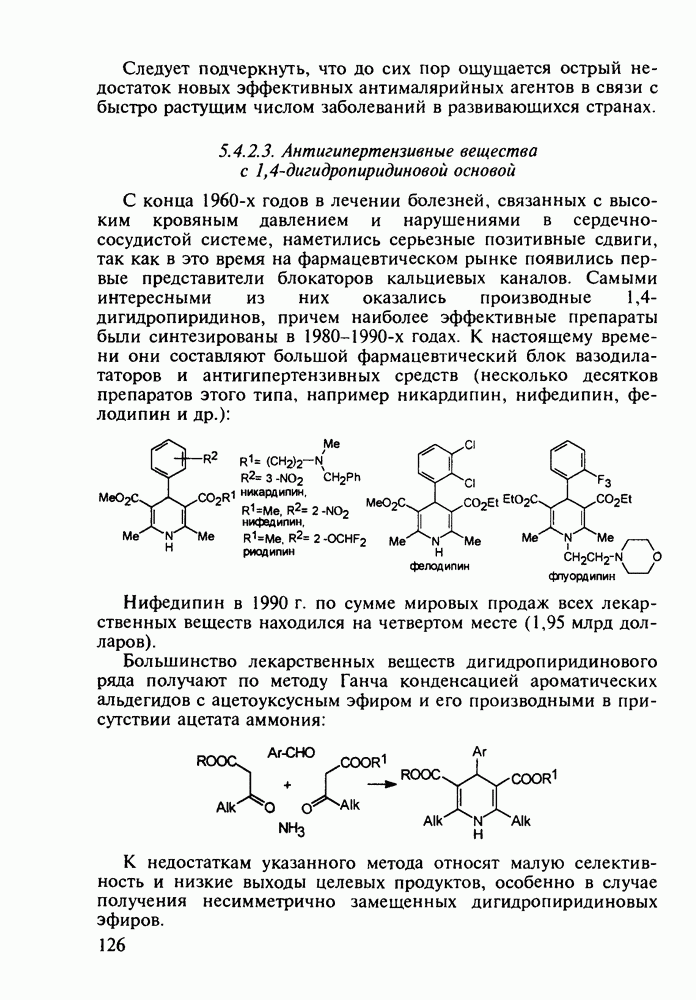
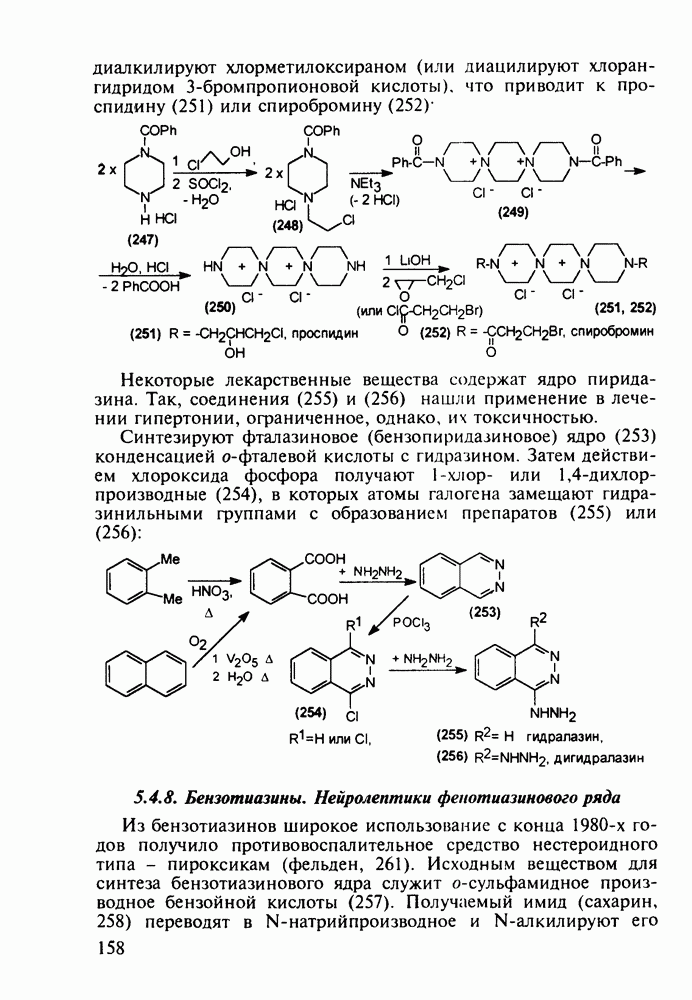
100 тыс. т в год. Известны его противовоспалительные, жаропонижающие и болеутоляющие свойства. Обнаружено также, что он препятствует образованию тромбов, оказывает сосудорасширяющее действие и начинает применяться даже для профилактики и лечения инфарктов и инсультов. Считают, что весь потенциал лечебных свойств этого вещества еще не исчерпан. В то же время аспирин раздражает слизистую оболочку желудочно-кишечного тракта, что может вызывать кровотечения. Возможны также аллергические реакции. Аспирин в организме влияет на синтез простагландинов (контролирующих, в частности, образование тромбов) и гормона гистамина (расширяющего сосуды и вызывающего приток иммунных клеток к месту воспаления; кроме того, он может препятствовать при воспалительных процессах биосинтезу болевых веществ).
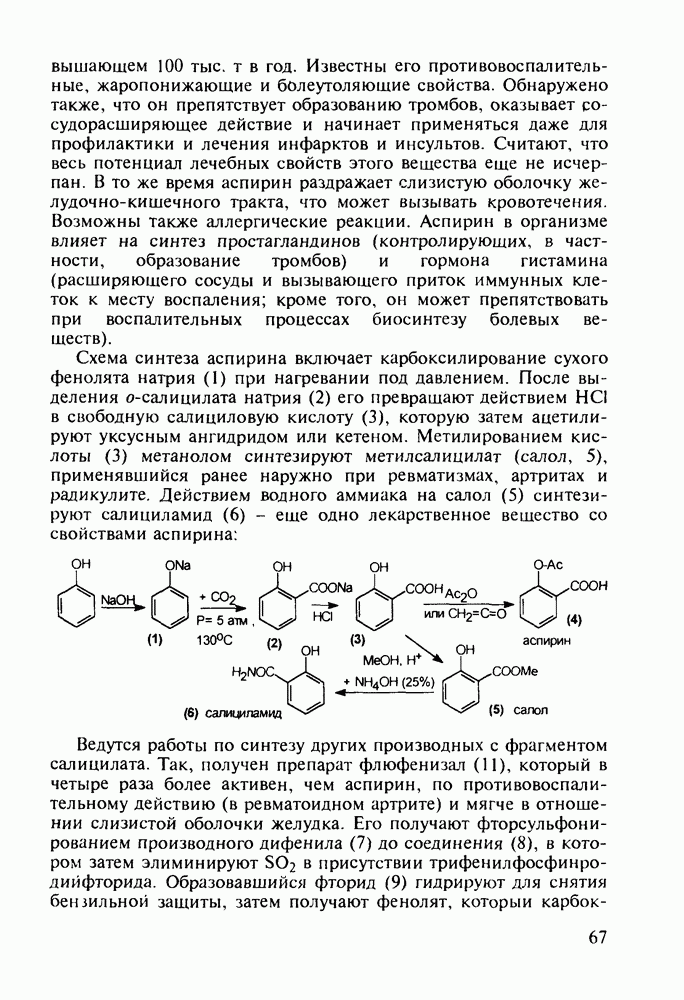
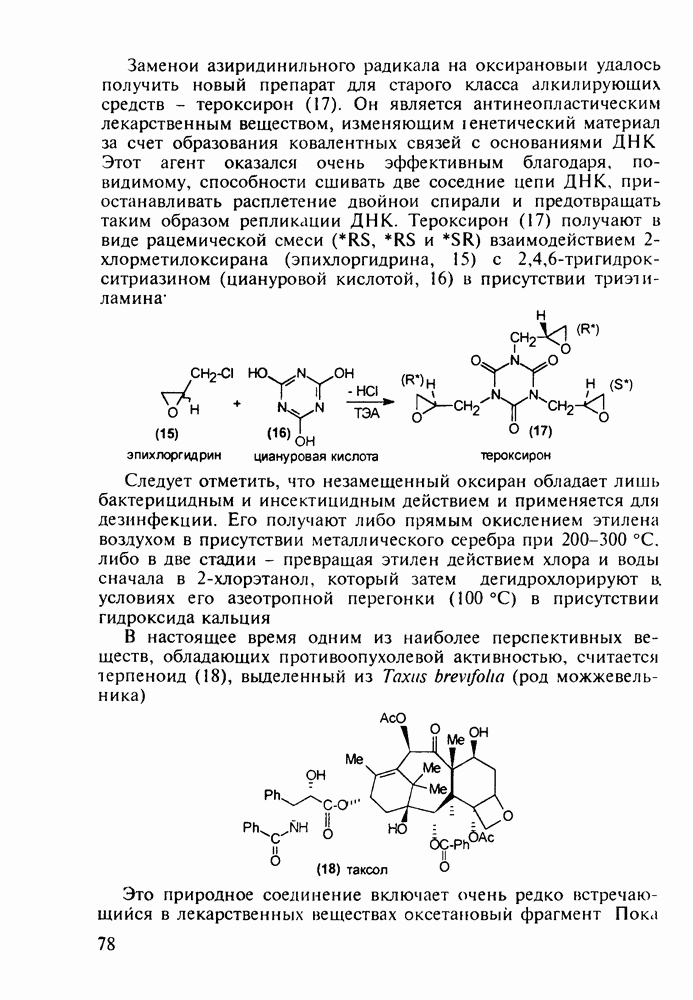
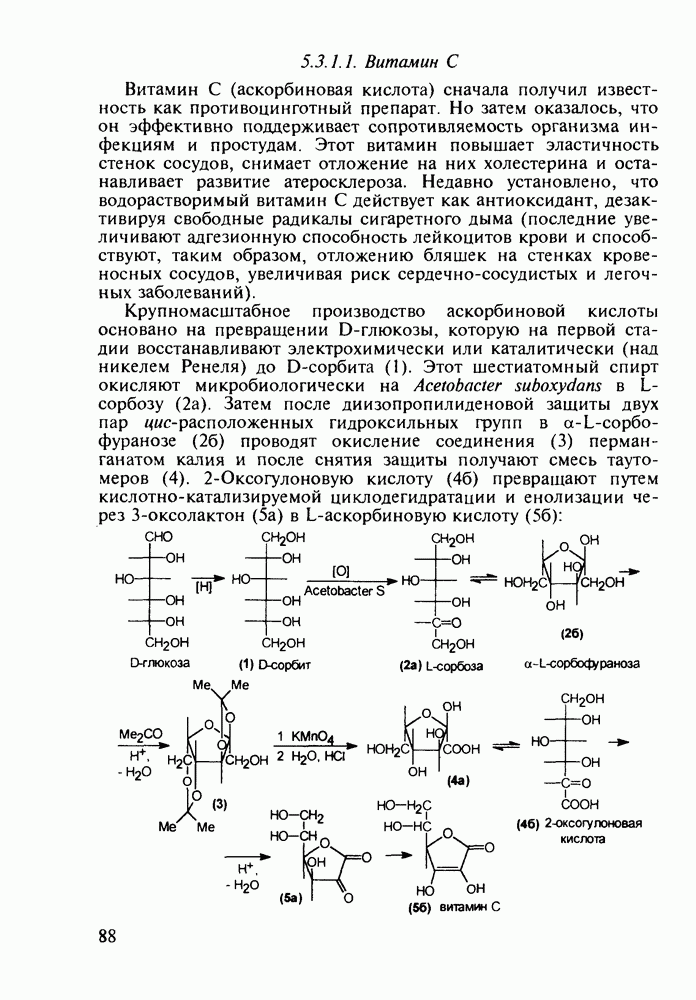
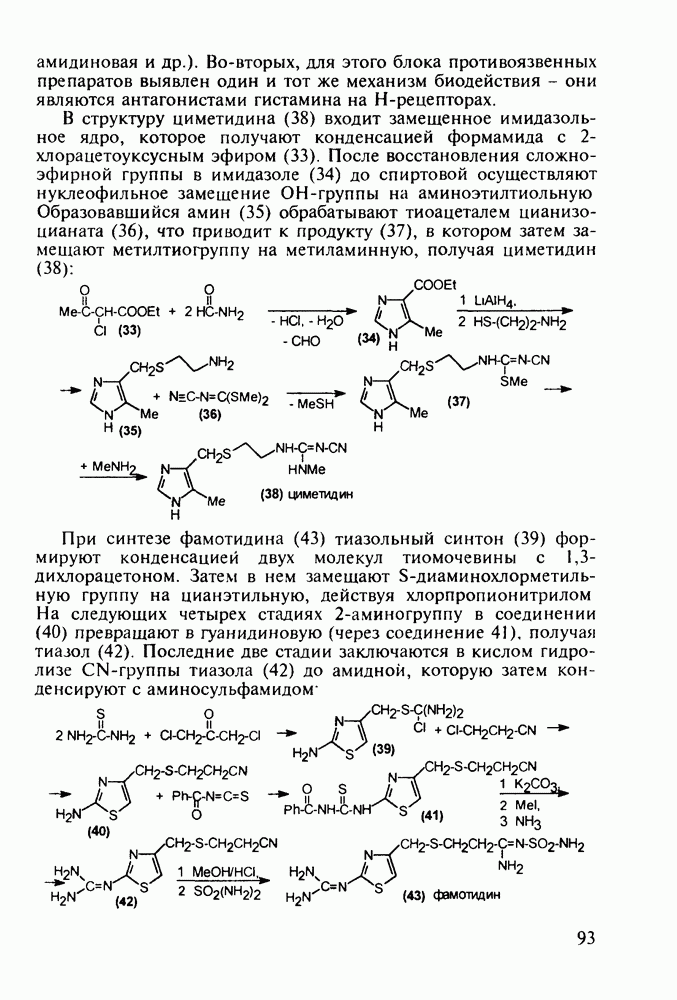
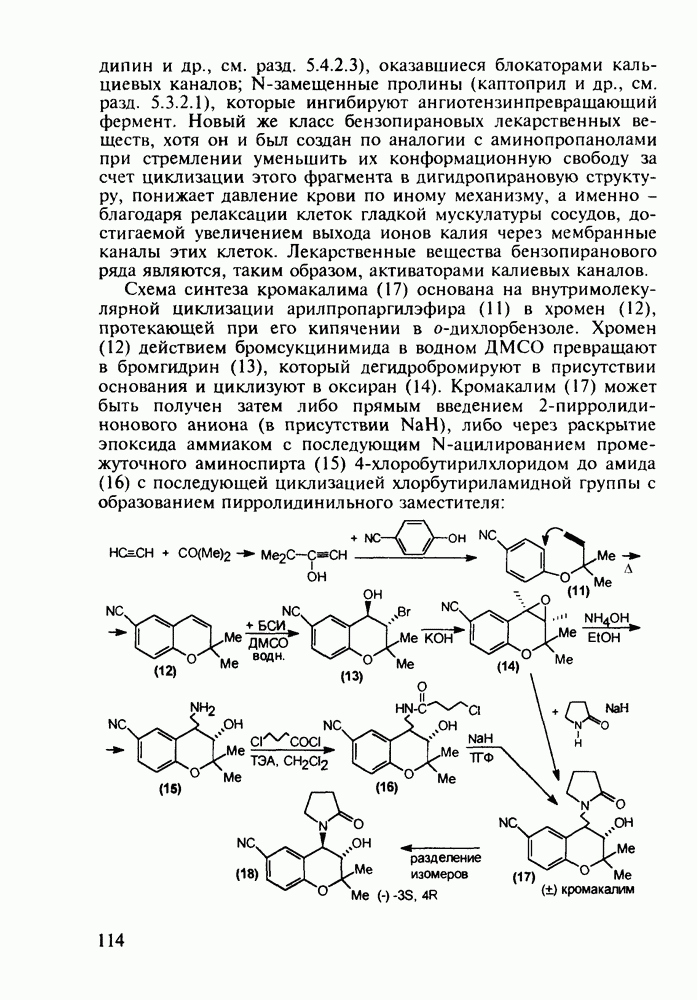
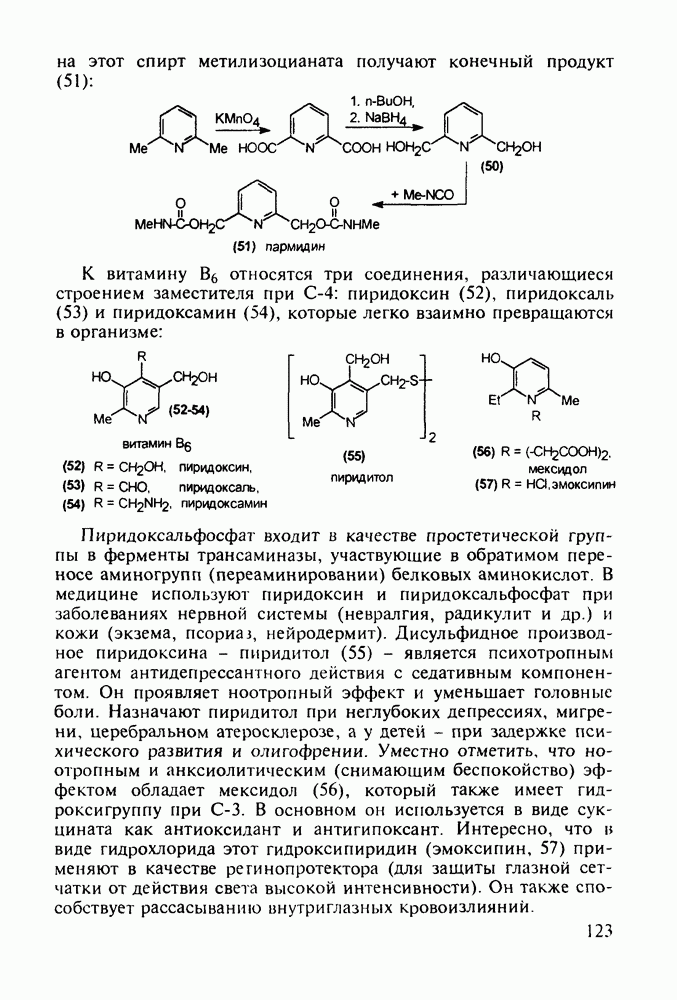
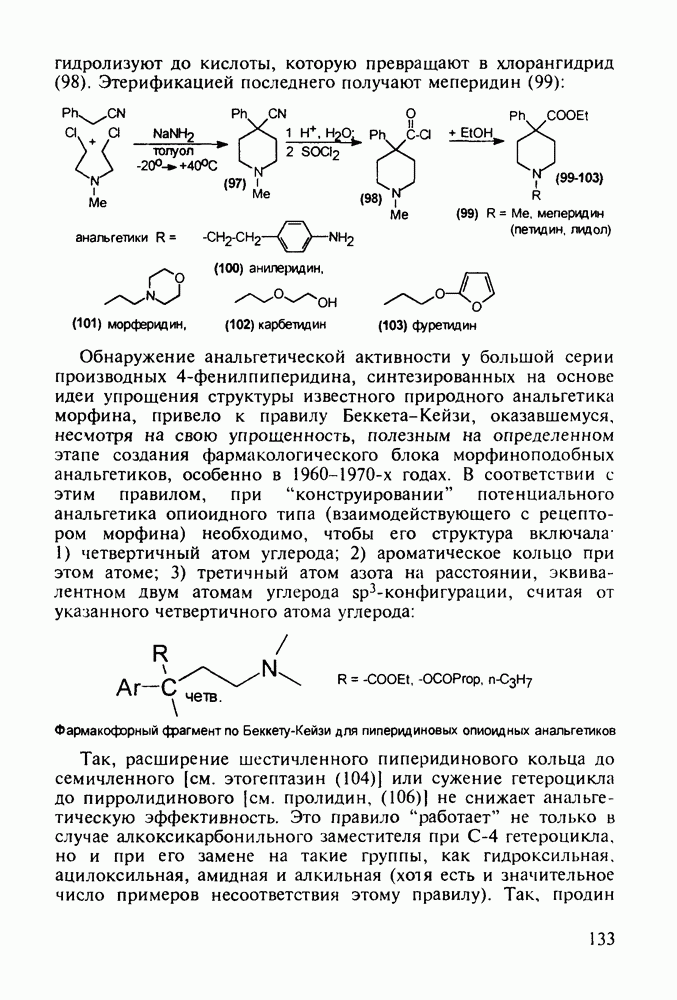
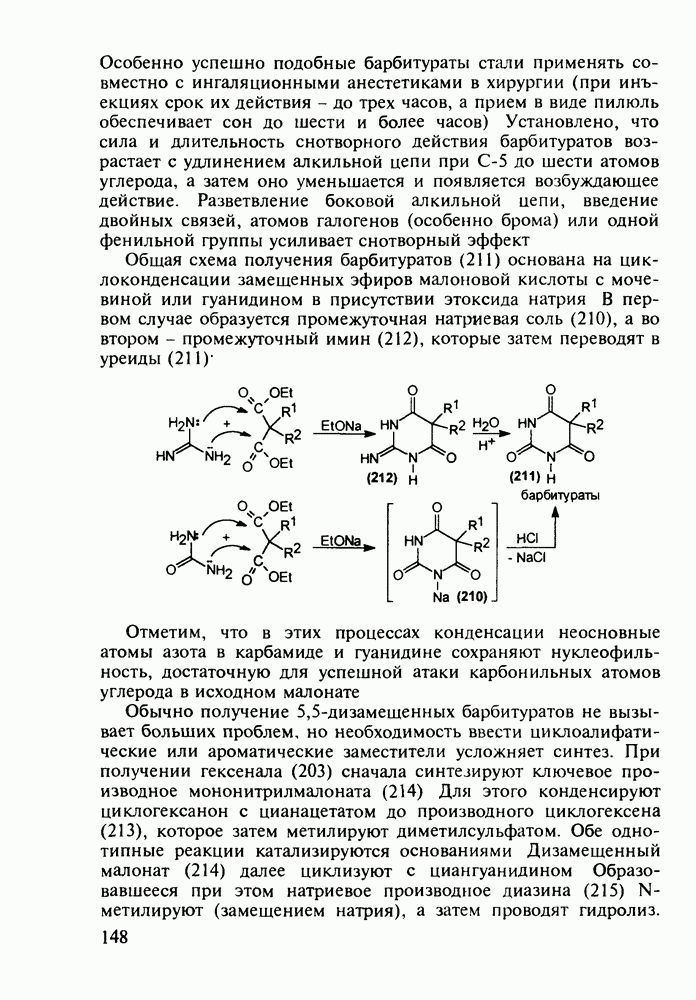
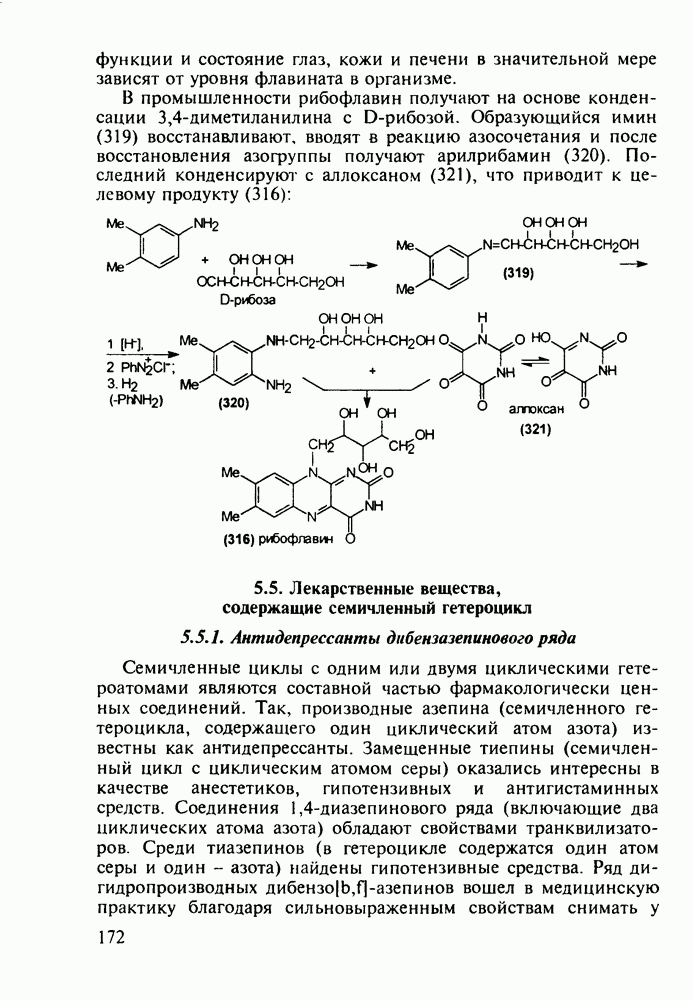
Схема синтеза аспирина включает карбоксилирование сухого фенолята натрия (1) при нагревании под давлением. После выделения  -салицилата натрия (2) его превращают действием
-салицилата натрия (2) его превращают действием  в свободную салициловую кислоту (3), которую затем ацетилируют уксусным ангидридом или кетеном. Метилированием кислоты (3) метанолом синтезируют метилсалицилат (салол, 5), применявшийся ранее наружно при ревматизмах, артритах и радикулите. Действием водного аммиака на салол (5) синтезируют салициламид (6) - еще одно лекарственное вещество со свойствами аспирина:
в свободную салициловую кислоту (3), которую затем ацетилируют уксусным ангидридом или кетеном. Метилированием кислоты (3) метанолом синтезируют метилсалицилат (салол, 5), применявшийся ранее наружно при ревматизмах, артритах и радикулите. Действием водного аммиака на салол (5) синтезируют салициламид (6) - еще одно лекарственное вещество со свойствами аспирина:

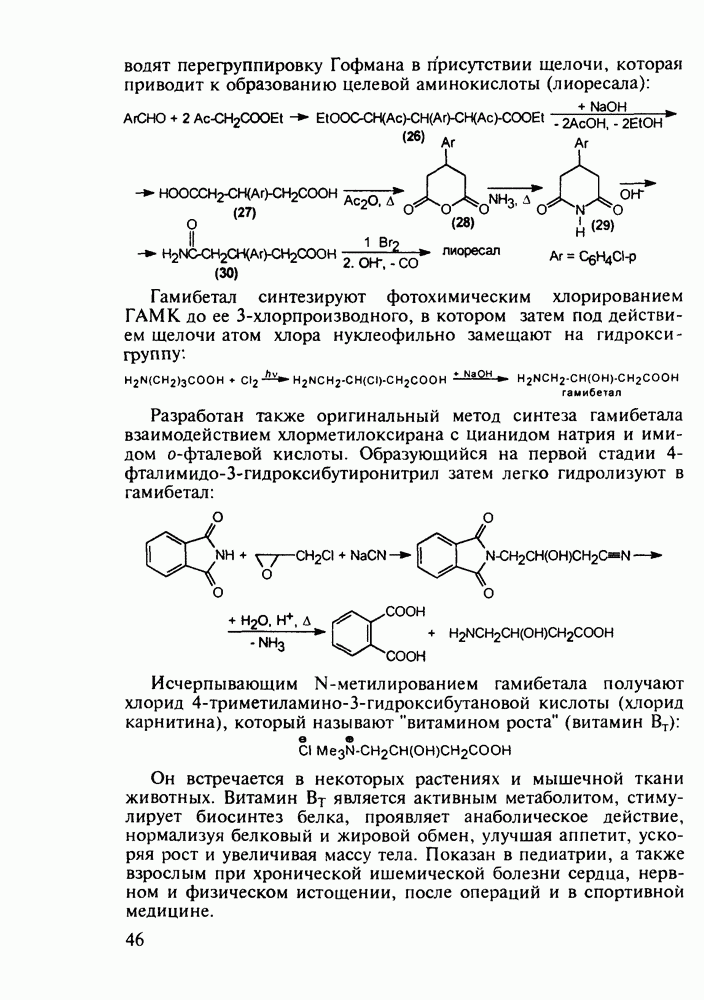
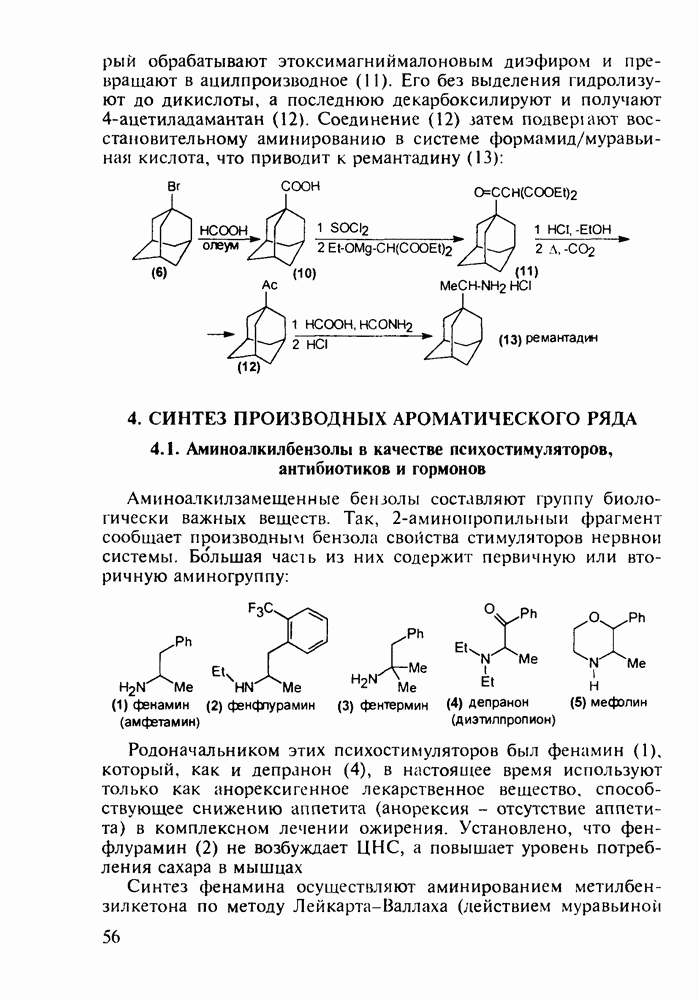
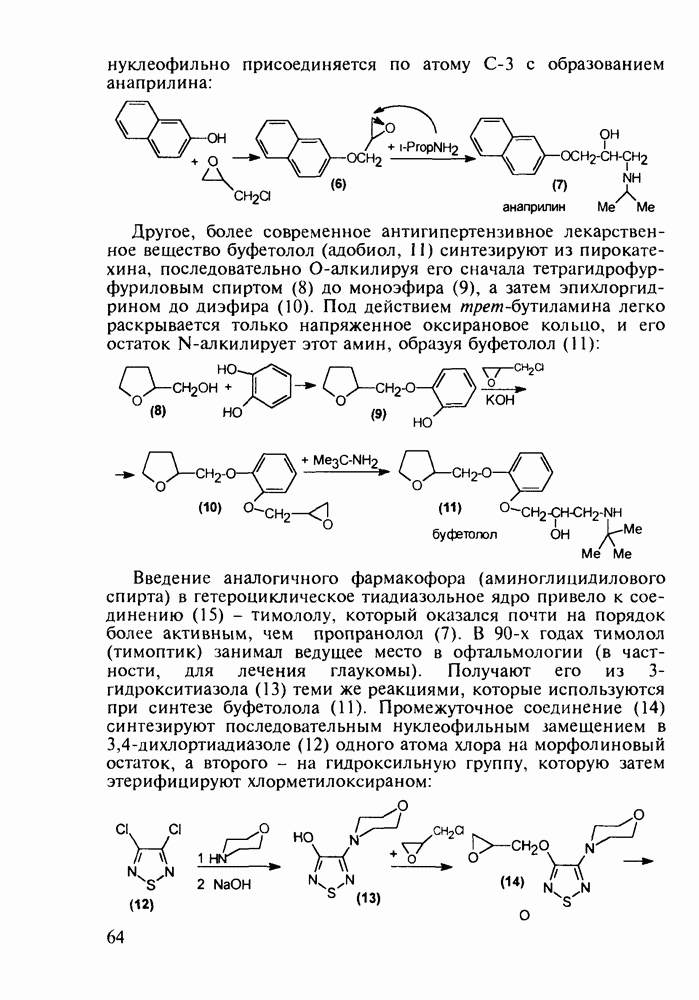
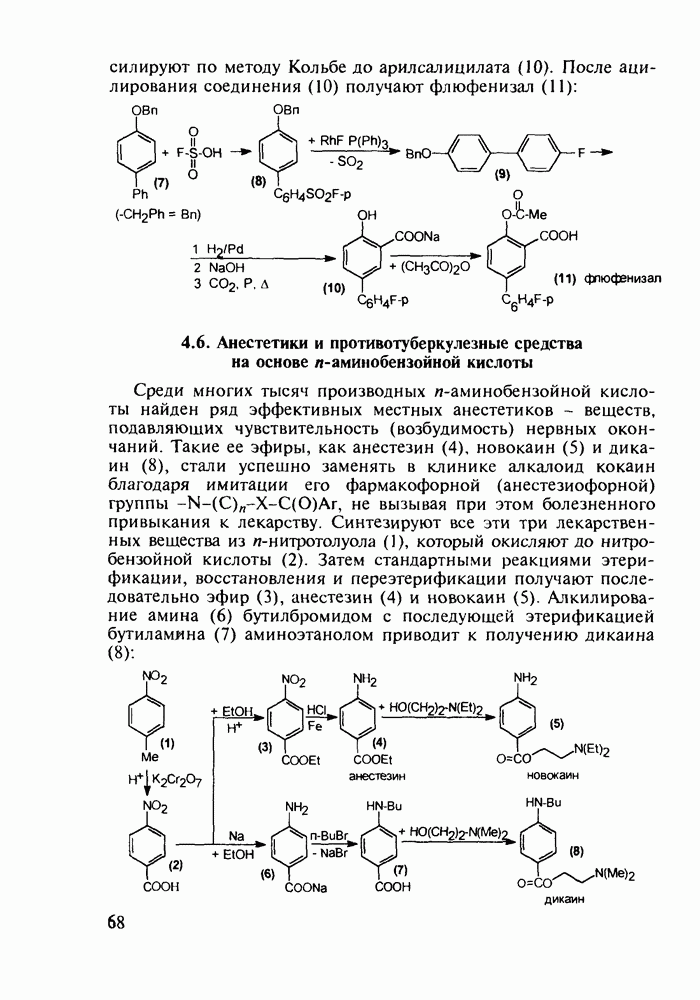
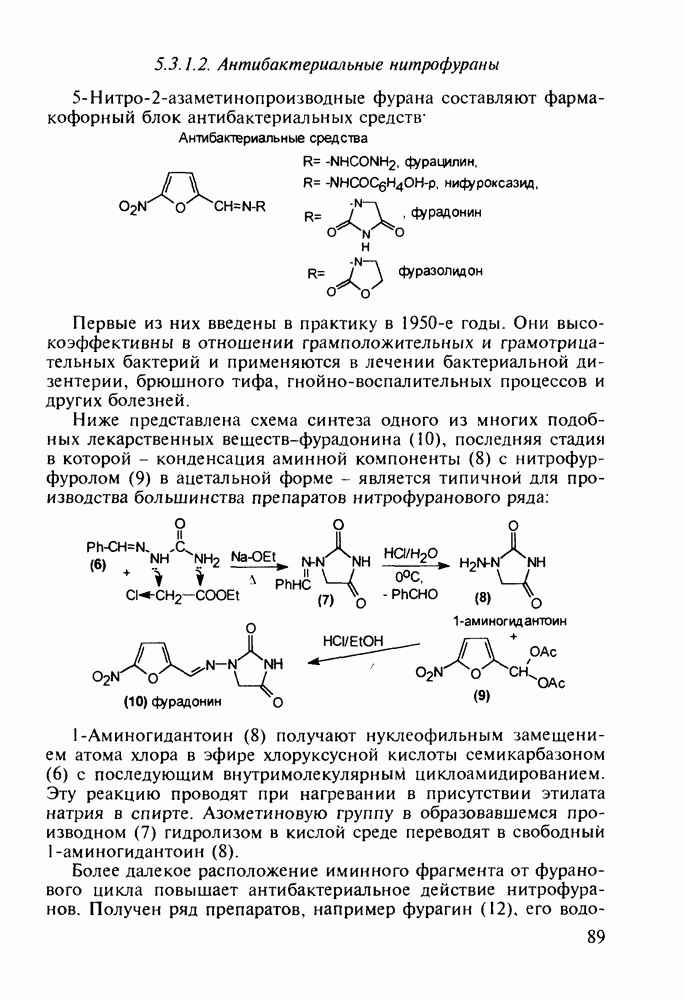
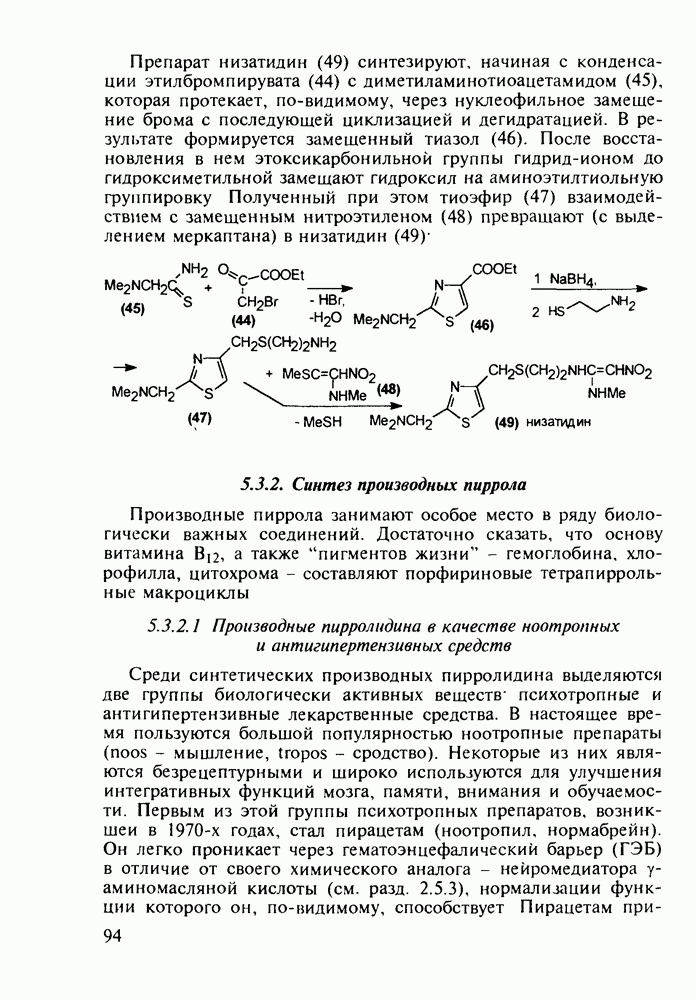
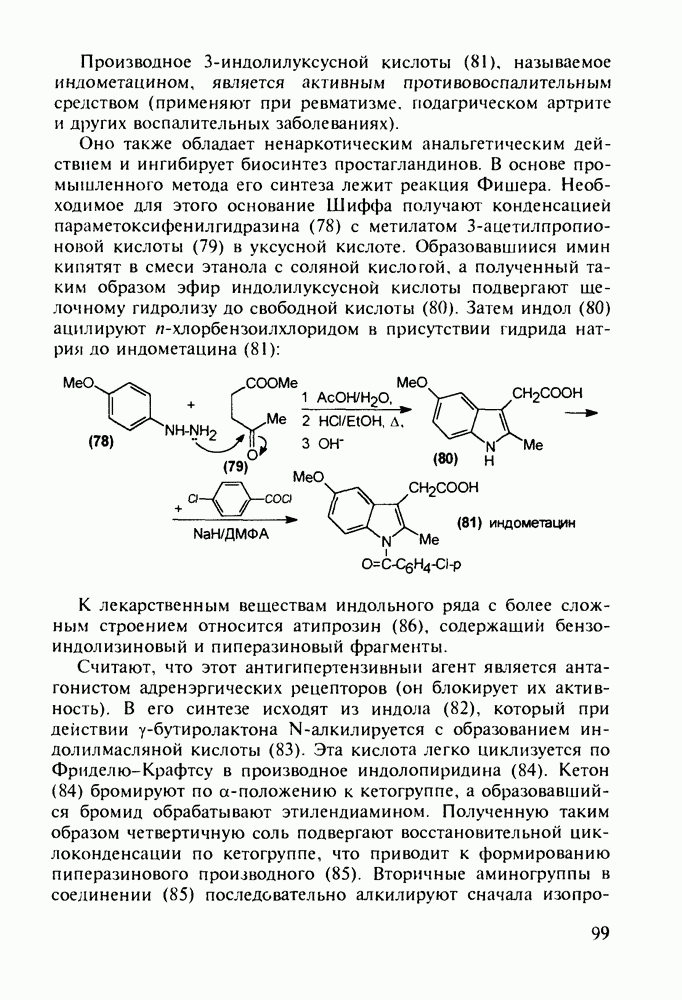
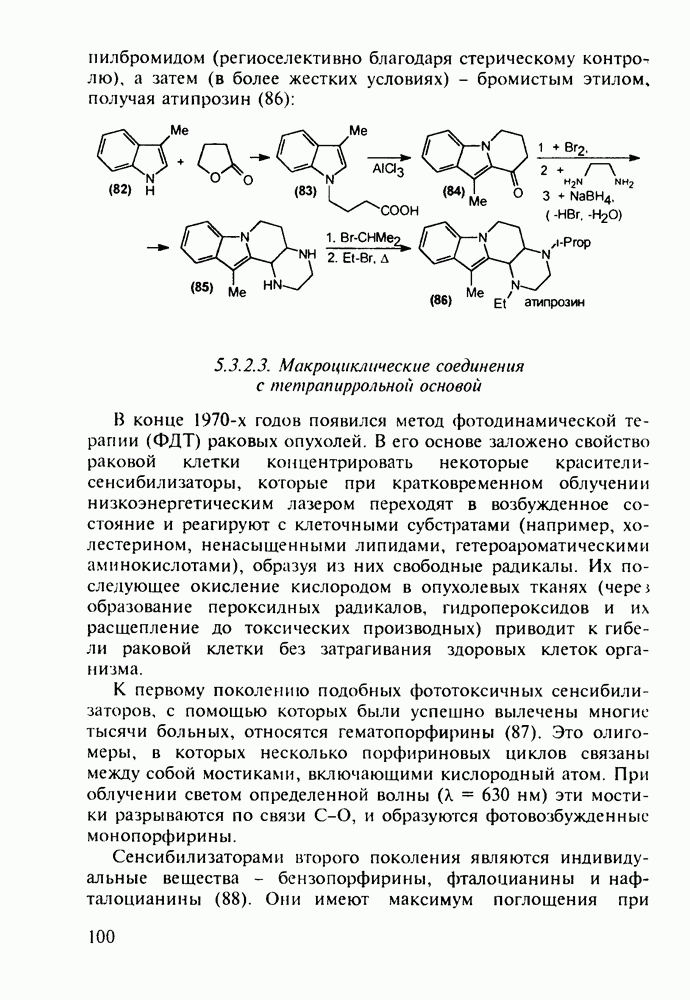
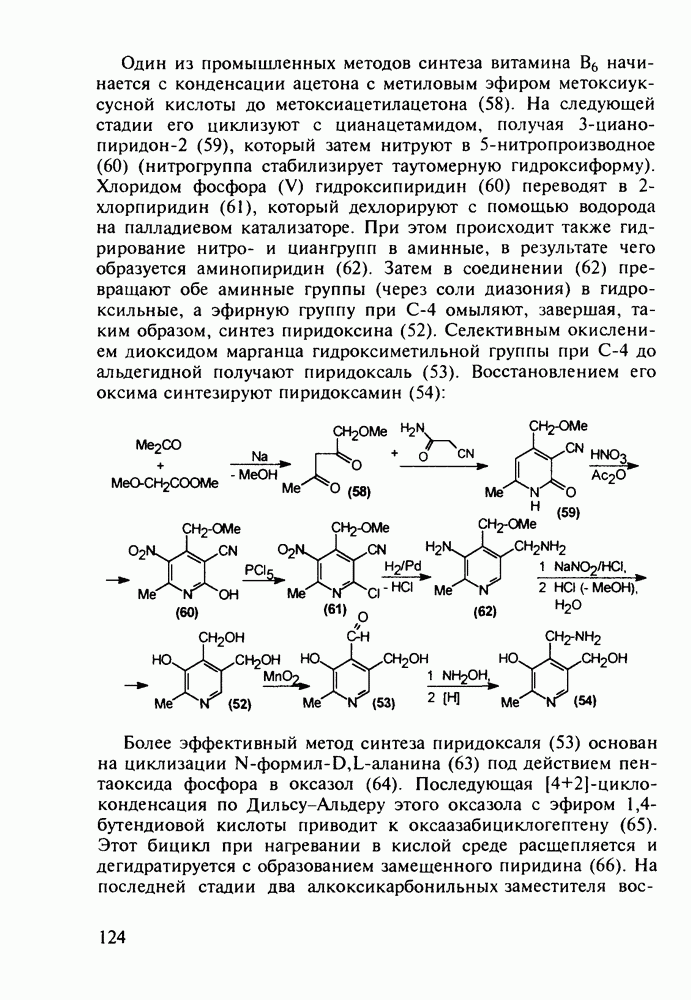
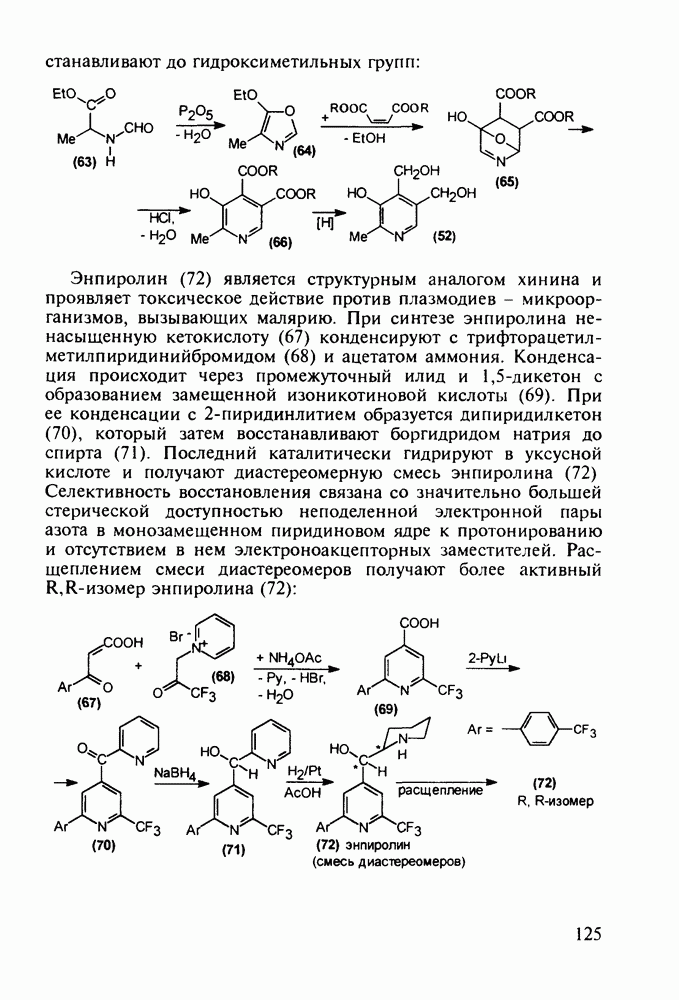
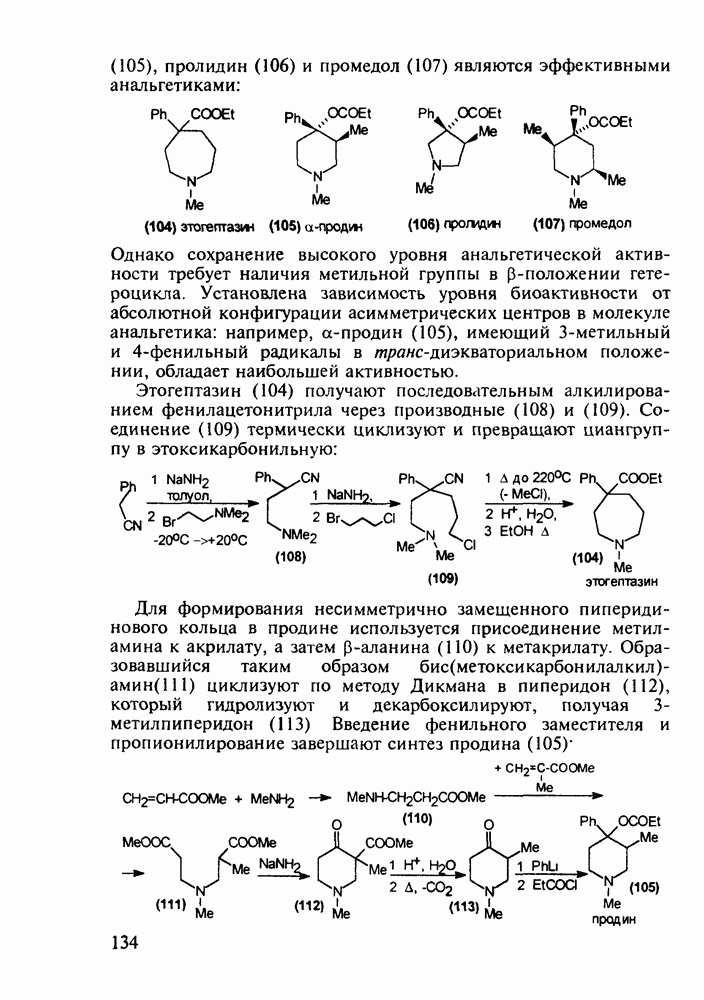
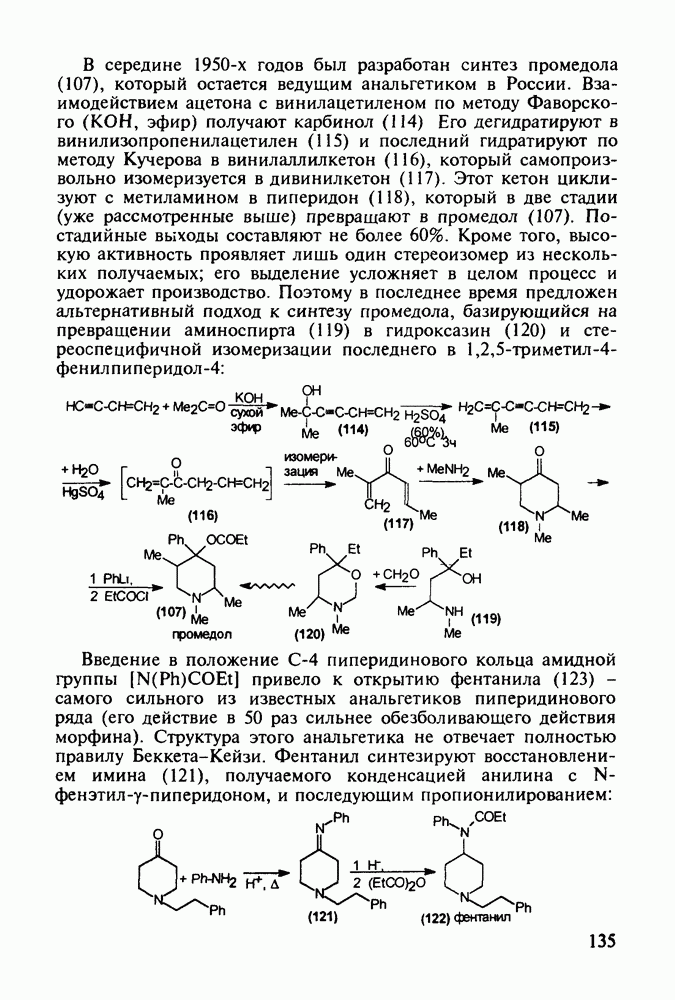
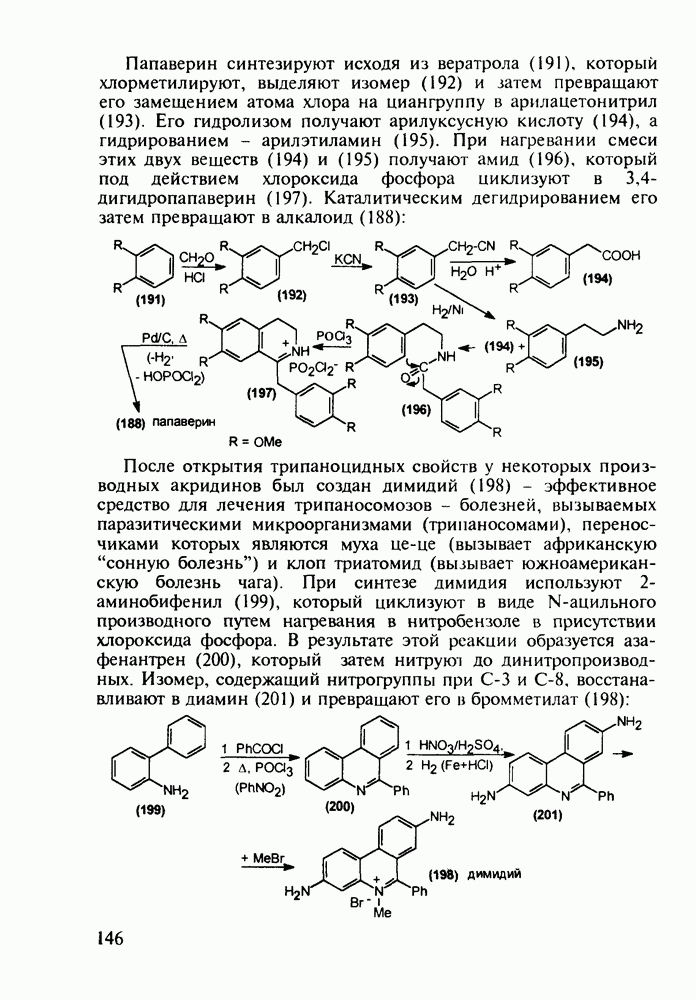
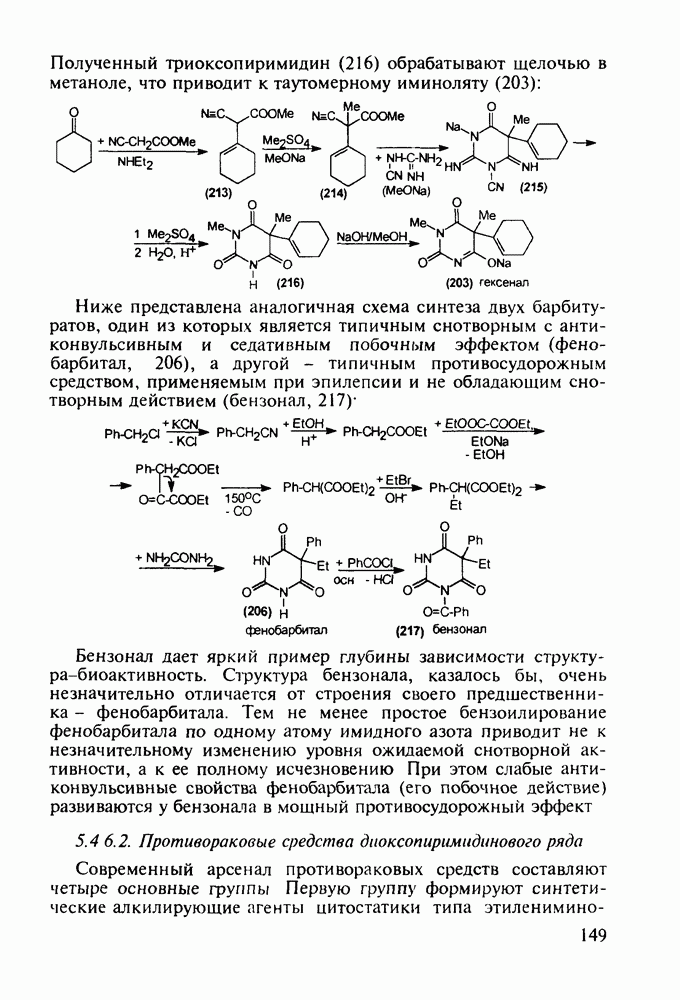
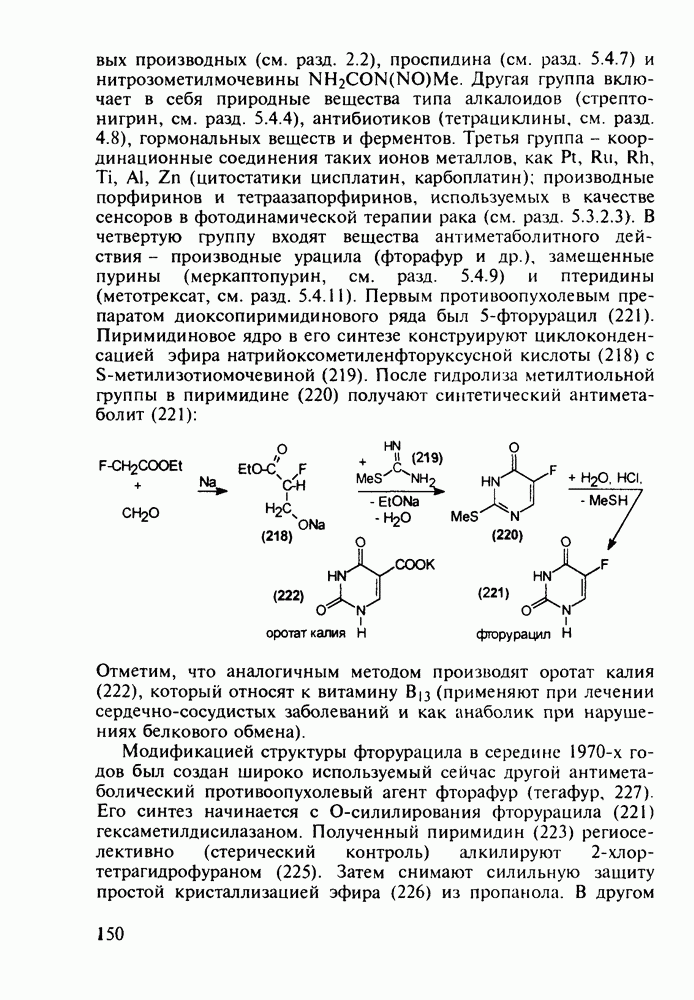
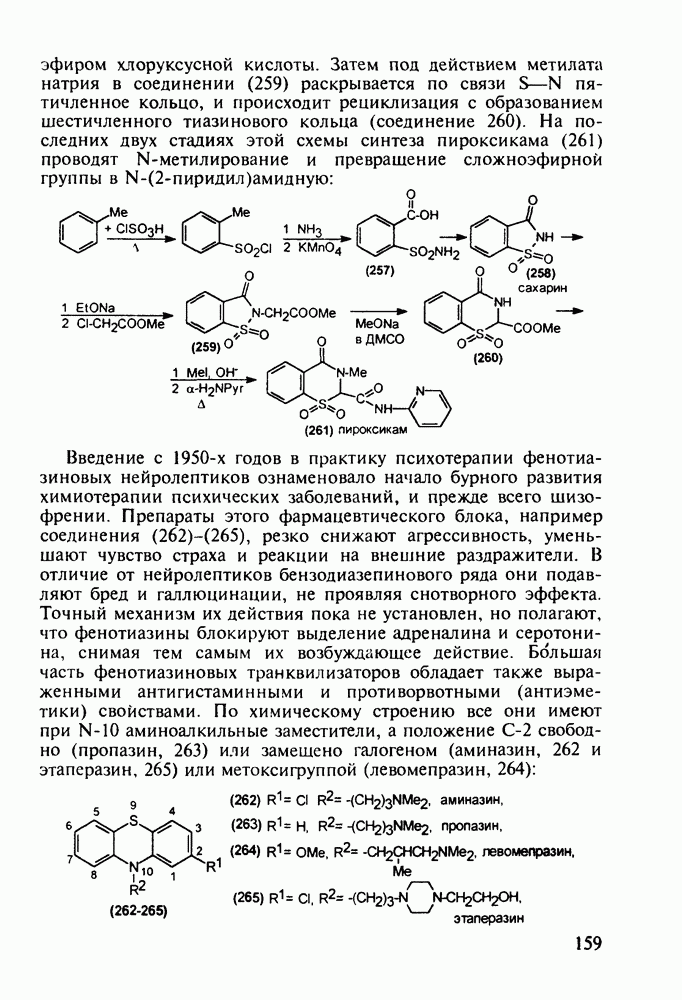
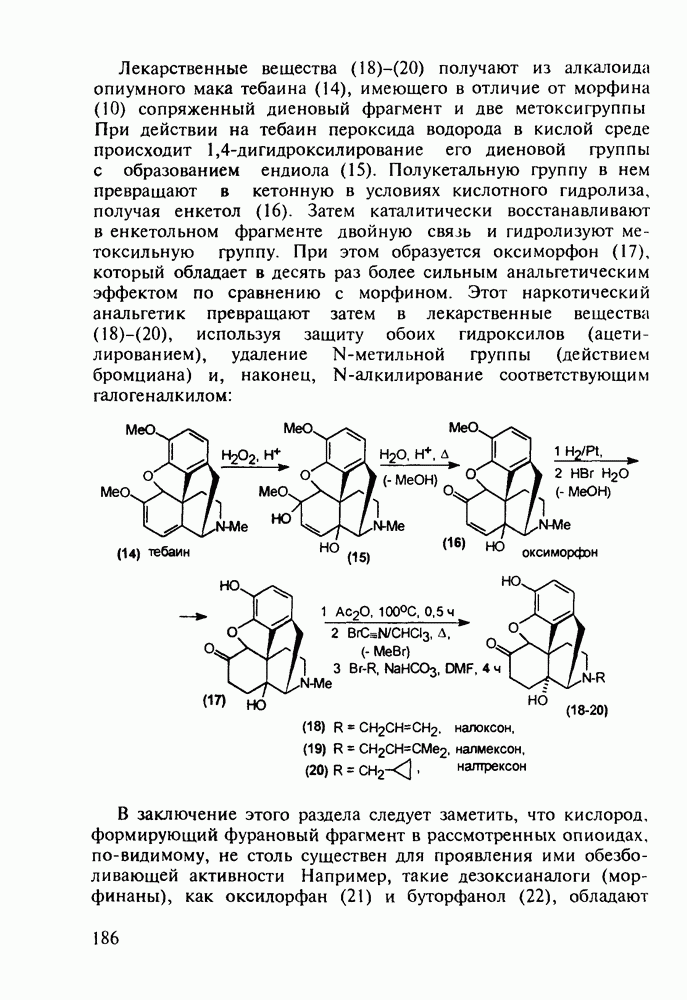
Ведутся работы по синтезу других производных с фрагментом салицилата. Так, получен препарат флюфенизал (11), который в четыре раза более активен, чем аспирин, по противовоспалительному действию (в ревматоидном артрите) и мягче в отношении слизистой оболочки желудка. Его получают фторсульфонированием производного дифенила (7) до соединения (8), в котором затем элиминируют  в присутствии трифенилфосфинродинфторида. Образовавшийся фторид (9) гидрируют для снятия бензильной защиты, затем получают фенолят, который карбоксилируют
в присутствии трифенилфосфинродинфторида. Образовавшийся фторид (9) гидрируют для снятия бензильной защиты, затем получают фенолят, который карбоксилируют
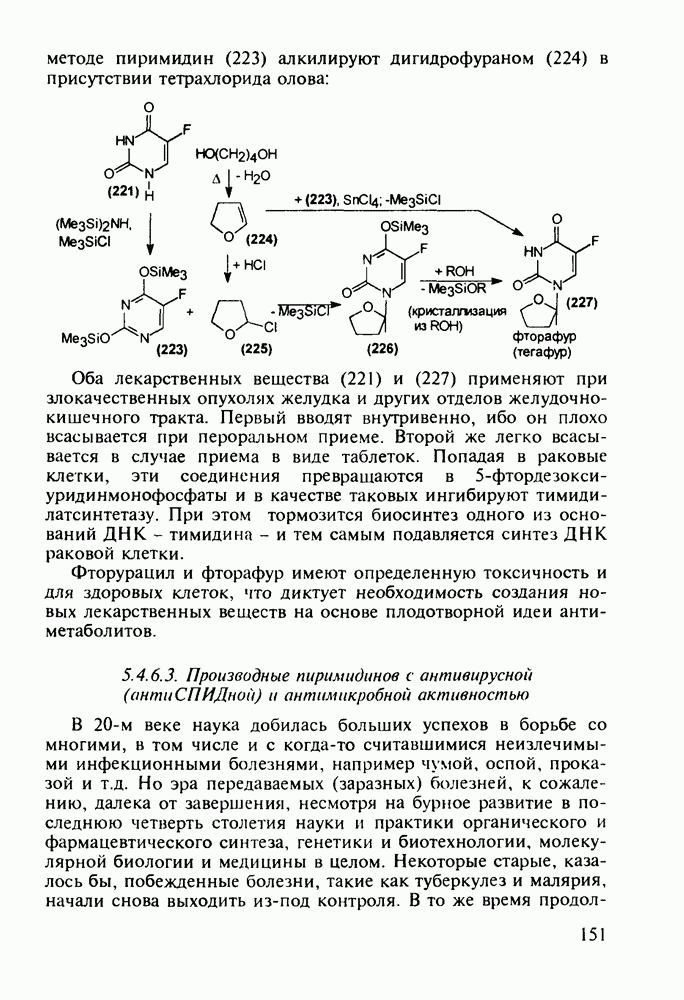
по методу Кольбе до арилсалицилата (10). После ацилирования соединения (10) получают флюфенизал (11):

| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- Предисловие
- 1. ВВЕДЕНИЕ
- 1.1. Эволюция органической химии лекарственных веществ
- 1.2. Современные требования к лекарственным веществам
- 1.3. Стадии биологического изучения лекарственного вещества
- 1.4. Основы стратегии создания новых синтетических лекарственных веществ
- 1.5. Связь структура-биологическая активность
- 1.6. Принципиальная схема разработки нового лекарственного вещества
- 1.7. Классификация лекарственных веществ
- 1.8. Основные болезни человека и ведущие группы лекарственных веществ на современном фармацевтическом рынке
- 2. СИНТЕЗ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ АЛИФАТИЧЕСКОГО РЯДА
- 2.2. Группа противораковых веществ с дихлордиэтиламинным фармакофором
- 2.3. Алканолы, аминоалканолы и их эфиры. Нейромедиатор ацетилхолин и холиномиметики
- 2.4. Альдегиды и кислоты. Витамины F и B15
- 2.5. Аминокислоты
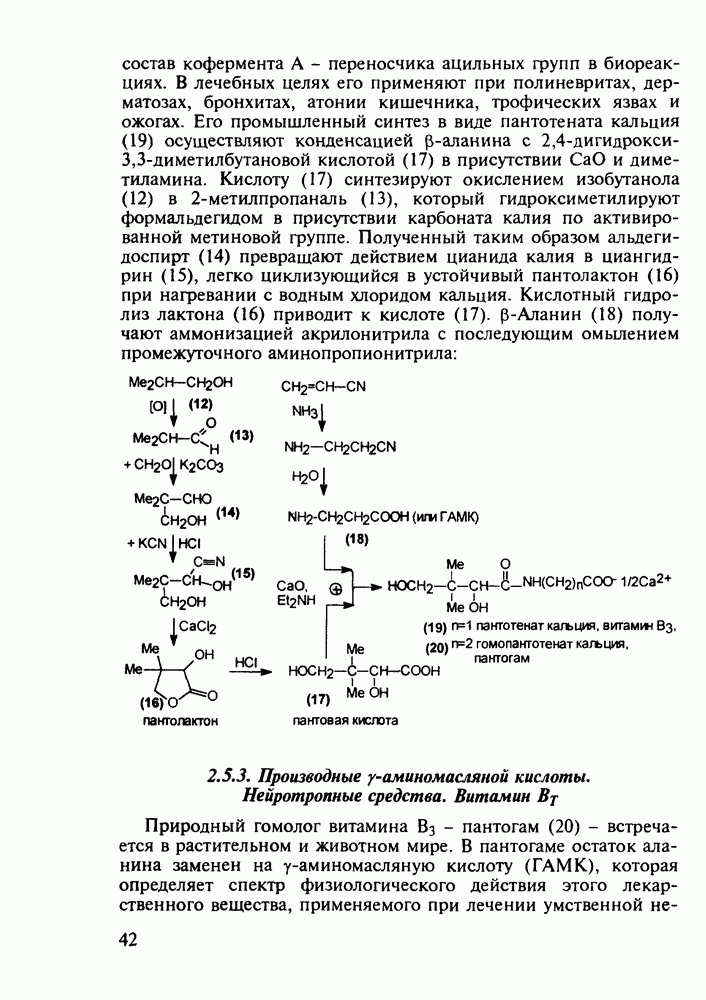
- 2.5.2. Производные b-аминокислот. Витамин B3
- 2.5.3. Производные у-аминомасляной кислоты. Нейротропные средства. Витамин BT
- 2.5.4. Другие аминокислоты
- 3. ЛЕКАРСТВЕННЫЕ ВЕЩЕСТВА АЛИЦИКЛИЧЕСКОГО РЯДА
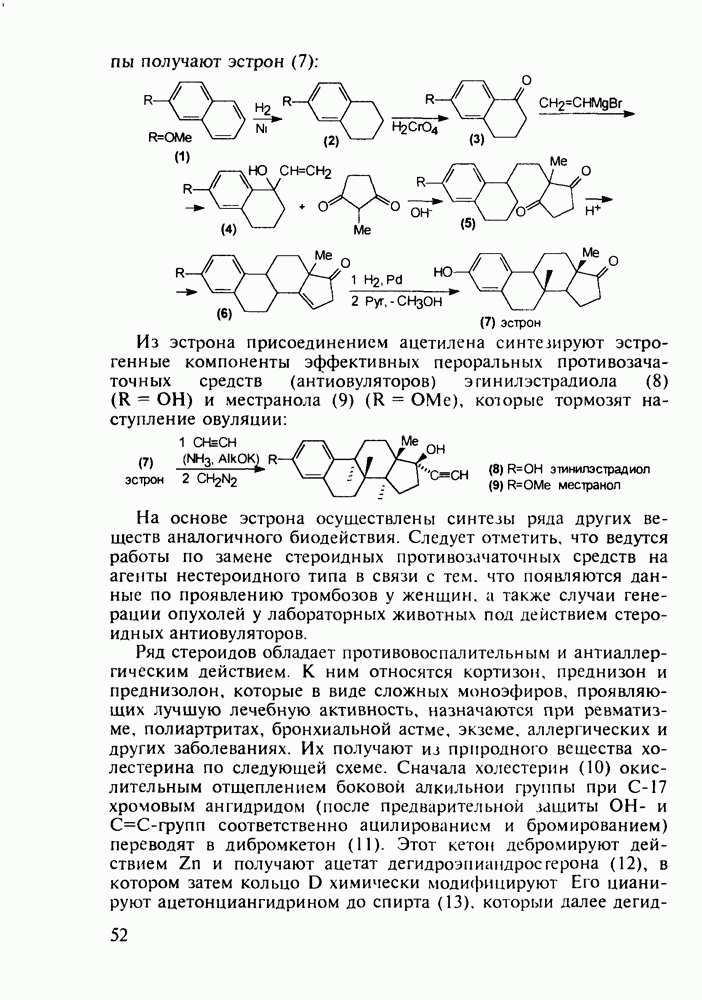
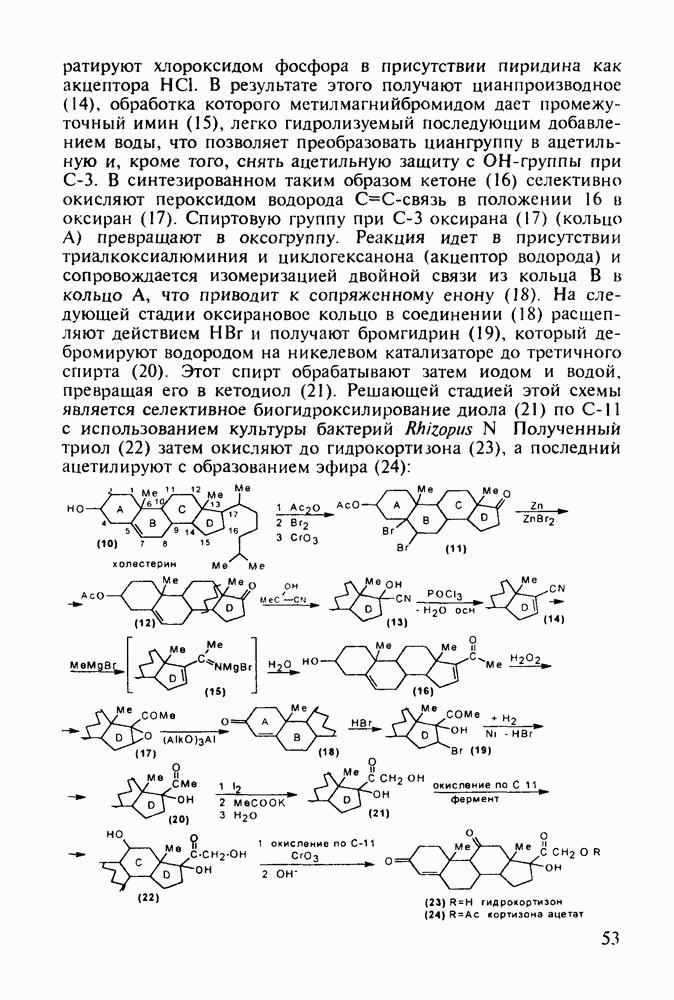
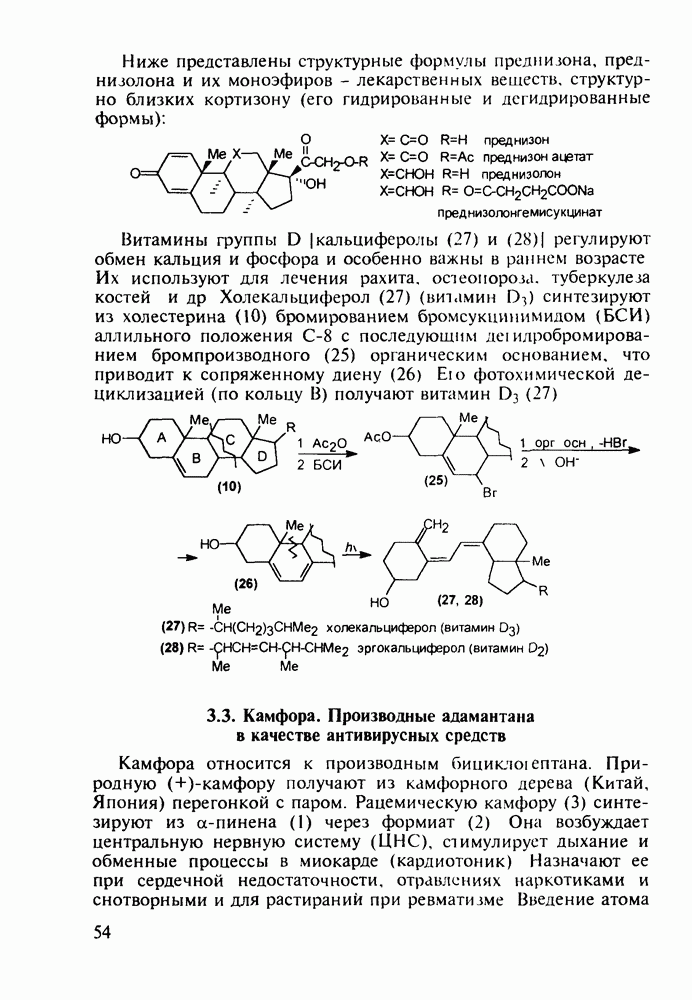
- 3.2. Противозачаточные и противовоспалительные вещества на основе циклопентафенантрена. Синтез витамина D
- 3.3. Камфора. Производные адамантана в качестве антивирусных средств
- 4. СИНТЕЗ ПРОИЗВОДНЫХ АРОМАТИЧЕСКОГО РЯДА
- 4.2. Антигистаминные препараты группы диарилметана
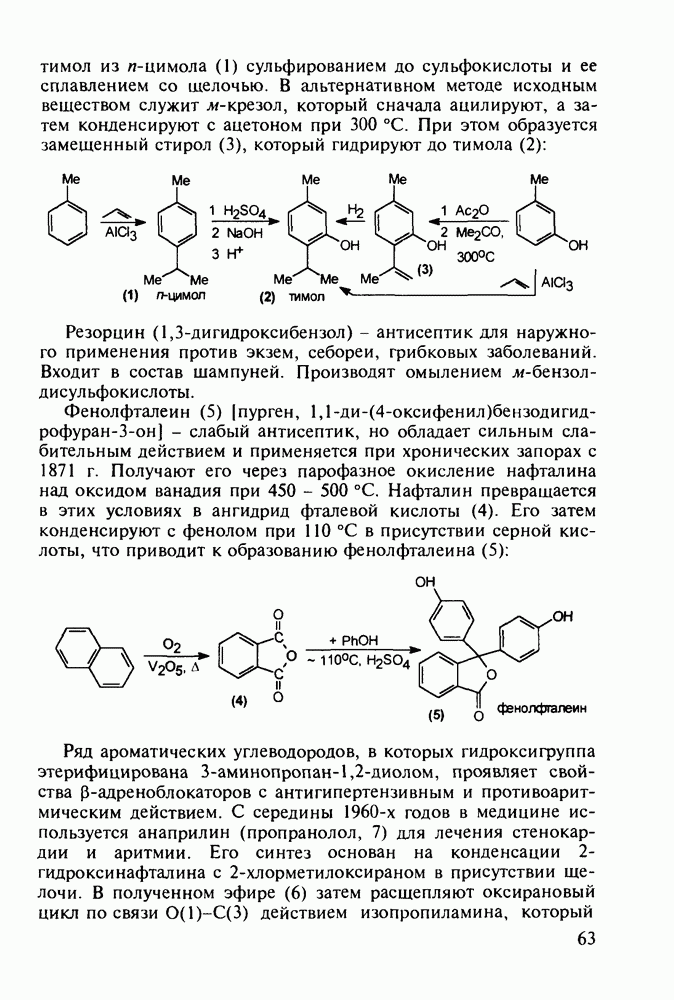
- 4.3. Антисептики и адреноблокаторы фенольного ряда
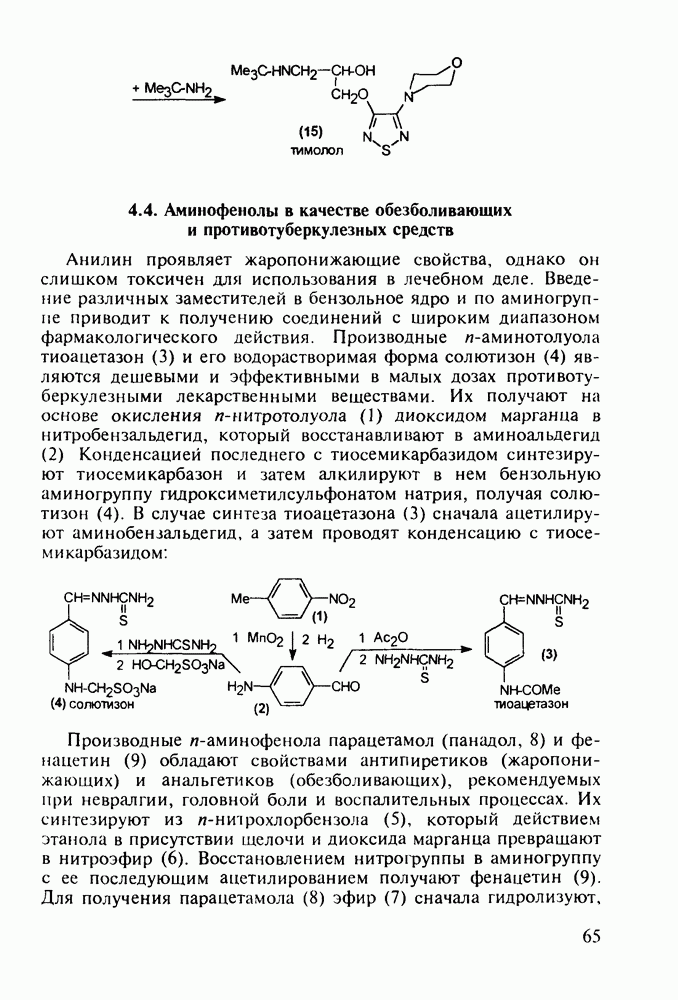
- 4.4. Аминофенолы в качестве обезболивающих и противотуберкулезных средств
- 4.5. Производные о-гидроксибензойной кислоты. Аспирин
- 4.6. Анестетики и противотуберкулезные средства на основе n-аминобензойной кислоты
- 4.7. Производные n-аминобензолсульфокислоты с антибактериальным и диуретическим действием
- 4.8. Оксопроизводные нафталина. Витамин К1. Оксолин
- 5. ХИМИЯ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ С БАЗОВЫМ ГЕТЕРОЦИКЛИЧЕСКИМ ФРАГМЕНТОМ
- 5.2. Антибиотики, содержащие четырехчленное азетидиновое ядро
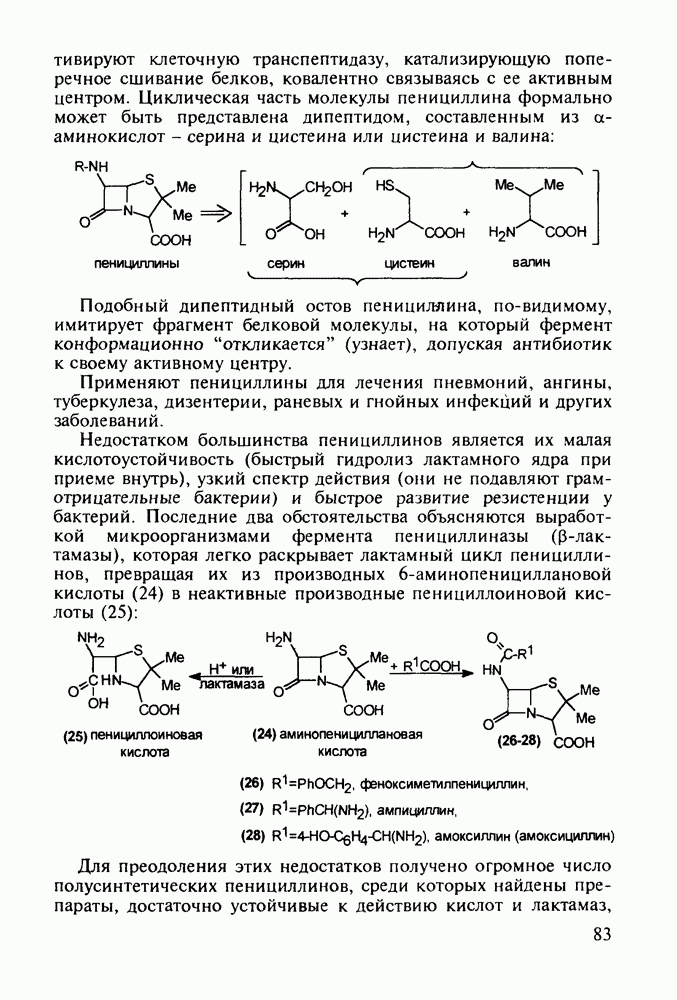
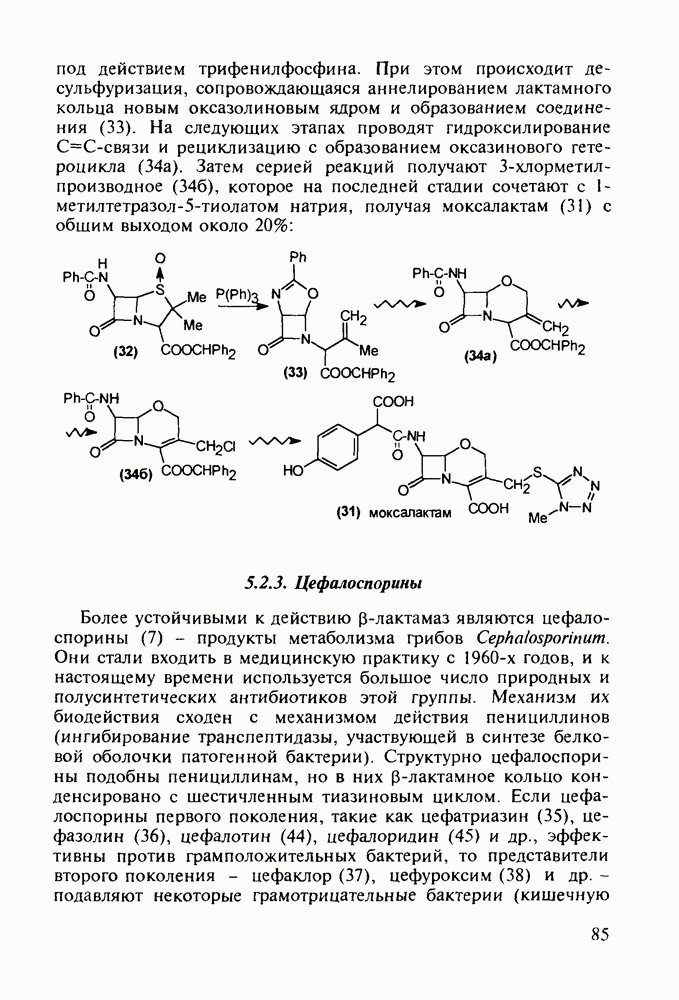
- 5.2.2. Пенициллины. Моксалактам
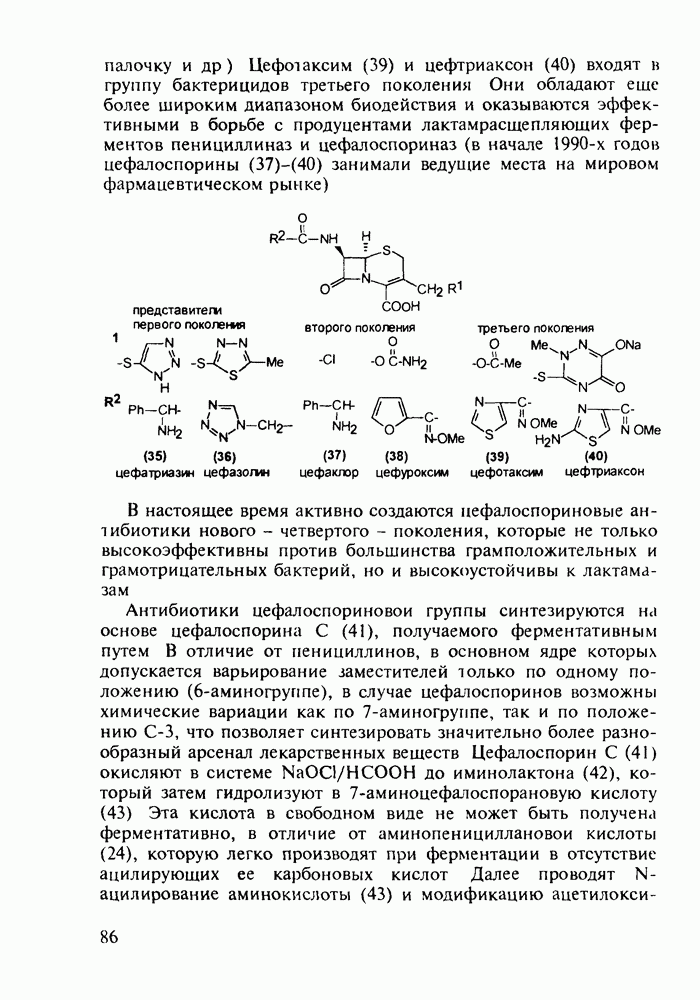
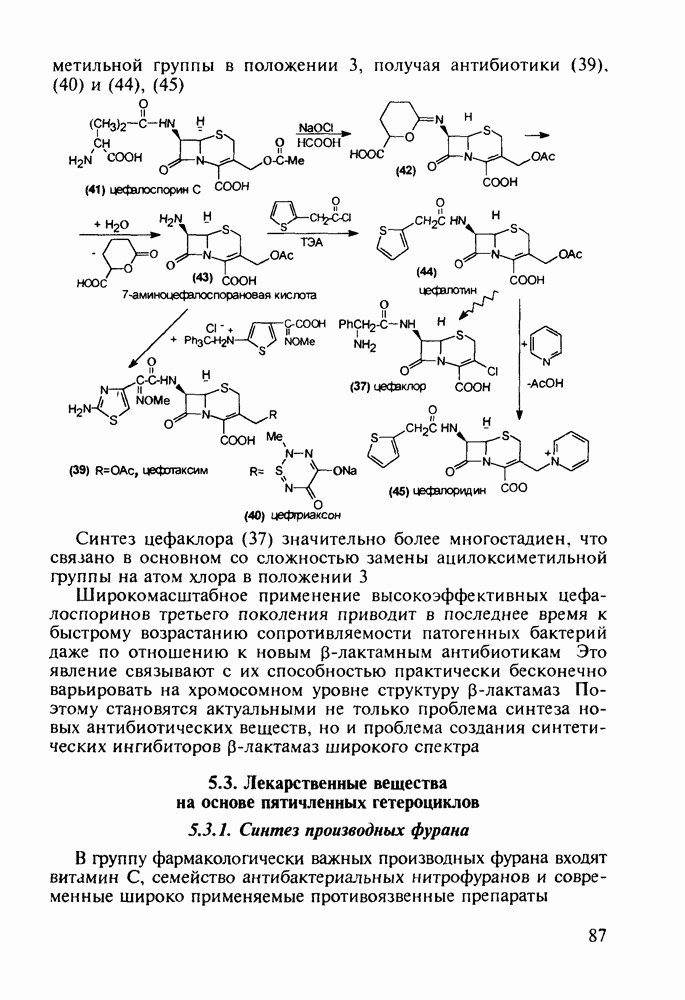
- 5.2.3. Цефалоспорины
- 5.3. Лекарственные вещества на основе пятичленных гетероциклов
- 5.3.2. Синтез производных пиррола
- 5.3.3. Оксазолидины. Антибиотик циклосерин
- 5.3.4. Антипиретики и анальгетики пиразолинового ряда
- 5.3.5. Имидазолы с противопаразитарной, антигипертензивной и другой биоактивностью
- 5.3.6. Производные тиазола. Витамин В1
- 5.3.7. Психостимуляторы с оксадиазольным и тетразольным гетероциклами
- 5.4. Синтез лекарственных веществ, содержащих шестичленные гетероциклы
- 5.4.2. Синтез лекарственных веществ пиридинового ряда
- 5.4.3. Анальгетики и транквилизаторы пиперидинового ряда
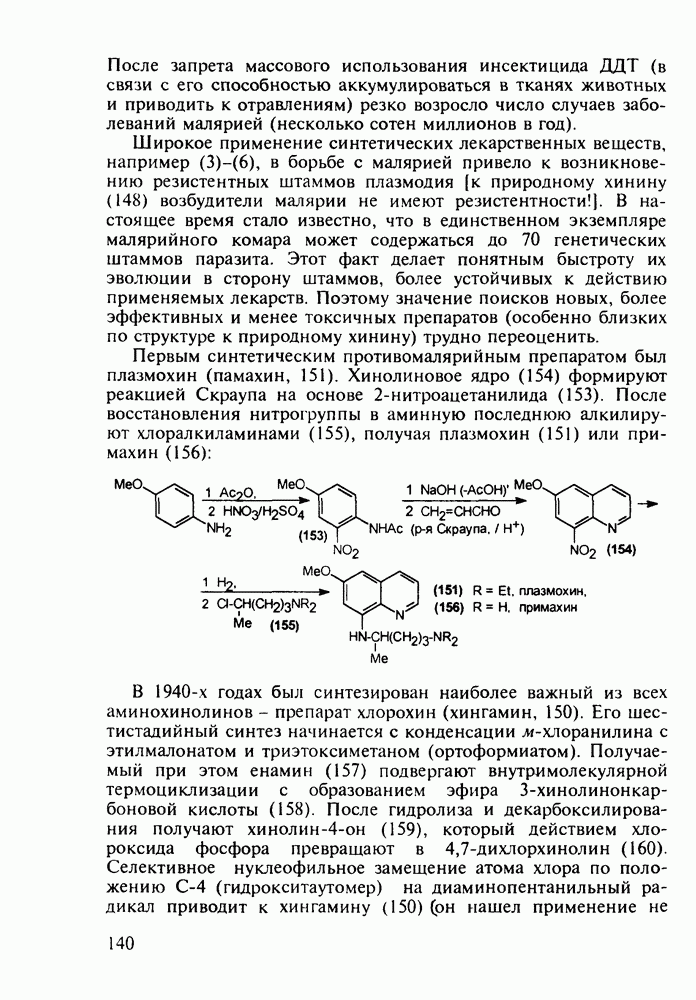
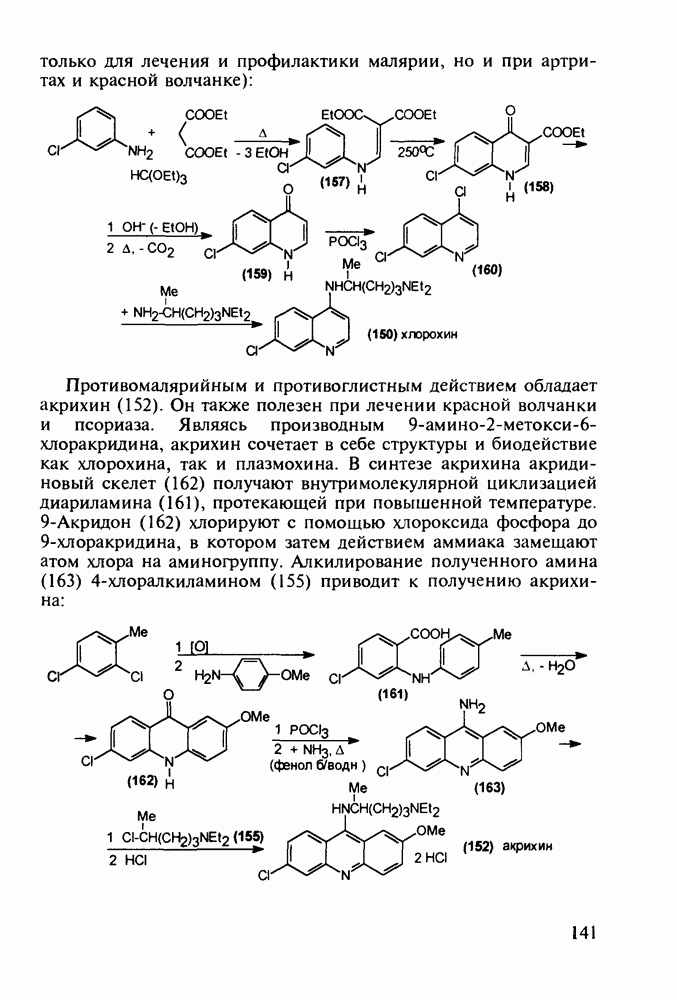
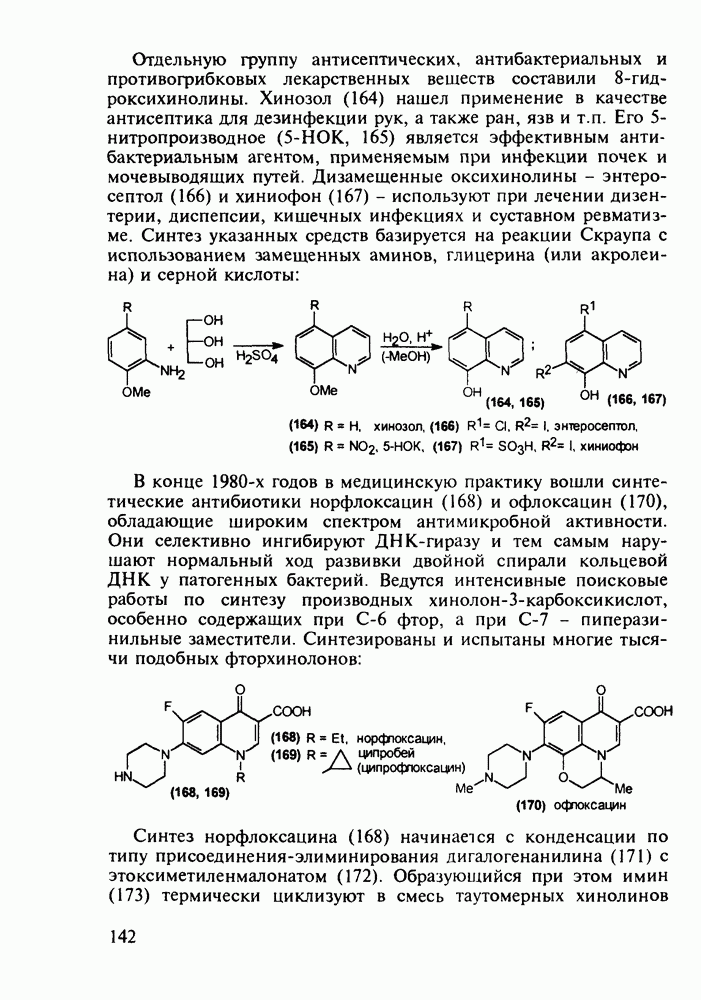
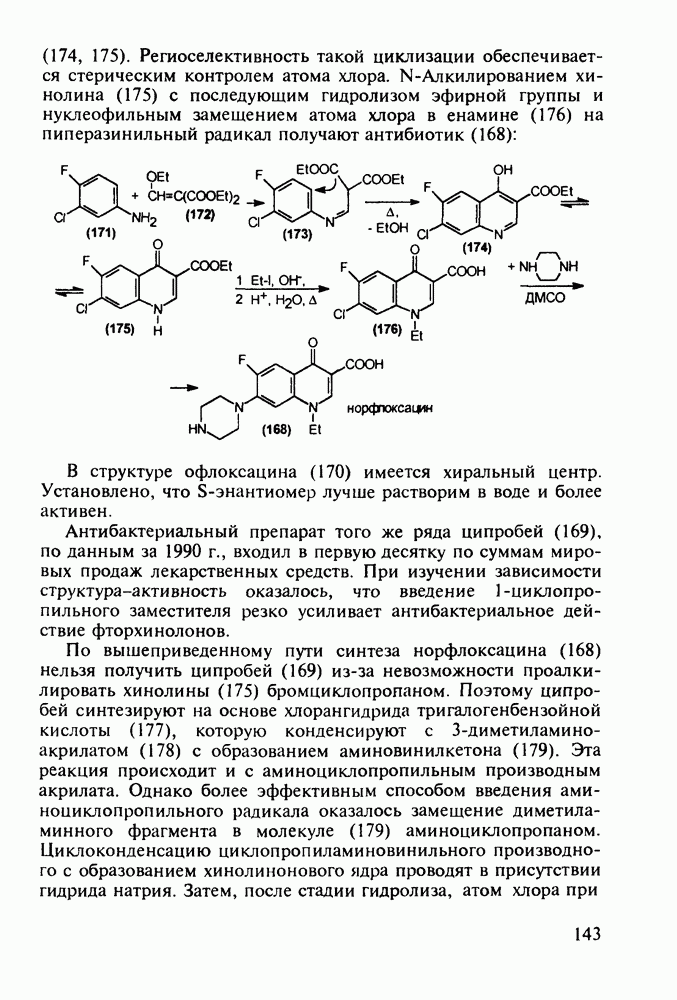
- 5.4.4. Производные хинолина с антималярийным и антибактериальным действием
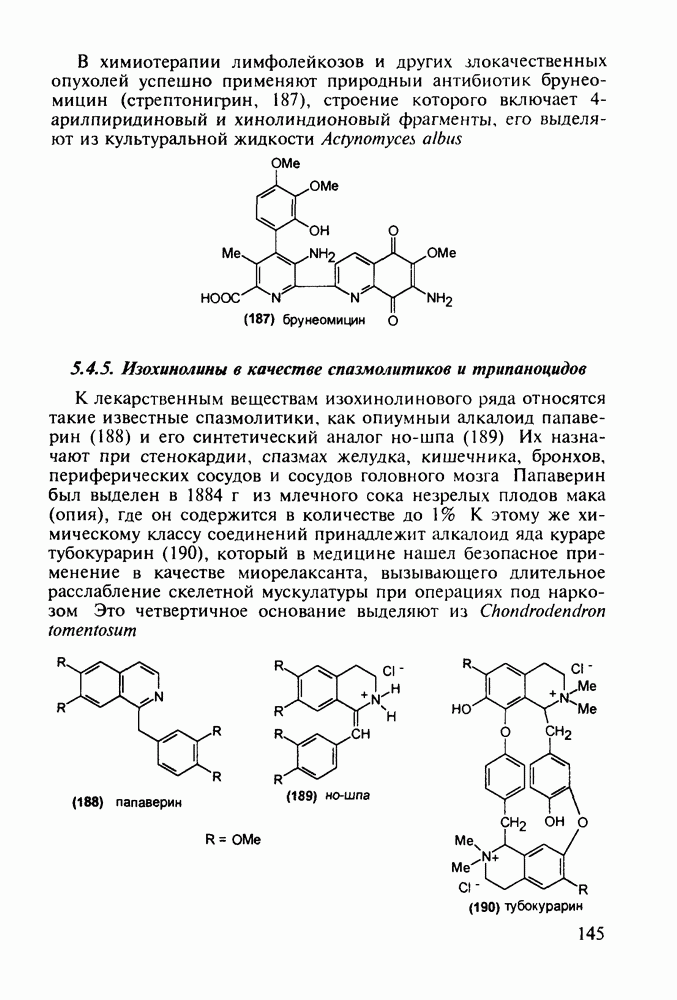
- 5.4.5. Изохинолины в качестве спазмолитиков и трипаноцидов
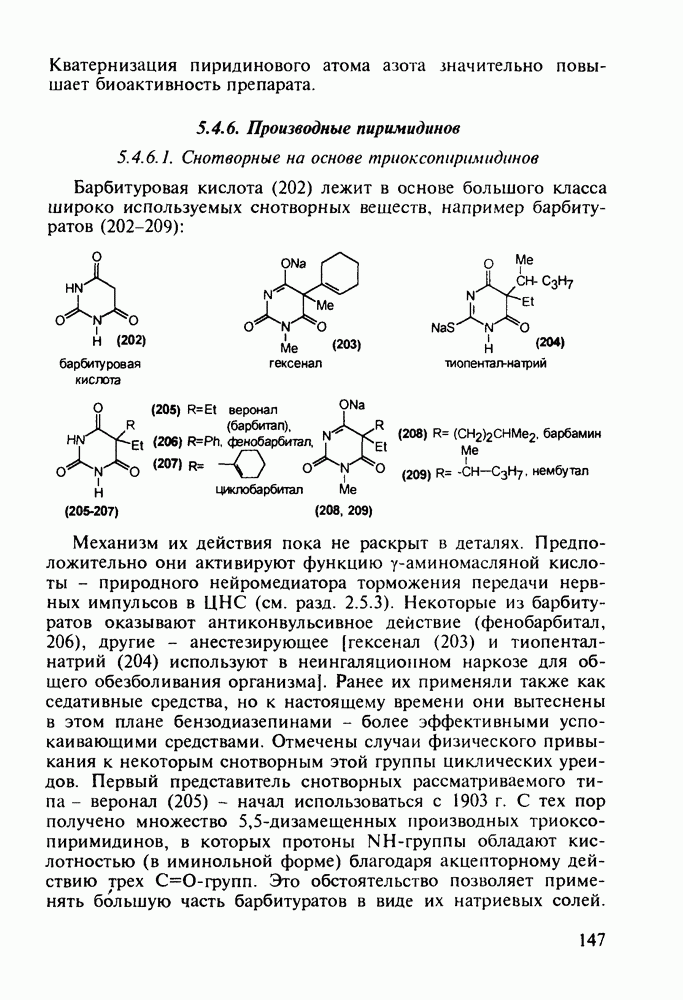
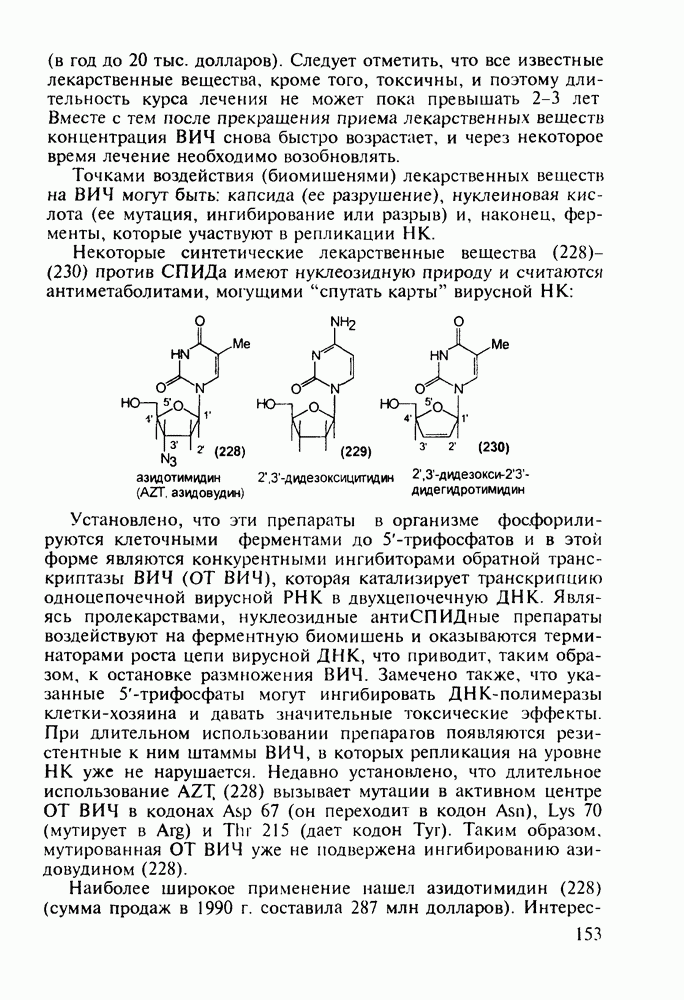
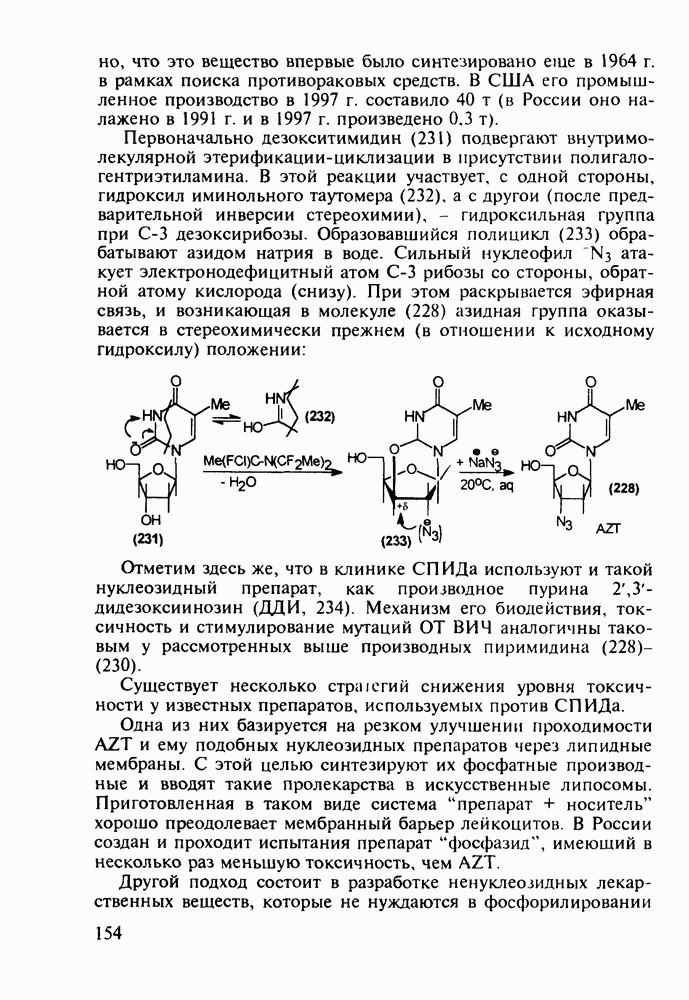
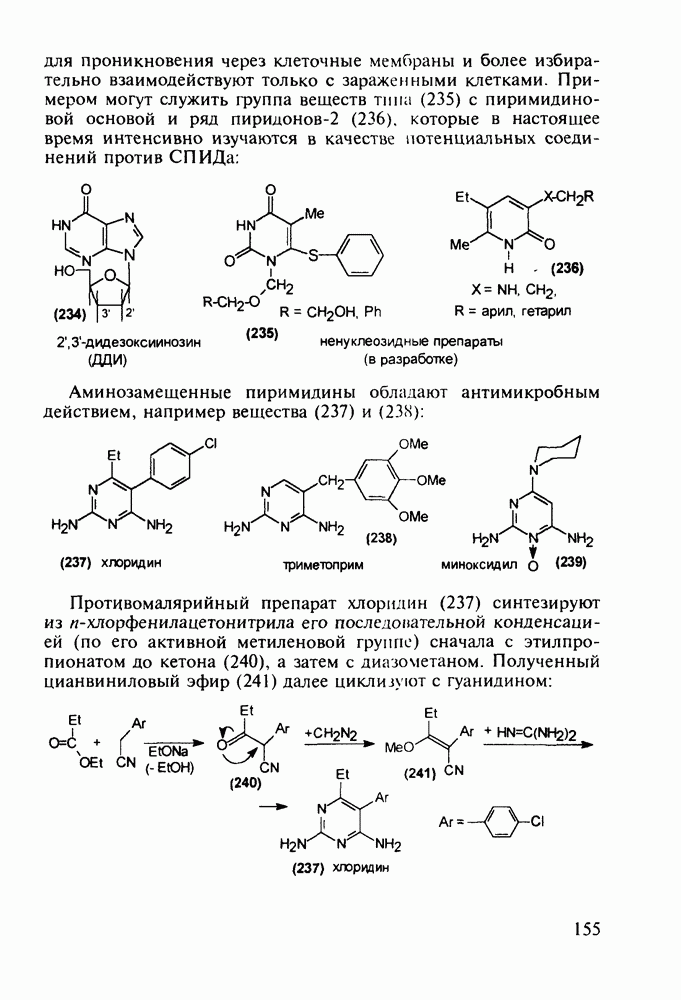
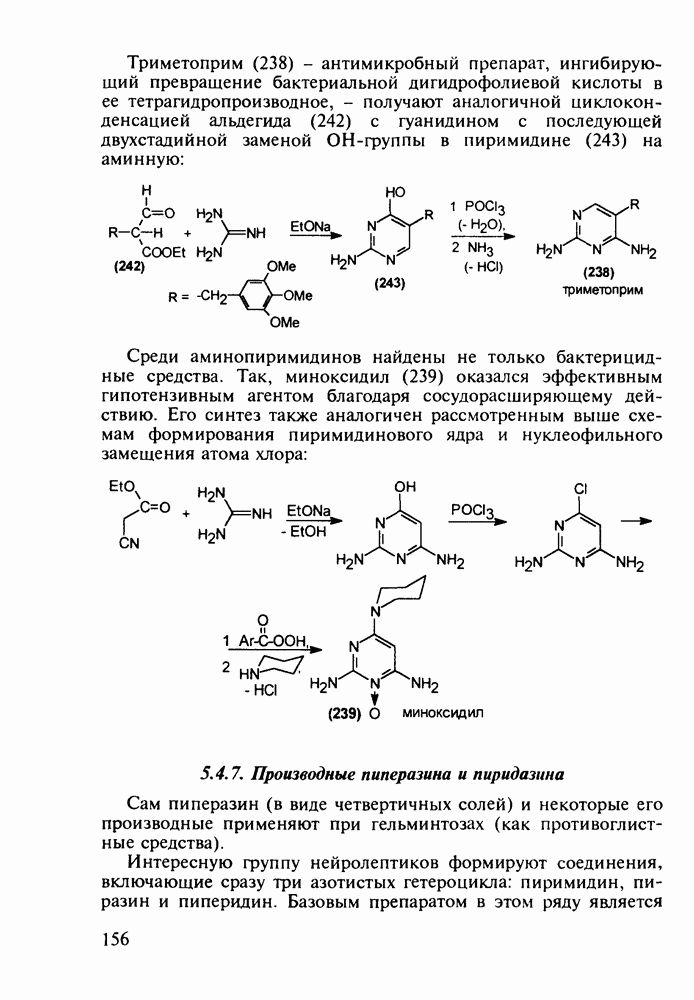
- 5.4.6. Производные пиримидинов
- 5.4.7. Производные пиперазина и пиридазина
- 5.4.8. Бензотиазины. Нейролептики фенотиазинового ряда
- 5.4.9. Пуриновые основания в качестве стимулирующих и антивирусных агентов
- 5.4.10. Производные аденозинфосфорной кислоты
- 5.4.11. Производные птеридина с витаминной (витамины Вс и В2) и противораковой активностью
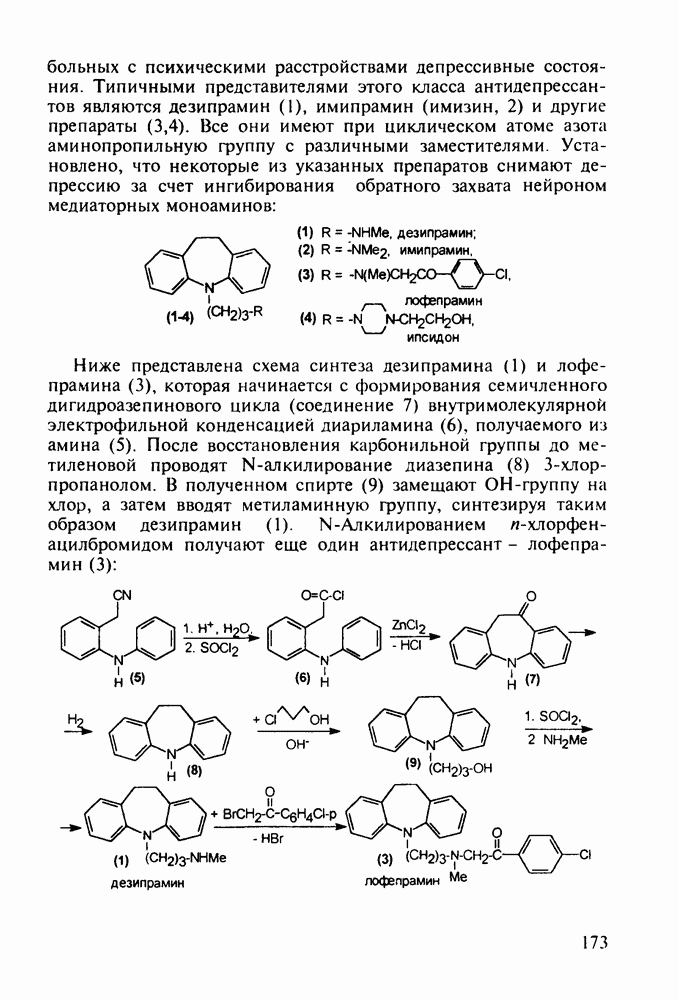
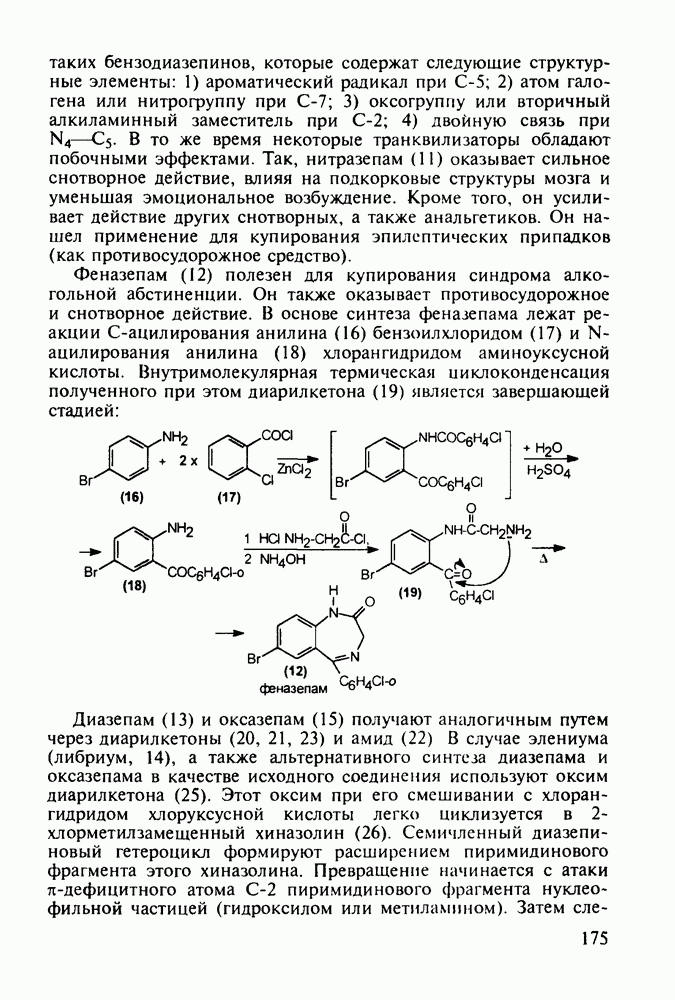
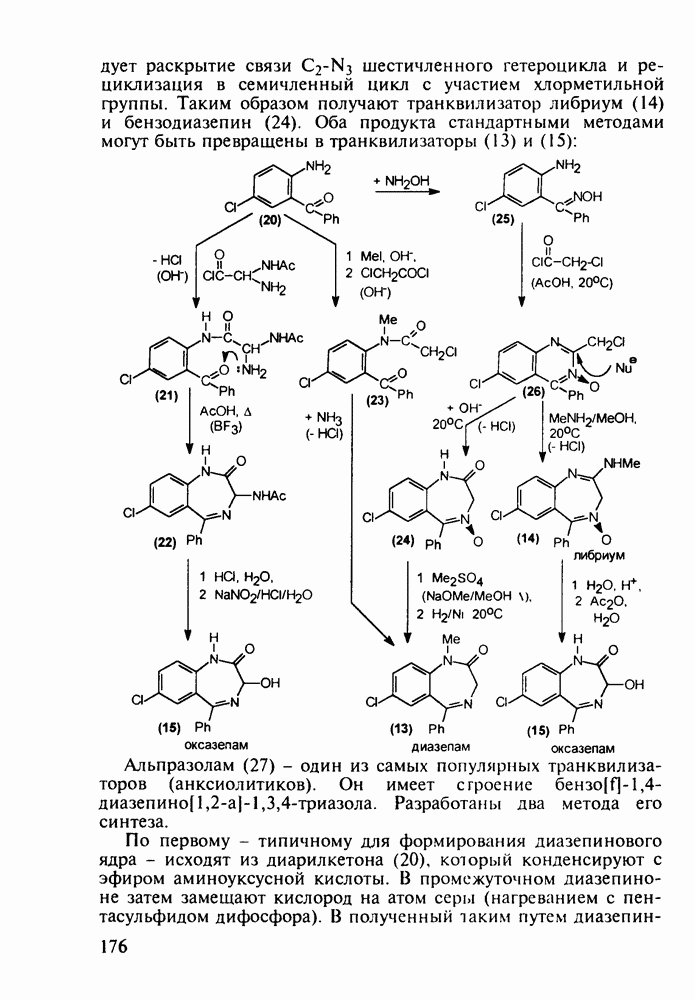
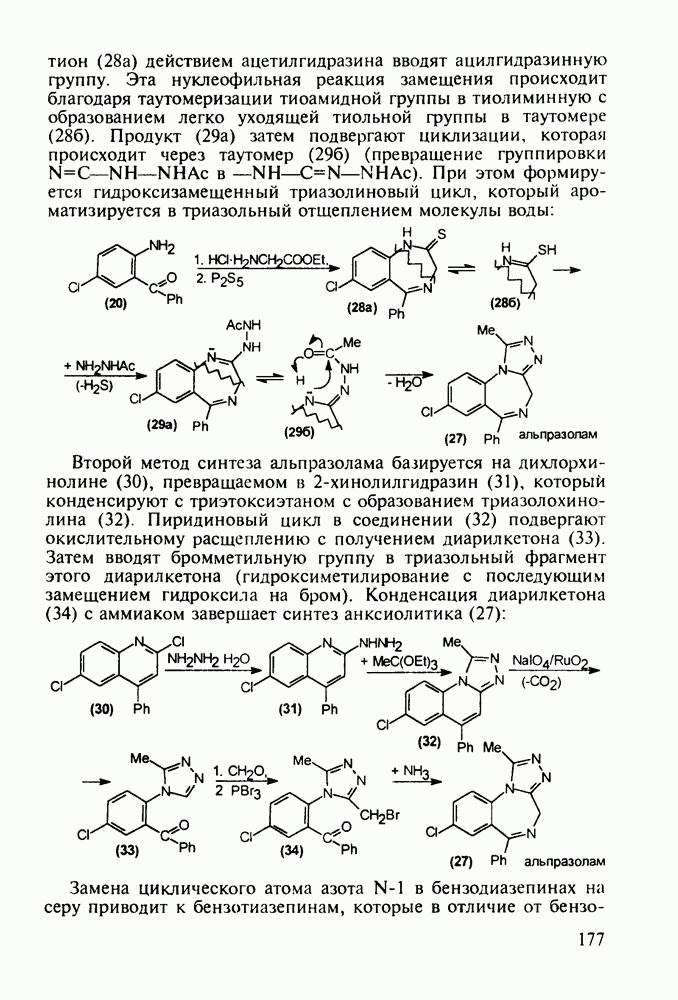
- 5.5. Лекарственные вещества, содержащие семичленный гетероцикл
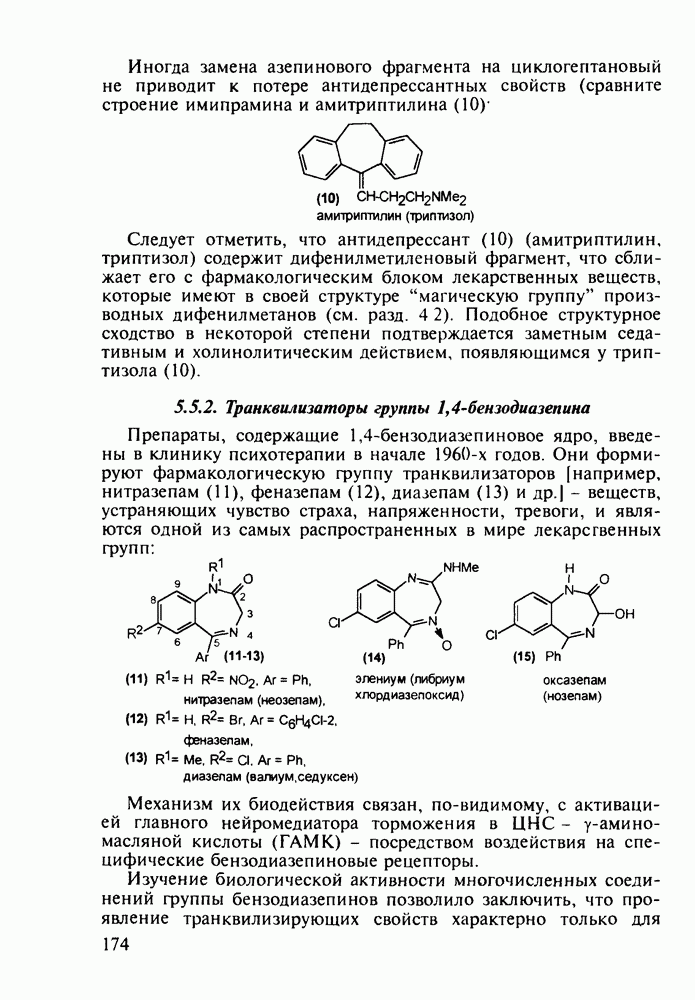
- 5.5.2. Транквилизаторы группы 1,4-бензодиазепина
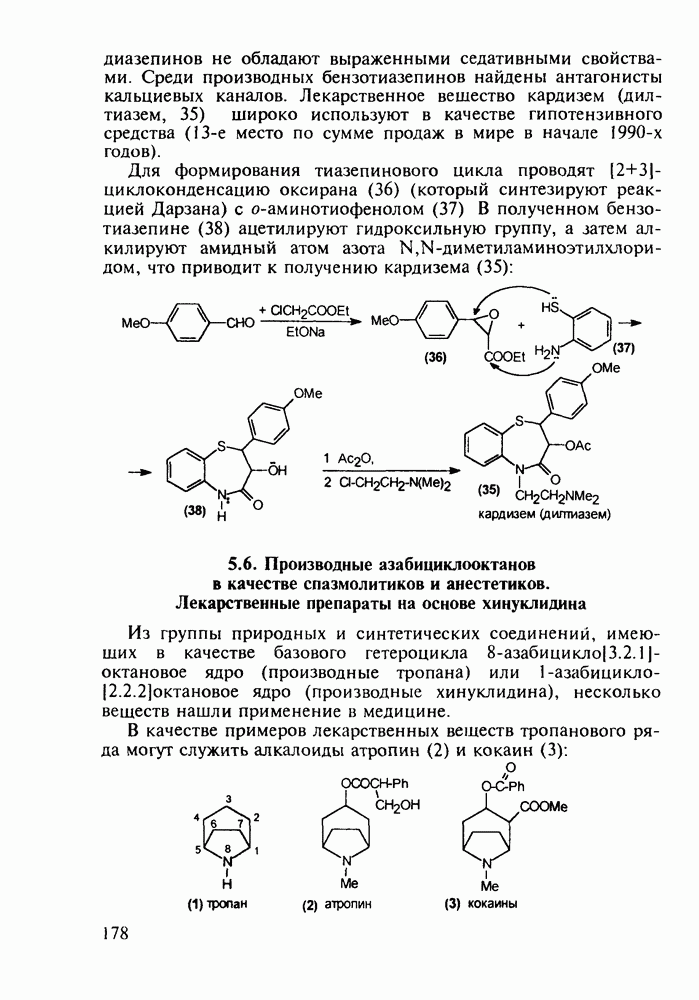
- 5.6. Производные азабициклооктанов в качестве спазмолитиков и анестетиков. Лекарственные препараты на основе хинуклидина
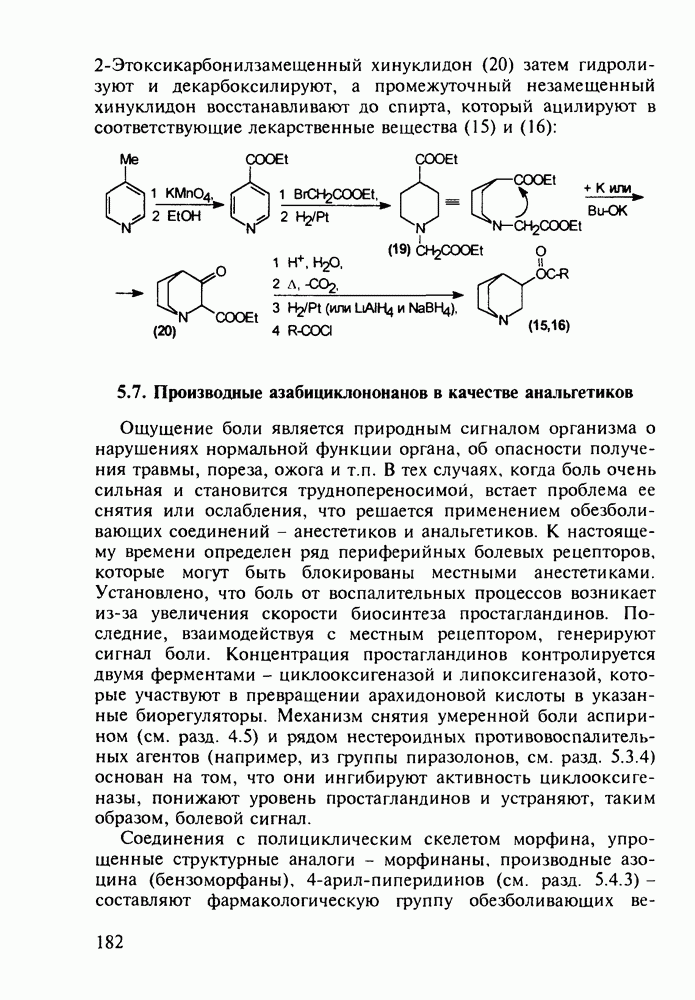
- 5.7. Производные азабициклононанов в качестве анальгетиков
- 5.7.1. Группа пентазоцина
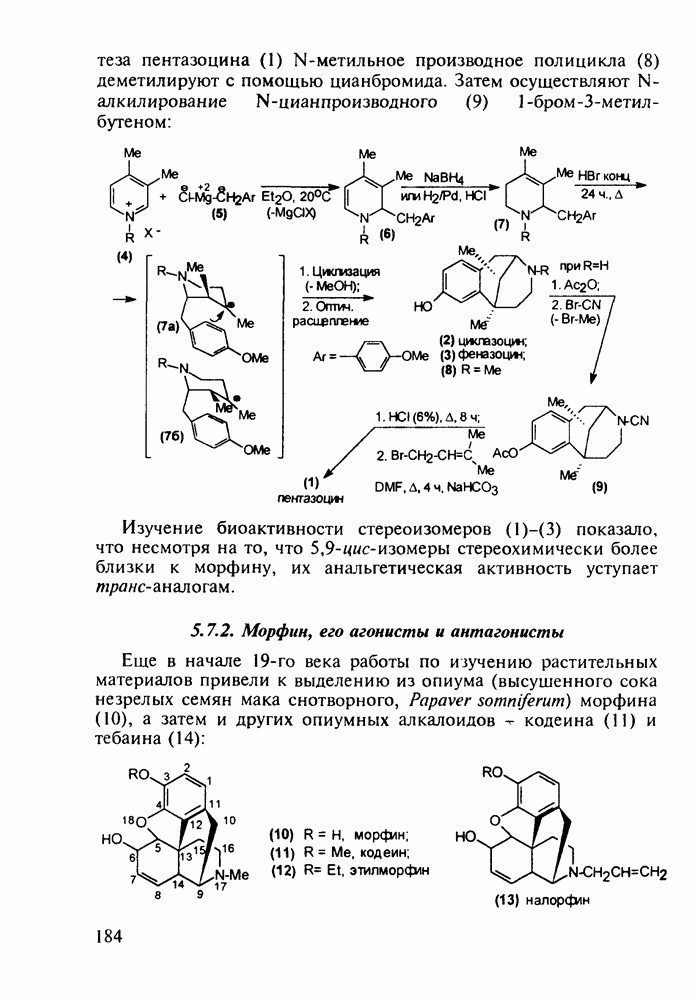
- 5.7.2. Морфин, его агонисты и антагонисты
- РЕКОМЕНДУЕМАЯ ЛИТЕРАТУРА