| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
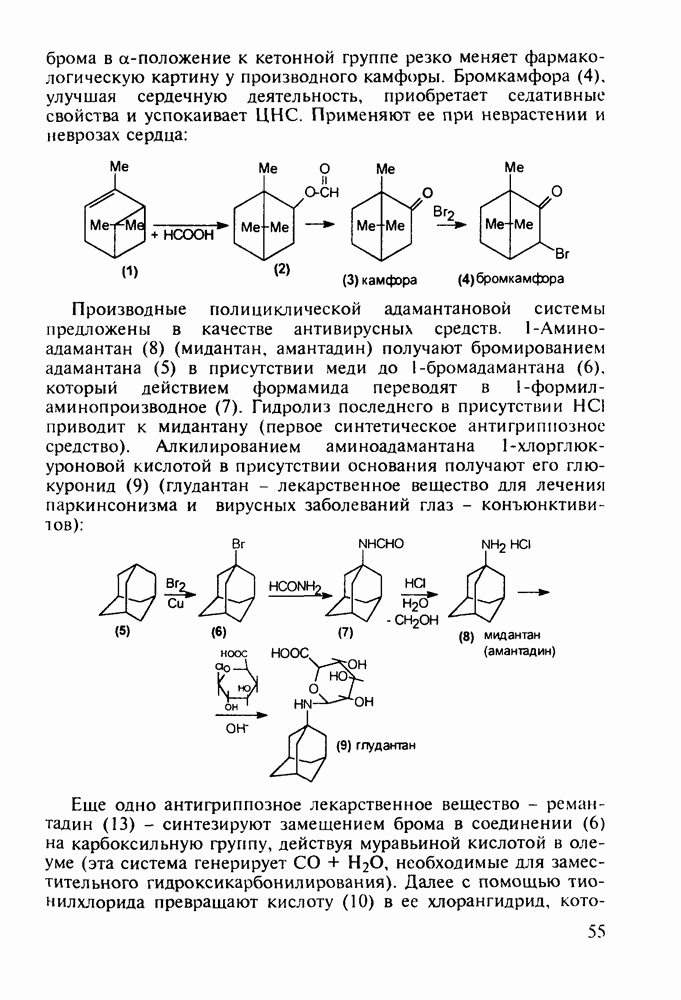
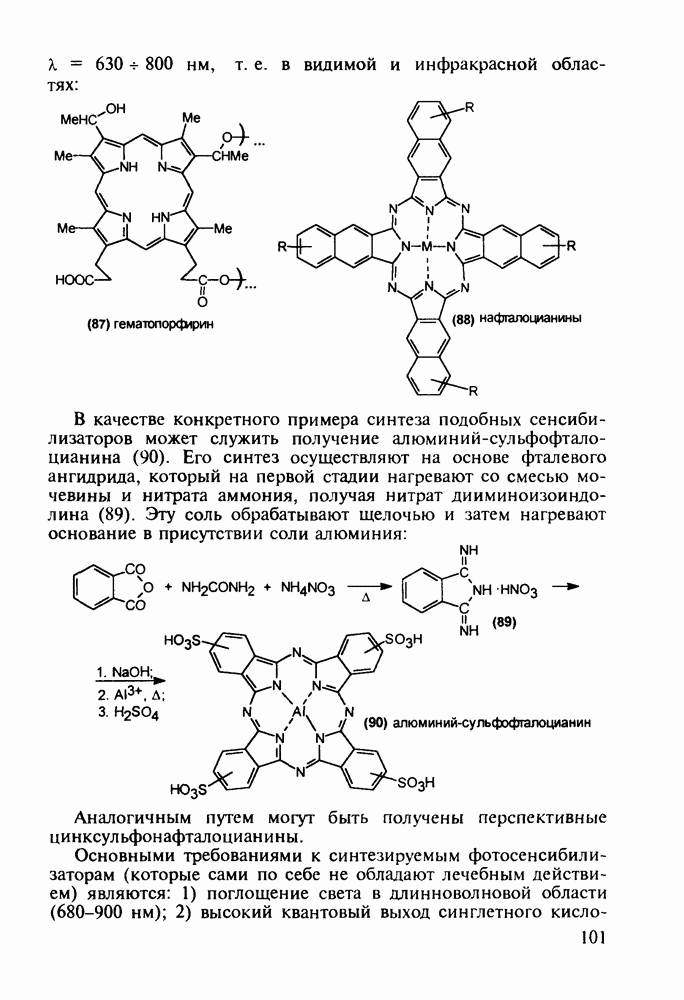
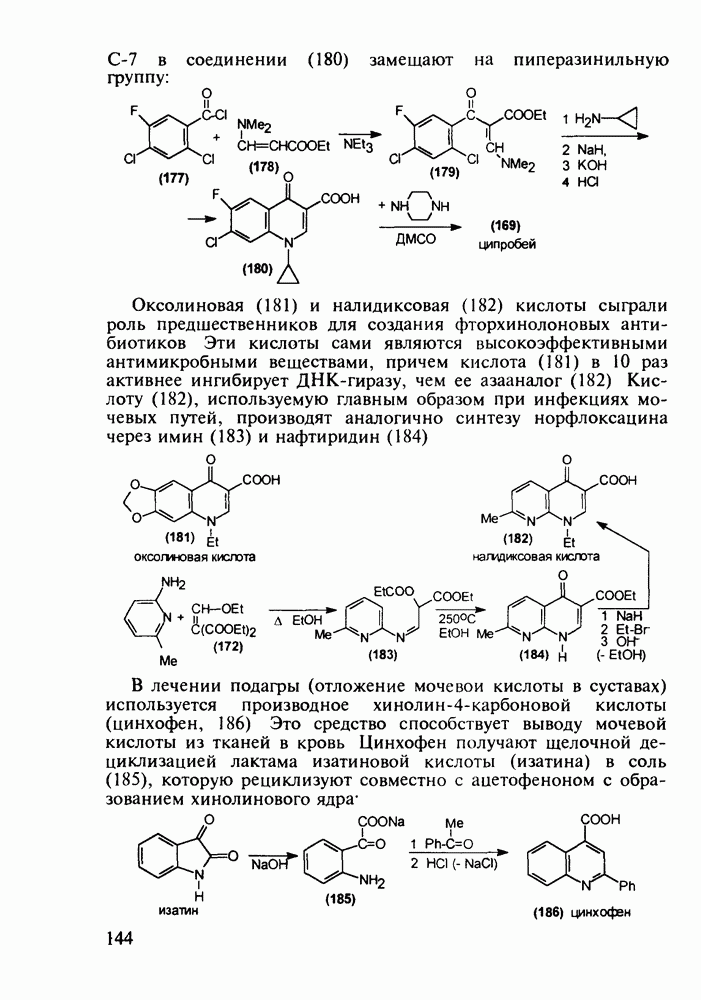
3.2. Противозачаточные и противовоспалительные вещества на основе циклопентафенантрена. Синтез витамина D
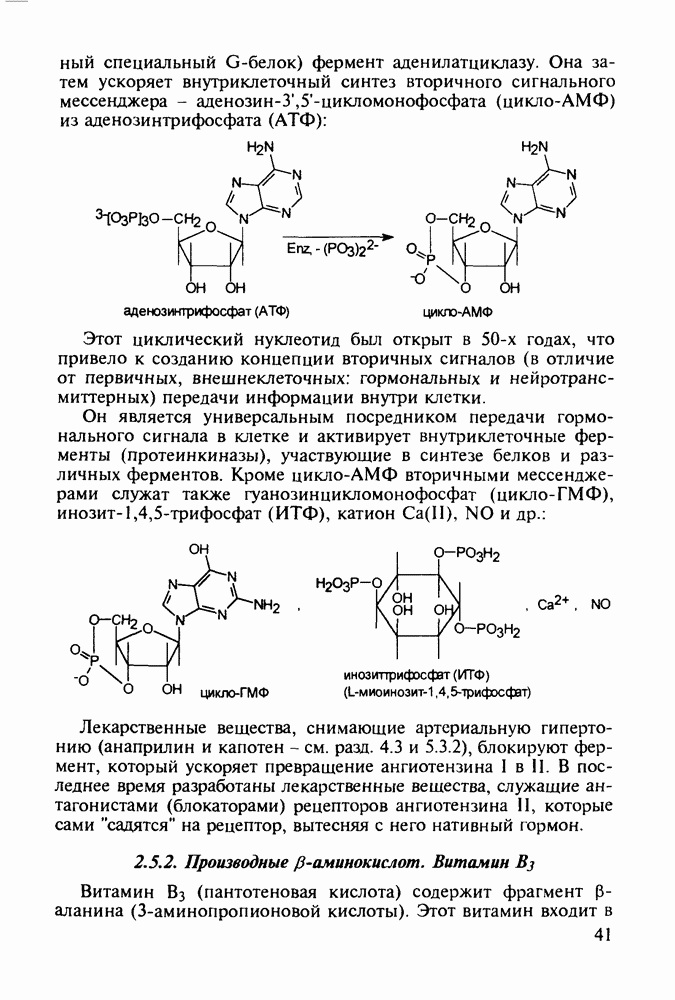
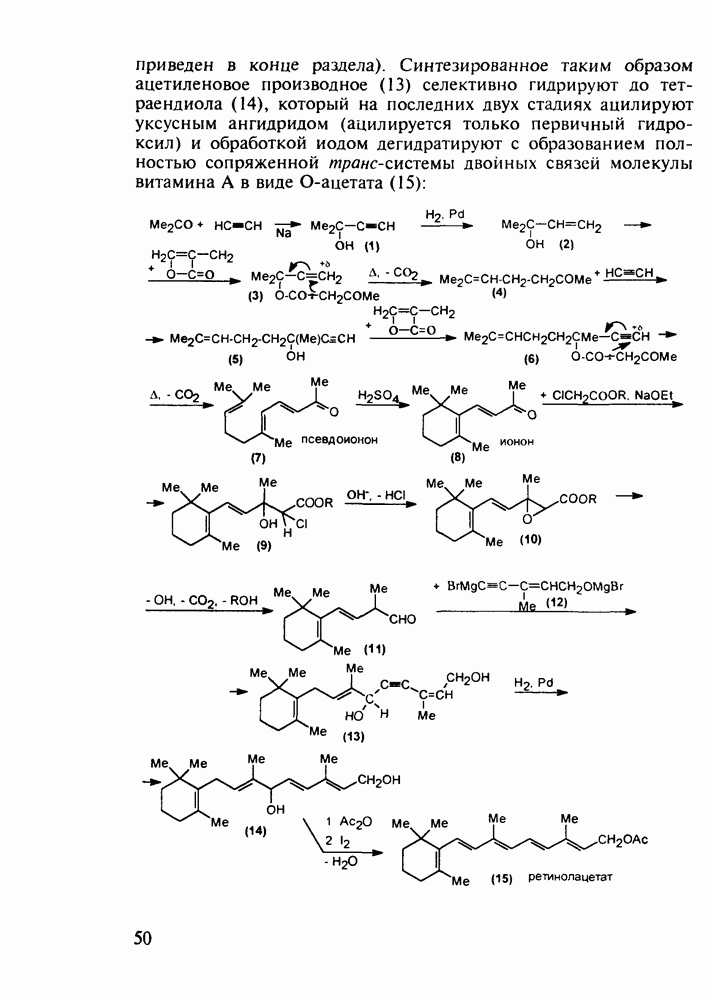
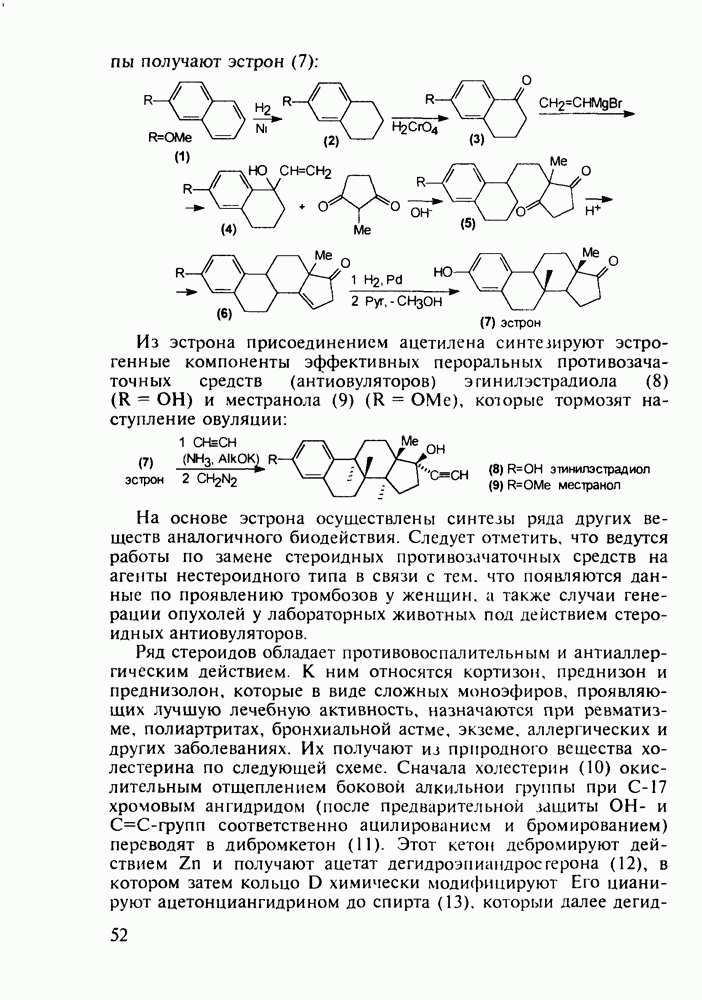
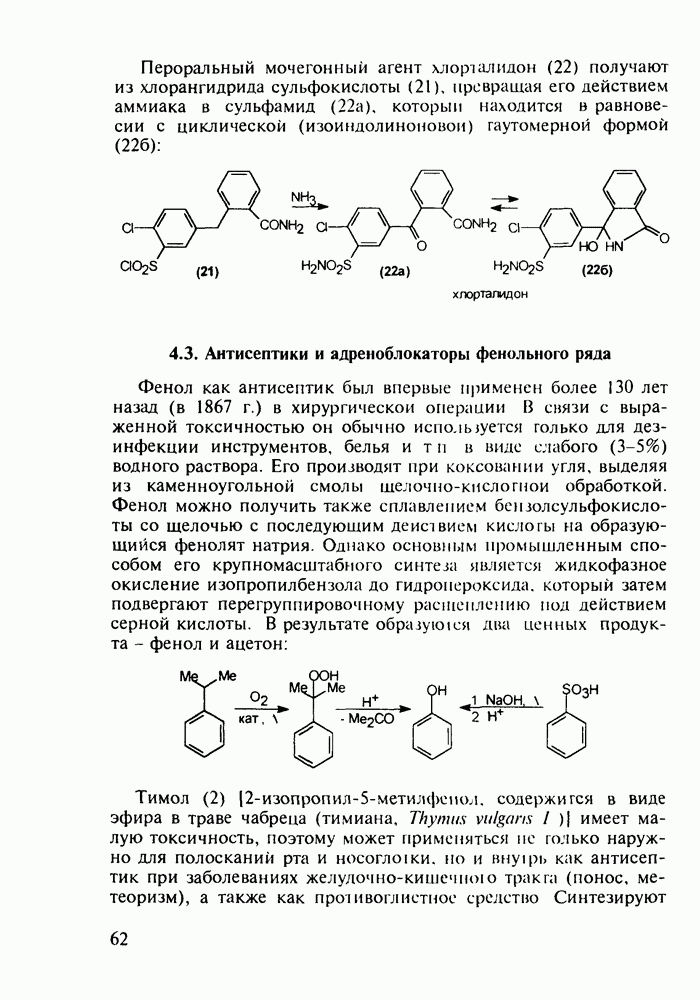
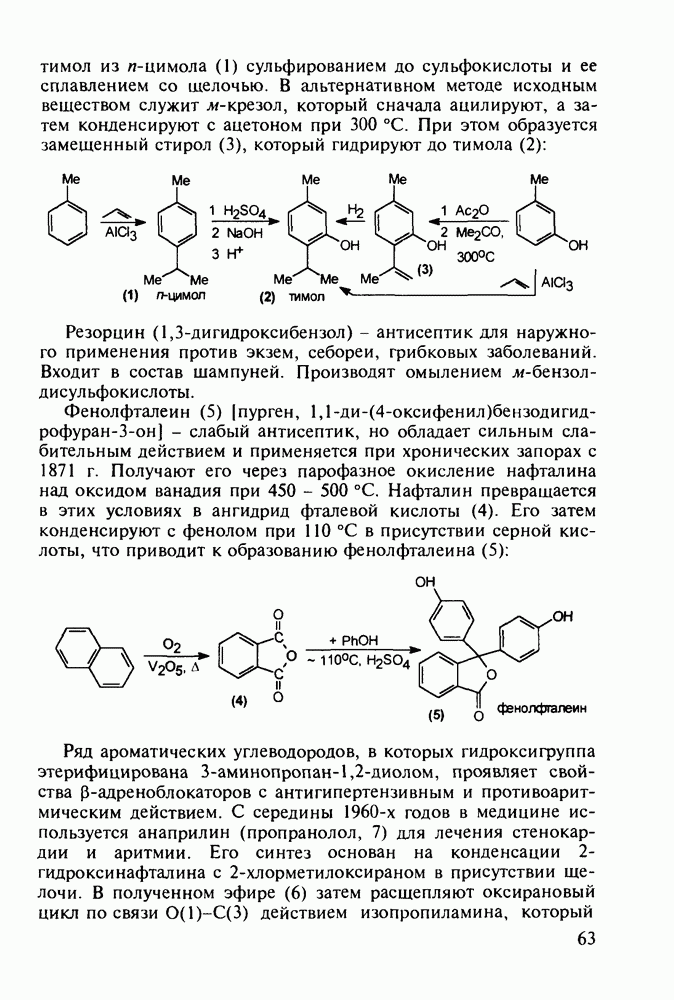
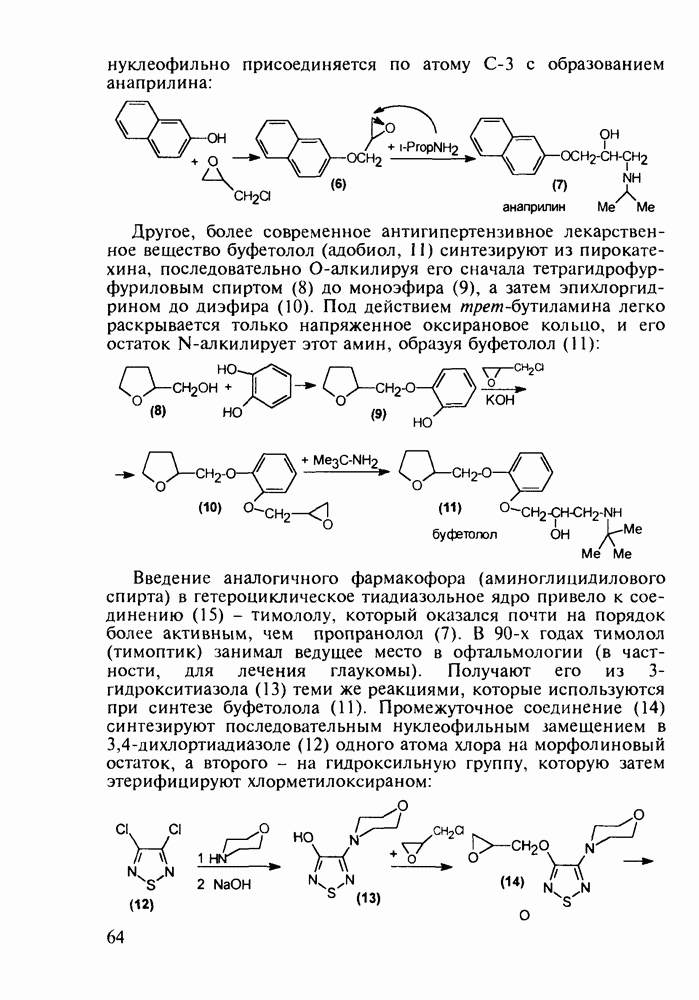
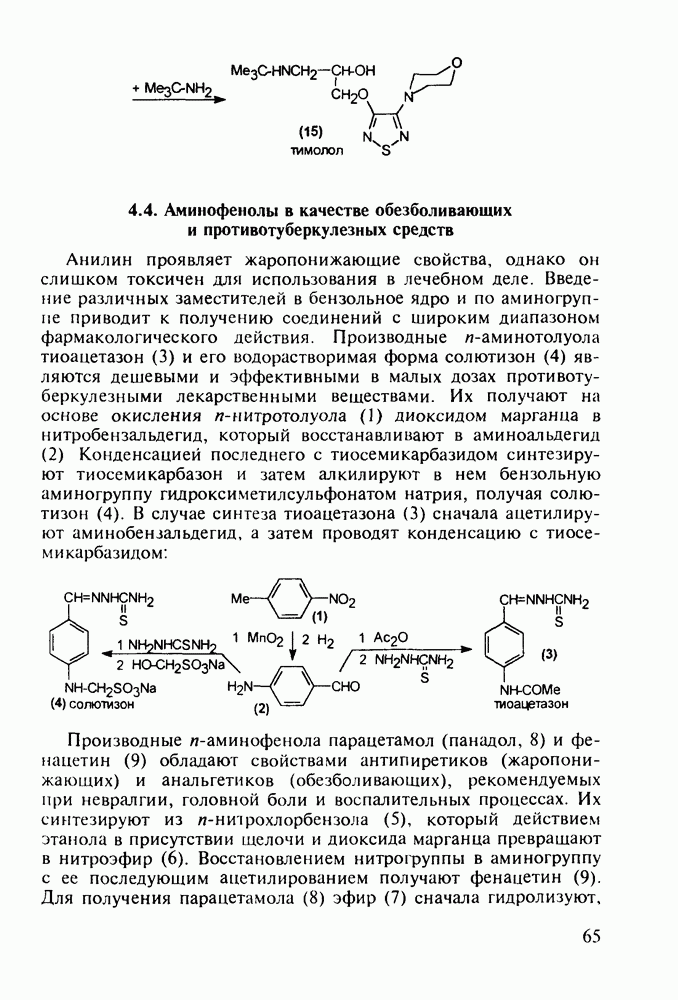
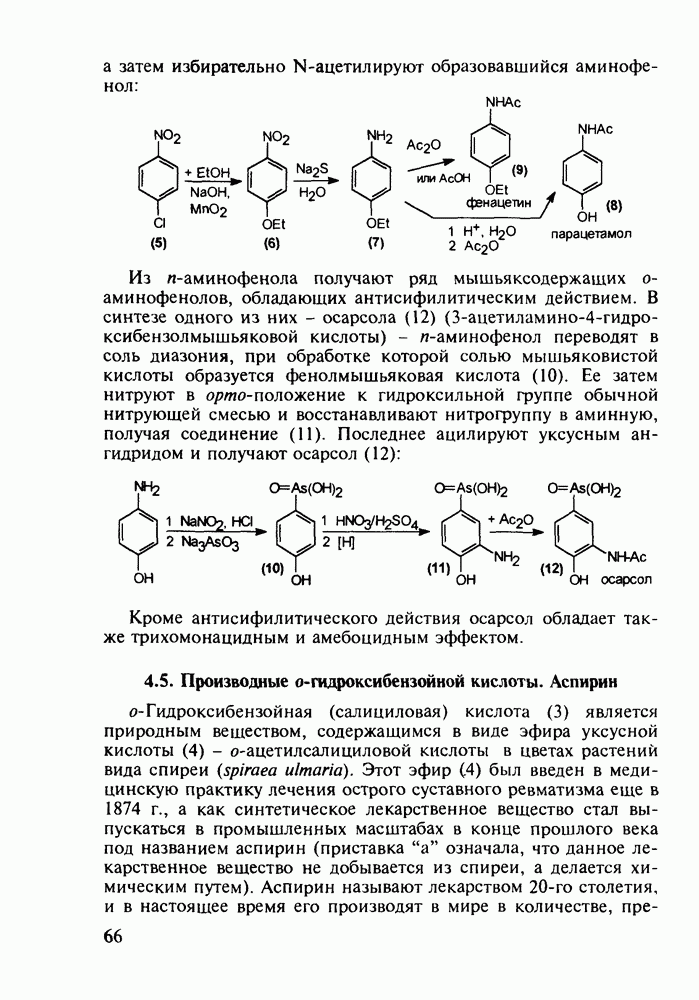
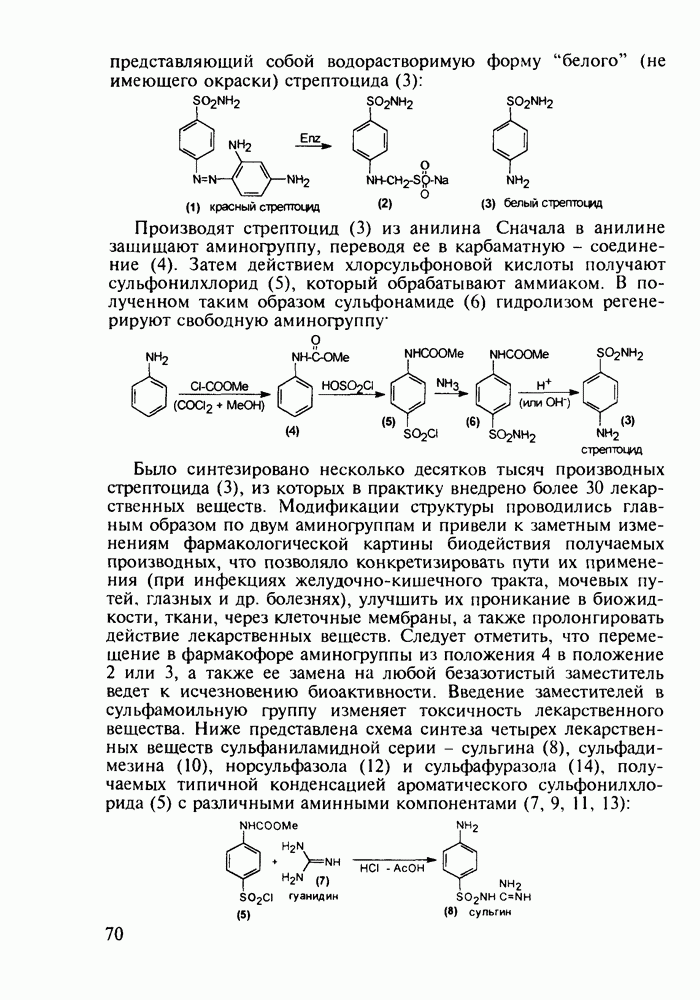
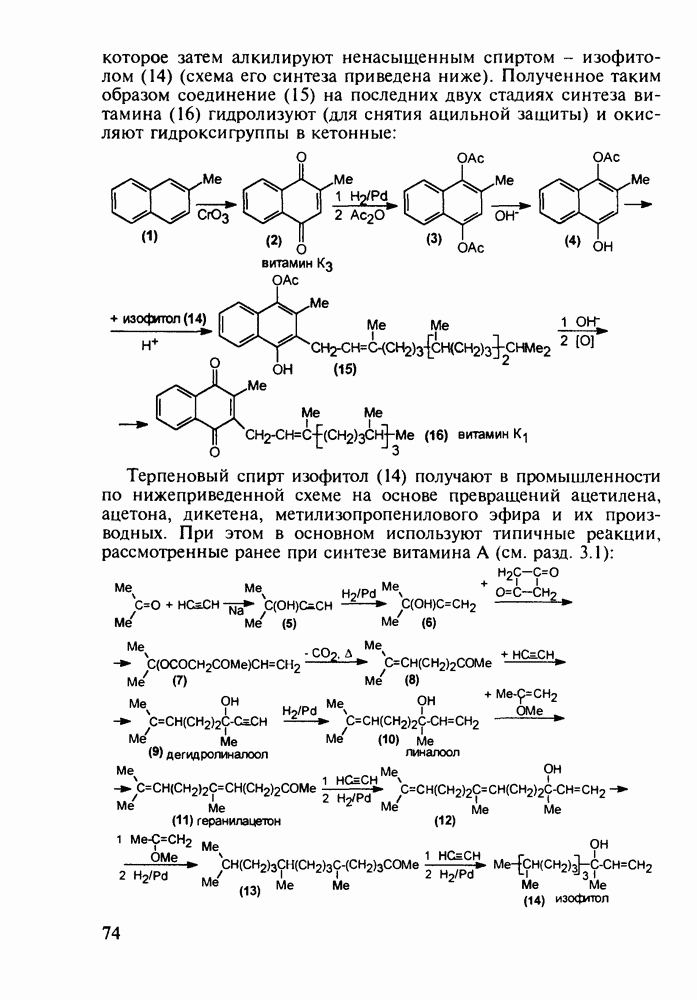
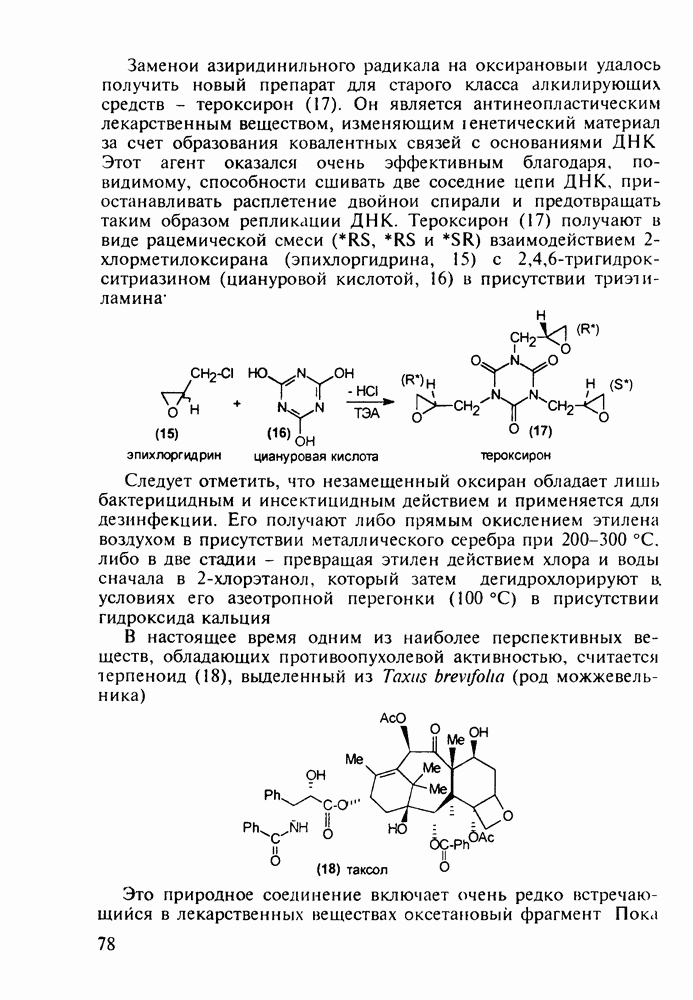
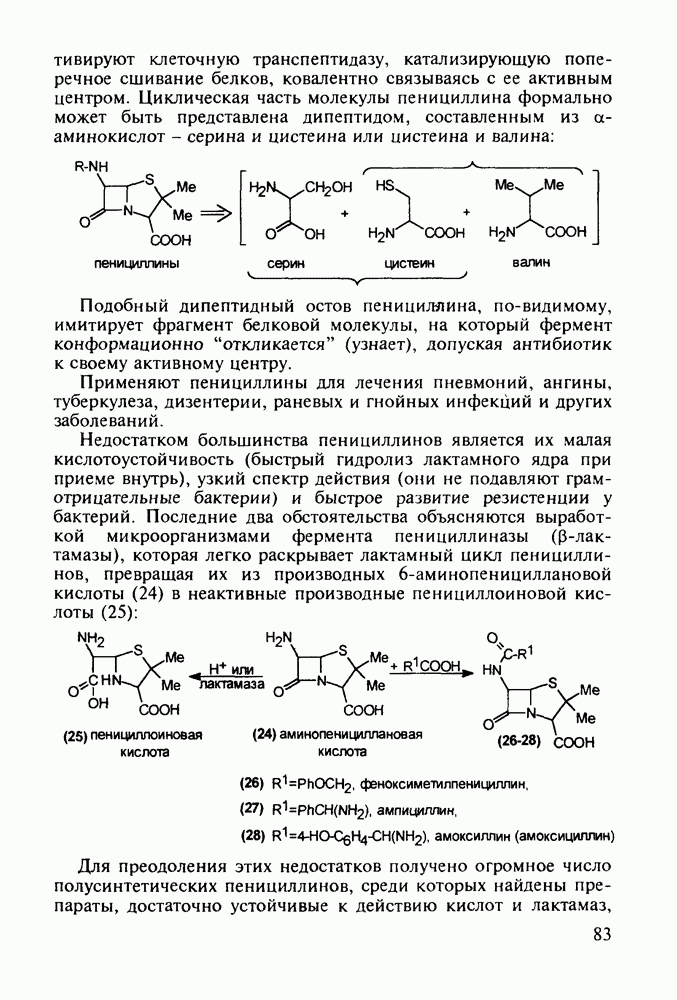
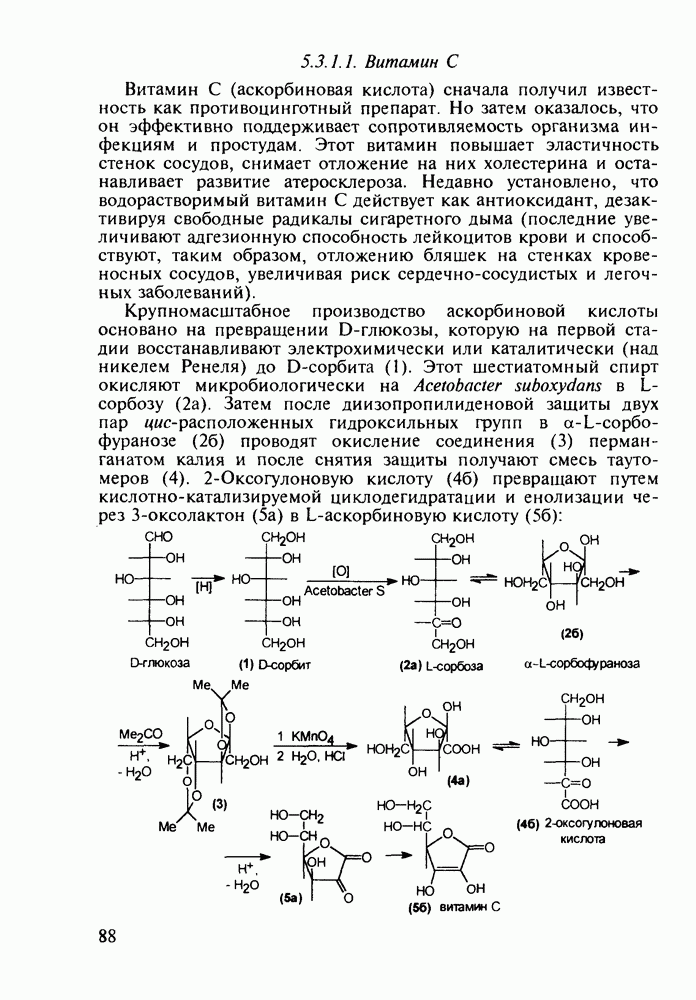
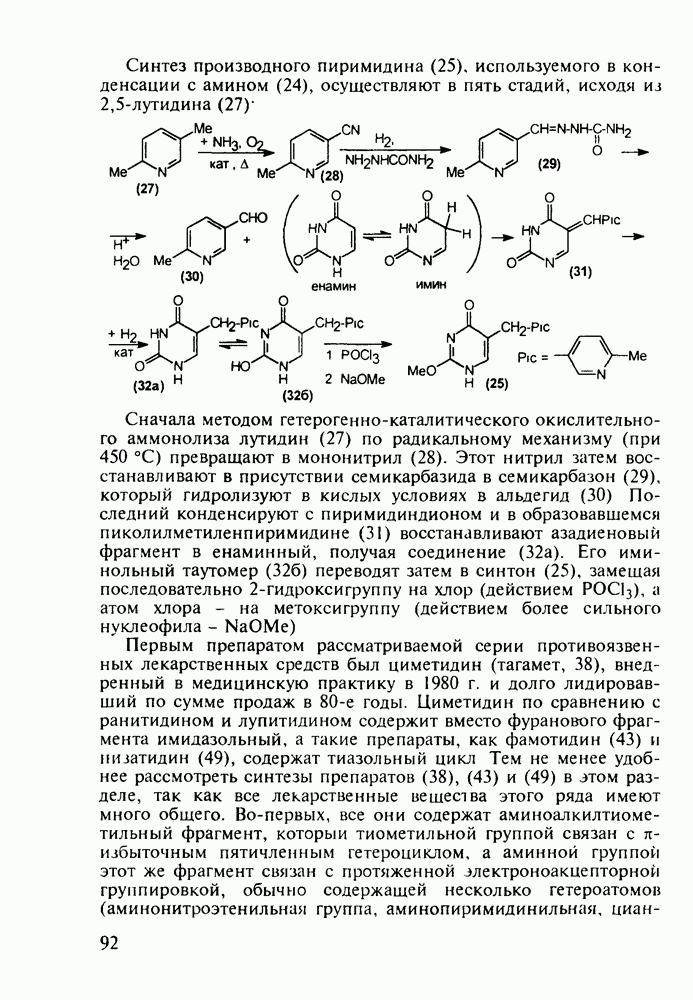
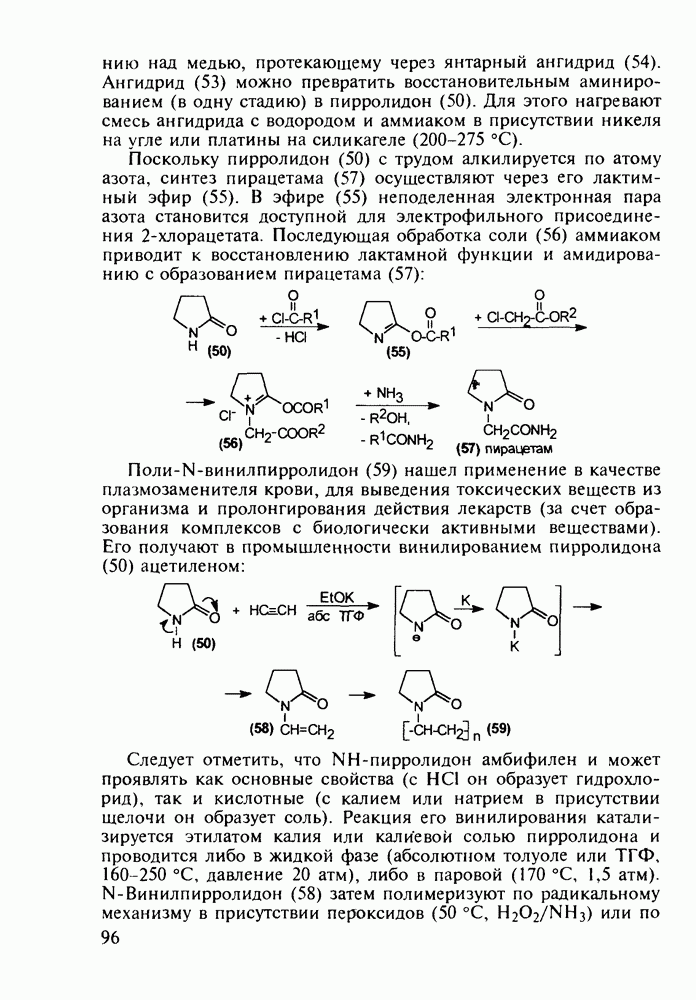
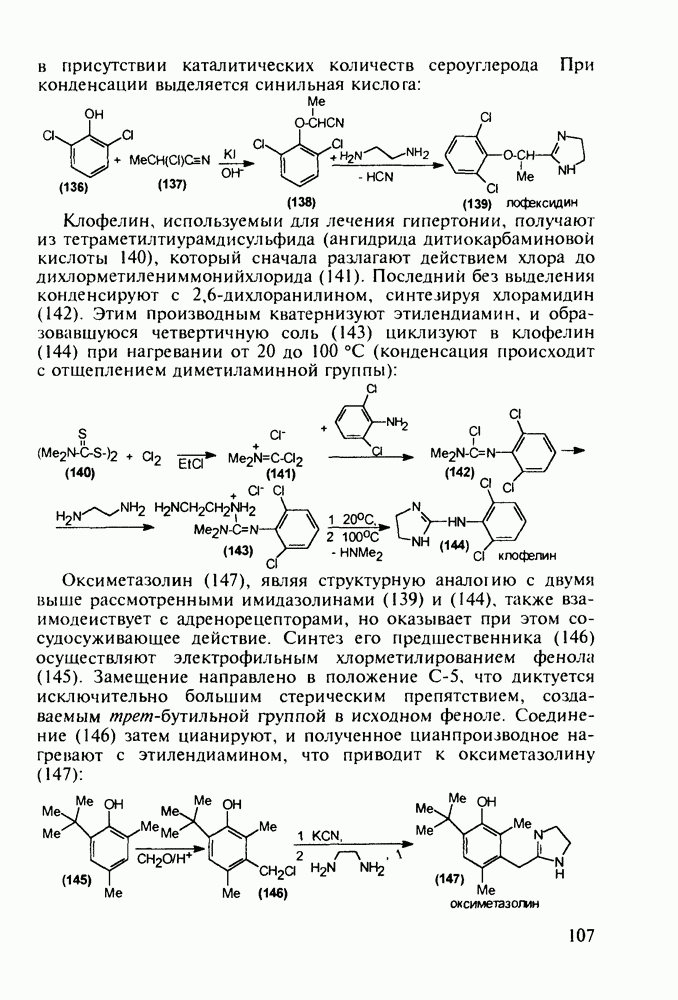
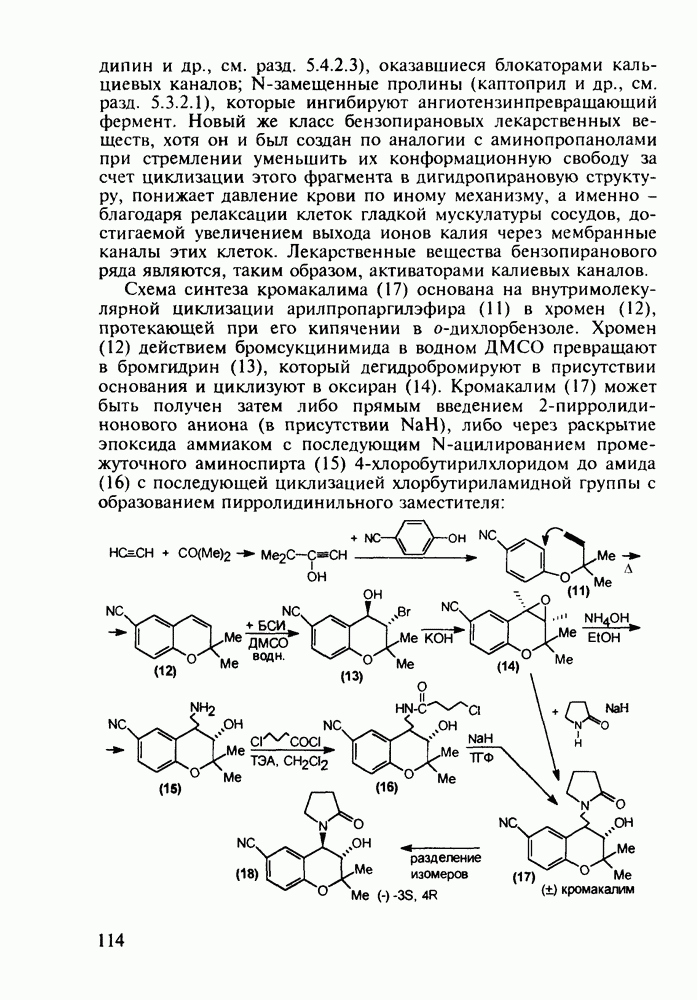
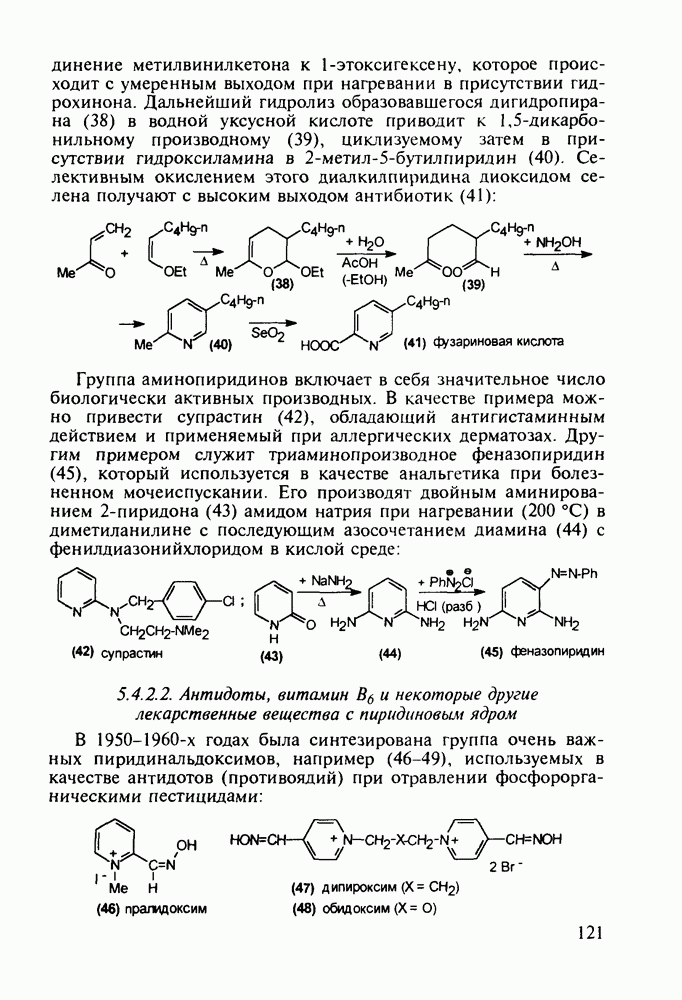
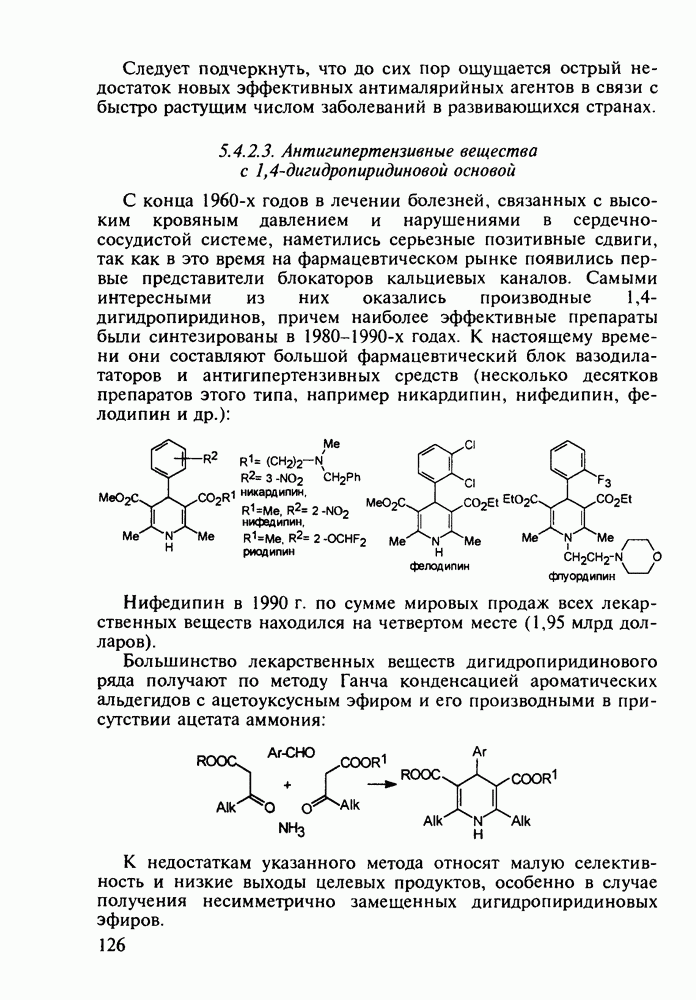
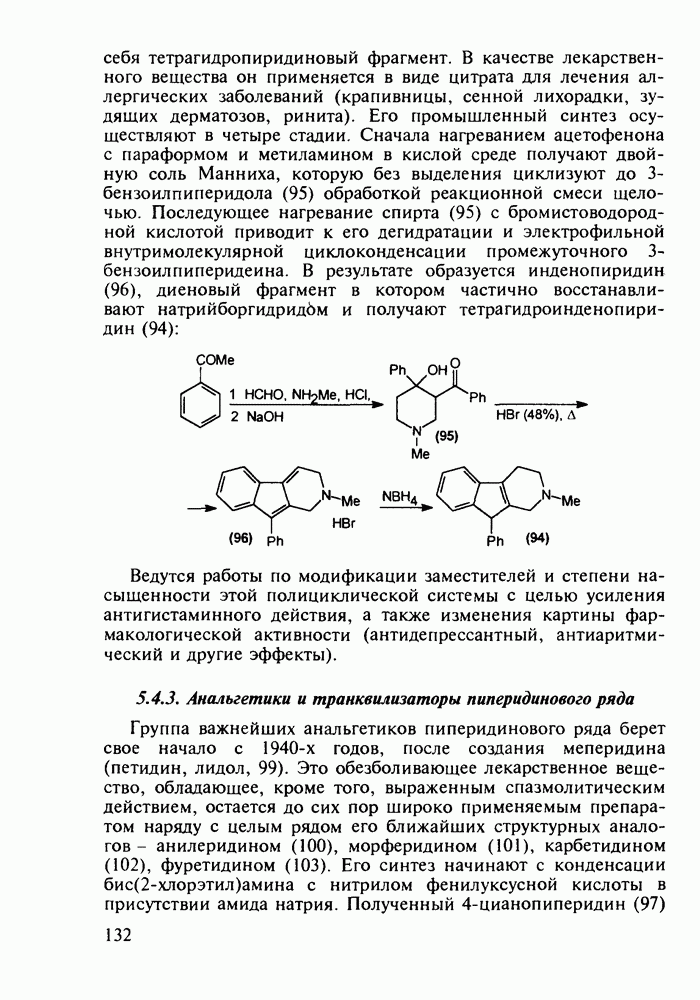
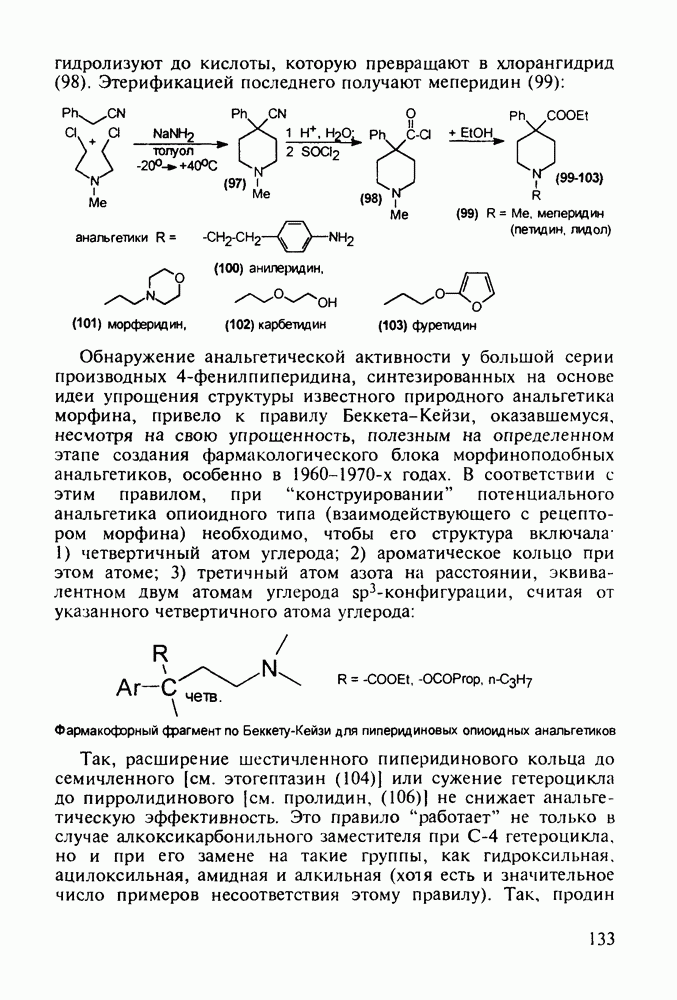
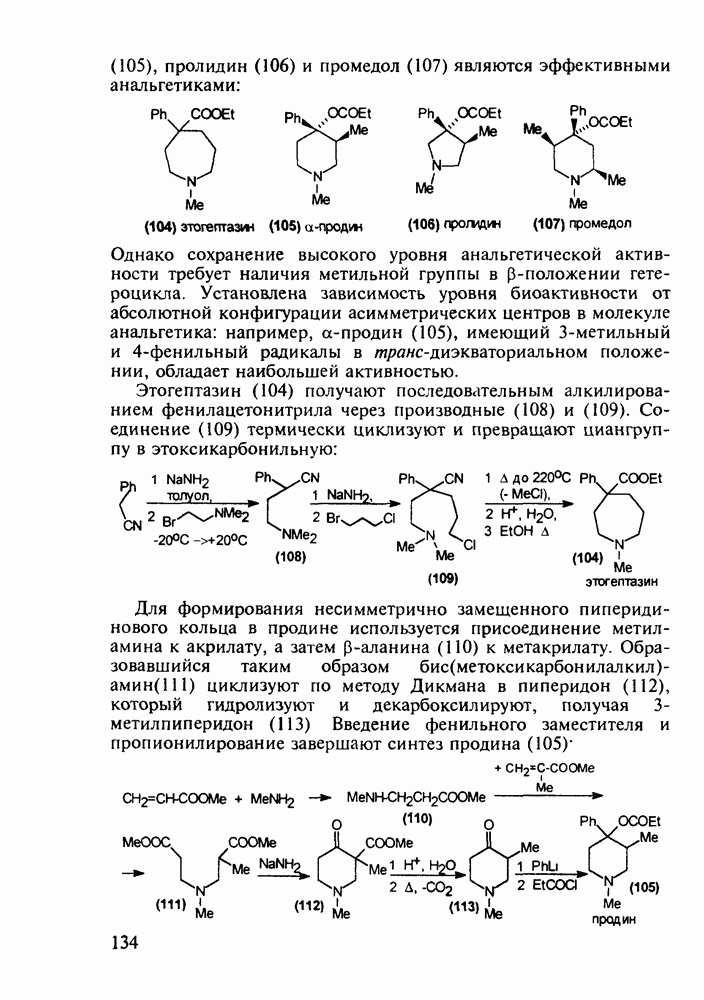
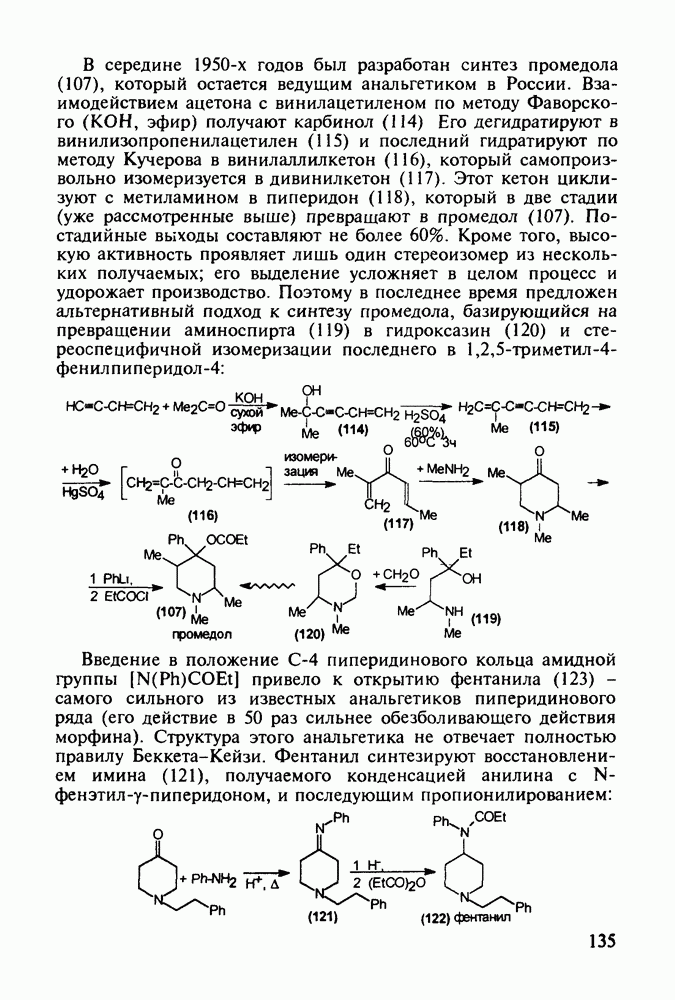
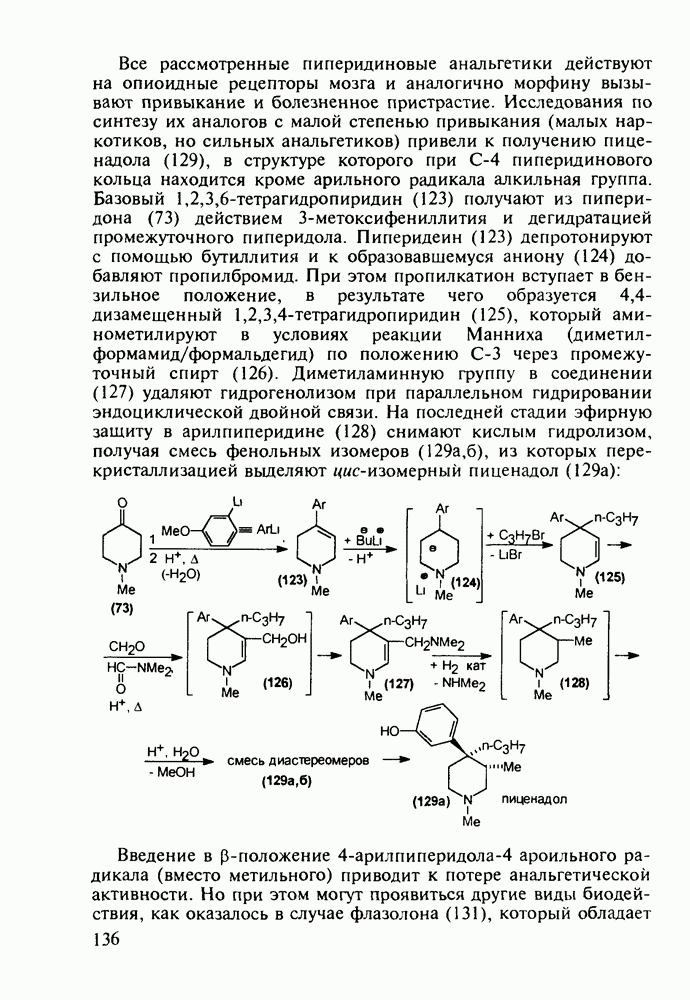
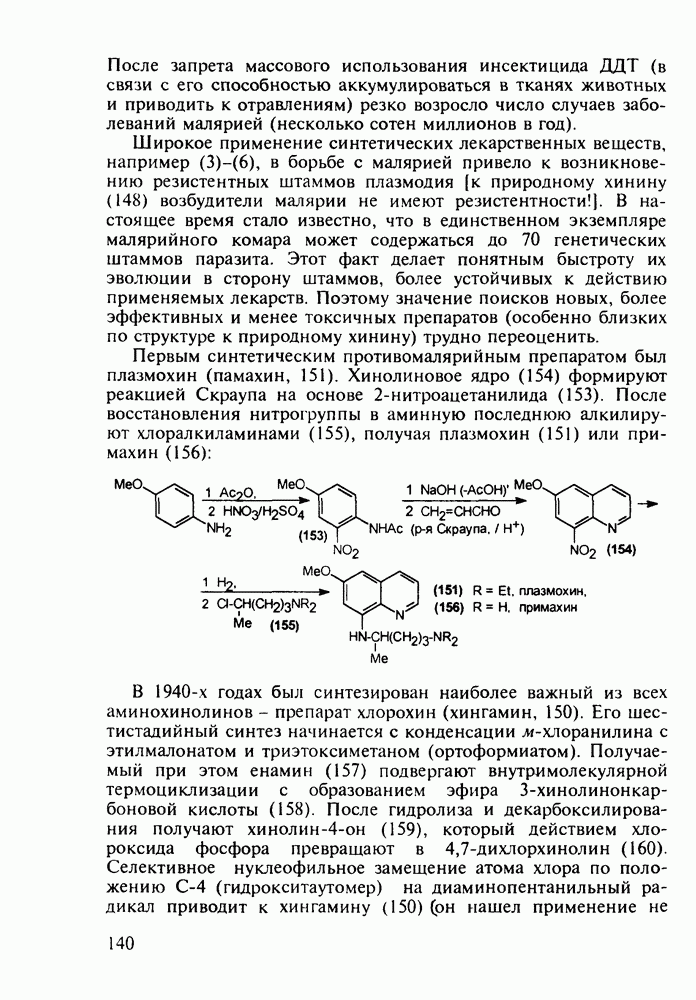
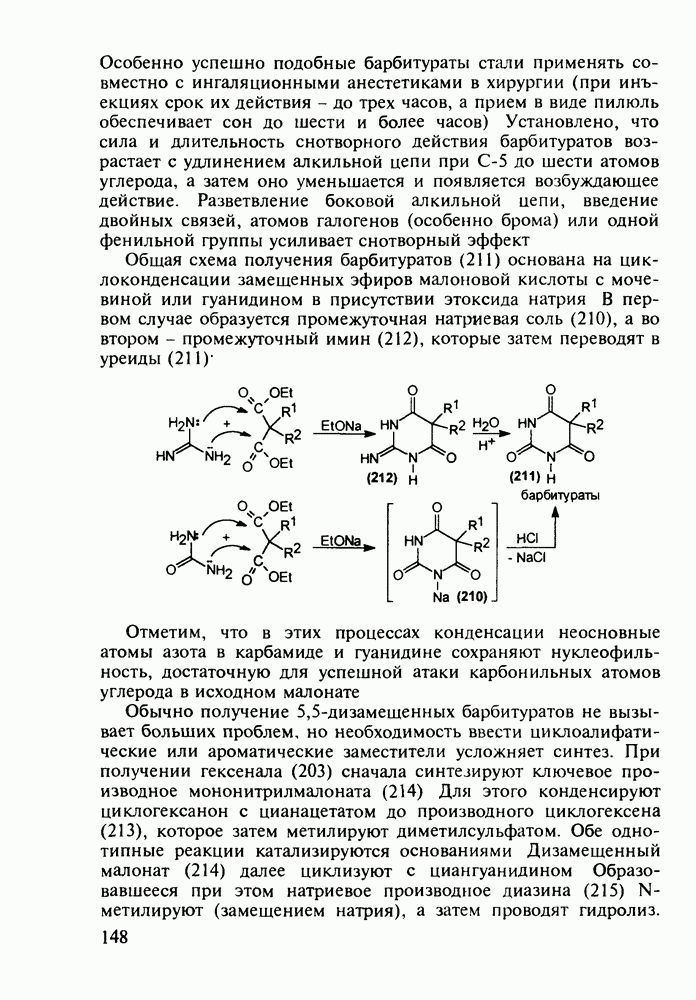
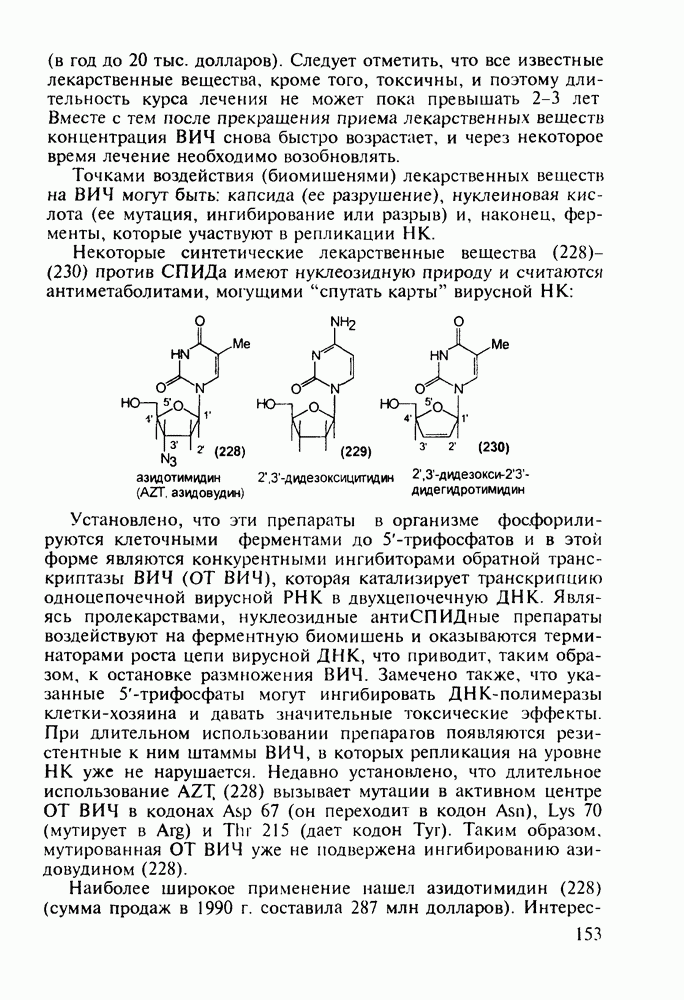
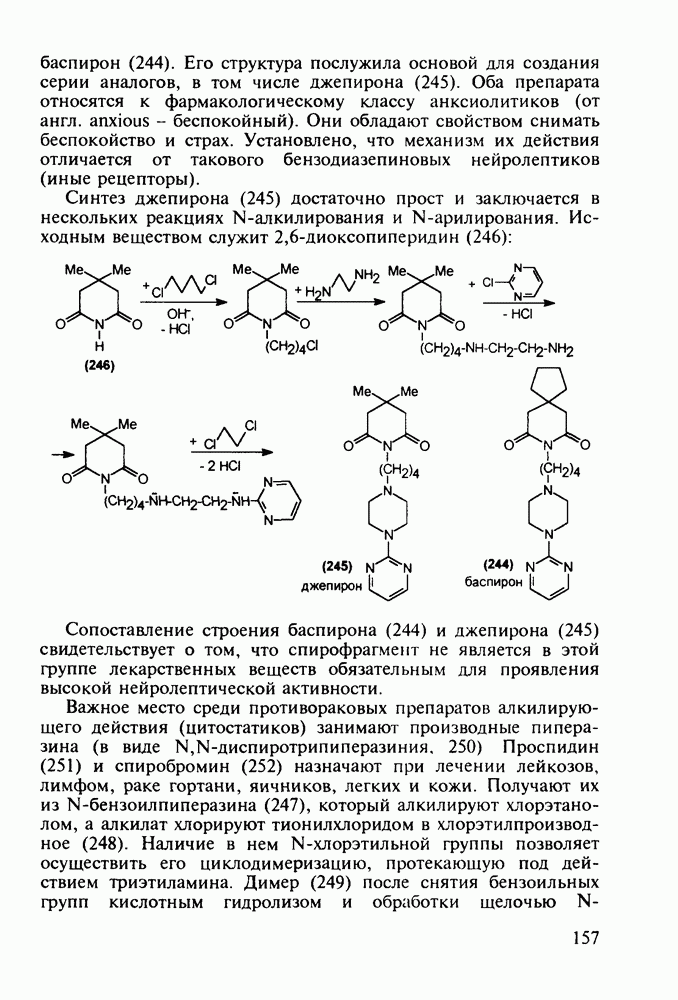
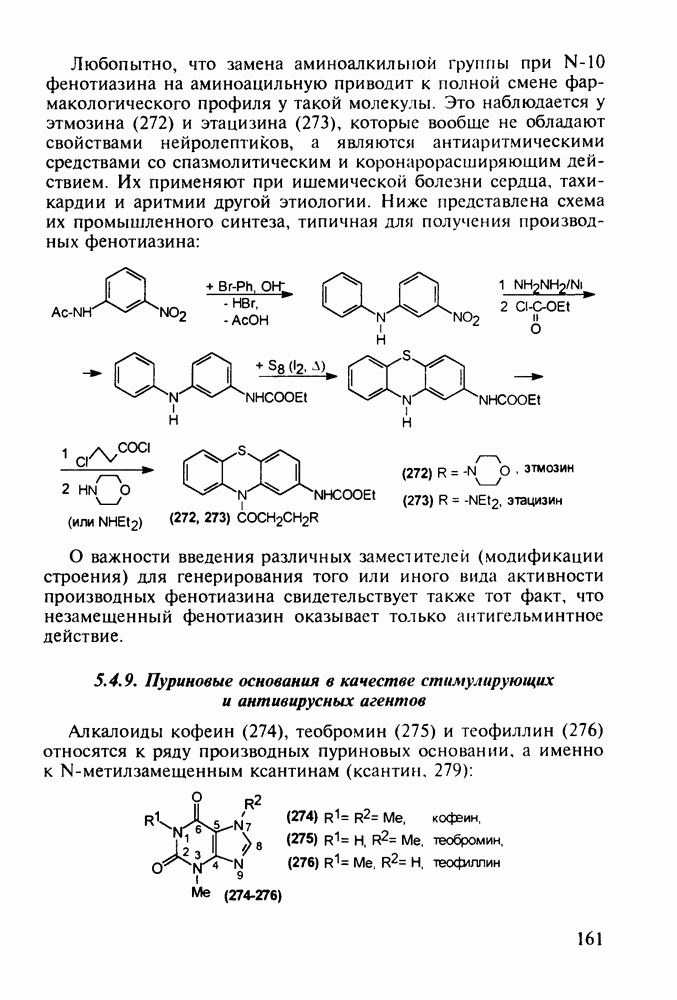
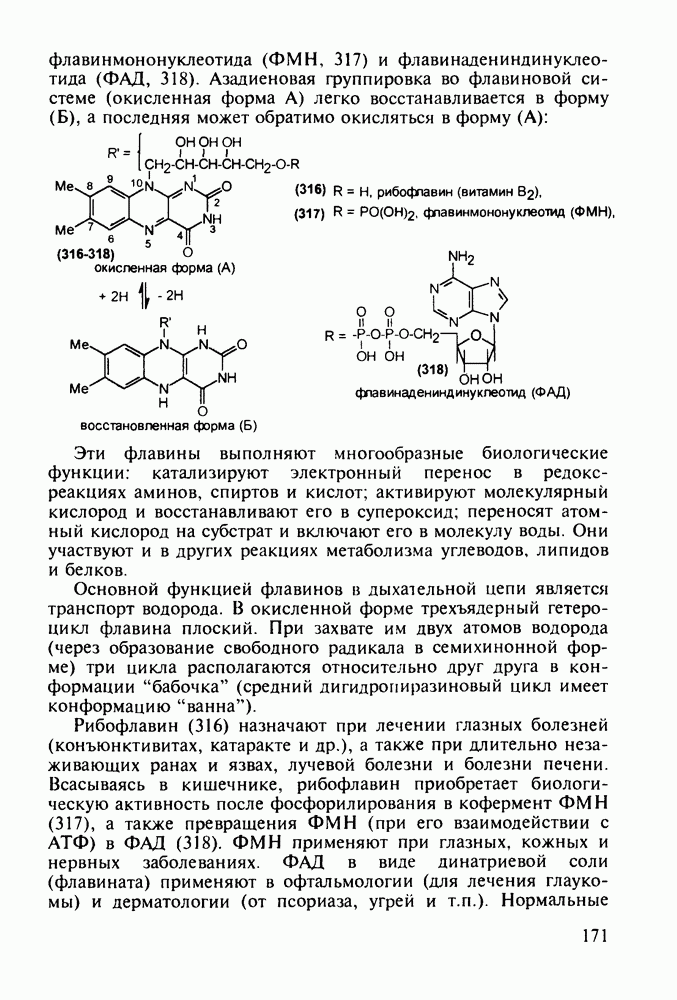
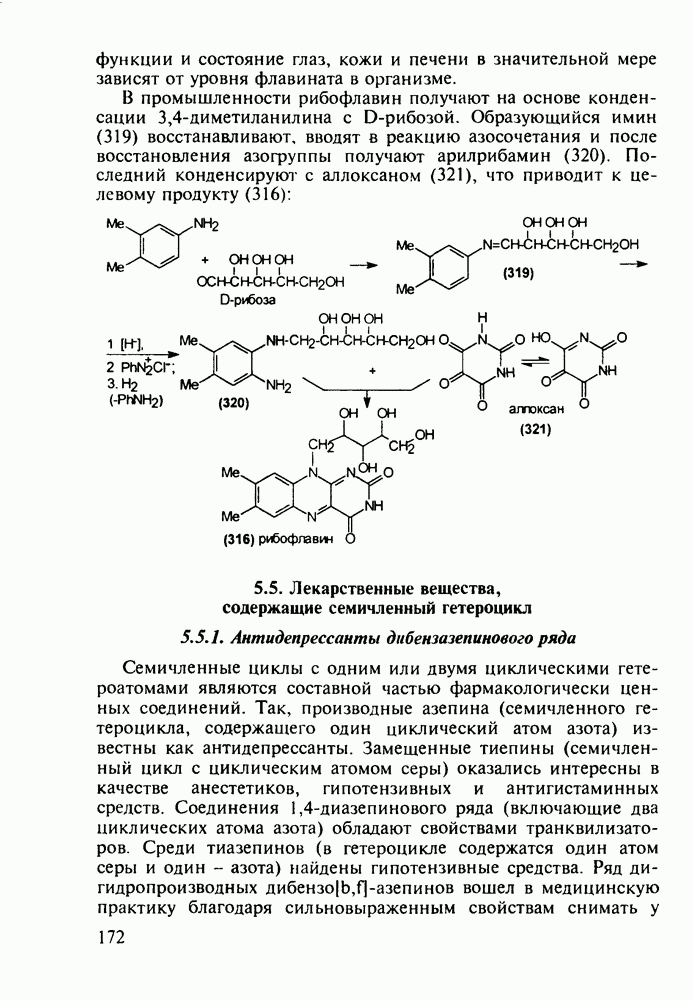
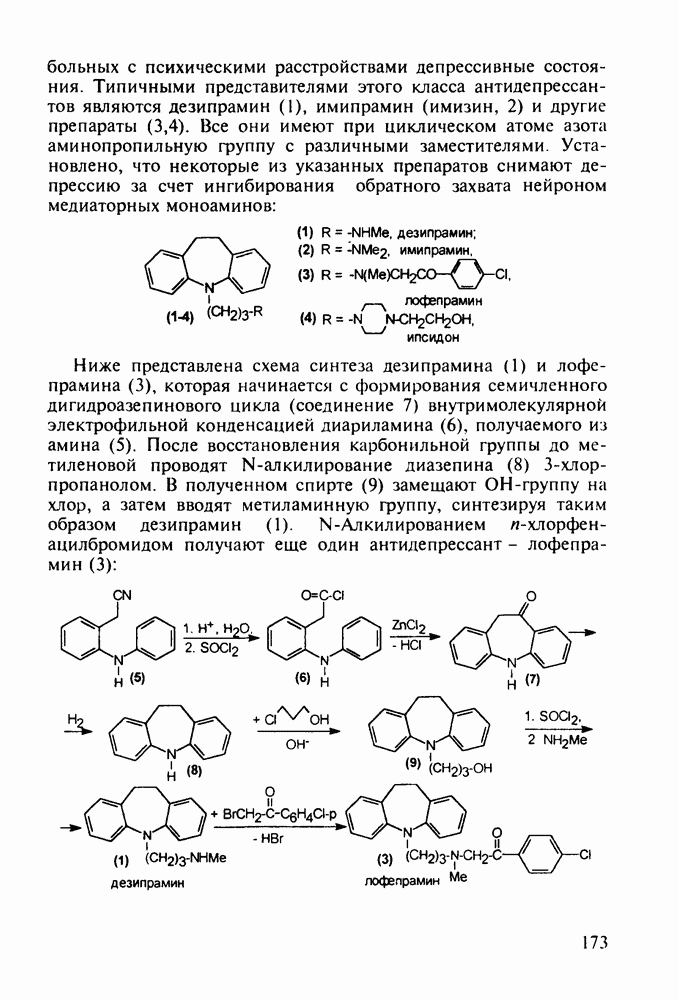
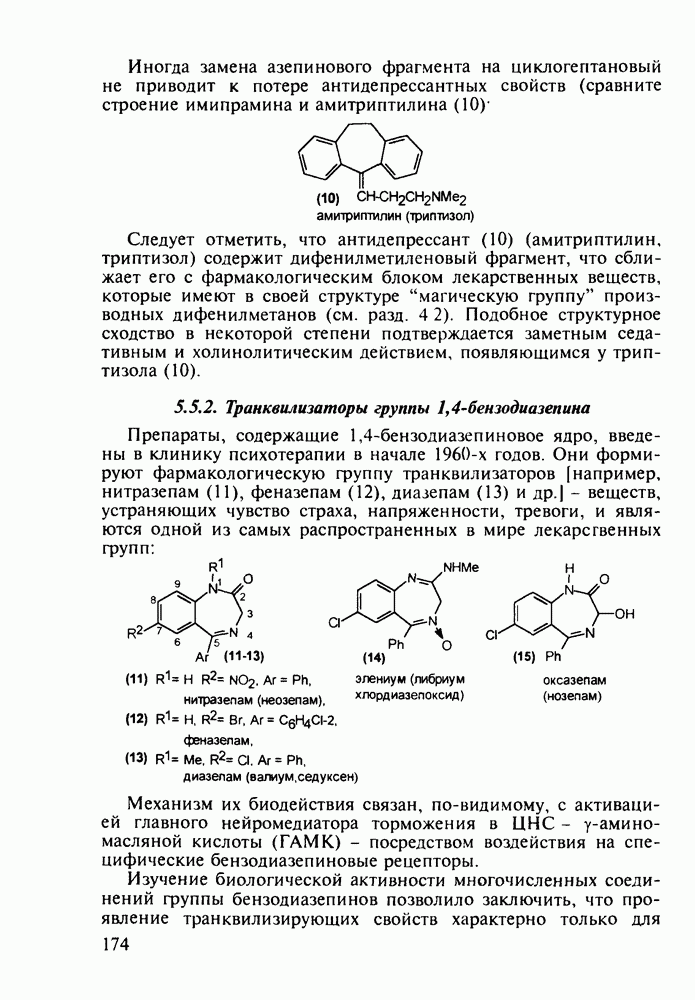
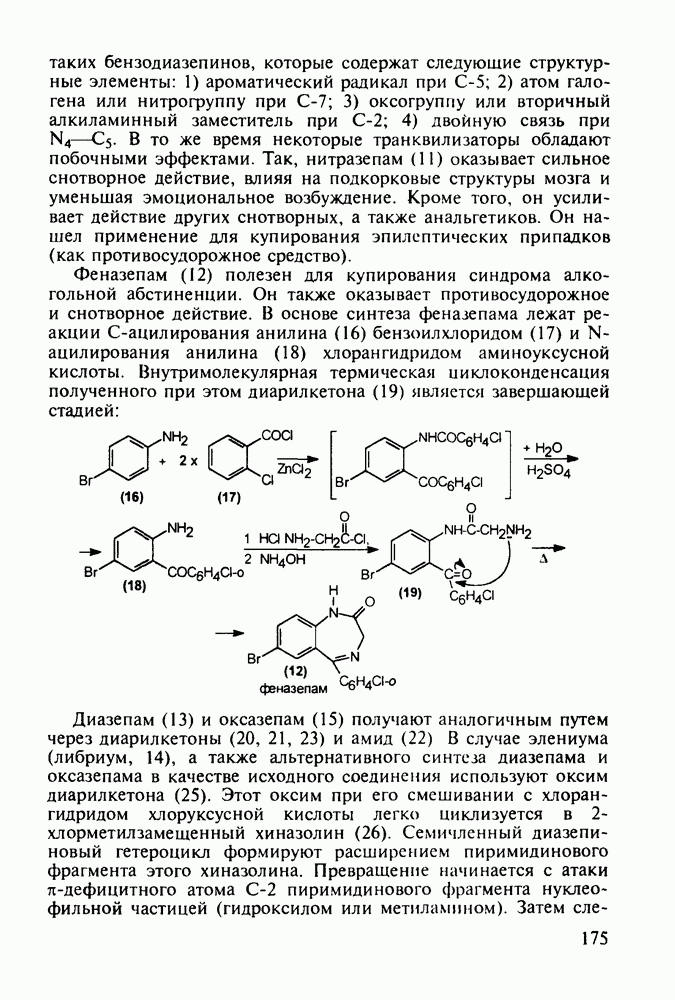
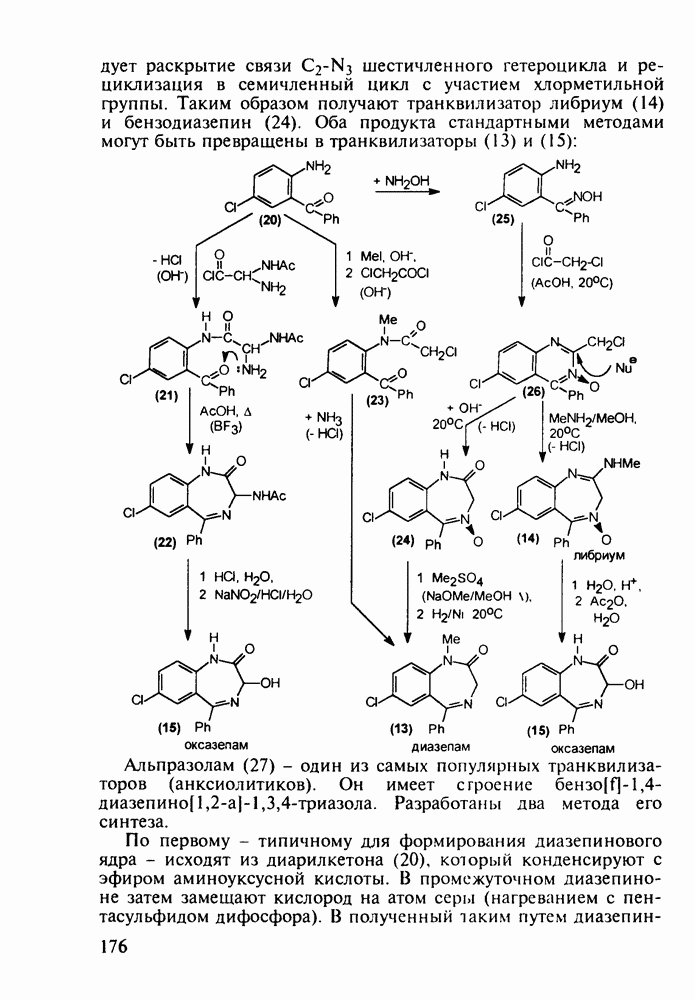
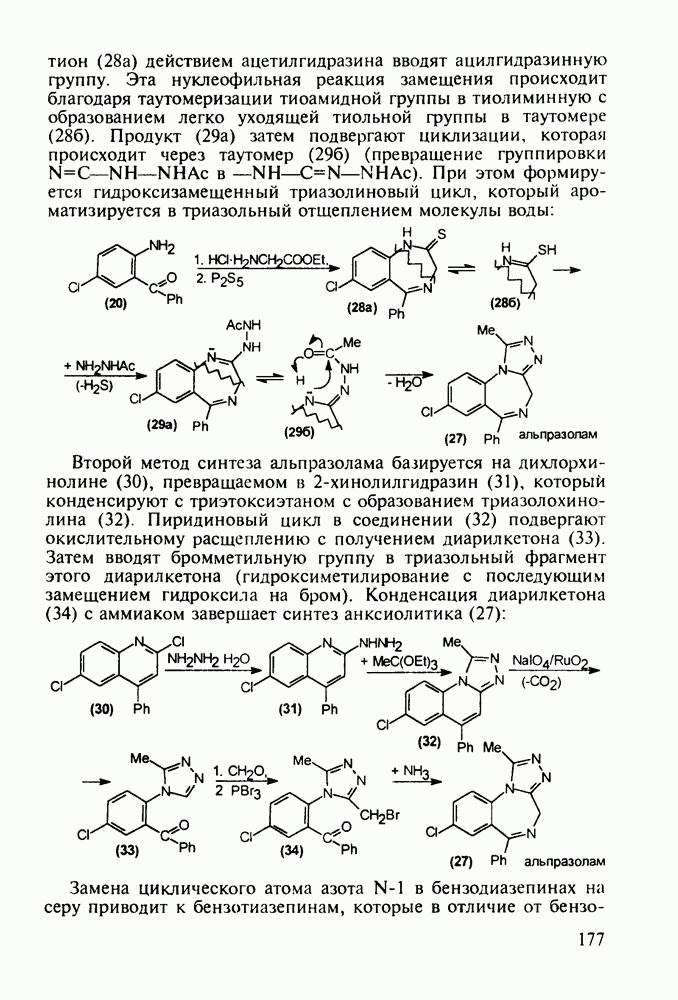
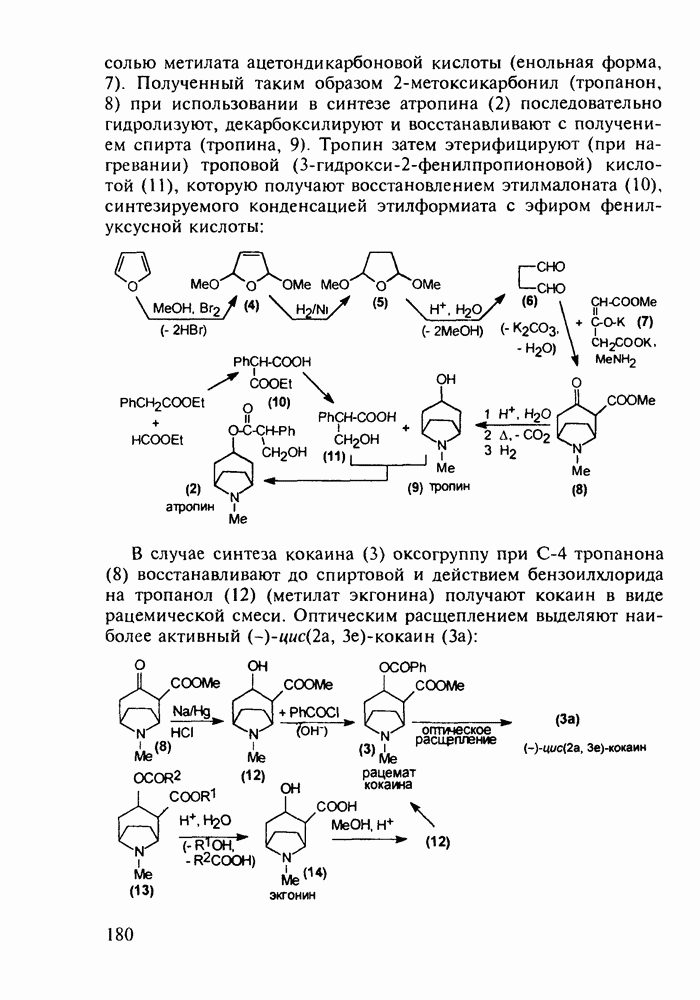
Структура стероидных гормонов - естественных метаболитов, выполняющих регуляторные функции в организме, - включает циклопентановый и циклогексановые фрагменты. Гормоны стероидного типа, в отличие от пептидных гормонов, могут проникать через мембрану в клетку в виде комплекса с рецептором и воздействовать на клеточное ядро и синтез нуклеиновых кислот. Некоторые из них, например эстрон (7) и его 17-этинилпроизводные (8, 9), используют и медицине. Женский половой гормон эстрон (7) обнаружен 70 лет назад в моче беременных женщин. Он контролирует в организме развитие и функционирование половых органов и отвечает за проявление вторичных половых признаков. Вещества (7-9) применяют в качестве противозачаточных средств. Их промышленный синтез основан на гидрировании 2-метоксинафталина (1) до тетралина (2), окислением которого хромовой кислотой до тетралона (3) и обработкой последнего винилмагнийбромидом получают спирт (4). 2-Метилциклопентандион-1,3 как СН-кислота легко присоединяется по винильной группе спирта (4), образуя после дегидратации щелочью соединение (5), которое далее подвергают кислотнокатализируемой циклизации с отщеплеиием одной молекулы воды. В результате возникает конденсированный четырехъядерный остов молекулы (6). Гидрированием  олефиновой связи с последующим гидролизом метоксильной группы
олефиновой связи с последующим гидролизом метоксильной группы
получают эстрон (7):

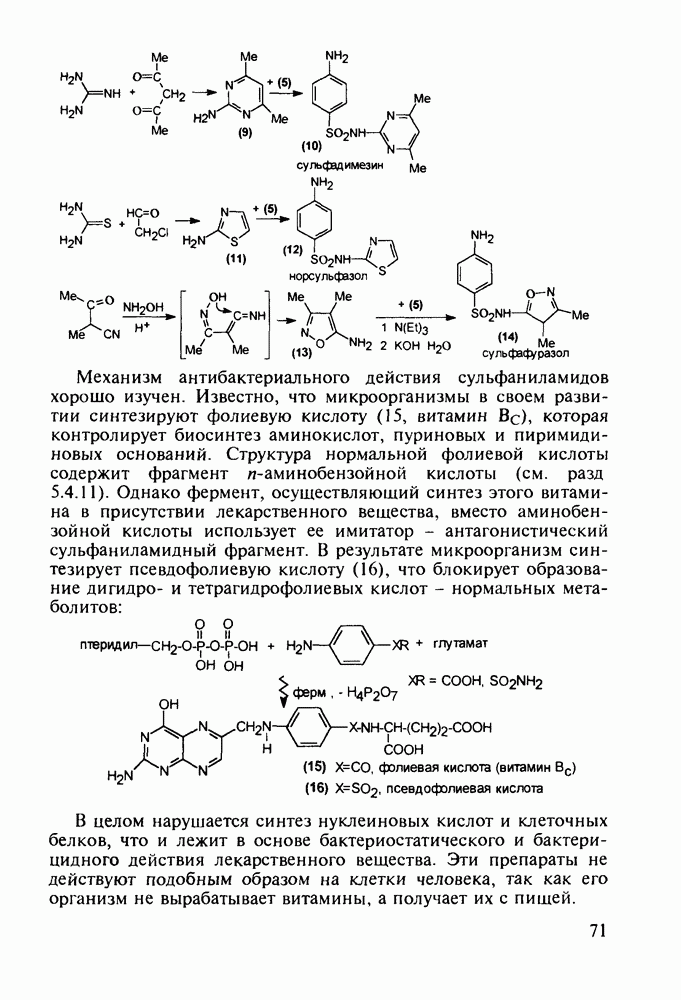
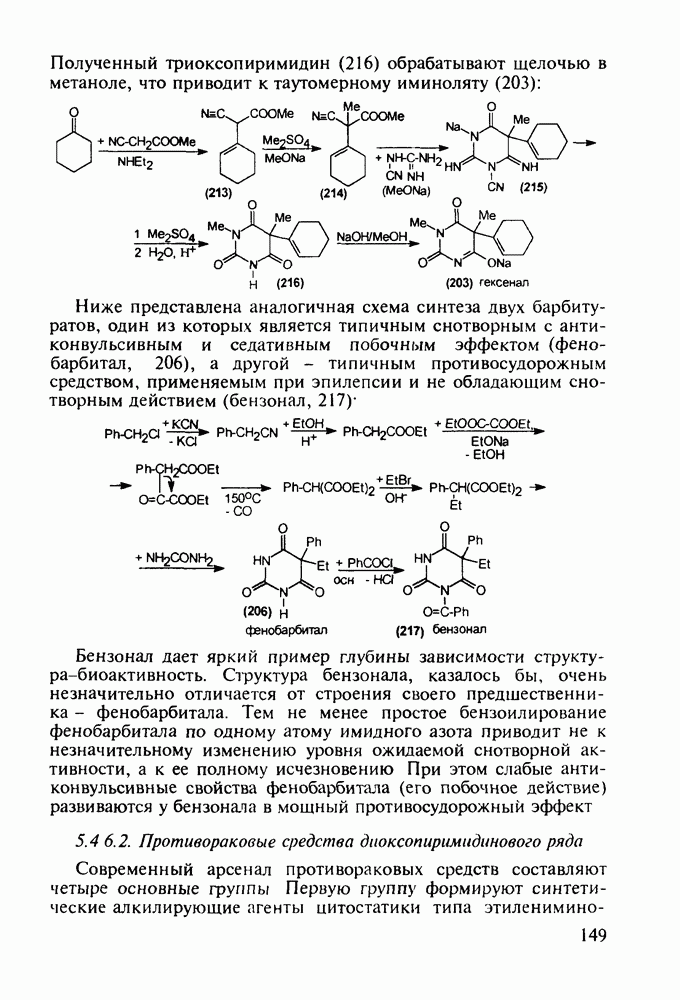
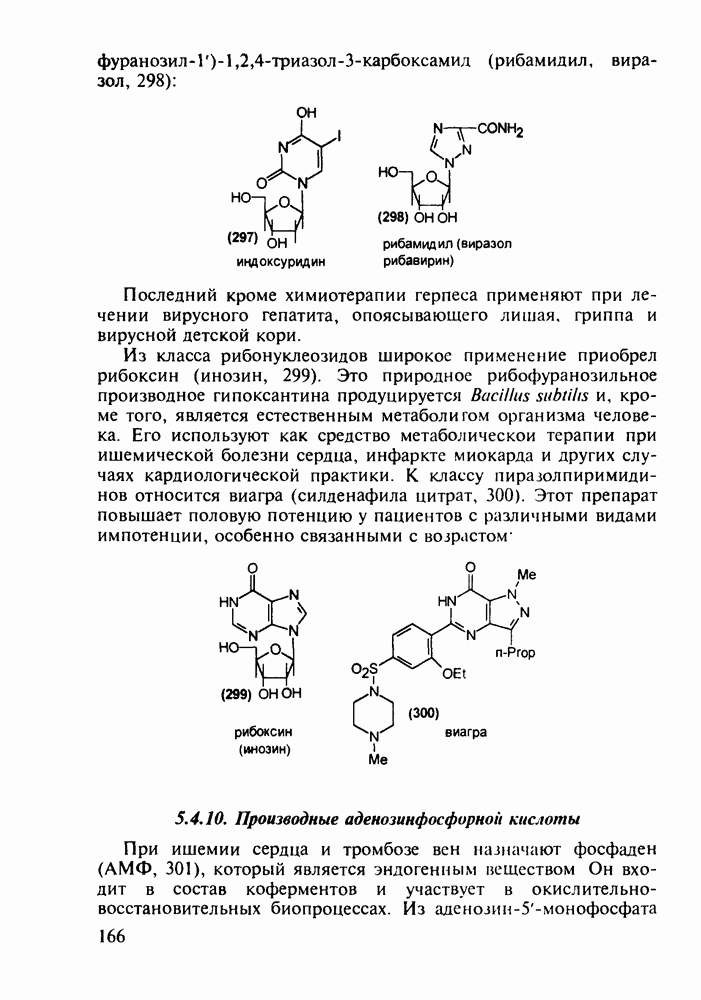
Из эстрона присоединением ацетилена синтезируют эстрогенные компоненты эффективных пероральных противозачаточных средств (антиовуляторов) эгинилэстрадиола  и местранола
и местранола  , которые тормозят наступление овуляции:
, которые тормозят наступление овуляции:

На основе эстрона осуществлены синтезы ряда других веществ аналогичного биодействия. Следует отметить, что ведутся работы по замене стероидных противозачаточных средств на агенты нестероидного типа в связи с тем. что появляются данные по проявлению тромбозов у женщин, а также случаи генерации опухолей у лабораторных животных под действием стероидных антиовуляторов.
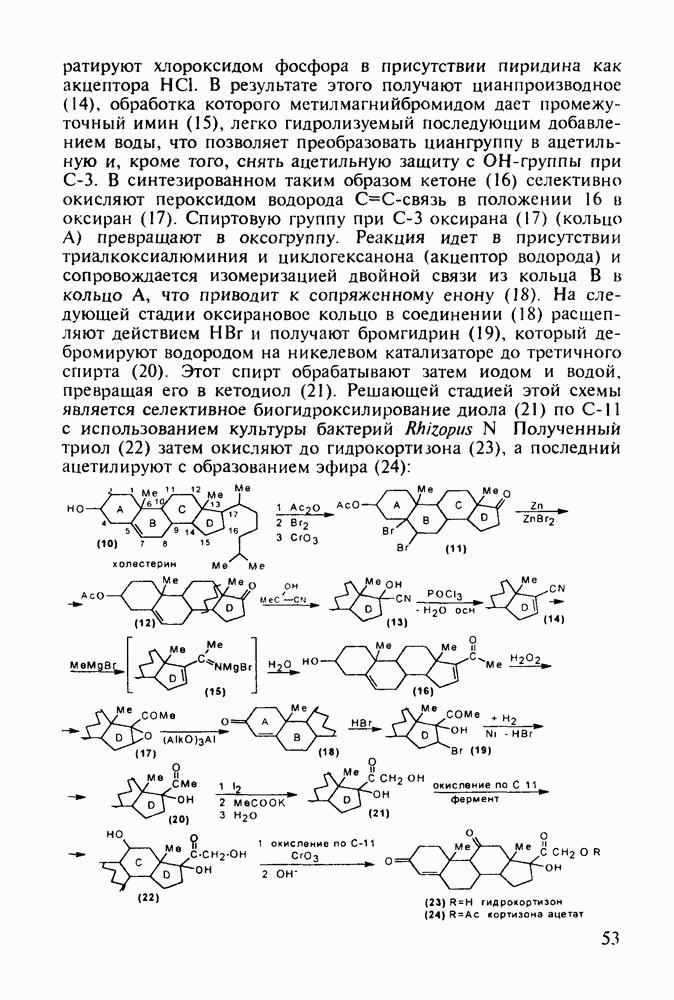
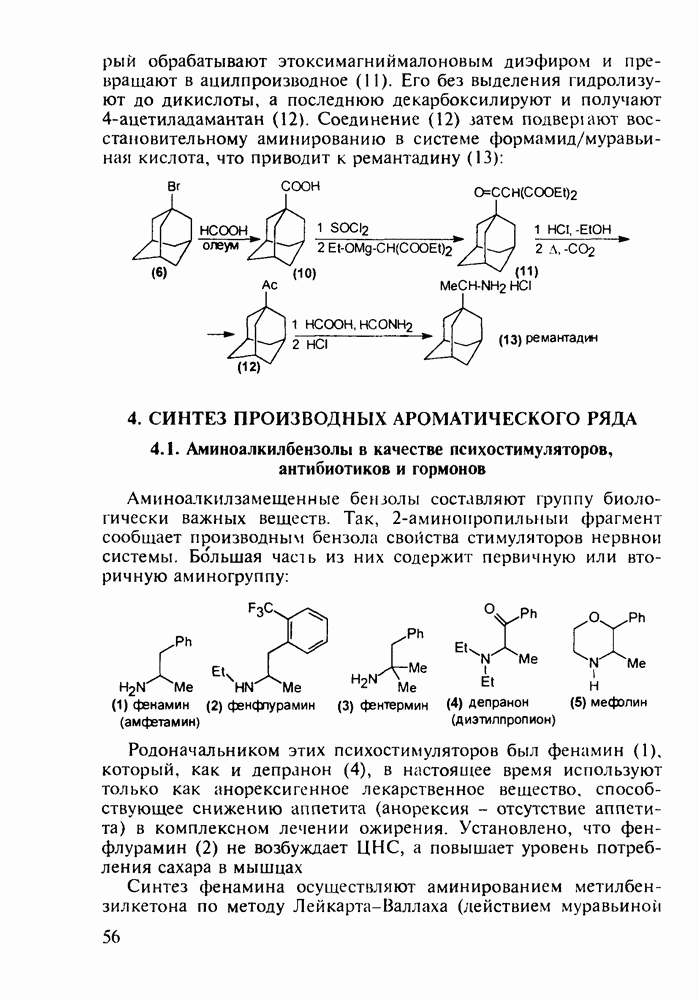
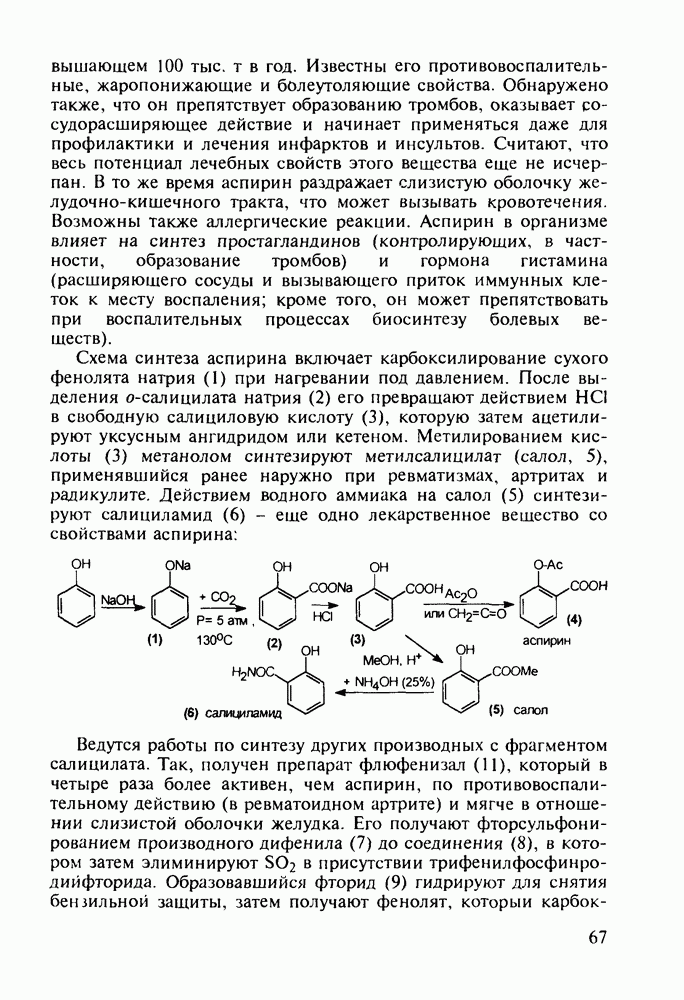
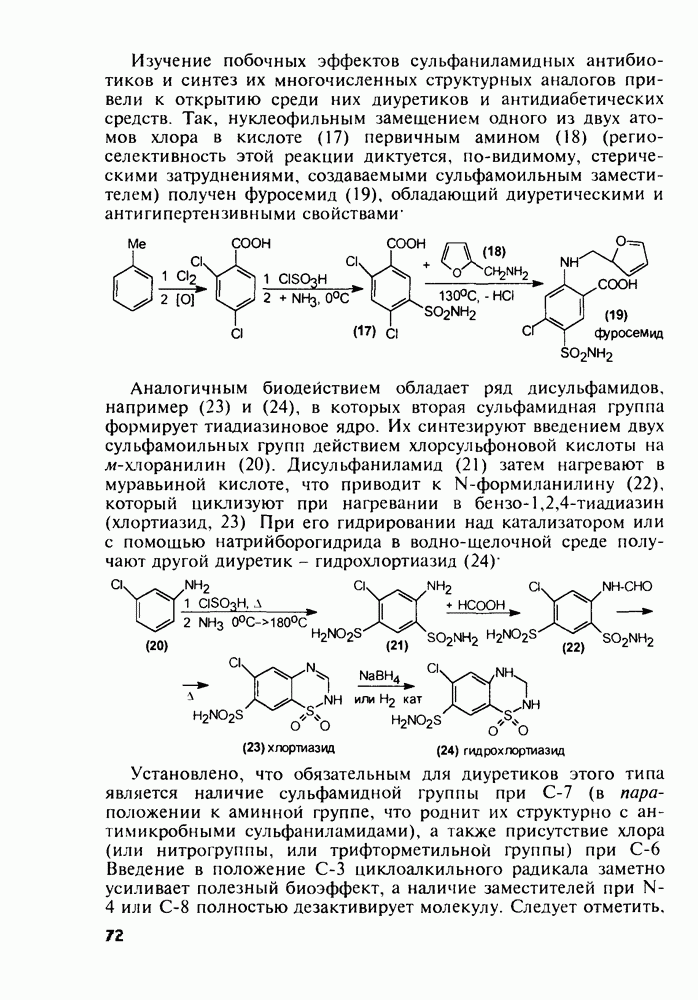
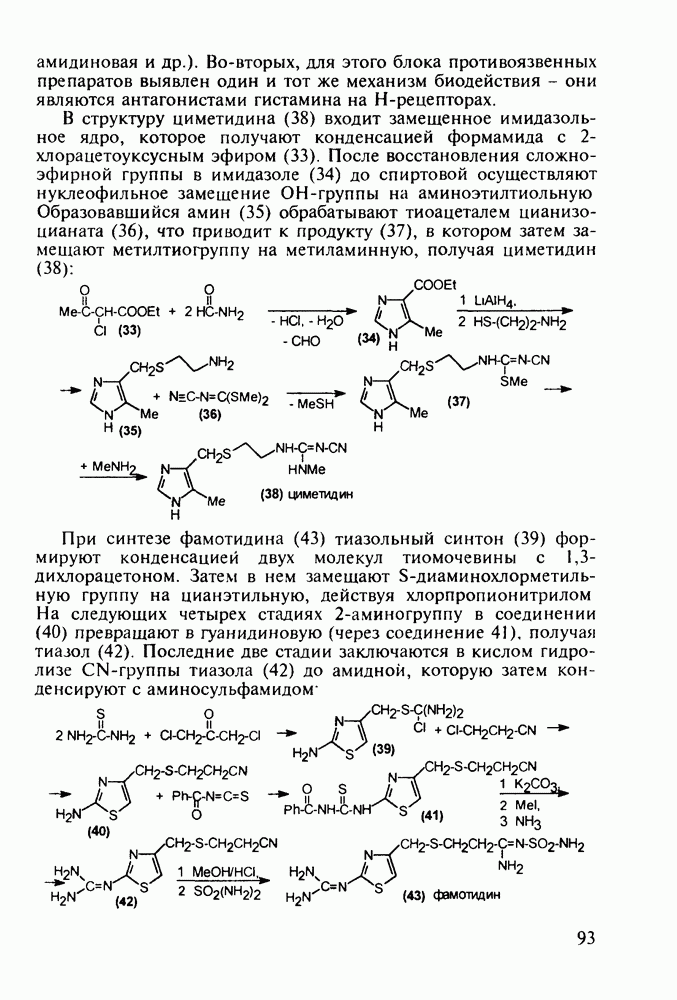
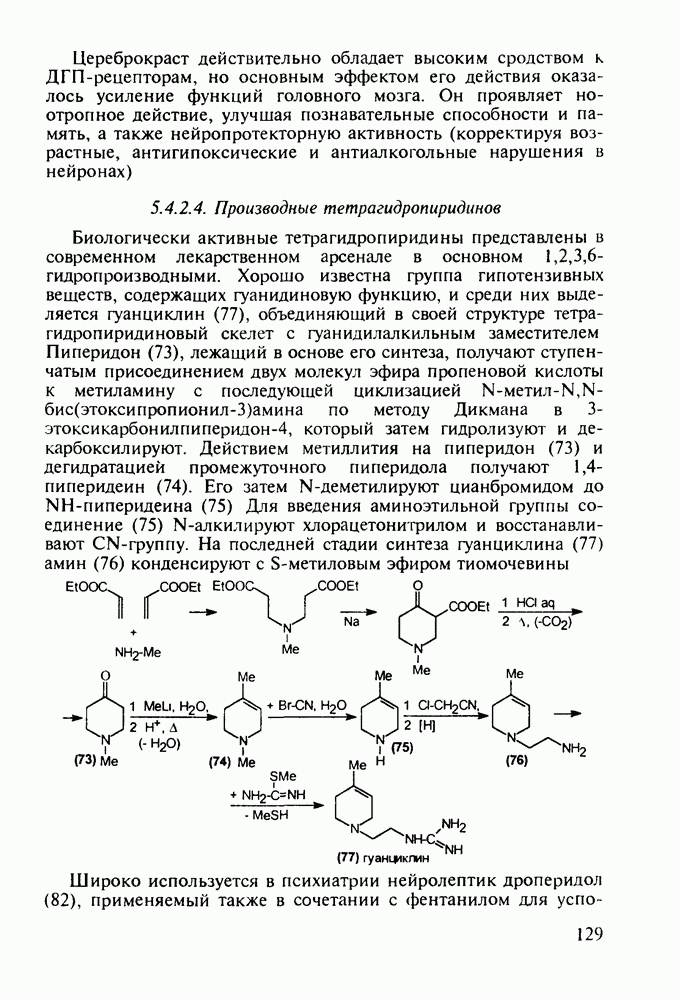
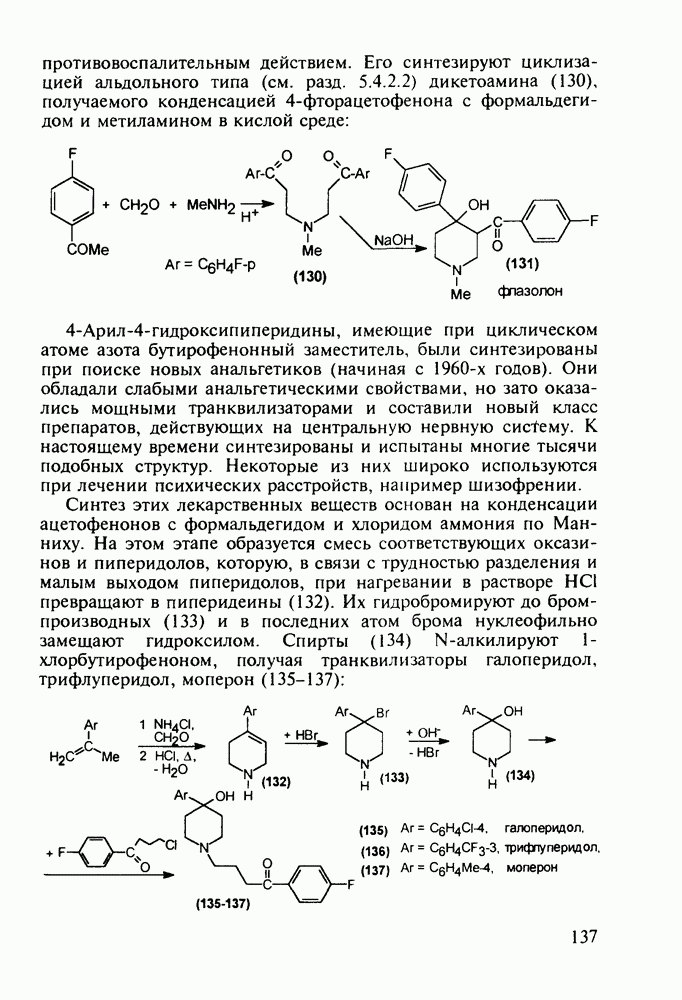
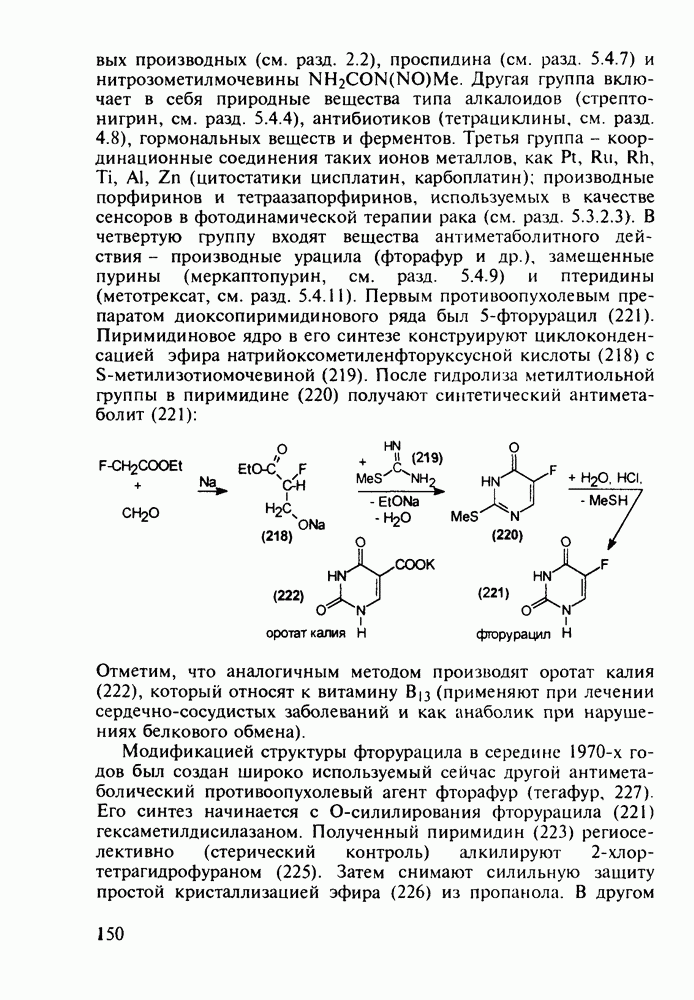
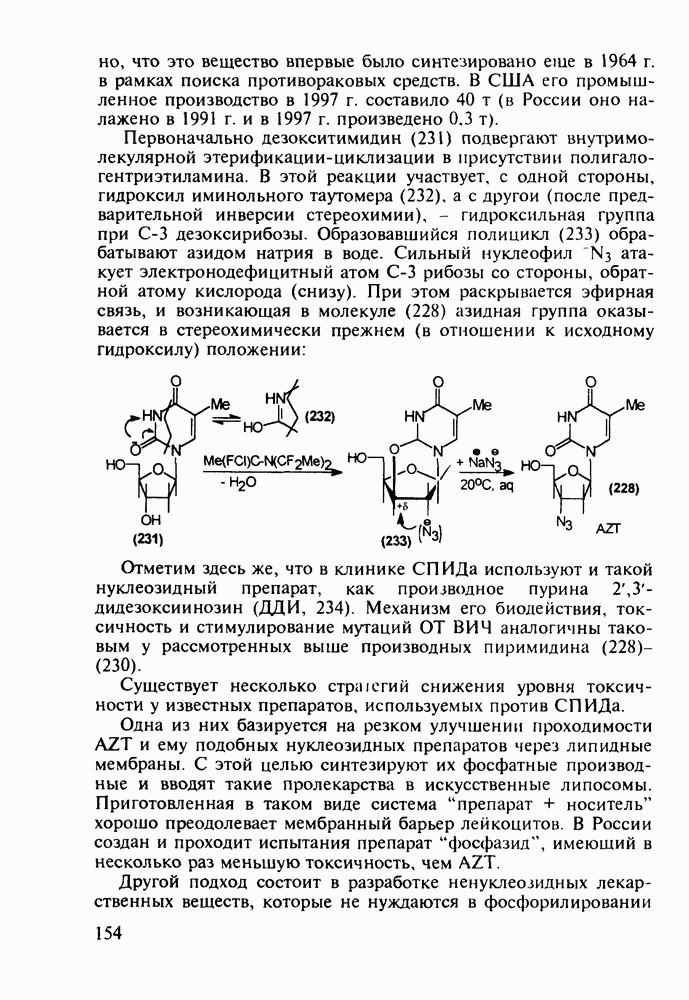
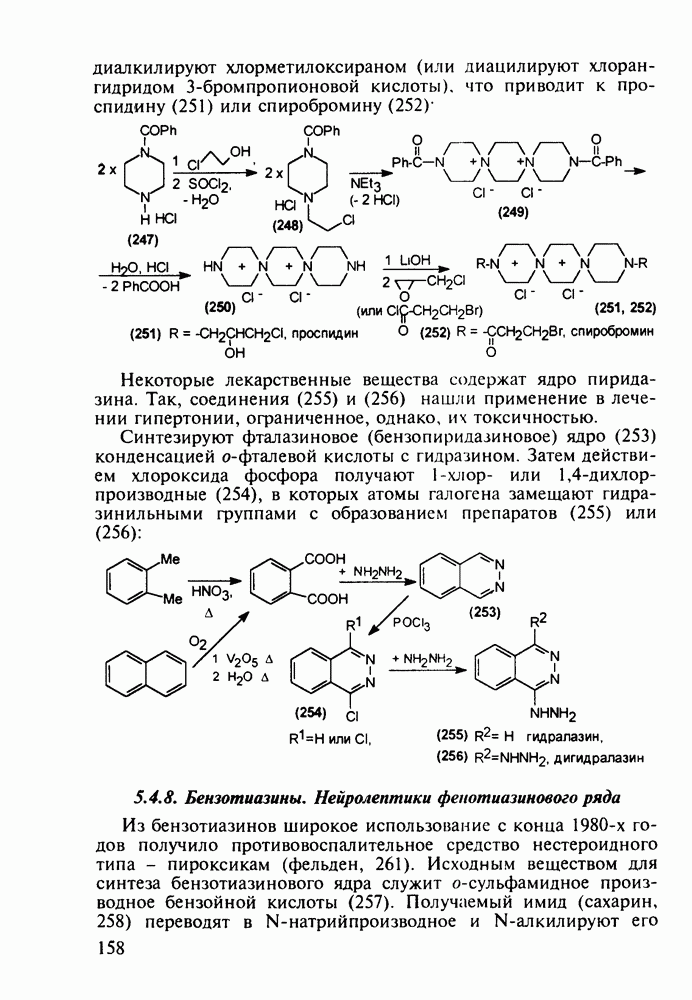
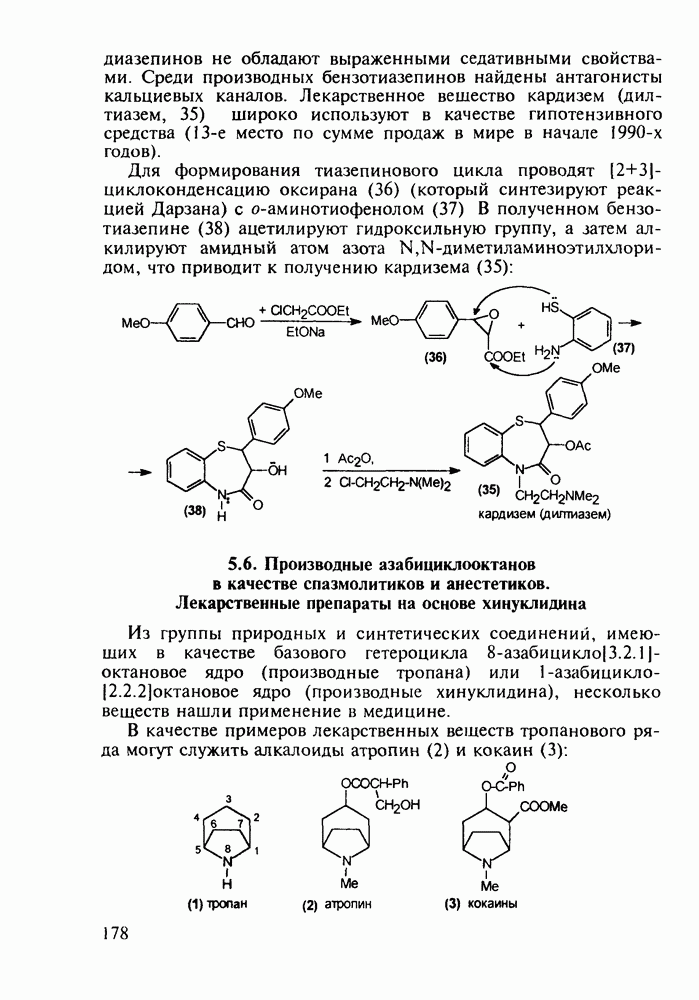
Ряд стероидов обладает противовоспалительным и антиаллергическим действием. К ним относятся кортизон, преднизон и преднизолон, которые в виде сложных моноэфиров, проявляющих лучшую лечебную активность, назначаются при ревматизме, полиартритах, бронхиальной астме, экземе, аллергических и других заболеваниях. Их получают из природного вещества холестерина по следующей схеме. Сначала холестерин (10) окислительным отщеплением боковой алкильнои группы при  хромовым ангидридом (после предварительной защиты ОН- и С=С-групп соответственно ацилированием и бромированием) переводят в дибромкетон (11). Этот кетон дебромируют действием Zn и получают ацетат дегидроэпиандросгерона (12), в котором затем кольцо D химически модифицируют Его цианируют ацетонциангидрином до спирта (13), который далее дегидратируют
хромовым ангидридом (после предварительной защиты ОН- и С=С-групп соответственно ацилированием и бромированием) переводят в дибромкетон (11). Этот кетон дебромируют действием Zn и получают ацетат дегидроэпиандросгерона (12), в котором затем кольцо D химически модифицируют Его цианируют ацетонциангидрином до спирта (13), который далее дегидратируют
хлороксидом фосфора в присутствии пиридина как акцептора  . В результате этого получают цианпроизводное (14), обработка которого метилмагнийбромидом дает промежуточный имин (15), легко гидролизуемый последующим добавлением воды, что позволяет преобразовать циангруппу в ацетильную и, кроме того, снять ацетильную защиту с ОН-группы при
. В результате этого получают цианпроизводное (14), обработка которого метилмагнийбромидом дает промежуточный имин (15), легко гидролизуемый последующим добавлением воды, что позволяет преобразовать циангруппу в ацетильную и, кроме того, снять ацетильную защиту с ОН-группы при  . В синтезированном таким образом кетоне (16) селективно окисляют пероксидом водорода
. В синтезированном таким образом кетоне (16) селективно окисляют пероксидом водорода  -связь в положении 16 и оксиран (17). Спиртовую группу при
-связь в положении 16 и оксиран (17). Спиртовую группу при  оксирана (17) (кольцо А) превращают в оксогруппу. Реакция идет в присутствии триалкоксиалюминия и циклогексанона (акцептор водорода) и сопровождается изомеризацией двойной связи из кольца В в кольцо А, что приводит к сопряженному енону (18). На следующей стадии оксирановое кольцо в соединении (18) расщепляют действием
оксирана (17) (кольцо А) превращают в оксогруппу. Реакция идет в присутствии триалкоксиалюминия и циклогексанона (акцептор водорода) и сопровождается изомеризацией двойной связи из кольца В в кольцо А, что приводит к сопряженному енону (18). На следующей стадии оксирановое кольцо в соединении (18) расщепляют действием  и получают бромгидрин (19), который дебромируют водородом на никелевом катализаторе до третичного спирта (20). Этот спирт обрабатывают затем иодом и водой, превращая его в кетодиол (21). Решающей стадией этой схемы является селективное биогидроксилирование диола (21) по
и получают бромгидрин (19), который дебромируют водородом на никелевом катализаторе до третичного спирта (20). Этот спирт обрабатывают затем иодом и водой, превращая его в кетодиол (21). Решающей стадией этой схемы является селективное биогидроксилирование диола (21) по  с использованием культуры бактерий Rhizopus N Полученный триол (22) затем окисляют до гидрокортизона (23), а последний ацетилируют с образованием эфира (24):
с использованием культуры бактерий Rhizopus N Полученный триол (22) затем окисляют до гидрокортизона (23), а последний ацетилируют с образованием эфира (24):

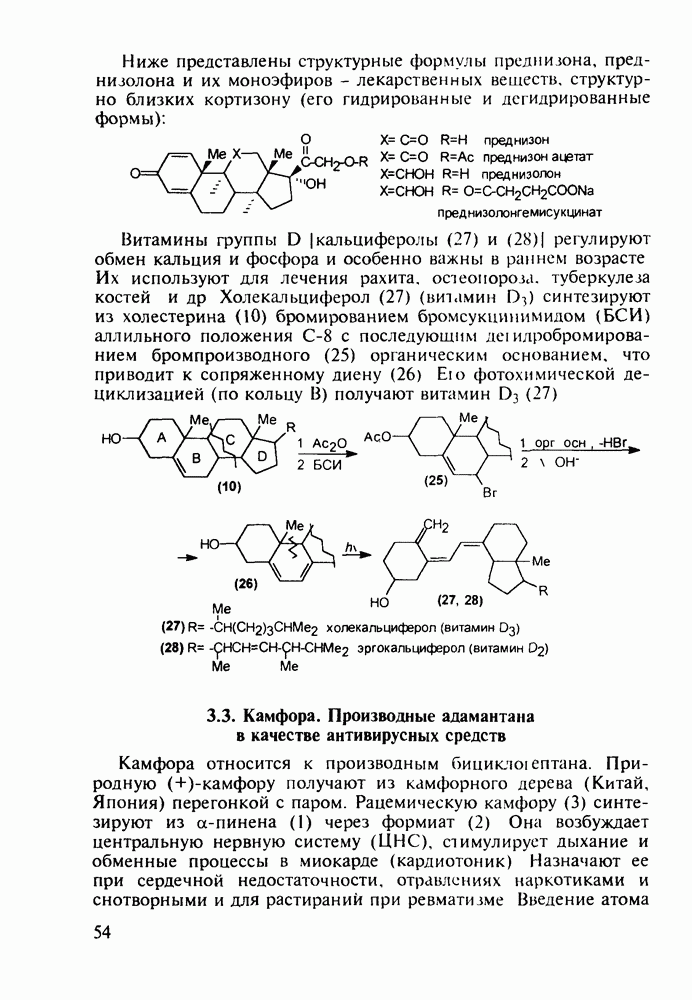
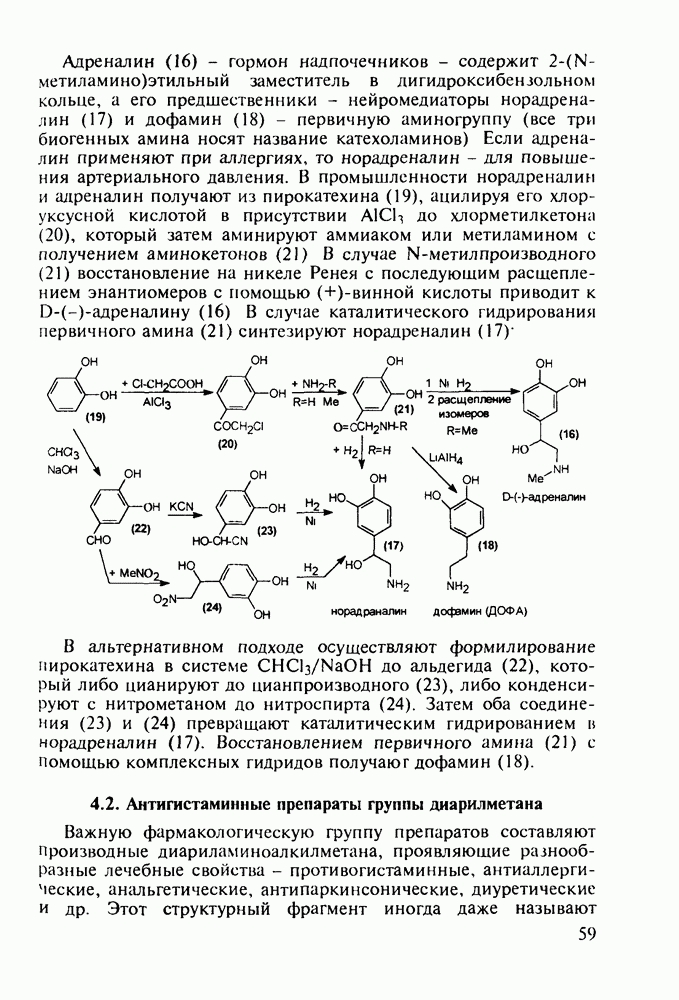
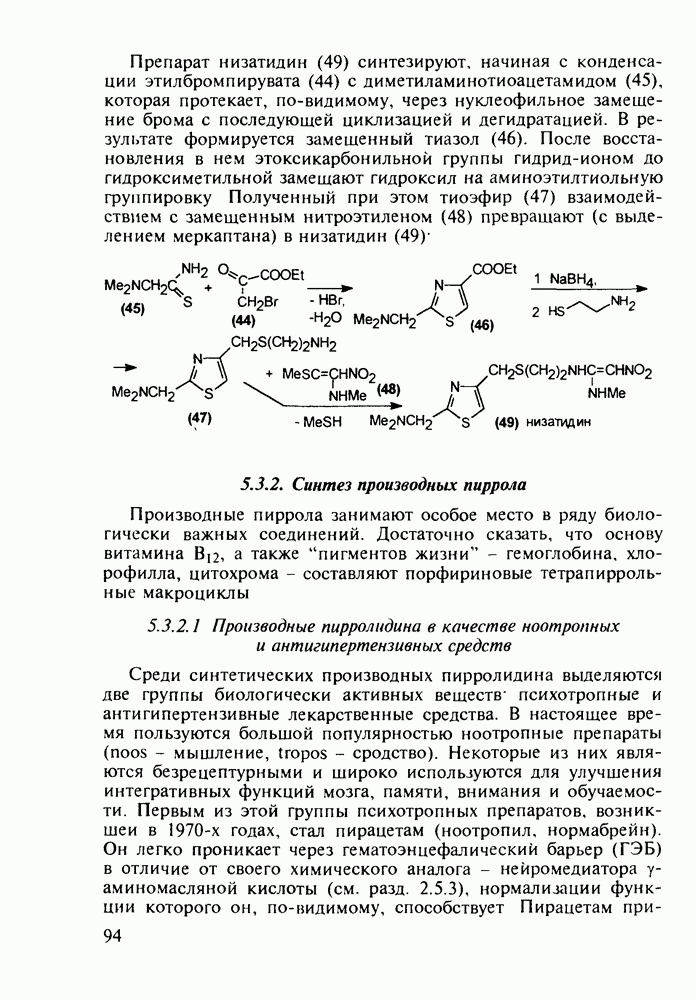
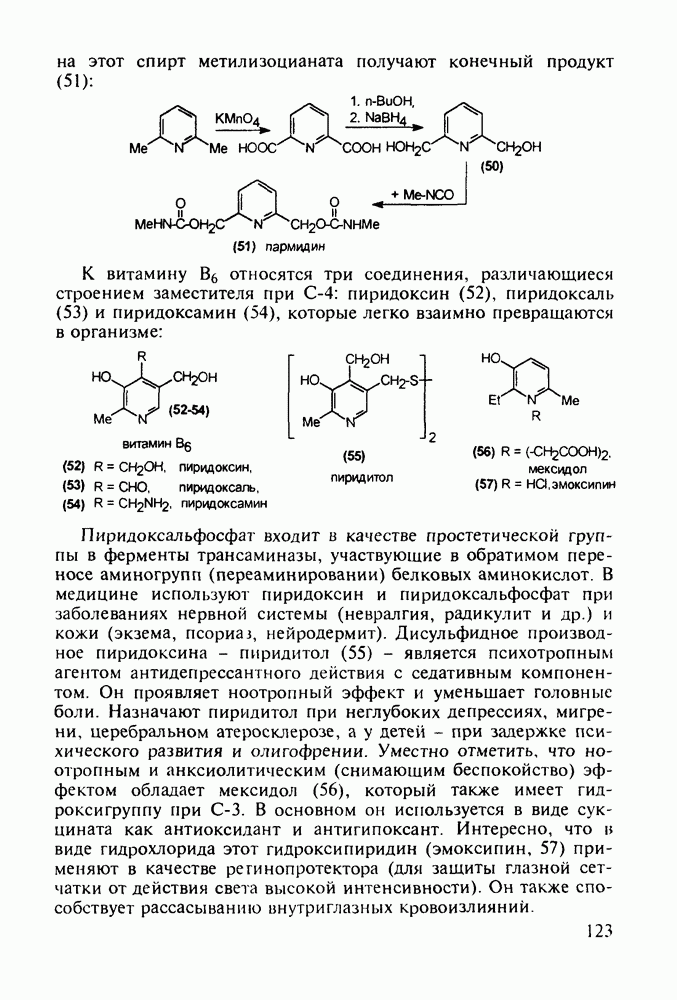
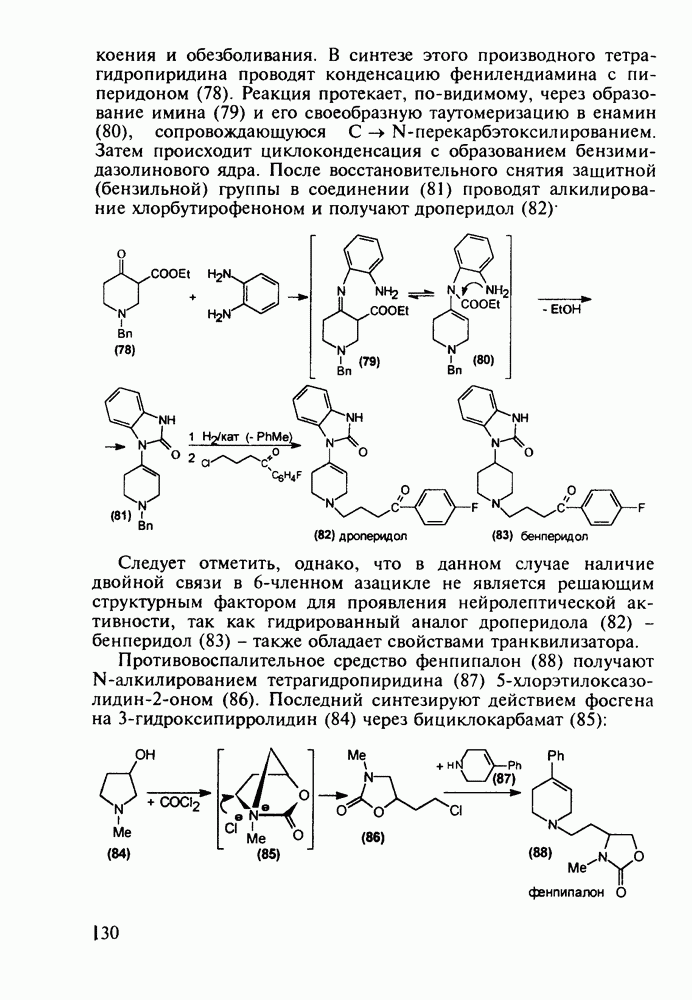
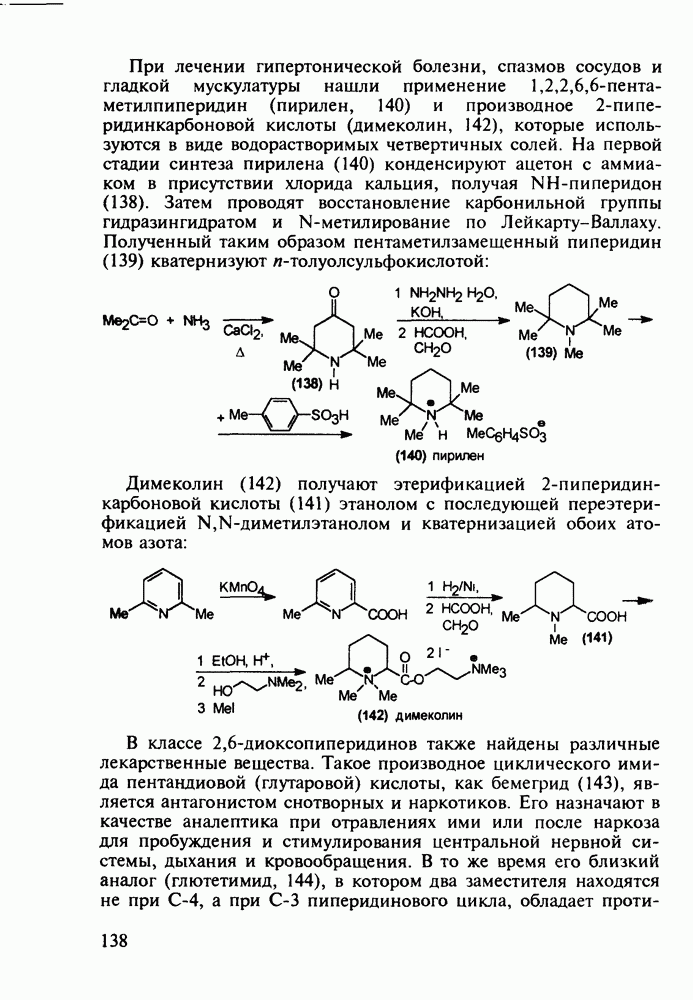
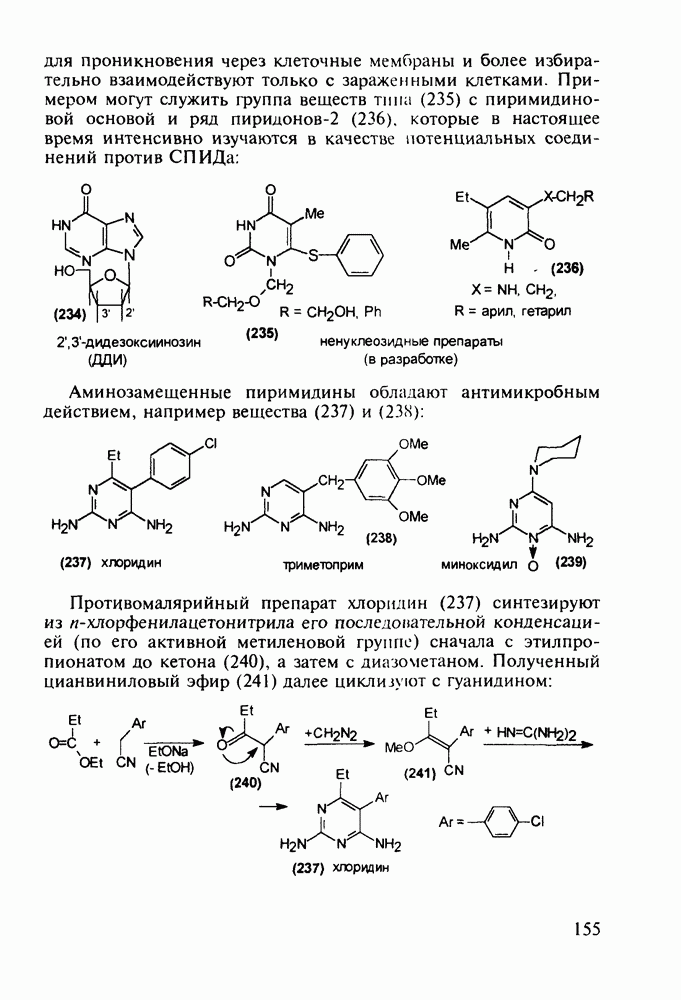
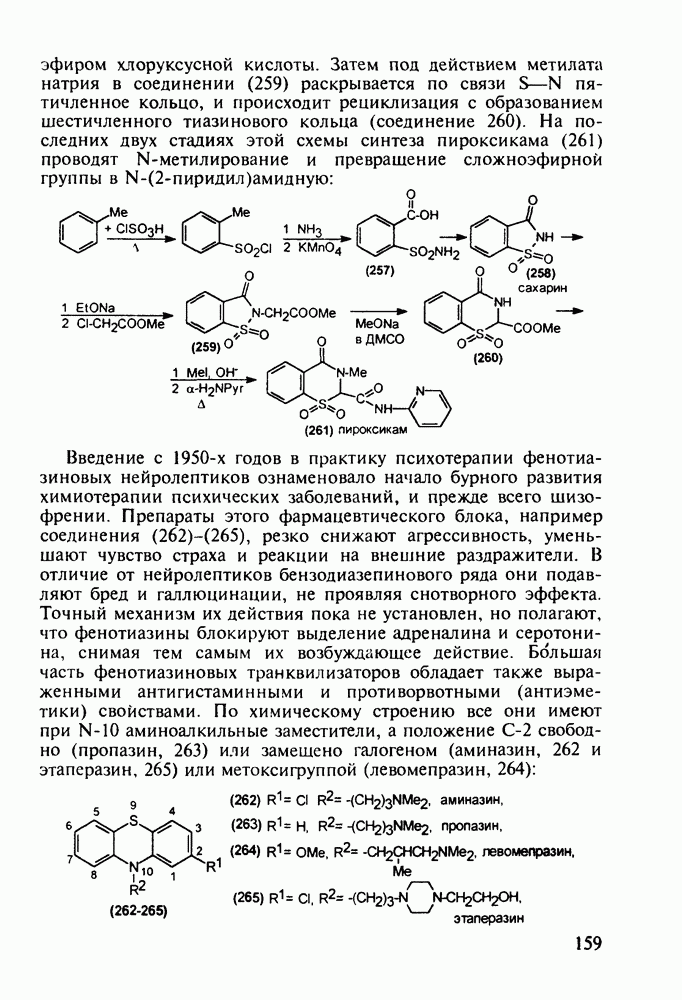
Ниже представлены структурные формулы преднизона, преднизолона и их моноэфиров - лекарственных веществ, структурно близких кортизону (его гидрированные и дегидрированные формы):

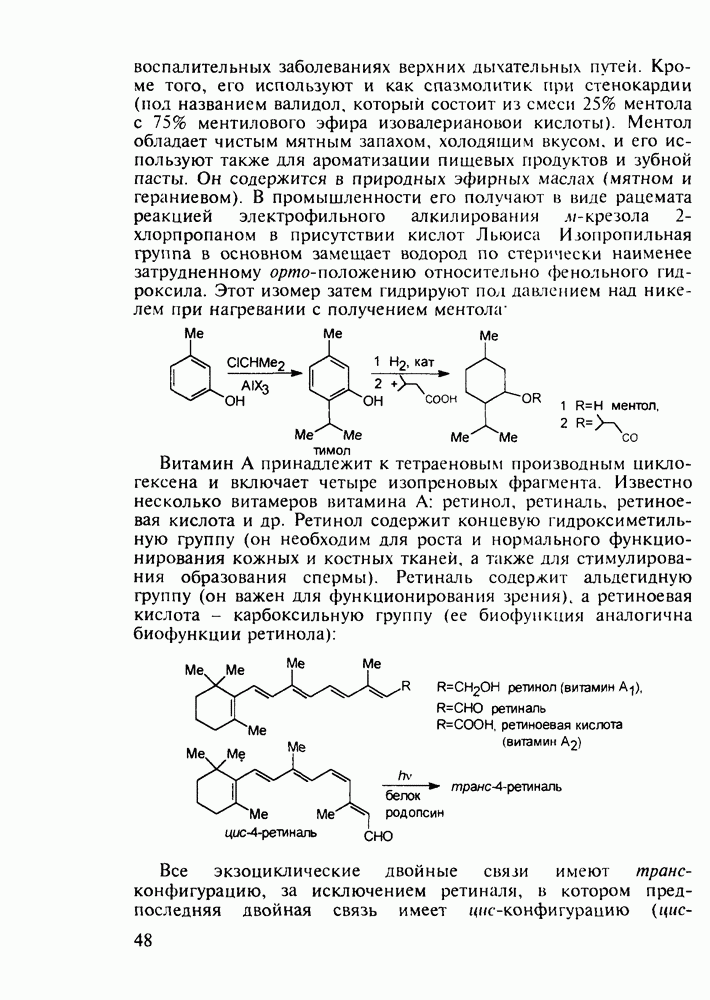
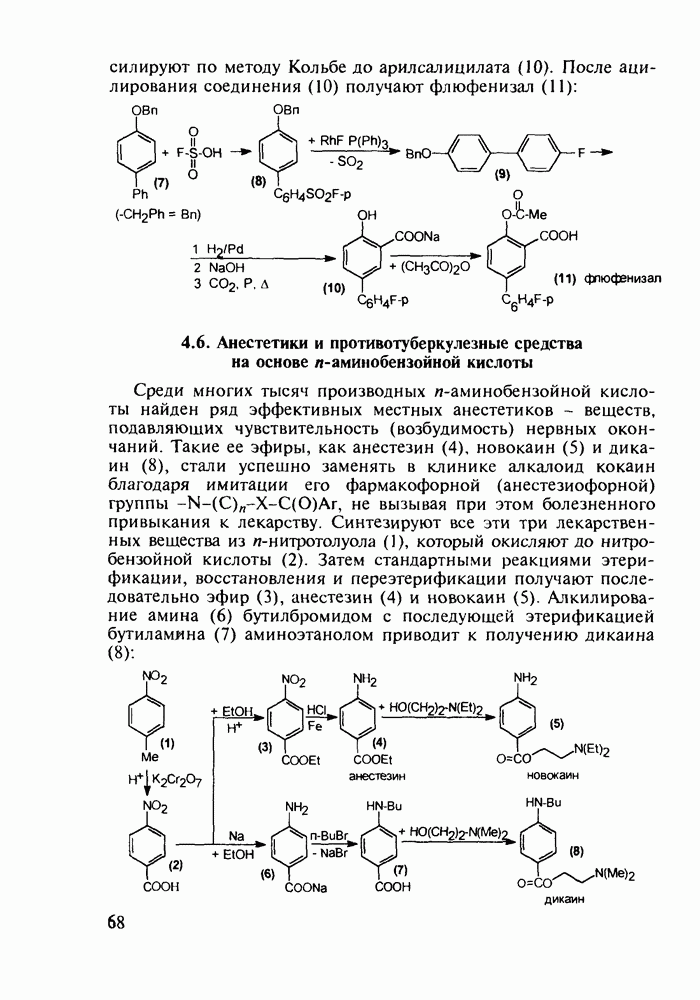
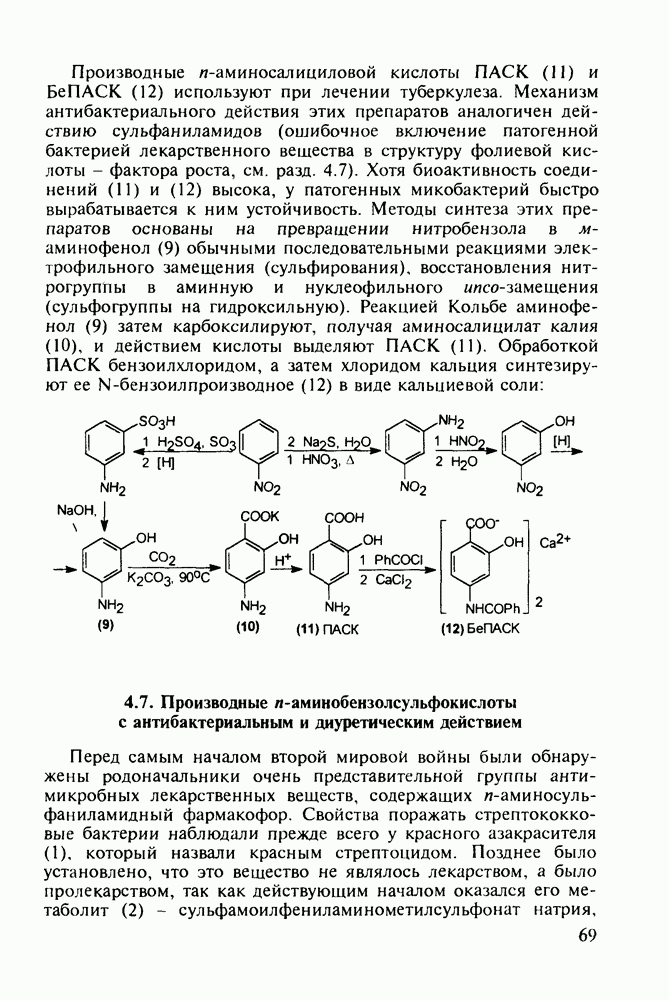
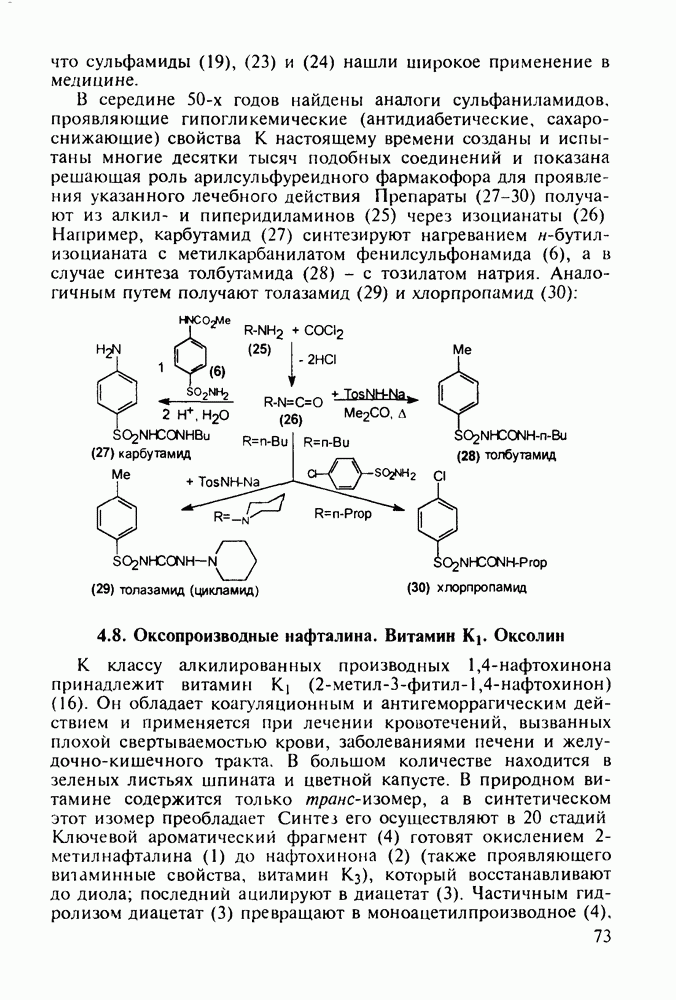
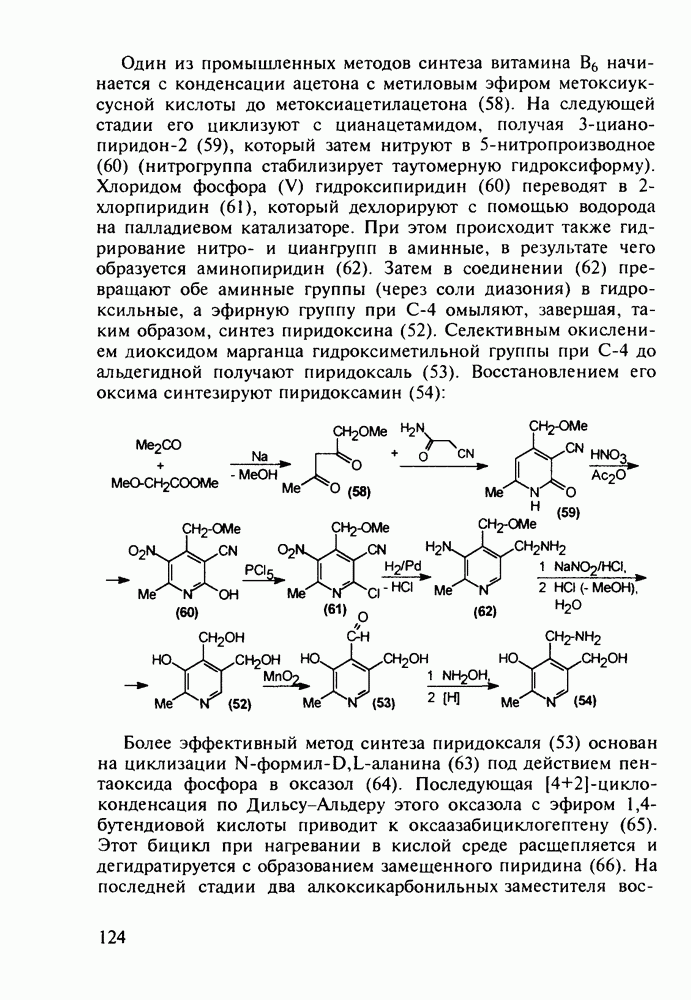
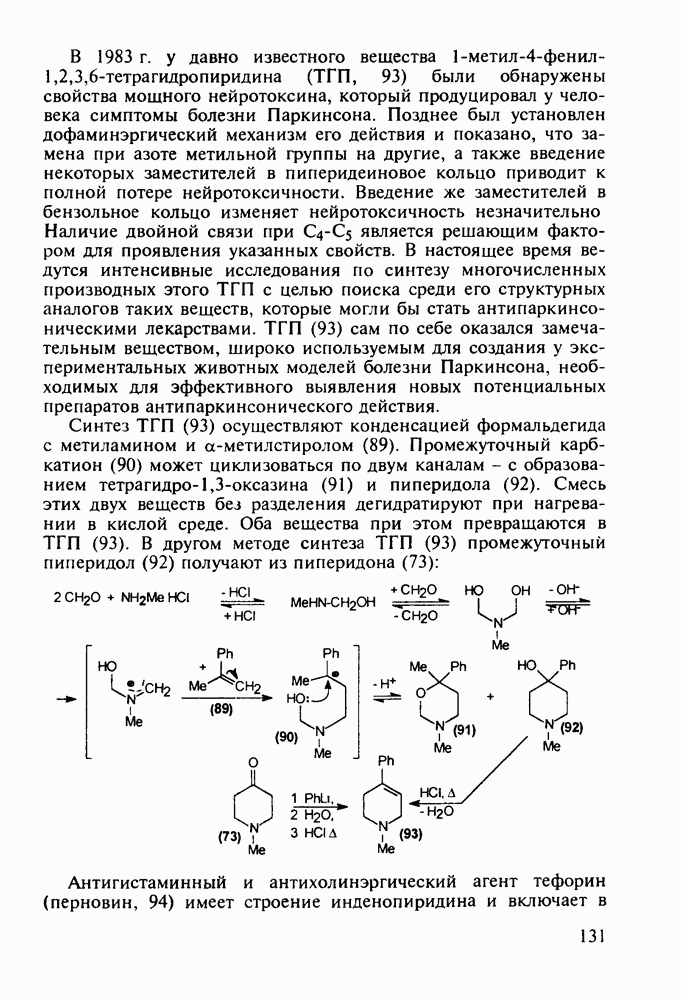
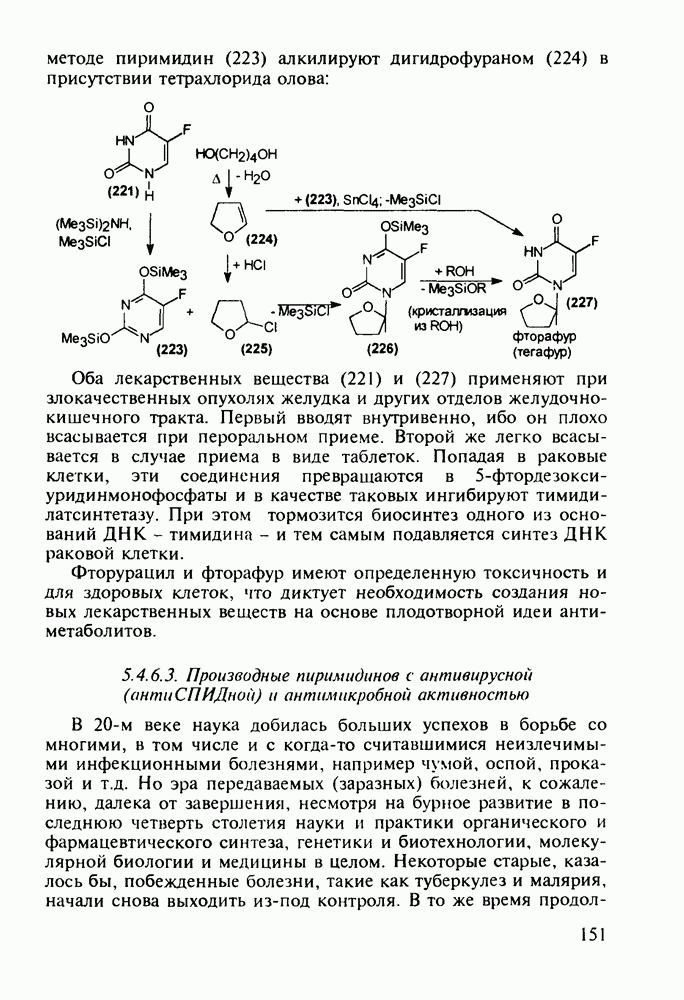
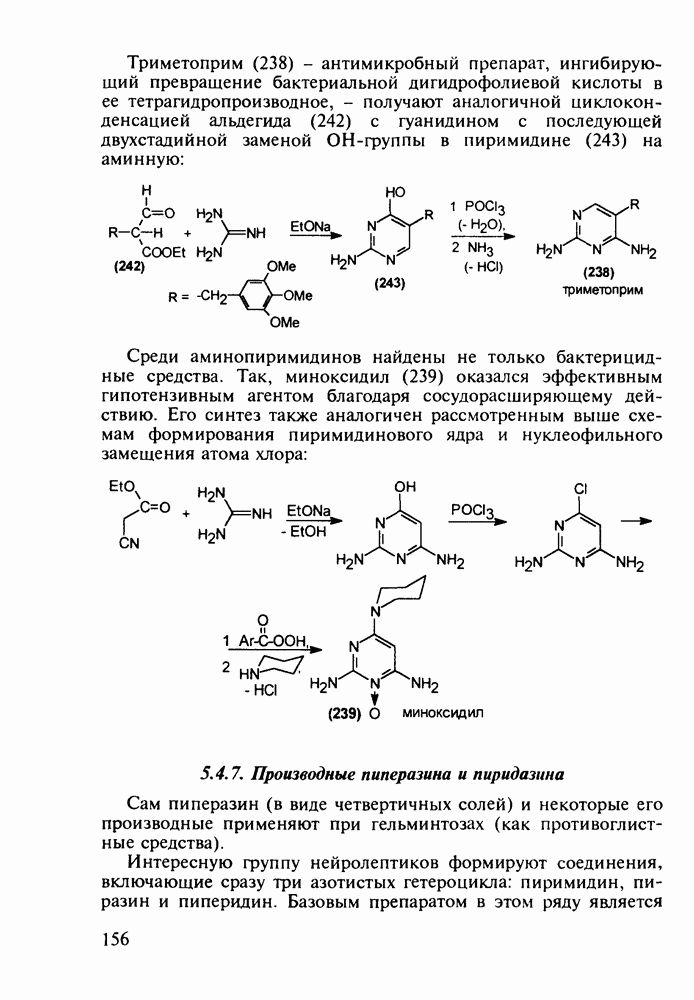
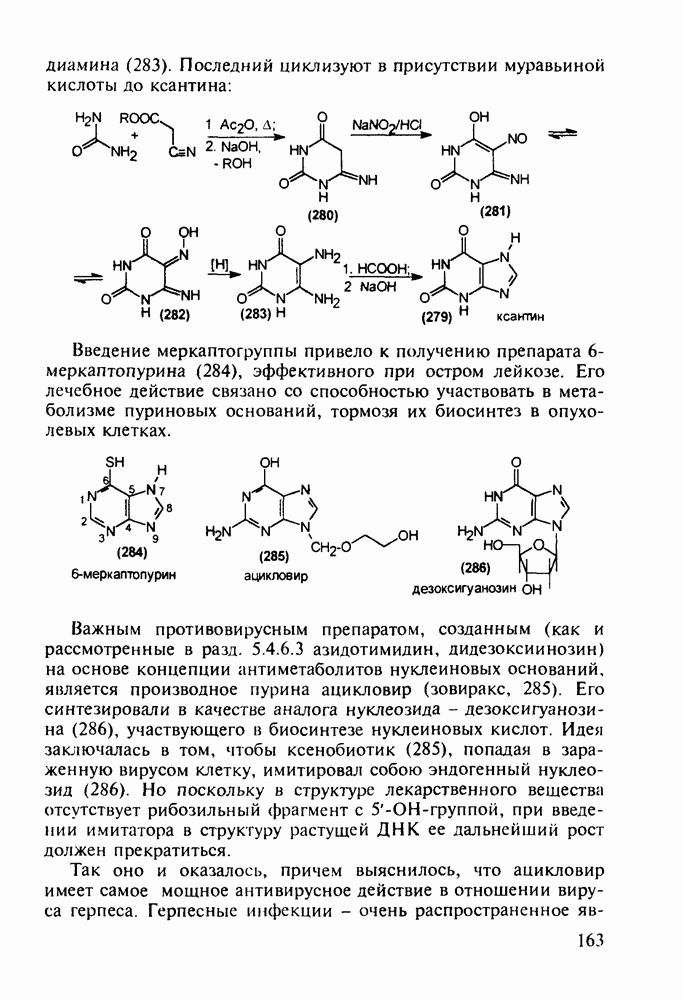
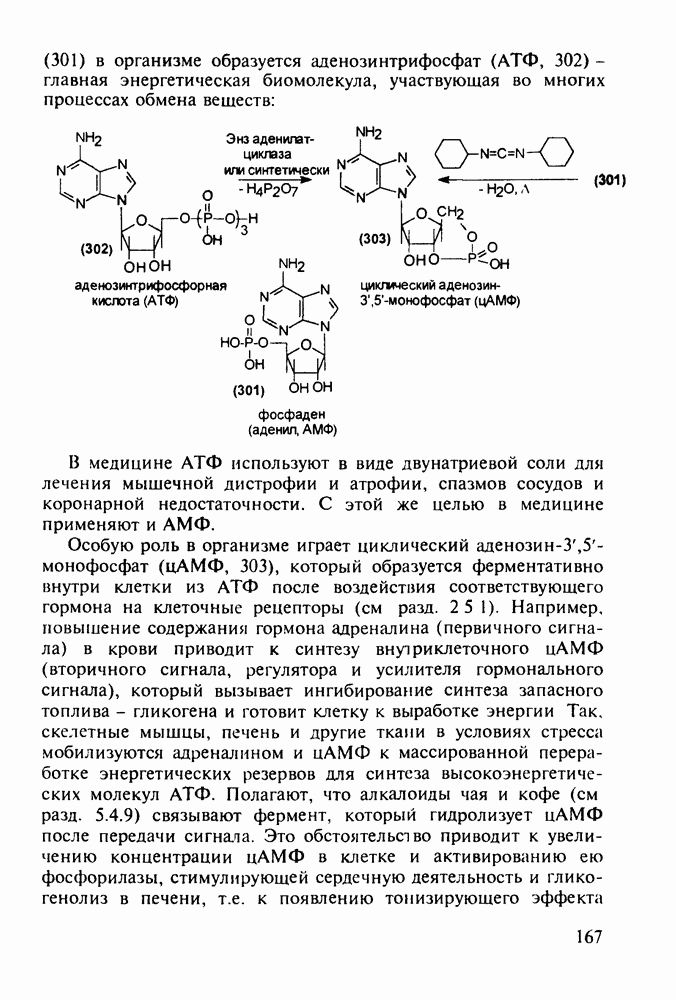
Витамины группы  регулируют обмен кальция и фосфора и особенно важны в раннем возрасте Их используют для лечения рахита, остеопороза. туберкулеза костей и др Холекальциферол (27) (витамин D) синтезируют из холестерина (10) бромированием бромсукцинимидом (БСИ) аллильного положения
регулируют обмен кальция и фосфора и особенно важны в раннем возрасте Их используют для лечения рахита, остеопороза. туберкулеза костей и др Холекальциферол (27) (витамин D) синтезируют из холестерина (10) бромированием бромсукцинимидом (БСИ) аллильного положения  с последующим
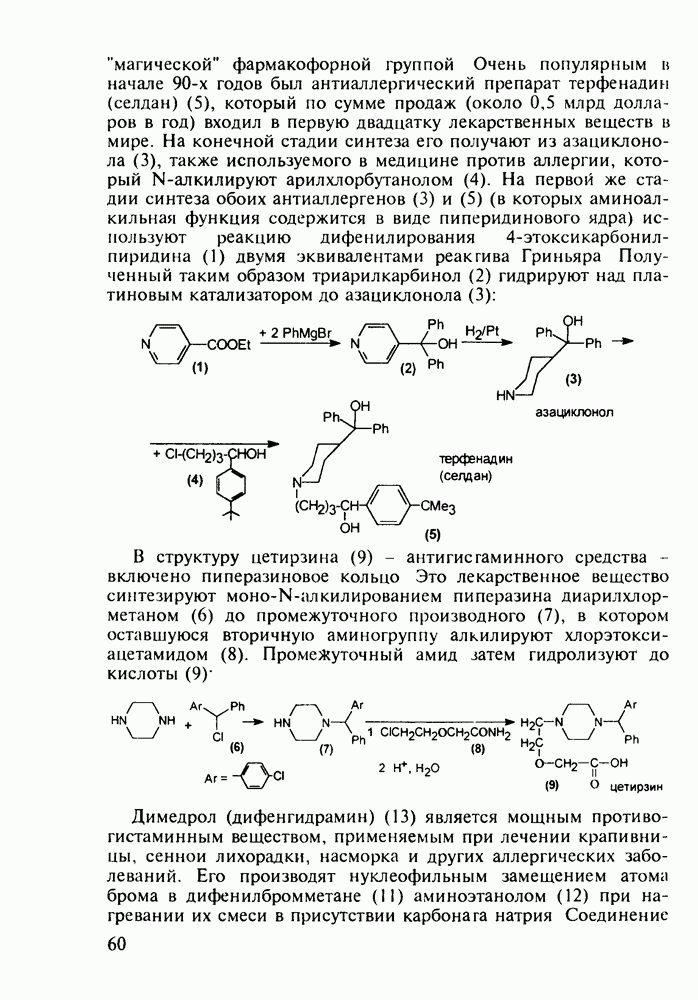
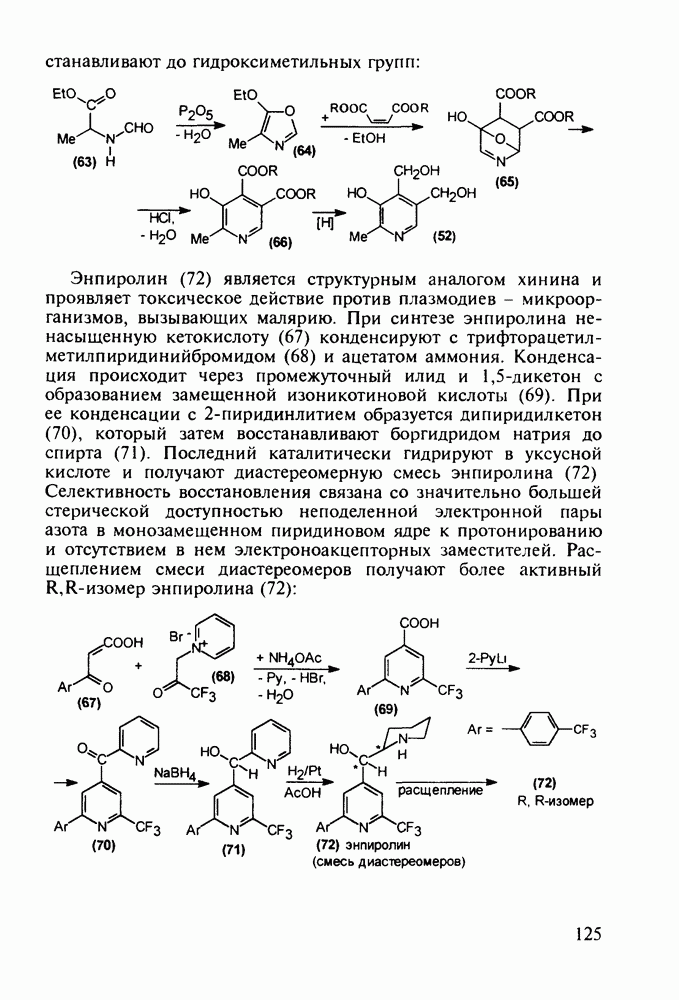
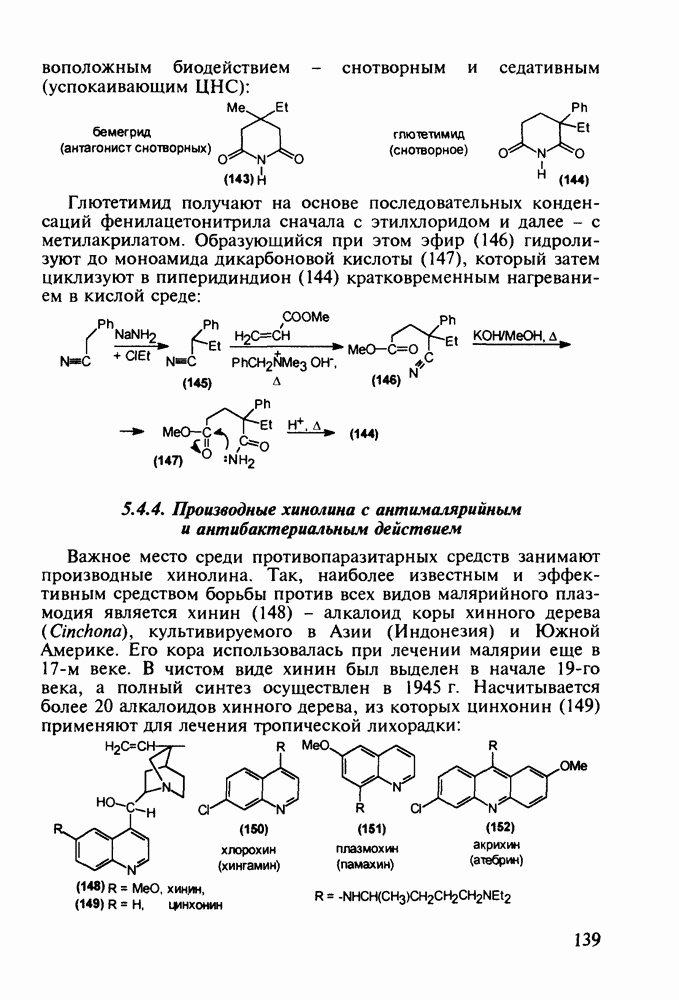
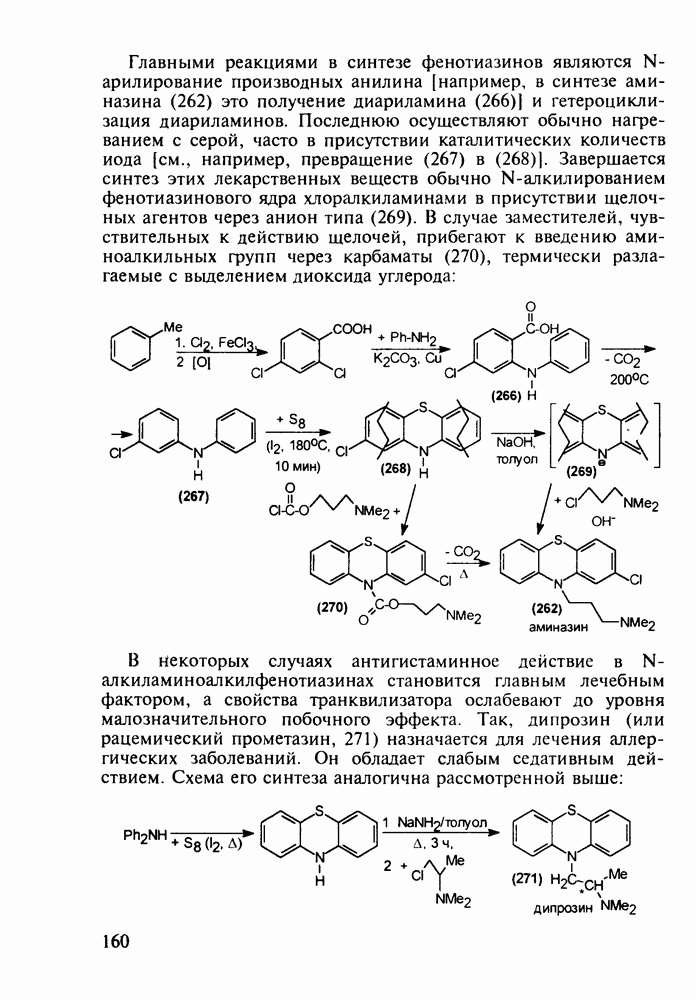
с последующим  идробромированием бромпроизводного (25) органическим основанием, что приводит к сопряженному диену (26) Ею фотохимической дециклизацией (по кольцу В) получают витамин
идробромированием бромпроизводного (25) органическим основанием, что приводит к сопряженному диену (26) Ею фотохимической дециклизацией (по кольцу В) получают витамин 

| << Предыдущий параграф | Следующий параграф >> |
- Предисловие
- 1. ВВЕДЕНИЕ
- 1.1. Эволюция органической химии лекарственных веществ
- 1.2. Современные требования к лекарственным веществам
- 1.3. Стадии биологического изучения лекарственного вещества
- 1.4. Основы стратегии создания новых синтетических лекарственных веществ
- 1.5. Связь структура-биологическая активность
- 1.6. Принципиальная схема разработки нового лекарственного вещества
- 1.7. Классификация лекарственных веществ
- 1.8. Основные болезни человека и ведущие группы лекарственных веществ на современном фармацевтическом рынке
- 2. СИНТЕЗ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ АЛИФАТИЧЕСКОГО РЯДА
- 2.2. Группа противораковых веществ с дихлордиэтиламинным фармакофором
- 2.3. Алканолы, аминоалканолы и их эфиры. Нейромедиатор ацетилхолин и холиномиметики
- 2.4. Альдегиды и кислоты. Витамины F и B15
- 2.5. Аминокислоты
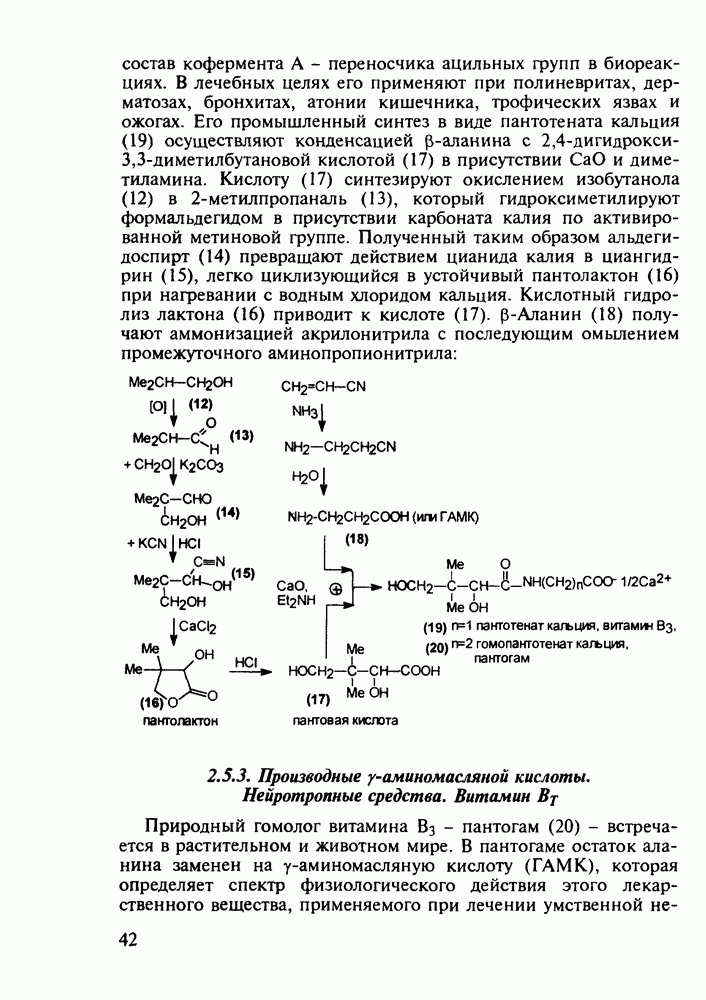
- 2.5.2. Производные b-аминокислот. Витамин B3
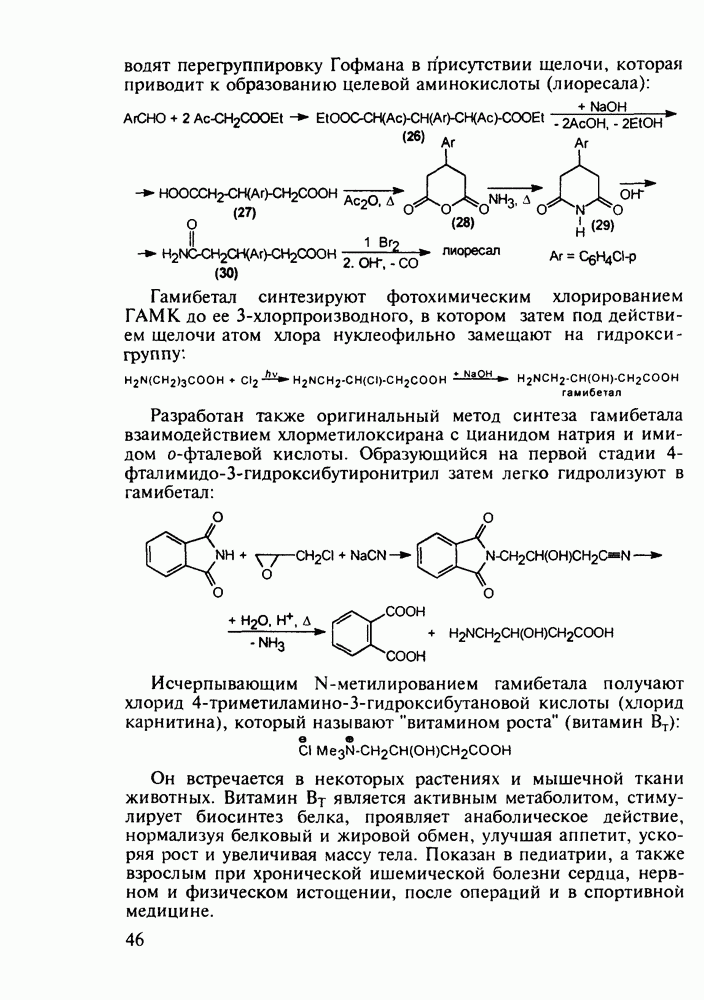
- 2.5.3. Производные у-аминомасляной кислоты. Нейротропные средства. Витамин BT
- 2.5.4. Другие аминокислоты
- 3. ЛЕКАРСТВЕННЫЕ ВЕЩЕСТВА АЛИЦИКЛИЧЕСКОГО РЯДА
- 3.2. Противозачаточные и противовоспалительные вещества на основе циклопентафенантрена. Синтез витамина D
- 3.3. Камфора. Производные адамантана в качестве антивирусных средств
- 4. СИНТЕЗ ПРОИЗВОДНЫХ АРОМАТИЧЕСКОГО РЯДА
- 4.2. Антигистаминные препараты группы диарилметана
- 4.3. Антисептики и адреноблокаторы фенольного ряда
- 4.4. Аминофенолы в качестве обезболивающих и противотуберкулезных средств
- 4.5. Производные о-гидроксибензойной кислоты. Аспирин
- 4.6. Анестетики и противотуберкулезные средства на основе n-аминобензойной кислоты
- 4.7. Производные n-аминобензолсульфокислоты с антибактериальным и диуретическим действием
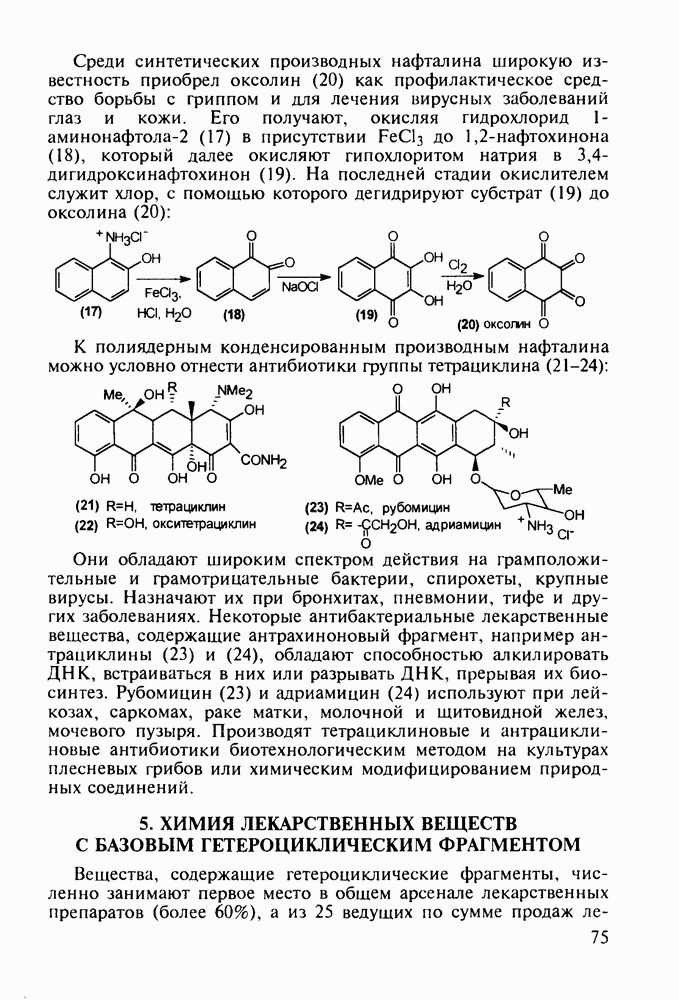
- 4.8. Оксопроизводные нафталина. Витамин К1. Оксолин
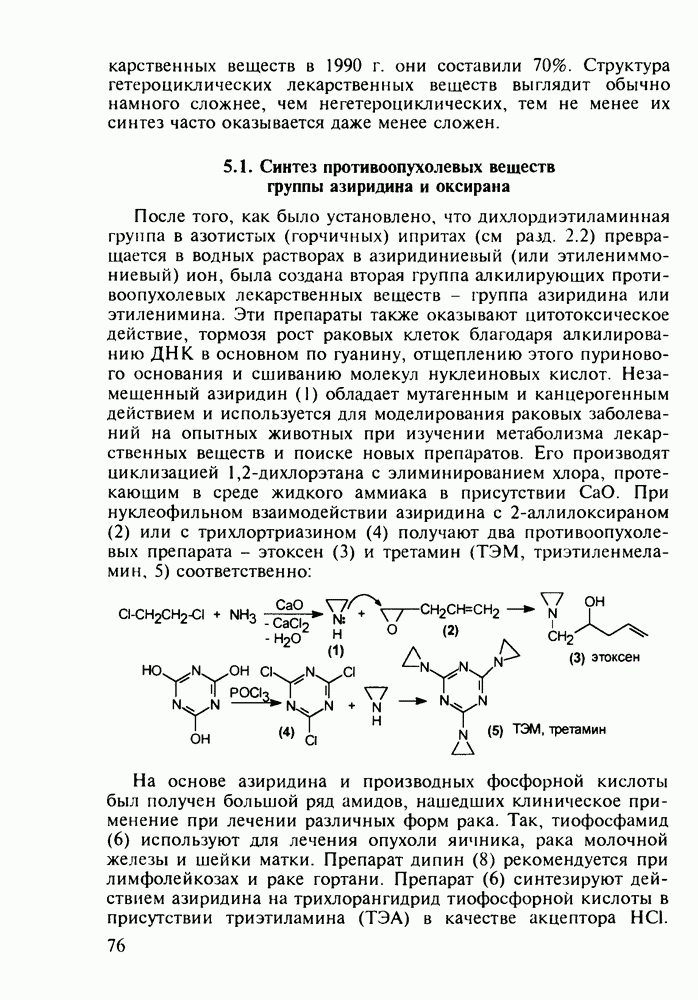
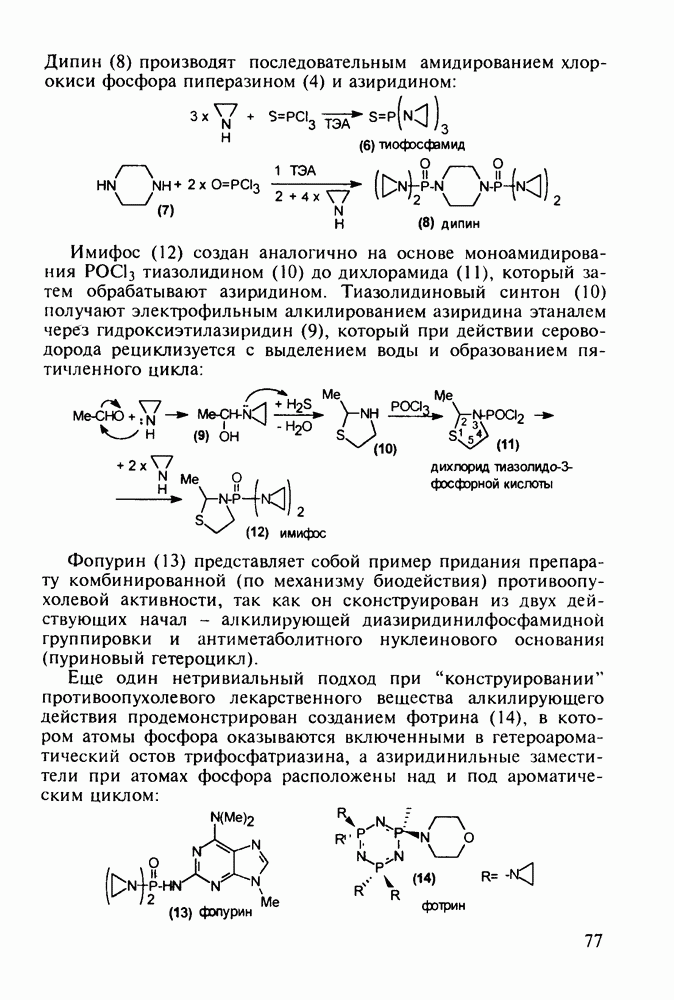
- 5. ХИМИЯ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ С БАЗОВЫМ ГЕТЕРОЦИКЛИЧЕСКИМ ФРАГМЕНТОМ
- 5.2. Антибиотики, содержащие четырехчленное азетидиновое ядро
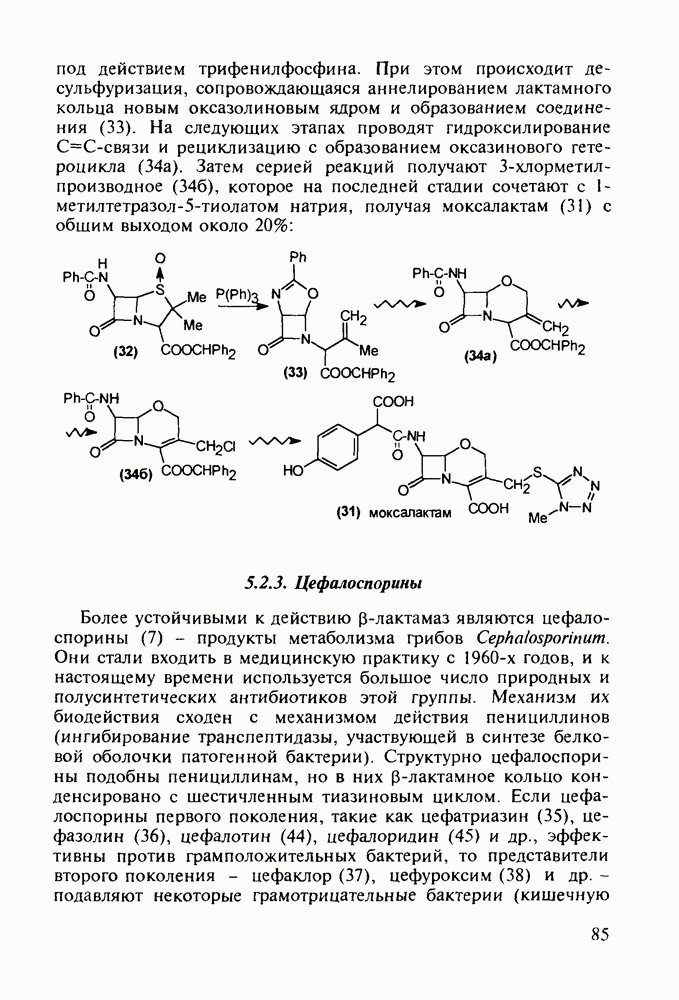
- 5.2.2. Пенициллины. Моксалактам
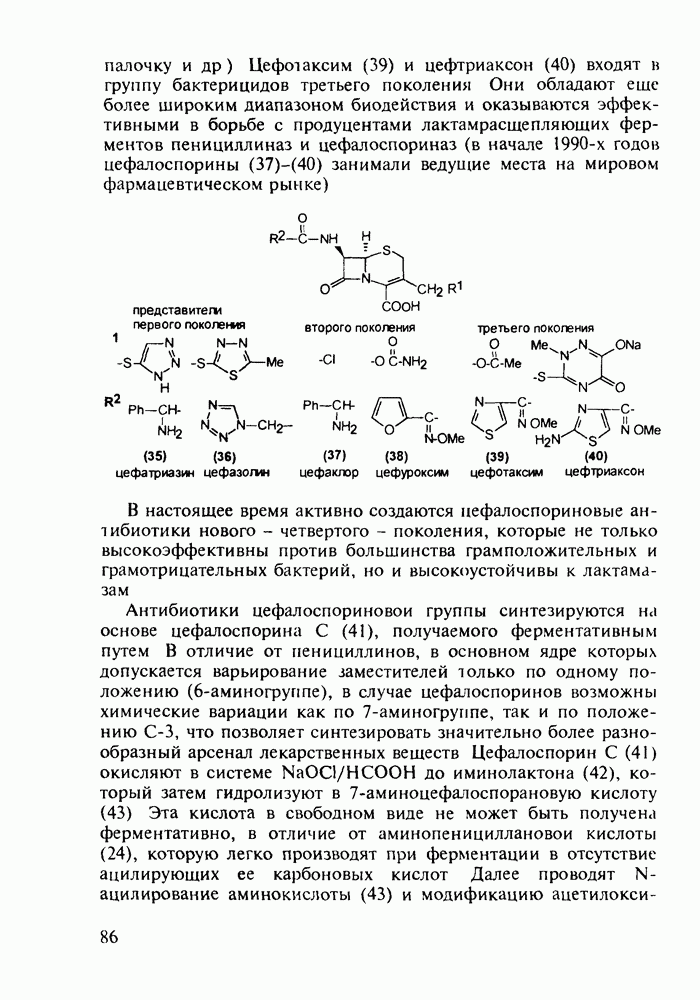
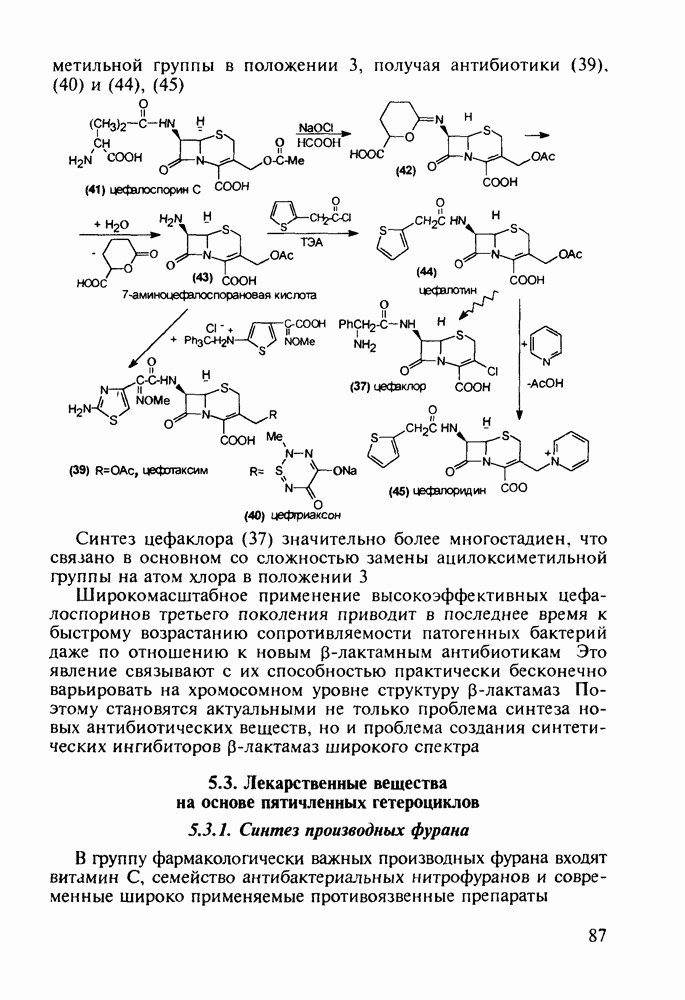
- 5.2.3. Цефалоспорины
- 5.3. Лекарственные вещества на основе пятичленных гетероциклов
- 5.3.2. Синтез производных пиррола
- 5.3.3. Оксазолидины. Антибиотик циклосерин
- 5.3.4. Антипиретики и анальгетики пиразолинового ряда
- 5.3.5. Имидазолы с противопаразитарной, антигипертензивной и другой биоактивностью
- 5.3.6. Производные тиазола. Витамин В1
- 5.3.7. Психостимуляторы с оксадиазольным и тетразольным гетероциклами
- 5.4. Синтез лекарственных веществ, содержащих шестичленные гетероциклы
- 5.4.2. Синтез лекарственных веществ пиридинового ряда
- 5.4.3. Анальгетики и транквилизаторы пиперидинового ряда
- 5.4.4. Производные хинолина с антималярийным и антибактериальным действием
- 5.4.5. Изохинолины в качестве спазмолитиков и трипаноцидов
- 5.4.6. Производные пиримидинов
- 5.4.7. Производные пиперазина и пиридазина
- 5.4.8. Бензотиазины. Нейролептики фенотиазинового ряда
- 5.4.9. Пуриновые основания в качестве стимулирующих и антивирусных агентов
- 5.4.10. Производные аденозинфосфорной кислоты
- 5.4.11. Производные птеридина с витаминной (витамины Вс и В2) и противораковой активностью
- 5.5. Лекарственные вещества, содержащие семичленный гетероцикл
- 5.5.2. Транквилизаторы группы 1,4-бензодиазепина
- 5.6. Производные азабициклооктанов в качестве спазмолитиков и анестетиков. Лекарственные препараты на основе хинуклидина
- 5.7. Производные азабициклононанов в качестве анальгетиков
- 5.7.1. Группа пентазоцина
- 5.7.2. Морфин, его агонисты и антагонисты
- РЕКОМЕНДУЕМАЯ ЛИТЕРАТУРА