| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
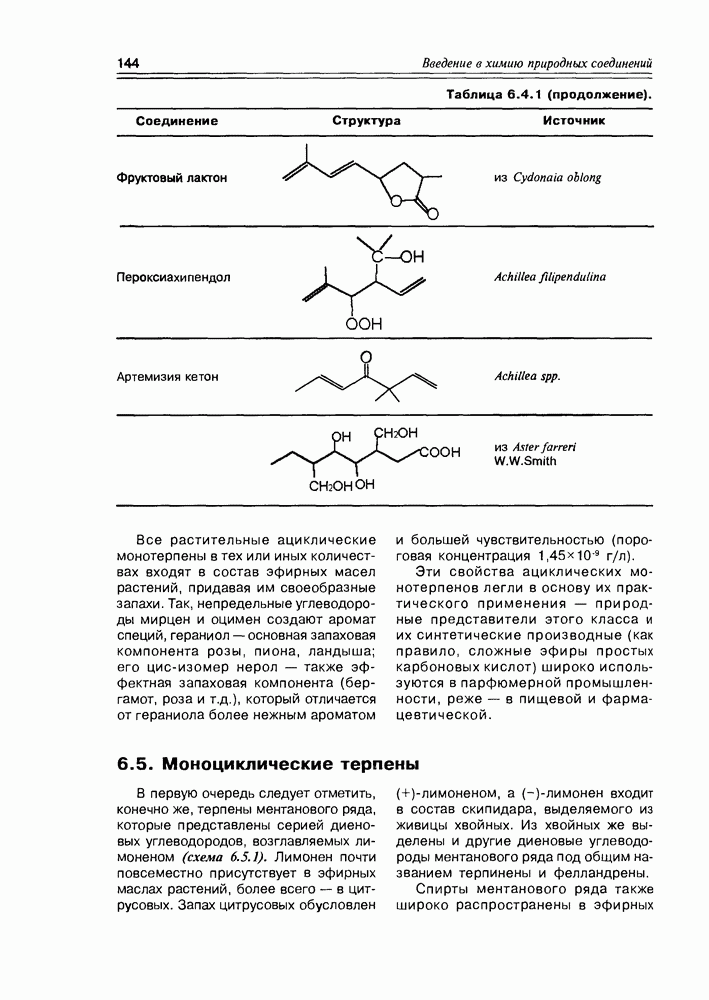
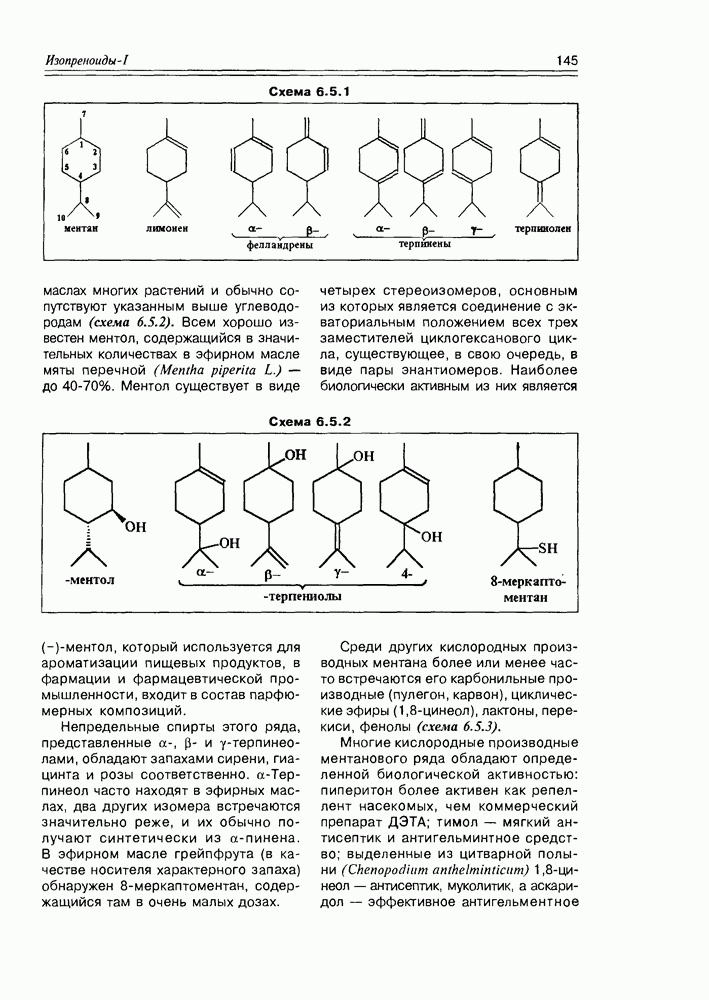
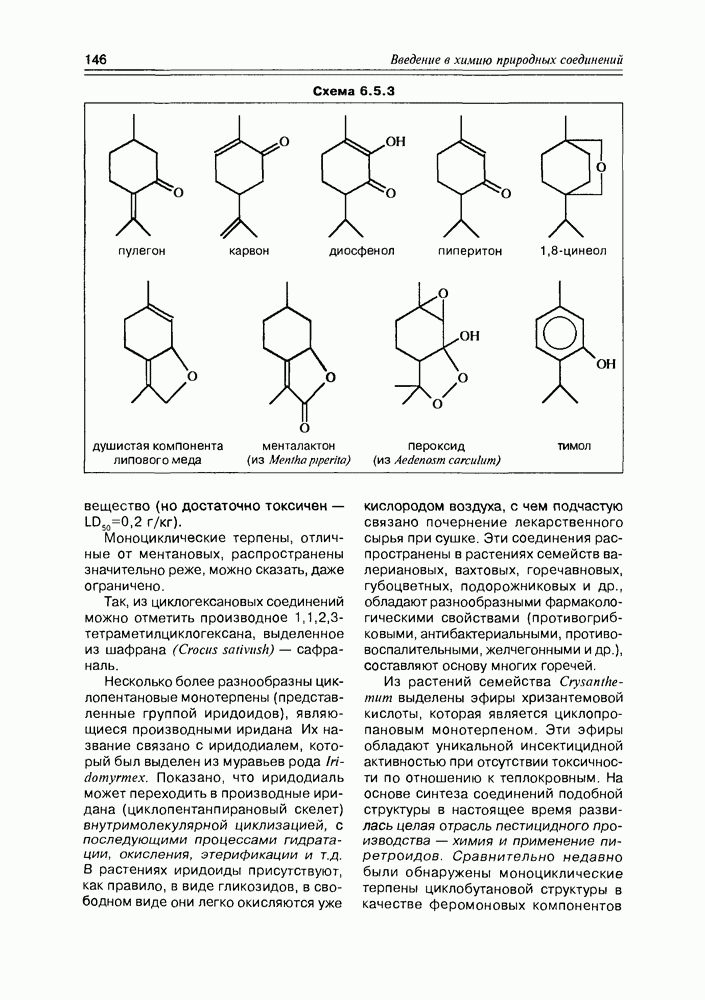
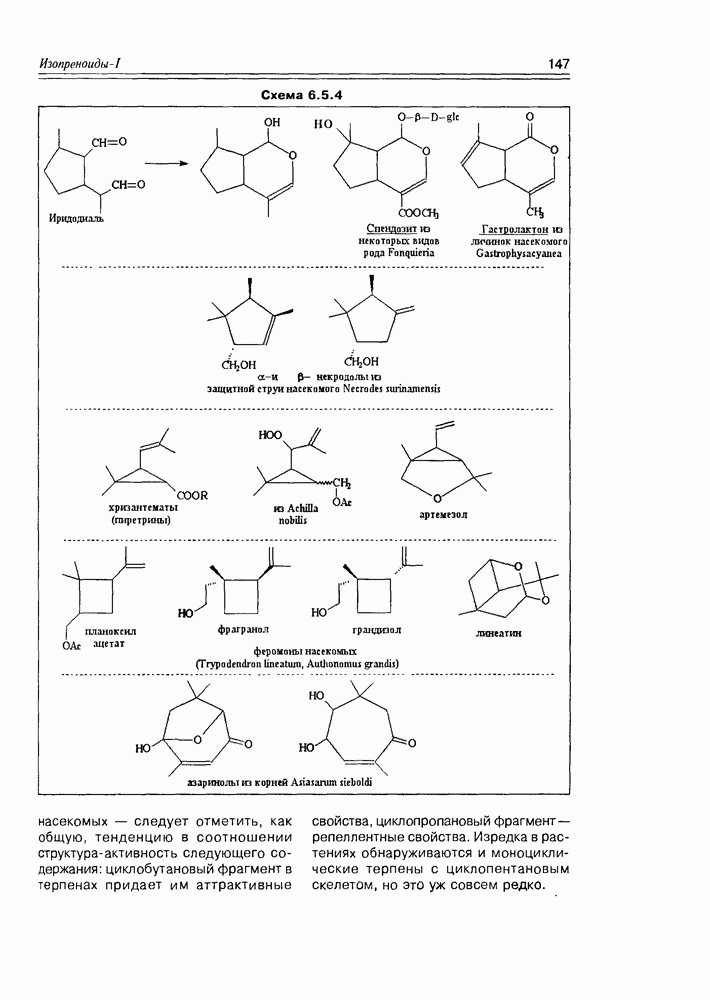
5.3. Жиры и жироподобные производные жирных кислот
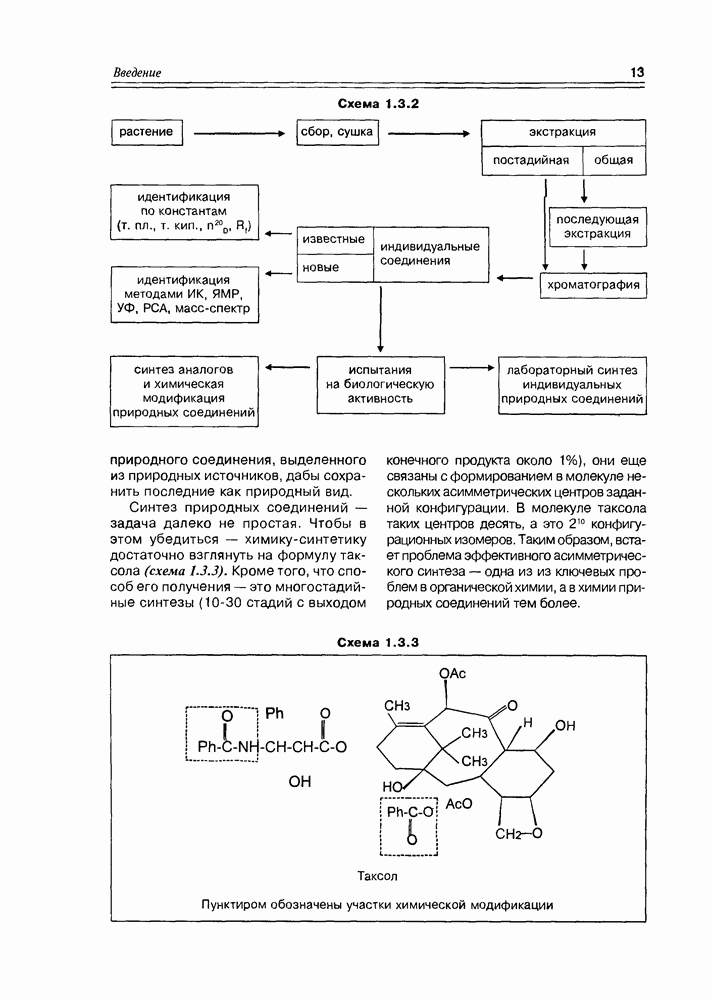
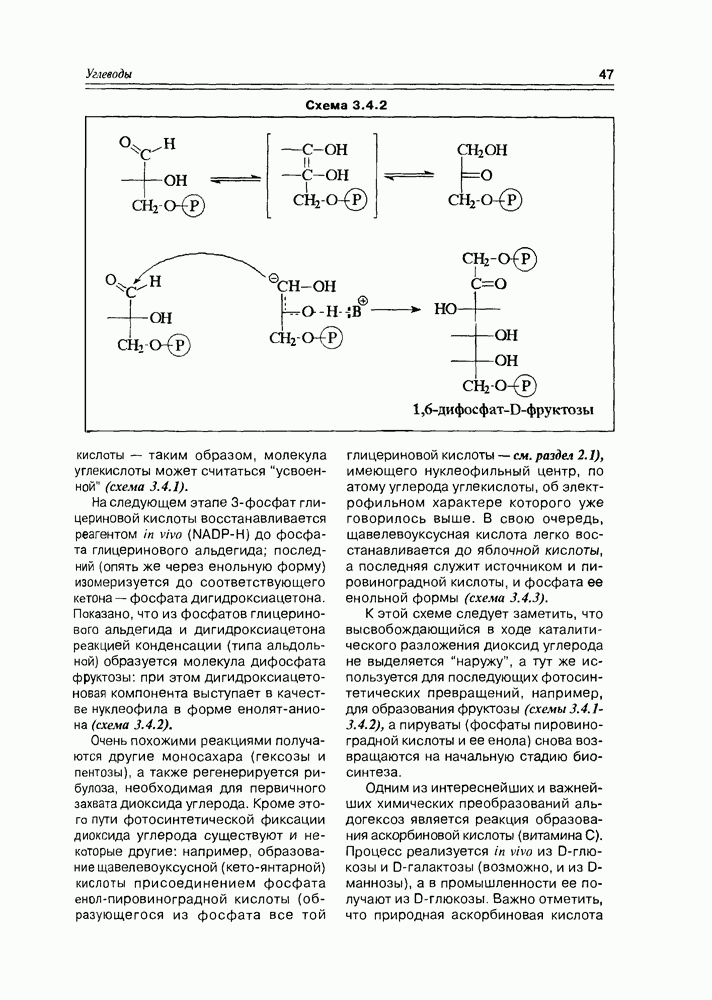
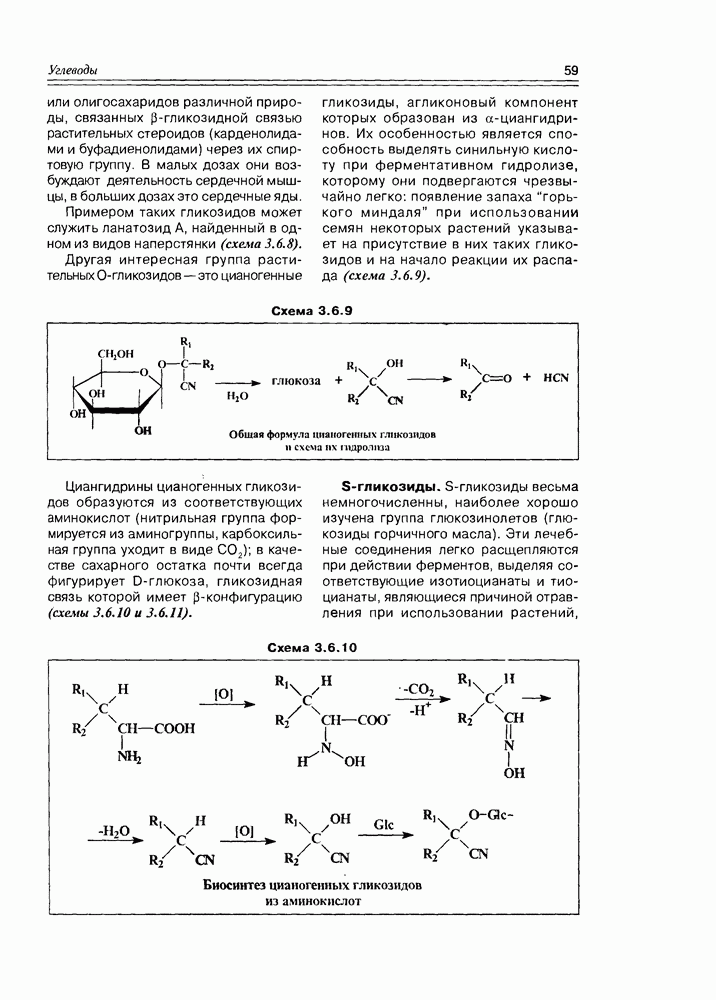
Образование сложных эфиров карбоновыми кислотами — наиболее типичный процесс для этой функциональной группы. Жирные кислоты не являются исключением в этом плане, скорее наоборот — это главный процесс для жирных кислот, протекающий in vivo Особую группу сложных эфиров жирные кислоты образуют с многоатомными спиртами (глицерином, в первую очередь) — как правило, это полные эфиры, т.е. этерифицированы все три гидроксила многоатомного спирта.
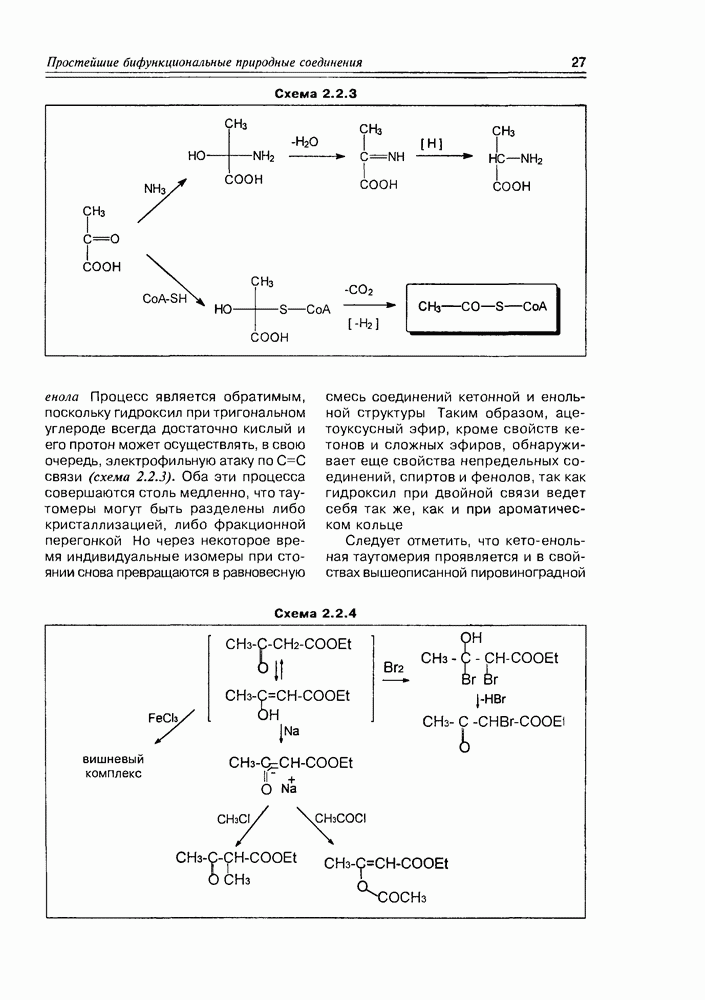
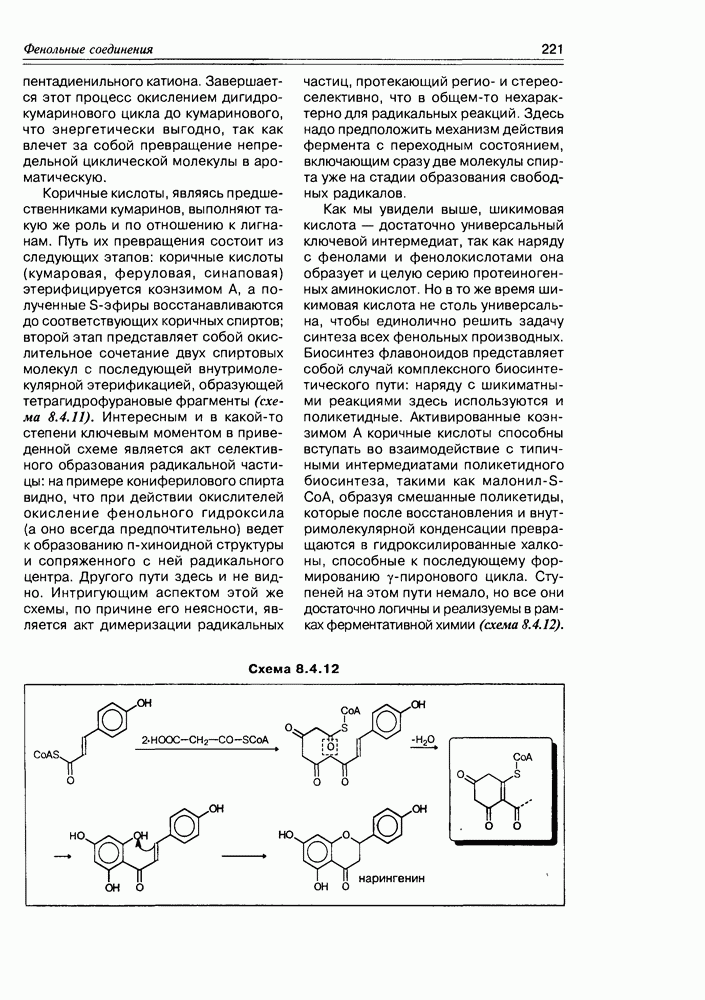
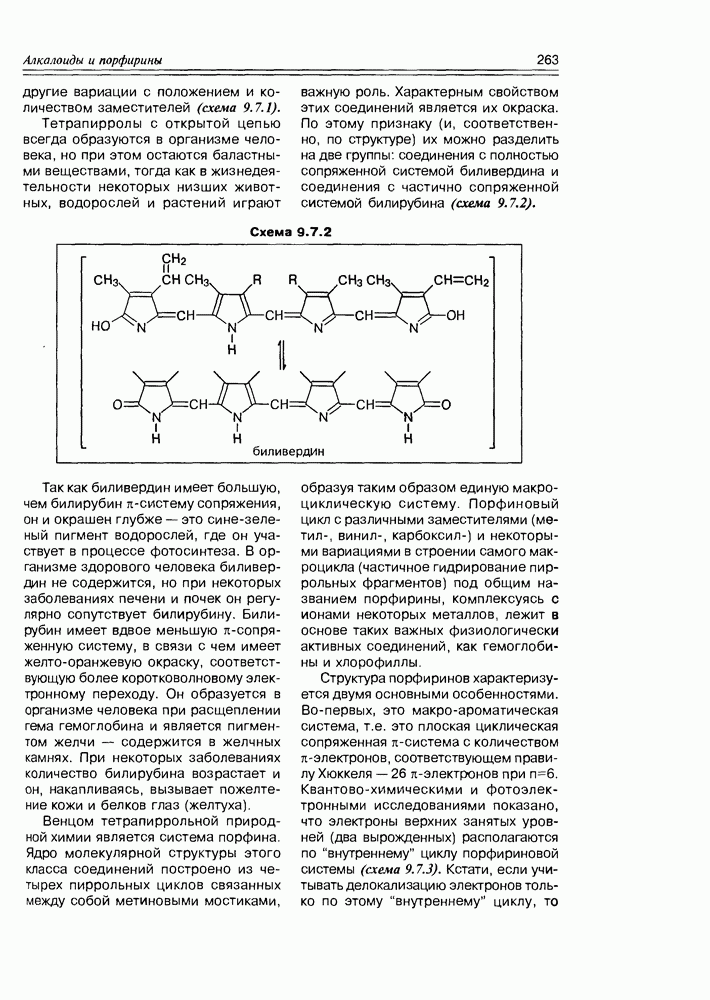
Жиры. Этерификация глицерина может осуществляться как одним типом жирных кислот, так и различными, причем последний вариант наиболее распространен. В том случае, когда все три кислоты насыщенные — образуются эфиры, называемые твердыми или животными жирами; если кислоты ненасыщенные — образуются жидкие или растительные жиры. Очень часто природные жиры образованы с одновременным участием насыщенных и ненасыщенных жирных кислот, а в качестве минорных — циклических и оксигенированных. О распространении жидких и твердых жиров в природе говорить не приходится — это резервные липиды большинства животных и растений, для микроорганизмов глицериды жирных кислот тоже не редкость. Общая формула жиров имеет вид, представленный на схеме 5.3.1.
Схема 5.3.1

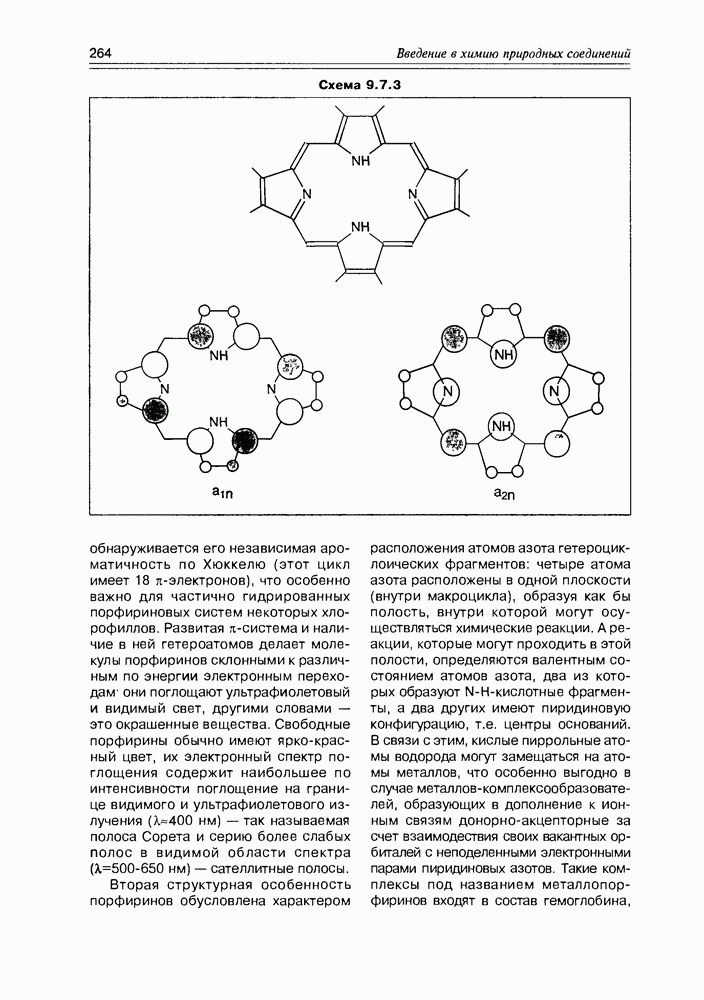
 — те самые длиноцепочечные углеводородные радикалы, которые описаны в разделе жирных кислот. Такие глицериды могут существовать в виде трех пар энантиомеров с учетом перестановки радикалов и наличием одного асимметрического центра. Для жиров (как жидких, так и твердых) характерна высокая степень гидрофобности (липофильности), т.е. они нерастворимы в воде, но хорошо растворимы в углеводородах, галогенал-канах, спиртах, эфирах Кроме того, жидкие жиры, т.е. глицериды ненасыщенных кислот, могут быть гидрогенизированы в присутствии катализаторов
— те самые длиноцепочечные углеводородные радикалы, которые описаны в разделе жирных кислот. Такие глицериды могут существовать в виде трех пар энантиомеров с учетом перестановки радикалов и наличием одного асимметрического центра. Для жиров (как жидких, так и твердых) характерна высокая степень гидрофобности (липофильности), т.е. они нерастворимы в воде, но хорошо растворимы в углеводородах, галогенал-канах, спиртах, эфирах Кроме того, жидкие жиры, т.е. глицериды ненасыщенных кислот, могут быть гидрогенизированы в присутствии катализаторов  до твердых жиров, в результате чего происходит превращение остатков ненасыщенных кислот в насыщенные. Жиры также используются для получения мыла и глицерина реакцией щелочного гидролиза. Жиры (по причине высокой доли связей
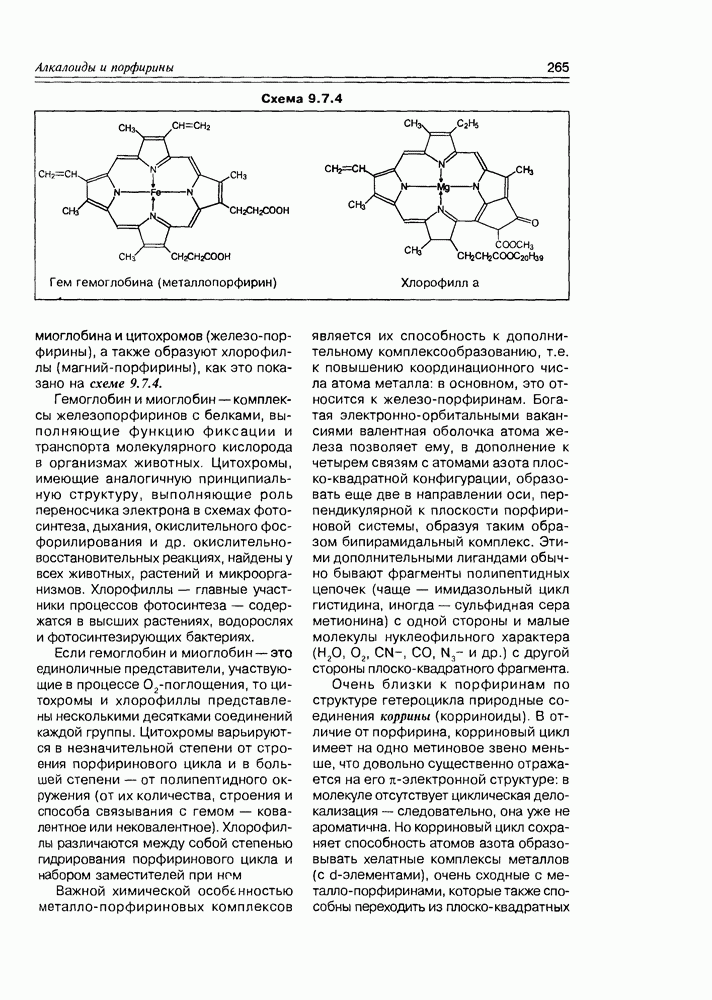
до твердых жиров, в результате чего происходит превращение остатков ненасыщенных кислот в насыщенные. Жиры также используются для получения мыла и глицерина реакцией щелочного гидролиза. Жиры (по причине высокой доли связей  в молекуле) обладают высокой калорийностью, т.е. при их сгорании (окислении) как спонтанном in vitro, так и ступенчатом in vivo, выделяется тепла почти столько же, как и при аналогичном превращении углеводородного топлива (газ, нефть, уголь). В древности (народами Севера
в молекуле) обладают высокой калорийностью, т.е. при их сгорании (окислении) как спонтанном in vitro, так и ступенчатом in vivo, выделяется тепла почти столько же, как и при аналогичном превращении углеводородного топлива (газ, нефть, уголь). В древности (народами Севера
Схема 5.3.2

и совсем недавно) жиры использовались в быту в качестве источника тепла и света. А наш организм использует жиры и поныне, в том числе и в качестве “топлива”.
Вышеуказанные производные жирных кислот и глицерина еще относят к классу так называемых нейтральных липидов, поскольку они не содержат свободных функциональных групп, обеспечивающих либо кислотные, либо основные свойства. Поэтому здесь же будет уместно описать и другие виды нейтральных липидов, распространенных в природе в той лил иной степени. Из жирнокислотных производных глицерина сюда относятся алкилдиацил-глицериды и плазмологены — это те соединения, в которых глицерин образует две сложноэфирных связи и одну связь простого эфира. Функция простого эфира может быть насыщенной (алкилдиацилглицериды) и ненасыщенной (плазмологены). Такие липиды найдены в различных органах животных (костный и головной мозг, сердце, плазма крови), в яичном желтке и молочном жире, в растениях и микроорганизмах; но более всего их в морских организмах (звезды, иглокожие, моллюски, некоторые виды рыб).
Схема 5.3.3

Интересно заметить здесь, что спирты, участвующие в образовании этого вида глицеридов, имеют такой же состав, что и обычные жирные кислоты — факт, указывающий на общность их биосинтеза.
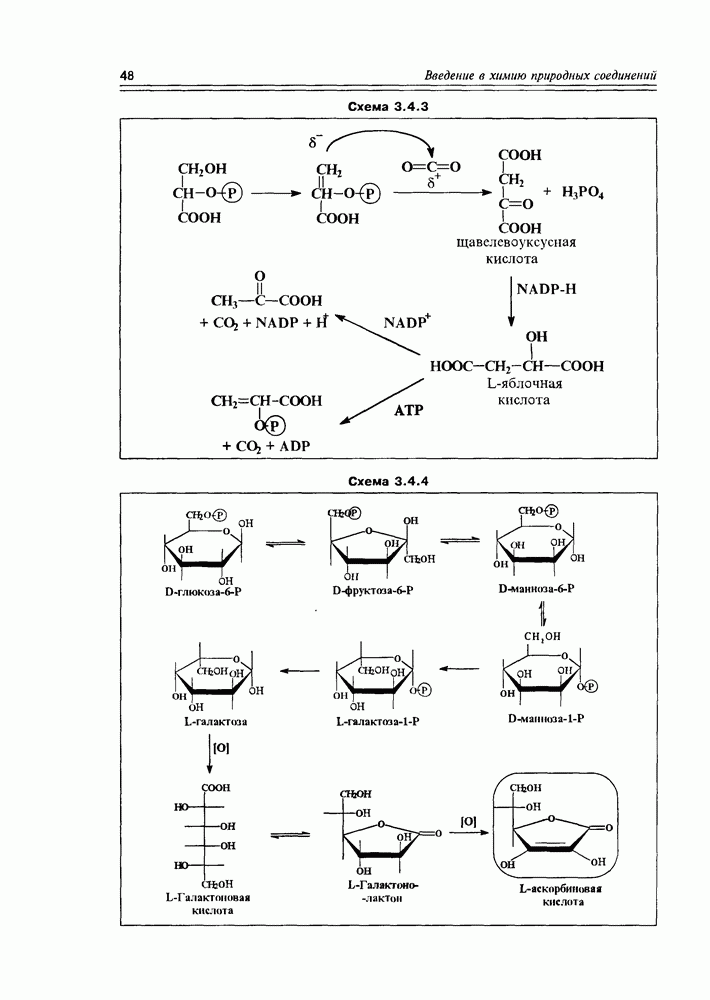
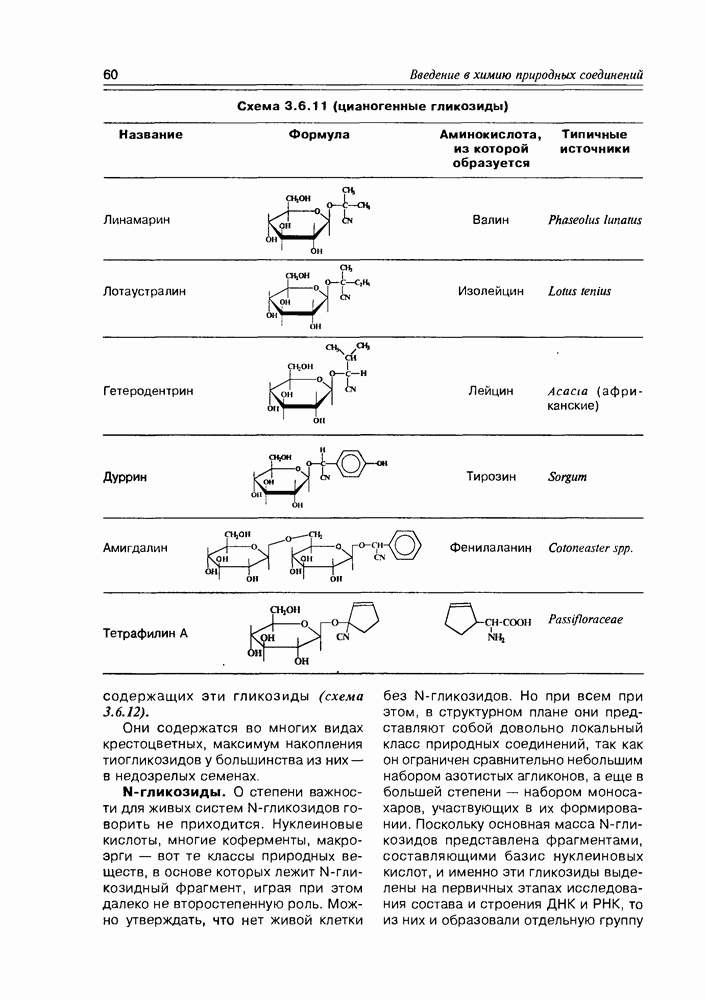
Фосфоглицериды образуются при совместной этерификации глицерина как карбоновыми (жирными), так и минеральными (фосфорной) кислотами. Образующиеся в этом случае фосфатидовые кислоты имеют кислый характер, поскольку фосфорная кислота многоосновная. По этой же причине фосфатидовая кислота сохраняет возможность последующих этерификаций,
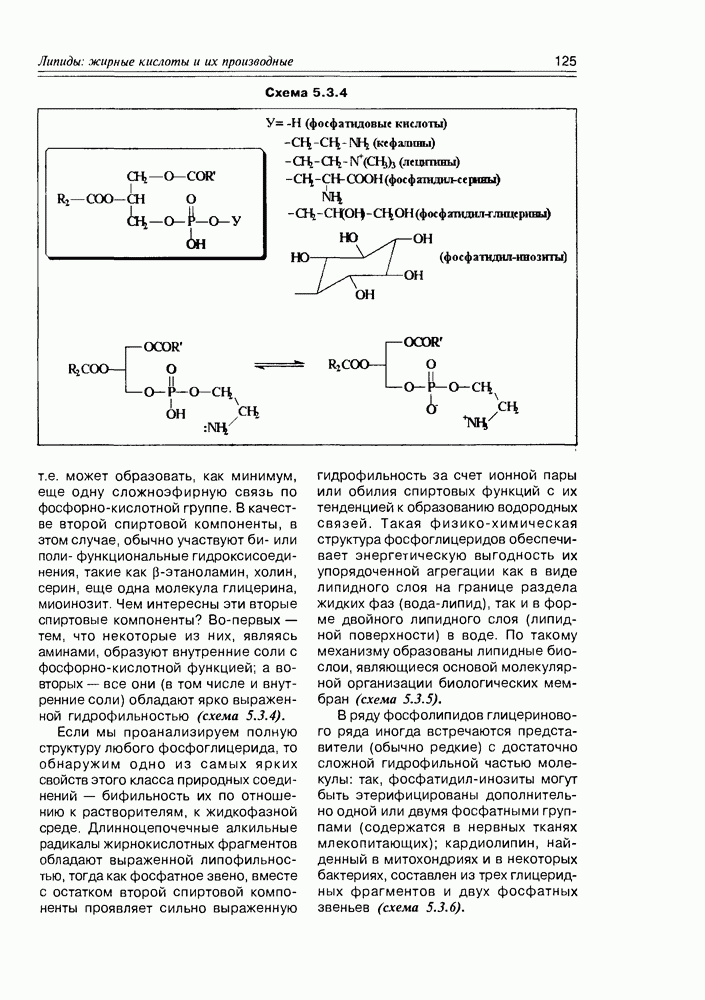
Схема 5.3.4

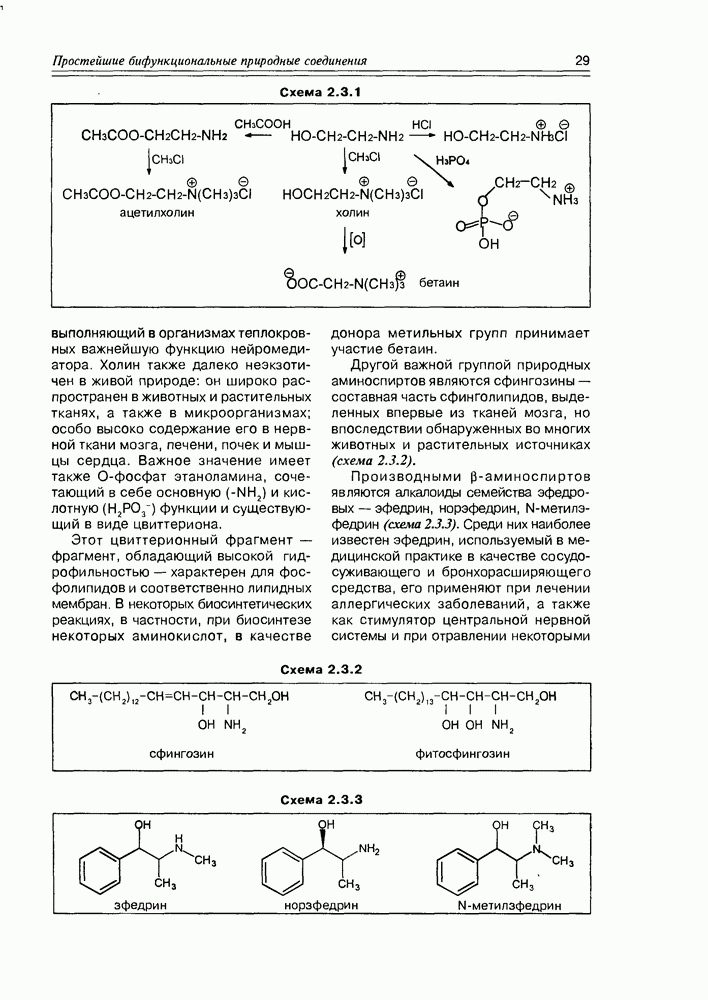
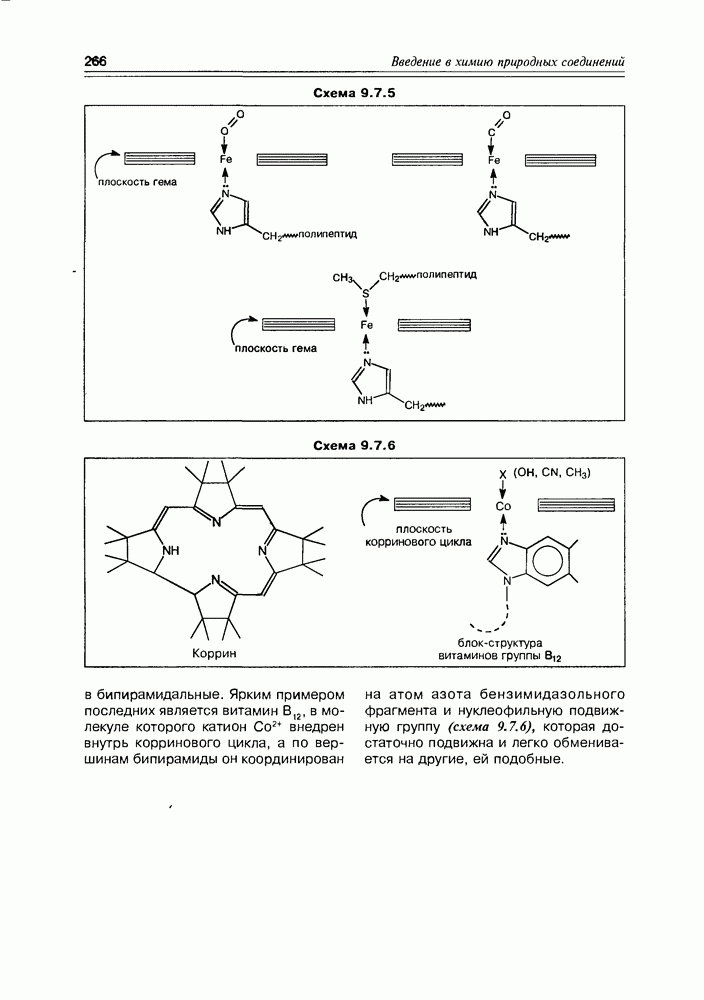
т.е. может образовать, как минимум, еще одну сложноэфирную связь по фосфорно-кислотной группе. В качестве второй спиртовой компоненты, в этом случае, обычно участвуют би- или поли- функциональные гидроксисоединения, такие как  -этаноламин, холин, серин, еще одна молекула глицерина, миоинозит. Чем интересны эти вторые спиртовые компоненты? Во-первых — тем, что некоторые из них, являясь аминами, образуют внутренние соли с фосфорно-кислотной функцией; а во-вторых — все они (в том числе и внутренние соли) обладают ярко выраженной гидрофильностью (схема 5.3.4).
-этаноламин, холин, серин, еще одна молекула глицерина, миоинозит. Чем интересны эти вторые спиртовые компоненты? Во-первых — тем, что некоторые из них, являясь аминами, образуют внутренние соли с фосфорно-кислотной функцией; а во-вторых — все они (в том числе и внутренние соли) обладают ярко выраженной гидрофильностью (схема 5.3.4).
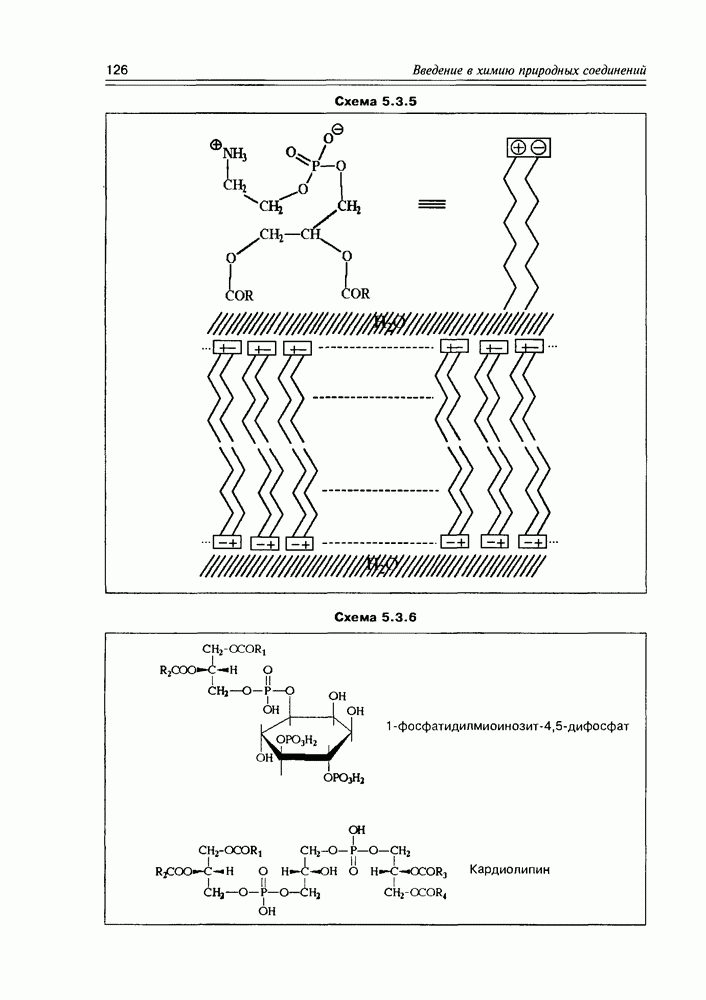
Если мы проанализируем полную структуру любого фосфоглицерида, то обнаружим одно из самых ярких свойств этого класса природных соединений — бифильность их по отношению к растворителям, к жидкофазной среде. Длинноцепочечные алкильные радикалы жирнокислотных фрагментов обладают выраженной липофильностью, тогда как фосфатное звено, вместе с остатком второй спиртовой компоненты проявляет сильно выраженную гидрофильность за счет ионной пары или обилия спиртовых функций с их тенденцией к образованию водородных связей. Такая физико-химическая структура фосфоглицеридов обеспечивает энергетическую выгодность их упорядоченной агрегации как в виде липидного слоя на границе раздела жидких фаз (вода-липид), так и в форме двойного липидного слоя (липидной поверхности) в воде. По такому механизму образованы липидные биослои, являющиеся основой молекулярной организации биологических мембран (схема 5.3.5).
В ряду фосфолипидов глицеринового ряда иногда встречаются представители (обычно редкие) с достаточно сложной гидрофильной частью молекулы: так, фосфатидил-инозиты могут быть этерифицированы дополнительно одной или двумя фосфатными группами (содержатся в нервных тканях млекопитающих); кардиолипин, найденный в митохондриях и в некоторых бактериях, составлен из трех глицеридных фрагментов и двух фосфатных звеньев (схема 5.3.6).
Схема 5.3.5
(см. скан)
Схема 5.3.6
(см. скан)
В тех случаях, когда вместо глицерина в качестве спиртовой компоненты во взаимодействие с жирными кислотами выступают двухатомные спирты (диолы) — образуется группа диольных липидов. Гликоли, участвующие в формировании соответствующих липидов, обычно имеют первичные спиртовые группы, разделенные несколькими метиленовыми звеньями (от 2 до 6), а их липидные производные, как и в случае глицерина, могут быть нейтральными или фосфатидными. Диольные липиды обычно содержаться в тканях животных, семенах растений и микроорганизмах в весьма незначительных количествах — в тысячи раз меньше по сравнению с глицеридами. Обнаружено, что их концентрация может возрастать при усиленной пролиферации клеток: регенерирующая печень, созревающие семена растений. Из их физиологических реакций можно отметить повышение проницаемости мембран и инициирование гемолиза эритроцитов.
Схема 5.3.7

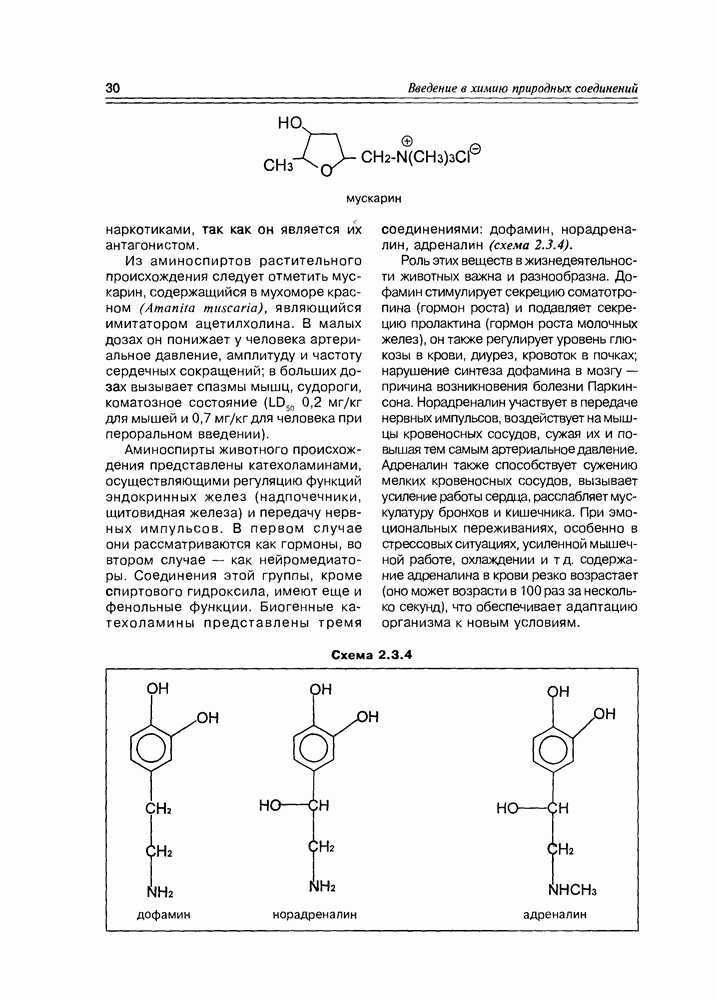
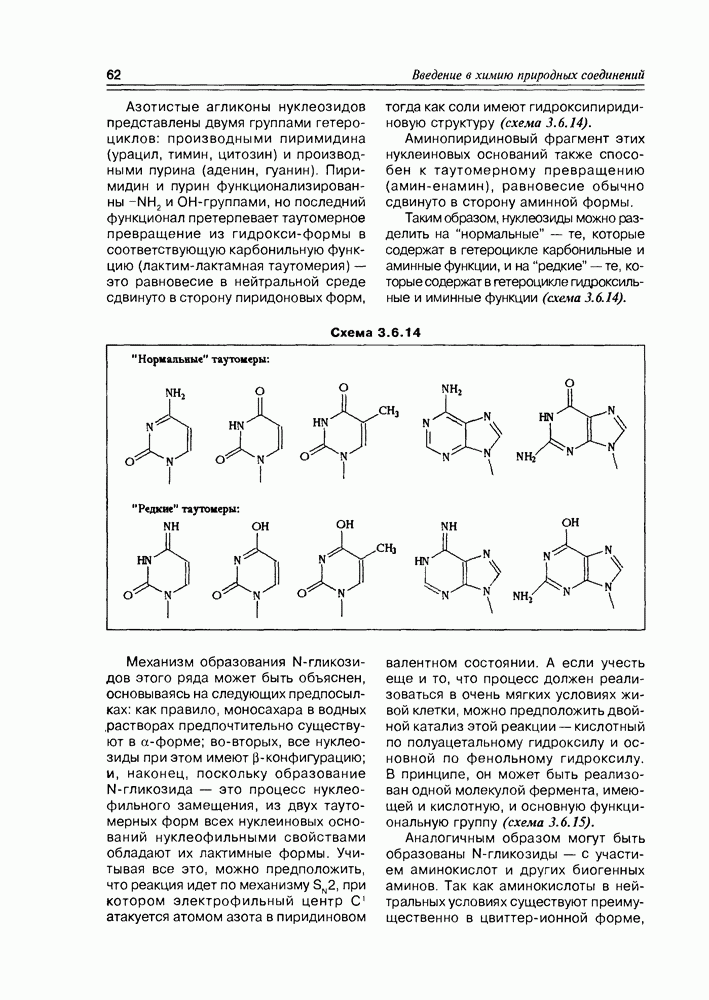
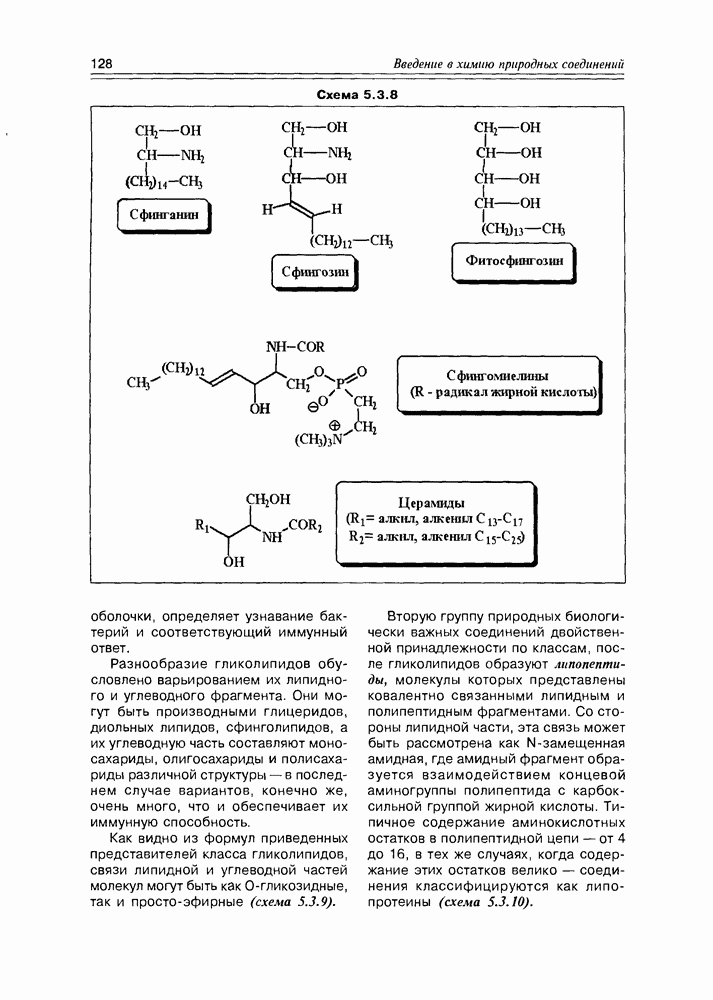
Весьма важную, разнообразную и интересную группу липидов под общим названием сфинголипиды, образуют длинноцепочечные аминоспирты — сфингонин, сфингозин и фитосфингозин. Указанные аминоспирты являются диольными. Они содержат алкильную цепочку от 12 до 22 атомов углерода. Сфингозины животных имеют олефиновую связь в основной цепи, сфингозины растений — дополнительную спиртовую группу (схема 5.3.8).
Как правило, жирная кислота, взаимодействуя со сфингозинами по аминогруппе, образует соответствующий замещенный амид, а фосфорная кислота этерифицирует первичную спиртовую группу, остальные спиртовые группы (одна или две) — обычно свободны. В церамидах все спиртовые группы остаются свободными. Фосфатная группа, как и во всех фосфолипидах, этерифицируется далее, образуя эффективную гидрофильную группу.
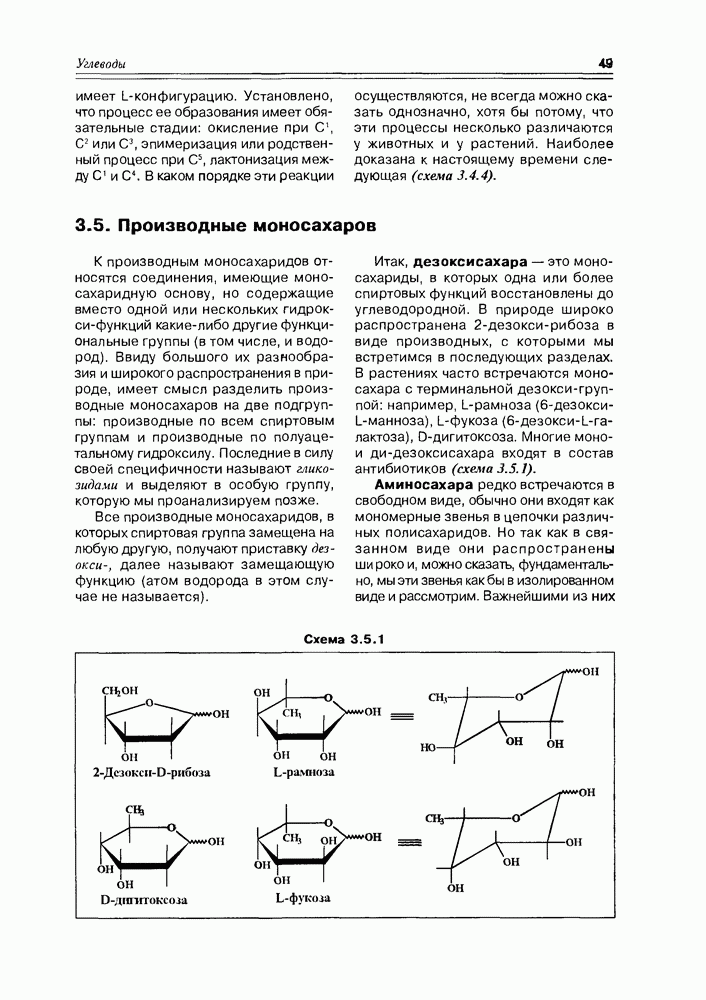
Интересная группа соединений образуется как бы на границе существования двух важных классов соединений — липидов и углеводов. В зависимости от соотношения липидных и углеводных фрагментов, эти соединения определяют как гликолипиды (в самом общем случае), выделяя в них группу липополисахаридов. В природе эти соединения распространены очень широко — они обнаружены в растениях, животных и микроорганизмах. В последнем случае, для микроорганизмов, характерно присутствие липополисахаридов, которые играют важную роль в их жизнедеятельности: участвуют в формировании клеточных мембран, в трансмембранном транспорте различных соединений, являются эндотоксинами, антигенами, рецепторами бактериофагов. В организмах человека и животных полисахаридный фрагмент этих липидов, направленный в сторону окружающей среды от клеточной
Схема 5.3.8

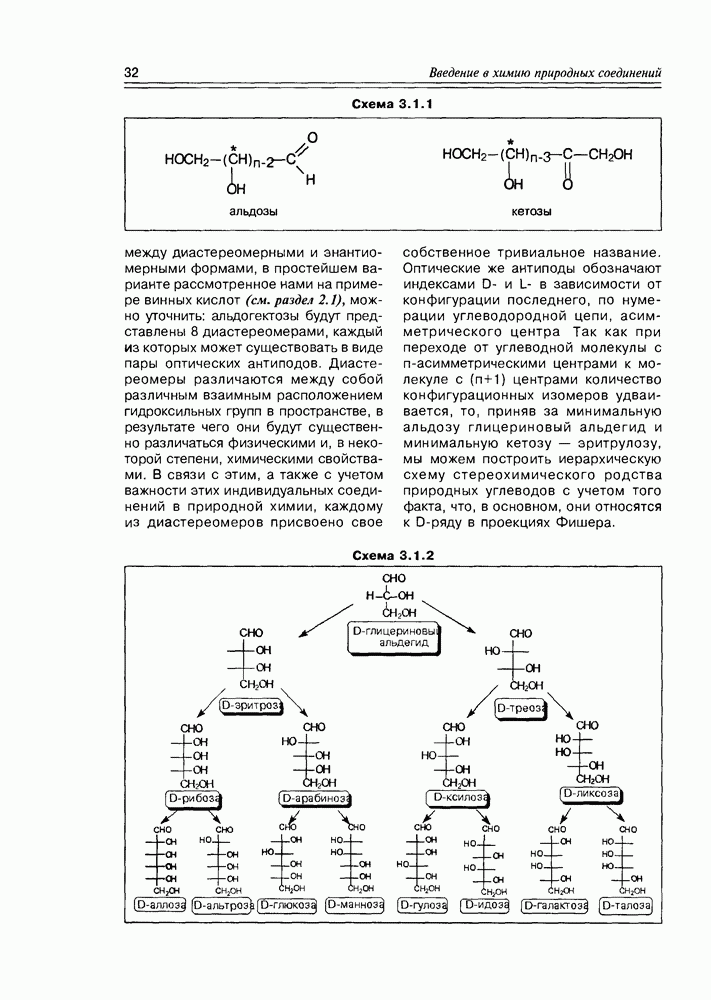
оболочки, определяет узнавание бактерий и соответствующий иммунный ответ.
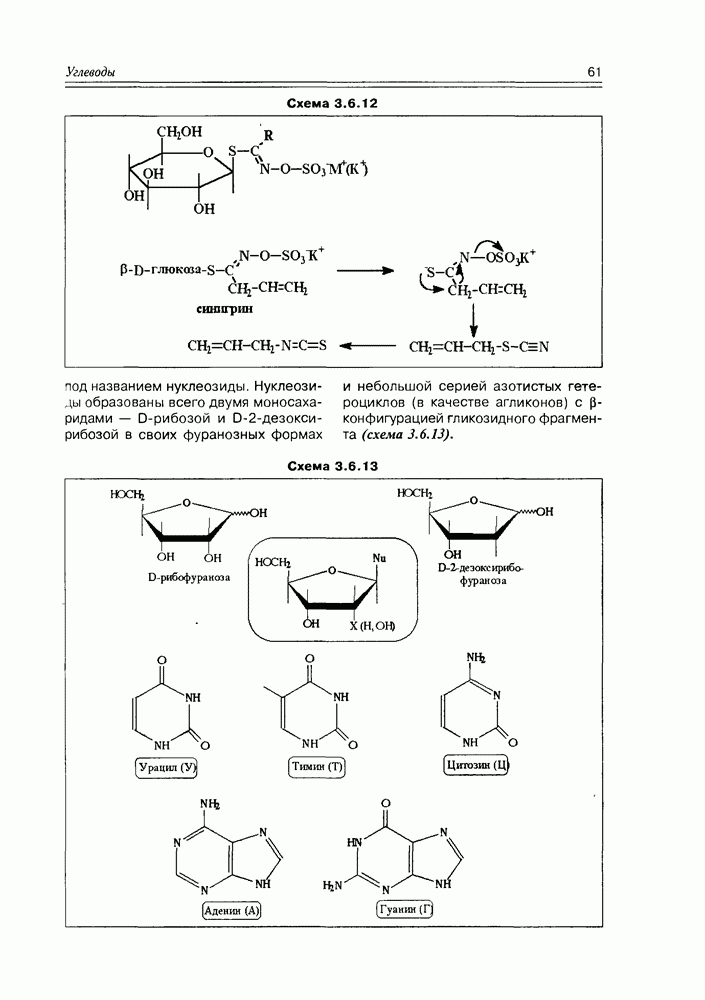
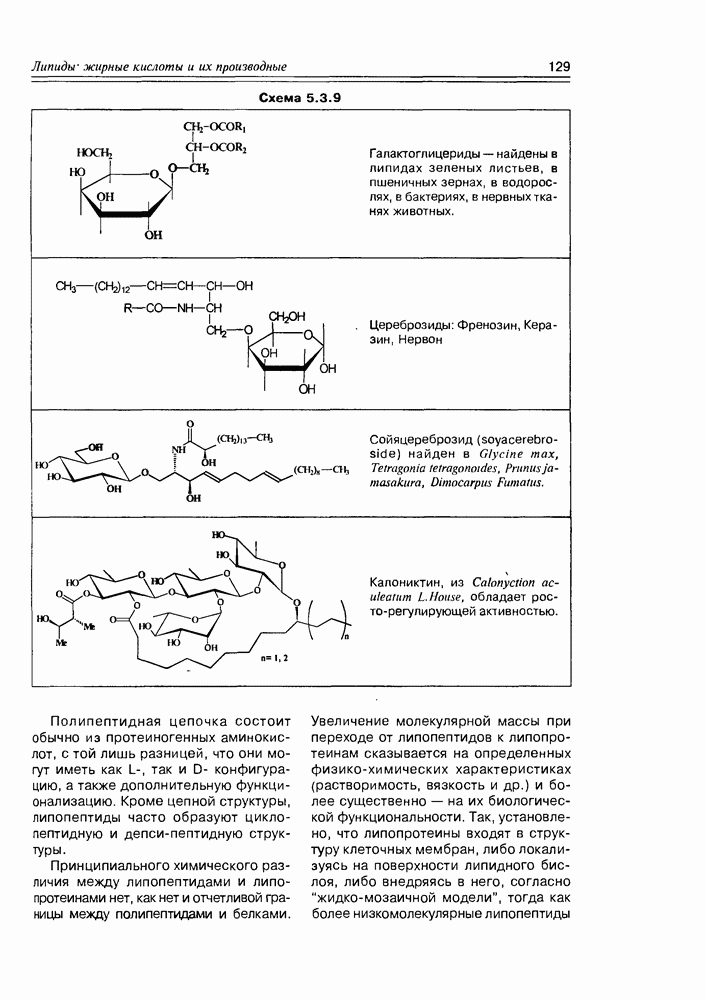
Разнообразие гликолипидов обусловлено варьированием их липидного и углеводного фрагмента. Они могут быть производными глицеридов, диольных липидов, сфинголипидов, а их углеводную часть составляют моносахариды, олигосахариды и полисахариды различной структуры — в последнем случае вариантов, конечно же, очень много, что и обеспечивает их иммунную способность.
Как видно из формул приведенных представителей класса гликолипидов, связи липидной и углеводной частей молекул могут быть как О-гликозидные, так и просто эфирные (схема 5.3.9).
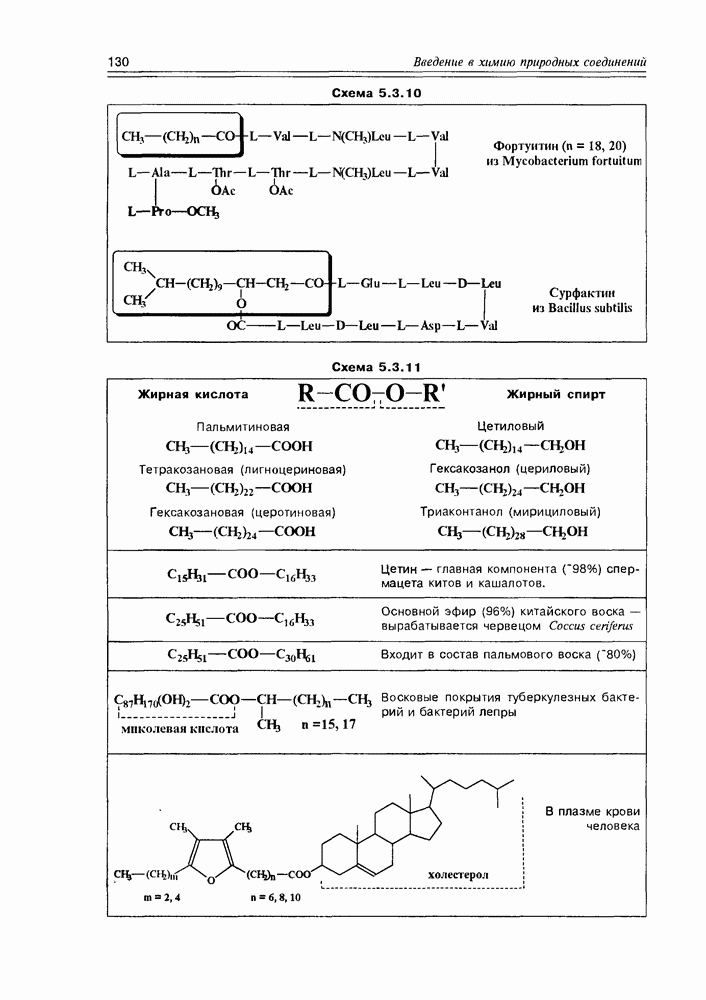
Вторую группу природных биологически важных соединений двойственной принадлежности по классам, после гликолипидов образуют липопептиды, молекулы которых представлены ковалентно связанными липидным и полипептидным фрагментами. Со стороны липидной части, эта связь может быть рассмотрена как N-замещенная амидная, где амидный фрагмент образуется взаимодействием концевой аминогруппы полипептида с карбоксильной группой жирной кислоты. Типичное содержание аминокислотных остатков в полипептидной цепи — от 4 до 16, в тех же случаях, когда содержание этих остатков велико — соединения классифицируются как липопротеины (схема 5.3.10).
Схема 5.3.9

Полипептидная цепочка состоит обычно из протеиногенных аминокислот, с той лишь разницей, что они могут иметь как L-, так и D- конфигурацию, а также дополнительную функци-онализацию. Кроме цепной структуры, липопептиды часто образуют циклопептидную и депсипептидную структуры.
Принципиального химического различия между липопептидами и липо-протеинами нет, как нет и отчетливой границы между полипептидами и белками.
Увеличение молекулярной массы при переходе от липопептидов к липопротеинам сказывается на определенных физико-химических характеристиках (растворимость, вязкость и др.) и более существенно — на их биологической функциональности. Так, установлено, что липопротеины входят в структуру клеточных мембран, либо локализуясь на поверхности липидного бислоя, либо внедряясь в него, согласно “жидко-мозаичной модели”, тогда как более низкомолекулярные липопептиды
Схема 5.3.10
(см. скан)
Схема 5.3.11
(см. скан)
не удерживаются клетками и выделяются (это характерно для микроорганизмов) в окружающую среду, выполняя определенную экологическую функцию — например, бактерицидную.
Липопептиды наиболее характерны для микроорганизмов (грам-положительных бактерий, актиномицет некоторых видов низших грибов).
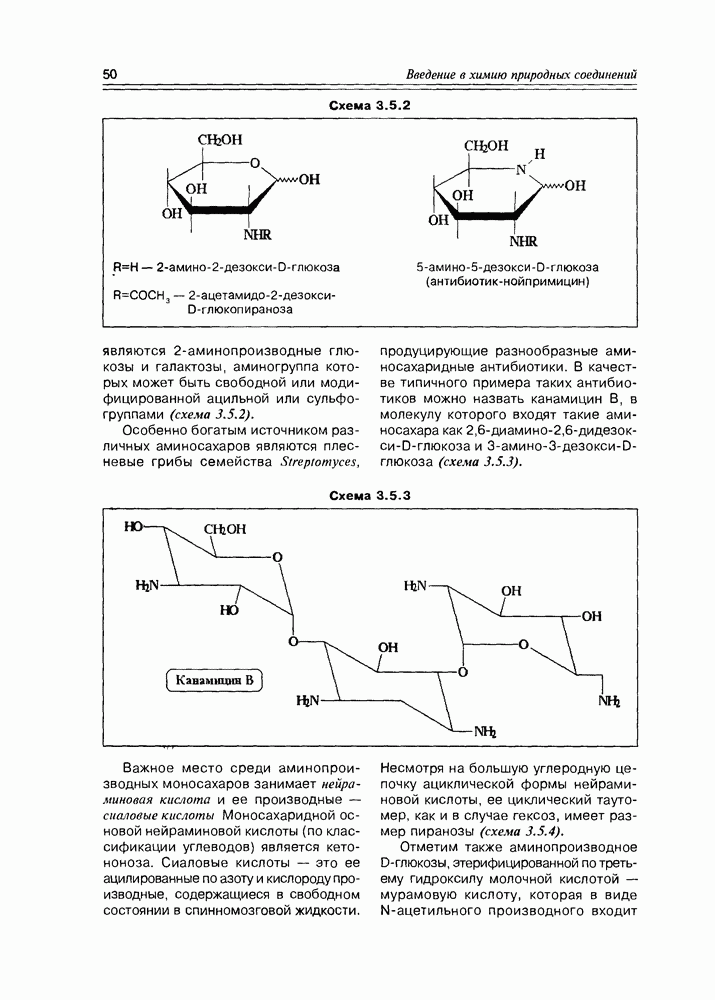
Не очень разнообразную, но все же заметную группу жироподобных производных жирных кислот представляют воски, являющиеся сложными эфирами неразветвленных жирных кислот и жирных спиртов. В состав этих “жирных” эфиров чаще всего входят пальмитиновая, церотиновая и маноцериновая кислоты, а также цетиловый и цериловый спирты. Все вышеуказанные спирты — неразветвленные первичные. Иногда в образовании восков участвуют и первичные спирты — такие как эйкозанол-2 и октадеканол-2. В состав некоторых животных восков (ланолин) входят сложные эфиры обычных жирных кислот и циклического спирта холестерола. Сложные эфиры холестерола и редких жирных кислот (например, фурановые жирные кислоты) достаточно часто встречаются в морских организмах, входят в состав плазмы крови человека. Кислотоупорные бактерии, в частности микобактерии туберкулеза и лепры, защищены восковой оболочкой, обеспечивающей им устойчивость к внешним воздействиям. Эта оболочка образована эфирами миколовых кислот и вышеуказанных вторичных спиртов  .
.
Растительные воски, покрывающие в виде тонкого налета или пленки листья, стебли и плоды растений, защищают последние от излишней потери влаги. Их примерами являются карнаубский воск, покрывающий листья бразильской пальмы Copernicia cerifera, и пальмовый воск, покрывающий ствол пальмы Geroxilon ondlicoka.
По химическим и физико-химическим свойствам воски близки к жирам, отличаясь от последних большей инертностью, особенной устойчивостью к гидролизу — они могут быть гидролизованы с трудом и только в щелочной среде. Для них также нехарактерно окисление по типу “прогоркания”. Гидрофобность восков также более ярко выражена по сравнению с глицеридами, фосфолипидами и другими жироподобными соединениями — они вообще не образуют поверхностно-активных пленок и макроструктур, подобных липидным бислоям.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ АВТОРА
- Глава 1. ВВЕДЕНИЕ
- 1.1. Предмет химии природных соединений
- 1.2. Классификация природных соединений
- 1.3. Методология химии природных соединений
- 1.4. Углерод и жизнь
- Глава 2. ПРОСТЕЙШИЕ БИФУНКЦИОНАЛЬНЫЕ ПРИРОДНЫЕ СОЕДИНЕНИЯ — МОСТИК К МАССИВУ ПРИРОДНЫХ СОЕДИНЕНИЙ
- 2.2. Оксокислоты
- 2.3. Аминоспирты
- Глава 3. УГЛЕВОДЫ
- 3.2. Свойства и структура моносахаридов
- 3.3. Химические свойства моносахаридов
- 3.4. Биосинтетические реакции углеводов
- 3.6. Гликозиды
- Глава 4. АМИНОКИСЛОТЫ, ПЕПТИДЫ, БЕЛКИ
- 4.2. Химические свойства а-аминокислот
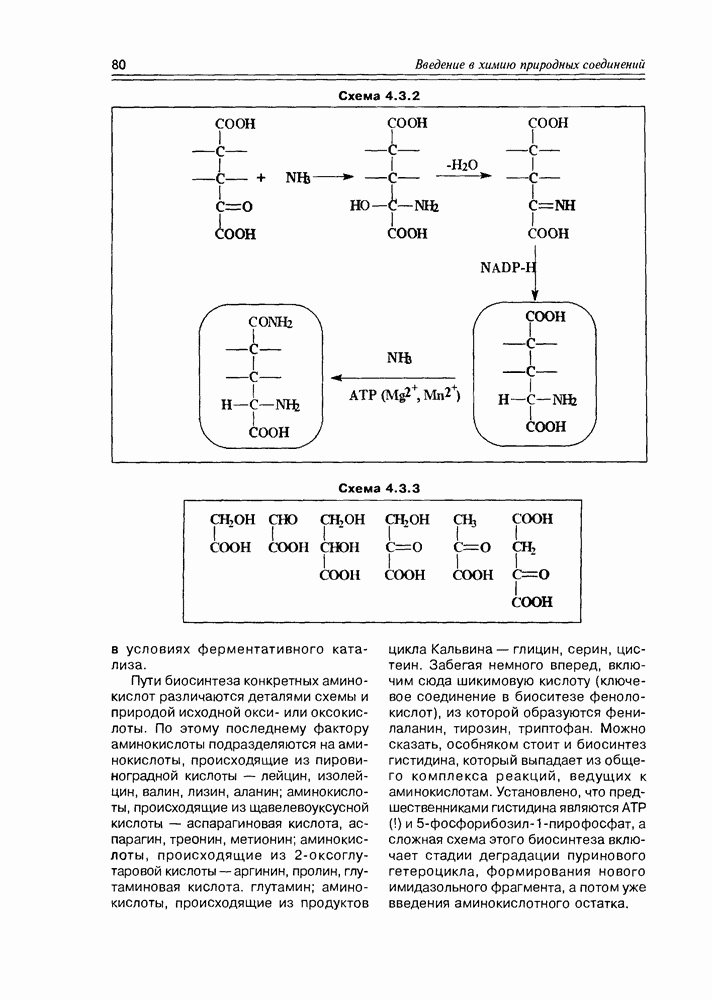
- 4.3. Биосинтез аминокислот
- 4.4. Полипептиды
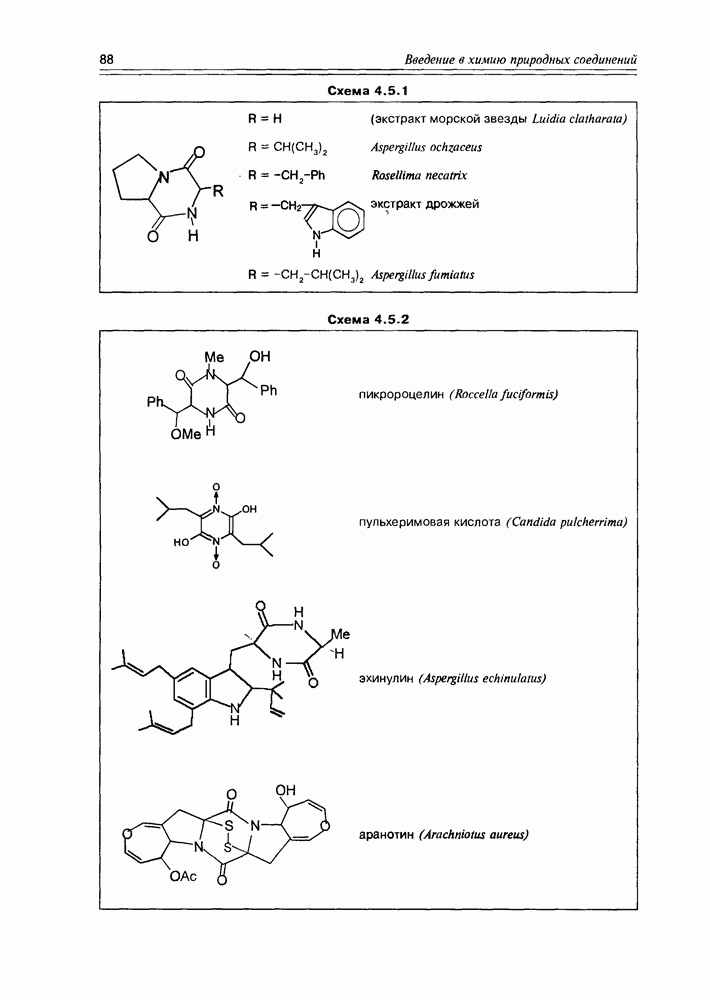
- 4.5. Дикетопиперазины
- 4.6. Циклопептиды
- 4.7. Депсипептиды
- 4.8. Белки
- Глава 5. ЛИПИДЫ: ЖИРНЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
- 5.1.1. Химические свойства жирных кислот
- 5.2. Метаболиты жирных кислот
- 5.2.2. Карбоциклические оксилипины
- 5.3. Жиры и жироподобные производные жирных кислот
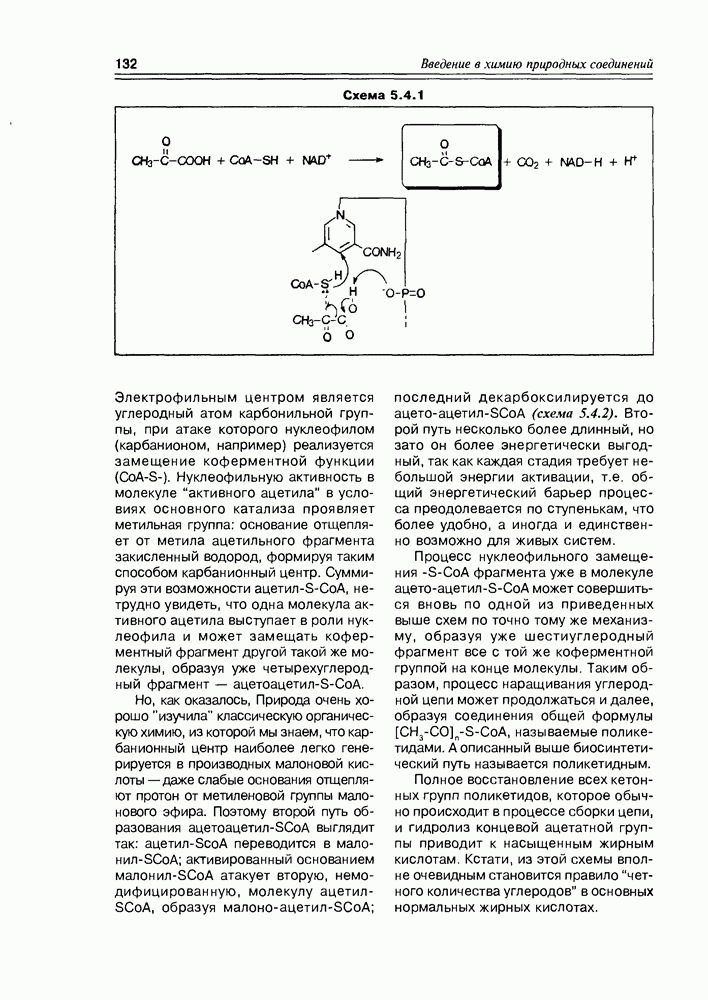
- 5.4. Биосинтез жирных кислот и их производных
- Глава 6. ИЗОПРЕНОИДЫ-1
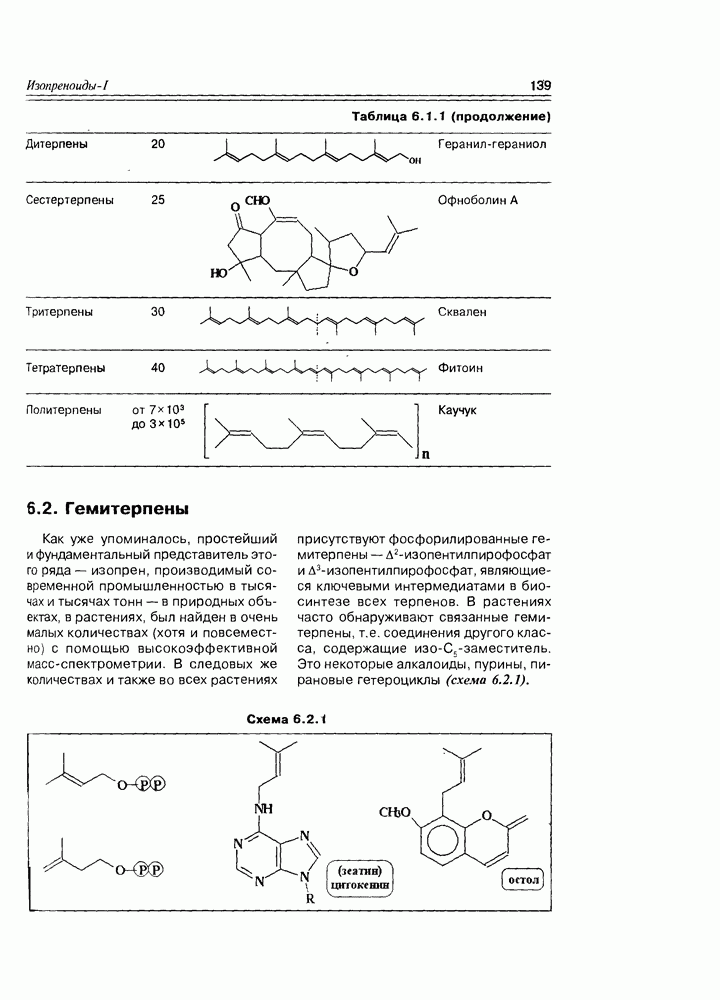
- 6.2. Гемитерпены
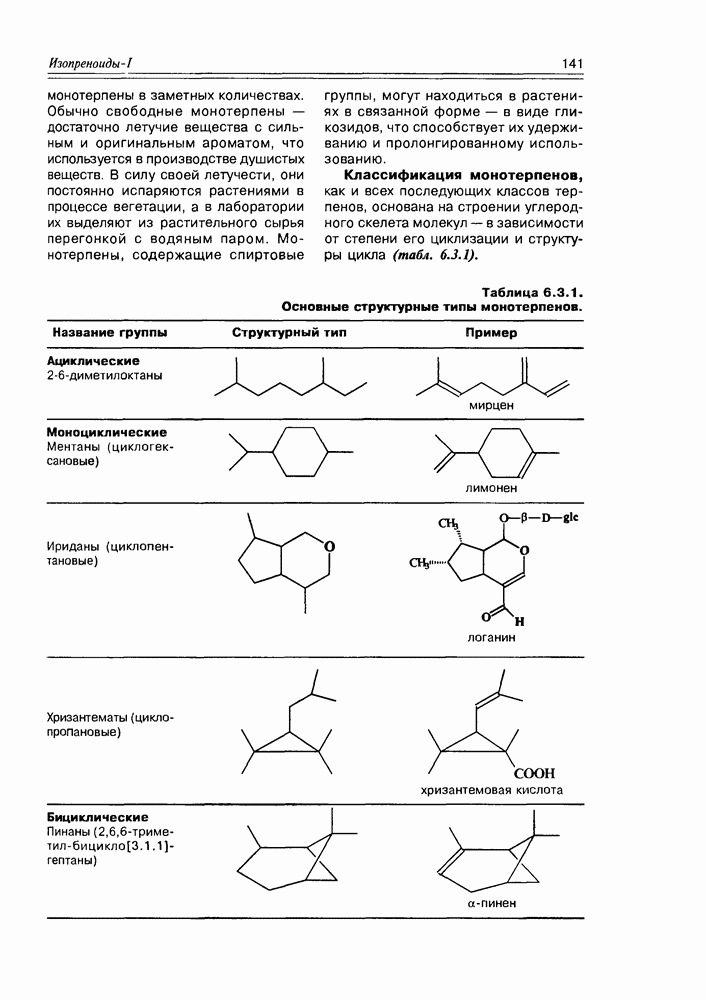
- 6.3. Монотерпены
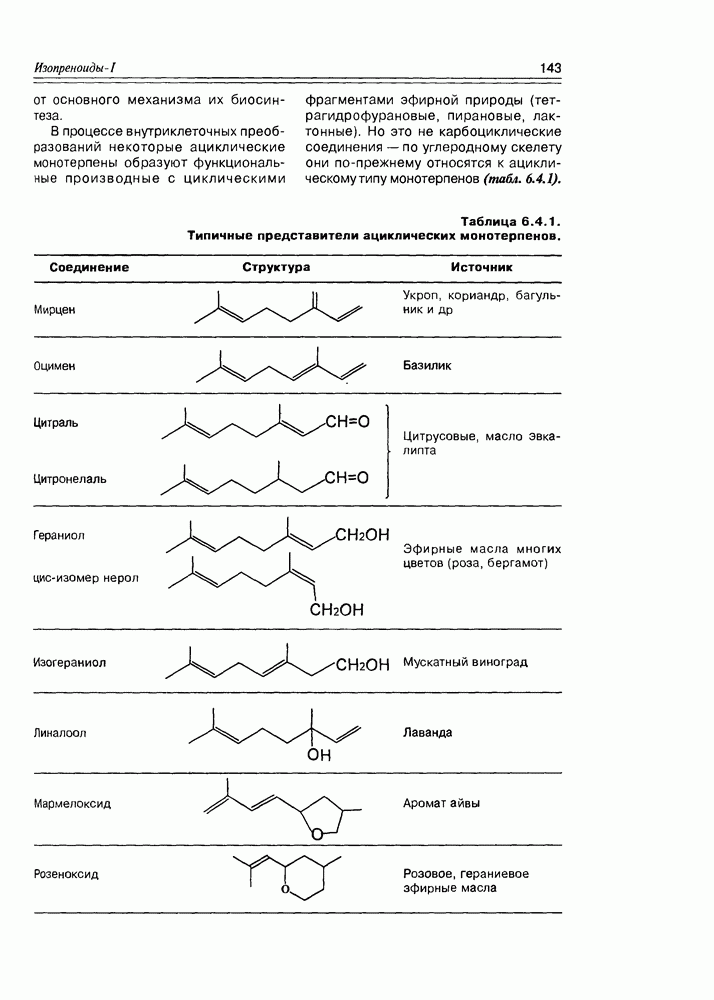
- 6.4. Ациклические монотерпены
- 6.5. Моноциклические терпены
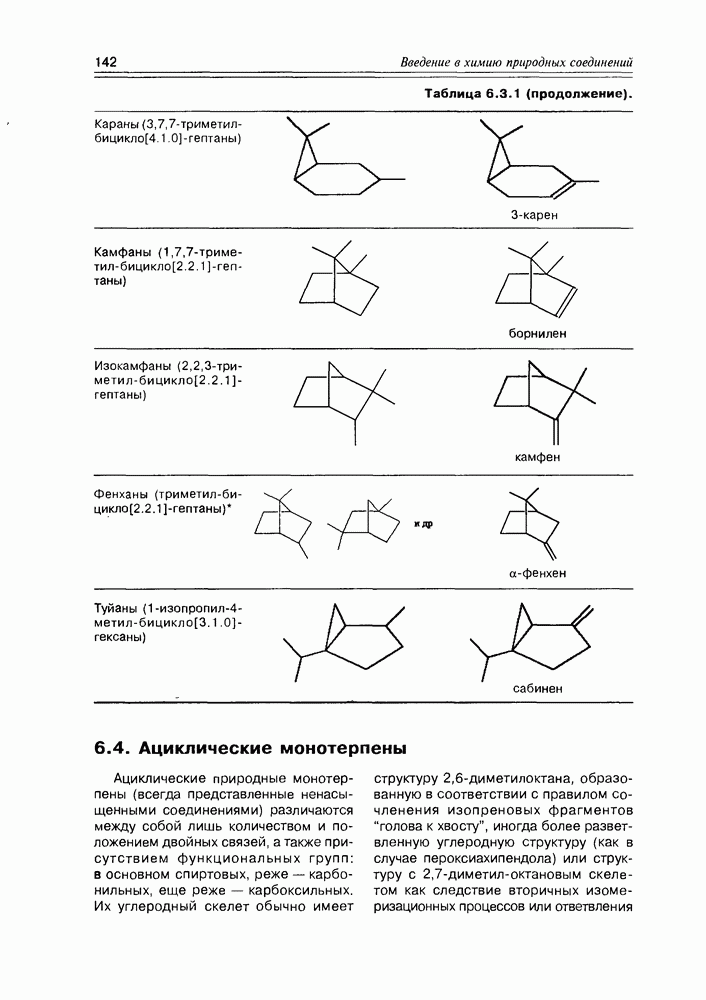
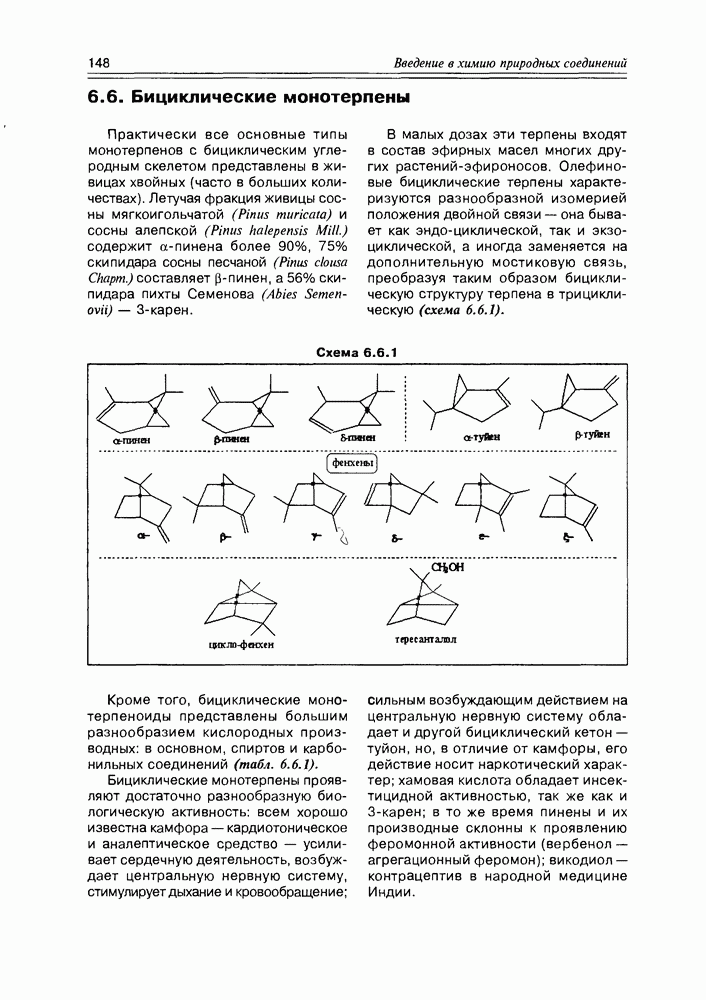
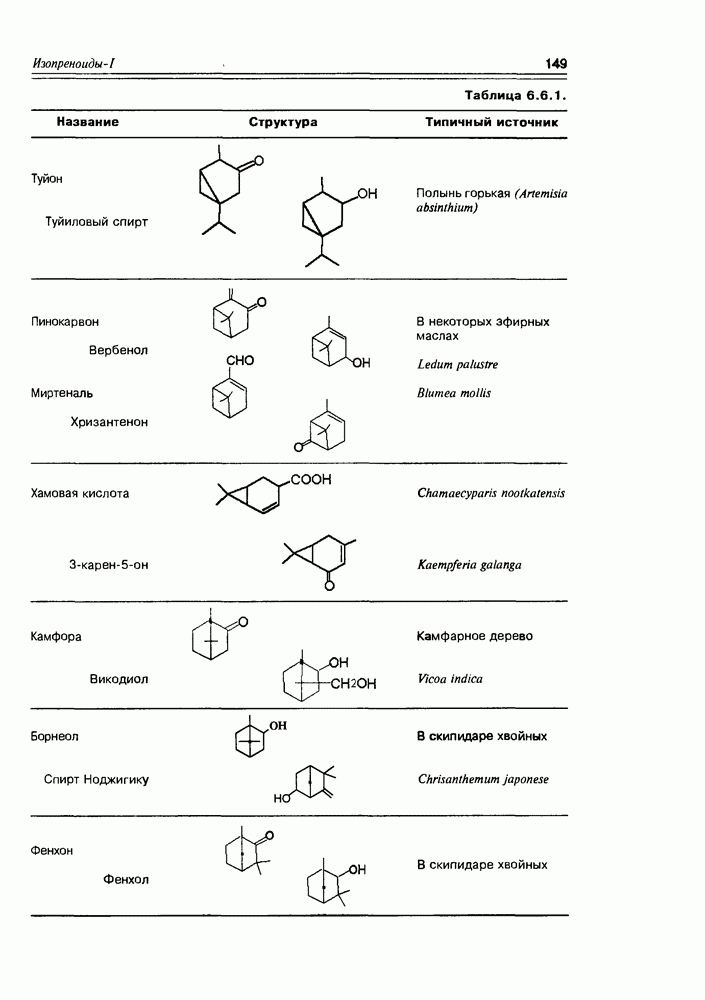
- 6.6. Бициклические монотерпены
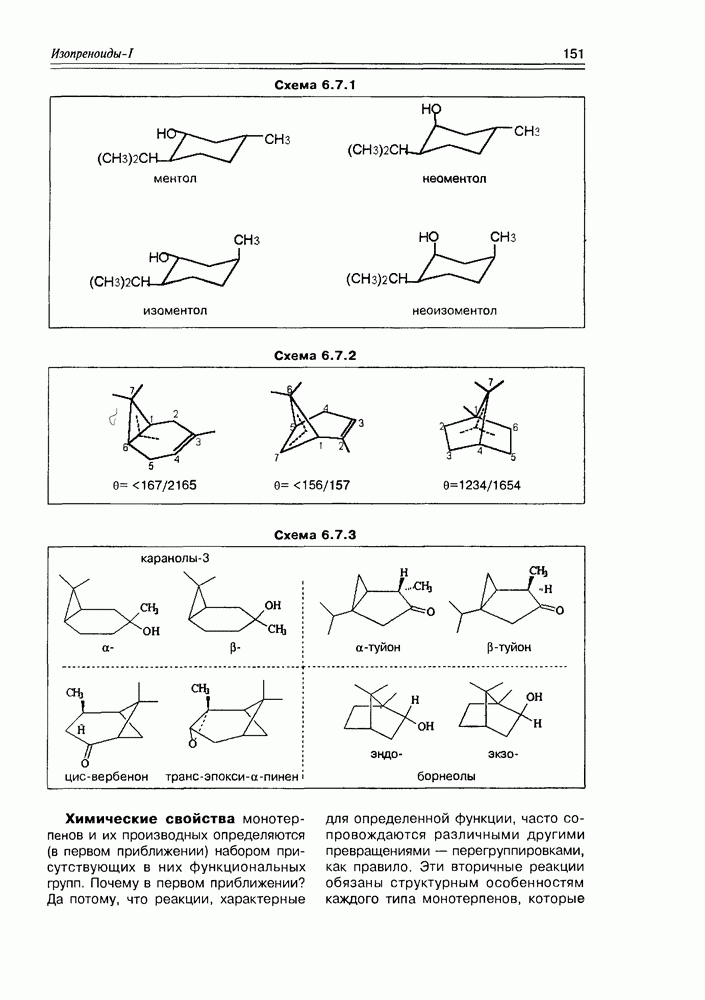
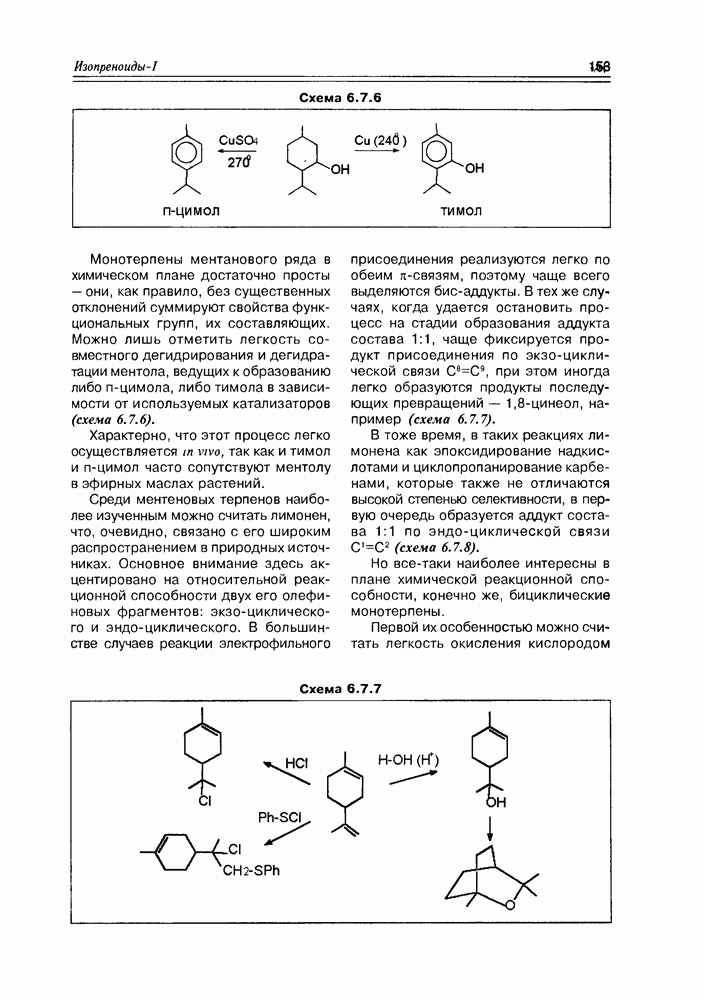
- 6.7. Строение и свойства монотерпенов
- 6.8. Биосинтез изопреноидов
- Глава 7. ИЗОПРЕНОИДЫ II. ОТ СЕСКВИТЕРПЕНОВ ДО ПОЛИТЕРПЕНОВ
- 7.2. Химические свойства сесквитерпенов
- 7.3. Дитерпены и сестертерпены
- 7.4. Тритерпеноиды и стероиды
- 7.5. Тетратерпеноиды — каротиноиды
- Глава 8. ФЕНОЛЬНЫЕ СОЕДИНЕНИЯ
- 8.2. Пираны
- 8.4. Биосинтез фенольных соединений
- Глава 9. АЛКАЛОИДЫ И ПОРФИРИНЫ
- 9.2. Истинные алкалоиды
- 9.3. Протоалкалоиды
- 9.5. Химические свойства и химические модификации алкалоидов
- 9.6. Аминокислоты и биосинтез алкалоидов
- 9.7. Порфирины
- Глава 10. ВИТАМИНЫ И КОФЕРМЕНТЫ
- 10.1. Витамины — собственно
- 10.2. Витамины-коферменты
- 10.3. Коферменты
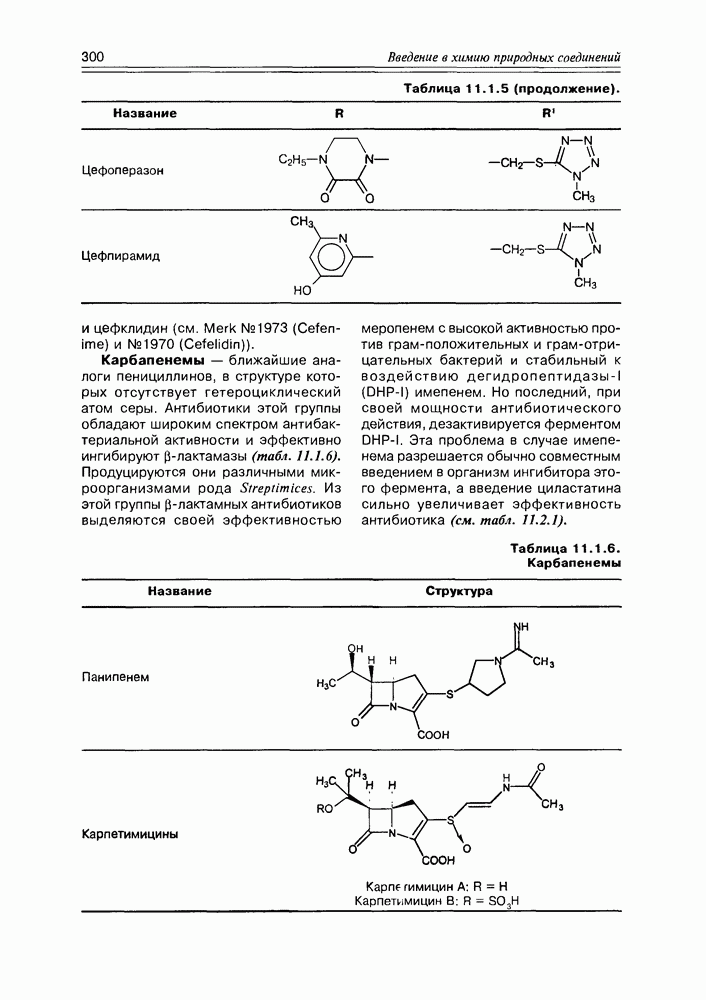
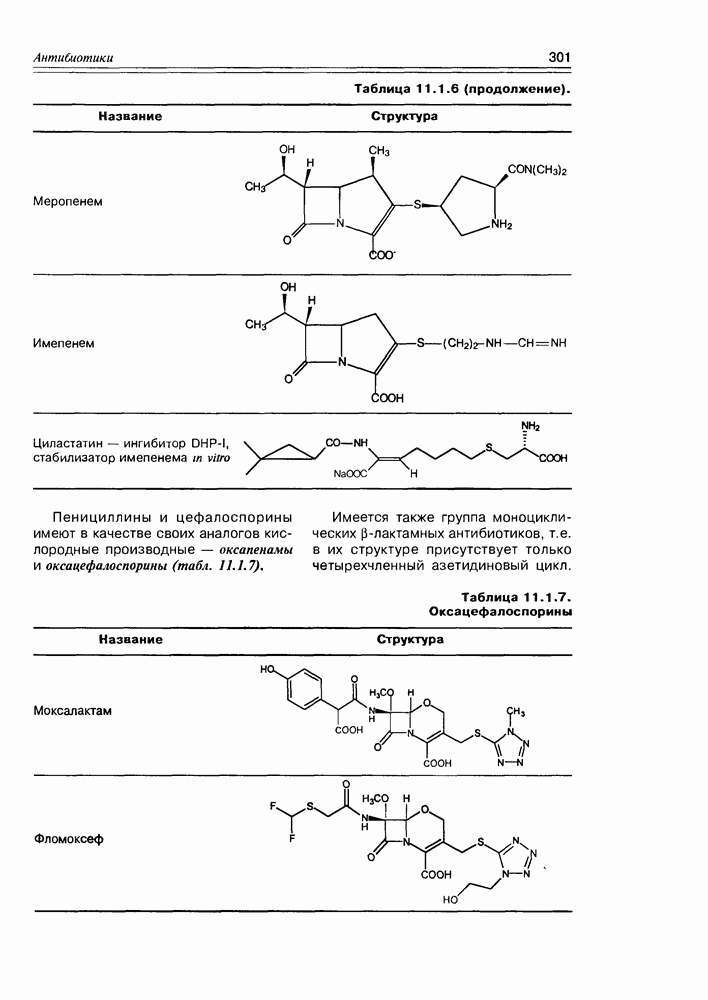
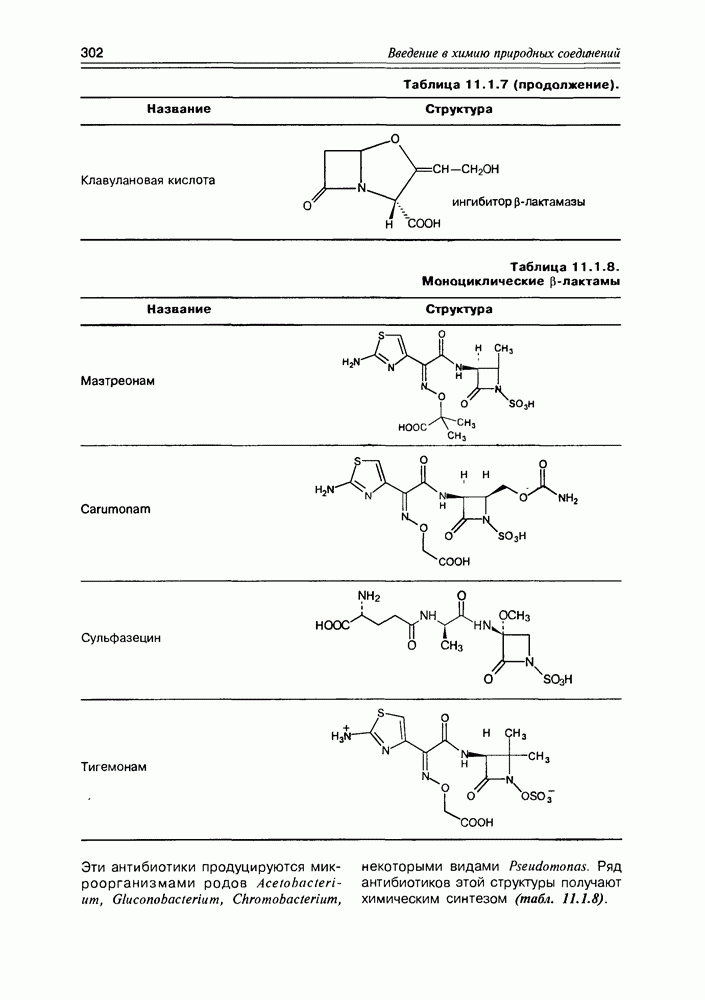
- Глава 11. АНТИБИОТИКИ
- 11.1. b-Лактамные антибиотики
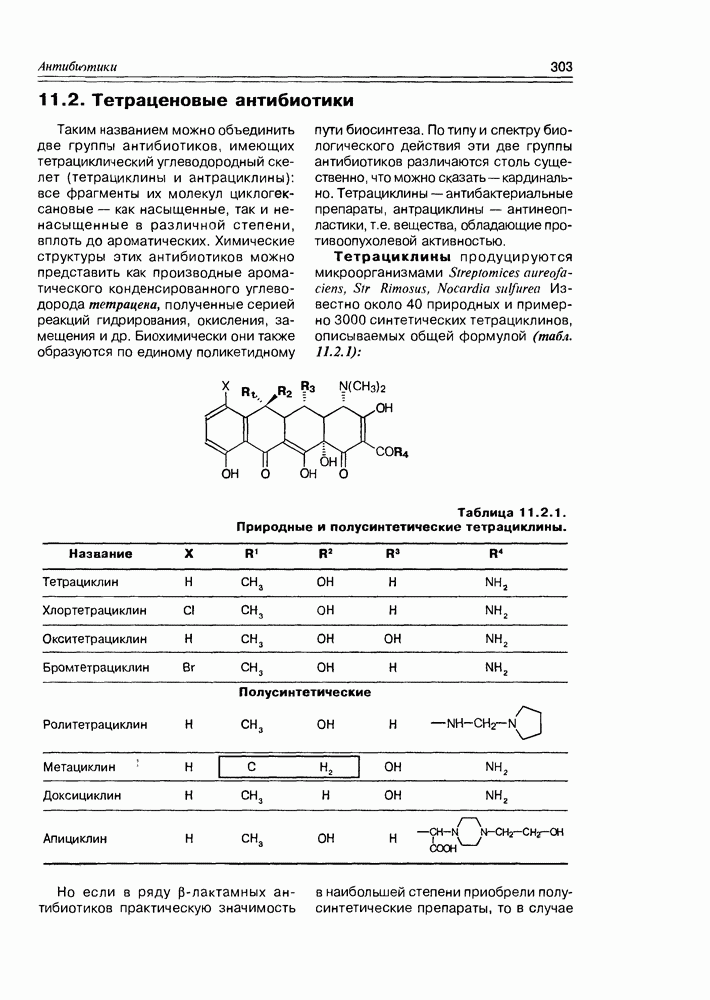
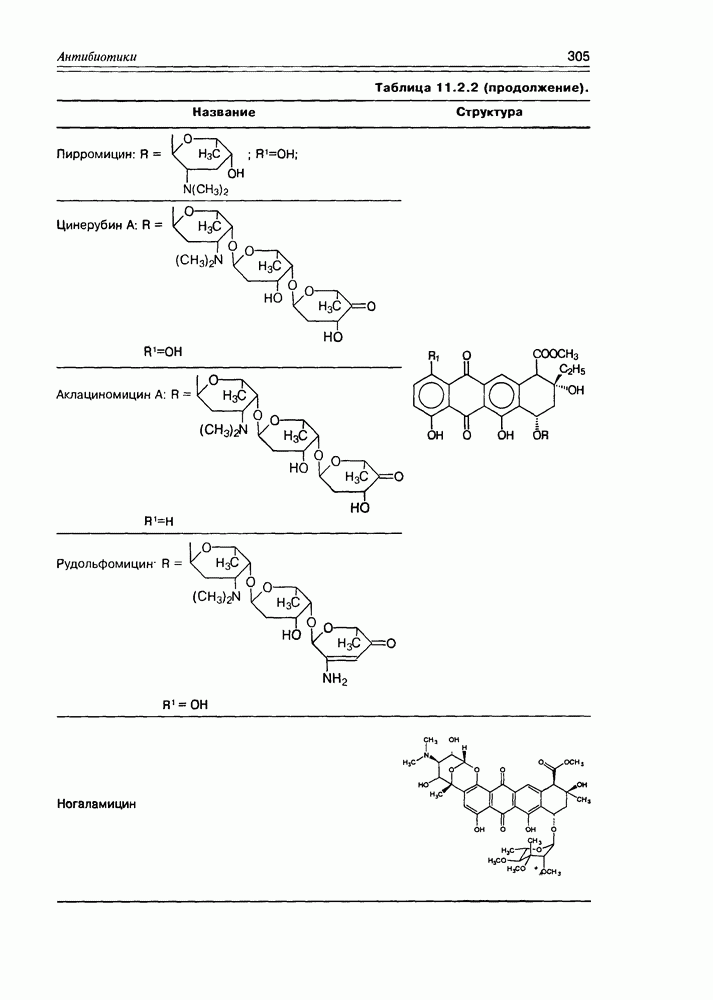
- 11.2. Тетраценовые антибиотики
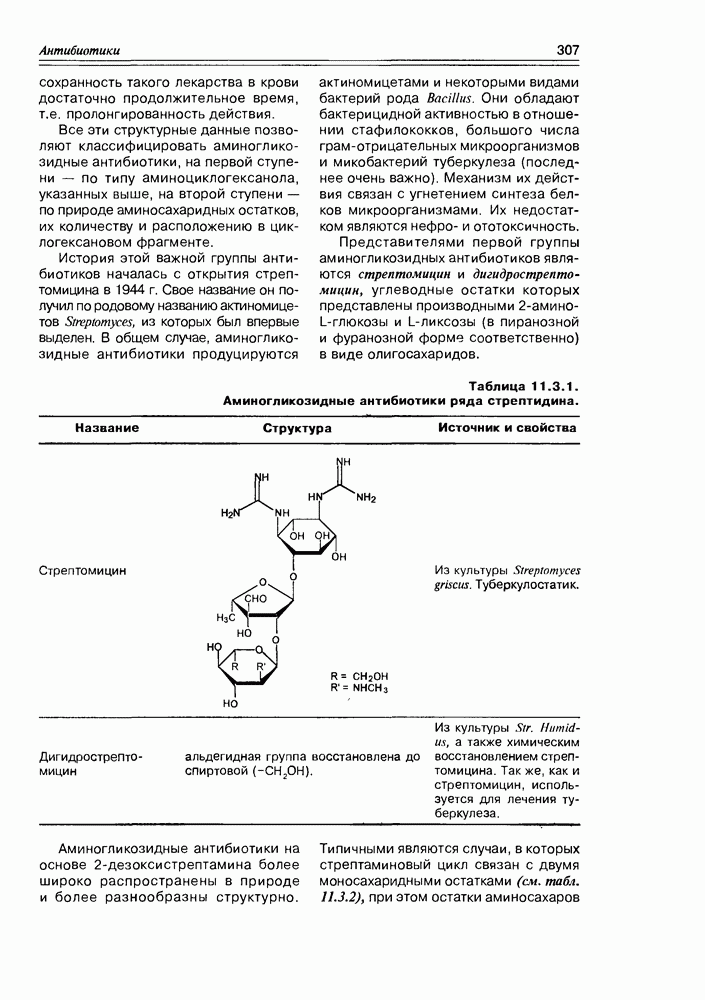
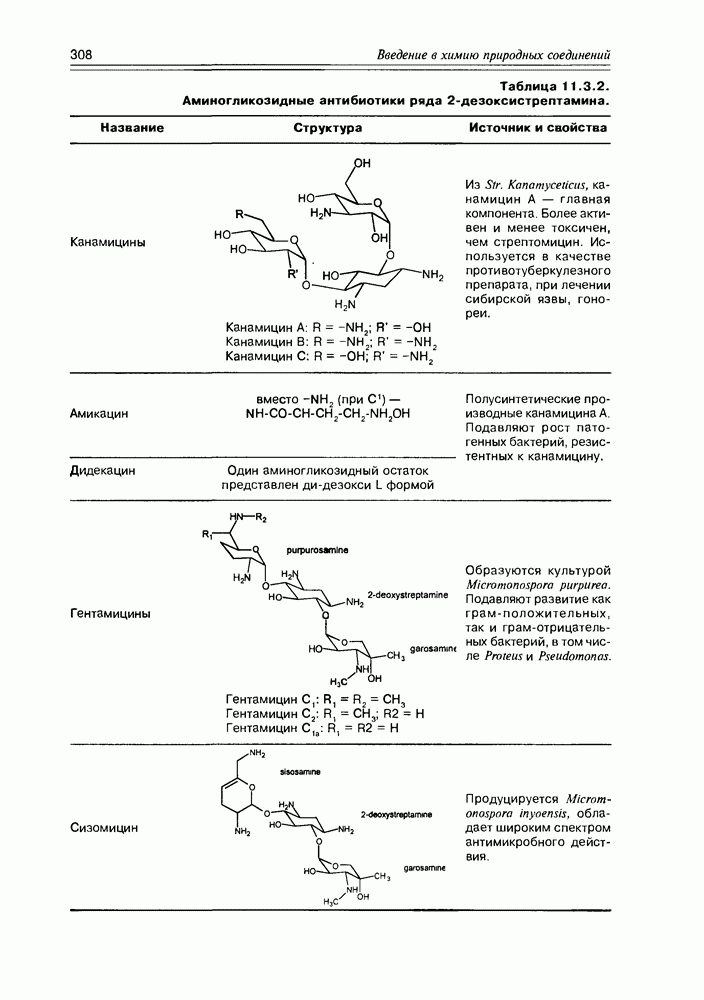
- 11.3. Аминогликозидные антибиотики
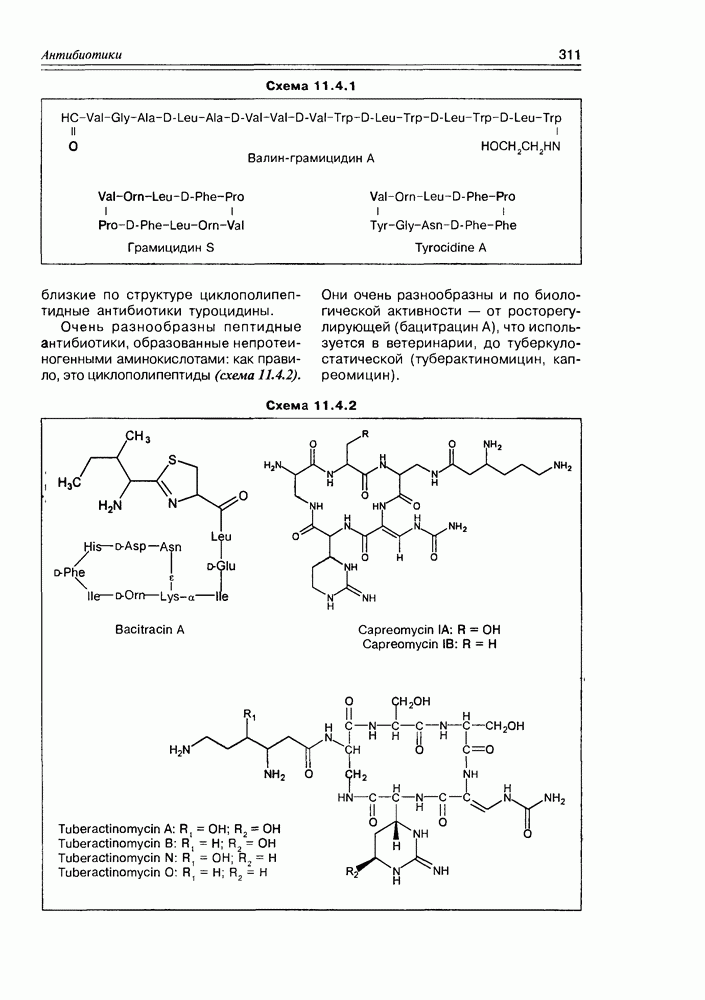
- 11.4. Пептидные антибиотики
- 11.5. Макролидные антибиотики
- 11.6. Полиэфирные антибиотики
- 11.7. Антибиотики разные
- Глава 12. РАЗНЫЕ ГРУППЫ ПРИРОДНЫХ СОЕДИНЕНИЙ
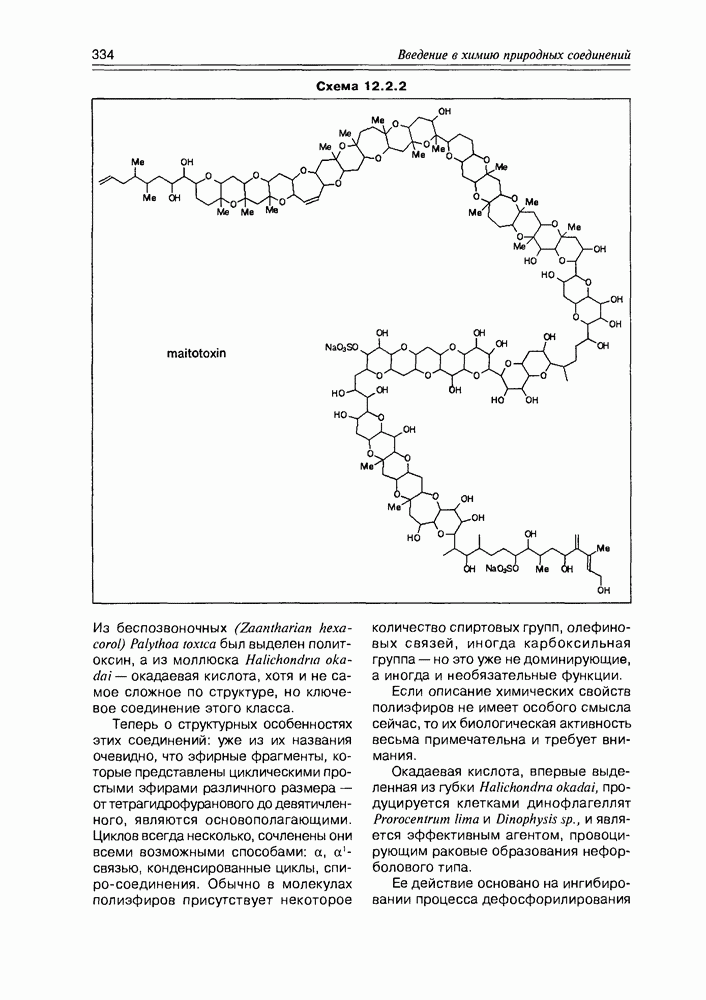
- 12.2. Полиэфиры
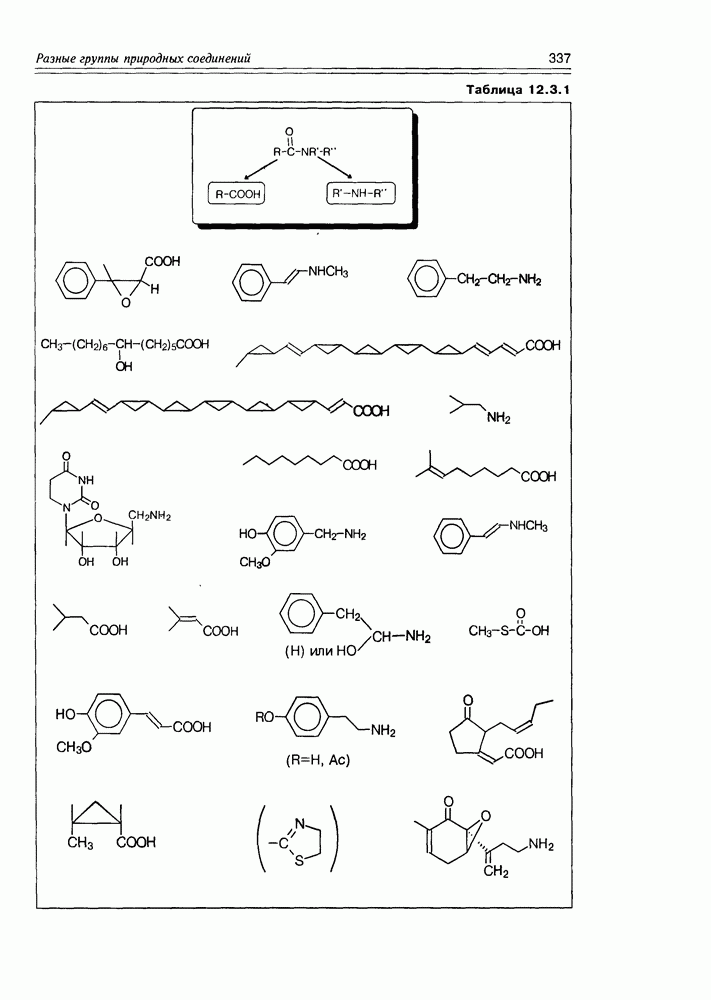
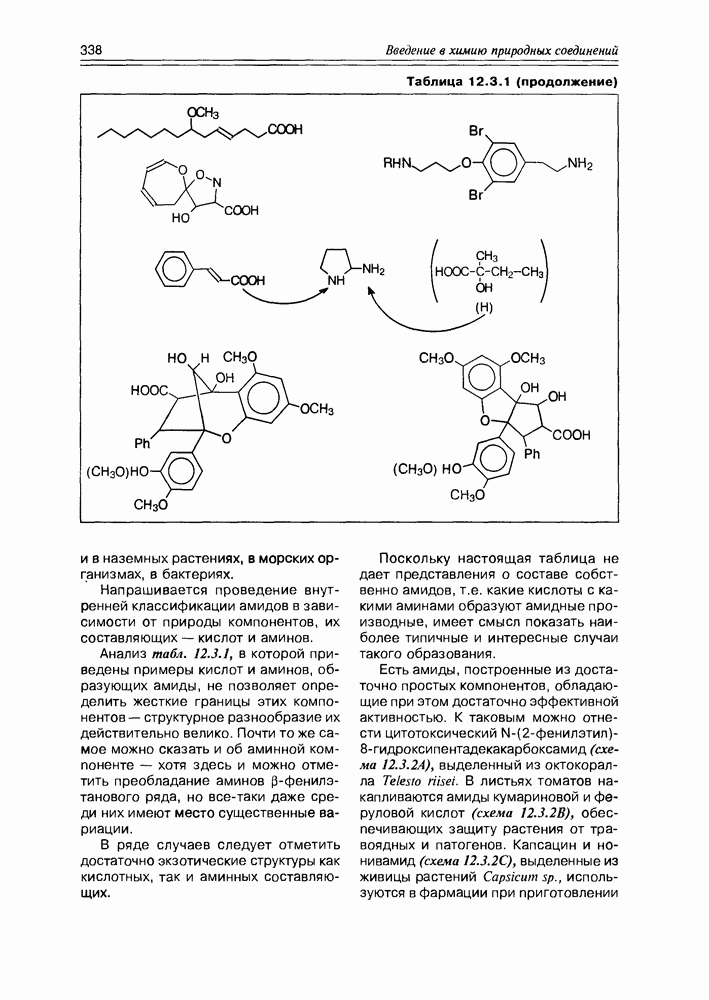
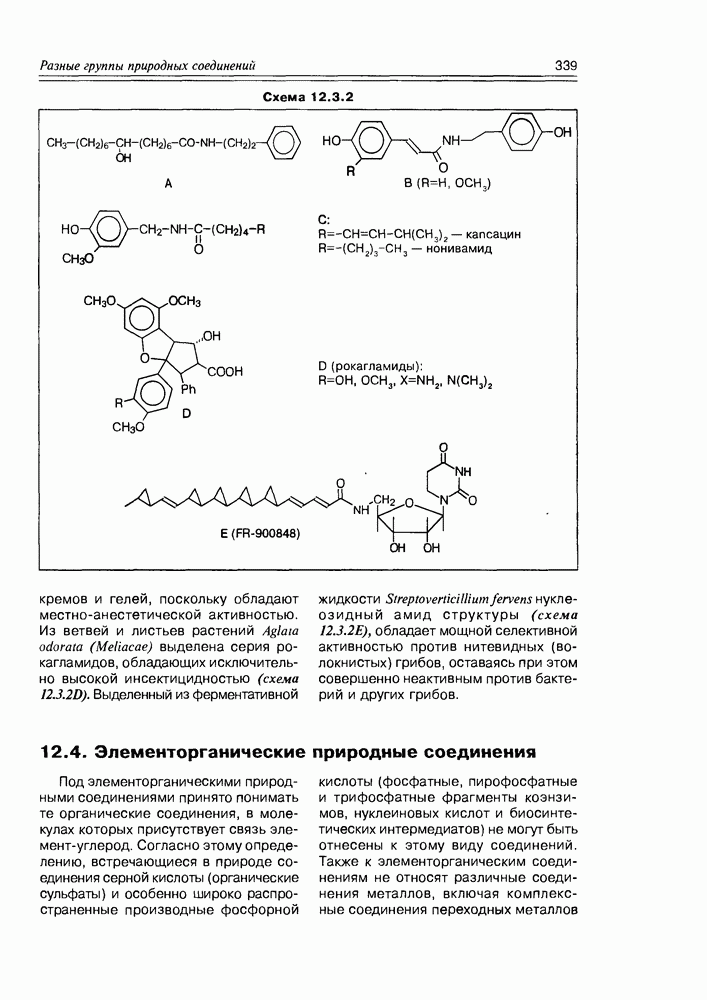
- 12.3. Амиды
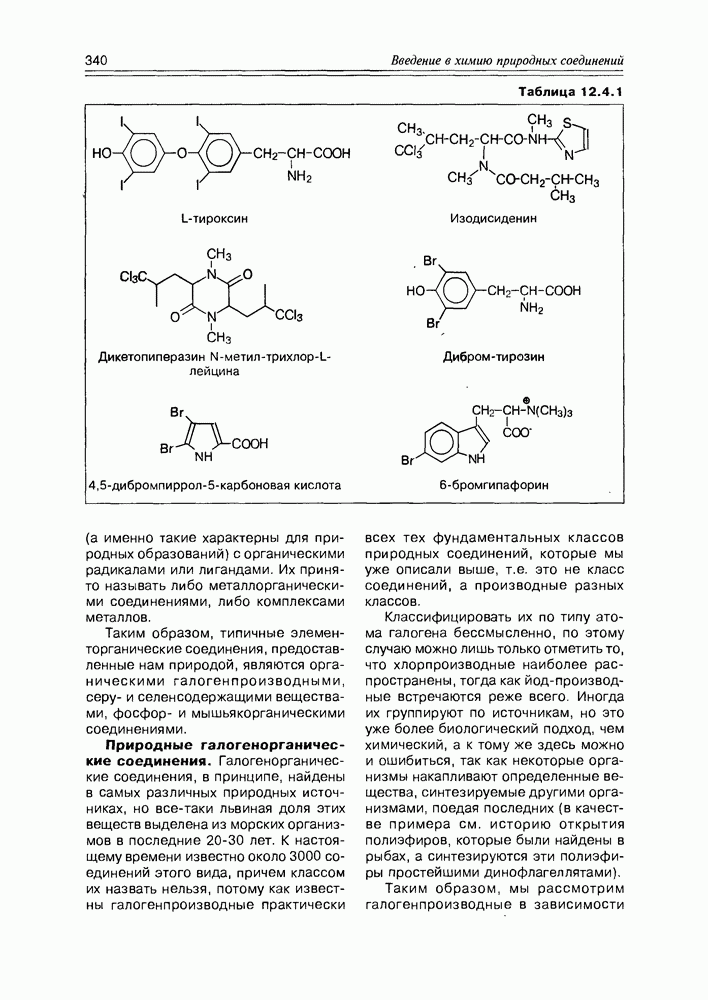
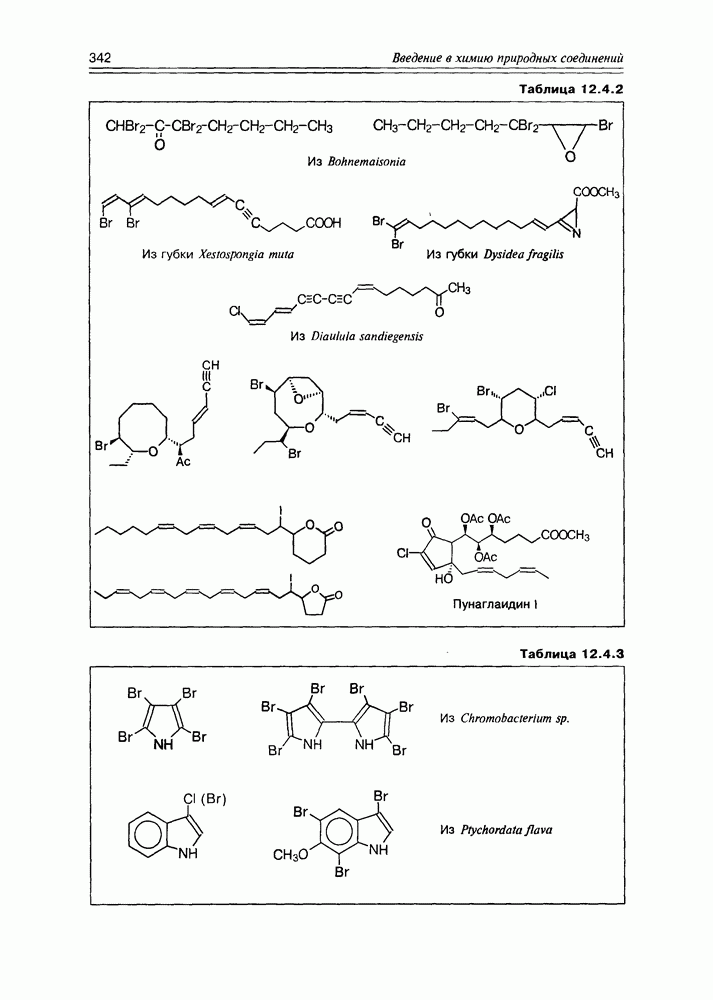
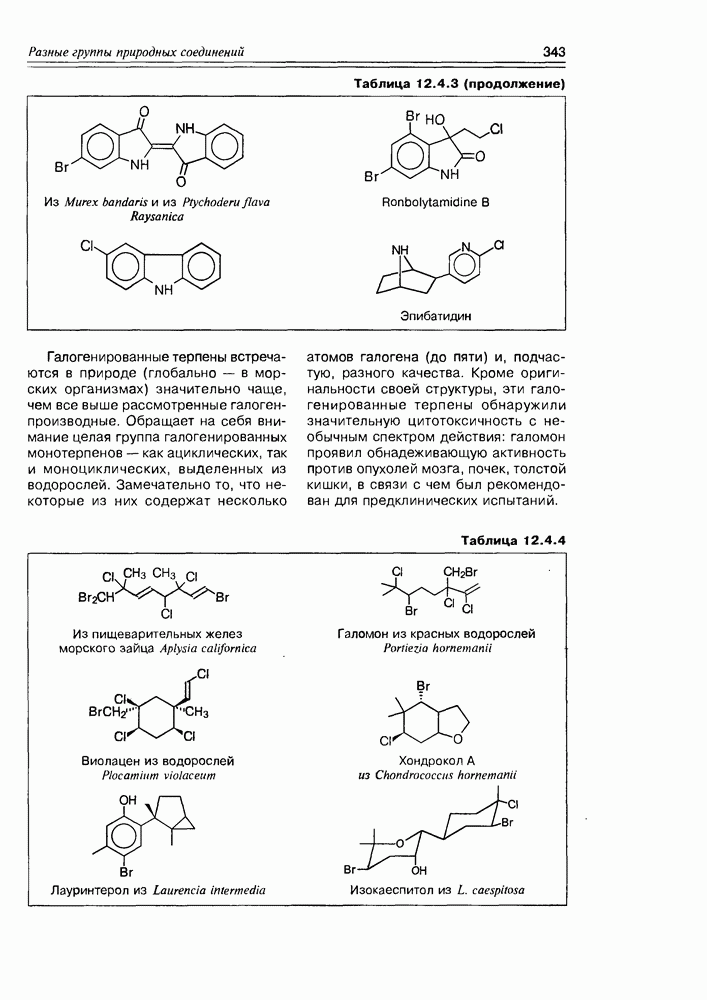
- 12.4. Элементорганические природные соединения
- Глава 13. МЕТАЛЛО-КОЭНЗИМЫ