| << Предыдущий параграф |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
Глава 13. МЕТАЛЛО-КОЭНЗИМЫ
Выделение металло-энзимов (металло-коэнзимов) в отдельную (в какой-то мере, особую) группу природных соединений связано с их химическим строением: они являются комплексными соединениями металлов и их солей с органическими лигандами различной природы, образуя класс природных соединений симбиозом органических и неорганических субстанций Т.е. это действительно тот класс соединений, который не может быть единолично отнесен ни к органической, ни к неорганической химии — он однозначно дитя химии природных соединений.
Возможно, включение металло-коэнзимов в общий раздел о витаминах и коферментах связано с их ключевой ролью в катализе широкого набора химических процессов in vivo и витаминно-подобной зависимостью живых организмов от металлов, их образующих: как и витамины, энзим-образующие элементы должны быть внесены экзогенно — не случайно поливитаминные препараты часто “идут” в комплексе с определенным набором микроэлементов. Но это уже медико-биологический подход. Таким образом, оставляя первенство за химией, мы выносим металло-энзимы в самостоятельный класс природных субстанций.
Общие положения. Металло-энзимы составляют приблизительно одну треть всех известных энзимов, они катализируют все типы биохимических реакций, включая митохондриальное восстановление кислорода, гидрокси-лирование углеводородов, фиксация азота, фотосинтетическая эволюция кислорода, деструкция токсических продуктов восстановления 02, скелетную изомеризацию, реакции метаногенеза, гидролиза, декарбоксилирования и др.
В первую очередь, в этом классе соединений, конечно же, необходимо определится по металлам, т.е. уяснить, какие металлы образуют коэнзимы, с какой частотой и как их классифицировать. Для наглядности проанализируем таблицу содержания металлов в организме человека (табл. 13.1).
Таблица 13.1.
Содержание металлов в организме человека (в весовых %).

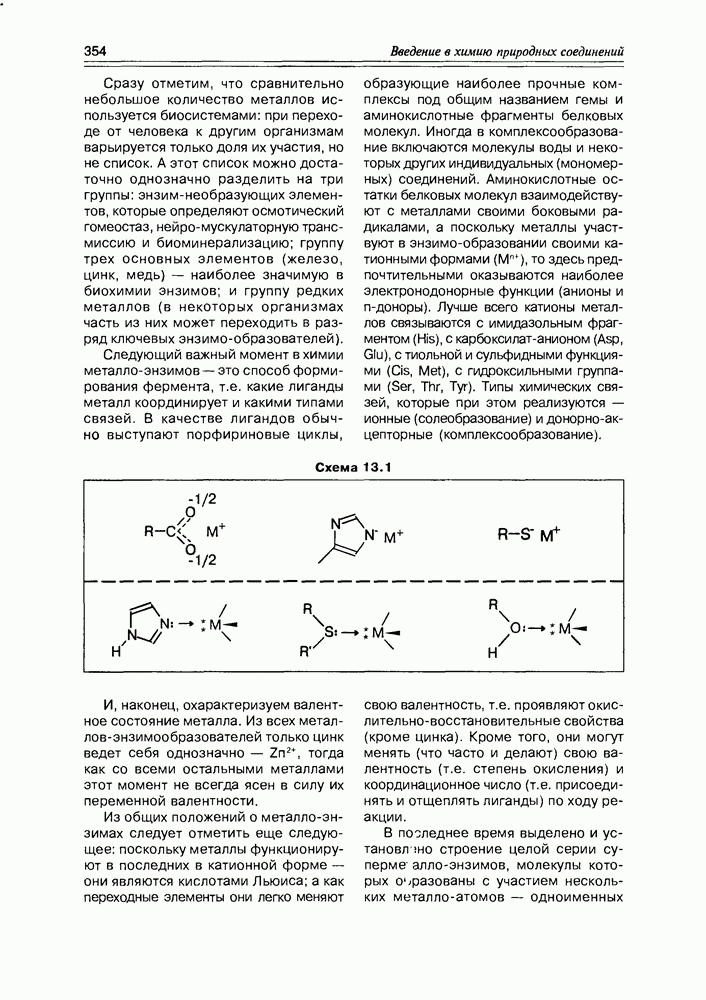
Сразу отметим, что сравнительно небольшое количество металлов используется биосистемами: при переходе от человека к другим организмам варьируется только доля их участия, но не список. А этот список можно достаточно однозначно разделить на три группы: энзим-необразующих элементов, которые определяют осмотический гомеостаз, нейро-мускулаторную трансмиссию и биоминерализацию; группу трех основных элементов (железо, цинк, медь) — наиболее значимую в биохимии энзимов; и группу редких металлов (в некоторых организмах часть из них может переходить в разряд ключевых энзимообразователей).
Следующий важный момент в химии металло-энзимов — это способ формирования фермента, т.е. какие лиганды металл координирует и какими типами связей. В качестве лигандов обычно выступают порфириновые циклы, образующие наиболее прочные комплексы под общим названием гемы и аминокислотные фрагменты белковых молекул. Иногда в комплексообразование включаются молекулы воды и некоторых других индивидуальных (мономерных) соединений. Аминокислотные остатки белковых молекул взаимодействуют с металлами своими боковыми радикалами, а поскольку металлы участвуют в энзимо-образовании своими катионными формами  , то здесь предпочтительными оказываются наиболее электронодонорные функции (анионы и
, то здесь предпочтительными оказываются наиболее электронодонорные функции (анионы и  -доноры). Лучше всего катионы металлов связываются с имидазольным фрагментом
-доноры). Лучше всего катионы металлов связываются с имидазольным фрагментом  с карбоксилат-анионом (Asp, Glu), с тиольной и сульфидными функциями
с карбоксилат-анионом (Asp, Glu), с тиольной и сульфидными функциями  с гидроксильными группами
с гидроксильными группами  . Типы химических связей, которые при этом реализуются — ионные (солеобразование) и донорно-акцепторные (комплексообразование).
. Типы химических связей, которые при этом реализуются — ионные (солеобразование) и донорно-акцепторные (комплексообразование).
Схема 13.1

И, наконец, охарактеризуем валентное состояние металла. Из всех металлов-энзимообразователей только цинк ведет себя однозначно  тогда как со всеми остальными металлами этот момент не всегда ясен в силу их переменной валентности.
тогда как со всеми остальными металлами этот момент не всегда ясен в силу их переменной валентности.
Из общих положений о металло-энзимах следует отметить еще следующее: поскольку металлы функционируют в последних в катионной форме — они являются кислотами Льюиса; а как переходные элементы они легко меняют свою валентность, т.е. проявляют окислительно-восстановительные свойства (кроме цинка). Кроме того, они могут менять (что часто и делают) свою валентность (т.е. степень окисления) и координационное число (т.е. присоединять и отщеплять лиганды) по ходу реакции.
В последнее время выделено и установлено строение целой серии супермеалло-энзимов, молекулы которых образованы с участием нескольких металло-атомов — одноименных
Таблица 13.2. Типичные реакции цинк-содержащих энзимов.

или различных, которые тесно связаны между собой либо непосредственно, либо сульфидными (иногда оксидными) мостиками, образуя иногда целые кластеры в качестве кофакторов ферментов. В деле установления структуры этих последних энзимов необходимо отдать должное методу рентгеноструктурного анализа — здесь он незаменим и однозначен.
В отличие от классической органической химии, где фигурирует понятие реакционного центра (или активного центра) молекулы, в химии природных соединений по отношению к реакциям, управляемым энзимами, a in vivo таковыми являются практически все, более подходящим является термин “активный сайт”, так как всегда несколько атомов и функциональных групп формируют ту область (“сайт") фермента, где происходит реакция. По этой же причине, здесь более употребительным будет и термин “сайт переходного состояния” реакции вместо классического “переходное состояние” реакции.
Цинк-энзимы. Первый цмнк-содержащий энзим был открыт в 1939 г. (Мапп и Keilin), сейчас их известно уже более 300. Точная структура (рентгеноструктурный анализ) установлена более чем у дюжины оных.
Энзимы этой группы катализируют следующие биохимические реакции (табл. 13.2.).
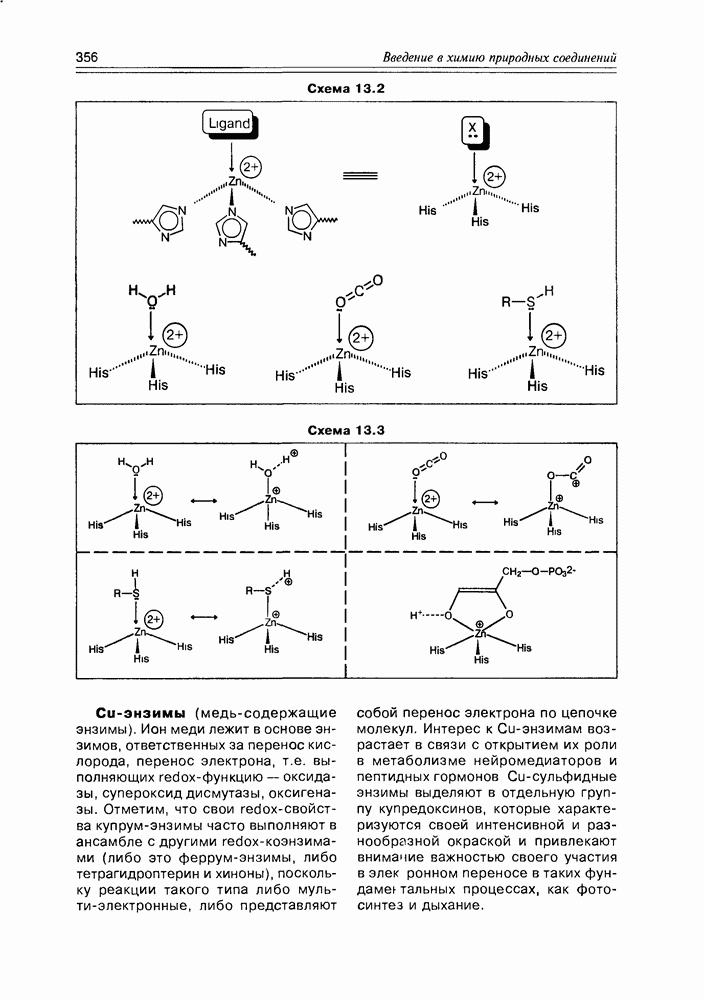
Цинк образует активный сайт координацией с аминокислотными остатками белковых молекул (гистидина, цистеина, аспарагиновой кислоты) с использованием как ионных, так и донорно-акцепторных связей. Обычно таких лигандов три-четыре, на оставшиеся координационные вакансии (одна-две) катион цинка присоединяет молекулы или фрагменты молекул, подлежащие активации (схема 13.2).
Цинк-энзимовая активация основана на Льюисовской кислотности этого металла, которая не осложнена redox-свойствами и влечет за собой увеличение либо кислотности, либо электро-фильности координируемой молекулы (схема 13.3).
Исключительными свойствами цинк-энзимов (кроме redox-неактивности) следует считать легкость лигандного обмена и сравнимая стабильность комплексов различной степени координации — от 4 до 6.
Схема 13.2

Схема 13.3

Cu-энзимы (медь-содержащие энзимы). Ион меди лежит в основе энзимов, ответственных за перенос кислорода, перенос электрона, т.е. выполняющих redox-функцию — оксидазы, супероксид дисмутазы, оксигеназы. Отметим, что свои redox-свойства купрум-энзимы часто выполняют в ансамбле с другими redox-коэнзимами (либо это феррум-энзимы, либо тетрагидроптерин и хиноны), поскольку реакции такого типа либо мультиэлектронные, либо представляют собой перенос электрона по цепочке молекул. Интерес к  -энзимам возрастает в связи с открытием их роли в метаболизме нейромедиаторов и пептидных гормонов Cu-сульфидные энзимы выделяют в отдельную группу купредоксинов, которые характеризуются своей интенсивной и разнообразной окраской и привлекают внимание важностью своего участия в элек ронном переносе в таких фундаментальных процессах, как фотосинтез и дыхание.
-энзимам возрастает в связи с открытием их роли в метаболизме нейромедиаторов и пептидных гормонов Cu-сульфидные энзимы выделяют в отдельную группу купредоксинов, которые характеризуются своей интенсивной и разнообразной окраской и привлекают внимание важностью своего участия в элек ронном переносе в таких фундаментальных процессах, как фотосинтез и дыхание.
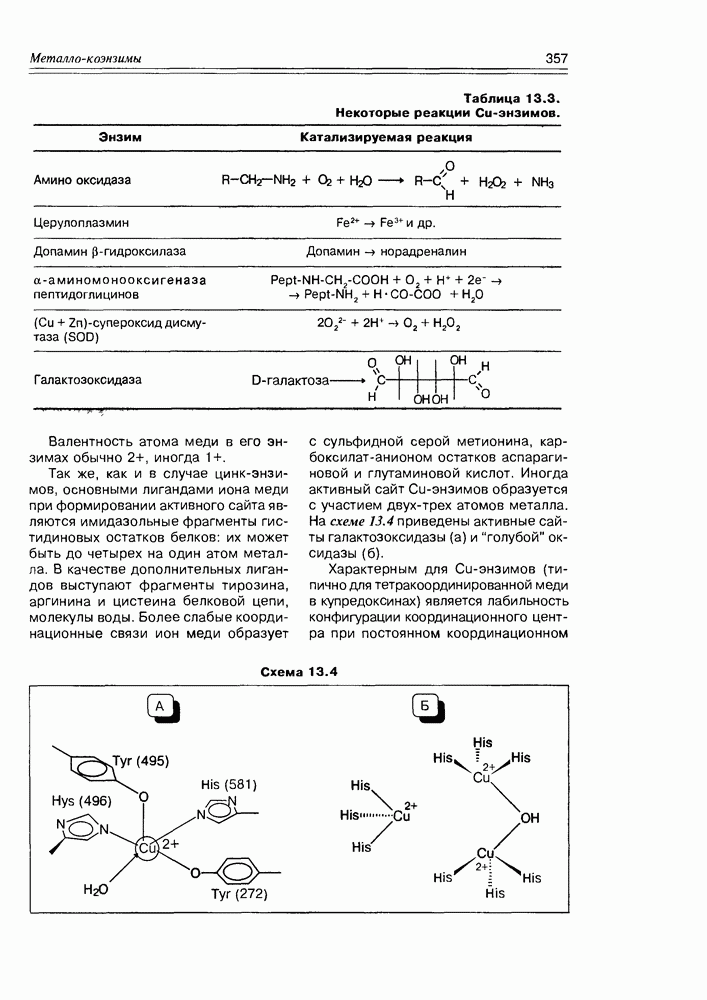
Таблица 13.3. Некоторые реакции Си-энзимов.

Валентность атома меди в его энзимах обычно  иногда
иногда 
Так же, как и в случае цинк-энзимов, основными лигандами иона меди при формировании активного сайта являются имидазольные фрагменты гистидиновых остатков белков: их может быть до четырех на один атом металла. В качестве дополнительных лигандов выступают фрагменты тирозина, аргинина и цистеина белковой цепи, молекулы воды. Более слабые координационные связи ион меди образует с сульфидной серой метионина, карбоксилат-анионом остатков аспарагиновой и глутаминовой кислот. Иногда активный сайт  -энзимов образуется с участием двух-трех атомов металла. На схеме 13.4 приведены активные сайты галактозоксидазы (а) и “голубой" оксидазы (б).
-энзимов образуется с участием двух-трех атомов металла. На схеме 13.4 приведены активные сайты галактозоксидазы (а) и “голубой" оксидазы (б).
Характерным для Cu-энзимов (типично для тетракоординированной меди в купредоксинах) является лабильность конфигурации координационного центра при постоянном координационном
Схема 13.4

Схема 13.5

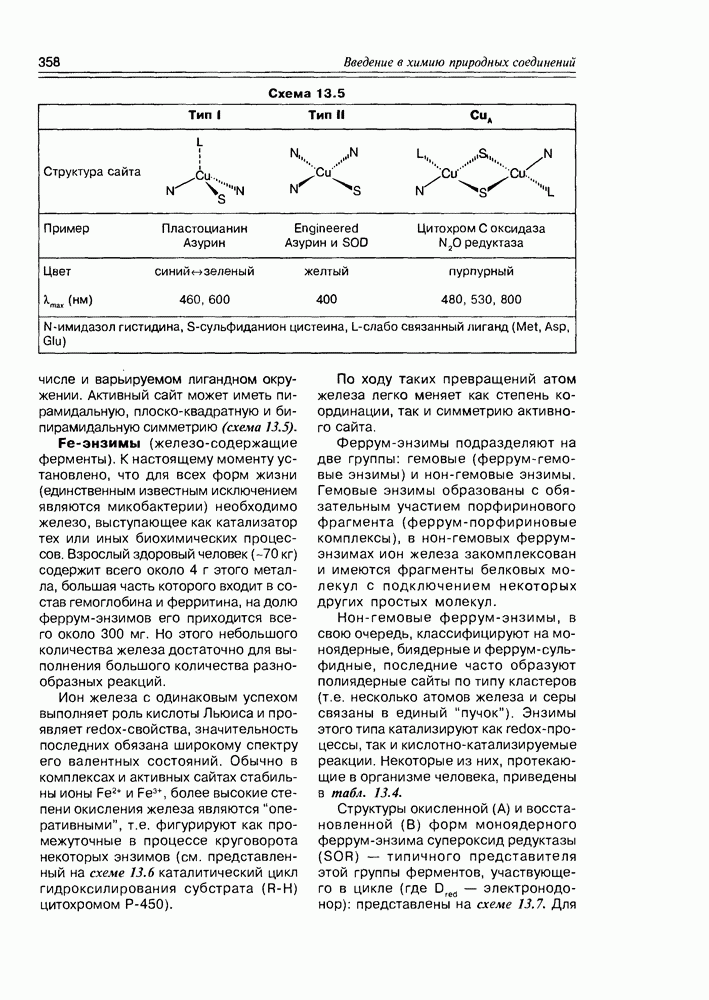
числе и варьируемом лигандном окружении. Активный сайт может иметь пирамидальную, плоско-квадратную и би-пирамидальную симметрию (схема 13.5).
Fe-энзимы (железо-содержащие ферменты). К настоящему моменту установлено, что для всех форм жизни (единственным известным исключением являются микобактерии) необходимо железо, выступающее как катализатор тех или иных биохимических процессов. Взрослый здоровый человек  кг) содержит всего около 4 г этого металла, большая часть которого входит в состав гемоглобина и ферритина, на долю феррум-энзимов его приходится всего около 300 мг. Но этого небольшого количества железа достаточно для выполнения большого количества разнообразных реакций.
кг) содержит всего около 4 г этого металла, большая часть которого входит в состав гемоглобина и ферритина, на долю феррум-энзимов его приходится всего около 300 мг. Но этого небольшого количества железа достаточно для выполнения большого количества разнообразных реакций.
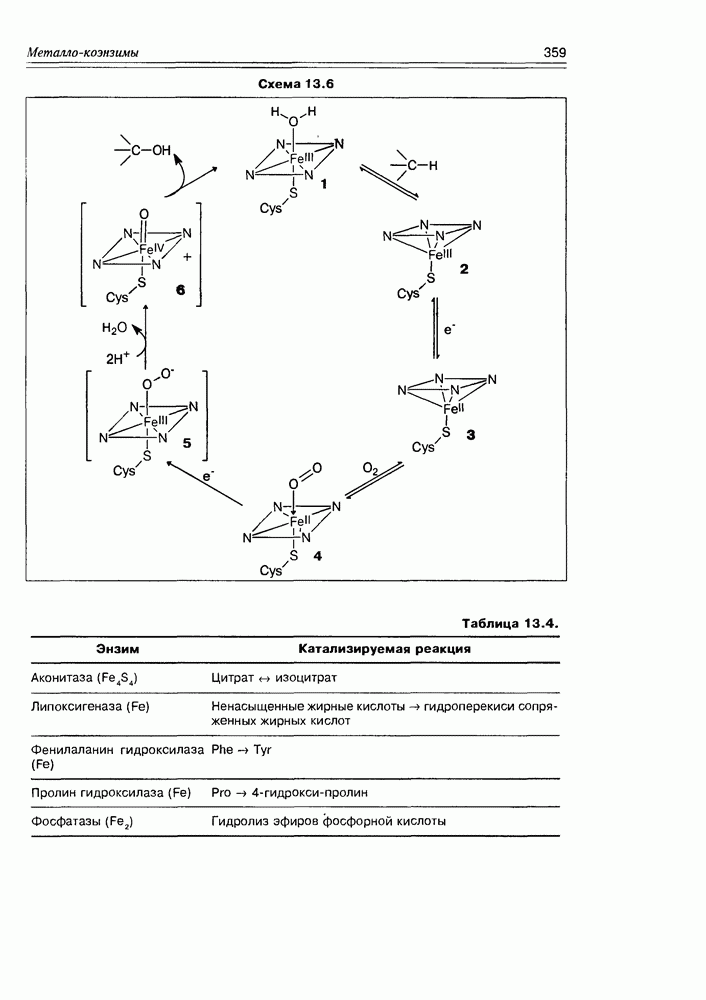
Ион железа с одинаковым успехом выполняет роль кислоты Льюиса и проявляет redox-свойства, значительность последних обязана широкому спектру его валентных состояний. Обычно в комплексах и активных сайтах стабильны ионы  более высокие степени окисления железа являются “оперативными", т.е. фигурируют как промежуточные в процессе круговорота некоторых энзимов (см. представленный на схеме 13.6 каталитический цикл гидроксилирования субстрата
более высокие степени окисления железа являются “оперативными", т.е. фигурируют как промежуточные в процессе круговорота некоторых энзимов (см. представленный на схеме 13.6 каталитический цикл гидроксилирования субстрата  ) цитохромом
) цитохромом 
По ходу таких превращений атом железа легко меняет как степень координации, так и симметрию активного сайта.
Феррум-энзимы подразделяют на две группы: гемовые (феррум-гемо-вые энзимы) и нон-гемовые энзимы. Гемовые энзимы образованы с обязательным участием порфиринового фрагмента (феррум-порфириновые комплексы), в нон-гемовых феррум-энзимах ион железа закомплексован и имеются фрагменты белковых молекул с подключением некоторых других простых молекул.
Нон-гемовые феррум-энзимы, в свою очередь, классифицируют на мо-ноядерные, биядерные и феррум-суль-фидные, последние часто образуют полиядерные сайты по типу кластеров (т.е. несколько атомов железа и серы связаны в единый “пучок”). Энзимы этого типа катализируют как redox-npoцессы, так и кислотно-катализируемые реакции. Некоторые из них, протекающие в организме человека, приведены в табл. 13.4.
Структуры окисленной (А) и восстановленной (В) форм моноядерного феррум-энзима супероксид редуктазы (SOR) — типичного представителя этой группы ферментов, участвующего в цикле (где Dred — электронодонор): представлены на схеме 13.7. Для
Схема 13.6
(см. скан)
Таблица 13.4.
(см. скан)

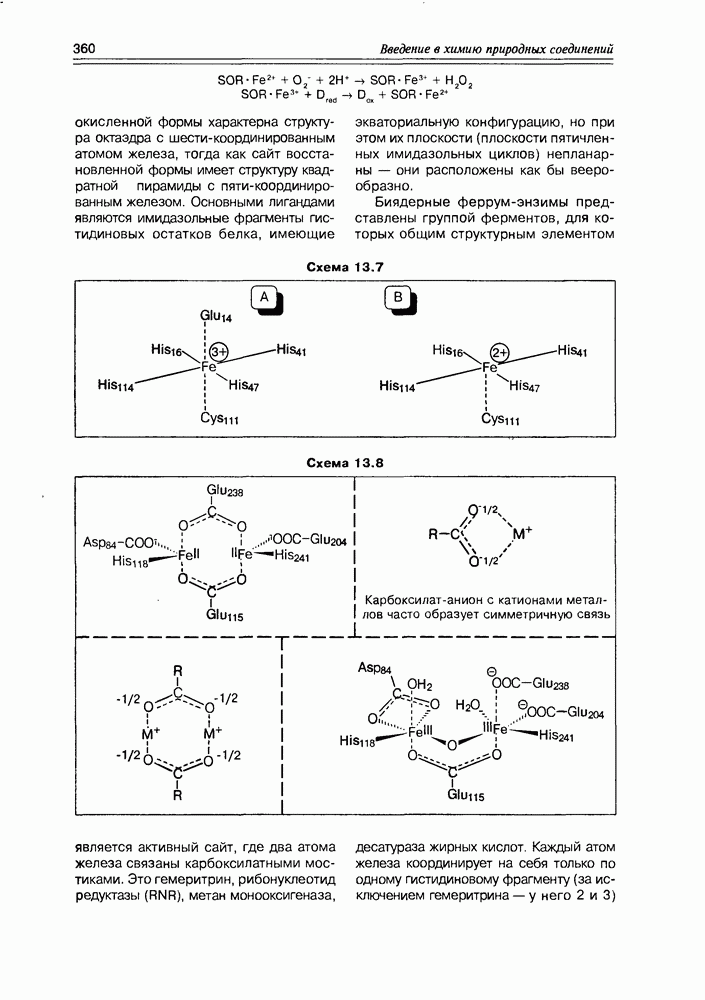
окисленной формы характерна структура октаэдра с шести-координированным атомом железа, тогда как сайт восстановленной формы имеет структуру квадратной пирамиды с пяти-координированным железом. Основными лигандами являются имидазольные фрагменты гистидиновых остатков белка, имеющие экваториальную конфигурацию, но при этом их плоскости (плоскости пятичленных имидазольных циклов) непланарны — они расположены как бы веерообразно.
Биядерные феррум-энзимы представлены группой ферментов, для которых общим структурным элементом является активный сайт, где два атома железа связаны карбоксилатными мостиками.
Схема 13.7

Схема 13.8

Это гемеритрин, рибонуклеотид редуктазы (RNR), метан монооксигеназа, десатураза жирных кислот. Каждый атом железа координирует на себя только по одному гистидиновому фрагменту (за исключением гемеритрина — у него 2 и 3)
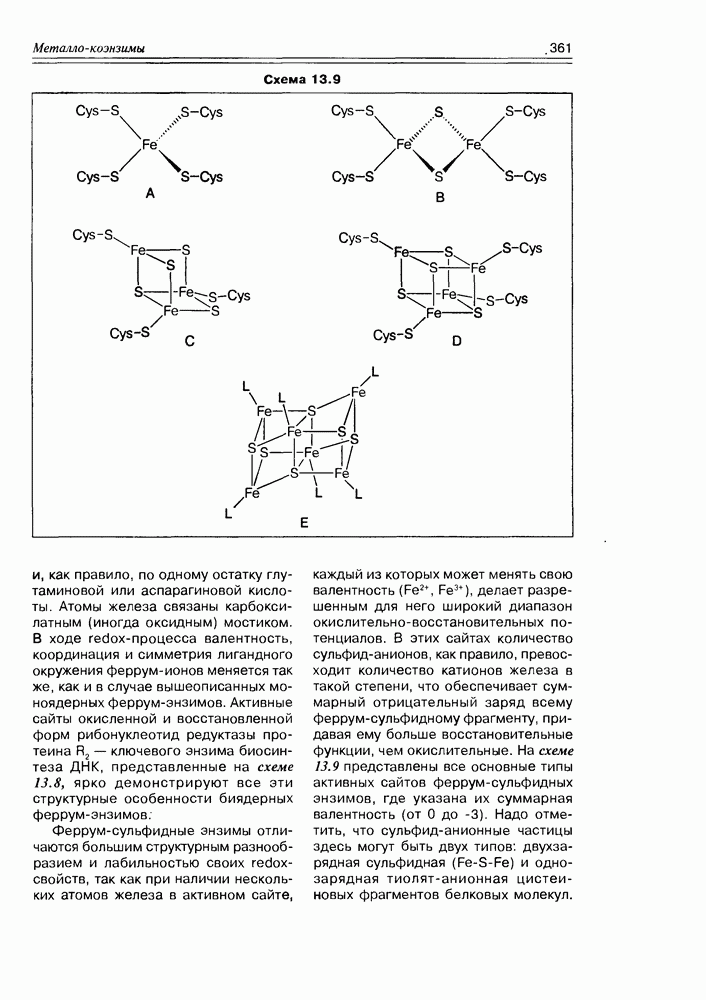
Схема 13.9

и, как правило, по одному остатку глутаминовой или аспарагиновой кислоты. Атомы железа связаны карбоксилатным (иногда оксидным) мостиком. В ходе redox-npouecca валентность, координация и симметрия лигандного окружения феррум-ионов меняется так же, как и в случае вышеописанных мо-ноядерных феррум-энзимов. Активные сайты окисленной и восстановленной форм рибонуклеотид редуктазы протеина  ключевого энзима биосинтеза ДНК, представленные на схеме 13.8, ярко демонстрируют все эти структурные особенности биядерных феррум-энзимов.
ключевого энзима биосинтеза ДНК, представленные на схеме 13.8, ярко демонстрируют все эти структурные особенности биядерных феррум-энзимов.
Феррум-сульфидные энзимы отличаются большим структурным разнообразием и лабильностью своих redox-свойств, так как при наличии нескольких атомов железа в активном сайте, каждый из которых может менять свою валентность  делает разрешенным для него широкий диапазон окислительно-восстановительных потенциалов. В этих сайтах количество сульфид-анионов, как правило, превосходит количество катионов железа в такой степени, что обеспечивает суммарный отрицательный заряд всему феррум-сульфидному фрагменту, придавая ему больше восстановительные функции, чем окислительные. На схеме 13.9 представлены все основные типы активных сайтов феррум-сульфидных энзимов, где указана их суммарная валентность (от 0 до -3). Надо отметить, что сульфид-анионные частицы здесь могут быть двух типов: двухзарядная сульфидная (Fe-S-Fe) и однозарядная тиолят-анионная цистеи-новых фрагментов белковых молекул.
делает разрешенным для него широкий диапазон окислительно-восстановительных потенциалов. В этих сайтах количество сульфид-анионов, как правило, превосходит количество катионов железа в такой степени, что обеспечивает суммарный отрицательный заряд всему феррум-сульфидному фрагменту, придавая ему больше восстановительные функции, чем окислительные. На схеме 13.9 представлены все основные типы активных сайтов феррум-сульфидных энзимов, где указана их суммарная валентность (от 0 до -3). Надо отметить, что сульфид-анионные частицы здесь могут быть двух типов: двухзарядная сульфидная (Fe-S-Fe) и однозарядная тиолят-анионная цистеи-новых фрагментов белковых молекул.
Таблица 13.5.

В принципе, от полипептидных цепей фермента на связывание фрагмента  могут быть использованы и другие электронодонорные функции сульфидная (Met), имидазольная (His), карбоксилат-анионная (Glu, Asp), фенолятанионная (Phe).
могут быть использованы и другие электронодонорные функции сульфидная (Met), имидазольная (His), карбоксилат-анионная (Glu, Asp), фенолятанионная (Phe).
Гем-энзимы играют буквально выдающуюся роль в химии живых организмов. В их функции входят: перенос электрона, транспорт  , активация
, активация  Последние две функции связаны с несколькими видами оксидоредуктаз: оксидаз, оксигеназ, пероксидаз и каталаз. Основные представители этого класса энзимов и реакции, ими катализируемые, представлены в табл. 13.5.
Последние две функции связаны с несколькими видами оксидоредуктаз: оксидаз, оксигеназ, пероксидаз и каталаз. Основные представители этого класса энзимов и реакции, ими катализируемые, представлены в табл. 13.5.
Одними из интересных и важных видов гемферрум-энзимов являются цитохромы  количество которых только в организме человека достигает 200. Их роль в метаболизме лекарств и стероидов (так же, как и в активации потенциальных канцерогенов конденсированной ароматической структуры) привели их к статусу самого интенсивно исследуемого семейства ферментов. Особенно привлекательны аспекты биохимии цитохромов
количество которых только в организме человека достигает 200. Их роль в метаболизме лекарств и стероидов (так же, как и в активации потенциальных канцерогенов конденсированной ароматической структуры) привели их к статусу самого интенсивно исследуемого семейства ферментов. Особенно привлекательны аспекты биохимии цитохромов  связанные с генной инженерией.
связанные с генной инженерией.
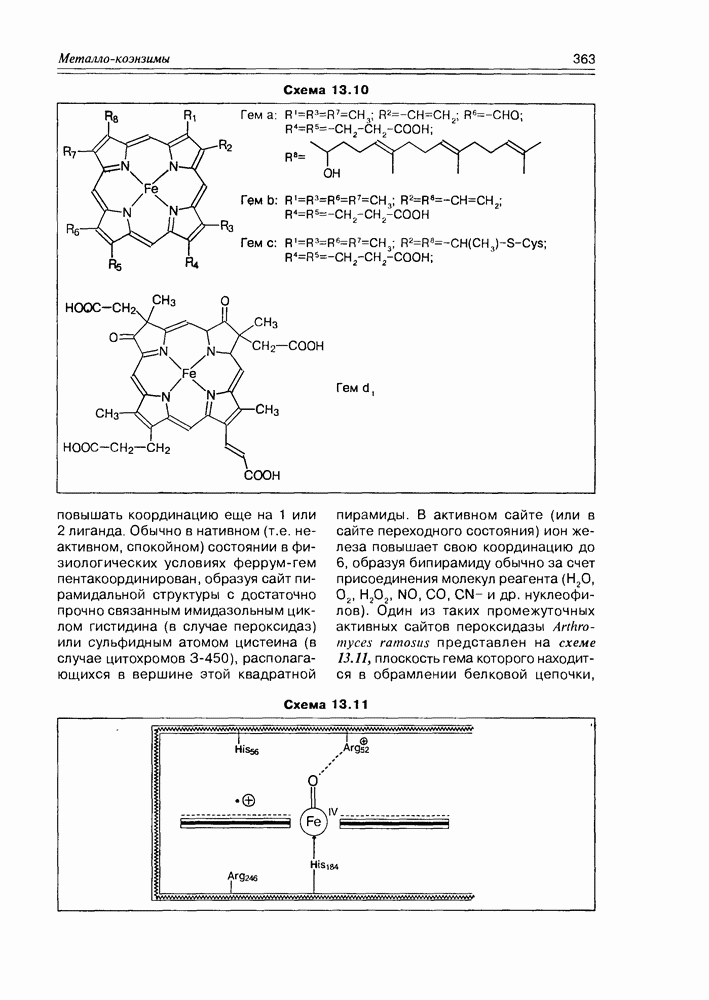
Структура гем-энзимов, в первую очередь, характеризуется наличием феррум-порфиринового комплекса, где атом железа включен внутрь порфиринового цикла, образуя единую планарную л-делокализованную систему (см. раздел 9.7). В зависимости от природы внешних заместителей порфиринового гетероцикла, выделяют четыре общих типа гемов (а, в, с,  ), которые в комбинации с серией белков и формируют все многообразие гем-феррум-энзимов (схема 13.10).
), которые в комбинации с серией белков и формируют все многообразие гем-феррум-энзимов (схема 13.10).
Тетракоординированный атом железа в порфириновом комплексе может
Схема 13.10

повышать координацию еще на 1 или 2 лиганда. Обычно в нативном (т.е. неактивном, спокойном) состоянии в физиологических условиях феррум-гем пентакоординирован, образуя сайт пирамидальной структуры с достаточно прочно связанным имидазольным циклом гистидина (в случае пероксидаз) или сульфидным атомом цистеина (в случае цитохромов 3-450), располагающихся в вершине этой квадратной пирамиды. В активном сайте (или в сайте переходного состояния) ион железа повышает свою координацию до 6, образуя бипирамиду обычно за счет присоединения молекул реагента ( и др. нуклеофилов). Один из таких промежуточных активных сайтов пероксидазы Arthromyces ramosus представлен на схеме 13.11, плоскость гема которого находится в обрамлении белковой цепочки,
и др. нуклеофилов). Один из таких промежуточных активных сайтов пероксидазы Arthromyces ramosus представлен на схеме 13.11, плоскость гема которого находится в обрамлении белковой цепочки,
Схема 13.11

удерживаемой феррум-имидазольной координационной  и водородной
и водородной  связями. Спектральными исследованиями этой пероксидазы установлено, что это соединение имеет оксигенировааный атом
связями. Спектральными исследованиями этой пероксидазы установлено, что это соединение имеет оксигенировааный атом  и катион-радикал (обозначено-
и катион-радикал (обозначено- ), делокализованный на протопорфириновом цикле.
), делокализованный на протопорфириновом цикле.
Металло-энзимы с участием других элементов  Со,
Со,  встречаются значительно реже, но для некоторых микроорганизмов и биохимических процессов часть из них является ключевыми.
встречаются значительно реже, но для некоторых микроорганизмов и биохимических процессов часть из них является ключевыми.
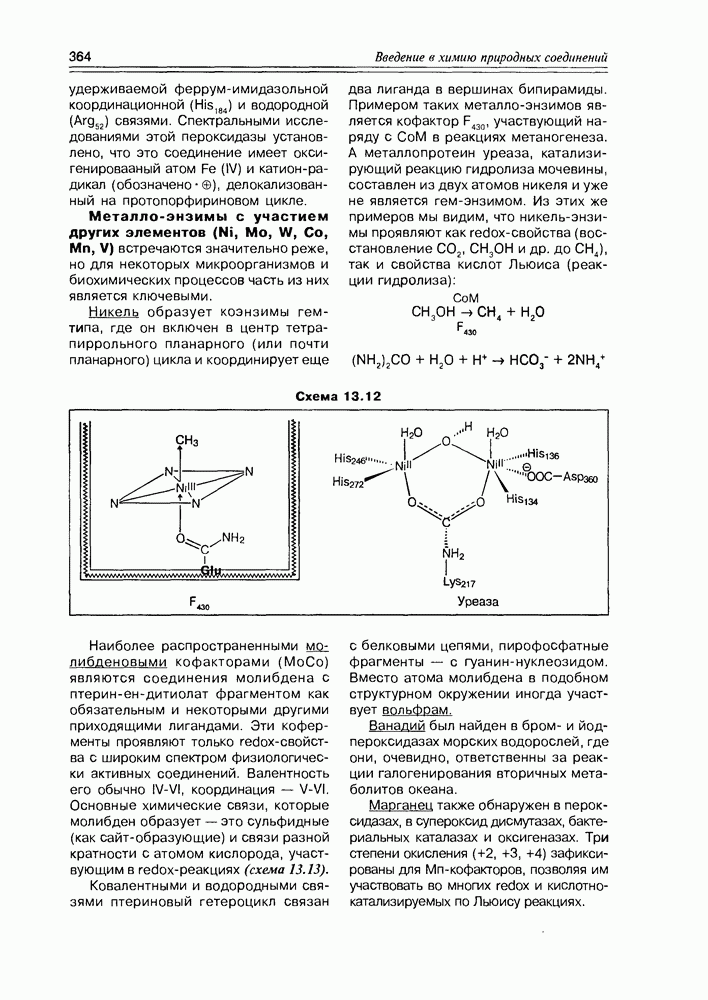
Никель образует коэнзимы гем-типа, где он включен в центр тетрапиррольного планарного (или почти планарного) цикла и координирует еще два лиганда в вершинах бипирамиды. Примером таких металло-энзимов является кофактор  участвующий наряду с СоМ в реакциях метаногенеза. А металлопротеин уреаза, катализирующий реакцию гидролиза мочевины, составлен из двух атомов никеля и уже не является гем-энзимом. Из этих же примеров мы видим, что никель-энзимы проявляют как redox-свойства (восстановление
участвующий наряду с СоМ в реакциях метаногенеза. А металлопротеин уреаза, катализирующий реакцию гидролиза мочевины, составлен из двух атомов никеля и уже не является гем-энзимом. Из этих же примеров мы видим, что никель-энзимы проявляют как redox-свойства (восстановление  и др. до
и др. до  ), так и свойства кислот Льюиса (реакции гидролиза):
), так и свойства кислот Льюиса (реакции гидролиза):

Схема 13.12

Наиболее распространенными молибденовыми кофакторами  являются соединения молибдена с птерин-ен-дитиолат фрагментом как обязательным и некоторыми другими приходящими лигандами. Эти коферменты проявляют только redox-свойства с широким спектром физиологически активных соединений. Валентность его обычно IV-VI, координация — V-VI. Основные химические связи, которые молибден образует — это сульфидные (как сайт-образующие) и связи разной кратности с атомом кислорода, участвующим в redox-реакциях (схема 13.13).
являются соединения молибдена с птерин-ен-дитиолат фрагментом как обязательным и некоторыми другими приходящими лигандами. Эти коферменты проявляют только redox-свойства с широким спектром физиологически активных соединений. Валентность его обычно IV-VI, координация — V-VI. Основные химические связи, которые молибден образует — это сульфидные (как сайт-образующие) и связи разной кратности с атомом кислорода, участвующим в redox-реакциях (схема 13.13).
Ковалентными и водородными связями птериновый гетероцикл связан с белковыми цепями, пирофосфатные фрагменты — с гуанин-нуклеозидом. Вместо атома молибдена в подобном структурном окружении иногда участвует вольфрам.
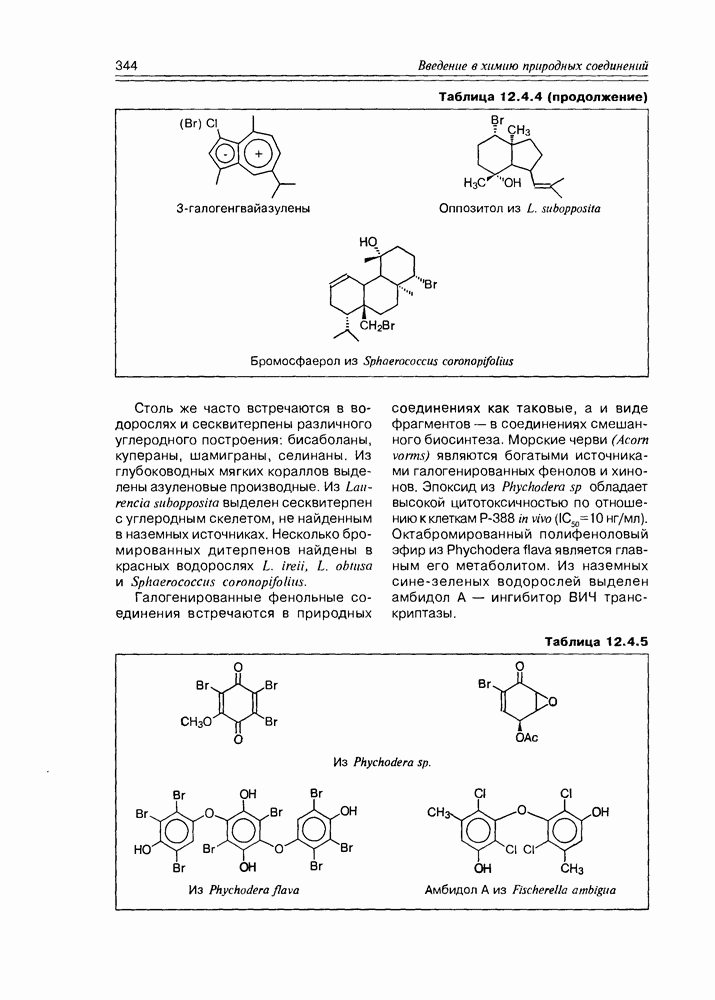
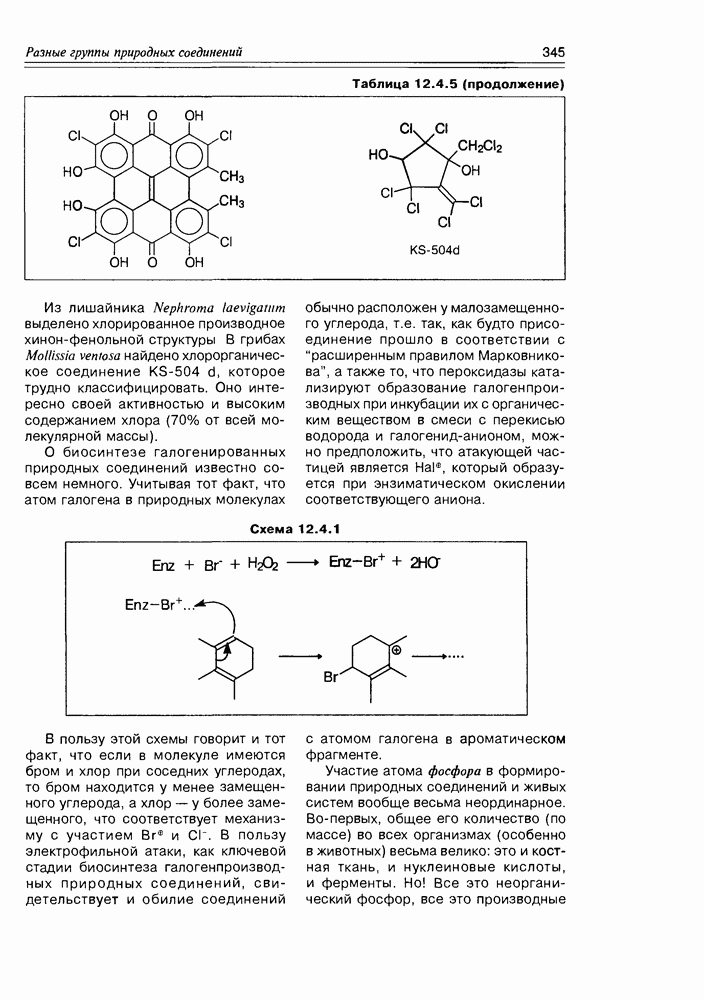
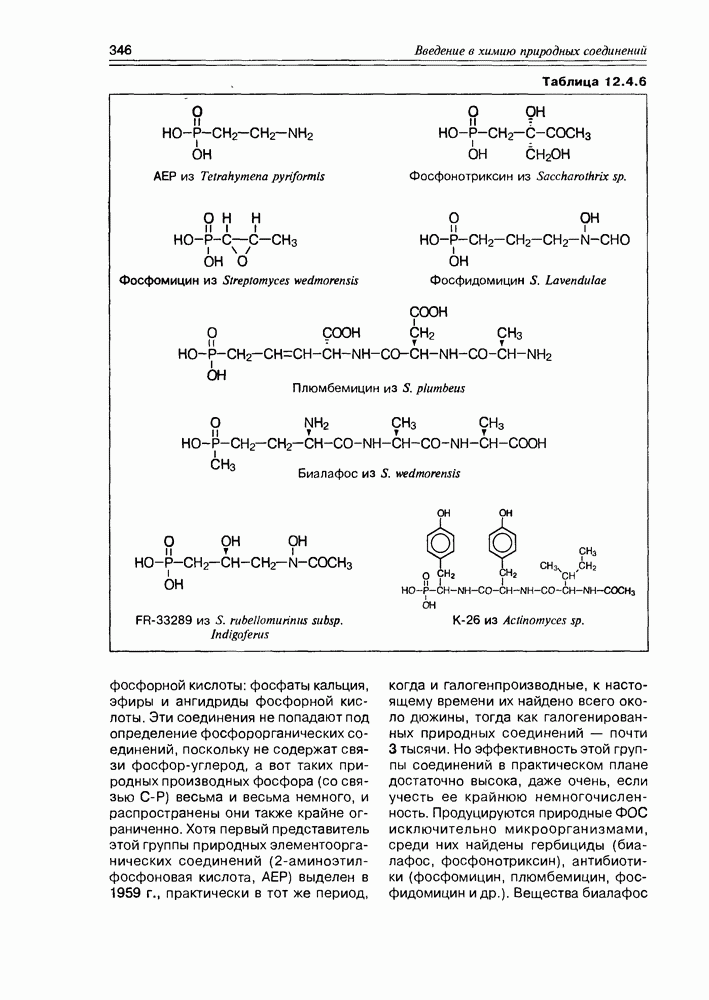
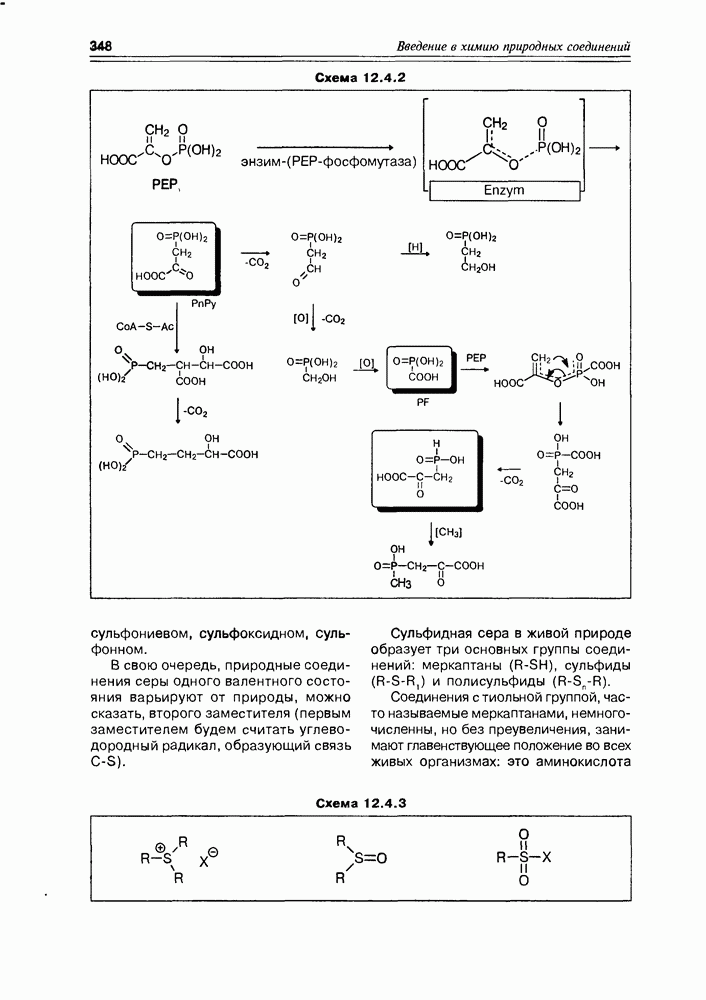
Ванадий был найден в бром- и йод-пероксидазах морских водорослей, где они, очевидно, ответственны за реакции галогенирования вторичных метаболитов океана.
Марганец также обнаружен в перок-сидазах, в супероксид дисмугазах, бактериальных каталазах и оксигеназах. Три степени окисления (+2, +3, +4) зафиксированы для  -кофакторов, позволяя им участвовать во многих redox и кислотно-катализируемых по Льюису реакциях.
-кофакторов, позволяя им участвовать во многих redox и кислотно-катализируемых по Льюису реакциях.
Схема 13.13

Гетеро-би(поли)-металло-энзимы - самая экзотическая группа металло-энзимов, а возможно, и энзимов вообще. Молекулы этих веществ, как правило, построены с участием атомов двух разных металлов, но при этом один из них может быть представлен в количестве, превышающим единицу Т.е. по содержанию металлов их можно подразделить как  . Разнообразие этих энзимов также обеспечивается сочетанием различных по природе металлов: обычно это
. Разнообразие этих энзимов также обеспечивается сочетанием различных по природе металлов: обычно это  При формировании биметаллических энзимов, ключевым элементом среди них является железо, которое участвует либо в виде одного атома, либо в виде целого кластера — обычно сульфидного. Поэтому мы можем теперь представить металлический состав основных типов этой группы энзимов более предметно: [Fe-Ni], [Fe-Cu], [Fen-Ni], [Fen-Mo],
При формировании биметаллических энзимов, ключевым элементом среди них является железо, которое участвует либо в виде одного атома, либо в виде целого кластера — обычно сульфидного. Поэтому мы можем теперь представить металлический состав основных типов этой группы энзимов более предметно: [Fe-Ni], [Fe-Cu], [Fen-Ni], [Fen-Mo],
Вполне очевидно, что энзимы, содержащие вышеуказанные сайты, должны обладать мощными redox-свойствами. Они участвуют в реакциях метаногенеза, гидрогенизации, азот-фиксации, оксидирования и др. В основном, такие энзимы найдены в различных бактериях.
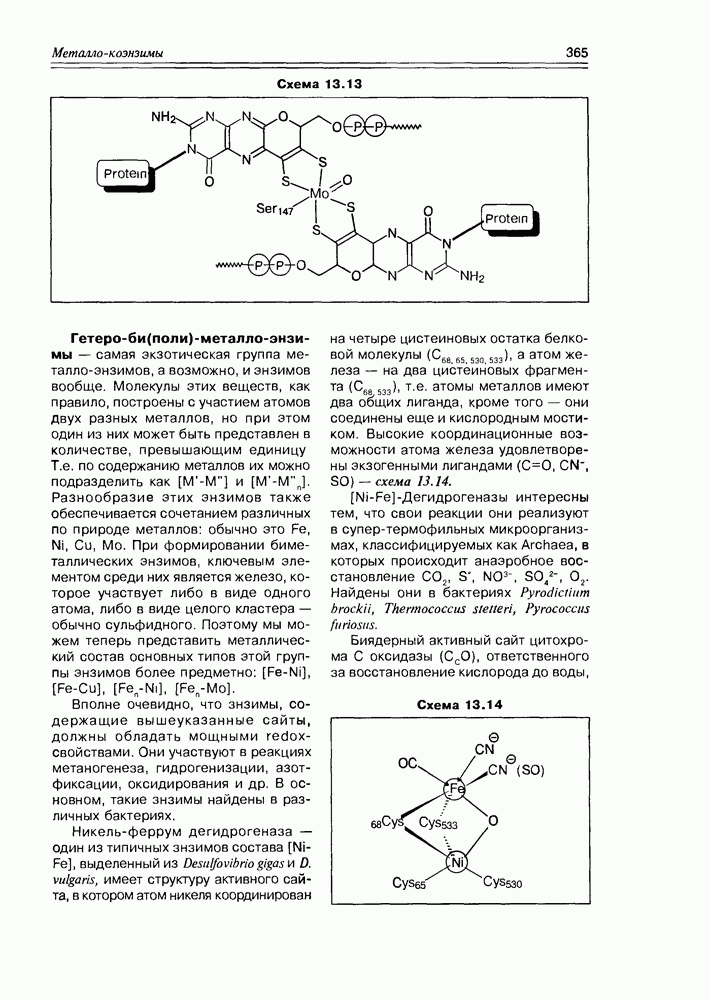
Никель-феррум дегидрогеназа — один из типичных энзимов состава [Ni-Fe], выделенный из Destilfovibrio gigas и D. vulgaris, имеет структуру активного сайта, в котором атом никеля координирован на четыре цистеиновых остатка белковой молекулы  , а атом железа — на два цистеиновых фрагмента
, а атом железа — на два цистеиновых фрагмента  , т.е. атомы металлов имеют два общих лиганда, кроме того — они соединены еще и кислородным мостиком. Высокие координационные возможности атома железа удовлетворены экзогенными лигандами
, т.е. атомы металлов имеют два общих лиганда, кроме того — они соединены еще и кислородным мостиком. Высокие координационные возможности атома железа удовлетворены экзогенными лигандами  схема 13.14.
схема 13.14.
 -Дегидрогеназы интересны тем, что свои реакции они реализуют в супер-термофильных микроорганизмах, классифицируемых как Archaea, в которых происходит анаэробное восстановление
-Дегидрогеназы интересны тем, что свои реакции они реализуют в супер-термофильных микроорганизмах, классифицируемых как Archaea, в которых происходит анаэробное восстановление  Найдены они в бактериях Pyrodictium brockii, Thermococcus stetteri, Pyrococcus furiostts.
Найдены они в бактериях Pyrodictium brockii, Thermococcus stetteri, Pyrococcus furiostts.
Биядерный активный сайт цитохрома С оксидазы  ответственного за восстановление кислорода до воды,
ответственного за восстановление кислорода до воды,
Схема 13.14

Схема 13.15

имеет металло-состав [Fe-Cu], где атом железа представлен ферро-гем фрагментом, атом меди координирован на три имидазольных фрагмента гистидиновых остатков белковой цепи. Оба атома металла связаны между собой перекисным мостиком.
Важным представителем коферментов [Fen-Mo] металло-состава является молибден-феррум кофактор нитро-геназы — фермент, ответственный за азот-фиксацию атмосферного азота.
Эти ферменты содержатся в азот-фикирующих бактериях рода Rhizobiitm, живущих симбиотрофно в корневых клетках растения-хозяина, в свободно живущих бактериях Klebsiellapneu-moniae и в фотосинтезирующих сине-зеленых водорослях. Они восстанавливают  до
до  Интересно, что ацетилен, электронное строение которого практически такое же, как и у азота, также легко восстанавливается этим ферментом.
Интересно, что ацетилен, электронное строение которого практически такое же, как и у азота, также легко восстанавливается этим ферментом.

Учитывая известную инертность молекулы азота в различных химических превращениях, в том числе и в реакциях гидрирования, можно оценить, насколько мощным восстановителем является феррум-молибденовый энзим. Структура его активного сайта представлена кластером, где один атом молибдена через три сульфидных мостика связан с тремя атомами железа. Последние, в свою очередь, связаны еще с “пучком” феррум-сульфидного содержания — весь этот кластер завязан на белковую цепь донорно-акцептор-ными взаимодействиями через имида-зольный (на молибден) и тиольный (на феррум) фрагменты.
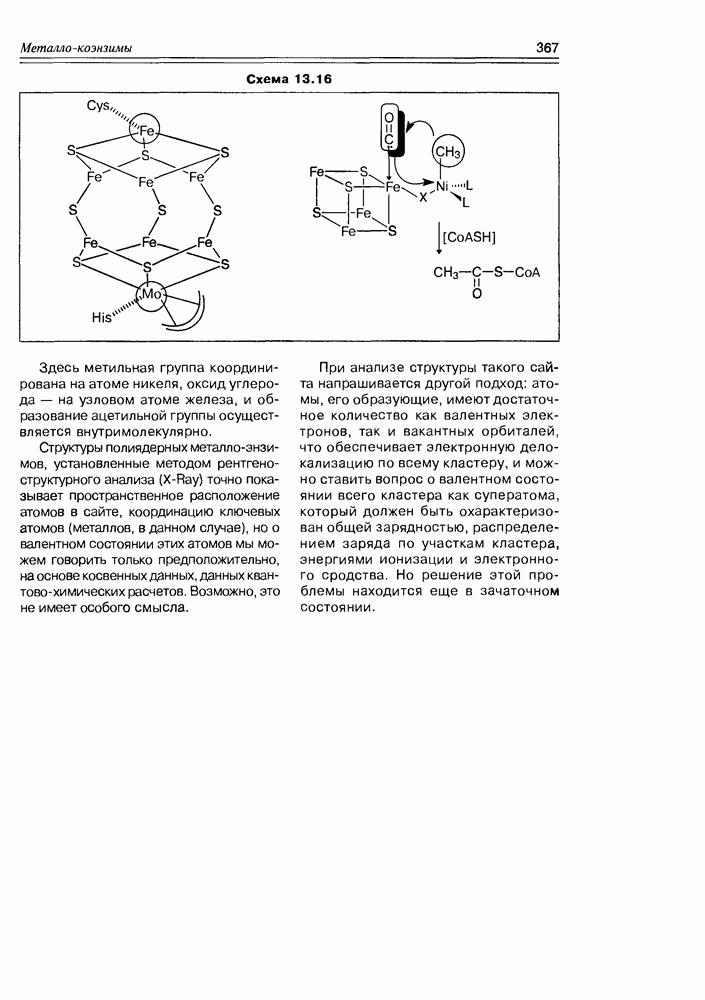
Похожую кластерную структуру активного сайта имеет металло-энзим карбон монооксид дегидрогеназы (CODH), образованный феррум-сульфидным “пучком" и атомом никеля. Феррум-сульфидный кластер состава  имеет кубическую упаковку, где все атомы железа (кроме одного — узлового) и серы трижды координированы. Узловой атом железа имеет координацию 5, он через атом X (О или S) связан со вторым металлом — никелем, который тетракоординирован. Этот энзим осуществляет конечную стадию образования ацетил-ScoA:
имеет кубическую упаковку, где все атомы железа (кроме одного — узлового) и серы трижды координированы. Узловой атом железа имеет координацию 5, он через атом X (О или S) связан со вторым металлом — никелем, который тетракоординирован. Этот энзим осуществляет конечную стадию образования ацетил-ScoA:

Схема 13.16

Здесь метильная группа координирована на атоме никеля, оксид углерода — на узловом атоме железа, и образование ацетильной группы осуществляется внутримолекулярно.
Структуры полиядерных металло-энзимов, установленные методом рентгеноструктурного анализа (X-Ray) точно показывает пространственное расположение атомов в сайте, координацию ключевых атомов (металлов, в данном случае), но о валентном состоянии этих атомов мы можем говорить только предположительно, на основе косвенных данных, данных квантово-химических расчетов. Возможно, это не имеет особого смысла.
При анализе структуры такого сайта напрашивается другой подход: атомы, его образующие, имеют достаточное количество как валентных электронов, так и вакантных орбиталей, что обеспечивает электронную делокализацию по всему кластеру, и можно ставить вопрос о валентном состоянии всего кластера как суператома, который должен быть охарактеризован общей зарядностью, распределением заряда по участкам кластера, энергиями ионизации и электронного сродства. Но решение этой проблемы находится еще в зачаточном состоянии.
| << Предыдущий параграф |
- ПРЕДИСЛОВИЕ АВТОРА
- Глава 1. ВВЕДЕНИЕ
- 1.1. Предмет химии природных соединений
- 1.2. Классификация природных соединений
- 1.3. Методология химии природных соединений
- 1.4. Углерод и жизнь
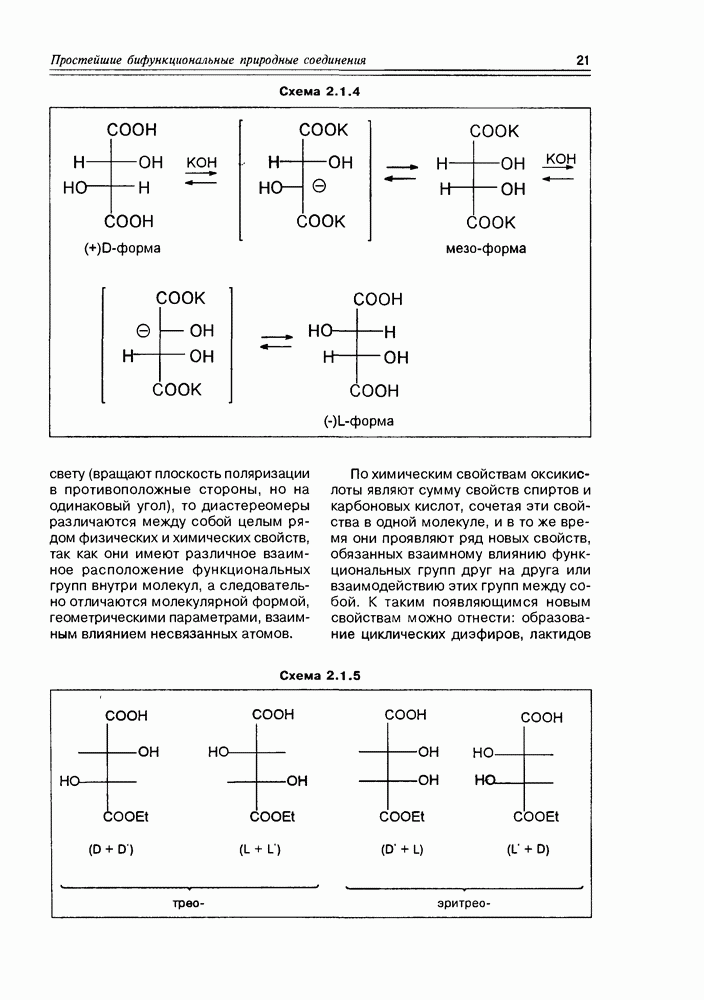
- Глава 2. ПРОСТЕЙШИЕ БИФУНКЦИОНАЛЬНЫЕ ПРИРОДНЫЕ СОЕДИНЕНИЯ — МОСТИК К МАССИВУ ПРИРОДНЫХ СОЕДИНЕНИЙ
- 2.2. Оксокислоты
- 2.3. Аминоспирты
- Глава 3. УГЛЕВОДЫ
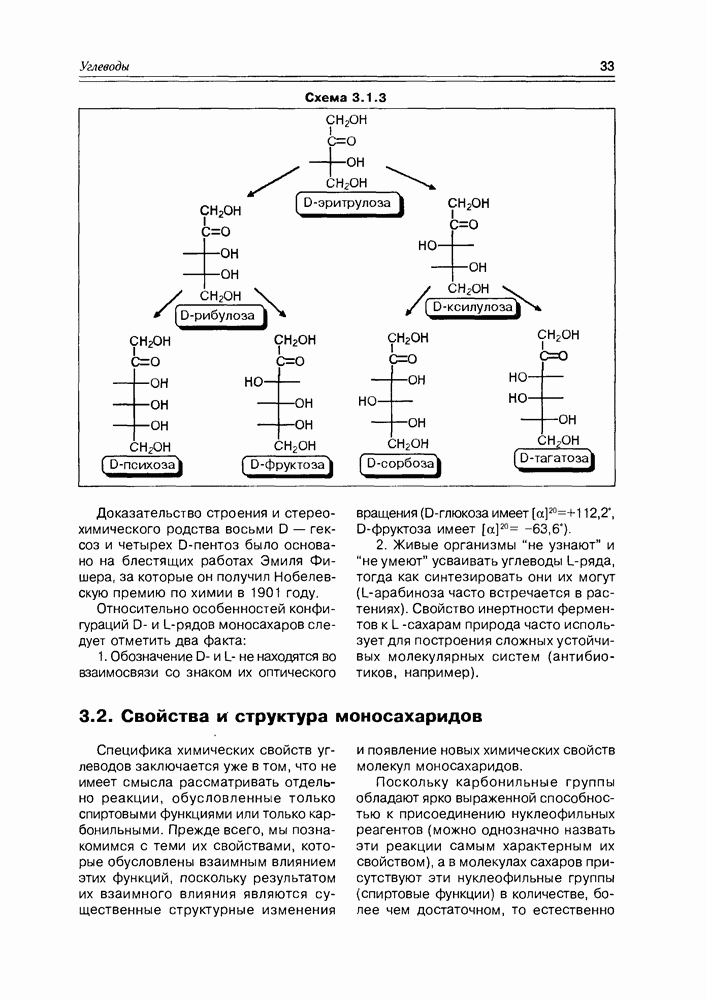
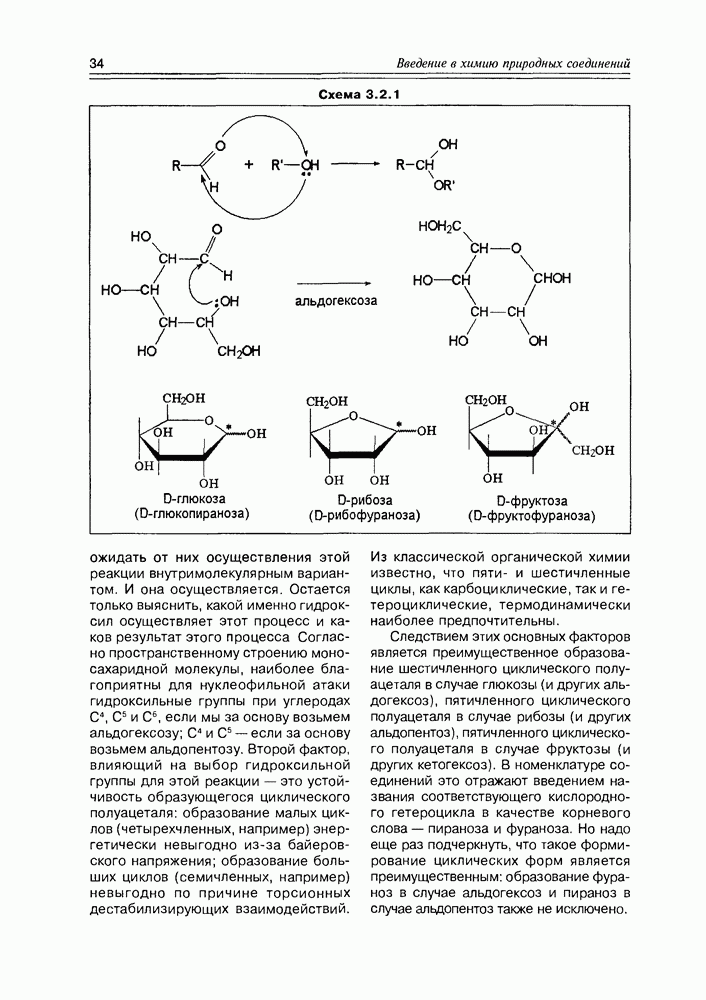
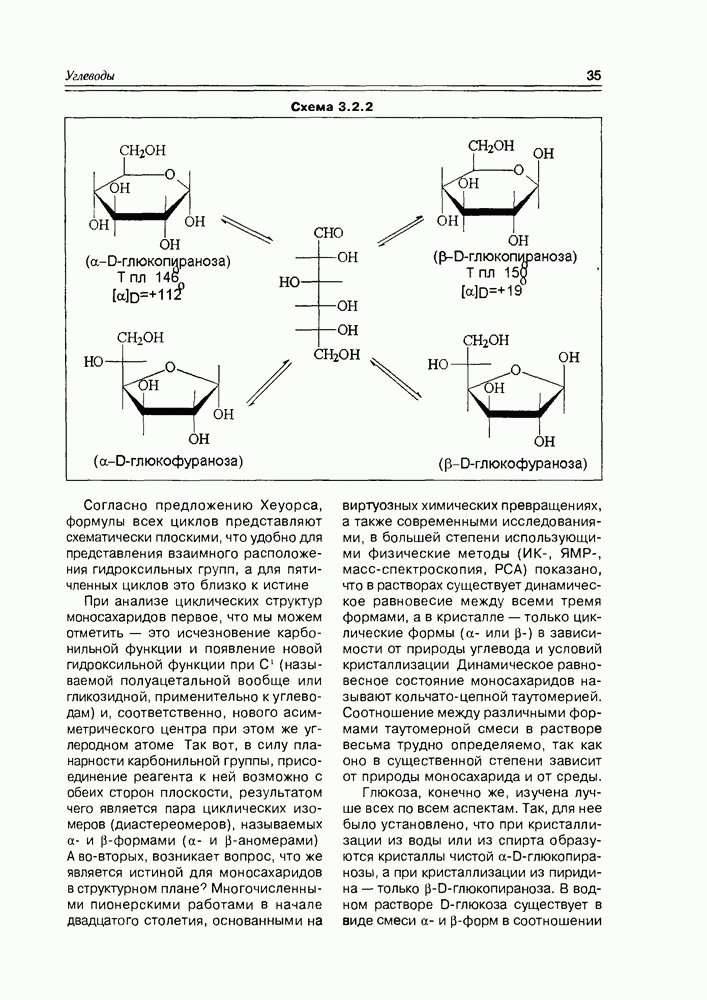
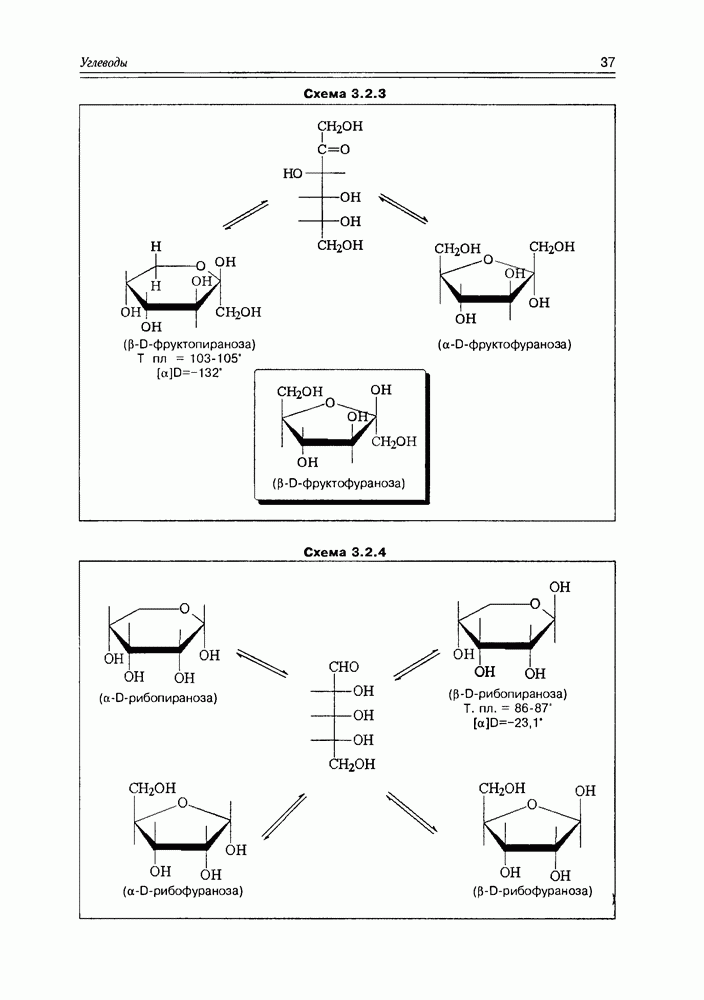
- 3.2. Свойства и структура моносахаридов
- 3.3. Химические свойства моносахаридов
- 3.4. Биосинтетические реакции углеводов
- 3.6. Гликозиды
- Глава 4. АМИНОКИСЛОТЫ, ПЕПТИДЫ, БЕЛКИ
- 4.2. Химические свойства а-аминокислот
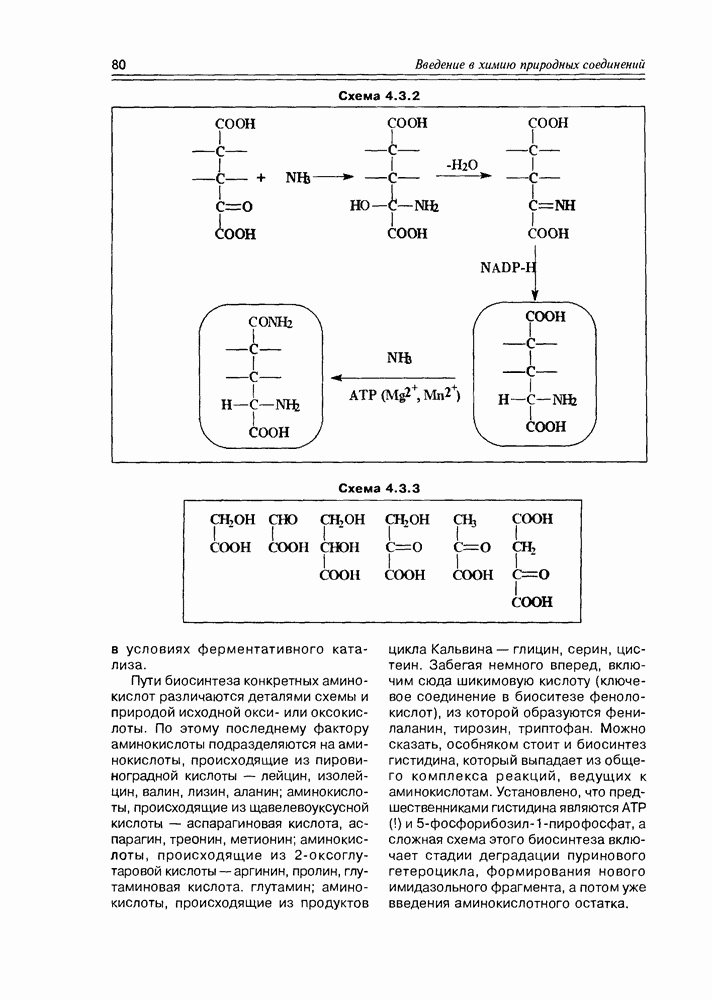
- 4.3. Биосинтез аминокислот
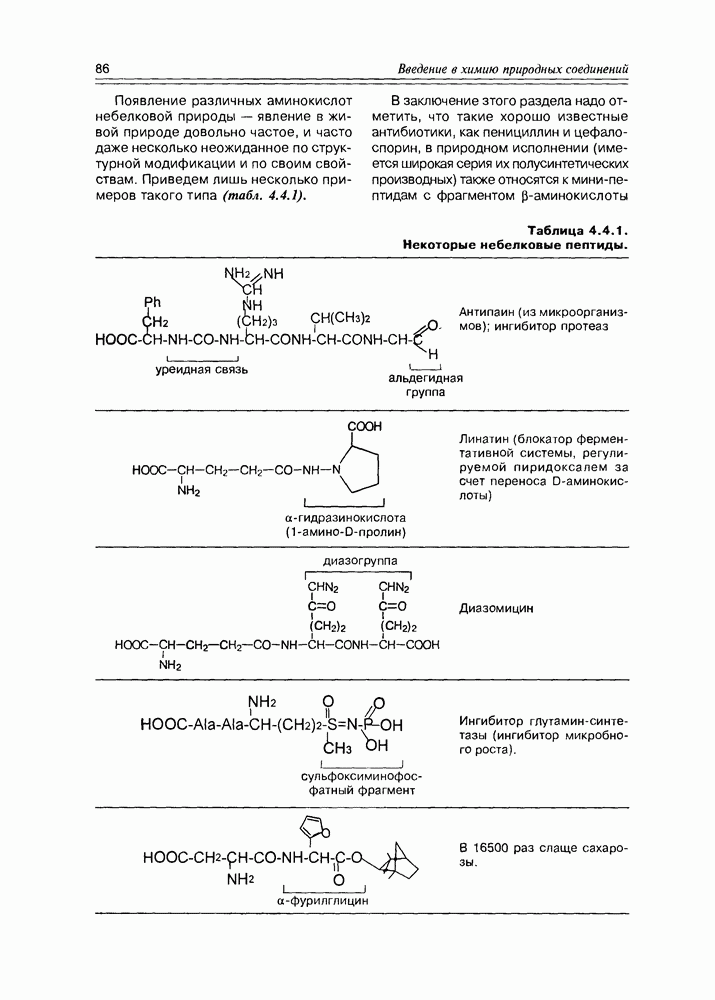
- 4.4. Полипептиды
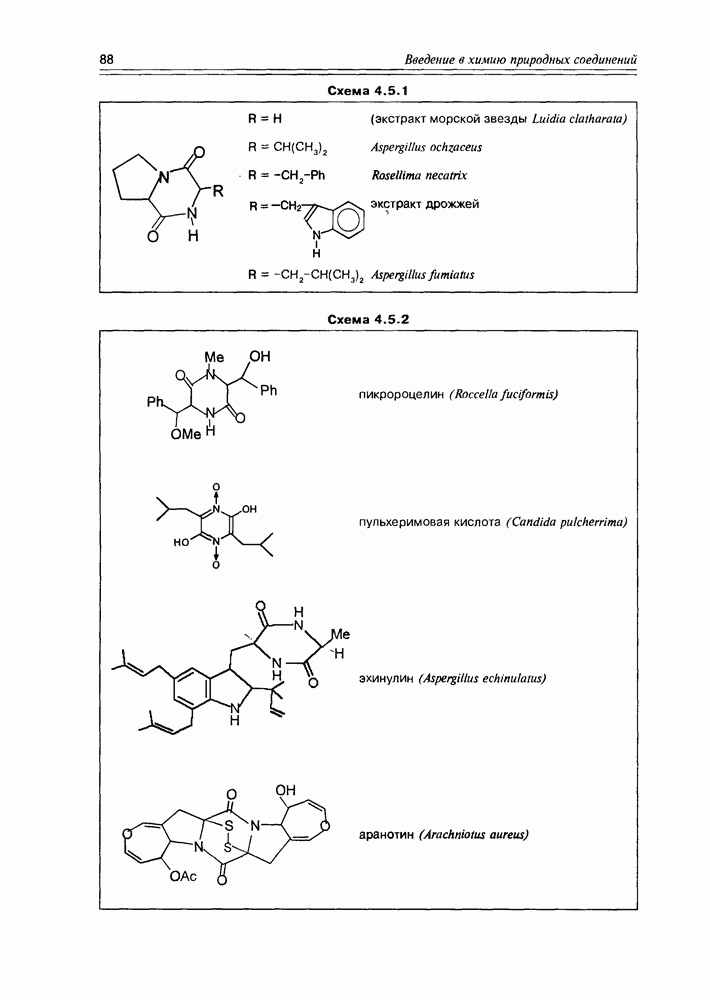
- 4.5. Дикетопиперазины
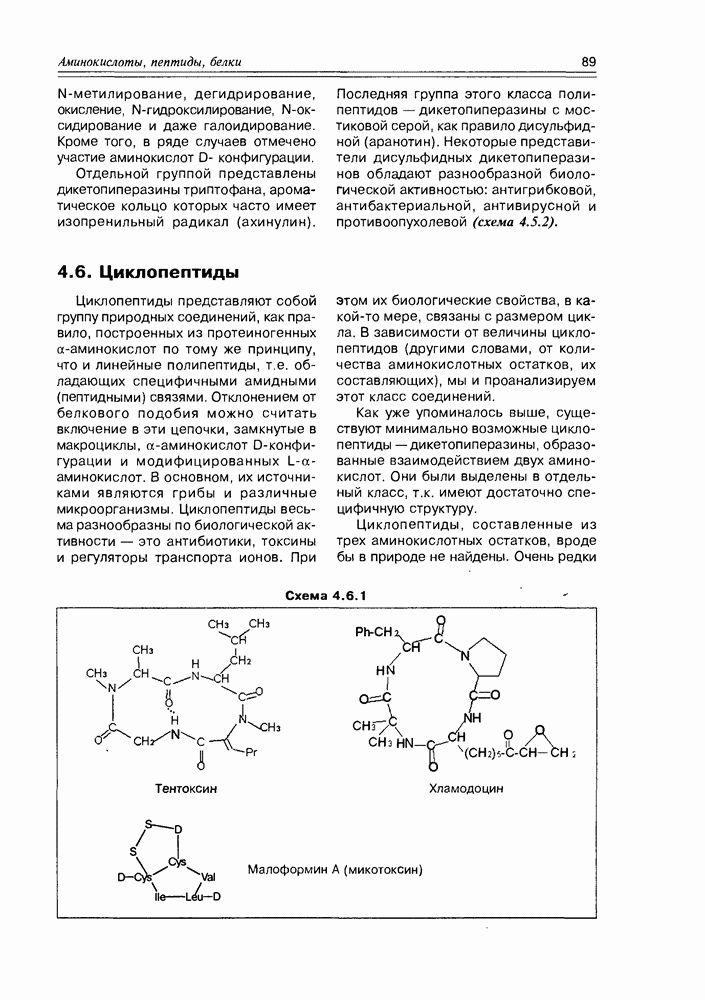
- 4.6. Циклопептиды
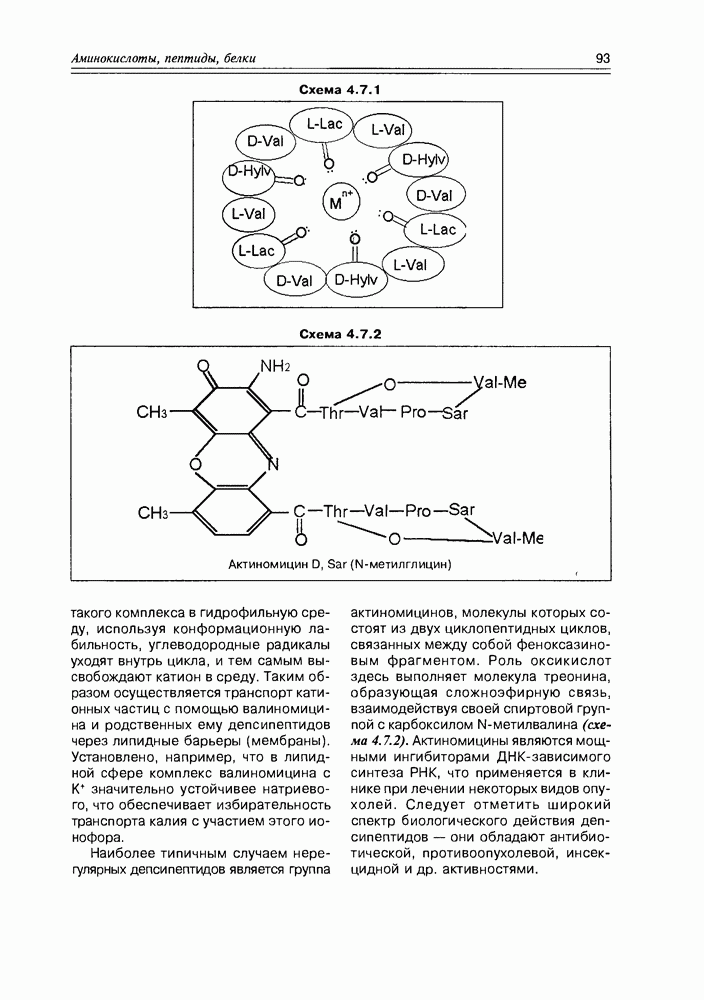
- 4.7. Депсипептиды
- 4.8. Белки
- Глава 5. ЛИПИДЫ: ЖИРНЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
- 5.1.1. Химические свойства жирных кислот
- 5.2. Метаболиты жирных кислот
- 5.2.2. Карбоциклические оксилипины
- 5.3. Жиры и жироподобные производные жирных кислот
- 5.4. Биосинтез жирных кислот и их производных
- Глава 6. ИЗОПРЕНОИДЫ-1
- 6.2. Гемитерпены
- 6.3. Монотерпены
- 6.4. Ациклические монотерпены
- 6.5. Моноциклические терпены
- 6.6. Бициклические монотерпены
- 6.7. Строение и свойства монотерпенов
- 6.8. Биосинтез изопреноидов
- Глава 7. ИЗОПРЕНОИДЫ II. ОТ СЕСКВИТЕРПЕНОВ ДО ПОЛИТЕРПЕНОВ
- 7.2. Химические свойства сесквитерпенов
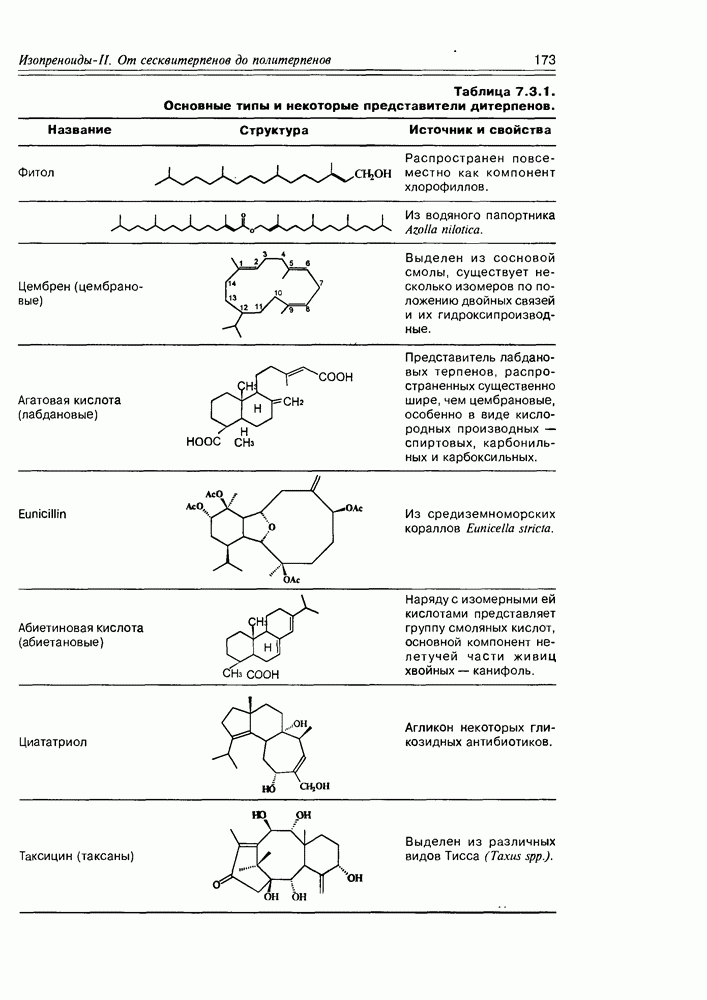
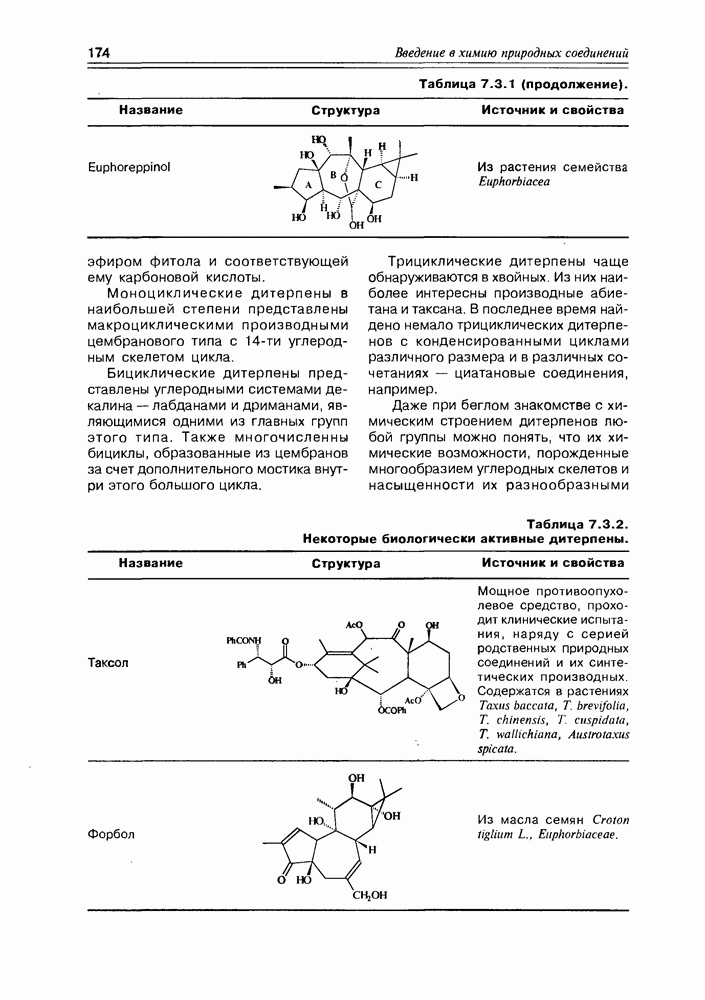
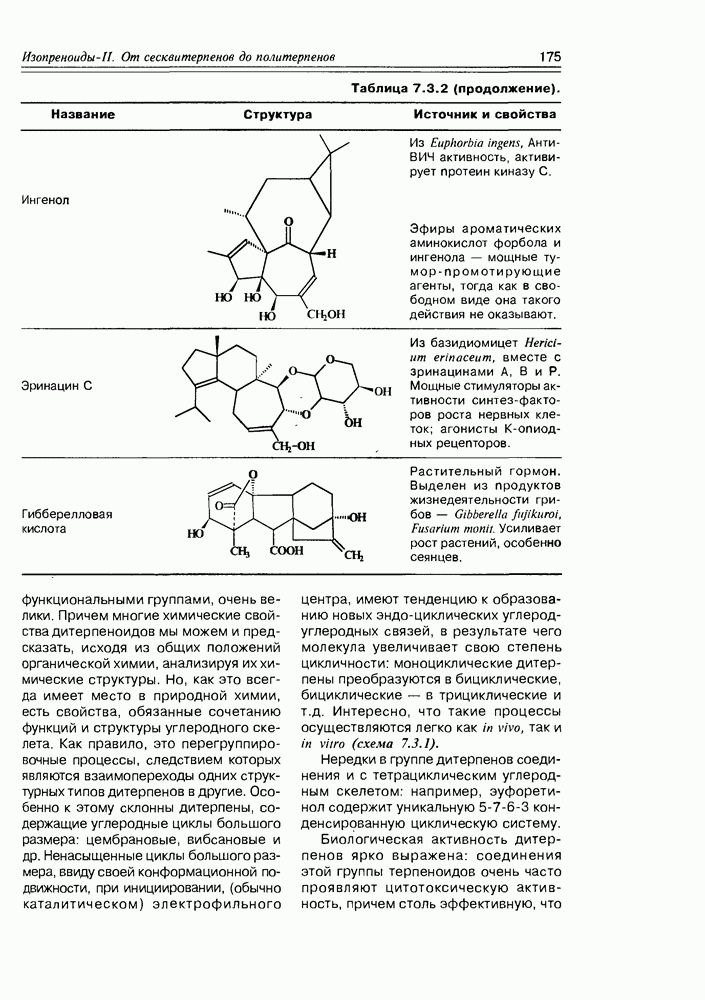
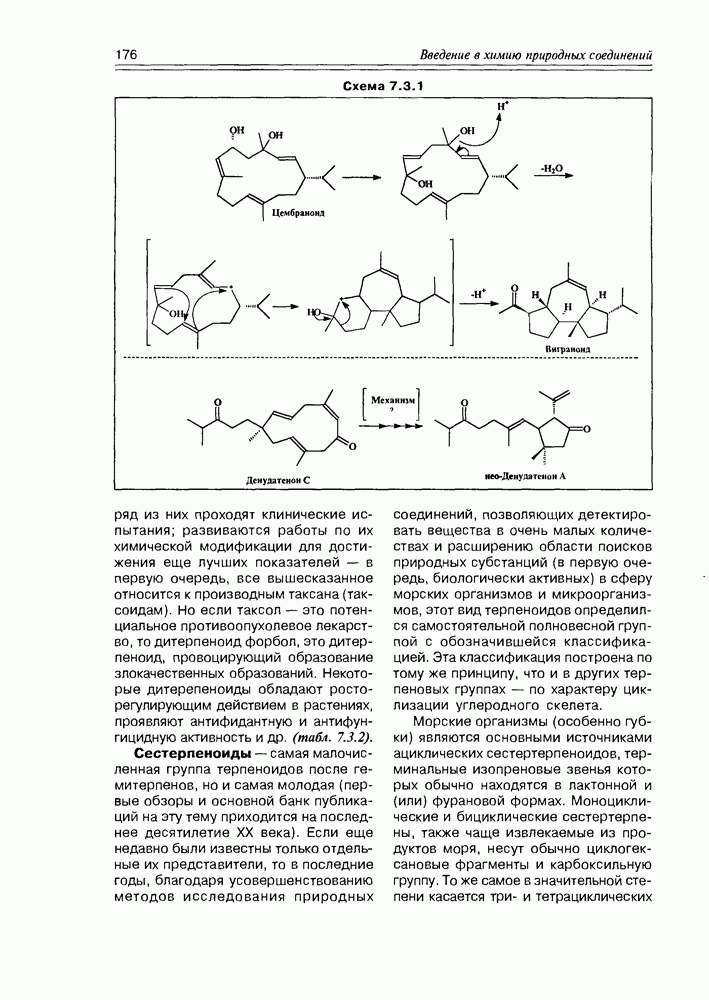
- 7.3. Дитерпены и сестертерпены
- 7.4. Тритерпеноиды и стероиды
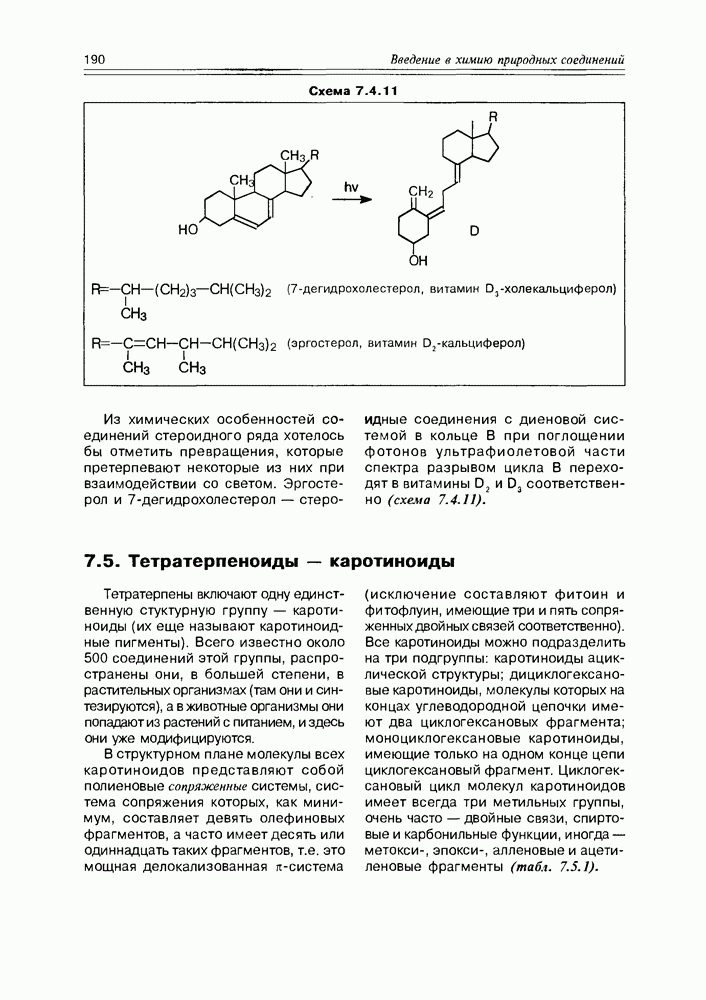
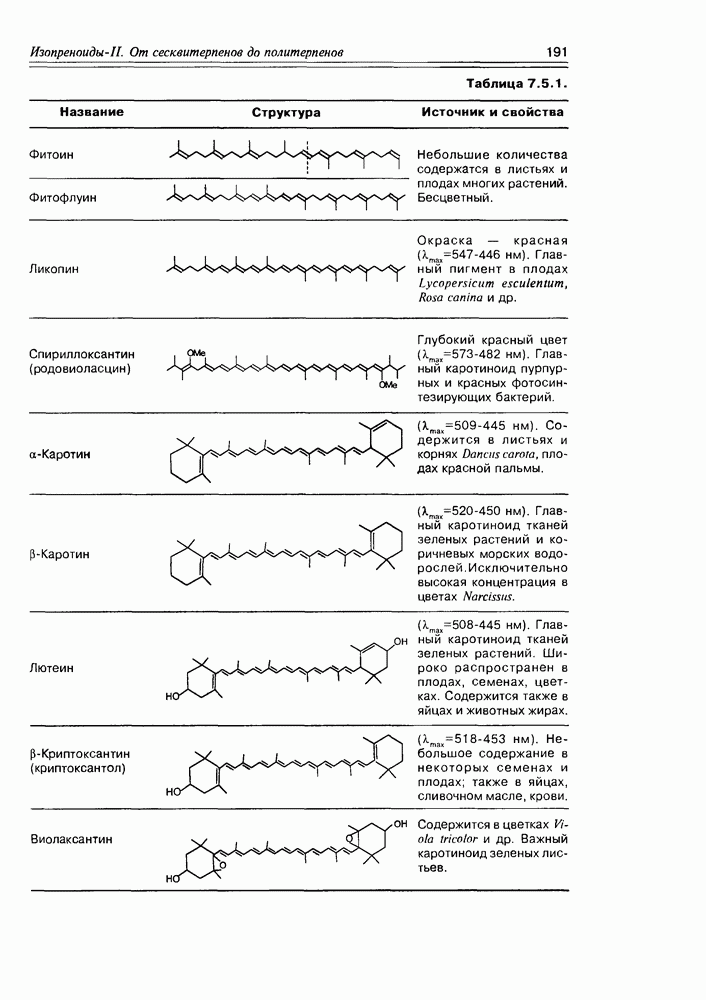
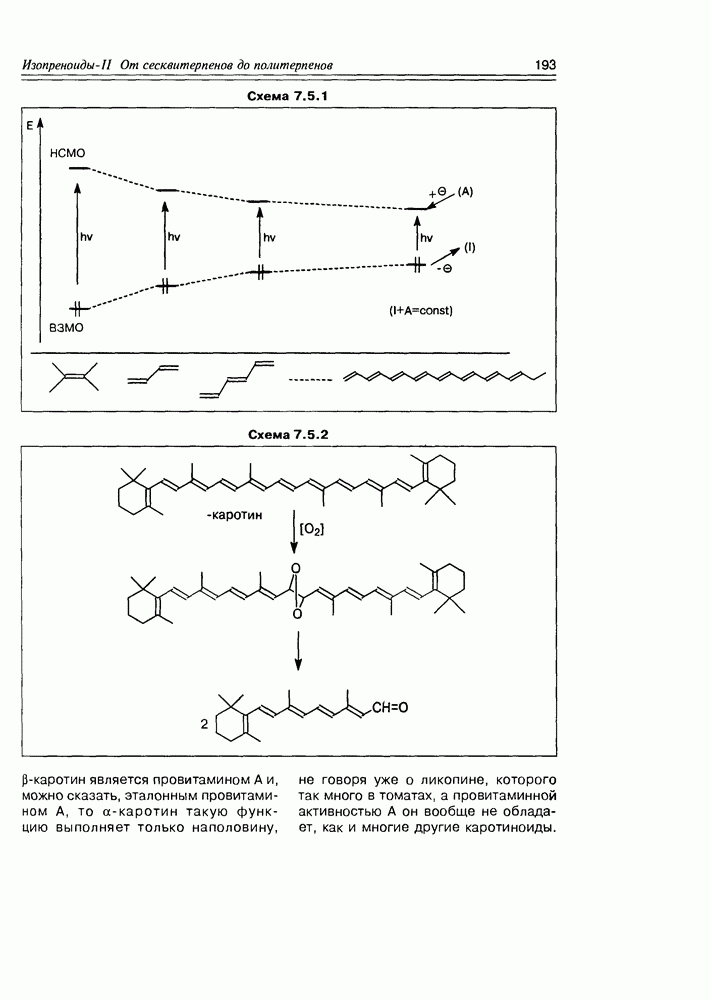
- 7.5. Тетратерпеноиды — каротиноиды
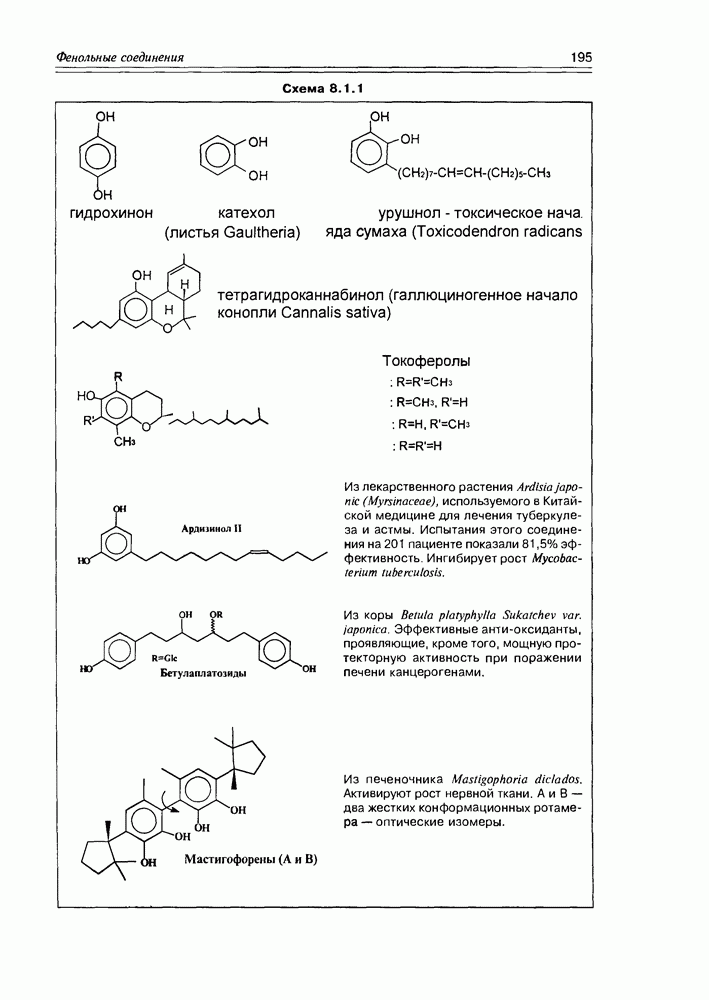
- Глава 8. ФЕНОЛЬНЫЕ СОЕДИНЕНИЯ
- 8.2. Пираны
- 8.4. Биосинтез фенольных соединений
- Глава 9. АЛКАЛОИДЫ И ПОРФИРИНЫ
- 9.2. Истинные алкалоиды
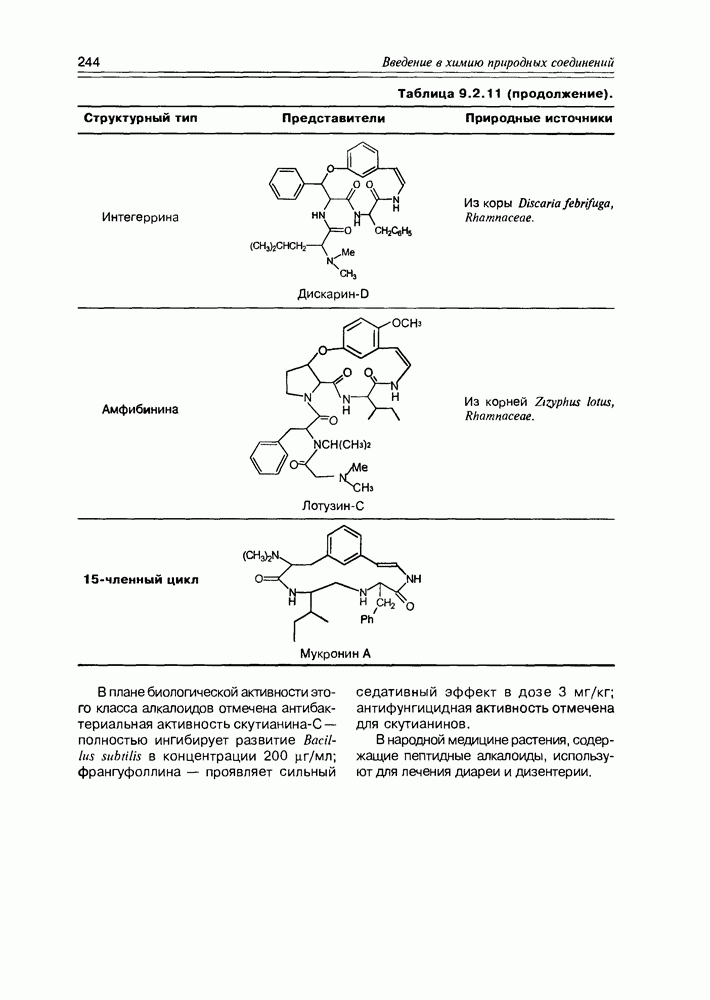
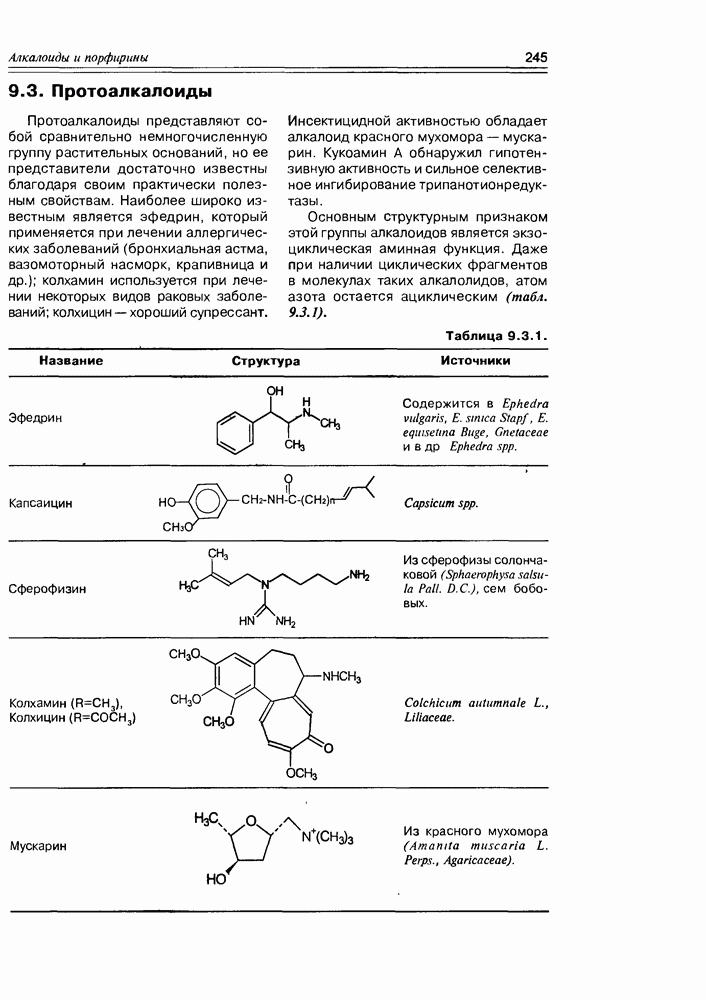
- 9.3. Протоалкалоиды
- 9.5. Химические свойства и химические модификации алкалоидов
- 9.6. Аминокислоты и биосинтез алкалоидов
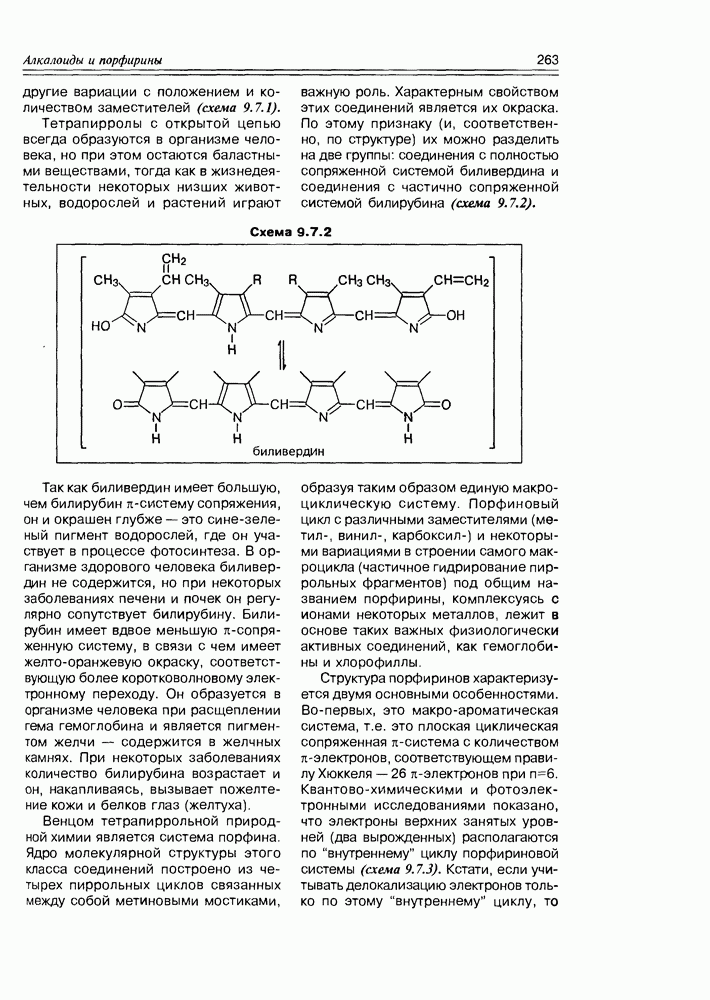
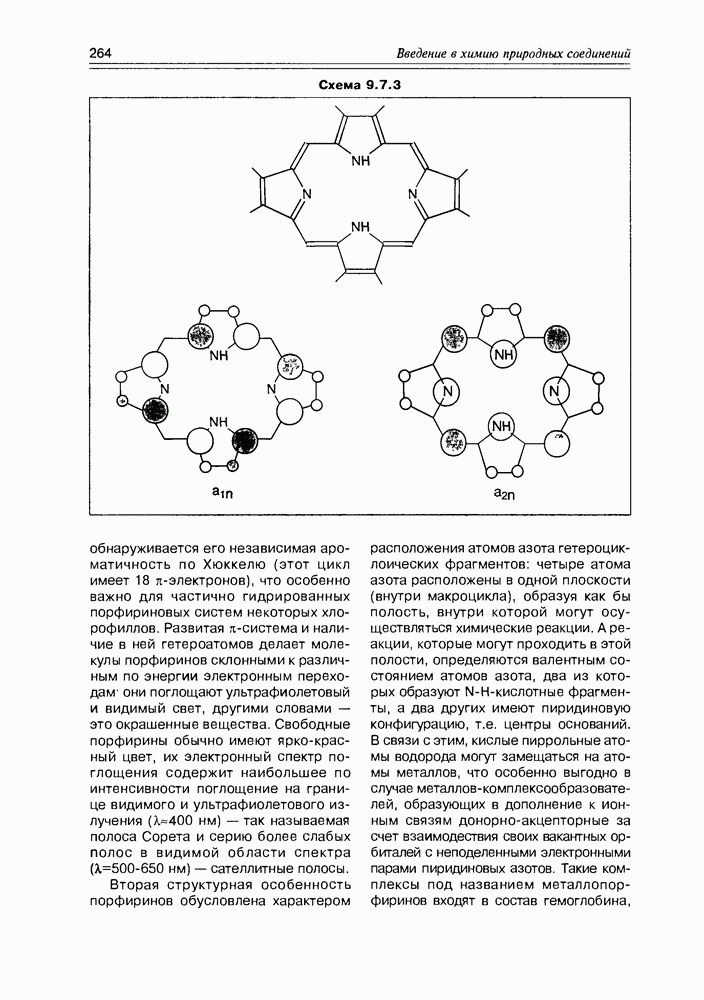
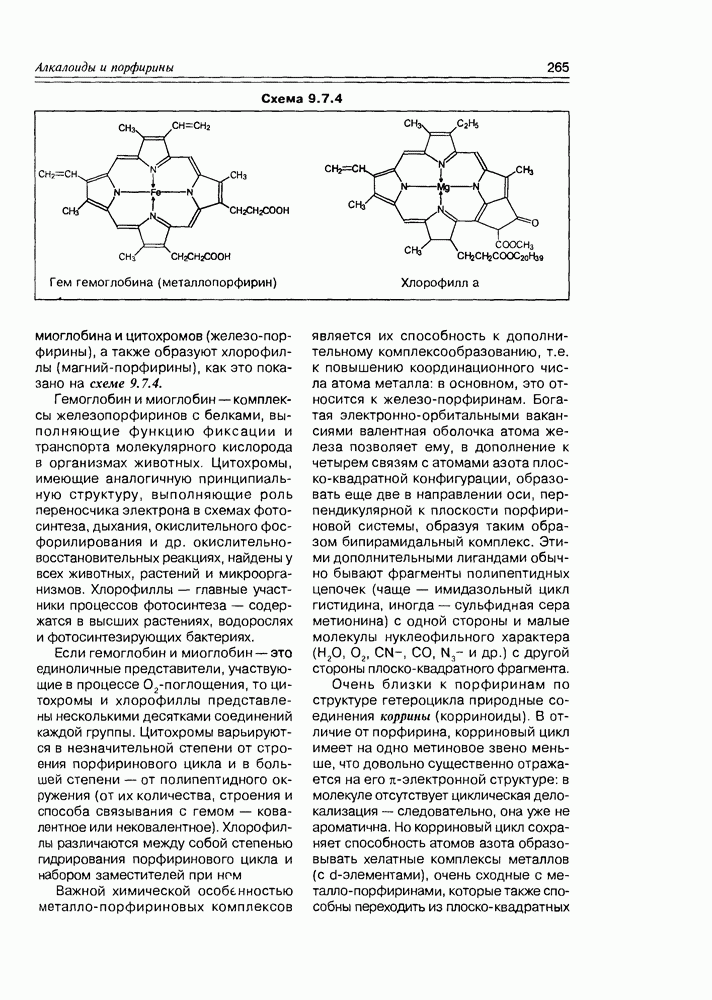
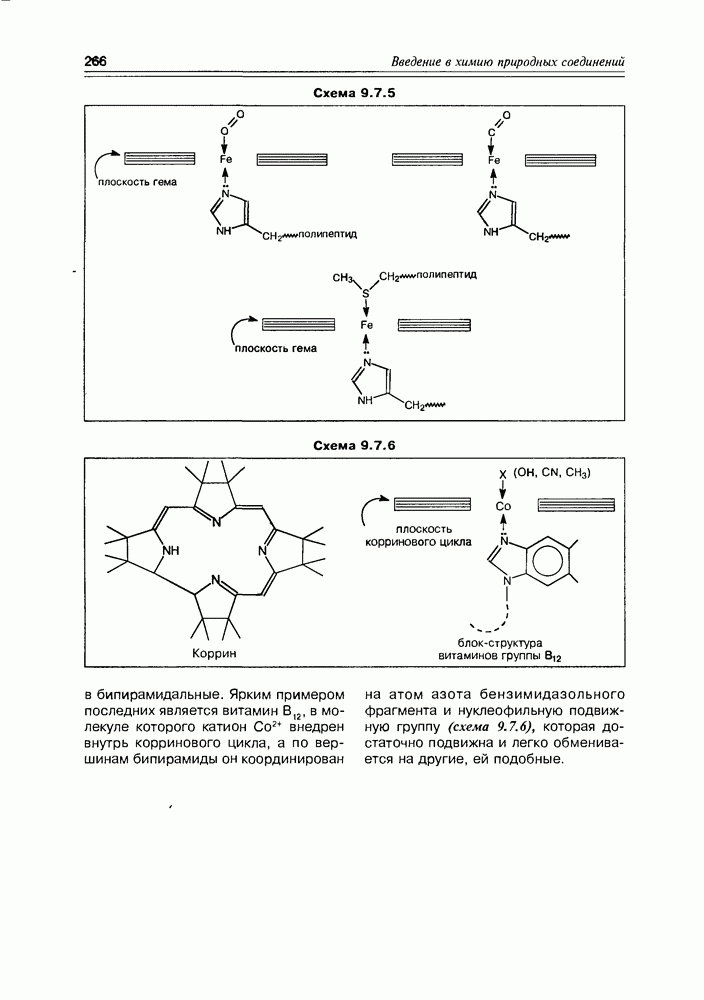
- 9.7. Порфирины
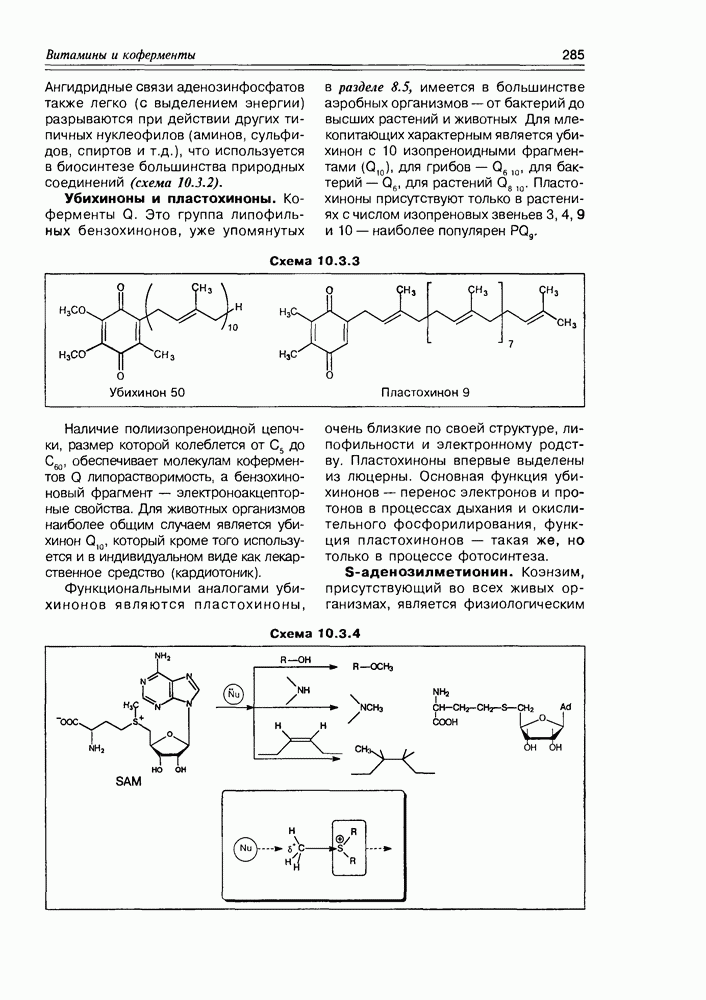
- Глава 10. ВИТАМИНЫ И КОФЕРМЕНТЫ
- 10.1. Витамины — собственно
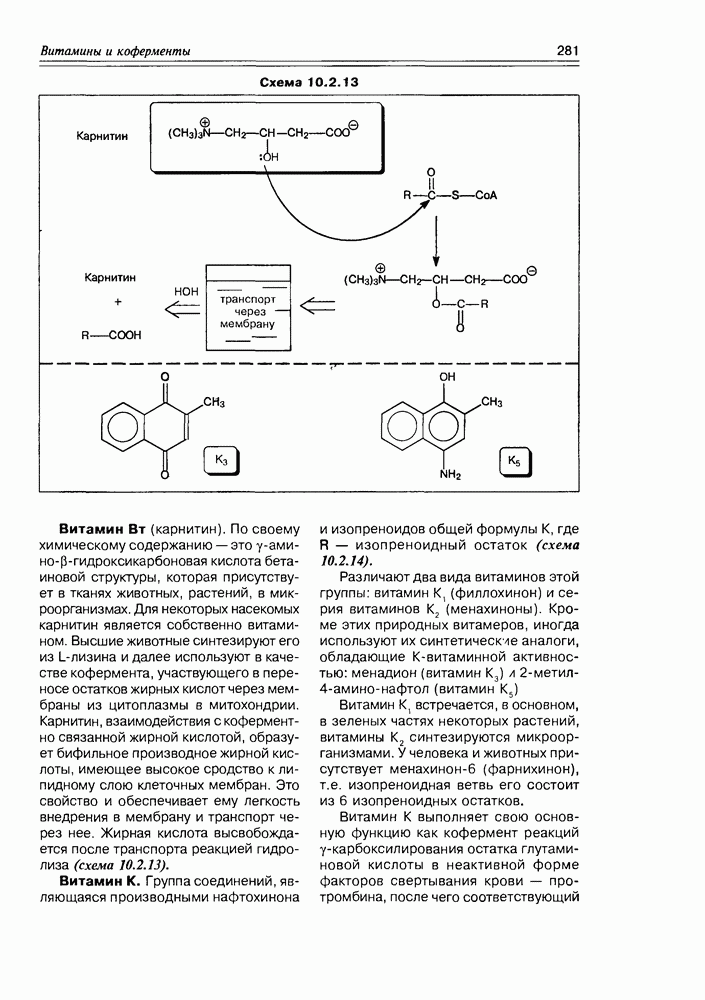
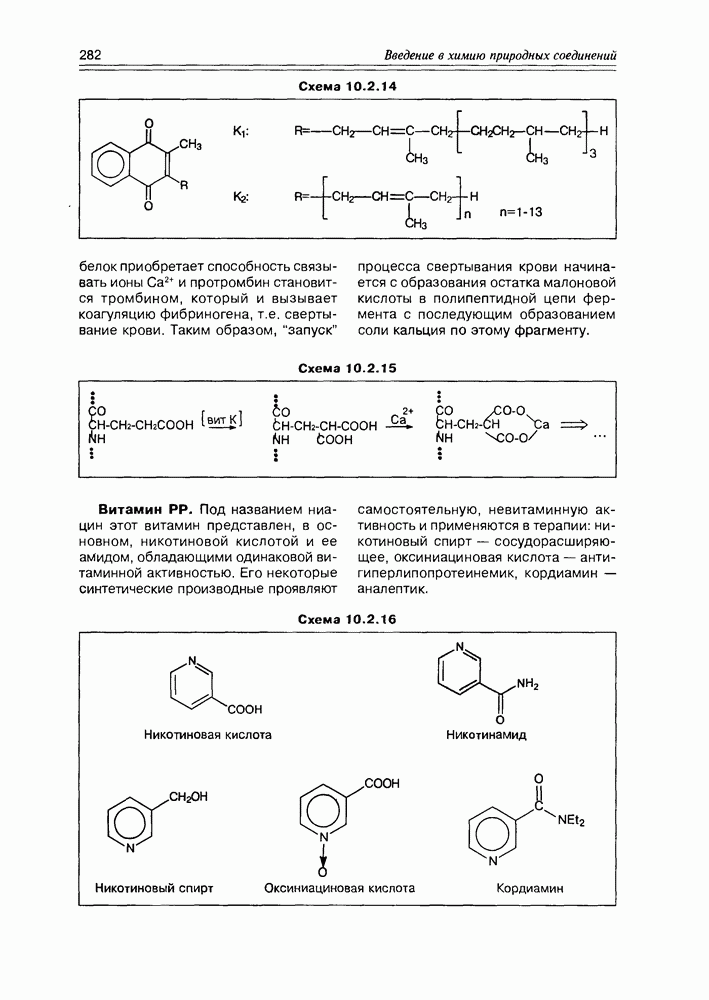
- 10.2. Витамины-коферменты
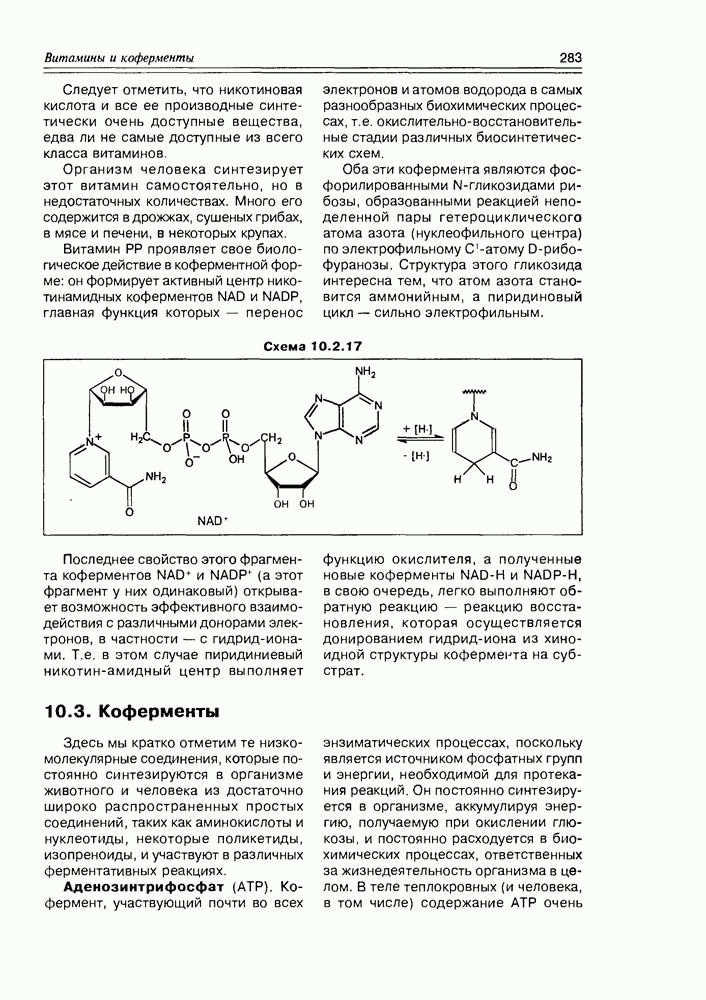
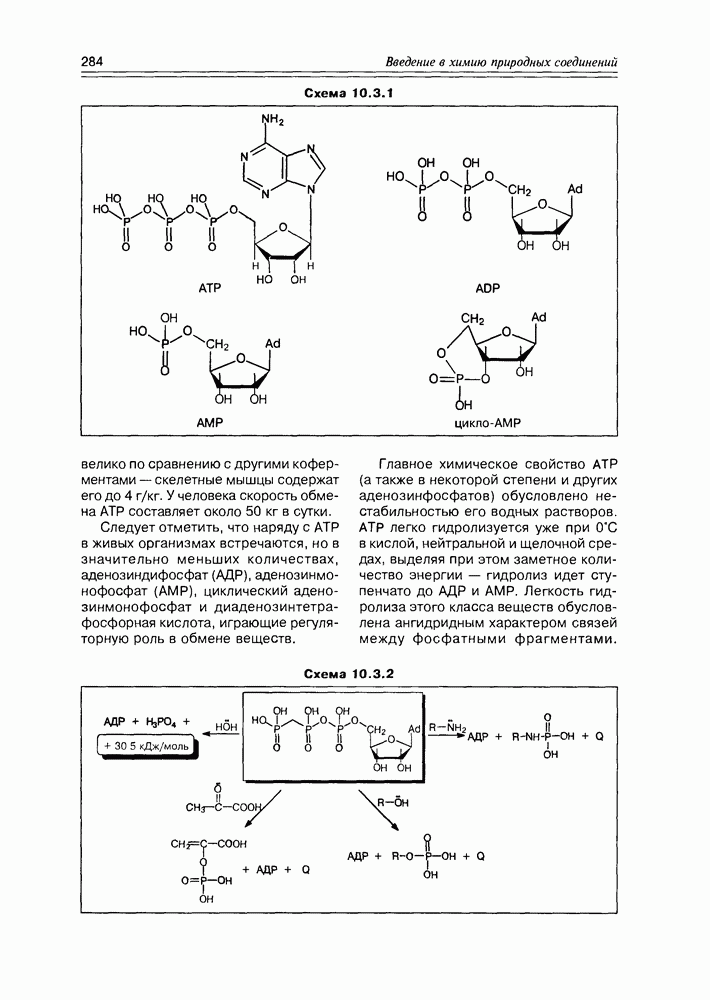
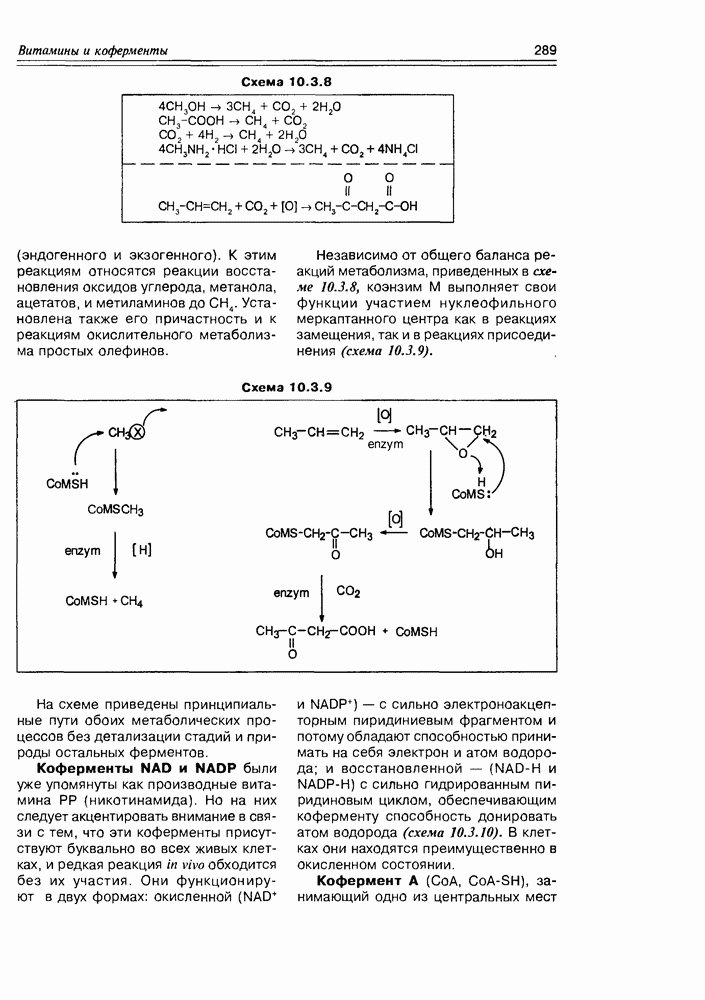
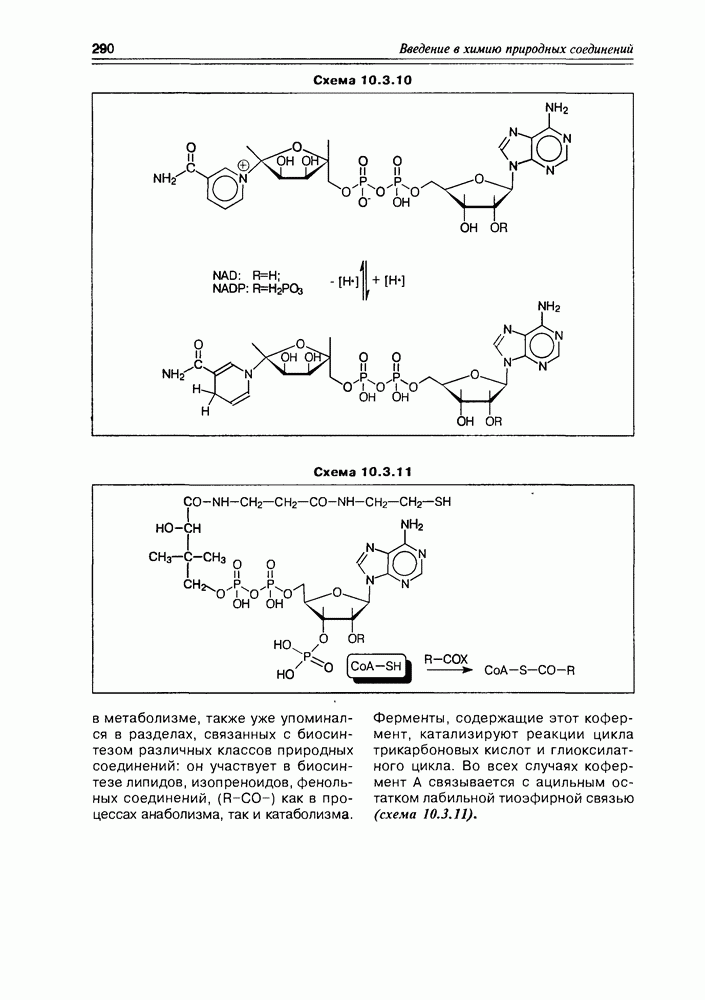
- 10.3. Коферменты
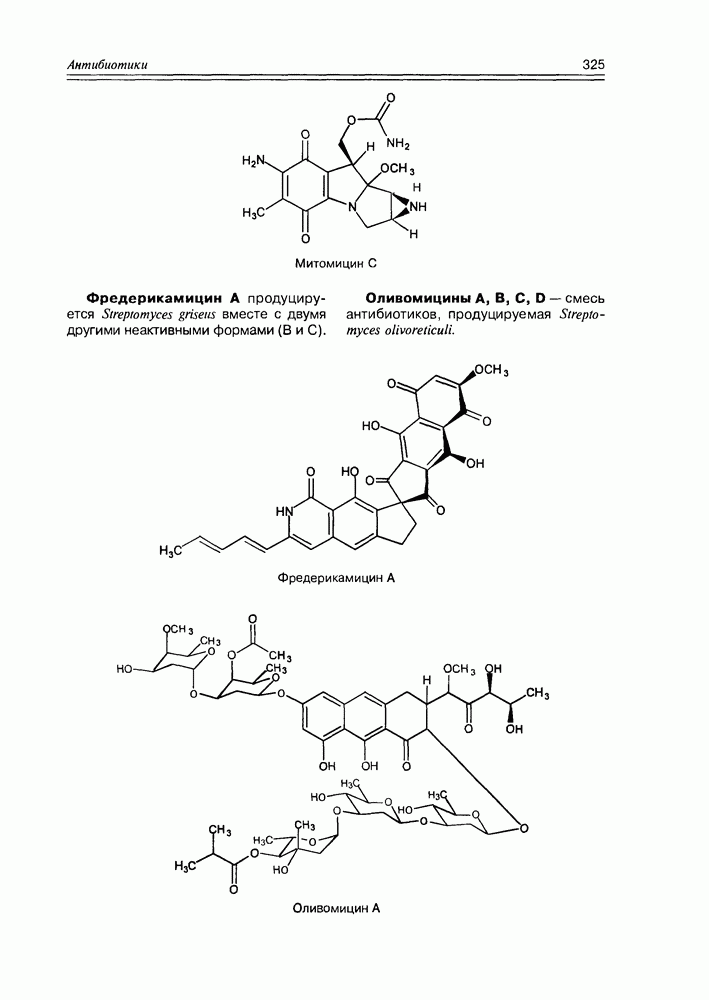
- Глава 11. АНТИБИОТИКИ
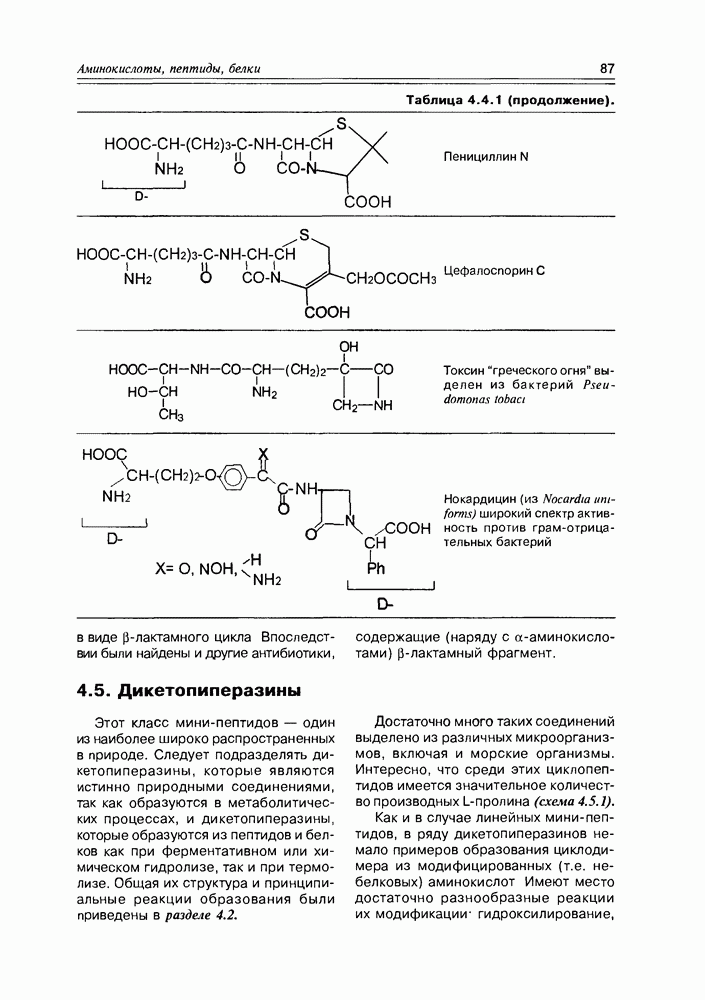
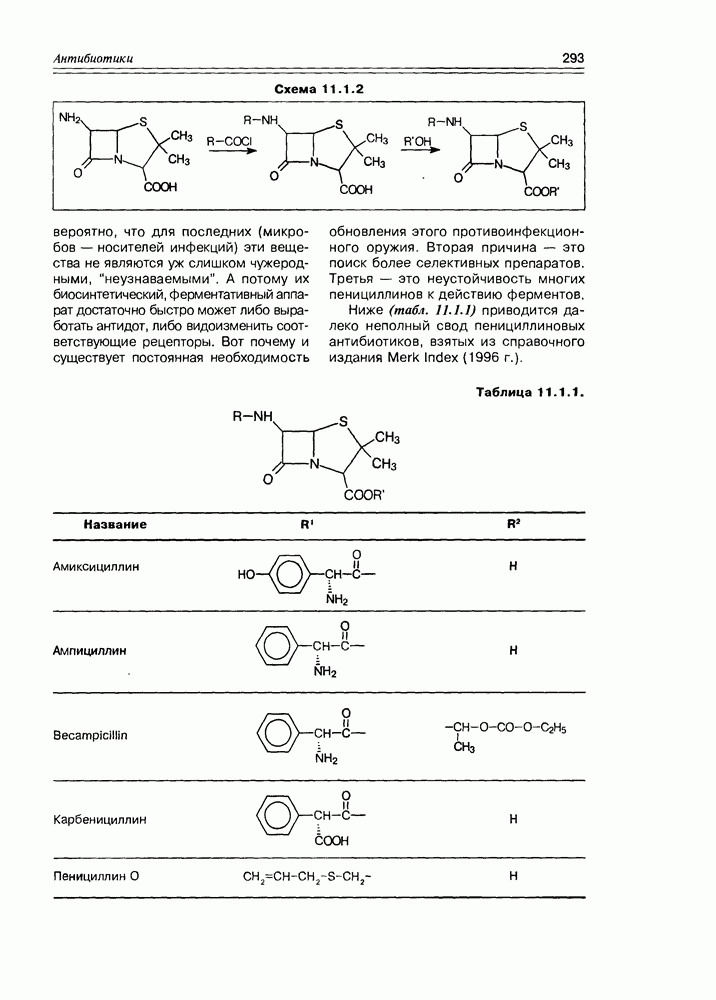
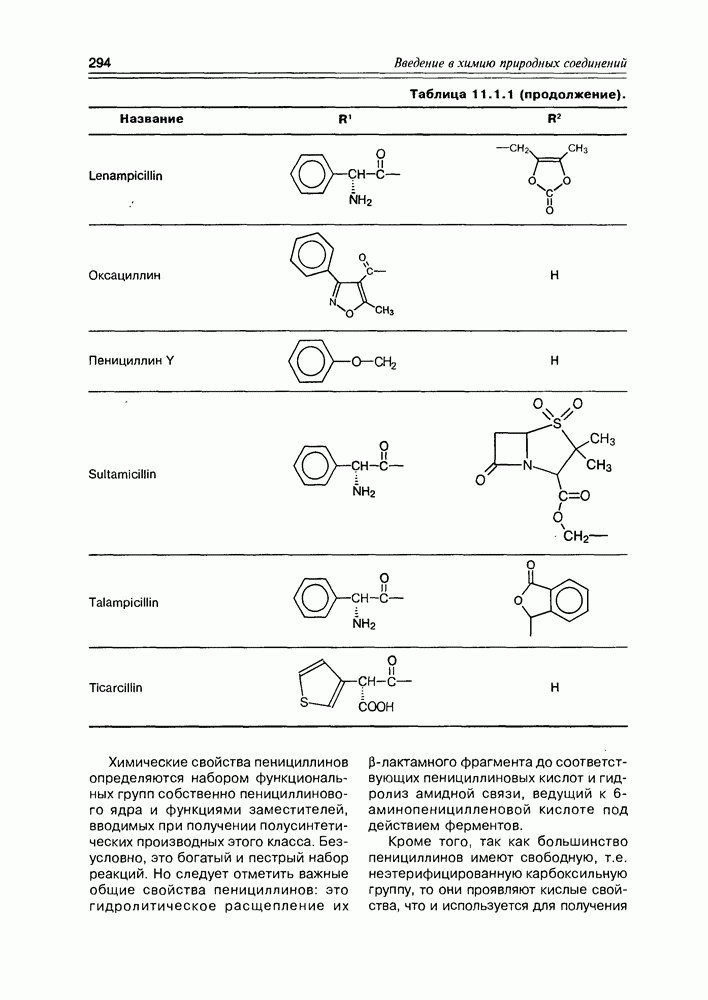
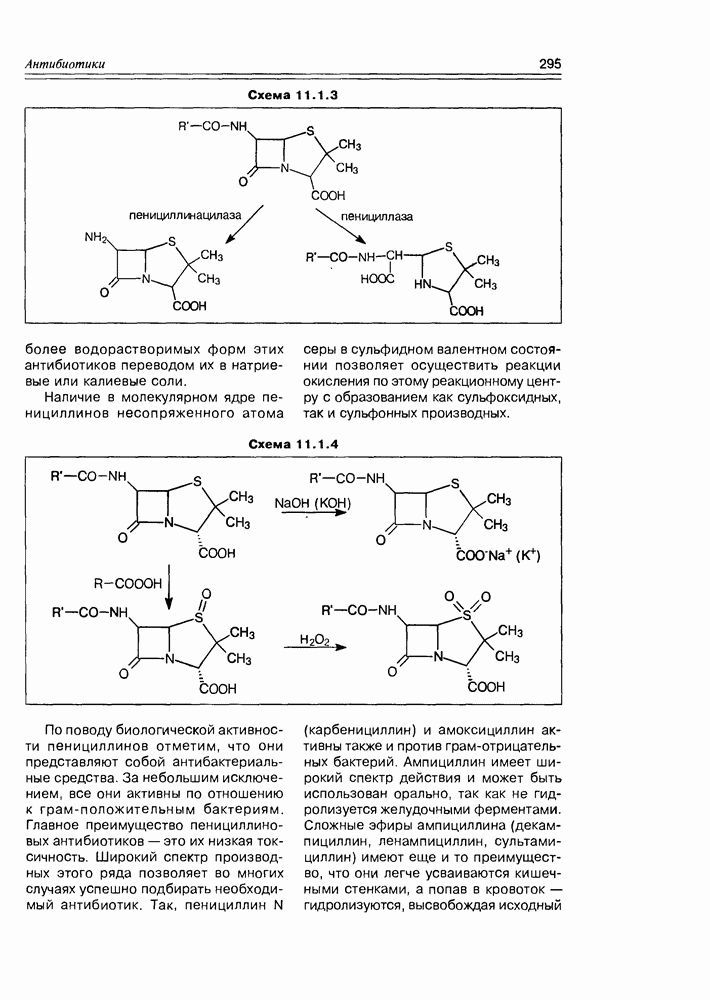
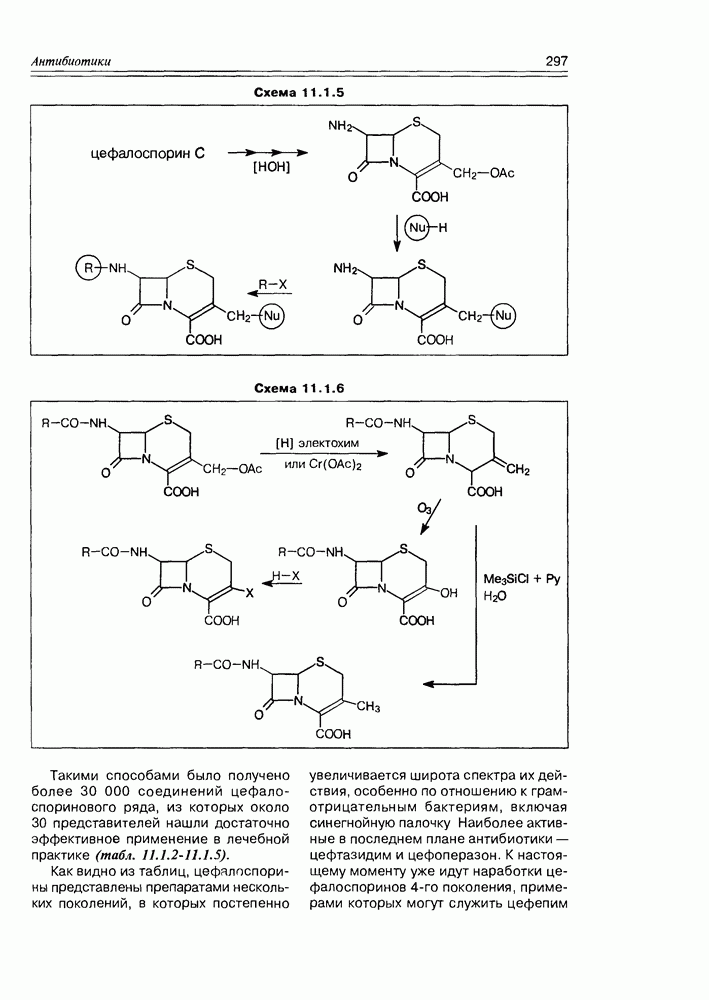
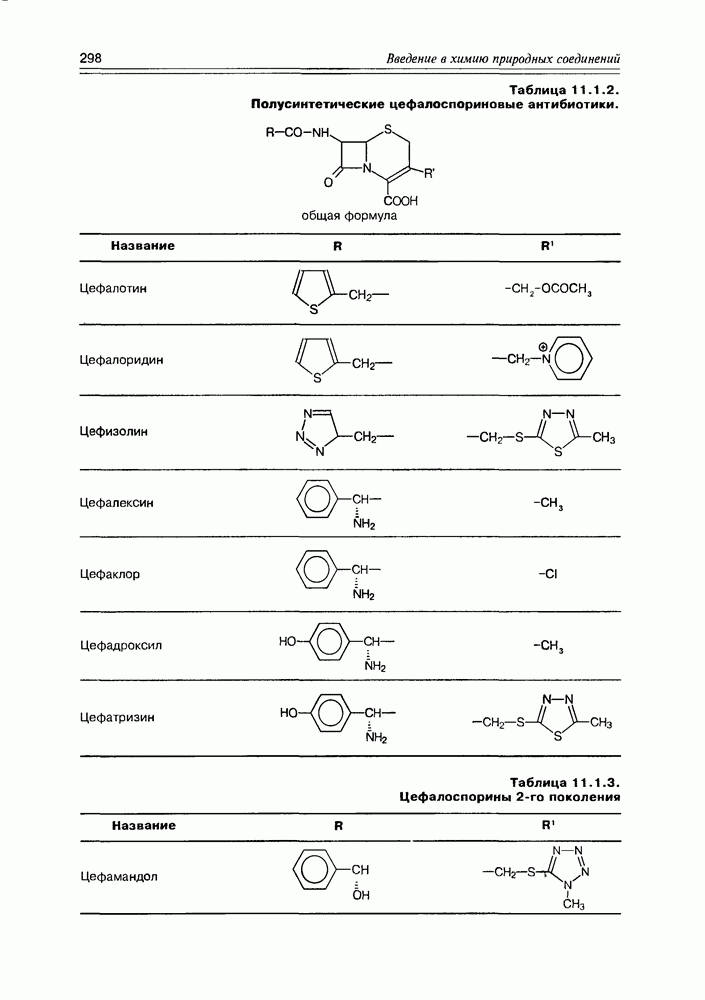
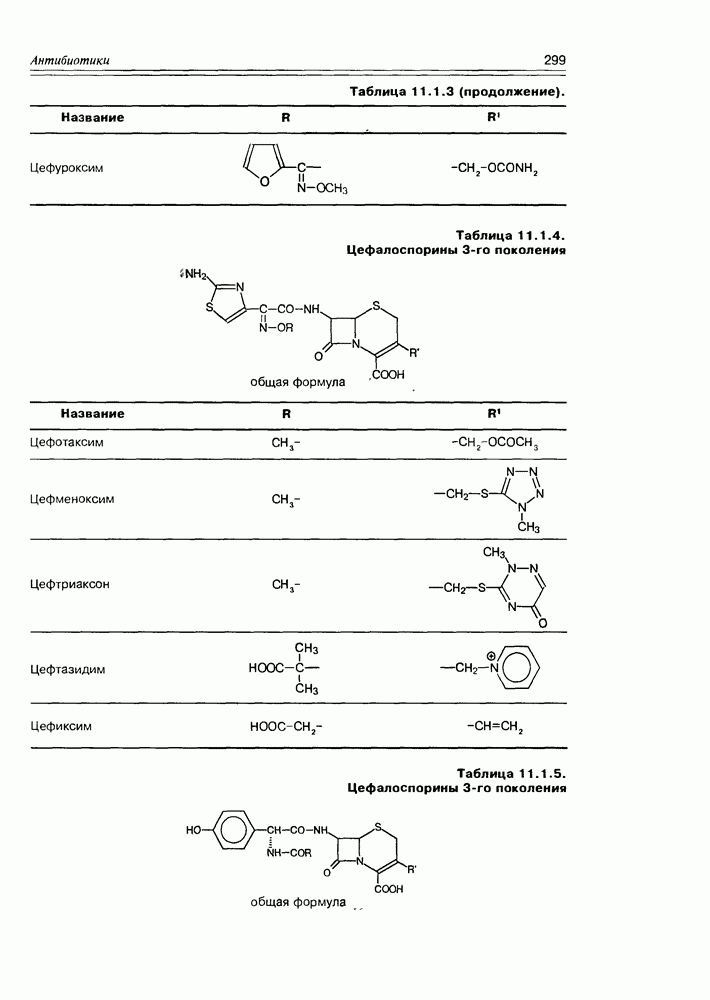
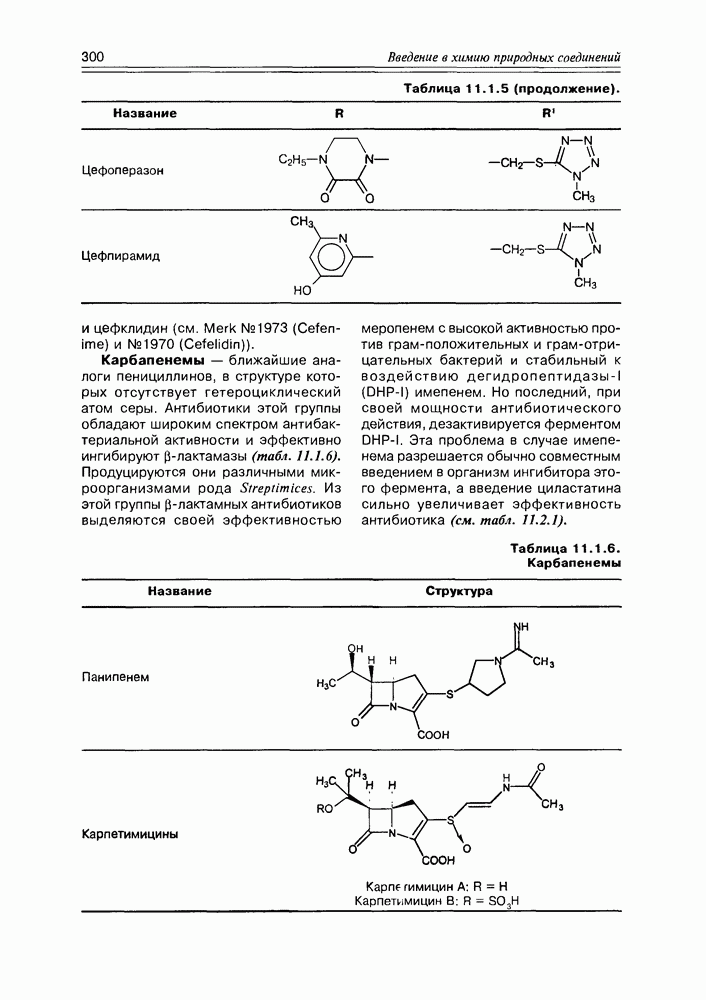
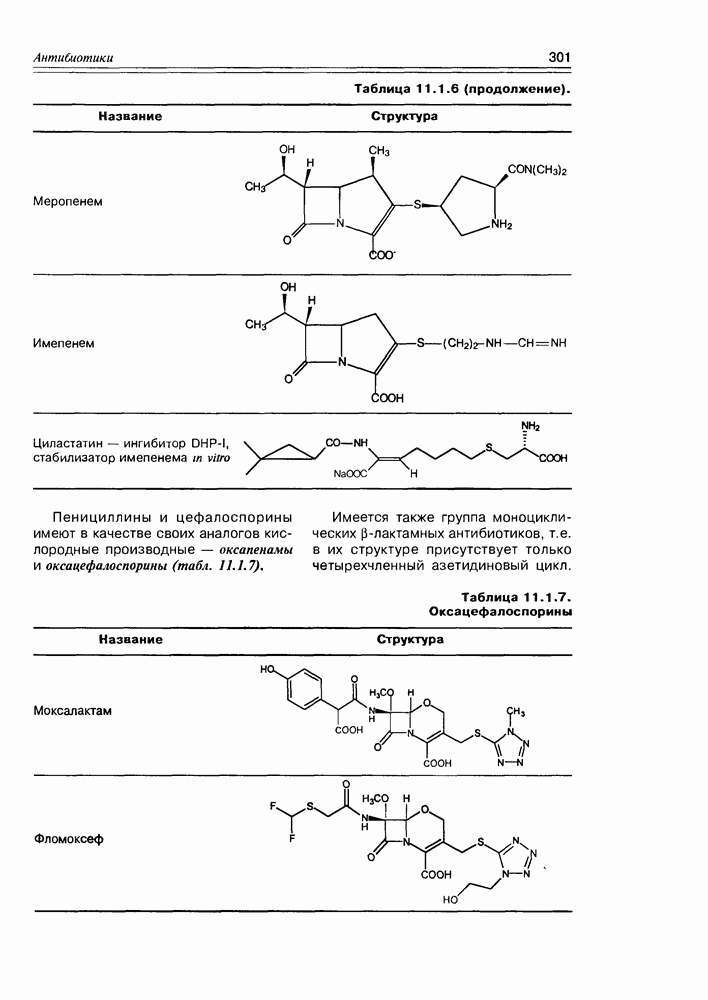
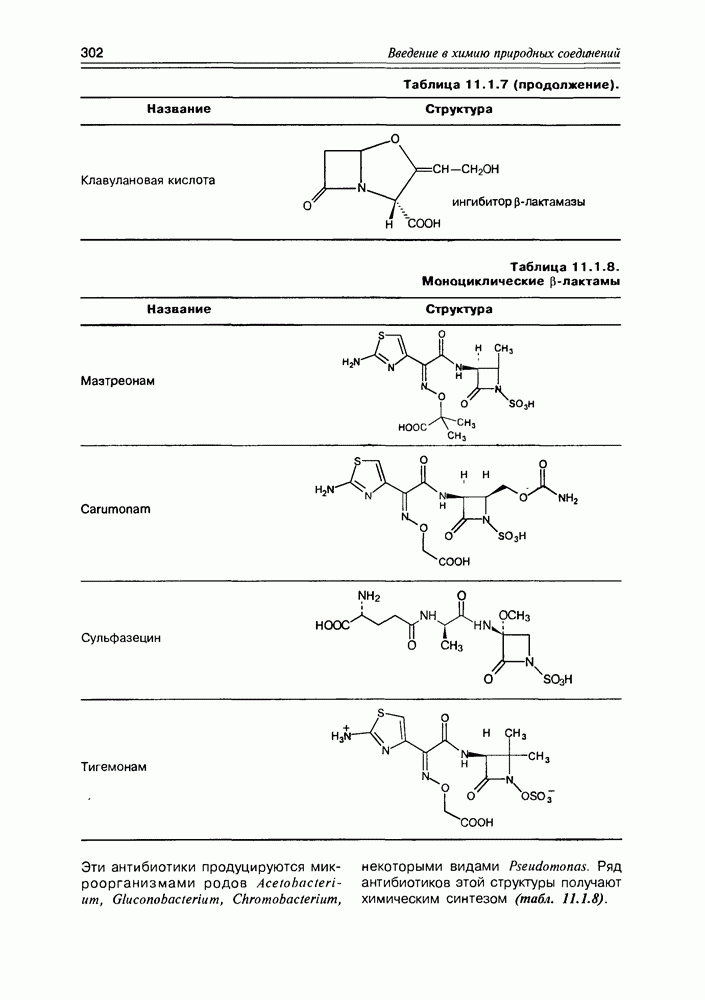
- 11.1. b-Лактамные антибиотики
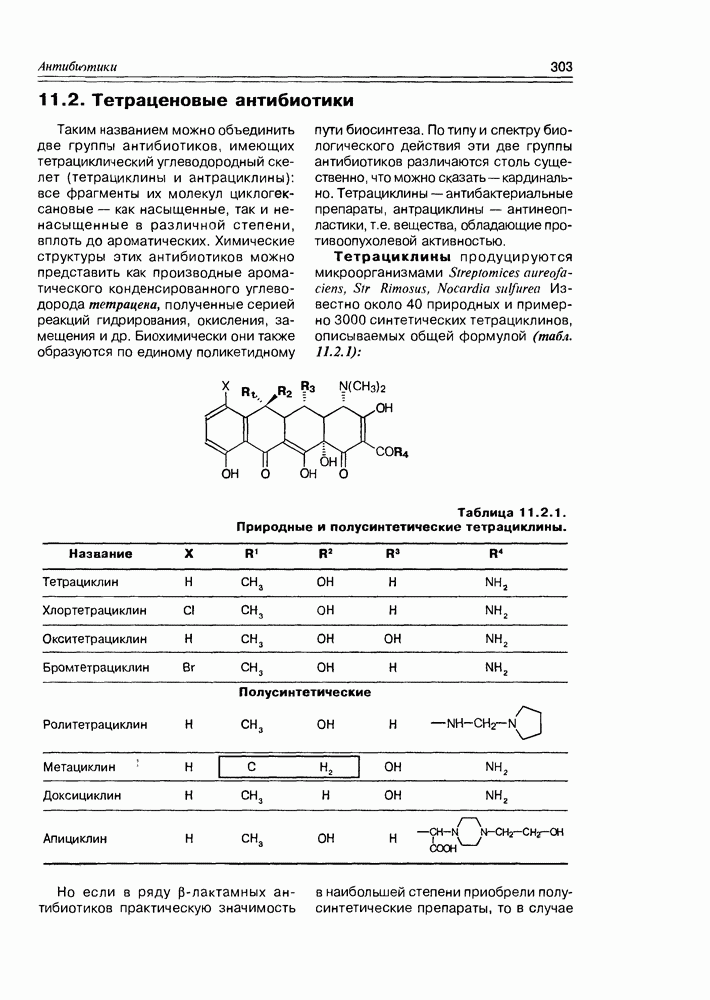
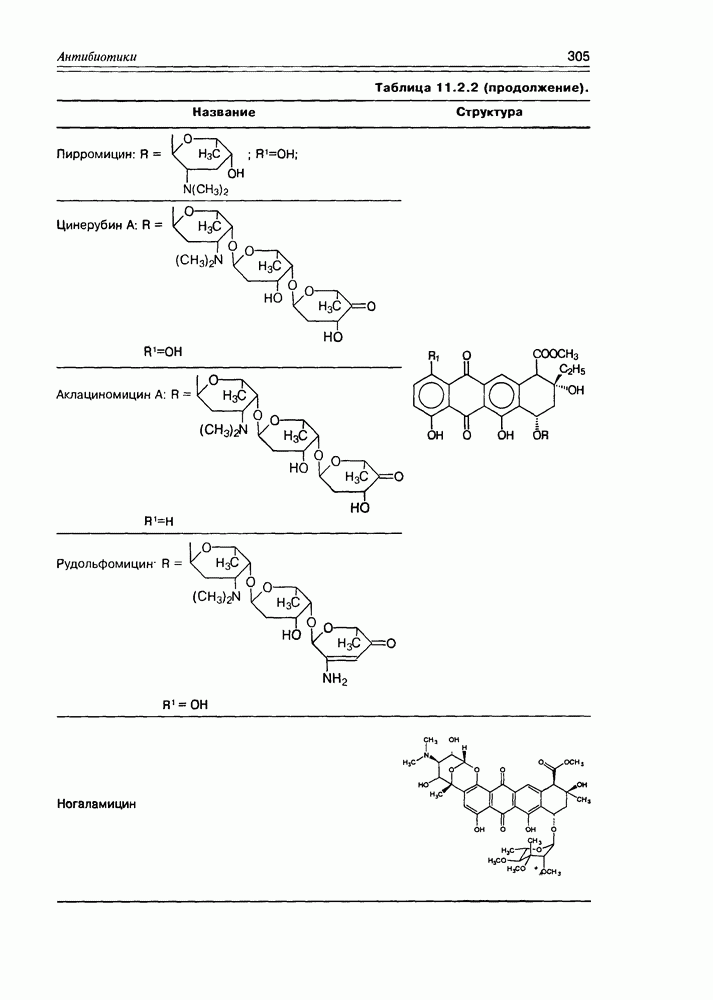
- 11.2. Тетраценовые антибиотики
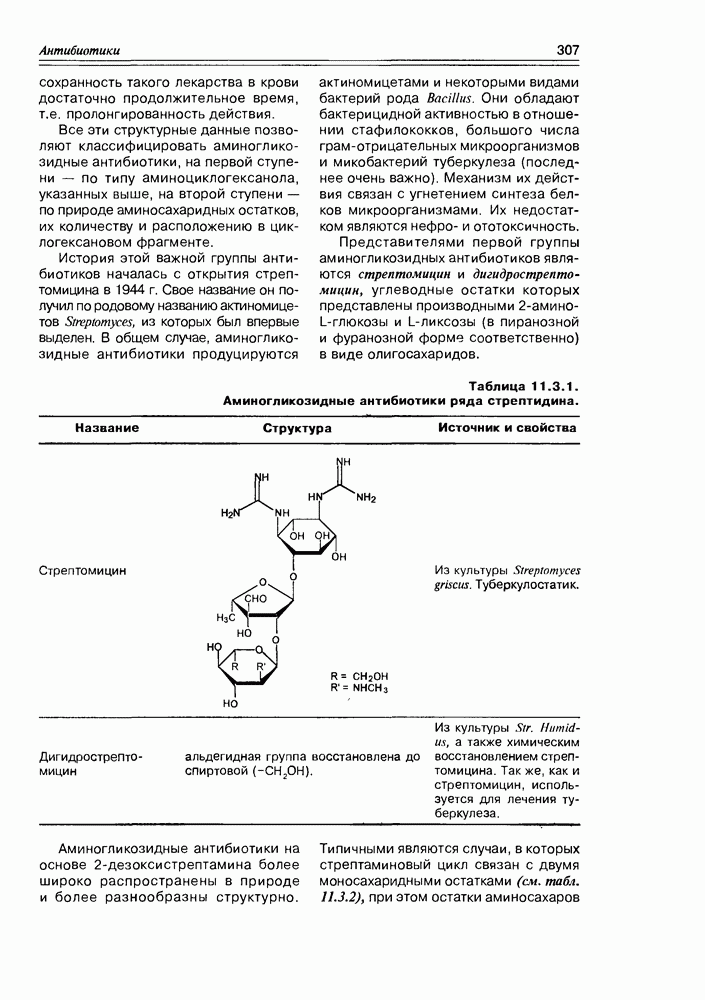
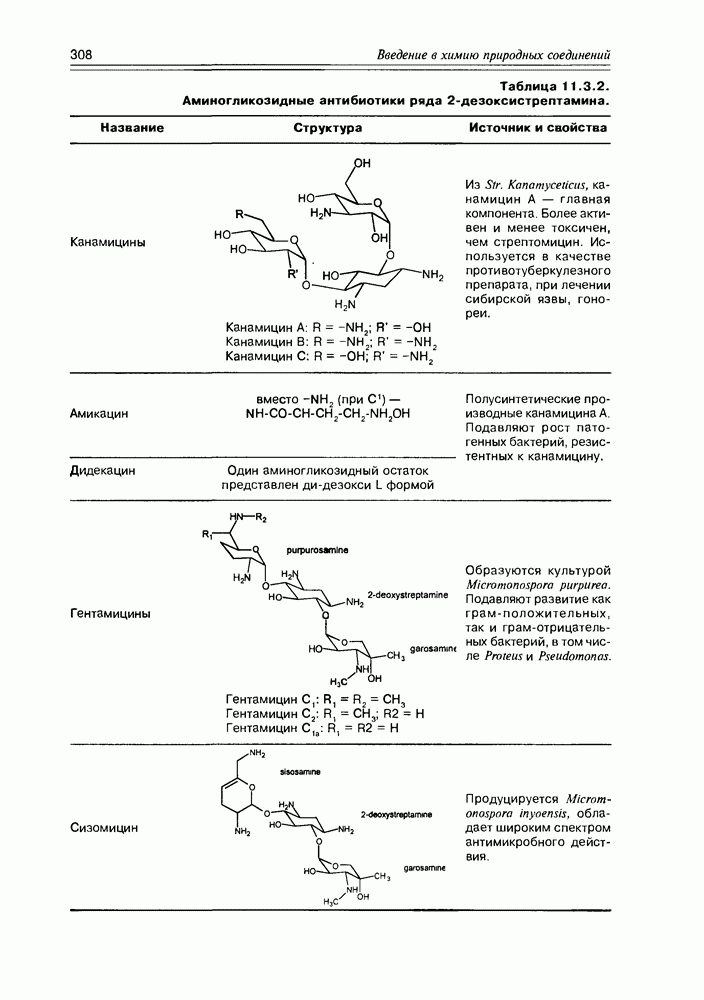
- 11.3. Аминогликозидные антибиотики
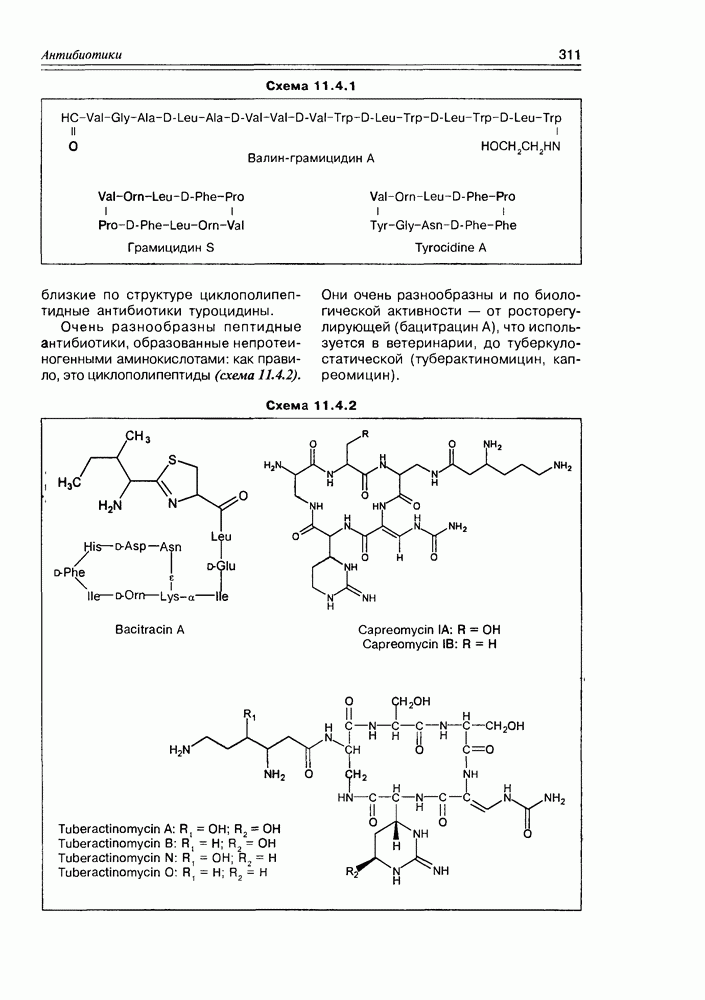
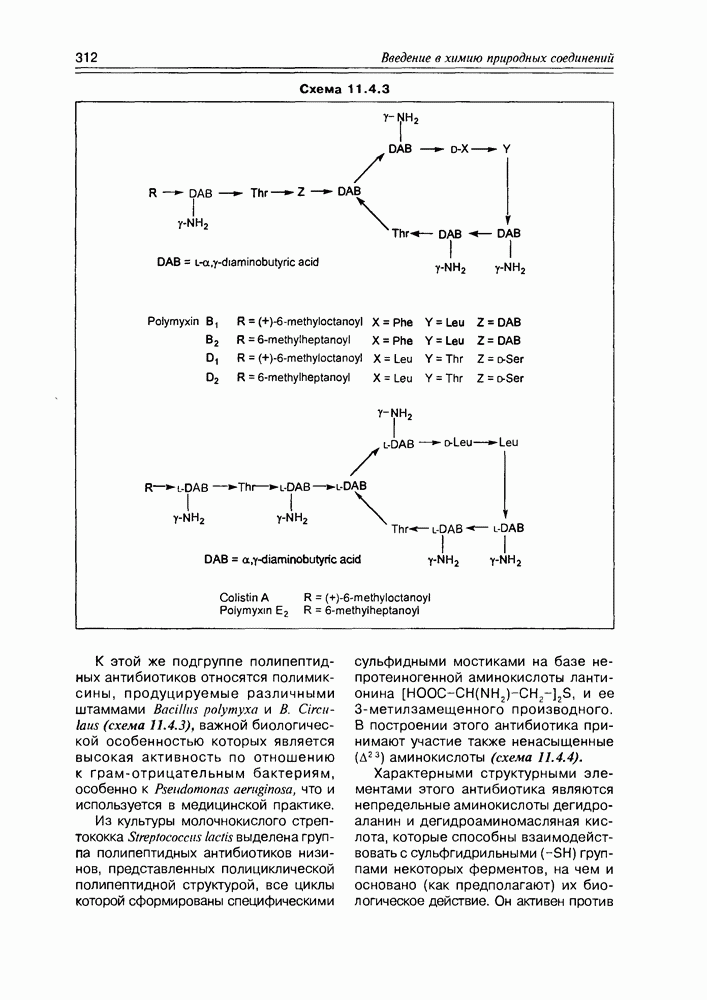
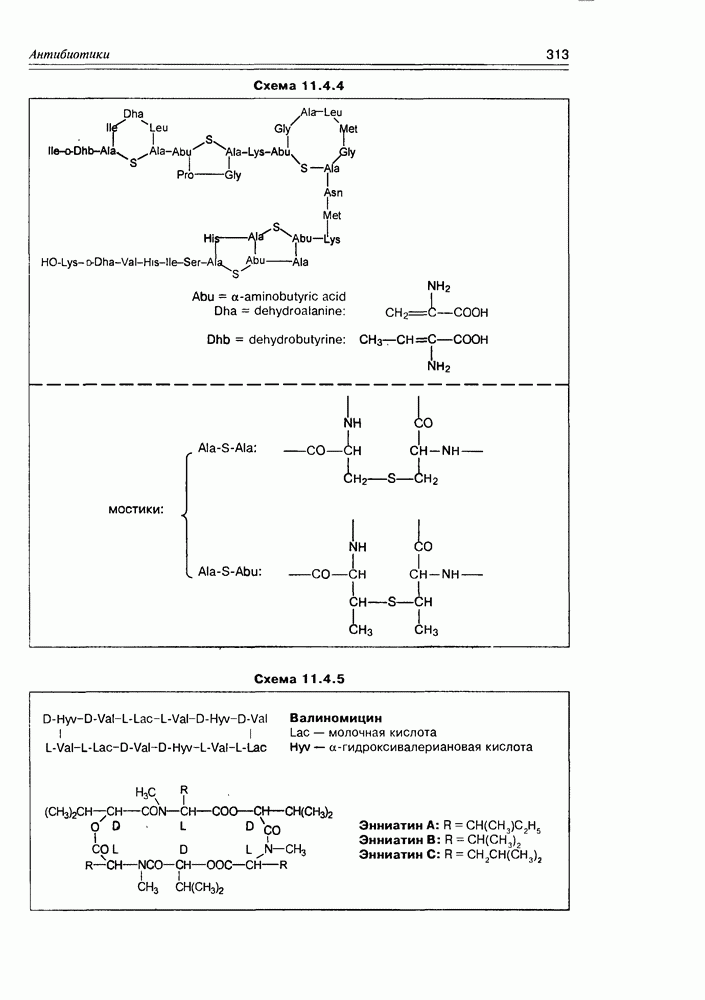
- 11.4. Пептидные антибиотики
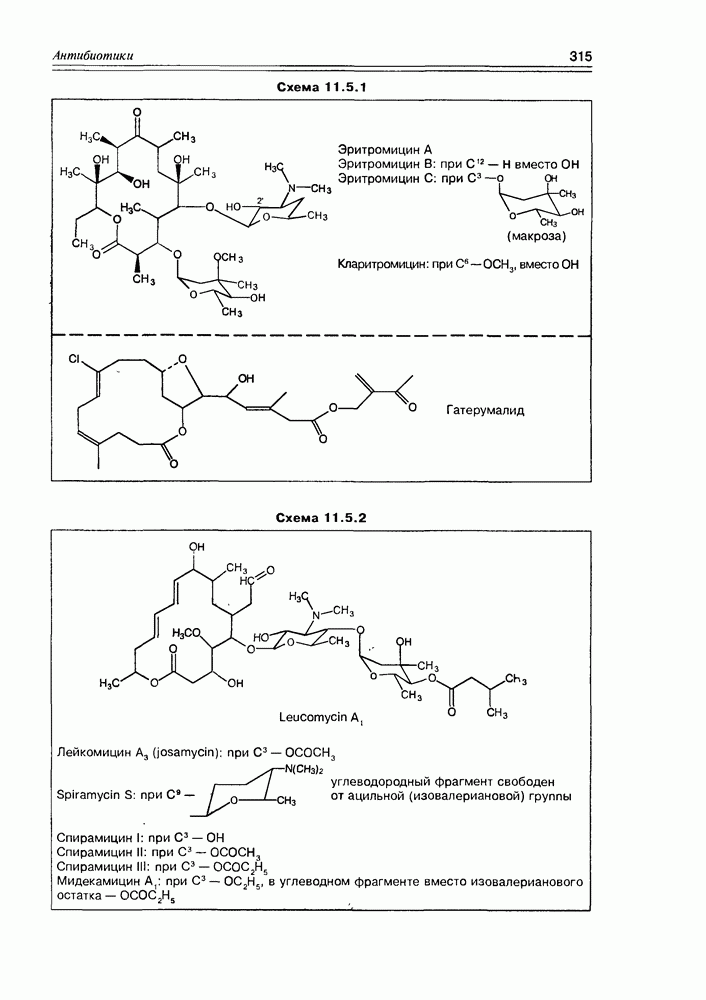
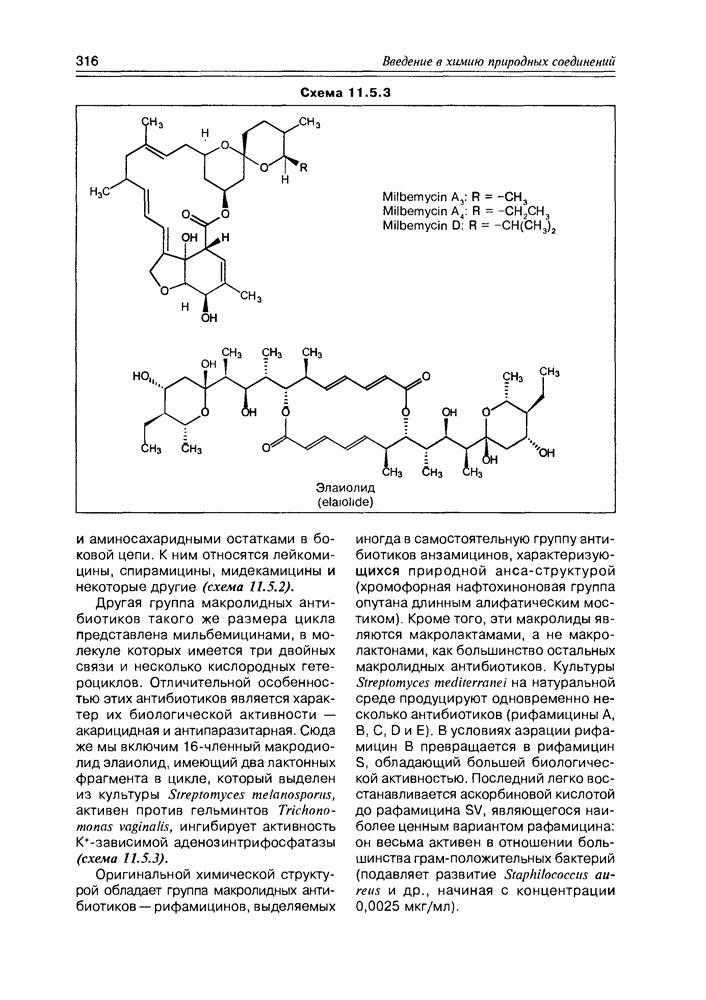
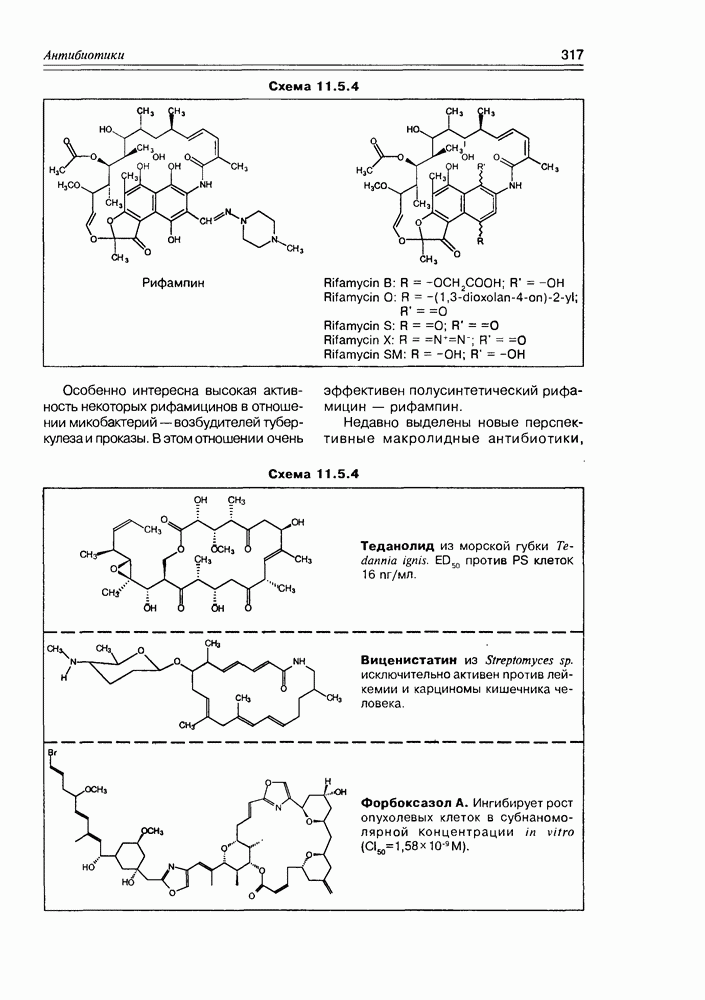
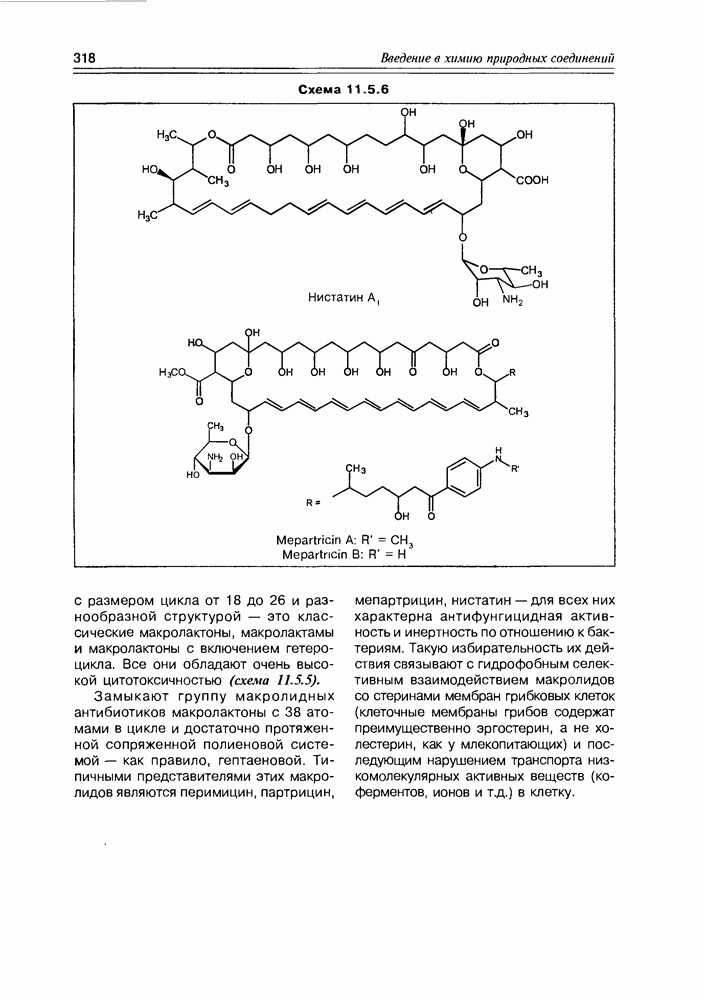
- 11.5. Макролидные антибиотики
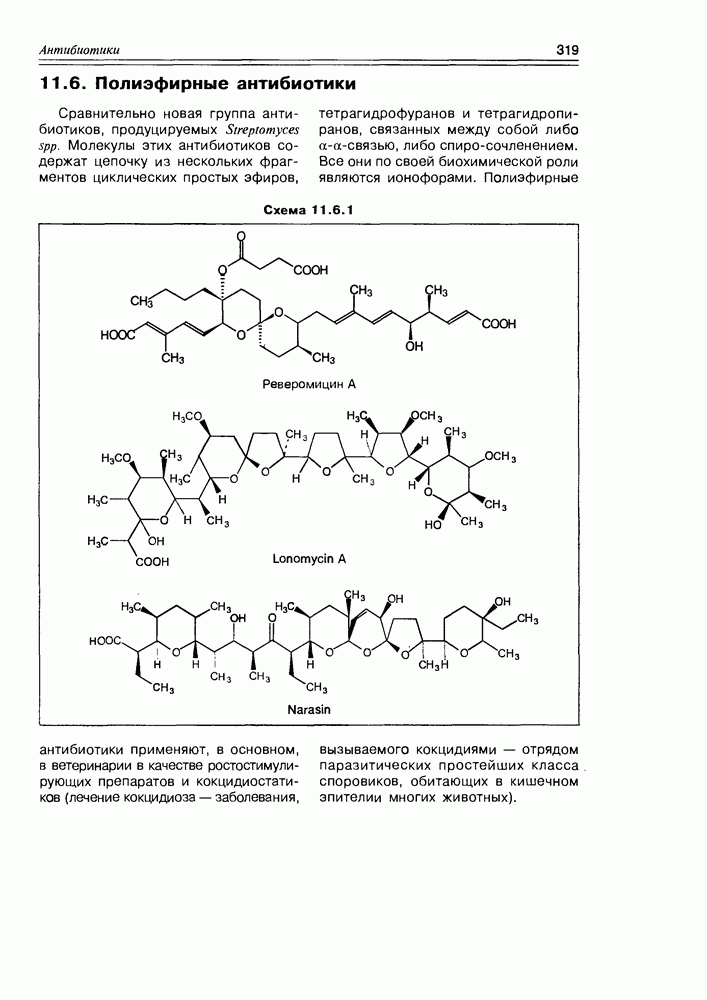
- 11.6. Полиэфирные антибиотики
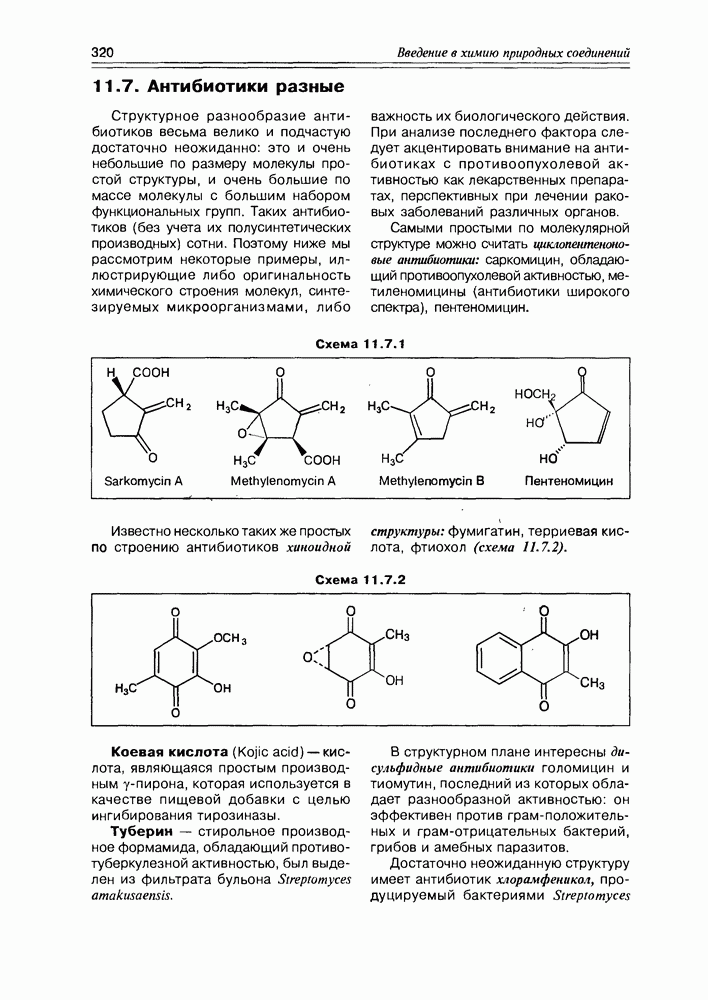
- 11.7. Антибиотики разные
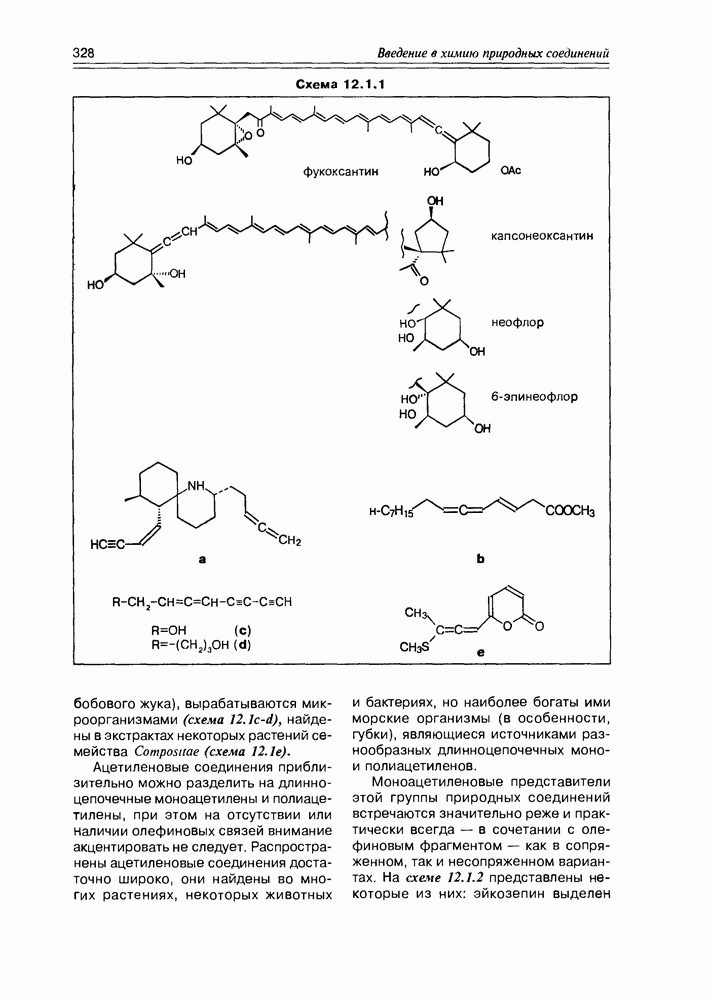
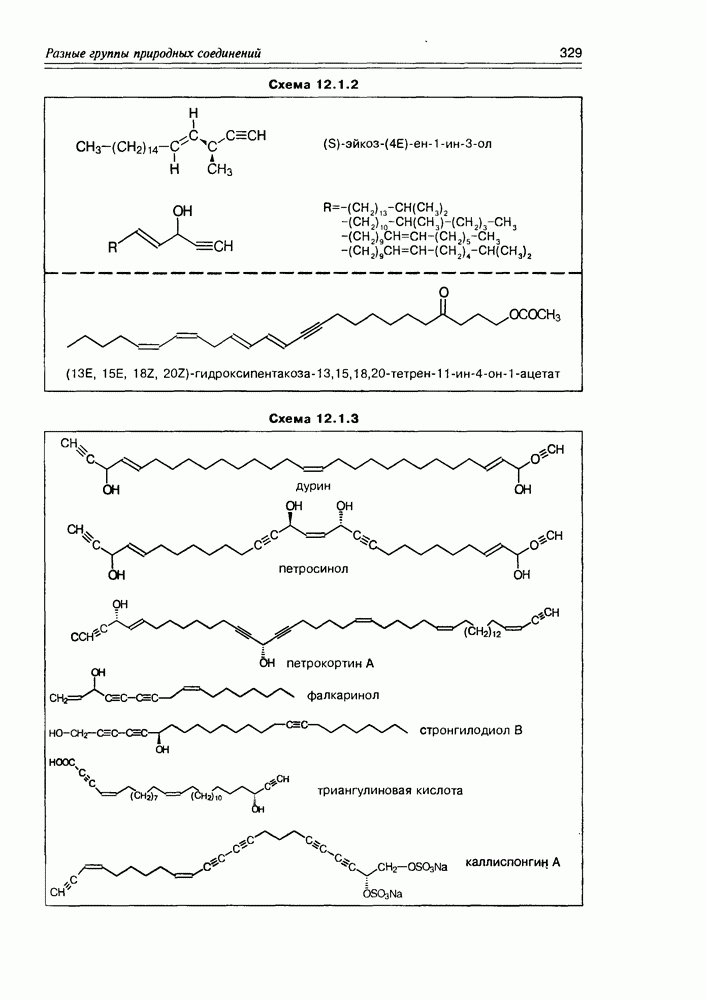
- Глава 12. РАЗНЫЕ ГРУППЫ ПРИРОДНЫХ СОЕДИНЕНИЙ
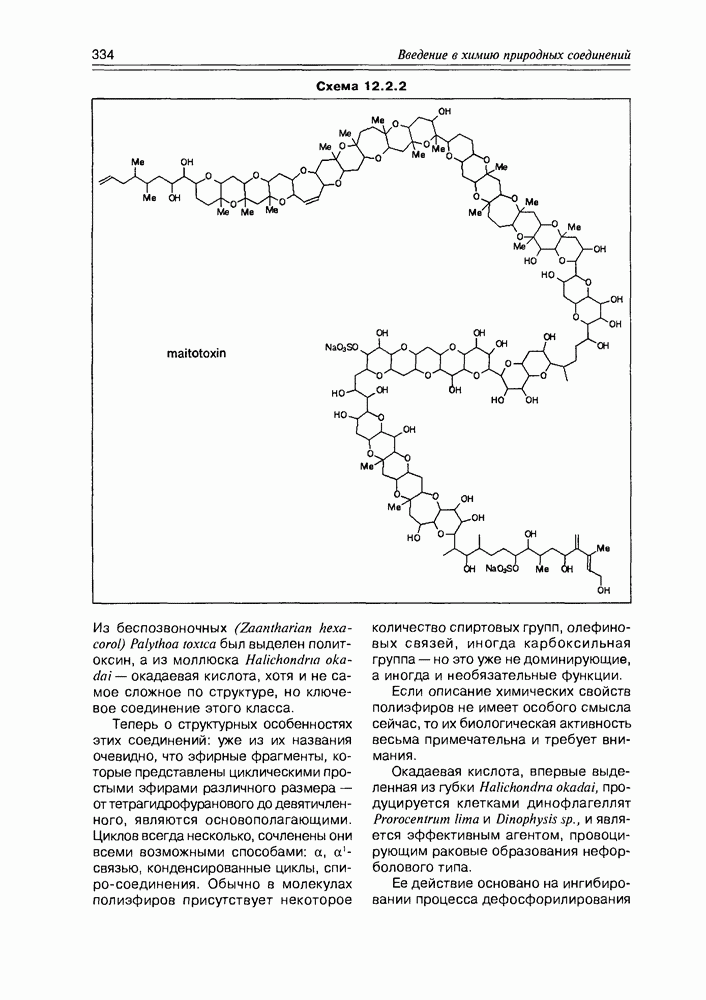
- 12.2. Полиэфиры
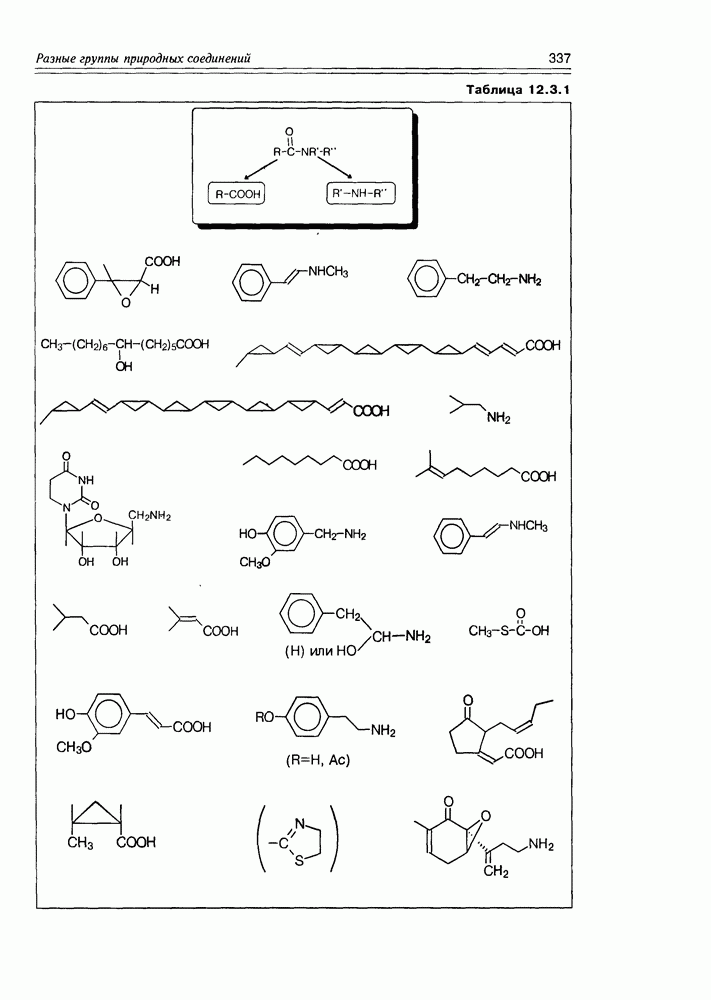
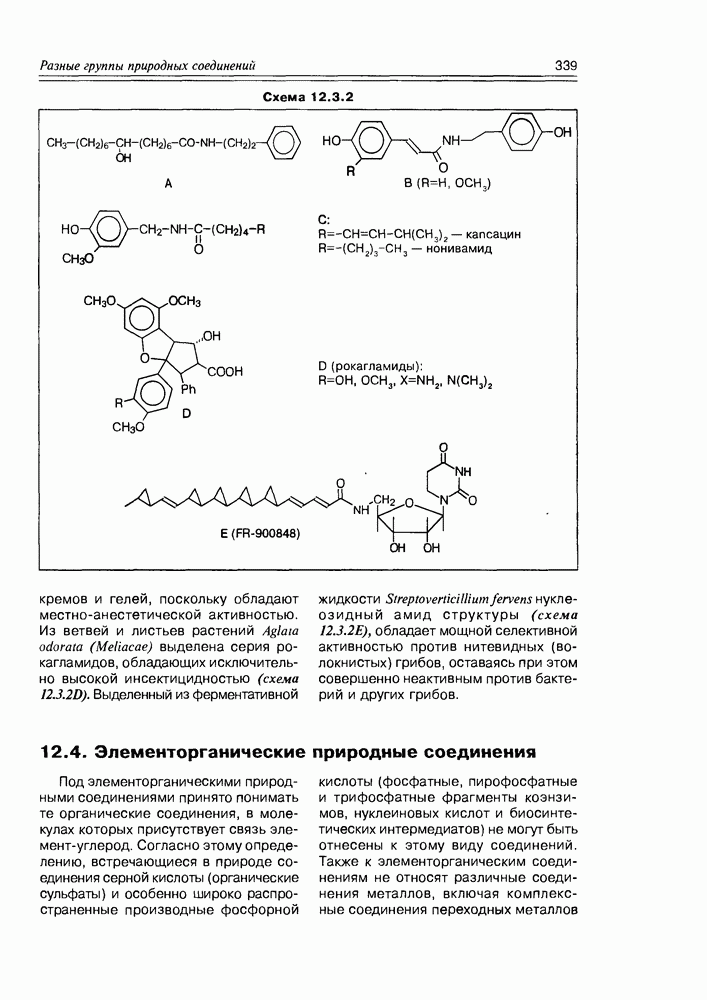
- 12.3. Амиды
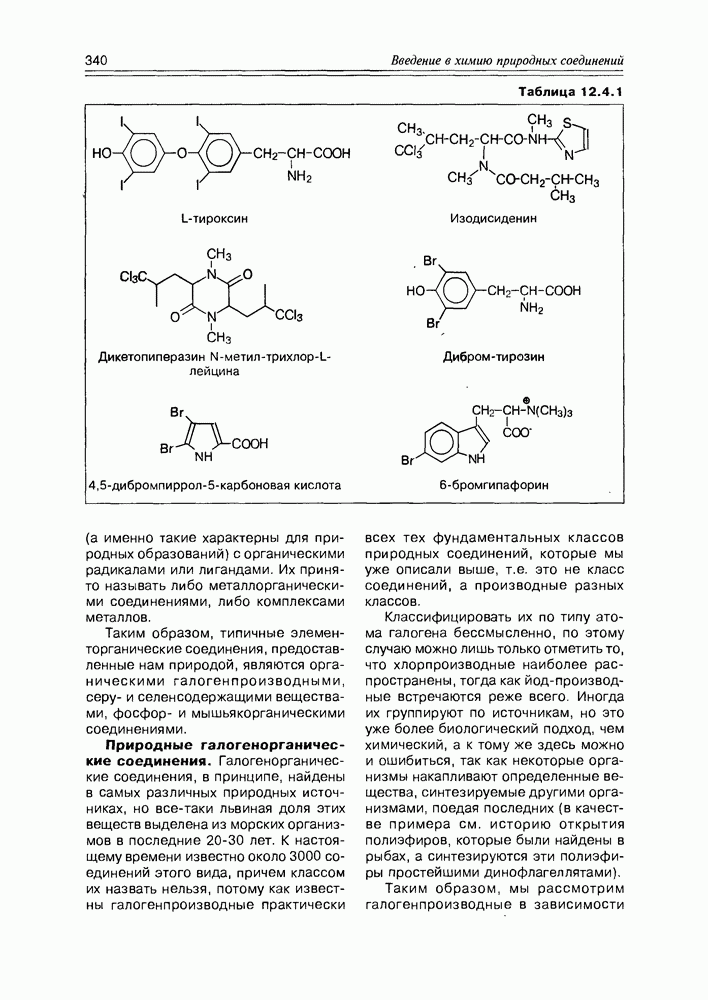
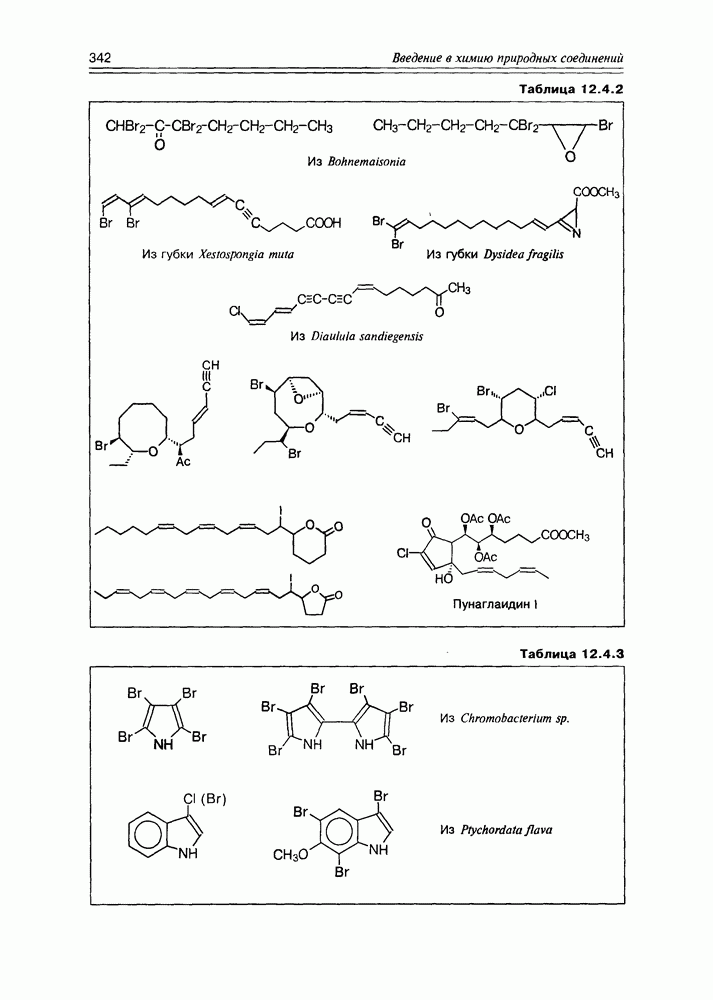
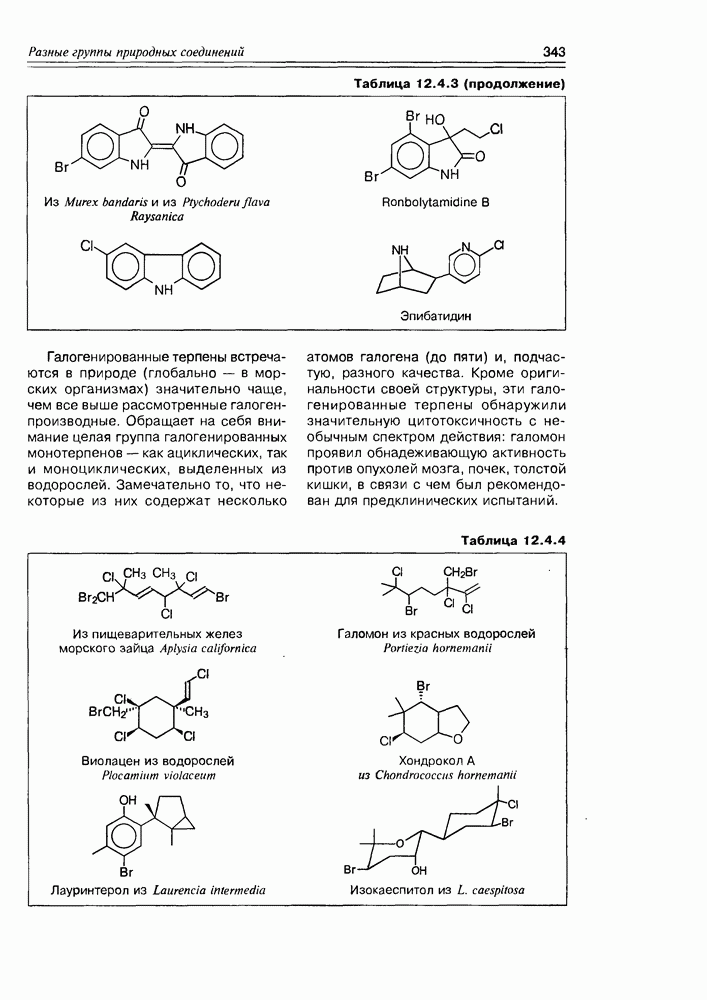
- 12.4. Элементорганические природные соединения
- Глава 13. МЕТАЛЛО-КОЭНЗИМЫ