| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
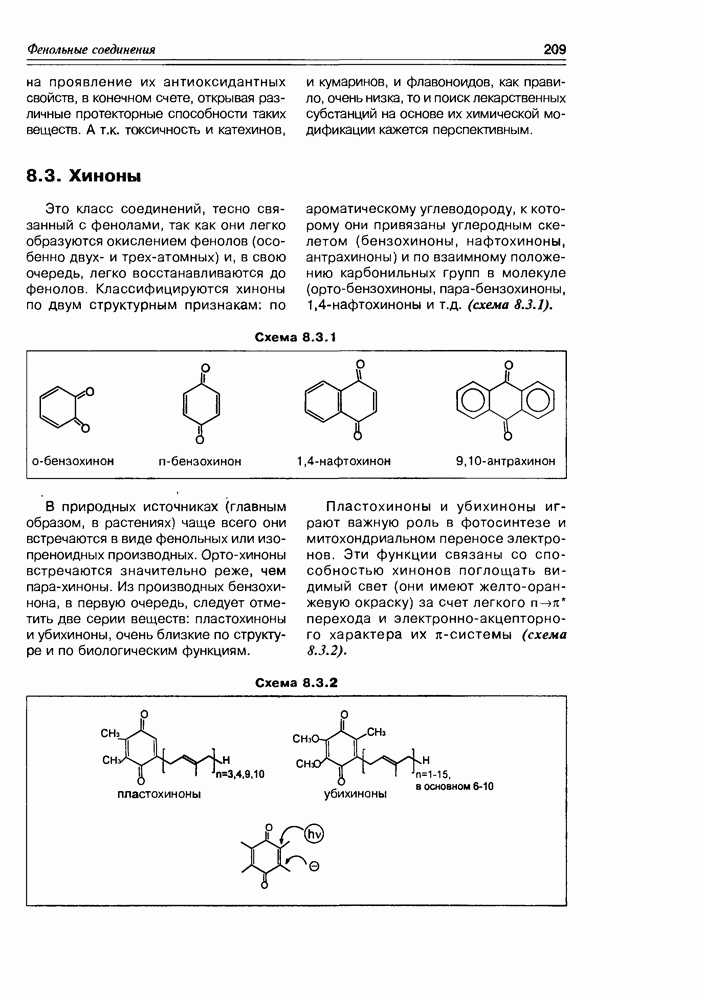
12.2. Полиэфиры
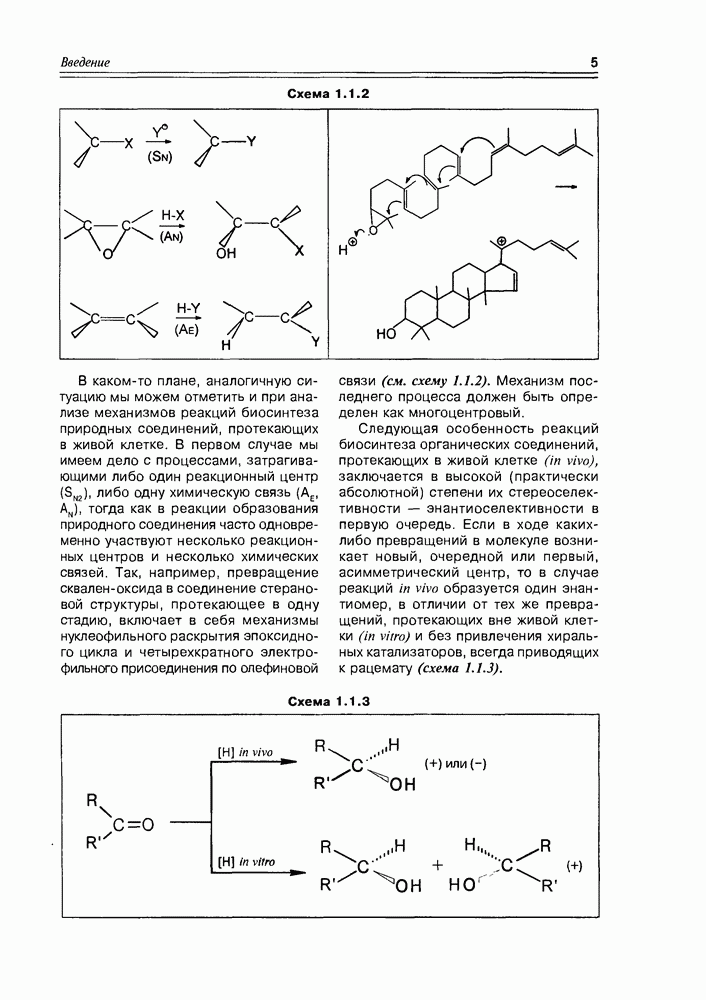
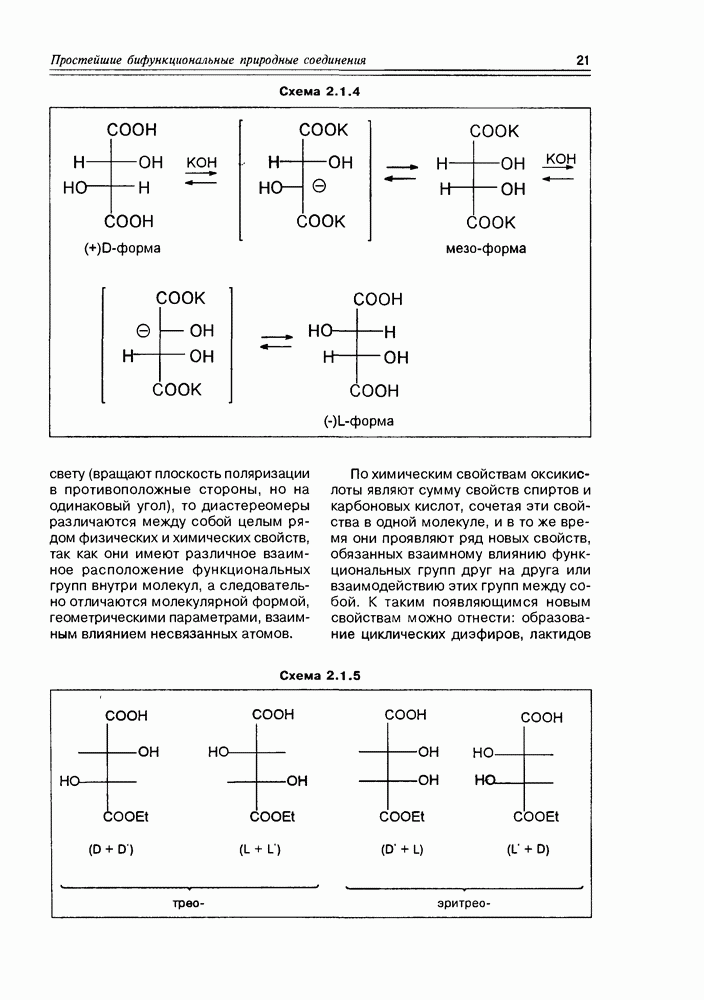
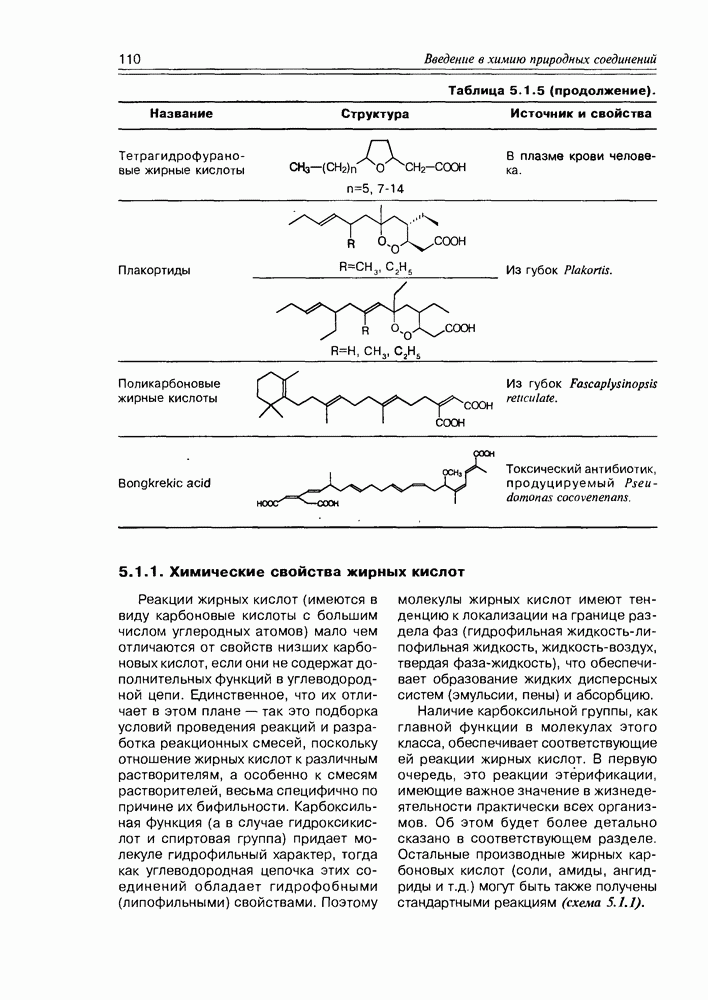
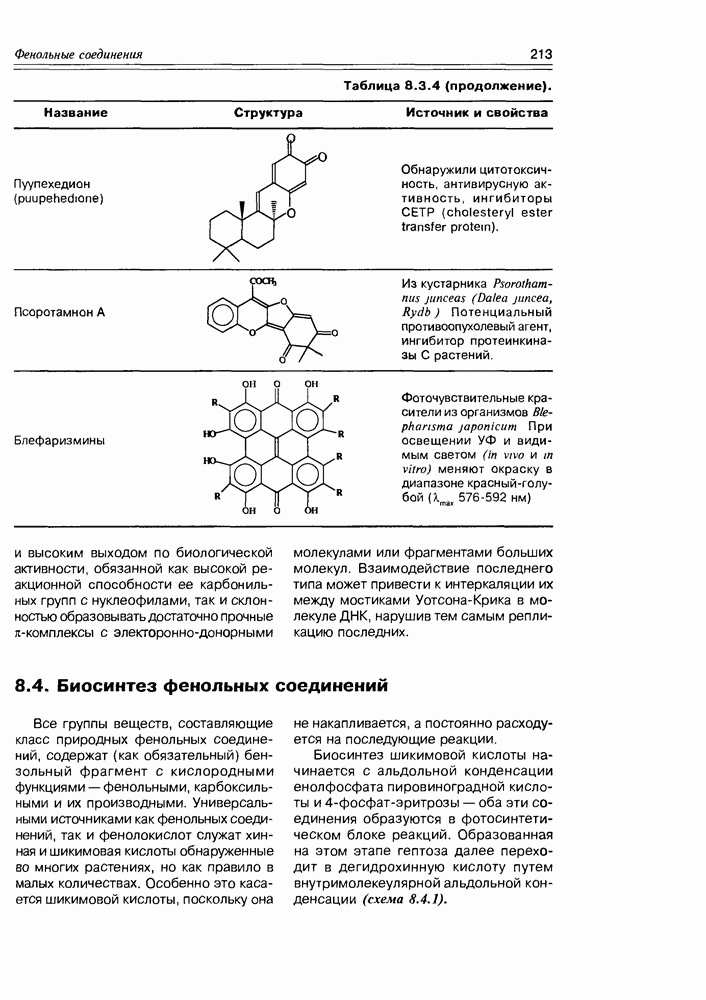
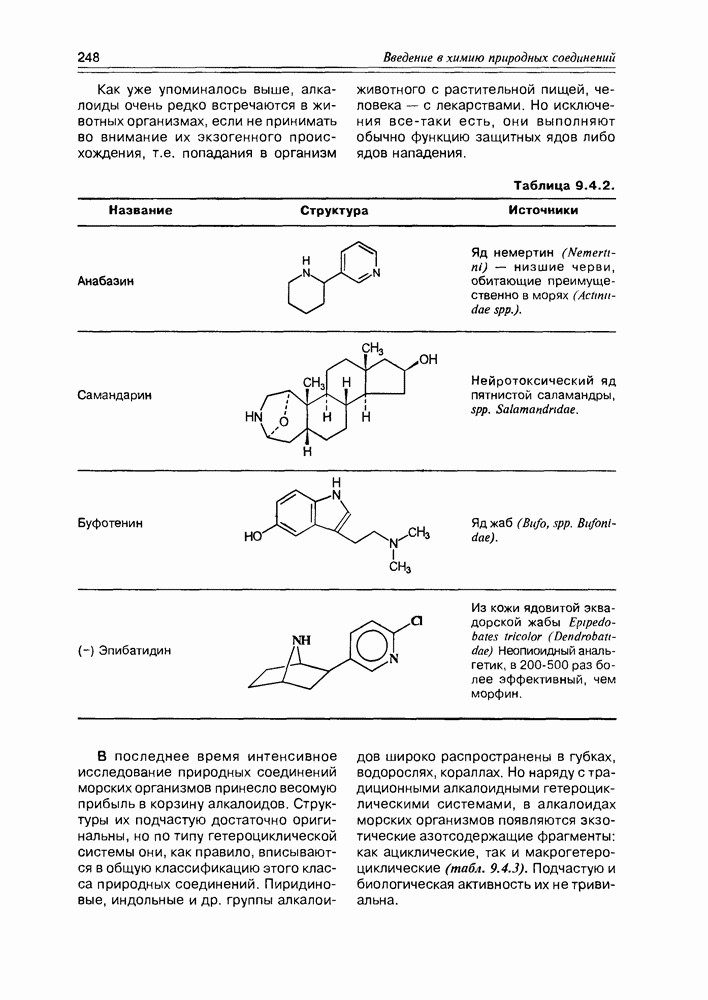
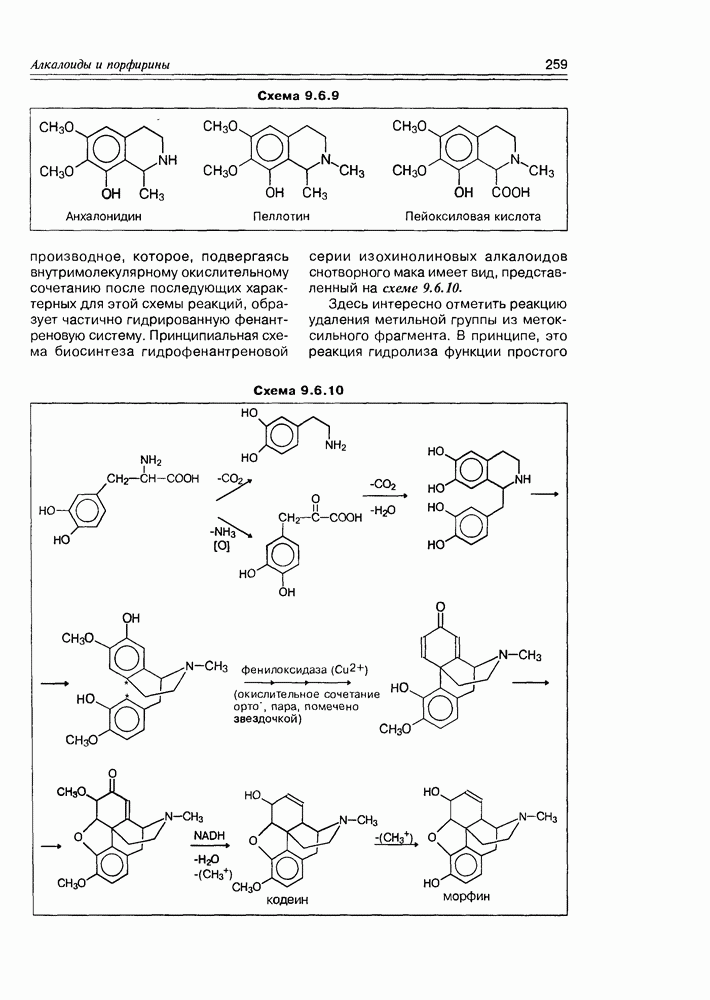
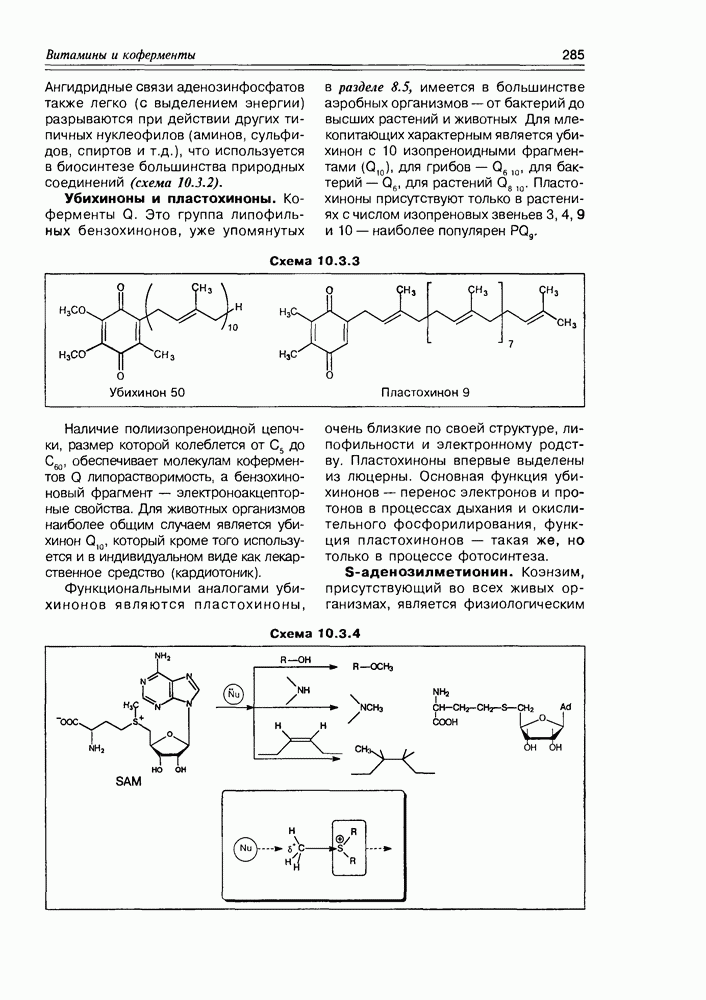
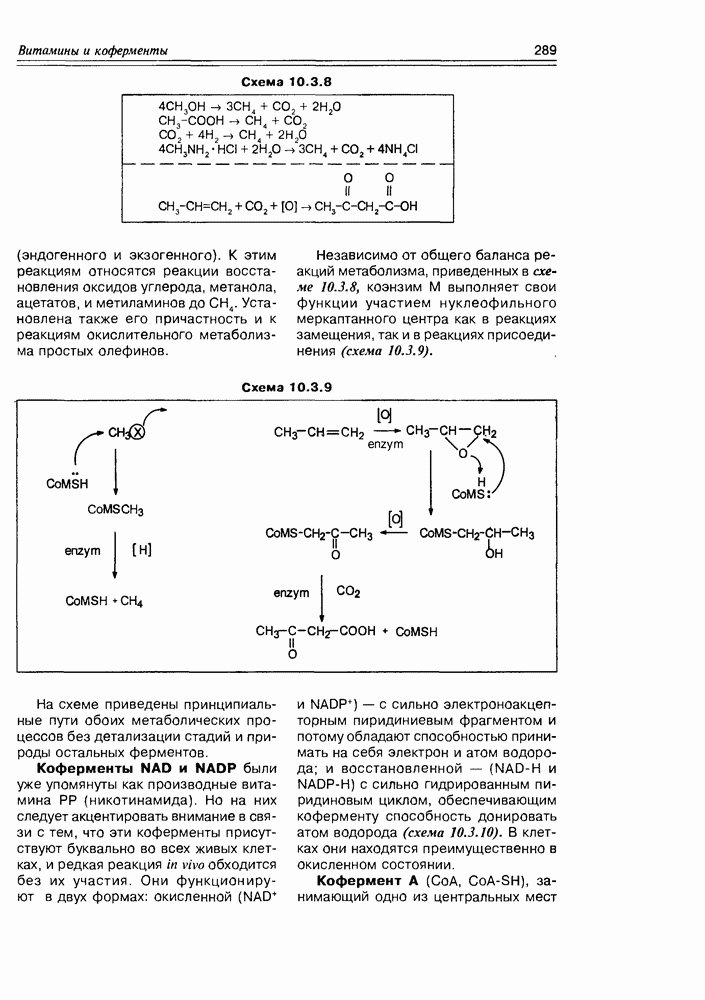
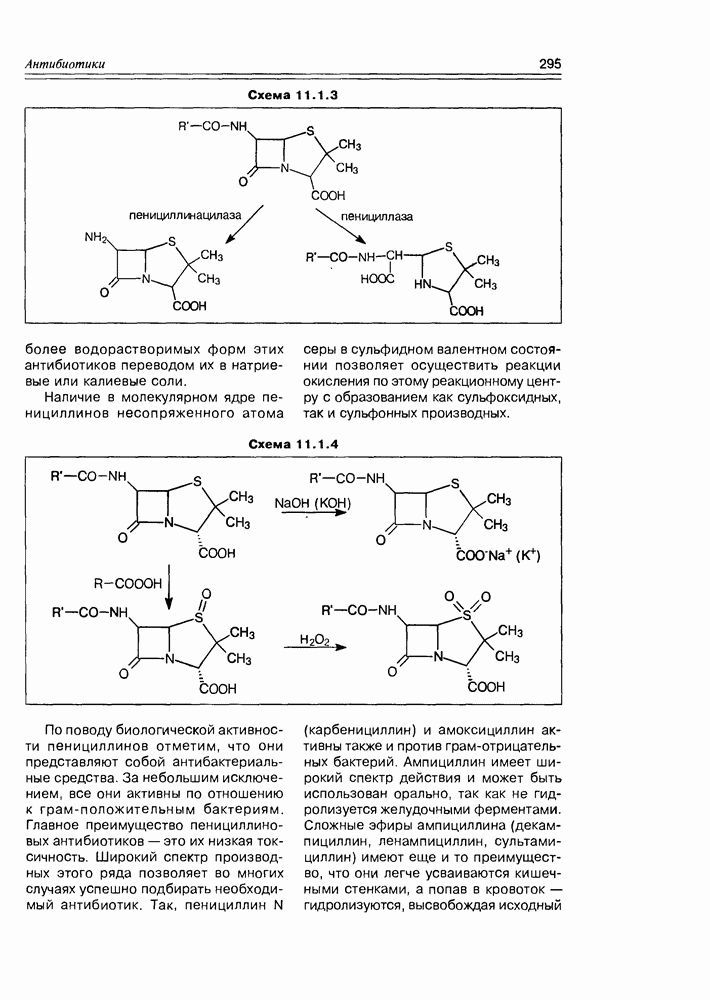
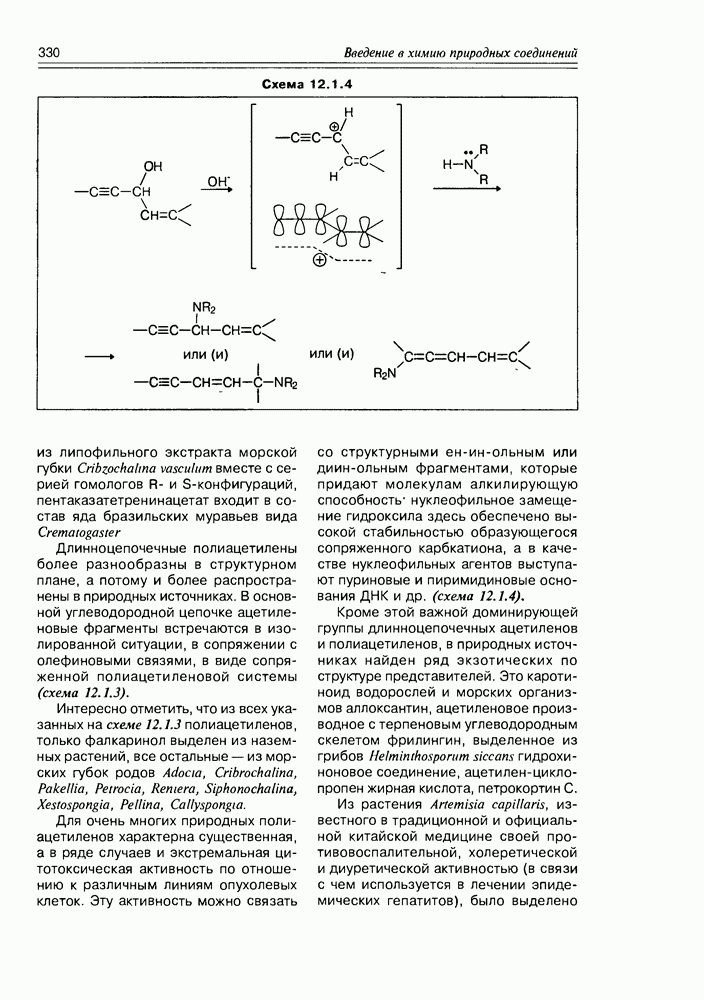
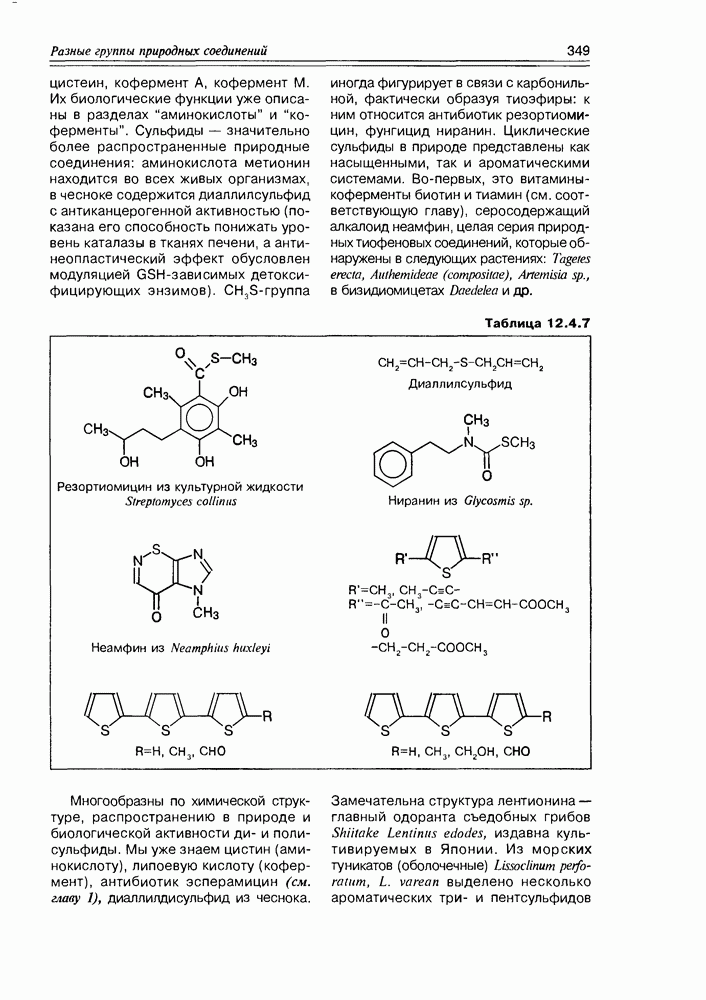
Открытие этого класса природных соединений — наверное, самого молодого класса, представляет собой захватывающую, почти детективную историю, начинается которая из медицины. Уже несколько столетий людям, проживающим в прибрежных тропических областях, было известно пищевое отравление при употреблении разнообразных рыб, обитающих в рифовых зонах. Таких рыб более 400 видов, а симптоматика отравления носит название "сигватера” (ciquatera). При поисках токсического начала этих рыб было установлено, что источником токсина являются динофлагелляты — микроорганизмы (возможно, вид планктона или одноклеточные “красные приливы”), которыми питаются рыбы, а также и многие моллюски, накапливая их в своем организме. Т.е. для рыб и моллюсков это экзогенные вещества, у диноф-лагеллят — эндогенные. Эти вещества оказались весьма устойчивыми термически (не разлагаются при кулинарной обработке) и очень токсичными ( для сигватоксина).
для сигватоксина).
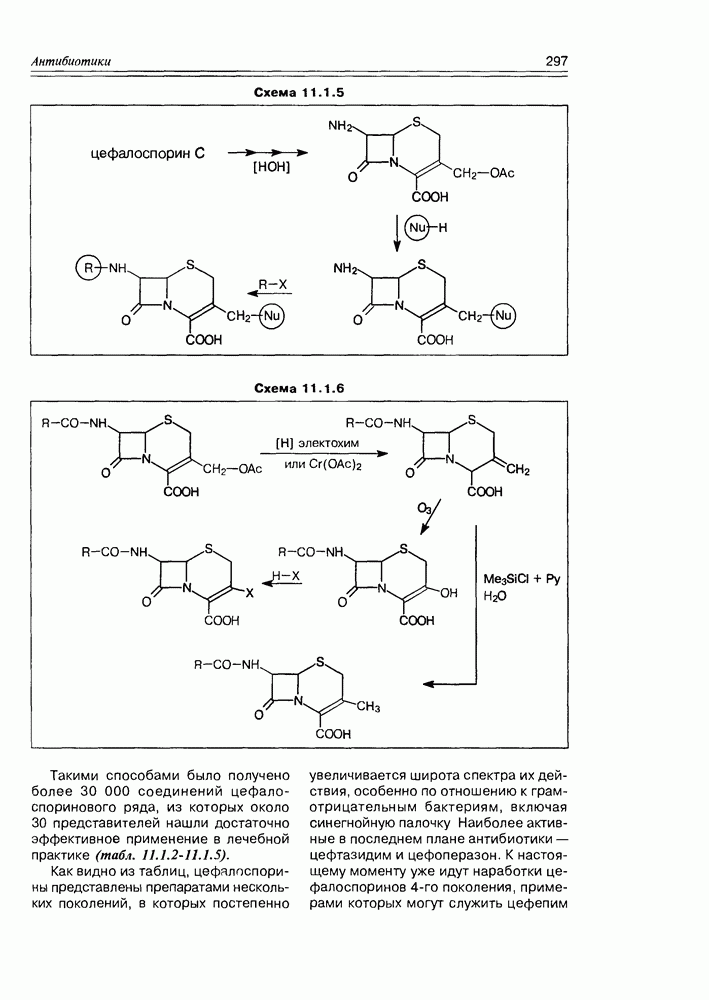
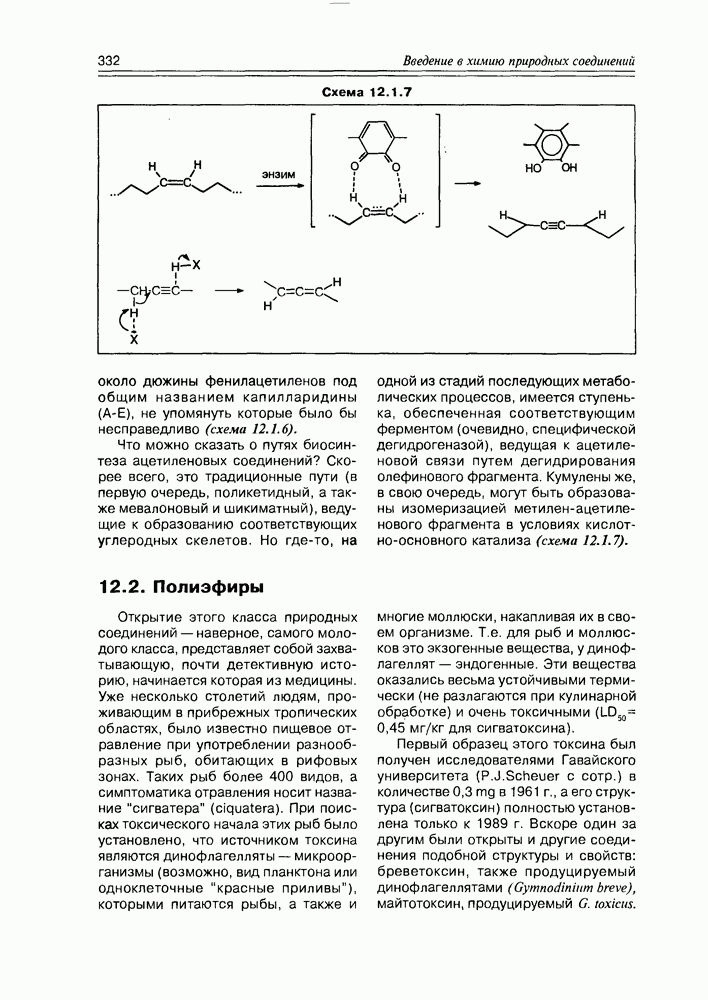
Первый образец этого токсина был получен исследователями Гавайского университета (P.J.Scheuer с сотр.) в количестве  в 1961 г., а его структура (сигватоксин) полностью установлена только к 1989 г. Вскоре один за другим были открыты и другие соединения подобной структуры и свойств: бреветоксин, также продуцируемый динофлагеллятами (Gymnodinium breve), майтотоксин, продуцируемый G. toxicus.
в 1961 г., а его структура (сигватоксин) полностью установлена только к 1989 г. Вскоре один за другим были открыты и другие соединения подобной структуры и свойств: бреветоксин, также продуцируемый динофлагеллятами (Gymnodinium breve), майтотоксин, продуцируемый G. toxicus.
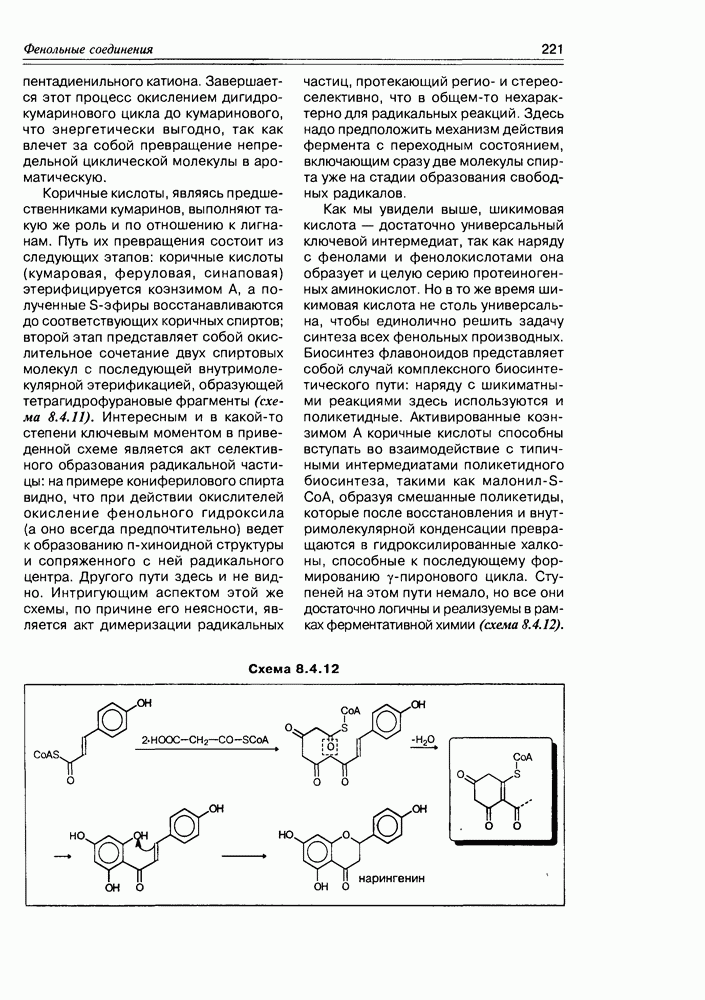
Схема 12.2.1
(см. скан)
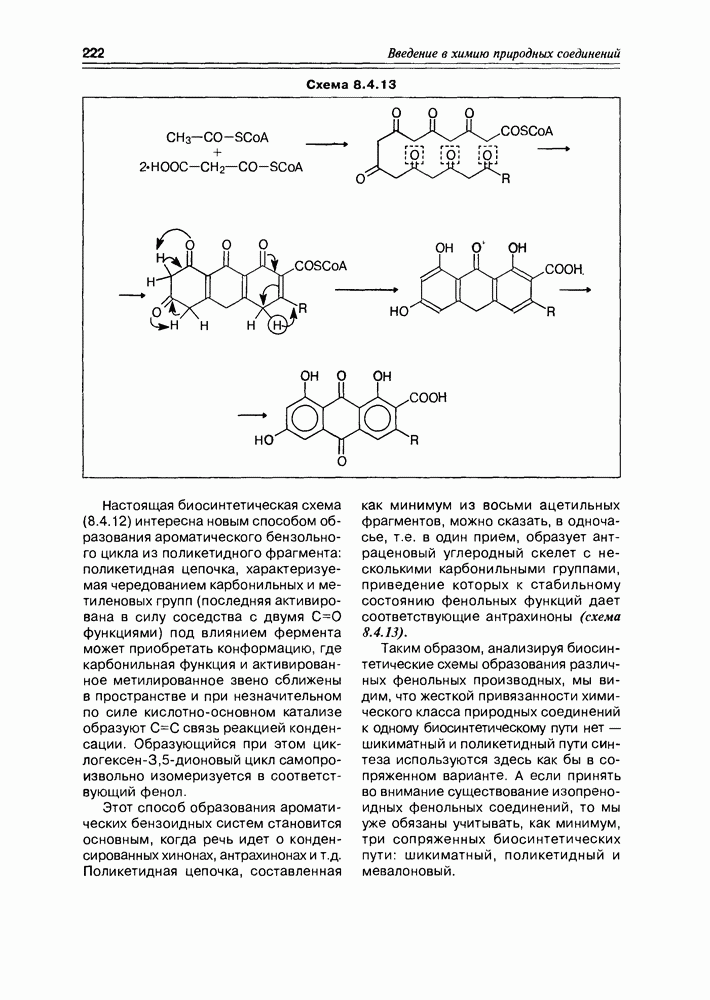
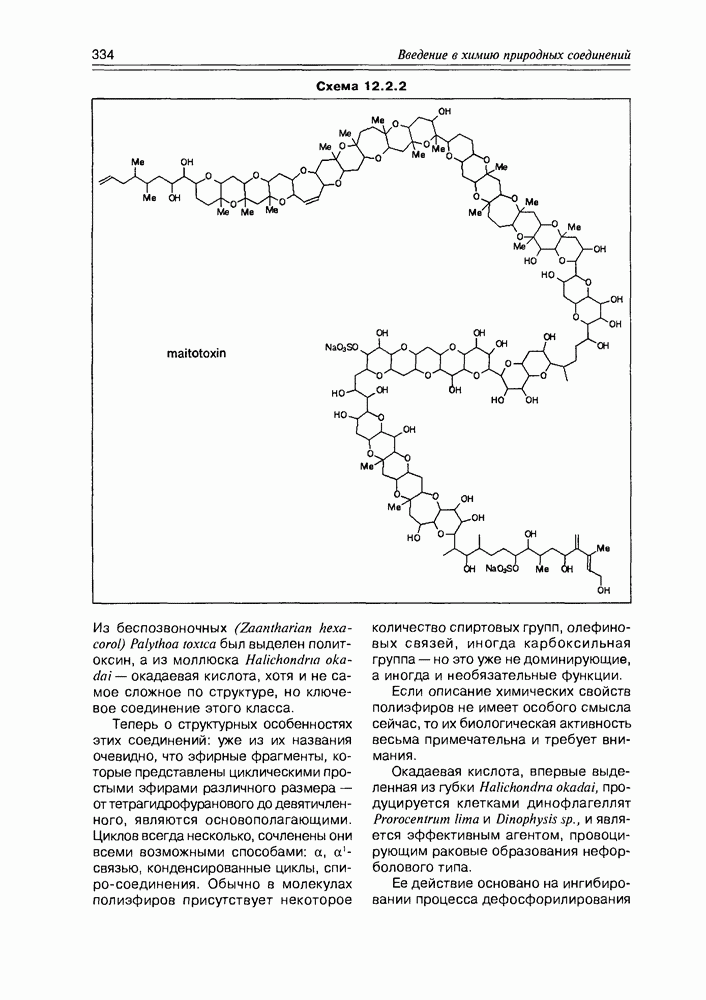
Схема 12.2.2

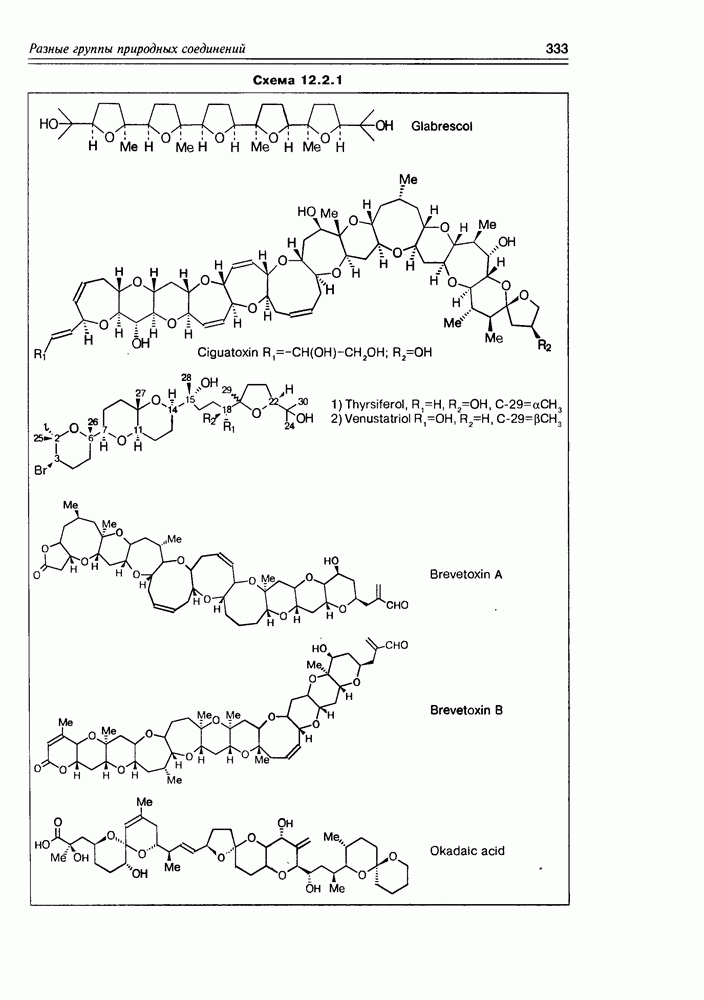
Из беспозвоночных (Zaantharian hexa-corol) Palythoa toxica был выделен политоксин, а из моллюска Halichondria ока-dai - окадаевая кислота, хотя и не самое сложное по структуре, но ключевое соединение этого класса.
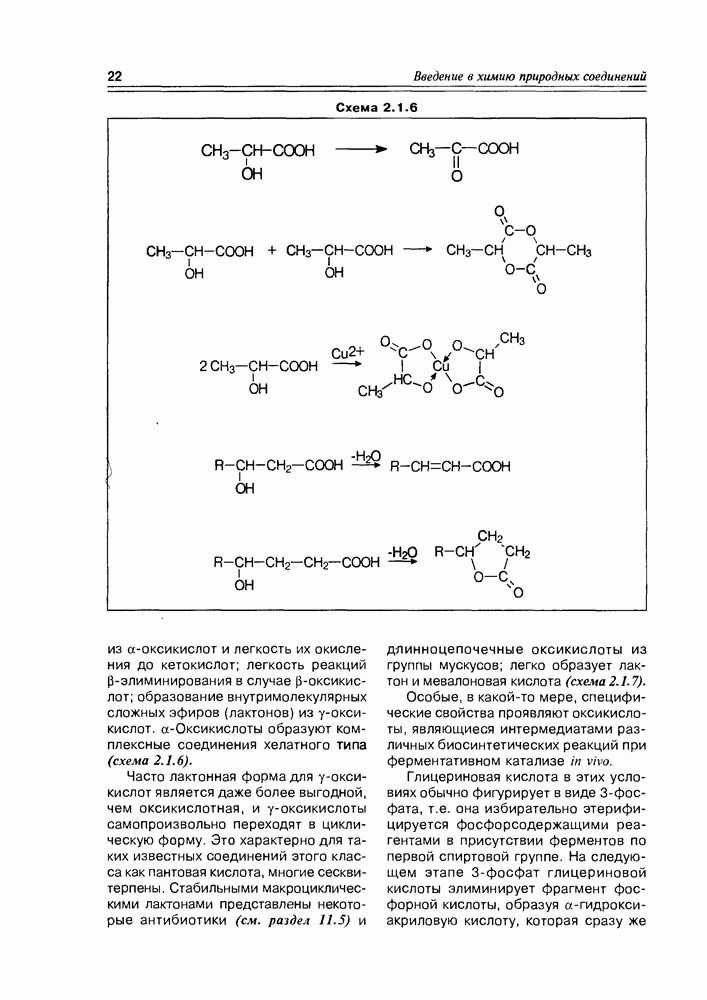
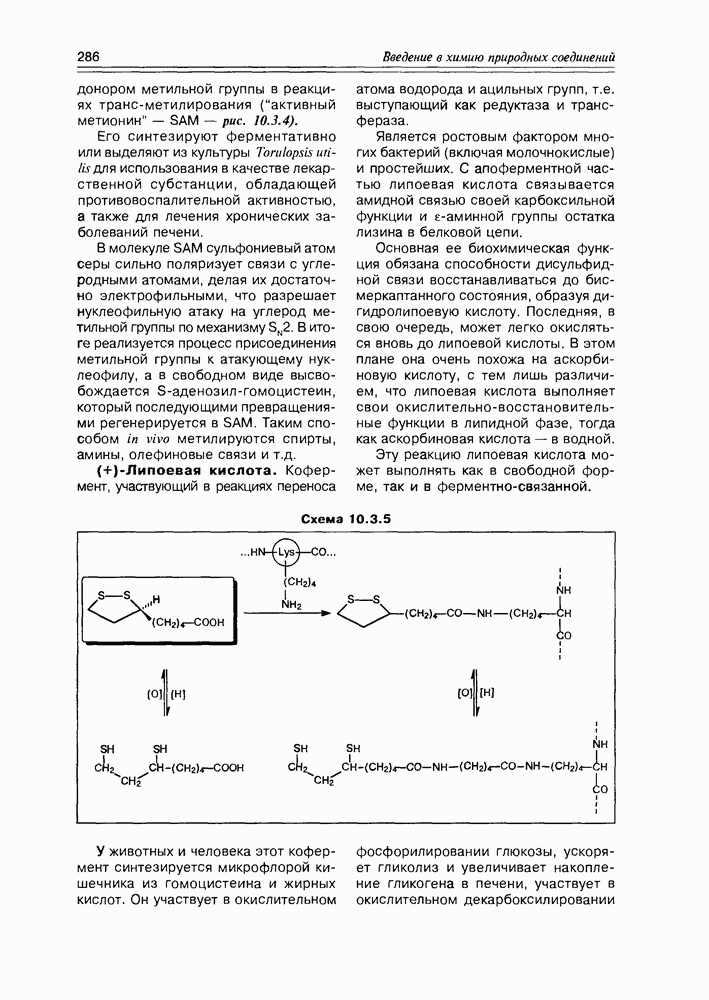
Теперь о структурных особенностях этих соединений: уже из их названия очевидно, что эфирные фрагменты, которые представлены циклическими простыми эфирами различного размера — оттетрагидрофуранового до девятичленного, являются основополагающими. Циклов всегда несколько, сочленены они всеми возможными способами:  -связью, конденсированные циклы, спиросоединения. Обычно в молекулах полиэфиров присутствует некоторое количество спиртовых групп, олефиновых связей, иногда карбоксильная группа — но это уже не доминирующие, а иногда и необязательные функции.
-связью, конденсированные циклы, спиросоединения. Обычно в молекулах полиэфиров присутствует некоторое количество спиртовых групп, олефиновых связей, иногда карбоксильная группа — но это уже не доминирующие, а иногда и необязательные функции.
Если описание химических свойств полиэфиров не имеет особого смысла сейчас, то их биологическая активность весьма примечательна и требует внимания.
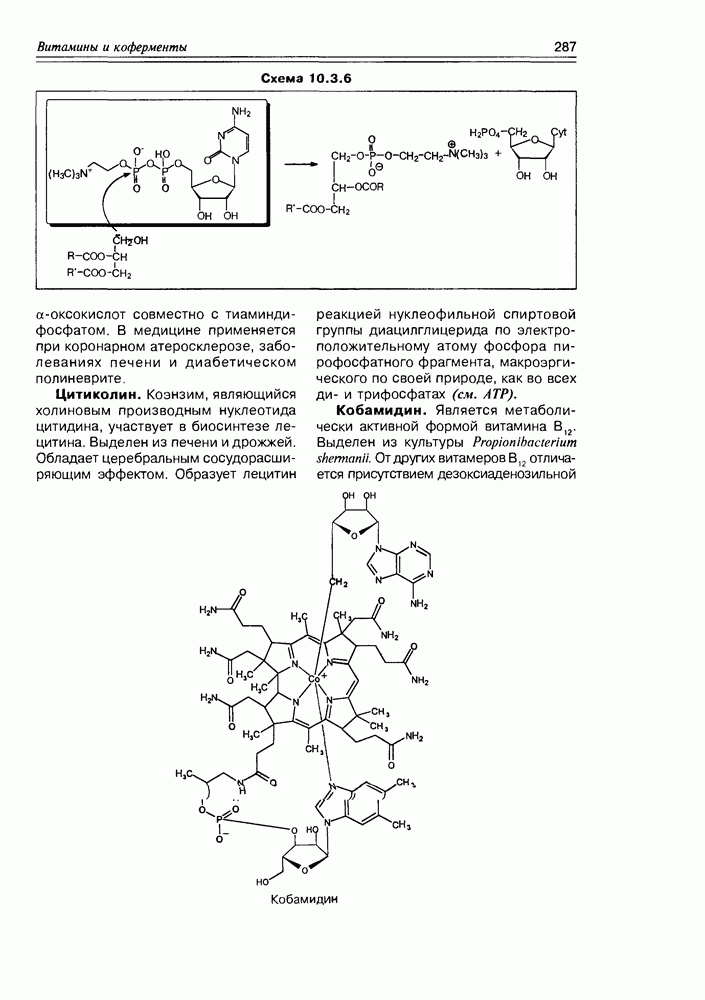
Окадаевая кислота, впервые выделенная из губки Halichondria okadai, продуцируется клетками динофлагеллят Prorocentrum lima и Dinophysis sp., и является эффективным агентом, провоцирующим раковые образования нефорболового типа.
Ее действие основано на ингибировании процесса дефосфорилирования
Схема 12.2.3

протеинов (преимущественно, серии треонин-остатков), поэтому она используется в качестве мощного теста при исследовании механизма действия фосфатазы 1 и 2а и клеточной регуляции.
Фармакологические исследования бреветоксинов и сигватоксина показали, что первичный “сайт" их действия (в общем-то, высокотоксического) есть натриевый канал (voltage-sensitive sodium cell, VSSC).
Следует отметить, что практически все полиэфиры являются ионофорами, а значит, механизм их действия на том или ином этапе связан с ионным транспортом.
Многие из полиэфиров проявляют высокую цитотоксичность: спонгипираны (например, спингостатин 1-9) — экстраординарно мощные противоопухолевые субстанции.
Майтотоксин (maitotoxin) — один из наиболее замечательных полиэфиров, — его можно назвать рекордсменом по размеру молекулы среди неполимерных веществ установленной структуры, а также рекордсменом по токсичности ( мыши) среди непротеинных токсинов.
мыши) среди непротеинных токсинов.
Молекулярные свойства, обеспечивающие высокую биологическую активность полиэфиров (морских полиэфиров) имеют химическую и физико-химическую природу: циклополиэфирные фрагменты придают веществам бифильность. Они достаточно липофильны и гидрофильны, последнее свойство возрастает с увеличением количества спиртовых функций, большое количество метильных групп увеличивает липофильность. Таким образом, эти вещества обладают высокой клеточной проникаемостью, а также комплексующей способностью по отношению к щелочным и щелочноземельным катионам. Обращает на себя внимание почти обязательное присутствие спиро-сочлененных циклоэфирных фрагментов — фактически, спиро-кетальных функций, способных к взаимодействию с нуклеофильными реагентами (схема 12.2.3).
Кроме того, высокая способность к образованию водородных связей, наряду с достаточно протяженной циклополиэфирной цепочкой, открывает возможность блокировать некоторые хорошо комплементирующие участки белковых молекул и молекул нуклеиновых кислот.
Учитывая экстранеординарную биологическую активность полиэфиров, основанную на глубоком вмешательстве во внутриклеточные процессы, многие исследователи высоко оценивают будущее этого класса биологически активных веществ, считая, что они могут стать основой нового поколения лекарственных субстанций, как в свое время стали таковыми алкалоиды, а потом стероиды.
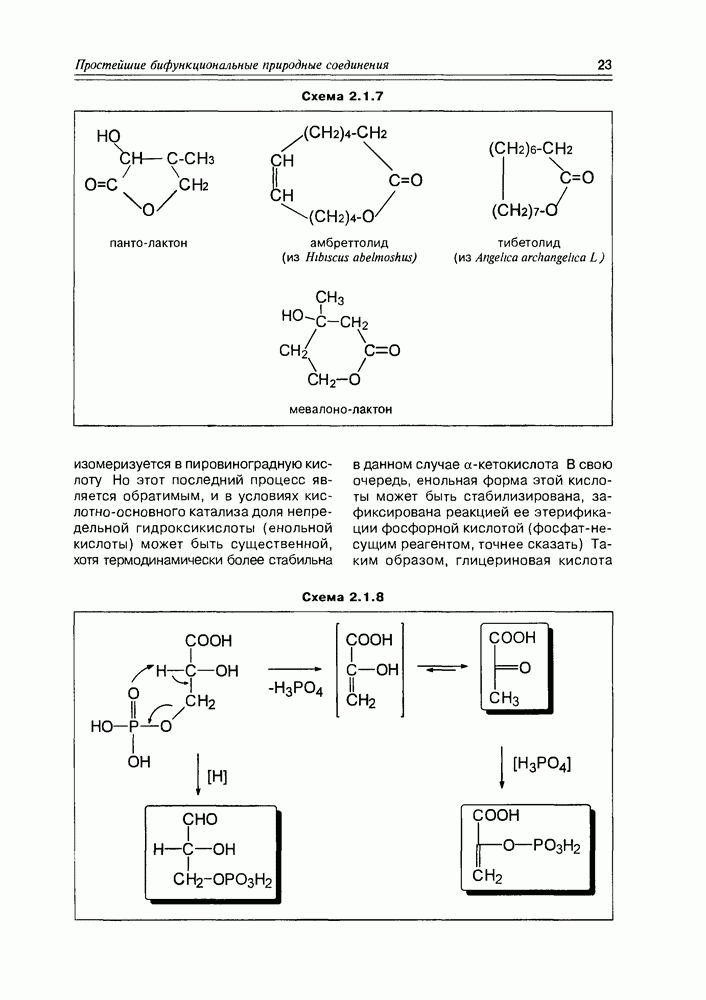
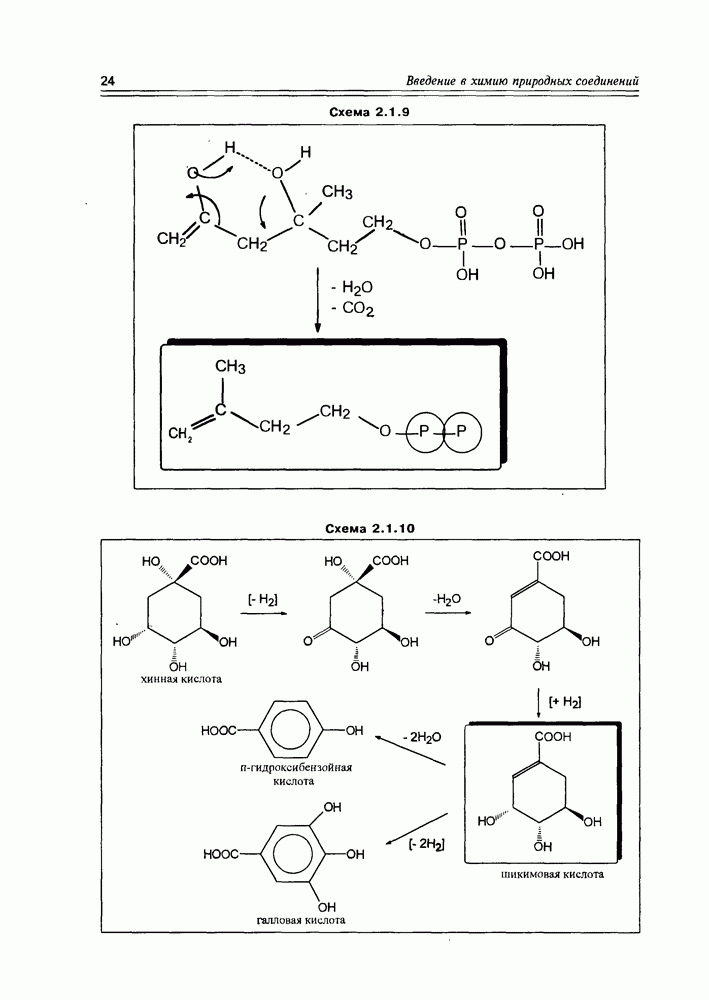
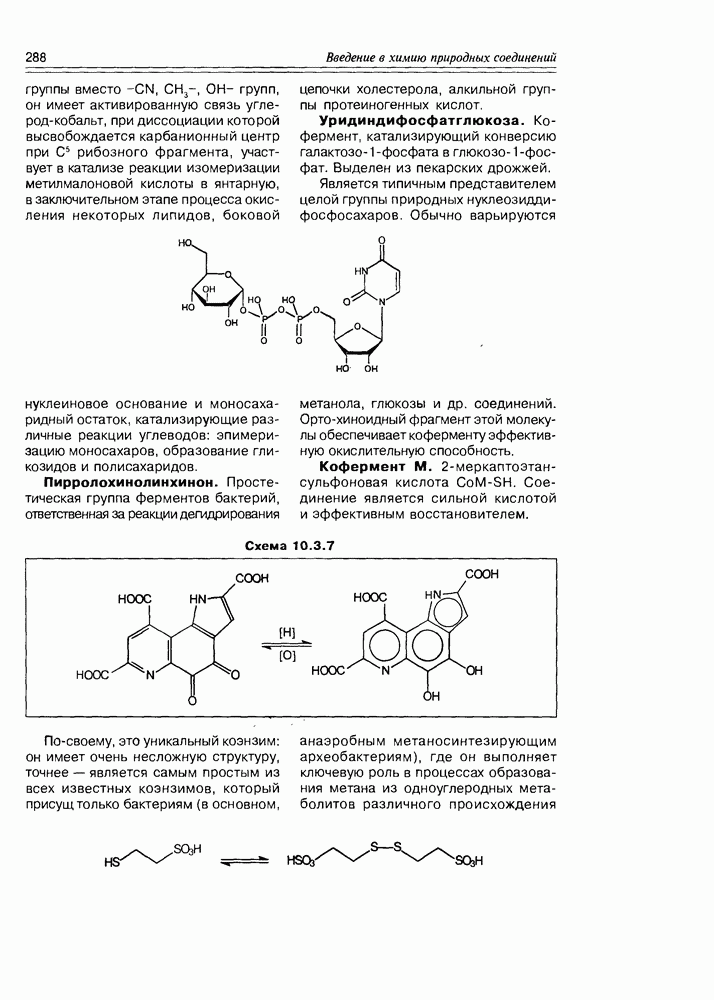
Относительно биосинтетического происхождения полиэфиров пока можно констатировать только то, что они образуются реакциями циклизации высоко оксигенированных метаболитов поликетидной и изопреноидной структуры. Так, сквален может быть полностью гидроксилирован по всем своим двойным связям, образуя молекулу многоатомного спирта, внутри которой
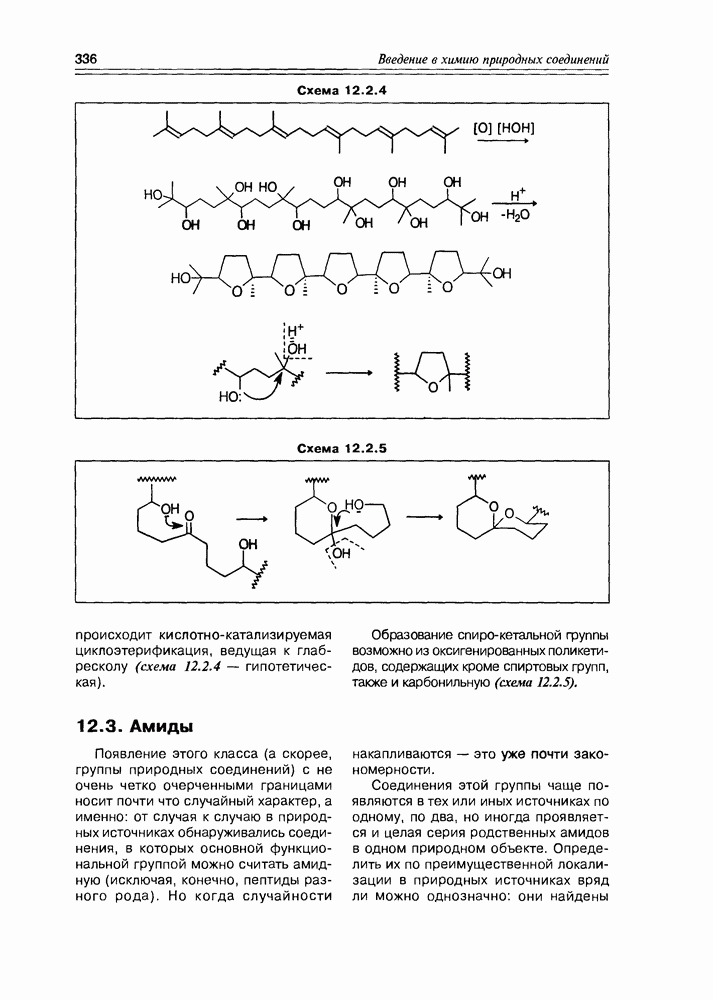
Схема 12.2.4

Схема 12.2.5

происходит кислотно-катализируемая циклоэтерификация, ведущая к глабресколу (схема 12.2.4 — гипотетическая).
Образование спирокетальной группы возможно из оксигенированных поликетидов, содержащих кроме спиртовых групп, также и карбонильную (схема 12.2.5).
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ АВТОРА
- Глава 1. ВВЕДЕНИЕ
- 1.1. Предмет химии природных соединений
- 1.2. Классификация природных соединений
- 1.3. Методология химии природных соединений
- 1.4. Углерод и жизнь
- Глава 2. ПРОСТЕЙШИЕ БИФУНКЦИОНАЛЬНЫЕ ПРИРОДНЫЕ СОЕДИНЕНИЯ — МОСТИК К МАССИВУ ПРИРОДНЫХ СОЕДИНЕНИЙ
- 2.2. Оксокислоты
- 2.3. Аминоспирты
- Глава 3. УГЛЕВОДЫ
- 3.2. Свойства и структура моносахаридов
- 3.3. Химические свойства моносахаридов
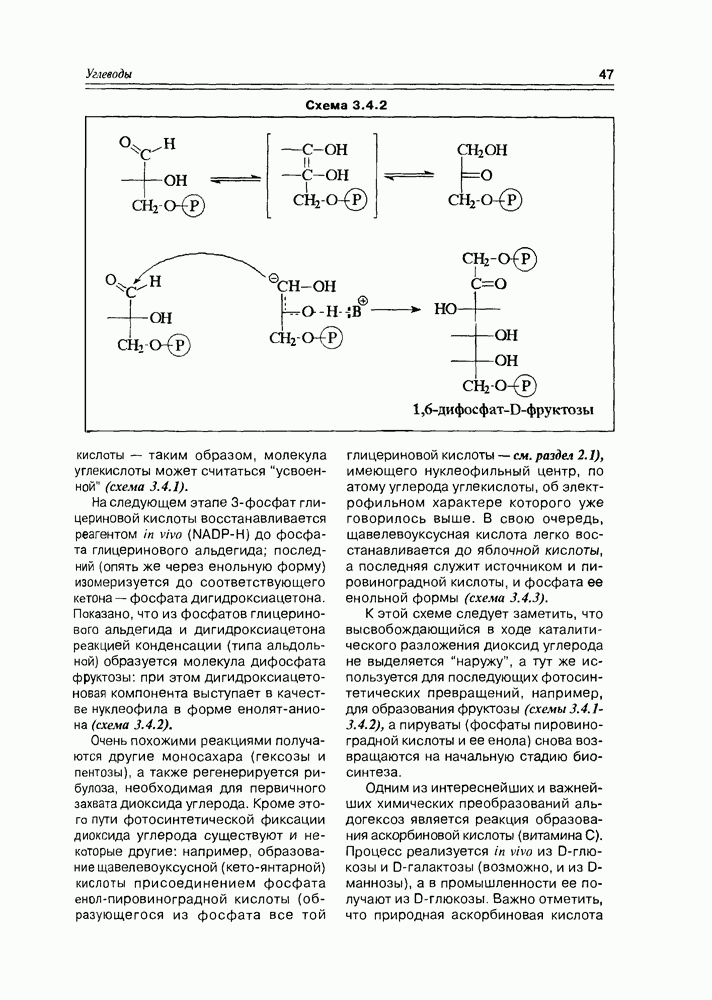
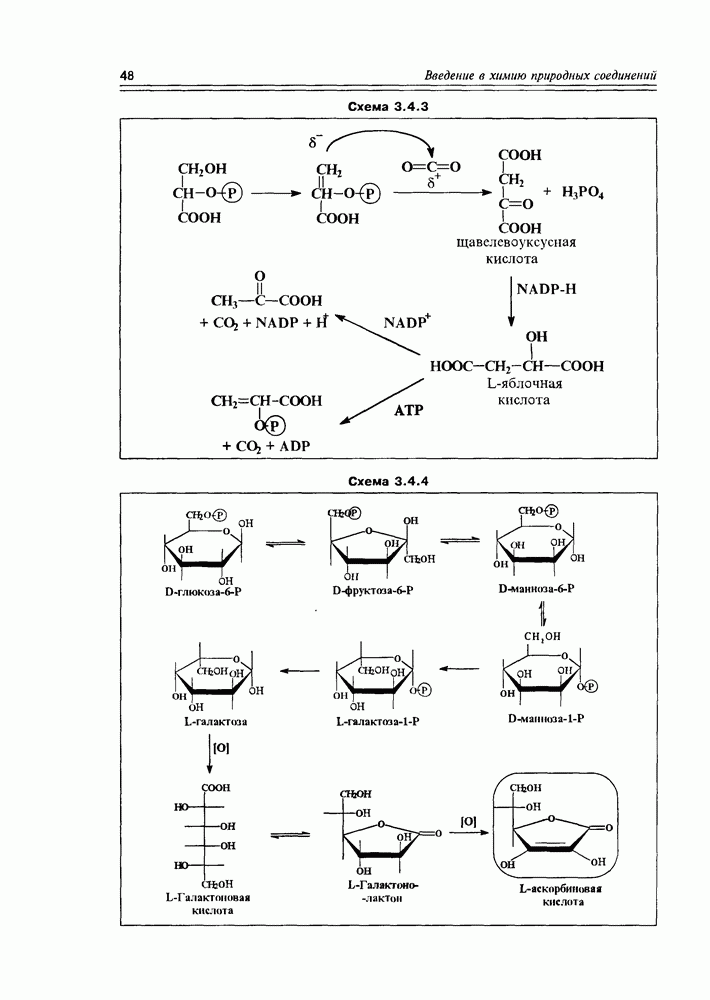
- 3.4. Биосинтетические реакции углеводов
- 3.6. Гликозиды
- Глава 4. АМИНОКИСЛОТЫ, ПЕПТИДЫ, БЕЛКИ
- 4.2. Химические свойства а-аминокислот
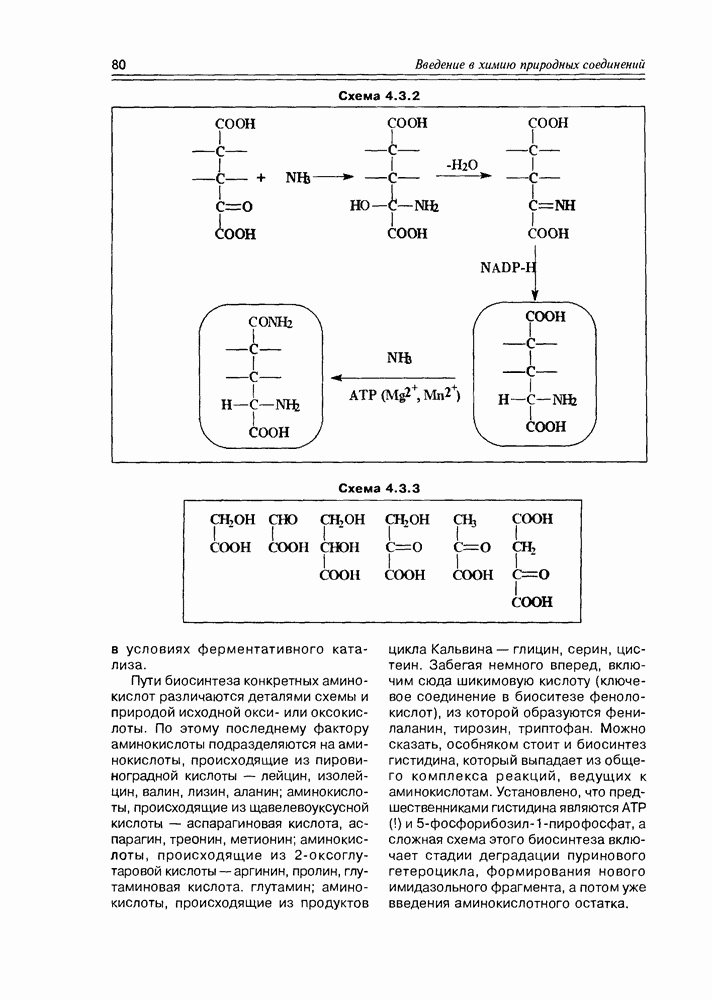
- 4.3. Биосинтез аминокислот
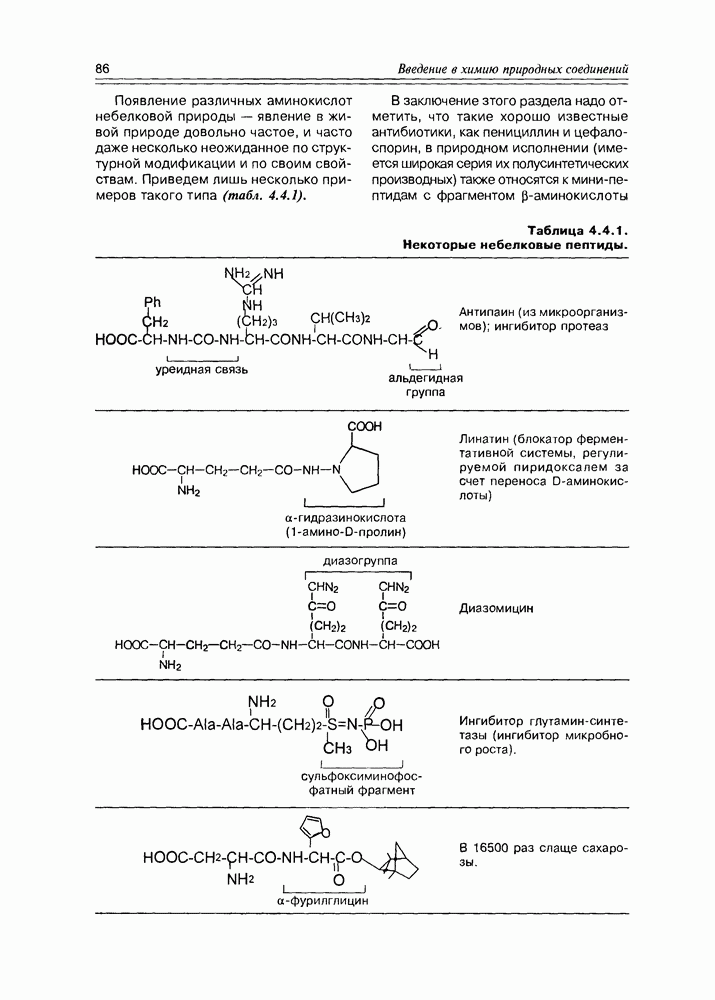
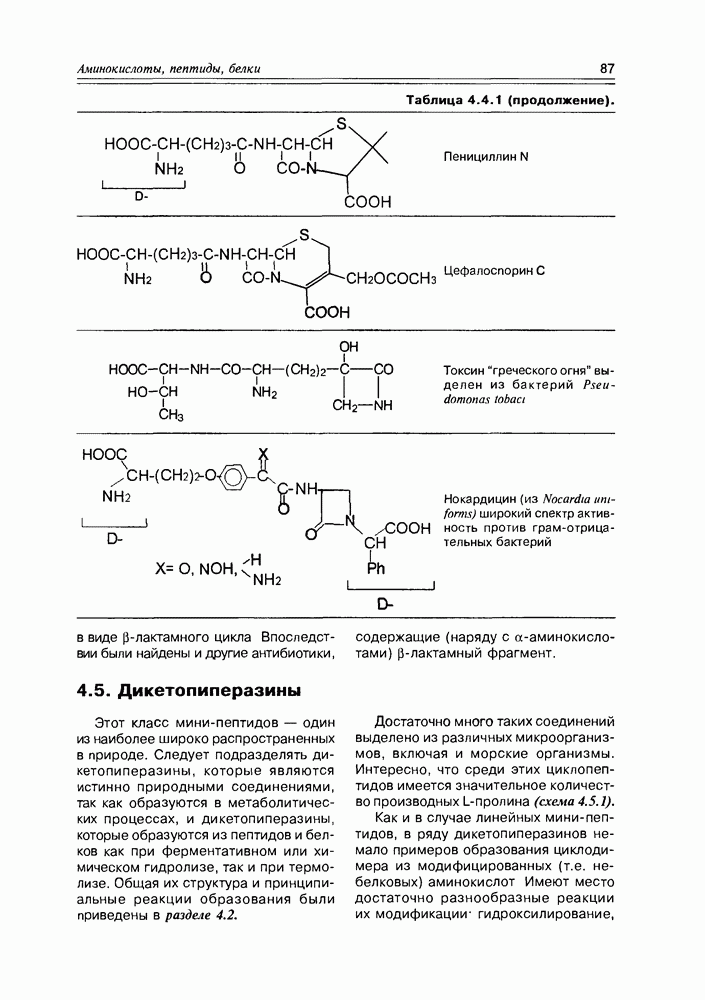
- 4.4. Полипептиды
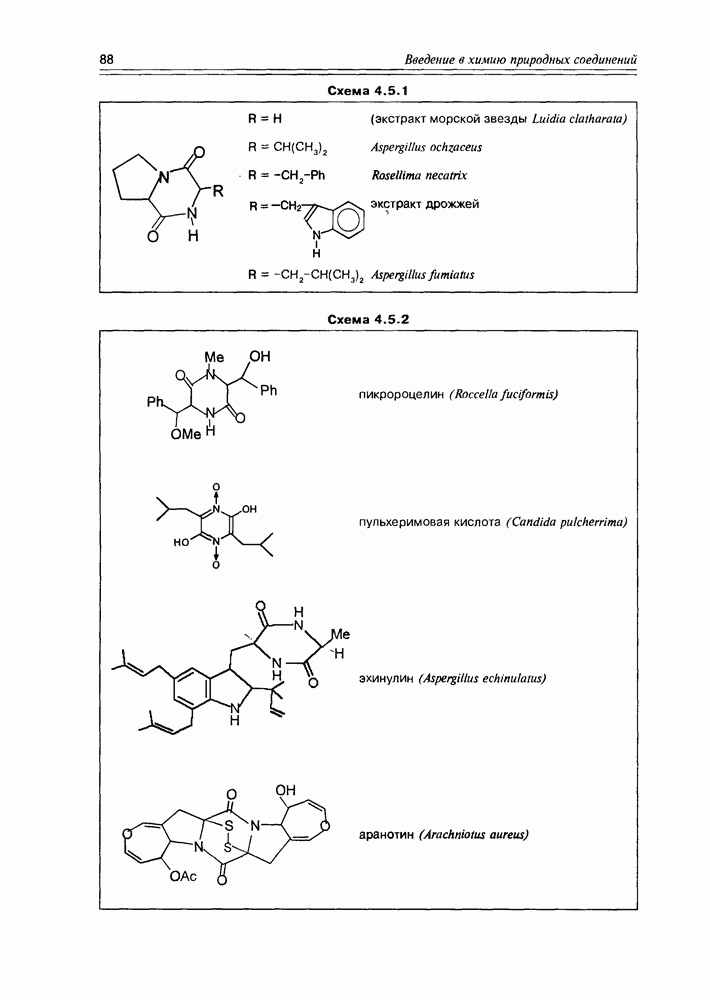
- 4.5. Дикетопиперазины
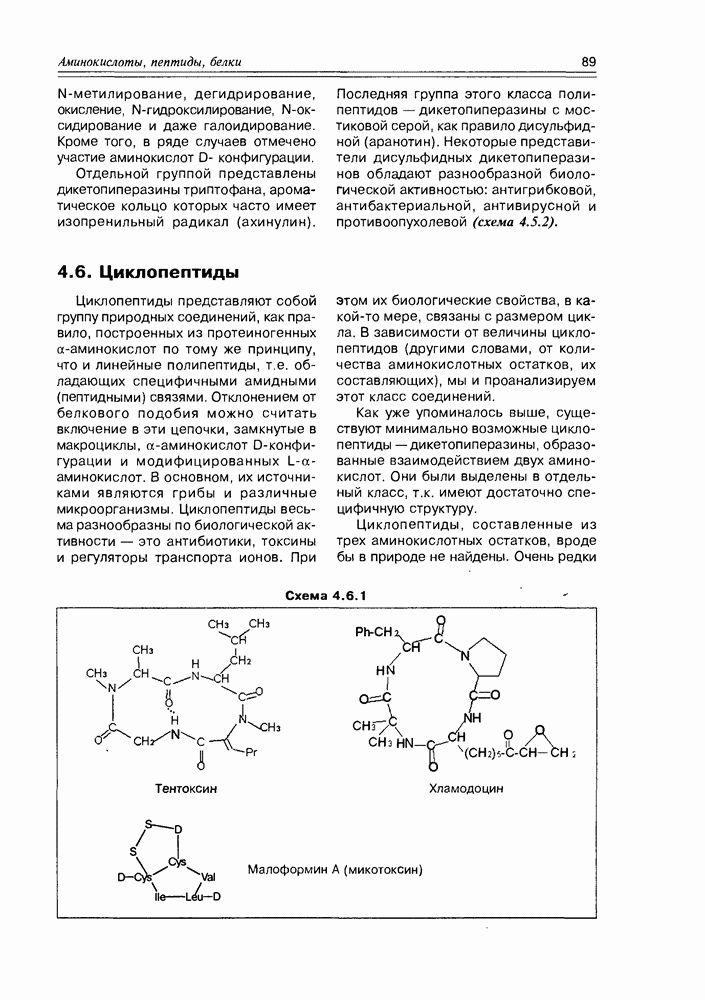
- 4.6. Циклопептиды
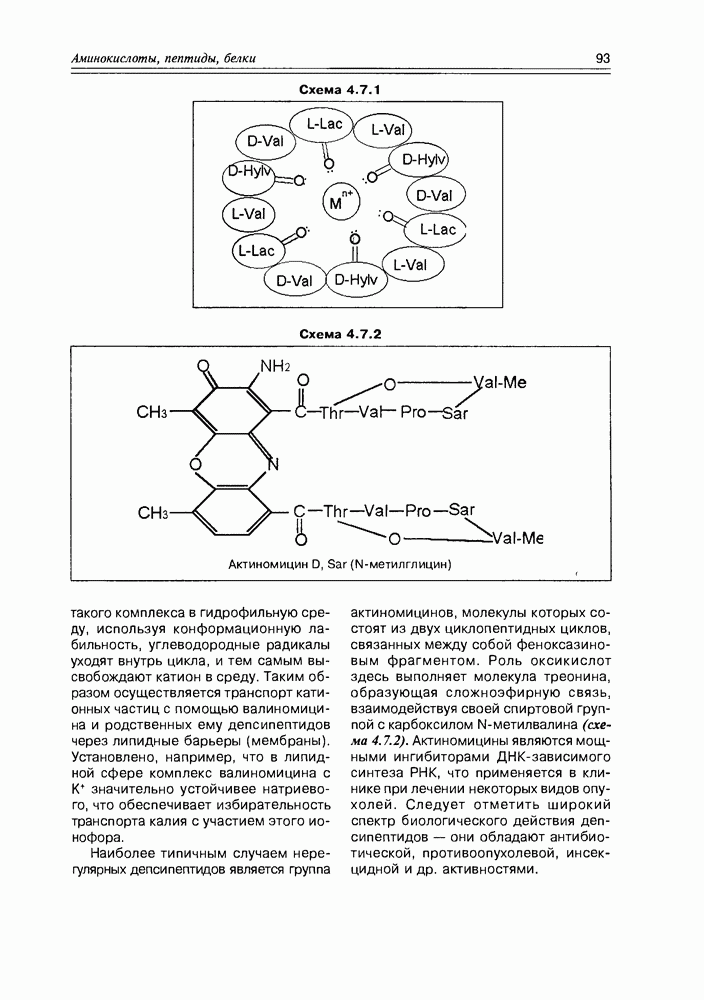
- 4.7. Депсипептиды
- 4.8. Белки
- Глава 5. ЛИПИДЫ: ЖИРНЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
- 5.1.1. Химические свойства жирных кислот
- 5.2. Метаболиты жирных кислот
- 5.2.2. Карбоциклические оксилипины
- 5.3. Жиры и жироподобные производные жирных кислот
- 5.4. Биосинтез жирных кислот и их производных
- Глава 6. ИЗОПРЕНОИДЫ-1
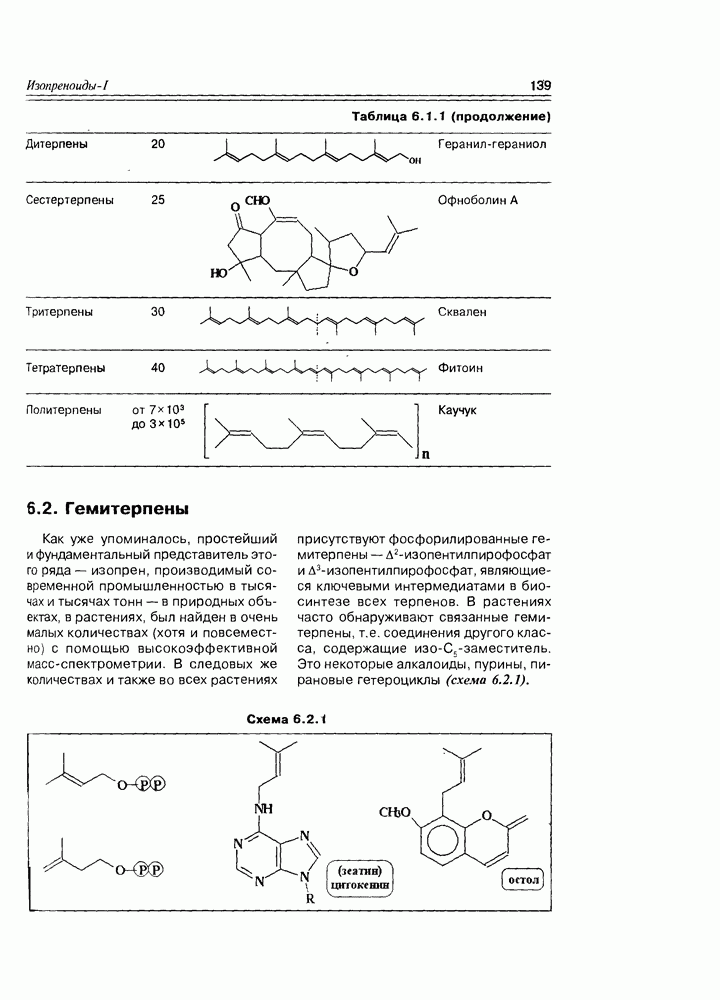
- 6.2. Гемитерпены
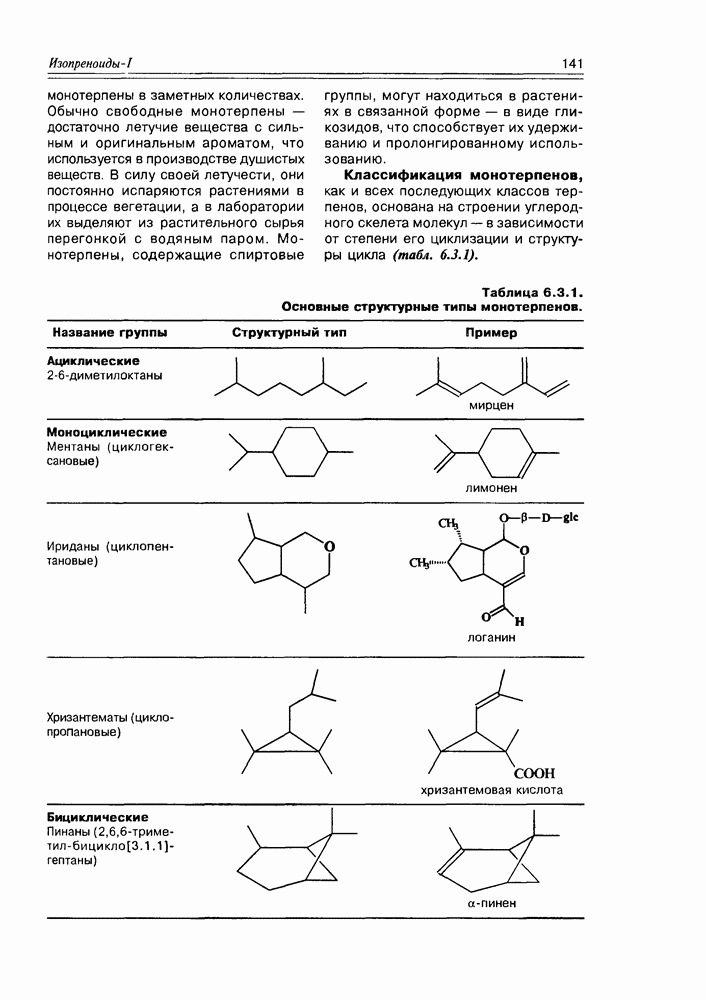
- 6.3. Монотерпены
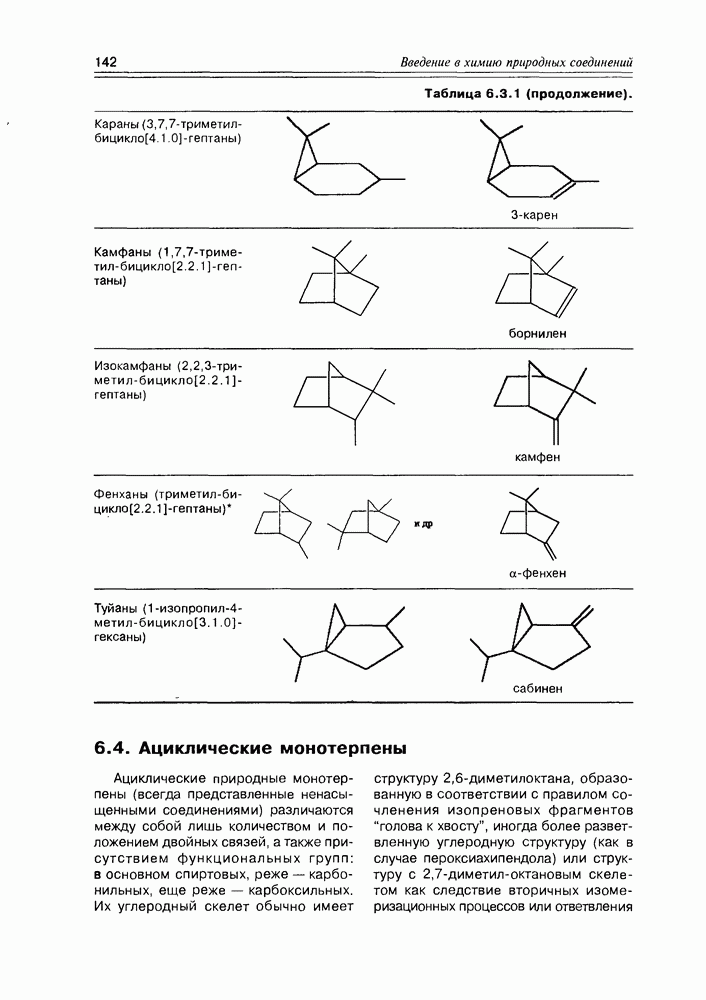
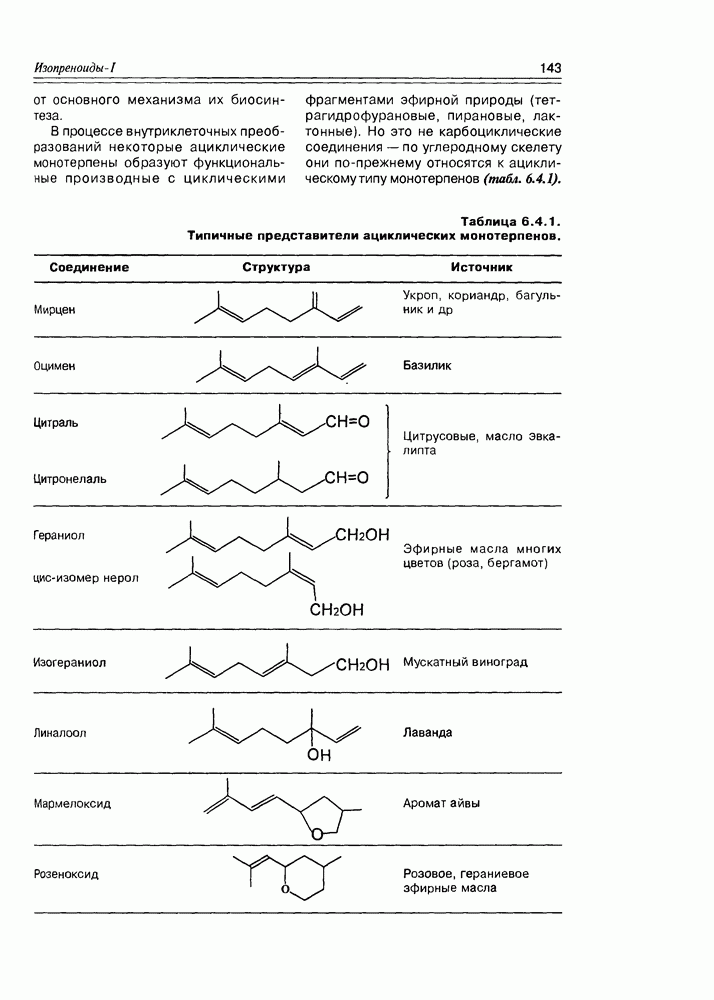
- 6.4. Ациклические монотерпены
- 6.5. Моноциклические терпены
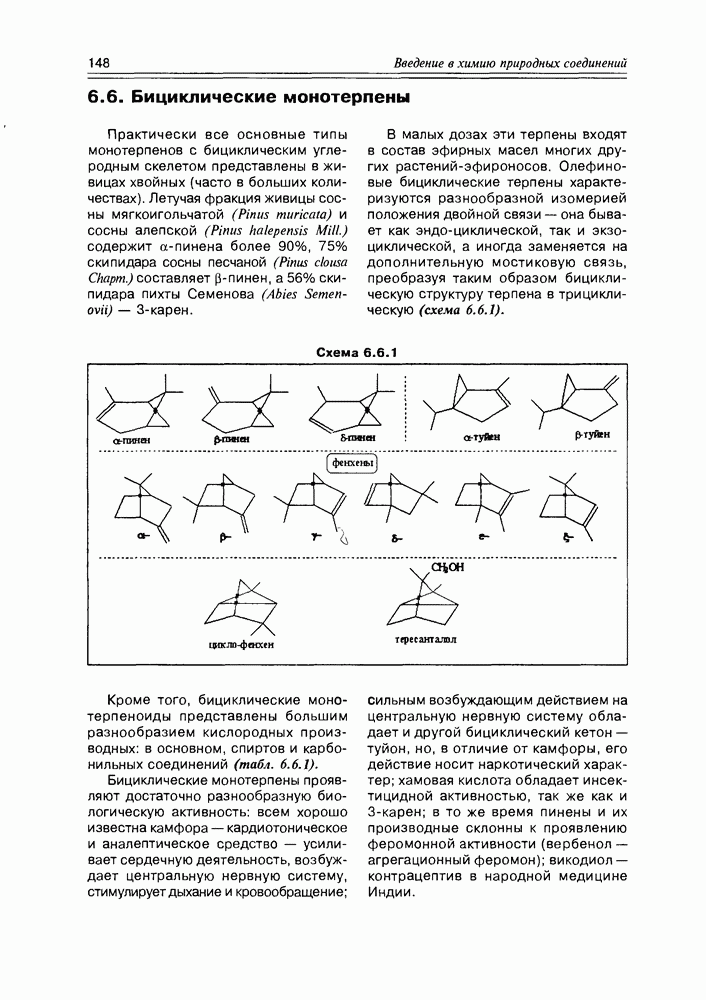
- 6.6. Бициклические монотерпены
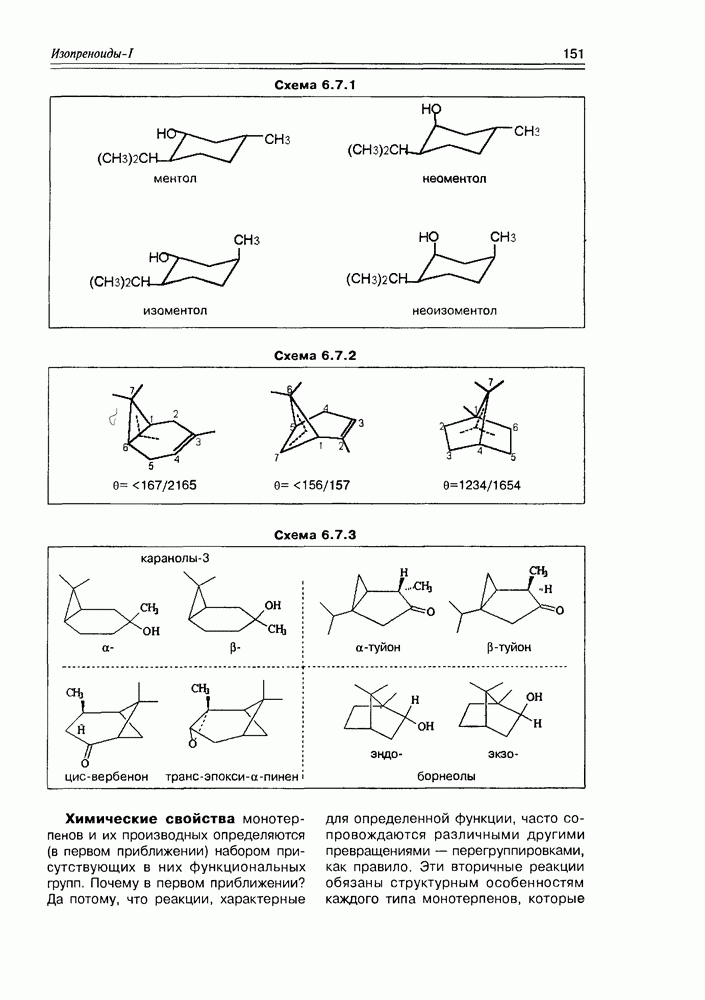
- 6.7. Строение и свойства монотерпенов
- 6.8. Биосинтез изопреноидов
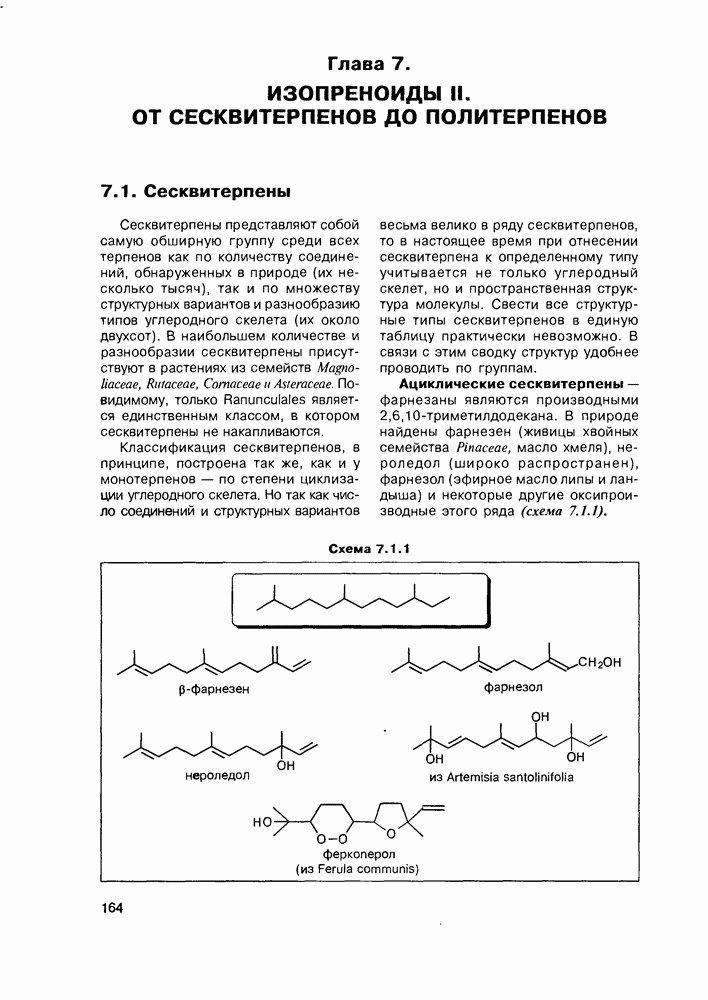
- Глава 7. ИЗОПРЕНОИДЫ II. ОТ СЕСКВИТЕРПЕНОВ ДО ПОЛИТЕРПЕНОВ
- 7.2. Химические свойства сесквитерпенов
- 7.3. Дитерпены и сестертерпены
- 7.4. Тритерпеноиды и стероиды
- 7.5. Тетратерпеноиды — каротиноиды
- Глава 8. ФЕНОЛЬНЫЕ СОЕДИНЕНИЯ
- 8.2. Пираны
- 8.4. Биосинтез фенольных соединений
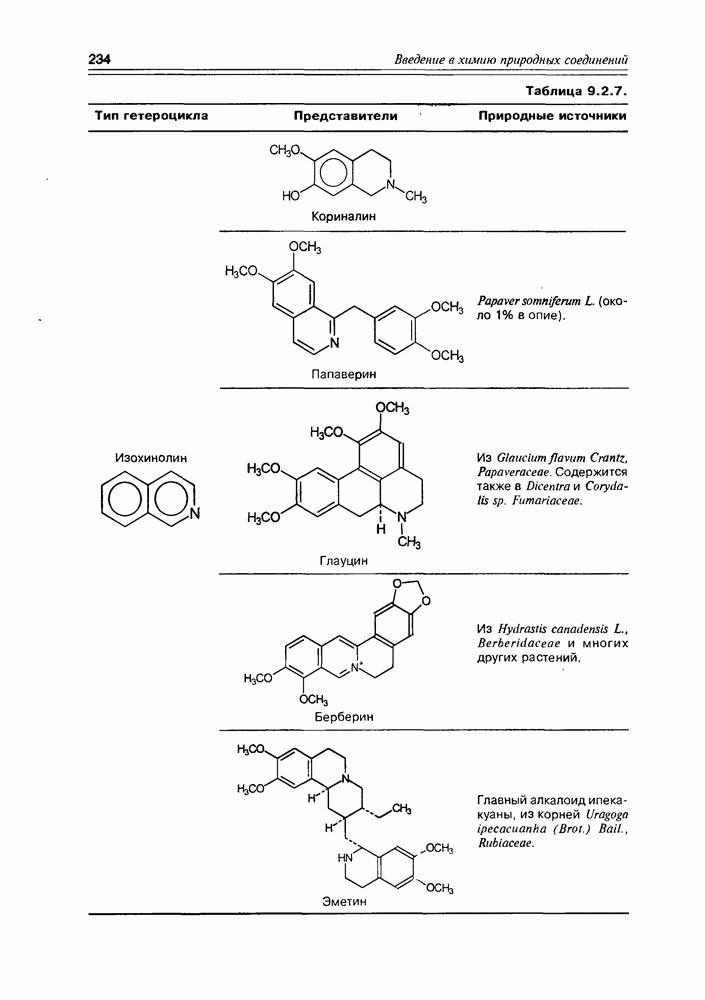
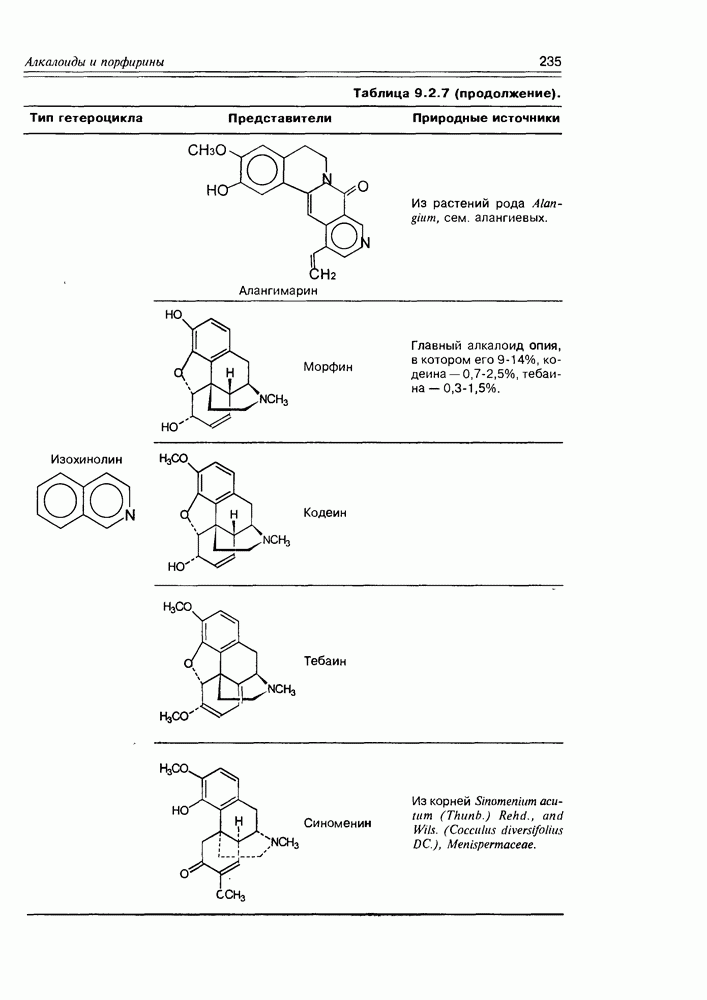
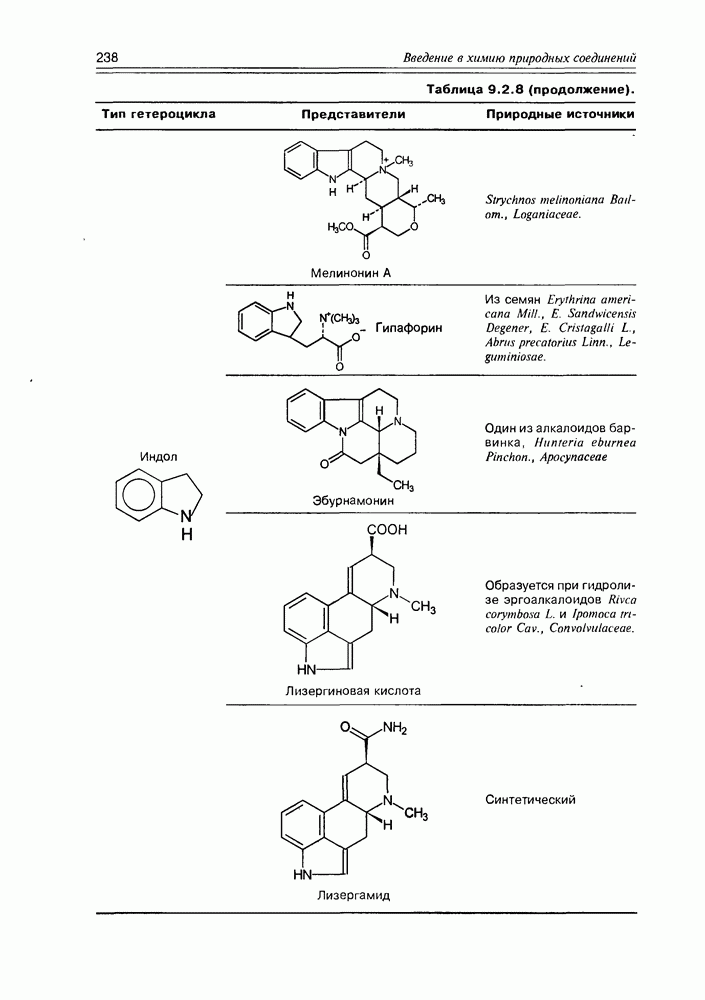
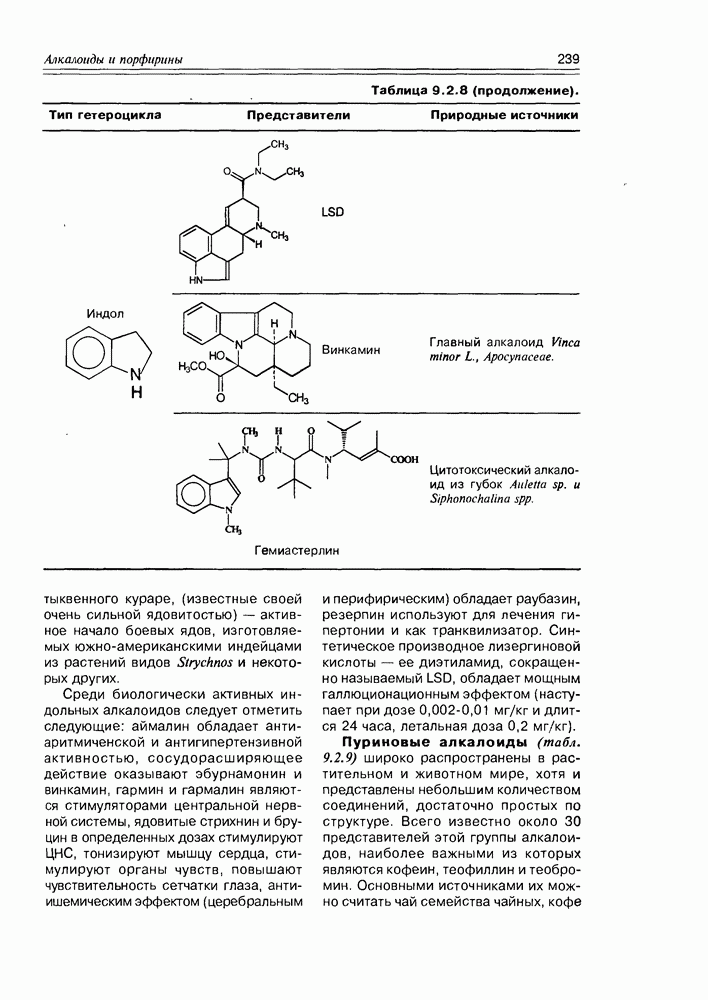
- Глава 9. АЛКАЛОИДЫ И ПОРФИРИНЫ
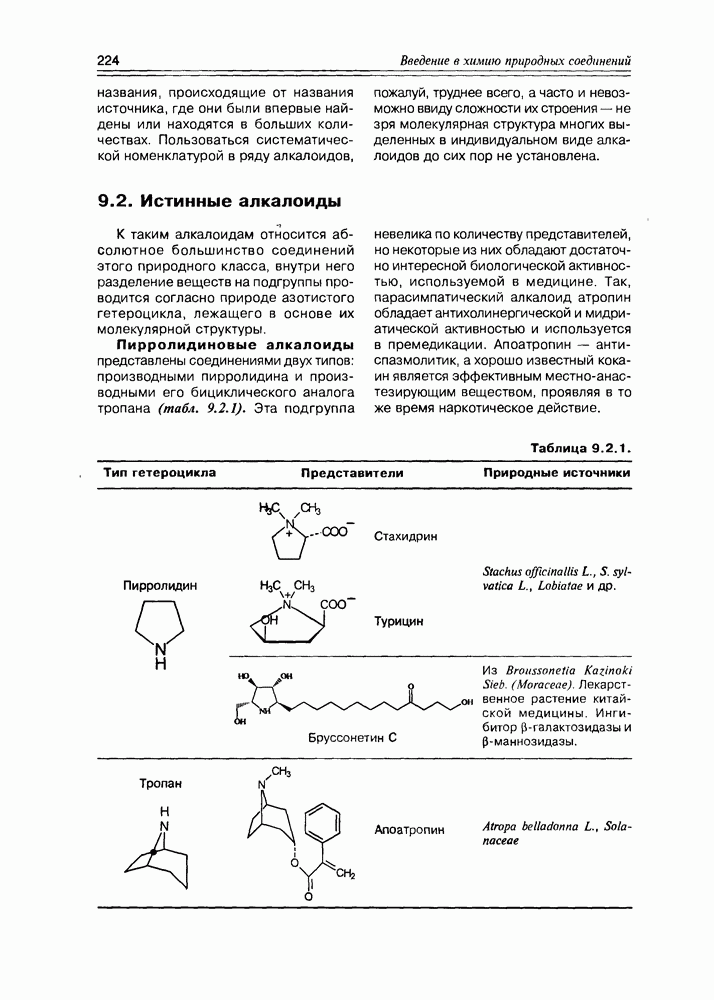
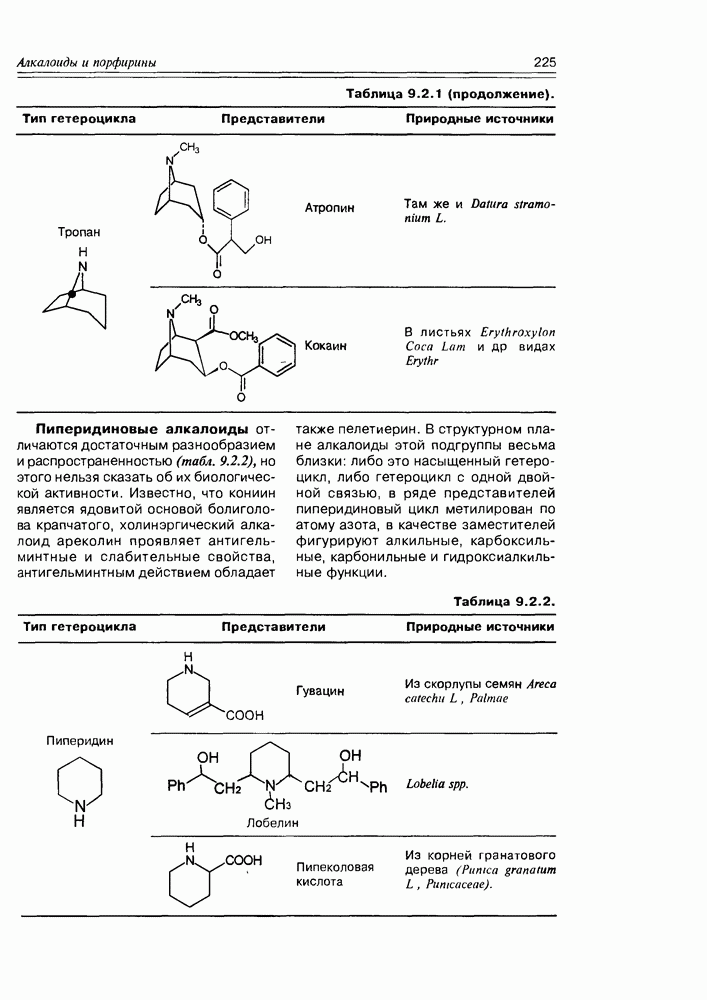
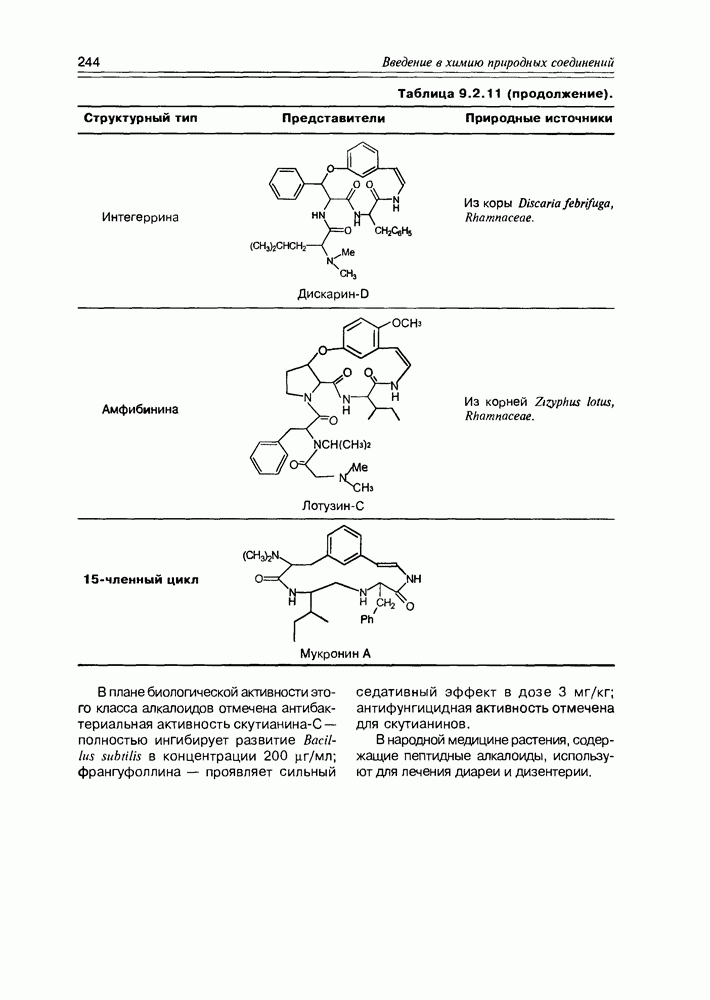
- 9.2. Истинные алкалоиды
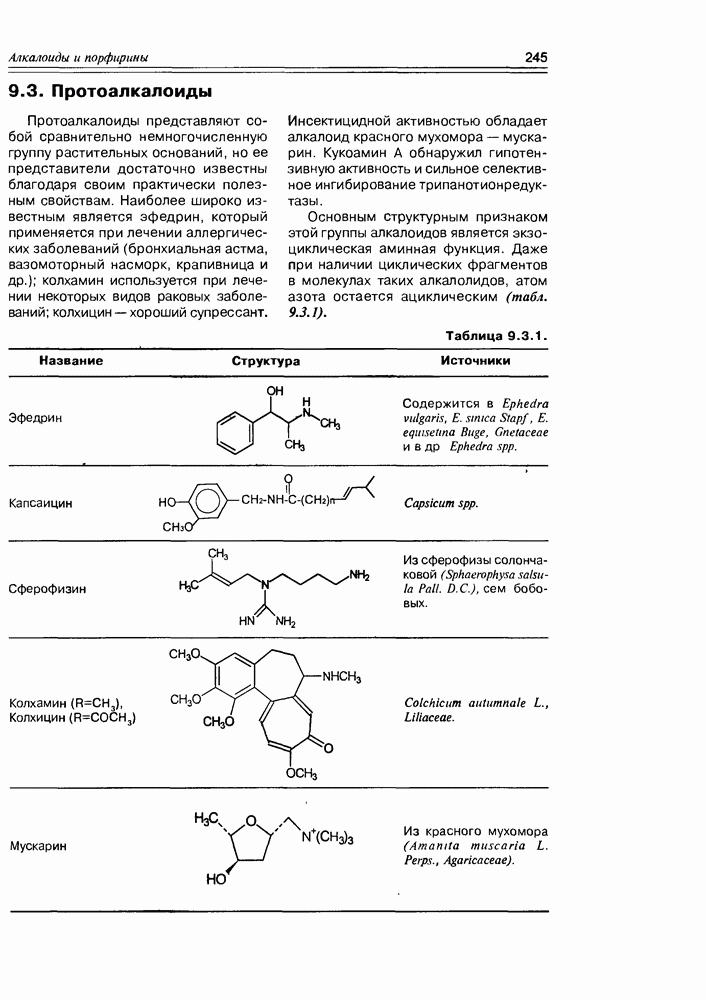
- 9.3. Протоалкалоиды
- 9.5. Химические свойства и химические модификации алкалоидов
- 9.6. Аминокислоты и биосинтез алкалоидов
- 9.7. Порфирины
- Глава 10. ВИТАМИНЫ И КОФЕРМЕНТЫ
- 10.1. Витамины — собственно
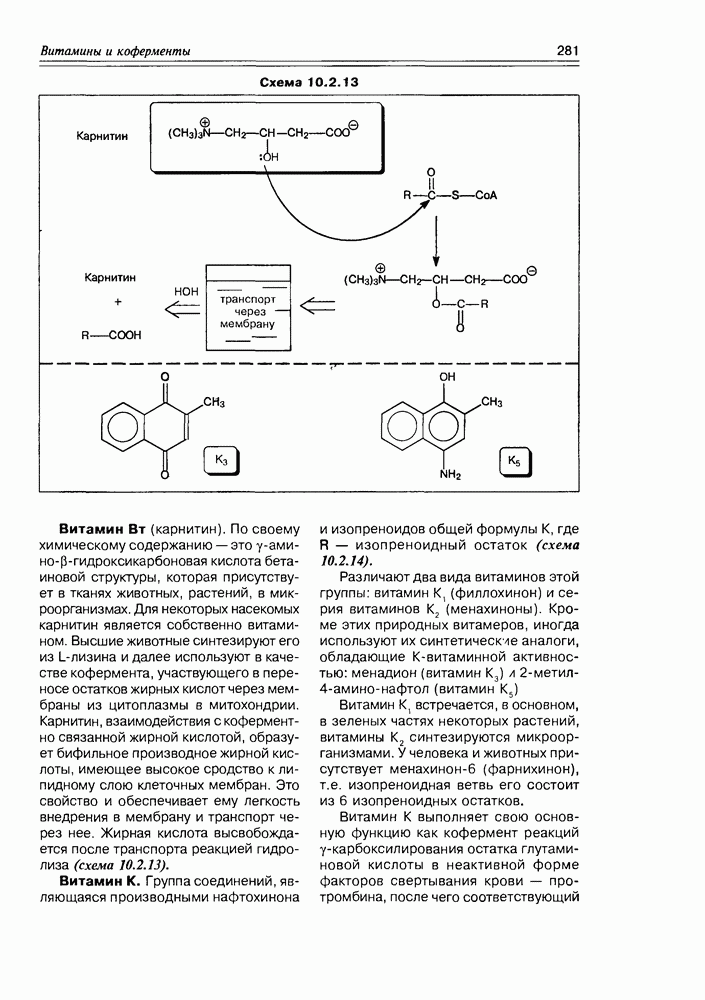
- 10.2. Витамины-коферменты
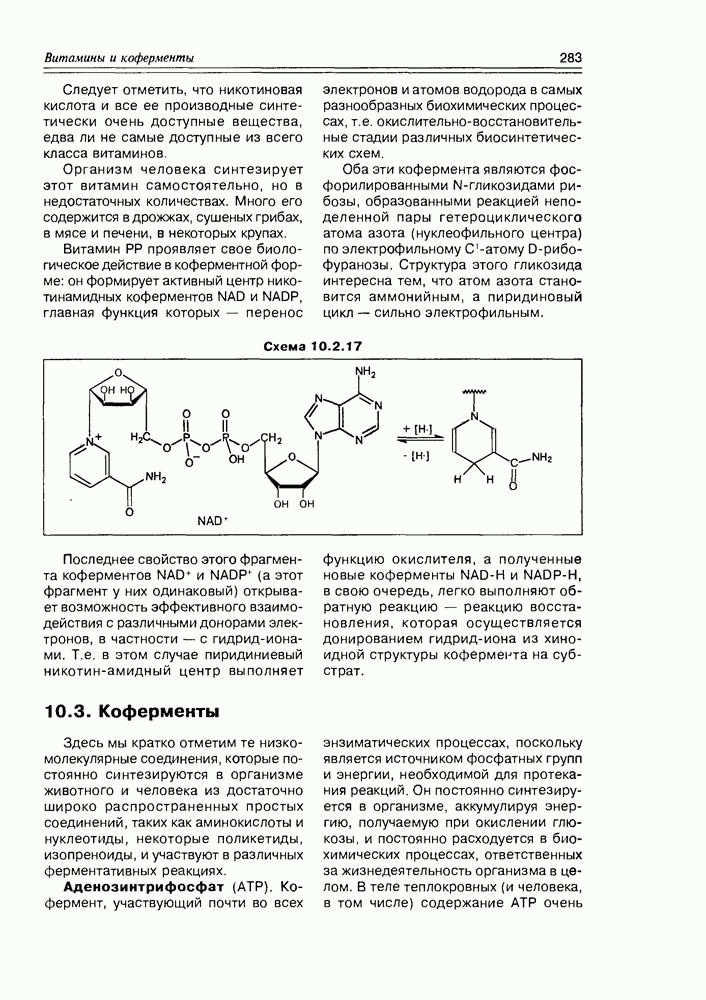
- 10.3. Коферменты
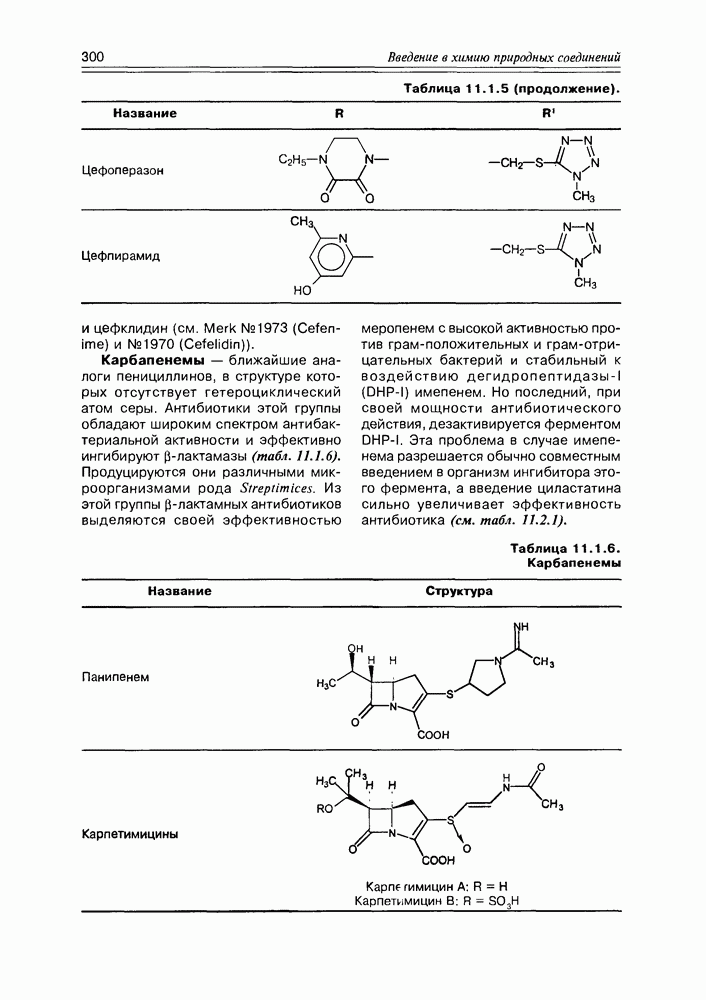
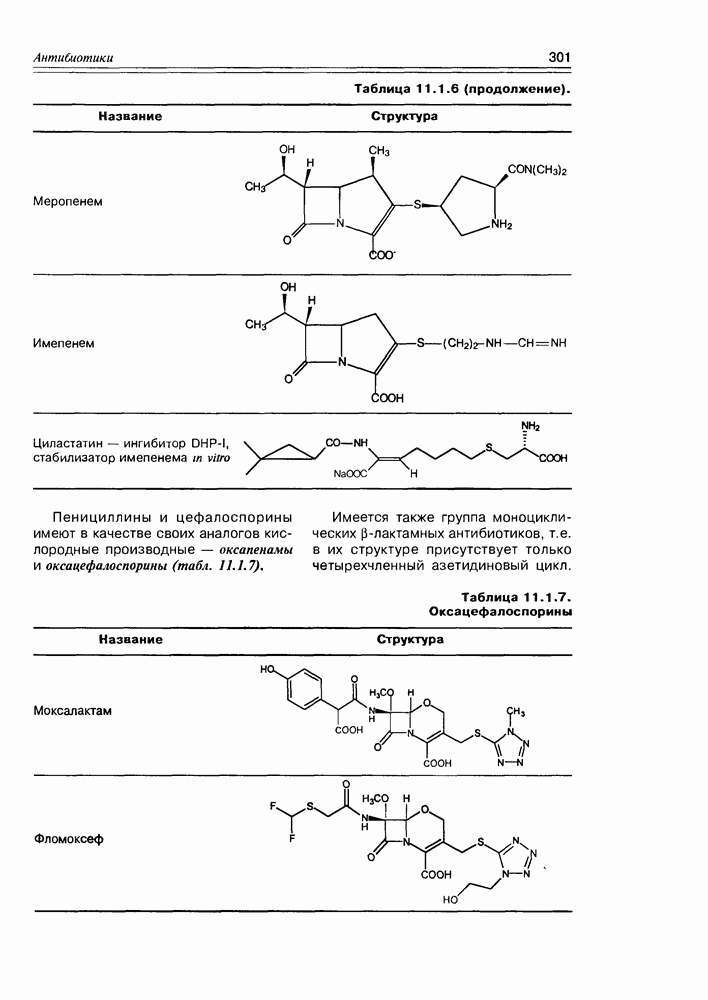
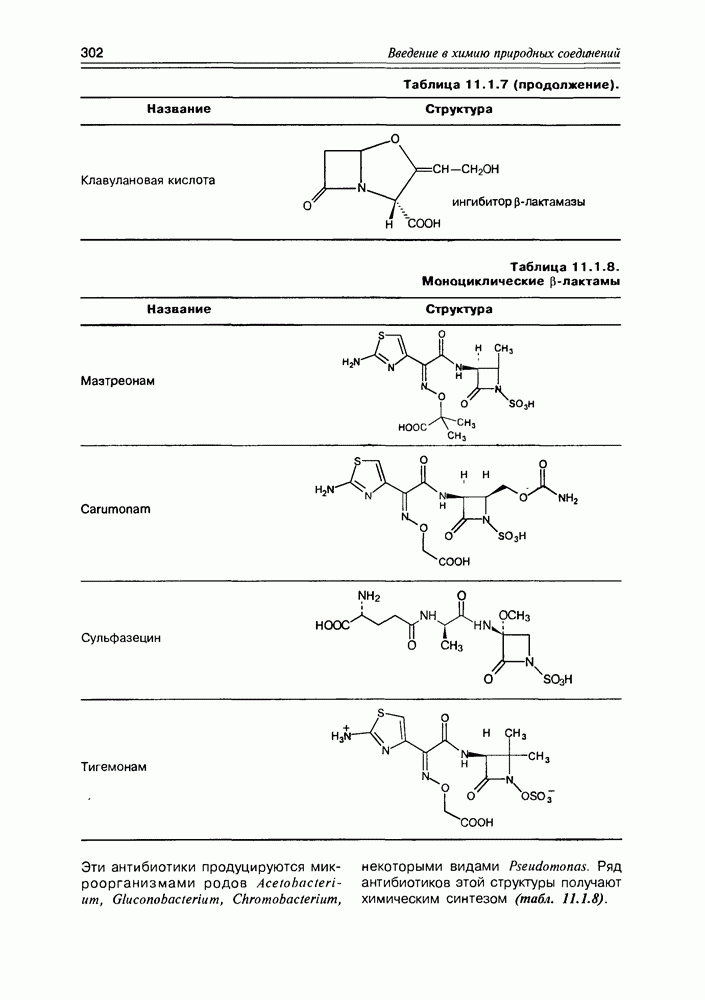
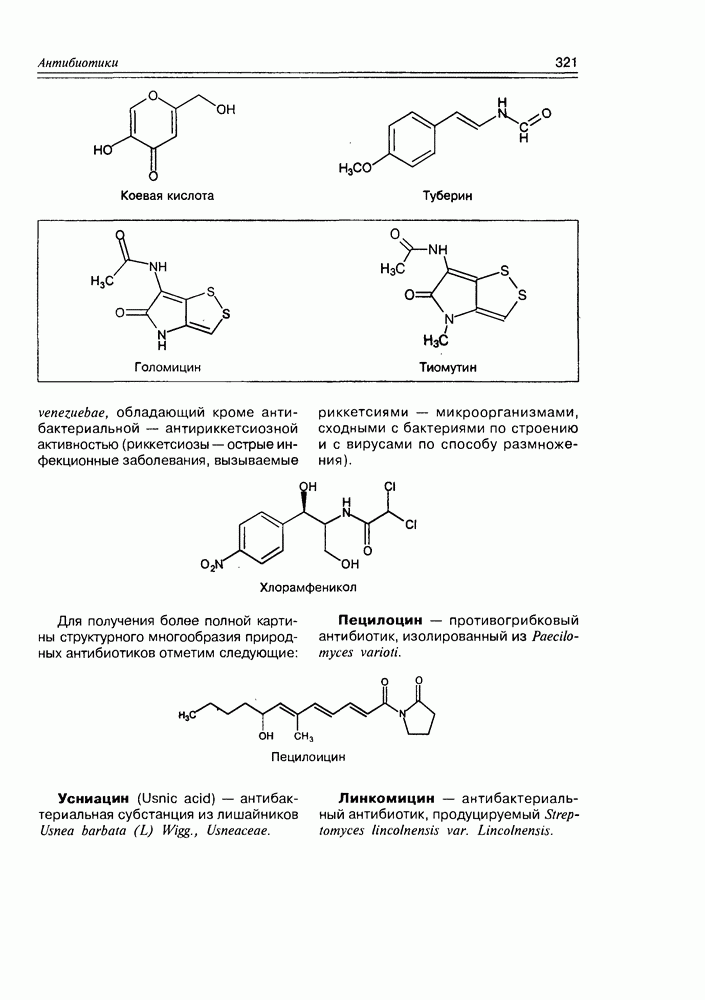
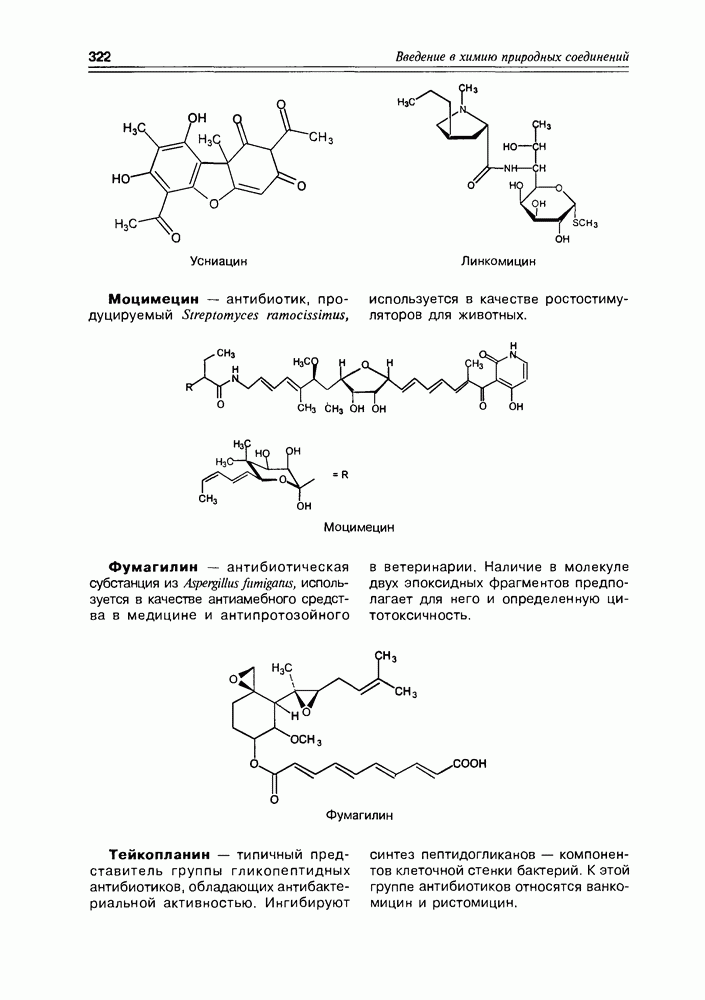
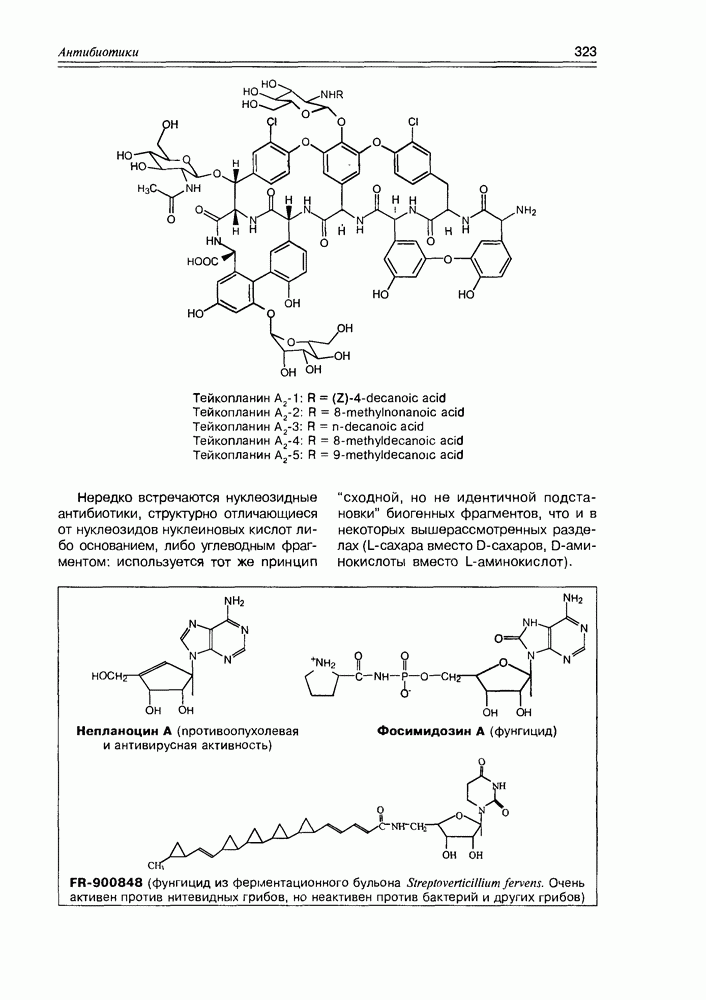
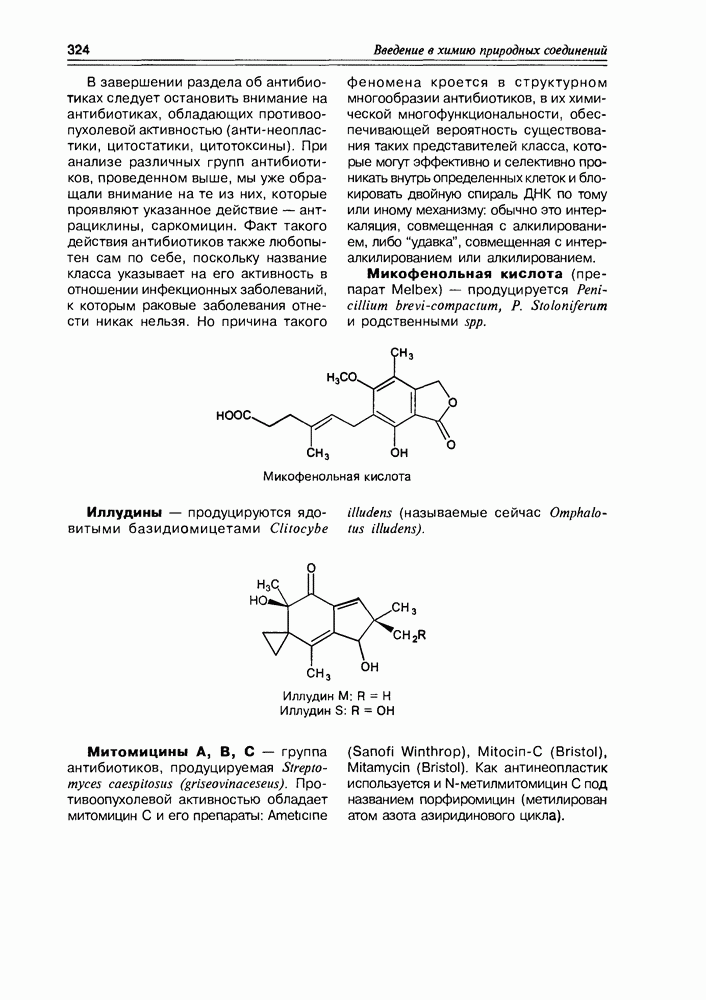
- Глава 11. АНТИБИОТИКИ
- 11.1. b-Лактамные антибиотики
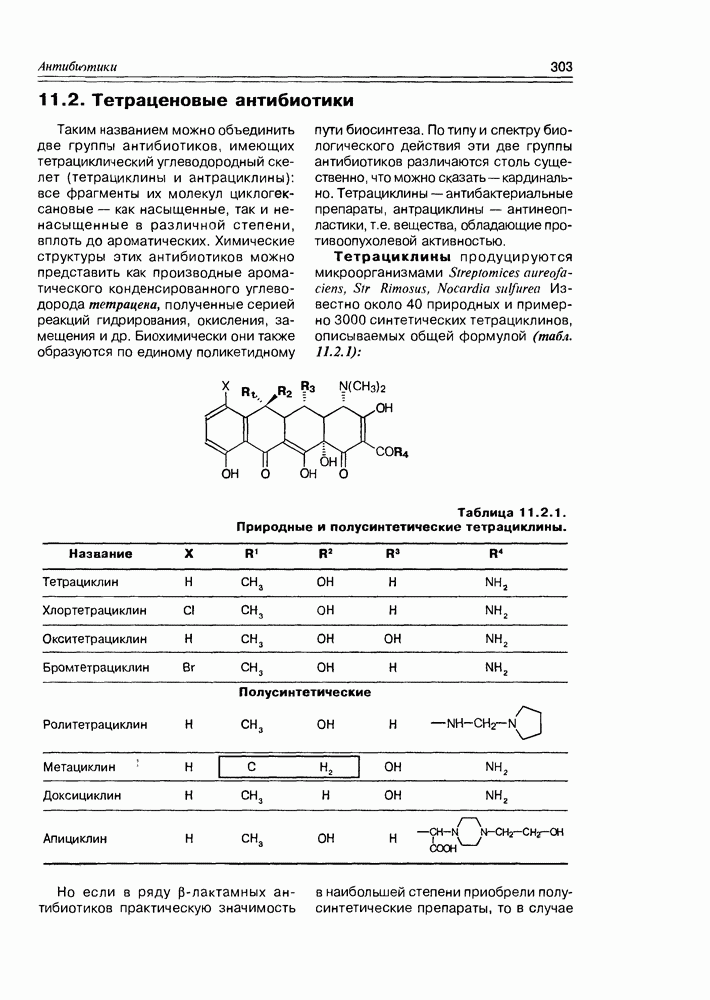
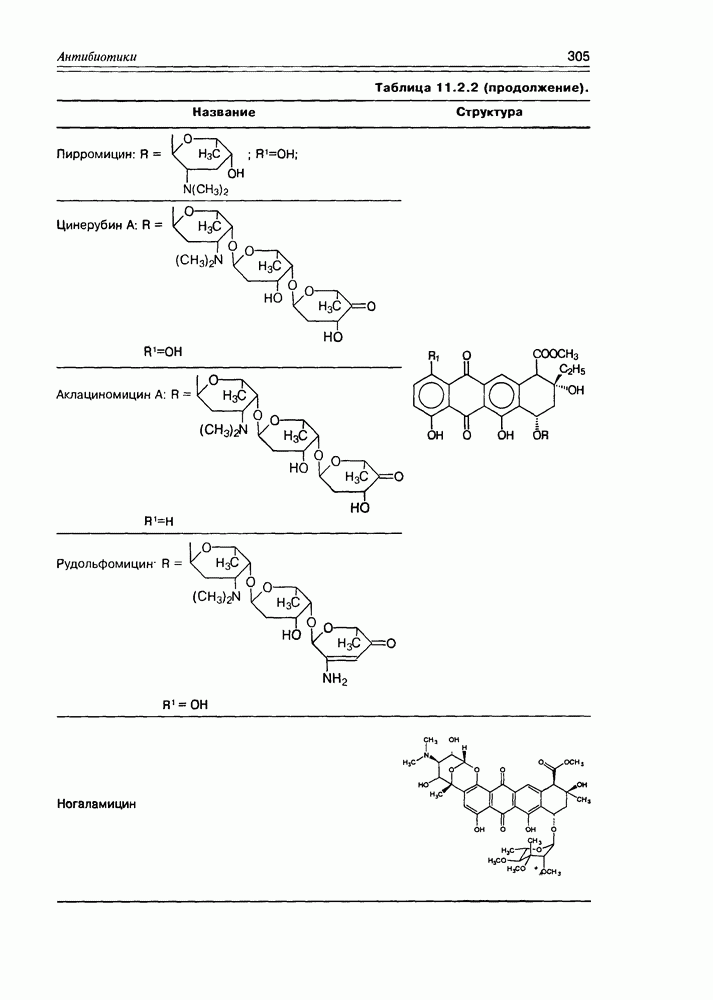
- 11.2. Тетраценовые антибиотики
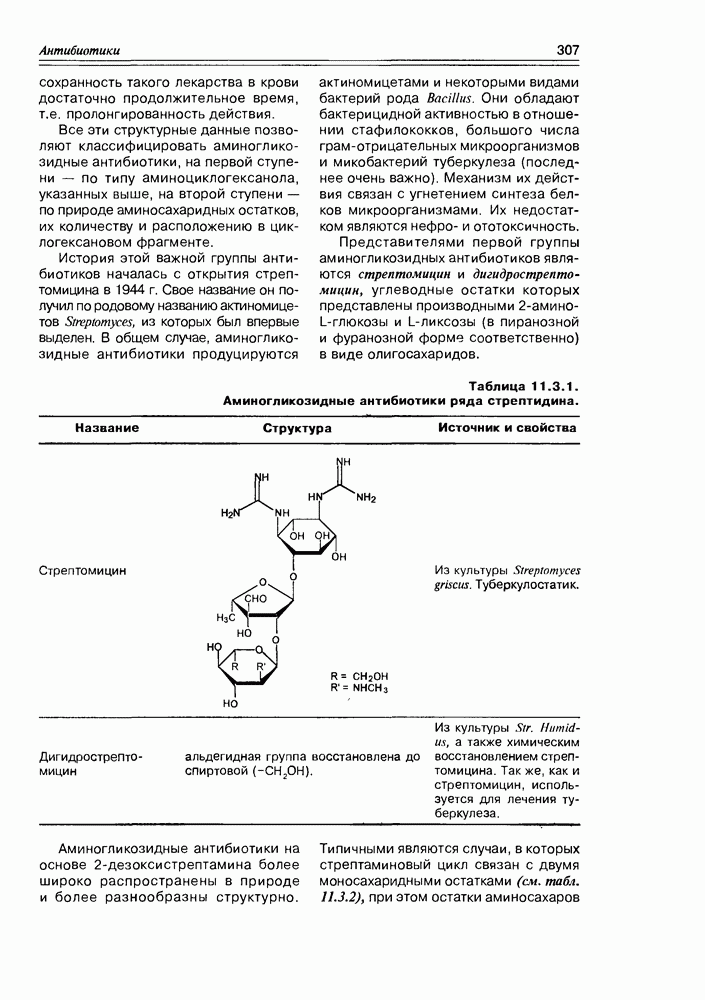
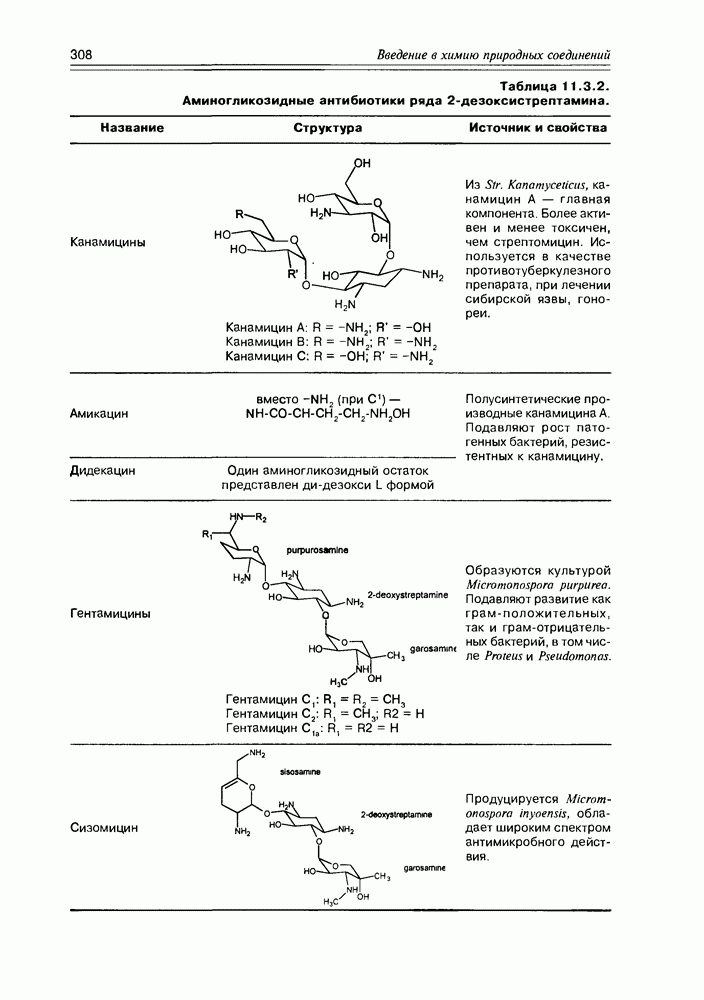
- 11.3. Аминогликозидные антибиотики
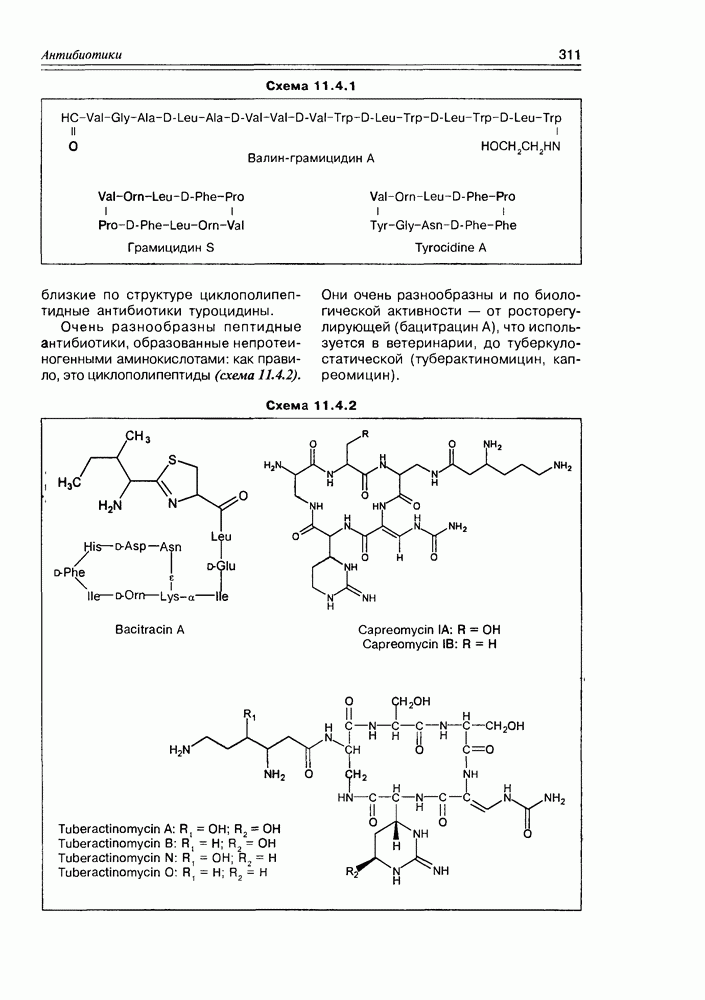
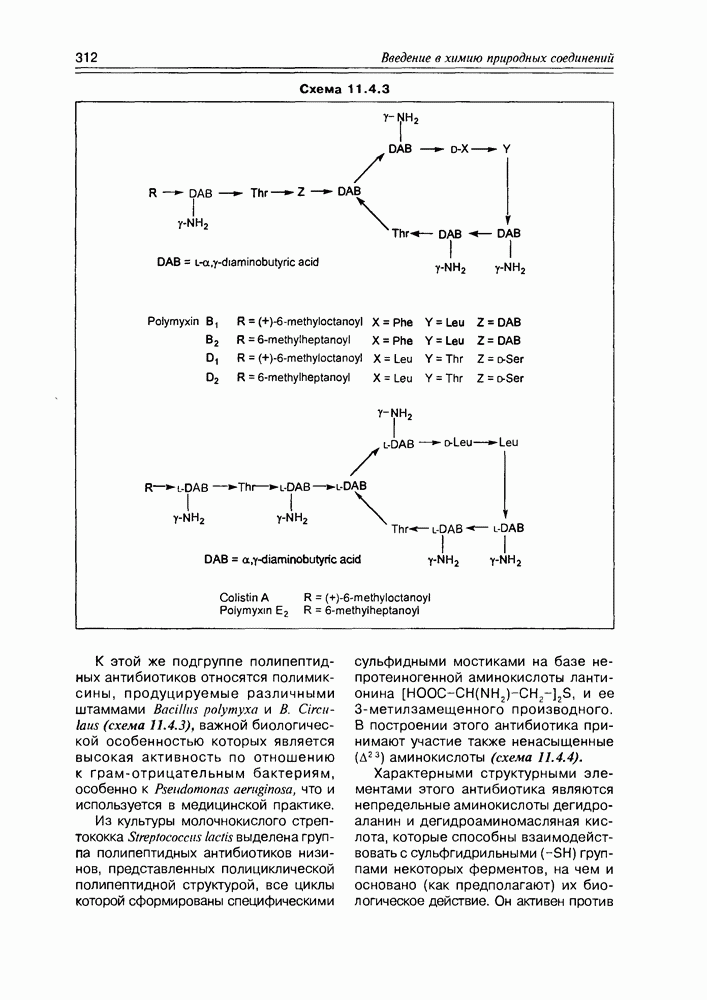
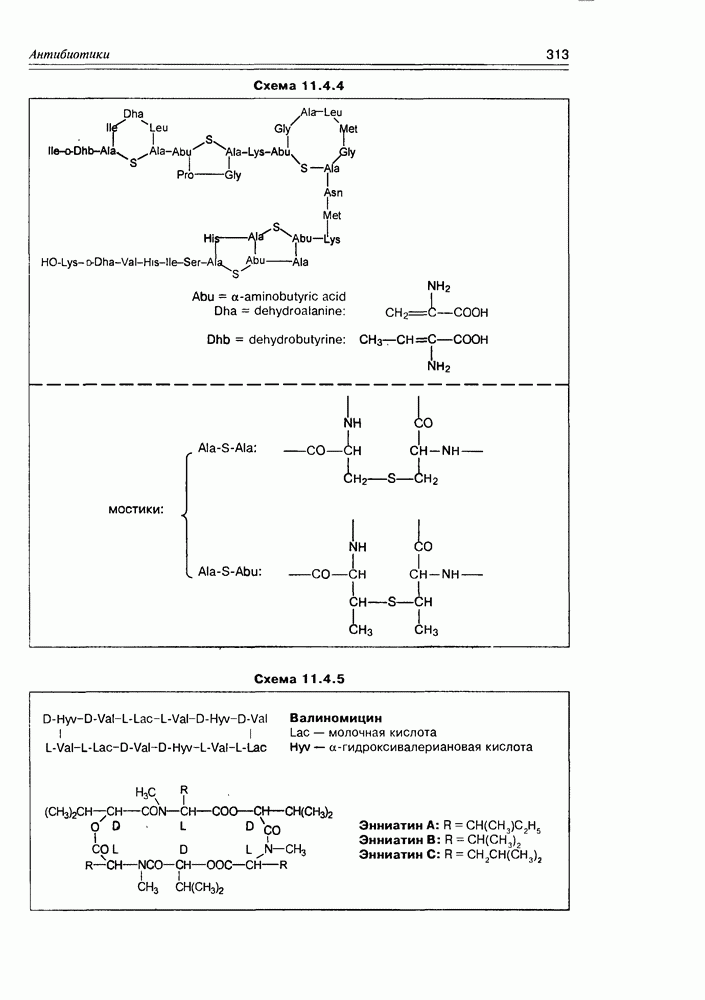
- 11.4. Пептидные антибиотики
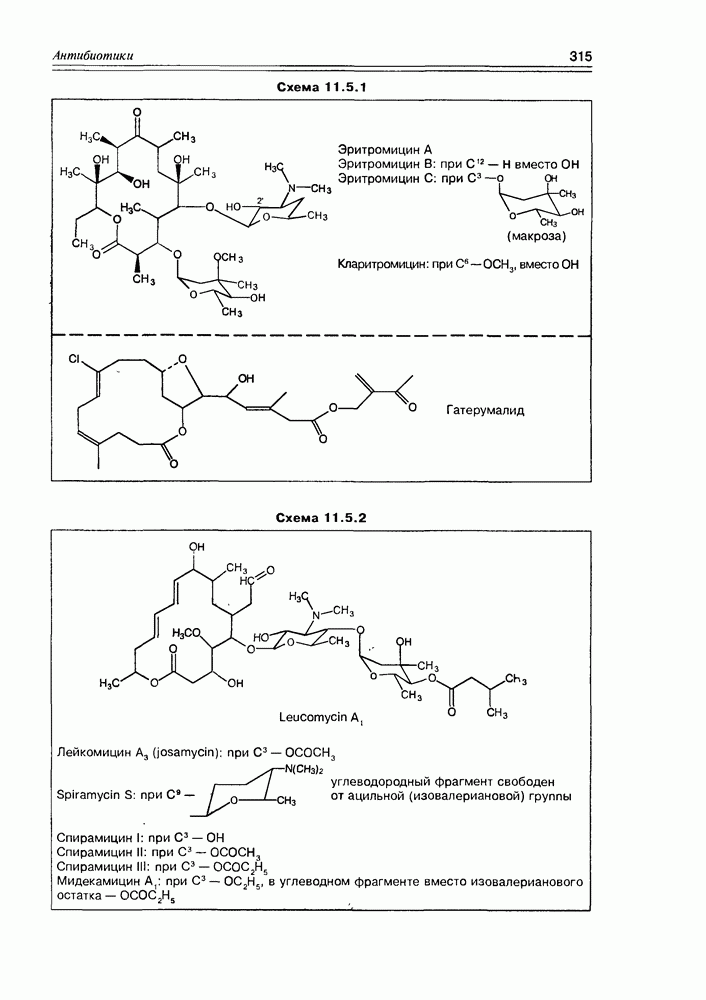
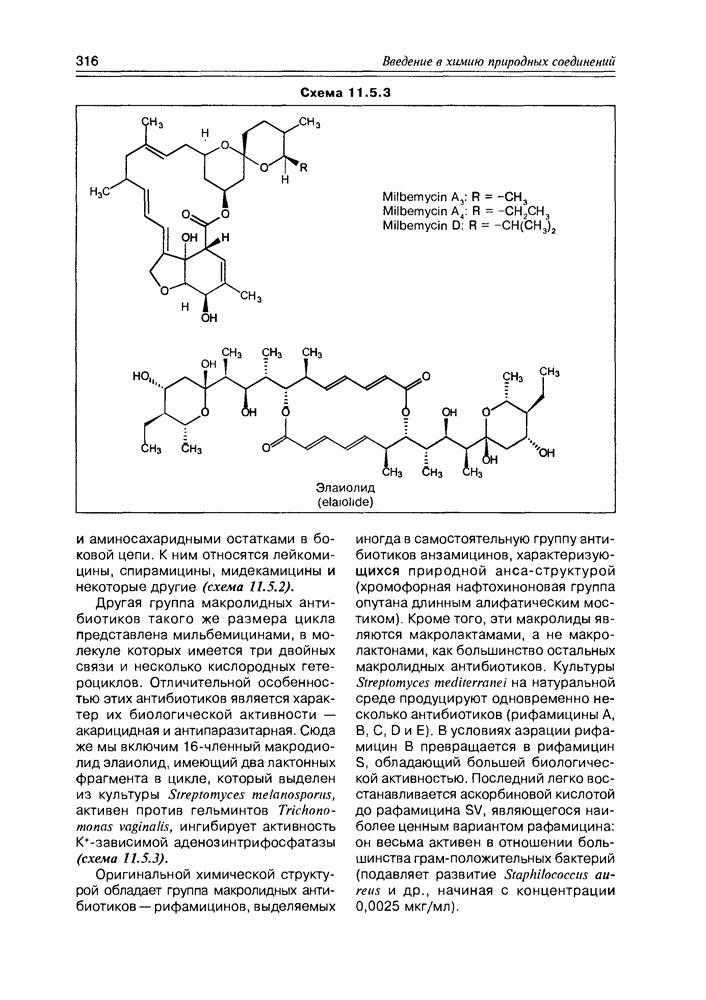
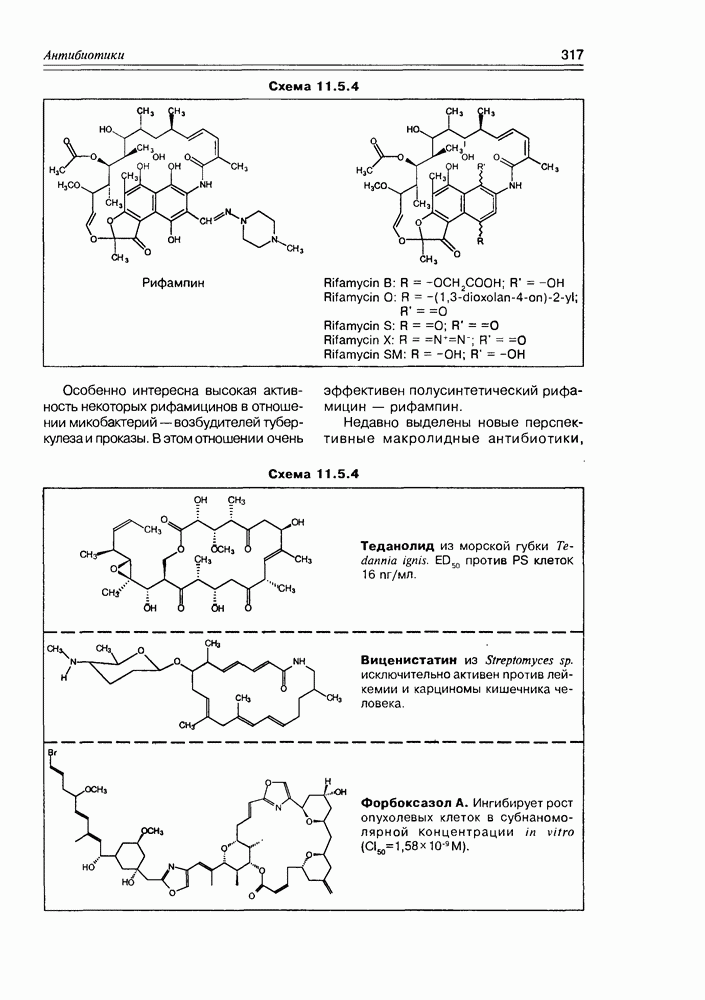
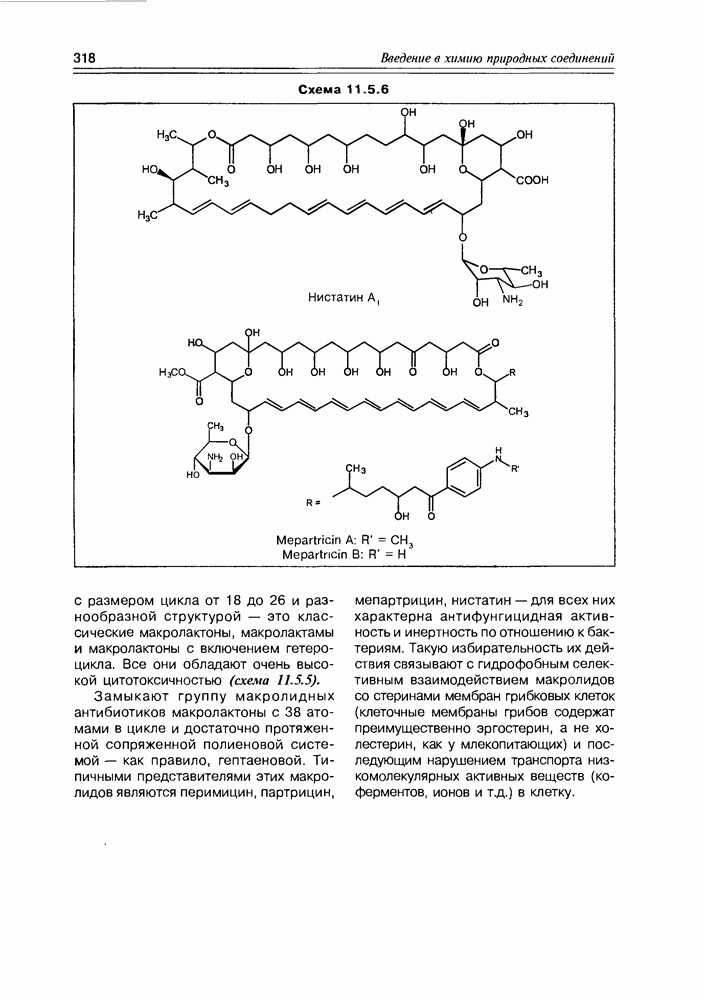
- 11.5. Макролидные антибиотики
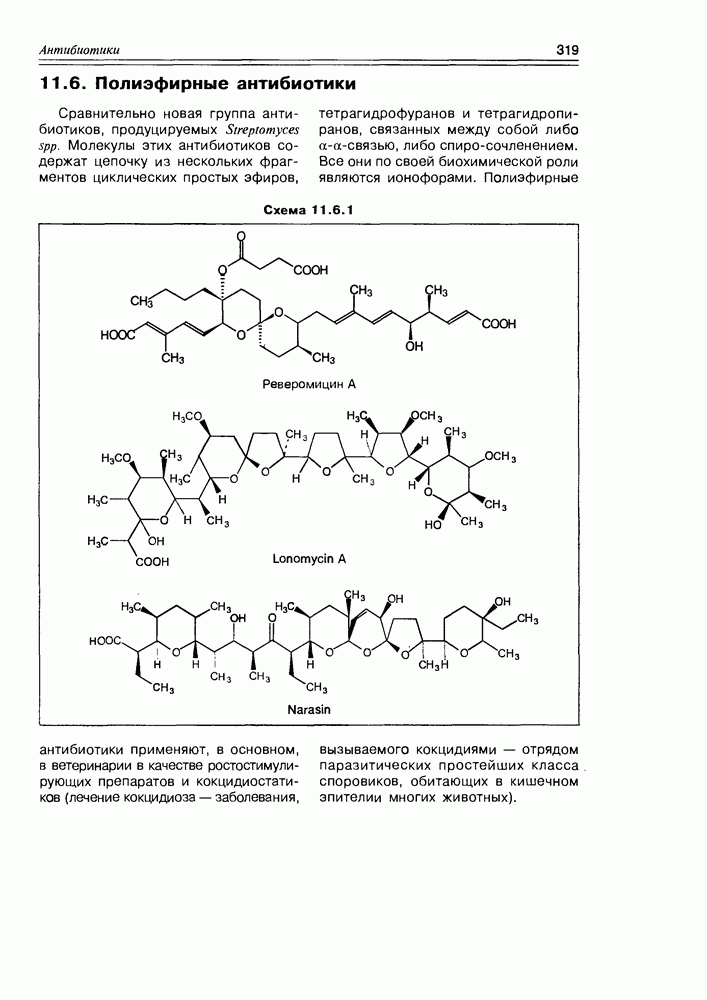
- 11.6. Полиэфирные антибиотики
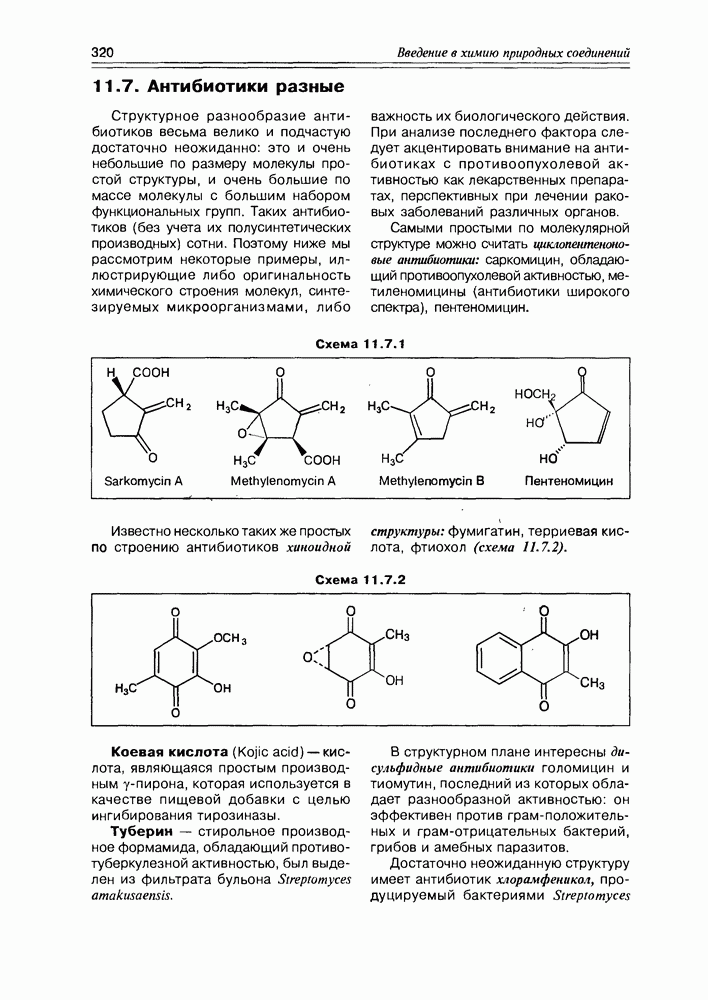
- 11.7. Антибиотики разные
- Глава 12. РАЗНЫЕ ГРУППЫ ПРИРОДНЫХ СОЕДИНЕНИЙ
- 12.2. Полиэфиры
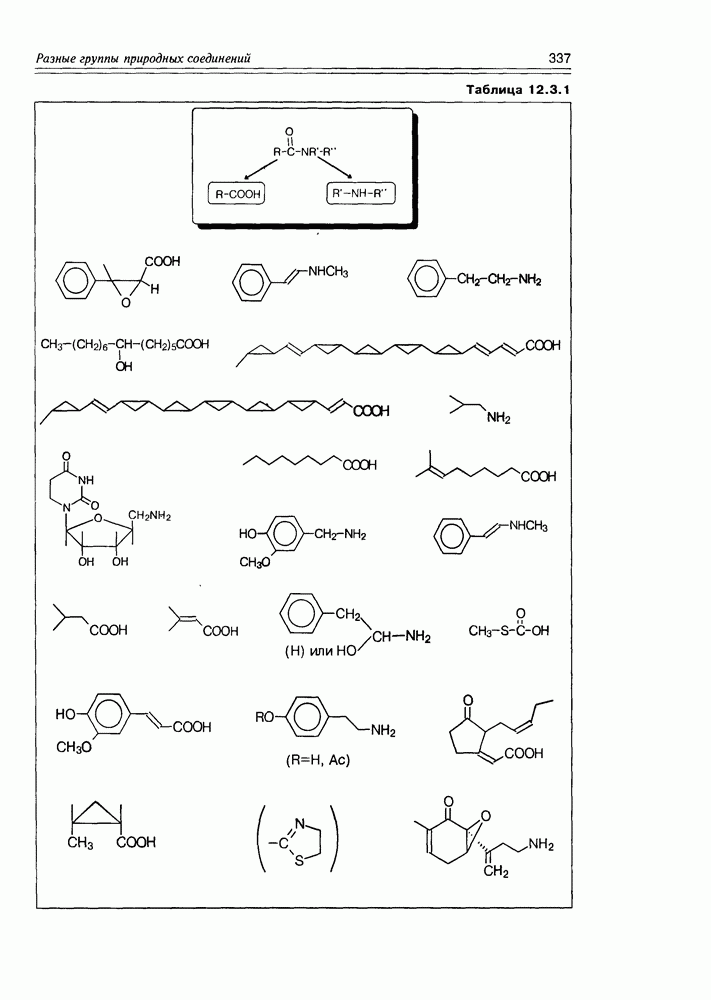
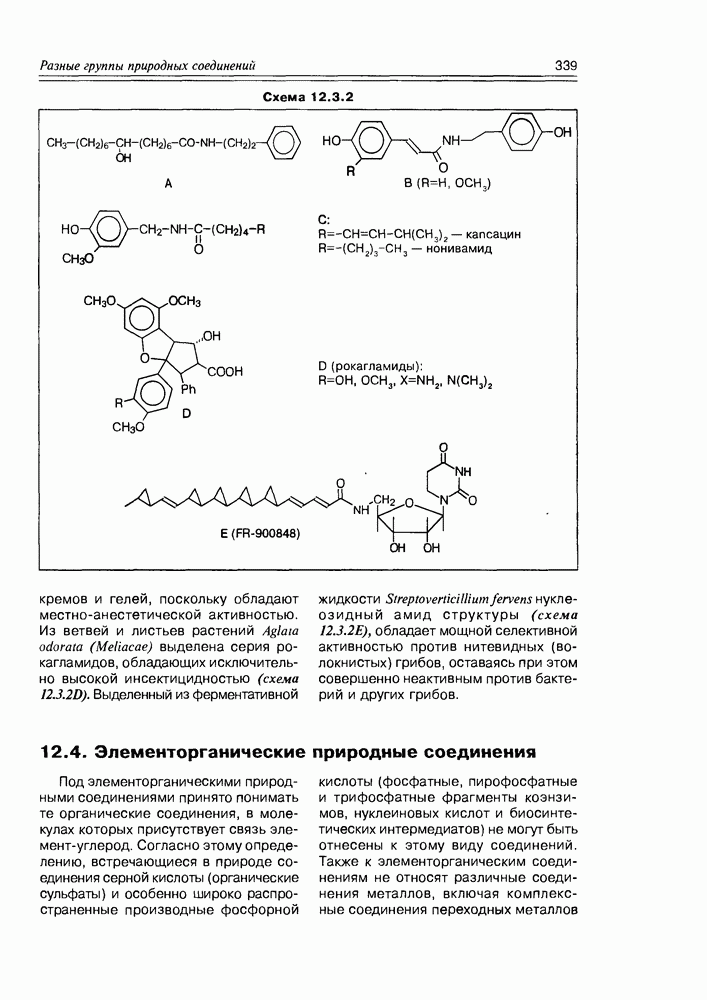
- 12.3. Амиды
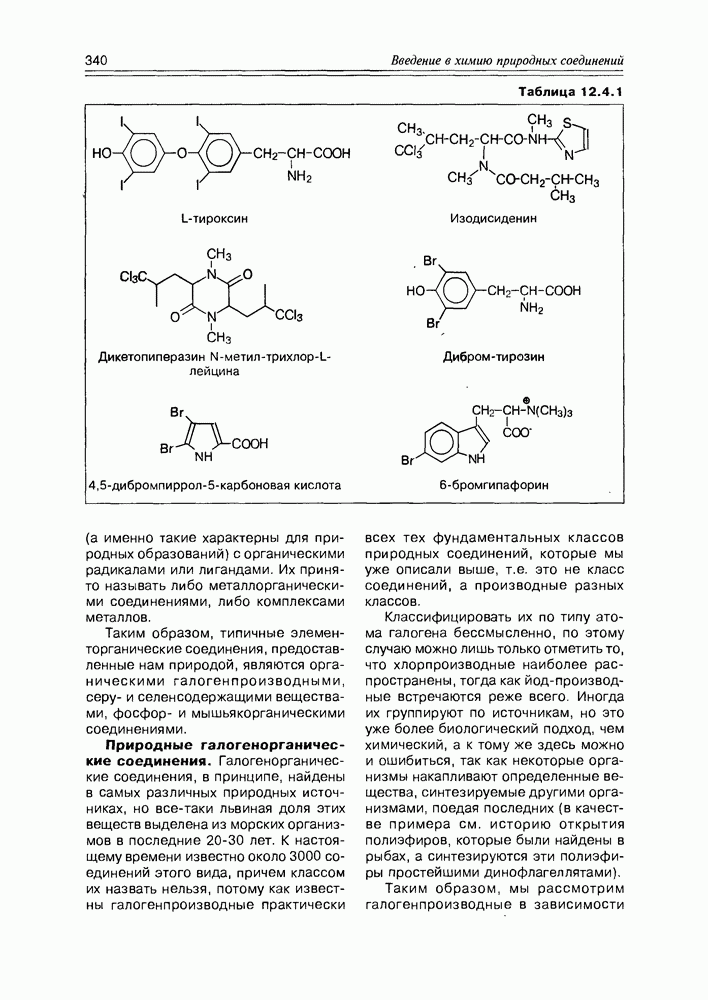
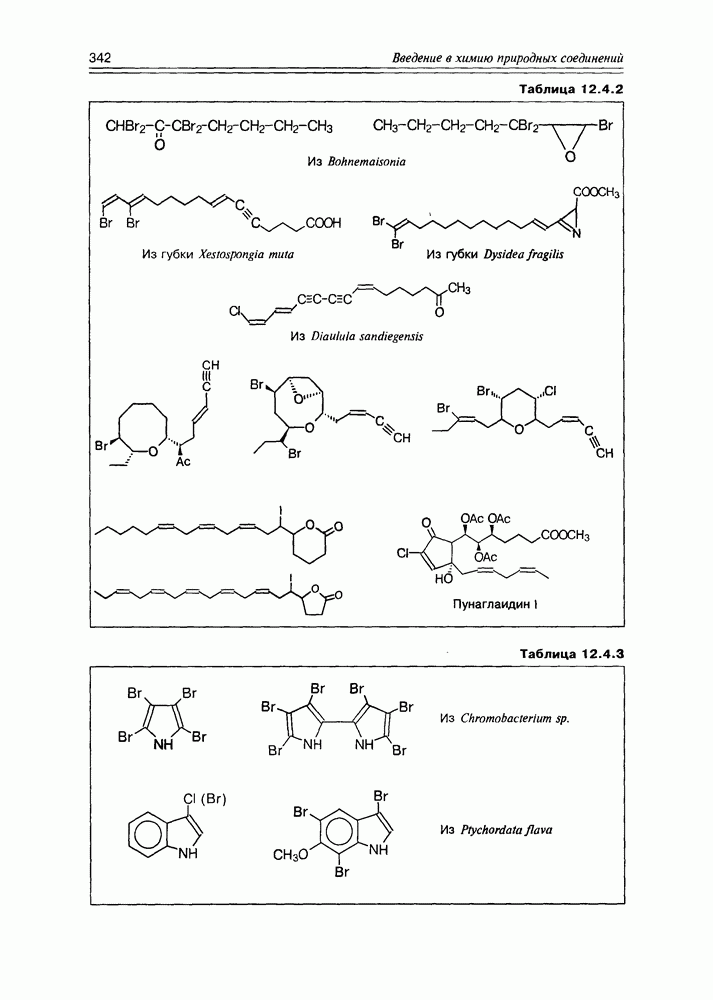
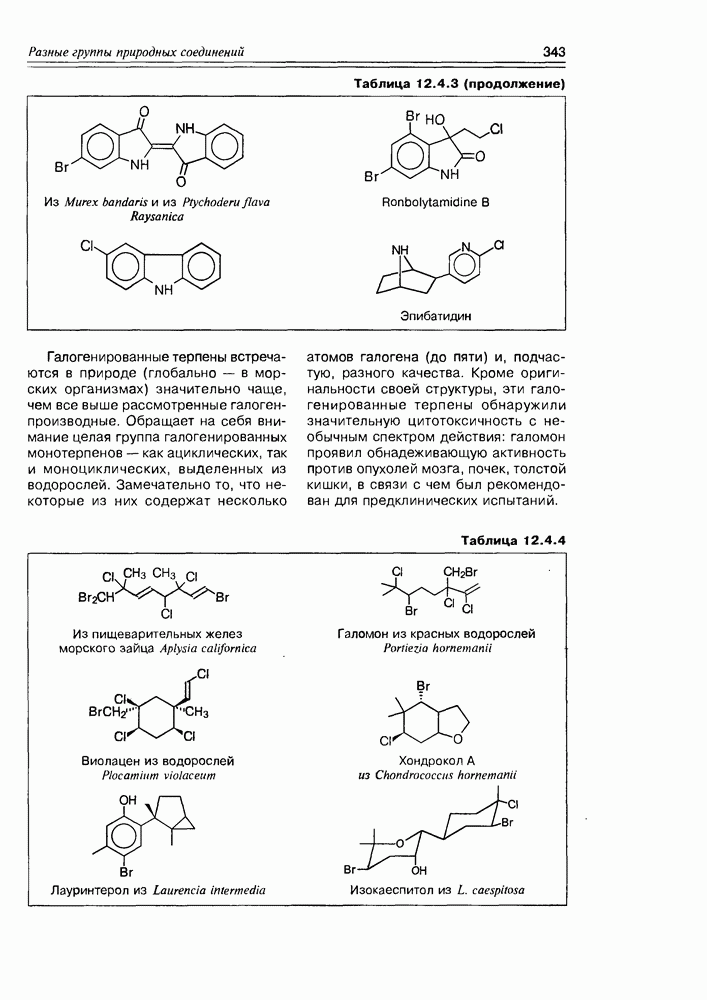
- 12.4. Элементорганические природные соединения
- Глава 13. МЕТАЛЛО-КОЭНЗИМЫ