| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
10.2. Витамины-коферменты
Витамин  . Водорастворимый витамин группы В, имеющий также тривиальное химическое название тиамин, широко распространен в живой природе, синтезируется многими растениями и микроорганизмами (но не животными). Наиболее богаты им дрожжи, мука грубого помола, крупы, бобовые, печень, нежирная свинина.
. Водорастворимый витамин группы В, имеющий также тривиальное химическое название тиамин, широко распространен в живой природе, синтезируется многими растениями и микроорганизмами (но не животными). Наиболее богаты им дрожжи, мука грубого помола, крупы, бобовые, печень, нежирная свинина.
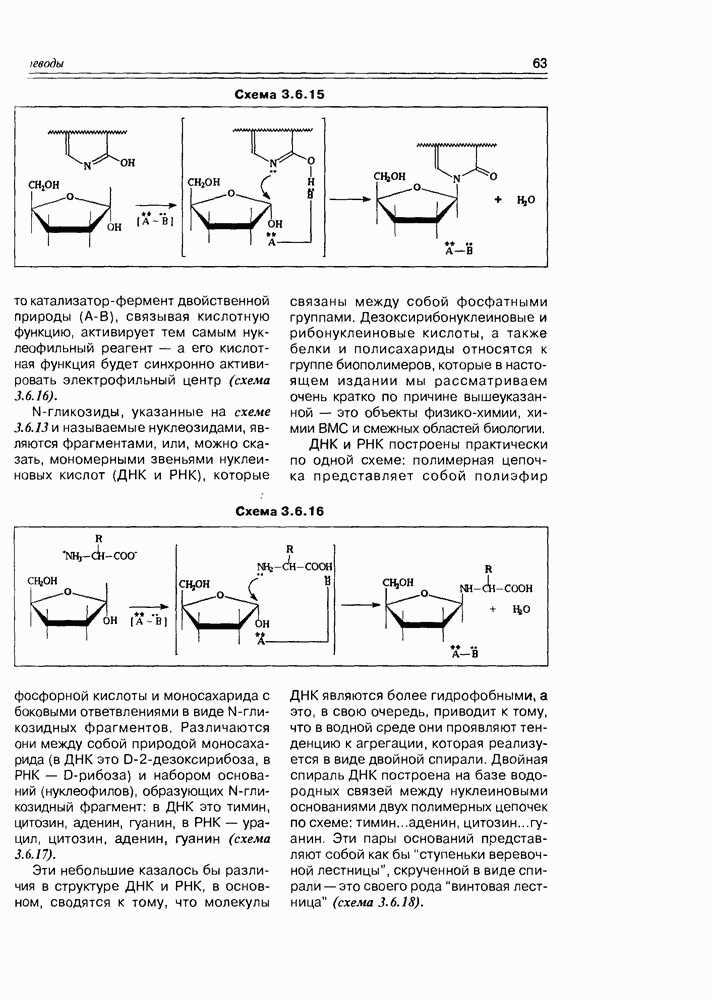
По химической структуре тиамин являет собой систему из двух гетероциклов (пиримидина и тиазола) с небольшим набором функциональных групп: аминогруппа в пиримидиновом цикле и спиртовая группа у тиазольного фрагмента. Атом азота тиазольного цикла находится в аммонийном состоянии, а само соединение — в виде соли, спиртовая группа этерифицирована фосфорной кислотой. В живых организмах тиамин присутствует либо в свободном виде, либо в виде моно-, ди- и трифосфатов с наибольшей долей дифосфата.
Схема 10.2.1

Витамин В, является как раз тем соединением, попадающим под понятие витамин, которое самостоятельно никаких функций не выполняет, но в виде кофермента (ТРР) ряда важнейших ферментов углеводного обмена участвует в серии биохимических процессов, связанных с реакциями окислительного декарбоксилирования пировиноградной кислоты (пируват-дегидрогеназа), 2-оксоглутаровой кислоты, декарбоксилирования 2-оксоизовале-риановой и других разветвленных кетокислот (а-оксоглутарат-дегидрогеназа) и переноса двухуглеродного фрагмента с карбонильной группой (транс-кетолаза).
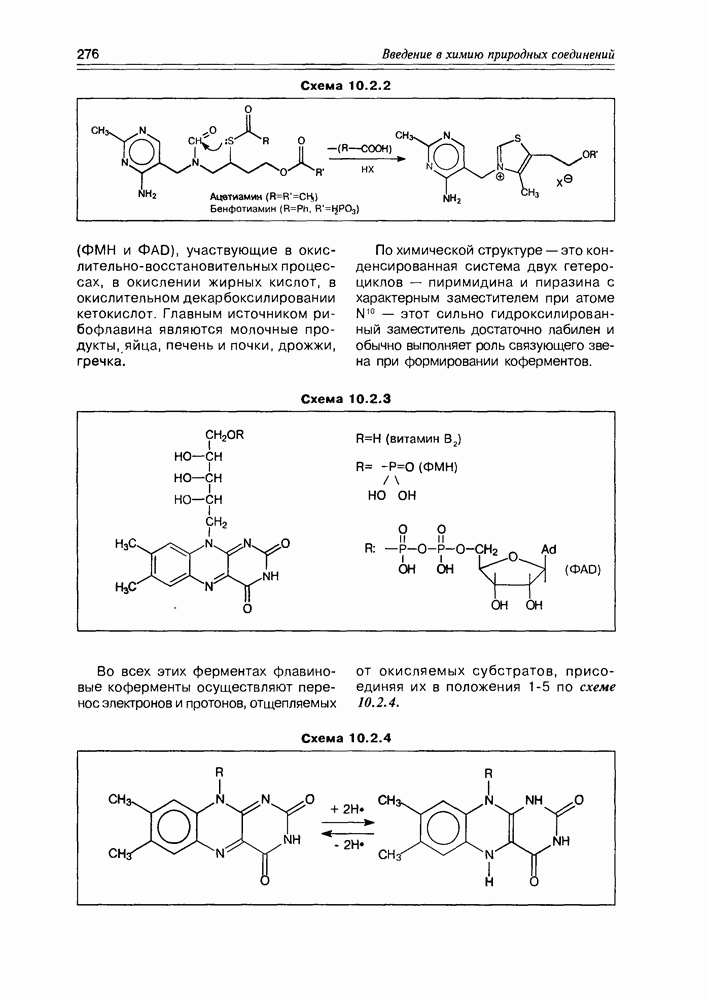
Известно несколько синтетических производных витамина  обладающих его активностью, но в отличие от оригинала — это жирорастворимые соединения, а по химической структуре их можно считать провитаминами В, так как нетрудно увидеть путь их превращения непосредственно в тиамин (схема 10.2.2).
обладающих его активностью, но в отличие от оригинала — это жирорастворимые соединения, а по химической структуре их можно считать провитаминами В, так как нетрудно увидеть путь их превращения непосредственно в тиамин (схема 10.2.2).
Витамин  , известный также под названием рибофлавин, по своей биологической роли похож на тиамин, поскольку самостоятельно в биохимических процессах не участвует (так как это делает, например, витамин А), а в качестве предшественника формирует флавиновые коферменты и ферменты
, известный также под названием рибофлавин, по своей биологической роли похож на тиамин, поскольку самостоятельно в биохимических процессах не участвует (так как это делает, например, витамин А), а в качестве предшественника формирует флавиновые коферменты и ферменты
Схема 10.2.2

(ФМН и ФАD), участвующие в окислительно-восстановительных процессах, в окислении жирных кислот, в окислительном декарбоксилировании кетокислот. Главным источником рибофлавина являются молочные продукты, яйца, печень и почки, дрожжи, гречка.
По химической структуре — это конденсированная система двух гетероциклов — пиримидина и пиразина с характерным заместителем при атоме  этот сильно гидроксилированный заместитель достаточно лабилен и обычно выполняет роль связующего звена при формировании коферментов.
этот сильно гидроксилированный заместитель достаточно лабилен и обычно выполняет роль связующего звена при формировании коферментов.
Схема 10.2.3

Во всех этих ферментах флавиновые коферменты осуществляют перенос электронов и протонов, отщепляемых от окисляемых субстратов, присоединяя их в положения 1-5 по схеме 10.2.4.
Схема 10.2.4

Витамин  известный также как пантотеновая кислота, синтезируется зелеными растениями и микроорганизмами, в том числе и микрофлорой млекопитающих (и человека, в том числе). Также не выполняет самостоятельной функции, а является составной частью широко распространенного в живой природе, чуть ли не ключевого во многих биосинтетических схемах кофермента А (КоА, KoA-SH).
известный также как пантотеновая кислота, синтезируется зелеными растениями и микроорганизмами, в том числе и микрофлорой млекопитающих (и человека, в том числе). Также не выполняет самостоятельной функции, а является составной частью широко распространенного в живой природе, чуть ли не ключевого во многих биосинтетических схемах кофермента А (КоА, KoA-SH).
По своим химическим свойствам это типичная оксикислота, которая может образовывать производные как по карбоксильной группе (амиды, сложные эфиры и т.д.), так и по спиртовым гидроксилам (сложные и простые эфиры), что используется природой при включении ее в структуру кофермента А, катализирующего реакции переноса ацетильного фрагмента (процесса, являющегося ключевым для многих биосинтетических путей), а также некоторых других кислотных остатков (R-CO-).
Химически эта кислота неустойчива в любой среде (кислой и щелочной) легко гидролизуется до р-аланина и пантолактона. Биологической активностью, ей подобной, обладают также пантотениловый спирт и пантетеин (схема 10.2.5).
Схема 10.2.5

Витамин В6 представляет собой группу производных 2-метил-3-гидрокси-5-метиленгидрокси пиридина.
Продуцируется витамин  разнообразными микроорганизмами, а также растениями. Им наиболее богаты зеленый перец, дрожжи, печень млекопитающих, зерна пшеницы. Как пиридиновые основания, все эти соединения легко образуют соли с минеральными кислотами (HCI наиболее подходящая), а как спирты — этерифицируются по спиртовым гидроксилам, in vivo фосфорилируется предпочтительно 5-мети-ленгидроксильный фрагмент. Из других функциональных производных этой группы соединений следует отметить пиридоксаль, альдегидная группа которого обеспечивает молекуле разнообразную и высокую химическую активность.
разнообразными микроорганизмами, а также растениями. Им наиболее богаты зеленый перец, дрожжи, печень млекопитающих, зерна пшеницы. Как пиридиновые основания, все эти соединения легко образуют соли с минеральными кислотами (HCI наиболее подходящая), а как спирты — этерифицируются по спиртовым гидроксилам, in vivo фосфорилируется предпочтительно 5-мети-ленгидроксильный фрагмент. Из других функциональных производных этой группы соединений следует отметить пиридоксаль, альдегидная группа которого обеспечивает молекуле разнообразную и высокую химическую активность.
Схема 10.2.6

Схема 10.2.7

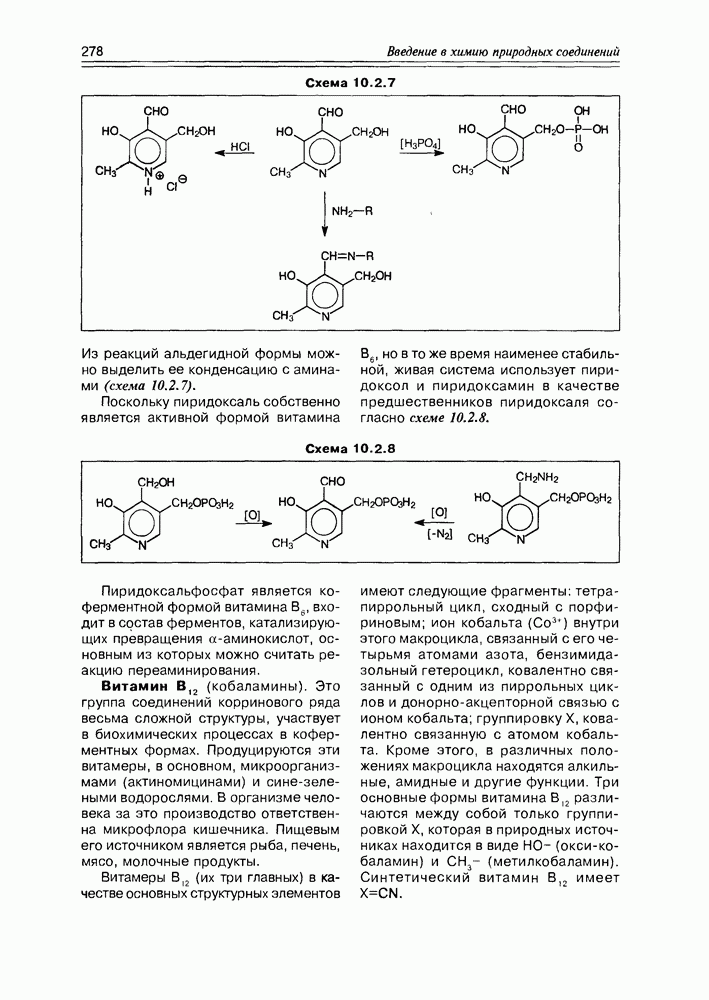
Из реакций альдегидной формы можно выделить ее конденсацию с аминами (схема 10.2.7).
Поскольку пиридоксаль собственно является активной формой витамина  но в то же время наименее стабильной, живая система использует пиридоксол и пиридоксамин в качестве предшественников пиридоксаля согласно схеме 10.2.8.
но в то же время наименее стабильной, живая система использует пиридоксол и пиридоксамин в качестве предшественников пиридоксаля согласно схеме 10.2.8.
Схема 10.2.8

Пиридоксальфосфат является коферментной формой витамина Вв, входит в состав ферментов, катализирующих превращения а-аминокислот, основным из которых можно считать реакцию переаминирования.
Витамин В12 (кобаламины). Это группа соединений корринового ряда весьма сложной структуры, участвует в биохимических процессах в коферментных формах. Продуцируются эти витамеры, в основном, микроорганизмами (актиномицинами) и сине-зелеными водорослями. В организме человека за это производство ответственна микрофлора кишечника. Пищевым его источником является рыба, печень, мясо, молочные продукты.
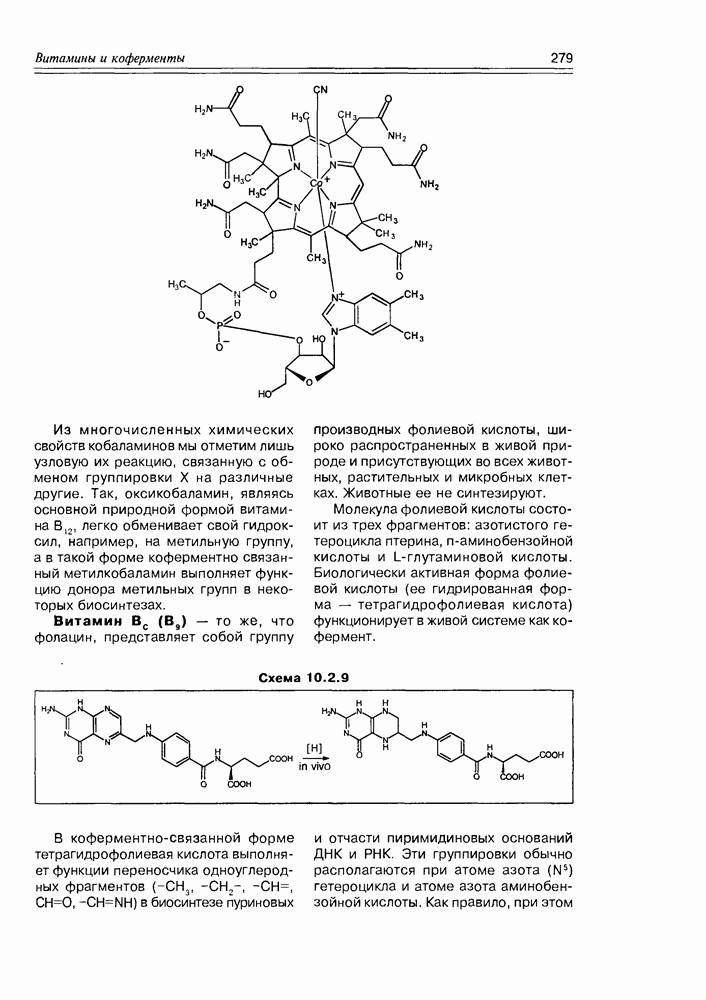
Витамеры  (их три главных) в качестве основных структурных элементов имеют следующие фрагменты: тетра-пиррольный цикл, сходный с порфириновым; ион кобальта
(их три главных) в качестве основных структурных элементов имеют следующие фрагменты: тетра-пиррольный цикл, сходный с порфириновым; ион кобальта  внутри этого макроцикла, связанный с его четырьмя атомами азота, бензимидазольный гетероцикл, ковалентно связанный с одним из пиррольных циклов и донорно-акцепторной связью с ионом кобальта; группировку X, ковалентно связанную с атомом кобальта. Кроме этого, в различных положениях макроцикла находятся алкильные, амидные и другие функции. Три основные формы витамина
внутри этого макроцикла, связанный с его четырьмя атомами азота, бензимидазольный гетероцикл, ковалентно связанный с одним из пиррольных циклов и донорно-акцепторной связью с ионом кобальта; группировку X, ковалентно связанную с атомом кобальта. Кроме этого, в различных положениях макроцикла находятся алкильные, амидные и другие функции. Три основные формы витамина  различаются между собой только группировкой X, которая в природных источниках находится в виде НО- (окси-кобаламин) и
различаются между собой только группировкой X, которая в природных источниках находится в виде НО- (окси-кобаламин) и  Синтетический витамин
Синтетический витамин  имеет
имеет 

Из многочисленных химических свойств кобаламинов мы отметим лишь узловую их реакцию, связанную с обменом группировки X на различные другие. Так, оксикобаламин, являясь основной природной формой витамина  легко обменивает свой гидроксил, например, на метильную группу, а в такой форме коферментно связанный метилкобаламин выполняет функцию донора метильных групп в некоторых биосинтезах.
легко обменивает свой гидроксил, например, на метильную группу, а в такой форме коферментно связанный метилкобаламин выполняет функцию донора метильных групп в некоторых биосинтезах.
Витамин  то же, что фолацин, представляет собой группу производных фолиевой кислоты, широко распространенных в живой природе и присутствующих во всех животных, растительных и микробных клетках. Животные ее не синтезируют.
то же, что фолацин, представляет собой группу производных фолиевой кислоты, широко распространенных в живой природе и присутствующих во всех животных, растительных и микробных клетках. Животные ее не синтезируют.
Молекула фолиевой кислоты состоит из трех фрагментов: азотистого гетероцикла птерина,  -аминобензойной кислоты и
-аминобензойной кислоты и  -глутаминовой кислоты. Биологически активная форма фолиевой кислоты (ее гидрированная форма — тетрагидрофолиевая кислота) функционирует в живой системе как кофермент.
-глутаминовой кислоты. Биологически активная форма фолиевой кислоты (ее гидрированная форма — тетрагидрофолиевая кислота) функционирует в живой системе как кофермент.
Схема 10.2.9

В коферментно-связанной форме тетрагидрофолиевая кислота выполняет функции переносчика одноуглеродных фрагментов  в биосинтезе пуриновых и отчасти пиримидиновых оснований ДНК и РНК. Эти группировки обычно располагаются при атоме азота
в биосинтезе пуриновых и отчасти пиримидиновых оснований ДНК и РНК. Эти группировки обычно располагаются при атоме азота  гетероцикла и атоме азота аминобензойной кислоты. Как правило, при этом
гетероцикла и атоме азота аминобензойной кислоты. Как правило, при этом
Схема 10.2.10

вместо одного остатка глутаминовой кислоты, содержится полипептидная цепочка из нескольких остатков глутаминовой кислоты — от 2 до 7.
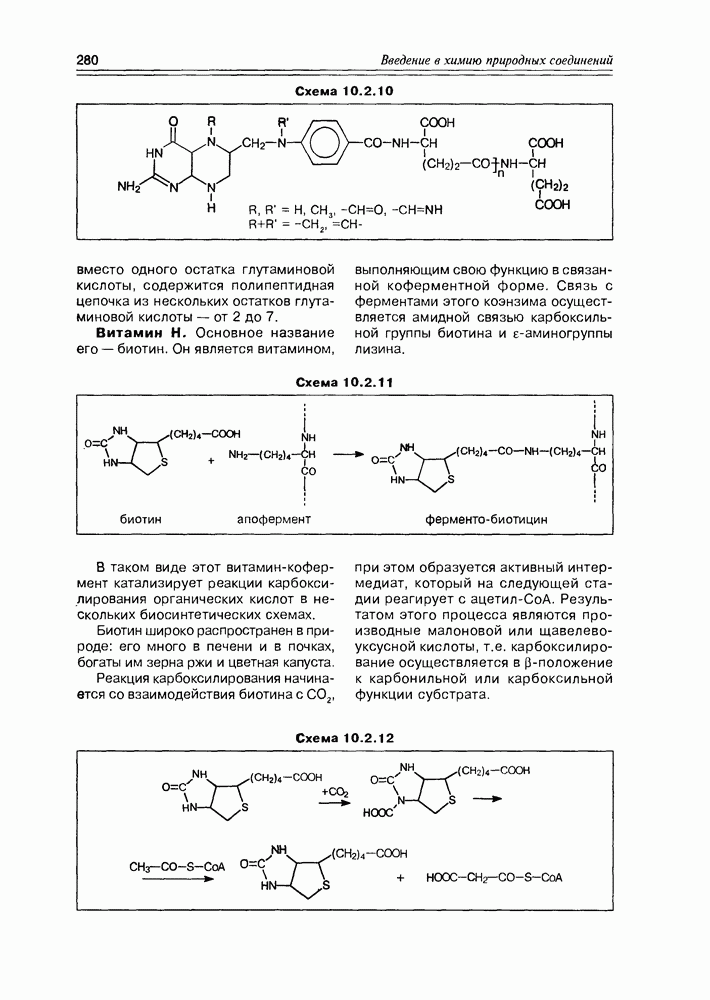
Витамин Н. Основное название его — биотин. Он является витамином, выполняющим свою функцию в связанной коферментной форме. Связь с ферментами этого коэнзима осуществляется амидной связью карбоксильной группы биотина и е-аминогруппы лизина.
Схема 10.2.11

В таком виде этот витамин-кофермент катализирует реакции карбокси-лирования органических кислот в нескольких биосинтетических схемах.
Биотин широко распространен в природе: его много в печени и в почках, богаты им зерна ржи и цветная капуста.
Реакция карбоксилирования начинается со взаимодействия биотина с  при этом образуется активный интермедиат, который на следующей стадии реагирует с ацетил-СоА. Результатом этого процесса являются производные малоновой или щавелевоуксусной кислоты, т.е. карбоксилиро-вание осуществляется в
при этом образуется активный интермедиат, который на следующей стадии реагирует с ацетил-СоА. Результатом этого процесса являются производные малоновой или щавелевоуксусной кислоты, т.е. карбоксилиро-вание осуществляется в  -положение к карбонильной или карбоксильной функции субстрата.
-положение к карбонильной или карбоксильной функции субстрата.
Схема 10.2.12

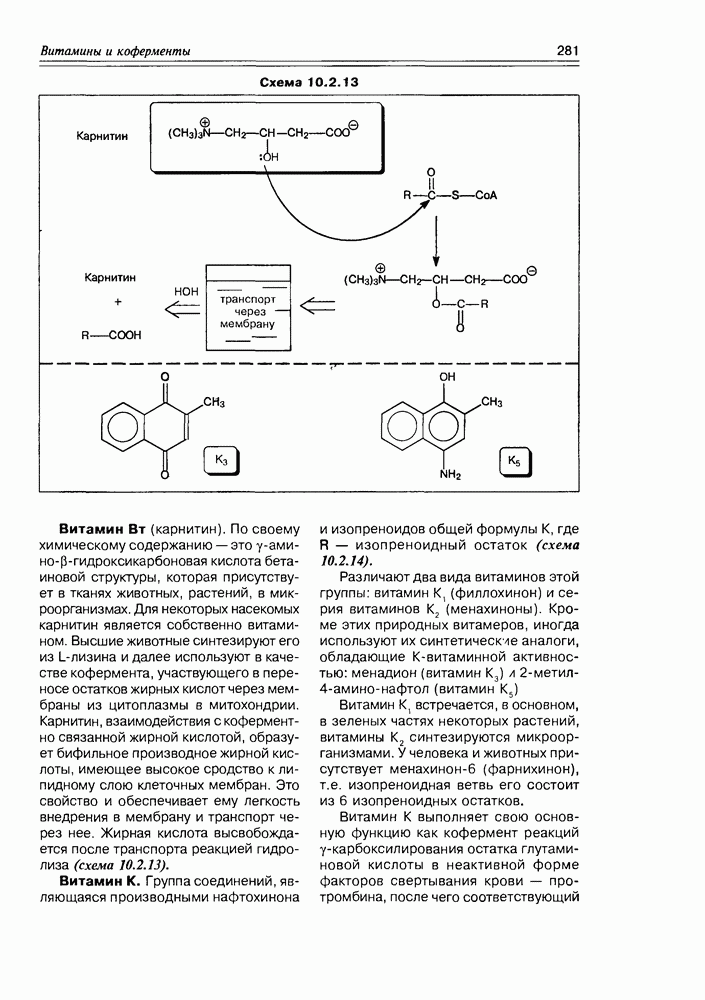
Схема 10.2.13

Витамин  По своему химическому содержанию — это у-амино-р-гидроксикарбоновая кислота бета-иновой структуры, которая присутствует в тканях животных, растений, в микроорганизмах. Для некоторых насекомых карнитин является собственно витамином. Высшие животные синтезируют его из L-лизина и далее используют в качестве кофермента, участвующего в переносе остатков жирных кислот через мембраны из цитоплазмы в митохондрии. Карнитин, взаимодействия с коферментно связанной жирной кислотой, образует бифильное производное жирной кислоты, имеющее высокое сродство к липидному слою клеточных мембран. Это свойство и обеспечивает ему легкость внедрения в мембрану и транспорт через нее. Жирная кислота высвобождается после транспорта реакцией гидролиза (схема 10.2.13).
По своему химическому содержанию — это у-амино-р-гидроксикарбоновая кислота бета-иновой структуры, которая присутствует в тканях животных, растений, в микроорганизмах. Для некоторых насекомых карнитин является собственно витамином. Высшие животные синтезируют его из L-лизина и далее используют в качестве кофермента, участвующего в переносе остатков жирных кислот через мембраны из цитоплазмы в митохондрии. Карнитин, взаимодействия с коферментно связанной жирной кислотой, образует бифильное производное жирной кислоты, имеющее высокое сродство к липидному слою клеточных мембран. Это свойство и обеспечивает ему легкость внедрения в мембрану и транспорт через нее. Жирная кислота высвобождается после транспорта реакцией гидролиза (схема 10.2.13).
Витамин К. Группа соединений, являющаяся производными нафтохинона и изопреноидов общей формулы К, где R — изопреноидный остаток (схема 10.2.14).
Различают два вида витаминов этой группы: витамин К, (филлохинон) и серия витаминов К2 (менахиноны). Кроме этих природных витамеров, иногда используют их синтетические аналоги, обладающие К-витаминной активностью: менадион (витамин К3) л 2-метил-4-амино-нафтол (витамин К5)
Витамин К, встречается, в основном, в зеленых частях некоторых растений, витамины  синтезируются микроорганизмами. У человека и животных присутствует менахинон-6 (фарнихинон), т.е. изопреноидная ветвь его состоит из 6 изопреноидных остатков.
синтезируются микроорганизмами. У человека и животных присутствует менахинон-6 (фарнихинон), т.е. изопреноидная ветвь его состоит из 6 изопреноидных остатков.
Витамин К выполняет свою основную функцию как кофермент реакций у-карбоксилирования остатка глутаминовой кислоты в неактивной форме факторов свертывания крови — протромбина, после чего соответствующий
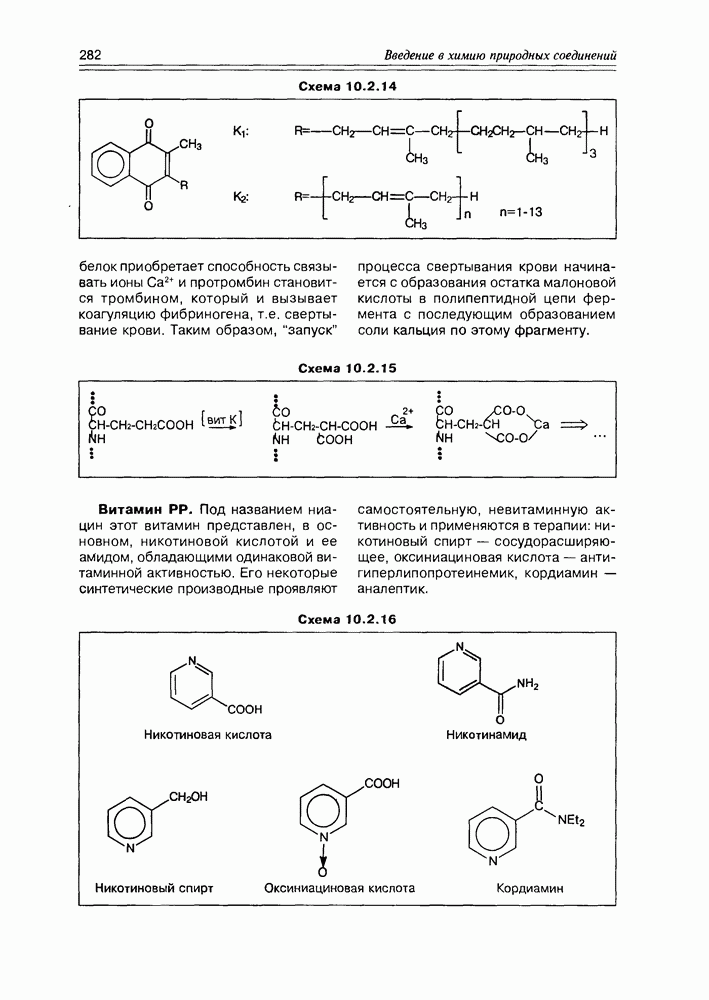
Схема 10.2.14

белок приобретает способность связывать ионы  и протромбин становится тромбином, который и вызывает коагуляцию фибриногена, т.е. свертывание крови. Таким образом, “запуск” процесса свертывания крови начинается с образования остатка малоновой кислоты в полипептидной цепи фермента с последующим образованием соли кальция по этому фрагменту.
и протромбин становится тромбином, который и вызывает коагуляцию фибриногена, т.е. свертывание крови. Таким образом, “запуск” процесса свертывания крови начинается с образования остатка малоновой кислоты в полипептидной цепи фермента с последующим образованием соли кальция по этому фрагменту.
Схема 10.2.15

Витамин PP. Под названием ниацин этот витамин представлен, в основном, никотиновой кислотой и ее амидом, обладающими одинаковой витаминной активностью. Его некоторые синтетические производные проявляют самостоятельную, невитаминную активность и применяются в терапии: никотиновый спирт — сосудорасширяющее, оксиниациновая кислота — антигиперлипопротеинемик, кордиамин — аналептик.
Схема 10.2.16

Следует отметить, что никотиновая кислота и все ее производные синтетически очень доступные вещества, едва ли не самые доступные из всего класса витаминов.
Организм человека синтезирует этот витамин самостоятельно, но в недостаточных количествах. Много его содержится в дрожжах, сушеных грибах, в мясе и печени, в некоторых крупах.
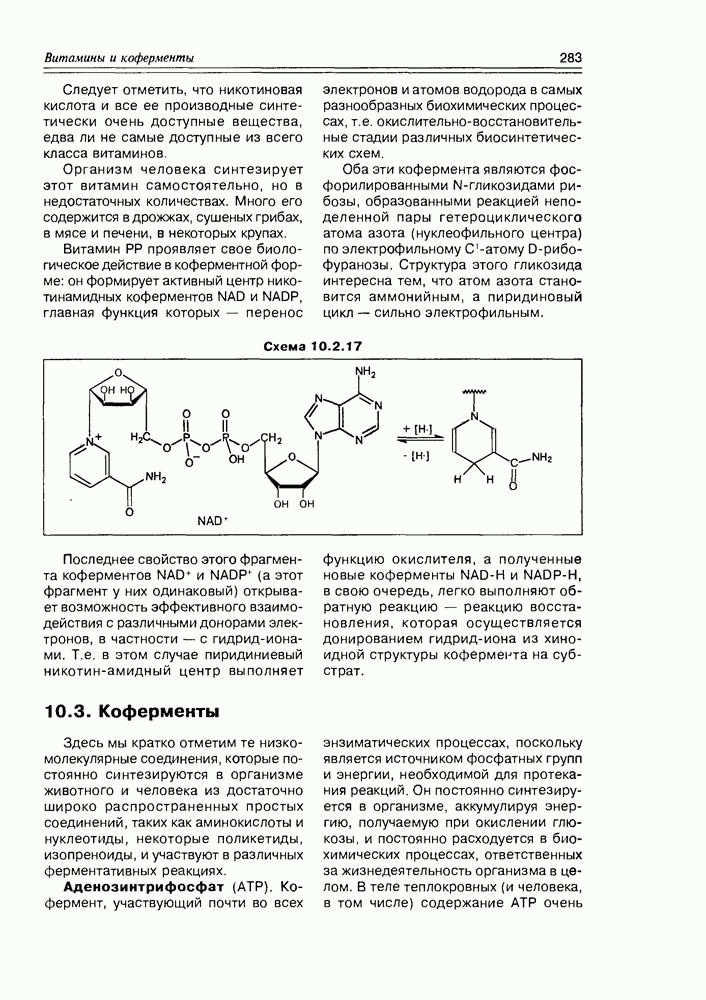
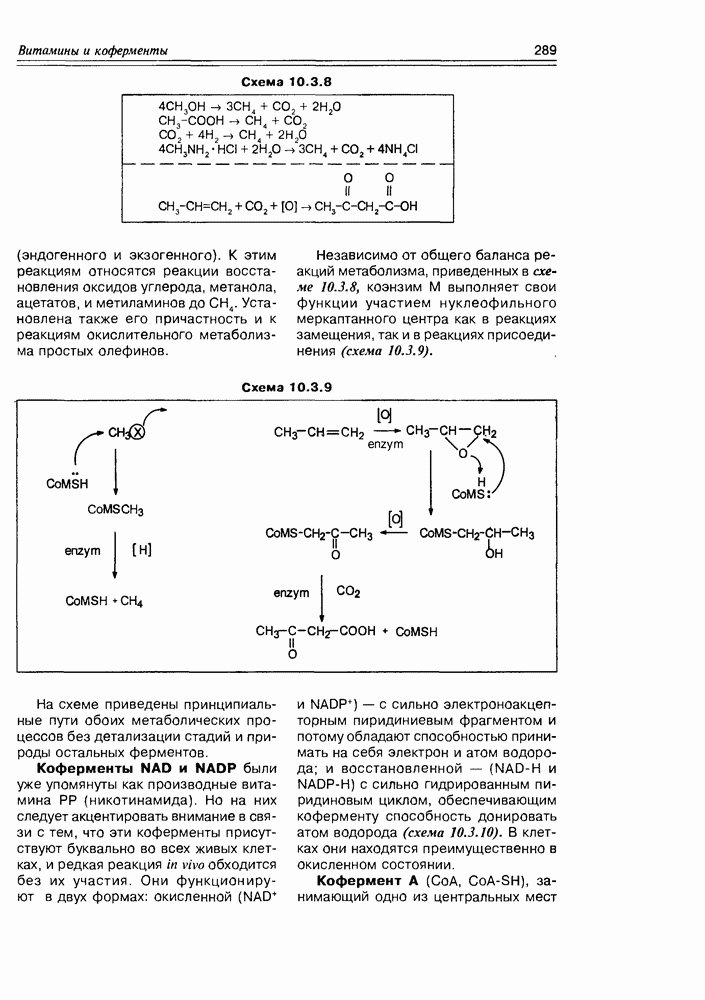
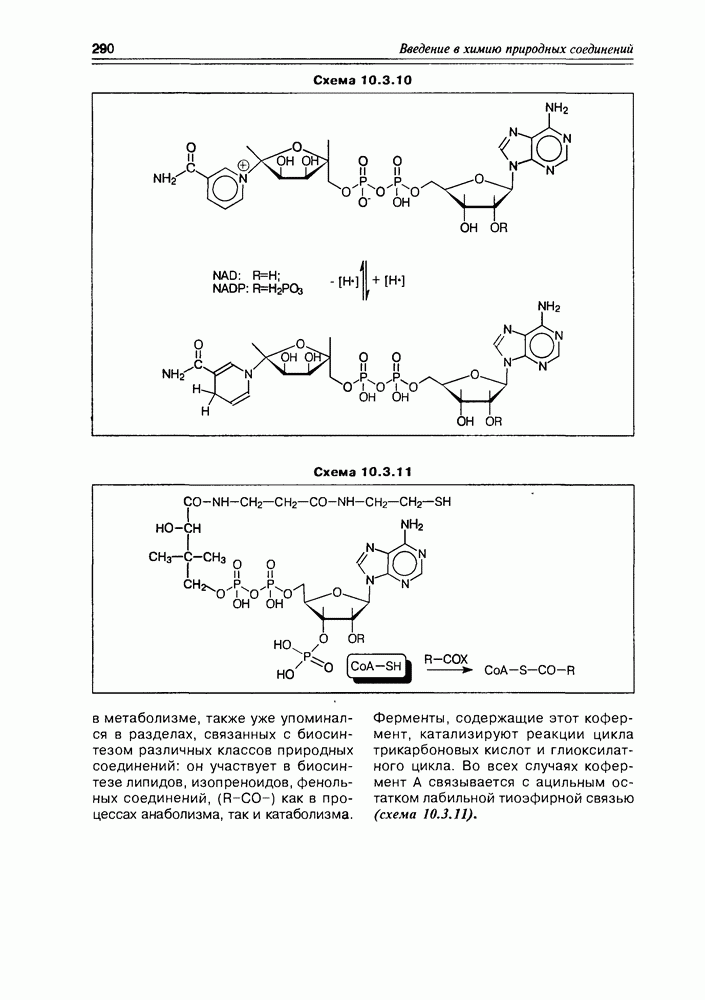
Витамин РР проявляет свое биологическое действие в коферментной форме: он формирует активный центр нико-тинамидных коферментов NAD и NADP, главная функция которых — перенос электронов и атомов водорода в самых разнообразных биохимических процессах, т.е. окислительно-восстановительные стадии различных биосинтетических схем.
Оба эти кофермента являются фосфорилированными N-гликозидами рибозы, образованными реакцией неподеленной пары гетероциклического атома азота (нуклеофильного центра) по электрофильному С-атому D-рибофуранозы. Структура этого гликозида интересна тем, что атом азота становится аммонийным, а пиридиновый цикл — сильно электрофильным.
Схема 10.2.17

Последнее свойство этого фрагмента коферментов  этот фрагмент у них одинаковый) открывает возможность эффективного взаимодействия с различными донорами электронов, в частности — с гидрид-ионами. Т.е. в этом случае пиридиниевый никотин-амидный центр выполняет
этот фрагмент у них одинаковый) открывает возможность эффективного взаимодействия с различными донорами электронов, в частности — с гидрид-ионами. Т.е. в этом случае пиридиниевый никотин-амидный центр выполняет
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ АВТОРА
- Глава 1. ВВЕДЕНИЕ
- 1.1. Предмет химии природных соединений
- 1.2. Классификация природных соединений
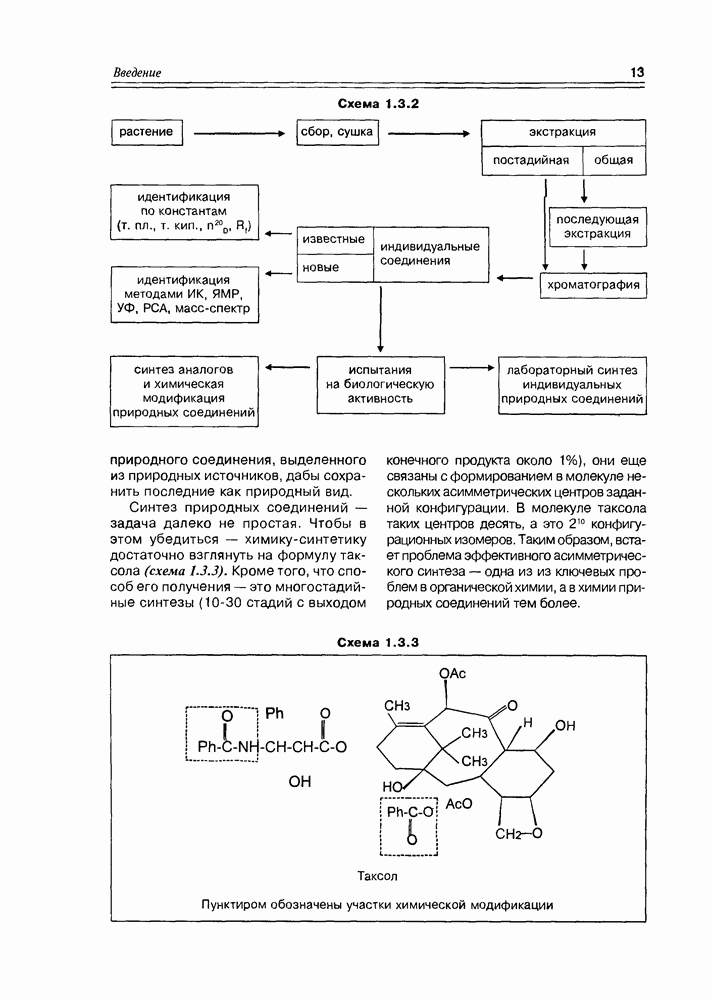
- 1.3. Методология химии природных соединений
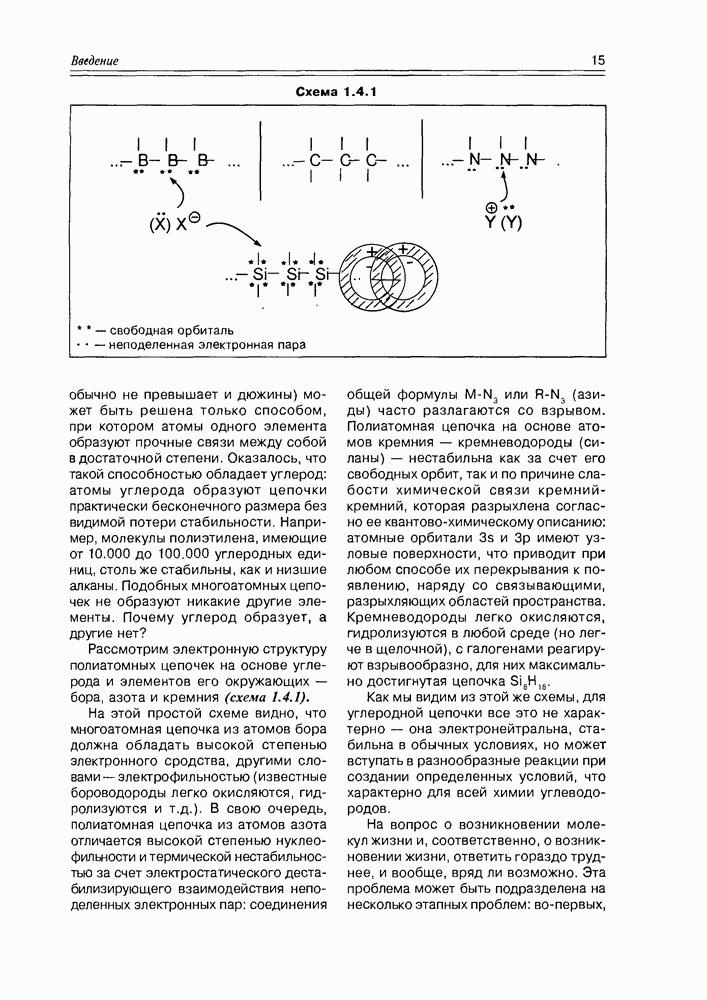
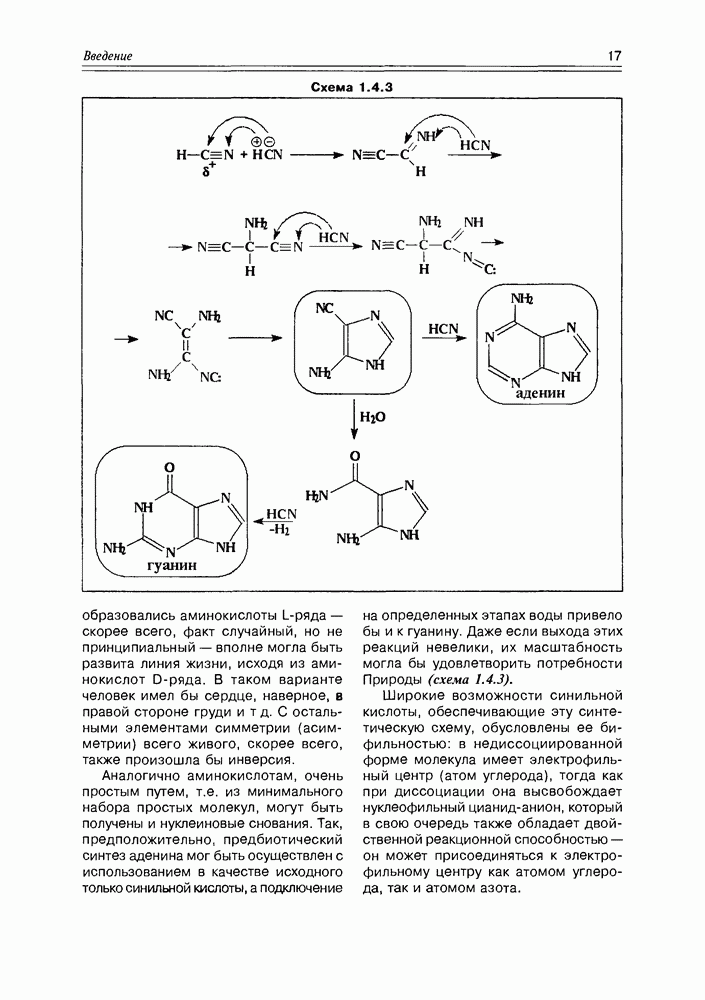
- 1.4. Углерод и жизнь
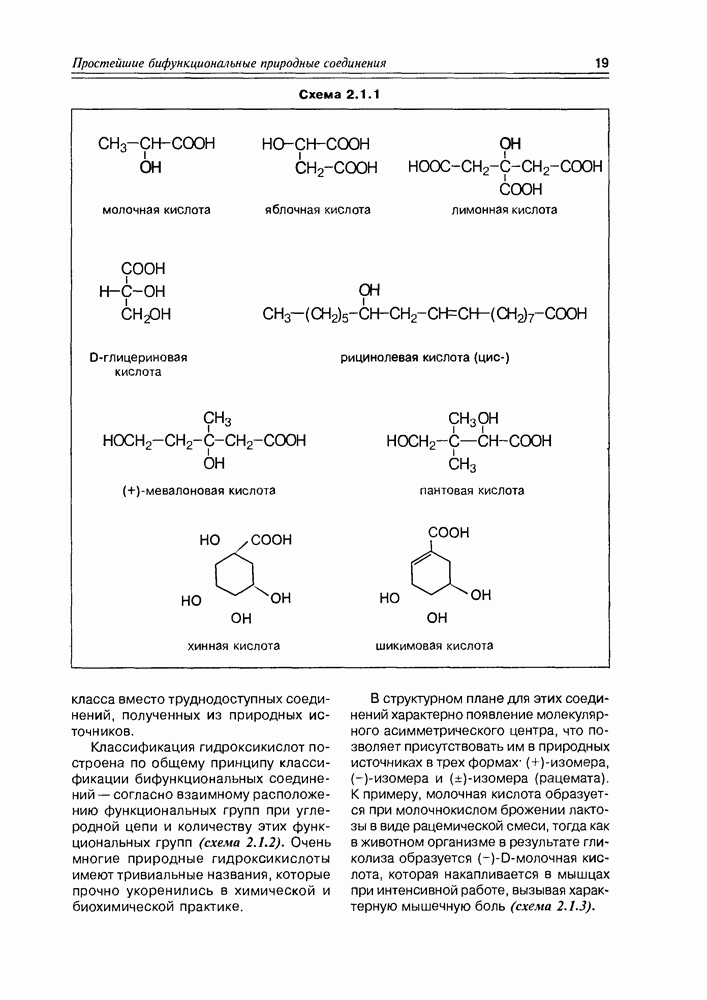
- Глава 2. ПРОСТЕЙШИЕ БИФУНКЦИОНАЛЬНЫЕ ПРИРОДНЫЕ СОЕДИНЕНИЯ — МОСТИК К МАССИВУ ПРИРОДНЫХ СОЕДИНЕНИЙ
- 2.2. Оксокислоты
- 2.3. Аминоспирты
- Глава 3. УГЛЕВОДЫ
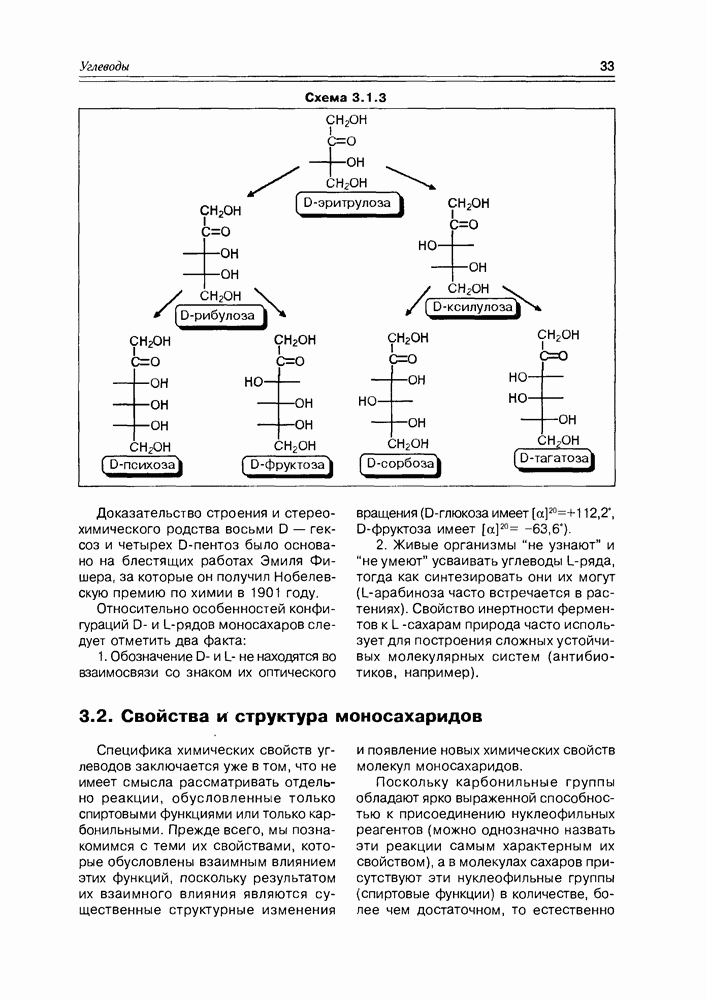
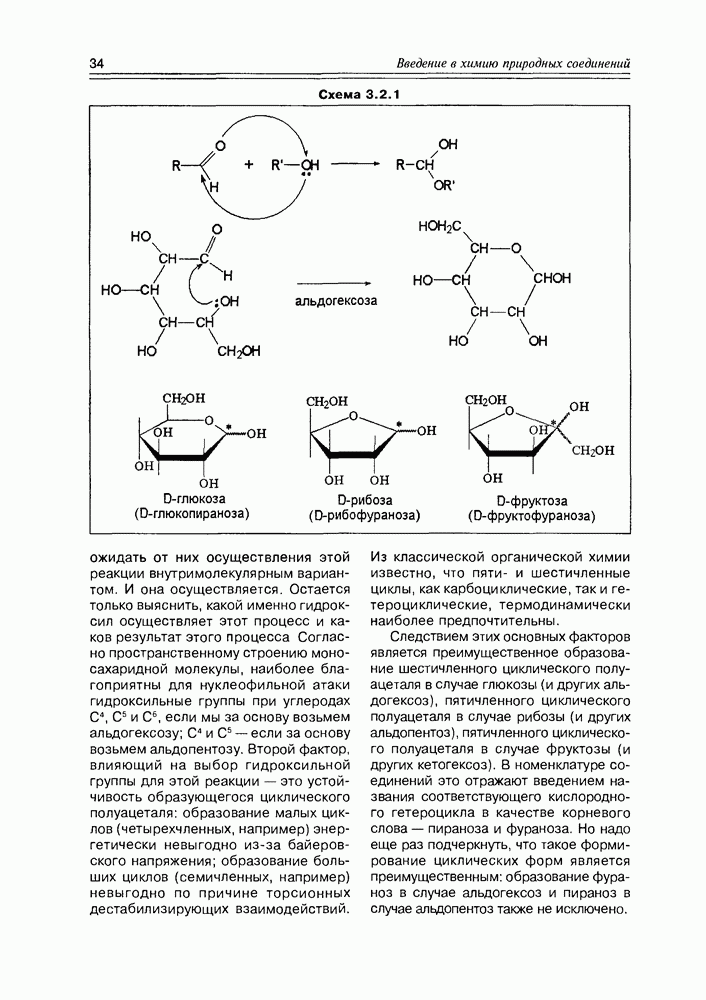
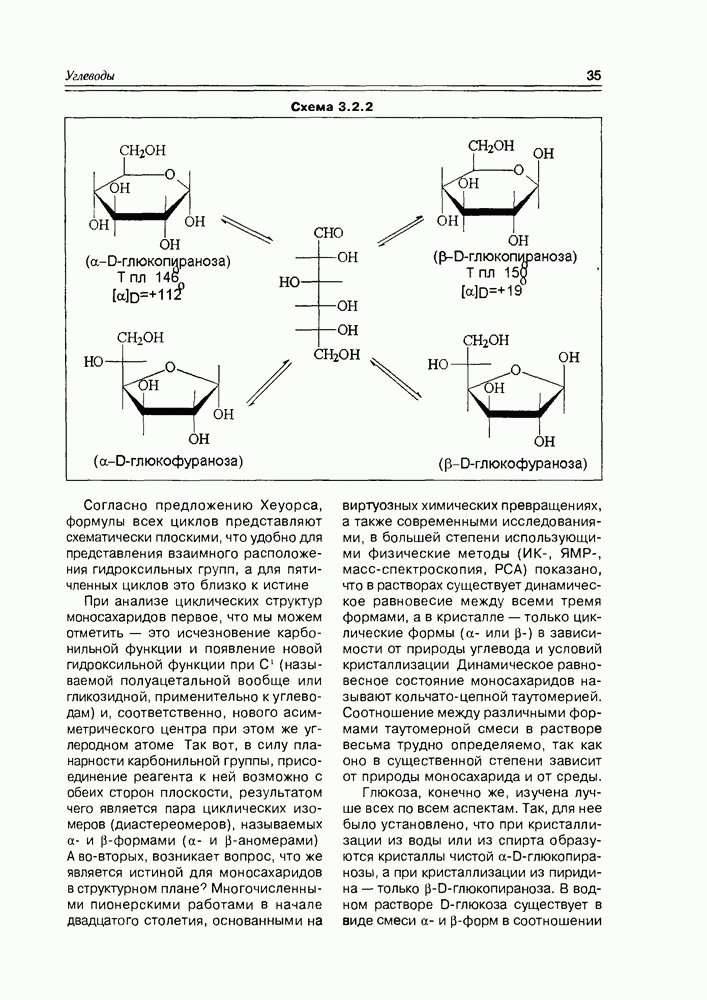
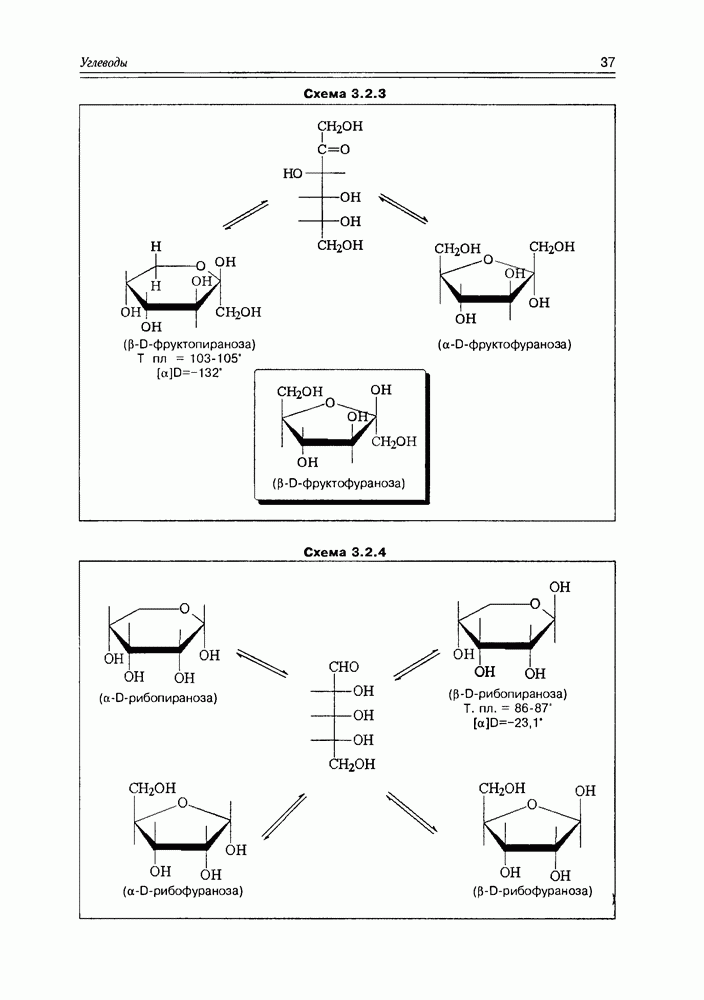
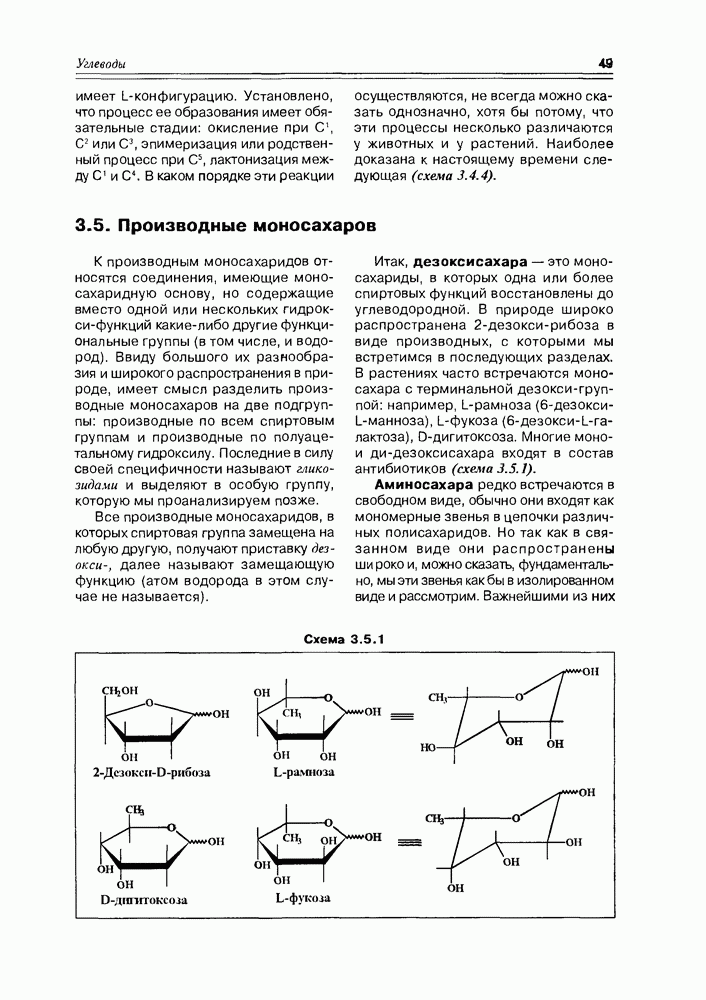
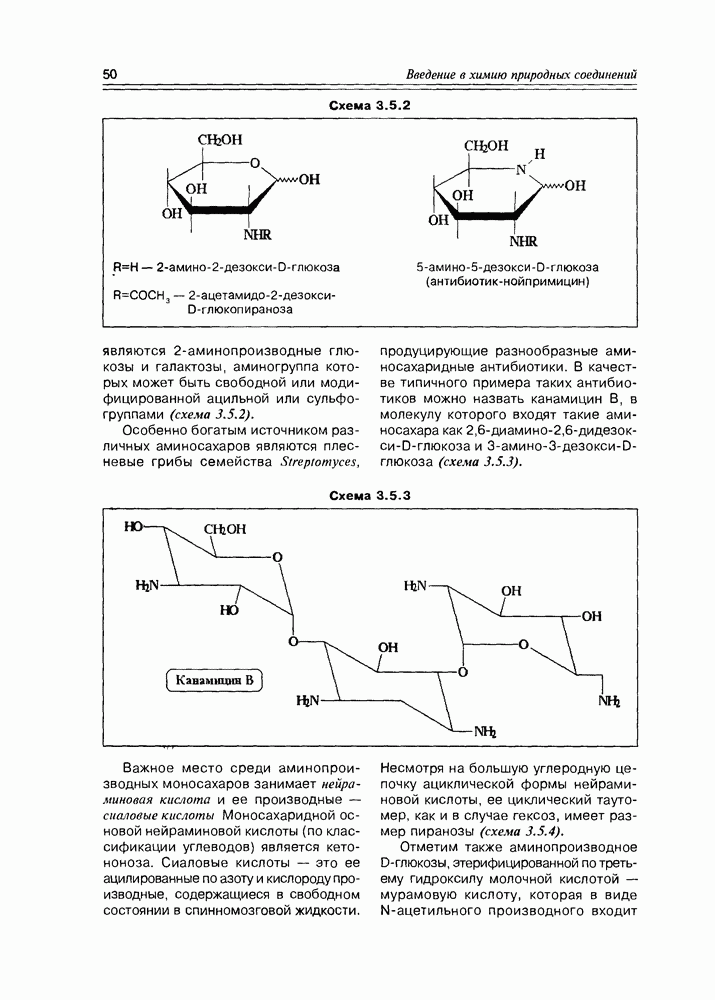
- 3.2. Свойства и структура моносахаридов
- 3.3. Химические свойства моносахаридов
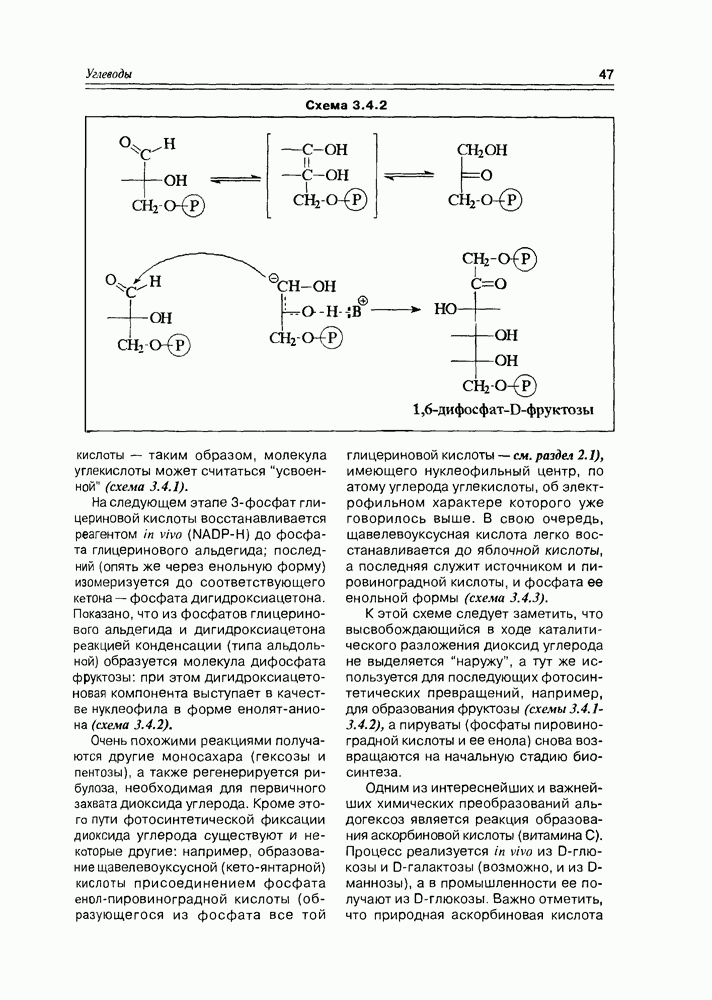
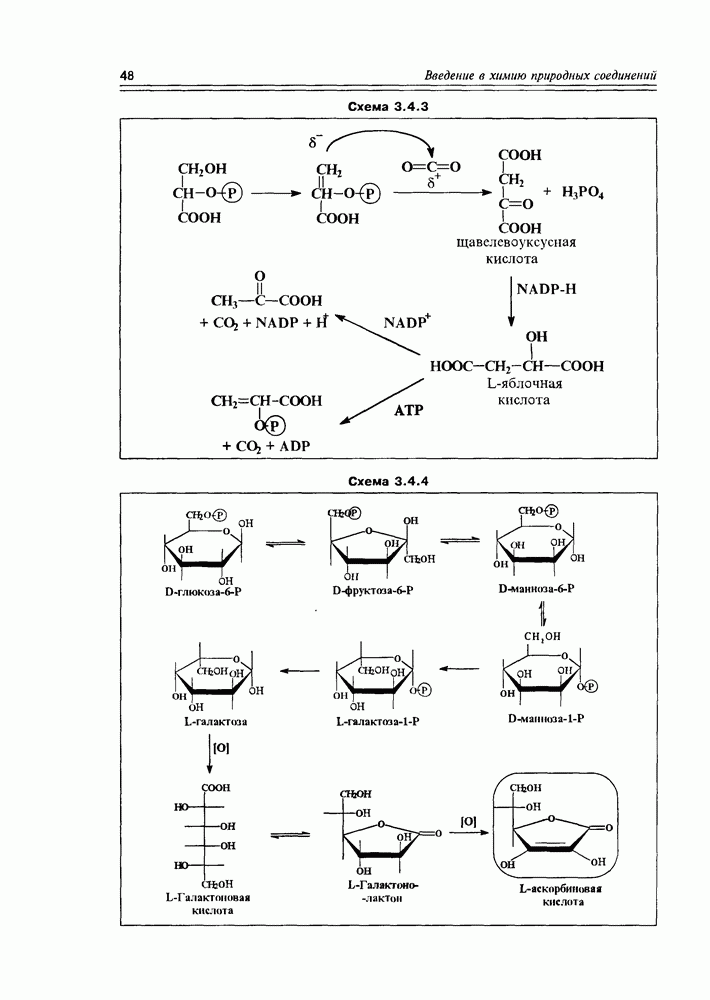
- 3.4. Биосинтетические реакции углеводов
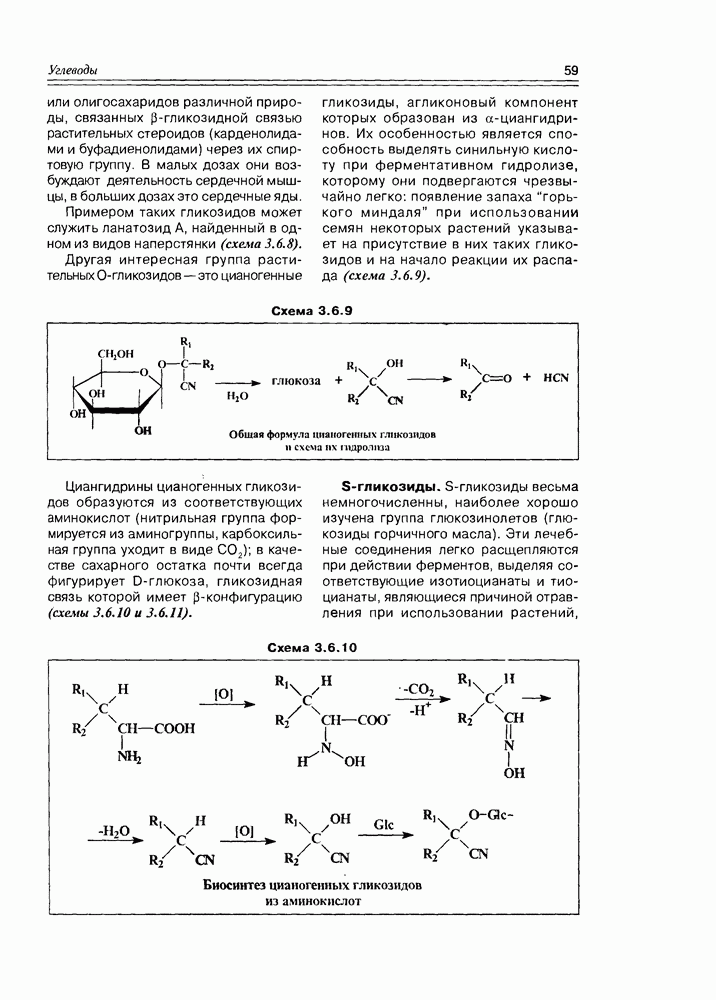
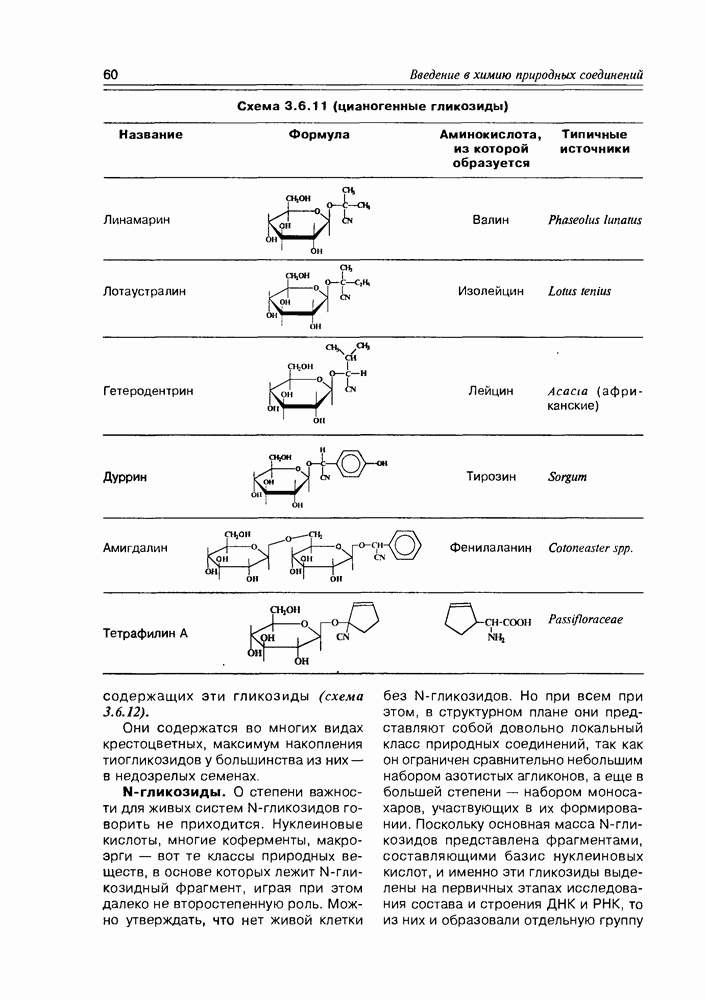
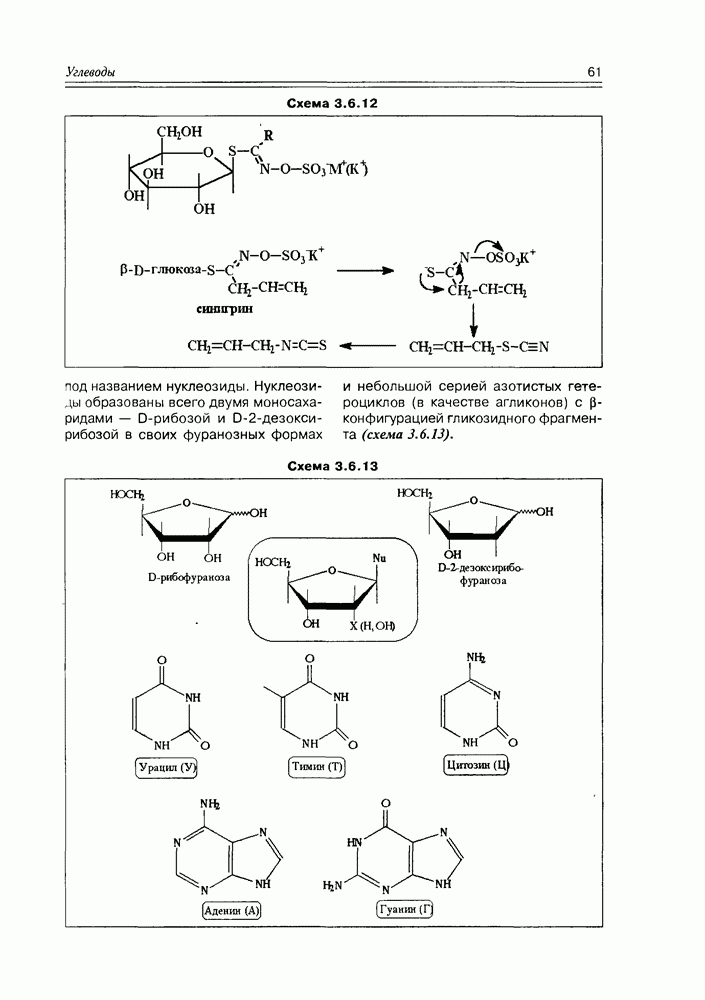
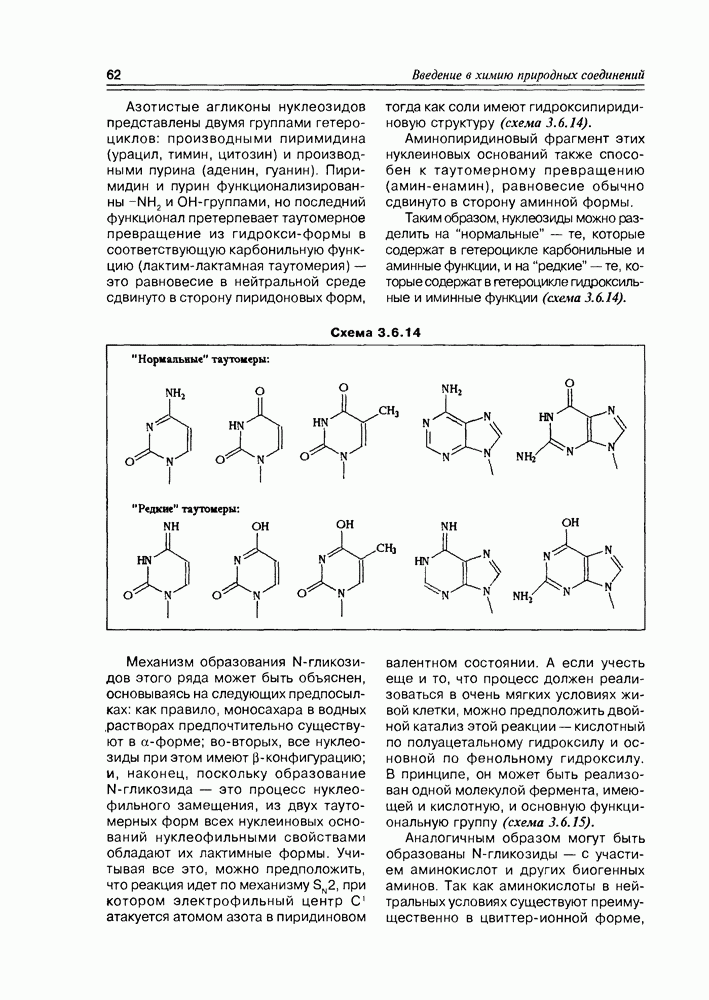
- 3.6. Гликозиды
- Глава 4. АМИНОКИСЛОТЫ, ПЕПТИДЫ, БЕЛКИ
- 4.2. Химические свойства а-аминокислот
- 4.3. Биосинтез аминокислот
- 4.4. Полипептиды
- 4.5. Дикетопиперазины
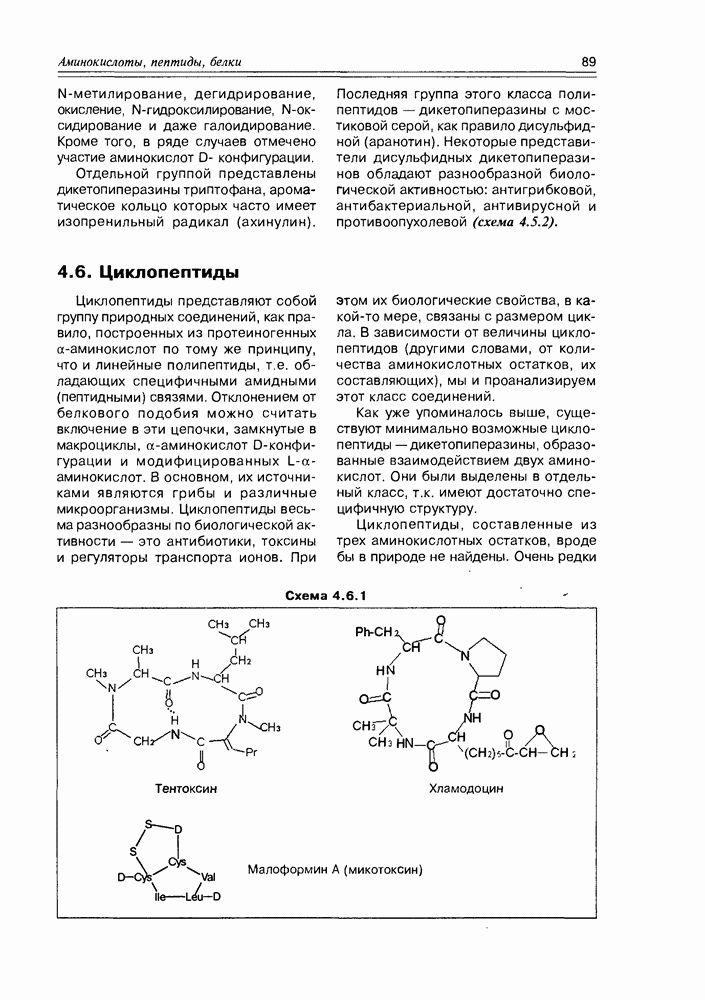
- 4.6. Циклопептиды
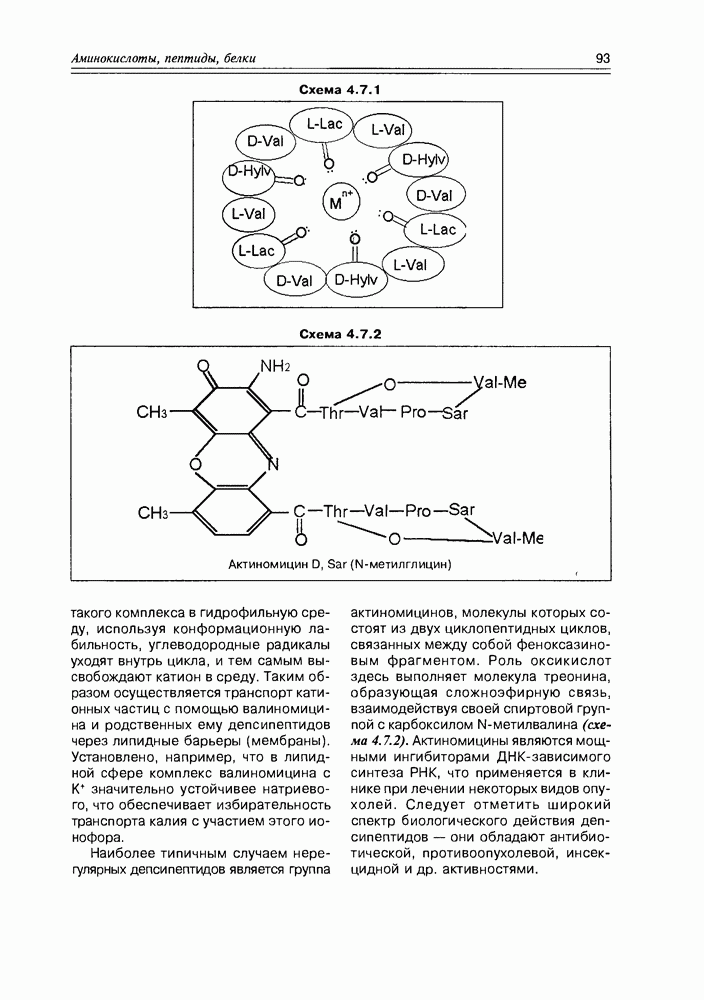
- 4.7. Депсипептиды
- 4.8. Белки
- Глава 5. ЛИПИДЫ: ЖИРНЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
- 5.1.1. Химические свойства жирных кислот
- 5.2. Метаболиты жирных кислот
- 5.2.2. Карбоциклические оксилипины
- 5.3. Жиры и жироподобные производные жирных кислот
- 5.4. Биосинтез жирных кислот и их производных
- Глава 6. ИЗОПРЕНОИДЫ-1
- 6.2. Гемитерпены
- 6.3. Монотерпены
- 6.4. Ациклические монотерпены
- 6.5. Моноциклические терпены
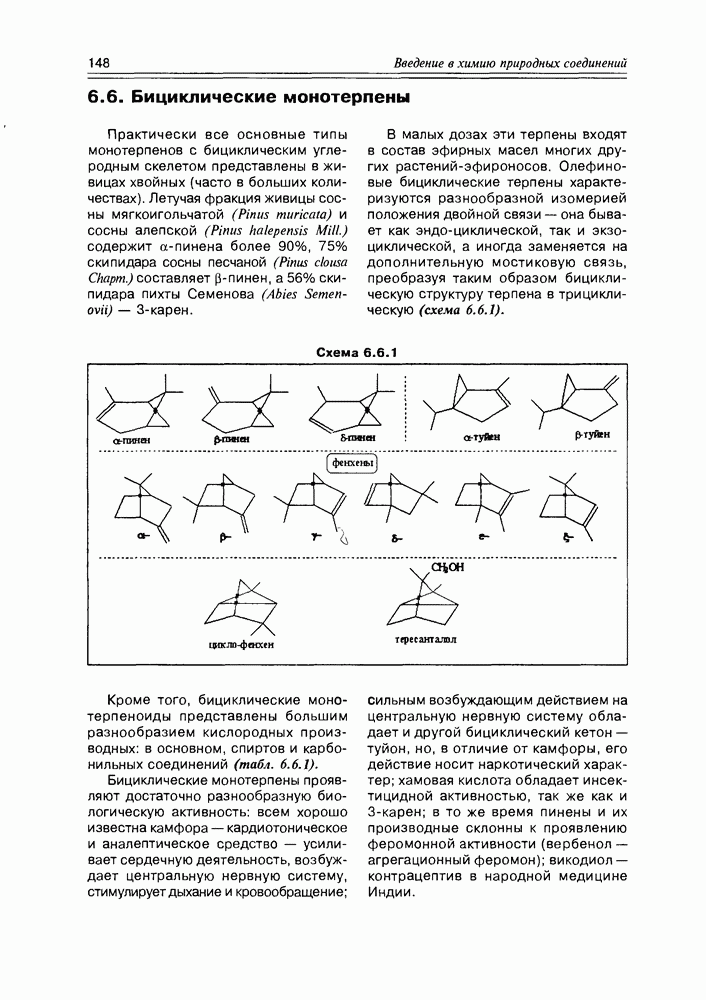
- 6.6. Бициклические монотерпены
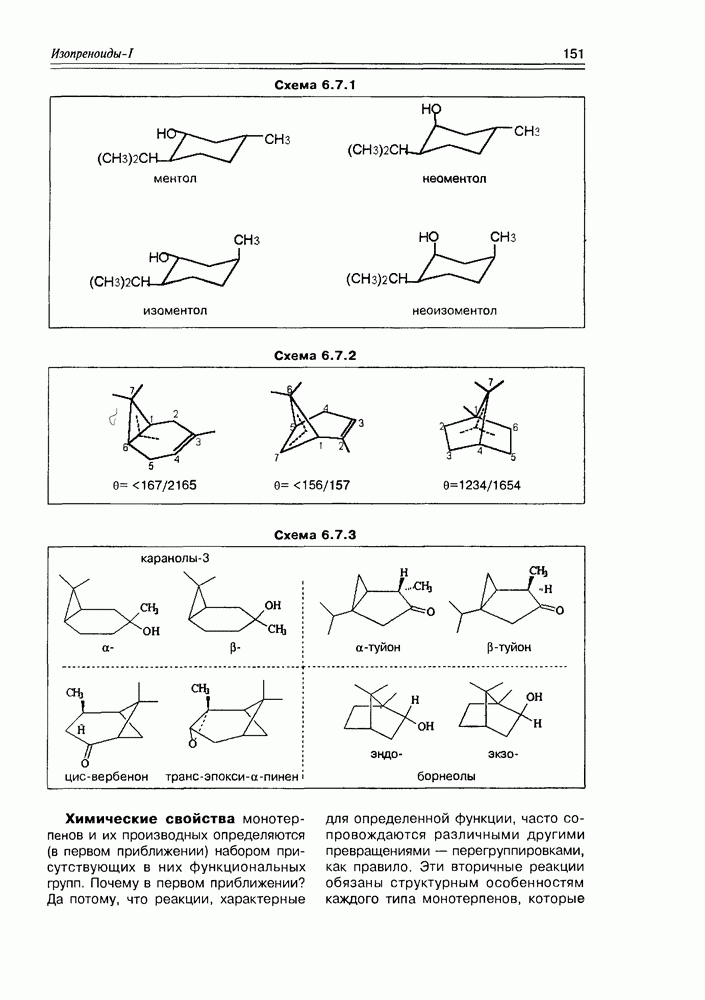
- 6.7. Строение и свойства монотерпенов
- 6.8. Биосинтез изопреноидов
- Глава 7. ИЗОПРЕНОИДЫ II. ОТ СЕСКВИТЕРПЕНОВ ДО ПОЛИТЕРПЕНОВ
- 7.2. Химические свойства сесквитерпенов
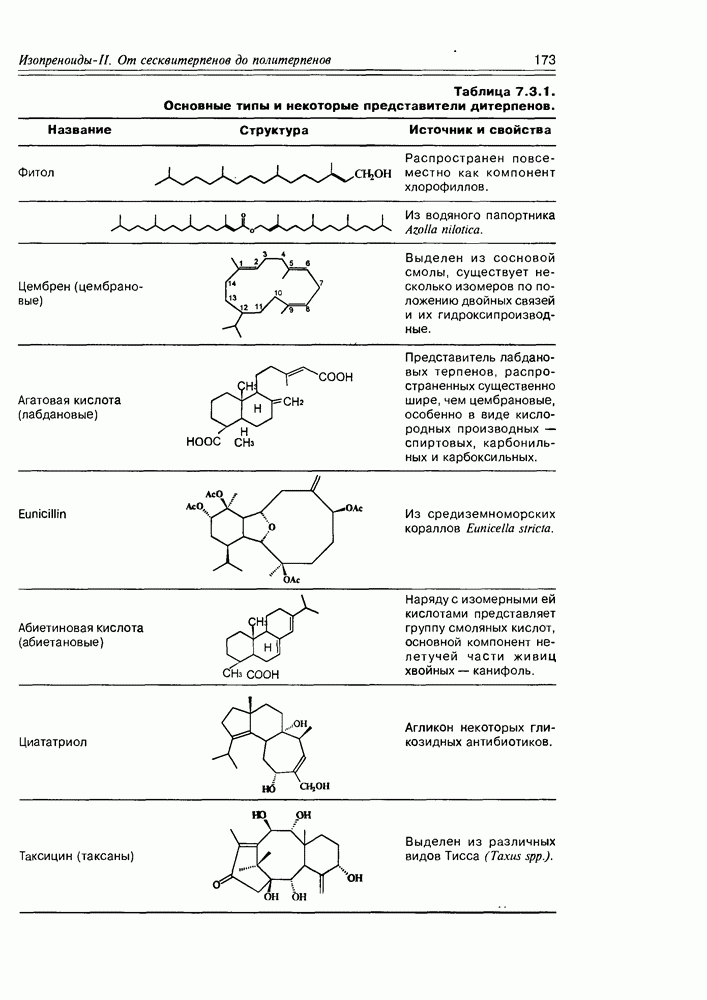
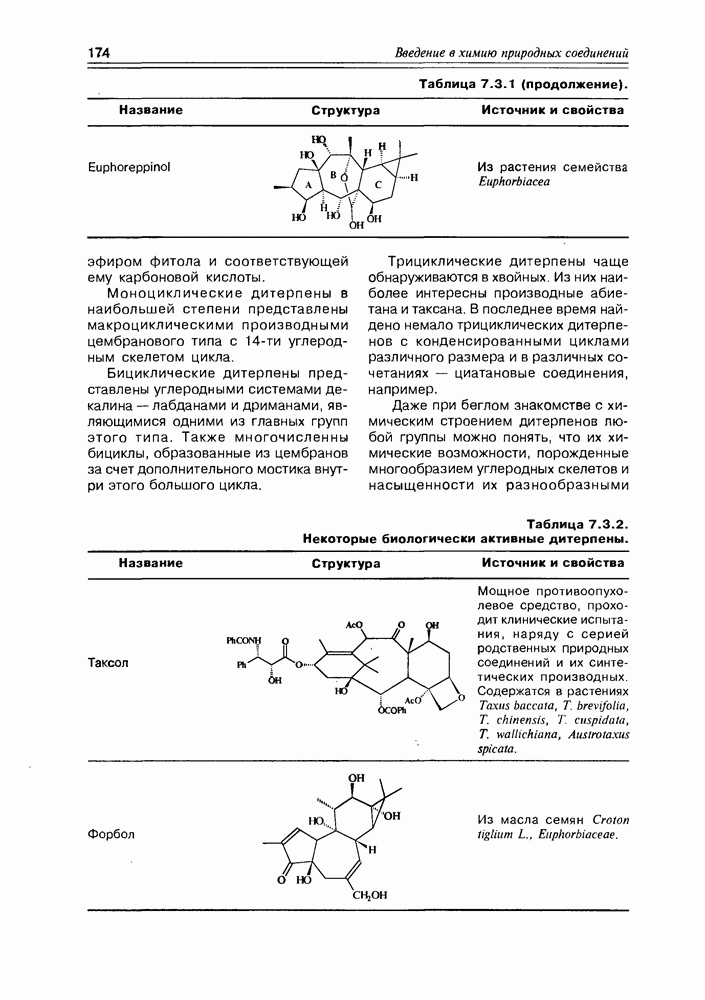
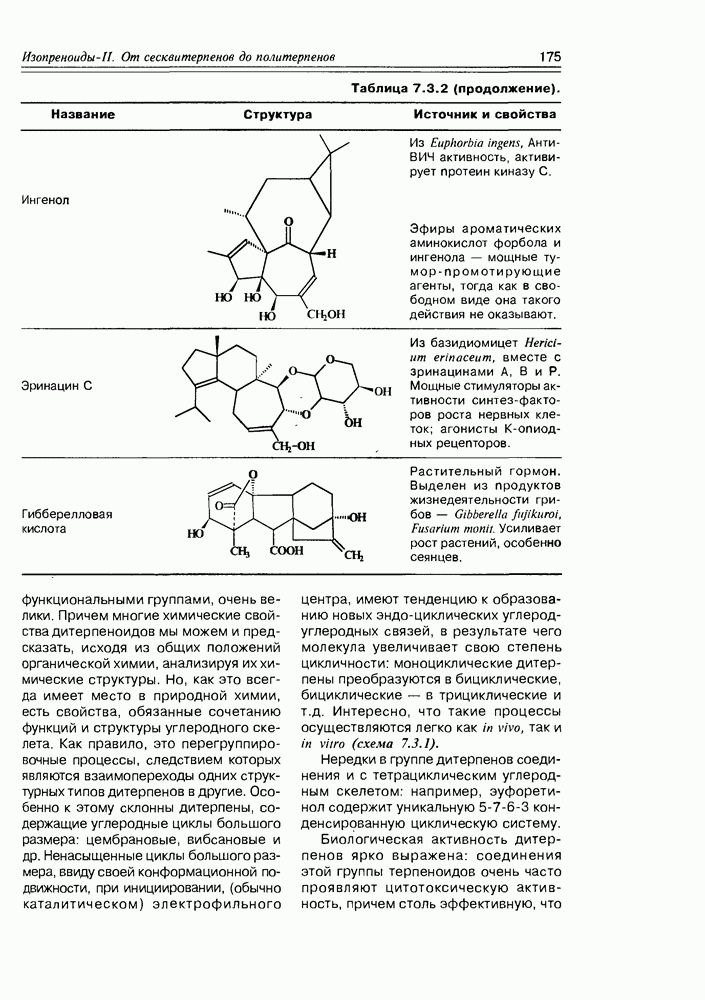
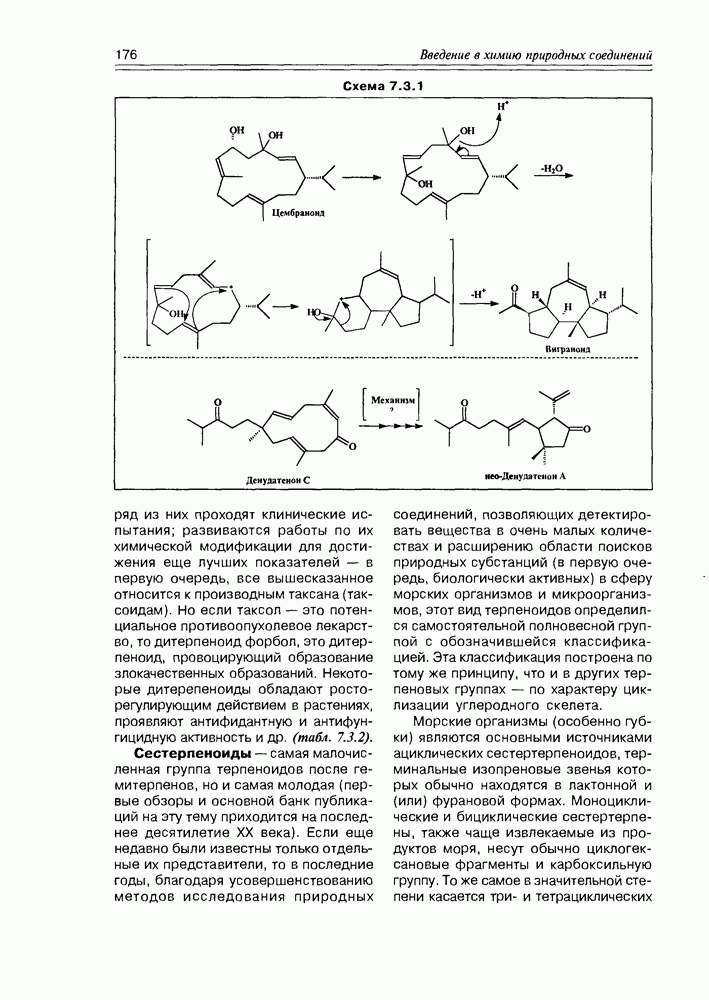
- 7.3. Дитерпены и сестертерпены
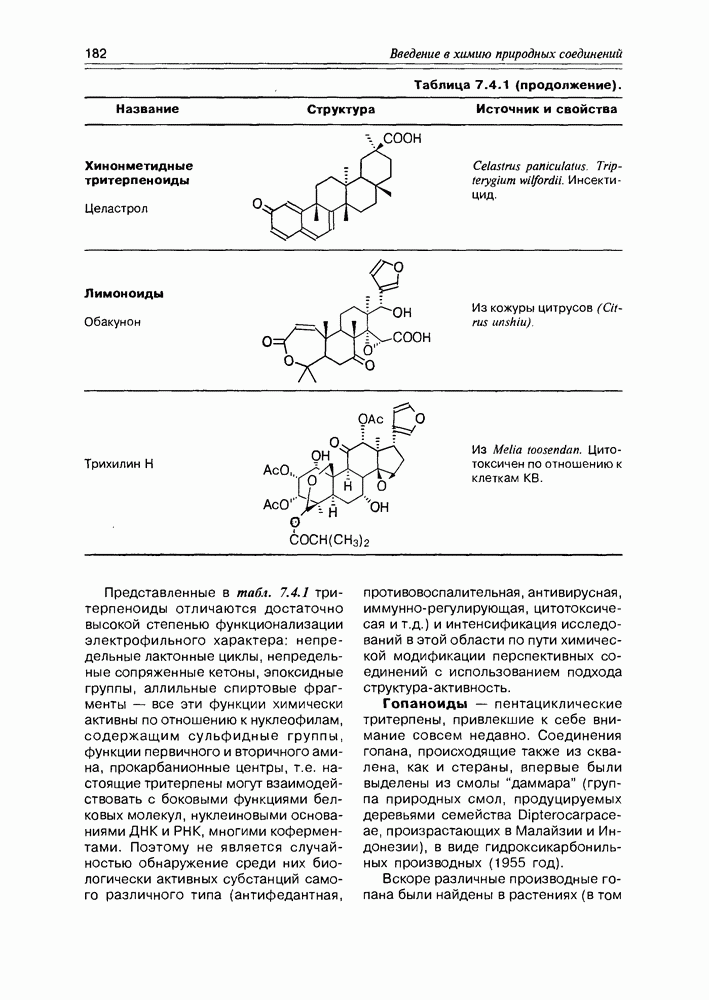
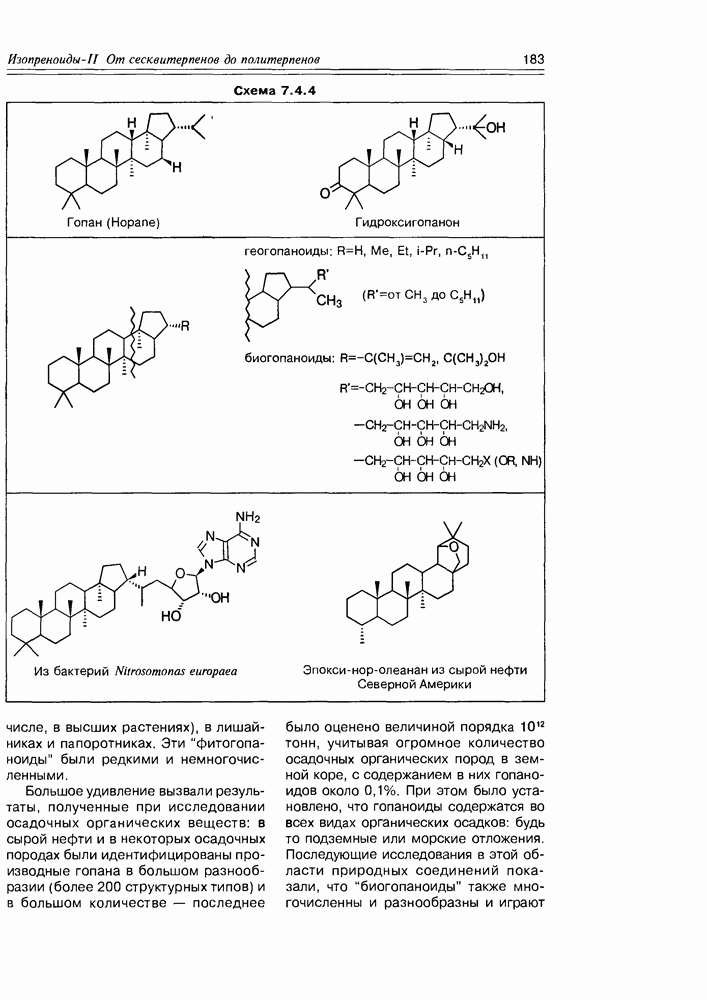
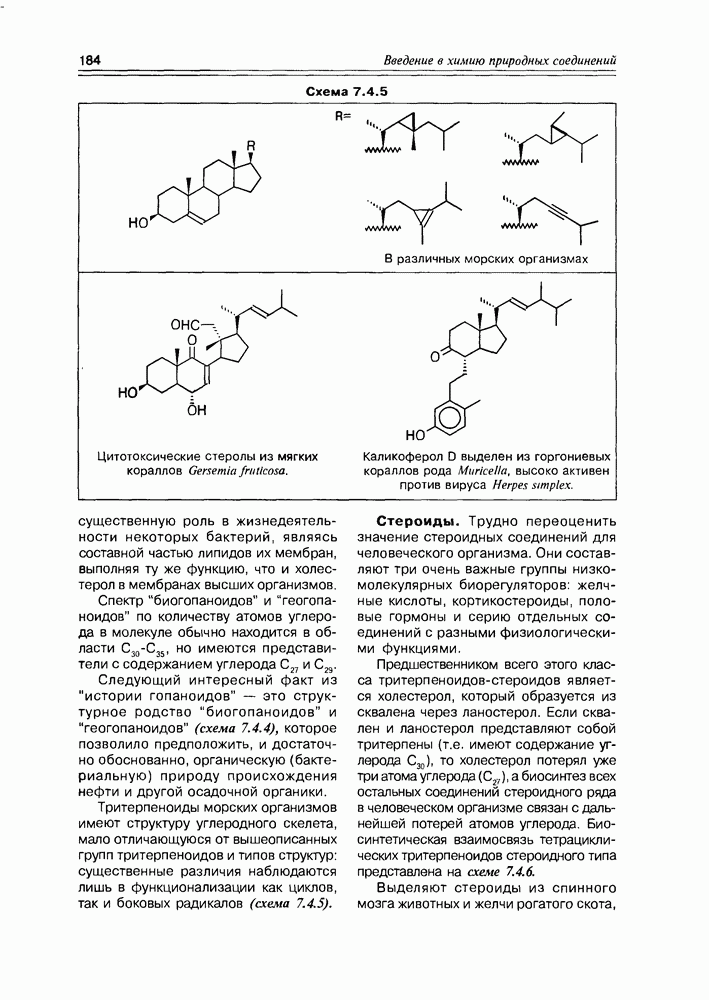
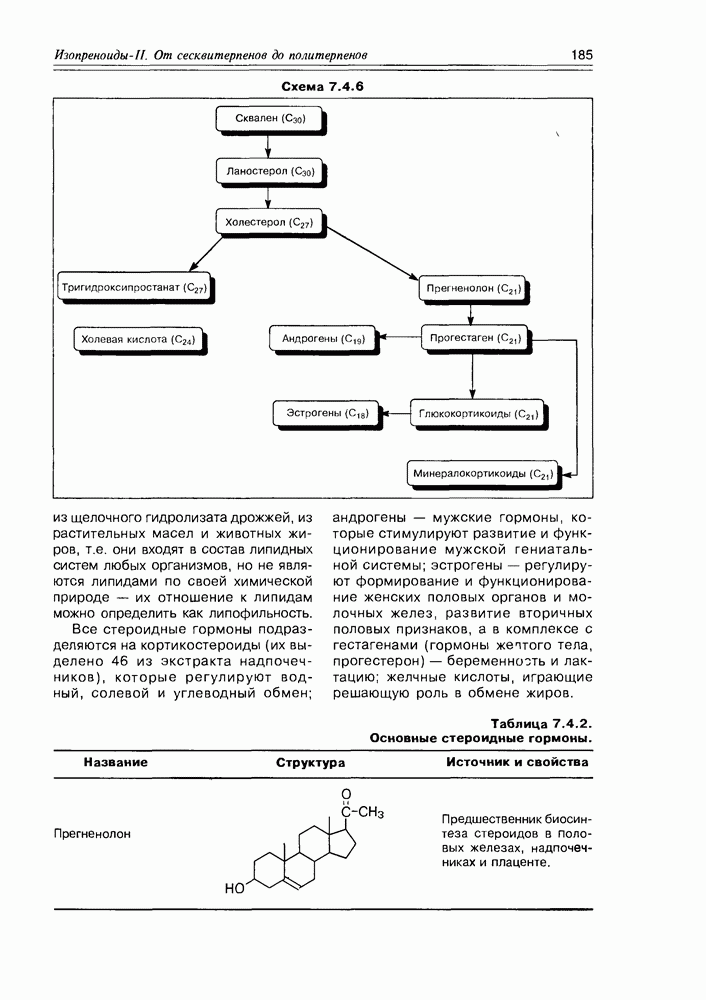
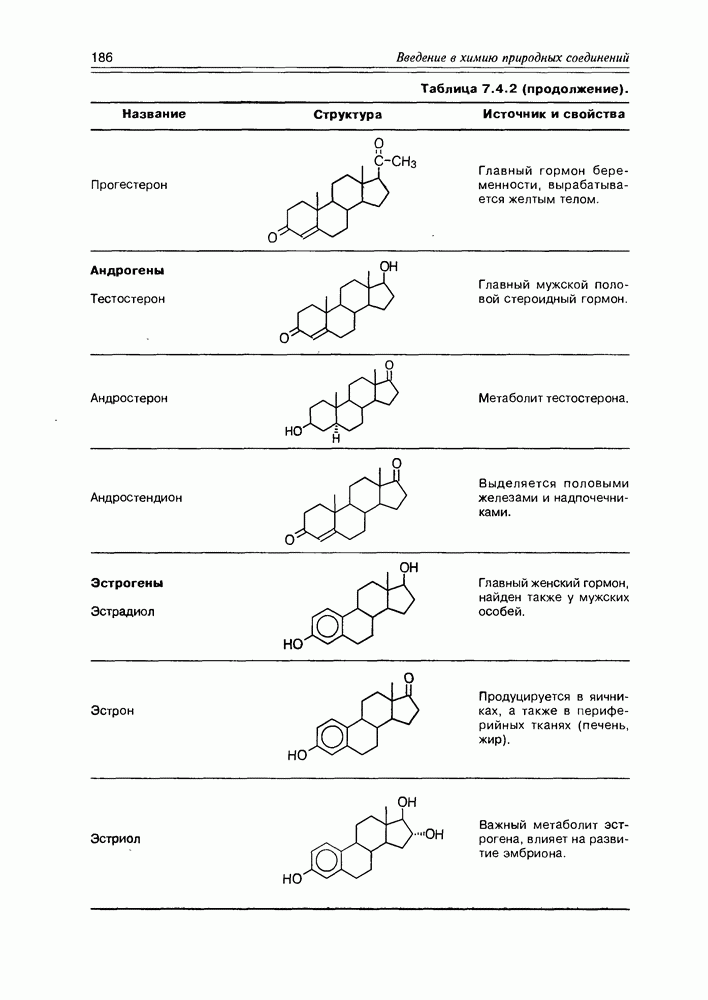
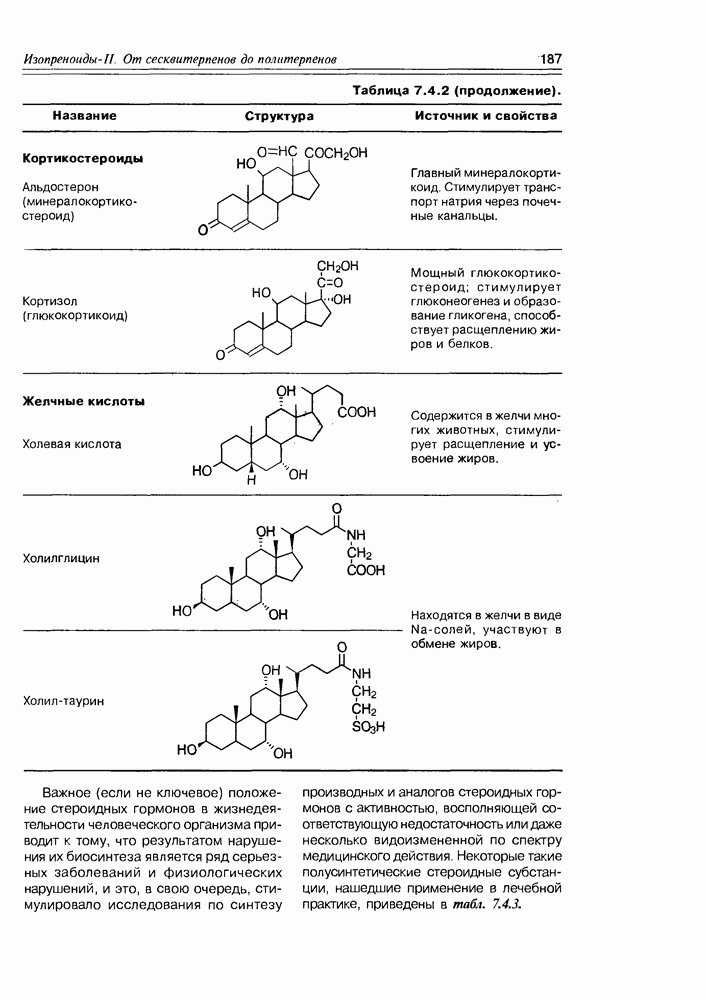
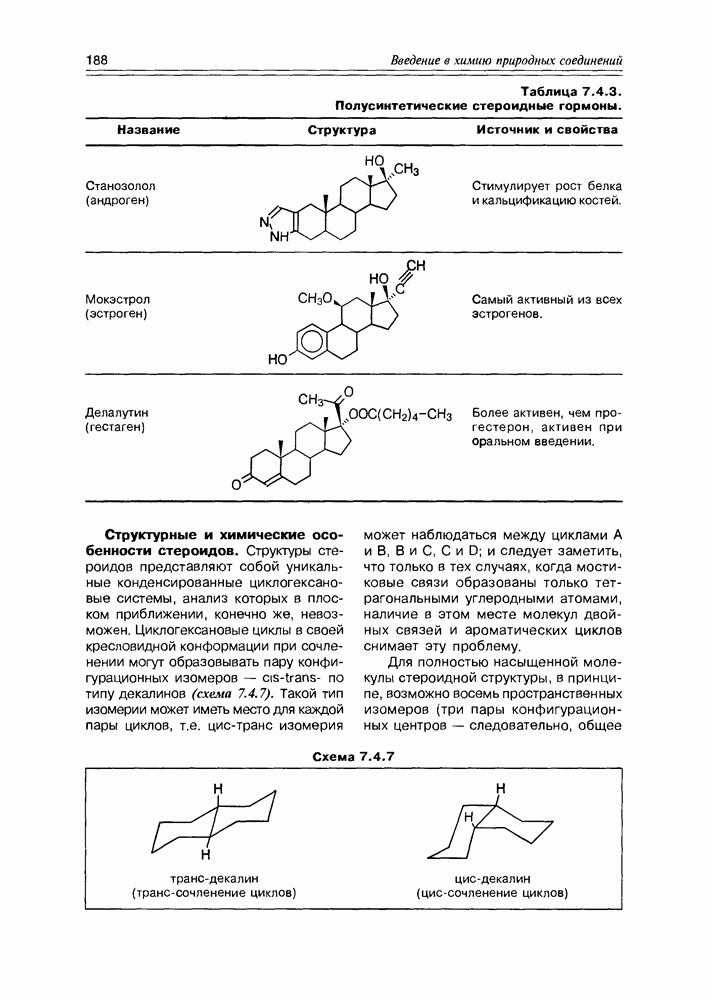
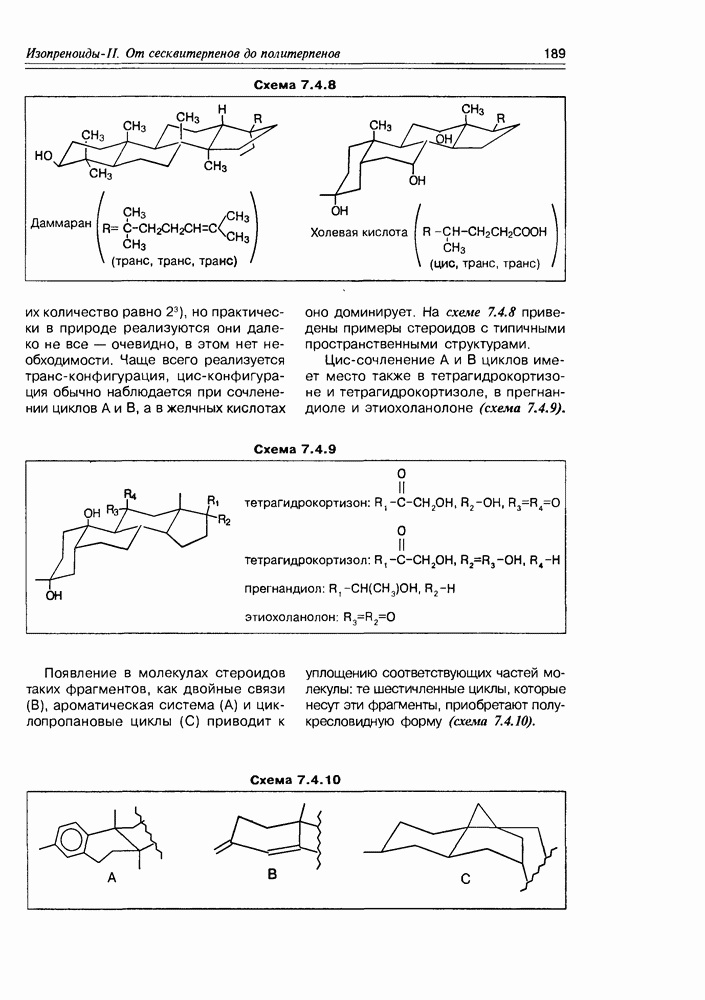
- 7.4. Тритерпеноиды и стероиды
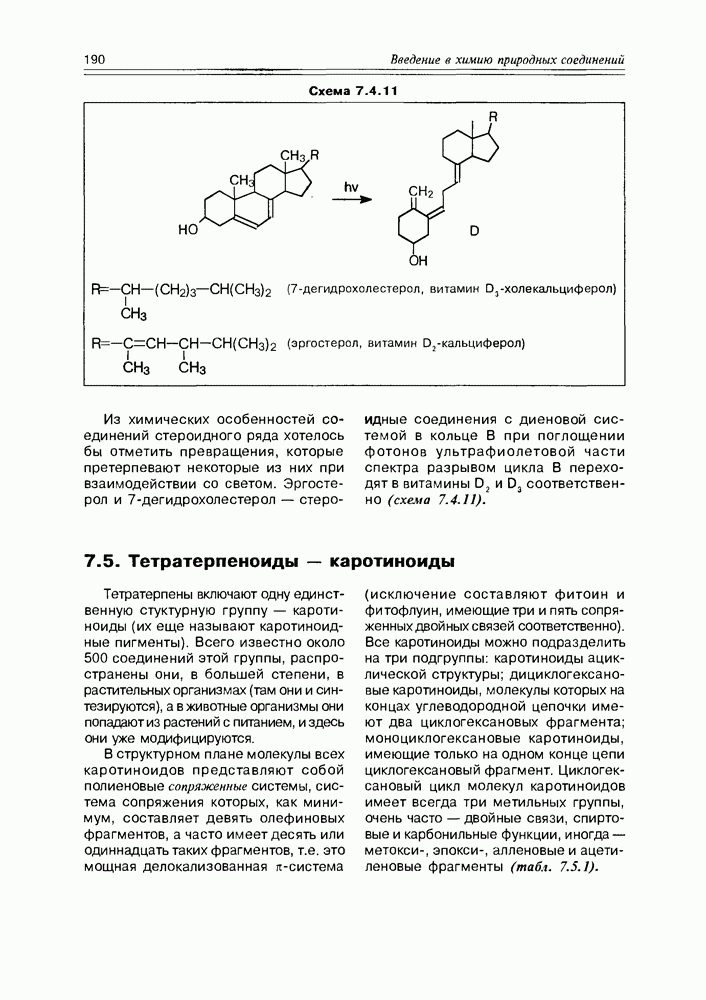
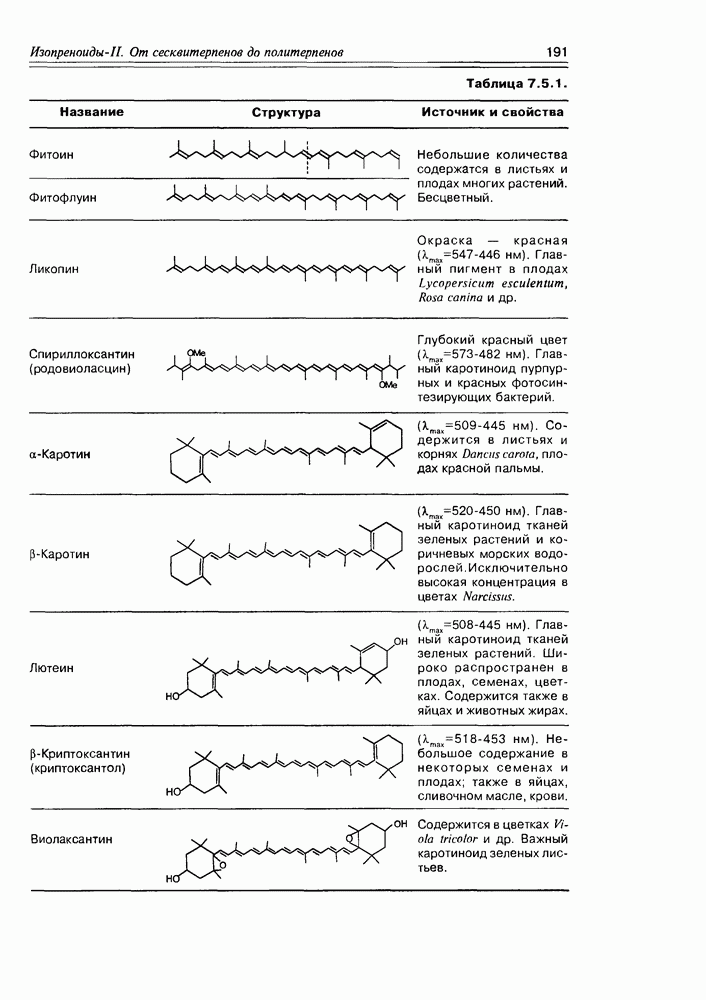
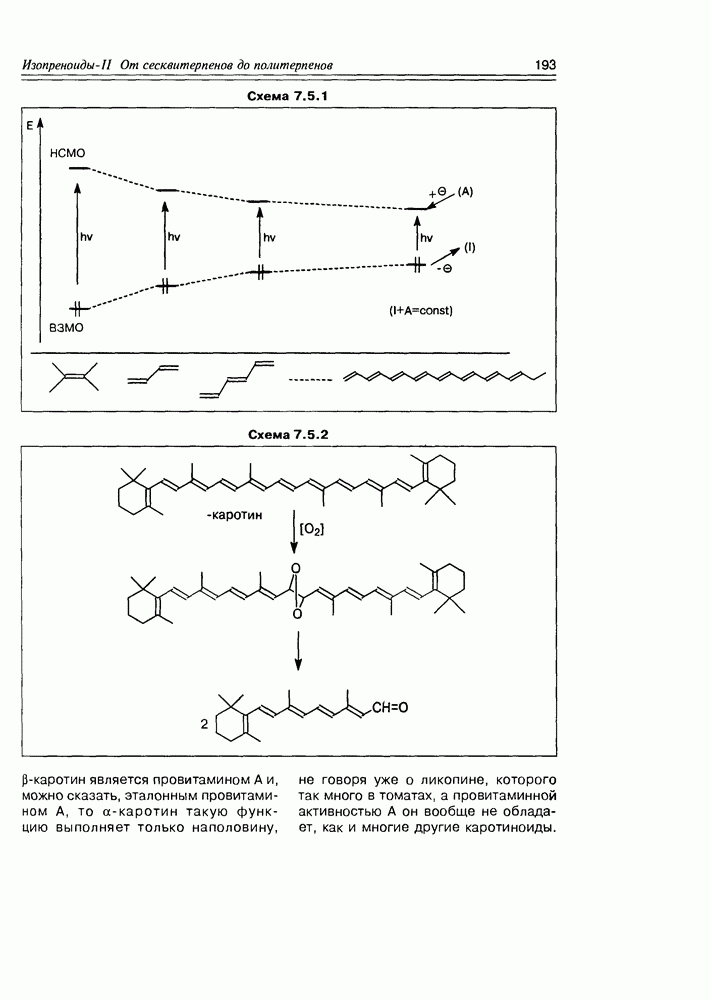
- 7.5. Тетратерпеноиды — каротиноиды
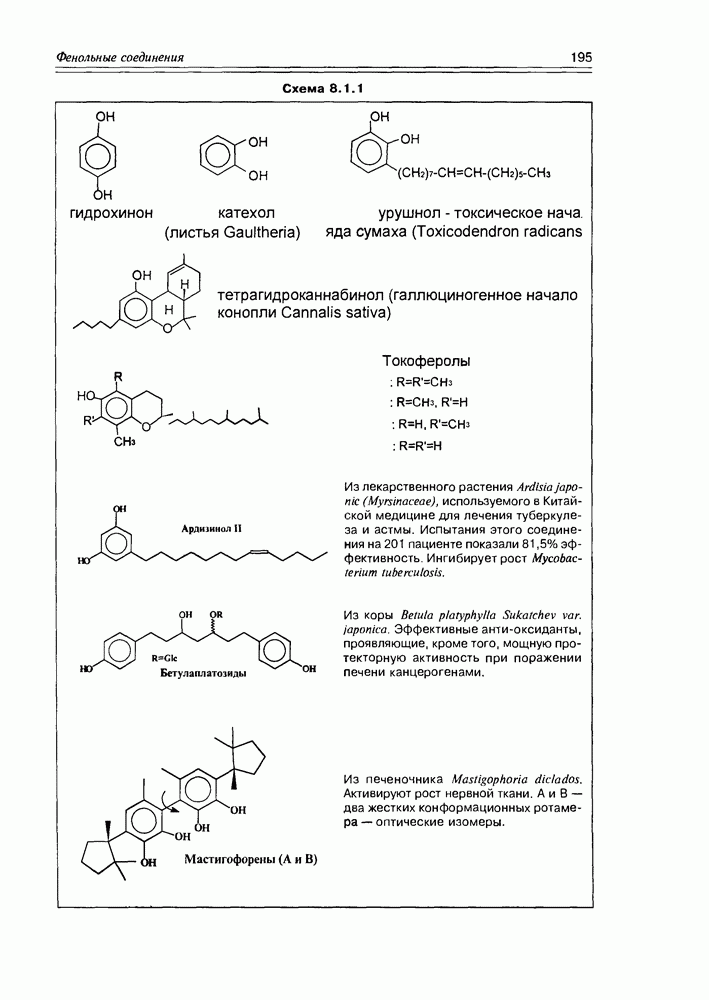
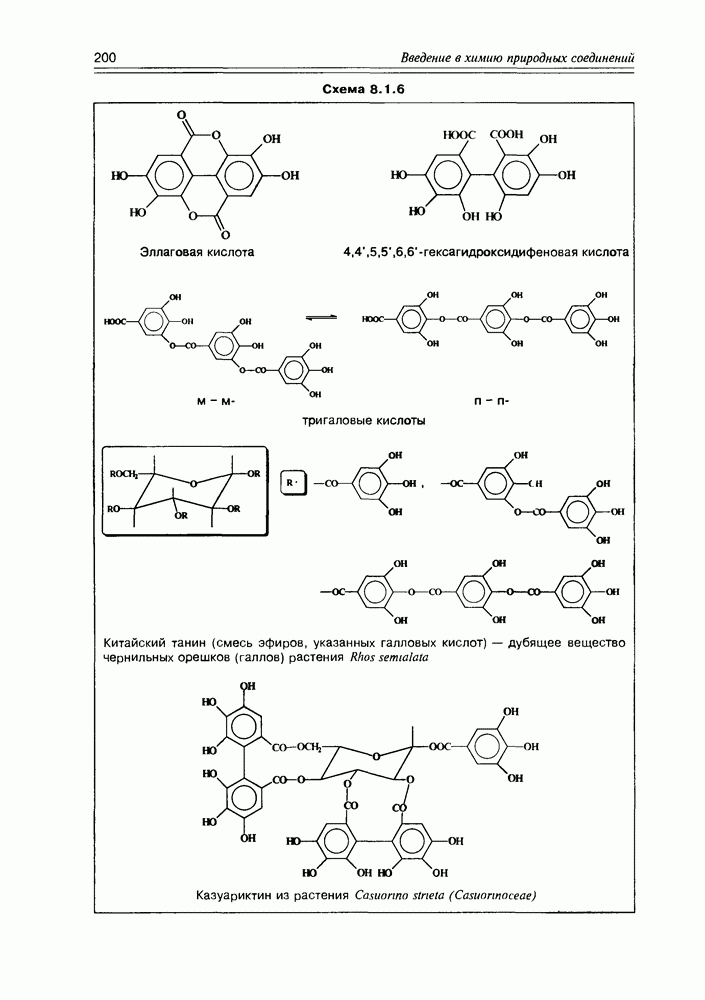
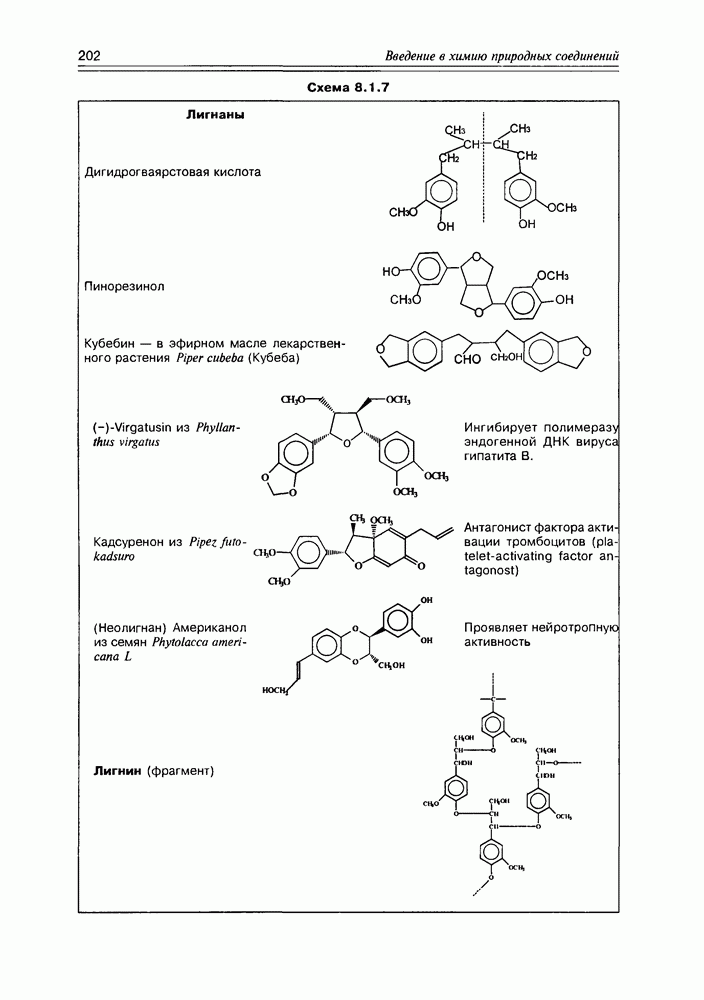
- Глава 8. ФЕНОЛЬНЫЕ СОЕДИНЕНИЯ
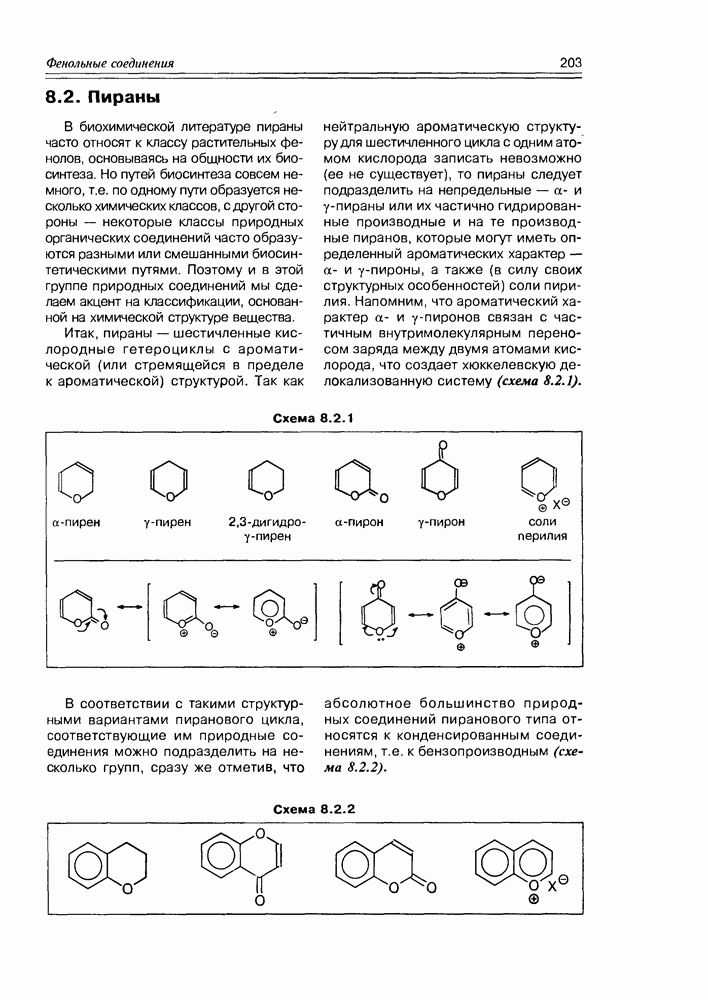
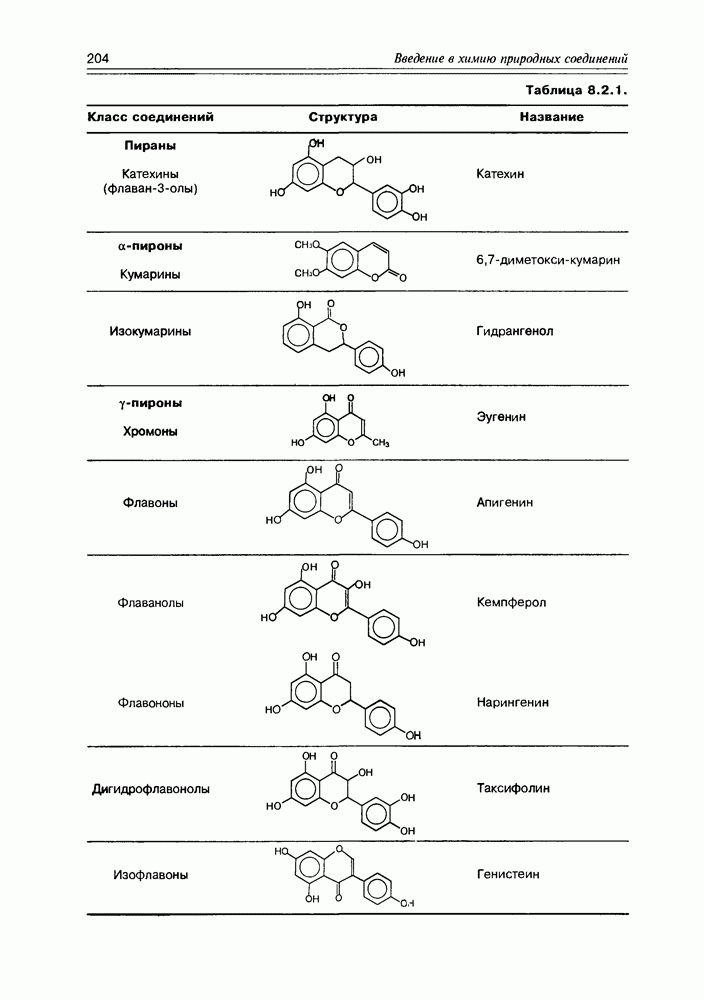
- 8.2. Пираны
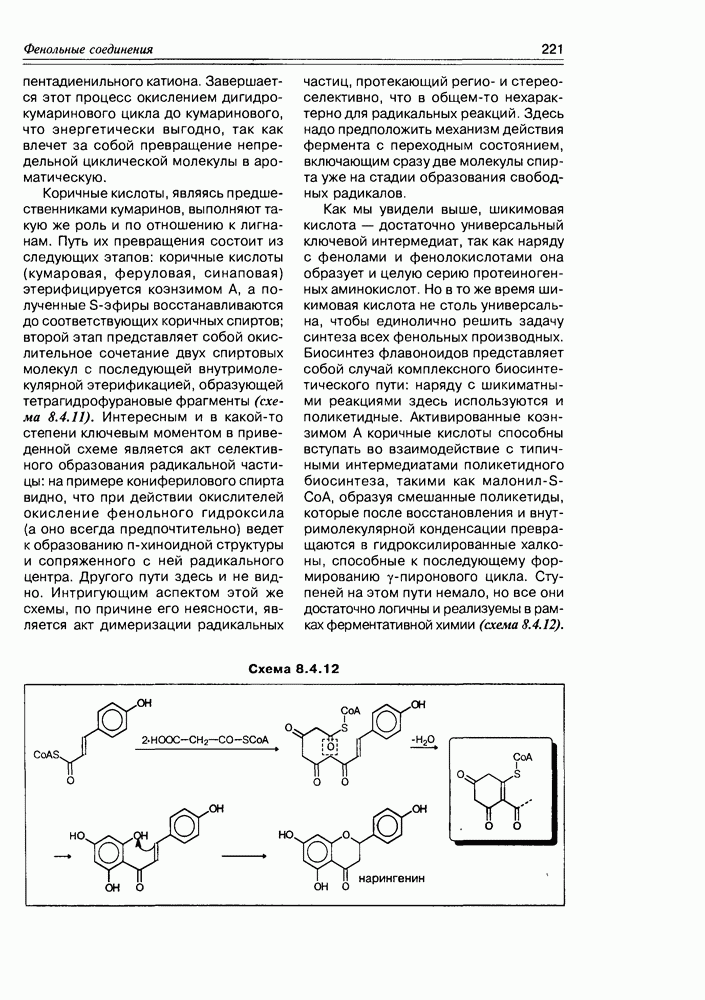
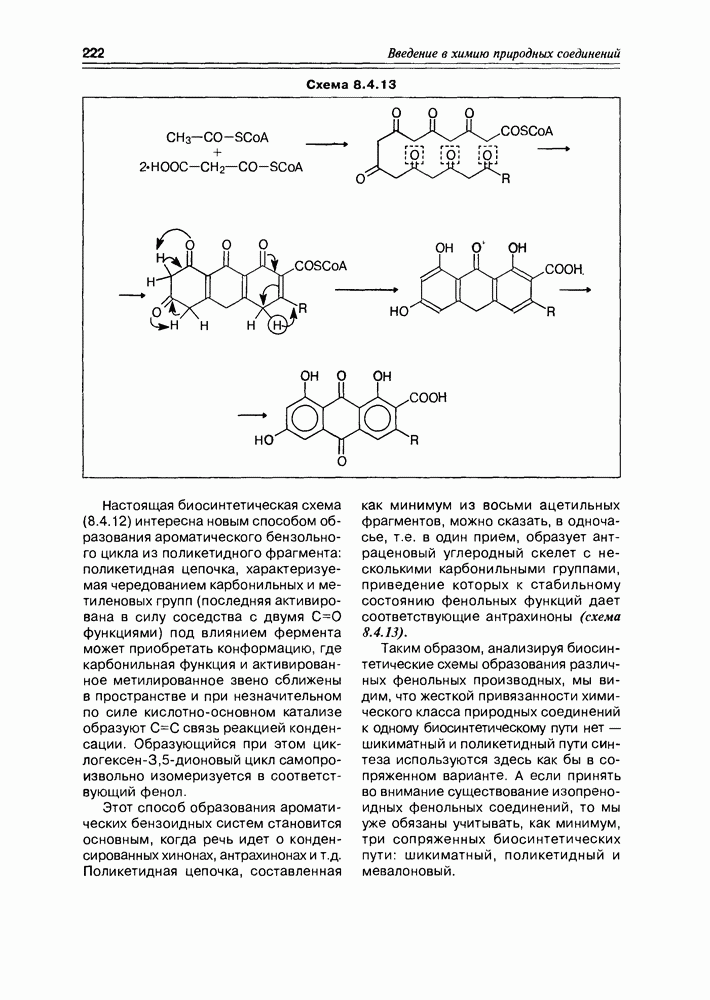
- 8.4. Биосинтез фенольных соединений
- Глава 9. АЛКАЛОИДЫ И ПОРФИРИНЫ
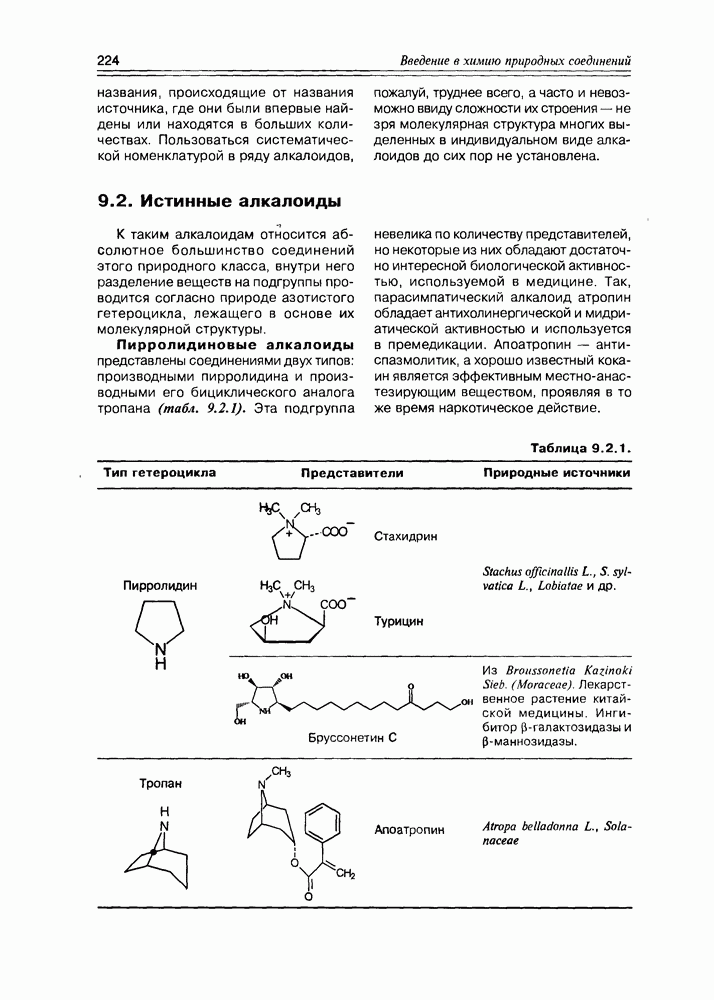
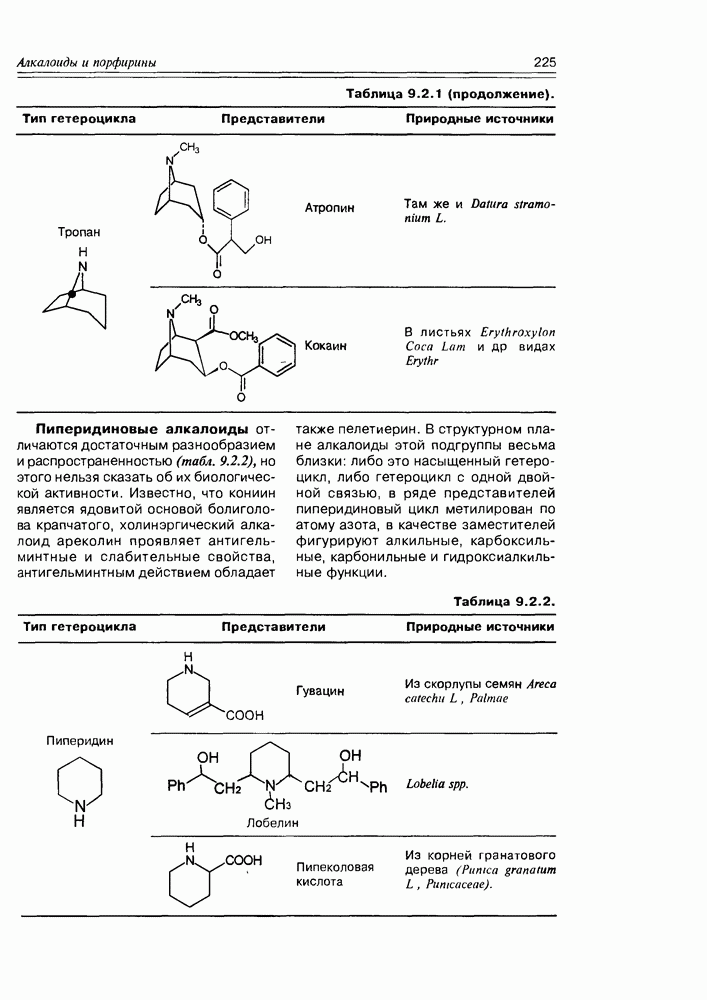
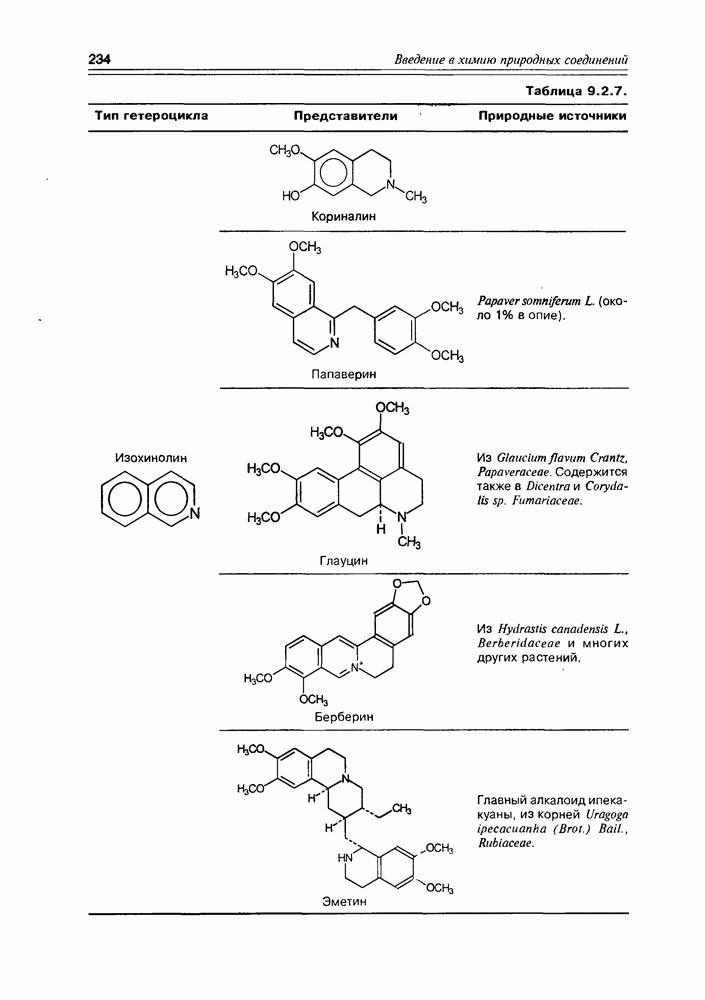
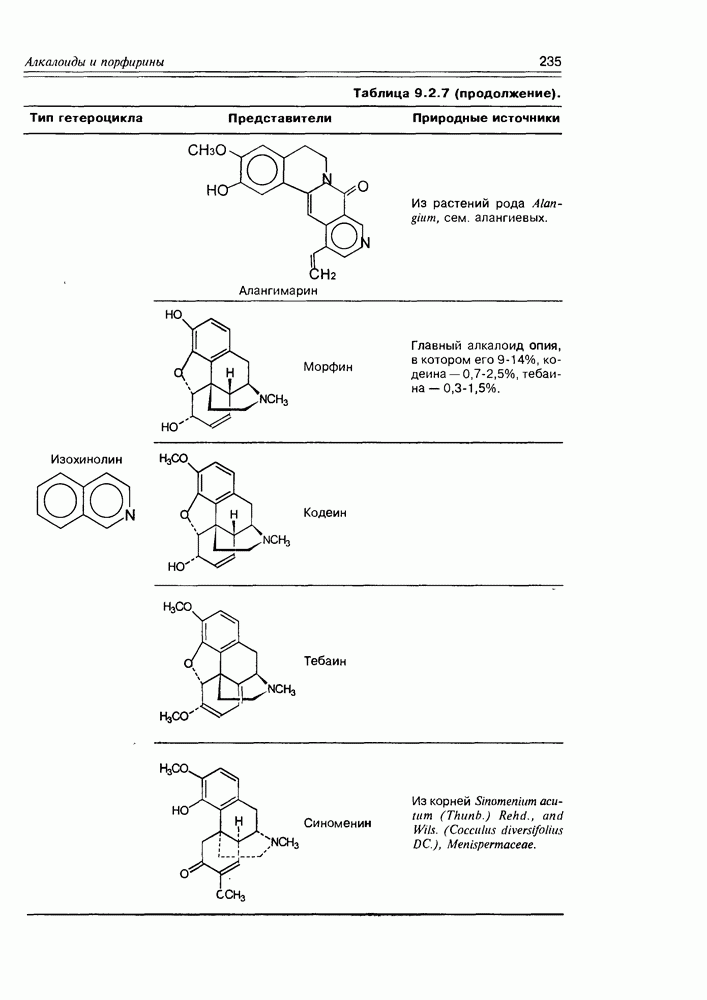
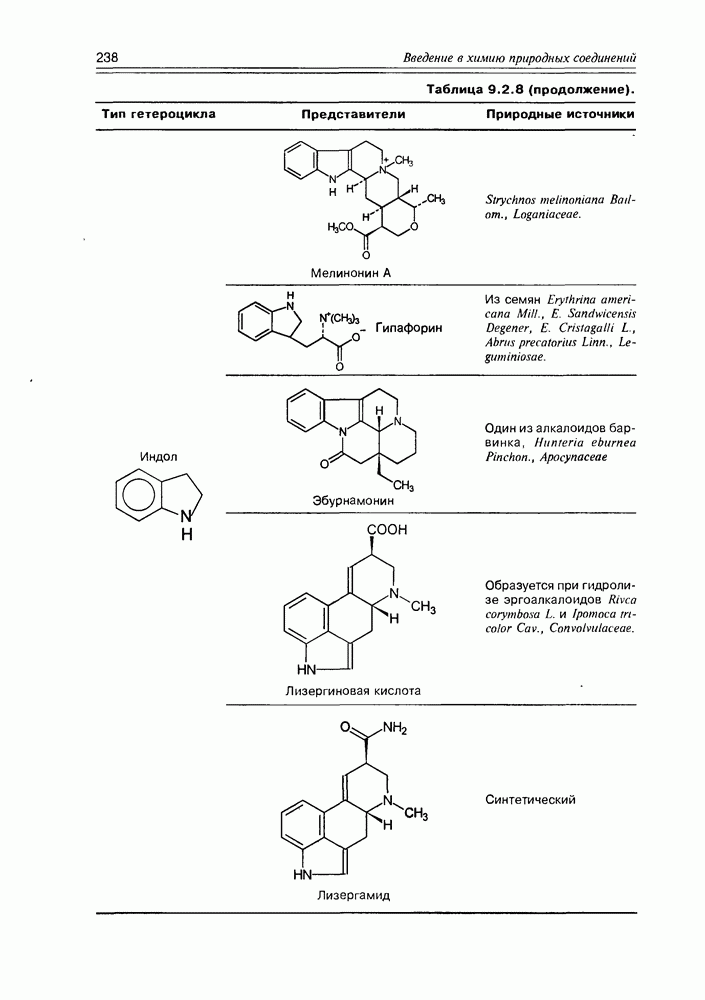
- 9.2. Истинные алкалоиды
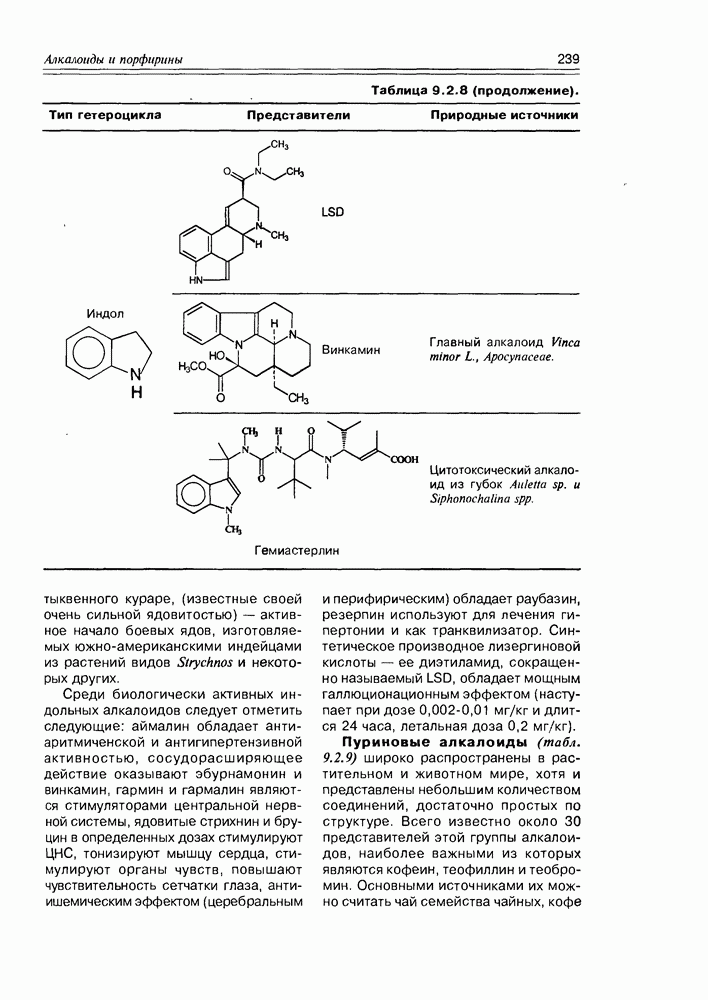
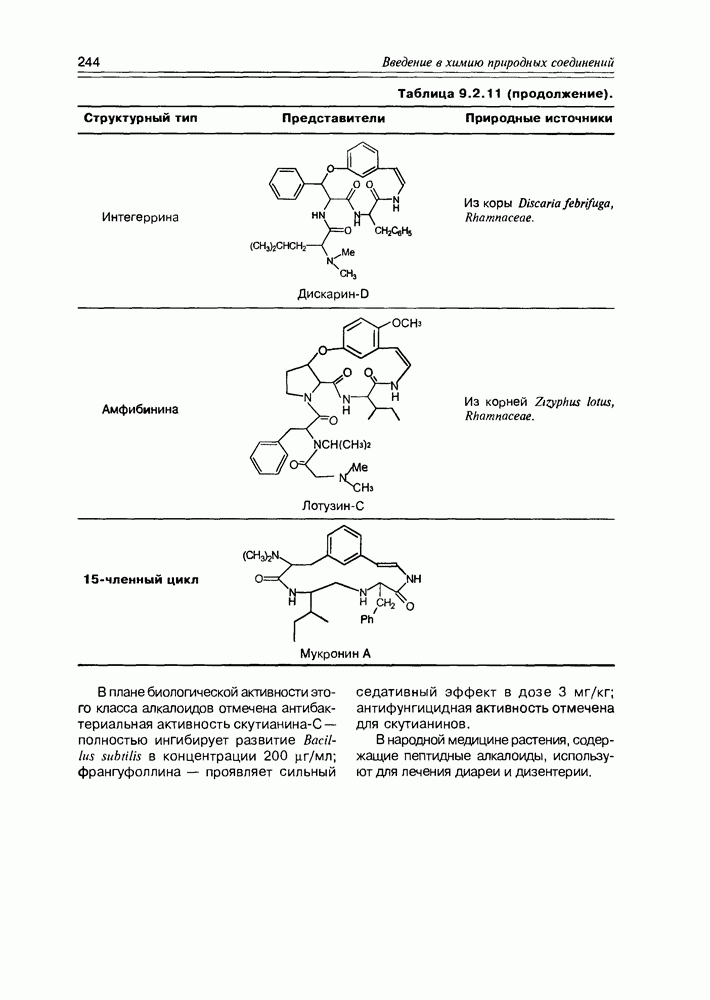
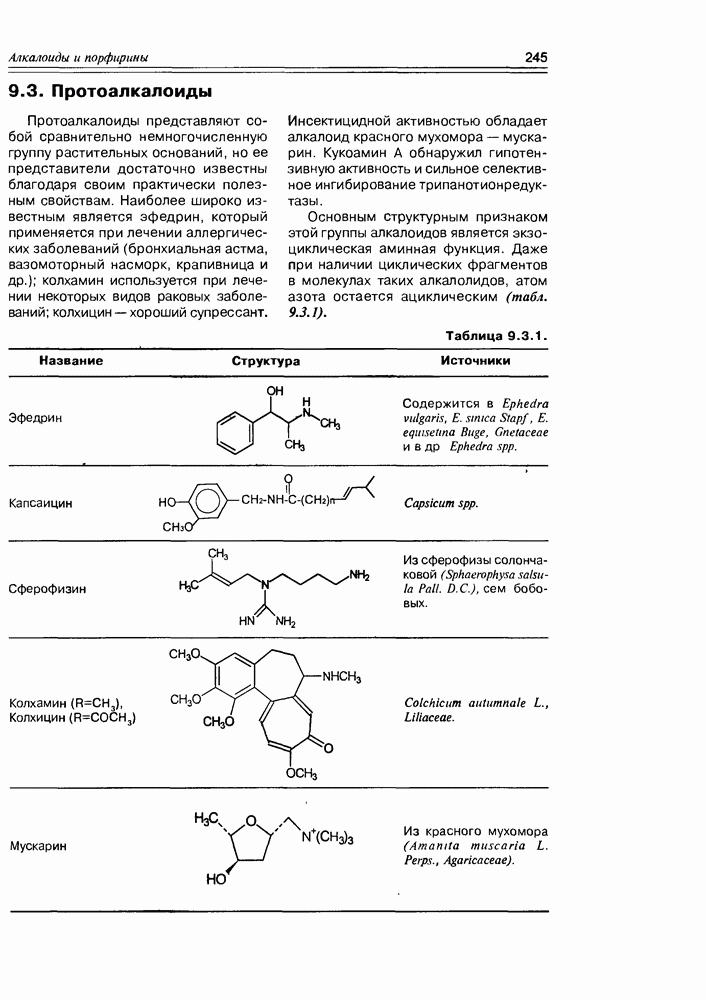
- 9.3. Протоалкалоиды
- 9.5. Химические свойства и химические модификации алкалоидов
- 9.6. Аминокислоты и биосинтез алкалоидов
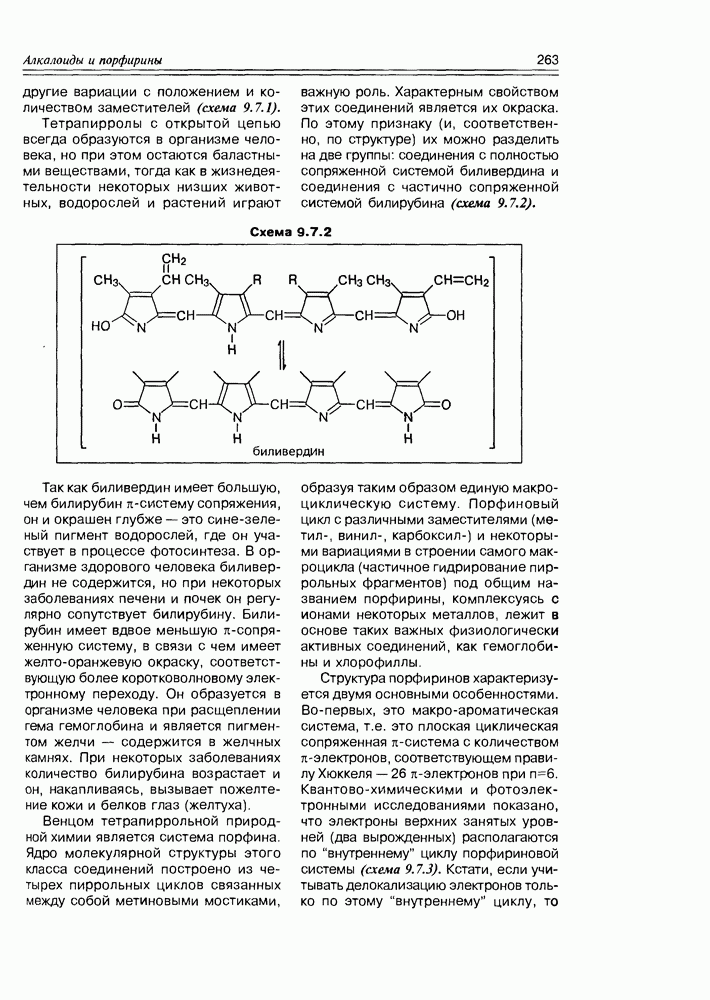
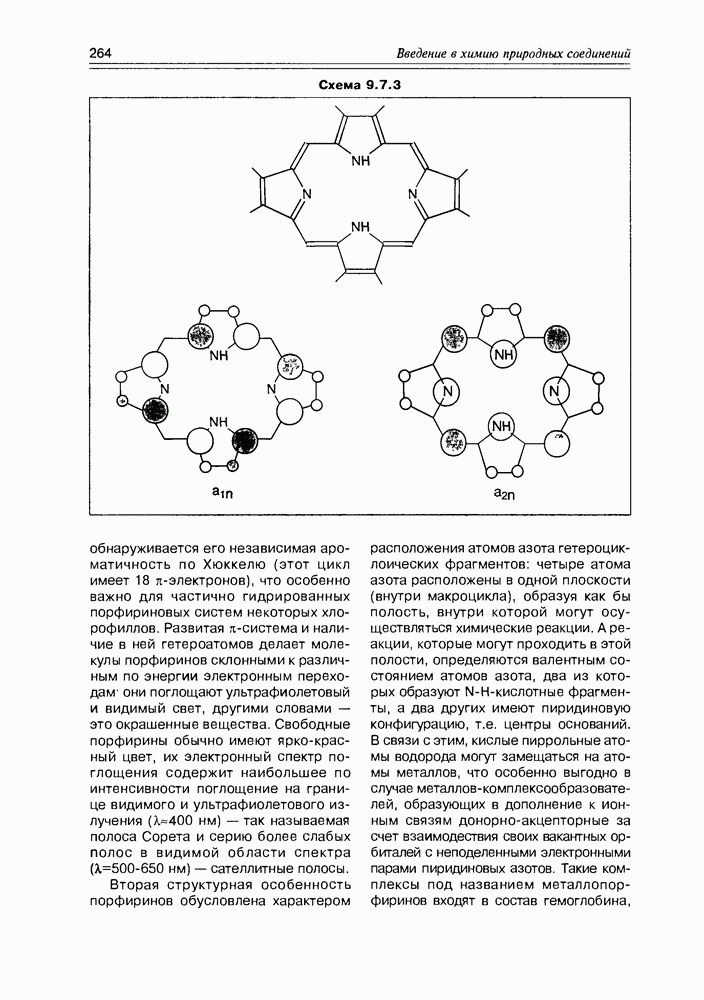
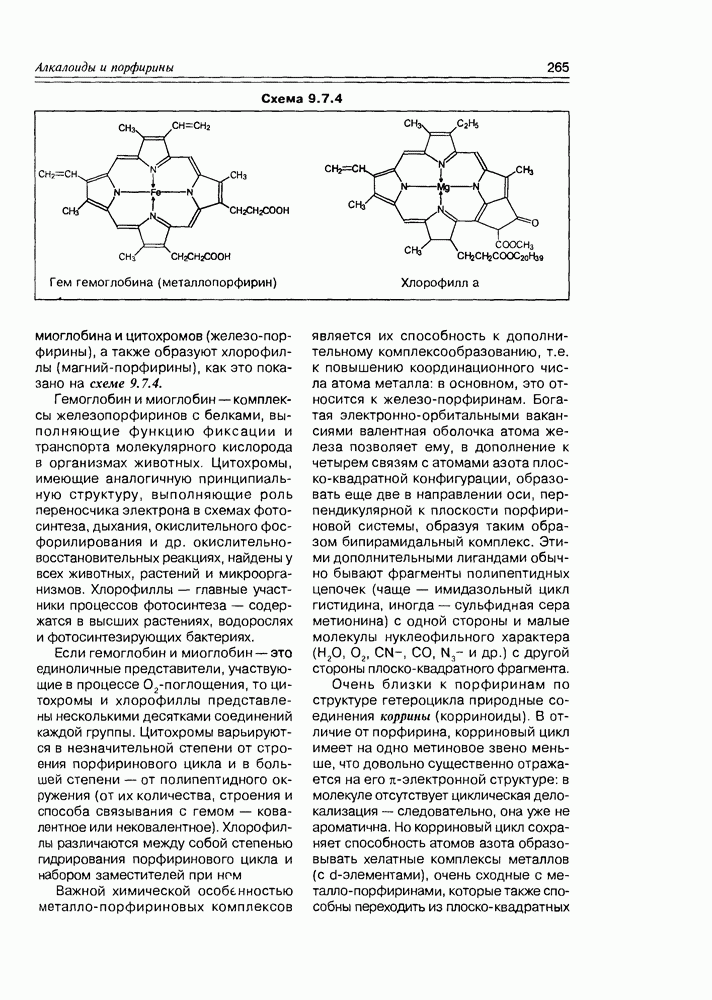
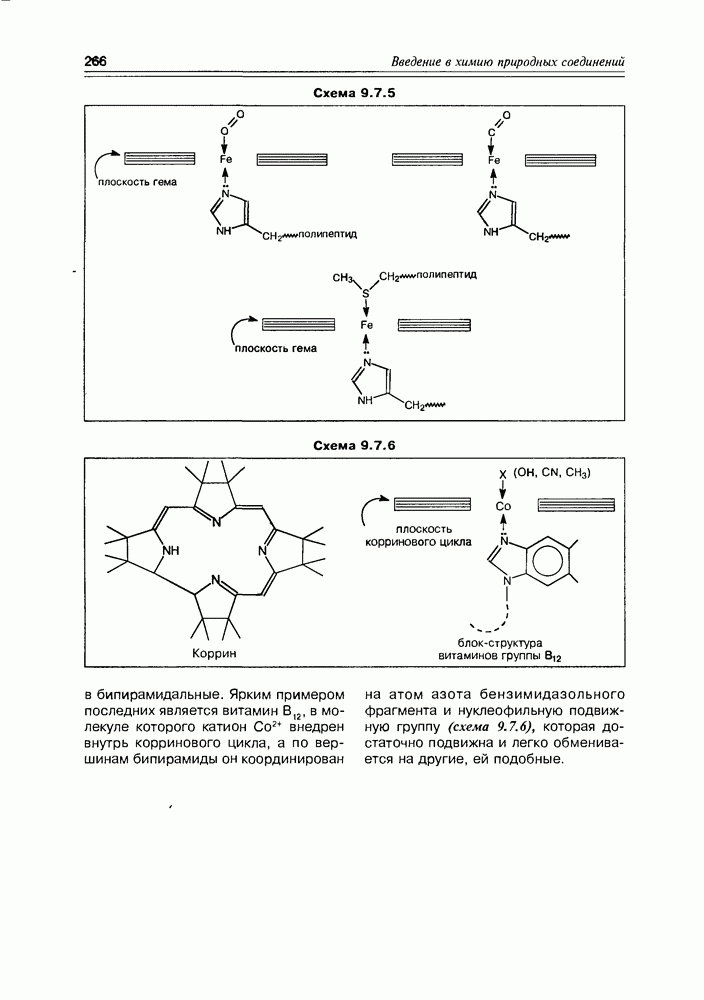
- 9.7. Порфирины
- Глава 10. ВИТАМИНЫ И КОФЕРМЕНТЫ
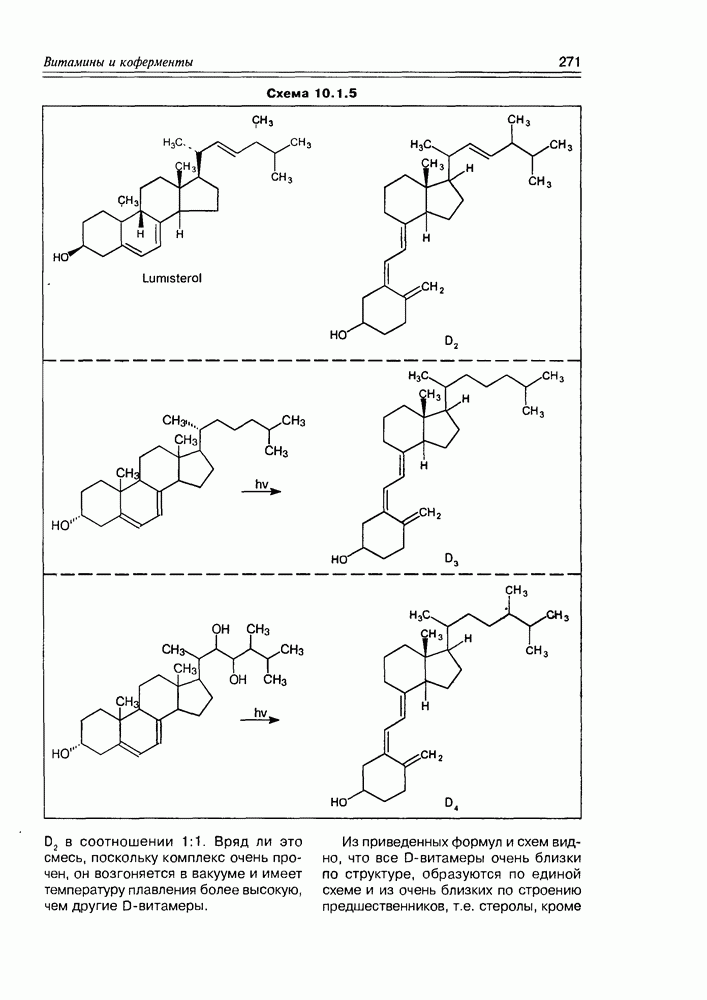
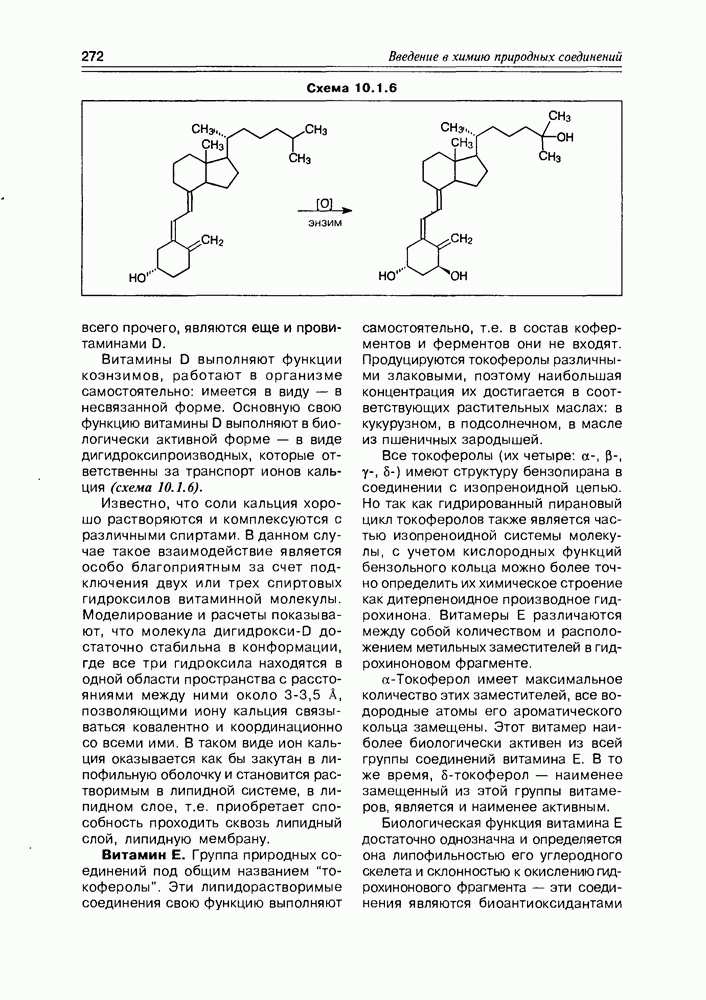
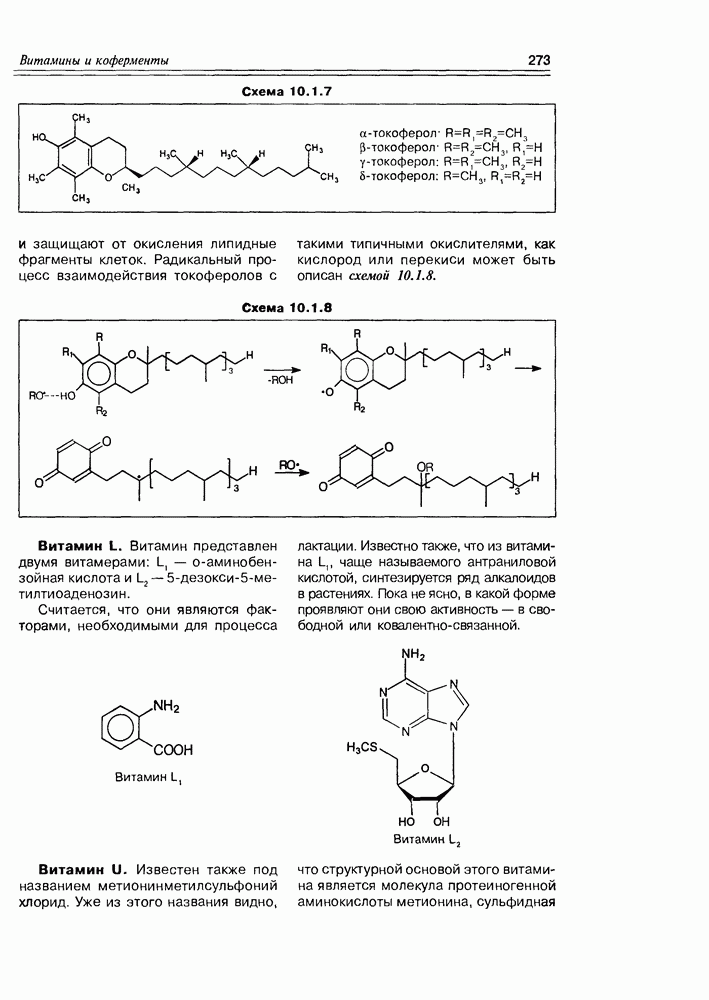
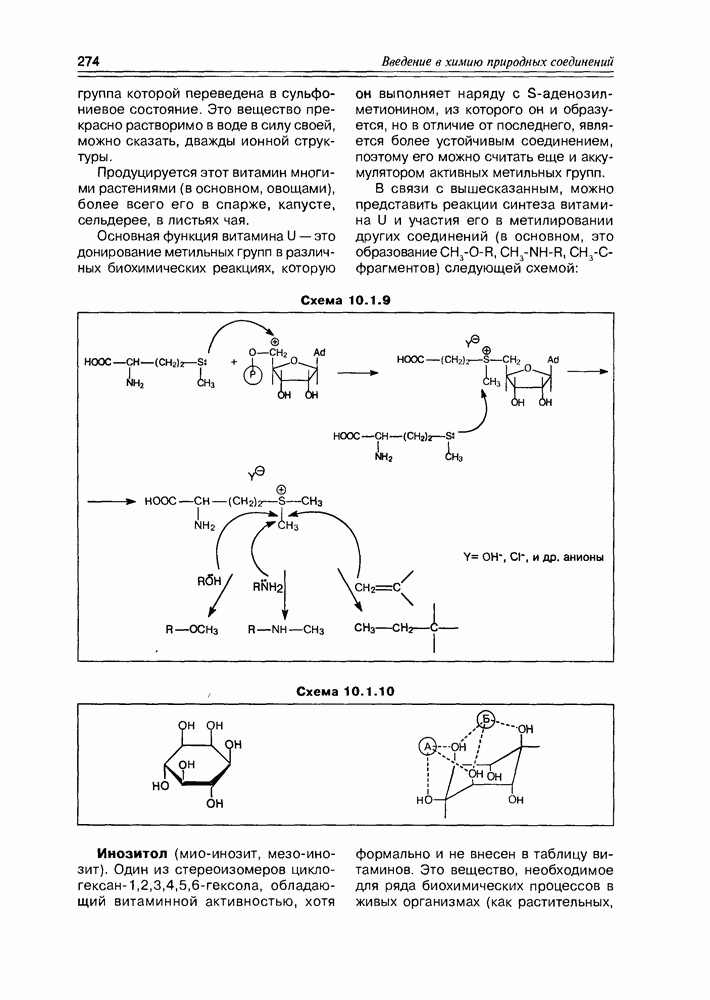
- 10.1. Витамины — собственно
- 10.2. Витамины-коферменты
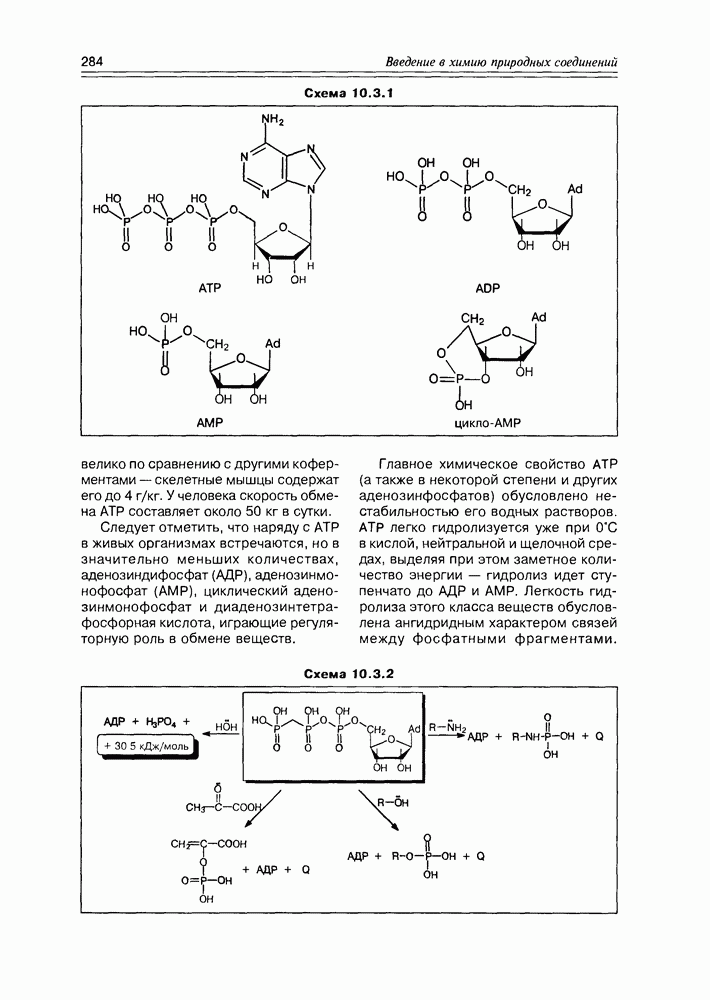
- 10.3. Коферменты
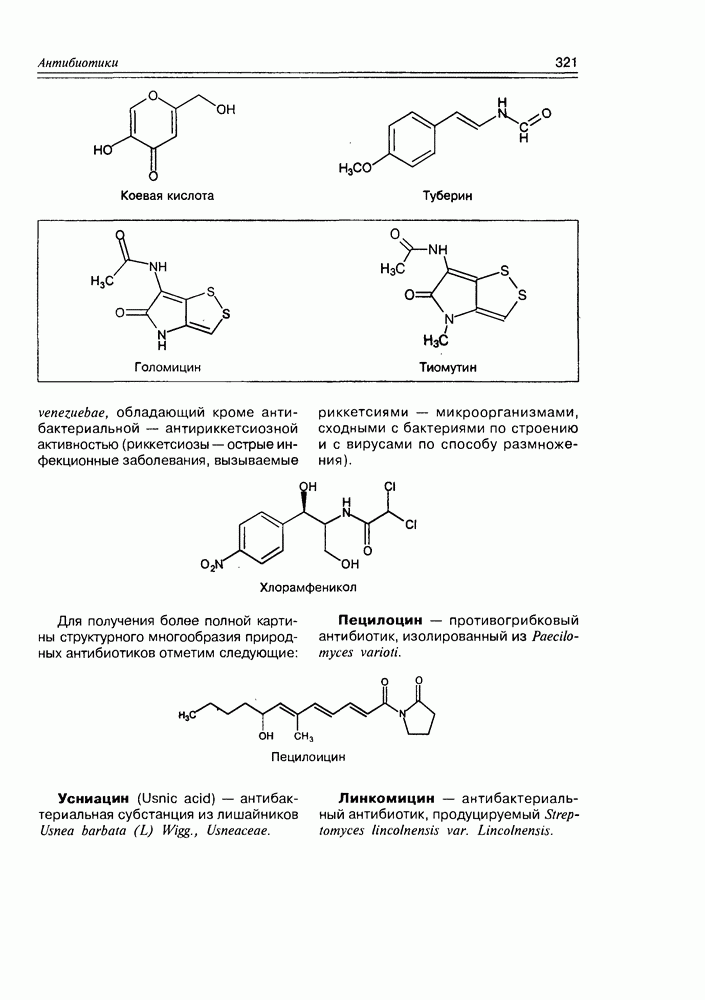
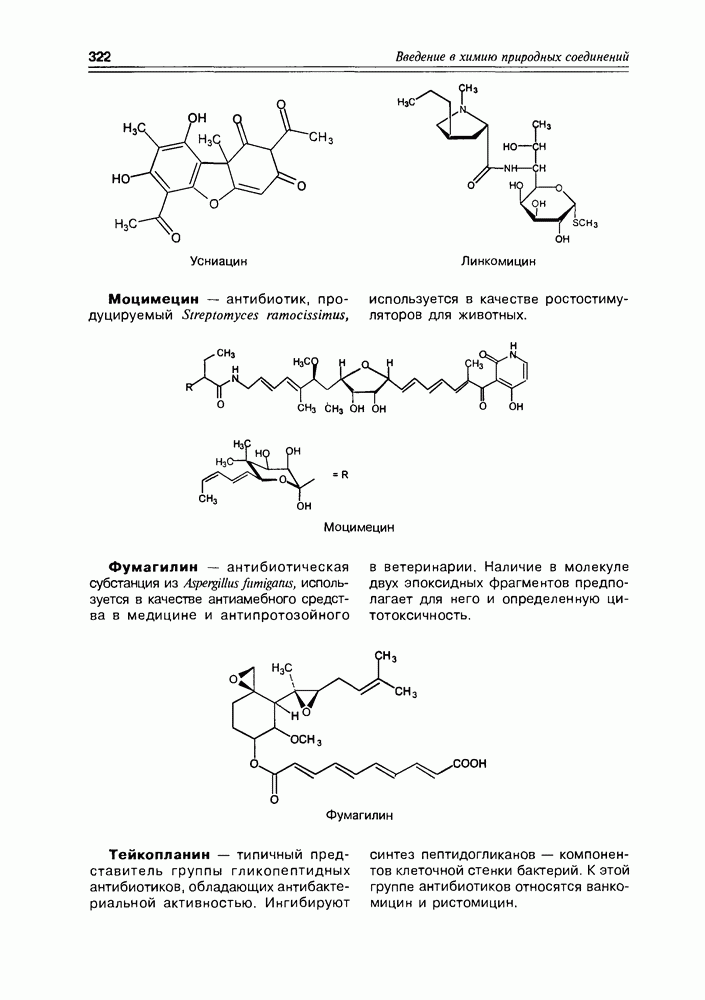
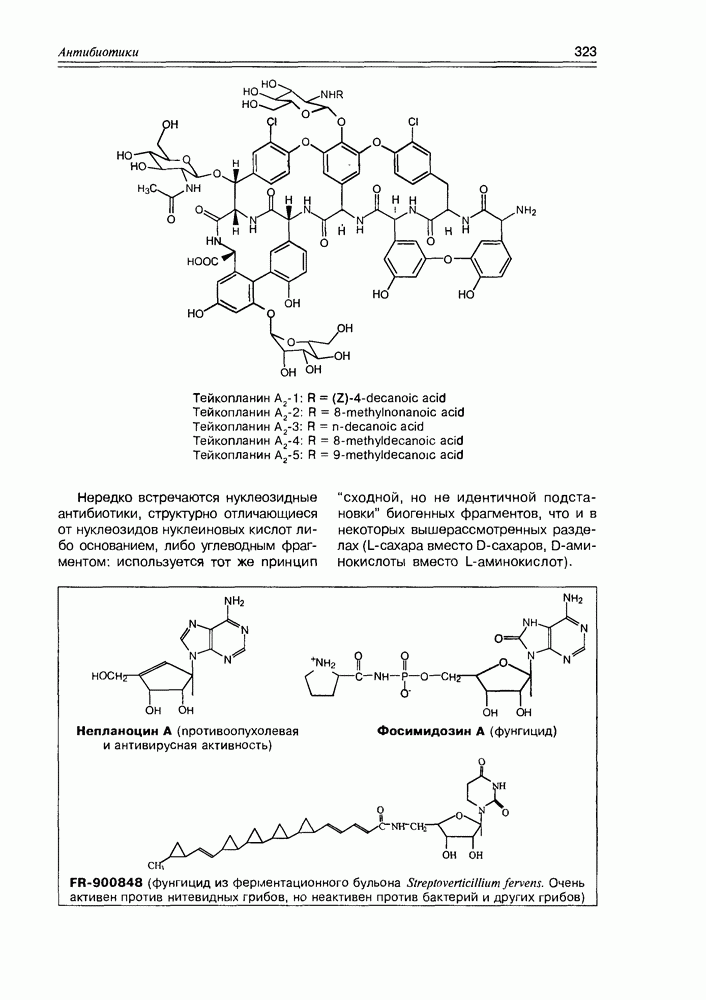
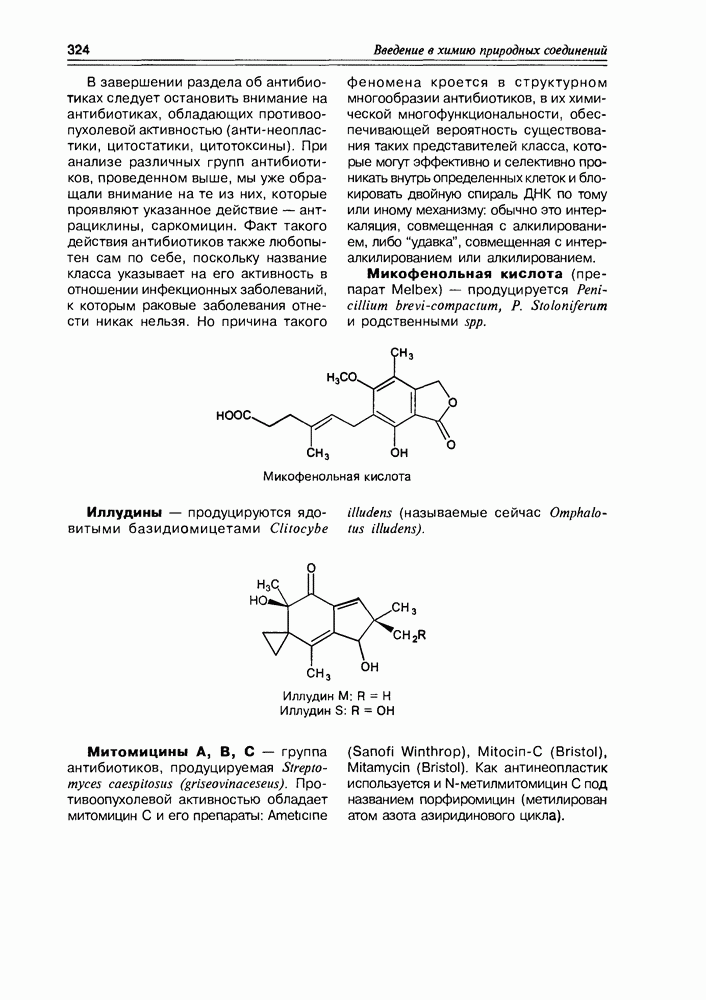
- Глава 11. АНТИБИОТИКИ
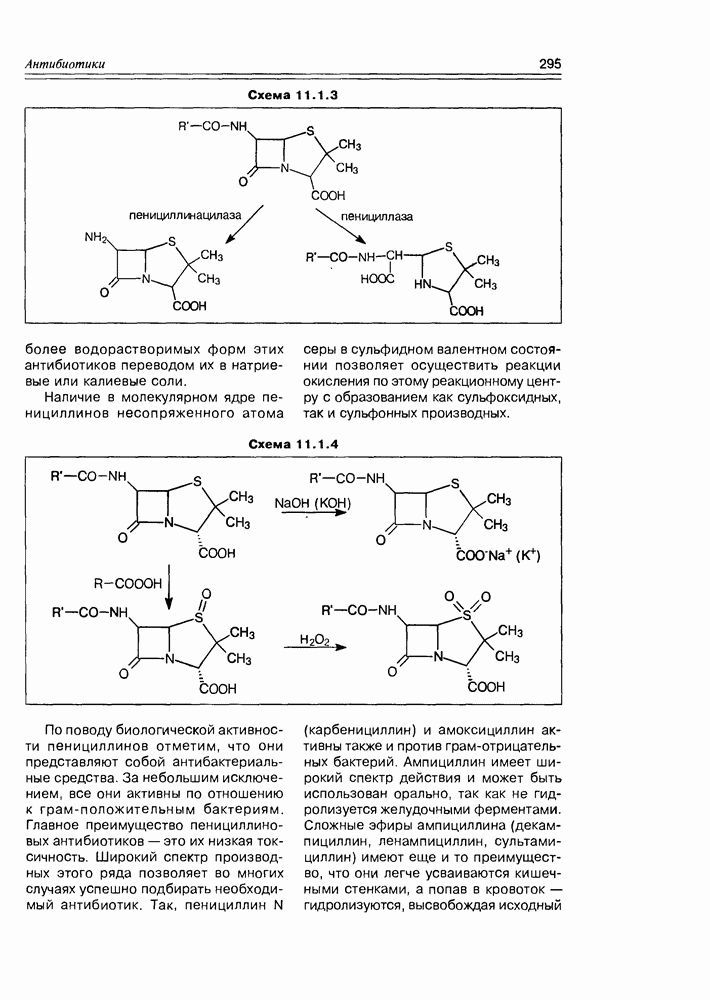
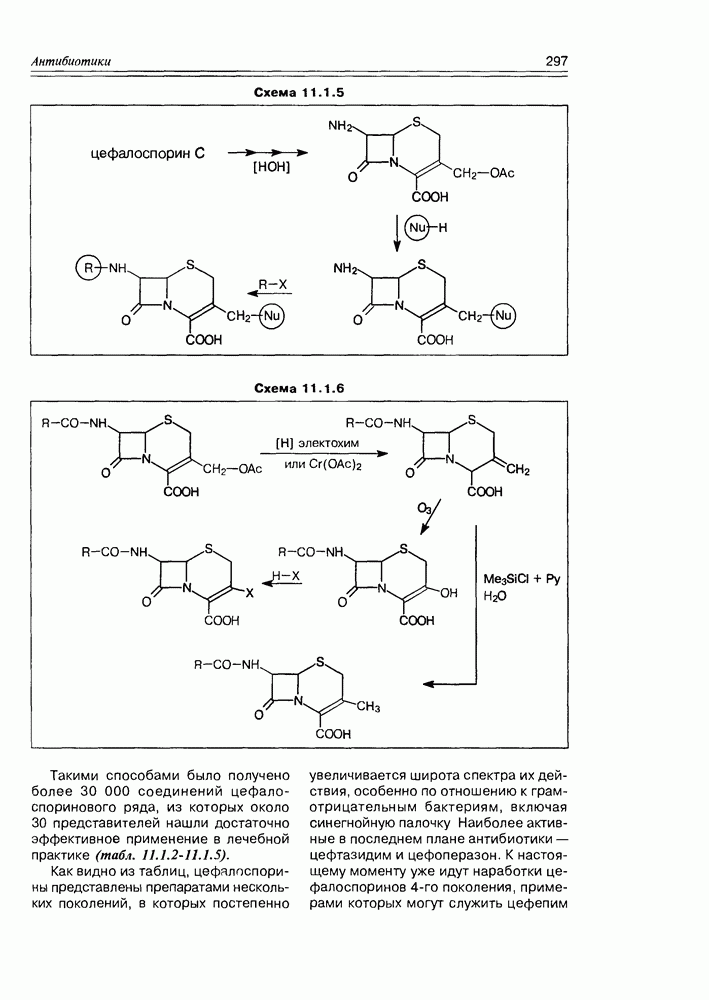
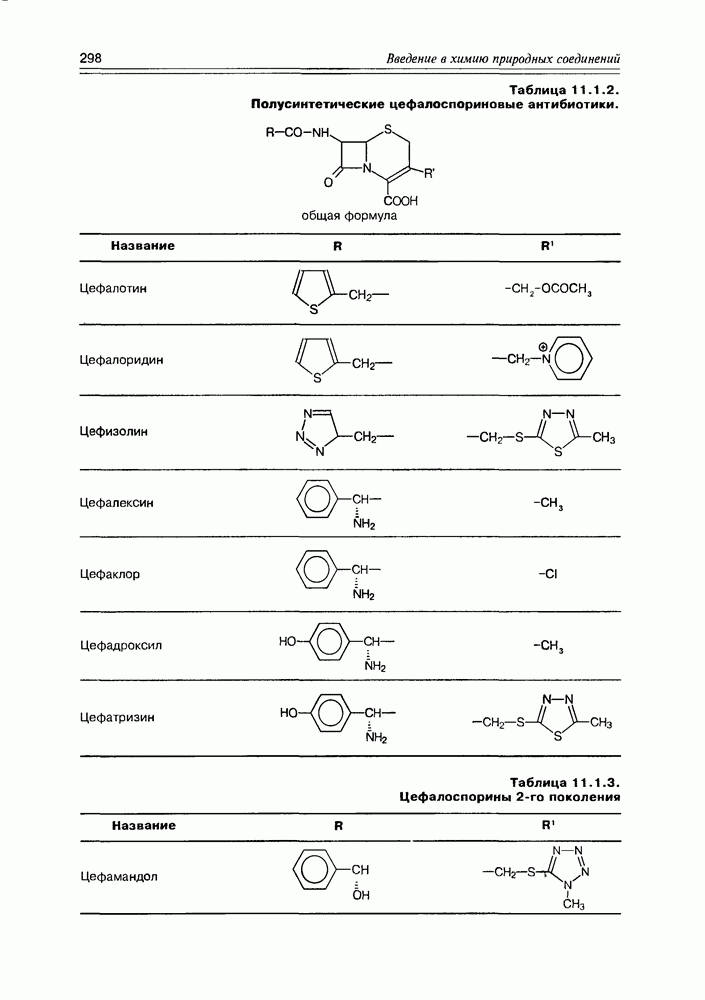
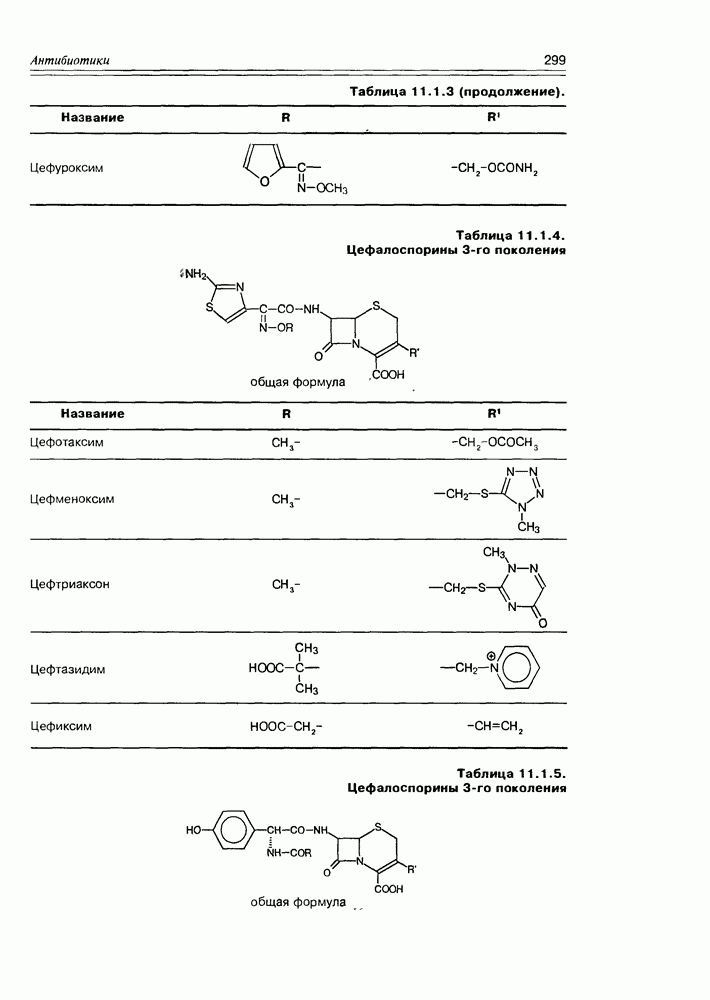
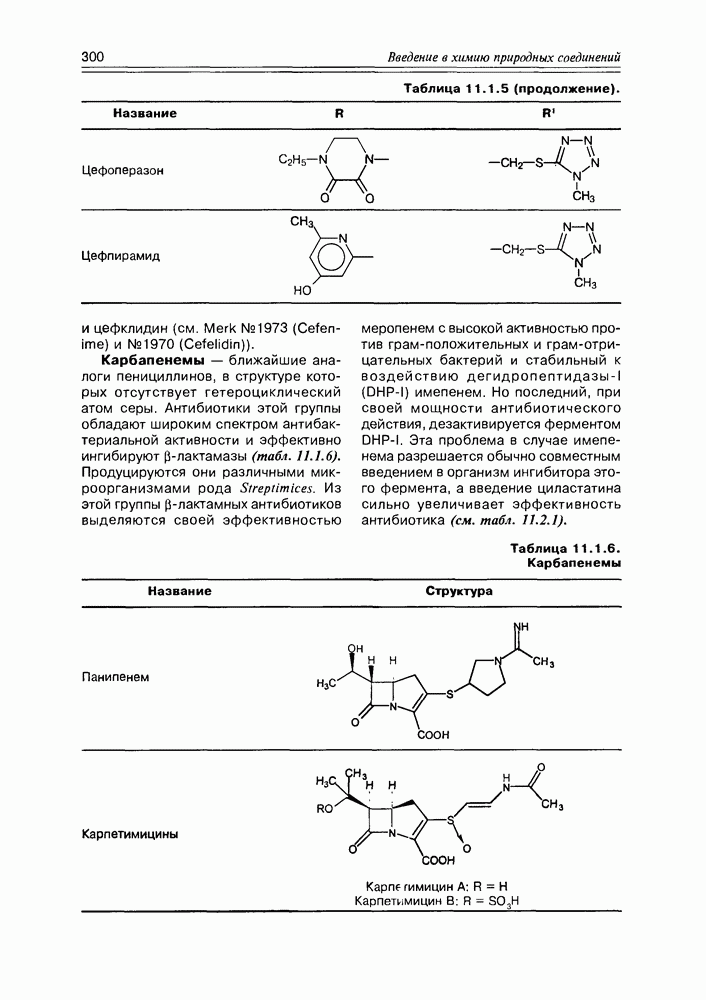
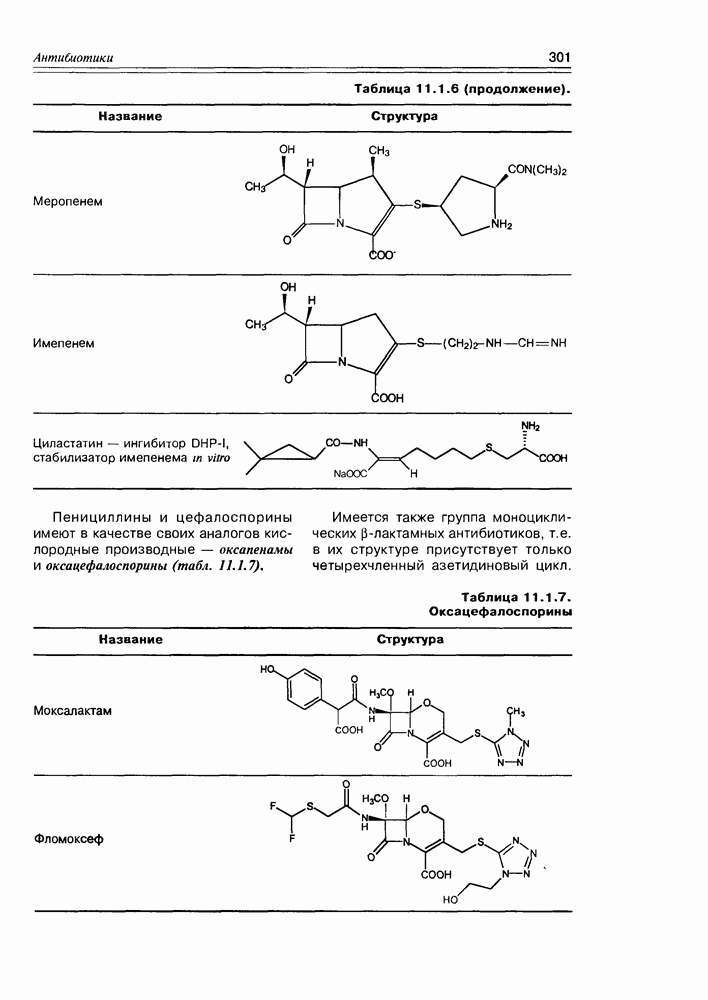
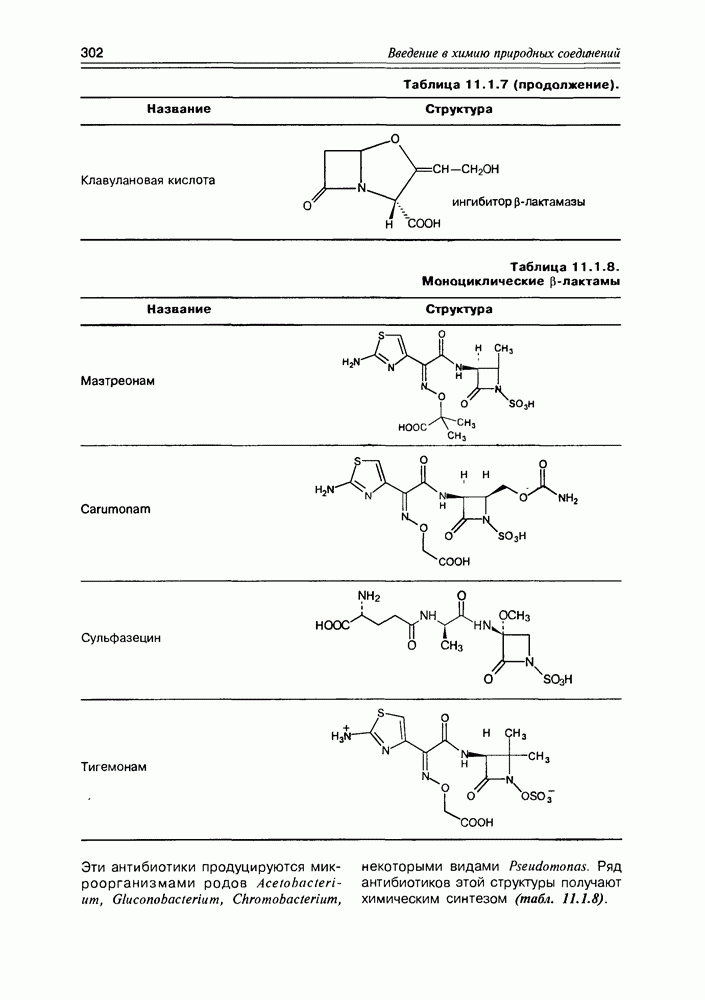
- 11.1. b-Лактамные антибиотики
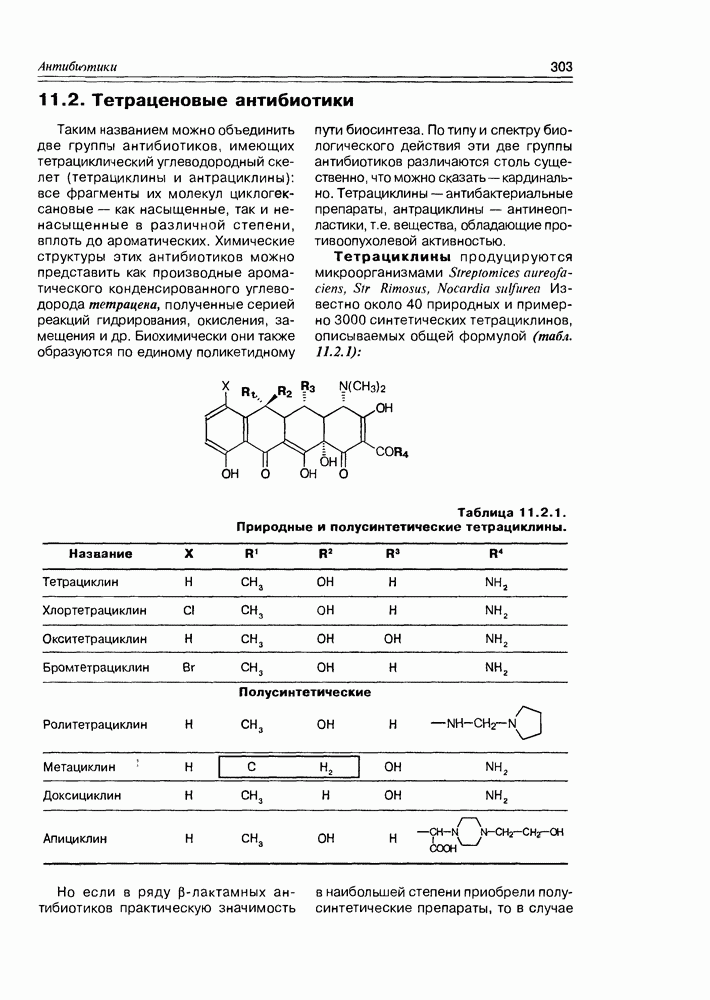
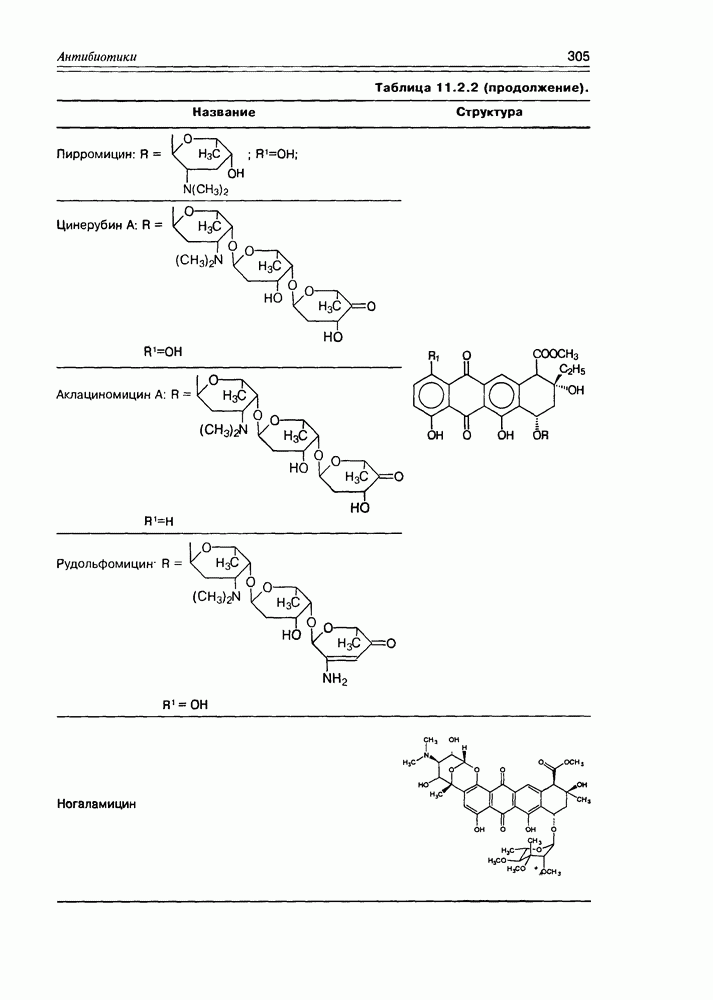
- 11.2. Тетраценовые антибиотики
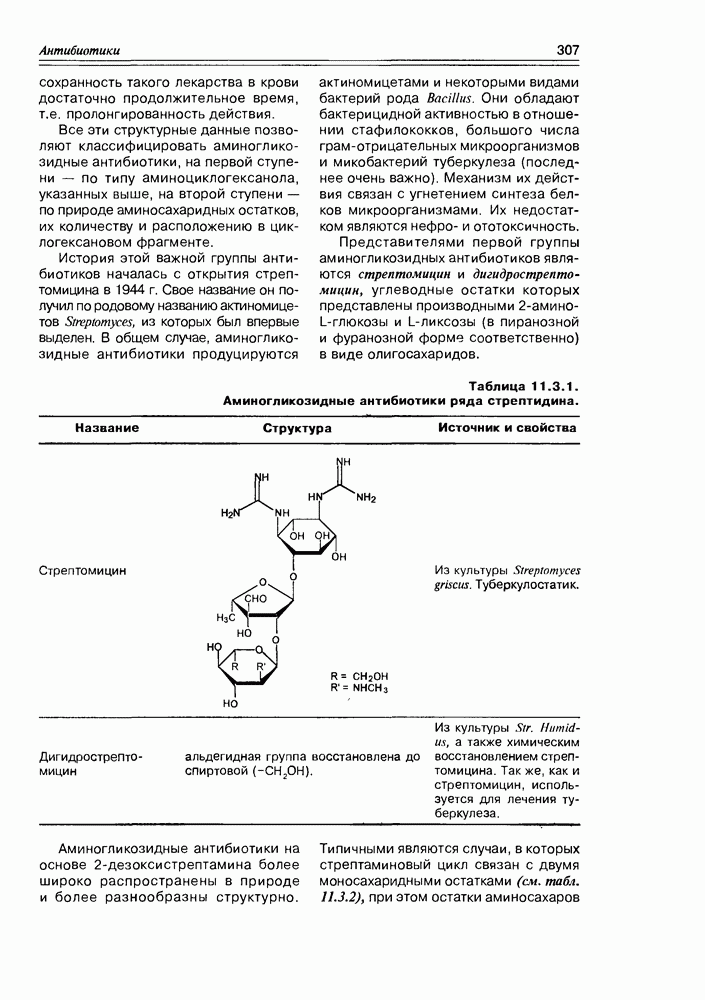
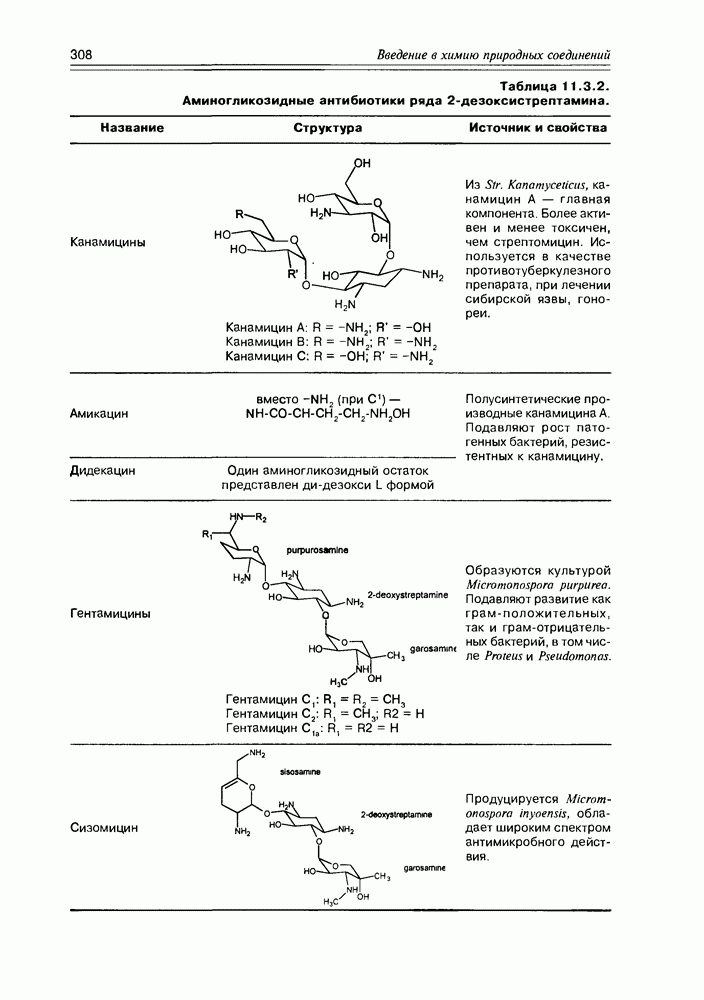
- 11.3. Аминогликозидные антибиотики
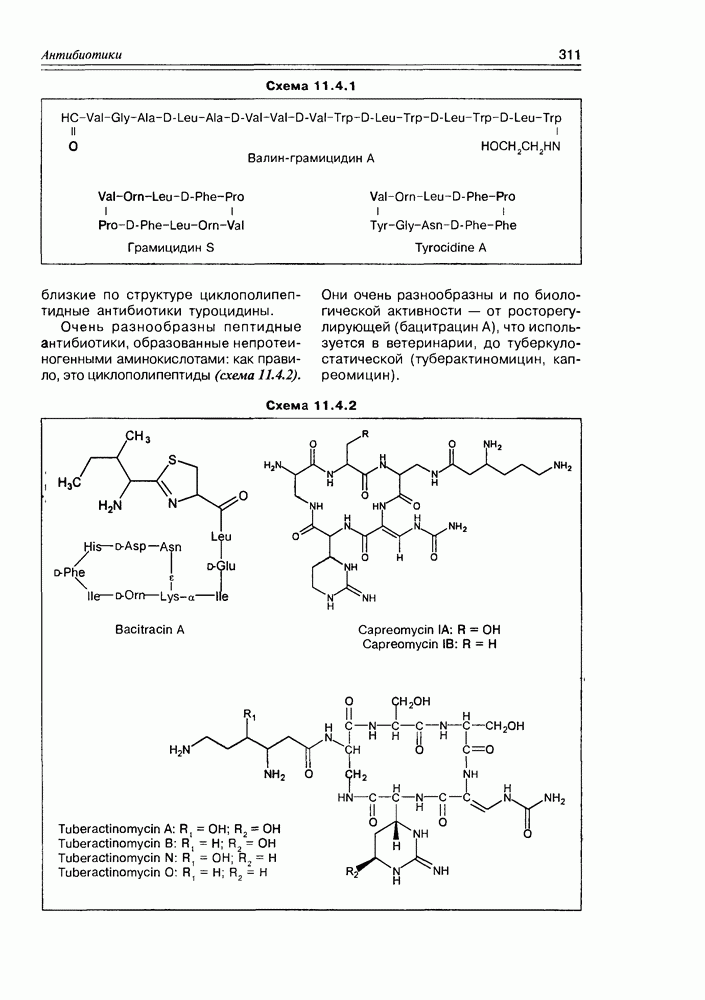
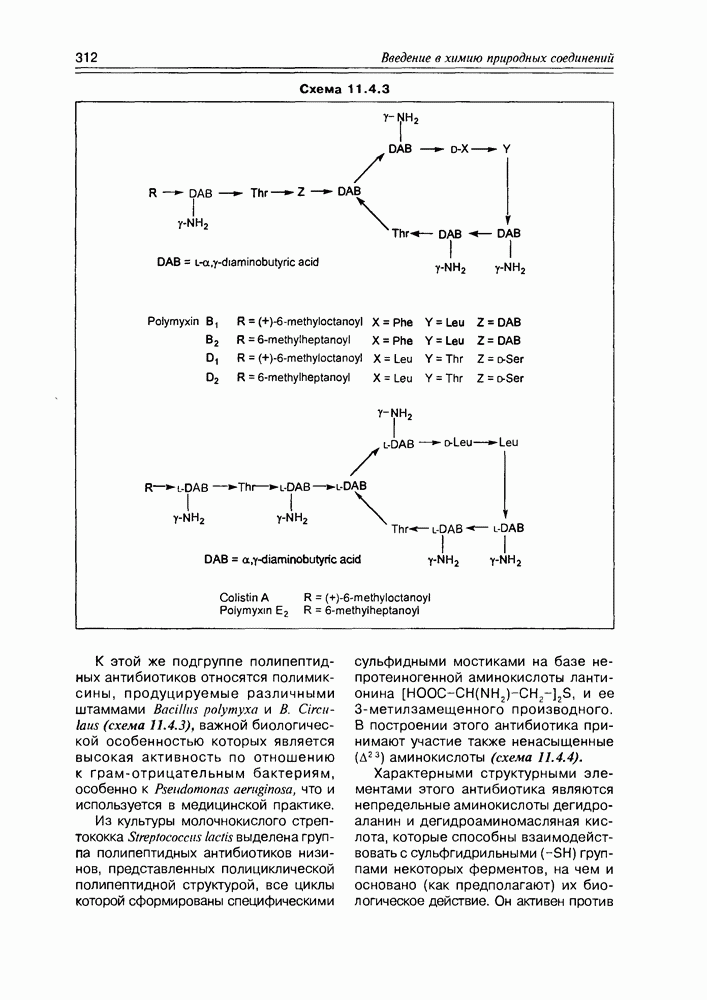
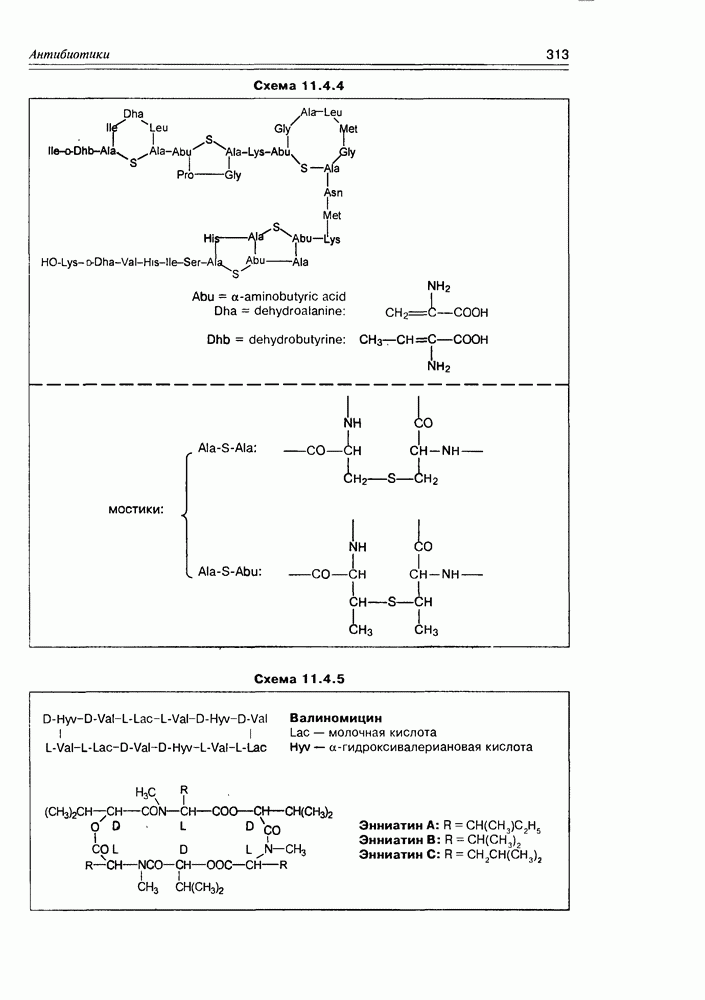
- 11.4. Пептидные антибиотики
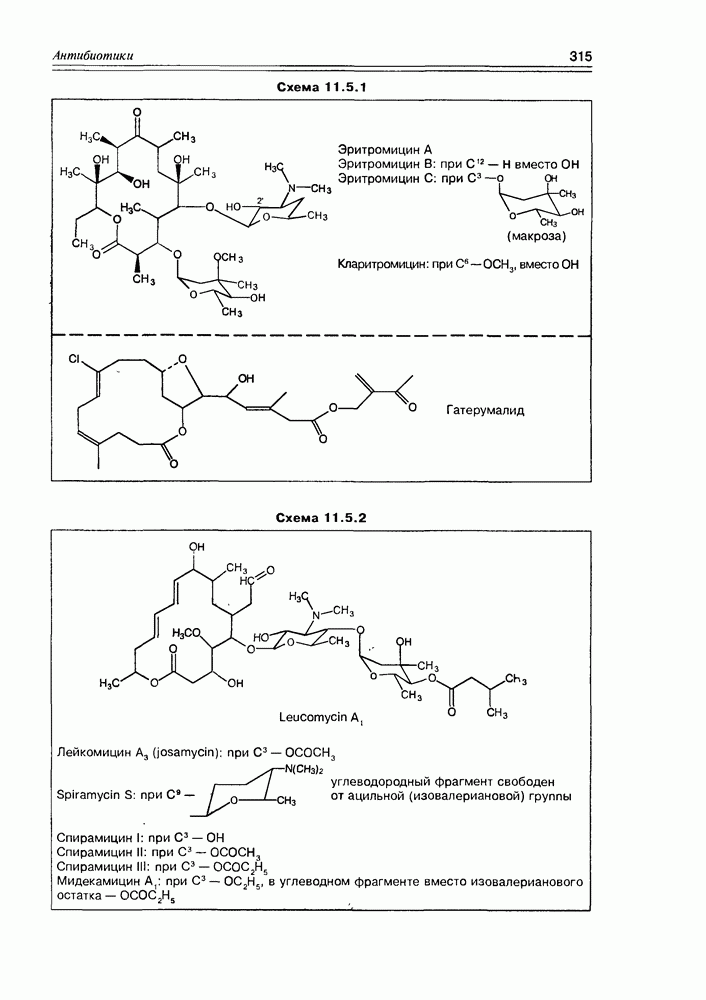
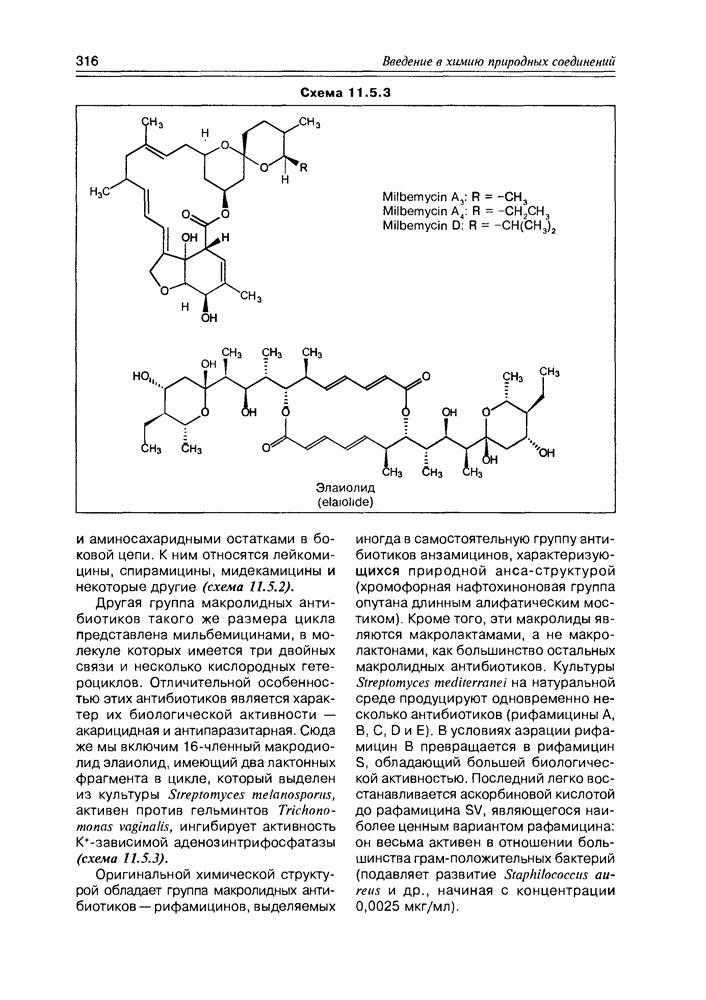
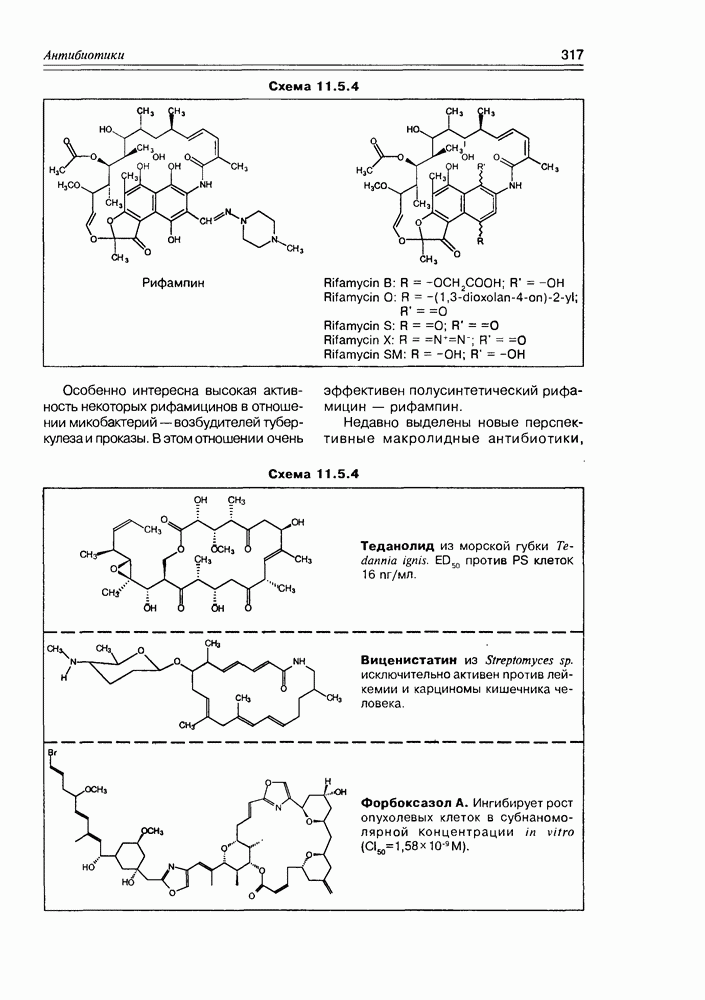
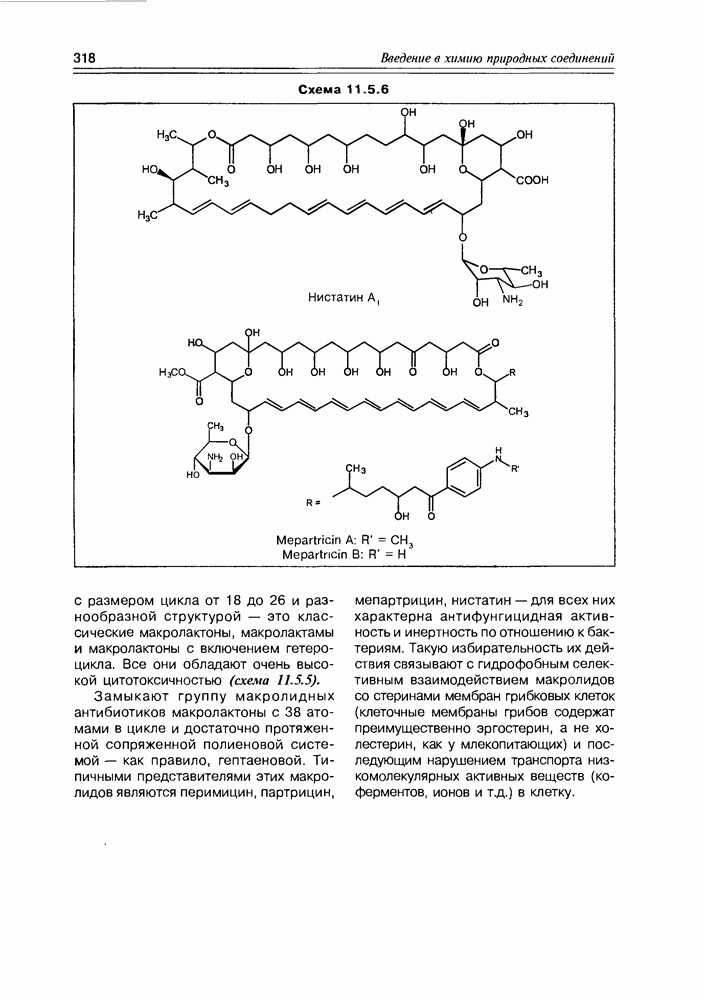
- 11.5. Макролидные антибиотики
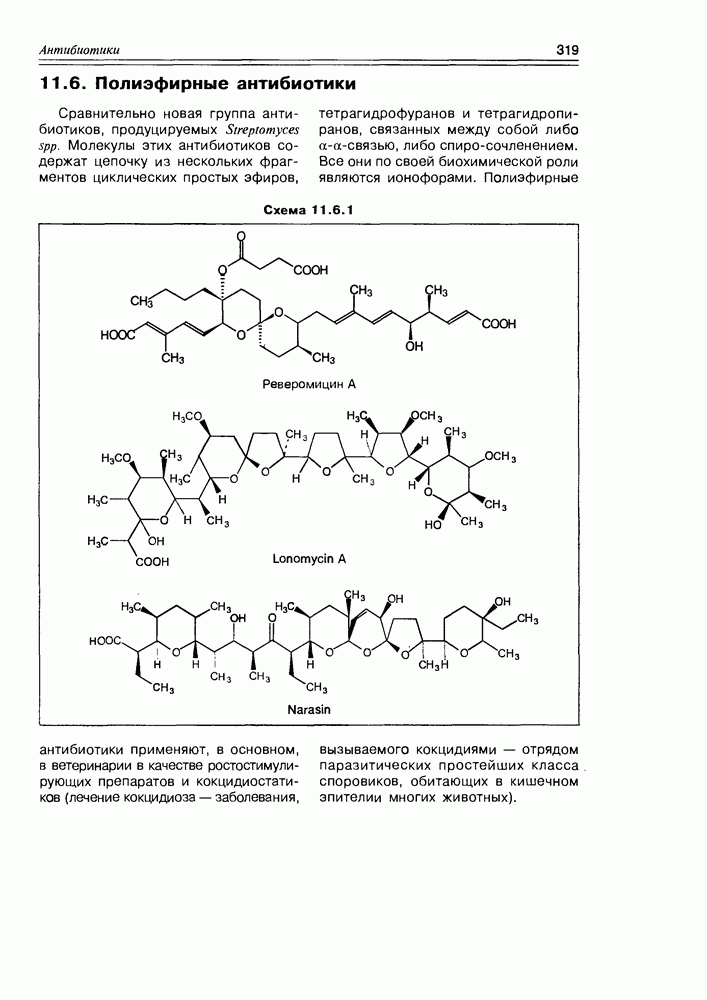
- 11.6. Полиэфирные антибиотики
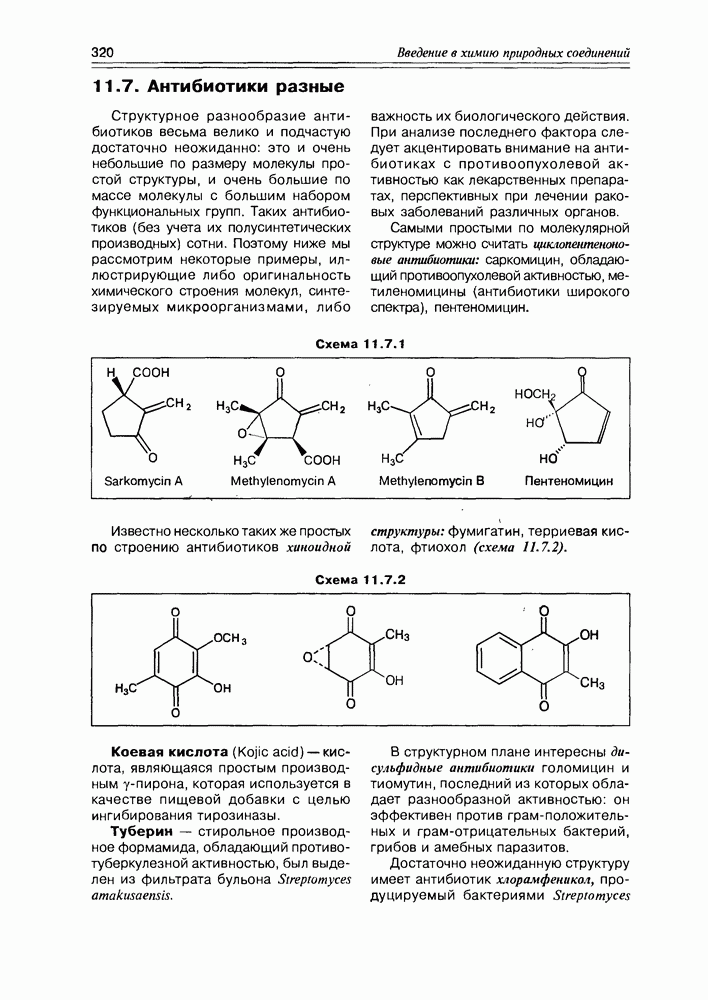
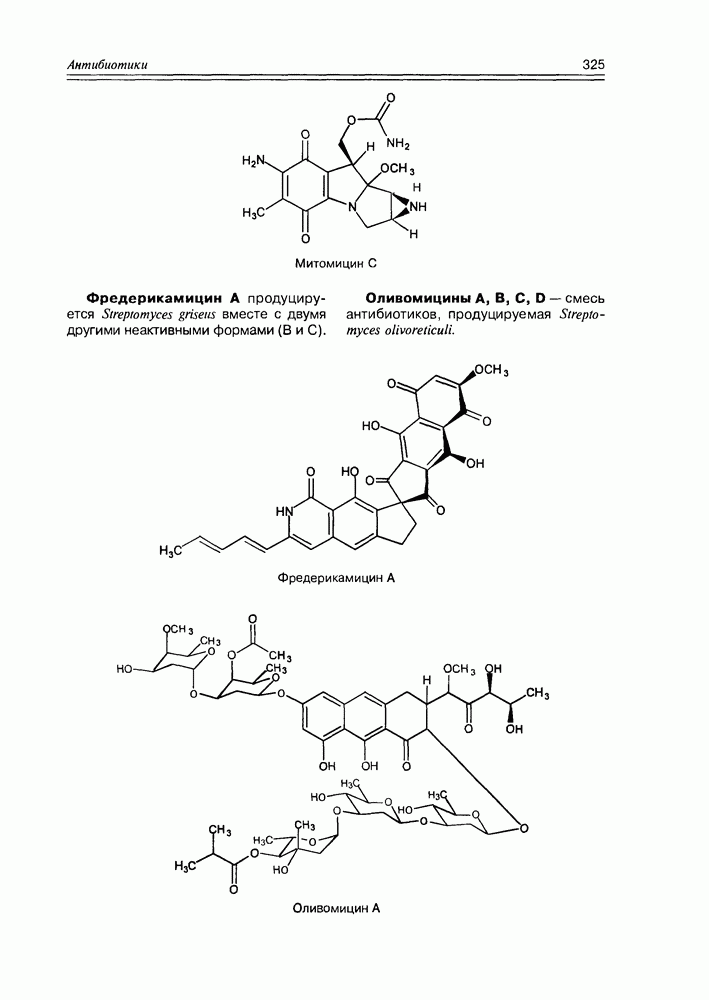
- 11.7. Антибиотики разные
- Глава 12. РАЗНЫЕ ГРУППЫ ПРИРОДНЫХ СОЕДИНЕНИЙ
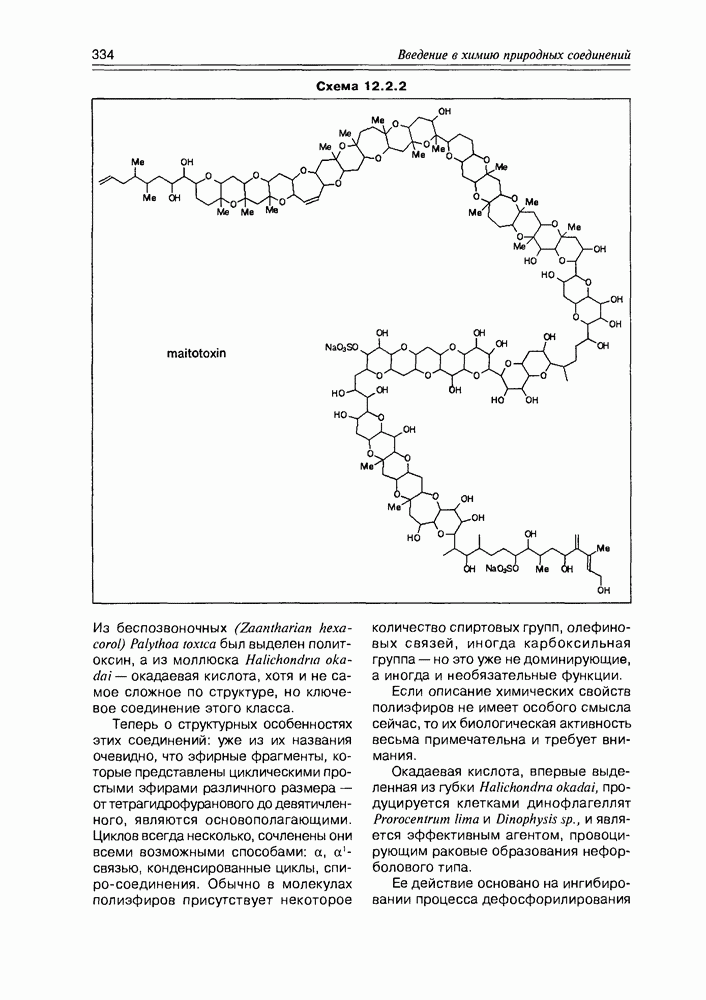
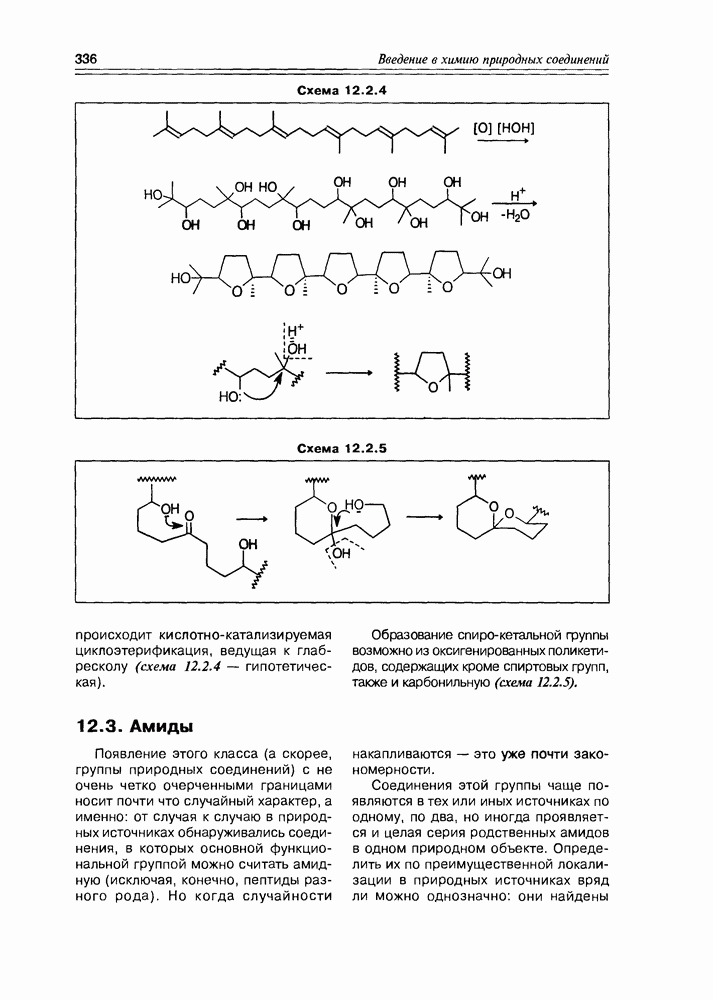
- 12.2. Полиэфиры
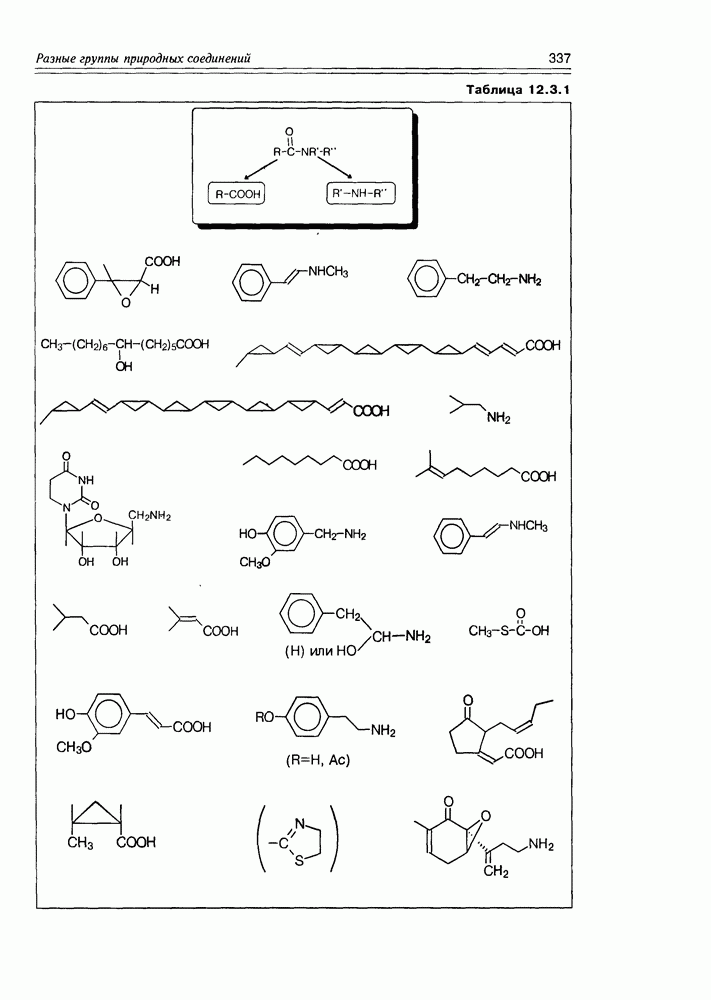
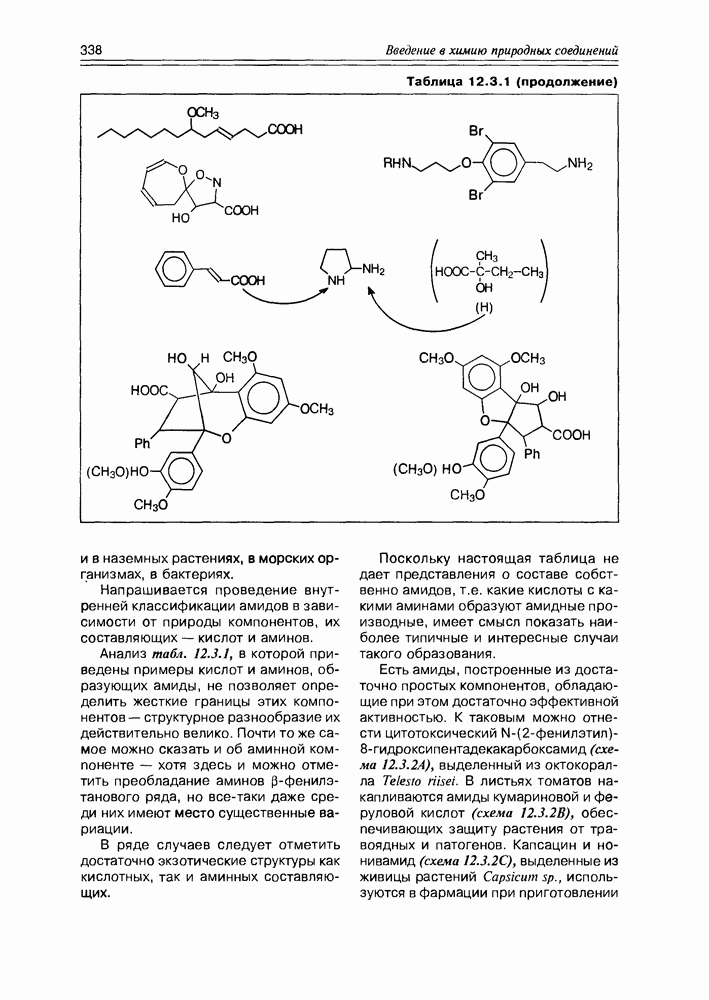
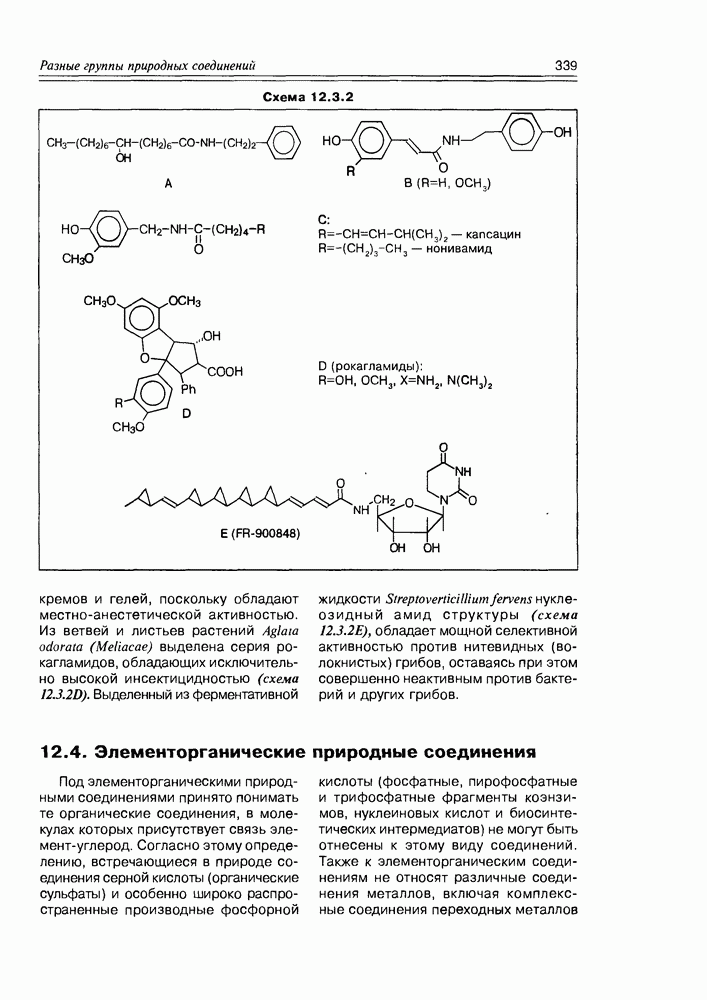
- 12.3. Амиды
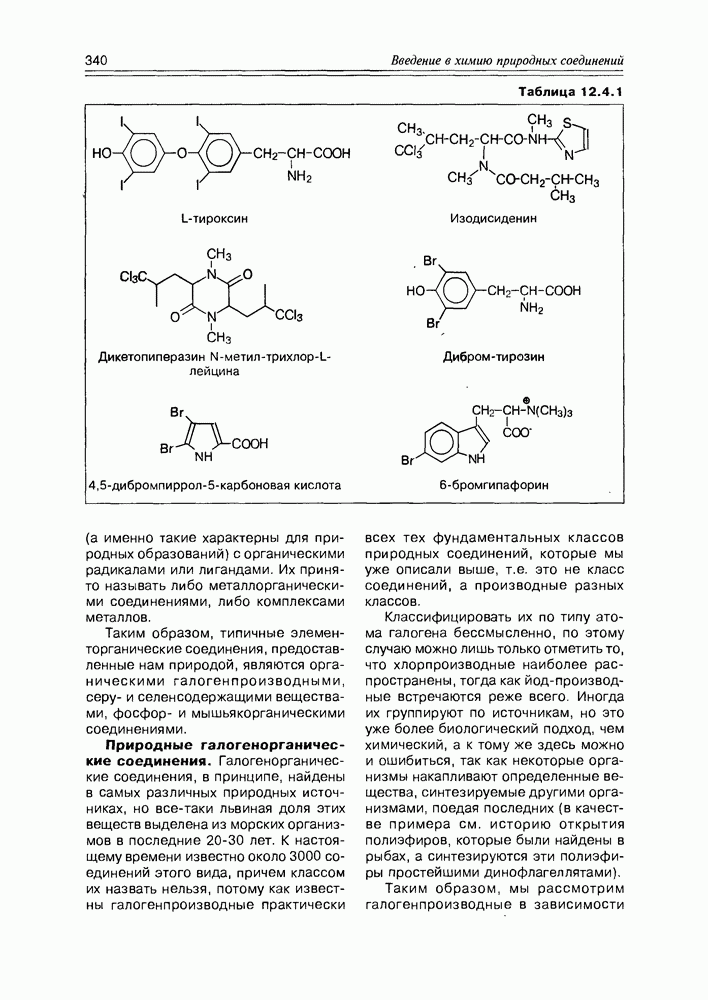
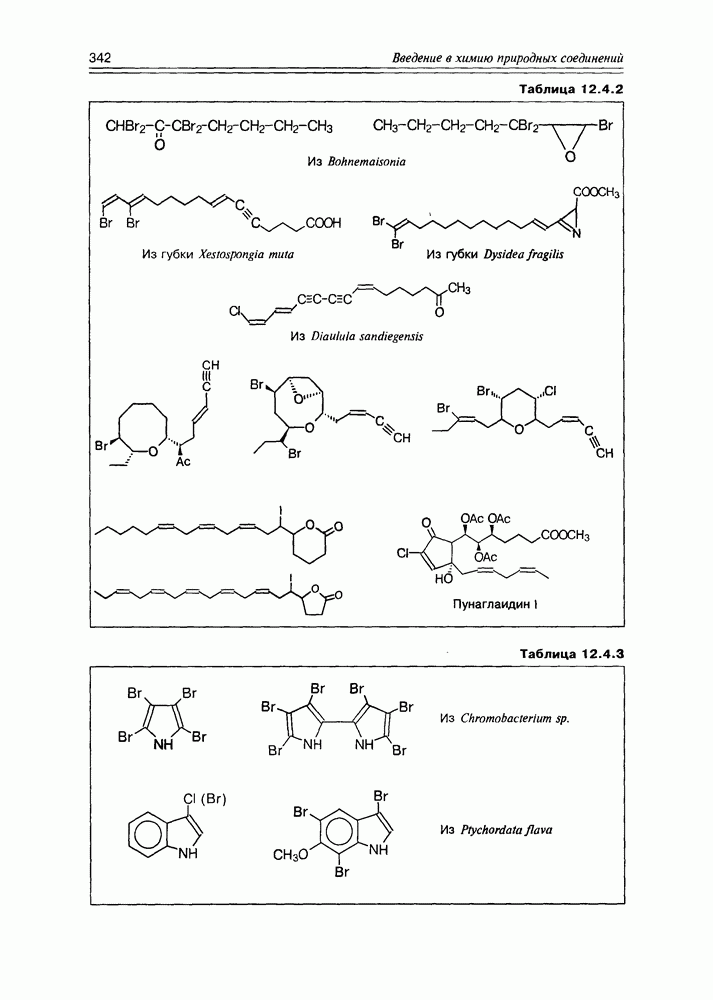
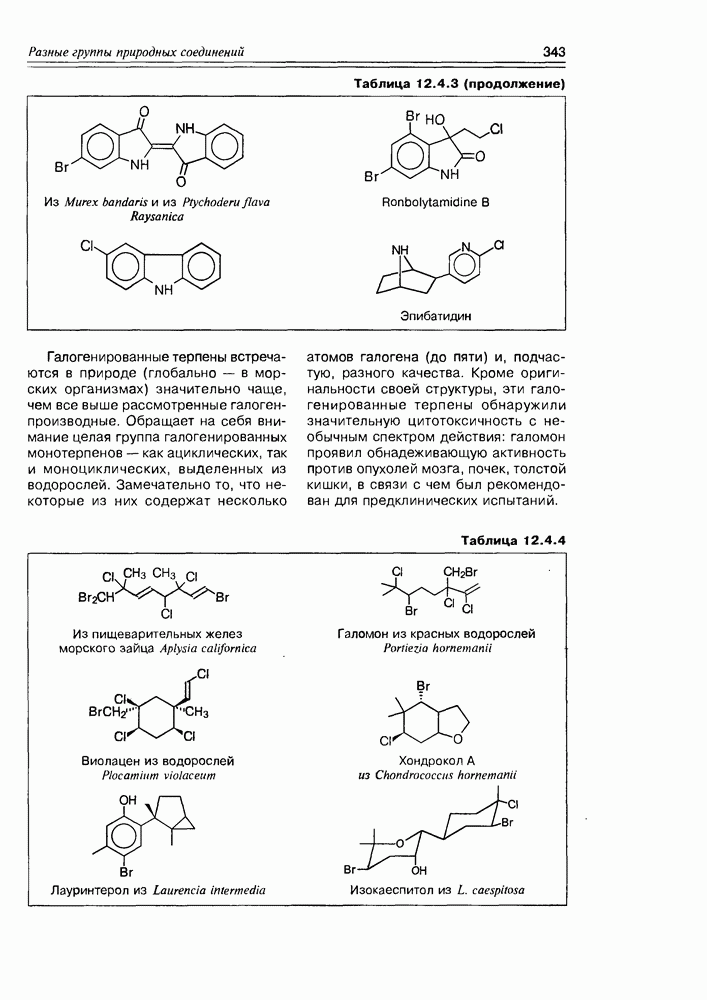
- 12.4. Элементорганические природные соединения
- Глава 13. МЕТАЛЛО-КОЭНЗИМЫ