| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
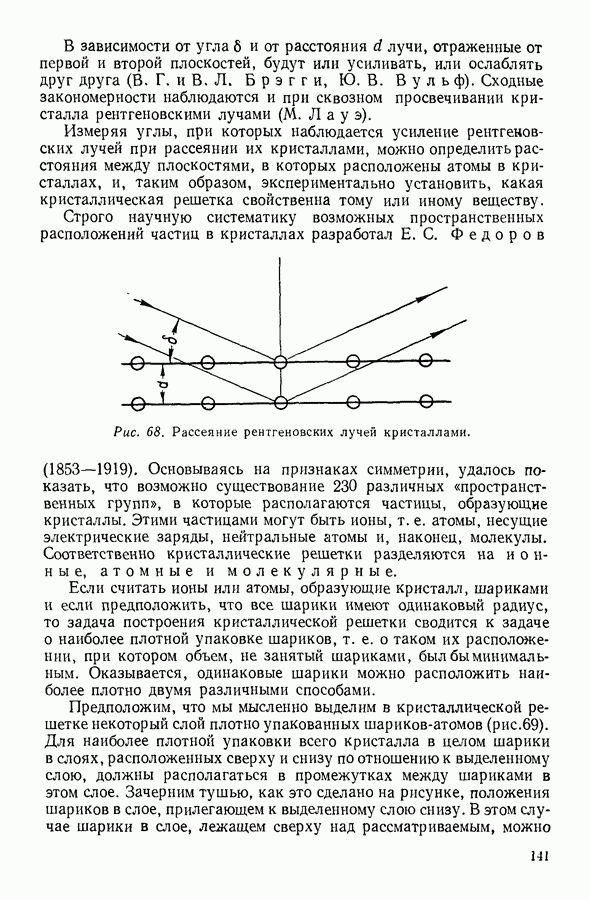
9. НЕКОТОРЫЕ СЛЕДСТВИЯ ИЗ ОСНОВНОГО УРАВНЕНИЯ КИНЕТИЧЕСКОЙ ТЕОРИИ ГАЗОВ
Если в сосуде объемом V находится смесь нескольких газов, то общая кинетическая энергия молекул газовой смеси равна сумме кинетических энергий молекул отдельных компонентов смеси,

где  — кинетические энергии молекул первого, второго, третьего и т. д. газов, входящих в состав смеси.
— кинетические энергии молекул первого, второго, третьего и т. д. газов, входящих в состав смеси.
Написанное равенство не изменится, если обе его части помножить на одну и ту же величину, равную  Проделав эту операцию, найдем:
Проделав эту операцию, найдем:

Проанализируем физический смысл полученного равенства. Выражение  стоящее в левой части уравнения, согласно выводам предыдущего параграфа, представляет собой общее давление газовой смеси
стоящее в левой части уравнения, согласно выводам предыдущего параграфа, представляет собой общее давление газовой смеси 
Первый член правой части уравнения  соответствует тому давлению
соответствует тому давлению  которое оказывал бы первый газ, входящий в состав газовой смеси, если бы он один занимал весь объем
которое оказывал бы первый газ, входящий в состав газовой смеси, если бы он один занимал весь объем  Это давление называют парциальным давлением первого компонента газовой смеси. Второй член правой части уравнения, очевидно, соответствует парциальному давлению второго компонента газовой смеси, третий — парциальному давлению третьего компонента смеси и т. д. Физический смысл полученного уравнения заключается, таким образом, в утверждении, что общее давление, оказываемое на стенки сосуда смесью нескольких газов, равно сумме парциальных давлений отдельных компонентов смеси. Этот важный физический закон был открыт эмпирически Д. Дальтоном и носит его имя.
Это давление называют парциальным давлением первого компонента газовой смеси. Второй член правой части уравнения, очевидно, соответствует парциальному давлению второго компонента газовой смеси, третий — парциальному давлению третьего компонента смеси и т. д. Физический смысл полученного уравнения заключается, таким образом, в утверждении, что общее давление, оказываемое на стенки сосуда смесью нескольких газов, равно сумме парциальных давлений отдельных компонентов смеси. Этот важный физический закон был открыт эмпирически Д. Дальтоном и носит его имя.
Закон Дальтона вытекает непосредственно из основных представлений кинетической теории газов. Действительно, выше предполагалось, что молекулы газа движутся, не соударяясь друг с другом. При этом условии молекулы какого-либо газа в смеси ударяются о стенки сосуда и создают давление независимо от присутствия других газов в сосуде. Очевидно, что общее давление газовой смеси будет при этом равно сумме парциальных давлений компонентов смеси.
Молекулярно-кинетическое истолкование возникновения давления газа позволяет объяснить и весомость газов. Вес газа возникает в результате того, что о верхнюю и нижнюю стенки сосуда
молекулы ударяются, двигаясь с различной скоростью. Для доказательства этого возвратимся еще раз к кубическому сосуду, которым пользовались при выводе основного уравнения кинетической теории газов (рис. 10).
Предположим, что какая-либо молекула ударилась о верхнюю стенку куба, двигаясь со скоростью  При последующем движении вниз скорость молекулы под действием силы тяготения возрастет. Если время движения рассматриваемой молекулы от верхней грани куба до нижней
При последующем движении вниз скорость молекулы под действием силы тяготения возрастет. Если время движения рассматриваемой молекулы от верхней грани куба до нижней  то при соударении с нижней гранью ее скорость
то при соударении с нижней гранью ее скорость  будет
будет

где  ускорение силы тяжести.
ускорение силы тяжести.
Изменение количества движения при ударах молекулы о верхнюю и нижнюю грани куба будут соответственно равны:  при ударе о верхнюю грань и
при ударе о верхнюю грань и  при ударе о нижнюю грань.
при ударе о нижнюю грань.
Время движения молекулы вверх равно времени движения ее вниз, и поэтому промежуток времени между двумя последующими ударами рассматриваемой молекулы об одну и ту же грань  будет равен удвоенному времени движения молекулы сверху вниз, т. е.
будет равен удвоенному времени движения молекулы сверху вниз, т. е.  В этом случае число ударов молекулы о стенку за 1 сек равно
В этом случае число ударов молекулы о стенку за 1 сек равно  а изменения количества движения за то же время на верхней и нижней гранях составит соответственно:
а изменения количества движения за то же время на верхней и нижней гранях составит соответственно:  Разность этих величин будет численно равна направленной вниз избыточной силе, возникающей в результате ударов рассматриваемой молекулы:
Разность этих величин будет численно равна направленной вниз избыточной силе, возникающей в результате ударов рассматриваемой молекулы:

Как мы видим, эта избыточная сила не зависит от скорости движения молекулы, а зависит лишь от ее массы. Поэтому для вычисления суммарной избыточной силы, действующей на нижнюю грань куба со стороны всех молекул, достаточно умножить найденную величину на число молекул  т. е.
т. е.

Здесь  общая масса газа. Таким образом, избыточная сила, действующая на нижнюю грань куба и возникающая в результате изменения скоростей движения молекул под действием поля земного тяготения, и обусловливает вес газа.
общая масса газа. Таким образом, избыточная сила, действующая на нижнюю грань куба и возникающая в результате изменения скоростей движения молекул под действием поля земного тяготения, и обусловливает вес газа.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ОСНОВНЫЕ ЕДИНИЦЫ СИ
- I. ГАЗООБРАЗНОЕ СОСТОЯНИЕ ВЕЩЕСТВА
- 1. РАЗВИТИЕ АТОМНЫХ ПРЕДСТАВЛЕНИЙ В НАУКЕ
- 2. ПОНЯТИЕ О СОСТОЯНИИ ВЕЩЕСТВА
- 3. ЗАКОН БОЙЛЯ — МАРИОТТА
- 4. ЗАКОН ГЕЙ-ЛЮССАКА
- 5. ОБЪЕДИНЕННЫЙ ГАЗОВЫЙ ЗАКОН
- 6. ПОНЯТИЕ ОБ ИДЕАЛЬНОМ ГАЗЕ
- 7. ОСНОВНЫЕ ПОЛОЖЕНИЯ КИНЕТИЧЕСКОЙ ТЕОРИИ ГАЗОВ
- 8. ОСНОВНОЕ УРАВНЕНИЕ КИНЕТИЧЕСКОЙ ТЕОРИИ ГАЗОВ
- 9. НЕКОТОРЫЕ СЛЕДСТВИЯ ИЗ ОСНОВНОГО УРАВНЕНИЯ КИНЕТИЧЕСКОЙ ТЕОРИИ ГАЗОВ
- 10. РАСПРЕДЕЛЕНИЕ МОЛЕКУЛ ГАЗА В ПОЛЕ ЗЕМНОГО ТЯГОТЕНИЯ
- 11. ЭКСПЕРИМЕНТАЛЬНОЕ ОПРЕДЕЛЕНИЕ ЧИСЛА АВОГАДРО
- 12. ЗАКОН РАСПРЕДЕЛЕНИЯ СКОРОСТЕЙ
- 13. ЭКСПЕРИМЕНТАЛЬНАЯ ПРОВЕРКА ЗАКОНА РАСПРЕДЕЛЕНИЯ МАКСВЕЛЛА
- 14. ЧИСЛО СОУДАРЕНИЙ И ДЛИНА СВОБОДНОГО ПРОБЕГА МОЛЕКУЛЫ
- 15. ЭКСПЕРИМЕНТАЛЬНОЕ ОПРЕДЕЛЕНИЕ ДЛИНЫ СРЕДНЕГО СВОБОДНОГО ПРОБЕГА МОЛЕКУЛ
- 16. ЯВЛЕНИЯ ПЕРЕНОСА. ВЯЗКОСТЬ ГАЗОВ
- 17. ТЕПЛОПРОВОДНОСТЬ ГАЗОВ
- 18. ДИФФУЗИЯ ГАЗОВ
- 19. ВАКУУМ. ПОЛУЧЕНИЕ И ИЗМЕРЕНИЕ ВАКУУМА
- 20. ВНУТРЕННЯЯ ЭНЕРГИЯ ИДЕАЛЬНОГО ГАЗА
- 21. ТЕПЛОЕМКОСТЬ ИДЕАЛЬНОГО ГАЗА
- 22. СООТНОШЕНИЕ МЕЖДУ ТЕПЛОЕМКОСТЬЮ ГАЗА ПРИ ПОСТОЯННОМ ОБЪЕМЕ И ТЕПЛОЕМКОСТЬЮ ГАЗА ПРИ ПОСТОЯННОМ ДАВЛЕНИИ
- 23. РЕАЛЬНЫЕ ГАЗЫ. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- 24. ИССЛЕДОВАНИЕ УРАВНЕНИЯ ВАН-ДЕР-ВААЛЬСА
- 25. ОПРЕДЕЛЕНИЕ КРИТИЧЕСКИХ ПАРАМЕТРОВ ВЕЩЕСТВА
- 26. ПРИРОДА СИЛ МОЛЕКУЛЯРНОГО ПРИТЯЖЕНИЯ
- 27. ВНУТРЕННЯЯ ЭНЕРГИЯ РЕАЛЬНОГО ГАЗА
- 28. СЖИЖЕНИЕ ГАЗОВ
- II. ЖИДКОЕ СОСТОЯНИЕ ВЕЩЕСТВА
- 1. СРАВНЕНИЕ СВОЙСТВ ЖИДКОСТЕЙ СО СВОЙСТВАМИ ГАЗОВ И ТВЕРДЫХ ТЕЛ
- 2. МОЛЕКУЛЯРНОЕ ДАВЛЕНИЕ
- 3. ПОВЕРХНОСТНЫЕ СВОЙСТВА ЖИДКОСТЕЙ
- 4. ЯВЛЕНИЯ НА ГРАНИЦЕ ЖИДКОСТИ С ТВЕРДЫМ ТЕЛОМ
- 5. ДАВЛЕНИЕ ПОД ИЗОГНУТОЙ ПОВЕРХНОСТЬЮ ЖИДКОСТИ
- 6. ПОВЕРХНОСТНО-АКТИВНЫЕ ВЕЩЕСТВА
- 7. ИСПАРЕНИЕ ЖИДКОСТЕЙ. НАСЫЩЕННЫЙ ПАР И ЕГО СВОЙСТВА
- 8. МОЛЕКУЛЯРНОЕ СТРОЕНИЕ ЖИДКОСТЕЙ
- 9. ВЯЗКОСТЬ ЖИДКОСТЕЙ
- 10. РАСТВОРЫ. ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ
- 11. ПОНИЖЕНИЕ ДАВЛЕНИЯ НАСЫЩЕННОГО ПАРА РАСТВОРИТЕЛЯ НАД РАСТВОРОМ
- 12. РАСТВОРЫ ЭЛЕКТРОЛИТОВ
- 13. ПРИМЕНЕНИЕ УЛЬТРААКУСТИЧЕСКИХ МЕТОДОВ К ИССЛЕДОВАНИЮ ГАЗОВ И ЖИДКОСТЕЙ
- III. ТВЕРДОЕ СОСТОЯНИЕ ВЕЩЕСТВА
- 1. КРИСТАЛЛИЧЕСКИЕ И АМОРФНЫЕ ТВЕРДЫЕ ТЕЛА
- 2. МОЛЕКУЛЯРНОЕ СТРОЕНИЕ КРИСТАЛЛОВ
- 3. ПОЛИМЕРЫ
- 4. СИЛЫ, ДЕЙСТВУЮЩИЕ МЕЖДУ ЧАСТИЦАМИ В ТВЕРДЫХ ТЕЛАХ
- 5. ТЕПЛОЕМКОСТЬ ТВЕРДЫХ ТЕЛ
- 6. СУБЛИМАЦИЯ, ПЛАВЛЕНИЕ И КРИСТАЛЛИЗАЦИЯ ТВЕРДЫХ ТЕЛ
- 7. КРИСТАЛЛИЗАЦИЯ РАСТВОРОВ. ДИАГРАММЫ ПЛАВКОСТИ
- 8. АДСОРБЦИЯ
- IV. ФИЗИЧЕСКИЕ ОСНОВЫ ТЕРМОДИНАМИКИ
- 1. МОЛЕКУЛЯРНО-КИНЕТИЧЕСКИЙ МЕТОД, МЕТОД СТАТИСТИЧЕСКОЙ МЕХАНИКИ И ТЕРМОДИНАМИЧЕСКИЙ МЕТОД
- 2. ПРЕДМЕТ ТЕРМОДИНАМИКИ. ОСНОВНЫЕ ТЕРМОДИНАМИЧЕСКИЕ ПОНЯТИЯ.
- 3. ФИЗИЧЕСКИЙ СМЫСЛ ПОНЯТИЯ «ТЕПЛОТА»
- 4. ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ
- 5. МЕТОДЫ НАХОЖДЕНИЯ ТЕРМОДИНАМИЧЕСКИХ СООТНОШЕНИЙ
- 6. АДИАБАТНЫЕ ПРОЦЕССЫ. УРАВНЕНИЕ ПУАССОНА
- 7. ПРИМЕНЕНИЕ ПЕРВОГО НАЧАЛА ТЕРМОДИНАМИКИ К НЕКОТОРЫМ ПРОЦЕССАМ В ГАЗАХ
- 8. КРУГОВЫЕ ПРОЦЕССЫ
- 9. ЦИКЛ КАРНО
- 10. ИСПОЛЬЗОВАНИЕ ЦИКЛИЧЕСКИХ ПРОЦЕССОВ В ТЕРМОДИНАМИЧЕСКИХ РАССУЖДЕНИЯХ
- 11. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ
- 12. СТАТИСТИЧЕСКИЙ СМЫСЛ ВТОРОГО НАЧАЛА ТЕРМОДИНАМИКИ
- 13. КРИТИКА ТАК НАЗЫВАЕМОЙ «ТЕОРИИ ТЕПЛОВОЙ СМЕРТИ ВСЕЛЕННОЙ»