| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
20. ВНУТРЕННЯЯ ЭНЕРГИЯ ИДЕАЛЬНОГО ГАЗА
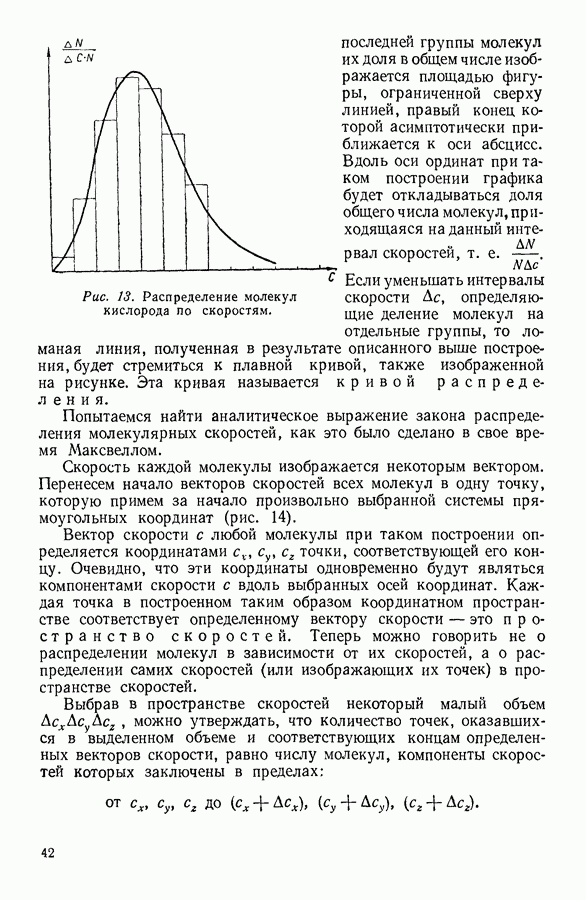
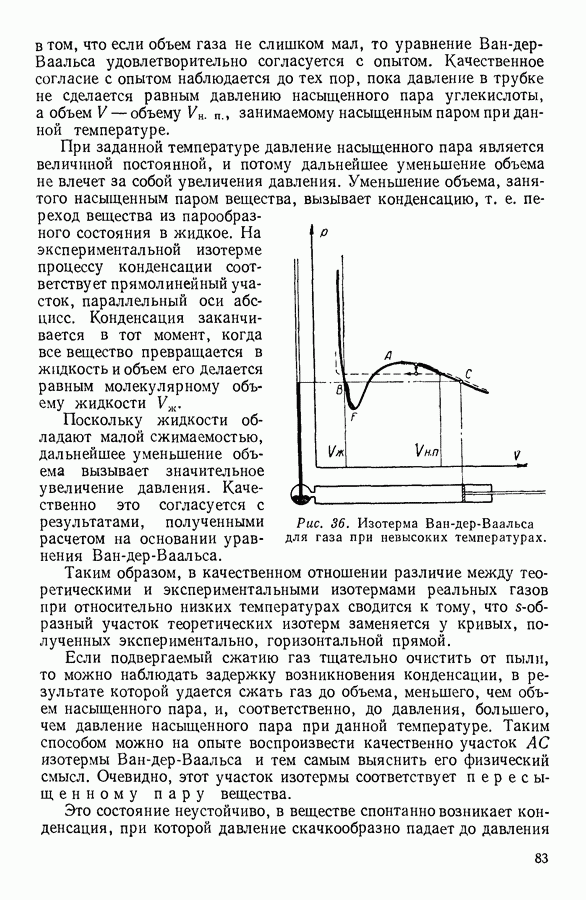
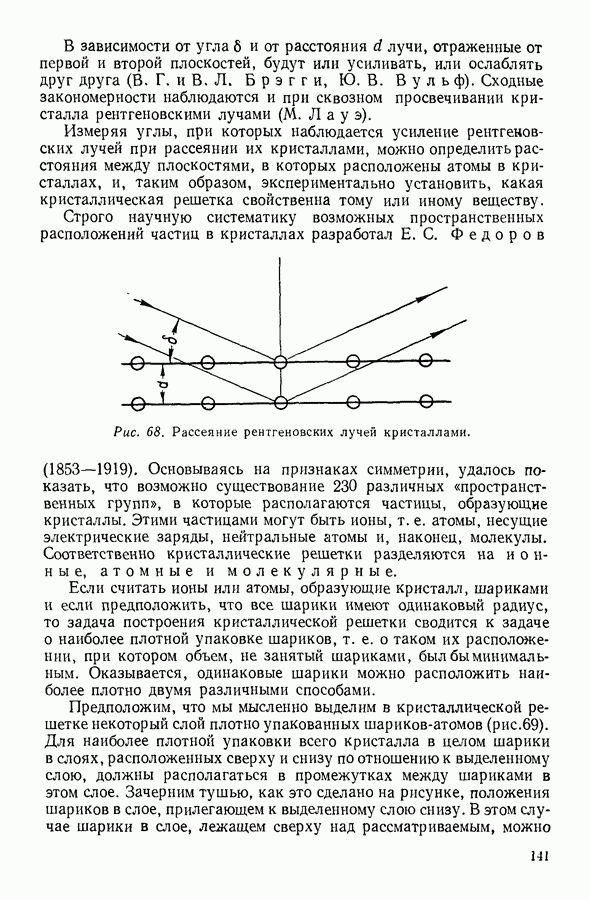
Газ состоит из движущихся с различными скоростями молекул, обладающих вследствие движения определенной кинетической энергией. Полная энергия, которой обладают в совокупности все молекулы газа, называется внутренней энергией газа.
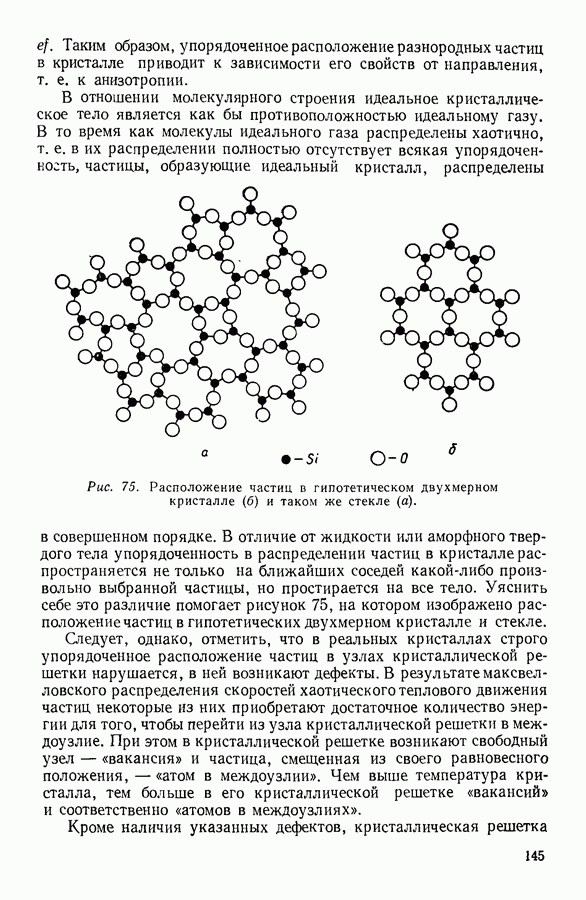
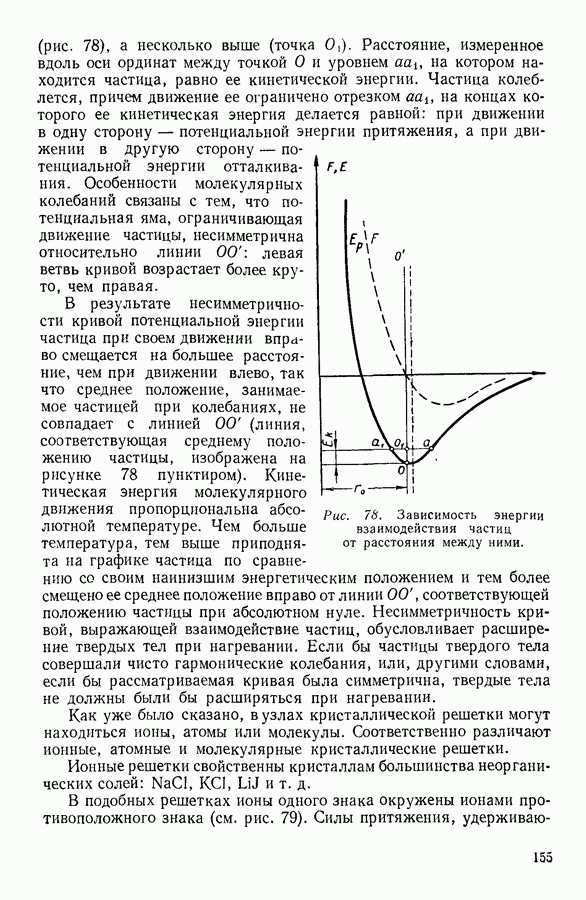
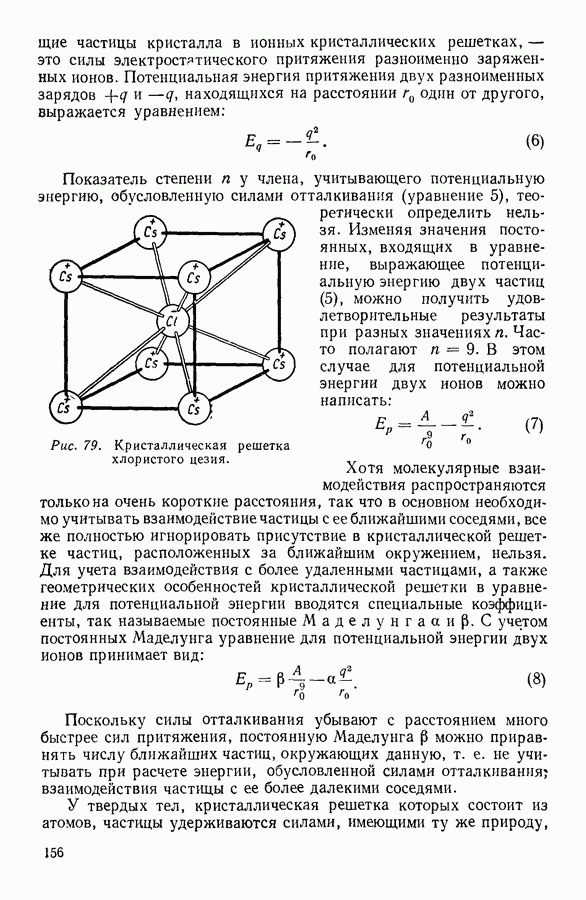
В общем случае внутренняя энергия газа представляет сумму всех видов энергии, которыми обладают молекулы, включая сюда и потенциальную энергию молекулярных взаимодействий, если таковые имеют место. В идеальном газе молекулярные взаимодействия отсутствуют, и поэтому внутренняя энергия его равна суммарной кинетической энергии молекул.
Выше (§ 8) было получено выражение для кинетической энергии молекул, обусловленной их перемещением в пространстве. В случае Молекул конечных размеров это движение соответствует поступательному движению. Поступательное движение твердого тела может быть разложено на три независимых движения, происходящих вдоль трех независимых осей координат. По предложению Максвелла эти независимые движения называют степенями свободы движения молекул. Заметим, что число степеней свободы совпадает с числом независимых координат, которые необходимо ввести для того, чтобы определить положение тела, в данном случае молекулы, в пространстве.
Любая молекула обладает тремя степенями свободы поступательного движения.
В классической кинетической теории молекулы, состоящие из одного атома, принимались за идеально гладкие твердые шарики, у которых при соударениях вращательного движения возникнуть не может. На этом основании предполагалось, что одноатомные молекулы не обладают степенями свободы вращательного движения. Хотя в настоящее время представление об атомах сильно отличается от этой простой модели, однако заключение о том, что при соударениях атомов не возникает вращательного движения, сохраняет свою силу.
Одноатомные молекулы обладают только тремя степенями свободы поступательного движения.
У двухатомной молекулы к трем степеням свободы поступательного движения следовало бы добавить три степени свободы вращательного движения (соответствующие трем взаимно перпендикулярным осям вращения). Однако одну из осей вращения всегда можно совместить с осью молекулы. Вращение вокруг этой оси равносильно вращению отдельных атомов, поэтому его не учитывают. Таким образом, всем двухатомным молекулам, а также тем многоатомным молекулам, атомы которых расположены вдоль прямой, следует приписать две степени свободы вращательного движения.
Общее число степеней свободы двухатомной молекулы равно пяти.
Это число совпадает с числом независимых координат, необходимых для определения положения двухатомной молекулы в пространстве. Действительно, для определения положения двухатомной молекулы в пространстве необходимо и достаточно указать координаты ее центра тяжести  и два угла
и два угла 
Для многоатомной молекулы с нелинейным расположением атомов сохраняются все три степени свободы вращательного движения, и поэтому общее число степеней свободы, обусловленных поступательным и вращательным движением молекулы, равно шести.
В приведенном подсчете числа степеней свободы принималось, что атомы в молекулах закреплены неподвижно и не могут колебаться друг относительно друга. Опыт показывает, что при комнатной температуре для двухатомных газов это предположение оправдывается.

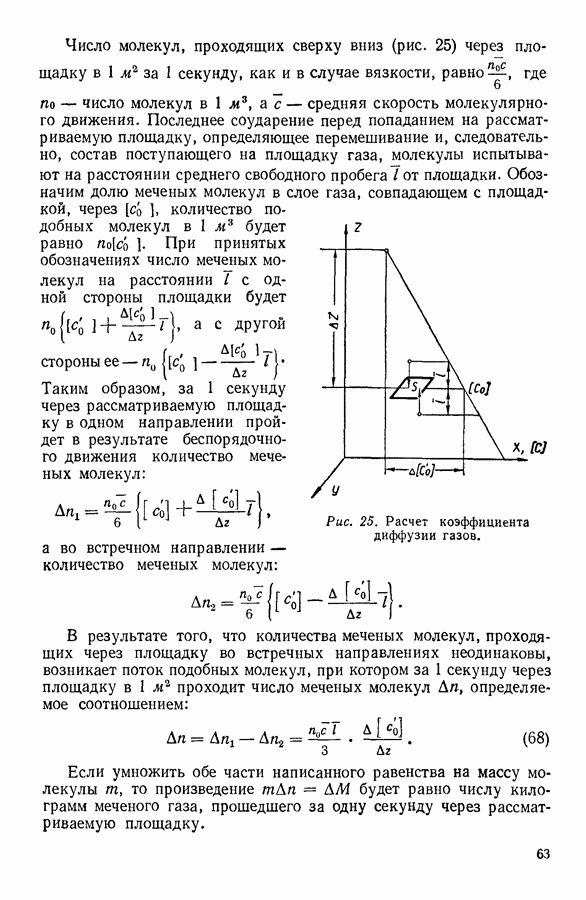
Рис. 31. Число степеней свободы двухатомной молекулы.
Средняя кинетическая энергия поступательного движения любой молекулы (уравнение 28) согласно молекулярно-кинетической теории является линейной функцией абсолютной температуры:

Эту величину можно разложить на три составляющие соответственно трем произвольно выбранным координатным осям, или, как можно теперь сказать, соответственно трем степеням свободы поступательного движения.
Хаотичность молекулярного движения требует, чтобы ни одно из направлений не было бы преимущественным в отношении движения, а это равносильно требованию равного распределения кинетической энергии, связанной с перемещением молекул, между тремя степенями свободы поступательного движения. Максвелл обобщил эту закономерность в знаменитом принципе равного распределения энергии, согласно которому в системе, состоящей из большого числа частиц, кинетическая энергия распределяется в среднем поровну между различными степенями свободы движения частиц.
На три степени свободы поступательного движения молекулы приходится в среднем кинетическая энергия, равная  следовательно, на одну степень свободы будет приходиться:
следовательно, на одну степень свободы будет приходиться:

Такое же количество кинетической энергии будет приходиться при температуре  на любую другую степень свободы движения молекулы.
на любую другую степень свободы движения молекулы.
Таким образом, если молекула газа обладает  степенями свободы, то средняя кинетическая энергия ее будет равна:
степенями свободы, то средняя кинетическая энергия ее будет равна:

Умножив среднюю кинетическую энергию молекулы на число Авогадро  получим кинетическую энергию одного киломоля газа, которая в случае идеального газа будет равна его внутренней энергии
получим кинетическую энергию одного киломоля газа, которая в случае идеального газа будет равна его внутренней энергии  Замечая, что
Замечая, что  можно написать:
можно написать:

| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ОСНОВНЫЕ ЕДИНИЦЫ СИ
- I. ГАЗООБРАЗНОЕ СОСТОЯНИЕ ВЕЩЕСТВА
- 1. РАЗВИТИЕ АТОМНЫХ ПРЕДСТАВЛЕНИЙ В НАУКЕ
- 2. ПОНЯТИЕ О СОСТОЯНИИ ВЕЩЕСТВА
- 3. ЗАКОН БОЙЛЯ — МАРИОТТА
- 4. ЗАКОН ГЕЙ-ЛЮССАКА
- 5. ОБЪЕДИНЕННЫЙ ГАЗОВЫЙ ЗАКОН
- 6. ПОНЯТИЕ ОБ ИДЕАЛЬНОМ ГАЗЕ
- 7. ОСНОВНЫЕ ПОЛОЖЕНИЯ КИНЕТИЧЕСКОЙ ТЕОРИИ ГАЗОВ
- 8. ОСНОВНОЕ УРАВНЕНИЕ КИНЕТИЧЕСКОЙ ТЕОРИИ ГАЗОВ
- 9. НЕКОТОРЫЕ СЛЕДСТВИЯ ИЗ ОСНОВНОГО УРАВНЕНИЯ КИНЕТИЧЕСКОЙ ТЕОРИИ ГАЗОВ
- 10. РАСПРЕДЕЛЕНИЕ МОЛЕКУЛ ГАЗА В ПОЛЕ ЗЕМНОГО ТЯГОТЕНИЯ
- 11. ЭКСПЕРИМЕНТАЛЬНОЕ ОПРЕДЕЛЕНИЕ ЧИСЛА АВОГАДРО
- 12. ЗАКОН РАСПРЕДЕЛЕНИЯ СКОРОСТЕЙ
- 13. ЭКСПЕРИМЕНТАЛЬНАЯ ПРОВЕРКА ЗАКОНА РАСПРЕДЕЛЕНИЯ МАКСВЕЛЛА
- 14. ЧИСЛО СОУДАРЕНИЙ И ДЛИНА СВОБОДНОГО ПРОБЕГА МОЛЕКУЛЫ
- 15. ЭКСПЕРИМЕНТАЛЬНОЕ ОПРЕДЕЛЕНИЕ ДЛИНЫ СРЕДНЕГО СВОБОДНОГО ПРОБЕГА МОЛЕКУЛ
- 16. ЯВЛЕНИЯ ПЕРЕНОСА. ВЯЗКОСТЬ ГАЗОВ
- 17. ТЕПЛОПРОВОДНОСТЬ ГАЗОВ
- 18. ДИФФУЗИЯ ГАЗОВ
- 19. ВАКУУМ. ПОЛУЧЕНИЕ И ИЗМЕРЕНИЕ ВАКУУМА
- 20. ВНУТРЕННЯЯ ЭНЕРГИЯ ИДЕАЛЬНОГО ГАЗА
- 21. ТЕПЛОЕМКОСТЬ ИДЕАЛЬНОГО ГАЗА
- 22. СООТНОШЕНИЕ МЕЖДУ ТЕПЛОЕМКОСТЬЮ ГАЗА ПРИ ПОСТОЯННОМ ОБЪЕМЕ И ТЕПЛОЕМКОСТЬЮ ГАЗА ПРИ ПОСТОЯННОМ ДАВЛЕНИИ
- 23. РЕАЛЬНЫЕ ГАЗЫ. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- 24. ИССЛЕДОВАНИЕ УРАВНЕНИЯ ВАН-ДЕР-ВААЛЬСА
- 25. ОПРЕДЕЛЕНИЕ КРИТИЧЕСКИХ ПАРАМЕТРОВ ВЕЩЕСТВА
- 26. ПРИРОДА СИЛ МОЛЕКУЛЯРНОГО ПРИТЯЖЕНИЯ
- 27. ВНУТРЕННЯЯ ЭНЕРГИЯ РЕАЛЬНОГО ГАЗА
- 28. СЖИЖЕНИЕ ГАЗОВ
- II. ЖИДКОЕ СОСТОЯНИЕ ВЕЩЕСТВА
- 1. СРАВНЕНИЕ СВОЙСТВ ЖИДКОСТЕЙ СО СВОЙСТВАМИ ГАЗОВ И ТВЕРДЫХ ТЕЛ
- 2. МОЛЕКУЛЯРНОЕ ДАВЛЕНИЕ
- 3. ПОВЕРХНОСТНЫЕ СВОЙСТВА ЖИДКОСТЕЙ
- 4. ЯВЛЕНИЯ НА ГРАНИЦЕ ЖИДКОСТИ С ТВЕРДЫМ ТЕЛОМ
- 5. ДАВЛЕНИЕ ПОД ИЗОГНУТОЙ ПОВЕРХНОСТЬЮ ЖИДКОСТИ
- 6. ПОВЕРХНОСТНО-АКТИВНЫЕ ВЕЩЕСТВА
- 7. ИСПАРЕНИЕ ЖИДКОСТЕЙ. НАСЫЩЕННЫЙ ПАР И ЕГО СВОЙСТВА
- 8. МОЛЕКУЛЯРНОЕ СТРОЕНИЕ ЖИДКОСТЕЙ
- 9. ВЯЗКОСТЬ ЖИДКОСТЕЙ
- 10. РАСТВОРЫ. ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ
- 11. ПОНИЖЕНИЕ ДАВЛЕНИЯ НАСЫЩЕННОГО ПАРА РАСТВОРИТЕЛЯ НАД РАСТВОРОМ
- 12. РАСТВОРЫ ЭЛЕКТРОЛИТОВ
- 13. ПРИМЕНЕНИЕ УЛЬТРААКУСТИЧЕСКИХ МЕТОДОВ К ИССЛЕДОВАНИЮ ГАЗОВ И ЖИДКОСТЕЙ
- III. ТВЕРДОЕ СОСТОЯНИЕ ВЕЩЕСТВА
- 1. КРИСТАЛЛИЧЕСКИЕ И АМОРФНЫЕ ТВЕРДЫЕ ТЕЛА
- 2. МОЛЕКУЛЯРНОЕ СТРОЕНИЕ КРИСТАЛЛОВ
- 3. ПОЛИМЕРЫ
- 4. СИЛЫ, ДЕЙСТВУЮЩИЕ МЕЖДУ ЧАСТИЦАМИ В ТВЕРДЫХ ТЕЛАХ
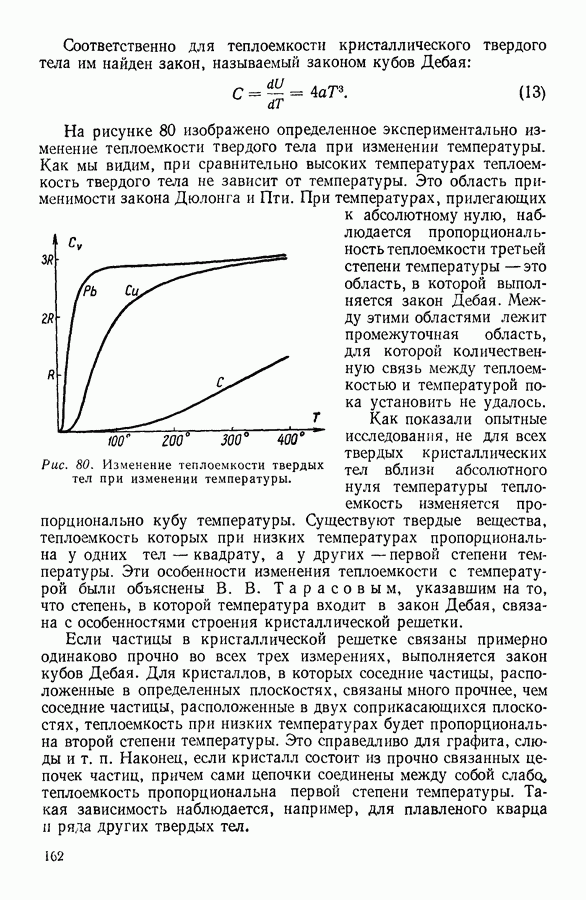
- 5. ТЕПЛОЕМКОСТЬ ТВЕРДЫХ ТЕЛ
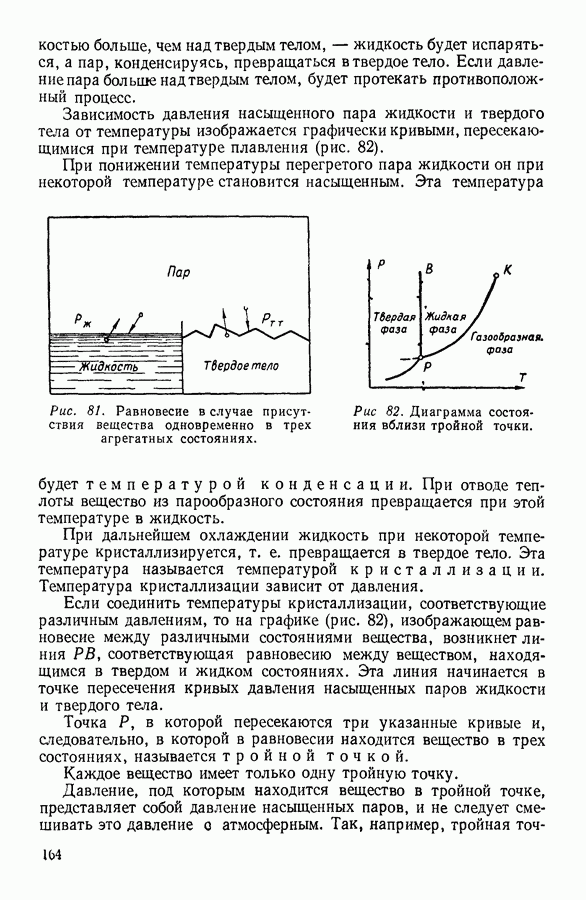
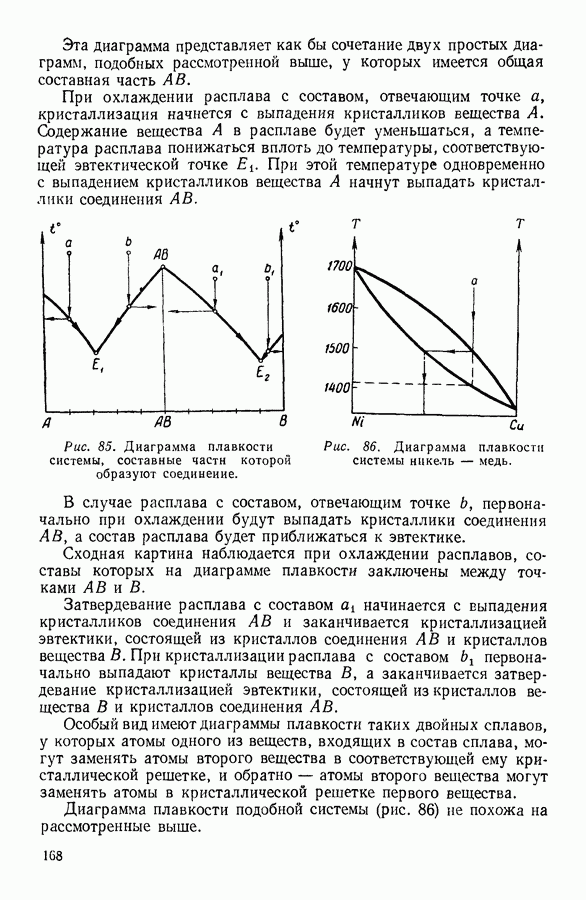
- 6. СУБЛИМАЦИЯ, ПЛАВЛЕНИЕ И КРИСТАЛЛИЗАЦИЯ ТВЕРДЫХ ТЕЛ
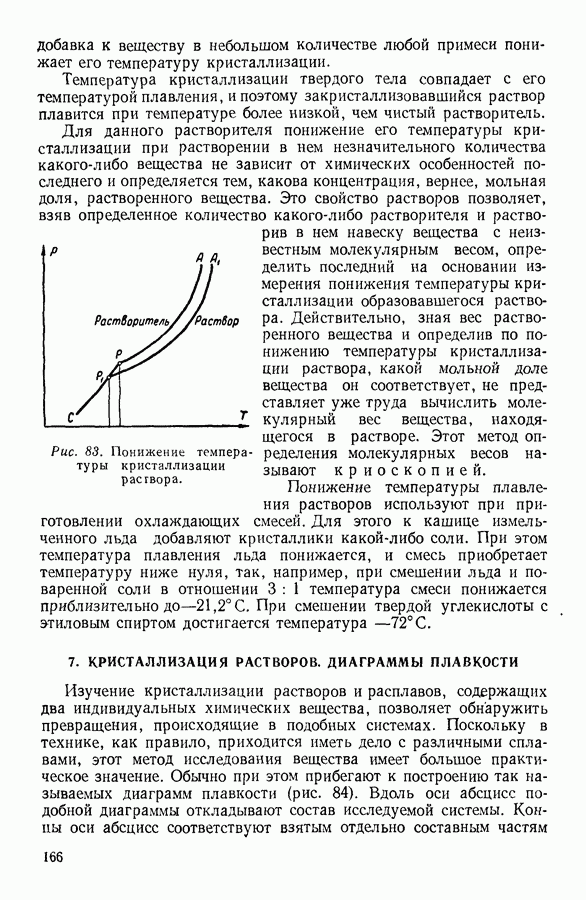
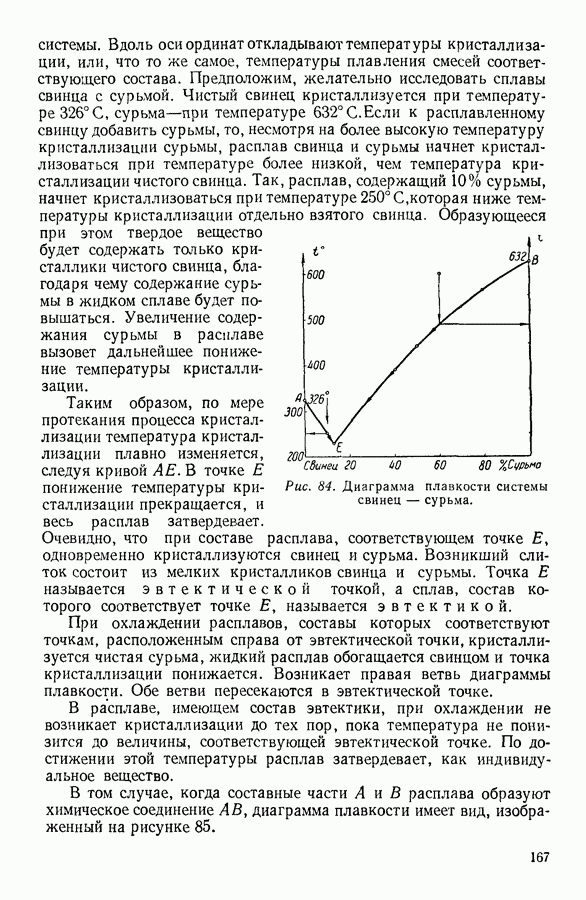
- 7. КРИСТАЛЛИЗАЦИЯ РАСТВОРОВ. ДИАГРАММЫ ПЛАВКОСТИ
- 8. АДСОРБЦИЯ
- IV. ФИЗИЧЕСКИЕ ОСНОВЫ ТЕРМОДИНАМИКИ
- 1. МОЛЕКУЛЯРНО-КИНЕТИЧЕСКИЙ МЕТОД, МЕТОД СТАТИСТИЧЕСКОЙ МЕХАНИКИ И ТЕРМОДИНАМИЧЕСКИЙ МЕТОД
- 2. ПРЕДМЕТ ТЕРМОДИНАМИКИ. ОСНОВНЫЕ ТЕРМОДИНАМИЧЕСКИЕ ПОНЯТИЯ.
- 3. ФИЗИЧЕСКИЙ СМЫСЛ ПОНЯТИЯ «ТЕПЛОТА»
- 4. ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ
- 5. МЕТОДЫ НАХОЖДЕНИЯ ТЕРМОДИНАМИЧЕСКИХ СООТНОШЕНИЙ
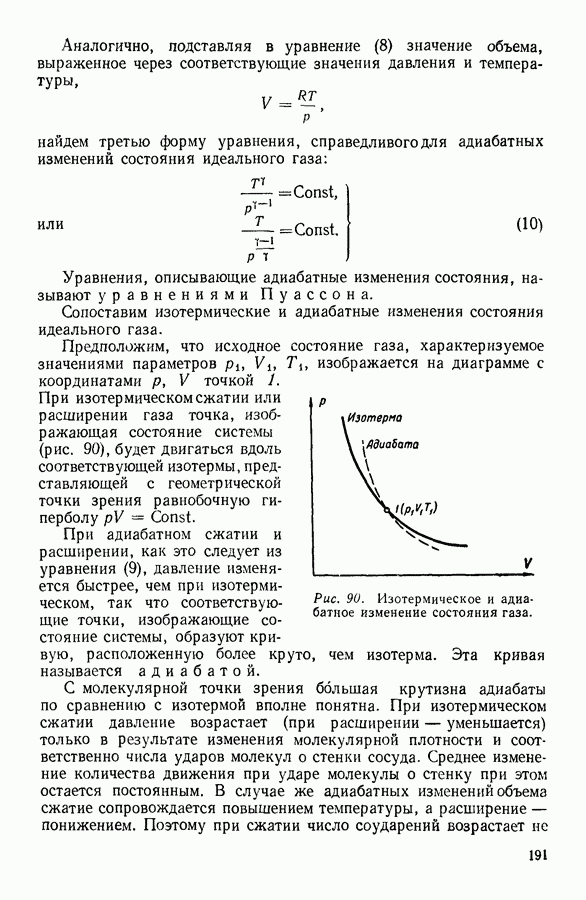
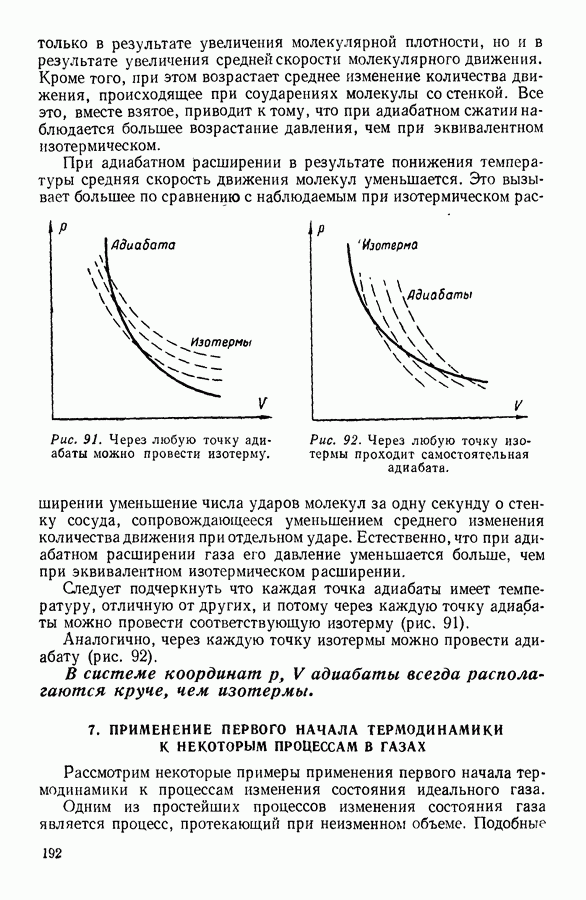
- 6. АДИАБАТНЫЕ ПРОЦЕССЫ. УРАВНЕНИЕ ПУАССОНА
- 7. ПРИМЕНЕНИЕ ПЕРВОГО НАЧАЛА ТЕРМОДИНАМИКИ К НЕКОТОРЫМ ПРОЦЕССАМ В ГАЗАХ
- 8. КРУГОВЫЕ ПРОЦЕССЫ
- 9. ЦИКЛ КАРНО
- 10. ИСПОЛЬЗОВАНИЕ ЦИКЛИЧЕСКИХ ПРОЦЕССОВ В ТЕРМОДИНАМИЧЕСКИХ РАССУЖДЕНИЯХ
- 11. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ
- 12. СТАТИСТИЧЕСКИЙ СМЫСЛ ВТОРОГО НАЧАЛА ТЕРМОДИНАМИКИ
- 13. КРИТИКА ТАК НАЗЫВАЕМОЙ «ТЕОРИИ ТЕПЛОВОЙ СМЕРТИ ВСЕЛЕННОЙ»