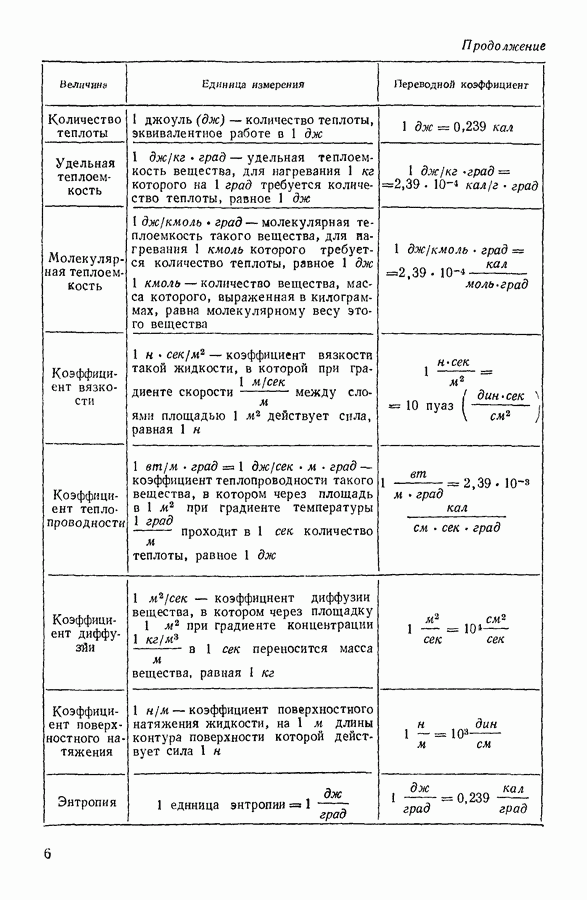
| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
5. ТЕПЛОЕМКОСТЬ ТВЕРДЫХ ТЕЛ
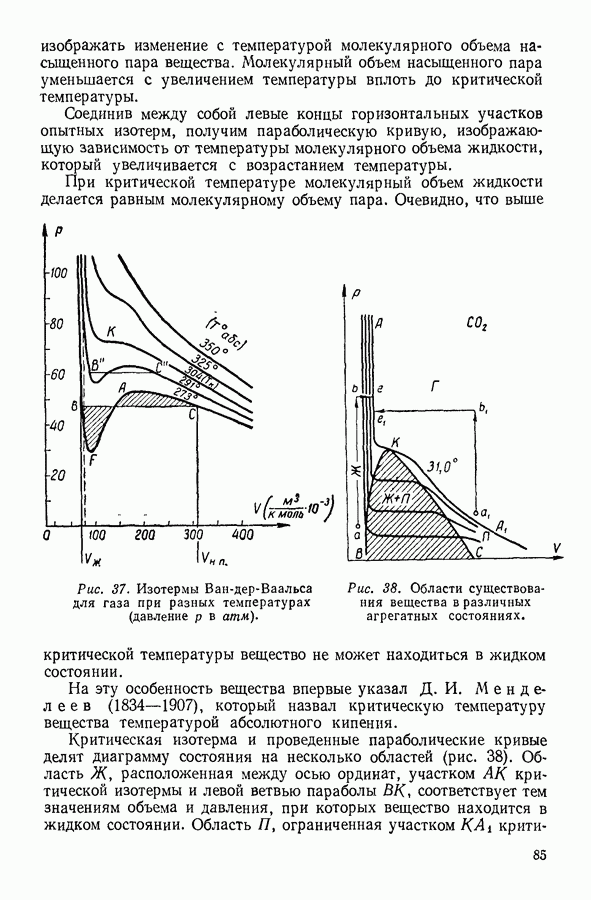
Образующие твердое тело частицы находятся в непрерывном тепловом движении — они колеблются около положений равновесия, совпадающих с узлами кристаллической решетки. Естественно, что каждая частица взаимодействует с окружающими ее частицами, и поэтому колебания всех частиц являются связанными между собой. Однако, как показывает сопоставление выводов теории с опытом, при достаточно высокой температуре эта связь невелика,
и можно считать, что каждая частица колеблется независимо от своих соседей.
Внутренняя энергия, приходящаяся на одну степень свободы движения атома или молекулы  пропорциональна абсолютной температуре:
пропорциональна абсолютной температуре:

здесь  постоянная Больцмана,
постоянная Больцмана,  абсолютная температура. Если атомы вещества обладают
абсолютная температура. Если атомы вещества обладают  степенями свободы, то внутренняя энергия
степенями свободы, то внутренняя энергия  одного килограмм-атома выражается соотношением:
одного килограмм-атома выражается соотношением:

Поскольку  а — число Авогадро,
а — число Авогадро,  то
то

Положение атома (как материальной точки) в пространстве определяется тремя координатами, следовательно, колеблющийся атом обладает тремя степенями свободы движения.
При подобном подсчете числа степеней свободы необходимо, однако, принять во внимание, что колеблющаяся материальная точка обладает одновременно кинетической и потенциальной энергией, и поэтому при вычислении внутренней энергии колеблющегося атома наряду со степенями свободы, приходящимися на кинетическую энергию, следует учитывать равное количество степеней свободы, приходящихся на долю потенциальной энергии. В результате этого колеблющийся атом оказывается обладающим не тремя степенями свободы, а шестью.
Внутренняя энергия килограмм-атома кристаллического твердого тела, таким образом, равна:

Поскольку твердые тела обладают малым коэффициентом термического расширения и, следовательно, мало увеличиваются в объеме при нагревании, для них часто не различают теплоемкость при постоянном объеме от теплоемкости при постоянном давлении, а говорят просто о теплоемкости твердого тела С, которая численно равна первой производной от внутренней энергии тела по температуре:

Подставляя в выражение для теплоемкости значение внутренней энергии твердого тела, найдем:

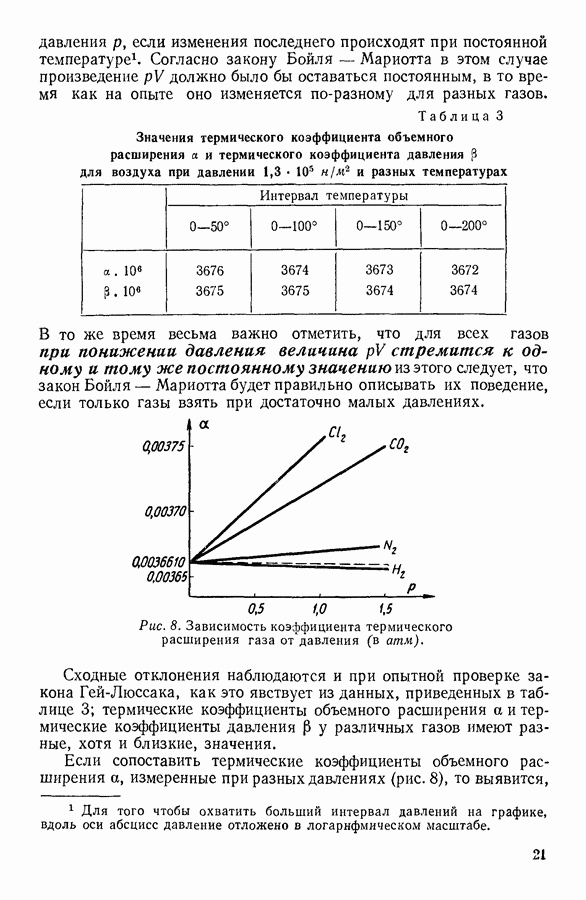
Таким образом, при достаточно высокой температуре атомная теплоемкость всех твердых тел не зависит от температуры и равна 
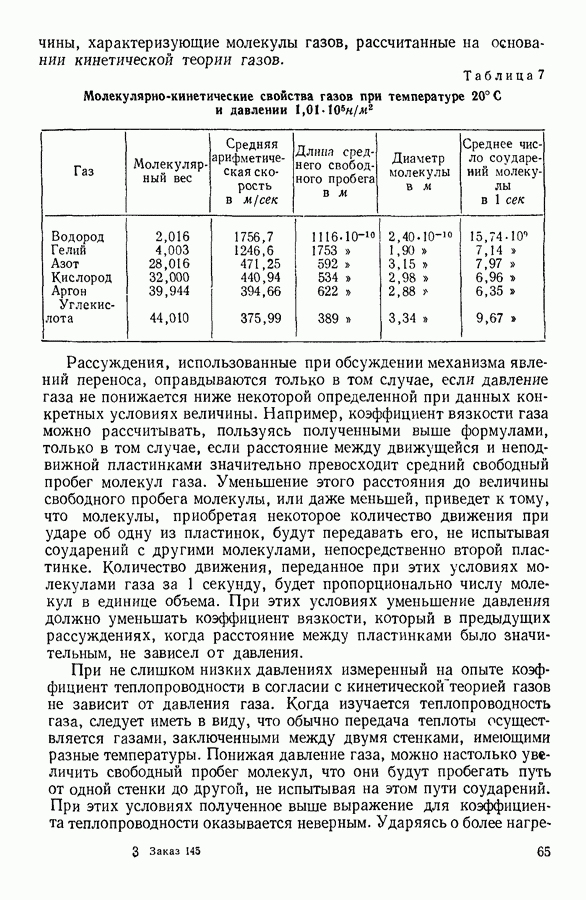
Этот закон был открыт эмпирически еще в XIX столетии Дюлонгом (1785—1838) и Пти (1791—1820) и носит их имя (закон Дюлонга и  Величины, приведенные в таблице 14, убеждают в том, что во многих случаях закон Дюлонга и
Величины, приведенные в таблице 14, убеждают в том, что во многих случаях закон Дюлонга и  удовлетворительно выполняется, и, следовательно, для указанных в таблице веществ колебания атомов уже при комнатной температуре можно считать независимыми. В то же время имеются и такие вещества, как, например, алмаз или бор, для которых измеренное при комнатной температуре значение темплоемкости существенно отличается от
удовлетворительно выполняется, и, следовательно, для указанных в таблице веществ колебания атомов уже при комнатной температуре можно считать независимыми. В то же время имеются и такие вещества, как, например, алмаз или бор, для которых измеренное при комнатной температуре значение темплоемкости существенно отличается от 
Таблица 14 (см. скан) Теплоемкость твердых тел
Таблица 15 (см. скан) Молекулярная теплоемкость химических соединений в твердом состоянии
Для этих веществ комнатная температура, очевидно, недостаточно высока для того, чтобы считать колебания атомов независимыми.
В случае кристаллов солей или каких-либо других химических соединений обычно определяется не атомная, а молекулярная теплоемкость.
Если по-прежнему считать, что кристалл построен из атомов или ионов, колеблющихся независимо друг от друга, то, очевидно, число частиц, движение которых необходимо учитывать при вычислении внутренней энергии одного килограмм-моля вещества, будет равно общему числу атомов в одном киломоле вещества или числу Авогадро, помноженному на число атомов в молекуле. Это объясняет найденное эмпирически правило, согласно которому молекулярная теплоемкость твердого соединения равна сумме атомных теплоемкостей элементов, входящих в состав соединения.
В случае твердых соединений, состоящих из двух атомов, наг пример  молекулярная теплоемкость согласно этому правилу должна равняться
молекулярная теплоемкость согласно этому правилу должна равняться  а для твердых соединений, состоящих из трех атомов, например
а для твердых соединений, состоящих из трех атомов, например  и т. д.,
и т. д.,
соответственно  В таблице 15 приведены величины молекулярных теплоемкостей некоторых соединений, подтверждающие сформулированное правило.
В таблице 15 приведены величины молекулярных теплоемкостей некоторых соединений, подтверждающие сформулированное правило.
Как показывает опыт, постоянство теплоемкости твердых тел нарушается при понижении температуры. Теплоемкости твердых тел уменьшаются при понижении температуры, стремясь к нулю при приближении температуры к абсолютному нулю.
Удовлетворительно объяснить зависимость теплоемкости твердых тел от температуры удалось Дебаю на основе теории квантов. Теория квантов, развитая  Планком (1858—1947), исходит из представления о том, что энергия, так же как и вещество, имеет дискретную (прерывную) природу. Энергия может передаваться от одних тел другим не сколь угодно малыми порциями, а лишь определенными дискретными количествами — квантами.
Планком (1858—1947), исходит из представления о том, что энергия, так же как и вещество, имеет дискретную (прерывную) природу. Энергия может передаваться от одних тел другим не сколь угодно малыми порциями, а лишь определенными дискретными количествами — квантами.
Величина кванта энергии колебательного движения  зависит от частоты колебаний
зависит от частоты колебаний  и определяется выражением:
и определяется выражением:

в котором  так называемая универсальная постоянная Планка, равная
так называемая универсальная постоянная Планка, равная  сек.
сек.
Квантовая природа энергии проявляется в тепловых явлениях тогда, когда энергия теплового движения атомов или молекул, приходящаяся на одну степень свободы —  делается сравнимой с величиной кванта энергии. Пока же величина кванта энергии очень мала по сравнению с величинои
делается сравнимой с величиной кванта энергии. Пока же величина кванта энергии очень мала по сравнению с величинои  квантовую природу энергии можно не учитывать. Частота колебаний частиц в кристаллической решетке имеет порядок
квантовую природу энергии можно не учитывать. Частота колебаний частиц в кристаллической решетке имеет порядок  так что соответствующий квант имеет величину, равную
так что соответствующий квант имеет величину, равную 
Таким образом, квантовую природу энергии необходимо учитывать при температурах  при которых выполняется неравенство:
при которых выполняется неравенство:

или

Исходя из квантовой теории, Дебай нашел, что при температурах, близких к абсолютному нулю, внутренняя энергия кристаллического твердого тела пропорциональна четвертой степени температуры:

где а — постоянная величина.
Соответственно для теплоемкости кристаллического твердого тела им найден закон, называемый законом кубов Дебая:

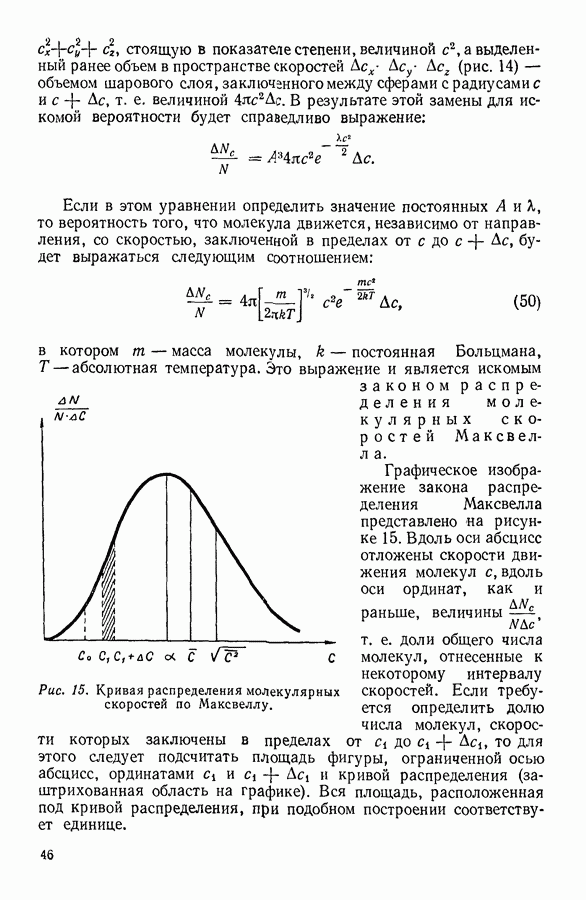
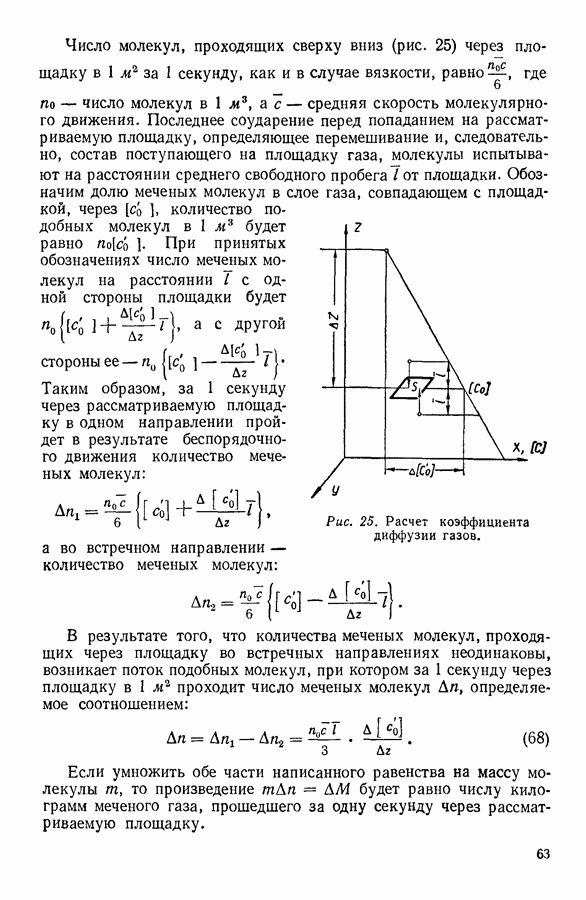
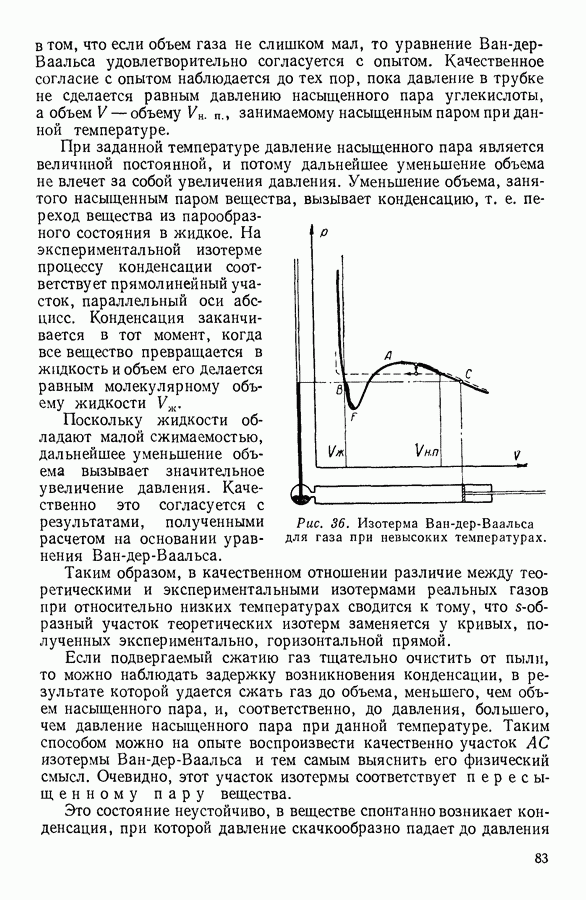
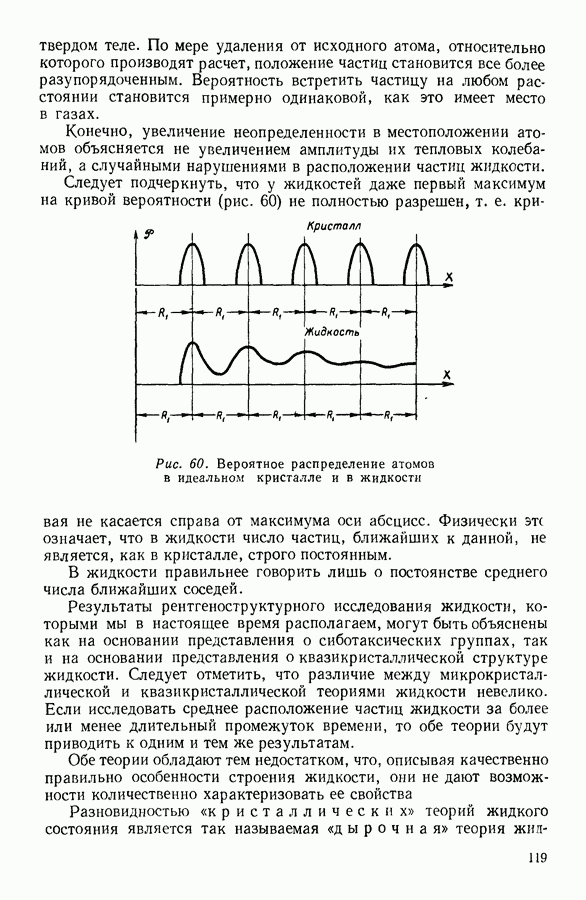
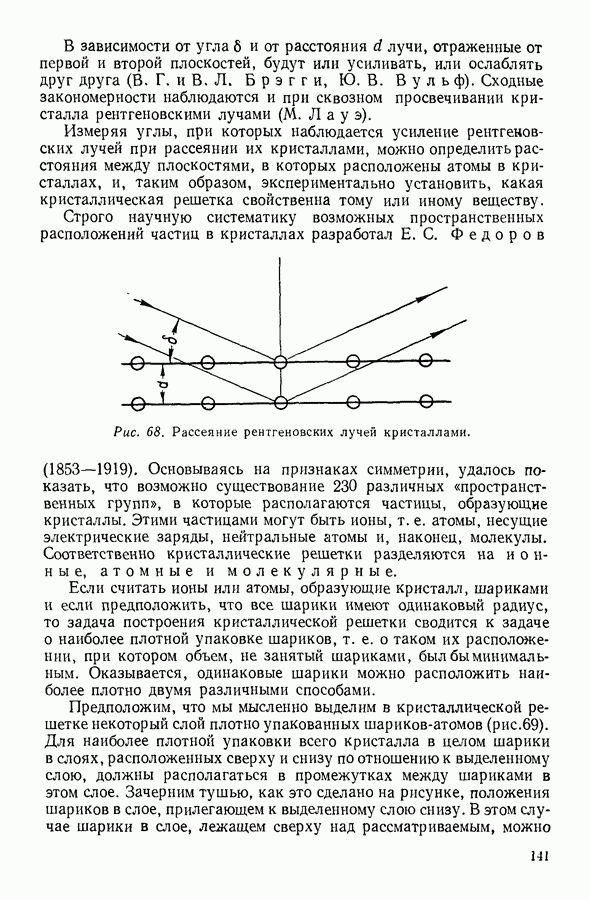
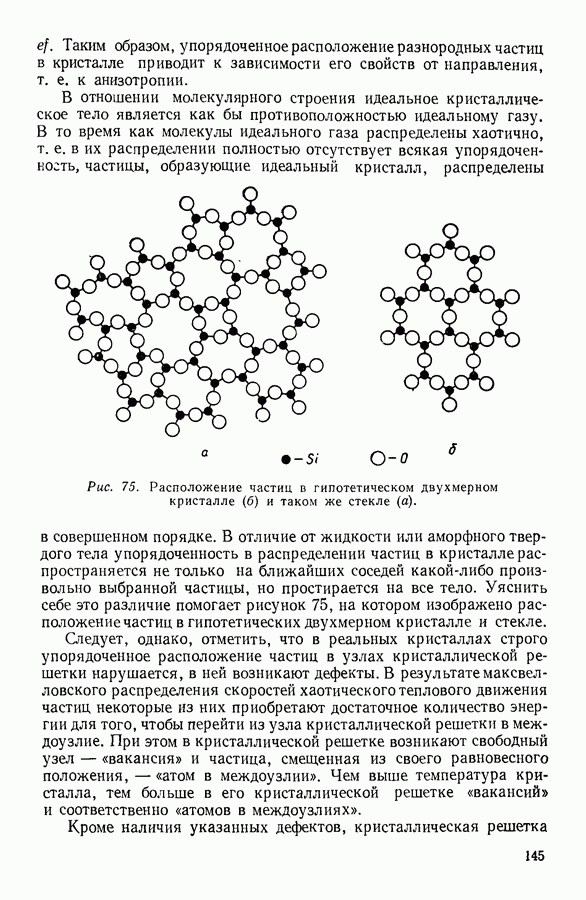
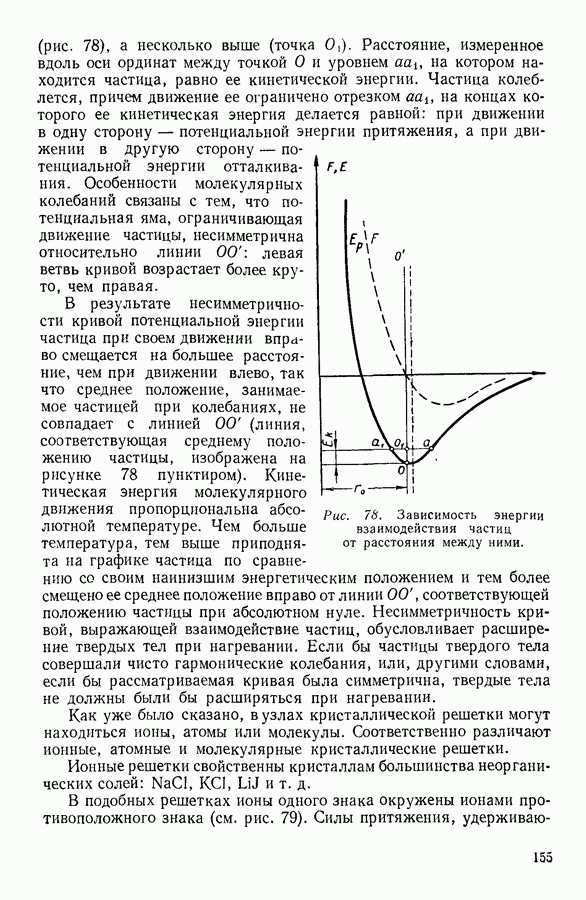
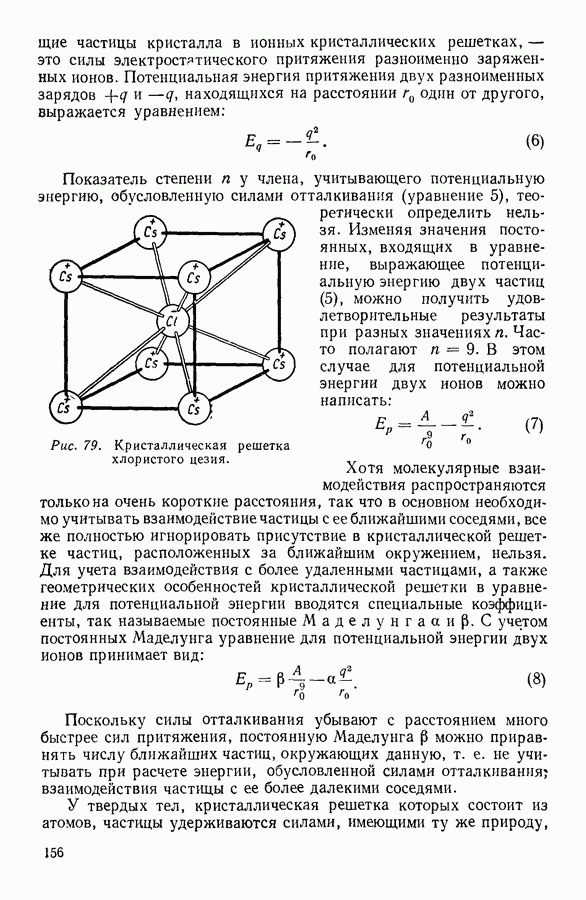
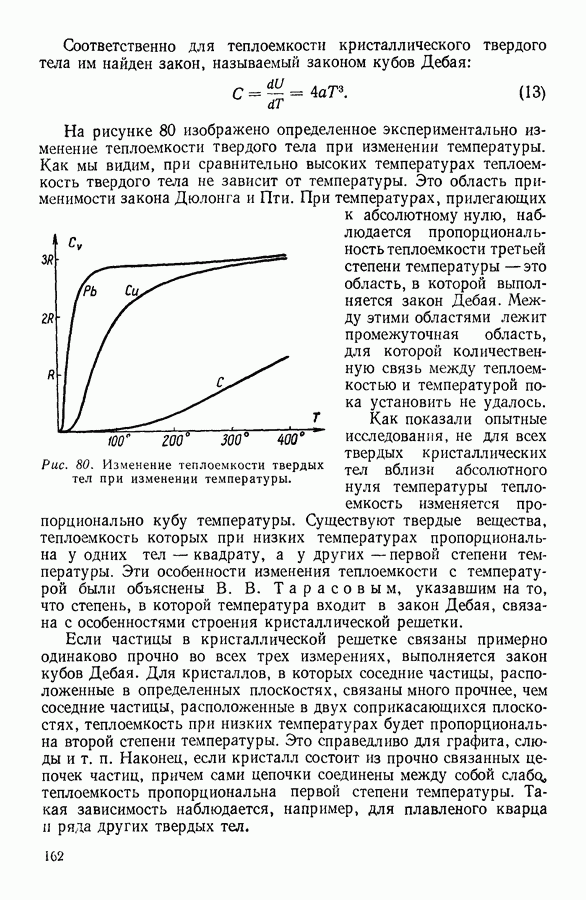
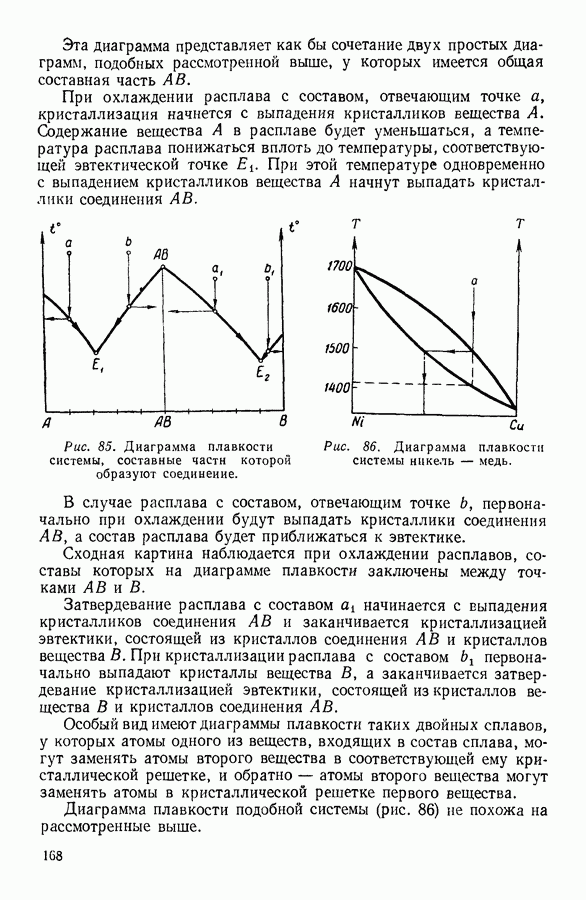
На рисунке 80 изображено определенное экспериментально изменение теплоемкости твердого тела при изменении температуры. Как мы видим, при сравнительно высоких температурах теплоемкость твердого тела не зависит от температуры. Это область применимости закона Дюлонга и Пти. При температурах, прилегающих к абсолютному нулю, наблюдается пропорциональность теплоемкости третьей степени температуры — это область, в которой выполняется закон Дебая. Между этими областями лежит промежуточная область, для которой количественную связь между теплоемкостью и температурой пока установить не удалось.

Рис. 80. Изменение теплоемкости твердых тел при изменении температуры.
Как показали опытные исследования, не для всех твердых кристаллических тел вблизи абсолютного нуля температуры теплоемкость изменяется пропорционально кубу температуры. Существуют твердые вещества, теплоемкость которых при низких температурах пропорциональна у одних тел — квадрату, а у других — первой степени температуры. Эти особенности изменения теплоемкости с температурой были объяснены В. В. Тарасовым, указавшим на то, что степень, в которой температура входит в закон Дебая, связана с особенностями строения кристаллической решетки.
Если частицы в кристаллической решетке связаны примерно одинаково прочно во всех трех измерениях, выполняется закон кубов Дебая. Для кристаллов, в которых соседние частицы, расположенные в определенных плоскостях, связаны много прочнее, чем соседние частицы, расположенные в двух соприкасающихся плоскостях, теплоемкость при низких температурах будет пропорциональна второй степени температуры. Это справедливо для графита, слюды и т. п. Наконец, если кристалл состоит из прочно связанных цепочек частиц, причем сами цепочки соединены между собой слабо, теплоемкость пропорциональна первой степени температуры. Такая зависимость наблюдается, например, для плавленого кварца  ряда других твердых тел.
ряда других твердых тел.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ОСНОВНЫЕ ЕДИНИЦЫ СИ
- I. ГАЗООБРАЗНОЕ СОСТОЯНИЕ ВЕЩЕСТВА
- 1. РАЗВИТИЕ АТОМНЫХ ПРЕДСТАВЛЕНИЙ В НАУКЕ
- 2. ПОНЯТИЕ О СОСТОЯНИИ ВЕЩЕСТВА
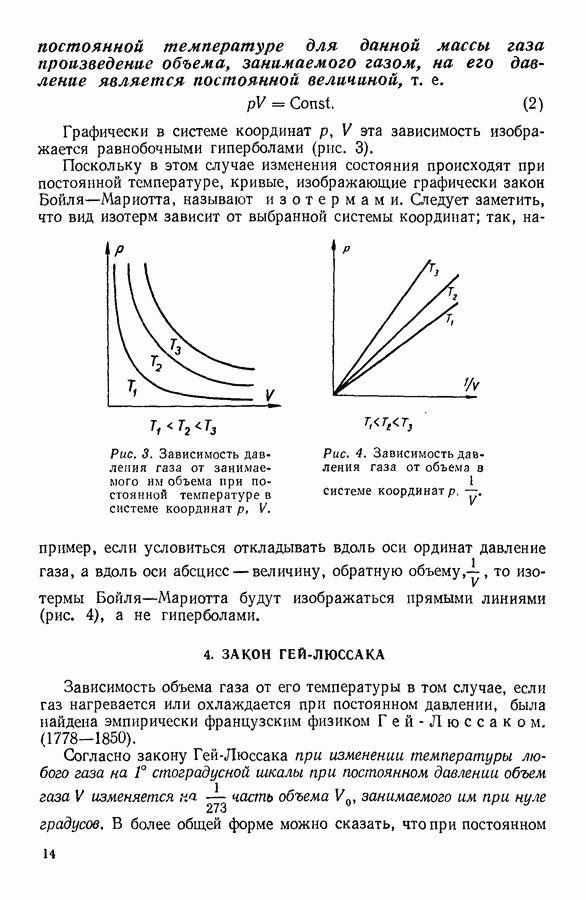
- 3. ЗАКОН БОЙЛЯ — МАРИОТТА
- 4. ЗАКОН ГЕЙ-ЛЮССАКА
- 5. ОБЪЕДИНЕННЫЙ ГАЗОВЫЙ ЗАКОН
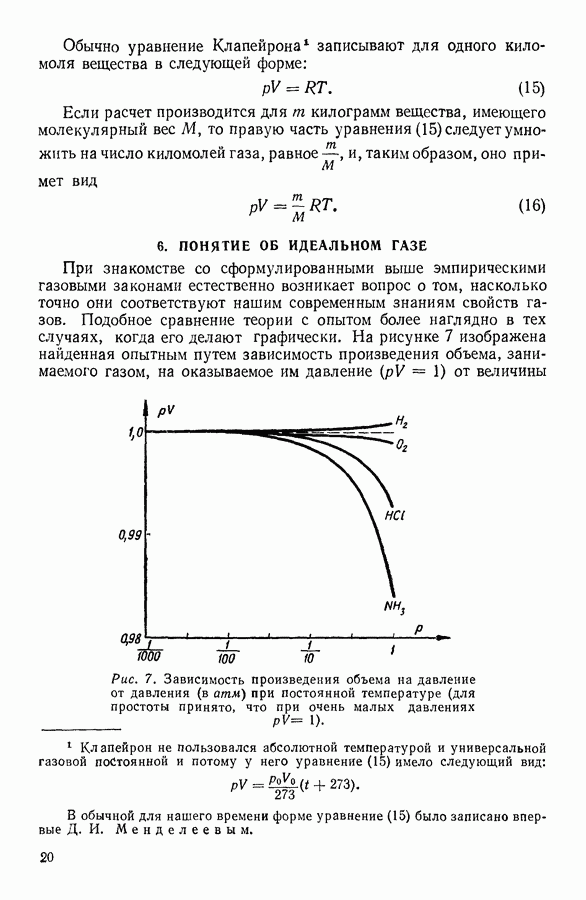
- 6. ПОНЯТИЕ ОБ ИДЕАЛЬНОМ ГАЗЕ
- 7. ОСНОВНЫЕ ПОЛОЖЕНИЯ КИНЕТИЧЕСКОЙ ТЕОРИИ ГАЗОВ
- 8. ОСНОВНОЕ УРАВНЕНИЕ КИНЕТИЧЕСКОЙ ТЕОРИИ ГАЗОВ
- 9. НЕКОТОРЫЕ СЛЕДСТВИЯ ИЗ ОСНОВНОГО УРАВНЕНИЯ КИНЕТИЧЕСКОЙ ТЕОРИИ ГАЗОВ
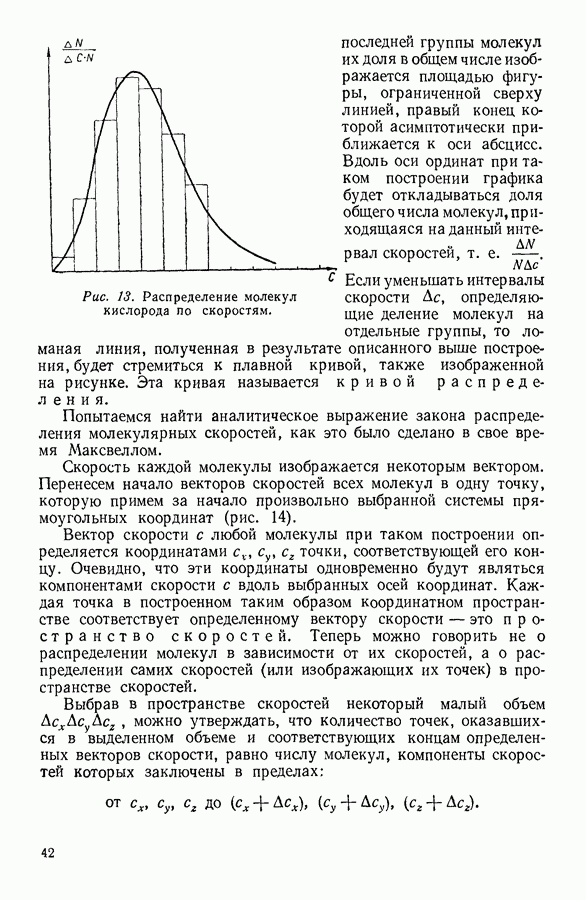
- 10. РАСПРЕДЕЛЕНИЕ МОЛЕКУЛ ГАЗА В ПОЛЕ ЗЕМНОГО ТЯГОТЕНИЯ
- 11. ЭКСПЕРИМЕНТАЛЬНОЕ ОПРЕДЕЛЕНИЕ ЧИСЛА АВОГАДРО
- 12. ЗАКОН РАСПРЕДЕЛЕНИЯ СКОРОСТЕЙ
- 13. ЭКСПЕРИМЕНТАЛЬНАЯ ПРОВЕРКА ЗАКОНА РАСПРЕДЕЛЕНИЯ МАКСВЕЛЛА
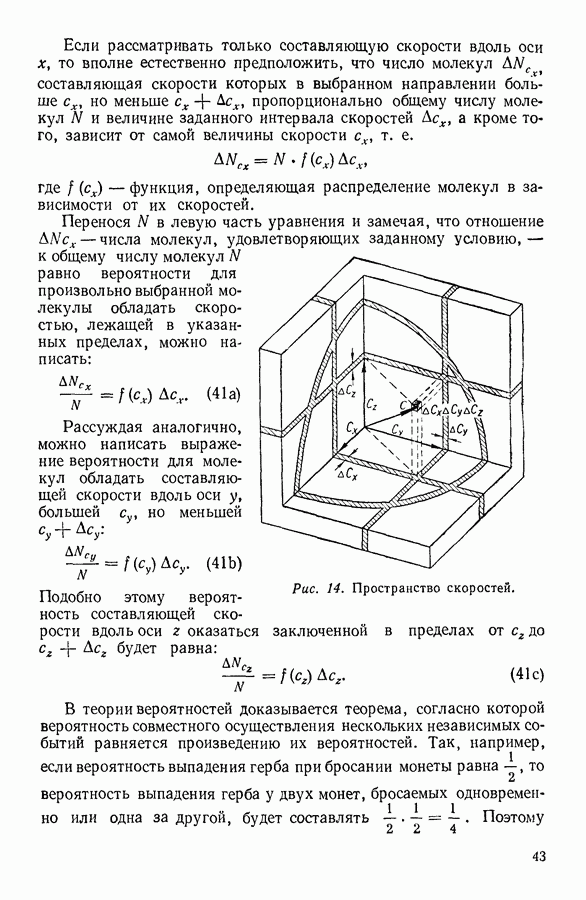
- 14. ЧИСЛО СОУДАРЕНИЙ И ДЛИНА СВОБОДНОГО ПРОБЕГА МОЛЕКУЛЫ
- 15. ЭКСПЕРИМЕНТАЛЬНОЕ ОПРЕДЕЛЕНИЕ ДЛИНЫ СРЕДНЕГО СВОБОДНОГО ПРОБЕГА МОЛЕКУЛ
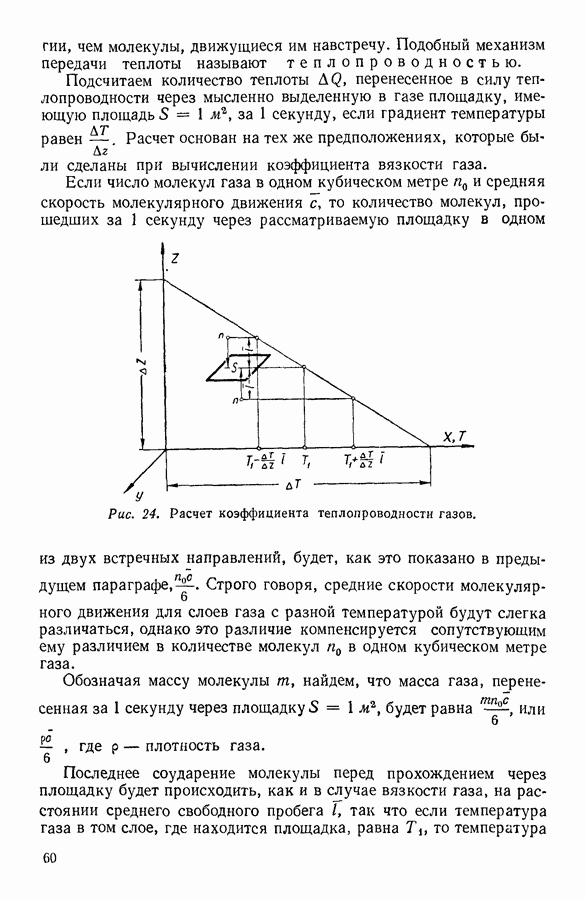
- 16. ЯВЛЕНИЯ ПЕРЕНОСА. ВЯЗКОСТЬ ГАЗОВ
- 17. ТЕПЛОПРОВОДНОСТЬ ГАЗОВ
- 18. ДИФФУЗИЯ ГАЗОВ
- 19. ВАКУУМ. ПОЛУЧЕНИЕ И ИЗМЕРЕНИЕ ВАКУУМА
- 20. ВНУТРЕННЯЯ ЭНЕРГИЯ ИДЕАЛЬНОГО ГАЗА
- 21. ТЕПЛОЕМКОСТЬ ИДЕАЛЬНОГО ГАЗА
- 22. СООТНОШЕНИЕ МЕЖДУ ТЕПЛОЕМКОСТЬЮ ГАЗА ПРИ ПОСТОЯННОМ ОБЪЕМЕ И ТЕПЛОЕМКОСТЬЮ ГАЗА ПРИ ПОСТОЯННОМ ДАВЛЕНИИ
- 23. РЕАЛЬНЫЕ ГАЗЫ. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- 24. ИССЛЕДОВАНИЕ УРАВНЕНИЯ ВАН-ДЕР-ВААЛЬСА
- 25. ОПРЕДЕЛЕНИЕ КРИТИЧЕСКИХ ПАРАМЕТРОВ ВЕЩЕСТВА
- 26. ПРИРОДА СИЛ МОЛЕКУЛЯРНОГО ПРИТЯЖЕНИЯ
- 27. ВНУТРЕННЯЯ ЭНЕРГИЯ РЕАЛЬНОГО ГАЗА
- 28. СЖИЖЕНИЕ ГАЗОВ
- II. ЖИДКОЕ СОСТОЯНИЕ ВЕЩЕСТВА
- 1. СРАВНЕНИЕ СВОЙСТВ ЖИДКОСТЕЙ СО СВОЙСТВАМИ ГАЗОВ И ТВЕРДЫХ ТЕЛ
- 2. МОЛЕКУЛЯРНОЕ ДАВЛЕНИЕ
- 3. ПОВЕРХНОСТНЫЕ СВОЙСТВА ЖИДКОСТЕЙ
- 4. ЯВЛЕНИЯ НА ГРАНИЦЕ ЖИДКОСТИ С ТВЕРДЫМ ТЕЛОМ
- 5. ДАВЛЕНИЕ ПОД ИЗОГНУТОЙ ПОВЕРХНОСТЬЮ ЖИДКОСТИ
- 6. ПОВЕРХНОСТНО-АКТИВНЫЕ ВЕЩЕСТВА
- 7. ИСПАРЕНИЕ ЖИДКОСТЕЙ. НАСЫЩЕННЫЙ ПАР И ЕГО СВОЙСТВА
- 8. МОЛЕКУЛЯРНОЕ СТРОЕНИЕ ЖИДКОСТЕЙ
- 9. ВЯЗКОСТЬ ЖИДКОСТЕЙ
- 10. РАСТВОРЫ. ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ
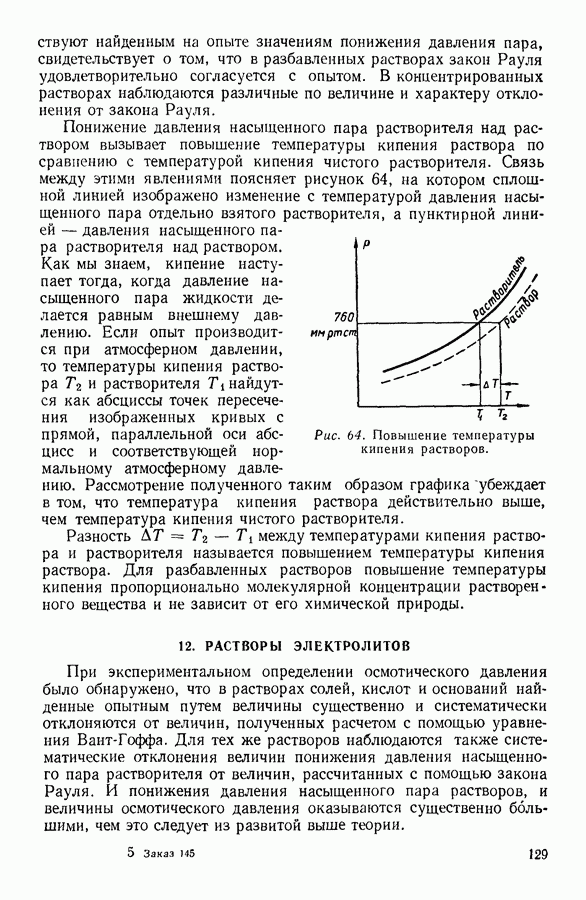
- 11. ПОНИЖЕНИЕ ДАВЛЕНИЯ НАСЫЩЕННОГО ПАРА РАСТВОРИТЕЛЯ НАД РАСТВОРОМ
- 12. РАСТВОРЫ ЭЛЕКТРОЛИТОВ
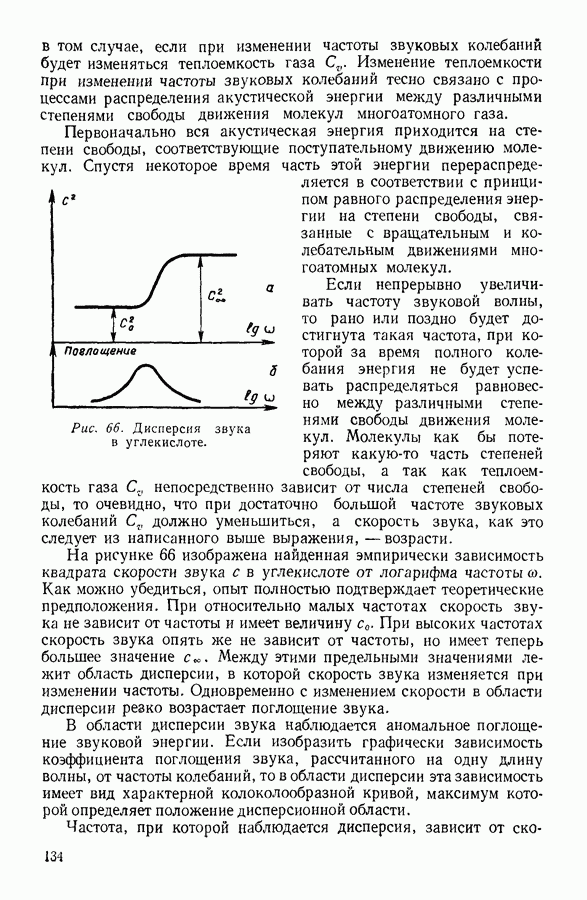
- 13. ПРИМЕНЕНИЕ УЛЬТРААКУСТИЧЕСКИХ МЕТОДОВ К ИССЛЕДОВАНИЮ ГАЗОВ И ЖИДКОСТЕЙ
- III. ТВЕРДОЕ СОСТОЯНИЕ ВЕЩЕСТВА
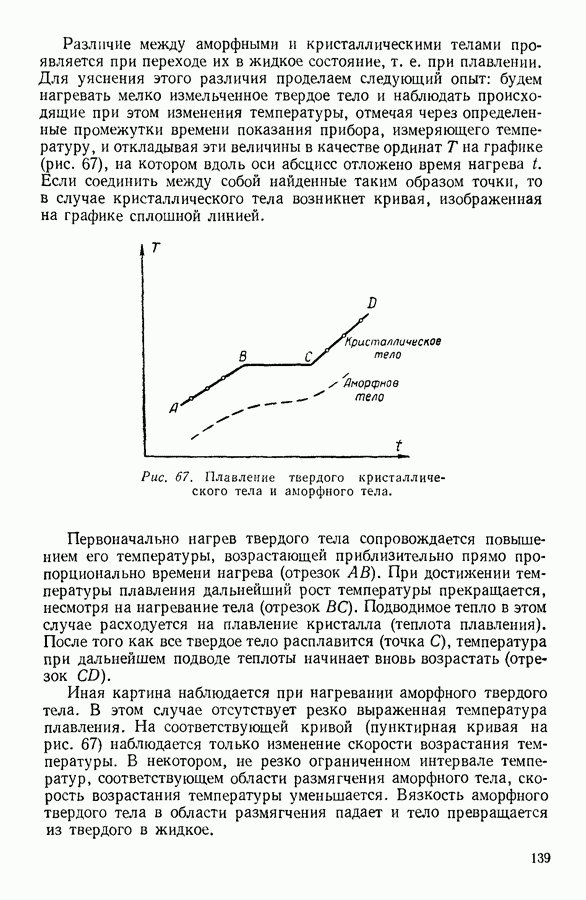
- 1. КРИСТАЛЛИЧЕСКИЕ И АМОРФНЫЕ ТВЕРДЫЕ ТЕЛА
- 2. МОЛЕКУЛЯРНОЕ СТРОЕНИЕ КРИСТАЛЛОВ
- 3. ПОЛИМЕРЫ
- 4. СИЛЫ, ДЕЙСТВУЮЩИЕ МЕЖДУ ЧАСТИЦАМИ В ТВЕРДЫХ ТЕЛАХ
- 5. ТЕПЛОЕМКОСТЬ ТВЕРДЫХ ТЕЛ
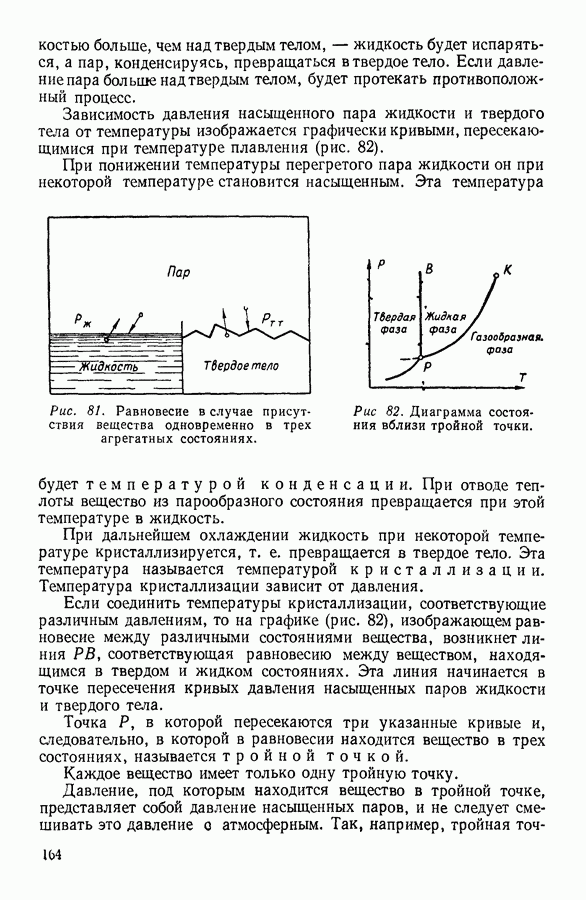
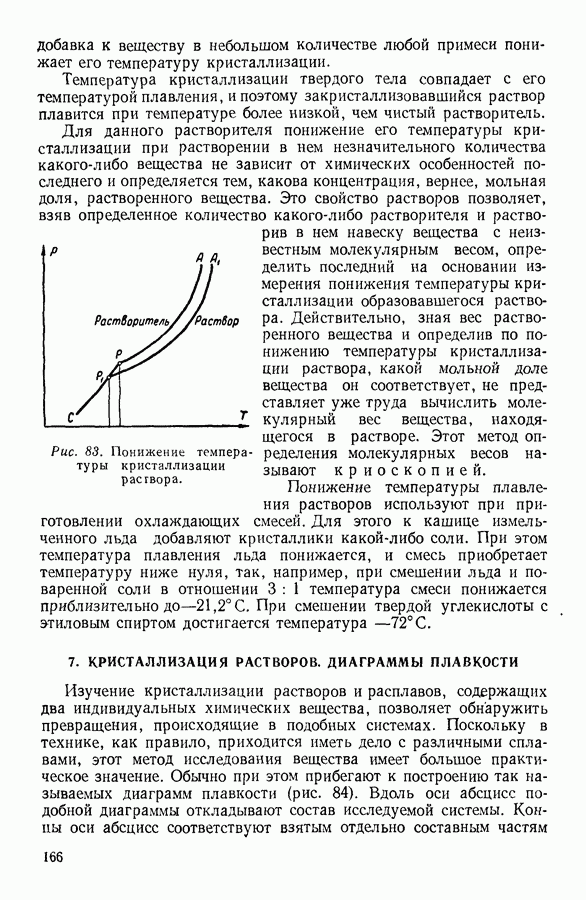
- 6. СУБЛИМАЦИЯ, ПЛАВЛЕНИЕ И КРИСТАЛЛИЗАЦИЯ ТВЕРДЫХ ТЕЛ
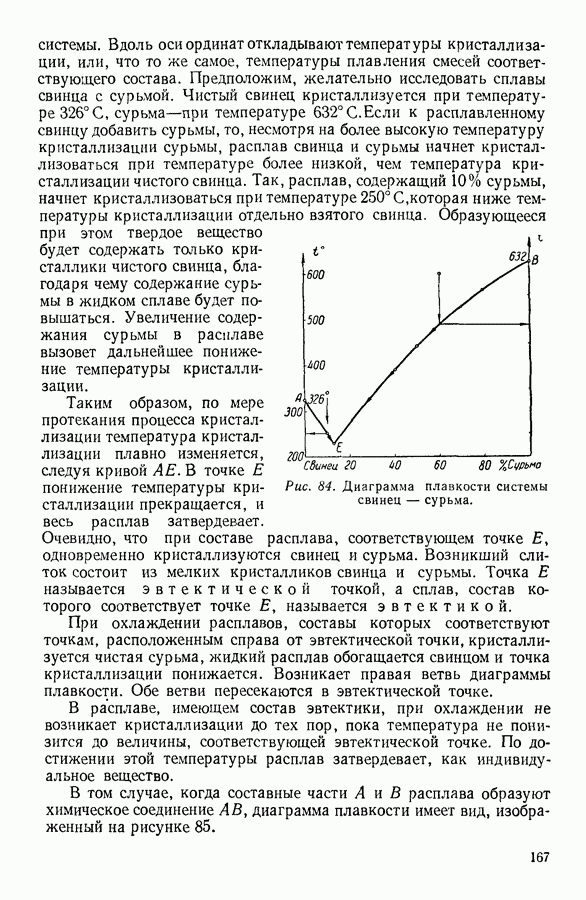
- 7. КРИСТАЛЛИЗАЦИЯ РАСТВОРОВ. ДИАГРАММЫ ПЛАВКОСТИ
- 8. АДСОРБЦИЯ
- IV. ФИЗИЧЕСКИЕ ОСНОВЫ ТЕРМОДИНАМИКИ
- 1. МОЛЕКУЛЯРНО-КИНЕТИЧЕСКИЙ МЕТОД, МЕТОД СТАТИСТИЧЕСКОЙ МЕХАНИКИ И ТЕРМОДИНАМИЧЕСКИЙ МЕТОД
- 2. ПРЕДМЕТ ТЕРМОДИНАМИКИ. ОСНОВНЫЕ ТЕРМОДИНАМИЧЕСКИЕ ПОНЯТИЯ.
- 3. ФИЗИЧЕСКИЙ СМЫСЛ ПОНЯТИЯ «ТЕПЛОТА»
- 4. ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ
- 5. МЕТОДЫ НАХОЖДЕНИЯ ТЕРМОДИНАМИЧЕСКИХ СООТНОШЕНИЙ
- 6. АДИАБАТНЫЕ ПРОЦЕССЫ. УРАВНЕНИЕ ПУАССОНА
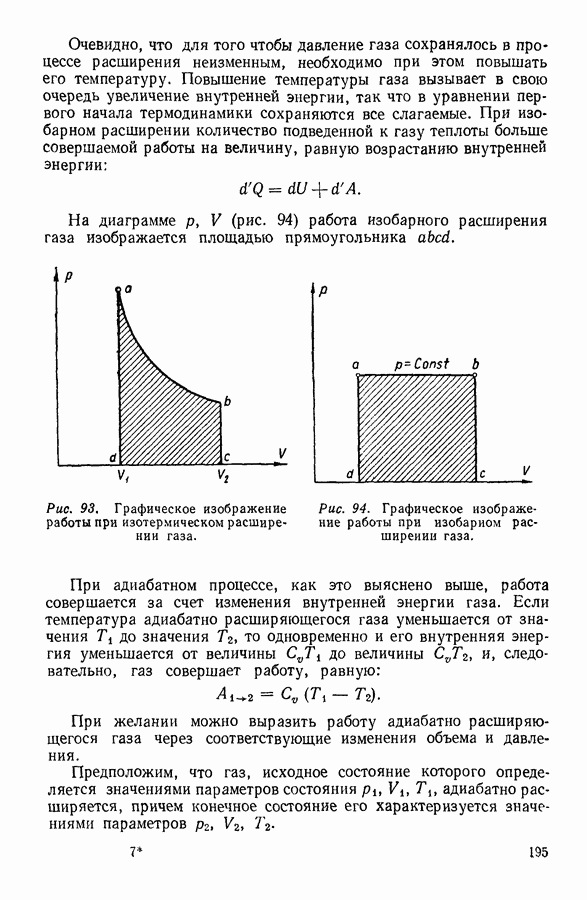
- 7. ПРИМЕНЕНИЕ ПЕРВОГО НАЧАЛА ТЕРМОДИНАМИКИ К НЕКОТОРЫМ ПРОЦЕССАМ В ГАЗАХ
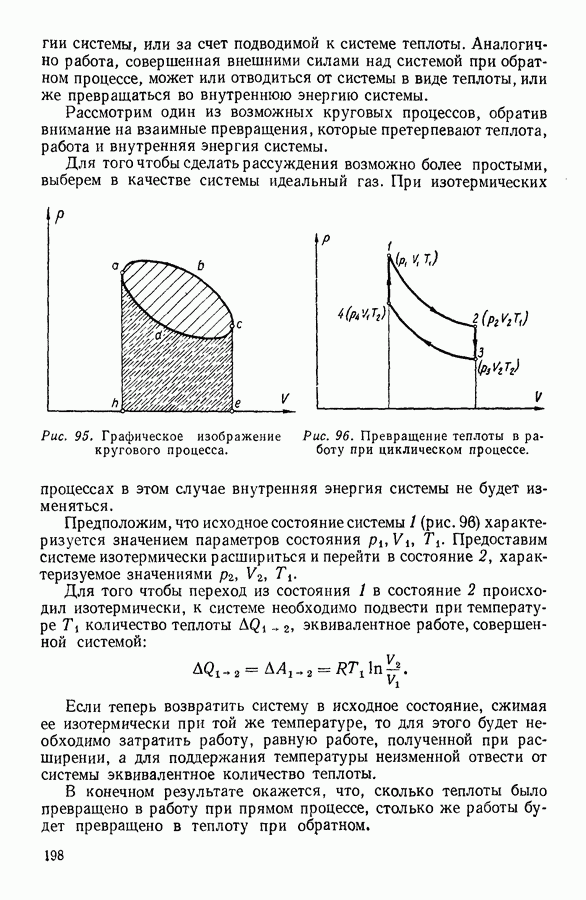
- 8. КРУГОВЫЕ ПРОЦЕССЫ
- 9. ЦИКЛ КАРНО
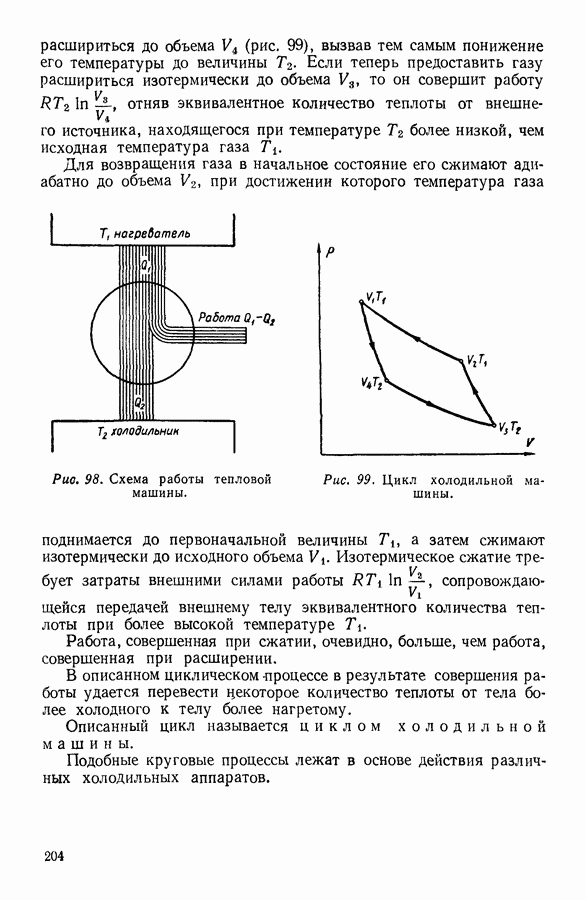
- 10. ИСПОЛЬЗОВАНИЕ ЦИКЛИЧЕСКИХ ПРОЦЕССОВ В ТЕРМОДИНАМИЧЕСКИХ РАССУЖДЕНИЯХ
- 11. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ
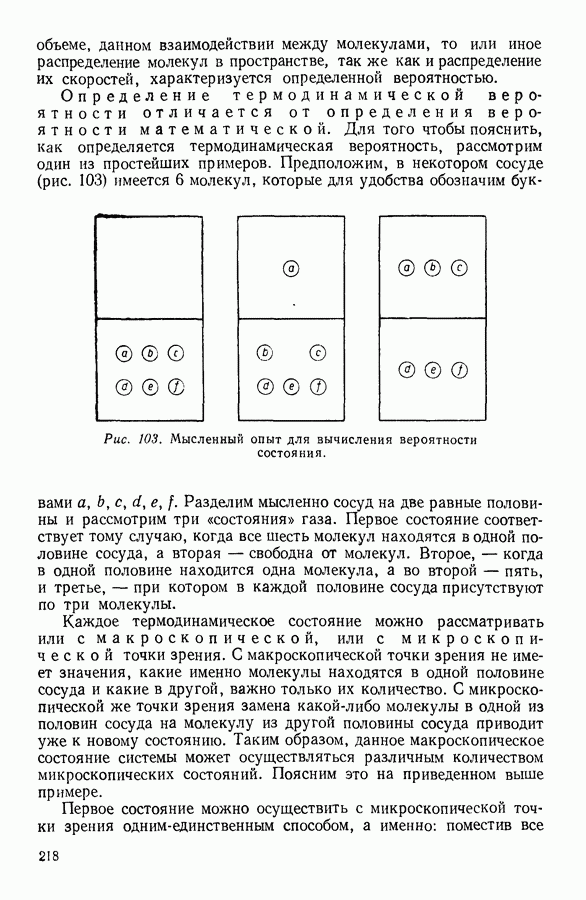
- 12. СТАТИСТИЧЕСКИЙ СМЫСЛ ВТОРОГО НАЧАЛА ТЕРМОДИНАМИКИ
- 13. КРИТИКА ТАК НАЗЫВАЕМОЙ «ТЕОРИИ ТЕПЛОВОЙ СМЕРТИ ВСЕЛЕННОЙ»