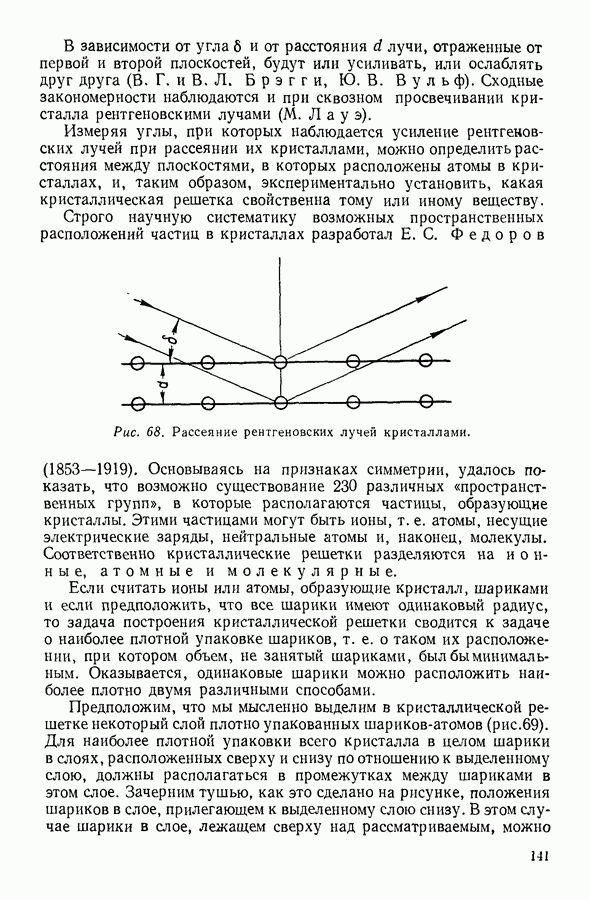
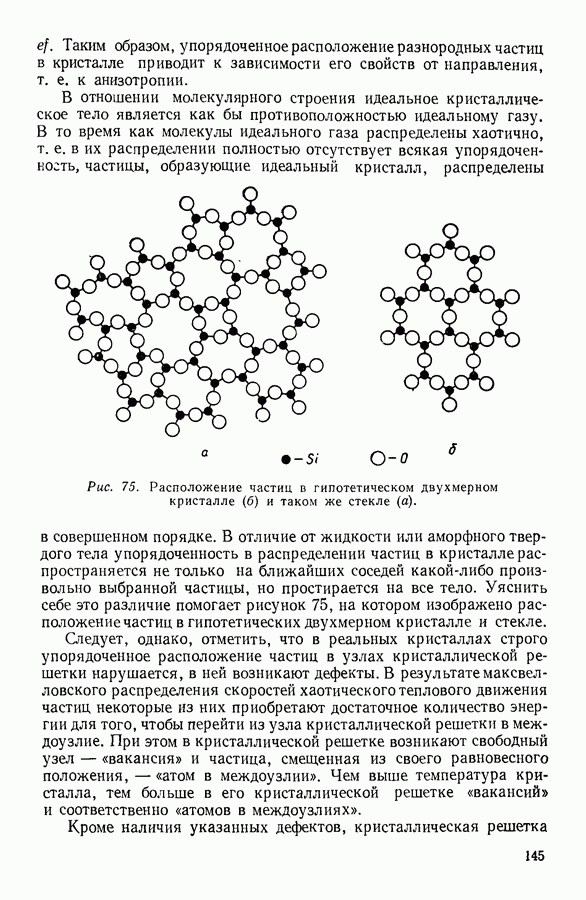
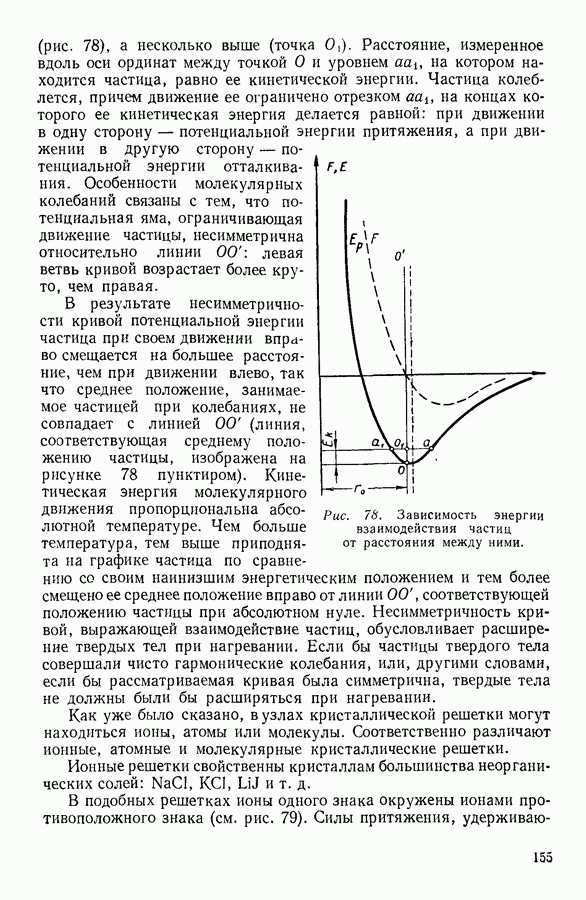
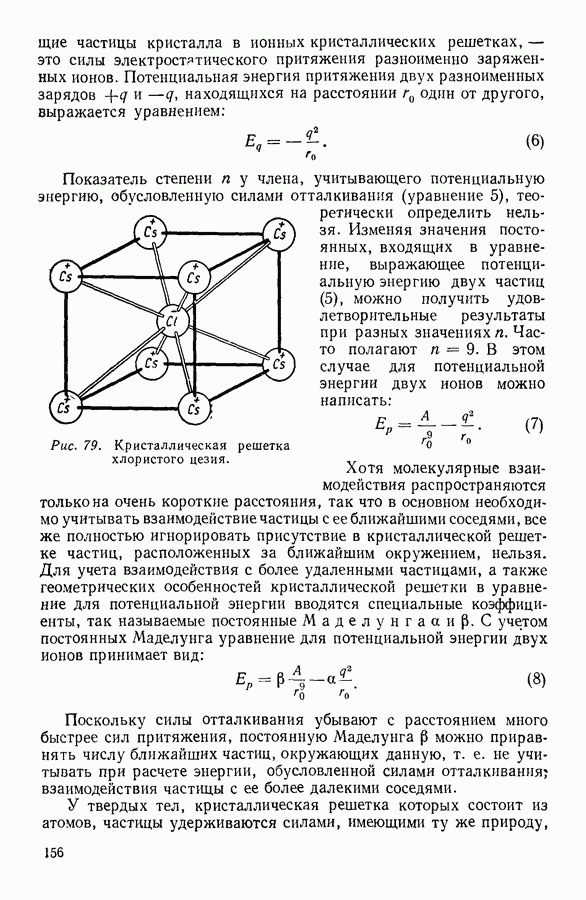
| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
11. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ
Выше мы познакомились с термодинамическим методом решения различных физических задач. Все рассуждения при этом основывались на использовании одного из основных законов природы: закона сохранения и превращения энергии, или первого начала термодинамики.
Как показал человеческий опыт, при всей важности этого закона, его, однако, недостаточно для того, чтобы объяснить своеобразие протекания различных явлений в природе. Для того чтобы убедиться в этом, рассмотрим первое начало термодинамики и следствия, вытекающие из него, с несколько иной точки зрения, чем это делалось выше. Математически первое начало термодинамики выражается уравнением:

физический смысл которого сводится к утверждению, что изменение внутренней энергии системы возможно или в результате
совершения работы, или в результате передачи некоторого количества теплоты. Чрезвычайно важно то, что написанное уравнение исчерпывает все возможные способы изменения внутренней энергии системы: внутренняя энергия системы может изменяться только в результате совершения работы или передачи некоторого количества теплоты.
Обратим теперь внимание на то обстоятельство, что оба указанных способа изменения внутренней энергии системы подразумевают взаимодействие ее с какими-то телами, не входящими в рассматриваемую систему. Работа совершается или внешними силами, т. е. силами, действующими на систему со стороны каких-либо не входящих в нее тел, или, наоборот, системой, преодолевающей действие этих внешних сил.
Точно так же количество теплоты, необходимое для изменения внутренней энергии системы, передается последней или от каких-либо тел, не входящих в нее, или от самой системы этим телам.
Необходимость для изменения внутренней энергии системы взаимодействия ее с телами, не входящими в нее, приводит к тому, что в изолированной системе, т. е. в системе, включающей все взаимодействующие тела, внутренняя энергия остается неизменной. Учитывая сказанное, первое начало термодинамики иногда так и формулируют, утверждая, что внутренняя энергия изолированной системы постоянна, или, что то же самое, в изолированной системе 
В различных термодинамических системах можно представить себе мысленно самые разнообразные процессы. Первое начало термодинамики позволяет выбрать из этого многообразия процессы, протекание которых с точки зрения энергетических соотношений принципиально возможно.
Предположим, например, что рассматриваемая система состоит из двух порций  одной и той же жидкости, имеющих соответственно температуры
одной и той же жидкости, имеющих соответственно температуры  При сливании этих порций жидкости в условиях изоляции от взаимодействия с какими-либо другими телами для всей смеси устанавливается некоторая общая температура
При сливании этих порций жидкости в условиях изоляции от взаимодействия с какими-либо другими телами для всей смеси устанавливается некоторая общая температура  Опираясь на первое начало термодинамики, можно утверждать, что конечная температура всей смеси не может быть больше температуры более теплой из смешиваемых порций жидкости. Процесс, приводящий к подобному результату, не допускается первым началом термодинамики. Более того, на том же основании можно утверждать, что в случае действительно изолированной системы возможны только такие процессы, при которых выполняется следующее равенство:
Опираясь на первое начало термодинамики, можно утверждать, что конечная температура всей смеси не может быть больше температуры более теплой из смешиваемых порций жидкости. Процесс, приводящий к подобному результату, не допускается первым началом термодинамики. Более того, на том же основании можно утверждать, что в случае действительно изолированной системы возможны только такие процессы, при которых выполняется следующее равенство:

Огромное значение первого начала термодинамики заключается именно в том, что оно указывает, каким образом выбрать из бесконечного количества процессов, которые человек может себе
представить, те процессы, протекание которых, вообще говоря, возможно.
Однако, помогая выделить возможные процессы, первое начало термодинамики не дает основания для дальнейшего различия между ними: с точки зрения первого начала термодинамики все отобранные процессы одинаково возможны.
Для того чтобы уяснить эту особенность, возвратимся к приведенному выше примеру. При смешении двух порций жидкости с разной температурой с точки зрения первого начала термодинамики возможен любой процесс, в результате которого температура смеси примет значение  соответствующее уравнению (21).
соответствующее уравнению (21).
Однако с точки зрения первого начала термодинамики вполне возможен и процесс, обратный рассмотренному: первое начало термодинамики допускает возможность того, что жидкость, масса которой  имеющая повсюду одинаковую температуру
имеющая повсюду одинаковую температуру  самопроизвольно разделится на две части
самопроизвольно разделится на две части  с различными температурами
с различными температурами  если только эти температуры удовлетворяют уравнению (21). Первое начало термодинамики не допускает лишь изменения внутренней энергии изолированной системы, но никак не ограничивает перераспределение внутренней энергии внутри данной изолированной системы.
если только эти температуры удовлетворяют уравнению (21). Первое начало термодинамики не допускает лишь изменения внутренней энергии изолированной системы, но никак не ограничивает перераспределение внутренней энергии внутри данной изолированной системы.
В то же время опыт учит человека тому, что в природе наблюдается иное положение.
Хорошо известно, что при смешении нескольких порций жид кости с разными температурами смесь всегда приобретает некоторую температуру, общую для всей жидкости. Также хорошо известно из опыта, что без воздействия извне в жидкости, имевшей повсюду одинаковую температуру, никогда не возникает разность температур, обусловленная самопроизвольным переходом некоторого количества теплоты от одной части жидкости к Другой.
Точно так же, при смешении водного раствора какой-либо соли с чистой водой всегда наблюдается диффузия растворенного вещества, приводящая к выравниванию концентрации раствора во всей жидкости, и никогда не наблюдается, чтобы растворенное в какой-либо жидкости вещество самопроизвольно собралось бы в одной ее части, в то время как во второй оказался бы чистый растворитель, хотя этот процесс и не противоречит первому началу термодинамики.
Наконец, можно постоянно наблюдать самопроизвольное превращение механической работы в теплоту. Так, например, можно заставить скользить тяжелый брусок по наклонной плоскости, (рис. 101), причем вся работа, совершаемая силой тяжести, будет благодаря трению превращаться в теплоту. В результате трения температура бруска и наклонной плоскости слегка возрастет, а внутренняя энергия системы останется постоянной.
В то же время, сколько бы ни ожидать, не удается наблюдать самопроизвольного охлаждения бруска и наклонной плоскости, в результате которого брусок сам начал бы двигаться вверх по наклонной плоскости, хотя этот процесс может также протекать при неизменной внутренней энергии системы.
Таким образом, возможные с точки зрения первого начала термодинамики процессы оказываются неравноценными в отношении их протекания в том смысле, что, как показывает опыт, в изолированной системе одни из этих процессов протекают, а другие не протекают.
На различие таких процессов и указывается вторым основным законом, или вторым началом, термодинамики.
Второе начало термодинамики утверждает, что существует функция состояния, называемая энтропией, которая обладает тем свойством, что при всех реальных процессах, протекающих в изолированной системе, она возрастает.

Рис. 101.
Таким образом, второму началу термодинамики можно придать следующую формулировку: в изолированной системе возможны только такие процессы, при которых энтропия системы возрастает.
Часто второе начало термодинамики формулируют несколько иначе, например Кельвин формулировал этот закон в форме утверждения, что невозможен процесс, единственным результатом которого было бы получение от какого-либо тела теплоты и превращение ее в эквивалентное количество работы.
Клаузиус предложил записать второе начало термодинамики как утверждение невозможности самопроизвольного перехода теплоты от более холодного тела к телу более теплому. Эти формулировки второго начала, так же как и еще несколько формулировок, встречающихся в литературе, приводят в конечном счете к одним и тем же выводам, и в этом отношении равноценны.
Формулировка, приведенная в качестве первой, отличается тем, что в ней более ясно выступает общность второго начала термодинамики.
Согласно второму началу термодинамики, для того чтобы ответить на вопрос, возможно ли в изолированной системе то или иное превращение, необходимо рассчитать приращение энтропии при этом превращении, и если это приращение окажется положительным, то рассматриваемое превращение возможно, так как в результате его энтропия изолированной системы возрастает. Те же
процессы, при которых приращение энтропии оказывается отрицательным, в изолированной системе невозможны, поскольку при подобных процессах энтропия изолированной системы должна убывать.
Количественно в термодинамике определяется не энтропия, а разность энтропии, соответствующая какому-либо изменению состояния системы. Новая функция состояния — энтропия — обозначается буквой  и согласно определению
и согласно определению

или

Дифференциальное изменение энтропии  определяется, таким образом, отношением дифференциально малого количества теплоты, полученного или отданного системой, к температуре, при которой происходит процесс. Для гого чтобы пояснить, как используются формулы (22) и (23), рассмотрим некоторые примеры.
определяется, таким образом, отношением дифференциально малого количества теплоты, полученного или отданного системой, к температуре, при которой происходит процесс. Для гого чтобы пояснить, как используются формулы (22) и (23), рассмотрим некоторые примеры.
1. Подсчитаем изменение энтропии при плавлении 1 кмоля  льда. Удельная теплота плавления льда
льда. Удельная теплота плавления льда  Плавление льда происходит при постоянной температуре 273° К, и поэтому в уравнении (23)
Плавление льда происходит при постоянной температуре 273° К, и поэтому в уравнении (23)  выносится за знак интеграла
выносится за знак интеграла  который в данном случае будет равен количеству теплоты, необходимому для плавления одного киломоля льда.
который в данном случае будет равен количеству теплоты, необходимому для плавления одного киломоля льда.
Таким образом:

2. Один киломоль идеального газа занимает при давлении  и температуре
и температуре  объем
объем  Определим изменение энтропии при равновесном переходе газа в состояние, характеризуемое параметрами состояния
Определим изменение энтропии при равновесном переходе газа в состояние, характеризуемое параметрами состояния 
Запишем первое начало термодинамики:

В случае идеального газа  Подставив эти значения в уравнение первого начала, запишем его в виде:
Подставив эти значения в уравнение первого начала, запишем его в виде:

Разделив это уравнение на  и приняв во внимание определение энтропии (уравнение 22), получим:
и приняв во внимание определение энтропии (уравнение 22), получим:

Интегрируя уравнение в пределах от  до
до  найдем искомое решение:
найдем искомое решение:

Читатель может самостоятельно записать приращение энтропии идеального газа при том же изменении состояния как функцию параметров состояния  и
и  или
или  и
и 
Рассмотрим простейшие примеры применения второго начала термодинамики для определения возможности протекания некоторых процессов в изолированных термодинамических системах.
Предположим, что в соприкосновение приведены два весьма больших куска железа, один при температуре 300° К, а второй при 400° К (рис. 102). Подсчитаем изменение энтропии, которое будет иметь место при переходе  теплоты один раз от более теплого куска к более холодному, а второй раз — в обратном направлении.
теплоты один раз от более теплого куска к более холодному, а второй раз — в обратном направлении.

Рис. 102. К расчету изменения энтропии при теплообмене.
Будем считать, что куски настолько велики, что при получении или потере  изменением температуры можно пренебречь. Когда теплота переходит от тела более теплого к телу более холодному, общее изменение энтропии в системе составит:
изменением температуры можно пренебречь. Когда теплота переходит от тела более теплого к телу более холодному, общее изменение энтропии в системе составит:

Знак минус ставится в том случае, когда теплота отдается телом, и плюс, когда тело получает некоторое количество теплоты.
В случае, когда теплота переходит от тела более холодного к телу более теплому, общее изменение энтропии системы составит:

Таким образом, переход теплоты от тела более нагретого к телу более холодному сопровождается положительным приращением энтропии, и, следовательно, этот процесс в изолированной системе возможен. Наоборот, переход теплоты от более холодного тела к телу более теплому сопровождается отрицательным приращением энтропии, и, следовательно, в изолированной системе такой процесс невозможен.
В качестве второго примера рассмотрим изменение энтропии при изменении объема идеального газа. Изменение энтропии в этом случае выражается формулой:

Если изменение объема происходит изотермически: 

т. е. изменение энтропии будет всегда положительно, когда конечный объем больше начального. Другими словами, идеальный газ, представляющий собой изолированную систему, будет самопроизвольно расширяться, стремясь занять весь предоставленный ему объем.
Выше были рассмотрены наиболее элементарные примеры применения второго начала для определения направления возможного процесса. Однако этот закон позволяет определить направление и более сложных процессов. Кроме того, он дает возможность предопределить, при каких именно условиях данный процесс будет протекать в желательном направлении.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- ОСНОВНЫЕ ЕДИНИЦЫ СИ
- I. ГАЗООБРАЗНОЕ СОСТОЯНИЕ ВЕЩЕСТВА
- 1. РАЗВИТИЕ АТОМНЫХ ПРЕДСТАВЛЕНИЙ В НАУКЕ
- 2. ПОНЯТИЕ О СОСТОЯНИИ ВЕЩЕСТВА
- 3. ЗАКОН БОЙЛЯ — МАРИОТТА
- 4. ЗАКОН ГЕЙ-ЛЮССАКА
- 5. ОБЪЕДИНЕННЫЙ ГАЗОВЫЙ ЗАКОН
- 6. ПОНЯТИЕ ОБ ИДЕАЛЬНОМ ГАЗЕ
- 7. ОСНОВНЫЕ ПОЛОЖЕНИЯ КИНЕТИЧЕСКОЙ ТЕОРИИ ГАЗОВ
- 8. ОСНОВНОЕ УРАВНЕНИЕ КИНЕТИЧЕСКОЙ ТЕОРИИ ГАЗОВ
- 9. НЕКОТОРЫЕ СЛЕДСТВИЯ ИЗ ОСНОВНОГО УРАВНЕНИЯ КИНЕТИЧЕСКОЙ ТЕОРИИ ГАЗОВ
- 10. РАСПРЕДЕЛЕНИЕ МОЛЕКУЛ ГАЗА В ПОЛЕ ЗЕМНОГО ТЯГОТЕНИЯ
- 11. ЭКСПЕРИМЕНТАЛЬНОЕ ОПРЕДЕЛЕНИЕ ЧИСЛА АВОГАДРО
- 12. ЗАКОН РАСПРЕДЕЛЕНИЯ СКОРОСТЕЙ
- 13. ЭКСПЕРИМЕНТАЛЬНАЯ ПРОВЕРКА ЗАКОНА РАСПРЕДЕЛЕНИЯ МАКСВЕЛЛА
- 14. ЧИСЛО СОУДАРЕНИЙ И ДЛИНА СВОБОДНОГО ПРОБЕГА МОЛЕКУЛЫ
- 15. ЭКСПЕРИМЕНТАЛЬНОЕ ОПРЕДЕЛЕНИЕ ДЛИНЫ СРЕДНЕГО СВОБОДНОГО ПРОБЕГА МОЛЕКУЛ
- 16. ЯВЛЕНИЯ ПЕРЕНОСА. ВЯЗКОСТЬ ГАЗОВ
- 17. ТЕПЛОПРОВОДНОСТЬ ГАЗОВ
- 18. ДИФФУЗИЯ ГАЗОВ
- 19. ВАКУУМ. ПОЛУЧЕНИЕ И ИЗМЕРЕНИЕ ВАКУУМА
- 20. ВНУТРЕННЯЯ ЭНЕРГИЯ ИДЕАЛЬНОГО ГАЗА
- 21. ТЕПЛОЕМКОСТЬ ИДЕАЛЬНОГО ГАЗА
- 22. СООТНОШЕНИЕ МЕЖДУ ТЕПЛОЕМКОСТЬЮ ГАЗА ПРИ ПОСТОЯННОМ ОБЪЕМЕ И ТЕПЛОЕМКОСТЬЮ ГАЗА ПРИ ПОСТОЯННОМ ДАВЛЕНИИ
- 23. РЕАЛЬНЫЕ ГАЗЫ. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- 24. ИССЛЕДОВАНИЕ УРАВНЕНИЯ ВАН-ДЕР-ВААЛЬСА
- 25. ОПРЕДЕЛЕНИЕ КРИТИЧЕСКИХ ПАРАМЕТРОВ ВЕЩЕСТВА
- 26. ПРИРОДА СИЛ МОЛЕКУЛЯРНОГО ПРИТЯЖЕНИЯ
- 27. ВНУТРЕННЯЯ ЭНЕРГИЯ РЕАЛЬНОГО ГАЗА
- 28. СЖИЖЕНИЕ ГАЗОВ
- II. ЖИДКОЕ СОСТОЯНИЕ ВЕЩЕСТВА
- 1. СРАВНЕНИЕ СВОЙСТВ ЖИДКОСТЕЙ СО СВОЙСТВАМИ ГАЗОВ И ТВЕРДЫХ ТЕЛ
- 2. МОЛЕКУЛЯРНОЕ ДАВЛЕНИЕ
- 3. ПОВЕРХНОСТНЫЕ СВОЙСТВА ЖИДКОСТЕЙ
- 4. ЯВЛЕНИЯ НА ГРАНИЦЕ ЖИДКОСТИ С ТВЕРДЫМ ТЕЛОМ
- 5. ДАВЛЕНИЕ ПОД ИЗОГНУТОЙ ПОВЕРХНОСТЬЮ ЖИДКОСТИ
- 6. ПОВЕРХНОСТНО-АКТИВНЫЕ ВЕЩЕСТВА
- 7. ИСПАРЕНИЕ ЖИДКОСТЕЙ. НАСЫЩЕННЫЙ ПАР И ЕГО СВОЙСТВА
- 8. МОЛЕКУЛЯРНОЕ СТРОЕНИЕ ЖИДКОСТЕЙ
- 9. ВЯЗКОСТЬ ЖИДКОСТЕЙ
- 10. РАСТВОРЫ. ОСМОТИЧЕСКОЕ ДАВЛЕНИЕ
- 11. ПОНИЖЕНИЕ ДАВЛЕНИЯ НАСЫЩЕННОГО ПАРА РАСТВОРИТЕЛЯ НАД РАСТВОРОМ
- 12. РАСТВОРЫ ЭЛЕКТРОЛИТОВ
- 13. ПРИМЕНЕНИЕ УЛЬТРААКУСТИЧЕСКИХ МЕТОДОВ К ИССЛЕДОВАНИЮ ГАЗОВ И ЖИДКОСТЕЙ
- III. ТВЕРДОЕ СОСТОЯНИЕ ВЕЩЕСТВА
- 1. КРИСТАЛЛИЧЕСКИЕ И АМОРФНЫЕ ТВЕРДЫЕ ТЕЛА
- 2. МОЛЕКУЛЯРНОЕ СТРОЕНИЕ КРИСТАЛЛОВ
- 3. ПОЛИМЕРЫ
- 4. СИЛЫ, ДЕЙСТВУЮЩИЕ МЕЖДУ ЧАСТИЦАМИ В ТВЕРДЫХ ТЕЛАХ
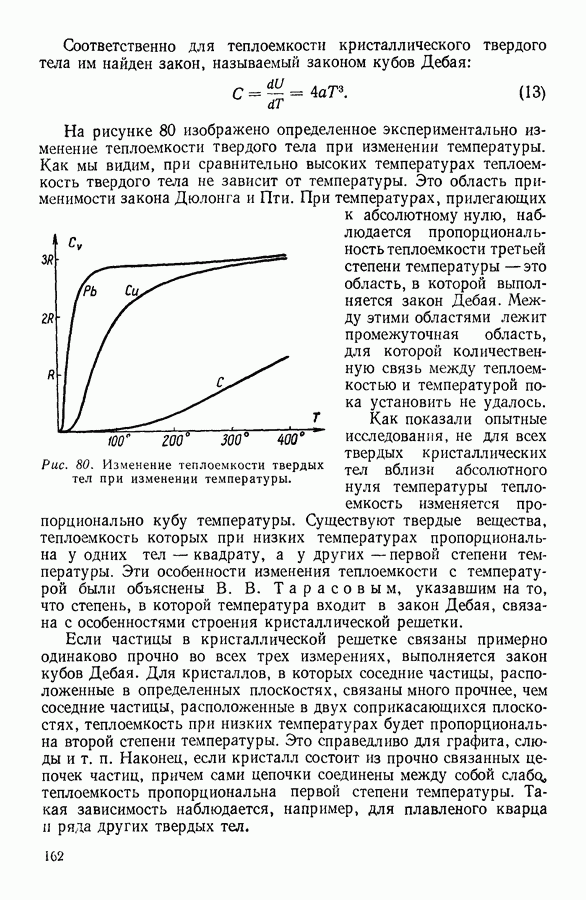
- 5. ТЕПЛОЕМКОСТЬ ТВЕРДЫХ ТЕЛ
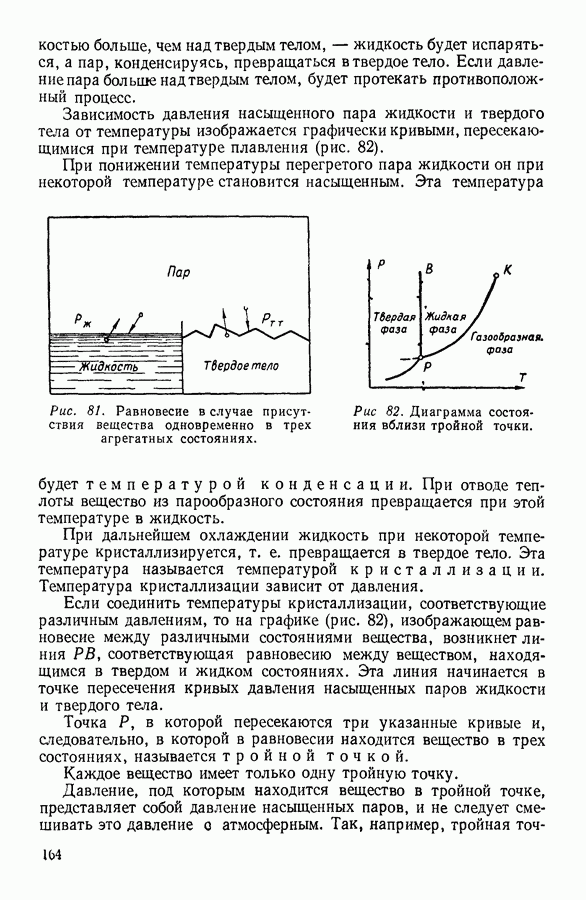
- 6. СУБЛИМАЦИЯ, ПЛАВЛЕНИЕ И КРИСТАЛЛИЗАЦИЯ ТВЕРДЫХ ТЕЛ
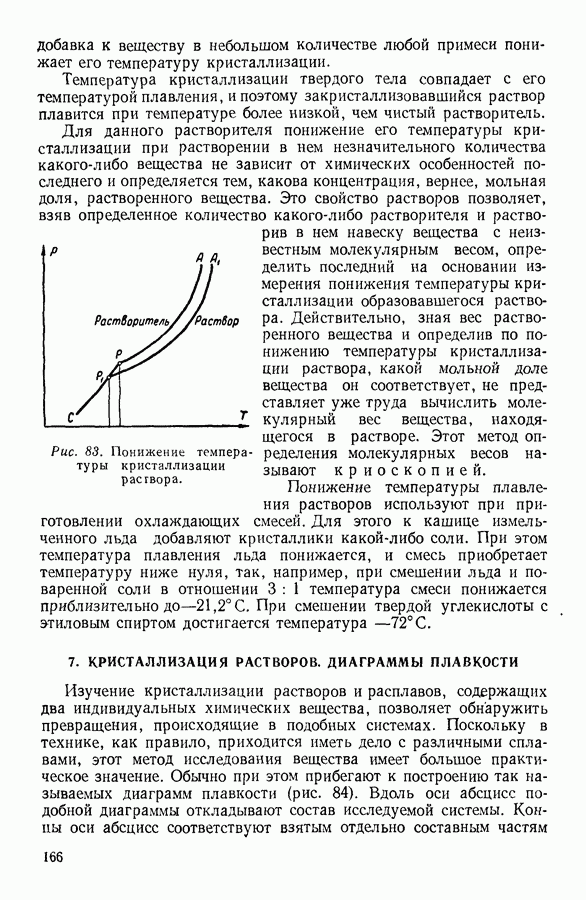
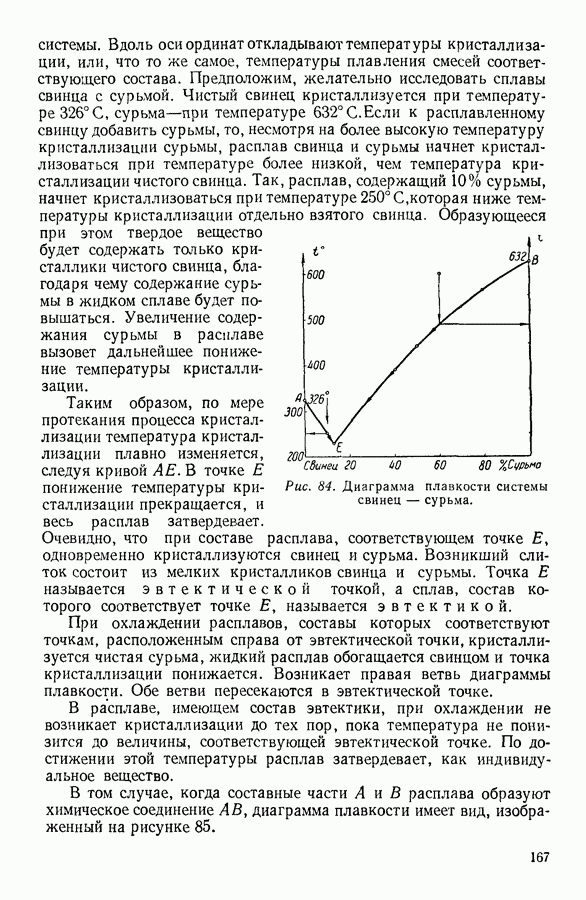
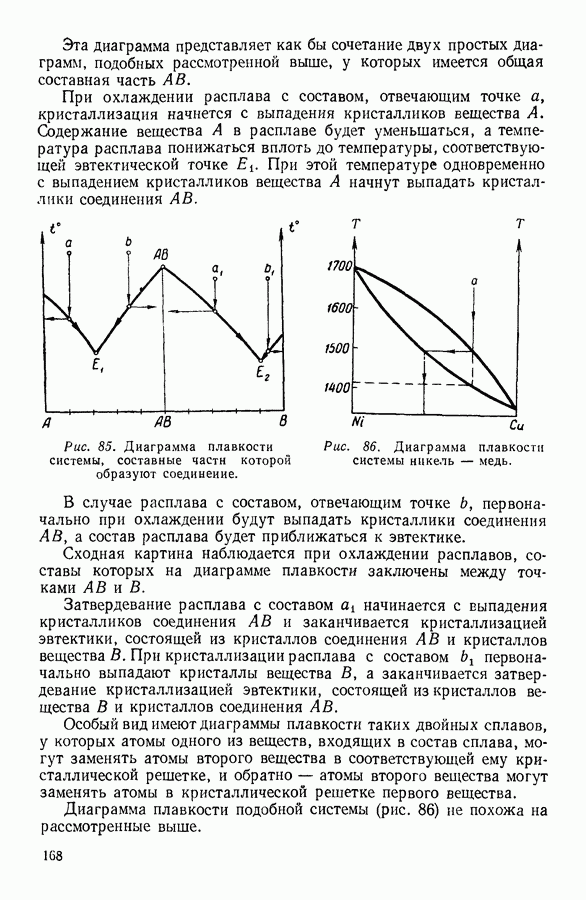
- 7. КРИСТАЛЛИЗАЦИЯ РАСТВОРОВ. ДИАГРАММЫ ПЛАВКОСТИ
- 8. АДСОРБЦИЯ
- IV. ФИЗИЧЕСКИЕ ОСНОВЫ ТЕРМОДИНАМИКИ
- 1. МОЛЕКУЛЯРНО-КИНЕТИЧЕСКИЙ МЕТОД, МЕТОД СТАТИСТИЧЕСКОЙ МЕХАНИКИ И ТЕРМОДИНАМИЧЕСКИЙ МЕТОД
- 2. ПРЕДМЕТ ТЕРМОДИНАМИКИ. ОСНОВНЫЕ ТЕРМОДИНАМИЧЕСКИЕ ПОНЯТИЯ.
- 3. ФИЗИЧЕСКИЙ СМЫСЛ ПОНЯТИЯ «ТЕПЛОТА»
- 4. ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ
- 5. МЕТОДЫ НАХОЖДЕНИЯ ТЕРМОДИНАМИЧЕСКИХ СООТНОШЕНИЙ
- 6. АДИАБАТНЫЕ ПРОЦЕССЫ. УРАВНЕНИЕ ПУАССОНА
- 7. ПРИМЕНЕНИЕ ПЕРВОГО НАЧАЛА ТЕРМОДИНАМИКИ К НЕКОТОРЫМ ПРОЦЕССАМ В ГАЗАХ
- 8. КРУГОВЫЕ ПРОЦЕССЫ
- 9. ЦИКЛ КАРНО
- 10. ИСПОЛЬЗОВАНИЕ ЦИКЛИЧЕСКИХ ПРОЦЕССОВ В ТЕРМОДИНАМИЧЕСКИХ РАССУЖДЕНИЯХ
- 11. ВТОРОЕ НАЧАЛО ТЕРМОДИНАМИКИ
- 12. СТАТИСТИЧЕСКИЙ СМЫСЛ ВТОРОГО НАЧАЛА ТЕРМОДИНАМИКИ
- 13. КРИТИКА ТАК НАЗЫВАЕМОЙ «ТЕОРИИ ТЕПЛОВОЙ СМЕРТИ ВСЕЛЕННОЙ»