| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
РЕГУЛЯЦИЯ ГЛИКОЛИЗА, ГЛЮКОНЕОГЕНЕЗА И ПЕНТОЗОФОСФАТНОГО ПУТИ
Индукция и репрессия синтеза ферментов
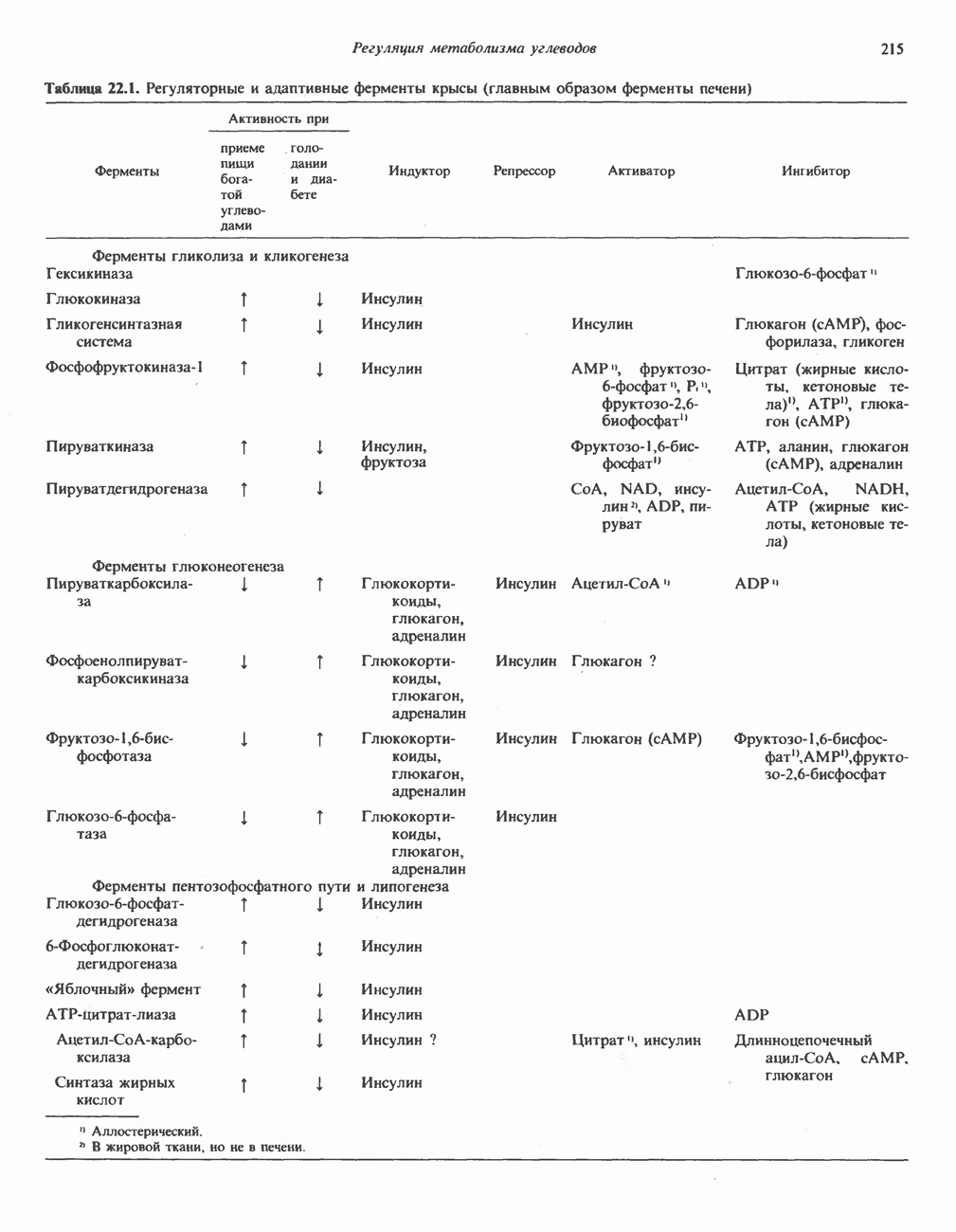
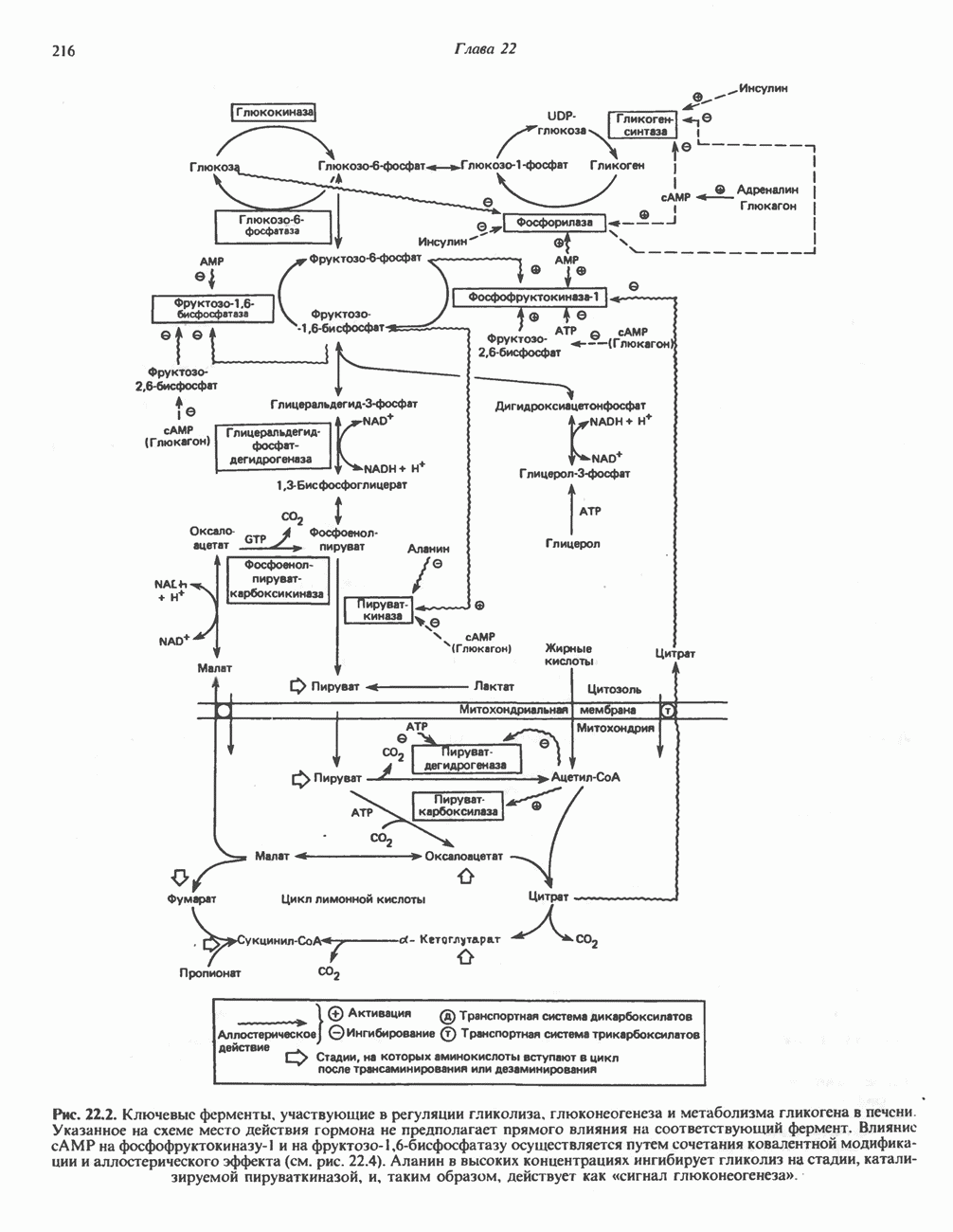
Наиболее полно изученные изменения активности ферментов, которые, как считают, происходят при различном состоянии обмена веществ, приведены в табл. 22.1. Данные, представленные в этой таблице, относятся главным образом к ферментам печени. Рассматриваемые ферменты катализируют неравновесные реакции, которые с точки зрения физиологии являются односторонними. Часто эффекты «в прямом направлении» оказываются более выраженными, поскольку одновременно противоположным образом меняется активность ферментов, катализирующих изменения в обратном направлении (рис. 22.2). Необходимо отметить, что все ключевые ферменты, участвующие в каком-либо пути метаболизма, активируются или ингибируются координированно, об этом свидетельствуют данные, представленные в табл. 22.1. Ферменты, участвующие в использовании глюкозы, т. е. ферменты гликолиза и
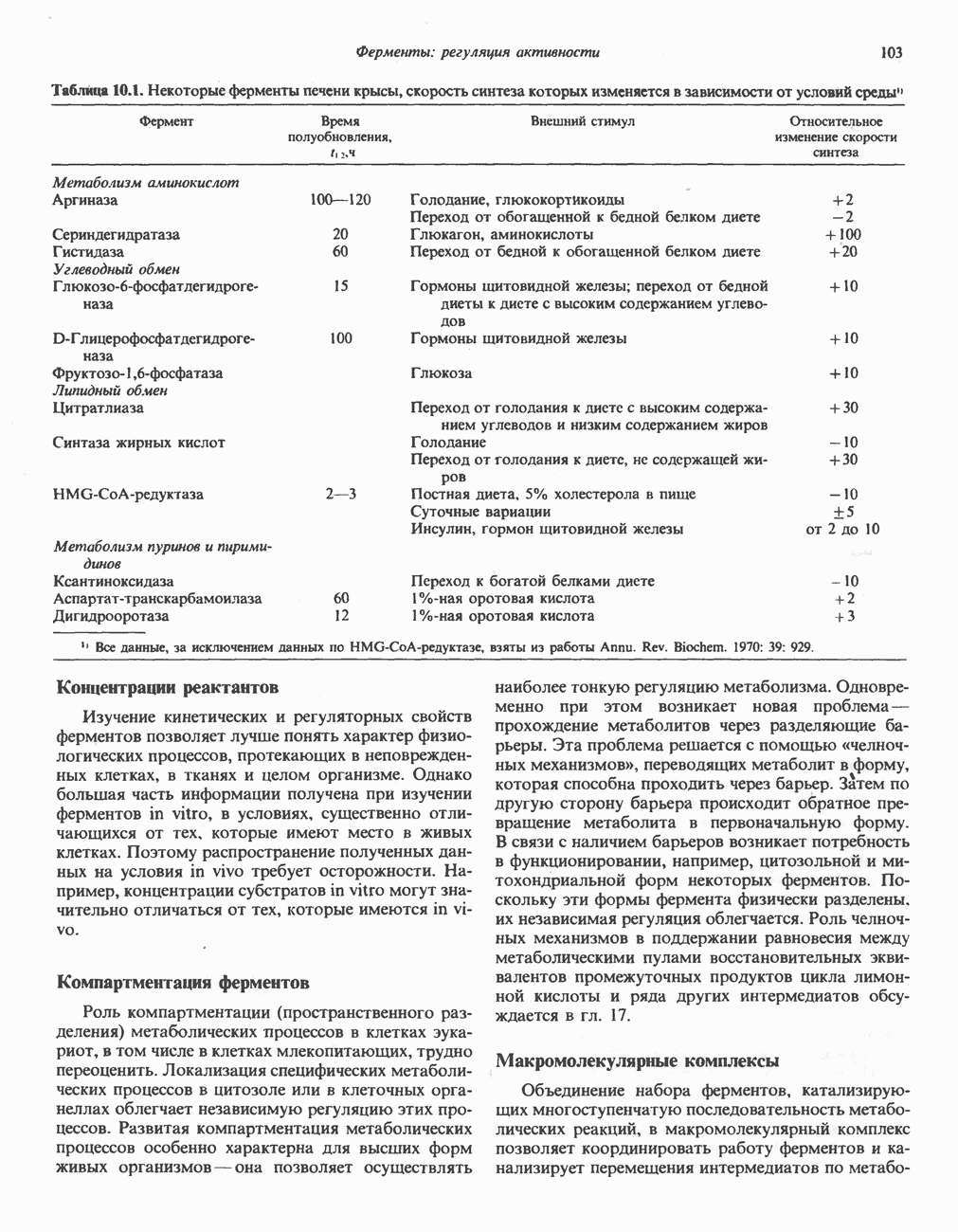
Таблица 22.1. Регуляторные и адаптивные ферменты крысы (главным образом ферменты печени)
(см. скан)
(см. скан)
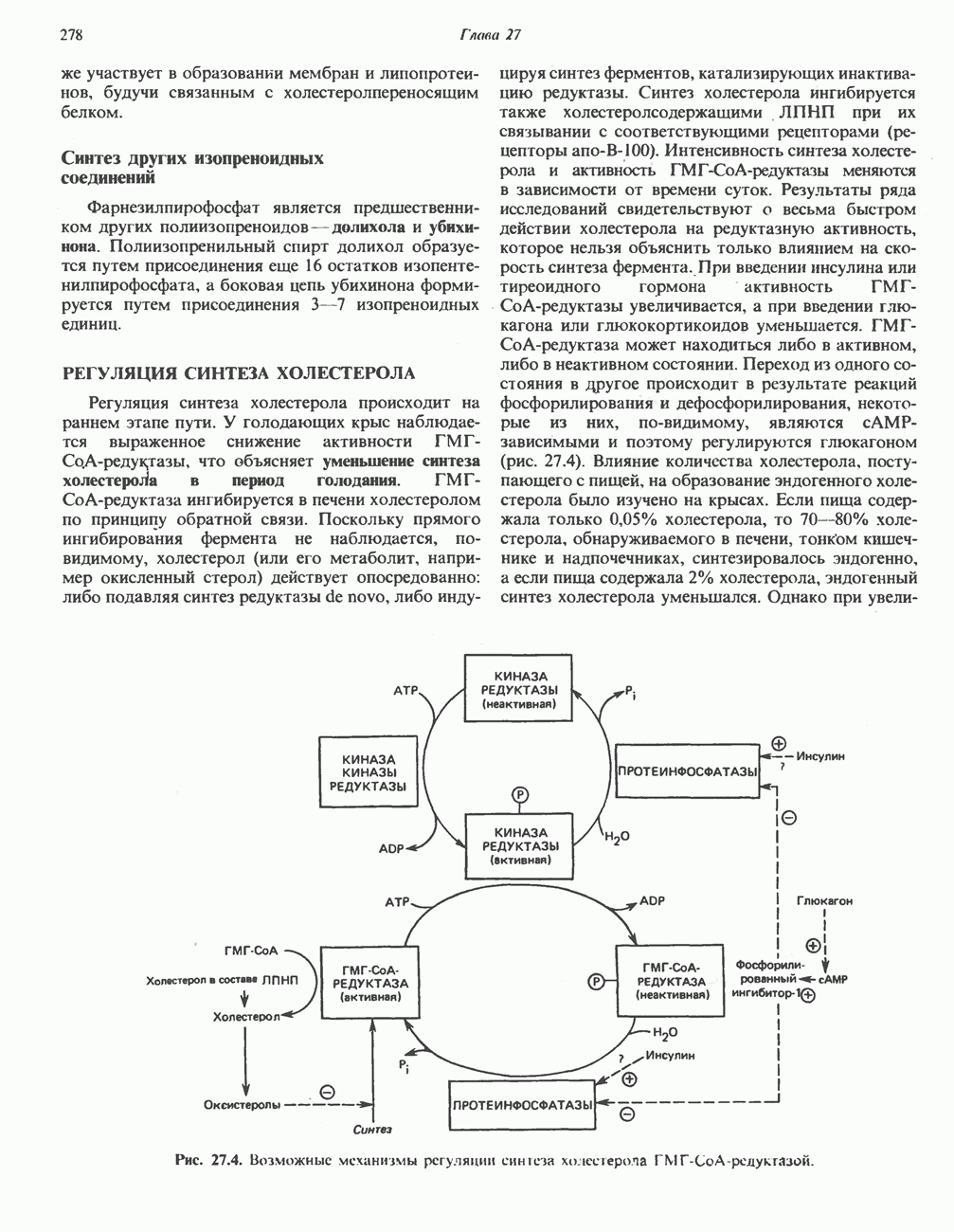
Рис. 22.2. Ключевые ферменты, участвующие в регуляции гликолиза, глюконеогенеза и метаболизма гликогена в печени. Указанное на схеме место действия гормона не предполагает прямого влияния на соответствующий фермент. Влияние сАМР на фосфофруктокиназу-1 и на фруктозо-1,6-бисфосфатазу осуществляется путем сочетания ковалентной модификации и аллостерического эффекта (см. рис. 22.4). Аланин в высоких концентрациях ингибирует гликолиз на стадии, катализируемой пируваткиназой, и, таким образом, действует как «сигнал глюконеогенеза».

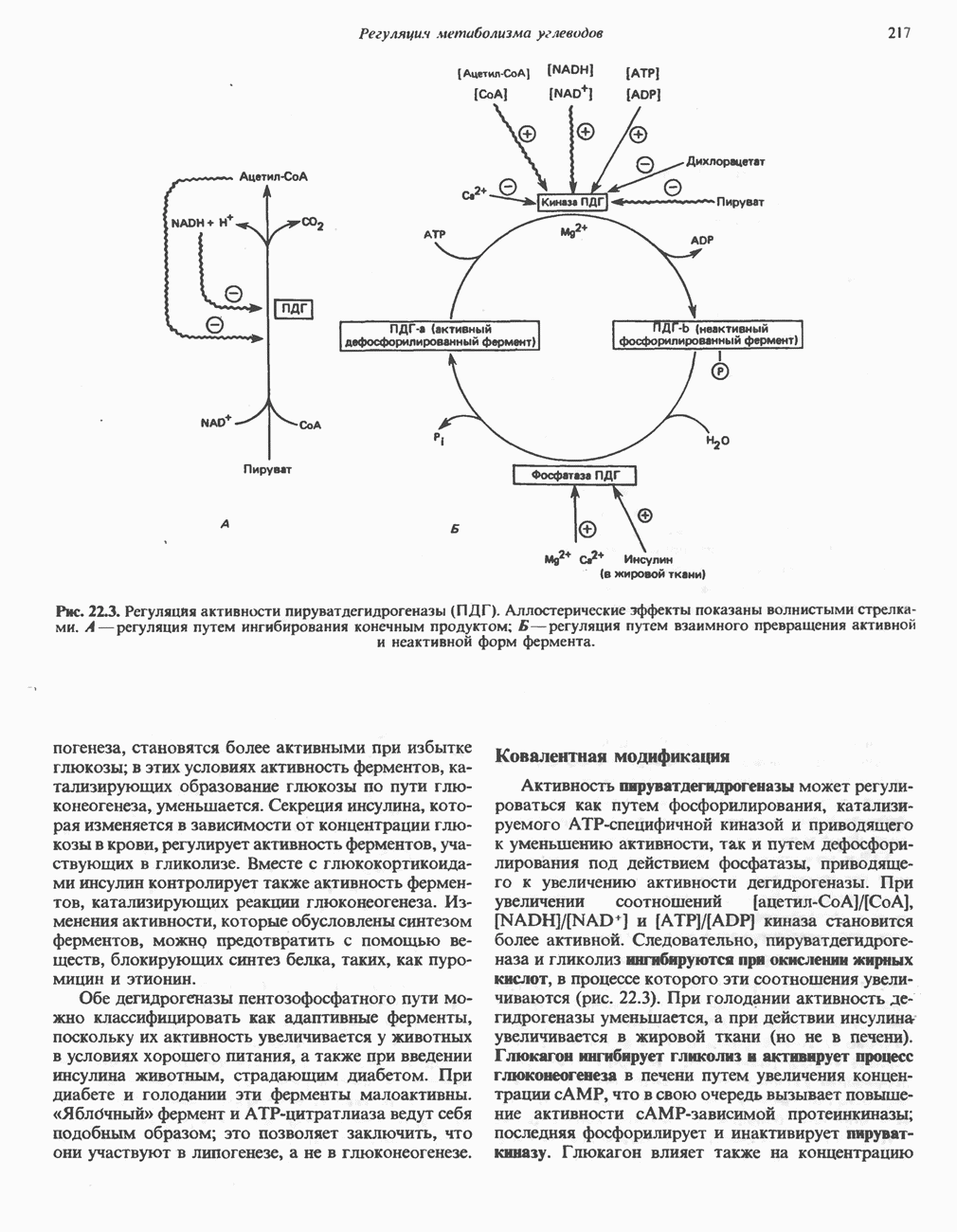
Рис. 22.3. Регуляция активности пируватдегидрогеназы (ПДГ). Аллостерические эффекты показаны волнистыми стрелками. А — регуляция путем ингибирования конечным продуктом; Б—регуляция путем взаимного превращения активной и неактивной форм фермента.
липогенеза, становятся более активными при избытке глюкозы; в этих условиях активность ферментов, катализирующих образование глюкозы по пути глюконеогенеза, уменьшается. Секреция инсулина, которая изменяется в зависимости от концентрации глюкозы в крови, регулирует активность ферментов, участвующих в гликолизе. Вместе с глюкокортикоидами инсулин контролирует также активность ферментов, катализирующих реакции глюконеогенеза. Изменения активности, которые обусловлены синтезом ферментов, можнр предотвратить с помощью веществ, блокирующих синтез белка, таких, как пуромицин и этионин.
Обе дегидрогеназы пентозофосфатного пути можно классифицировать как адаптивные ферменты, поскольку их активность увеличивается у животных в условиях хорошего питания, а также при введении инсулина животным, страдающим диабетом. При диабете и голодании эти ферменты малоактивны. «Яблочный» фермент и АТР-цитратлиаза ведут себя подобным образом; это позволяет заключить, что они участвуют в липогенезе, а не в глюконеогенезе.
Ковалентная модификация
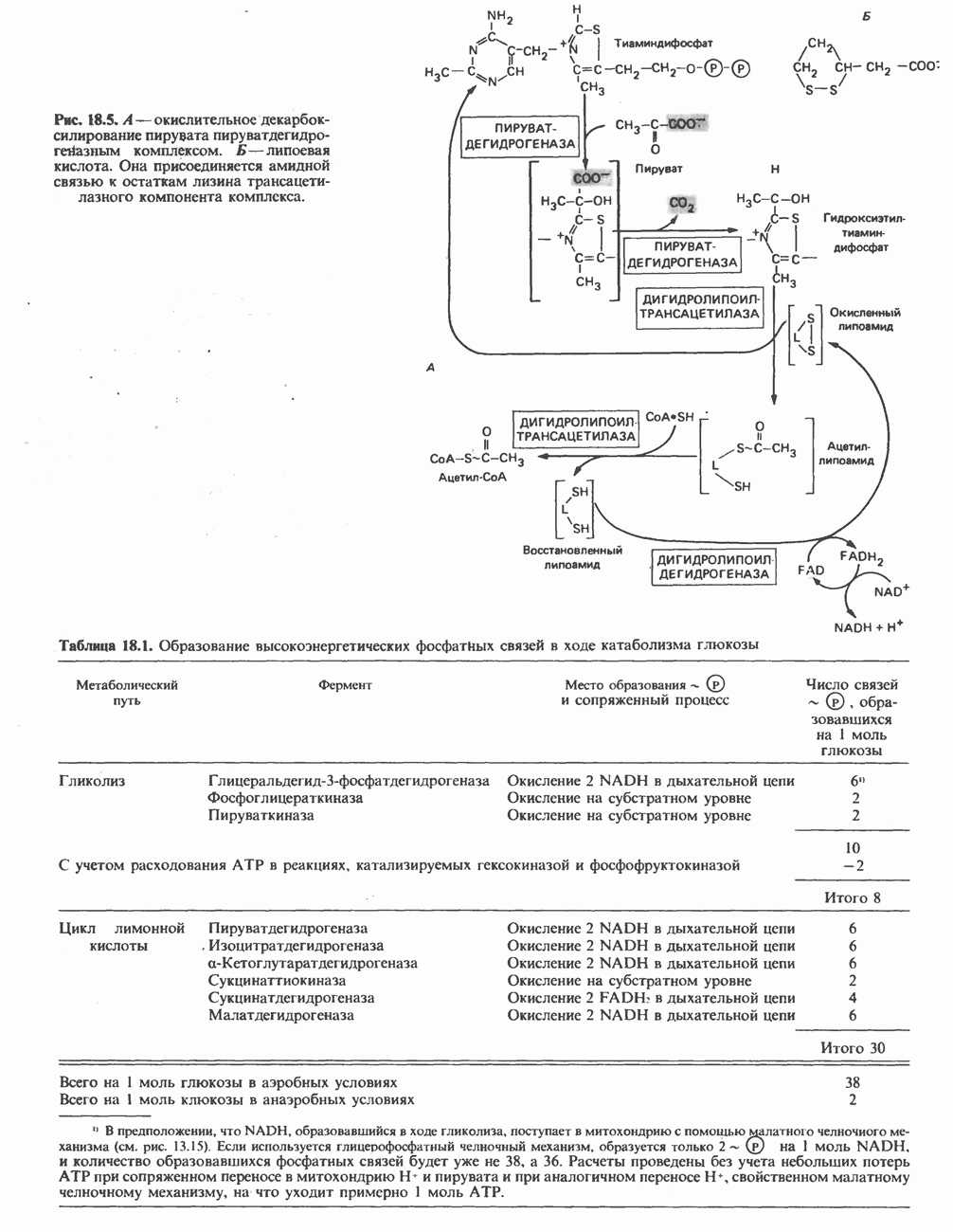
Активность пируватдегидрогеназы может регулироваться как путем фосфорилирования, катализируемого ATP-специфичной киназой и приводящего к уменьшению активности, так и путем дефосфорилирования под действием фосфатазы, приводящего к увеличению активности дегидрогеназы. При увеличении соотношений  киназа становится более активной. Следовательно, пируватдегидрогеназа и гликолиз ингибируются при окислении жирных кислот, в процессе которого эти соотношения увеличиваются (рис. 22.3). При голодании активность дегидрогеназы уменьшается, а при действии инсулина увеличивается в жировой ткани (но не в печени). Глюкагон ингибирует гликолиз и активирует процесс глюконеогенеза в печени путем увеличения концентрации сАМР, что в свою очередь вызывает повышение активности сАМР-зависимой протеинкиназы; последняя фосфорилирует и инактивирует пируваткиназу. Глюкагон влияет также на концентрацию
киназа становится более активной. Следовательно, пируватдегидрогеназа и гликолиз ингибируются при окислении жирных кислот, в процессе которого эти соотношения увеличиваются (рис. 22.3). При голодании активность дегидрогеназы уменьшается, а при действии инсулина увеличивается в жировой ткани (но не в печени). Глюкагон ингибирует гликолиз и активирует процесс глюконеогенеза в печени путем увеличения концентрации сАМР, что в свою очередь вызывает повышение активности сАМР-зависимой протеинкиназы; последняя фосфорилирует и инактивирует пируваткиназу. Глюкагон влияет также на концентрацию
фруктозо-2,6-бисфосфата, а следовательно, и на протекание гликолиза и глюконеогенеза; эти вопросы рассматриваются ниже.
Аллостерическая модификация
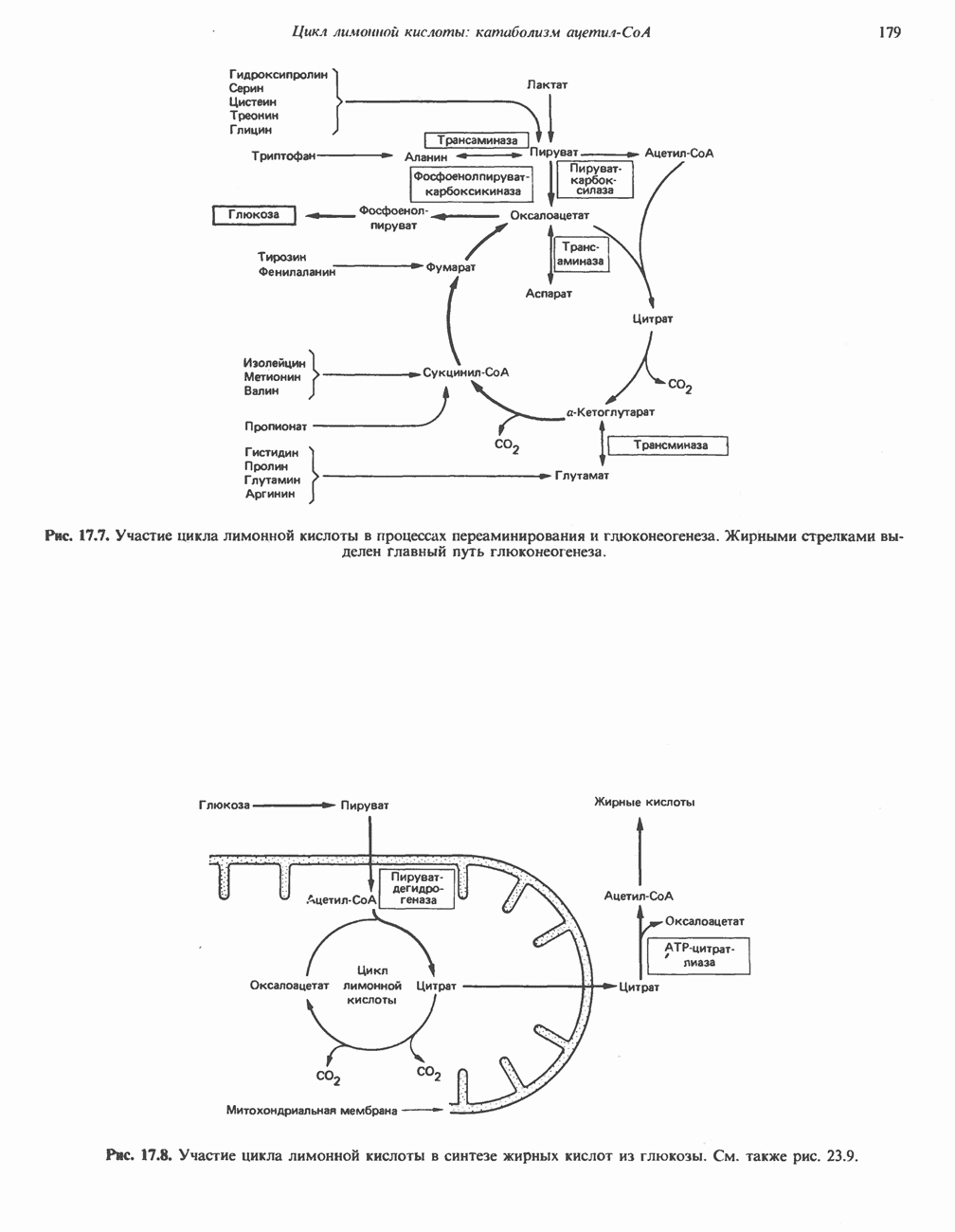
Аллостерический контроль осуществляется при регуляции активности ряда ферментов углеводного обмена. При биосинтезе в ходе глюконеогенеза оксалоацетата из бикарбоната и пирувата, катализируемого пируваткарбоксилазой, в качестве аллостерического активатора выступает ацетил-СоА. Последний изменяет конформацию белка, в результате уменьшается величина  для бикарбоната. Этот эффект имеет важное значение для саморегуляции промежуточного обмена веществ, поскольку ацетил-СоА, образующийся из пирувата, активирует пируваткарбоксилазу и тем самым способствует образованию оксалоацетата и его дальнейшему окислению в цикле лимонной кислоты. Активация пируваткарбоксилазы и ингибирование пируватдегидрогеназы, которые вызываются ацетил-СоА, образующимся при окислении жирных кислот, позволяют понять тормозящее действие окисления жирных кислот на окисление пирувата и активирующее влияние на глюконеогенез в печени. Как в печени, так и в почках регуляция активностей пируватдегидрогеназы и пируваткарбоксилазы имеет реципрокный характер, благодаря этому метаболическая судьба пирувата изменяется при переходе от окисления углеводов, начинающегося с гликолиза, к глюконеогенезу (рис. 22.2). Окисление жирных кислот обеспечивает глюконеогенез, поставляя АТР, необходимый для протекания реакций, которые катализируются пируваткарбоксилазой и фосфоенолпируваткарбоксикиназой.
для бикарбоната. Этот эффект имеет важное значение для саморегуляции промежуточного обмена веществ, поскольку ацетил-СоА, образующийся из пирувата, активирует пируваткарбоксилазу и тем самым способствует образованию оксалоацетата и его дальнейшему окислению в цикле лимонной кислоты. Активация пируваткарбоксилазы и ингибирование пируватдегидрогеназы, которые вызываются ацетил-СоА, образующимся при окислении жирных кислот, позволяют понять тормозящее действие окисления жирных кислот на окисление пирувата и активирующее влияние на глюконеогенез в печени. Как в печени, так и в почках регуляция активностей пируватдегидрогеназы и пируваткарбоксилазы имеет реципрокный характер, благодаря этому метаболическая судьба пирувата изменяется при переходе от окисления углеводов, начинающегося с гликолиза, к глюконеогенезу (рис. 22.2). Окисление жирных кислот обеспечивает глюконеогенез, поставляя АТР, необходимый для протекания реакций, которые катализируются пируваткарбоксилазой и фосфоенолпируваткарбоксикиназой.
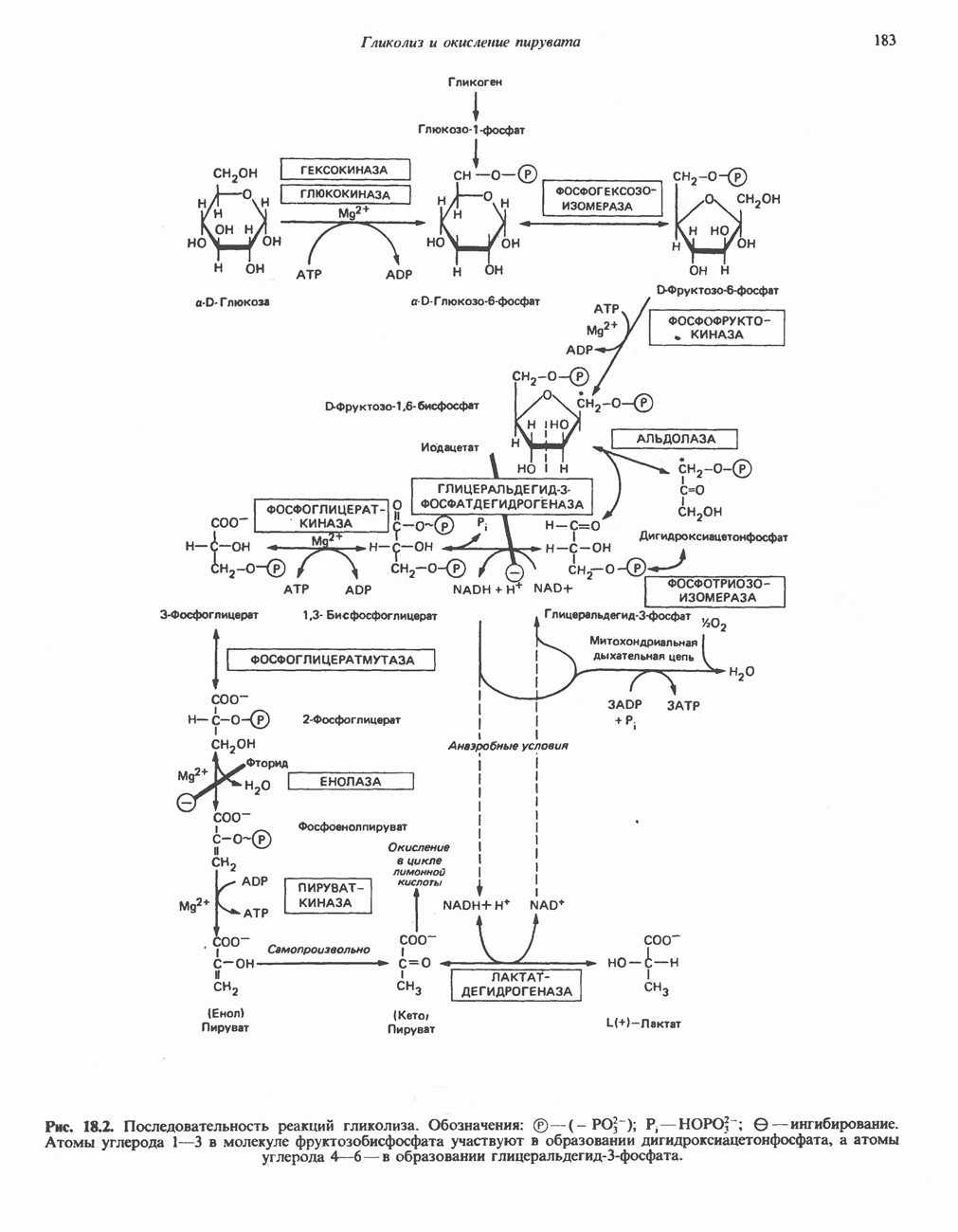
Фосфофруктокиназа (фосфофруктокиназа-1) является еще одним ферментом, регуляция которого осуществляется по принципу обратной связи. Этот фермент играет ключевую роль в регуляции гликолиза. Фосфофруктокиназа-1 ингибируется цитратом и АТР и активируется АМР. Последний функционирует как своего рода индикатор энергетического состояния клетки. Благодаря присутствию аденилаткиназы в клетках печени и многих других тканей быстро достигается равновесие в реакции

Таким образом, при расходовании АТР в потребляющих энергию реакциях и образовании ADP возрастает концентрация АМР. Поскольку в исходном равновесии концентрация АТР может в 50 раз превышать концентрацию АМР, то при сравнительно небольшом уменьшении концентрации АТР может многократно увеличиться концентрация АМР. Таким образом, большое увеличение концентрации АМР действует как своего рода метаболический усилитель при незначительном изменении концентрации АТР. Данный механизм делает фосфофруктокиназу-1 высокочувствительной к небольшим изменениям энергетического состояния клетки и позволяет регулировать количество углеводов, подвергающихся гликолизу, до их вступления в цикл лимонной кислоты. Увеличение концентрации АМР позволяет также объяснить, почему процесс гликолиза усиливается при недостатке кислорода, когда концентрация АТР снижается. Одновременно АМР активирует фосфорилазу и тем самым усиливает гликогенолиз. Ингибирование фосфофруктокиназы-1 цитратом и АТР является еще одним путем, который объясняет тормозящее действие окисления жирных кислот на окисление глюкозы; это ингибирование объясняет также эффект Пастера, заключающийся в том, что аэробное окисление субстратов в цикле лимонной кислоты ингибирует анаэробное расщепление глюкозы. Следствием ингибирования фосфофруктокиназы-1 является также накопление глюкозобфосфата, который снижает поступление глюкозы во внепеченочные ткани путем аллостерического ингибирования гексокиназы.
Роль фруктозо-2,6-бисфосфата
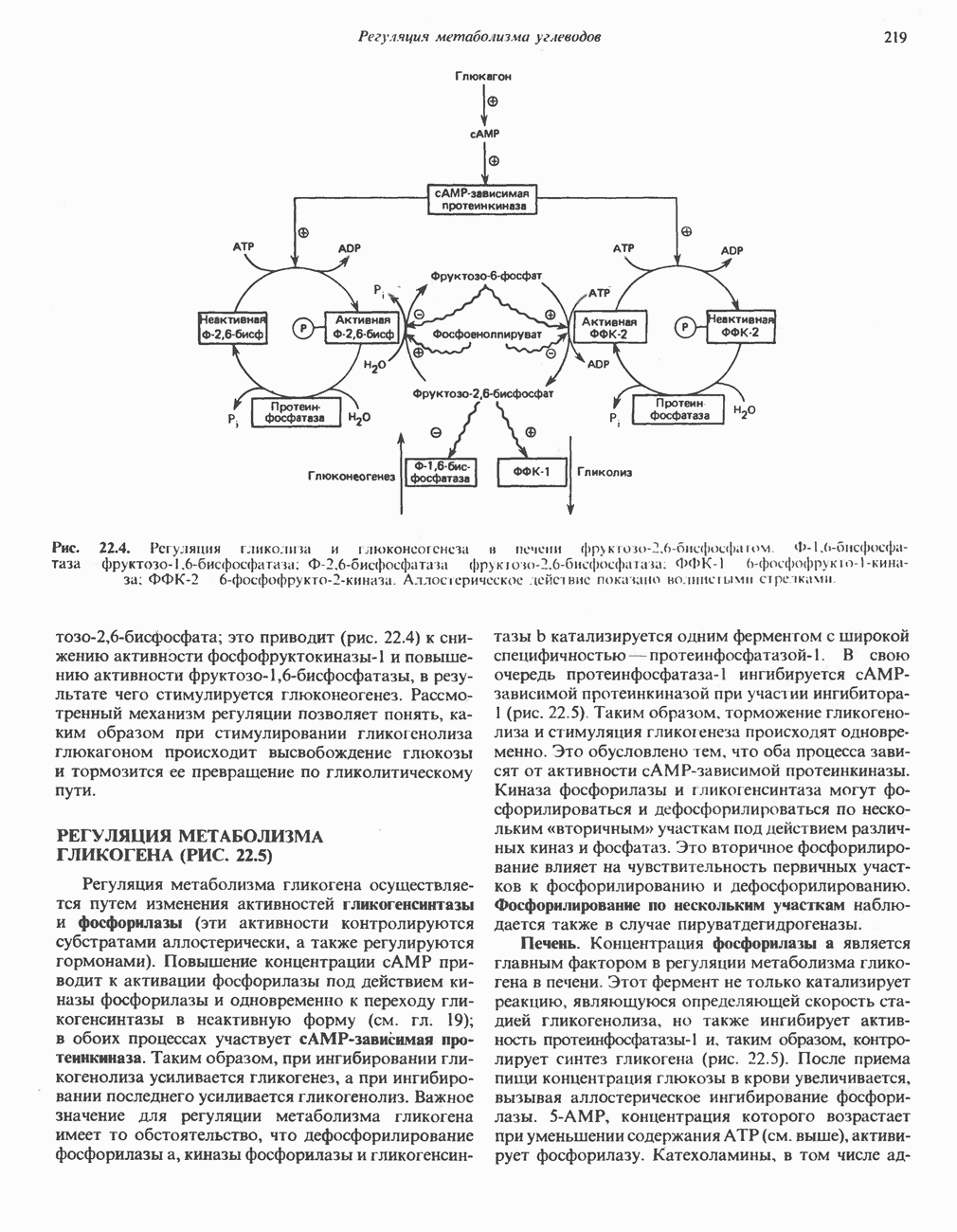
Наиболее мощным аллостерическим активатором фосфофруктокиназы-1 и ингибитором фруктозо-1, 6-бисфосфатазы печени является фруктозо-2.6-бисфосфат. Он снижает ингибирующее действие АТР на фосфофруктокиназу-1 и увеличивает сродство этого фермента к фруктозо-6-фосфату. При ингибировании фруктозо-1,6-бисфосфатазы фруктозо-2.6-бисфосфатом происходит увеличение  для фруктозо-1,6-бисфосфата. Концентрация фруктозо-2.6-бисфосфата регулируется концентрацией фруктозо-6-фосфата и гормонами (рис. 22.4). Фруктозо-2.6-бисфосфат образуется при фосфорилировании фруктозо-6-фосфата, катализируемом фосфофруктокиназой-2. Этот фермент является бифункциональным (он обладает также фруктозо-2.6-бисфосфатазной активностью) и находится под аллостерическим контролем фруктозо-6-фосфата (при повышении концентрации фруктозо-6-фосфата, наблюдаемой в случае избытка глюкозы, происходит стимулирование киназной и ингибирование фосфатазной активности). С другой стороны, при снижении концентрации глюкозы глюкагон стимулирует образование сАМР; последний активирует сАМР-зависимую протеинкиназу, которая в свою очередь ингибирует фосфофруктокиназу-2 и активирует фруктозо-2,6-бисфосфатазу путем фосфорилирования. Таким образом, при избытке глюкозы увеличивается концентрация фруктозо-2,6-бисфосфата, который активирует фосфофруктокиназу-1 и ингибирует фруктозо-1,6-бисфосфатазу; в результате происходит стимулирование гликолиза. При недостатке глюкозы гликагон уменьшает концентрацию фруктозо-2,6-бисфосфата;
для фруктозо-1,6-бисфосфата. Концентрация фруктозо-2.6-бисфосфата регулируется концентрацией фруктозо-6-фосфата и гормонами (рис. 22.4). Фруктозо-2.6-бисфосфат образуется при фосфорилировании фруктозо-6-фосфата, катализируемом фосфофруктокиназой-2. Этот фермент является бифункциональным (он обладает также фруктозо-2.6-бисфосфатазной активностью) и находится под аллостерическим контролем фруктозо-6-фосфата (при повышении концентрации фруктозо-6-фосфата, наблюдаемой в случае избытка глюкозы, происходит стимулирование киназной и ингибирование фосфатазной активности). С другой стороны, при снижении концентрации глюкозы глюкагон стимулирует образование сАМР; последний активирует сАМР-зависимую протеинкиназу, которая в свою очередь ингибирует фосфофруктокиназу-2 и активирует фруктозо-2,6-бисфосфатазу путем фосфорилирования. Таким образом, при избытке глюкозы увеличивается концентрация фруктозо-2,6-бисфосфата, который активирует фосфофруктокиназу-1 и ингибирует фруктозо-1,6-бисфосфатазу; в результате происходит стимулирование гликолиза. При недостатке глюкозы гликагон уменьшает концентрацию фруктозо-2,6-бисфосфата;

Рис. 22.4. Регуляция гликолнга и i лкжонеогенеза и печени  Аллосгерическое действие показано волнистыми стрелками.
Аллосгерическое действие показано волнистыми стрелками.
это приводит (рис. 22.4) к снижению активности фосфофруктокиназы-1 и повышению активности фруктозо-1,6-бисфосфатазы, в результате чего стимулируется глюконеогенез. Рассмотренный механизм регуляции позволяет понять, каким образом при стимулировании гликогенолиза глюкагоном происходит высвобождение глюкозы и тормозится ее превращение по гликолитическому пути.
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие к русскому изданию
- Предисловие
- Глава 1. Биохимия и медицина
- Глава 2. Биомолекулы и биохимические методы
- КЛЕТКА
- ОБЩИЙ ЭКСПЕРИМЕНТАЛЬНЫЙ ПОДХОД, ИСПОЛЬЗУЕМЫЙ В БИОХИМИИ
- ОСНОВНЫЕ ДОСТИЖЕНИЯ БИОХИМИИ
- Раздел I. Структура и функции белков и ферментов
- Глава 3. Аминокислоты
- АМИНОКИСЛОТЫ
- ИОННЫЕ ФОРМЫ АМИНОКИСЛОТ
- СТРУКТУРА АМИНОКИСЛОТ
- РАСТВОРИМОСТЬ АМИНОКИСЛОТ
- ОБЩИЕ ХИМИЧЕСКИЕ РЕАКЦИИ
- СВОЙСТВА ИНДИВИДУАЛЬНЫХ АМИНОКИСЛОТ
- МЕТОДЫ РАЗДЕЛЕНИЯ АМИНОКИСЛОТ
- Глава 4. Пептиды
- СТРУКТУРА ПЕПТИДОВ
- ИОННЫЕ ФОРМЫ ПЕПТИДОВ
- КОНФОРМАЦИЯ ПЕПТИДОВ В РАСТВОРЕ
- МЕТОДЫ РАЗДЕЛЕНИЯ ПЕПТИДОВ
- ОПРЕДЕЛЕНИЕ АМИНОКИСЛОТНОГО СОСТАВА ПЕПТИДОВ
- ОПРЕДЕЛЕНИЕ ПЕРВИЧНОЙ СТРУКТУРЫ ПОЛИПЕПТИДОВ
- АВТОМАТИЧЕСКОЕ ОПРЕДЕЛЕНИЕ АМИНОКИСЛОТНОЙ ПОСЛЕДОВАТЕЛЬНОСТИ ПОЛИПЕПТИДОВ МЕТОДОМ ЭДМАНА
- АВТОМАТИЧЕСКИЙ СИНТЕЗ ПЕПТИДОВ
- ЛИТЕРАТУРА
- Глава 5. Белки: структура и свойства
- КЛАССИФИКАЦИЯ БЕЛКОВ
- СВЯЗИ, ОТВЕТСТВЕННЫЕ ЗА ФОРМИРОВАНИЕ СТРУКТУРЫ БЕЛКА
- УПОРЯДОЧЕННЫЕ КОНФОРМАЦИИ ПОЛИПЕПТИДОВ
- УРОВНИ СТРУКТУРНОЙ ОРГАНИЗАЦИИ БЕЛКА
- ДЕНАТУРАЦИЯ
- МЕТОДЫ ОПРЕДЕЛЕНИЯ ПЕРВИЧНОЙ СТРУКТУРЫ
- ОПРЕДЕЛЕНИЕ ВТОРИЧНОЙ И ТРЕТИЧНОЙ СТРУКТУРЫ МЕТОДОМ РЕНТГЕНОВСКОЙ КРИСТАЛЛОГРАФИИ
- ОПРЕДЕЛЕНИЕ ЧЕТВЕРТИЧНОЙ СТРУКТУРЫ
- ГЛАВА 6. Белки: миоглобин и гемоглобин
- ГЕМОПРОТЕИНЫ — МИОГЛОБИН И ГЕМОГЛОБИН
- МИОГЛОБИН
- ГЕМОГЛОБИНЫ
- Глава 7. Ферменты: общие свойства
- КОФЕРМЕНТЫ
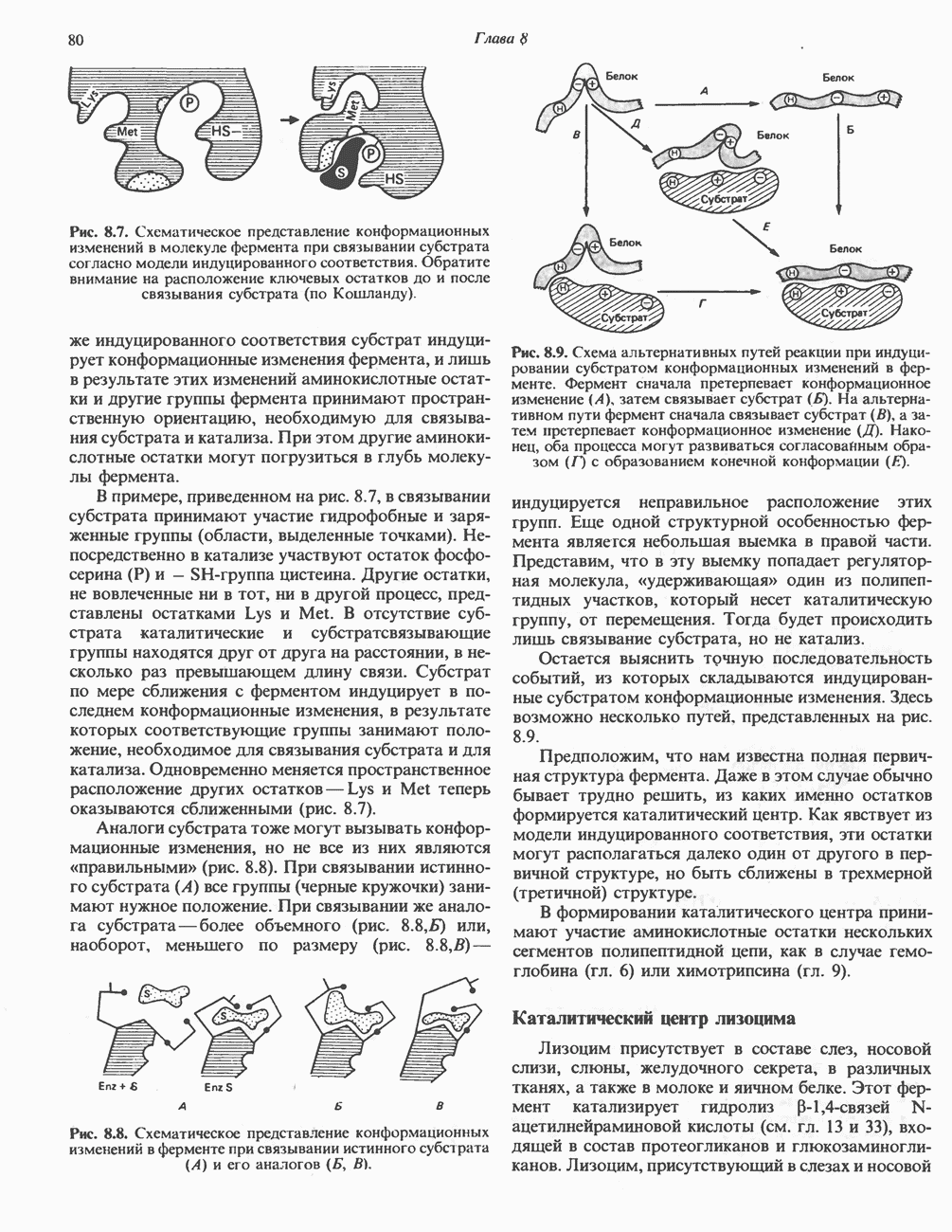
- «ТРЕХТОЧЕЧНАЯ ФИКСАЦИЯ» СУБСТРАТОВ НА ФЕРМЕНТАХ
- СПЕЦИФИЧНОСТЬ ФЕРМЕНТОВ
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ФЕРМЕНТАТИВНОЙ АКТИВНОСТИ
- ВЫДЕЛЕНИЕ ФЕРМЕНТОВ
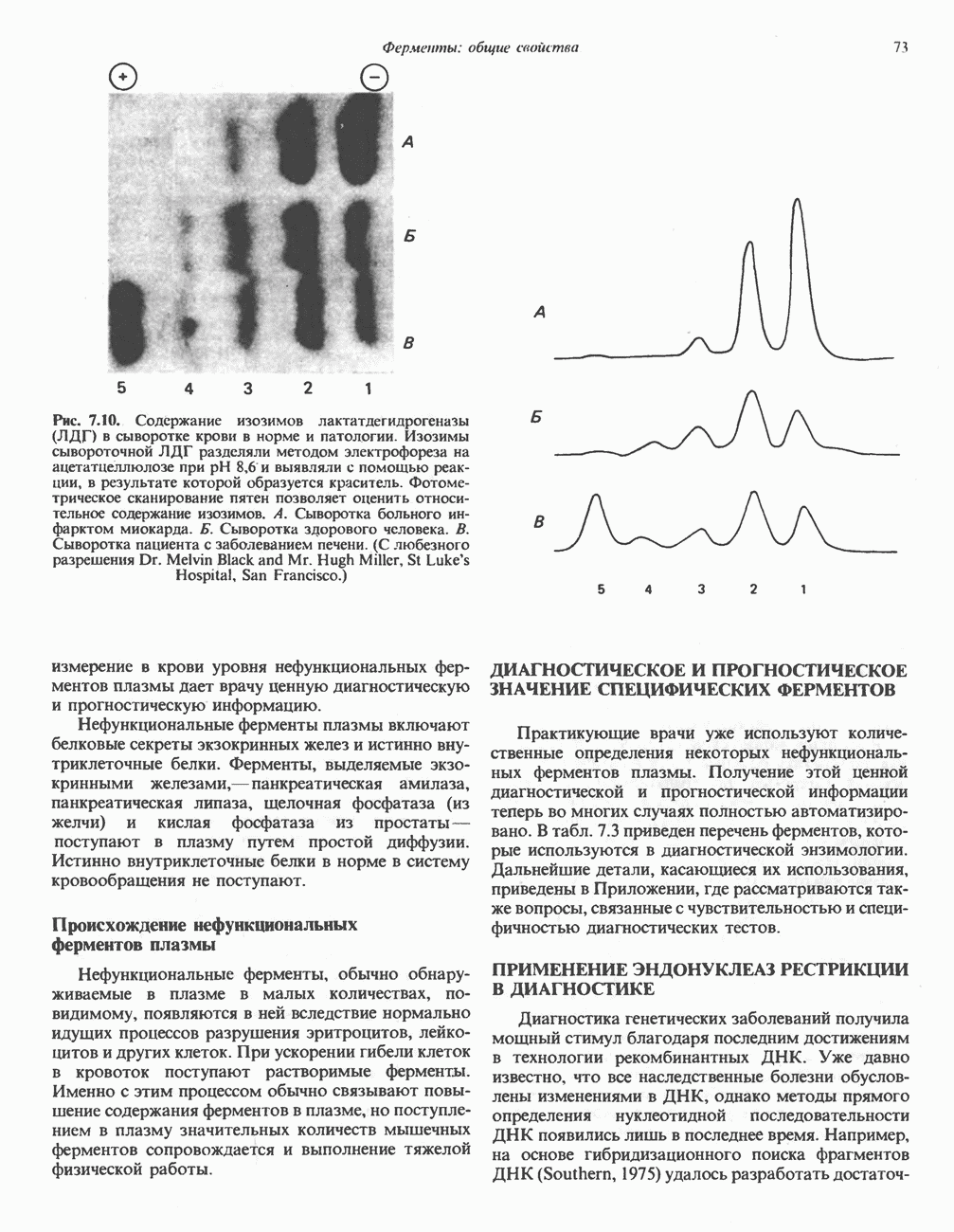
- ИЗОФЕРМЕНТЫ (ИЗОЗИМЫ)
- ФЕРМЕНТЫ В КЛИНИЧЕСКОЙ ДИАГНОСТИКЕ
- ДИАГНОСТИЧЕСКОЕ И ПРОГНОСТИЧЕСКОЕ ЗНАЧЕНИЕ СПЕЦИФИЧЕСКИХ ФЕРМЕНТОВ
- ПРИМЕНЕНИЕ ЭНДОНУКЛЕАЗ РЕСТРИКЦИИ В ДИАГНОСТИКЕ
- ЛИТЕРАТУРА
- Глава 8. ФЕРМЕНТЫ: КИНЕТИКА
- ОБРАЗОВАНИЕ И РАСПАД ПЕРЕХОДНЫХ СОСТОЯНИЙ
- ИЗМЕНЕНИЯ СВОБОДНОЙ ЭНЕРГИИ, СВЯЗАННЫЕ С ОБРАЗОВАНИЕМ И РАСПАДОМ ПЕРЕХОДНЫХ СОСТОЯНИЙ
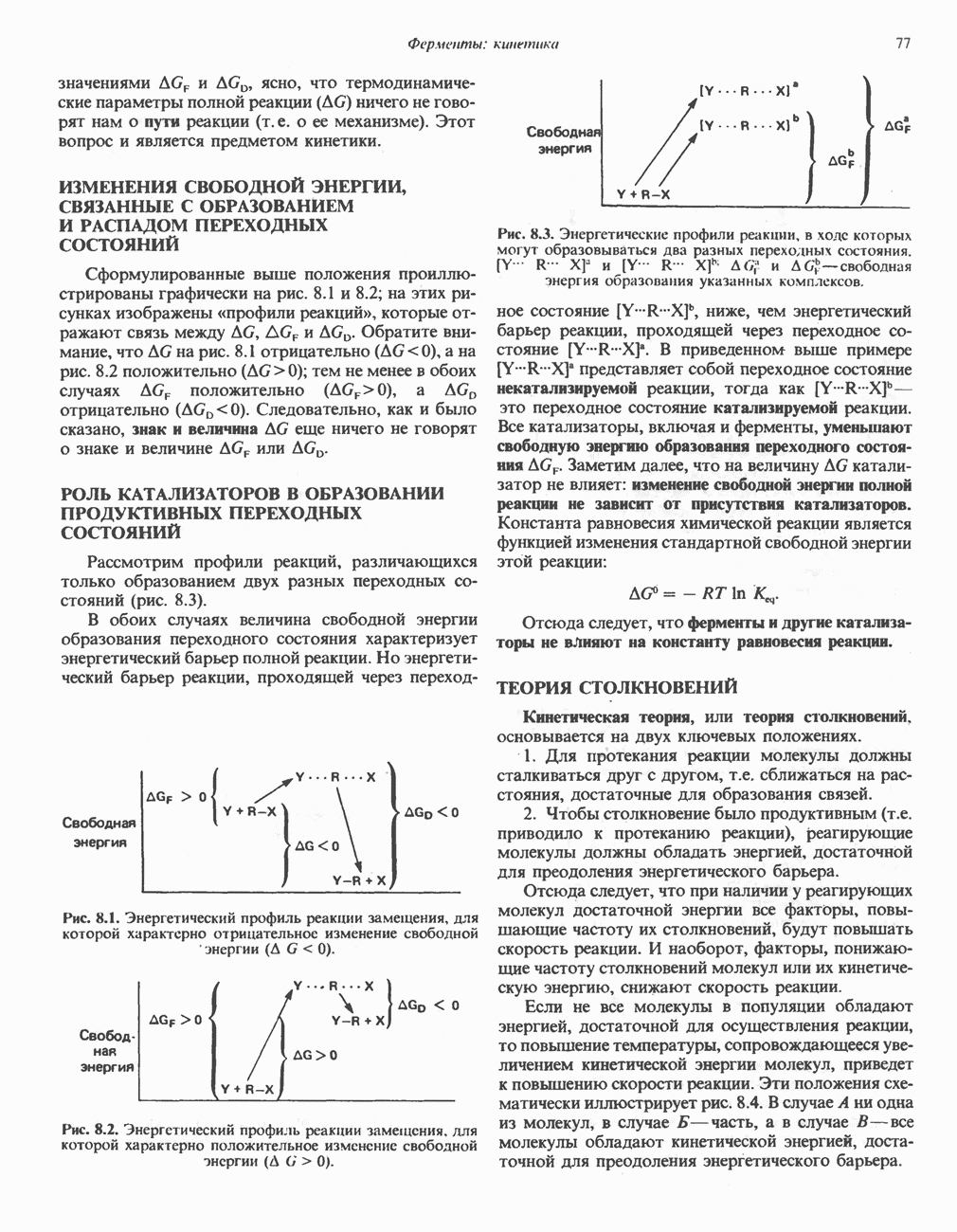
- РОЛЬ КАТАЛИЗАТОРОВ В ОБРАЗОВАНИИ ПРОДУКТИВНЫХ ПЕРЕХОДНЫХ СОСТОЯНИЙ
- ТЕОРИЯ СТОЛКНОВЕНИЙ
- РОЛЬ ФЕРМЕНТОВ В РАЗРЫВЕ И ОБРАЗОВАНИИ КОВАЛЕНТНЫХ СВЯЗЕЙ
- КАТАЛИТИЧЕСКИЙ ЦЕНТР
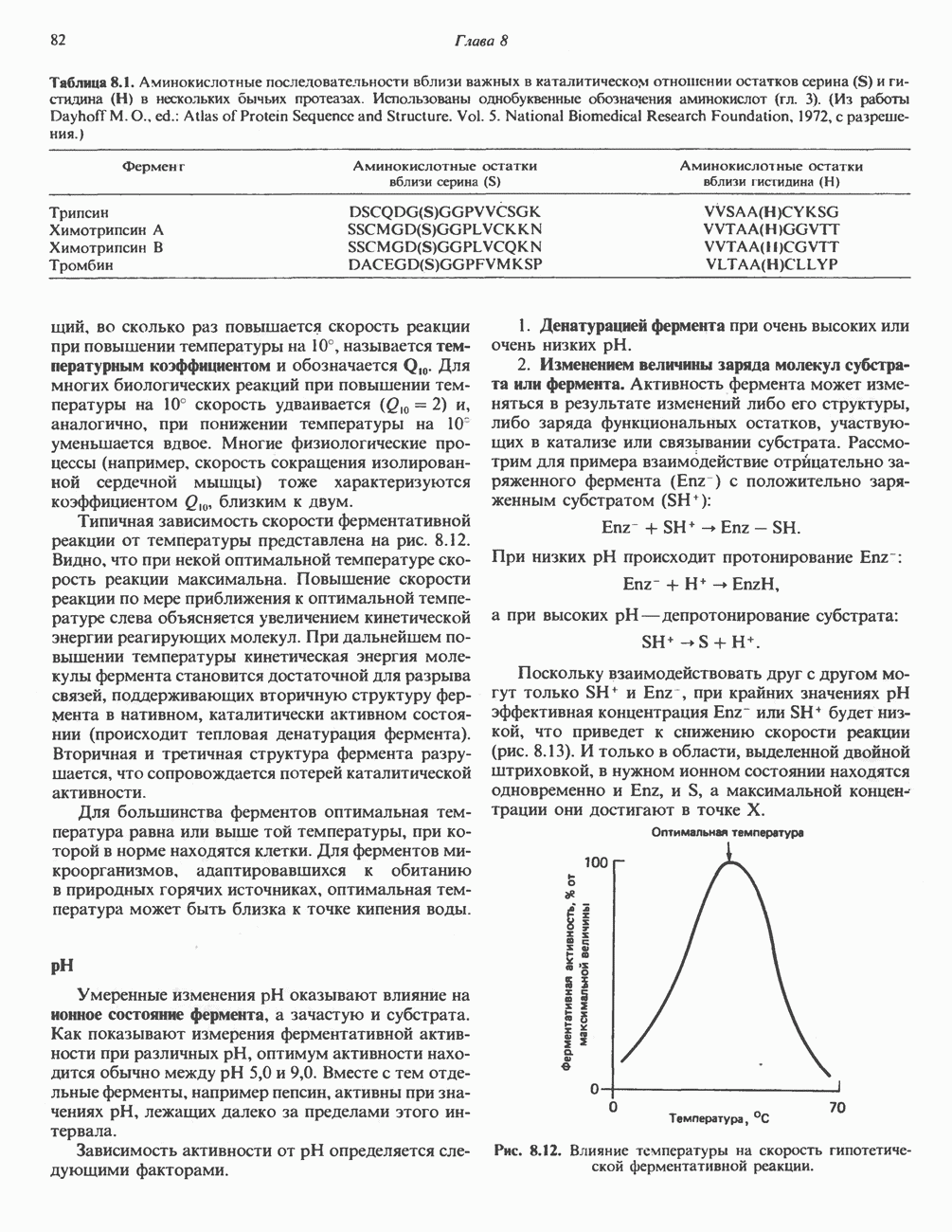
- ФАКТОРЫ, ВЛИЯЮЩИЕ НА АКТИВНОСТЬ ФЕРМЕНТОВ
- КОНСТАНТА РАВНОВЕСИЯ
- КОНЦЕНТРАЦИЯ ФЕРМЕНТА
- КОНЦЕНТРАЦИЯ СУБСТРАТА
- УРАВНЕНИЕ МИХАЭЛИСА—МЕНТЕН
- ОГРАНИЧЕНИЯ, ПРИСУЩИЕ УРАВНЕНИЮ МИХАЭЛИСА — МЕНТЕН
- ИНГИБИРОВАНИЕ АКТИВНОСТИ ФЕРМЕНТОВ
- МОДУЛЯТОРЫ ФЕРМЕНТАТИВНОЙ АКТИВНОСТИ
- Глава 9. Ферменты: механизм действия
- МЕХАНИЗМ КАТАЛИТИЧЕСКОГО ДЕЙСТВИЯ ХИМОТРИПСИНА
- РОЛЬ ИЗБИРАТЕЛЬНОГО ПРОТЕОЛИЗА В ФОРМИРОВАНИИ АКТИВНЫХ ЦЕНТРОВ ФЕРМЕНТОВ
- УПОРЯДОЧЕННОЕ И НЕУПОРЯДОЧЕННОЕ СВЯЗЫВАНИЕ СУБСТРАТОВ
- ФЕРМЕНТЫ КАК КАТАЛИЗАТОРЫ ОБЩЕГО КИСЛОТНОГО И ОБЩЕГО ОСНОВНОГО ТИПА
- ИОНЫ МЕТАЛЛОВ
- Глава 10. Ферменты: регуляция активности
- РЕГУЛЯЦИЯ МЕТАБОЛИЗМА
- РЕГУЛЯЦИЯ КОЛИЧЕСТВА ФЕРМЕНТА ПУТЕМ РЕГУЛЯЦИИ СКОРОСТИ ЕГО СИНТЕЗА И РАСПАДА
- РЕГУЛЯЦИЯ КАТАЛИТИЧЕСКОЙ АКТИВНОСТИ ФЕРМЕНТОВ
- АЛЛОСТЕРИЧЕСКАЯ РЕГУЛЯЦИЯ
- КОВАЛЕНТНАЯ МОДИФИКАЦИЯ ФЕРМЕНТОВ
- Раздел II. Биоэнергетика и метаболизм углеводов и липидов
- Глава 11. Биоэнергетика
- СВОБОДНАЯ ЭНЕРГИЯ И ЗАКОНЫ ТЕРМОДИНАМИКИ
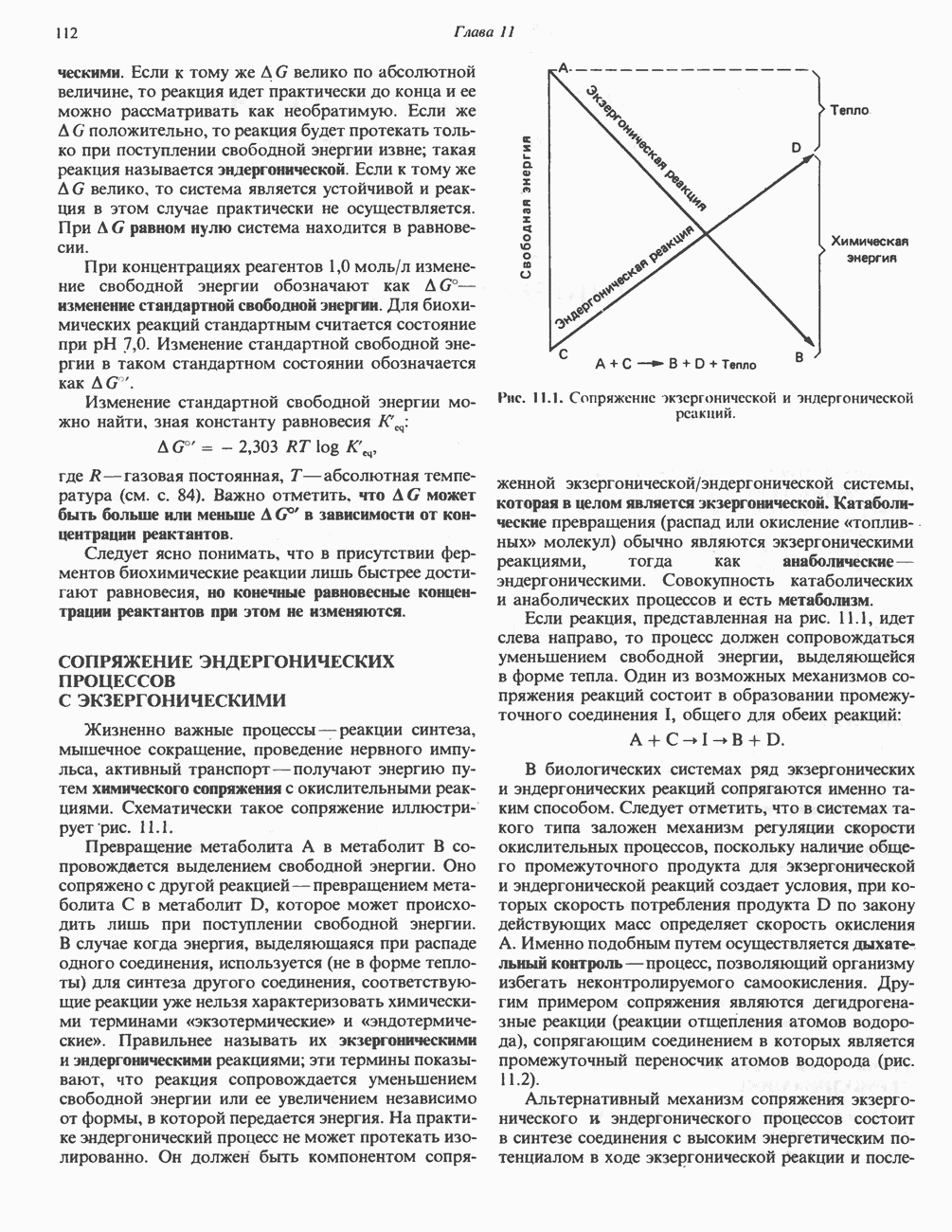
- СОПРЯЖЕНИЕ ЭНДЕРГОНИЧЕСКИХ ПРОЦЕССОВ С ЭКЗЕРГОНИЧЕСКИМИ
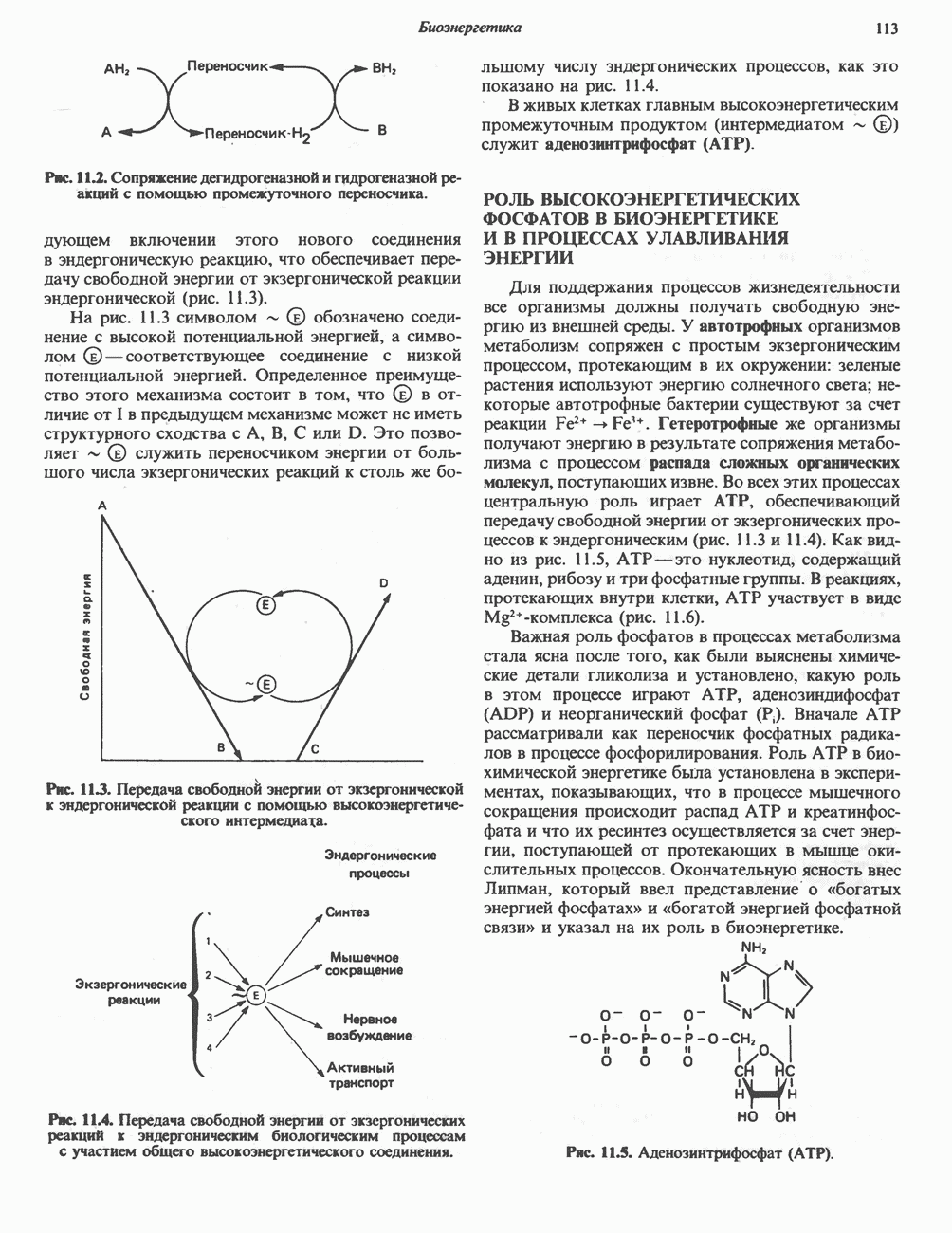
- РОЛЬ ВЫСОКОЭНЕРГЕТИЧЕСКИХ ФОСФАТОВ В БИОЭНЕРГЕТИКЕ И В ПРОЦЕССАХ УЛАВЛИВАНИЯ ЭНЕРГИИ
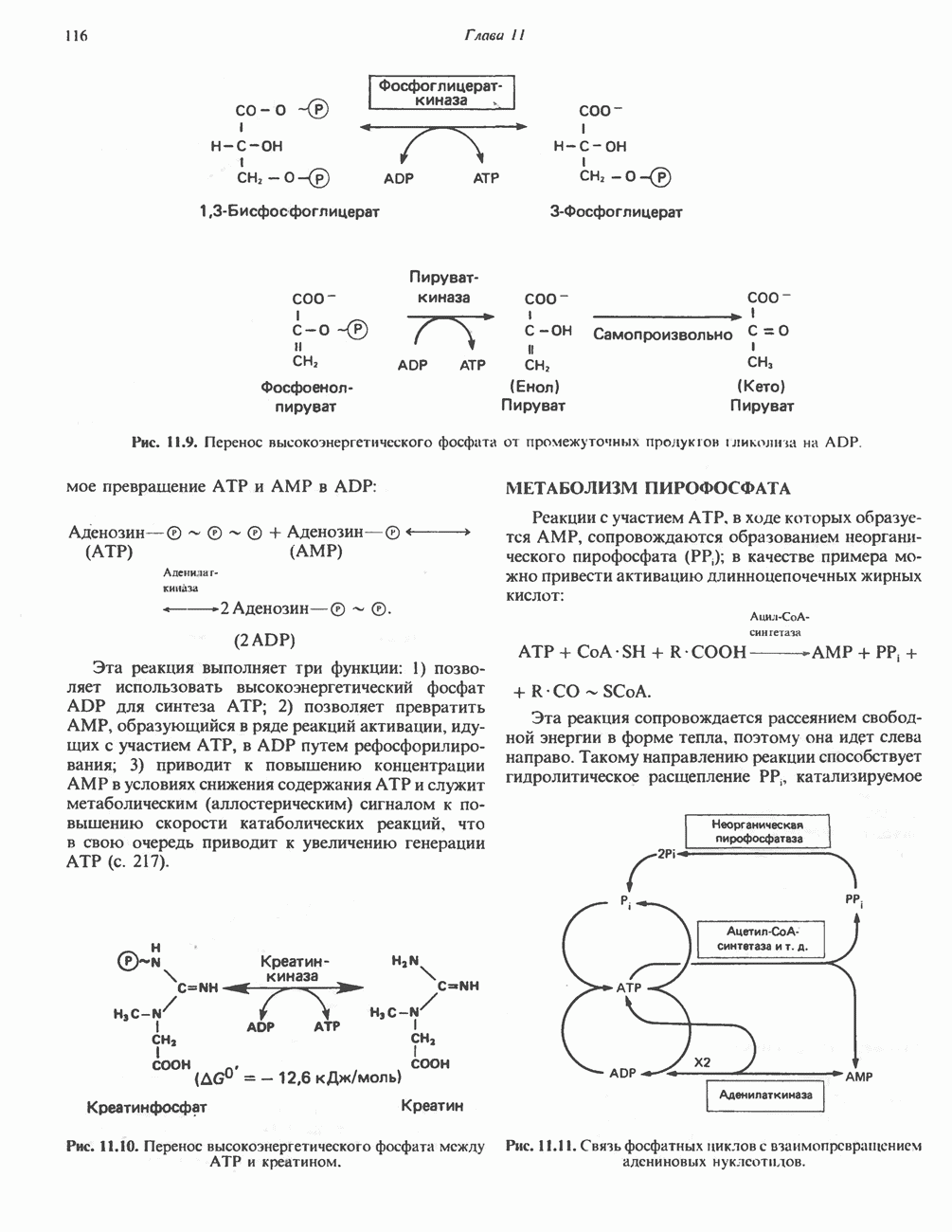
- МЕТАБОЛИЗМ ПИРОФОСФАТА
- Глава 12. Биологическое окисление
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНОЕ РАВНОВЕСИЕ, ОКИСЛИТЕЛЬНОВОССТАНОВИТЕЛЬНЫЙ ПОТЕНЦИАЛ
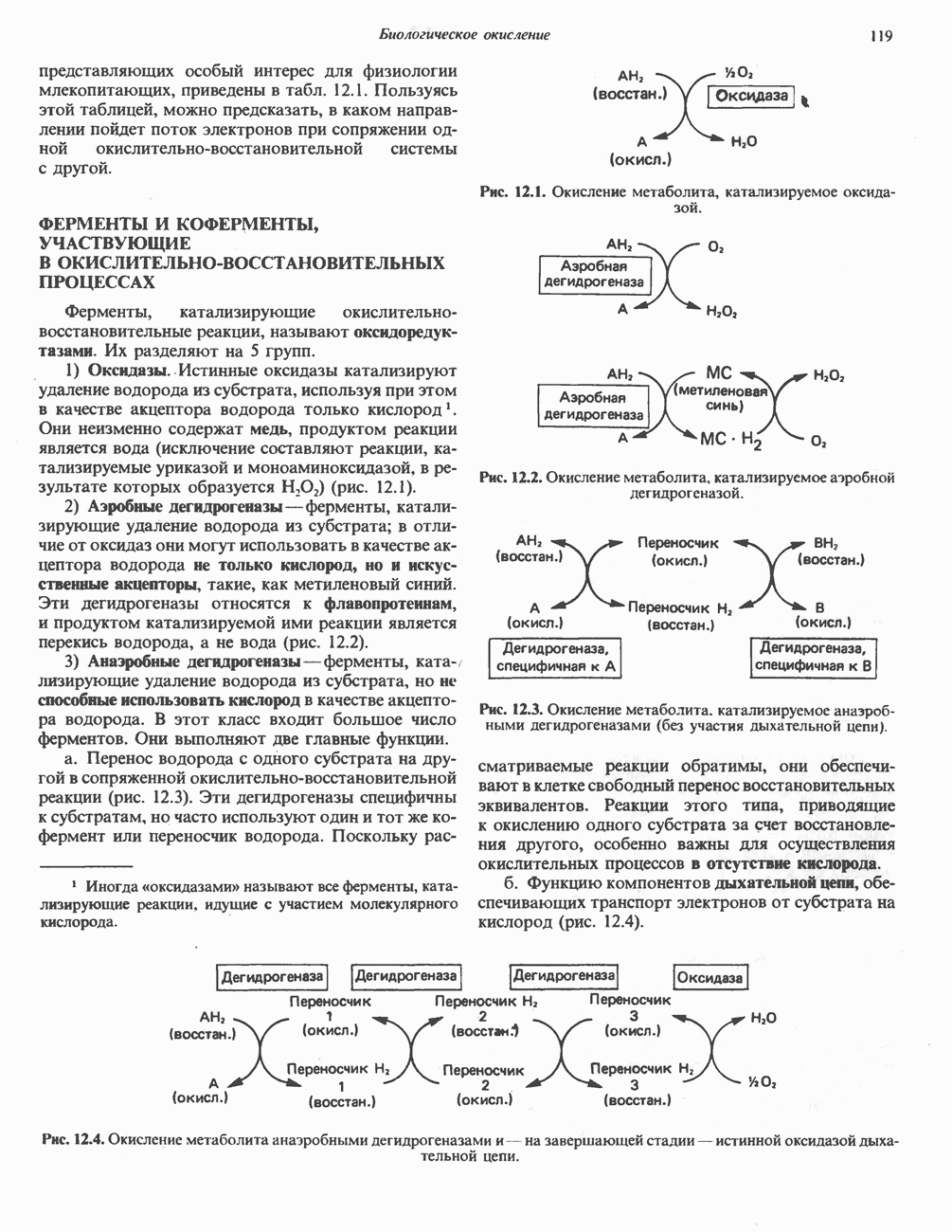
- ФЕРМЕНТЫ И КОФЕРМЕНТЫ, УЧАСТВУЮЩИЕ В ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ ПРОЦЕССАХ
- Глава 13. Окислительное фосфорилирование и транспортные системы митохондрий
- ДЫХАТЕЛЬНАЯ ЦЕПЬ
- ОРГАНИЗАЦИЯ ДЫХАТЕЛЬНОЙ ЦЕПИ В МИТОХОНДРИЯХ
- РОЛЬ ДЫХАТЕЛЬНОЙ ЦЕПИ В УЛАВЛИВАНИИ ЭНЕРГИИ
- ДЫХАТЕЛЬНЫЙ КОНТРОЛЬ
- ИНГИБИТОРЫ ДЫХАТЕЛЬНОЙ ЦЕПИ И ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ
- МЕХАНИЗМ ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ
- МИТОХОНДРИАЛЬНЫЕ ТРАНСПОРТНЫЕ СИСТЕМЫ
- Глава 14. Физиологически важные углеводы
- КЛАССИФИКАЦИЯ УГЛЕВОДОВ
- МОНОСАХАРИДЫ
- ДИСАХАРИДЫ
- ПОЛИСАХАРИДЫ
- УГЛЕВОДЫ КЛЕТОЧНЫХ МЕМБРАН
- Глава 15. Физиологически важные липиды
- КЛАССИФИКАЦИЯ ЛИПИДОВ
- ЖИРНЫЕ КИСЛОТЫ
- ТРИАЦИЛГЛИЦЕРОЛЫ (триглицериды)
- ФОСФОЛИПИДЫ
- ГЛИКОЛИПИДЫ (ГЛИКОСФИНГОЛИПИДЫ)
- СТЕРОИДЫ
- ПЕРЕКИСНОЕ ОКИСЛЕНИЕ ЛИПИДОВ
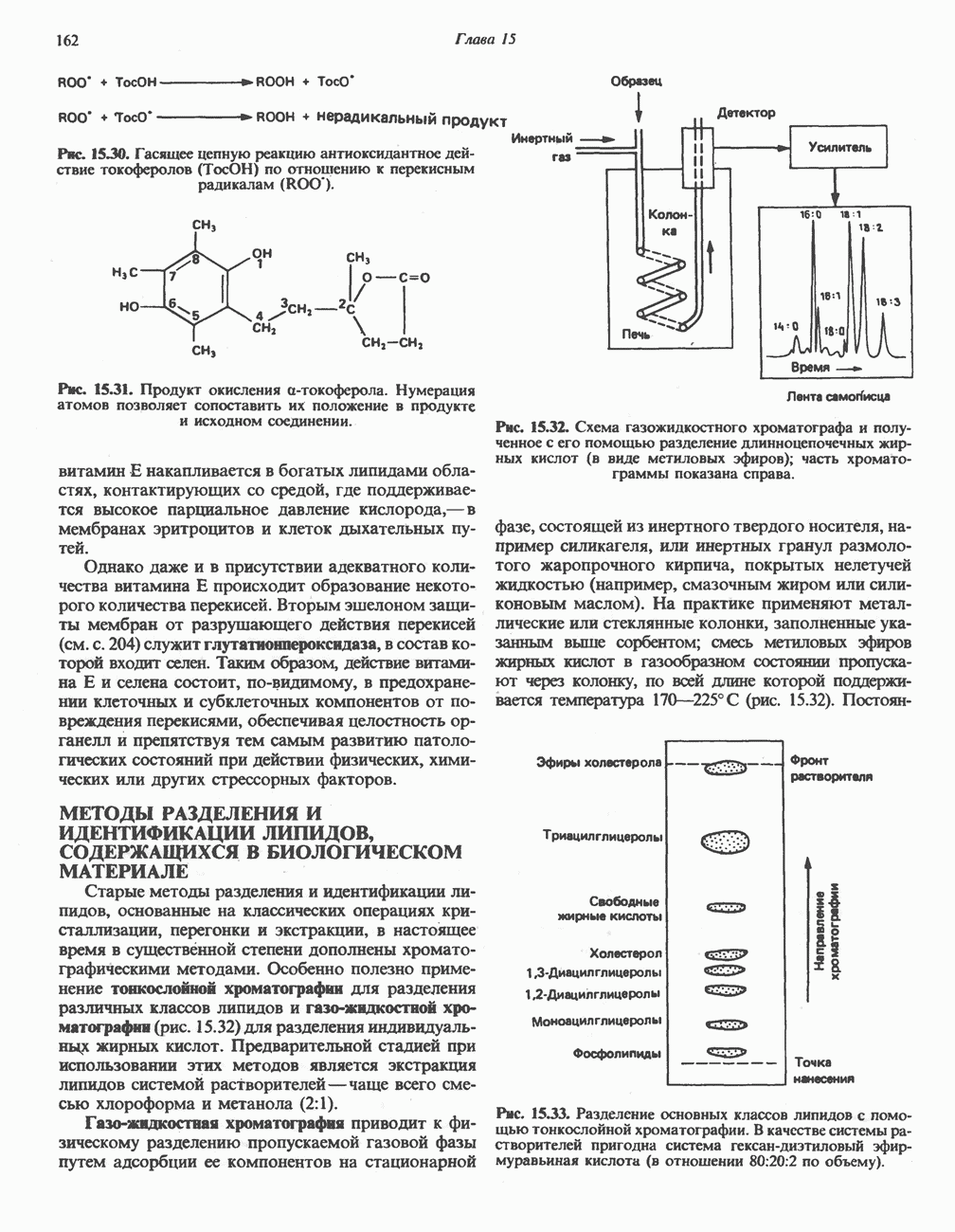
- МЕТОДЫ РАЗДЕЛЕНИЯ И ИДЕНТИФИКАЦИИ ЛИПИДОВ, СОДЕРЖАЩИХСЯ В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ
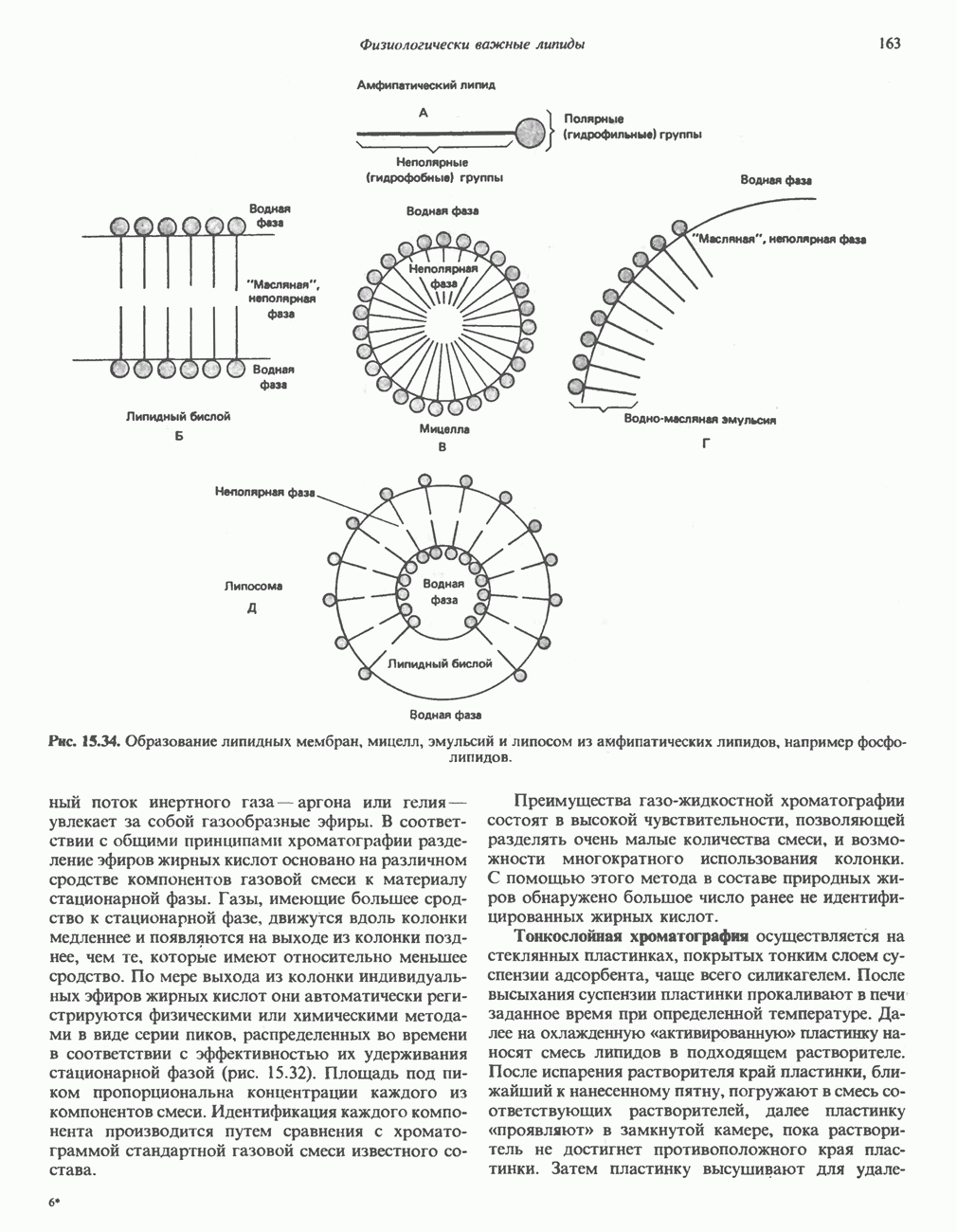
- АМФИПАТИЧЕСКИЕ ЛИПИДЫ
- Глава 16. Промежуточный обмен
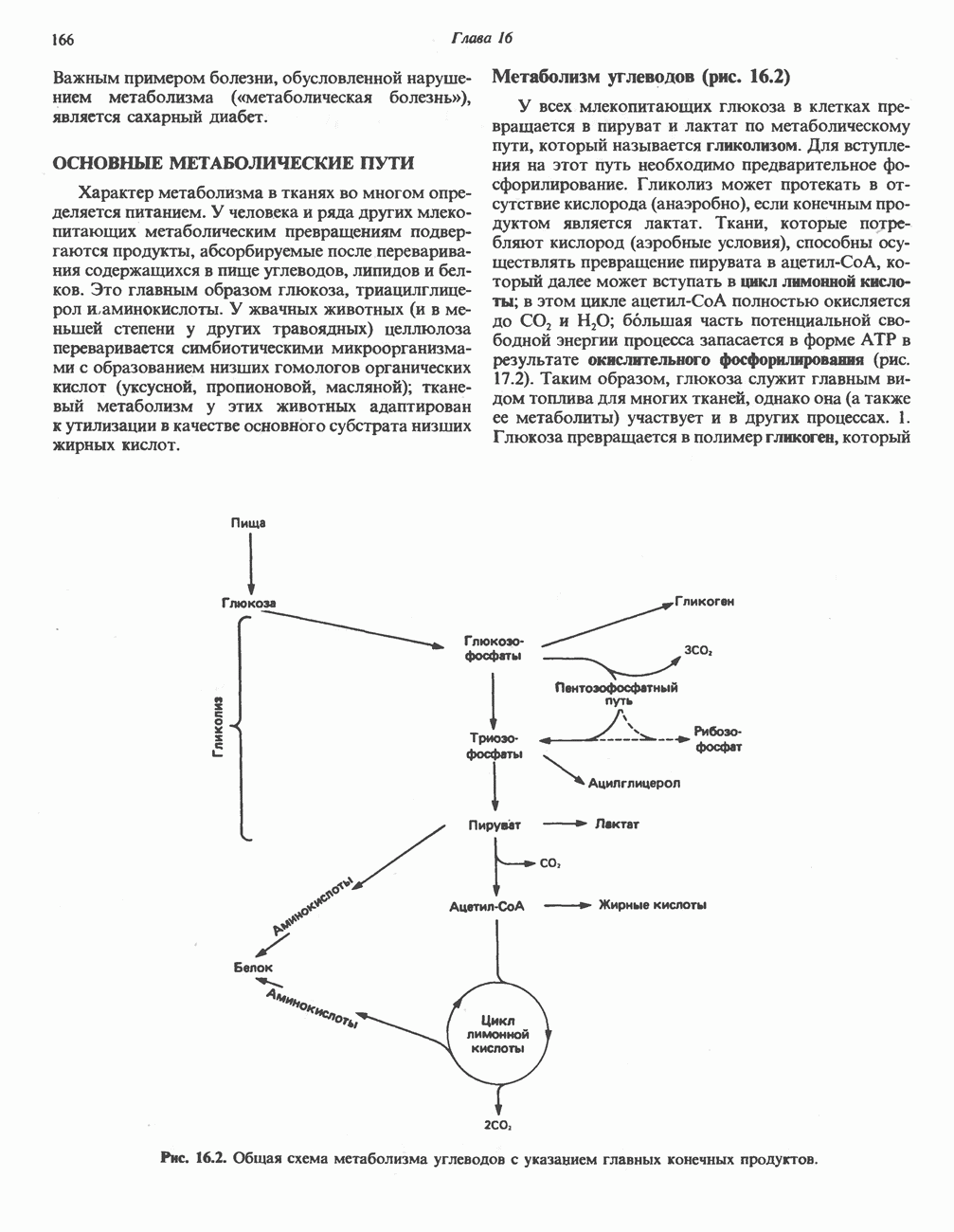
- ОСНОВНЫЕ МЕТАБОЛИЧЕСКИЕ ПУТИ
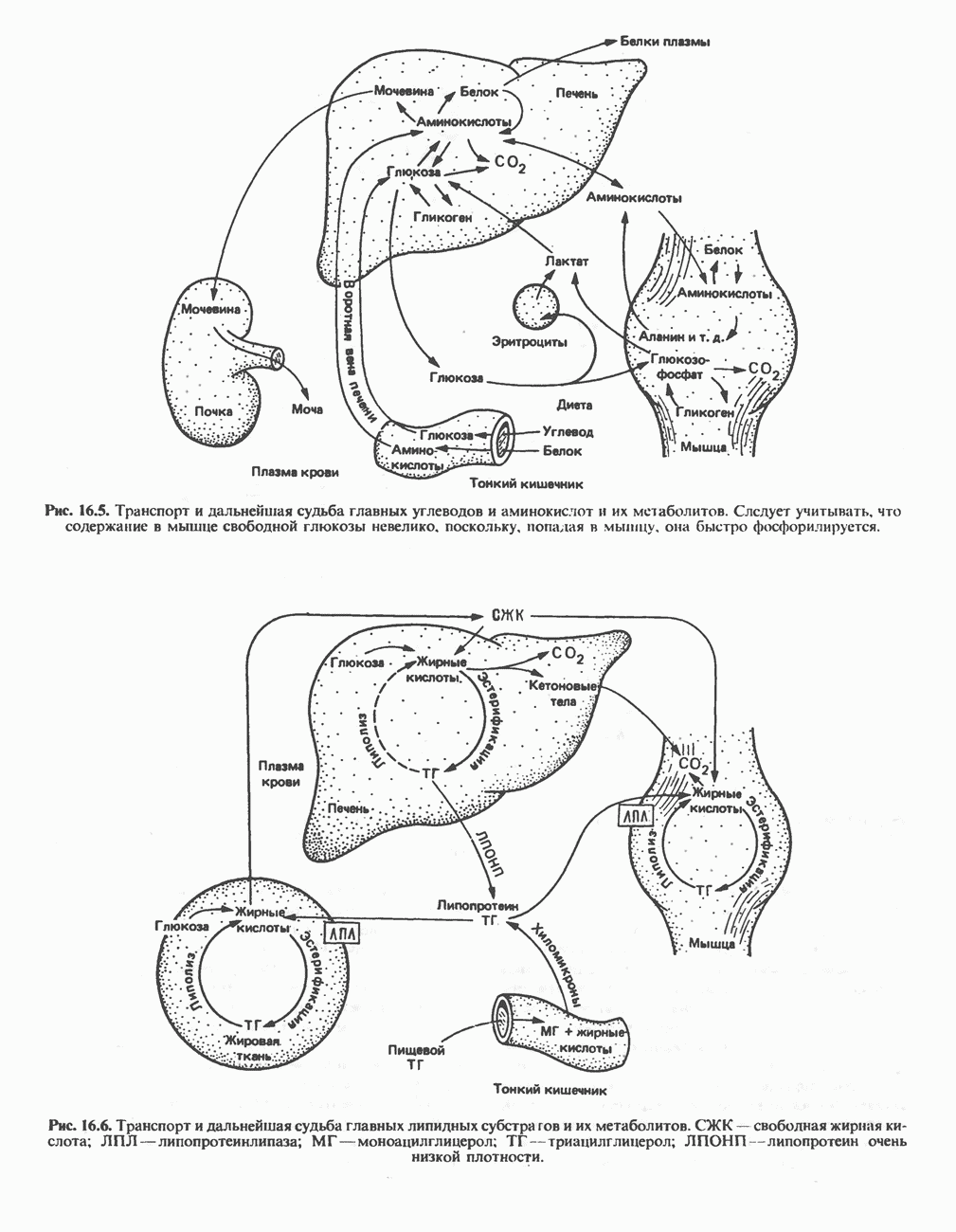
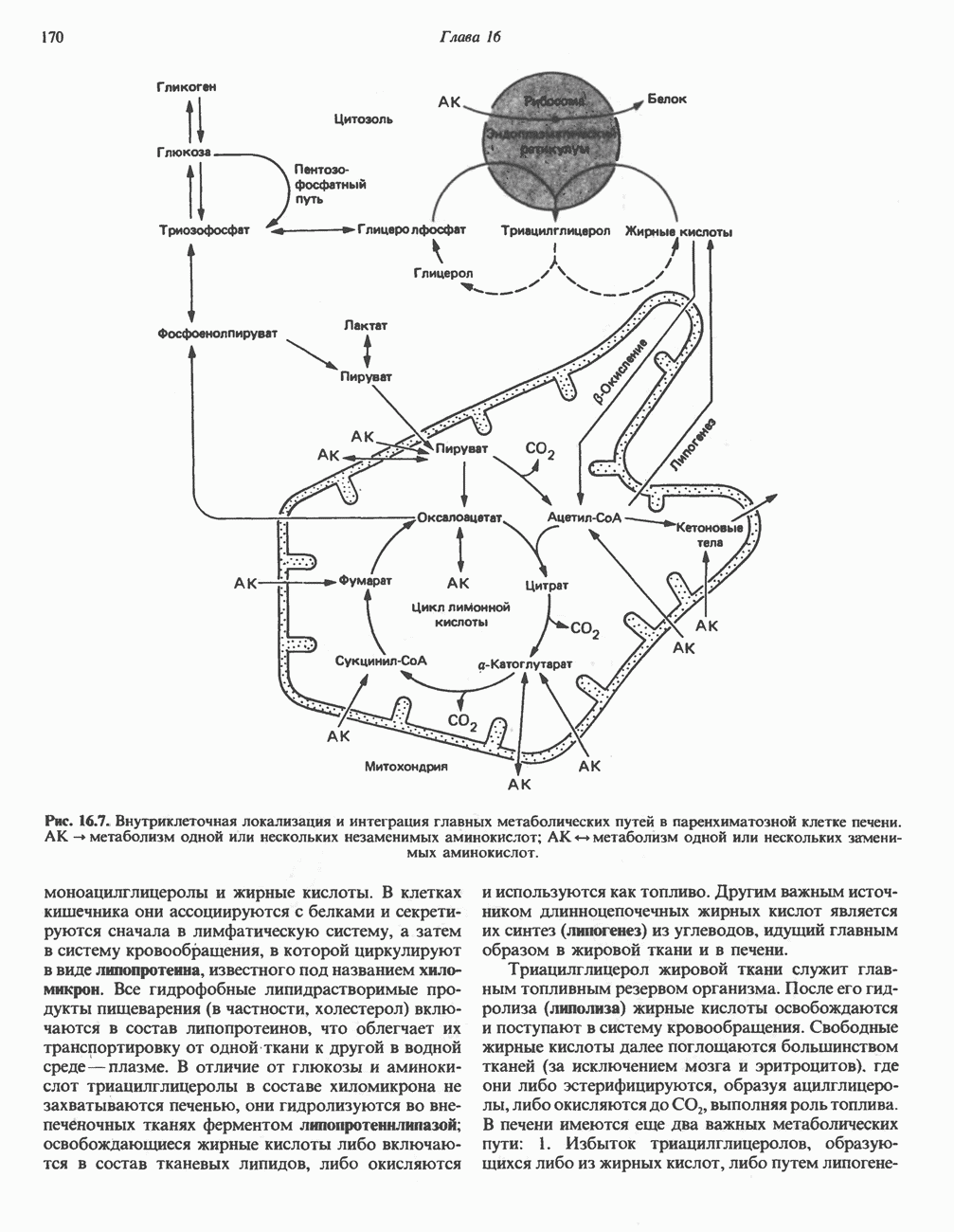
- ЛОКАЛИЗАЦИЯ МЕТАБОЛИЧЕСКИХ ПУТЕЙ
- Глава 17. Цикл лимонной кислоты: катаболизм ацетил-СоА
- КАТАБОЛИЧЕСКАЯ РОЛЬ ЦИКЛА ЛИМОННОЙ КИСЛОТЫ
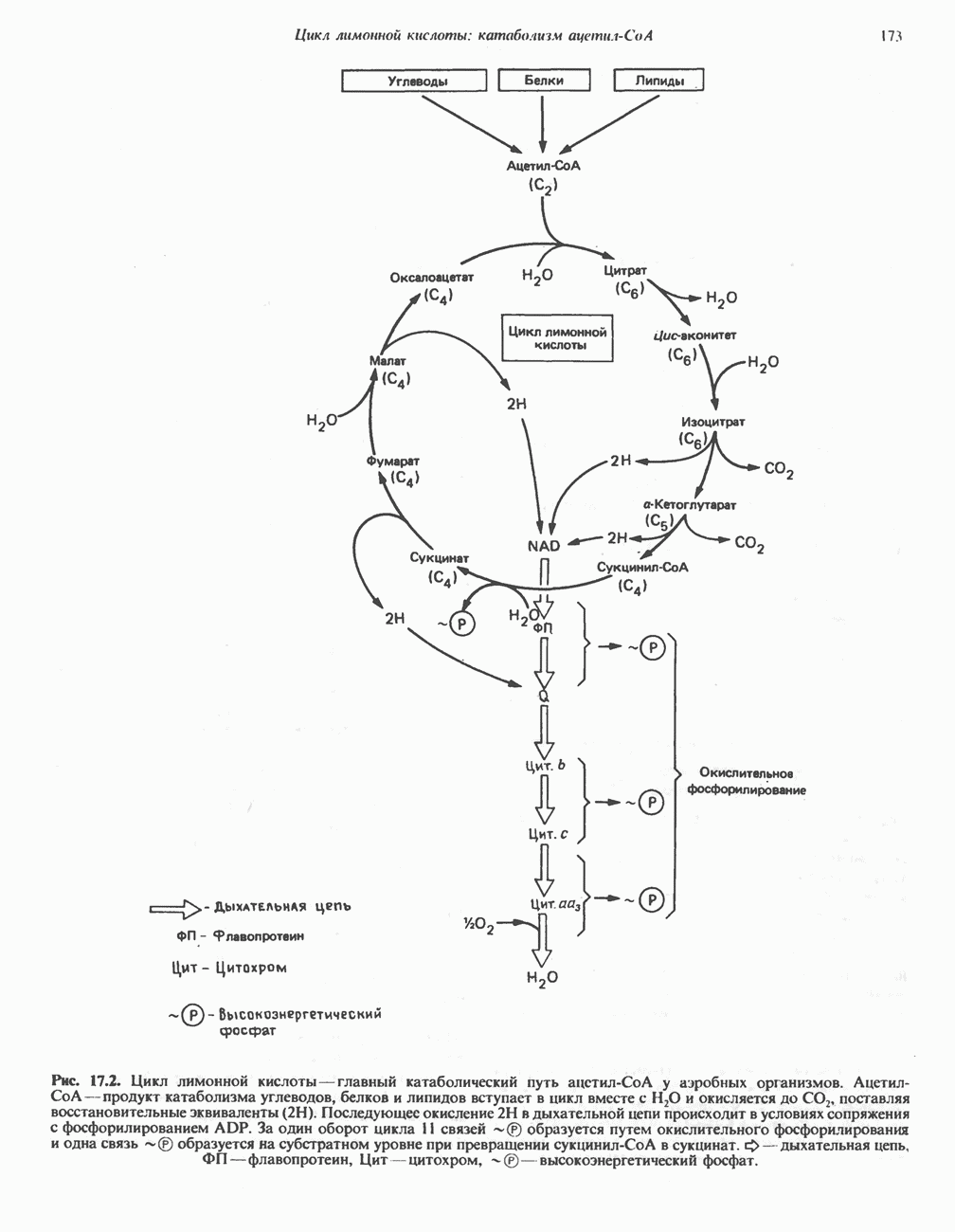
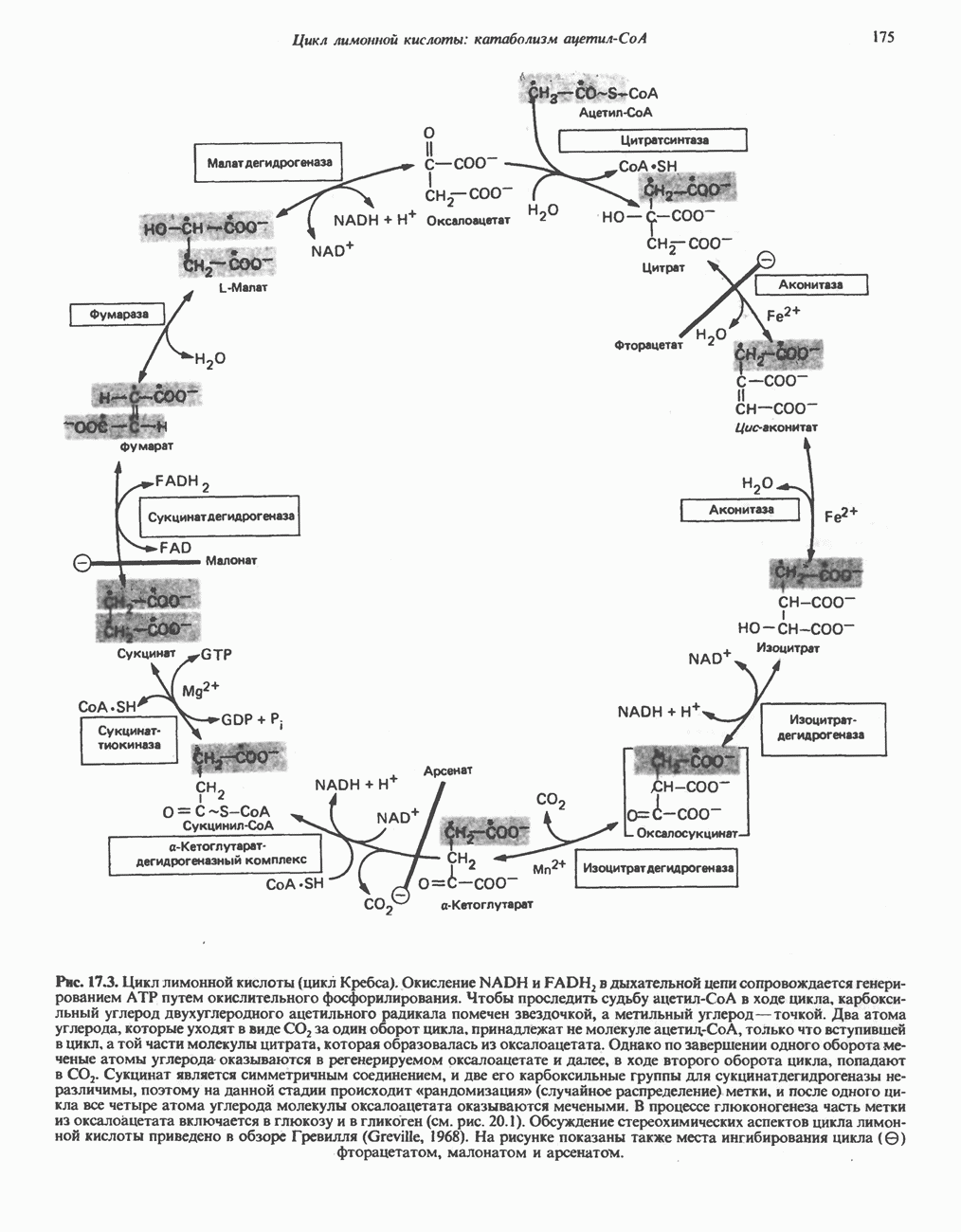
- РЕАКЦИИ ЦИКЛА ЛИМОННОЙ КИСЛОТЫ (рис. 17.3)
- ЭНЕРГЕТИКА ЦИКЛА ЛИМОННОЙ КИСЛОТЫ
- РОЛЬ ВИТАМИНОВ В ЦИКЛЕ ЛИМОННОЙ КИСЛОТЫ
- АМФИБОЛИЧЕСКАЯ РОЛЬ ЦИКЛА ЛИМОННОЙ КИСЛОТЫ
- Глава 18. Гликолиз и окисление пирувата
- ГЛИКОЛИТИЧЕСКИЙ ПУТЬ
- ПОСЛЕДОВАТЕЛЬНЫЕ СТАДИИ ГЛИКОЛИЗА
- ОКИСЛЕНИЕ ПИРУВАТА В АЦЕТИЛ-СоА
- Глава 19. Метаболизм гликогена
- ГЛИКОГЕНЕЗ
- ГЛИКОГЕНОЛИЗ
- МЕХАНИЗМЫ КОНТРОЛЯ ГЛИКОГЕНОЛИЗА И ГЛИКОГЕНЕЗА
- БОЛЕЗНИ, СВЯЗАННЫЕ С НАКОПЛЕНИЕМ ГЛИКОГЕНА (ГЛИКОГЕНОЗЫ)
- Глава 20. Глюконеогенез и пентозофосфатный путь
- МЕТАБОЛИЧЕСКИЕ ПУТИ, УЧАСТВУЮЩИЕ В ГЛЮКОНЕОГЕНЕЗЕ (рис. 20.1)
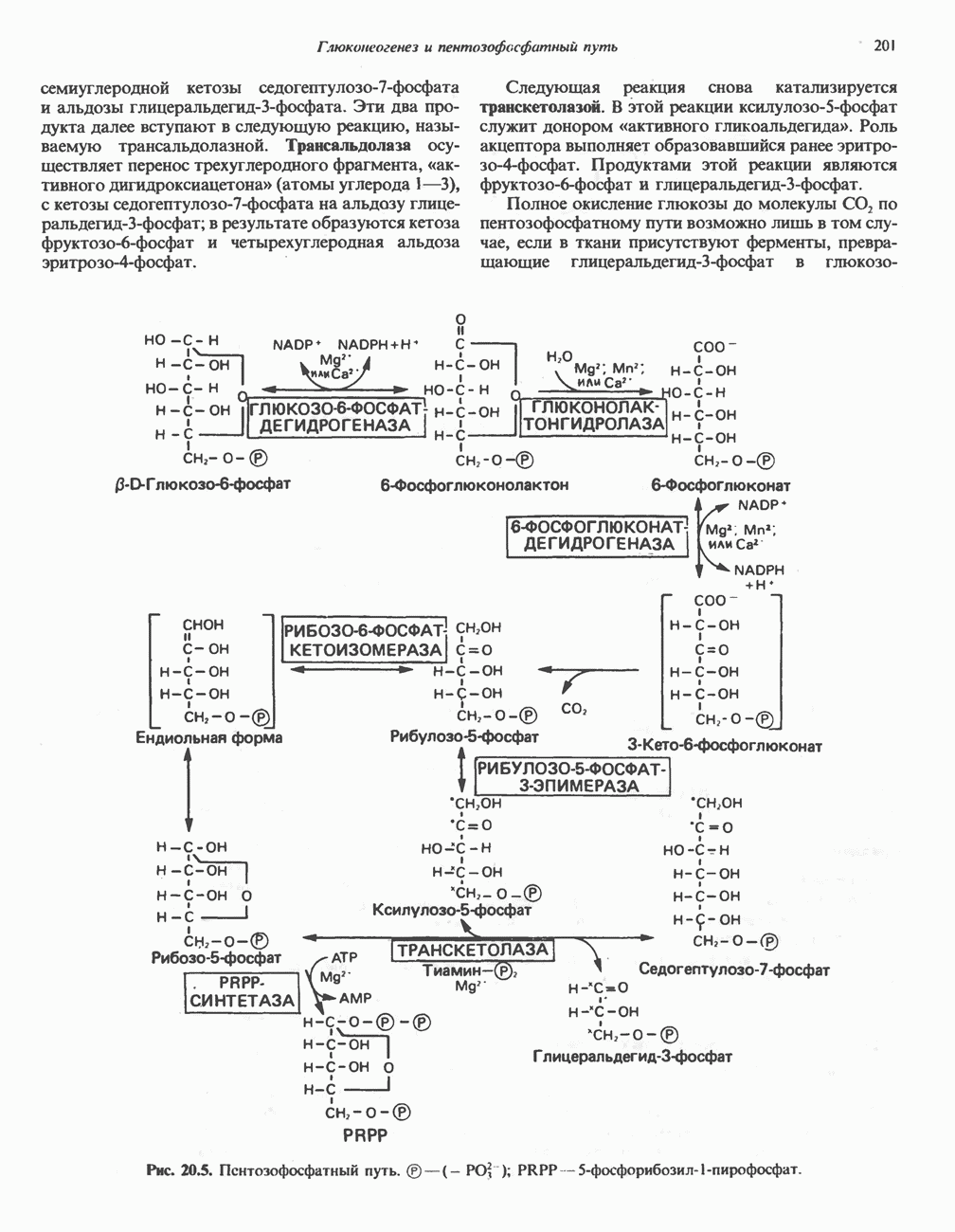
- ПЕНТОЗОФОСФАТНЫЙ ПУТЬ ИЛИ ГЕКСОЗОМОНОФОСФАТНЫЙ ШУНТ
- ПОСЛЕДОВАТЕЛЬНОСТЬ РЕАКЦИЙ
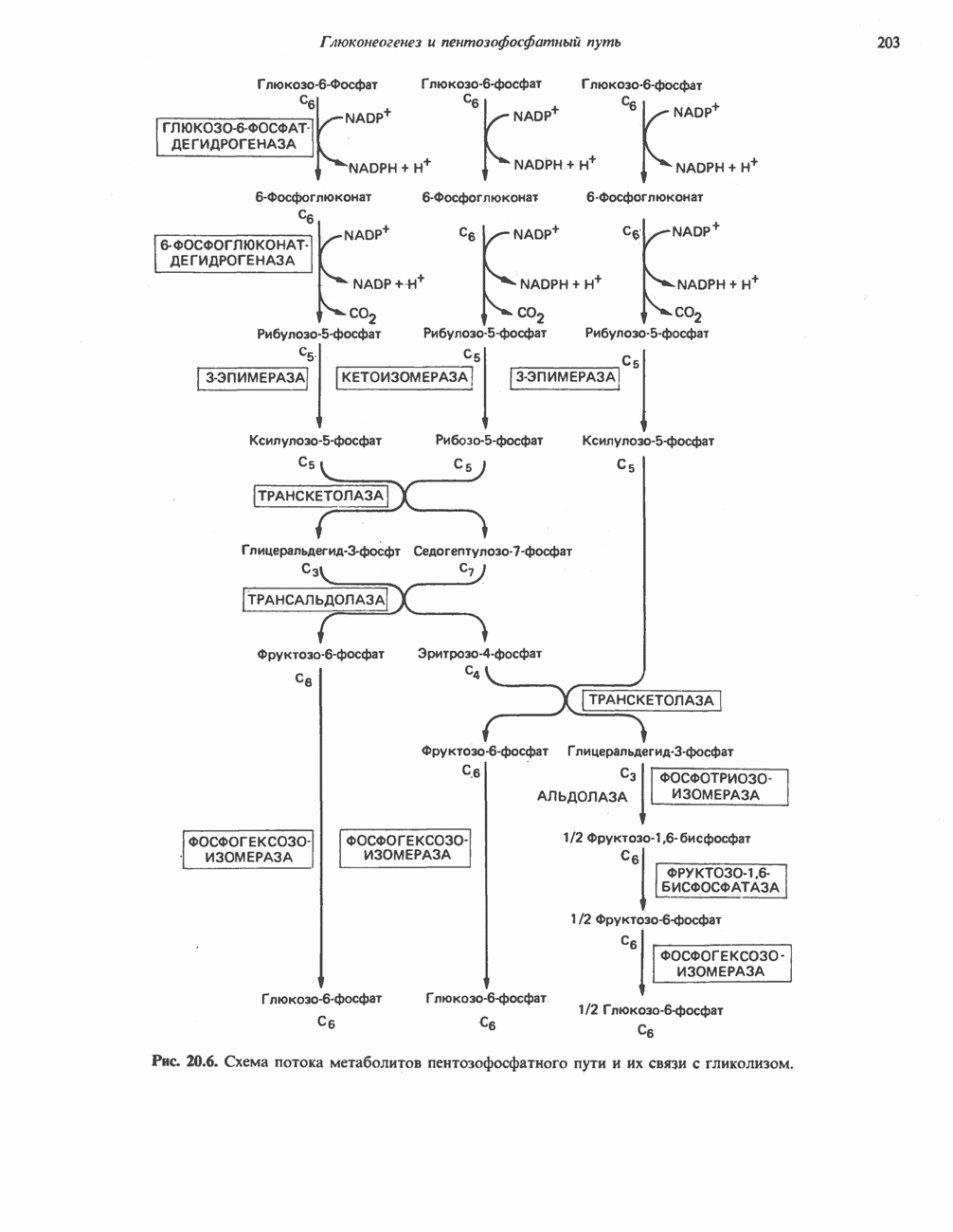
- МЕТАБОЛИЧЕСКОЕ ЗНАЧЕНИЕ ПЕНТОЗОФОСФАТНОГО ПУТИ
- КЛИНИЧЕСКИЕ АСПЕКТЫ
- Глава 21. Метаболизм наиболее важных гексоз
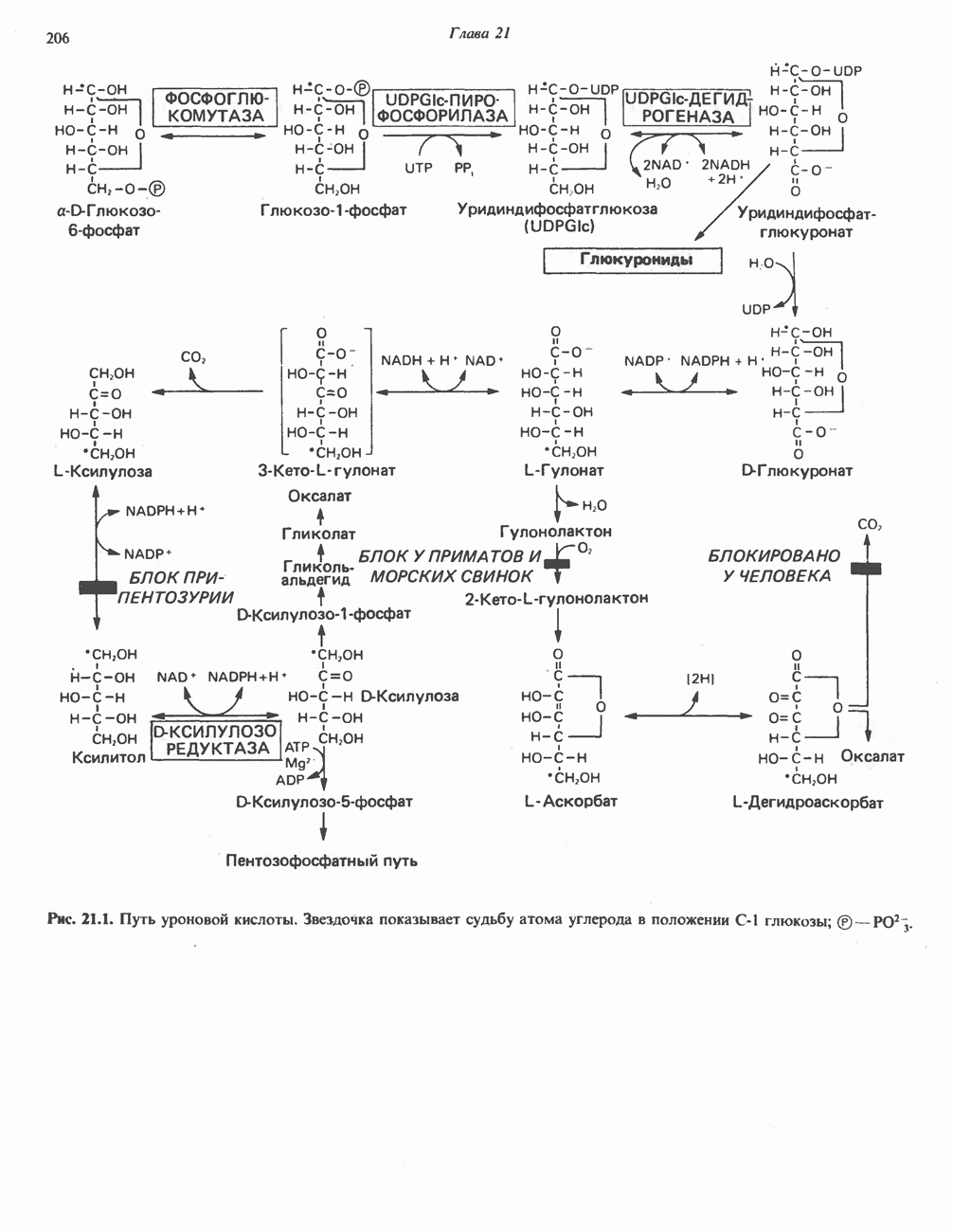
- ПУТЬ УРОНОВЫХ КИСЛОТ
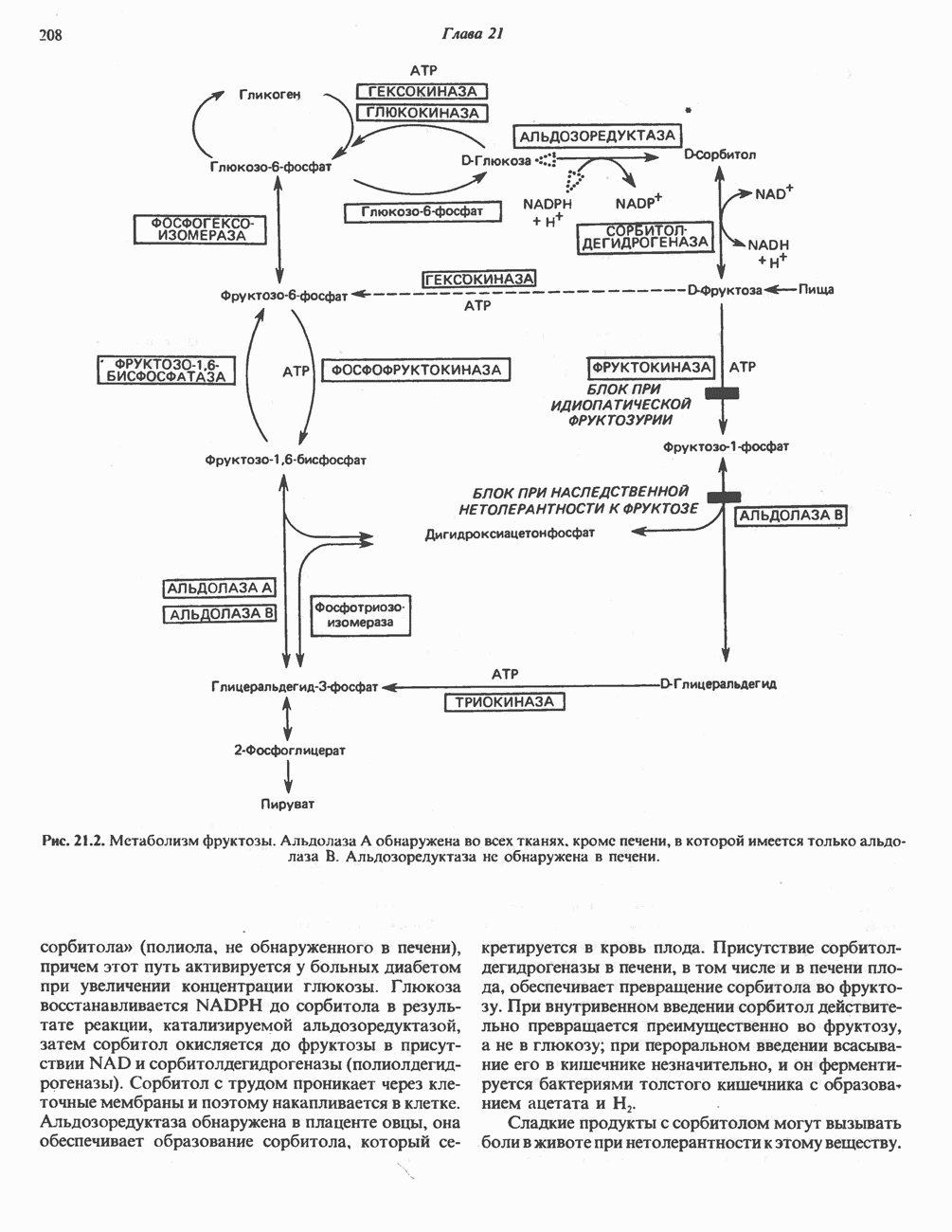
- МЕТАБОЛИЗМ ФРУКТОЗЫ
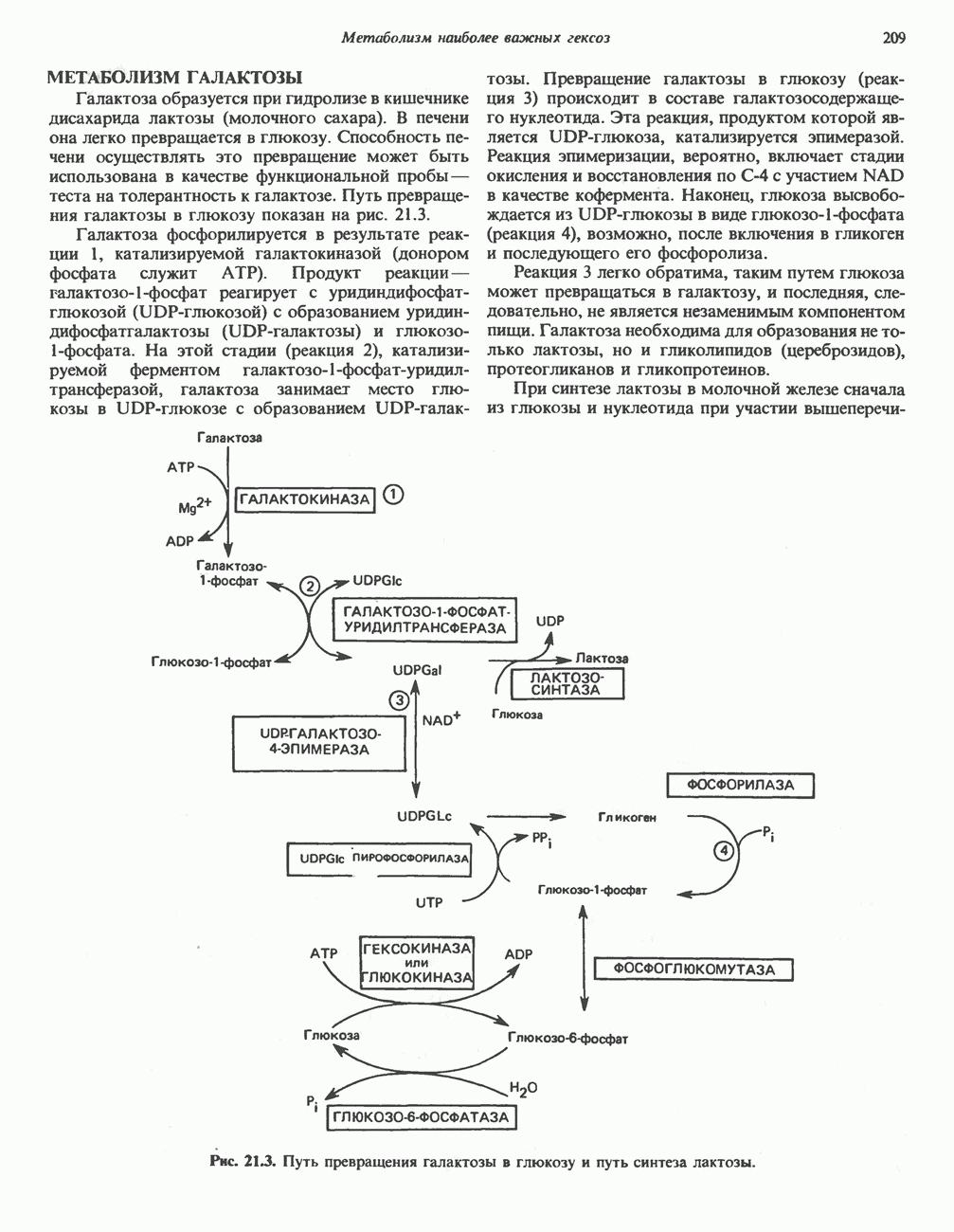
- МЕТАБОЛИЗМ ГАЛАКТОЗЫ
- Глава 22. Регуляция метаболизма углеводов
- ОБЩИЕ ПРИНЦИПЫ РЕГУЛЯЦИИ ПУТЕЙ МЕТАБОЛИЗМА
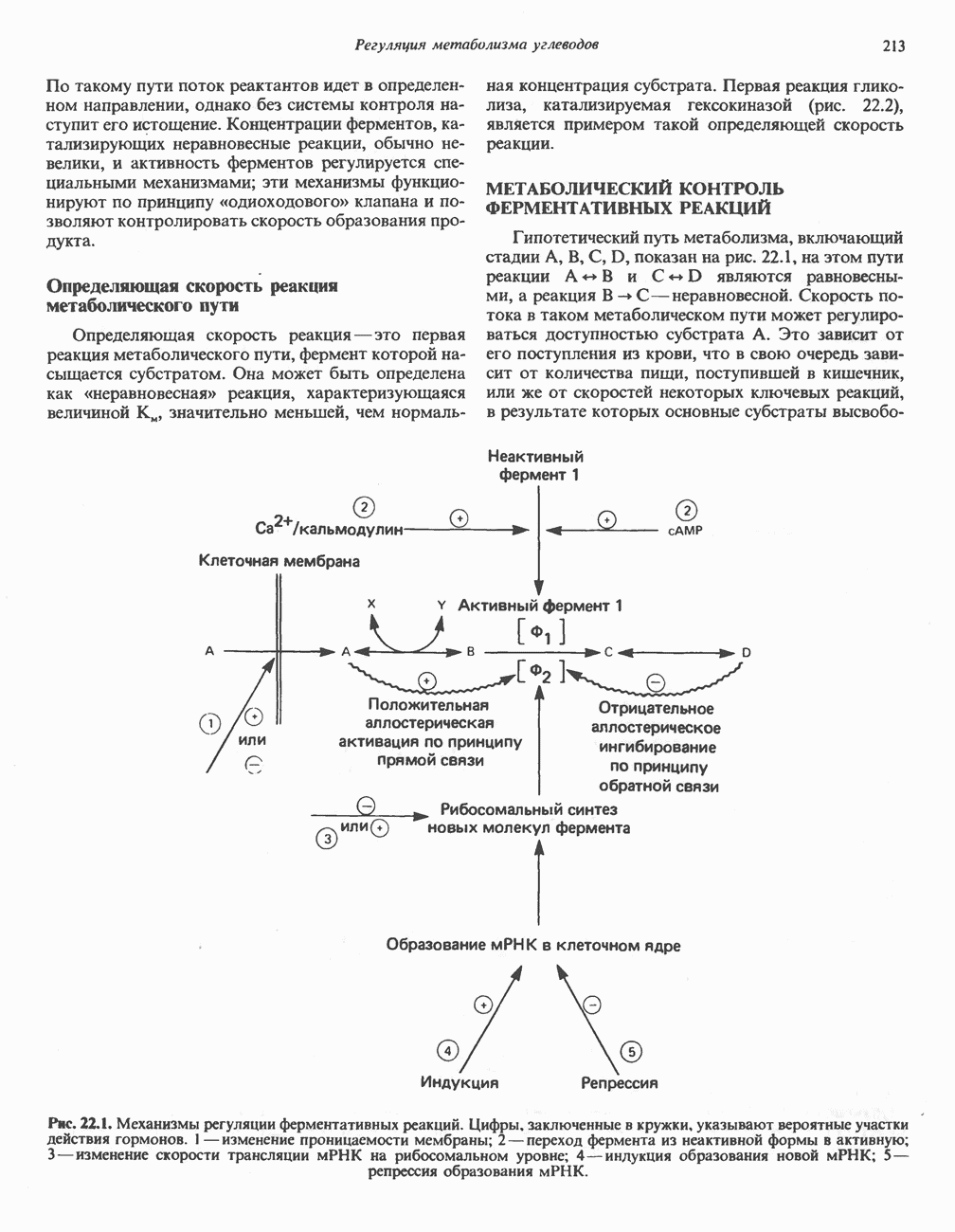
- МЕТАБОЛИЧЕСКИЙ КОНТРОЛЬ ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ
- РЕГУЛЯЦИЯ МЕТАБОЛИЗМА УГЛЕВОДОВ НА КЛЕТОЧНОМ И ФЕРМЕНТНОМ УРОВНЕ
- РЕГУЛЯЦИЯ ГЛИКОЛИЗА, ГЛЮКОНЕОГЕНЕЗА И ПЕНТОЗОФОСФАТНОГО ПУТИ
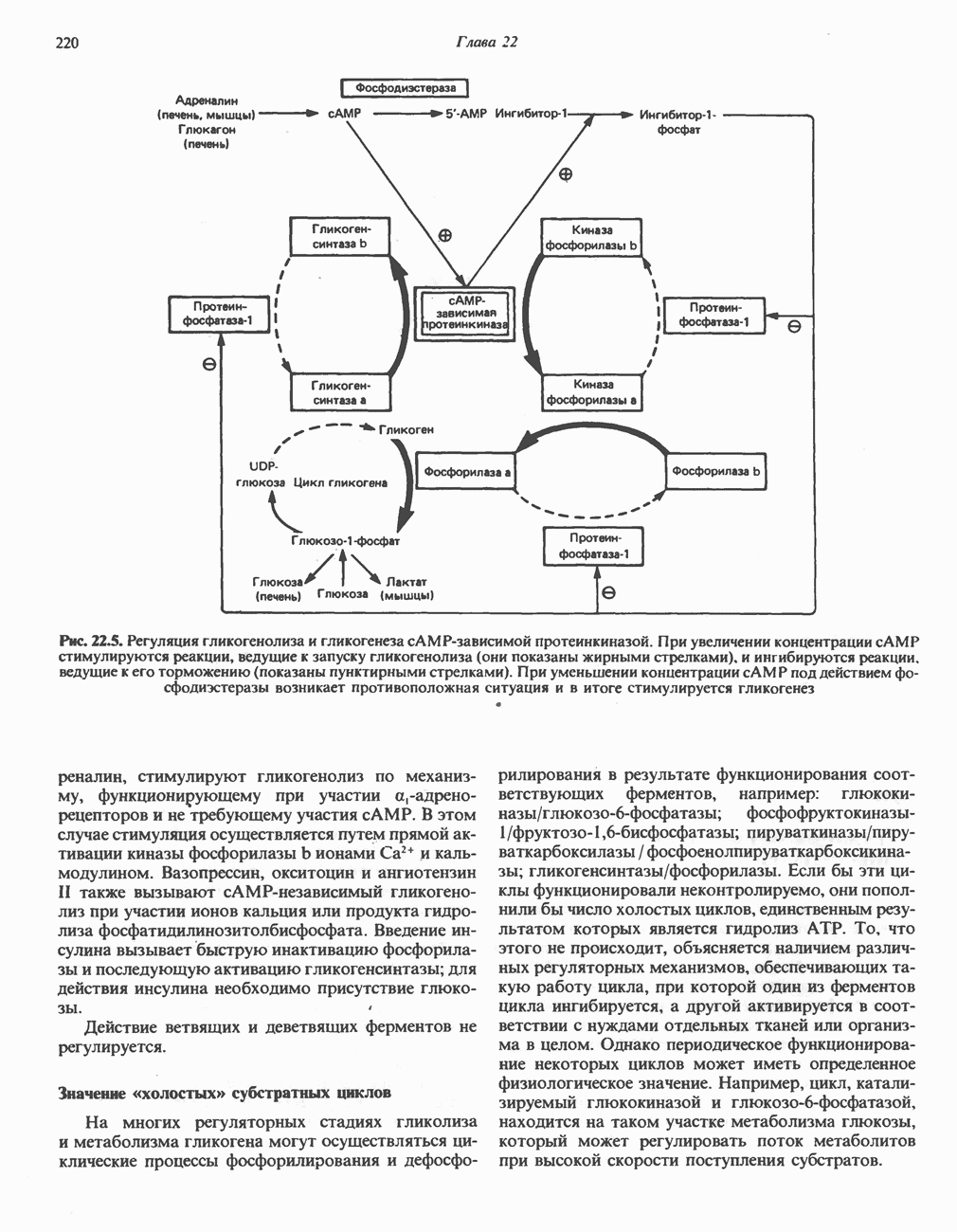
- РЕГУЛЯЦИЯ МЕТАБОЛИЗМА ГЛИКОГЕНА (РИС. 22.5)
- РЕГУЛЯЦИЯ ЦИКЛА ЛИМОННОЙ КИСЛОТЫ (СМ. РИС. 18.3)
- РЕГУЛЯЦИЯ УРОВНЯ ГЛЮКОЗЫ В КРОВИ
- Глава 23. Окисление и биосинтез жирных кислот
- ОКИСЛЕНИЕ ЖИРНЫХ КИСЛОТ
- БИОСИНТЕЗ НАСЫЩЕННЫХ ЖИРНЫХ КИСЛОТ
- Глава 24. Метаболизм ненасыщенных жирных кислот и эйкозаноидов
- МЕТАБОЛИЗМ НЕНАСЫЩЕННЫХ ЖИРНЫХ КИСЛОТ
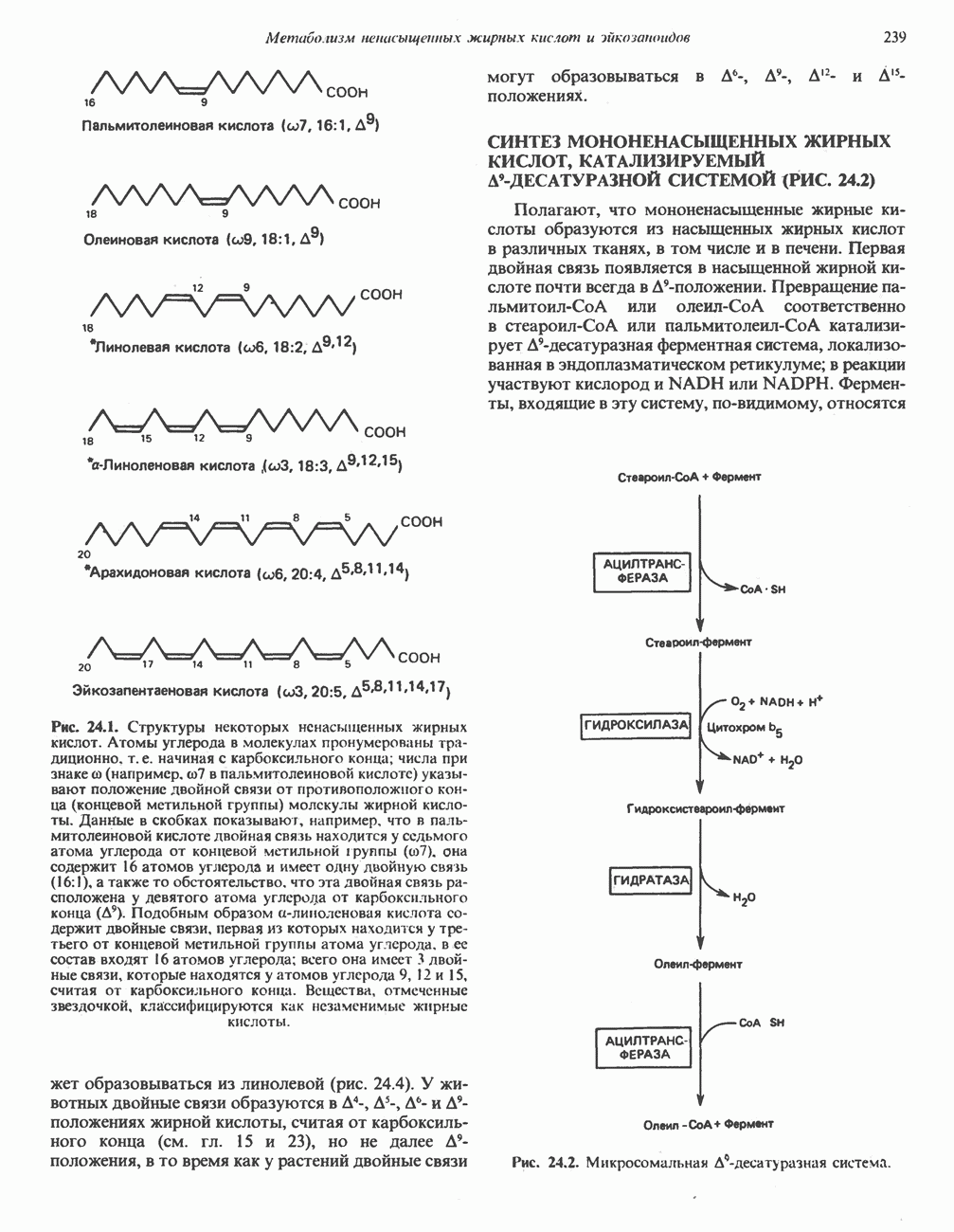
- СИНТЕЗ МОНОНЕНАСЫЩЕННЫХ ЖИРНЫХ КИСЛОТ, КАТАЛИЗИРУЕМЫЙ Д9-ДЕСАТУРАЗНОЙ СИСТЕМОЙ (РИС. 24.2)
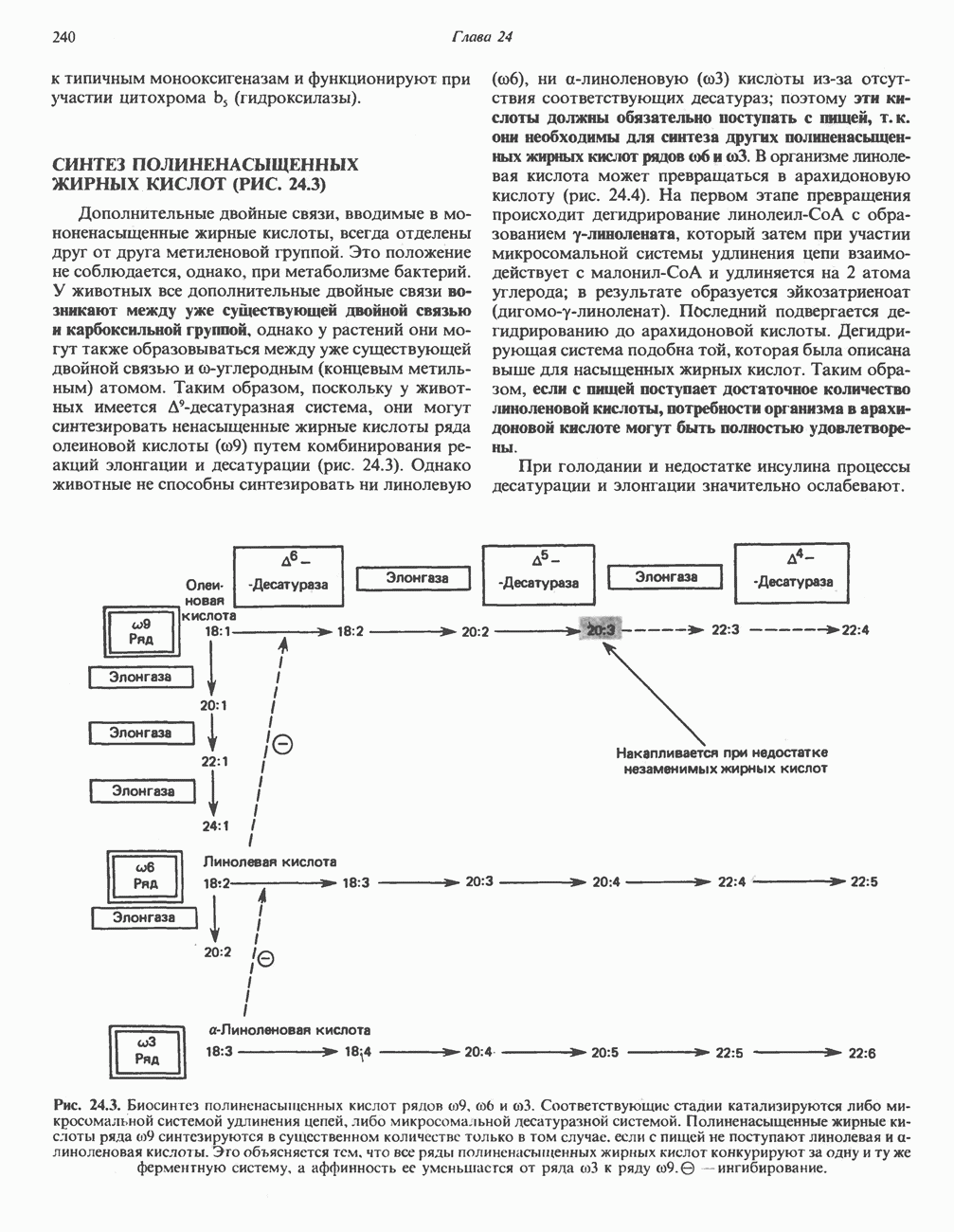
- СИНТЕЗ ПОЛИНЕНАСЫЩЕННЫХ ЖИРНЫХ КИСЛОТ (РИС. 24.3)
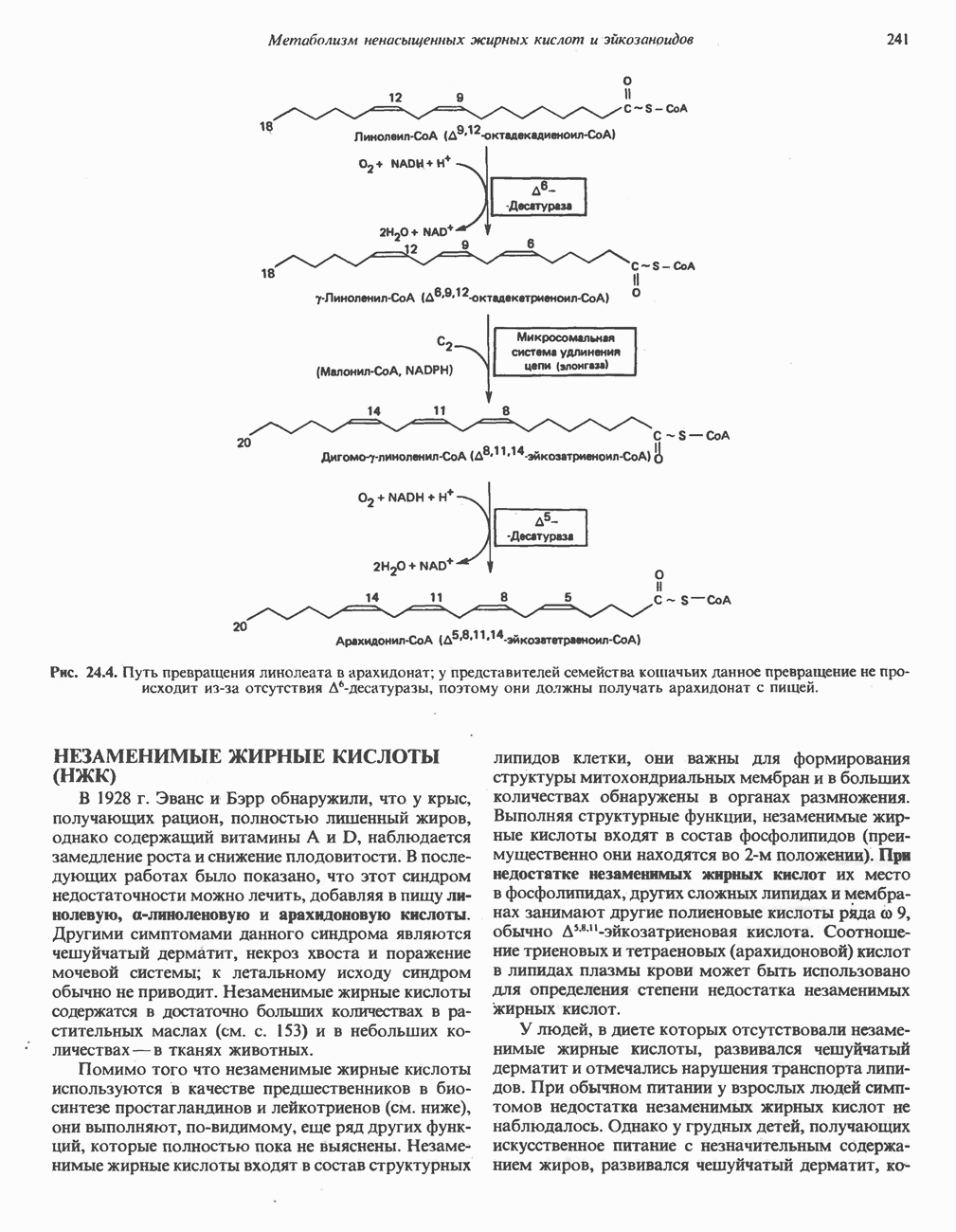
- НЕЗАМЕНИМЫЕ ЖИРНЫЕ КИСЛОТЫ (НЖК)
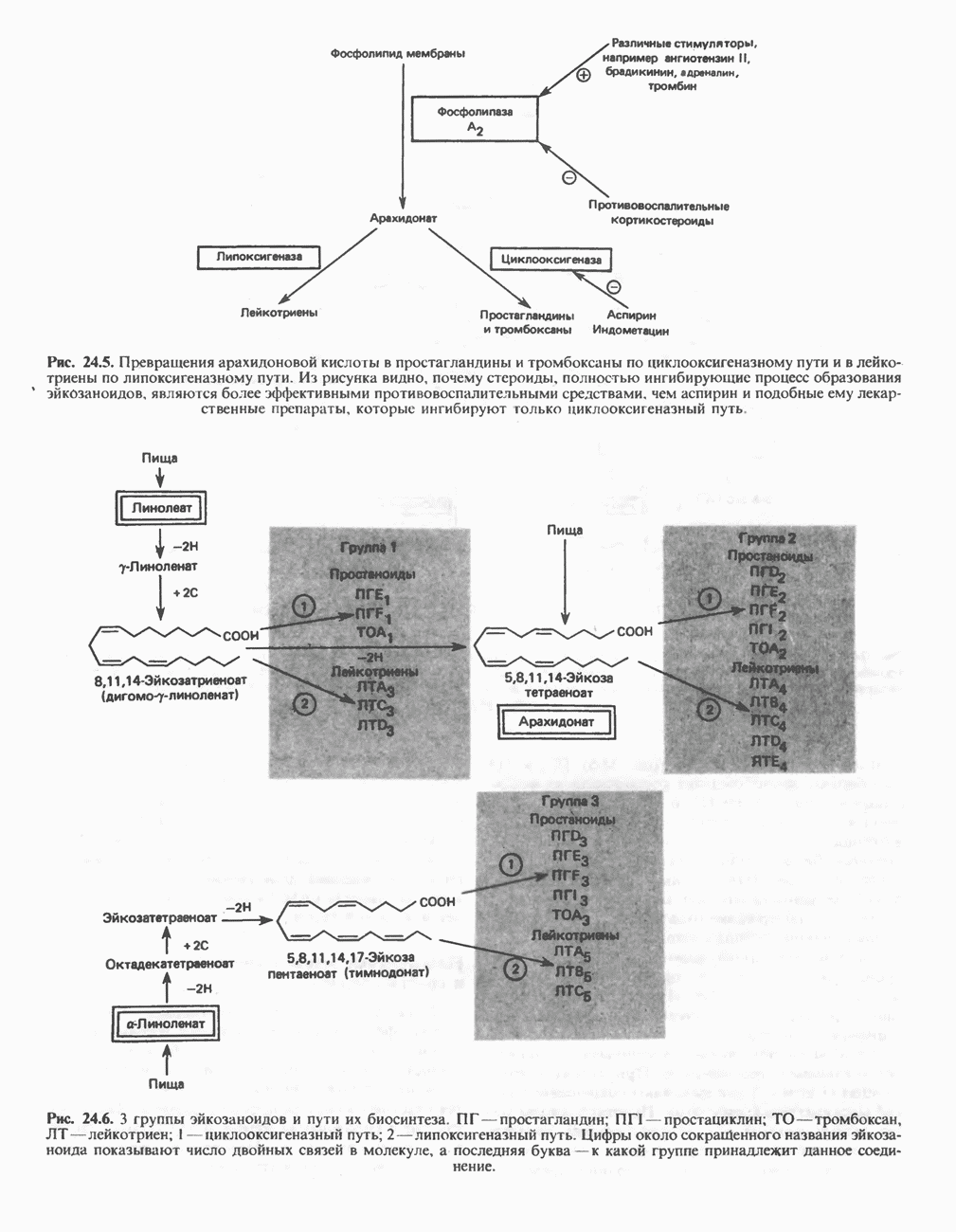
- ЭЙКОЗАНОИДЫ
- ПРОСТАНОИДЫ
- ЛЕЙКОТРИЕНЫ
- Глава 25. Метаболизм ацилглицеролов и сфинголипидов
- МЕТАБОЛИЗМ АЦИЛГЛИЦЕРОЛОВ
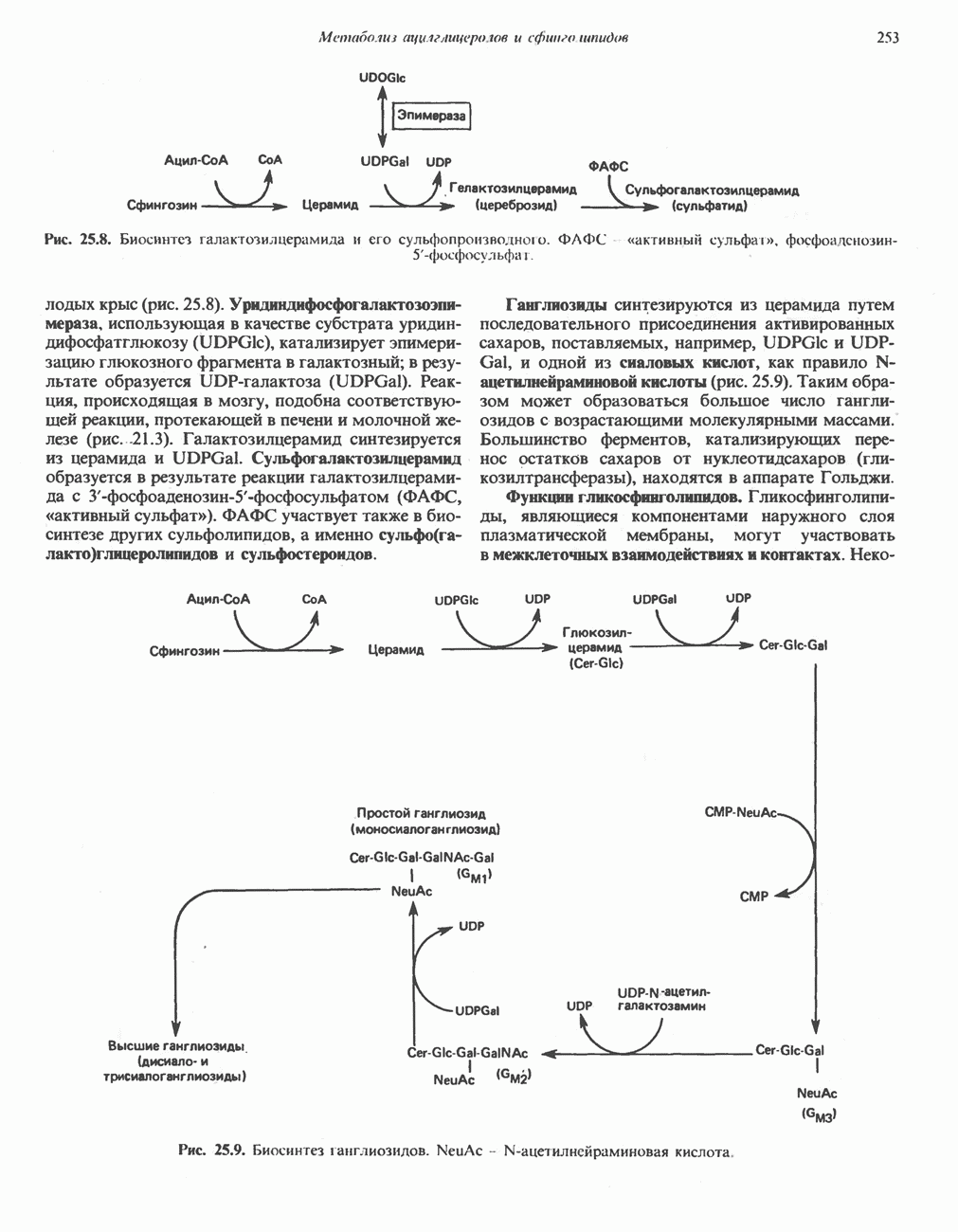
- МЕТАБОЛИЗМ СФИНГОЛИПИДОВ
- ГЛИКОЛИПИДЫ
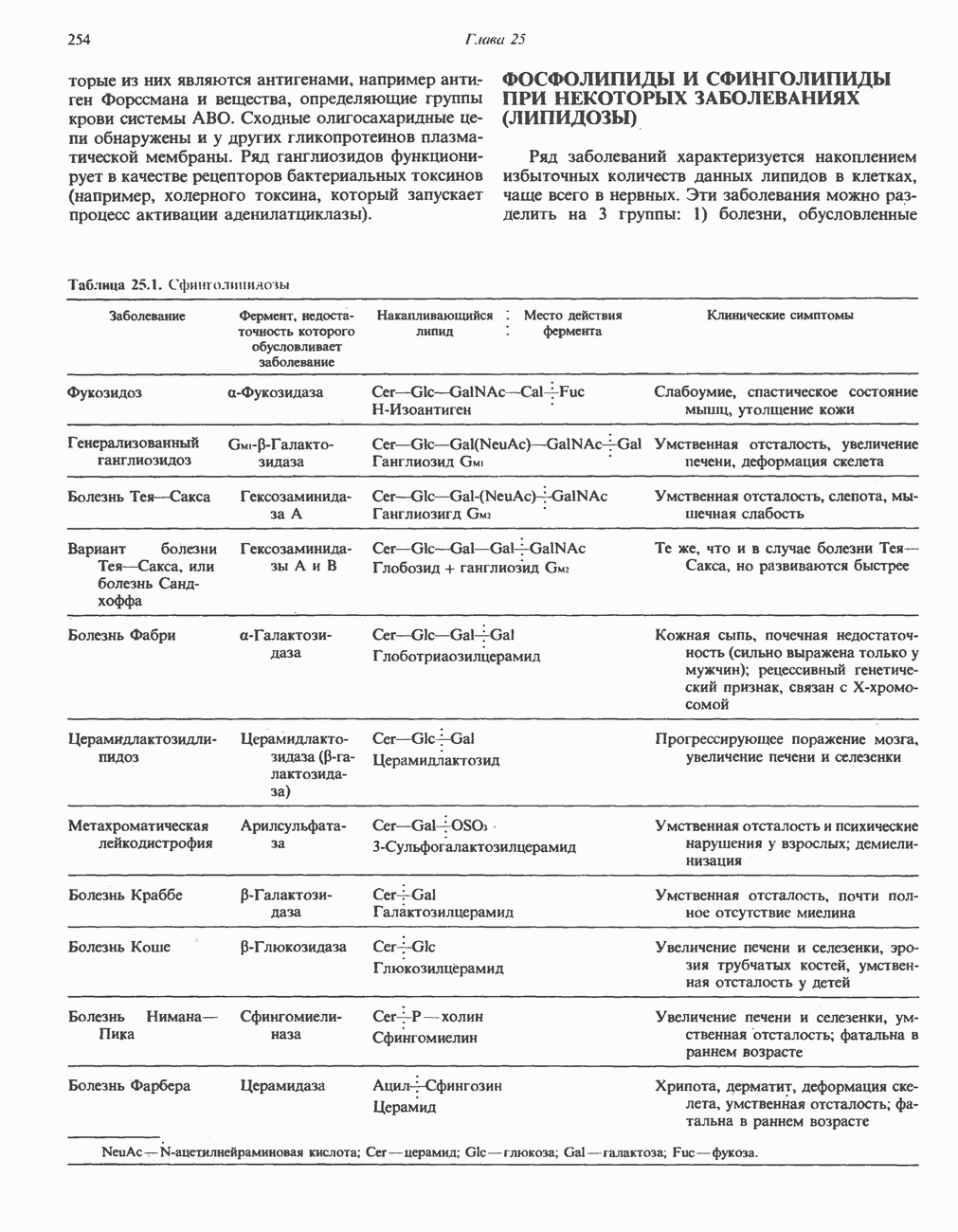
- ФОСФОЛИПИДЫ И СФИНГОЛИПИДЫ ПРИ НЕКОТОРЫХ ЗАБОЛЕВАНИЯХ (ЛИПИДОЗЫ)
- Глава 26. Транспорт и запасание липидов
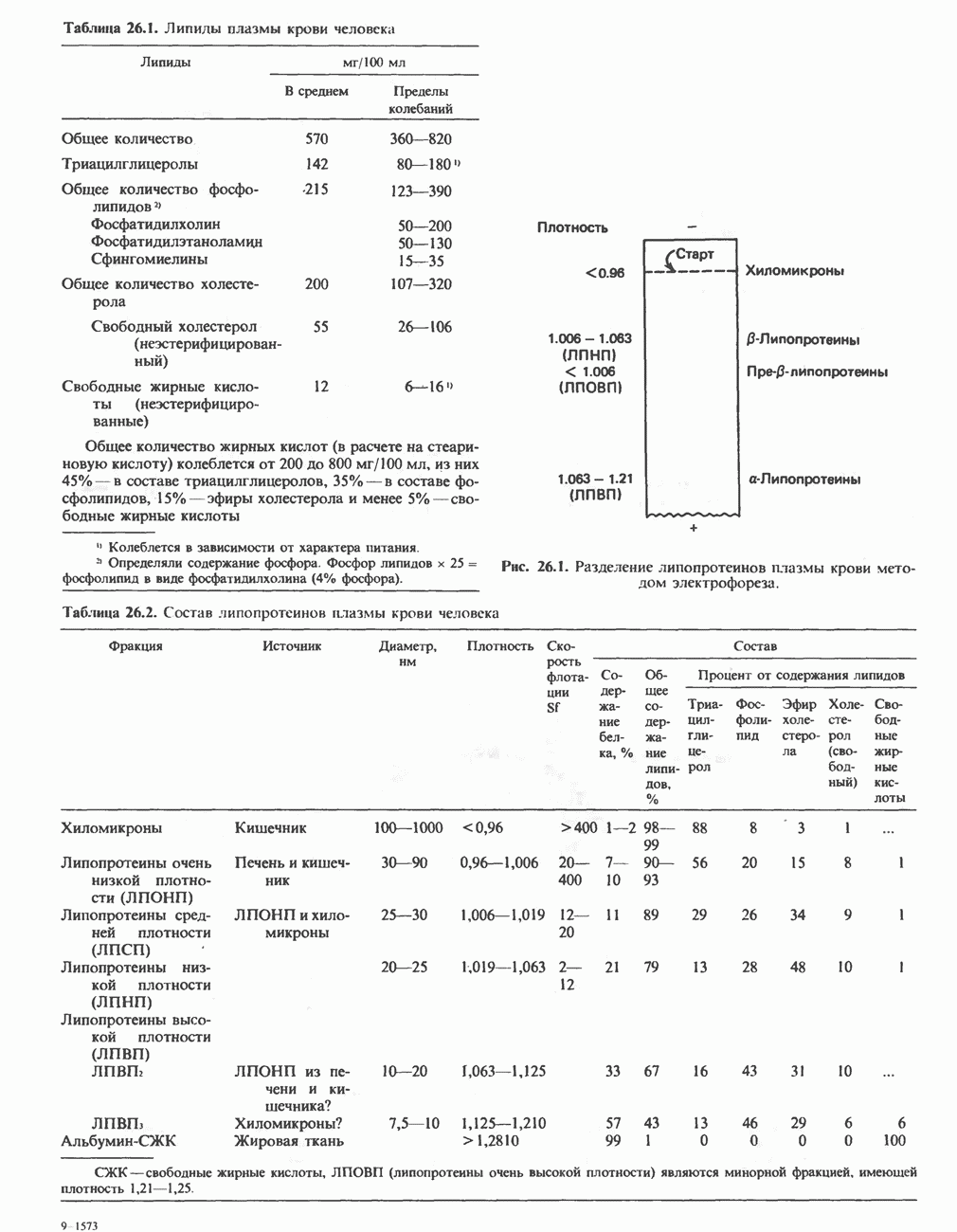
- ЛИПИДЫ ПЛАЗМЫ КРОВИ И ЛИПОПРОТЕИНЫ
- МЕТАБОЛИЗМ ЛИПОПРОТЕИНОВ ПЛАЗМЫ КРОВИ
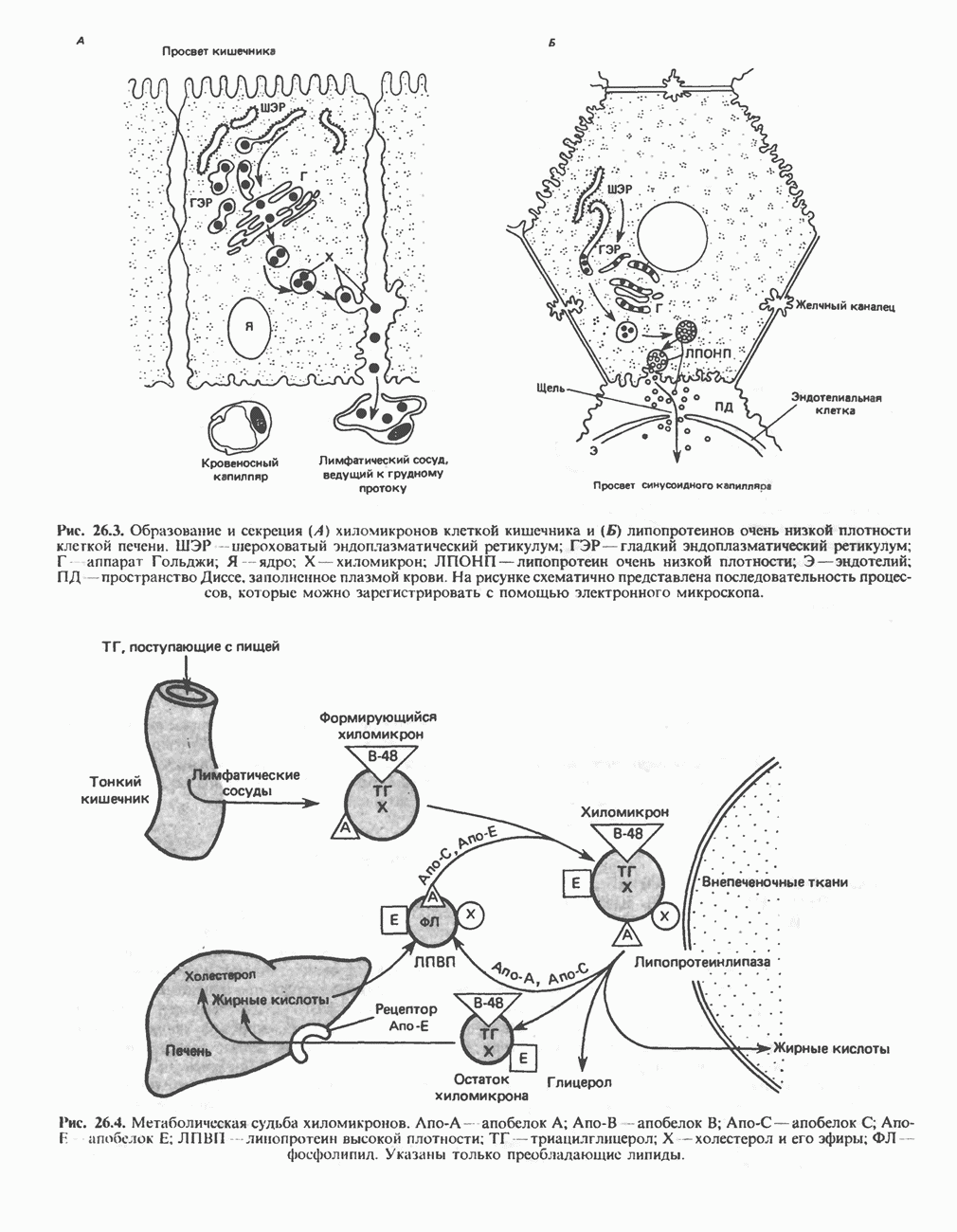
- ОБРАЗОВАНИЕ ХИЛОМИКРОНОВ И ЛИПОПРОТЕИНОВ ОЧЕНЬ НИЗКОЙ ПЛОТНОСТИ (ЛПОНП)
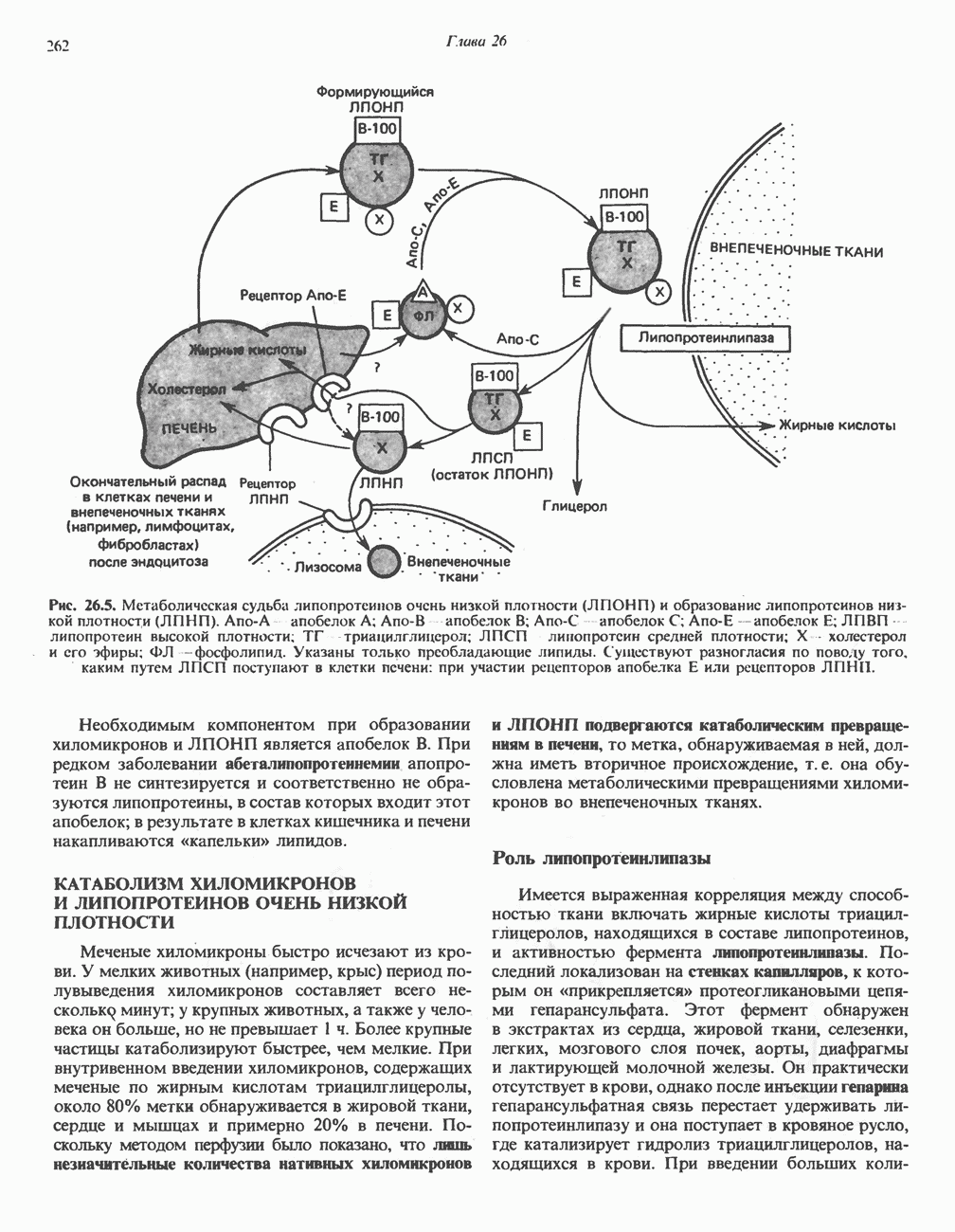
- КАТАБОЛИЗМ ХИЛОМИКРОНОВ И ЛИПОПРОТЕИНОВ ОЧЕНЬ НИЗКОЙ ПЛОТНОСТИ
- МЕТАБОЛИЗМ ЛПНП
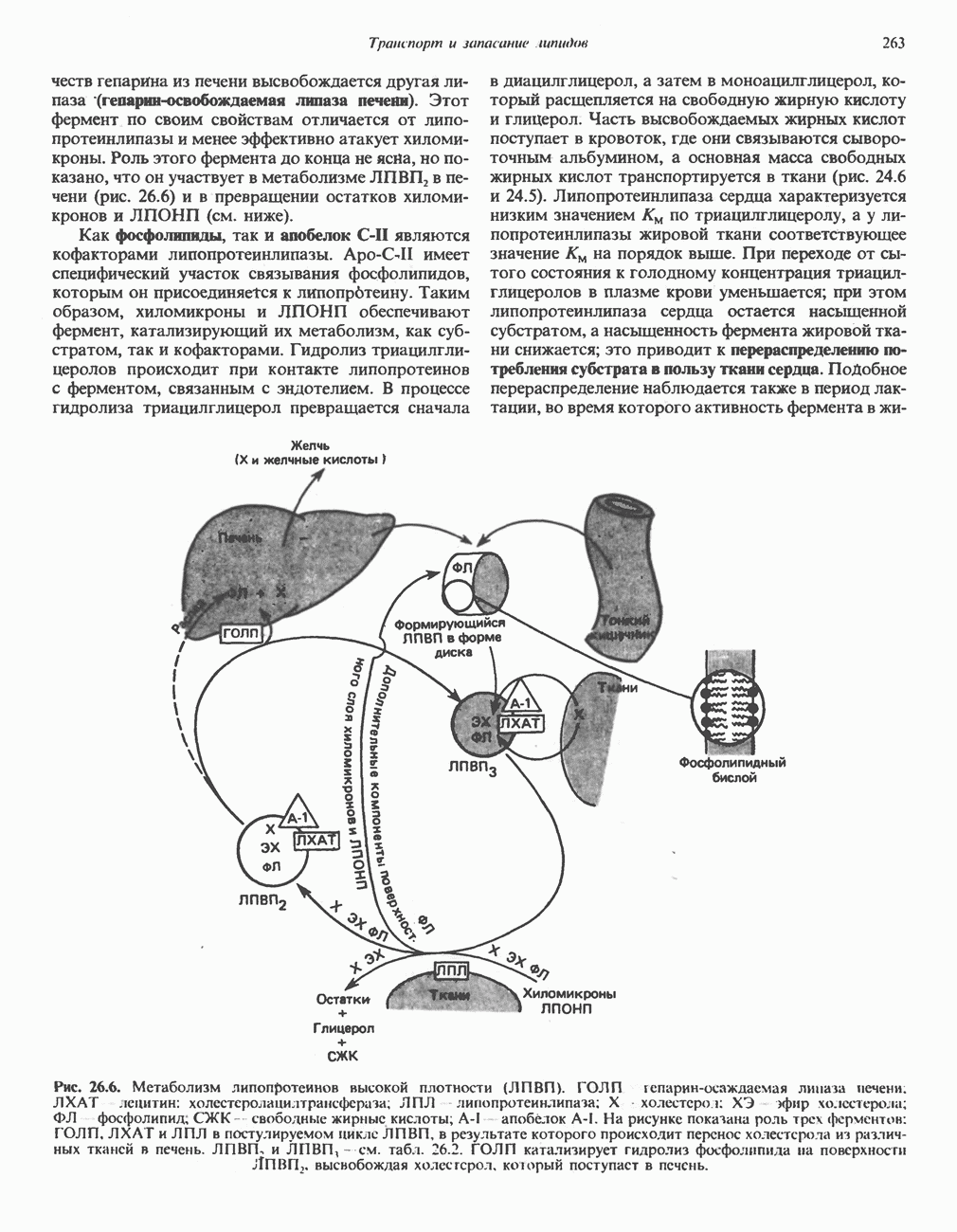
- МЕТАБОЛИЗМ ЛПВП (рис. 26.6)
- РОЛЬ ПЕЧЕНИ В ТРАНСПОРТЕ И МЕТАБОЛИЗМЕ ЛИПИДОВ
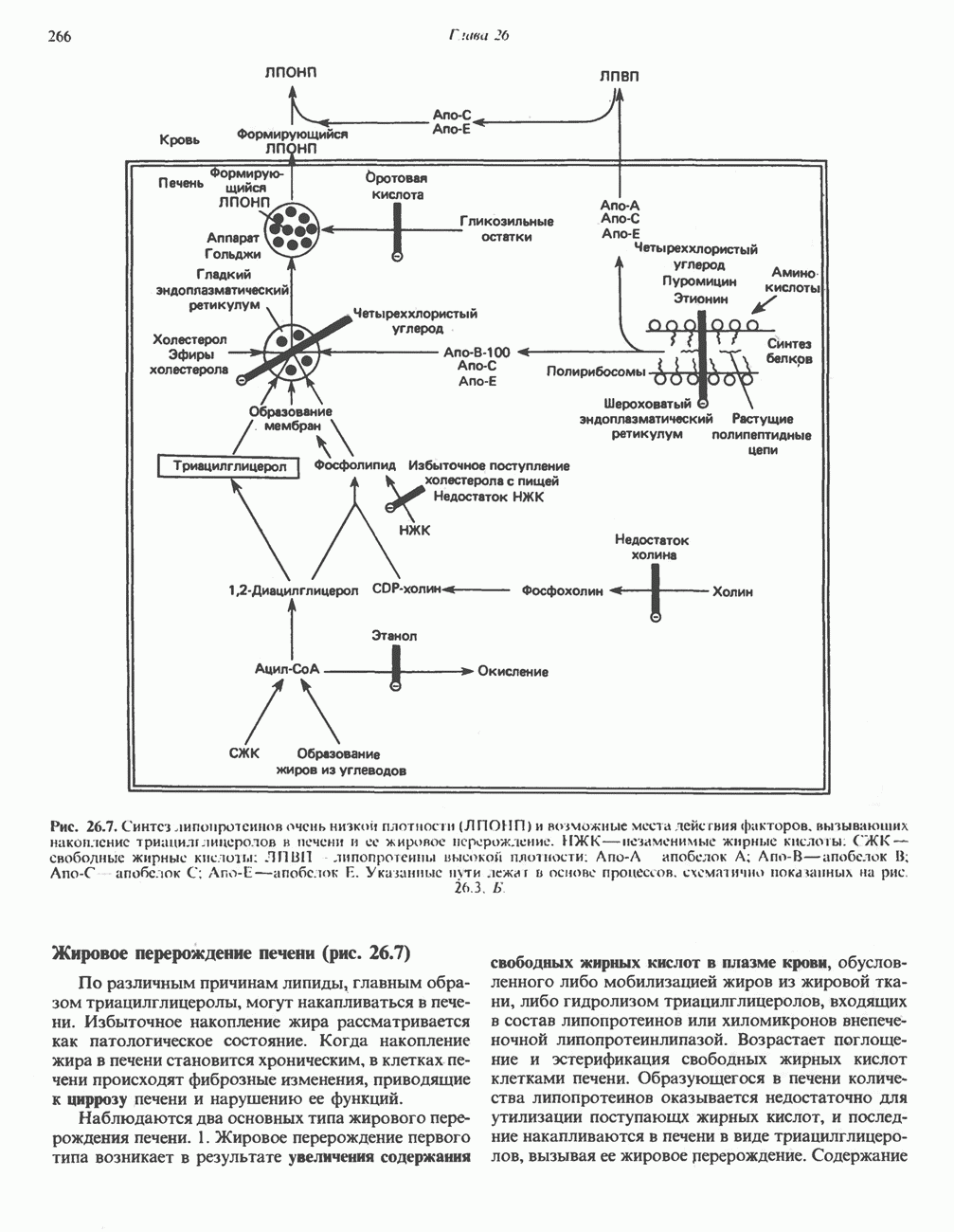
- СИНТЕЗ ТРИАЦИЛГЛИЦЕРОЛОВ И ОБРАЗОВАНИЕ ЛПОНП (рис. 26.7)
- МЕТАБОЛИЧЕСКИЕ ПРЕВРАЩЕНИЯ В ЖИРОВОЙ ТКАНИ И МОБИЛИЗАЦИЯ ЖИРОВ
- РОЛЬ ГОРМОНОВ В МОБИЛИЗАЦИИ ЖИРОВ
- СРАВНИТЕЛЬНЫЕ АСПЕКТЫ
- РОЛЬ БУРОЙ ЖИРОВОЙ ТКАНИ В ТЕРМОГЕНЕЗЕ
- Глава 27. Синтез, транспорт и экскреция холестерола
- БИОСИНТЕЗ ХОЛЕСТЕРОЛА
- РЕГУЛЯЦИЯ СИНТЕЗА ХОЛЕСТЕРОЛА
- ТРАНСПОРТ ХОЛЕСТЕРОЛА
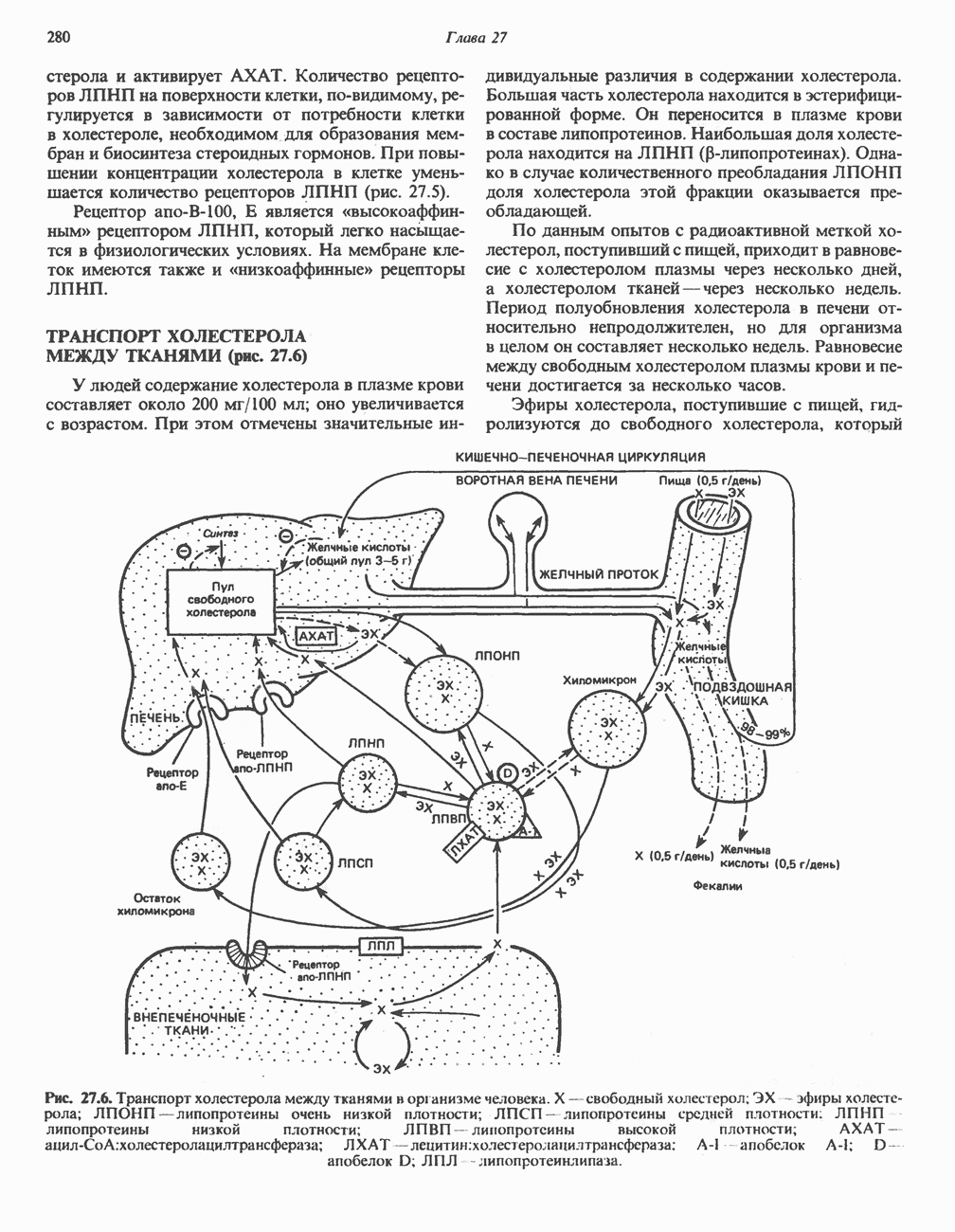
- ТРАНСПОРТ ХОЛЕСТЕРОЛА МЕЖДУ ТКАНЯМИ (рис. 27.6)
- ВЫВЕДЕНИЕ ХОЛЕСТЕРОЛА И ОБРАЗОВАНИЕ СОЛЕЙ ЖЕЛЧНЫХ КИСЛОТ
- КИШЕЧНО-ПЕЧЕНОЧНАЯ ЦИРКУЛЯЦИЯ ЖЕЛЧНЫХ КИСЛОТ
- КЛИНИЧЕСКИЕ АСПЕКТЫ
- Глава 28. Регуляция метаболизма липидов и источники энергии в тканях
- РЕГУЛЯЦИЯ БИОСИНТЕЗА ЖИРНЫХ КИСЛОТ (ЛИПОГЕНЕЗА)
- МОЛЕКУЛЯРНЫЕ ФАКТОРЫ, РЕГУЛИРУЮЩИЕ ЛИПОГЕНЕЗ
- РЕГУЛЯЦИЯ ОКИСЛЕНИЯ ЖИРНЫХ КИСЛОТ
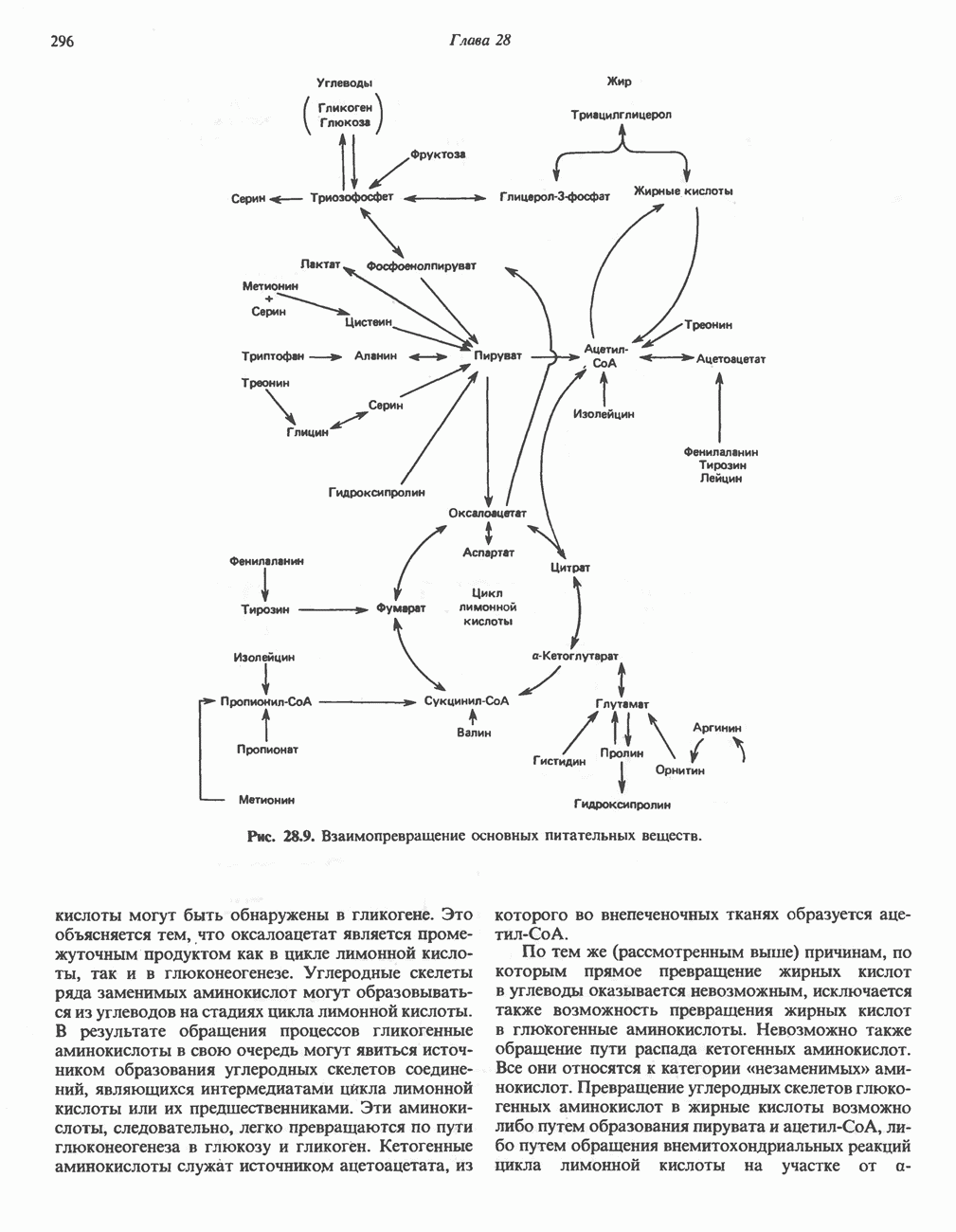
- ВЗАИМНОЕ ПРЕВРАЩЕНИЕ ОСНОВНЫХ ПИТАТЕЛЬНЫХ ВЕЩЕСТВ (рис. 28.9)
- ЭКОНОМИКА УГЛЕВОДНОГО И ЛИПИДНОГО ОБМЕНА В ОРГАНИЗМЕ
- ГОЛОДАНИЕ
- Раздел III. Метаболизм белков и аминокислот
- Глава 29. Биосинтез аминокислот
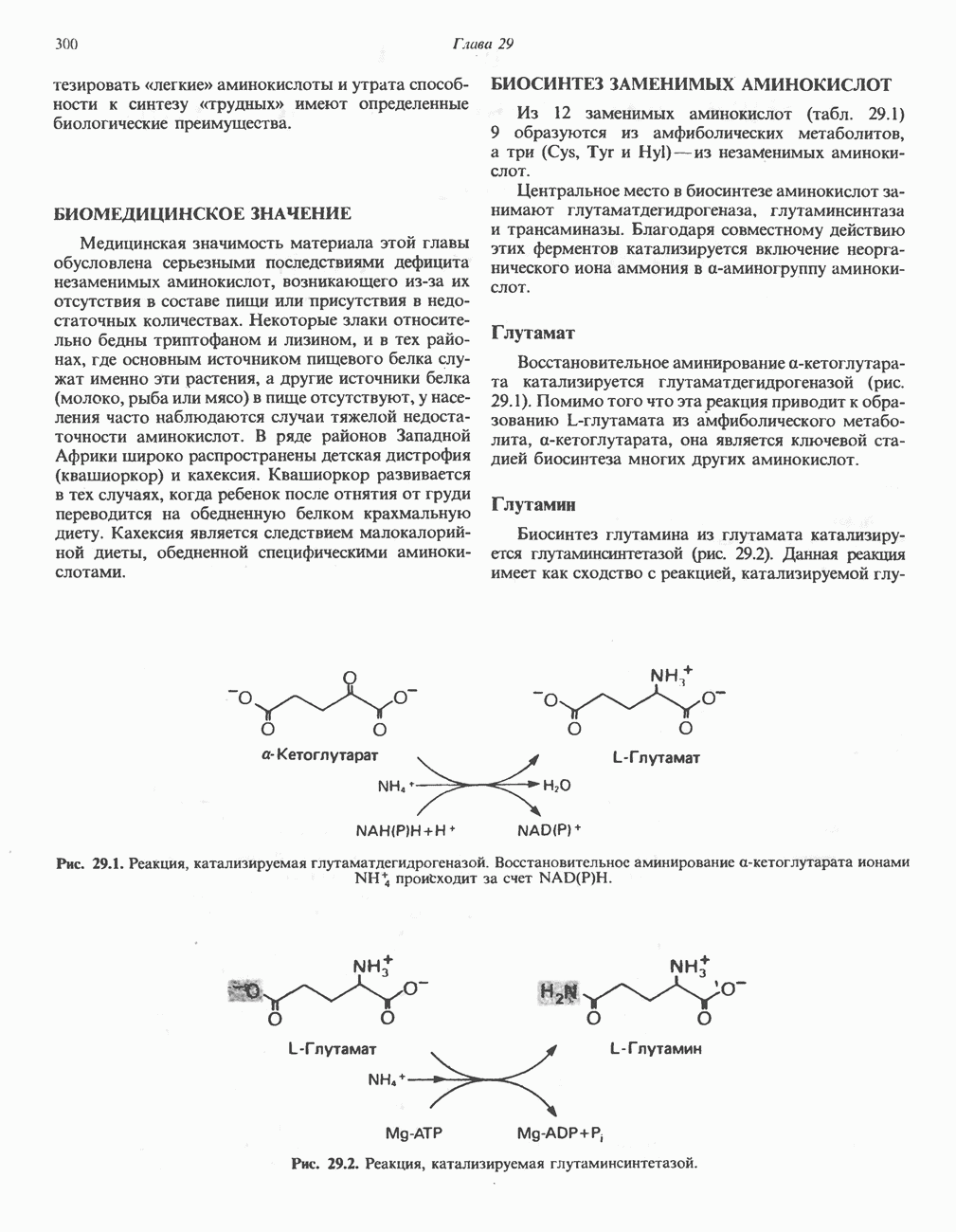
- БИОСИНТЕЗ ЗАМЕНИМЫХ АМИНОКИСЛОТ
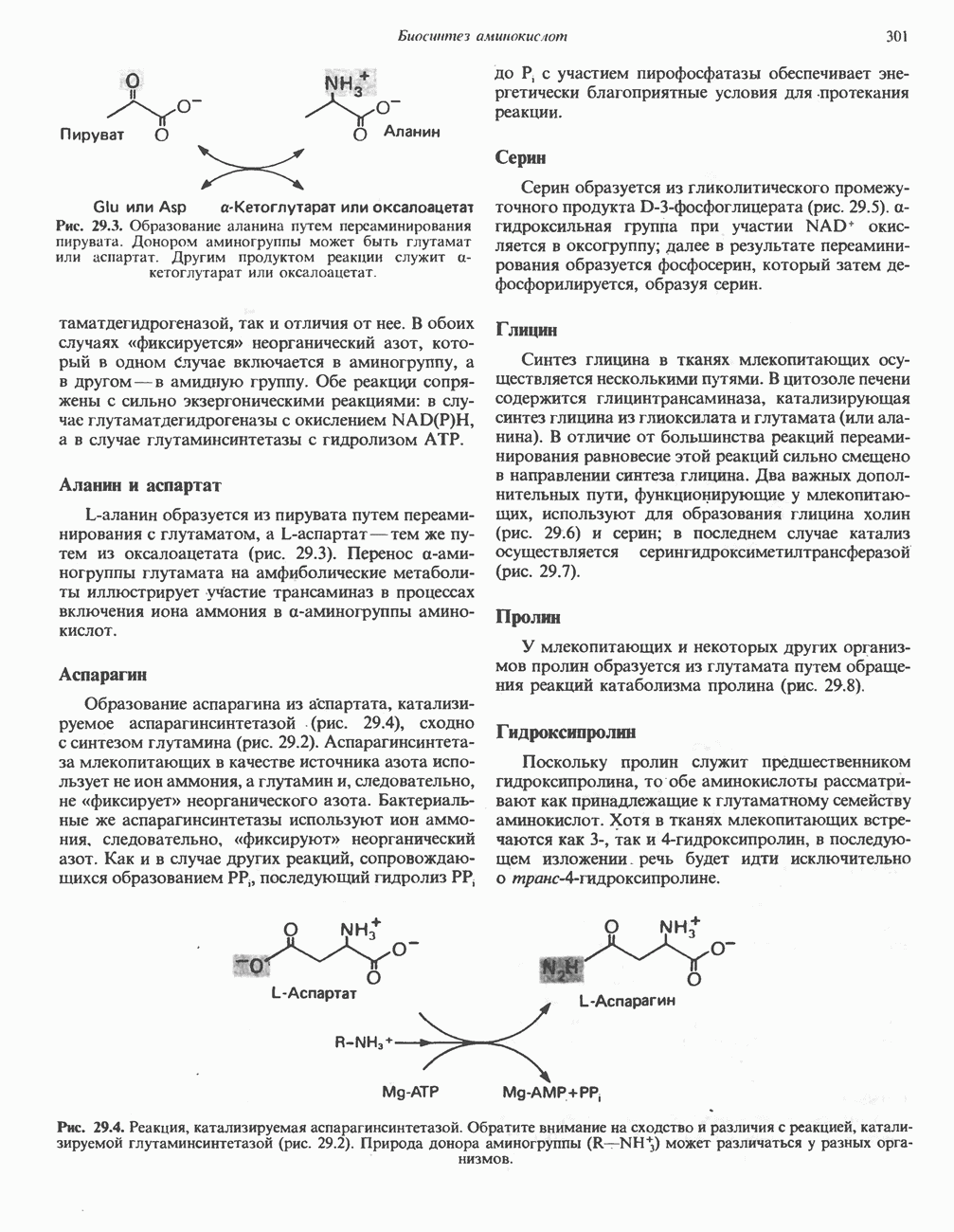
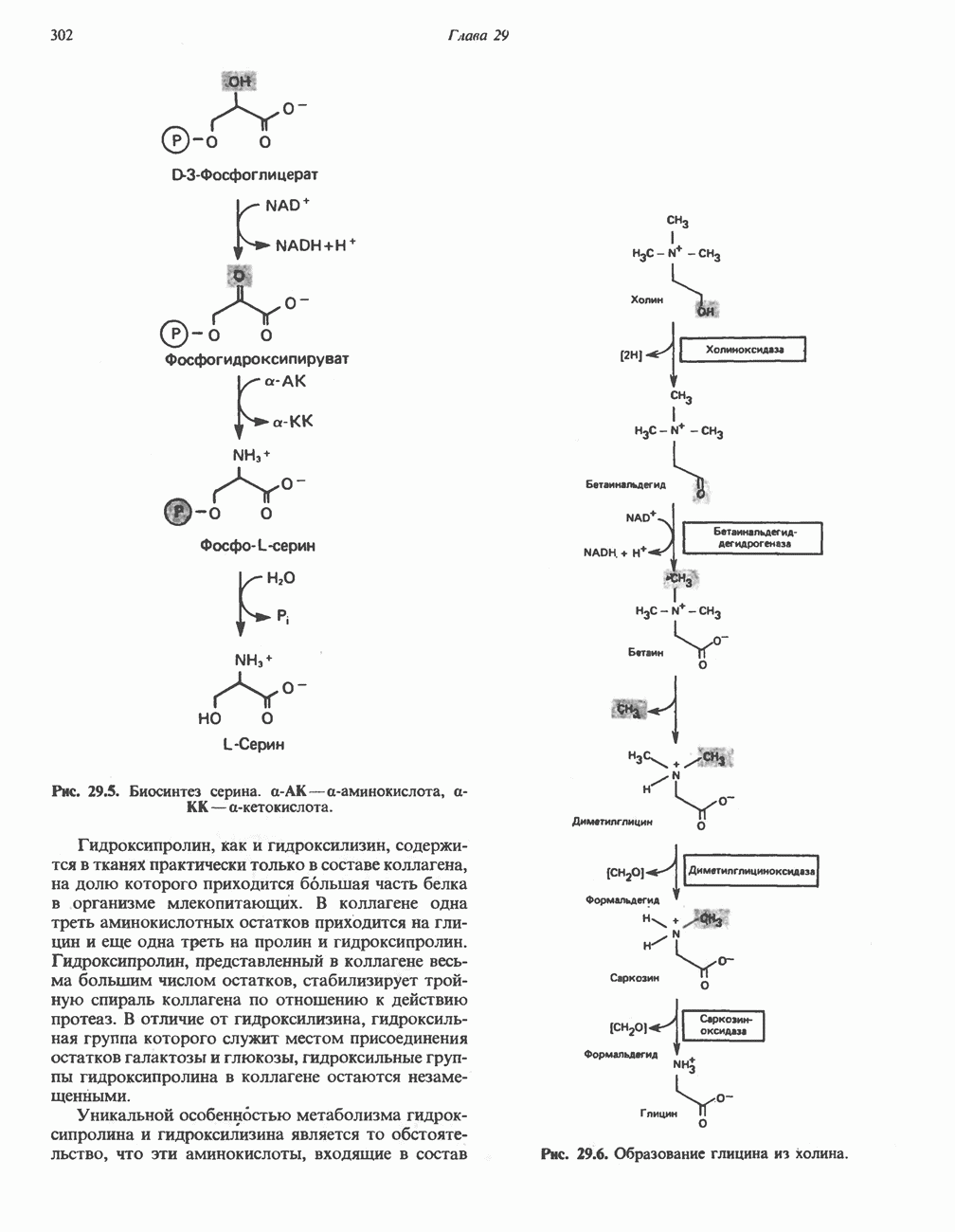
- БИОСИНТЕЗ НЕЗАМЕНИМЫХ АМИНОКИСЛОТ
- Глава 30. Катаболизм азота аминокислот
- ПЕРЕАМИНИРОВАНИЕ
- ОКИСЛИТЕЛЬНОЕ ДЕЗАМИНИРОВАНИЕ
- ОБРАЗОВАНИЕ АММИАКА
- ТРАНСПОРТ АММИАКА
- ОБМЕН АМИНОКИСЛОТАМИ МЕЖДУ ОРГАНАМИ В ПОСТАБСОРБТИВНОМ СОСТОЯНИИ
- ОБМЕН АМИНОКИСЛОТ МЕЖДУ ОРГАНАМИ ПОСЛЕ ПРИЕМА ПИЩИ
- БИОСИНТЕЗ МОЧЕВИНЫ
- РЕГУЛЯЦИЯ СИНТЕЗА МОЧЕВИНЫ
- МЕТАБОЛИЧЕСКИЕ НАРУШЕНИЯ ЦИКЛА МОЧЕВИНЫ
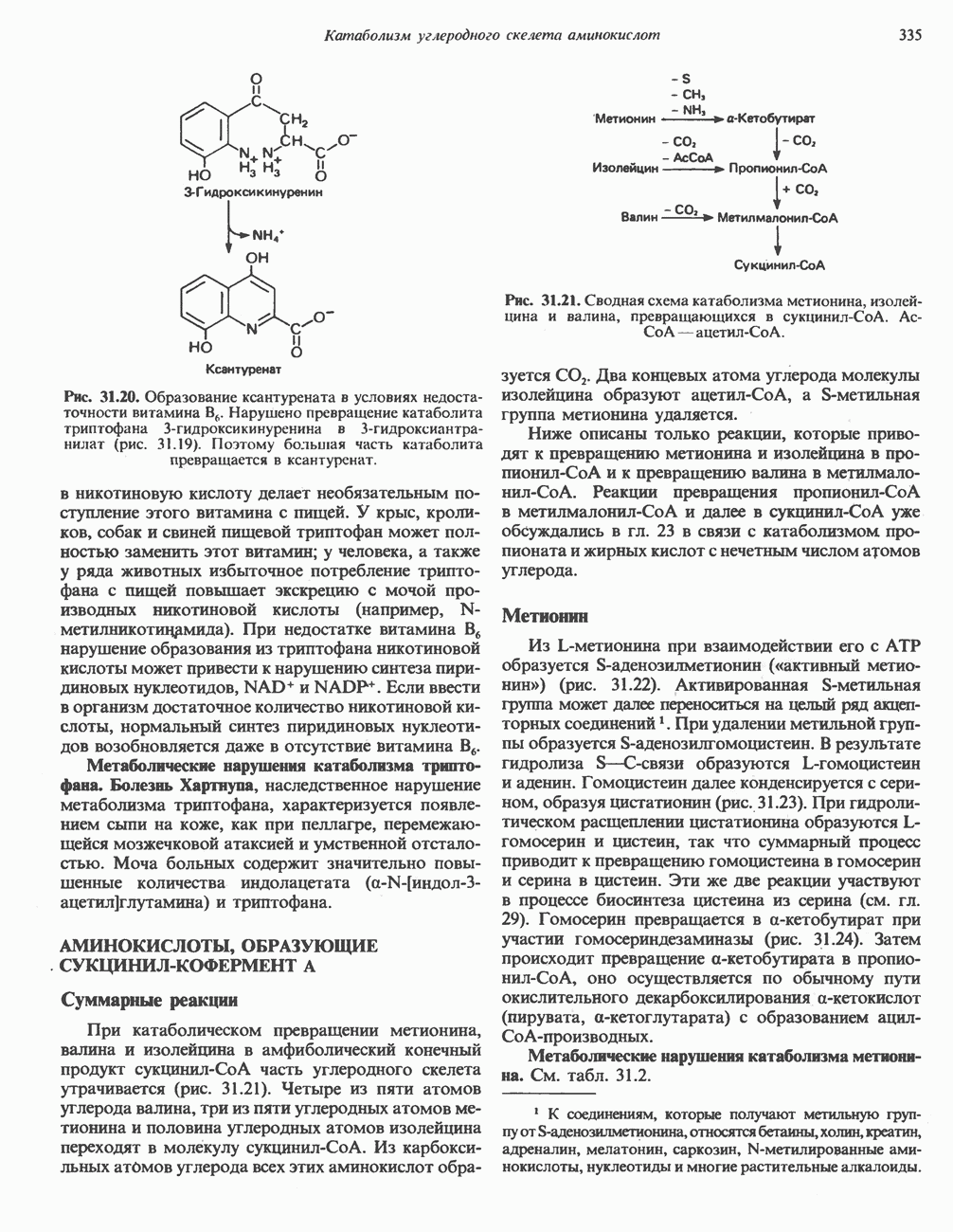
- Глава 31. Катаболизм углеродного скелета аминокислот
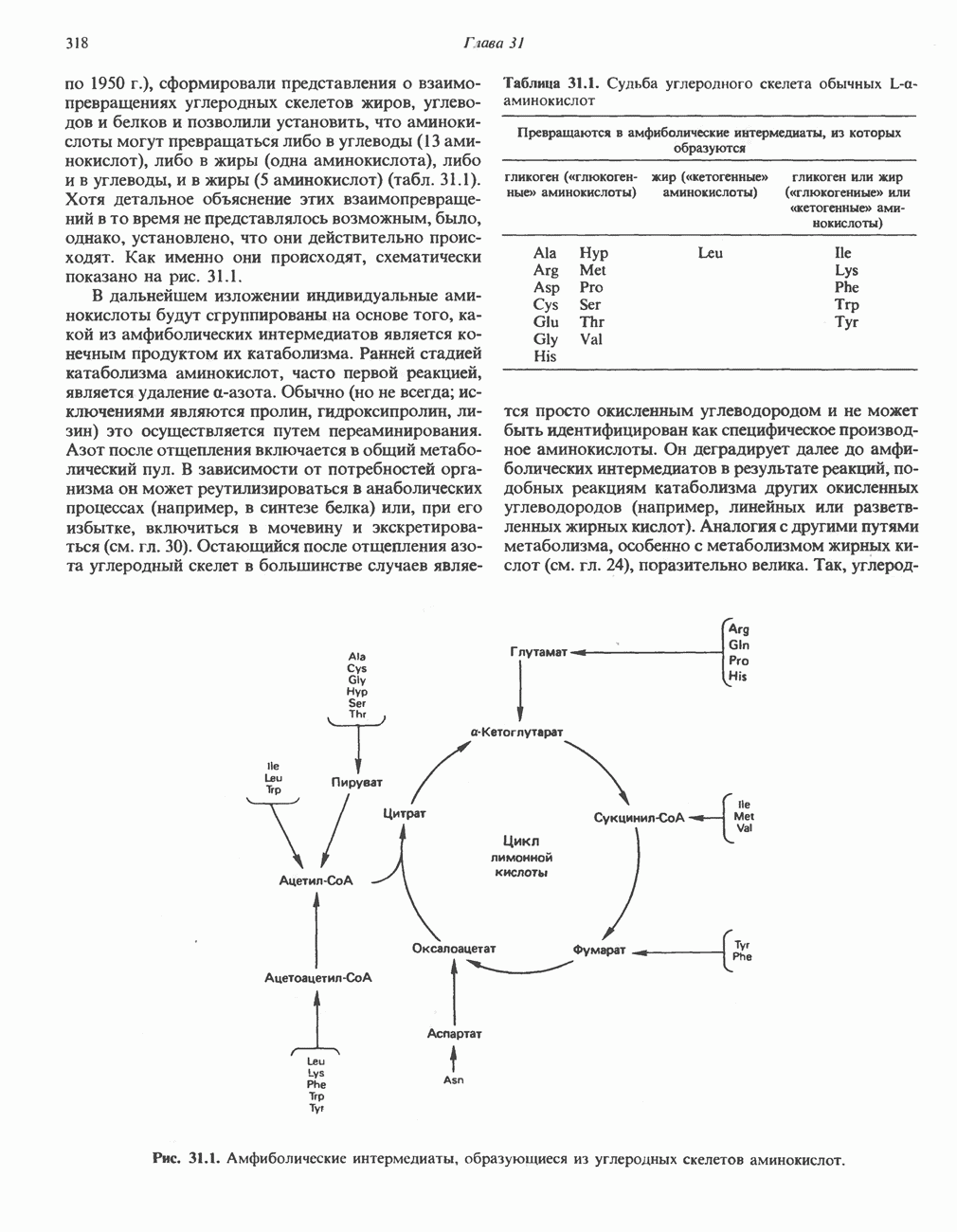
- ПРЕВРАЩЕНИЕ УГЛЕРОДНОГО СКЕЛЕТА ОБЫЧНЫХ L-a-АМИНОКИСЛОТ В АМФИБОЛИЧЕСКИЕ ИНТЕРМЕДИАТЫ
- АМИНОКИСЛОТЫ, ОБРАЗУЮЩИЕ ОКСАЛОАЦЕТАТ
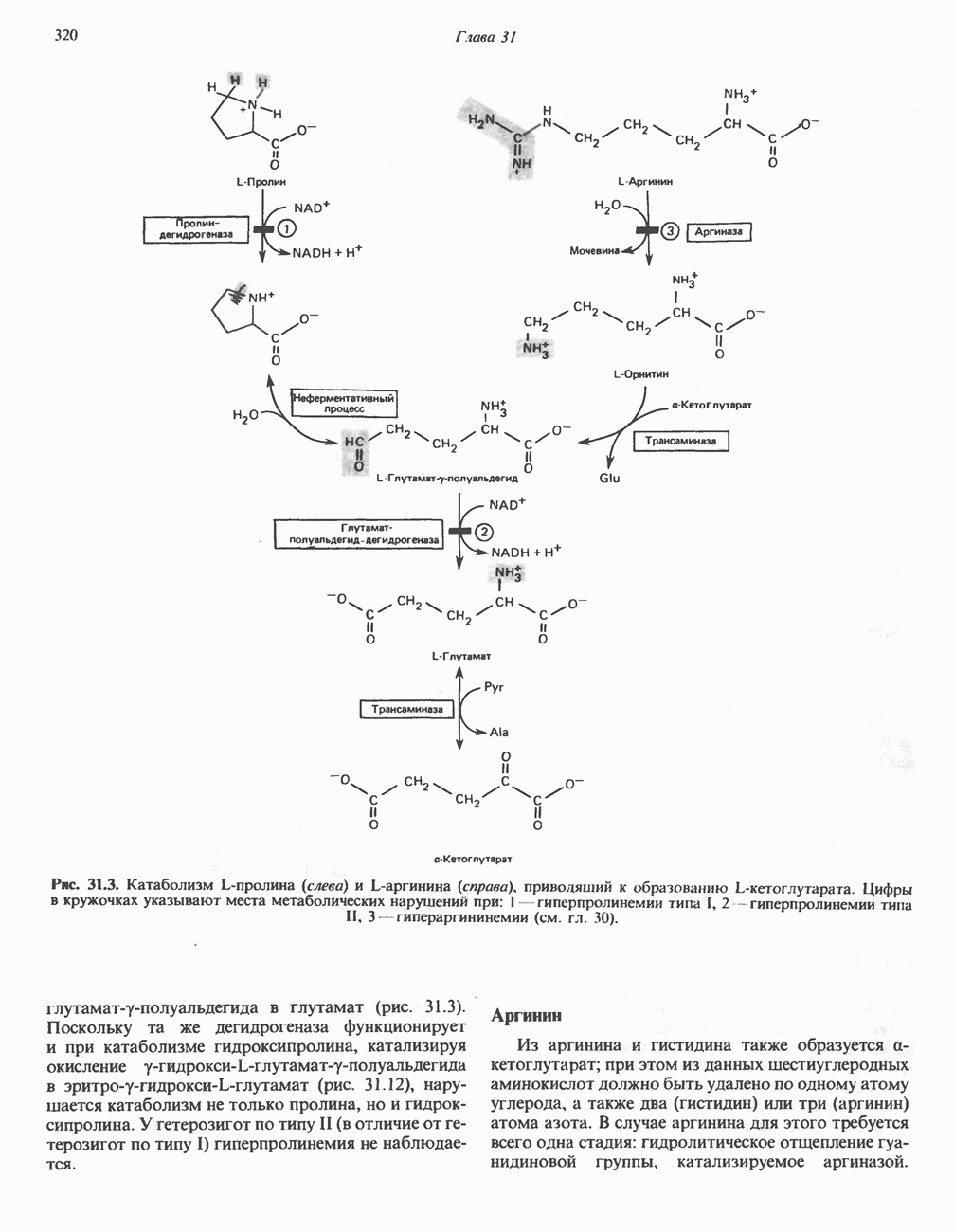
- АМИНОКИСЛОТЫ, ОБРАЗУЮЩИЕ а-КЕТОГЛУТАРАТ
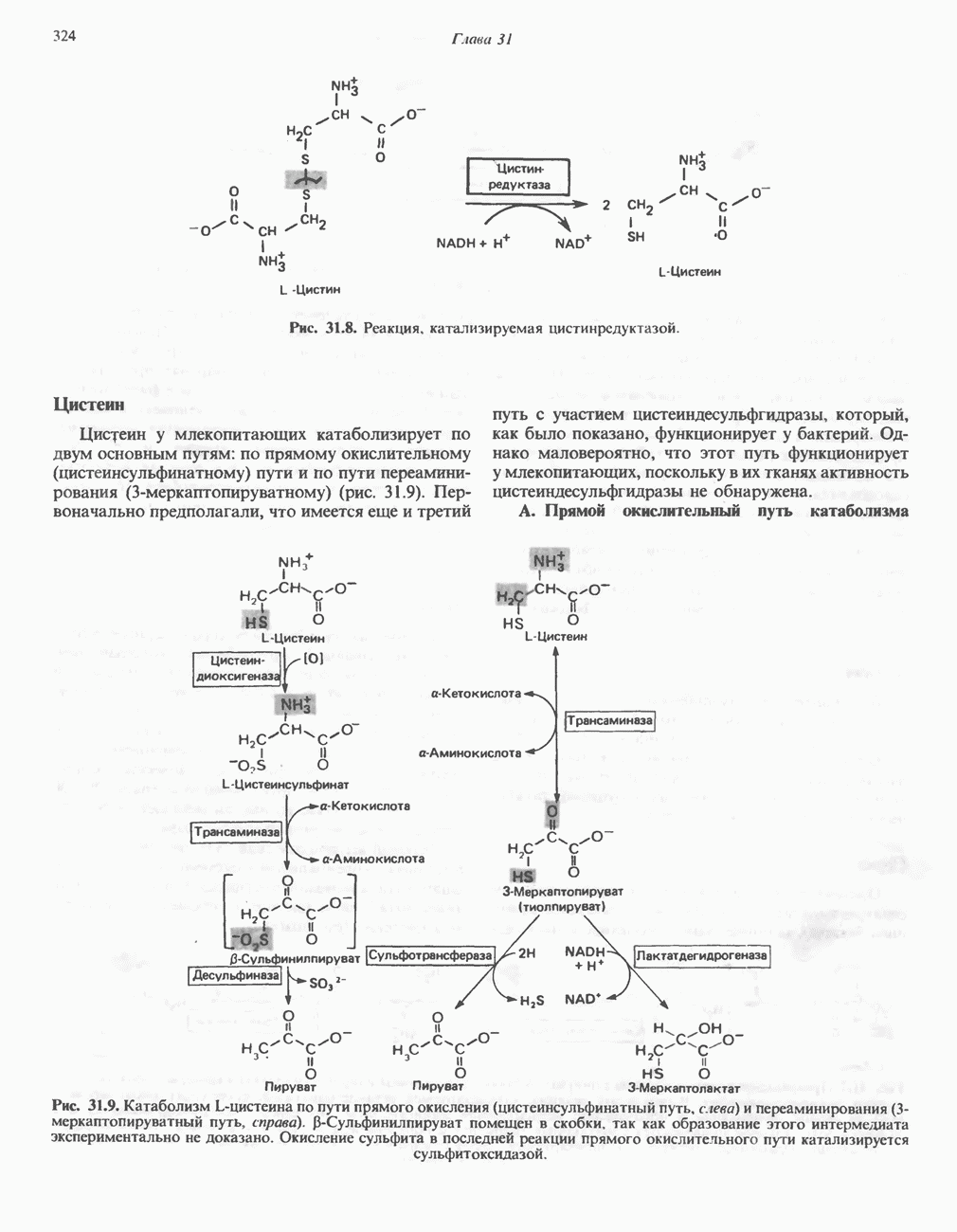
- АМИНОКИСЛОТЫ, ОБРАЗУЮЩИЕ ПИРУВАТ
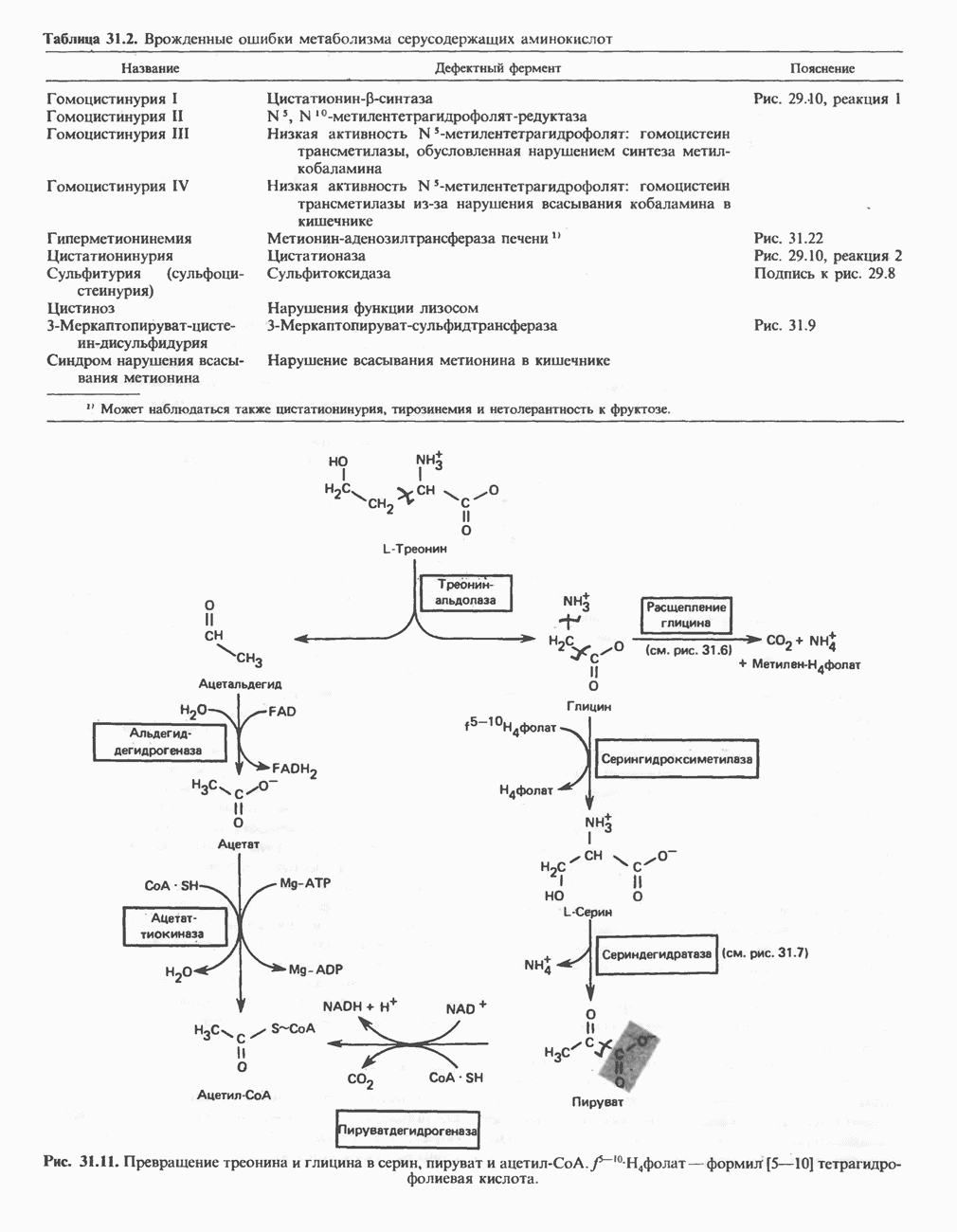
- АМИНОКИСЛОТЫ, ОБРАЗУЮЩИЕ АЦЕТИЛ-КОФЕРМЕНТ А
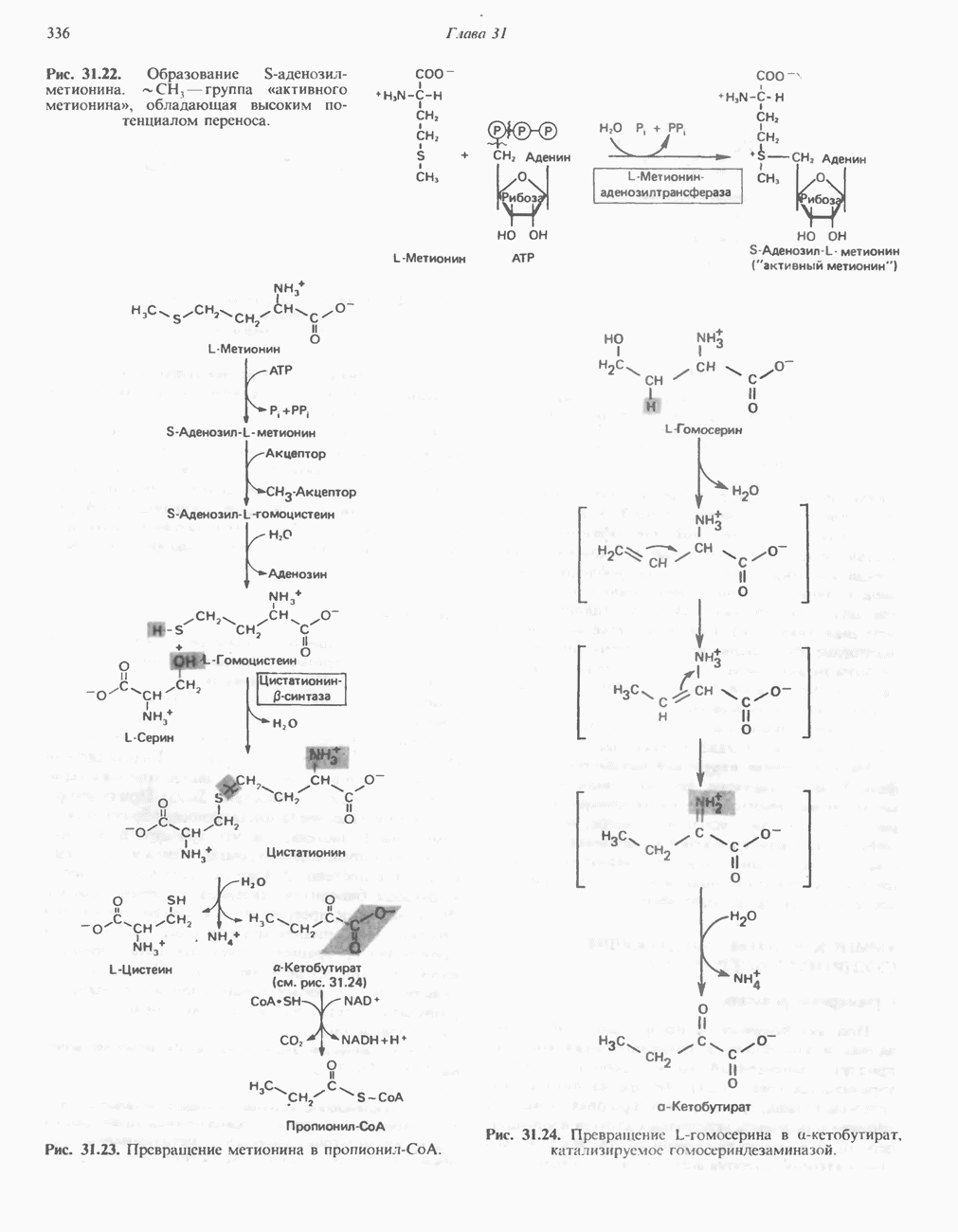
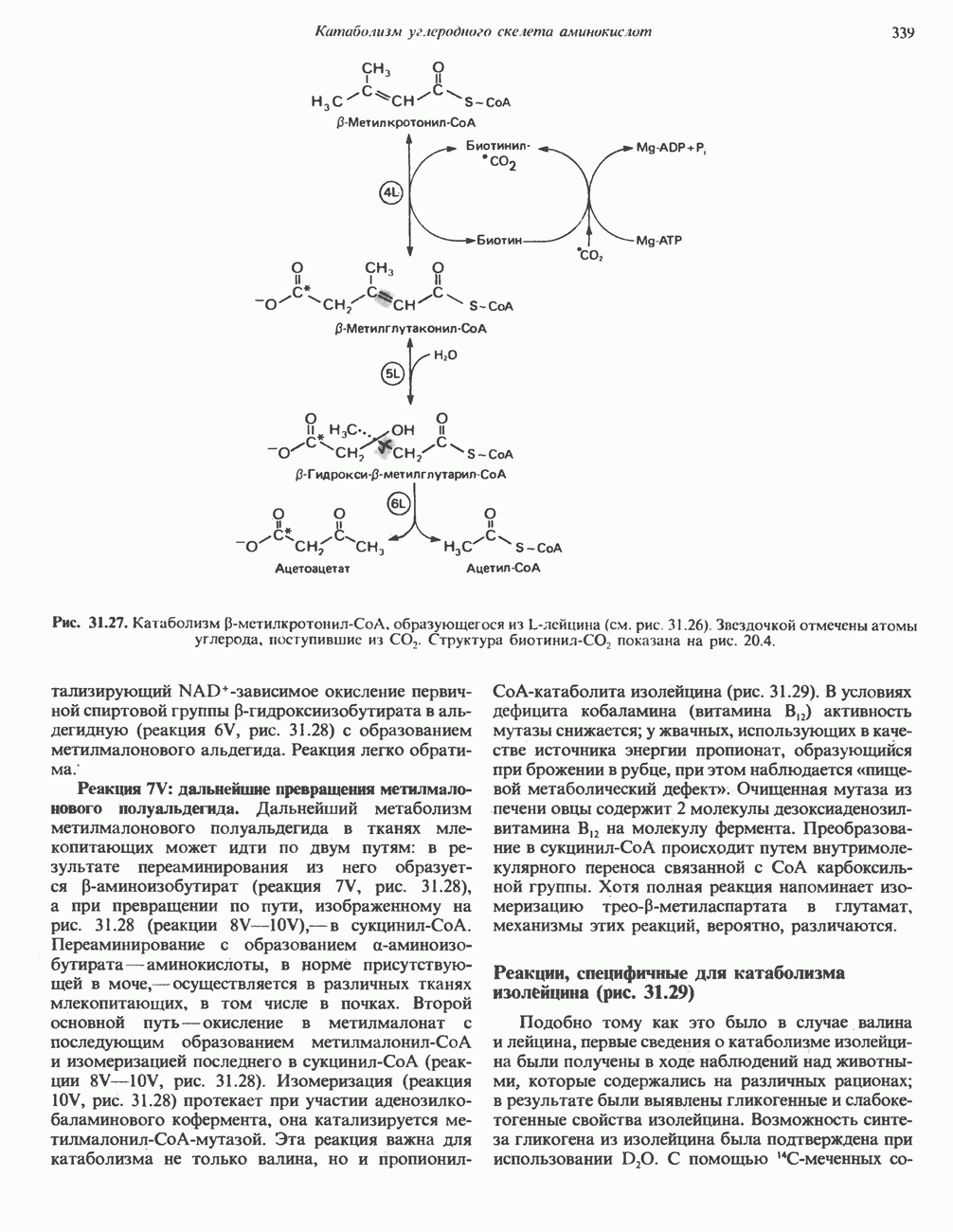
- АМИНОКИСЛОТЫ, ОБРАЗУЮЩИЕ СУКЦИНИЛ-КОФЕРМЕНТ А
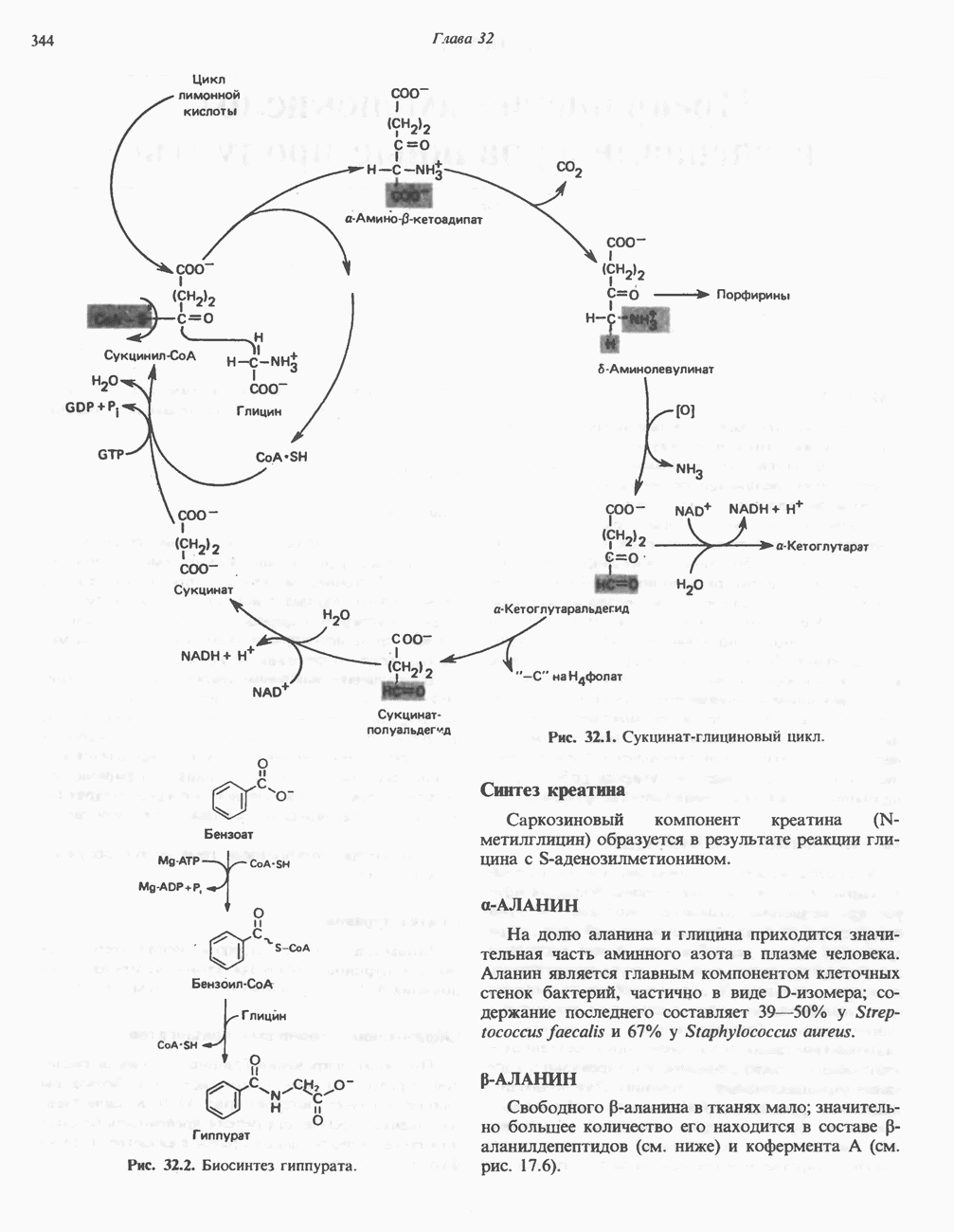
- Глава 32. Превращение аминокислот в специализированные продукты
- ГЛИЦИН
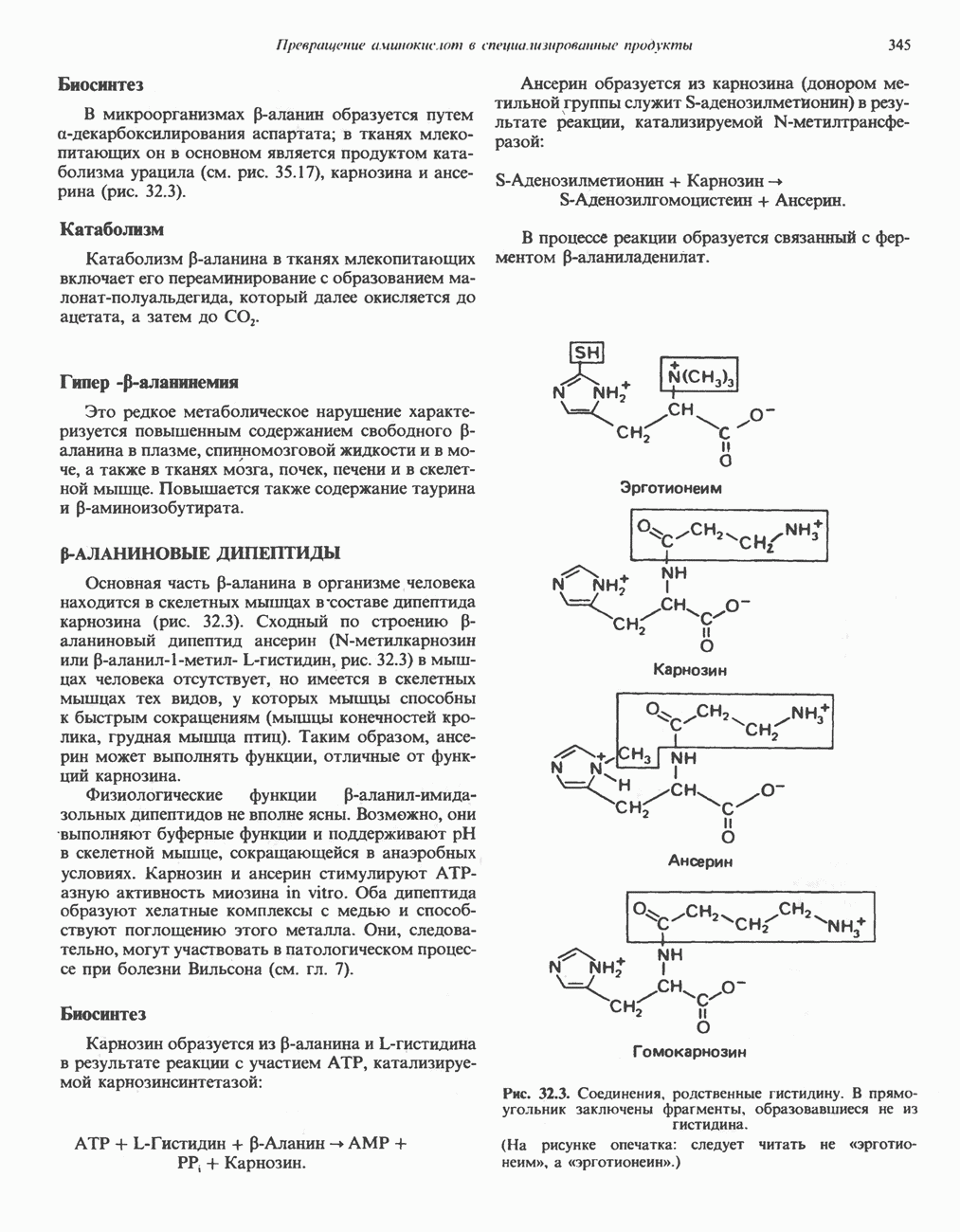
- р-АЛАНИНОВЫЕ ДИПЕПТИДЫ
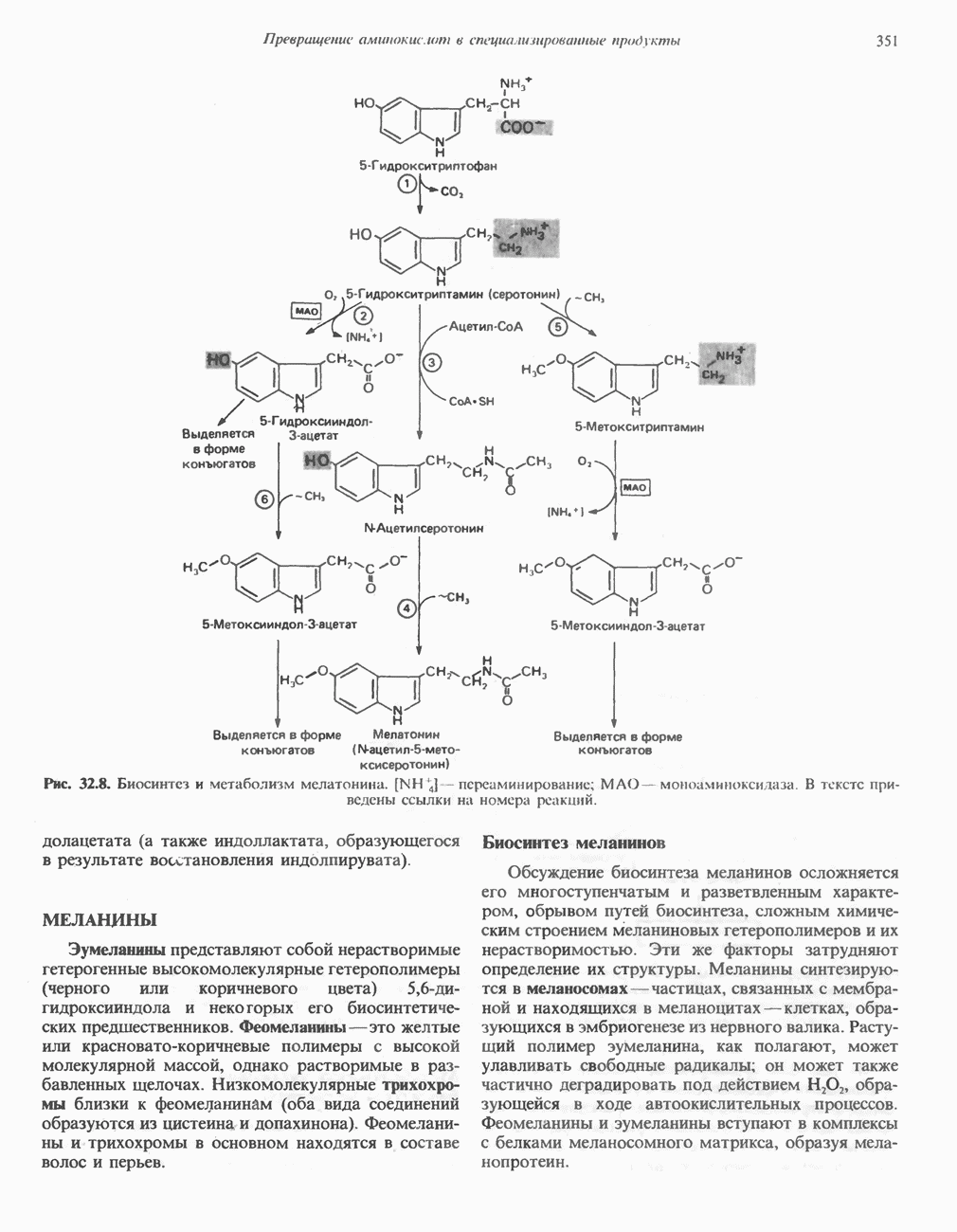
- ТРИПТОФАН
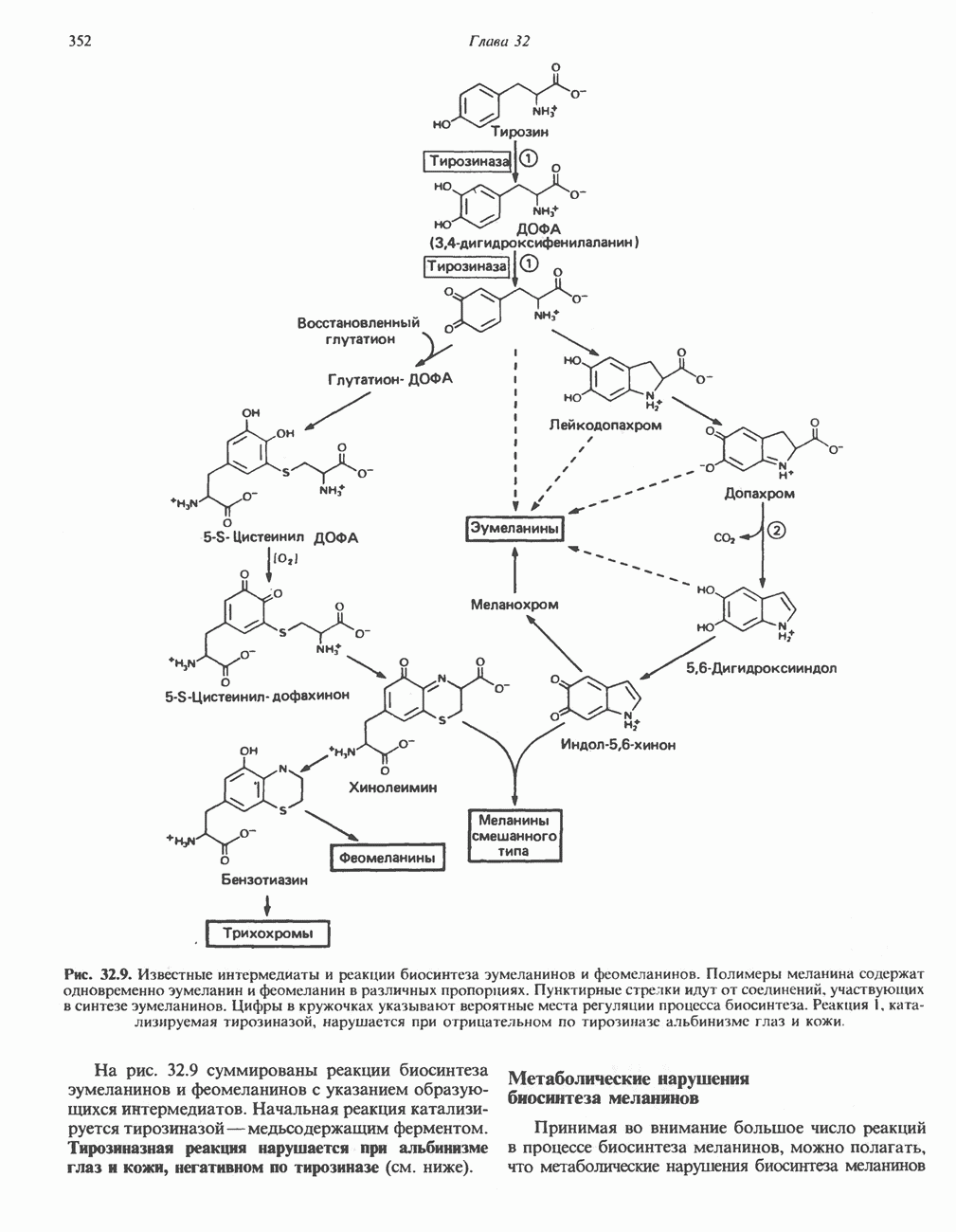
- МЕЛАНИНЫ
- ТИРОЗИН
- КРЕАТИН И КРЕАТИНИН
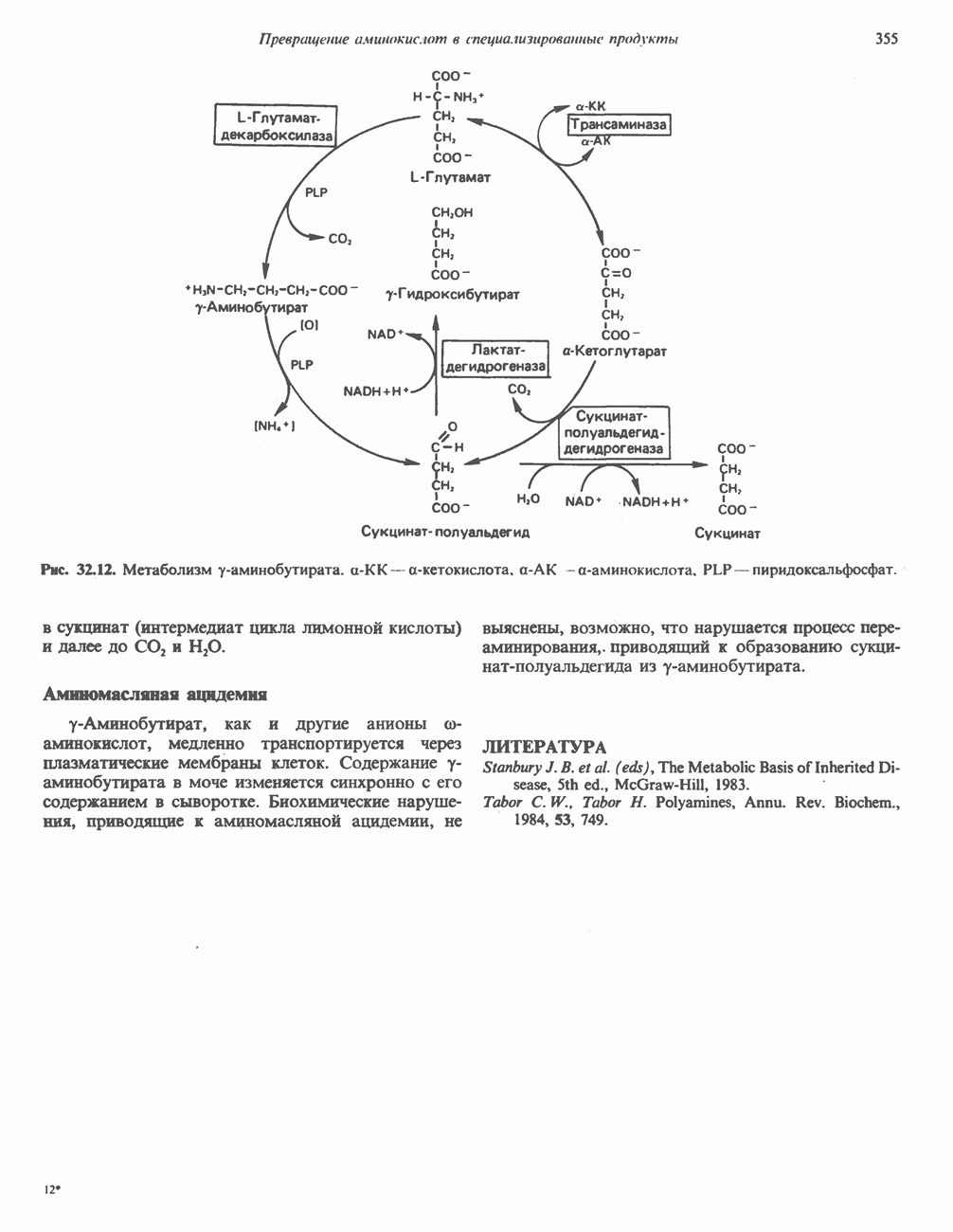
- у-АМИНОБУТИРАТ
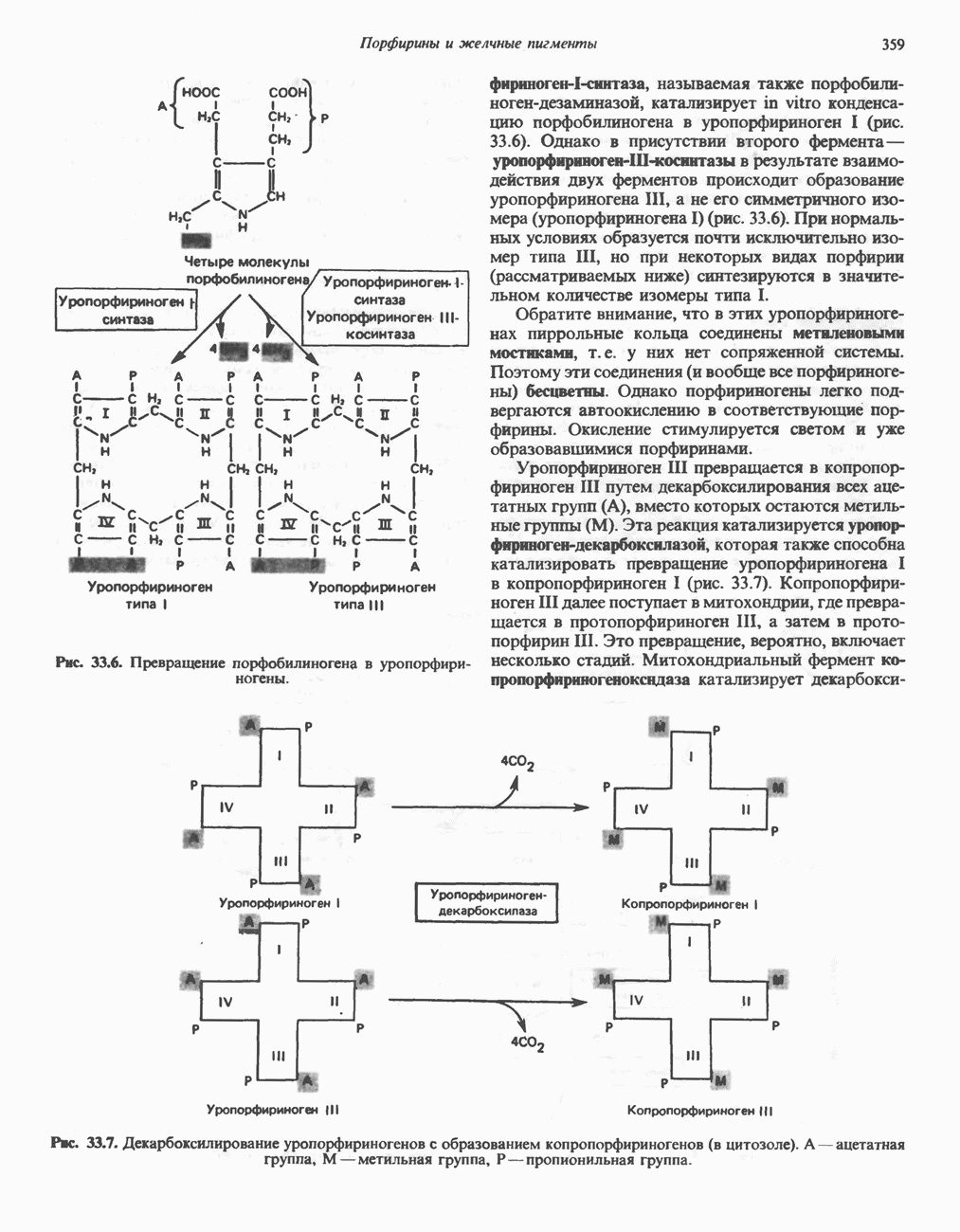
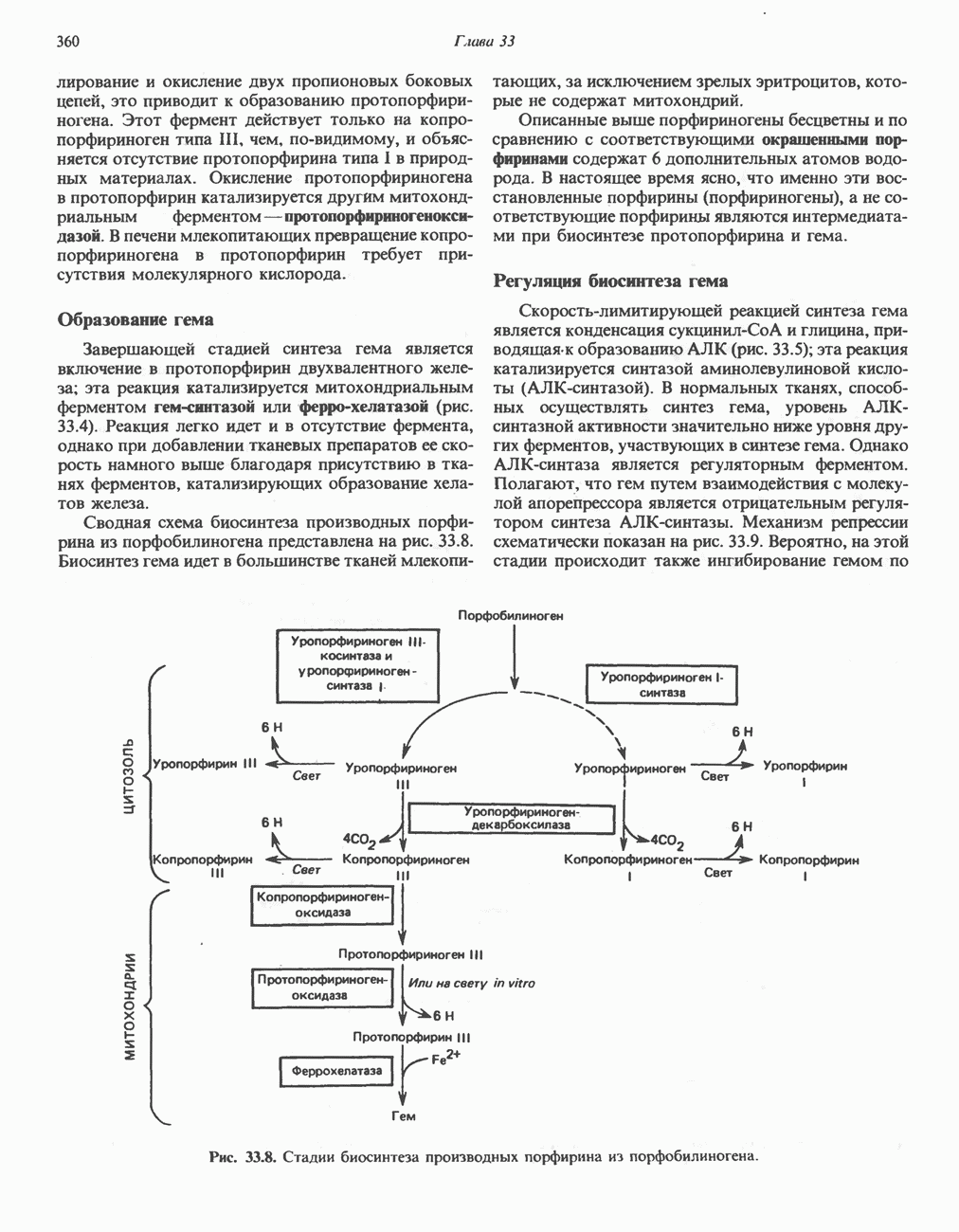
- Глава 33. Порфирины и желчные пигменты
- ПОРФИРИНЫ
- ПОРФИРИН
- КАТАБОЛИЗМ ГЕМА: ОБРАЗОВАНИЕ ЖЕЛЧНЫХ ПИГМЕНТОВ
- МЕТАБОЛИЗМ БИЛИРУБИНА В КИШЕЧНИКЕ
- ГИПЕРБИЛИРУБИНЕМИЯ
- Список сокращений