| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
РЕГУЛЯЦИЯ КОЛИЧЕСТВА ФЕРМЕНТА ПУТЕМ РЕГУЛЯЦИИ СКОРОСТИ ЕГО СИНТЕЗА И РАСПАДА
Общие принципы
Абсолютное количество фермента в клетке определяется скоростями его синтеза  и распада (расп) (Рис. 10.2). Соответственно количество фермента увеличивается либо в результате повышения скорости его синтеза (увеличением
и распада (расп) (Рис. 10.2). Соответственно количество фермента увеличивается либо в результате повышения скорости его синтеза (увеличением  ), либо снижения скорости распада (уменьшением к), либо обоими способами сразу. Подобным же образом
), либо снижения скорости распада (уменьшением к), либо обоими способами сразу. Подобным же образом

Рис. 10.2. Количество фермента определяется балансом процессов его синтеза и распада.
количество фермента уменьшается в результате либо уменьшения  либо увеличения
либо увеличения  либо и тем и другим путем. В клетках человека может происходить изменение и
либо и тем и другим путем. В клетках человека может происходить изменение и  и к. У всех живых организмов синтез ферментов (и всех других белков) из аминокислот и распад фермента (белка) на аминокислоты представляют собой разные процессы, которые катализируются совершенно разными наборами ферментов. В этих условиях легко осуществляется независимая регуляция скорости синтеза фермента и скорости его распада.
и к. У всех живых организмов синтез ферментов (и всех других белков) из аминокислот и распад фермента (белка) на аминокислоты представляют собой разные процессы, которые катализируются совершенно разными наборами ферментов. В этих условиях легко осуществляется независимая регуляция скорости синтеза фермента и скорости его распада.
Синтез ферментов детерминируется информацией, содержащейся в ДНК
Первичная структура фермента, как и любого другого белка, определяется той информацией, которая записана в информационной (матричной) РНК  и считывается с помощью трехбуквенного (триплетного) кода. Нуклеотидная последовательность
и считывается с помощью трехбуквенного (триплетного) кода. Нуклеотидная последовательность  в свою очередь определяется комплементарной последовательностью оснований ДНК-матрицы, т.е. соответствующего гена (см. гл. 38 и 40).
в свою очередь определяется комплементарной последовательностью оснований ДНК-матрицы, т.е. соответствующего гена (см. гл. 38 и 40).
В результате мутаций нуклеотидная последовательность ДНК может измениться, и будут синтезироваться белки с измененной первичной структурой. Если новая аминокислота сильно отличается по своим свойствам от исходной, изменения могут охватить высокие уровни структурной организации и может произойти частичная или полная утрата каталитической активности (впрочем, в редких случаях наблюдается, напротив, ее повышение). Мутации в различных генетических локусах могут приводить к нарушению синтеза самых разных ферментов и тем самым к развитию многих генетических заболеваний.
Индукция ферментов
Клетки могут синтезировать специфические ферменты в ответ на присутствие специфических низкомолекулярных индукторов. Индукцию ферментов можно проиллюстрировать на следующем примере. Клетки Escherichia coli, выращенные на глюкозе, не способны сбраживать лактозу из-за отсутствия фермента р-галактозидазы, гидролизующей лактозу, которая распадается на глюкозу и галактозу. Если в питательную среду добавить лактозу или некоторые другие Р-галактозиды, то индуцируется синтез р-галактозидазы, и культура клеток обретает способность сбраживать лактозу.
Индуктор (лактоза) является субстратом индуцируемого белка ф-галактозидазы). Многие индукторы одновременно служат субстратами ферментов, которые они индуцируют, однако в роли индукторов могут выступать и соединения, структурно сходные с субстратом, но сами не являющиеся субстратами. И наоборот, соединение может быть субстратом, но не являться индуктором. Нередко какое-либо соединение индуцирует сразу несколько ферментов данного катаболического пути. В этих случаях говорят, что структурные гены, кодирующие группу катаболических ферментов, составляют оперон, и все ферменты, кодируемые генами оперона, индуцируются единственным индуктором (координированная индукция). Способность регулировать синтез ферментов с помощью того или иного питательного вещества позволяет бактерии использовать это питательное вещество с максимальным для себя преимуществом; в то же время «ненужные» ферменты бактерия не синтезирует.
Ферменты, концентрация которых в клетке не зависит от добавления индукторов, называются конститутивными. Данный фермент может быть конститутивным для одного штамма, индуцируемым для другого и вообще отсутствовать в третьем. Обычно клетки содержат небольшое, но измеримое количество соответствующего фермента даже в отсутствие индуктора. Это — базовый уровень. Величина отклика данного организма на введение индуктора определяется генетически (см. гл. 41). При индукции различных штаммов может наблюдаться повышение содержания фермента, варьирующее от двукратного до тысячекратного. Таким образом, содержащаяся в клетке наследственная генетическая информация определяет и характер, и величину реакции на введение индуктора. Следовательно, понятия «конститутивный» и «индуцируемый» относительны: они характеризуют лишь крайние точки всего спектра возможных реакций.
Индукция ферментов наблюдается и у эукариот. Примерами индуцируемых ферментов у млекопитающих являются триптофанпирролаза, треониндегидраза, тирозин-а-оксоглутарат—грансаминаза, инвертаза, ферменты цикла мочевины, HMG-СоА-редуктаза и цитохром 
Репрессия и дерепрессия ферментов
Бактерии, способные синтезировать определенный метаболит, при наличии этого метаболита в среде могут приостановить его синтез в результате репрессии. В этом случае небольшая молекула,
например пурин или аминокислота, действуя как корепрессор, блокирует синтез ферментов, участвующих в биосинтезе самого корепрессора. Например, добавление гистидина в среду, на которой растет бактерия Salmonella typhimurium, подавляет (репрессирует) синтез всех ферментов биосинтеза гистидина; добавление в среду лейцина репрессирует синтез первых трех ферментов, которые участвуют исключительно в биосинтезе лейцина. В обоих случаях гены ферментов, ответственных за биосинтез данного метаболита, образуют оперон: добавление в среду конечного продукта биосинтеза, гистидина или лейцина, вызывает координированную репрессию. Координированная репрессия наблюдается не для всех путей биосинтеза. После удаления из среды корепрессора или же при истощении его запасов биосинтез соответствующих ферментов возобновляется. Это явление называют дерепрессиен. Дерепрессия может быть координированной и некоординированной.
Приведенные выше примеры иллюстрируют репрессию конечным продуктом по принципу обратной связи, характерную для процессов биосинтеза в бактериях. Сходное явление —катаболитная репрессия — состоит в том, что одно из промежуточных соединений в цепочке катаболических ферментативных реакций репрессирует синтез катаболических ферментов. Оно было впервые обнаружено при изучении культуры Е. coli, растущей на среде, которая содержит в качестве источника углерода не глюкозу, а другое соединение  . Добавление глюкозы репрессировало синтез ферментов, участвующих в катаболизме X. Это явление вначале называли «эффект глюкозы», но потом обнаружилось, что сходные эффекты могут вызывать и другие окисляемые питательные вещества; поэтому был предложен термин «катаболитная репрессия». Катаболитная репрессия осуществляется при участии
. Добавление глюкозы репрессировало синтез ферментов, участвующих в катаболизме X. Это явление вначале называли «эффект глюкозы», но потом обнаружилось, что сходные эффекты могут вызывать и другие окисляемые питательные вещества; поэтому был предложен термин «катаболитная репрессия». Катаболитная репрессия осуществляется при участии  Молекулярные механизмы индукции, репрессии и дерепрессии осуждаются в гл. 41.
Молекулярные механизмы индукции, репрессии и дерепрессии осуждаются в гл. 41.
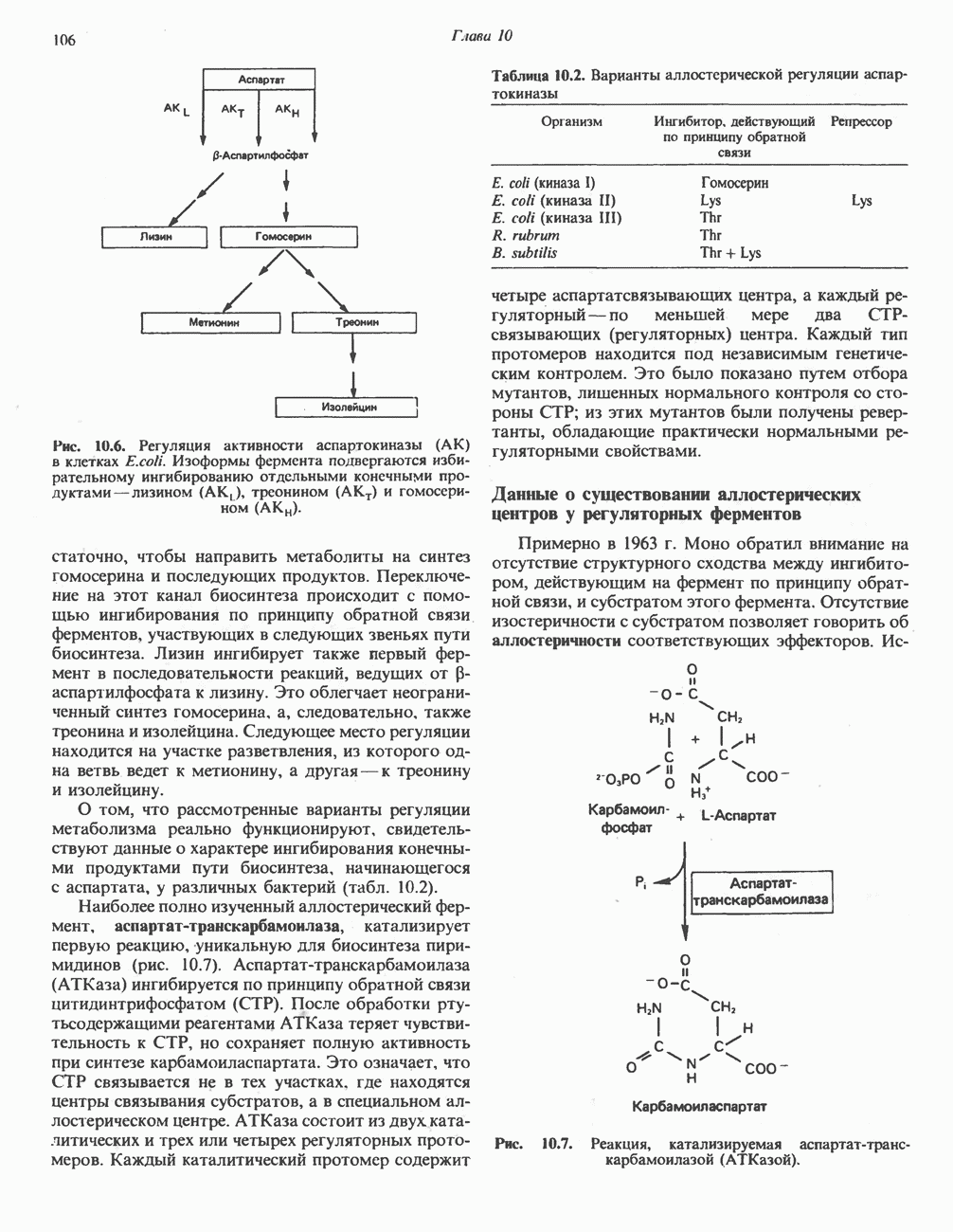
В разветвленных процессах биосинтеза, например при биосинтезе аминокислот с разветвленными боковыми цепями или аминокислот семейства аспартата, ферменты начальных стадий участвуют в биосинтезе нескольких аминокислот (рис. 10.3). Если в среду, на которой растут бактерии, добавить лизин, репрессируется синтез ферментов, участвующих исключительно в биосинтезе лизина  Добавление в среду треонина вызывает репрессию ферментов, участвующих только в биосинтезе треонина
Добавление в среду треонина вызывает репрессию ферментов, участвующих только в биосинтезе треонина  Это — примеры простой репрессии конечным продуктом. В то же время ферменты
Это — примеры простой репрессии конечным продуктом. В то же время ферменты  участвуют одновременно в биосинтезе и лизина, и треонина. Если бы репрессию их синтеза вызывал каждый из конечных продуктов по отдельности, то наблюдался бы недостаток другой аминокислоты.
участвуют одновременно в биосинтезе и лизина, и треонина. Если бы репрессию их синтеза вызывал каждый из конечных продуктов по отдельности, то наблюдался бы недостаток другой аминокислоты.

Рис. 10.3. Синтез аминокислот семейства аспартата. Под  подразумеваются группы ферментов, участвующих в биосинтезе лизина и треонина соответственно. Число стрелок соответствует числу стадий.
подразумеваются группы ферментов, участвующих в биосинтезе лизина и треонина соответственно. Число стрелок соответствует числу стадий.
Если же в среду добавить одновременно и лизин, и треонин, то ферменты  окажутся излишними; их репрессия была бы выгодна бактерии, поскольку позволила бы более эффективно использовать имеющиеся питательные вещества.
окажутся излишними; их репрессия была бы выгодна бактерии, поскольку позволила бы более эффективно использовать имеющиеся питательные вещества.
В присутствии всех конечных продуктов, образующихся на различных ответвлениях пути биосинтеза, может наблюдаться мультивалентная репрессия. Это происходит только тогда, когда все конечные продукты, синтезируемые данным набором ферментов, присутствуют в избытке. Следовательно, для полной репрессии аспартокиназы  необходимо присутствие не только лизина и треонина, но также еще и метионина, и изолейцина.
необходимо присутствие не только лизина и треонина, но также еще и метионина, и изолейцина.
Обновление ферментов
В быстро растущих бактериях общая скорость распада белков составляет около 2% в час. Иное положение складывается, когда бактерии находятся в условиях голодания или их переносят на свежую среду, бедную углеродом. В этих условиях распад бактериальных белков идет со скоростью 7—10% в час.
Сочетание процессов синтеза и распада ферментов называют обновлением ферментов. Обновление происходит и у бактерий, и у млекопитающих, однако значение распада ферментов как средства регуляции их количества у бактерий недооценивалось.
В клетках млекопитающих обновление белков было обнаружено гораздо раньше, чем у бактерий. Указания на этот процесс у человека были получены более ста лет назад на основании наблюдений за людьми, получавшими специальную диету. Однако лишь после классических работ Шёнхеймера, начатых незадолго до второй мировой войны, было твердо установлено, что обновление клеточных белков происходит на протяжении всей жизни. Измеряя скорость включения в данный белок 15 N-меченных аминокислот и скорость утраты метки белком, Шёнхеймер пришел к выводу, что белки в организме человека находятся в состоянии «динамического равновесия»; это представление позднее было распространено на другие компоненты организма, включая липиды и нуклеиновые кислоты.
Регуляция синтеза и распада ферментов
Основные этапы синтеза белков достаточно хорошо изучены, чего нельзя сказать о процессах распада ферментов. Распад ферментов происходит в результате их гидролиза протеолитическими ферментами, но о механизме регуляции этой протеолитической активности мало что известно. Установлено только, что процессы регуляции могут быть сопряжены с расходованием АТР. Чувствительность фермента к протеолизу зависит от его конформации. Присутствие или отсутствие субстратов, коферментов, ионов металлов — все это способно влиять на конформацию белка и его чувствительность к протеолизу. Поэтому скорость распада специфических ферментов может зависеть от концентрации в клетке субстратов, коферментов и, возможно, ионов. Эти представления можно хорошо проиллюстрировать на примере аргиназы и триптофаноксигеназы (триптофанпирролазы). Регуляция содержания аргиназы в печени может осуществляться путем изменения либо  либо красп. Переход на обогащенную белковую диету приводит к возрастанию содержания аргиназы из-за повышения скорости ее синтеза. Содержание фермента в печени возрастает также у голодающих животных. Но это обусловлено снижением скорости распада аргиназы, поскольку значение
либо красп. Переход на обогащенную белковую диету приводит к возрастанию содержания аргиназы из-за повышения скорости ее синтеза. Содержание фермента в печени возрастает также у голодающих животных. Но это обусловлено снижением скорости распада аргиназы, поскольку значение  остается постоянным. Теперь о ситуации, которая наблюдается со вторым ферментом: инъекция млекопитающим глюкокортикоидов, как и инъекция триптофана, повышает содержание триптофаноксигеназы. Гормон вызывает повышение скорости синтеза фермента
остается постоянным. Теперь о ситуации, которая наблюдается со вторым ферментом: инъекция млекопитающим глюкокортикоидов, как и инъекция триптофана, повышает содержание триптофаноксигеназы. Гормон вызывает повышение скорости синтеза фермента  тогда как
тогда как  не оказывает влияния на а понижает
не оказывает влияния на а понижает  повышая устойчивость оксигеназы к протеолизу. Сравним оба этих примера с индукцией ферментов у бактерий. В случае аргиназы повышенное потребление азота при нахождении на обогащенной белковой диете может увеличить содержание аргиназы (см. гл. 30). Повышение скорости синтеза аргиназы внешне напоминает индукцию субстратом, наблюдающуюся у бактерий. Для триптофанпирролазы ситуация иная: в бактериальных клетках
повышая устойчивость оксигеназы к протеолизу. Сравним оба этих примера с индукцией ферментов у бактерий. В случае аргиназы повышенное потребление азота при нахождении на обогащенной белковой диете может увеличить содержание аргиназы (см. гл. 30). Повышение скорости синтеза аргиназы внешне напоминает индукцию субстратом, наблюдающуюся у бактерий. Для триптофанпирролазы ситуация иная: в бактериальных клетках  может действовать как индуктор (увеличивая ксшп), но в тканях млекопитающих он действует только на процесс распада фермента (уменьшает
может действовать как индуктор (увеличивая ксшп), но в тканях млекопитающих он действует только на процесс распада фермента (уменьшает  ).
).
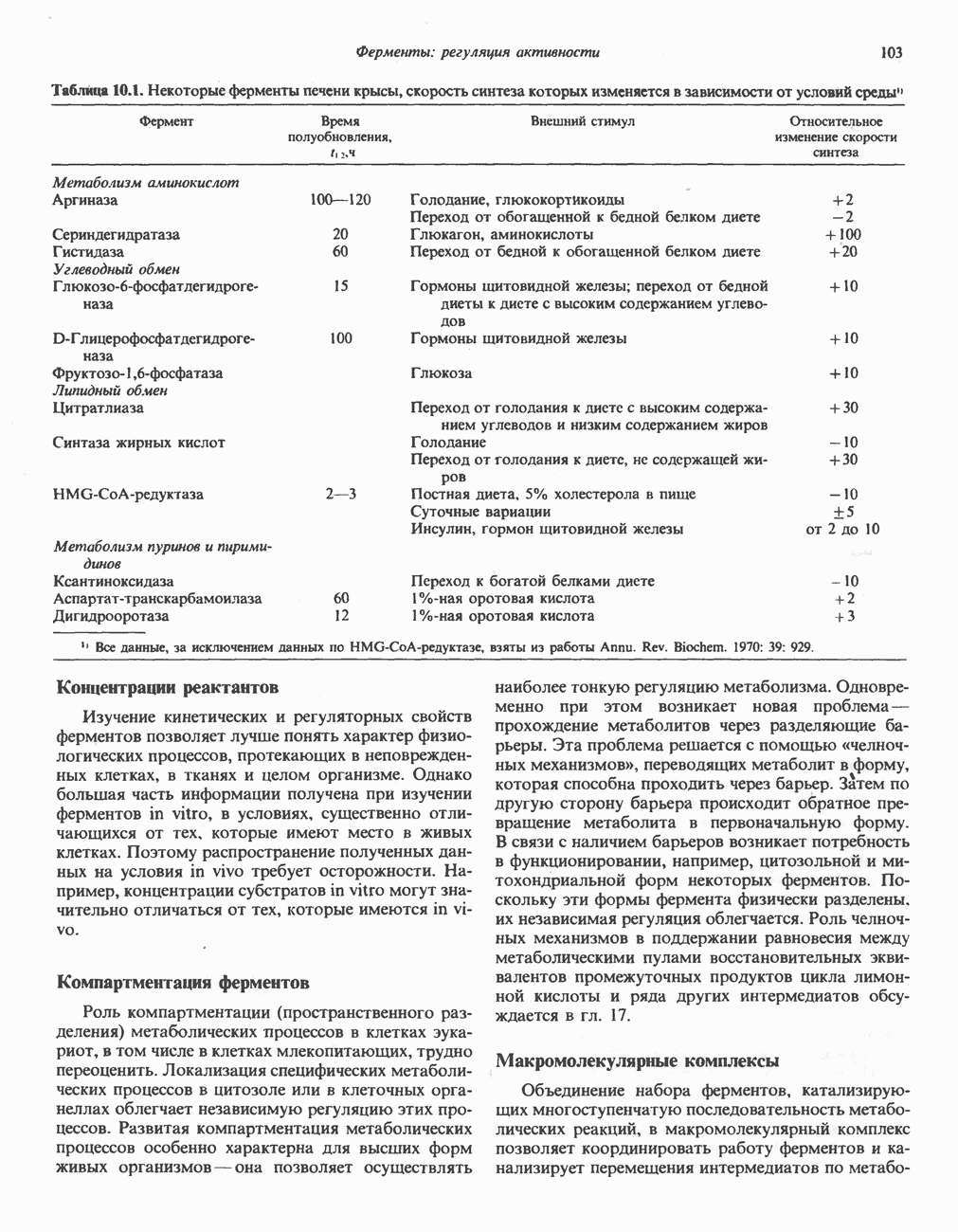
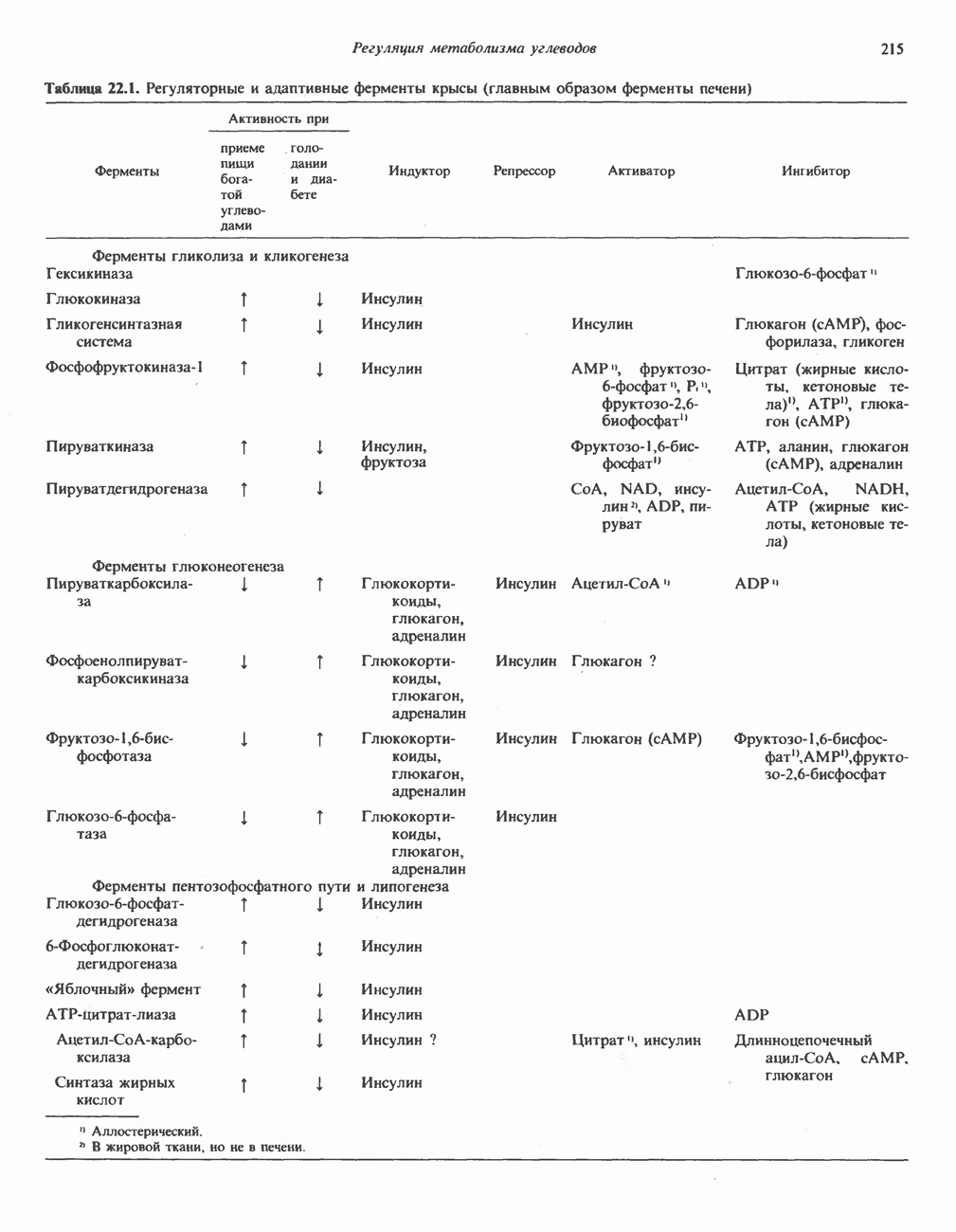
Содержание ферментов в тканях млекопитающих может изменяться в результате действия различных физиологических и гормональных факторов, а также под влиянием диеты. Известно много примеров такого рода для разных тканей и различных метаболических путей (табл. 10.1), однако наши знания о молекулярном механизме процессов носят фрагментарный характер.
Глюкокортикоиды повышают концентрацию тирозин-трансаминазы, увеличивая  На этом примере была впервые четко показана гормональная регуляция синтеза фермента в тканях млекопитающих. Инсулин и глюкагон, несмотря на взаимный антагонизм их физиологического действия, оба независимо повышают
На этом примере была впервые четко показана гормональная регуляция синтеза фермента в тканях млекопитающих. Инсулин и глюкагон, несмотря на взаимный антагонизм их физиологического действия, оба независимо повышают  в 4—5 раз. Действие глюкагона, вероятно, опосредуется
в 4—5 раз. Действие глюкагона, вероятно, опосредуется  который оказывает аналогичное гормону действие в органной культуре печени крысы.
который оказывает аналогичное гормону действие в органной культуре печени крысы.
Превращение проферментов в активные ферменты
Ферментативная активность может регулироваться путем превращения неактивного профермента в каталитически активную форму. Чтобы перейти в такую форму, профермент должен подвергнуться ограниченному протеолизу, сопровождающемуся конформационными изменениями; при этом происходит либо демаскирование каталитического центра, либо его формирование (см. гл. 8). Синтез в форме каталитически неактивных проферментов является характерным свойством пищеварительных ферментов, а также ферментов системы свертывания крови и системы фибринолиза (см. гл. 55).
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие к русскому изданию
- Предисловие
- Глава 1. Биохимия и медицина
- Глава 2. Биомолекулы и биохимические методы
- КЛЕТКА
- ОБЩИЙ ЭКСПЕРИМЕНТАЛЬНЫЙ ПОДХОД, ИСПОЛЬЗУЕМЫЙ В БИОХИМИИ
- ОСНОВНЫЕ ДОСТИЖЕНИЯ БИОХИМИИ
- Раздел I. Структура и функции белков и ферментов
- Глава 3. Аминокислоты
- АМИНОКИСЛОТЫ
- ИОННЫЕ ФОРМЫ АМИНОКИСЛОТ
- СТРУКТУРА АМИНОКИСЛОТ
- РАСТВОРИМОСТЬ АМИНОКИСЛОТ
- ОБЩИЕ ХИМИЧЕСКИЕ РЕАКЦИИ
- СВОЙСТВА ИНДИВИДУАЛЬНЫХ АМИНОКИСЛОТ
- МЕТОДЫ РАЗДЕЛЕНИЯ АМИНОКИСЛОТ
- Глава 4. Пептиды
- СТРУКТУРА ПЕПТИДОВ
- ИОННЫЕ ФОРМЫ ПЕПТИДОВ
- КОНФОРМАЦИЯ ПЕПТИДОВ В РАСТВОРЕ
- МЕТОДЫ РАЗДЕЛЕНИЯ ПЕПТИДОВ
- ОПРЕДЕЛЕНИЕ АМИНОКИСЛОТНОГО СОСТАВА ПЕПТИДОВ
- ОПРЕДЕЛЕНИЕ ПЕРВИЧНОЙ СТРУКТУРЫ ПОЛИПЕПТИДОВ
- АВТОМАТИЧЕСКОЕ ОПРЕДЕЛЕНИЕ АМИНОКИСЛОТНОЙ ПОСЛЕДОВАТЕЛЬНОСТИ ПОЛИПЕПТИДОВ МЕТОДОМ ЭДМАНА
- АВТОМАТИЧЕСКИЙ СИНТЕЗ ПЕПТИДОВ
- ЛИТЕРАТУРА
- Глава 5. Белки: структура и свойства
- КЛАССИФИКАЦИЯ БЕЛКОВ
- СВЯЗИ, ОТВЕТСТВЕННЫЕ ЗА ФОРМИРОВАНИЕ СТРУКТУРЫ БЕЛКА
- УПОРЯДОЧЕННЫЕ КОНФОРМАЦИИ ПОЛИПЕПТИДОВ
- УРОВНИ СТРУКТУРНОЙ ОРГАНИЗАЦИИ БЕЛКА
- ДЕНАТУРАЦИЯ
- МЕТОДЫ ОПРЕДЕЛЕНИЯ ПЕРВИЧНОЙ СТРУКТУРЫ
- ОПРЕДЕЛЕНИЕ ВТОРИЧНОЙ И ТРЕТИЧНОЙ СТРУКТУРЫ МЕТОДОМ РЕНТГЕНОВСКОЙ КРИСТАЛЛОГРАФИИ
- ОПРЕДЕЛЕНИЕ ЧЕТВЕРТИЧНОЙ СТРУКТУРЫ
- ГЛАВА 6. Белки: миоглобин и гемоглобин
- ГЕМОПРОТЕИНЫ — МИОГЛОБИН И ГЕМОГЛОБИН
- МИОГЛОБИН
- ГЕМОГЛОБИНЫ
- Глава 7. Ферменты: общие свойства
- КОФЕРМЕНТЫ
- «ТРЕХТОЧЕЧНАЯ ФИКСАЦИЯ» СУБСТРАТОВ НА ФЕРМЕНТАХ
- СПЕЦИФИЧНОСТЬ ФЕРМЕНТОВ
- КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ФЕРМЕНТАТИВНОЙ АКТИВНОСТИ
- ВЫДЕЛЕНИЕ ФЕРМЕНТОВ
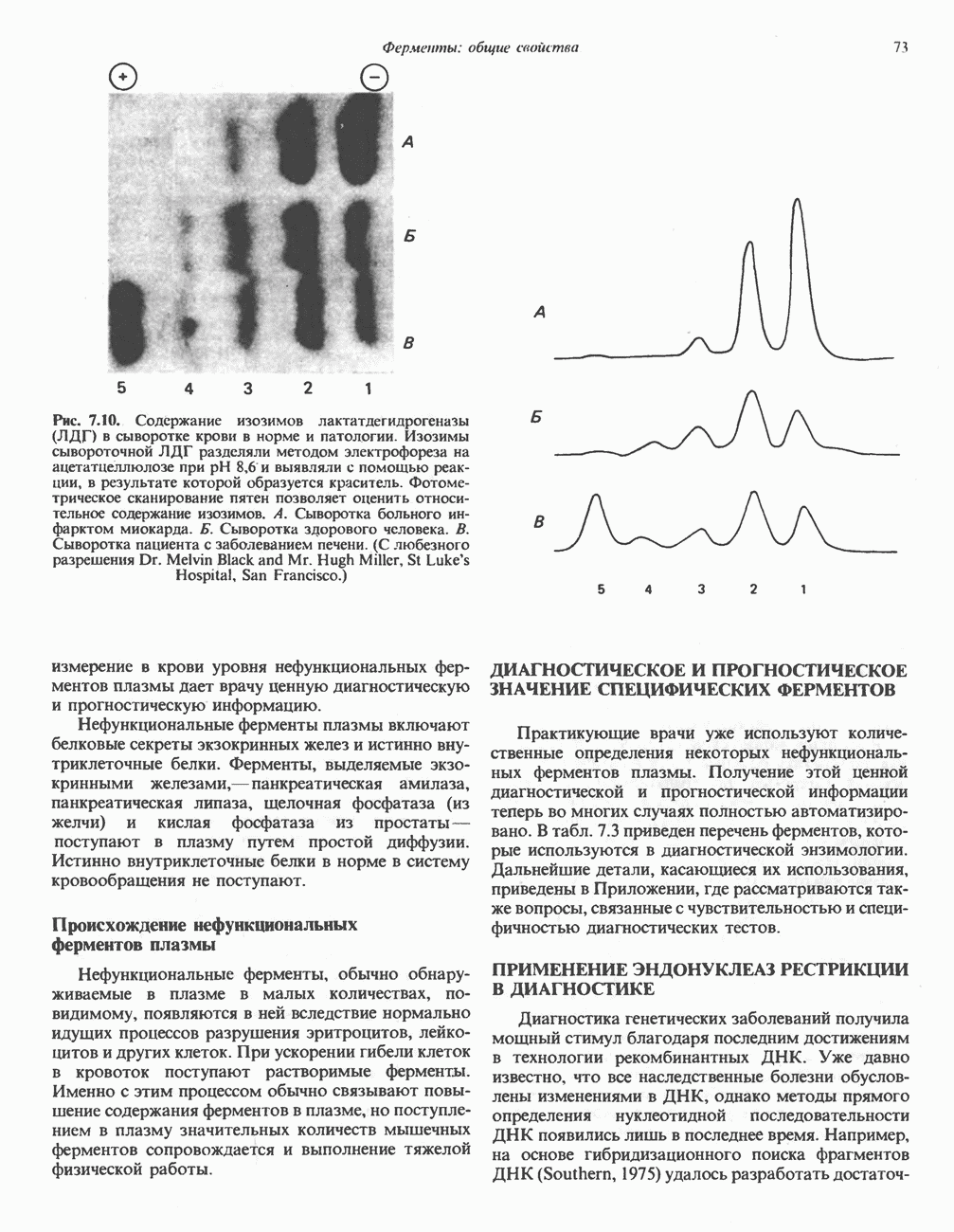
- ИЗОФЕРМЕНТЫ (ИЗОЗИМЫ)
- ФЕРМЕНТЫ В КЛИНИЧЕСКОЙ ДИАГНОСТИКЕ
- ДИАГНОСТИЧЕСКОЕ И ПРОГНОСТИЧЕСКОЕ ЗНАЧЕНИЕ СПЕЦИФИЧЕСКИХ ФЕРМЕНТОВ
- ПРИМЕНЕНИЕ ЭНДОНУКЛЕАЗ РЕСТРИКЦИИ В ДИАГНОСТИКЕ
- ЛИТЕРАТУРА
- Глава 8. ФЕРМЕНТЫ: КИНЕТИКА
- ОБРАЗОВАНИЕ И РАСПАД ПЕРЕХОДНЫХ СОСТОЯНИЙ
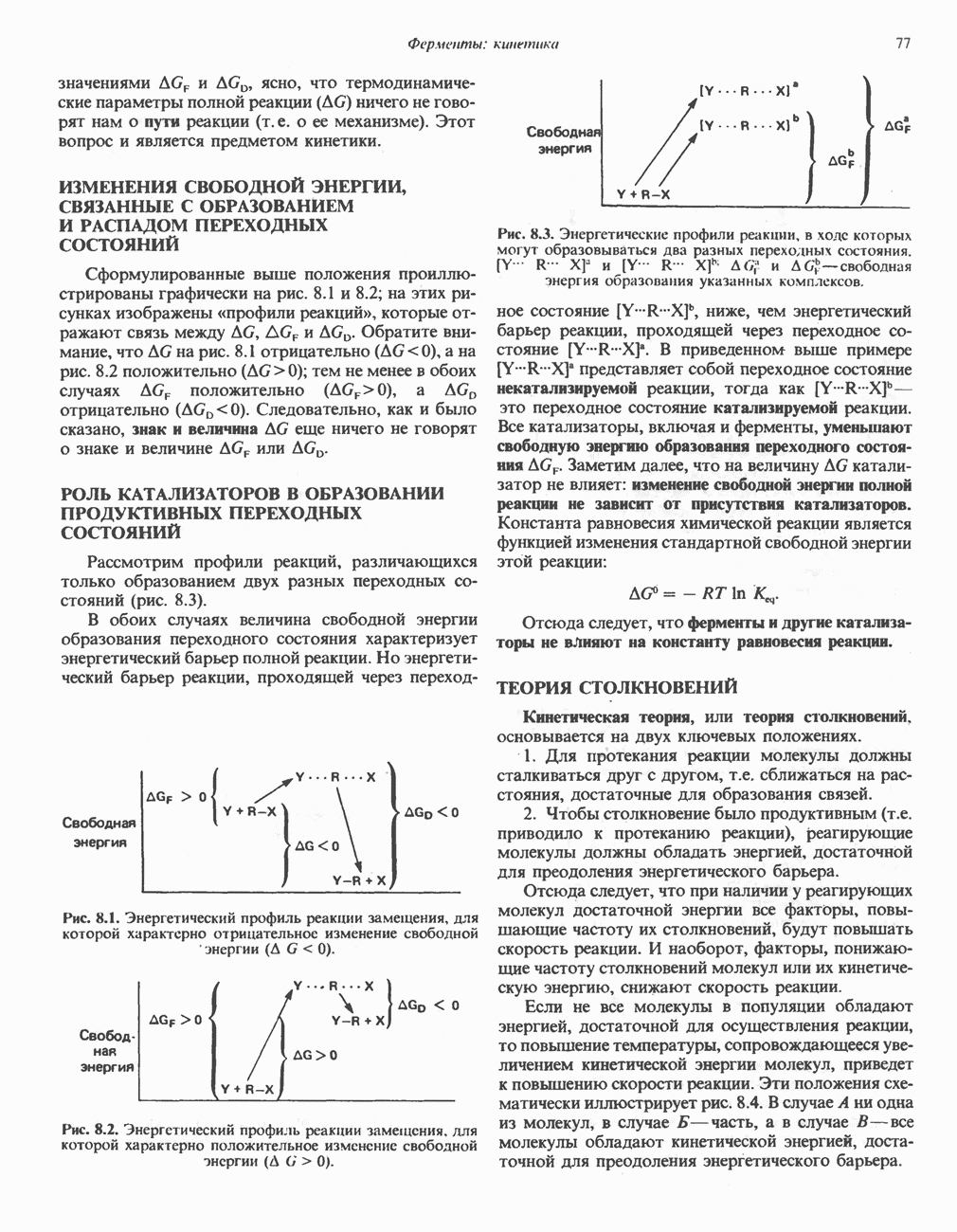
- ИЗМЕНЕНИЯ СВОБОДНОЙ ЭНЕРГИИ, СВЯЗАННЫЕ С ОБРАЗОВАНИЕМ И РАСПАДОМ ПЕРЕХОДНЫХ СОСТОЯНИЙ
- РОЛЬ КАТАЛИЗАТОРОВ В ОБРАЗОВАНИИ ПРОДУКТИВНЫХ ПЕРЕХОДНЫХ СОСТОЯНИЙ
- ТЕОРИЯ СТОЛКНОВЕНИЙ
- РОЛЬ ФЕРМЕНТОВ В РАЗРЫВЕ И ОБРАЗОВАНИИ КОВАЛЕНТНЫХ СВЯЗЕЙ
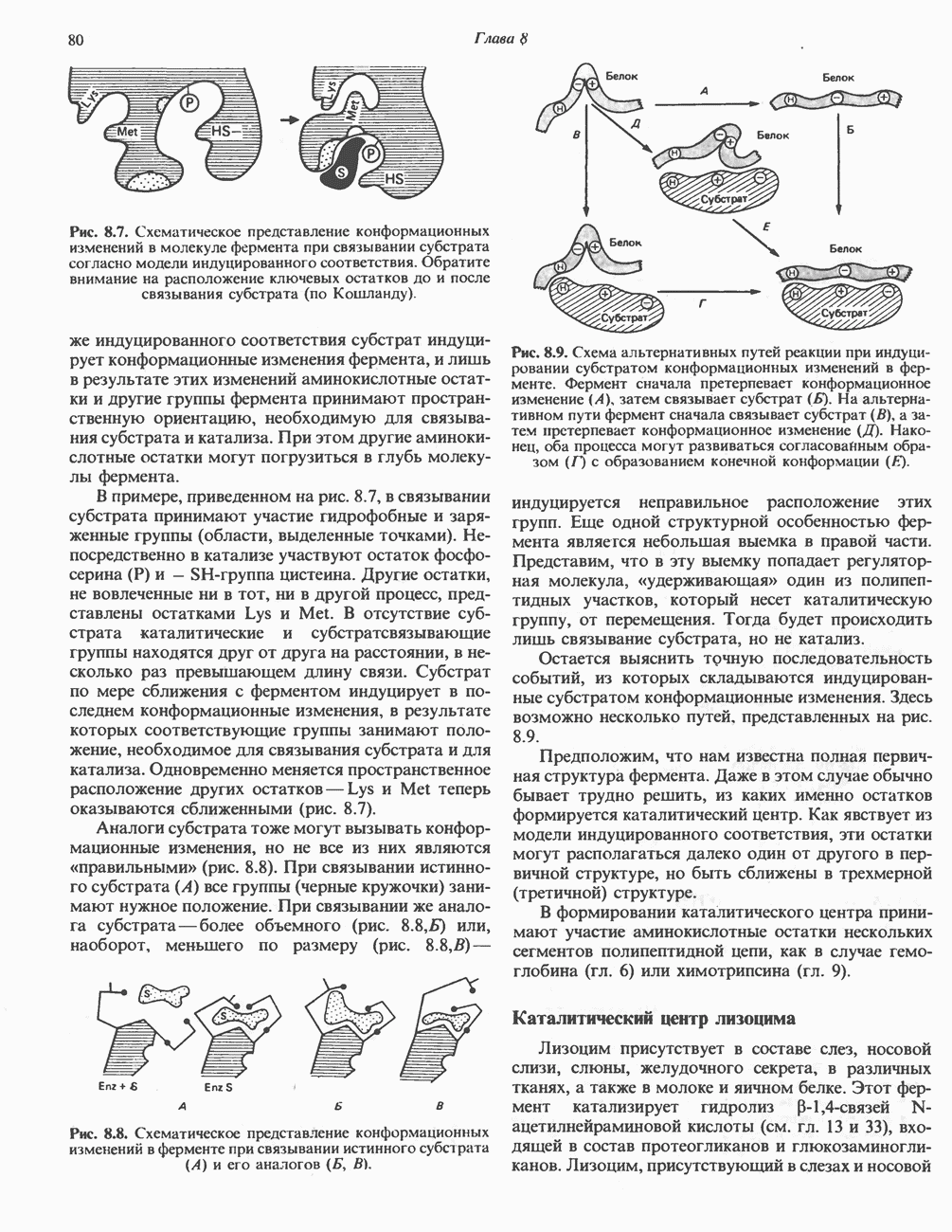
- КАТАЛИТИЧЕСКИЙ ЦЕНТР
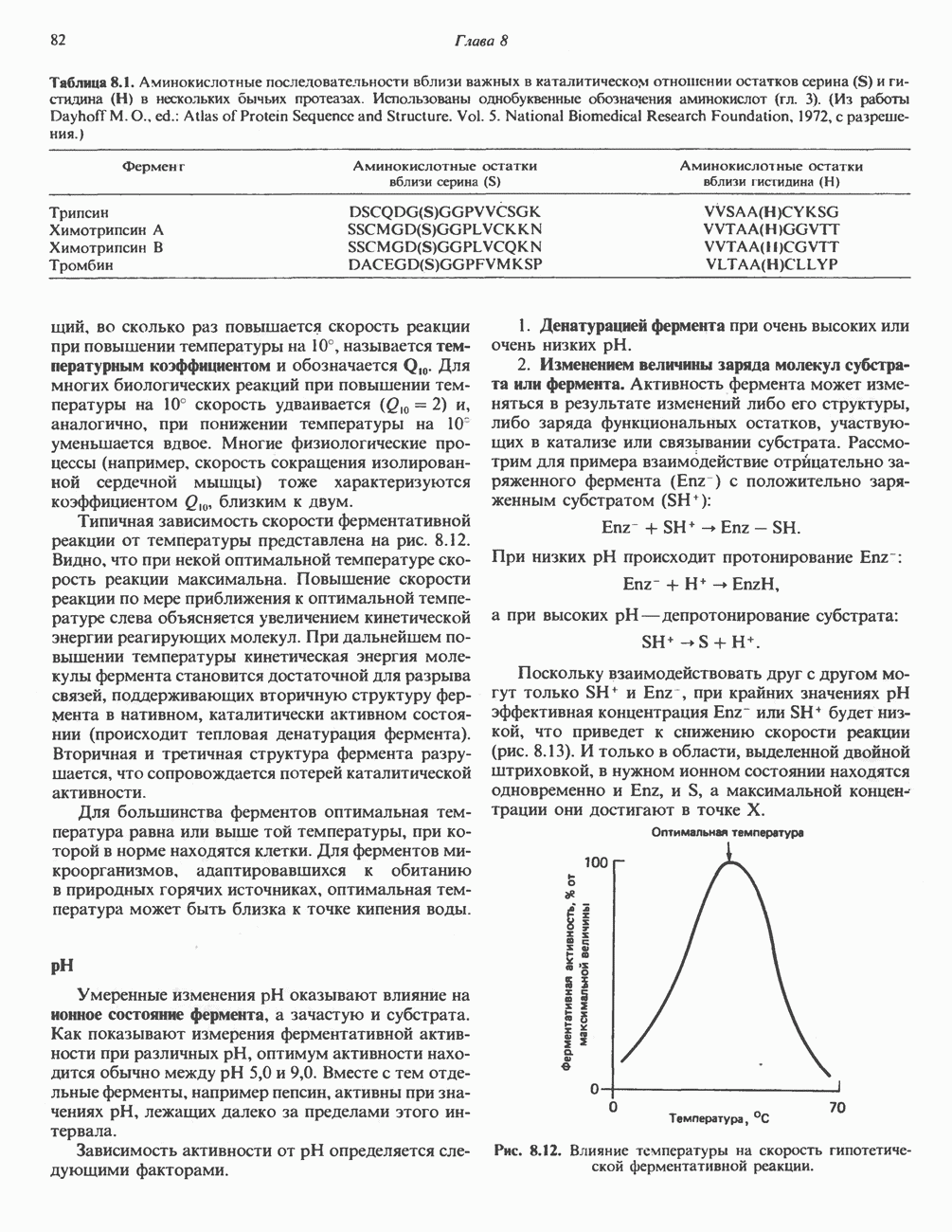
- ФАКТОРЫ, ВЛИЯЮЩИЕ НА АКТИВНОСТЬ ФЕРМЕНТОВ
- КОНСТАНТА РАВНОВЕСИЯ
- КОНЦЕНТРАЦИЯ ФЕРМЕНТА
- КОНЦЕНТРАЦИЯ СУБСТРАТА
- УРАВНЕНИЕ МИХАЭЛИСА—МЕНТЕН
- ОГРАНИЧЕНИЯ, ПРИСУЩИЕ УРАВНЕНИЮ МИХАЭЛИСА — МЕНТЕН
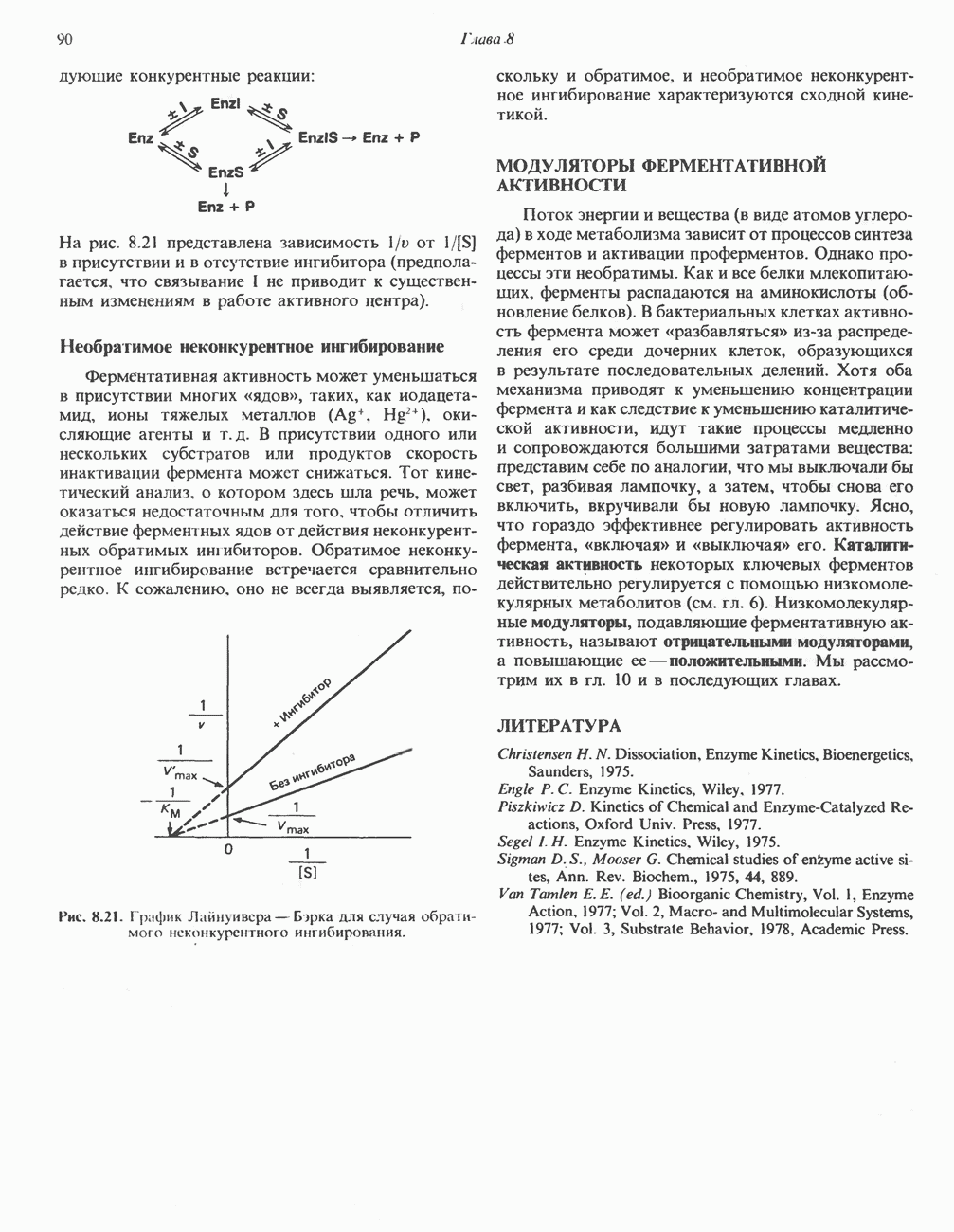
- ИНГИБИРОВАНИЕ АКТИВНОСТИ ФЕРМЕНТОВ
- МОДУЛЯТОРЫ ФЕРМЕНТАТИВНОЙ АКТИВНОСТИ
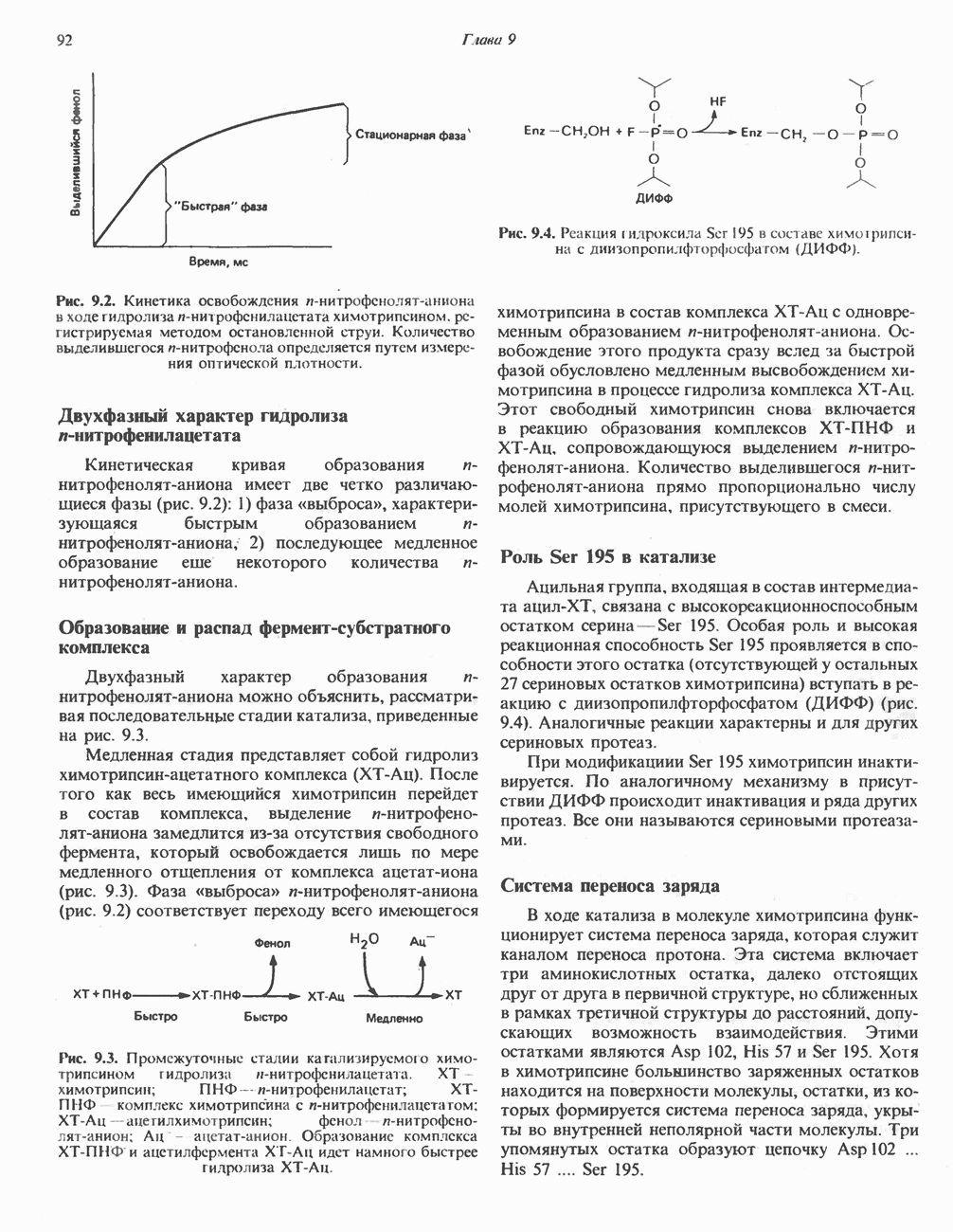
- Глава 9. Ферменты: механизм действия
- МЕХАНИЗМ КАТАЛИТИЧЕСКОГО ДЕЙСТВИЯ ХИМОТРИПСИНА
- РОЛЬ ИЗБИРАТЕЛЬНОГО ПРОТЕОЛИЗА В ФОРМИРОВАНИИ АКТИВНЫХ ЦЕНТРОВ ФЕРМЕНТОВ
- УПОРЯДОЧЕННОЕ И НЕУПОРЯДОЧЕННОЕ СВЯЗЫВАНИЕ СУБСТРАТОВ
- ФЕРМЕНТЫ КАК КАТАЛИЗАТОРЫ ОБЩЕГО КИСЛОТНОГО И ОБЩЕГО ОСНОВНОГО ТИПА
- ИОНЫ МЕТАЛЛОВ
- Глава 10. Ферменты: регуляция активности
- РЕГУЛЯЦИЯ МЕТАБОЛИЗМА
- РЕГУЛЯЦИЯ КОЛИЧЕСТВА ФЕРМЕНТА ПУТЕМ РЕГУЛЯЦИИ СКОРОСТИ ЕГО СИНТЕЗА И РАСПАДА
- РЕГУЛЯЦИЯ КАТАЛИТИЧЕСКОЙ АКТИВНОСТИ ФЕРМЕНТОВ
- АЛЛОСТЕРИЧЕСКАЯ РЕГУЛЯЦИЯ
- КОВАЛЕНТНАЯ МОДИФИКАЦИЯ ФЕРМЕНТОВ
- Раздел II. Биоэнергетика и метаболизм углеводов и липидов
- Глава 11. Биоэнергетика
- СВОБОДНАЯ ЭНЕРГИЯ И ЗАКОНЫ ТЕРМОДИНАМИКИ
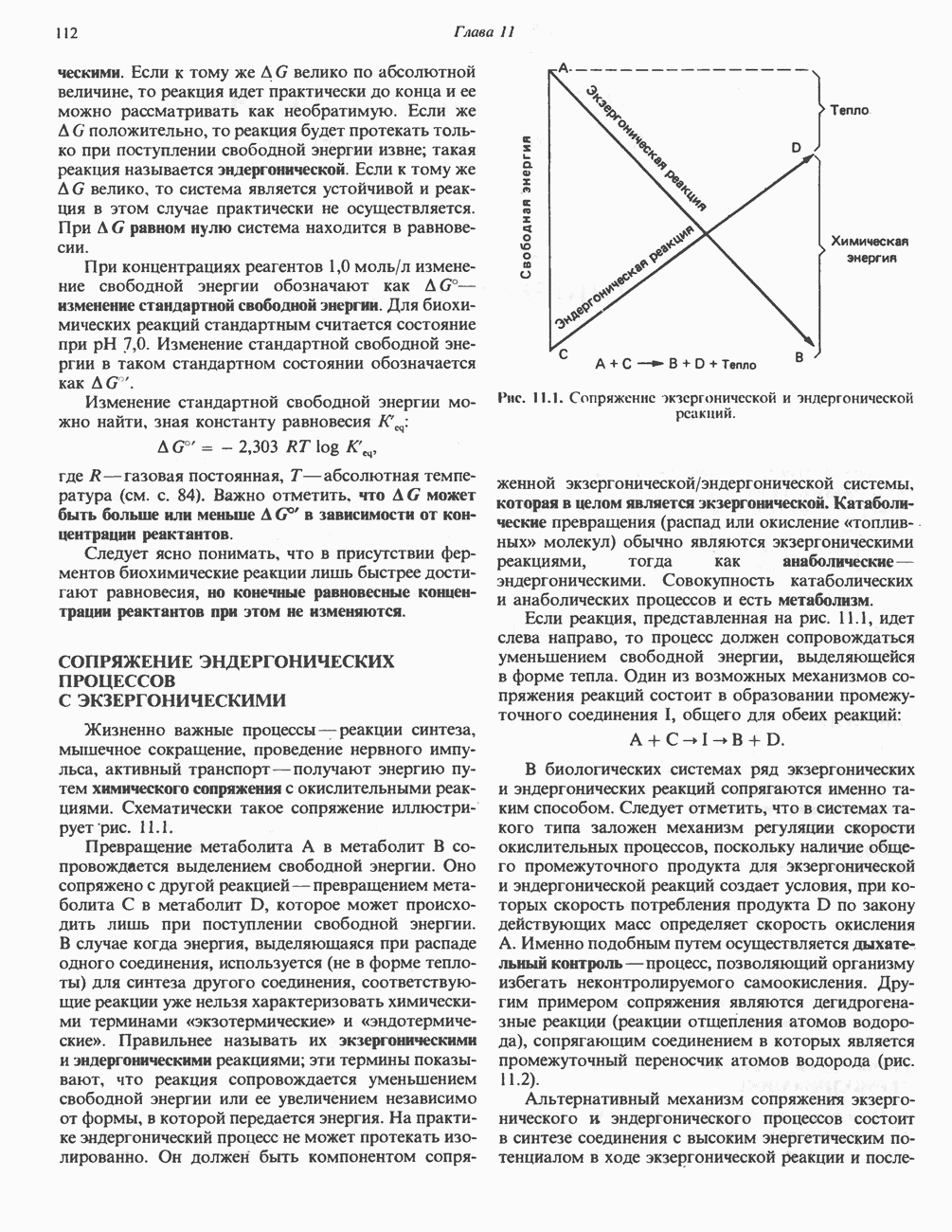
- СОПРЯЖЕНИЕ ЭНДЕРГОНИЧЕСКИХ ПРОЦЕССОВ С ЭКЗЕРГОНИЧЕСКИМИ
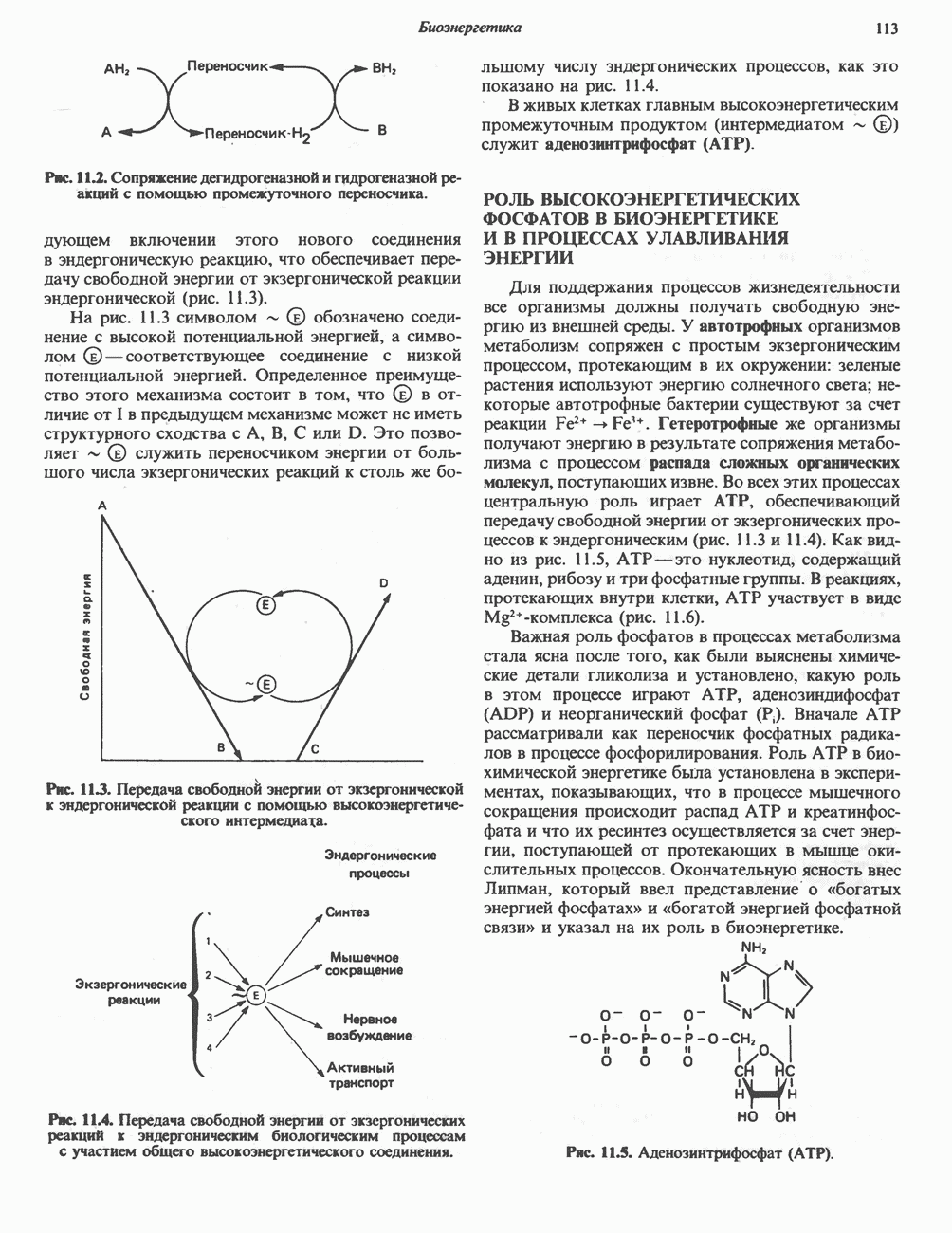
- РОЛЬ ВЫСОКОЭНЕРГЕТИЧЕСКИХ ФОСФАТОВ В БИОЭНЕРГЕТИКЕ И В ПРОЦЕССАХ УЛАВЛИВАНИЯ ЭНЕРГИИ
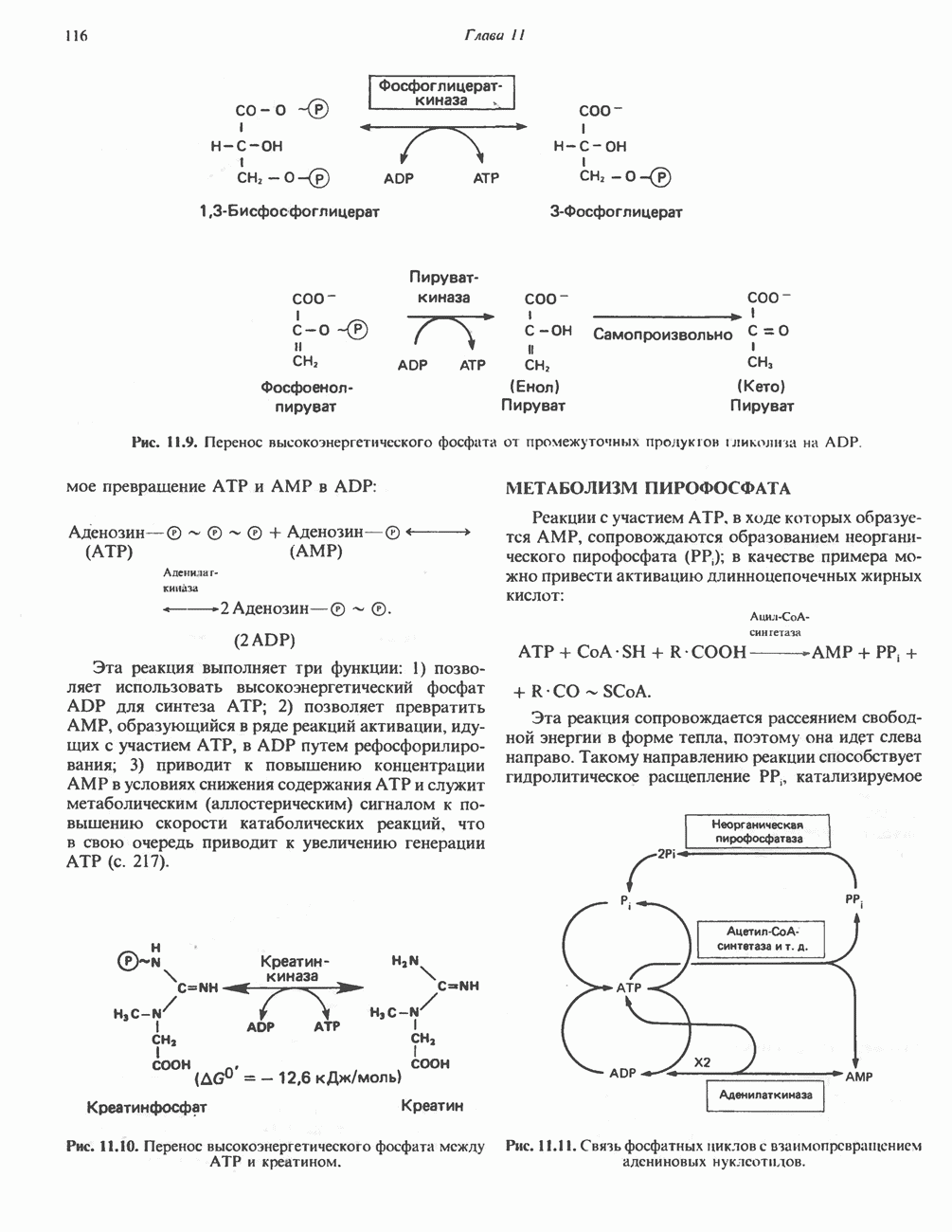
- МЕТАБОЛИЗМ ПИРОФОСФАТА
- Глава 12. Биологическое окисление
- ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНОЕ РАВНОВЕСИЕ, ОКИСЛИТЕЛЬНОВОССТАНОВИТЕЛЬНЫЙ ПОТЕНЦИАЛ
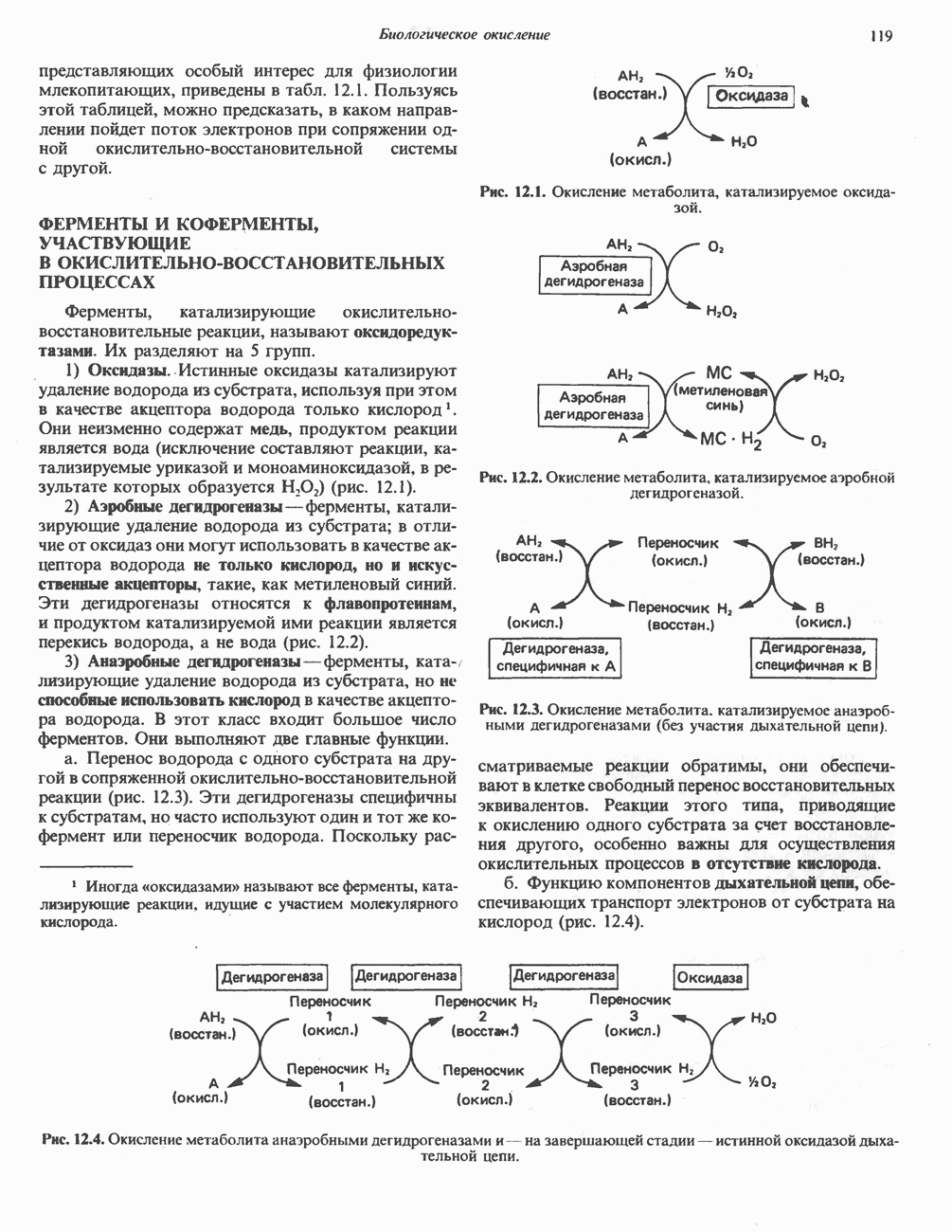
- ФЕРМЕНТЫ И КОФЕРМЕНТЫ, УЧАСТВУЮЩИЕ В ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ ПРОЦЕССАХ
- Глава 13. Окислительное фосфорилирование и транспортные системы митохондрий
- ДЫХАТЕЛЬНАЯ ЦЕПЬ
- ОРГАНИЗАЦИЯ ДЫХАТЕЛЬНОЙ ЦЕПИ В МИТОХОНДРИЯХ
- РОЛЬ ДЫХАТЕЛЬНОЙ ЦЕПИ В УЛАВЛИВАНИИ ЭНЕРГИИ
- ДЫХАТЕЛЬНЫЙ КОНТРОЛЬ
- ИНГИБИТОРЫ ДЫХАТЕЛЬНОЙ ЦЕПИ И ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ
- МЕХАНИЗМ ОКИСЛИТЕЛЬНОГО ФОСФОРИЛИРОВАНИЯ
- МИТОХОНДРИАЛЬНЫЕ ТРАНСПОРТНЫЕ СИСТЕМЫ
- Глава 14. Физиологически важные углеводы
- КЛАССИФИКАЦИЯ УГЛЕВОДОВ
- МОНОСАХАРИДЫ
- ДИСАХАРИДЫ
- ПОЛИСАХАРИДЫ
- УГЛЕВОДЫ КЛЕТОЧНЫХ МЕМБРАН
- Глава 15. Физиологически важные липиды
- КЛАССИФИКАЦИЯ ЛИПИДОВ
- ЖИРНЫЕ КИСЛОТЫ
- ТРИАЦИЛГЛИЦЕРОЛЫ (триглицериды)
- ФОСФОЛИПИДЫ
- ГЛИКОЛИПИДЫ (ГЛИКОСФИНГОЛИПИДЫ)
- СТЕРОИДЫ
- ПЕРЕКИСНОЕ ОКИСЛЕНИЕ ЛИПИДОВ
- МЕТОДЫ РАЗДЕЛЕНИЯ И ИДЕНТИФИКАЦИИ ЛИПИДОВ, СОДЕРЖАЩИХСЯ В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ
- АМФИПАТИЧЕСКИЕ ЛИПИДЫ
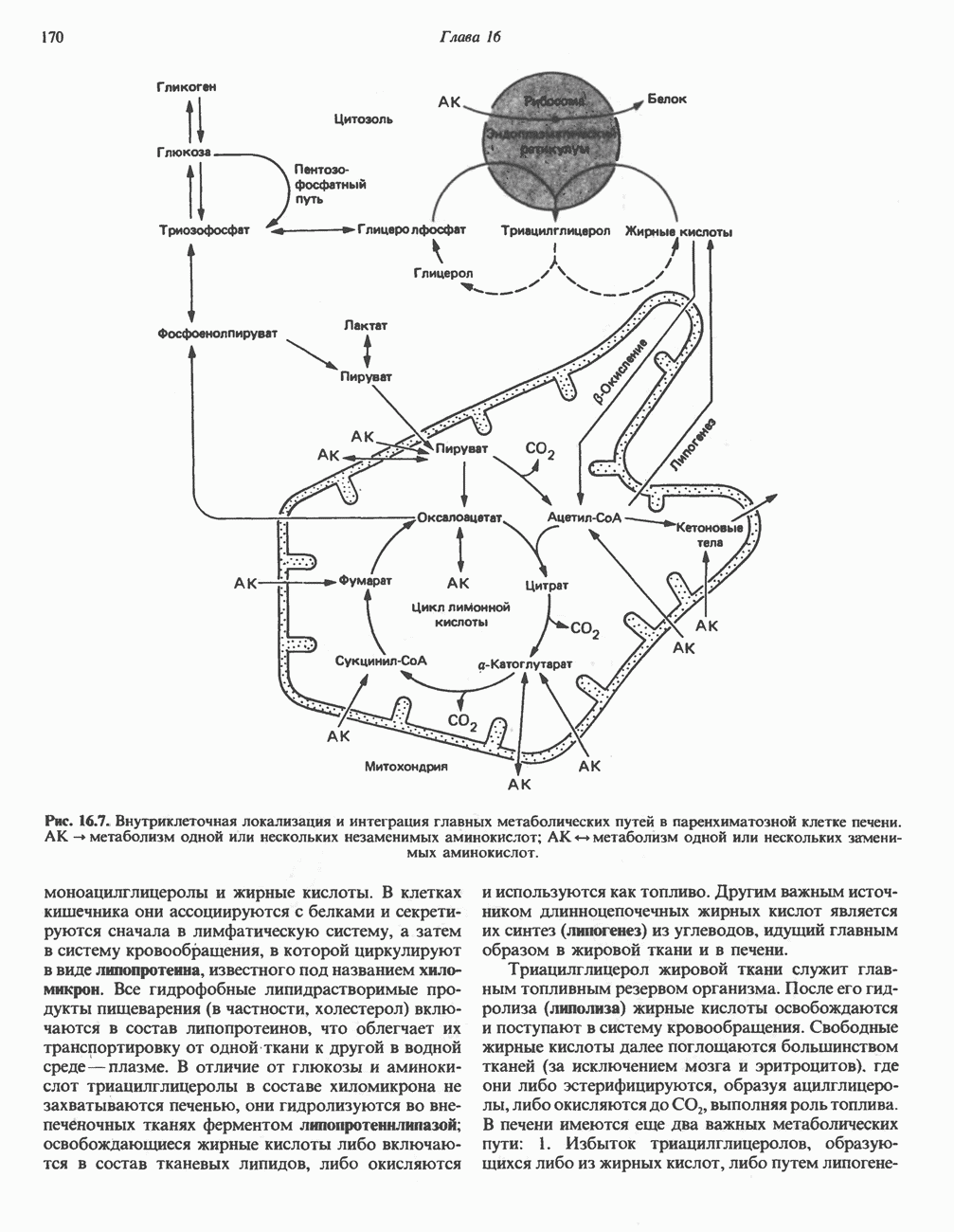
- Глава 16. Промежуточный обмен
- ОСНОВНЫЕ МЕТАБОЛИЧЕСКИЕ ПУТИ
- ЛОКАЛИЗАЦИЯ МЕТАБОЛИЧЕСКИХ ПУТЕЙ
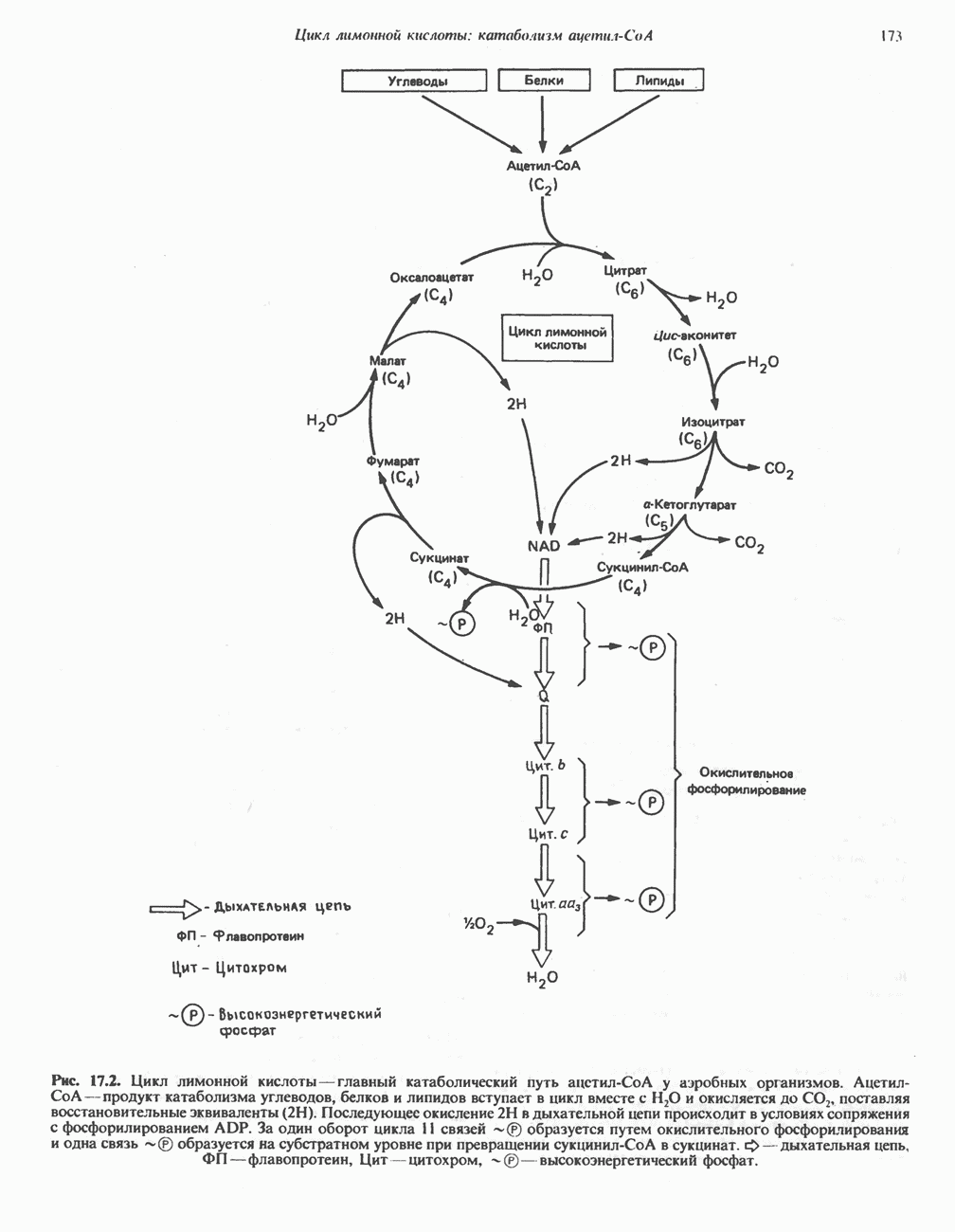
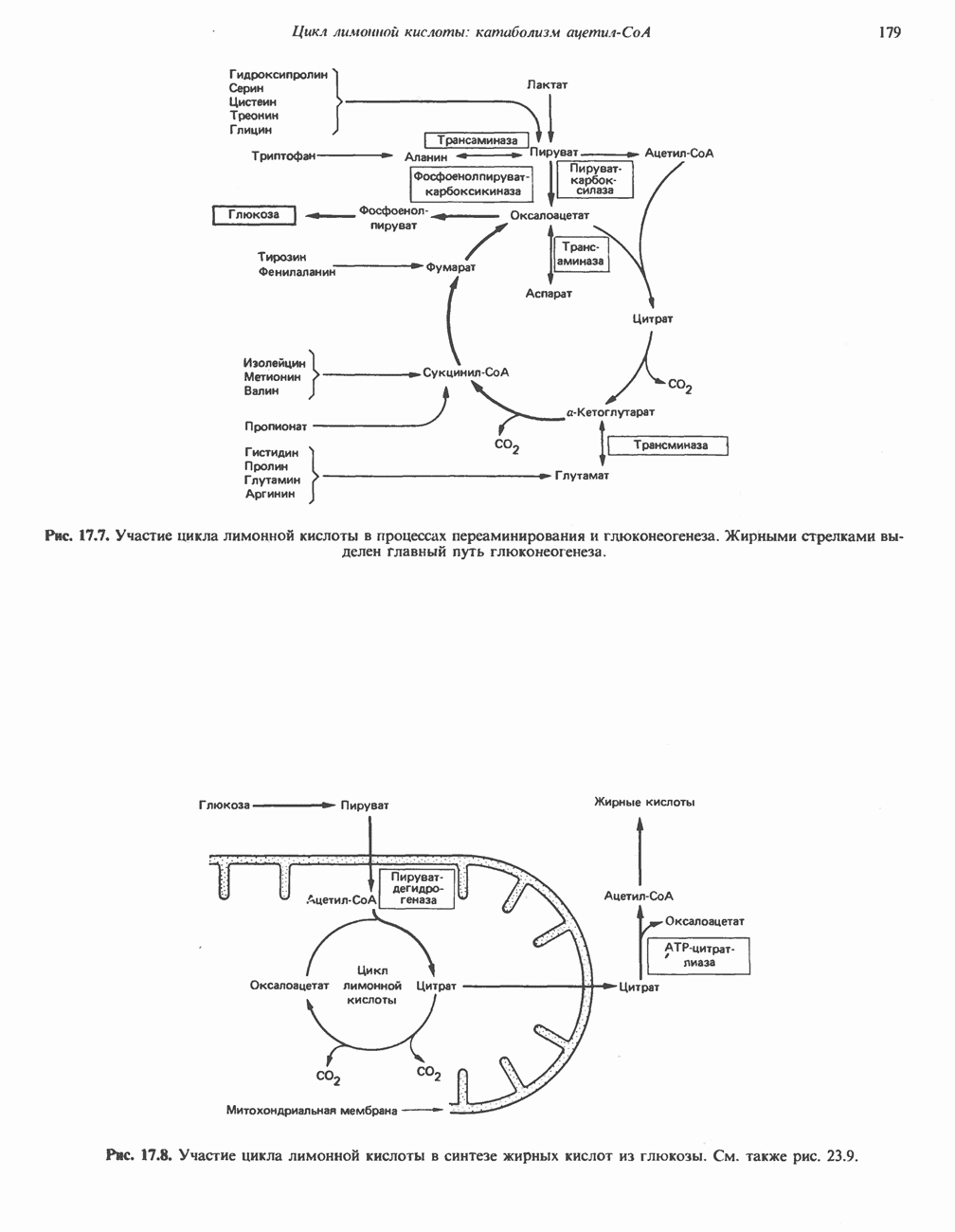
- Глава 17. Цикл лимонной кислоты: катаболизм ацетил-СоА
- КАТАБОЛИЧЕСКАЯ РОЛЬ ЦИКЛА ЛИМОННОЙ КИСЛОТЫ
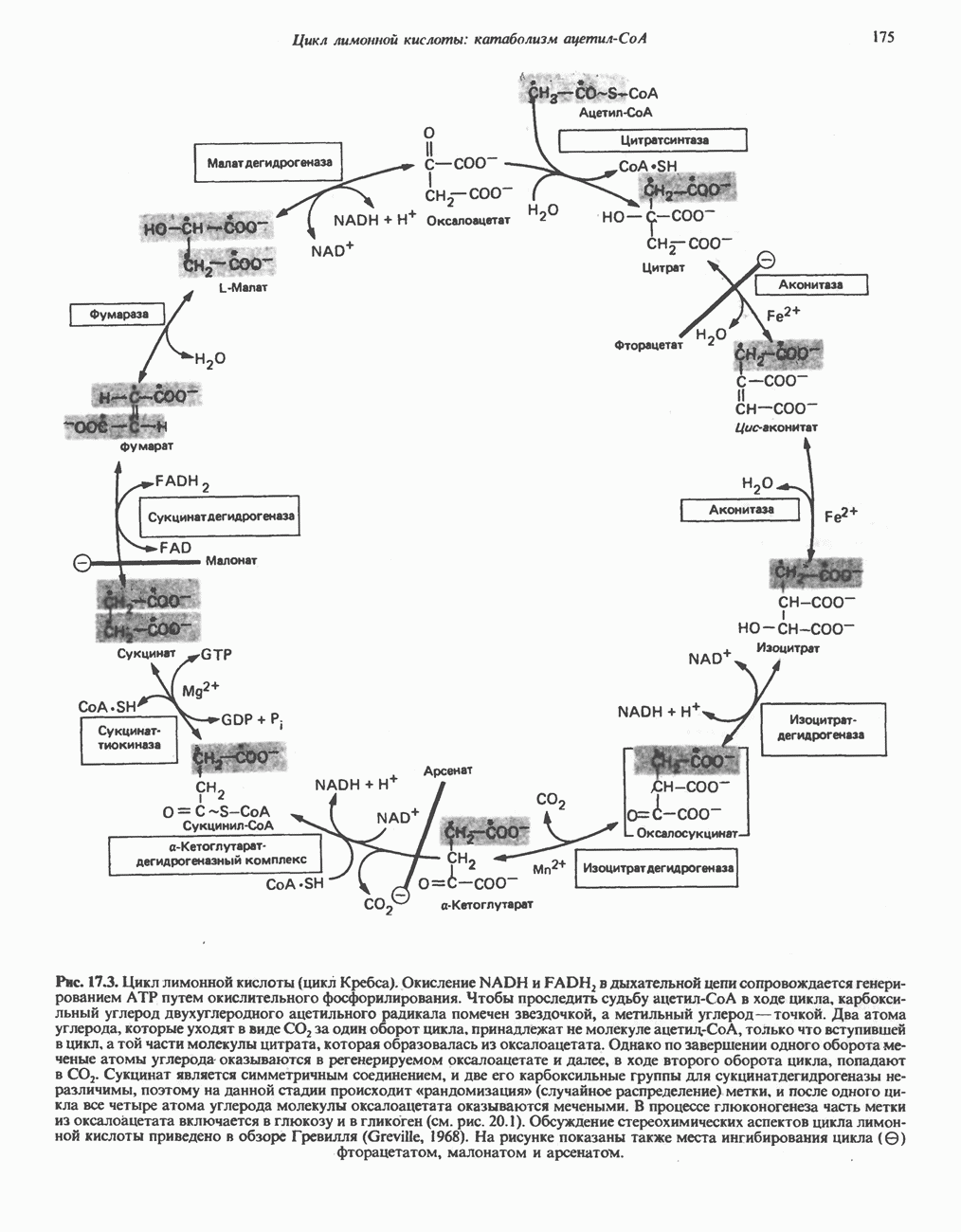
- РЕАКЦИИ ЦИКЛА ЛИМОННОЙ КИСЛОТЫ (рис. 17.3)
- ЭНЕРГЕТИКА ЦИКЛА ЛИМОННОЙ КИСЛОТЫ
- РОЛЬ ВИТАМИНОВ В ЦИКЛЕ ЛИМОННОЙ КИСЛОТЫ
- АМФИБОЛИЧЕСКАЯ РОЛЬ ЦИКЛА ЛИМОННОЙ КИСЛОТЫ
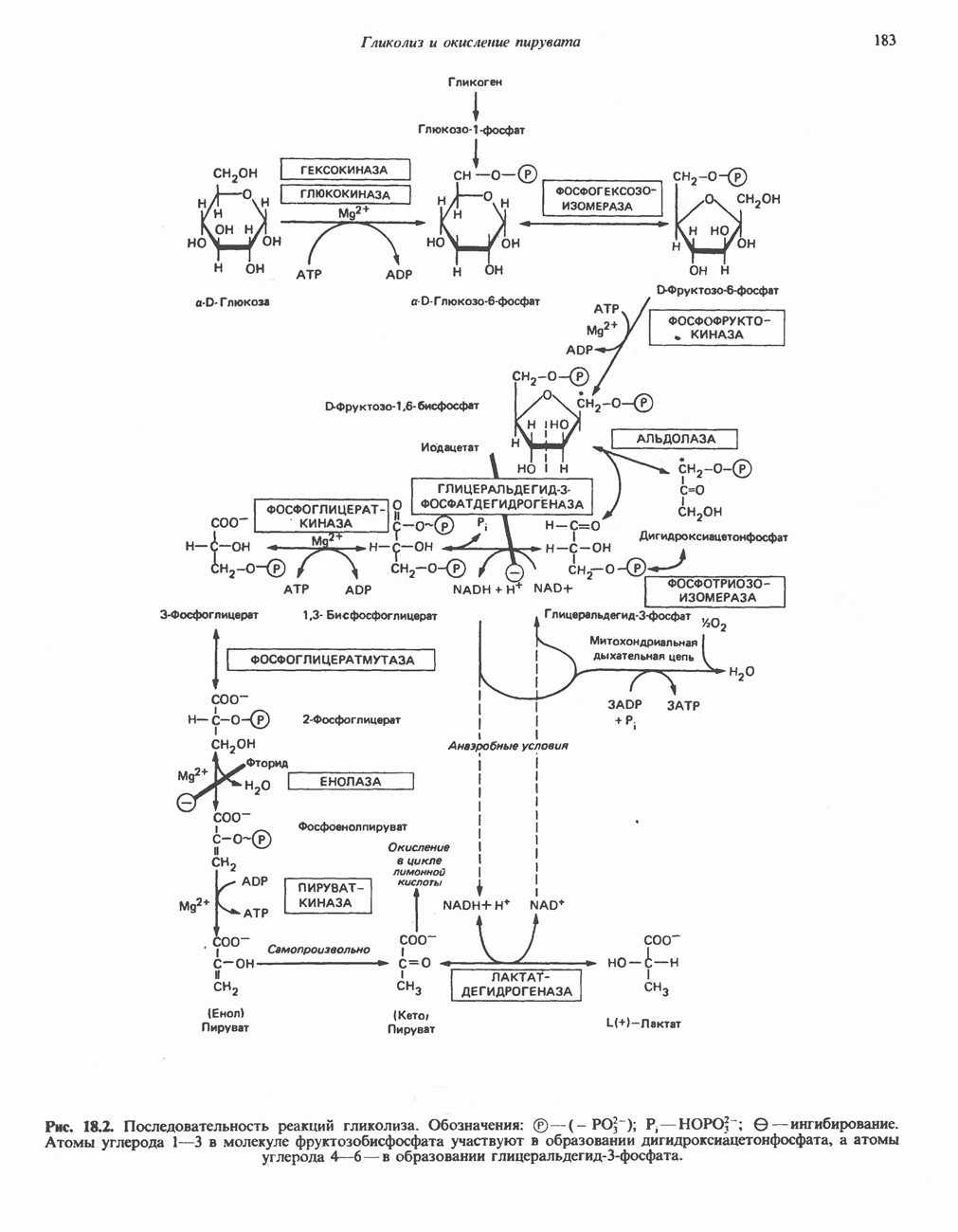
- Глава 18. Гликолиз и окисление пирувата
- ГЛИКОЛИТИЧЕСКИЙ ПУТЬ
- ПОСЛЕДОВАТЕЛЬНЫЕ СТАДИИ ГЛИКОЛИЗА
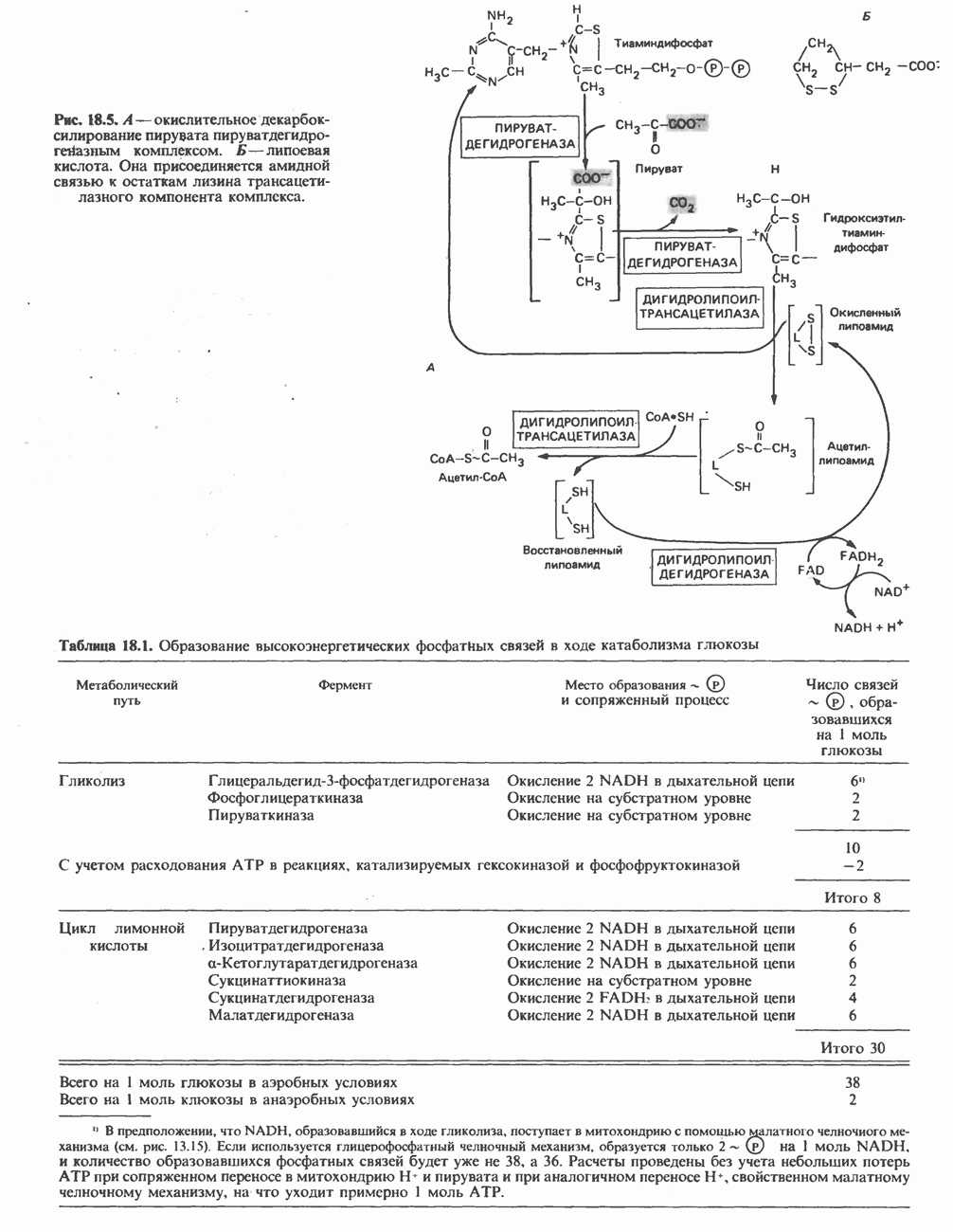
- ОКИСЛЕНИЕ ПИРУВАТА В АЦЕТИЛ-СоА
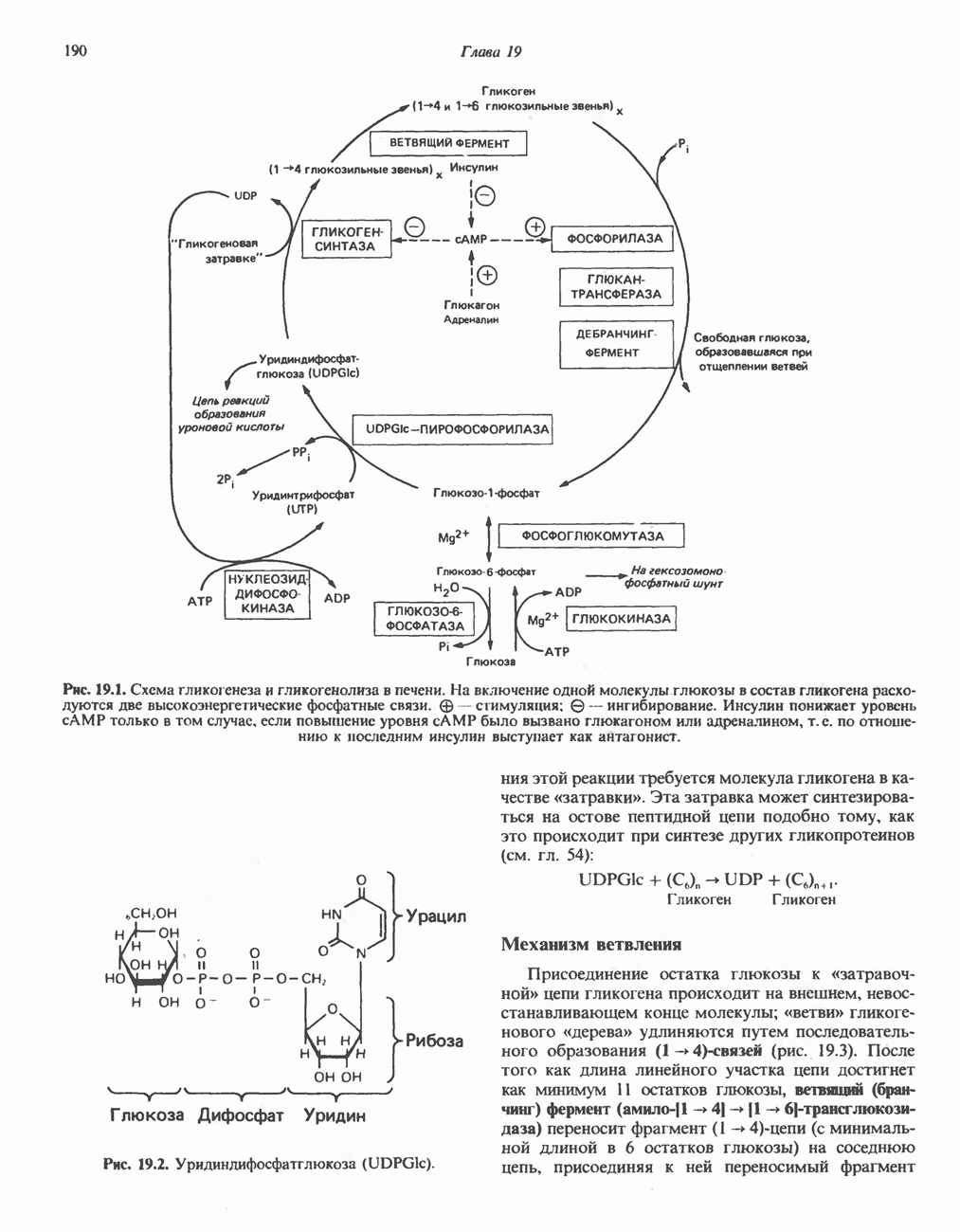
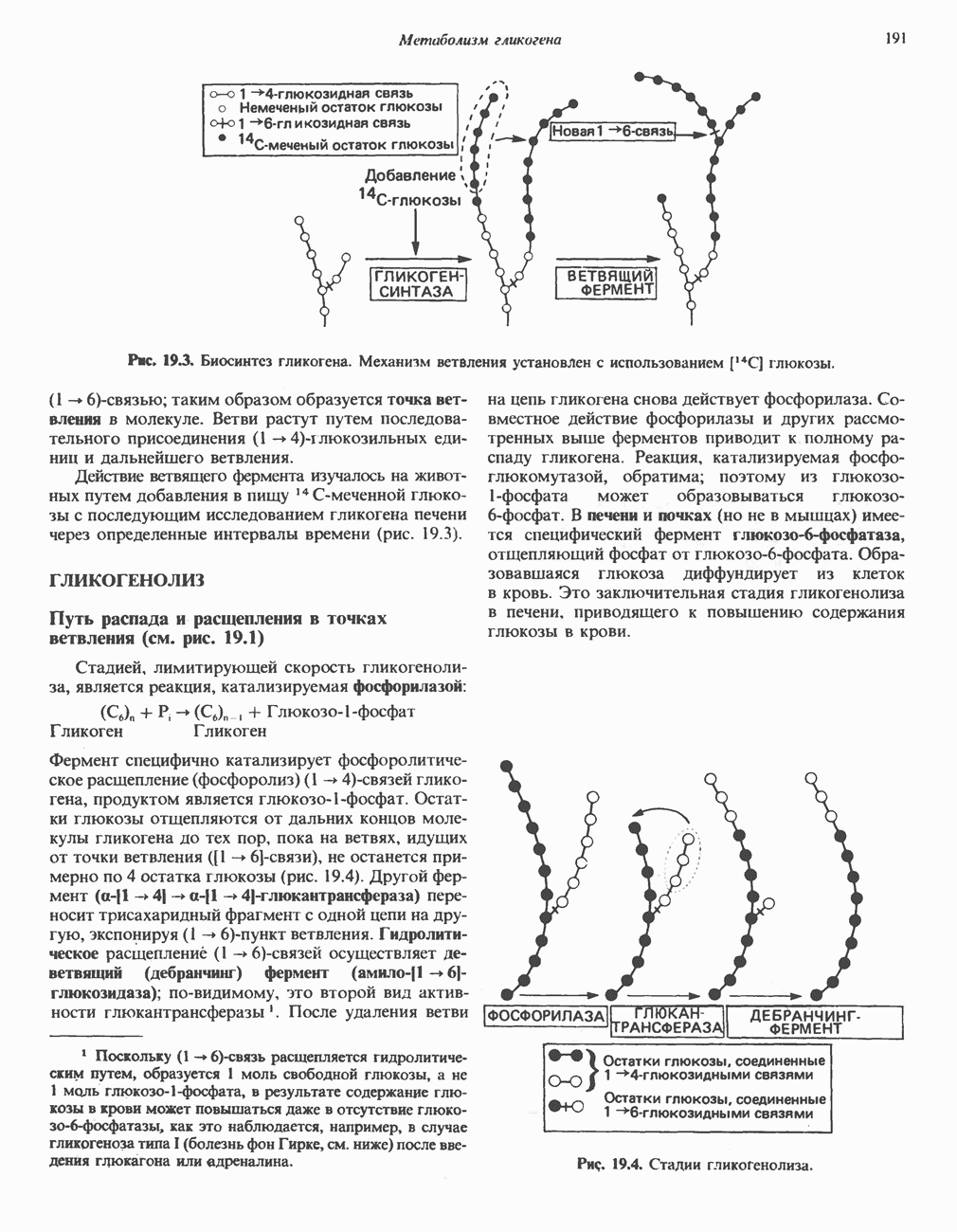
- Глава 19. Метаболизм гликогена
- ГЛИКОГЕНЕЗ
- ГЛИКОГЕНОЛИЗ
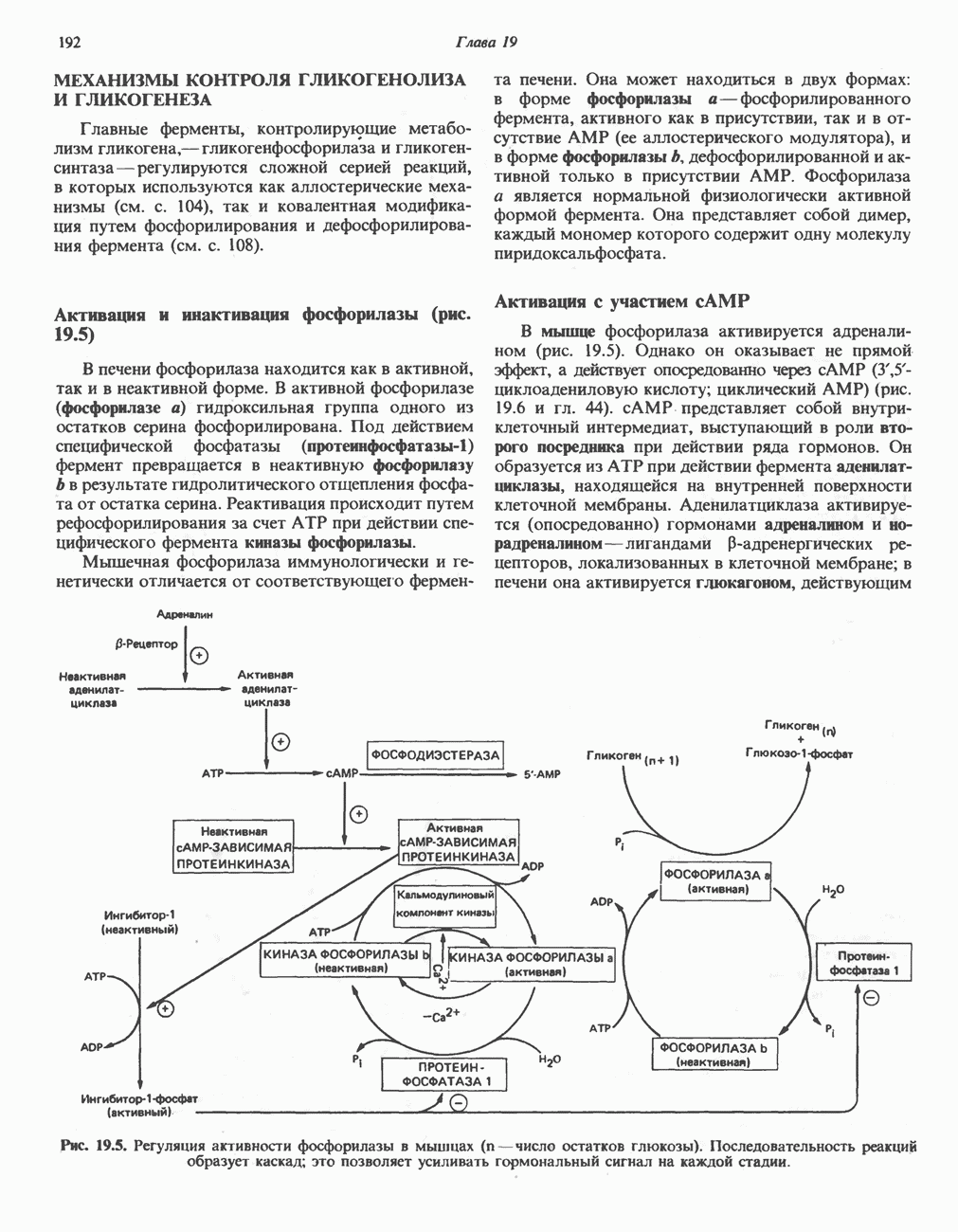
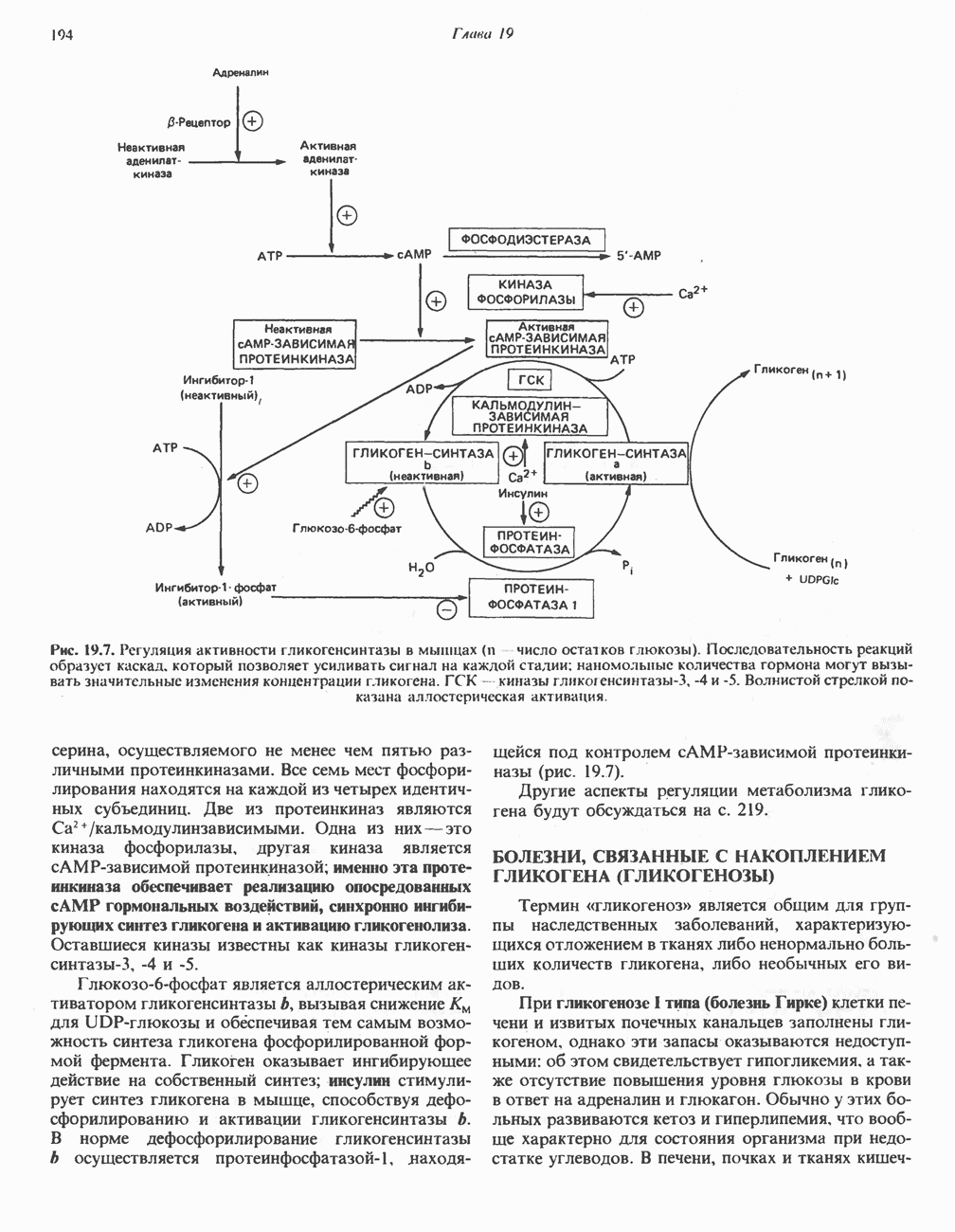
- МЕХАНИЗМЫ КОНТРОЛЯ ГЛИКОГЕНОЛИЗА И ГЛИКОГЕНЕЗА
- БОЛЕЗНИ, СВЯЗАННЫЕ С НАКОПЛЕНИЕМ ГЛИКОГЕНА (ГЛИКОГЕНОЗЫ)
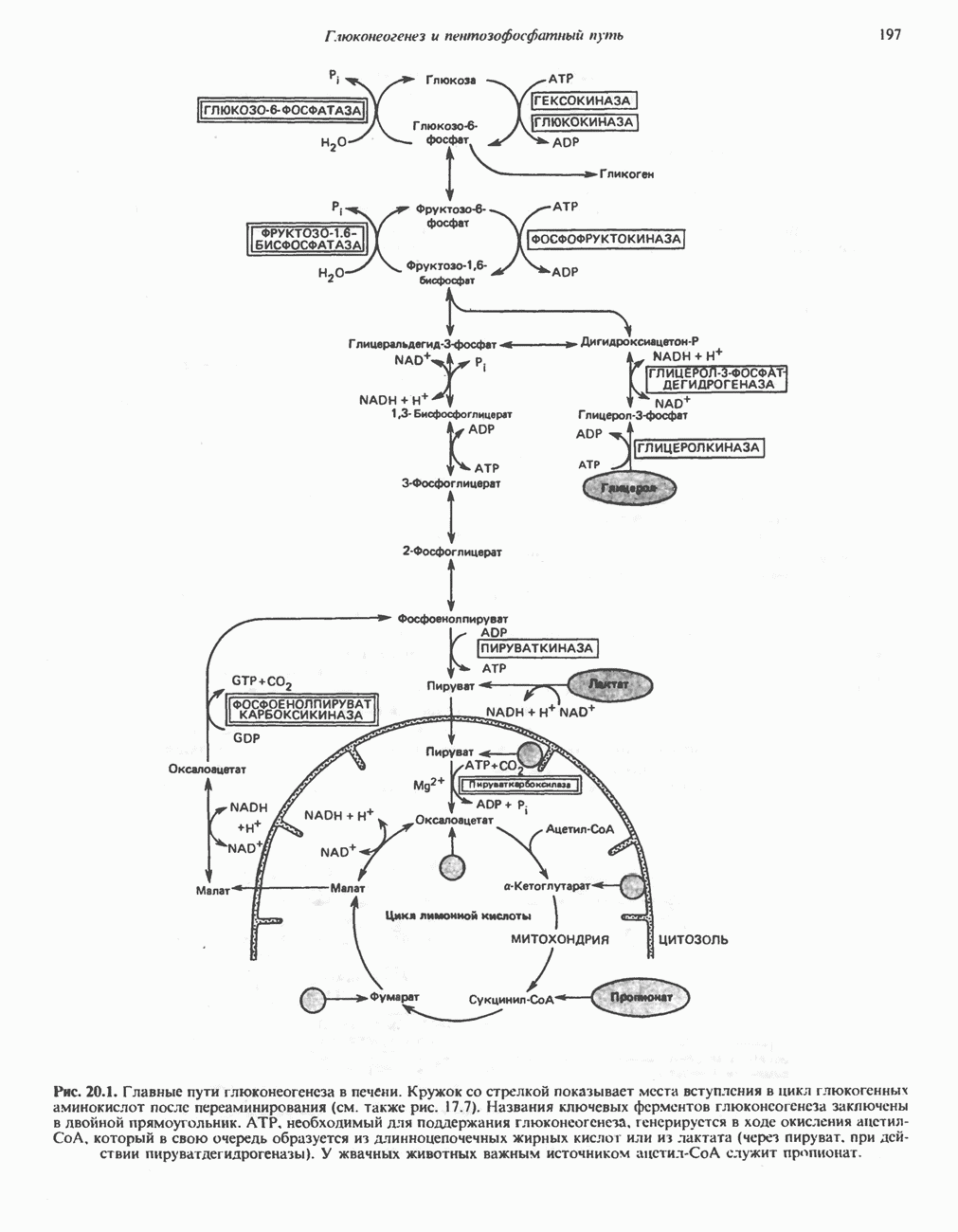
- Глава 20. Глюконеогенез и пентозофосфатный путь
- МЕТАБОЛИЧЕСКИЕ ПУТИ, УЧАСТВУЮЩИЕ В ГЛЮКОНЕОГЕНЕЗЕ (рис. 20.1)
- ПЕНТОЗОФОСФАТНЫЙ ПУТЬ ИЛИ ГЕКСОЗОМОНОФОСФАТНЫЙ ШУНТ
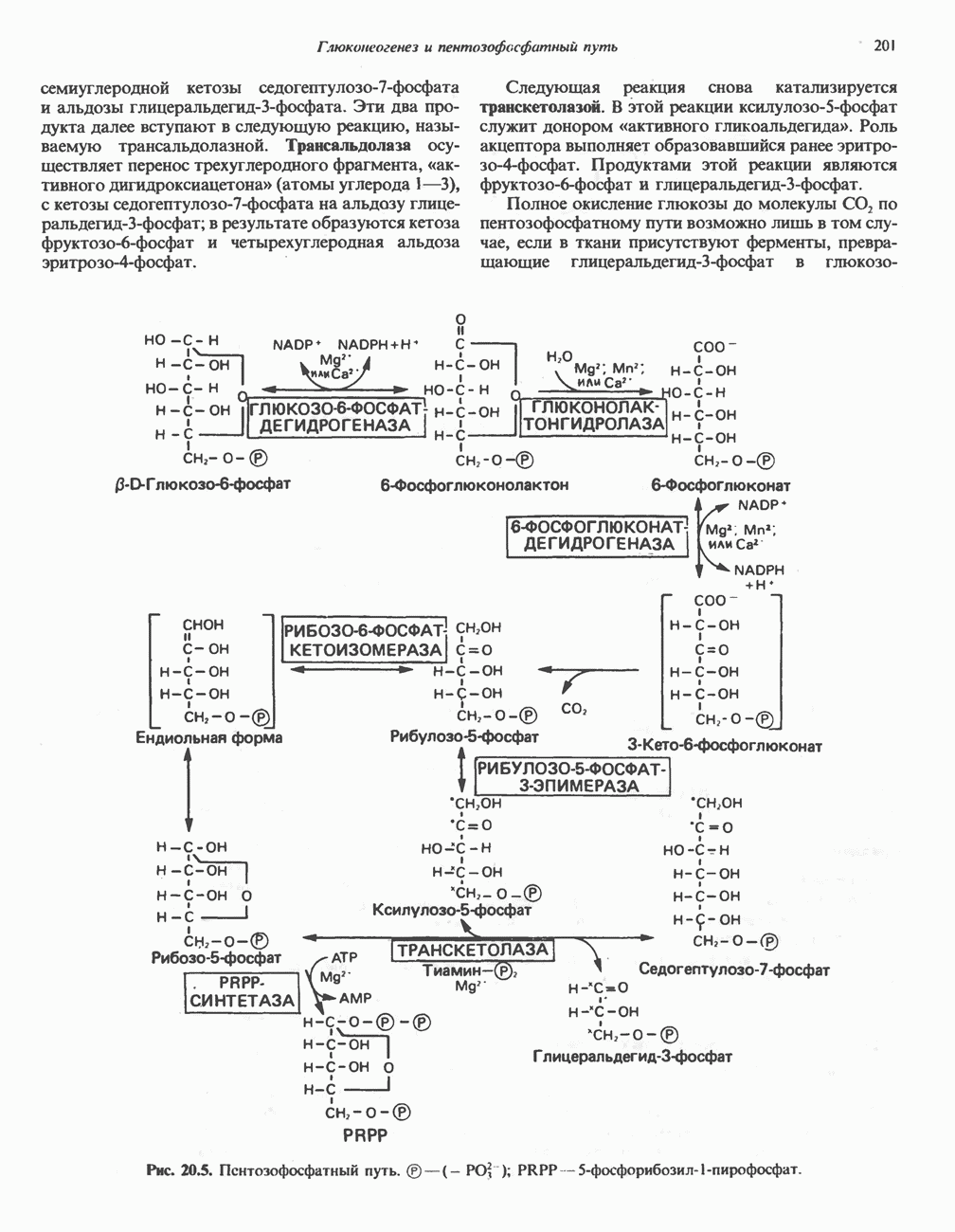
- ПОСЛЕДОВАТЕЛЬНОСТЬ РЕАКЦИЙ
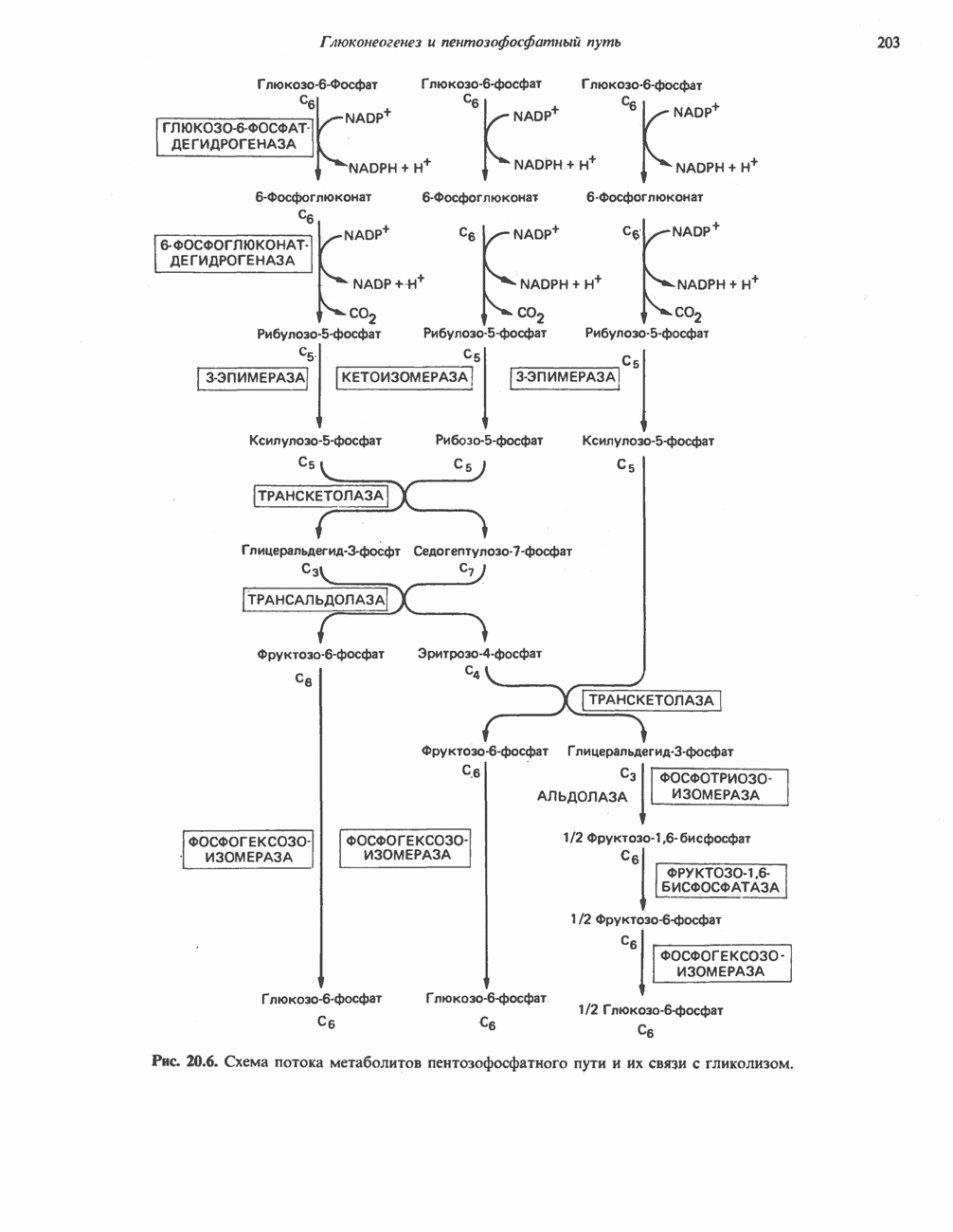
- МЕТАБОЛИЧЕСКОЕ ЗНАЧЕНИЕ ПЕНТОЗОФОСФАТНОГО ПУТИ
- КЛИНИЧЕСКИЕ АСПЕКТЫ
- Глава 21. Метаболизм наиболее важных гексоз
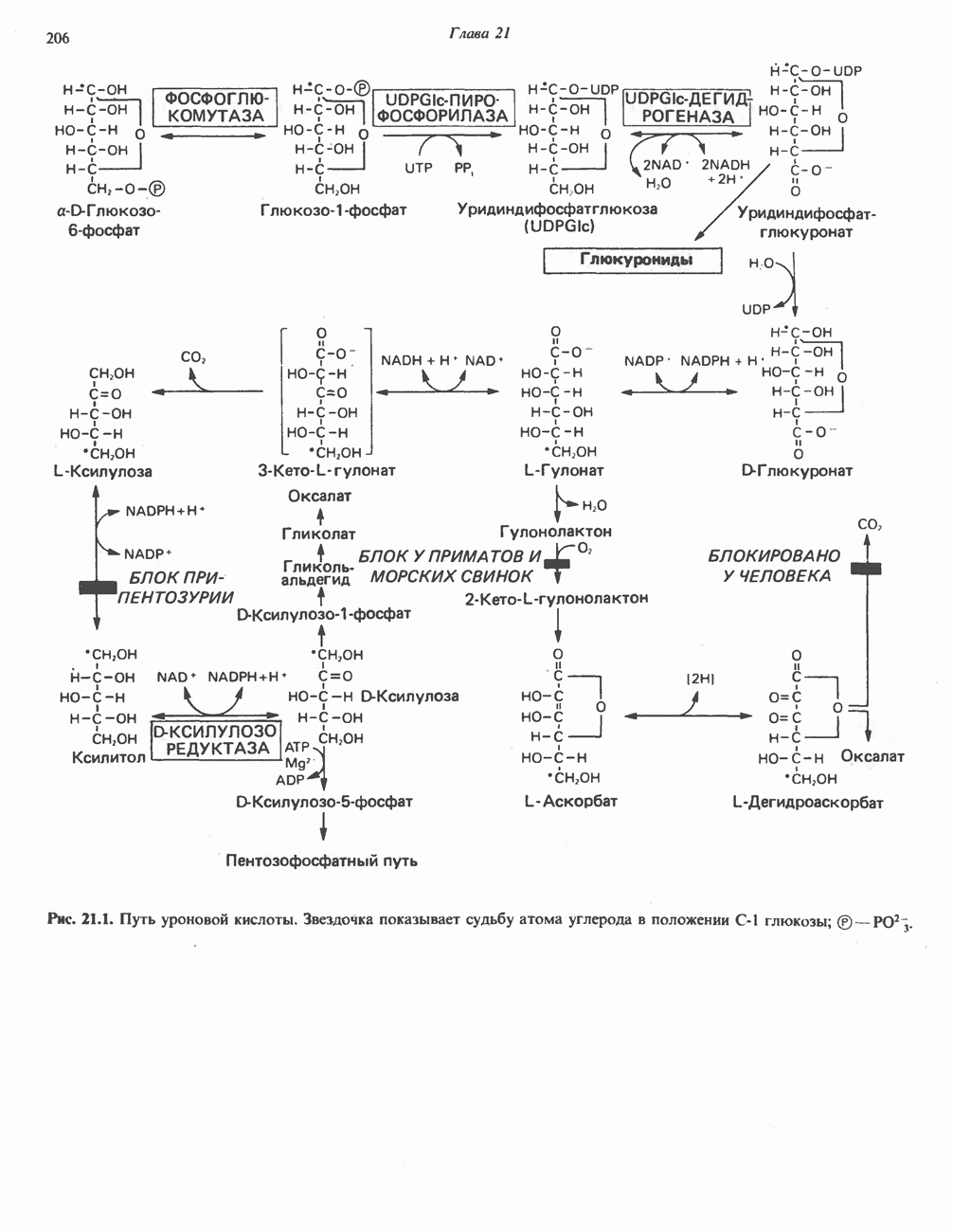
- ПУТЬ УРОНОВЫХ КИСЛОТ
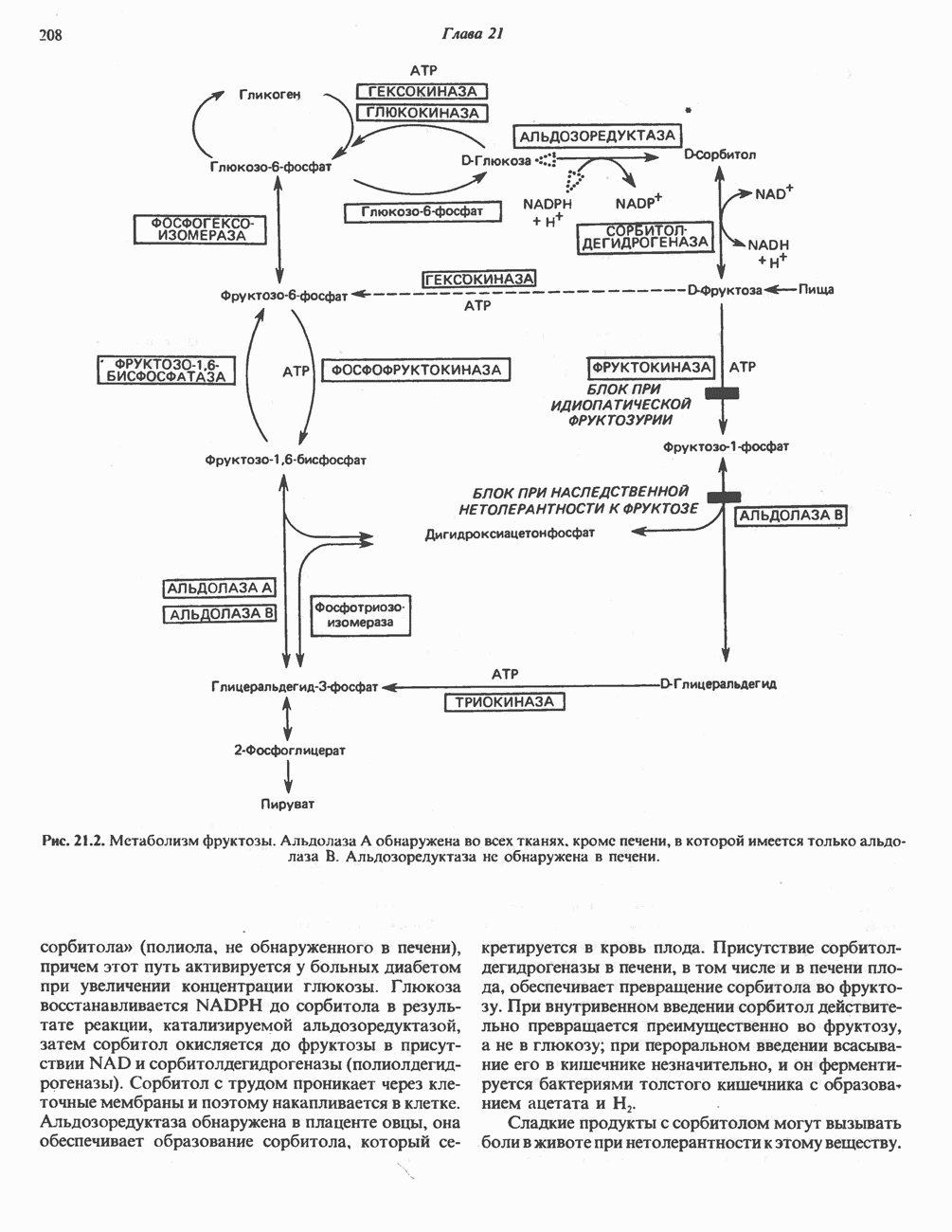
- МЕТАБОЛИЗМ ФРУКТОЗЫ
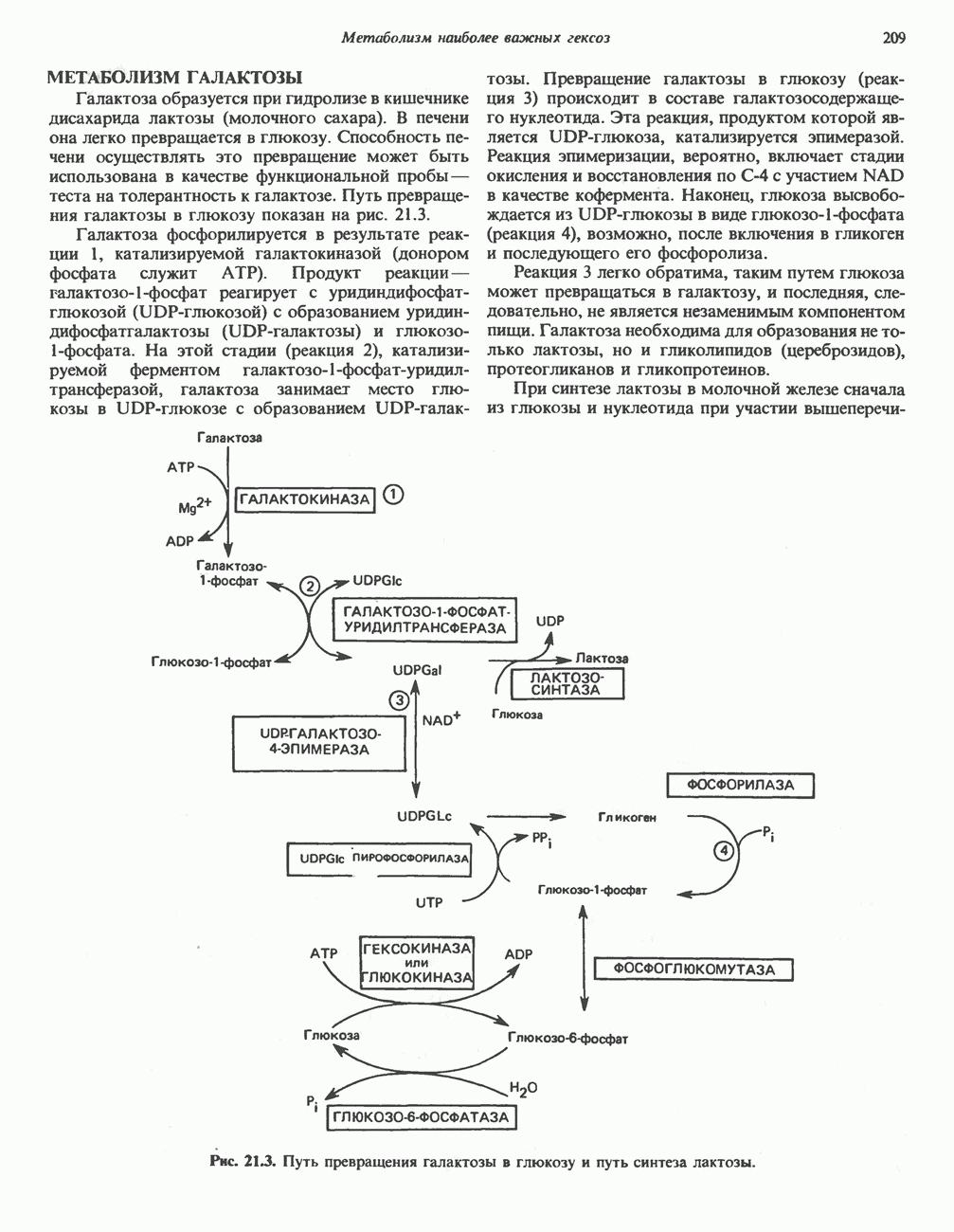
- МЕТАБОЛИЗМ ГАЛАКТОЗЫ
- Глава 22. Регуляция метаболизма углеводов
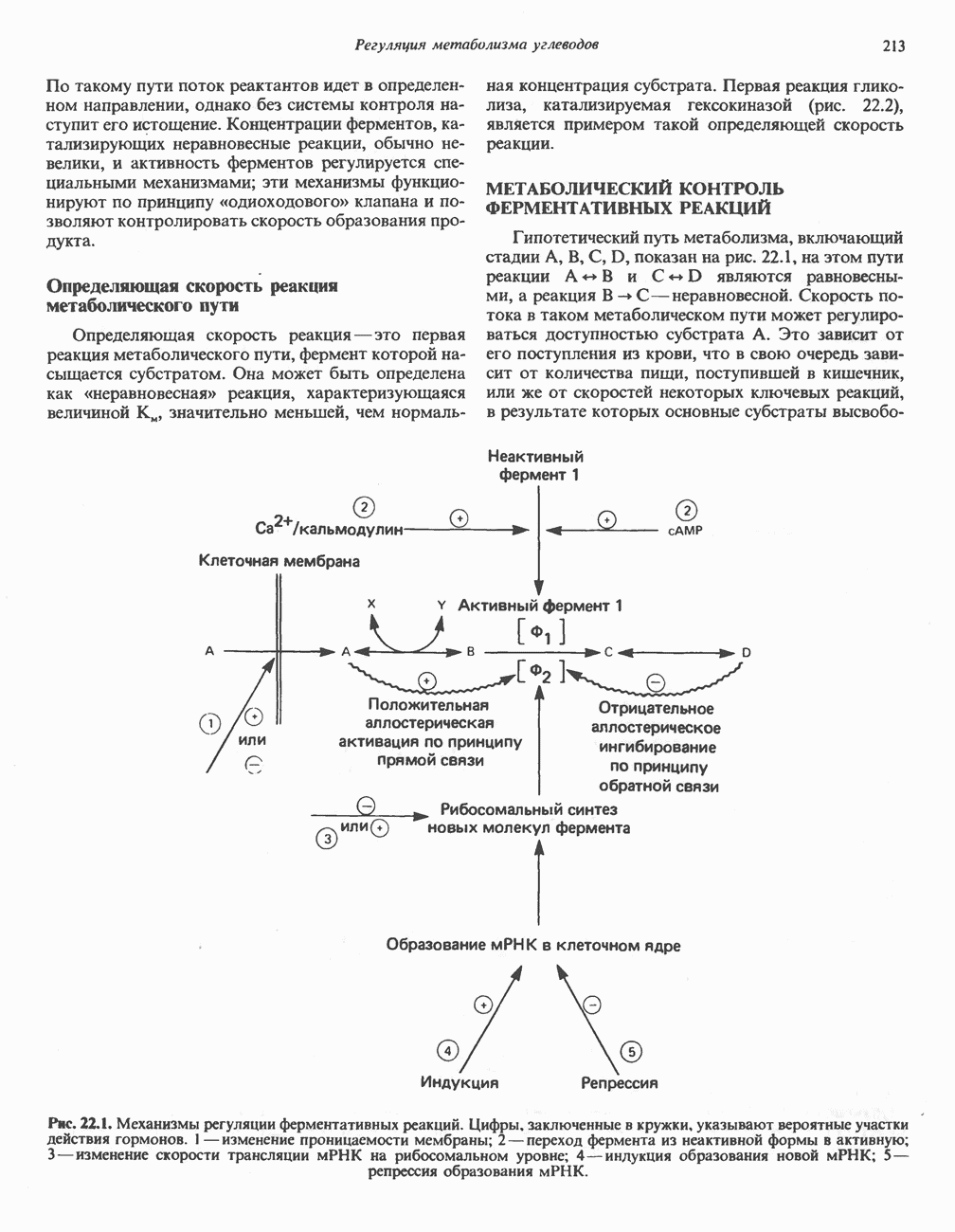
- ОБЩИЕ ПРИНЦИПЫ РЕГУЛЯЦИИ ПУТЕЙ МЕТАБОЛИЗМА
- МЕТАБОЛИЧЕСКИЙ КОНТРОЛЬ ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ
- РЕГУЛЯЦИЯ МЕТАБОЛИЗМА УГЛЕВОДОВ НА КЛЕТОЧНОМ И ФЕРМЕНТНОМ УРОВНЕ
- РЕГУЛЯЦИЯ ГЛИКОЛИЗА, ГЛЮКОНЕОГЕНЕЗА И ПЕНТОЗОФОСФАТНОГО ПУТИ
- РЕГУЛЯЦИЯ МЕТАБОЛИЗМА ГЛИКОГЕНА (РИС. 22.5)
- РЕГУЛЯЦИЯ ЦИКЛА ЛИМОННОЙ КИСЛОТЫ (СМ. РИС. 18.3)
- РЕГУЛЯЦИЯ УРОВНЯ ГЛЮКОЗЫ В КРОВИ
- Глава 23. Окисление и биосинтез жирных кислот
- ОКИСЛЕНИЕ ЖИРНЫХ КИСЛОТ
- БИОСИНТЕЗ НАСЫЩЕННЫХ ЖИРНЫХ КИСЛОТ
- Глава 24. Метаболизм ненасыщенных жирных кислот и эйкозаноидов
- МЕТАБОЛИЗМ НЕНАСЫЩЕННЫХ ЖИРНЫХ КИСЛОТ
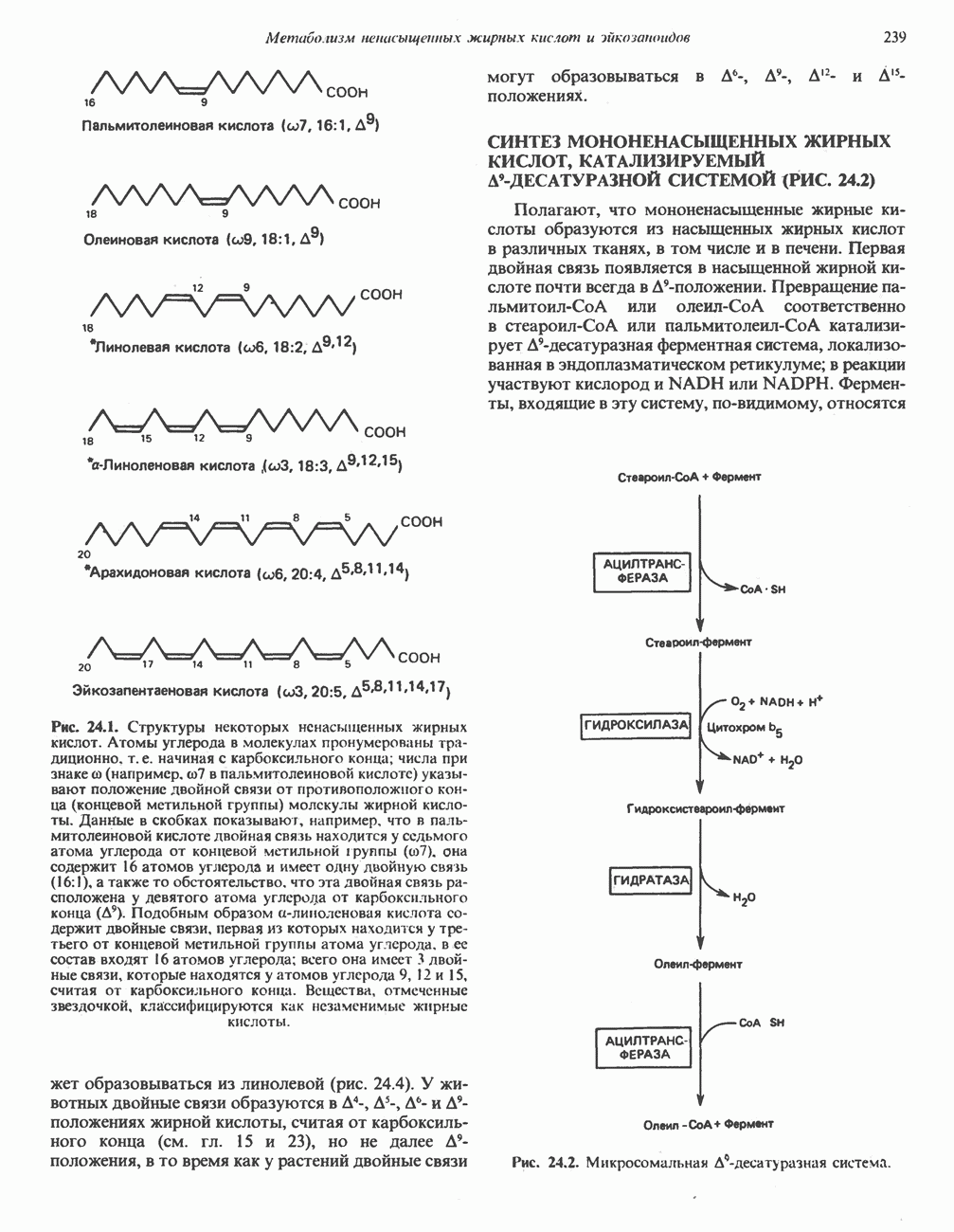
- СИНТЕЗ МОНОНЕНАСЫЩЕННЫХ ЖИРНЫХ КИСЛОТ, КАТАЛИЗИРУЕМЫЙ Д9-ДЕСАТУРАЗНОЙ СИСТЕМОЙ (РИС. 24.2)
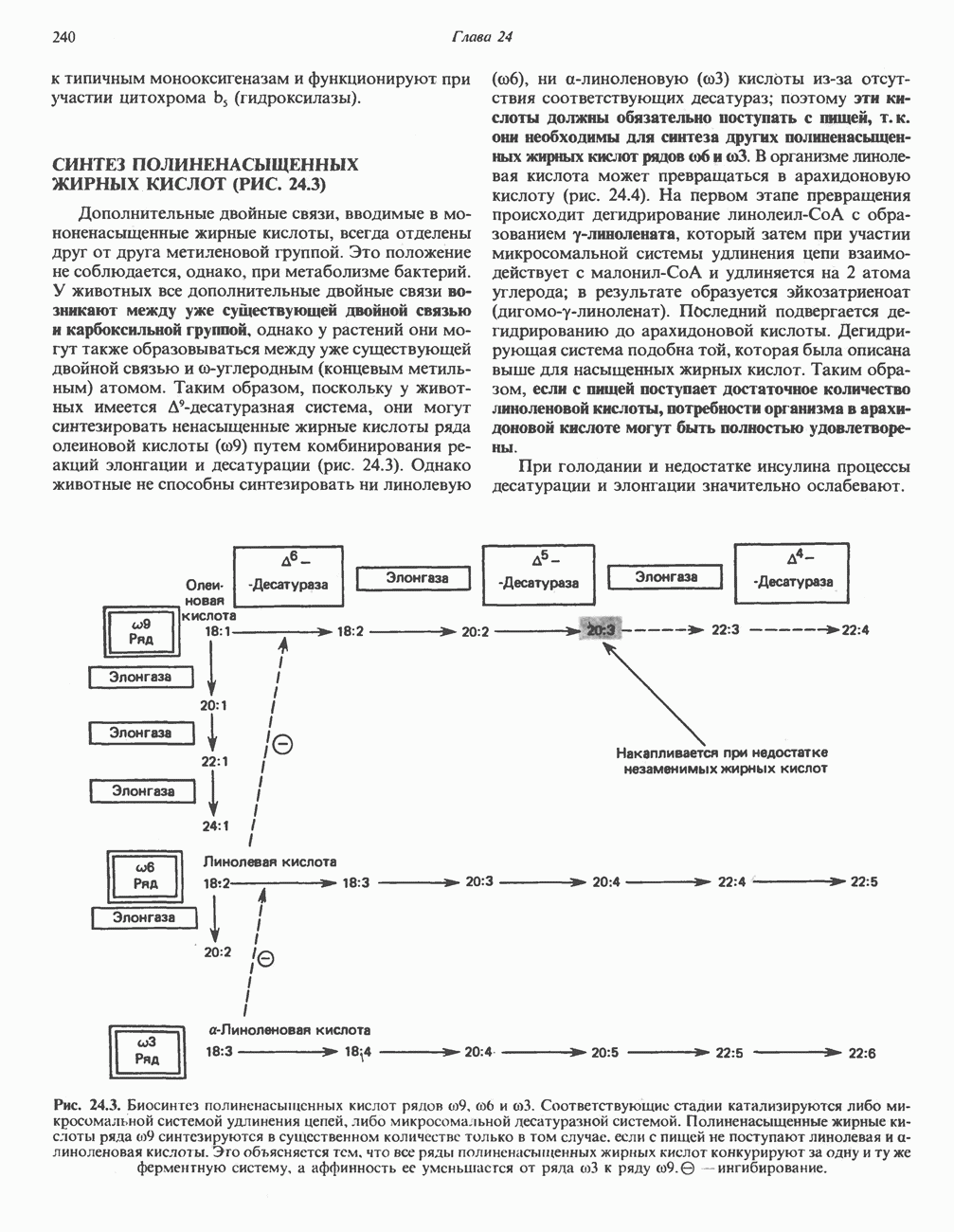
- СИНТЕЗ ПОЛИНЕНАСЫЩЕННЫХ ЖИРНЫХ КИСЛОТ (РИС. 24.3)
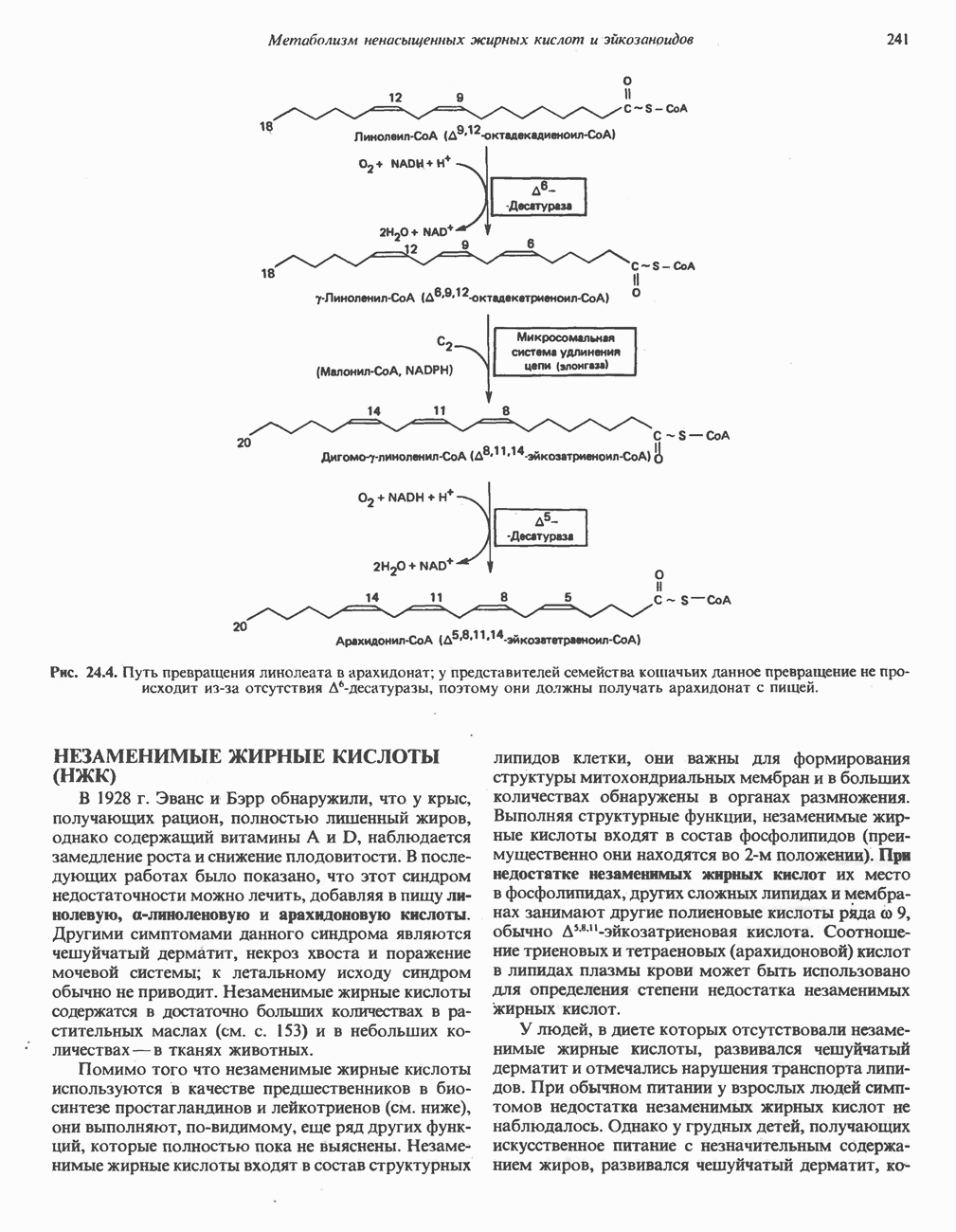
- НЕЗАМЕНИМЫЕ ЖИРНЫЕ КИСЛОТЫ (НЖК)
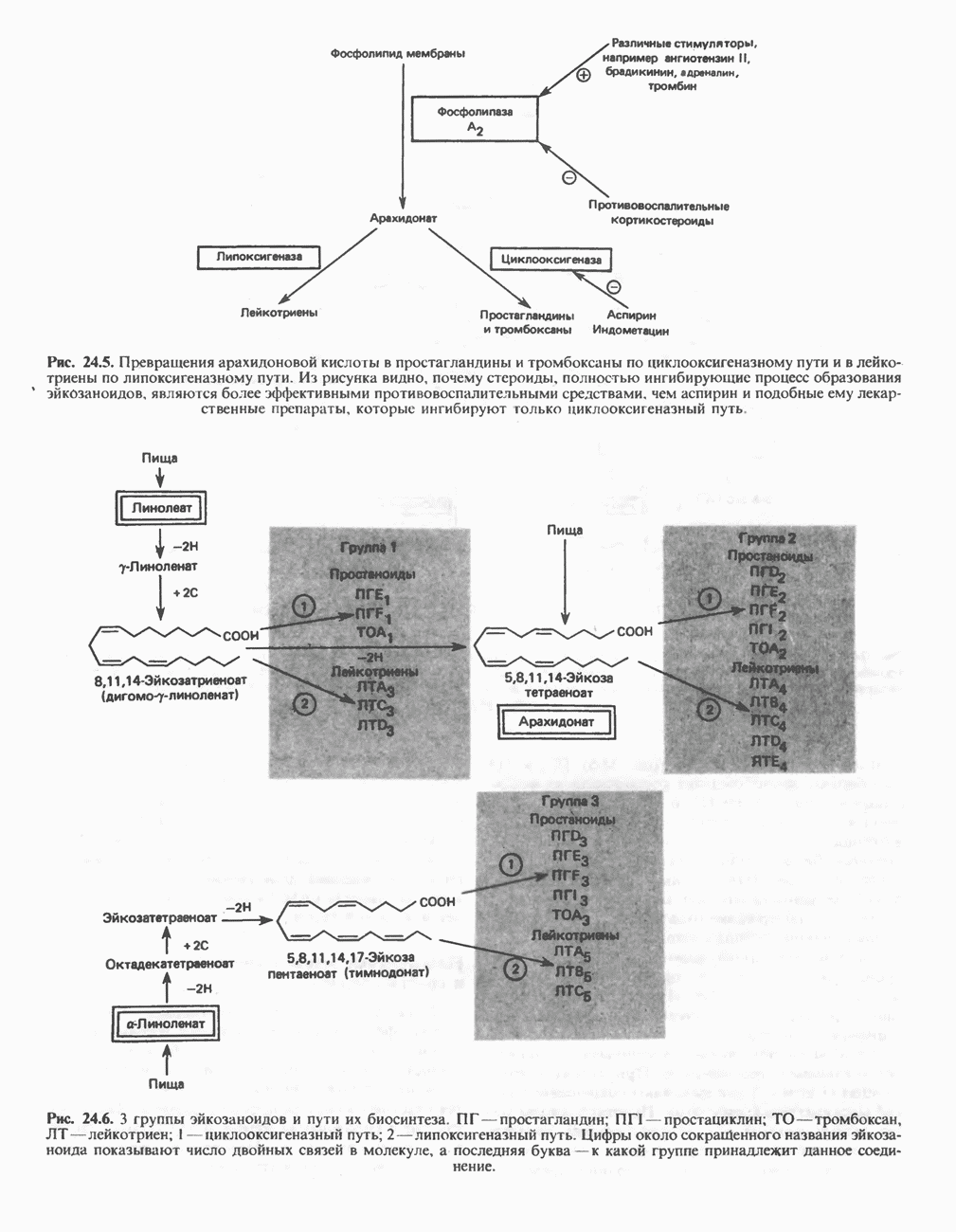
- ЭЙКОЗАНОИДЫ
- ПРОСТАНОИДЫ
- ЛЕЙКОТРИЕНЫ
- Глава 25. Метаболизм ацилглицеролов и сфинголипидов
- МЕТАБОЛИЗМ АЦИЛГЛИЦЕРОЛОВ
- МЕТАБОЛИЗМ СФИНГОЛИПИДОВ
- ГЛИКОЛИПИДЫ
- ФОСФОЛИПИДЫ И СФИНГОЛИПИДЫ ПРИ НЕКОТОРЫХ ЗАБОЛЕВАНИЯХ (ЛИПИДОЗЫ)
- Глава 26. Транспорт и запасание липидов
- ЛИПИДЫ ПЛАЗМЫ КРОВИ И ЛИПОПРОТЕИНЫ
- МЕТАБОЛИЗМ ЛИПОПРОТЕИНОВ ПЛАЗМЫ КРОВИ
- ОБРАЗОВАНИЕ ХИЛОМИКРОНОВ И ЛИПОПРОТЕИНОВ ОЧЕНЬ НИЗКОЙ ПЛОТНОСТИ (ЛПОНП)
- КАТАБОЛИЗМ ХИЛОМИКРОНОВ И ЛИПОПРОТЕИНОВ ОЧЕНЬ НИЗКОЙ ПЛОТНОСТИ
- МЕТАБОЛИЗМ ЛПНП
- МЕТАБОЛИЗМ ЛПВП (рис. 26.6)
- РОЛЬ ПЕЧЕНИ В ТРАНСПОРТЕ И МЕТАБОЛИЗМЕ ЛИПИДОВ
- СИНТЕЗ ТРИАЦИЛГЛИЦЕРОЛОВ И ОБРАЗОВАНИЕ ЛПОНП (рис. 26.7)
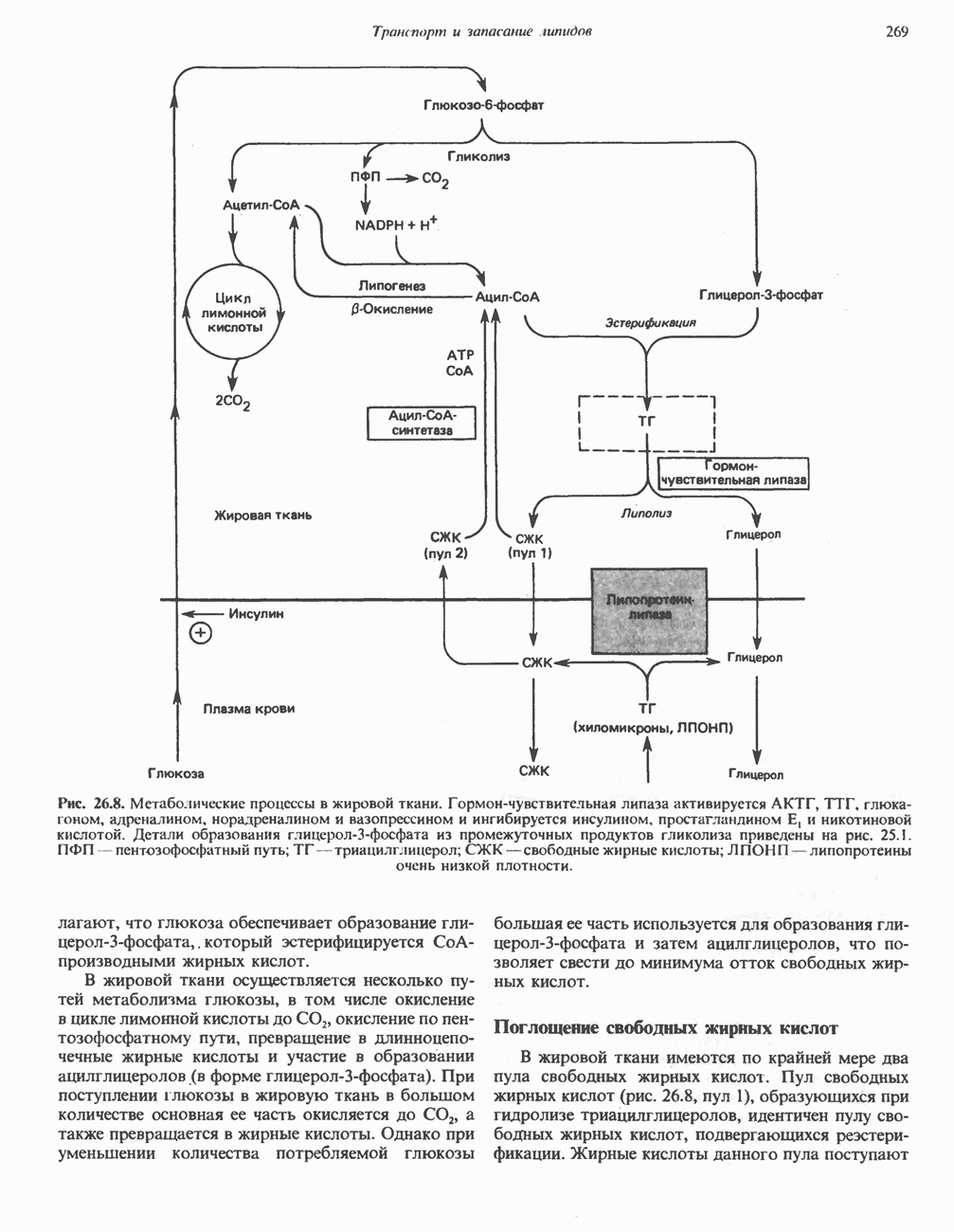
- МЕТАБОЛИЧЕСКИЕ ПРЕВРАЩЕНИЯ В ЖИРОВОЙ ТКАНИ И МОБИЛИЗАЦИЯ ЖИРОВ
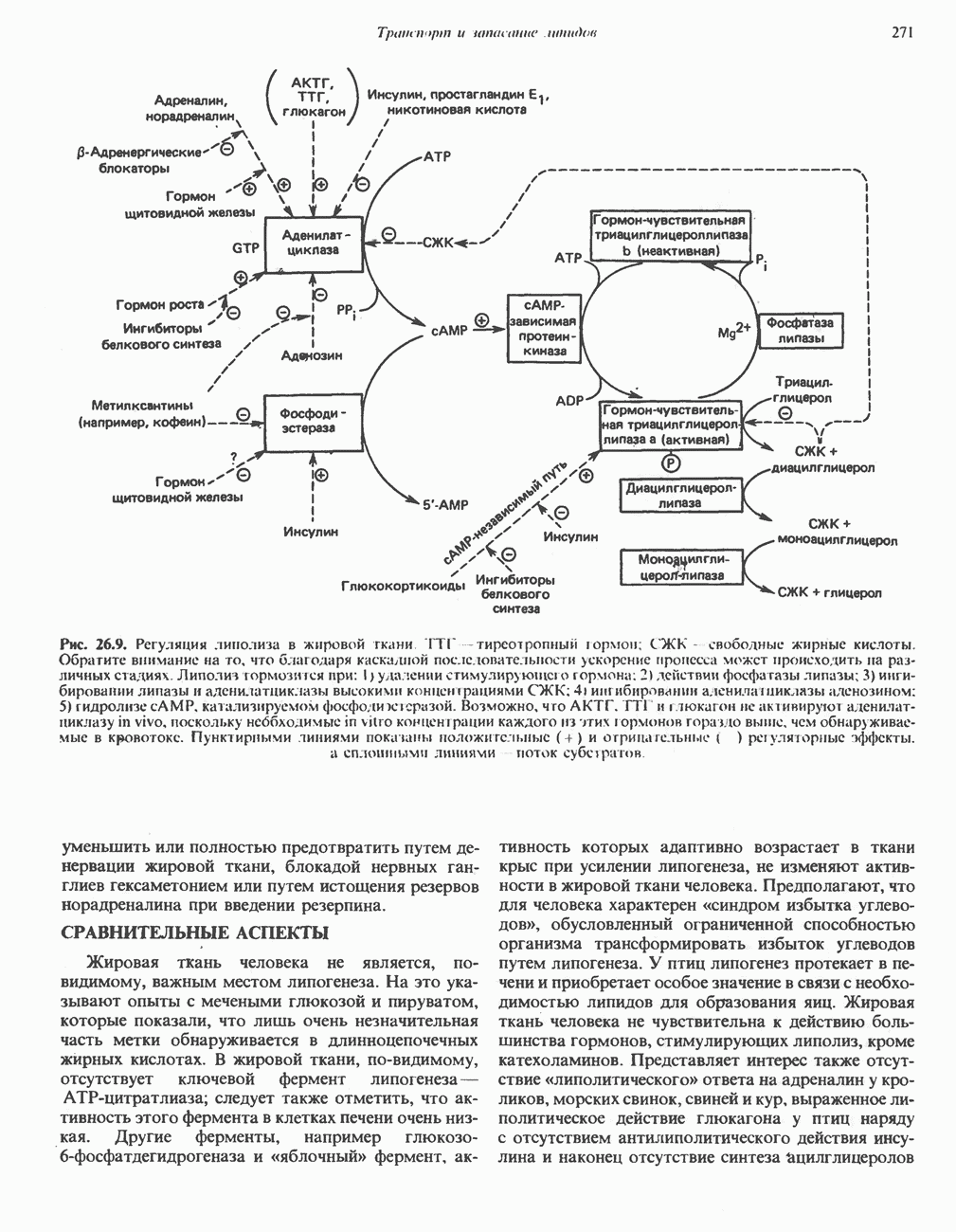
- РОЛЬ ГОРМОНОВ В МОБИЛИЗАЦИИ ЖИРОВ
- СРАВНИТЕЛЬНЫЕ АСПЕКТЫ
- РОЛЬ БУРОЙ ЖИРОВОЙ ТКАНИ В ТЕРМОГЕНЕЗЕ
- Глава 27. Синтез, транспорт и экскреция холестерола
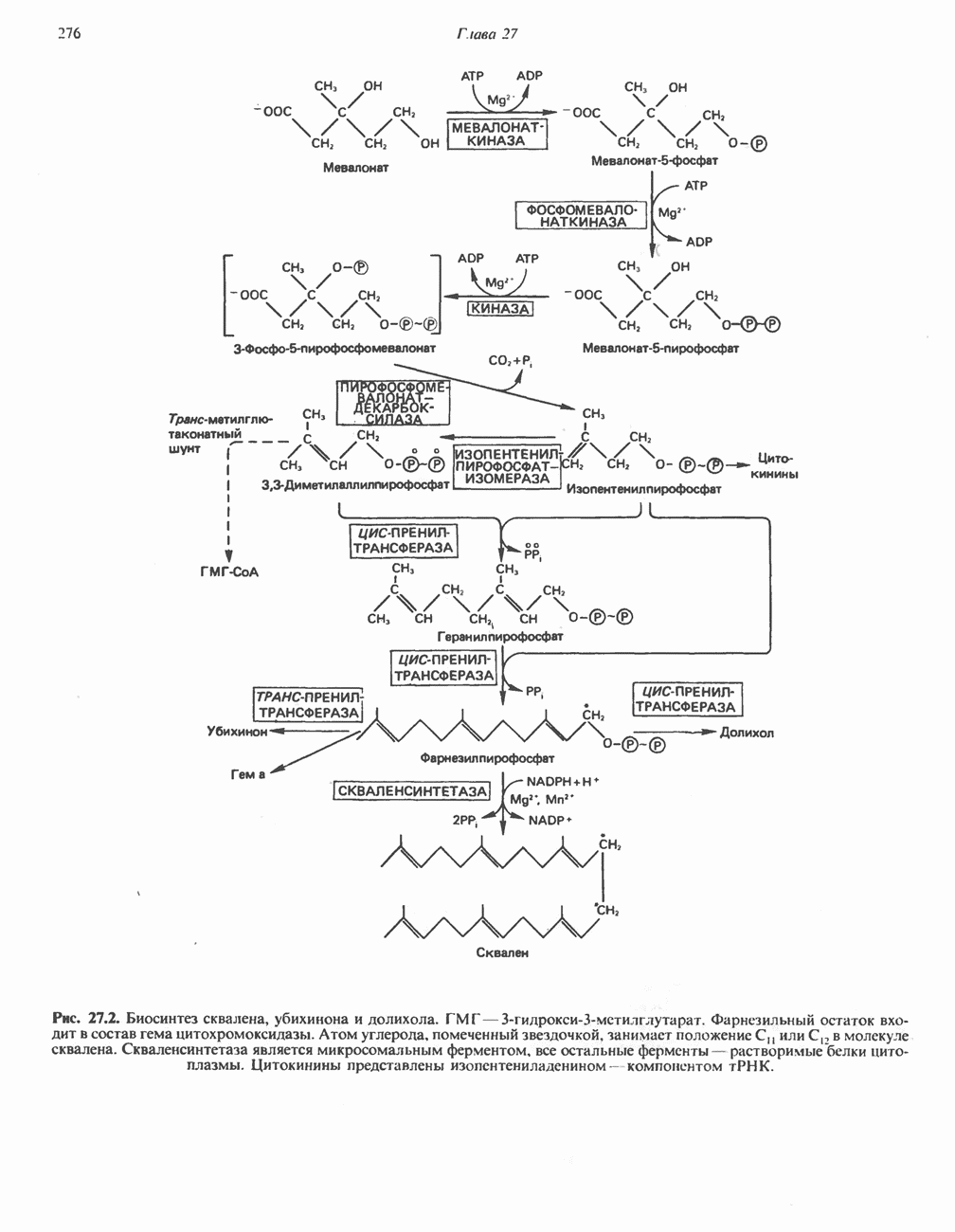
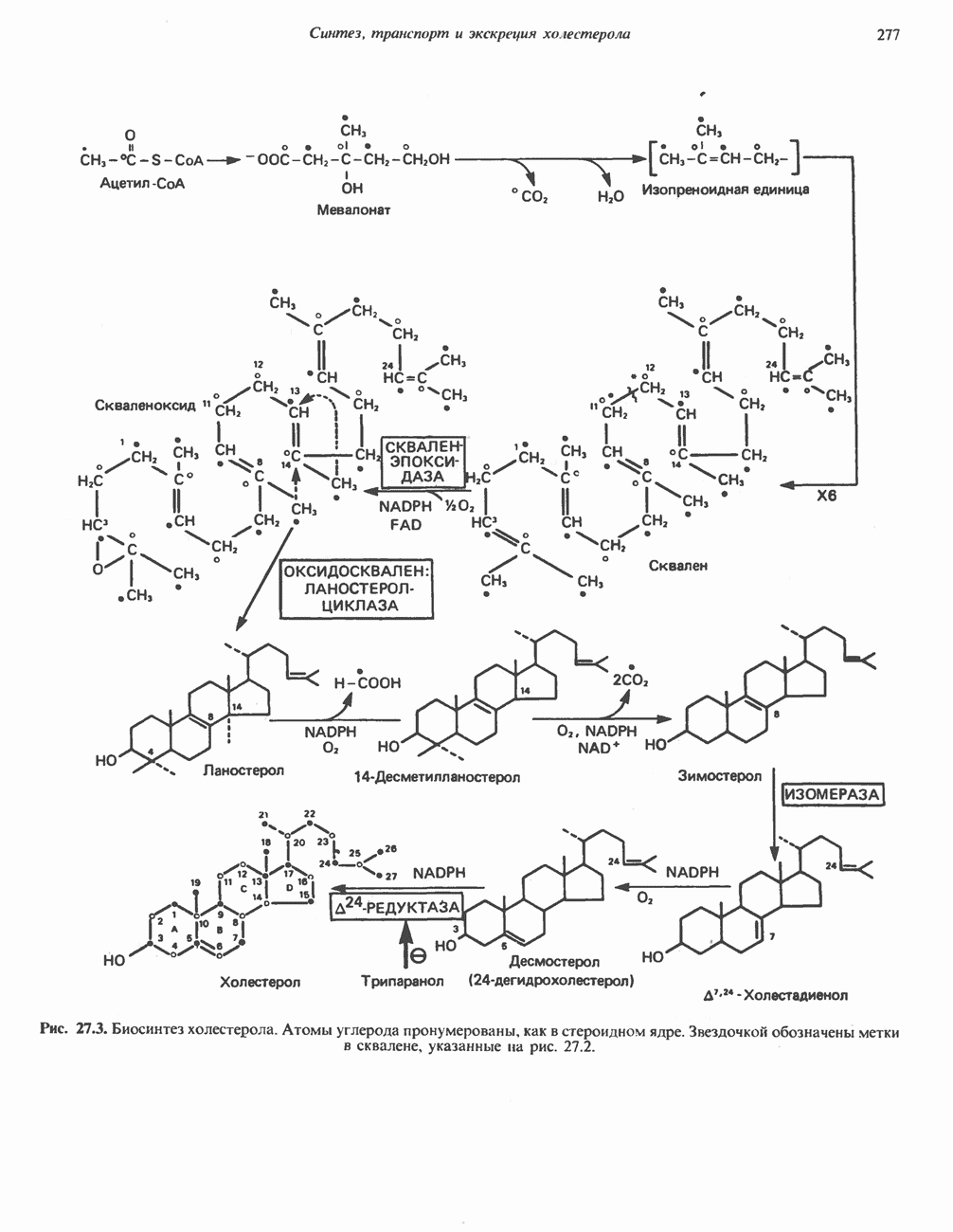
- БИОСИНТЕЗ ХОЛЕСТЕРОЛА
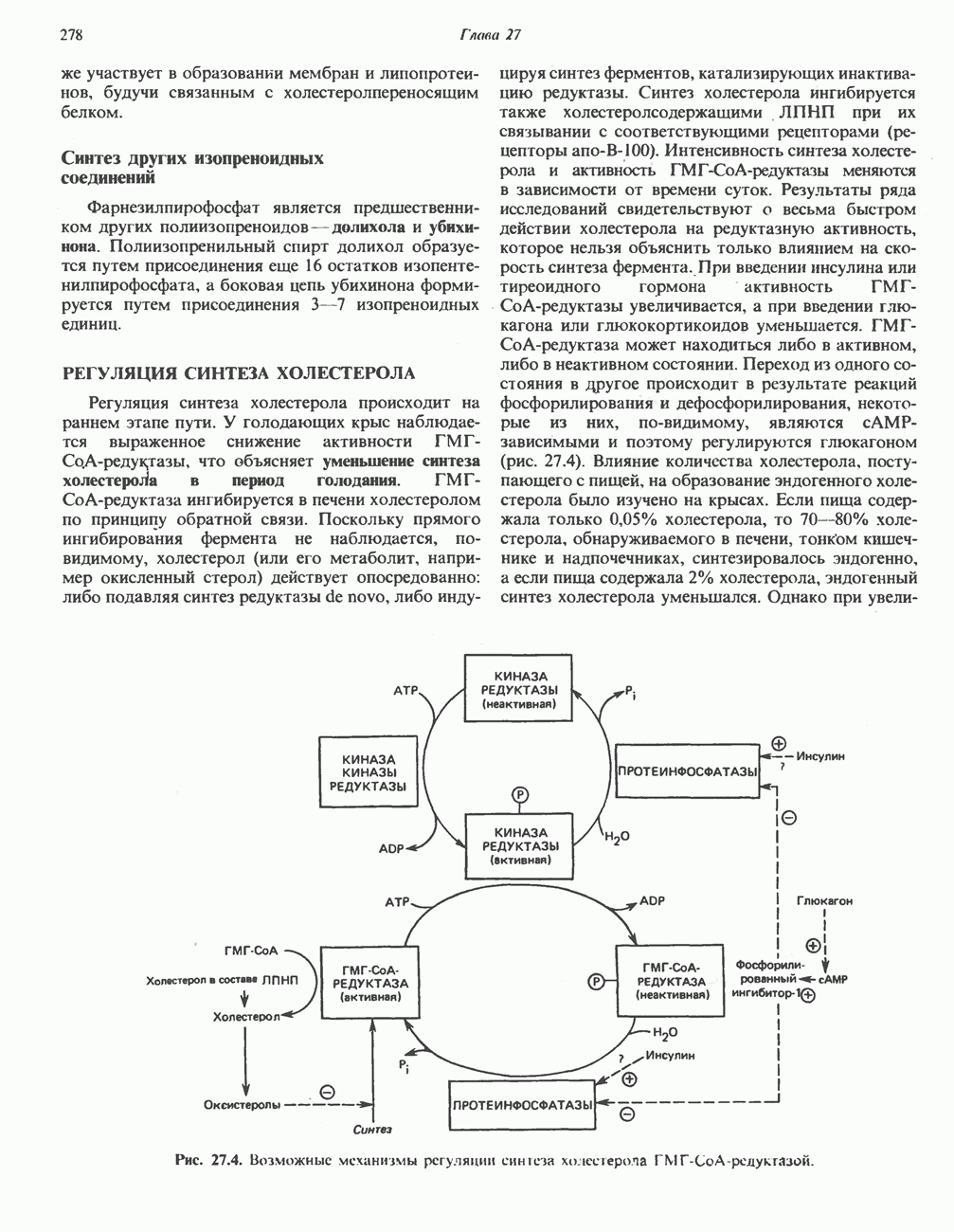
- РЕГУЛЯЦИЯ СИНТЕЗА ХОЛЕСТЕРОЛА
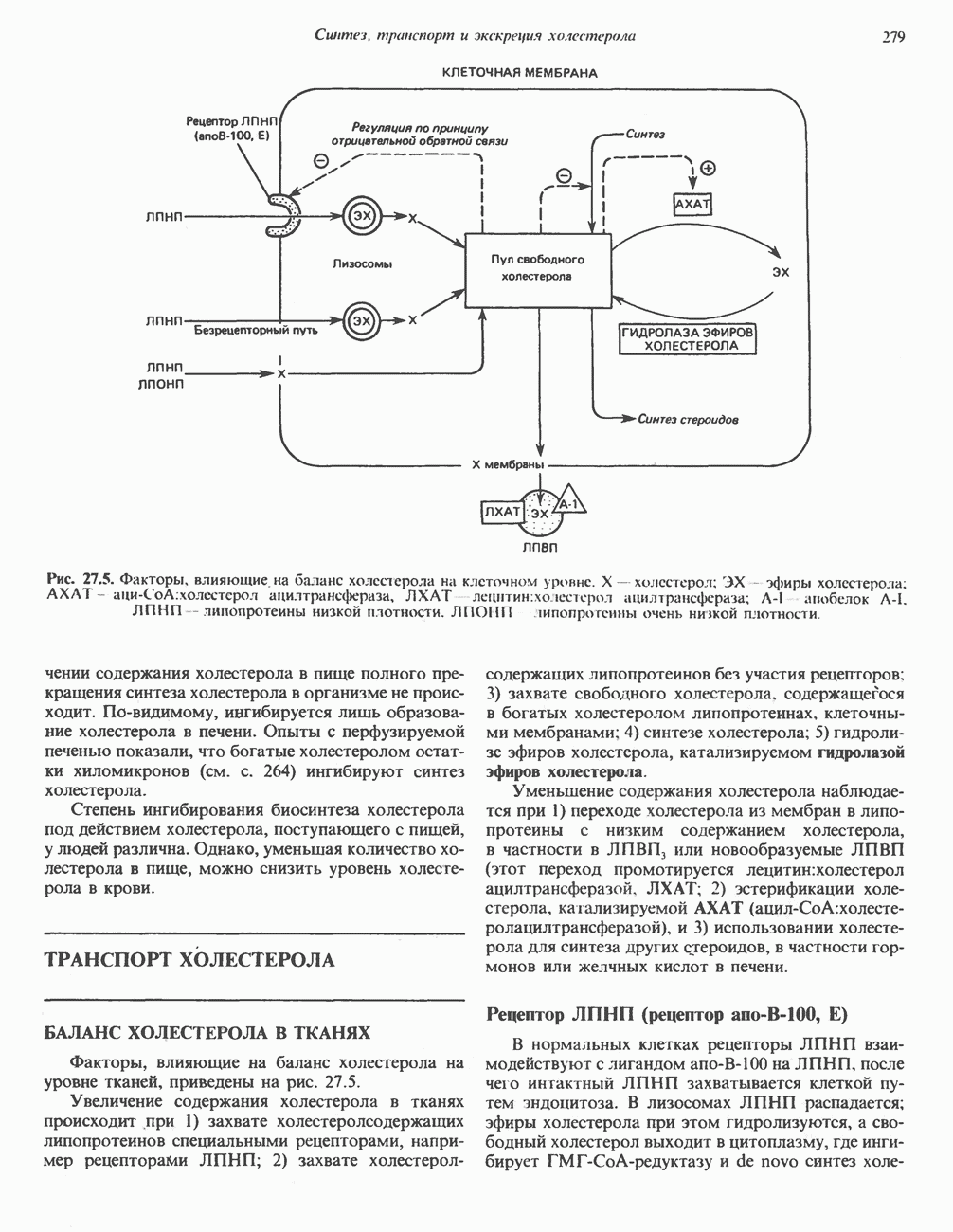
- ТРАНСПОРТ ХОЛЕСТЕРОЛА
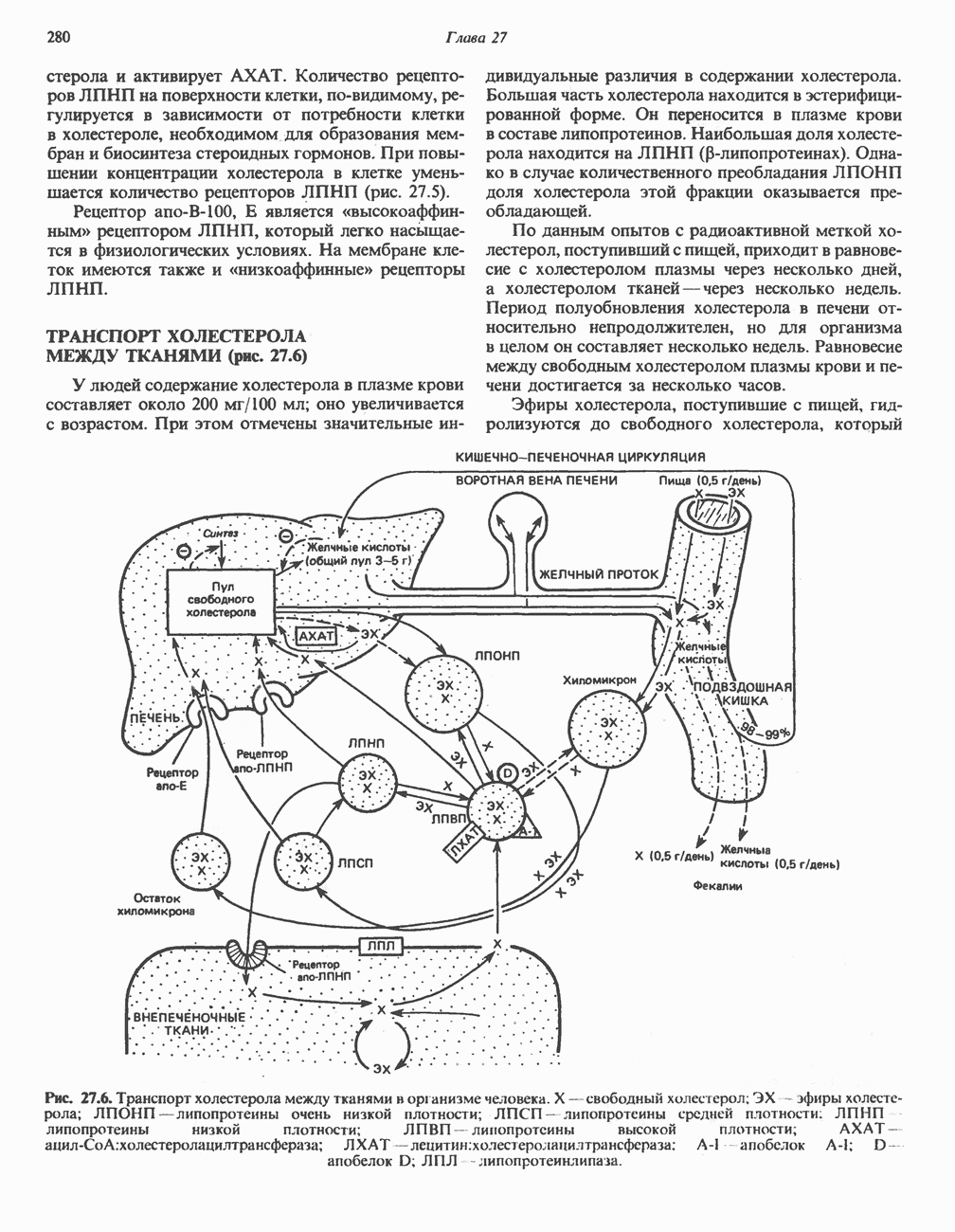
- ТРАНСПОРТ ХОЛЕСТЕРОЛА МЕЖДУ ТКАНЯМИ (рис. 27.6)
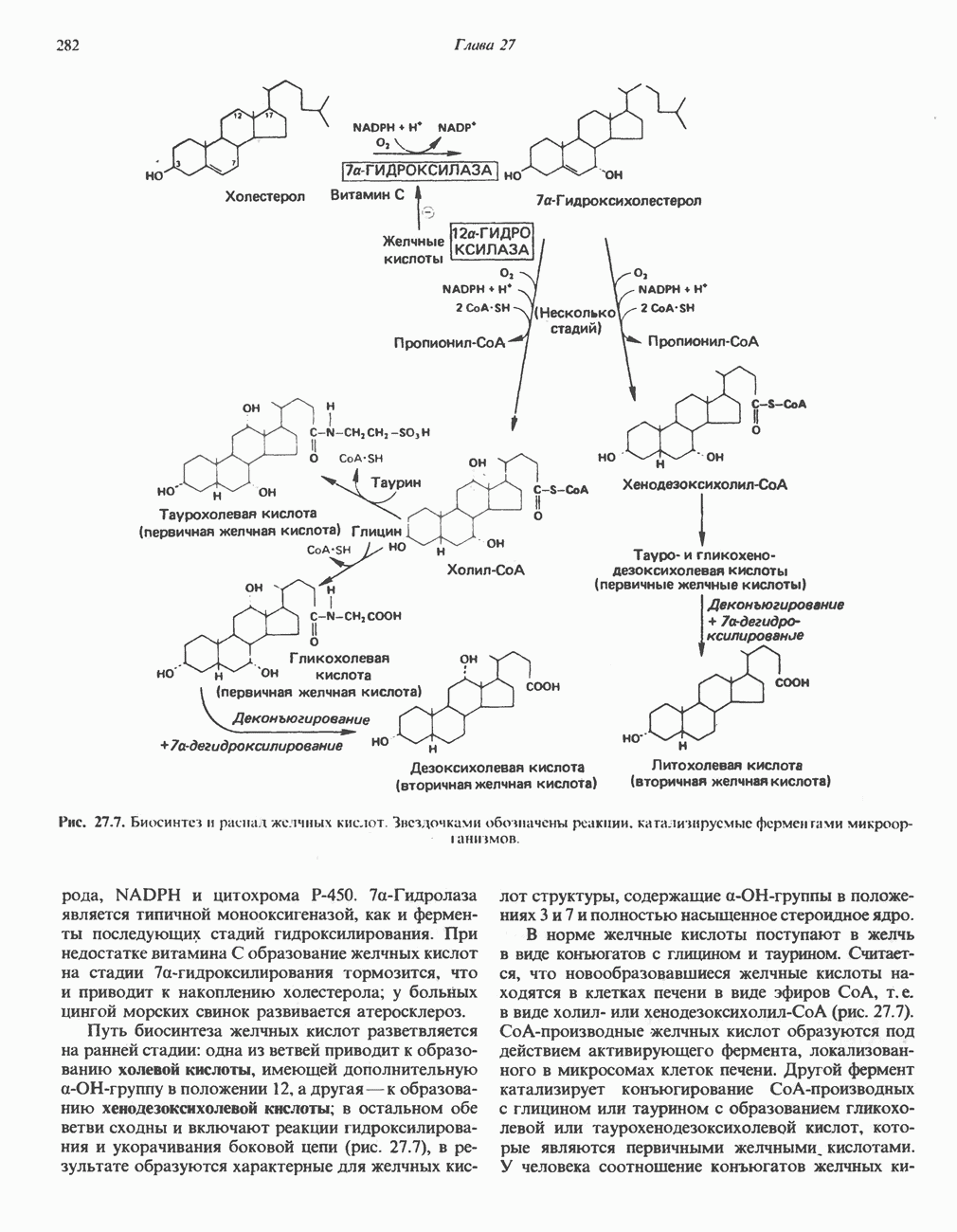
- ВЫВЕДЕНИЕ ХОЛЕСТЕРОЛА И ОБРАЗОВАНИЕ СОЛЕЙ ЖЕЛЧНЫХ КИСЛОТ
- КИШЕЧНО-ПЕЧЕНОЧНАЯ ЦИРКУЛЯЦИЯ ЖЕЛЧНЫХ КИСЛОТ
- КЛИНИЧЕСКИЕ АСПЕКТЫ
- Глава 28. Регуляция метаболизма липидов и источники энергии в тканях
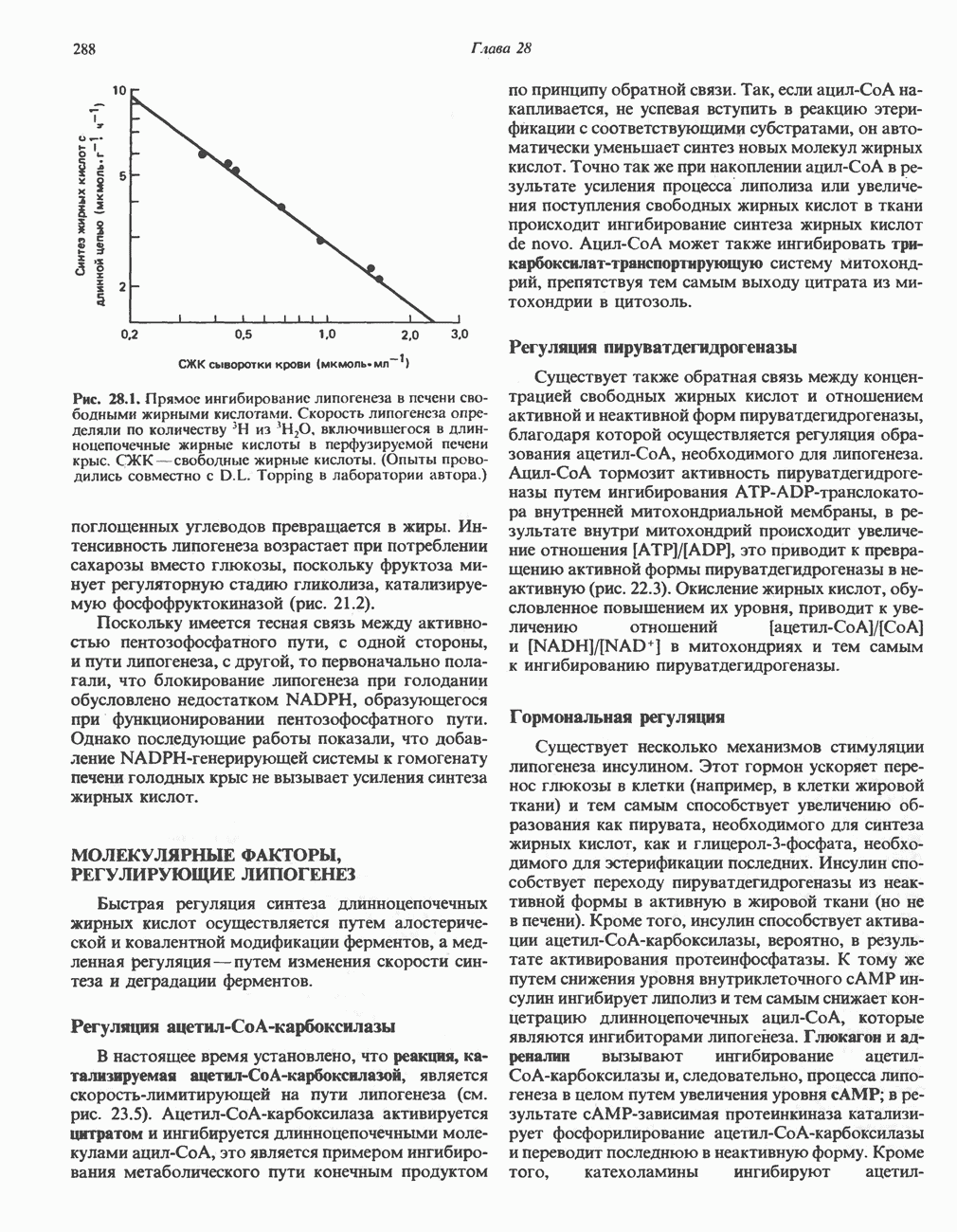
- РЕГУЛЯЦИЯ БИОСИНТЕЗА ЖИРНЫХ КИСЛОТ (ЛИПОГЕНЕЗА)
- МОЛЕКУЛЯРНЫЕ ФАКТОРЫ, РЕГУЛИРУЮЩИЕ ЛИПОГЕНЕЗ
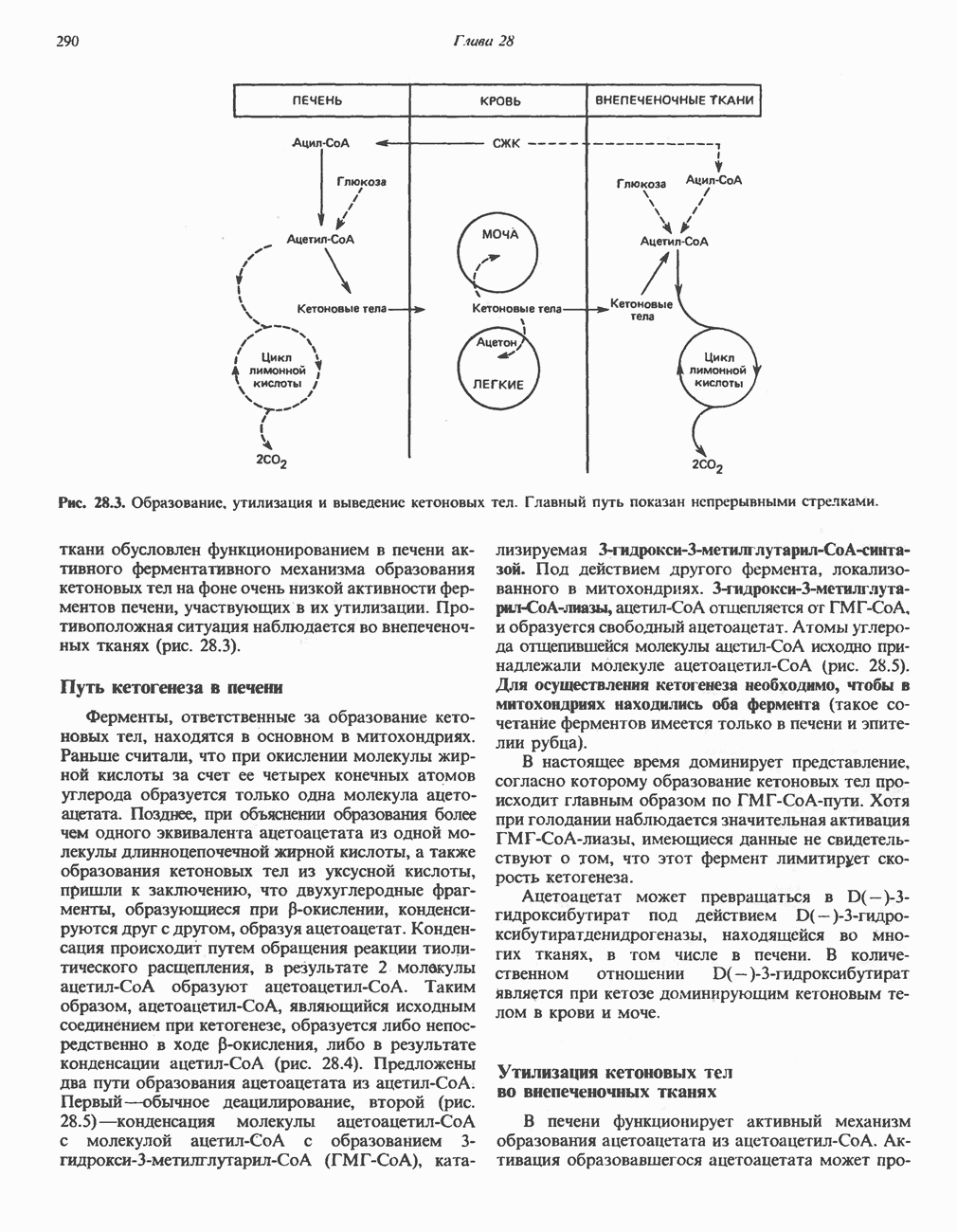
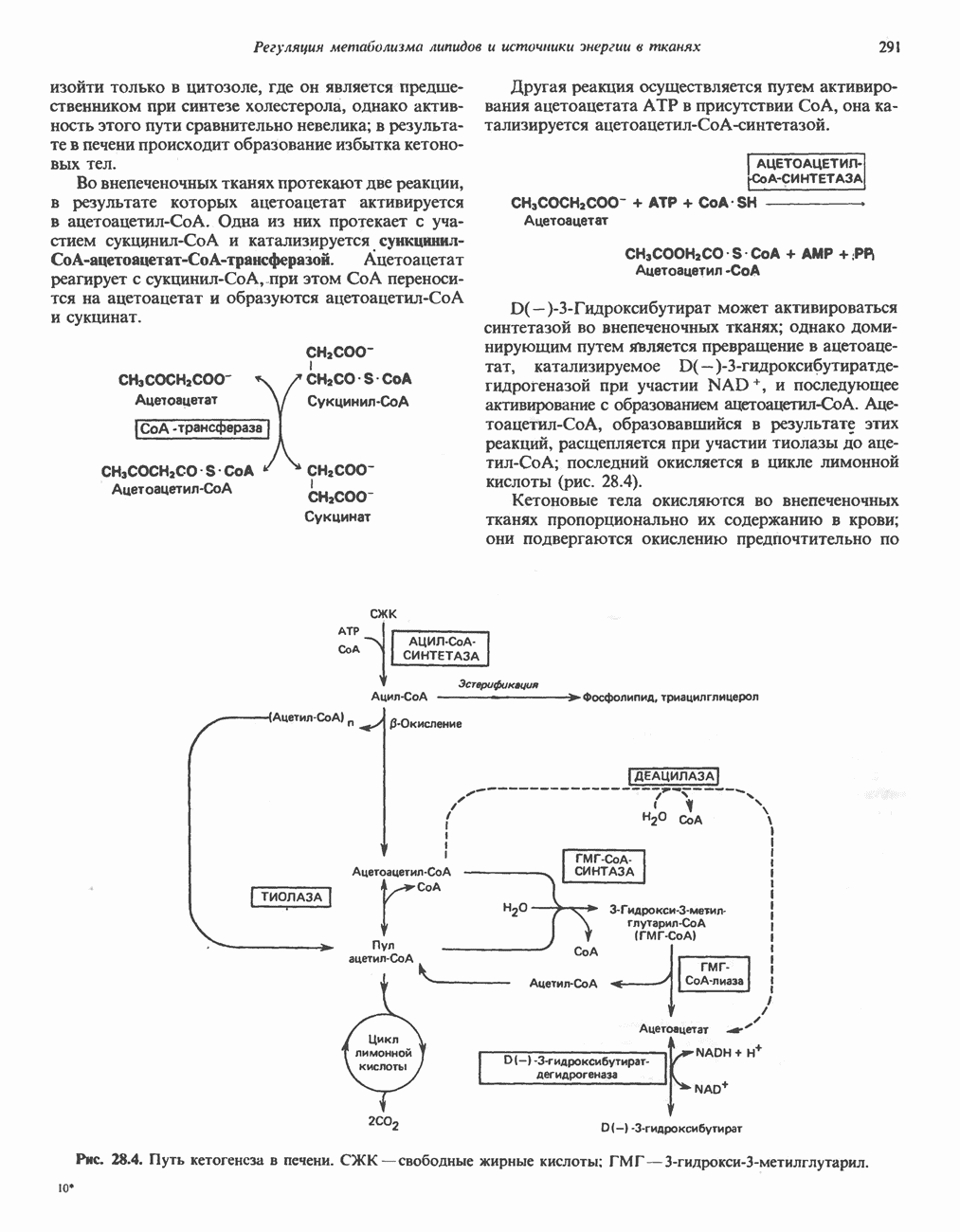
- РЕГУЛЯЦИЯ ОКИСЛЕНИЯ ЖИРНЫХ КИСЛОТ
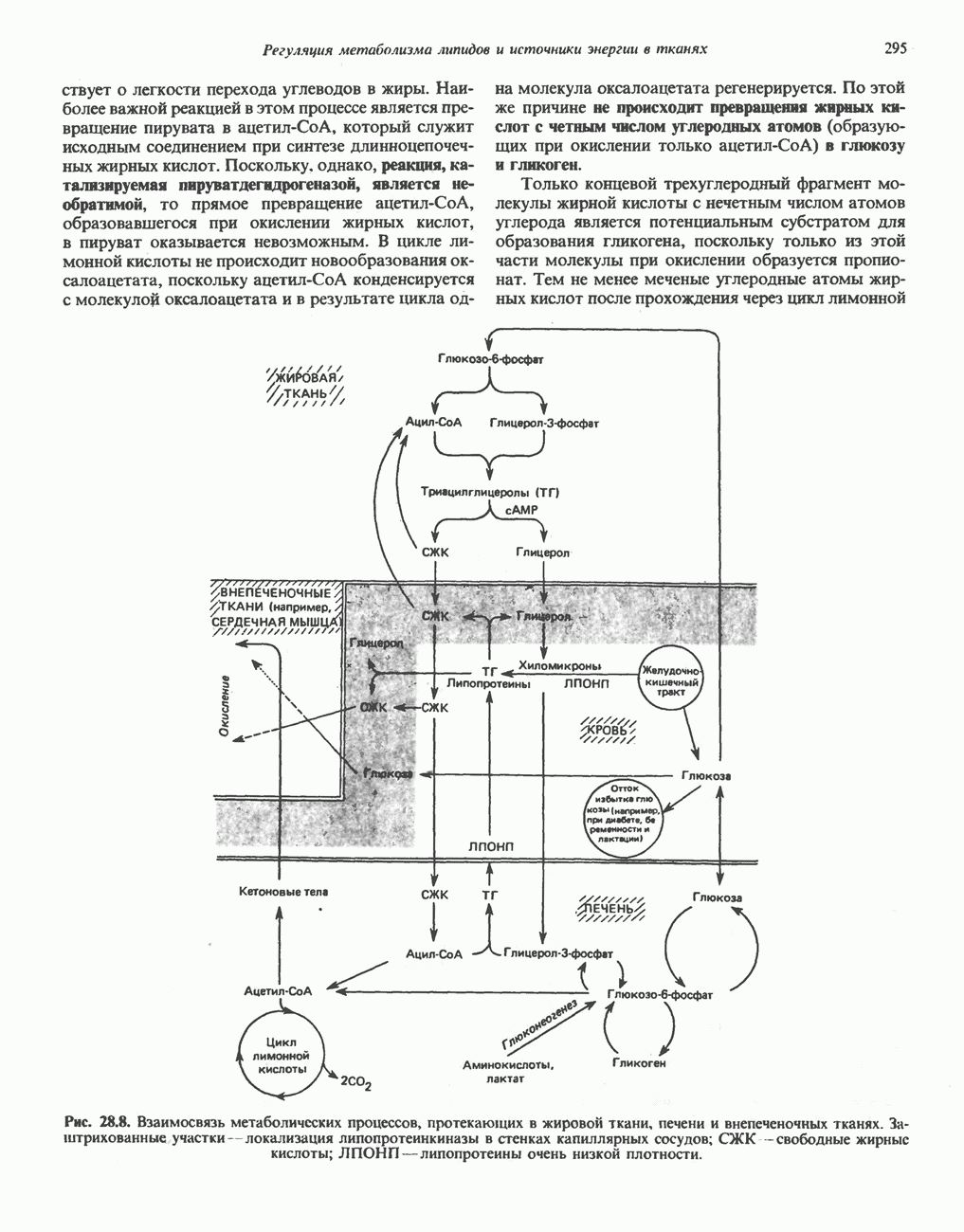
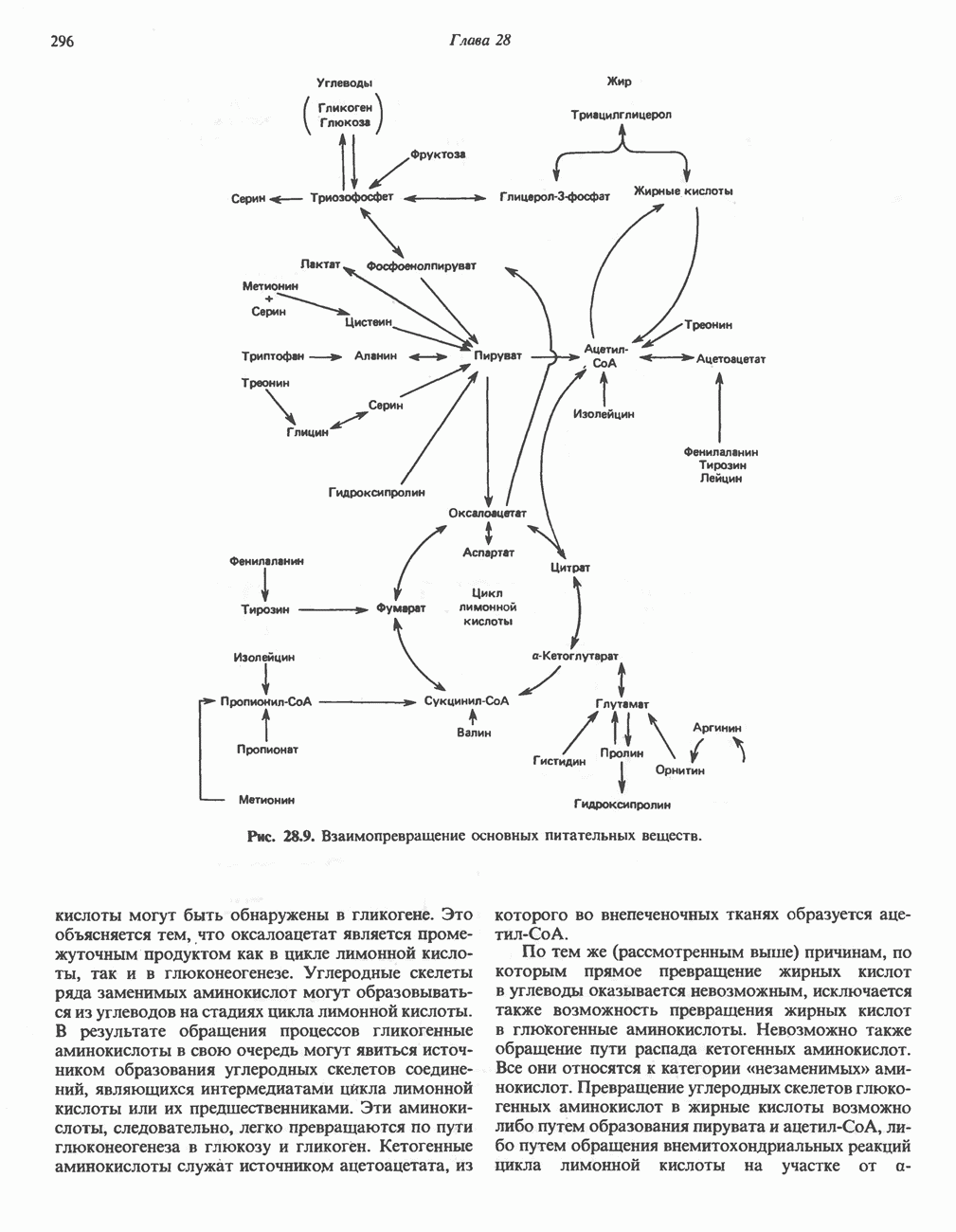
- ВЗАИМНОЕ ПРЕВРАЩЕНИЕ ОСНОВНЫХ ПИТАТЕЛЬНЫХ ВЕЩЕСТВ (рис. 28.9)
- ЭКОНОМИКА УГЛЕВОДНОГО И ЛИПИДНОГО ОБМЕНА В ОРГАНИЗМЕ
- ГОЛОДАНИЕ
- Раздел III. Метаболизм белков и аминокислот
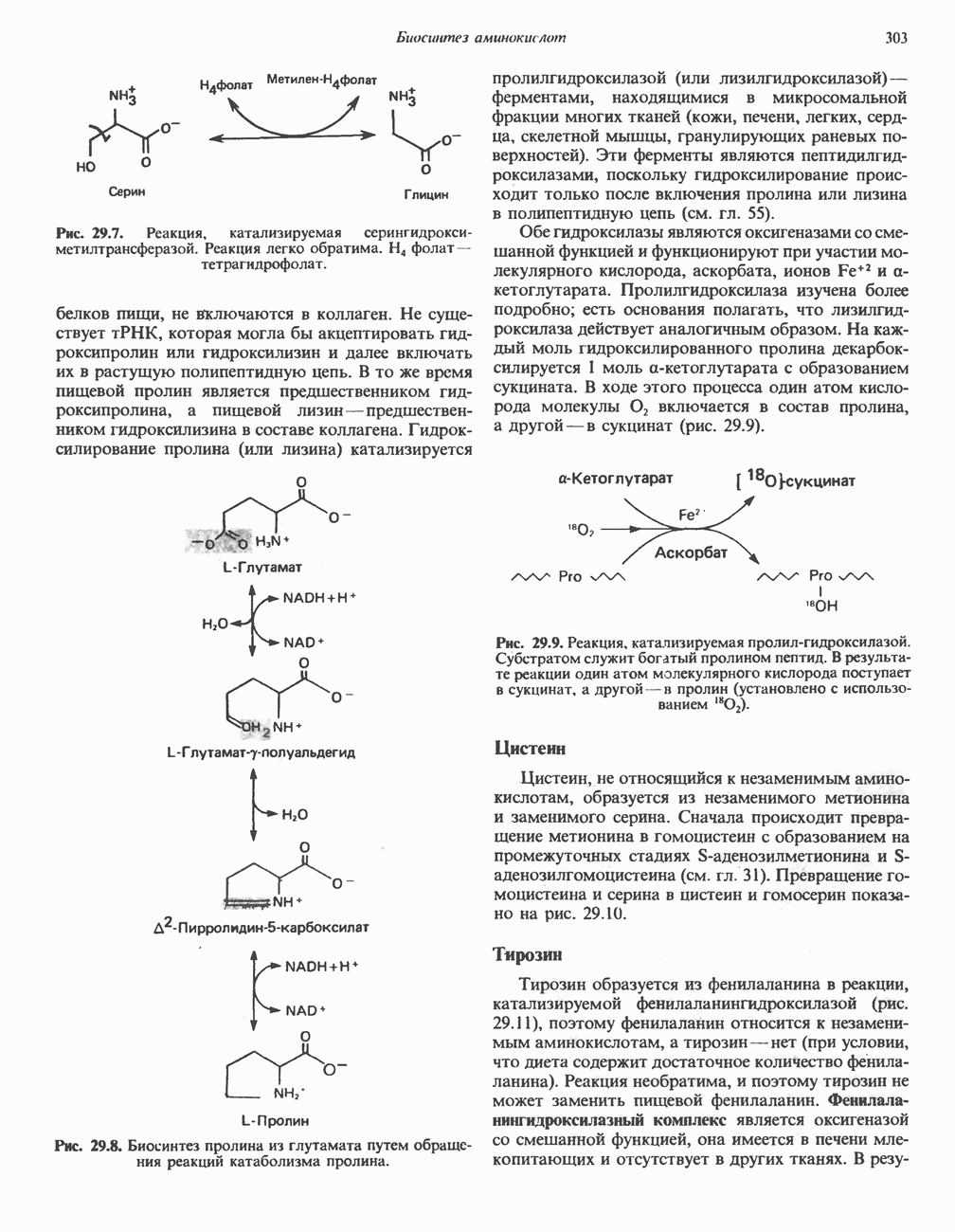
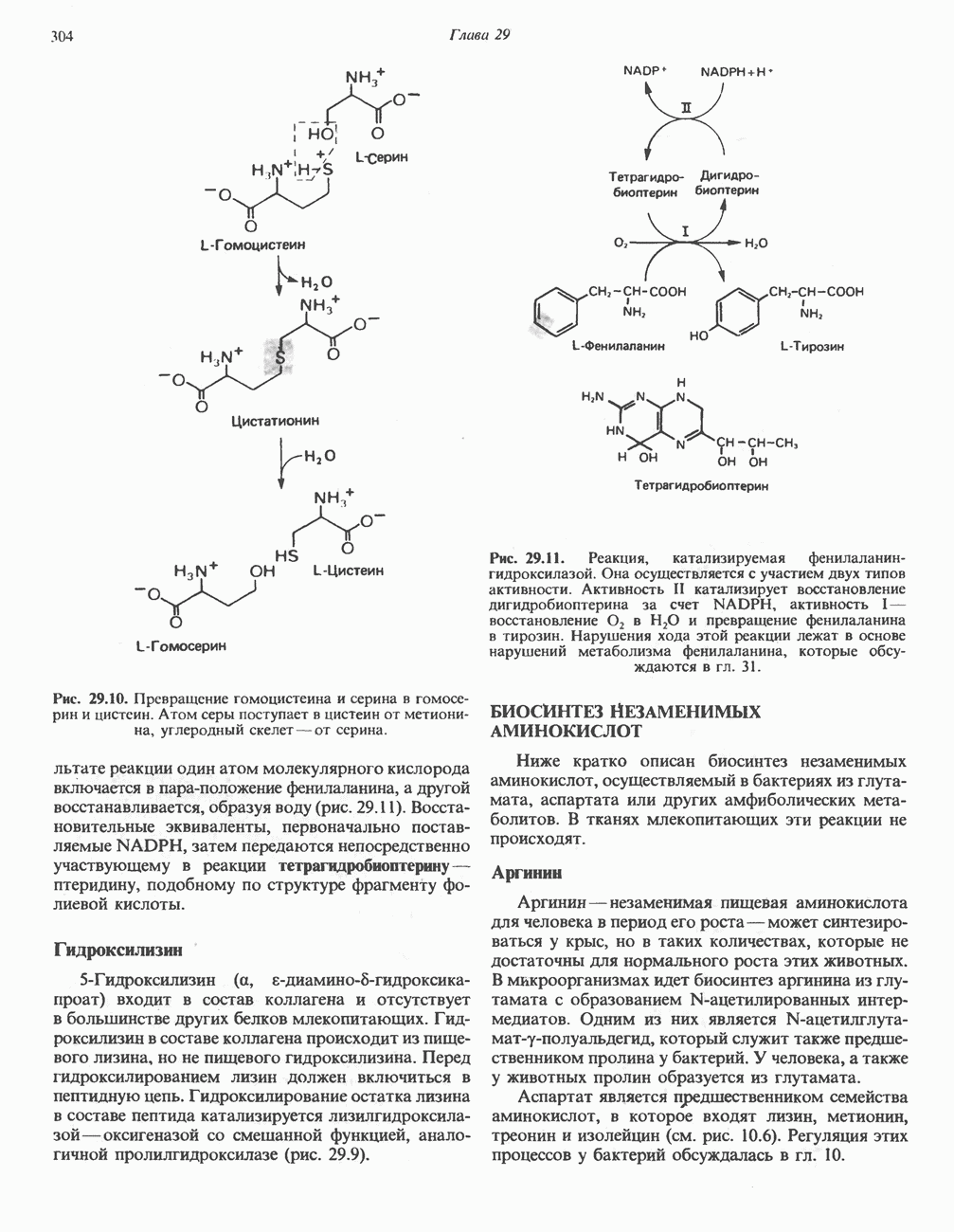
- Глава 29. Биосинтез аминокислот
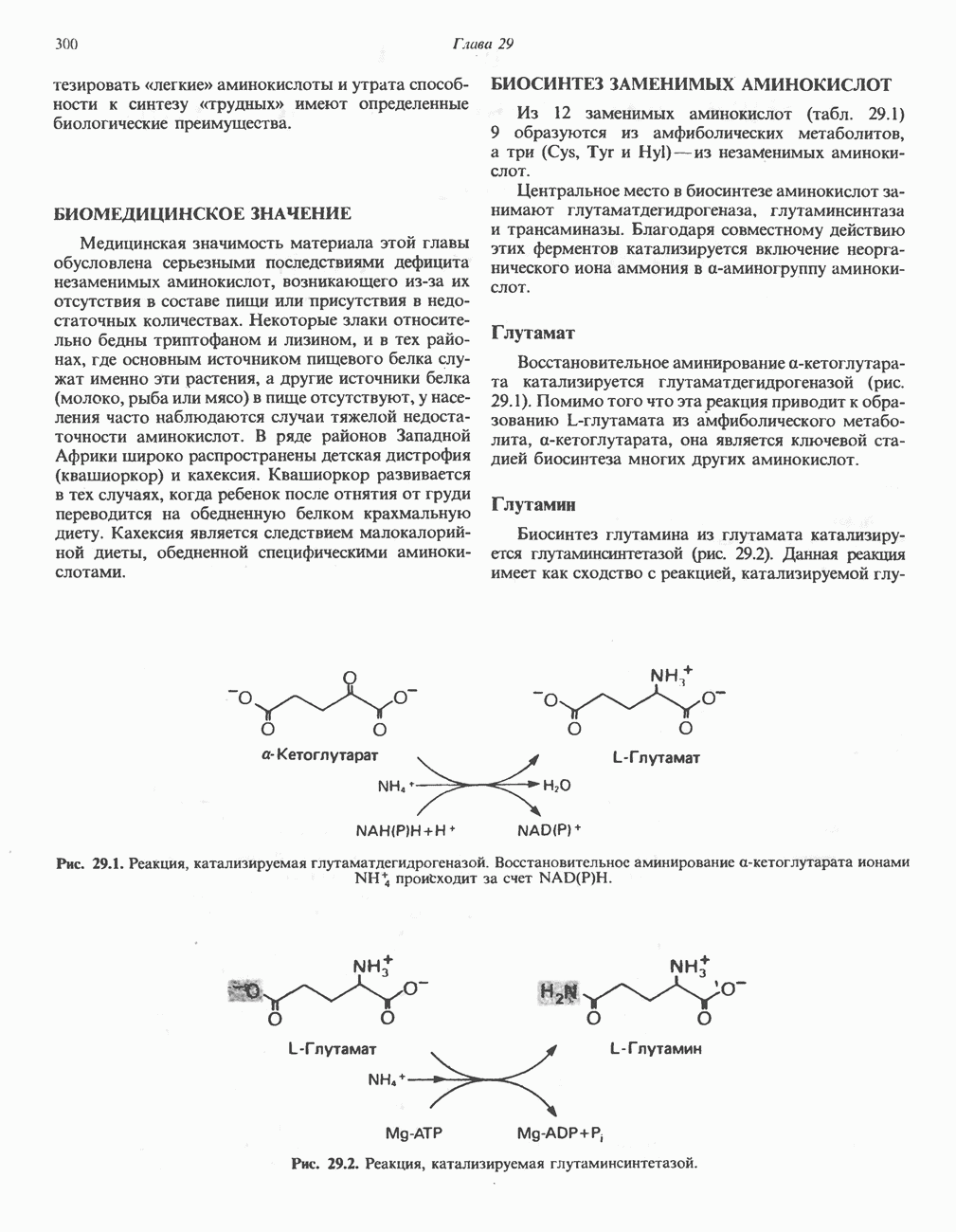
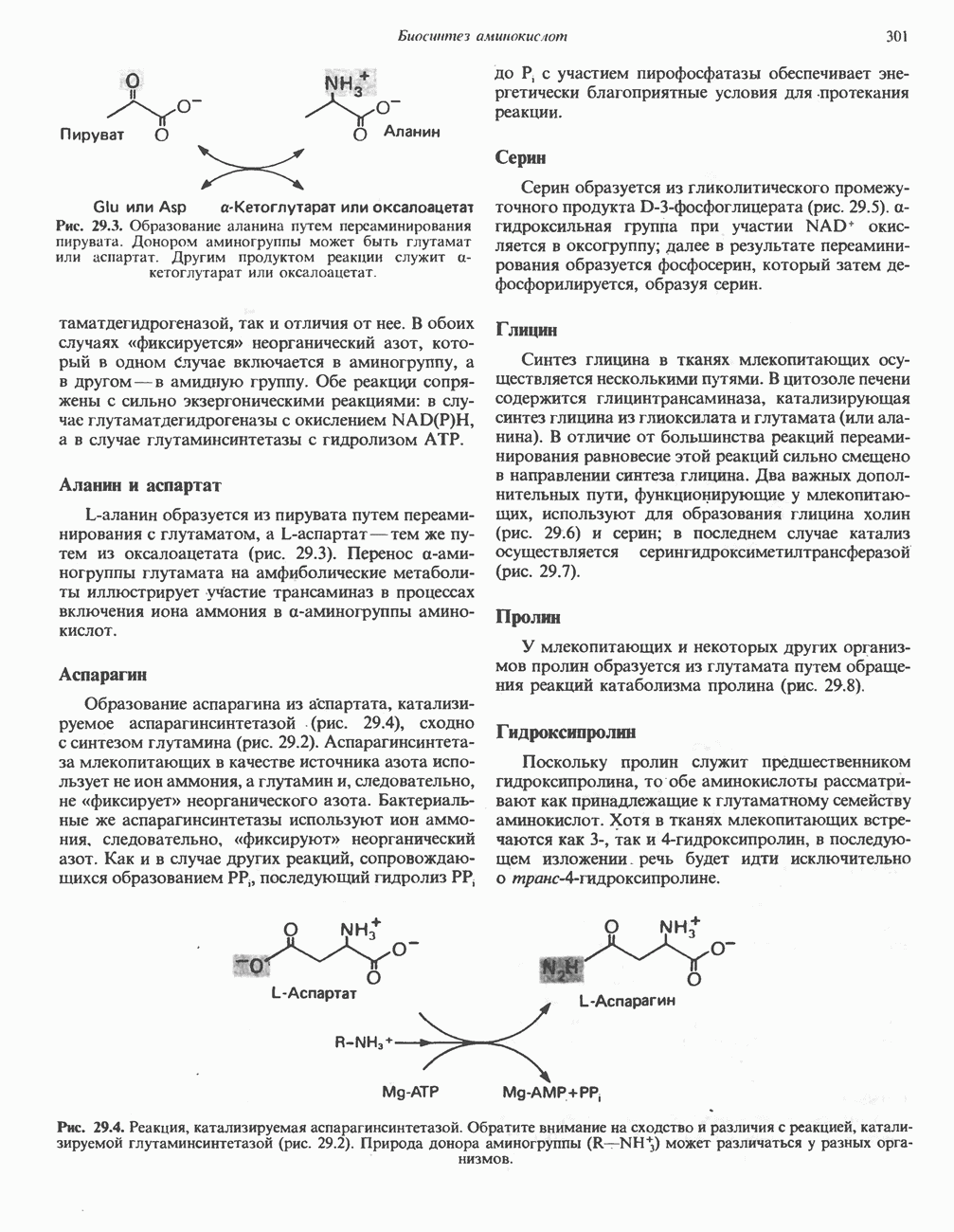
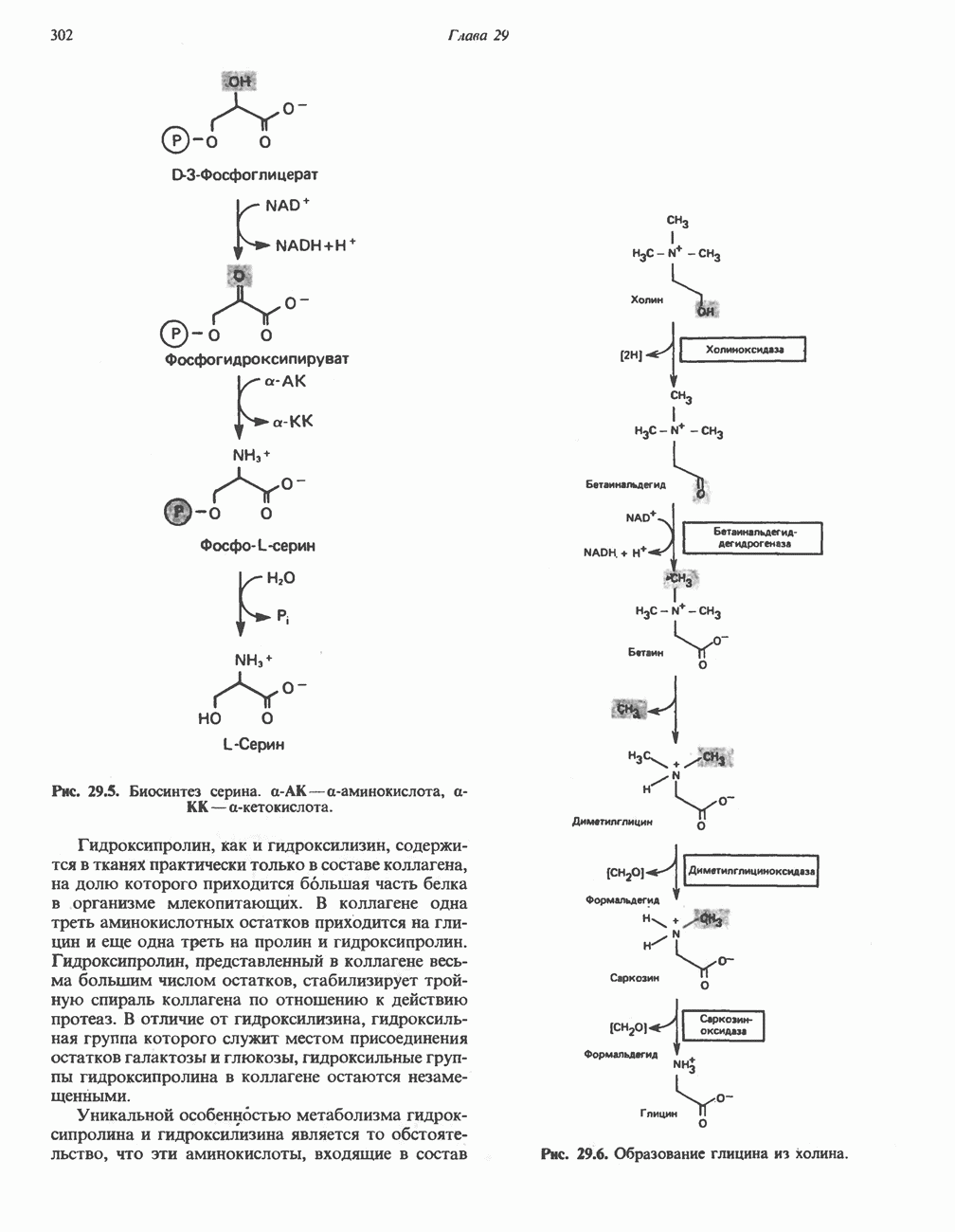
- БИОСИНТЕЗ ЗАМЕНИМЫХ АМИНОКИСЛОТ
- БИОСИНТЕЗ НЕЗАМЕНИМЫХ АМИНОКИСЛОТ
- Глава 30. Катаболизм азота аминокислот
- ПЕРЕАМИНИРОВАНИЕ
- ОКИСЛИТЕЛЬНОЕ ДЕЗАМИНИРОВАНИЕ
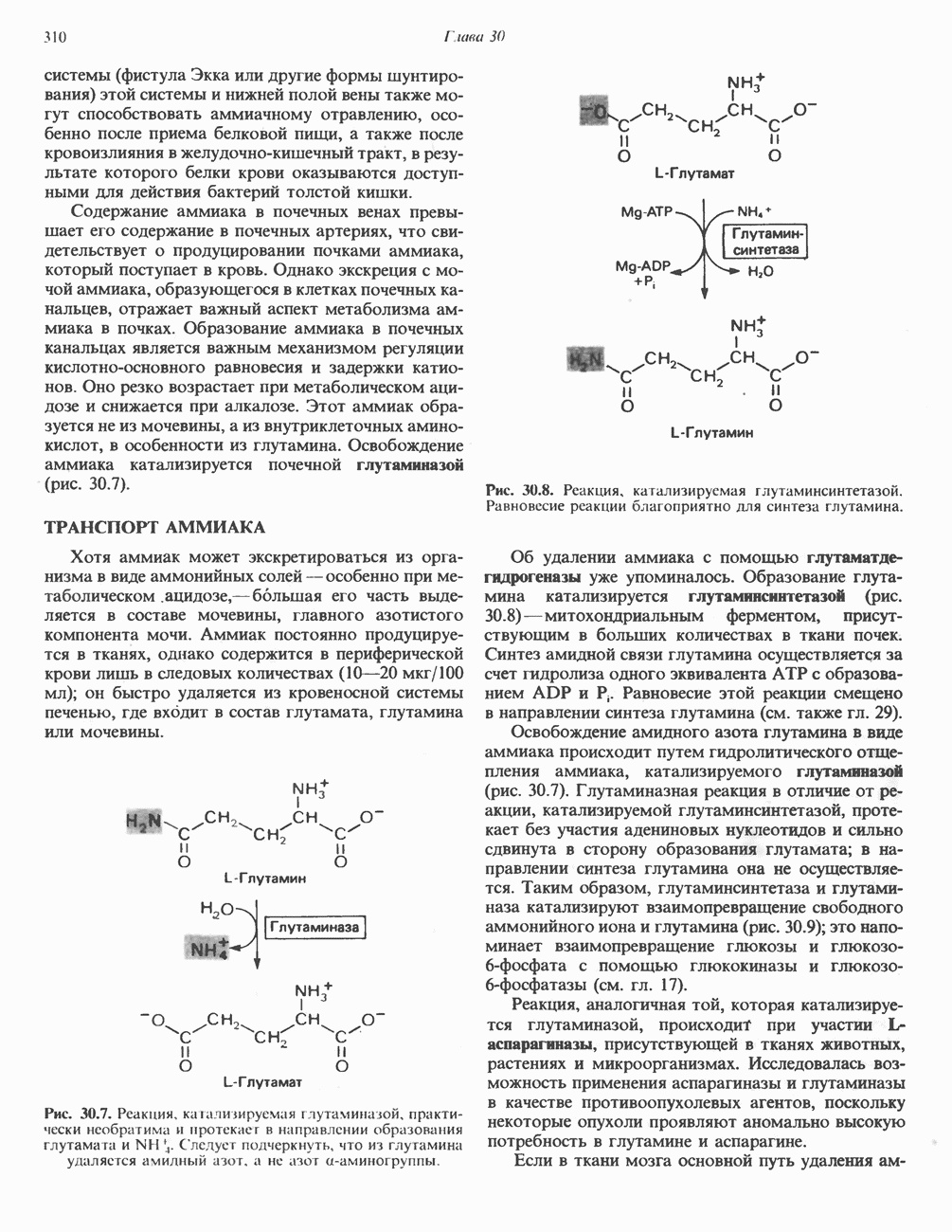
- ОБРАЗОВАНИЕ АММИАКА
- ТРАНСПОРТ АММИАКА
- ОБМЕН АМИНОКИСЛОТАМИ МЕЖДУ ОРГАНАМИ В ПОСТАБСОРБТИВНОМ СОСТОЯНИИ
- ОБМЕН АМИНОКИСЛОТ МЕЖДУ ОРГАНАМИ ПОСЛЕ ПРИЕМА ПИЩИ
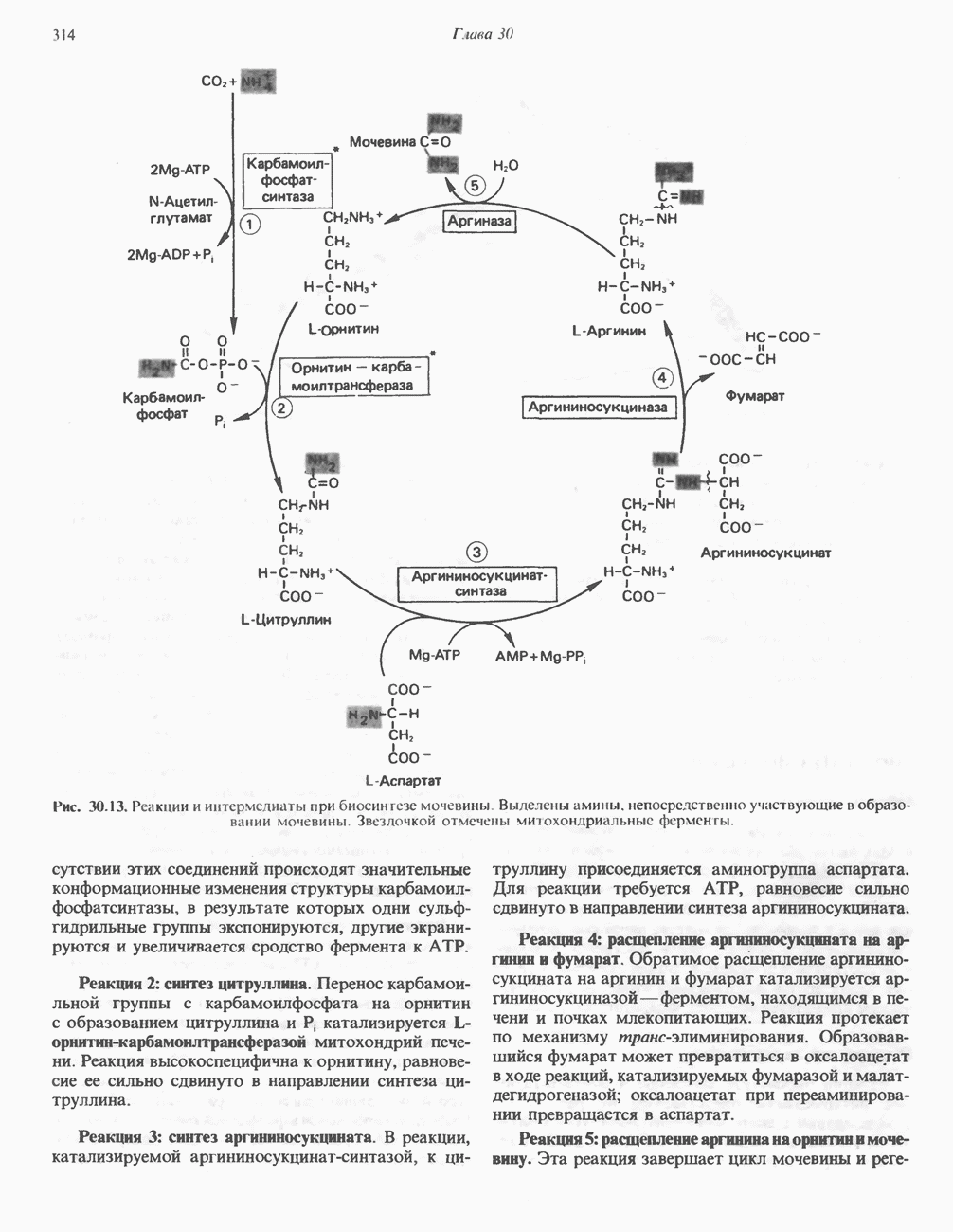
- БИОСИНТЕЗ МОЧЕВИНЫ
- РЕГУЛЯЦИЯ СИНТЕЗА МОЧЕВИНЫ
- МЕТАБОЛИЧЕСКИЕ НАРУШЕНИЯ ЦИКЛА МОЧЕВИНЫ
- Глава 31. Катаболизм углеродного скелета аминокислот
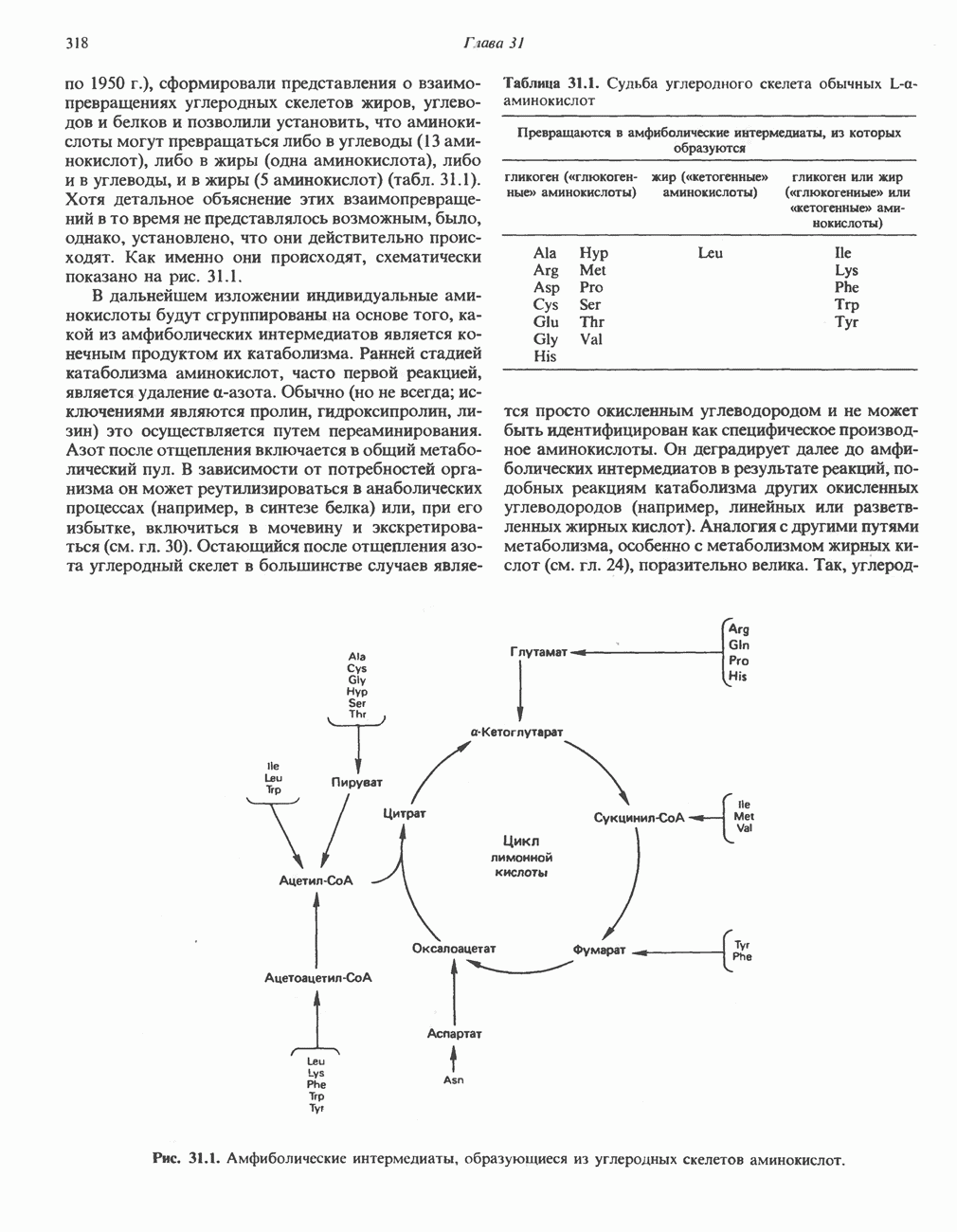
- ПРЕВРАЩЕНИЕ УГЛЕРОДНОГО СКЕЛЕТА ОБЫЧНЫХ L-a-АМИНОКИСЛОТ В АМФИБОЛИЧЕСКИЕ ИНТЕРМЕДИАТЫ
- АМИНОКИСЛОТЫ, ОБРАЗУЮЩИЕ ОКСАЛОАЦЕТАТ
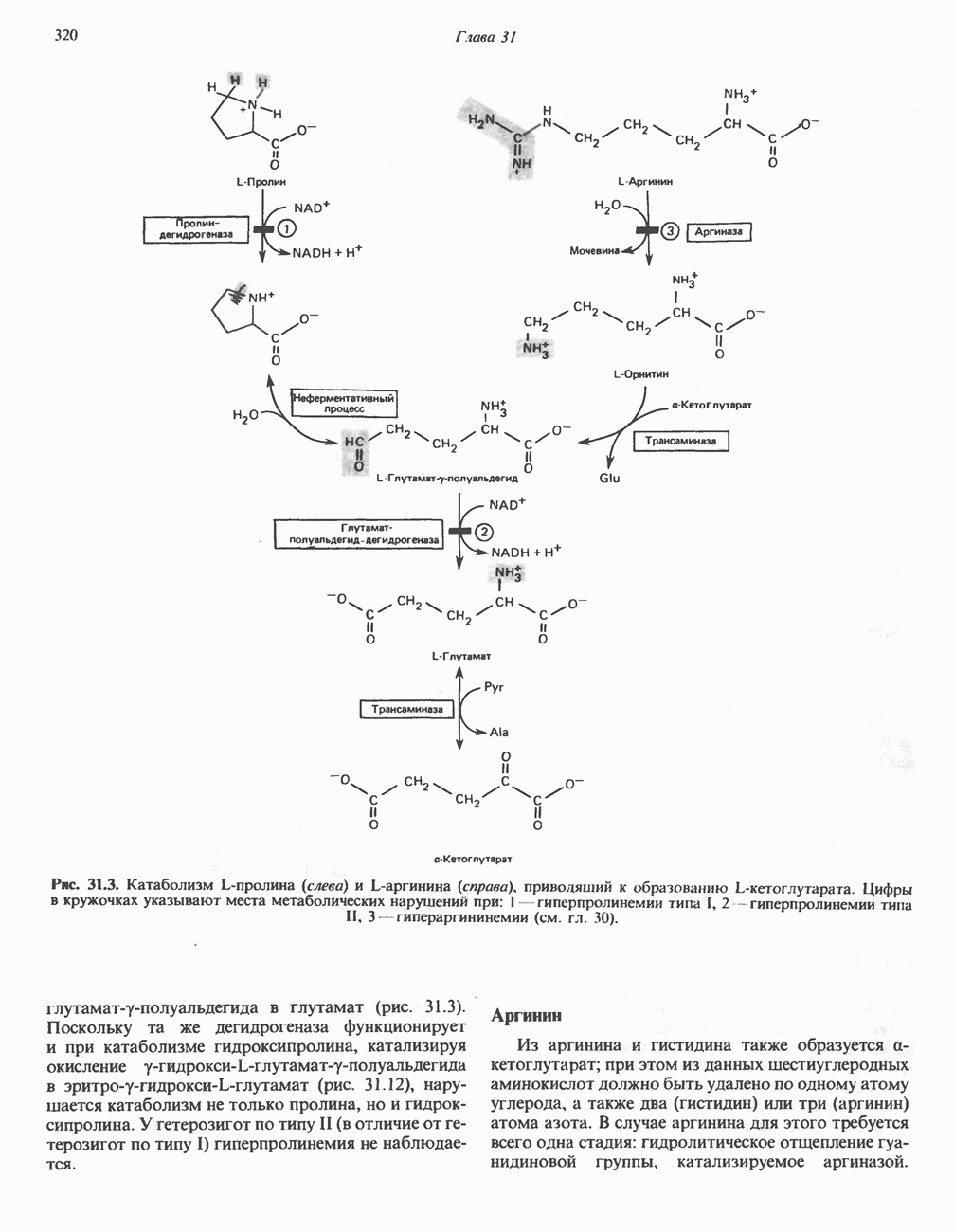
- АМИНОКИСЛОТЫ, ОБРАЗУЮЩИЕ а-КЕТОГЛУТАРАТ
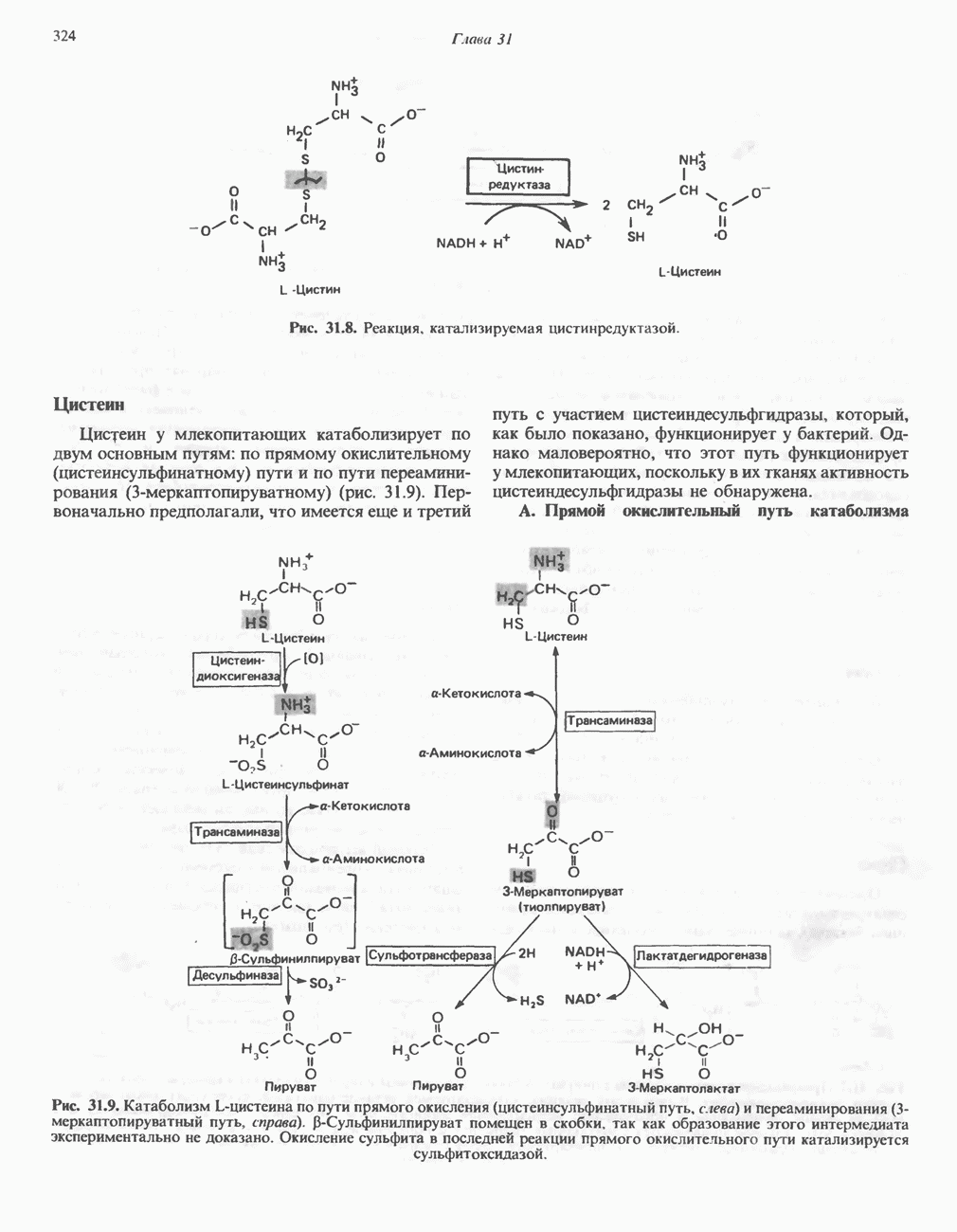
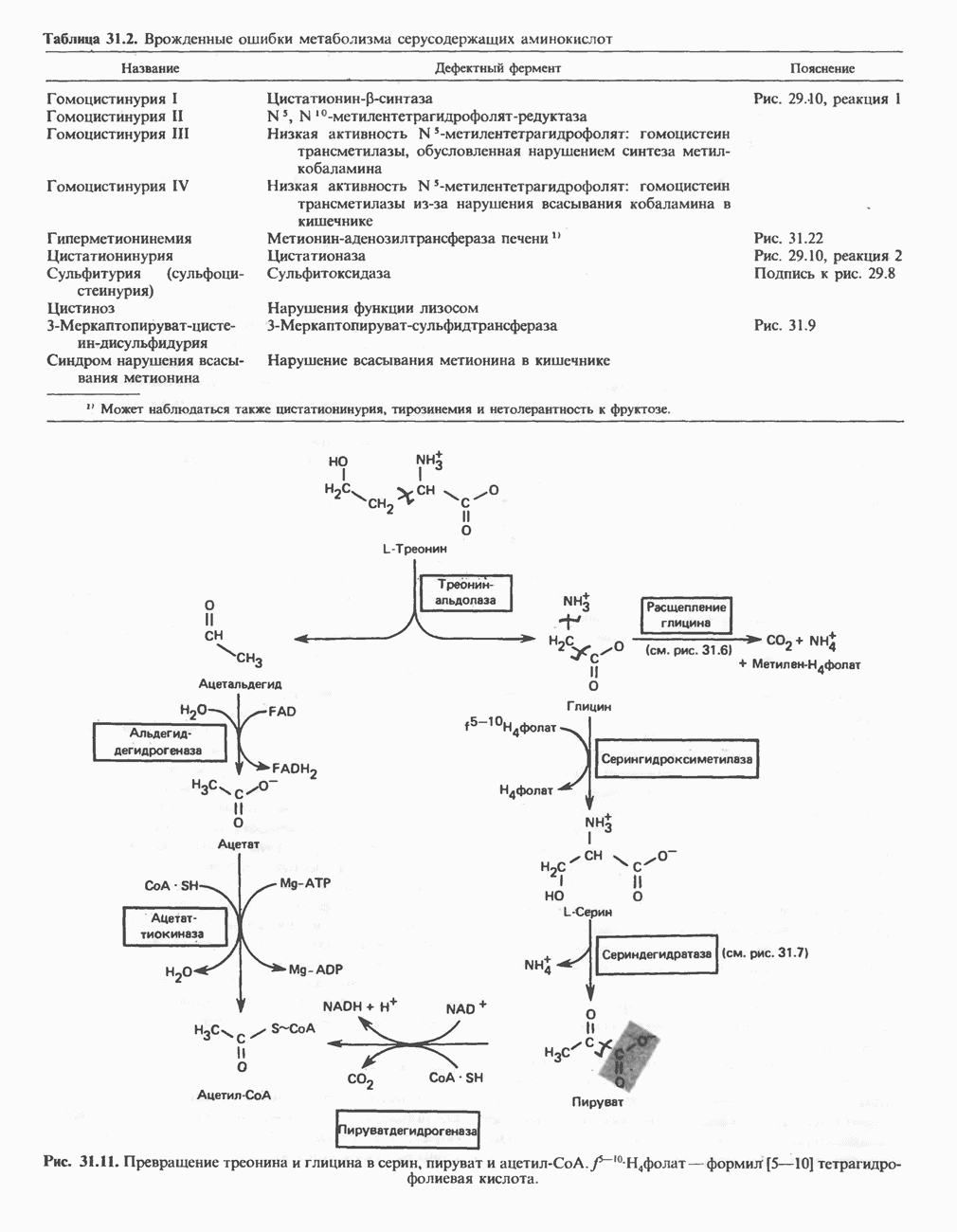
- АМИНОКИСЛОТЫ, ОБРАЗУЮЩИЕ ПИРУВАТ
- АМИНОКИСЛОТЫ, ОБРАЗУЮЩИЕ АЦЕТИЛ-КОФЕРМЕНТ А
- АМИНОКИСЛОТЫ, ОБРАЗУЮЩИЕ СУКЦИНИЛ-КОФЕРМЕНТ А
- Глава 32. Превращение аминокислот в специализированные продукты
- ГЛИЦИН
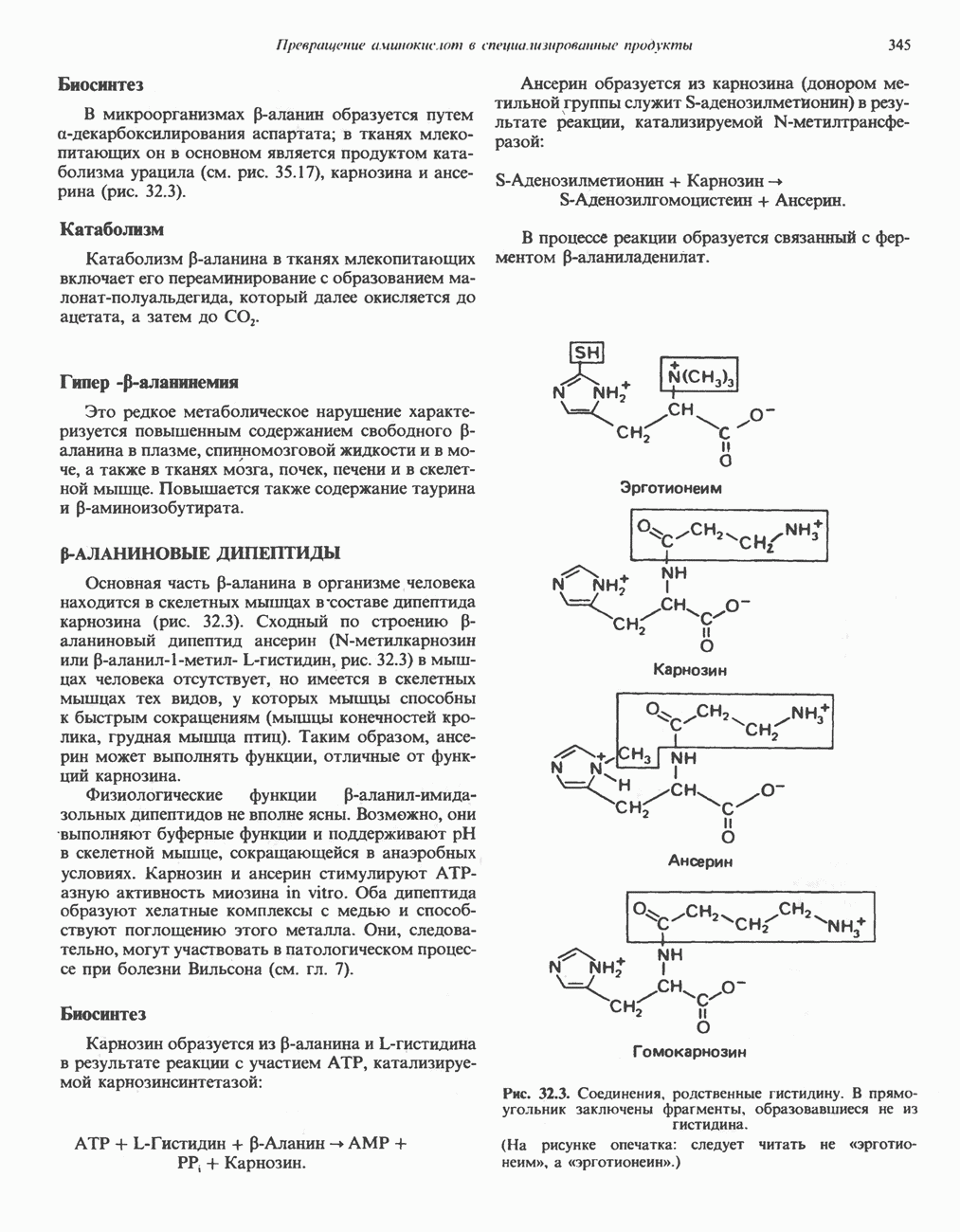
- р-АЛАНИНОВЫЕ ДИПЕПТИДЫ
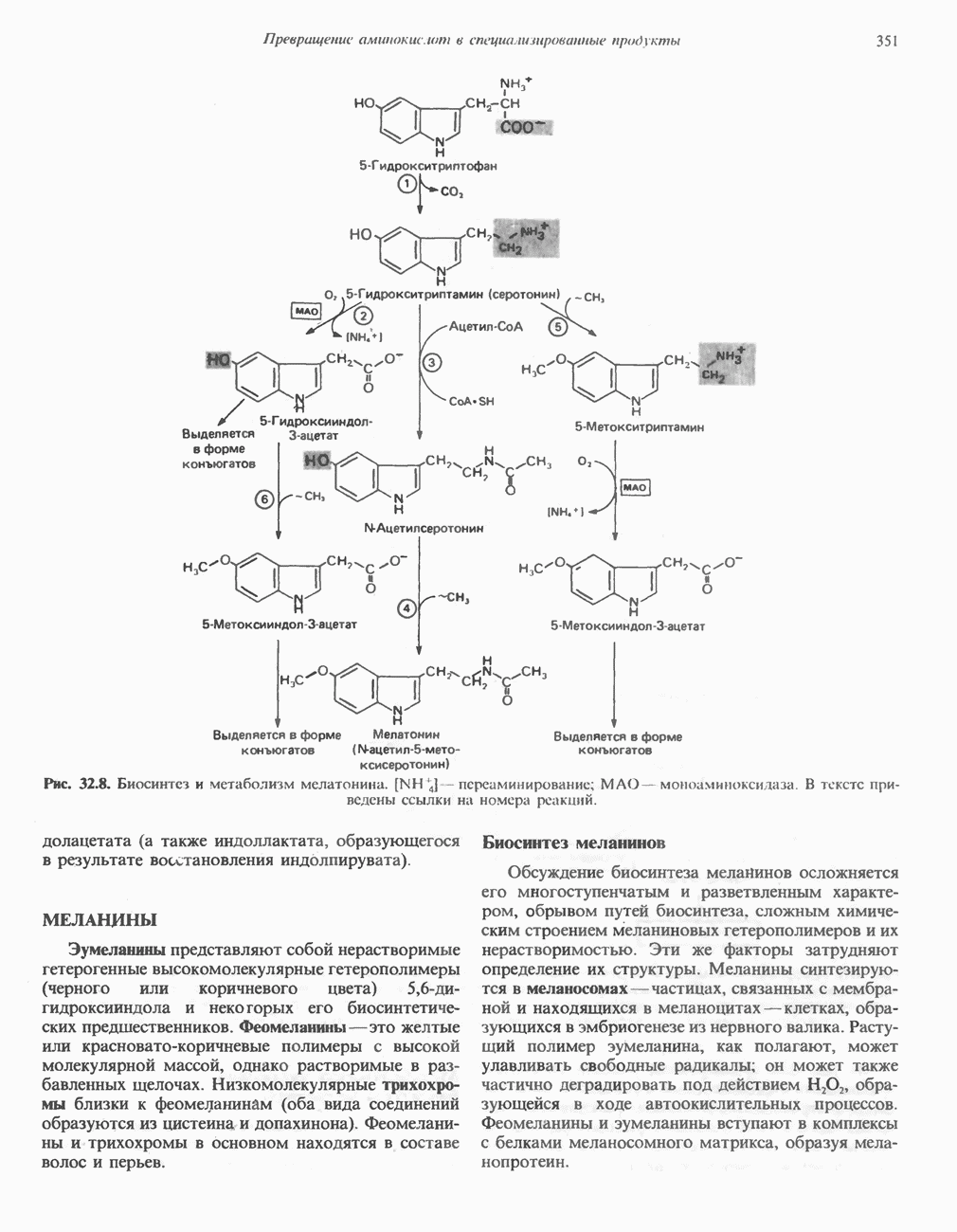
- ТРИПТОФАН
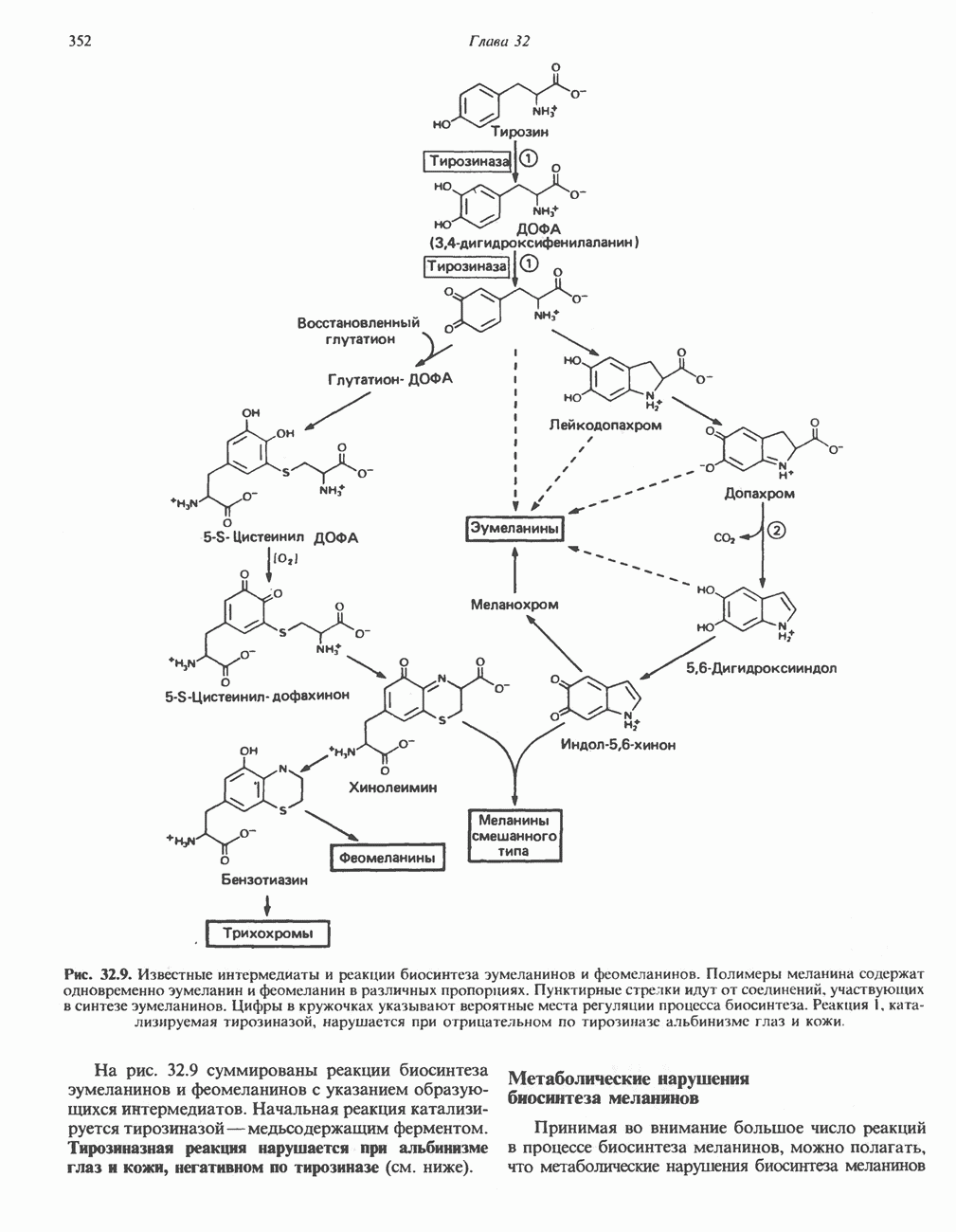
- МЕЛАНИНЫ
- ТИРОЗИН
- КРЕАТИН И КРЕАТИНИН
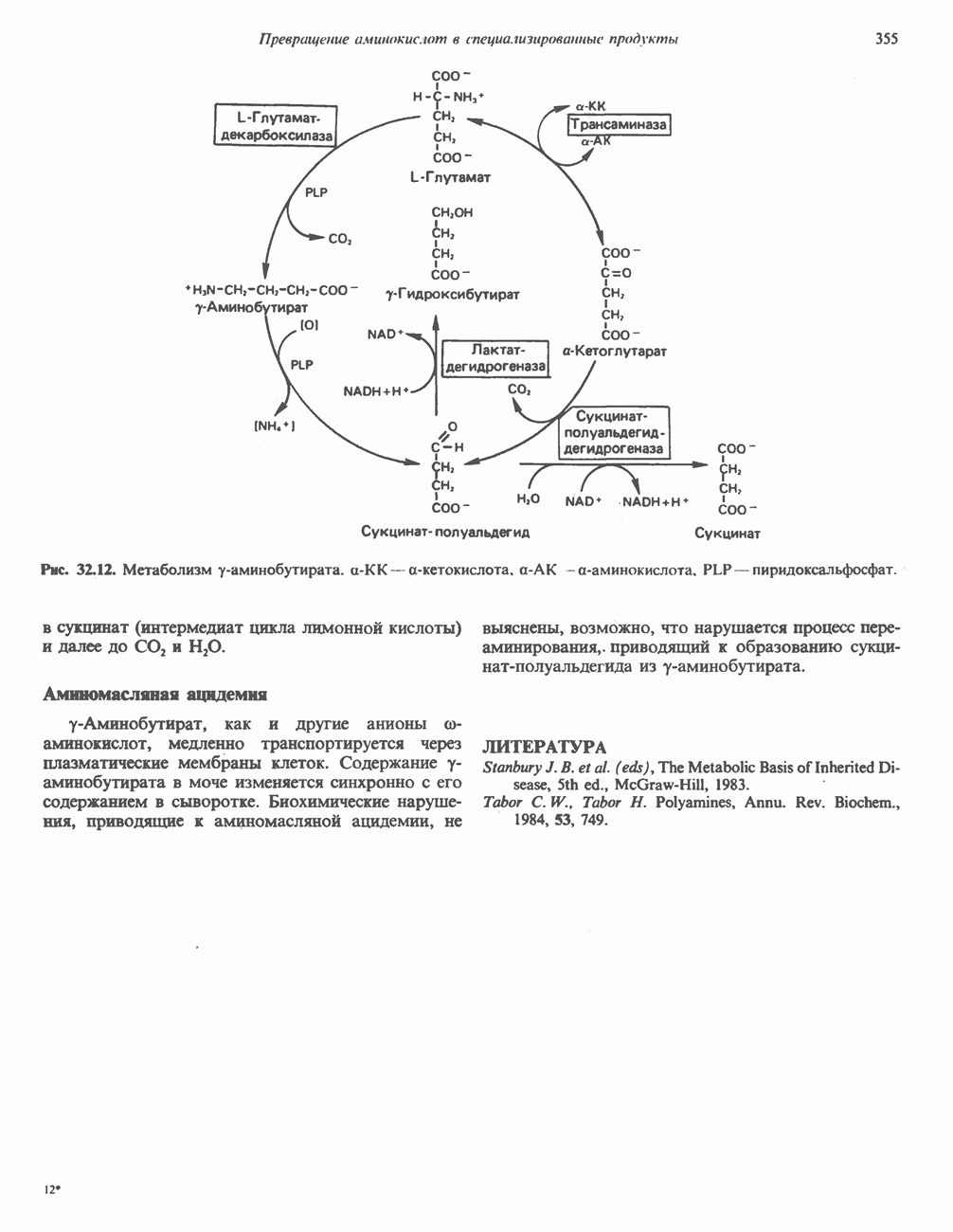
- у-АМИНОБУТИРАТ
- Глава 33. Порфирины и желчные пигменты
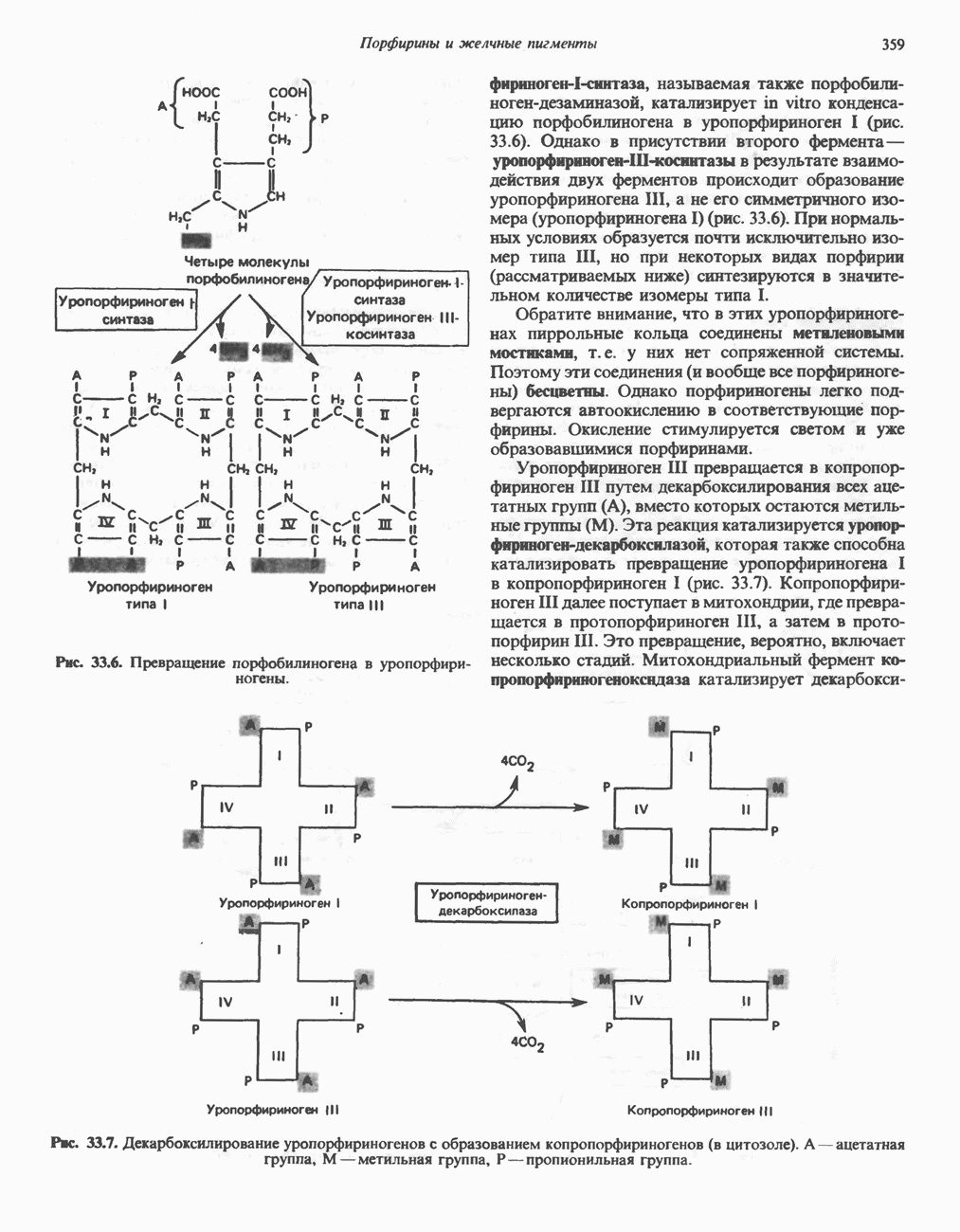
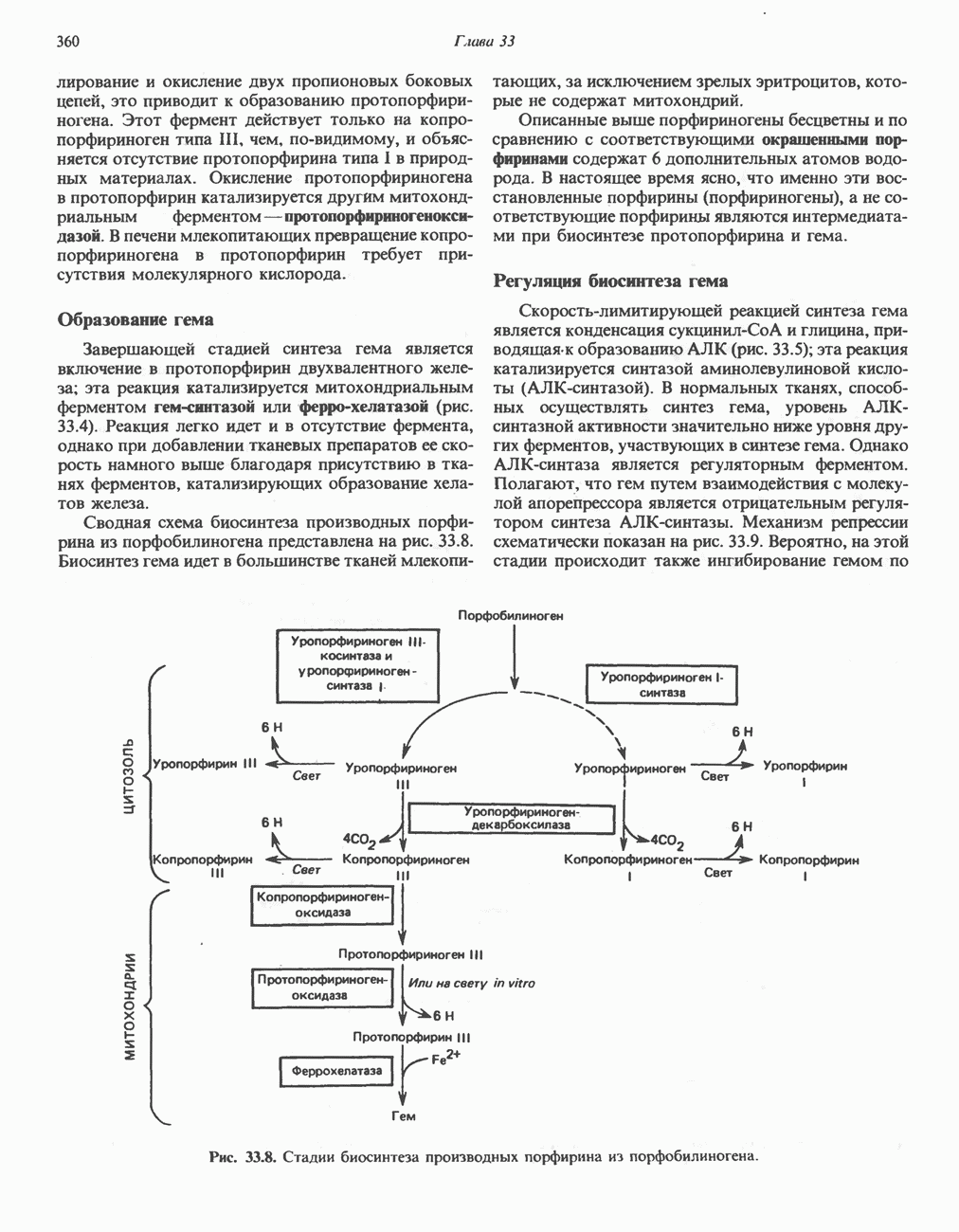
- ПОРФИРИНЫ
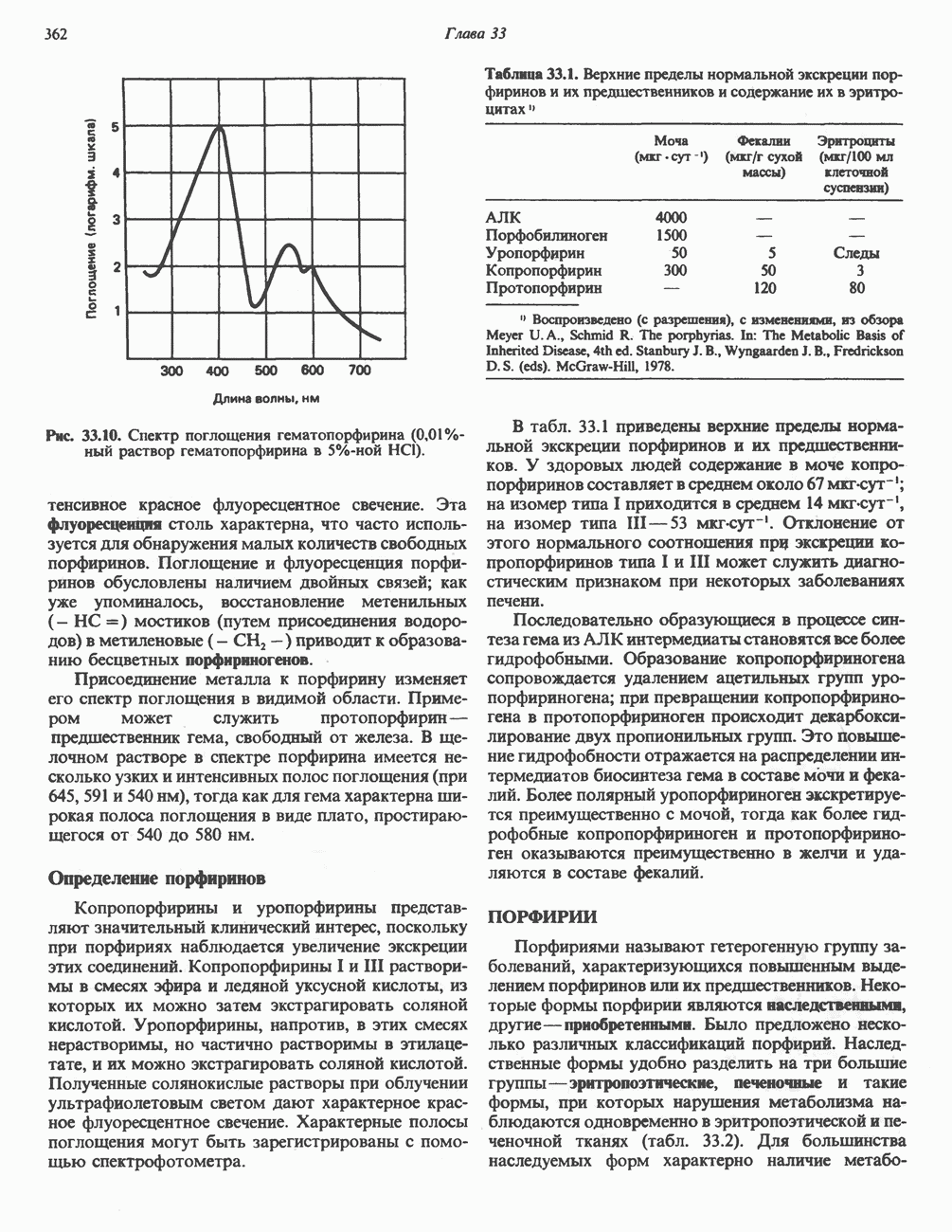
- ПОРФИРИН
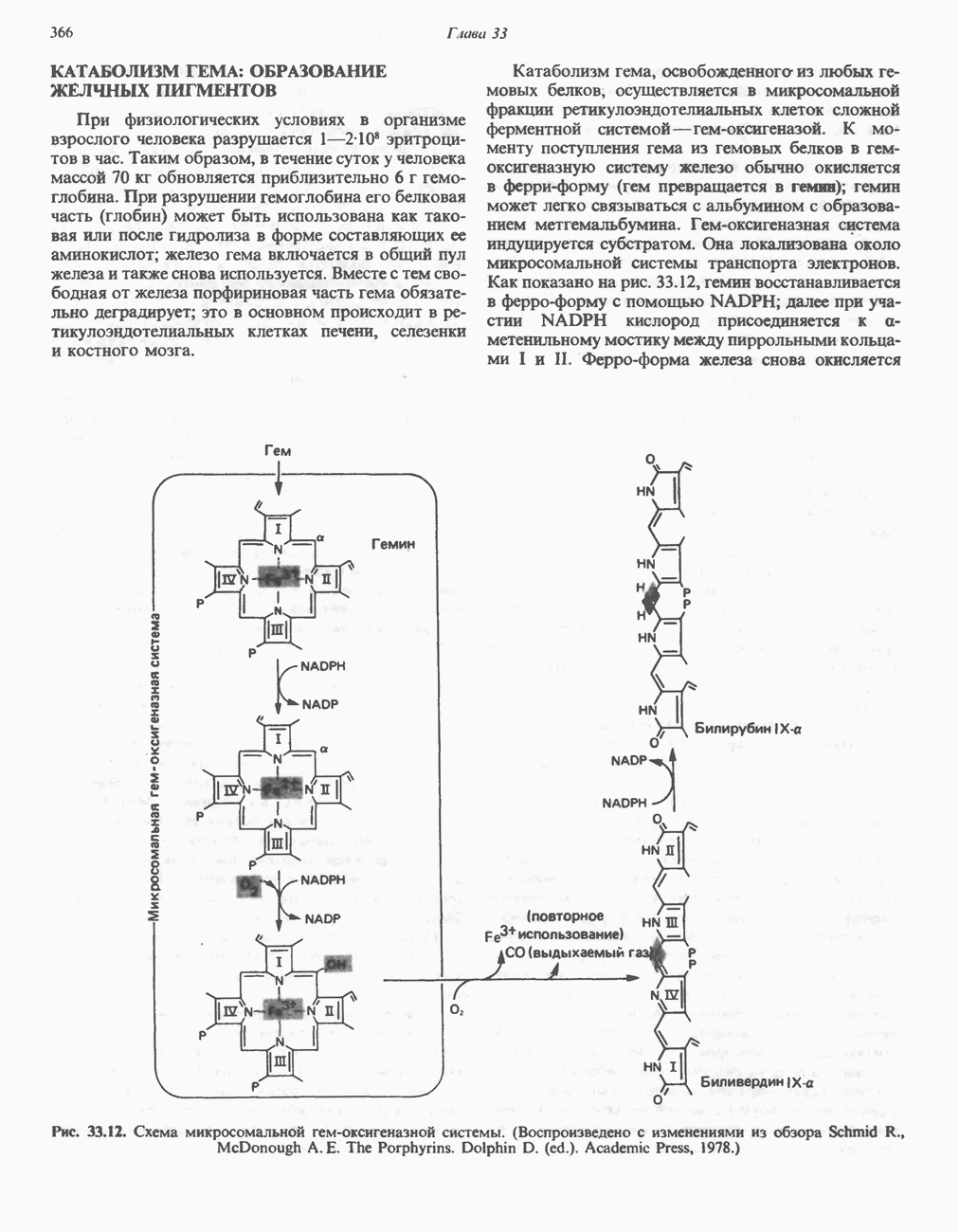
- КАТАБОЛИЗМ ГЕМА: ОБРАЗОВАНИЕ ЖЕЛЧНЫХ ПИГМЕНТОВ
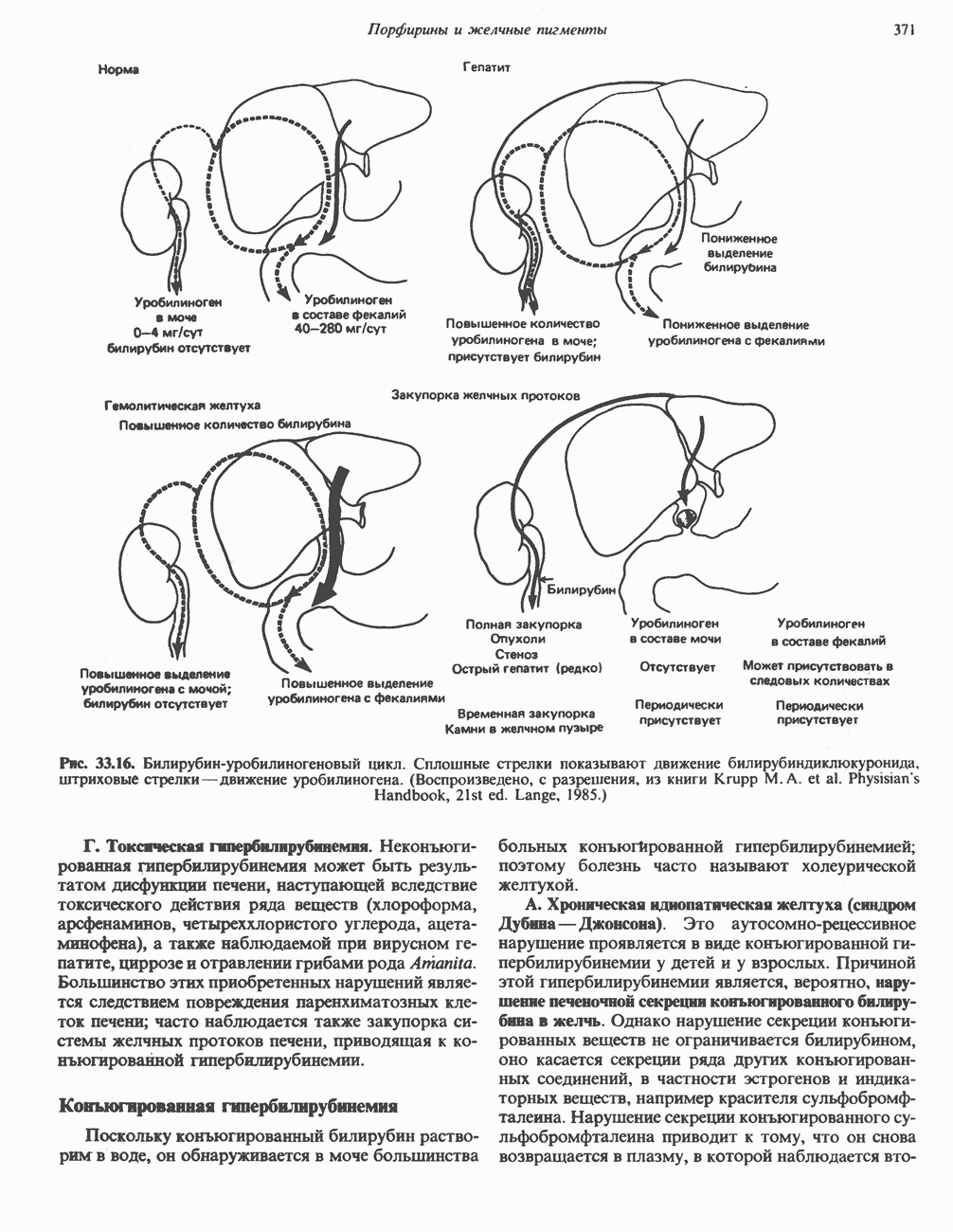
- МЕТАБОЛИЗМ БИЛИРУБИНА В КИШЕЧНИКЕ
- ГИПЕРБИЛИРУБИНЕМИЯ
- Список сокращений