| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
2.4.3. Методы выращивания кристаллов из растворов
Общие положения. При выращивании кристаллов из растворов появляется возможность использовать в качестве движущей силы кристаллизации градиент концентрации. Это позволяет более гибко управлять процессом и создает большое разнообразие методов, но
одновременно увеличивает значение гидродинамических условий процесса для кинетики кристаллизации, так как в системах с концентрационным градиентом диффузия всегда играет важную роль. Поскольку вблизи поверхности кристалла имеется пограничный диффузионный слой, то в процессе кристаллизации можно выделить два этапа:
1) диффузионный перенос вещества из объема раствора к поверхности кристалла

2) межфазовый массоперенос и встраивание частиц, обусловленные химической активностью данной поверхности кристалла,

где  толщина диффузионного слоя;
толщина диффузионного слоя;  — коэффициент диффузии;
— коэффициент диффузии;  — поверхность кристалла; К — коэффициент скорости реакции; с — концентрация вещества в объеме раствора;
— поверхность кристалла; К — коэффициент скорости реакции; с — концентрация вещества в объеме раствора;  — равновесная концентрация раствор — кристалл, т. е. концентрация насыщения;
— равновесная концентрация раствор — кристалл, т. е. концентрация насыщения;  — концентрация вещества у растущей поверхности кристалла.
— концентрация вещества у растущей поверхности кристалла.
Решая уравнения (2.96) и (2.97) совместно для условия, когда скорости обоих этапов равны, получаем

При большой скорости химического процесса  выражение (2.98) превращается в (2.96), т. е. процесс роста кристалла лимитируется диффузией. При малом К выражение (2.98) приближается к (2.97), т. е. межфазная химическая реакция протекает настолько медленно, что диффузия уже не играет никакой роли.
выражение (2.98) превращается в (2.96), т. е. процесс роста кристалла лимитируется диффузией. При малом К выражение (2.98) приближается к (2.97), т. е. межфазная химическая реакция протекает настолько медленно, что диффузия уже не играет никакой роли.
Поскольку коэффициент диффузии зависит от вязкости раствора, а коэффициент скорости роста — от химической активности растворителя, то эти параметры являются определяющими при выборе растворителя и метода выращивания кристалла из раствора. При повышенной вязкости раствора явно преобладает диффузионный механизм, возможен захват жидкой фазы растущим кристаллом, дендритный и поликристаллический рост.
Химическая активность растворителя по отношению к граням кристалла характеризуется величиной (растворимости. Однои то же вещество при кристаллизации из разных растворителей образует кристаллы различной огранкн, так как растворимость одной и той же грани кристалла в различных растворителях различна. Наибольшая информация о растворимости в данной системе содержится в фазовых диаграммах растворимости:  и
и  .
.
Выбор (метода кристаллизации и растворителя начинается обычно с рассмотрения диаграммы температура — растворимость  Поэтому часто говорят об изотермических и политермических методах кристаллизации. Возможны четыре основных типа кривых растворимости.
Поэтому часто говорят об изотермических и политермических методах кристаллизации. Возможны четыре основных типа кривых растворимости.
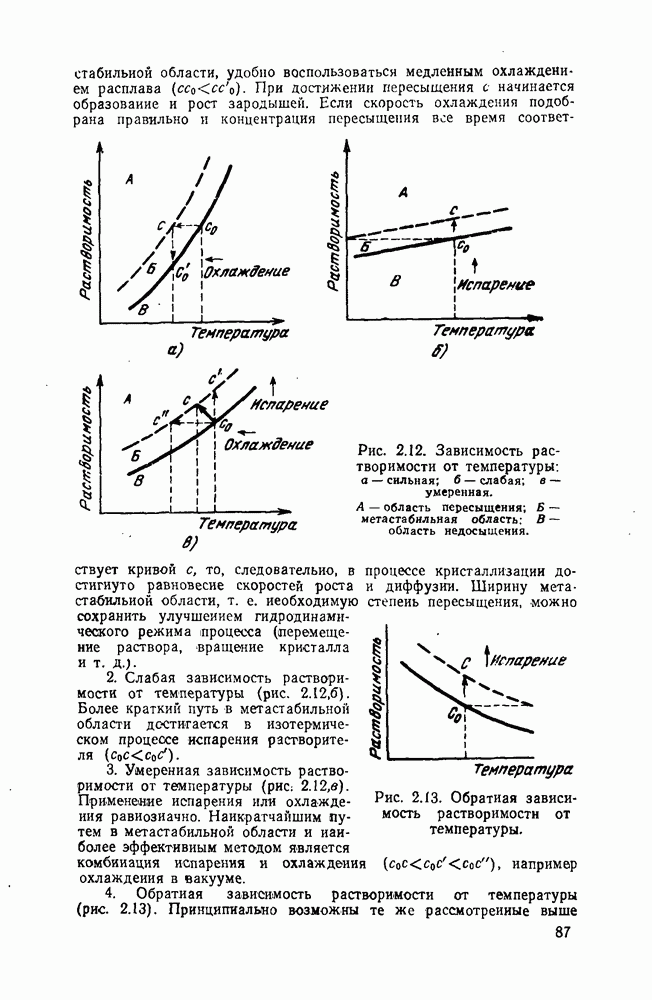
1. Сильная зависимость растворимости от температуры (рис. 2.12,а). Чтобы вести процесс по более краткому пути в
метастабильной области, удобно воспользоваться медленным охлаждением расплава  При достижении пересыщения с начинается образование и рост зародышей. Если скорость охлаждения подобрана правильно и концентрация пересыщения все время соответствует кривой с, то, следовательно, в процессе кристаллизации достигнуто равновесие скоростей роста и диффузии.
При достижении пересыщения с начинается образование и рост зародышей. Если скорость охлаждения подобрана правильно и концентрация пересыщения все время соответствует кривой с, то, следовательно, в процессе кристаллизации достигнуто равновесие скоростей роста и диффузии.

Рис. 2.12. Зависимость растворимости от температуры: а — сильная; б — слабая; в — умеренная. А — область пересыщения; Б — метастабильная область: В — область недосыщения.
Ширину метастабильной области, т. е. необходимую степень пересыщения, можно сохранить улучшением гидродинамического режима процесса (перемещение раствора, вращение кристалла и т. д.).
2. Слабая зависимость растворимости от температуры (рис. 2.12, б).

Рис. 2.13. Обратная зависимость растворимости от температуры.
Более краткий путь в метастабильной области достигается в изотермическом процессе испарения растворителя 
3. Умеренная зависимость растворимости от температуры (рис: 2.12,в).
Применение испарения или охлаждения равнозначно. Наикратчайшим путем в метастабильной области и наиболее эффективным методом является комбинация испарения и охлаждения  например охлаждения в вакууме.
например охлаждения в вакууме.
4. Обратная зависимость растворимости от температуры (рис. 2.13). Принципиально возможны те же рассмотренные выше
варианты, но иместо охлаждения необходим программный нагрев. При удачной организации подпитки раствора из газовой фазы или с помощью циркуляции раствора у растущей поверхности возможны изотермические методы без испарения растворителя.
Наибольшее развитие и распространение получили статические и динамические методы выращивания кристаллов из растворов в таких растворителях, как вода, спирт, эфир и т. д. Используя вращение или более сложные движения кристалла, циркуляцию пересыщенного раствора и стабилизацию или программное понижение температуры, удается выращивать однородные совершенные кристаллы рекордных размеров. Так были выращены кристаллы сегнетовой соли  весом
весом 
Методы кристаллизации из водных растворов успешно применяются для выращивания модуляционных кристаллов типа дигидрофосфата аммония  и дигидрофосфата калия
и дигидрофосфата калия 
Кристаллизация из раствора в расплаве (метод флюсов). Особенно удобен этот метод для синтеза и выращивания монокристаллов тугоплавких или инконгруэнтяо плавящихся соединений, получение которых из стехиометрнческих расплавов крайне затруднительно. Выращивание кристаллов по этому методу происходит следующим образом. Исходные компоненты выращиваемого кристалла растворяются в иизкоплавкой солевой смеси до насыщения при температуре, превышающей температуру плавления чистой смеси. Раствор выдерживается при этой температуре в течение нескольких часов для достижения однородности расплава. Затем после введения в раствор затравочного кристалла, а Иногда и без него, начинают медленное  охлаждение раствора, вследствие чего в расплаве создается пересыщение и происходит кристаллизация растворенных компонентов растущего кристалла. Рост кристаллов продолжается в течение нескольких суток с линейной скоростью
охлаждение раствора, вследствие чего в расплаве создается пересыщение и происходит кристаллизация растворенных компонентов растущего кристалла. Рост кристаллов продолжается в течение нескольких суток с линейной скоростью  Обычно выращивание происходит в режиме молекулярной диффузии, хотя, конечно, более эффективны конвективный или вынужденный гидродинамический режим.
Обычно выращивание происходит в режиме молекулярной диффузии, хотя, конечно, более эффективны конвективный или вынужденный гидродинамический режим.
Выбор растворителя производится с учетом следующих соображений.
1. Растворитель и растворяемые вещества в жидком состоянии должны обладать полной смешиваемостью и не должны образовывать твердых растворов. Неполная смешиваемость и образование твердых растворов могут привести к нарушениям химического состава и параметров структуры растущего кристалла вследствие включений побочных фаз. Наиболее удобен растворитель, который образует с растворенным веществом эвтектику с высоким содержанием растворителя.
2. Растворитель не должен влиять на свойства выращиваемого кристалла. Например, железо и другие тяжелые металлы способны «тушить» люминесценцию, посторонние редкоземельные или переходные металлы могут образовывать дополнительные центры окраски.
3. Во избежание попадания примесей в выращиваемый кристалл в результате изоморфного замещения желательно, чтобы растворитель имел с кристаллизуемым веществом общий ион  а другие ионы имели сильно отличающиеся размерные параметры (ионные радиусы).
а другие ионы имели сильно отличающиеся размерные параметры (ионные радиусы).
4. Солевая смесь должна обладать малой вязкостью. Это облегчает диффузию компонентов раствора и ускоряет выравнивание концентрации в расплаве по мере обеднения кристаллизующимся веществом.
5. Давление паров компонентов солевой смеси должно быть по возможности малым, так как в результате испарения какого-либо компонента будет меняться состав расплава, а следовательно, и его свойства (температура плавления, вязкость, растворимость). Поэтому температуры плавления и кипения растворителя должны сильно различаться между собой.
6. Температура плавления расплава должна быть значительно ниже температуры плавления кристаллизуемого вещества для того, чтобы рабочая температура сохранялась низкой.
7. Желательно, чтобы оставшийся расплав легко отделялся от выращенного кристалла простыми методами (например, растворением в воде).
Методом кристаллизации из раствора в расплаве выращивают гранаты, рубин, ферриты, силикаты (в том числе изумруд, фенакит, циркон), ниобаты. вольфраматы и другие кристаллы.
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие
- Введение
- Глава первая. ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ИЗЛУЧЕНИЯ И ПРИНЦИП ДЕЙСТВИЯ КВАНТОВЫХ ГЕНЕРАТОРОВ
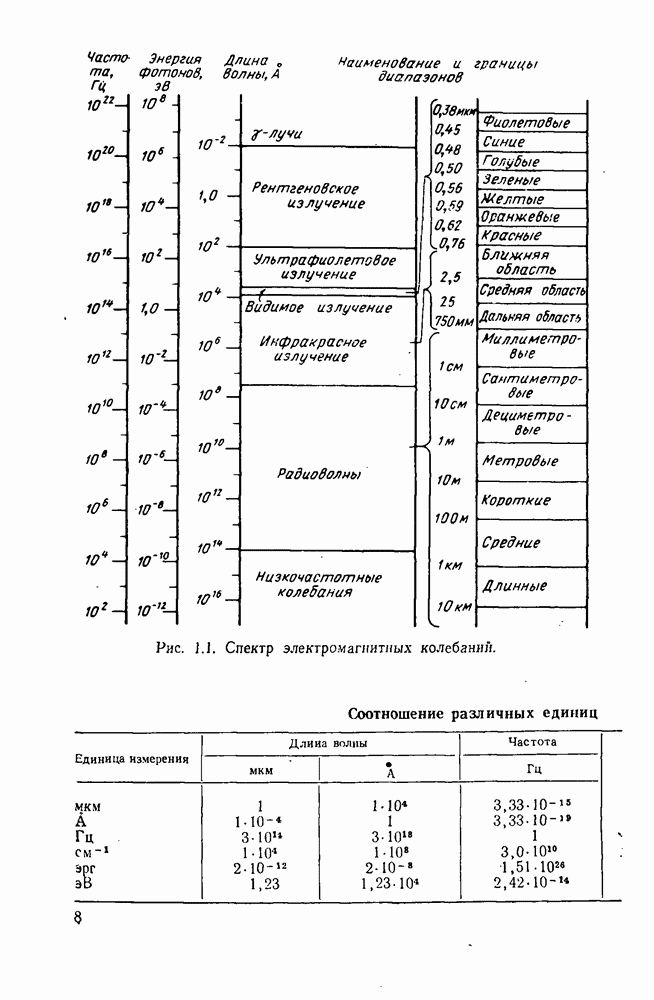
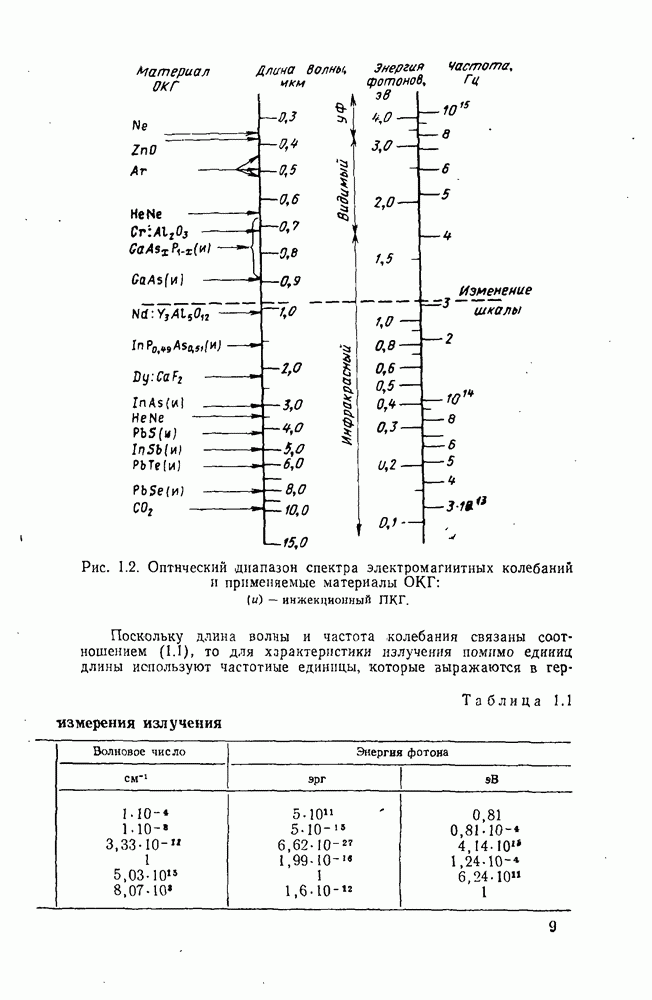
- 1.1. Спектр электромагнитных колебаний
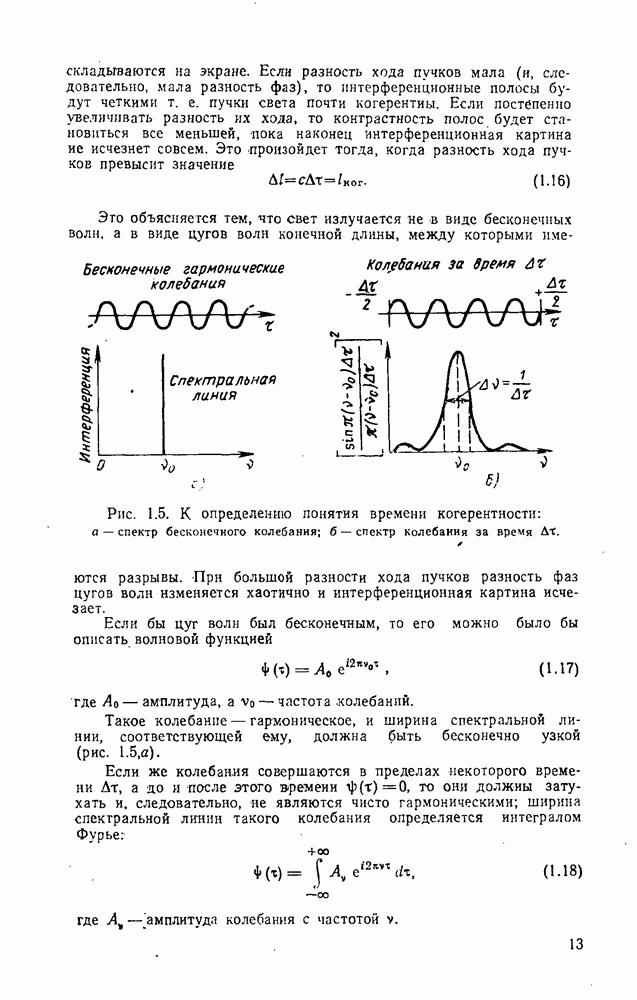
- 1.2. Когерентность
- 1.3. Направленность излучения
- 1.4. Символика энергетических уровней атомов и ионов
- 1.5. Инверсная населенность
- 1.6. Вероятности спонтанных и вынужденных переходов
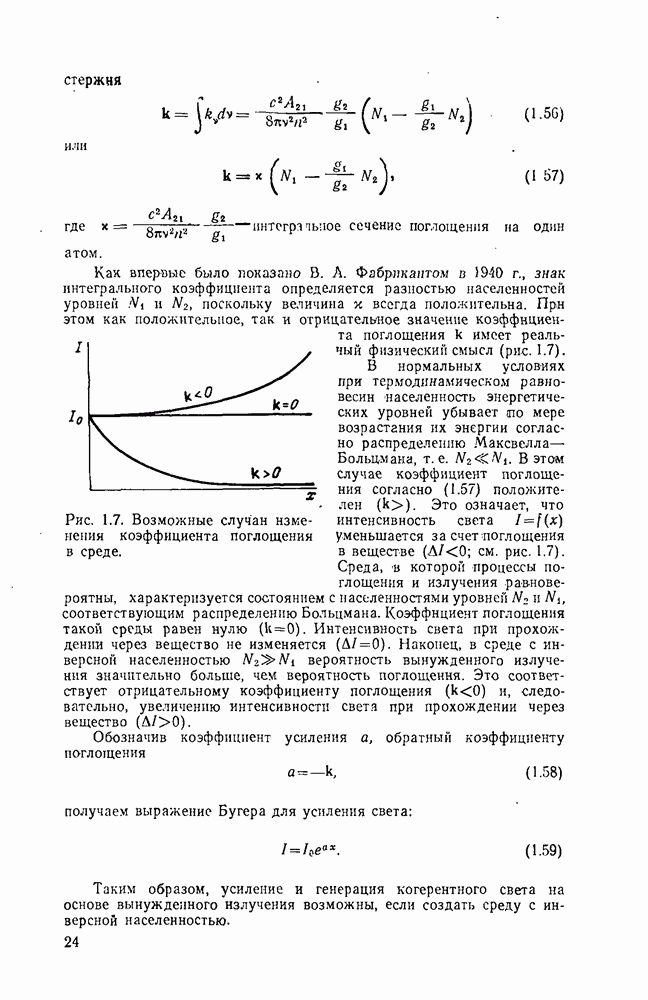
- 1.7. Усиление света при прохождении через вещество
- 1.8. Двухуровневая система
- 1.9. Трехуровневая система
- 1.10. Четырехуровневая система
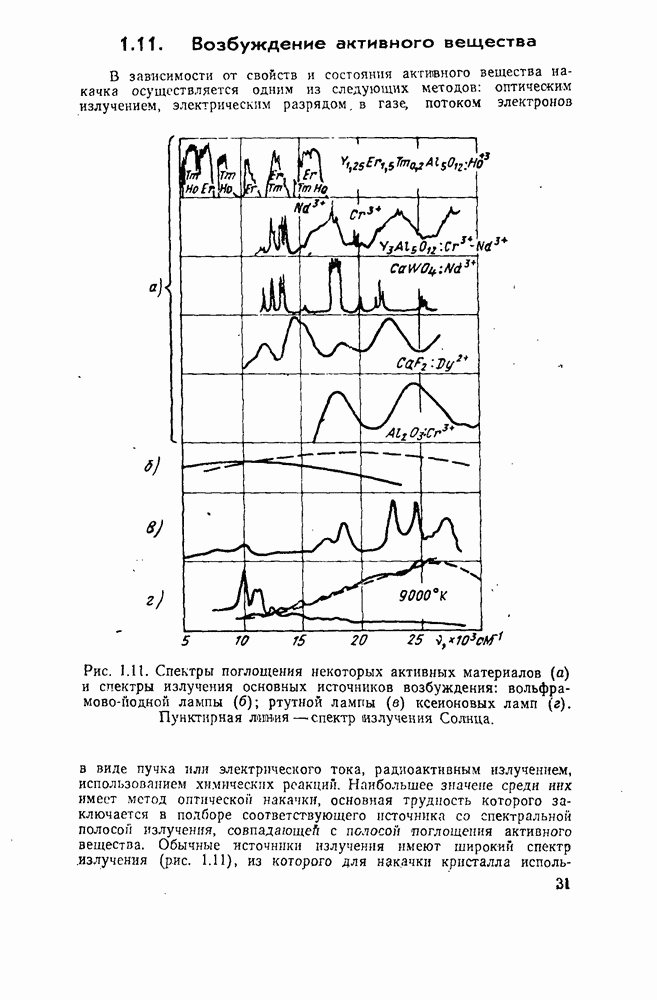
- 1.11. Возбуждение активного вещества
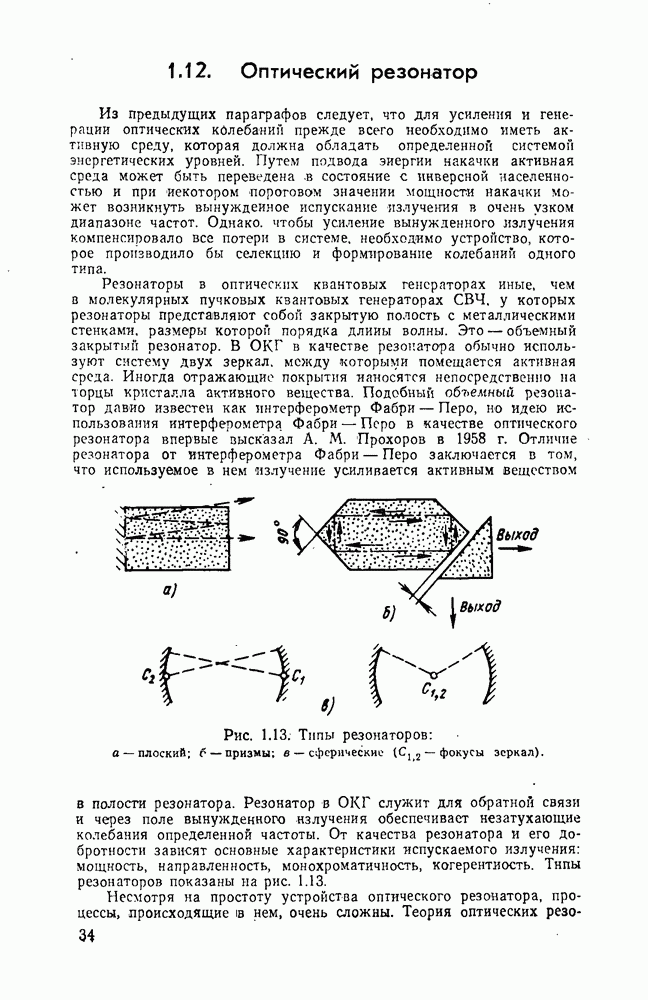
- 1.12. Оптический резонатор
- 1.13 Условие генерации
- 1.14. Потери энергии в квантовом генераторе
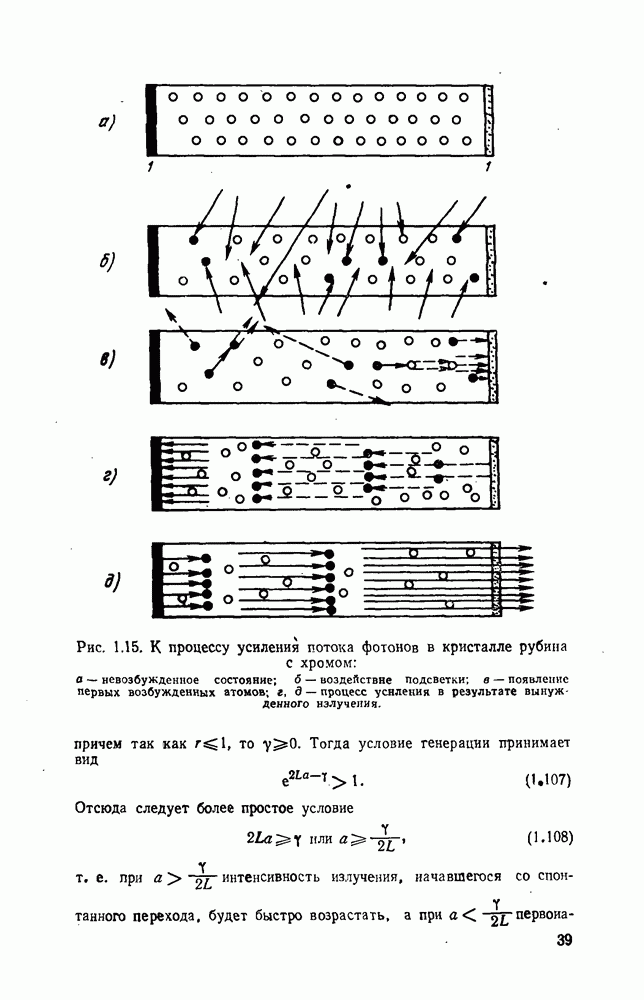
- 1.15. Устройство ОКГ на твердом теле
- Глава вторая. ОБЩИЕ ВОПРОСЫ ТЕХНОЛОГИИ МАТЕРИАЛОВ ТВЕРДОТЕЛЬНЫХ ОКГ
- 2.1. Особенности активного вещества ионных квантовых систем
- 2.2. Особенности технологии твердотельных материалов квантовых генераторов
- 2.3. Физико-химические основы кристаллизации
- 2.3.2. Гетерогенное зародышеобразование
- 2.3.3. Скорость зарождения новой фазы
- 2.3.4. Рост кристаллов
- 2.3.5. Общее кинетическое уравнение кристаллизации
- 2.3.6. Распределение примеси в процессе роста кристалла
- 2.4. Основные методы синтеза и выращивания кристаллов
- 2.4.2. Выращивание из стехиометрических расплавов
- 2.4.3. Методы выращивания кристаллов из растворов
- 2.4.4. Гидротермальный синтез и рост кристаллов
- 2.4.5. Выращивание кристаллов из газовой фазы
- 2.5. Кристалло-химическая классификация материалов твердотельных квантовых генераторов
- Глава третья. КИСЛОРОДНЫЕ СОЕДИНЕНИЯ
- 3.1. Окислы элементов III группы
- 3.1.2. Окислы редкоземельных элементов и иттрия
- 3.3.1. Гранаты
- 3.2. Материалы на основе кислородных соединений элементов VI группы
- 3.2.2. Молибдаты
- 3.3. Материалы на основе кислородных соединений элементов V группы
- 3.3.2. Ниобаты
- 3.3.3. Фосфаты
- Выращивание кристаллов фторфосфата кальция [47]
- Глава четвертая. ФТОРИСТЫЕ СОЕДИНЕНИЯ
- 4.1. Фториды элементов II группы
- 4.2. Фториды редкоземельных элементов
- 4.3. Смешанные фториды
- 4.4. Фториды элементов VII группы
- Глава пятая. СТЕКЛО
- 5.1. Особенности стекла как активного материала ОКГ
- 5.2. Общая характеристика стекол для ОКГ
- 5.3. Особенности положения атомов активатора в стекле
- 5.4. Стекло с неодимом
- Глава шестая. МАТЕРИАЛЫ ЖИДКОСТНЫХ ОКГ
- 6.2. Механизм излучения в органических растворах
- 6.3. Растворы металлоорганических соединений
- 6.4. Растворы органических красителей
- 6.5. Растворы неорганических соединений редкоземельных элементов
- Глава седьмая. ОБЩАЯ ХАРАКТЕРИСТИКА ПОЛУПРОВОДНИКОВЫХ КВАНТОВЫХ ГЕНЕРАТОРОВ (ПКГ)
- 7.2. Основные сведения из теории люминесценции инжекционных ПКГ
- 7.3. Рабочие характеристики инжекционных ПКГ
- 7.3.2. Пространственные свойства
- 7.3.3. Пороговый ток
- 7.3.4. Квантовый выход
- 7.4. Тепловые условия работы лазерного диода
- 7.4.2. Работа в квазинепрерывном режиме
- 7.5. Другие типы ПКГ
- 7.5.1. ПКГ с электронным возбуждением
- 7.5.2. ПКГ с оптической накачкой
- 7.5.3. ПКГ с прямым электрическим возбуждением
- Глава восьмая. АРСЕНИД ГАЛЛИЯ И ТЕХНОЛОГИЯ ИЗГОТОВЛЕНИЯ ДИОДОВ ПКГ
- 8.1. Физические свойства арсенида галлия
- 8.2. Методы выращивания монокристаллов арсенида галлия
- 8.3. Методы изготовления р-n-переходов
- 8.3.2. Эпитаксия из жидкой фазы
- 8.3.3. Эпитаксия из газовой фазы
- 8.4. Изготовление невыпрямляющих низкоомных контактов к арсениду галлия
- 8.5. Изготовление резонатора
- 8.6. Общая технологическая схема изготовления диодов ПКГ
- 8.7. Конструкция ПКГ
- 8.8. Гетероструктуры на основе арсенида галлия
- 8.9. Другие материалы с прямыми переходами
- Глава девятая. МАТЕРИАЛЫ ГАЗОВЫХ ОКГ
- 9.1. Особенности газового активного вещества ОКГ и методы создания инверсной населенности
- 9.2. Газоразрядные ОКГ
- 9.2.2. Ионные газоразрядные ОКГ
- 9.2.3. Молекулярные газоразрядные ОКГ
- 9.3. Газовые ОКГ с оптической накачкой
- 9.4. Химические ОКГ
- Глава десятая. МАТЕРИАЛЫ МОДУЛЯТОРОВ ОПТИЧЕСКОГО ИЗЛУЧЕНИЯ
- 10.1. Некоторые физические основы модуляции оптического излучения
- 10.2. Требования к материалам модуляторов излучения ОКГ
- 10.3. Материалы с линейным электрооптическим эффектом
- 10.3.1. Тетрагональные кристаллы типа KDP
- 10.3.2. Ромбические кристаллы
- 10.3.3. Тригональные кристаллы
- 10.3.4. Кубические кристаллы
- 10.4. Кристаллы с квадратичным электрооптическим эффектом
- Литература