| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
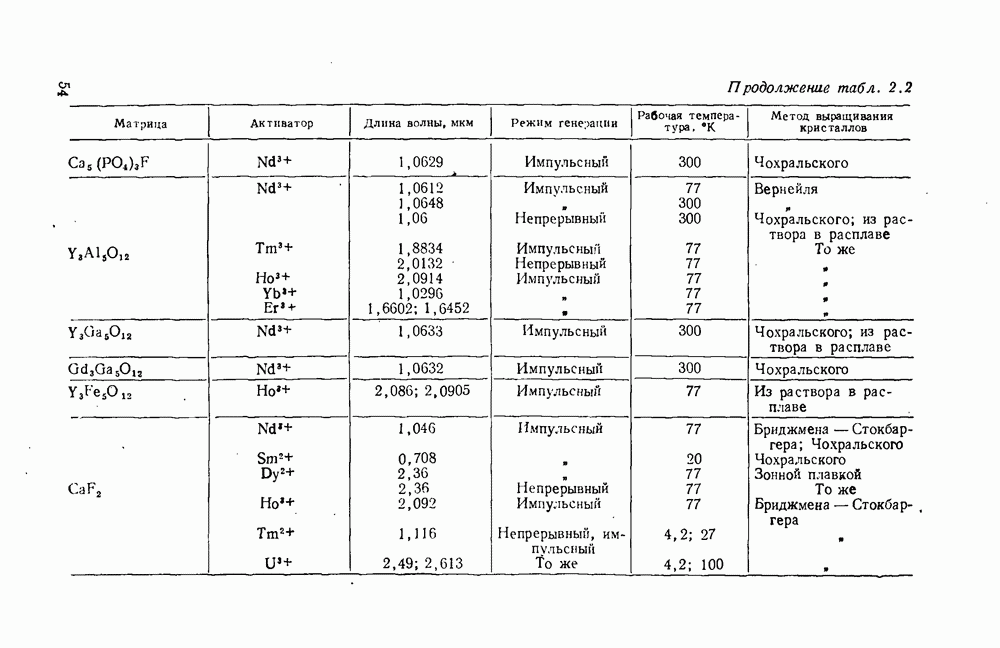
Глава четвертая. ФТОРИСТЫЕ СОЕДИНЕНИЯ
4.1. Фториды элементов II группы
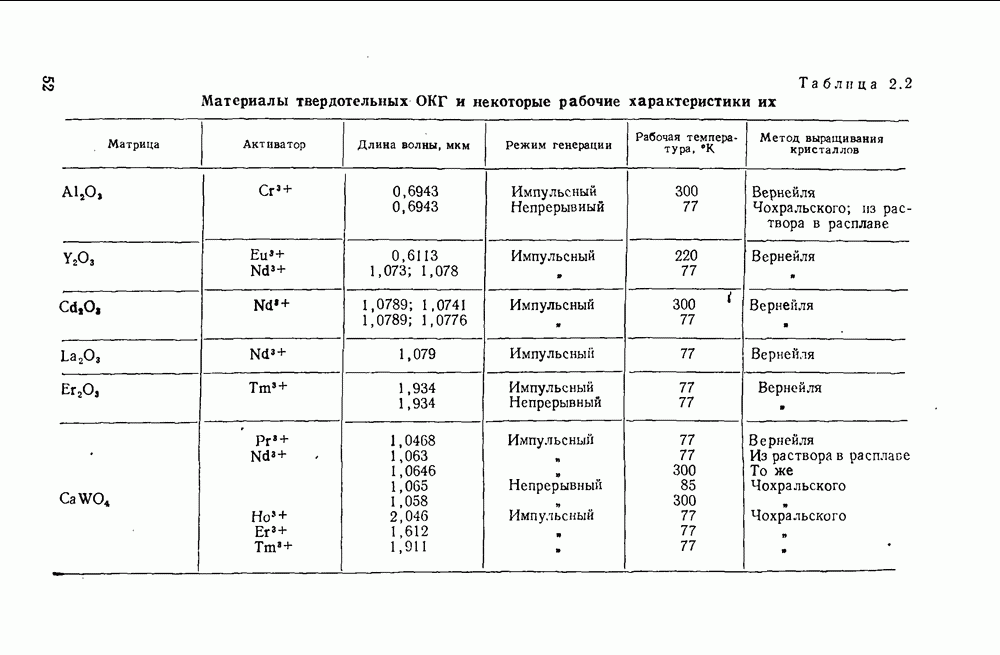
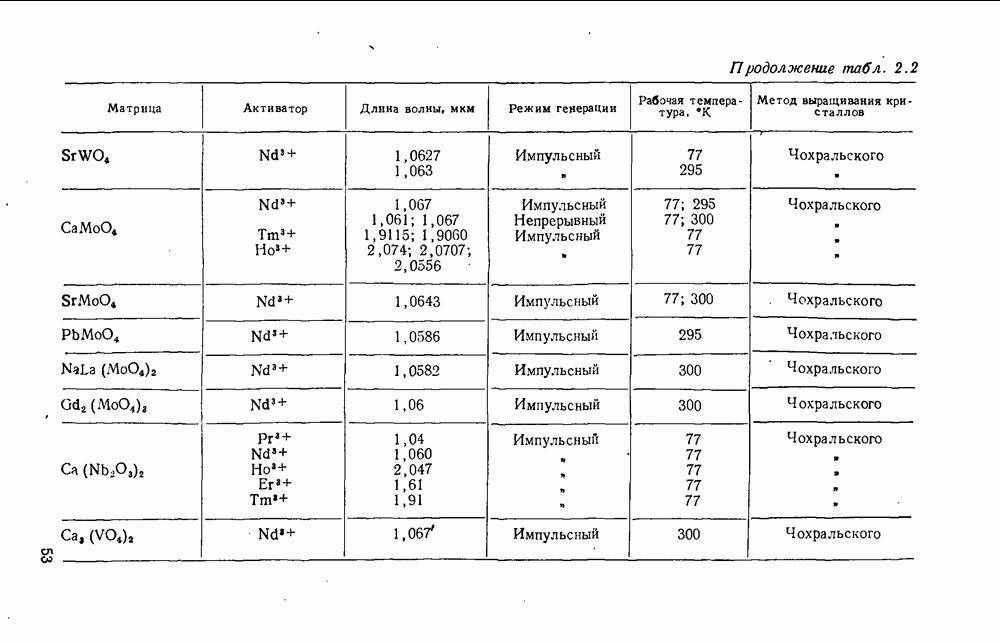
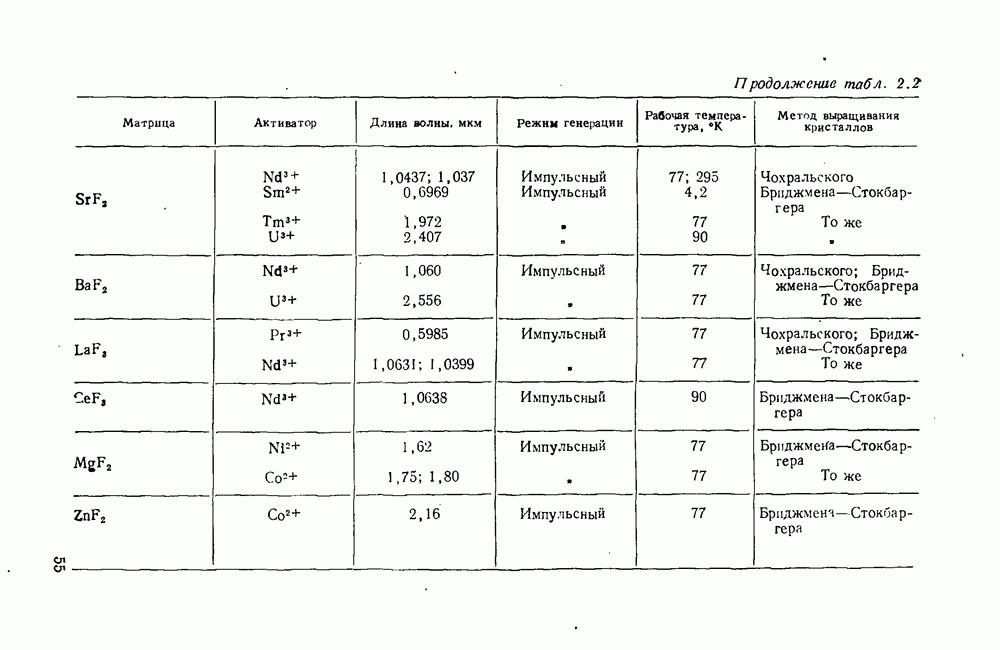
В качестве активных материалов ОКГ в настоящее время применяются следующие фторады щелочноземельных металлов:

а также фторид цинка  Эти фториды, кроме
Эти фториды, кроме  имеют кубическую структуру типа флюорита
имеют кубическую структуру типа флюорита 

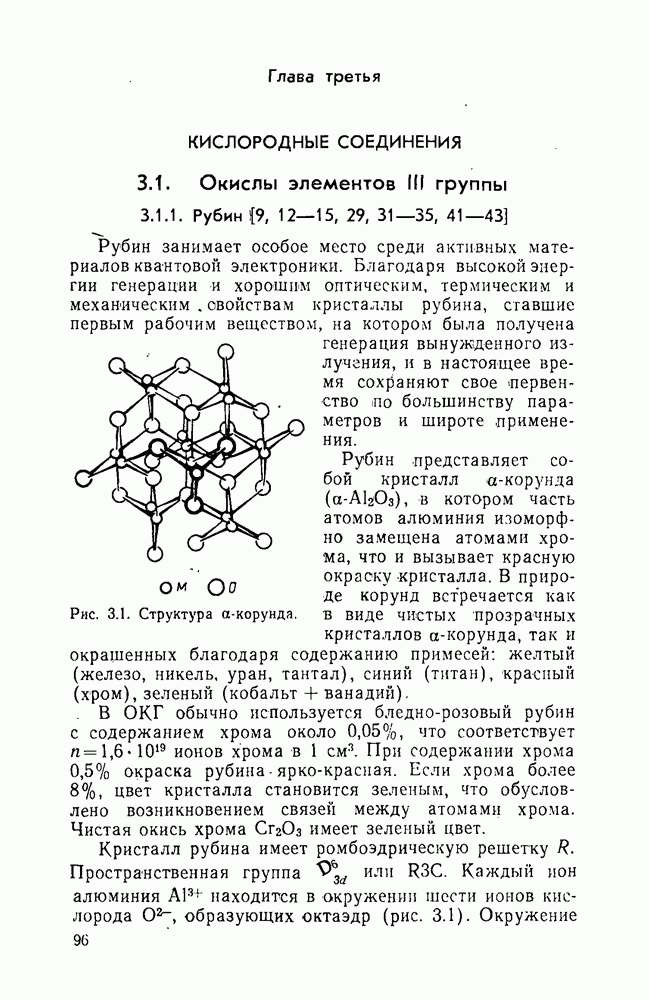
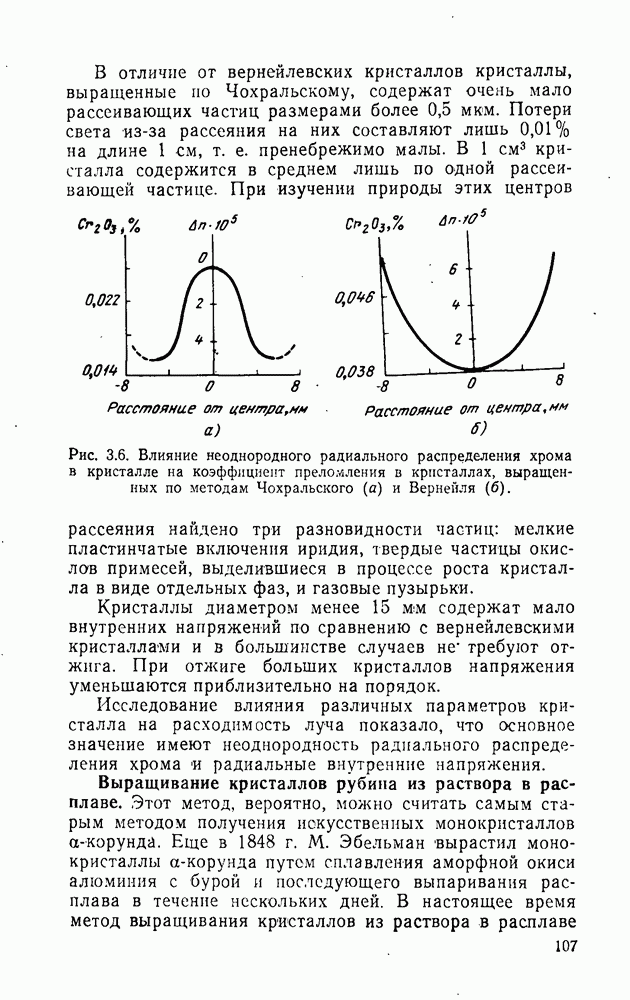
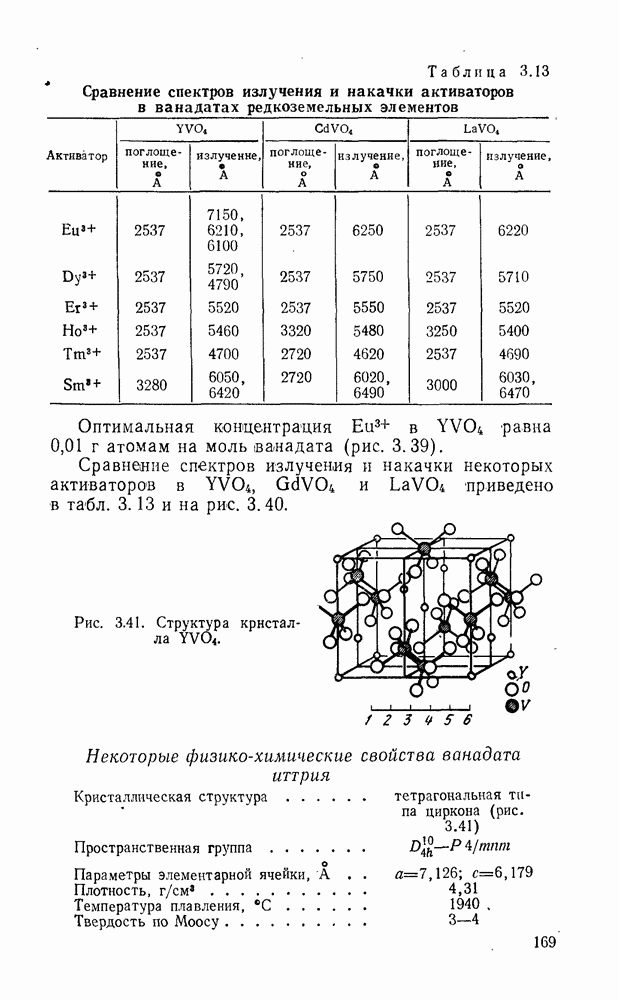
Рис. 4.1. Структура элементарной ячейки кристаллов типа флюорита.
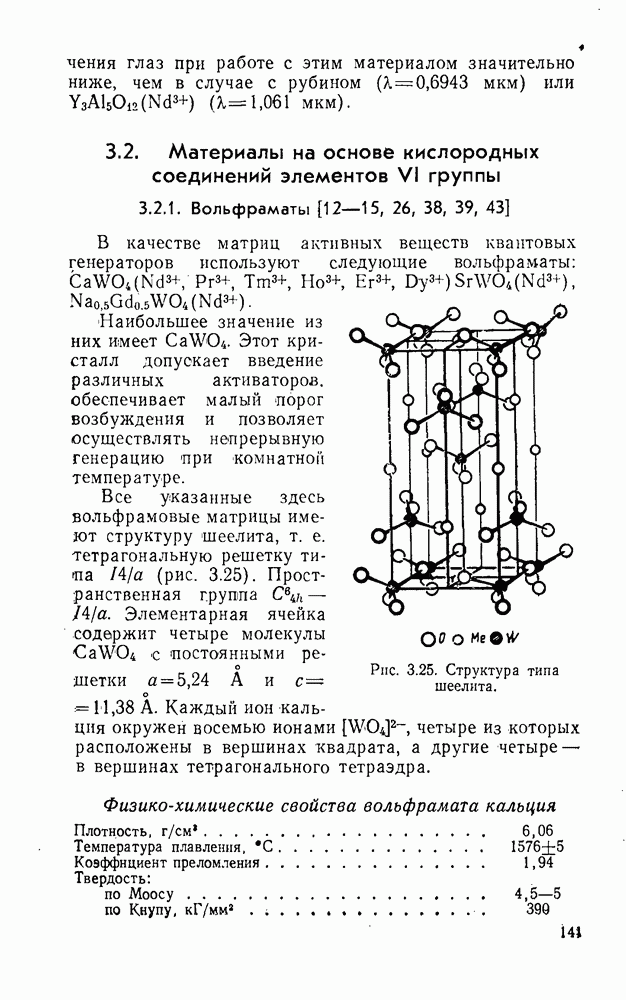
Пространственная группа  элементарная ячейка содержит четыре молекулы. Катионы координированы восемью ионами фтора, расположенными
элементарная ячейка содержит четыре молекулы. Катионы координированы восемью ионами фтора, расположенными
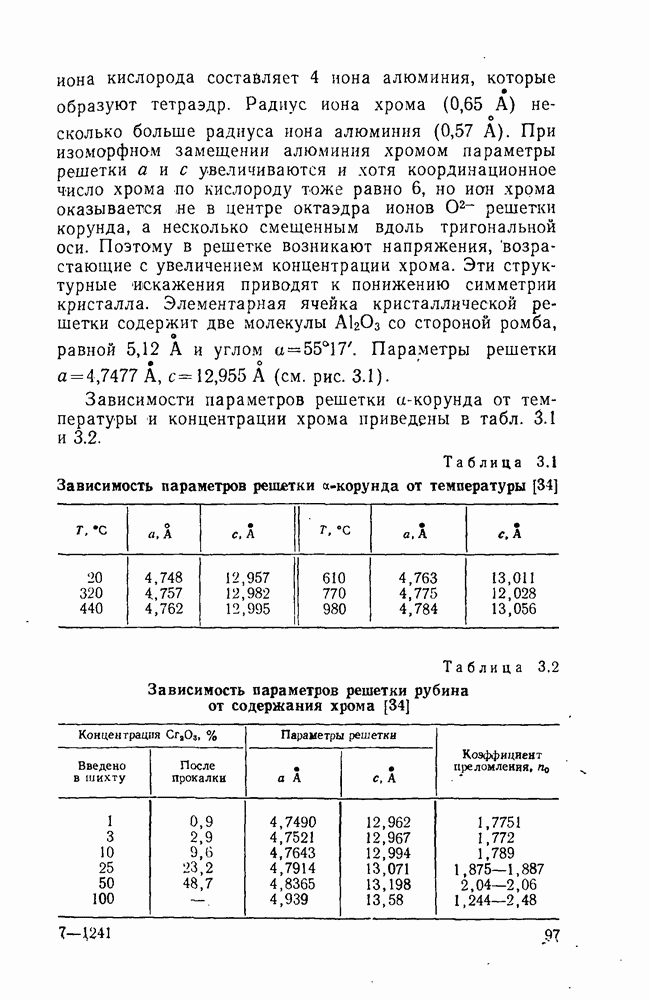
Таблица 4.1 Параметры кристаллической структуры 

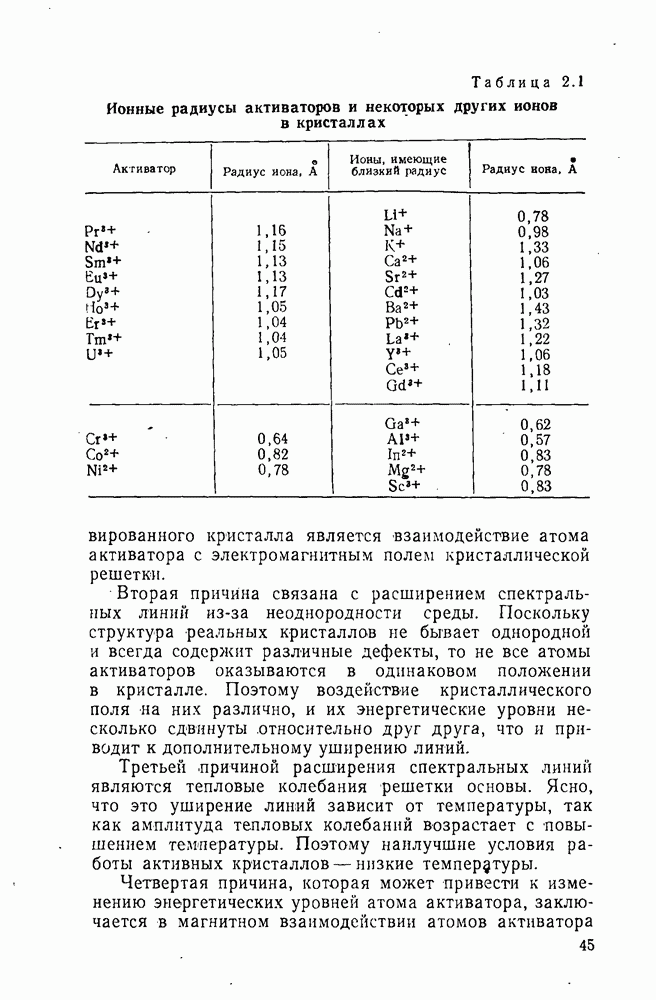
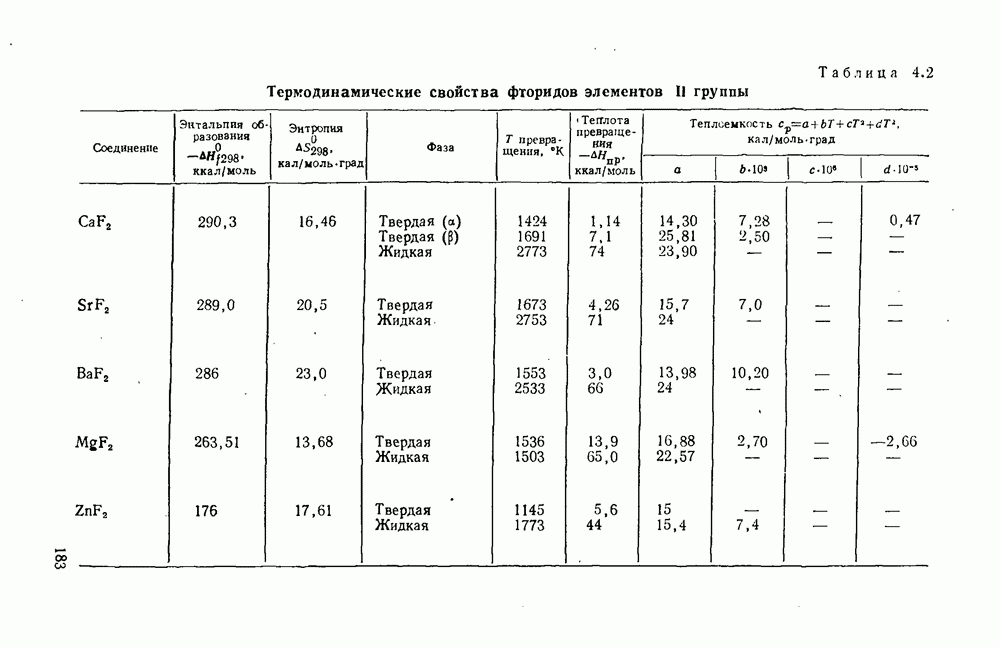
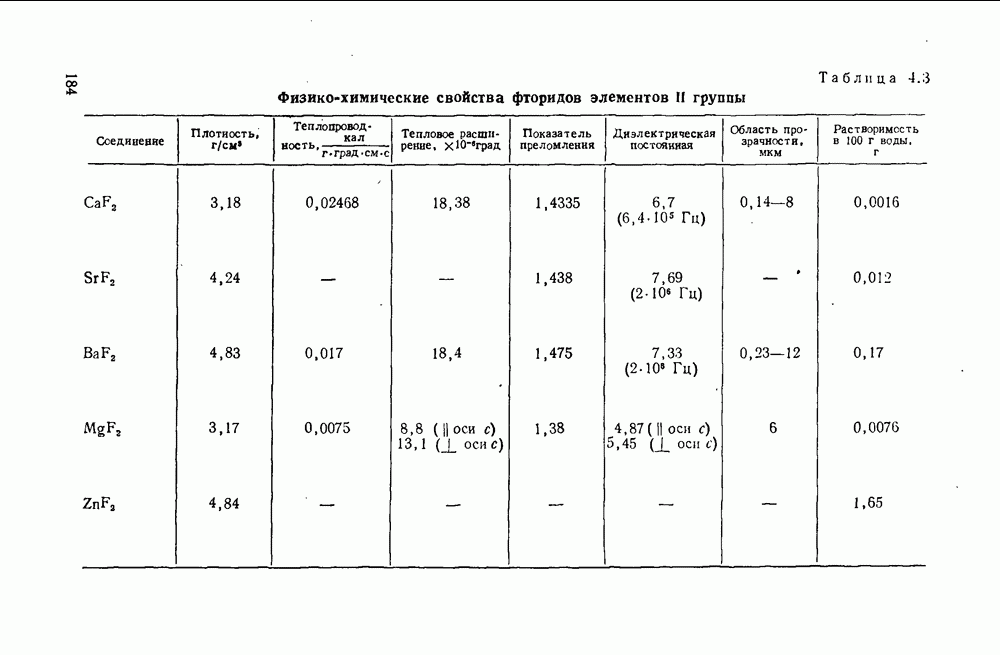
в вершинах куба; ионы фтора — четырьмя катионами, образующими тетраэдр (рис. 4. 1). Параметры кристаллической структуры и ионные радиусы этих фторидов даны в табл. 4.1, а термодинамические и физико-химические свойства — в табл. 4.2 и 4.3.
Некоторые свойства монокристаллов фтористого кальция
(см. скан)
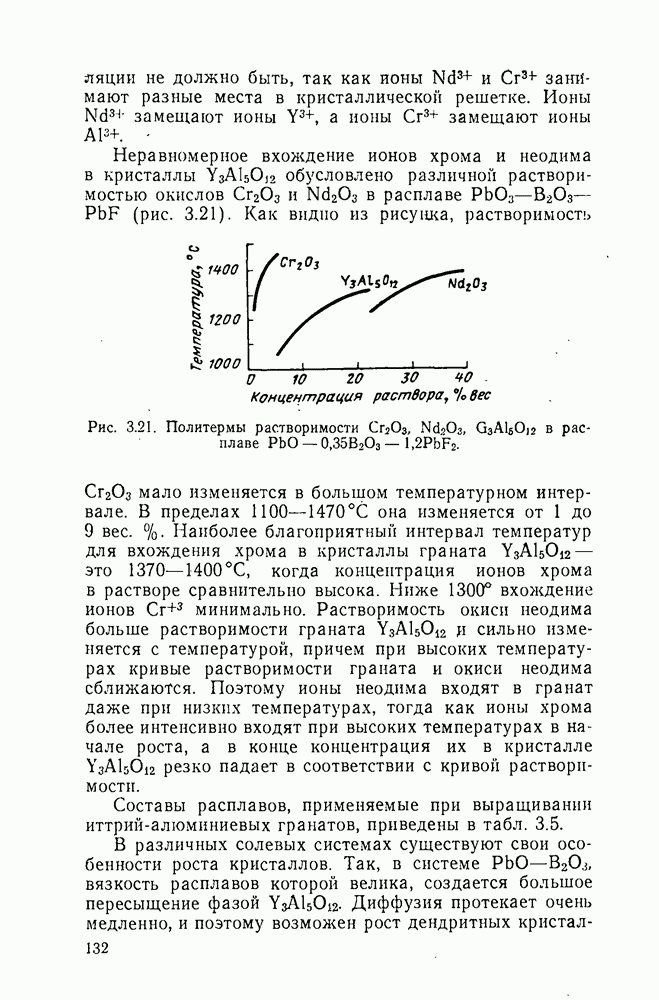
Сравнение температурных зависимостей свободных энергий образования фторидов и окислов щелочноземельных металлов показывает, что фториды кальция и магния менее устойчивы, чем окислы. Это означает, что фториды этих элементов могут взаимодействовать с кислородом и водяным паром с образованием окислов  Действительно, при высоких температурах процесс гидролиза фторида кальция заметен, но при нормальной температуре фтористый кальций очень мало растворим в воде и кислотах. Горячая концентрированная серная кислота разлагает фторид кальция с образованием плавиковой кислоты.
Действительно, при высоких температурах процесс гидролиза фторида кальция заметен, но при нормальной температуре фтористый кальций очень мало растворим в воде и кислотах. Горячая концентрированная серная кислота разлагает фторид кальция с образованием плавиковой кислоты.
Фтористый кальций встречается в природе в виде плавикового шпата — флюорита, как прозрачного, так и окрашенного. Окраска объясняется наличием примесей: зеленоватая — присутствием ионов  красноватая — ионов
красноватая — ионов 
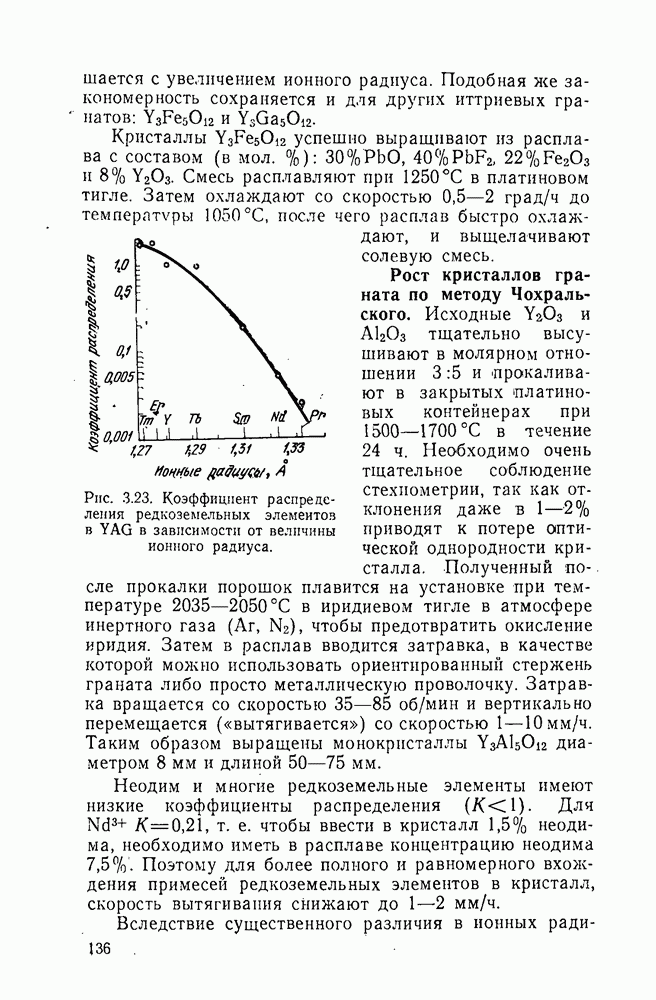
Ионы редкоземельных элементов легко входят в решетку фтористого кальция благодаря хорошему совпадению значений ионных радиусов. Ионный радиус  равен 1,04 А, а ионные радиусы редкоземельных элементов от
равен 1,04 А, а ионные радиусы редкоземельных элементов от  до
до  составляют
составляют 

(кликните для просмотра скана)

(кликните для просмотра скана)
(см. табл. 2.1). Наилучшее совпадение у неодима, ионный радиус которого равен 1,04 А. Кроме того, лишний ион фтора  образующийся при легировании флюорита фторидом трехваленгного элемента, свободно встраивается в октаэдрические междоузлия флюоритовой структуры, не вызывая при этом больших искажений решетки.
образующийся при легировании флюорита фторидом трехваленгного элемента, свободно встраивается в октаэдрические междоузлия флюоритовой структуры, не вызывая при этом больших искажений решетки.
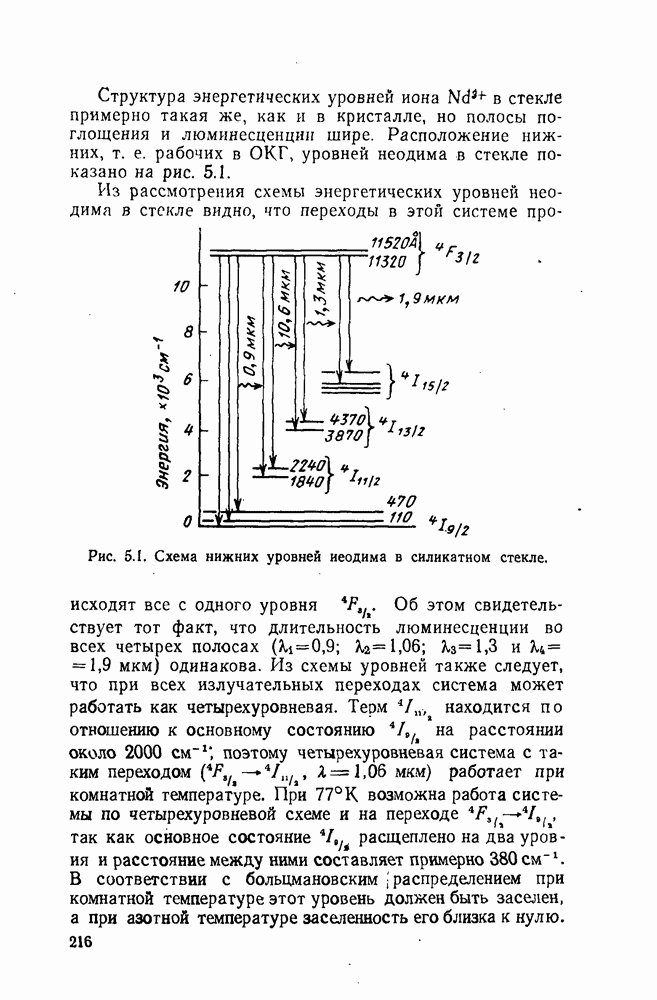
 Исторически вторым осуществленным лазером после рубинового был лазер на кристалле флюорита с ураном. Буквально через несколько месяцев после удачного опыта Меймана, впервые получившего генерацию на
Исторически вторым осуществленным лазером после рубинового был лазер на кристалле флюорита с ураном. Буквально через несколько месяцев после удачного опыта Меймана, впервые получившего генерацию на  т. е. в трехуровневой системе, в том же 1960 г. П. Сорокин и М. Стивенсон получили вынужденное излучение на кристалле
т. е. в трехуровневой системе, в том же 1960 г. П. Сорокин и М. Стивенсон получили вынужденное излучение на кристалле  и впервые показали существенные преимущества четырехуровневой системы. Они использовали кристаллы с содержанием урана 0,05 мол.
и впервые показали существенные преимущества четырехуровневой системы. Они использовали кристаллы с содержанием урана 0,05 мол.  Было получено излучение с длиной волны 2,51 мкм при температуре жидкого гелия. Впоследствии было получено излучение в этих кристаллах и при комнатной температуре. Вынужденное излучение ионов
Было получено излучение с длиной волны 2,51 мкм при температуре жидкого гелия. Впоследствии было получено излучение в этих кристаллах и при комнатной температуре. Вынужденное излучение ионов  было получено также и в кристаллах
было получено также и в кристаллах  .
.
В атомах актиноидных элементов идет достраивание  -оболочки О-слоя. Эта незаполненная оболочка экранируется от внешних электрических полей (например, решетки матричного кристалла) оболочками
-оболочки О-слоя. Эта незаполненная оболочка экранируется от внешних электрических полей (например, решетки матричного кристалла) оболочками  но их экранирующее действие невелико и положение энергетических уровней ионов
но их экранирующее действие невелико и положение энергетических уровней ионов  в кристаллической решетке значительно смещено по сравнению со свободными ионами урана.
в кристаллической решетке значительно смещено по сравнению со свободными ионами урана.
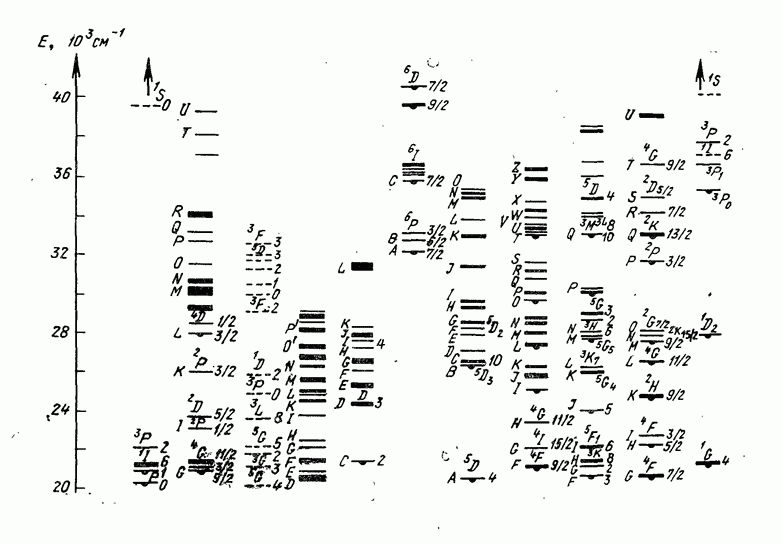
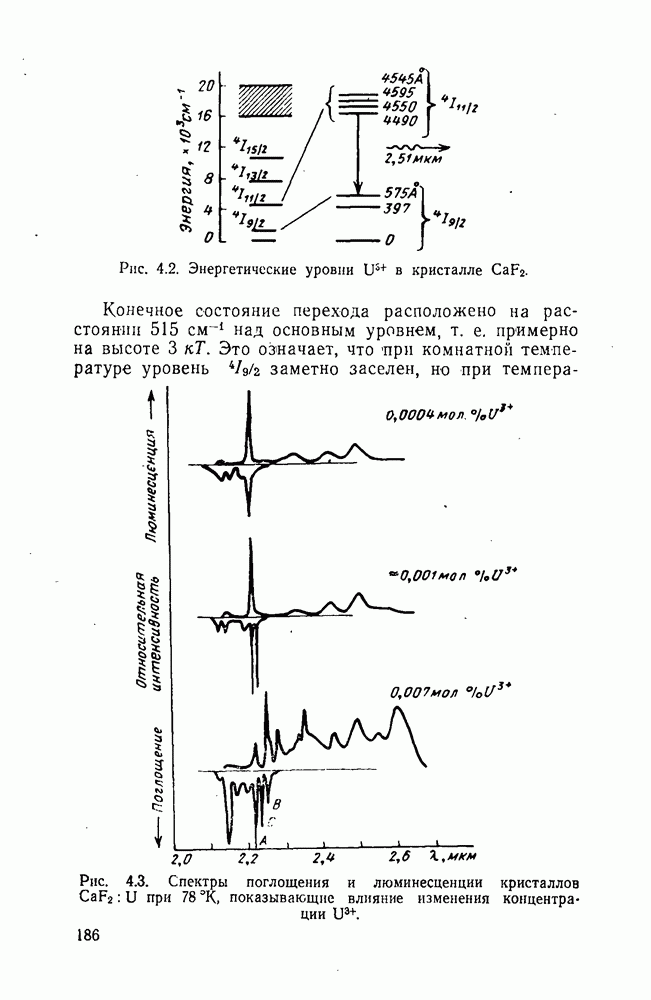
Диаграмма энергетических уровней  во фтористом кальции приведена на рис. 4.2. Наиболее сильные полосы поглощения находятся в видимой и ультрафиолетовой областях спектра
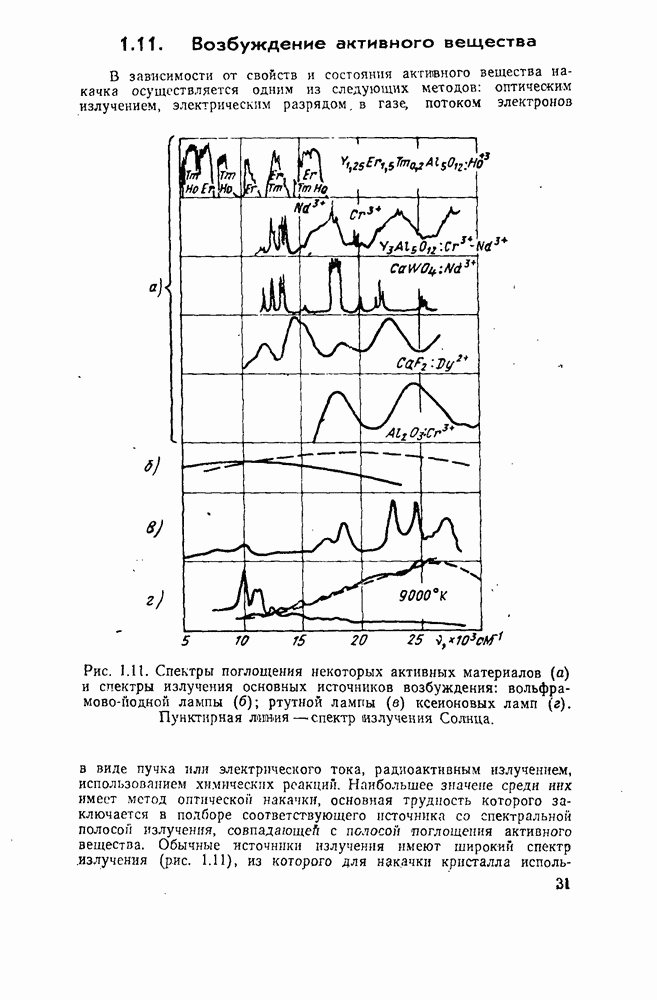
во фтористом кальции приведена на рис. 4.2. Наиболее сильные полосы поглощения находятся в видимой и ультрафиолетовой областях спектра  , ширина полосы — около 1 000 А), а также несколько полос в ближней инфракрасной области (0,84; 0,89; 1,23 мкм). Следовательно, наиболее удобным для возбуждения системы источником накачки является ксеноновая лампа-вспышка. Спектр излучения в зависимости от концентрации урана может находиться в пределах
, ширина полосы — около 1 000 А), а также несколько полос в ближней инфракрасной области (0,84; 0,89; 1,23 мкм). Следовательно, наиболее удобным для возбуждения системы источником накачки является ксеноновая лампа-вспышка. Спектр излучения в зависимости от концентрации урана может находиться в пределах  мкм (рис. 4.3). При концентрации 0,05 мол.
мкм (рис. 4.3). При концентрации 0,05 мол.  излучение происходит на волне
излучение происходит на волне  мкм, что соответствует переходу
мкм, что соответствует переходу 

Рис. 4.2. Энергетические уровни  в кристалле
в кристалле 
Конечное состояние перехода расположено на расстоянии  над основным уровнем, т. е. примерно на высоте
над основным уровнем, т. е. примерно на высоте  Это означает, что при комнатной температуре уровень
Это означает, что при комнатной температуре уровень  заметно заселен, но при температуре
заметно заселен, но при температуре
Рис. 4.3. (см. скан) Спектры поглощения и люминесценции кристаллов  при
при  показывающие влияние изменения концентрации
показывающие влияние изменения концентрации 
жидкого азота  он практически свободен, и генерация происходит по четырехуровневой схеме. С повышением температуры уменьшается время жизни метастабпльного состояния с
он практически свободен, и генерация происходит по четырехуровневой схеме. С повышением температуры уменьшается время жизни метастабпльного состояния с  с при
с при  до
до  с при
с при  Сокращение времени жизни метастабильного состояния в 10 раз приводит к повышению пороговой энергии накачки с 3,28 Дж
Сокращение времени жизни метастабильного состояния в 10 раз приводит к повышению пороговой энергии накачки с 3,28 Дж  до 1200 Дж
до 1200 Дж 
При более высоких концентрациях урана (0,1%) кристалл флюорита генерирует одновременно на длинах волн 2,51 и 2,61 мкм, причем пороговая энергия возбуждения генерации для 2,61 мкм в несколько раз ниже. Это происходит потому, что при высоких концентрациях активатора повышается населенность более высоких подуровней метастабильного состояния. Так как пороговая энергия накачки для линии 2,61 мкм при  составляет единицы джоулей, то при этой температуре на длине волны 2,61 мкм получена непрерывная генерация. Выходная мощность излучения составила
составляет единицы джоулей, то при этой температуре на длине волны 2,61 мкм получена непрерывная генерация. Выходная мощность излучения составила  при мощности накачки 700 Вт. Минимальная пороговая мощность накачки 250 Вт.
при мощности накачки 700 Вт. Минимальная пороговая мощность накачки 250 Вт.
 Из трехвалентных ионов редкоземельных элементов в качестве активаторов в решетках типа флюорита успешно применяют
Из трехвалентных ионов редкоземельных элементов в качестве активаторов в решетках типа флюорита успешно применяют  При этом энергетические уровни, например
При этом энергетические уровни, например  аналогичны энергетическим уровням
аналогичны энергетическим уровням  Как указывалось, вхождение этих ионов в решетку флюорита происходит легко, и достигается практически равномерное распределение примеси (коэффициент распределения близок к единице).
Как указывалось, вхождение этих ионов в решетку флюорита происходит легко, и достигается практически равномерное распределение примеси (коэффициент распределения близок к единице).
Введение трехвалентных ионов Ln3+ в решетку флюорита вместо двухвалентных ионов кальция связано с необходимостью компенсации заряда в кристалле. Эта компенсация может быть выполнена одним из трех способов:
1) один ион Ln3+ замещает один ион Са2+, а в соседнюю ячейку кубической решетки вводится дополнительный ион 
2) один ион Ln3+ замещает один ион Са2+, а второй ион Са2+ замещается ионом какого-либо одновалентного металла 
3) два иона Ln3+ замещают три иона Са2+.
Однако все эти способы приводят к искажению симметрии структуры и появлению дополнительных центров
окраски и люминесценции. В кристаллической решетке флюорита возможны несколько типов оптических центров Ln3+, различающихся структурой. Это обусловлено многообразием элементарных точечных дефектов в кристаллах решетки и существованием у дефектов эффективных электрических зарядов. Различные комбинации дефектов с ионами Ln3+ и обусловливают наблюдающееся на практике многообразие.оптических центров.

Рис. 4.4. Структуры оптических центров Ln3+ в кристаллах: а — кубический центр; б — тетрагональный; в — тригональный; г — ромбический.
Структуры некоторых центров  в кристаллах типа флюорита показаны на рис. 4.4. Возможности образования центров различной структуры обусловливает сильная изменчивость оптических свойств кристаллов флюорита с Ln3+ при небольших изменениях процессов синтеза и выращивания кристаллов или концентрации активатора
в кристаллах типа флюорита показаны на рис. 4.4. Возможности образования центров различной структуры обусловливает сильная изменчивость оптических свойств кристаллов флюорита с Ln3+ при небольших изменениях процессов синтеза и выращивания кристаллов или концентрации активатора  других примесей. К этим другим примесям относятся анионные примеси типа кислорода. Влияние кислорода на спектры люминесценции очень заметно: изменяется не только положение, но и число линий. Кислород легко входит в решетку флюорита, изоморфно замещая ион фтора, так как ионные радиусы их близки
других примесей. К этим другим примесям относятся анионные примеси типа кислорода. Влияние кислорода на спектры люминесценции очень заметно: изменяется не только положение, но и число линий. Кислород легко входит в решетку флюорита, изоморфно замещая ион фтора, так как ионные радиусы их близки  . При этом появляется новая ось симметрии. Такие центры участвуют в генерации.
. При этом появляется новая ось симметрии. Такие центры участвуют в генерации.
Оптические спектры кристаллов флюорита с Ln3+ сильно изменяются при добавлении другого  Например, если при выращивании кристалла
Например, если при выращивании кристалла  добавлено 1—2 вес.
добавлено 1—2 вес.  то в полученном кристалле наблюдается появление новых типов центров, способных к генерации. Во-первых, образуются центры, в состав которых входят ионы
то в полученном кристалле наблюдается появление новых типов центров, способных к генерации. Во-первых, образуются центры, в состав которых входят ионы  и во-вторых, вследствие добавки
и во-вторых, вследствие добавки  равновесие центров Nd3+ смещается в сторону их ассоциации.
равновесие центров Nd3+ смещается в сторону их ассоциации.
На оптические свойства кристаллов флюорита сильное влияние оказывает облучение жестким рентгеновским или излучением. При этом ионы Ln3+ частично восстанавливаются в  электромагнитное поле решетки изменяется; это обусловливает перестройку структур оптических центров оставшихся ионов
электромагнитное поле решетки изменяется; это обусловливает перестройку структур оптических центров оставшихся ионов  Как правило, сложные центры (например, ромбические) исчезают. Однако после отжига этих кристаллов при
Как правило, сложные центры (например, ромбические) исчезают. Однако после отжига этих кристаллов при  первоначальные спектры их полностью восстанавливаются.
первоначальные спектры их полностью восстанавливаются.
 При введении в решетку флюорита двухвалентных ионов
При введении в решетку флюорита двухвалентных ионов  (например,
(например,  дело обстоит проще, так как в этом случае проблема компенсации заряда отпадает. Кстати, после рубина и флюорита с ураном система
дело обстоит проще, так как в этом случае проблема компенсации заряда отпадает. Кстати, после рубина и флюорита с ураном система  была третьим по счету веществом, на котором было получено вынужденное излучение. Спектральные свойства двухвалентных ионов редкоземельных элементов отличаются существенными особенностями по сравнению со свойствами ионов
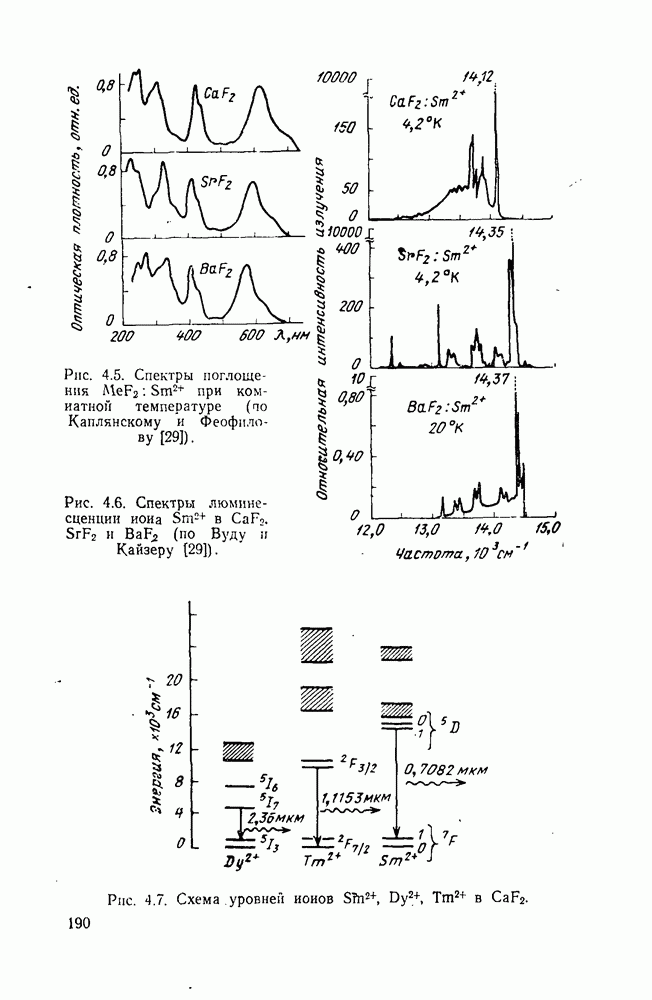
была третьим по счету веществом, на котором было получено вынужденное излучение. Спектральные свойства двухвалентных ионов редкоземельных элементов отличаются существенными особенностями по сравнению со свойствами ионов  Прежде всего, эти особенности касаются спектров поглощения. Двухвалентные ионы редкоземельных элементов обладают широкими и интенсивными полюсами поглощения в видимой и ближней инфракрасной области спектра, что очень удобно для оптической накачки (рис. 4.5). Если коэффициенты поглощения ионов Ln3+ при рабочих концентрациях
Прежде всего, эти особенности касаются спектров поглощения. Двухвалентные ионы редкоземельных элементов обладают широкими и интенсивными полюсами поглощения в видимой и ближней инфракрасной области спектра, что очень удобно для оптической накачки (рис. 4.5). Если коэффициенты поглощения ионов Ln3+ при рабочих концентрациях  составляют
составляют  то для большинства
то для большинства  они достигают
они достигают  . С другой стороны, спектры люминесценции ионов
. С другой стороны, спектры люминесценции ионов  наблюдаемые при низких температурах, состоят из узких и отчетливо разделенных линий, на которые почти не влияет кристаллическая структура матрицы (рис. 4. 6).
наблюдаемые при низких температурах, состоят из узких и отчетливо разделенных линий, на которые почти не влияет кристаллическая структура матрицы (рис. 4. 6).
Эти особенности объясняются тем, что поглощение сопровождается переходом с уровней  на
на  а люминесценция при переходах
а люминесценция при переходах  как и трехвалентных ионов, т. е. между уровнями внутренней оболочки
как и трехвалентных ионов, т. е. между уровнями внутренней оболочки  хорошо защищенной от внешних влияний оболочками
хорошо защищенной от внешних влияний оболочками  Схемы энергетических уровней ионов
Схемы энергетических уровней ионов  показаны на рис. 4. 7.
показаны на рис. 4. 7.
Поскольку ионы  легко замещают ионы Са2+ в решетке флюорита без каких-либо искажений симметрии и без необходимости компенсации заряда, то никаких новых центров окраски при этом не возникает, и спектр таких кристаллов значительно более стабилен,
легко замещают ионы Са2+ в решетке флюорита без каких-либо искажений симметрии и без необходимости компенсации заряда, то никаких новых центров окраски при этом не возникает, и спектр таких кристаллов значительно более стабилен,

(кликните для просмотра скана)
чем кристаллов с ионами Ln3+, и почти не зависит от условий выращивания, концентрации примесей и других технологических изменений. Однако при попадании в решетку примеси кислорода в больших концентрациях в спектре поглощения, например  появляются полосы, обусловленные новыми оптическими центрами и возникающие в связи с образованием вакансий фтора и замещением их кислородом.
появляются полосы, обусловленные новыми оптическими центрами и возникающие в связи с образованием вакансий фтора и замещением их кислородом.
Вынужденное излучение ионов  возникает на длине волны 0,7082 мкм при переходе между состояниями
возникает на длине волны 0,7082 мкм при переходе между состояниями  причем конечный уровень
причем конечный уровень  расположен на расстоянии
расположен на расстоянии  над основным уровнем
над основным уровнем  Ширина линии люминесценции составляет
Ширина линии люминесценции составляет  (при
(при  ) и
) и  (при
(при  ). Время жизни метастабильного уровня
). Время жизни метастабильного уровня  при
при  равно
равно  , квантовый выход люминесценции равен 0,2. Наиболее интенсивная полоса поглощения находится между 0,6 и 0,06 мкм
, квантовый выход люминесценции равен 0,2. Наиболее интенсивная полоса поглощения находится между 0,6 и 0,06 мкм
Большой интерес представляют ОКГ на  Этот кристалл имеет низкий пороговый уровень накачки (1 Дж при 77 °К и 0,1 Дж при 4,2 °К) и излучение его характеризуется очень малой шириной линии люминесценции:
Этот кристалл имеет низкий пороговый уровень накачки (1 Дж при 77 °К и 0,1 Дж при 4,2 °К) и излучение его характеризуется очень малой шириной линии люминесценции:  при
при  при
при  Это позволяет получить генерацию на одном продольном типе колебаний (нулевой моды) и перестройку частоты излучения с помощью магнитного поля (эффект Зеемана). Излучение происходит на длине волны 2,36 мкм при переходе 517—518. Время жизни состояния
Это позволяет получить генерацию на одном продольном типе колебаний (нулевой моды) и перестройку частоты излучения с помощью магнитного поля (эффект Зеемана). Излучение происходит на длине волны 2,36 мкм при переходе 517—518. Время жизни состояния  зависит от концентрации
зависит от концентрации  и изменяется от
и изменяется от  при низких концентрациях до
при низких концентрациях до  при содержании в кристалле
при содержании в кристалле
0,2% диспрозия. От температуры время жизни не зависит. Конечный уровень перехода 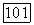 находится на расстоянии
находится на расстоянии 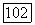 над основным уровнем. В непрерывном режиме генерации пороговая мощность возбуждения составляет при температуре
над основным уровнем. В непрерывном режиме генерации пороговая мощность возбуждения составляет при температуре 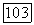 менее
менее 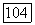 что является очень низкой величиной для твердотельных ОКГ. При накачке мощностью
что является очень низкой величиной для твердотельных ОКГ. При накачке мощностью 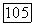 от вольфрамовой лампы получена выходная мощность 1,2 Вт.
от вольфрамовой лампы получена выходная мощность 1,2 Вт.
Выращивание монокристаллов флюорита производится только из стехиометрических расплавов. Обычно используют три метода: метод Стокбаргера, метод Чохральского и метод зонной плавки. Для получения кристаллов высокого оптического совершенства большое значение имеет качество исходных материалов, так как
наличие в них посторонних примесей (особенно кислорода, воды) приводит к снижению качества монокристалла. Раньше за исходный материал брали природный флюорит, но и он требовал очистки от кислорода и влаги. В настоящее время применяют в основном синтетический флюорит. Исходный материал для выращивания кристаллов приготавливают одним из следующих способов.
1. Осаждение фторида кальция из водного раствора какой-либо соли кальция, например, по реакции

Исходные реактивы должны быть особой чистоты. Недостатком этого метода является образование студенистого осадка фтористого кальция, который содержит много воды, окислов и оксифторидов. Поэтому для получения сухого бескислородного продукта этот осадок необходимо выдержать при 800 °С в потоке безводного фтористого водорода в течение 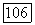
2. Фторирование некоторых соединений кальция (хлорида, окиси), безводным фтористым водородом в тех же условиях 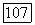
3. Фторирование окиси кальция в расплаве фтористым свинцом по реакции замещения

Этот способ применяется также для очистки исходного фтористого кальция от содержащейся в нем окиси. Исходный продукт смешивают с 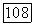 взятым в избытке. Смесь нагревают до 1400 °С в вакууме
взятым в избытке. Смесь нагревают до 1400 °С в вакууме 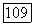 до полной отгонки
до полной отгонки 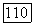 и остаточного
и остаточного 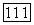 Такую реакцию применяют также и для создания фторирующей атмосферы в процессе выращивания кристаллов флюорита. В расплав добавляют около
Такую реакцию применяют также и для создания фторирующей атмосферы в процессе выращивания кристаллов флюорита. В расплав добавляют около 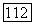 для предотвращения образования окиси кальция и вообще попадания кислорода в растущий кристалл.
для предотвращения образования окиси кальция и вообще попадания кислорода в растущий кристалл.
Вообще к атмосфере, в которой должна производиться плавка фторида кальция, предъявляются очень жесткие требования, и она должна быть строго контролируемой. Для этой цели применяют инертные газы (аргон или гелий), очищенные от кислорода пропусканием над медным катализатороми от влаги — пропусканием через молекулярные сита и вымораживающие ловушки.
К инертному газу для создания восстановительной среды добавляют водород. Однако чаще используют активные фторирующие среды. Практика показала, что использование активных фторирующих сред значительно повышает выход качественных монокристаллов флюорита.
В качестве фторирующей среды чаще всего используют безводный фтористый водород. Из других фторирующих агентов используют упомянутый выше фтористый свинец, который добавляют в расплав, и тетрафторэтилен 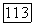 — тефлон, который в результате пиролиза при высоких температурах плавки образует активные газообразные фторирующие агенты. При этом окислы, содержащиеся в расплаве, будут фторироваться согласно суммарной реакции
— тефлон, который в результате пиролиза при высоких температурах плавки образует активные газообразные фторирующие агенты. При этом окислы, содержащиеся в расплаве, будут фторироваться согласно суммарной реакции

Чистоту атмосферы можно контролировать по цвету расплава. В расплав флюорита вводят небольшое количество (менее 0,05 ат. %) ионов 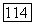 Если самарий остается в расплаве в двухвалентном состоянии, то расплав окрашен в интенсивно зеленый цвет. При наличии окислителей ионы
Если самарий остается в расплаве в двухвалентном состоянии, то расплав окрашен в интенсивно зеленый цвет. При наличии окислителей ионы 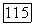 переходят в
переходят в 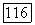 и кристалл флюорита становится бесцветным. Таким образом, интенсивность зеленой окраски характеризует чистоту атмосферы в аппарате для выращивания монокристаллов флюорита.
и кристалл флюорита становится бесцветным. Таким образом, интенсивность зеленой окраски характеризует чистоту атмосферы в аппарате для выращивания монокристаллов флюорита.
Химическая агрессивность фторирующих сред и высокие температуры плавления фторидов предъявляют жесткие требования к материалу тигля и аппаратуры. Наиболее надежными материалами тигля являются графит, платина, молибден. Части аппаратуры, соприкасающиеся с активной фторирующей средой, изготавливаются из платины. Тигель или лодочка перемещаются в алундовой трубке.
Выращивание монокристаллов флюорита методом Бриджмена — Стокбаргера. Важнейшими факторами, влияющими на рост кристаллов в этом случае, являются величина температурного градиента и возможно плоский фронт кристаллизации. С увеличением диаметра кристалла выполнение этих условий становится все более затруднительным. Экспериментально показано, что для флюорита достаточен градиент 7 град/см, но, например,
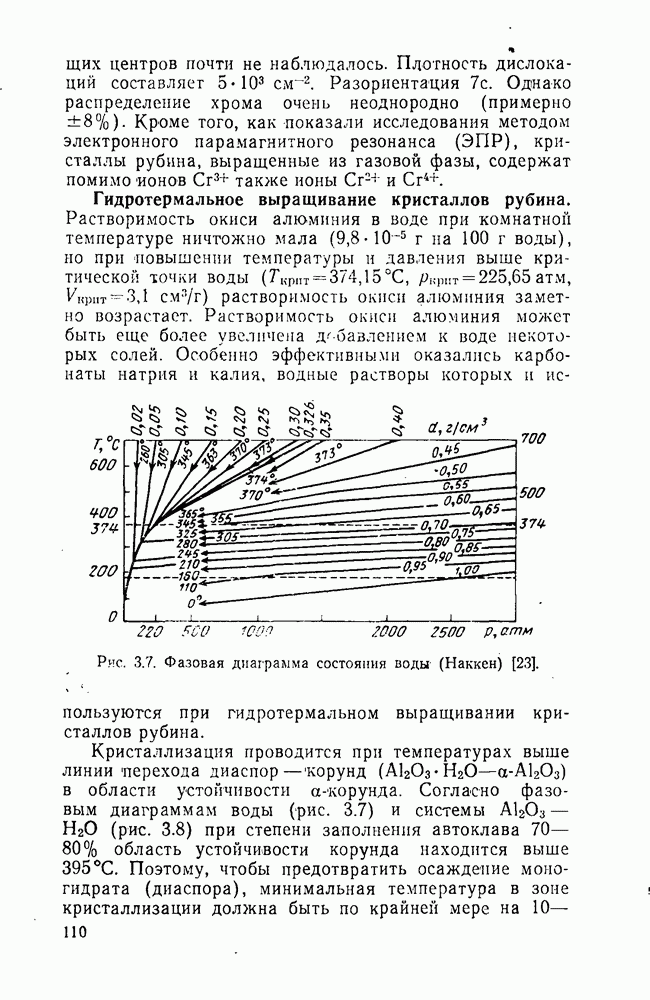
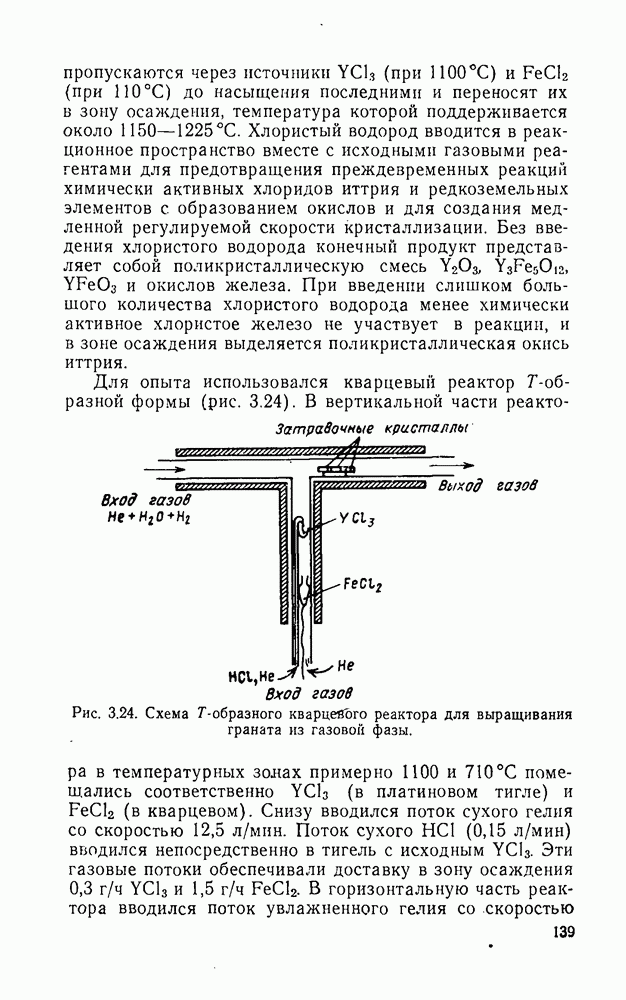
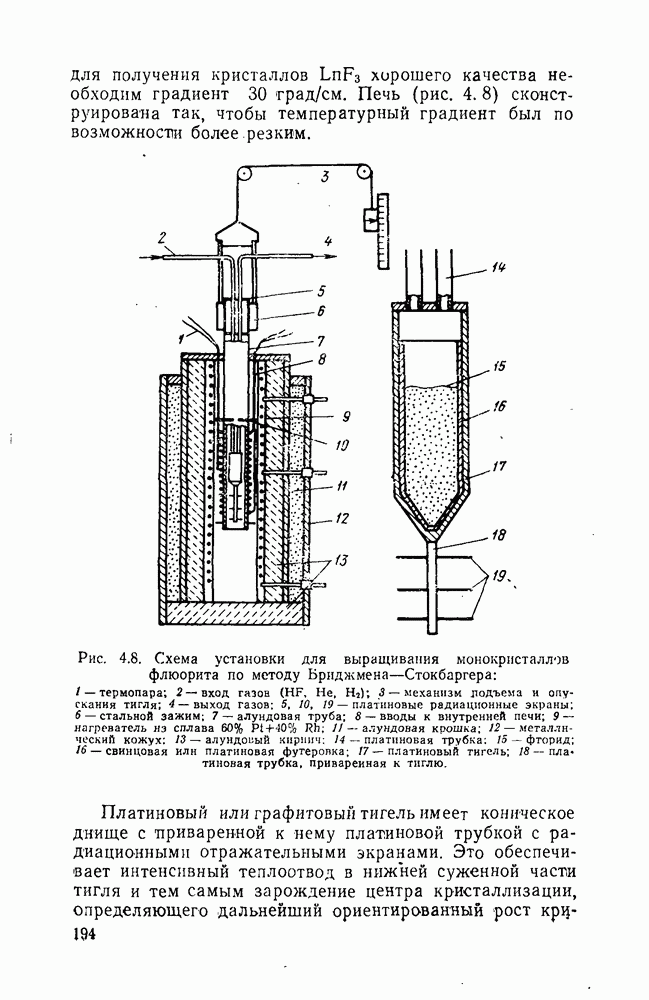
для получения кристаллов 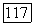 хорошего качества необходим градиент 30 град/см. Печь (рис. 4. 8) сконструирована так, чтобы температурный градиент был по возможности более резким.
хорошего качества необходим градиент 30 град/см. Печь (рис. 4. 8) сконструирована так, чтобы температурный градиент был по возможности более резким.

Рис. 4.8. Схема установки для выращивания монокристаллов флюорита по методу Бриджмена—Стокбаргера: 1 — термопара; 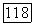 -вход газон
-вход газон 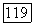 Не,
Не, 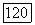 — механизм лодъема и опускания тигля; 4 — выход газов; 5, 10, 19 — платиновые радиационные экраны; 6 — стальной зажим; 7 — алундовая труба; 8 — вводы к внутренней печи; 9 — нагреватель
— механизм лодъема и опускания тигля; 4 — выход газов; 5, 10, 19 — платиновые радиационные экраны; 6 — стальной зажим; 7 — алундовая труба; 8 — вводы к внутренней печи; 9 — нагреватель 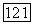 сплава
сплава 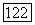 — алундовая крошка; 12 — металлический кожух; 13 — алундоиый кирпич; 14 — платиновая трубка: 15 — фторид; 16 — свинцовая или платиновая футеровка; 17 — платиновый тигель; 18- платиновая трубка, приваренная к тиглю.
— алундовая крошка; 12 — металлический кожух; 13 — алундоиый кирпич; 14 — платиновая трубка: 15 — фторид; 16 — свинцовая или платиновая футеровка; 17 — платиновый тигель; 18- платиновая трубка, приваренная к тиглю.
Платиновый или графитовый тигельимеет коническое днище с приваренной к нему платиновой трубкой с радиационными отражательными экранами. Это обеспечивает интенсивный теплоотвод в нижней суженной части тигля и тем самым зарождение центра кристаллизации, определяющего дальнейший ориентированный рост
кристалла из расплава. Фронт кристаллизации медленно перемещается с постоянной скоростью до тех пор, пока не закристаллизуется весь материал.
Ввиду жесткости медных и платиновых трубок осуществляется перемещение не тигля, а горячей зоны. Внутри большой печи с платиновыми нагревателями помещается малая платиновая печь, которая связана с механизмом перемещения. Внутрь малой печи помещают тигель с исходной шихтой. После этого система продувается потоком сухого гелия 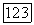 в течение нескольких часов, после чего к гелию добавляют безводный фтористый водород (парциальное давление
в течение нескольких часов, после чего к гелию добавляют безводный фтористый водород (парциальное давление 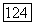 ).
).
Температуру печи медленно поднимают так, чтобы горячая зона была нагрета на 50° выше точки плавления фторида кальция, т. е. примерно до 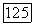 . В течение нескольких часов тигель выдерживают при этой температуре, затем газ отключают и начинают перемещение малой печи со скоростью
. В течение нескольких часов тигель выдерживают при этой температуре, затем газ отключают и начинают перемещение малой печи со скоростью 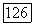 После того как весь материал пройдет через зону с температурным градиентом, печь охлаждают со скоростью
После того как весь материал пройдет через зону с температурным градиентом, печь охлаждают со скоростью 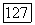 до комнатной температуры.
до комнатной температуры.
В Советском Союзе промышленный способ выращивания монокристаллов флюорита был разработан И. В. Степановым и П. П. Феофиловым. Основную массу кристаллов флюорита получают по методу Бриджмена—Стокбаргера.
Выращивание монокристаллов флюорита по методу Чохральского. Метод Чохральского имеет некоторые преимущества перед методом Бриджмена—Стокбаргера. Он позволяет выбирать заданную ориентацию (с помощью затравки), визуально контролировать рост кристалла и распределение концентрации примесных атомов в кристалле. Однако резкий температурный градиент на выходе кристалла из расплава приводит к большим внутренним напряжениям. Поэтому во избежание раскалывания монокристаллов в верхней части над тиглем помещают дополнительный нагреватель с температурой 800—1000°С, благодаря которому происходит отжиг вытягиваемого кристалла. Скорость вращения затравки составляет около 30 об/мин, а скорость вытягивания — 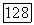 Таким образом получают высококачественные монокристаллы флюорита диаметром 10—12 мм и длиной 80—100 мм.
Таким образом получают высококачественные монокристаллы флюорита диаметром 10—12 мм и длиной 80—100 мм.
Выращивание монокристаллов флюорита методом зонной кристаллизации. Для выращивания крупных кристаллов флюорита обычно используют горизонтальную зонную перекристаллизацию в графитовой лодочке, покрытой пиролитическим графитом. Скорость перемещения расплавленной зоны составляет около 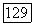 Температура расплавленной зоны около
Температура расплавленной зоны около 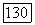 Иногда осуществляют несколько проходов расплавленной зоны по кристаллу с целью зонной очистки от нежелательных примесей или зонного выравнивания концентрации активатора по длине кристалла. Поместив перед исходным поликристаллическим стержнем затравочный кристалл, можно вырастить монокристалл заданной ориентации, размеры которого определяются размерами лодочки или ампулы.
Иногда осуществляют несколько проходов расплавленной зоны по кристаллу с целью зонной очистки от нежелательных примесей или зонного выравнивания концентрации активатора по длине кристалла. Поместив перед исходным поликристаллическим стержнем затравочный кристалл, можно вырастить монокристалл заданной ориентации, размеры которого определяются размерами лодочки или ампулы.
Отжиг кристаллов флюорита. Для снятия напряжений выращенные кристаллы флюорита подвергают отжигу независимо от метода выращивания кристалла. Обычно отжиг флюорита проводят в том же аппарате и в том же тигле, где кристалл выращен. Если же кристалл был извлечен из аппарата, то перед помещением его в печь отжига он должен быть тщательно высушен во избежание гидролиза и диффузии кислорода:

Отжиг проводится в глубоком вакууме в защитной фторирующей среде при температуре 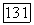 в течение
в течение 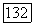 Продолжительность отжига определяется диаметром кристалла и коэффициентом диффузии кислорода во фтористом кальции, который составляет около
Продолжительность отжига определяется диаметром кристалла и коэффициентом диффузии кислорода во фтористом кальции, который составляет около 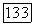 при
при 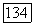 После отжига кристалл медленно охлаждают со скоростью
После отжига кристалл медленно охлаждают со скоростью 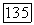 Кристалл диаметром 5 мм необходимо отжечь при 1 200°С в течение
Кристалл диаметром 5 мм необходимо отжечь при 1 200°С в течение  Отжиг кристаллов других фторидов обычно производят при температурах на 200 — 300° ниже точки плавления данного фторида.
Отжиг кристаллов других фторидов обычно производят при температурах на 200 — 300° ниже точки плавления данного фторида.
Введение примесей (активаторов) в кристалл флюорита
1. Введение трехвалентных ионов частично рассмотрено нами выше. Однако помимо необходимости компенсации заряда при введении трехвалентных ионов 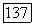 имеется еще ряд трудностей. Например, при легировании флюорита ураном необходимо приготовить чистый трифторид урана
имеется еще ряд трудностей. Например, при легировании флюорита ураном необходимо приготовить чистый трифторид урана 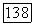 который бы не содержал ионов
который бы не содержал ионов 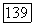 искажающих спектр люминесценции
искажающих спектр люминесценции
кристалла. Фториды редкоземельных элементов получают относительно легко путем фторирования соответствующих металлов или их окислов фтористым водородом. В случае урана при таком взаимодействии получается тетрафторид 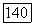 Трифторид урана получают по реакции взаимодействия тетрафторида урана с чистым порошкообразным металлическим ураном при 1050°С в среде инертного газа с небольшой добавкой водорода
Трифторид урана получают по реакции взаимодействия тетрафторида урана с чистым порошкообразным металлическим ураном при 1050°С в среде инертного газа с небольшой добавкой водорода

Химически активный порошок урана получают термическим разложением гидрида урана при температуре около 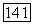 Можно обе эти реакции объединить в один процесс:
Можно обе эти реакции объединить в один процесс:

Этот процесс необходимо проводить при температуре 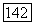
Концентрация ионов 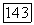 в кристаллах флюорита составляет
в кристаллах флюорита составляет 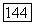 по отношению к кальцию. При этом кристалл окрашивается в темно-красный цвет.
по отношению к кальцию. При этом кристалл окрашивается в темно-красный цвет.
2. Введение двухвалентных ионов 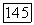 в флюорит. Для большинства редкоземельных элементов двухвалентное состояние не характерно и менее устойчиво, чем трехвалентное. Поэтому получение и сохранение в процессе выращивания фторидов
в флюорит. Для большинства редкоземельных элементов двухвалентное состояние не характерно и менее устойчиво, чем трехвалентное. Поэтому получение и сохранение в процессе выращивания фторидов 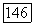 затруднительно. В связи с этим в качестве исходных соединений берут трифториды редкоземельных элементов и восстанавливают их либо в процессе роста монокристалла флюорита, либо путем специальной обработки готового кристалла, содержащего ионы
затруднительно. В связи с этим в качестве исходных соединений берут трифториды редкоземельных элементов и восстанавливают их либо в процессе роста монокристалла флюорита, либо путем специальной обработки готового кристалла, содержащего ионы 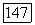 Из обычно используемых активаторов во флюорите
Из обычно используемых активаторов во флюорите 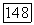 лучше других восстанавливается самарий. Для этого достаточно создать восстановительные условия в процессе роста кристалла (водород в газовой фазе, порошок графита в шихте и т. д.), но при этом оказывается невозможным применение защитных фторирующих сред, так как при фторировании ионы
лучше других восстанавливается самарий. Для этого достаточно создать восстановительные условия в процессе роста кристалла (водород в газовой фазе, порошок графита в шихте и т. д.), но при этом оказывается невозможным применение защитных фторирующих сред, так как при фторировании ионы 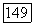 окисляются до
окисляются до 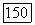 Поэтому обычно восстановление ионов Ln3+ до
Поэтому обычно восстановление ионов Ln3+ до 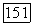 производится в готовых, выращенных кристаллах. Такое восстановление осуществляют одним из следующих методов.
производится в готовых, выращенных кристаллах. Такое восстановление осуществляют одним из следующих методов.
1. Радиационное восстановление. Кристалл подвергают действию гамма-лучей и быстрых электронов. При таком восстановлении двухвалентные редкоземельные
ионы образуются за счет перераспределения электронов в кристалле. Избыточные свободные электроны не покидают кристалл. Поэтому такое состояние ионов 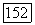 неустойчиво и под действием тепла или света происходит релаксация — обратный процесс окисления
неустойчиво и под действием тепла или света происходит релаксация — обратный процесс окисления 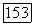 до
до 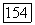 Фото- и термонеустойчивость радиационно восстановленных кристаллов, а также неполнота восстановления (менее 30% атомов примеси) являются существенными недостатками этого метода. Неполнота восстановления, вероятно, связана с тем, что способностью захватывать электрон и переходить в двухвалентное состояние обладают не все центры
Фото- и термонеустойчивость радиационно восстановленных кристаллов, а также неполнота восстановления (менее 30% атомов примеси) являются существенными недостатками этого метода. Неполнота восстановления, вероятно, связана с тем, что способностью захватывать электрон и переходить в двухвалентное состояние обладают не все центры 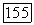 а только «кубические», так как только эти центры имеют доложительные эффективные заряды.
а только «кубические», так как только эти центры имеют доложительные эффективные заряды.
Исследование ЭПР и эффекта Зеемана подтвердили, что двухвалентные редкоземельные ионы в кристаллах флюорита находятся в электрическом поле кубической симметрии. Поскольку концентрация кубических центров невелика, то и в двухвалентное состояние переходит небольшая часть ионов 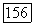 Достоинством радиационного метода восстановления является высокое оптическое качество монокристаллов.
Достоинством радиационного метода восстановления является высокое оптическое качество монокристаллов.
2. Метод аддитивного окрашивания или метод диффузии. Кристалл флюорита, легированный редкоземельным элементом, выдерживают при температуре 600 — 900 °С в парах щелочноземельного металла (или другого электроположительного элемента) в течение времени, достаточного для диффузии атомов металла в кристалл. При этом они отдают свои валентные электроны редкоземельным ионам:

Во избежание окисления флюорита процесс проводят в эвакуированных и запаянных ампулах или при непрерывной откачке. Таким образом получены кристаллы 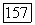 с хорошей оптической однородностью, фото- и термоустойчивые. Проведение процесса при высокой температуре обусловливает почти полное восстановление всех введенных в кристалл атомов.
с хорошей оптической однородностью, фото- и термоустойчивые. Проведение процесса при высокой температуре обусловливает почти полное восстановление всех введенных в кристалл атомов.
3. Метод электродиффузии (твердофазный электролиз). К кристаллу флюорита, содержащему трехвалентные редкоземельные ионы, прикладывают постоянное напряжение. Кристалл нагревают до температуры,
обеспечивающей ионную проводимость, и выдерживают в течение нескольких часов под напряжением. Восстановленные таким способом ионы 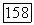 в кристалле флюорита также фото- и термоустойчивы.
в кристалле флюорита также фото- и термоустойчивы.
Фториды магния и цинка 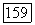
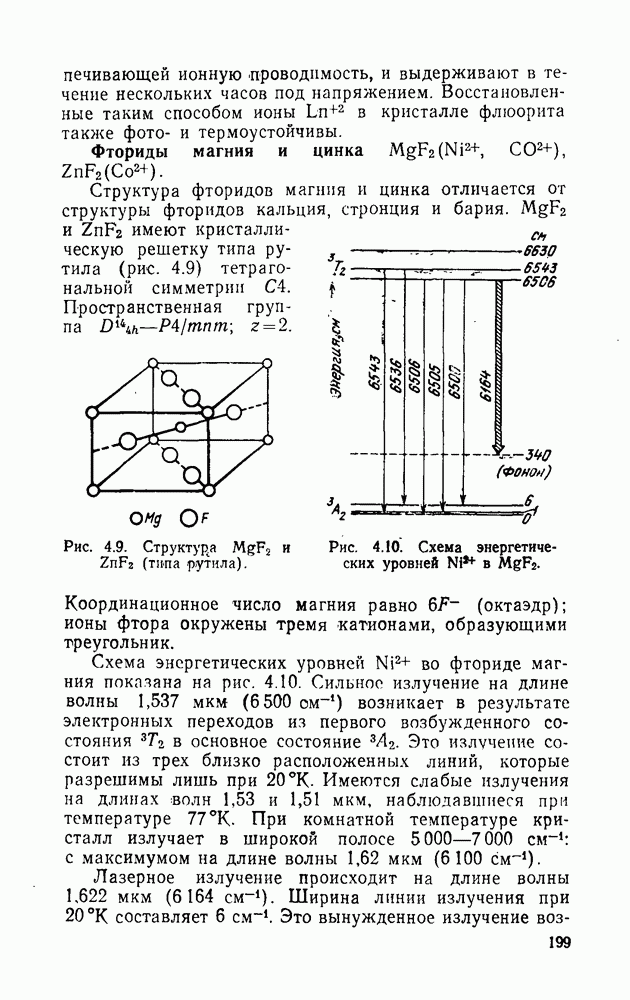
Структура фторидов магния и цинка отличается от структуры фторидов кальция, стронция и бария. 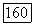 имеют кристаллическую решетку типа рутила (рис. 4.9) тетрагональной симметрии
имеют кристаллическую решетку типа рутила (рис. 4.9) тетрагональной симметрии 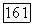
Пространственная группа 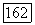

Рис. 4.9. Структуру 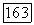 (пита рутила).
(пита рутила).

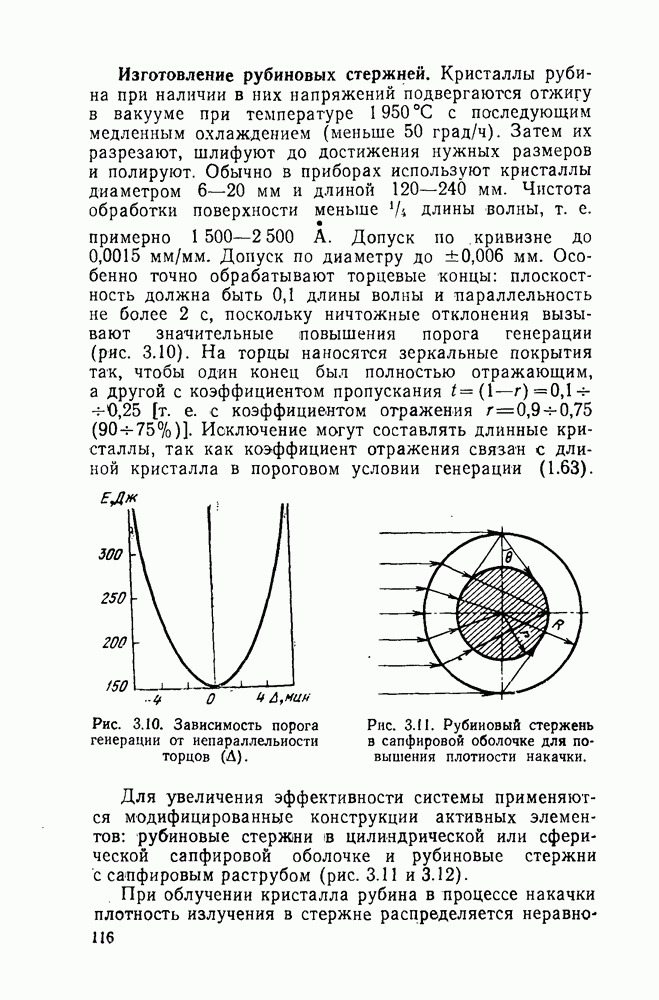
Рис. 4.10. Схема энергетических уровней 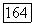
Координационное число магния равно 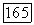 (октаэдр); ионы фтора окружены тремя катионами, образующими треугольник.
(октаэдр); ионы фтора окружены тремя катионами, образующими треугольник.
Схема энергетических уровней  во фториде магния показана на рис. 4.10. Сильное излучение на длине волны 1,537 мкм
во фториде магния показана на рис. 4.10. Сильное излучение на длине волны 1,537 мкм  возникает в результате электронных переходов из первого возбужденного состояния
возникает в результате электронных переходов из первого возбужденного состояния  в основное состояние 3/12. Это излучение состоит из трех близко расположенных линий, которые разрешимы лишь при
в основное состояние 3/12. Это излучение состоит из трех близко расположенных линий, которые разрешимы лишь при  Имеются слабые излучения на длинах волн 1,53 и 1,51 мкм, наблюдавшиеся при температуре
Имеются слабые излучения на длинах волн 1,53 и 1,51 мкм, наблюдавшиеся при температуре 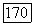 При комнатной температуре кристалл излучает в широкой полосе
При комнатной температуре кристалл излучает в широкой полосе 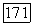 : с максимумом на длине волны 1,62 мкм
: с максимумом на длине волны 1,62 мкм 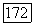
Лазерное излучение происходит на длине волны 1,622 мкм 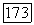 Ширина линии излучения при
Ширина линии излучения при 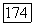 составляет
составляет 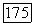 Это вынужденное излучение
Это вынужденное излучение
возникает в результате перехода с самого низкого уровня состояния 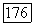 в основное состояние иона
в основное состояние иона 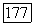 с одновременным возбуждением колебаний решетки (испускание фотона). Следовательно, в этом переходе участвует весь кристалл в целом. Хотя ион
с одновременным возбуждением колебаний решетки (испускание фотона). Следовательно, в этом переходе участвует весь кристалл в целом. Хотя ион 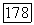 в результате перехода оказывается в основном состоянии, конечным состоянием лазерного перехода является возбужденное состояние решетки кристалла в целом.
в результате перехода оказывается в основном состоянии, конечным состоянием лазерного перехода является возбужденное состояние решетки кристалла в целом.
Монокристаллы фторидов магния и цинка выращивают из расплава методом зонной кристаллизации в инертной среде. Уровень легирования кристаллов активаторами (никелем или кобальтом) составляет 1—5%.
Для выращивания по методу Чохральского исходные фториды предварительно высушивают в вакууме при температуре 300°С в течение нескольких часов. Рост монокристаллов проводят из платинового тигля в атмосфере сухого гелия. Нагрев индукционный. Затравление осуществляют на платиновой проволоке. Кристаллы с малым светорассеянием получаются лишь при скоростях вытягивания менее 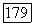 Светорассеяние в кристаллах вызывается газовыми пузырьками и твердыми включениями частиц окиси магния. Выращены кристаллы диаметром 7 мм.
Светорассеяние в кристаллах вызывается газовыми пузырьками и твердыми включениями частиц окиси магния. Выращены кристаллы диаметром 7 мм.
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие
- Введение
- Глава первая. ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ИЗЛУЧЕНИЯ И ПРИНЦИП ДЕЙСТВИЯ КВАНТОВЫХ ГЕНЕРАТОРОВ
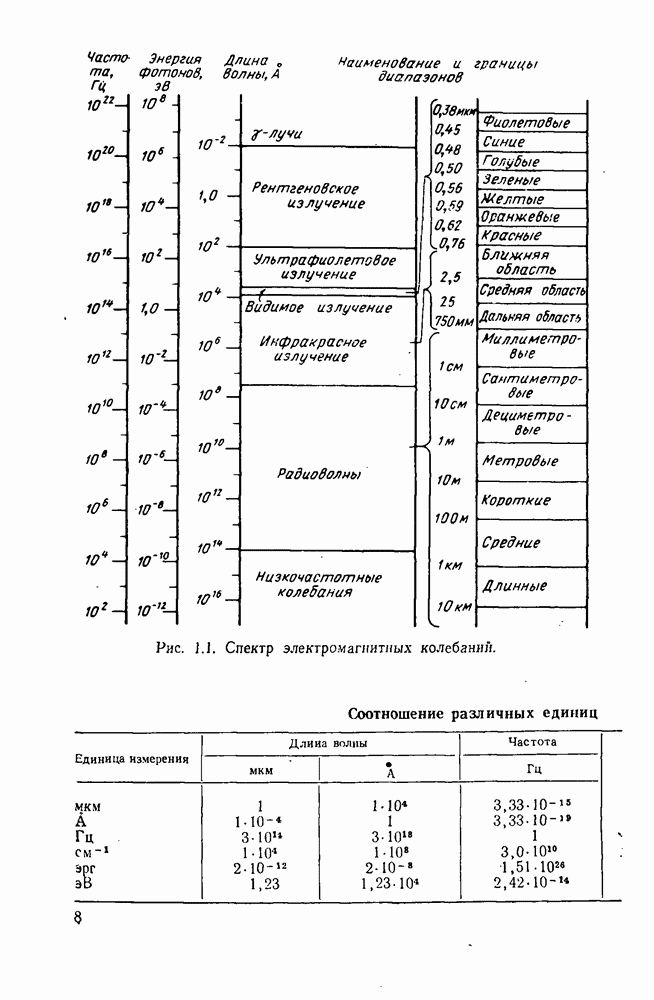
- 1.1. Спектр электромагнитных колебаний
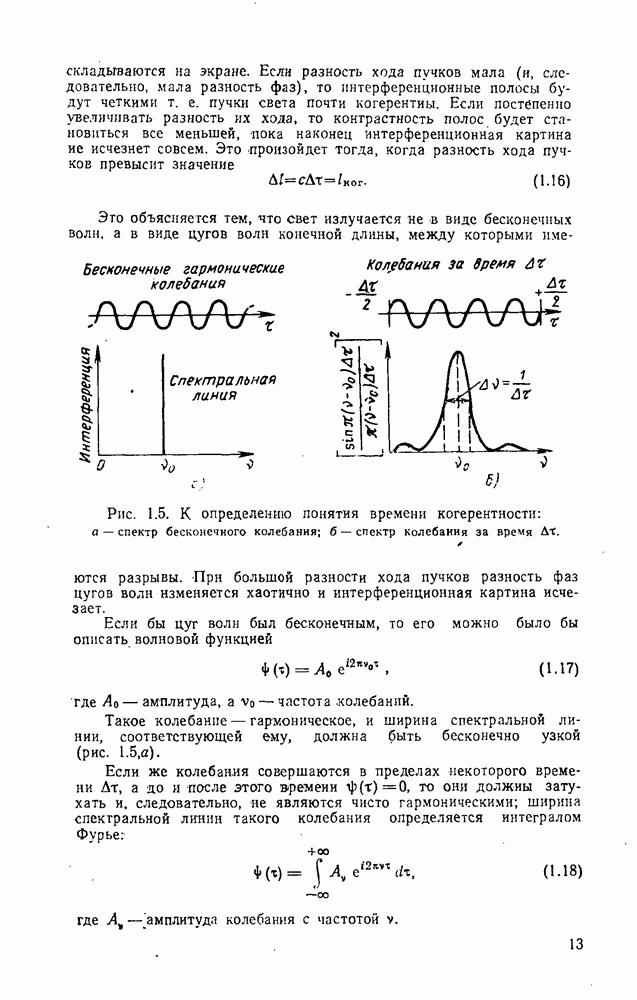
- 1.2. Когерентность
- 1.3. Направленность излучения
- 1.4. Символика энергетических уровней атомов и ионов
- 1.5. Инверсная населенность
- 1.6. Вероятности спонтанных и вынужденных переходов
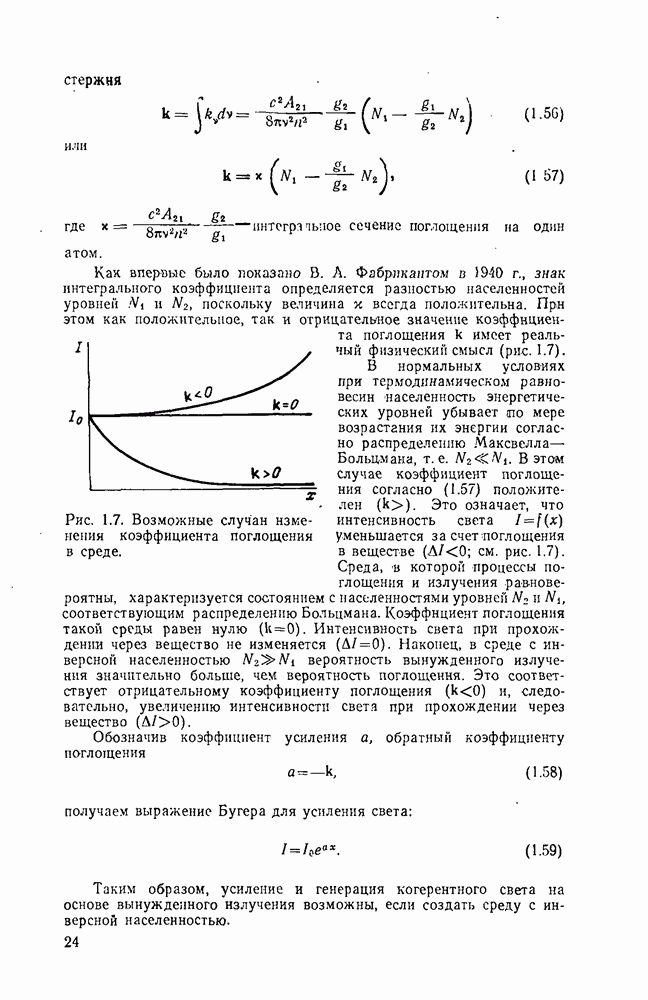
- 1.7. Усиление света при прохождении через вещество
- 1.8. Двухуровневая система
- 1.9. Трехуровневая система
- 1.10. Четырехуровневая система
- 1.11. Возбуждение активного вещества
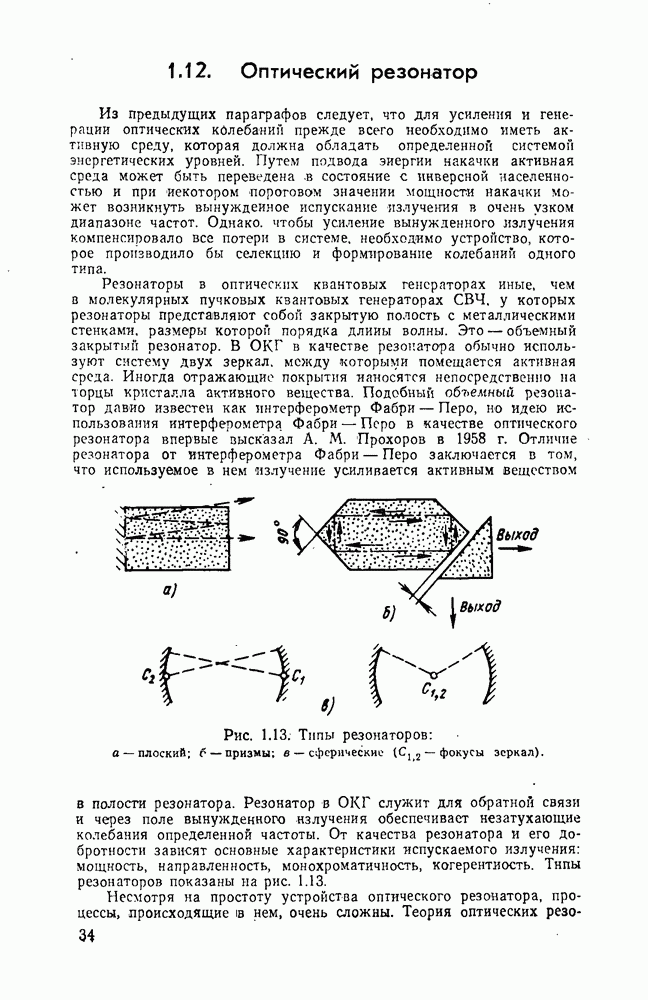
- 1.12. Оптический резонатор
- 1.13 Условие генерации
- 1.14. Потери энергии в квантовом генераторе
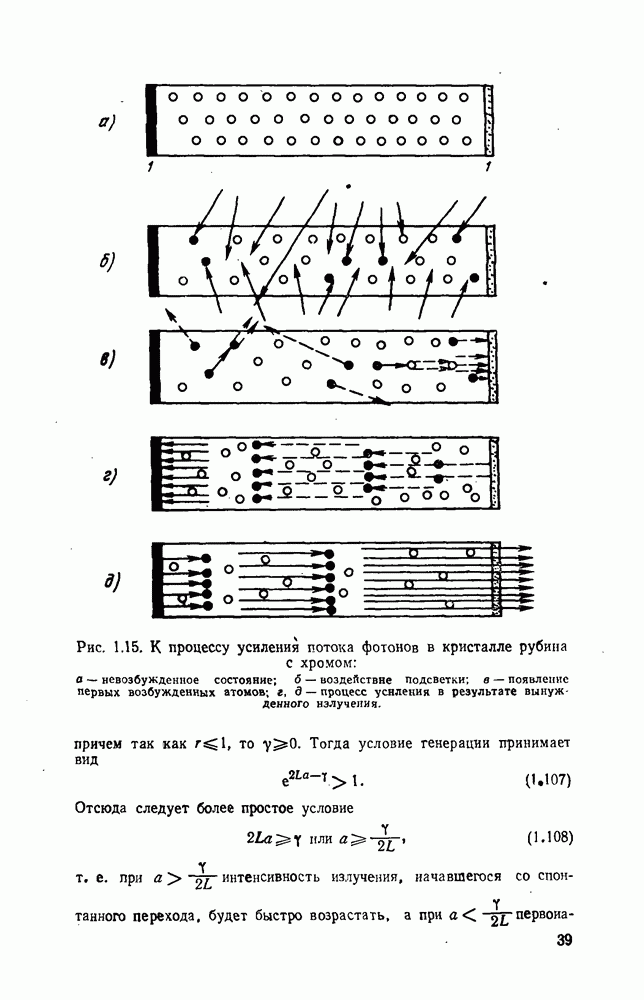
- 1.15. Устройство ОКГ на твердом теле
- Глава вторая. ОБЩИЕ ВОПРОСЫ ТЕХНОЛОГИИ МАТЕРИАЛОВ ТВЕРДОТЕЛЬНЫХ ОКГ
- 2.1. Особенности активного вещества ионных квантовых систем
- 2.2. Особенности технологии твердотельных материалов квантовых генераторов
- 2.3. Физико-химические основы кристаллизации
- 2.3.2. Гетерогенное зародышеобразование
- 2.3.3. Скорость зарождения новой фазы
- 2.3.4. Рост кристаллов
- 2.3.5. Общее кинетическое уравнение кристаллизации
- 2.3.6. Распределение примеси в процессе роста кристалла
- 2.4. Основные методы синтеза и выращивания кристаллов
- 2.4.2. Выращивание из стехиометрических расплавов
- 2.4.3. Методы выращивания кристаллов из растворов
- 2.4.4. Гидротермальный синтез и рост кристаллов
- 2.4.5. Выращивание кристаллов из газовой фазы
- 2.5. Кристалло-химическая классификация материалов твердотельных квантовых генераторов
- Глава третья. КИСЛОРОДНЫЕ СОЕДИНЕНИЯ
- 3.1. Окислы элементов III группы
- 3.1.2. Окислы редкоземельных элементов и иттрия
- 3.3.1. Гранаты
- 3.2. Материалы на основе кислородных соединений элементов VI группы
- 3.2.2. Молибдаты
- 3.3. Материалы на основе кислородных соединений элементов V группы
- 3.3.2. Ниобаты
- 3.3.3. Фосфаты
- Выращивание кристаллов фторфосфата кальция [47]
- Глава четвертая. ФТОРИСТЫЕ СОЕДИНЕНИЯ
- 4.1. Фториды элементов II группы
- 4.2. Фториды редкоземельных элементов
- 4.3. Смешанные фториды
- 4.4. Фториды элементов VII группы
- Глава пятая. СТЕКЛО
- 5.1. Особенности стекла как активного материала ОКГ
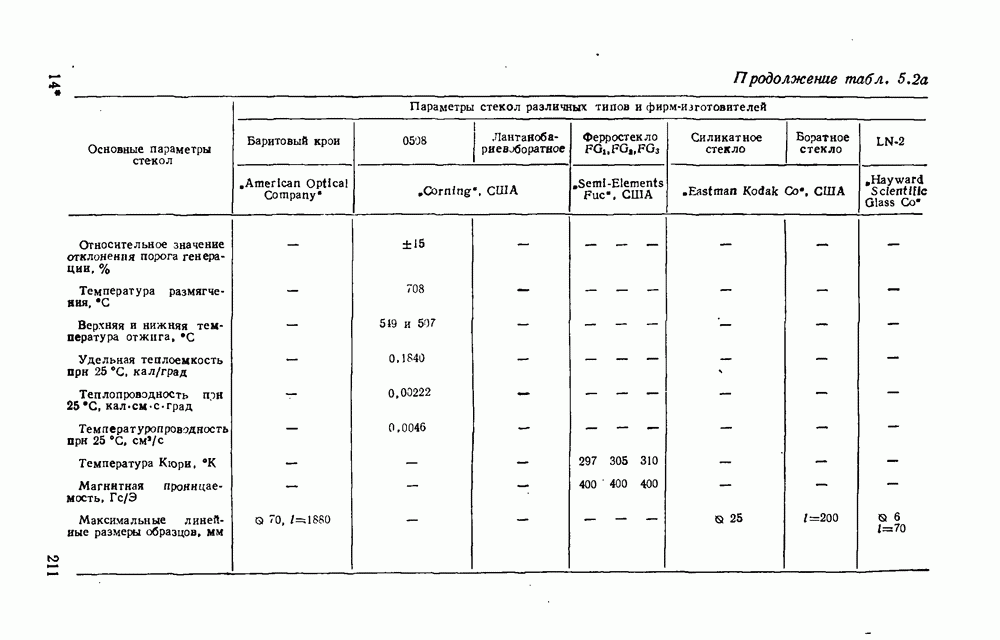
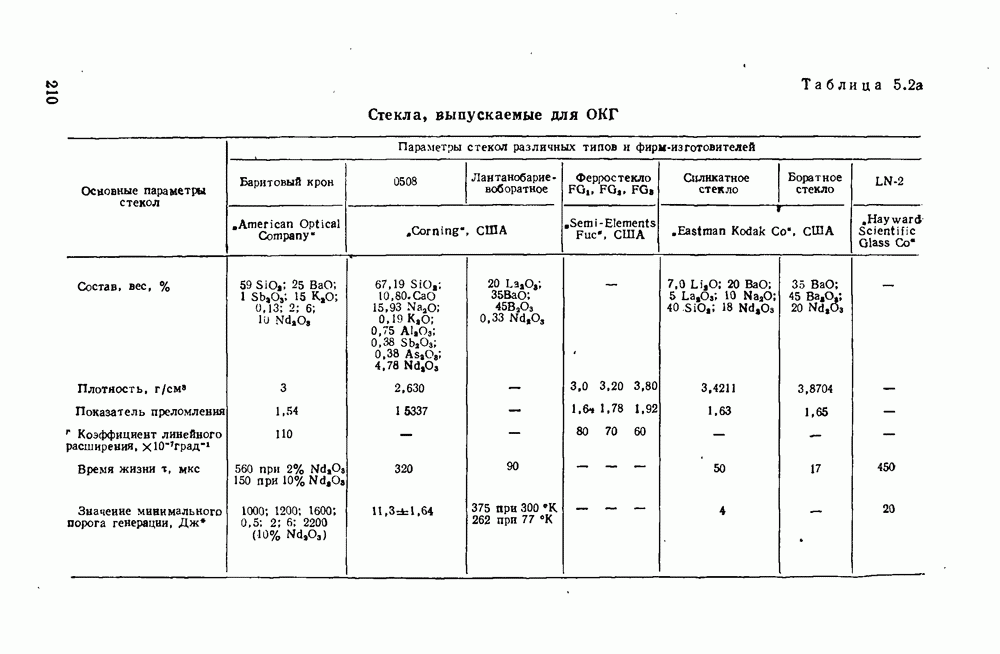
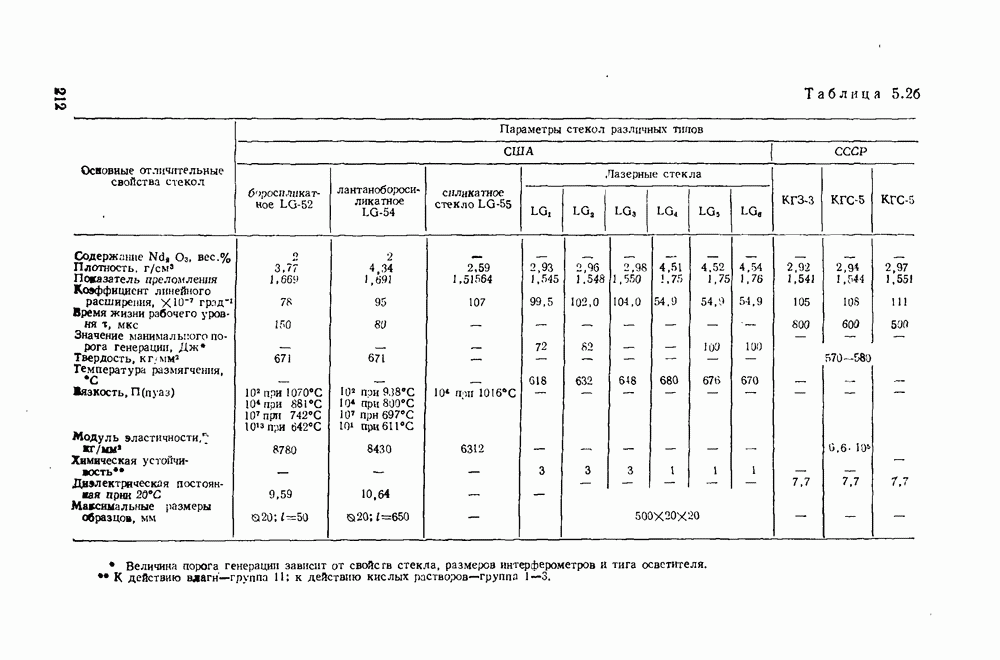
- 5.2. Общая характеристика стекол для ОКГ
- 5.3. Особенности положения атомов активатора в стекле
- 5.4. Стекло с неодимом
- Глава шестая. МАТЕРИАЛЫ ЖИДКОСТНЫХ ОКГ
- 6.2. Механизм излучения в органических растворах
- 6.3. Растворы металлоорганических соединений
- 6.4. Растворы органических красителей
- 6.5. Растворы неорганических соединений редкоземельных элементов
- Глава седьмая. ОБЩАЯ ХАРАКТЕРИСТИКА ПОЛУПРОВОДНИКОВЫХ КВАНТОВЫХ ГЕНЕРАТОРОВ (ПКГ)
- 7.2. Основные сведения из теории люминесценции инжекционных ПКГ
- 7.3. Рабочие характеристики инжекционных ПКГ
- 7.3.2. Пространственные свойства
- 7.3.3. Пороговый ток
- 7.3.4. Квантовый выход
- 7.4. Тепловые условия работы лазерного диода
- 7.4.2. Работа в квазинепрерывном режиме
- 7.5. Другие типы ПКГ
- 7.5.1. ПКГ с электронным возбуждением
- 7.5.2. ПКГ с оптической накачкой
- 7.5.3. ПКГ с прямым электрическим возбуждением
- Глава восьмая. АРСЕНИД ГАЛЛИЯ И ТЕХНОЛОГИЯ ИЗГОТОВЛЕНИЯ ДИОДОВ ПКГ
- 8.1. Физические свойства арсенида галлия
- 8.2. Методы выращивания монокристаллов арсенида галлия
- 8.3. Методы изготовления р-n-переходов
- 8.3.2. Эпитаксия из жидкой фазы
- 8.3.3. Эпитаксия из газовой фазы
- 8.4. Изготовление невыпрямляющих низкоомных контактов к арсениду галлия
- 8.5. Изготовление резонатора
- 8.6. Общая технологическая схема изготовления диодов ПКГ
- 8.7. Конструкция ПКГ
- 8.8. Гетероструктуры на основе арсенида галлия
- 8.9. Другие материалы с прямыми переходами
- Глава девятая. МАТЕРИАЛЫ ГАЗОВЫХ ОКГ
- 9.1. Особенности газового активного вещества ОКГ и методы создания инверсной населенности
- 9.2. Газоразрядные ОКГ
- 9.2.2. Ионные газоразрядные ОКГ
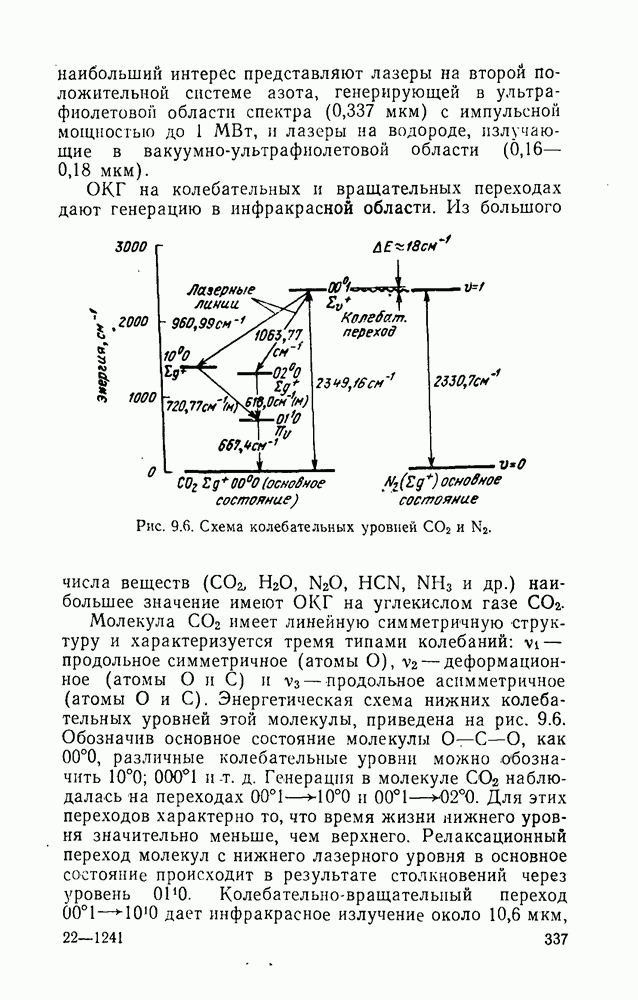
- 9.2.3. Молекулярные газоразрядные ОКГ
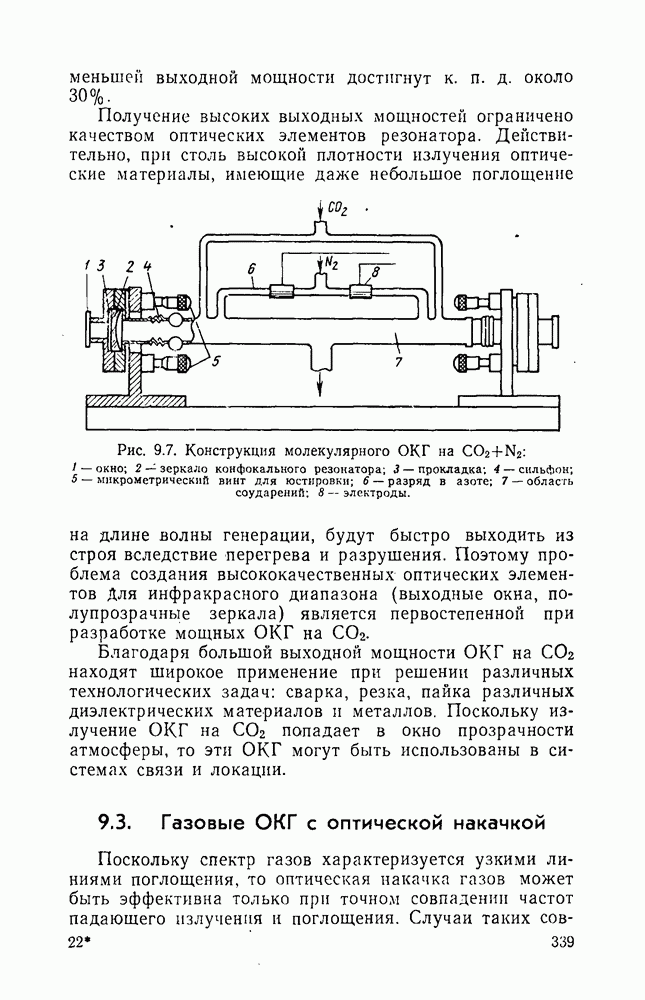
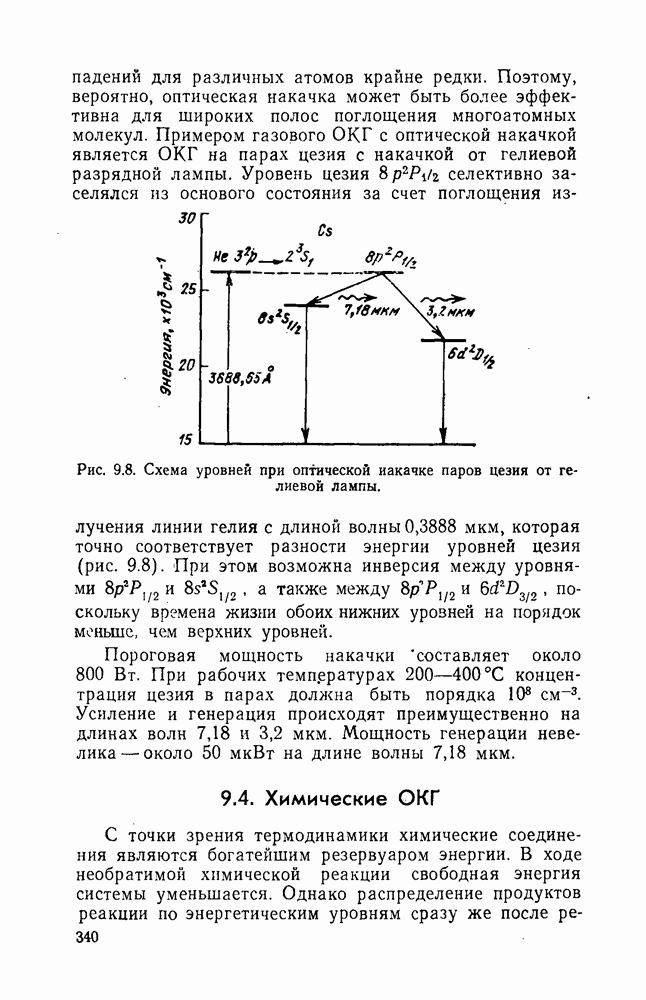
- 9.3. Газовые ОКГ с оптической накачкой
- 9.4. Химические ОКГ
- Глава десятая. МАТЕРИАЛЫ МОДУЛЯТОРОВ ОПТИЧЕСКОГО ИЗЛУЧЕНИЯ
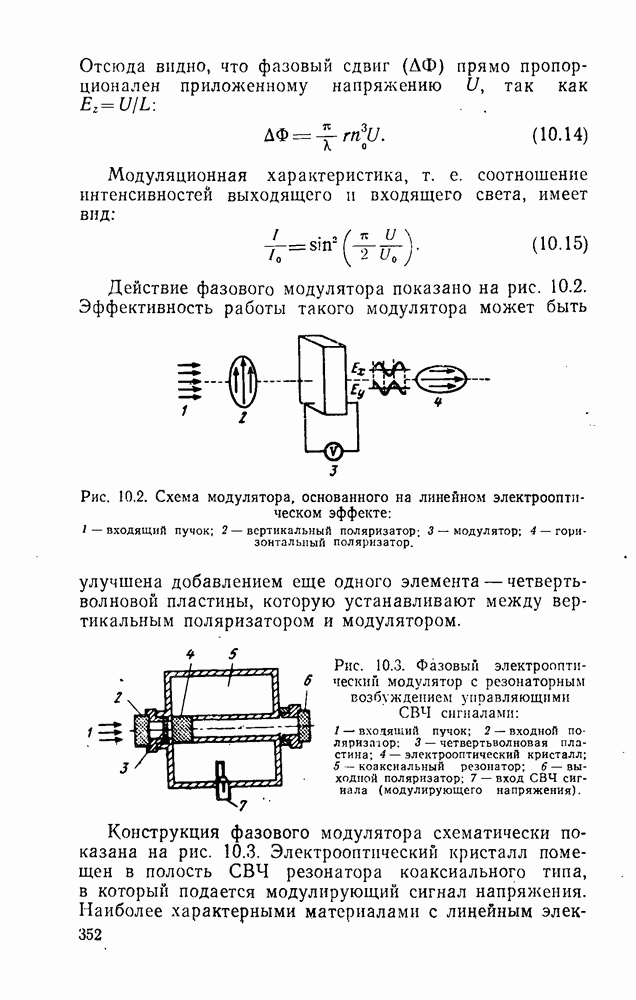
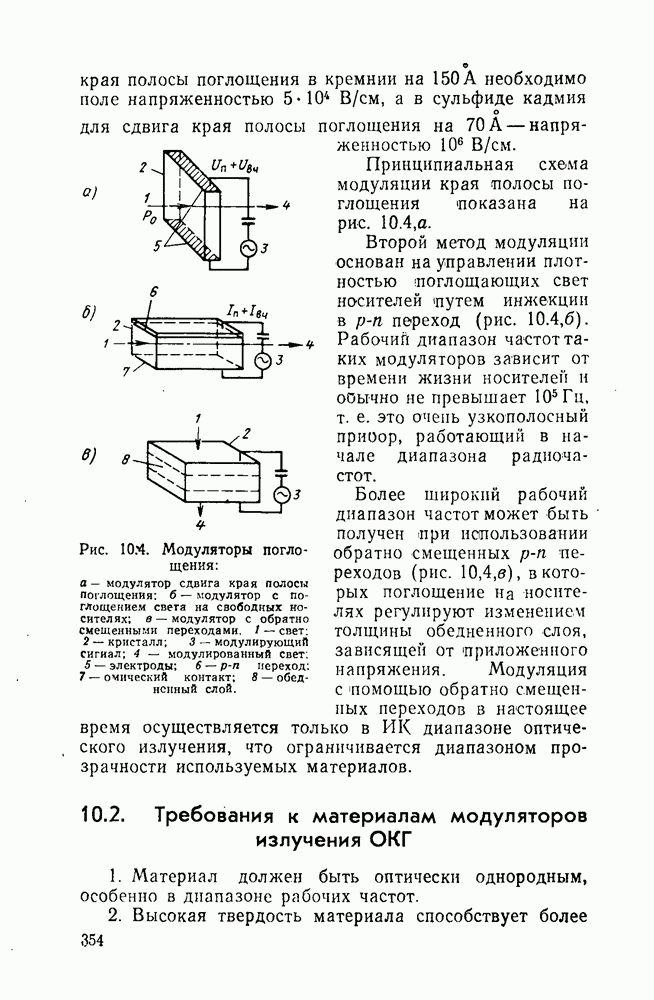
- 10.1. Некоторые физические основы модуляции оптического излучения
- 10.2. Требования к материалам модуляторов излучения ОКГ
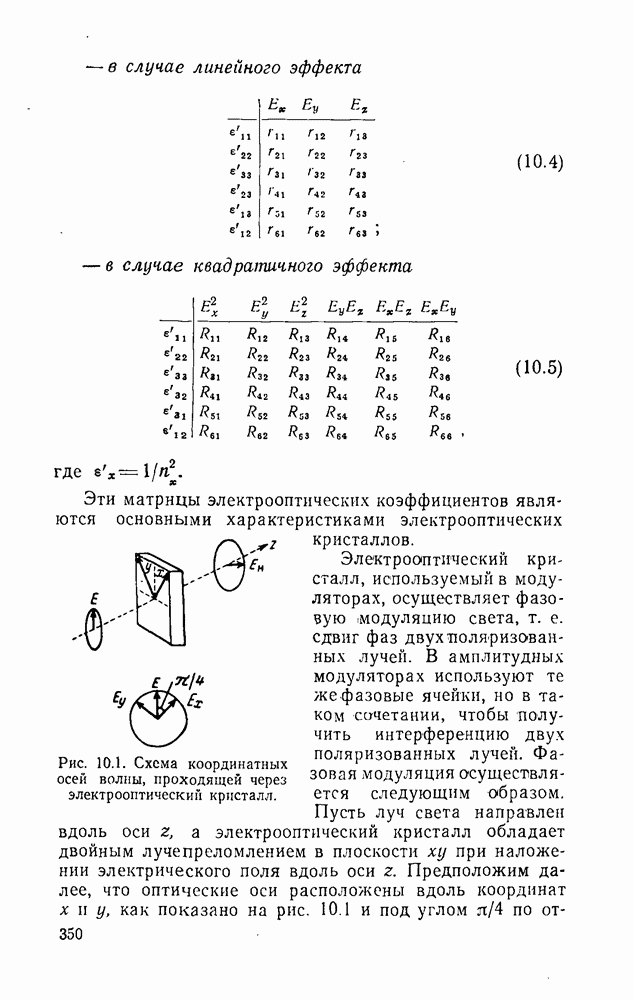
- 10.3. Материалы с линейным электрооптическим эффектом
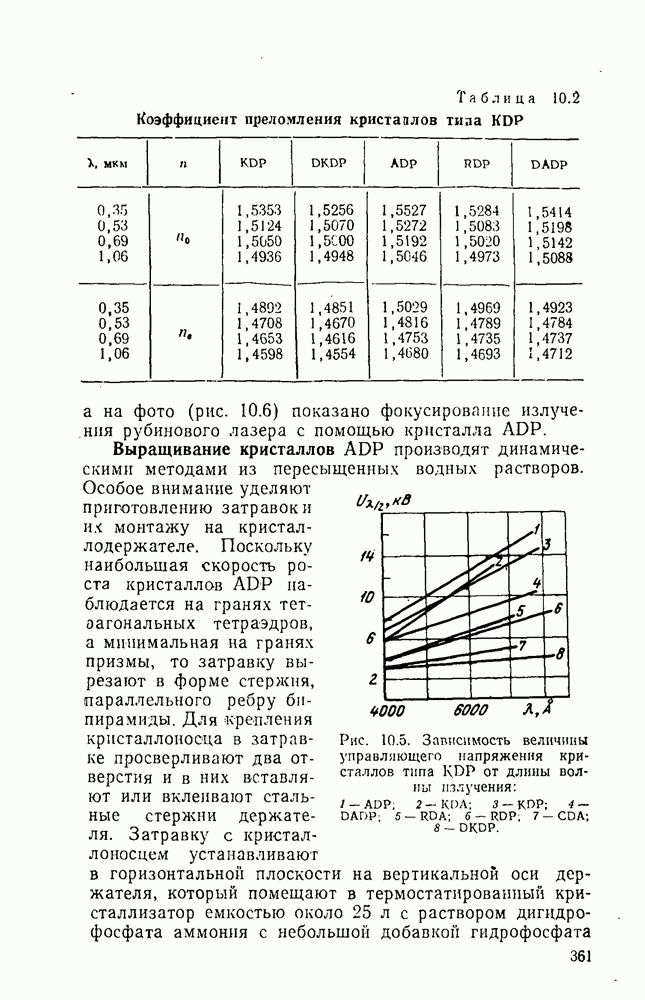
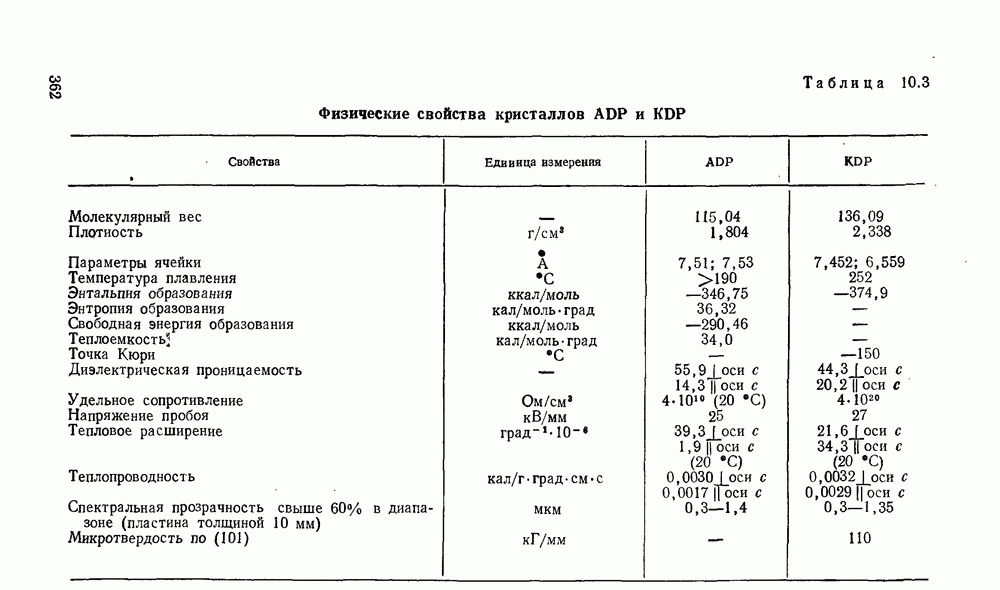
- 10.3.1. Тетрагональные кристаллы типа KDP
- 10.3.2. Ромбические кристаллы
- 10.3.3. Тригональные кристаллы
- 10.3.4. Кубические кристаллы
- 10.4. Кристаллы с квадратичным электрооптическим эффектом
- Литература