| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
2.4.5. Выращивание кристаллов из газовой фазы
Методы выращивания кристаллов из газовой фазы известны давно. Теоретические основы зарождения и роста кристаллов разработаны на моделях кристаллизации из газовой фазы. Однако в технологии материалов квантовой электроники эти методы пока не получили распространения вследствие малых размеров получаемых кристаллов. Размеры кристаллов, выращенных из газовой фазы, ограничиваются главным образом концентрационными, а также тепло- и массодинамическими условиями. Во-первых, это низкие концентрации газовой фазы по сравнению, например, с растворами. Во-вторых, трудности отвода теплоты кристаллизации с поверхности кристалла. В-третьих, возникновение турбулентных потоков газовой фазы вокруг кристалла может привести к неоднородному дендритному или поликристаллнческому росту.
Все же в ряде случаев методы кристаллизации из газовой фазы обладают столь явными преимуществами перед другими методами, что оказываются наиболее эффективными или даже единственно возможными. Так, только из газовой фазы удается вырастить ряд тугоплавких или инконгруэнгно плавящихся соединений. Путем ориентированной кристаллизации из газовой фазы получают монокристаллнческие слои полупроводников с однородным распределением примеси. Из газовой фазы осуществляется нанесение просветляющих или защитных покрытий, контактов, металлических или многослойных диэлектрических зеркал и т. д.
Достоинствами методов выращивания кристаллов из газовой фазы являются более низкие температуры кристаллизации и малые пересыщения, а следовательно, и более высокое совершенство кристаллов, малое содержание дефектов, относительная простота аппаратуры и возможность управление составом. Существуют две основные группы методов выращивания кристаллов из газовой фазы: методы молекулярных пучков (напыление, сублимация) и методы химических реакций (в том числе химический перенос).
Методы молекулярных пучков (дискретные методы) заключаются в следующем. Вещество испаряется путем нагревания в вакууме, образуя прямолинейный поток атомов и молекул. Последние при сюлкиовснии с поверхностью подложки адсорбируются на ней и ?мигрируют. Если частица встречает участок активного роста, он а встраивается в кристалл, если нет — уходит в газовую фазу. Механизм встраивания (двумерное зарождение, дислокационный росг, нормальный рост) зависит от разности температур молекулярного пучка и поверхности подложки, т. е. от степени пересыщения.
Таким образом, при взаимодействии падающей молекулы с поверхностью кристалла возможны два случая: адсорбция молекулы или отражение ее, что аналогично конденсации или испарению. Вероятность превалирования того или иного процесса характеризуется коэффициентом аккомодации а, который может быть выражен через энергии или температуры падающих и испаряющихся молекул:

где  — энергия падающих молекул;
— энергия падающих молекул;  — энергия испарившихся молекул;
— энергия испарившихся молекул;  — энергия адсорбированных на поверхности молекул (для температуры Т — обозначения аналогичные).
— энергия адсорбированных на поверхности молекул (для температуры Т — обозначения аналогичные).
Нетрудно видеть, что если молекула после столкновения с поверхностью сохранила энергию, меньшую энергии поверхностных молекул, она остается на поверхности,  е. конденсируется. Следовательно, при
е. конденсируется. Следовательно, при  имеет место конденсация. При
имеет место конденсация. При  более вероятно испарение, так как молекула после столкновения имеет достаточную энергию, чтобы преодолеть поверхностные силы.
более вероятно испарение, так как молекула после столкновения имеет достаточную энергию, чтобы преодолеть поверхностные силы.
Согласно кинетической теории для идеального газа скорость конденсации может быть найдена из уравнения Кнудсена

где  — равновесное давление пара при температуре поверхности Г;
— равновесное давление пара при температуре поверхности Г;  — давление пара в молекулярном пучке, приведенное к температуре поверхности
— давление пара в молекулярном пучке, приведенное к температуре поверхности  , т. е. если
, т. е. если  то
то  определяется как доля, равная
определяется как доля, равная  истинного давления;
истинного давления;  — масса молекул;
— масса молекул;  — постоянная Больцмана.
— постоянная Больцмана.
В реальных системах отклонения от идеальности учитываются коэффициентам конденсации  при
при  и коэффициентом испарения
и коэффициентом испарения  при
при 

Коэффициент  характеризует долю конденсирующихся молекул из всех падающих на поверхность.
характеризует долю конденсирующихся молекул из всех падающих на поверхность.
Среднее время жизни молекул в адсорбированном состоянии равно

где  — частота колебаний атомов на поверхности;
— частота колебаний атомов на поверхности;  — энергия десорбции молекулы.
— энергия десорбции молекулы.
Миграция молекулы по поверхности в течение этого времени Тадс характеризуется коэффициентом поверхностной диффузии

где  — длина свободного пробега молекулы на поверхности;
— длина свободного пробега молекулы на поверхности;  энергия активации поверхностной диффузии.
энергия активации поверхностной диффузии.
За время тадо молекулэ либо находит активный участок роста и встраивается в кристалл, либо десорбируется в газовую фазу. Среднее расстояние, которое она успевает пройти по поверхности кристалла до момента десорбции, равно

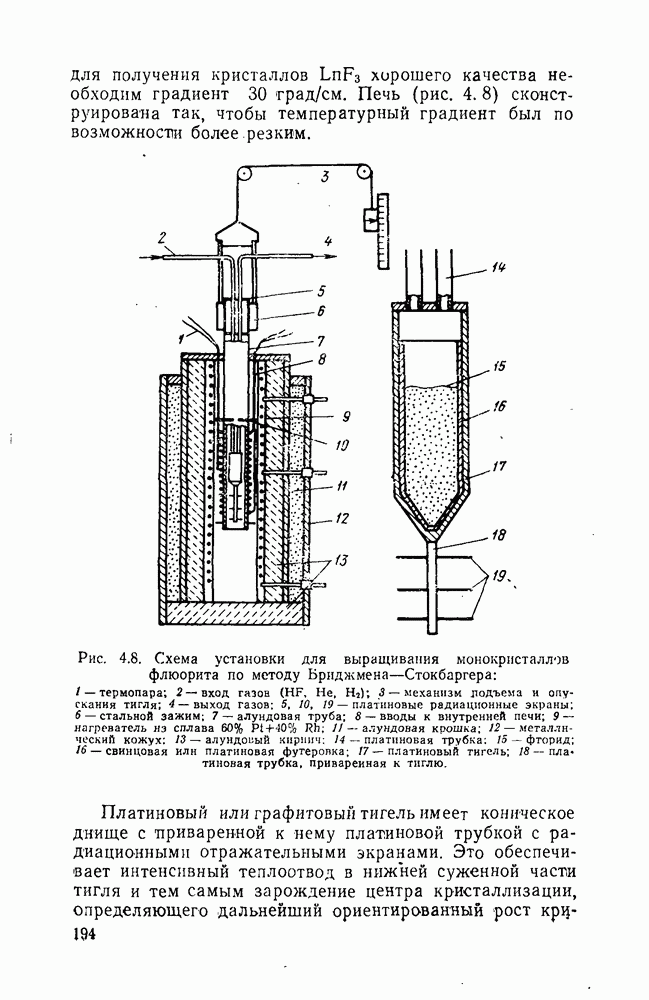
В большинстве случаев крупные кристаллы не удается вырастить этим методом потому, что вследствие большого и резкого температурного
турного градиента образуется много зародышей и вырастаю! мелкие кристаллы. Чтобы вырастить крупные кристаллы, необходимо управлять образованием зародышей. Это возможно путем регулирования температуры подложки. Действительно, при конденсации паров на «горячую» подложку удается выращивать толстые монокристаллические слои большой площади.
Методы химических реакций очень разнообразны. При выращивании кристаллов этими методами состав газовой фазы отличается от состава растущего кристалла. Частицы (атомы или молекулы) газовой фазы хемосорбпруются на поверхности с образованием основного продукта — частиц, встраивающихся в кристалл, и побочных продуктов, уходящих в газовую фазу. Обычно используются реакции термического разложения, восстановления, окисления, сульфирования и др.
Методы химического переноса являются важнейшими среди методов химических реакций. Они применяются для выращивания нелетучих, тугоплавких и ннконгруэнтно плавящихся веществ, выращивание кристаллов которых из расплавов или дискретными методами невозможно или представляет существенные трудности вследствие необходимости проводить процесс при высоких температурах и давлениях из-за большой разницы в давлениях паров элементов над соединением при температуре плавления. Сущность методов химического переноса заключается в том, что твердое вещество (или его компоненты), взаимодействуя по обратимой реакции с газом, образует только газообразные продукты, которые после переноса в другую часть системы при изменении условий равновесия разлагаются с выделением конечного продукта и ростом кристалла. Внешне это похоже на испарение и конденсацию, но процесс протекает при таких низких температурах, при которых это вещество не обладает заметным давлением пара. В большинстве случаев перенос осуществляется вследствие градиента концентраций, создаваемого температурным градиентом.
Таким образом, с помощью химического переноса снижается температура кристаллизации и создается возможность проводить ее при малых пересыщениях. Кроме того, обратимость химической реакции создает возможность управления совершенством и однородностью растущего кристалла. В качестве газов-носителей используют водород, галогены, гатондоводороды, пары воды, сероводород и т.д.
Существуют различные варианты организации процессов химического переноса, различающиеся гидродинамическим режимом потоков. Закрытая система, использующая естественный гидродинамический режим (диффузию и конвекцию), аналогична рассмотренной выше гидротермальной системе. Все стадии процесса и закономерности их протекания совершенно аналогичны. Одиако, поскольку перенос в закрытой системе обычно проводят в горизонтальной ампуле, конвекция в ряде случаев играет менее существенную роль, чем диффузия. Так как в системах газозого переноса удобнее пользоваться величинами не концентраций, а парциальных давлений, то концентрации в этих уравнениях можно выразить с помощью уравнения Клапейрона

где  — число молей; V — объем;
— число молей; V — объем;  — газовая постоянная.
— газовая постоянная.
Более эффективна открытая система с иынужденным гидродинамическим режимом — регулируемым и кондиционированным потоком газа. Под кондиционированным газовым потоком понимается поток, однородный по парциальным давлениям компонентов. В открытой системе при оптимальном скорости потока процесс переноса не является лимитирующей стадией, и скорость роста кристаллов определяется процессами, протекающими на границе раздела фаз, т. е. процессами диффузии через пограничный слой, хсмосорбции и встраивания в кристаллическую решетку. Для рассмотрения этих процессов справедливы положения, относящиеся к конденсации, а также теории зарождения и роста кристаллов из паров.
Следует отметить, что хотя метод переноса в потоке пока не используется для выращивания активных кристаллов квантовой электроники, он, несомненно, является весьма перспективным методом.
| << Предыдущий параграф | Следующий параграф >> |
- Предисловие
- Введение
- Глава первая. ОСНОВНЫЕ ХАРАКТЕРИСТИКИ ИЗЛУЧЕНИЯ И ПРИНЦИП ДЕЙСТВИЯ КВАНТОВЫХ ГЕНЕРАТОРОВ
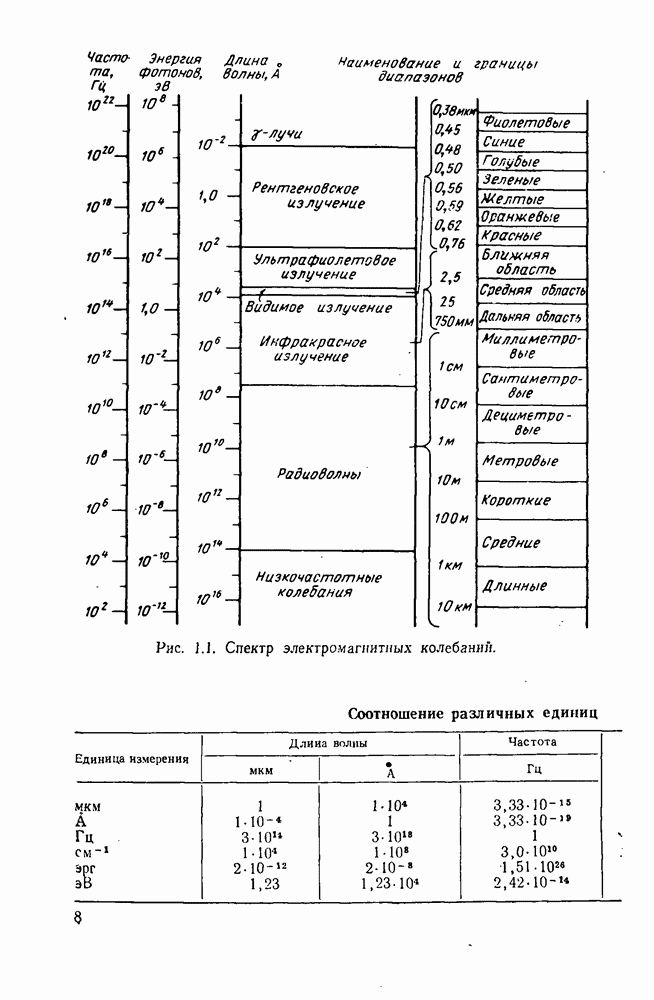
- 1.1. Спектр электромагнитных колебаний
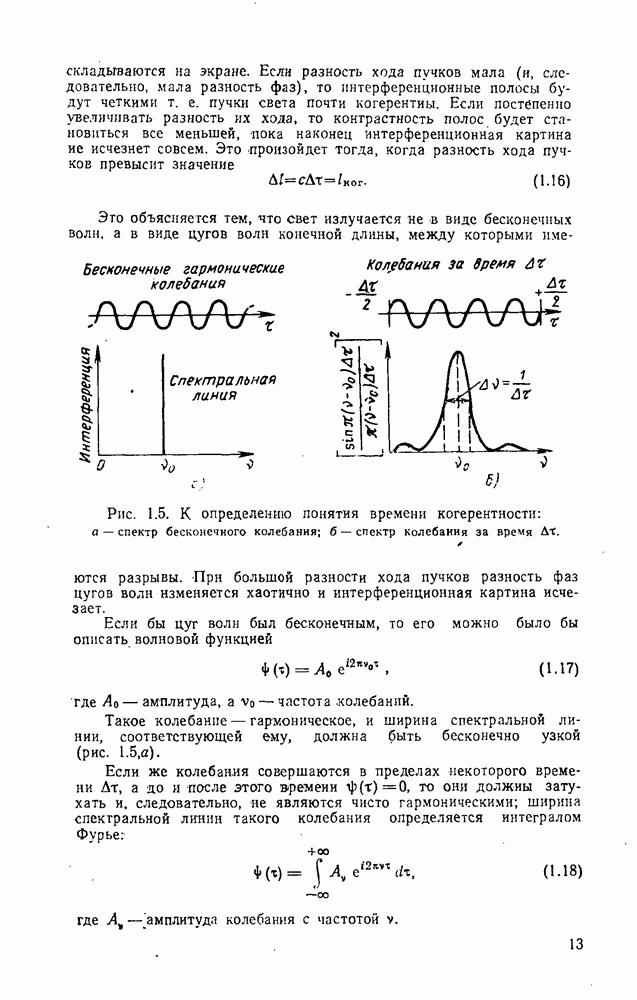
- 1.2. Когерентность
- 1.3. Направленность излучения
- 1.4. Символика энергетических уровней атомов и ионов
- 1.5. Инверсная населенность
- 1.6. Вероятности спонтанных и вынужденных переходов
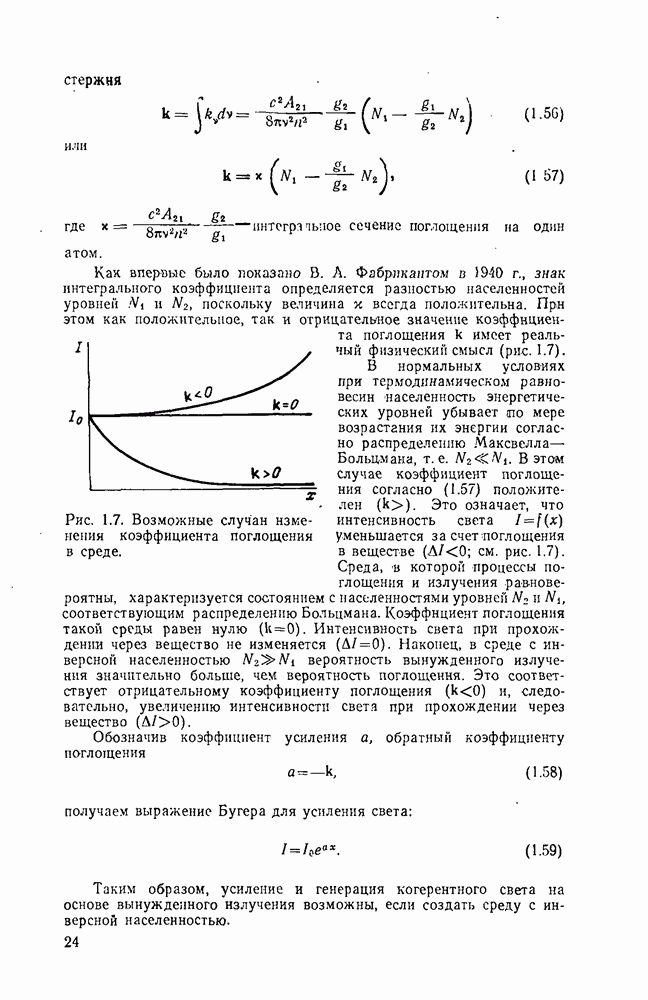
- 1.7. Усиление света при прохождении через вещество
- 1.8. Двухуровневая система
- 1.9. Трехуровневая система
- 1.10. Четырехуровневая система
- 1.11. Возбуждение активного вещества
- 1.12. Оптический резонатор
- 1.13 Условие генерации
- 1.14. Потери энергии в квантовом генераторе
- 1.15. Устройство ОКГ на твердом теле
- Глава вторая. ОБЩИЕ ВОПРОСЫ ТЕХНОЛОГИИ МАТЕРИАЛОВ ТВЕРДОТЕЛЬНЫХ ОКГ
- 2.1. Особенности активного вещества ионных квантовых систем
- 2.2. Особенности технологии твердотельных материалов квантовых генераторов
- 2.3. Физико-химические основы кристаллизации
- 2.3.2. Гетерогенное зародышеобразование
- 2.3.3. Скорость зарождения новой фазы
- 2.3.4. Рост кристаллов
- 2.3.5. Общее кинетическое уравнение кристаллизации
- 2.3.6. Распределение примеси в процессе роста кристалла
- 2.4. Основные методы синтеза и выращивания кристаллов
- 2.4.2. Выращивание из стехиометрических расплавов
- 2.4.3. Методы выращивания кристаллов из растворов
- 2.4.4. Гидротермальный синтез и рост кристаллов
- 2.4.5. Выращивание кристаллов из газовой фазы
- 2.5. Кристалло-химическая классификация материалов твердотельных квантовых генераторов
- Глава третья. КИСЛОРОДНЫЕ СОЕДИНЕНИЯ
- 3.1. Окислы элементов III группы
- 3.1.2. Окислы редкоземельных элементов и иттрия
- 3.3.1. Гранаты
- 3.2. Материалы на основе кислородных соединений элементов VI группы
- 3.2.2. Молибдаты
- 3.3. Материалы на основе кислородных соединений элементов V группы
- 3.3.2. Ниобаты
- 3.3.3. Фосфаты
- Выращивание кристаллов фторфосфата кальция [47]
- Глава четвертая. ФТОРИСТЫЕ СОЕДИНЕНИЯ
- 4.1. Фториды элементов II группы
- 4.2. Фториды редкоземельных элементов
- 4.3. Смешанные фториды
- 4.4. Фториды элементов VII группы
- Глава пятая. СТЕКЛО
- 5.1. Особенности стекла как активного материала ОКГ
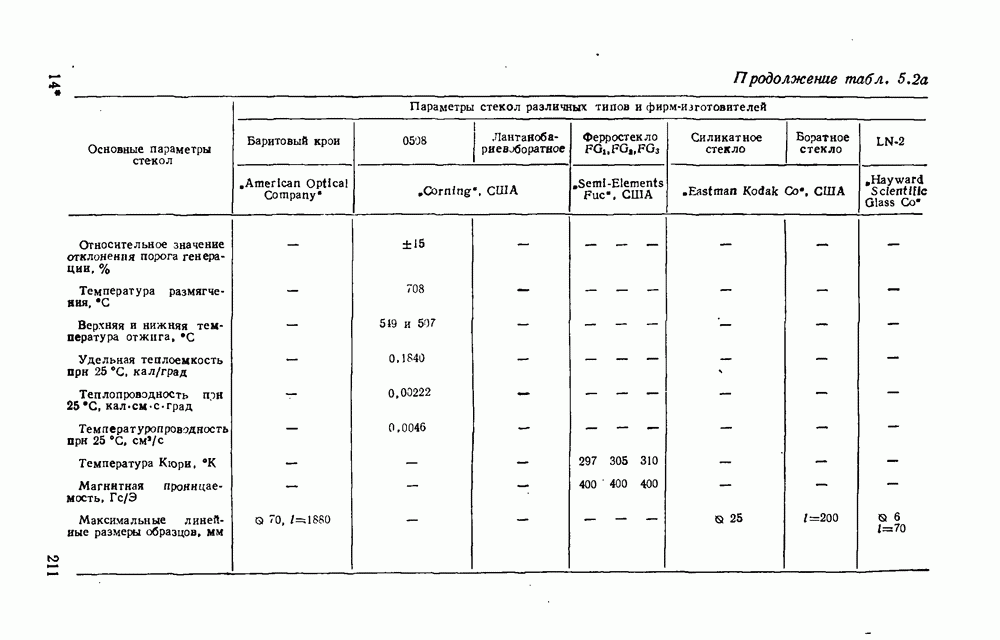
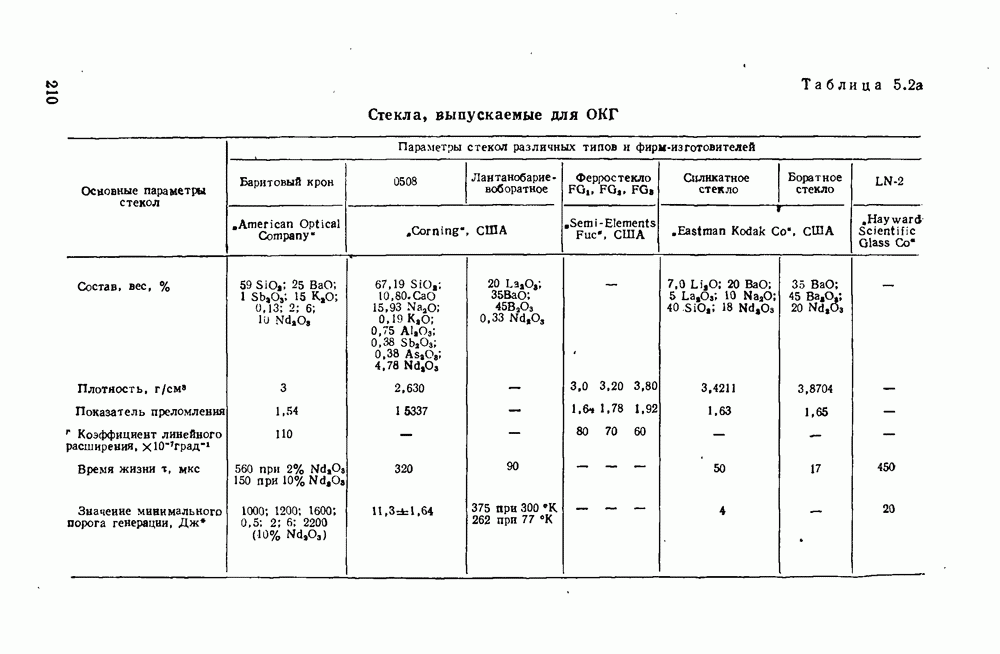
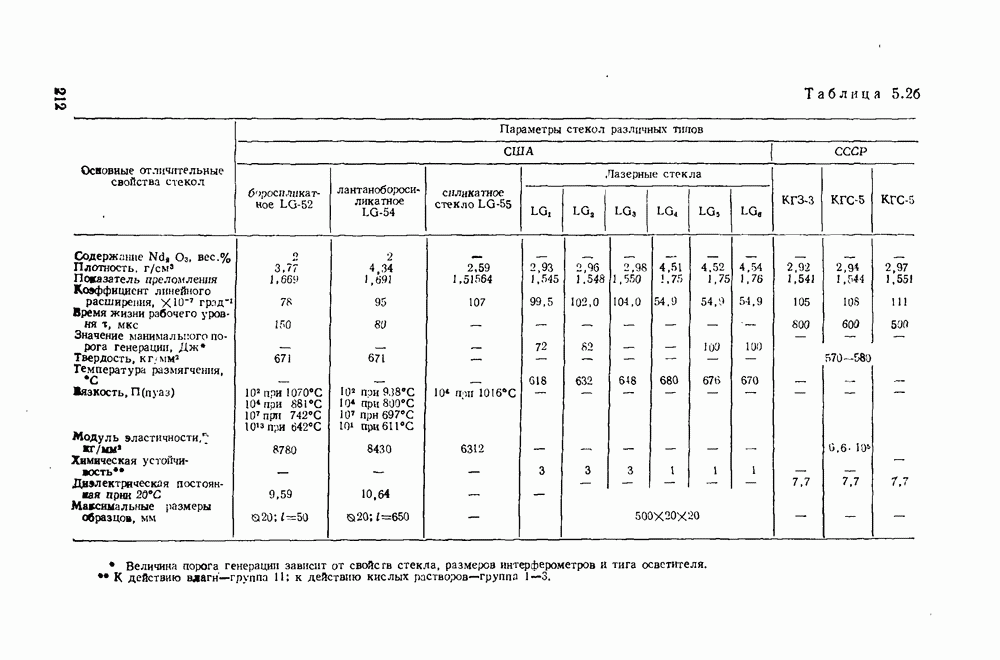
- 5.2. Общая характеристика стекол для ОКГ
- 5.3. Особенности положения атомов активатора в стекле
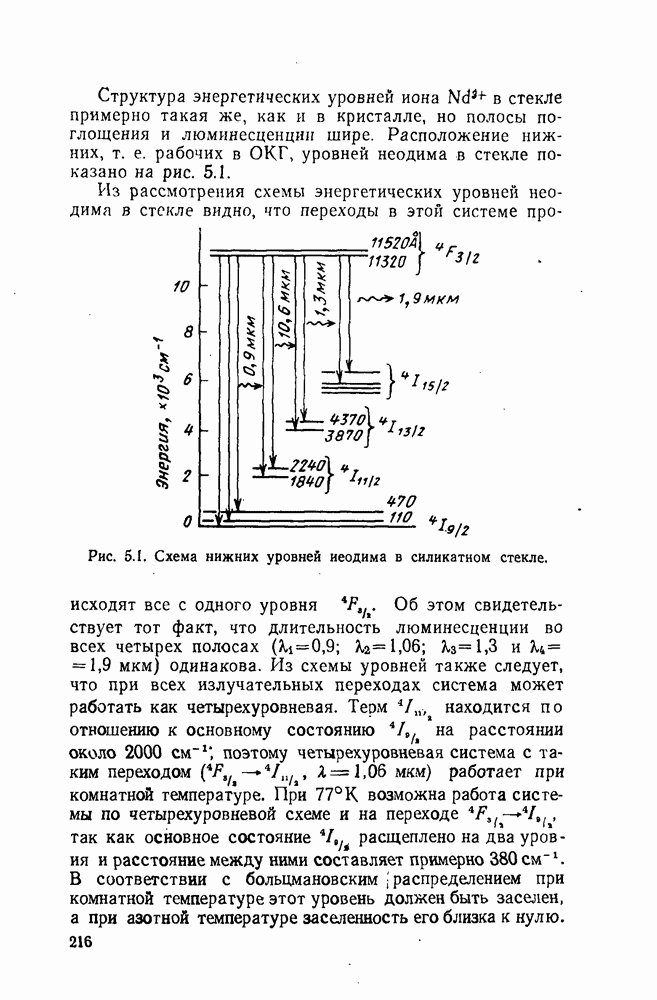
- 5.4. Стекло с неодимом
- Глава шестая. МАТЕРИАЛЫ ЖИДКОСТНЫХ ОКГ
- 6.2. Механизм излучения в органических растворах
- 6.3. Растворы металлоорганических соединений
- 6.4. Растворы органических красителей
- 6.5. Растворы неорганических соединений редкоземельных элементов
- Глава седьмая. ОБЩАЯ ХАРАКТЕРИСТИКА ПОЛУПРОВОДНИКОВЫХ КВАНТОВЫХ ГЕНЕРАТОРОВ (ПКГ)
- 7.2. Основные сведения из теории люминесценции инжекционных ПКГ
- 7.3. Рабочие характеристики инжекционных ПКГ
- 7.3.2. Пространственные свойства
- 7.3.3. Пороговый ток
- 7.3.4. Квантовый выход
- 7.4. Тепловые условия работы лазерного диода
- 7.4.2. Работа в квазинепрерывном режиме
- 7.5. Другие типы ПКГ
- 7.5.1. ПКГ с электронным возбуждением
- 7.5.2. ПКГ с оптической накачкой
- 7.5.3. ПКГ с прямым электрическим возбуждением
- Глава восьмая. АРСЕНИД ГАЛЛИЯ И ТЕХНОЛОГИЯ ИЗГОТОВЛЕНИЯ ДИОДОВ ПКГ
- 8.1. Физические свойства арсенида галлия
- 8.2. Методы выращивания монокристаллов арсенида галлия
- 8.3. Методы изготовления р-n-переходов
- 8.3.2. Эпитаксия из жидкой фазы
- 8.3.3. Эпитаксия из газовой фазы
- 8.4. Изготовление невыпрямляющих низкоомных контактов к арсениду галлия
- 8.5. Изготовление резонатора
- 8.6. Общая технологическая схема изготовления диодов ПКГ
- 8.7. Конструкция ПКГ
- 8.8. Гетероструктуры на основе арсенида галлия
- 8.9. Другие материалы с прямыми переходами
- Глава девятая. МАТЕРИАЛЫ ГАЗОВЫХ ОКГ
- 9.1. Особенности газового активного вещества ОКГ и методы создания инверсной населенности
- 9.2. Газоразрядные ОКГ
- 9.2.2. Ионные газоразрядные ОКГ
- 9.2.3. Молекулярные газоразрядные ОКГ
- 9.3. Газовые ОКГ с оптической накачкой
- 9.4. Химические ОКГ
- Глава десятая. МАТЕРИАЛЫ МОДУЛЯТОРОВ ОПТИЧЕСКОГО ИЗЛУЧЕНИЯ
- 10.1. Некоторые физические основы модуляции оптического излучения
- 10.2. Требования к материалам модуляторов излучения ОКГ
- 10.3. Материалы с линейным электрооптическим эффектом
- 10.3.1. Тетрагональные кристаллы типа KDP
- 10.3.2. Ромбические кристаллы
- 10.3.3. Тригональные кристаллы
- 10.3.4. Кубические кристаллы
- 10.4. Кристаллы с квадратичным электрооптическим эффектом
- Литература