| << Предыдущий параграф | Следующий параграф >> |
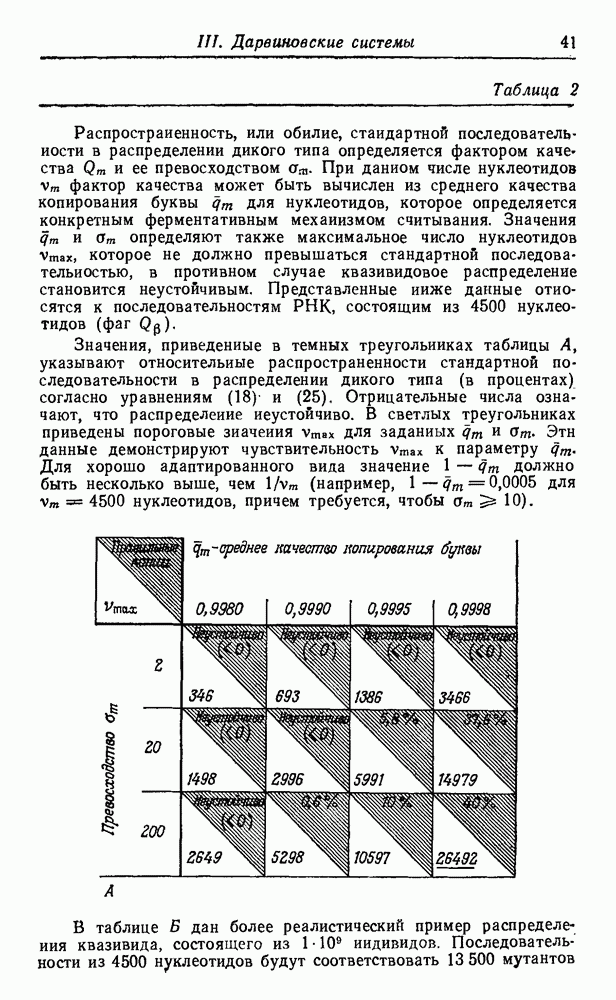
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
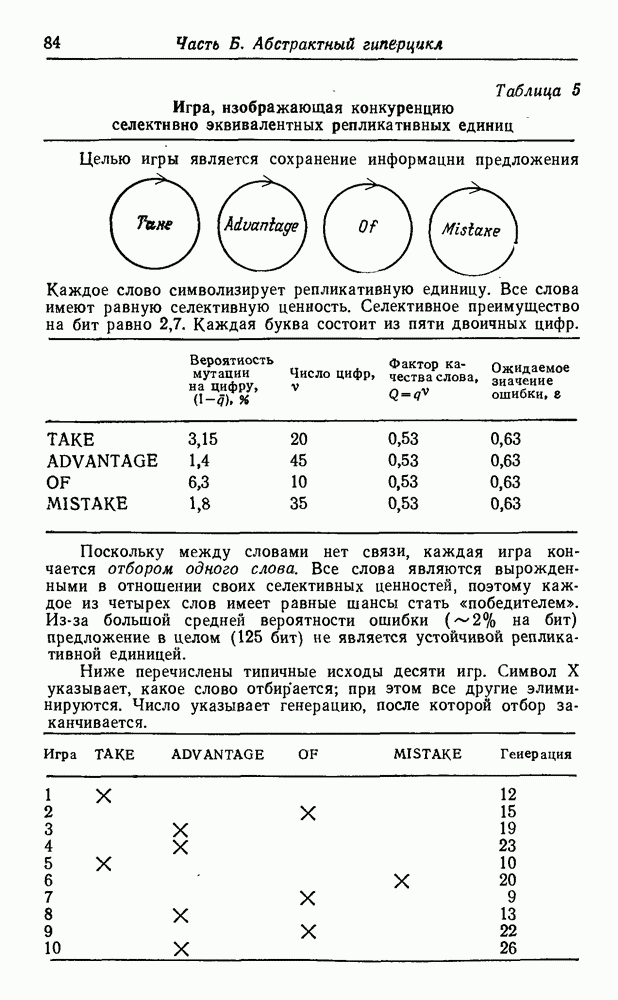
XIV.4. Первичный алфавит аминокислот
Первичные распространенности различных аминокислот могут быть оценены очень надежно. Основные указания, необходимые для оценки вероятностей
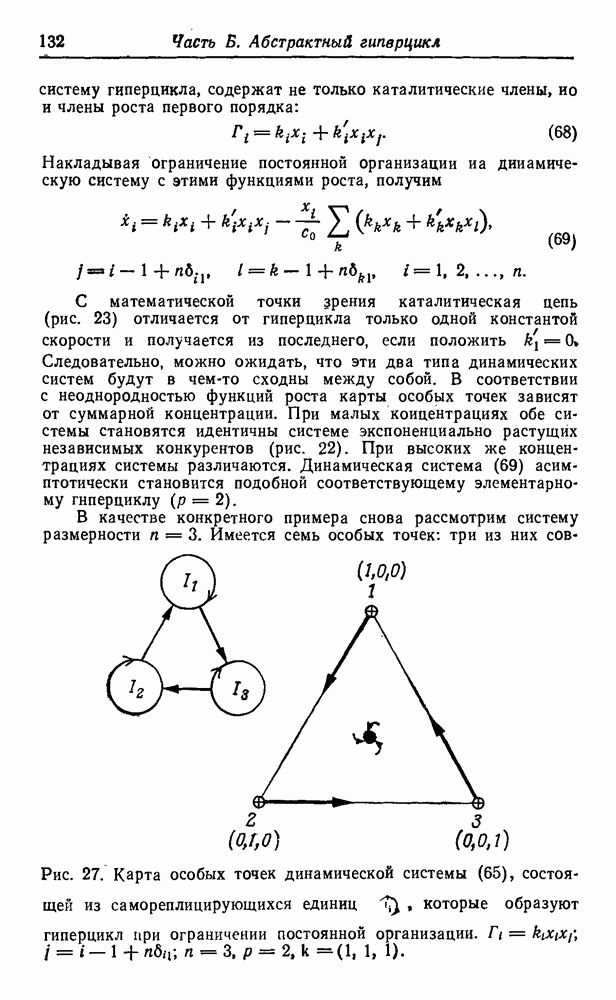
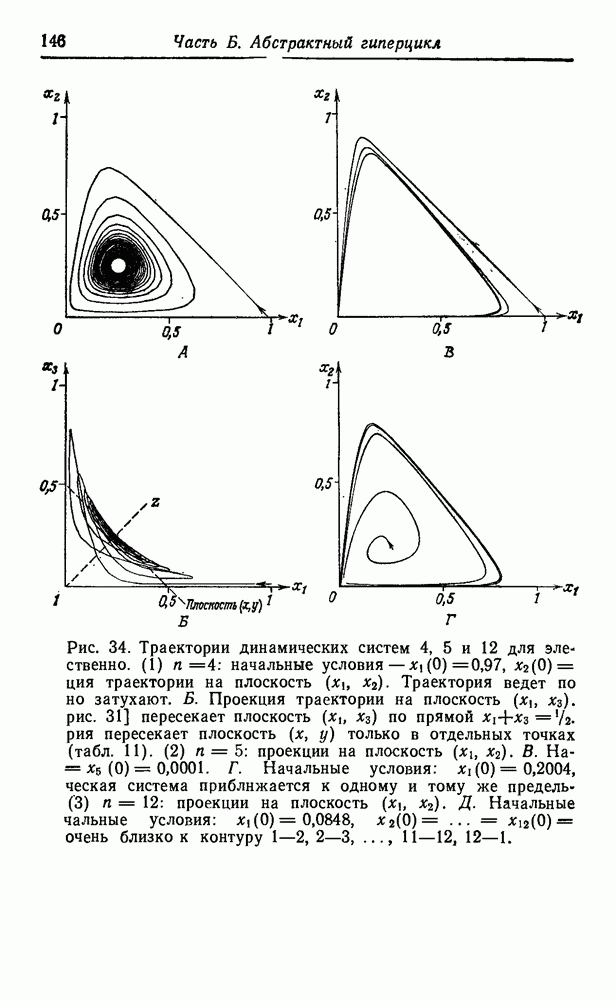
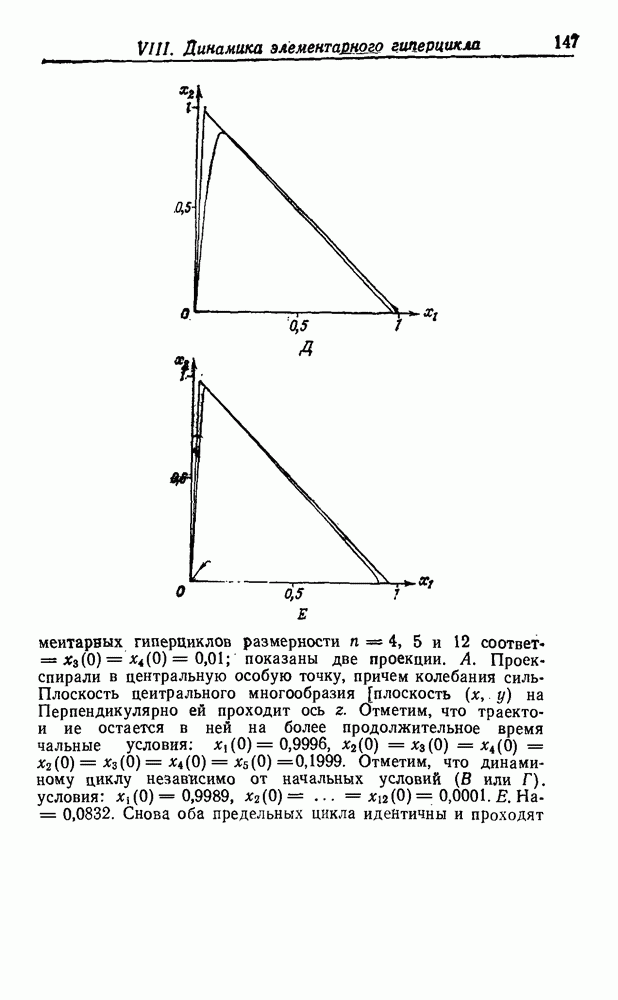
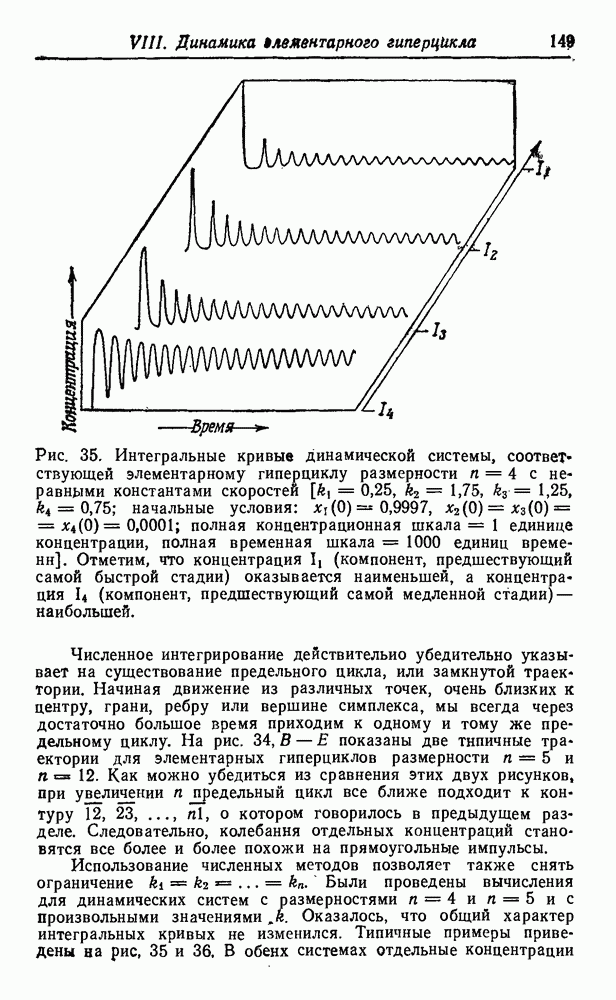
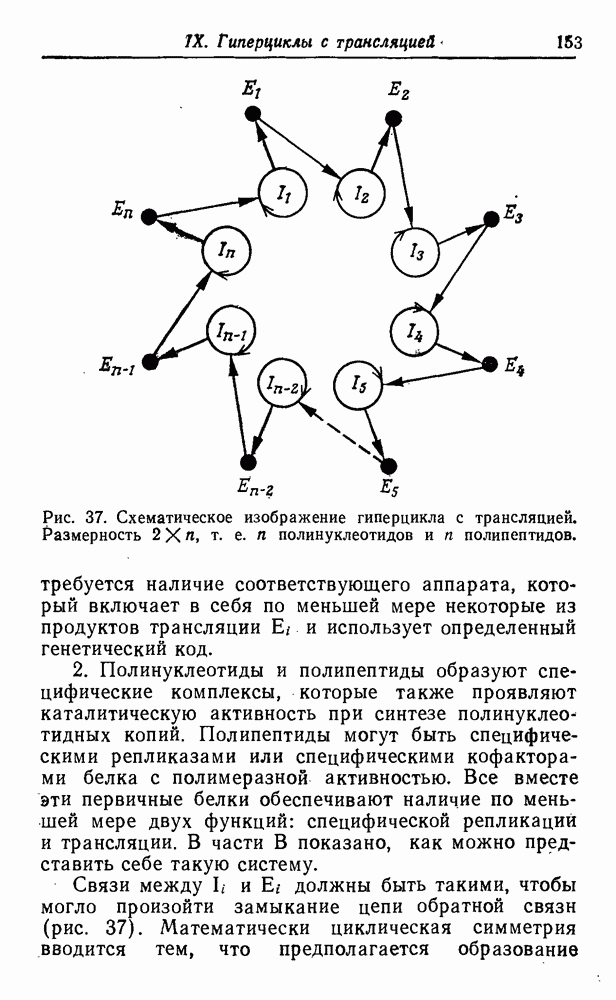
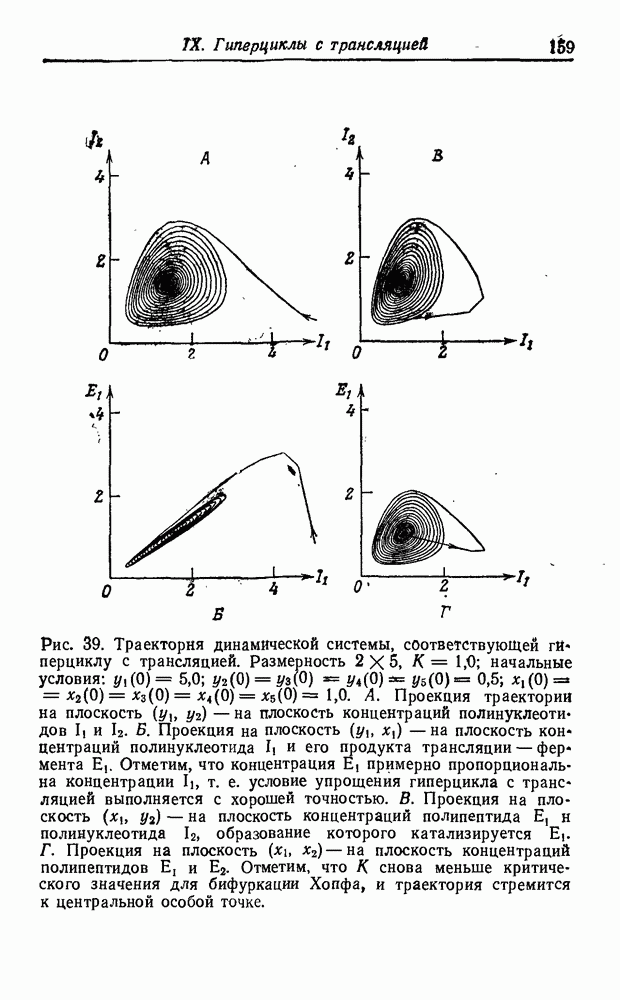
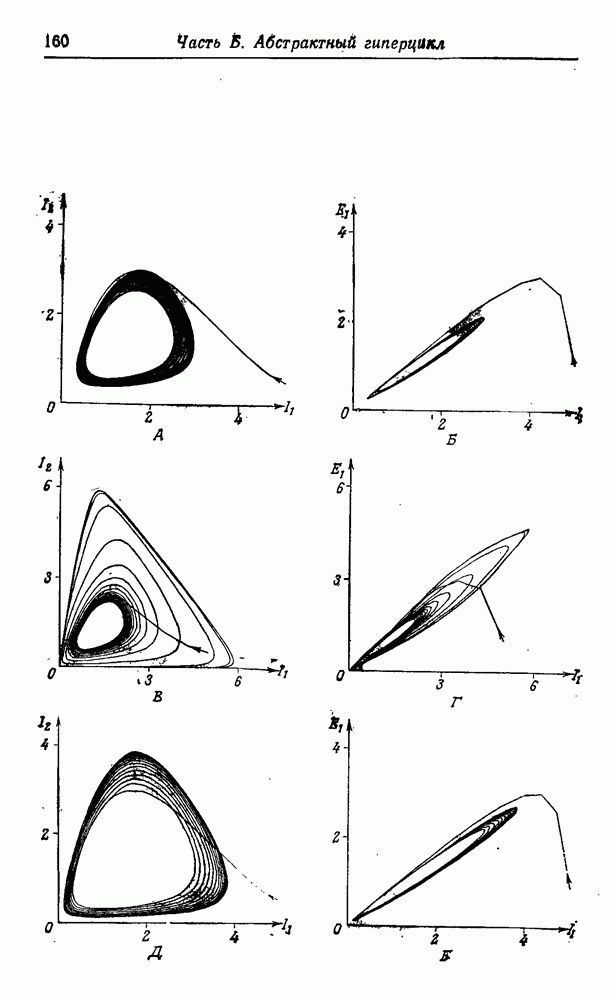
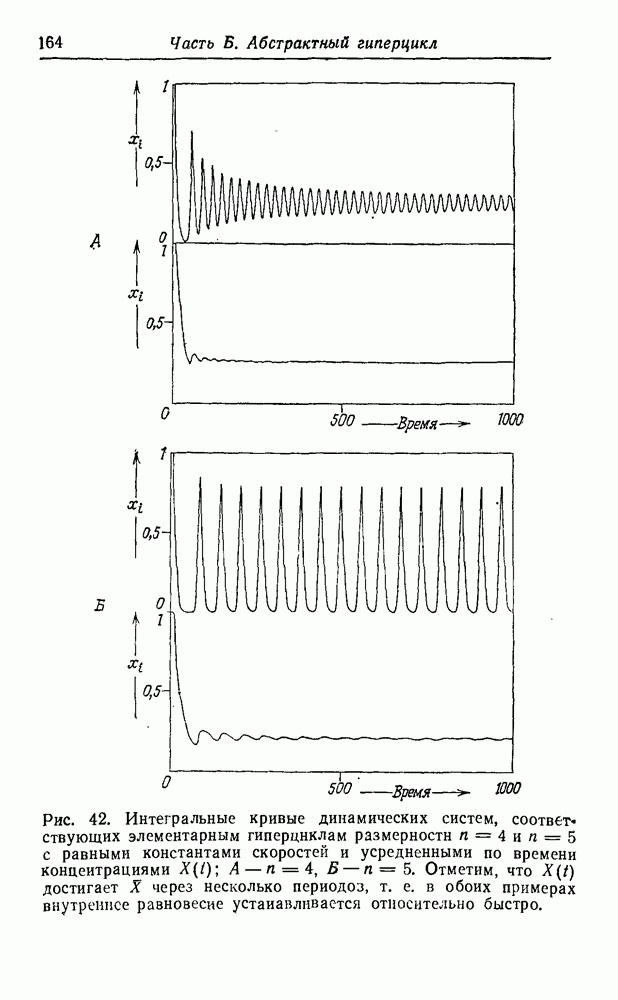
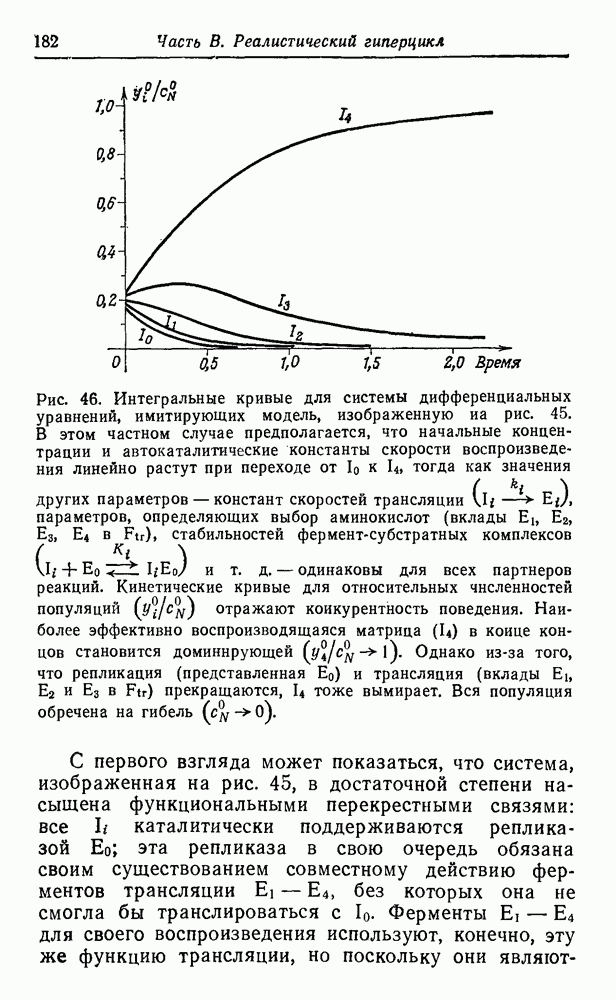
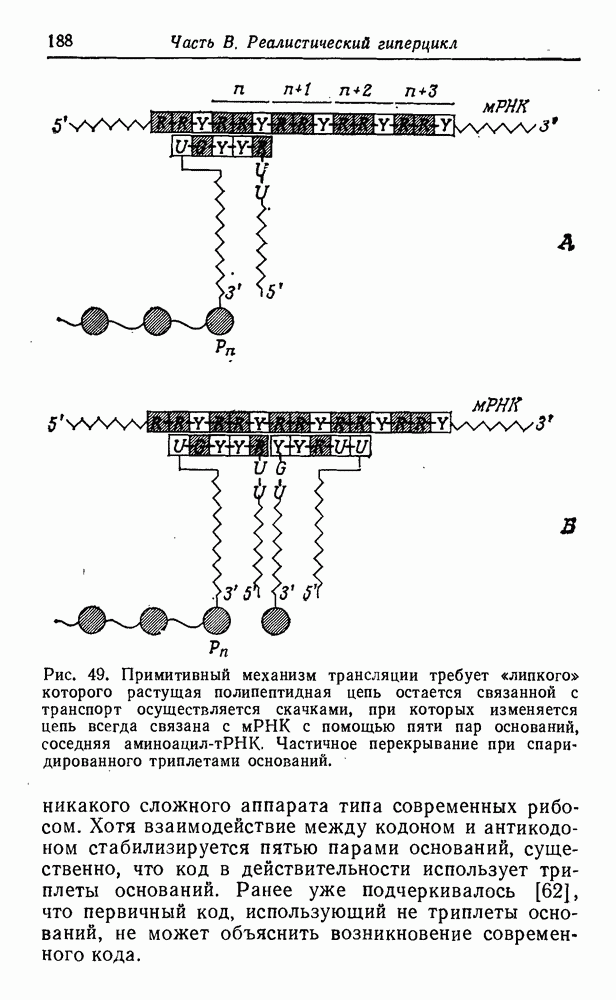
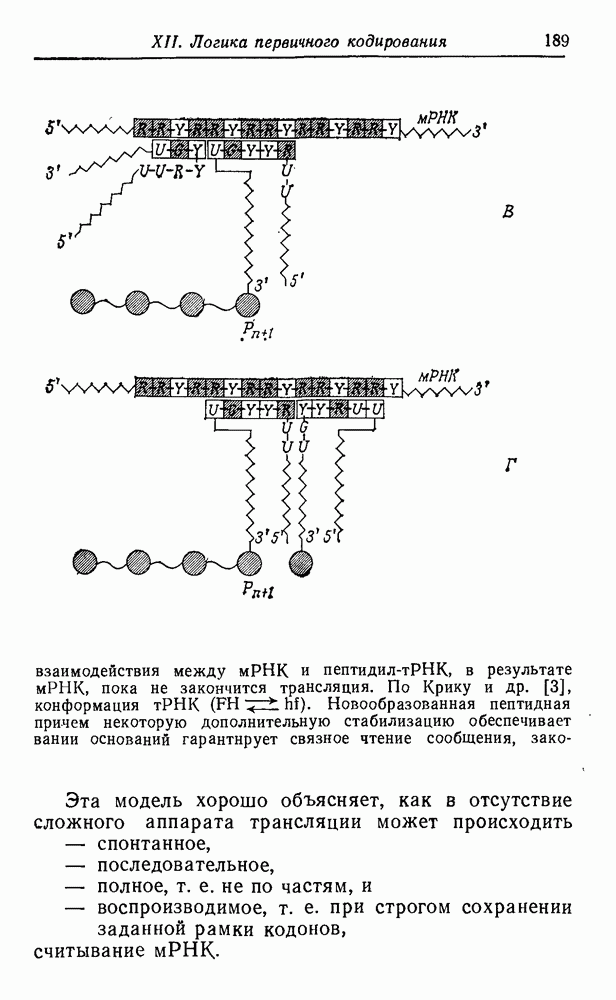
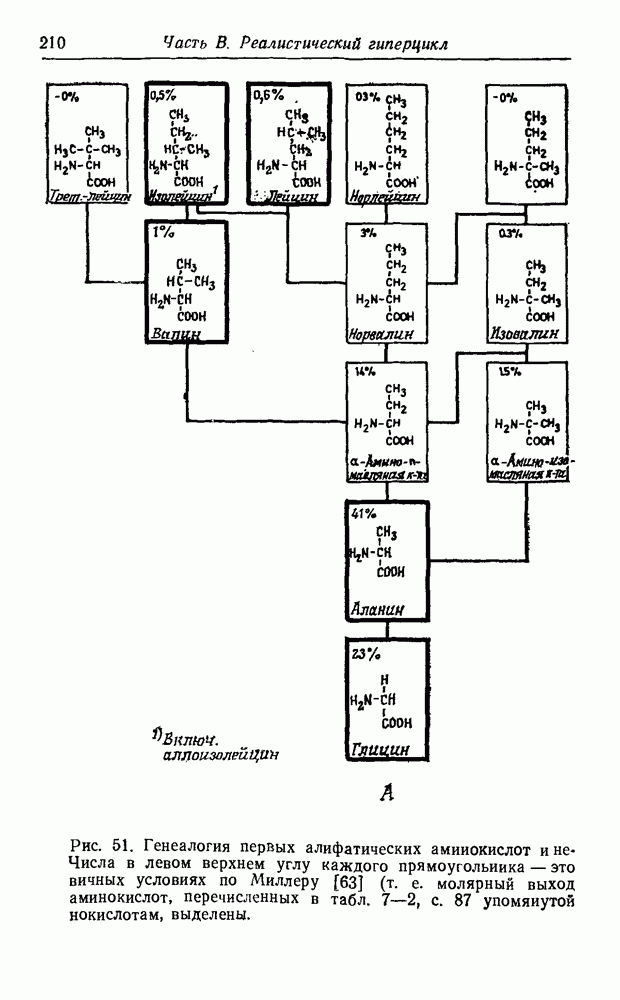
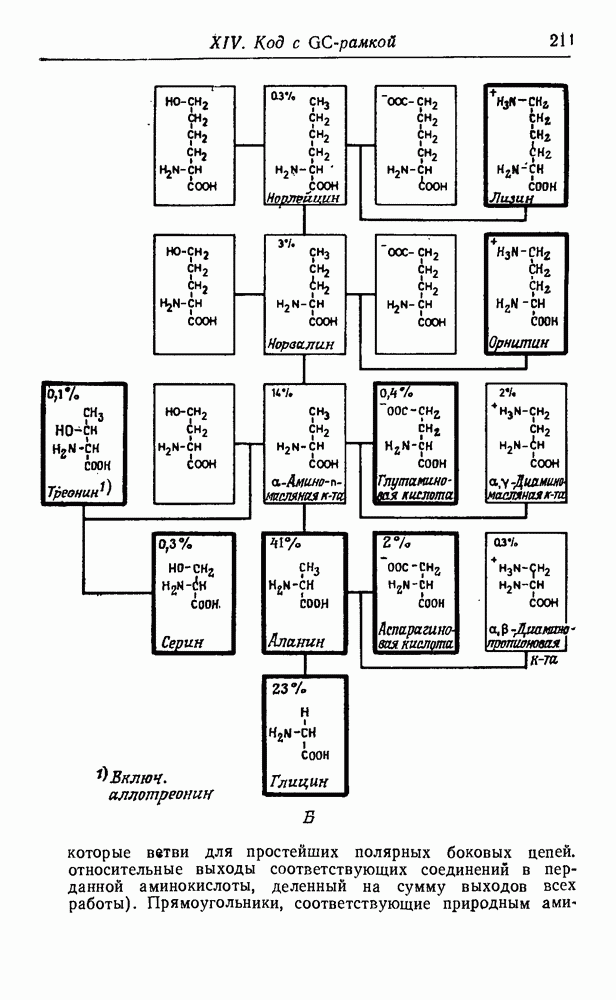
синтеза этих соединений в первичных условиях, дают уже их структура и состав. На рис. 51 приведена «родословная» первых 12 неполярных алифатических аминокислот, а также несколько ветвей, показывающих родственные отношения для простейших полярных боковых цепей. При рассмотрении этой схемы возникают интересные вопросы, касающиеся выбора Природой белкового алфавита.
Две простейшие аминокислоты — глицин и аланин — являются «природными». Видимо, требования гидрофобного взаимодействия легче было выполнить, добавив некоторые высшие гомологи — такие, как валин, лейцин и изолейцин. Возможно, этот выбор был. случайным, а может быть, на него повлияли дискриминирующие взаимодействия с имеющимися адапторами. Среди полярных соединений мы обнаруживаем некоторые алифатические карбоновые кислоты (аспарагиновая и глутаминовая кислота), а также спирты (серин и треонин), но не соответствующие амины  -диаминопропионовая кислота и а, у-диаминомасляная кислота). Из двадцати «природных» аминокислот появляется только второй следующий гомолог (лизин), в то время как интермедиат (ор-нитин) представлен лишь в следовых количествах. Это может объясняться тем, что после активации второй аминогруппы происходит образование лактама или элиминация, которая обрывает полимеризацию. Более того, наличие второй аминогруппы может привести к разветвлению полипептидной цепи (хотя такой же аргумент можно привести и в отношении карбоксильных групп). Для первых функциональных компонентов наличие положительно заряженных боковых депей вполне могло быть необязательным. Даже в воде современных морей концентрация
-диаминопропионовая кислота и а, у-диаминомасляная кислота). Из двадцати «природных» аминокислот появляется только второй следующий гомолог (лизин), в то время как интермедиат (ор-нитин) представлен лишь в следовых количествах. Это может объясняться тем, что после активации второй аминогруппы происходит образование лактама или элиминация, которая обрывает полимеризацию. Более того, наличие второй аминогруппы может привести к разветвлению полипептидной цепи (хотя такой же аргумент можно привести и в отношении карбоксильных групп). Для первых функциональных компонентов наличие положительно заряженных боковых депей вполне могло быть необязательным. Даже в воде современных морей концентрация  достаточно высока
достаточно высока  чтобы вызвать заметное комплексообразование с карбоксильными группами. При восстановительных условиях в океанах могло быть растворено еще больше двухвалентных ионов (например,
чтобы вызвать заметное комплексообразование с карбоксильными группами. При восстановительных условиях в океанах могло быть растворено еще больше двухвалентных ионов (например,  Такие ионы металлов, связанные с карбоксильными группами и все-таки сохранившие свободные координирующие сайты, особенно
Такие ионы металлов, связанные с карбоксильными группами и все-таки сохранившие свободные координирующие сайты, особенно
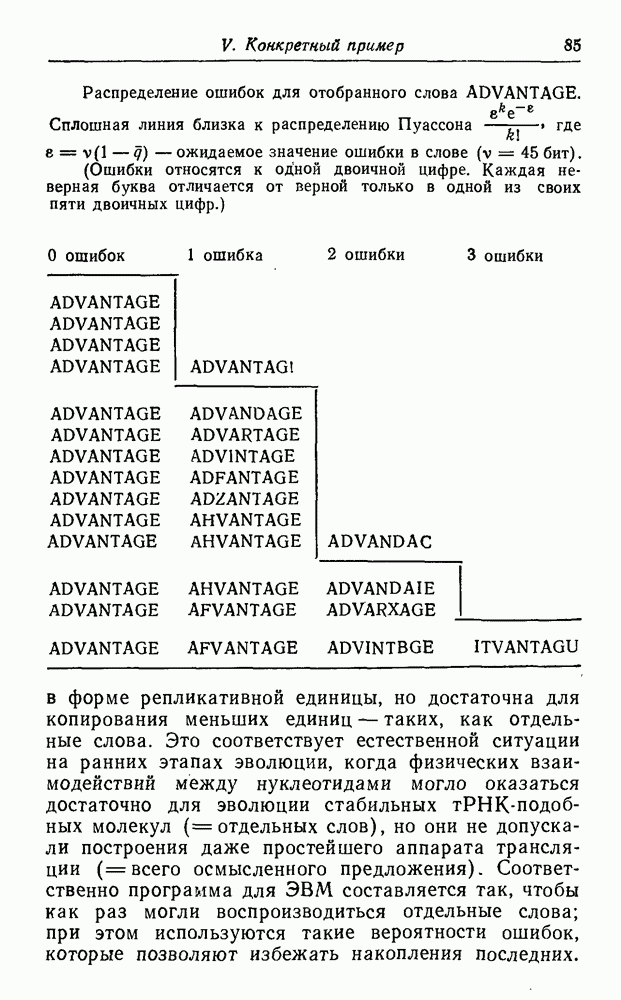
Рис. 51. (см. скан) Генеалогия первых алифатических аминокислот и 
Числа в левом верхнем углу каждого прямоугольника — это вичных условиях по Миллеру [63] (т. е. молярный выход аминокислот, перечисленных в табл. 7—2, с. 87 упомянутой
(см. скан)
некоторые ветви для простейших полярных боковых цепей, относительные выходы соответствующих соединений в перданной аминокислоты, деленный на сумму выходов всех работы). Прямоугольники, соответствующие природным аминокислотам, выделены.
важны для облегчения взаимодействий между ранними белками и (отрицательно заряженными) полинуклеотидами. С этой точки зрения боковые цепи, содержащие отрицательно заряженные лиганды, кажутся более необходимыми, чем боковые цепи с положительными зарядами.
«Природные» аминокислоты, не представленные на рис. 51, имеют значительно более сложные боковые цепи, и поэтому их концентрации в первичном бульоне были сравнительно низки.
Предположения, основанные на данных о структуре и составе аминокислот, великолепно согласуются с результатами экспериментов, имитирующих предбиологический синтез указанных соединений (Миллер и др.; см. обзор в [63]). Выходы, полученные для природных аминокислот (как впрочем и для других ветвей генеалогического древа), примерно соответствуют величинам, ожидаемым из чисто химических данных (см. численные значения на рис. 51); в ходе этих экспериментов было выявлено также много других интересных деталей. Более того, эти результаты находятся в хорошем согласии с данными, полученными из анализа метеоритов [69, 70], которые отражают встречаемость аминокислот в межзвездном пространстве. Табл. 16 содержит сводку данных (взятых из работы [63]), имеющих отношение к предмету нашей дискуссии.
Первичный бульон без сомнения был очень богат глицином и аланином. В опытах Миллера эти аминокислоты образуются примерно в двадцатикратном избытке по сравнению с любой другой природной аминокислотой. Следующие два места на шкале распространенностей природных аминокислот занимают аспарагиновая кислота и валин, причем между ними и лейцином, глутаминовой кислотой, серином, изолейцином, треонином и пролином имеется большой разрыв.
Есть все основания предполагать, что соответствия между кодонами и аминокислотами в действительности возникали в порядке уменьшения
распространенностей последних. Если глицин и аланин по своим распространенностям далеко превосходят все другие аминокислоты, то они вполне могли быть закодированы раньше всех, сразу же после того, как сформировались химические механизмы активации.
Таблица 16 (см. скан)
Выход природных аминокислот при имитации предбиологического синтеза и содержание их в метеорите Мерчисон. В первом столбце перечислены аминокислоты содержащиеся в белках, Во втором столбце приведены типичные результаты экспериментов Миллера (из обзора [63]). Эти данные были получены, когда через метан ( в присутствии азота и воды пропускали искровой разряд. Суммарный выход аминокислот (включая те, которые не содержатся в белках) по углероду был равен 1,9%, соответствующие выходы глицина и аланина — 0,26 и 0,71%. Аналогичные результаты были получены и в других условиях, причем в наибольшем количестве из природных аминокислот присутствовали обычно
в присутствии азота и воды пропускали искровой разряд. Суммарный выход аминокислот (включая те, которые не содержатся в белках) по углероду был равен 1,9%, соответствующие выходы глицина и аланина — 0,26 и 0,71%. Аналогичные результаты были получены и в других условиях, причем в наибольшем количестве из природных аминокислот присутствовали обычно  Данные по содержанию аминокислот в метеорите получены Оро и др. [70] И Квенволденом и др. [69]. Во всех случаях
Данные по содержанию аминокислот в метеорите получены Оро и др. [70] И Квенволденом и др. [69]. Во всех случаях  -изомеры составляли почти точно 50%. Другие ссылки можно найти в работе [63].
-изомеры составляли почти точно 50%. Другие ссылки можно найти в работе [63].
(см. скан)
В таком случае первыми предбиологическими полипептидами — как инструктированными, так и неинструктированными — были, вероятно, в основном, сополимеры  со случайными замещениями
со случайными замещениями
другими аминокислотами, среди которых, по-видимому, встречались и такие, которые в конечном счете так и не стали кодироваться.
Соответствие между распространенностями природных аминокислот и очередностью их сопоставления первым четырем кодонам поразительно. Следует подчеркнуть, что наш выбор кодонов основан исключительно на аргументах, относящихся к структуре нуклеиновых кислот. Не только первые четыре кодона с GC-рамкой точно отвечают распространенностям соответствующих аминокислот, но и четыре следующих RNY-кодона сопоставляются именно с теми аминокислотами, которые — за исключением аспарагина — представлены в таблице Миллера со значительными выходами. Однако возникает вопрос — является ли соответствие  аспарагину первичным или же (как подсказывает близкое сходство с кодоном лизина) этот кодон сначала отвечал одной из низших гомологичных диаминокислот, которые в таблице Миллера имеют обращенный порядок выходов по сравнению с аспарагиновой кислотой
аспарагину первичным или же (как подсказывает близкое сходство с кодоном лизина) этот кодон сначала отвечал одной из низших гомологичных диаминокислот, которые в таблице Миллера имеют обращенный порядок выходов по сравнению с аспарагиновой кислотой  -диамино-масляная кислота) и глутаминовой кислотой
-диамино-масляная кислота) и глутаминовой кислотой  -диаминопропионовая кислота). Следует признать, что в отсутствие дополнительных данных все предположения по этому поводу могут носить только спекулятивный характер.
-диаминопропионовая кислота). Следует признать, что в отсутствие дополнительных данных все предположения по этому поводу могут носить только спекулятивный характер.
В этой связи важны также некоторые новые результаты, полученные из анализа аминокислотных последовательностей нуклеотид-связывающих ферментов, которые, по-видимому, существовали еще более  лет назад в доклеточных условиях [71, 72]. Эти данные позволяют предположить наличие последовательности-предшественника нуклеотид-связывающей поверхности, которая включала аминокислоты валин, аспарагиновую (и глутаминовую) кислоты, аланин и глицин, а кроме того, изолейцин, лизин и треоиин (хотя эти данные в действительности относятся к более поздней стадии доклеточной эволюции, нежели та, которая обсуждается в этой работе).
лет назад в доклеточных условиях [71, 72]. Эти данные позволяют предположить наличие последовательности-предшественника нуклеотид-связывающей поверхности, которая включала аминокислоты валин, аспарагиновую (и глутаминовую) кислоты, аланин и глицин, а кроме того, изолейцин, лизин и треоиин (хотя эти данные в действительности относятся к более поздней стадии доклеточной эволюции, нежели та, которая обсуждается в этой работе).
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРОВ ПЕРЕВОДА
- ЧАСТЬ А. ВОЗНИКНОВЕНИЕ ГИПЕРЦИКЛА
- II. Что такое гиперцикл?
- III. Дарвиновские системы
- III.2. Необходимые предпосылки возникновения дарвиновских систем
- III.3. Динамика отбора
- III.4. Концепция квазивида
- III.5. Реалистические аппроксимации
- III.6. Обобщения
- III.7. Информационное содержание квазивида
- IV. Порог ошибок и эволюция
- IV.2. Экспериментальные исследования с РНК-содержащими фагами
- IV.3. Репликация ДНК
- IV.4. Первые репликативные единицы
- IV.5. Необходимость возникновения гиперциклов
- ЧАСТЬ Б. АБСТРАКТНЫЙ ГИПЕРЦИКЛ
- VI. Общая классификация динамических систем
- VI.2. Неограниченный рост
- VI.3. Ограниченный рост и отбор
- VI.4. Внутреннее уравновешивание в растущих системах
- VII. Исследование особых точек самоорганизующихся сетей реакций
- VII.2. Топологические свойства
- VII.3. Адекватное пространство: симплекс концентраций
- VII.4. Исследование нормальных мод
- VII.5. Растущие системы
- VII.6. Анализ конкретных систем
- VII.7. Исследование особых точек гиперциклов
- VIII. Динамика элементарного гиперцикла
- VIII.2. Численное интегрирование
- X. Гиперциклы с трансляцией
- IX.2. Кинетические уравнения
- IX.3. Численные решения
- X. Сети гиперциклов
- Х.2. Паразитная связь и каталитические сети
- Х.3. Иерархия связей между гиперциклами
- ЧАСТЬ В. РЕАЛИСТИЧЕСКИЙ ГИПЕРЦИКЛ
- XII. Логика первичного кодирования
- XII.2. Код RNY
- XIII. Физика первичного кодирования
- XIII.2. Распространенность нуклеотидов
- XIII.3. Стабильность комплементарных структур
- XIV. Код с GC-рамкой
- XIV.2. «Апериодическая линейная GC-решетка»
- XIV.3. От GNC к RNY
- XIV.4. Первичный алфавит аминокислот
- XV. Гиперциклическая организация раннего аппарата трансляции
- XVI. Десять вопросов, касающихся наших самых ранних молекулярных предков и тех следов, которые они оставили в биосинтетическом аппарате современных клеток
- XVI.2. Что означает селективное преимущество для молекулы?
- XVI.3. Почему нужна гиперциклическая организация отдельных мутантных генов, а не один постоянно растущий геном?
- XVI.4. Необходимы ли при старте тРНК?
- XVI.5. Дают ли современные тРНК какие-либо указания на свое происхождение
- XVI.6. Как в информационной РНК могли возникнуть кодонные паттерны без запятых?
- XVI.7. Какими были первые функционально активные белки?
- XVI.8. Необходимы ли при старте синтетазы?
- XVI.9. Какими были первые ферменты?
- XVI.10. Почему же в конечном счете — клетки с объединенными геномами?
- XVII. Реалистические граничные условия
- XVIII. Непрерывность эволюции