| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
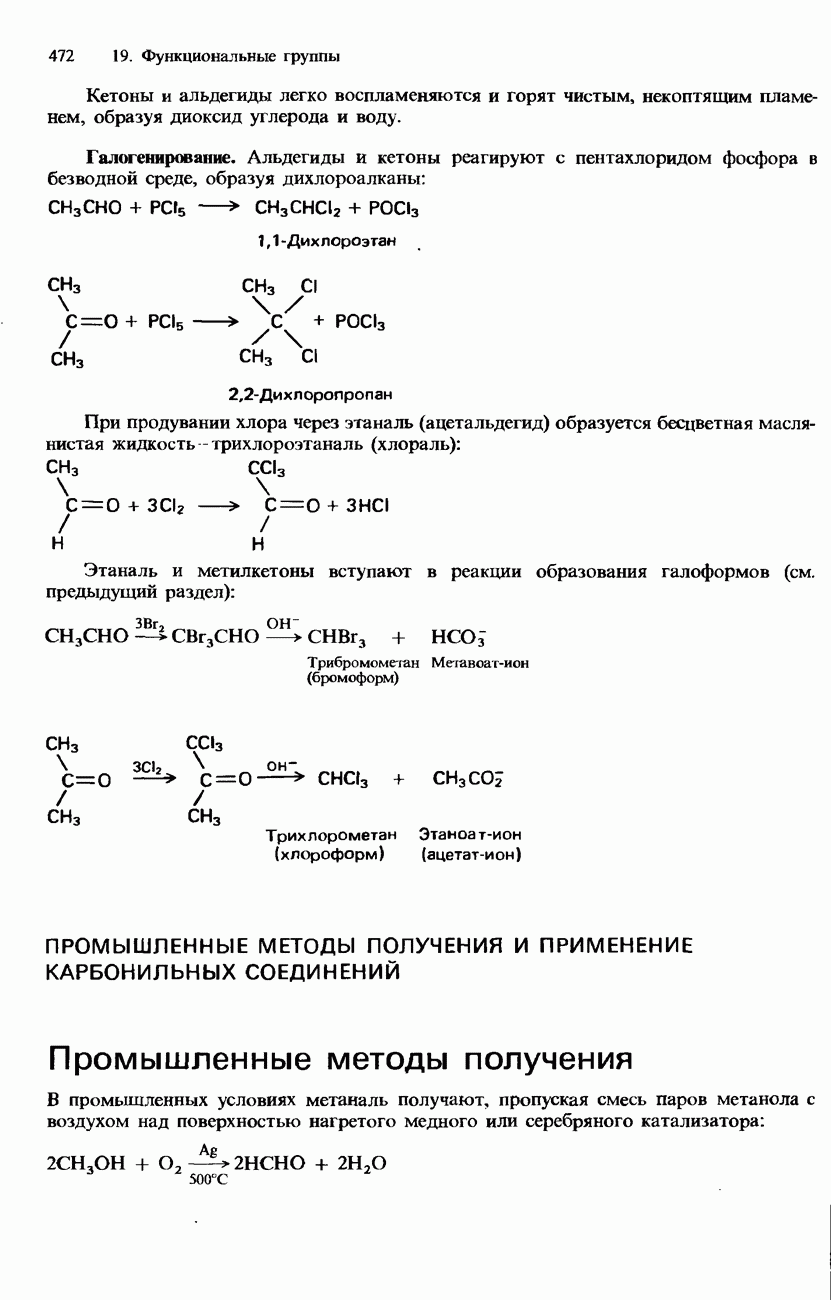
АМИНОКИСЛОТЫ
Аминокислотами называются бифункциональные соединения, содержащие карбоксильные группы с кислотными свойствами и аминогруппы с основными свойствами. Аминокислоты, входящие в состав белков, преимущественно относятся к  -аминокислотам. Так называются аминокислоты, в которых и карбоксильная группа, и аминогруппа присоединены к одному и тому же атому углерода. Простейшим примером а-аминокислоты является глицин:
-аминокислотам. Так называются аминокислоты, в которых и карбоксильная группа, и аминогруппа присоединены к одному и тому же атому углерода. Простейшим примером а-аминокислоты является глицин:

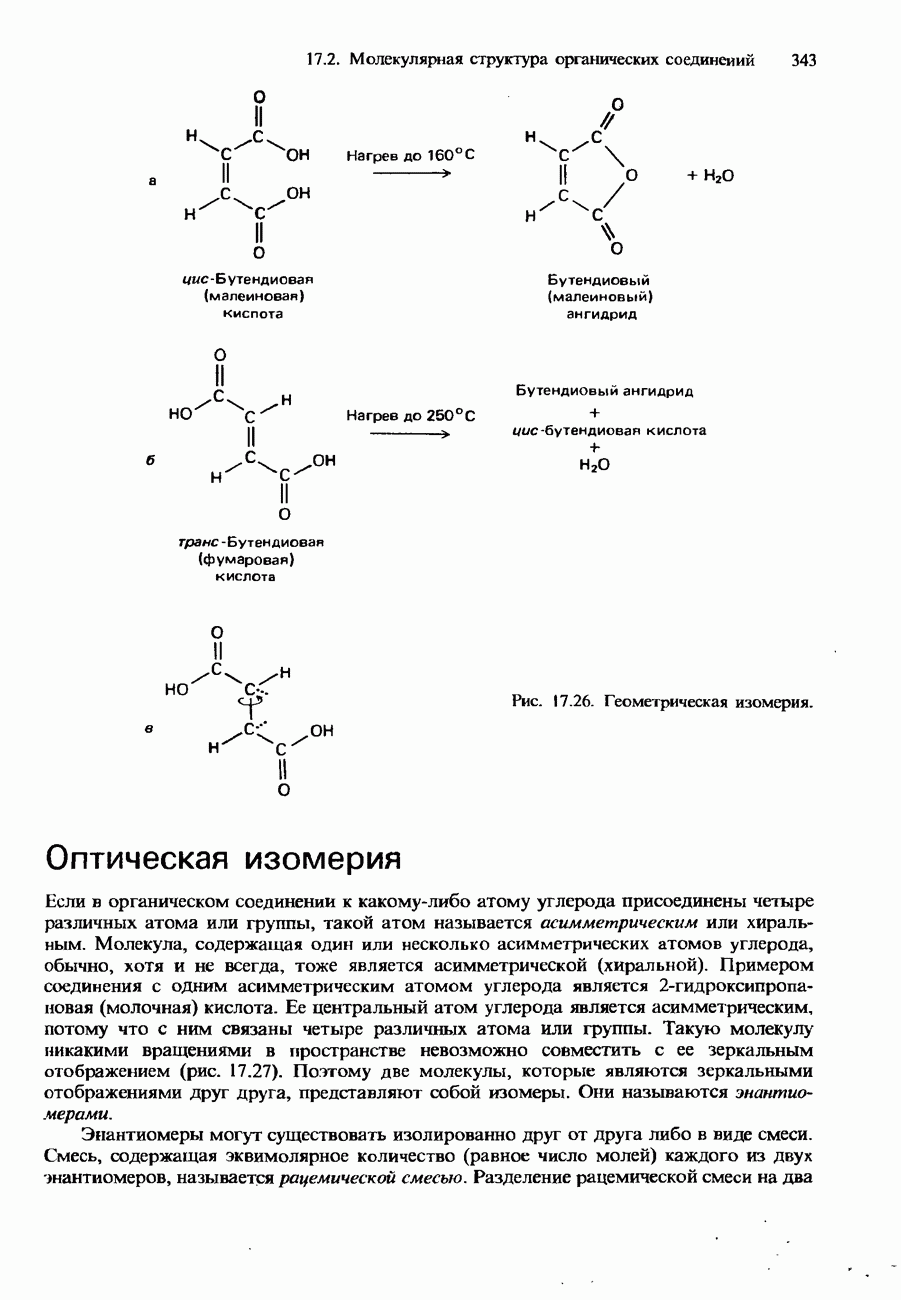
а-Атом углерода во всех а-аминокислотах, за исключением глицина, является асимметрическим. Поэтому все а-аминокислоты, за исключением глицина, обладают хиральностью (см. разд. 17.2) и, следовательно, обнаруживают оптическую изомерию.

Оптические изомеры аланина Все аминокислоты, входящие в состав белков, представляют собой L-изомеры.
Аминокислоты содержат первичные аминогруппы. В качестве примера приведем глицин. Пролин, который тоже встречается в белках, включает вторичную аминогруппу как часть гетероциклической структуры. Он тоже представляет собой аминокислоту.

Двадцать аминокислот (18  -аминокислот и две иминокислоты) входят в состав почти всех белков. Эти аминокислоты отличаются одна от другой своими боковыми цепями. При записи структурных формул белков или полипептидов принято кратко обозначать каждую аминокислоту условным трехбуквенным символом, В табл. 20.2 приведены тривиальные названия аминокислот, которыми обычно пользуются на практике. Однако каждая аминокислота имеет и систематическое название. Например, глицин имеет систематическое название аминоэтановая (аминоуксусная) кислота, а аланин - систематическое название 2-аминопропионовая кислота.
-аминокислот и две иминокислоты) входят в состав почти всех белков. Эти аминокислоты отличаются одна от другой своими боковыми цепями. При записи структурных формул белков или полипептидов принято кратко обозначать каждую аминокислоту условным трехбуквенным символом, В табл. 20.2 приведены тривиальные названия аминокислот, которыми обычно пользуются на практике. Однако каждая аминокислота имеет и систематическое название. Например, глицин имеет систематическое название аминоэтановая (аминоуксусная) кислота, а аланин - систематическое название 2-аминопропионовая кислота.
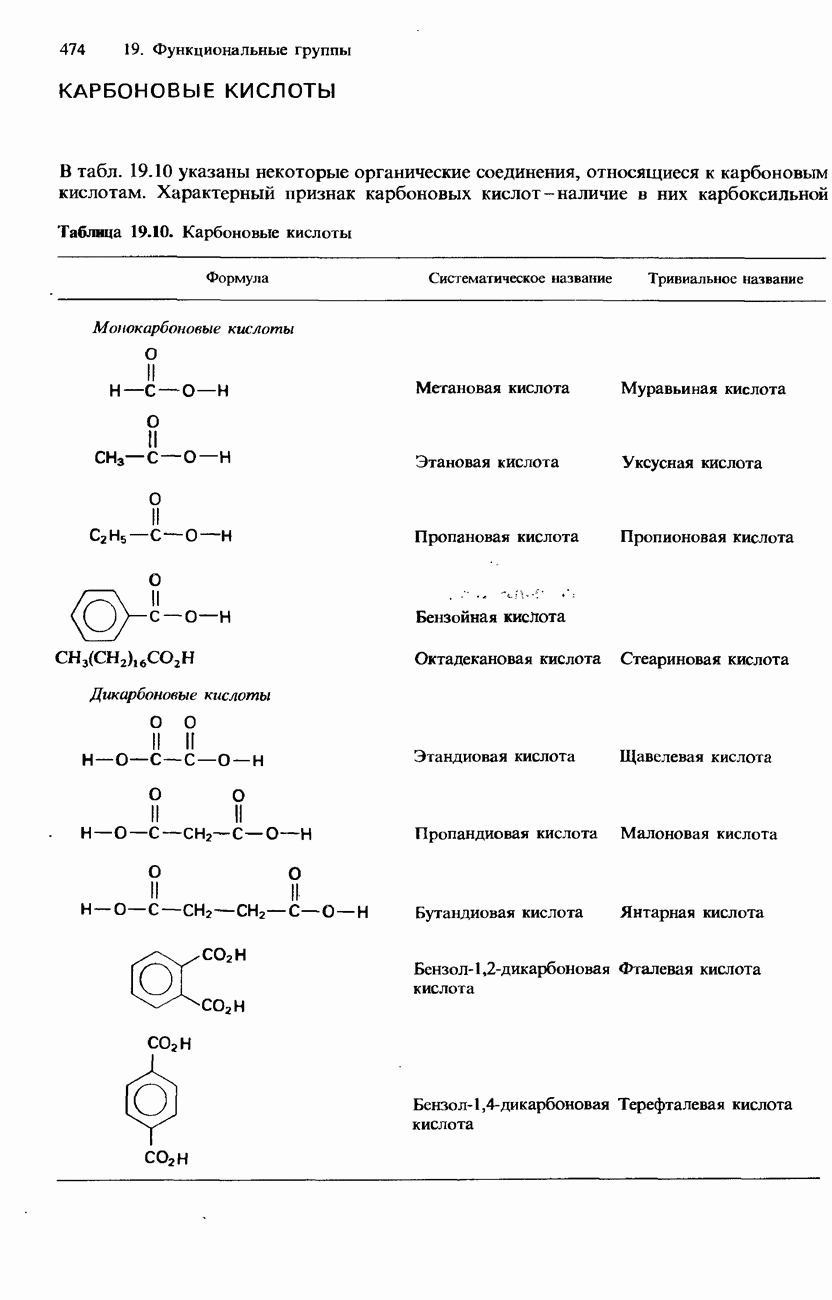
Таблица 20.2. Некоторые аминокислоты общей формулы 

Двенадцать из 20 аминокислот, входящих в состав белков, могут синтезироваться в человеческом организме. Остальные восемь должны содержаться в нашей диете. Они называются незаменимыми аминокислотами.
Аминокислоты подразделяются на нейтральные, основные и кислотные в зависимости от того, сколько они содержат аминогрупп и карбоксильных групп. Например, глицин и аланин принадлежат к числу нейтральных аминокислот, поскольку в каждой из них содержится по одной аминогруппе и по одной карбоксигруппе. Аспарагиновая кислота, содержащая две карбоксигруппы, представляет собой кислотную аминокислоту. В отличие от этого лизин, который содержит две аминогруппы, представляет собой основную аминокислоту.
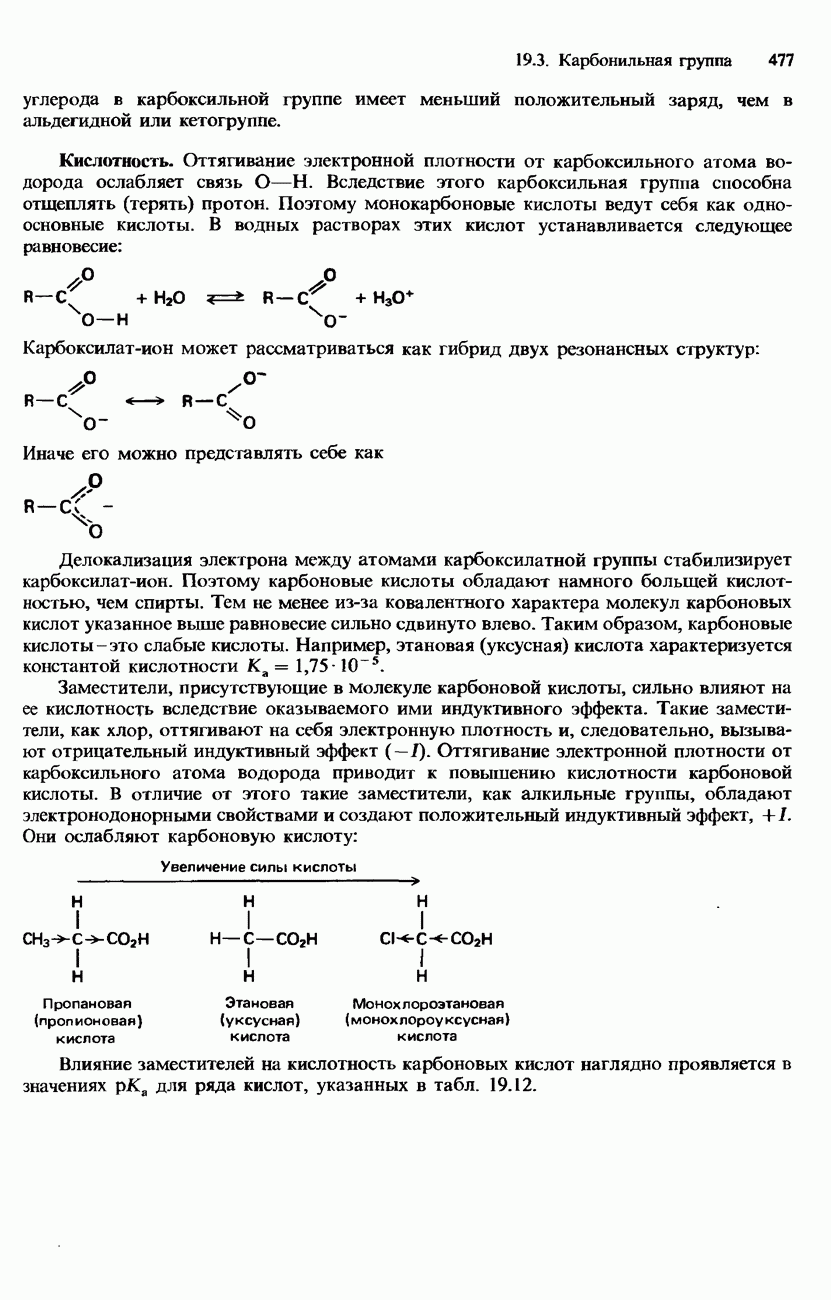
В водных растворах аминокислоты могут существовать в различных ионных формах в зависимости от pH и от того, принадлежат ли они к нейтральным, кислотным либо основным аминокислотам. В водном растворе нейтральной аминокислоты, в зависимости от pH, могут содержаться следующие формы:

Форма, в которой одновременно присутствуют положительный и отрицательный заряды, называется цвиттер-ион. Такая форма является преобладающей в нейтральном растворе. Значение pH, при котором аминокислота не имеет результирующего заряда, называется изоэлектрической точкой. Каждой аминокислоте соответствует характерная для нее изоэлектрическая точка. Для многих  -аминокислот изоэлектрическая точка находится вблизи pH 6,00. Например, изоэлектрические точки глицина и аланина имеют значения 5,97 и 6,02 соответственно.
-аминокислот изоэлектрическая точка находится вблизи pH 6,00. Например, изоэлектрические точки глицина и аланина имеют значения 5,97 и 6,02 соответственно.
Разделение и аналитическое обнаружение аминокислот
Смесь аминокислот можно разделить следующими методами: 1) хроматографии на бумаге (см. разд. 6.3), 2) ионообменной хроматографии (см. разд. 8.2), 3) электрофореза (см. разд. 9.1).
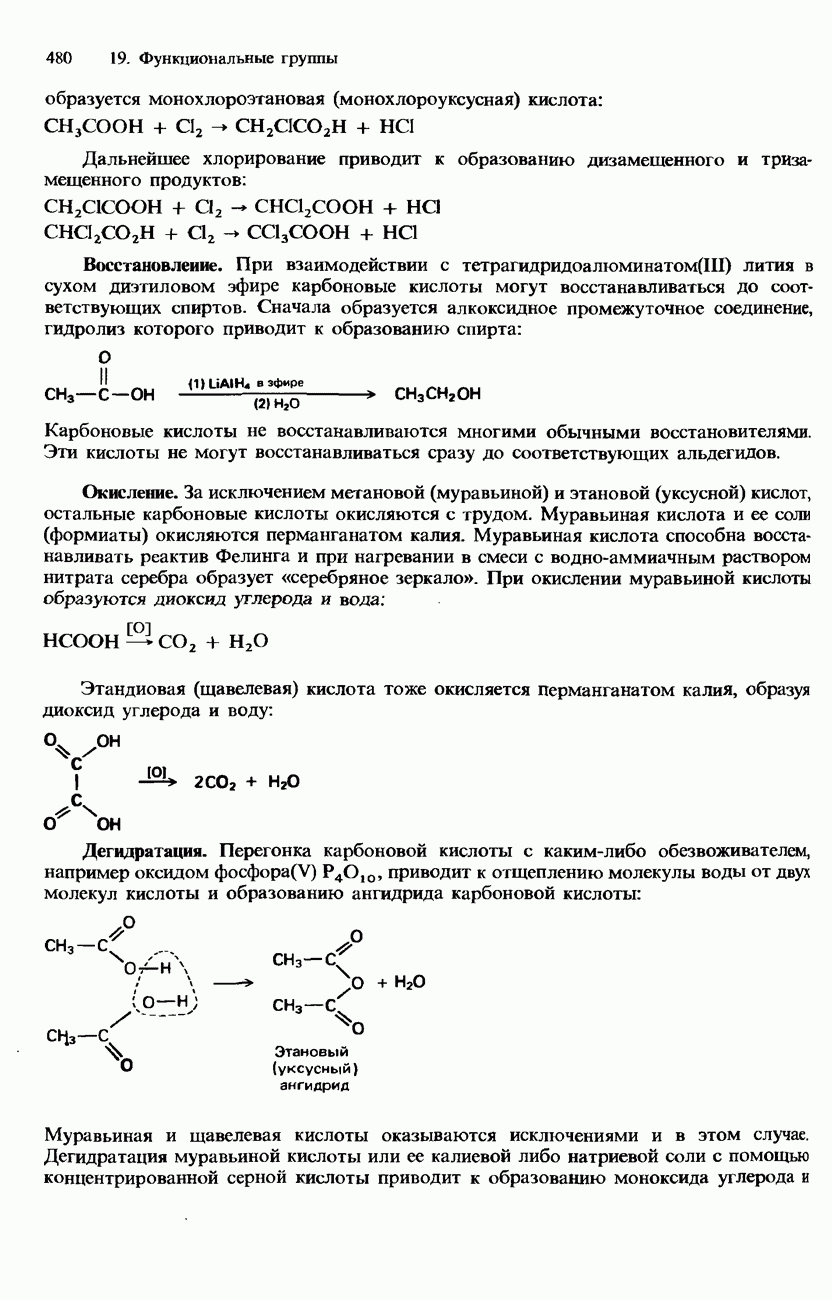
Для аналитического обнаружения аминокислот используется нингидрин:

Нингидрин окисляет аминокислоты, в результате чего образуются окрашенные продукты. Большинство а-аминокислог при взаимодействии с нингидрииом образуют продукты синего или фиолетового цвета. Пролин при реакции с нингидрином дает желтую окраску.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- 11. ПЕРИОДИЧЕСКИЙ ЗАКОН
- 11.1 Периодичность
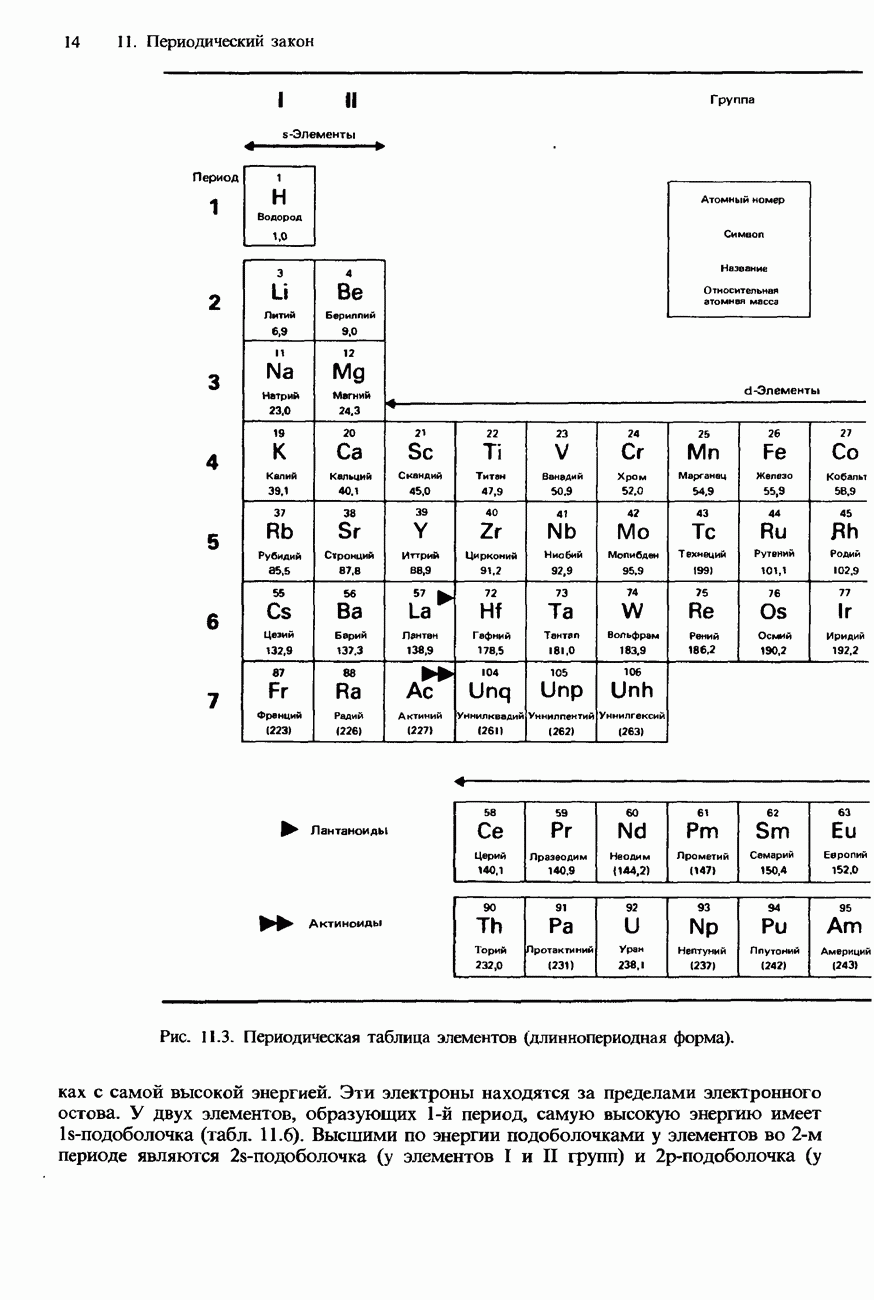
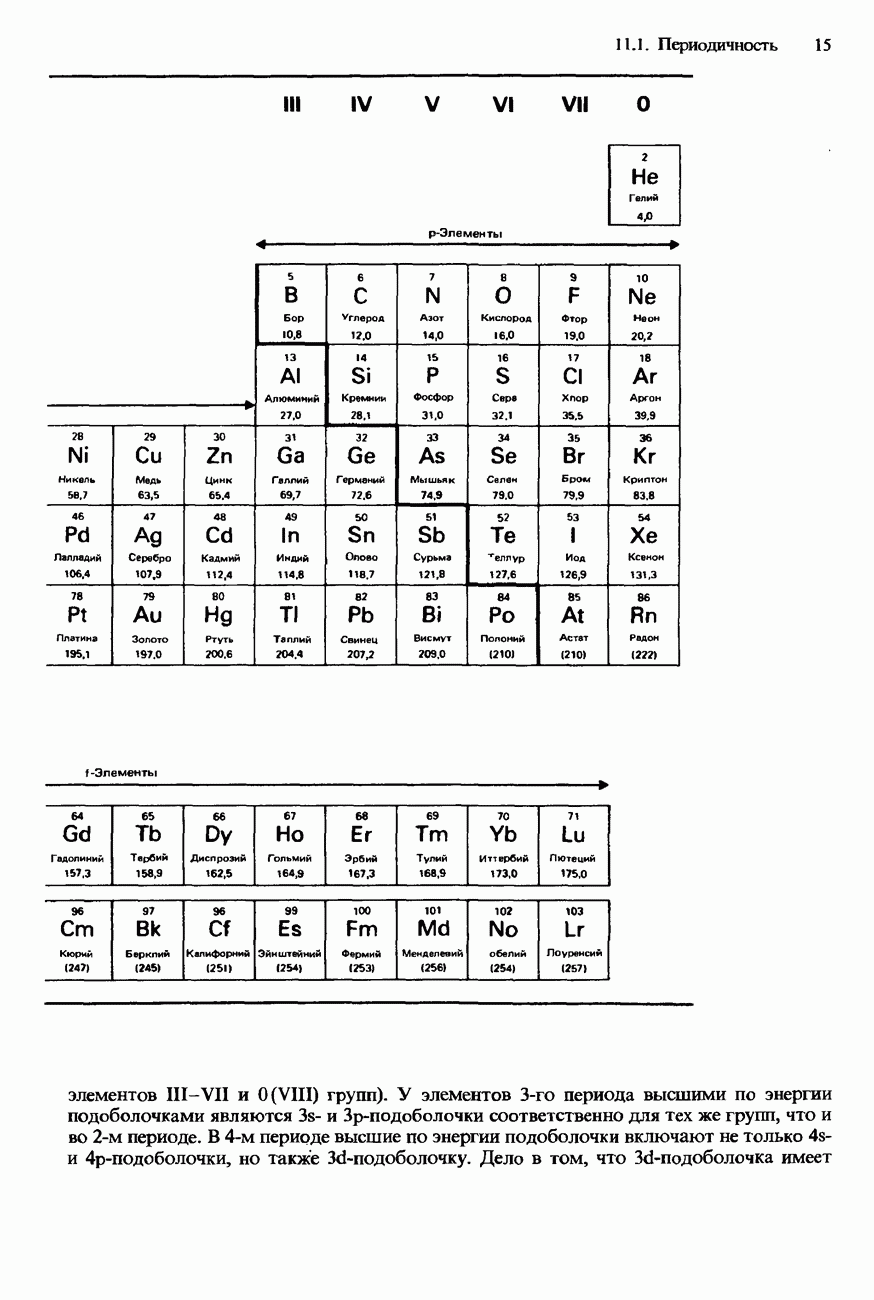
- СОВРЕМЕННАЯ ФОРМА ПЕРИОДИЧЕСКОЙ ТАБЛИЦЫ
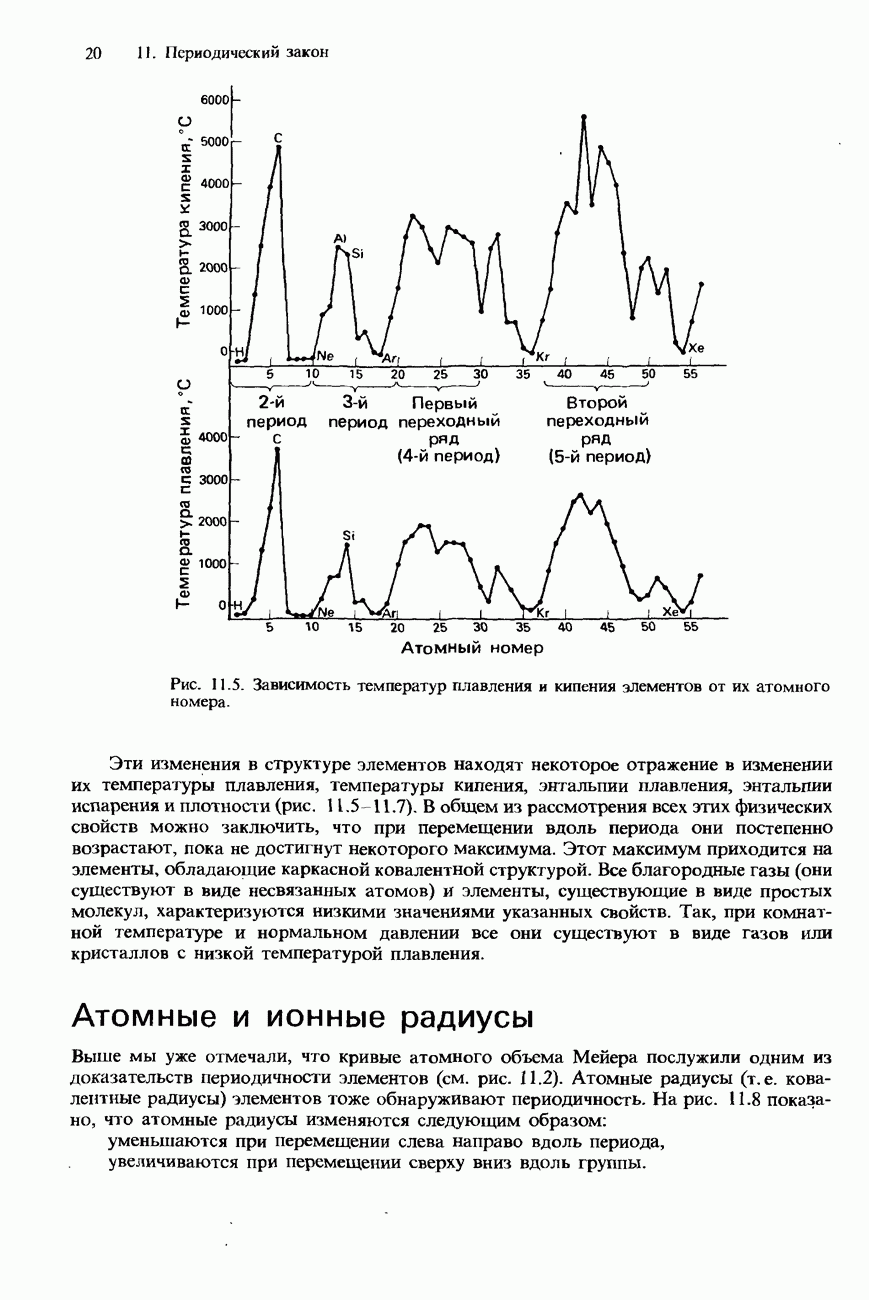
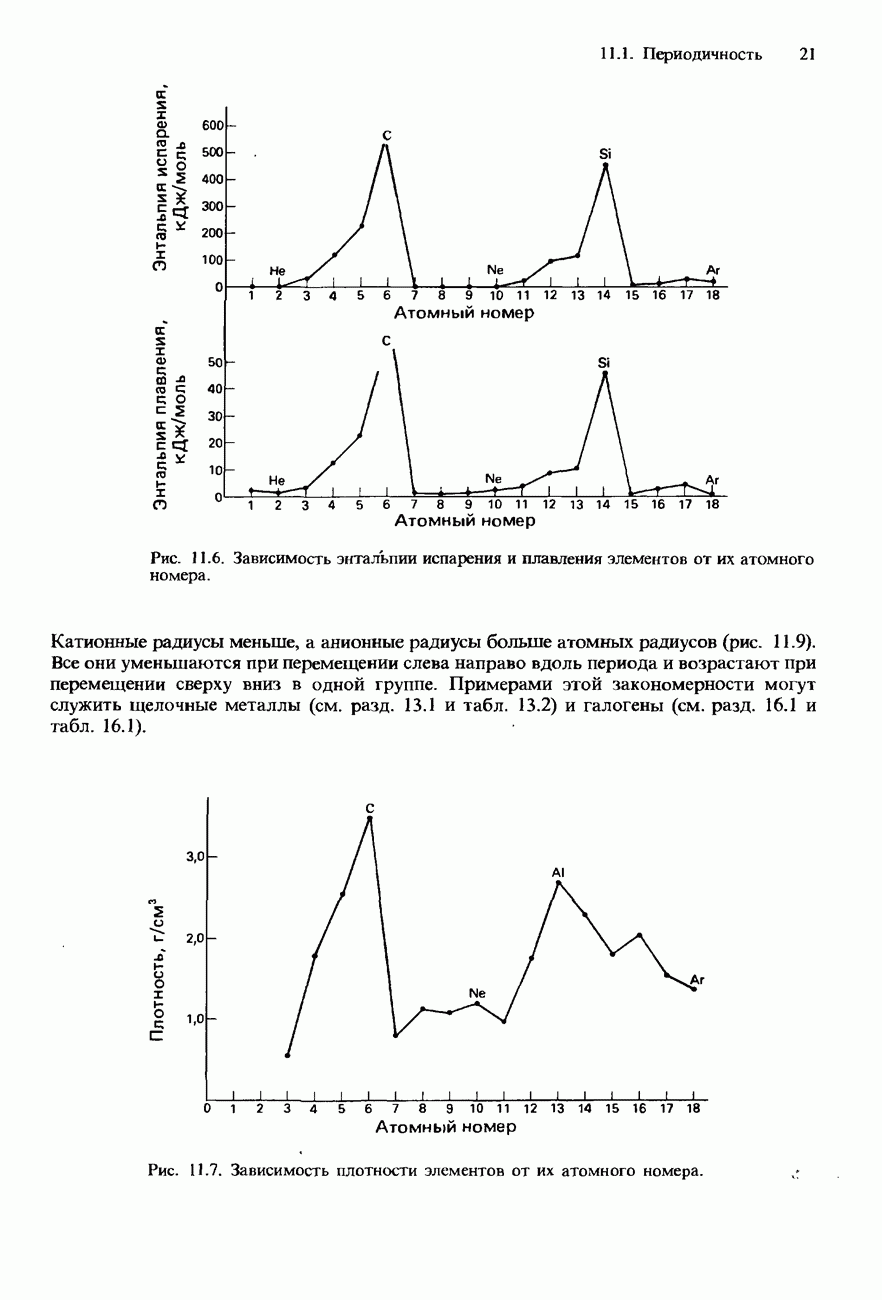
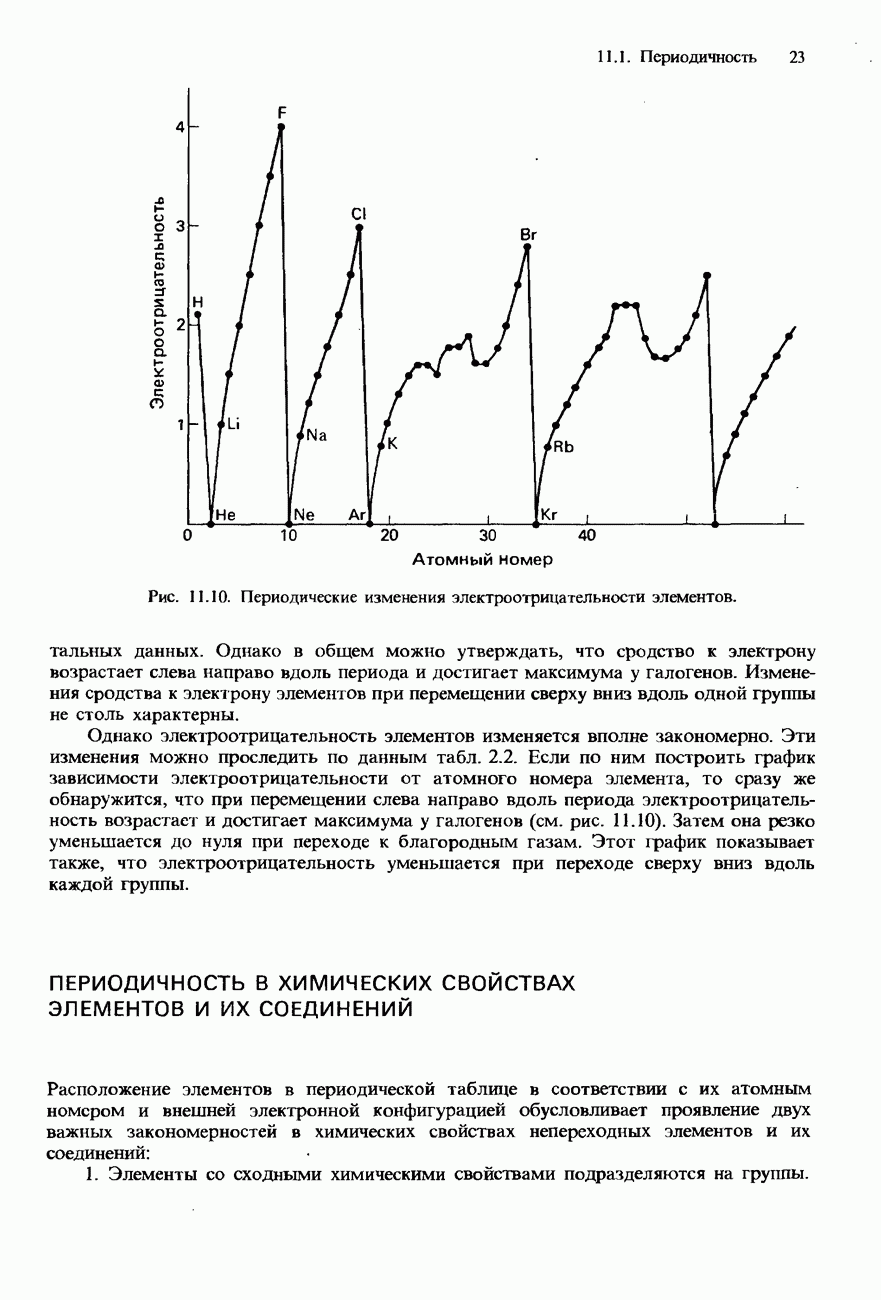
- ПЕРИОДИЧНОСТЬ
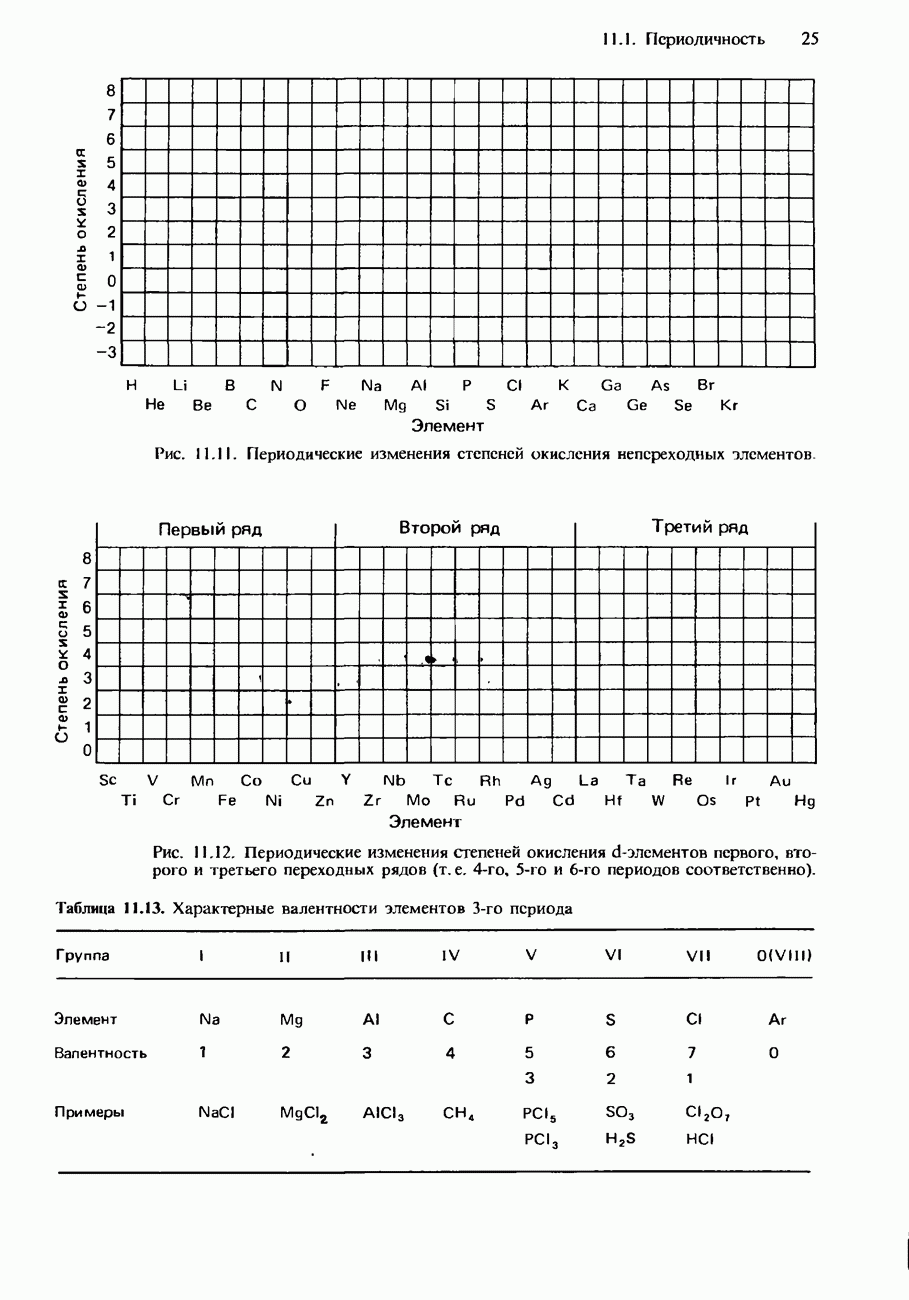
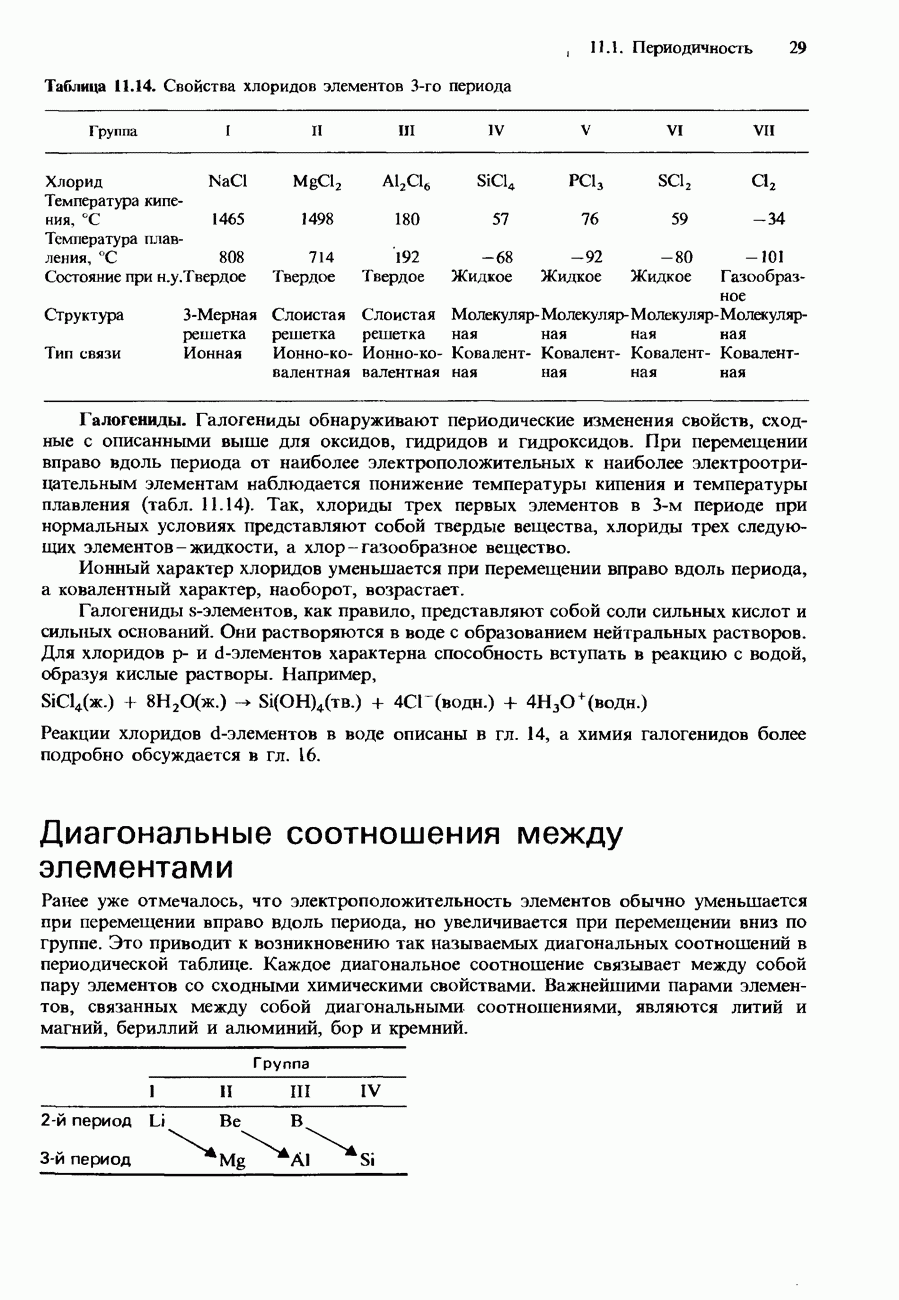
- ПЕРИОДИЧНОСТЬ В ХИМИЧЕСКИХ СВОЙСТВАХ ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 12. ВОДОРОД И ВОДА
- 12.1. ВОДОРОД
- ПОЛУЧЕНИЕ ВОДОРОДА В ЛАБОРАТОРНЫХ УСЛОВИЯХ
- РАЗЛИЧНЫЕ ФОРМЫ ВОДОРОДА
- ФИЗИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
- ХИМИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
- ТИПЫ СОЕДИНЕНИЙ ВОДОРОДА
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ, ПОЛУЧЕНИЕ И ИСПОЛЬЗОВАНИЕ ВОДОРОДА
- 12.2 Вода
- ХИМИЧЕСКИЕ РЕАКЦИИ С УЧАСТИЕМ ВОДЫ
- ИСТОЧНИКИ ПРЕСНОЙ ВОДЫ И ЕЕ ИСПОЛЬЗОВАНИЕ
- КАЧЕСТВО ВОДЫ
- ЗАГРЯЗНЕНИЕ ВОДЫ
- ОЧИСТКА И ПОДГОТОВКА ВОДЫ
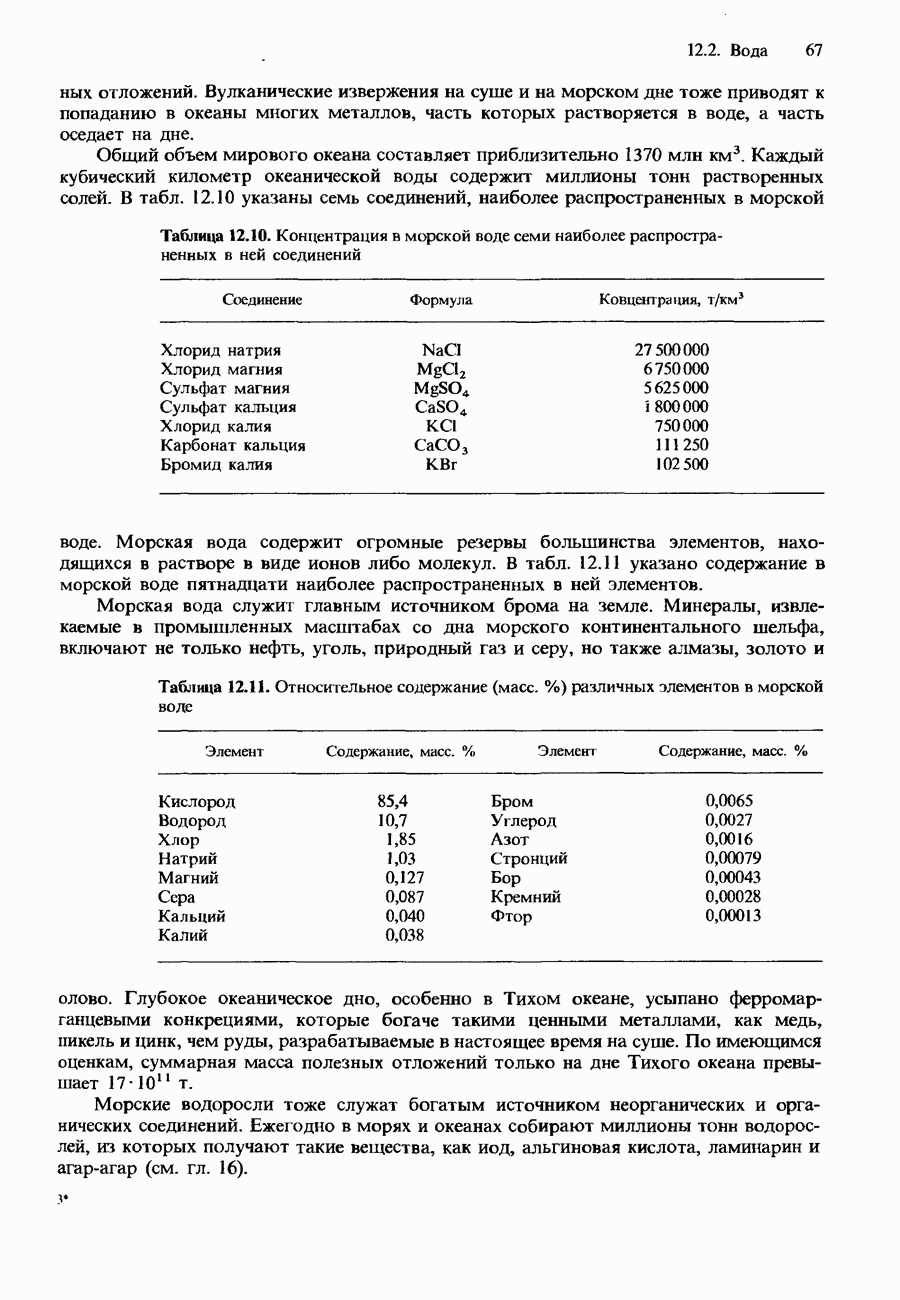
- ОКЕАНЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 13. s-Металлы
- 13.1 Структура и свойства s-металлов
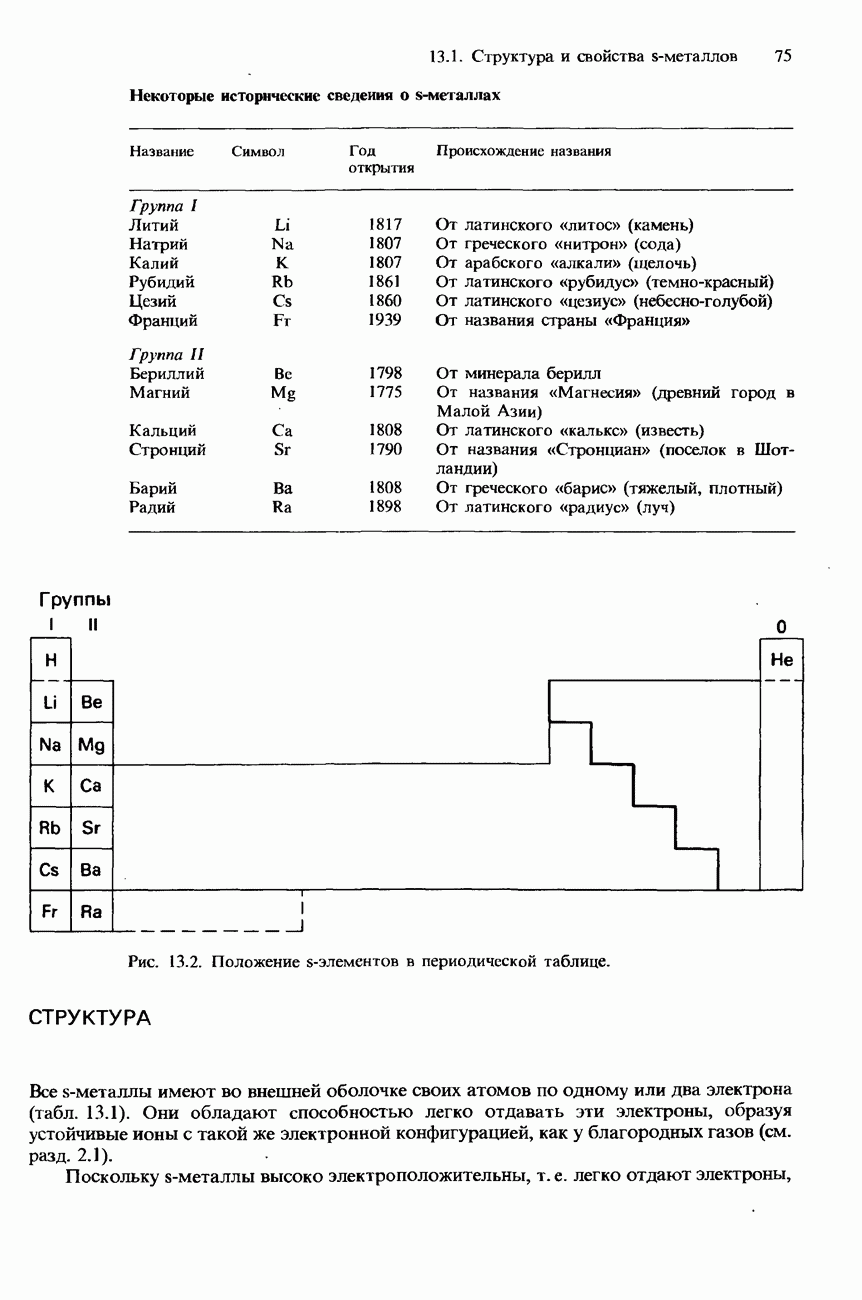
- СТРУКТУРА
- ФИЗИЧЕСКИЕ СВОЙСТВА
- РЕАКЦИОННАЯ СПОСОБНОСТЬ S-МЕТАЛЛОВ
- 13.2 Соединения, образуемые s-металлами
- ДРУГИЕ БИНАРНЫЕ СОЕДИНЕНИЯ
- ГИДРОКСИДЫ
- КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ
- ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- ТЕРМИЧЕСКАЯ УСТОЙЧИВОСТЬ ОКСОСОЕДИНЕНИЙ S-МЕТАЛЛОВ
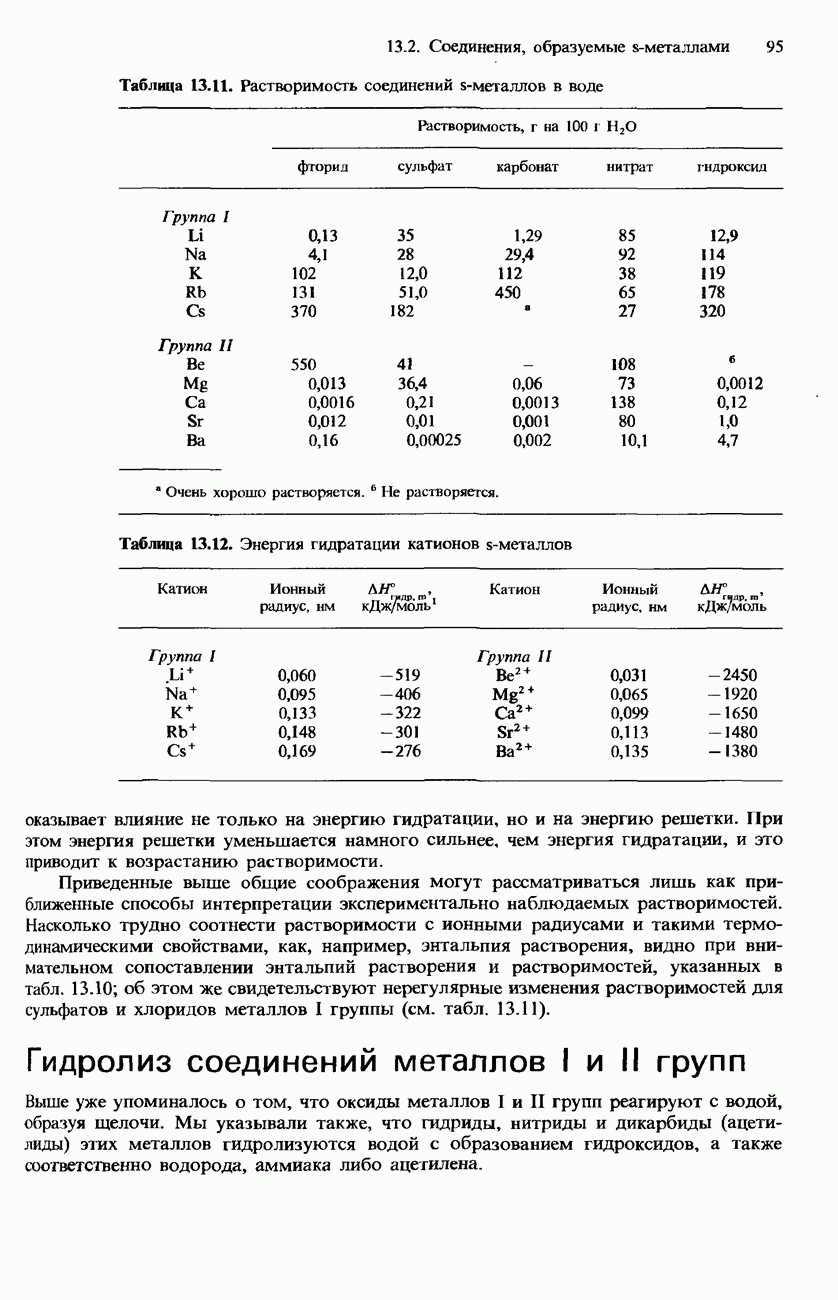
- РАСТВОРИМОСТЬ СОЛЕЙ И ГИДРОКСИДОВ МЕТАЛЛОВ I И II ГРУПП В ВОДЕ
- АНОМАЛЬНЫЕ СВОЙСТВА ЛИТИЯ И БЕРИЛЛИЯ, А ТАКЖЕ ИХ СОЕДИНЕНИЙ
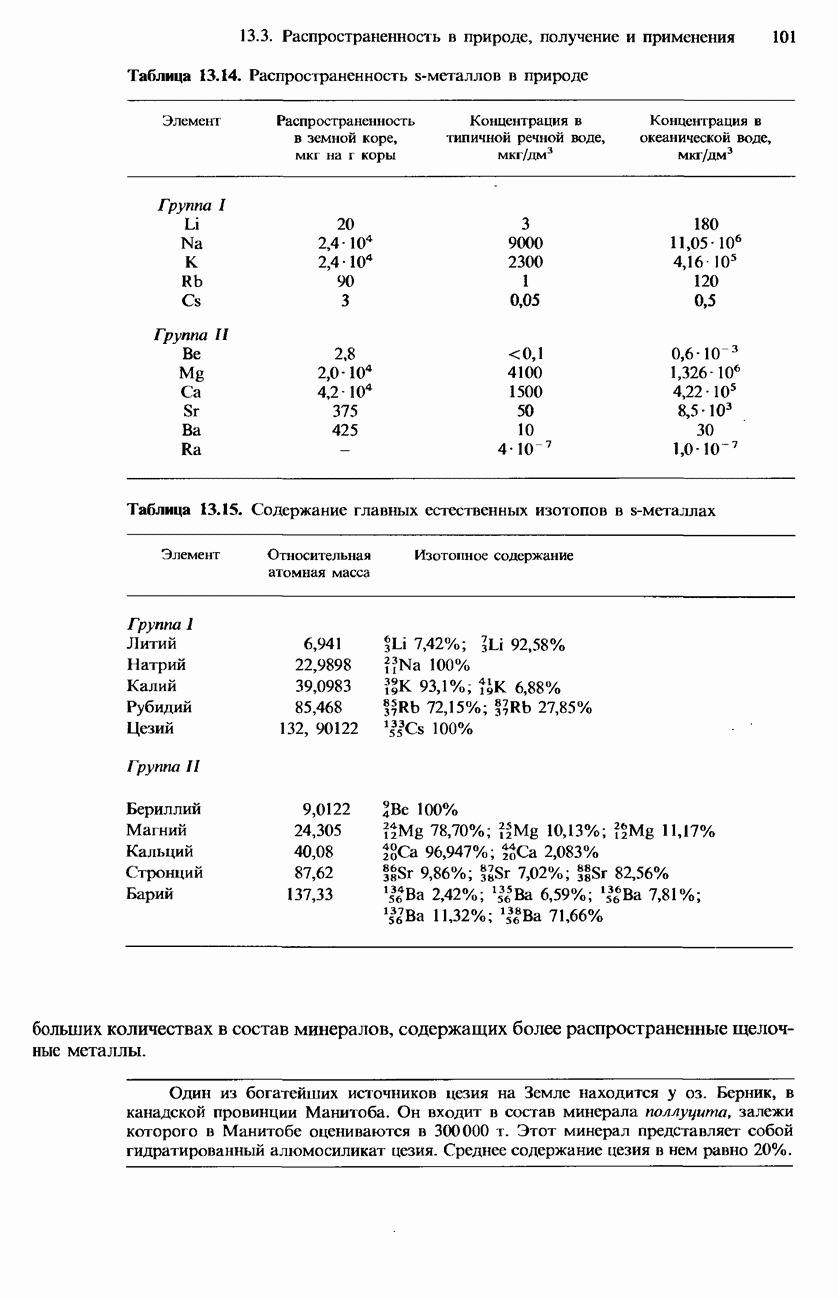
- 13.3. Распространенность в природе, получение и применение
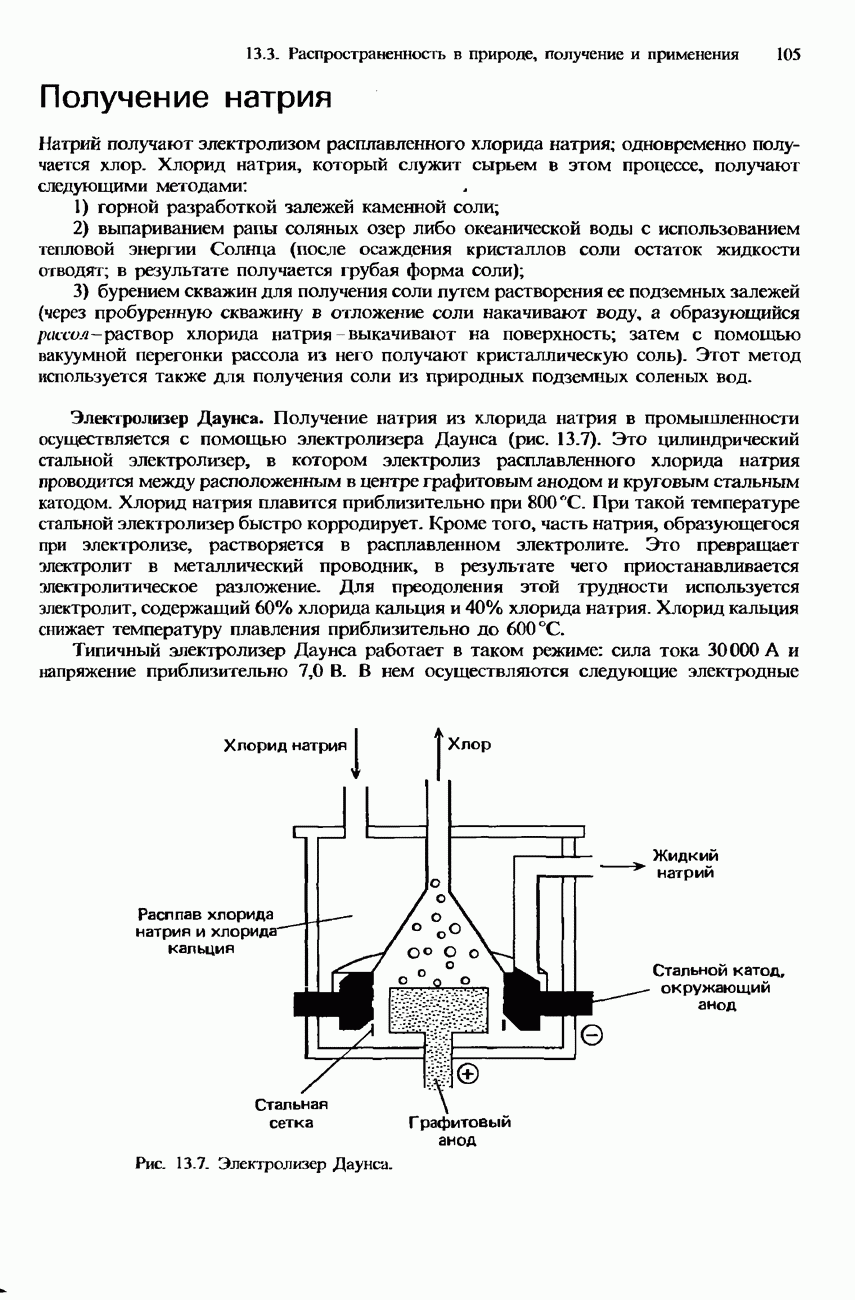
- ПОЛУЧЕНИЕ S-МЕТАЛЛОВ
- ПОЛУЧЕНИЕ СОЕДИНЕНИЙ S-МЕТАЛЛОВ
- ПРИМЕНЕНИЕ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 14. d-ЭЛЕМЕНТЫ
- 14.1. Структура и свойства d-элементов
- d-ЭЛЕМЕНТЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА
- ХИМИЧЕСКИЕ СВОЙСТВА
- 14.2 Химия семи d-элементов
- МАРГАНЕЦ
- ЖЕЛЕЗО
- КОБАЛЬТ
- НИКЕЛЬ
- МЕДЬ
- ЦИНК
- 14.3. Распространенность в природе, получение и применения
- ПРОИЗВОДСТВО ЖЕЛЕЗА И СТАЛИ
- ПОЛУЧЕНИЕ ДРУГИХ МЕТАЛЛОВ ПЕРВОГО ПЕРЕХОДНОГО РЯДА
- ПРИМЕНЕНИЯ d-ЭЛЕМЕНТОВ И ИХ СОЕДИНЕНИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 15. ЭЛЕМЕНТЫ III-VI ГРУПП
- 15.1. Алюминий и другие элементы III группы
- БОР
- ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА АЛЮМИНИЯ
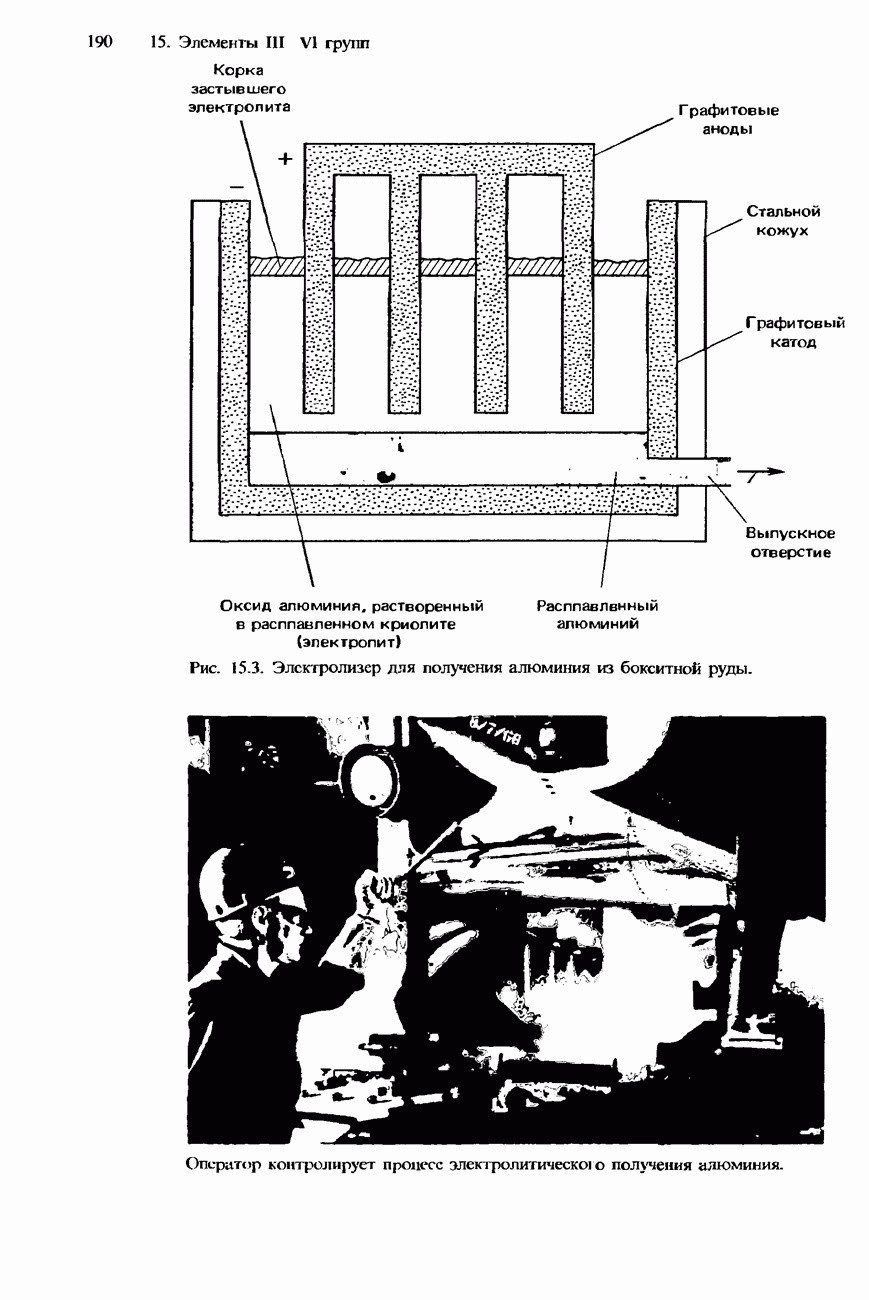
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ И ПОЛУЧЕНИЕ АЛЮМИНИЯ
- ПРИМЕНЕНИЯ АЛЮМИНИЯ И ЕГО СОЕДИНЕНИЙ
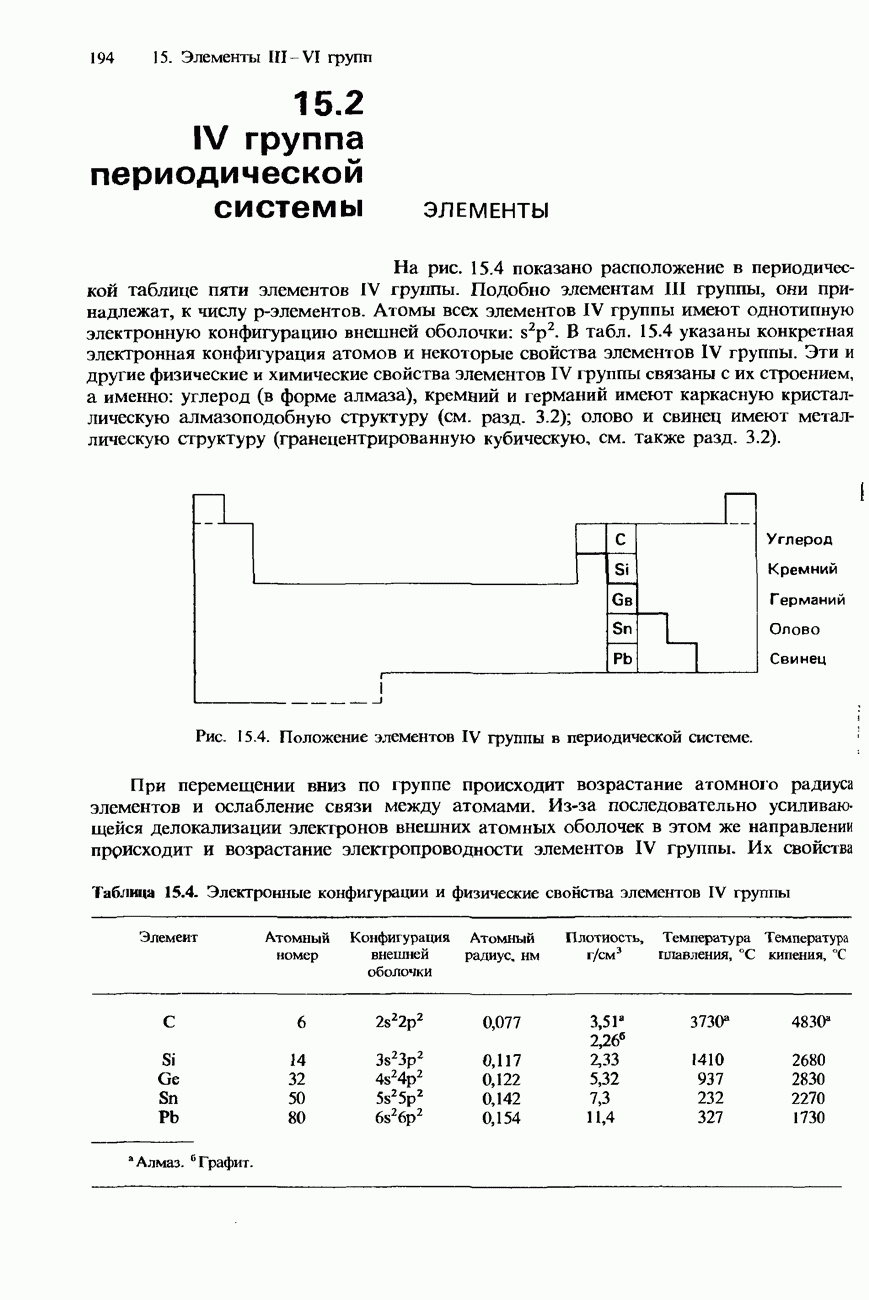
- 15.2. IV группа периодической системы
- СОЕДИНЕНИЯ
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ И ПОЛУЧЕНИЕ ИЗ РУД
- ПРИМЕНЕНИЯ УГЛЕРОДА
- ПРИМЕНЕНИЯ КРЕМНИЯ
- ПРИМЕНЕНИЯ ГЕРМАНИЯ, ОЛОВА И СВИНЦА
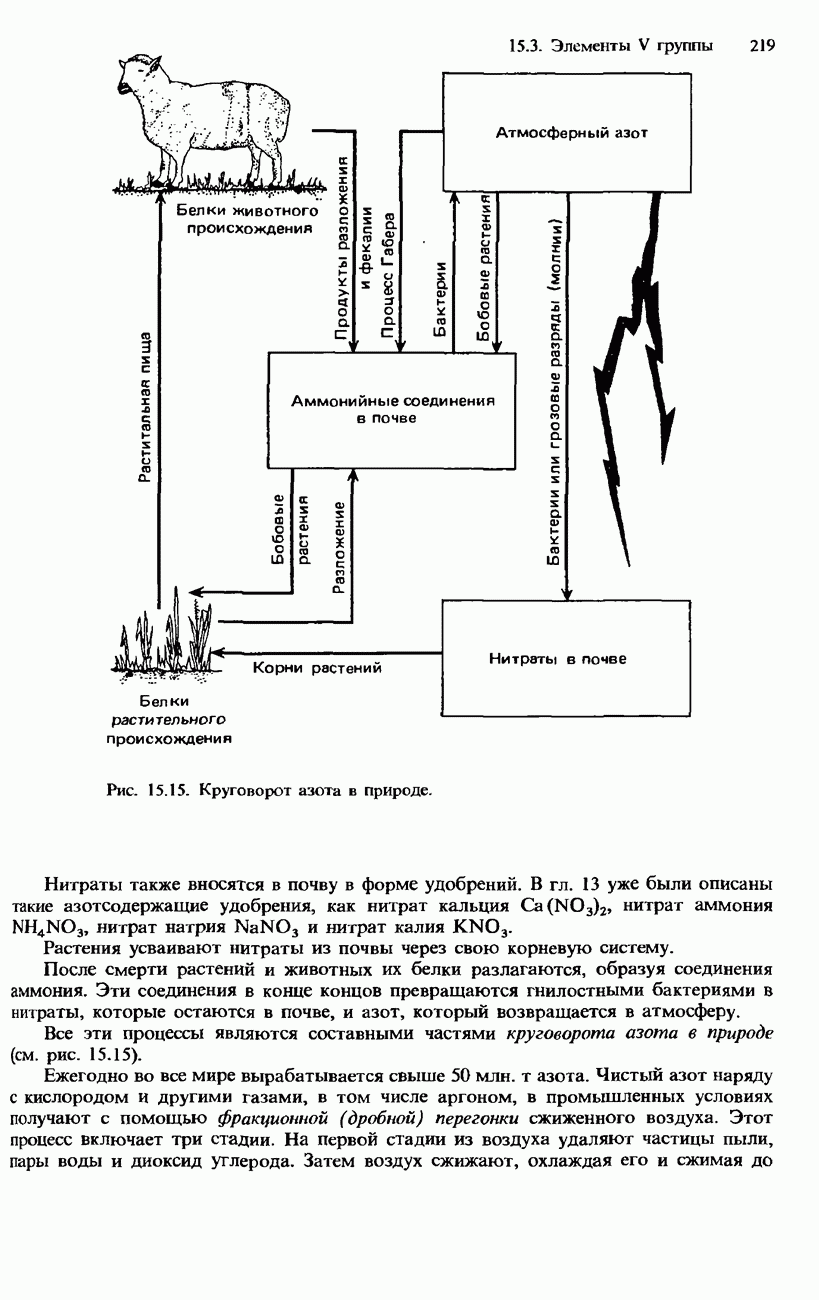
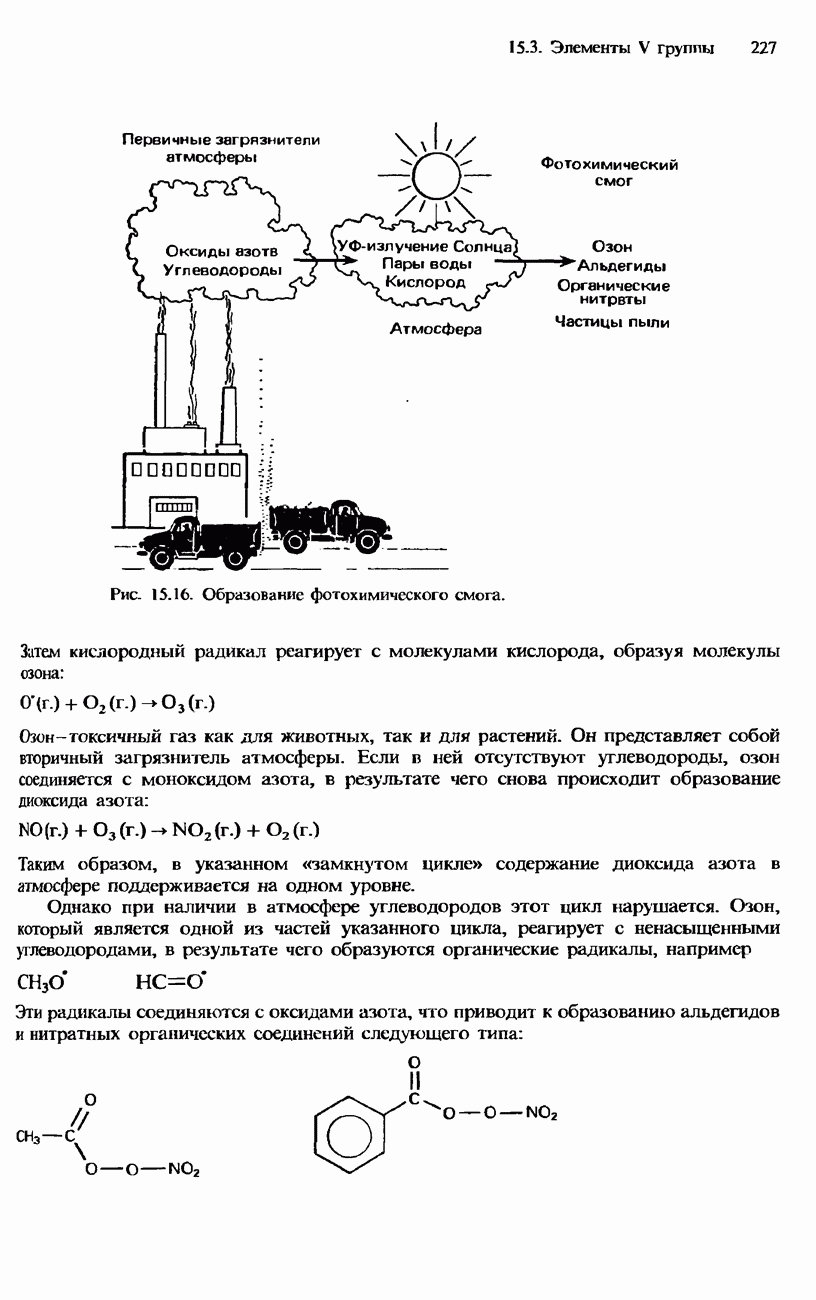
- 15.3. Элементы V группы
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ. ПОЛУЧЕНИЕ И ПРИМЕНЕНИЯ АЗОТА И ФОСФОРА
- СОЕДИНЕНИЯ АЗОТА
- СОЕДИНЕНИЯ ФОСФОРА
- 15.4. Элементы VI группы. Кислород и сера
- КИСЛОРОД
- СОЕДИНЕНИЯ КИСЛОРОДА
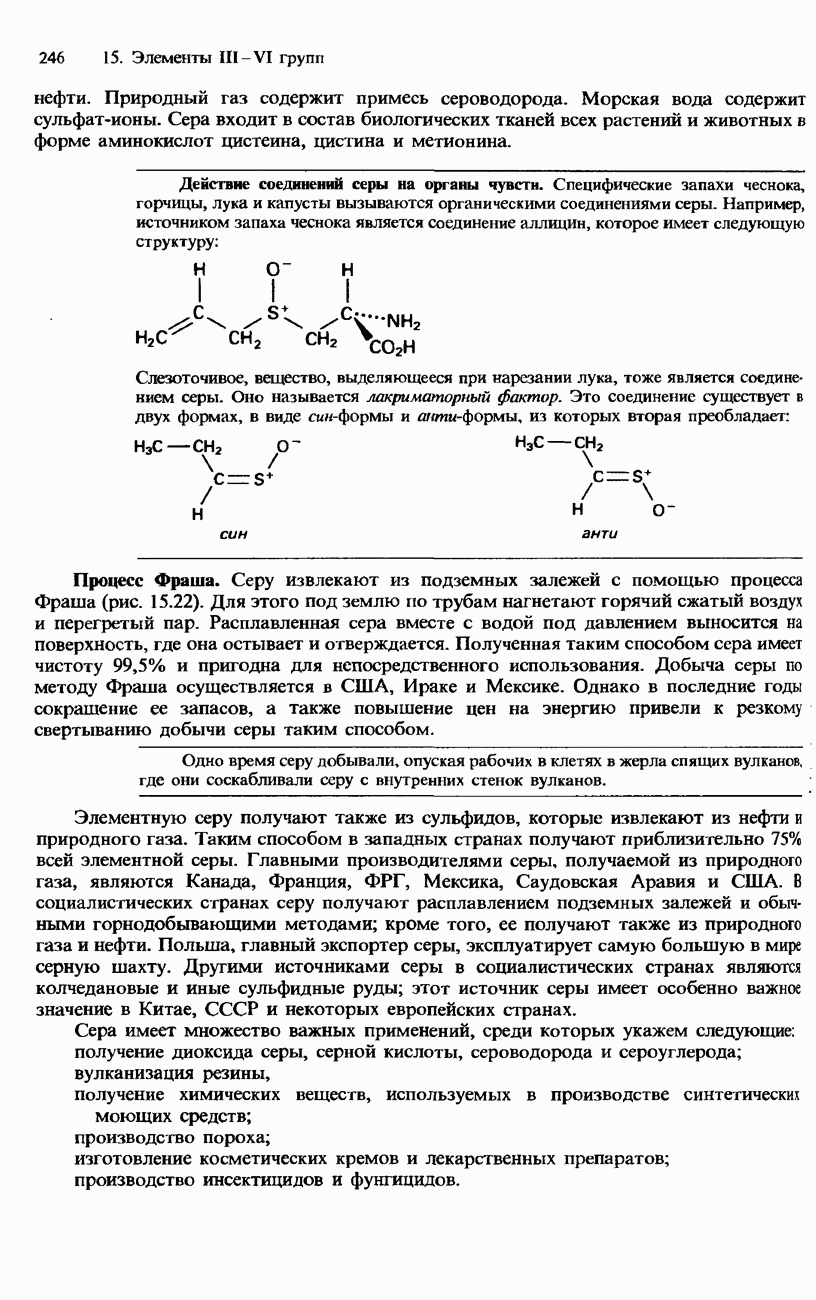
- СЕРА
- СОЕДИНЕНИЯ СЕРЫ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 16. ГАЛОГЕНЫ И БЛАГОРОДНЫЕ ГАЗЫ
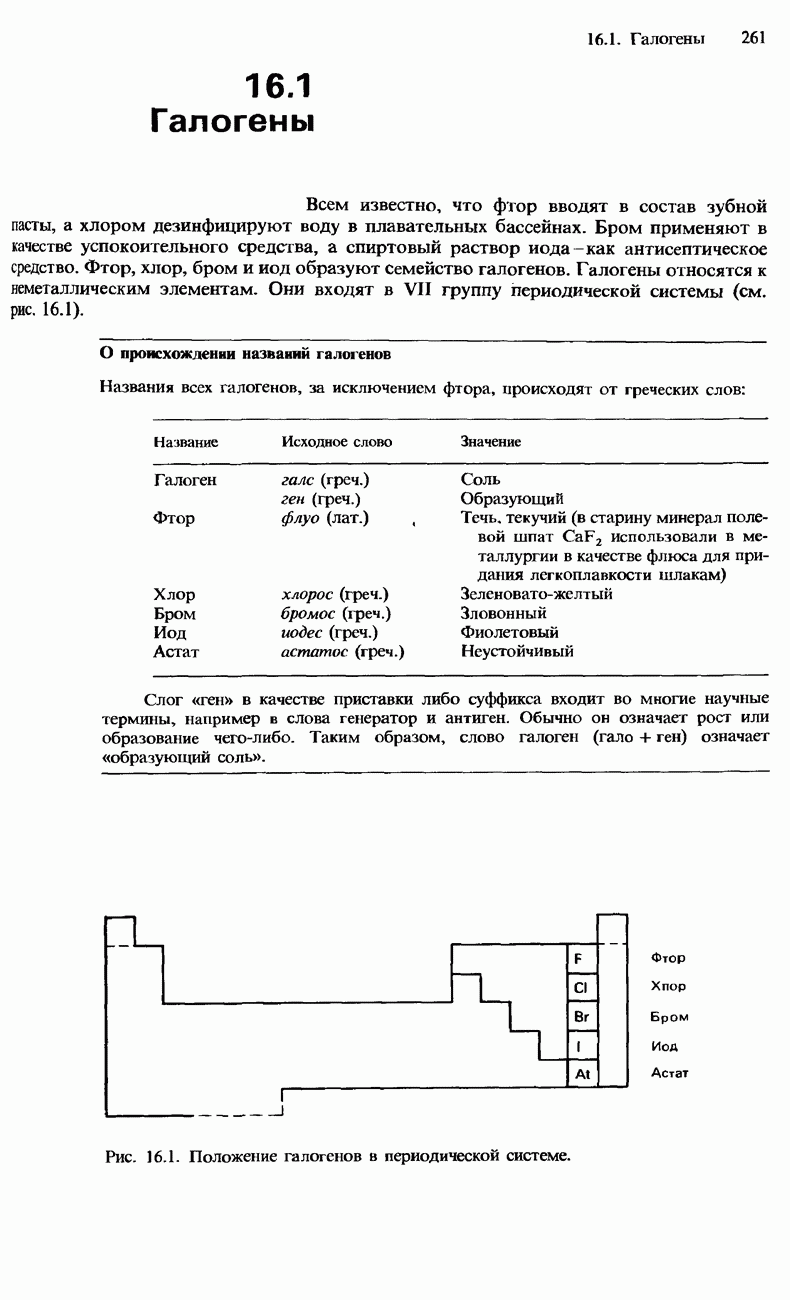
- 16.1. Галогены
- ЭЛЕКТРОННАЯ СТРУКТУРА АТОМОВ ГАЛОГЕНОВ
- ЛАБОРАТОРНЫЕ МЕТОДЫ ПОЛУЧЕНИЯ ГАЛОГЕНОВ
- ФИЗИЧЕСКИЕ И БИОЛОГИЧЕСКИЕ СВОЙСТВА
- РЕАКЦИОННАЯ СПОСОБНОСТЬ ГАЛОГЕНОВ
- 16.2. Соединения галогенов
- ГАЛОГЕНОВОДОРОДЫ
- КИСЛОРОДСОДЕРЖАЩИЕ СОЕДИНЕНИЯ ГАЛОГЕНОВ
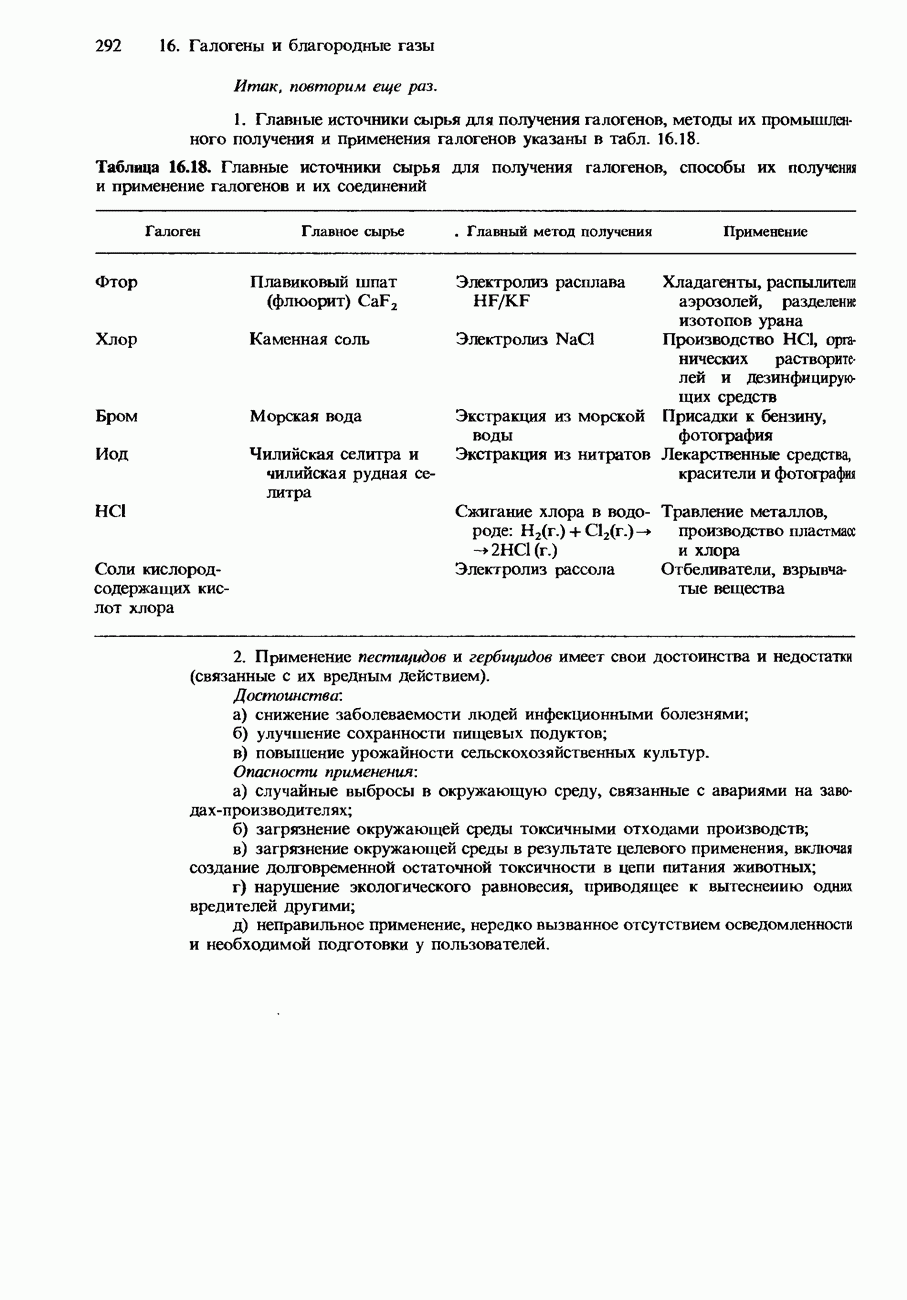
- 16.3. Распространенность, получение и применение галогенов и их соединений
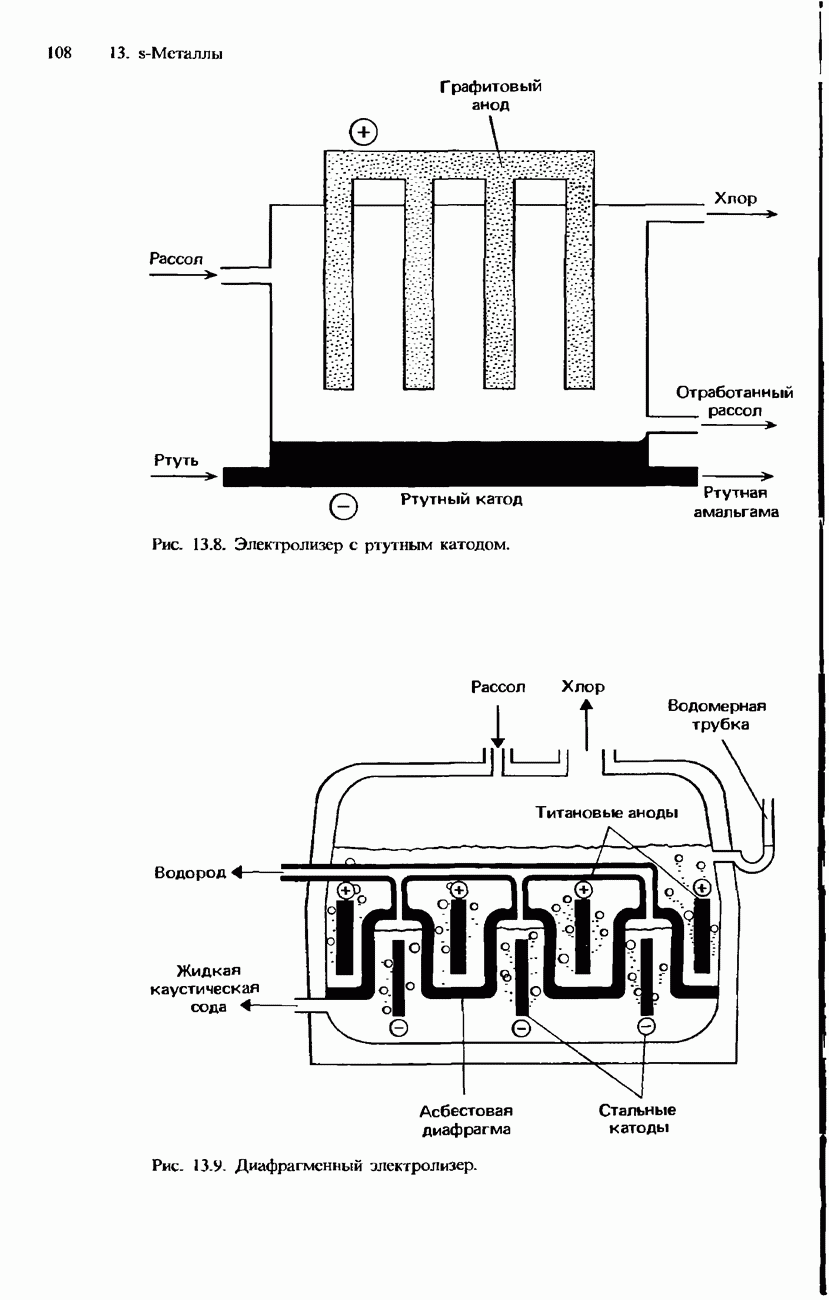
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ ХЛОРА
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ ДРУГИХ ГАЛОГЕНОВ
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ СОЕДИНЕНИЙ ХЛОРА
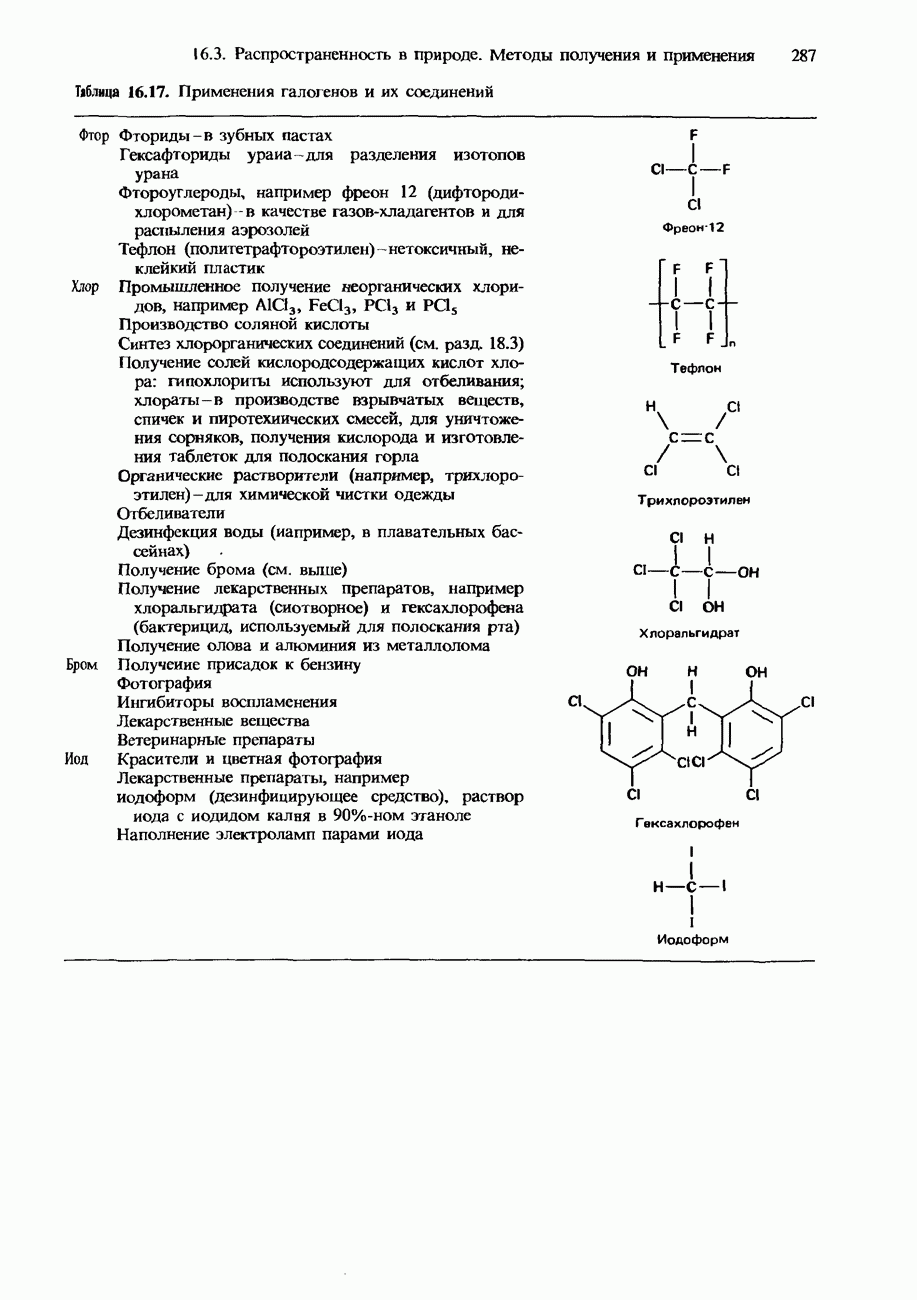
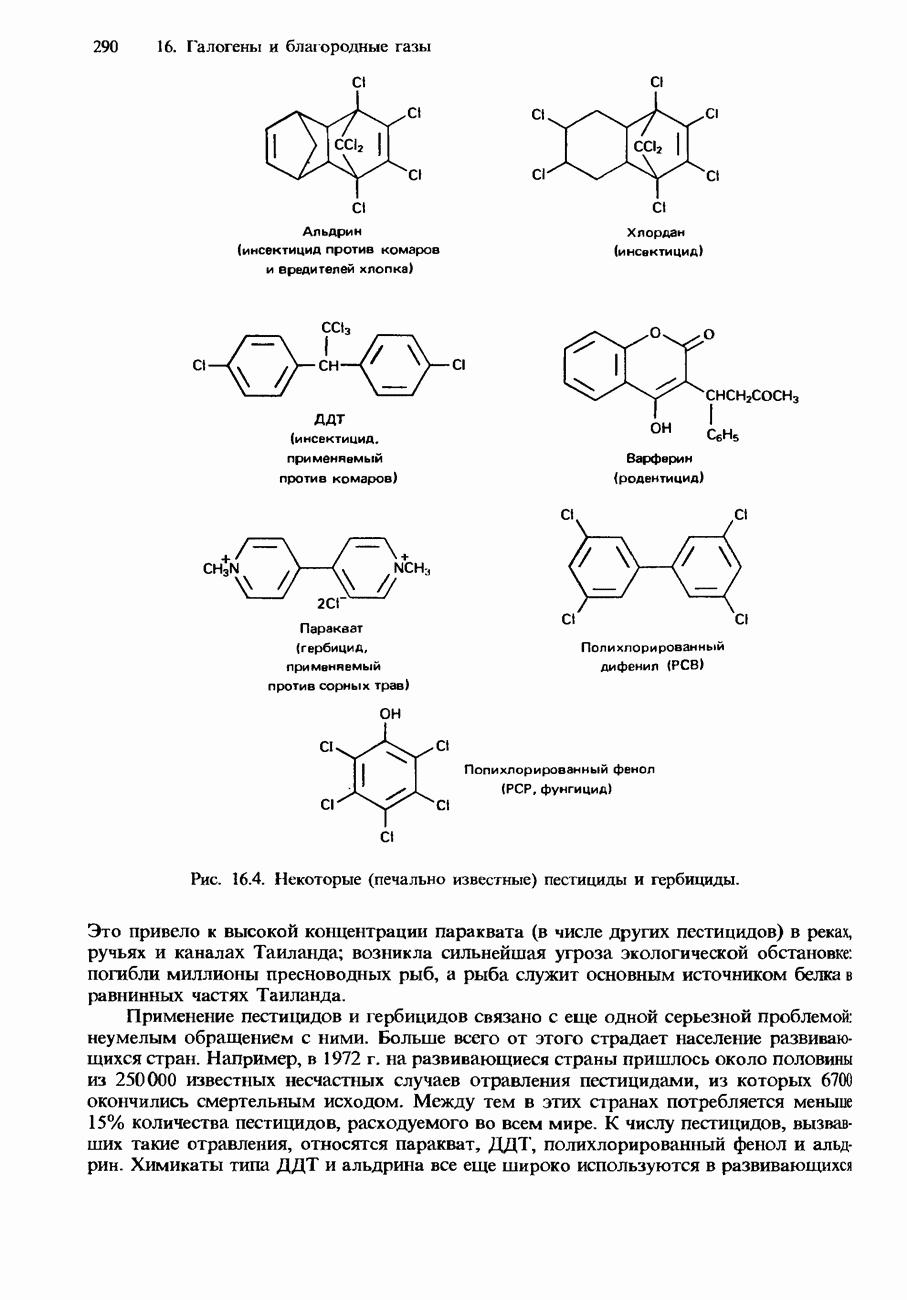
- ПРИМЕНЕНИЯ ГАЛОГЕНОВ И ИХ СОЕДИНЕНИЙ
- ТОКСИЧНОСТЬ ХЛОРСОДЕРЖАЩИХ ПРОДУКТОВ
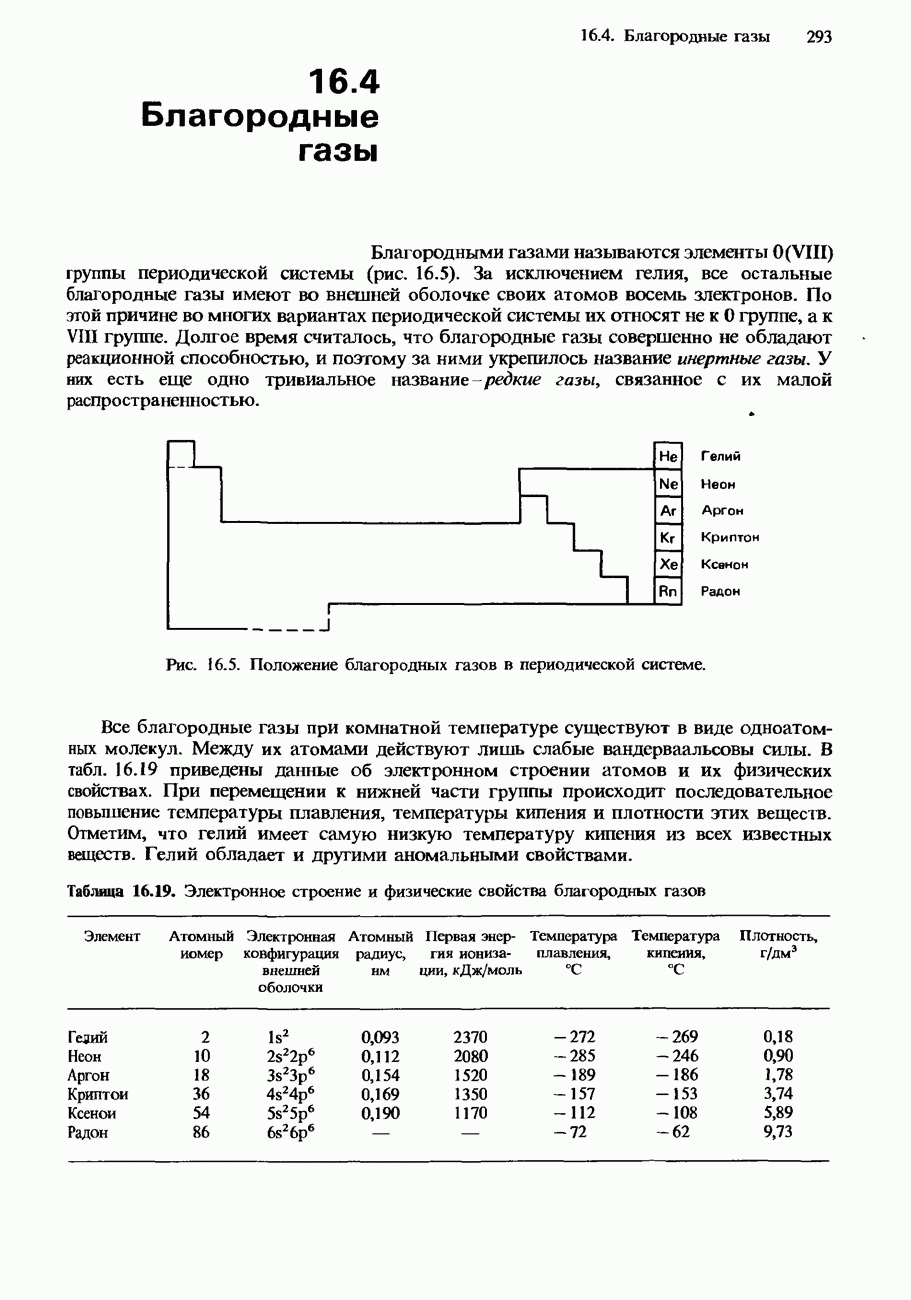
- 16.4. Благородные газы
- СОЕДИНЕНИЯ БЛАГОРОДНЫХ ГАЗОВ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 17. ОСНОВЫ ОРГАНИЧЕСКОЙ ХИМИИ
- 7.1. Органическая химия
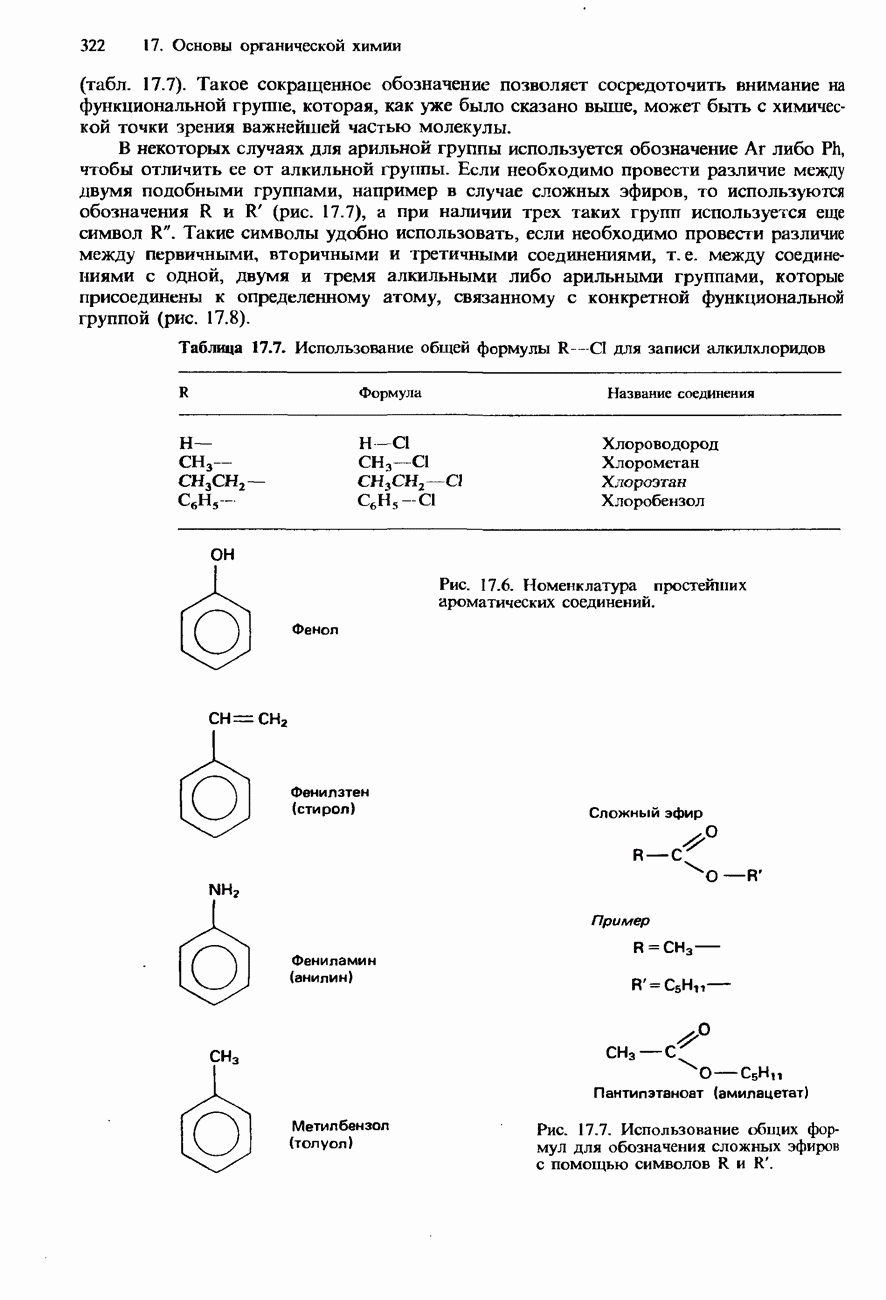
- НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
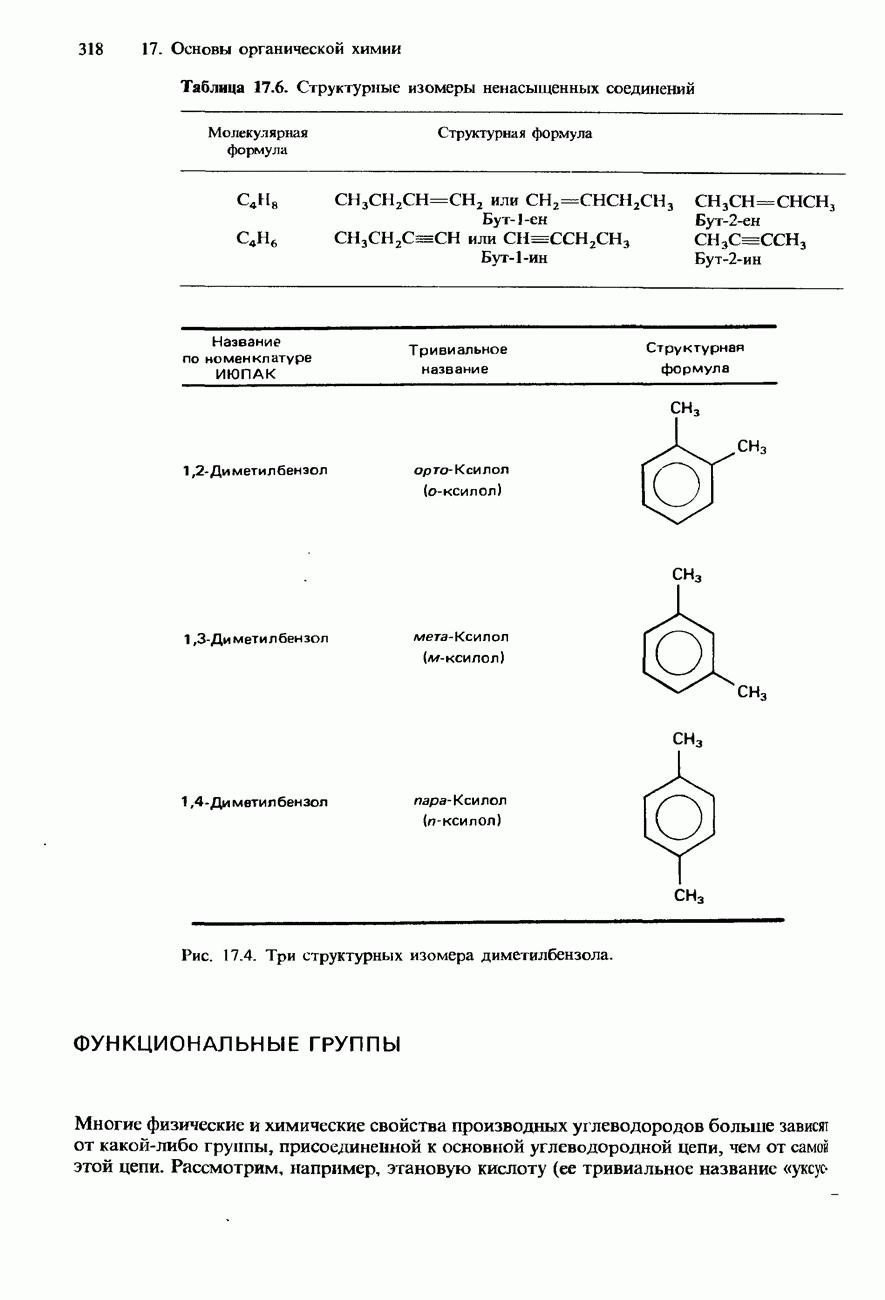
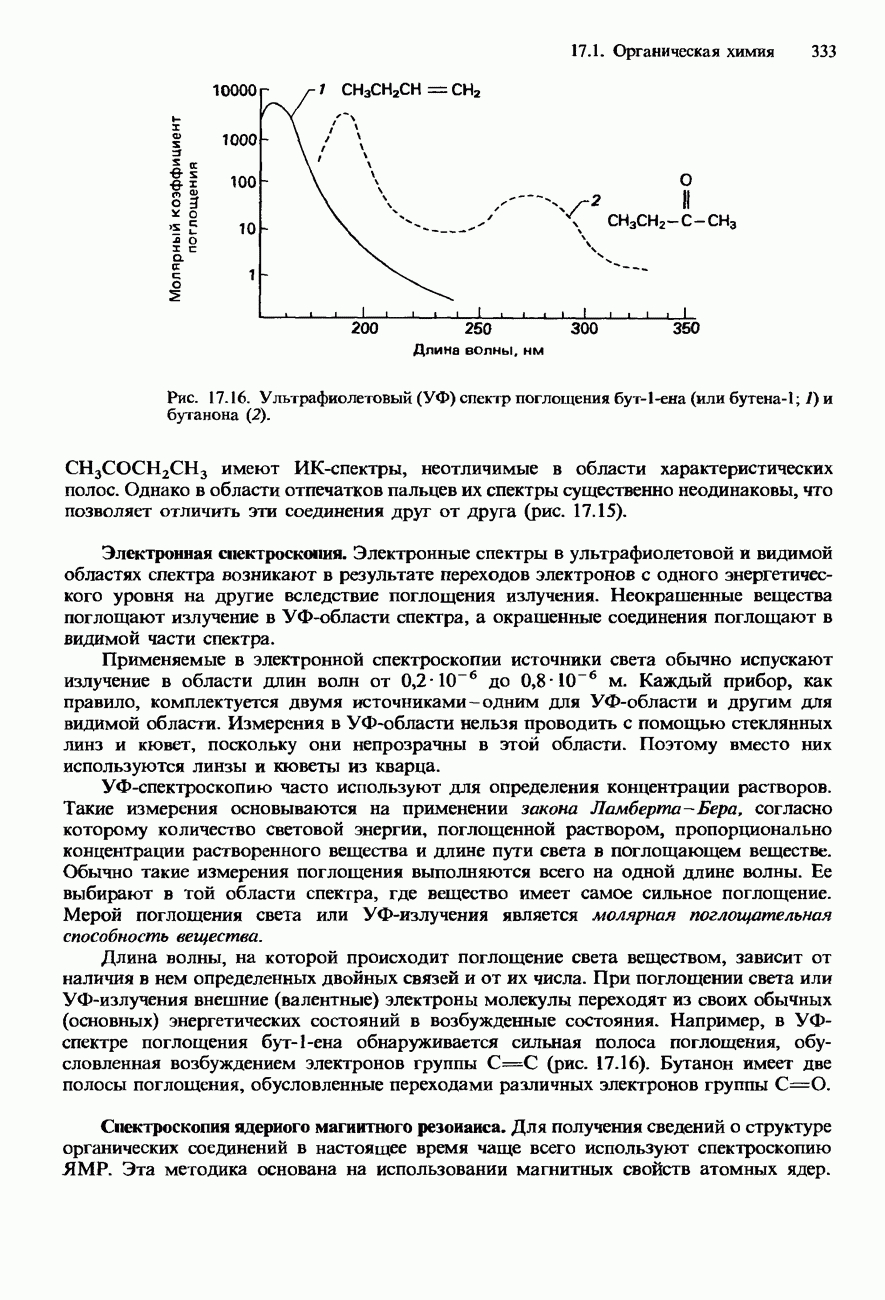
- УГЛЕВОДОРОДЫ
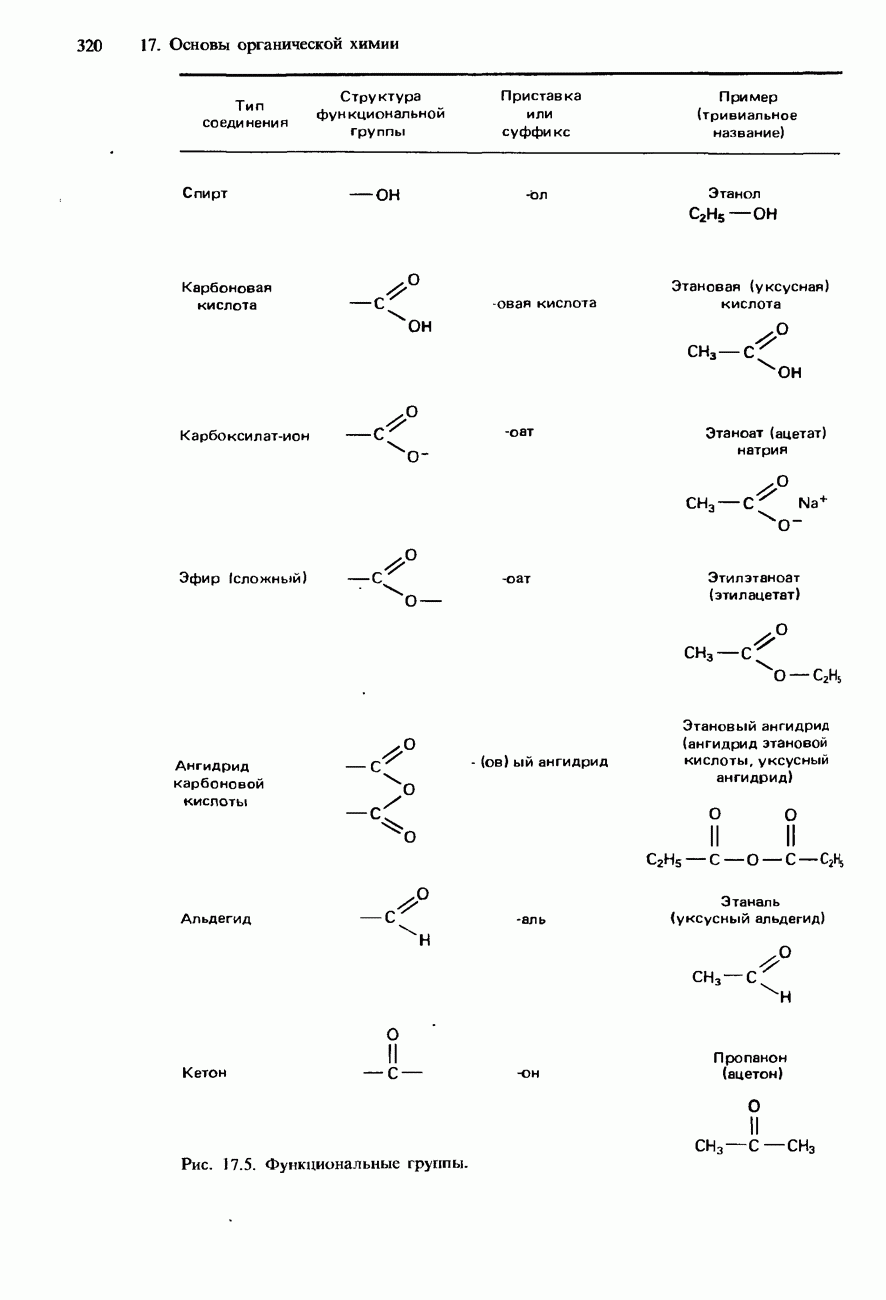
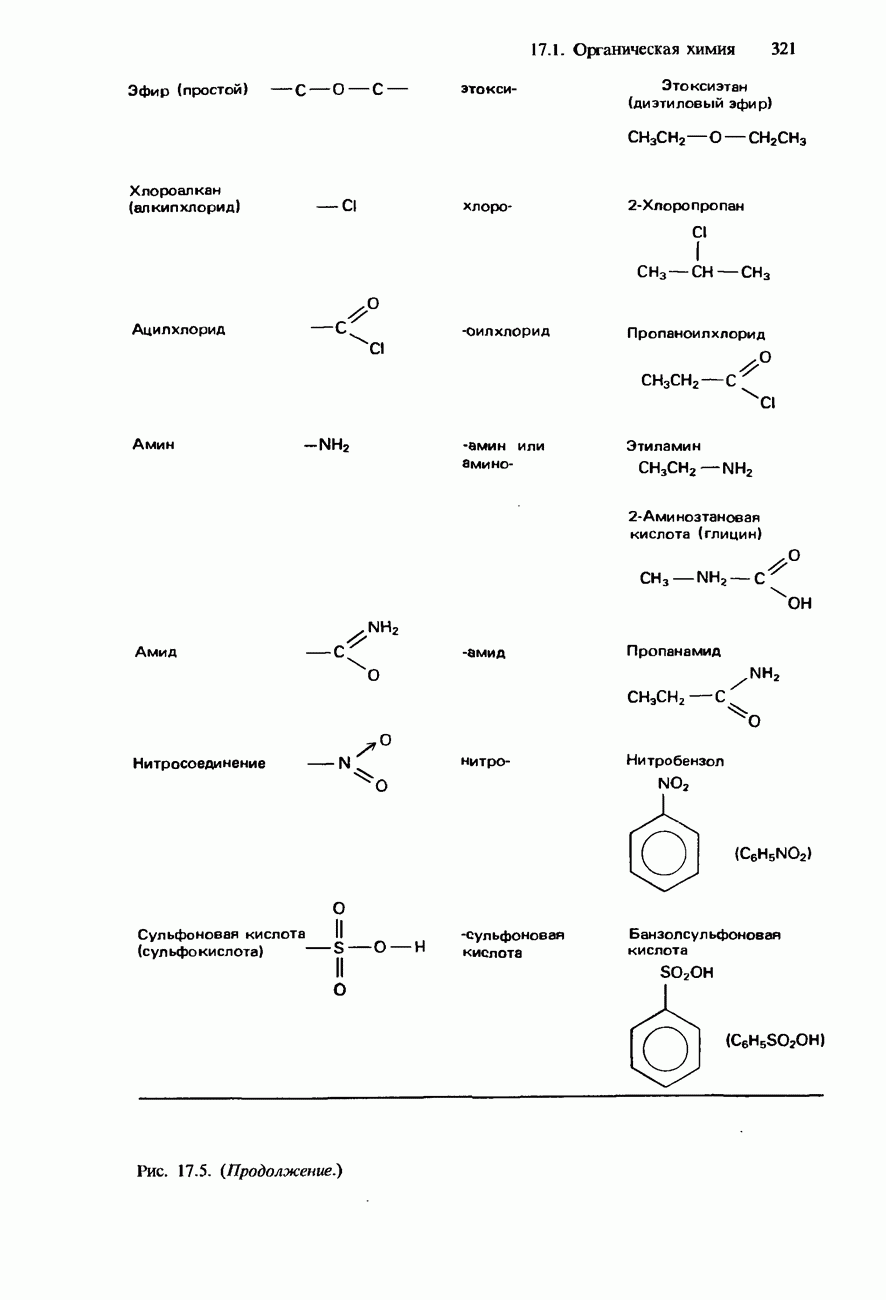
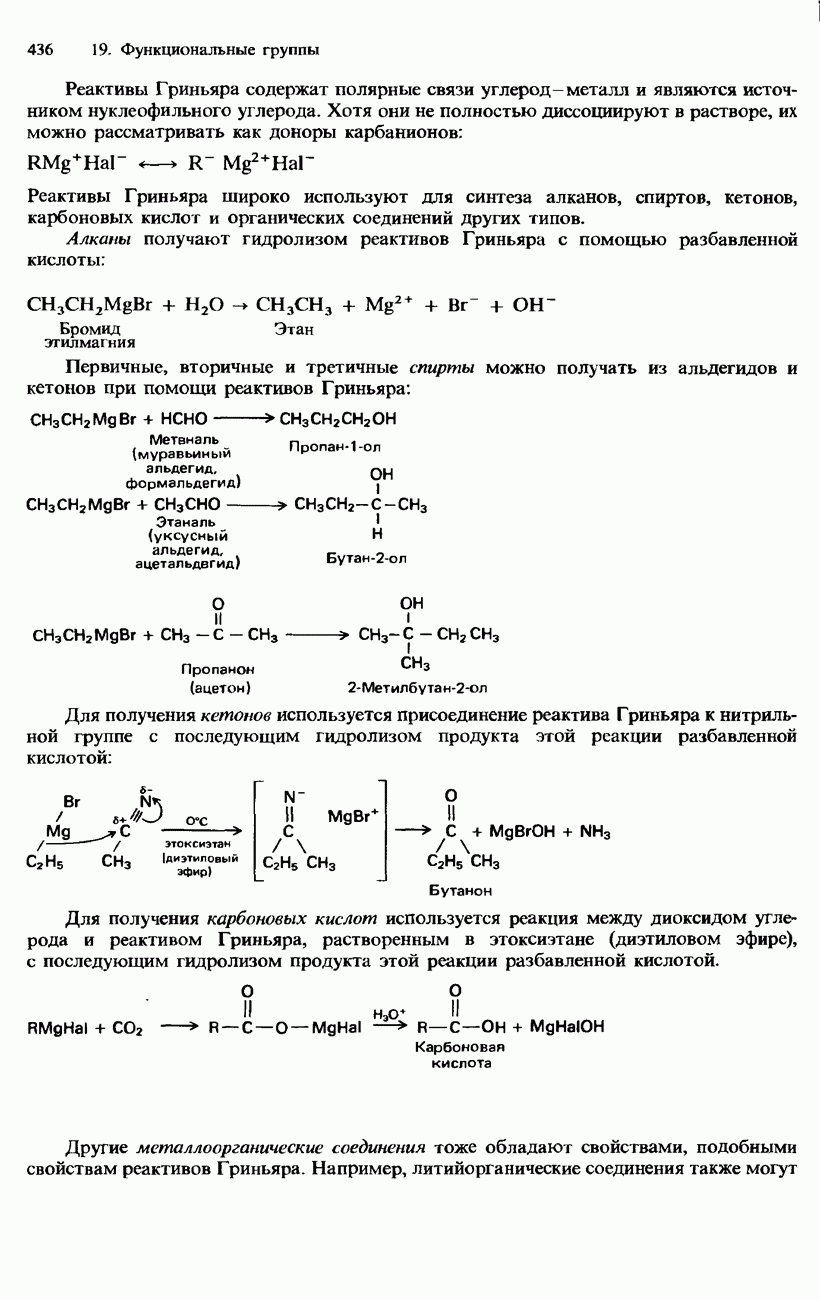
- ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- ПОЛУЧЕНИЕ И ИДЕНТИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 17.2. Молекулярная структура органических соединений
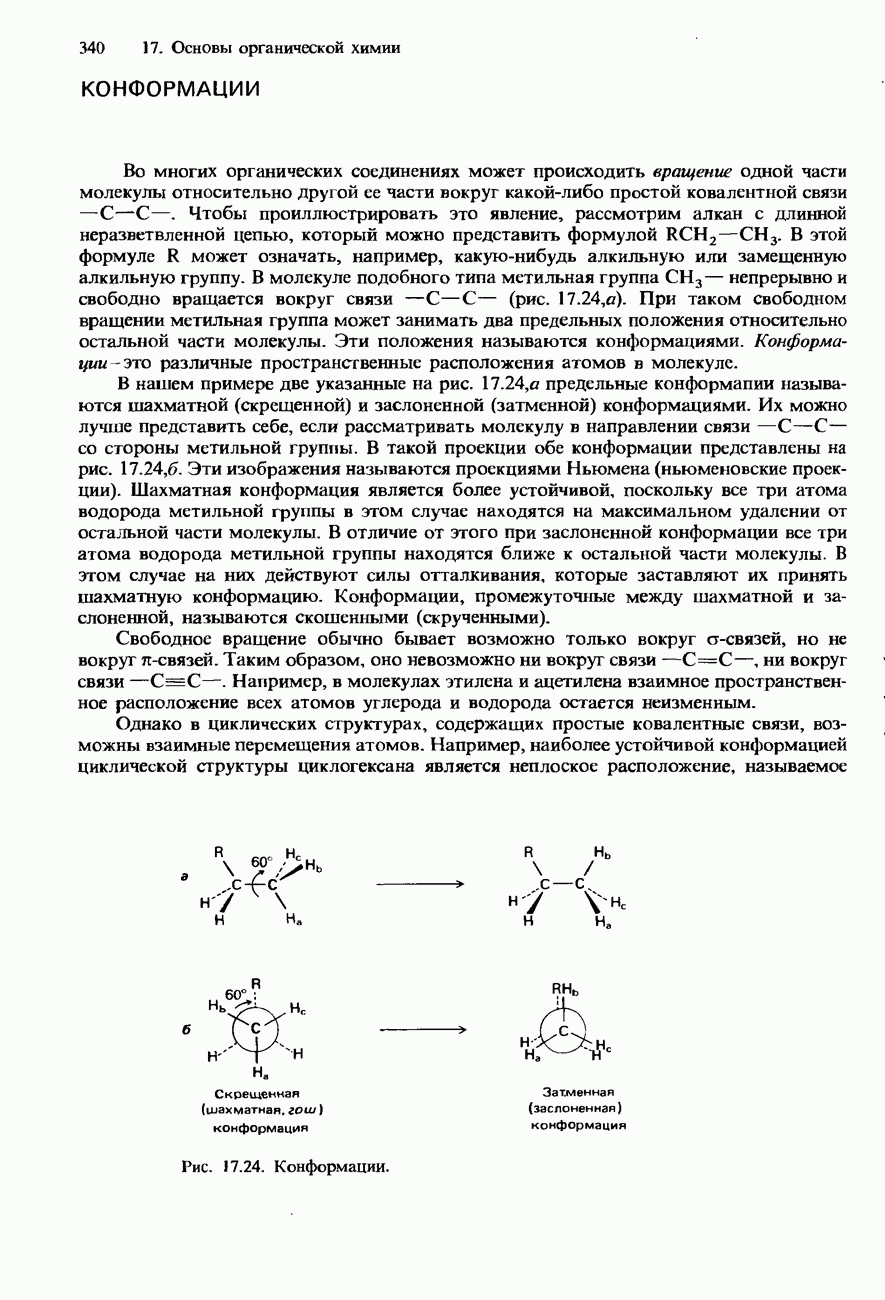
- КОНФОРМАЦИИ
- СТЕРЕОИЗОМЕРИЯ
- 17.3. Механизмы органических реакций
- ФАКТОРЫ, ВЛИЯЮЩИЕ НА РЕАКЦИОННУЮ СПОСОБНОСТЬ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- НУКЛЕОФИЛЫ И ЭЛЕКТРОФИЛЫ
- ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 18. УГЛЕВОДОРОДЫ
- 18.1. Алифатические углеводороды
- АЛКАНЫ
- АЛКЕНЫ
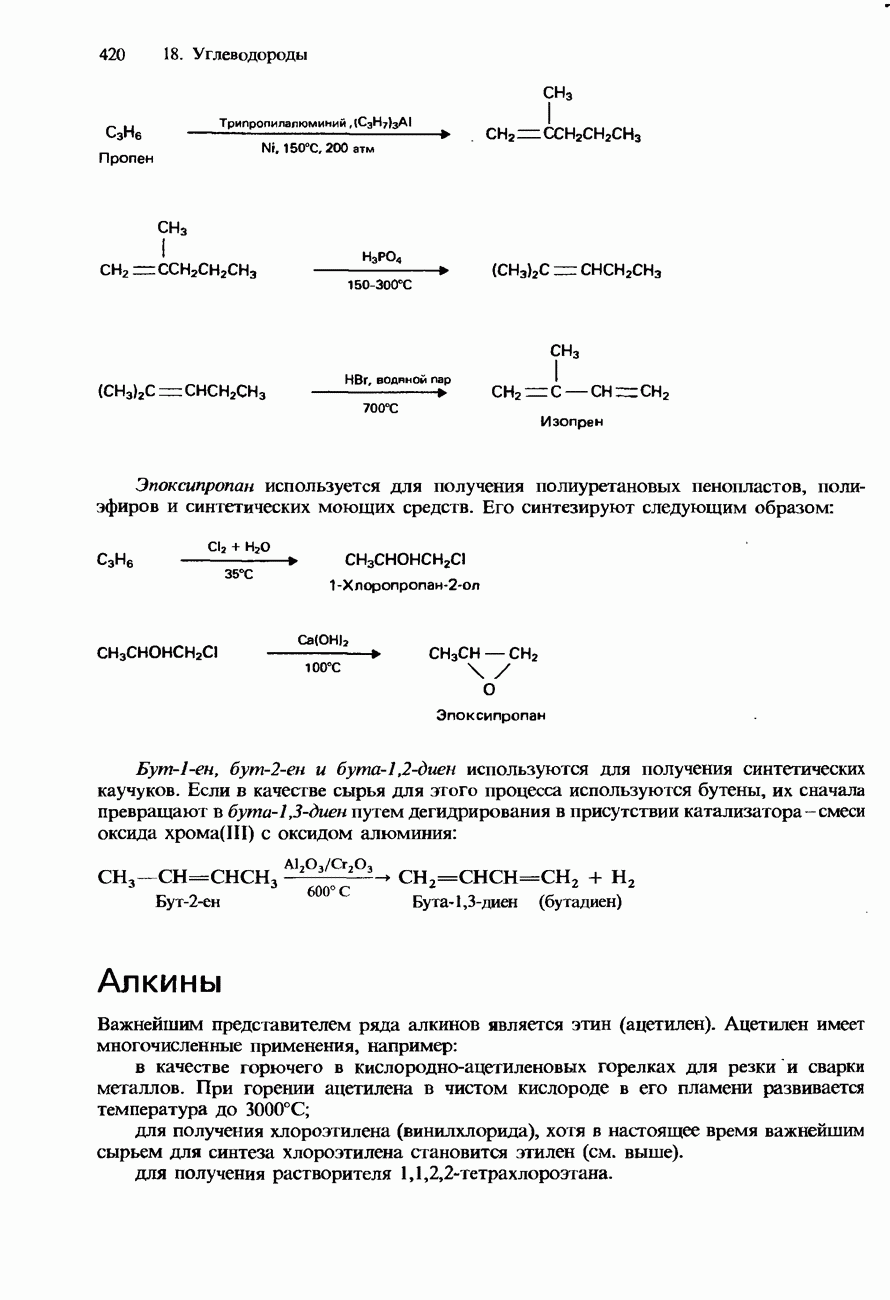
- АЛКИНЫ
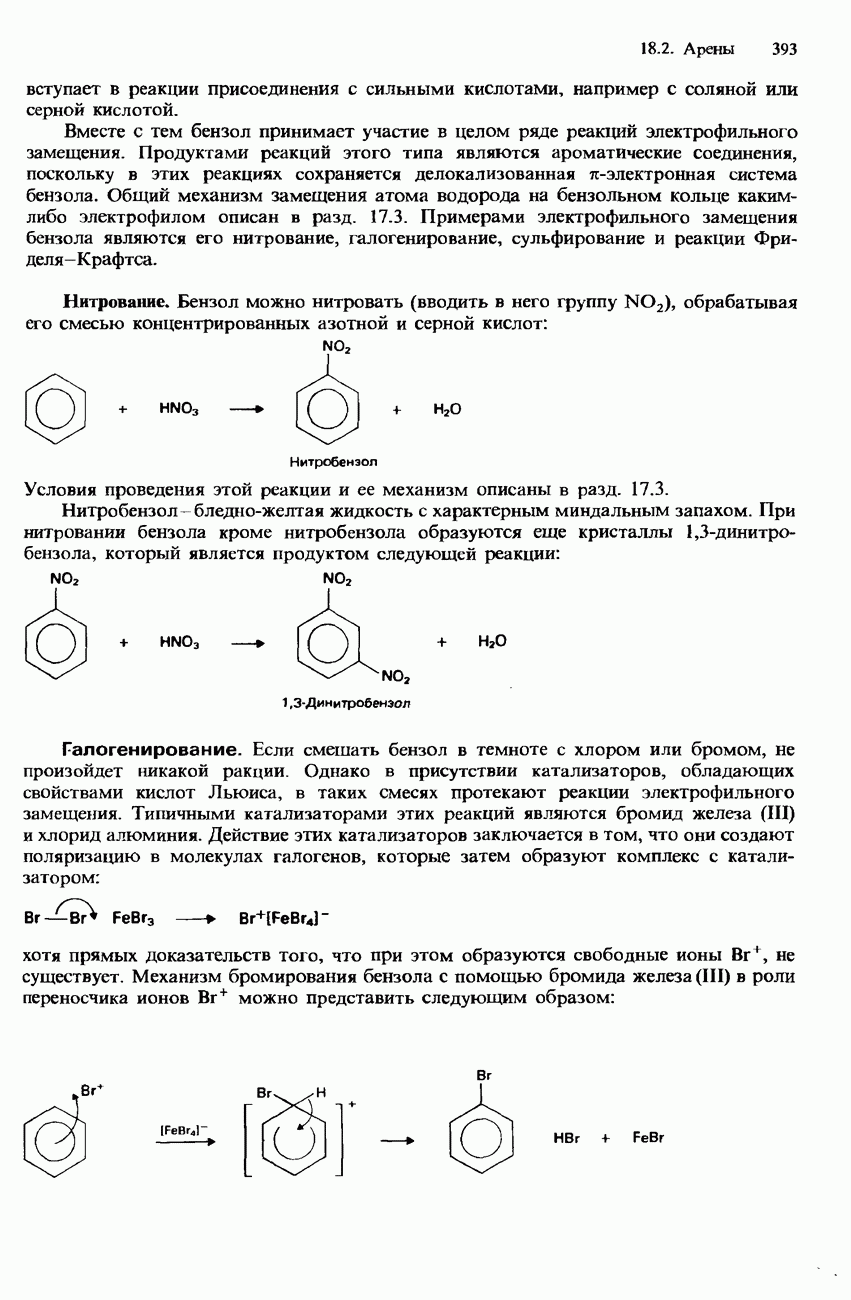
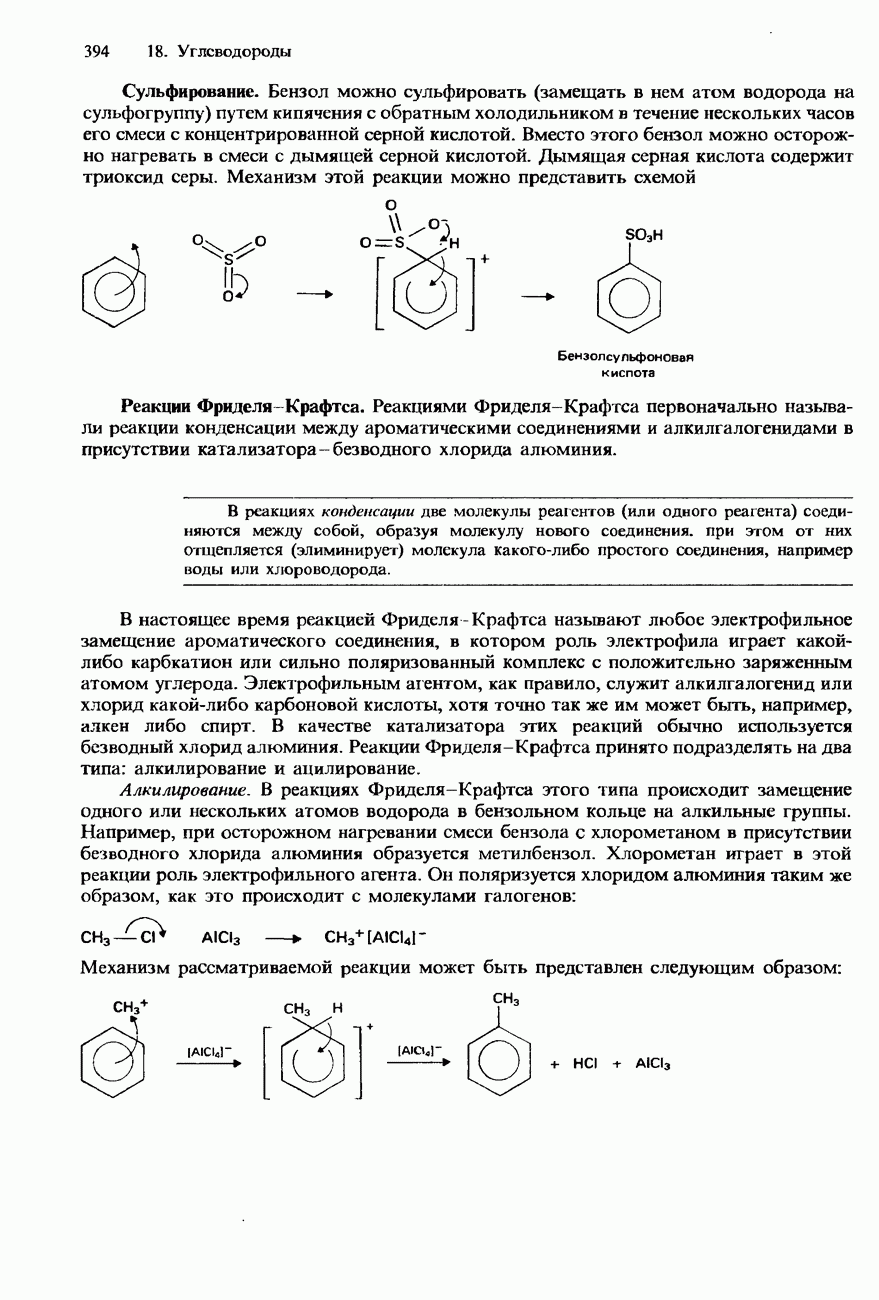
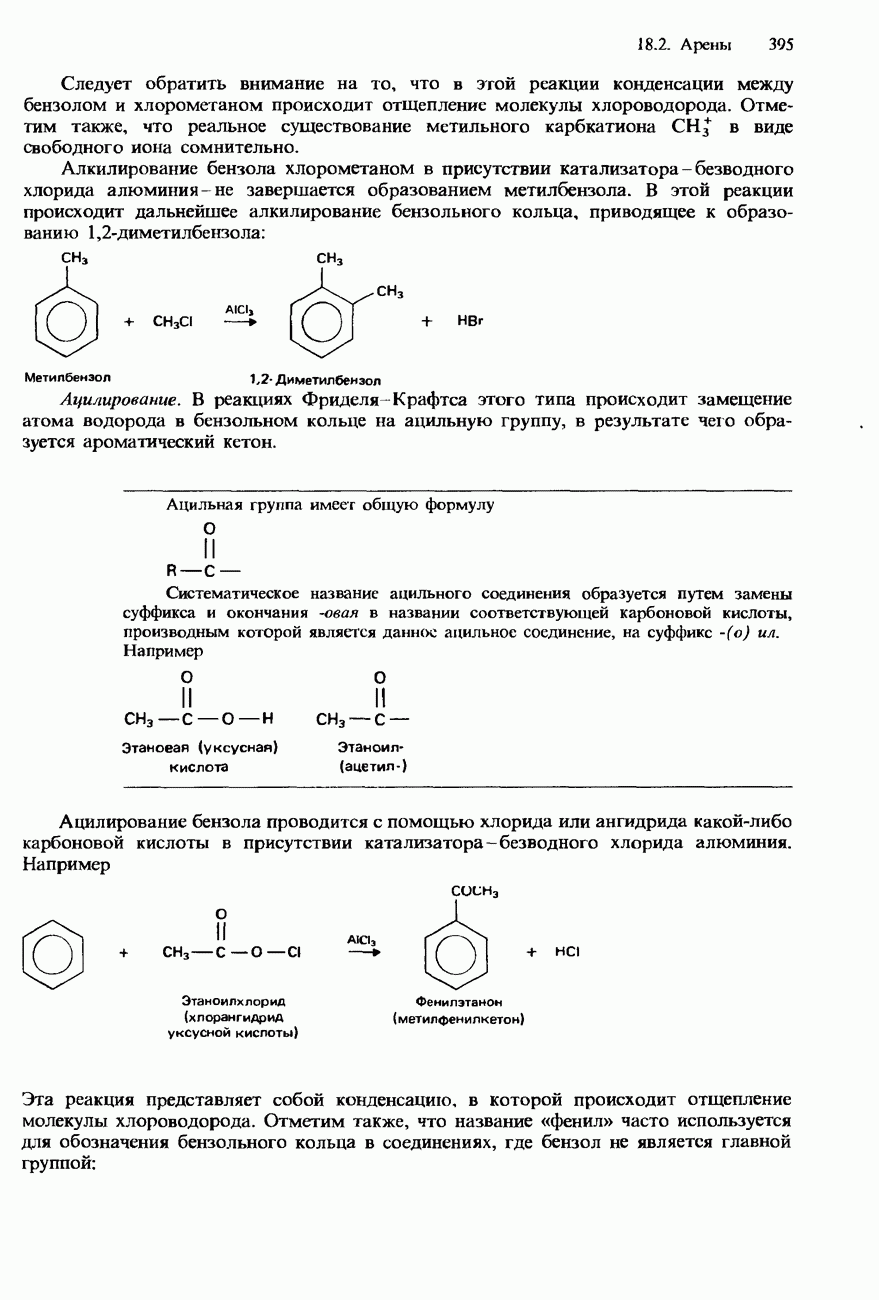
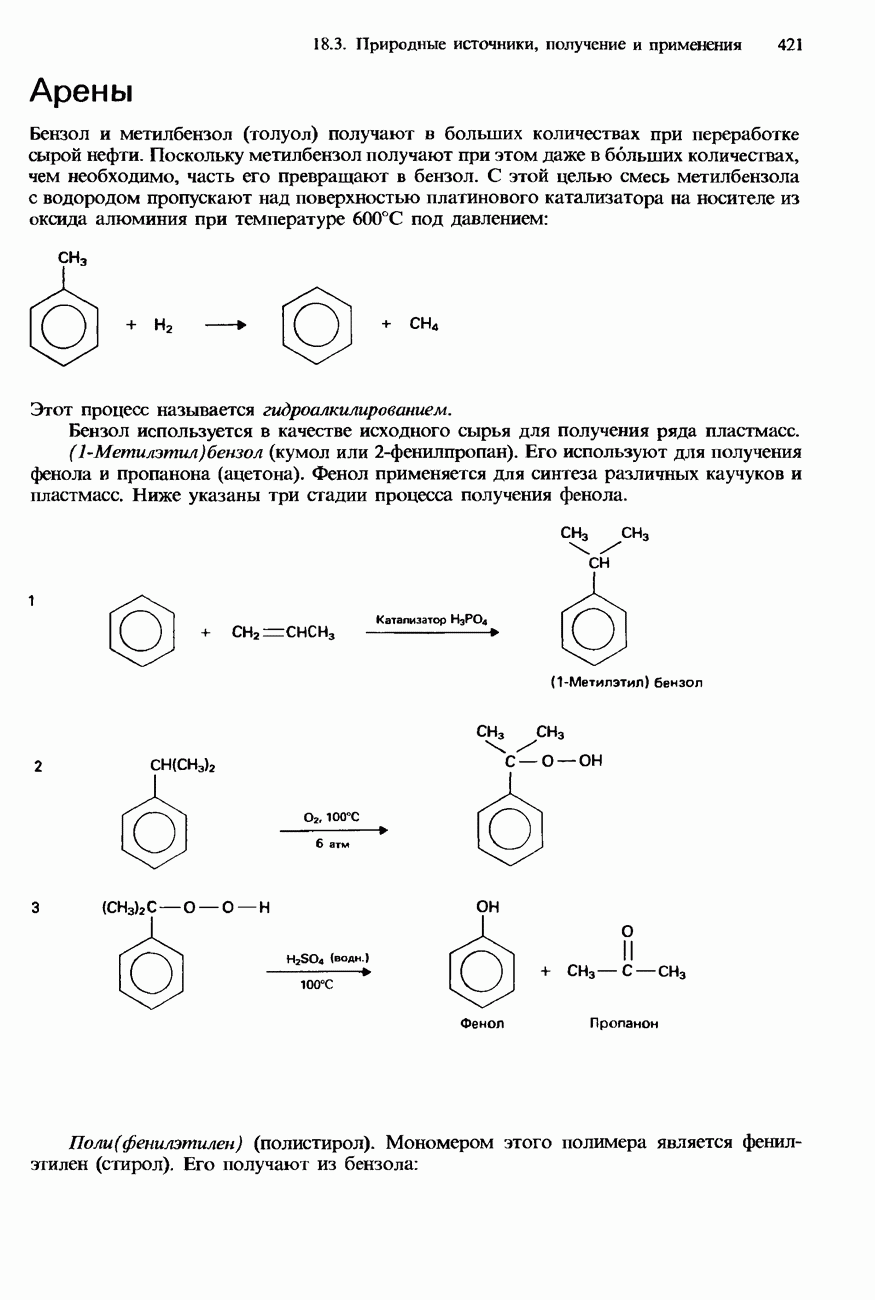
- 18.2. Арены
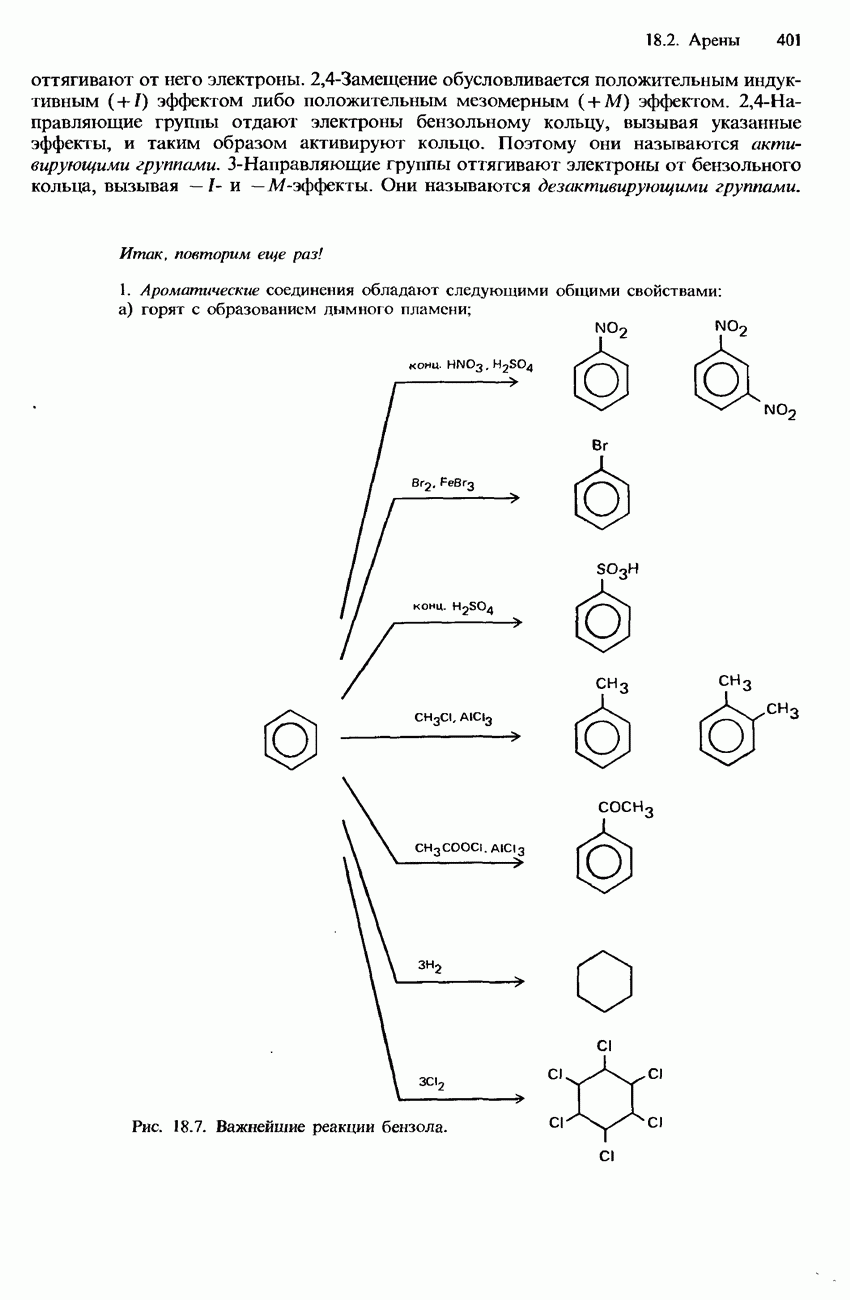
- БЕНЗОЛ
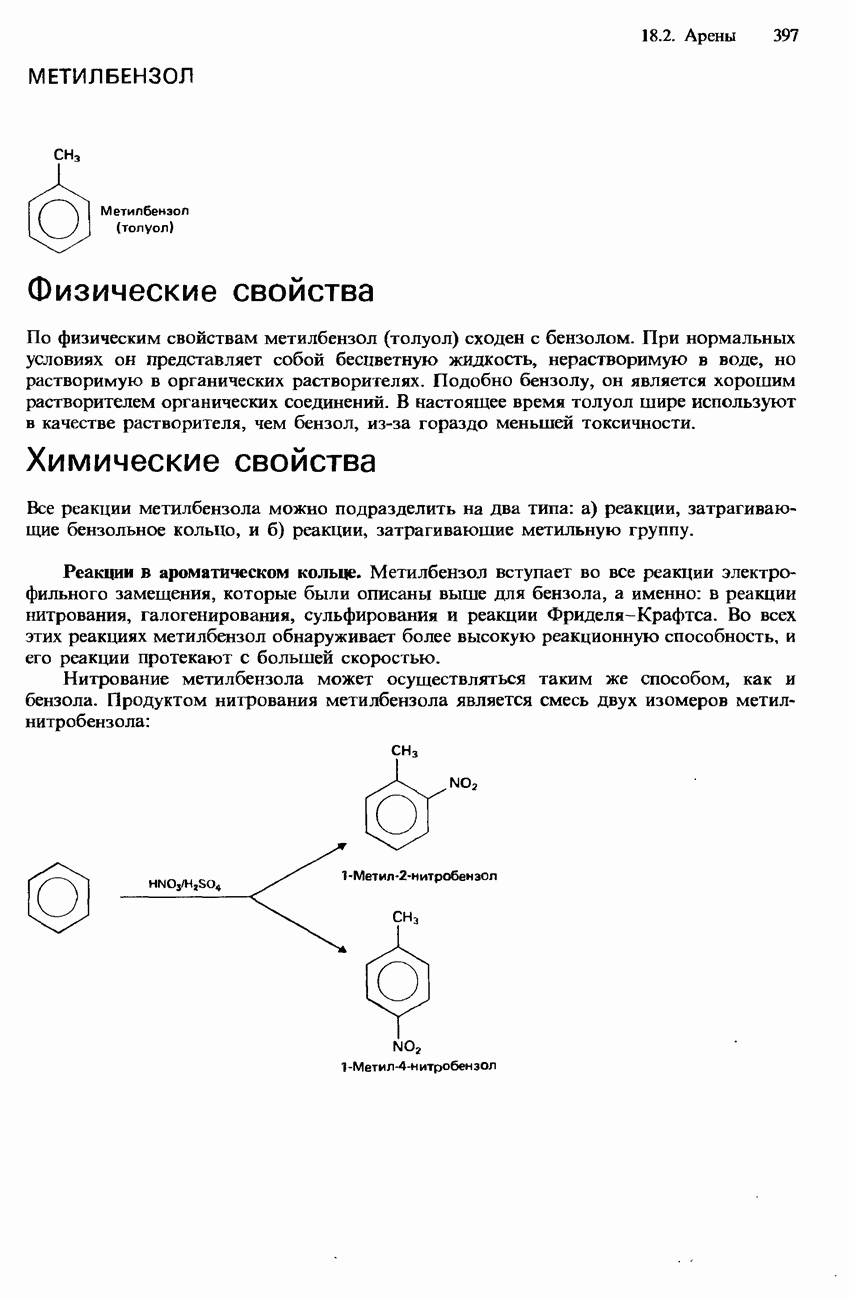
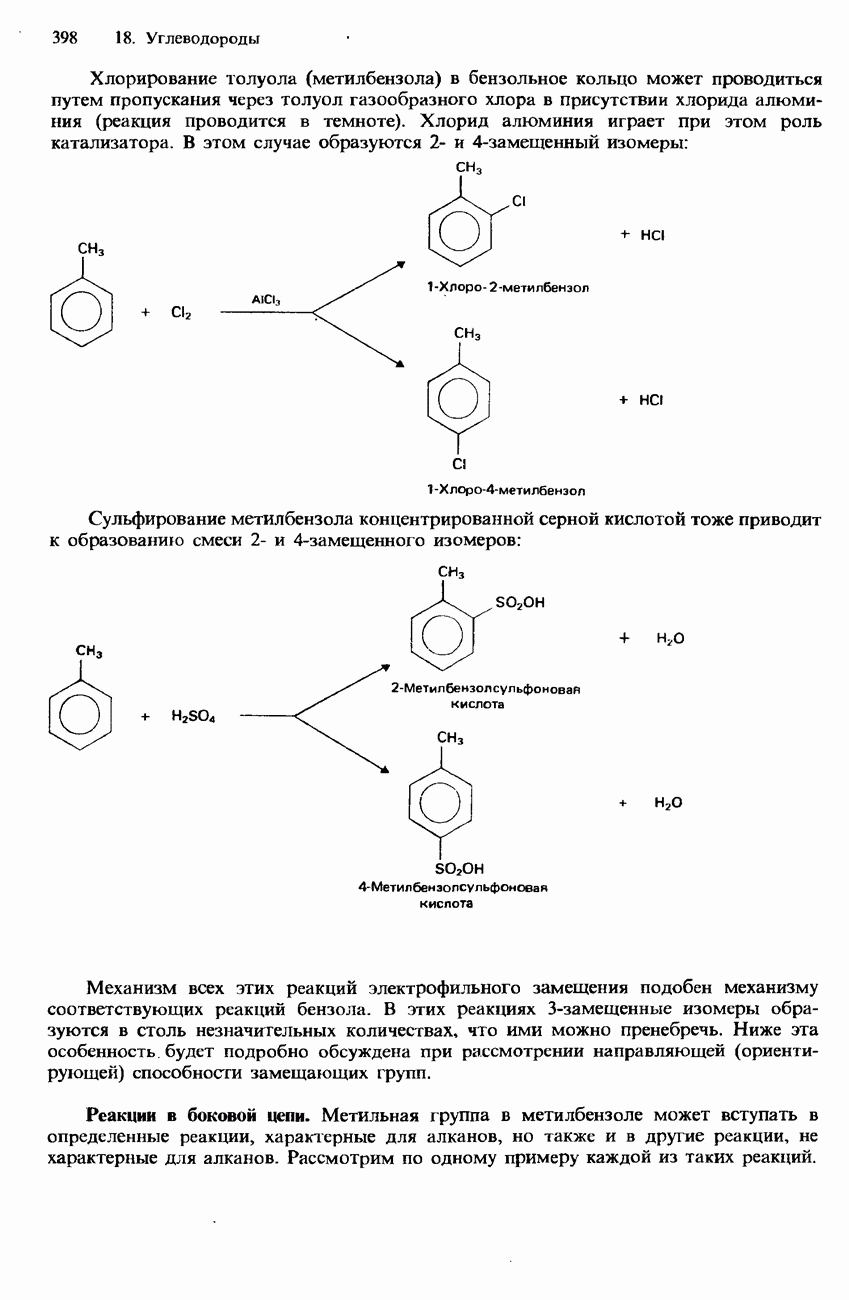
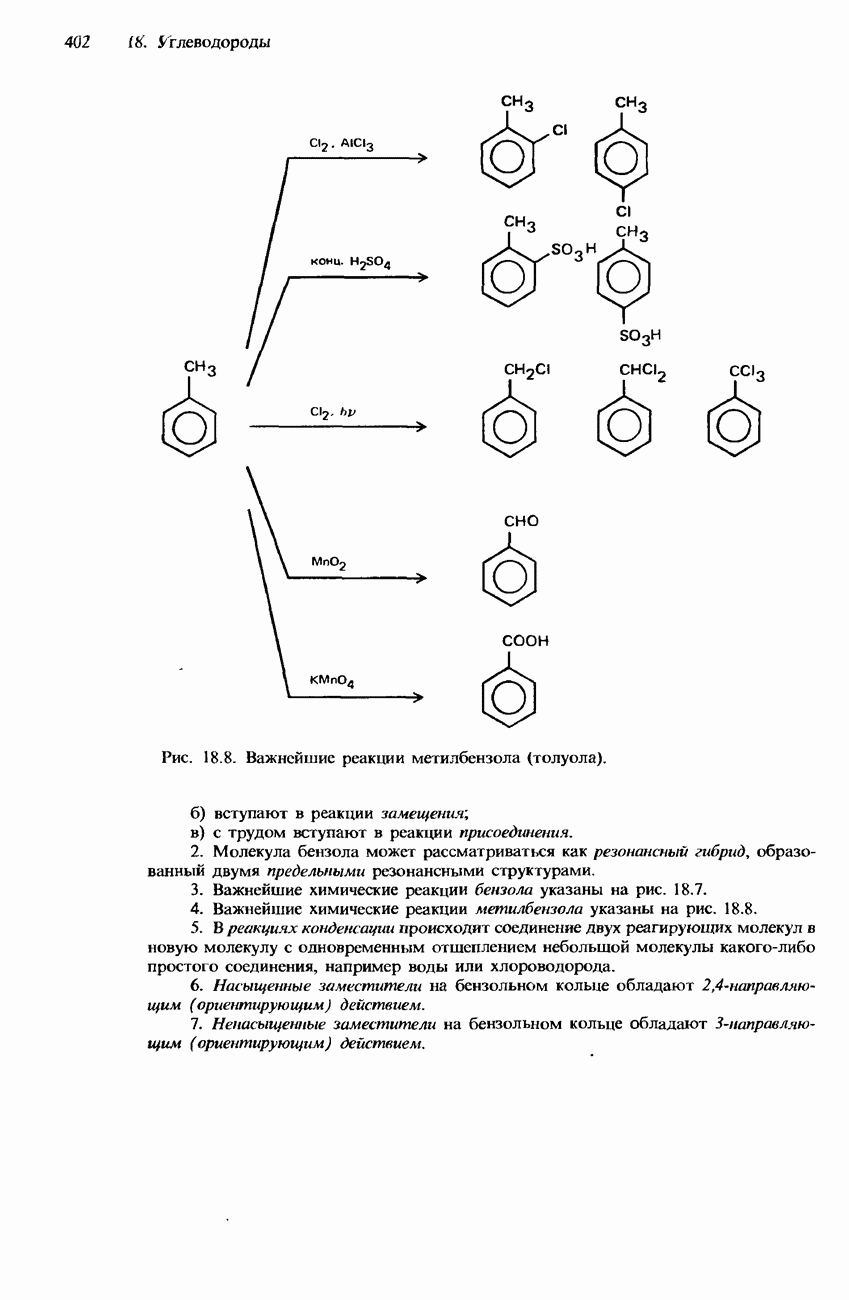
- МЕТИЛБЕНЗОЛ
- 18.3. Природные источники, получение и применения
- ПРОМЫШЛЕННОЕ ПОЛУЧЕНИЕ УГЛЕВОДОРОДОВ
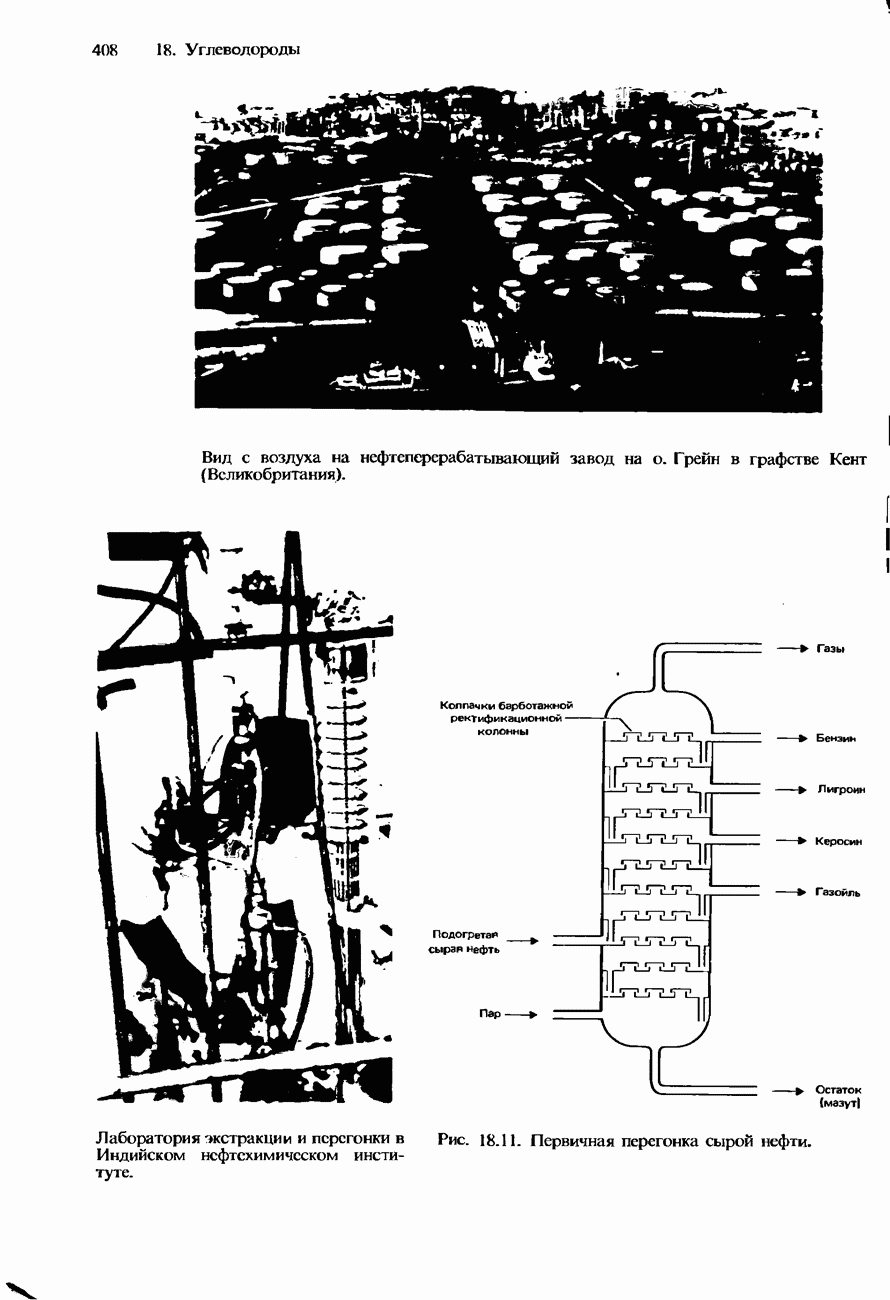
- ПЕРЕРАБОТКА НЕФТИ
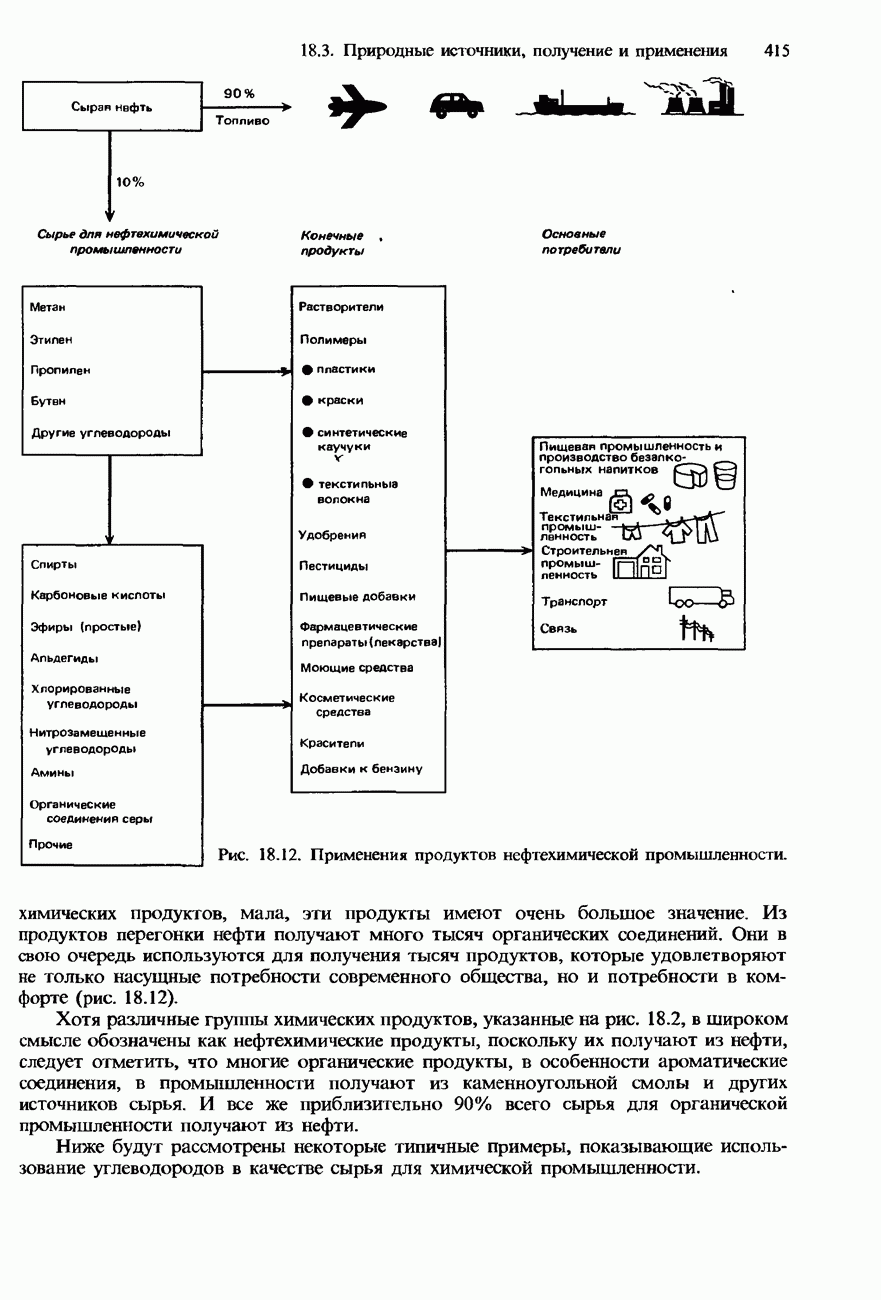
- ПРИМЕНЕНИЯ УГЛЕВОДОРОДОВ
- ЗАГРЯЗНЕНИЕ ОКРУЖАЮЩЕЙ СРЕДЫ НЕФТЬЮ И ПРОДУКТАМИ ЕЕ СГОРАНИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 19. ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
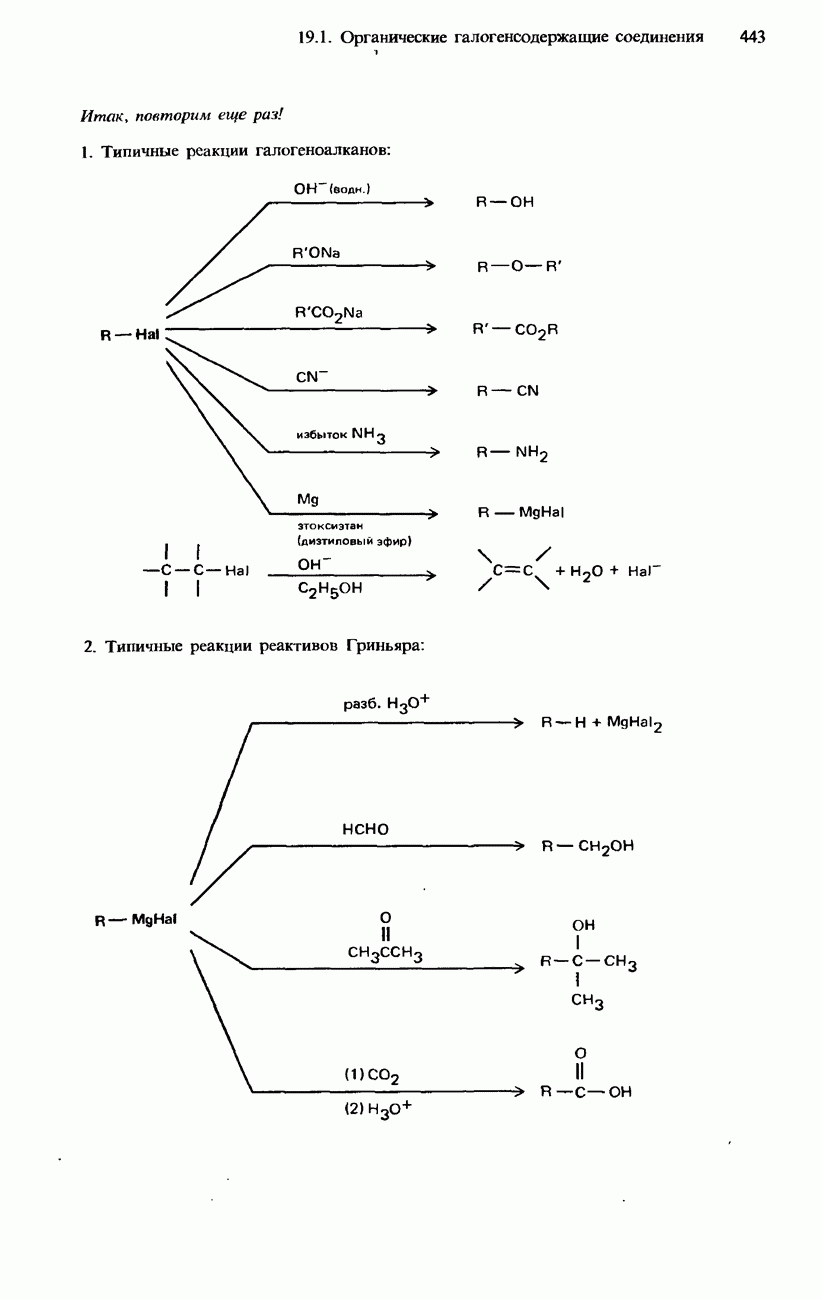
- 19.1. Органические галогенсодержащие соединения
- ГАЛОГЕНОАЛКЕНЫ
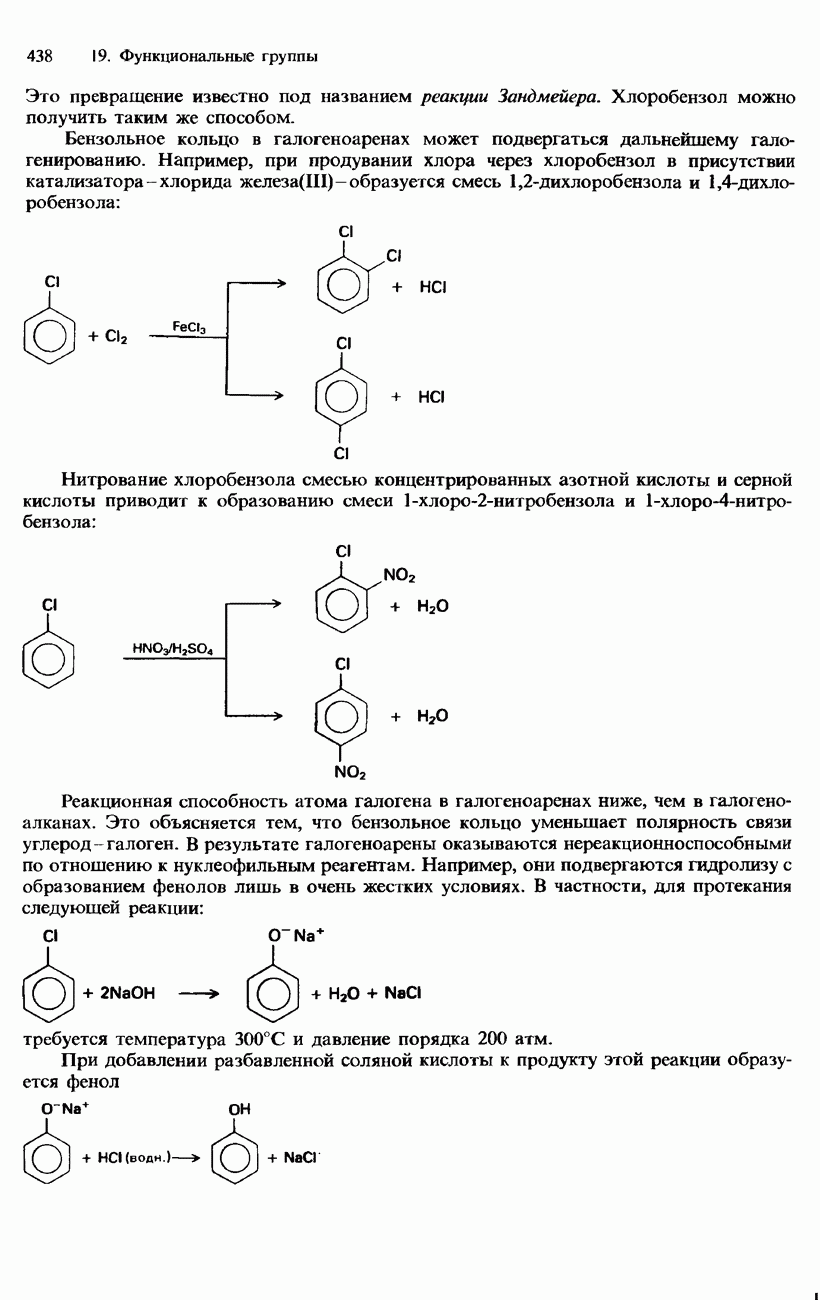
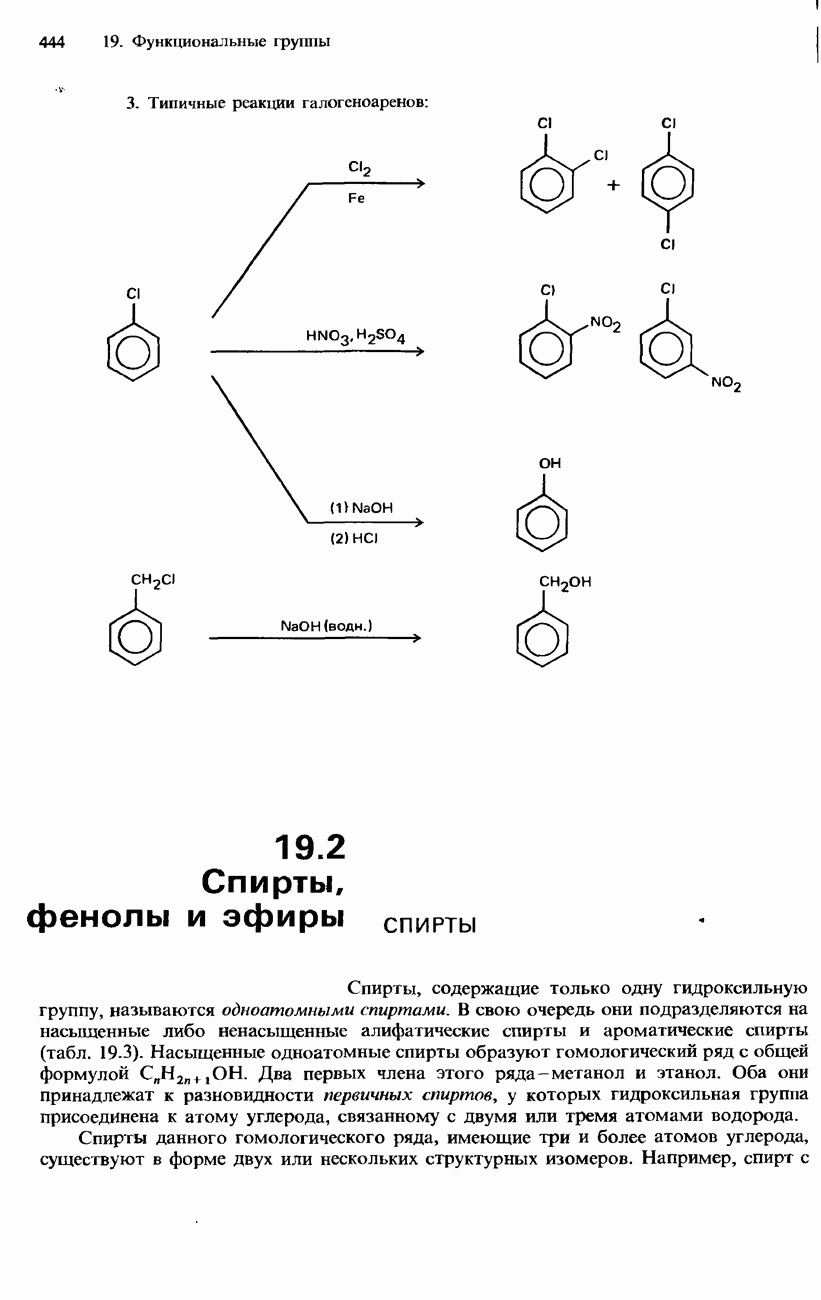
- ГАЛОГЕНОАРЕНЫ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ ОРГАНИЧЕСКИХ ГАЛОГЕНСОДЕРЖАЩИХ СОЕДИНЕНИЙ
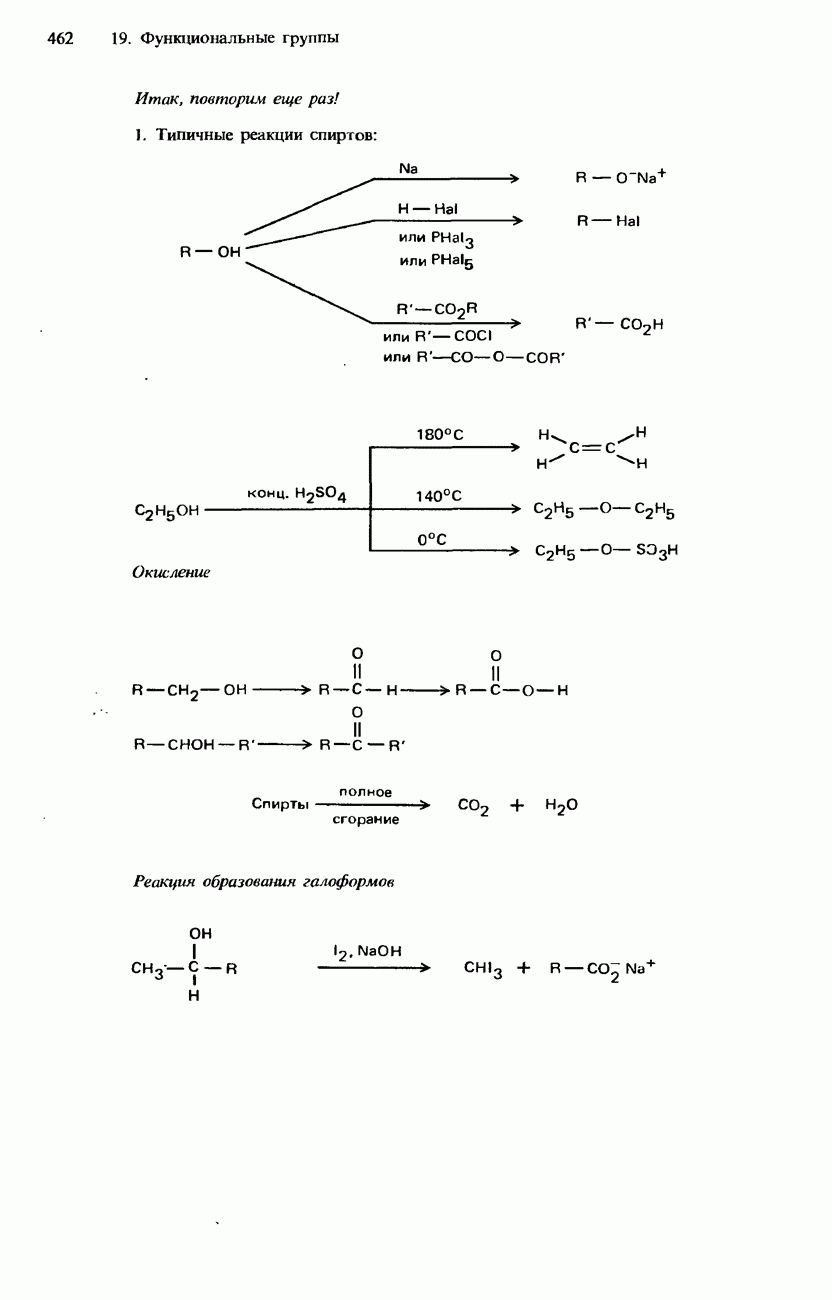
- 19.2. Спирты, фенолы и эфиры
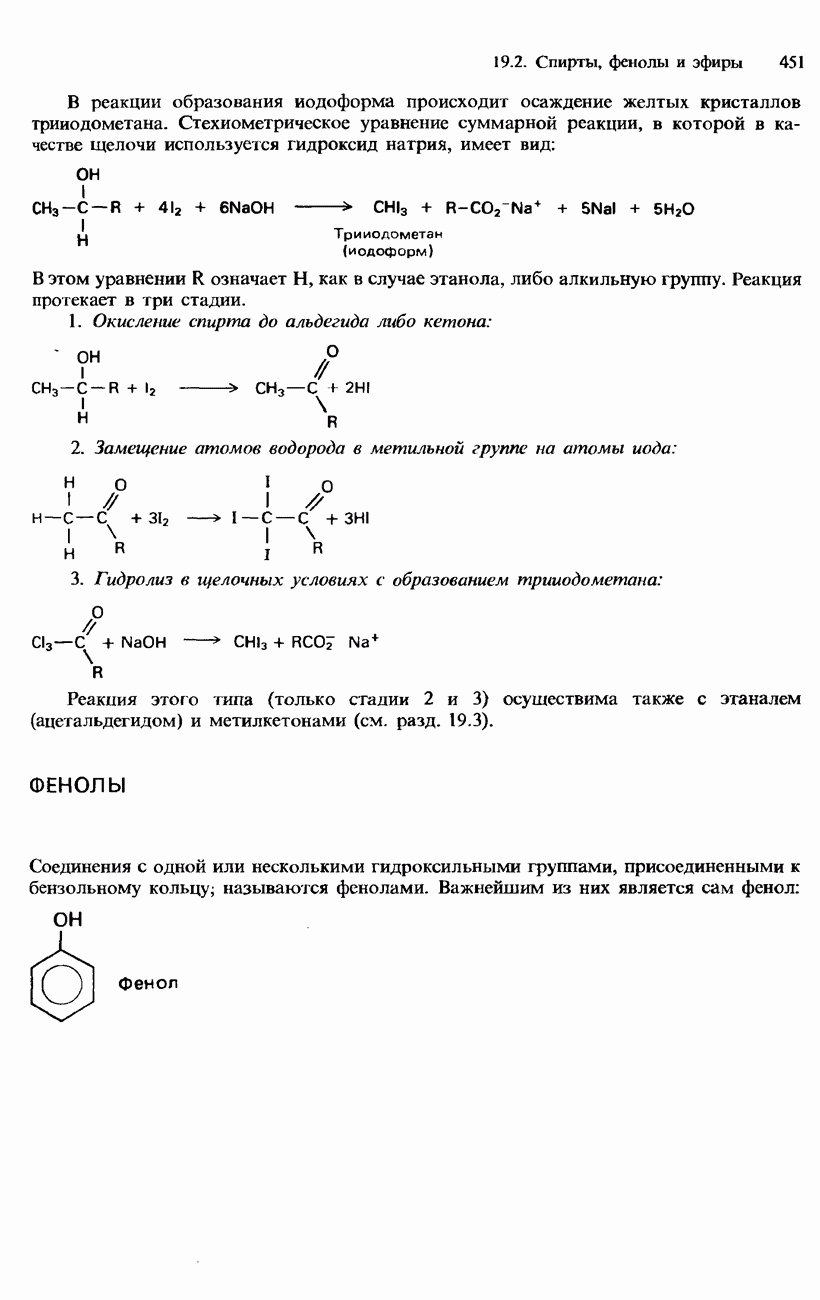
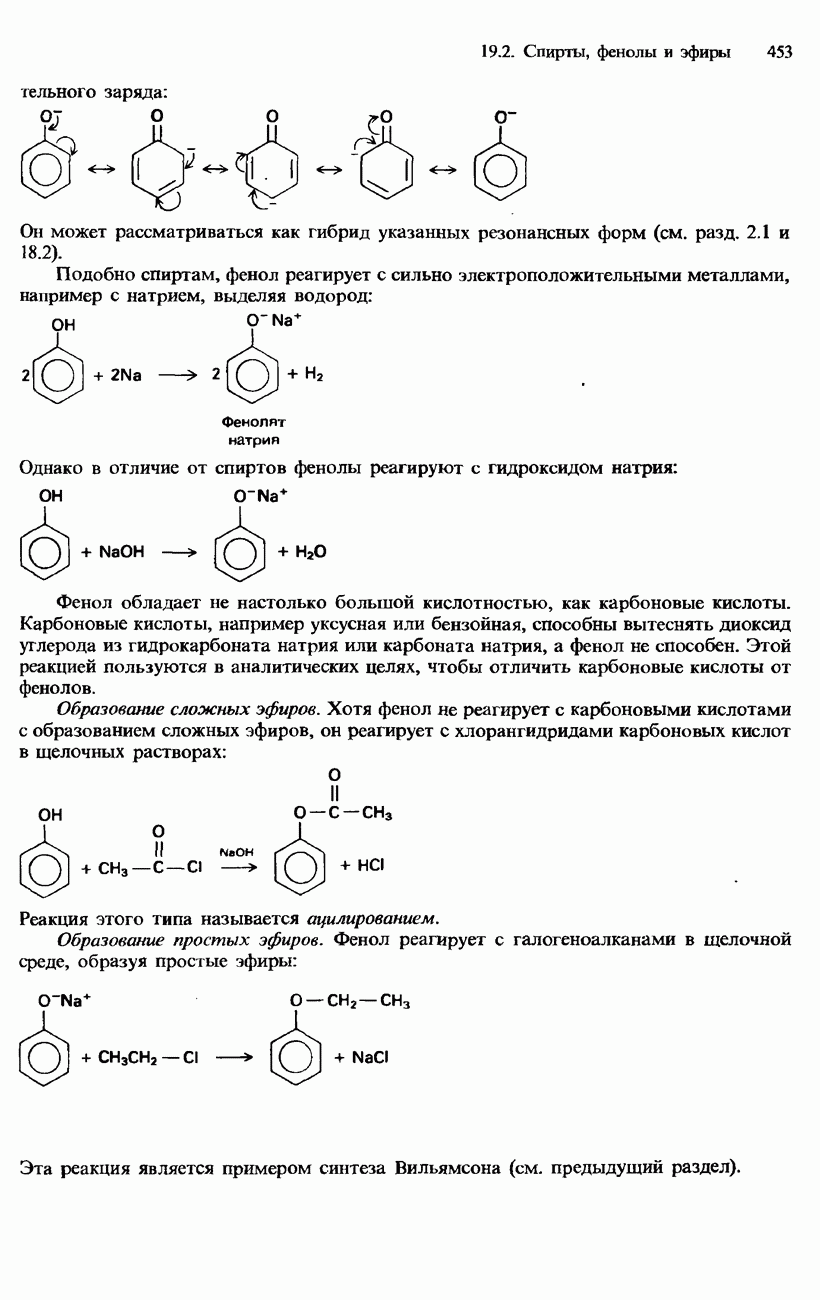
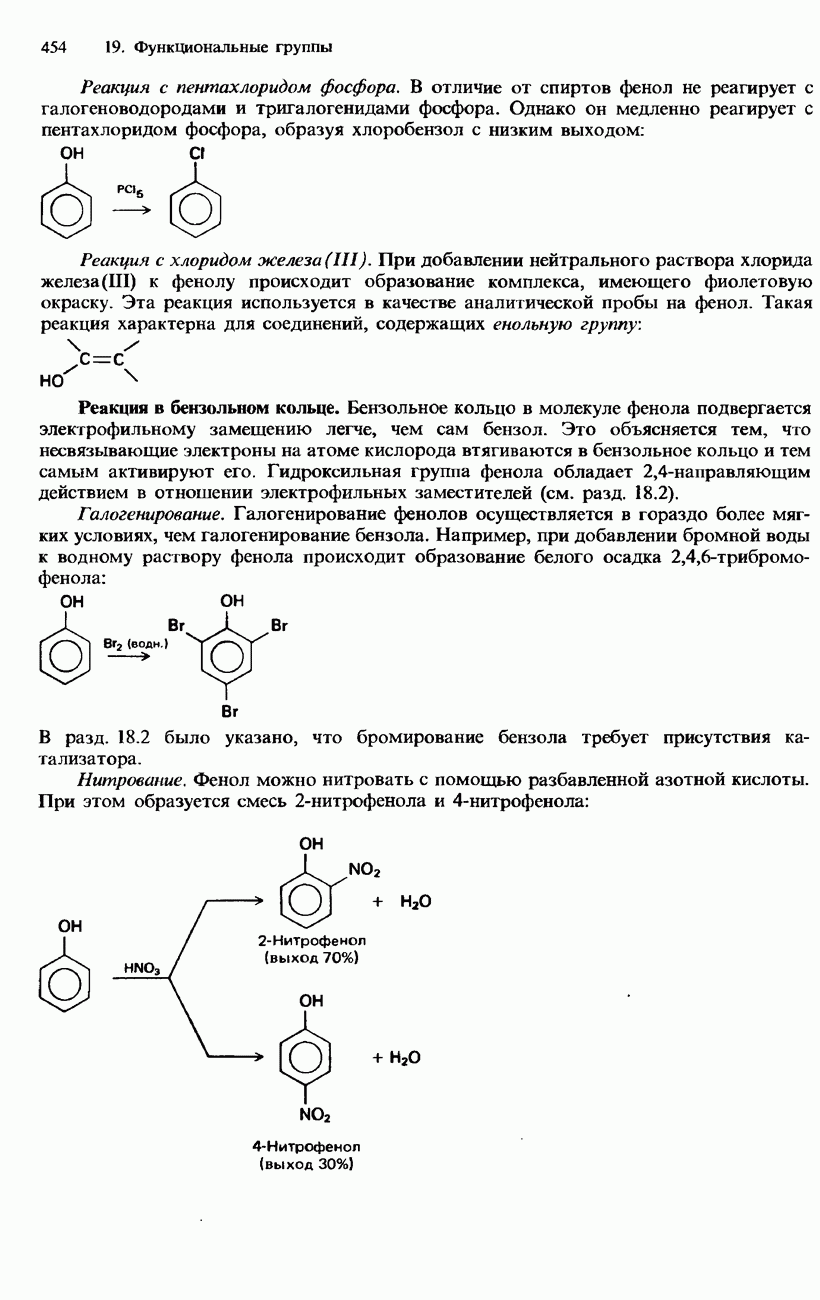
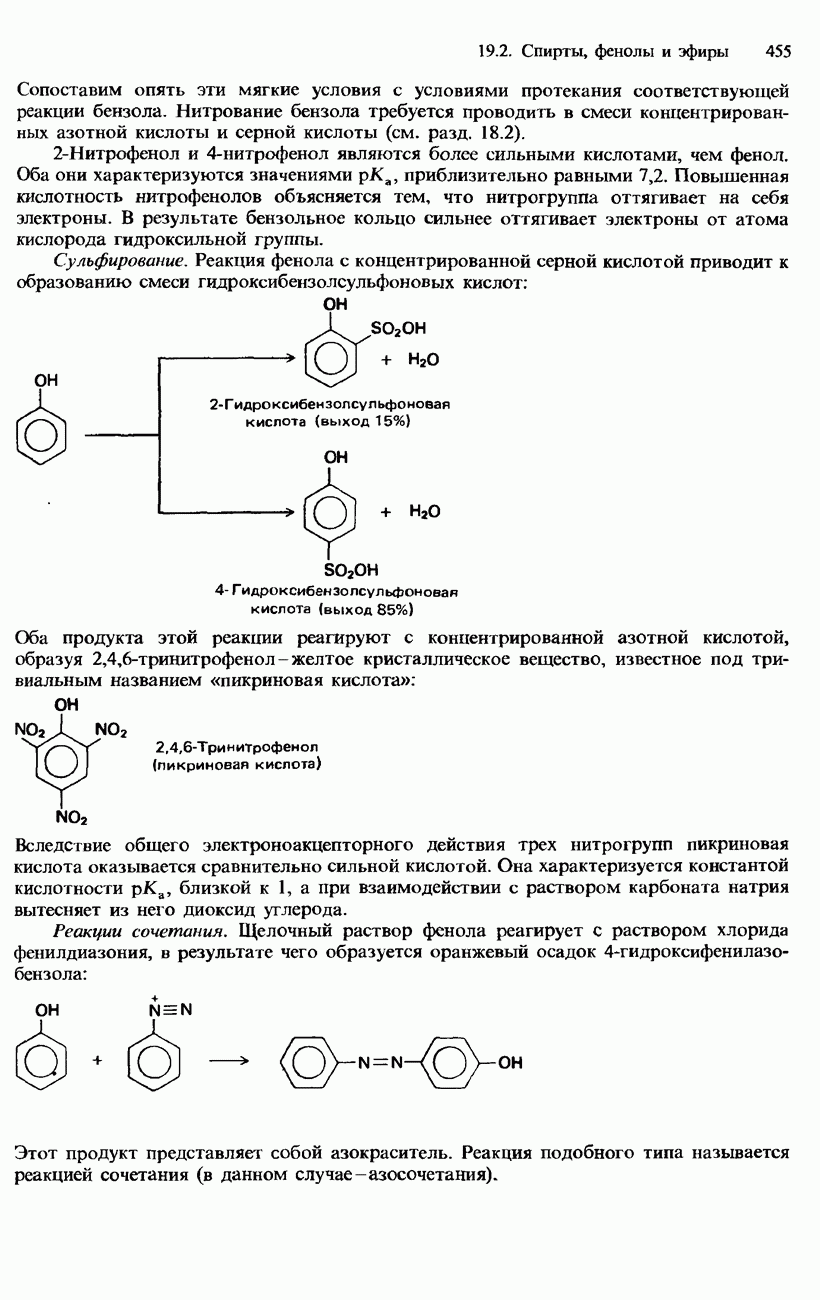
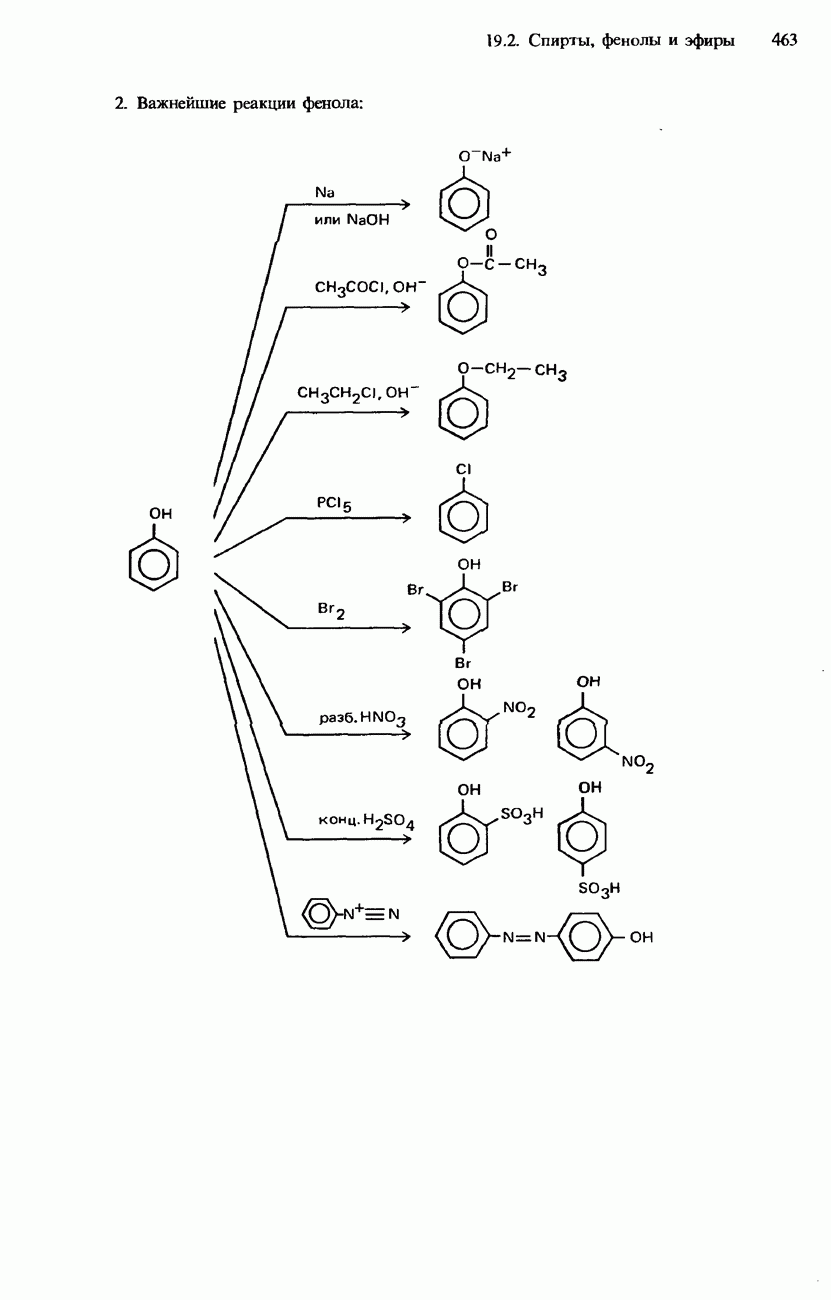
- ФЕНОЛЫ
- ПРОСТЫЕ ЭФИРЫ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ СПИРТОВ, ФЕНОЛОВ И ПРОСТЫХ ЭФИРОВ
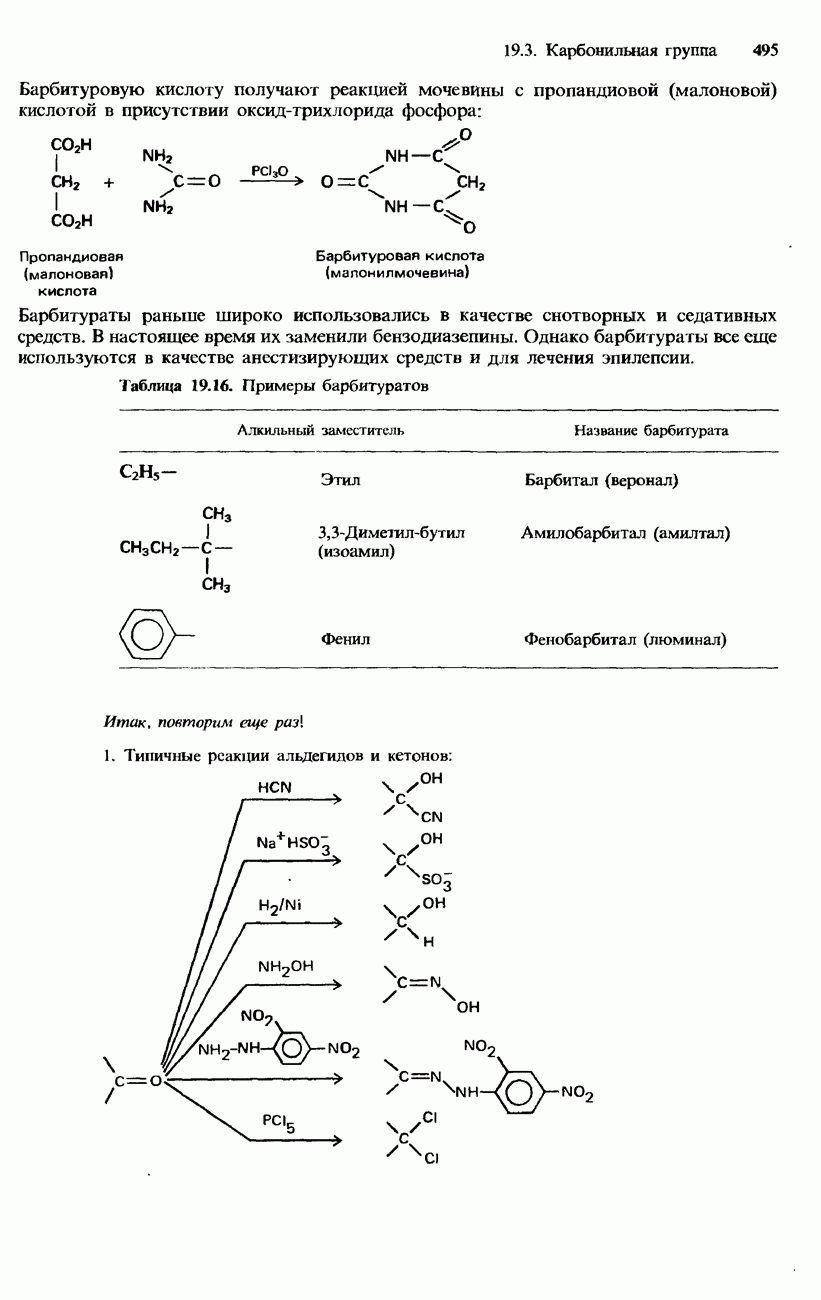
- 19.3. Карбонильная группа
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ
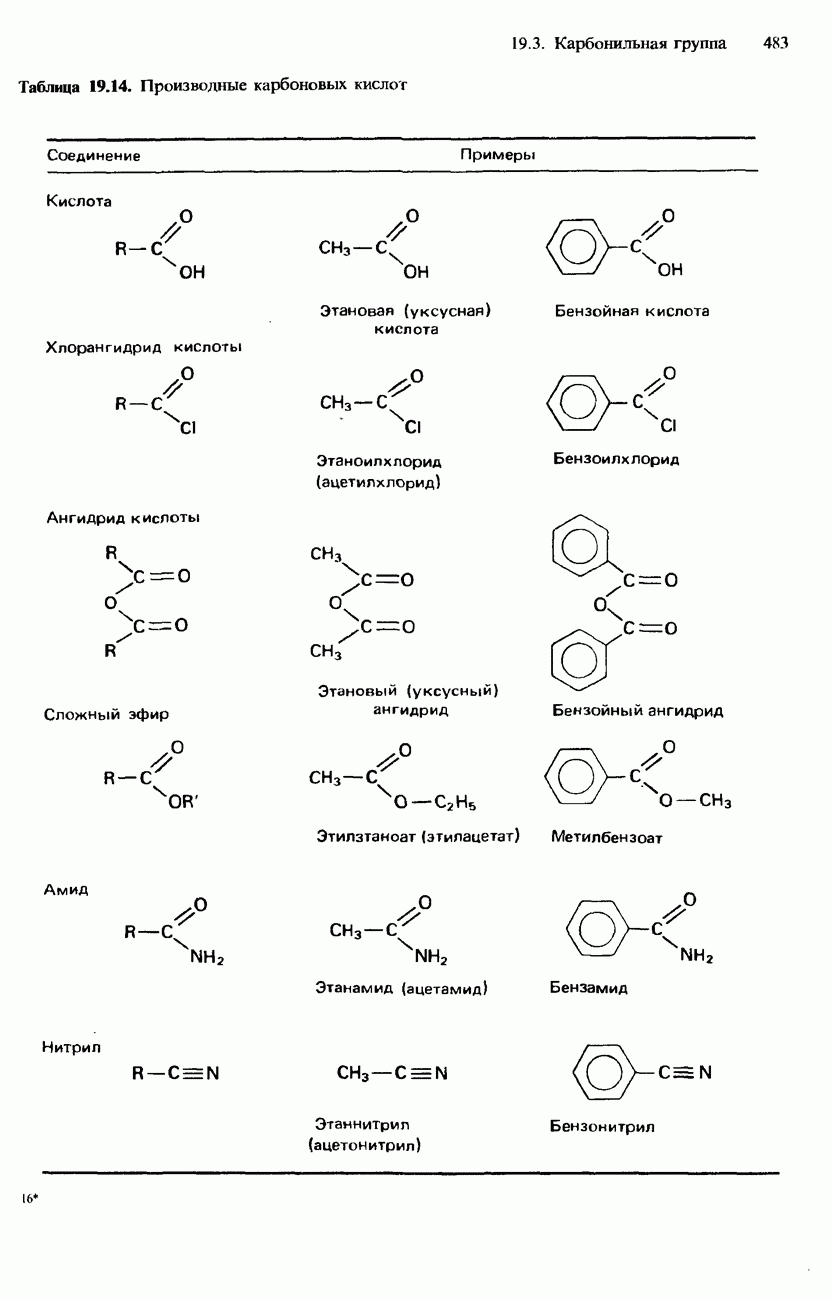
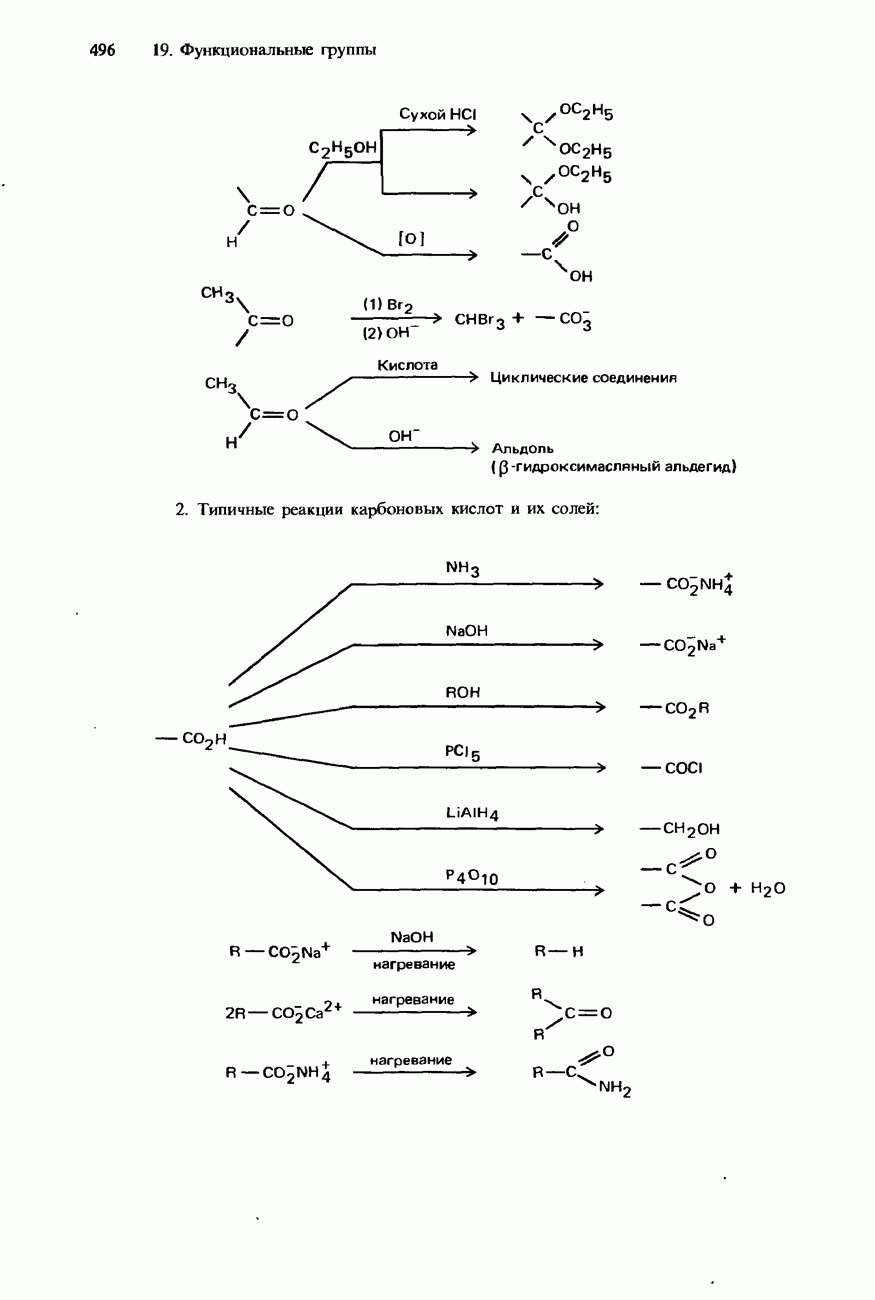
- КАРБОНОВЫЕ КИСЛОТЫ
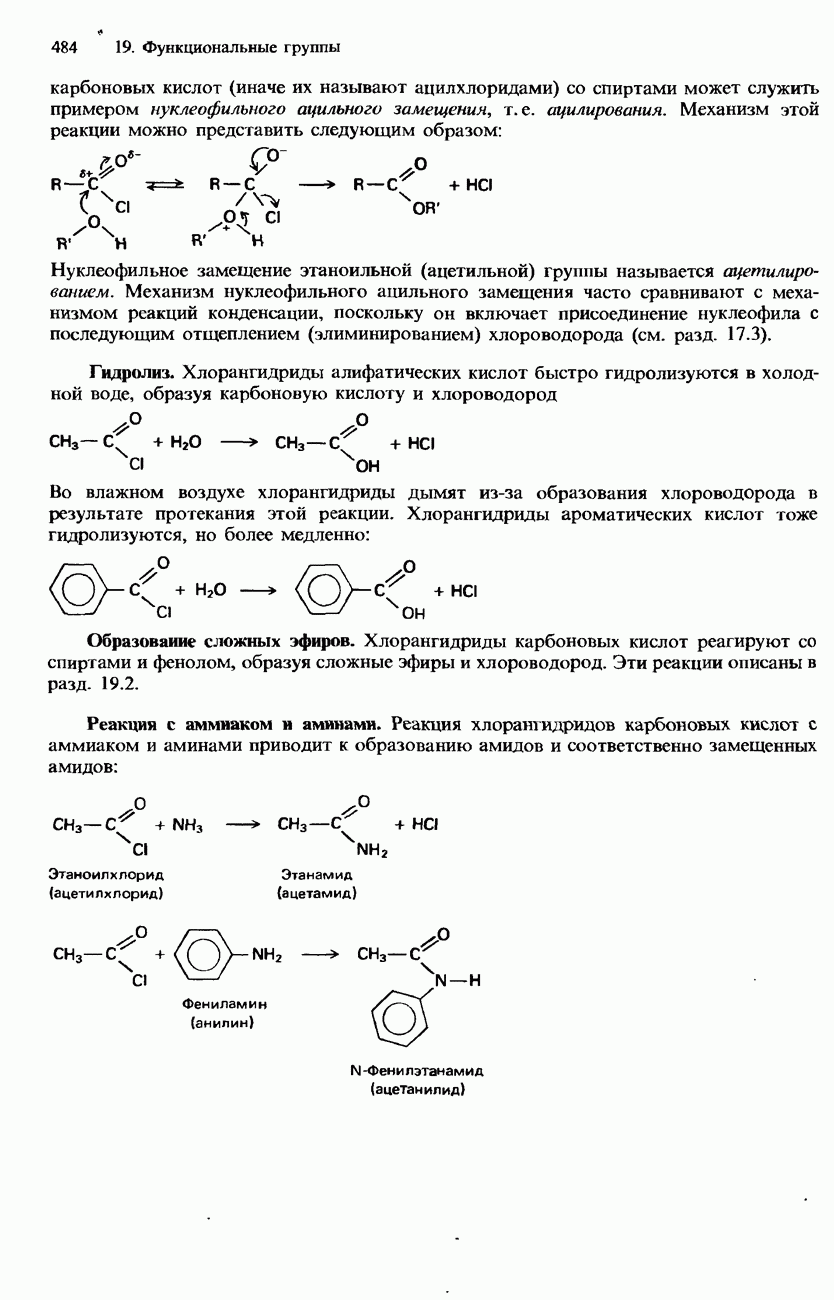
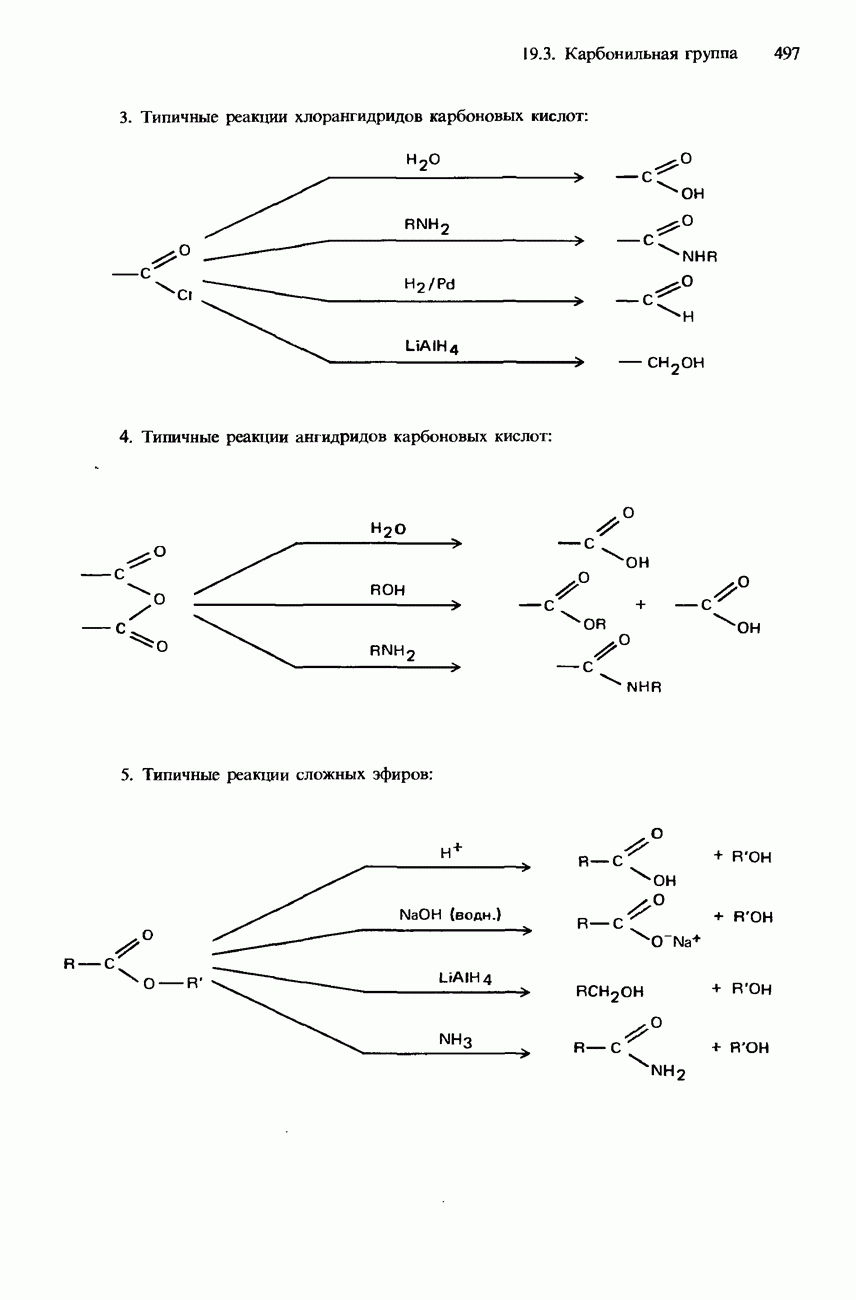
- ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ
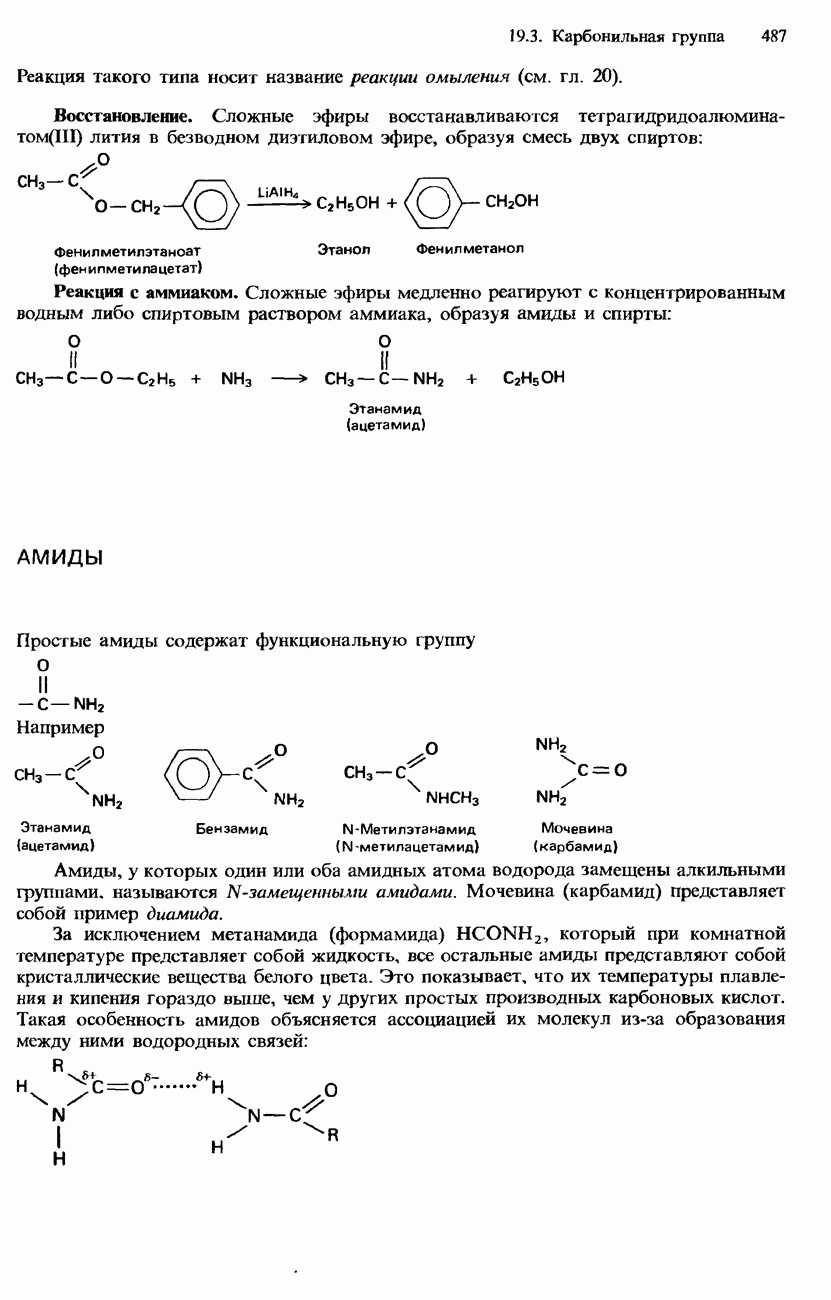
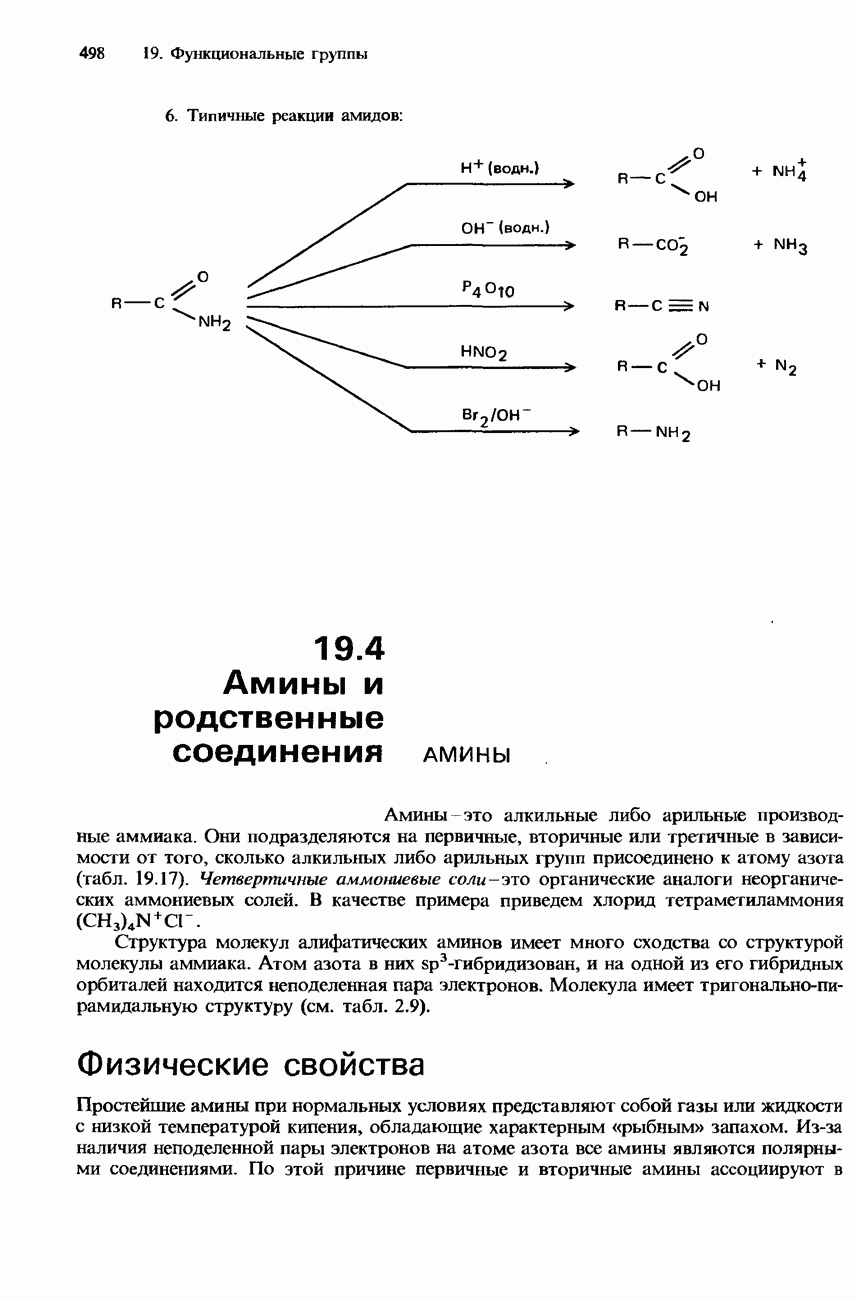
- АМИДЫ
- РАСПРОСТРАНЕННОСТЬ В ПРИРОДЕ, ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ КАРБОНОВЫХ КИСЛОТ И ИХ ПРОИЗВОДНЫХ
- 19.4 Амины и родственные соединения
- СОЛИ ДИАЗОНИЯ
- ПРОМЫШЛЕННЫЕ МЕТОДЫ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЯ
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- 20. ПРИРОДНЫЕ СОЕДИНЕНИЯ И ПОЛИМЕРЫ
- 20.1. Аминокислоты, пептиды и белки
- АМИНОКИСЛОТЫ
- ПЕПТИДЫ
- БЕЛКИ
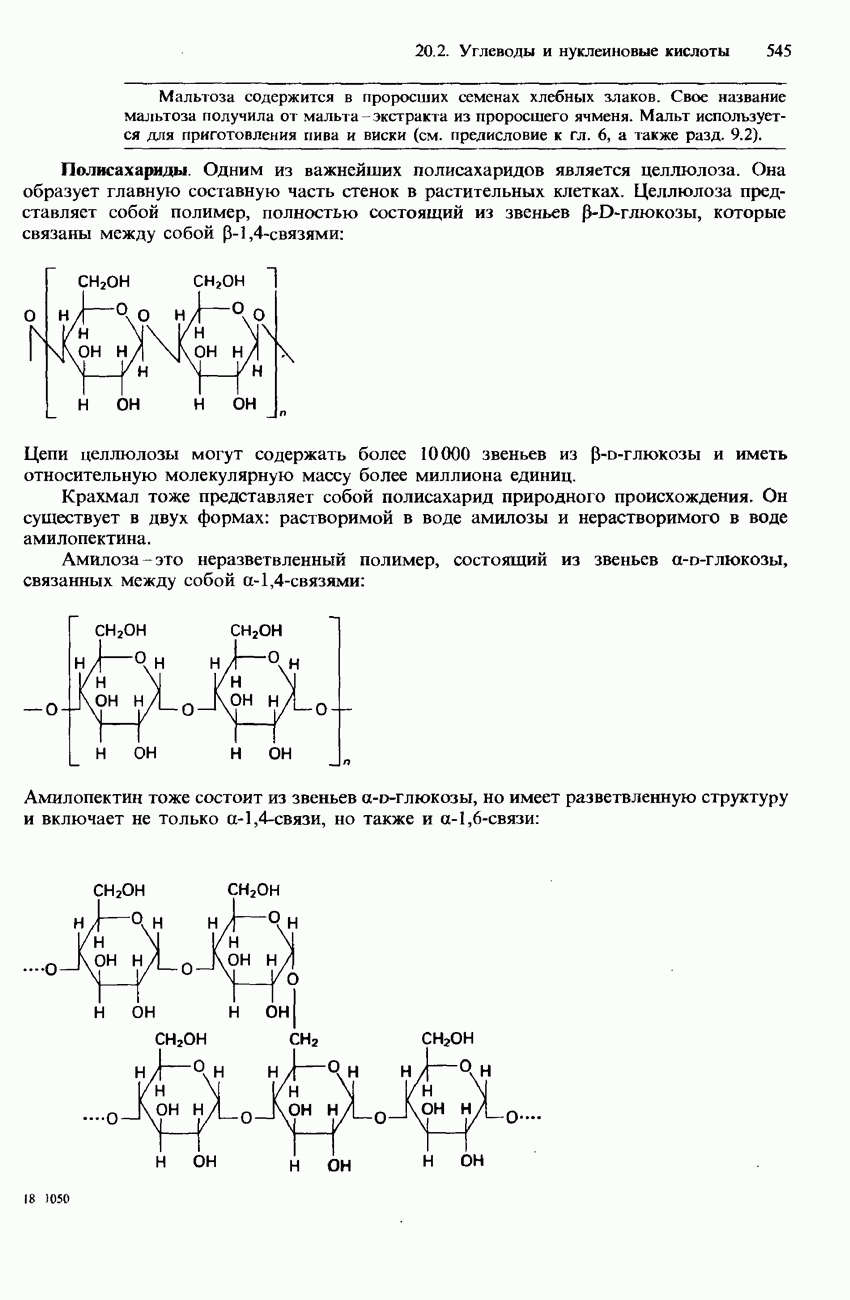
- 20.2. Углеводы и нуклеиновые кислоты
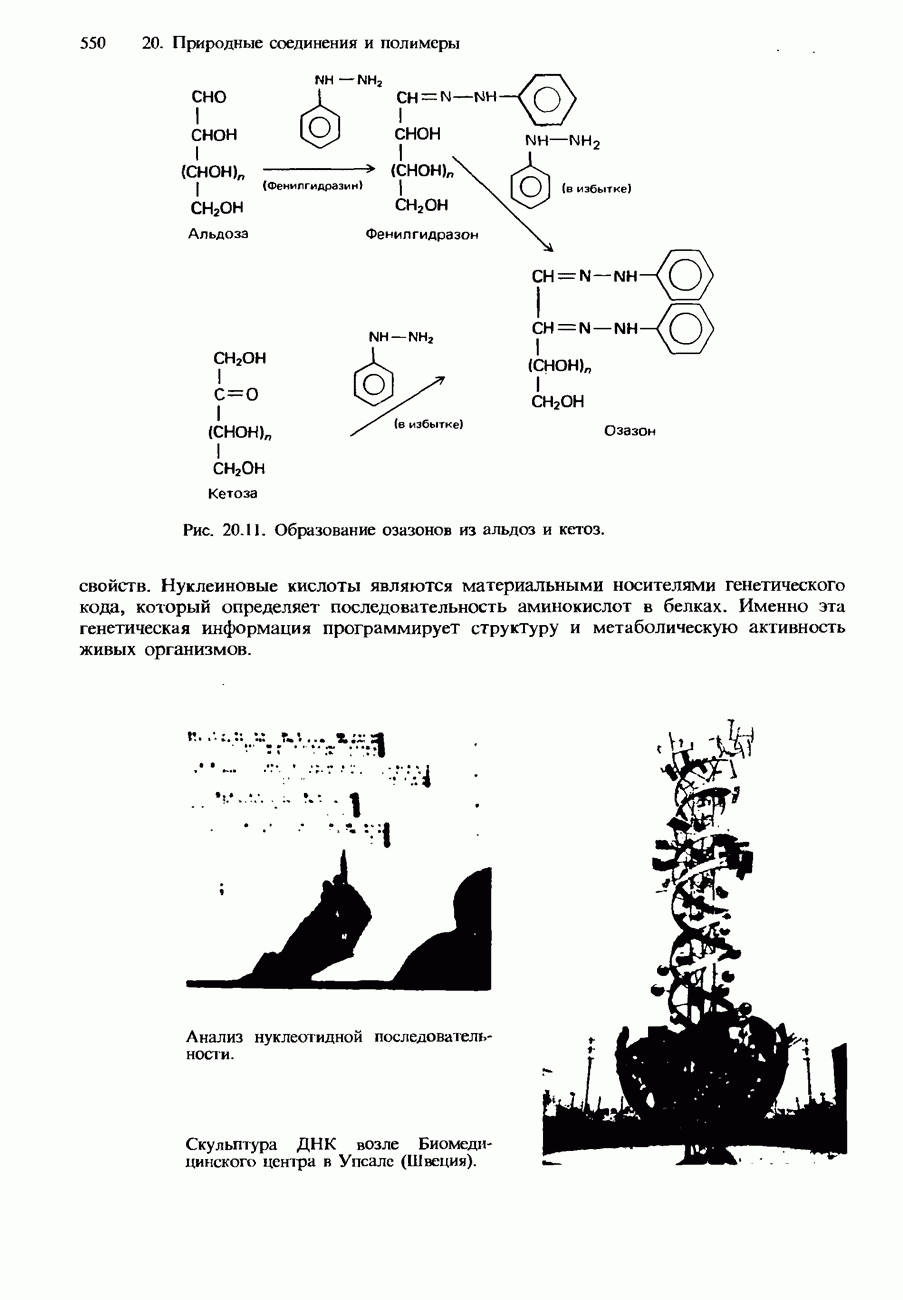
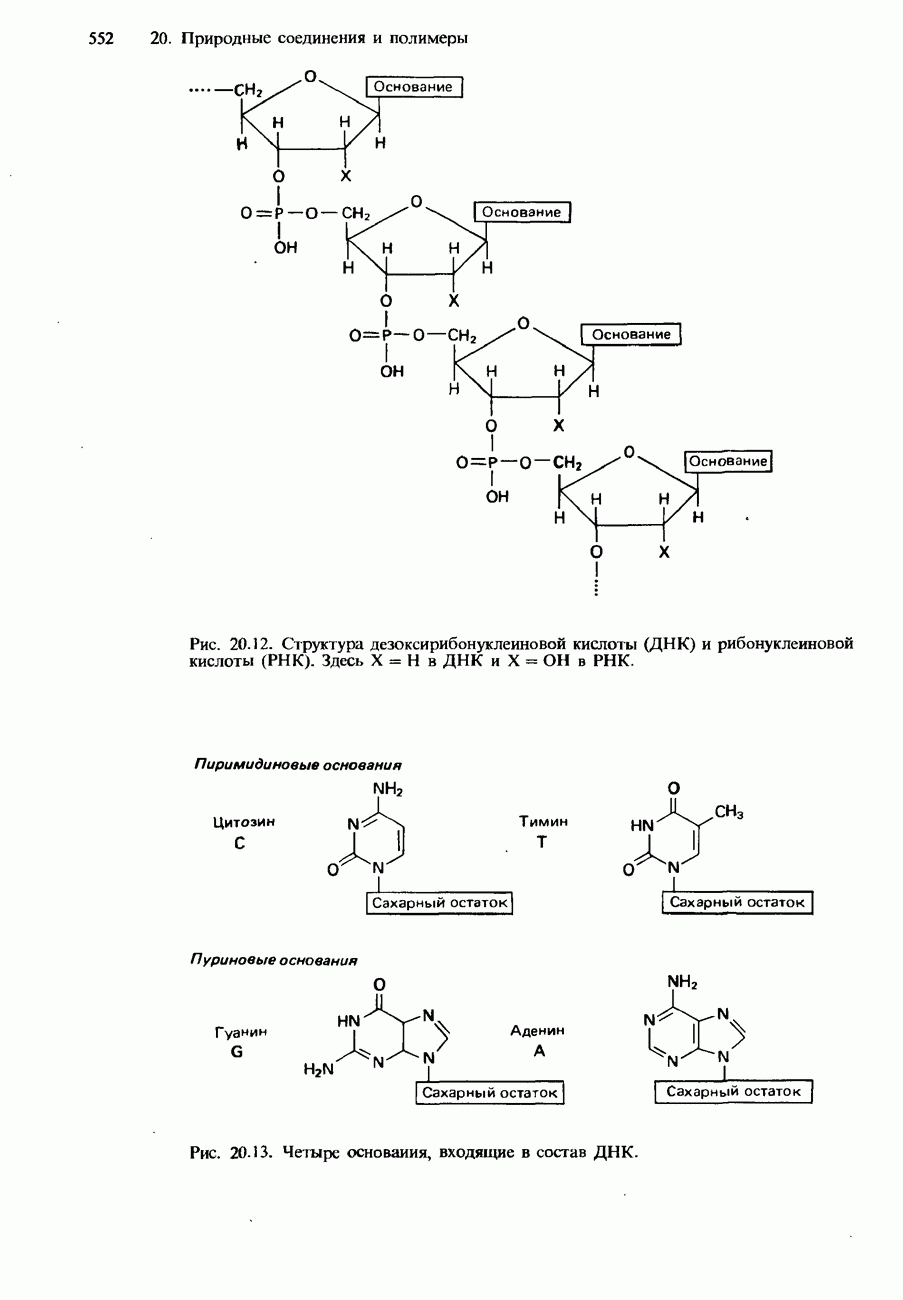
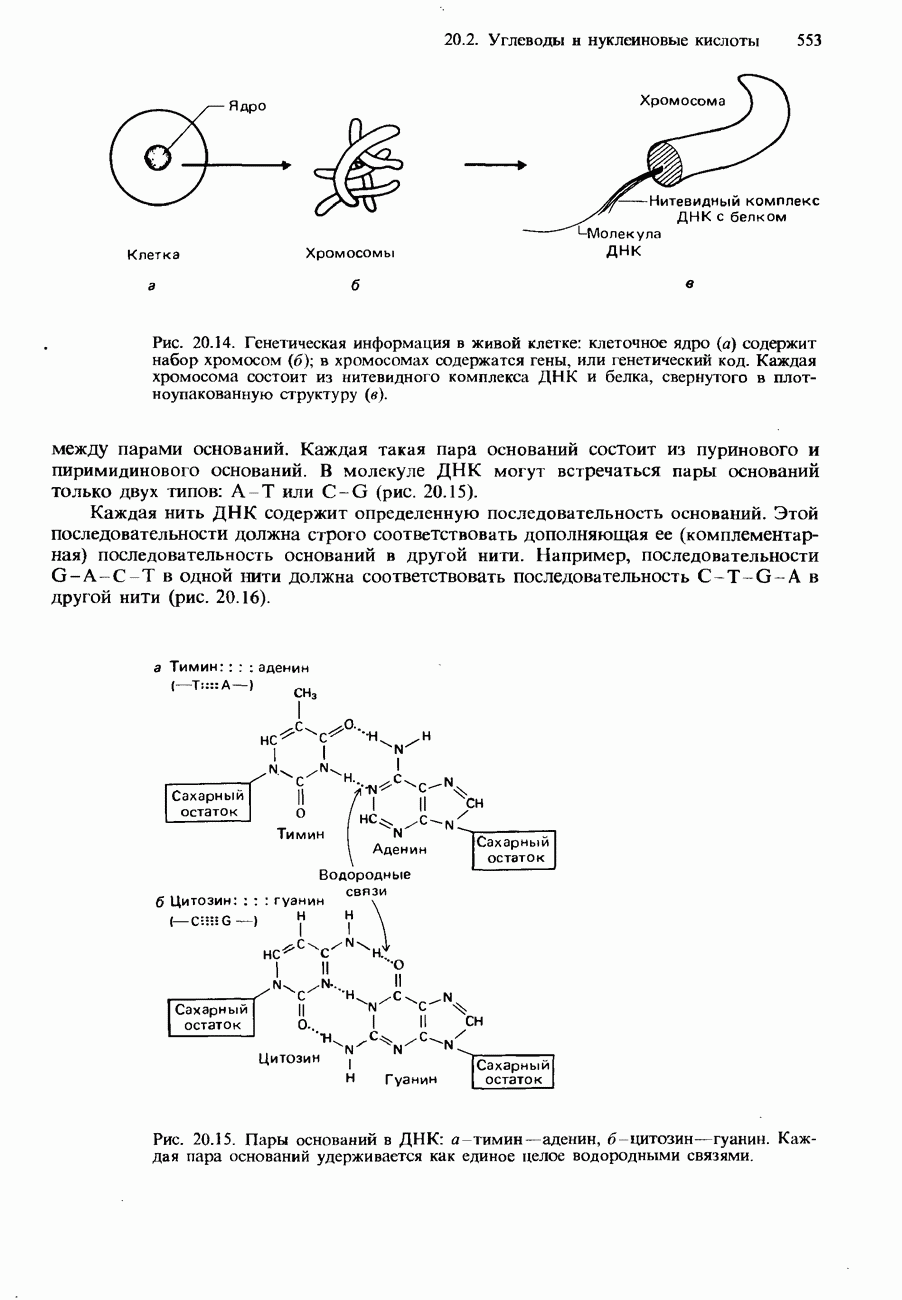
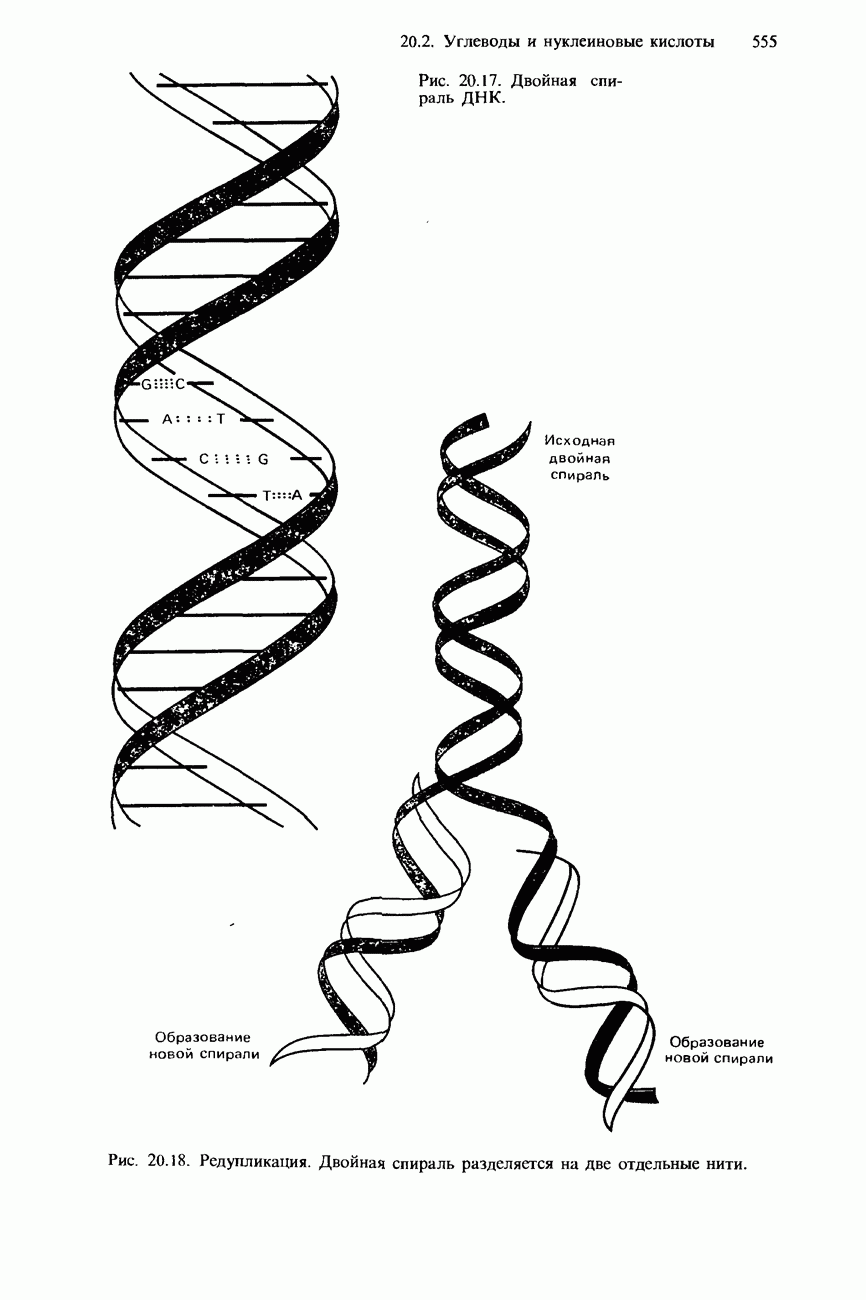
- НУКЛЕИНОВЫЕ КИСЛОТЫ
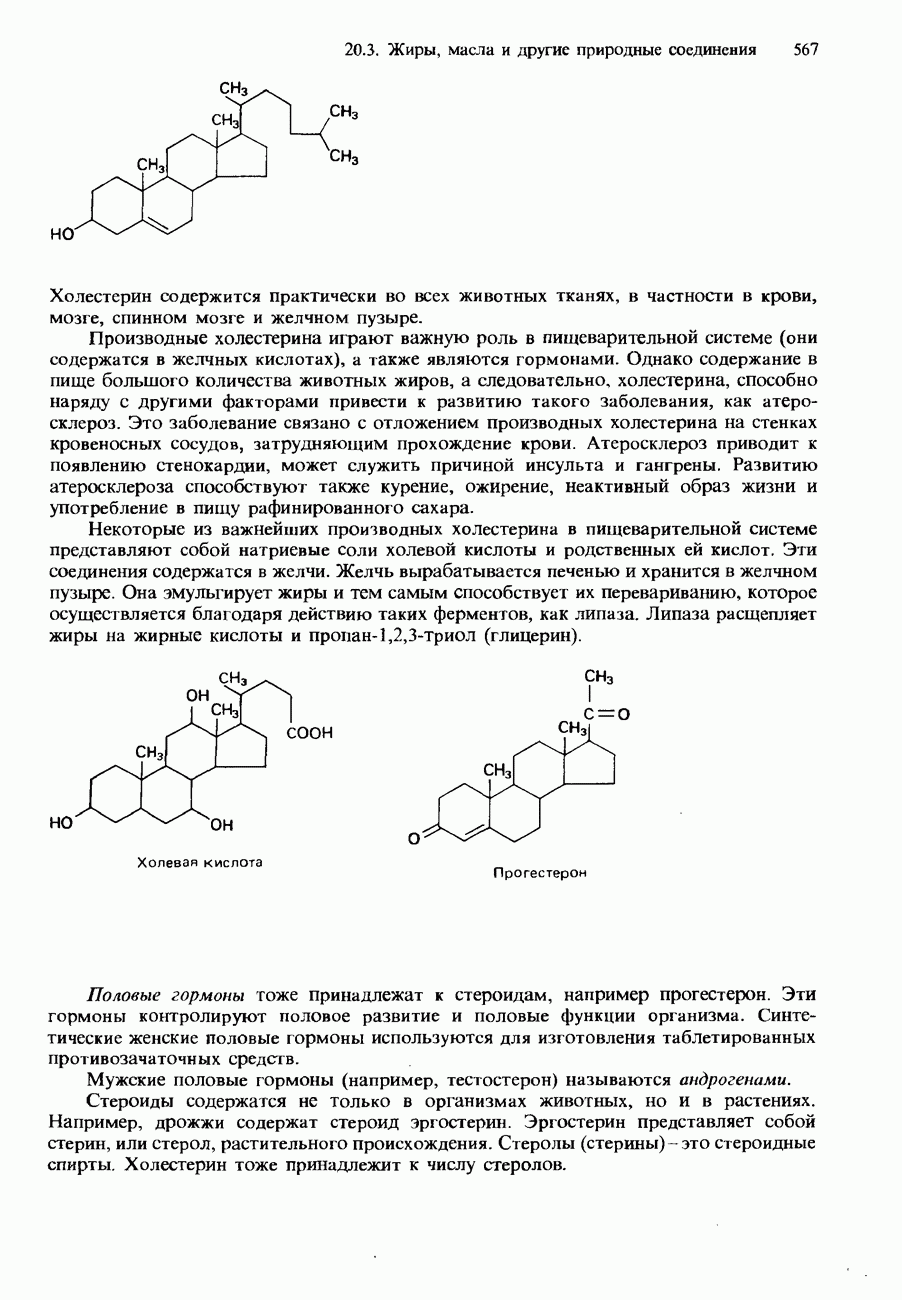
- 20.3. Жиры, масла и другие природные соединения
- ЖИРНЫЕ КИСЛОТЫ И ТРИГЛИЦЕРИДЫ
- ВОСКИ
- ФОСФОЛИПИДЫ И ГЛИКОЛИПИДЫ
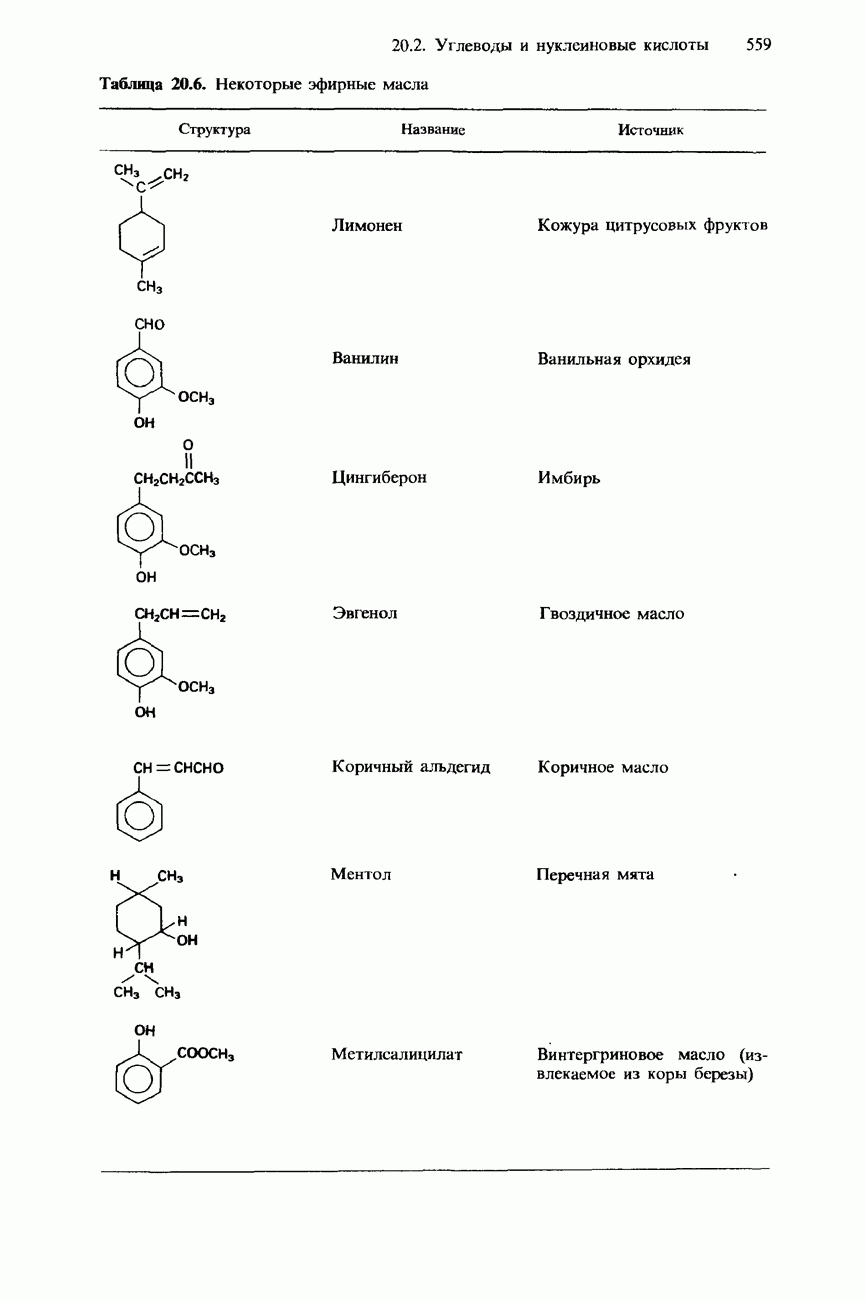
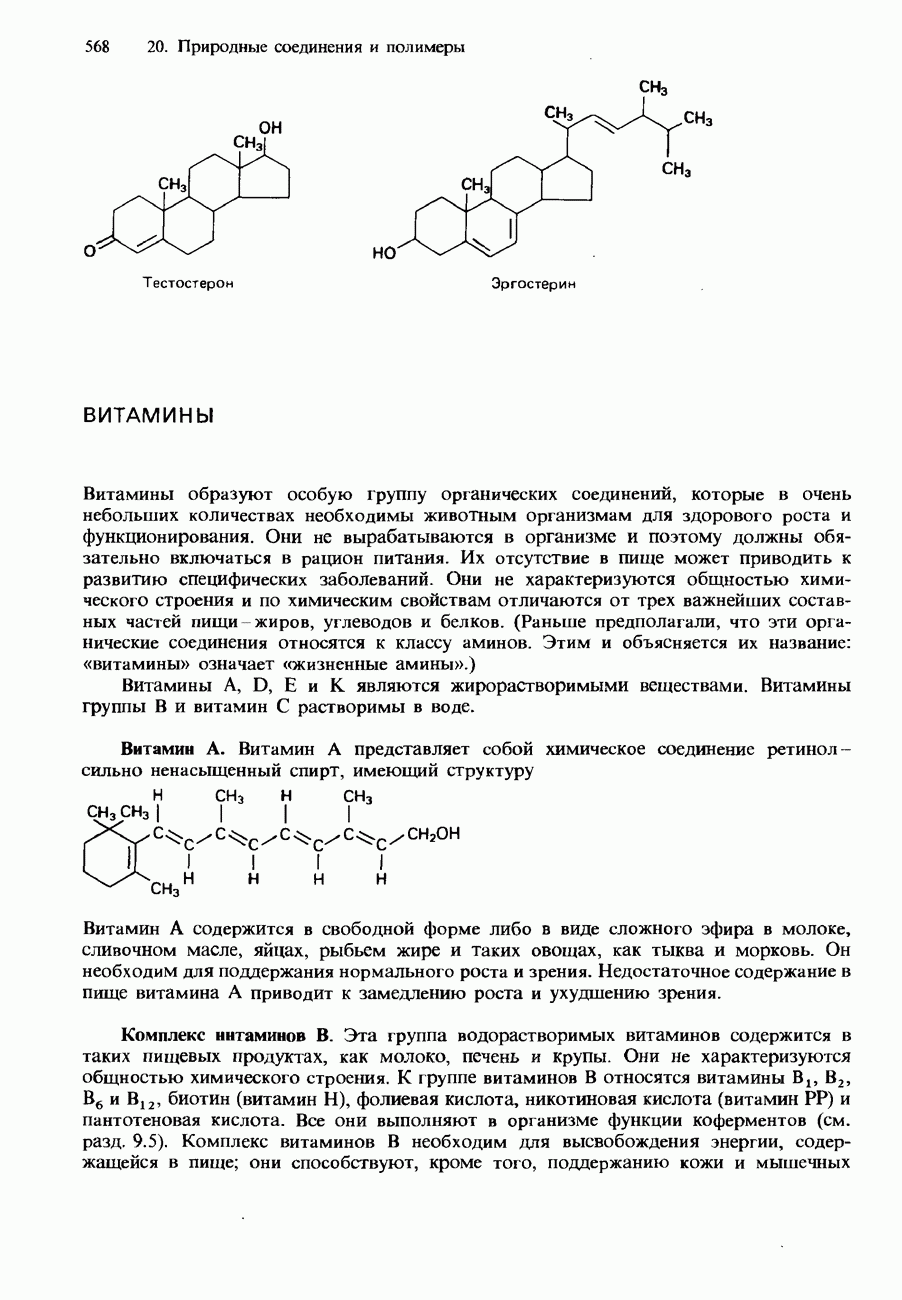
- ВИТАМИНЫ
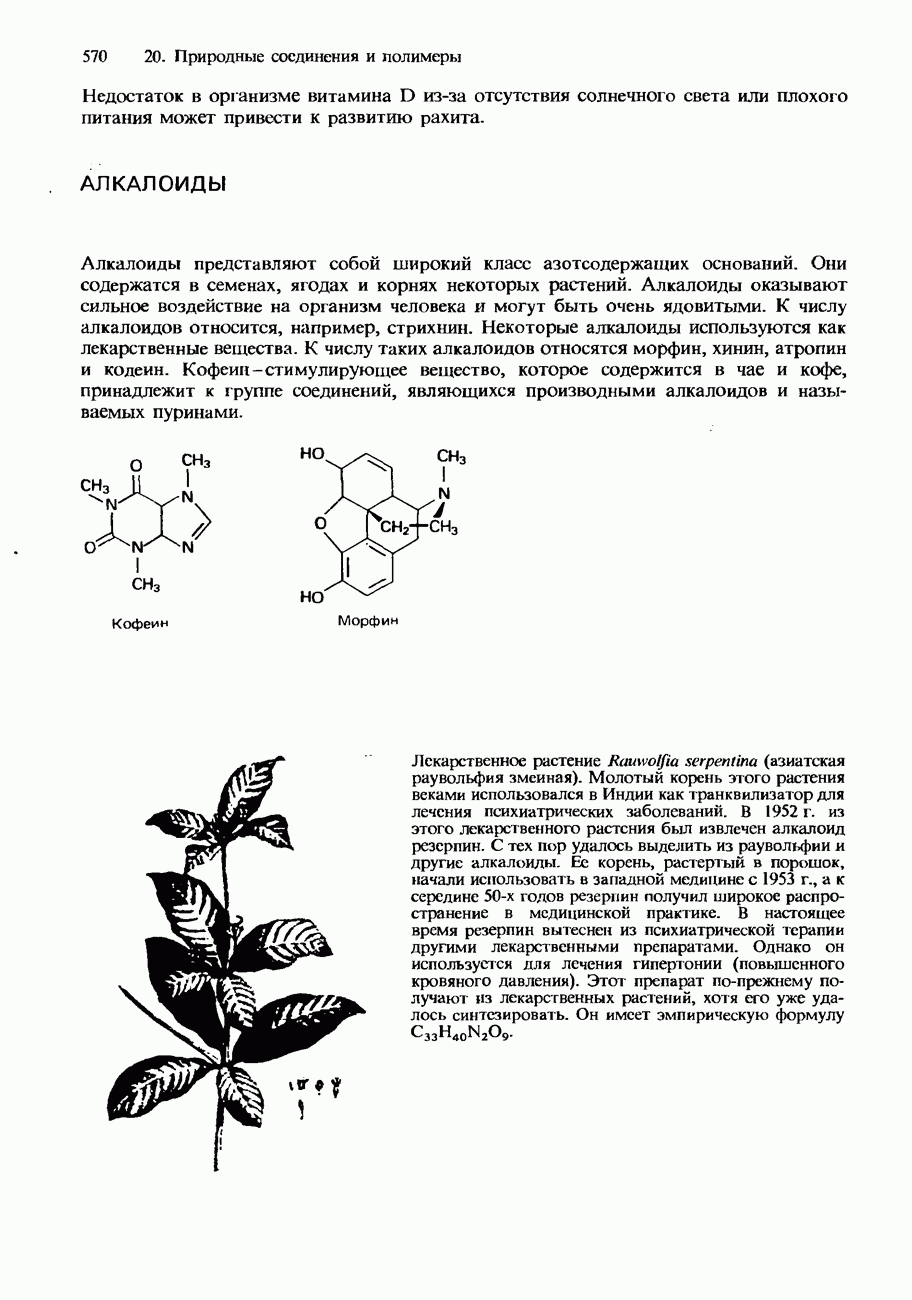
- АЛКАЛОИДЫ
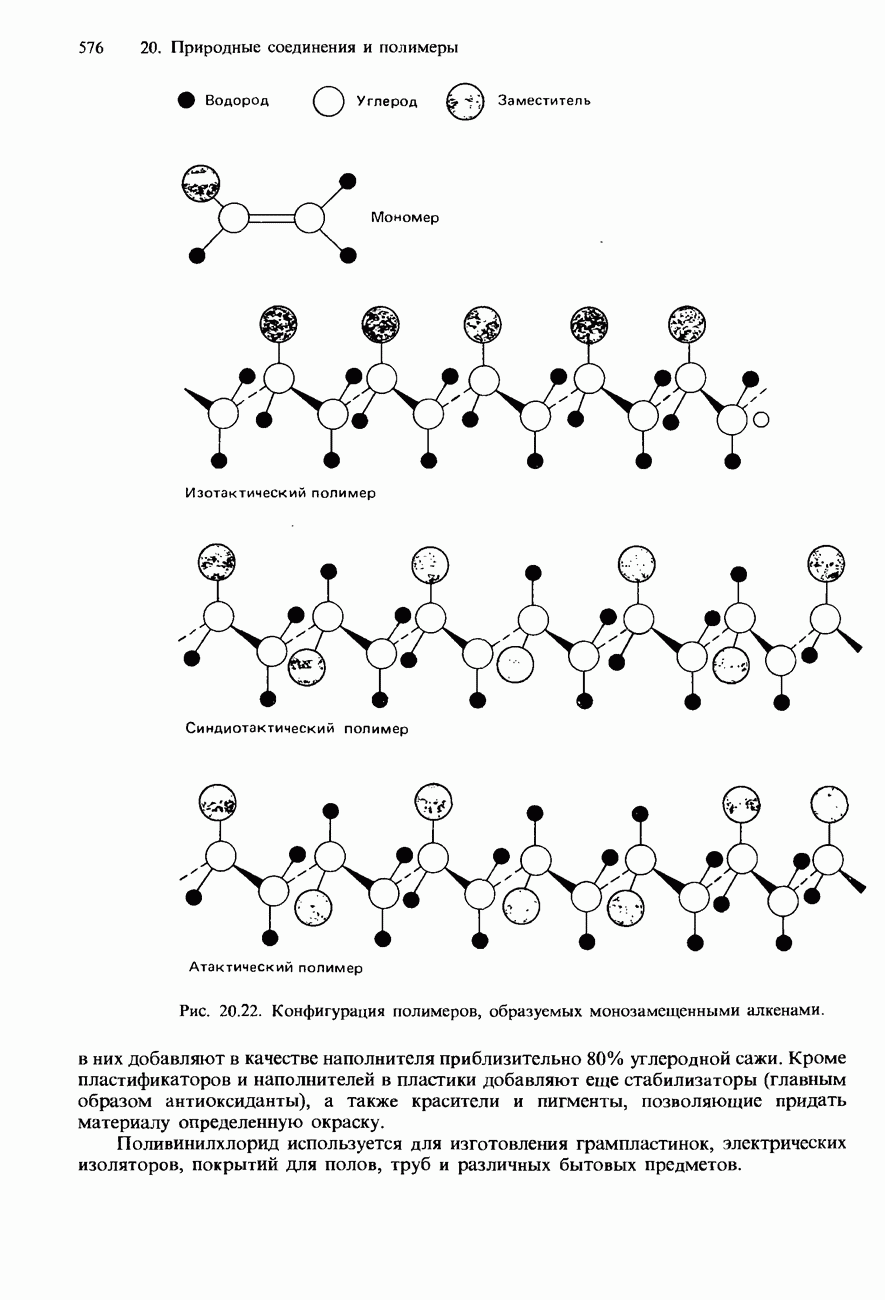
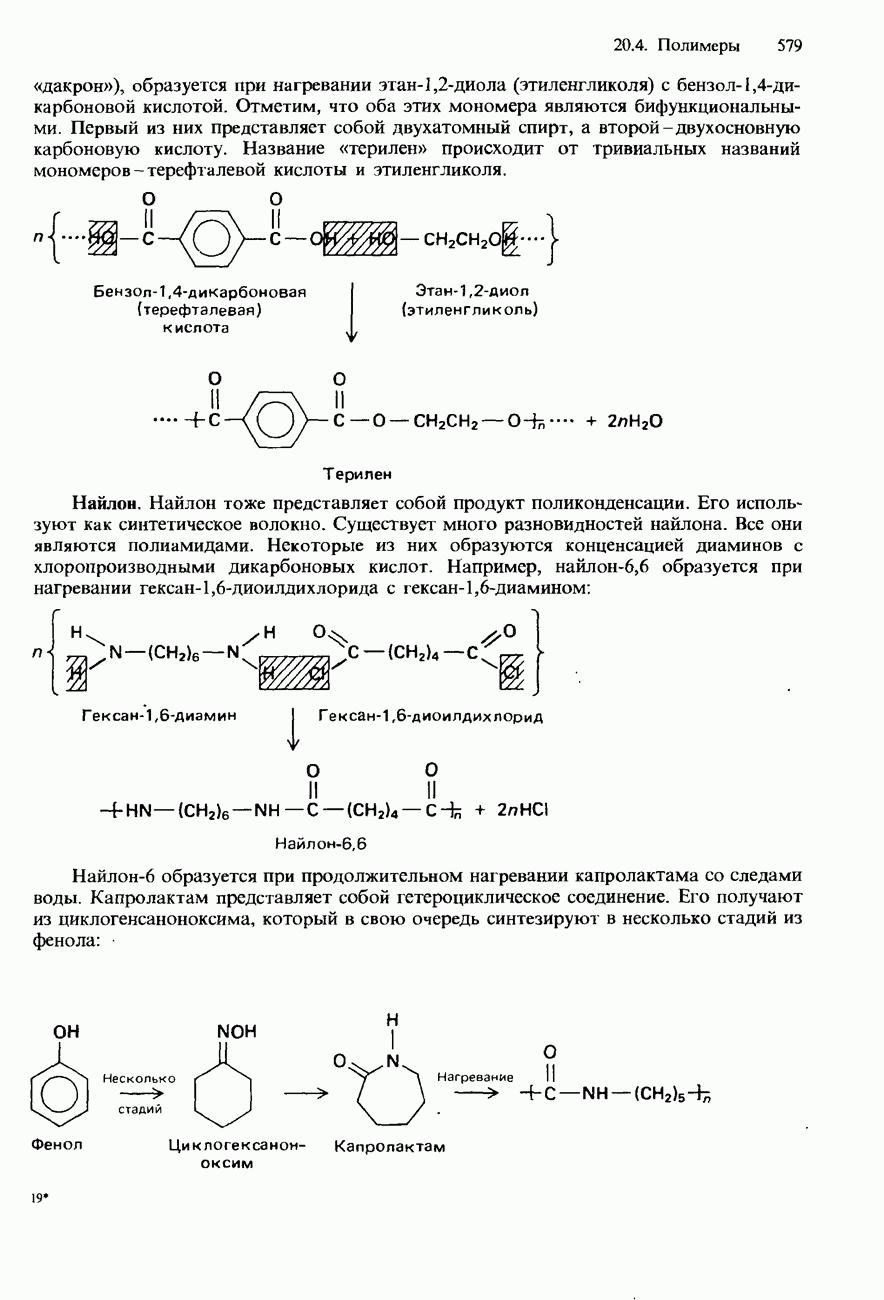
- 20.4. Полимеры
- ПОЛИМЕРИЗАЦИЯ
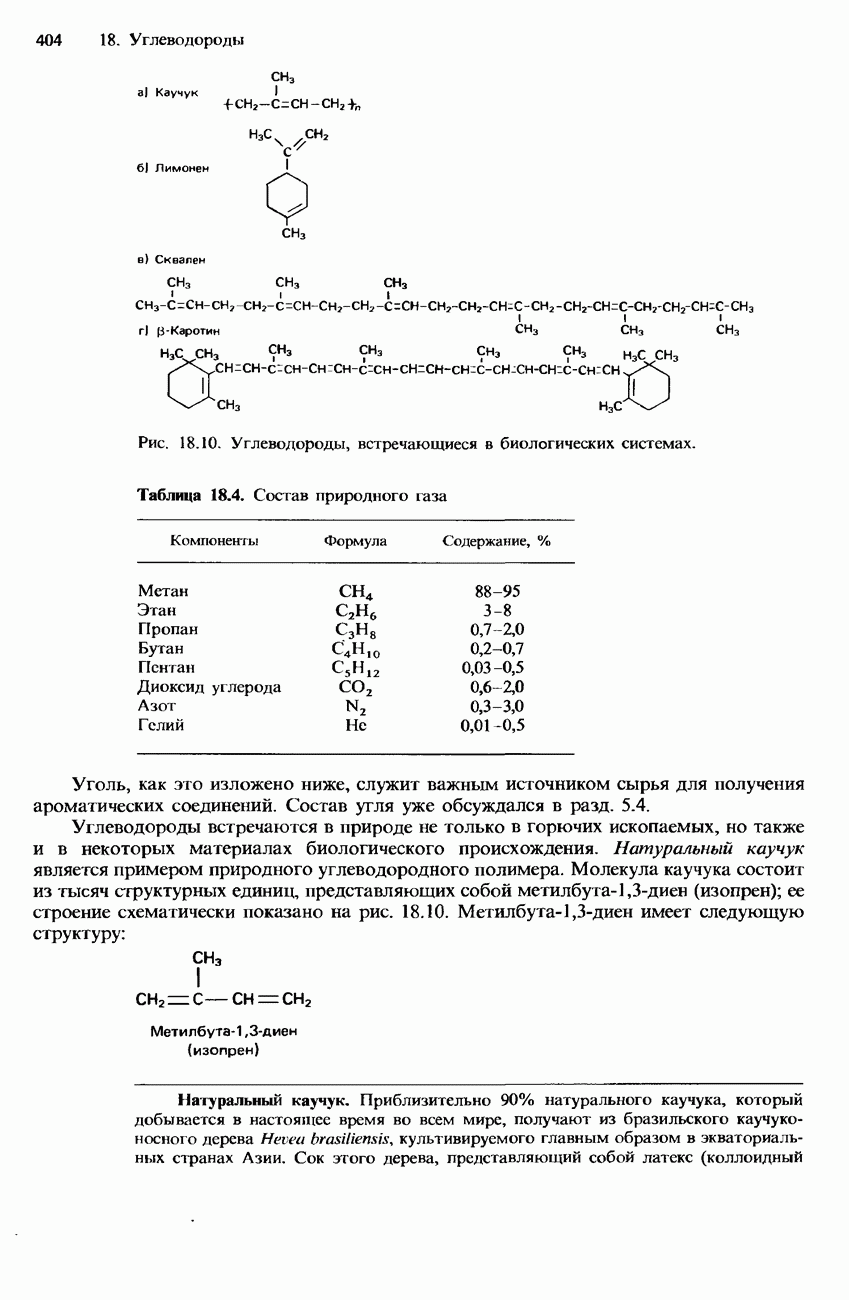
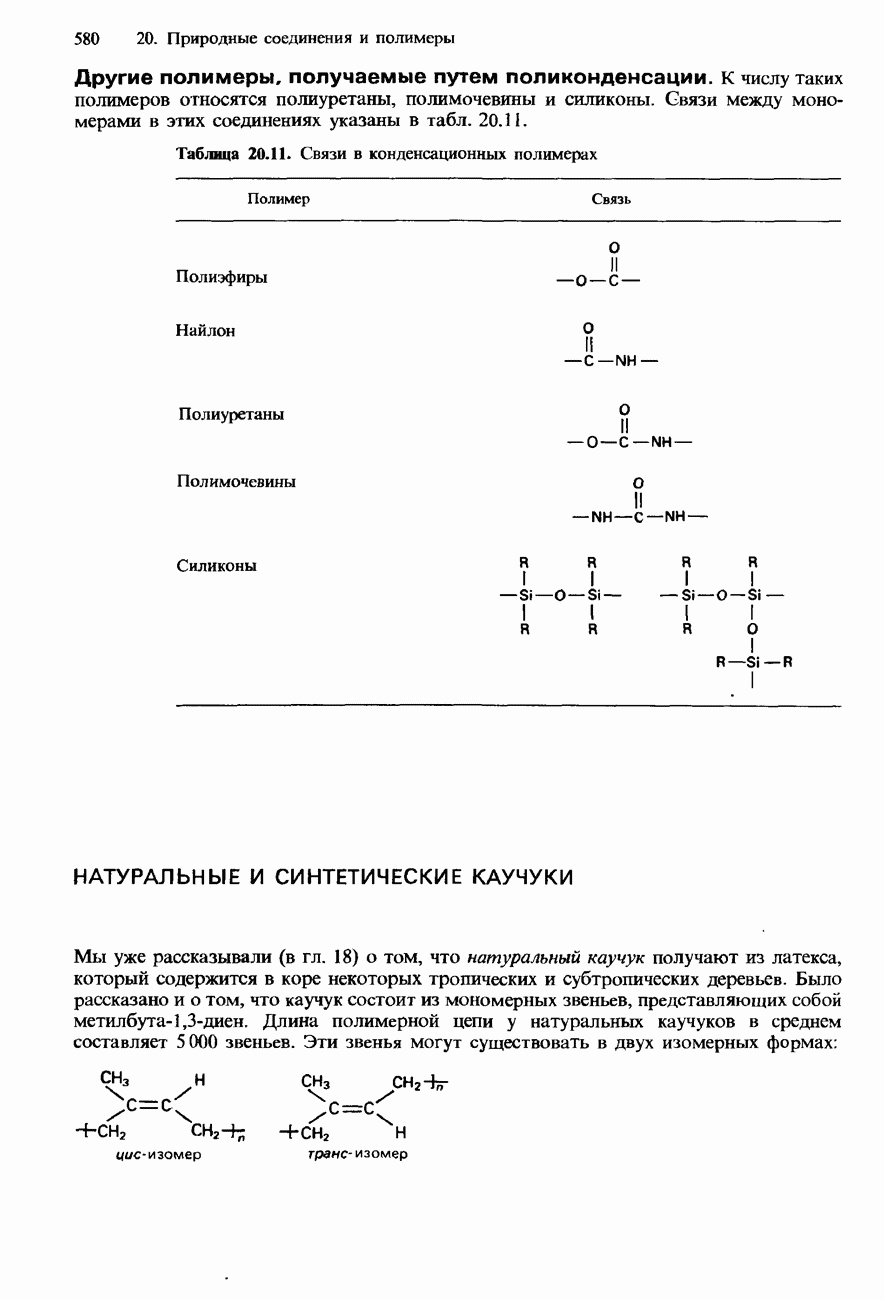
- НАТУРАЛЬНЫЕ И СИНТЕТИЧЕСКИЕ КАУЧУКИ
- ЦЕЛЛЮЛОЗНОЕ ВОЛОКНО
- ВОПРОСЫ ДЛЯ ПРОВЕРКИ
- ПРИЛОЖЕНИЯ