| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
§ 36. Принцип Паули. Распределение электронов по энергетическим уровням атома
Каждый электрон в атоме движется в первом приближении в центрально-симметричном некулоновском поле Состояние электрона в этом случае определяется тремя квантовыми числами  , физический смысл которых был выяснен в § 28. В связи с существованием спина электрона к указанным квантовым числам нужно добавить квантовое число
, физический смысл которых был выяснен в § 28. В связи с существованием спина электрона к указанным квантовым числам нужно добавить квантовое число  которое может принимать значения
которое может принимать значения  и определяет проекцию спина на заданное направление. В дальнейшем для магнитного квантового числа мы будем вместо
и определяет проекцию спина на заданное направление. В дальнейшем для магнитного квантового числа мы будем вместо  пользоваться обозначением
пользоваться обозначением  чтобы подчеркнуть то обстоятельство, что это число определяет проекцию орбитального момента, величина которого дается квантовым числом l.
чтобы подчеркнуть то обстоятельство, что это число определяет проекцию орбитального момента, величина которого дается квантовым числом l.
Таким образом, состояние каждого электрона в атоме характеризуется четырьмя квантовыми числами:

Энергия состояния зависит в основном от чисел  .
.
Кроме того, имеется слабая зависимость энергии от чисел  поскольку их значения связаны с взаимной ориентацией моментов
поскольку их значения связаны с взаимной ориентацией моментов  от которой зависит величина взаимодействия между орбитальным и собственным магнитными моментами электрона. Энергия состояния сильнее возрастает с увеличением числа
от которой зависит величина взаимодействия между орбитальным и собственным магнитными моментами электрона. Энергия состояния сильнее возрастает с увеличением числа  , чем с увеличением
, чем с увеличением  Поэтому, как правило, состояние с большим
Поэтому, как правило, состояние с большим  обладает, независимо от значения
обладает, независимо от значения  большей энергией.
большей энергией.
В нормальном (невозбужденном) состоянии атома электроны должны располагаться на самых низких доступных для них энергетических уровнях. Поэтому, казалось бы, в любом атоме в нормальном состоянии все электроны должны находиться в состоянии  а основные термы всех атомов должны быть типа
а основные термы всех атомов должны быть типа  -термов
-термов  Однако опыт показывает, что это не так.
Однако опыт показывает, что это не так.
Объяснение наблюдаемых типов термов заключается в следующем. Согласно одному из законов квантовой механики, называемому принципом Паули, в одном и том же атоме (или в какой-либо другой квантовой системе) не может быть двух электронов, обладающих одинаковой совокупностью квантовых чисел. Иными словами, в одном и том же состоянии не могут находиться одновременно два электрона.
В § 28 было показано, что данному  соответствует
соответствует  состояний, отличающихся значениями l и
состояний, отличающихся значениями l и  Квантовое число
Квантовое число  может принимать два значения:
может принимать два значения:  Поэтому в состояниях с данным значением
Поэтому в состояниях с данным значением  могут находиться в атоме не более
могут находиться в атоме не более  электронов:
электронов:

Совокупность электронов, имеющих одинаковые значения квантового числа  , образует оболочку. Оболочки подразделяются на подоболочки, отличающиеся значением квантового числа l. В соответствии с значением
, образует оболочку. Оболочки подразделяются на подоболочки, отличающиеся значением квантового числа l. В соответствии с значением  оболочкам дают обозначения, заимствованные из спектроскопии рентгеновских лучей:
оболочкам дают обозначения, заимствованные из спектроскопии рентгеновских лучей:

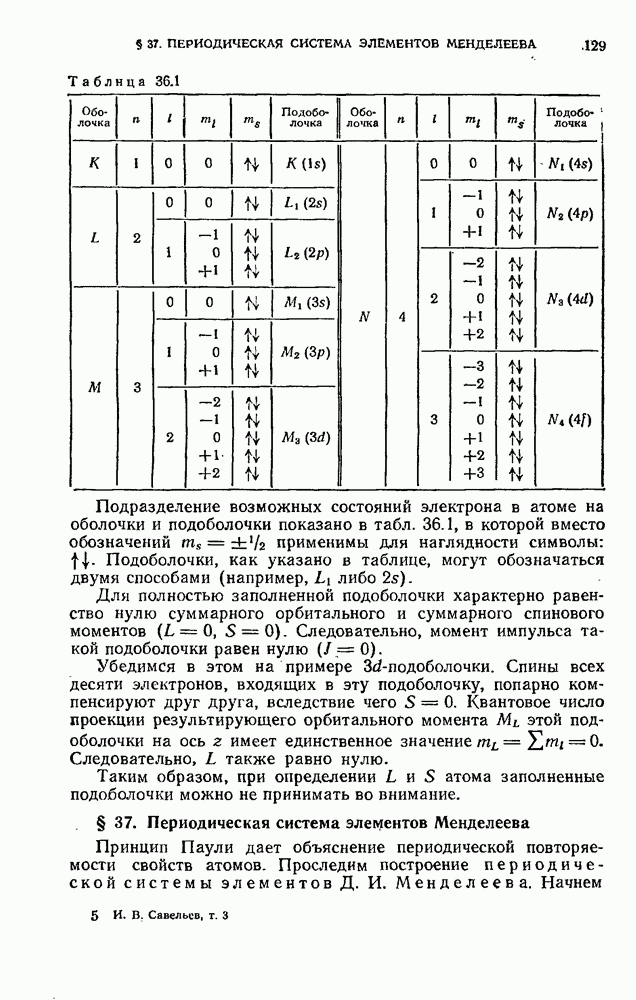
Таблица 36.1

Подразделение возможных состояний электрона в атоме на оболочки и подоболочки показано в табл. 36.1, в которой вместо обозначений  применимы для наглядности символы:
применимы для наглядности символы:  . Подоболочки, как указано в таблице, могут обозначаться двумя способами (например,
. Подоболочки, как указано в таблице, могут обозначаться двумя способами (например,  либо
либо  ).
).
Для полностью заполненной подоболочки характерно равенство нулю суммарного орбитального и суммарного спинового моментов  . Следовательно, момент импульса такой подоболочки равен нулю
. Следовательно, момент импульса такой подоболочки равен нулю 
Убедимся в этом на примере  -подоболочки. Спины всех десяти электронов, входящих в эту подоболочку, попарно компенсируют друг друга, вследствие чего
-подоболочки. Спины всех десяти электронов, входящих в эту подоболочку, попарно компенсируют друг друга, вследствие чего  Квантовое число проекции результирующего орбитального момента
Квантовое число проекции результирующего орбитального момента  этой подоболочки на ось z имеет единственное значение
этой подоболочки на ось z имеет единственное значение  -Следовательно, L также равно нулю.
-Следовательно, L также равно нулю.
Таким образом, при определении L и S атома заполненные подоболочки можно не принимать во внимание.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ
- ЧАСТЬ 1. КВАНТОВАЯ ОПТИКА
- § 1. Тепловое излучение и люминесценция
- § 2. Закон Кирхгофа
- § 3. Равновесная плотность энергии излучения
- § 4. Закон Стефана — Больцмана и закон Вина
- § 5. Стоячие волны в пространстве трех измерений
- § 6. Формула Рэлея — Джинса
- § 7. Формула Планка
- ГЛАВА II. ФОТОНЫ
- § 8. Тормозное рентгеновское излучение
- § 9. Фотоэффект
- § 10. Опыт Боте. Фотоны
- § 11. Эффект Комптона
- ЧАСТЬ 2. АТОМНАЯ ФИЗИКА
- § 12. Закономерности в атомных спектрах
- § 13. Модель атома Томсона
- § 14. Опыты по рассеянию а-частиц. Ядерная модель атома
- § 15. Постулаты Бора. Опыт Франка и Герца
- § 16. Правило квантования круговых орбит
- § 17. Элементарная боровская теория водородного атома
- ГЛАВА IV. ЭЛЕМЕНТЫ КВАНТОВОЙ МЕХАНИКИ
- § 18. Гипотеза де-Бройля. Волновые свойства вещества
- § 19. Необычные свойства микрочастиц
- § 20. Принцип неопределенности
- § 21. Уравнение Шрёдингера
- § 22. Смысл пси-функции
- § 23. Квантование энергии
- § 24. Квантование момента импульса
- § 25. Принцип суперпозиции
- § 26. Прохождение частиц через потенциальный барьер
- § 27. Гармонический осциллятор
- ГЛАВА V. ФИЗИКА АТОМОВ И МОЛЕКУЛ
- § 28. Атом водорода
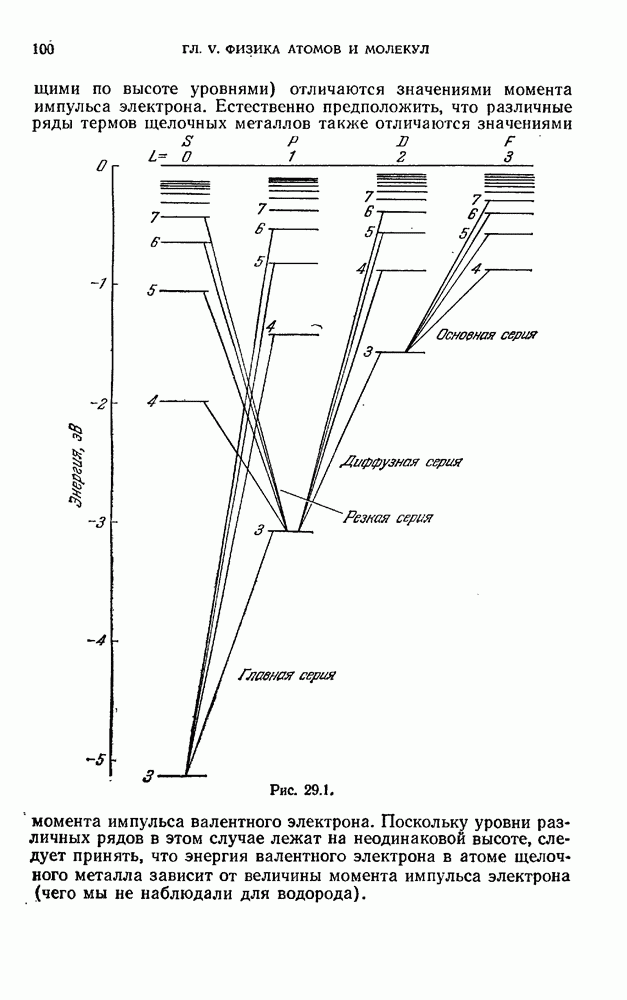
- § 29. Спектры щелочных металлов
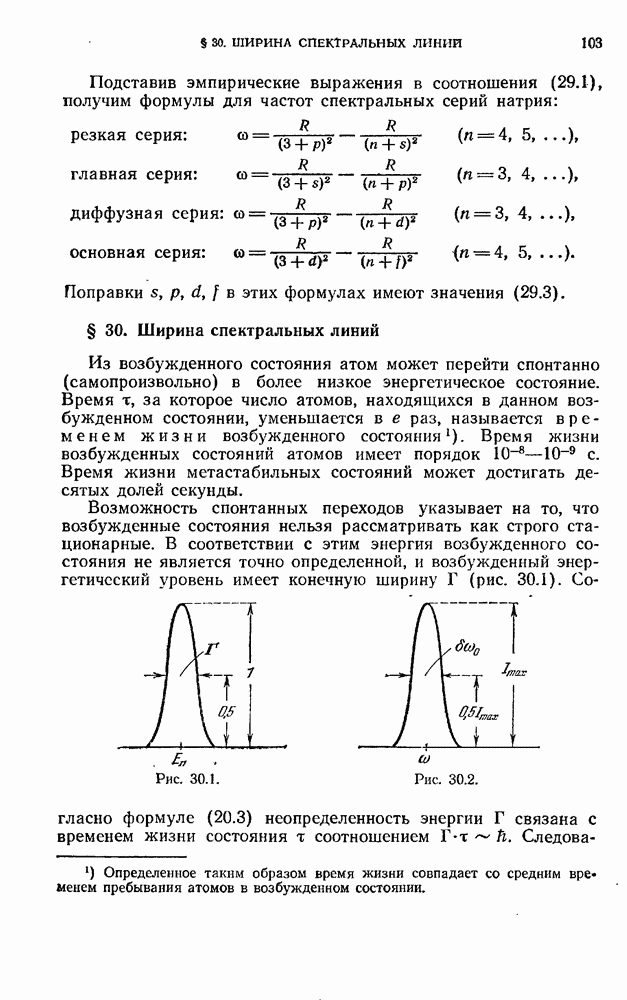
- § 30. Ширина спектральных линий
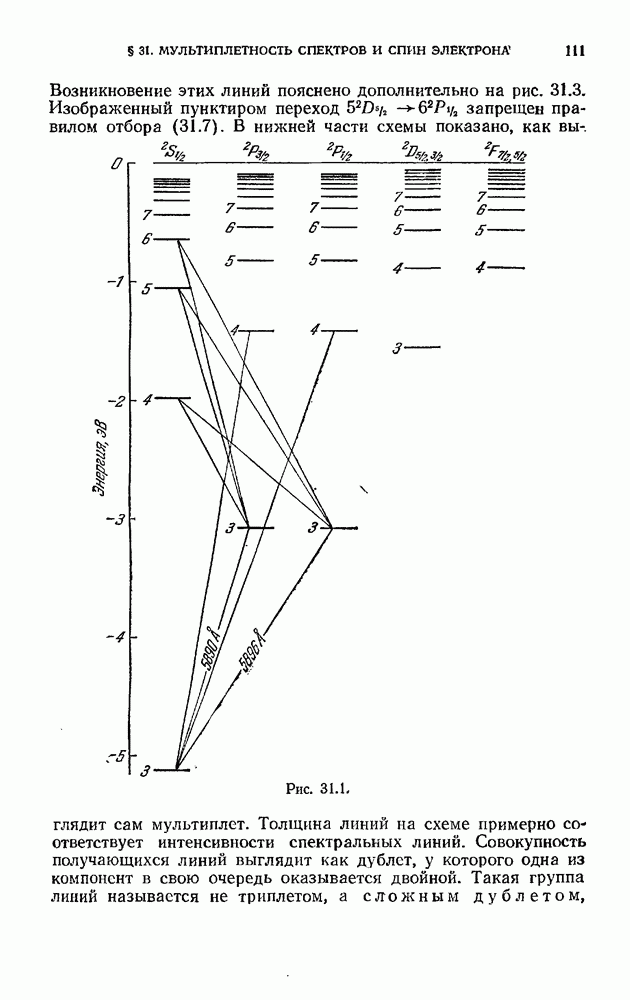
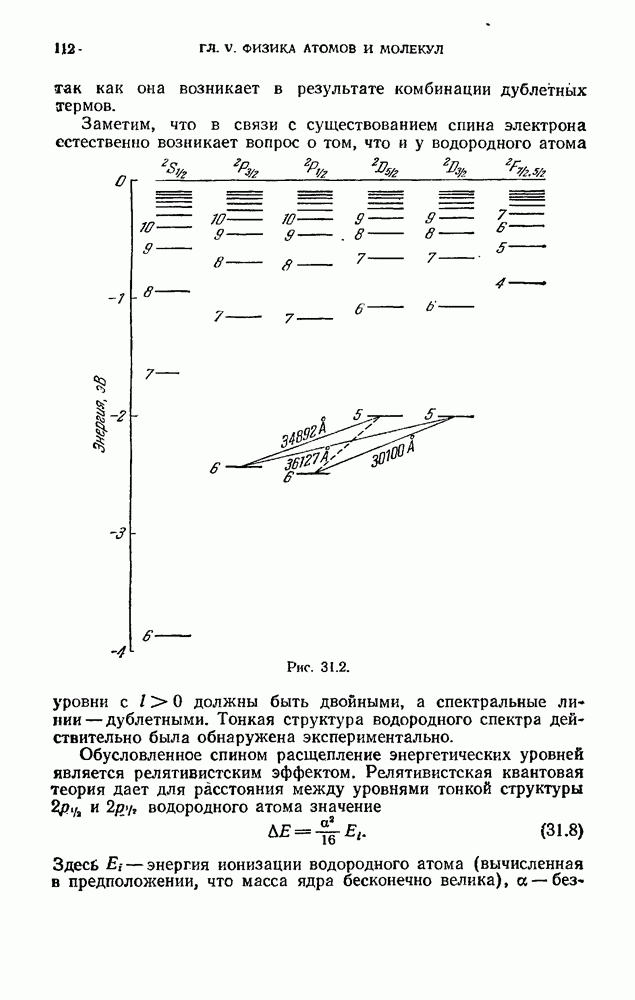
- § 31. Мультиплетность спектров и спин электрона
- § 32. Результирующий механический момент многоэлектронного атома
- § 33. Магнитный момент атома
- § 34. Эффект Зеемана
- § 35. Электронный парамагнитный резонанс
- § 36. Принцип Паули. Распределение электронов по энергетическим уровням атома
- § 37. Периодическая система элементов Менделеева
- § 38. Рентгеновские спектры
- § 39. Энергия молекулы
- § 40. Молекулярные спектры
- § 41. Комбинационное рассеяние света
- § 42. Вынужденное излучение
- § 43. Лазеры
- § 44. Нелинейная оптика
- ЧАСТЬ 3. ФИЗИКА ТВЕРДОГО ТЕЛА
- § 45. Кристаллическая решетка. Индексы Миллера
- § 46. Теплоемкость кристаллов. Теория Эйнштейна
- § 47. Колебания систем с большим числом степеней свободы
- § 48. Теория Дебая
- § 49. Фононы
- § 50. Эффект Мёссбауэра
- ГЛАВА VII. ЗОННАЯ ТЕОРИЯ ТВЕРДЫХ ТЕЛ
- § 51. Квантовая теория свободных электронов в металле
- § 52. Распределение Ферми — Дирака
- § 53. Энергетические зоны в кристаллах
- § 54. Динамика электронов в кристаллической решетке
- ГЛАВА VIII. ЭЛЕКТРОПРОВОДНОСТЬ МЕТАЛЛОВ И ПОЛУПРОВОДНИКОВ
- § 55. Электропроводность металлов
- § 56. Сверхпроводимость
- § 57. Полупроводники
- § 58. Собственная проводимость полупроводников
- § 59. Примесная проводимость полупроводников
- ГЛАВА IX. КОНТАКТНЫЕ И ТЕРМОЭЛЕКТРИЧЕСКИЕ ЯВЛЕНИЯ
- § 60. Работа выхода
- § 61. Термоэлектронная эмиссия. Электронные лампы
- § 62. Контактная разность потенциалов
- § 63. Термоэлектрические явления
- § 64. Полупроводниковые диоды и триоды
- § 65. Внутренний фотоэффект
- ЧАСТЬ 4. ФИЗИКА АТОМНОГО ЯДРА И ЭЛЕМЕНТАРНЫХ ЧАСТИЦ
- § 66. Состав и характеристики атомного ядра
- § 67. Масса и энергия связи ядра
- § 68. Модели атомного ядра
- § 69. Ядерные силы
- § 70. Радиоактивность
- § 71. Ядерные реакции
- § 72. Деление ядер
- § 73. Термоядерные реакции
- ГЛАВА XI. ЭЛЕМЕНТАРНЫЕ ЧАСТИЦЫ
- § 74. Виды взаимодействий и классы элементарных частиц
- § 75. Методы регистрации элементарных частиц
- § 76. Космические лучи
- § 77. Частицы и античастицы
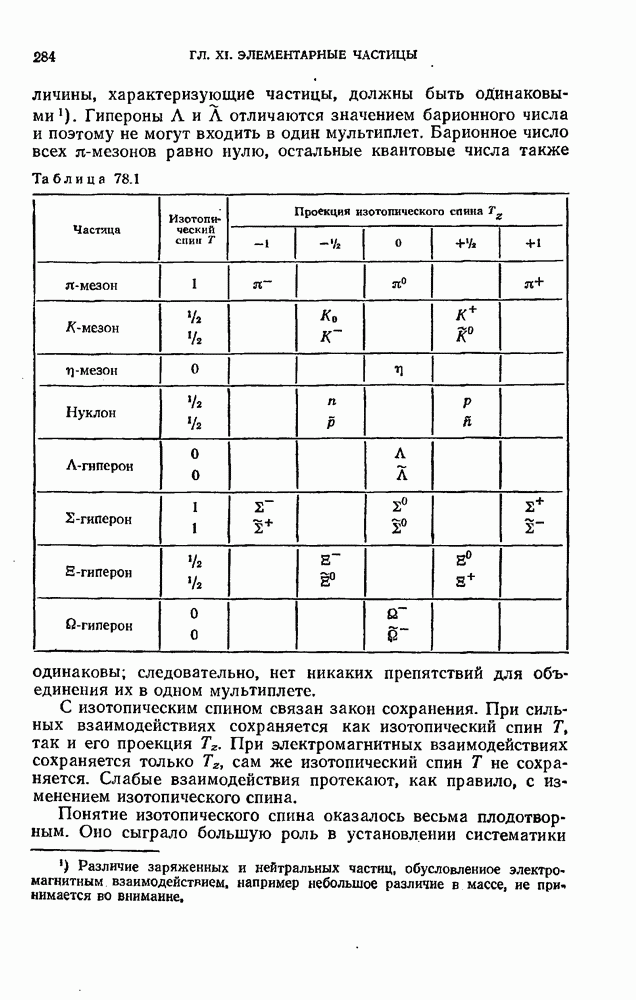
- § 78. Изотопический спин
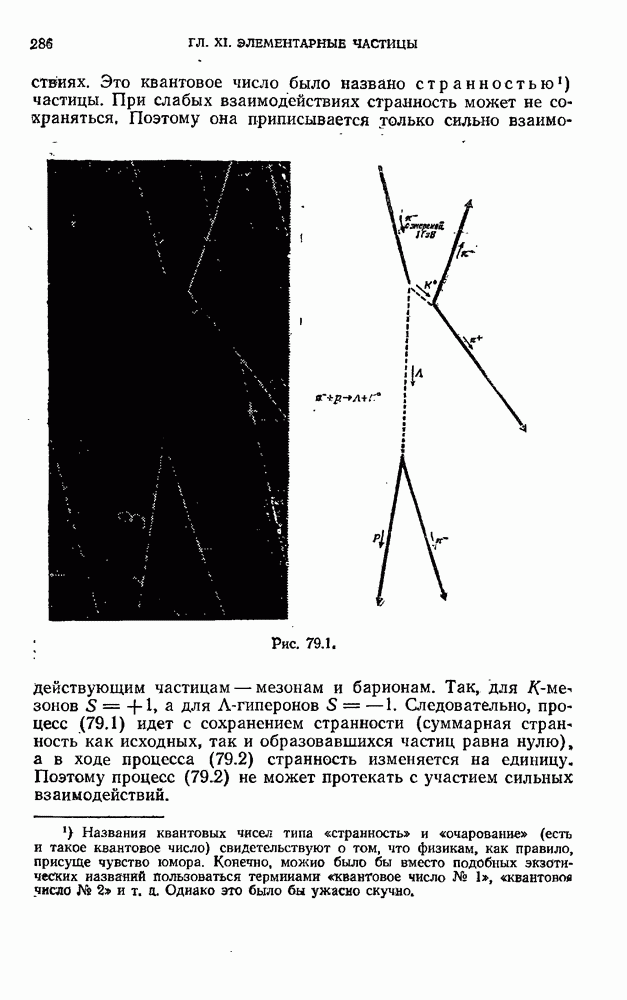
- § 79. Странные частицы
- § 80. Несохранение четности в слабых взаимодействиях
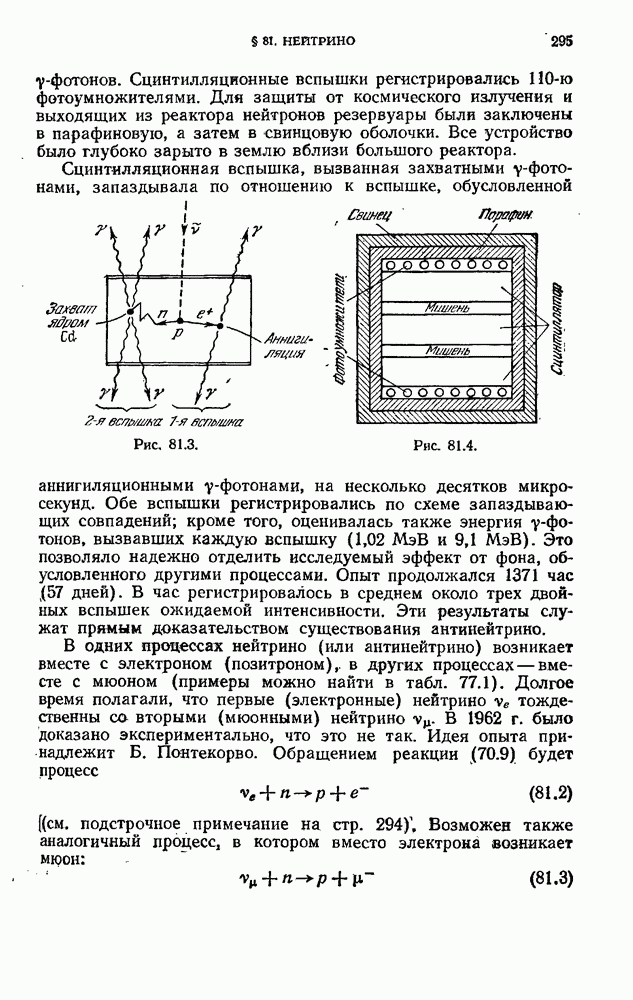
- § 81. Нейтрино
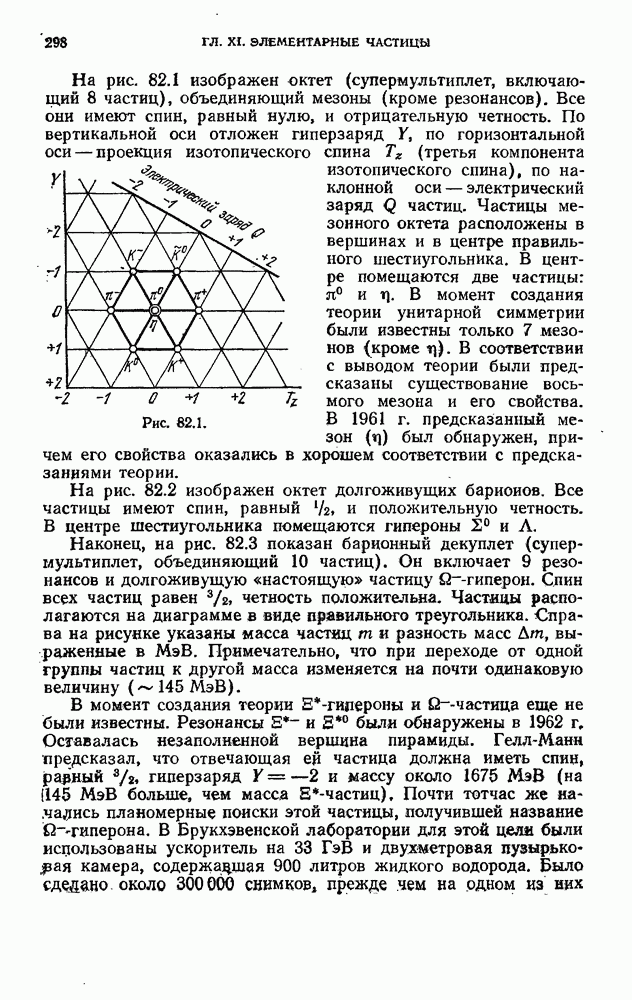
- § 82. Систематика элементарных частиц
- § 83. Кварки
- § 84. Великое объединение
- ПРИЛОЖЕНИЯ
- I. ГРАВИТАЦИОННОЕ ВЗАИМОДЕЙСТВИЕ