| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
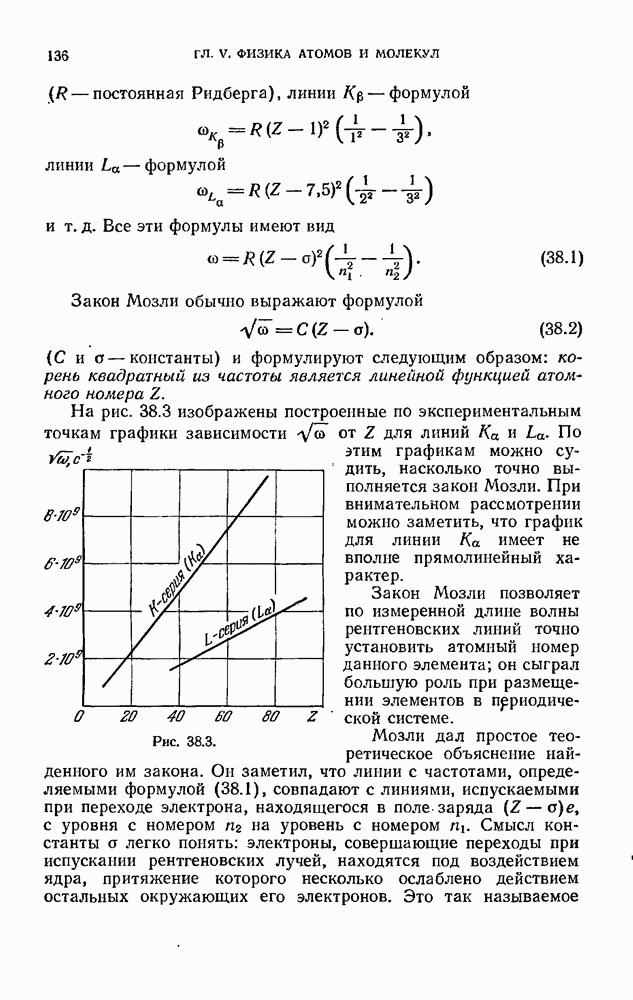
§ 39. Энергия молекулы
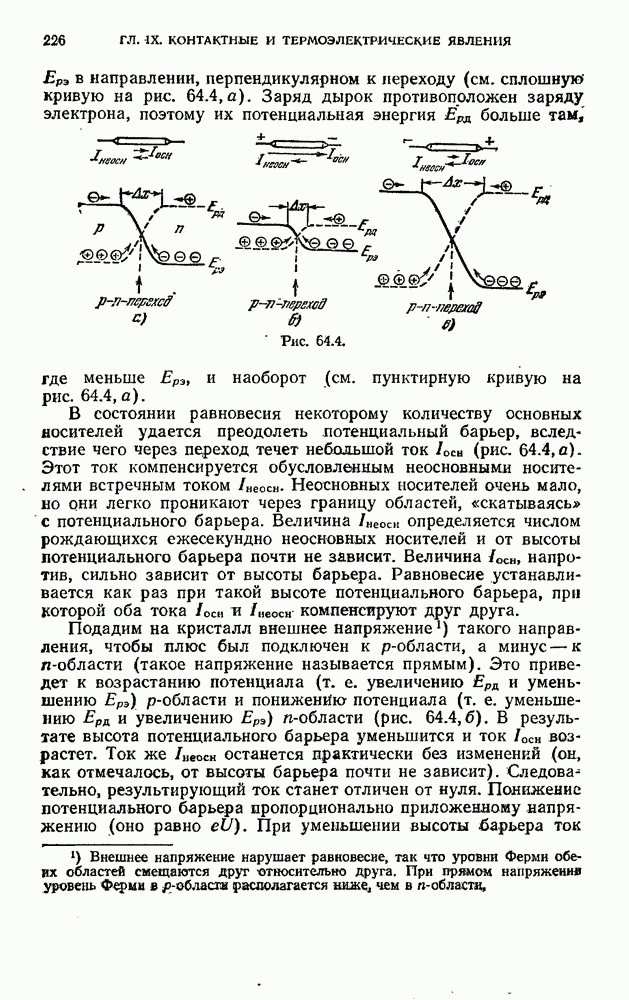
Опыт дает, что рентгеновские спектры тяжелых элементов не зависят от того, в состав какого химического соединения входит данный элемент. Отсюда следует, что силы, удерживающие атомы в молекуле, вызваны взаимодействием внешних электронов. Электроны внутренних оболочек при объединении атомов в молекулу остаются в прежних состояниях.
В дальнейшем мы ограничимся рассмотрением только двухатомных молекул. Различают два вида связи между атомами в молекуле. Один из них осуществляется в том случае, когда электроны в молекуле можно разделить на две группы, каждая из которых все время находится около одного из ядер. Электроны распределяются так, что около одного из ядер образуется избыток электронов, а около другого — их недостаток. Таким образом, молекула как бы состоит из двух ионов противоположных знаков, притягивающихся друг к другу. Связь этого типа называется гетерополярной (или ионной). Примером молекул с гетерополярной связью могут служить  и т.д.
и т.д.
Второй вид связи наблюдается в тех молекулах, в которых часть электронов движется около обоих ядер. Такая связь называется гомеополяр ной (или ковалентной, или атомной). Она образуется парами электронов с противоположно направленными спинами. Среди молекул этого типа следует различать молекулы с одинаковыми ядрами (Н2, N2, О2) и молекулы с разными ядрами (например, CN). В молекулах первого рода электроны распределены симметрично. В молекулах второго рода имеется некоторая асимметрия в распределении электронов, благодаря чему молекулы приобретают электрический дипольный момент.
Простейшей молекулой с гомеополярной связью является молекула водорода. Вскоре после создания квантовой механики Гайтлер и Лондон (1927) предприняли успешную попытку квантовомеханического расчета основного состояния молекулы 
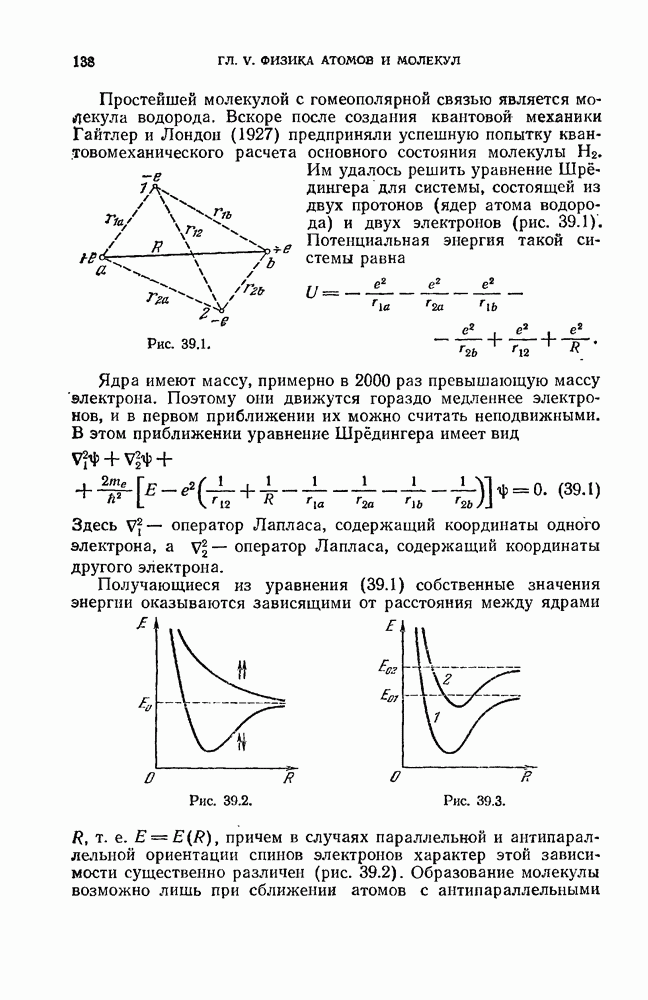
Им удалось решить уравнение Шрёдингера для системы, состоящей из двух протонов (ядер атома водорода) и двух электронов (рис. 39.1). Потенциальная энергия такой системы равна


Рис. 39.1.
Ядра имеют массу, примерно в 2000 раз превышающую массу электрона. Поэтому они движутся гораздо медленнее электронов, и в первом приближении их можно считать неподвижными. В этом приближении уравнение Шрёдингера имеет вид

Здесь  — оператор Лапласа, содержащий координаты одного электрона,
— оператор Лапласа, содержащий координаты одного электрона,  — оператор Лапласа, содержащий координаты другого электрона.
— оператор Лапласа, содержащий координаты другого электрона.

Рис. 39.2.

Рис. 39.3.
Получающиеся из уравнения (39.1) собственные значения энергии оказываются зависящими от расстояния между ядрами R, т. е.  , причем в случаях параллельной и антипараллельной ориентации спинов электронов характер этой зависимости существенно различен (рис. 39.2). Образование молекулы возможно лишь при сближении атомов с антипараллельными спинами.
, причем в случаях параллельной и антипараллельной ориентации спинов электронов характер этой зависимости существенно различен (рис. 39.2). Образование молекулы возможно лишь при сближении атомов с антипараллельными спинами.
Асимптотическое значение  к которому стремится энергия молекулы при
к которому стремится энергия молекулы при  для обеих изображенных на рисунке кривых, одинаково и равно сумме энергий изолированных атомов.
для обеих изображенных на рисунке кривых, одинаково и равно сумме энергий изолированных атомов.
Аналогично обстоит дело и в случае других двухатомных молекул. Энергия, обусловленная электронной конфигурацией (электронная энергия), имеет минимум при некотором значении R и изображается кривой такого же вида, как для водородной молекулы (см. кривую 1 на рис. 39.3).
Изменение электронной конфигурации молекулы приводит к изменению кривой зависимости электронной энергии от расстояния между ядрами R. Асимптотическое значение энергии также становится иным — равным суммарной энергии изолированных атомов в новом квантовом состоянии (см. кривую 2 на рис. 39.3).
В основном изменение энергетического запаса молекулы происходит, как и в атоме, в результате изменений в электронной конфигурации, образующей периферическую часть молекулы. Однако при заданной электронной конфигурации ядра молекулы могут различным образом колебаться и вращаться относительно общего центра масс. С этими видами движения связаны запасы колебательной и вращательной энергии, которые должны быть учтены в общем балансе. Введем обозначения:
Ее — энергия, обусловленная электронной конфигурацией (электронная энергия);
 — энергия, соответствующая колебаниям молекулы (колебательная или вибрационная энергия);
— энергия, соответствующая колебаниям молекулы (колебательная или вибрационная энергия);
 — энергия, связанная с вращением молекулы (вращательная или ротационная энергия).
— энергия, связанная с вращением молекулы (вращательная или ротационная энергия).
В первом приближении отдельные виды молекулярных движений — движение электронов, колебание и вращение молекулы — можно считать независимыми друг от друга. Поэтому полную энергию молекулы можно представить в виде

Согласно (27.3) энергия гармонического осциллятора определяется выражением

где v — колебательное квантовое число,  — классическая частота осциллятора (в формуле (27.3) эти величины обозначены буквами
— классическая частота осциллятора (в формуле (27.3) эти величины обозначены буквами  Напомним, что для колебательного квантового числа имеется правило отбора
Напомним, что для колебательного квантового числа имеется правило отбора

(см. (27.4)).
Кривая потенциальной энергии молекулы (см. рис. 39.3) совпадает с параболой только при малых колебаниях.
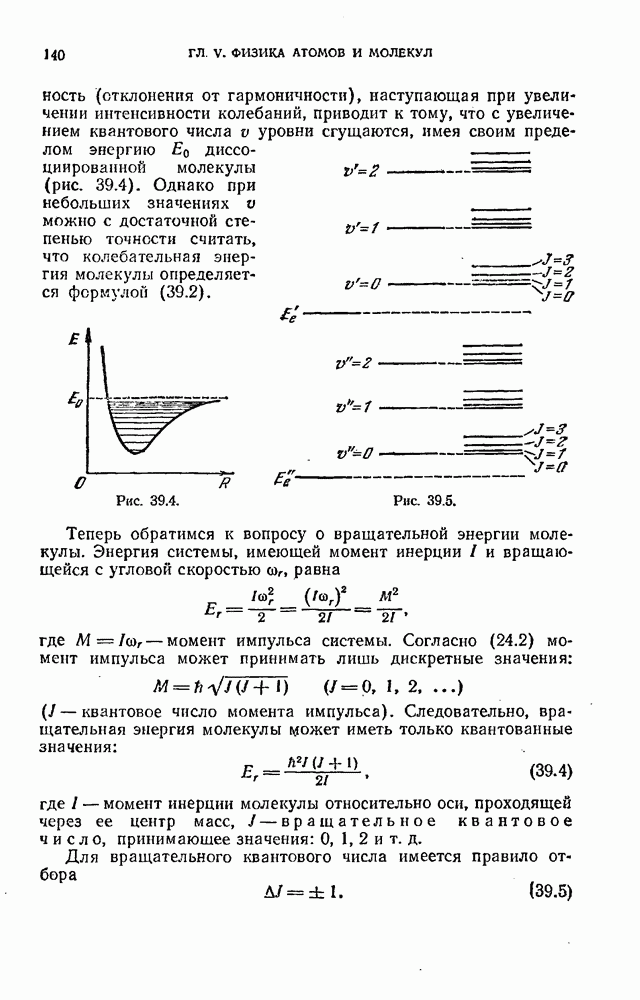
Ангармоничность (отклонения от гармоничности), наступающая при увеличении интенсивности колебаний, приводит к тому, что с увеличением квантового числа v уровни сгущаются, имея своим пределом энергию  диссоциированной молекулы (рис. 39.4). Однако при небольших значениях v можно с достаточной степенью точности считать, что колебательная энергия молекулы определяется формулой (39.2).
диссоциированной молекулы (рис. 39.4). Однако при небольших значениях v можно с достаточной степенью точности считать, что колебательная энергия молекулы определяется формулой (39.2).

Рис. 39.4.

Рис. 39.5.
Теперь обратимся к вопросу о вращательной энергии молекулы. Энергия системы, имеющей момент инерции  и вращающейся с угловой скоростью
и вращающейся с угловой скоростью  равна
равна

где  — момент импульса системы. Согласно (24.2) момент импульса может принимать лишь дискретные значения:
— момент импульса системы. Согласно (24.2) момент импульса может принимать лишь дискретные значения:

 — квантовое число момента импульса). Следовательно, вращательная энергия молекулы может иметь только квантованные значения:
— квантовое число момента импульса). Следовательно, вращательная энергия молекулы может иметь только квантованные значения:

где l — момент инерции молекулы относительно оси, проходящей через ее центр масс,  — вращательное квантовое число, принимающее значения: 0, 1, 2 и т. д.
— вращательное квантовое число, принимающее значения: 0, 1, 2 и т. д.
Для вращательного квантового числа имеется правило отбора

Итак, в соответствии с (39.2) и (39.4) полная энергия молекулы равна

Опыт и теория показывают, что расстояние между вращательными уровнями  значительно меньше расстояния между колебательными уровнями
значительно меньше расстояния между колебательными уровнями  которое в свою очередь значительно меньше, чем расстояние между электронными уровнями
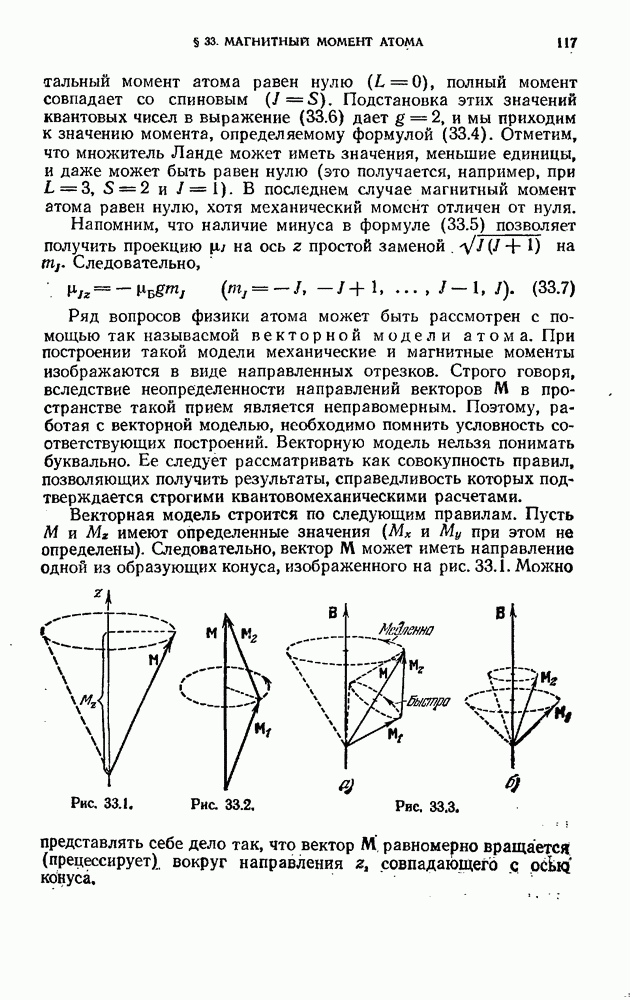
которое в свою очередь значительно меньше, чем расстояние между электронными уровнями  Следовательно, схема энергетических уровней двухатомной молекулы выглядит так, как показано на рис. 39.5 (приведены только два электронных уровня). Совокупность уровней содержится в правом столбце. Первые два столбца лишь поясняют возникновение уровней.
Следовательно, схема энергетических уровней двухатомной молекулы выглядит так, как показано на рис. 39.5 (приведены только два электронных уровня). Совокупность уровней содержится в правом столбце. Первые два столбца лишь поясняют возникновение уровней.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ
- ЧАСТЬ 1. КВАНТОВАЯ ОПТИКА
- § 1. Тепловое излучение и люминесценция
- § 2. Закон Кирхгофа
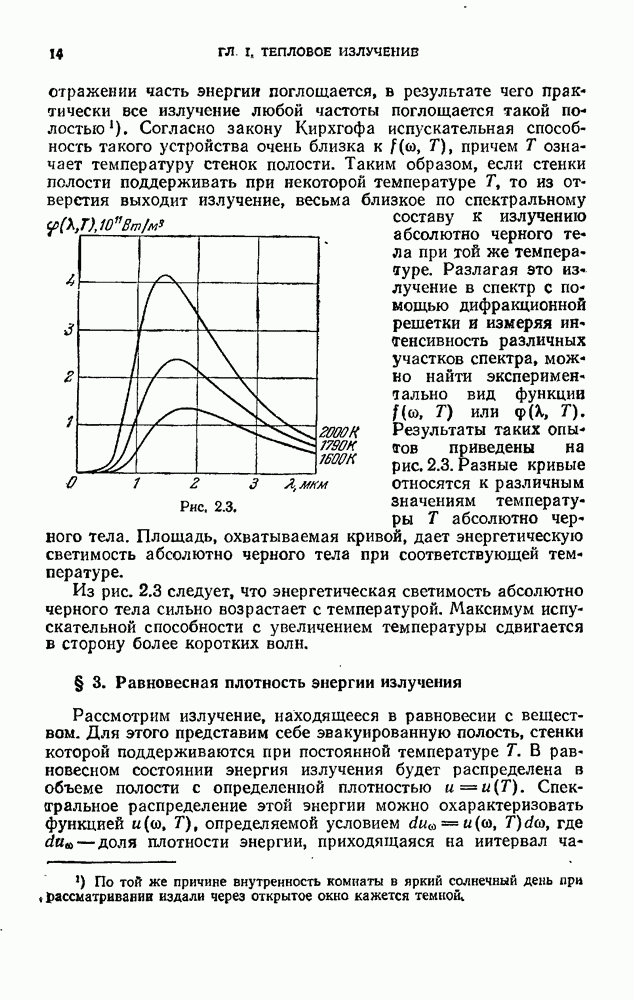
- § 3. Равновесная плотность энергии излучения
- § 4. Закон Стефана — Больцмана и закон Вина
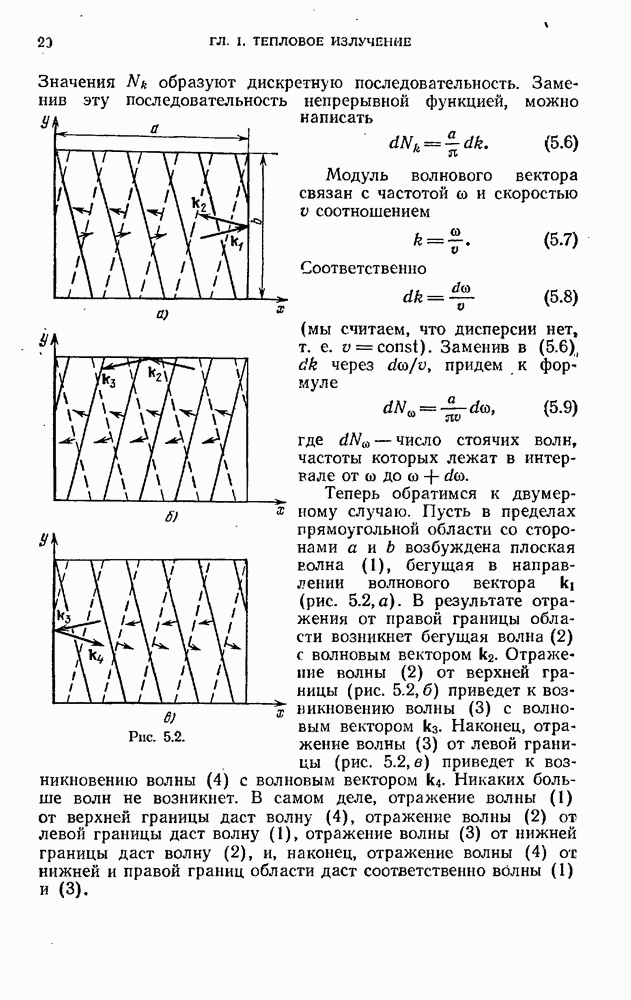
- § 5. Стоячие волны в пространстве трех измерений
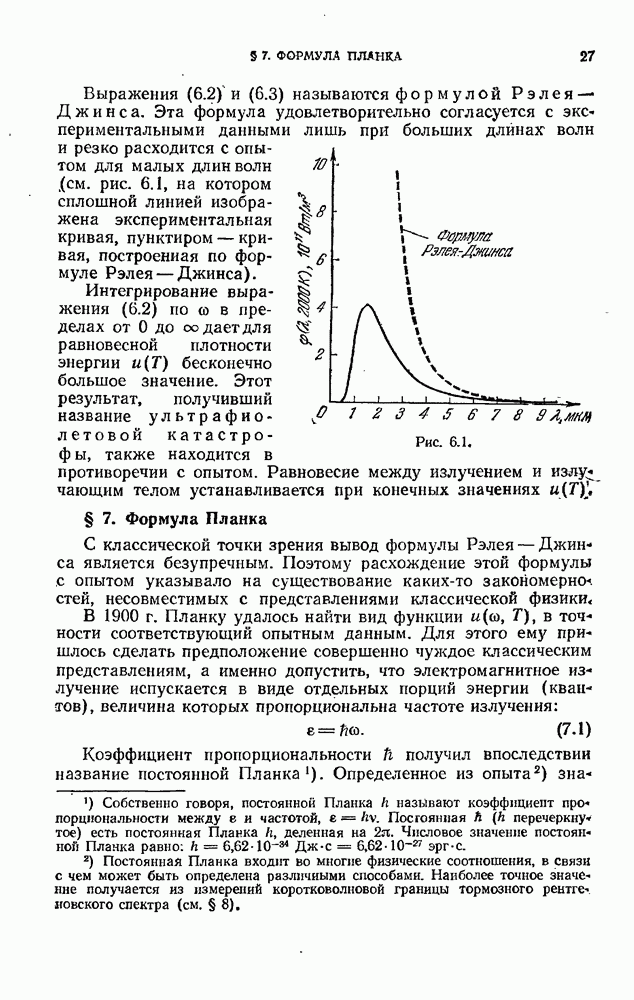
- § 6. Формула Рэлея — Джинса
- § 7. Формула Планка
- ГЛАВА II. ФОТОНЫ
- § 8. Тормозное рентгеновское излучение
- § 9. Фотоэффект
- § 10. Опыт Боте. Фотоны
- § 11. Эффект Комптона
- ЧАСТЬ 2. АТОМНАЯ ФИЗИКА
- § 12. Закономерности в атомных спектрах
- § 13. Модель атома Томсона
- § 14. Опыты по рассеянию а-частиц. Ядерная модель атома
- § 15. Постулаты Бора. Опыт Франка и Герца
- § 16. Правило квантования круговых орбит
- § 17. Элементарная боровская теория водородного атома
- ГЛАВА IV. ЭЛЕМЕНТЫ КВАНТОВОЙ МЕХАНИКИ
- § 18. Гипотеза де-Бройля. Волновые свойства вещества
- § 19. Необычные свойства микрочастиц
- § 20. Принцип неопределенности
- § 21. Уравнение Шрёдингера
- § 22. Смысл пси-функции
- § 23. Квантование энергии
- § 24. Квантование момента импульса
- § 25. Принцип суперпозиции
- § 26. Прохождение частиц через потенциальный барьер
- § 27. Гармонический осциллятор
- ГЛАВА V. ФИЗИКА АТОМОВ И МОЛЕКУЛ
- § 28. Атом водорода
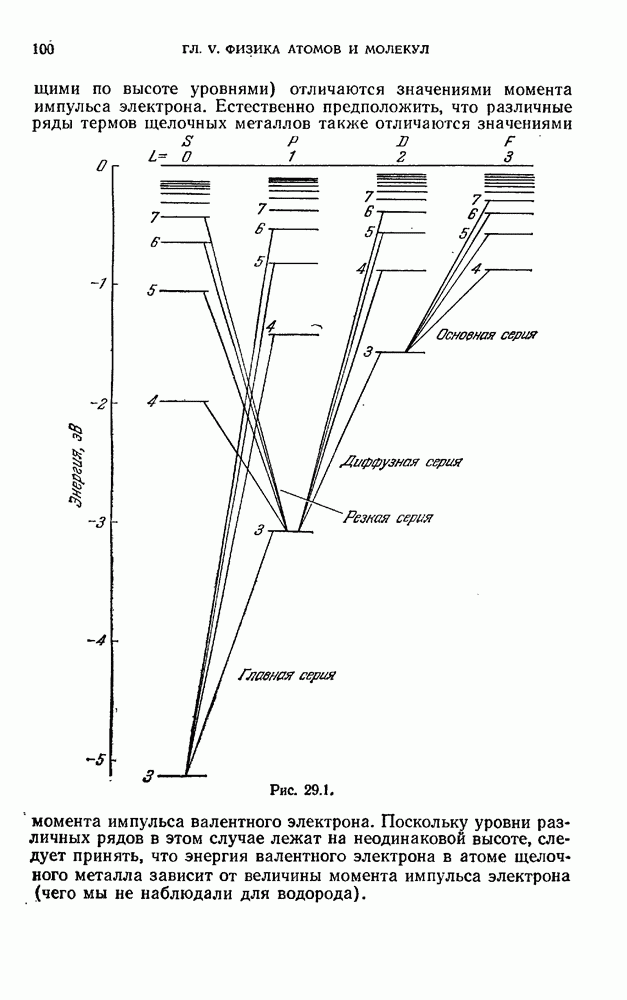
- § 29. Спектры щелочных металлов
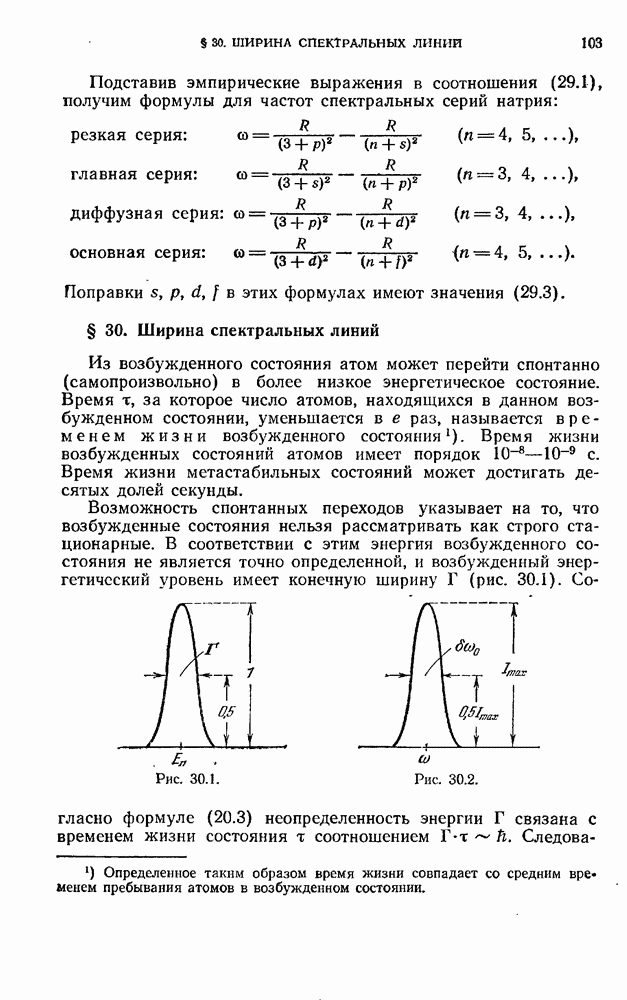
- § 30. Ширина спектральных линий
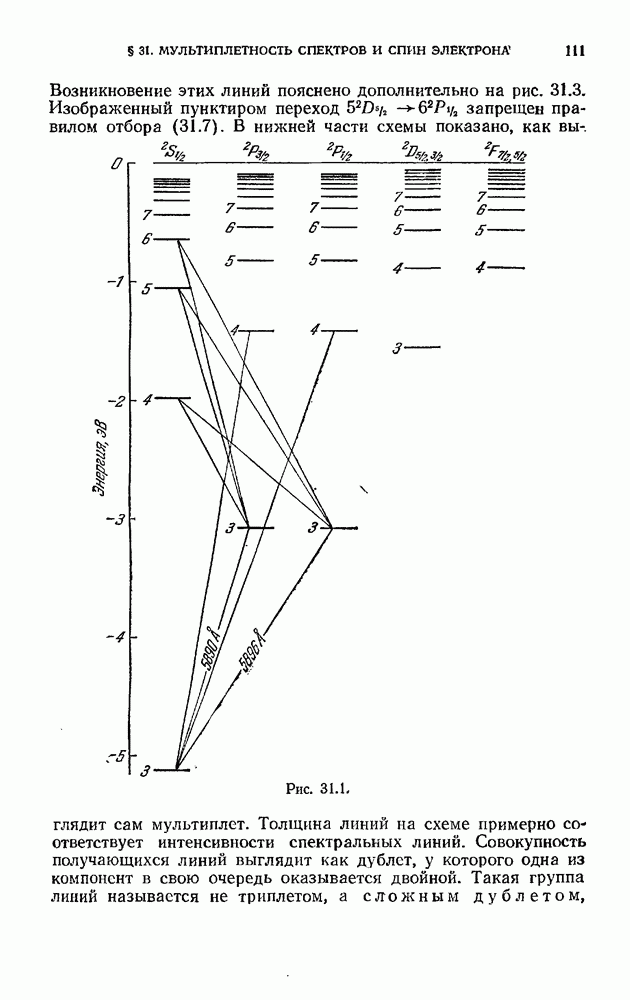
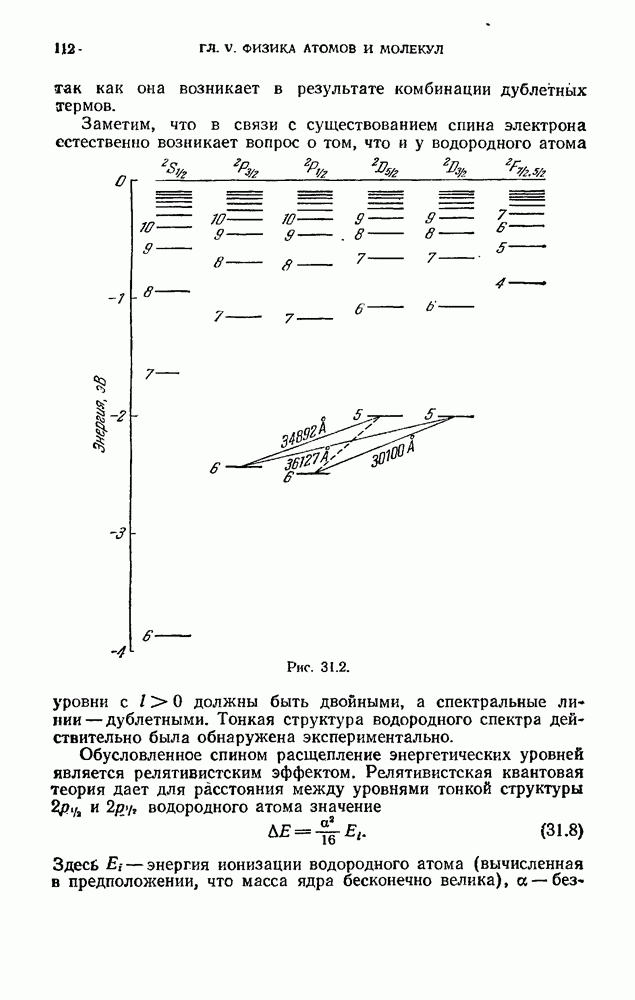
- § 31. Мультиплетность спектров и спин электрона
- § 32. Результирующий механический момент многоэлектронного атома
- § 33. Магнитный момент атома
- § 34. Эффект Зеемана
- § 35. Электронный парамагнитный резонанс
- § 36. Принцип Паули. Распределение электронов по энергетическим уровням атома
- § 37. Периодическая система элементов Менделеева
- § 38. Рентгеновские спектры
- § 39. Энергия молекулы
- § 40. Молекулярные спектры
- § 41. Комбинационное рассеяние света
- § 42. Вынужденное излучение
- § 43. Лазеры
- § 44. Нелинейная оптика
- ЧАСТЬ 3. ФИЗИКА ТВЕРДОГО ТЕЛА
- § 45. Кристаллическая решетка. Индексы Миллера
- § 46. Теплоемкость кристаллов. Теория Эйнштейна
- § 47. Колебания систем с большим числом степеней свободы
- § 48. Теория Дебая
- § 49. Фононы
- § 50. Эффект Мёссбауэра
- ГЛАВА VII. ЗОННАЯ ТЕОРИЯ ТВЕРДЫХ ТЕЛ
- § 51. Квантовая теория свободных электронов в металле
- § 52. Распределение Ферми — Дирака
- § 53. Энергетические зоны в кристаллах
- § 54. Динамика электронов в кристаллической решетке
- ГЛАВА VIII. ЭЛЕКТРОПРОВОДНОСТЬ МЕТАЛЛОВ И ПОЛУПРОВОДНИКОВ
- § 55. Электропроводность металлов
- § 56. Сверхпроводимость
- § 57. Полупроводники
- § 58. Собственная проводимость полупроводников
- § 59. Примесная проводимость полупроводников
- ГЛАВА IX. КОНТАКТНЫЕ И ТЕРМОЭЛЕКТРИЧЕСКИЕ ЯВЛЕНИЯ
- § 60. Работа выхода
- § 61. Термоэлектронная эмиссия. Электронные лампы
- § 62. Контактная разность потенциалов
- § 63. Термоэлектрические явления
- § 64. Полупроводниковые диоды и триоды
- § 65. Внутренний фотоэффект
- ЧАСТЬ 4. ФИЗИКА АТОМНОГО ЯДРА И ЭЛЕМЕНТАРНЫХ ЧАСТИЦ
- § 66. Состав и характеристики атомного ядра
- § 67. Масса и энергия связи ядра
- § 68. Модели атомного ядра
- § 69. Ядерные силы
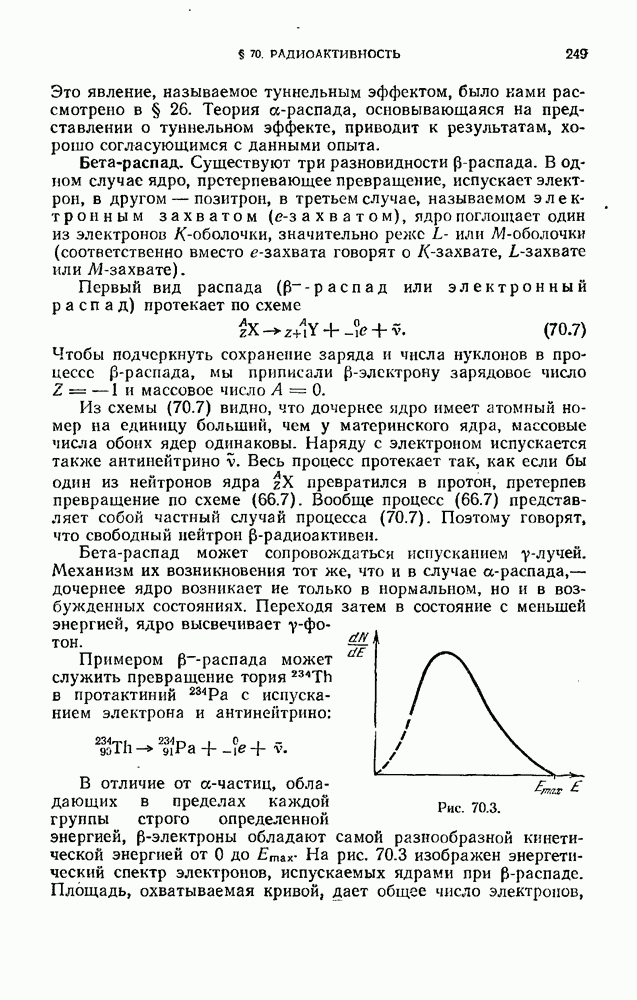
- § 70. Радиоактивность
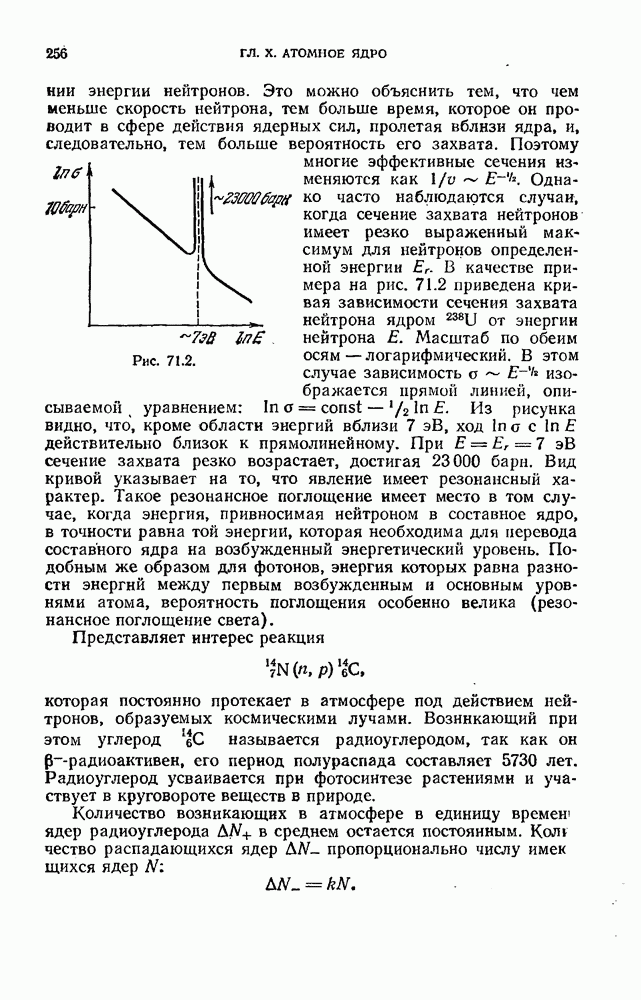
- § 71. Ядерные реакции
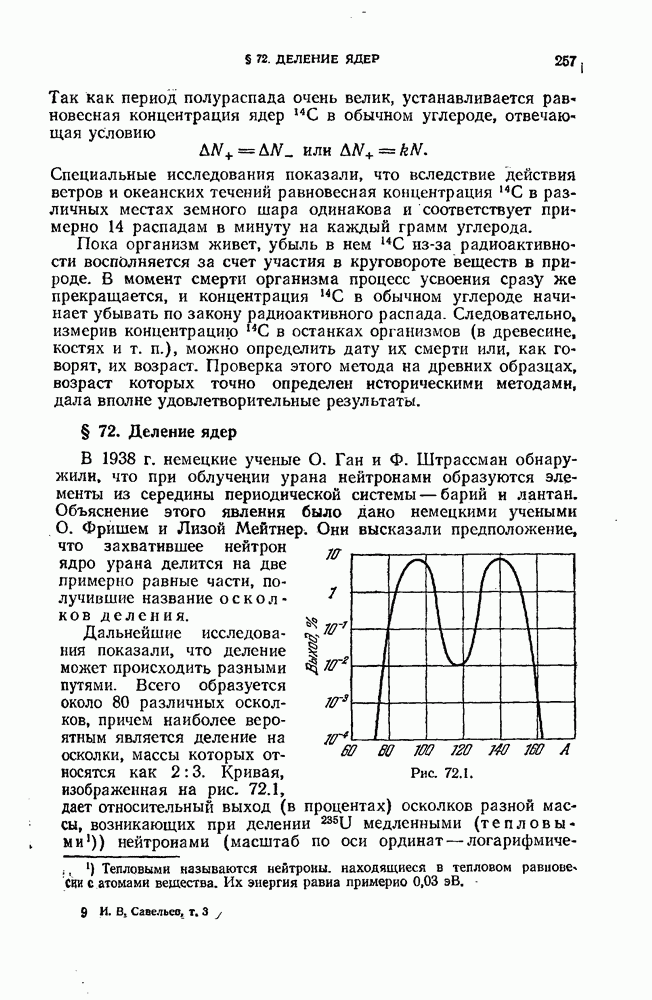
- § 72. Деление ядер
- § 73. Термоядерные реакции
- ГЛАВА XI. ЭЛЕМЕНТАРНЫЕ ЧАСТИЦЫ
- § 74. Виды взаимодействий и классы элементарных частиц
- § 75. Методы регистрации элементарных частиц
- § 76. Космические лучи
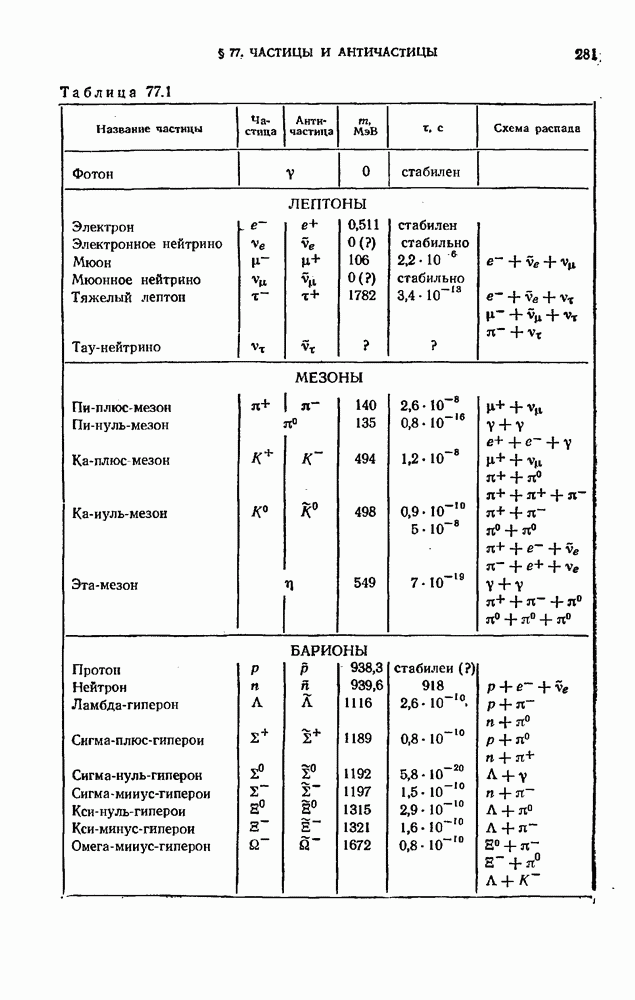
- § 77. Частицы и античастицы
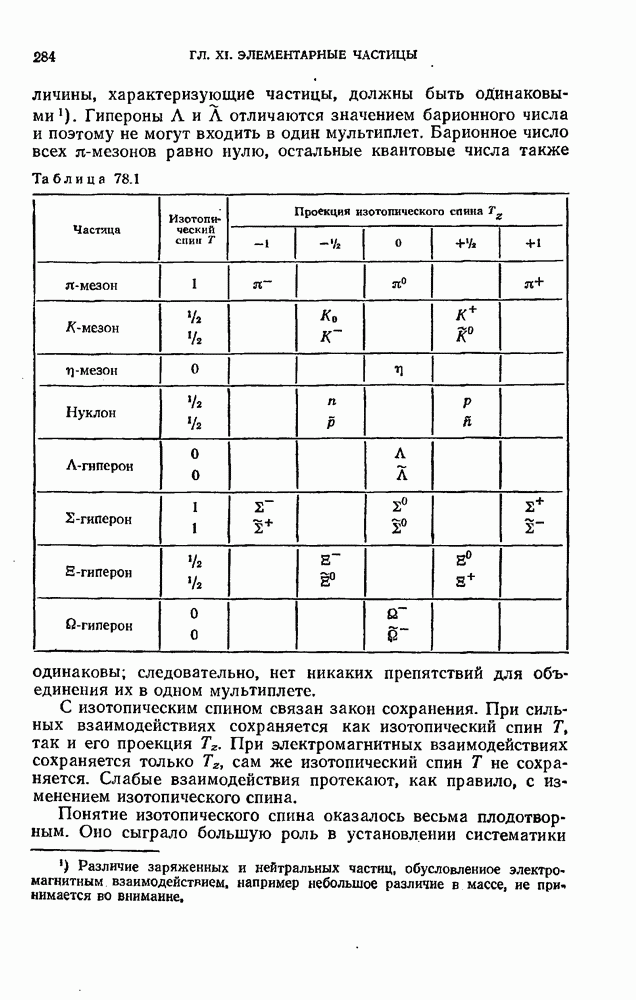
- § 78. Изотопический спин
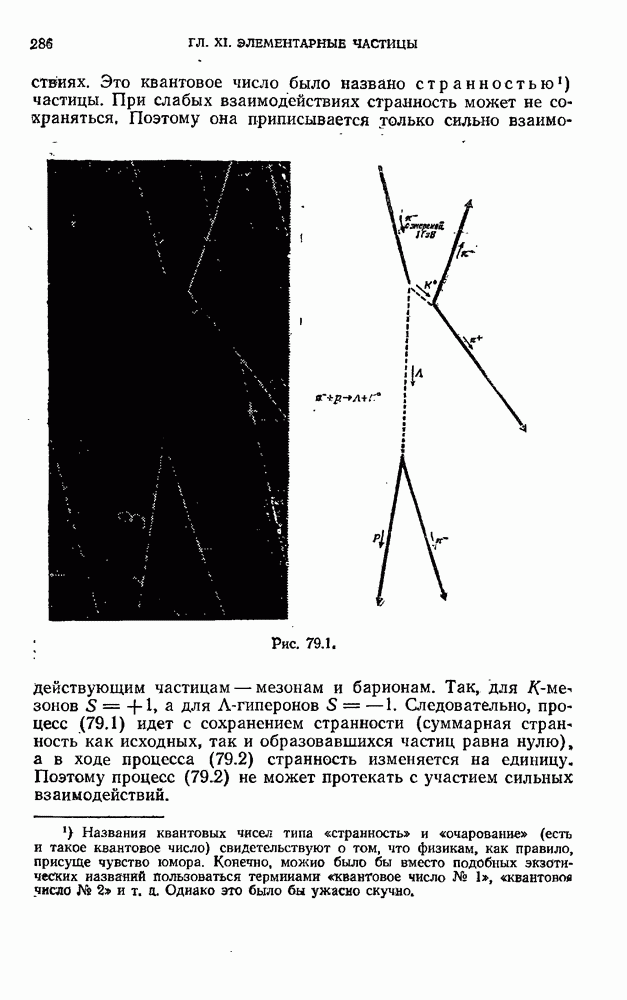
- § 79. Странные частицы
- § 80. Несохранение четности в слабых взаимодействиях
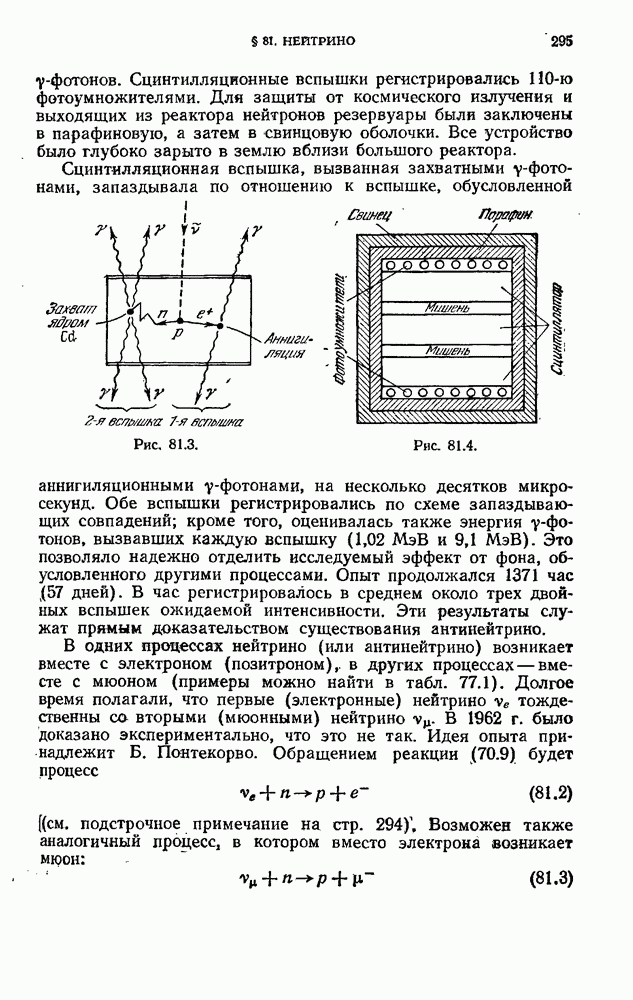
- § 81. Нейтрино
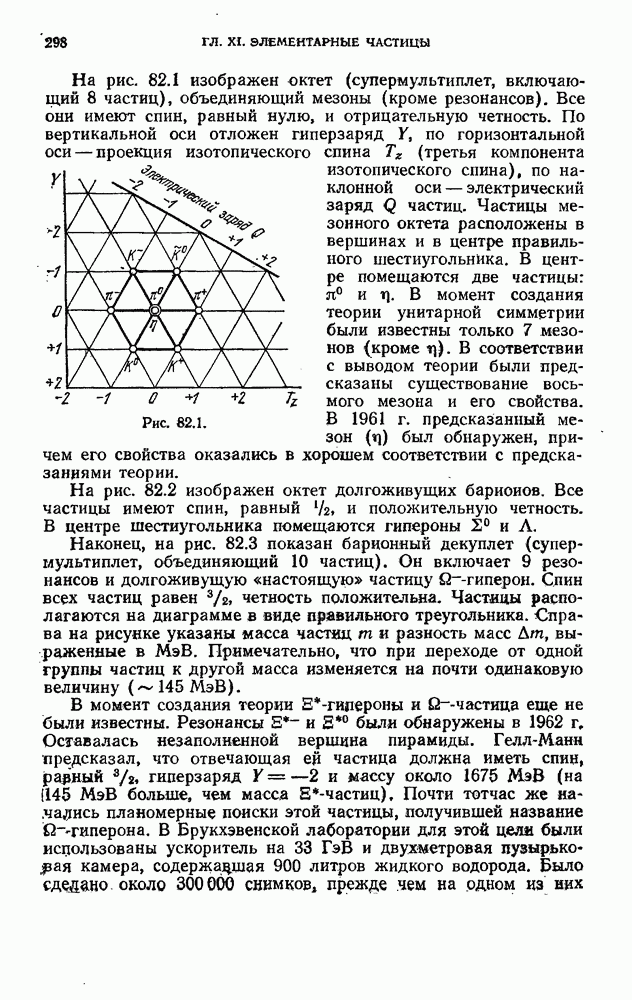
- § 82. Систематика элементарных частиц
- § 83. Кварки
- § 84. Великое объединение
- ПРИЛОЖЕНИЯ
- I. ГРАВИТАЦИОННОЕ ВЗАИМОДЕЙСТВИЕ