| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
Сложные эфиры карбоновых кислот
Сложные эфиры карбоновых кислот можно рассматривать как продукты замещения гидроксила кислоты на спиртовый остаток

а также как производные спиртов и как смешанные ангидриды кислот и спиртов.
Номенклатура. Названия сложных эфиров производятся от названий тех кислот и спиртов, которые образуют эфиры, например:

Физические свойства. Сложные эфиры предельных кислот — легколетучие жидкости. Они легче воды. Интересно отметить, что большинство предельных карбоновых кислот обладает очень неприятным запахом, однако их сложные эфиры, наоборот, имеют приятный фруктовый запах. Поэтому многие сложные эфиры (уксусноизоамиловый, масляноэтиловый и др.) применяются для изготовления «фруктовых эссенций».
Все сложные эфиры хорошо растворимы в сшфте и диэтиловом эфире.
Химические свойства. Гидролиз (омыление). При действии водных растворов едкой щелочи или минеральной кислоты сложные эфиры распадаются на молекулы исходной кислоты и спирта:

Восстановление. При восстановлении сложных эфиров образуются два спирта: один из них по числу углеродных атомов соответствует исходной кислоте, а другой — спирту, входящему в состав сложного эфира:

Образование амидов кислот происходит при действии на сложные эфиры аммиака: 4

Способы получения. Реакция этерификации. Важнейшим методом получения сложных эфиров является реакция этерификации — взаимодействие спирта с кислотой:

Современными методами исследования доказано, что при реакции этерификации от молекулы, кислоты отщепляется гидроксил, а от молекулы спирта — водород.
Наряду с этерификацией протекает и обратная реакция гидролиза {омыления), при которой сложный эфир расщепляется на кислоту и спирт. В зависимости от природы и количества участвующих в реакции этерификации кислоты и спирта равновесие реакции сдвигается в ту или иную сторону.
Для ускорения реакции этерификации, т. е. для ускорения образования сложного эфира, необходим катализатор — водородные ионы. С этой целью в реакционную смесь пропускают обычно газообразный хлористый водород или добавляют концентрированную серную кислоту. В присутствии водоотнимающих средств равновесие реакции этерификации также сдвигается в сторону образования сложного эфира.
Получение сложных эфиров из галоидпроизводных углеводородов и серебряных солей карбоновых кислот. Реакция лротекает по схеме

Способы получения сложных эфиров из хлорангидридов и ангидридов описанына стр. 132 и 133.
Уксусноэтиловый эфир  (этилацетат). Бесцветная, легколетучая жидкость, кипящая при 78 °С. Обладает приятным запахом. Применяется в качестве растворителя и промежуточного вещества для синтеза различных органических соединений.
(этилацетат). Бесцветная, легколетучая жидкость, кипящая при 78 °С. Обладает приятным запахом. Применяется в качестве растворителя и промежуточного вещества для синтеза различных органических соединений. 
В промышленности этилацетат получают из ацетальдегида по реакции Тищенко (стр. 110):

Процесс проводится при 0 °С. В качестве катализатора применяют смесь этилата алюминия, хлористого алюминия и этилата цинка.
Уксусновиниловый эфир  (винилацетат).
(винилацетат).
Жидкость. обладающая слезоточивым действием; темп. кип. 73 °С. Винилацетат нашел широкое применение в производстве пластических масс вследствие очень легкой полимеризации его в поливинилацетат, превращающийся после омылёния в поливиниловый спирт:

Получается винилацетат взаимодействием ацетилена с уксусной кислотой:

Катализатором этой реакции служат соли ртути.
| << Предыдущий параграф | Следующий параграф >> |
- ВВЕДЕНИЕ
- АЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ (АЛИФАТИЧЕСКИЕ, ИЛИ ЖИРНЫЕ, СОЕДИНЕНИЯ
- 1. ПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
- 2. НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
- Углеводороды ряда этилена (олефины, алкены)
- Углеводороды ряда ацетилена (алкины)
- Углеводороды с двумя этиленовыми связями. (диолефины, диены)
- 3. НЕФТЬ. ПРИРОДНЫЕ ГАЗЫ И ГАЗЫ НЕФТЕПЕРАРАБОТКИ
- Природные газы и газы нефтепереработки как сырье для получения химических веществ
- 4. ГАЛОИДПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
- Галоидпроизводные этиленовых углеводородов
- 5. СПИРТЫ И ИХ ПРОИЗВОДНЫЕ
- Непредельные спирты
- Многоатомные спирты
- Простые эфиры
- Эпоксиды
- 6. ТИОСПИРТЫ И ТИОЭФИРЫ
- 7. АЛЬДЕГИДЫ И КЕТОНЫ
- 8. КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
- Непредельные кислоты
- Галоидангидриды кислот
- Ангидриды кислот
- Сложные эфиры минеральных кислот
- Сложные эфиры карбоновых кислот
- Жиры
- Мыла
- Синтетические моющие средства
- Амиды кислот
- Нитрилы кислот
- Предельные двухосновные кислоты
- 9. СОЕДИНЕНИЯ ЦИАНА И ПРОИЗВОДНЫЕ УГОЛЬНОЙ КИСЛОТЫ
- Производные угольной кислоты
- 10. НИТРОСОЕДИНЕНИЯ
- 11. АМИНЫ
- Диамины
- 12. ЭЛЕМЕНТООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- Кремнийорганические соединения
- Фосфорорганические соединения
- Мышьякорганические соединения
- 13. ОКСИКИСЛОТЫ
- Двухосновные оксикислоты
- 14. АЛЬДЕГИДОКИСЛОТЫ И КЕТОНОКИСЛОТЫ
- 15. УГЛЕВОДЫ (САХАРА)
- Простые углеводы (моносахариды, монозы)
- Сложные углеводы (полисахариды)
- 16. АМИНОКИСЛОТЫ
- ЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 17. АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- Терпены
- 18. АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
- Ароматические углеводороды ряда бензола
- Ароматические углеводороды с непредельными боковыми цепями
- 19. ГАЛОИДПРОИЗВОДНЫЕ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ
- Галоидпроизводные ароматических углеводородов, содержащие галоид в боковой цепи
- 20. НИТРОСОЕДИНЕНИЯ АРОМАТИЧЕСКОГО РЯДА
- 21. СУЛЬФОКИСЛОТЫ АРОМАТИЧЕСКОГО РЯДА
- 22. ФЕНОЛЫ И АРОМАТИЧЕСКИЕ СПИРТЫ
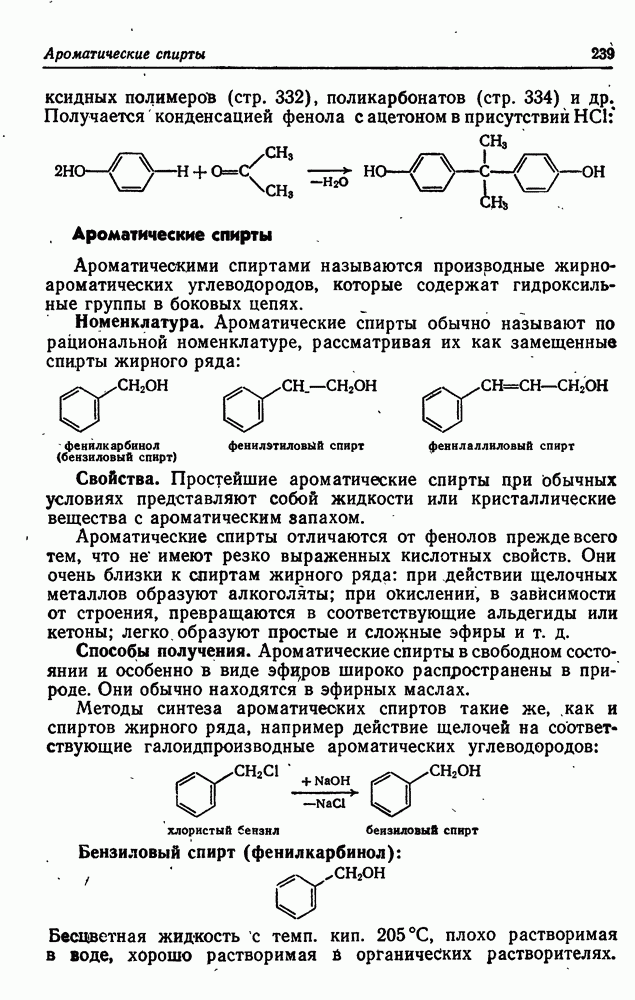
- Ароматические спирты
- 23. ХИНОНЫ И ХИНОНИМИНЫ
- 24. АРОМАТИЧЕСКИЕ АЛЬДЕГИДЫ И КЕТОНЫ
- Ароматические кетоны
- 25. АРОМАТИЧЕСКИЕ КИСЛОТЫ
- Двухосновные кислоты ряда бензола
- 26. АРОМАТИЧЕСКИЕ АМИНЫ
- Ароматические амины с аминогруппой в боковой цепи
- Ароматические диамины
- Хинониминовые красители
- 27. АРОМАТИЧЕСКИЕ ДИАЗОСОЕДИНЕНИЯ И АЗОКРАСИТЕЛИ
- Азокрасители
- Активные красители
- О зависимости между строением и окраской органических соединений
- 28. МНОГОЯДЕРНЫЕ АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
- Трифенилметановые красители
- Ароматические соединения с конденсированными ядрами
- 29. ХИМИЧЕСКИЕ СРЕДСТВА ЗАЩИТЫ РАСТЕНИЯ И ЖИВОТНЫХ (ПЕСТИЦИДЫ)
- Средства борьбы с болезнями растений (фунгициды и протравители)
- Средства борьбы с сорной растительностью (гербициды)
- Регуляторы роста растений
- Химические средства защиты животных
- 30. ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- Пятичленные гетероциклические соединения
- Шестичленные гетероциклические соединения
- Алкалоиды
- ВЫСОКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ
- 31. ОСНОВНЫЕ СВЕДЕНИЯ О ХИМИИ И ТЕХНОЛОГИЯ ПОЛИМЕРОВ
- Понятие о синтезе полимеров
- Понятие о технологии полимеров
- 32. ПЛАСТИЧЕСКИЕ МАССЫ
- 33. СИНТЕТИЧЕСКИЕ ИОНИТЫ
- 34. ЭЛЕМЕНТООРГАНИЧЕСКИЕ ПОЛИМЕРЫ
- 35. ХИМИЧЕСКИЕ ВОЛОКНА (ИСКУССТВЕННЫЕ И СИНТЕТИЧЕСКИЕ)
- Понятие о технологии изготовления химических волокон
- Искусственные волокна
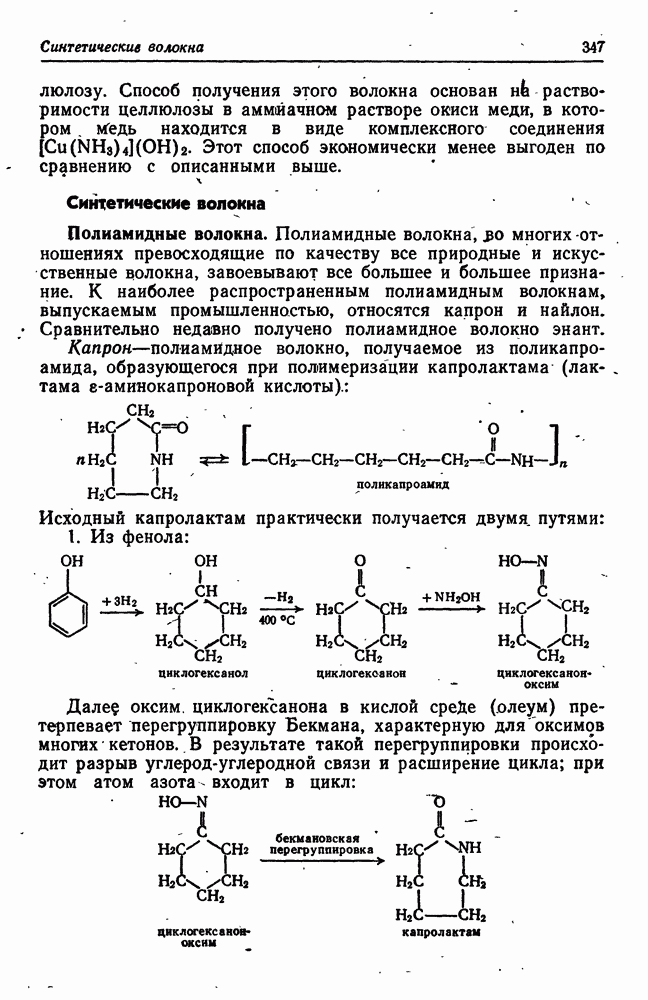
- Синтетические волокна
- 36. КАУЧУКИ
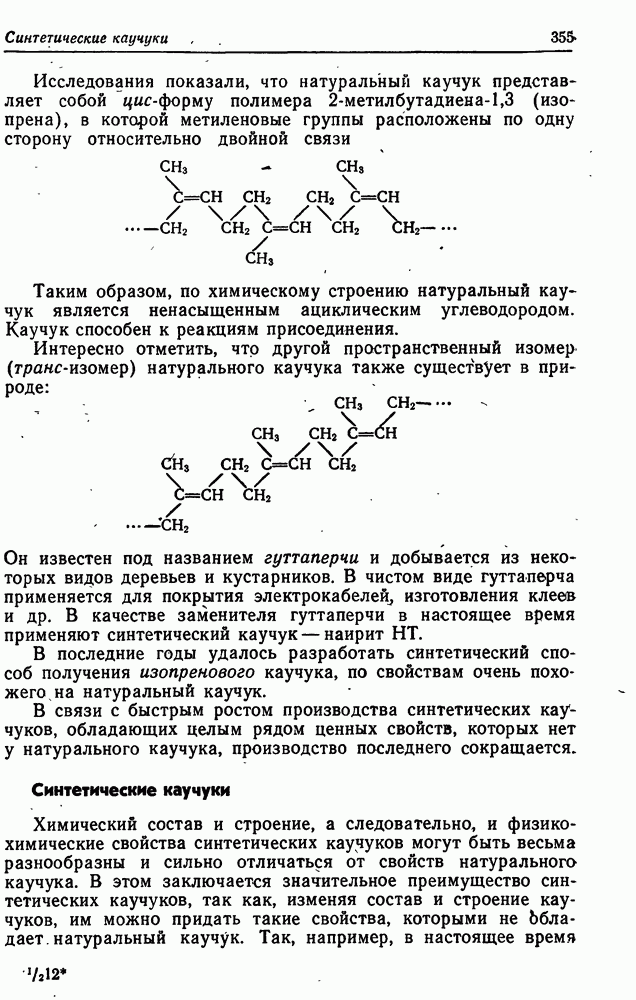
- Натуральный каучук
- Синтетические каучуки
- Синтетические латексы
- 37. СИНТЕТИЧЕСКИЕ КЛЕИ
- ХИМИЧЕСКИЕ ОСНОВЫ ЖИЗНЕДЕЯТЕЛЬНОСТИ
- 38. БЕЛКИ
- 39. НУКЛЕИНОВЫЕ КИСЛОТЫ
- 40. ЖИРЫ И УГЛЕВОДЫ
- 41. РОЛЬ БЕЛКОВ В ПРОЦЕССАХ ЖИЗНЕДЕЯТЕЛЬНОСТИ
- 42. СИНТЕЗ БЕЛКА В ОРГАНИЗМЕ
- ФИЗИОЛОГИЧЕСКИ АКТИВНЫЕ ВЕЩЕСТВА
- 43. ВИТАМИНЫ
- Витамин А
- Витамин С (аскорбиновая кислота)
- Витамины группы D
- 44. ГОРМОНЫ
- 45. АНТИБИОТИКИ