| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
26. АРОМАТИЧЕСКИЕ АМИНЫ
Простейшим ароматическим амином является аминобензол  который получил название анилин (от испанского
который получил название анилин (от испанского  индщо, так как впервые анилин был получен в 1826 г. из красителя индиго).
индщо, так как впервые анилин был получен в 1826 г. из красителя индиго).
В зависимости от числа углеводородных радикалов, связанных с азотом аминогруппы, ароматические амины, как и алифатические, подразделяются на первичные, вторичные и третичные. Кроме того, в зависимости от характера углеводородных радикалов, они делятся на чисто ароматические и жирно-ароматические.
Ароматические амины с аминогруппой в ядре
Номенклатура. Названия ароматических аминов по рациональной номенклатуре производят от названий заместителей у атома азота и названия ароматического радикала. Положения заместителей в бензольном кольце обозначают или. цифрами или (если их не более двух) названиями изомеров — орто-, мета-, пара-, например:

Ароматические амины — производные толуола, называют толуидинами:

Ароматические амины — производные ксилола, называют ксилидинами:

Свойства. Ароматические амины представляют собой бесцветные твердые или жидкие вещества с характерным запахом. Плотность их около единицы. Простейшие амины слабо растворимы в воде, высшие амины в воде нерастворимы.
Первичные ароматические амины, например анилин  являются значительно более слабыми основаниями, чем амины жирного ряда. Они образуют соли с сильными кислотами:
являются значительно более слабыми основаниями, чем амины жирного ряда. Они образуют соли с сильными кислотами:

Чисто ароматические вторичные амины, например дифениламин  представляют собой еще более слабый основания, чем первичные ароматические амины. Жирноароматические вторичные амины, например
представляют собой еще более слабый основания, чем первичные ароматические амины. Жирноароматические вторичные амины, например  (метил-анилин), являются более сильными основаниями, чем ароматические первичные амины, но более слабыми, чем амины жирного ряда. Жирноароматические третичные амины, найример диметиланилин
(метил-анилин), являются более сильными основаниями, чем ароматические первичные амины, но более слабыми, чем амины жирного ряда. Жирноароматические третичные амины, найример диметиланилин  обладают ярко выраженными основными свойствами. Чисто ароматические третичные амины, например, трифениламин
обладают ярко выраженными основными свойствами. Чисто ароматические третичные амины, например, трифениламин  совершенно лишены основных свойств. Таким образом, накопление фенильных остатков
совершенно лишены основных свойств. Таким образом, накопление фенильных остатков
в молекуле ароматических аминов приводит к ослаблению их основных свойств.
Замещение атомов водорода аминогруппы, а) Замещение алкильными остатками. При действии на первичные и вторичные ароматические амины галоидных алкилов происходит образование соответствующих вторичных и третичных аминов:

б) Замещение остатком кислоты (ацилом). При действии на первичные ароматические амины, например, уксусного ангидрида образуются анилиды:

Анилиды можно рассматривать как производные амидов кислот. Например, ацетанилид можно рассматривать как амид уксусной кислоты  в котором один водород замещен на фенильный радикал
в котором один водород замещен на фенильный радикал 
Действие азотистой кислоты, а) Соли первичных ароматических аминов при действии на них азотистой кислоты образуют диазосоединения:

Эта реакция носит название диазотирования. Диазосоединения очень реакционноспособны и имеют большое значение для. синтеза различных органических веществ (подробнее о диазосоединениях см. стр. 260).
б) При действии азотистой кислоты на вторичные амины (как чисто ароматические, так и жирно-ароматические) происходит замещение атома водорода, находящегося при атоме азота, на нитрозогруппу  Образующиеся при этом вещества называются нитрозаминами:
Образующиеся при этом вещества называются нитрозаминами:

Буква  перед названием соединения указывает, что замещающая группа
перед названием соединения указывает, что замещающая группа  непосредственно связана с атомом азота.
непосредственно связана с атомом азота.
в) При действии азотистой кислоты на третичные жирно-ароматические амины происходит реакция - нитрозирования, т. е. замещение подвижного атома водорода в бензольном ядре в пара-положении к аминогруппе на нитрозогруппу:

Замещение атомов водорода в ароматическом кольце. Аминогруппа очень заметно усиливает подвижность водородных атомов бензольного кольца, находящихся в орто,- и пара-положениях, вследствие чего они легко замещаются некоторыми атомами и группами.
а) Замещение на атомы галоидов (галдидирование). Замещение атомов водорода на галоиды происходит очень легко уже при действии бромной (или хлорной) воды на холоду. При этом согласно правилам замещения в бензольном ядре атомы галоида становятся в орто-, и пара-положения относительно аминогруппы:

б) Замещение на сульфо- и нитрогруппы. Водородные атомы бензольного кольца легко замещаются на сульфогруппу:

Образующаяся при этой реакции  -аминобензолсульфокислота (сульфаниловая кислота), является важным промежуточным продуктом при синтезе красителей и других органических соединений. У сульфаниловой кислоты ярко выражены кислотные свойства.
-аминобензолсульфокислота (сульфаниловая кислота), является важным промежуточным продуктом при синтезе красителей и других органических соединений. У сульфаниловой кислоты ярко выражены кислотные свойства.
Так же легко водородные атомы бензольного кольца в ароматических аминах замещаются на нитрогруппу.
Окисление. При окислении анилина можно получить хинон и его производные:

При этой реакции образуется целый ряд сложных соединений (например, краситель анилиновый черный). В зависимости от условий окисления могут образовываться различные соединения, в том числе и аналогичные получающимся при восстановлении нитробензола.
Способы получения. Важнейшим способом получения первичных ароматических аминов. является восстановление нитросоединений (стр. 223):

Эта реакция была открыта выдающимся русским ученым Н. Н. Зининым и играет громадную роль в синтезе многочисленных органических соединений.. В качестве восстанавливающих средств применяются самые разнообразные вещества.
С одним способом получения вторичных и третичных жирно-ароматических аминов мы уже знакомы (стр. 254).
Чисто ароматический вторичный амин, например дифениламин, можно получить при нагревании соли анилина со свободным анилином:

Чисто ароматический третичный амин, например, трифениламин, получается из дифениламина и иодбензола в присутствии поташа и меди:

Анилин (фениламин)  Бесцветная жидкость с темп. кип. 184°С, буреющая на воздухе вследствие постепенного окисления. В воде растворим плохо; смешивается в любых соотношениях со спиртом, эфиром и бензолом.
Бесцветная жидкость с темп. кип. 184°С, буреющая на воздухе вследствие постепенного окисления. В воде растворим плохо; смешивается в любых соотношениях со спиртом, эфиром и бензолом.
Анилин является основным сырьем анилинокрасочной промышленности и производится десятками тысяч тонн ежегодно. Помимо производства красителей анилин широко используется для синтеза самых разнообразных органических соединений.
Промышленным способом получения анилина является восстановление нитробензола железом в присутствии электролитов. Ввиду наличия раствора электролита (обычно  и незначительного количества соляной кислоты в реакционной смеси процесс восстановления нитробензола в этом случае по существу протекает почти в нейтральной среде:
и незначительного количества соляной кислоты в реакционной смеси процесс восстановления нитробензола в этом случае по существу протекает почти в нейтральной среде:

В качестве катализатора применяется чугунная стружка и производственный процесс осложнен образованием большого количества побочных отходов — железного шлама.
Этот старый промышленный способ вытесняется современным контактным, лишенным этих недостатков. При получении анилина контактным способом смесь паров нитробензола и водорода (в соотношении  поступает в контактный аппарат, в котором находится катализатор (окислы или сульфиды металлов). Реакция проводится при
поступает в контактный аппарат, в котором находится катализатор (окислы или сульфиды металлов). Реакция проводится при  Продукты реакции охлаждают и направляют на разделение и очистку
Продукты реакции охлаждают и направляют на разделение и очистку
Дифениламин  Вторичный чисто аромати ческий амин. При обычных условиях кристаллическое вещество с темп. пл. 54 °С; нерастворим в воде и разбавленных кислотах. Хорошо растворим в органических растворителях.
Вторичный чисто аромати ческий амин. При обычных условиях кристаллическое вещество с темп. пл. 54 °С; нерастворим в воде и разбавленных кислотах. Хорошо растворим в органических растворителях.
Дифениламин применяется в качестве промежуточного продукта в производстве красителей.
Диметилзннлин  Третичный жирноароматический амин. Представляет собой жидкость с характерным запахом; темп. кип. 193 °С.
Третичный жирноароматический амин. Представляет собой жидкость с характерным запахом; темп. кип. 193 °С.
Благодаря большой подвижности атома водорода, находящегося в пара-положении относительно аминогруппы, диметил-анилин широко используется для синтеза красителей и других органических соединений. Так, например, при взаимодействии двух молекул диметиланилина с фосгеном образуется аминокетон (кетон Михлера), играющий важную роль в производстве красителей:

Диметиланилин получается взаимодействием сернокислого анилина с метанолом при нагревании, под давлением:

| << Предыдущий параграф | Следующий параграф >> |
- ВВЕДЕНИЕ
- АЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ (АЛИФАТИЧЕСКИЕ, ИЛИ ЖИРНЫЕ, СОЕДИНЕНИЯ
- 1. ПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
- 2. НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
- Углеводороды ряда этилена (олефины, алкены)
- Углеводороды ряда ацетилена (алкины)
- Углеводороды с двумя этиленовыми связями. (диолефины, диены)
- 3. НЕФТЬ. ПРИРОДНЫЕ ГАЗЫ И ГАЗЫ НЕФТЕПЕРАРАБОТКИ
- Природные газы и газы нефтепереработки как сырье для получения химических веществ
- 4. ГАЛОИДПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
- Галоидпроизводные этиленовых углеводородов
- 5. СПИРТЫ И ИХ ПРОИЗВОДНЫЕ
- Непредельные спирты
- Многоатомные спирты
- Простые эфиры
- Эпоксиды
- 6. ТИОСПИРТЫ И ТИОЭФИРЫ
- 7. АЛЬДЕГИДЫ И КЕТОНЫ
- 8. КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
- Непредельные кислоты
- Галоидангидриды кислот
- Ангидриды кислот
- Сложные эфиры минеральных кислот
- Сложные эфиры карбоновых кислот
- Жиры
- Мыла
- Синтетические моющие средства
- Амиды кислот
- Нитрилы кислот
- Предельные двухосновные кислоты
- 9. СОЕДИНЕНИЯ ЦИАНА И ПРОИЗВОДНЫЕ УГОЛЬНОЙ КИСЛОТЫ
- Производные угольной кислоты
- 10. НИТРОСОЕДИНЕНИЯ
- 11. АМИНЫ
- Диамины
- 12. ЭЛЕМЕНТООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- Кремнийорганические соединения
- Фосфорорганические соединения
- Мышьякорганические соединения
- 13. ОКСИКИСЛОТЫ
- Двухосновные оксикислоты
- 14. АЛЬДЕГИДОКИСЛОТЫ И КЕТОНОКИСЛОТЫ
- 15. УГЛЕВОДЫ (САХАРА)
- Простые углеводы (моносахариды, монозы)
- Сложные углеводы (полисахариды)
- 16. АМИНОКИСЛОТЫ
- ЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 17. АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- Терпены
- 18. АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
- Ароматические углеводороды ряда бензола
- Ароматические углеводороды с непредельными боковыми цепями
- 19. ГАЛОИДПРОИЗВОДНЫЕ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ
- Галоидпроизводные ароматических углеводородов, содержащие галоид в боковой цепи
- 20. НИТРОСОЕДИНЕНИЯ АРОМАТИЧЕСКОГО РЯДА
- 21. СУЛЬФОКИСЛОТЫ АРОМАТИЧЕСКОГО РЯДА
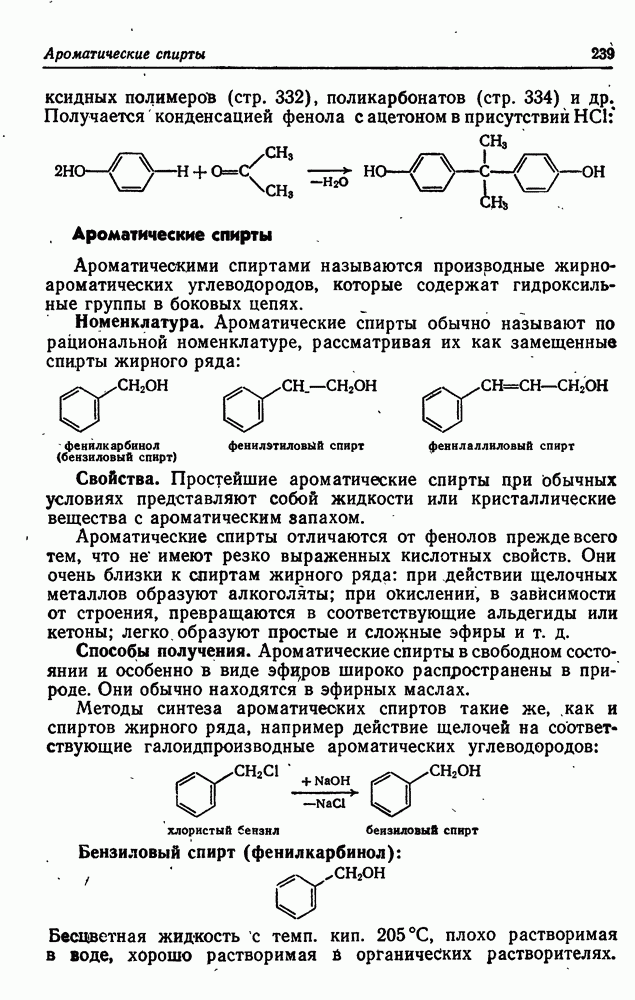
- 22. ФЕНОЛЫ И АРОМАТИЧЕСКИЕ СПИРТЫ
- Ароматические спирты
- 23. ХИНОНЫ И ХИНОНИМИНЫ
- 24. АРОМАТИЧЕСКИЕ АЛЬДЕГИДЫ И КЕТОНЫ
- Ароматические кетоны
- 25. АРОМАТИЧЕСКИЕ КИСЛОТЫ
- Двухосновные кислоты ряда бензола
- 26. АРОМАТИЧЕСКИЕ АМИНЫ
- Ароматические амины с аминогруппой в боковой цепи
- Ароматические диамины
- Хинониминовые красители
- 27. АРОМАТИЧЕСКИЕ ДИАЗОСОЕДИНЕНИЯ И АЗОКРАСИТЕЛИ
- Азокрасители
- Активные красители
- О зависимости между строением и окраской органических соединений
- 28. МНОГОЯДЕРНЫЕ АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
- Трифенилметановые красители
- Ароматические соединения с конденсированными ядрами
- 29. ХИМИЧЕСКИЕ СРЕДСТВА ЗАЩИТЫ РАСТЕНИЯ И ЖИВОТНЫХ (ПЕСТИЦИДЫ)
- Средства борьбы с болезнями растений (фунгициды и протравители)
- Средства борьбы с сорной растительностью (гербициды)
- Регуляторы роста растений
- Химические средства защиты животных
- 30. ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- Пятичленные гетероциклические соединения
- Шестичленные гетероциклические соединения
- Алкалоиды
- ВЫСОКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ
- 31. ОСНОВНЫЕ СВЕДЕНИЯ О ХИМИИ И ТЕХНОЛОГИЯ ПОЛИМЕРОВ
- Понятие о синтезе полимеров
- Понятие о технологии полимеров
- 32. ПЛАСТИЧЕСКИЕ МАССЫ
- 33. СИНТЕТИЧЕСКИЕ ИОНИТЫ
- 34. ЭЛЕМЕНТООРГАНИЧЕСКИЕ ПОЛИМЕРЫ
- 35. ХИМИЧЕСКИЕ ВОЛОКНА (ИСКУССТВЕННЫЕ И СИНТЕТИЧЕСКИЕ)
- Понятие о технологии изготовления химических волокон
- Искусственные волокна
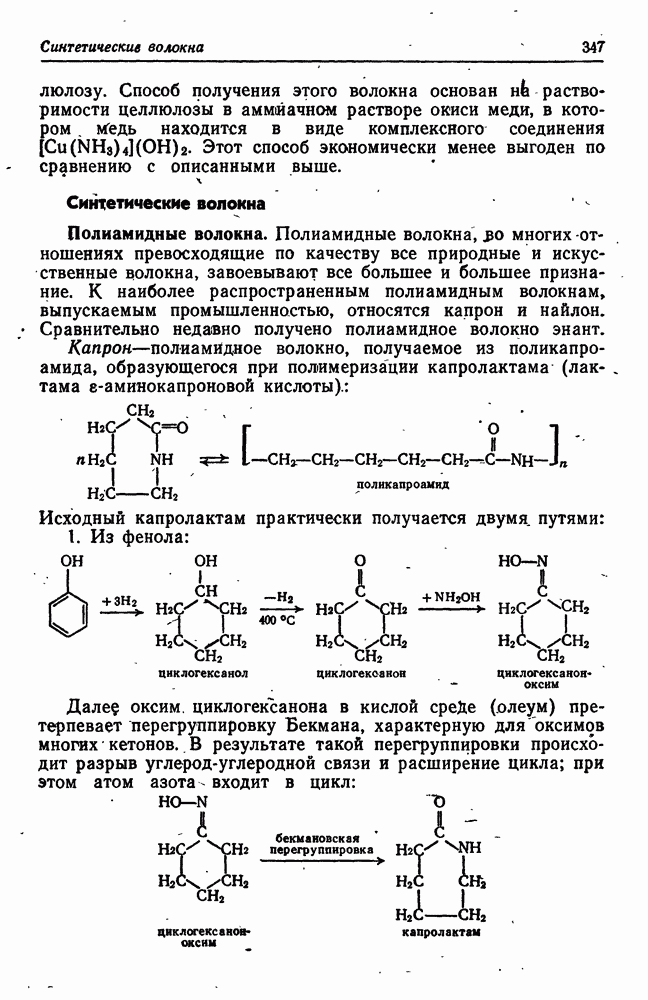
- Синтетические волокна
- 36. КАУЧУКИ
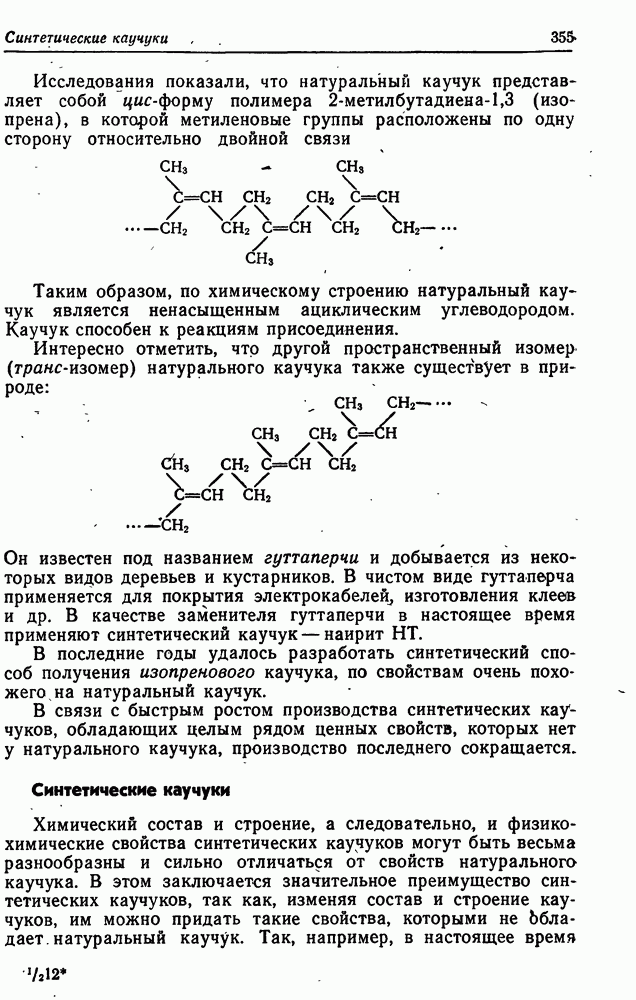
- Натуральный каучук
- Синтетические каучуки
- Синтетические латексы
- 37. СИНТЕТИЧЕСКИЕ КЛЕИ
- ХИМИЧЕСКИЕ ОСНОВЫ ЖИЗНЕДЕЯТЕЛЬНОСТИ
- 38. БЕЛКИ
- 39. НУКЛЕИНОВЫЕ КИСЛОТЫ
- 40. ЖИРЫ И УГЛЕВОДЫ
- 41. РОЛЬ БЕЛКОВ В ПРОЦЕССАХ ЖИЗНЕДЕЯТЕЛЬНОСТИ
- 42. СИНТЕЗ БЕЛКА В ОРГАНИЗМЕ
- ФИЗИОЛОГИЧЕСКИ АКТИВНЫЕ ВЕЩЕСТВА
- 43. ВИТАМИНЫ
- Витамин А
- Витамин С (аскорбиновая кислота)
- Витамины группы D
- 44. ГОРМОНЫ
- 45. АНТИБИОТИКИ