| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
Двухосновные кислоты ряда бензола
Существуют три изомерные двухосновные кислоты ряда бензола:  -фенилендикарбоновая кислота (фталевая кислота),
-фенилендикарбоновая кислота (фталевая кислота),  -фенилендикарбоновая (терефталевая) и
-фенилендикарбоновая (терефталевая) и  -фенилендикарбоновая (изофталевая):
-фенилендикарбоновая (изофталевая):

Фталевая ( -фенилендикарбоновая) кислота Кристаллическое вещество. При нагревании до 200-230 °С теряет молекулу воды и превращается во фталевый ангидрид:
-фенилендикарбоновая) кислота Кристаллическое вещество. При нагревании до 200-230 °С теряет молекулу воды и превращается во фталевый ангидрид:

Получается фталевая кислота обычно путем окисления нафталина или  -ксилола. Пары нафталина при высокой температуре (около 450 °С) пропускают над катализатором, осажденным на окиси кремния. Образующаяся фталевая кислота теряет молекулу воды и превращается во фталевый ангидрид:
-ксилола. Пары нафталина при высокой температуре (около 450 °С) пропускают над катализатором, осажденным на окиси кремния. Образующаяся фталевая кислота теряет молекулу воды и превращается во фталевый ангидрид:

Окисление  -ксилола проводят при температуре около 600 °С над катализатором
-ксилола проводят при температуре около 600 °С над катализатором  осажденном на окиси алюминия:
осажденном на окиси алюминия:

Фталевый ангидрид — блестящие кристаллы с темп. пл. 131 °С. Очень реакдионноспособное соединение.
При действии аммиака на фталевый ангидрид образуется фталимид:

Фталимид — важное исходное вещество для синтеза красителей и различных других органических соединений.
Большое значение имеют продукты взаимодействия фталевого ангидрида с фенолами — фталеины. Широко известен, например, индикатор фенолфталеин:

Фенолфталеин — бесцветное соединение, способное изменять свою окраску в щелочной среде. В связи с этим фенолфталеин применяется в качестве индикатора на щелочи. В щелочной среде образуется соль (с разрывом кольца), причем одно из бензольных ядер приобретает хиноидное строение, что вызывает появление красного окрашивания:

Фенолфталеин под названием пурген применяют в медицине в качестве слабительного средства. 
Терефталевая ( -фенилендикарбонова) кислота. Аморфный порошок. При конденсации с этиленгликолем образует высокомолекулярный эфир, называемый полиэтилентерефталатом. Полиэтилентерефталат служит для получения синтетического волокна лавсан (стр. 350).
-фенилендикарбонова) кислота. Аморфный порошок. При конденсации с этиленгликолем образует высокомолекулярный эфир, называемый полиэтилентерефталатом. Полиэтилентерефталат служит для получения синтетического волокна лавсан (стр. 350).
Существуют два промышленных способа получения терефталевой кислоты:
1. Окисление  -ксилола.
-ксилола.
2. Диспропорциониров&ние бензоата калия.
Окисление  -ксилола проводится кислородом воздуха в жидкой фазе в присутствии катализатора (марганец или кобальт) и связанного брома:
-ксилола проводится кислородом воздуха в жидкой фазе в присутствии катализатора (марганец или кобальт) и связанного брома:

Воздух пропускают через раствор  -ксилола в уксусной кислоте, в которой терефталевая кислота нерастворима, а примеси, образующиеся при реакции, хорошо растворимь. Окисление проводят при температуре около
-ксилола в уксусной кислоте, в которой терефталевая кислота нерастворима, а примеси, образующиеся при реакции, хорошо растворимь. Окисление проводят при температуре около  и давлении около
и давлении около  в окислительной колонне из хасталлоя (сплав
в окислительной колонне из хасталлоя (сплав 
Диспропорционирование бензоата калия проводится в среде двуокиси углерода при  в присутствии кадмиевых катализаторов:
в присутствии кадмиевых катализаторов:

При подкислении серной кислотой образуется терефталевая кислота:

Для получения полиэтилентерефталата требуется терефталевая кислота высшей степени очистки.
Диметиловый эфир терефтале вой кислоты  кристаллическое вещество с темп,
кристаллическое вещество с темп,  Применяется в значительных количествах для получения волокна лавсан.
Применяется в значительных количествах для получения волокна лавсан.
Получение диметилового эфира терефталевой кислоты может быть осуществлено несколькими способами. Промышленным методом является окисление  -ксилола по схеме:
-ксилола по схеме:

Окисление  -ксилола до
-ксилола до  -толуиловой кислоты проводят кислородом воздуха при 140 °С и давлении 5—6 кгс/см. Катализаторы процесса — соли кобальта или марганца. Далее полученную
-толуиловой кислоты проводят кислородом воздуха при 140 °С и давлении 5—6 кгс/см. Катализаторы процесса — соли кобальта или марганца. Далее полученную  -толуиловую кислоту этерифицируют метиловым спиртом и образовавшийся метиловый эфир
-толуиловую кислоту этерифицируют метиловым спиртом и образовавшийся метиловый эфир  -толуиловой кислоты окисляют (в условиях, аналогичных окислению
-толуиловой кислоты окисляют (в условиях, аналогичных окислению  -ксилола) в неполный эфир терефталевой кислоты, который на последней стадии этерифицируют и получают полный эфир. Выход диметилового эфира терефталевой кислоты (считая на исходный ксилол) составляет около 85%.
-ксилола) в неполный эфир терефталевой кислоты, который на последней стадии этерифицируют и получают полный эфир. Выход диметилового эфира терефталевой кислоты (считая на исходный ксилол) составляет около 85%.
| << Предыдущий параграф | Следующий параграф >> |
- ВВЕДЕНИЕ
- АЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ (АЛИФАТИЧЕСКИЕ, ИЛИ ЖИРНЫЕ, СОЕДИНЕНИЯ
- 1. ПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
- 2. НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
- Углеводороды ряда этилена (олефины, алкены)
- Углеводороды ряда ацетилена (алкины)
- Углеводороды с двумя этиленовыми связями. (диолефины, диены)
- 3. НЕФТЬ. ПРИРОДНЫЕ ГАЗЫ И ГАЗЫ НЕФТЕПЕРАРАБОТКИ
- Природные газы и газы нефтепереработки как сырье для получения химических веществ
- 4. ГАЛОИДПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
- Галоидпроизводные этиленовых углеводородов
- 5. СПИРТЫ И ИХ ПРОИЗВОДНЫЕ
- Непредельные спирты
- Многоатомные спирты
- Простые эфиры
- Эпоксиды
- 6. ТИОСПИРТЫ И ТИОЭФИРЫ
- 7. АЛЬДЕГИДЫ И КЕТОНЫ
- 8. КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
- Непредельные кислоты
- Галоидангидриды кислот
- Ангидриды кислот
- Сложные эфиры минеральных кислот
- Сложные эфиры карбоновых кислот
- Жиры
- Мыла
- Синтетические моющие средства
- Амиды кислот
- Нитрилы кислот
- Предельные двухосновные кислоты
- 9. СОЕДИНЕНИЯ ЦИАНА И ПРОИЗВОДНЫЕ УГОЛЬНОЙ КИСЛОТЫ
- Производные угольной кислоты
- 10. НИТРОСОЕДИНЕНИЯ
- 11. АМИНЫ
- Диамины
- 12. ЭЛЕМЕНТООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- Кремнийорганические соединения
- Фосфорорганические соединения
- Мышьякорганические соединения
- 13. ОКСИКИСЛОТЫ
- Двухосновные оксикислоты
- 14. АЛЬДЕГИДОКИСЛОТЫ И КЕТОНОКИСЛОТЫ
- 15. УГЛЕВОДЫ (САХАРА)
- Простые углеводы (моносахариды, монозы)
- Сложные углеводы (полисахариды)
- 16. АМИНОКИСЛОТЫ
- ЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 17. АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- Терпены
- 18. АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
- Ароматические углеводороды ряда бензола
- Ароматические углеводороды с непредельными боковыми цепями
- 19. ГАЛОИДПРОИЗВОДНЫЕ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ
- Галоидпроизводные ароматических углеводородов, содержащие галоид в боковой цепи
- 20. НИТРОСОЕДИНЕНИЯ АРОМАТИЧЕСКОГО РЯДА
- 21. СУЛЬФОКИСЛОТЫ АРОМАТИЧЕСКОГО РЯДА
- 22. ФЕНОЛЫ И АРОМАТИЧЕСКИЕ СПИРТЫ
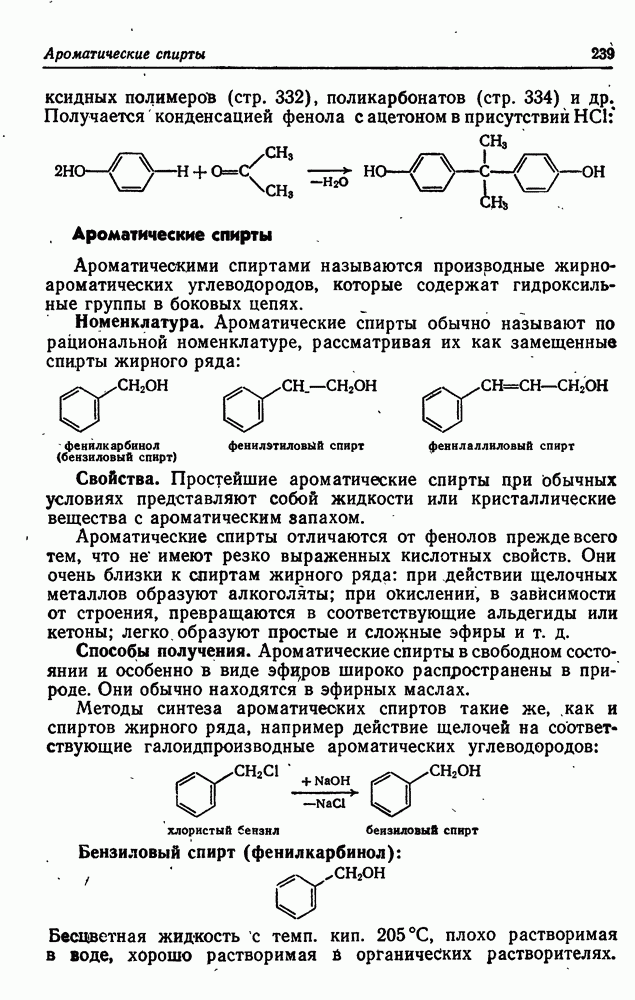
- Ароматические спирты
- 23. ХИНОНЫ И ХИНОНИМИНЫ
- 24. АРОМАТИЧЕСКИЕ АЛЬДЕГИДЫ И КЕТОНЫ
- Ароматические кетоны
- 25. АРОМАТИЧЕСКИЕ КИСЛОТЫ
- Двухосновные кислоты ряда бензола
- 26. АРОМАТИЧЕСКИЕ АМИНЫ
- Ароматические амины с аминогруппой в боковой цепи
- Ароматические диамины
- Хинониминовые красители
- 27. АРОМАТИЧЕСКИЕ ДИАЗОСОЕДИНЕНИЯ И АЗОКРАСИТЕЛИ
- Азокрасители
- Активные красители
- О зависимости между строением и окраской органических соединений
- 28. МНОГОЯДЕРНЫЕ АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
- Трифенилметановые красители
- Ароматические соединения с конденсированными ядрами
- 29. ХИМИЧЕСКИЕ СРЕДСТВА ЗАЩИТЫ РАСТЕНИЯ И ЖИВОТНЫХ (ПЕСТИЦИДЫ)
- Средства борьбы с болезнями растений (фунгициды и протравители)
- Средства борьбы с сорной растительностью (гербициды)
- Регуляторы роста растений
- Химические средства защиты животных
- 30. ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- Пятичленные гетероциклические соединения
- Шестичленные гетероциклические соединения
- Алкалоиды
- ВЫСОКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ
- 31. ОСНОВНЫЕ СВЕДЕНИЯ О ХИМИИ И ТЕХНОЛОГИЯ ПОЛИМЕРОВ
- Понятие о синтезе полимеров
- Понятие о технологии полимеров
- 32. ПЛАСТИЧЕСКИЕ МАССЫ
- 33. СИНТЕТИЧЕСКИЕ ИОНИТЫ
- 34. ЭЛЕМЕНТООРГАНИЧЕСКИЕ ПОЛИМЕРЫ
- 35. ХИМИЧЕСКИЕ ВОЛОКНА (ИСКУССТВЕННЫЕ И СИНТЕТИЧЕСКИЕ)
- Понятие о технологии изготовления химических волокон
- Искусственные волокна
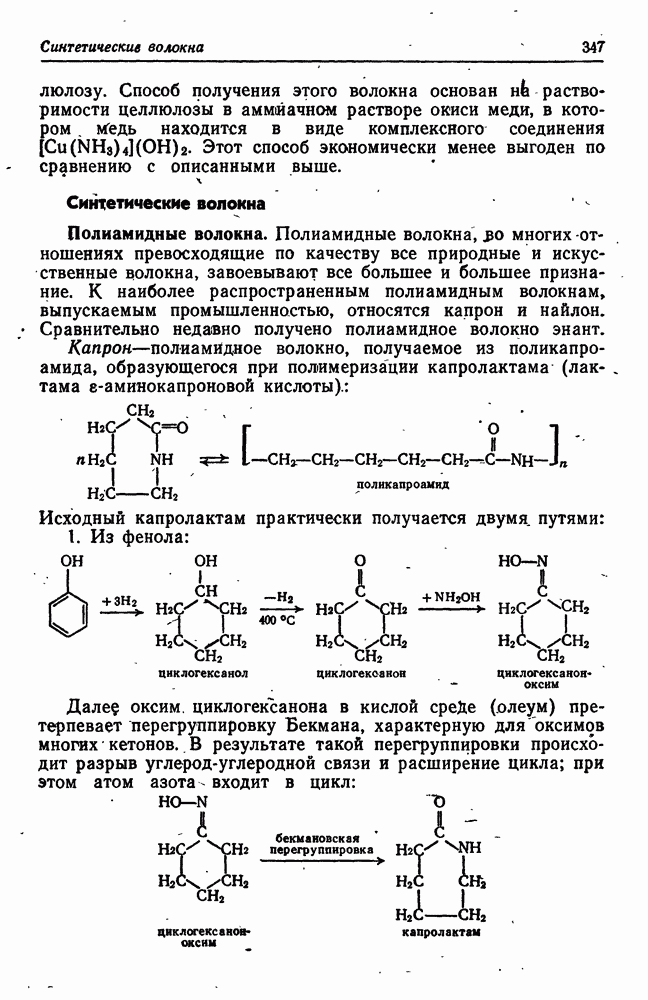
- Синтетические волокна
- 36. КАУЧУКИ
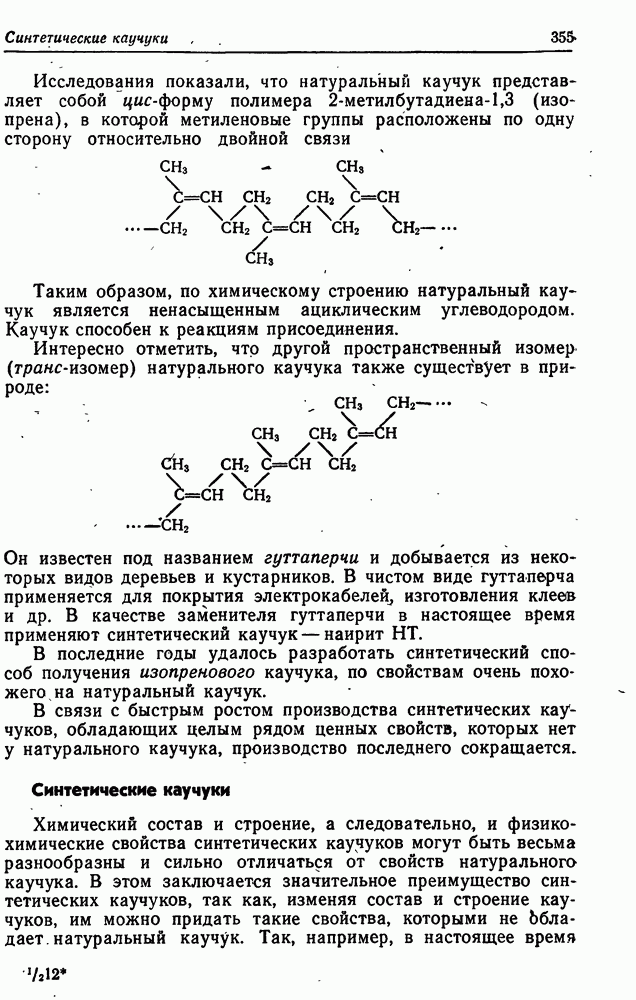
- Натуральный каучук
- Синтетические каучуки
- Синтетические латексы
- 37. СИНТЕТИЧЕСКИЕ КЛЕИ
- ХИМИЧЕСКИЕ ОСНОВЫ ЖИЗНЕДЕЯТЕЛЬНОСТИ
- 38. БЕЛКИ
- 39. НУКЛЕИНОВЫЕ КИСЛОТЫ
- 40. ЖИРЫ И УГЛЕВОДЫ
- 41. РОЛЬ БЕЛКОВ В ПРОЦЕССАХ ЖИЗНЕДЕЯТЕЛЬНОСТИ
- 42. СИНТЕЗ БЕЛКА В ОРГАНИЗМЕ
- ФИЗИОЛОГИЧЕСКИ АКТИВНЫЕ ВЕЩЕСТВА
- 43. ВИТАМИНЫ
- Витамин А
- Витамин С (аскорбиновая кислота)
- Витамины группы D
- 44. ГОРМОНЫ
- 45. АНТИБИОТИКИ