| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
20. НИТРОСОЕДИНЕНИЯ АРОМАТИЧЕСКОГО РЯДА
Номенклатура. Названия нитросоединеиий ароматического ряда обычно производят от названий соответствующих арома: тических углеводородов с приставкой нитро, динитро или тринитро в зависимости от числа нитрогрупп.
Положение нитрогрупп  ядре обозначают либо буквами
ядре обозначают либо буквами  либо цифрами:
либо цифрами:

Свойства. Мононитросоединения обычно представляют собой жидкие  твердые вещества с характерным запахом горького миндаля. Перегоняются без разложения. Ядовиты. Ароматические нитросоединения нерастворимы в воде, щелочах и кислотах.
твердые вещества с характерным запахом горького миндаля. Перегоняются без разложения. Ядовиты. Ароматические нитросоединения нерастворимы в воде, щелочах и кислотах.
Полинитросоединения, как правило, — кристаллические вещества желтого цвета. При перегонке разлагаются (некоторые со взрывом).
Важнейшим свойством нитросоединений является их способность к восстановлению с образованием ароматических аминов. Эту реакцию, играющую громадную роль в органической химии, открыл выдающийся русский ученый Н. Н. Зинин. Ароматические амины применяются для производства очень болыйой группы органических красителей, лекарственных соединений, пластических масс и др.
Восстановление нитросоединений в ароматические амины можно проводить несколькими способами.
В кислой среде восстановление идет через образование нескольких промежуточных веществ. В качестве восстановителя применяют водород, который образуется при взаимодействии металлов (цинк, олово, железо и др.) с соляной кислотой. Конечным продуктом восстановления является анилин:

В нейтральной или слабокислой среде водород для восстановления нитросоединений получается обычно при взаимодействии цинка с родным раствором хлористого аммония. В результате восстановления нитробензола в нейтральной или слабокислой среде образуется фенилгидроксиламин (который может быть восстановлен далее до анилина).
В щелочной среде водород для восстановления получается при реакции металла (обычно цинка) со щелочью.
В щелочной среде вначале восстановление идет обычным путем:

Затем образующийся в реакционной смеси нитрозобензол и фенилгидроксиламин в результате каталитического влияния щелочи реагируют друг с другом и образуют азоксибензол, который далее постепенно восстанавливается до гидразобензола:

При дальнейшем восстановлении гидр азобензол превращается в анилин:

Н. Н. Зинин открыл, что гидразобензол под действием сильных минеральных кислот перегруппировывается в так называемый бензидин. Эта реакция получила название бёнзидиновой перегруппировки:

В промышленности огромные количества анилина получают восстановлением нитробензола железом в нейтральной среде. Полинитросоединения восстанавливаются в полиаминосоединения аналогичным путем.
В случае необходимости частичного восстановления (одной нитрогрупны в динитропроизводном) в качестве восстановителя применяют, например, сернистый аммоний:

Нитрогруппы (особенно в симметричных тринитросоединениях) сильно повышают способность атома углерода, находящегося в орто-положении к нитрогруппам, к окислению. Так, тринитробензол даже при действии слабых окислителей превращается в тринитрофенол:

Нитрогруппа сильно влияет также на подвижность галоида, находящегося в орто- и пара-положении. По мере увеличения числа нитрогрупп в ароматическом ядре подвижность галоида увеличивается. Так, например, атом хлора в тринитрохлорбензоле уже при нагревании с водой легко замещается на гидроксил:

Способы получения. Нитросоединения получают действием смеси концентрированных азотной и серной кислот (нитрующей смеси) на ароматические углеводороды. При действии нитрующей смеси на бензол получается простейший представитель этого ряда соединений — нитробензол:

Механизм реакции следующий: сначала азотная и серная кислоты взаимодействуют с образованием нитросерной кислоты:

Затем нитросерная кислота диссоциирует на катион и анион:

Катион  (так называемый нитроний) замещает один из атомов водорода ароматического кольца, который отщепляется в виде протона
(так называемый нитроний) замещает один из атомов водорода ароматического кольца, который отщепляется в виде протона 

Вступление каждой последующей нитрогруппы в ароматическое кольцо происходит все более и более трудно. Согласно правилу замещения, следующая нитрогруппа вступает в мета-положение относительно уже имеющейся нитрогруппы. Нитрование гомологов бензола протекает легче, чем самого бензола.
Нитросоединения с нитрогруппой в боковой цепи, например фенилнитрометан  получаются способами, описанными для нитросоединений жирного ряда (стр. 158). По свойствам они также аналогичны алифатическим нитросоединениям.
получаются способами, описанными для нитросоединений жирного ряда (стр. 158). По свойствам они также аналогичны алифатическим нитросоединениям.
Нитробензол  Бесцветная жидкость с темп.
Бесцветная жидкость с темп.  с резким запахом, напоминающим запах горького миндаля. Ядовит. В воде нерастворим. Перегоняется с водяным паром. Нитробензол производится в громадных количествах для получения анилина — исходного вещества для производства различных органических соединений. В промышленности нитробензол получают действием нитрующей смеси (68%
с резким запахом, напоминающим запах горького миндаля. Ядовит. В воде нерастворим. Перегоняется с водяным паром. Нитробензол производится в громадных количествах для получения анилина — исходного вещества для производства различных органических соединений. В промышленности нитробензол получают действием нитрующей смеси (68%  и 32%
и 32%  ) на бензол при 60 °С. Нитрование осуществляется в виде периодического или непрерывного процесса. Наиболее прогрессивным является непрерывный процесс нитрования в нитраторах колонного типа.
) на бензол при 60 °С. Нитрование осуществляется в виде периодического или непрерывного процесса. Наиболее прогрессивным является непрерывный процесс нитрования в нитраторах колонного типа.
2,4,6-Тринитротолуол (тротил):

Желтое кристаллическое вещество с темп. пл. 81 °С; горит коптящим пламенем без взрыва. Взрывает только от детонации.  Получается тринитротолуол путем постепенного нитрования толуола. Широко применяется в качестве взрывчатого вещества.
Получается тринитротолуол путем постепенного нитрования толуола. Широко применяется в качестве взрывчатого вещества.
| << Предыдущий параграф | Следующий параграф >> |
- ВВЕДЕНИЕ
- АЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ (АЛИФАТИЧЕСКИЕ, ИЛИ ЖИРНЫЕ, СОЕДИНЕНИЯ
- 1. ПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
- 2. НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
- Углеводороды ряда этилена (олефины, алкены)
- Углеводороды ряда ацетилена (алкины)
- Углеводороды с двумя этиленовыми связями. (диолефины, диены)
- 3. НЕФТЬ. ПРИРОДНЫЕ ГАЗЫ И ГАЗЫ НЕФТЕПЕРАРАБОТКИ
- Природные газы и газы нефтепереработки как сырье для получения химических веществ
- 4. ГАЛОИДПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
- Галоидпроизводные этиленовых углеводородов
- 5. СПИРТЫ И ИХ ПРОИЗВОДНЫЕ
- Непредельные спирты
- Многоатомные спирты
- Простые эфиры
- Эпоксиды
- 6. ТИОСПИРТЫ И ТИОЭФИРЫ
- 7. АЛЬДЕГИДЫ И КЕТОНЫ
- 8. КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
- Непредельные кислоты
- Галоидангидриды кислот
- Ангидриды кислот
- Сложные эфиры минеральных кислот
- Сложные эфиры карбоновых кислот
- Жиры
- Мыла
- Синтетические моющие средства
- Амиды кислот
- Нитрилы кислот
- Предельные двухосновные кислоты
- 9. СОЕДИНЕНИЯ ЦИАНА И ПРОИЗВОДНЫЕ УГОЛЬНОЙ КИСЛОТЫ
- Производные угольной кислоты
- 10. НИТРОСОЕДИНЕНИЯ
- 11. АМИНЫ
- Диамины
- 12. ЭЛЕМЕНТООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- Кремнийорганические соединения
- Фосфорорганические соединения
- Мышьякорганические соединения
- 13. ОКСИКИСЛОТЫ
- Двухосновные оксикислоты
- 14. АЛЬДЕГИДОКИСЛОТЫ И КЕТОНОКИСЛОТЫ
- 15. УГЛЕВОДЫ (САХАРА)
- Простые углеводы (моносахариды, монозы)
- Сложные углеводы (полисахариды)
- 16. АМИНОКИСЛОТЫ
- ЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 17. АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- Терпены
- 18. АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
- Ароматические углеводороды ряда бензола
- Ароматические углеводороды с непредельными боковыми цепями
- 19. ГАЛОИДПРОИЗВОДНЫЕ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ
- Галоидпроизводные ароматических углеводородов, содержащие галоид в боковой цепи
- 20. НИТРОСОЕДИНЕНИЯ АРОМАТИЧЕСКОГО РЯДА
- 21. СУЛЬФОКИСЛОТЫ АРОМАТИЧЕСКОГО РЯДА
- 22. ФЕНОЛЫ И АРОМАТИЧЕСКИЕ СПИРТЫ
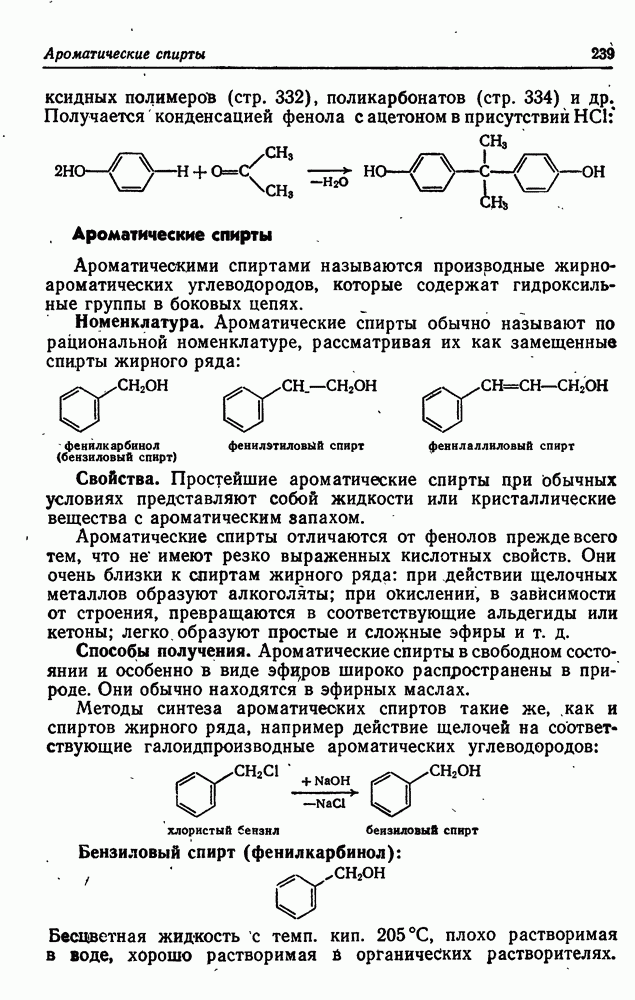
- Ароматические спирты
- 23. ХИНОНЫ И ХИНОНИМИНЫ
- 24. АРОМАТИЧЕСКИЕ АЛЬДЕГИДЫ И КЕТОНЫ
- Ароматические кетоны
- 25. АРОМАТИЧЕСКИЕ КИСЛОТЫ
- Двухосновные кислоты ряда бензола
- 26. АРОМАТИЧЕСКИЕ АМИНЫ
- Ароматические амины с аминогруппой в боковой цепи
- Ароматические диамины
- Хинониминовые красители
- 27. АРОМАТИЧЕСКИЕ ДИАЗОСОЕДИНЕНИЯ И АЗОКРАСИТЕЛИ
- Азокрасители
- Активные красители
- О зависимости между строением и окраской органических соединений
- 28. МНОГОЯДЕРНЫЕ АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
- Трифенилметановые красители
- Ароматические соединения с конденсированными ядрами
- 29. ХИМИЧЕСКИЕ СРЕДСТВА ЗАЩИТЫ РАСТЕНИЯ И ЖИВОТНЫХ (ПЕСТИЦИДЫ)
- Средства борьбы с болезнями растений (фунгициды и протравители)
- Средства борьбы с сорной растительностью (гербициды)
- Регуляторы роста растений
- Химические средства защиты животных
- 30. ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- Пятичленные гетероциклические соединения
- Шестичленные гетероциклические соединения
- Алкалоиды
- ВЫСОКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ
- 31. ОСНОВНЫЕ СВЕДЕНИЯ О ХИМИИ И ТЕХНОЛОГИЯ ПОЛИМЕРОВ
- Понятие о синтезе полимеров
- Понятие о технологии полимеров
- 32. ПЛАСТИЧЕСКИЕ МАССЫ
- 33. СИНТЕТИЧЕСКИЕ ИОНИТЫ
- 34. ЭЛЕМЕНТООРГАНИЧЕСКИЕ ПОЛИМЕРЫ
- 35. ХИМИЧЕСКИЕ ВОЛОКНА (ИСКУССТВЕННЫЕ И СИНТЕТИЧЕСКИЕ)
- Понятие о технологии изготовления химических волокон
- Искусственные волокна
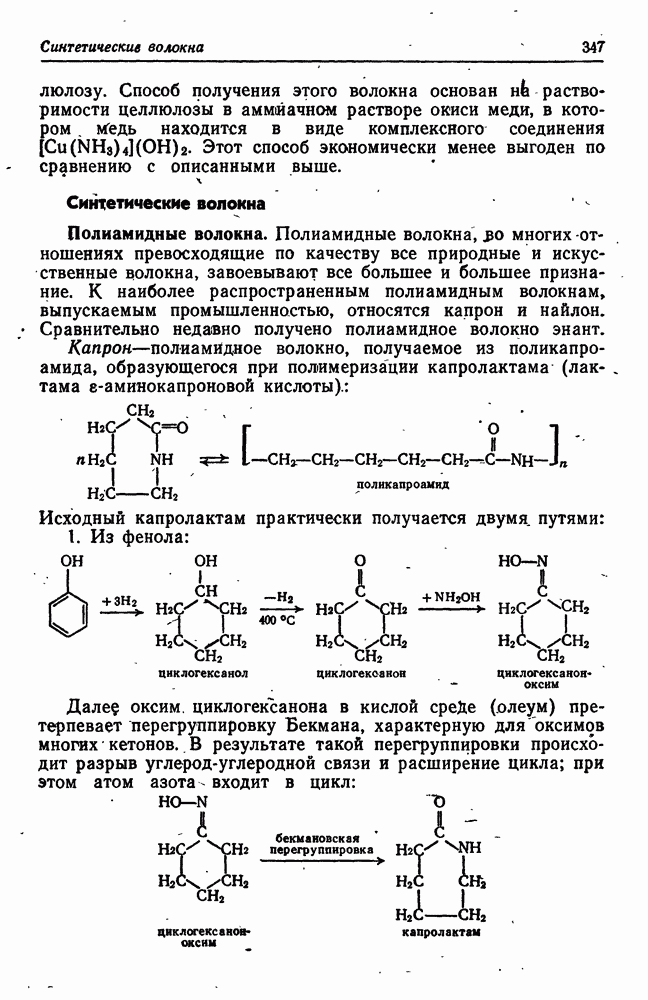
- Синтетические волокна
- 36. КАУЧУКИ
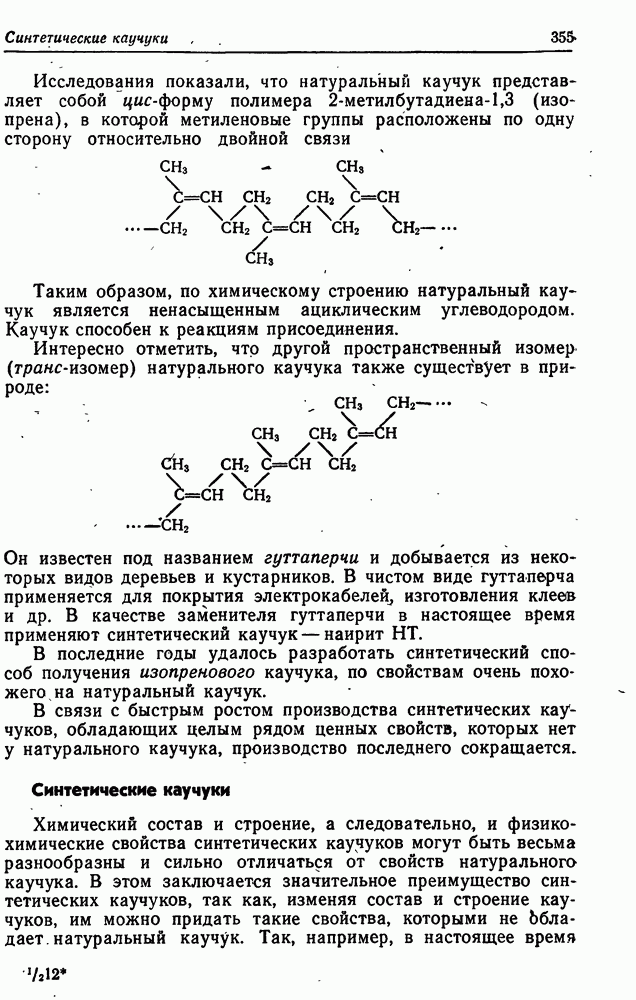
- Натуральный каучук
- Синтетические каучуки
- Синтетические латексы
- 37. СИНТЕТИЧЕСКИЕ КЛЕИ
- ХИМИЧЕСКИЕ ОСНОВЫ ЖИЗНЕДЕЯТЕЛЬНОСТИ
- 38. БЕЛКИ
- 39. НУКЛЕИНОВЫЕ КИСЛОТЫ
- 40. ЖИРЫ И УГЛЕВОДЫ
- 41. РОЛЬ БЕЛКОВ В ПРОЦЕССАХ ЖИЗНЕДЕЯТЕЛЬНОСТИ
- 42. СИНТЕЗ БЕЛКА В ОРГАНИЗМЕ
- ФИЗИОЛОГИЧЕСКИ АКТИВНЫЕ ВЕЩЕСТВА
- 43. ВИТАМИНЫ
- Витамин А
- Витамин С (аскорбиновая кислота)
- Витамины группы D
- 44. ГОРМОНЫ
- 45. АНТИБИОТИКИ