| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
Предельные двухосновные кислоты
Карбоновые кислоты, имеющие в своеймолекуле две карбоксильные группы  , называются двухосновными или дикарбоновыми кислотами. Дикарбоновые кислоты, как и монокарбоновые, могут быть предельного или непредельного ряда»
, называются двухосновными или дикарбоновыми кислотами. Дикарбоновые кислоты, как и монокарбоновые, могут быть предельного или непредельного ряда»
Номенклатура. Дикарбоновые кислоты, как и монокарбоновые, чаще всего называются исторически сложившимися названиями {возникшими в связи с первоначальным способом их получения). По рациональной номенклатуре их названия производят от названий углеводородов, остатки которых входят состав кислот, с прибавлением слов дикарбоновая кислота.
Ниже приведены формулы  названия первых пяти дикарбоновых кислот. Сначала даны исторические (тривиальные) названия кислот, а затем рациональные. Для успешного усвоения номенклатуры органических соединений особенно полезно запомнить названия этих кислот, так как они часто встречаются в литературе:
названия первых пяти дикарбоновых кислот. Сначала даны исторические (тривиальные) названия кислот, а затем рациональные. Для успешного усвоения номенклатуры органических соединений особенно полезно запомнить названия этих кислот, так как они часто встречаются в литературе:

Свойства. Дикарбоновые кислоты предельного ряда представляют собой кристаллические вещества, растворимые в воде. Все дикарбоновые кислоты являются более сильными кислотами, чем монокарбоновые.
Для двухосновных кислот характерны все реакции, свойственные одноосновным кислотам. Двухосновные кислоты могут образовывать два ряда производных в зависимости от тогр, участвуют ли в реакции одна или две карбоксильные группы:

Некоторые простейшие двухосновные кислоты обладают специфическими химическими свойствами, например превращаются при нагревании (с отщеплением  или воды) в одноосновные кислоты или ангидриды циклического строения.
или воды) в одноосновные кислоты или ангидриды циклического строения.
Способы получения. Дикарбоновые кислоты получаются теми же способами, что и монокарбоновые, с той лишь разницей, что для их синтеза в качестве исходных продуктов применяются вещества, содержащие вместо одной две функциональные группы, которые в результате реакции превращаются в карбоксильные:
группы. Если, например, одноосновные кислоты могут быть получены окислением одноатомных спиртов, то двухосновные — окислением двухатомных спиртов (гликолей):

Одним из наиболее важных способов получения двухосновных кислот является синтез их с помощью производных малоновой кислоты (стр. 151-152).
Щавелевая кислота  Бесцветные кристаллы
Бесцветные кристаллы  темп. пл. 189 °С (с разл.). В виде солей (оксалатов) щавелевая кислота широко распространена в природе. Она находится во многих растениях (особенно в щавеле).
темп. пл. 189 °С (с разл.). В виде солей (оксалатов) щавелевая кислота широко распространена в природе. Она находится во многих растениях (особенно в щавеле).
Щавелевая кислота легко окисляется

и поэтому используется иногда как восстановитель.
При нагревании щавелевая кислота разлагается:

В промышленности щавелевая кислота получается из солей муравьиной кислоты при нагревании до 

Малоновая кислота  Кристаллическое вещество; темп.
Кристаллическое вещество; темп. 
Очень большое значение в органической химии имеет диэтиловый эфир малоновой кислоты, который обычно сокращенно называют малоновым эфиром:

Малоновын эфир — жидкость с темп. кип.  обладает высокой реакционной способностью и широко используется при разнообразных органических синтезах.
обладает высокой реакционной способностью и широко используется при разнообразных органических синтезах.
Малоновый эфир обладает двумя особенностями:
1) водородные атомы метиленовой группы  находящейся между двумя карбонильными группами, очень подвижны и легко
находящейся между двумя карбонильными группами, очень подвижны и легко
замещаются на атомы натрия, образуя натрималоновый эфир

2) после омыления из малонового эфира получается малоновая кислота, которая легко превращается в одноосновную кислоту:

Этими реакциями малонового эфира широко пользуются для синтеза различных органических соединений. Например, для получения масляной кислоты проводят следующие превращения

С помощью малонового эфира можно получать различные двухосновные кислоты; например адипиновую кислоту можно
синтезировать из натриймалонового эфира и этилового эфира у-иодмасляной кислоты:

Адипиновая кислота  Белое кристаллическое вещество с темп. пл. 153 °С. Растворима в горячей воде. Содержится в продуктах окисления жиров. Является важным «сходным веществом для получения синтетических волокон (стр. 349).
Белое кристаллическое вещество с темп. пл. 153 °С. Растворима в горячей воде. Содержится в продуктах окисления жиров. Является важным «сходным веществом для получения синтетических волокон (стр. 349).
В промышленности адипиновая кислота получается окислением циклогексанола при  избытком 62%-ной азотной жислоты:
избытком 62%-ной азотной жислоты:

В качестве побочных веществ образуются глутаровая, янтарная и щавелевая кислоты.
При охлаждении реакционной смеси выпавшую кристаллическую адипиновую кислоту отфильтровывают, -а маточный раствор используют для разбавления азотной кислоты до 62%.
Адипиновая кислота служит исходным веществом для синтеза гексаметилендиамина (стр. 162), также применяемого для получения синтетических волокон.
| << Предыдущий параграф | Следующий параграф >> |
- ВВЕДЕНИЕ
- АЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ (АЛИФАТИЧЕСКИЕ, ИЛИ ЖИРНЫЕ, СОЕДИНЕНИЯ
- 1. ПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
- 2. НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
- Углеводороды ряда этилена (олефины, алкены)
- Углеводороды ряда ацетилена (алкины)
- Углеводороды с двумя этиленовыми связями. (диолефины, диены)
- 3. НЕФТЬ. ПРИРОДНЫЕ ГАЗЫ И ГАЗЫ НЕФТЕПЕРАРАБОТКИ
- Природные газы и газы нефтепереработки как сырье для получения химических веществ
- 4. ГАЛОИДПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
- Галоидпроизводные этиленовых углеводородов
- 5. СПИРТЫ И ИХ ПРОИЗВОДНЫЕ
- Непредельные спирты
- Многоатомные спирты
- Простые эфиры
- Эпоксиды
- 6. ТИОСПИРТЫ И ТИОЭФИРЫ
- 7. АЛЬДЕГИДЫ И КЕТОНЫ
- 8. КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
- Непредельные кислоты
- Галоидангидриды кислот
- Ангидриды кислот
- Сложные эфиры минеральных кислот
- Сложные эфиры карбоновых кислот
- Жиры
- Мыла
- Синтетические моющие средства
- Амиды кислот
- Нитрилы кислот
- Предельные двухосновные кислоты
- 9. СОЕДИНЕНИЯ ЦИАНА И ПРОИЗВОДНЫЕ УГОЛЬНОЙ КИСЛОТЫ
- Производные угольной кислоты
- 10. НИТРОСОЕДИНЕНИЯ
- 11. АМИНЫ
- Диамины
- 12. ЭЛЕМЕНТООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- Кремнийорганические соединения
- Фосфорорганические соединения
- Мышьякорганические соединения
- 13. ОКСИКИСЛОТЫ
- Двухосновные оксикислоты
- 14. АЛЬДЕГИДОКИСЛОТЫ И КЕТОНОКИСЛОТЫ
- 15. УГЛЕВОДЫ (САХАРА)
- Простые углеводы (моносахариды, монозы)
- Сложные углеводы (полисахариды)
- 16. АМИНОКИСЛОТЫ
- ЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 17. АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- Терпены
- 18. АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
- Ароматические углеводороды ряда бензола
- Ароматические углеводороды с непредельными боковыми цепями
- 19. ГАЛОИДПРОИЗВОДНЫЕ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ
- Галоидпроизводные ароматических углеводородов, содержащие галоид в боковой цепи
- 20. НИТРОСОЕДИНЕНИЯ АРОМАТИЧЕСКОГО РЯДА
- 21. СУЛЬФОКИСЛОТЫ АРОМАТИЧЕСКОГО РЯДА
- 22. ФЕНОЛЫ И АРОМАТИЧЕСКИЕ СПИРТЫ
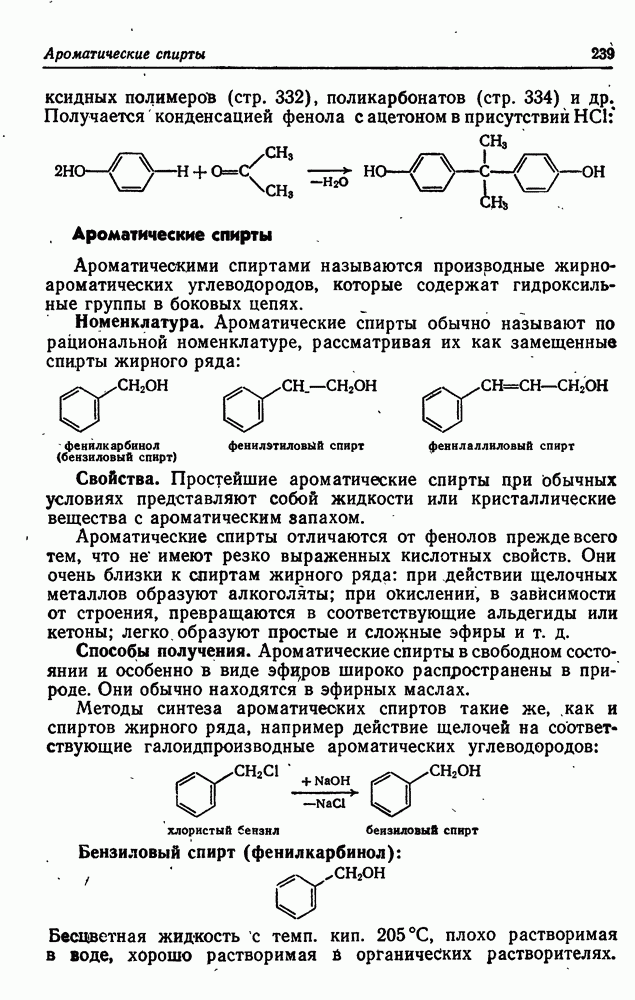
- Ароматические спирты
- 23. ХИНОНЫ И ХИНОНИМИНЫ
- 24. АРОМАТИЧЕСКИЕ АЛЬДЕГИДЫ И КЕТОНЫ
- Ароматические кетоны
- 25. АРОМАТИЧЕСКИЕ КИСЛОТЫ
- Двухосновные кислоты ряда бензола
- 26. АРОМАТИЧЕСКИЕ АМИНЫ
- Ароматические амины с аминогруппой в боковой цепи
- Ароматические диамины
- Хинониминовые красители
- 27. АРОМАТИЧЕСКИЕ ДИАЗОСОЕДИНЕНИЯ И АЗОКРАСИТЕЛИ
- Азокрасители
- Активные красители
- О зависимости между строением и окраской органических соединений
- 28. МНОГОЯДЕРНЫЕ АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
- Трифенилметановые красители
- Ароматические соединения с конденсированными ядрами
- 29. ХИМИЧЕСКИЕ СРЕДСТВА ЗАЩИТЫ РАСТЕНИЯ И ЖИВОТНЫХ (ПЕСТИЦИДЫ)
- Средства борьбы с болезнями растений (фунгициды и протравители)
- Средства борьбы с сорной растительностью (гербициды)
- Регуляторы роста растений
- Химические средства защиты животных
- 30. ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- Пятичленные гетероциклические соединения
- Шестичленные гетероциклические соединения
- Алкалоиды
- ВЫСОКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ
- 31. ОСНОВНЫЕ СВЕДЕНИЯ О ХИМИИ И ТЕХНОЛОГИЯ ПОЛИМЕРОВ
- Понятие о синтезе полимеров
- Понятие о технологии полимеров
- 32. ПЛАСТИЧЕСКИЕ МАССЫ
- 33. СИНТЕТИЧЕСКИЕ ИОНИТЫ
- 34. ЭЛЕМЕНТООРГАНИЧЕСКИЕ ПОЛИМЕРЫ
- 35. ХИМИЧЕСКИЕ ВОЛОКНА (ИСКУССТВЕННЫЕ И СИНТЕТИЧЕСКИЕ)
- Понятие о технологии изготовления химических волокон
- Искусственные волокна
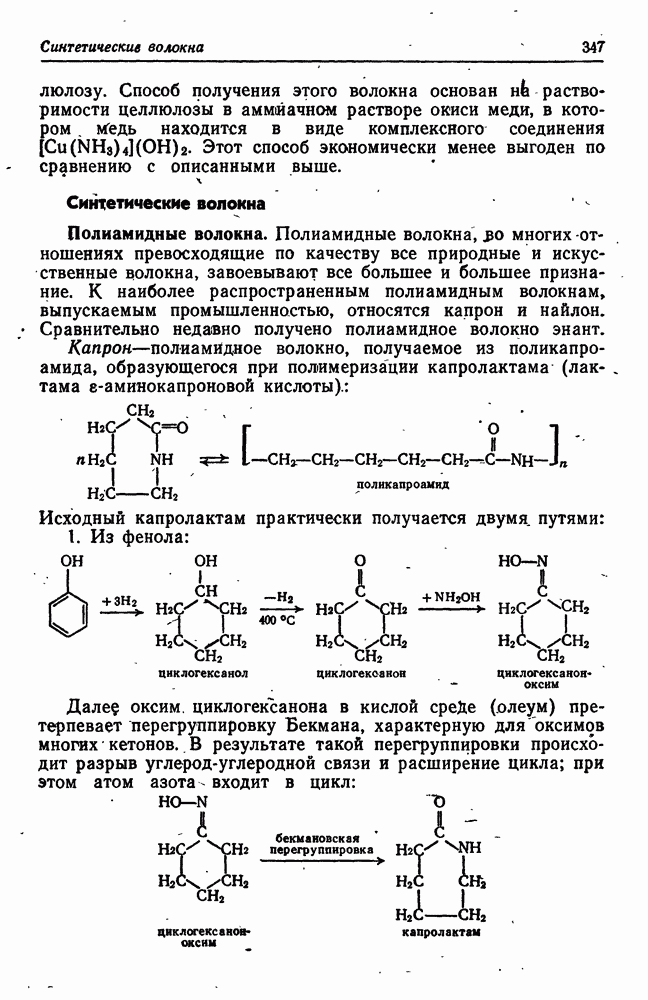
- Синтетические волокна
- 36. КАУЧУКИ
- Натуральный каучук
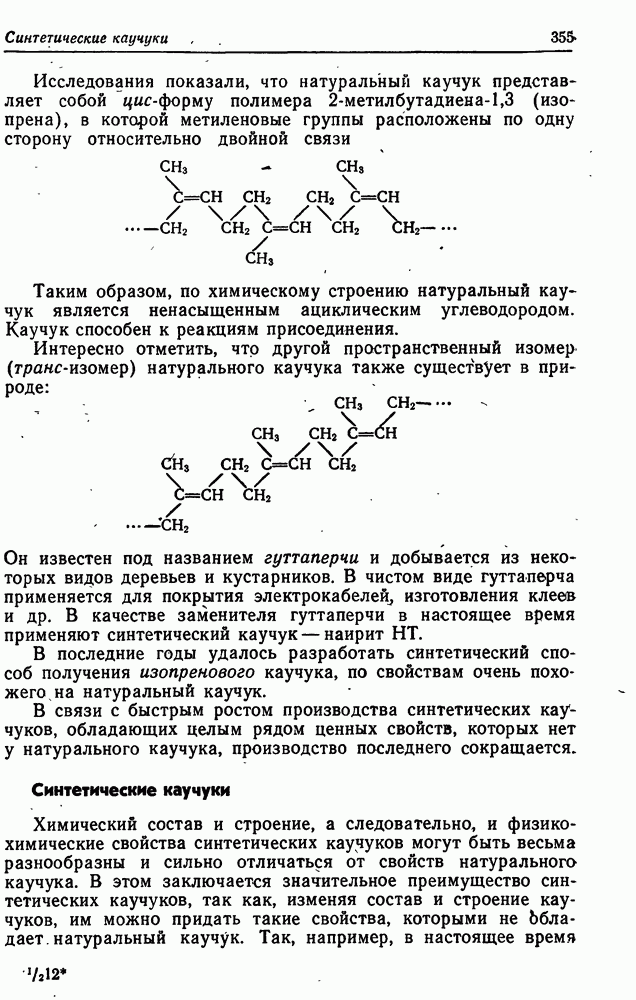
- Синтетические каучуки
- Синтетические латексы
- 37. СИНТЕТИЧЕСКИЕ КЛЕИ
- ХИМИЧЕСКИЕ ОСНОВЫ ЖИЗНЕДЕЯТЕЛЬНОСТИ
- 38. БЕЛКИ
- 39. НУКЛЕИНОВЫЕ КИСЛОТЫ
- 40. ЖИРЫ И УГЛЕВОДЫ
- 41. РОЛЬ БЕЛКОВ В ПРОЦЕССАХ ЖИЗНЕДЕЯТЕЛЬНОСТИ
- 42. СИНТЕЗ БЕЛКА В ОРГАНИЗМЕ
- ФИЗИОЛОГИЧЕСКИ АКТИВНЫЕ ВЕЩЕСТВА
- 43. ВИТАМИНЫ
- Витамин А
- Витамин С (аскорбиновая кислота)
- Витамины группы D
- 44. ГОРМОНЫ
- 45. АНТИБИОТИКИ