| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
12. ЭЛЕМЕНТООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
Органические соединения, которые содержат в составе своей молекулы атом металла (Na, К, Li, Zn, Al, Mg, Sn, Hg, Pb и др.) или неметалла (Р, Si, As, В и др.), связанный непосредственно с атомом углерода, называются элементоорганическими соединениями:

Металлоорггнические соединения
Металлоорганические соединения могут быть двух типов:
1. Полные — у которых все валентности металла затрачены на соединение с атомами углерода:

2. Смешанные — у которых часть валентностей металла затрачена на соединение с углеродными атомами, а Другая часть — с атомами других элементов (чаще всего галоидами), например 
Названия металлоорганических соединений Яроизводятся от названий углеводородных радикалов и металлов, входящих в состав их молекул:

Наиболее распространенным общим методом получения металлоорганических соединений является действие металлов на галоидные алкилы. Этот метод пригоден для получения как полных, так и смешанных металлоорганических соединений. Так, например, при действии цинка на ибдистый метил вначале образуется смешанное металлоорганическое соединение — иодистый метилцинк, который при нагревании превращается в диметилцинк:

Свойства. Полные металлоорганнческйе соединения представляют собой в большинстве случаев жидкости; смешанные — кристаллические вещества.
Металлорганические соединения отличаются очень большой реакционной способностью, которая объясняется слабой связью атома металла с углеродом. Благодаря большой реакционной способности, относительной простоте их получения и использования металлоорганнческйе соединения получили широкое применение в органическом синтезе.
Из очень большого числа металлоррганических соединений мы рассмотрим лишь соединения металлов второй группы периодической системы — цинка и магния, играющие наиболее важную роль для получения органических соединений различных классов.
Цинкорганические соединения самовоспламеняются на воздухе, вследствие чего работать с ними приходится в атмосфере азота или водорода. Значительно удобней для работы оказались смешанные магнийорганические соединения. Они были впервые изучены французским химиком Гриньяром и получили название реактивов Гриньяра. - 
Смешанные магнийорганические соединения быстро разлагаются под действием воды:

Обычно их получают, прибавляя галоидный алкил к стружкам магния, находящимся под слоем обезвоженного («абсолютного») эфира, который играет роль как растворителя, так и катализатора реакции. Через некоторое время после прибавления галоидного алкила начинается бурная реакция и образуется эфирный раствор смешанного магнийорганического соединения,

Для проведения дальнейших синтезов с помощью магнийорганических соединений последние обычно не выделяют в чистом виде, а применяют их эфирные растворы.
Синтезы с помощью магнийорганических соединений. 1. Получение предельных углеводородов из галоидных алкилов. Сначала действуют металлическим магнием на галоидный алкил, а затем разлагают образовавшееся магний-, органическое соединение водой:

2. Синтез спиртов. Первичные спирты получают при действии магнийорганических соединений на формальдегид:

торичнйе спирты получают из любых других альдегидов, например:

Третичные спирты получают из кетонов, например:

3. Синтез карбоновых кислот. Если через эфирный раствор магнийорганического соединения пропустить  получится смешанная магниевая соль карбоновой и галоидоводородной кислот:
получится смешанная магниевая соль карбоновой и галоидоводородной кислот:

При разложении этой соли водой образуется кароновая кислота:  у
у

Из металлоорганических соединений других металлов особое место занимает тетраэтилсвинец  - бесцветная, тяжелая жидкость (плотность
- бесцветная, тяжелая жидкость (плотность  с неприятным запахом, очень ядовитая. Тетраэтилсвинец нерастворим в воде, хорошо растворим в органических растворителях. Горюч. Прибавляется в количестве 0,1-0,3% к бензину в качестве антидетонатора. Получается взаимодействием хлористого этила со сплавом натрия и свинца:
с неприятным запахом, очень ядовитая. Тетраэтилсвинец нерастворим в воде, хорошо растворим в органических растворителях. Горюч. Прибавляется в количестве 0,1-0,3% к бензину в качестве антидетонатора. Получается взаимодействием хлористого этила со сплавом натрия и свинца:

Из элементоорганических соединений, содержащих неметаллические атомы, рассмотрим производные кремния, фосфора и мышьяка.
| << Предыдущий параграф | Следующий параграф >> |
- ВВЕДЕНИЕ
- АЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ (АЛИФАТИЧЕСКИЕ, ИЛИ ЖИРНЫЕ, СОЕДИНЕНИЯ
- 1. ПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
- 2. НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ
- Углеводороды ряда этилена (олефины, алкены)
- Углеводороды ряда ацетилена (алкины)
- Углеводороды с двумя этиленовыми связями. (диолефины, диены)
- 3. НЕФТЬ. ПРИРОДНЫЕ ГАЗЫ И ГАЗЫ НЕФТЕПЕРАРАБОТКИ
- Природные газы и газы нефтепереработки как сырье для получения химических веществ
- 4. ГАЛОИДПРОИЗВОДНЫЕ УГЛЕВОДОРОДОВ
- Галоидпроизводные этиленовых углеводородов
- 5. СПИРТЫ И ИХ ПРОИЗВОДНЫЕ
- Непредельные спирты
- Многоатомные спирты
- Простые эфиры
- Эпоксиды
- 6. ТИОСПИРТЫ И ТИОЭФИРЫ
- 7. АЛЬДЕГИДЫ И КЕТОНЫ
- 8. КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
- Непредельные кислоты
- Галоидангидриды кислот
- Ангидриды кислот
- Сложные эфиры минеральных кислот
- Сложные эфиры карбоновых кислот
- Жиры
- Мыла
- Синтетические моющие средства
- Амиды кислот
- Нитрилы кислот
- Предельные двухосновные кислоты
- 9. СОЕДИНЕНИЯ ЦИАНА И ПРОИЗВОДНЫЕ УГОЛЬНОЙ КИСЛОТЫ
- Производные угольной кислоты
- 10. НИТРОСОЕДИНЕНИЯ
- 11. АМИНЫ
- Диамины
- 12. ЭЛЕМЕНТООРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
- Кремнийорганические соединения
- Фосфорорганические соединения
- Мышьякорганические соединения
- 13. ОКСИКИСЛОТЫ
- Двухосновные оксикислоты
- 14. АЛЬДЕГИДОКИСЛОТЫ И КЕТОНОКИСЛОТЫ
- 15. УГЛЕВОДЫ (САХАРА)
- Простые углеводы (моносахариды, монозы)
- Сложные углеводы (полисахариды)
- 16. АМИНОКИСЛОТЫ
- ЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- 17. АЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- Терпены
- 18. АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ
- Ароматические углеводороды ряда бензола
- Ароматические углеводороды с непредельными боковыми цепями
- 19. ГАЛОИДПРОИЗВОДНЫЕ АРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ
- Галоидпроизводные ароматических углеводородов, содержащие галоид в боковой цепи
- 20. НИТРОСОЕДИНЕНИЯ АРОМАТИЧЕСКОГО РЯДА
- 21. СУЛЬФОКИСЛОТЫ АРОМАТИЧЕСКОГО РЯДА
- 22. ФЕНОЛЫ И АРОМАТИЧЕСКИЕ СПИРТЫ
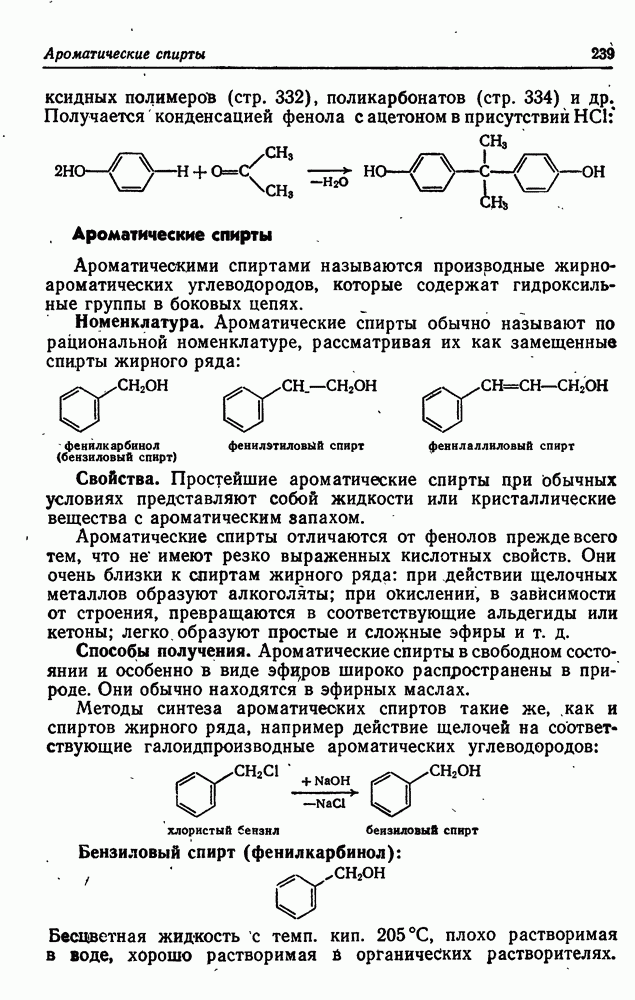
- Ароматические спирты
- 23. ХИНОНЫ И ХИНОНИМИНЫ
- 24. АРОМАТИЧЕСКИЕ АЛЬДЕГИДЫ И КЕТОНЫ
- Ароматические кетоны
- 25. АРОМАТИЧЕСКИЕ КИСЛОТЫ
- Двухосновные кислоты ряда бензола
- 26. АРОМАТИЧЕСКИЕ АМИНЫ
- Ароматические амины с аминогруппой в боковой цепи
- Ароматические диамины
- Хинониминовые красители
- 27. АРОМАТИЧЕСКИЕ ДИАЗОСОЕДИНЕНИЯ И АЗОКРАСИТЕЛИ
- Азокрасители
- Активные красители
- О зависимости между строением и окраской органических соединений
- 28. МНОГОЯДЕРНЫЕ АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
- Трифенилметановые красители
- Ароматические соединения с конденсированными ядрами
- 29. ХИМИЧЕСКИЕ СРЕДСТВА ЗАЩИТЫ РАСТЕНИЯ И ЖИВОТНЫХ (ПЕСТИЦИДЫ)
- Средства борьбы с болезнями растений (фунгициды и протравители)
- Средства борьбы с сорной растительностью (гербициды)
- Регуляторы роста растений
- Химические средства защиты животных
- 30. ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ
- Пятичленные гетероциклические соединения
- Шестичленные гетероциклические соединения
- Алкалоиды
- ВЫСОКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ
- 31. ОСНОВНЫЕ СВЕДЕНИЯ О ХИМИИ И ТЕХНОЛОГИЯ ПОЛИМЕРОВ
- Понятие о синтезе полимеров
- Понятие о технологии полимеров
- 32. ПЛАСТИЧЕСКИЕ МАССЫ
- 33. СИНТЕТИЧЕСКИЕ ИОНИТЫ
- 34. ЭЛЕМЕНТООРГАНИЧЕСКИЕ ПОЛИМЕРЫ
- 35. ХИМИЧЕСКИЕ ВОЛОКНА (ИСКУССТВЕННЫЕ И СИНТЕТИЧЕСКИЕ)
- Понятие о технологии изготовления химических волокон
- Искусственные волокна
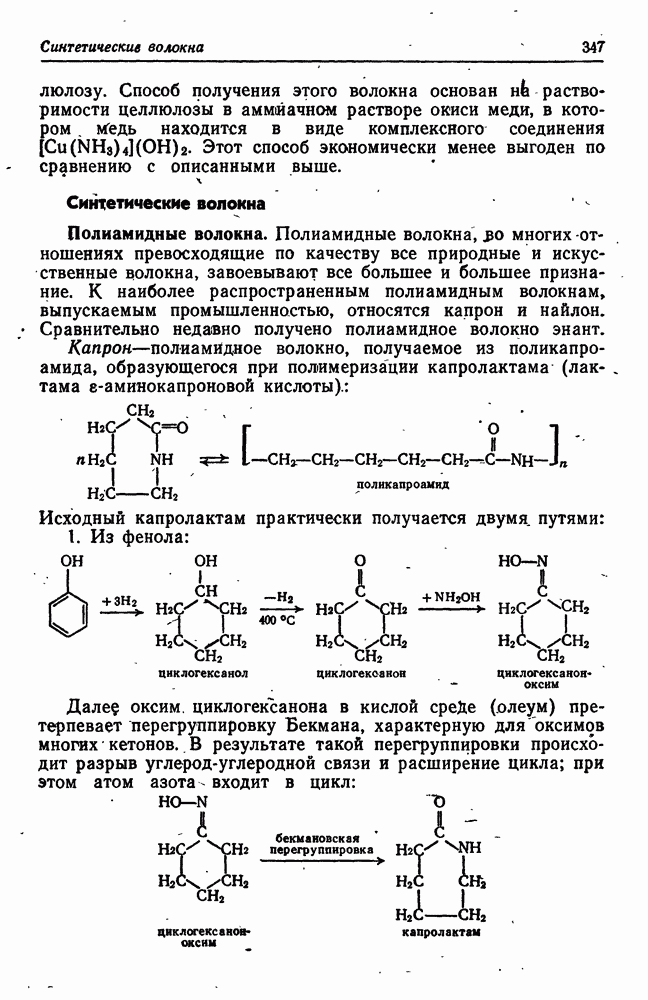
- Синтетические волокна
- 36. КАУЧУКИ
- Натуральный каучук
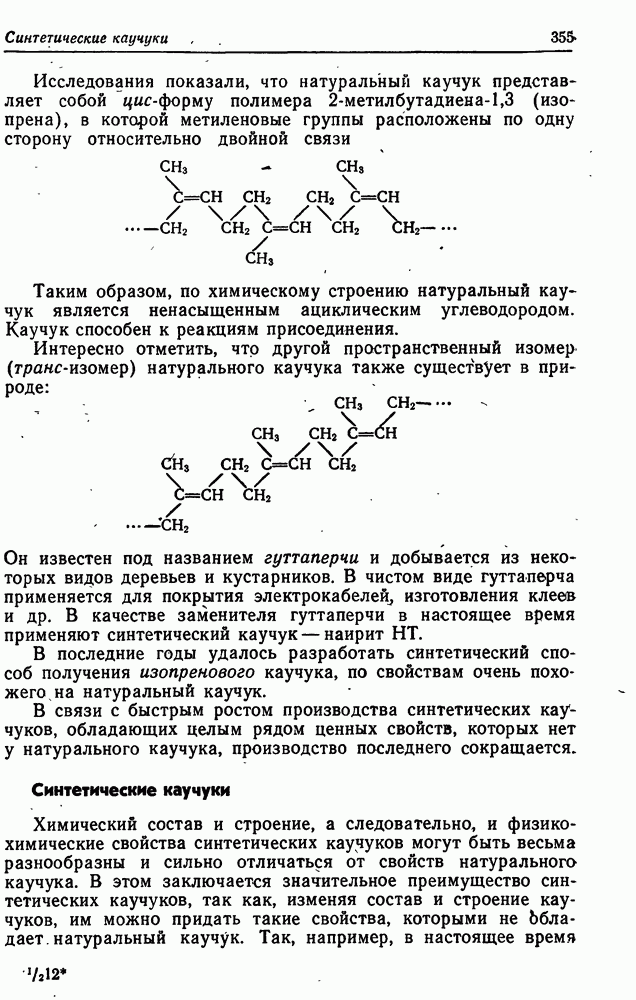
- Синтетические каучуки
- Синтетические латексы
- 37. СИНТЕТИЧЕСКИЕ КЛЕИ
- ХИМИЧЕСКИЕ ОСНОВЫ ЖИЗНЕДЕЯТЕЛЬНОСТИ
- 38. БЕЛКИ
- 39. НУКЛЕИНОВЫЕ КИСЛОТЫ
- 40. ЖИРЫ И УГЛЕВОДЫ
- 41. РОЛЬ БЕЛКОВ В ПРОЦЕССАХ ЖИЗНЕДЕЯТЕЛЬНОСТИ
- 42. СИНТЕЗ БЕЛКА В ОРГАНИЗМЕ
- ФИЗИОЛОГИЧЕСКИ АКТИВНЫЕ ВЕЩЕСТВА
- 43. ВИТАМИНЫ
- Витамин А
- Витамин С (аскорбиновая кислота)
- Витамины группы D
- 44. ГОРМОНЫ
- 45. АНТИБИОТИКИ