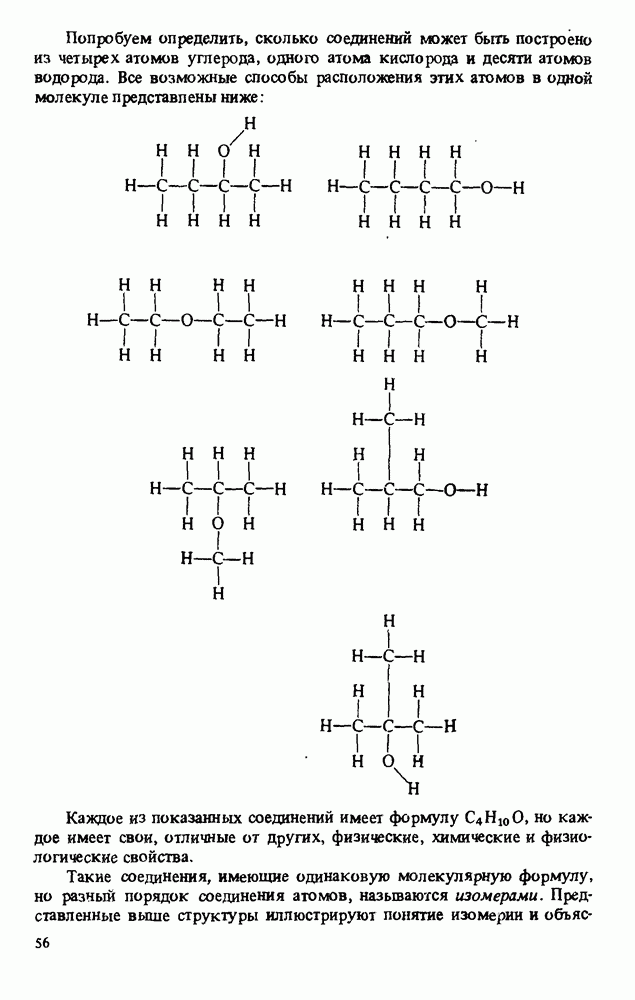| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ГИБРИДИЗАЦИЯ
Валентные электроны атома углерода располагаются на одной  -opбитали и двух
-opбитали и двух  -орбиталях.
-орбиталях.  -Орбитали расположены под углом 90° друг к другу, а
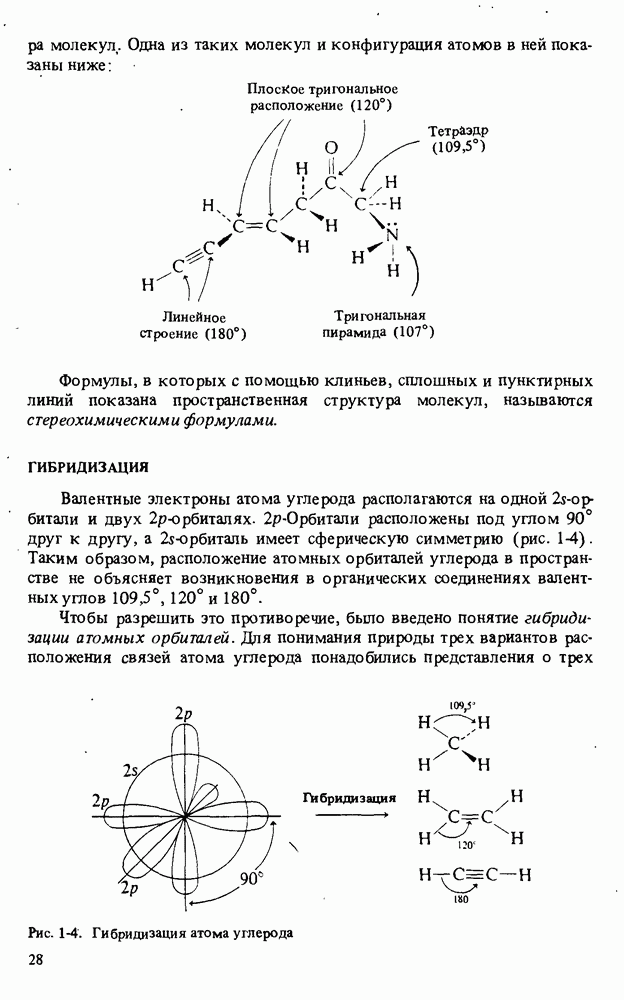
-Орбитали расположены под углом 90° друг к другу, а  -орбиталь имеет сферическую симметрию (рис. 1-4). Таким образом, расположение атомных орбиталей углерода в пространстве не объясняет возникновения в органических соединениях валентных углов 109,5°, 120° и 180°.
-орбиталь имеет сферическую симметрию (рис. 1-4). Таким образом, расположение атомных орбиталей углерода в пространстве не объясняет возникновения в органических соединениях валентных углов 109,5°, 120° и 180°.
Чтобы разрешить это противоречие, было введено понятие гибридизации атомных орбиталей. Для понимания природы трех вариантов расположения связей атома углерода понадобились представления о трех

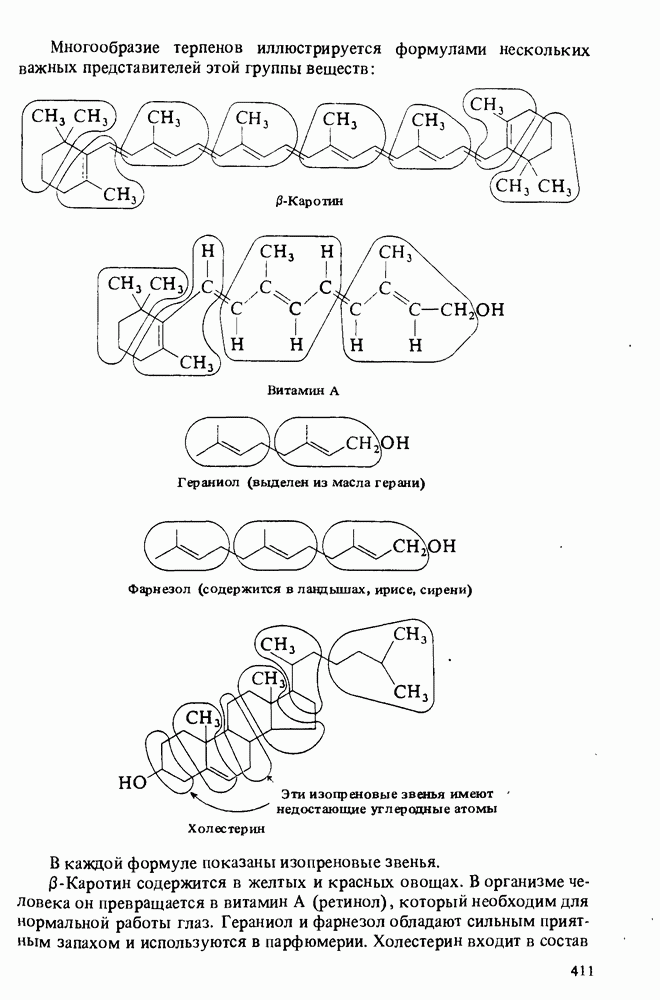
Рис. 1-4. Гибридизация атома углерода

Рис. 1-5. Гибридизация атома углерода в метане; 1 — атом углерода в основном состоянии; 2 — возбуждение (проматирование); 3 -  -гибридизация; 4 -
-гибридизация; 4 -  -гибридизированный атом углерода; 5 — образование четырех связей с атомами водорода; 6 - молекула метана
-гибридизированный атом углерода; 5 — образование четырех связей с атомами водорода; 6 - молекула метана
типах гибридизации (рис. 14). Возникновением концепции гибридизации мы обязаны Лайнусу Полингу, много сделавшему для развития теории химической связи.
Концепция гибридизации объясняет, каким образом атом углерода видоизменяет свои орбитали при образовании соединений. Ниже мы будем рассматривать этот процесс трансформации орбиталей постадийно. При этом надо иметь в виду, что расчленение процесса гибридизации на стадии или этапы есть, на самом деле, не более чем мысленный прием, позволяющий более логично и доступно изложить концепцию. Тем не менее заключения, о пространственной ориентации связей углеродного атома, к которым мы в итоге придем, полностью соответствуют реальному положению дел.
Посмотрите на рис. 1-5, где показана электронная конфигурация атома углерода. Нас интересует только судьба валентных электронов. В результате первого шага, который называют возбуждением или промотированием, один из двух  -электронов перемещается на свободную
-электронов перемещается на свободную  -орбиталь. На втором этапе происходит собственно процесс гибридизации, который несколько условно можно представить себе как смешение
-орбиталь. На втором этапе происходит собственно процесс гибридизации, который несколько условно можно представить себе как смешение
одной  и трех
и трех  -орбиталей и образование из них четырех новых одинаковых орбиталей, каждая из которых на одну четверть сохраняет свойства
-орбиталей и образование из них четырех новых одинаковых орбиталей, каждая из которых на одну четверть сохраняет свойства  -орбитали и на три четверти — свойства рорбиталей. Эти новые орбитали получили название
-орбитали и на три четверти — свойства рорбиталей. Эти новые орбитали получили название  -гибридных. Здесь надстрочный индекс 3 обозначает не число электронов, занимающих орбитали, а число
-гибридных. Здесь надстрочный индекс 3 обозначает не число электронов, занимающих орбитали, а число  -орбиталей, принявших участие в гибридизации. Гибридные орбитали направлены к вершинам тетраэдра, в центре которого находится атом углерода. На каждой
-орбиталей, принявших участие в гибридизации. Гибридные орбитали направлены к вершинам тетраэдра, в центре которого находится атом углерода. На каждой  -гибридной орбитали находится по одному электрону. Эти электроны и участвуют на третьем этапе в образовании связей с четырьмя атомами водорода, образуя валентные углы 109,5°. Чтобы облегчить восприятие материала, рядом с изображениями орбиталей показаны электронные конфигурации углеродного атома.
-гибридной орбитали находится по одному электрону. Эти электроны и участвуют на третьем этапе в образовании связей с четырьмя атомами водорода, образуя валентные углы 109,5°. Чтобы облегчить восприятие материала, рядом с изображениями орбиталей показаны электронные конфигурации углеродного атома.
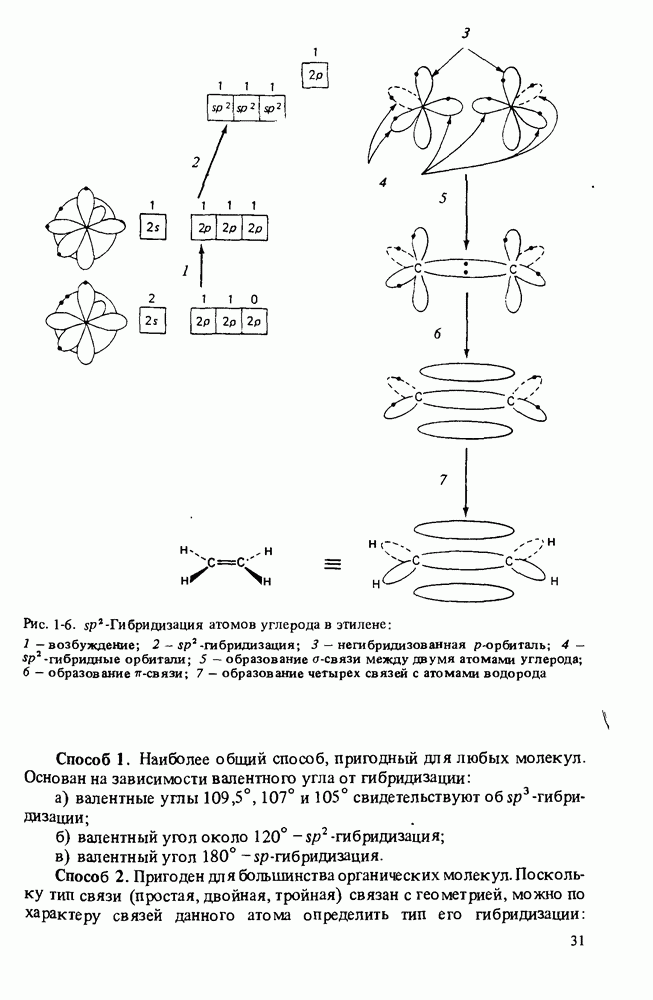
Образование плоских молекул с валентными углами 120° показано на рис. 1-6. Здесь, как и в случае  -гибридизации, первый шаг — возбуждение. На втором этапе в гибридизации участвуют одна
-гибридизации, первый шаг — возбуждение. На втором этапе в гибридизации участвуют одна  и две
и две  -орбитали, образуя три
-орбитали, образуя три  -гибридных орбитали, расположенных в одной плоскости под углом 120° друг к другу. Одна
-гибридных орбитали, расположенных в одной плоскости под углом 120° друг к другу. Одна  -орбиталь остается негибридизованной и располагается перпендикулярно плоскости
-орбиталь остается негибридизованной и располагается перпендикулярно плоскости  -гибридных орбиталей. Затем (третий шаг) две
-гибридных орбиталей. Затем (третий шаг) две  -гибридные орбитали двух углеродных атомов объединяют электроны, образуя ко валентную связь. Такая связь, образующаяся в результате перекрывания "оконечностей" двух атомных орбиталей, называется
-гибридные орбитали двух углеродных атомов объединяют электроны, образуя ко валентную связь. Такая связь, образующаяся в результате перекрывания "оконечностей" двух атомных орбиталей, называется  -связью. Четвертый этап - образование второй связи между двумя углеродными атомами. Связь образуется в результате перекрывания обращенных друг к другу краев негибридизованных
-связью. Четвертый этап - образование второй связи между двумя углеродными атомами. Связь образуется в результате перекрывания обращенных друг к другу краев негибридизованных  -орбиталей и называется
-орбиталей и называется  -связью. Новая молекулярная орбиталь представляет собой совокупность двух занятых электронами
-связью. Новая молекулярная орбиталь представляет собой совокупность двух занятых электронами  -связи областей — над и под
-связи областей — над и под  -связью. Обе связи (
-связью. Обе связи ( и
и  ) вместе составляют двойную связь между атомами углерода. И наконец, последний, пятый шаг - образование связей между атомами углерода и водорода с помощью электронов четырех оставшихся
) вместе составляют двойную связь между атомами углерода. И наконец, последний, пятый шаг - образование связей между атомами углерода и водорода с помощью электронов четырех оставшихся  -гибридных орбиталей.
-гибридных орбиталей.
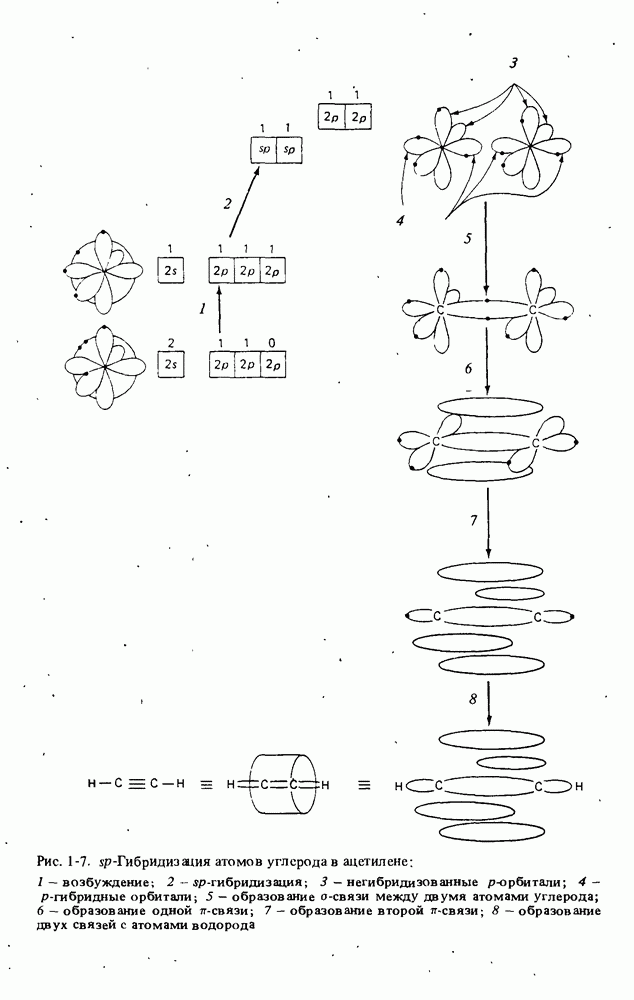
Третий, последний тип гибридизации, показан на примере простейшей молекулы, содержащей тройную связь молекулы ацетилена (рис. 1-7). Первый шаг — такой же, как раньше. На втором этапе происходит гибридизация одной  и одной
и одной  -орбиталей с образованием двух
-орбиталей с образованием двух  -гибрид-ных орбиталей и остаются неизмененными две
-гибрид-ных орбиталей и остаются неизмененными две  -орбитали, необходимые для образования двух
-орбитали, необходимые для образования двух  -связей. Следующий (третий) шаг — образование
-связей. Следующий (третий) шаг — образование  -связи между двумя
-связи между двумя  -гибридизовэнными углеродными атомами, затем образуются две
-гибридизовэнными углеродными атомами, затем образуются две  -связи (четвертый и пятый этапы). Одна
-связи (четвертый и пятый этапы). Одна  -связь и две
-связь и две  -связи между двумя атомами углерода вместе составляют тройную связь. И наконец, нашестом этапе образуются связи с двумя атомами водорода. Молекула ацетилена имеет линейное строение, все четыре атома лежат на одной прямой.
-связи между двумя атомами углерода вместе составляют тройную связь. И наконец, нашестом этапе образуются связи с двумя атомами водорода. Молекула ацетилена имеет линейное строение, все четыре атома лежат на одной прямой.
Мы показали, каким образом три основных в органической химии типа геометрии молекул возникают в результате различных трансформаций атомных орбиталей углерода. Можно предложить два способа определения типа гибридизации различных атомов в молекуле.
Рис. 1-6. (см. скан)  -Гибридизация атомов углерода в этилене: 1 - возбуждение; 2 -
-Гибридизация атомов углерода в этилене: 1 - возбуждение; 2 -  -гибридизация; 3 - негибридизованная
-гибридизация; 3 - негибридизованная  -орбиталь;
-орбиталь;  -гибридные орбитали; 5 — образование
-гибридные орбитали; 5 — образование  -связи между двумя атомами углерода; 6 — образование
-связи между двумя атомами углерода; 6 — образование  -связи; 7 - образование четырех связей с атомами водорода
-связи; 7 - образование четырех связей с атомами водорода
Способ 1. Наиболее общий способ, пригодный для любых молекул. Основан на зависимости валентного угла от гибридизации:
а) валентные углы 109,5°, 107° и 105° свидетельствуют  -гибридизации;
-гибридизации;
б) валентный угол около  -гибридизация;
-гибридизация;
в) валентный угол 180°  -гибридизация.
-гибридизация.
Способ 2. Пригоден для большинства органических молекул. Поскольку тип связи (простая, двойная, тройная) связан с геометрией, можно по характеру связей данного атома определить тип его гибридизации:

(кликните для просмотра скана)
а) все связи простые -  -гибридизация;
-гибридизация;
б) одна двойная связь -  -гибридизация;
-гибридизация;
в) одна тройная связь -  -гибридизация.
-гибридизация.
Для заряженных частиц и соединений некоторых нечасто встречающихся в органической химии элементов, таких, как бор  или бериллий
или бериллий  следует принимать во внимание конфигурацию атомов. Полезно обратиться к учебнику общей химии.
следует принимать во внимание конфигурацию атомов. Полезно обратиться к учебнику общей химии.
Для обычных органических молекул следует пользоваться простым и удобным способом 2.
Гибридизация — это мысленная операция превращения обычных (энергетически наиболее выгодных) атомных орбиталей в новые орбитали, геометрия которых соответствует экспериментально определенной геометрии молекул.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- Глава 1. КЛЮЧЕВЫЕ ПОНЯТИЯ ХИМИИ
- АТОМНАЯ ТЕОРИЯ
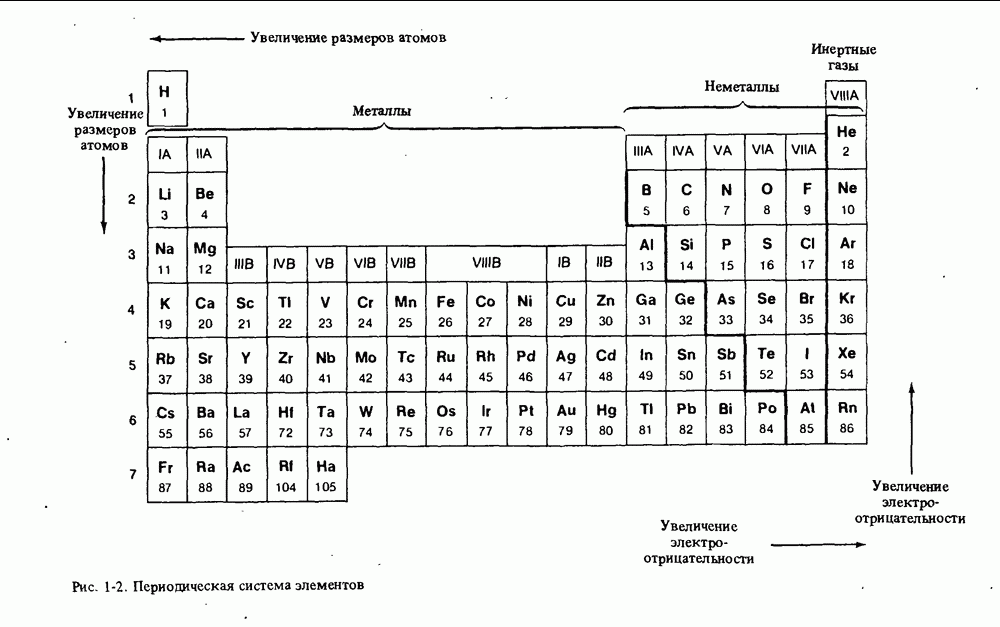
- ПЕРИОДИЧЕСКАЯ СИСТЕМА
- ХИМИЧЕСКАЯ СВЯЗЬ
- ФОРМУЛЫ ЛЬЮИСА
- ФОРМАЛЬНЫЙ ЗАРЯД
- РЕЗОНАНС
- ГЕОМЕТРИЯ МОЛЕКУЛ
- ГИБРИДИЗАЦИЯ
- ХИМИЧЕСКИЕ ФОРМУЛЫ
- СОВЕТЫ ИЗУЧАЮЩЕМУ ОРГАНИЧЕСКУЮ ХИМИЮ
- СВОДКА ОСНОВНЫХ ПОЛОЖЕНИЙ ГЛ. 1
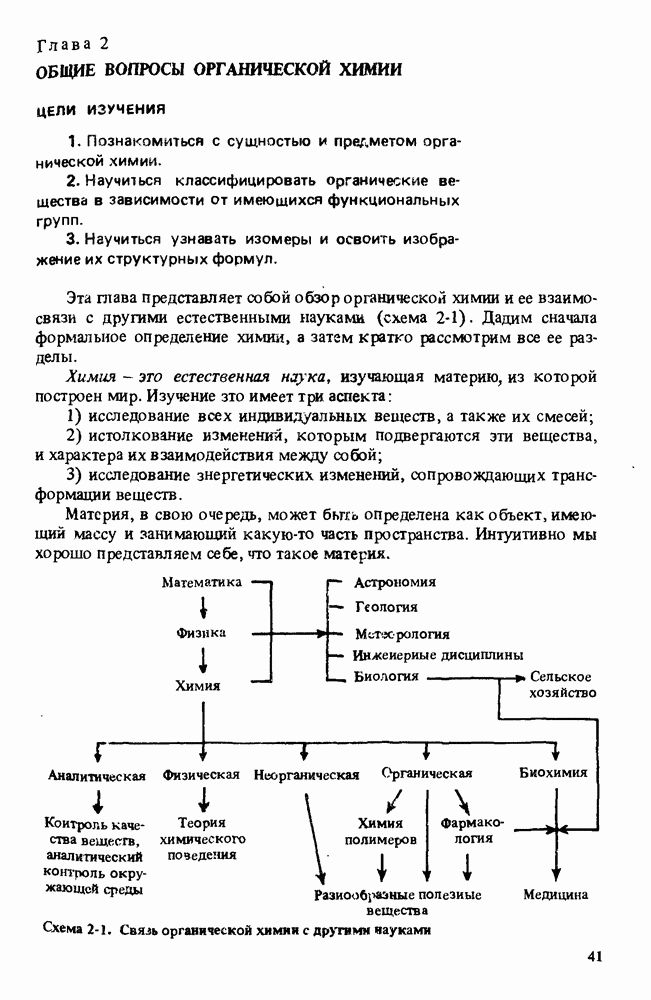
- Глава 2. ОБЩИЕ ВОПРОСЫ ОРГАНИЧЕСКОЙ ХИМИИ
- РАЗДЕЛЫ ХИМИИ
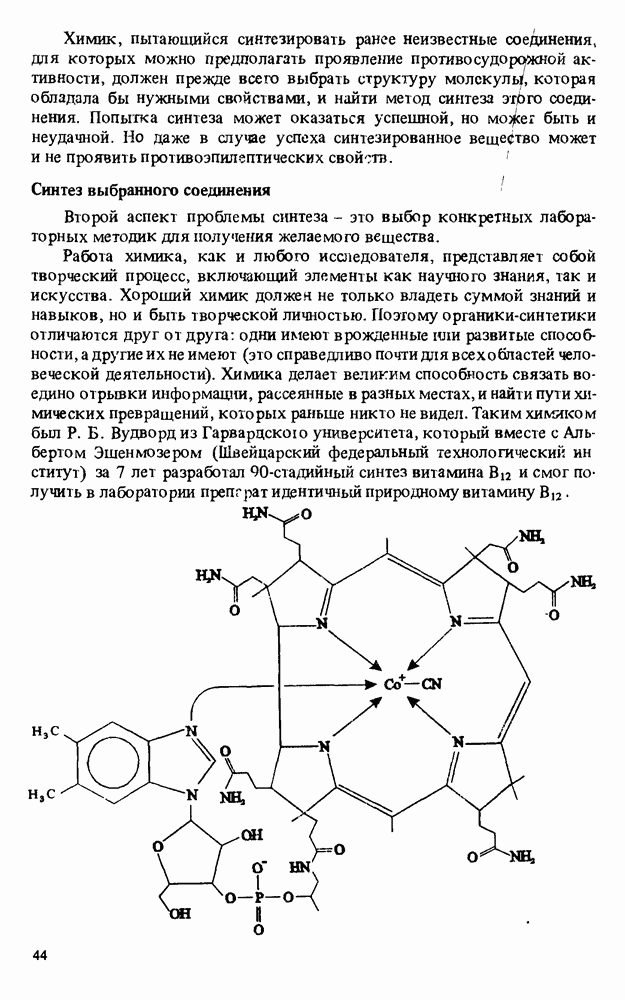
- СИНТЕТИЧЕСКАЯ ОРГАНИЧЕСКАЯ ХИМИЯ
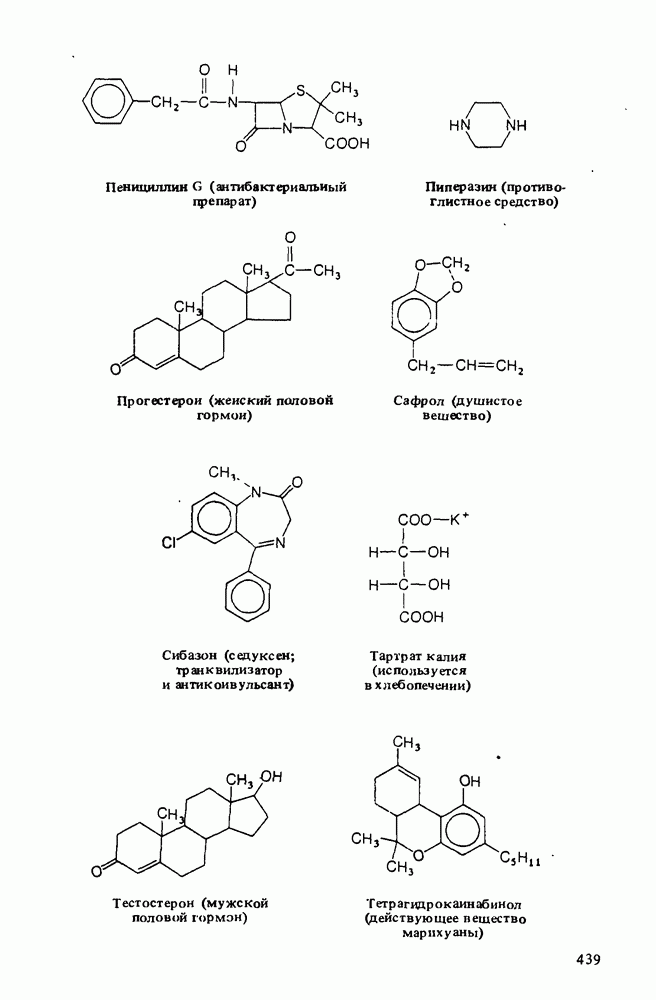
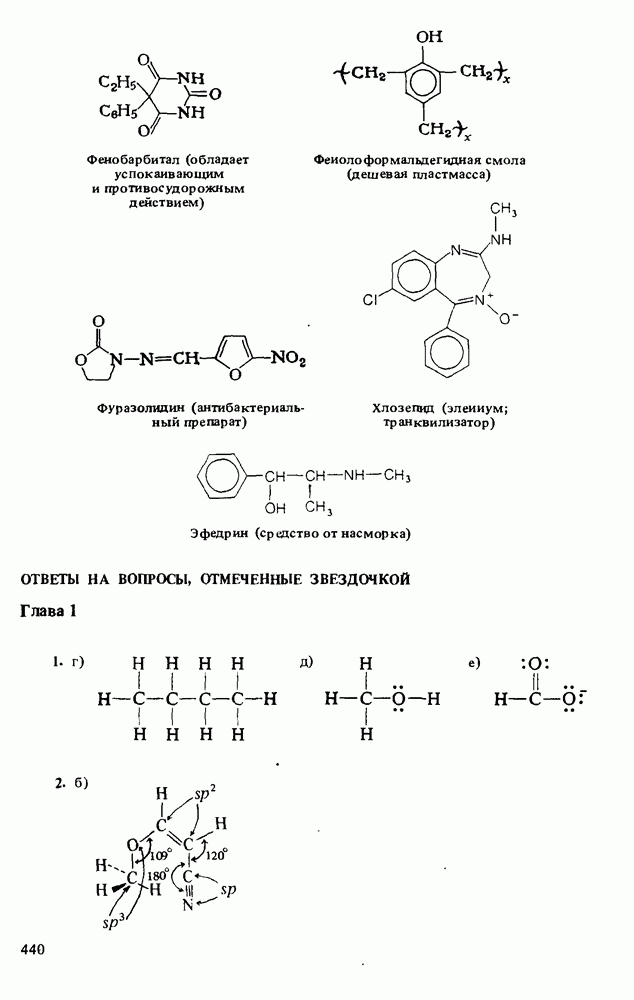
- ПОЛЕЗНЫЕ ОРГАНИЧЕСКИЕ ВЕЩЕСТВА
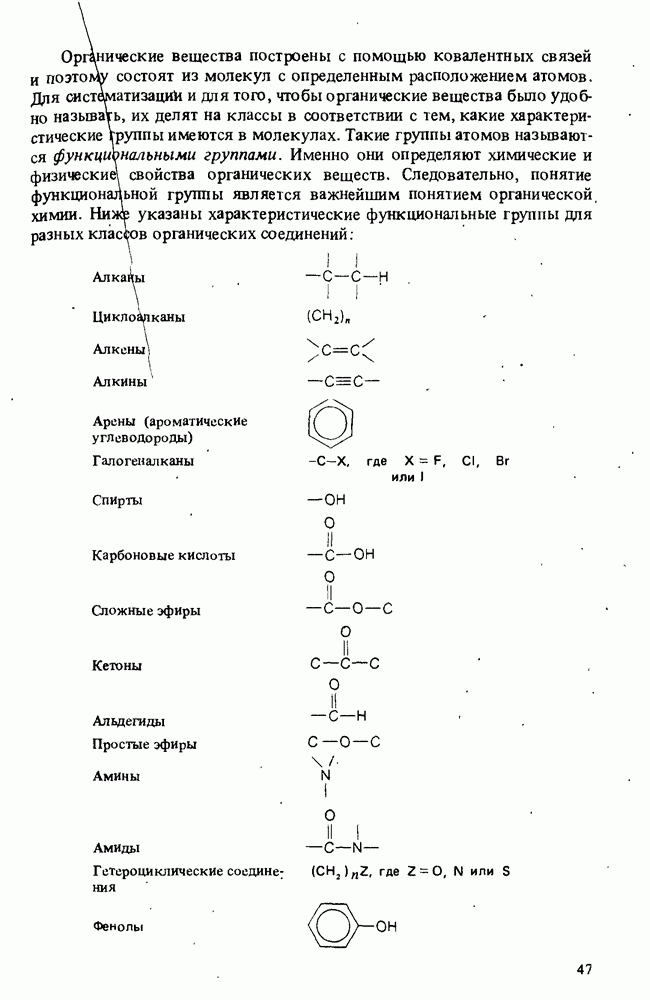
- КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ. ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
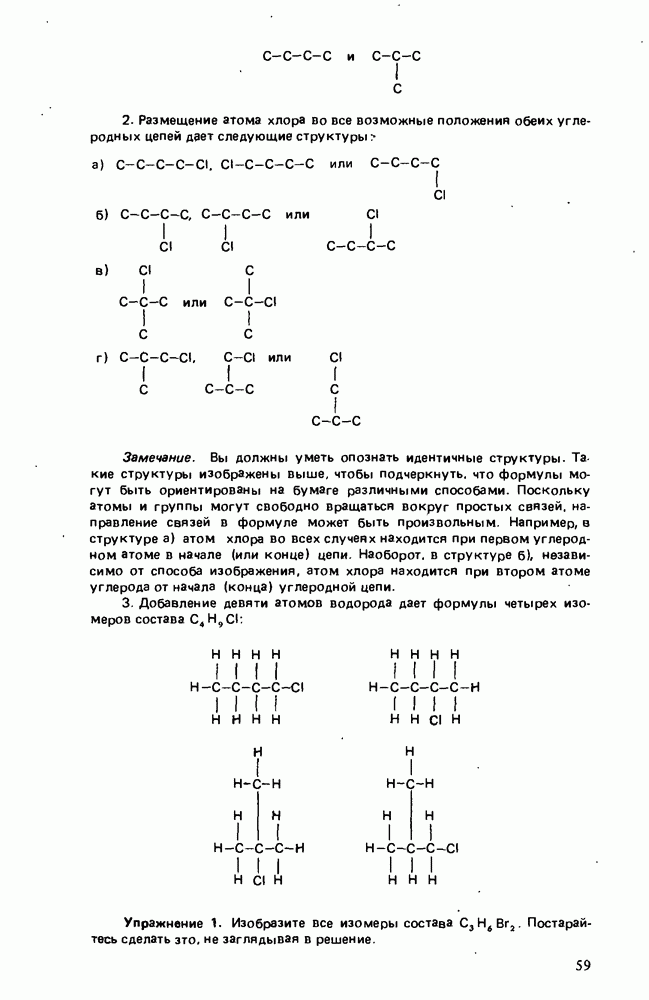
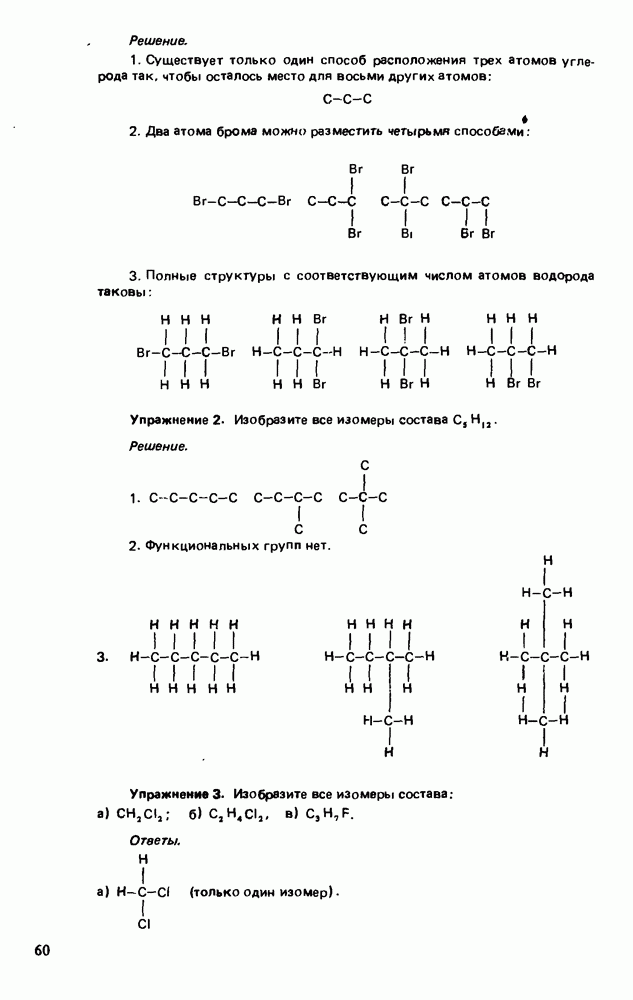
- ИЗОМЕРИЯ
- СВОДКА ОСНОВНЫХ ПОЛОЖЕНИЙ ГЛ. 2
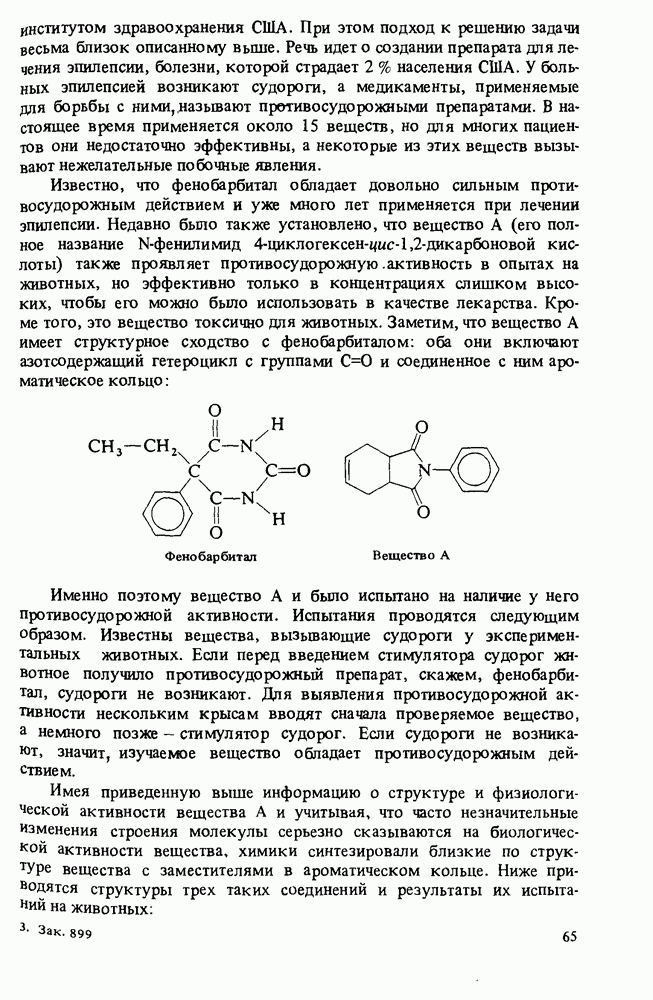
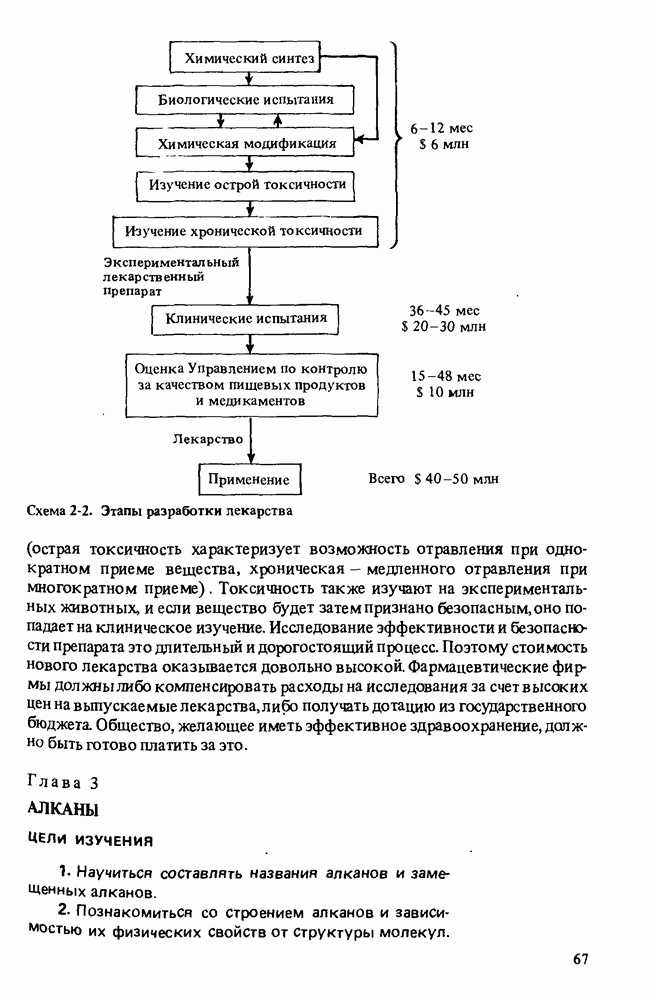
- Прикладная органическая химия: ХИМИЧЕСКИЙ СИНТЕЗ И МЕДИЦИНСКИЕ ИССЛЕДОВАНИЯ
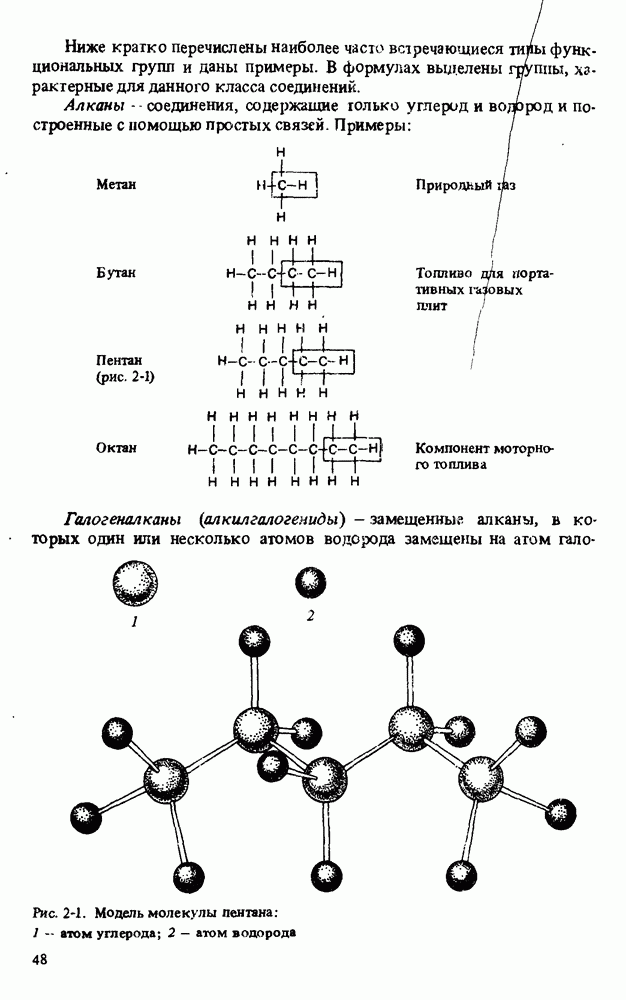
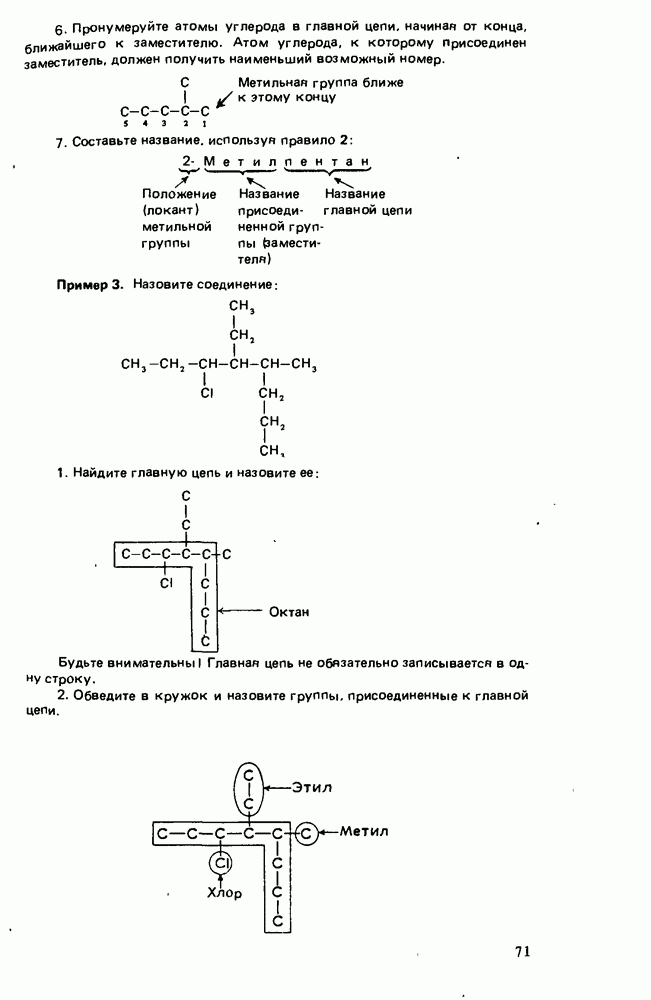
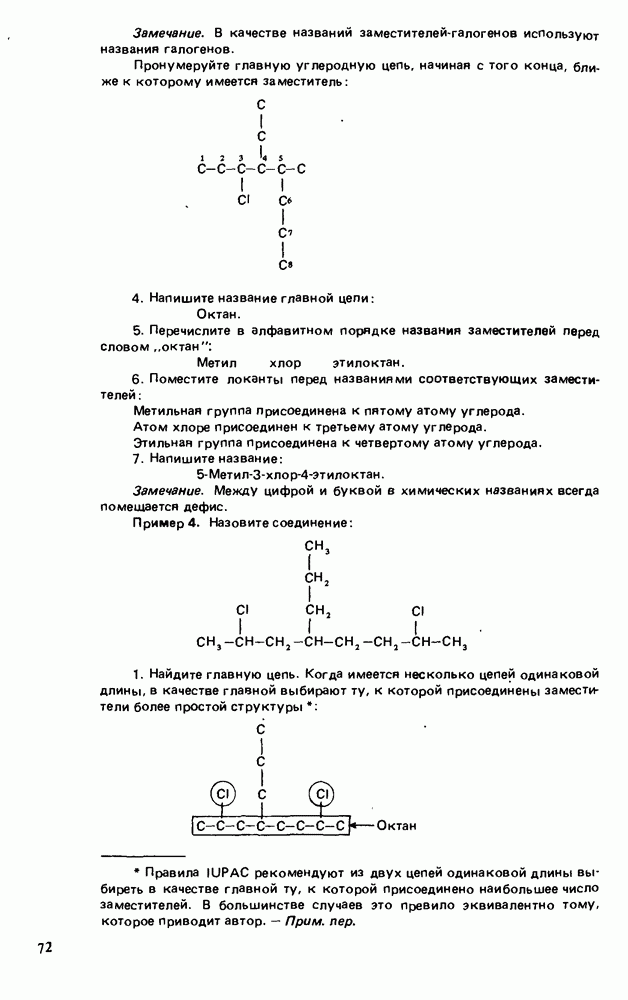
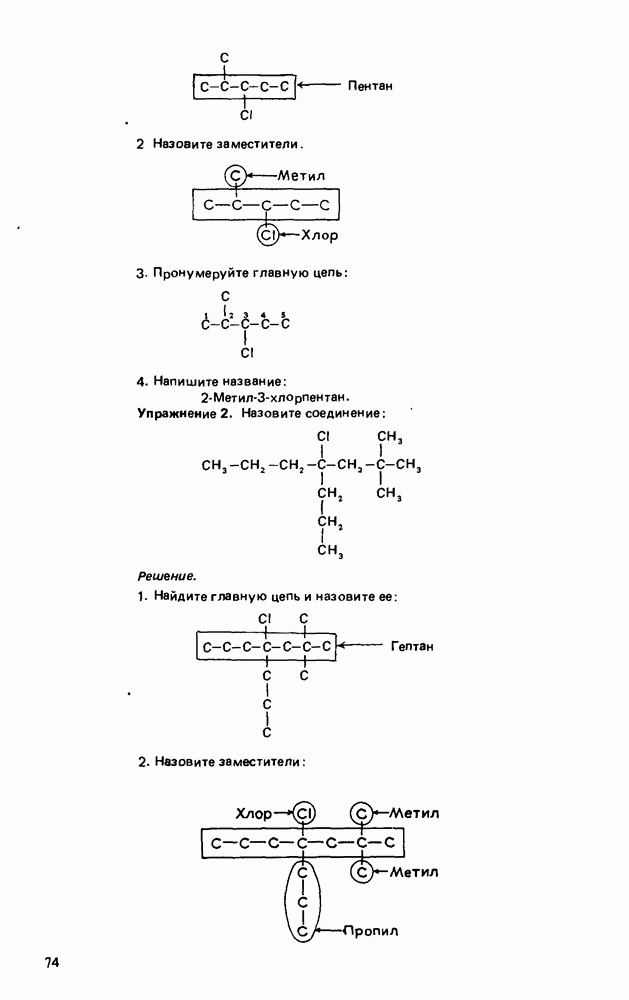
- Глава 3. АЛКАНЫ
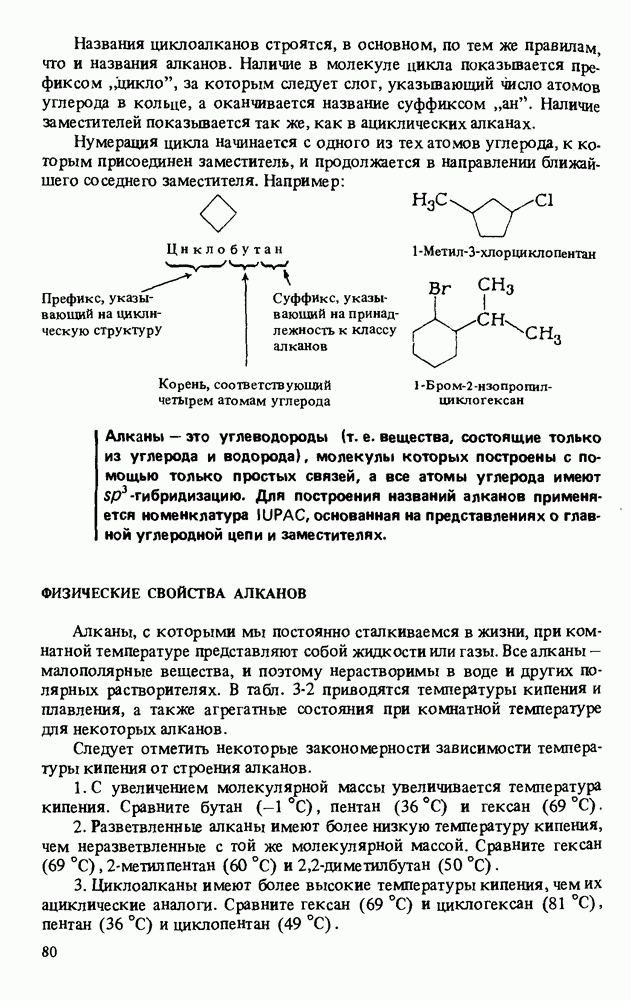
- ФИЗИЧЕСКИЕ СВОЙСТВА АЛКАНОВ
- СТРОЕНИЕ АЛКАНОВ
- ПОЛУЧЕНИЕ АЛКАНОВ
- РЕАКЦИИ АЛКАНОВ
- ХИМИЯ НЕФТИ
- СОВЕТЫ ИЗУЧАЮЩЕМУ ОРГАНИЧЕСКУЮ ХИМИЮ. ИЗУЧЕНИЕ РЕАКЦИЙ
- Глава 4. СТЕРЕОХИМИЯ И ОПТИЧЕСКАЯ АКТИВНОСТЬ
- СПОСОБЫ ИЗОБРАЖЕНИЯ ЭНАНТИОМЕРОВ
- ОБОЗНАЧЕНИЕ АБСОЛЮТНОЙ КОНФИГУРАЦИИ
- НАЗВАНИЯ ХИРАЛЬНЫХ МОЛЕКУЛ
- ИЗОБРАЖЕНИЕ МОЛЕКУЛ С ПРОТИВОПОЛОЖНОЙ КОНФИГУРАЦИЕЙ
- D,L-НОМЕНКЛАТУРА ЭНАНТИОМЕРОВ
- ТЕРМИНОЛОГИЯ, ПРИМЕНЯЕМАЯ В СТЕРЕОХИМИИ
- ЗНАЧЕНИЕ ОПТИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ
- Глава 5. ОРГАНИЧЕСКИЕ ГАЛОГЕНСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
- ПОЛУЧЕНИЕ ГАЛОГЕНАЛКАНОВ
- РЕАКЦИИ ГАЛОГЕНАЛКАНОВ
- ПРАКТИЧЕСКИ ВАЖНЫЕ ГАЛОГЕНАЛКАНЫ
- Прикладная органическая химия: ОРГАНИЧЕСКИЕ ПЕСТИЦИДЫ
- Глава 6. НЕНАСЫЩЕННЫЕ УГЛЕВОДОРОДЫ
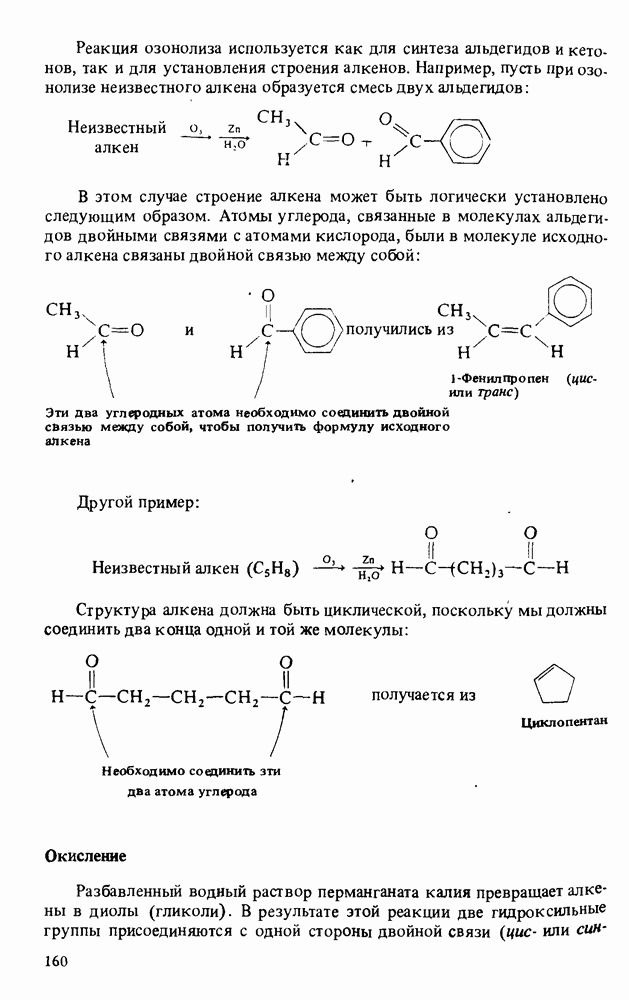
- НОМЕНКЛАТУРА АЛКЕНОВ
- ПОЛУЧЕНИЕ АЛКЕНОВ
- ОСНОВНЫЕ РЕАКЦИИ АЛКЕНОВ
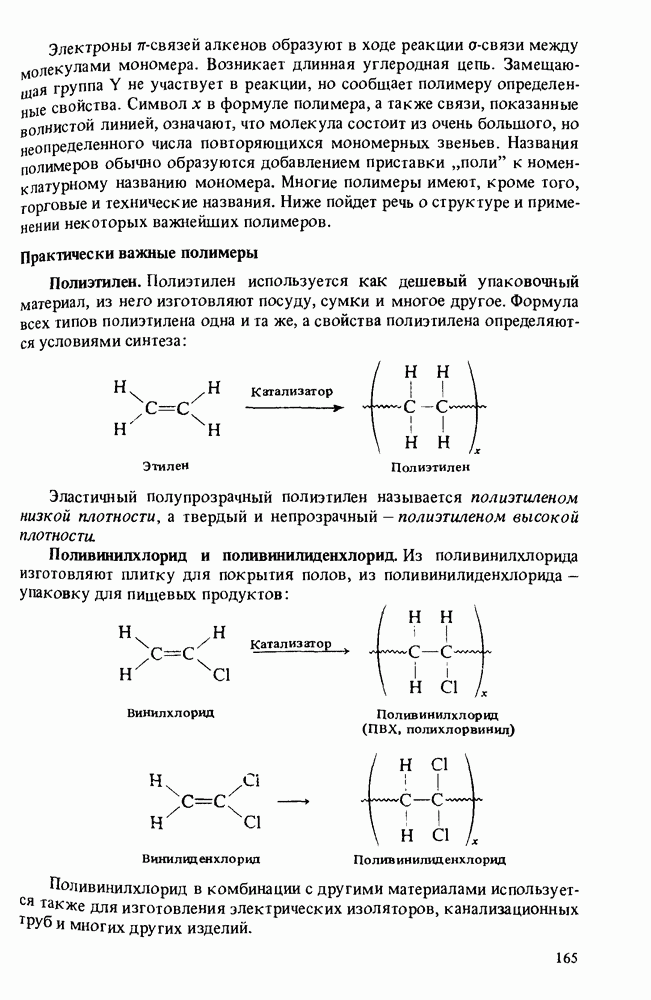
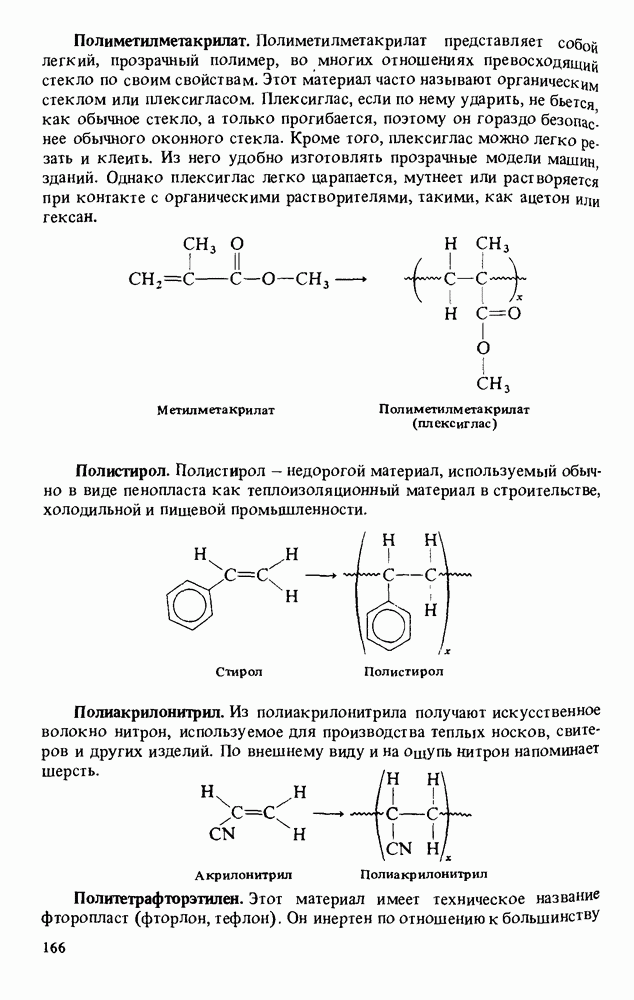
- ПОЛИМЕРЫ
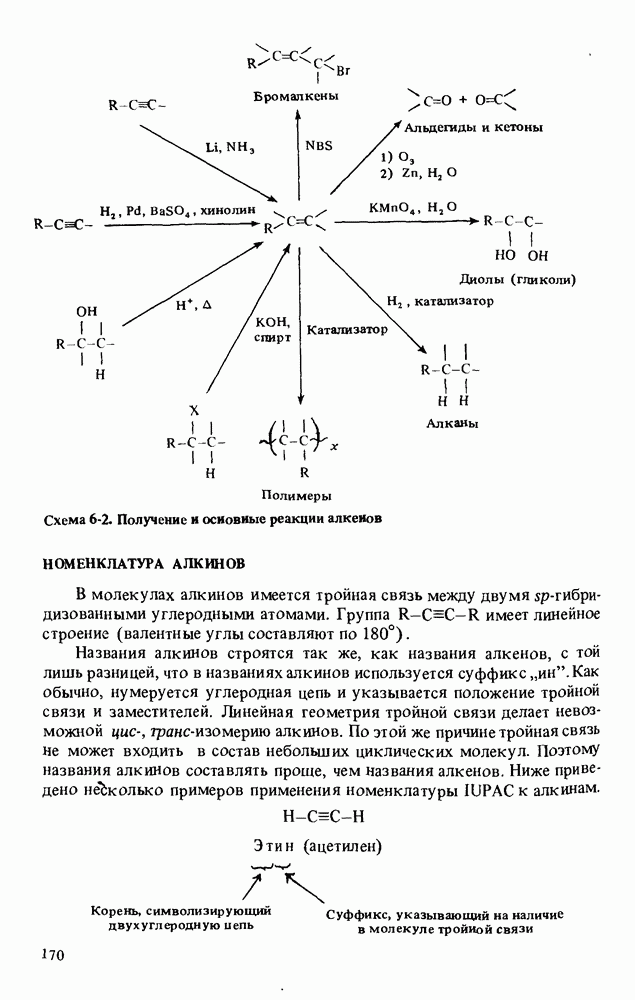
- НОМЕНКЛАТУРА АЛКИНОВ
- ПОЛУЧЕНИЕ АЛКИНОВ
- РЕАКЦИИ АЛКИНОВ
- НАПИСАНИЕ ОРГАНИЧЕСКИХ РЕАКЦИЙ
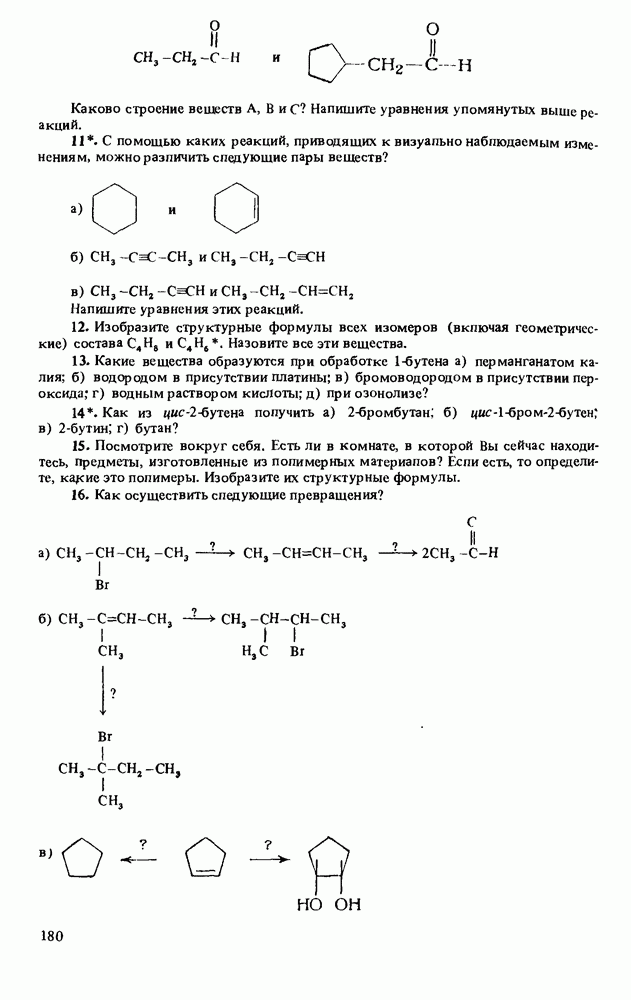
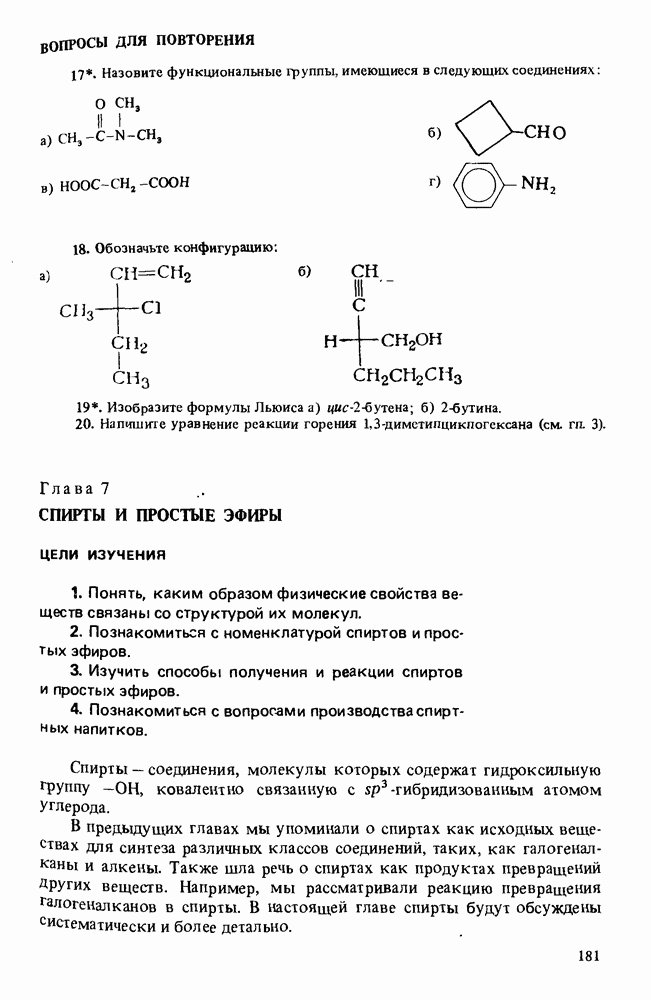
- Глава 7. СПИРТЫ И ПРОСТЫЕ ЭФИРЫ
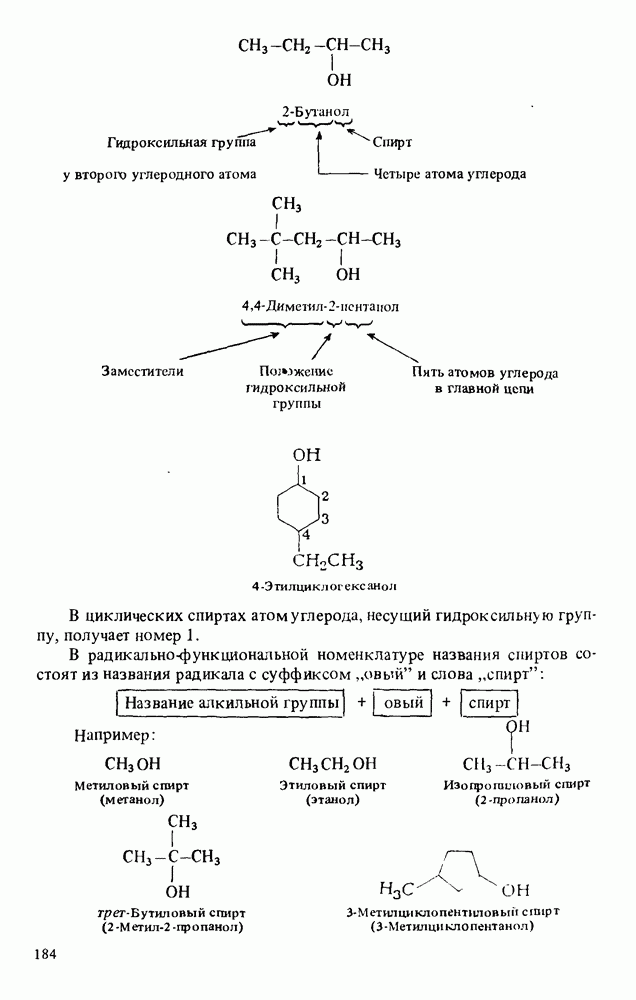
- НОМЕНКЛАТУРА СПИРТОВ
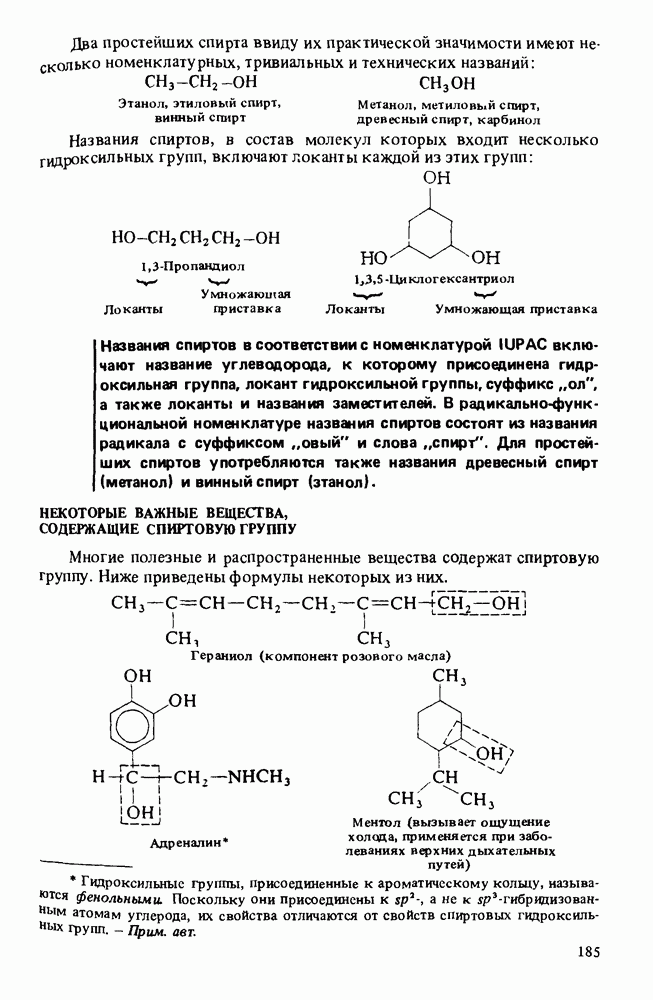
- НЕКОТОРЫЕ ВАЖНЫЕ ВЕЩЕСТВА, СОДЕРЖАЩИЕ СПИРТОВУЮ ГРУППУ
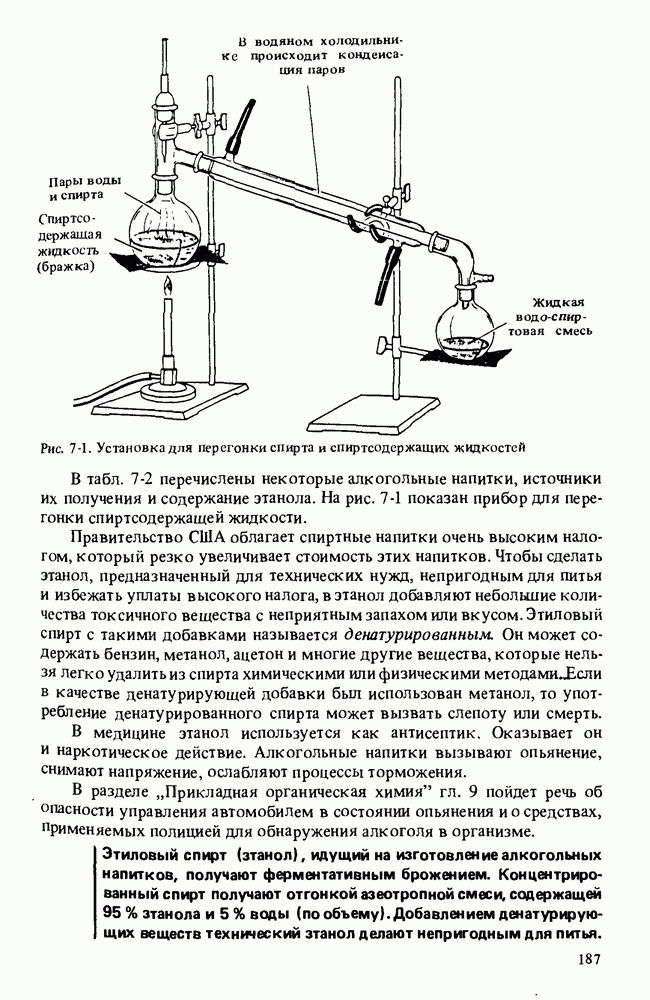
- ЭТИЛОВЫЙ СПИРТ. ПРОИЗВОДСТВО СПИРТНЫХ НАПИТКОВ
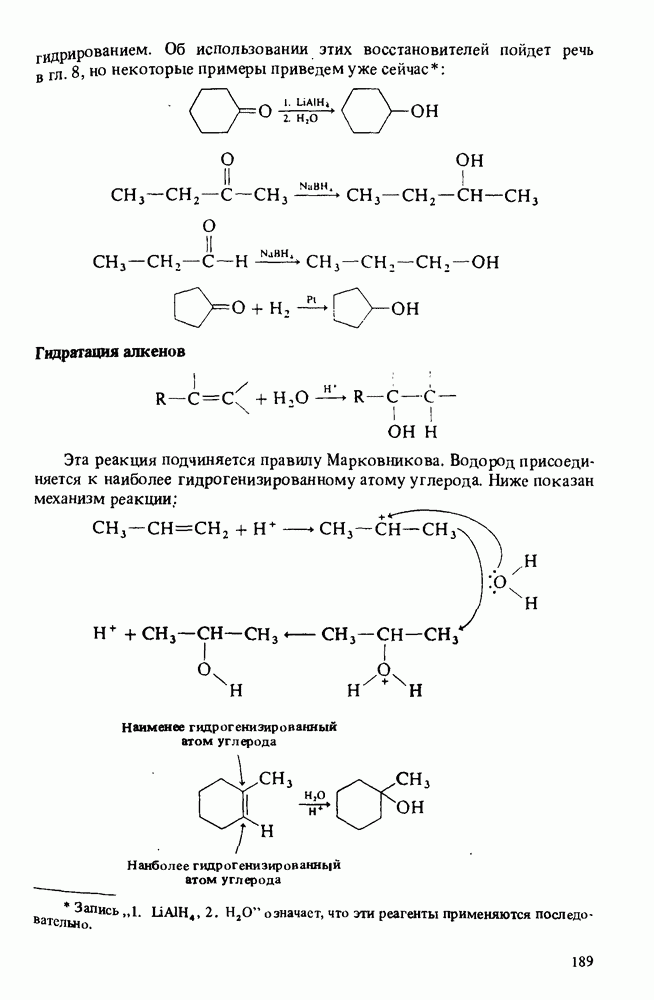
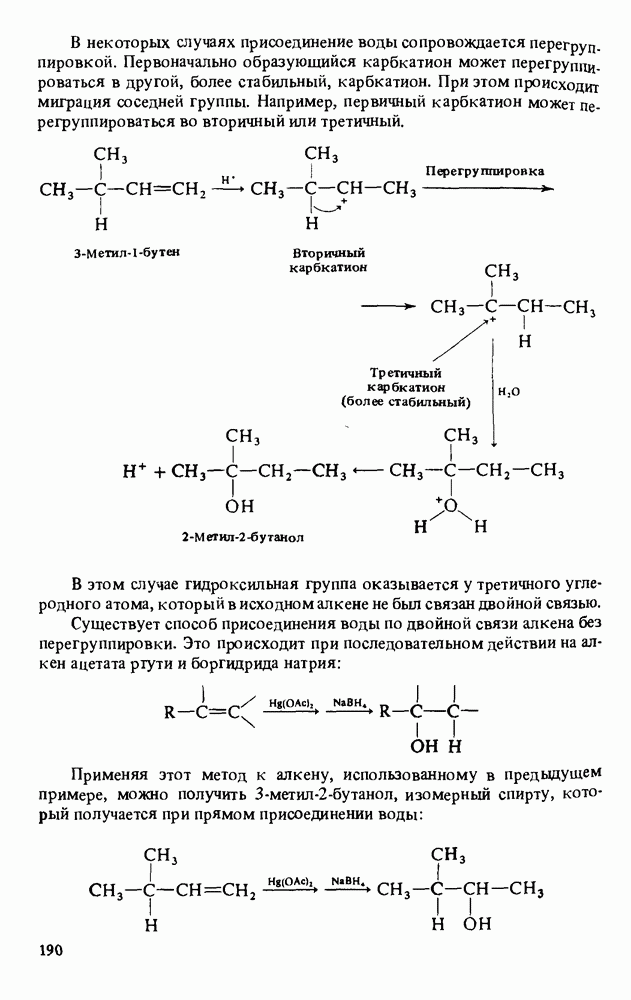
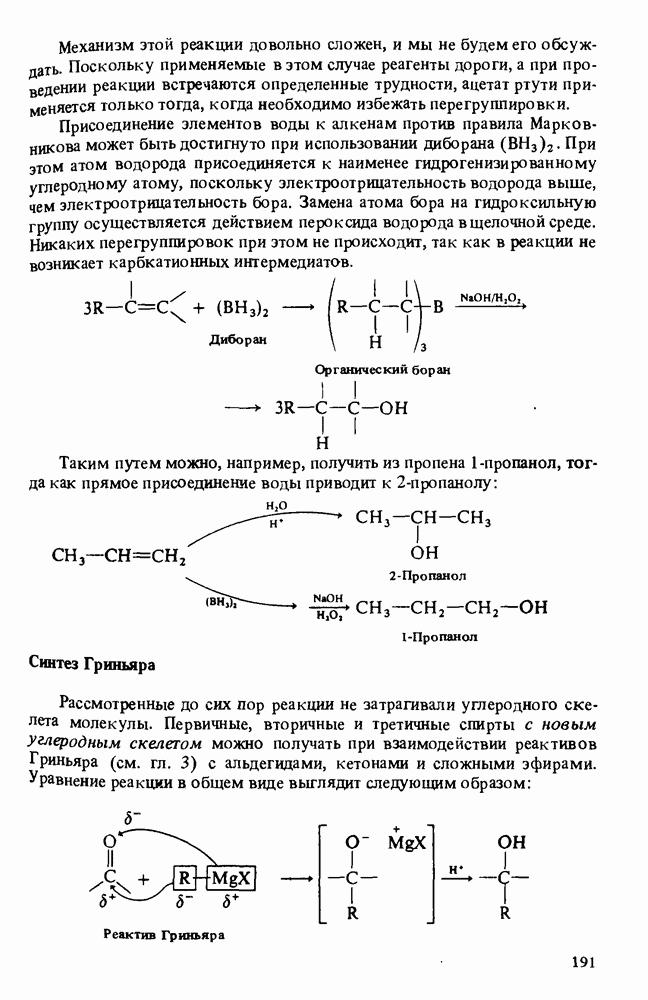
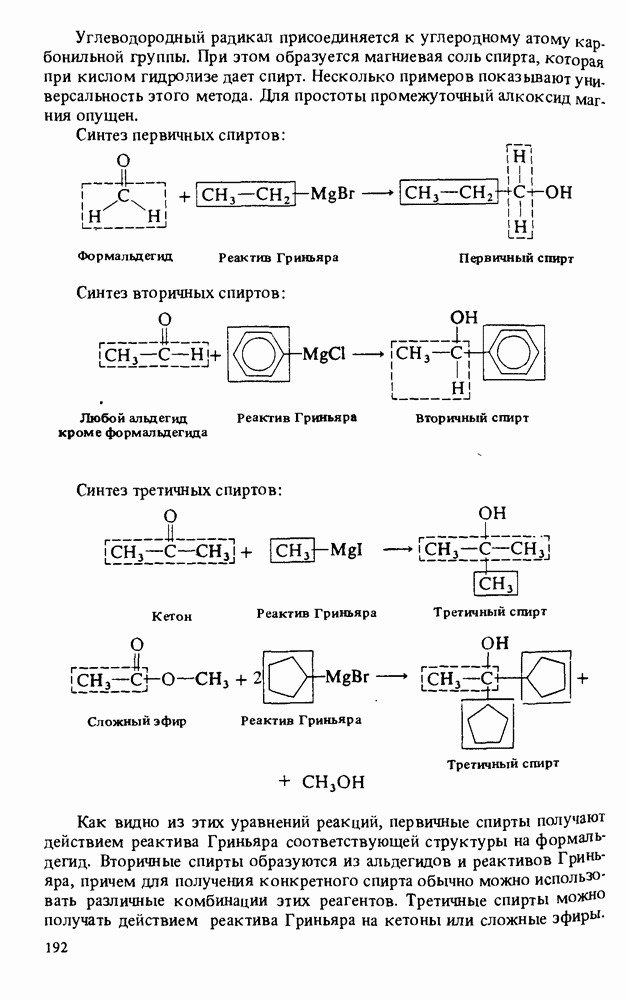
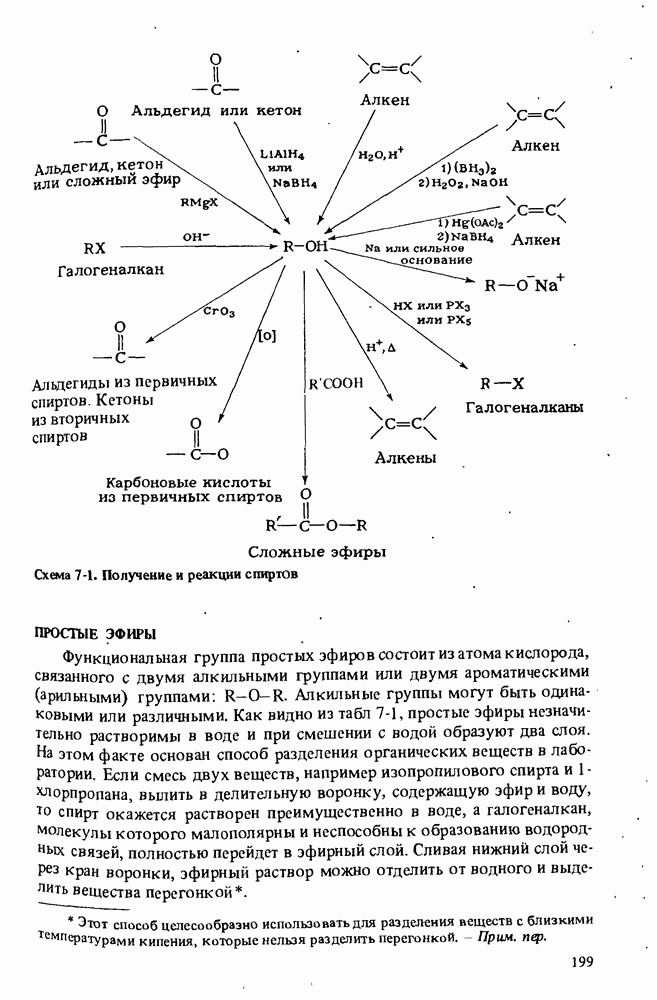
- ПОЛУЧЕНИЕ СПИРТОВ
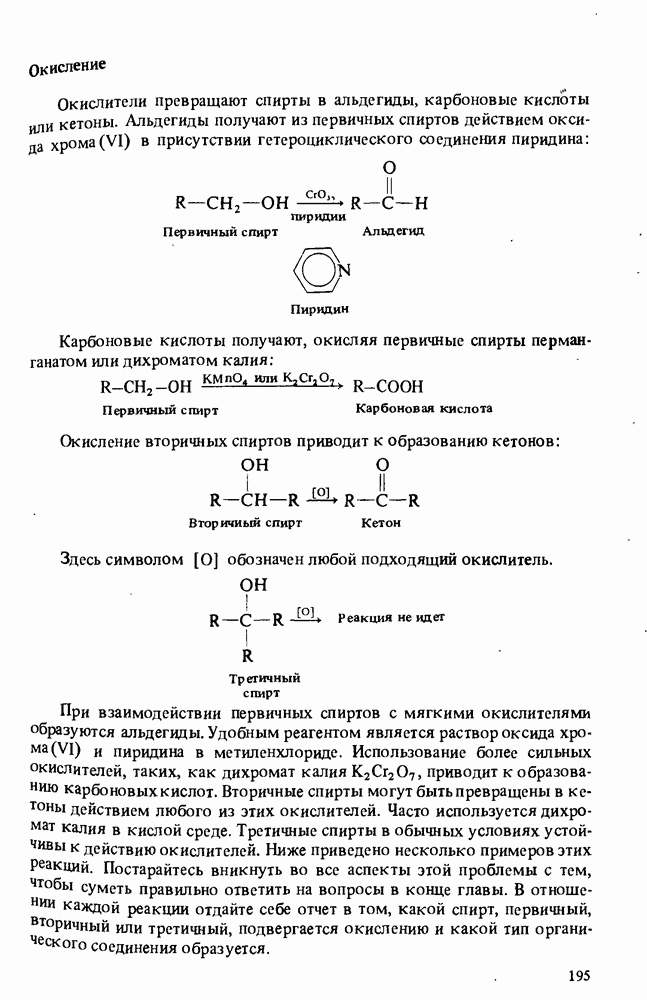
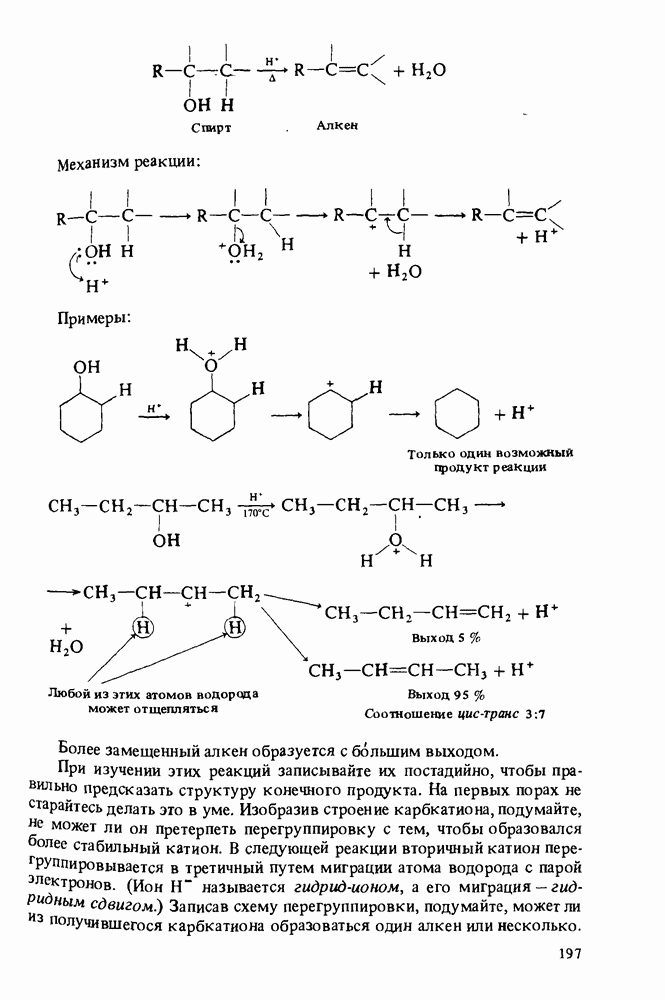
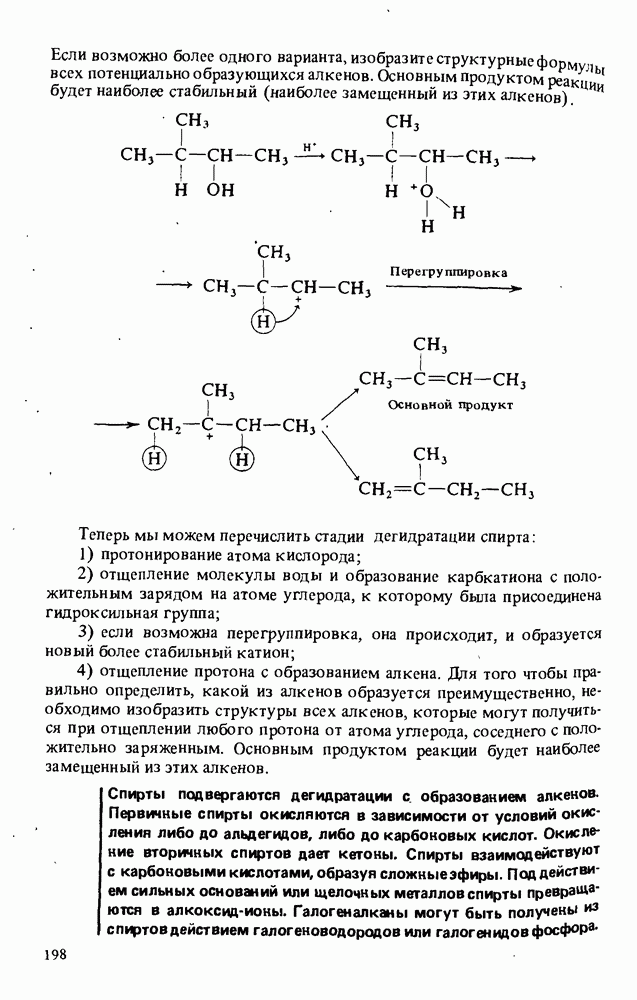
- РЕАКЦИИ СПИРТОВ
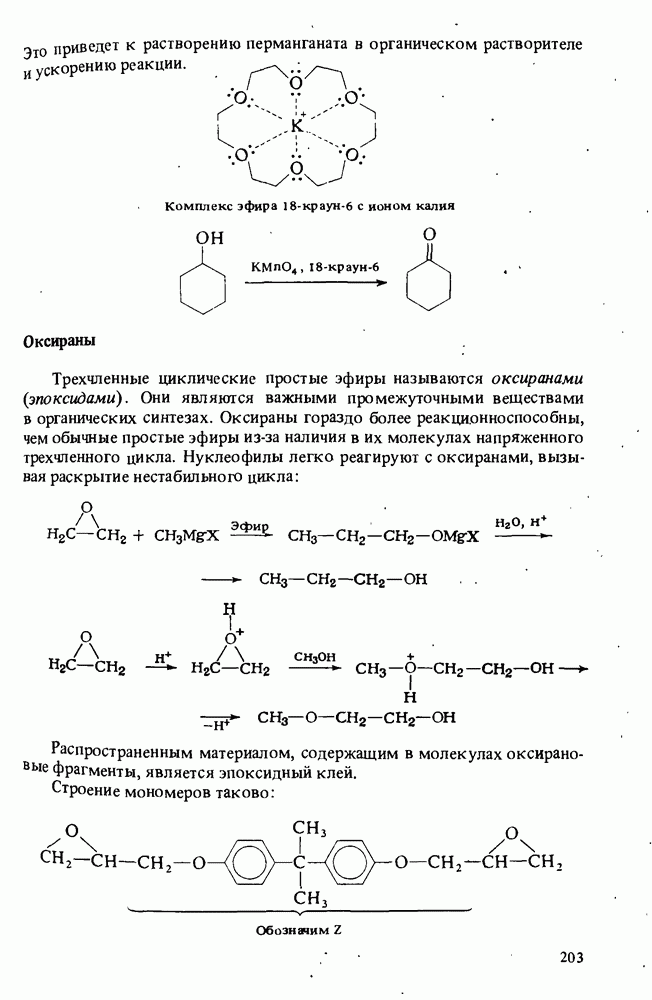
- ПРОСТЫЕ ЭФИРЫ
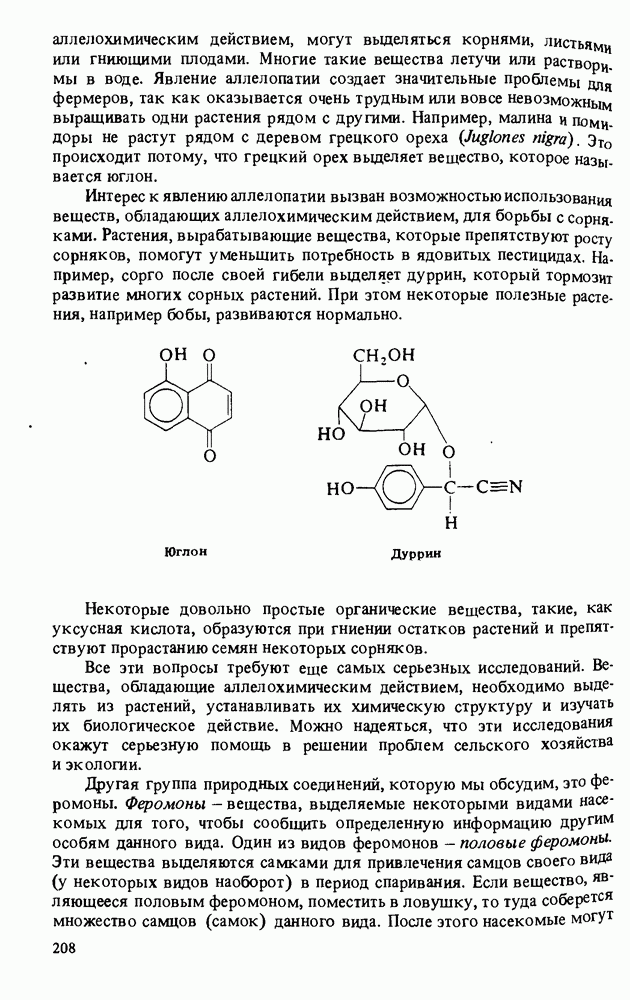
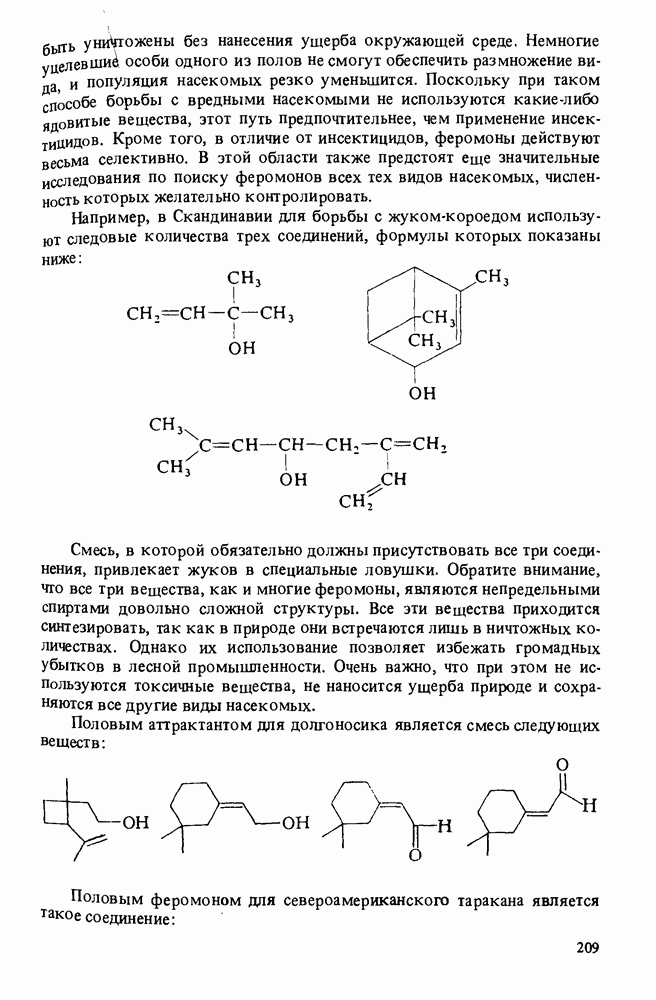
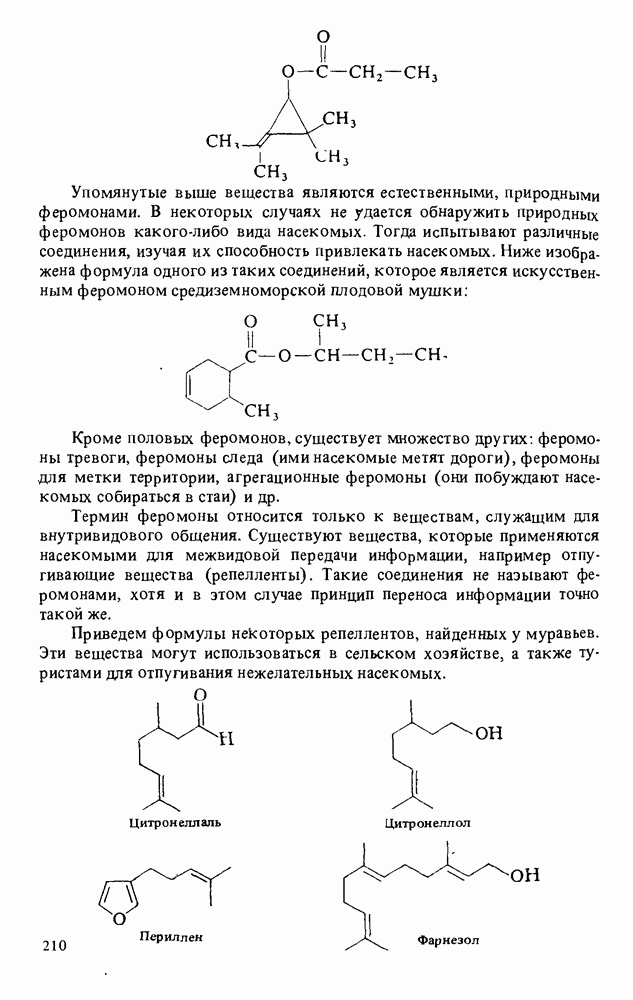
- Прикладная органическая химия: ВЕЩЕСТВА, ОБЛАДАЮЩИЕ АЛЛЕЛОХИМИЧЕСКИМ ДЕЙСТВИЕМ. ФЕРОМОНЫ
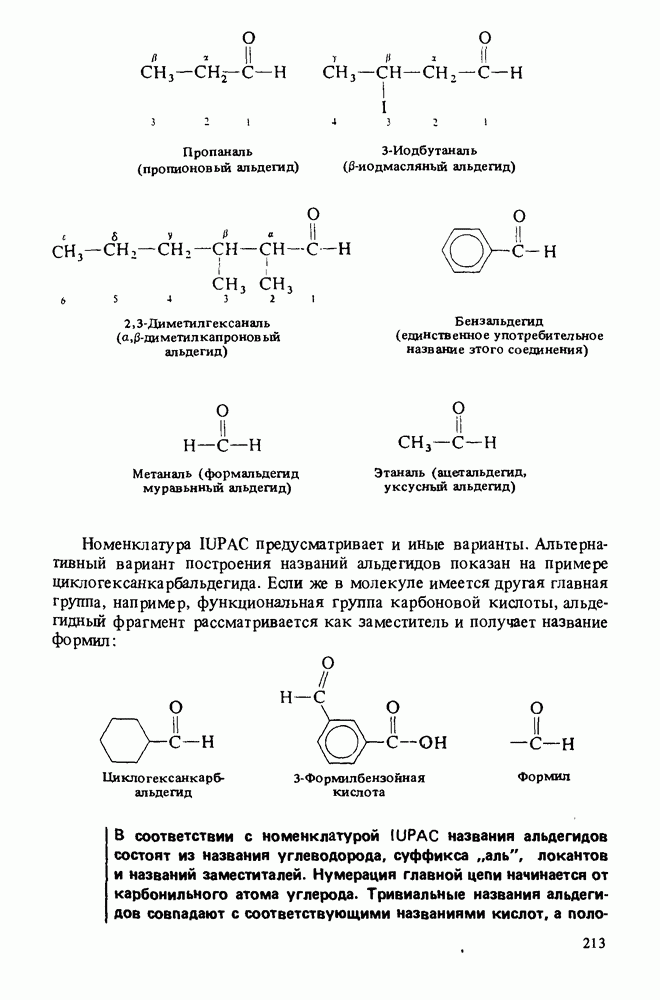
- Глава 8. АЛЬДЕГИДЫ И КЕТОНЫ
- ПОЛУЧЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ
- РЕАКЦИИ АЛЬДЕГИДОВ И КЕТОНОВ
- Глава 9. АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
- НОМЕНКЛАТУРА АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ
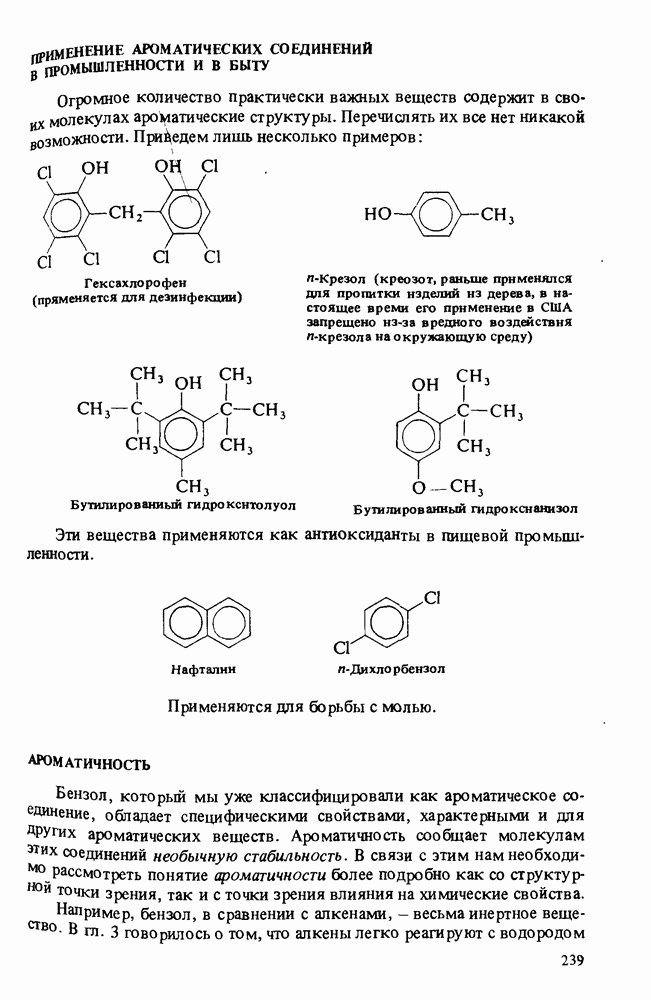
- ПРИМЕНЕНИЕ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ В ПРОМЫШЛЕННОСТИ И В БЫТУ
- АРОМАТИЧНОСТЬ
- ПОЛУЧЕНИЕ АЛКИЛЬБЕНЗОЛОВ
- РЕАКЦИИ БЕНЗОЛА И ЕГО ПРОИЗВОДНЫХ
- АРОМАТИЧЕСКОЕ ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ
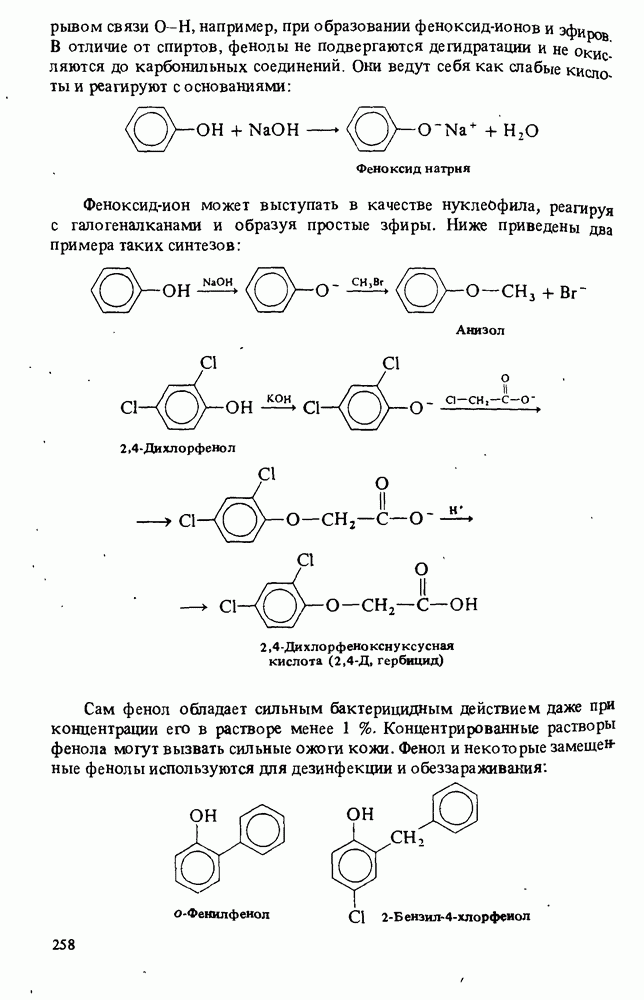
- ФЕНОЛЫ
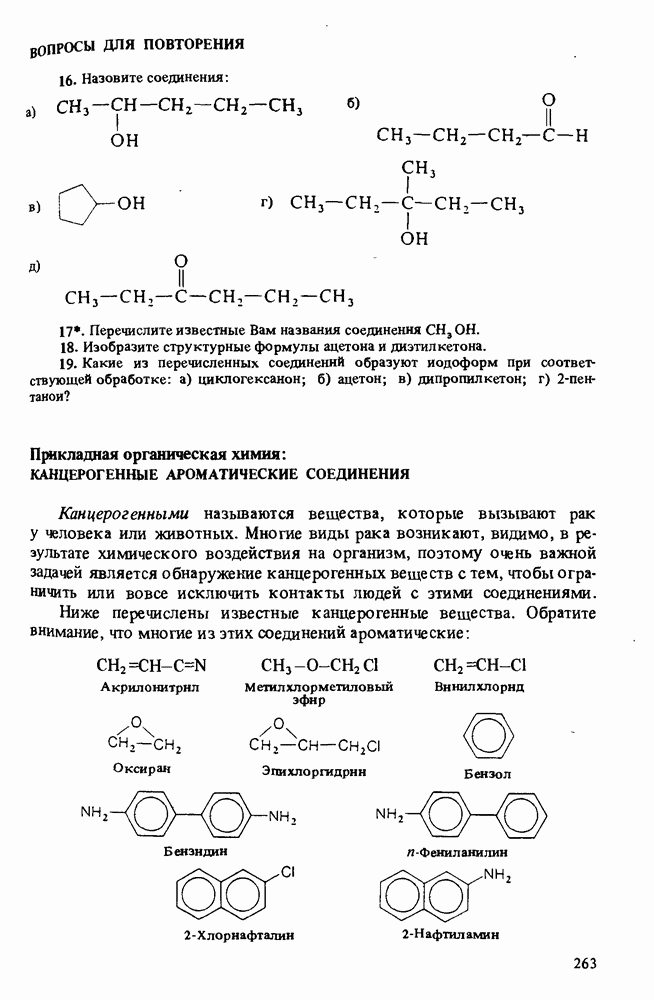
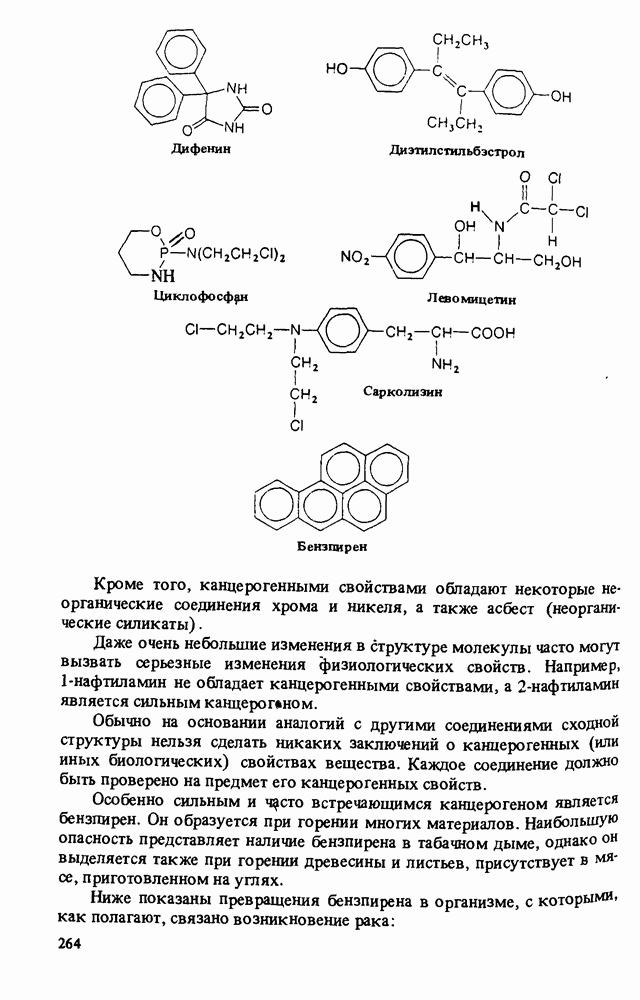
- Прикладная органическая химия: КАНЦЕРОГЕННЫЕ АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
- Глава 10. ОРГАНИЧЕСКИЙ СИНТЕЗ
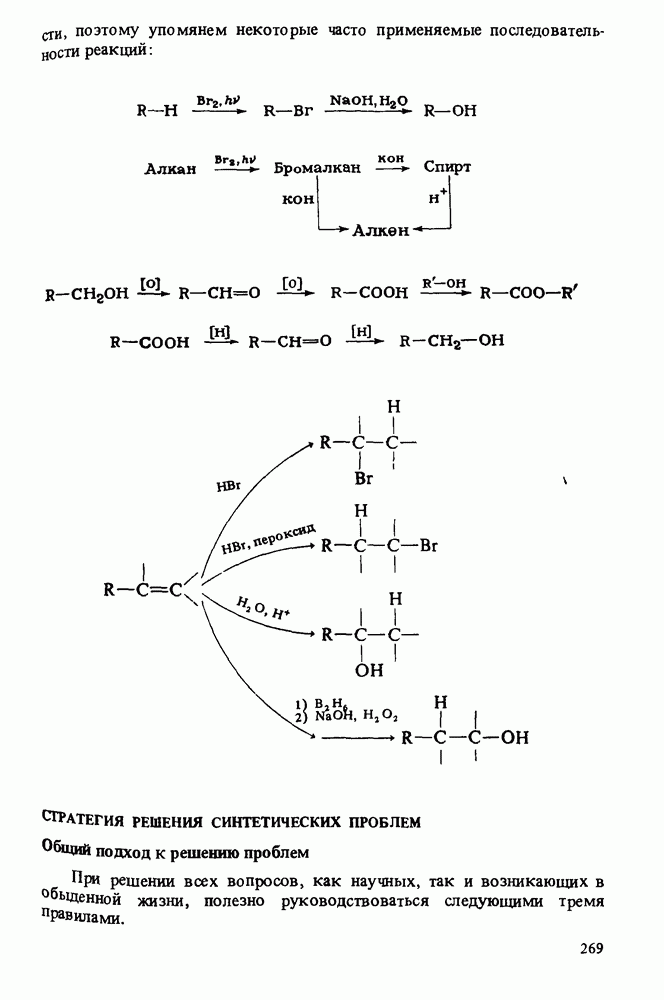
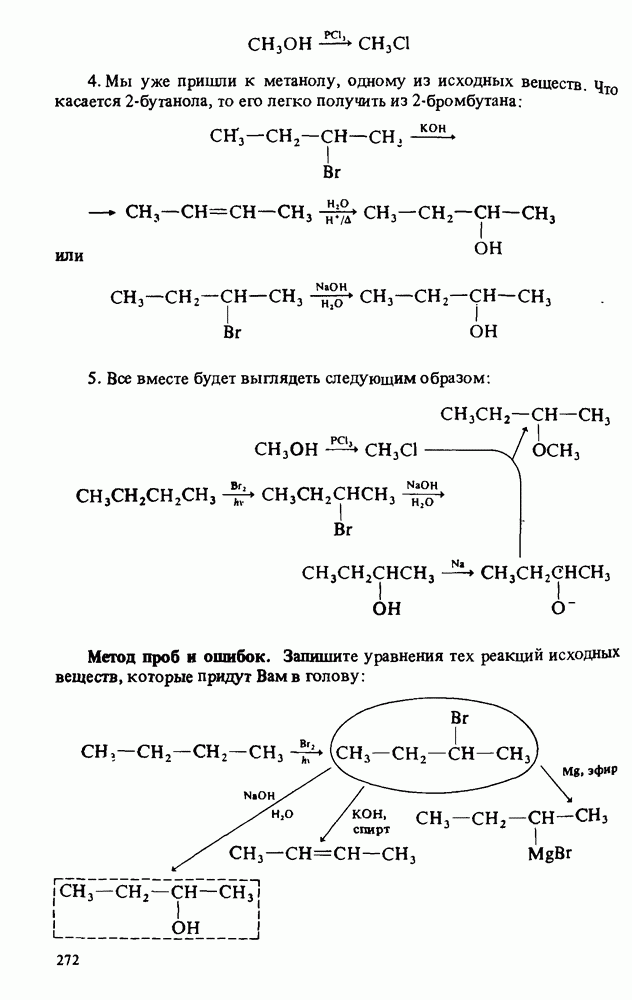
- СТРАТЕГИЯ РЕШЕНИЯ СИНТЕТИЧЕСКИХ ПРОБЛЕМ
- Глава 11. МОЛЕКУЛЯРНАЯ СПЕКТРОСКОПИЯ
- ИНФРАКРАСНАЯ СПЕКТРОСКОПИЯ
- СПЕКТРОСКОПИЯ ЯДЕРНОГО МАГНИТНОГО РЕЗОНАНСА
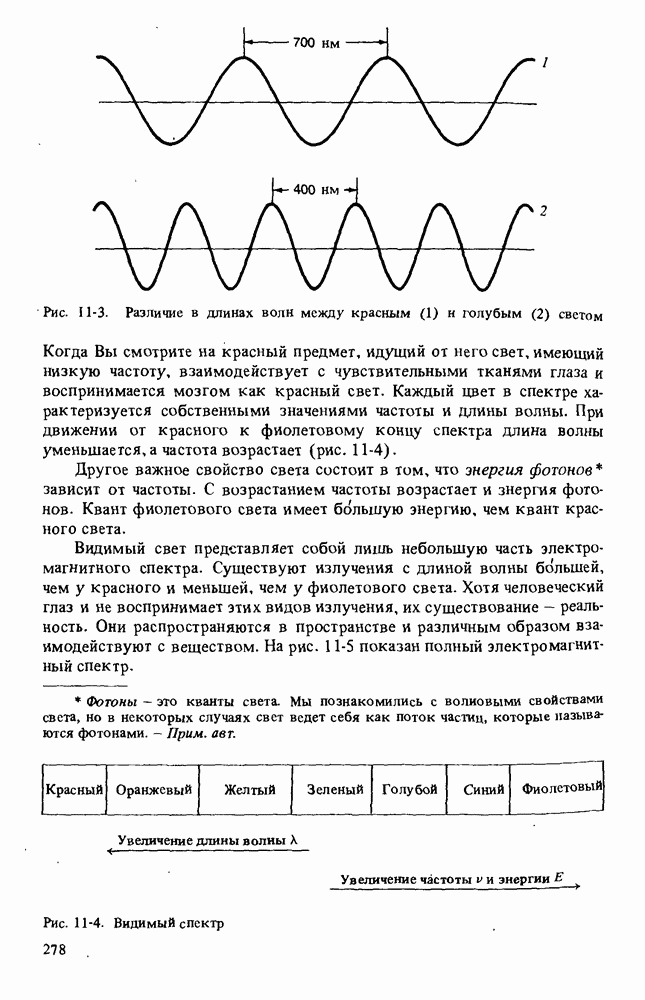
- УЛЬТРАФИОЛЕТОВАЯ СПЕКТРОСКОПИЯ
- МАСС-СПЕКТРОМЕТРИЯ
- ОПРЕДЕЛЕНИЕ СТРУКТУРЫ ОРГАНИЧЕСКОГО СОЕДИНЕНИЯ
- Прикладная органическая химия: ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ АЛКОГОЛЯ В КРОВИ
- Глава 12. КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
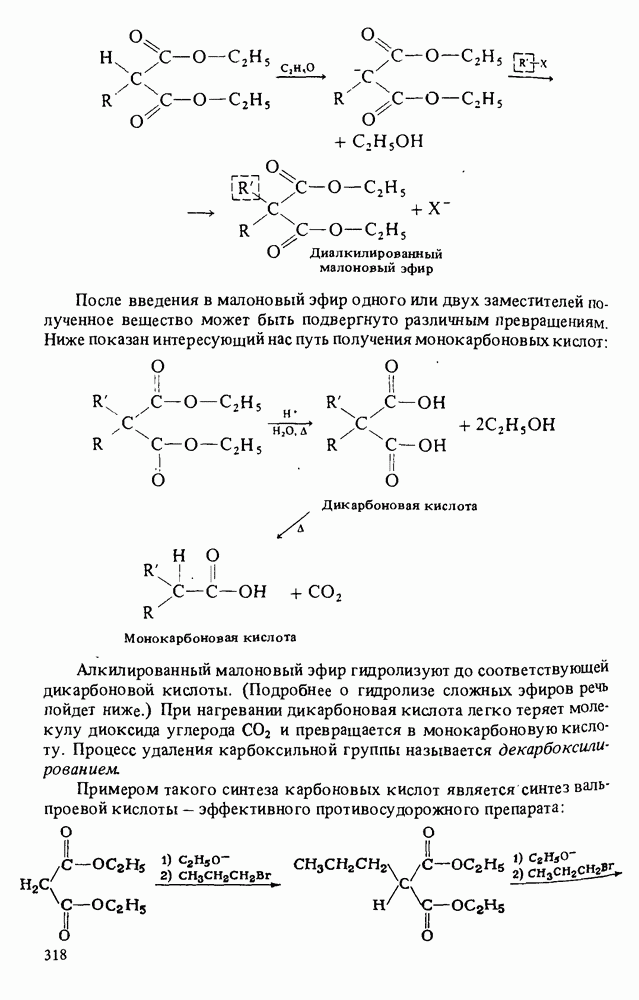
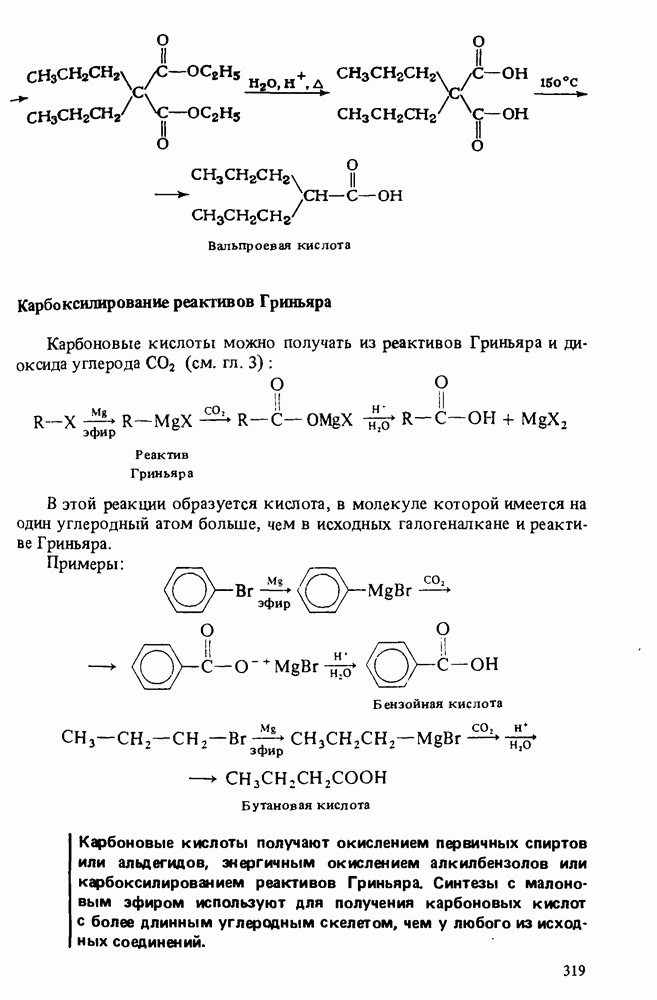
- ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ
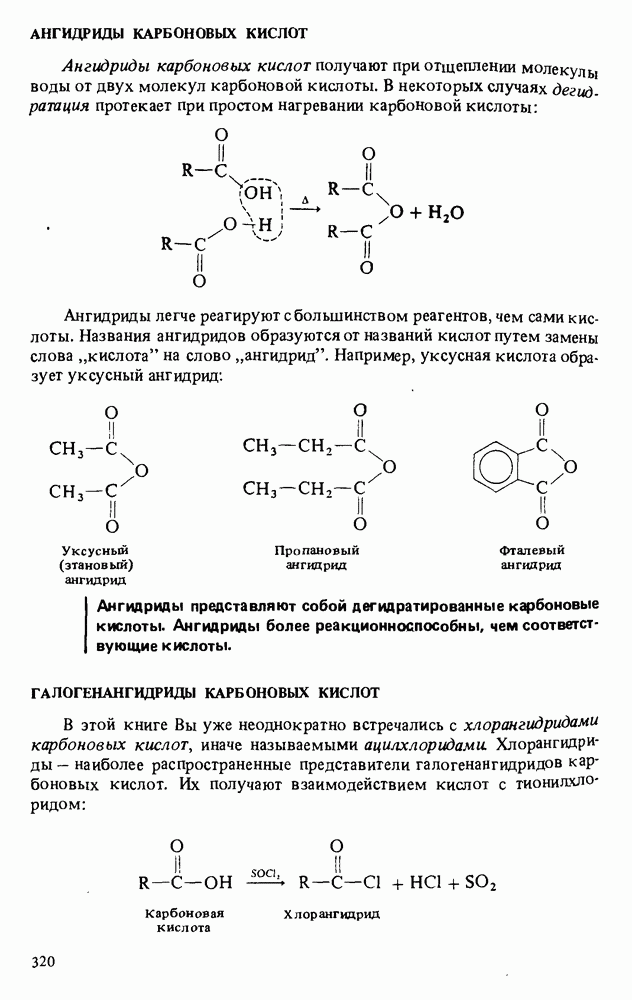
- АНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
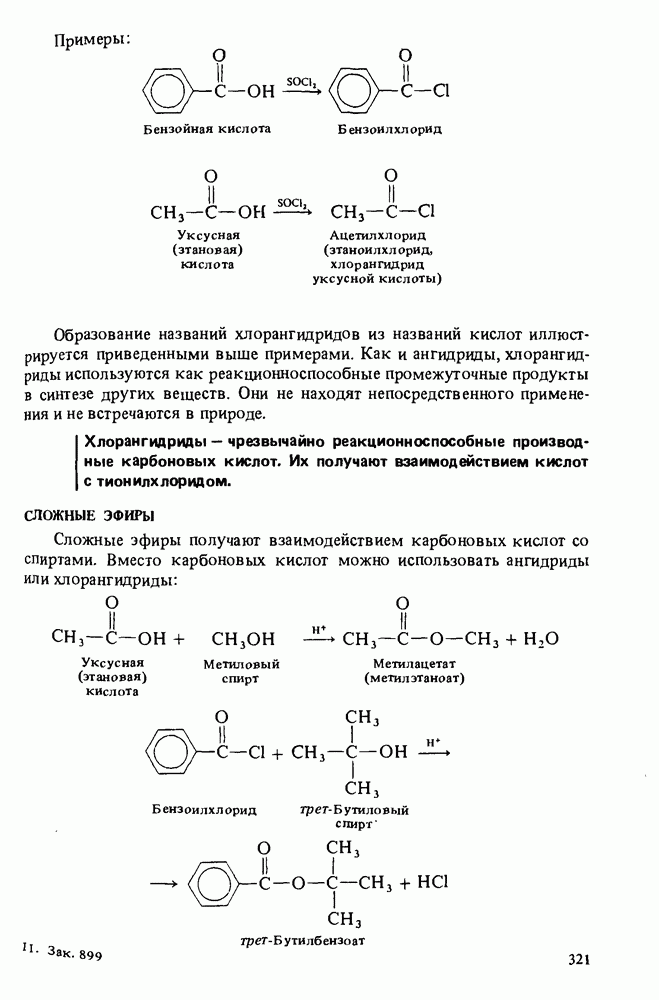
- ГАЛОГЕНАНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
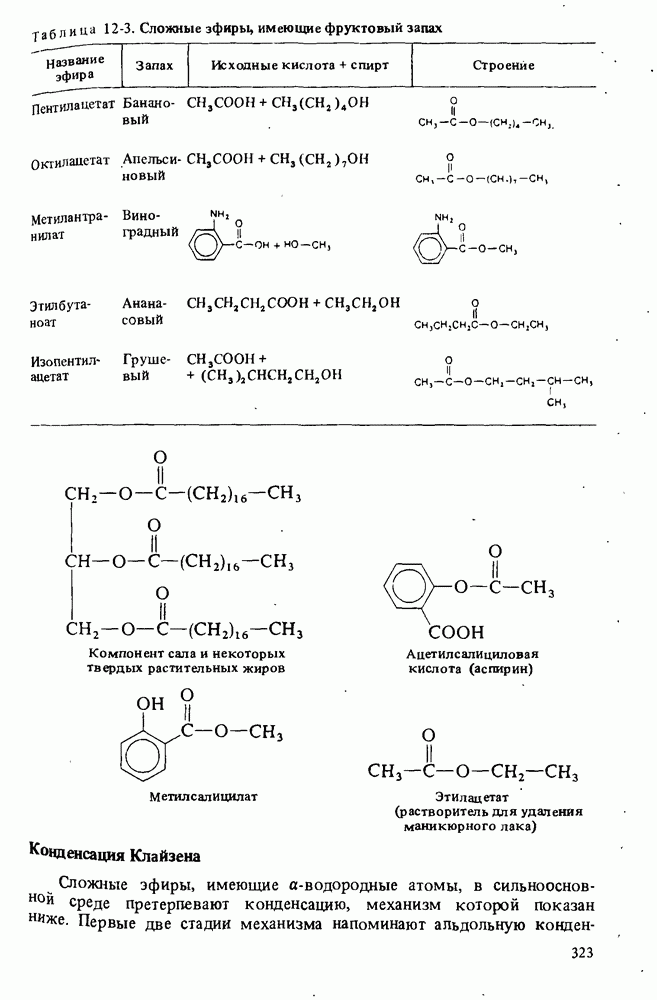
- СЛОЖНЫЕ ЭФИРЫ
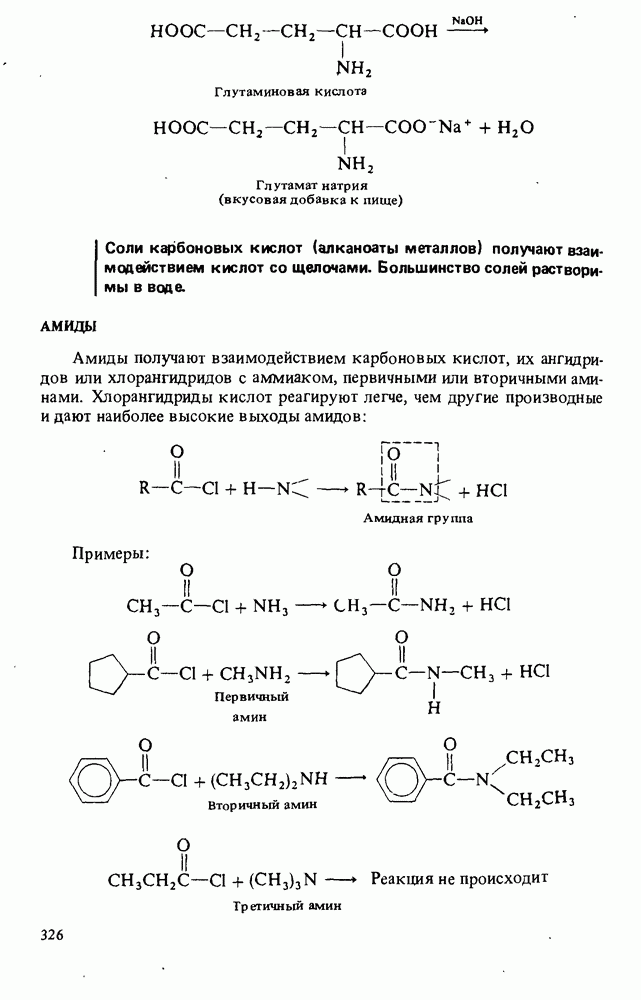
- СОЛИ
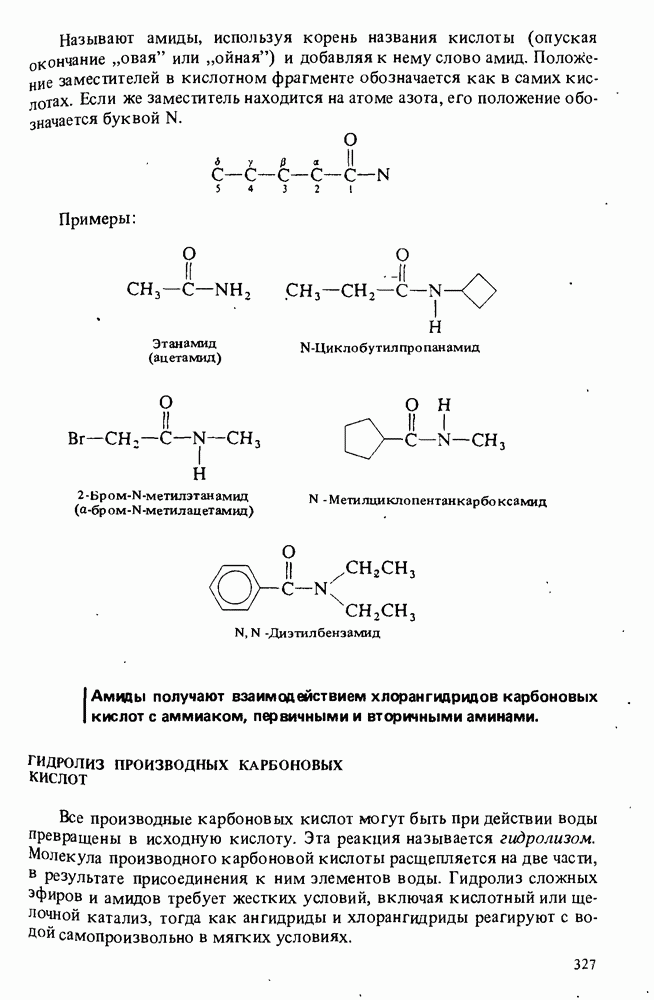
- АМИДЫ
- ГИДРОЛИЗ ПРОИЗВОДНЫХ КАРБОНОВЫХ КИСЛОТ
- СИНТЕТИЧЕСКИЕ ВОЛОКНА
- МОЮЩИЕ СРЕДСТВА
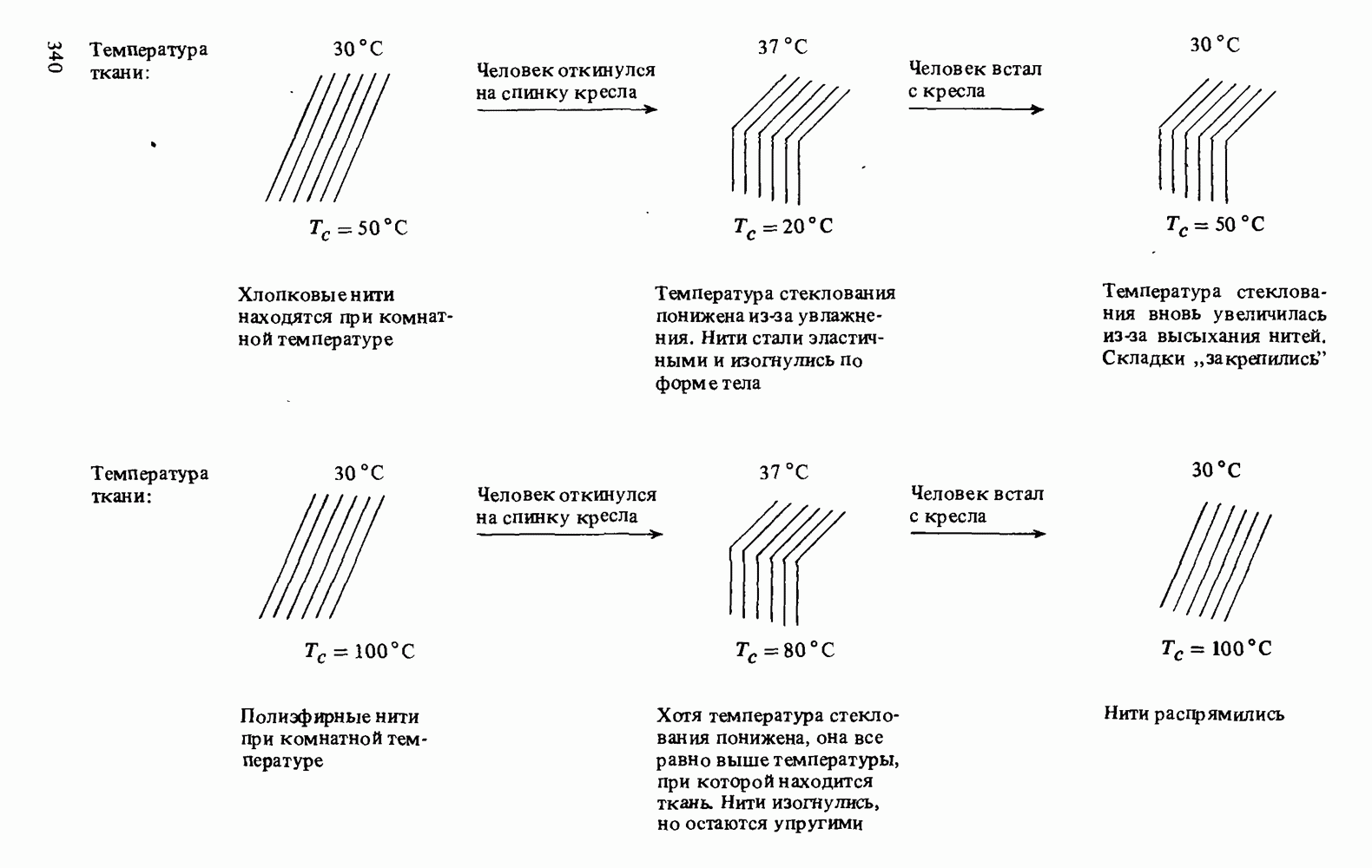
- Прикладная органическая химия: СВОЙСТВА ВОЛОКОН
- Глава 13. АМИНЫ
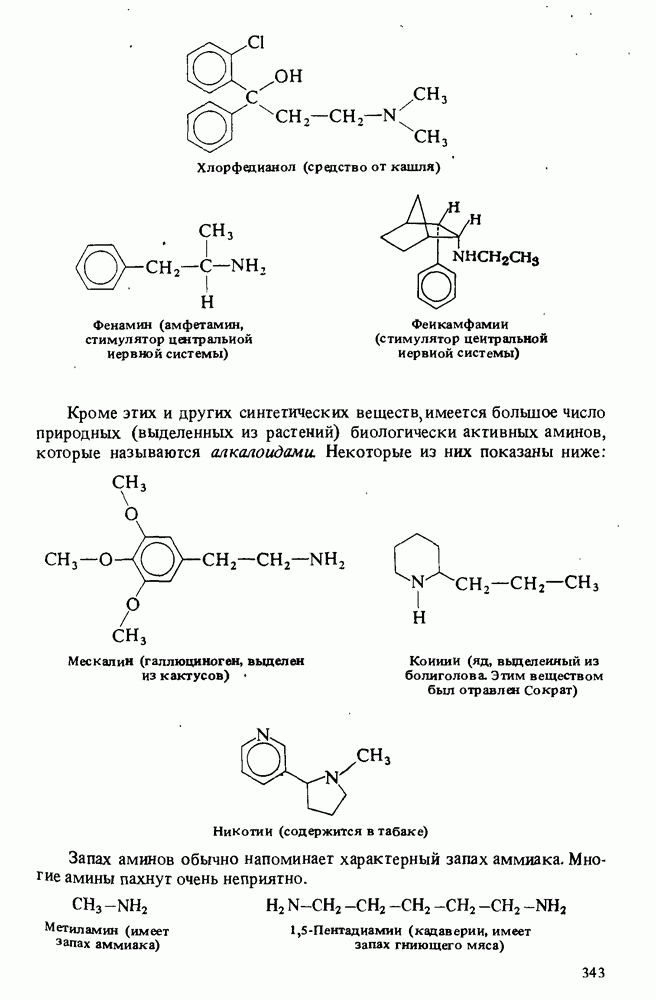
- БИОЛОГИЧЕСКИ АКТИВНЫЕ АМИНЫ
- ОСНОВНОСТЬ АМИНОВ
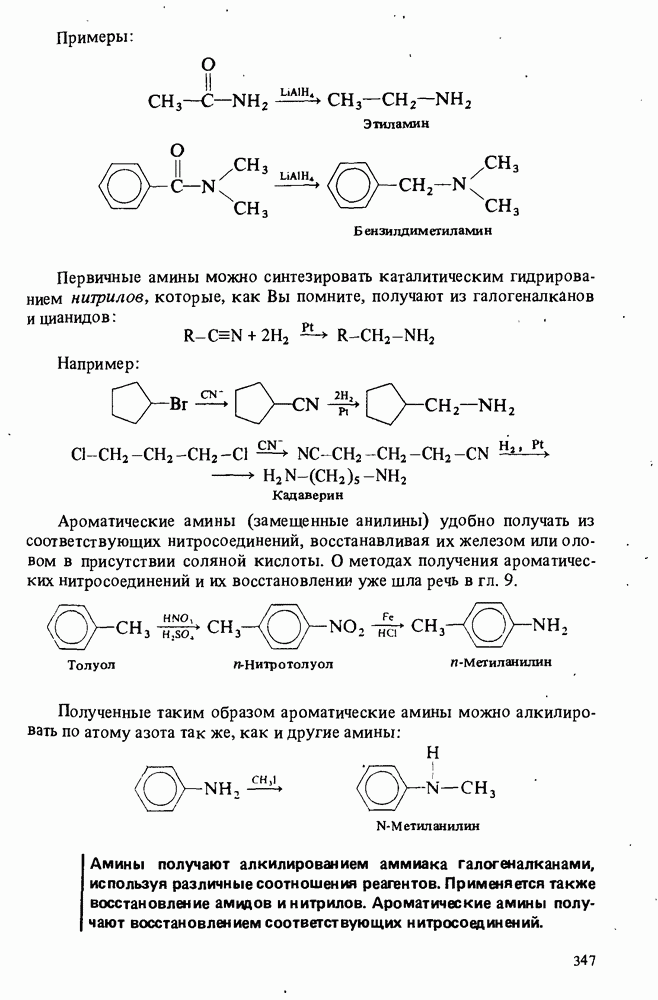
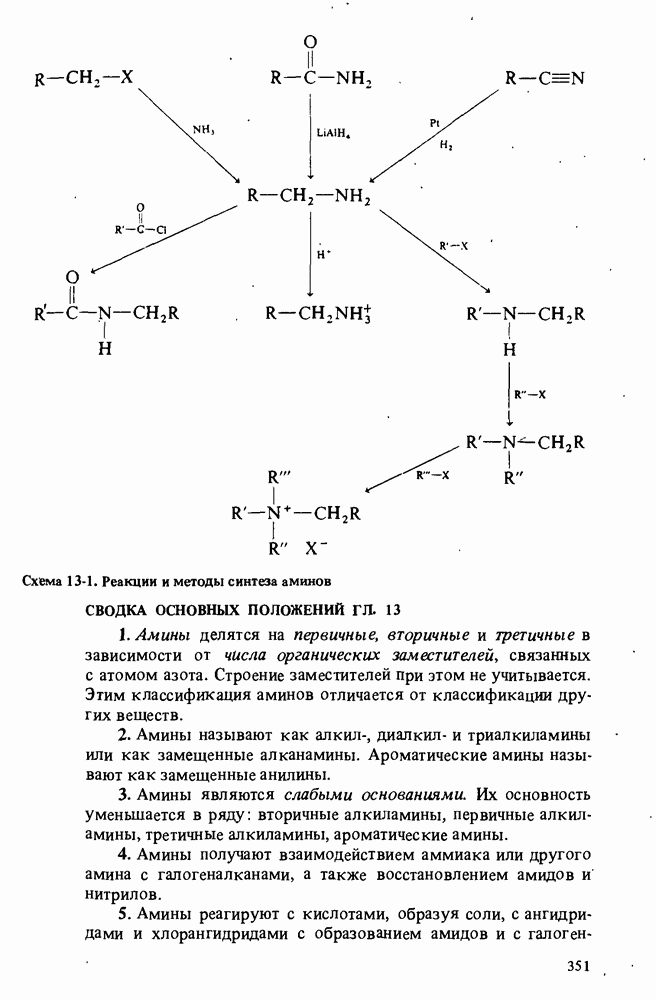
- ПОЛУЧЕНИЕ АМИНОВ
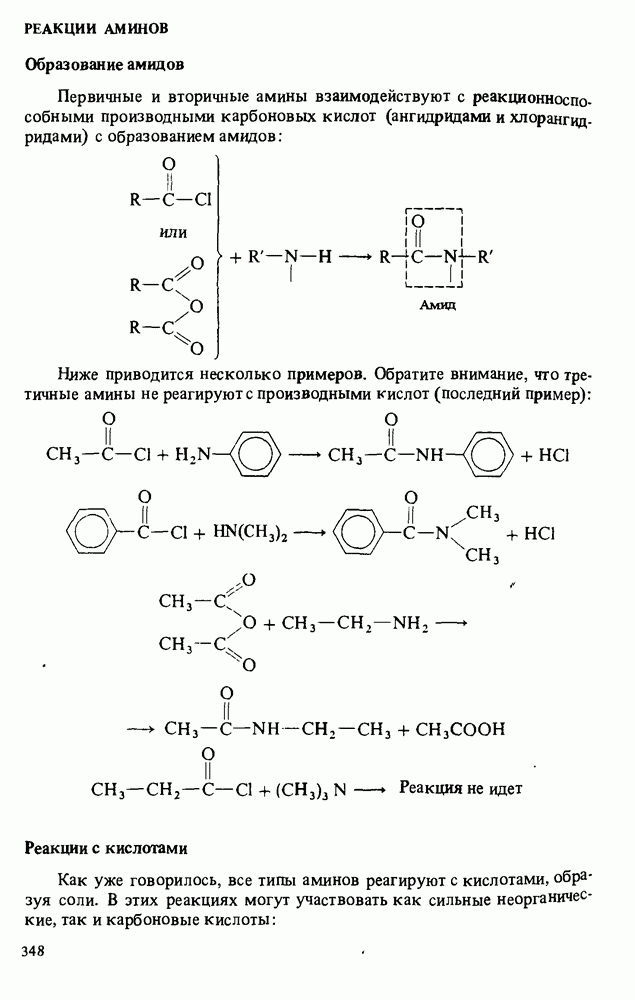
- РЕАКЦИИ АМИНОВ
- Прикладная органическая химия: ПОЛИМЕРЫ, ПОДВЕРГАЮЩИЕСЯ БИОЛОГИЧЕСКОЙ ДЕСТРУКЦИИ
- Глава 14. УГЛЕВОДЫ
- МОНОСАХАРИДЫ
- РЕАКЦИИ МОНОСАХАРИДОВ
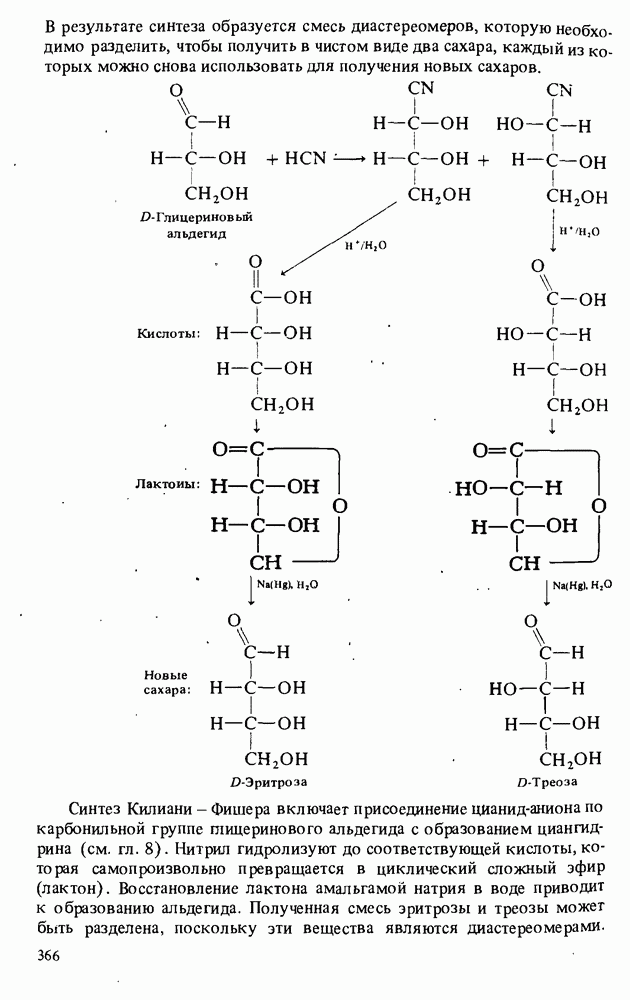
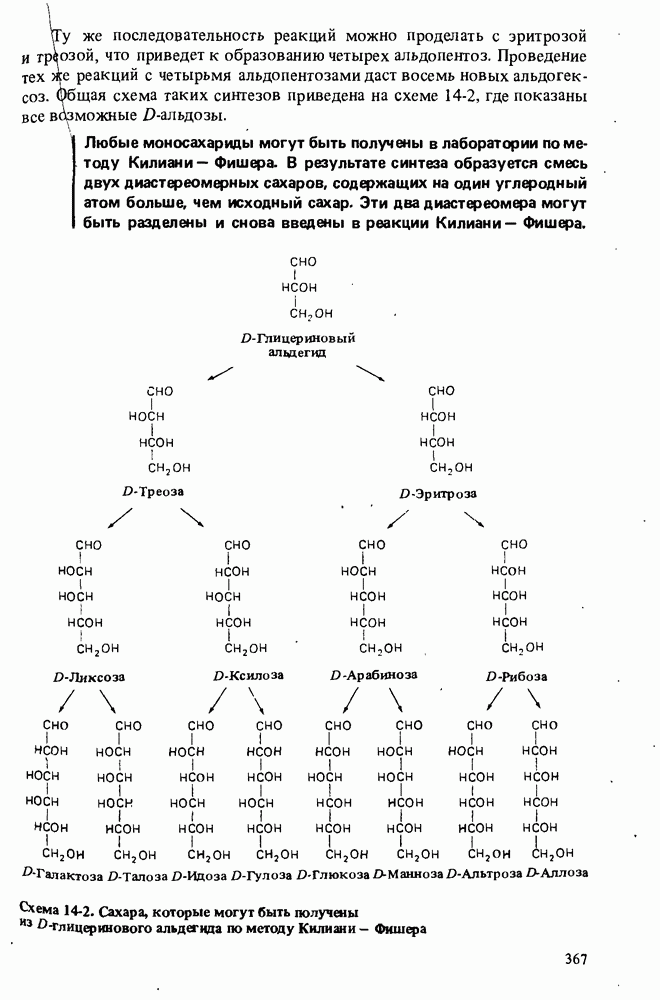
- СИНТЕЗЫ САХАРОВ
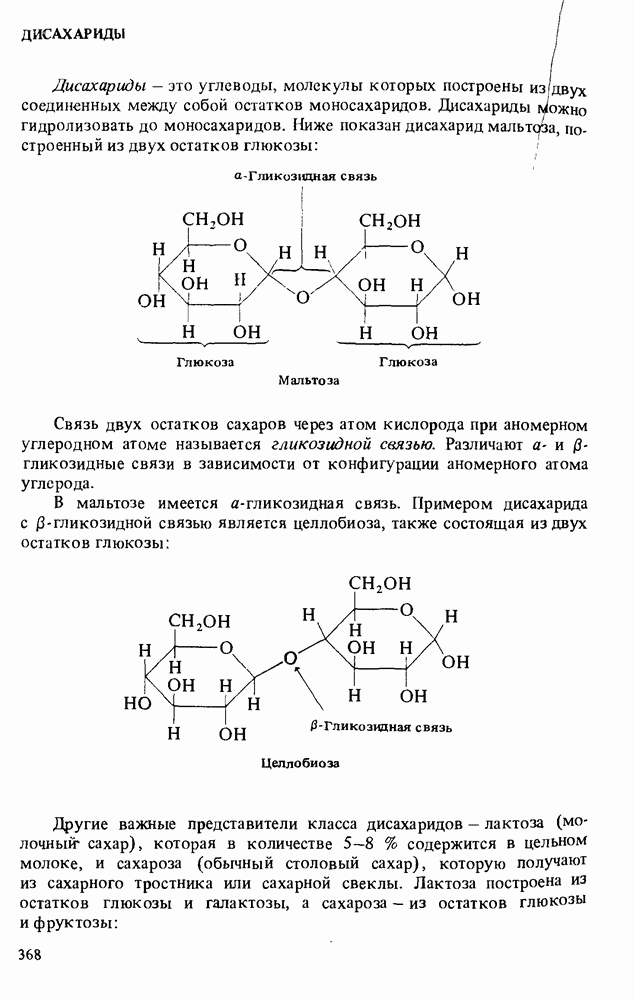
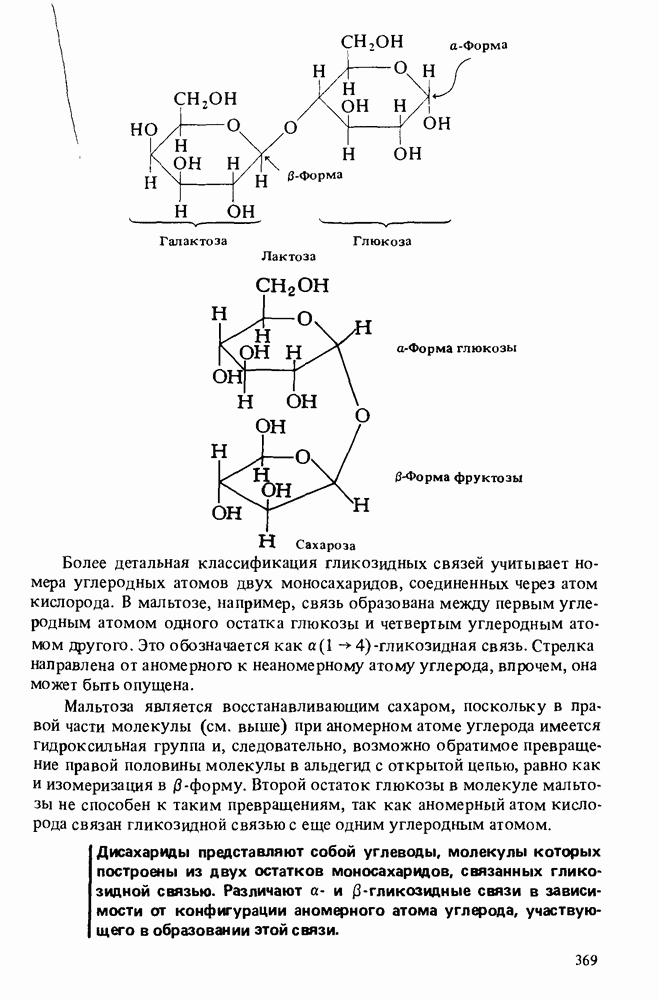
- ДИСАХАРИДЫ
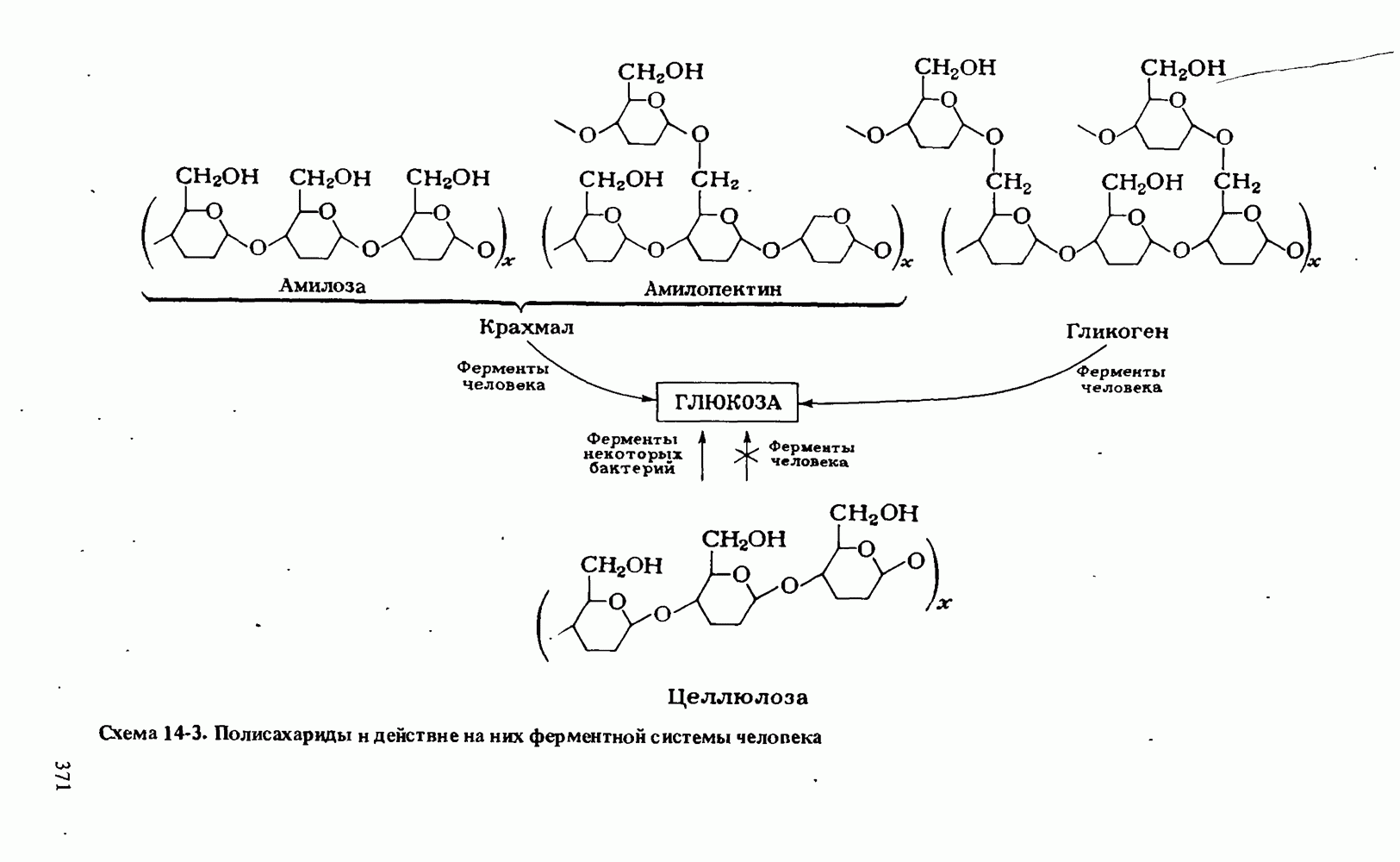
- ПОЛИСАХАРИДЫ
- Прикладная органическая химия: ПИЩЕВЫЕ СВОЙСТВА УГЛЕВОДОВ
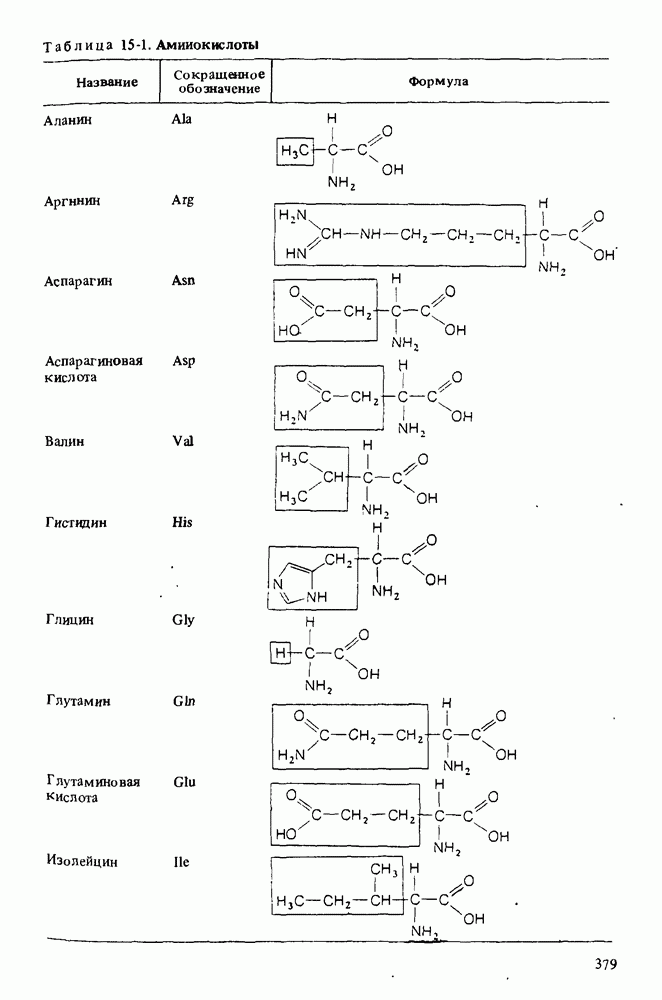
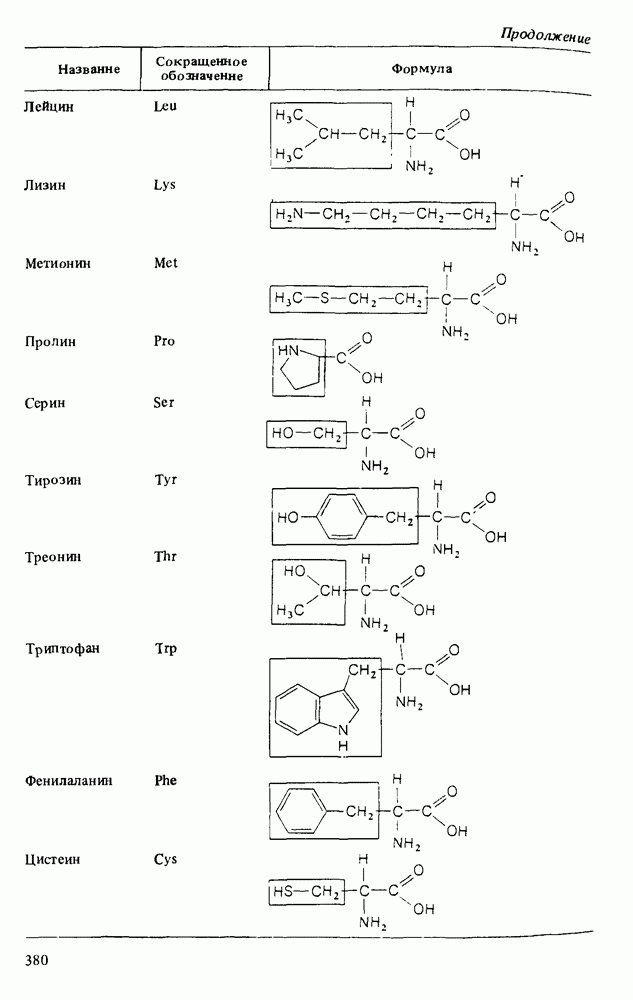
- Глава 15. АМИНОКИСЛОТЫ И БЕЛКИ
- КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА АМИНОКИСЛОТ
- АНАЛИЗ АМИНОКИСЛОТ
- СТРОЕНИЕ БЕЛКОВ
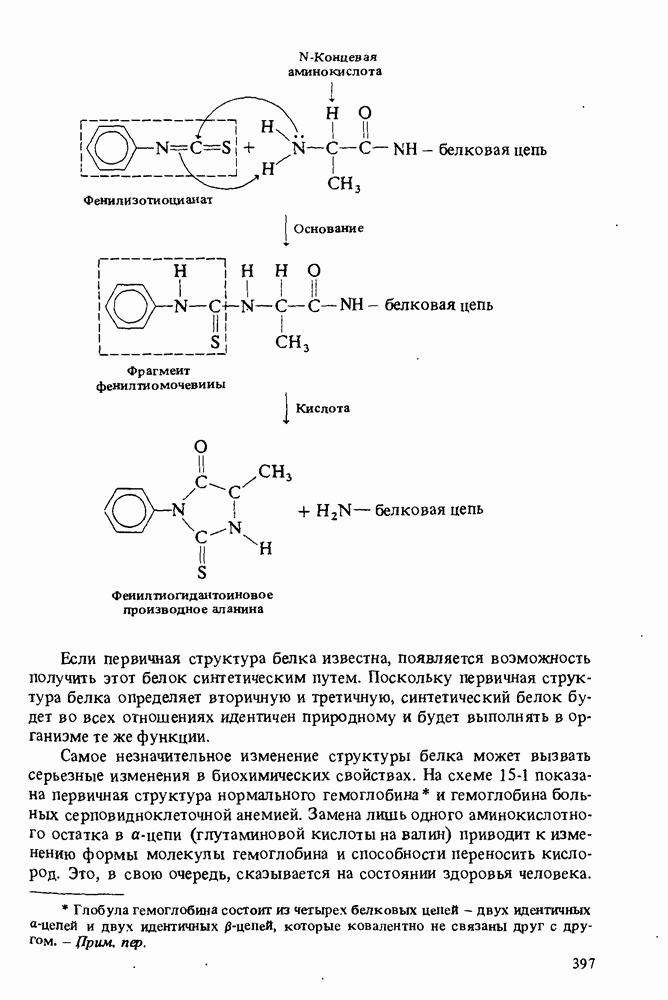
- УСТАНОВЛЕНИЕ ПЕРВИЧНОЙ СТРУКТУРЫ БЕЛКОВ
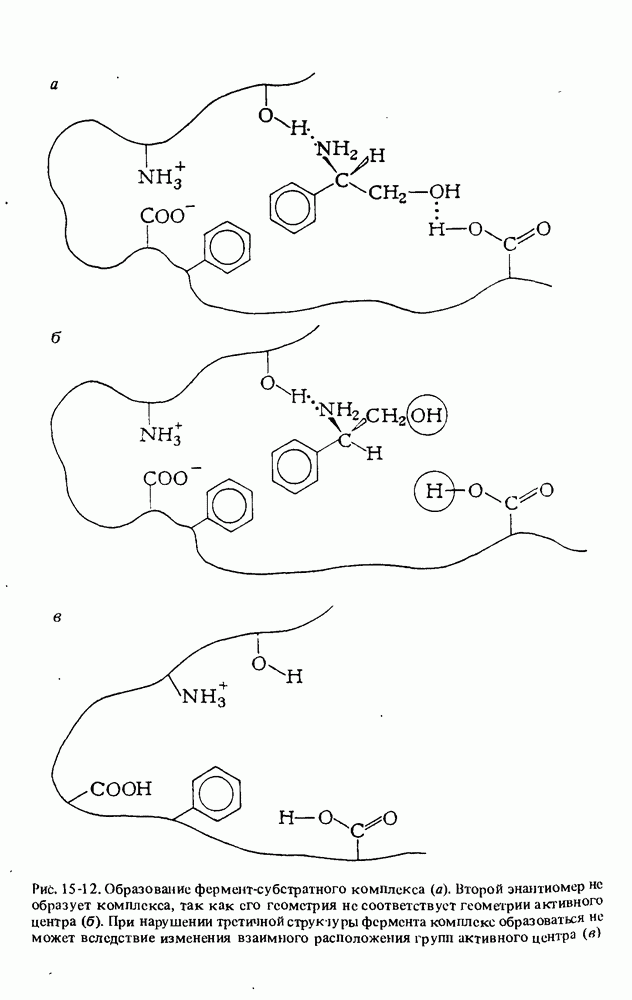
- ФЕРМЕНТЫ
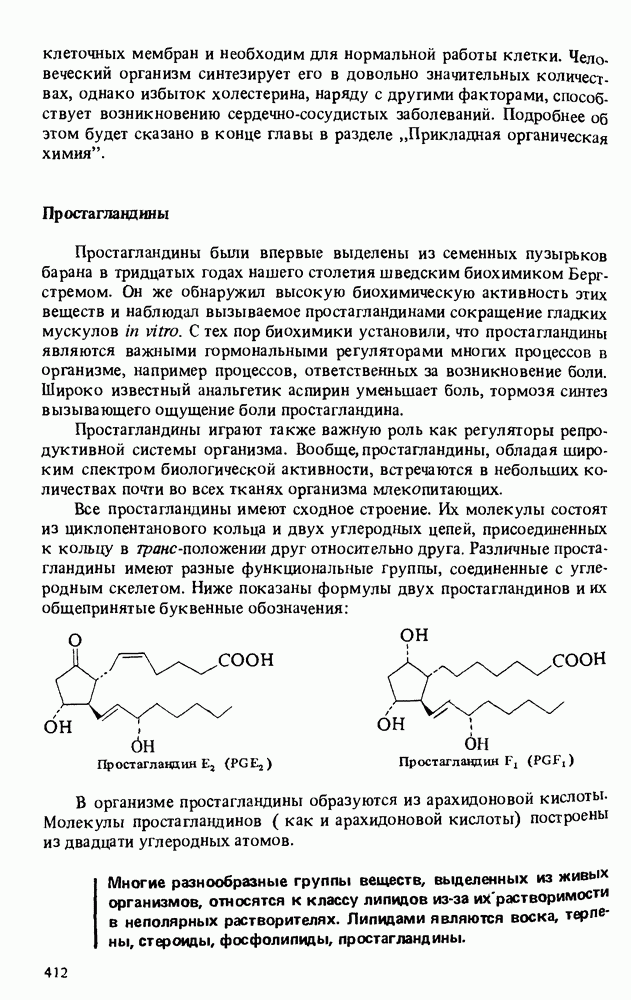
- Глава 16. ЛИПИДЫ
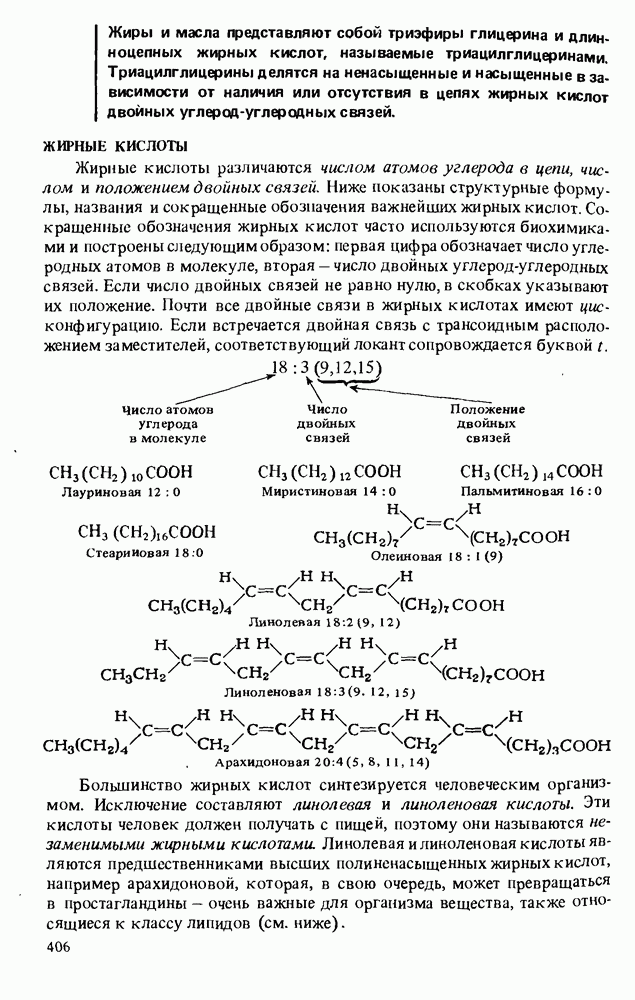
- ЖИРНЫЕ КИСЛОТЫ
- НАЗВАНИЯ ТРИАЦИЛГЛИЦЕРИНОВ
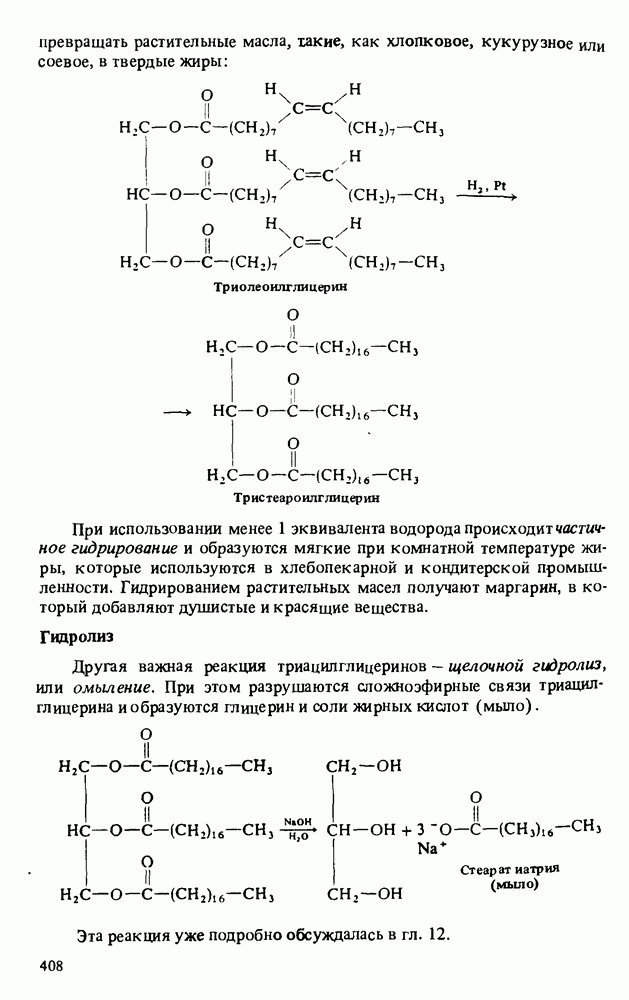
- РЕАКЦИИ ТРИАЦИЛГЛИЦЕРИНОВ
- ЛИПИДЫ, ОТЛИЧНЫЕ ОТ ТРИАЦИЛГЛИЦЕРИНОВ
- Прикладная органическая химия: ПИЩЕВЫЕ СВОЙСТВА ЛИПИДОВ
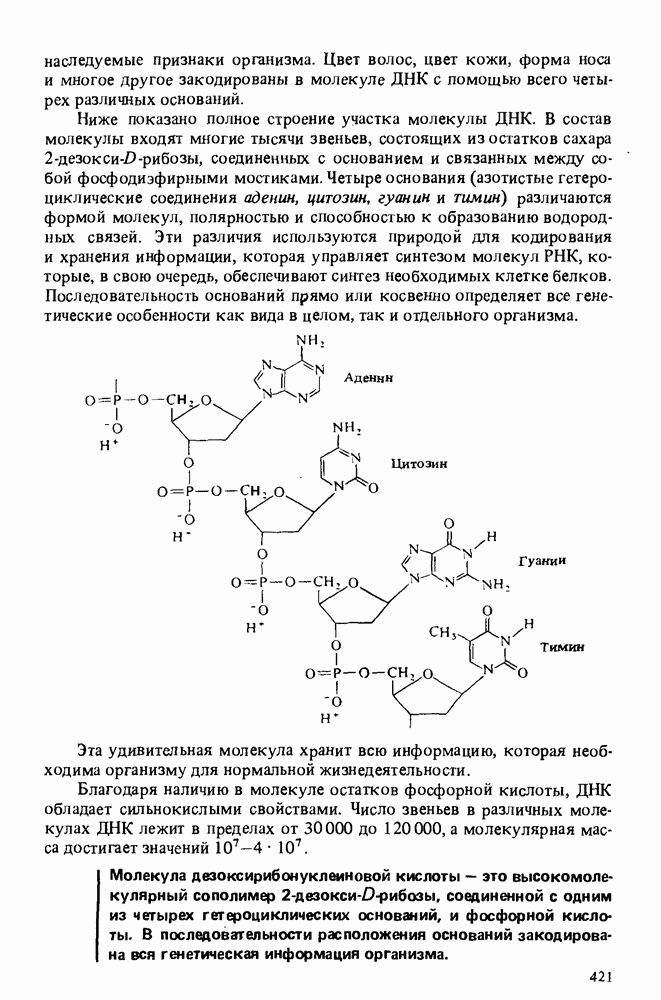
- Глава 17. НУКЛЕИНОВЫЕ КИСЛОТЫ
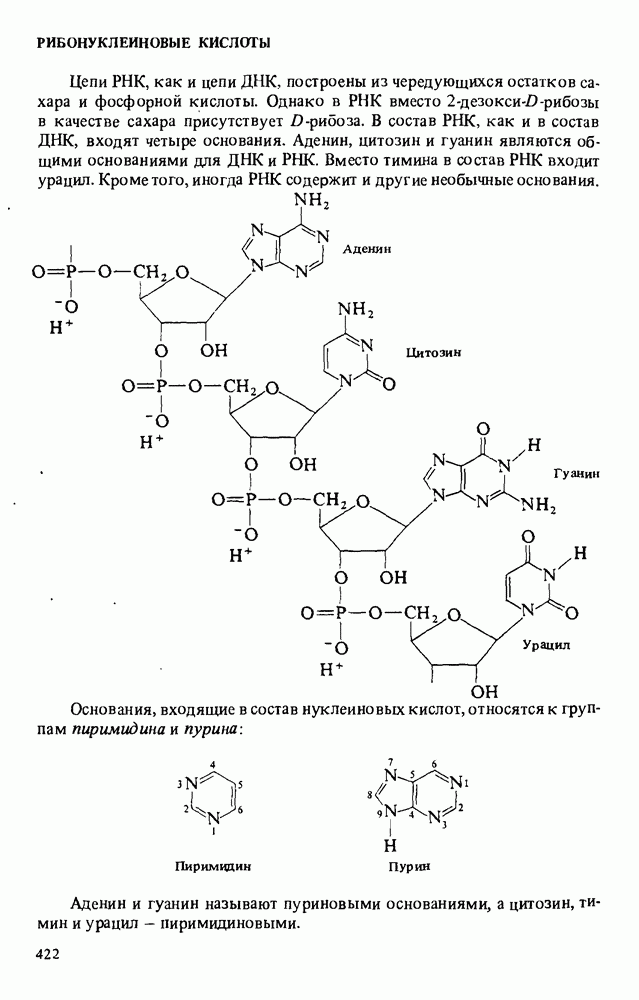
- РИБОНУКЛЕИНОВЫЕ КИСЛОТЫ
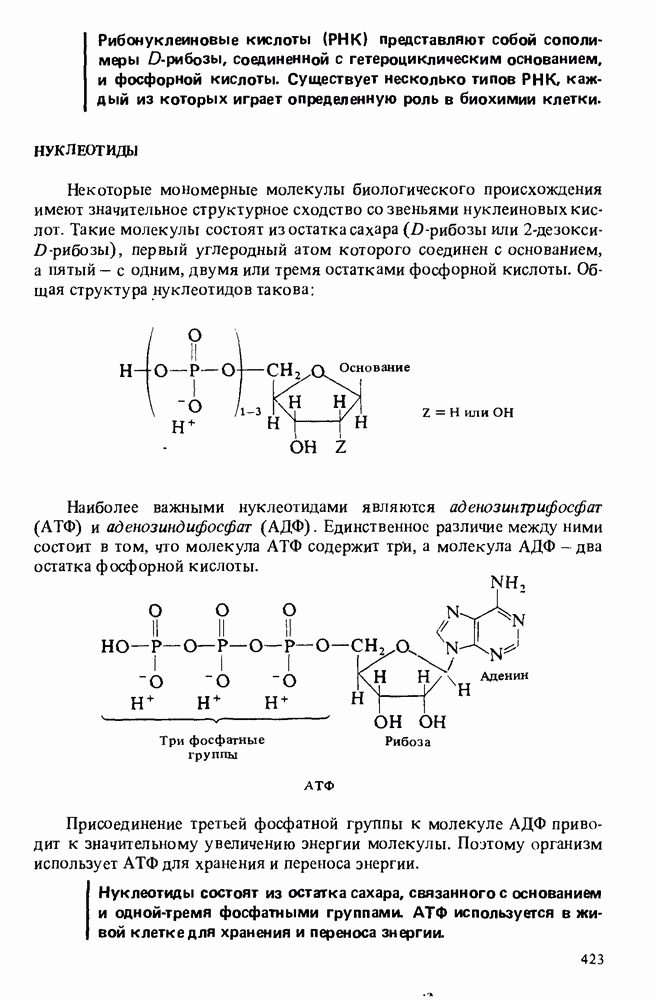
- НУКЛЕОТИДЫ
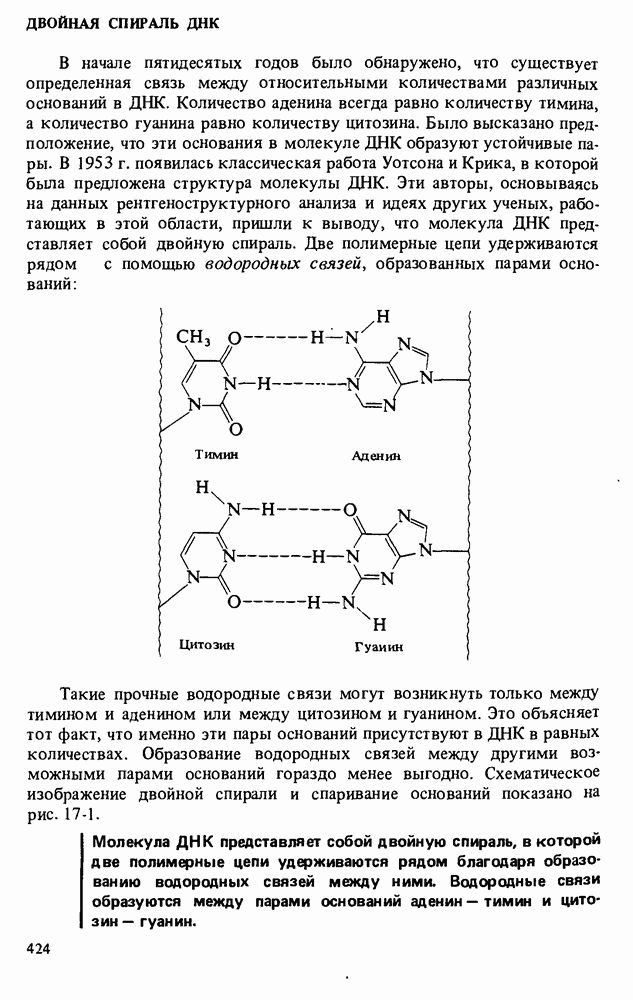
- ДВОЙНАЯ СПИРАЛЬ ДНК
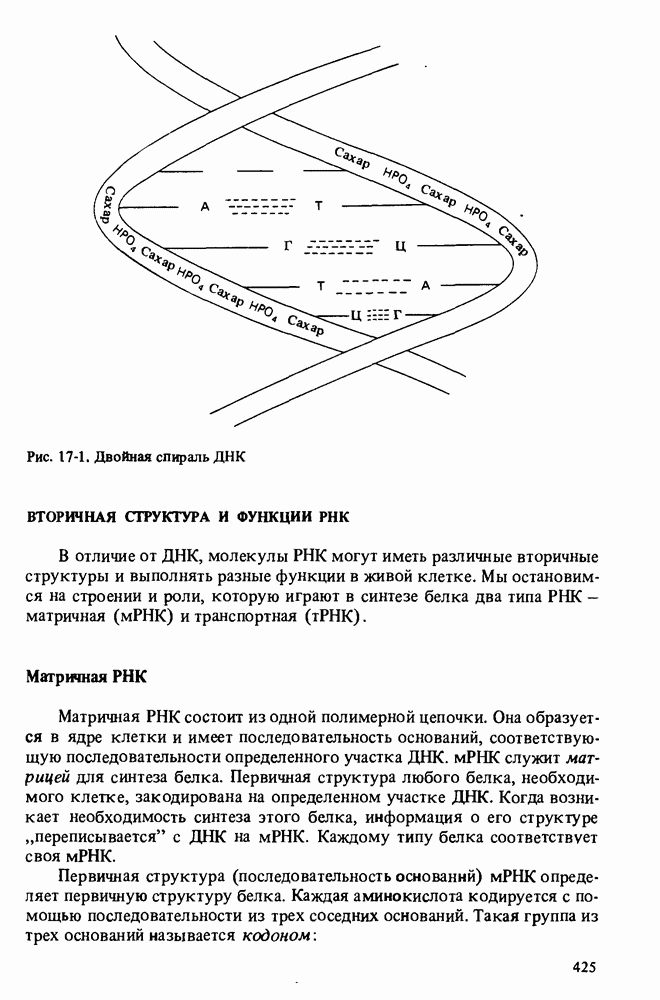
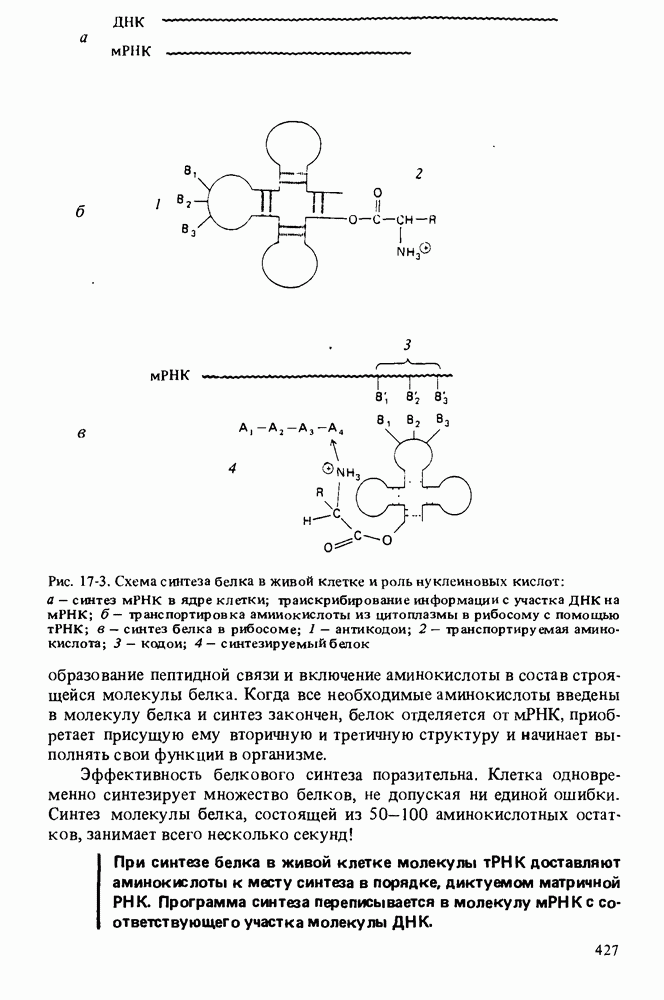
- ВТОРИЧНАЯ СТРУКТУРА И ФУНКЦИИ РНК
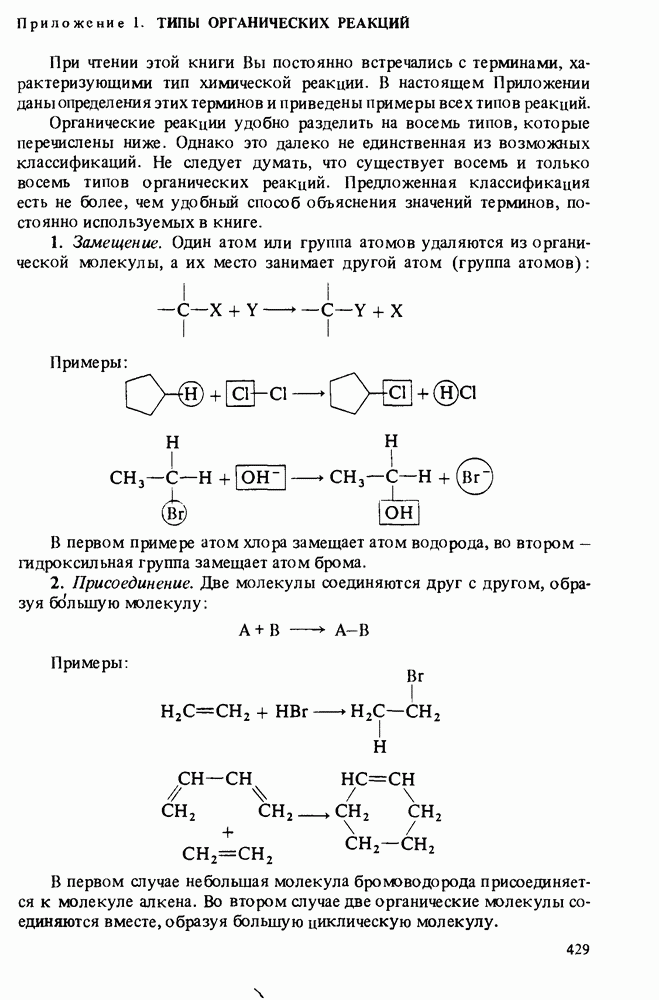
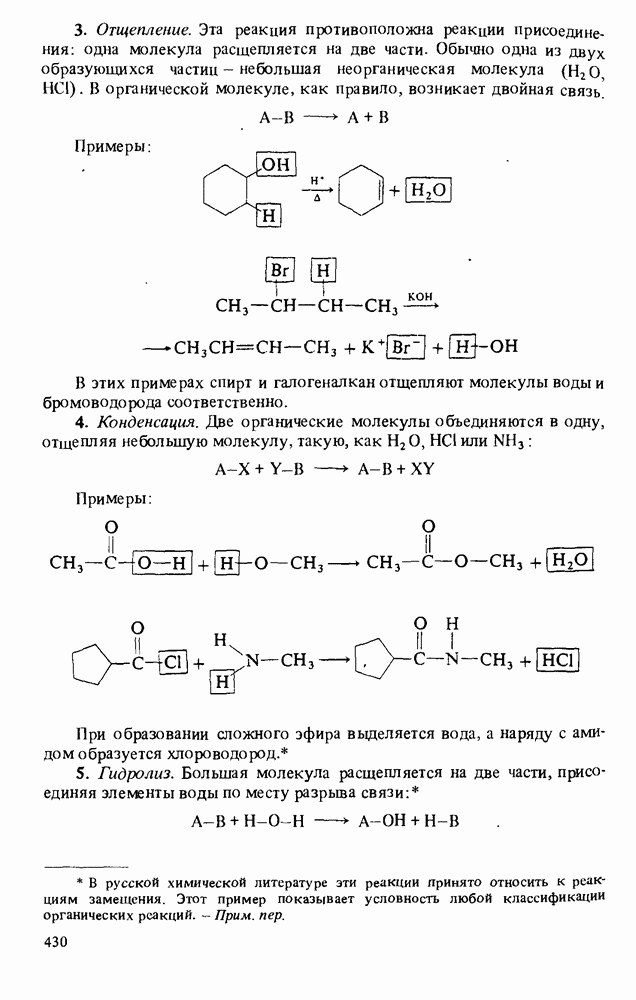
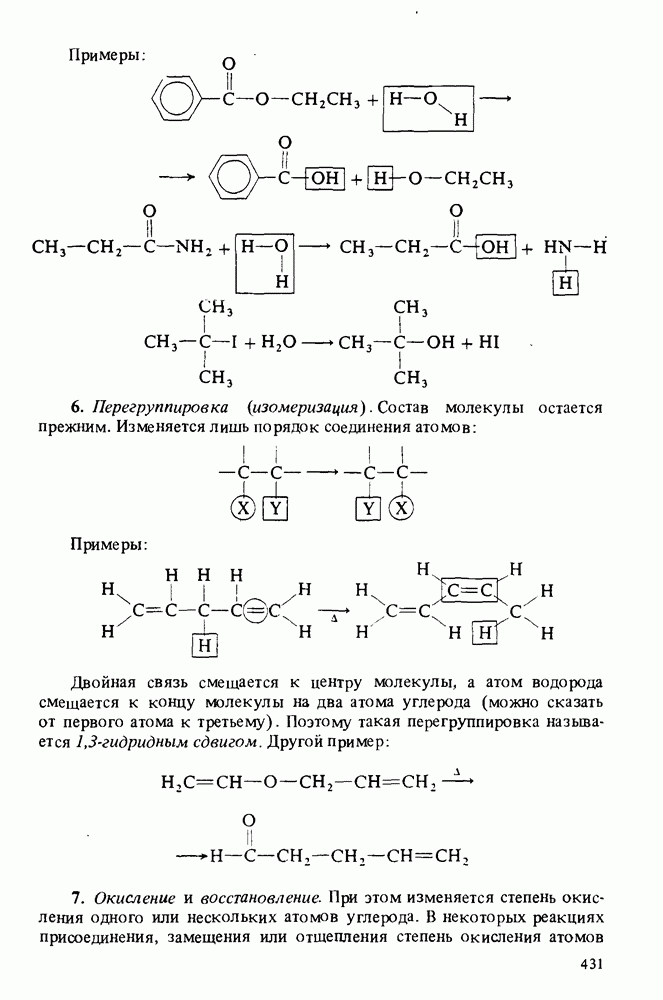
- Приложение 1. ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ
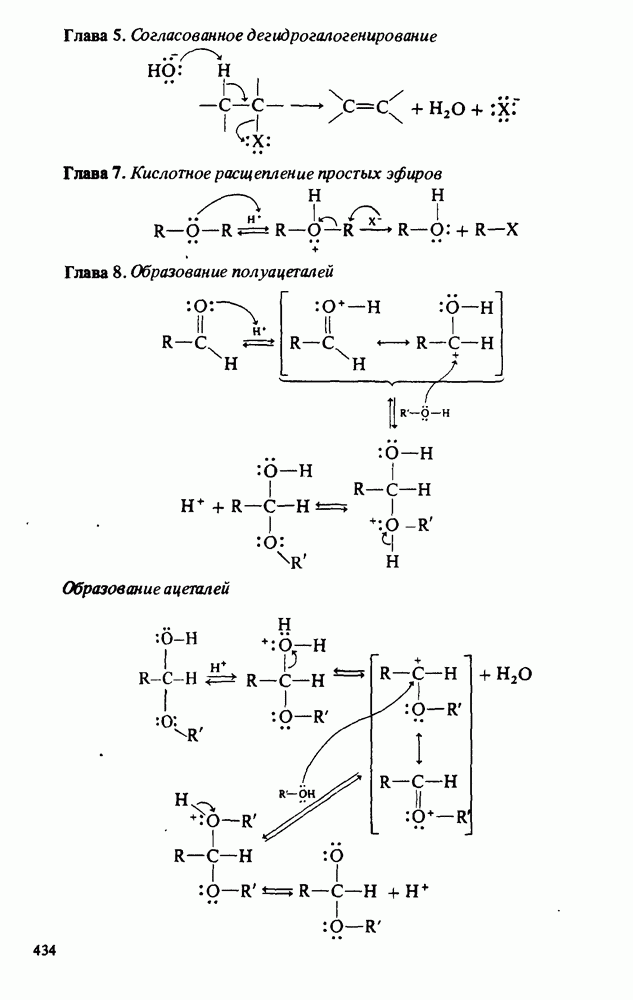
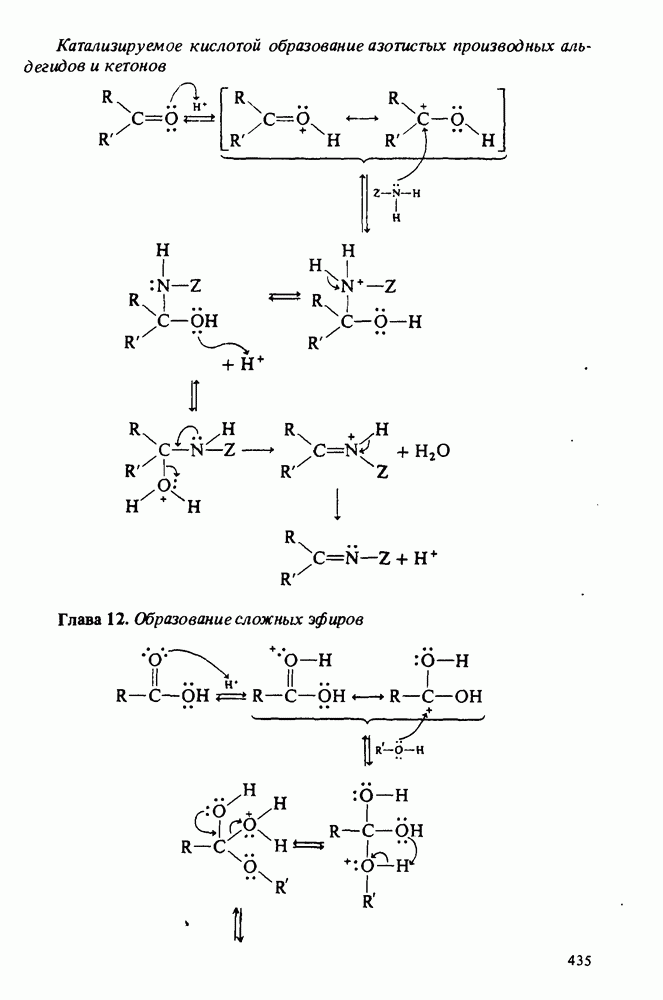
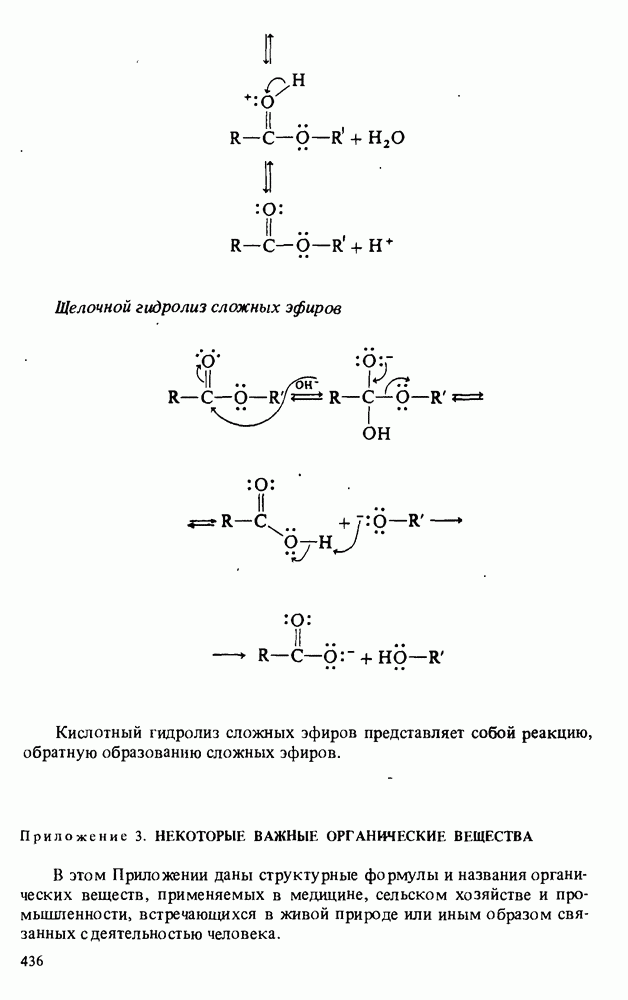
- Приложение 2. МЕХАНИЗМЫ НЕКОТОРЫХ РЕАКЦИЙ
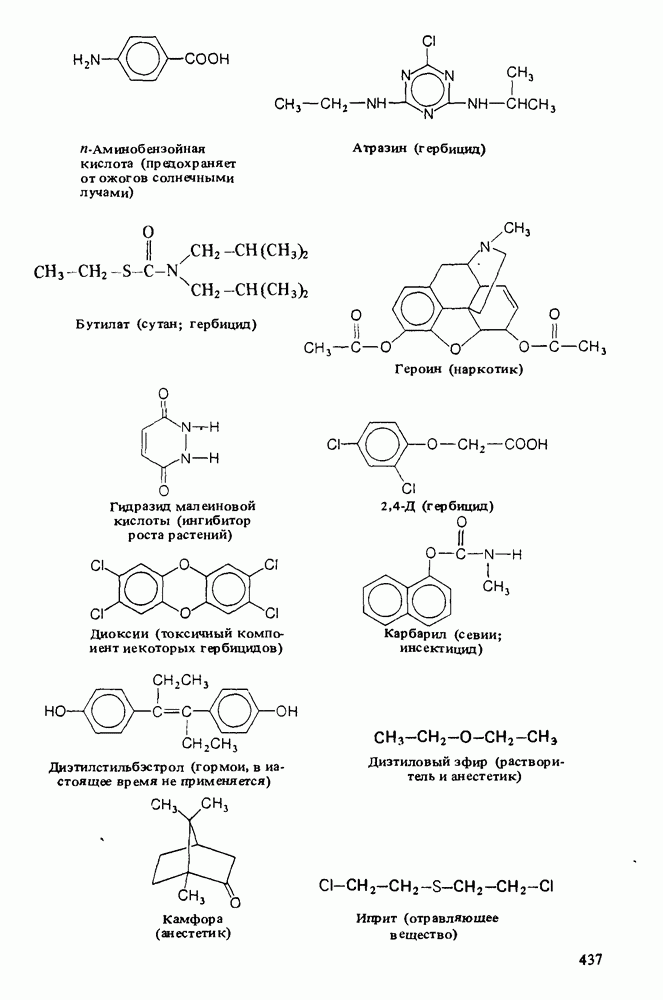
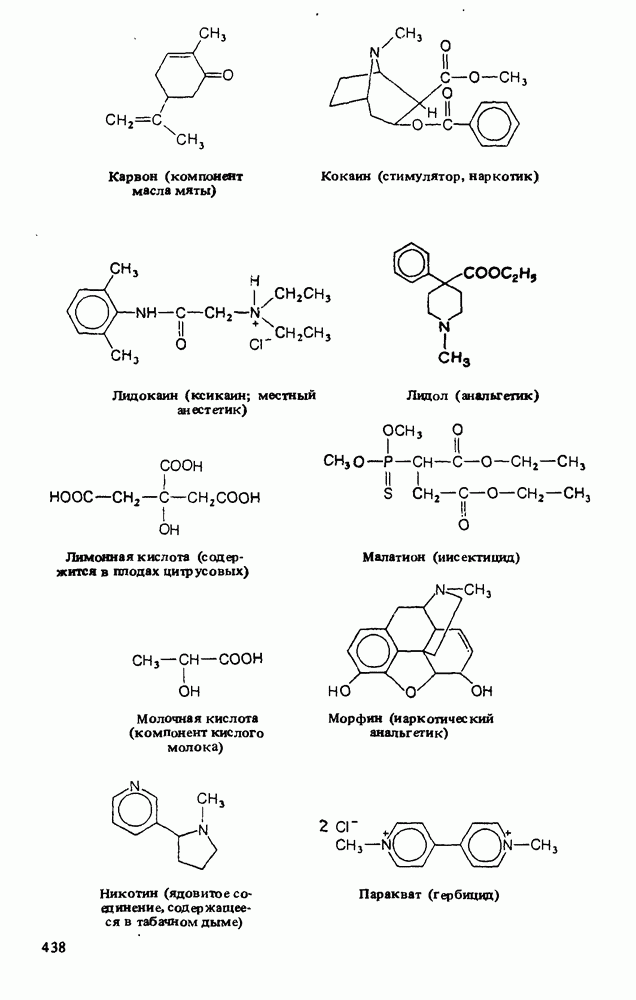
- Приложение 3. НЕКОТОРЫЕ ВАЖНЫЕ ОРГАНИЧЕСКИЕ ВЕЩЕСТВА