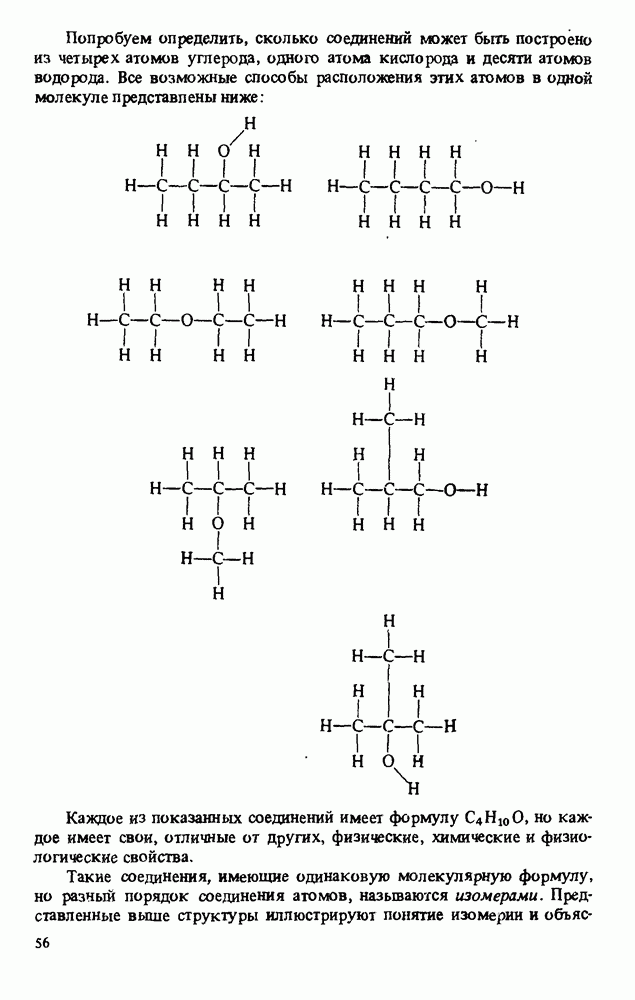| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
АНАЛИЗ АМИНОКИСЛОТ
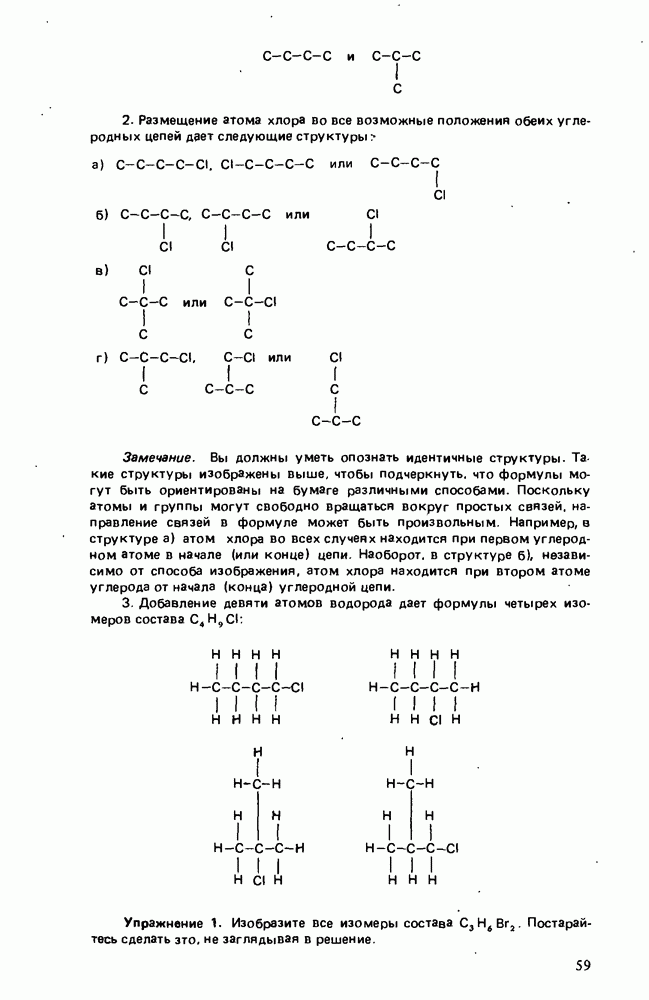
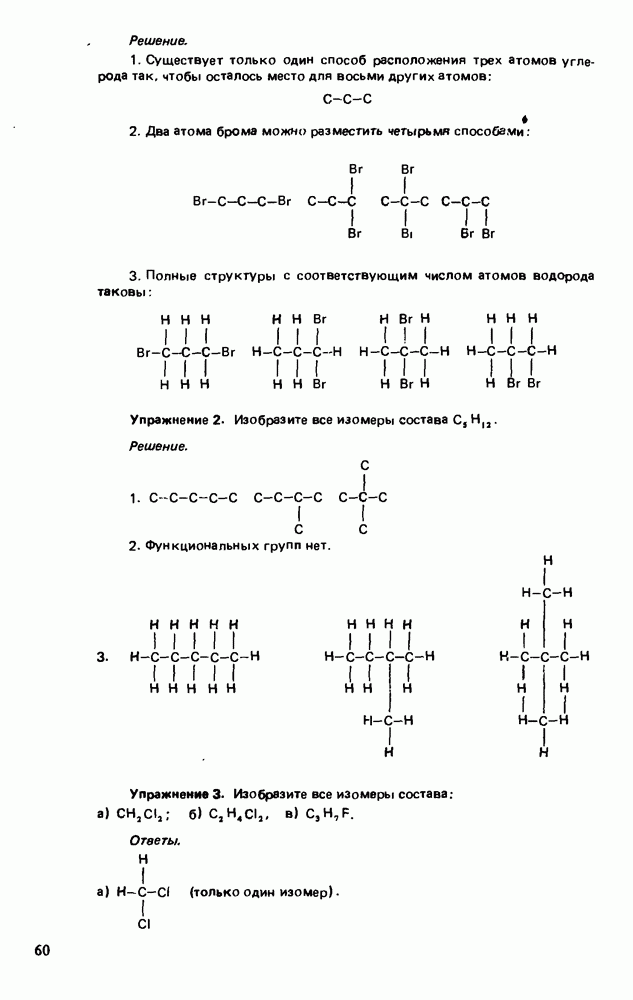
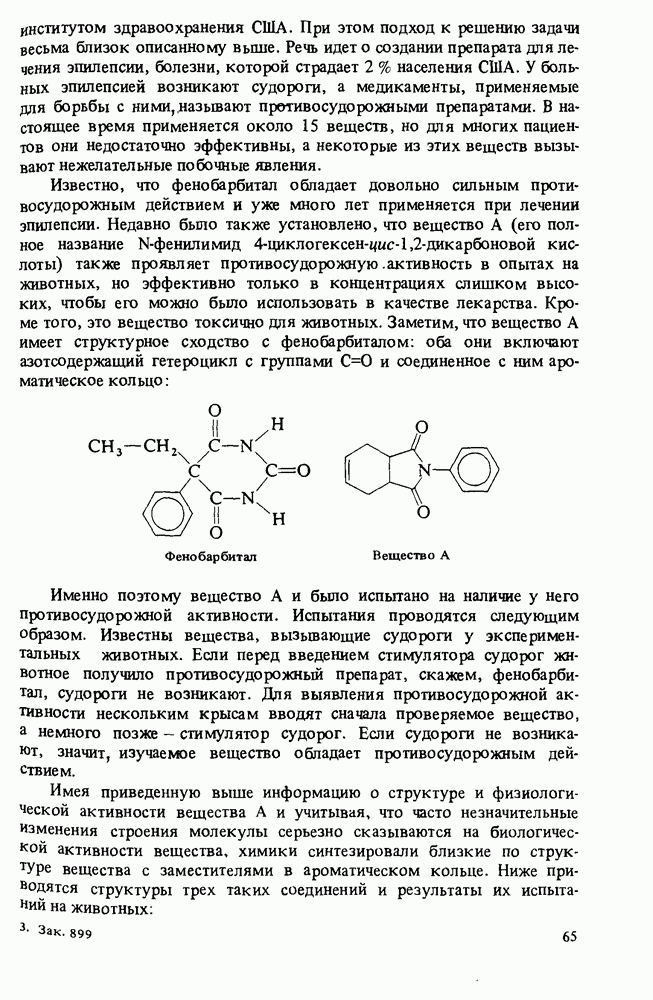
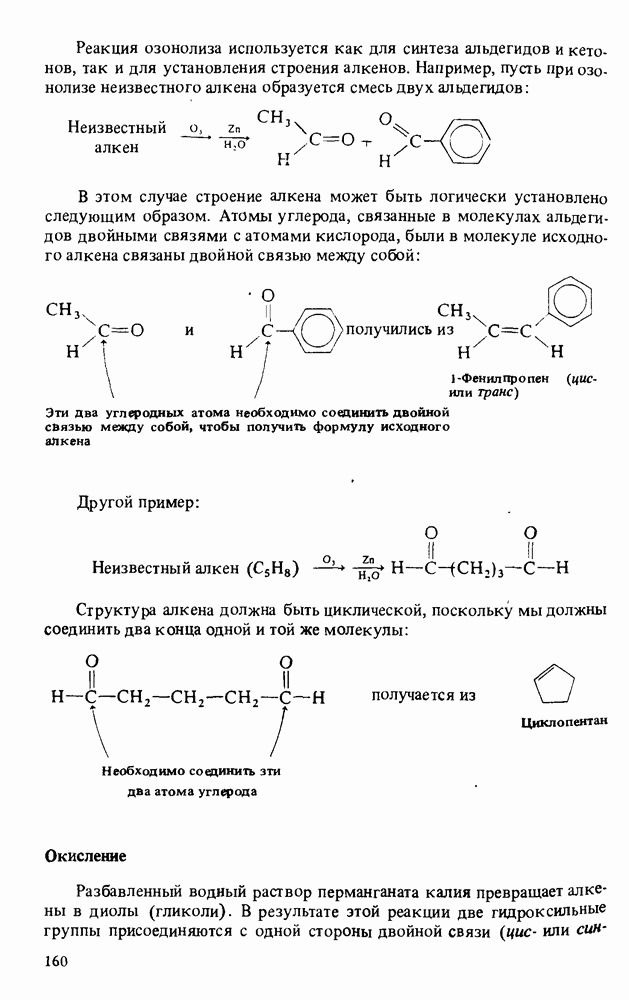
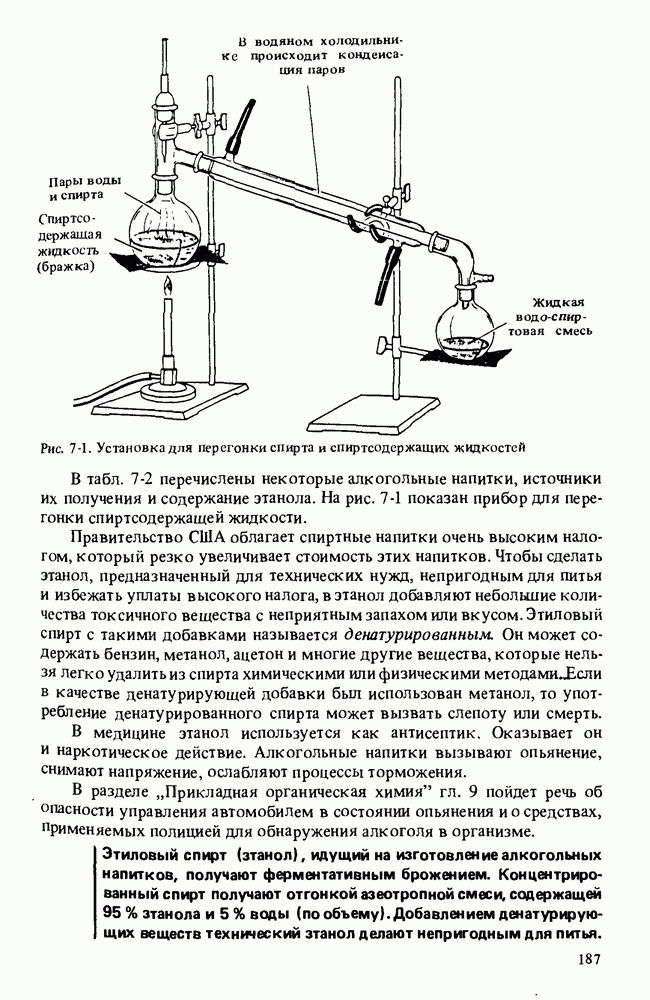
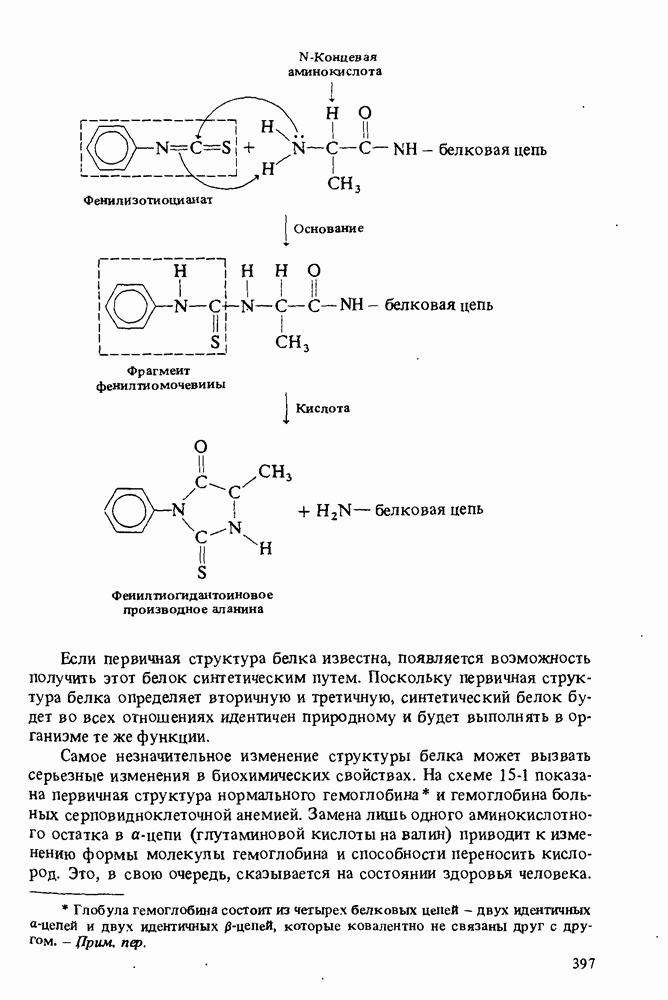
Один из способов определения структуры белка включает его гидролиз, а затем качественный и количественный анализ образовавшейся при этом смеси аминокислот. Ниже обсуждается несколько методов такого анализа.
Тонкослойная хроматография
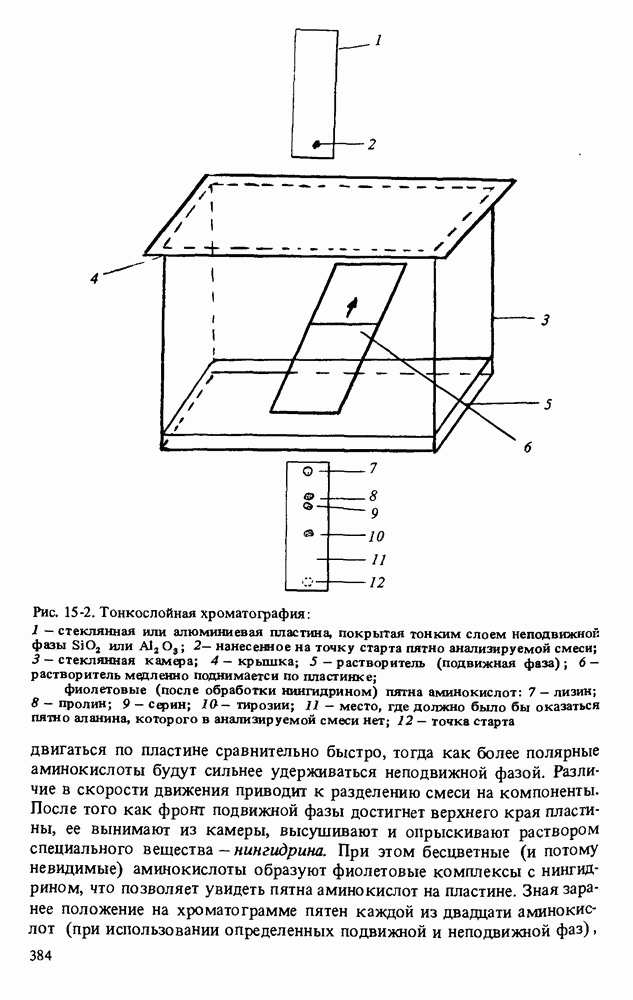
Смесь известных аминокислот наносится в виде пятна на стеклянную пластину, покрытую тонким слоем оксида кремния или оксида алюминия (рис. 15-2). В качестве пластины можно также использовать специальную бумагу без всякого покрытия. Пластину помещают в стеклянную камеру, на дно которой налито небольшое количество растворителя. Благодаря действию капиллярных сил растворитель начинает постепенно подниматься по пластине, увлекая за собой компоненты нанесенной на пластину смеси. Различные вещества движутся по пластине с различными скоростями. Относительная скорость движения компонентов смеси определяется относительной полярностью вещества, покрывающего пластину (неподвижной фазы), и растворителя (подвижной фазы). Например, если подвижная фаза малополярна, то менее полярные аминокислоты будут
Рис. 15-2. (см. скан) Тонкослойная хроматография: 1 — стеклянная или алюминиевая пластина, покрытая тонким слоем неподвижной фазы  или
или  нанесенное на точку старта пятно анализируемой смеси; 3 - стеклянная камера; 4 - крышка; 5 - растворитель (подвижная фаза)
нанесенное на точку старта пятно анализируемой смеси; 3 - стеклянная камера; 4 - крышка; 5 - растворитель (подвижная фаза)  растворитель медленно поднимаете и по пластинке; фиолетовые (после обработки нингидрином) пятна аминокислот: 7 - лизин; 8 - пролин; 9 - серин; 10 - тирозии; 11 - место, где должно было бы оказаться пятно аланина, которого в анализируемой смеси нет; 12 — точка старта
растворитель медленно поднимаете и по пластинке; фиолетовые (после обработки нингидрином) пятна аминокислот: 7 - лизин; 8 - пролин; 9 - серин; 10 - тирозии; 11 - место, где должно было бы оказаться пятно аланина, которого в анализируемой смеси нет; 12 — точка старта
двигаться по пластине сравнительно быстро, тогда как более полярные аминокислоты будут сильнее удерживаться неподвижной фазой. Различие в скорости движения приводит к разделению смеси на компоненты. После того как фронт подвижной фазы достигнет верхнего края пластины, ее вынимают из камеры, высушивают и опрыскивают раствором специального вещества - нингидрина. При этом бесцветные (и потому невидимые) аминокислоты образуют фиолетовые комплексы с нингидрином, что позволяет увидеть пятна аминокислот на пластине. Зная заранее положение на хроматограмме пятен каждой из двадцати аминокислот (при использовании определенных подвижной и неподвижной фаз),
легко определить, какие именно аминокислоты содержатся в исследуемой смеси. На рис. 15-2 показана хроматограмма смеси тирозина, серина, пролина и лизина.
Тонкослойная хроматография (ТСХ) позволяет провести лишь качественный анализ белков или смесей аминокислот. Очень приблизительно относительное содержание аминокислот в смеси можно оценить по интенсивности окраски пятен. Чем темнее пятно, тем выше содержание аминокислоты в изучаемом образце.
Электрофорез
Еще одним методом определения аминокислот служит электрофорез, который имеет значительное сходство с ТСХ. Анализируемую смесь аминокислот помещают в центр расположенного горизонтально бумажного листа, который смочен буферным раствором, обеспечивающим желаемое значение рН. Под действием внешнего электрического поля молекулы аминокислот, в зависимости от знака заряда, начинают двигаться либо к катоду, либо к аноду (рис. 15-3, табл. 15-3). Если значение рН буферного раствора выше  данной аминокислоты, то аминокислота существует в виде аниона и в электрическом поле будет двигаться к аноду. Наоборот, если
данной аминокислоты, то аминокислота существует в виде аниона и в электрическом поле будет двигаться к аноду. Наоборот, если  аминокислота находится в катионной форме и будет двигаться к катоду. Чем больше разница между
аминокислота находится в катионной форме и будет двигаться к катоду. Чем больше разница между  тем быстрее (дальше) будет двигаться аминокислота. В табл. 15-3 приведены значения
тем быстрее (дальше) будет двигаться аминокислота. В табл. 15-3 приведены значения  и относительные подвижности некоторых аминокислот при
и относительные подвижности некоторых аминокислот при 
На рис. 15-4 показана электрофореграмма, полученная после проявления нингидрином.
Электрофорез используется для анализа смесей аминокислот, полученных в результате гидролиза белков. В некоторых случаях электрофоретическое обнаружение необычных аминокислот в плазме крови позволяет поставить больному правильный диагноз.

Рис. 15-3- Схема установки для электрофореза: а - вид сбоку; б - вид сверху; 1 — бумажный лист; 2 — пятно исследуемой смеси; 3 - буферный раствор

Рис. 15-4, Электрофореграмма: 1 — точка старта; 2 — лейцин; 3 — фенил аланин; 4 — аспарагиновая кислота; 5 - лизин
Анализ аминокислот с помощью автоматического анализатора
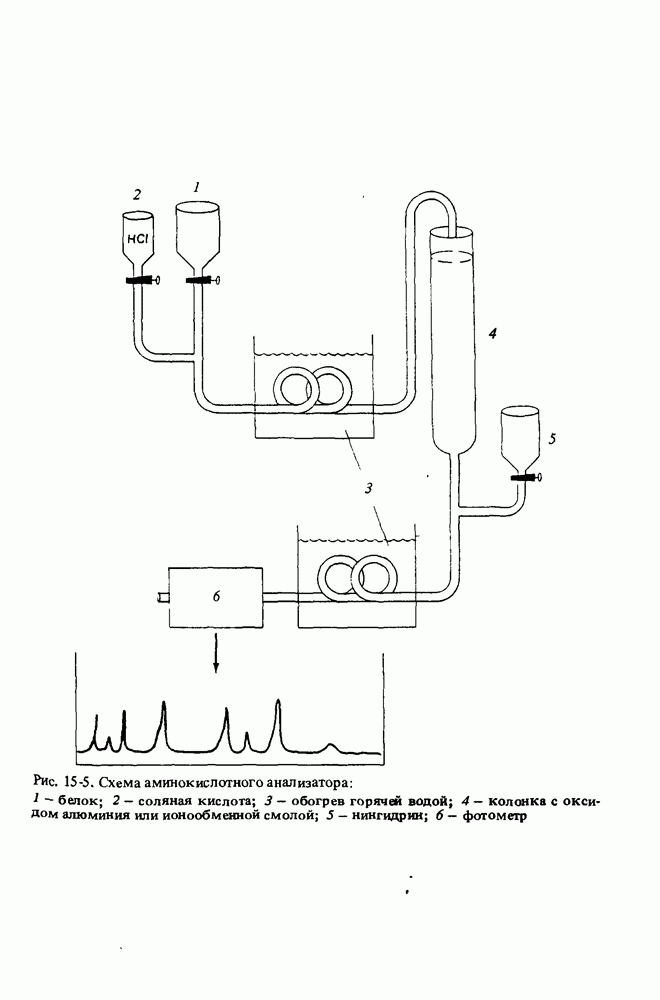
На рис. 15-5 показана принципиальная схема аминокислотного анализатора, который позволяет устанавливать как качественный, так и количественный состав смесей аминокислот, полученных в результате гидролиза белка.
Белок, чей аминокислотный состав анализируется, смешивают с соляной кислотой. Нагревание смеси приводит к гидролизу белка до аминокислот. Затем смесь аминокислот пропускают через колонку, заполненную оксидом алюминия или ионообменной смолой. В колонке аминокислоты разделяются и выходят из нее с различной скоростью. Разделенные аминокислоты смешивают с нингидрином и снова нагревают для ускорения образования окрашенного комплекса. Затем раствор проходит через фотометр, который регистрирует наличие и интенсивность окраски и изображает график зависимости оптической плотности раствора от времени. Поскольку время удерживания каждой из двадцати аминокислот в колонке известно, можно установить, какие именно аминокислоты входят в состав исследуемого белка. Площадь пика пропорциональна количеству данной аминокислоты, что позволяет установить относительное содержание аминокислот в белке.
Аминокислотный состав белка может быть установлен несколькими способами. После гидролиза белка до аминокислот смесь последних можно анализировать с помощью тонкослойной хроматографии или электрофореза. Оба эти метода дают только качественный состав смеси аминокислот. С помощью автоматического аминокислотного анализатора можно установить и качественными количественный аминокислотный состав белка.
Таблица 15-3. (см. скан) Относительные подвижности некоторых аминокислот в электрическом поле

(кликните для просмотра скана)
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- Глава 1. КЛЮЧЕВЫЕ ПОНЯТИЯ ХИМИИ
- АТОМНАЯ ТЕОРИЯ
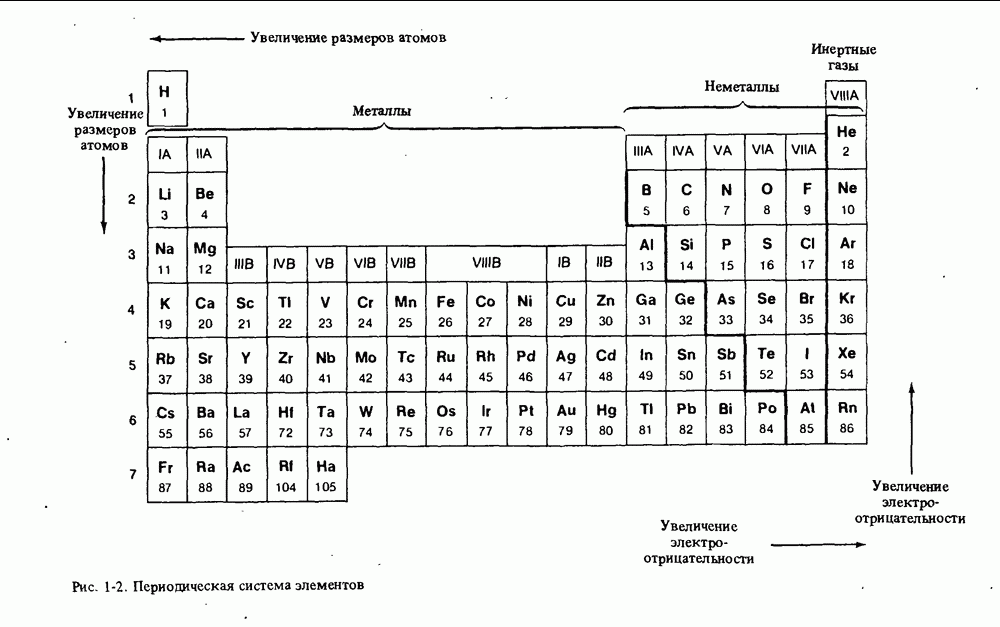
- ПЕРИОДИЧЕСКАЯ СИСТЕМА
- ХИМИЧЕСКАЯ СВЯЗЬ
- ФОРМУЛЫ ЛЬЮИСА
- ФОРМАЛЬНЫЙ ЗАРЯД
- РЕЗОНАНС
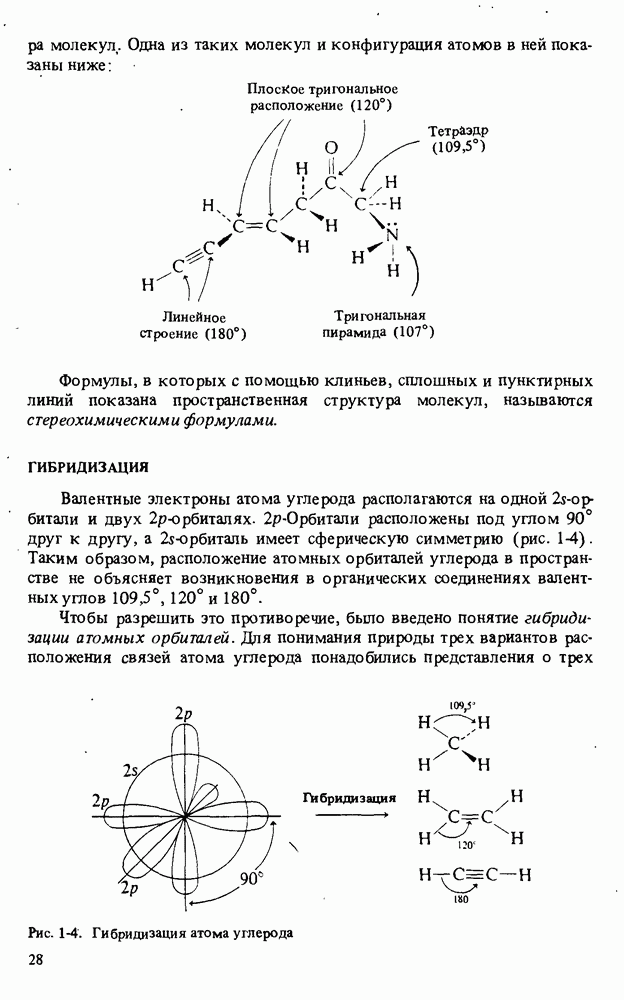
- ГЕОМЕТРИЯ МОЛЕКУЛ
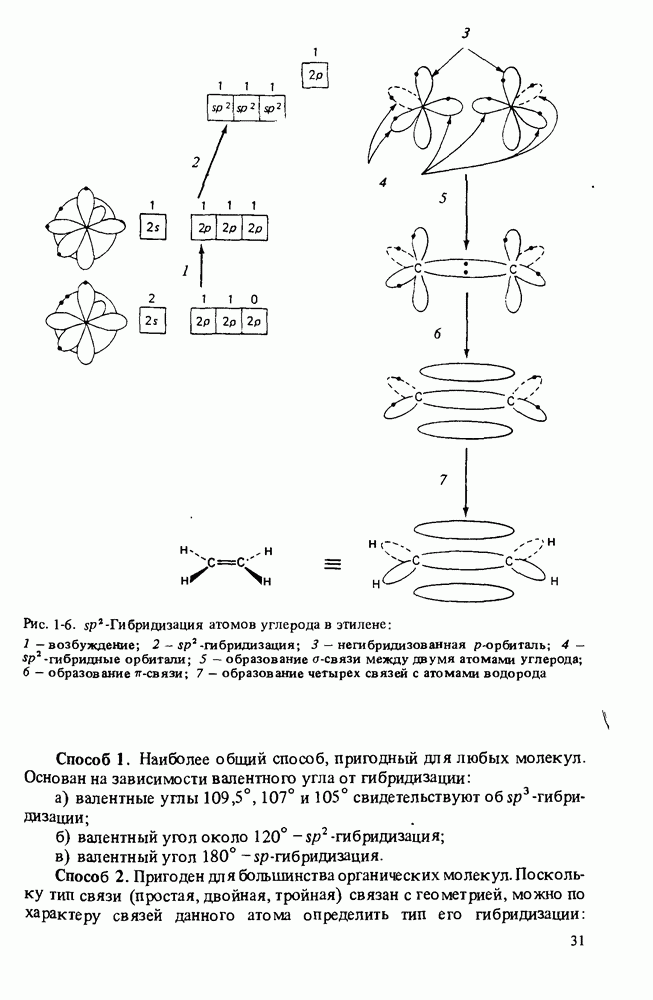
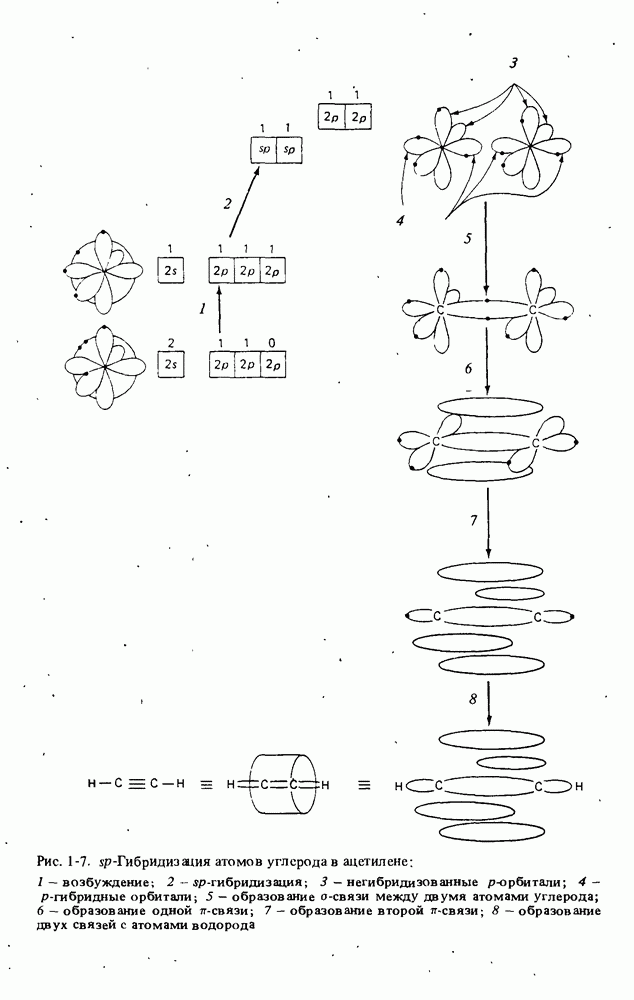
- ГИБРИДИЗАЦИЯ
- ХИМИЧЕСКИЕ ФОРМУЛЫ
- СОВЕТЫ ИЗУЧАЮЩЕМУ ОРГАНИЧЕСКУЮ ХИМИЮ
- СВОДКА ОСНОВНЫХ ПОЛОЖЕНИЙ ГЛ. 1
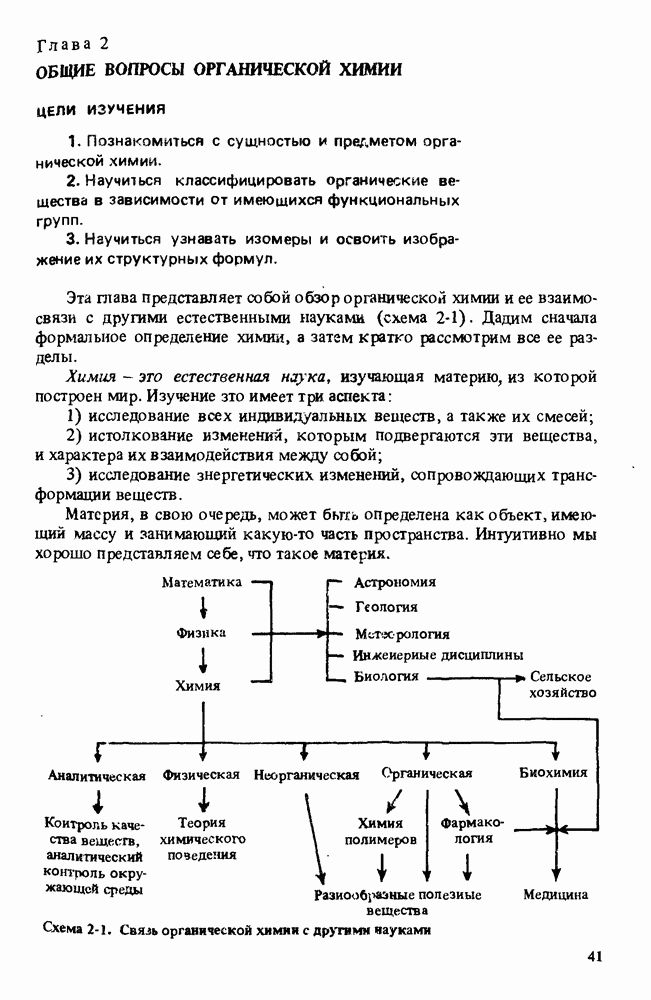
- Глава 2. ОБЩИЕ ВОПРОСЫ ОРГАНИЧЕСКОЙ ХИМИИ
- РАЗДЕЛЫ ХИМИИ
- СИНТЕТИЧЕСКАЯ ОРГАНИЧЕСКАЯ ХИМИЯ
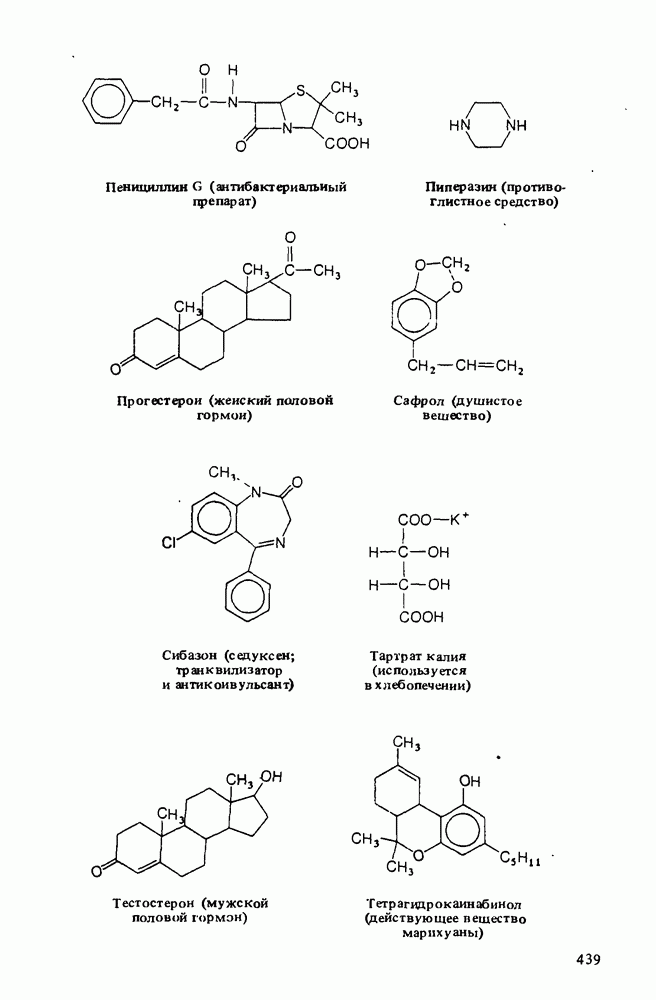
- ПОЛЕЗНЫЕ ОРГАНИЧЕСКИЕ ВЕЩЕСТВА
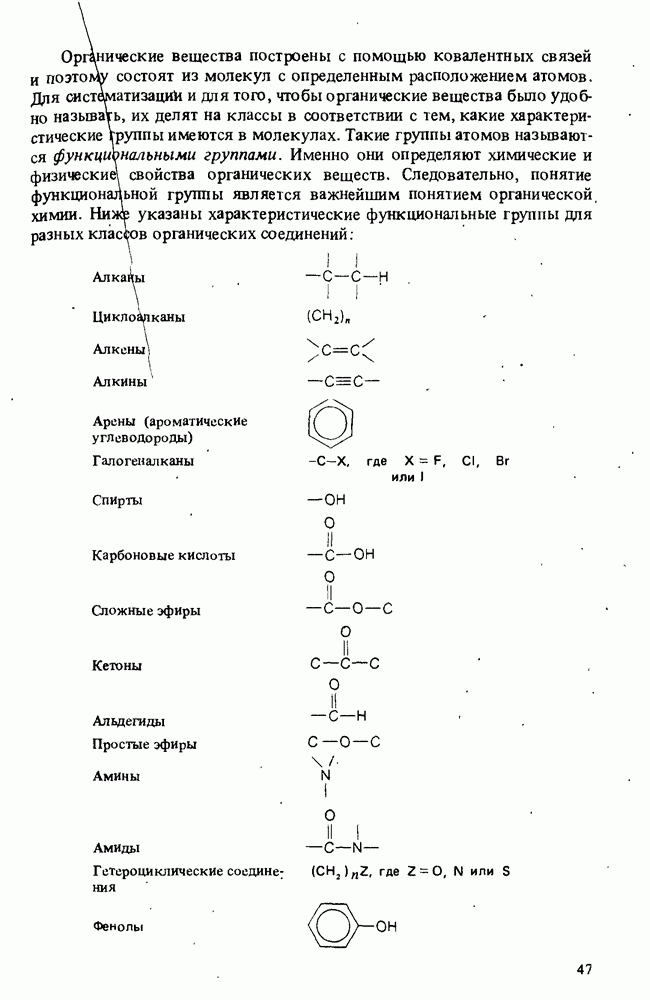
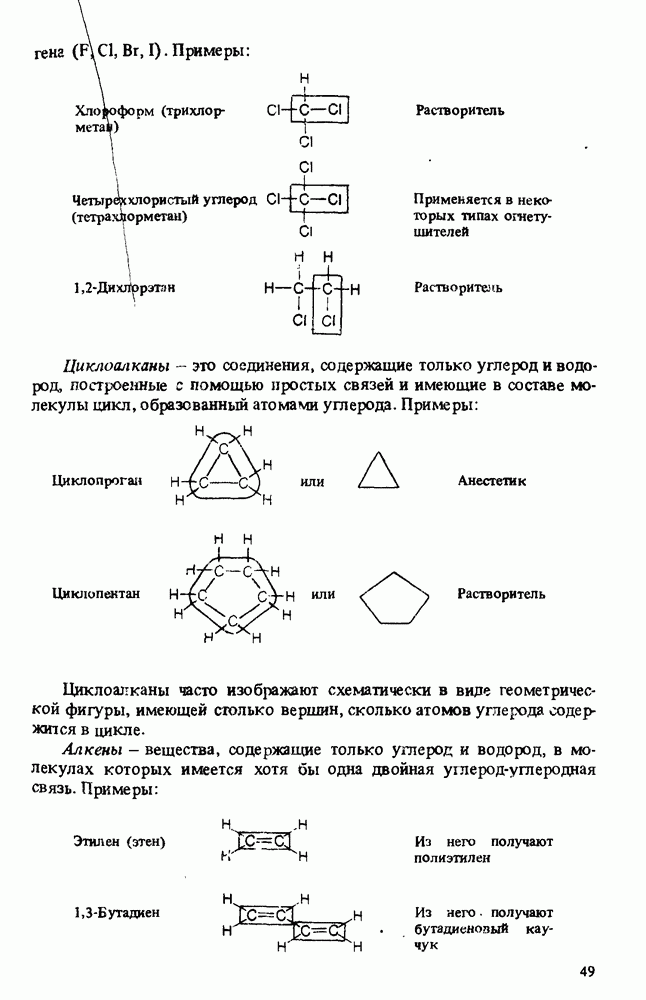
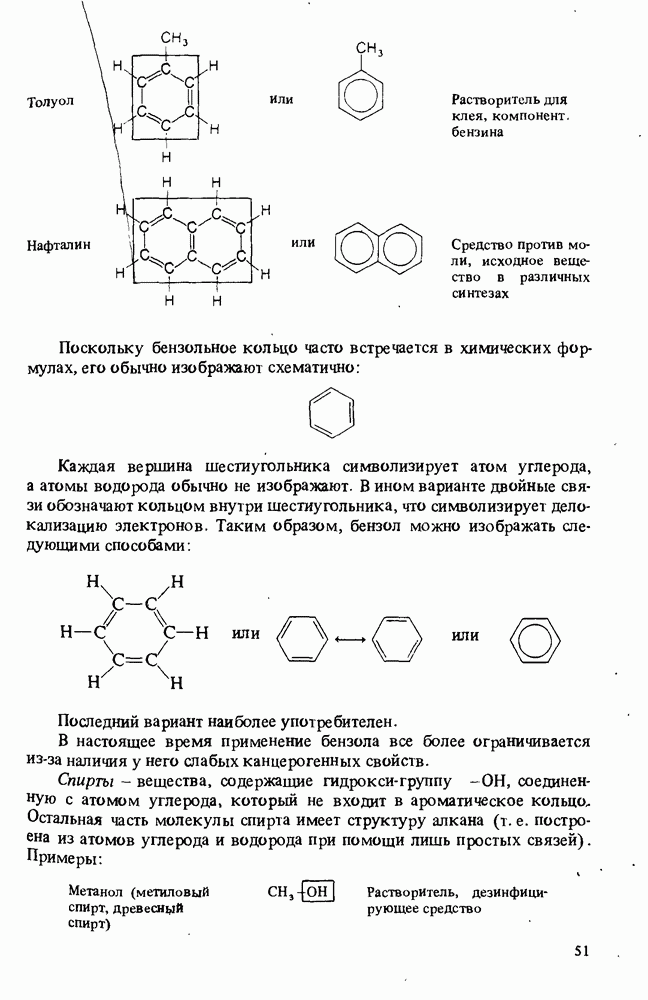
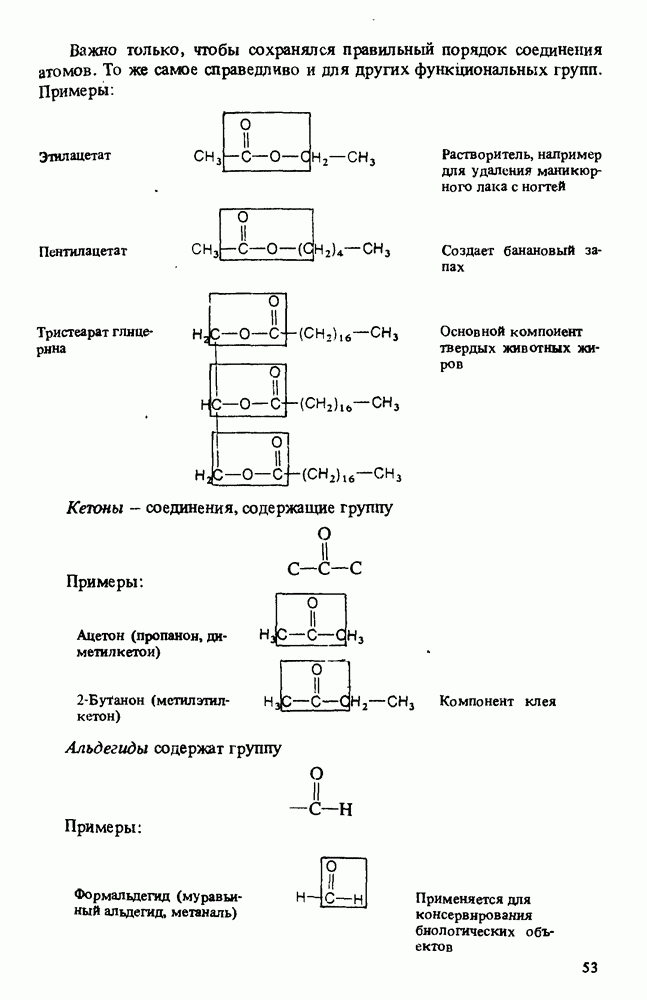
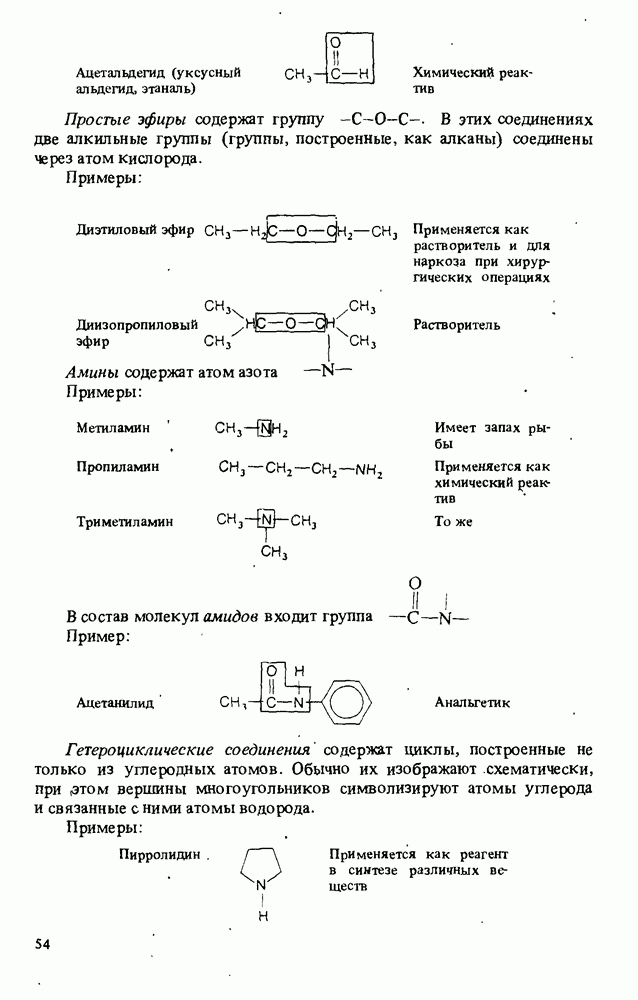
- КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ. ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
- ИЗОМЕРИЯ
- СВОДКА ОСНОВНЫХ ПОЛОЖЕНИЙ ГЛ. 2
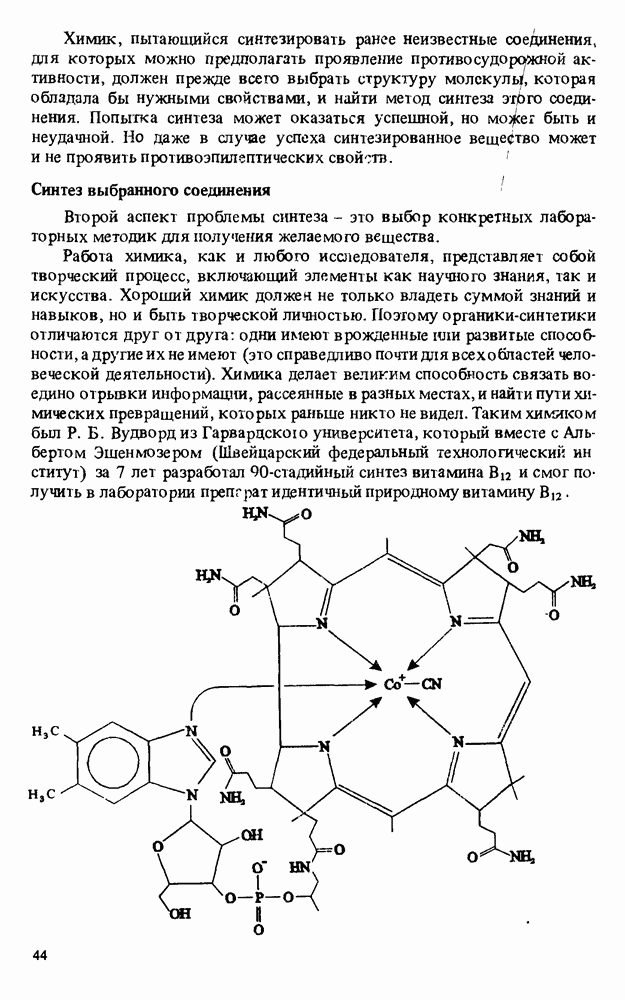
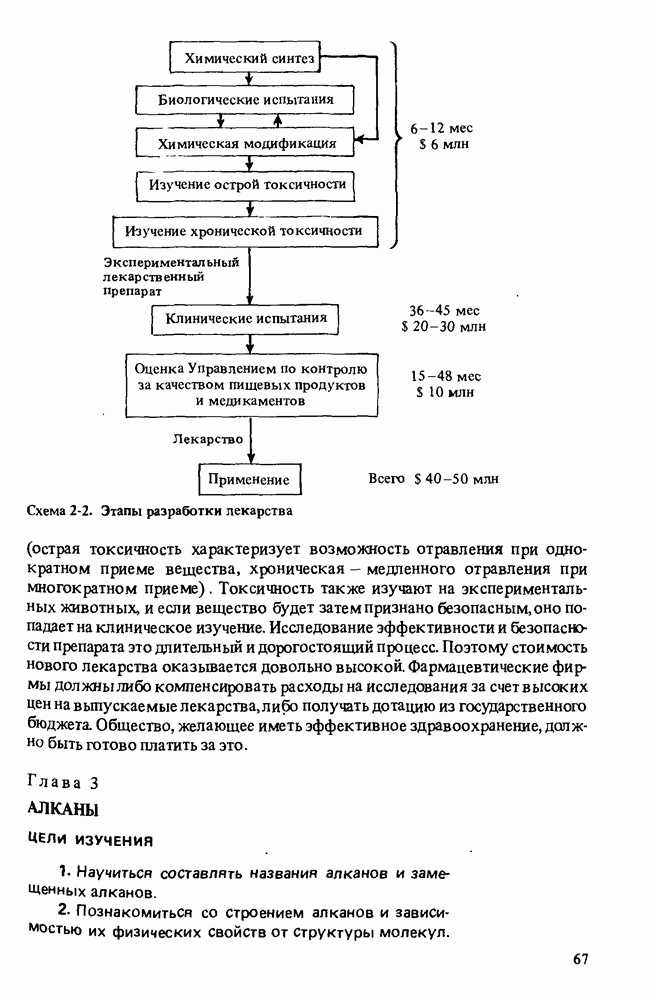
- Прикладная органическая химия: ХИМИЧЕСКИЙ СИНТЕЗ И МЕДИЦИНСКИЕ ИССЛЕДОВАНИЯ
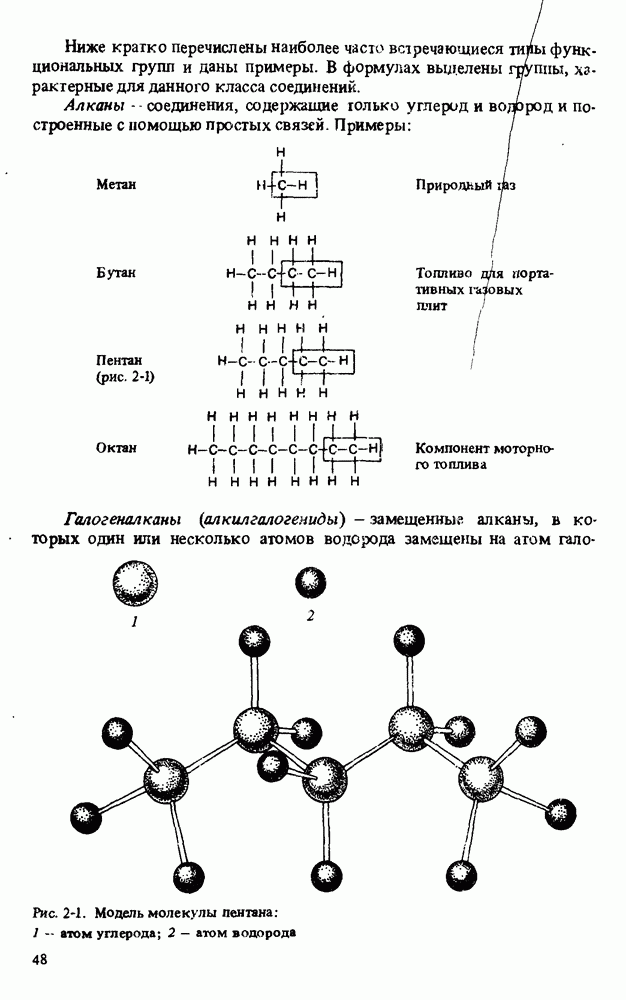
- Глава 3. АЛКАНЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА АЛКАНОВ
- СТРОЕНИЕ АЛКАНОВ
- ПОЛУЧЕНИЕ АЛКАНОВ
- РЕАКЦИИ АЛКАНОВ
- ХИМИЯ НЕФТИ
- СОВЕТЫ ИЗУЧАЮЩЕМУ ОРГАНИЧЕСКУЮ ХИМИЮ. ИЗУЧЕНИЕ РЕАКЦИЙ
- Глава 4. СТЕРЕОХИМИЯ И ОПТИЧЕСКАЯ АКТИВНОСТЬ
- СПОСОБЫ ИЗОБРАЖЕНИЯ ЭНАНТИОМЕРОВ
- ОБОЗНАЧЕНИЕ АБСОЛЮТНОЙ КОНФИГУРАЦИИ
- НАЗВАНИЯ ХИРАЛЬНЫХ МОЛЕКУЛ
- ИЗОБРАЖЕНИЕ МОЛЕКУЛ С ПРОТИВОПОЛОЖНОЙ КОНФИГУРАЦИЕЙ
- D,L-НОМЕНКЛАТУРА ЭНАНТИОМЕРОВ
- ТЕРМИНОЛОГИЯ, ПРИМЕНЯЕМАЯ В СТЕРЕОХИМИИ
- ЗНАЧЕНИЕ ОПТИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ
- Глава 5. ОРГАНИЧЕСКИЕ ГАЛОГЕНСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
- ПОЛУЧЕНИЕ ГАЛОГЕНАЛКАНОВ
- РЕАКЦИИ ГАЛОГЕНАЛКАНОВ
- ПРАКТИЧЕСКИ ВАЖНЫЕ ГАЛОГЕНАЛКАНЫ
- Прикладная органическая химия: ОРГАНИЧЕСКИЕ ПЕСТИЦИДЫ
- Глава 6. НЕНАСЫЩЕННЫЕ УГЛЕВОДОРОДЫ
- НОМЕНКЛАТУРА АЛКЕНОВ
- ПОЛУЧЕНИЕ АЛКЕНОВ
- ОСНОВНЫЕ РЕАКЦИИ АЛКЕНОВ
- ПОЛИМЕРЫ
- НОМЕНКЛАТУРА АЛКИНОВ
- ПОЛУЧЕНИЕ АЛКИНОВ
- РЕАКЦИИ АЛКИНОВ
- НАПИСАНИЕ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- Глава 7. СПИРТЫ И ПРОСТЫЕ ЭФИРЫ
- НОМЕНКЛАТУРА СПИРТОВ
- НЕКОТОРЫЕ ВАЖНЫЕ ВЕЩЕСТВА, СОДЕРЖАЩИЕ СПИРТОВУЮ ГРУППУ
- ЭТИЛОВЫЙ СПИРТ. ПРОИЗВОДСТВО СПИРТНЫХ НАПИТКОВ
- ПОЛУЧЕНИЕ СПИРТОВ
- РЕАКЦИИ СПИРТОВ
- ПРОСТЫЕ ЭФИРЫ
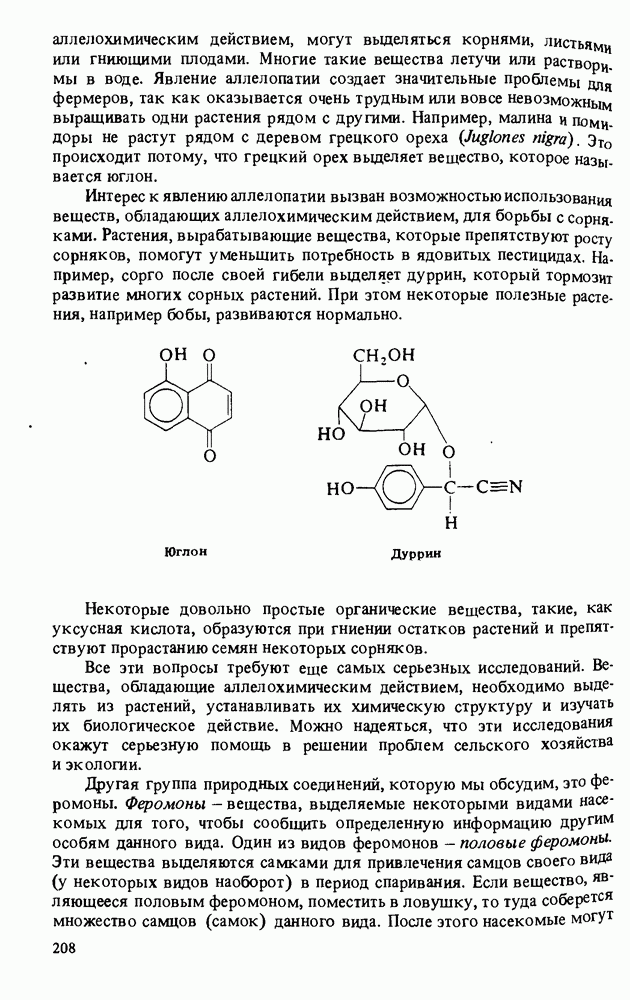
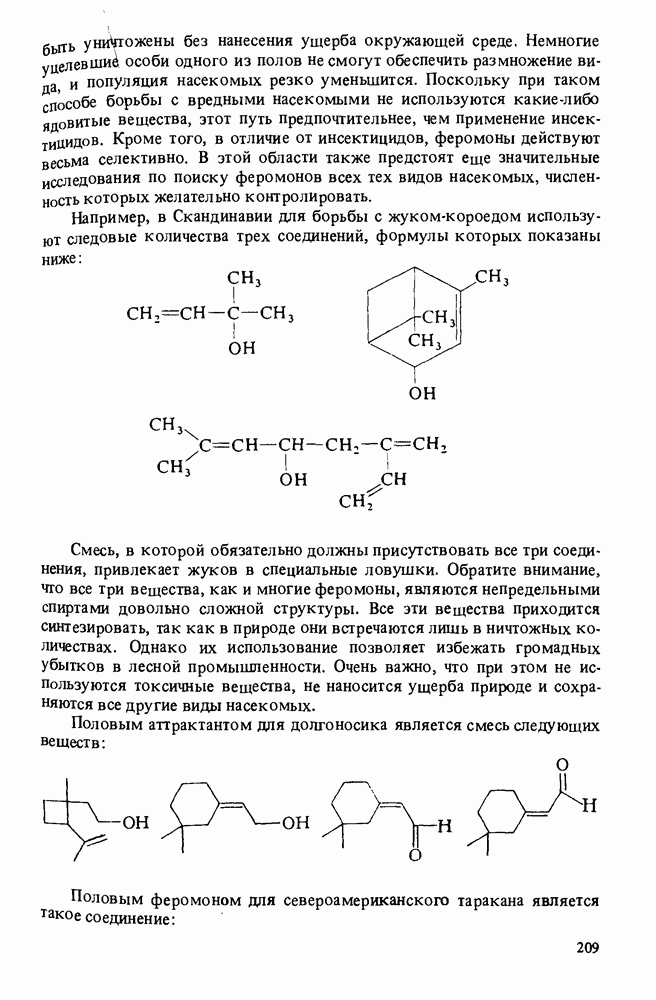
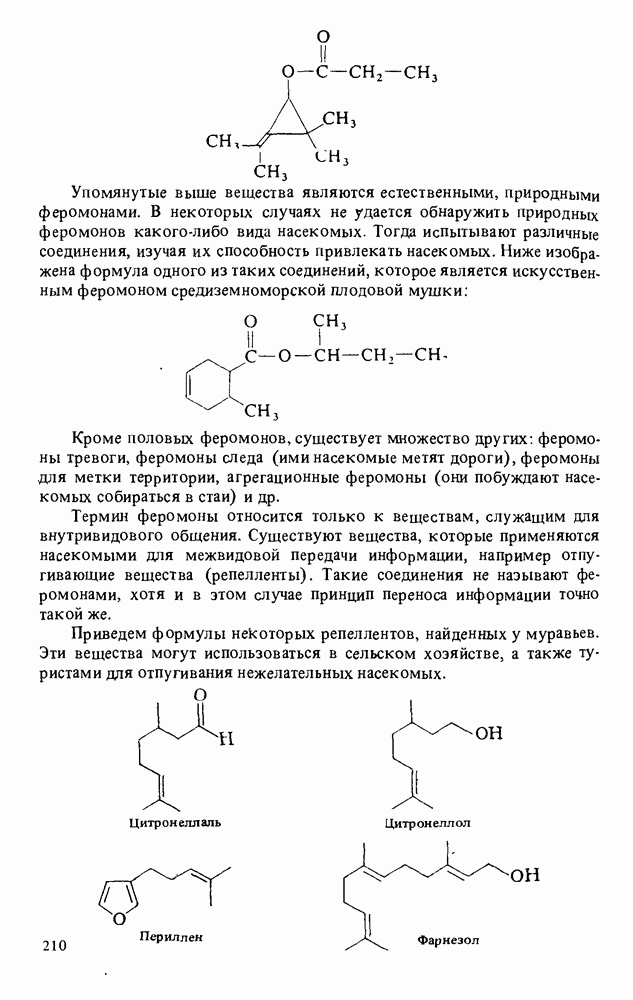
- Прикладная органическая химия: ВЕЩЕСТВА, ОБЛАДАЮЩИЕ АЛЛЕЛОХИМИЧЕСКИМ ДЕЙСТВИЕМ. ФЕРОМОНЫ
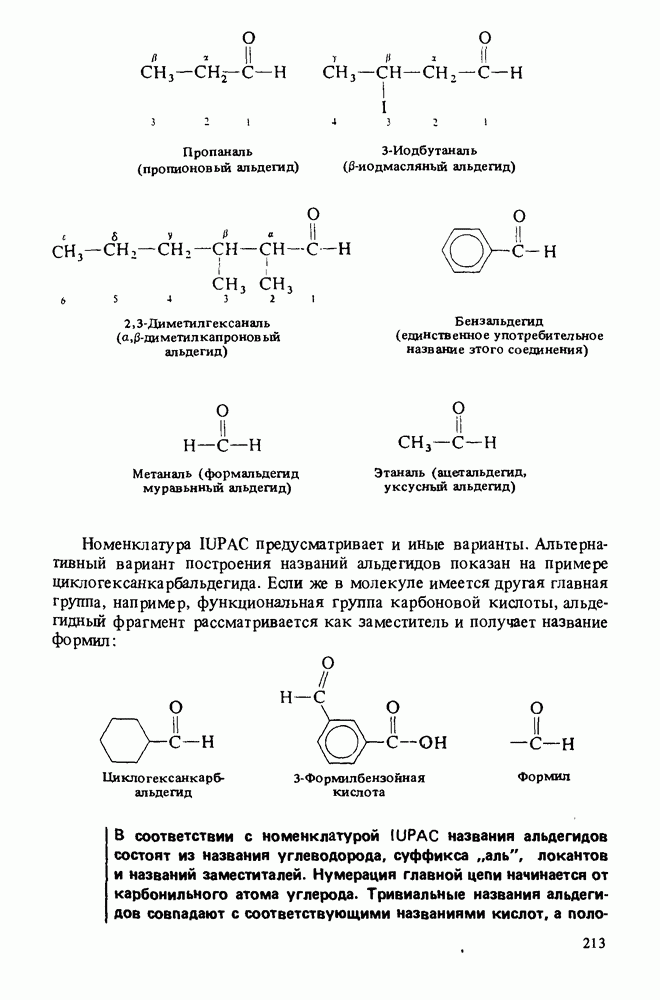
- Глава 8. АЛЬДЕГИДЫ И КЕТОНЫ
- ПОЛУЧЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ
- РЕАКЦИИ АЛЬДЕГИДОВ И КЕТОНОВ
- Глава 9. АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
- НОМЕНКЛАТУРА АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ
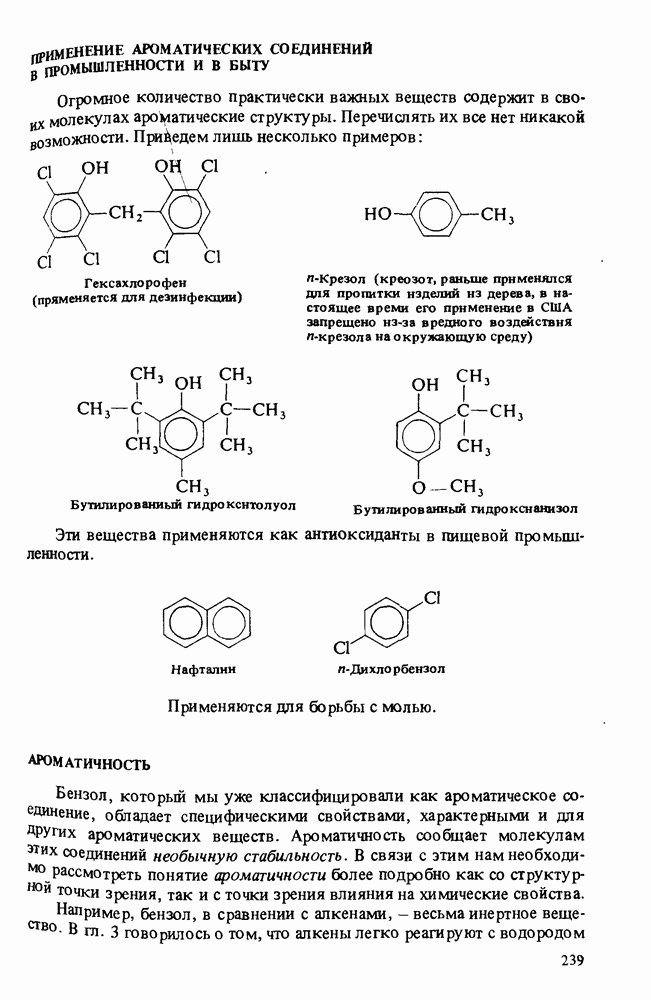
- ПРИМЕНЕНИЕ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ В ПРОМЫШЛЕННОСТИ И В БЫТУ
- АРОМАТИЧНОСТЬ
- ПОЛУЧЕНИЕ АЛКИЛЬБЕНЗОЛОВ
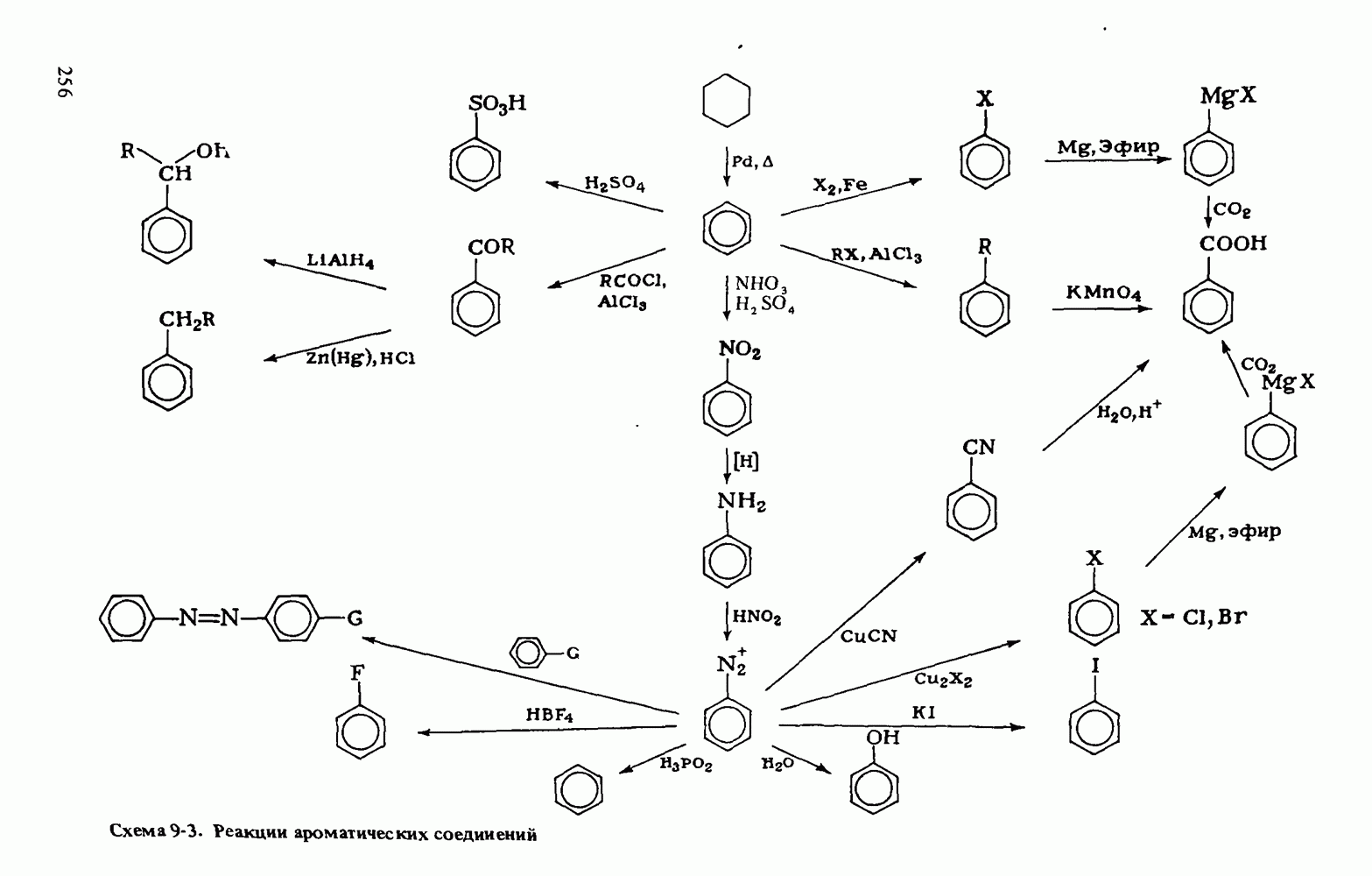
- РЕАКЦИИ БЕНЗОЛА И ЕГО ПРОИЗВОДНЫХ
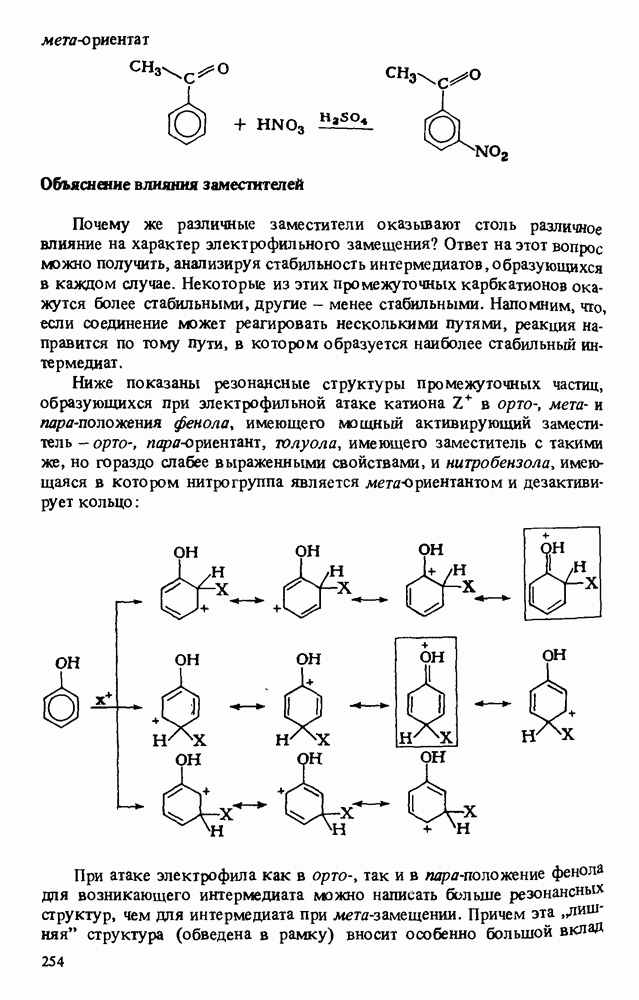
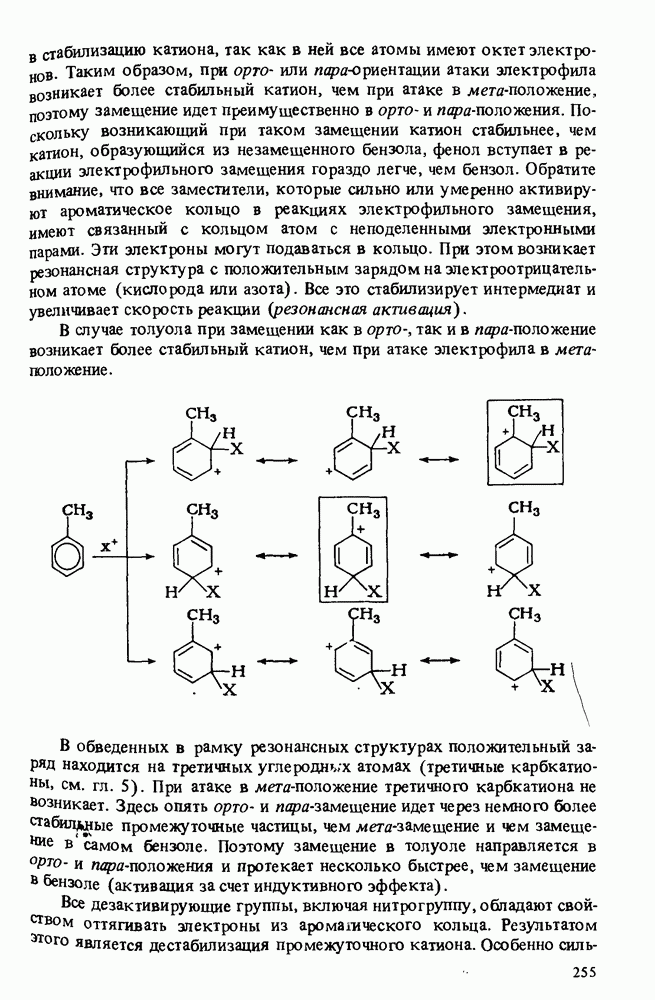
- АРОМАТИЧЕСКОЕ ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ
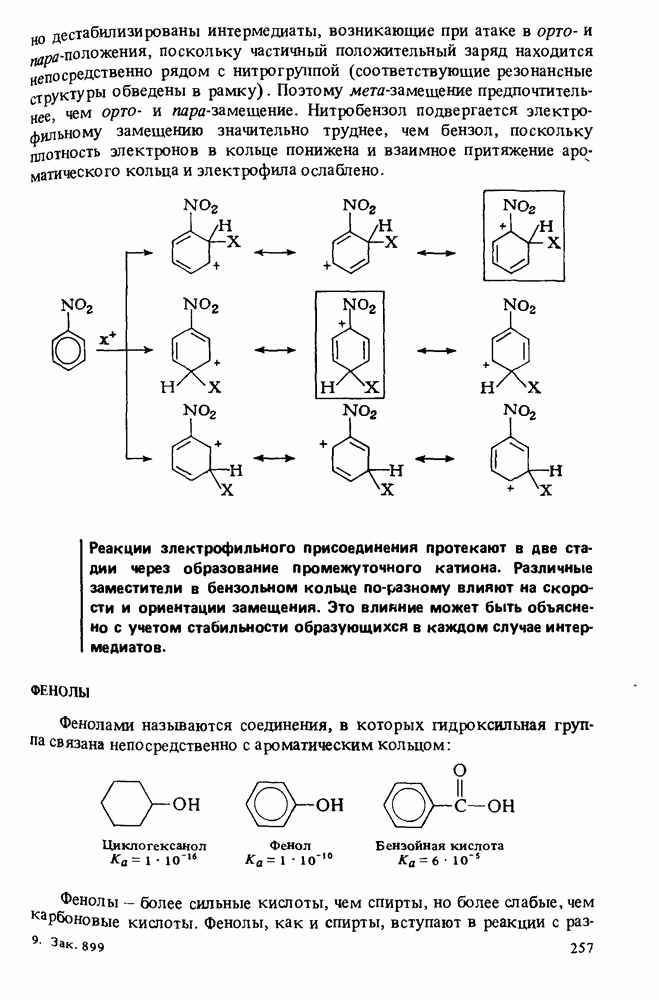
- ФЕНОЛЫ
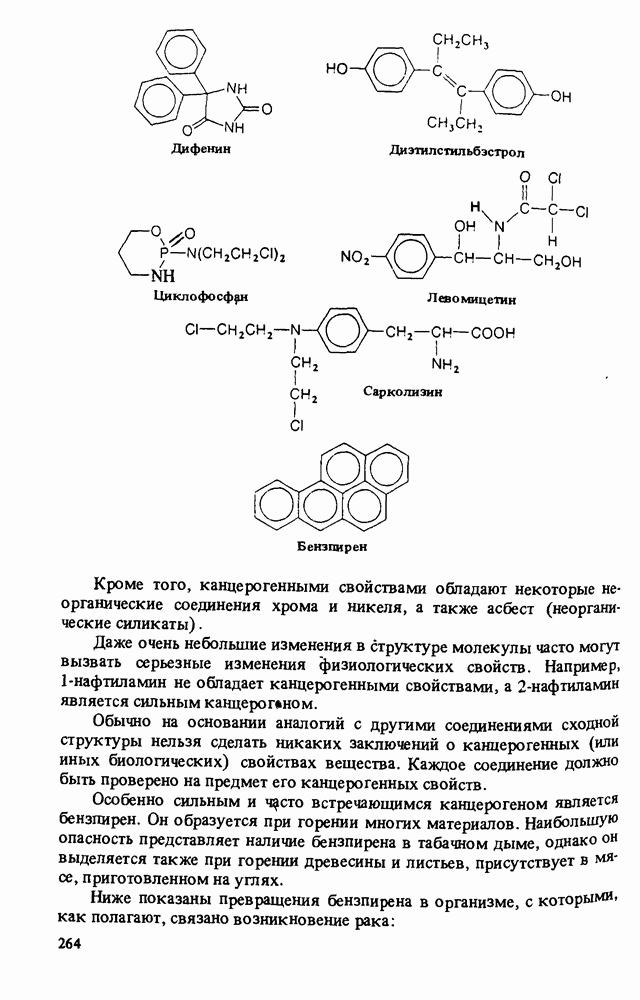
- Прикладная органическая химия: КАНЦЕРОГЕННЫЕ АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
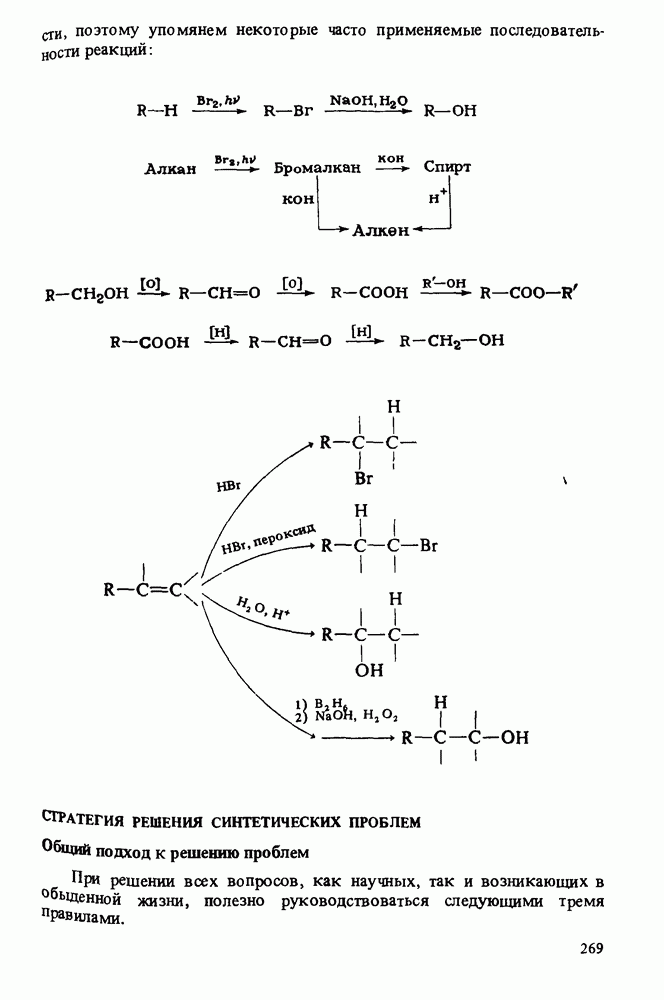
- Глава 10. ОРГАНИЧЕСКИЙ СИНТЕЗ
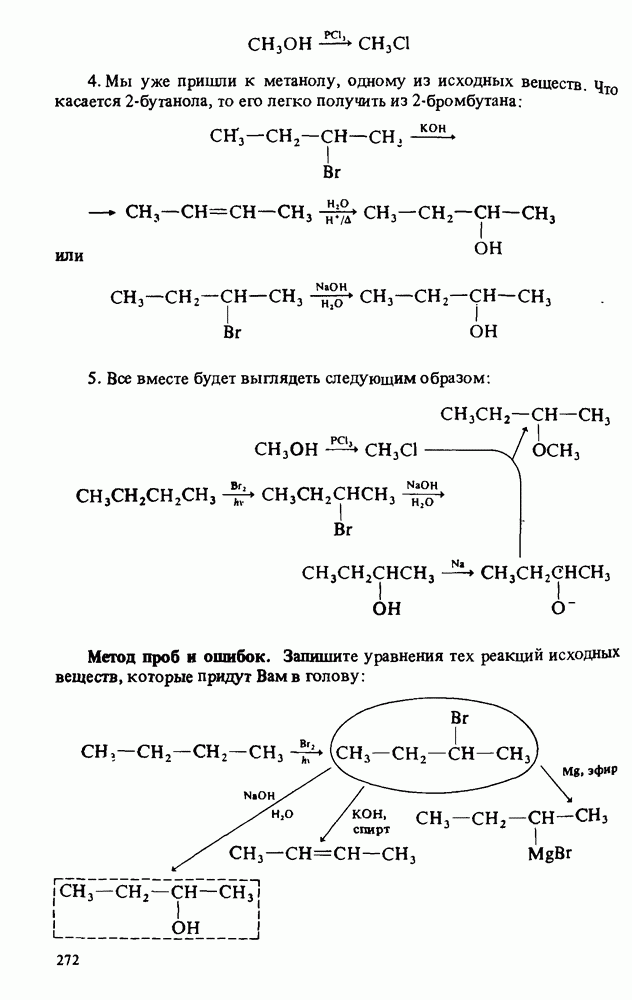
- СТРАТЕГИЯ РЕШЕНИЯ СИНТЕТИЧЕСКИХ ПРОБЛЕМ
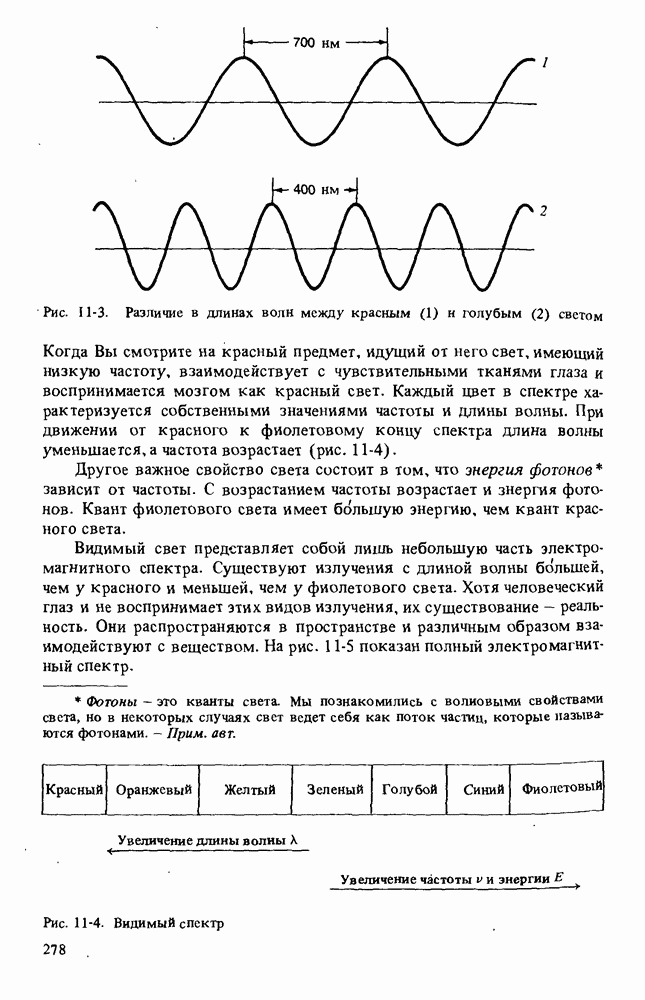
- Глава 11. МОЛЕКУЛЯРНАЯ СПЕКТРОСКОПИЯ
- ИНФРАКРАСНАЯ СПЕКТРОСКОПИЯ
- СПЕКТРОСКОПИЯ ЯДЕРНОГО МАГНИТНОГО РЕЗОНАНСА
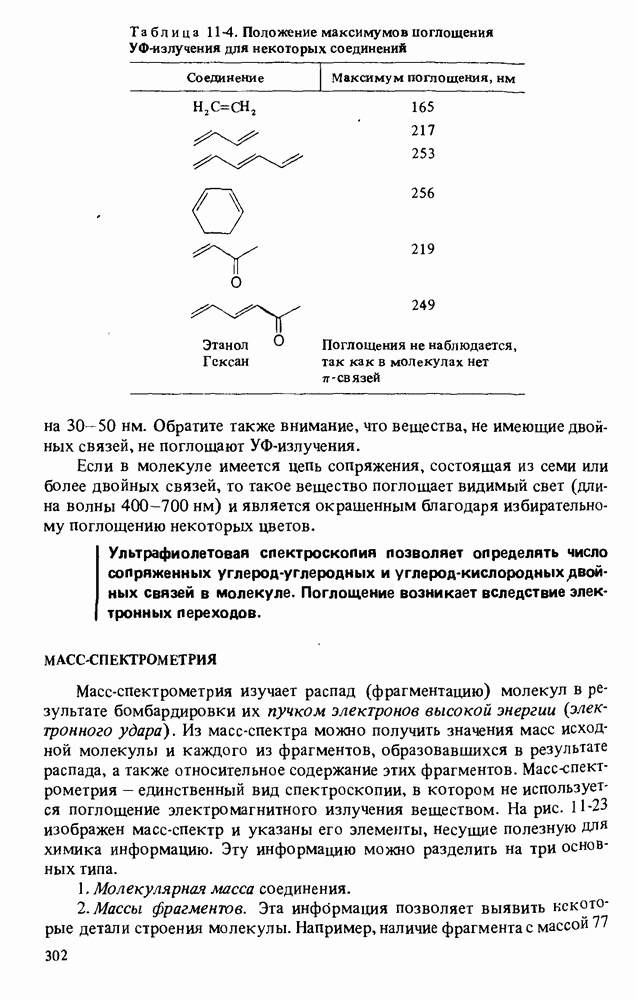
- УЛЬТРАФИОЛЕТОВАЯ СПЕКТРОСКОПИЯ
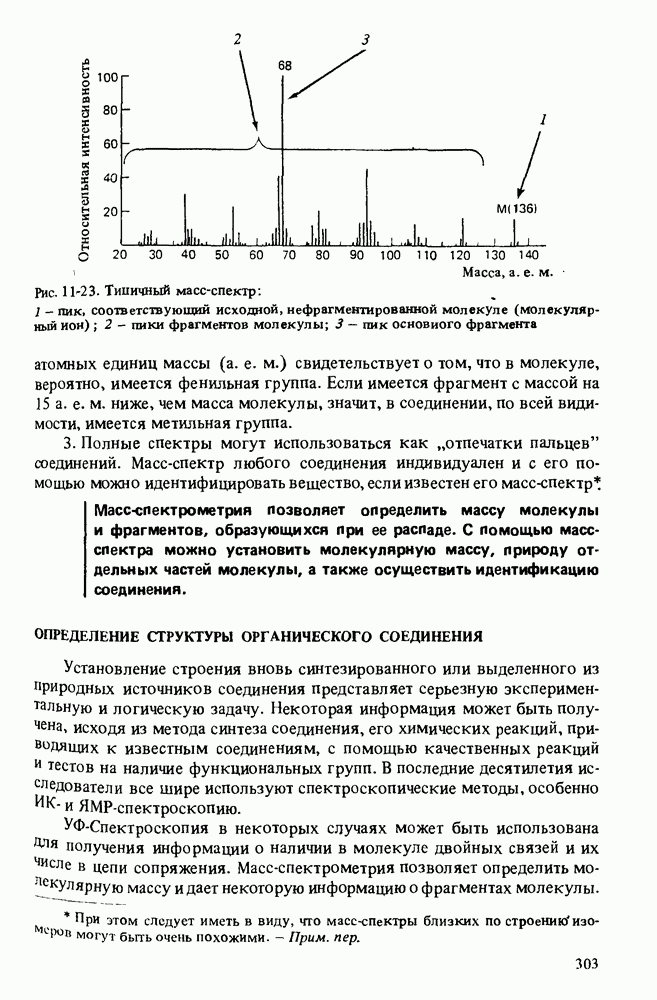
- МАСС-СПЕКТРОМЕТРИЯ
- ОПРЕДЕЛЕНИЕ СТРУКТУРЫ ОРГАНИЧЕСКОГО СОЕДИНЕНИЯ
- Прикладная органическая химия: ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ АЛКОГОЛЯ В КРОВИ
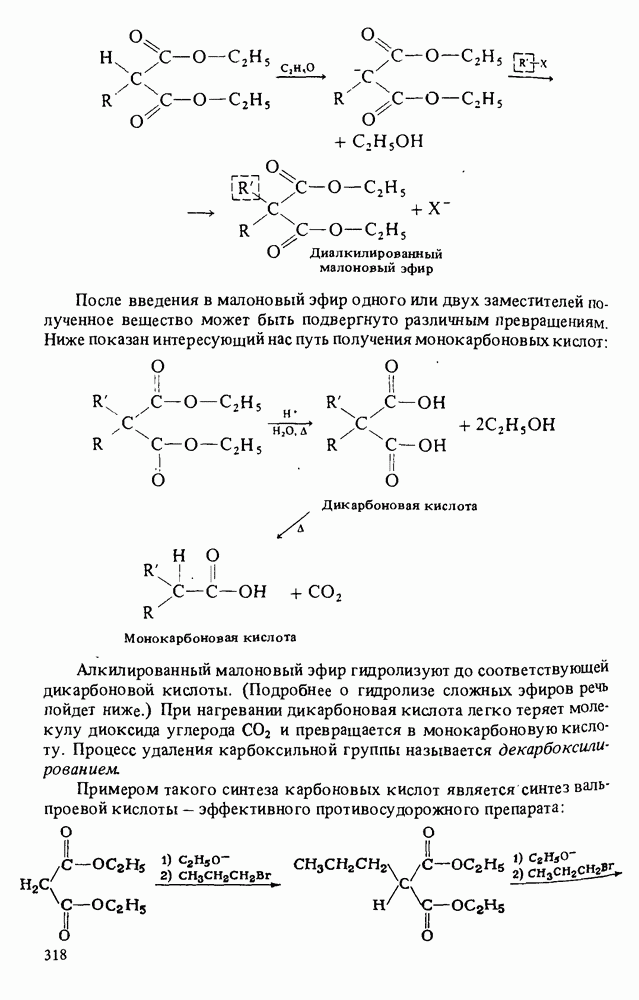
- Глава 12. КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
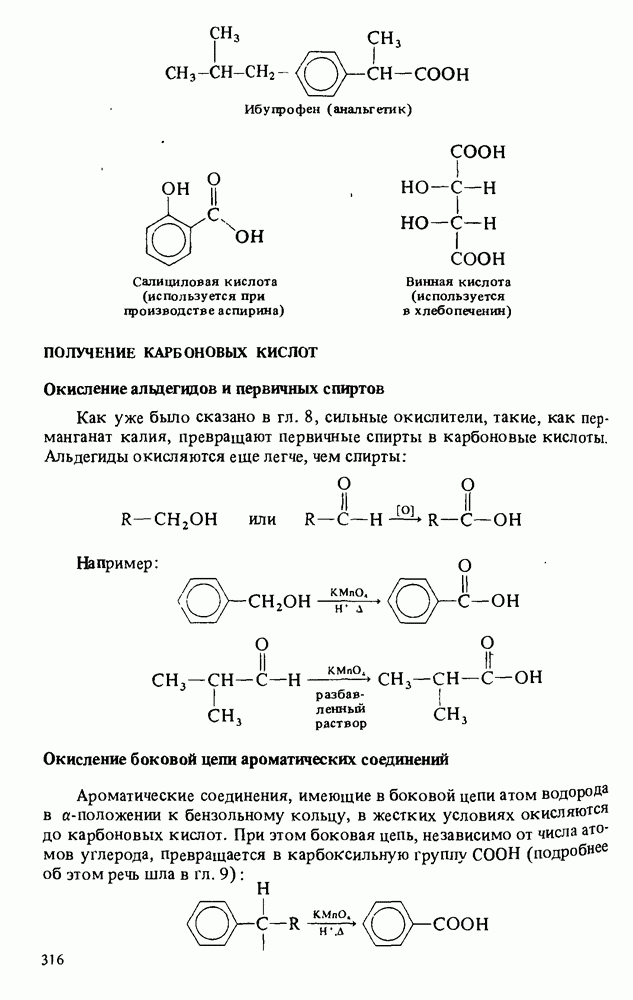
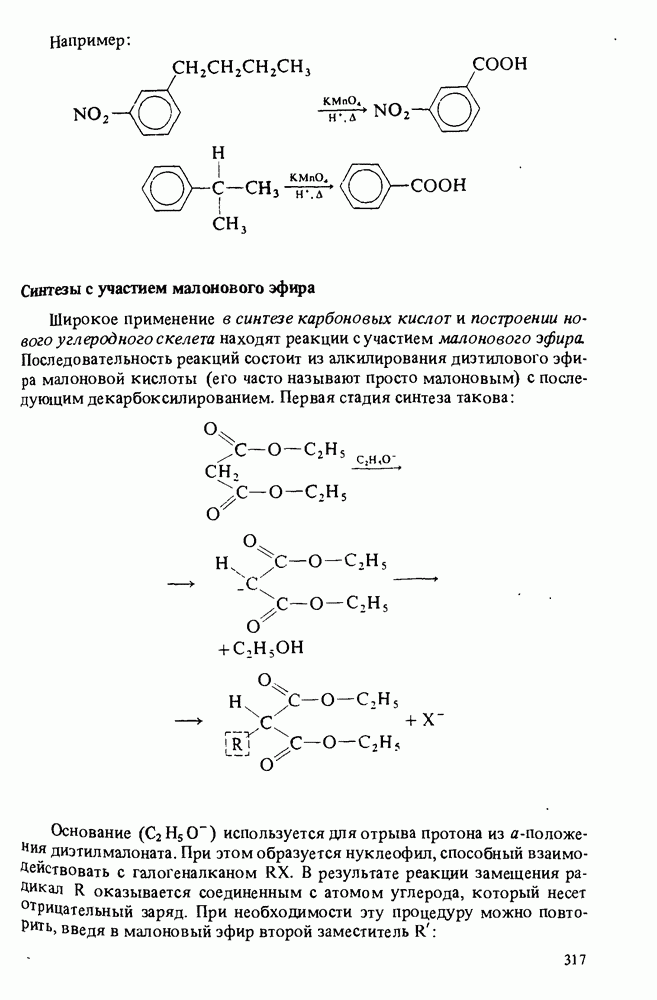
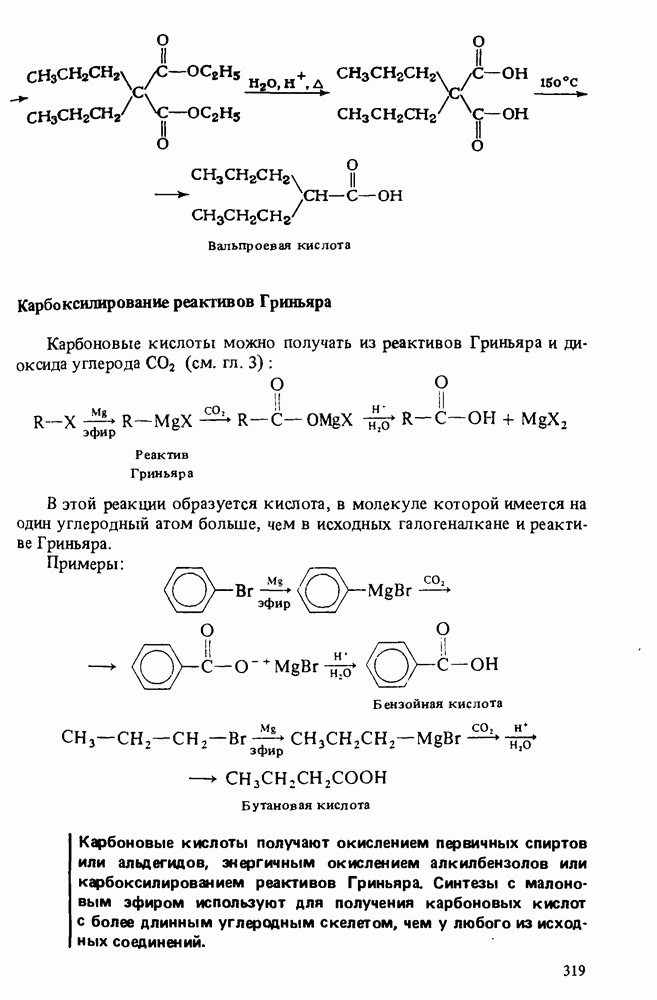
- ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ
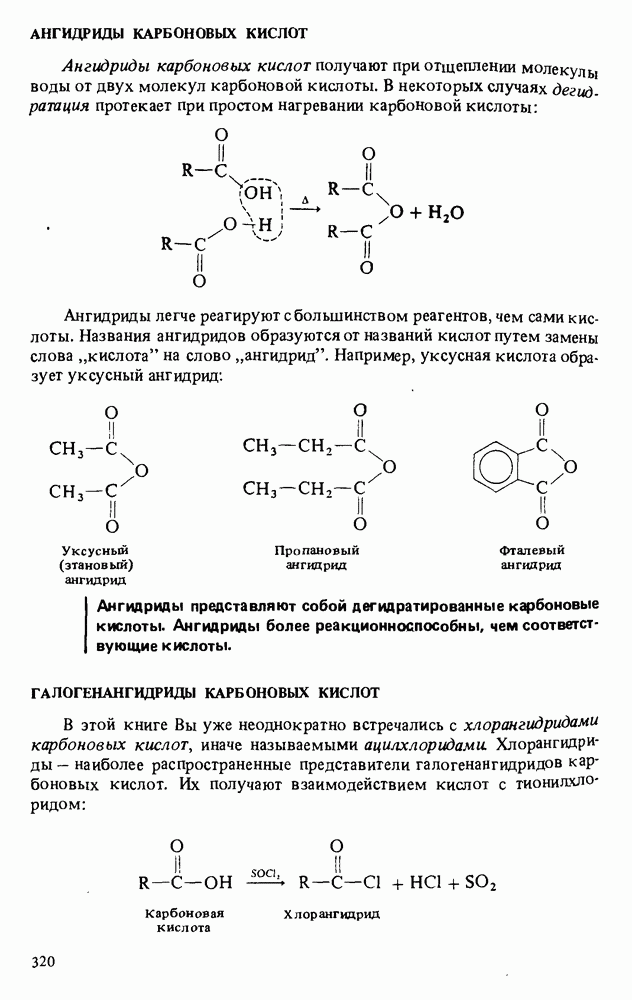
- АНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
- ГАЛОГЕНАНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
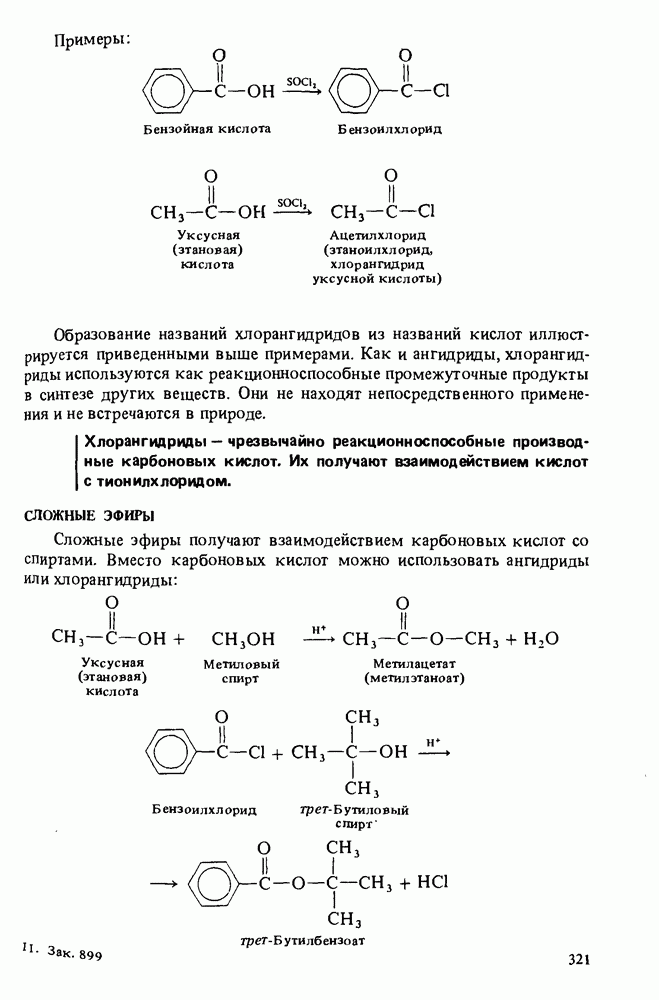
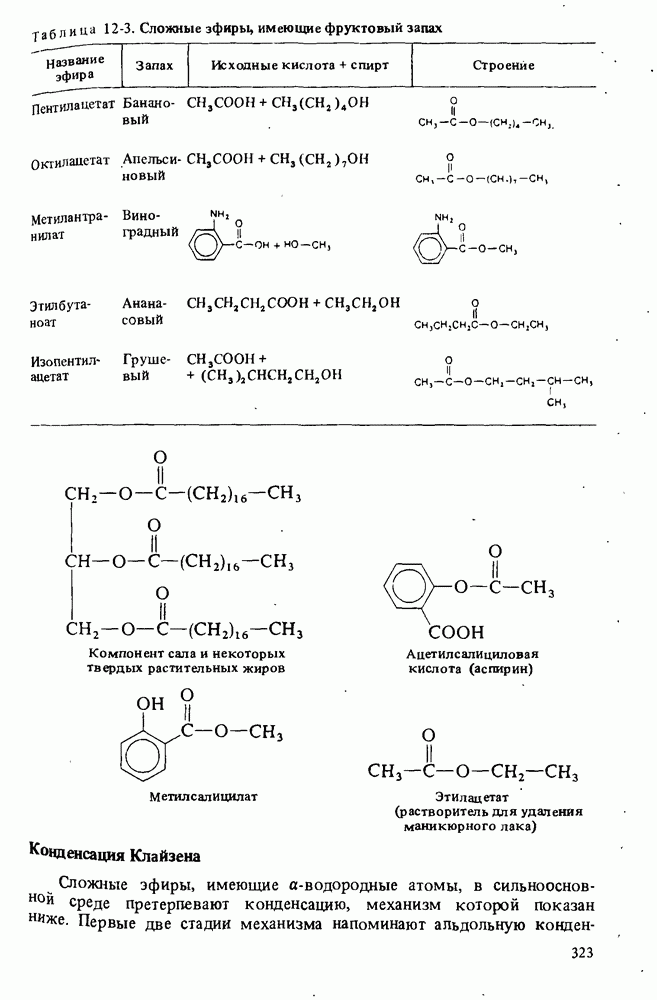
- СЛОЖНЫЕ ЭФИРЫ
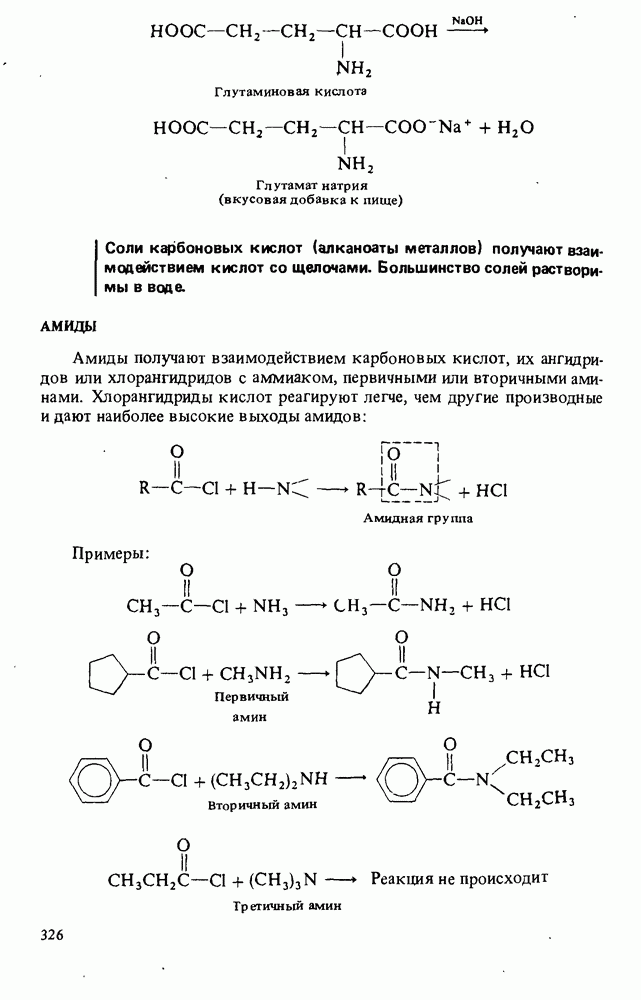
- СОЛИ
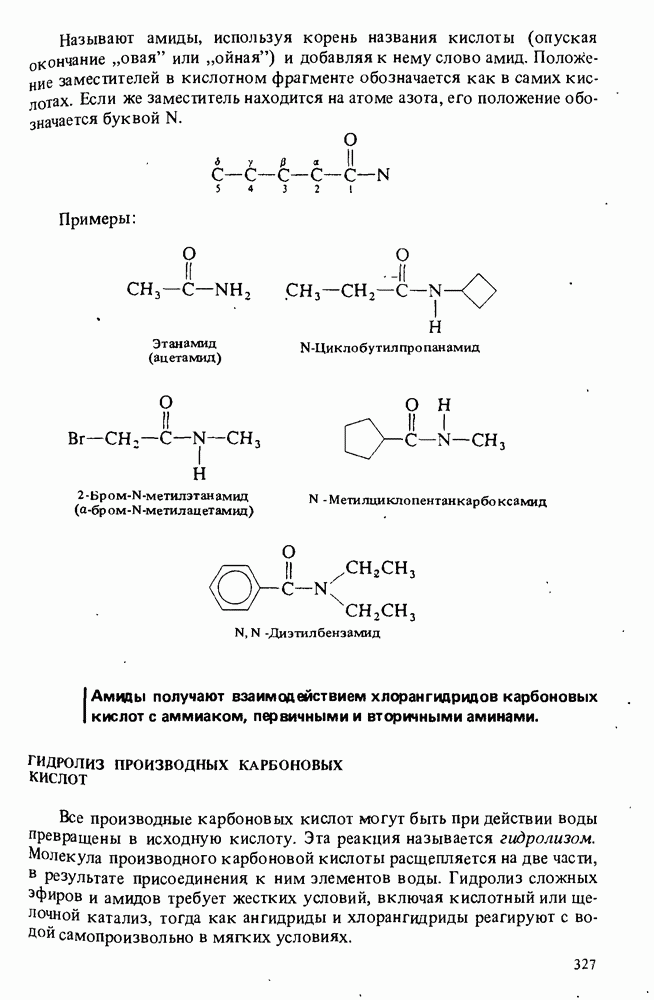
- АМИДЫ
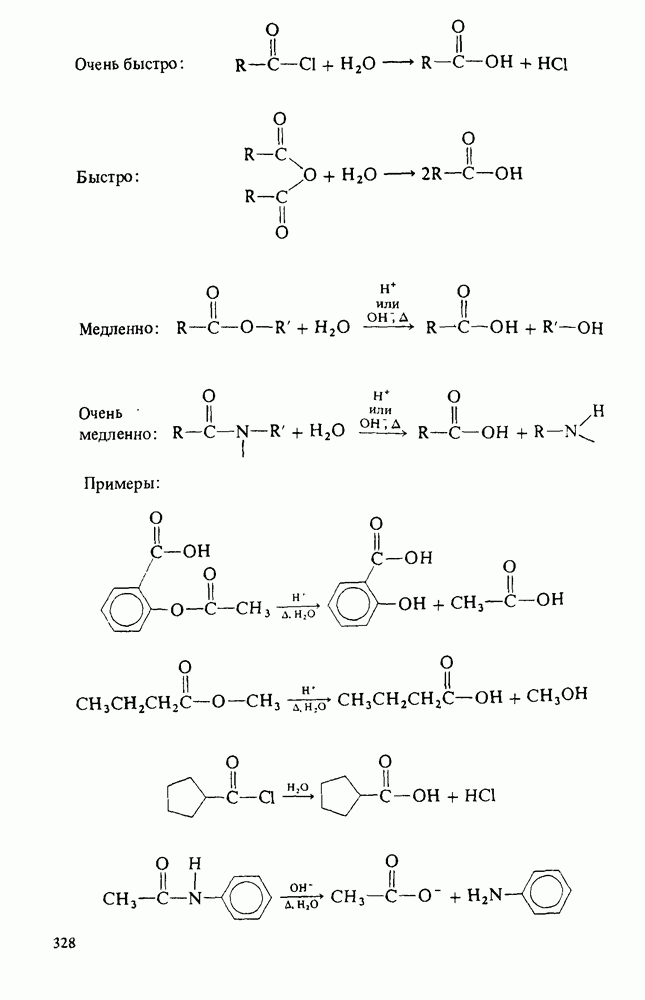
- ГИДРОЛИЗ ПРОИЗВОДНЫХ КАРБОНОВЫХ КИСЛОТ
- СИНТЕТИЧЕСКИЕ ВОЛОКНА
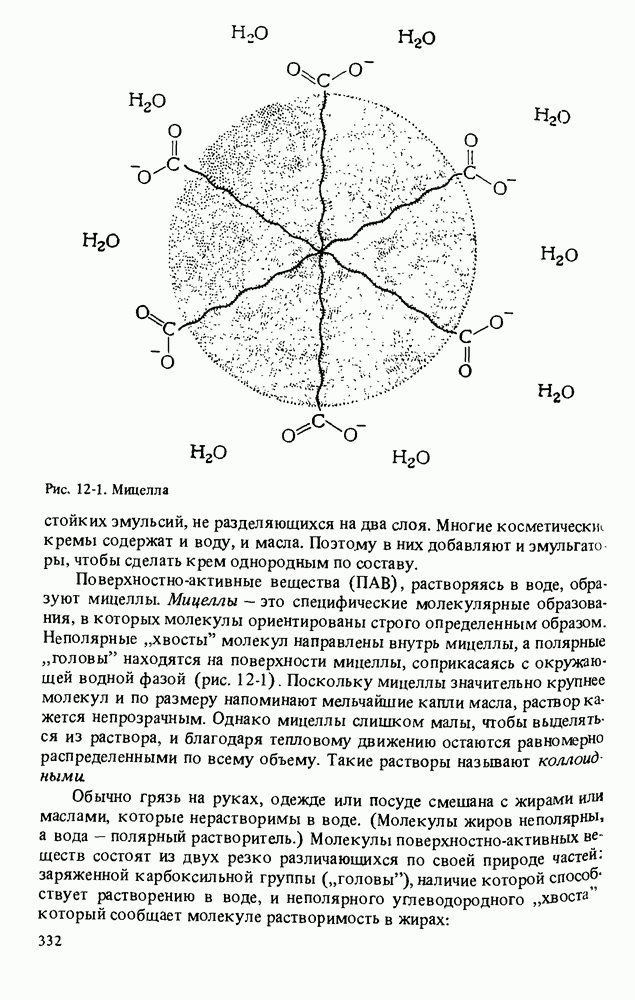
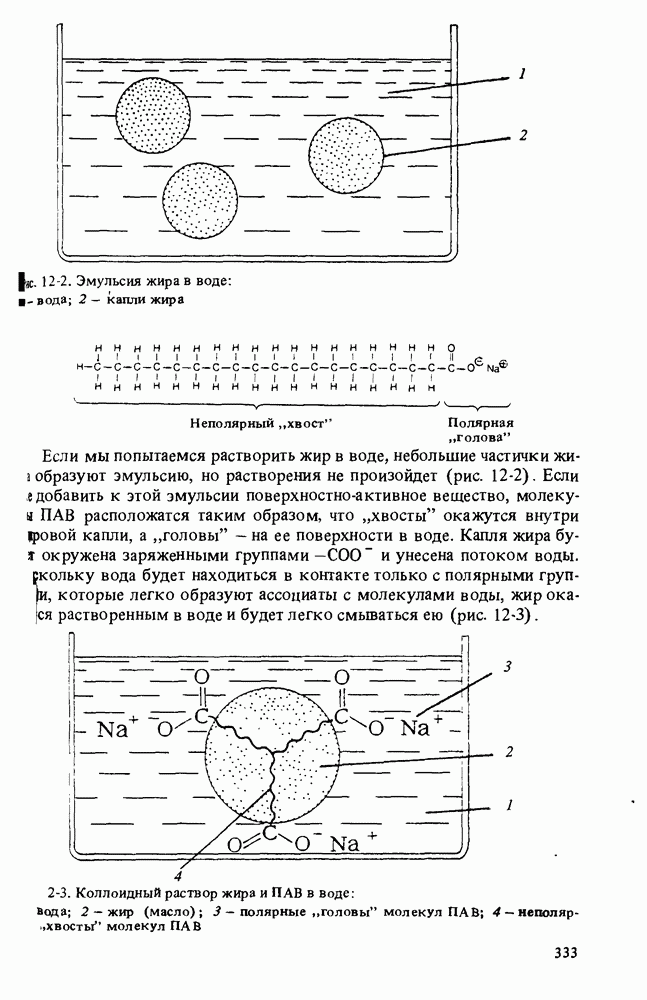
- МОЮЩИЕ СРЕДСТВА
- Прикладная органическая химия: СВОЙСТВА ВОЛОКОН
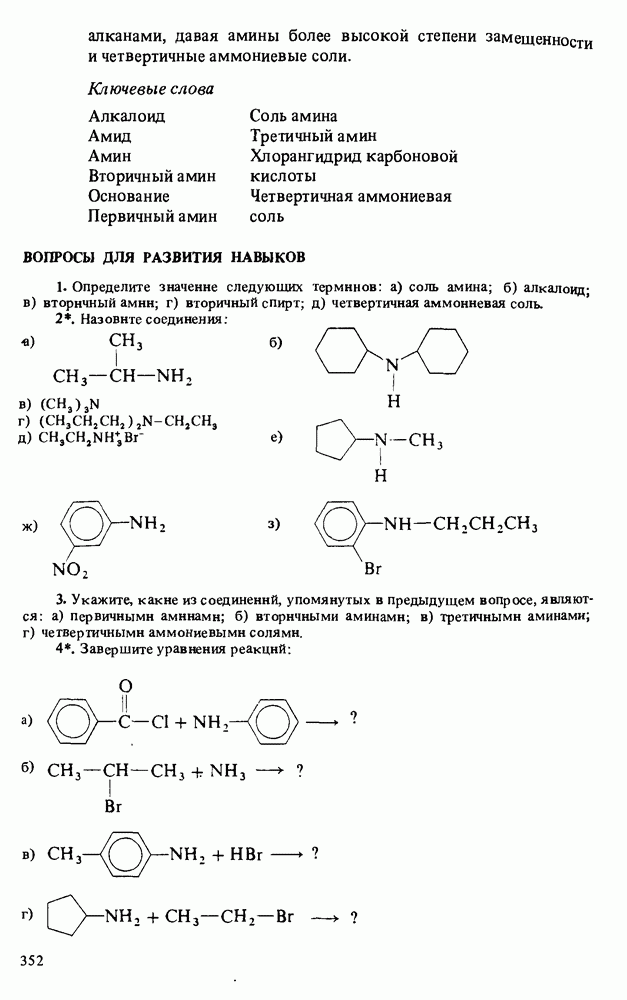
- Глава 13. АМИНЫ
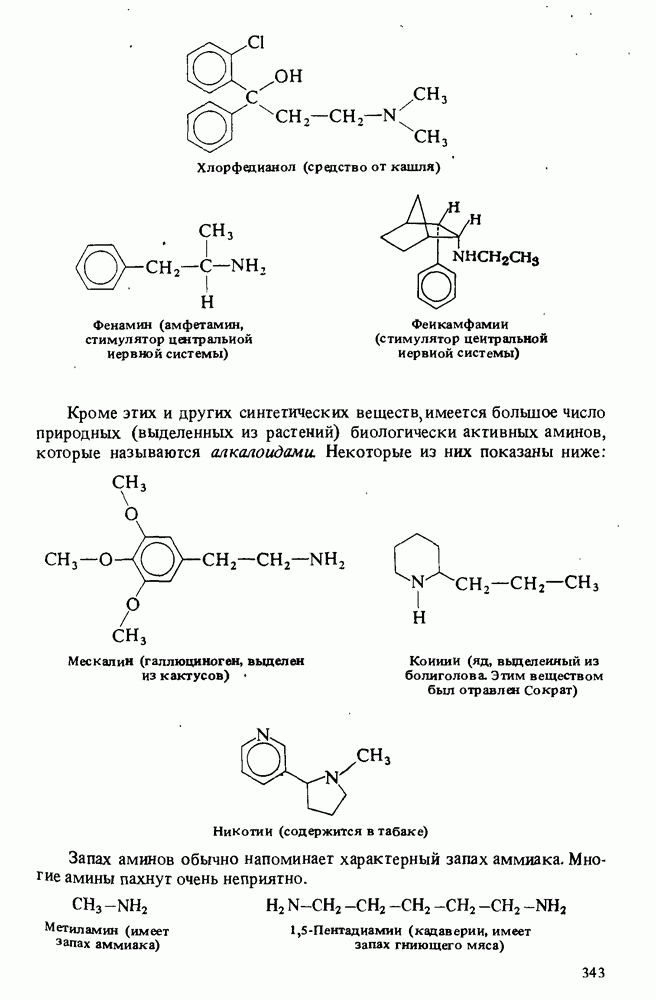
- БИОЛОГИЧЕСКИ АКТИВНЫЕ АМИНЫ
- ОСНОВНОСТЬ АМИНОВ
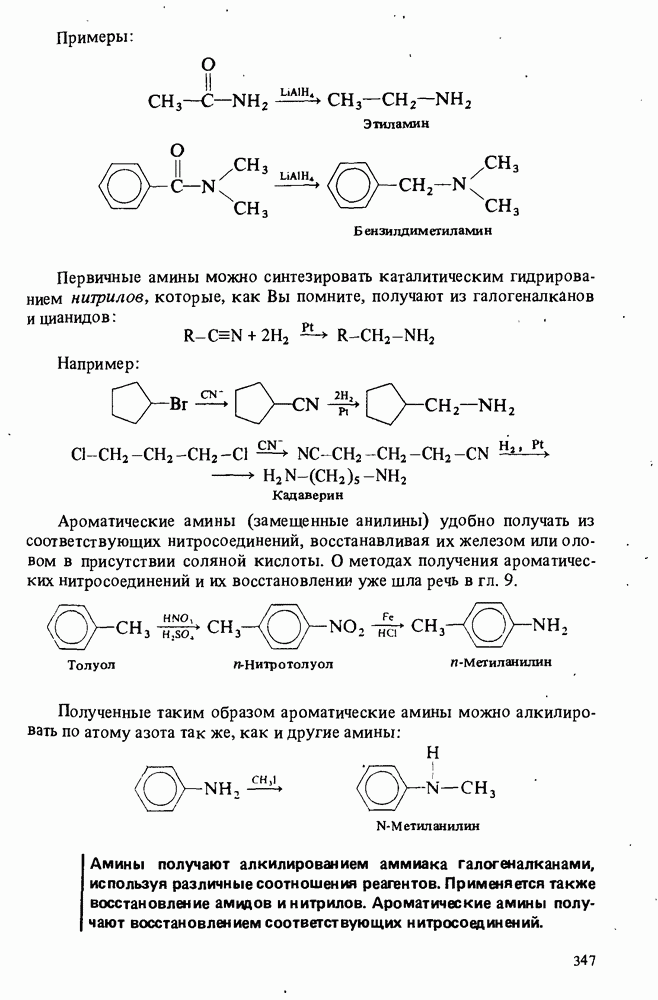
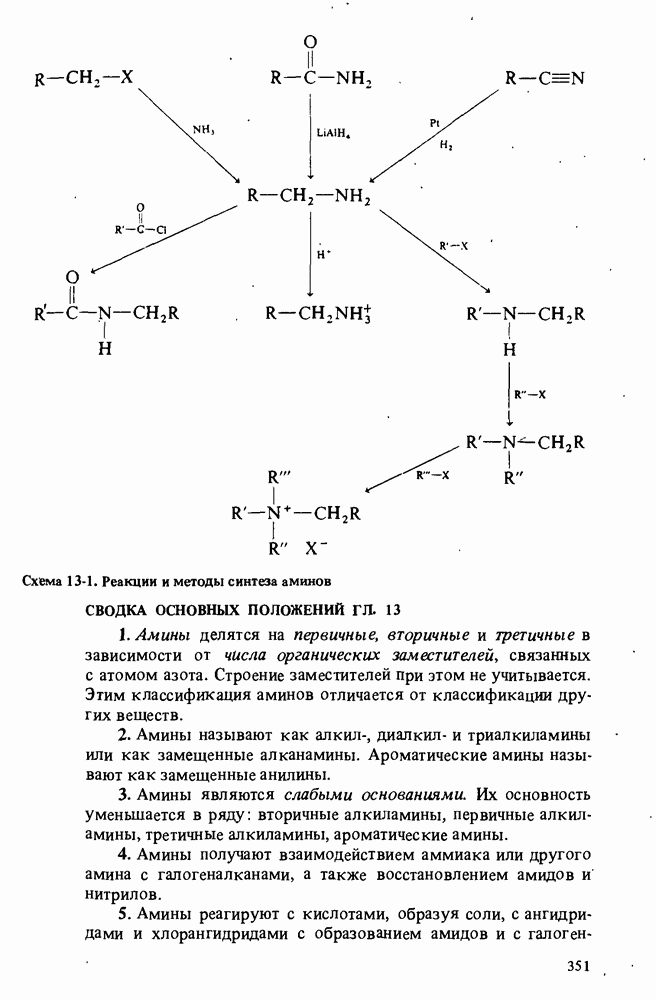
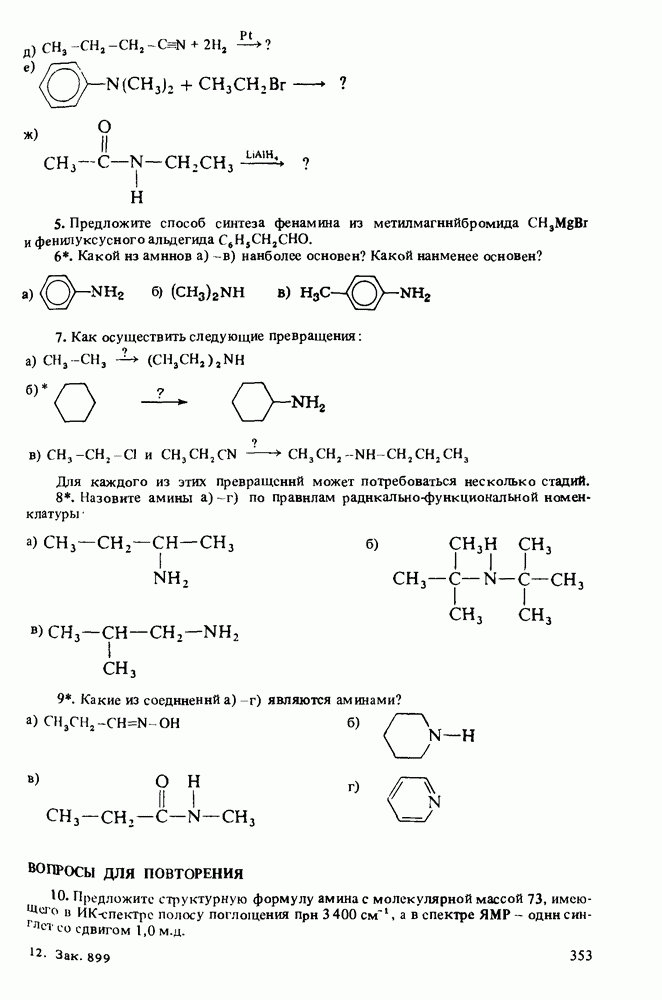
- ПОЛУЧЕНИЕ АМИНОВ
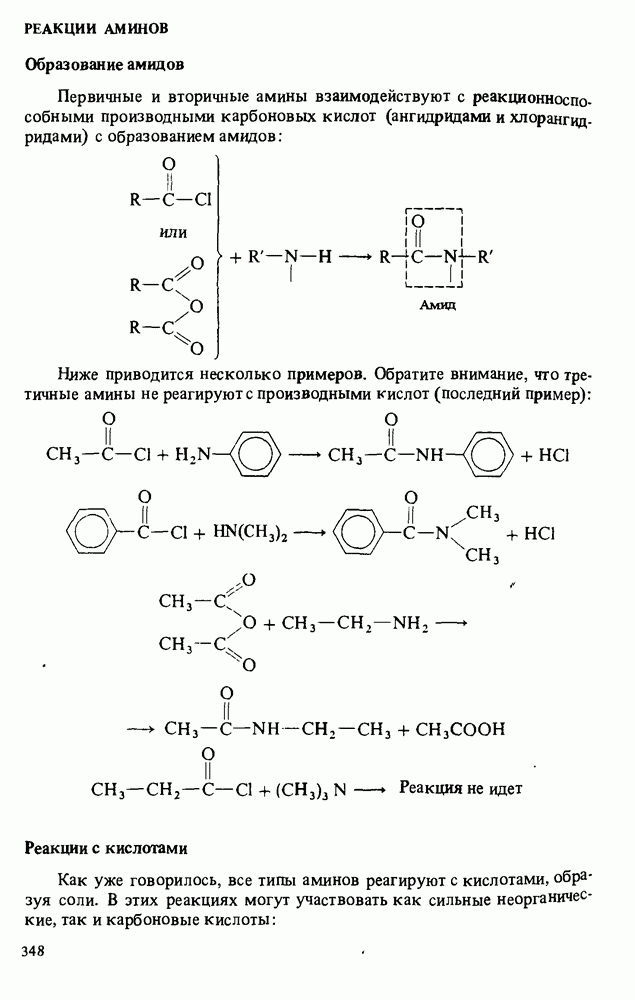
- РЕАКЦИИ АМИНОВ
- Прикладная органическая химия: ПОЛИМЕРЫ, ПОДВЕРГАЮЩИЕСЯ БИОЛОГИЧЕСКОЙ ДЕСТРУКЦИИ
- Глава 14. УГЛЕВОДЫ
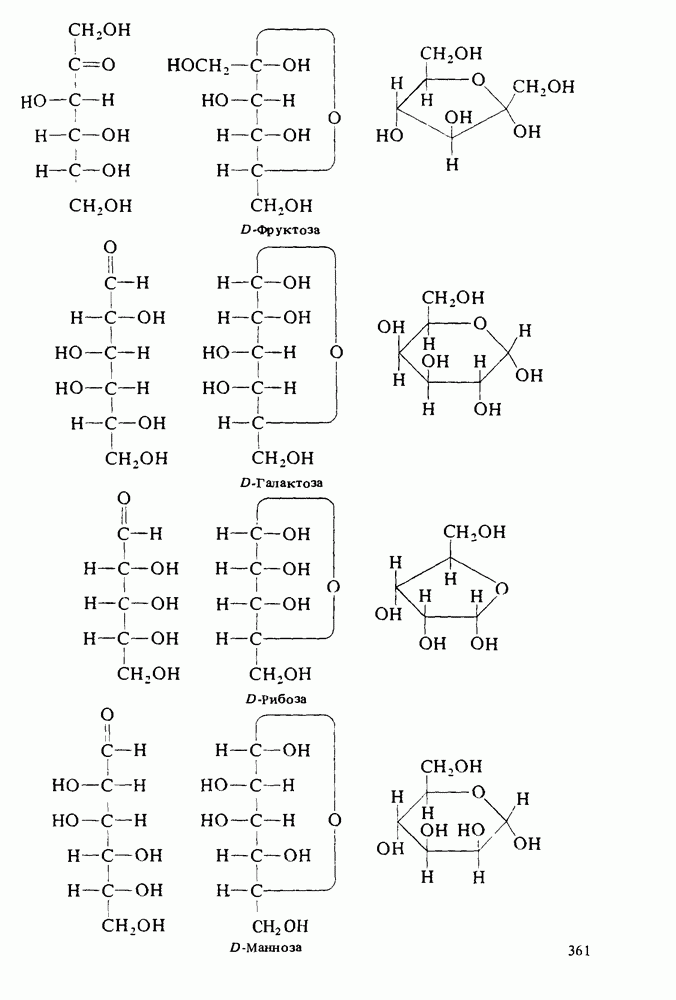
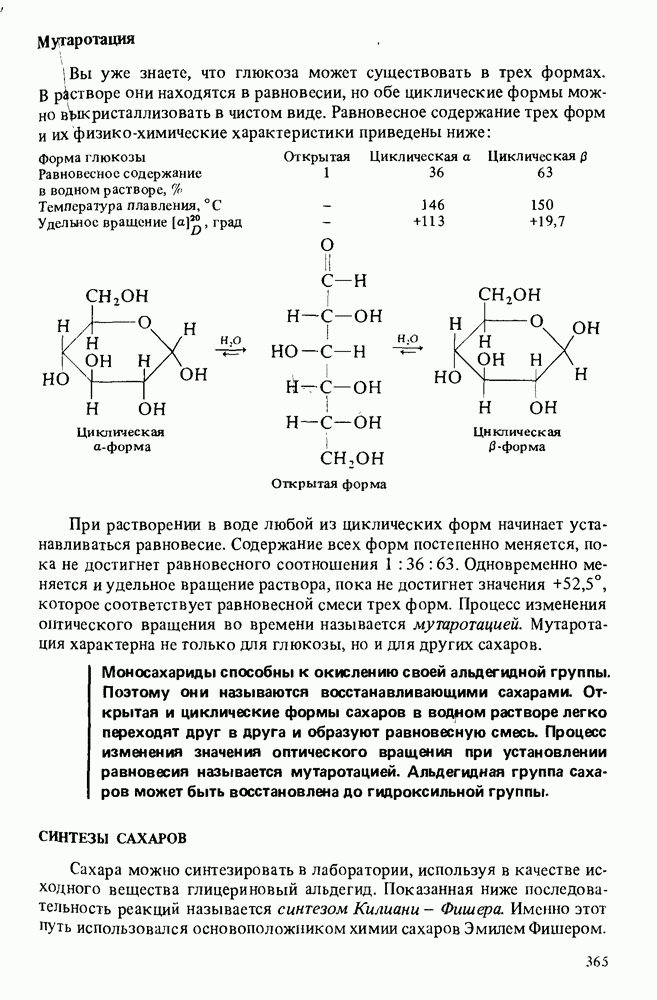
- МОНОСАХАРИДЫ
- РЕАКЦИИ МОНОСАХАРИДОВ
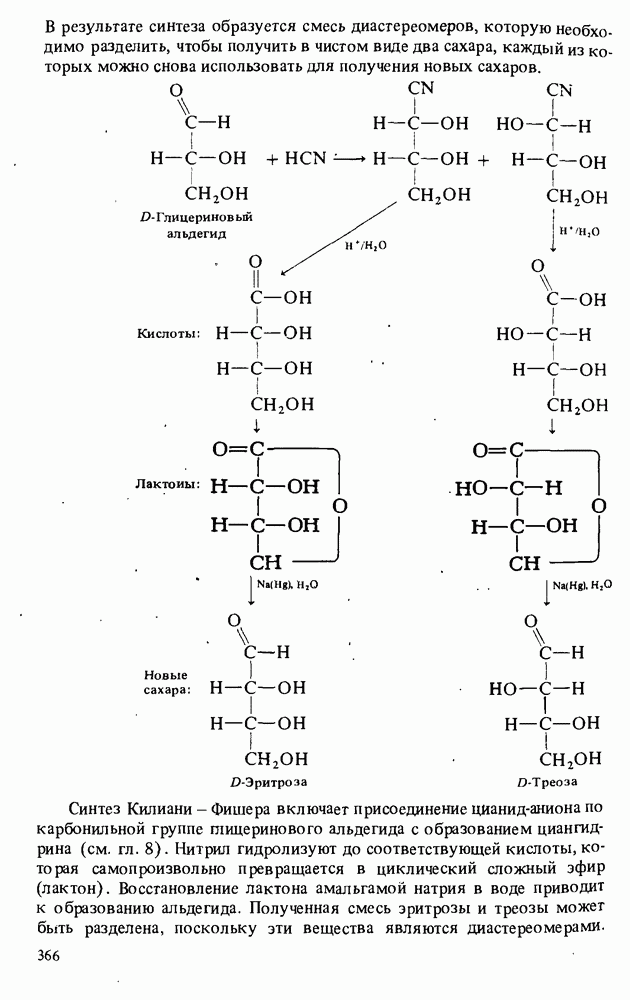
- СИНТЕЗЫ САХАРОВ
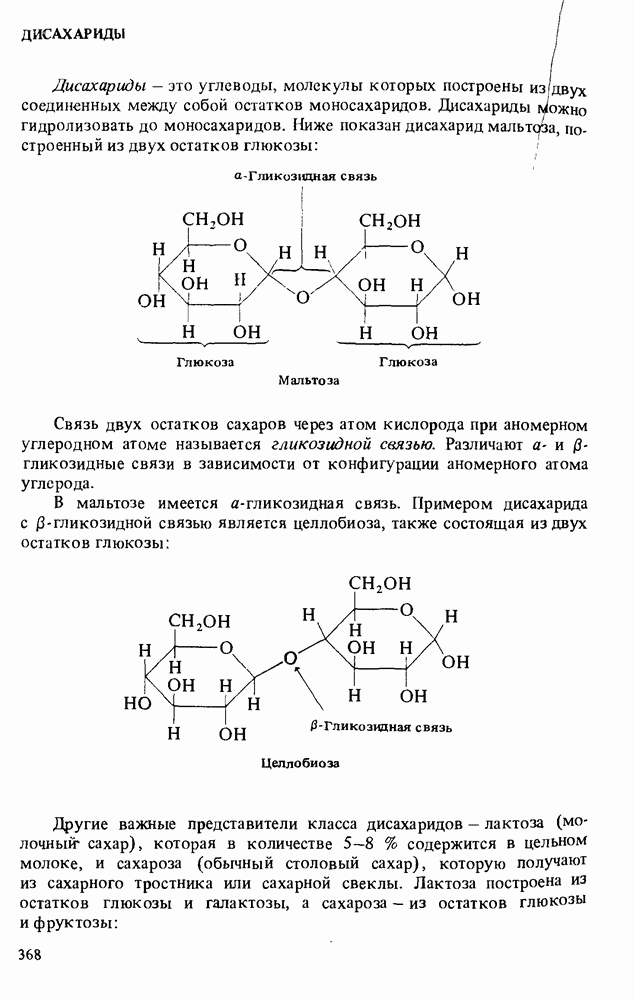
- ДИСАХАРИДЫ
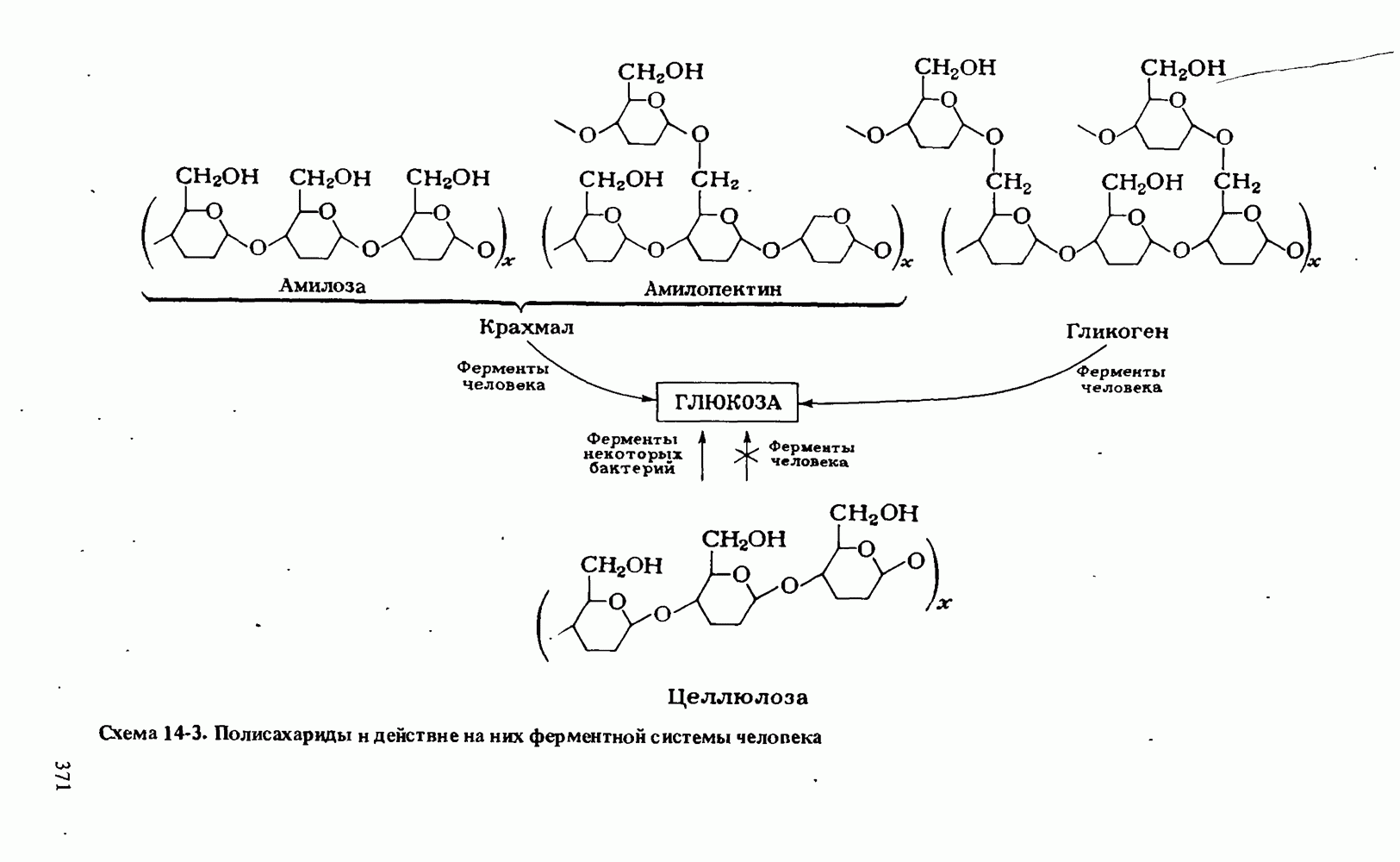
- ПОЛИСАХАРИДЫ
- Прикладная органическая химия: ПИЩЕВЫЕ СВОЙСТВА УГЛЕВОДОВ
- Глава 15. АМИНОКИСЛОТЫ И БЕЛКИ
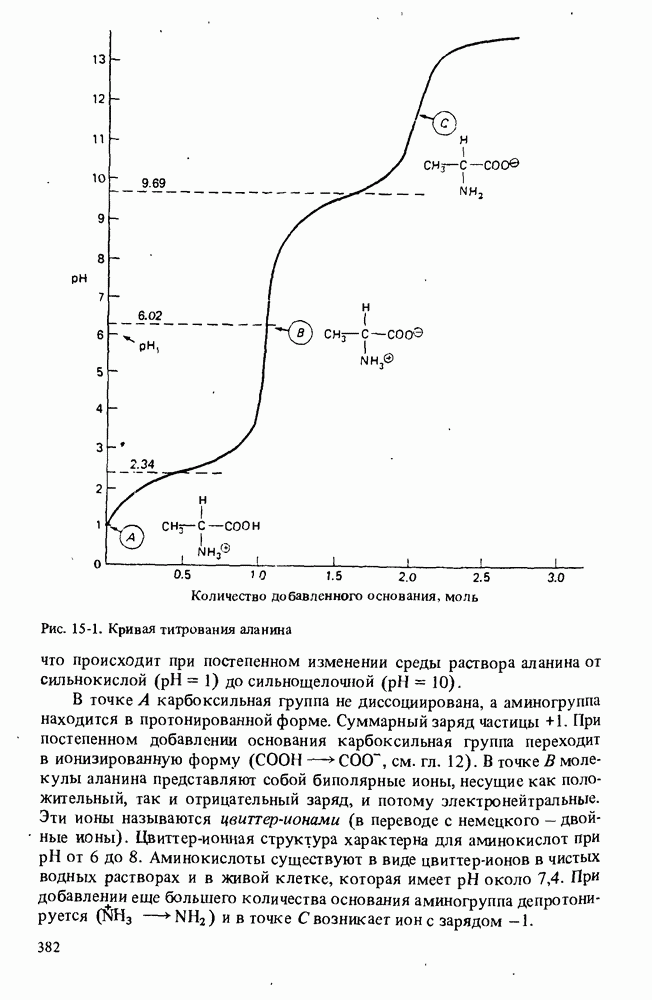
- КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА АМИНОКИСЛОТ
- АНАЛИЗ АМИНОКИСЛОТ
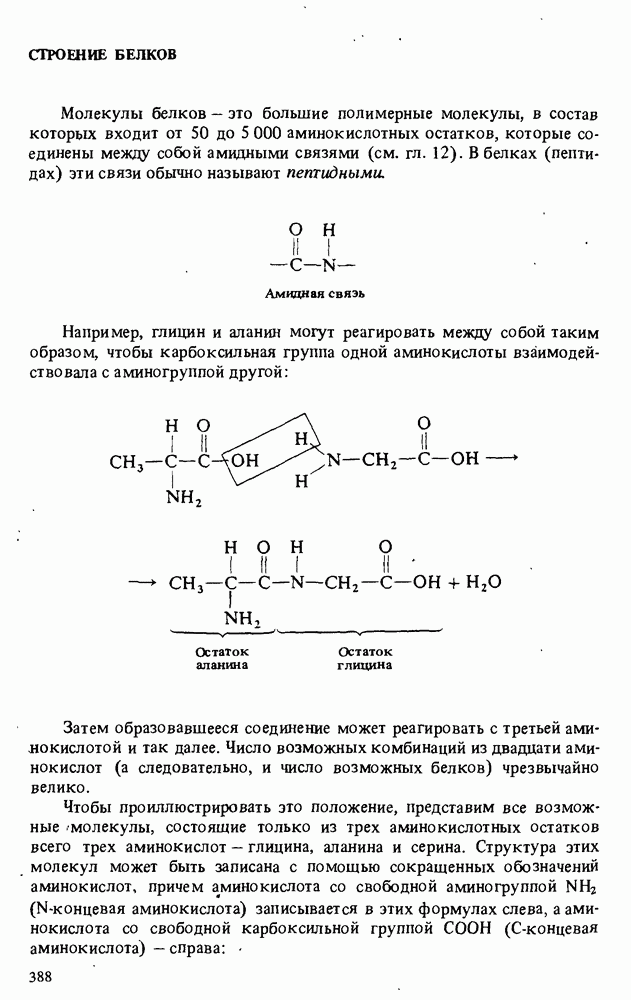
- СТРОЕНИЕ БЕЛКОВ
- УСТАНОВЛЕНИЕ ПЕРВИЧНОЙ СТРУКТУРЫ БЕЛКОВ
- ФЕРМЕНТЫ
- Глава 16. ЛИПИДЫ
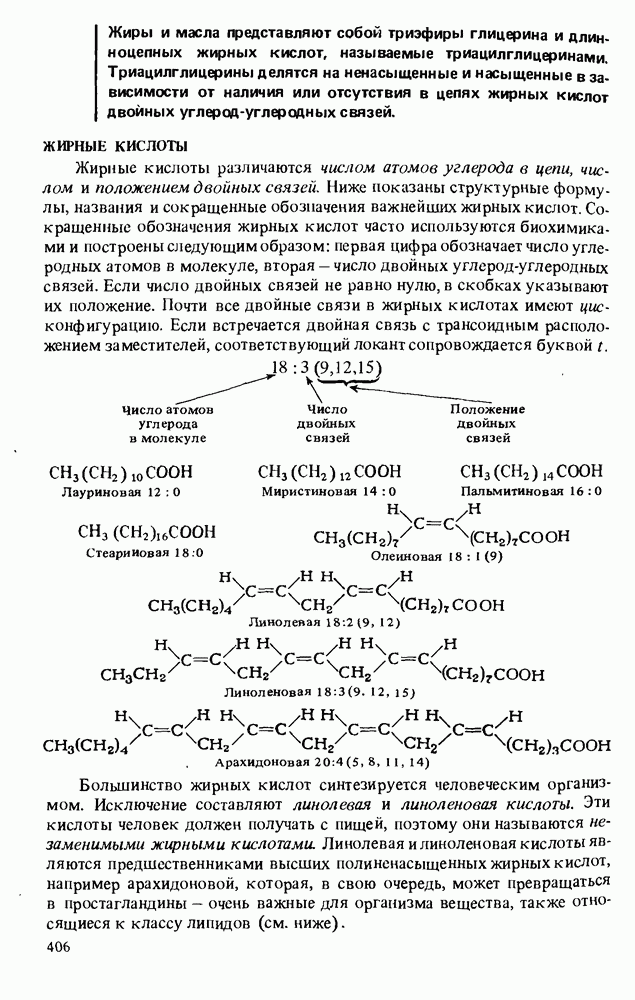
- ЖИРНЫЕ КИСЛОТЫ
- НАЗВАНИЯ ТРИАЦИЛГЛИЦЕРИНОВ
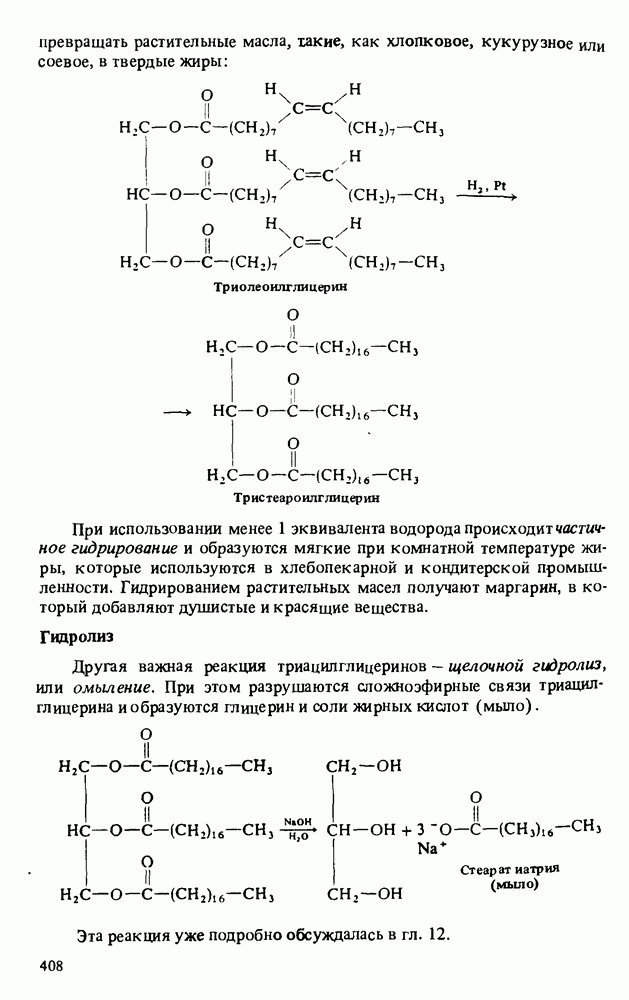
- РЕАКЦИИ ТРИАЦИЛГЛИЦЕРИНОВ
- ЛИПИДЫ, ОТЛИЧНЫЕ ОТ ТРИАЦИЛГЛИЦЕРИНОВ
- Прикладная органическая химия: ПИЩЕВЫЕ СВОЙСТВА ЛИПИДОВ
- Глава 17. НУКЛЕИНОВЫЕ КИСЛОТЫ
- РИБОНУКЛЕИНОВЫЕ КИСЛОТЫ
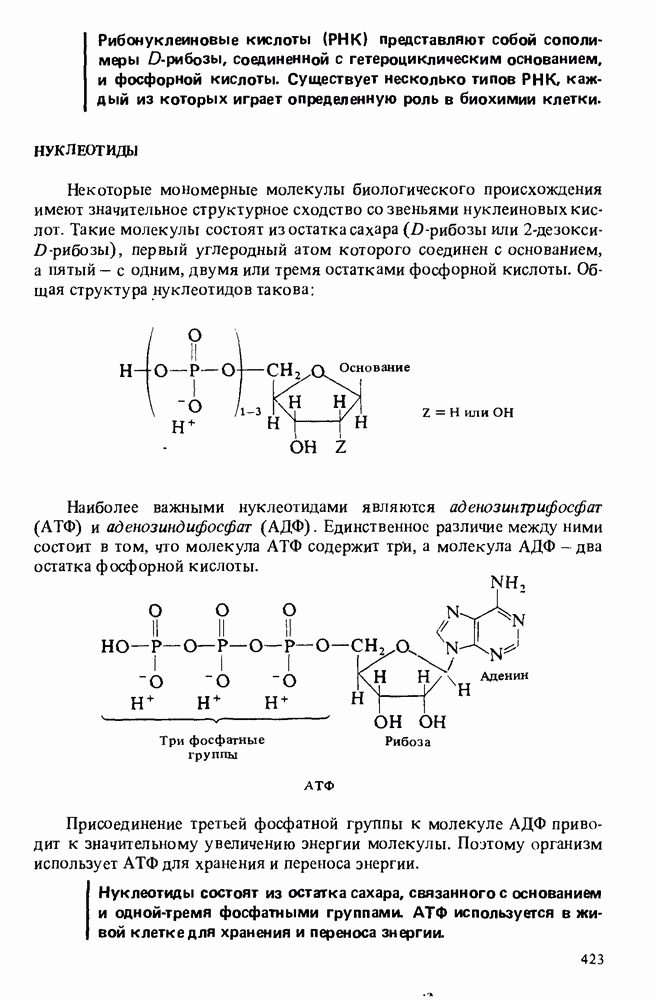
- НУКЛЕОТИДЫ
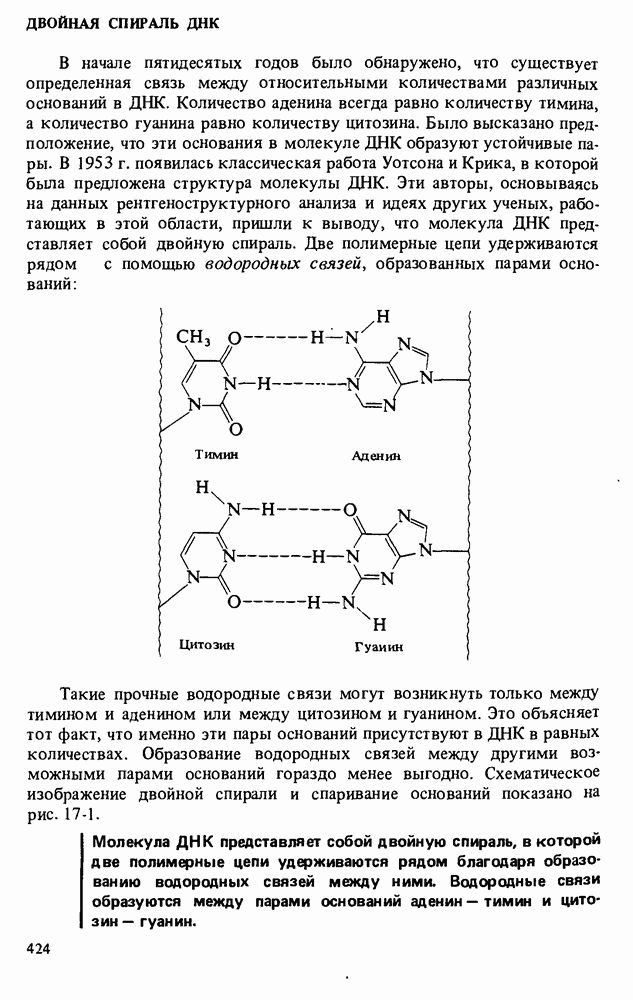
- ДВОЙНАЯ СПИРАЛЬ ДНК
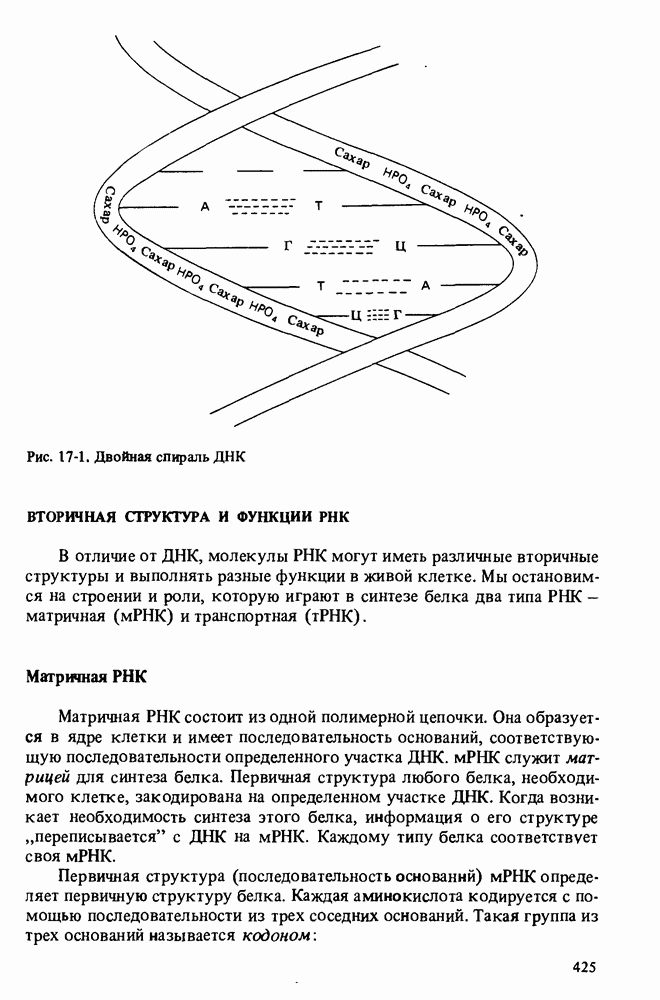
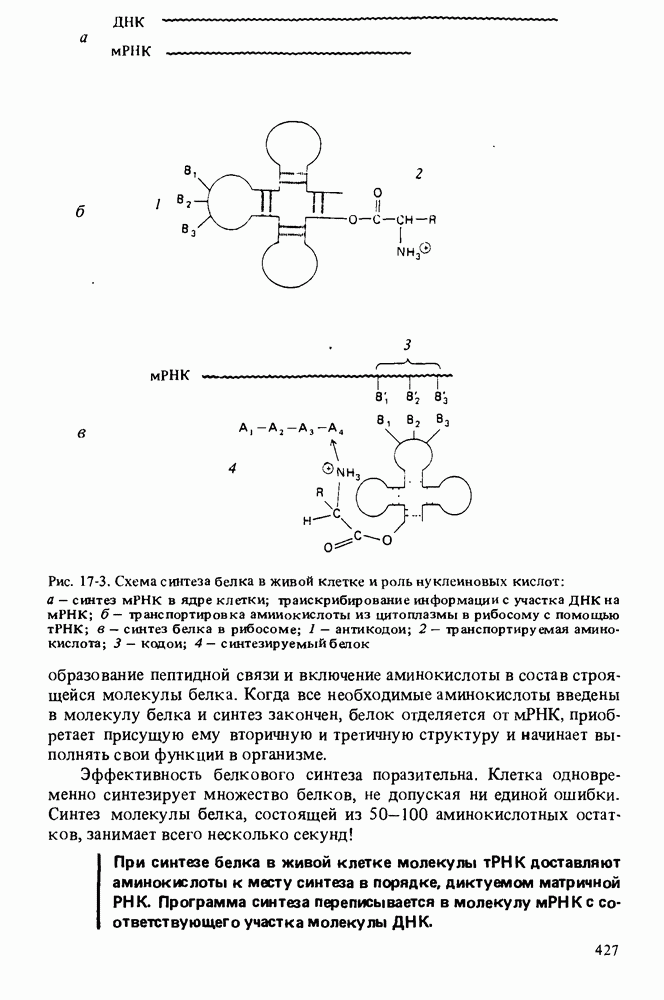
- ВТОРИЧНАЯ СТРУКТУРА И ФУНКЦИИ РНК
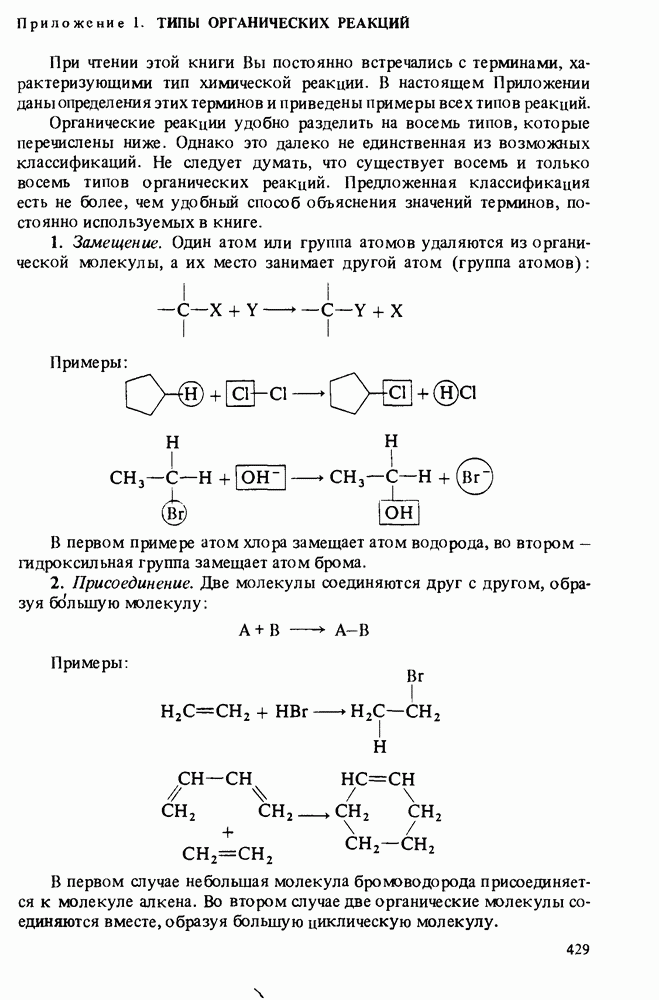
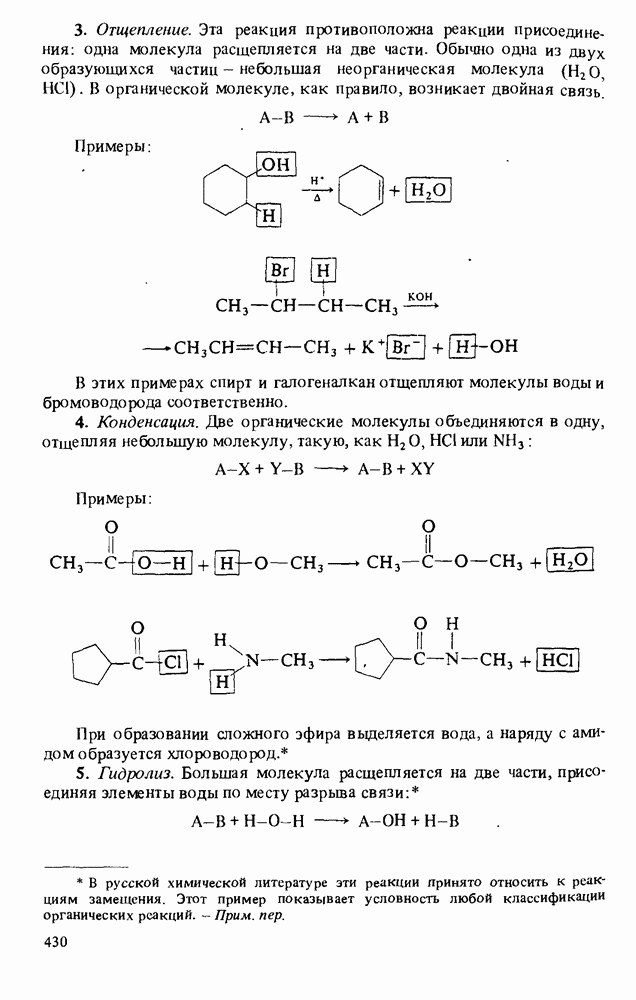
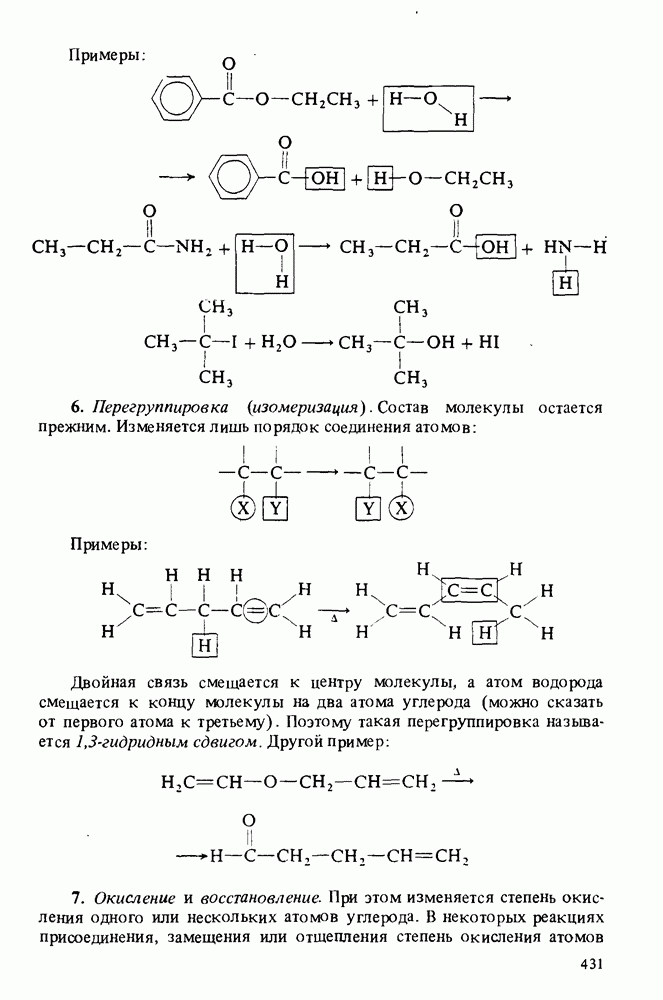
- Приложение 1. ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ
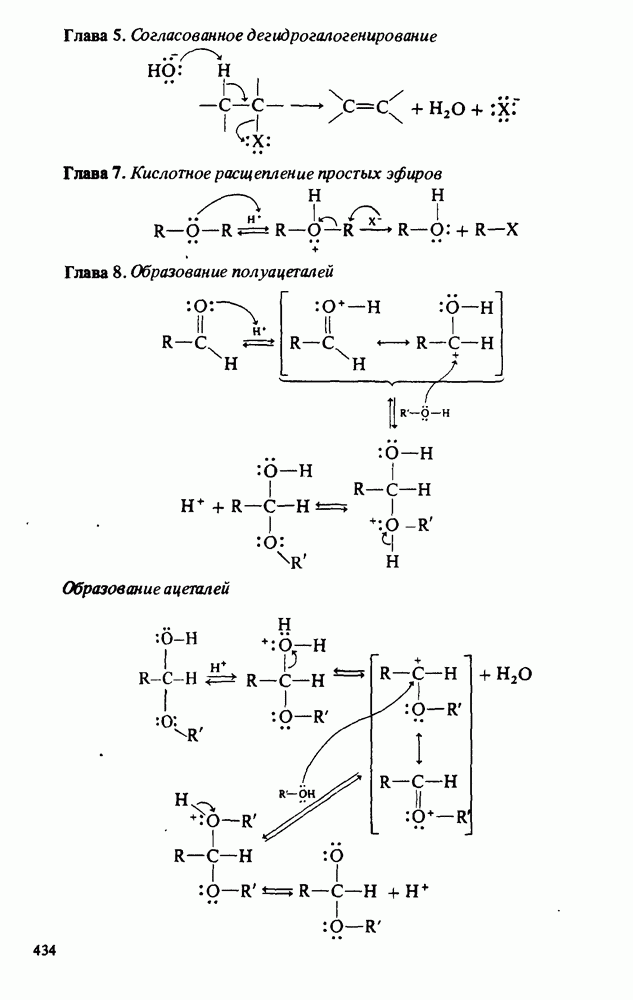
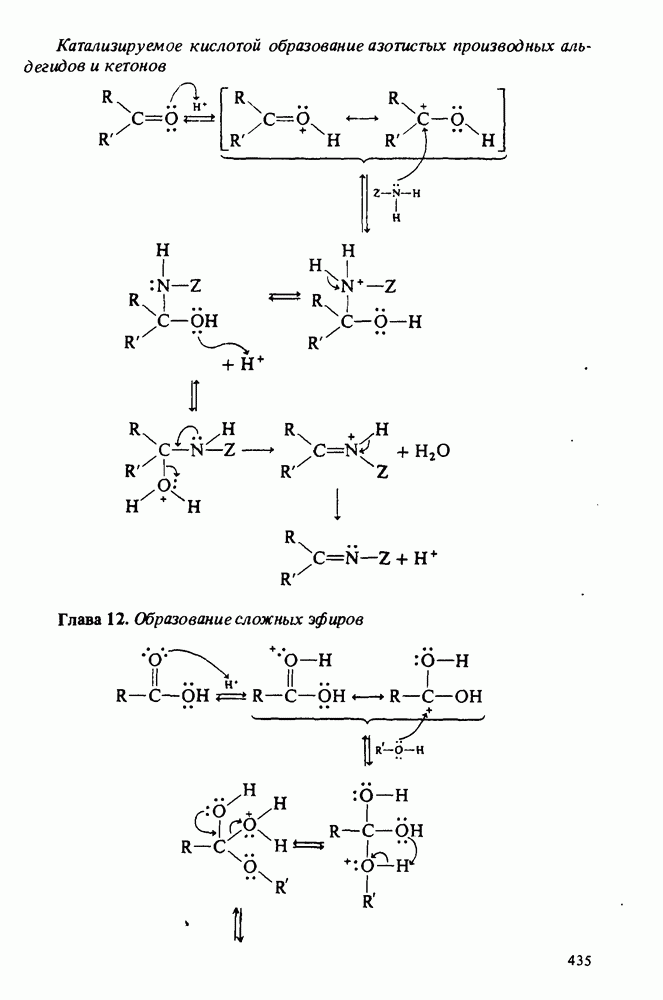
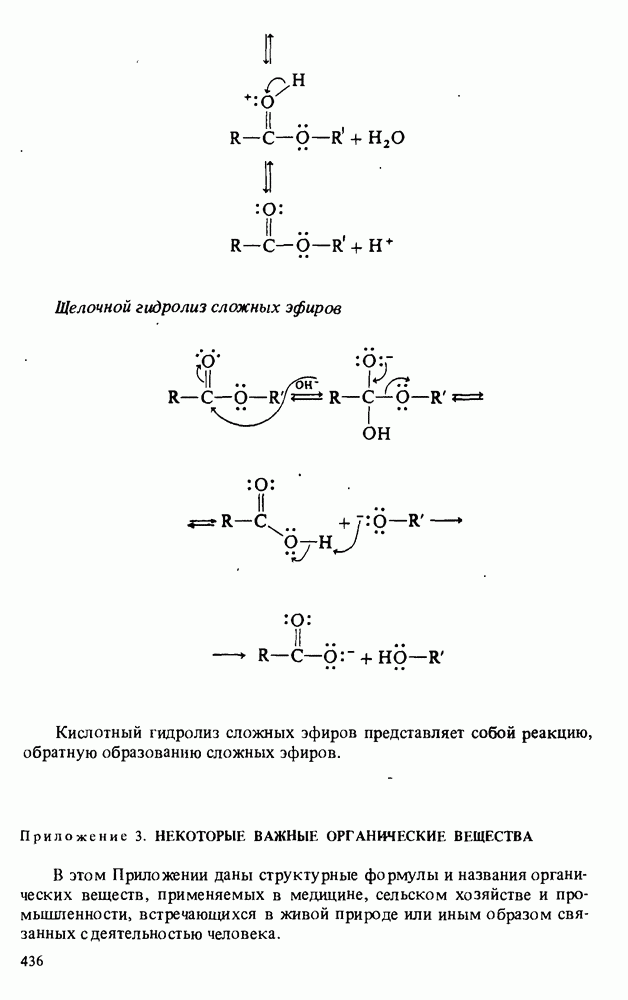
- Приложение 2. МЕХАНИЗМЫ НЕКОТОРЫХ РЕАКЦИЙ
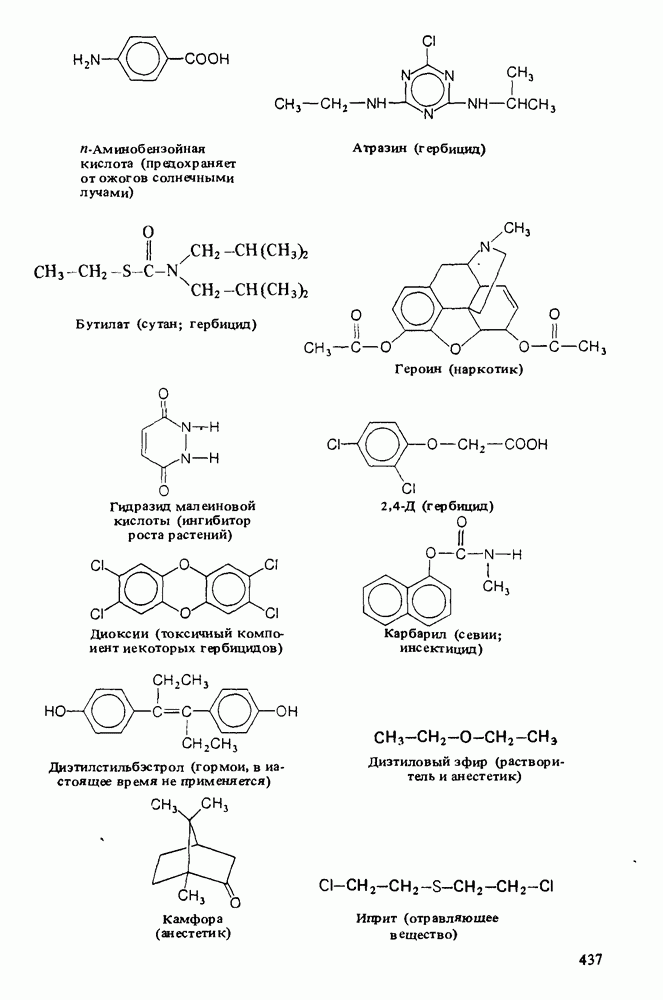
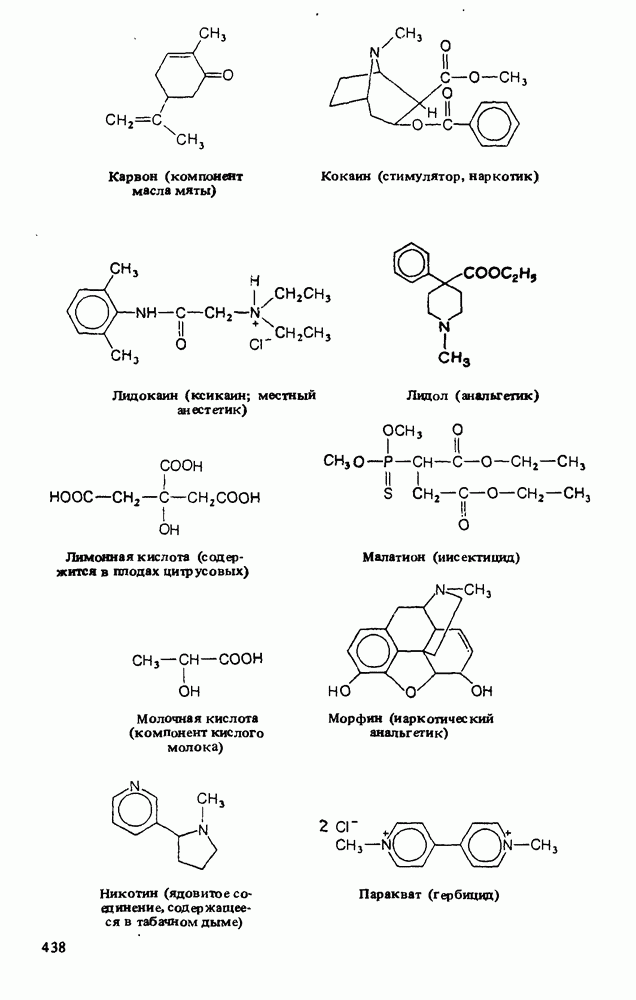
- Приложение 3. НЕКОТОРЫЕ ВАЖНЫЕ ОРГАНИЧЕСКИЕ ВЕЩЕСТВА