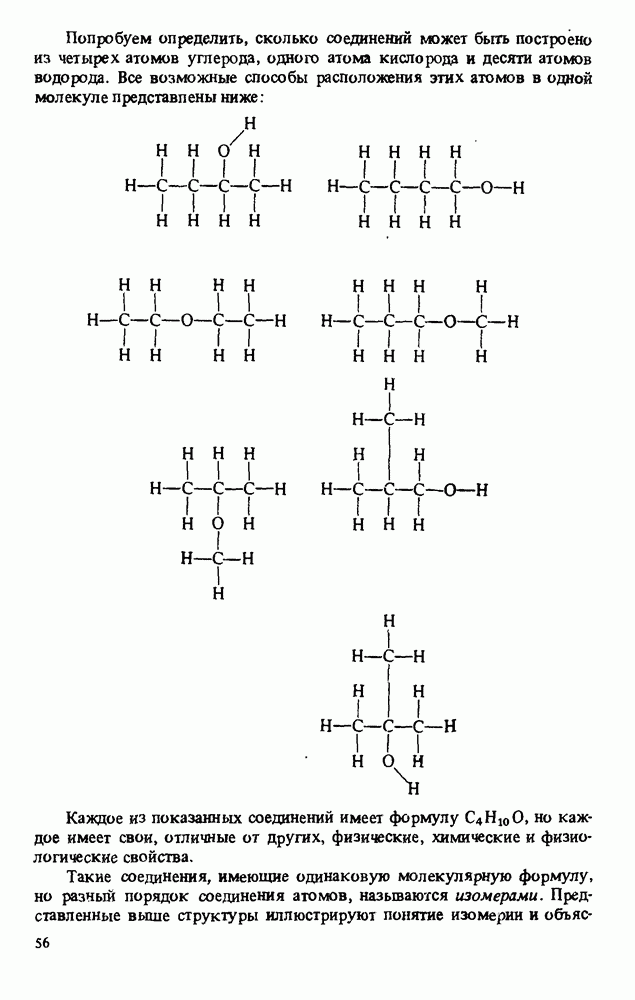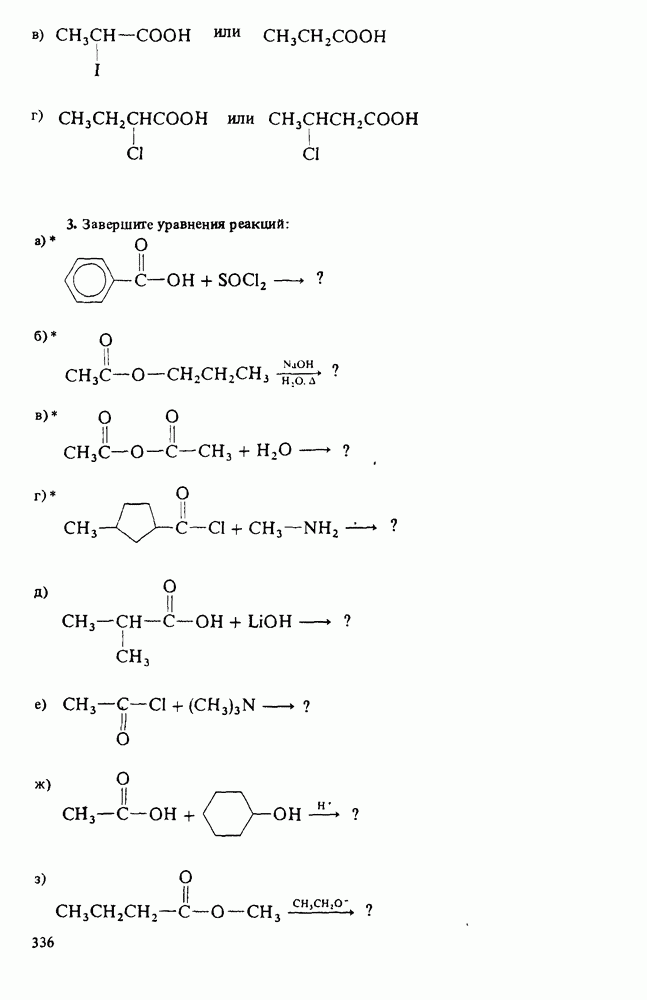| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
РЕАКЦИИ АМИНОВ
Образование амидов
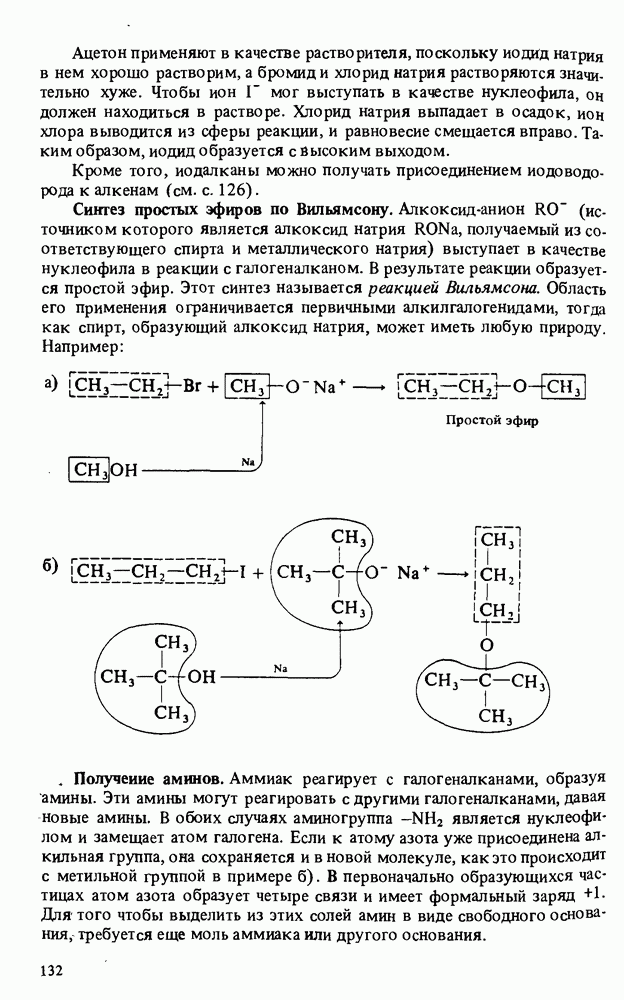
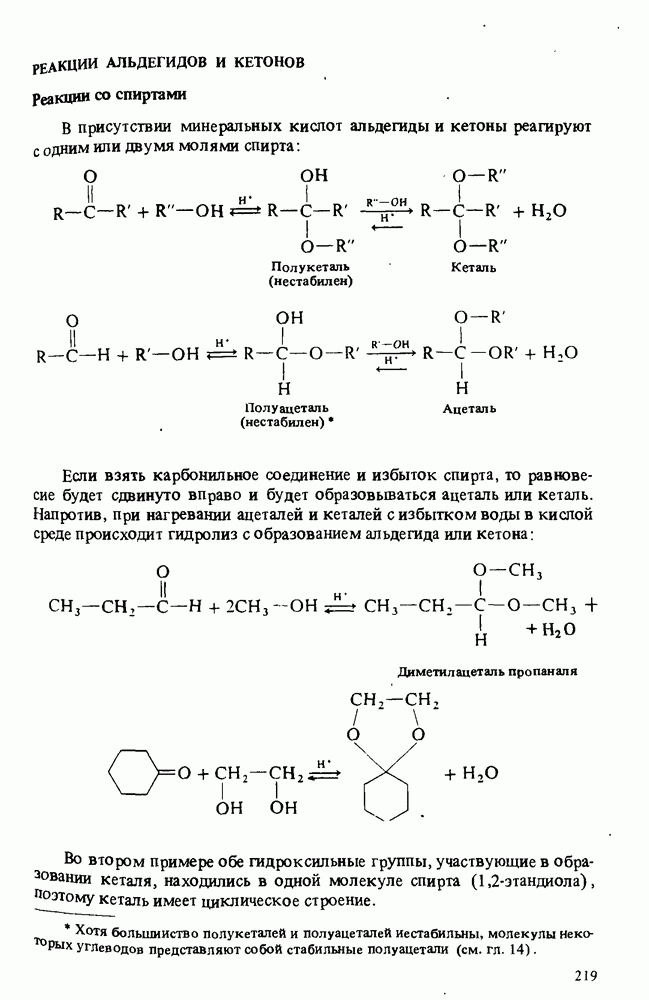
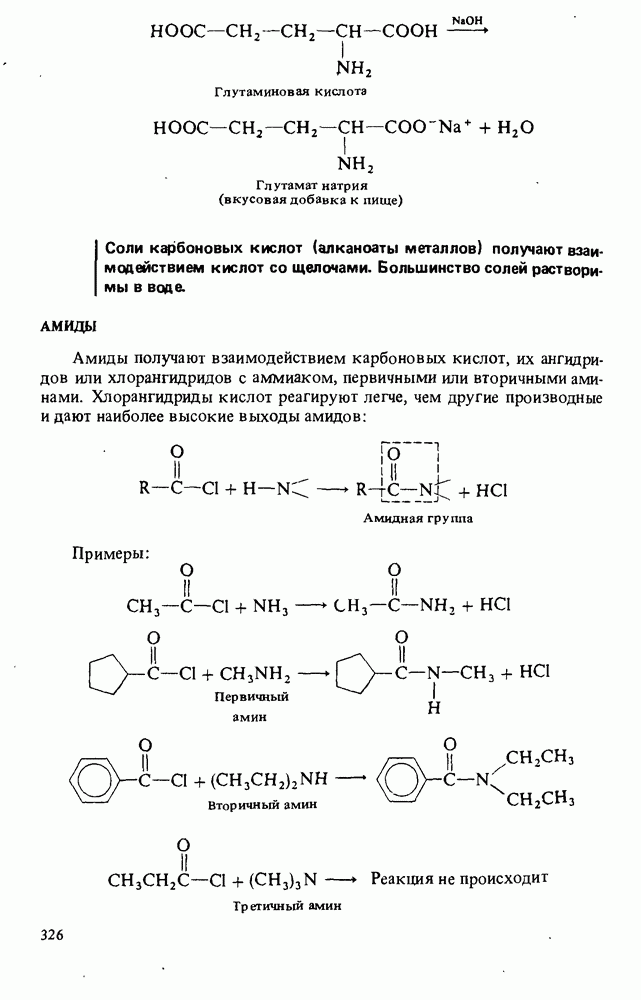
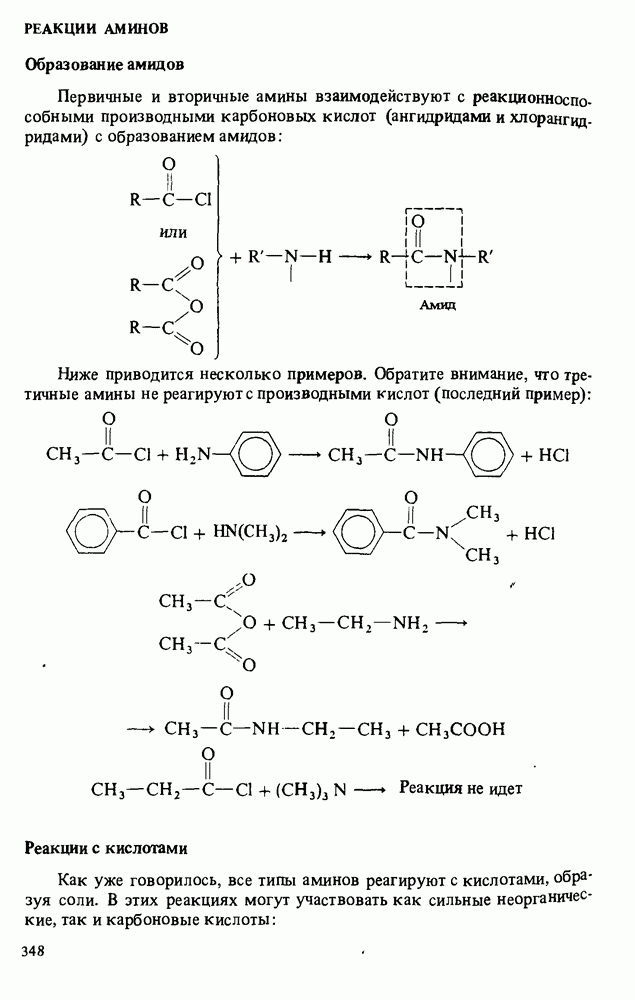
Первичные и вторичные амины взаимодействуют с реакционноспособными производными карбоновых кислот (ангидридами и хлорангид-ридами) с образованием амидов:

Циже приводится несколько примеров. Обратите внимание, что третичные амины не реагируют с производными кислот (последний пример):

Реакции с кислотами
Как уже говорилось, все типы аминов реагируют с кислотами, образуя соли. В этих реакциях могут участвовать как сильные неорганические, так и карбоновые кислоты:

Примеры:

Соли аминов называют солями замещенного аммония.
Соли аминов, как и другие соли, хорошо растворимы в воде. В то же время свободные амины, имеющие в молекуле более четырех углеродных атомов, в воде не растворяются. В отличие от самих аминов, их соли нелетучи. Реакция метиланилина с уксусной кислотой иллюстрирует процесс, происходящий при вымачивании рыбы в уксусе. Амины, сообщающие рыбе специфический запах, при этом превращаются в нелетучие соли, и поэтому не пахнут; рыбный запах исчезает или сильно ослабевает. Слабым раствором уксуса рекомендуется споласкивать руки для удаления неприятного запаха после приготовления рыбы. Амины при этом превращаются в растворимые соли, которые легко смываются водой:

Образование солей используется и для увеличения растворимости в воде аминов, являющихся лекарственными веществами. Соединение, формула которого изображена ниже, применяется как средство от кашля:

Этот амин в виде свободного основания нерастворим в воде, поэтому используется его бромоводородная соль.
Особой группой родственных аминам соединений являются четвертичные аммониевые соли. Как уже говорилось, они образуются при взаимодействии третичных аминов с галогеналканами. Четвертичные аммониевые соли, как и соли аминов, представляют собой ионные, нелетучие растворимые в воде вещества.

Некоторые четвертичные аммониевые соли, молекулы которых имеют в своем составе длинноцепные алкильные радикалы, являются детергентами и обладают бактерицидным действием:

Амины реагируют с галогеналканами, образуя новые амины более высокой степени замещенности и четвертичные аммониевые соли. При обработке минеральными и карбоновыми кислотами амины образуют соли, которые лучше растворимы в воде и гораздо менее летучи, чем свободные амины. При взаимодействии с реакционноспособными производными карбоновых кислот (ангидридами и хлорангидридами) амины дают амиды.
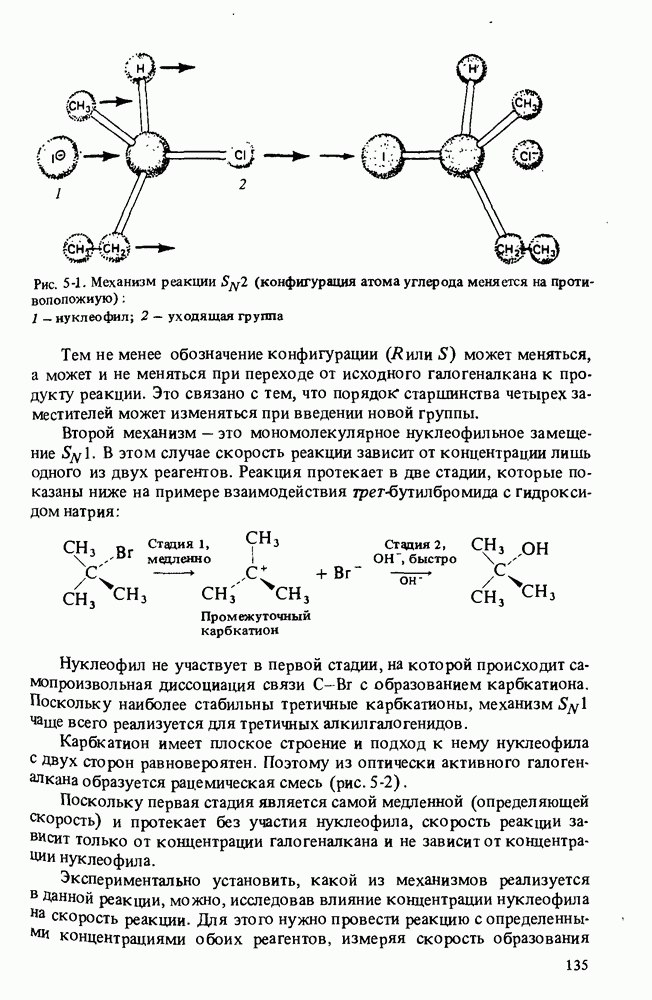
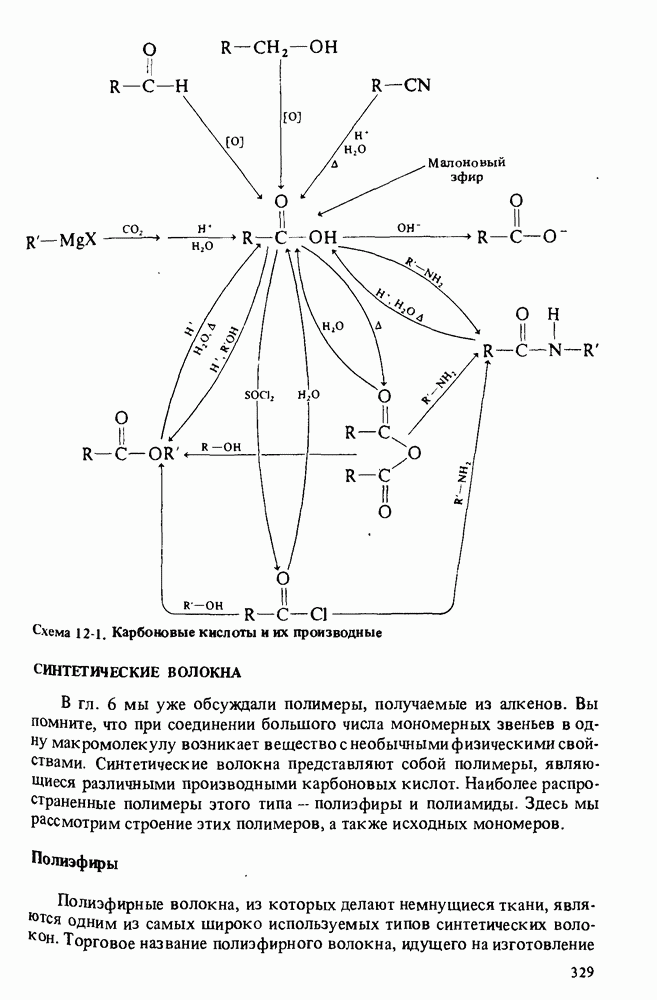
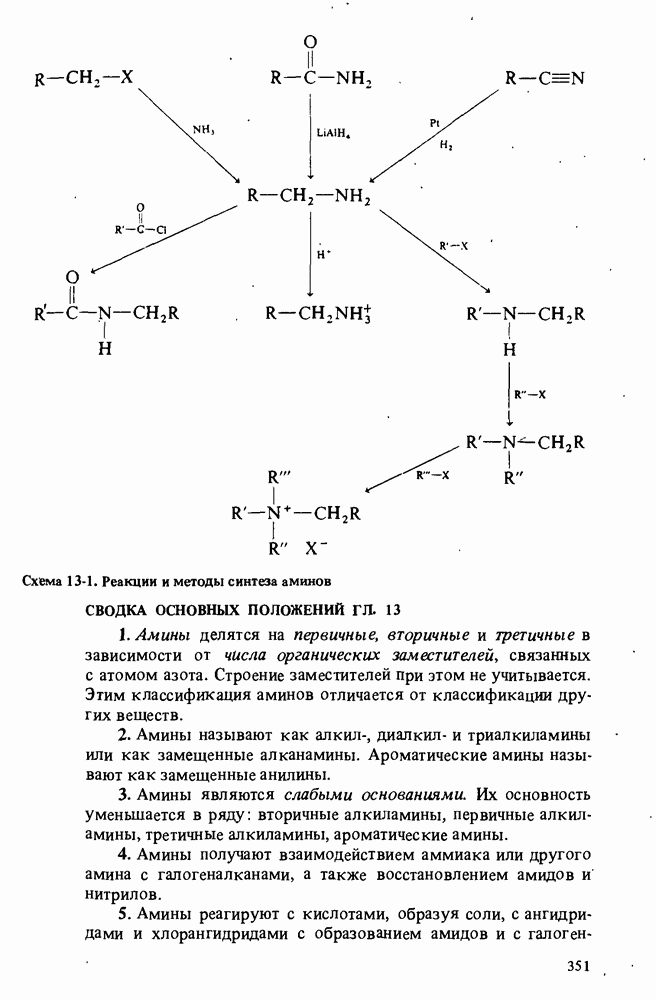
Схема 13-1. (см. скан) Реакции и методы синтеза аминов
СВОДКА ОСНОВНЫХ ПОЛОЖЕНИЙ ГЛ. 13
1. Амины делятся на первичные; вторичные и третичные в зависимости от числа органических заместителей, связанных с атомом азота. Строение заместителей при этом не учитывается. Этим классификация аминов отличается от классификации других веществ.
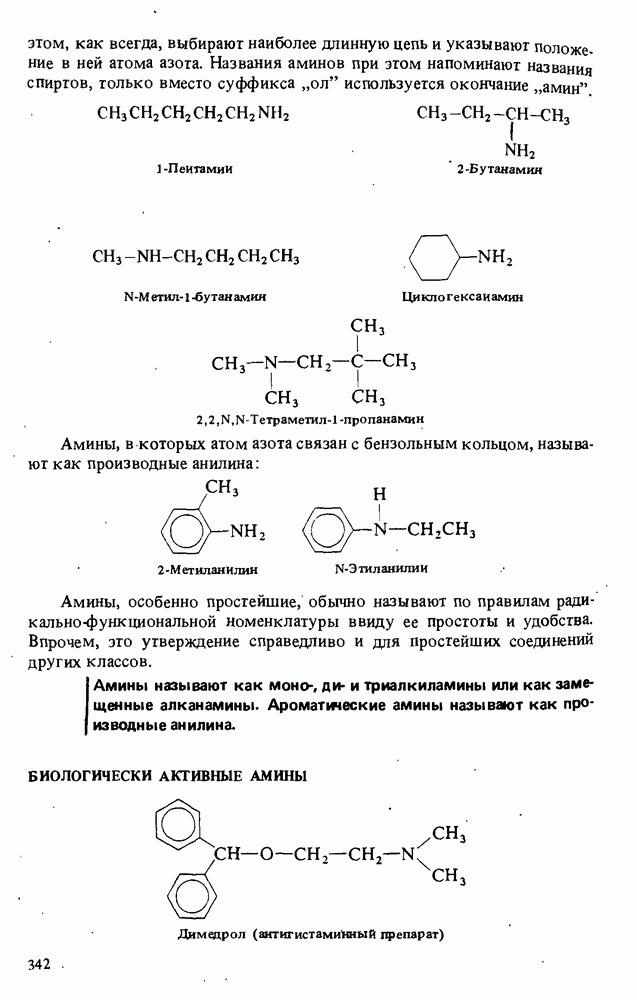
2. Амины называют как алкил-, диалкил- и триалкиламины или как замещенные алканамины. Ароматические амины называют как замещенные анилины.
3. Амины являются слабыми основаниями. Их основность уменьшается в ряду: вторичные алкиламины, первичные алкиламины, третичные алкиламины, ароматические амины.
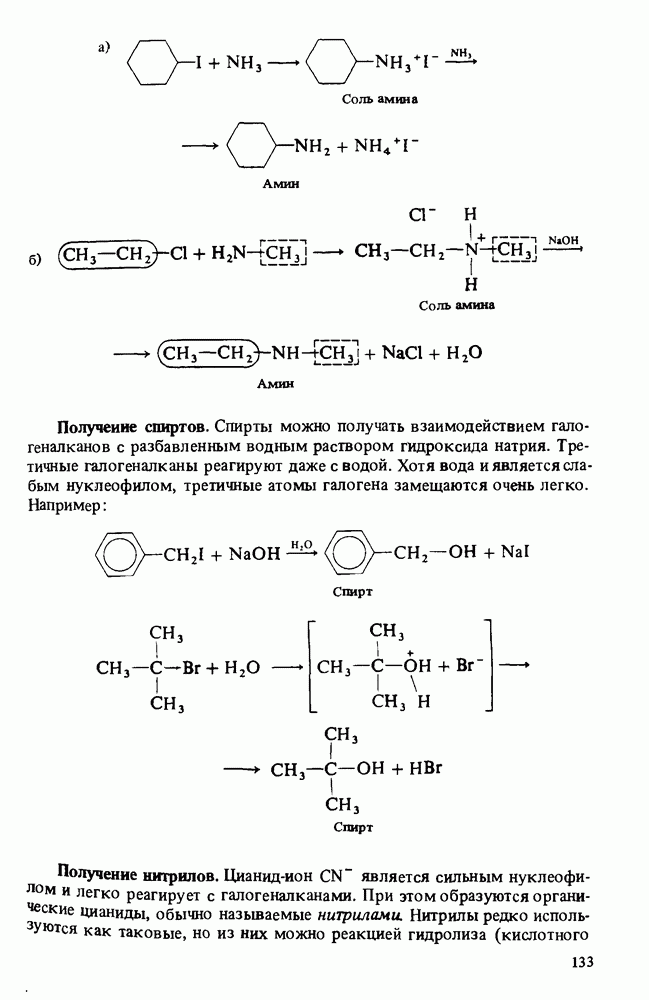
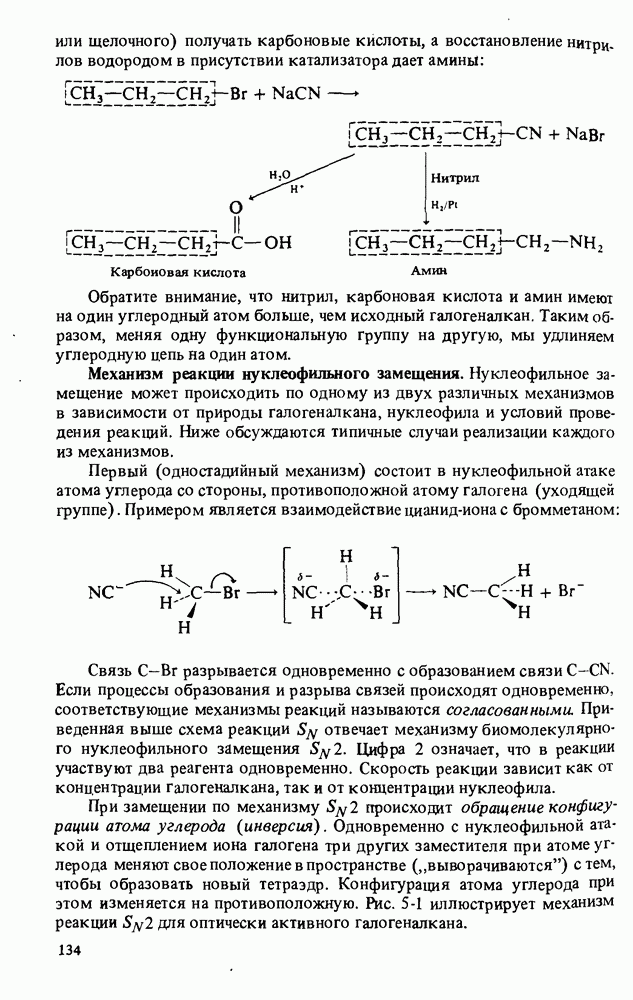
4. Амины получают взаимодействием аммиака или другого амина с галогеналканами, а также восстановлением амидов и нитрилов.
5. Амины реагируют с кислотами, образуя соли, с ангидридами и хлорангидридами с образованием амидов и с
галоген-алканами, давая амины более высокой степени замещенности и четвертичные аммониевые соли.
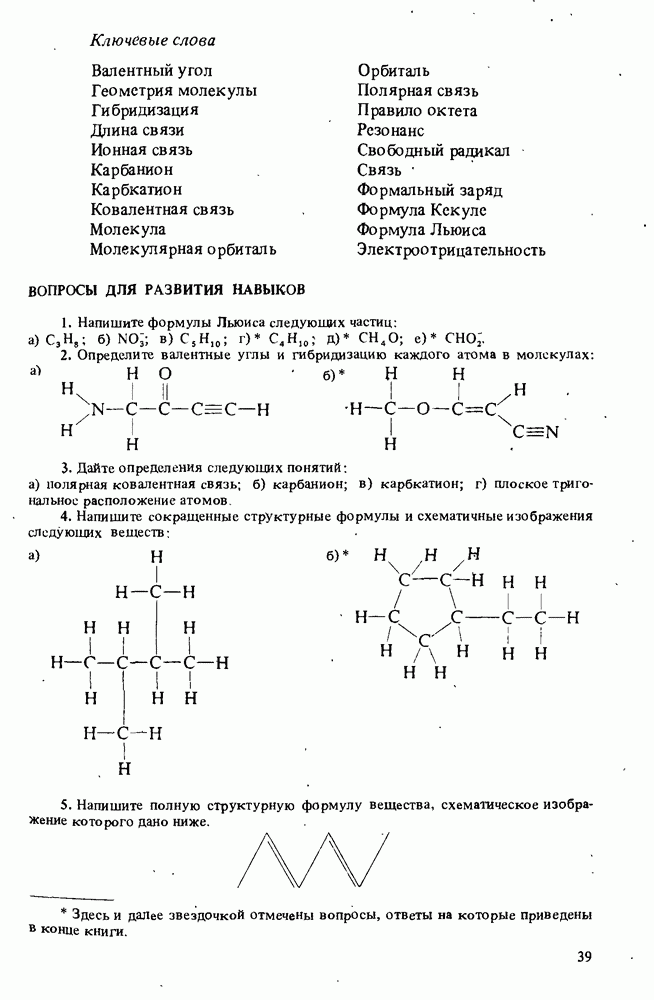
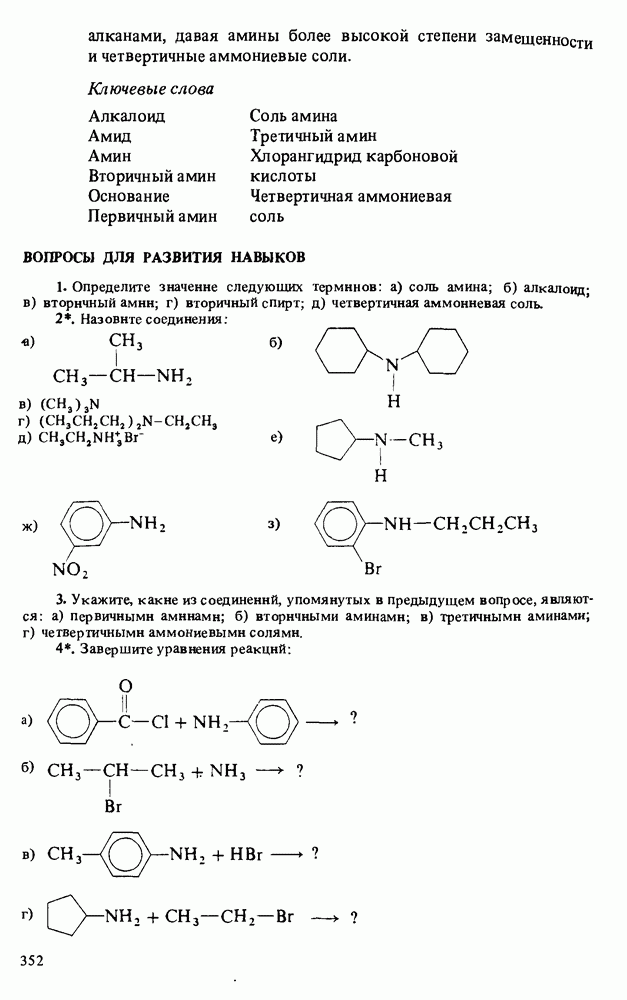
Ключевые слова
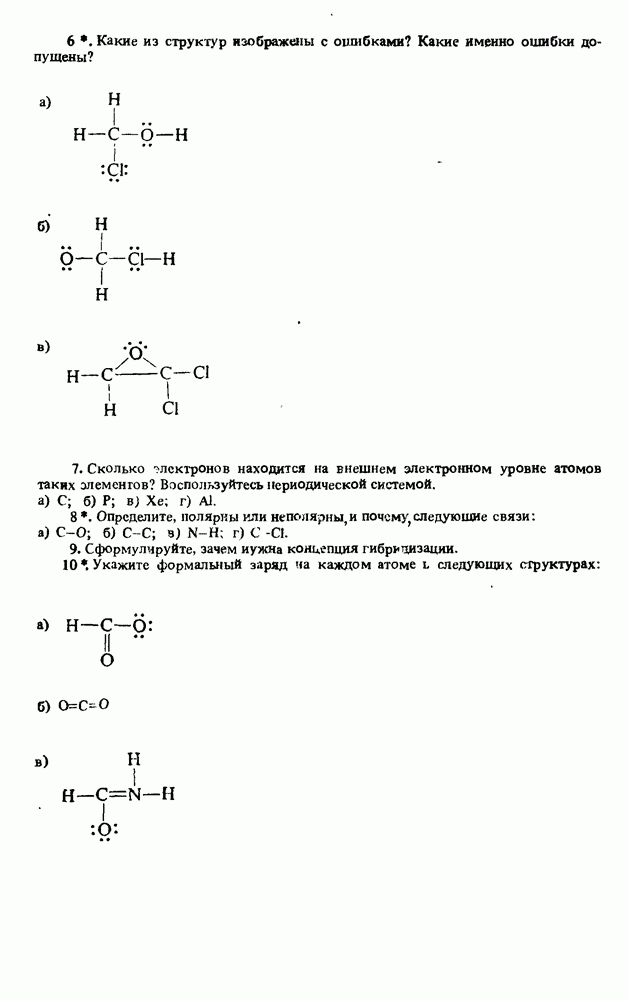
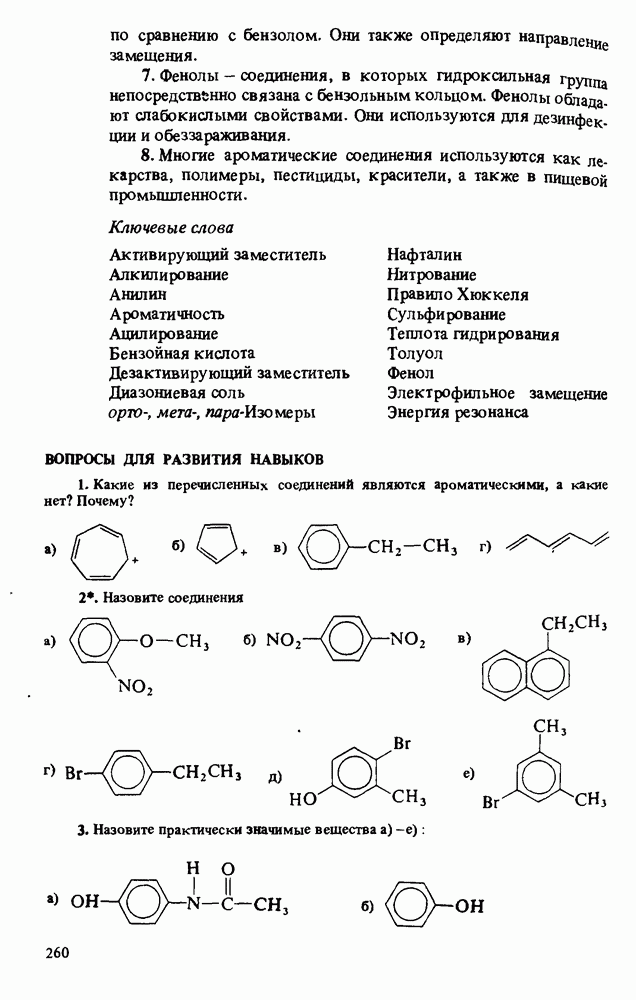
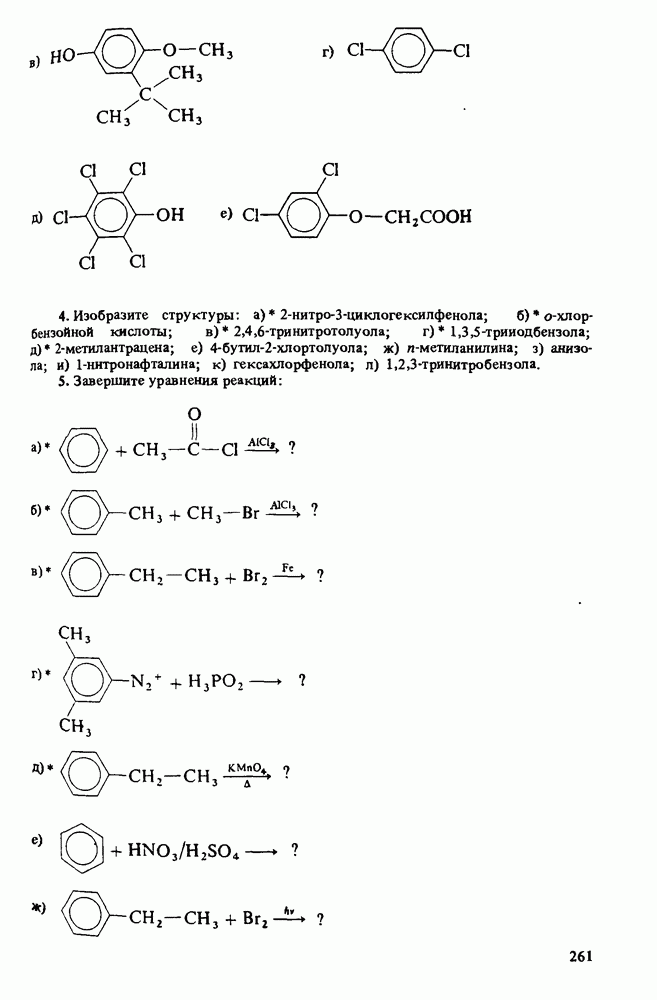
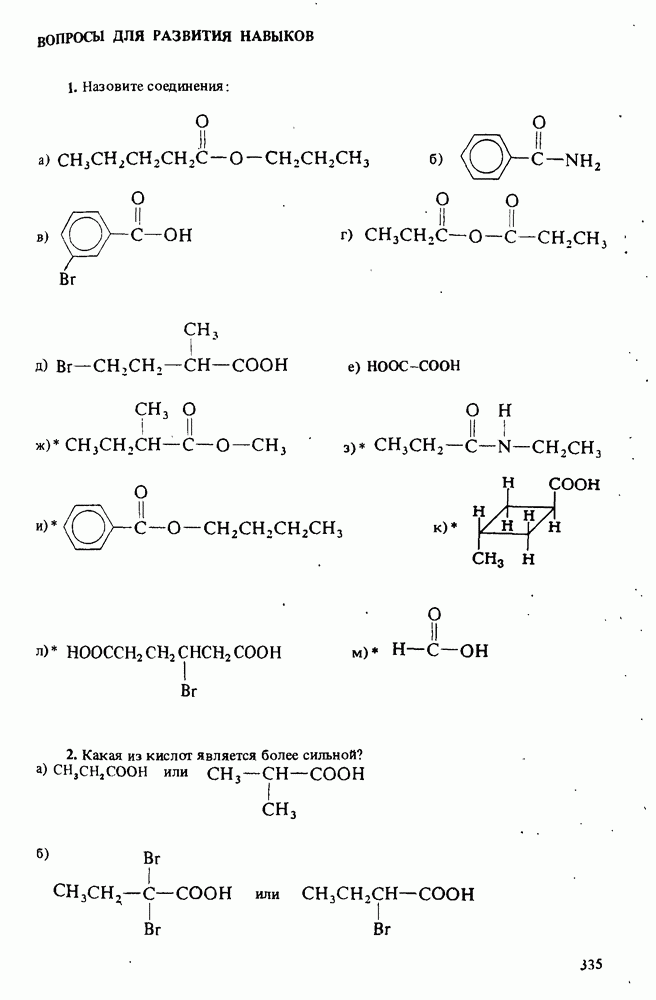
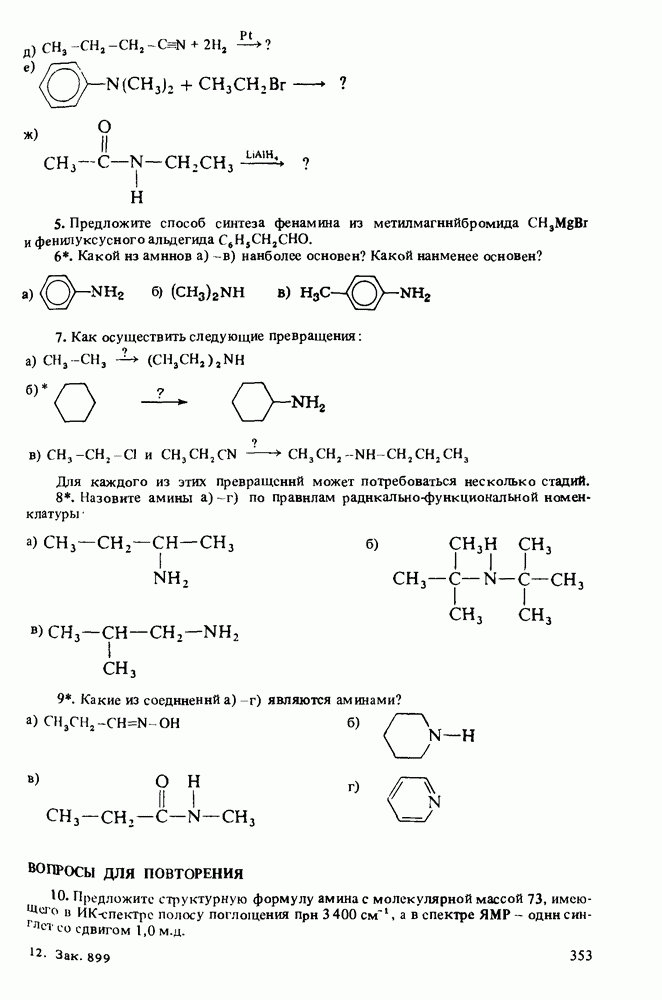
ВОПРОСЫ ДЛЯ РАЗВИТИЯ НАВЫКОВ
(см. скан)
(см. скан)
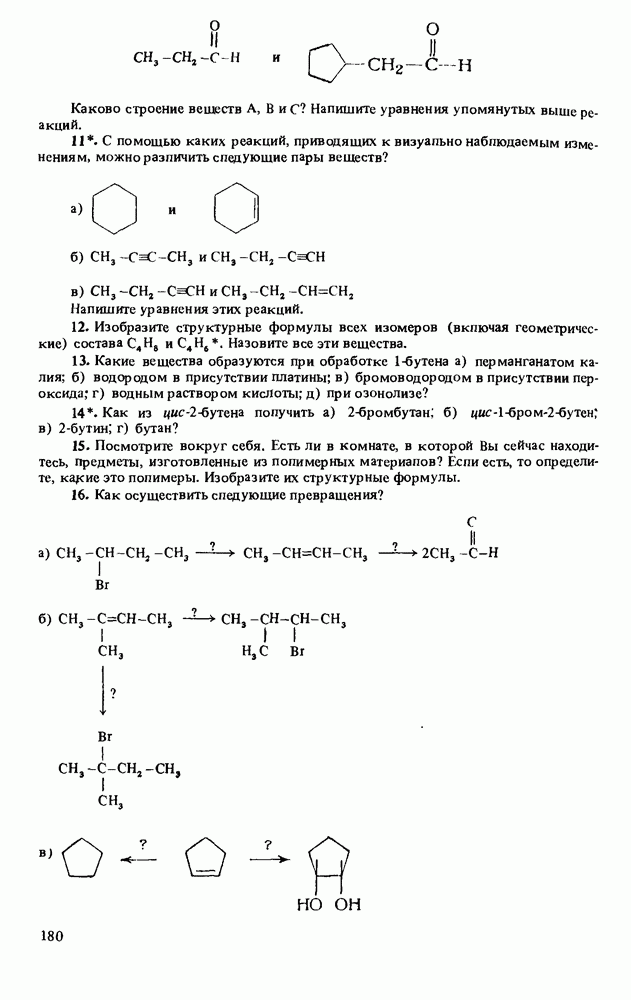
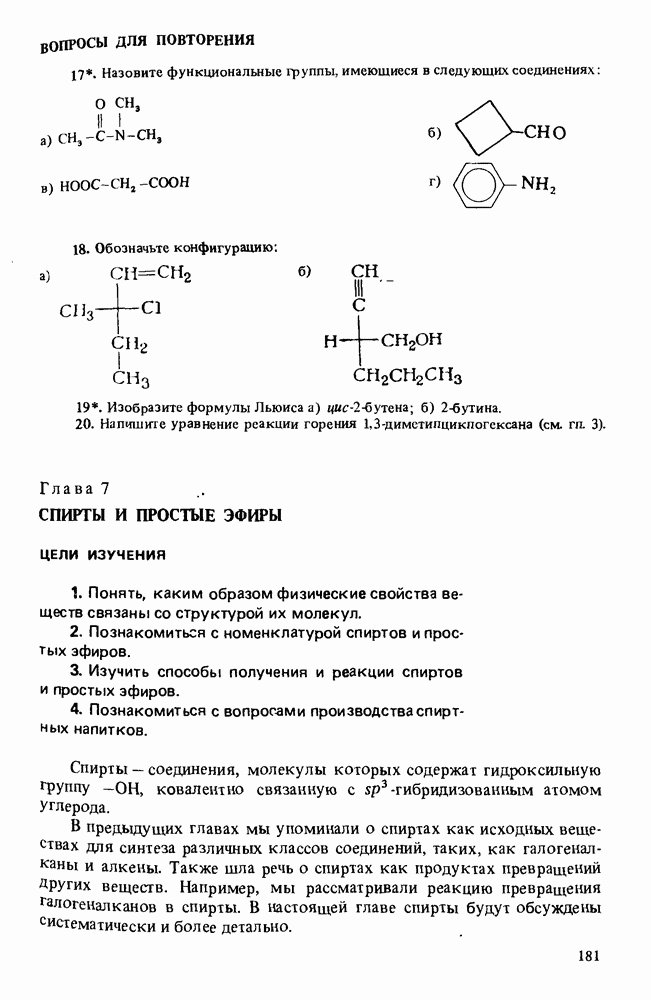
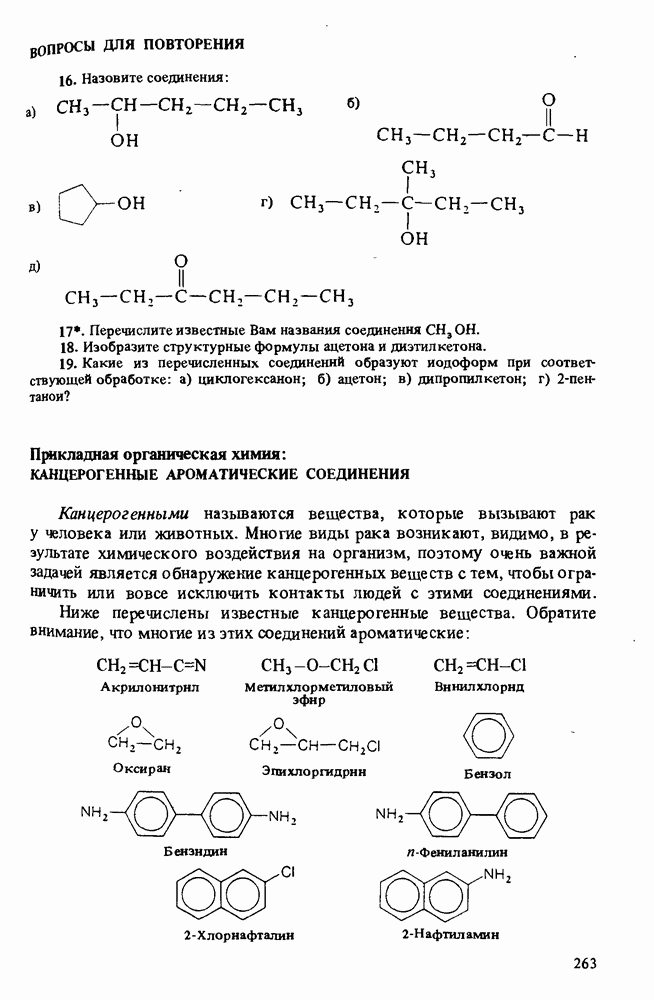
ВОПРОСЫ ДЛЯ ПОВТОРЕНИЯ
(см. скан)
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- Глава 1. КЛЮЧЕВЫЕ ПОНЯТИЯ ХИМИИ
- АТОМНАЯ ТЕОРИЯ
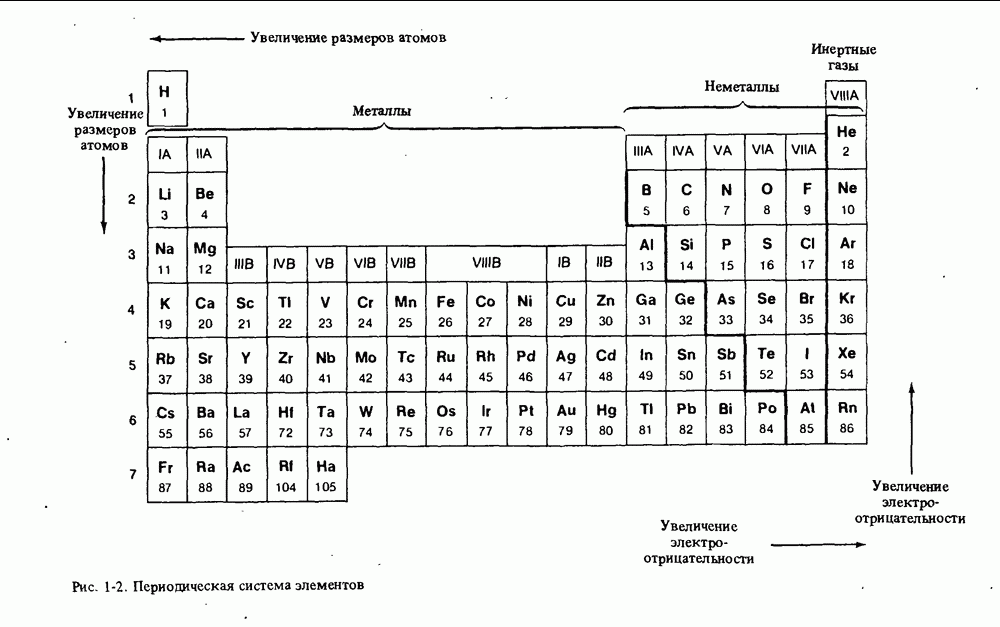
- ПЕРИОДИЧЕСКАЯ СИСТЕМА
- ХИМИЧЕСКАЯ СВЯЗЬ
- ФОРМУЛЫ ЛЬЮИСА
- ФОРМАЛЬНЫЙ ЗАРЯД
- РЕЗОНАНС
- ГЕОМЕТРИЯ МОЛЕКУЛ
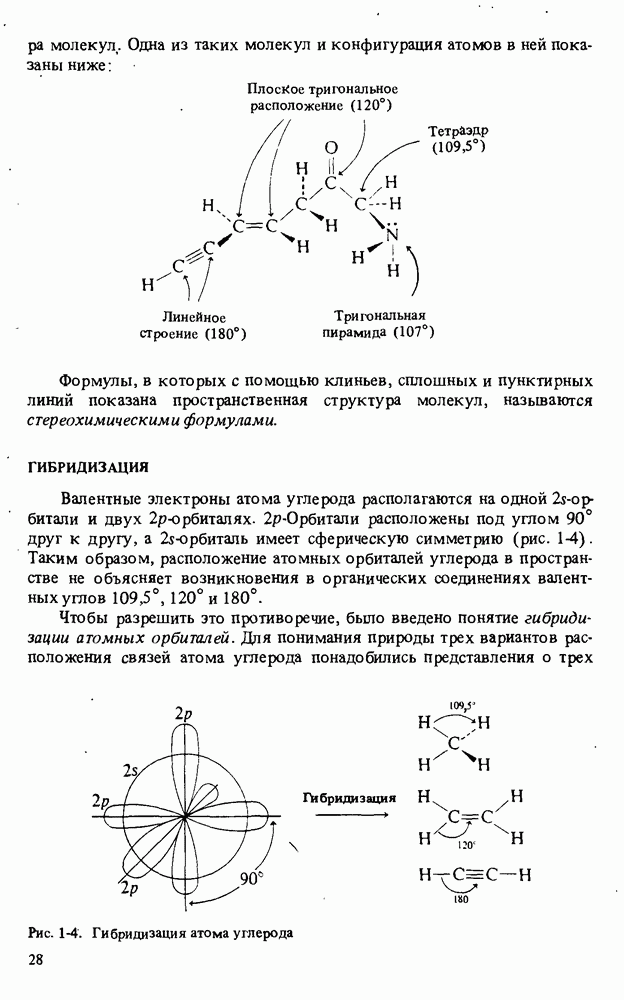
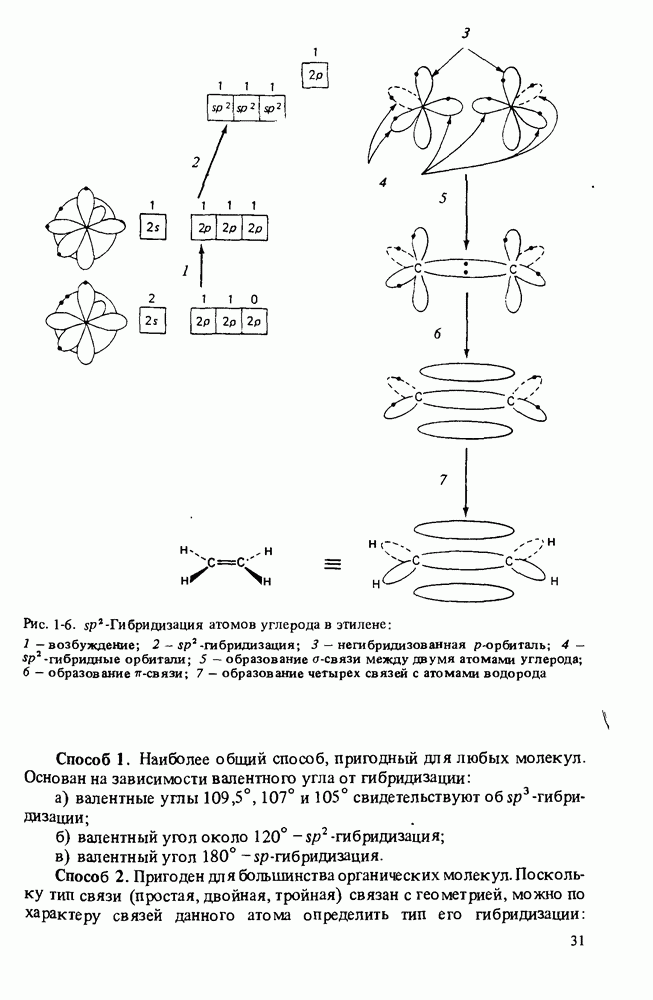
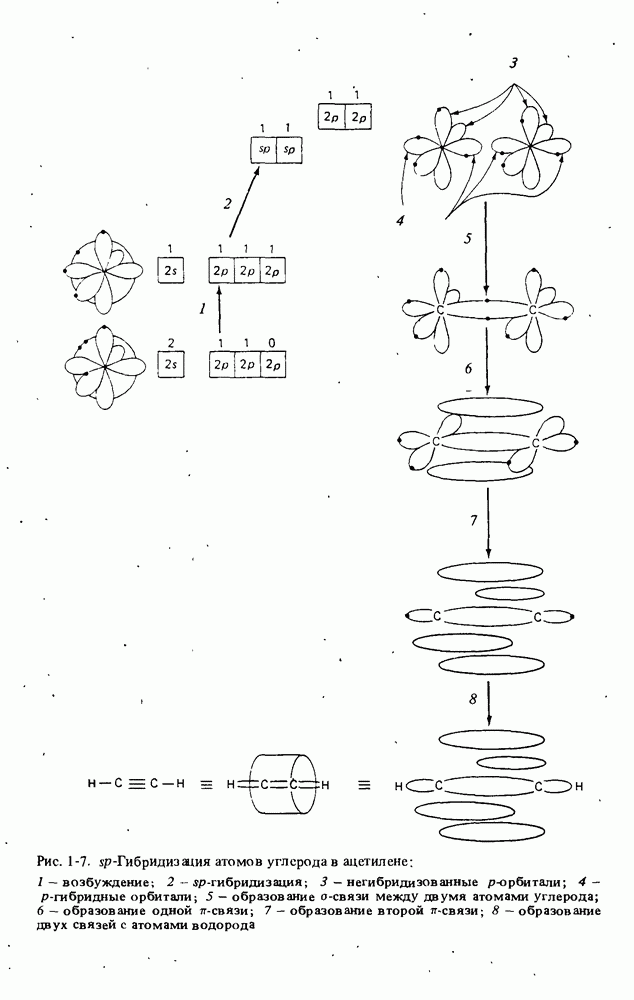
- ГИБРИДИЗАЦИЯ
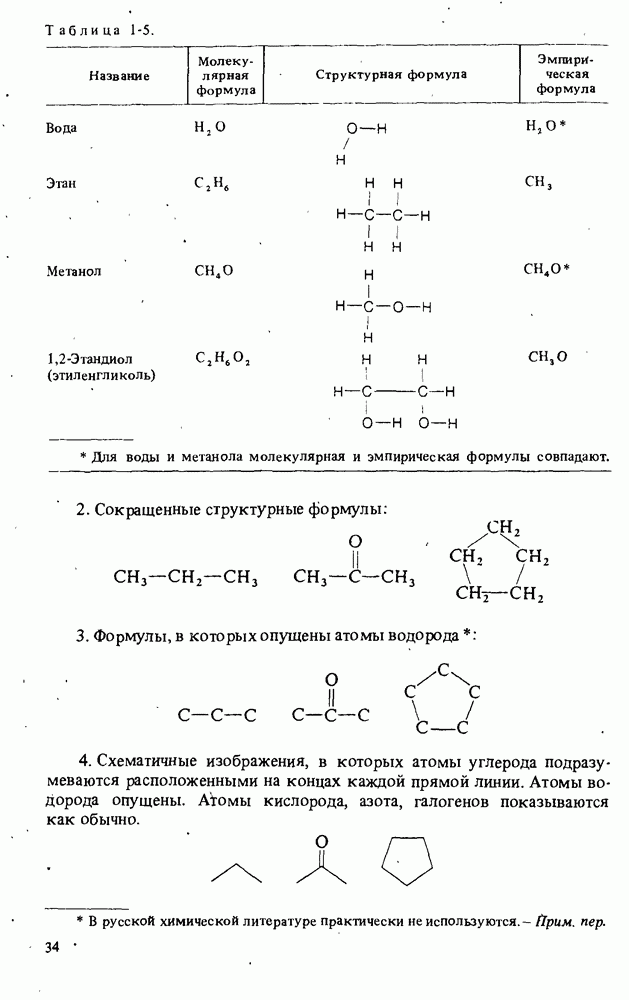
- ХИМИЧЕСКИЕ ФОРМУЛЫ
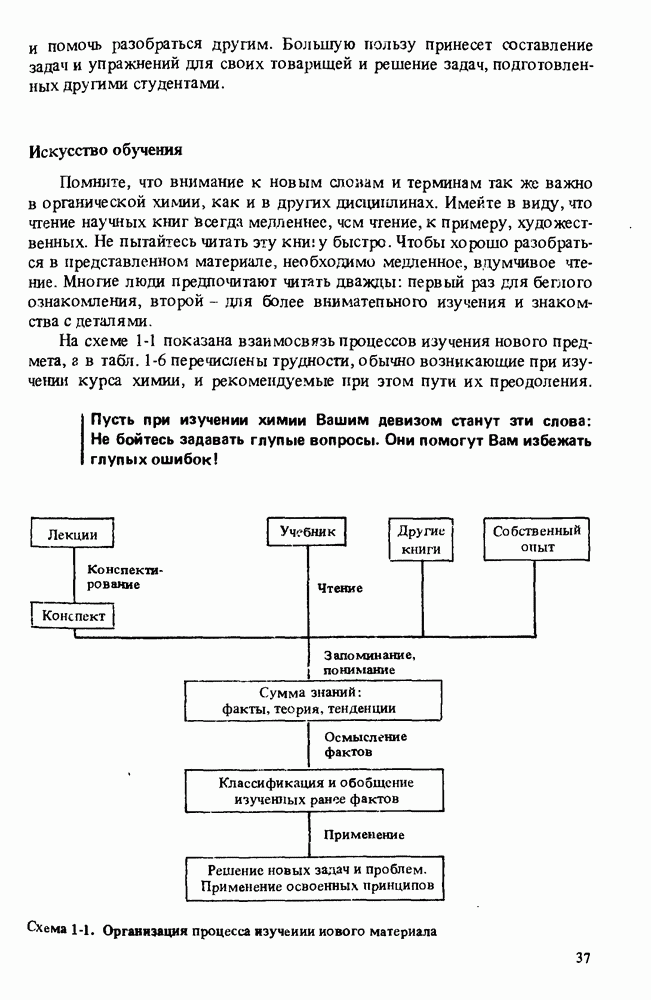
- СОВЕТЫ ИЗУЧАЮЩЕМУ ОРГАНИЧЕСКУЮ ХИМИЮ
- СВОДКА ОСНОВНЫХ ПОЛОЖЕНИЙ ГЛ. 1
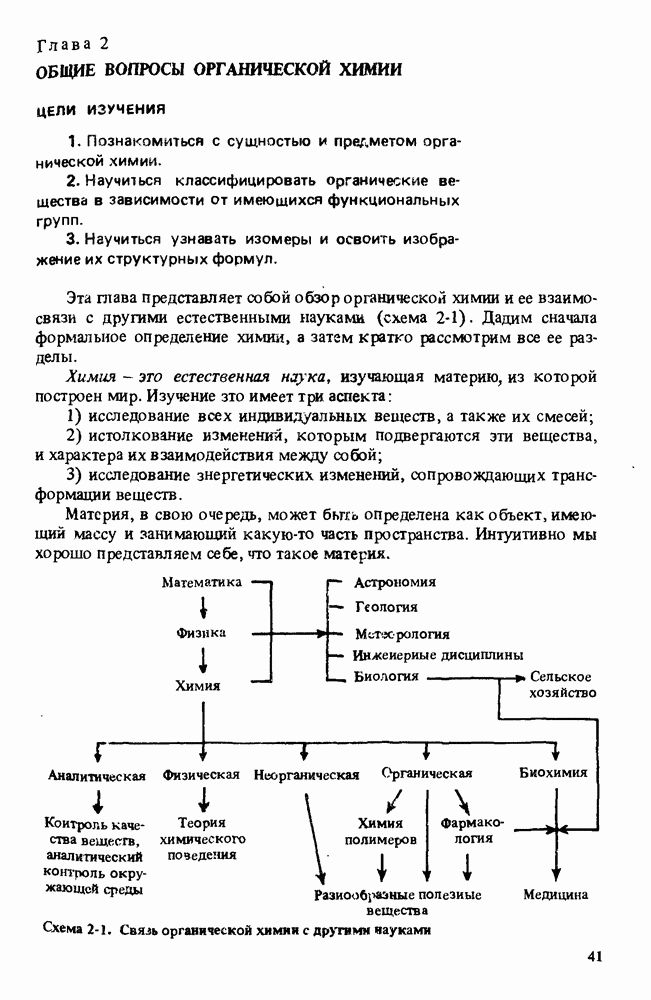
- Глава 2. ОБЩИЕ ВОПРОСЫ ОРГАНИЧЕСКОЙ ХИМИИ
- РАЗДЕЛЫ ХИМИИ
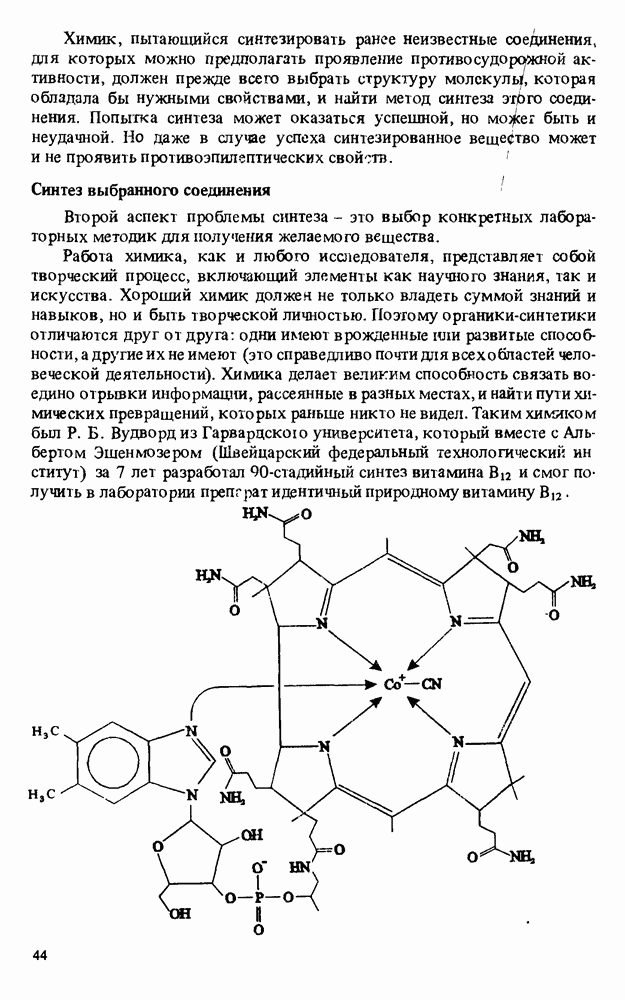
- СИНТЕТИЧЕСКАЯ ОРГАНИЧЕСКАЯ ХИМИЯ
- ПОЛЕЗНЫЕ ОРГАНИЧЕСКИЕ ВЕЩЕСТВА
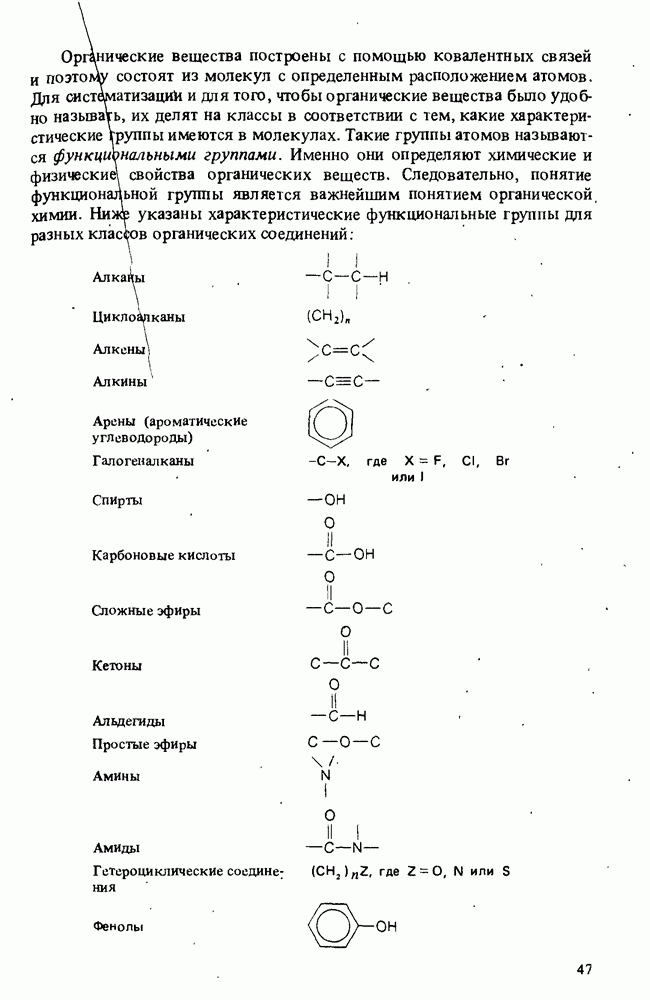
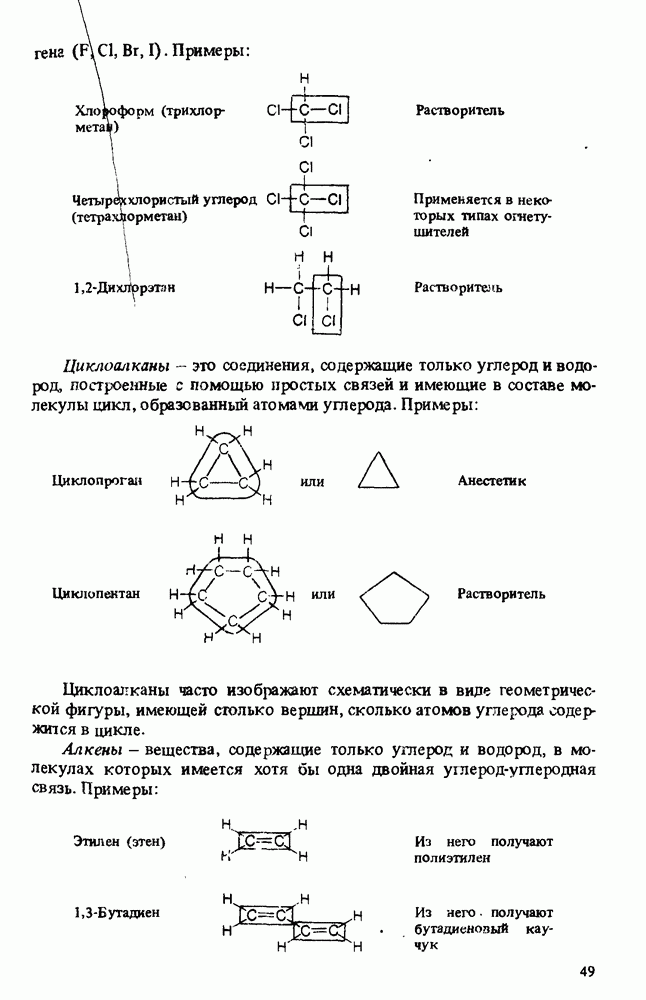
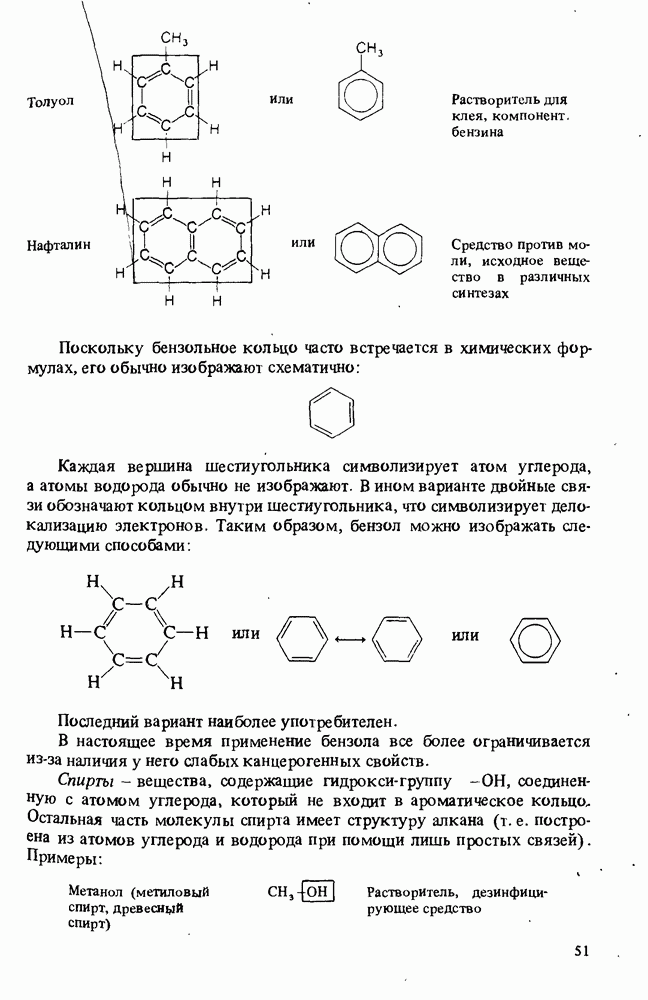
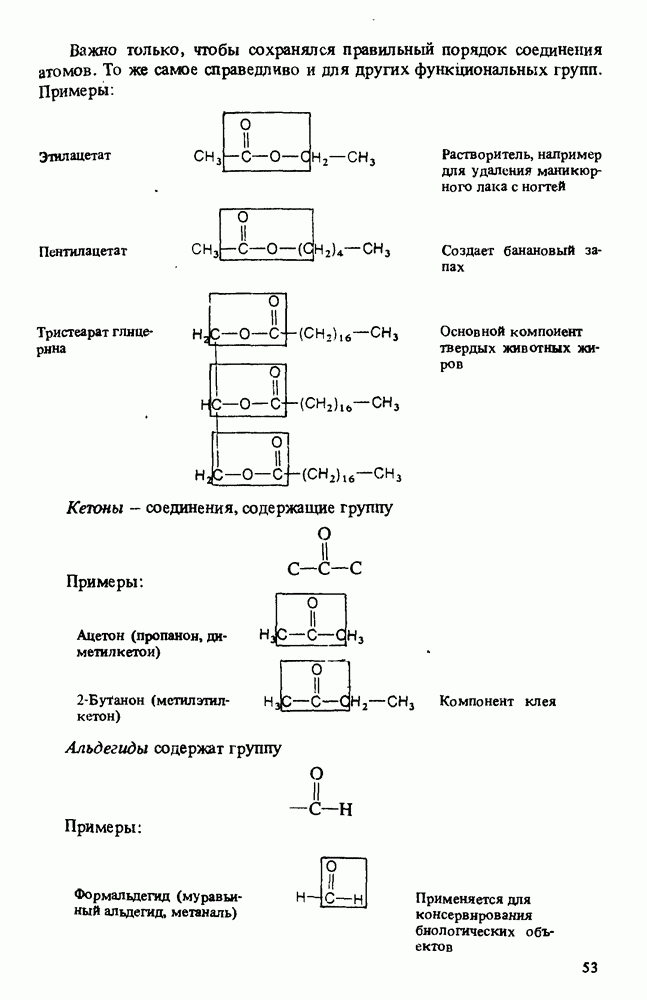
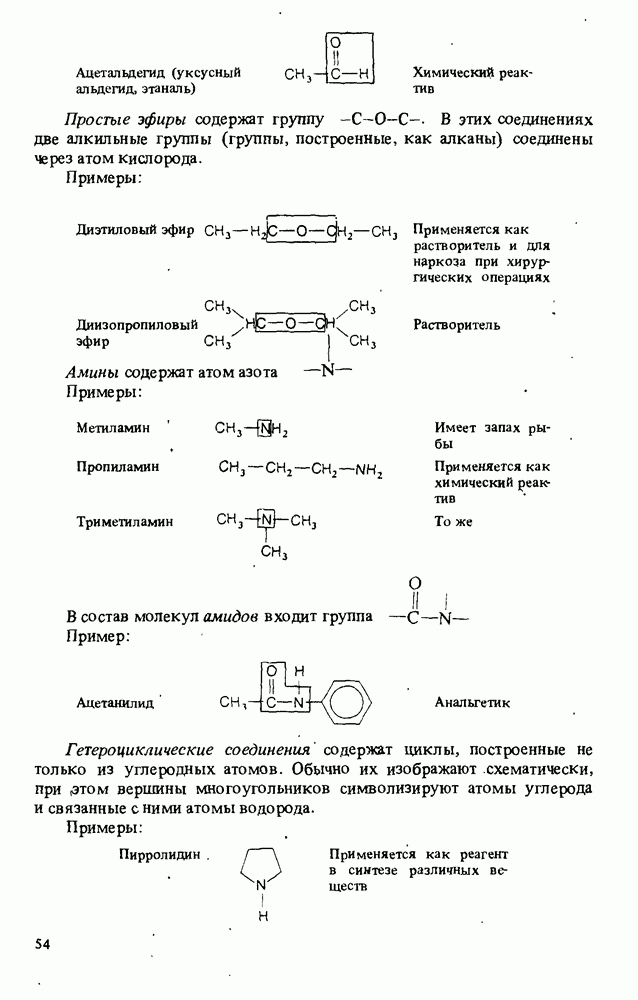
- КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ. ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
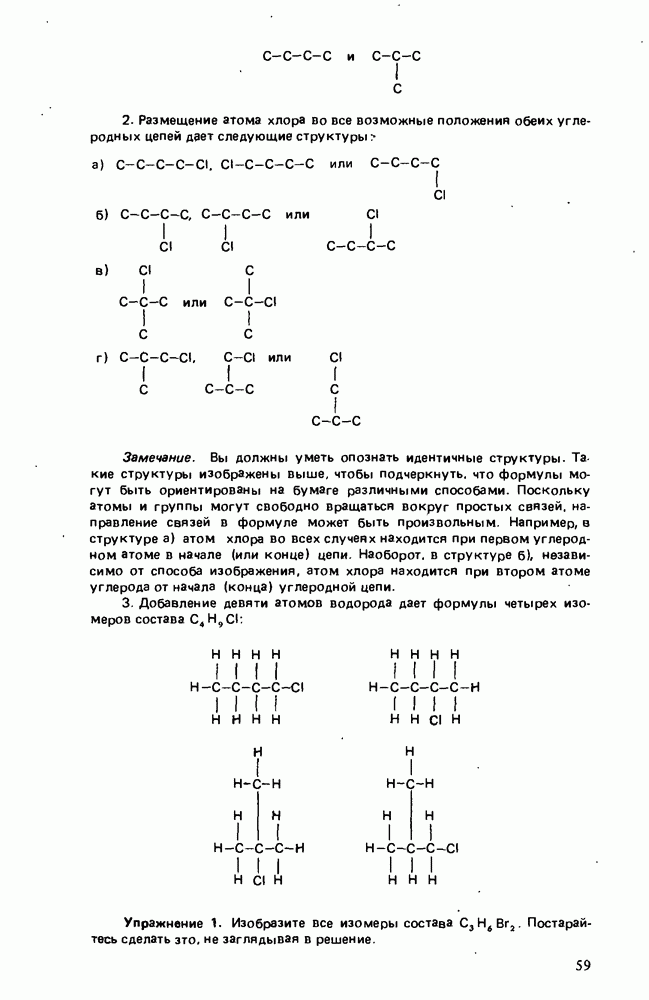
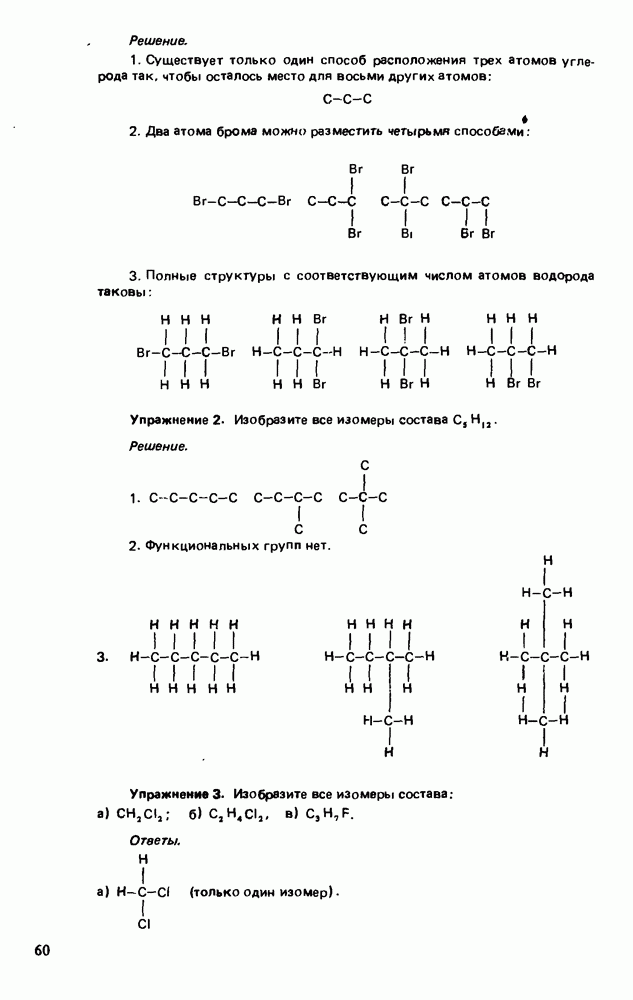
- ИЗОМЕРИЯ
- СВОДКА ОСНОВНЫХ ПОЛОЖЕНИЙ ГЛ. 2
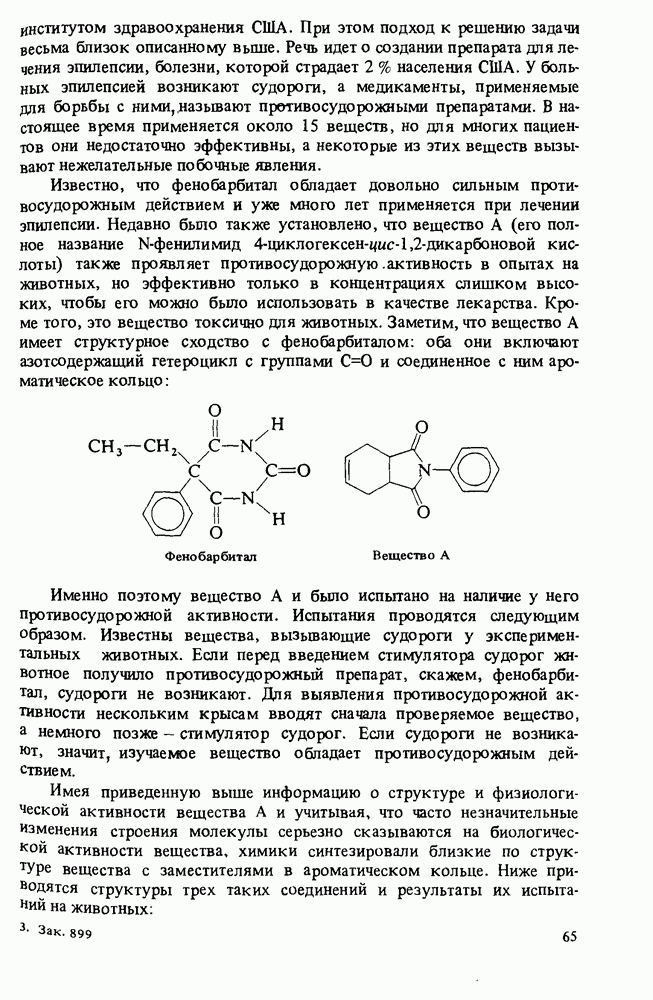
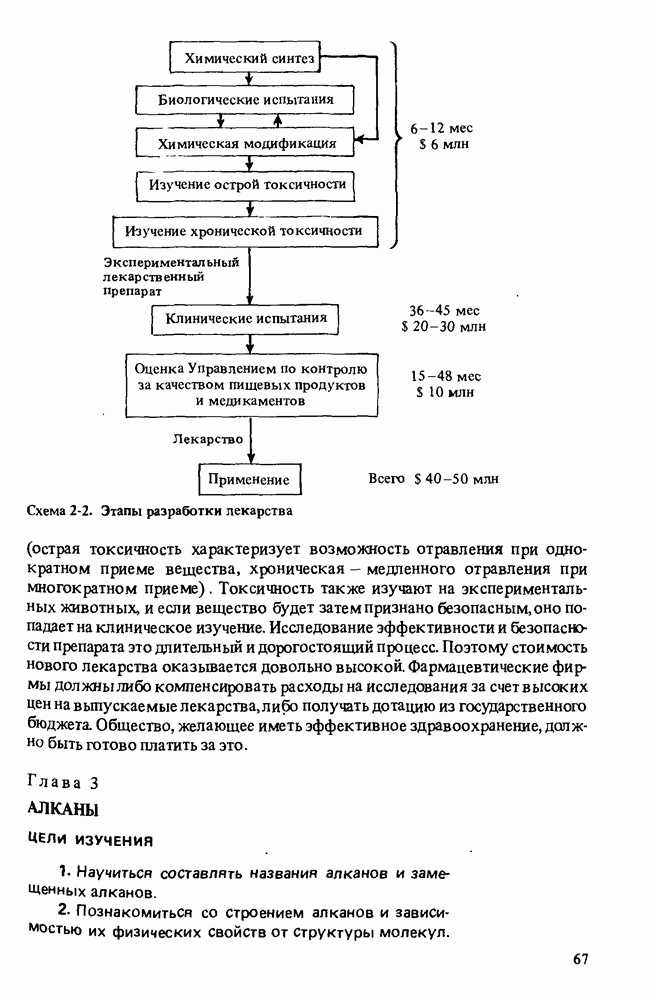
- Прикладная органическая химия: ХИМИЧЕСКИЙ СИНТЕЗ И МЕДИЦИНСКИЕ ИССЛЕДОВАНИЯ
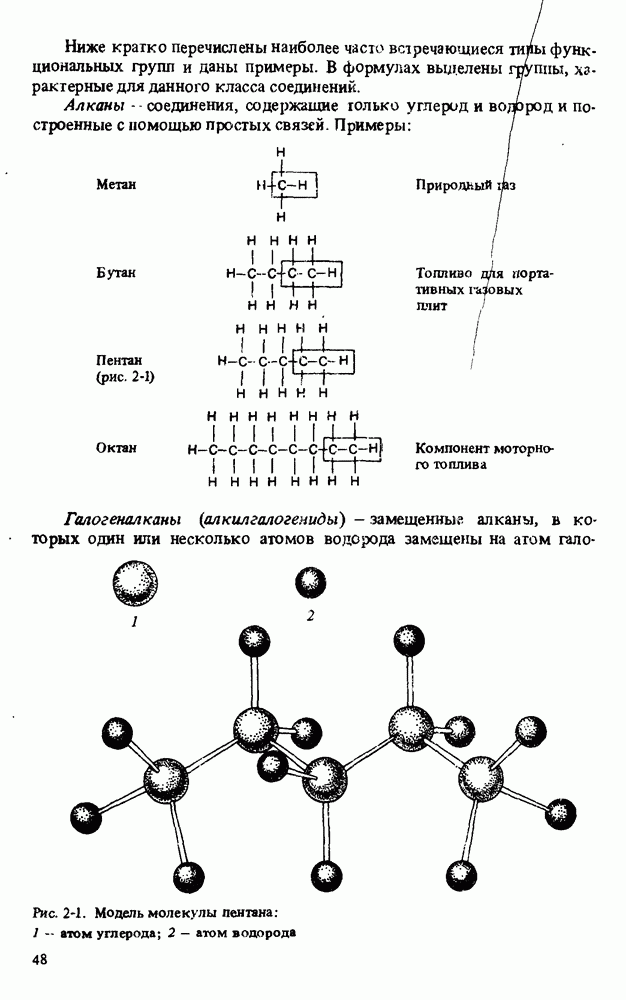
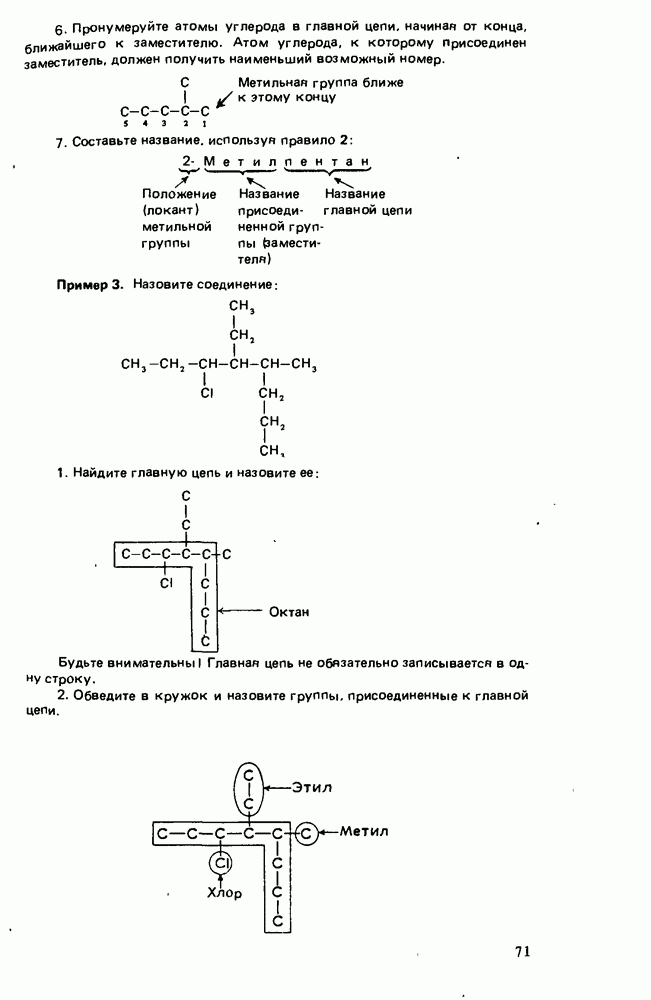
- Глава 3. АЛКАНЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА АЛКАНОВ
- СТРОЕНИЕ АЛКАНОВ
- ПОЛУЧЕНИЕ АЛКАНОВ
- РЕАКЦИИ АЛКАНОВ
- ХИМИЯ НЕФТИ
- СОВЕТЫ ИЗУЧАЮЩЕМУ ОРГАНИЧЕСКУЮ ХИМИЮ. ИЗУЧЕНИЕ РЕАКЦИЙ
- Глава 4. СТЕРЕОХИМИЯ И ОПТИЧЕСКАЯ АКТИВНОСТЬ
- СПОСОБЫ ИЗОБРАЖЕНИЯ ЭНАНТИОМЕРОВ
- ОБОЗНАЧЕНИЕ АБСОЛЮТНОЙ КОНФИГУРАЦИИ
- НАЗВАНИЯ ХИРАЛЬНЫХ МОЛЕКУЛ
- ИЗОБРАЖЕНИЕ МОЛЕКУЛ С ПРОТИВОПОЛОЖНОЙ КОНФИГУРАЦИЕЙ
- D,L-НОМЕНКЛАТУРА ЭНАНТИОМЕРОВ
- ТЕРМИНОЛОГИЯ, ПРИМЕНЯЕМАЯ В СТЕРЕОХИМИИ
- ЗНАЧЕНИЕ ОПТИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ
- Глава 5. ОРГАНИЧЕСКИЕ ГАЛОГЕНСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
- ПОЛУЧЕНИЕ ГАЛОГЕНАЛКАНОВ
- РЕАКЦИИ ГАЛОГЕНАЛКАНОВ
- ПРАКТИЧЕСКИ ВАЖНЫЕ ГАЛОГЕНАЛКАНЫ
- Прикладная органическая химия: ОРГАНИЧЕСКИЕ ПЕСТИЦИДЫ
- Глава 6. НЕНАСЫЩЕННЫЕ УГЛЕВОДОРОДЫ
- НОМЕНКЛАТУРА АЛКЕНОВ
- ПОЛУЧЕНИЕ АЛКЕНОВ
- ОСНОВНЫЕ РЕАКЦИИ АЛКЕНОВ
- ПОЛИМЕРЫ
- НОМЕНКЛАТУРА АЛКИНОВ
- ПОЛУЧЕНИЕ АЛКИНОВ
- РЕАКЦИИ АЛКИНОВ
- НАПИСАНИЕ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- Глава 7. СПИРТЫ И ПРОСТЫЕ ЭФИРЫ
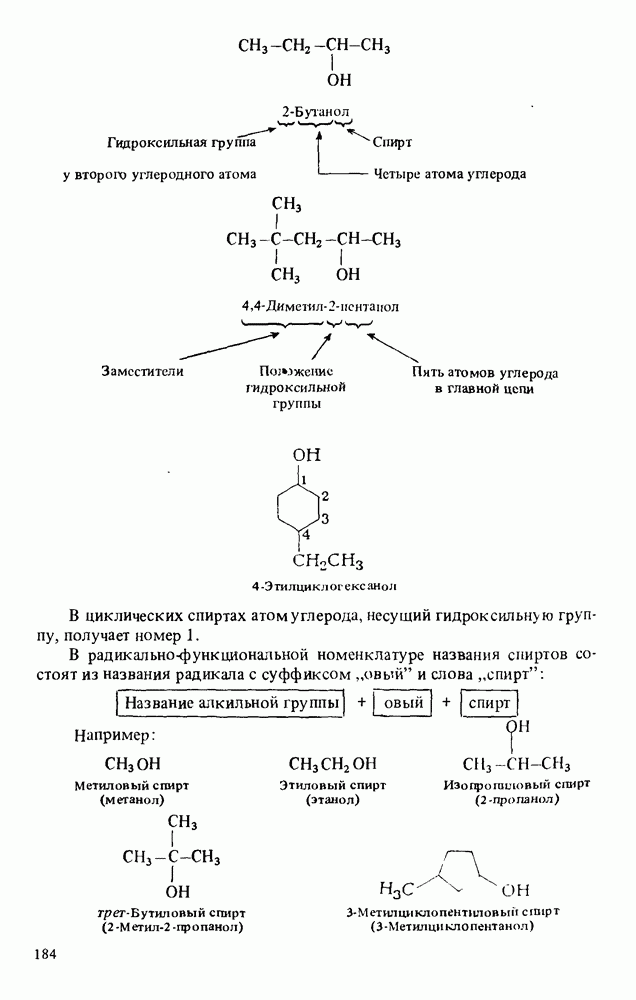
- НОМЕНКЛАТУРА СПИРТОВ
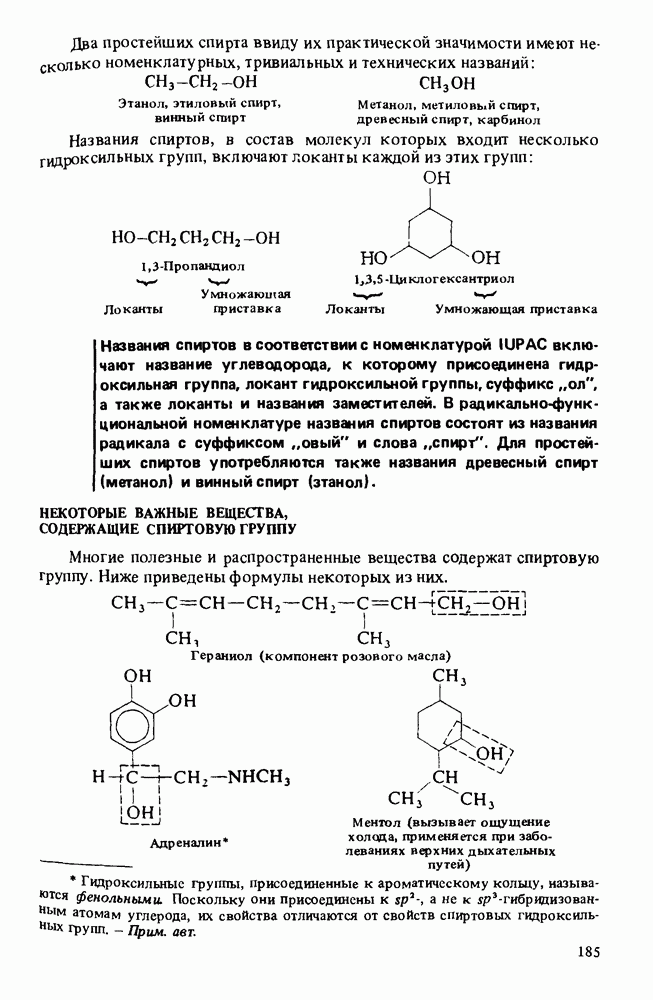
- НЕКОТОРЫЕ ВАЖНЫЕ ВЕЩЕСТВА, СОДЕРЖАЩИЕ СПИРТОВУЮ ГРУППУ
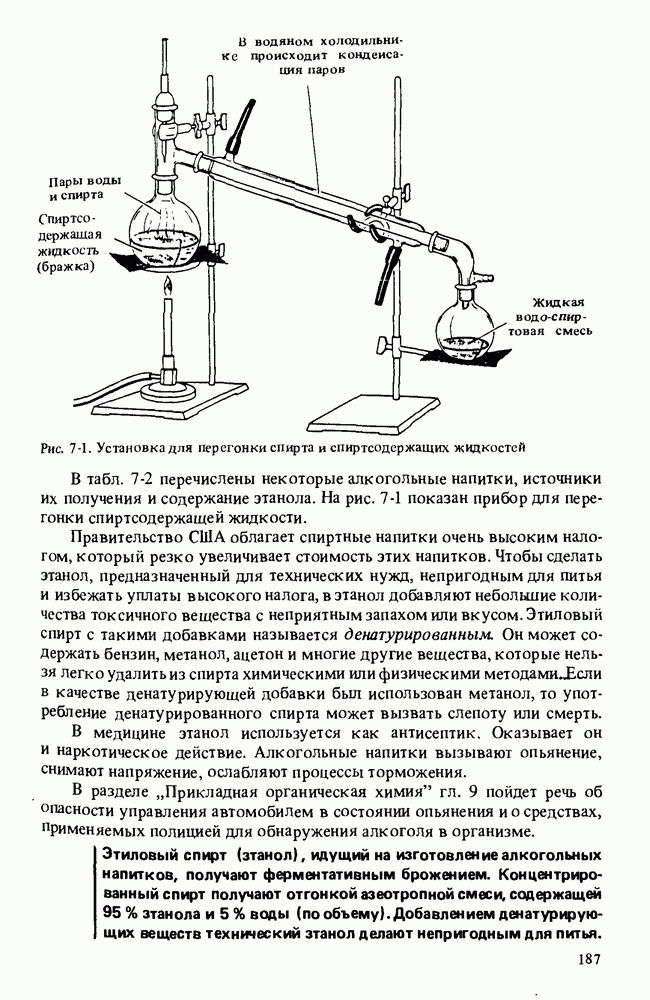
- ЭТИЛОВЫЙ СПИРТ. ПРОИЗВОДСТВО СПИРТНЫХ НАПИТКОВ
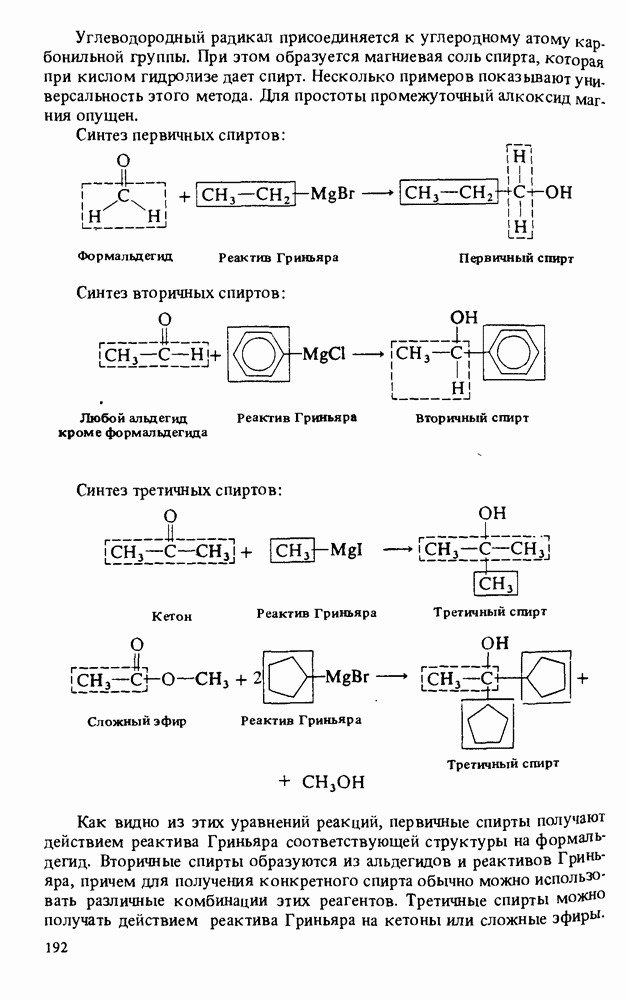
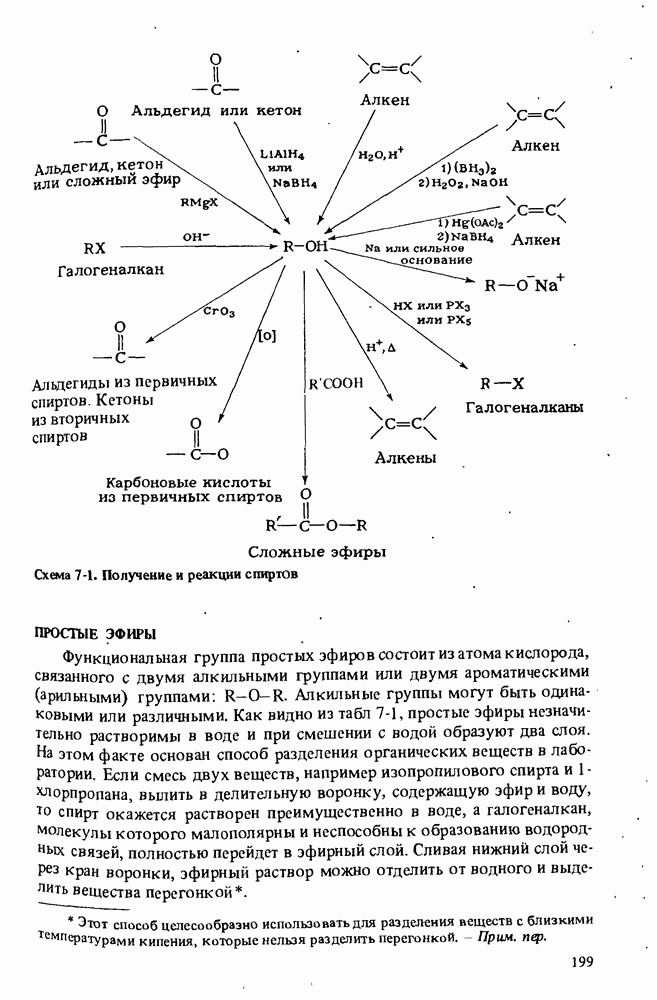
- ПОЛУЧЕНИЕ СПИРТОВ
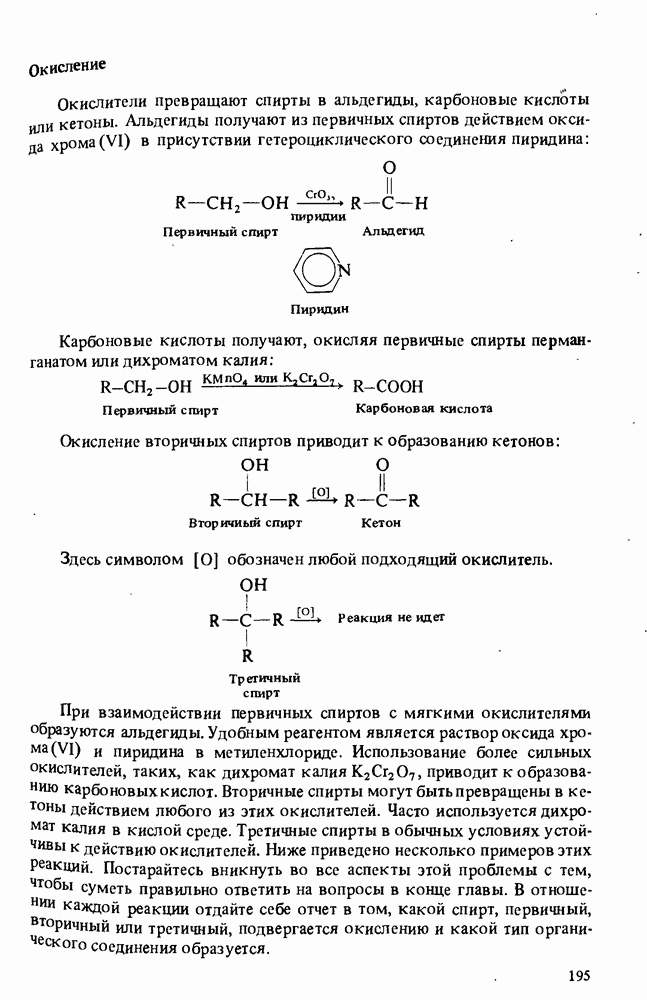
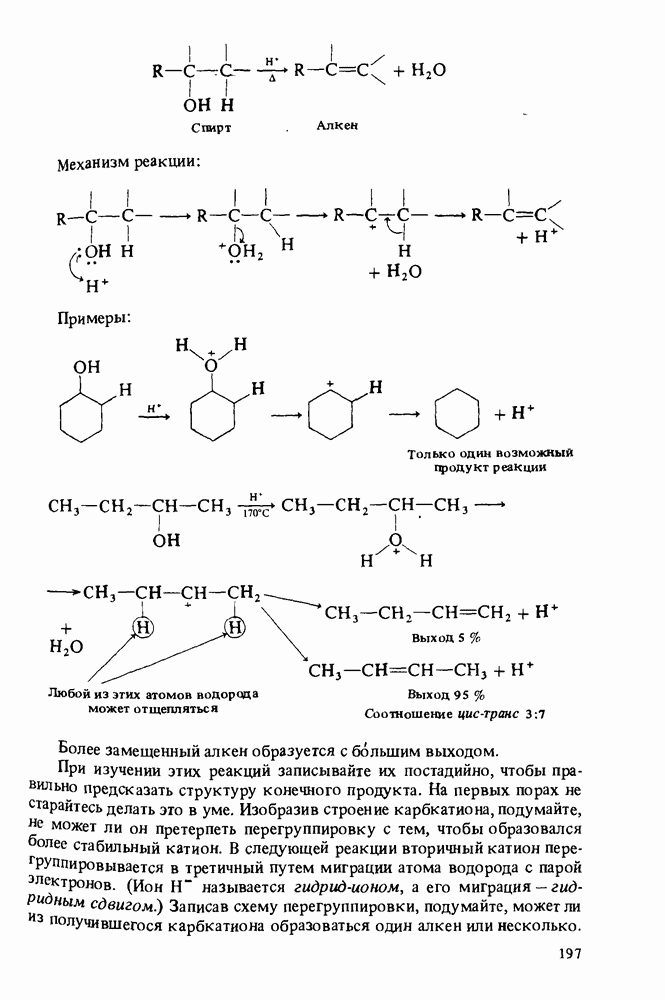
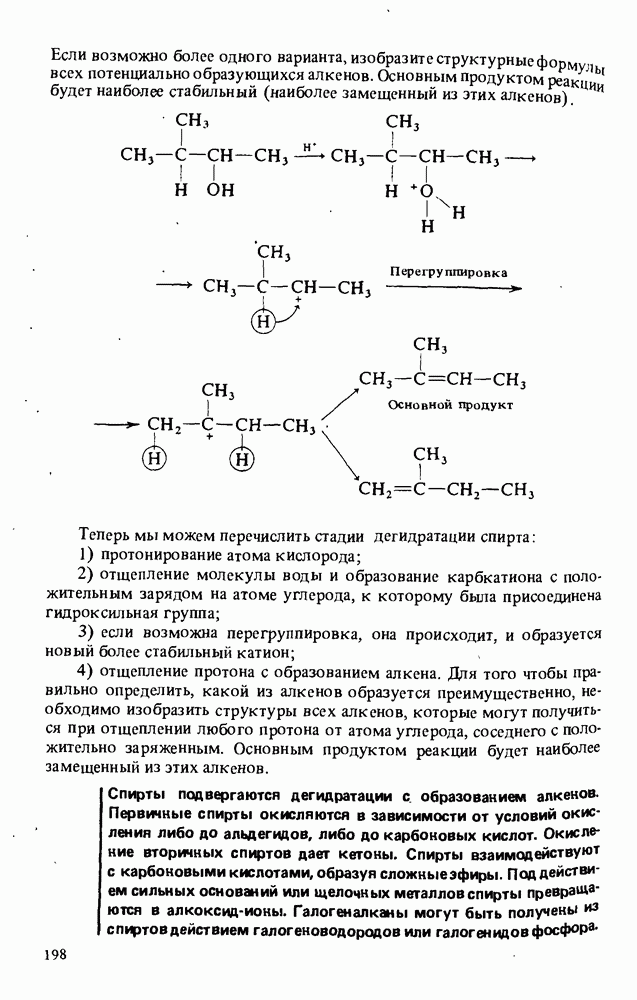
- РЕАКЦИИ СПИРТОВ
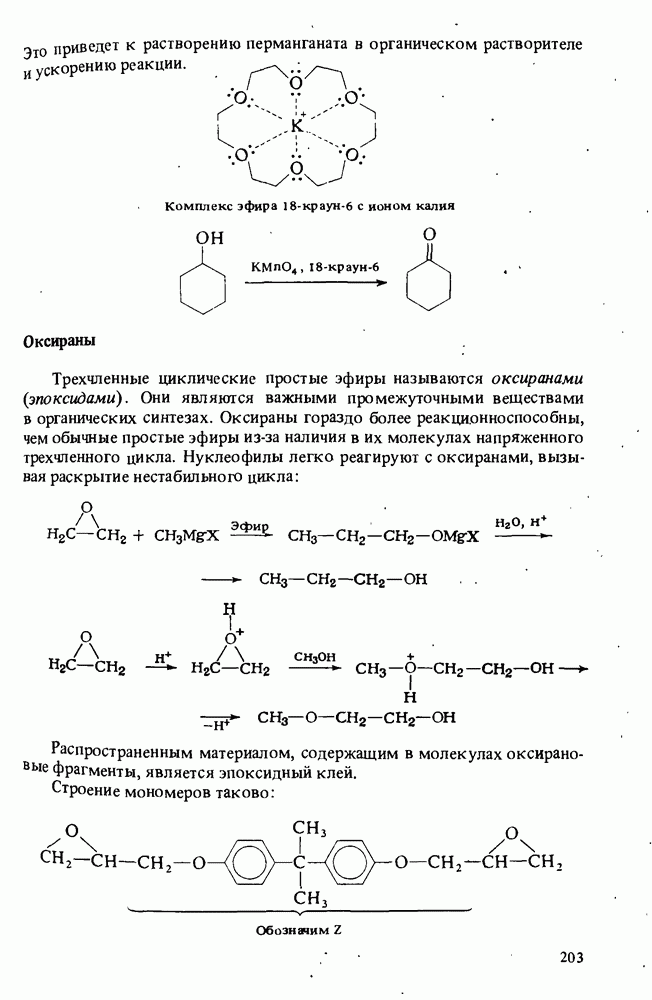
- ПРОСТЫЕ ЭФИРЫ
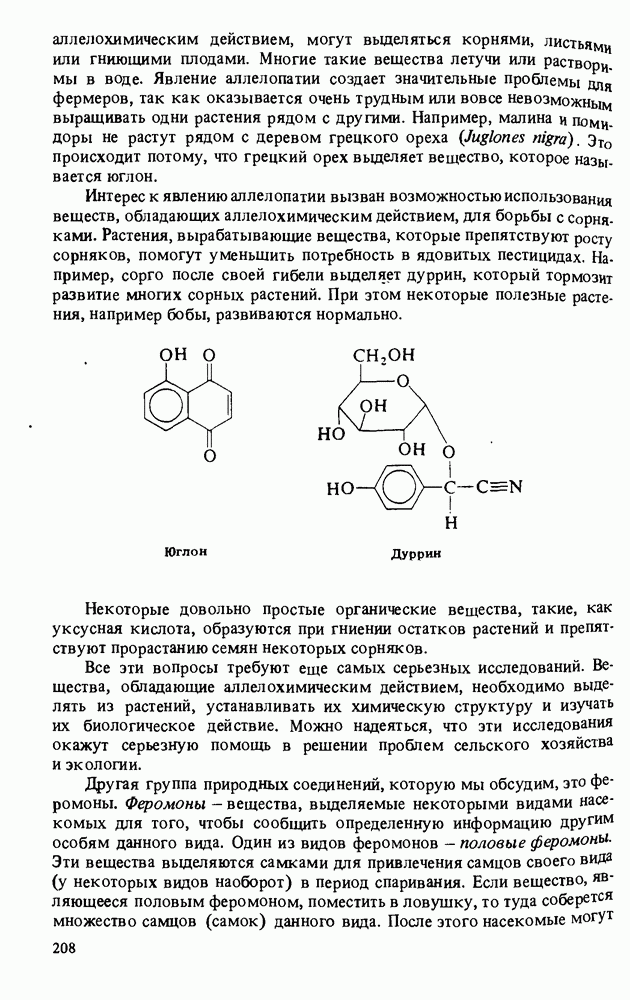
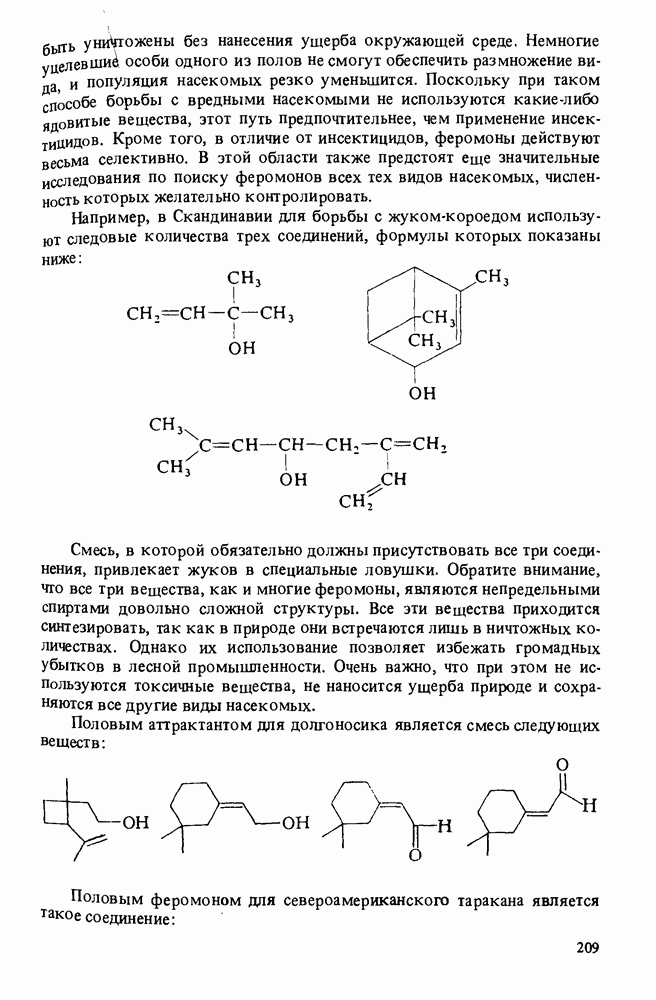
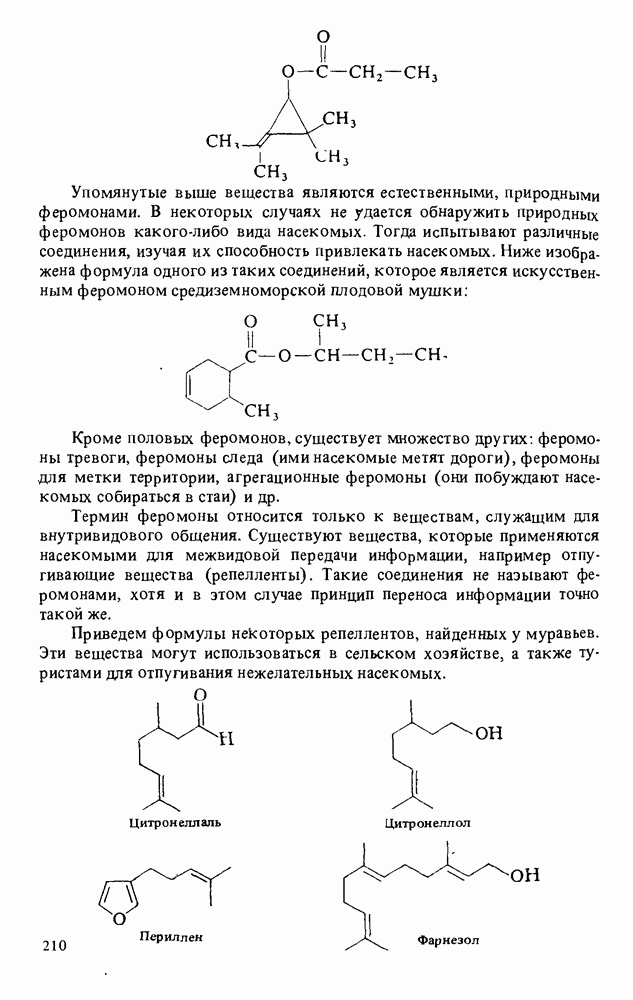
- Прикладная органическая химия: ВЕЩЕСТВА, ОБЛАДАЮЩИЕ АЛЛЕЛОХИМИЧЕСКИМ ДЕЙСТВИЕМ. ФЕРОМОНЫ
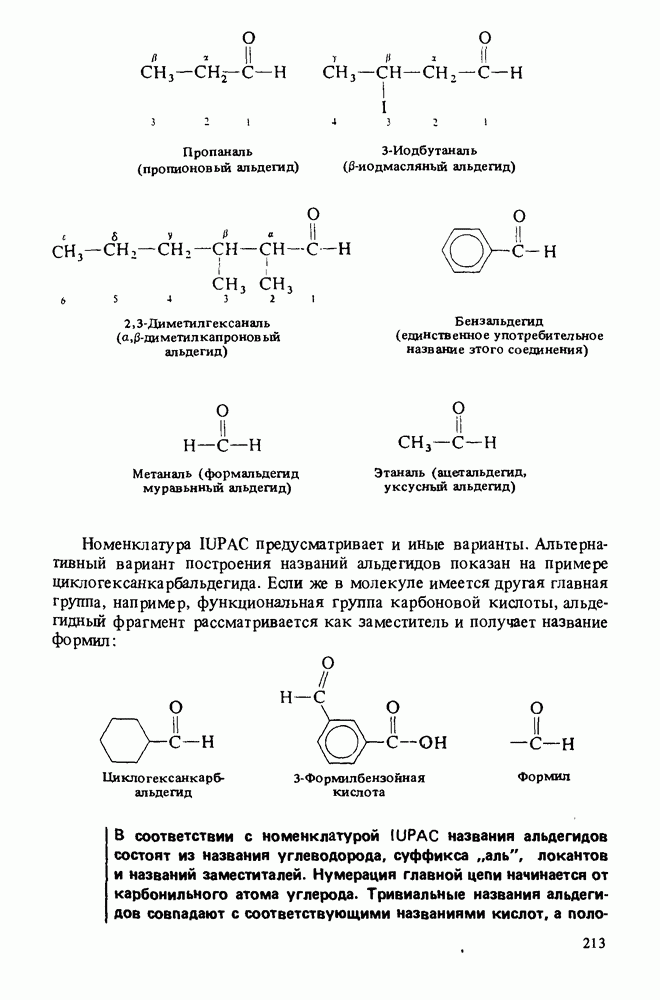
- Глава 8. АЛЬДЕГИДЫ И КЕТОНЫ
- ПОЛУЧЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ
- РЕАКЦИИ АЛЬДЕГИДОВ И КЕТОНОВ
- Глава 9. АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
- НОМЕНКЛАТУРА АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ
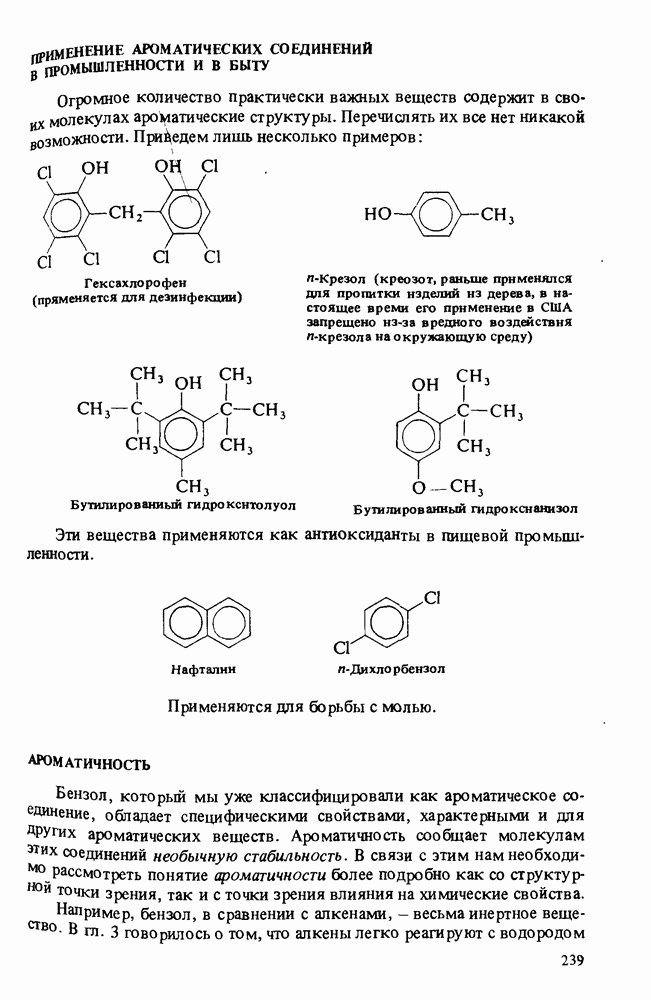
- ПРИМЕНЕНИЕ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ В ПРОМЫШЛЕННОСТИ И В БЫТУ
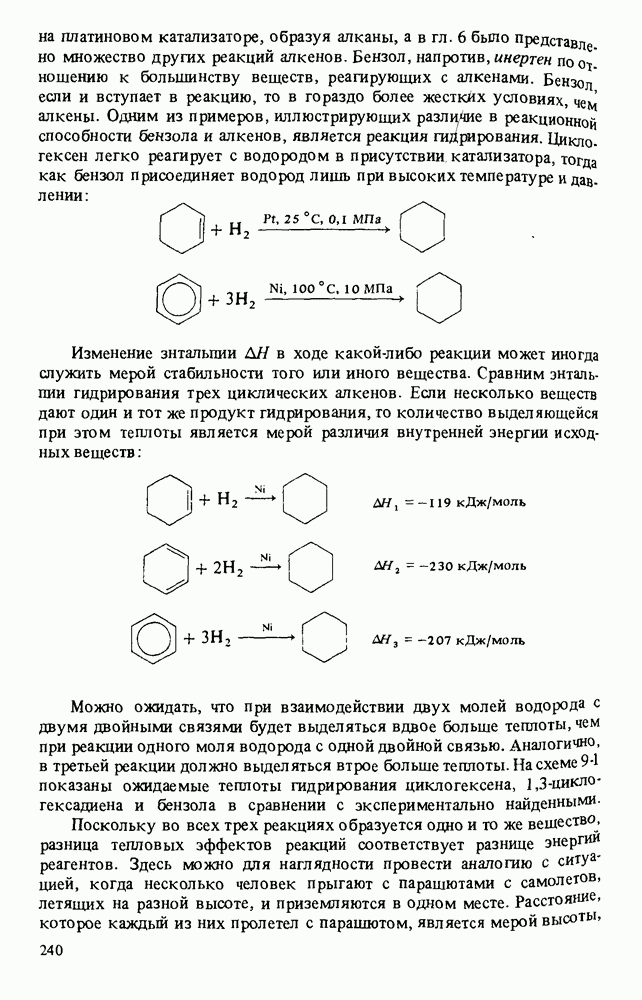
- АРОМАТИЧНОСТЬ
- ПОЛУЧЕНИЕ АЛКИЛЬБЕНЗОЛОВ
- РЕАКЦИИ БЕНЗОЛА И ЕГО ПРОИЗВОДНЫХ
- АРОМАТИЧЕСКОЕ ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ
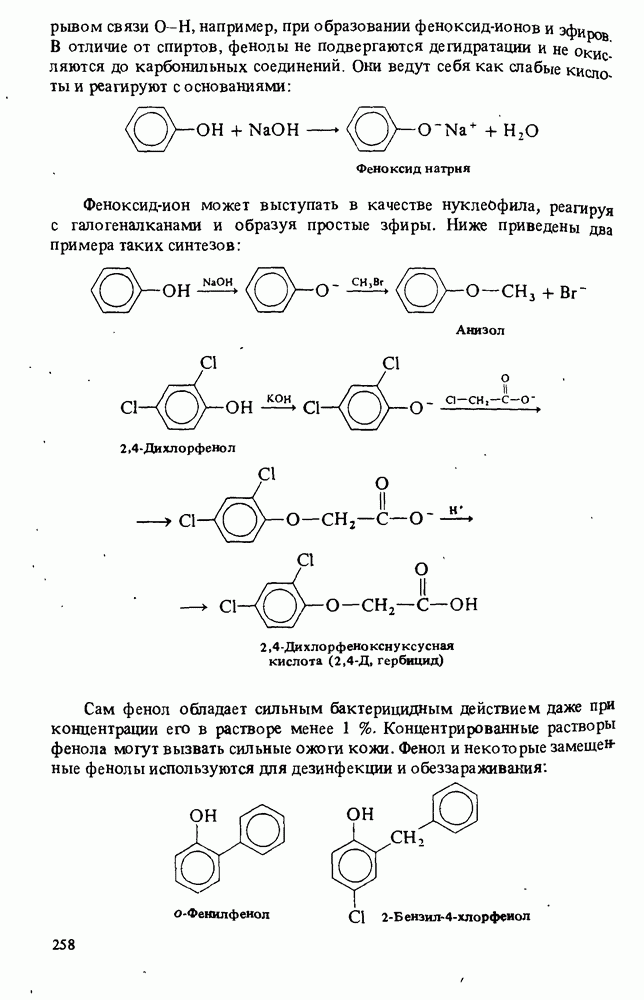
- ФЕНОЛЫ
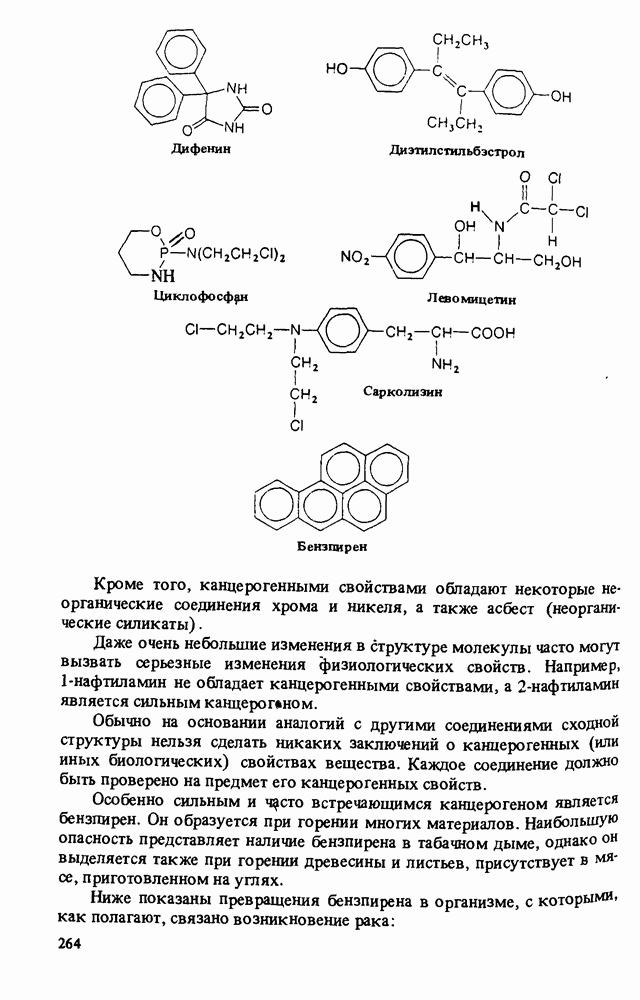
- Прикладная органическая химия: КАНЦЕРОГЕННЫЕ АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
- Глава 10. ОРГАНИЧЕСКИЙ СИНТЕЗ
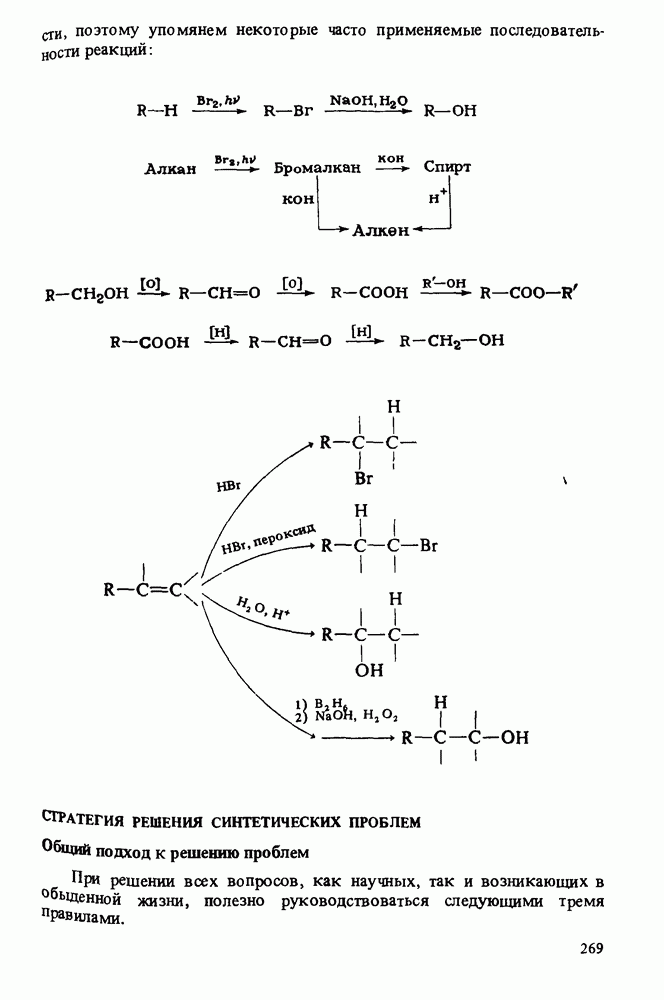
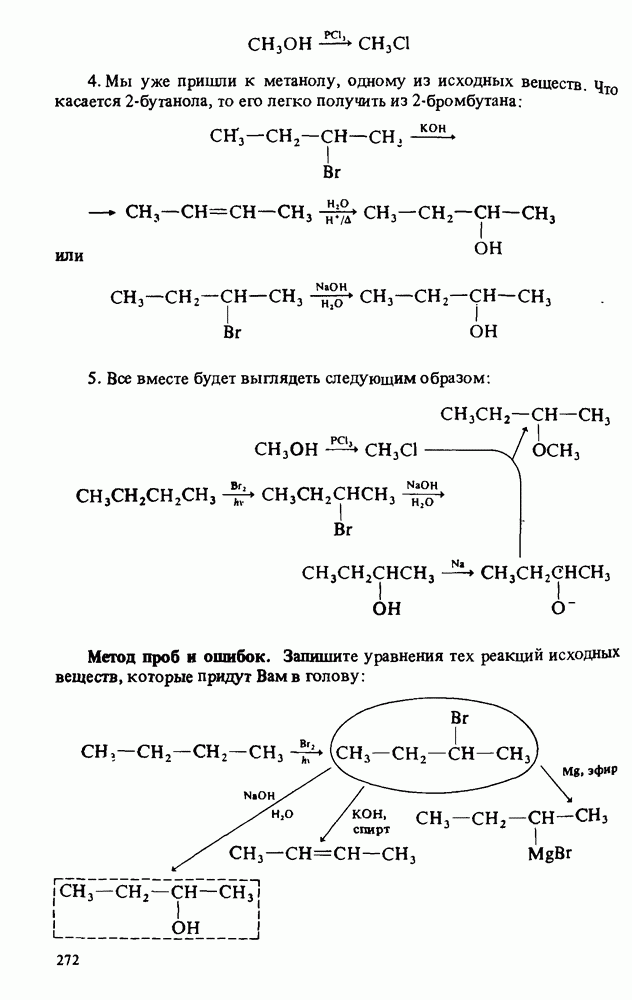
- СТРАТЕГИЯ РЕШЕНИЯ СИНТЕТИЧЕСКИХ ПРОБЛЕМ
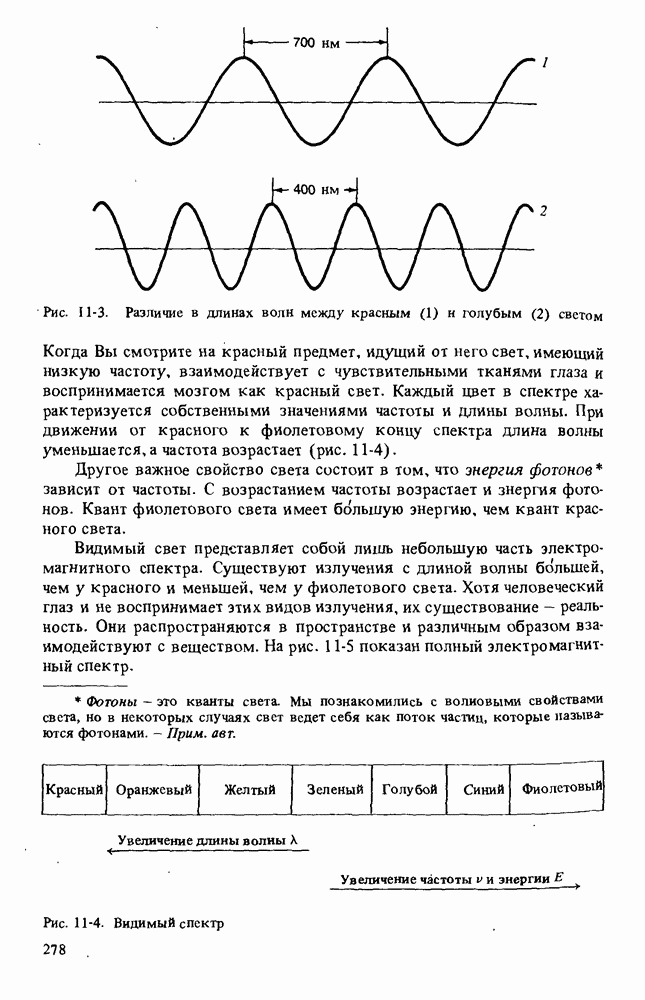
- Глава 11. МОЛЕКУЛЯРНАЯ СПЕКТРОСКОПИЯ
- ИНФРАКРАСНАЯ СПЕКТРОСКОПИЯ
- СПЕКТРОСКОПИЯ ЯДЕРНОГО МАГНИТНОГО РЕЗОНАНСА
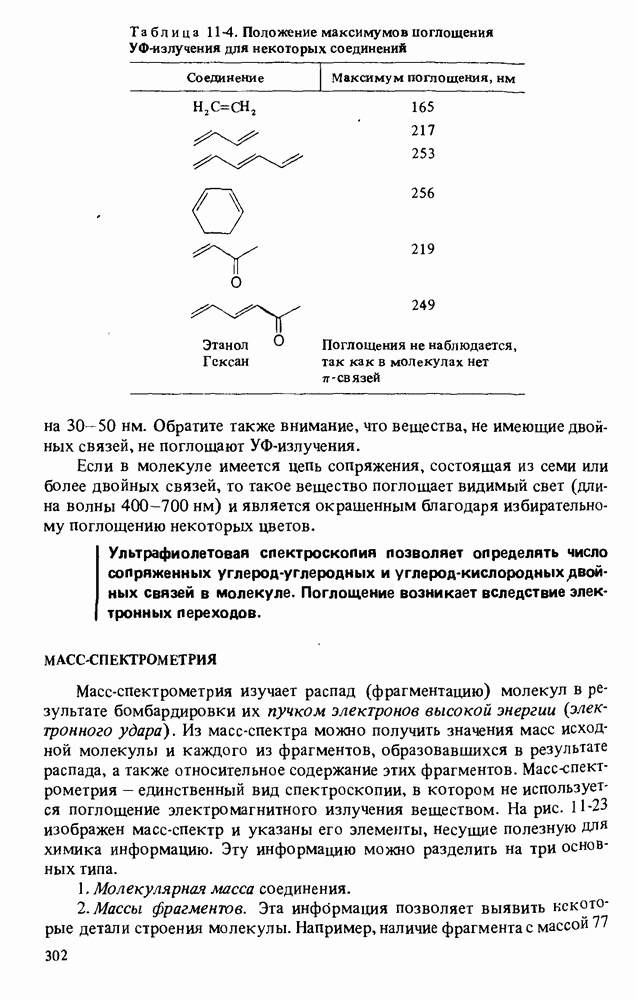
- УЛЬТРАФИОЛЕТОВАЯ СПЕКТРОСКОПИЯ
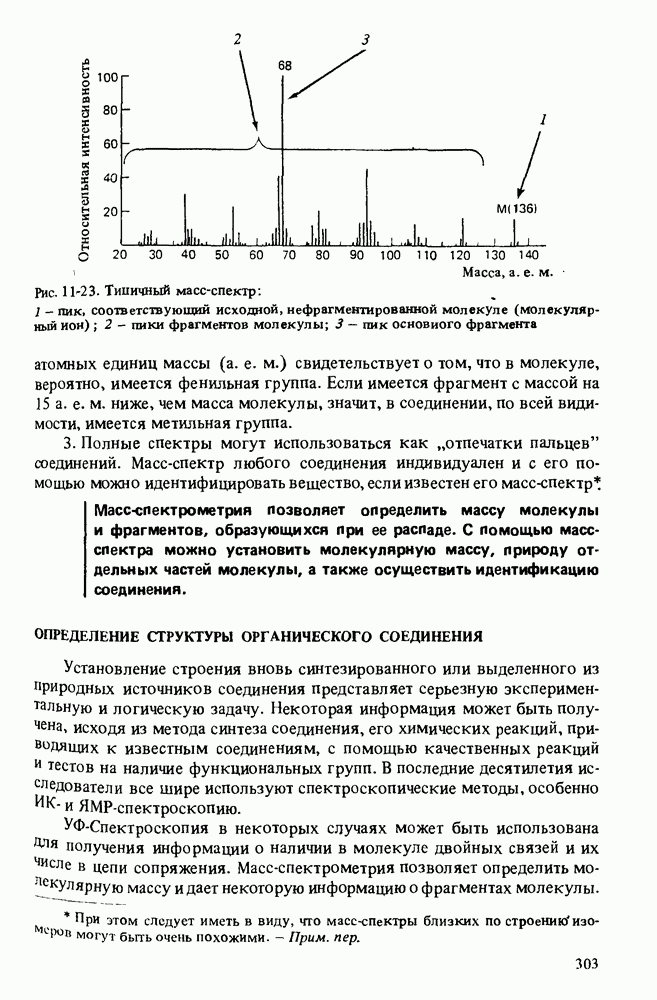
- МАСС-СПЕКТРОМЕТРИЯ
- ОПРЕДЕЛЕНИЕ СТРУКТУРЫ ОРГАНИЧЕСКОГО СОЕДИНЕНИЯ
- Прикладная органическая химия: ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ АЛКОГОЛЯ В КРОВИ
- Глава 12. КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
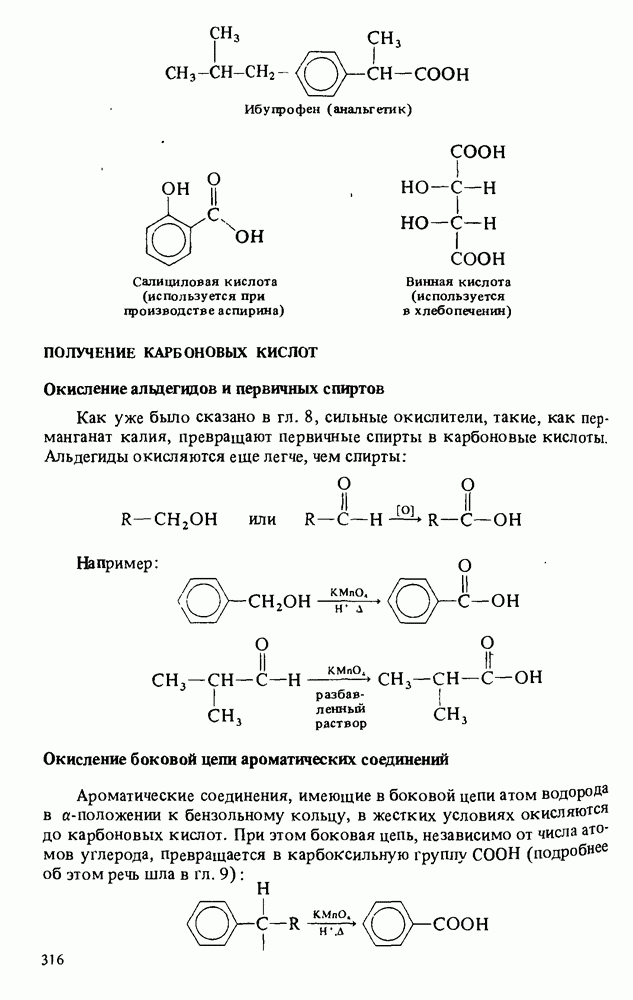
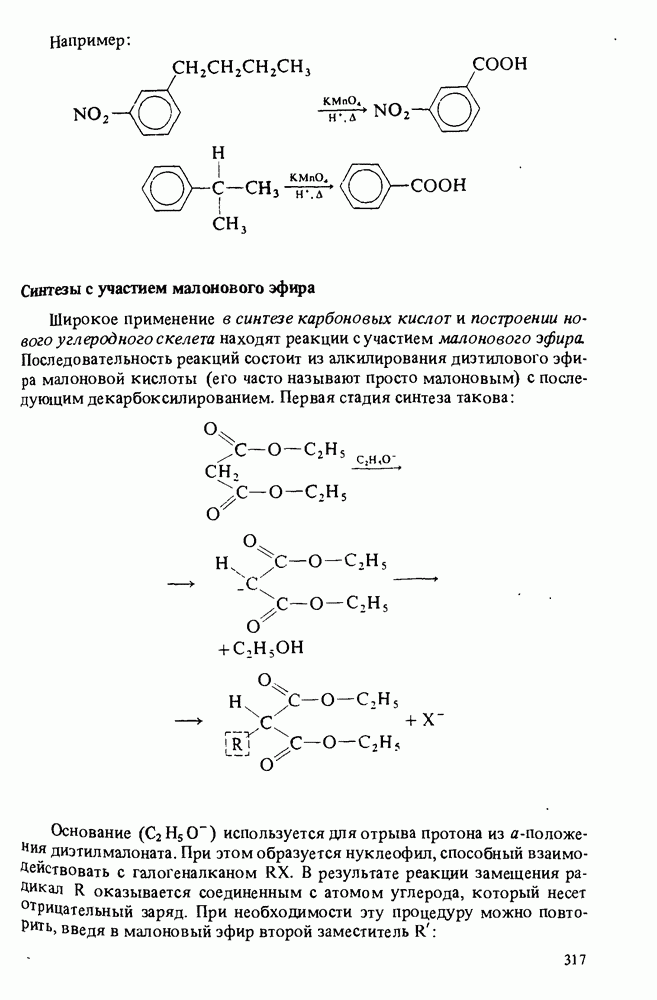
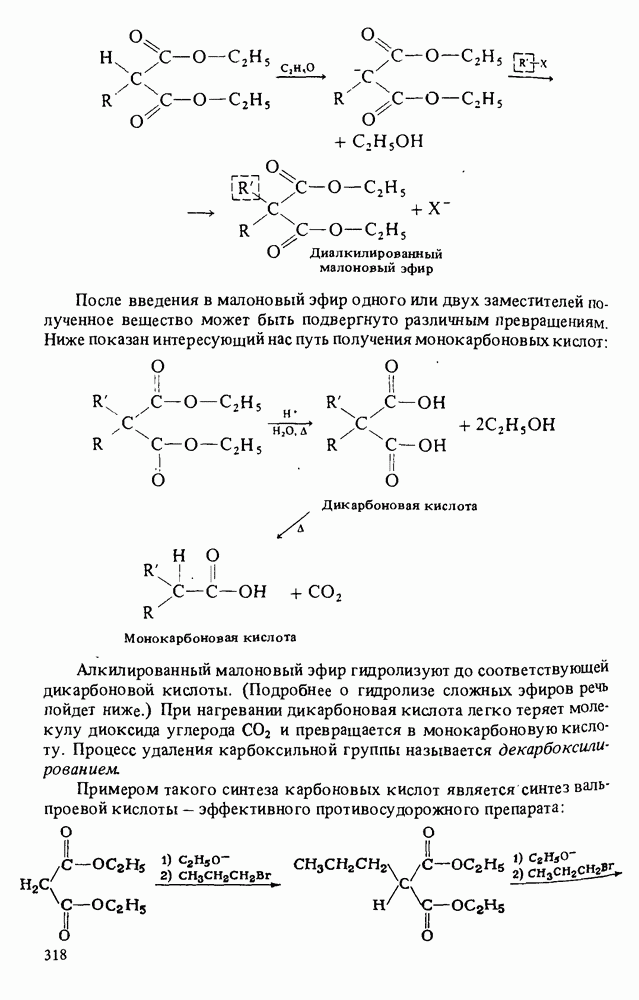
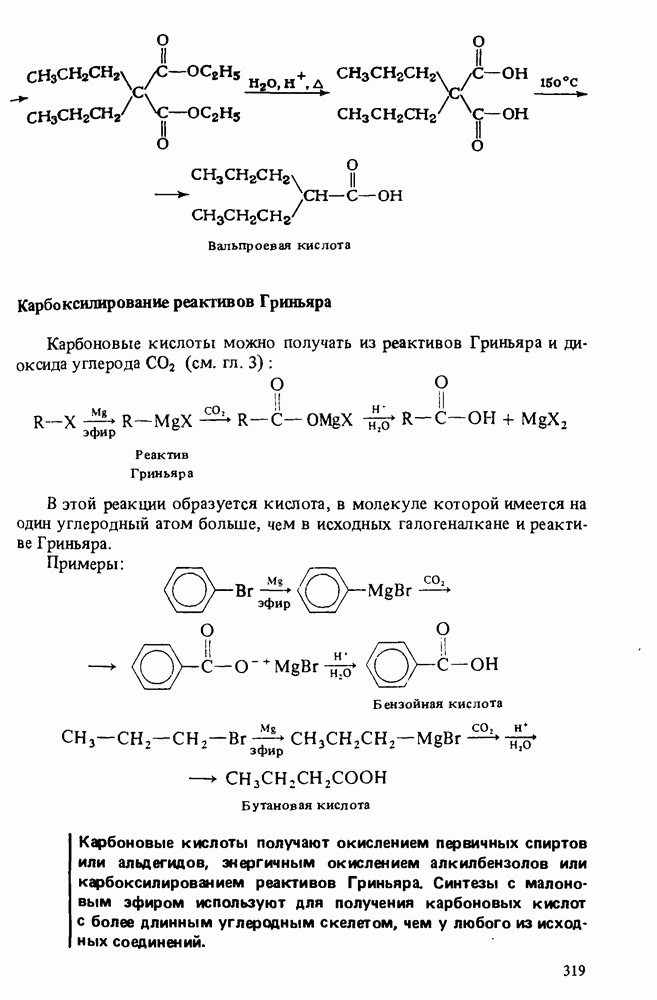
- ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ
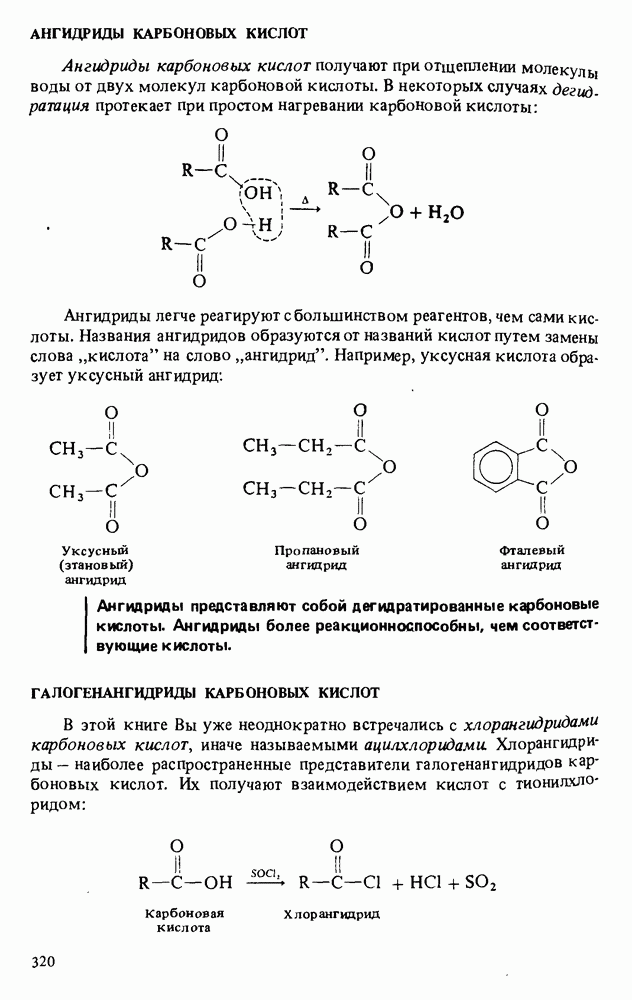
- АНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
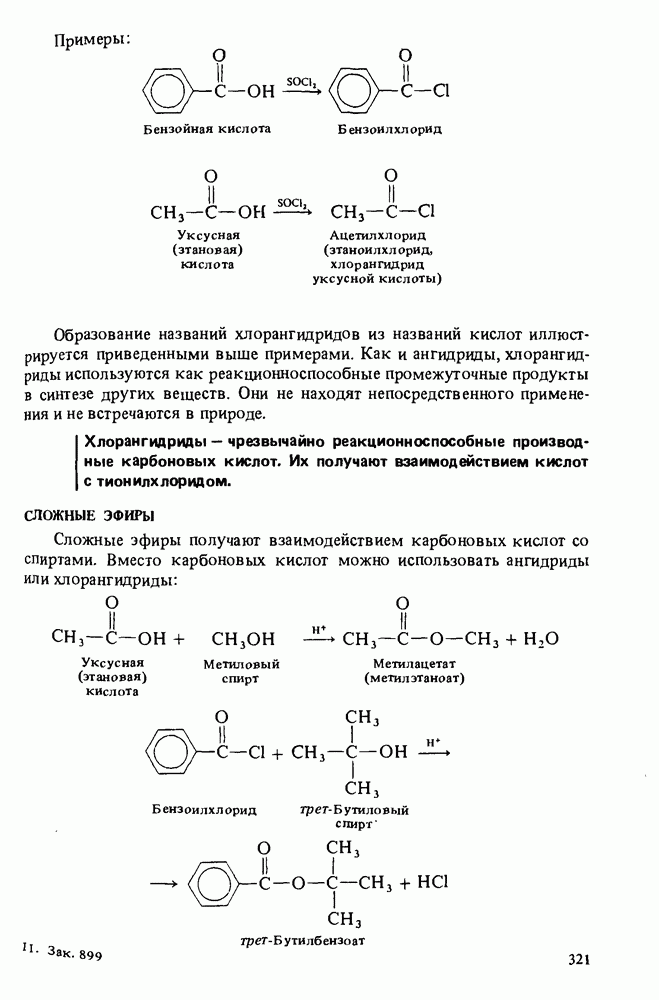
- ГАЛОГЕНАНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
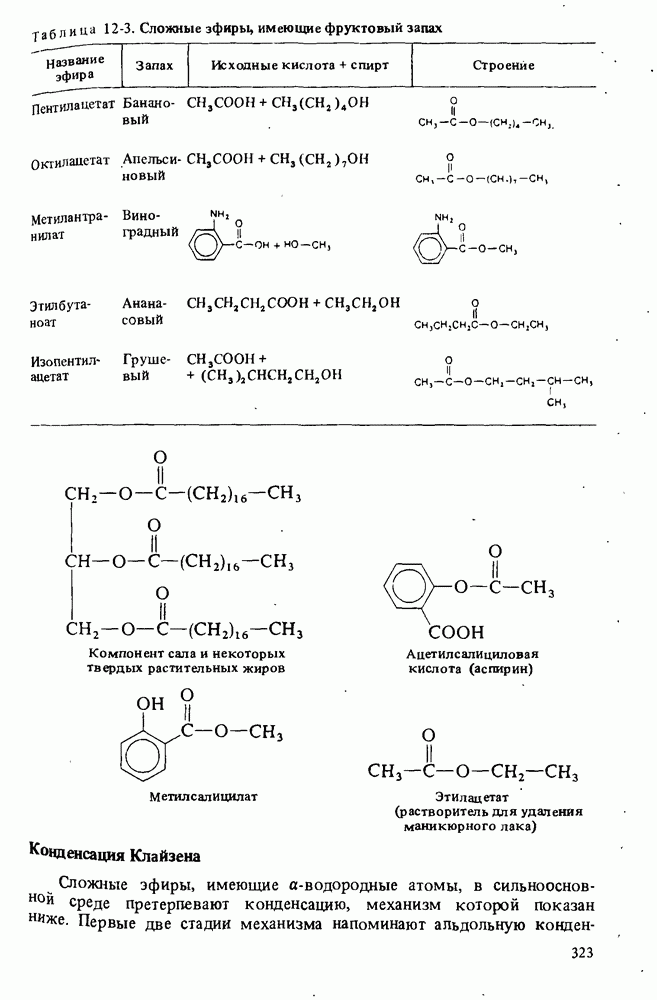
- СЛОЖНЫЕ ЭФИРЫ
- СОЛИ
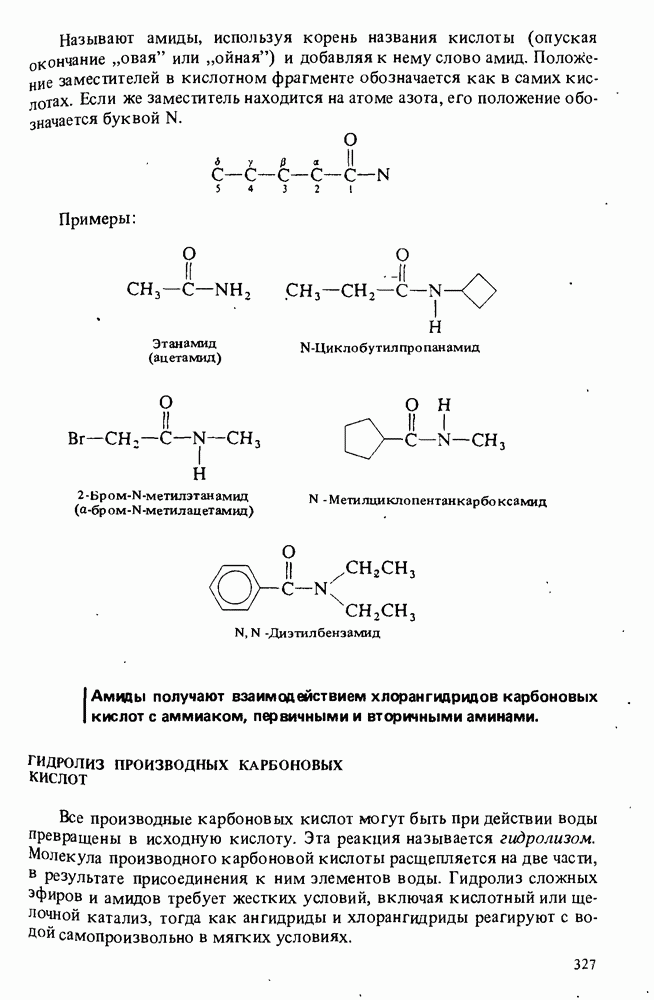
- АМИДЫ
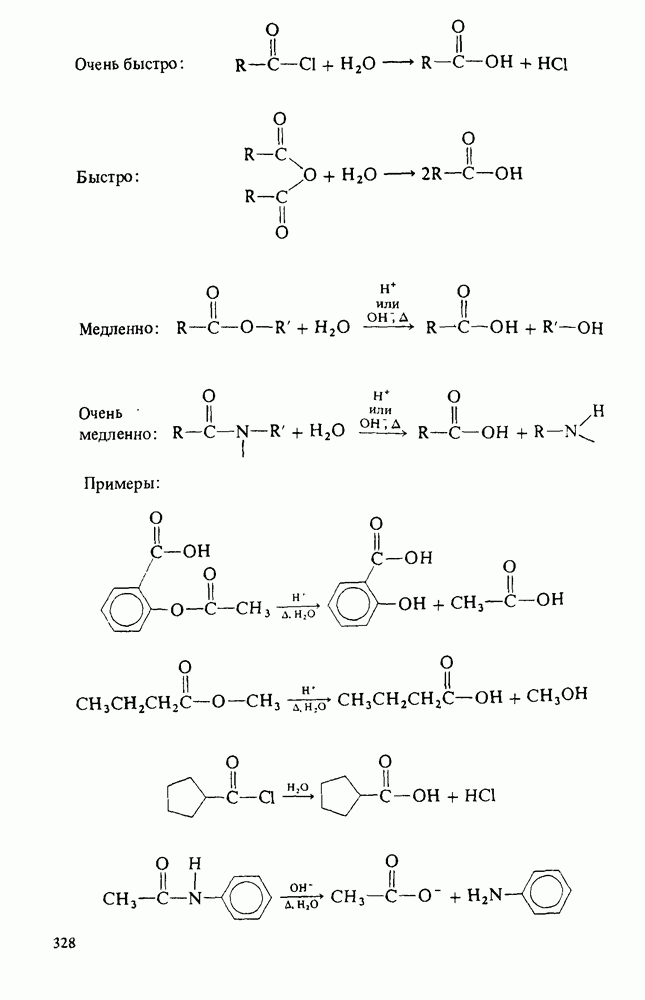
- ГИДРОЛИЗ ПРОИЗВОДНЫХ КАРБОНОВЫХ КИСЛОТ
- СИНТЕТИЧЕСКИЕ ВОЛОКНА
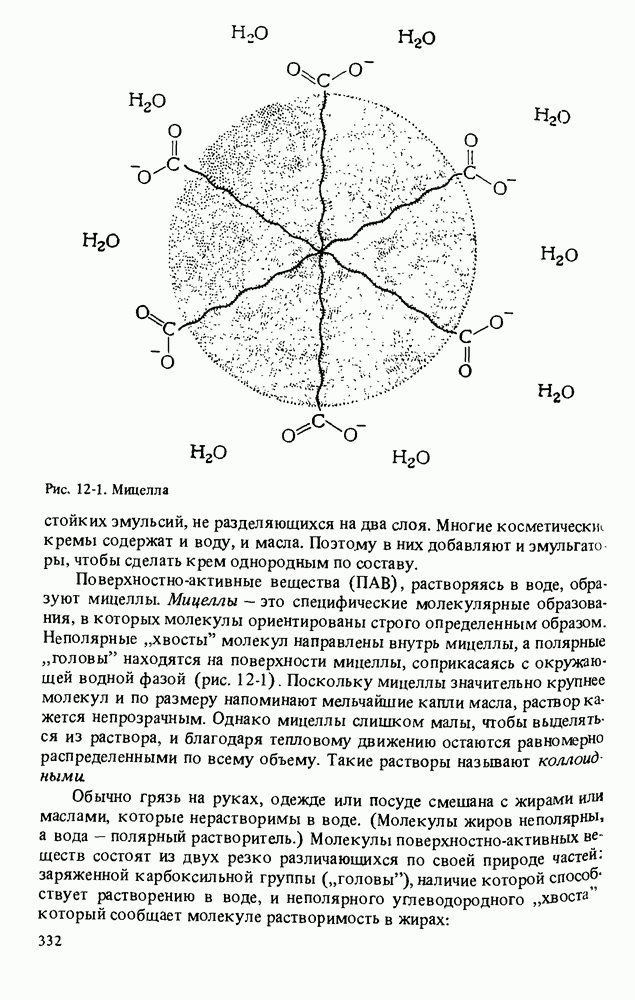
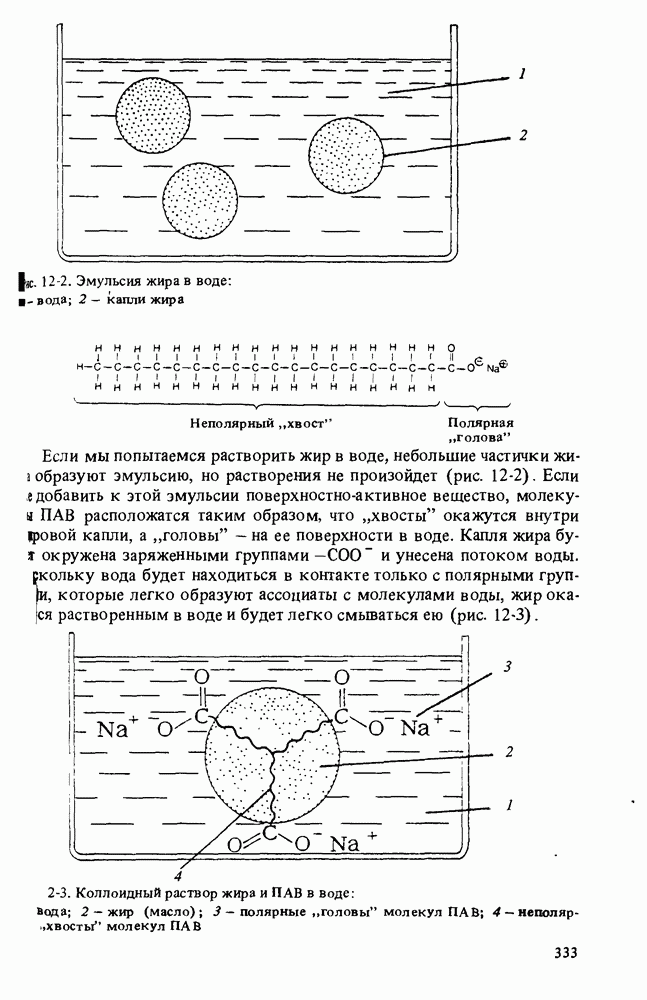
- МОЮЩИЕ СРЕДСТВА
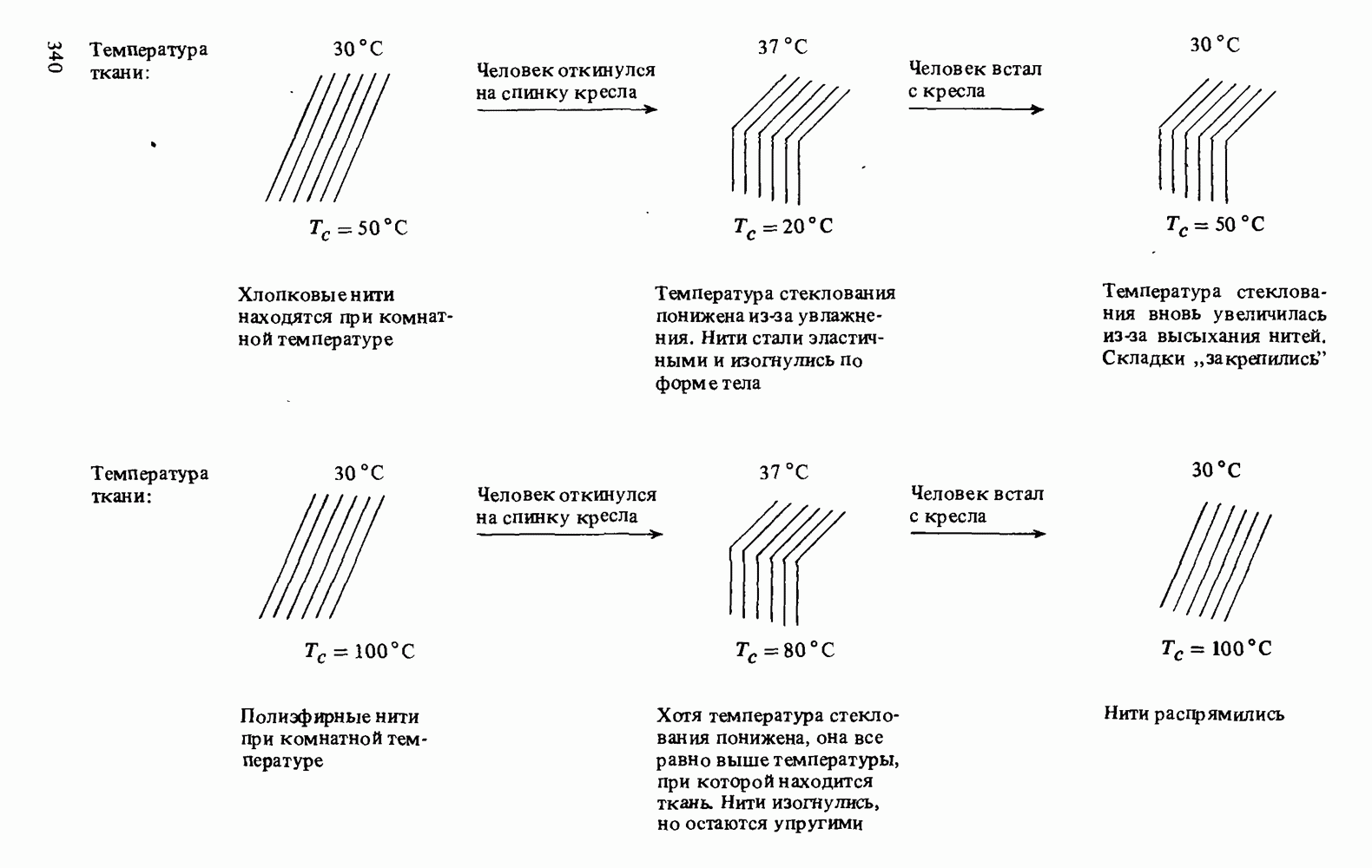
- Прикладная органическая химия: СВОЙСТВА ВОЛОКОН
- Глава 13. АМИНЫ
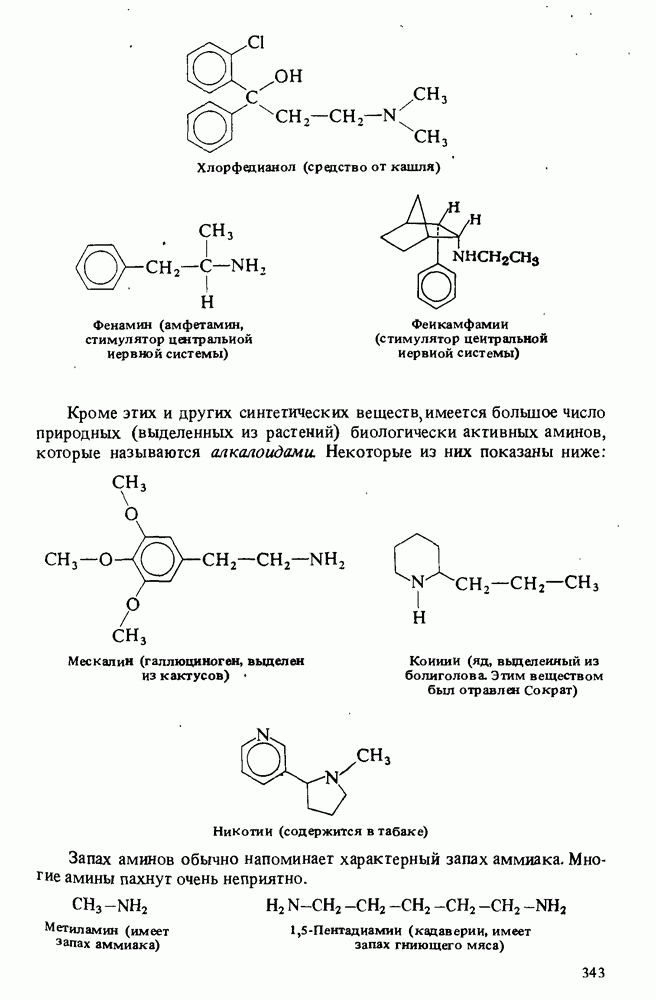
- БИОЛОГИЧЕСКИ АКТИВНЫЕ АМИНЫ
- ОСНОВНОСТЬ АМИНОВ
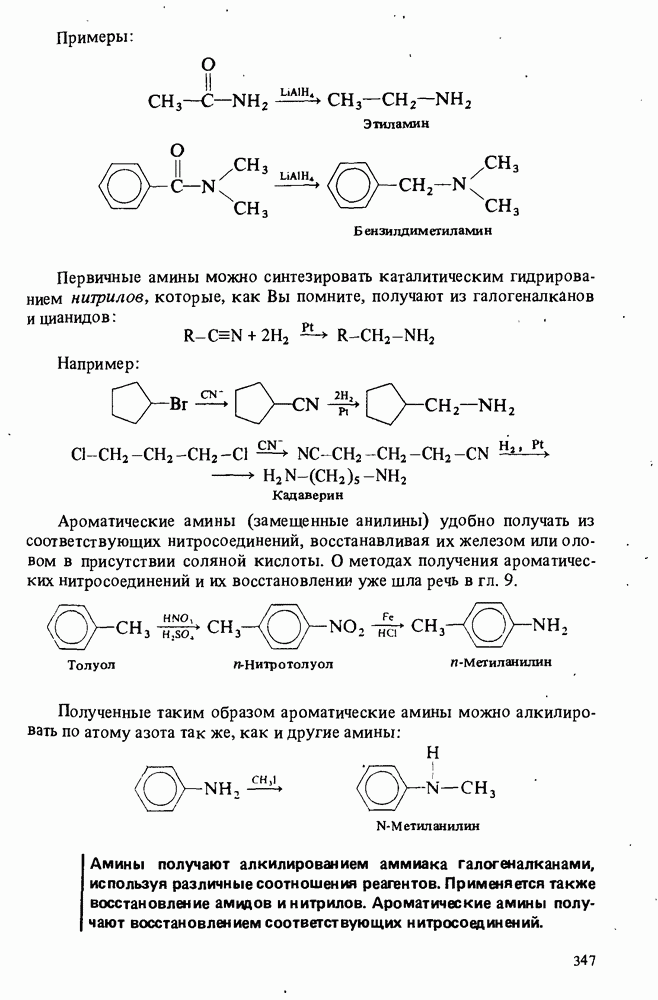
- ПОЛУЧЕНИЕ АМИНОВ
- РЕАКЦИИ АМИНОВ
- Прикладная органическая химия: ПОЛИМЕРЫ, ПОДВЕРГАЮЩИЕСЯ БИОЛОГИЧЕСКОЙ ДЕСТРУКЦИИ
- Глава 14. УГЛЕВОДЫ
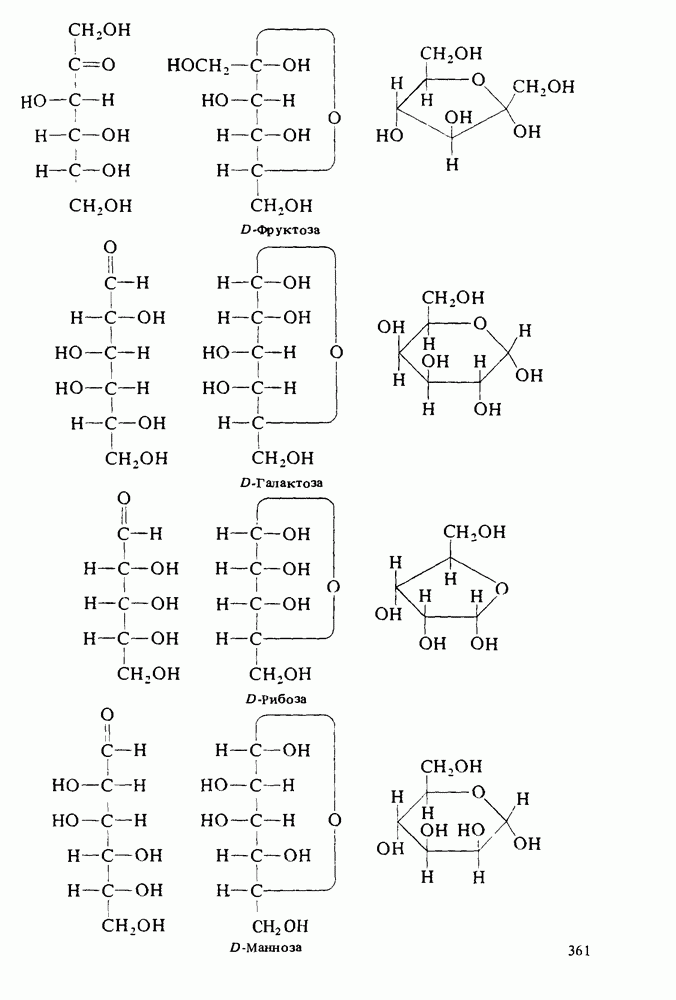
- МОНОСАХАРИДЫ
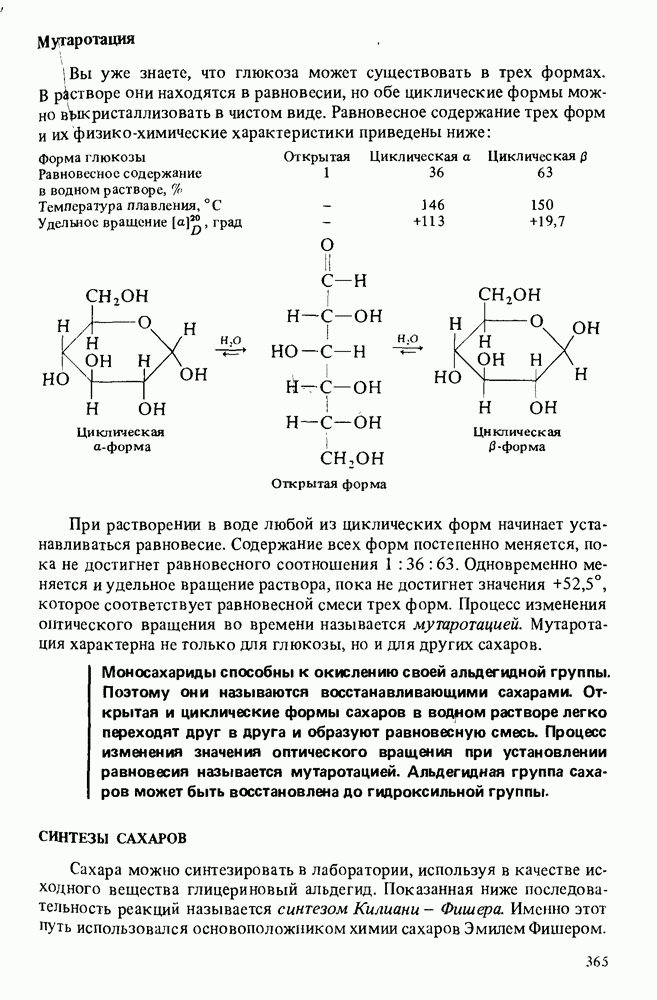
- РЕАКЦИИ МОНОСАХАРИДОВ
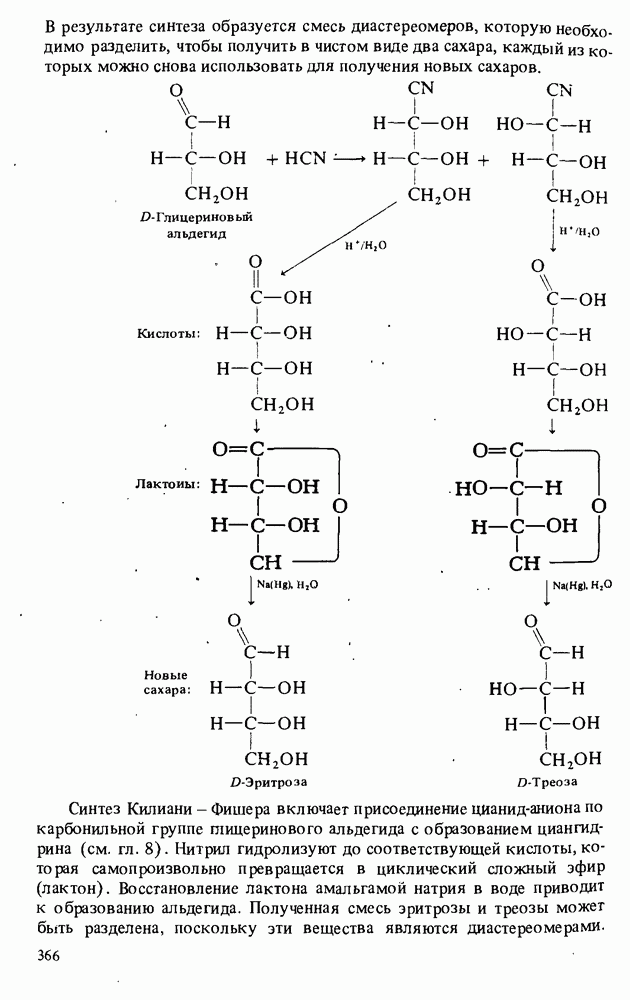
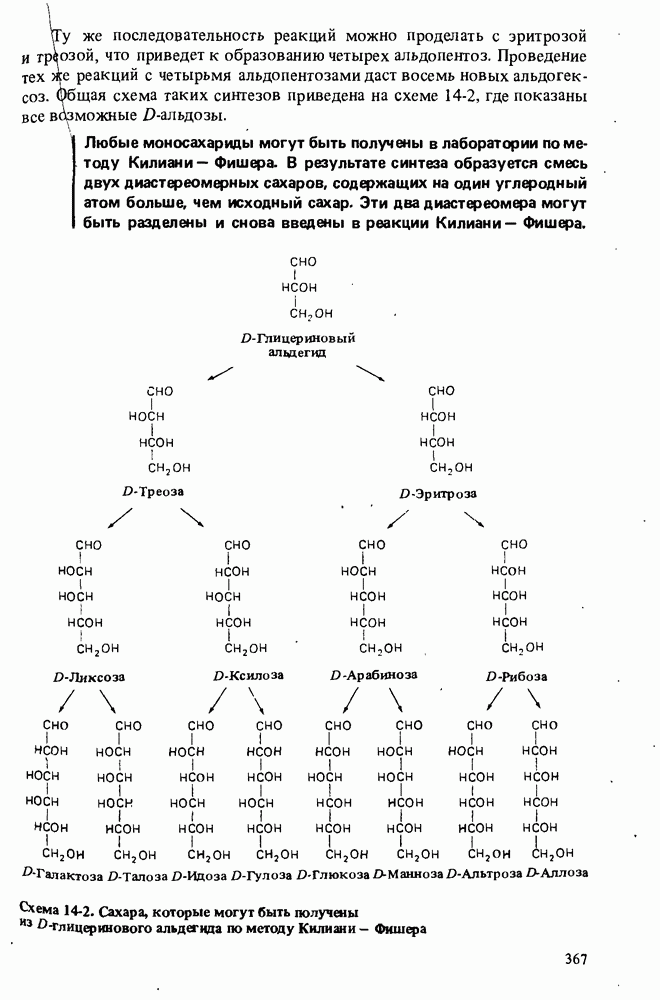
- СИНТЕЗЫ САХАРОВ
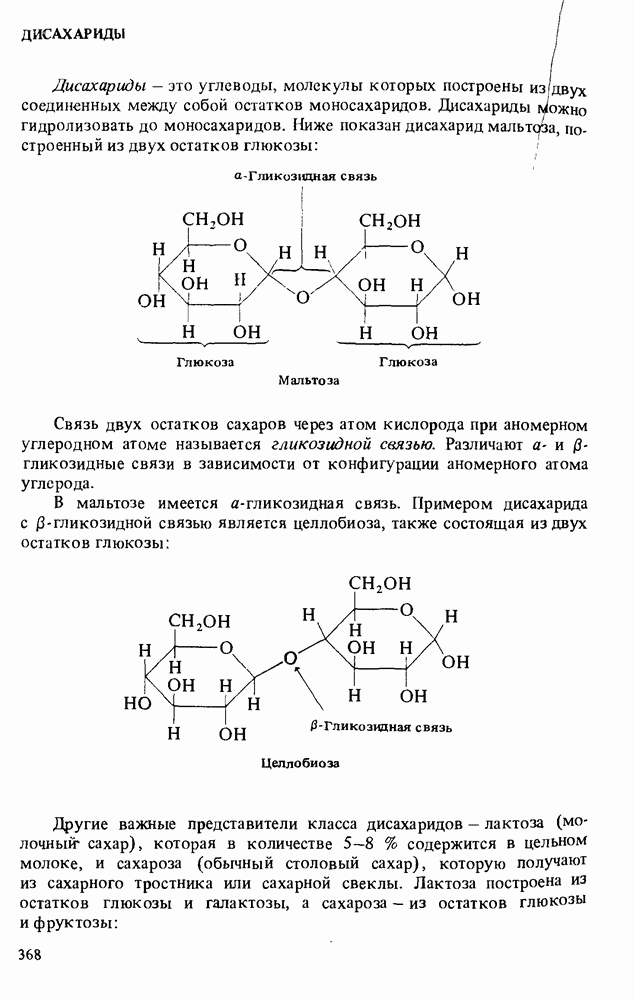
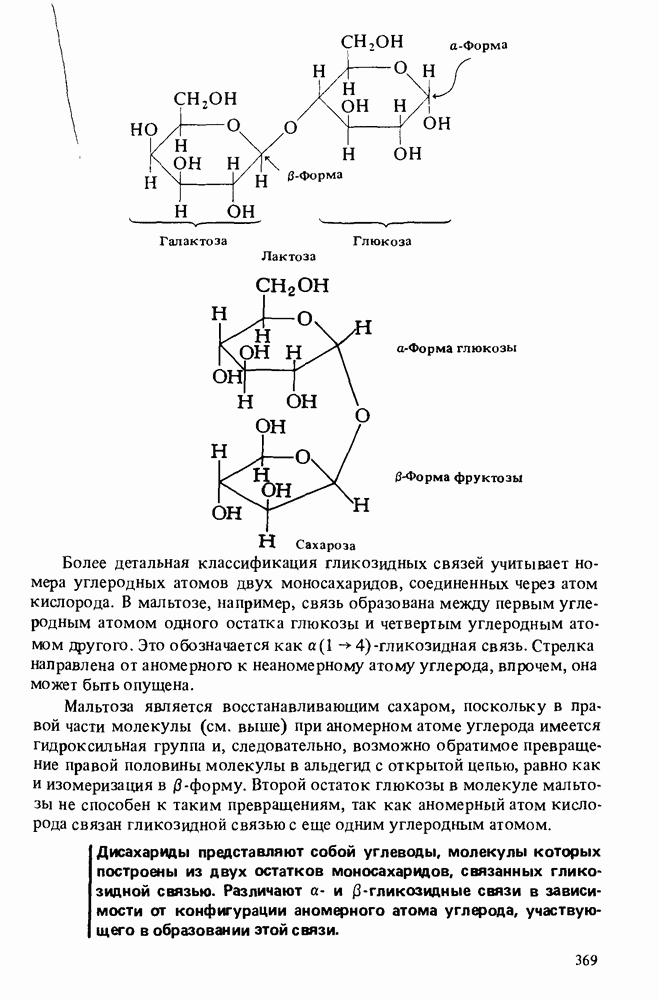
- ДИСАХАРИДЫ
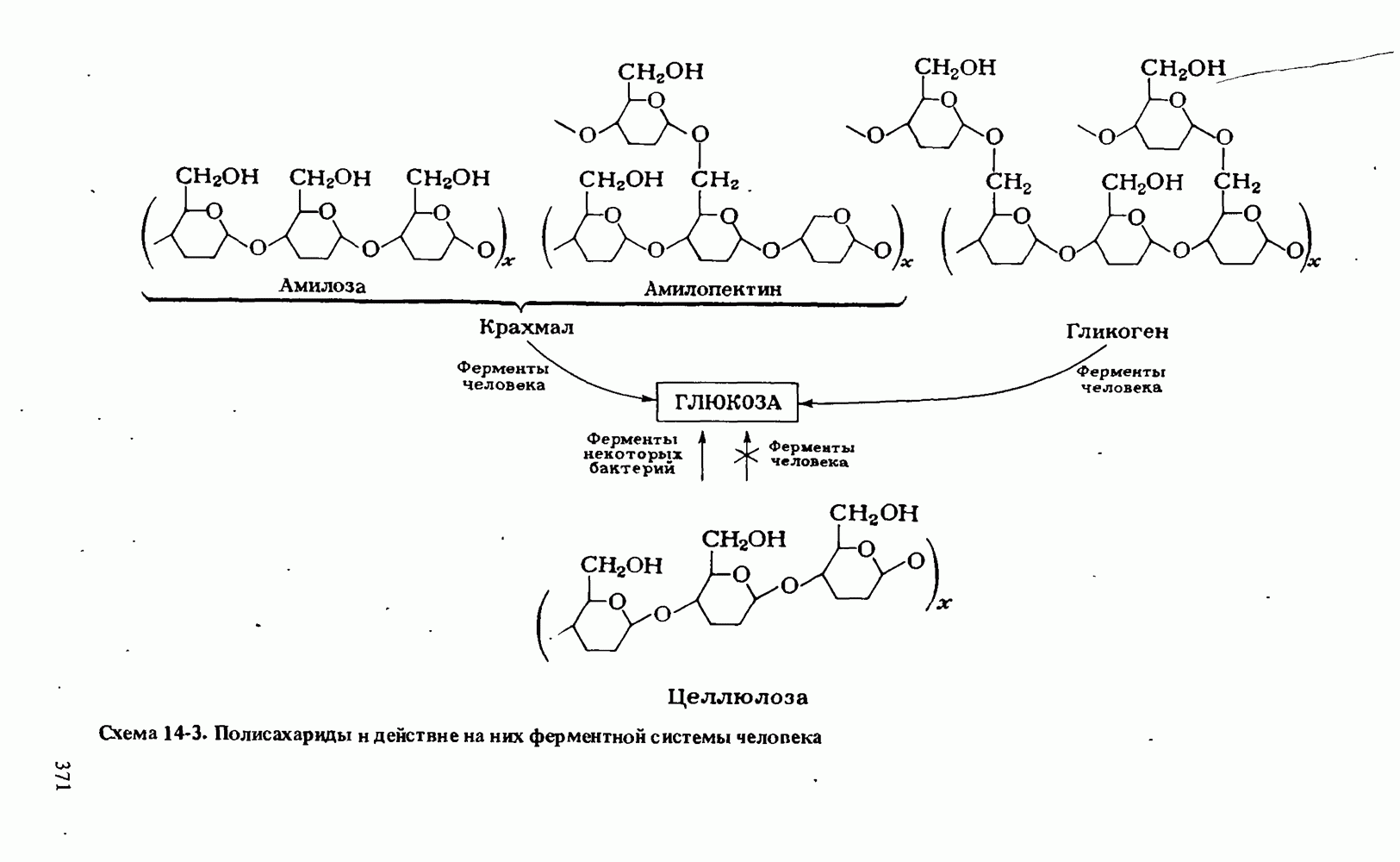
- ПОЛИСАХАРИДЫ
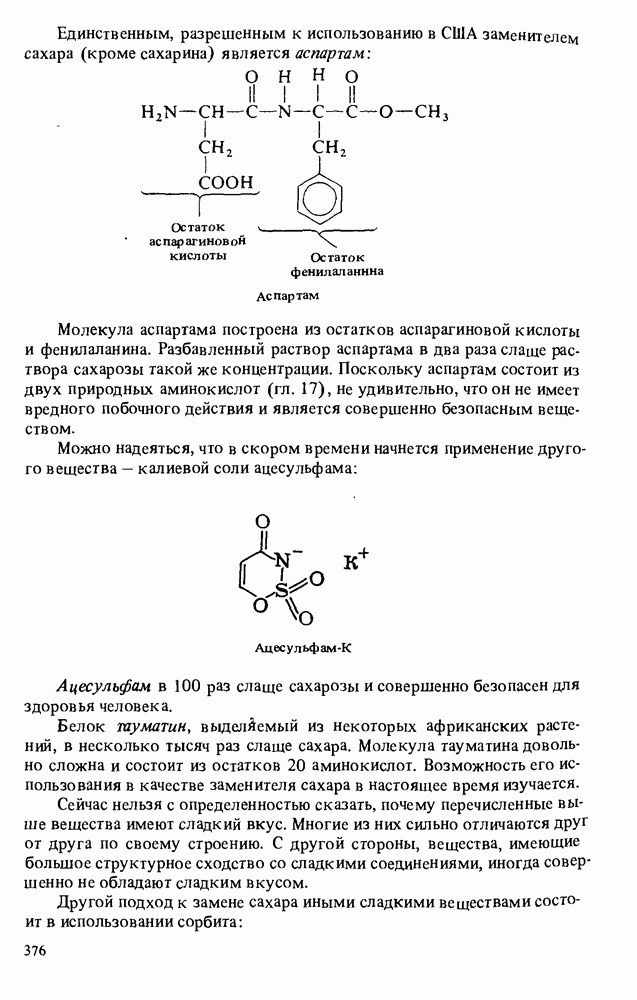
- Прикладная органическая химия: ПИЩЕВЫЕ СВОЙСТВА УГЛЕВОДОВ
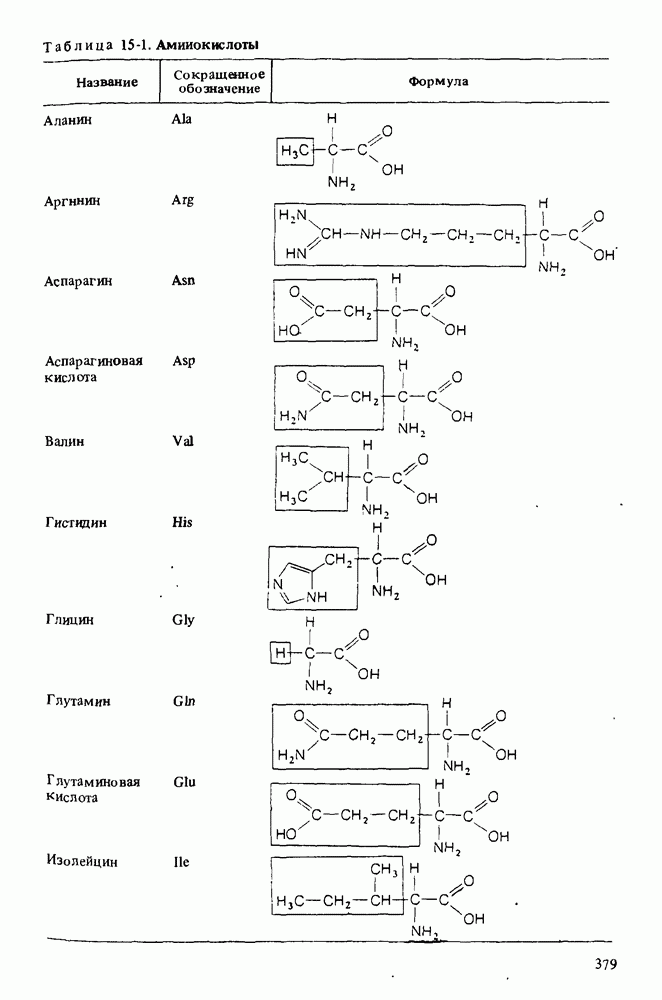
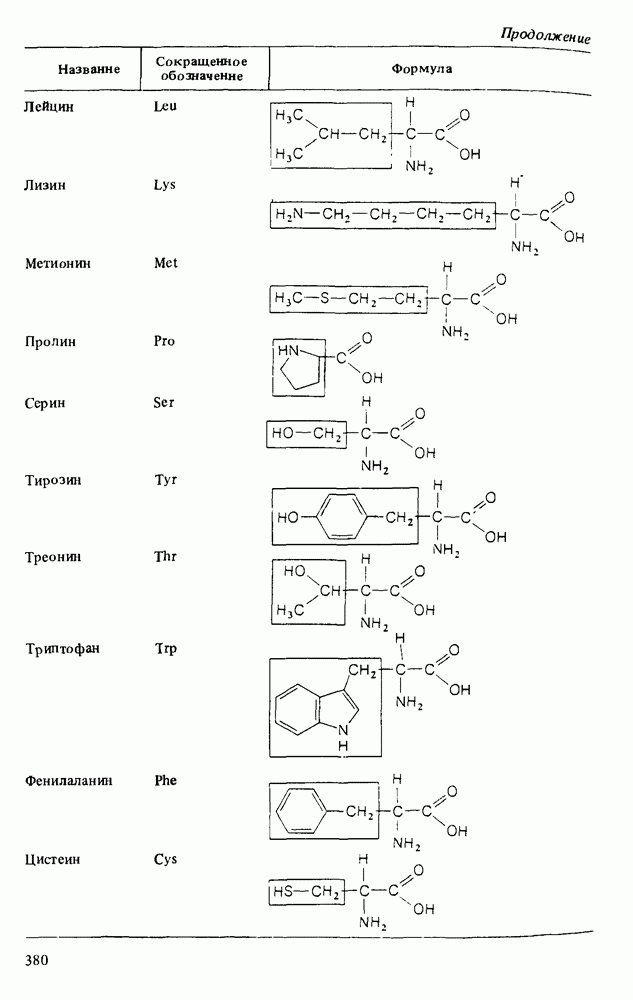
- Глава 15. АМИНОКИСЛОТЫ И БЕЛКИ
- КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА АМИНОКИСЛОТ
- АНАЛИЗ АМИНОКИСЛОТ
- СТРОЕНИЕ БЕЛКОВ
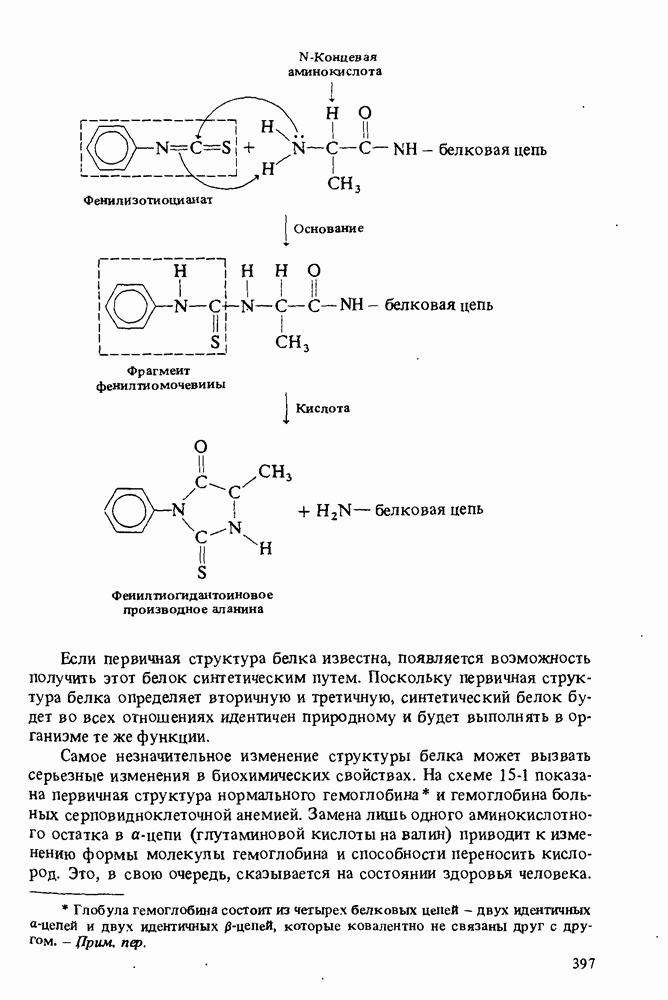
- УСТАНОВЛЕНИЕ ПЕРВИЧНОЙ СТРУКТУРЫ БЕЛКОВ
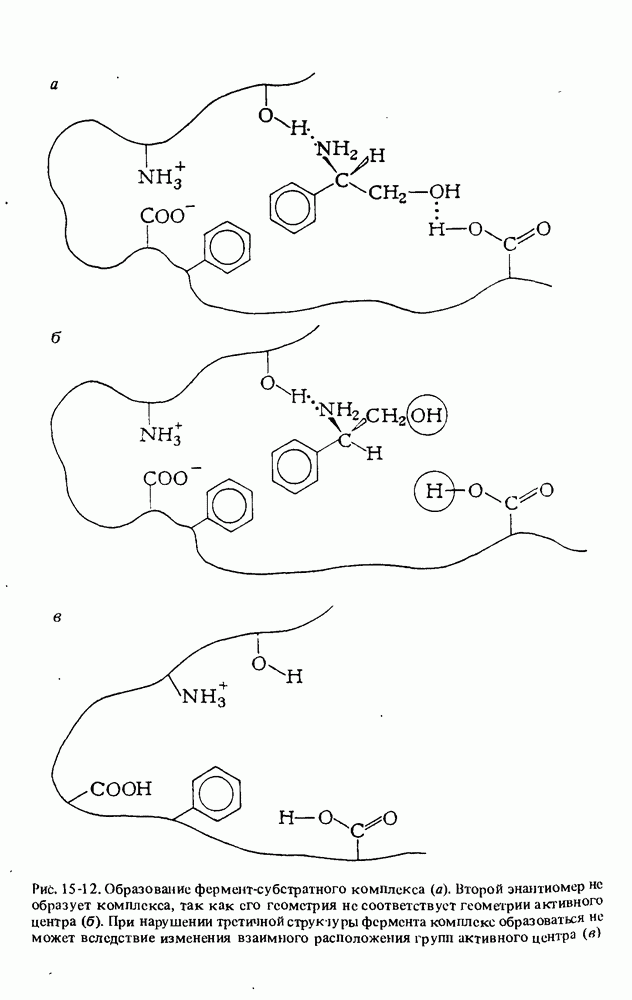
- ФЕРМЕНТЫ
- Глава 16. ЛИПИДЫ
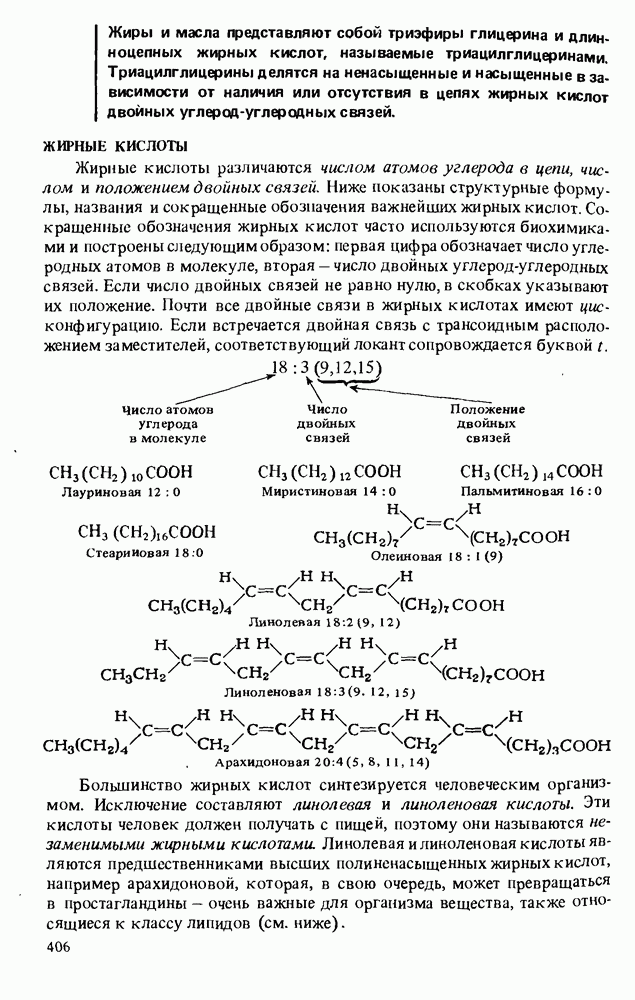
- ЖИРНЫЕ КИСЛОТЫ
- НАЗВАНИЯ ТРИАЦИЛГЛИЦЕРИНОВ
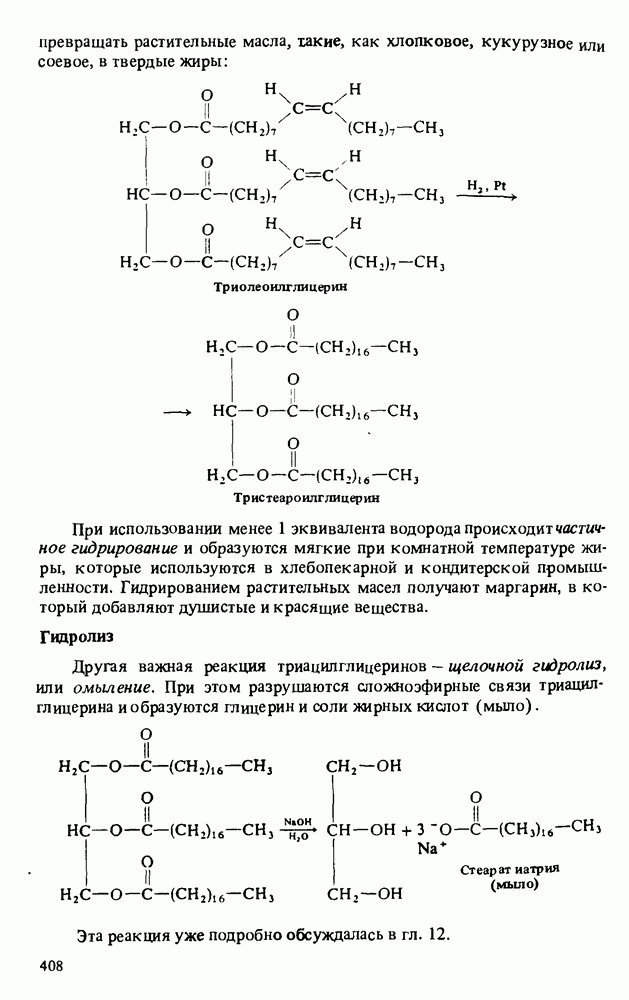
- РЕАКЦИИ ТРИАЦИЛГЛИЦЕРИНОВ
- ЛИПИДЫ, ОТЛИЧНЫЕ ОТ ТРИАЦИЛГЛИЦЕРИНОВ
- Прикладная органическая химия: ПИЩЕВЫЕ СВОЙСТВА ЛИПИДОВ
- Глава 17. НУКЛЕИНОВЫЕ КИСЛОТЫ
- РИБОНУКЛЕИНОВЫЕ КИСЛОТЫ
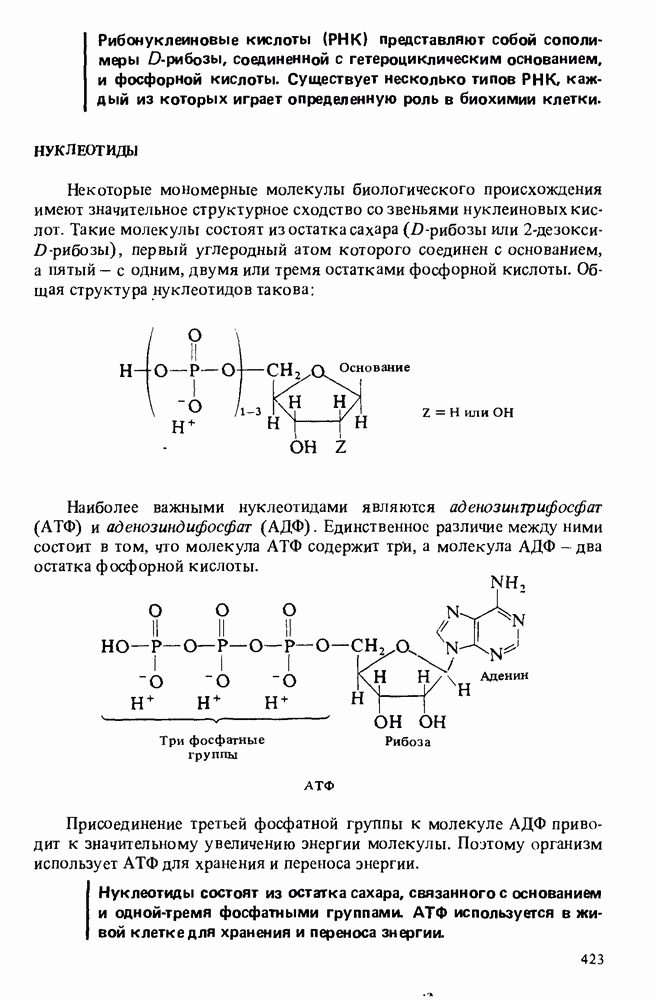
- НУКЛЕОТИДЫ
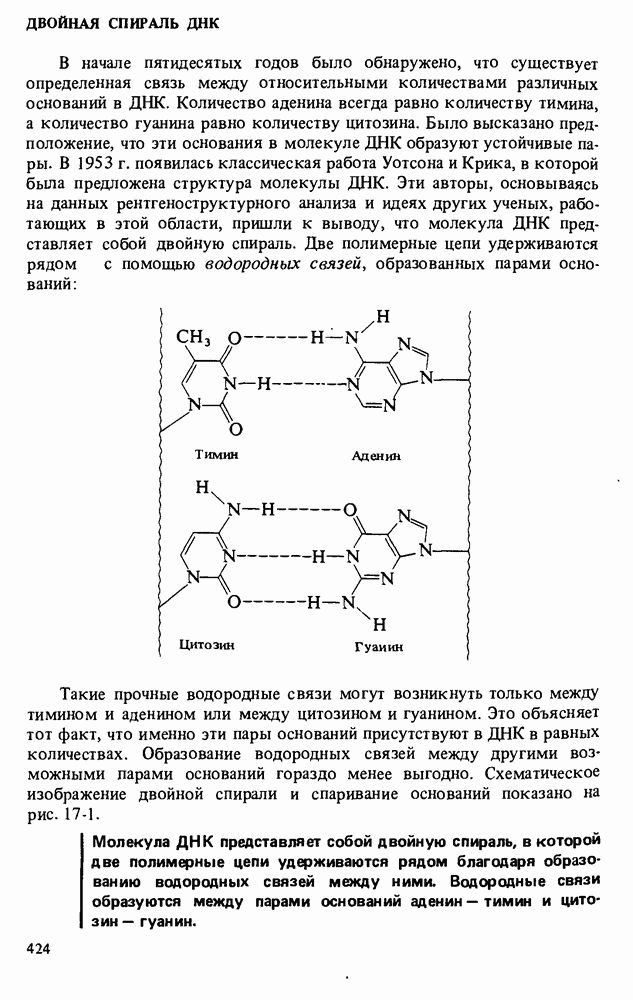
- ДВОЙНАЯ СПИРАЛЬ ДНК
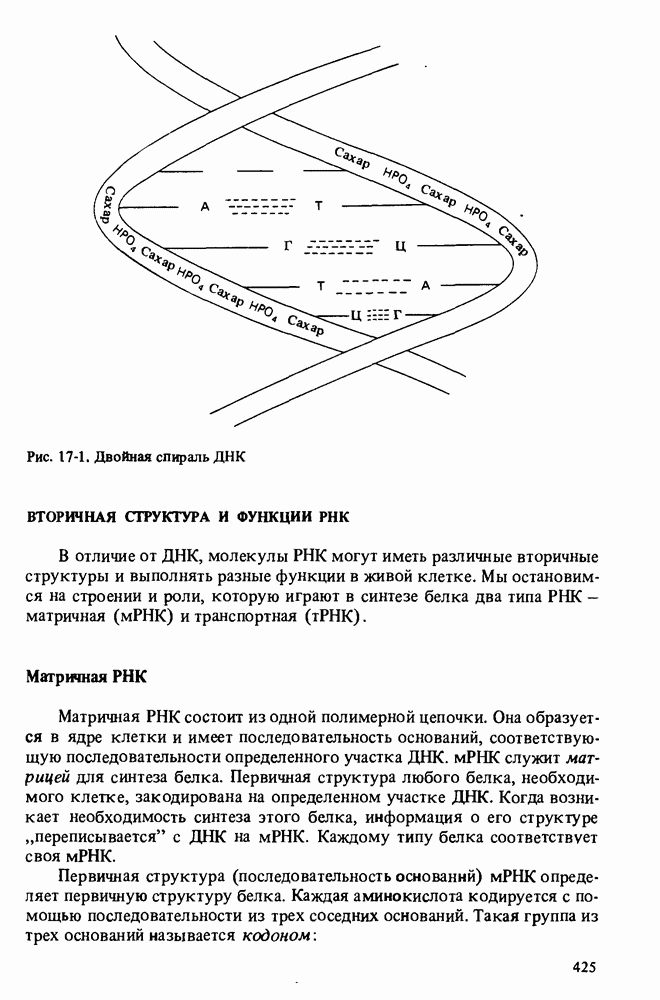
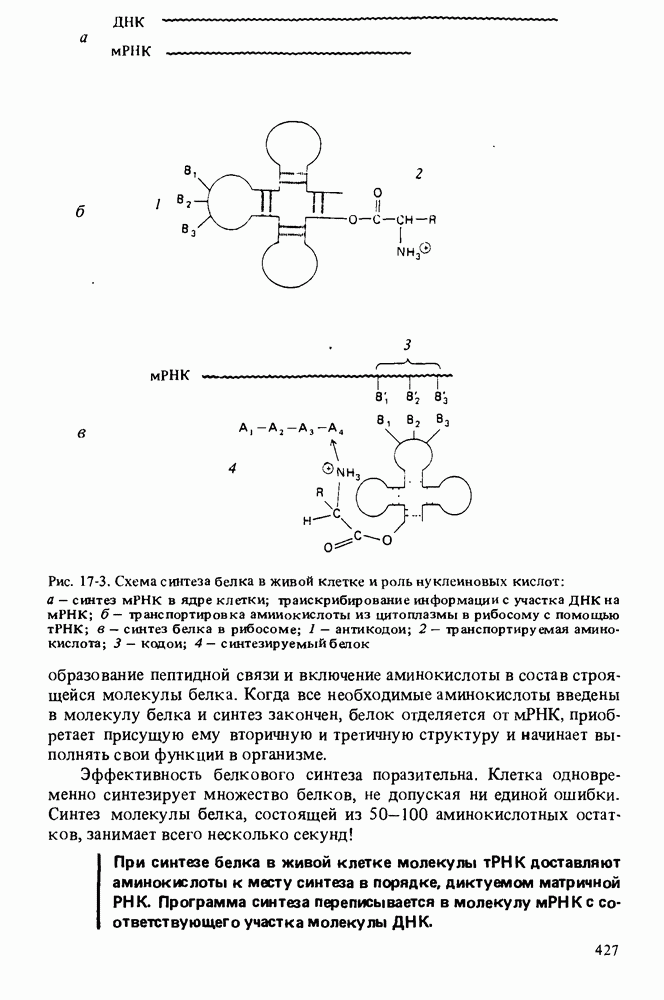
- ВТОРИЧНАЯ СТРУКТУРА И ФУНКЦИИ РНК
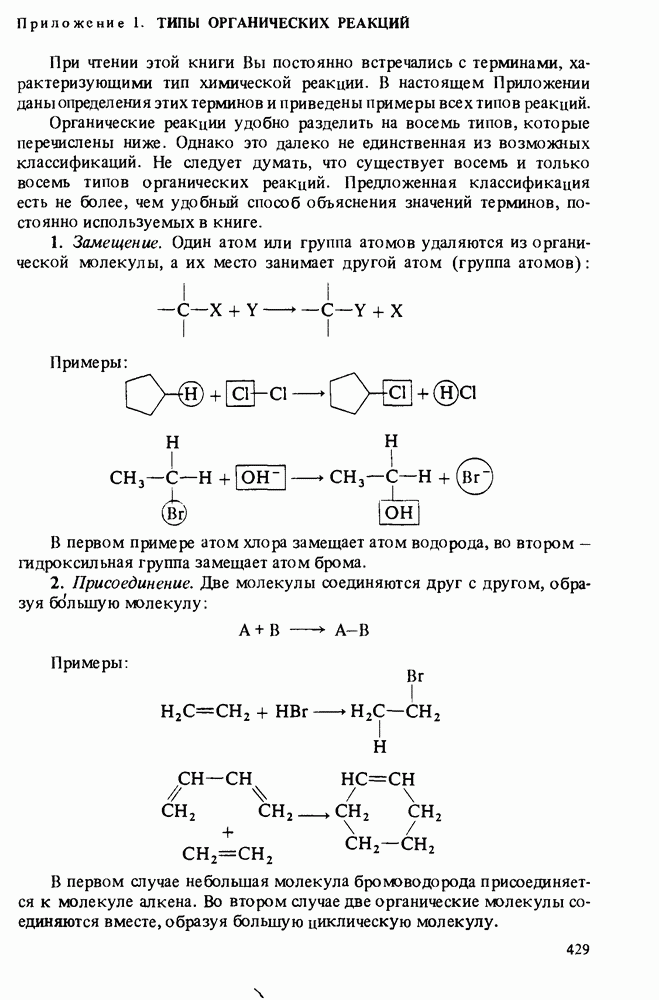
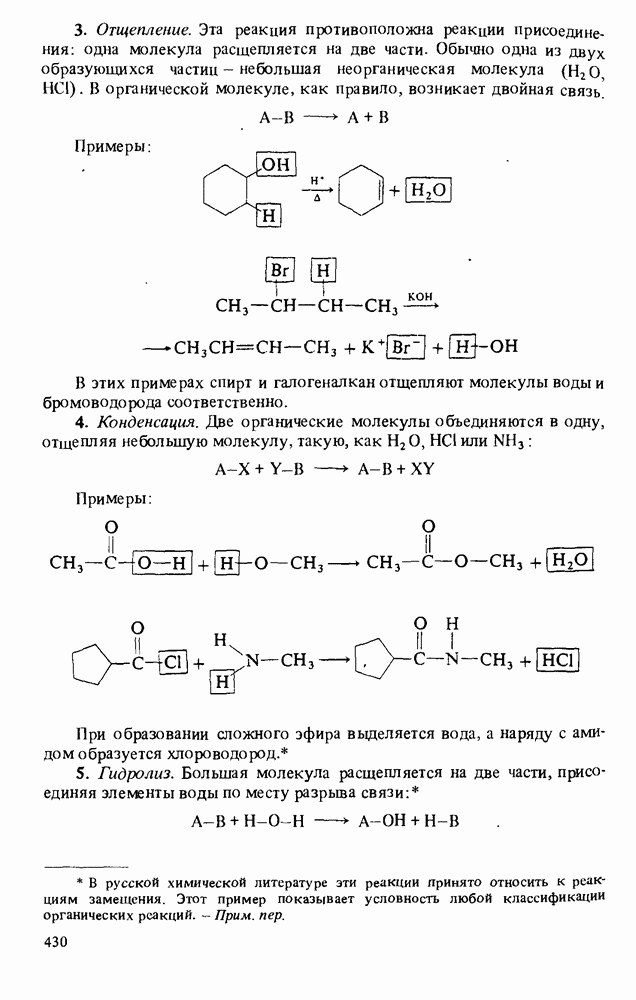
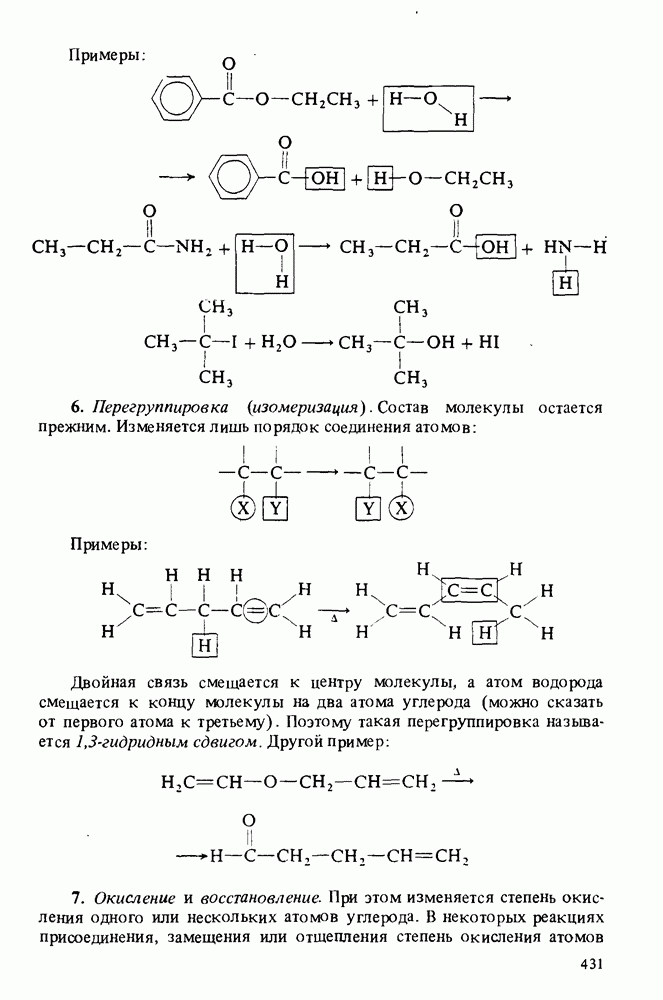
- Приложение 1. ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ
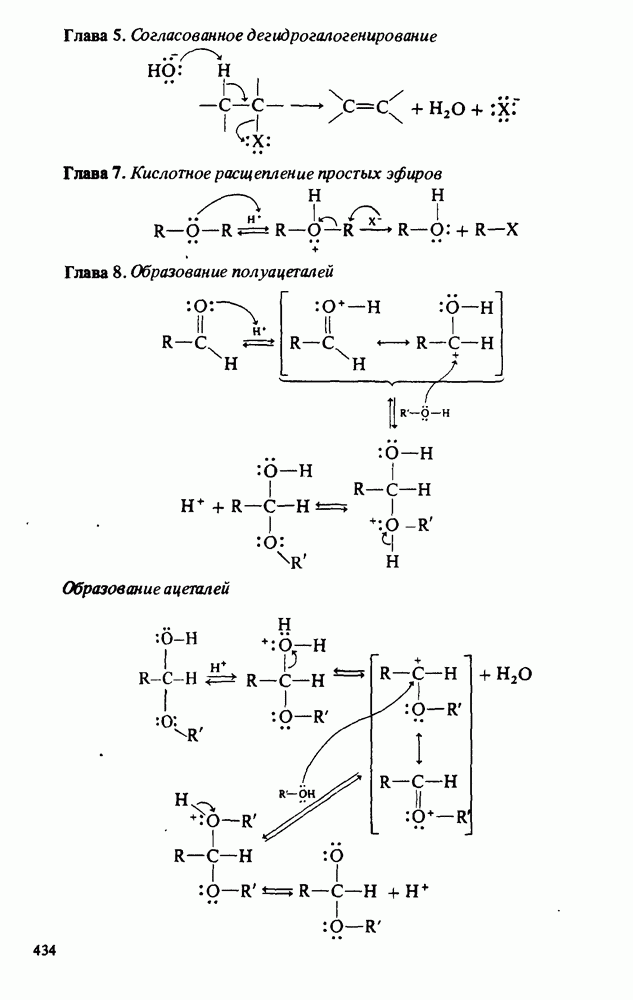
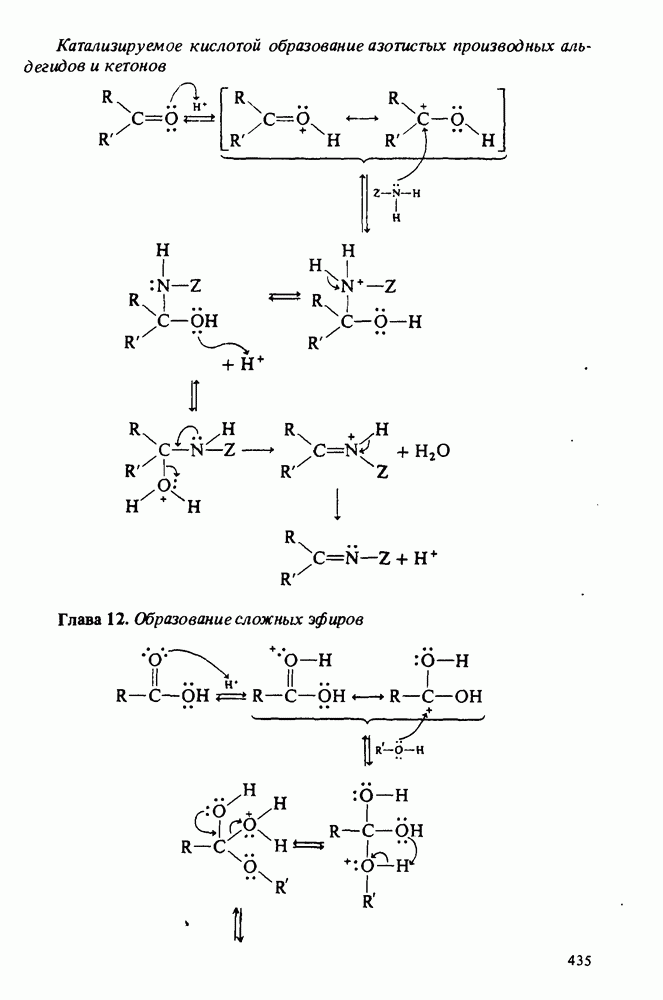
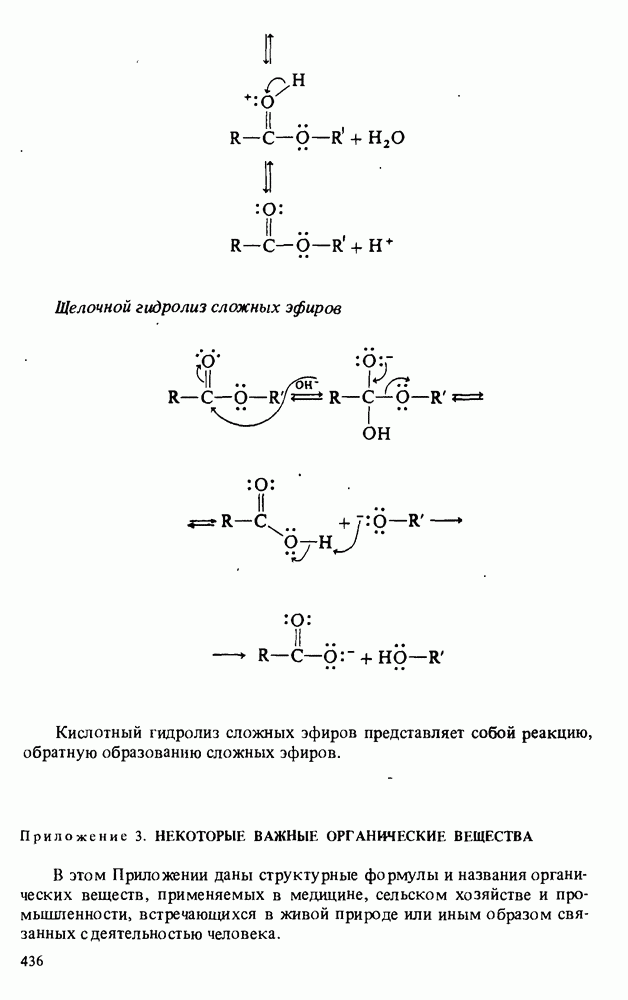
- Приложение 2. МЕХАНИЗМЫ НЕКОТОРЫХ РЕАКЦИЙ
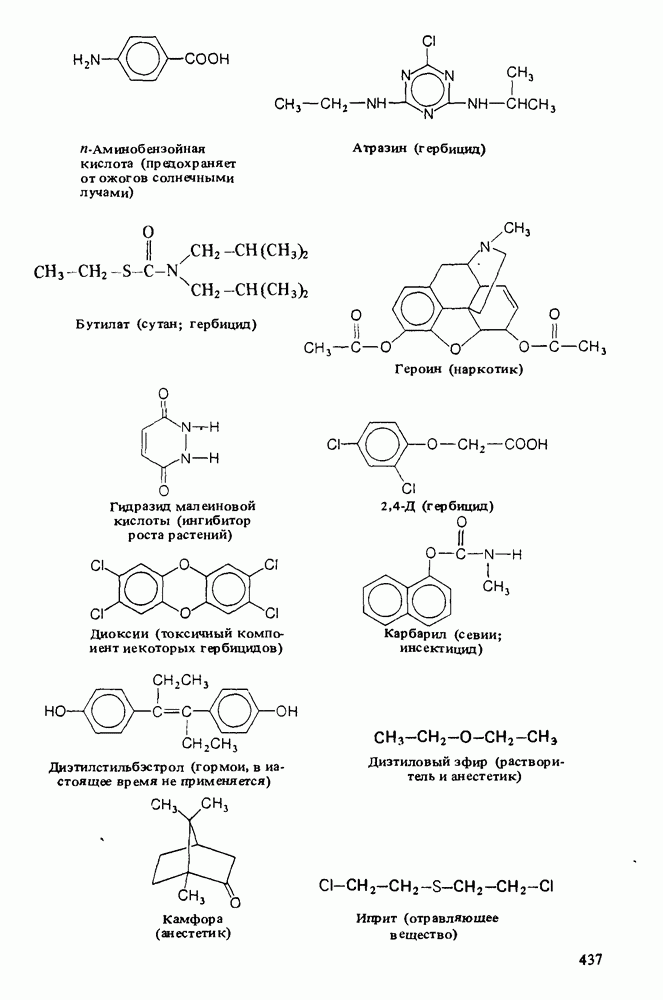
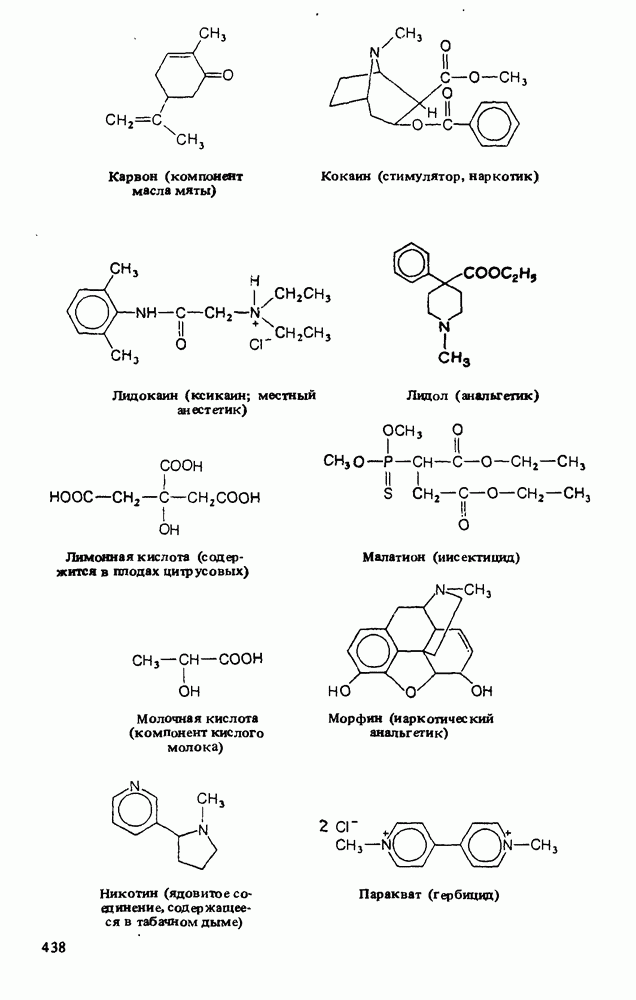
- Приложение 3. НЕКОТОРЫЕ ВАЖНЫЕ ОРГАНИЧЕСКИЕ ВЕЩЕСТВА