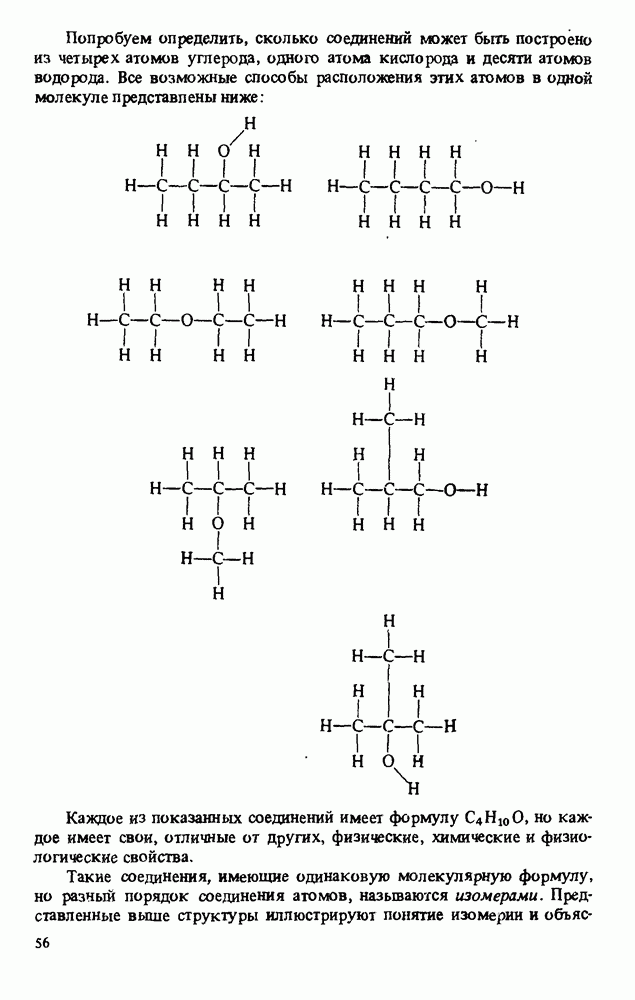| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
АТОМНАЯ ТЕОРИЯ
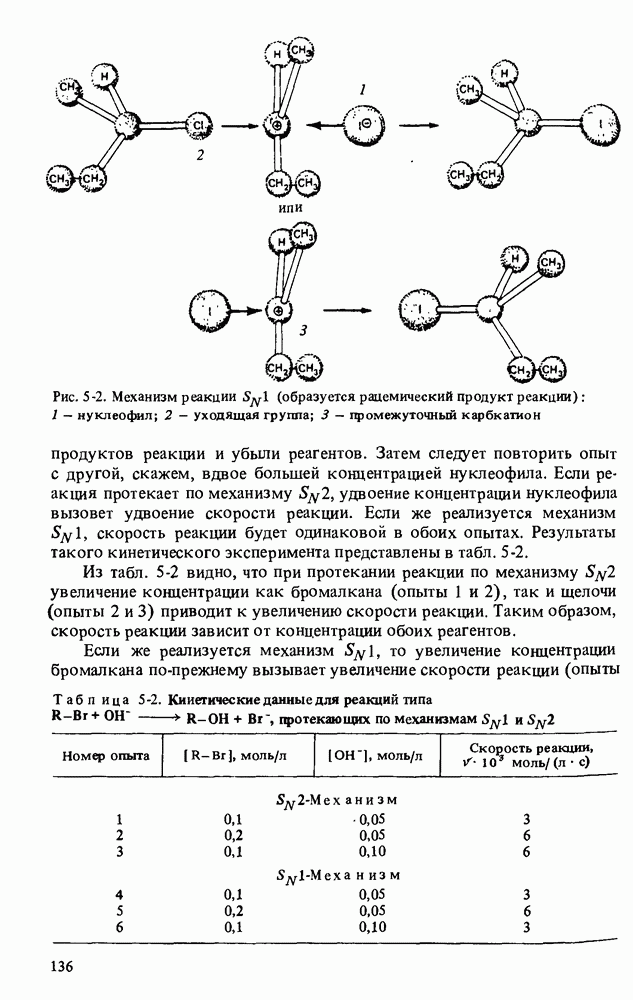
Материя построена из атомов, состоящих, в свою очередь, из еще меньших частиц — протонов, нейтронов и электронов, главнейшие сведения о которых помещены в табл. 1-1
Анализ фактов, обнаруженных разными учеными, видную роль среди которых играл Резерфорд, привел к пониманию того, что в атомах имеются небольшие тяжелые ядра, в состав которых входят протоны и нейтроны и в которых сосредоточена почти вся масса атома. Большая часть атома заполнена электронами и представляет собой почти пустое пространство.
Последующие работы химиков, физиков и математиков выявили характер расположения электронов внутри атомов. Здесь будут представлены только основные положения теории электронного строения для некоторых атомов и главные принципы, используемые в дальнейшем изложении.
Электроны расположены в трехмерном пространстве вокруг ядра атома. Несколько упрощенно можно считать, что внутри этого пространства имеются области, в которых могут располагаться электроны. Эти области называются орбиталями. Каждая орбиталь характеризуется размером, формой и ориентацией внутри атома, и каждой присвоено буквенно-цифровое обозначение.
Хотя в атоме имеется большое число орбиталей, в обычных условиях только сравнительно малая их часть занята электронами. Ниже приводится список общепринятых обозначений первых (т. е. ближайших к ядру) восемнадцати орбиталей. Цифра (номер) характеризует размерили средний диаметр орбитали, а буква — форму орбитали. s-Орбиталь представляет собой сферу, центр которой совпадает с центром (ядром) атома, а три  -орбитали напоминают объемные восьмерки, оси которых
-орбитали напоминают объемные восьмерки, оси которых
Таблица 1-1. (см. скан) Субатомные частицы

Рис. 1-1. Расположение атомных орбиталей: 1 - s-oрбиталь, имеет одну возможную ориентацию; 2 —  -орбиталь, имеет три возможные ориентации; точкой показано ядро атома
-орбиталь, имеет три возможные ориентации; точкой показано ядро атома
перпендикулярны друг другу (рис. 1-1). Таким образом,  рбиталь - сферическая и наименьшая по размерам;
рбиталь - сферическая и наименьшая по размерам;  -орбиталь — также сферическая, но большего размера;
-орбиталь — также сферическая, но большего размера;  -орбитали имеют форму восьмерок и по размеру сопоставимы с
-орбитали имеют форму восьмерок и по размеру сопоставимы с  . Орбитали имеют более сложную форму. Существуют также
. Орбитали имеют более сложную форму. Существуют также  -орбитали, но мы не будем рассматривать их в этой книге, так как большинство атомов, встречающихся в органических соединениях, не имеют занятых электронами
-орбитали, но мы не будем рассматривать их в этой книге, так как большинство атомов, встречающихся в органических соединениях, не имеют занятых электронами  Список 18 атомных орбиталей таков:
Список 18 атомных орбиталей таков:

Орбитали группируются в соответствии с их размерами и эти группы называются слоями или оболочками. В первой электронной оболочке имеется лишь одна орбиталь —  На второй оболочке их уже четыре, а на третьей — девять. Каждая орбиталь может быть свободной (пустой) или занятой одним или двумя электронами. Заметим, что в каждой оболочке (кроме первой) существует три
На второй оболочке их уже четыре, а на третьей — девять. Каждая орбиталь может быть свободной (пустой) или занятой одним или двумя электронами. Заметим, что в каждой оболочке (кроме первой) существует три  -орбитали и пять
-орбитали и пять  -орбиталей (во всех оболочках, кроме двух первых). Поскольку на каждой орбитали может находиться по 2 электрона, группу
-орбиталей (во всех оболочках, кроме двух первых). Поскольку на каждой орбитали может находиться по 2 электрона, группу  -орбиталей могут занимать 6 электронов, а группу
-орбиталей могут занимать 6 электронов, а группу  -орбиталей — 10 электронов. Электроны сначала
-орбиталей — 10 электронов. Электроны сначала
занимают орбитали низших слоев и только затем — орбитали более высоких уровней. Легкость заполнения орбиталей уменьшается от начала к концу списка. Иными словами, электроны, занимающие более высокие орбитали, имеют большую энергию.
Ниже приведены электронные конфигурации атомов бериллия, углерода и железа. Надстрочные индексы показывают число электронов на каждой орбитали:

Атом бериллия  имеет
имеет  электрона на
электрона на  и
и  -орбиталях. Углеродный атом С имеет по 2 электрона на
-орбиталях. Углеродный атом С имеет по 2 электрона на  и
и  -орбиталях и по одному на двух
-орбиталях и по одному на двух  -рбиталях. Больший по размеру атом, такой, как железа
-рбиталях. Больший по размеру атом, такой, как железа  имеет больше электронов и более сложную электронную конфигурацию. Чтобы упростить запись, заполнение
имеет больше электронов и более сложную электронную конфигурацию. Чтобы упростить запись, заполнение  и
и  -орбиталей иногда суммируют и обозначают как
-орбиталей иногда суммируют и обозначают как  Строение электронных оболочек атомов элементов I, IV и VII групп периодической системы можно изобразить следующим образом:
Строение электронных оболочек атомов элементов I, IV и VII групп периодической системы можно изобразить следующим образом:

| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- Глава 1. КЛЮЧЕВЫЕ ПОНЯТИЯ ХИМИИ
- АТОМНАЯ ТЕОРИЯ
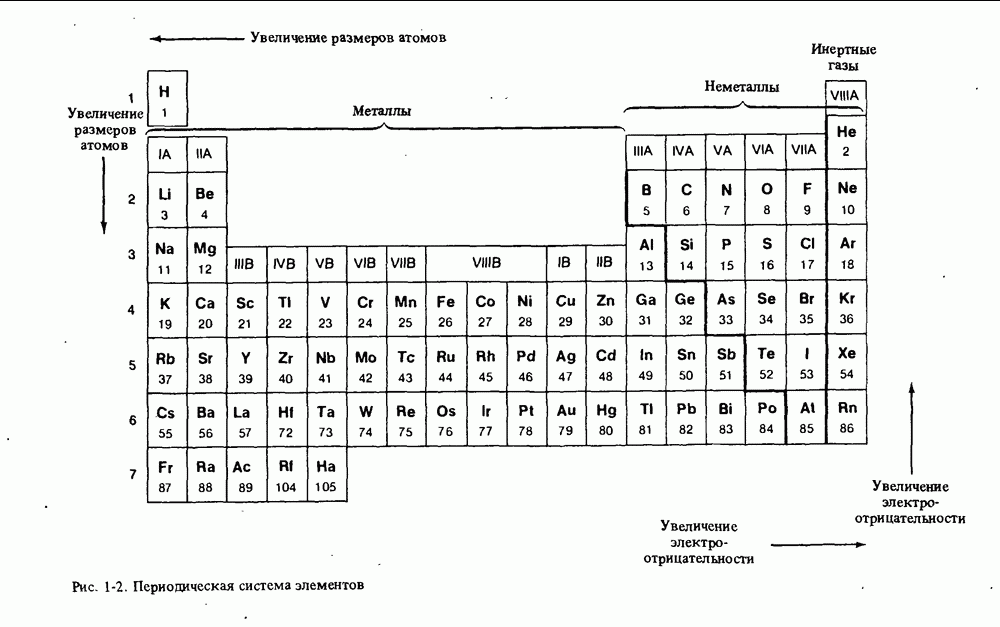
- ПЕРИОДИЧЕСКАЯ СИСТЕМА
- ХИМИЧЕСКАЯ СВЯЗЬ
- ФОРМУЛЫ ЛЬЮИСА
- ФОРМАЛЬНЫЙ ЗАРЯД
- РЕЗОНАНС
- ГЕОМЕТРИЯ МОЛЕКУЛ
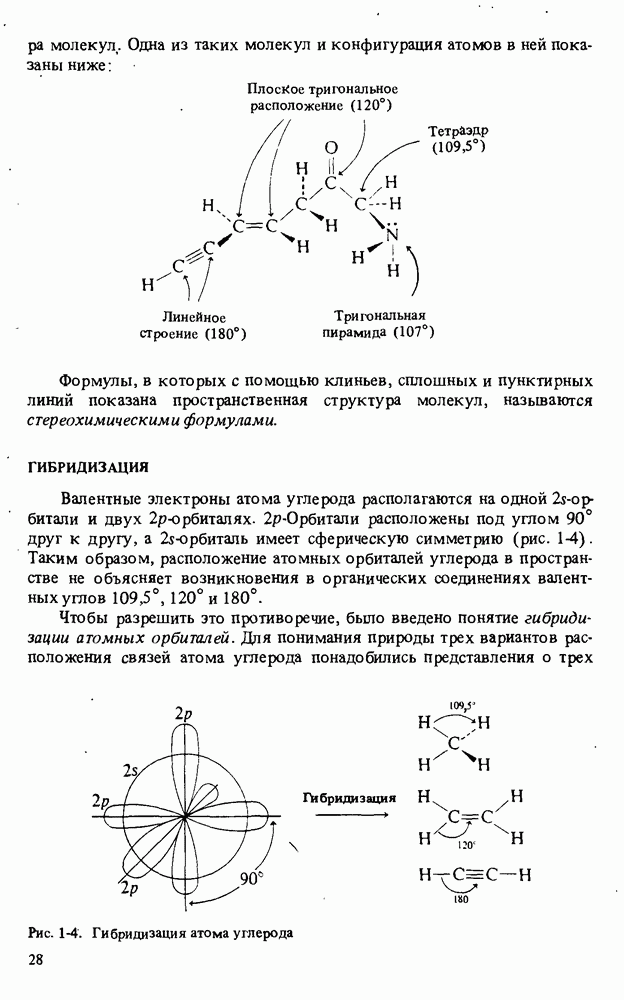
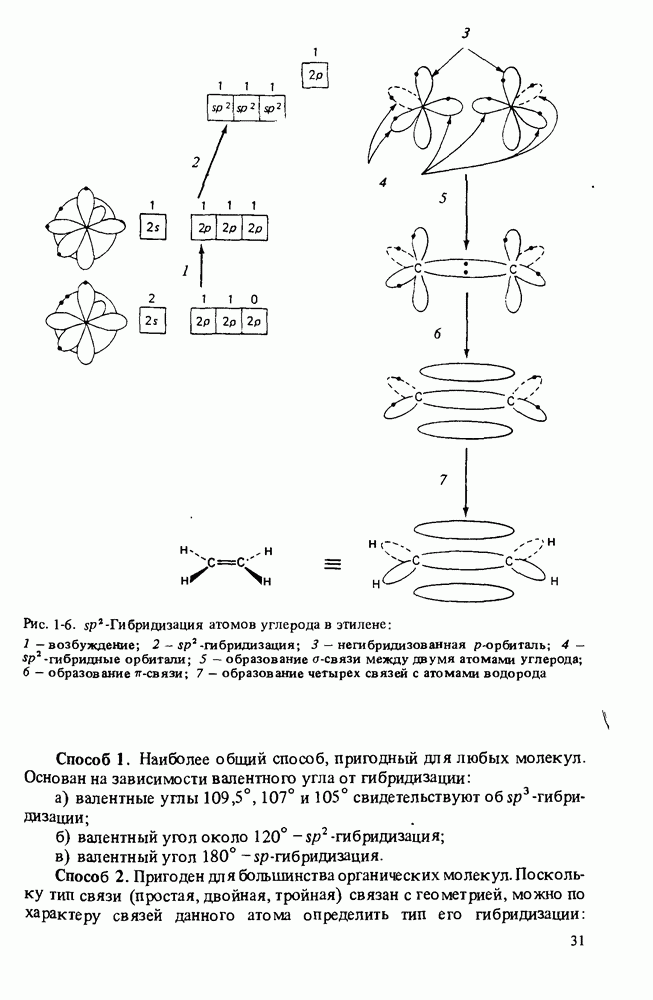
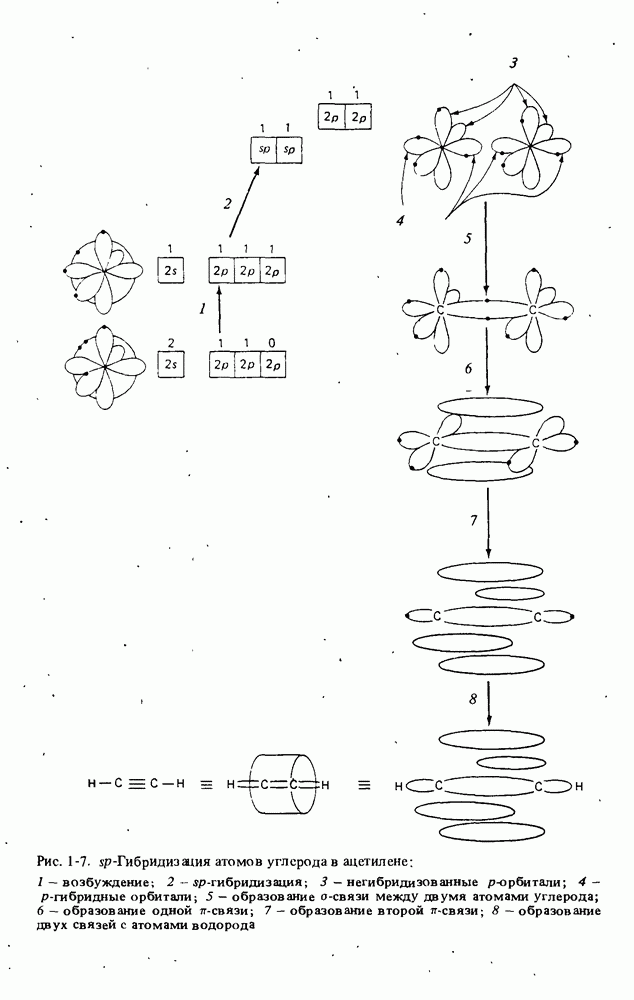
- ГИБРИДИЗАЦИЯ
- ХИМИЧЕСКИЕ ФОРМУЛЫ
- СОВЕТЫ ИЗУЧАЮЩЕМУ ОРГАНИЧЕСКУЮ ХИМИЮ
- СВОДКА ОСНОВНЫХ ПОЛОЖЕНИЙ ГЛ. 1
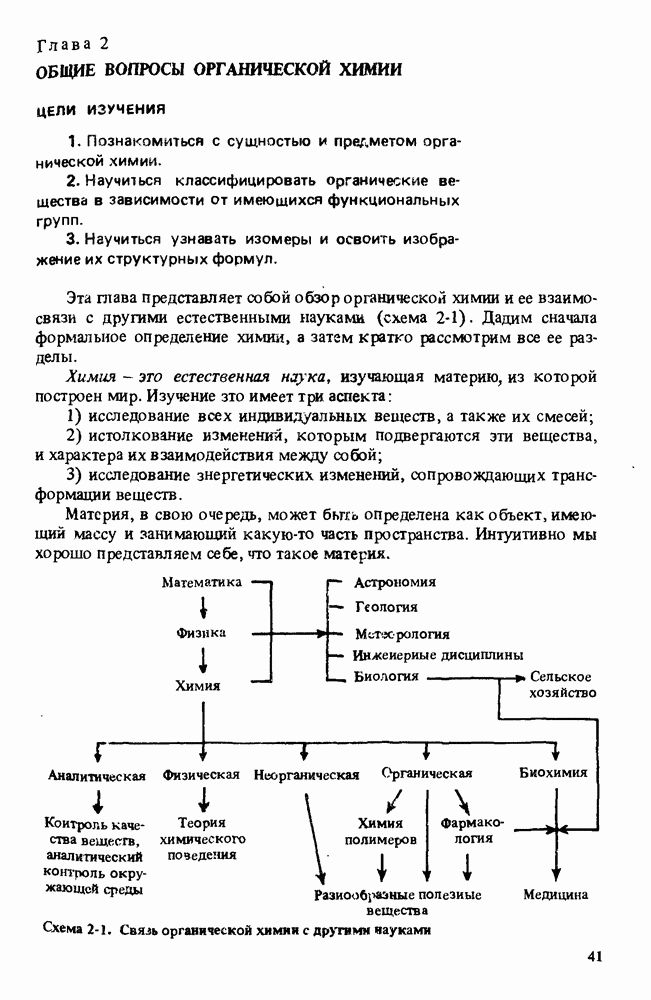
- Глава 2. ОБЩИЕ ВОПРОСЫ ОРГАНИЧЕСКОЙ ХИМИИ
- РАЗДЕЛЫ ХИМИИ
- СИНТЕТИЧЕСКАЯ ОРГАНИЧЕСКАЯ ХИМИЯ
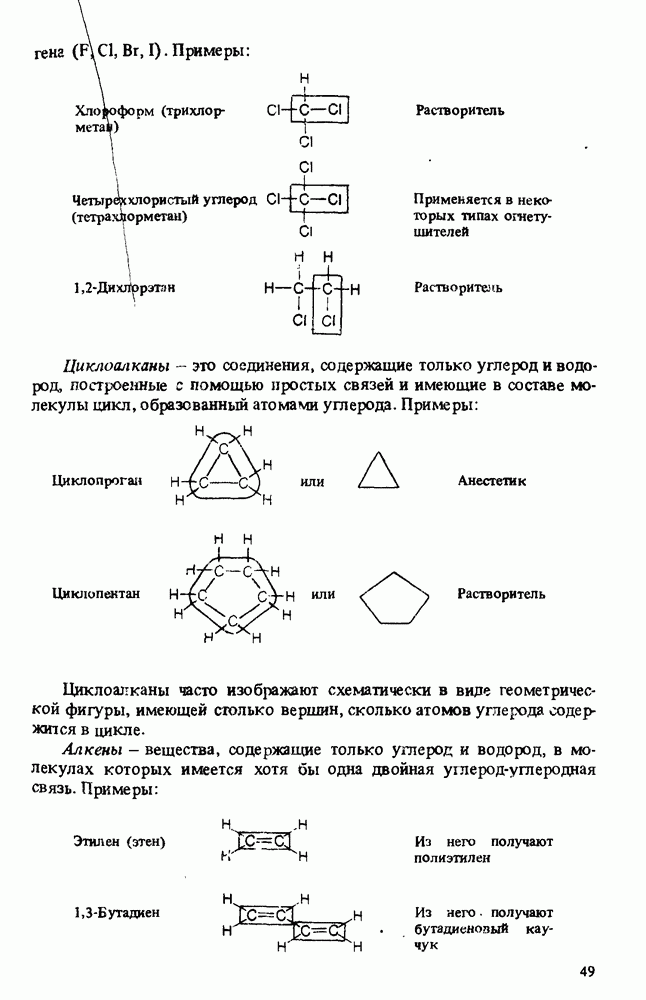
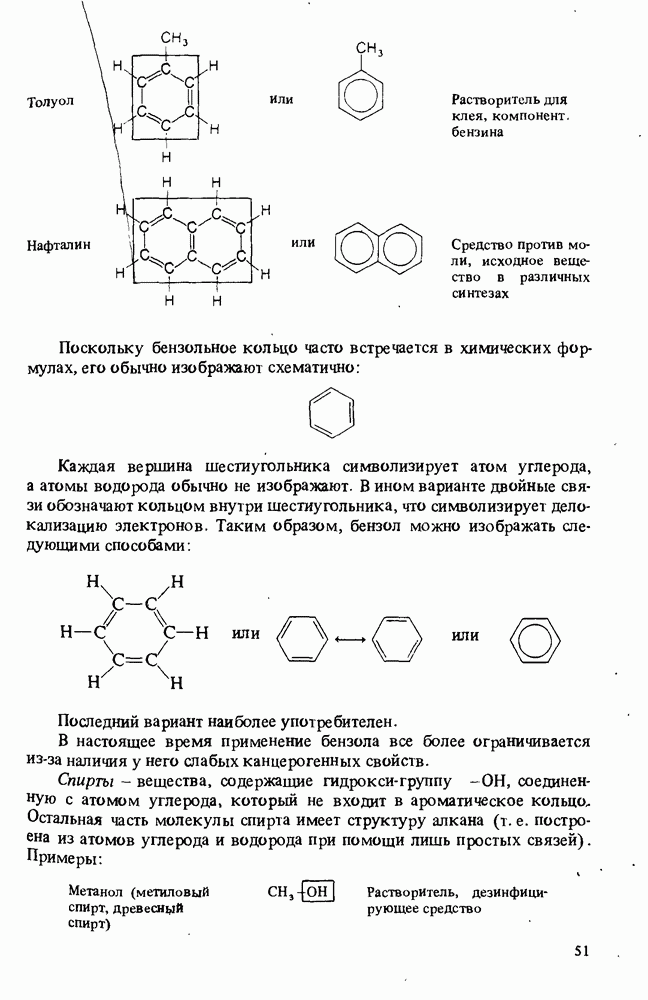
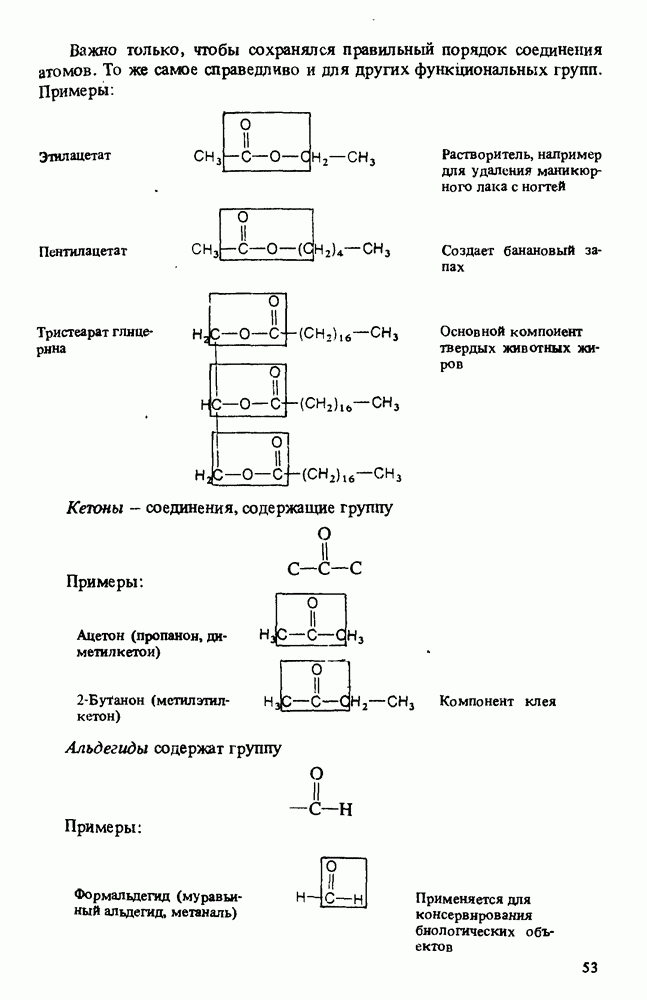
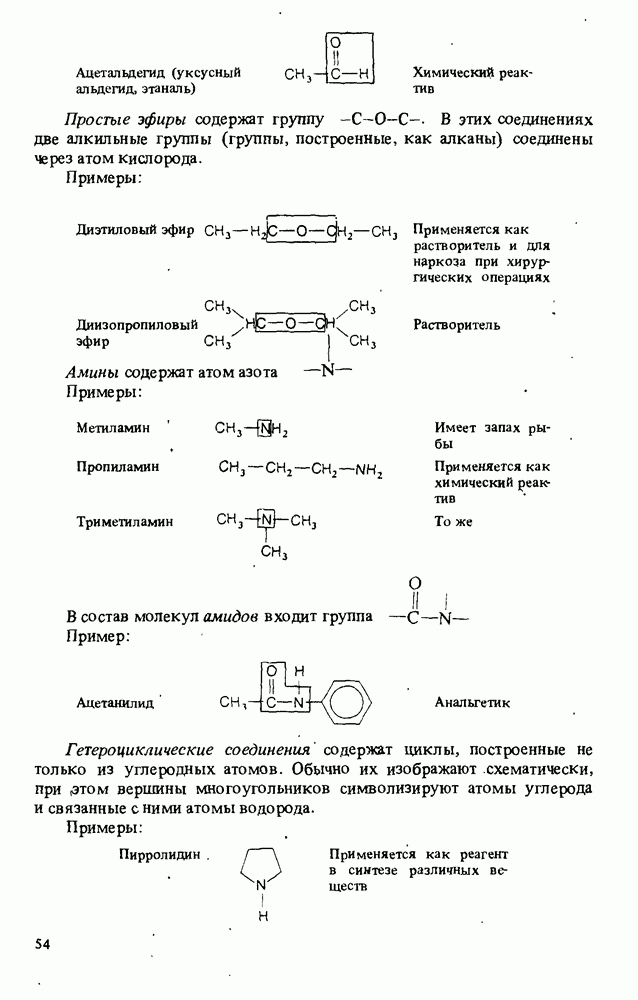
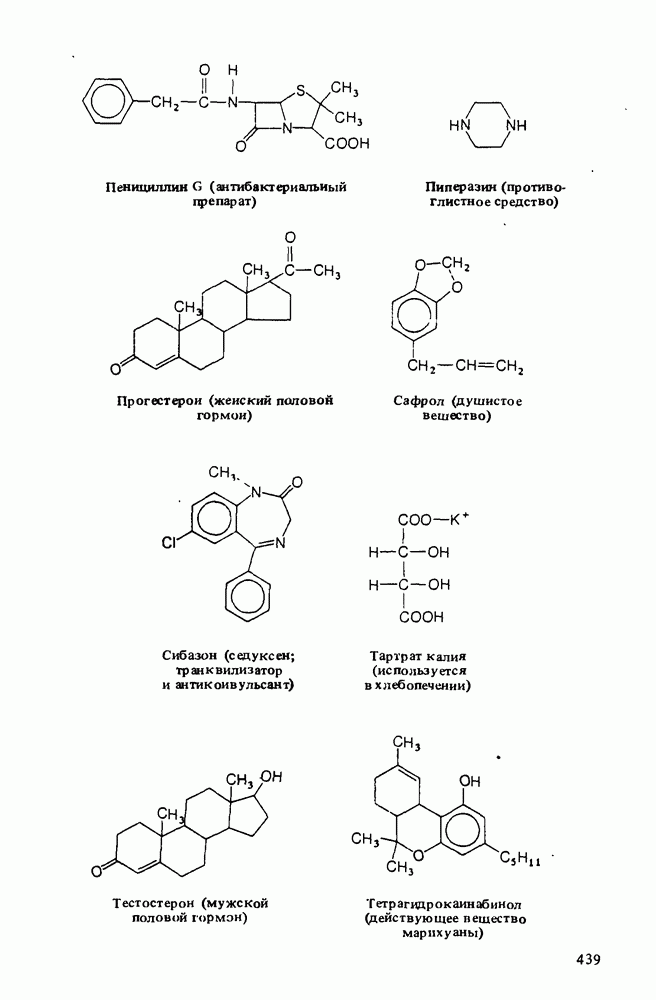
- ПОЛЕЗНЫЕ ОРГАНИЧЕСКИЕ ВЕЩЕСТВА
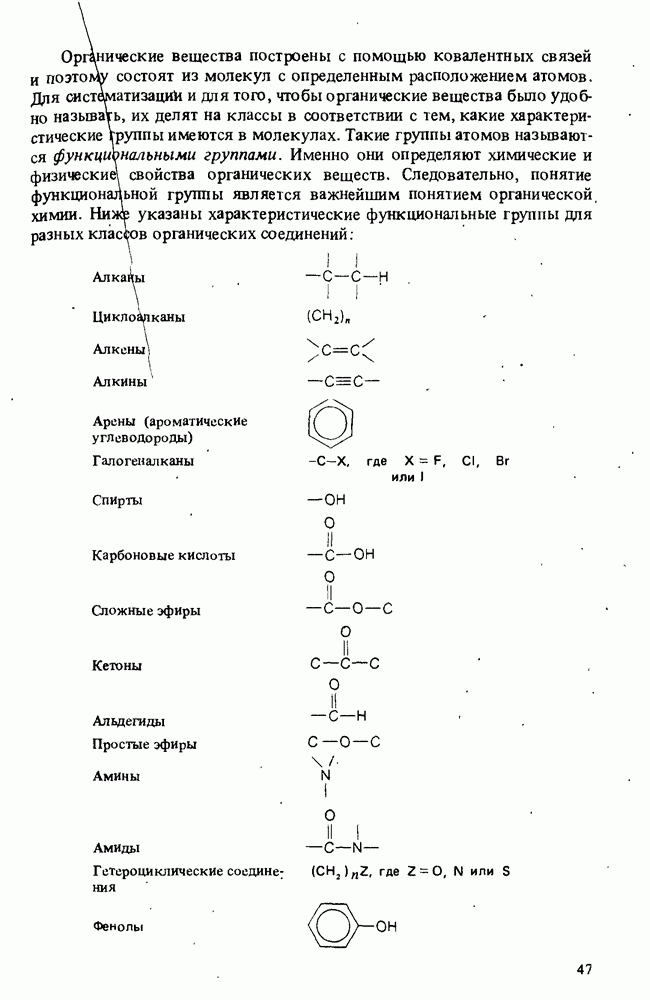
- КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ. ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
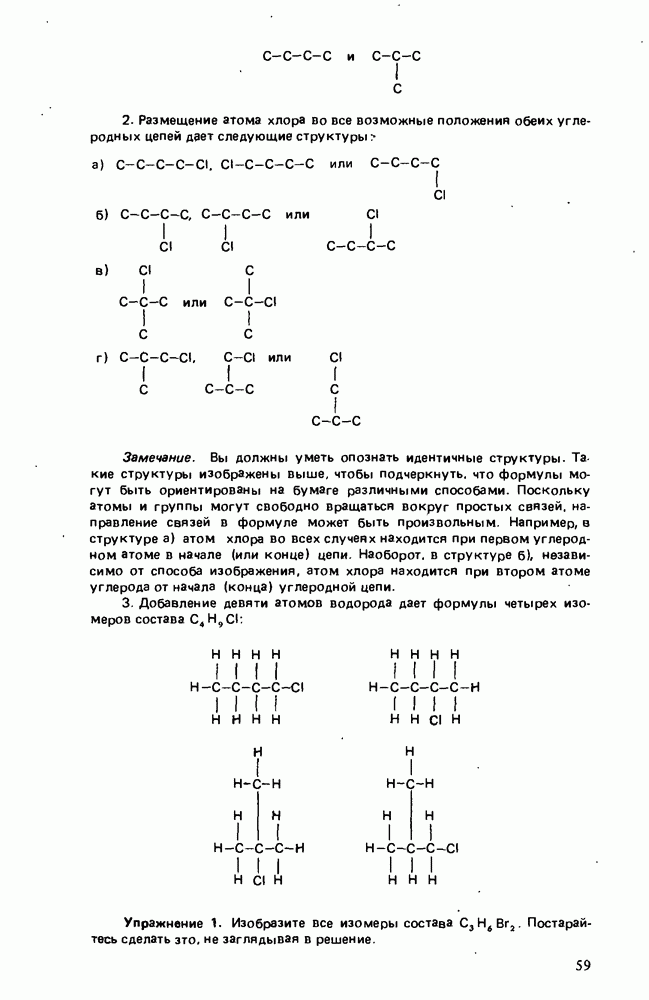
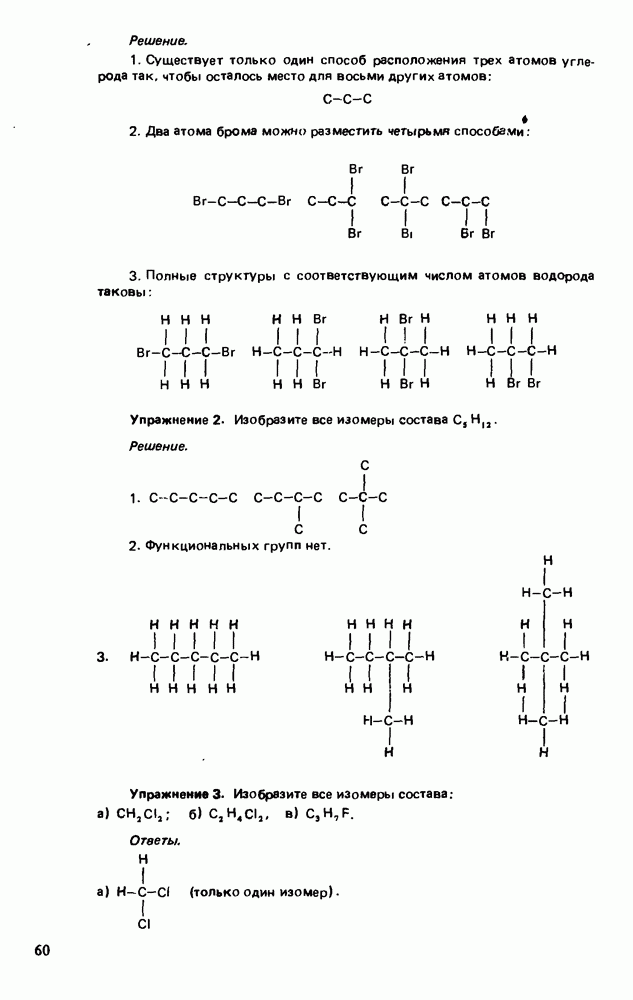
- ИЗОМЕРИЯ
- СВОДКА ОСНОВНЫХ ПОЛОЖЕНИЙ ГЛ. 2
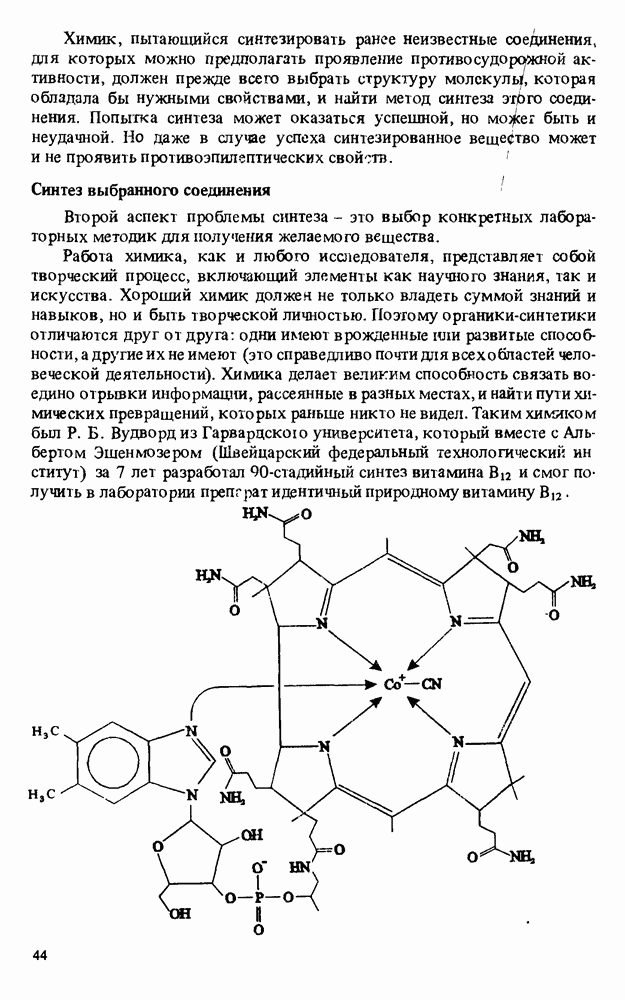
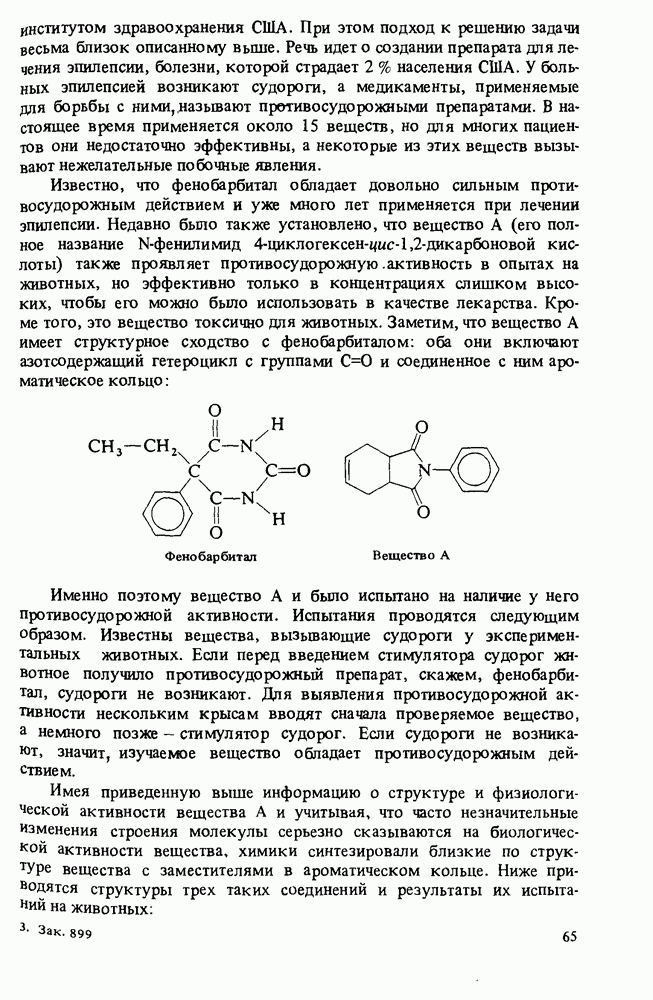
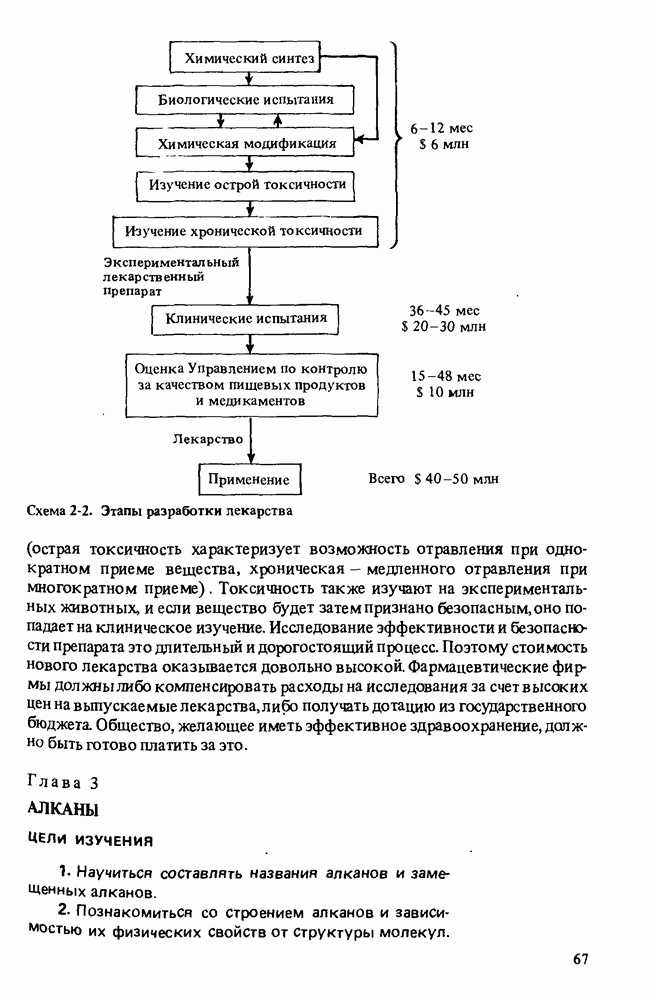
- Прикладная органическая химия: ХИМИЧЕСКИЙ СИНТЕЗ И МЕДИЦИНСКИЕ ИССЛЕДОВАНИЯ
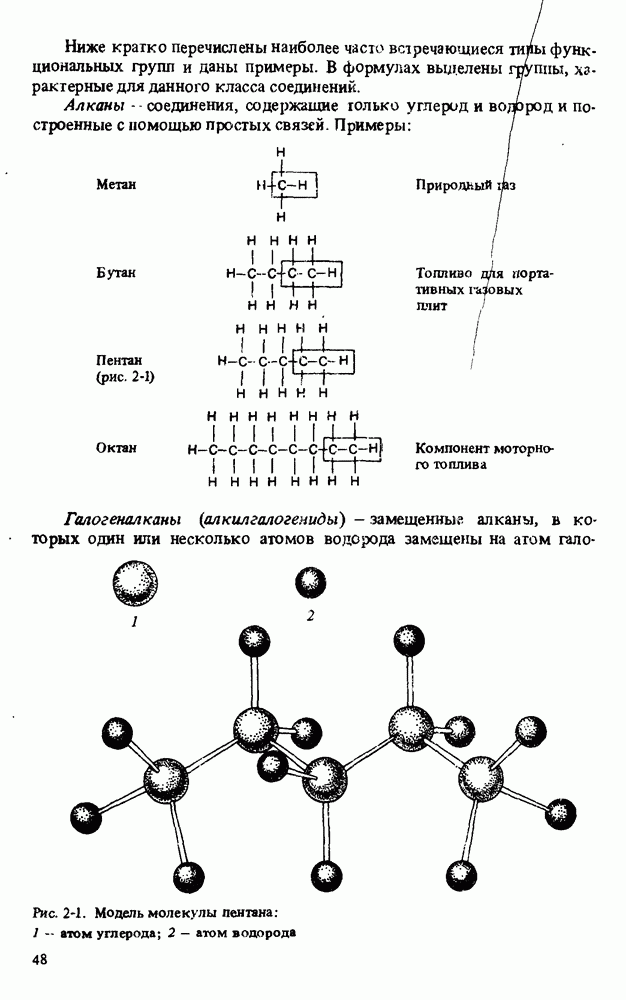
- Глава 3. АЛКАНЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА АЛКАНОВ
- СТРОЕНИЕ АЛКАНОВ
- ПОЛУЧЕНИЕ АЛКАНОВ
- РЕАКЦИИ АЛКАНОВ
- ХИМИЯ НЕФТИ
- СОВЕТЫ ИЗУЧАЮЩЕМУ ОРГАНИЧЕСКУЮ ХИМИЮ. ИЗУЧЕНИЕ РЕАКЦИЙ
- Глава 4. СТЕРЕОХИМИЯ И ОПТИЧЕСКАЯ АКТИВНОСТЬ
- СПОСОБЫ ИЗОБРАЖЕНИЯ ЭНАНТИОМЕРОВ
- ОБОЗНАЧЕНИЕ АБСОЛЮТНОЙ КОНФИГУРАЦИИ
- НАЗВАНИЯ ХИРАЛЬНЫХ МОЛЕКУЛ
- ИЗОБРАЖЕНИЕ МОЛЕКУЛ С ПРОТИВОПОЛОЖНОЙ КОНФИГУРАЦИЕЙ
- D,L-НОМЕНКЛАТУРА ЭНАНТИОМЕРОВ
- ТЕРМИНОЛОГИЯ, ПРИМЕНЯЕМАЯ В СТЕРЕОХИМИИ
- ЗНАЧЕНИЕ ОПТИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ
- Глава 5. ОРГАНИЧЕСКИЕ ГАЛОГЕНСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
- ПОЛУЧЕНИЕ ГАЛОГЕНАЛКАНОВ
- РЕАКЦИИ ГАЛОГЕНАЛКАНОВ
- ПРАКТИЧЕСКИ ВАЖНЫЕ ГАЛОГЕНАЛКАНЫ
- Прикладная органическая химия: ОРГАНИЧЕСКИЕ ПЕСТИЦИДЫ
- Глава 6. НЕНАСЫЩЕННЫЕ УГЛЕВОДОРОДЫ
- НОМЕНКЛАТУРА АЛКЕНОВ
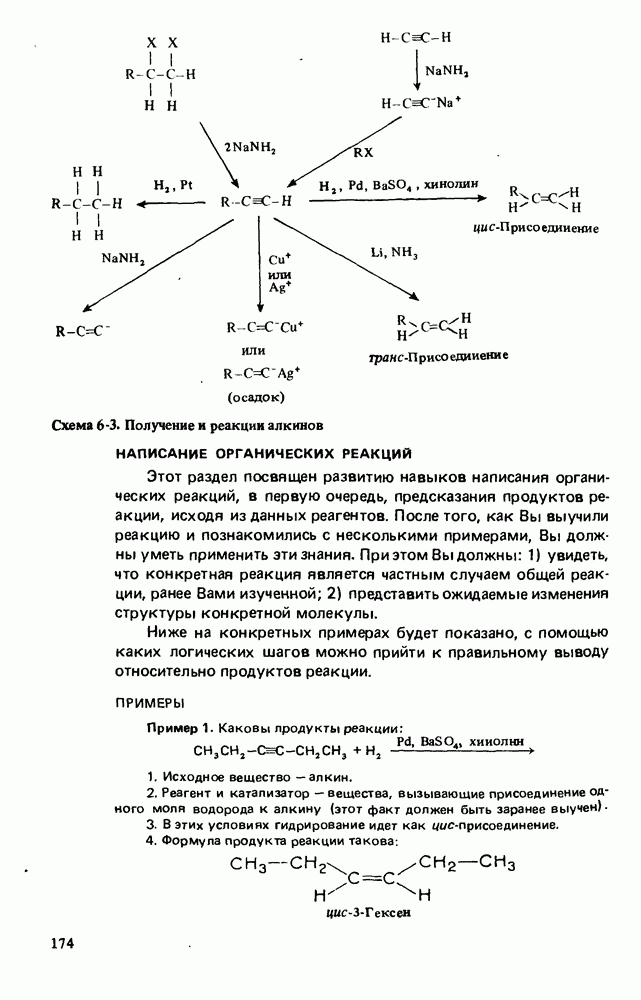
- ПОЛУЧЕНИЕ АЛКЕНОВ
- ОСНОВНЫЕ РЕАКЦИИ АЛКЕНОВ
- ПОЛИМЕРЫ
- НОМЕНКЛАТУРА АЛКИНОВ
- ПОЛУЧЕНИЕ АЛКИНОВ
- РЕАКЦИИ АЛКИНОВ
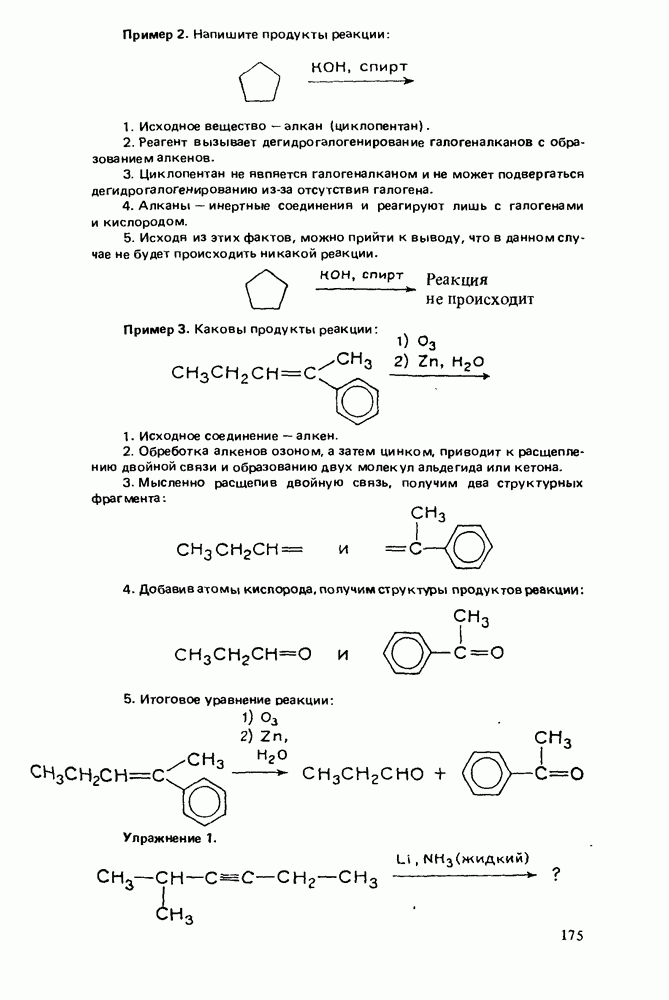
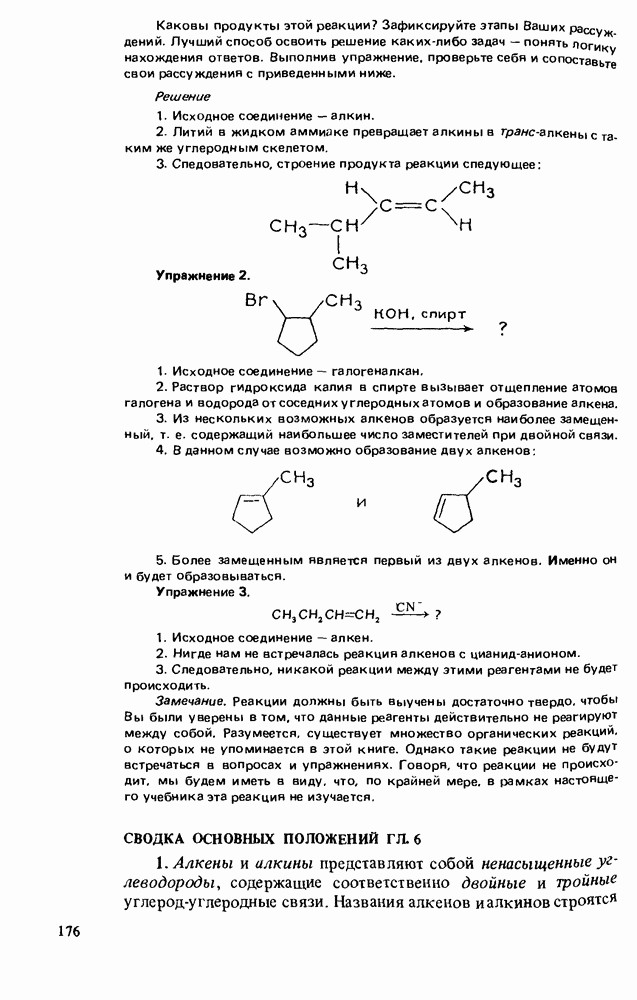
- НАПИСАНИЕ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- Глава 7. СПИРТЫ И ПРОСТЫЕ ЭФИРЫ
- НОМЕНКЛАТУРА СПИРТОВ
- НЕКОТОРЫЕ ВАЖНЫЕ ВЕЩЕСТВА, СОДЕРЖАЩИЕ СПИРТОВУЮ ГРУППУ
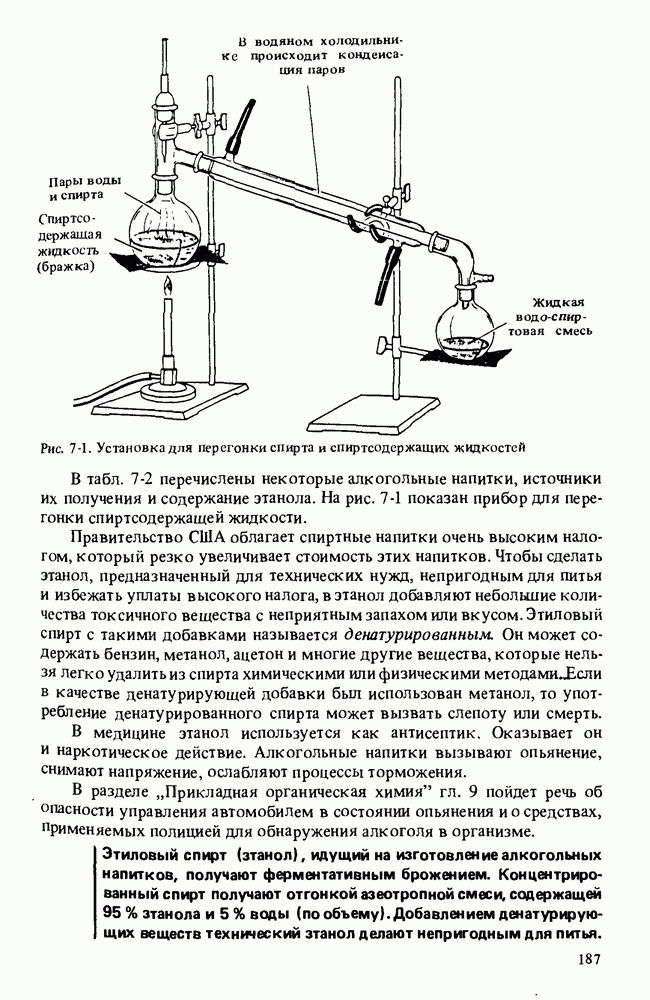
- ЭТИЛОВЫЙ СПИРТ. ПРОИЗВОДСТВО СПИРТНЫХ НАПИТКОВ
- ПОЛУЧЕНИЕ СПИРТОВ
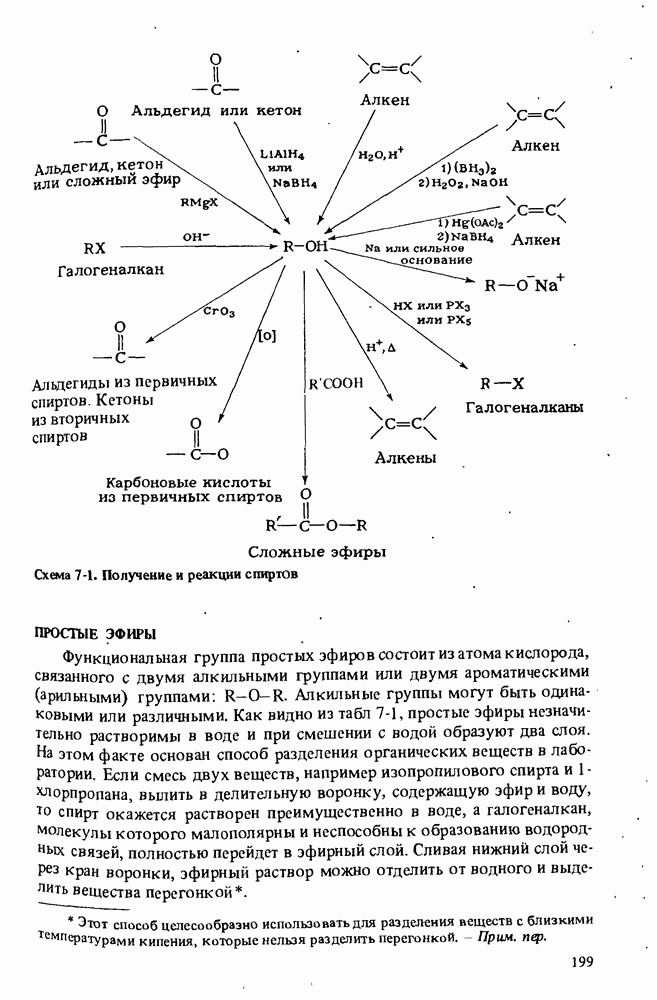
- РЕАКЦИИ СПИРТОВ
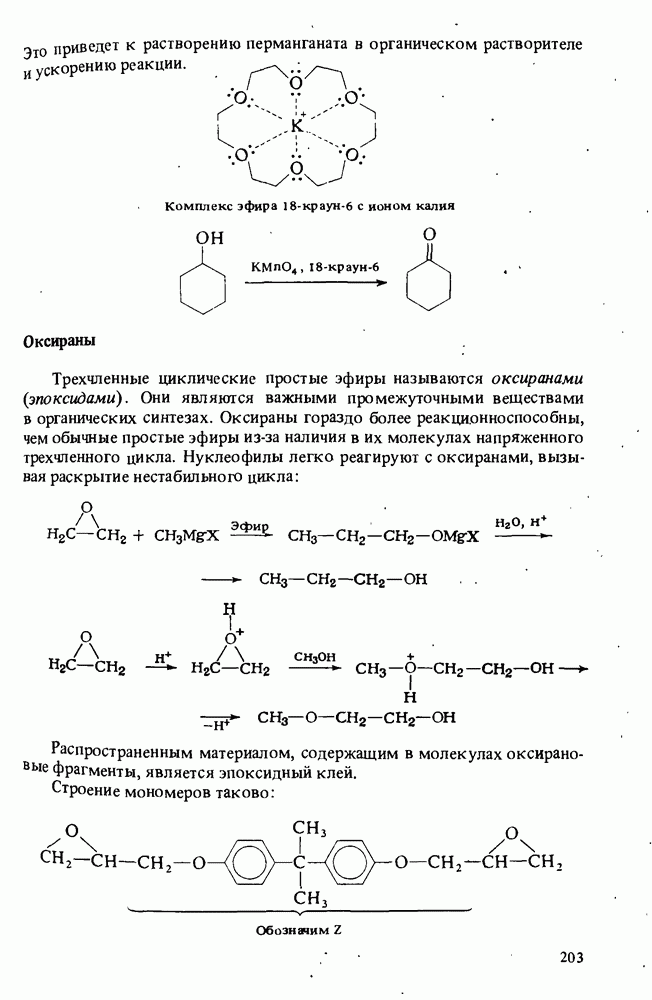
- ПРОСТЫЕ ЭФИРЫ
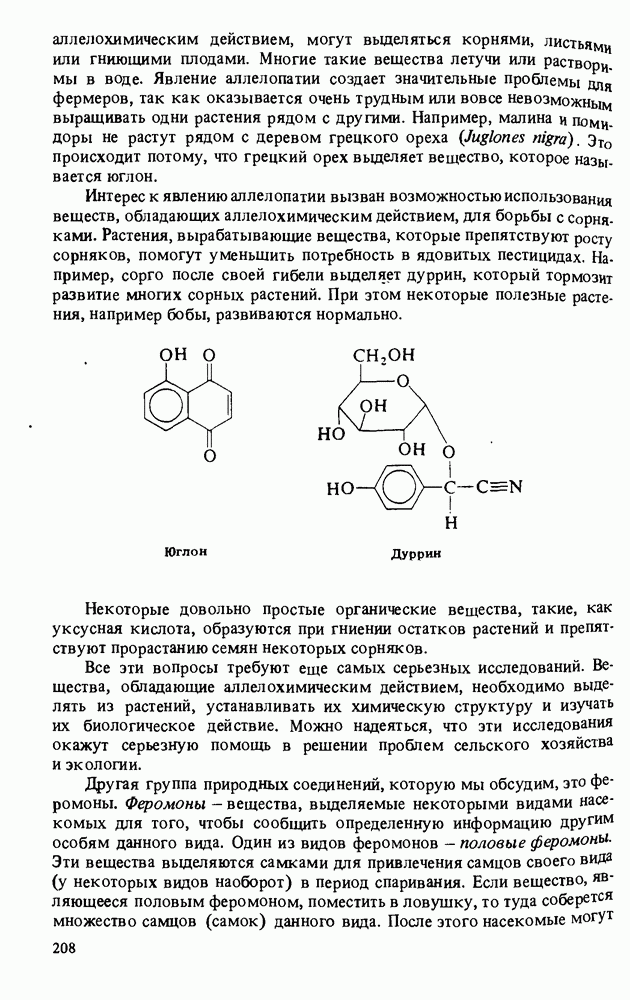
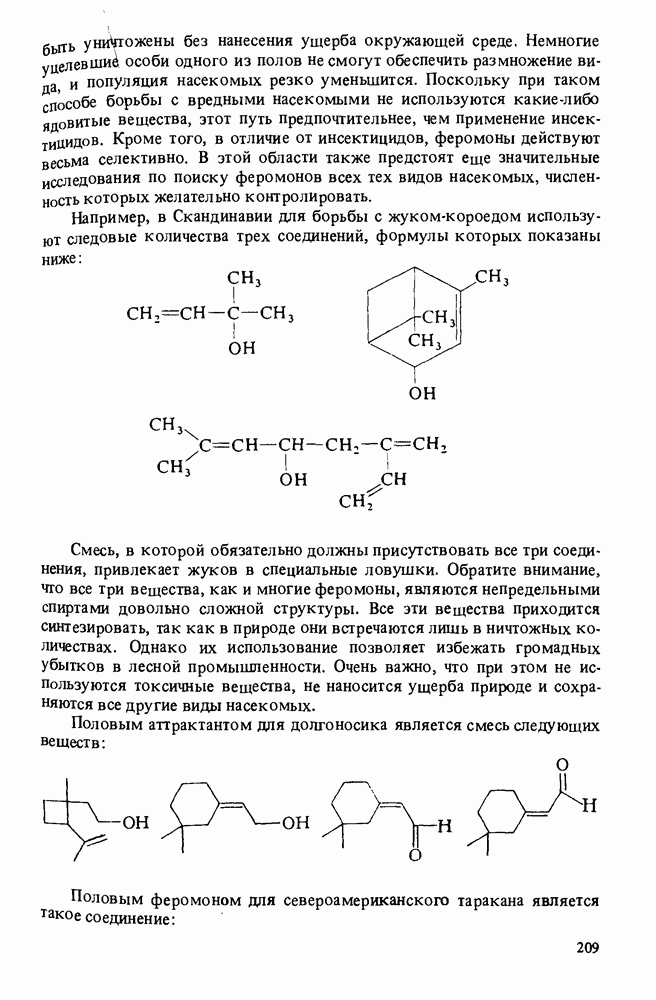
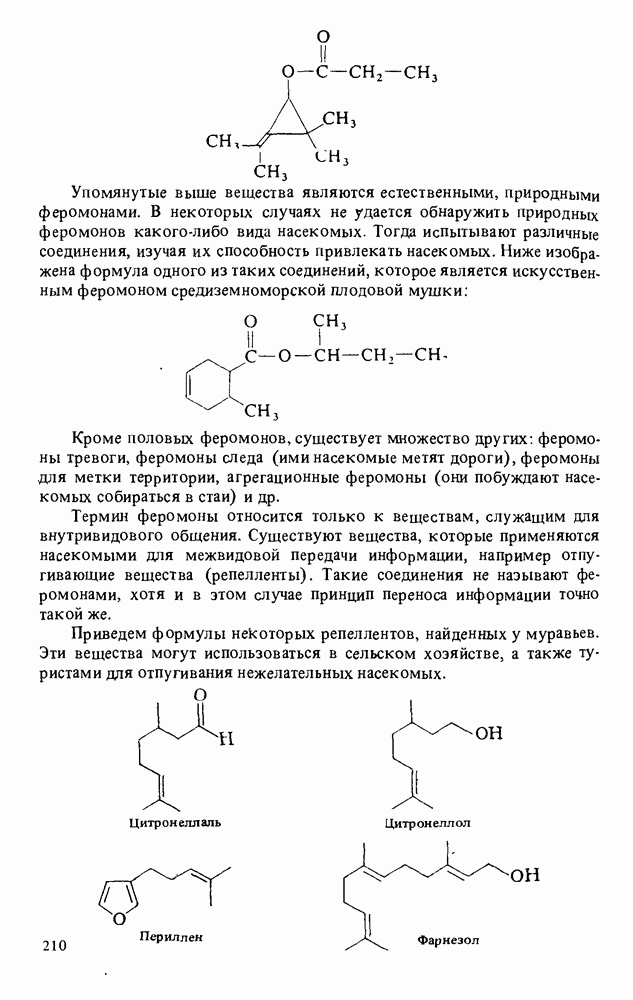
- Прикладная органическая химия: ВЕЩЕСТВА, ОБЛАДАЮЩИЕ АЛЛЕЛОХИМИЧЕСКИМ ДЕЙСТВИЕМ. ФЕРОМОНЫ
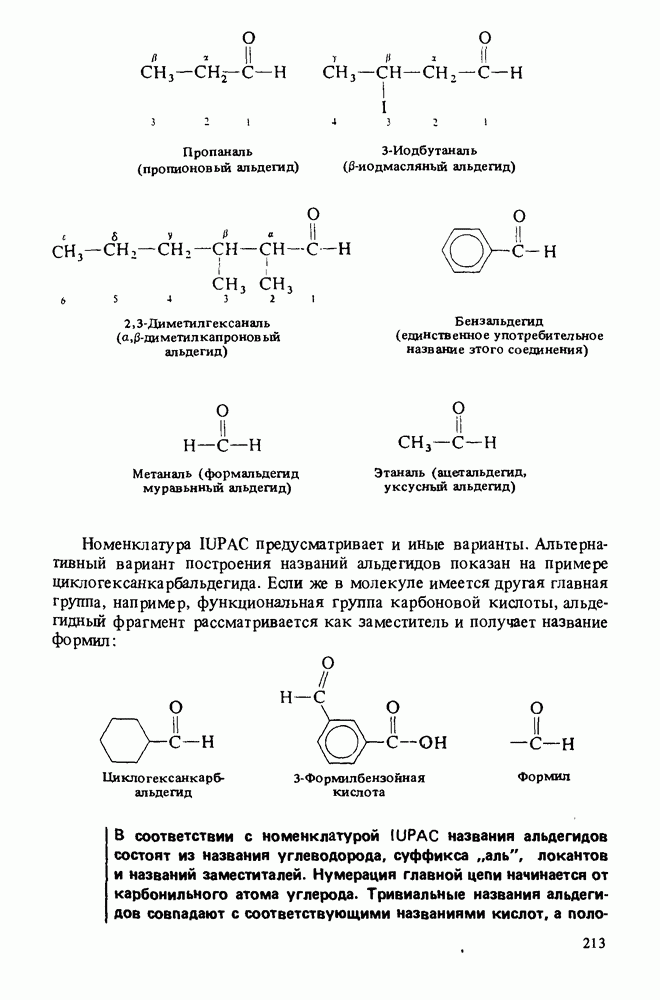
- Глава 8. АЛЬДЕГИДЫ И КЕТОНЫ
- ПОЛУЧЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ
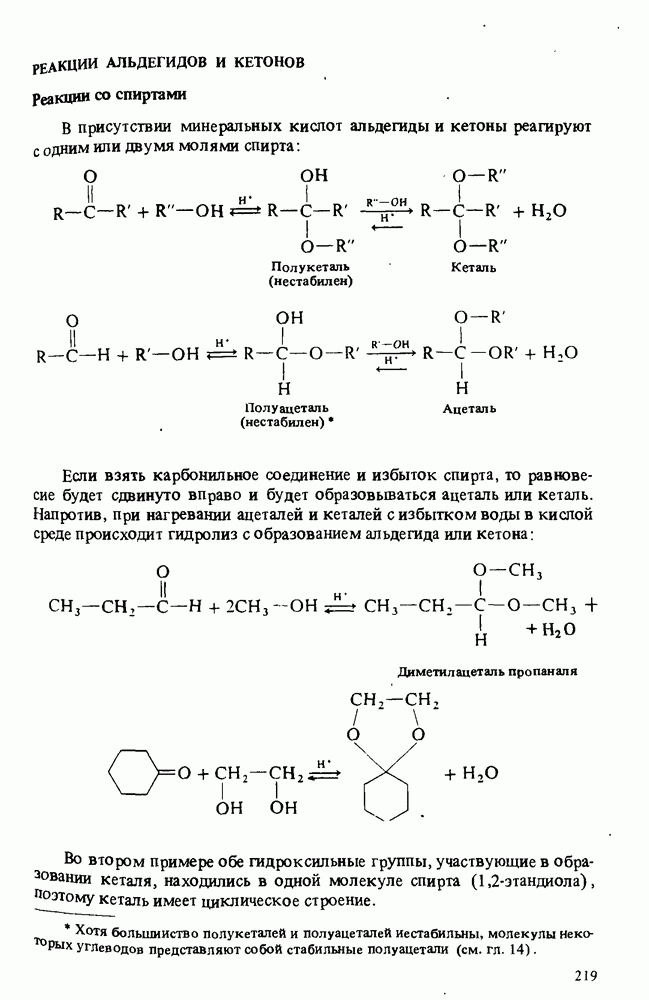
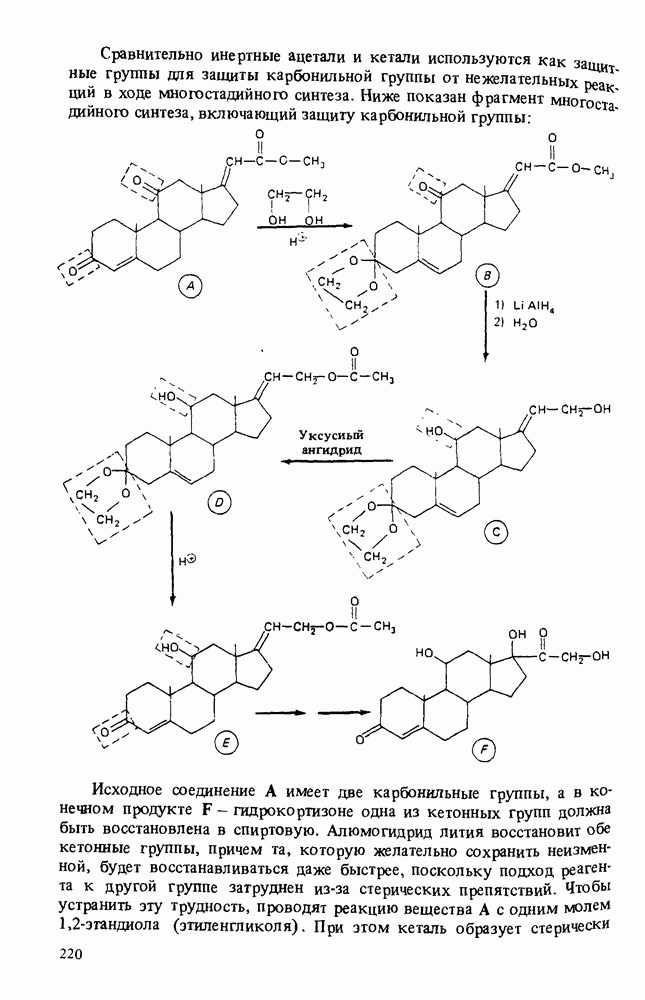
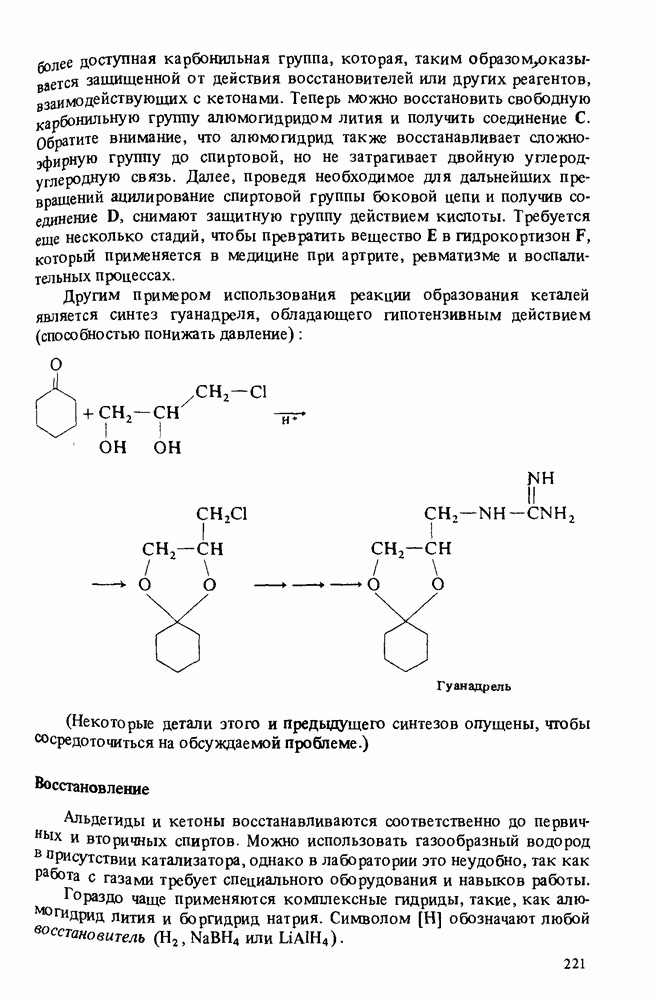
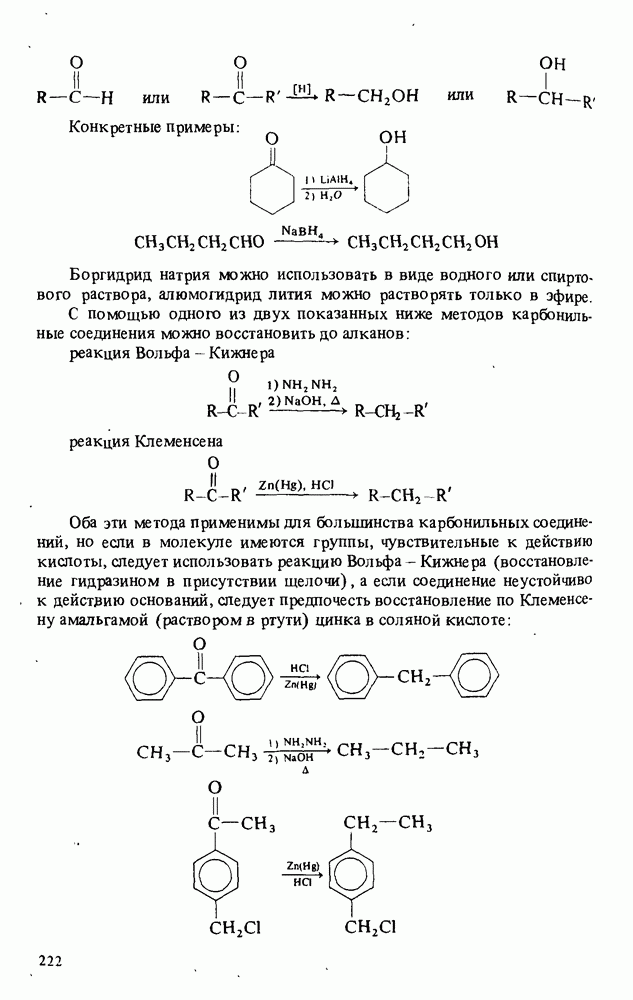
- РЕАКЦИИ АЛЬДЕГИДОВ И КЕТОНОВ
- Глава 9. АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
- НОМЕНКЛАТУРА АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ
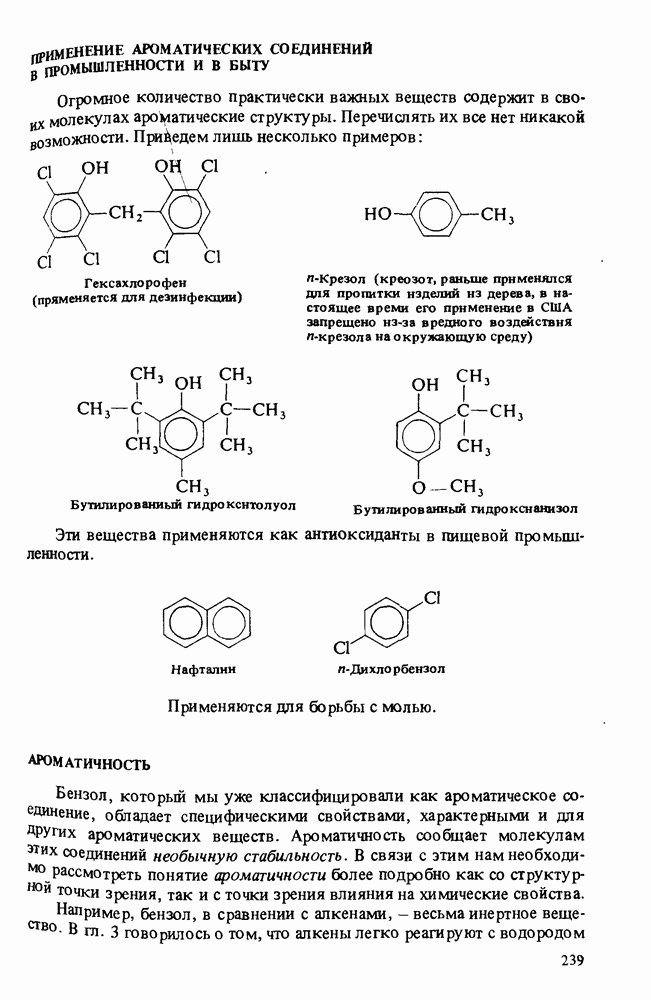
- ПРИМЕНЕНИЕ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ В ПРОМЫШЛЕННОСТИ И В БЫТУ
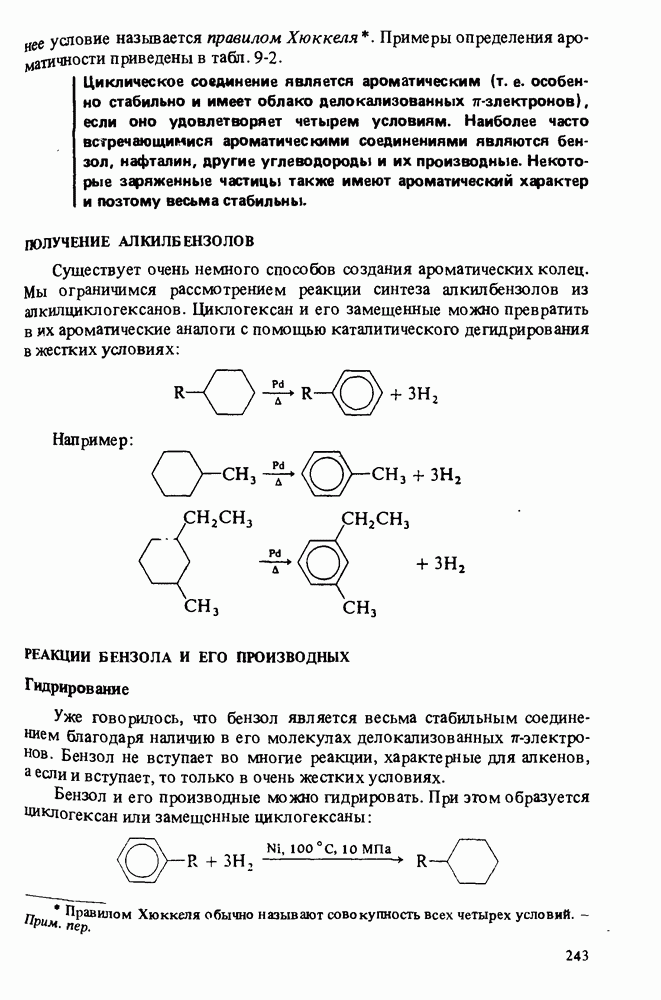
- АРОМАТИЧНОСТЬ
- ПОЛУЧЕНИЕ АЛКИЛЬБЕНЗОЛОВ
- РЕАКЦИИ БЕНЗОЛА И ЕГО ПРОИЗВОДНЫХ
- АРОМАТИЧЕСКОЕ ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ
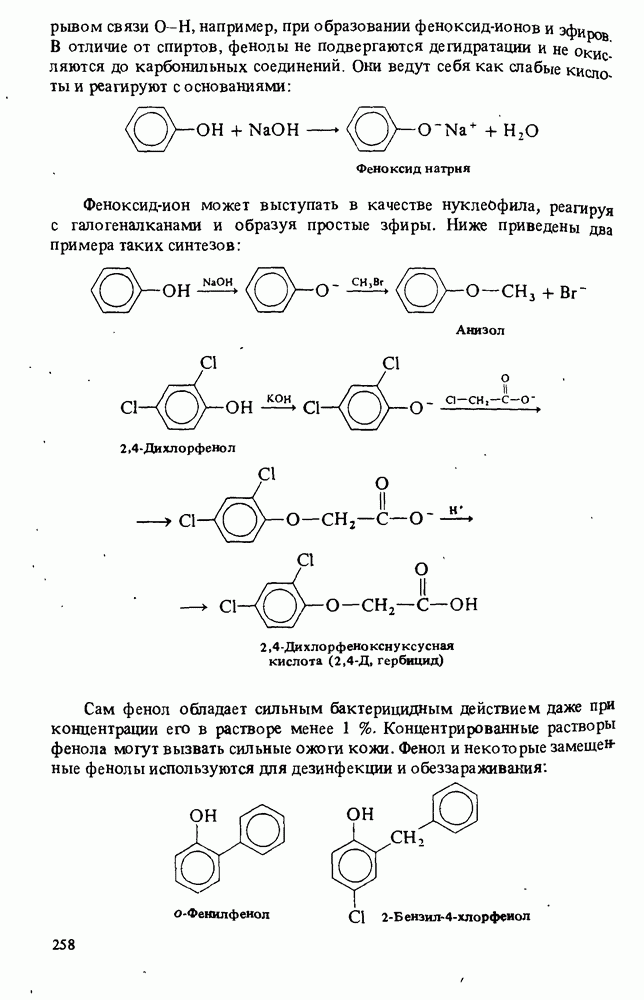
- ФЕНОЛЫ
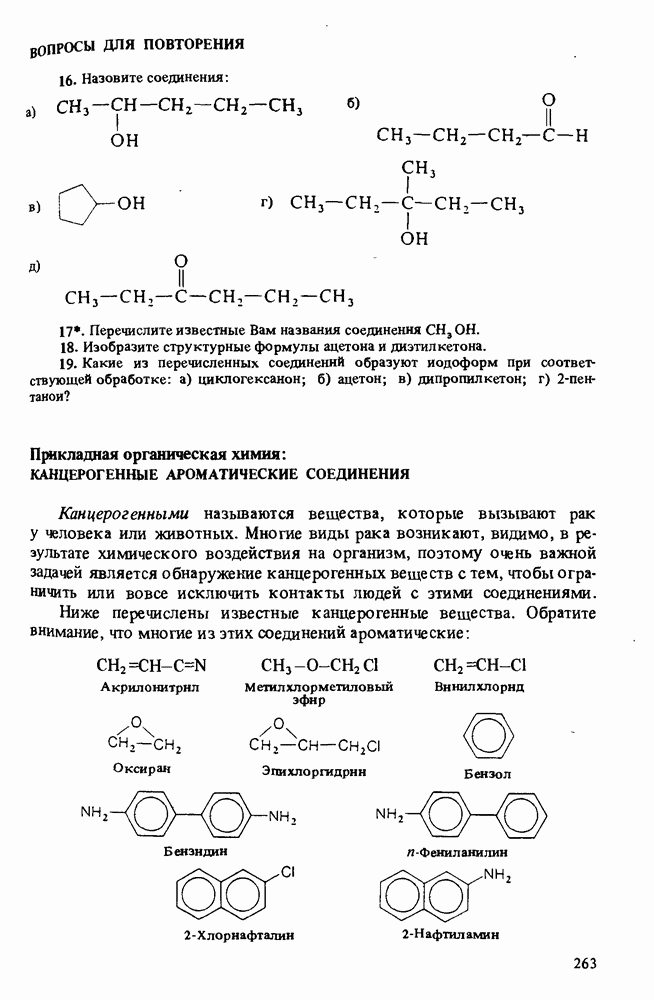
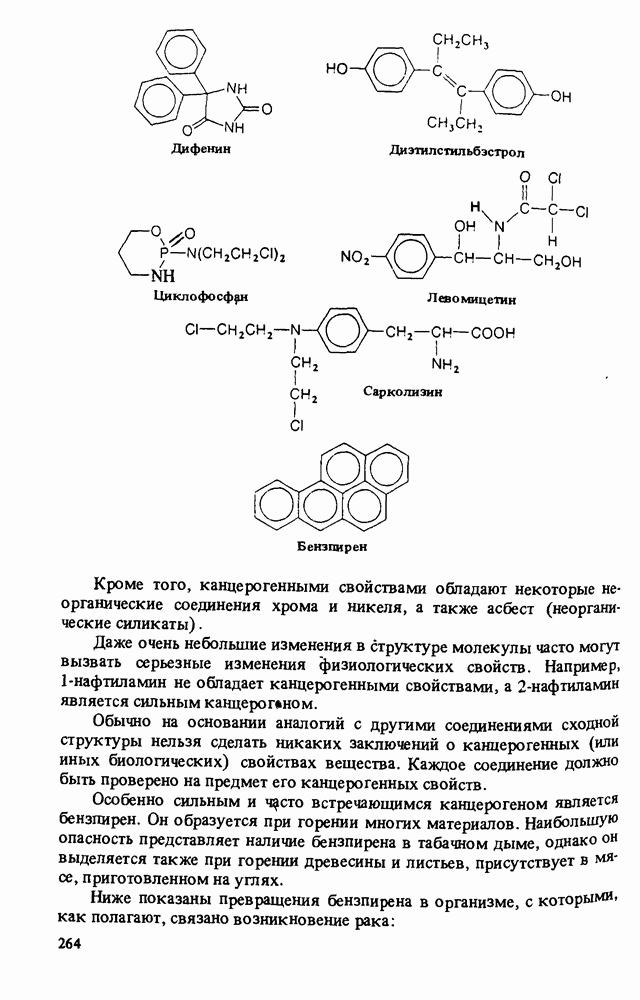
- Прикладная органическая химия: КАНЦЕРОГЕННЫЕ АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
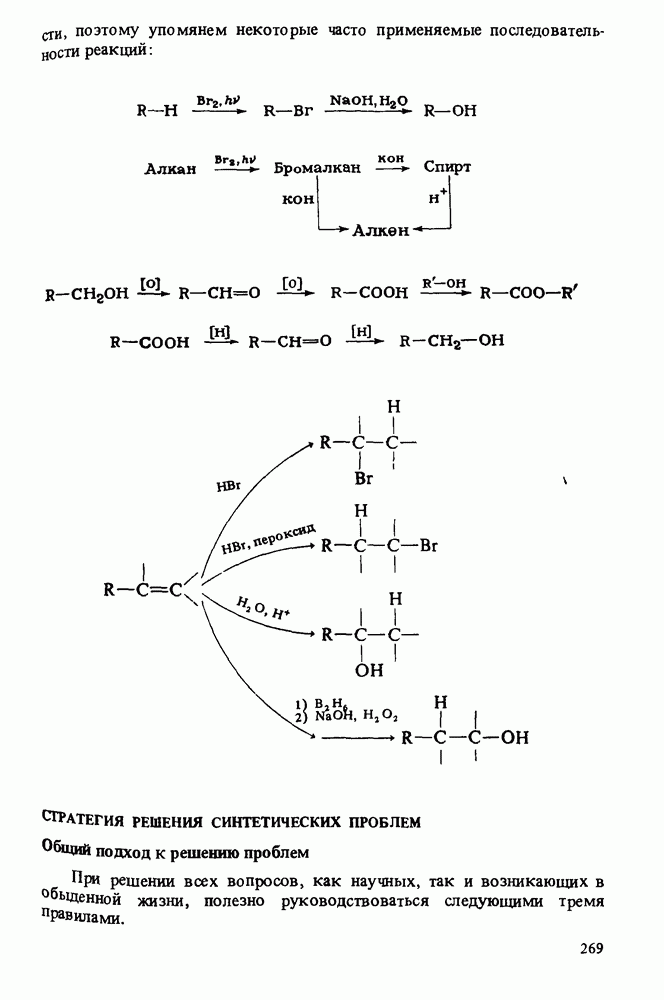
- Глава 10. ОРГАНИЧЕСКИЙ СИНТЕЗ
- СТРАТЕГИЯ РЕШЕНИЯ СИНТЕТИЧЕСКИХ ПРОБЛЕМ
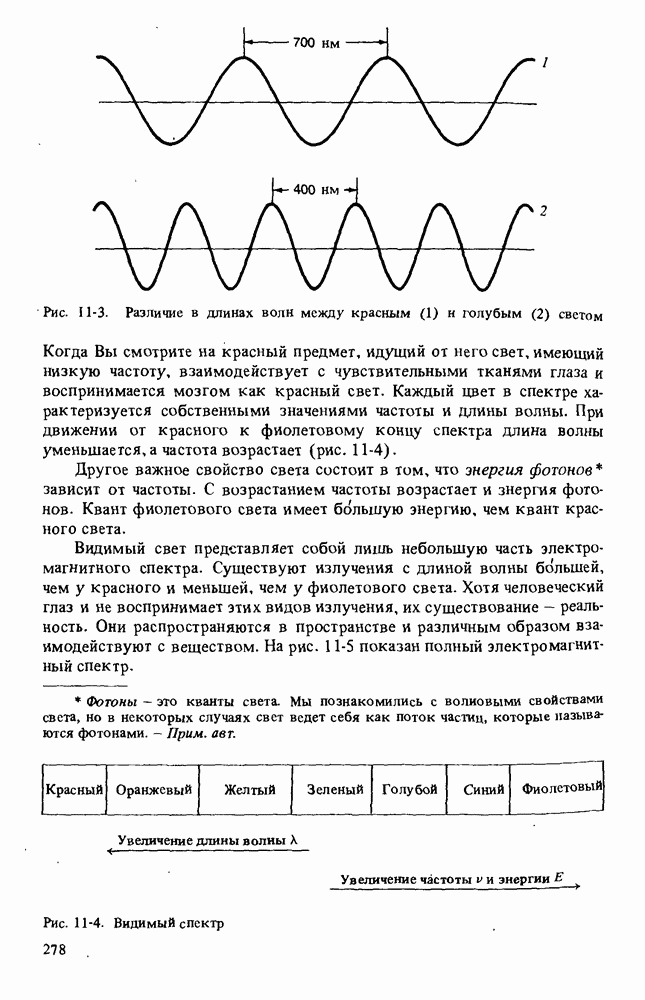
- Глава 11. МОЛЕКУЛЯРНАЯ СПЕКТРОСКОПИЯ
- ИНФРАКРАСНАЯ СПЕКТРОСКОПИЯ
- СПЕКТРОСКОПИЯ ЯДЕРНОГО МАГНИТНОГО РЕЗОНАНСА
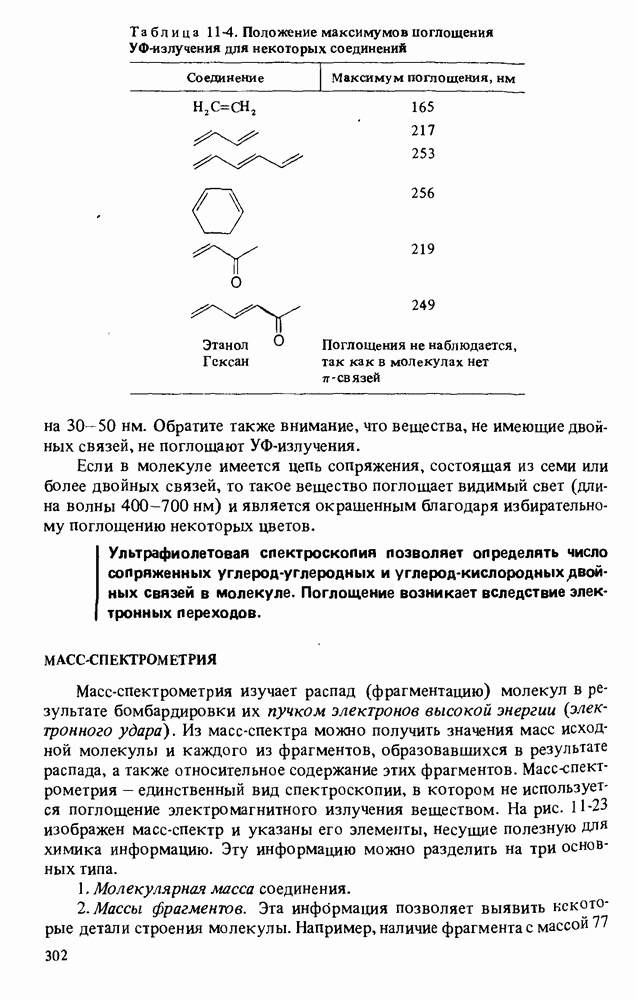
- УЛЬТРАФИОЛЕТОВАЯ СПЕКТРОСКОПИЯ
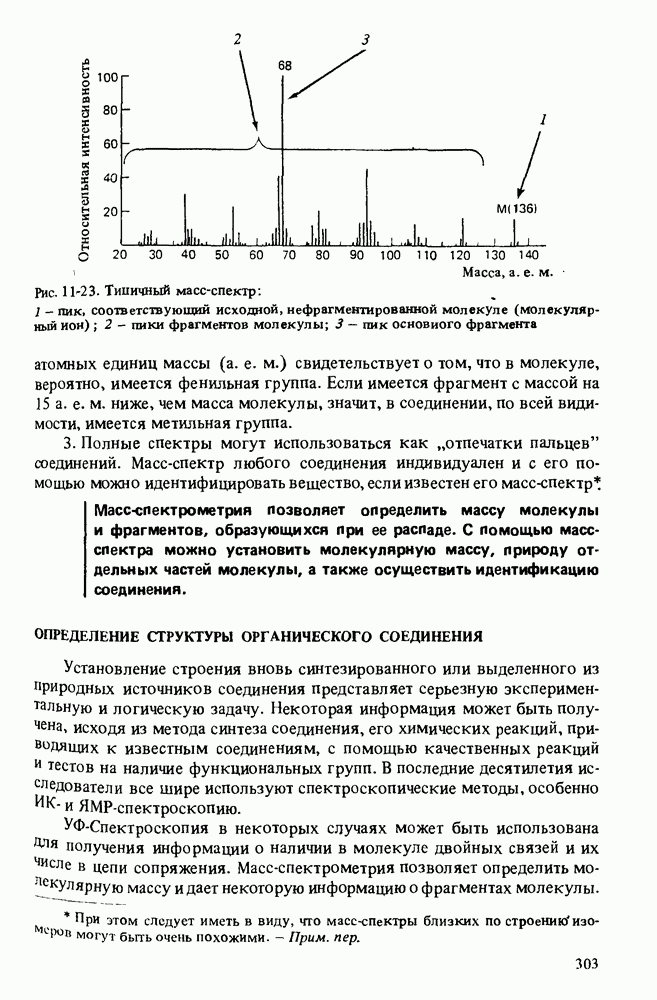
- МАСС-СПЕКТРОМЕТРИЯ
- ОПРЕДЕЛЕНИЕ СТРУКТУРЫ ОРГАНИЧЕСКОГО СОЕДИНЕНИЯ
- Прикладная органическая химия: ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ АЛКОГОЛЯ В КРОВИ
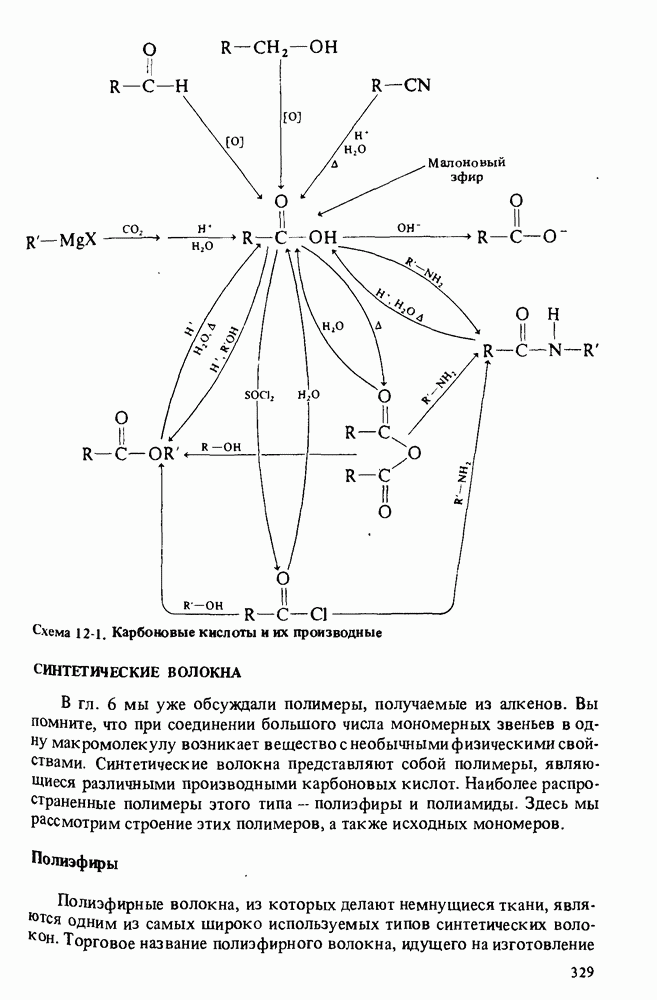
- Глава 12. КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
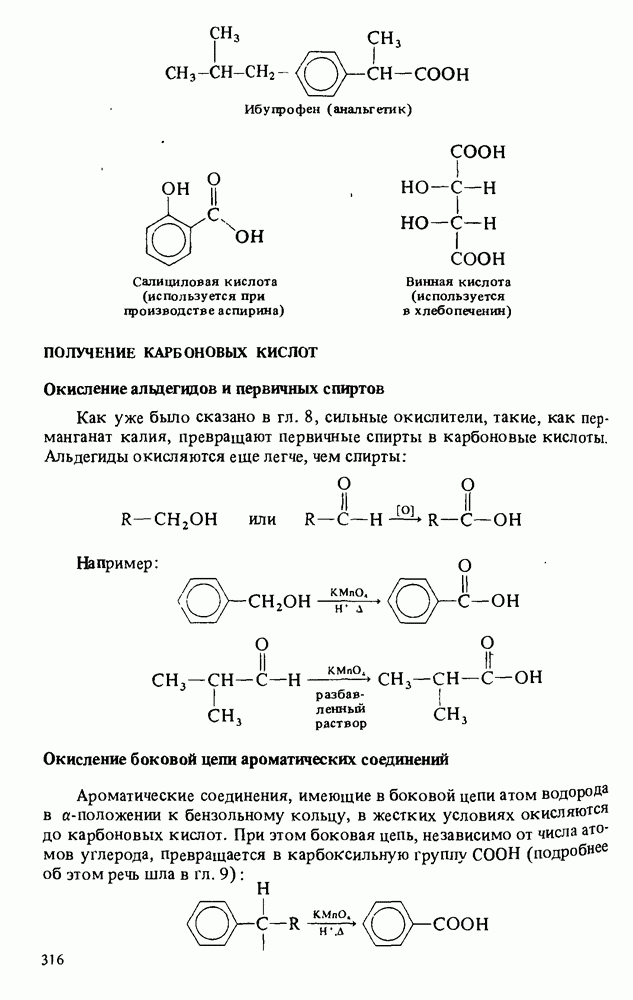
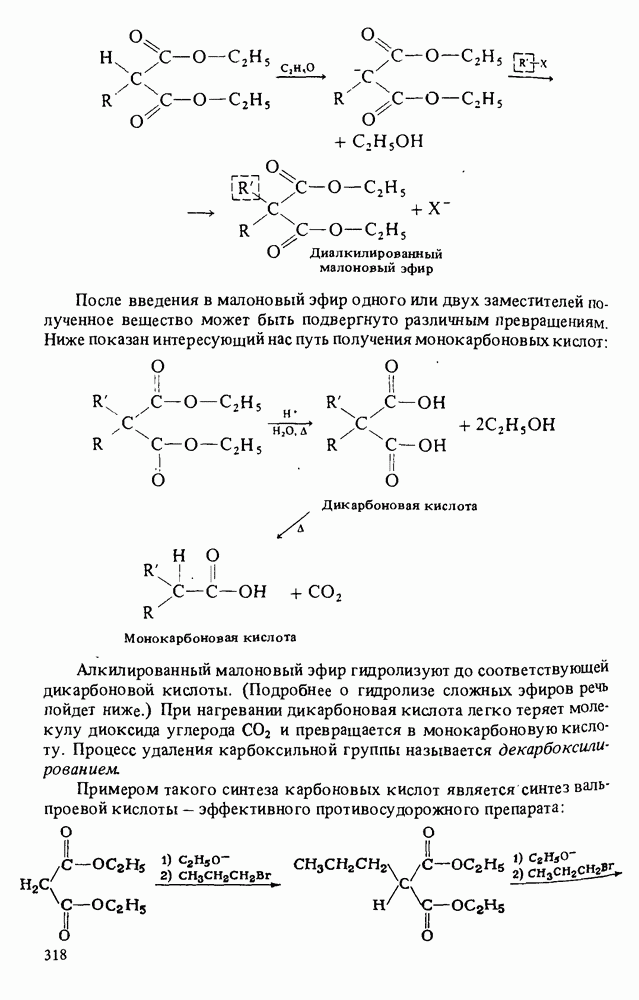
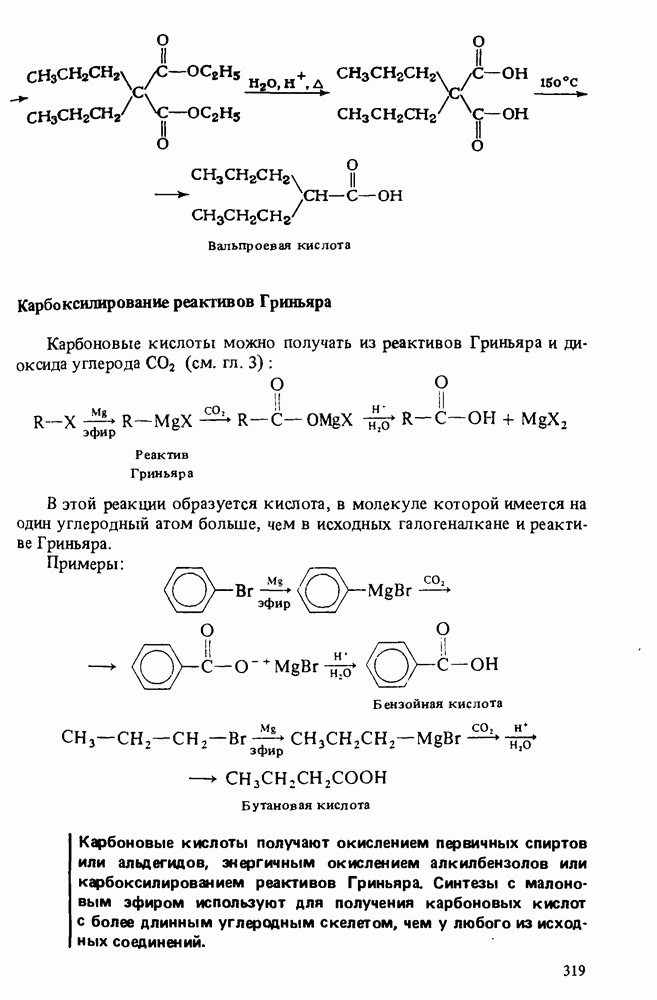
- ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ
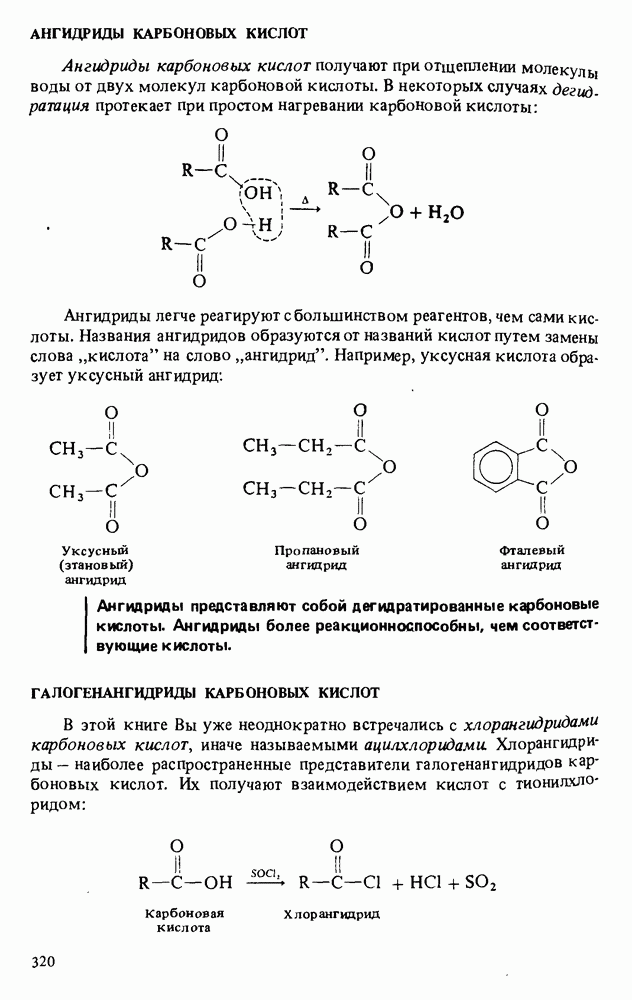
- АНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
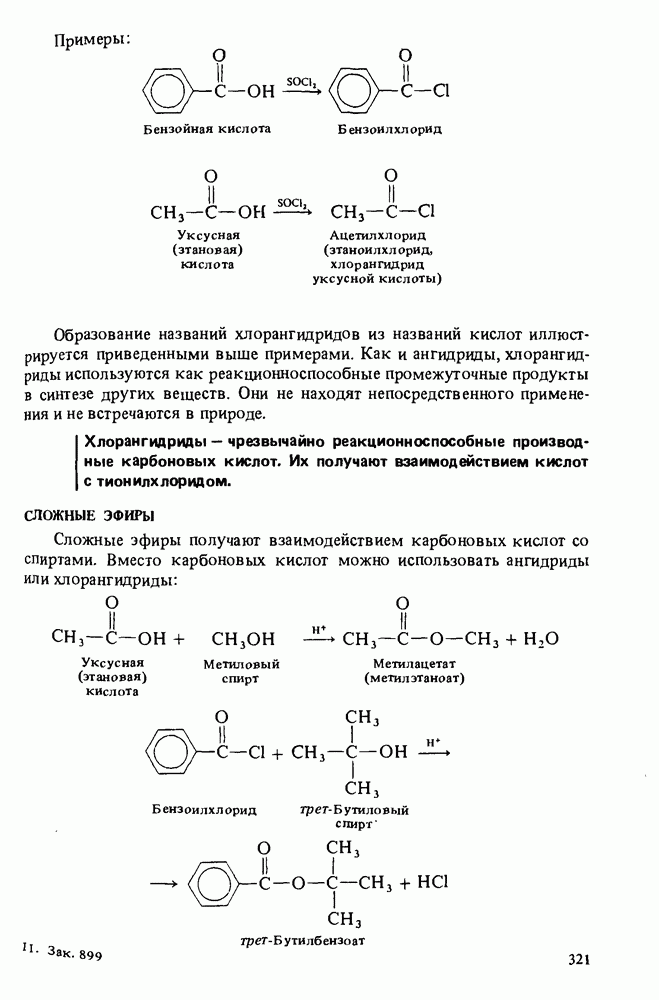
- ГАЛОГЕНАНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
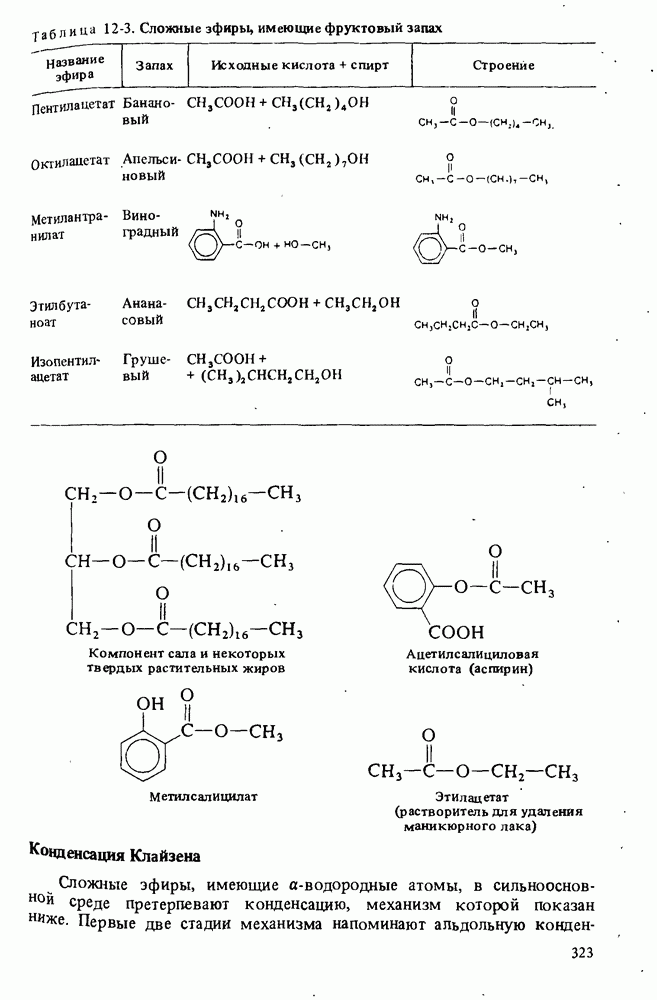
- СЛОЖНЫЕ ЭФИРЫ
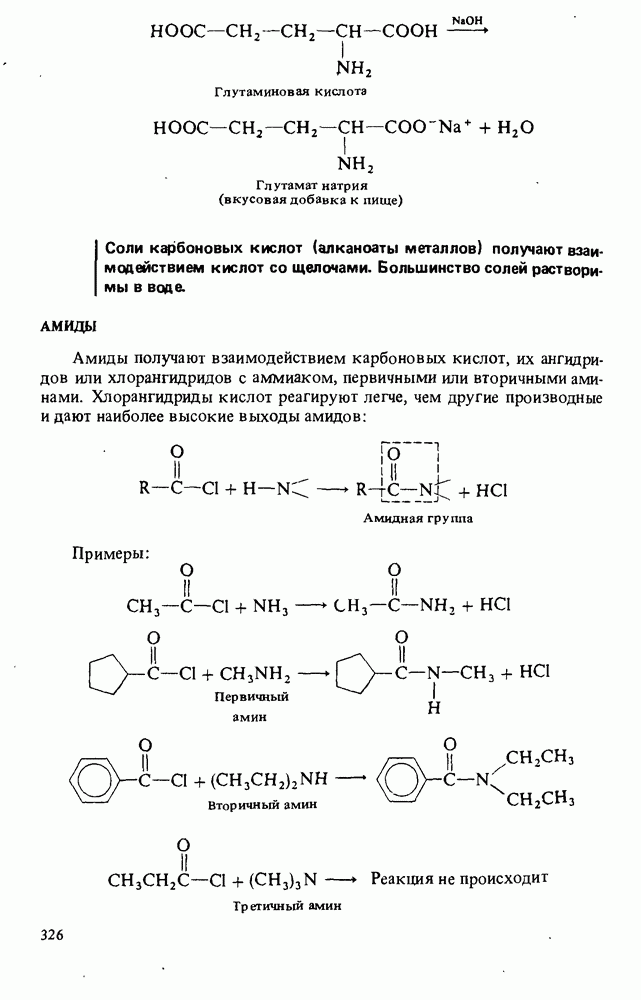
- СОЛИ
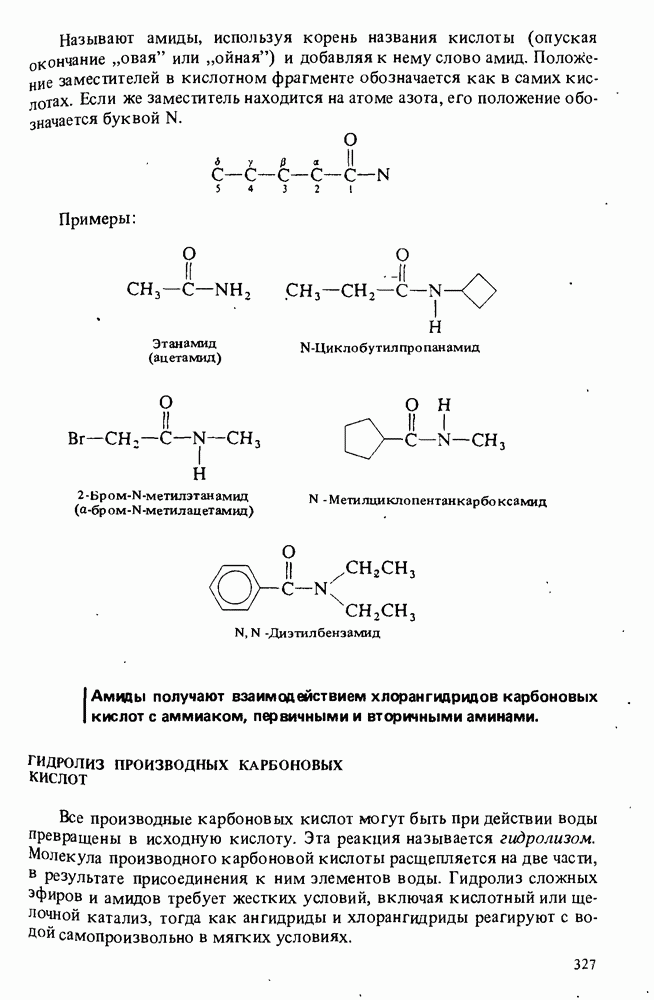
- АМИДЫ
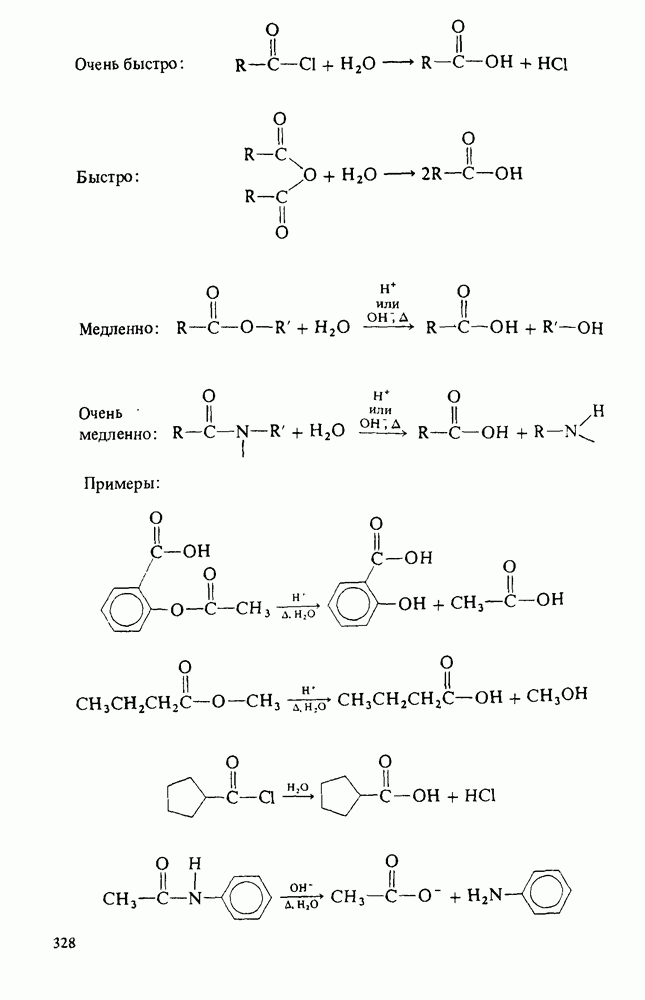
- ГИДРОЛИЗ ПРОИЗВОДНЫХ КАРБОНОВЫХ КИСЛОТ
- СИНТЕТИЧЕСКИЕ ВОЛОКНА
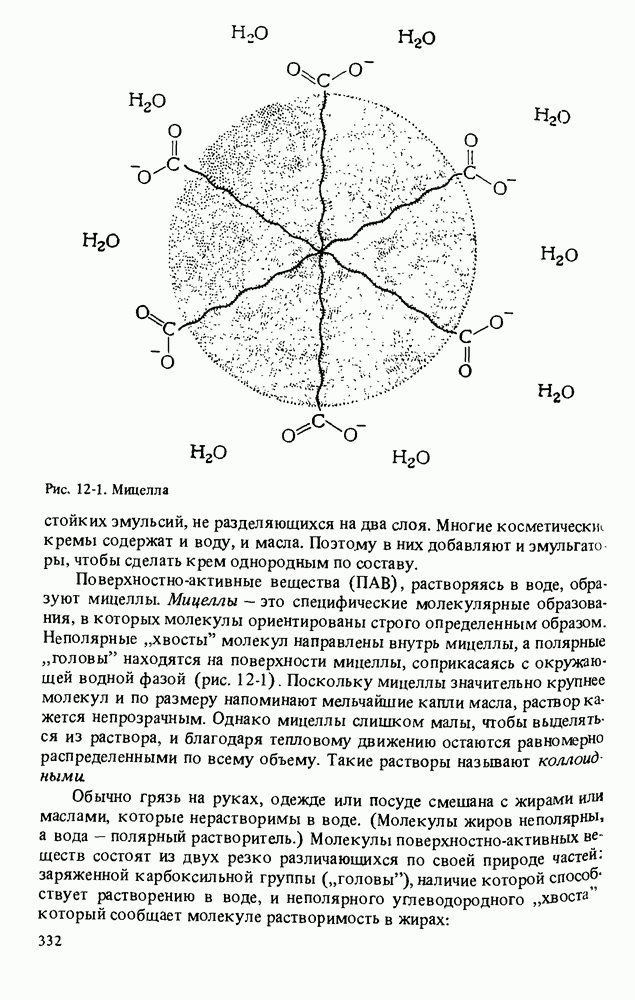
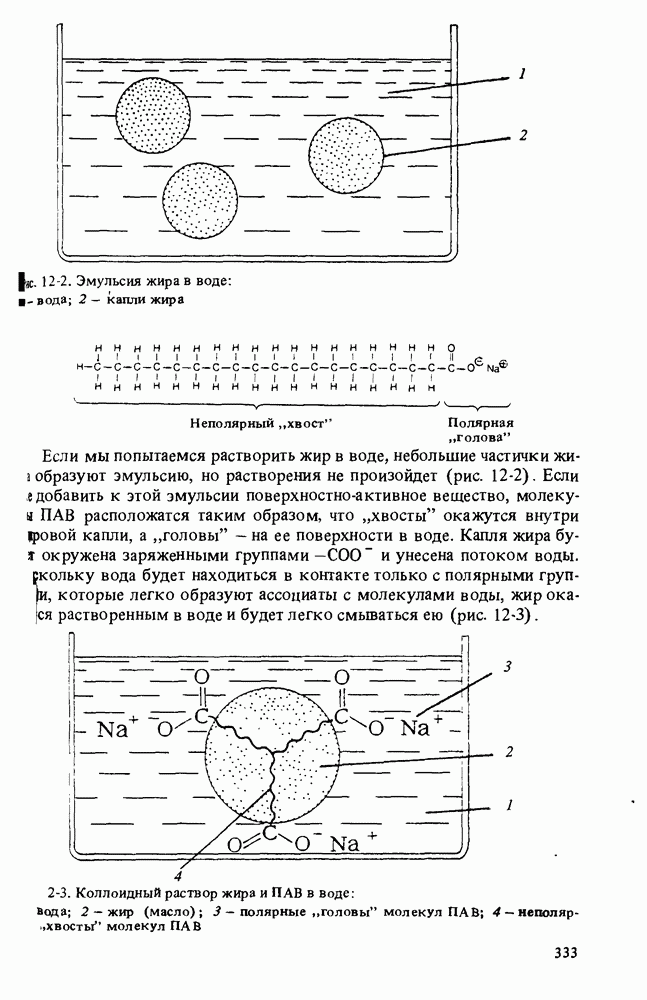
- МОЮЩИЕ СРЕДСТВА
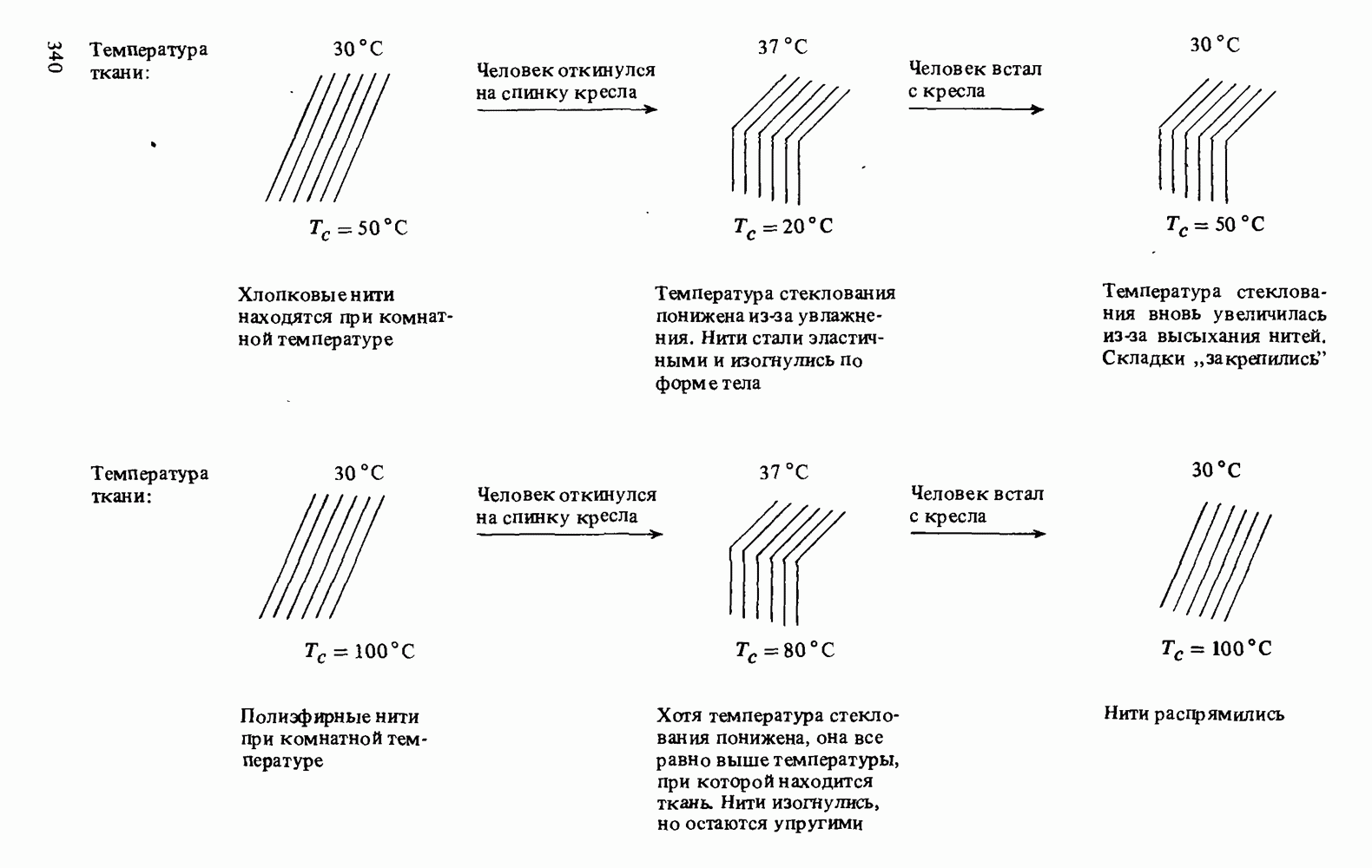
- Прикладная органическая химия: СВОЙСТВА ВОЛОКОН
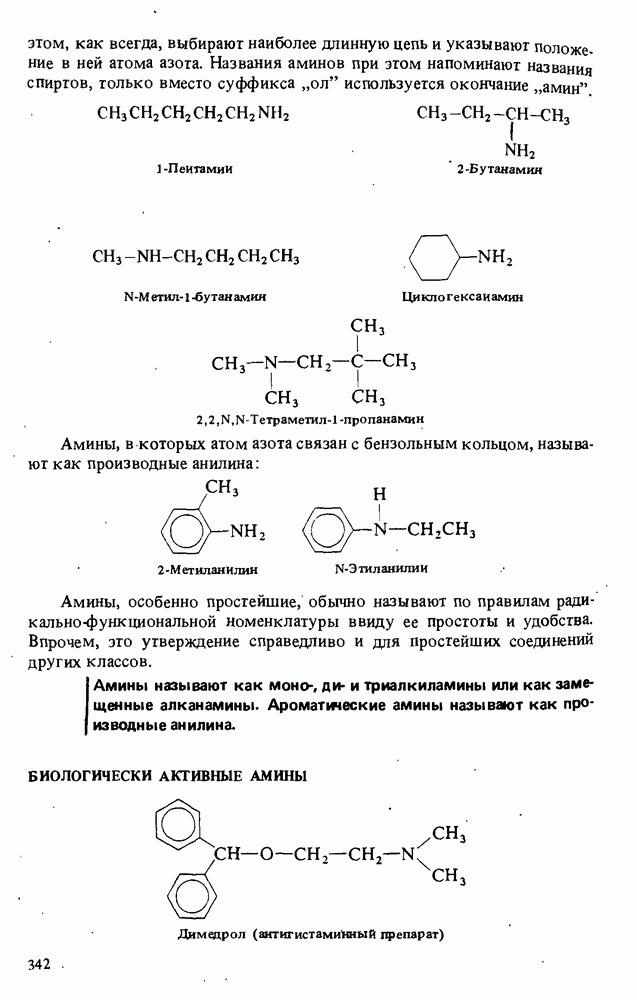
- Глава 13. АМИНЫ
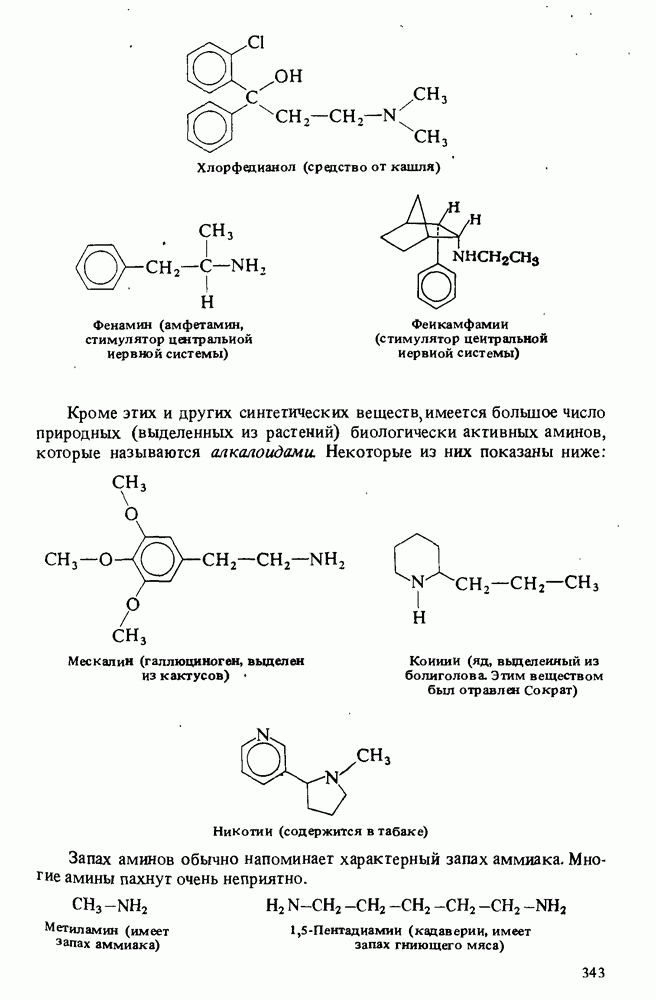
- БИОЛОГИЧЕСКИ АКТИВНЫЕ АМИНЫ
- ОСНОВНОСТЬ АМИНОВ
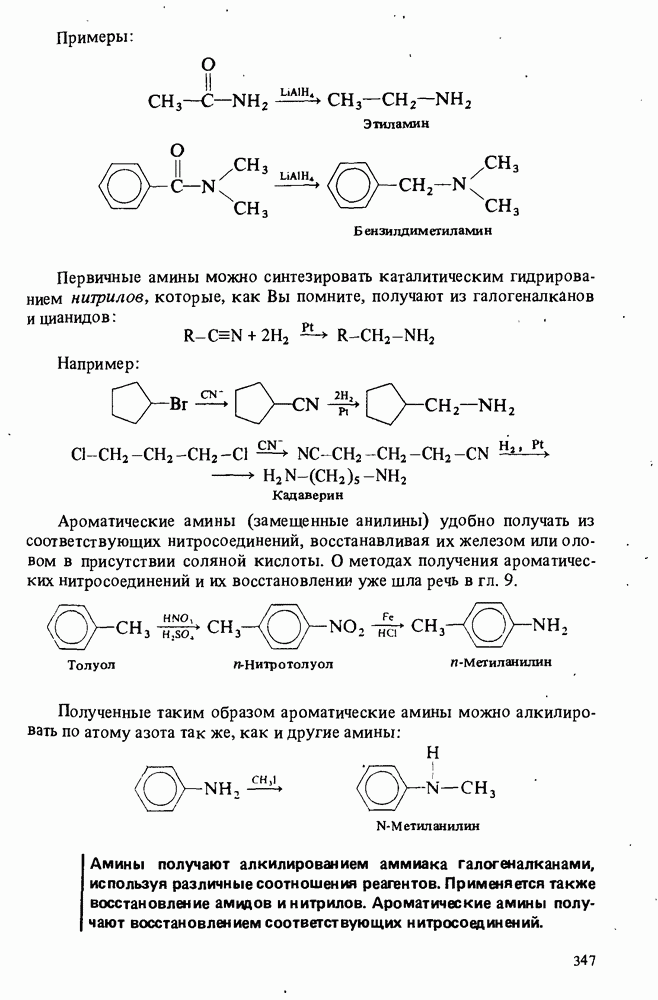
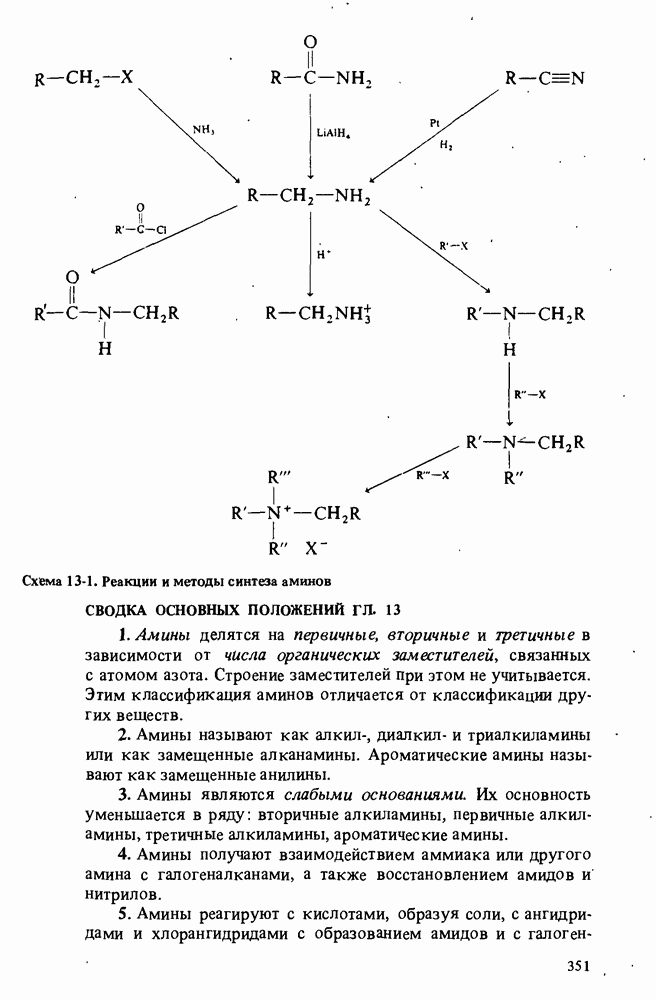
- ПОЛУЧЕНИЕ АМИНОВ
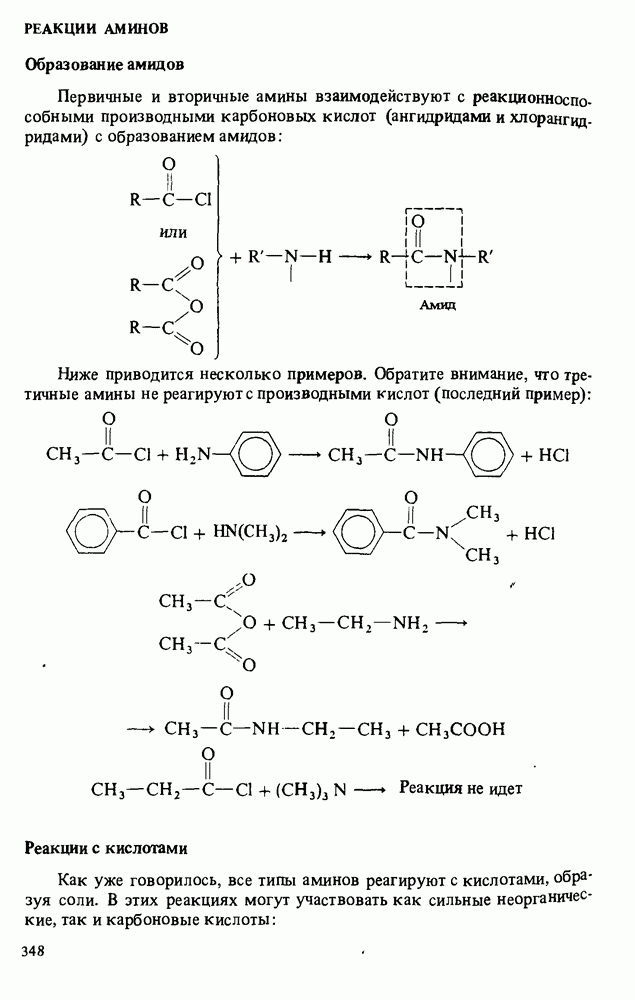
- РЕАКЦИИ АМИНОВ
- Прикладная органическая химия: ПОЛИМЕРЫ, ПОДВЕРГАЮЩИЕСЯ БИОЛОГИЧЕСКОЙ ДЕСТРУКЦИИ
- Глава 14. УГЛЕВОДЫ
- МОНОСАХАРИДЫ
- РЕАКЦИИ МОНОСАХАРИДОВ
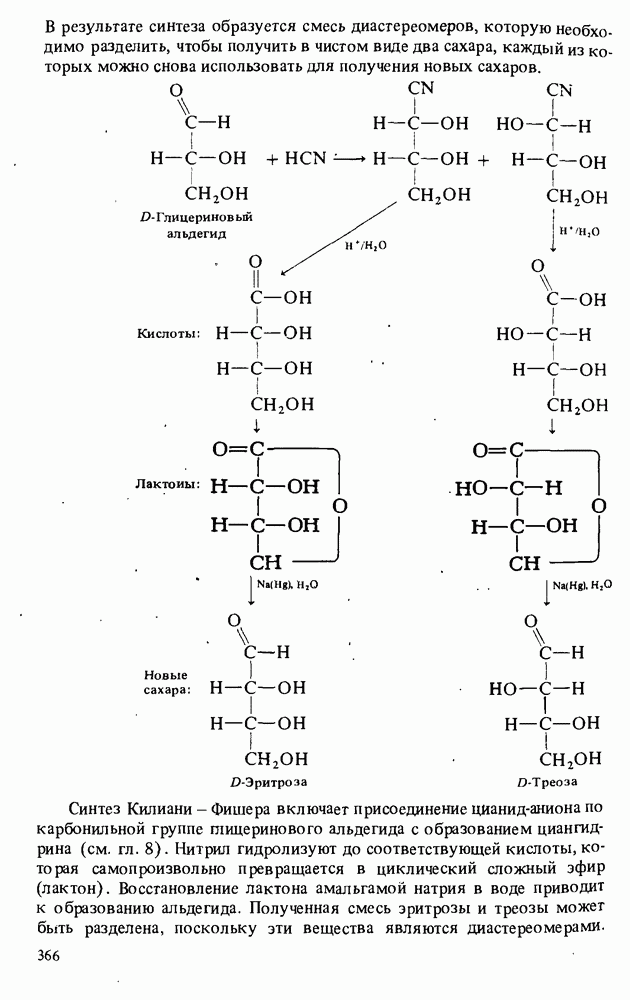
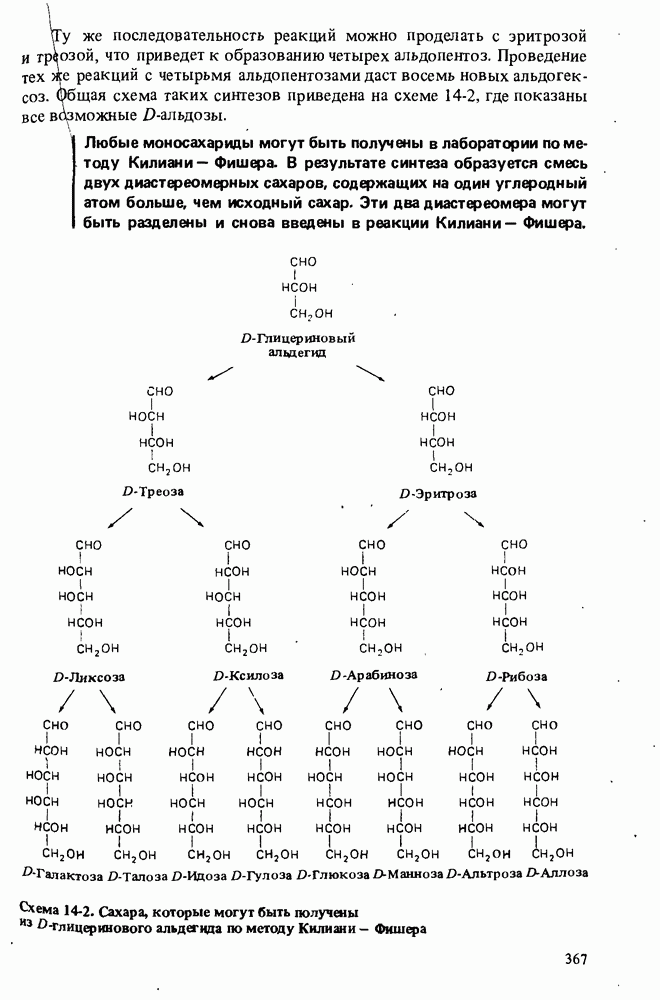
- СИНТЕЗЫ САХАРОВ
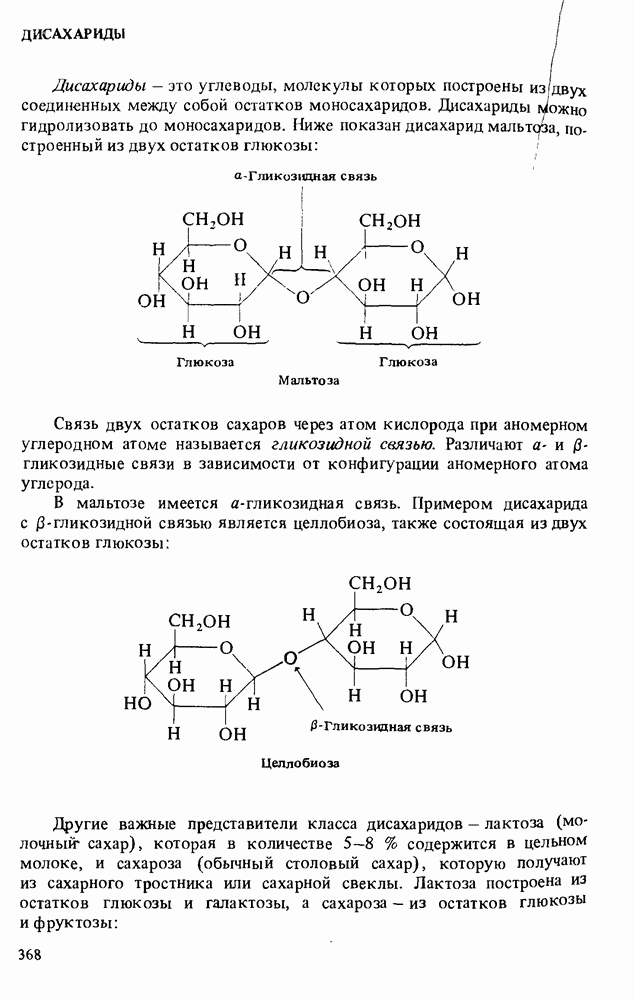
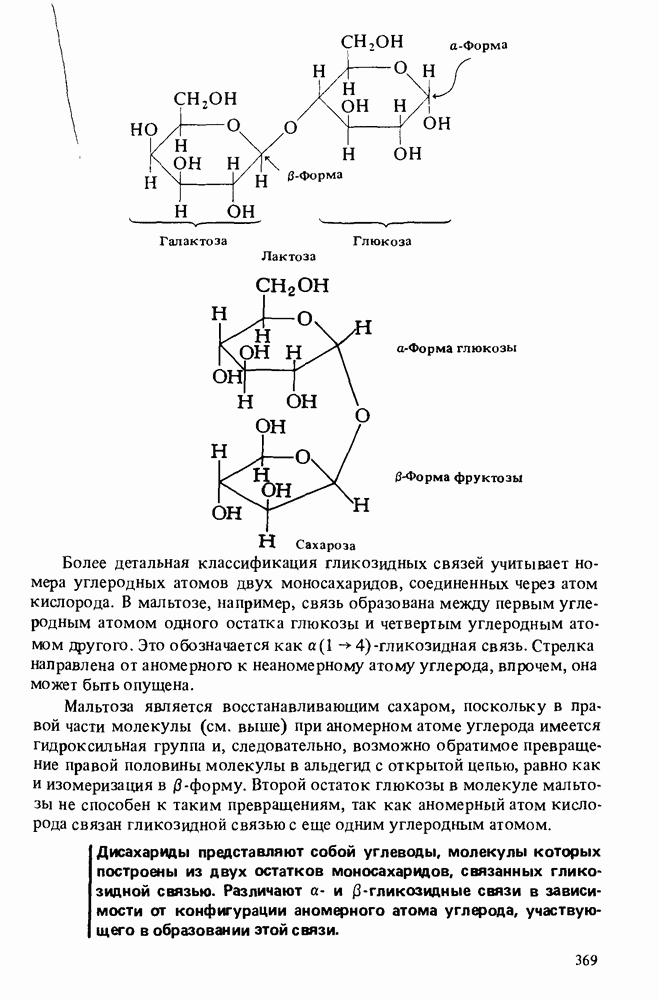
- ДИСАХАРИДЫ
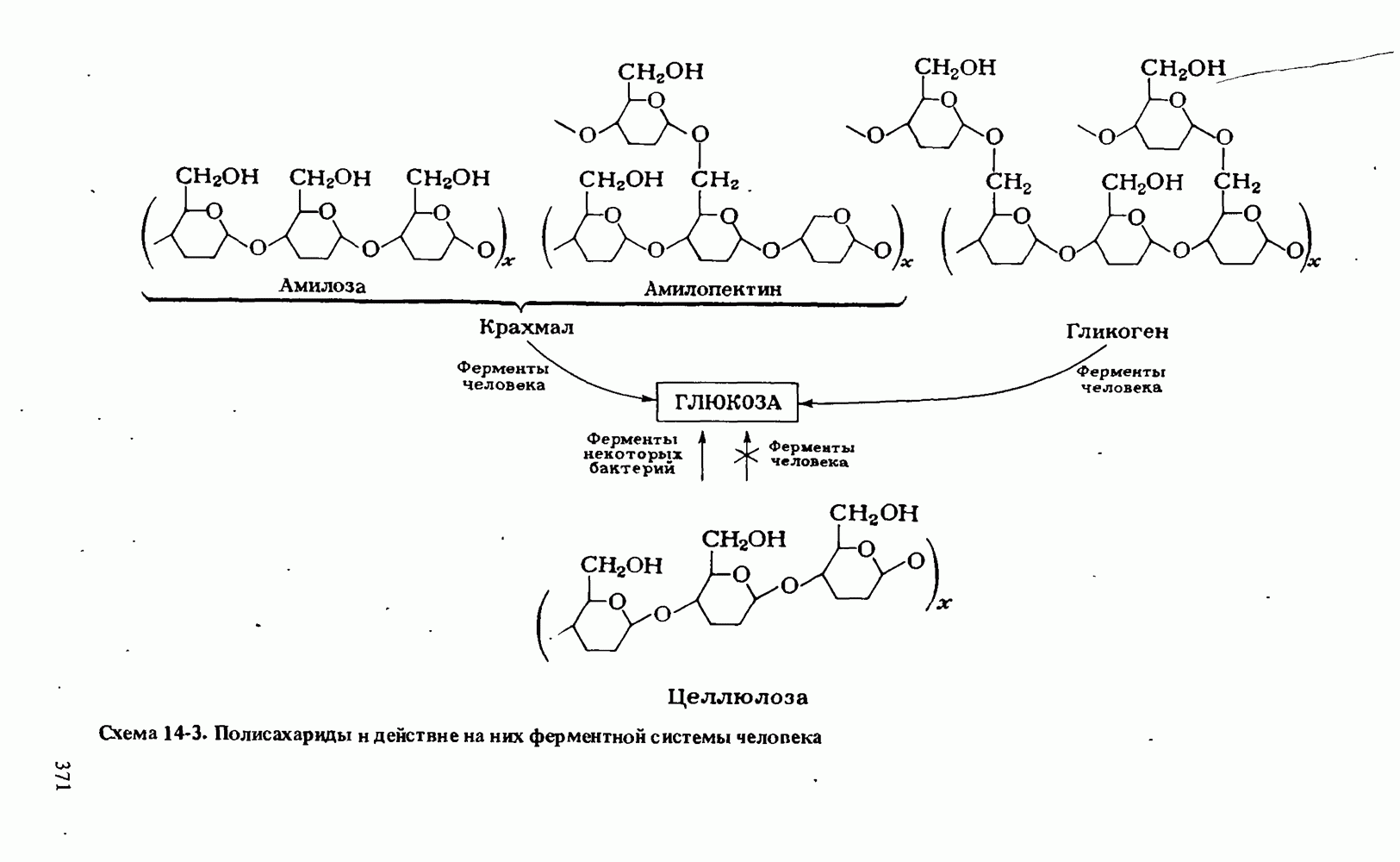
- ПОЛИСАХАРИДЫ
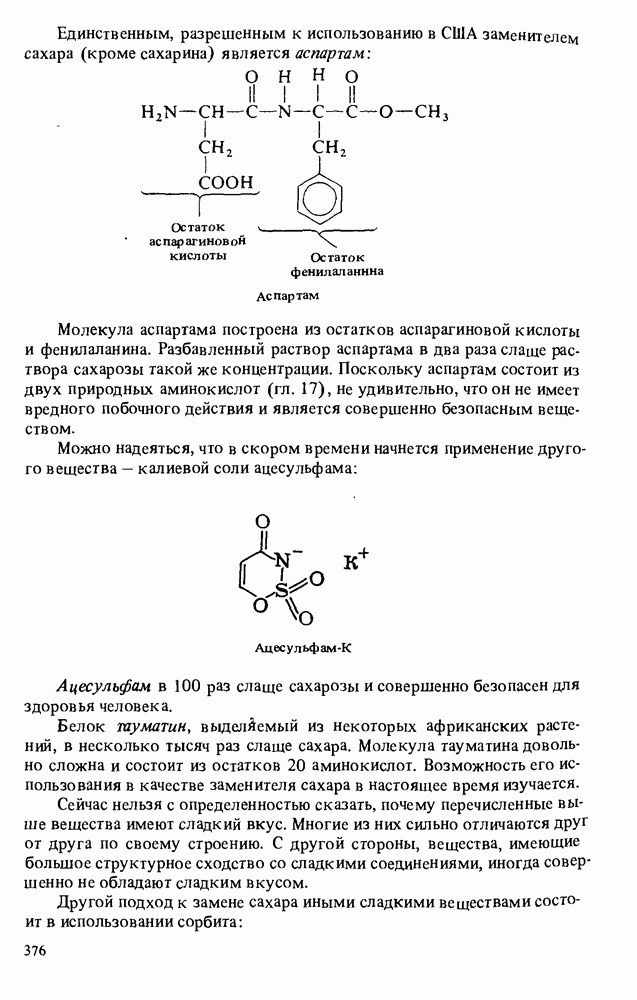
- Прикладная органическая химия: ПИЩЕВЫЕ СВОЙСТВА УГЛЕВОДОВ
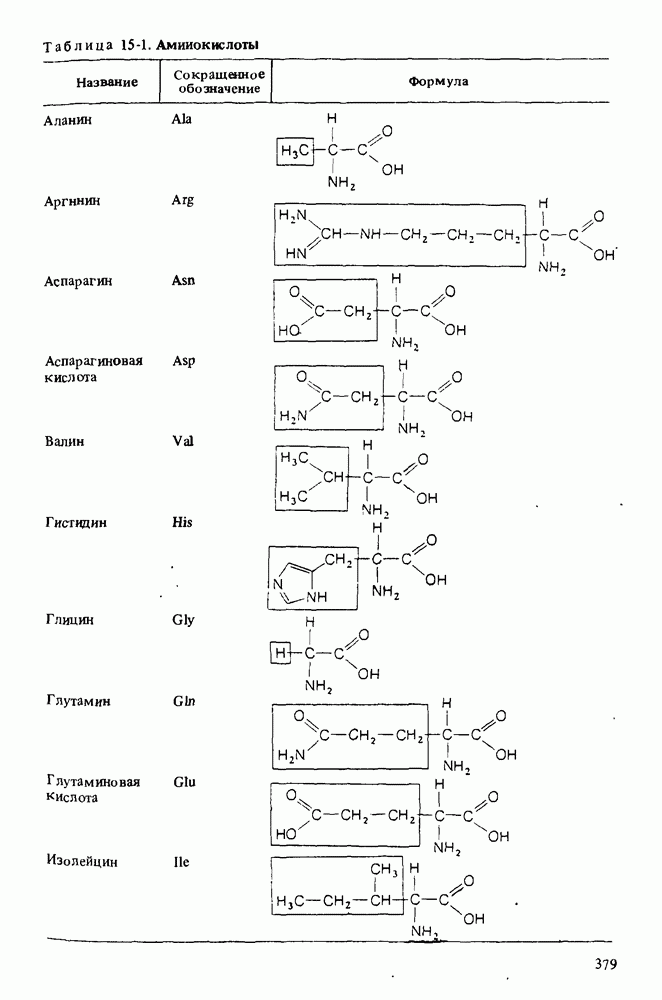
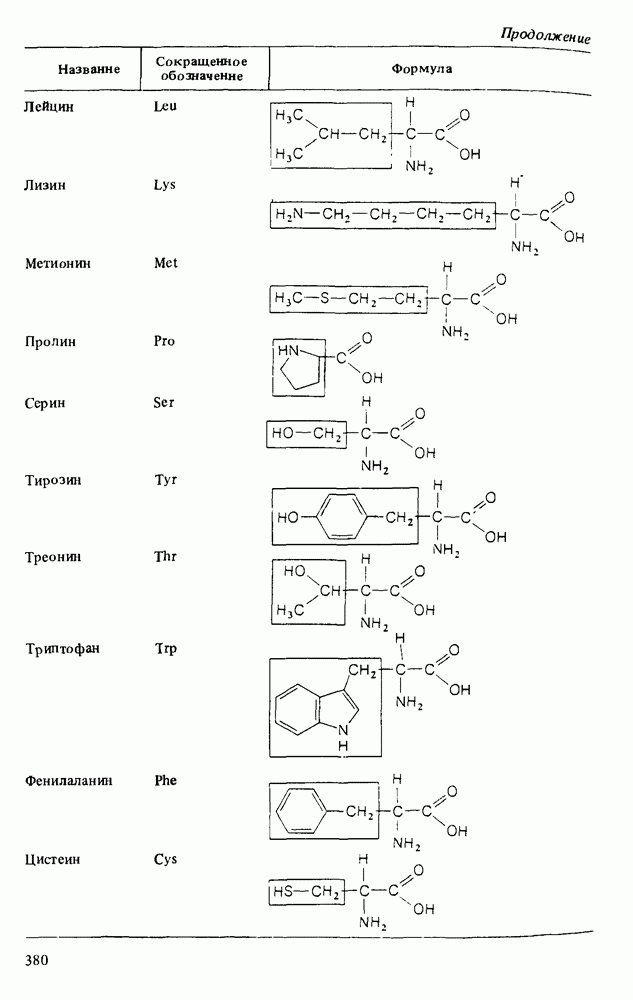
- Глава 15. АМИНОКИСЛОТЫ И БЕЛКИ
- КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА АМИНОКИСЛОТ
- АНАЛИЗ АМИНОКИСЛОТ
- СТРОЕНИЕ БЕЛКОВ
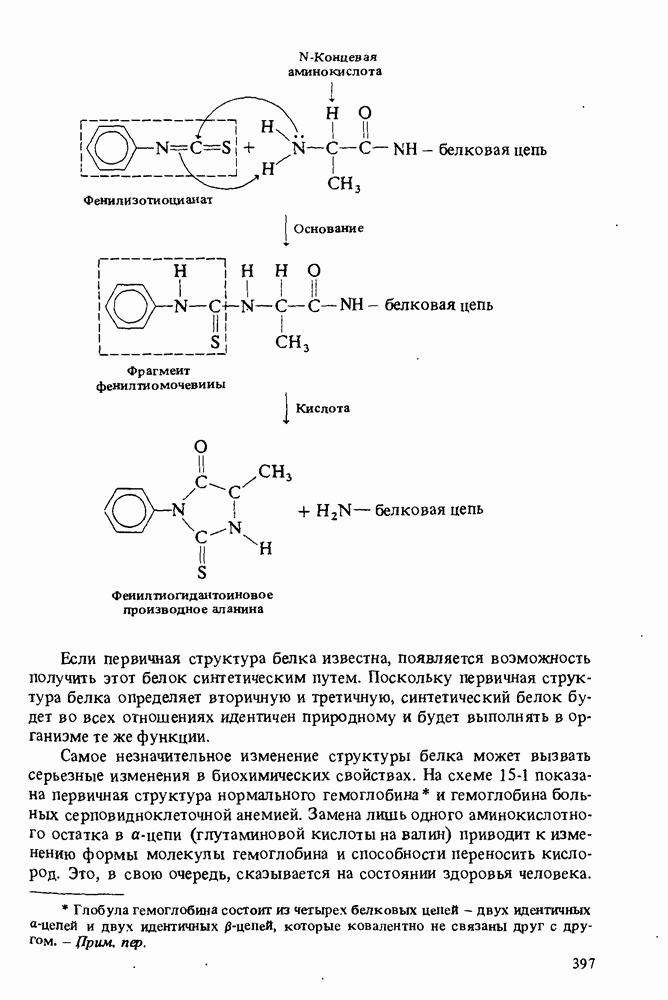
- УСТАНОВЛЕНИЕ ПЕРВИЧНОЙ СТРУКТУРЫ БЕЛКОВ
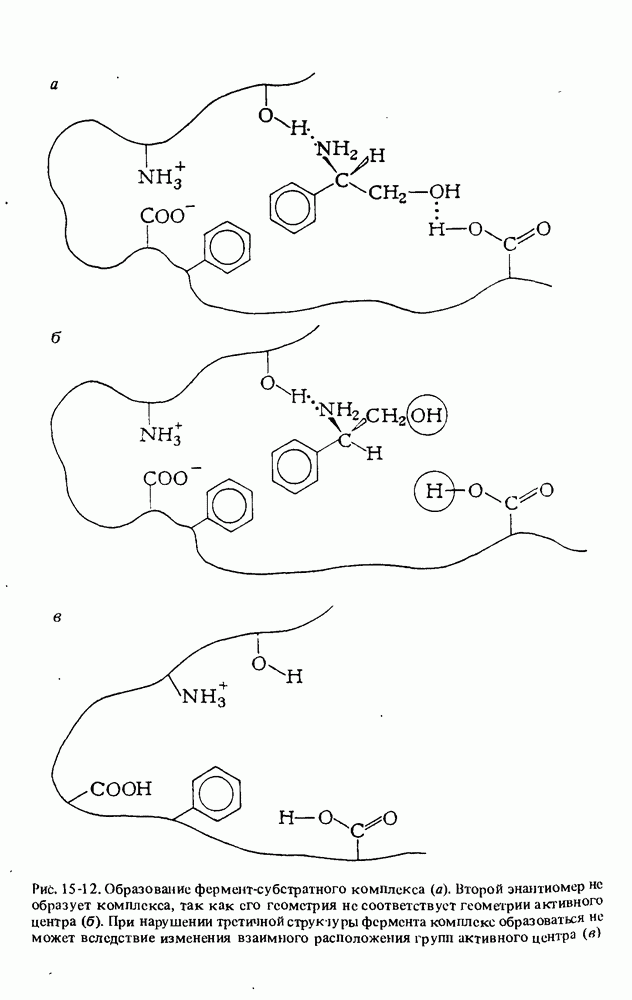
- ФЕРМЕНТЫ
- Глава 16. ЛИПИДЫ
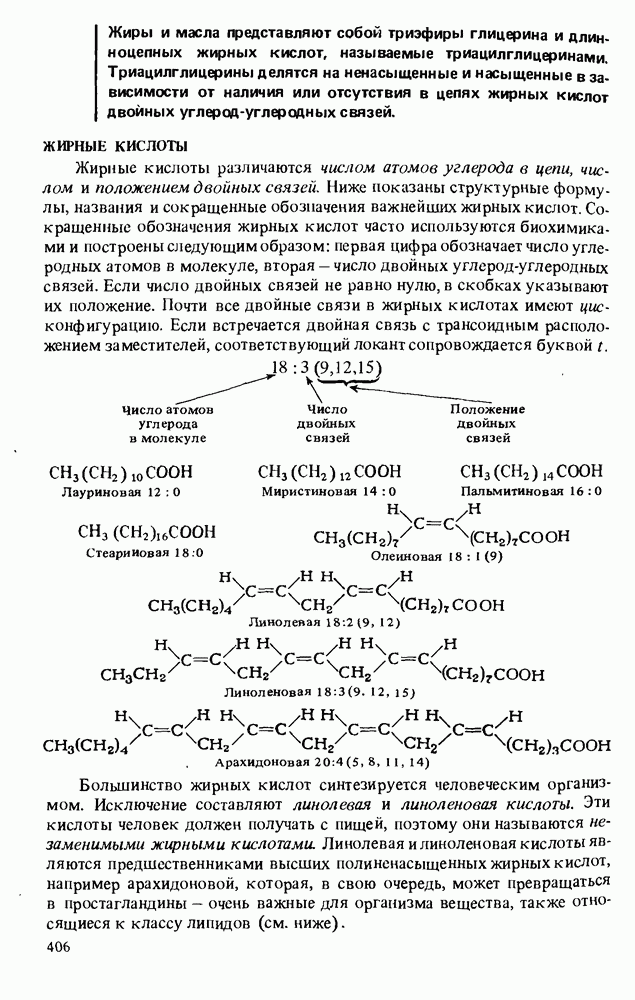
- ЖИРНЫЕ КИСЛОТЫ
- НАЗВАНИЯ ТРИАЦИЛГЛИЦЕРИНОВ
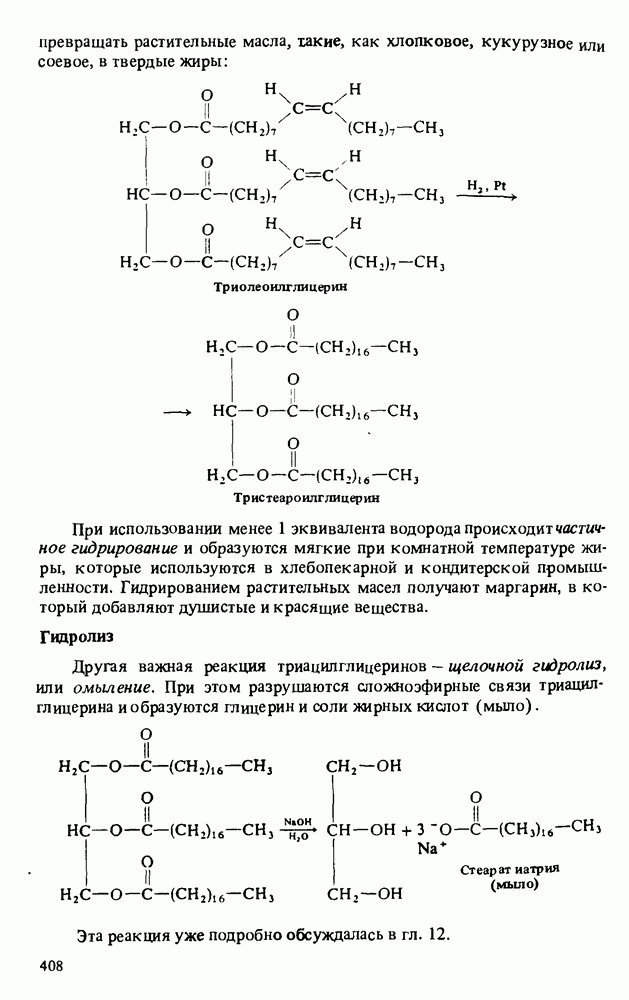
- РЕАКЦИИ ТРИАЦИЛГЛИЦЕРИНОВ
- ЛИПИДЫ, ОТЛИЧНЫЕ ОТ ТРИАЦИЛГЛИЦЕРИНОВ
- Прикладная органическая химия: ПИЩЕВЫЕ СВОЙСТВА ЛИПИДОВ
- Глава 17. НУКЛЕИНОВЫЕ КИСЛОТЫ
- РИБОНУКЛЕИНОВЫЕ КИСЛОТЫ
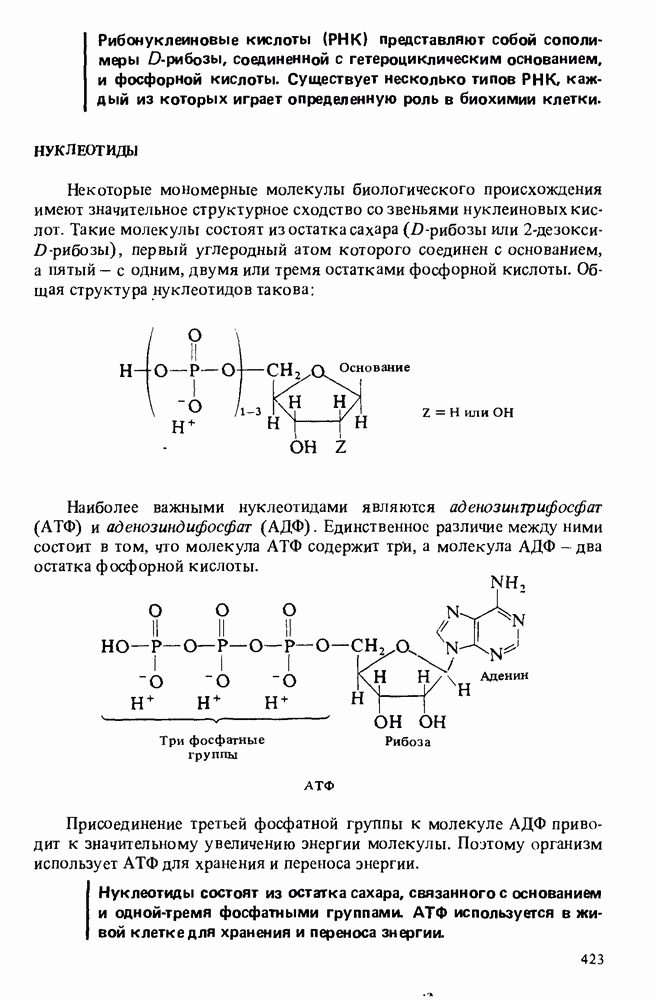
- НУКЛЕОТИДЫ
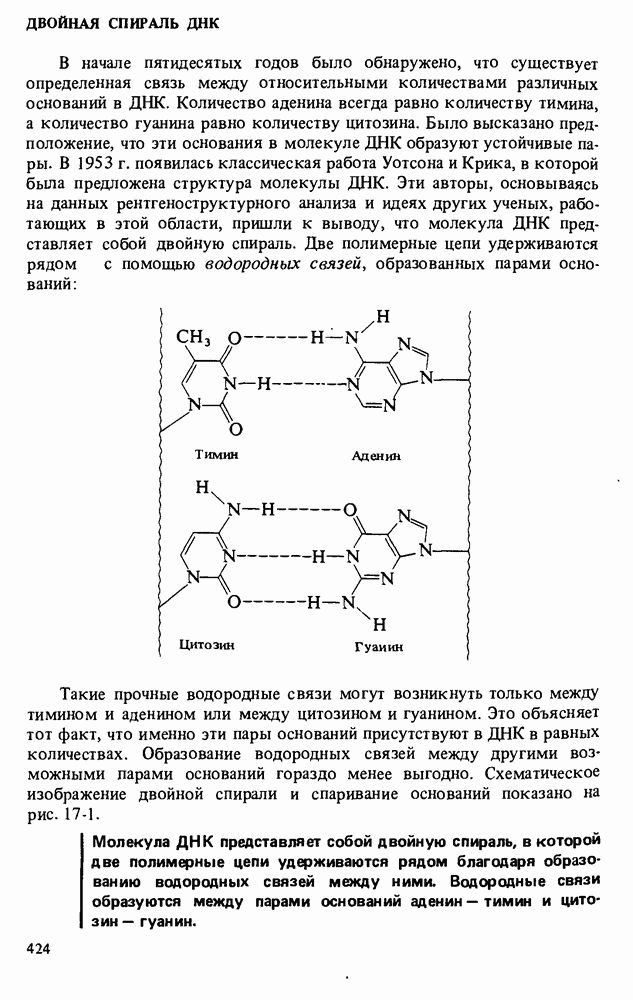
- ДВОЙНАЯ СПИРАЛЬ ДНК
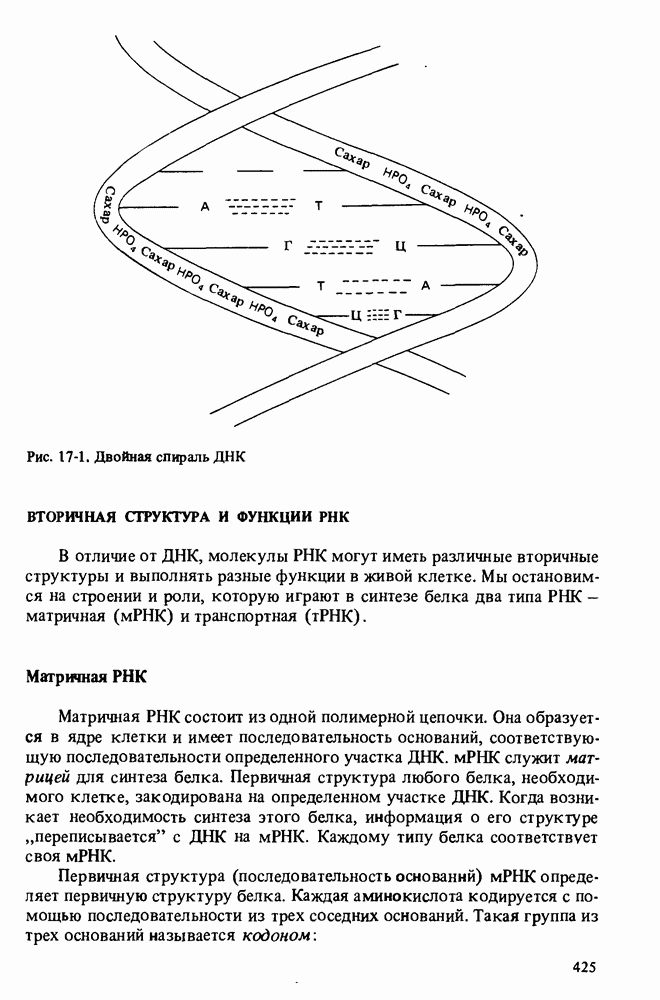
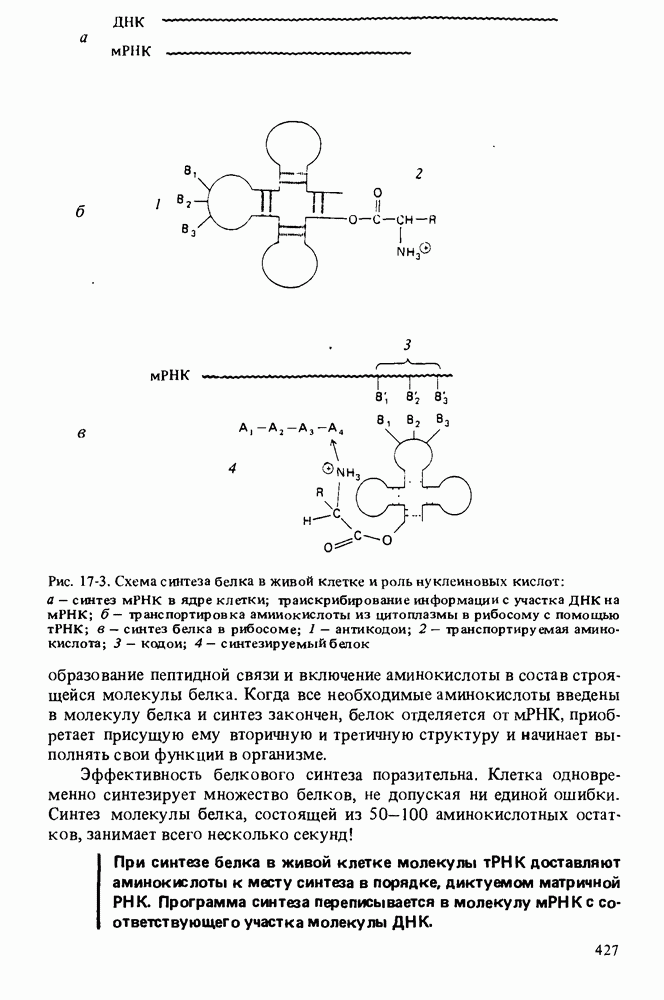
- ВТОРИЧНАЯ СТРУКТУРА И ФУНКЦИИ РНК
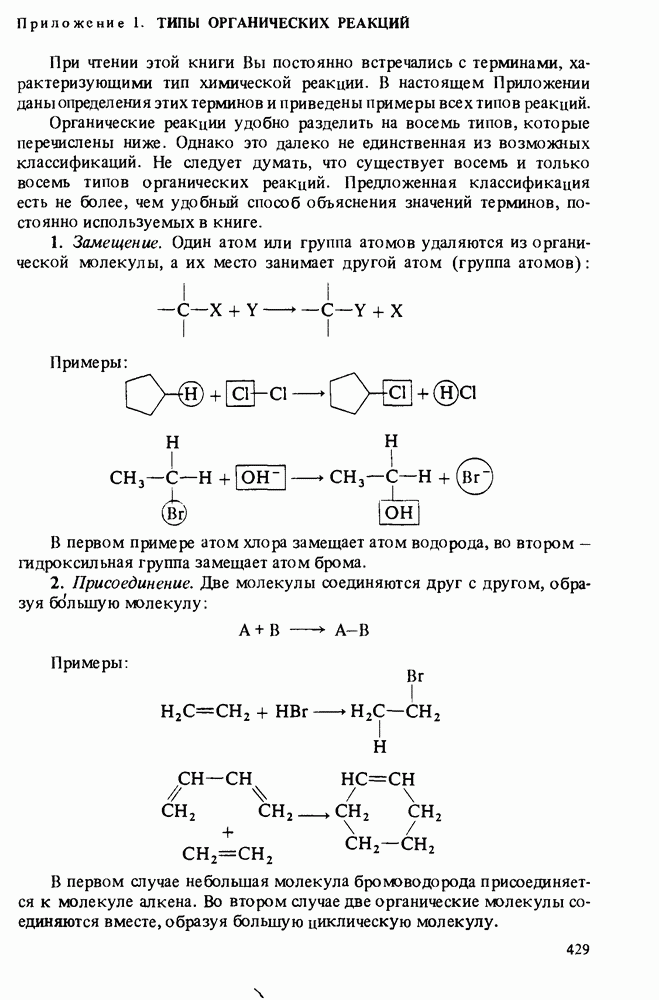
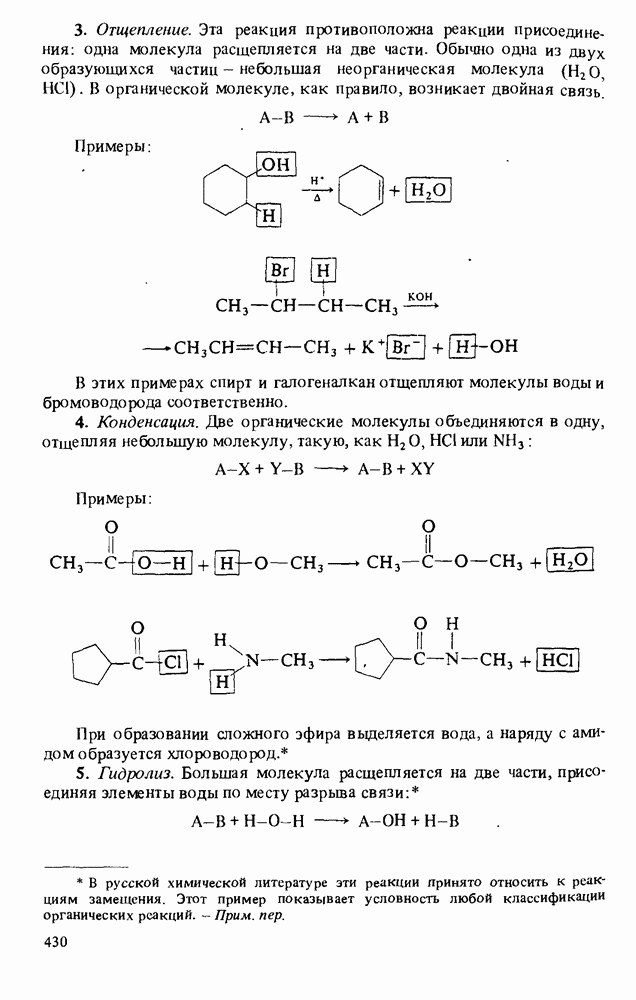
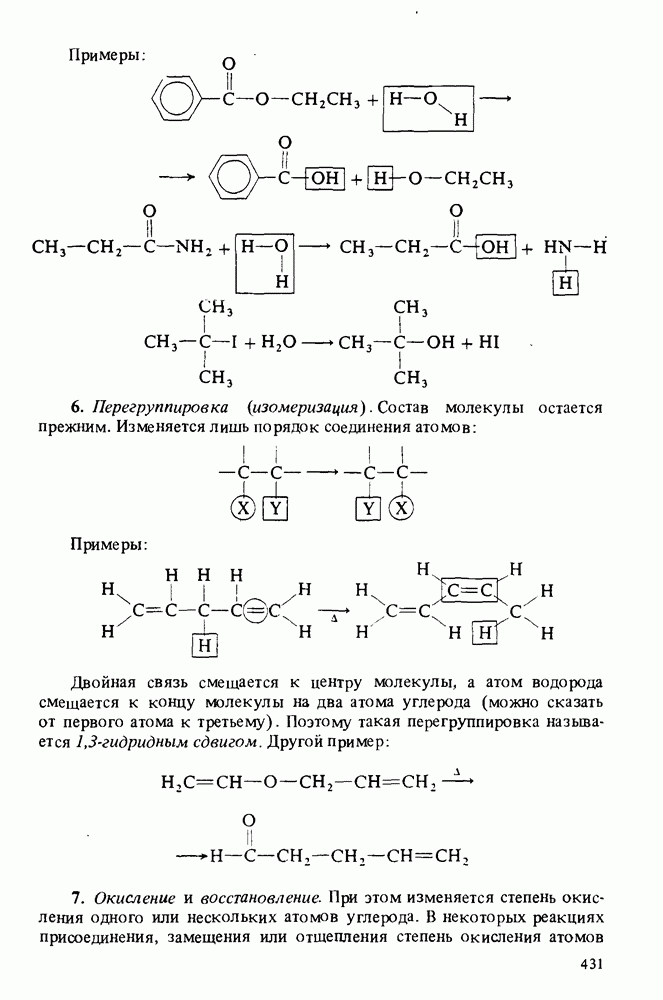
- Приложение 1. ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ
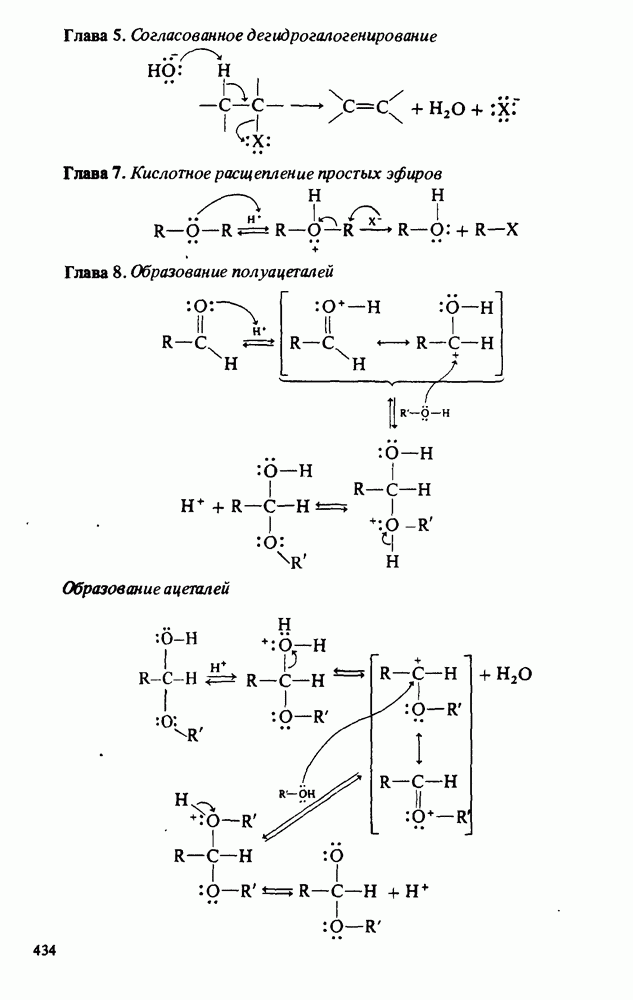
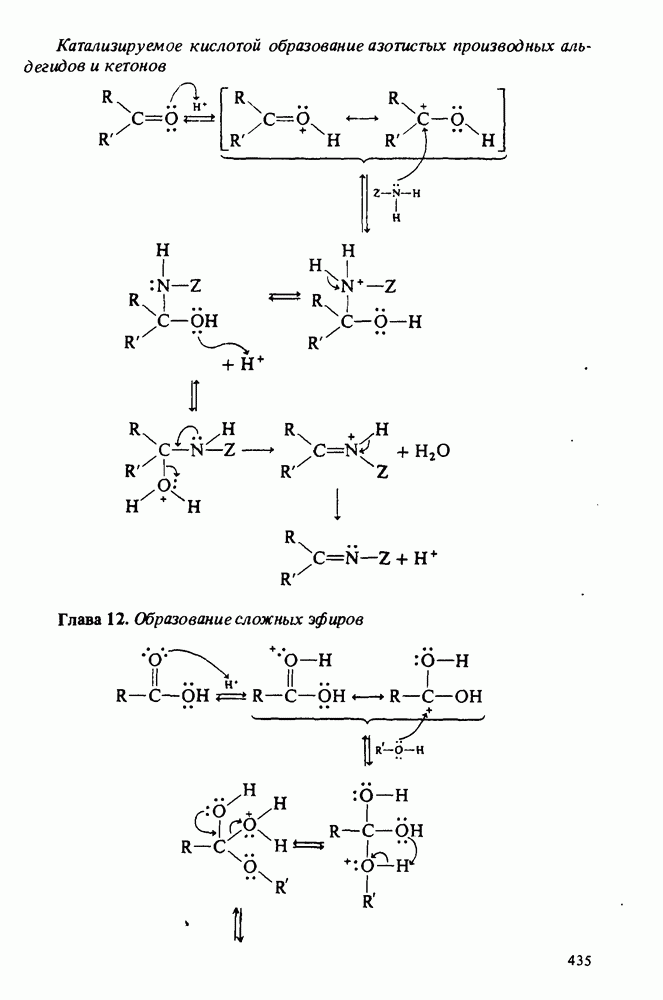
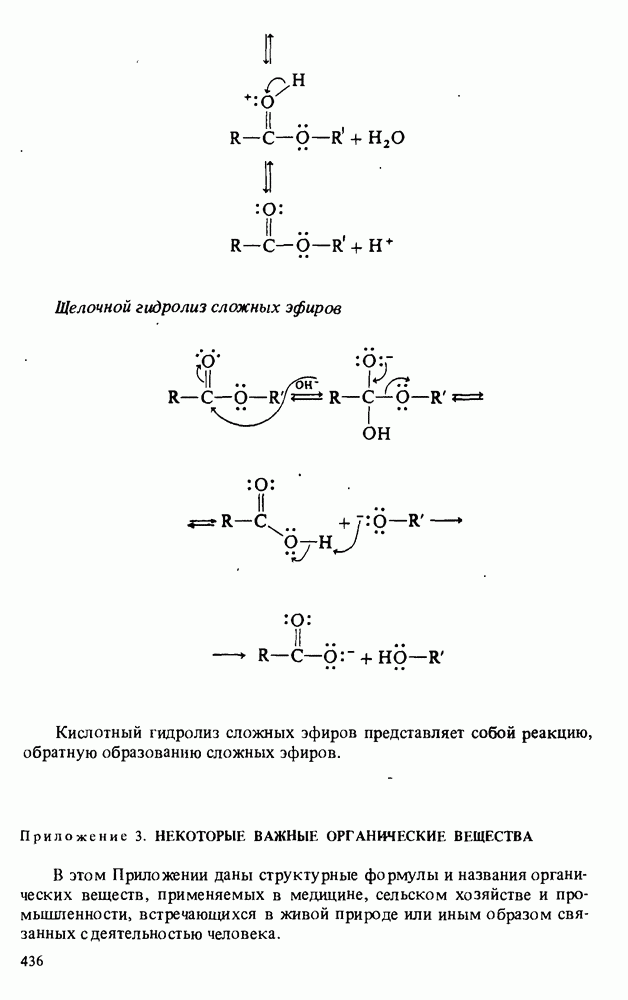
- Приложение 2. МЕХАНИЗМЫ НЕКОТОРЫХ РЕАКЦИЙ
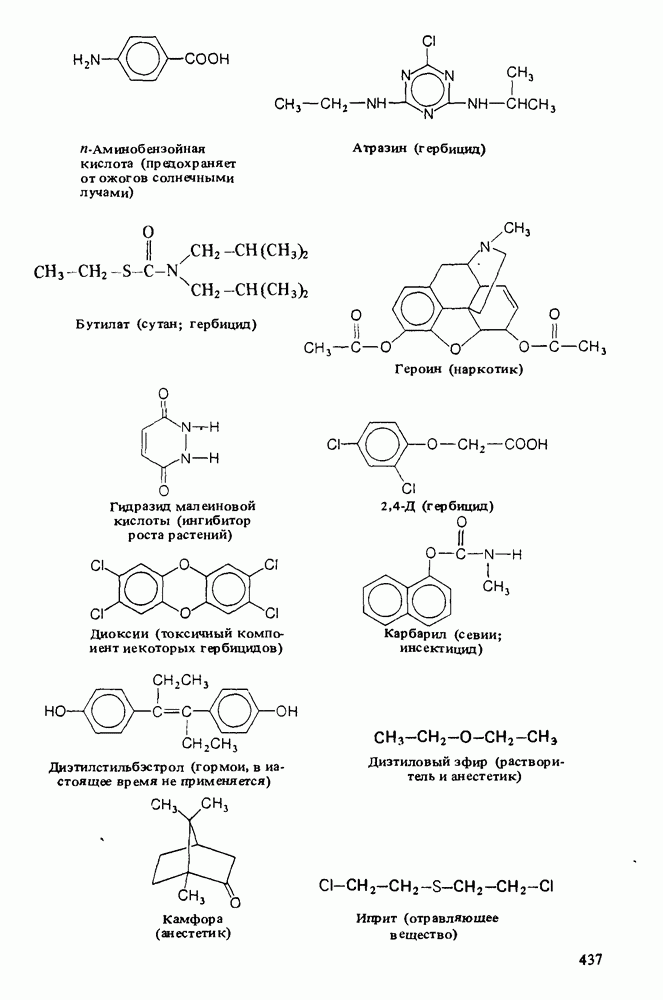
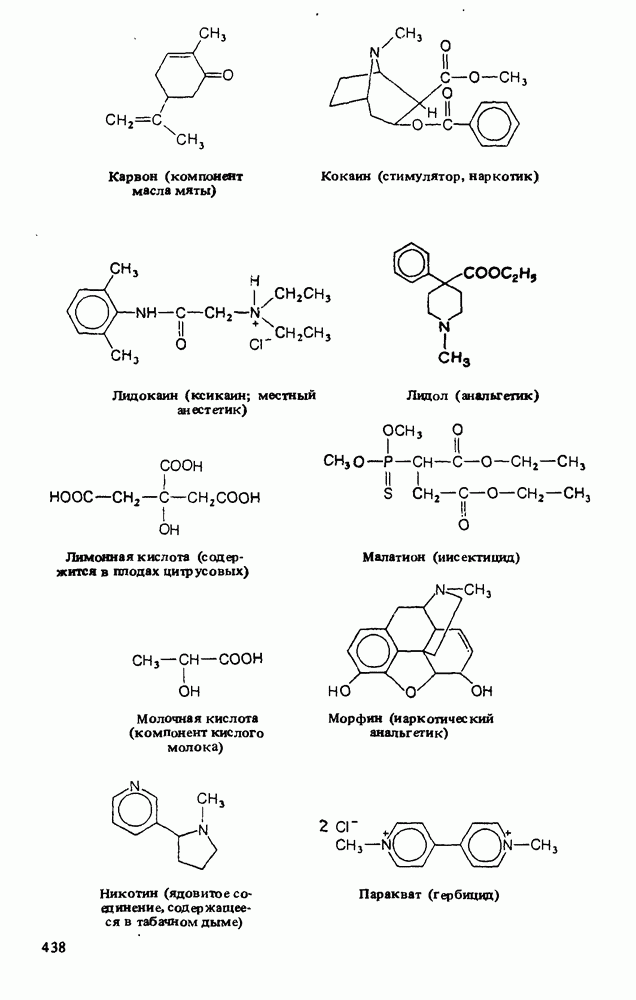
- Приложение 3. НЕКОТОРЫЕ ВАЖНЫЕ ОРГАНИЧЕСКИЕ ВЕЩЕСТВА