| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
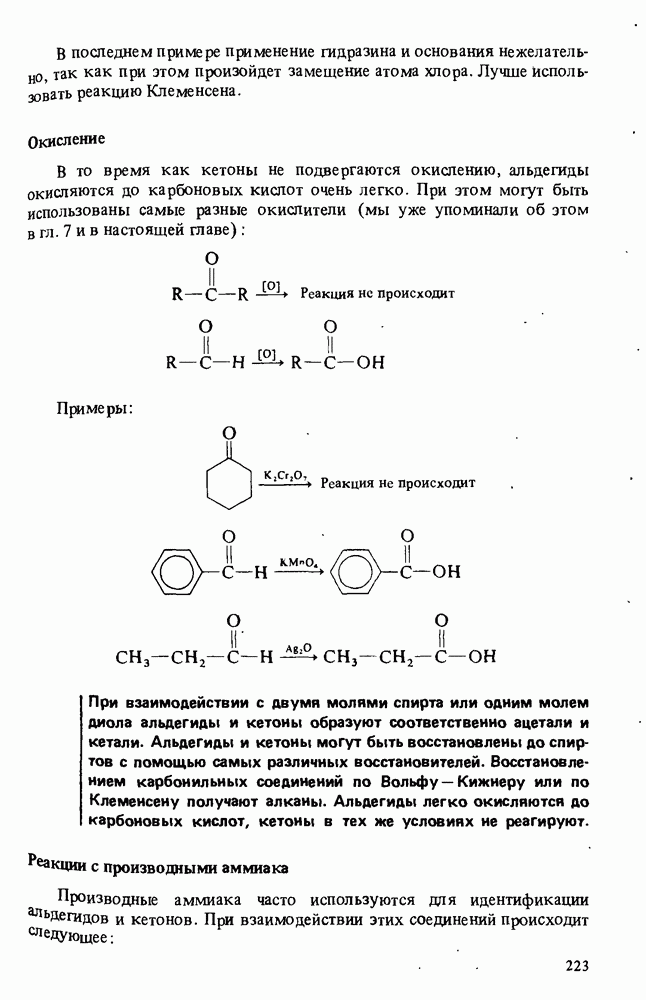
ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ
Окисление альдегидов и первичных спиртов
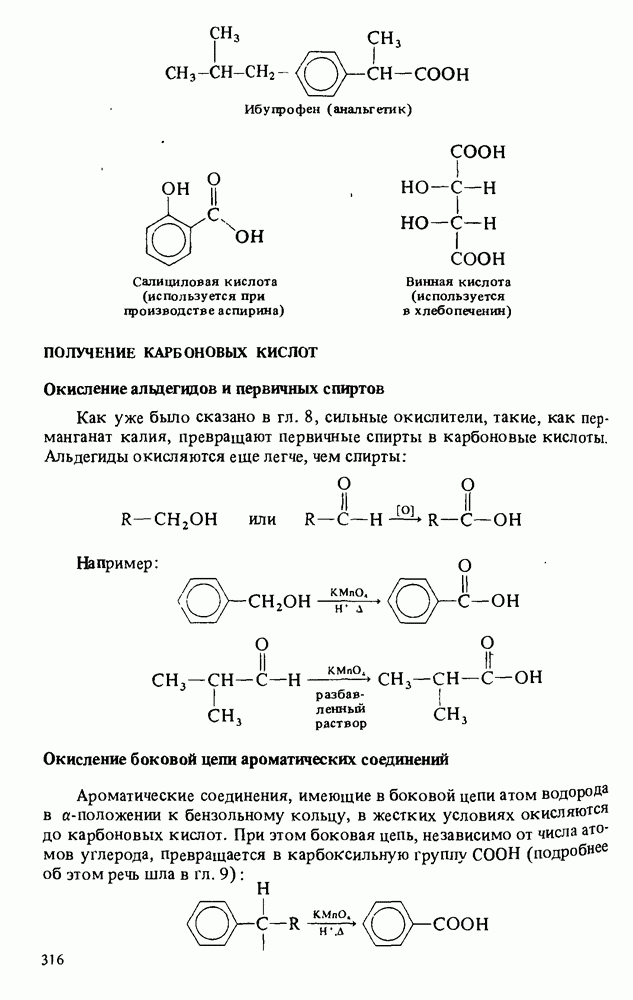
Как уже было сказано в гл. 8, сильные окислители, такие, как перманганат калия, превращают первичные спирты в карбоновые кислоты. Альдегиды окисляются еще легче, чем спирты:

Например:

Окисление боковой цепи ароматических соединений
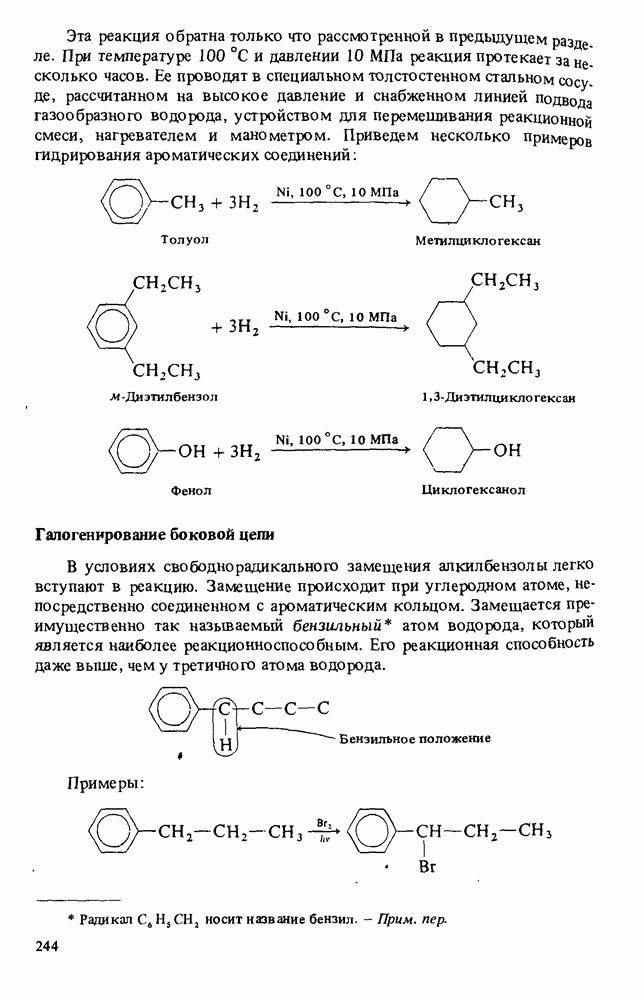
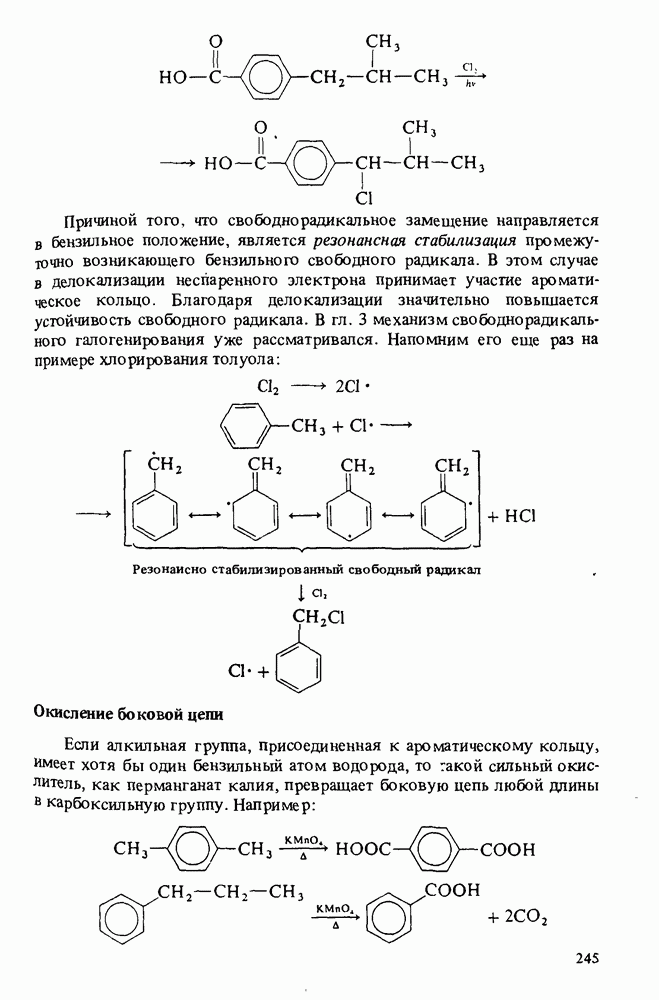
Ароматические соединения, имеющие в боковой цепи атом водорода в  -положении к бензольному кольцу, в жестких условиях окисляются до карбоновых кислот. При этом боковая цепь, независимо от числа атомов углерода, превращается в карбоксильную группу СООН (подробнее об этом речь шла в гл. 9):
-положении к бензольному кольцу, в жестких условиях окисляются до карбоновых кислот. При этом боковая цепь, независимо от числа атомов углерода, превращается в карбоксильную группу СООН (подробнее об этом речь шла в гл. 9):

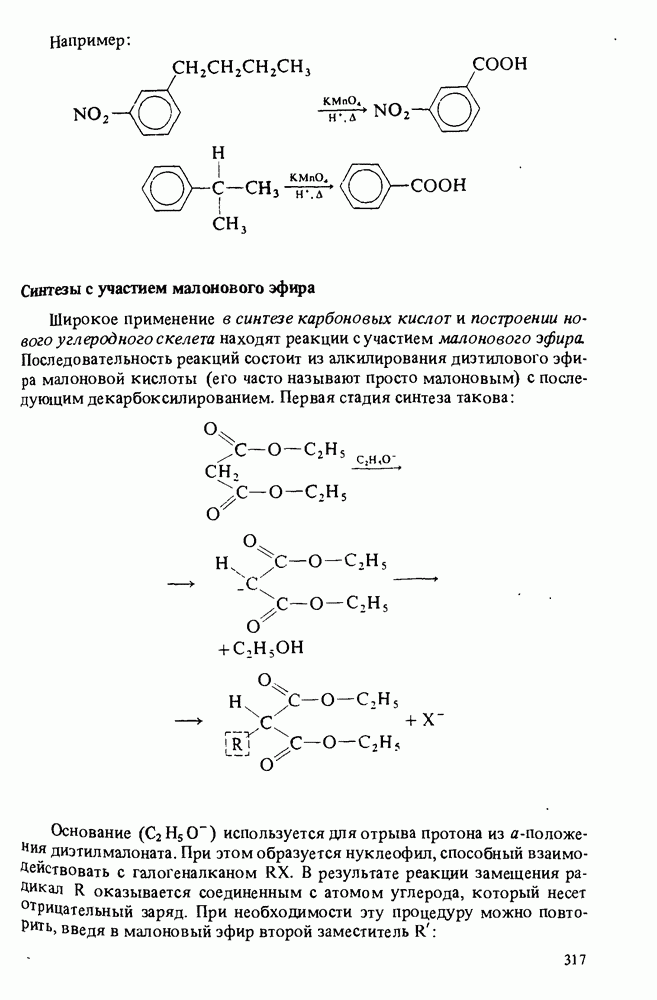
Например:

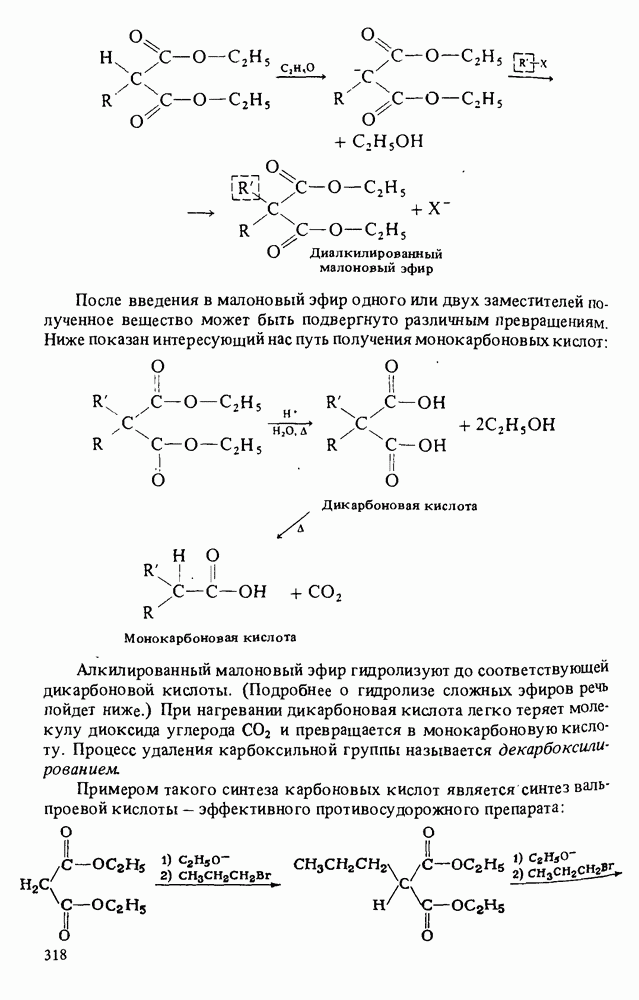
Синтезы с участием малонового эфира
Широкое применение в синтезе карбоновых кислот и построении нового углеродного скелета находят реакции с участием малонового эфира. Последовательность реакций состоит из алкилирования диэтилового эфира малоновой кислоты (его часто называют просто малоновым) с последующим декарбоксилированием. Первая стадия синтеза такова:

Основание  используется для отрыва протона из
используется для отрыва протона из  -положения диэтилмалоната. При этом образуется нуклеофил, способный взаимодействовать с галогеналканом
-положения диэтилмалоната. При этом образуется нуклеофил, способный взаимодействовать с галогеналканом  . В результате реакции замещения радикал R оказывается соединенным с атомом углерода, который несет отрицательный заряд. При необходимости эту процедуру можно повторить, введя в малоновый эфир второй заместитель
. В результате реакции замещения радикал R оказывается соединенным с атомом углерода, который несет отрицательный заряд. При необходимости эту процедуру можно повторить, введя в малоновый эфир второй заместитель 

После введения в малоновый эфир одного или двух заместителей полученное вещество может быть подвергнуто различным превращениям. Ниже показан интересующий нас путь получения монокарбоновых кислот:

Алкилированный малоновый эфир гидролизуют до соответствующей дикарбоновой кислоты. (Подробнее о гидролизе сложных эфиров речь пойдет ниже.) При нагревании дикарбоновая кислота легко теряет молекулу диоксида углерода  и превращается в монокарбоновую кислоту. Процесс удаления карбоксильной группы называется декарбоксилированием.
и превращается в монокарбоновую кислоту. Процесс удаления карбоксильной группы называется декарбоксилированием.
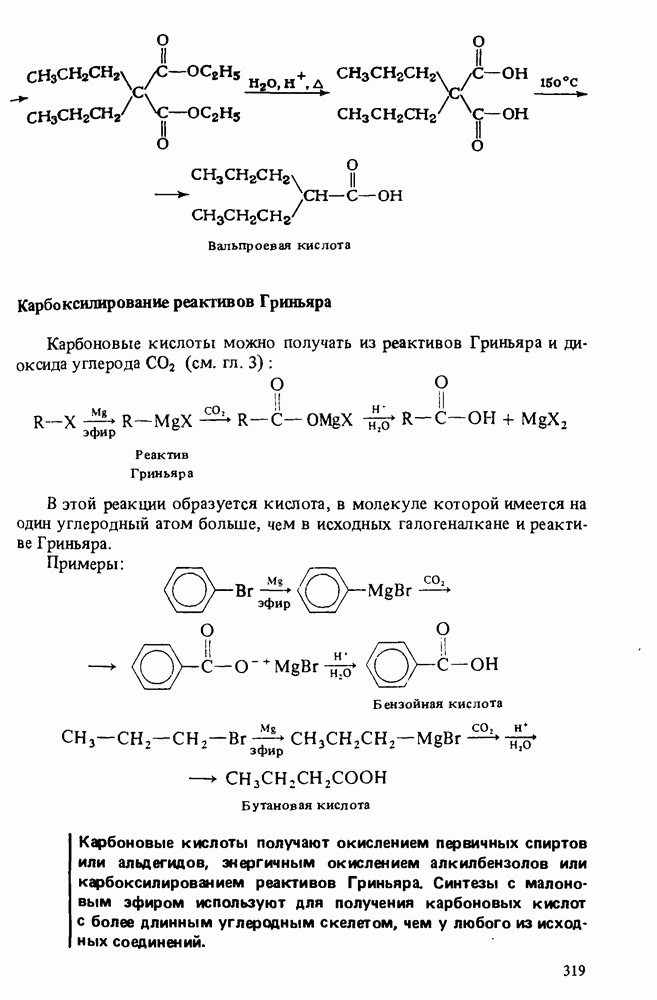
Примером такого синтеза карбоновых кислот является синтез вальпроевой кислоты — эффективного противосудорожного препарата:


Карбоксилирование реактивов Гриньяра
Карбоновые кислоты можно получать из реактивов Гриньяра и диоксида углерода  (см. гл. 3):
(см. гл. 3):

В этой реакции образуется кислота, в молекуле которой имеется на один углеродный атом больше, чем в исходных галогеналкане и реактиве Гриньяра.
Примеры:

Карбоновые кислоты получают окислением первичных спиртов или альдегидов, энергичным окислением алкилбензолов или карбоксилированием реактивов Гриньяра. Синтезы с малоновым эфиром используют для получения карбоновых кислот с более длинным углеродным скелетом, чем у любого из исходных соединений.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ
- Глава 1. КЛЮЧЕВЫЕ ПОНЯТИЯ ХИМИИ
- АТОМНАЯ ТЕОРИЯ
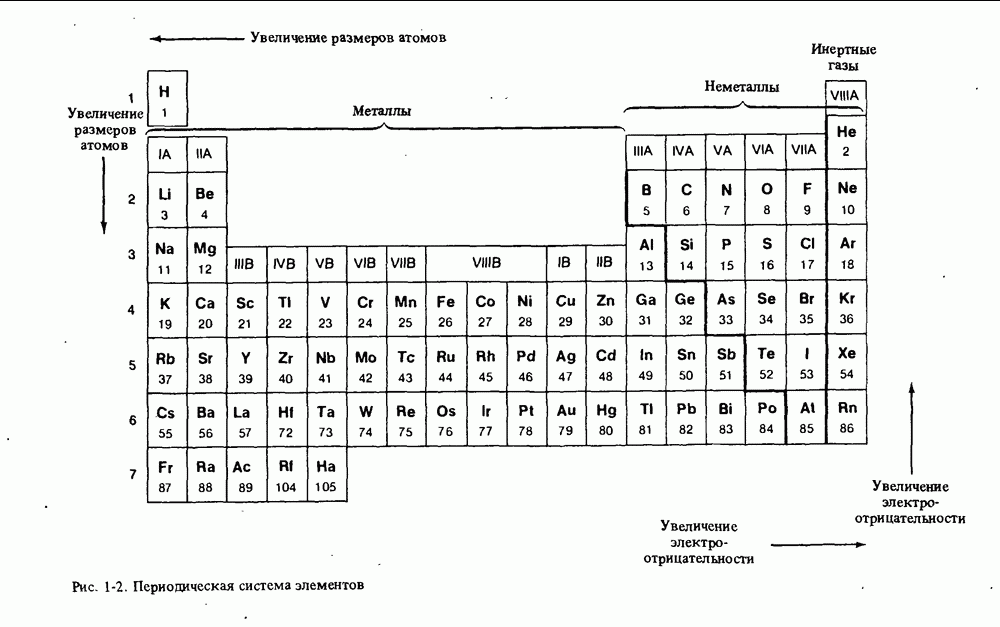
- ПЕРИОДИЧЕСКАЯ СИСТЕМА
- ХИМИЧЕСКАЯ СВЯЗЬ
- ФОРМУЛЫ ЛЬЮИСА
- ФОРМАЛЬНЫЙ ЗАРЯД
- РЕЗОНАНС
- ГЕОМЕТРИЯ МОЛЕКУЛ
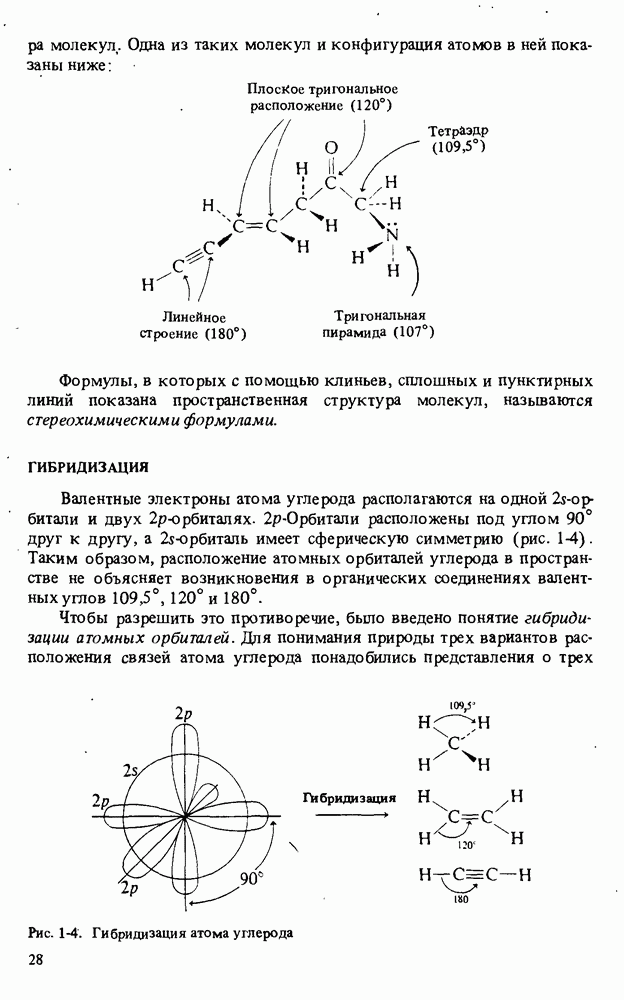
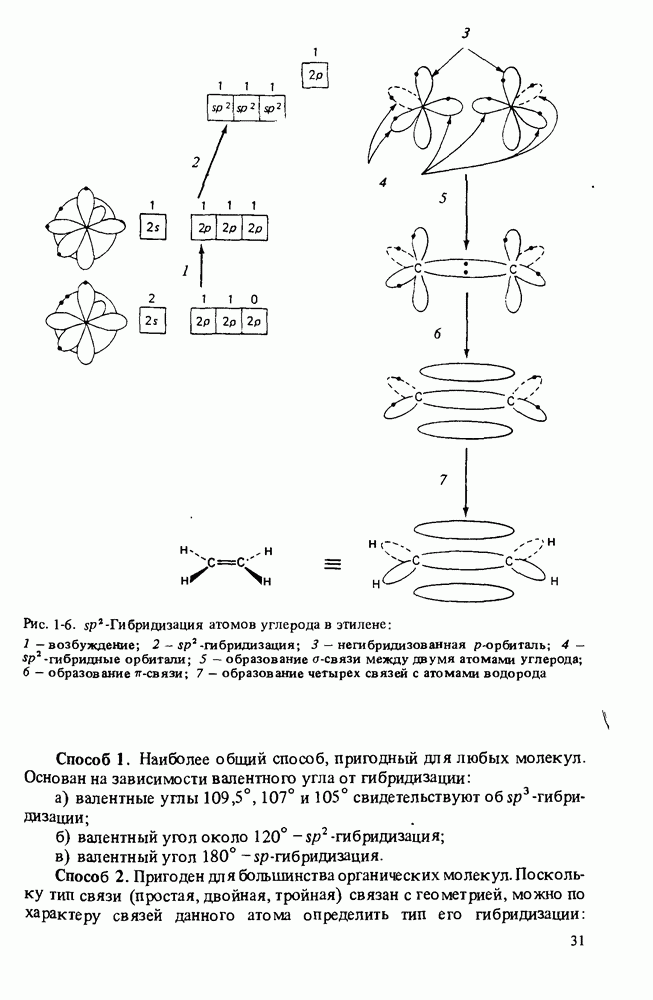
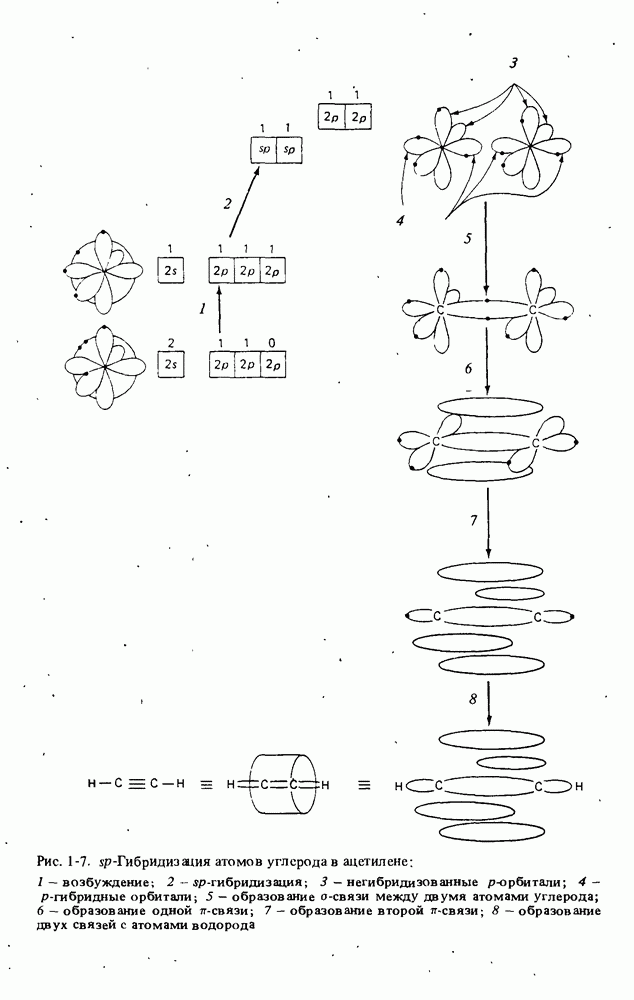
- ГИБРИДИЗАЦИЯ
- ХИМИЧЕСКИЕ ФОРМУЛЫ
- СОВЕТЫ ИЗУЧАЮЩЕМУ ОРГАНИЧЕСКУЮ ХИМИЮ
- СВОДКА ОСНОВНЫХ ПОЛОЖЕНИЙ ГЛ. 1
- Глава 2. ОБЩИЕ ВОПРОСЫ ОРГАНИЧЕСКОЙ ХИМИИ
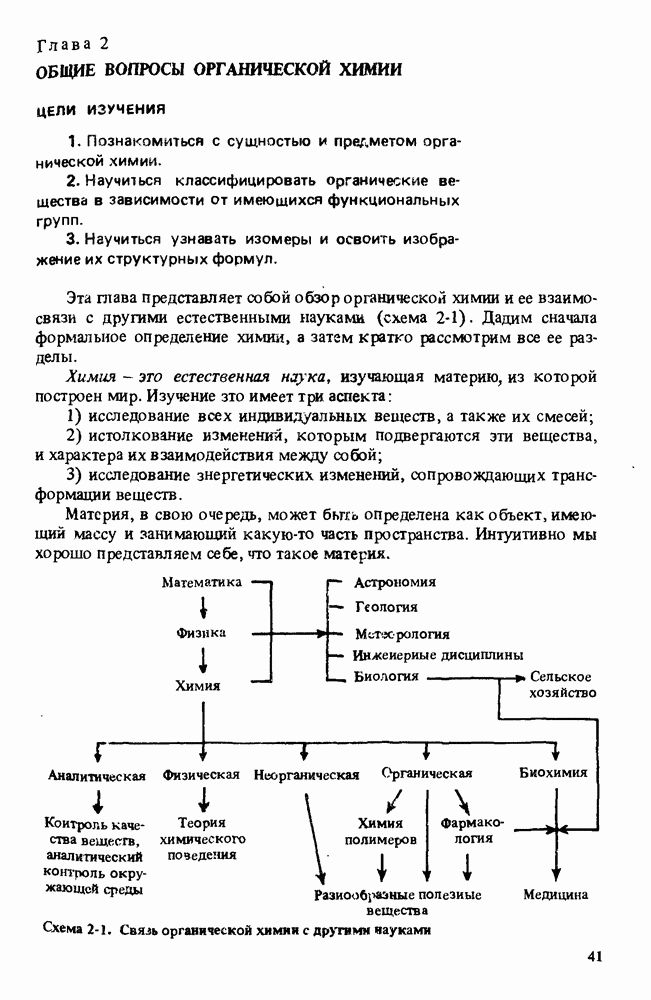
- РАЗДЕЛЫ ХИМИИ
- СИНТЕТИЧЕСКАЯ ОРГАНИЧЕСКАЯ ХИМИЯ
- ПОЛЕЗНЫЕ ОРГАНИЧЕСКИЕ ВЕЩЕСТВА
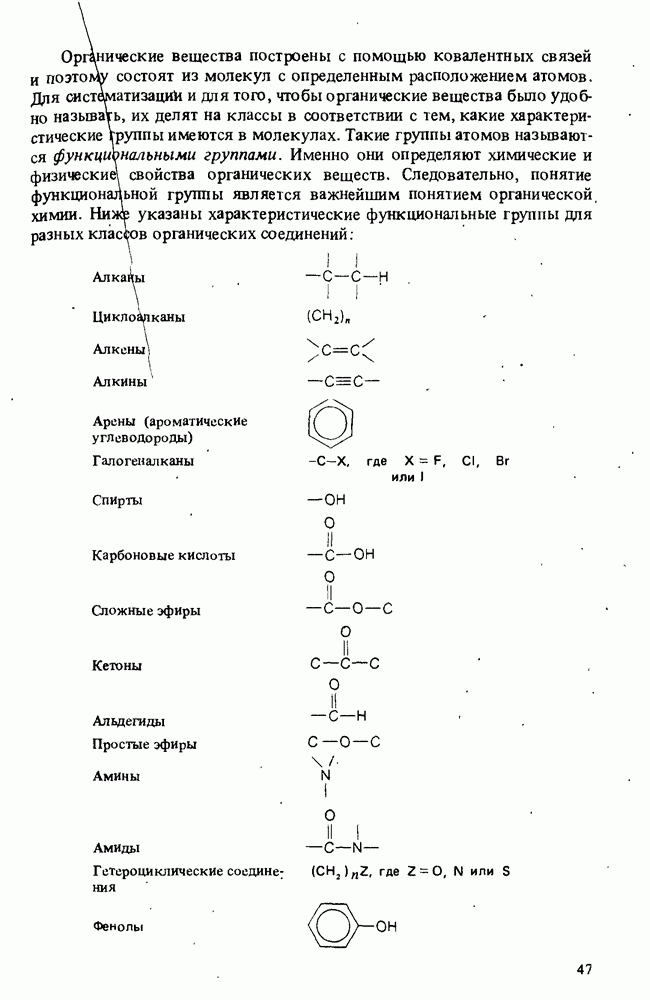
- КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ. ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
- ИЗОМЕРИЯ
- СВОДКА ОСНОВНЫХ ПОЛОЖЕНИЙ ГЛ. 2
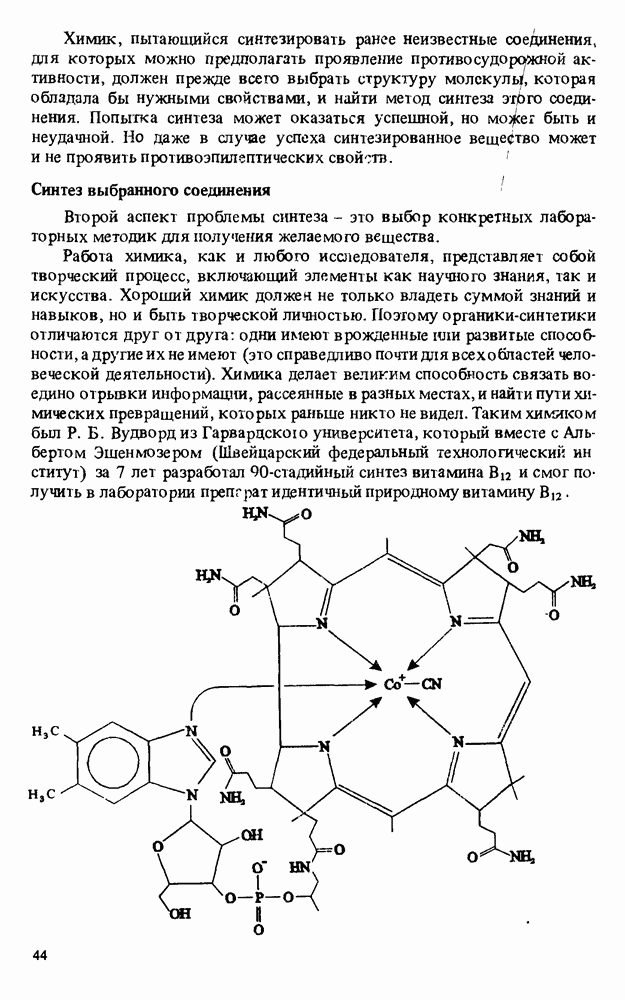
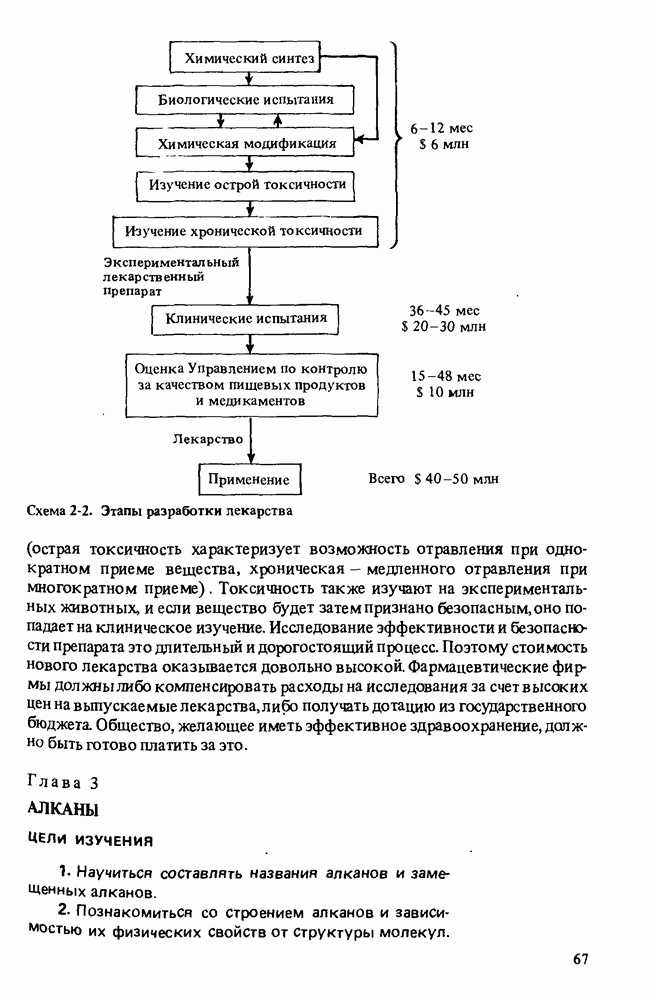
- Прикладная органическая химия: ХИМИЧЕСКИЙ СИНТЕЗ И МЕДИЦИНСКИЕ ИССЛЕДОВАНИЯ
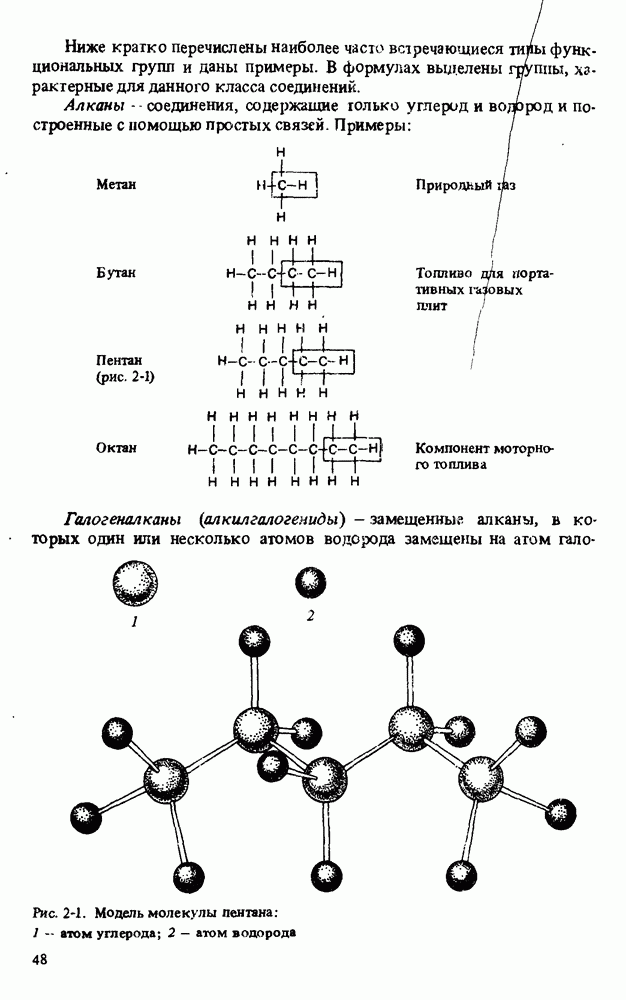
- Глава 3. АЛКАНЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА АЛКАНОВ
- СТРОЕНИЕ АЛКАНОВ
- ПОЛУЧЕНИЕ АЛКАНОВ
- РЕАКЦИИ АЛКАНОВ
- ХИМИЯ НЕФТИ
- СОВЕТЫ ИЗУЧАЮЩЕМУ ОРГАНИЧЕСКУЮ ХИМИЮ. ИЗУЧЕНИЕ РЕАКЦИЙ
- Глава 4. СТЕРЕОХИМИЯ И ОПТИЧЕСКАЯ АКТИВНОСТЬ
- СПОСОБЫ ИЗОБРАЖЕНИЯ ЭНАНТИОМЕРОВ
- ОБОЗНАЧЕНИЕ АБСОЛЮТНОЙ КОНФИГУРАЦИИ
- НАЗВАНИЯ ХИРАЛЬНЫХ МОЛЕКУЛ
- ИЗОБРАЖЕНИЕ МОЛЕКУЛ С ПРОТИВОПОЛОЖНОЙ КОНФИГУРАЦИЕЙ
- D,L-НОМЕНКЛАТУРА ЭНАНТИОМЕРОВ
- ТЕРМИНОЛОГИЯ, ПРИМЕНЯЕМАЯ В СТЕРЕОХИМИИ
- ЗНАЧЕНИЕ ОПТИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ
- Глава 5. ОРГАНИЧЕСКИЕ ГАЛОГЕНСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
- ПОЛУЧЕНИЕ ГАЛОГЕНАЛКАНОВ
- РЕАКЦИИ ГАЛОГЕНАЛКАНОВ
- ПРАКТИЧЕСКИ ВАЖНЫЕ ГАЛОГЕНАЛКАНЫ
- Прикладная органическая химия: ОРГАНИЧЕСКИЕ ПЕСТИЦИДЫ
- Глава 6. НЕНАСЫЩЕННЫЕ УГЛЕВОДОРОДЫ
- НОМЕНКЛАТУРА АЛКЕНОВ
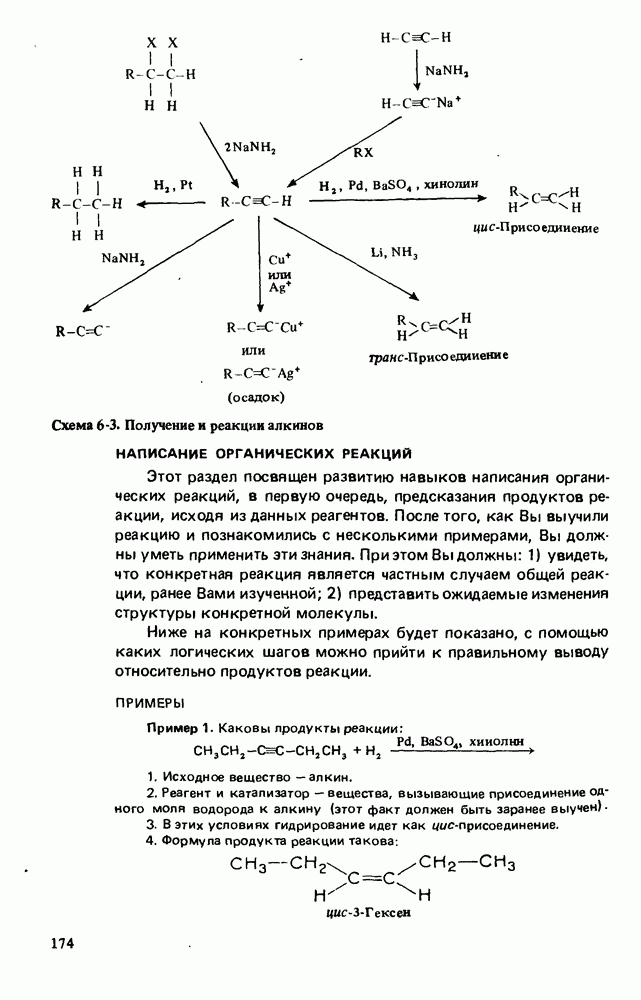
- ПОЛУЧЕНИЕ АЛКЕНОВ
- ОСНОВНЫЕ РЕАКЦИИ АЛКЕНОВ
- ПОЛИМЕРЫ
- НОМЕНКЛАТУРА АЛКИНОВ
- ПОЛУЧЕНИЕ АЛКИНОВ
- РЕАКЦИИ АЛКИНОВ
- НАПИСАНИЕ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- Глава 7. СПИРТЫ И ПРОСТЫЕ ЭФИРЫ
- НОМЕНКЛАТУРА СПИРТОВ
- НЕКОТОРЫЕ ВАЖНЫЕ ВЕЩЕСТВА, СОДЕРЖАЩИЕ СПИРТОВУЮ ГРУППУ
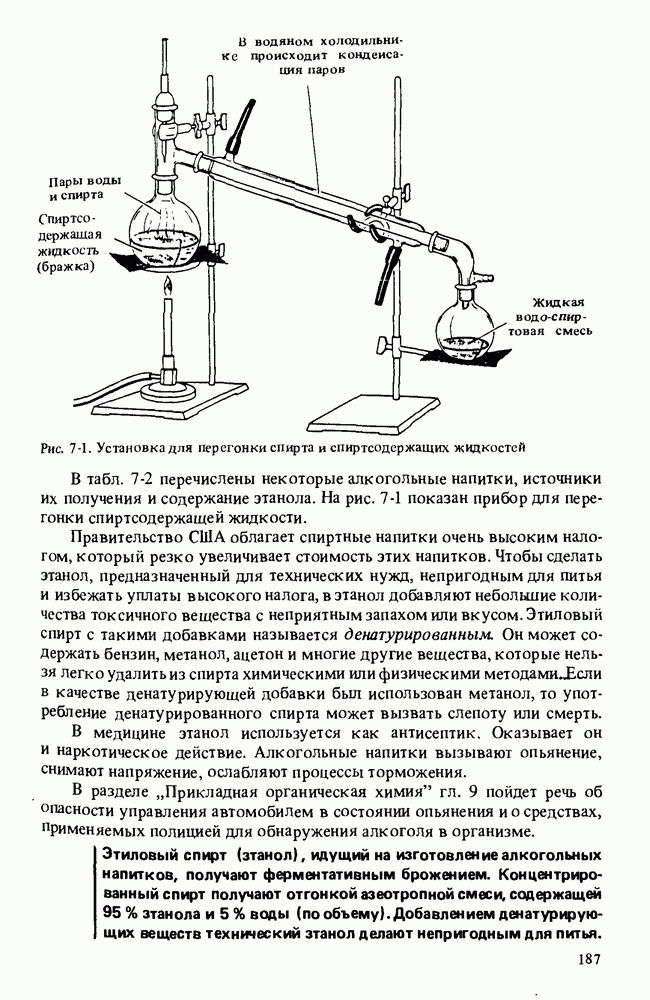
- ЭТИЛОВЫЙ СПИРТ. ПРОИЗВОДСТВО СПИРТНЫХ НАПИТКОВ
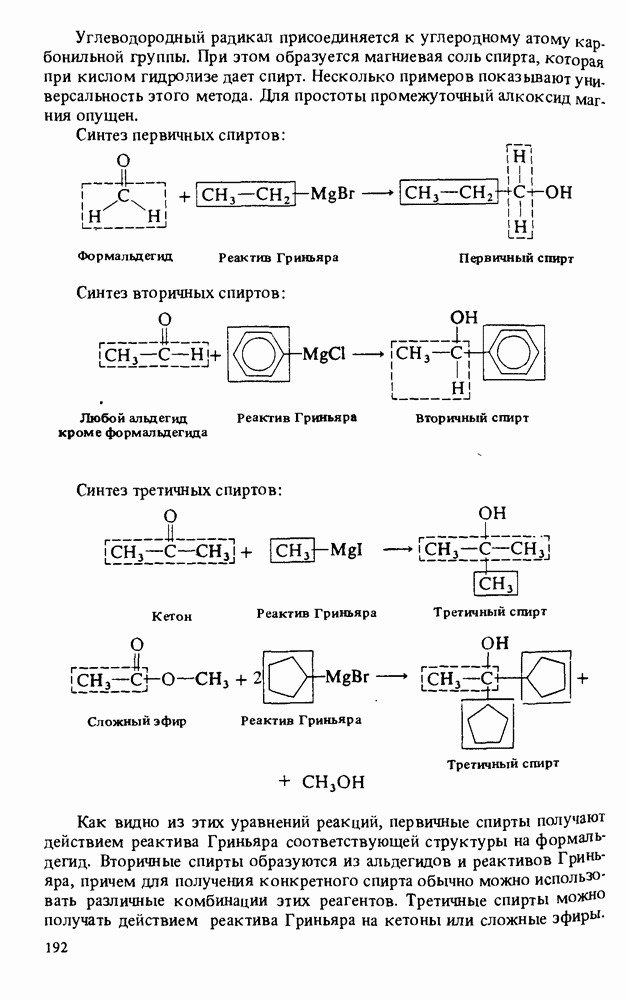
- ПОЛУЧЕНИЕ СПИРТОВ
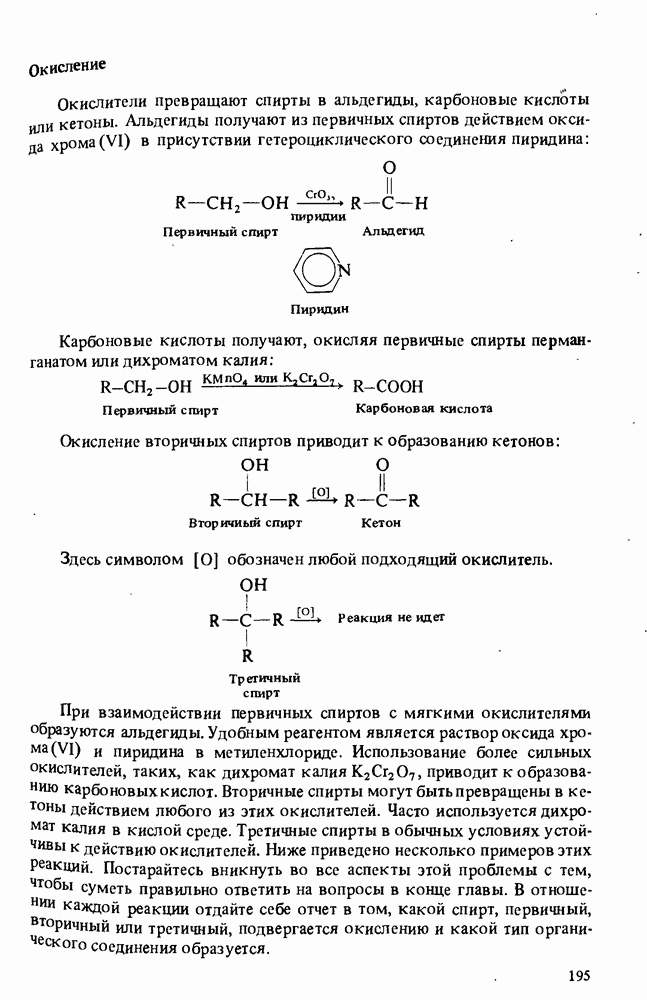
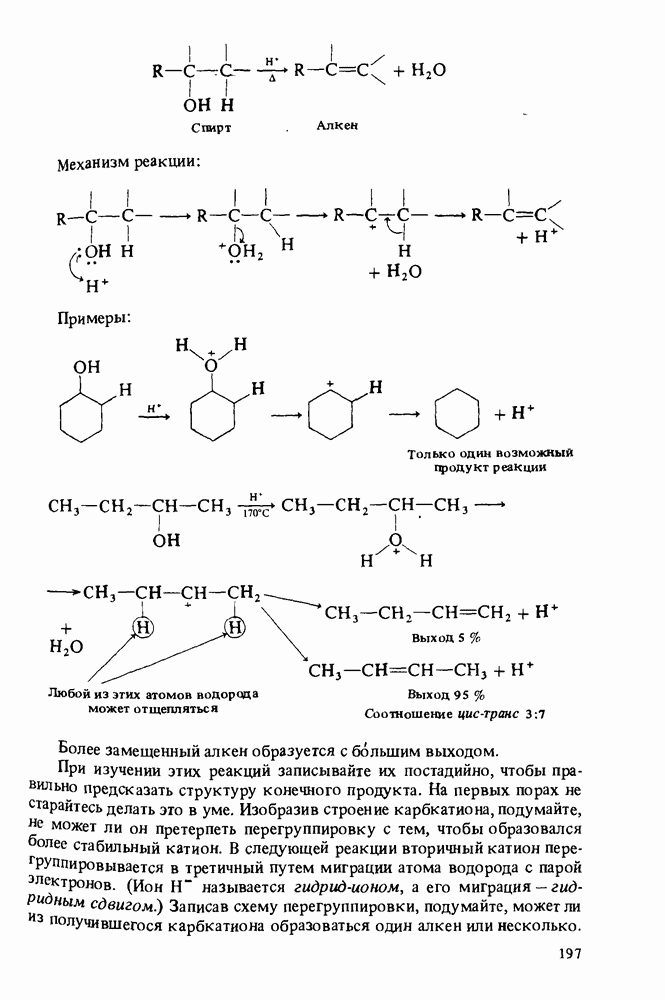
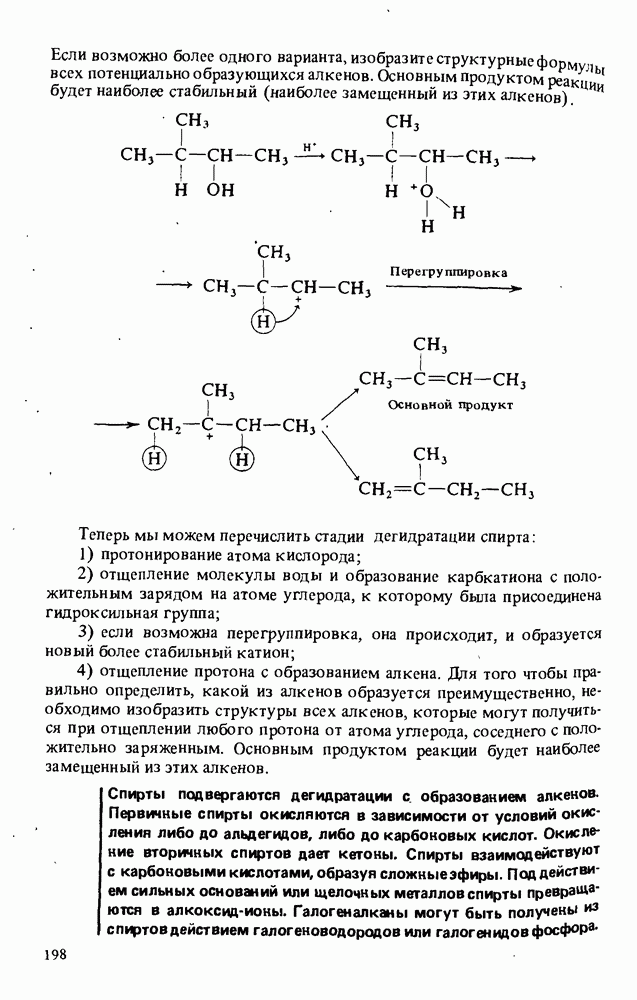
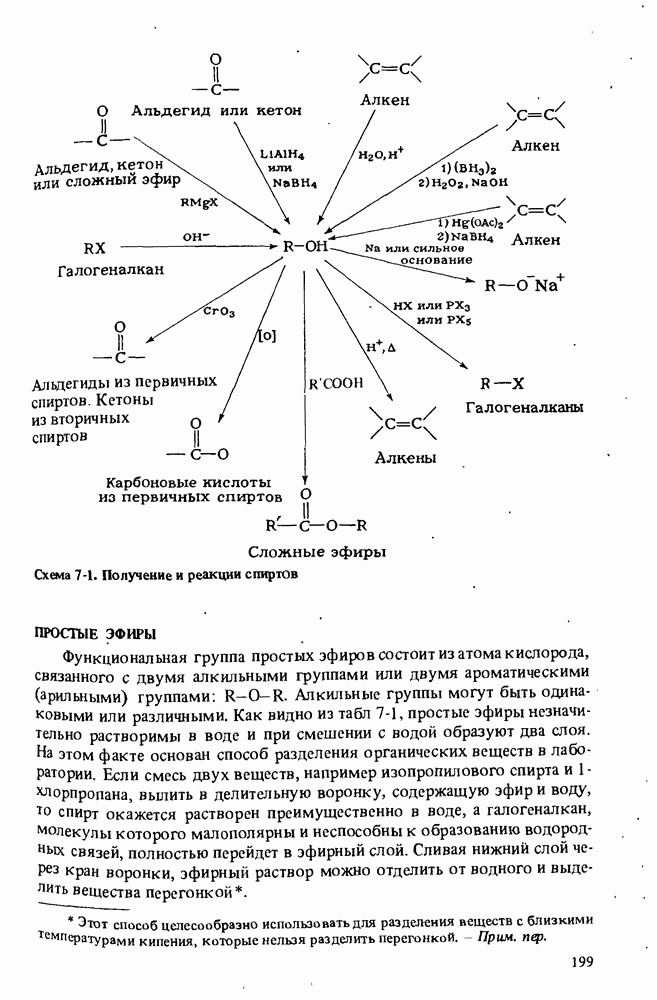
- РЕАКЦИИ СПИРТОВ
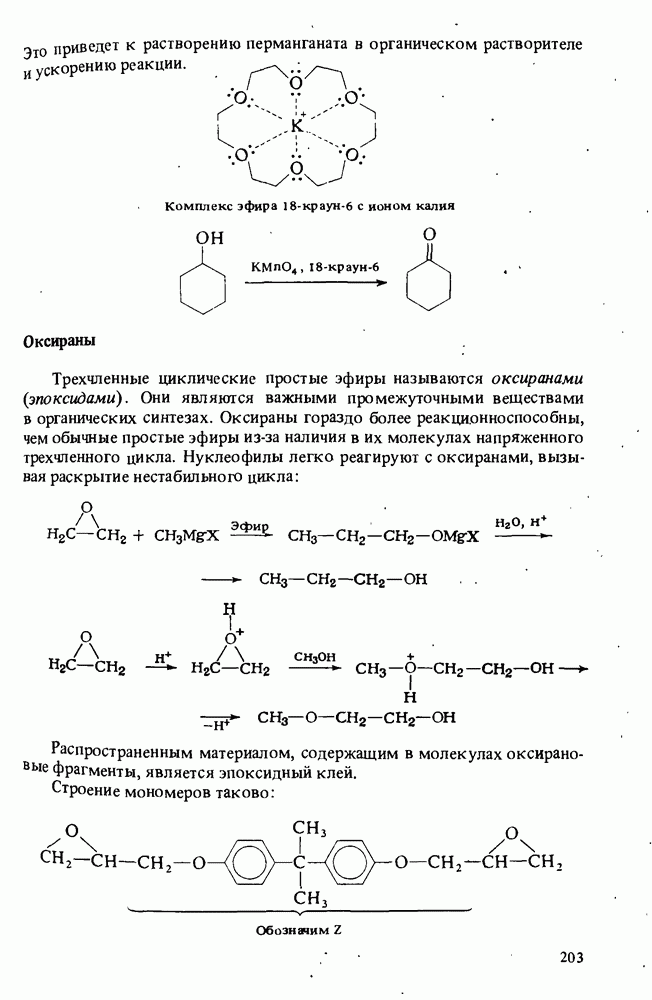
- ПРОСТЫЕ ЭФИРЫ
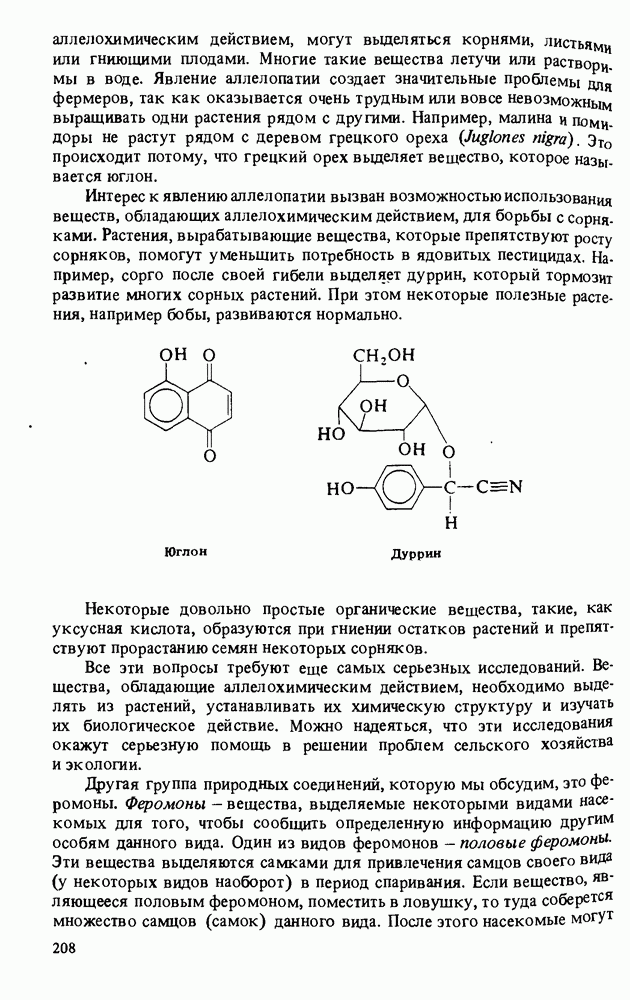
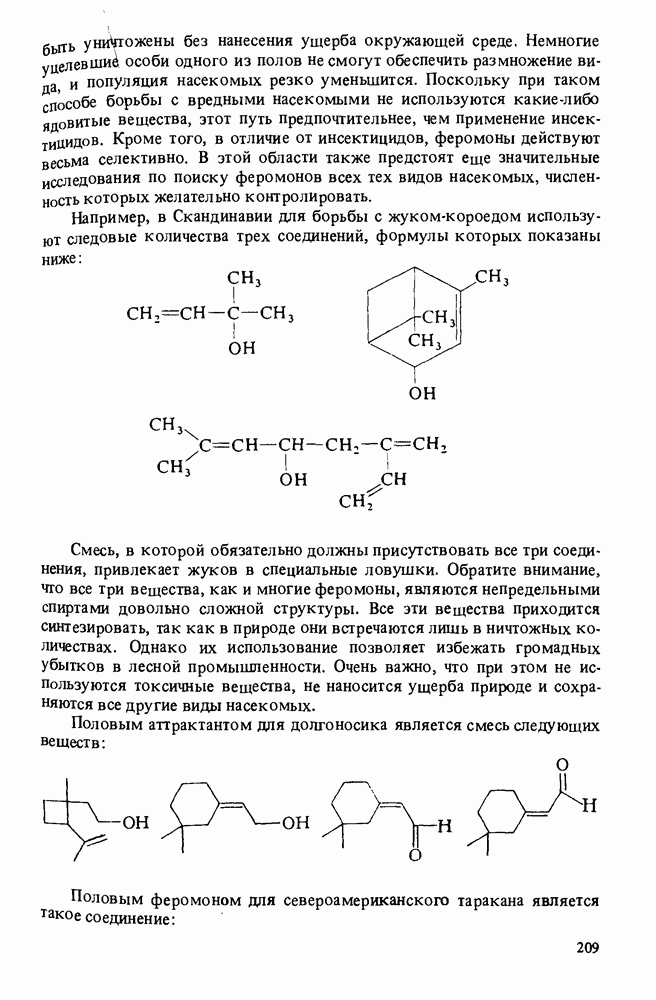
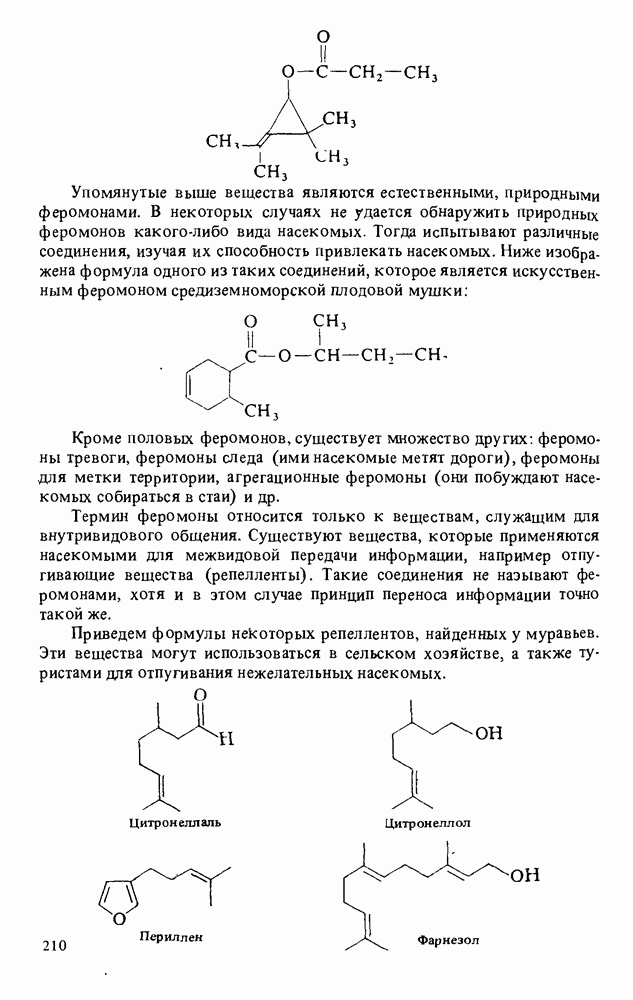
- Прикладная органическая химия: ВЕЩЕСТВА, ОБЛАДАЮЩИЕ АЛЛЕЛОХИМИЧЕСКИМ ДЕЙСТВИЕМ. ФЕРОМОНЫ
- Глава 8. АЛЬДЕГИДЫ И КЕТОНЫ
- ПОЛУЧЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ
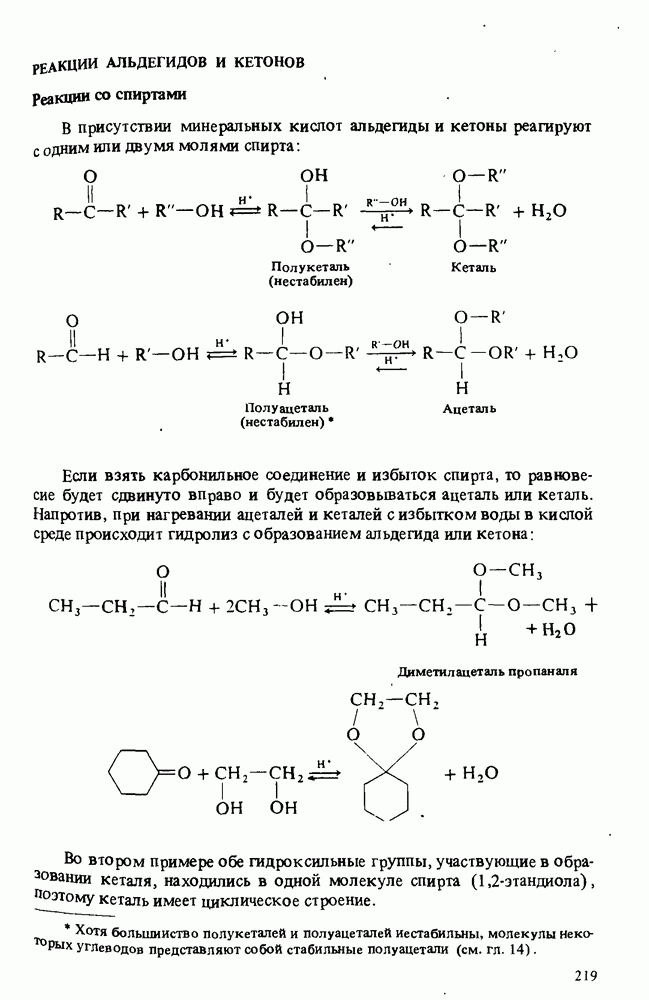
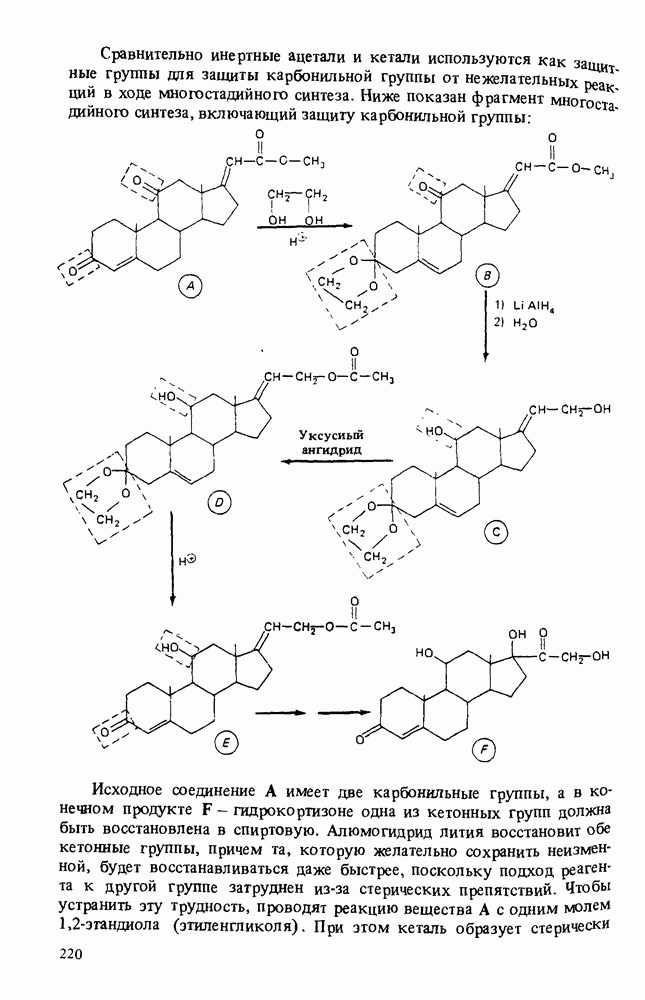
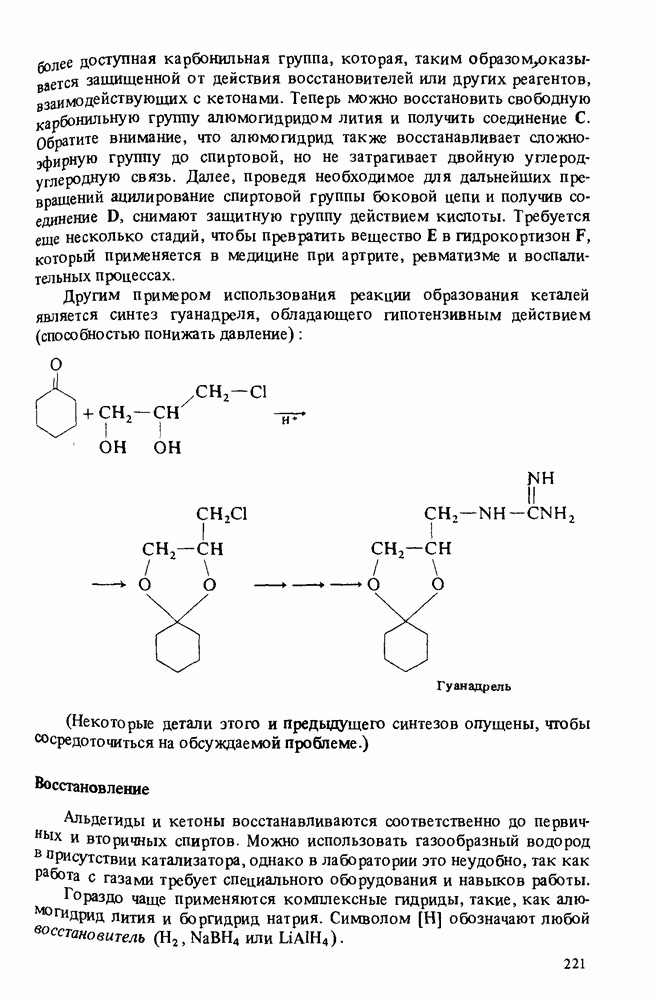
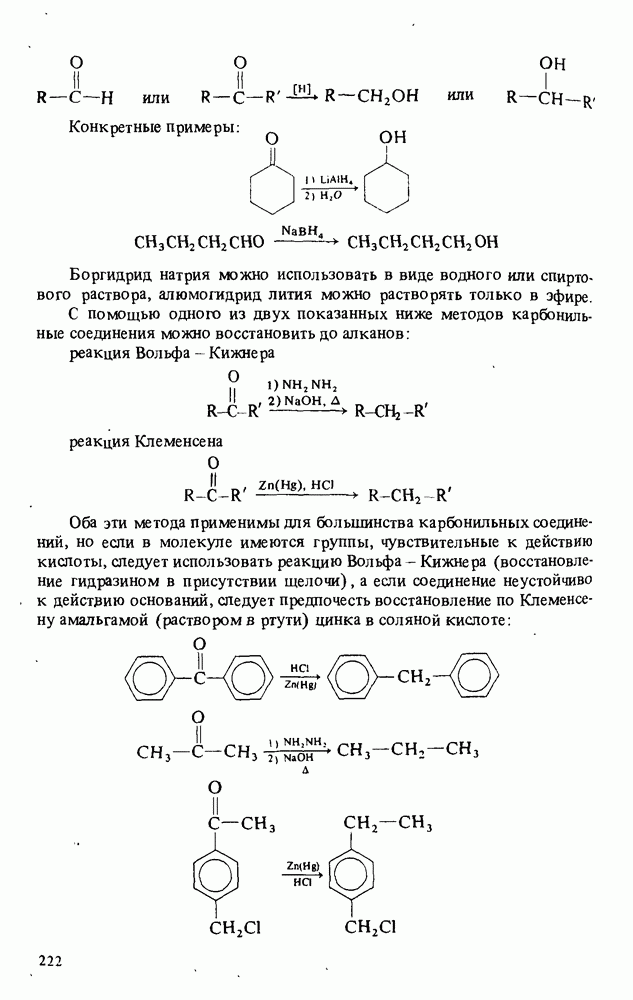
- РЕАКЦИИ АЛЬДЕГИДОВ И КЕТОНОВ
- Глава 9. АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
- НОМЕНКЛАТУРА АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ
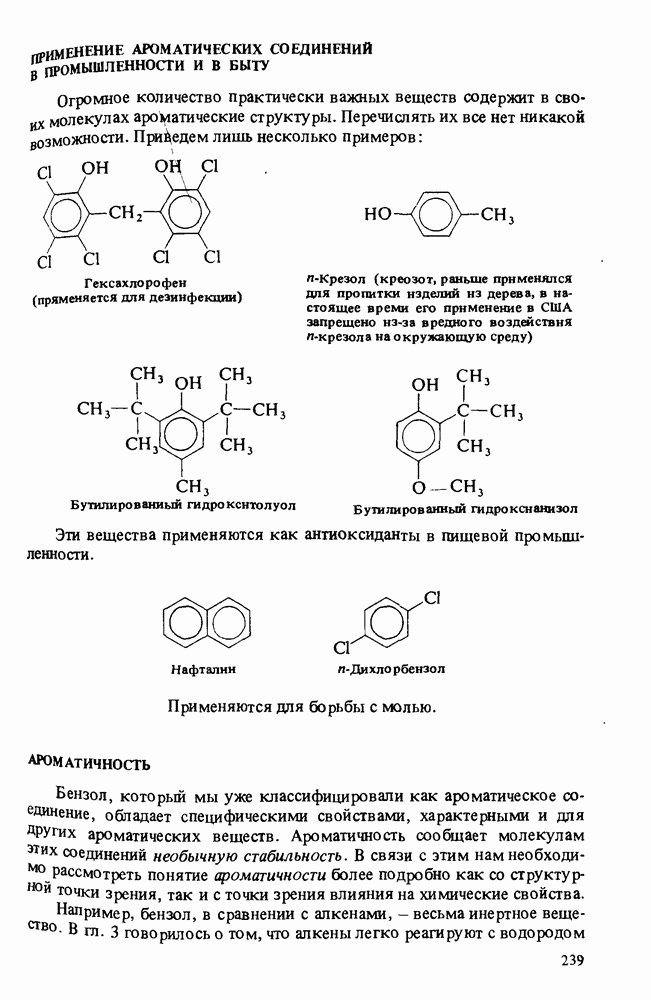
- ПРИМЕНЕНИЕ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ В ПРОМЫШЛЕННОСТИ И В БЫТУ
- АРОМАТИЧНОСТЬ
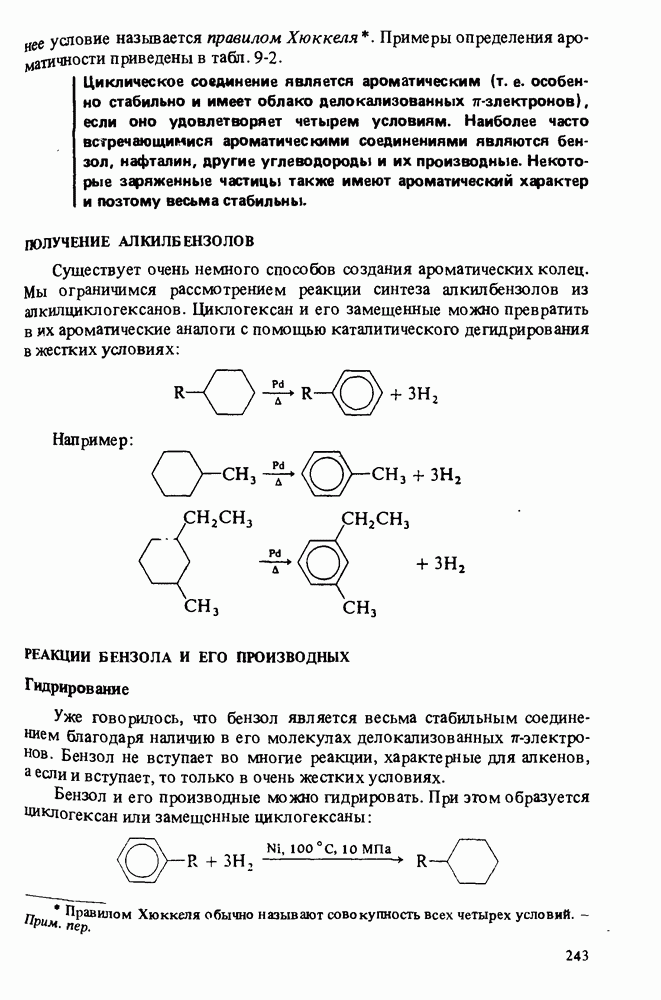
- ПОЛУЧЕНИЕ АЛКИЛЬБЕНЗОЛОВ
- РЕАКЦИИ БЕНЗОЛА И ЕГО ПРОИЗВОДНЫХ
- АРОМАТИЧЕСКОЕ ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ
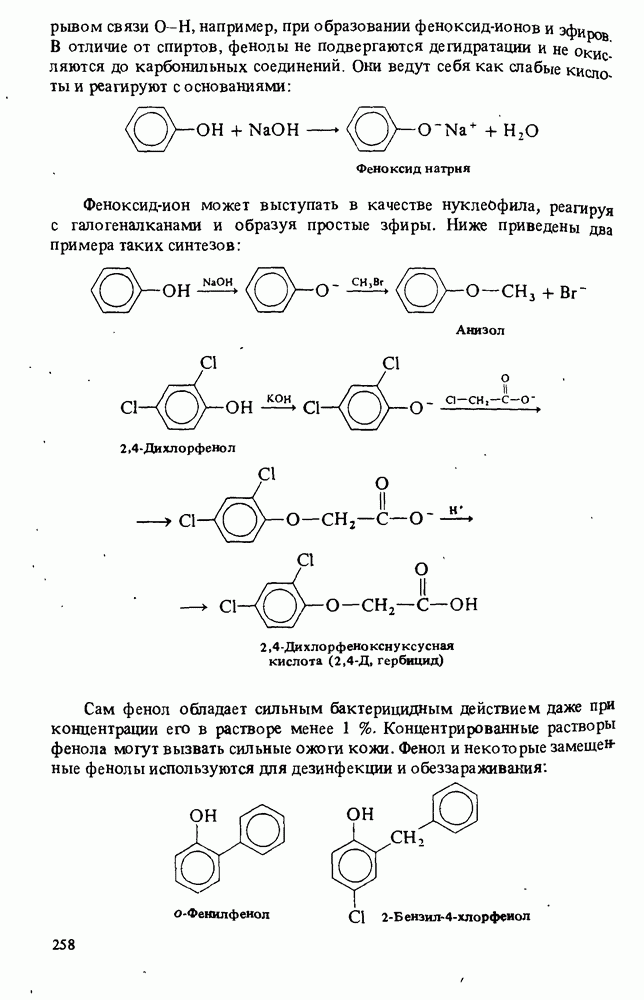
- ФЕНОЛЫ
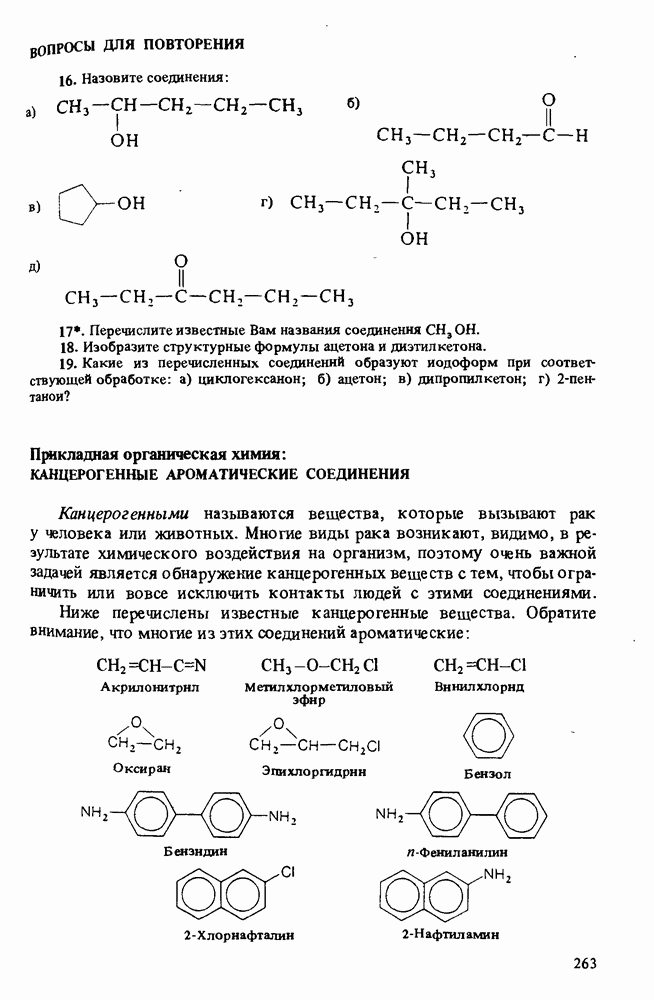
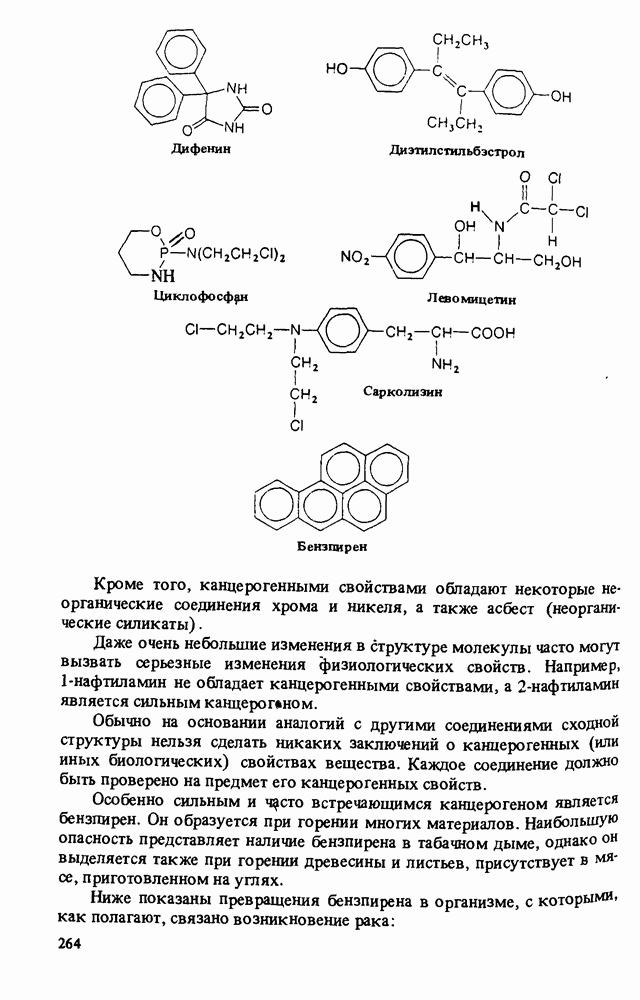
- Прикладная органическая химия: КАНЦЕРОГЕННЫЕ АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
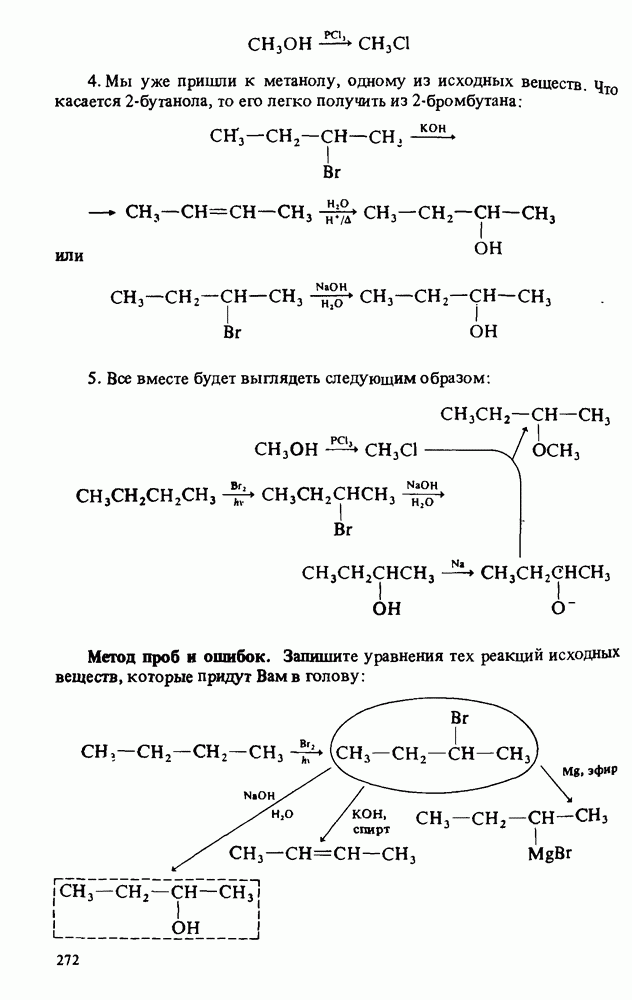
- Глава 10. ОРГАНИЧЕСКИЙ СИНТЕЗ
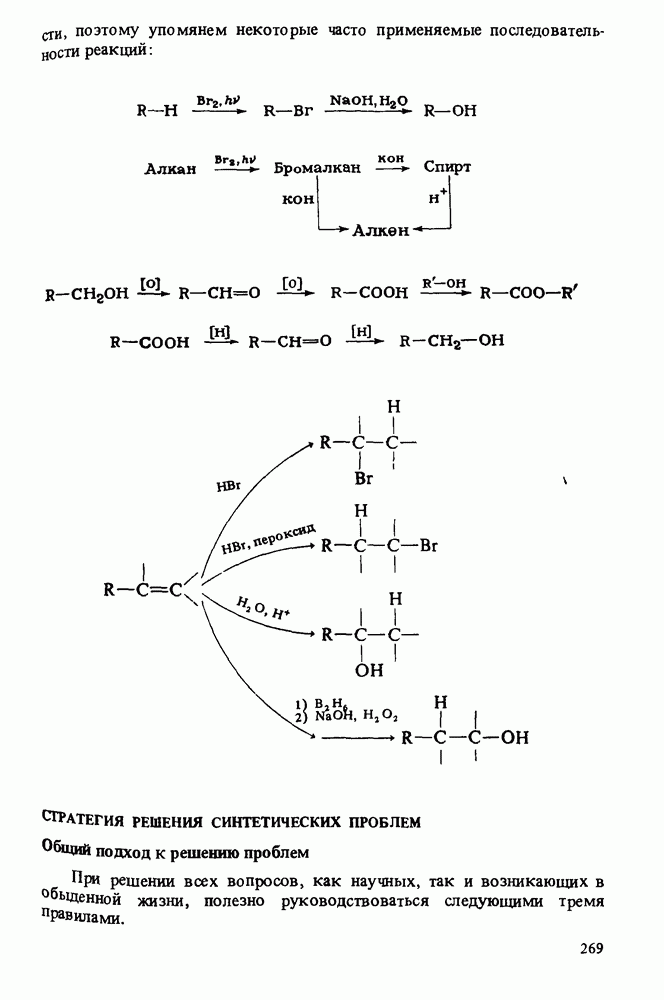
- СТРАТЕГИЯ РЕШЕНИЯ СИНТЕТИЧЕСКИХ ПРОБЛЕМ
- Глава 11. МОЛЕКУЛЯРНАЯ СПЕКТРОСКОПИЯ
- ИНФРАКРАСНАЯ СПЕКТРОСКОПИЯ
- СПЕКТРОСКОПИЯ ЯДЕРНОГО МАГНИТНОГО РЕЗОНАНСА
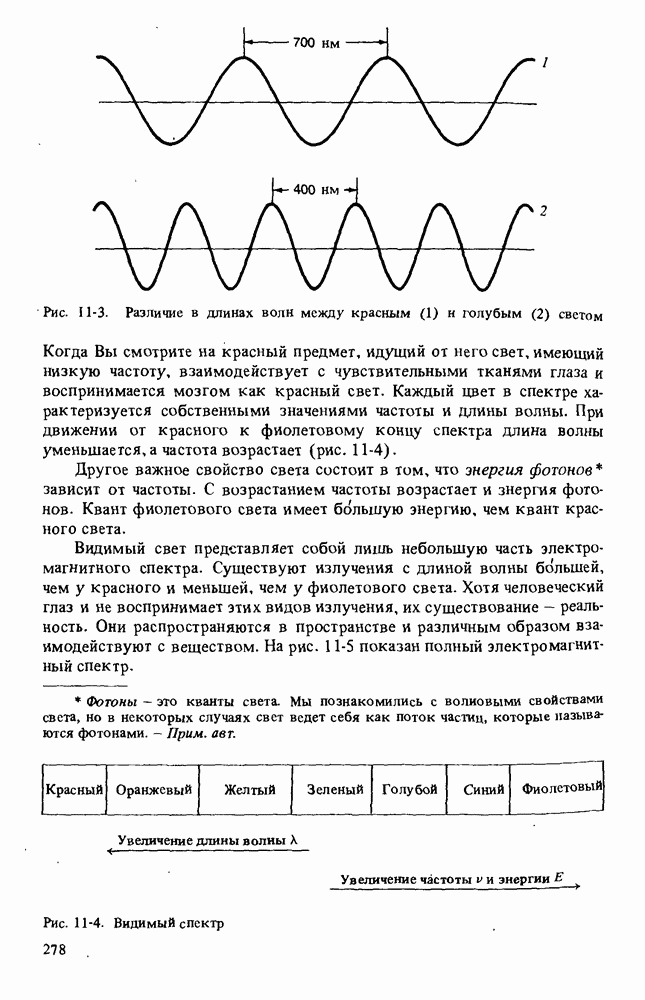
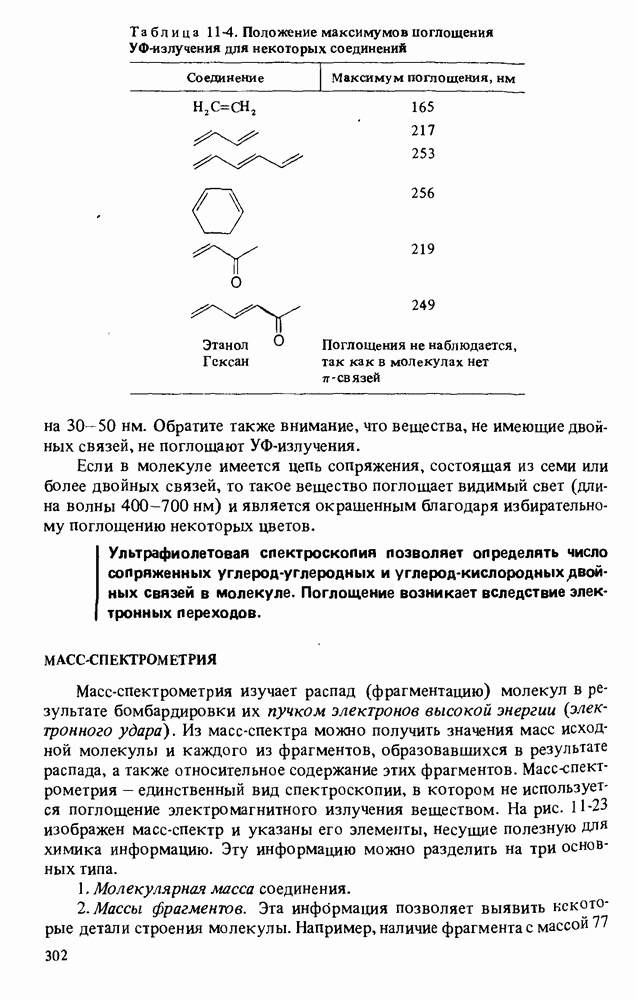
- УЛЬТРАФИОЛЕТОВАЯ СПЕКТРОСКОПИЯ
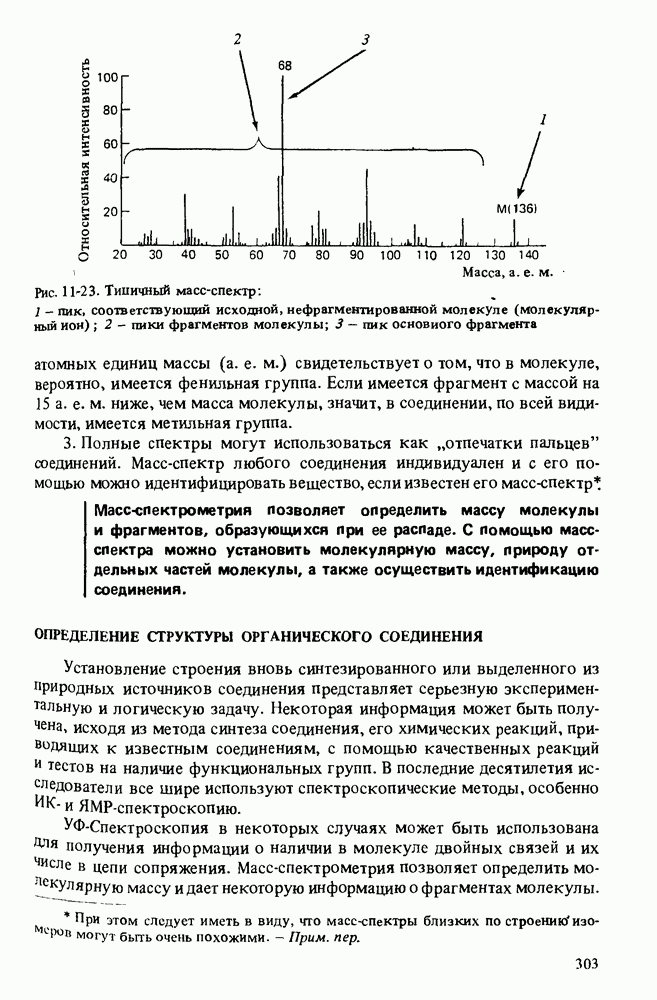
- МАСС-СПЕКТРОМЕТРИЯ
- ОПРЕДЕЛЕНИЕ СТРУКТУРЫ ОРГАНИЧЕСКОГО СОЕДИНЕНИЯ
- Прикладная органическая химия: ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ АЛКОГОЛЯ В КРОВИ
- Глава 12. КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
- ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ
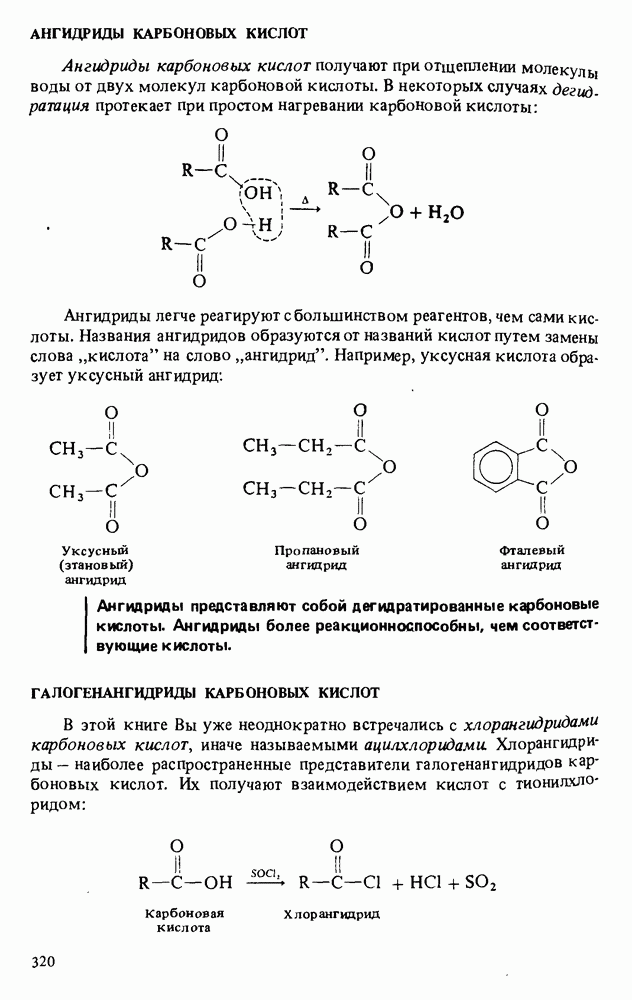
- АНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
- ГАЛОГЕНАНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
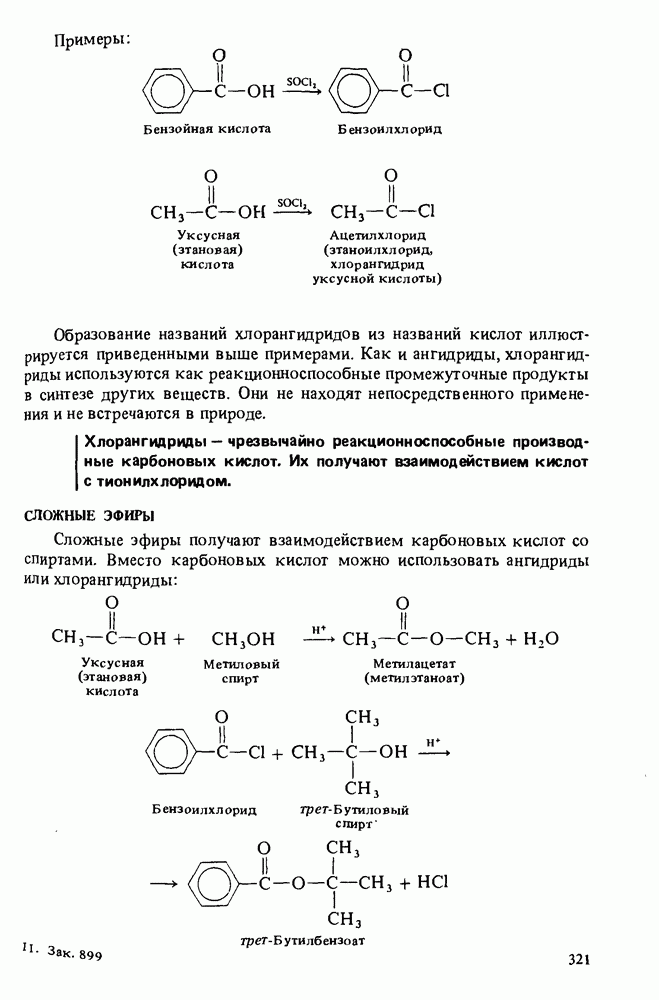
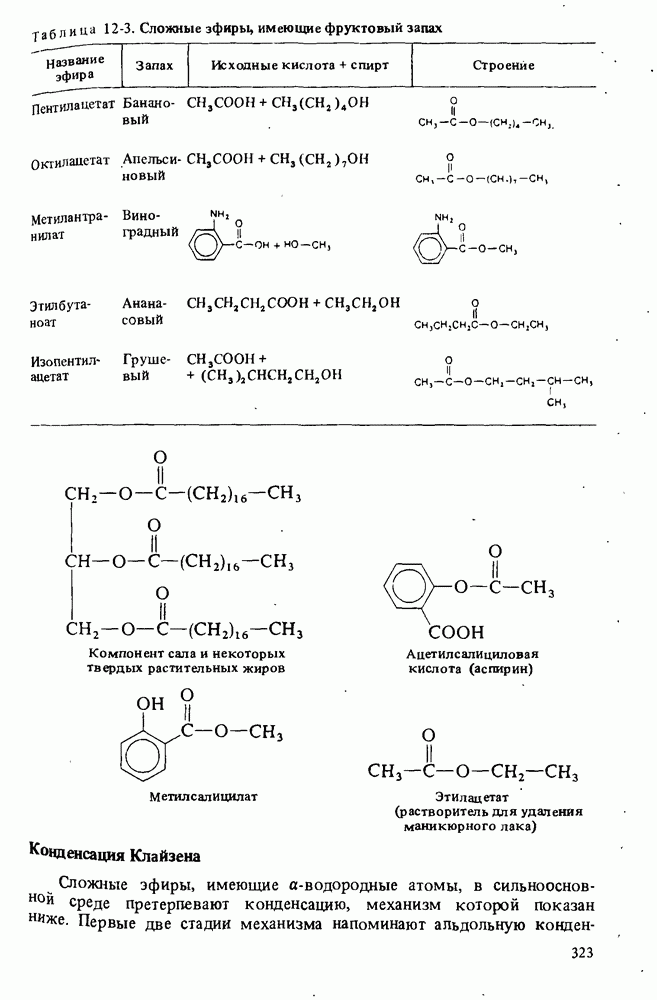
- СЛОЖНЫЕ ЭФИРЫ
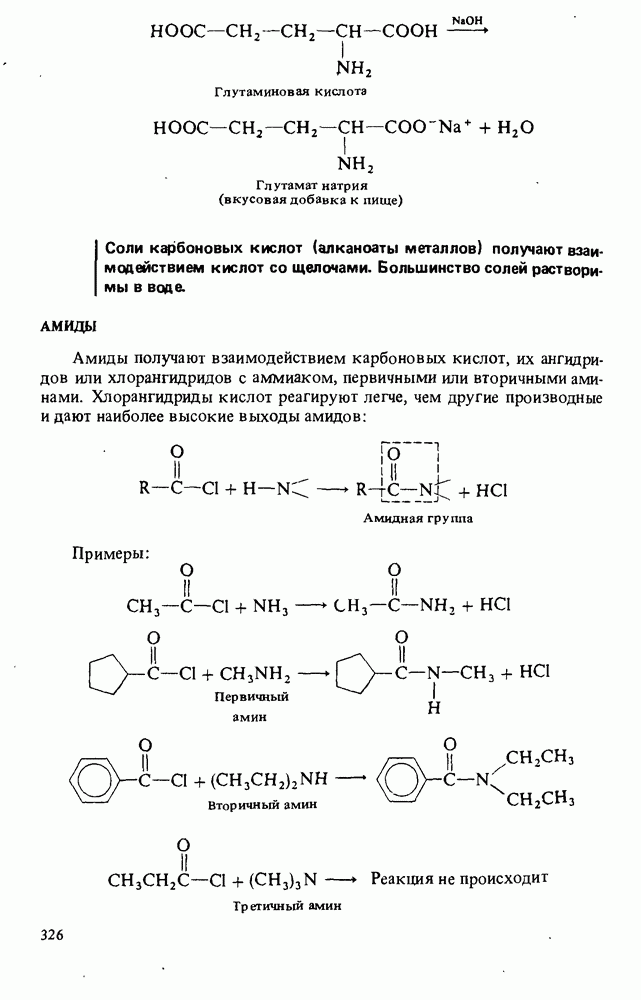
- СОЛИ
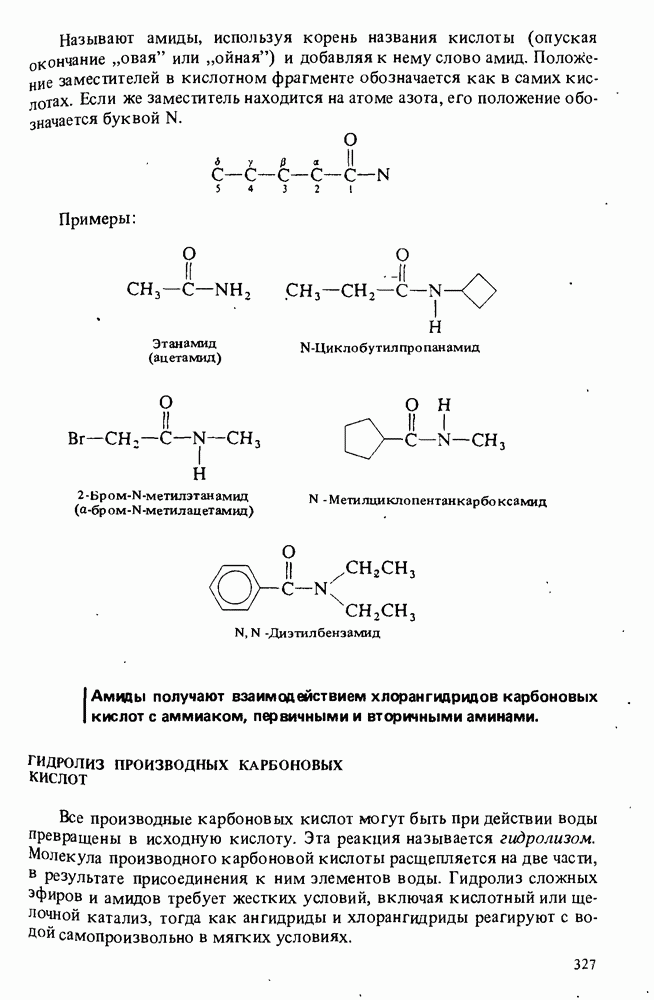
- АМИДЫ
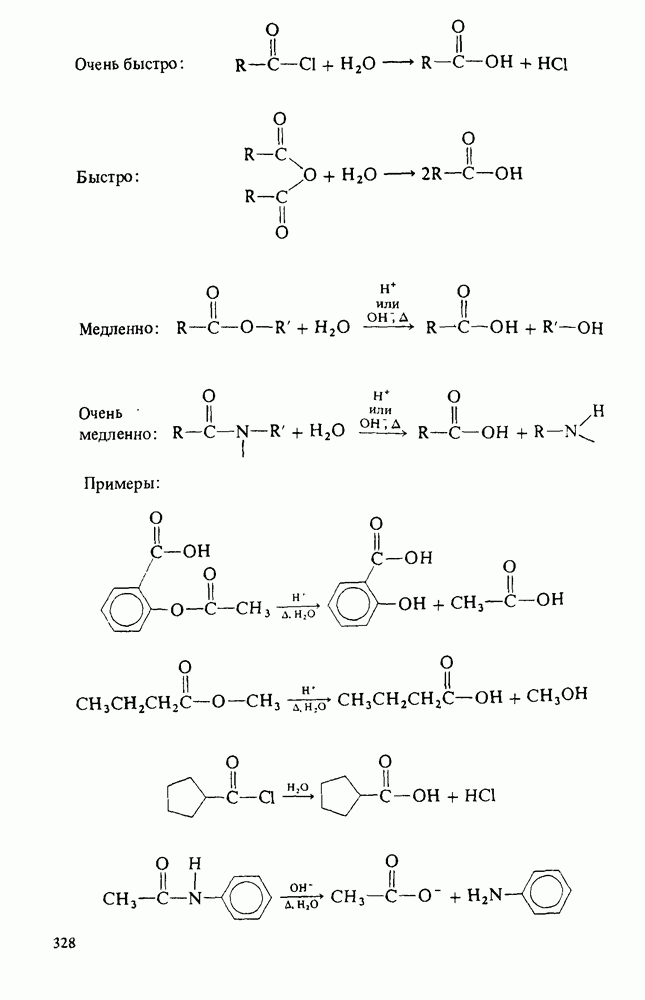
- ГИДРОЛИЗ ПРОИЗВОДНЫХ КАРБОНОВЫХ КИСЛОТ
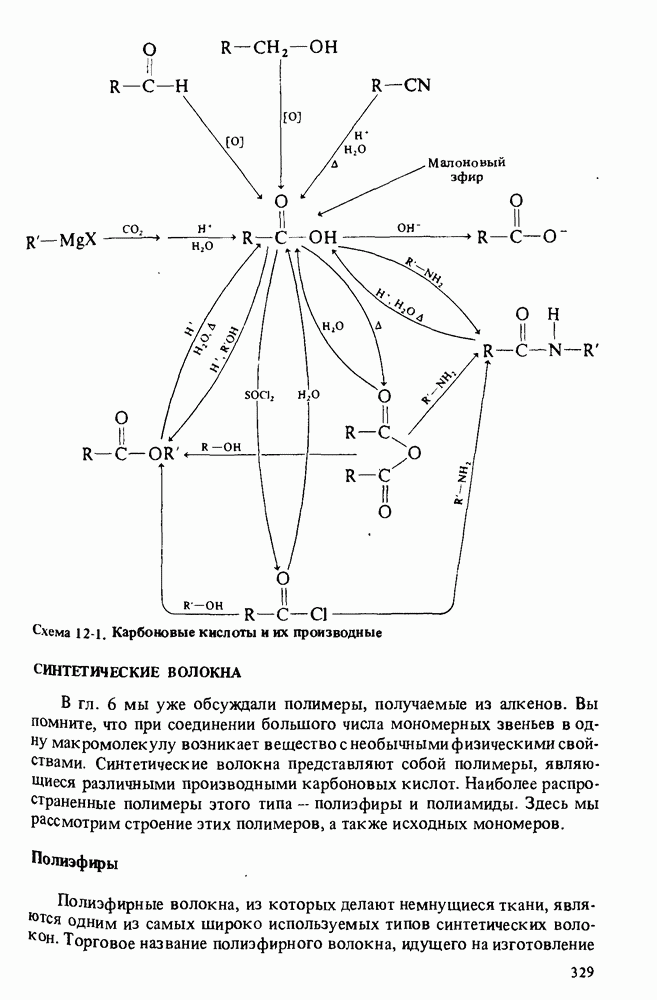
- СИНТЕТИЧЕСКИЕ ВОЛОКНА
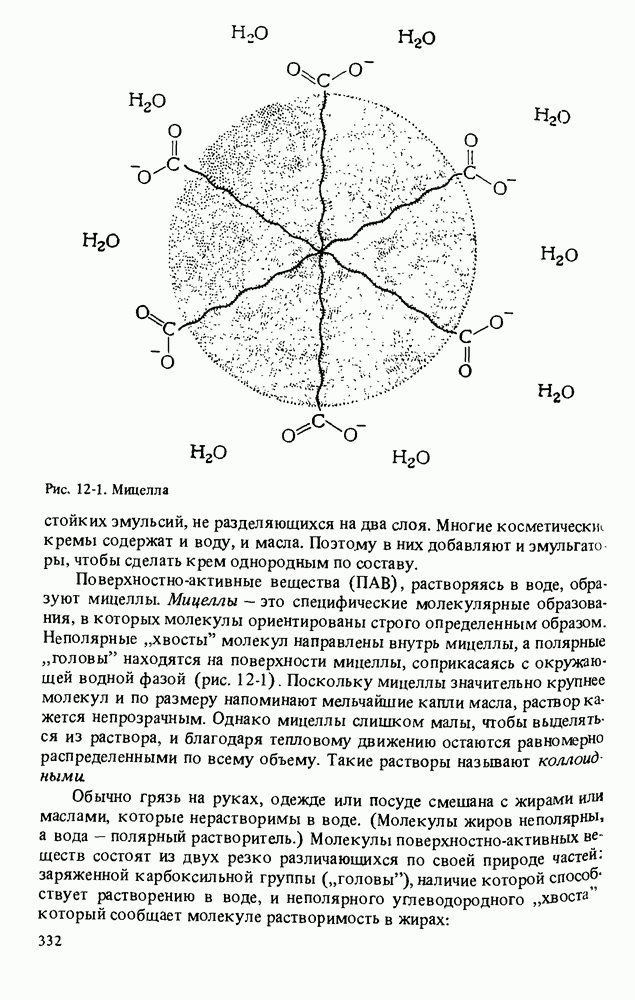
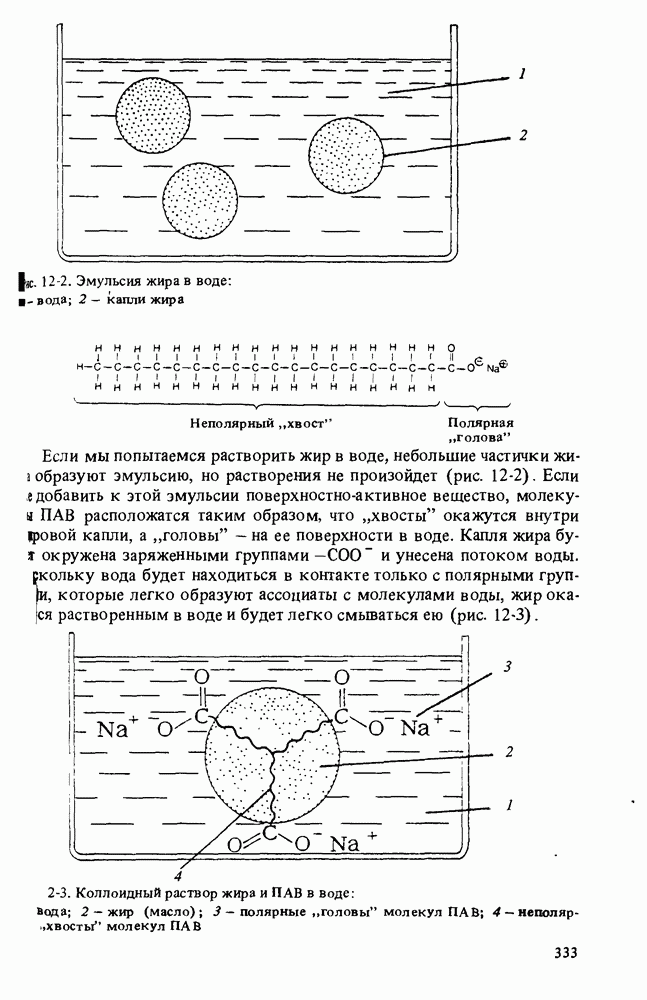
- МОЮЩИЕ СРЕДСТВА
- Прикладная органическая химия: СВОЙСТВА ВОЛОКОН
- Глава 13. АМИНЫ
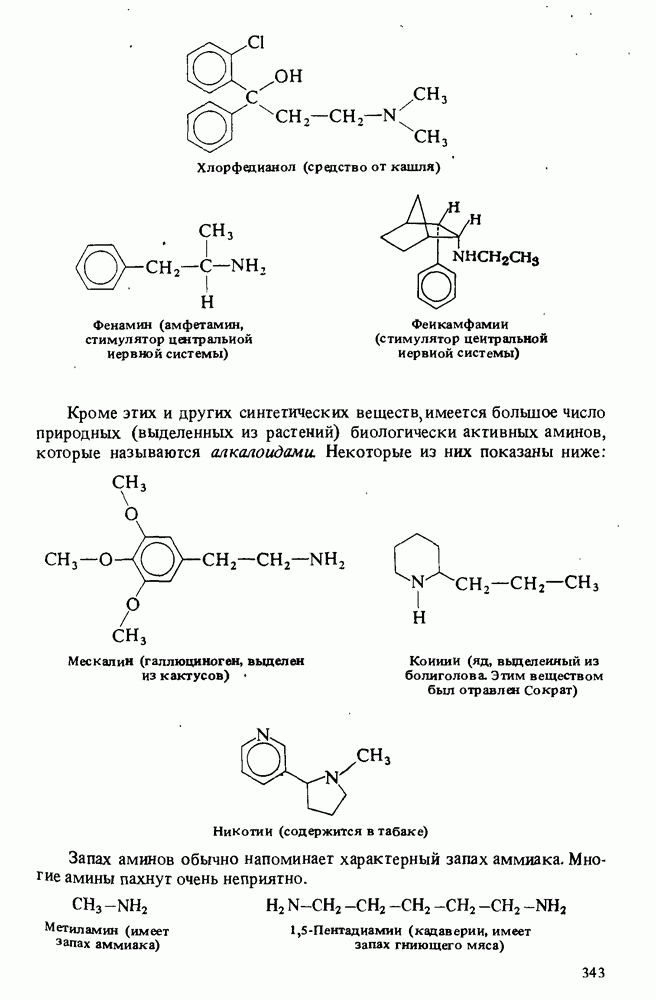
- БИОЛОГИЧЕСКИ АКТИВНЫЕ АМИНЫ
- ОСНОВНОСТЬ АМИНОВ
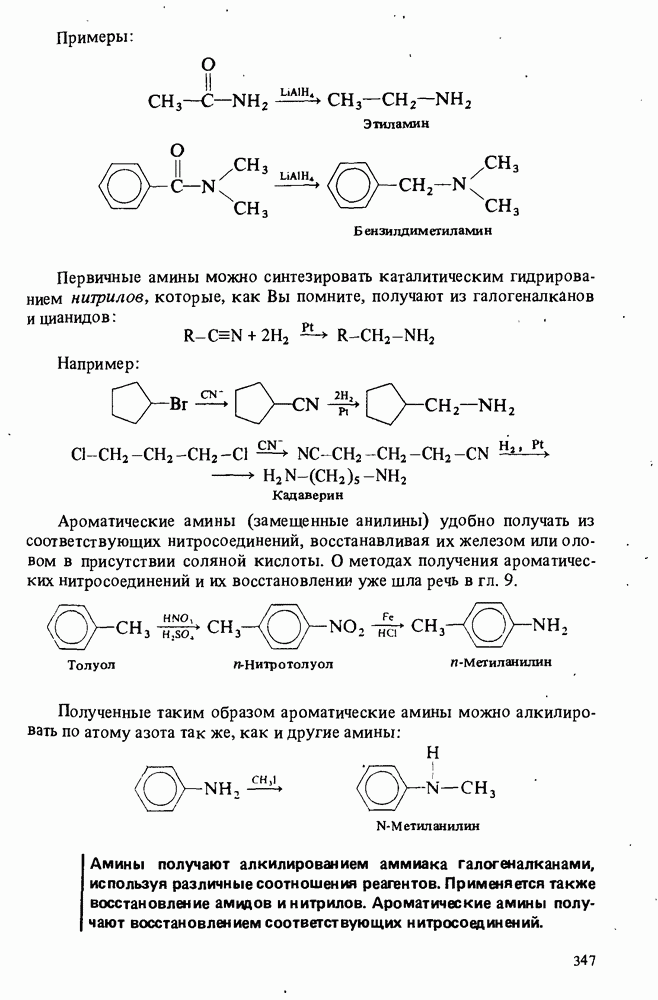
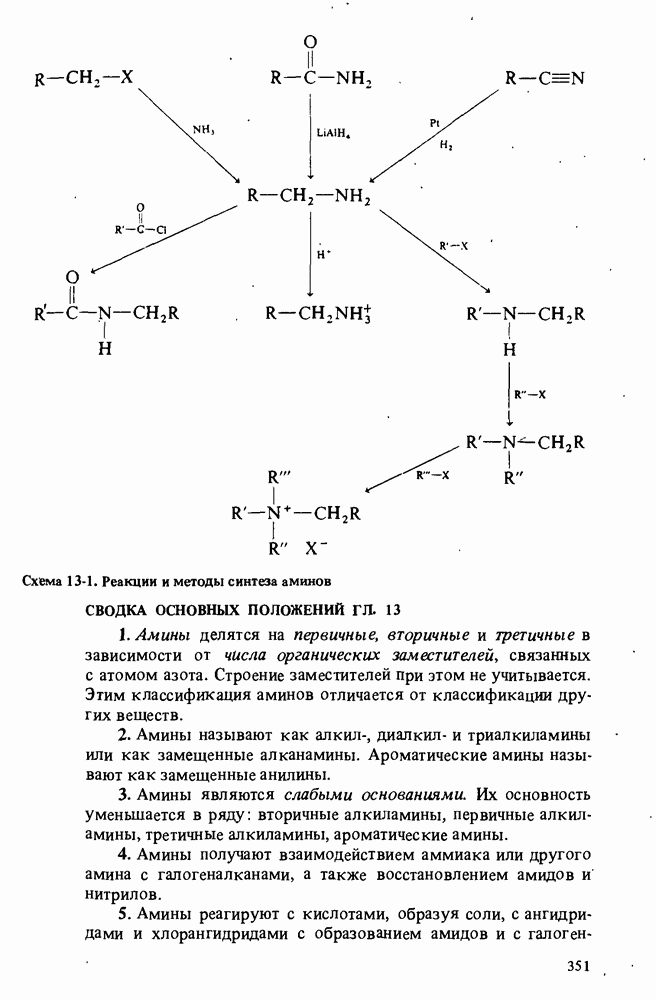
- ПОЛУЧЕНИЕ АМИНОВ
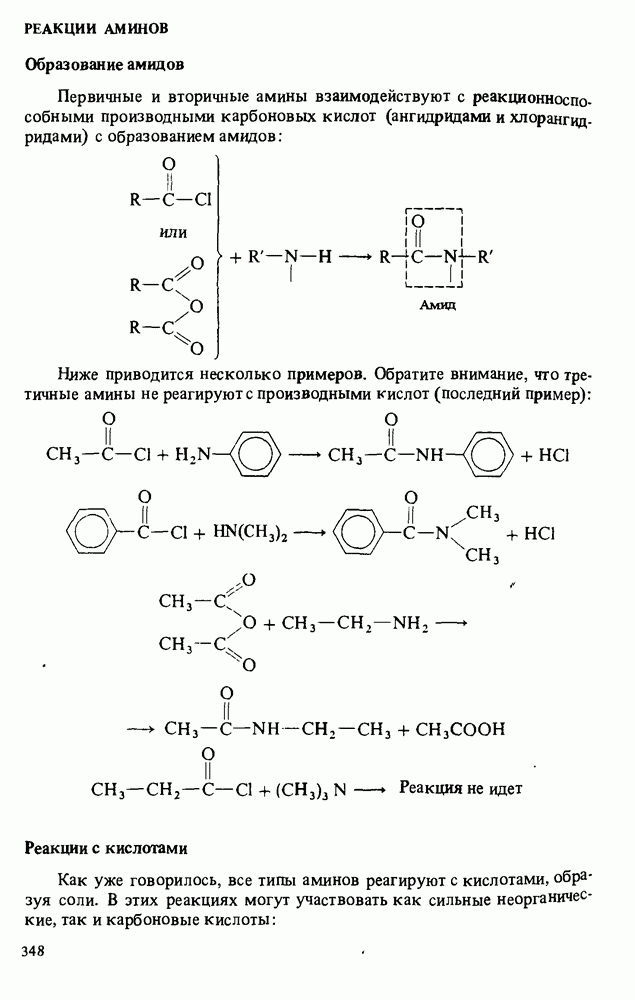
- РЕАКЦИИ АМИНОВ
- Прикладная органическая химия: ПОЛИМЕРЫ, ПОДВЕРГАЮЩИЕСЯ БИОЛОГИЧЕСКОЙ ДЕСТРУКЦИИ
- Глава 14. УГЛЕВОДЫ
- МОНОСАХАРИДЫ
- РЕАКЦИИ МОНОСАХАРИДОВ
- СИНТЕЗЫ САХАРОВ
- ДИСАХАРИДЫ
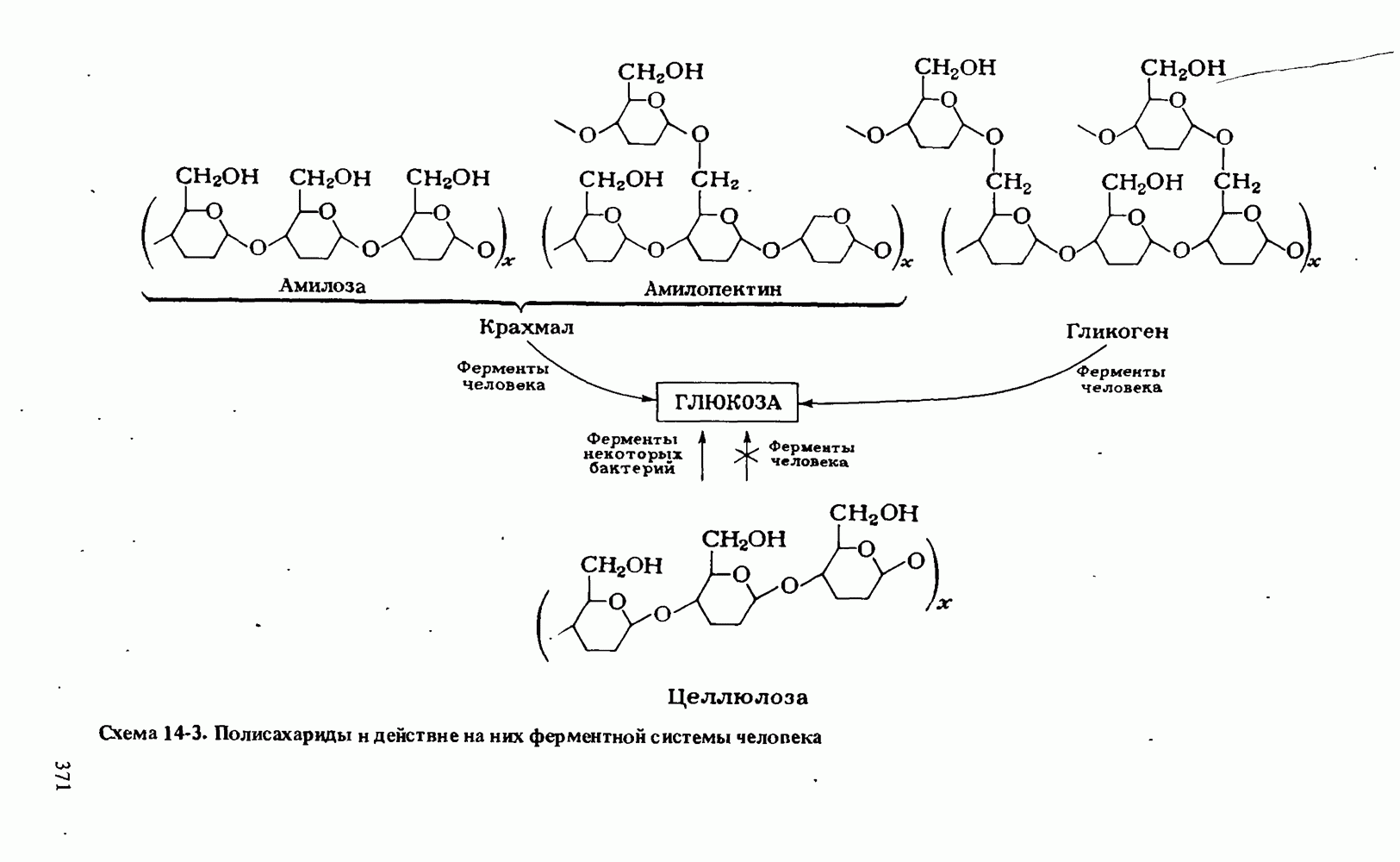
- ПОЛИСАХАРИДЫ
- Прикладная органическая химия: ПИЩЕВЫЕ СВОЙСТВА УГЛЕВОДОВ
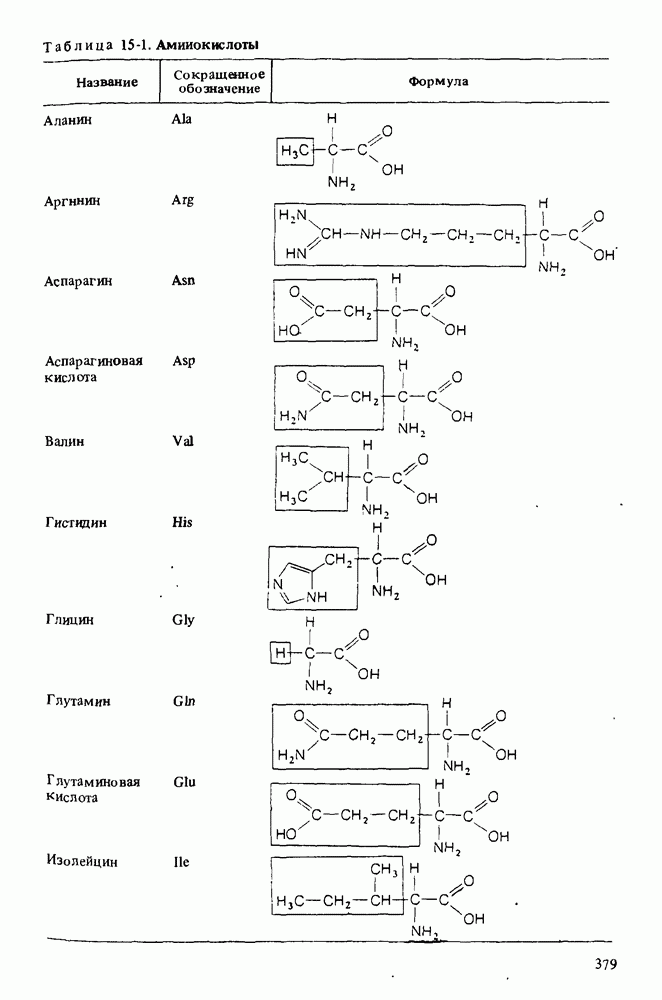
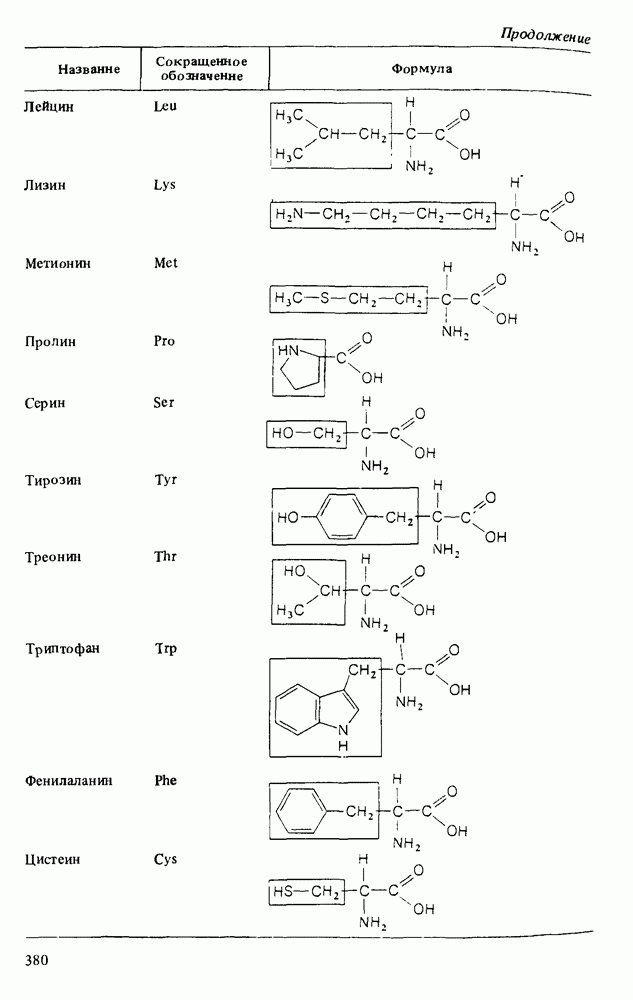
- Глава 15. АМИНОКИСЛОТЫ И БЕЛКИ
- КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА АМИНОКИСЛОТ
- АНАЛИЗ АМИНОКИСЛОТ
- СТРОЕНИЕ БЕЛКОВ
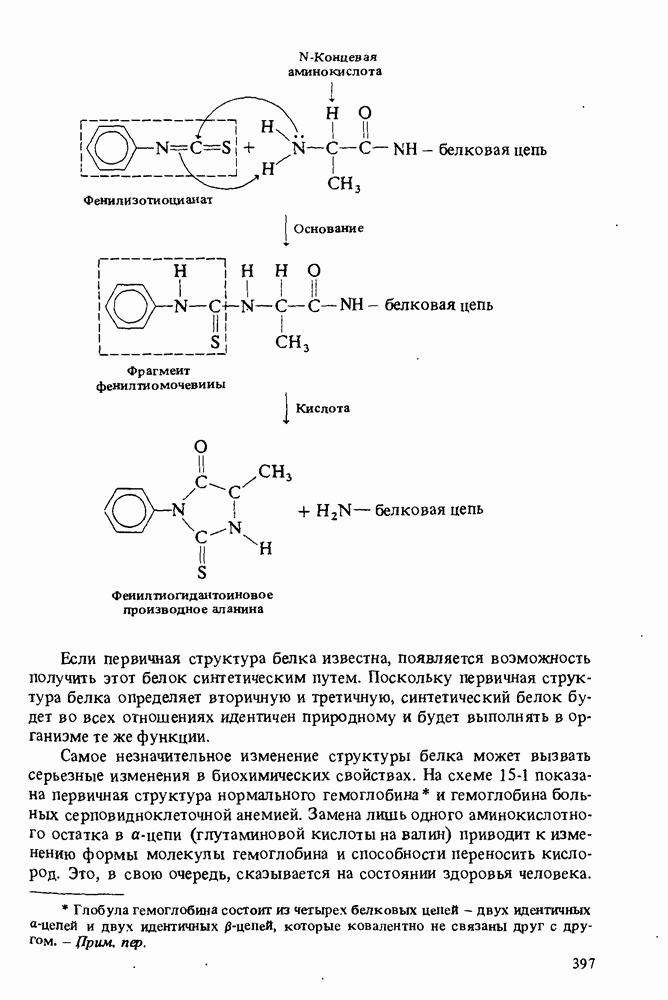
- УСТАНОВЛЕНИЕ ПЕРВИЧНОЙ СТРУКТУРЫ БЕЛКОВ
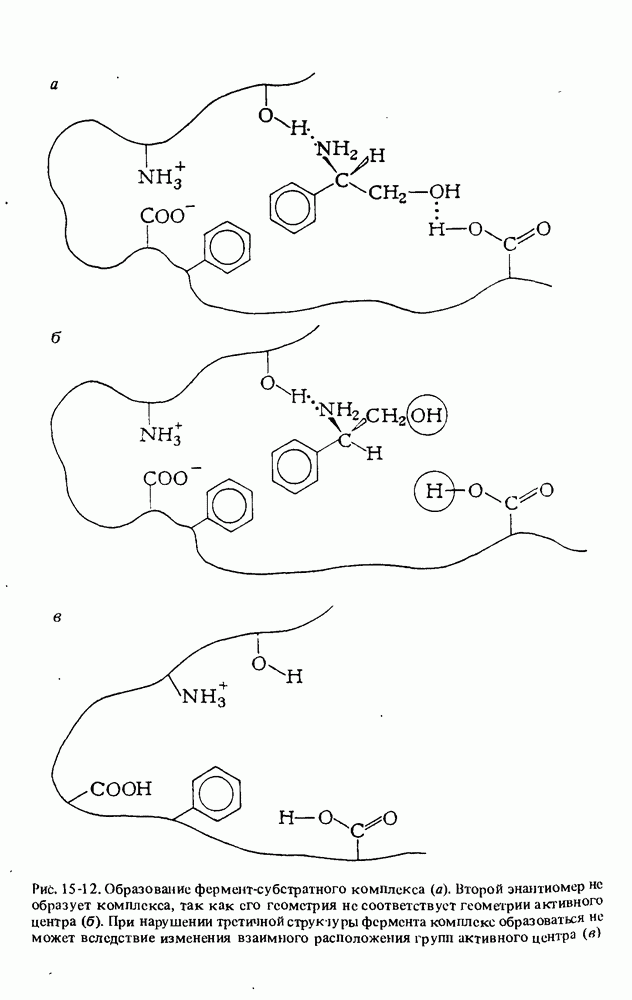
- ФЕРМЕНТЫ
- Глава 16. ЛИПИДЫ
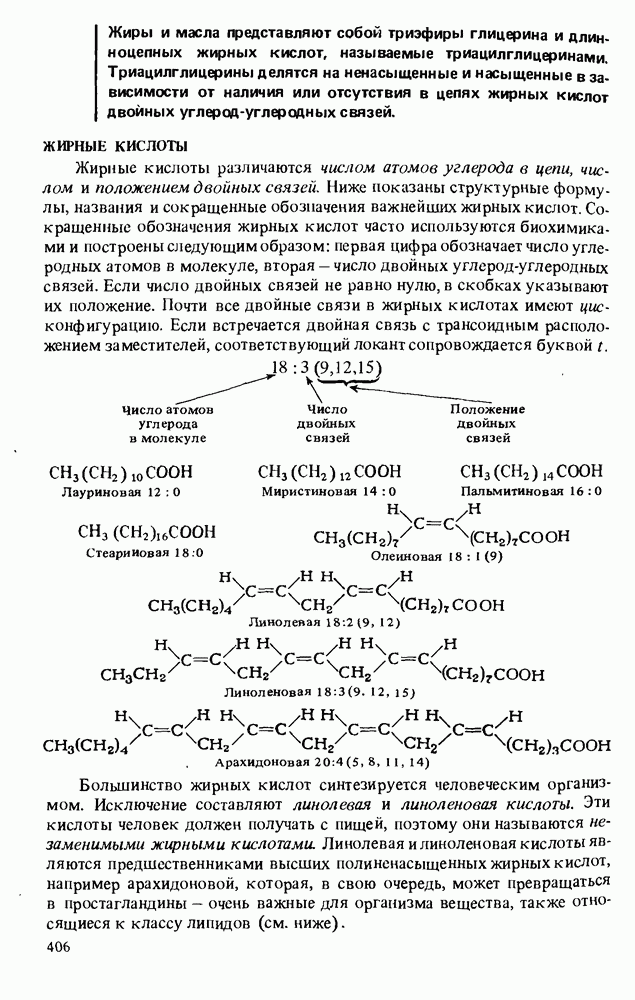
- ЖИРНЫЕ КИСЛОТЫ
- НАЗВАНИЯ ТРИАЦИЛГЛИЦЕРИНОВ
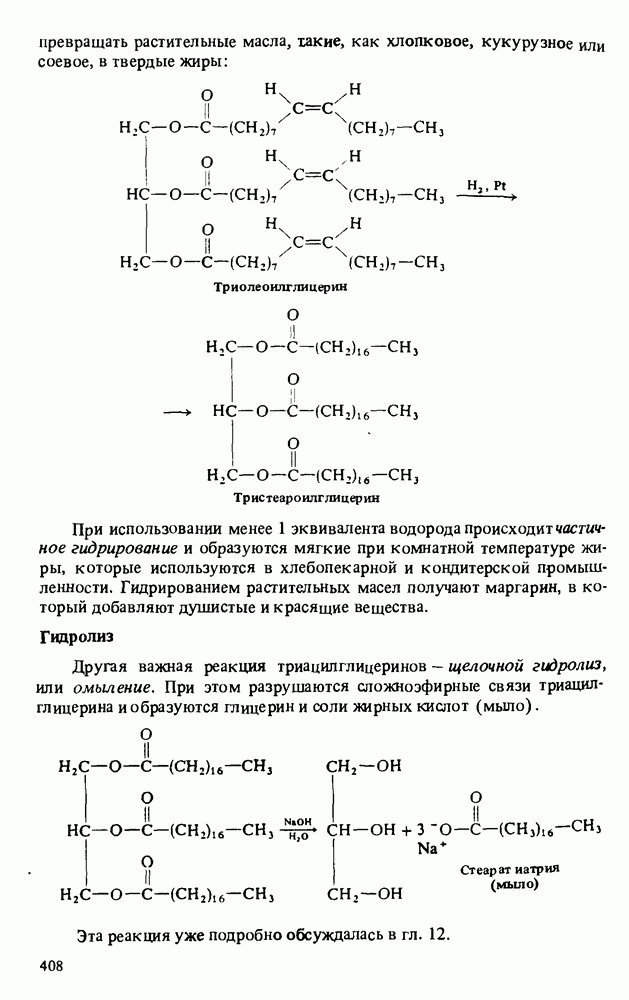
- РЕАКЦИИ ТРИАЦИЛГЛИЦЕРИНОВ
- ЛИПИДЫ, ОТЛИЧНЫЕ ОТ ТРИАЦИЛГЛИЦЕРИНОВ
- Прикладная органическая химия: ПИЩЕВЫЕ СВОЙСТВА ЛИПИДОВ
- Глава 17. НУКЛЕИНОВЫЕ КИСЛОТЫ
- РИБОНУКЛЕИНОВЫЕ КИСЛОТЫ
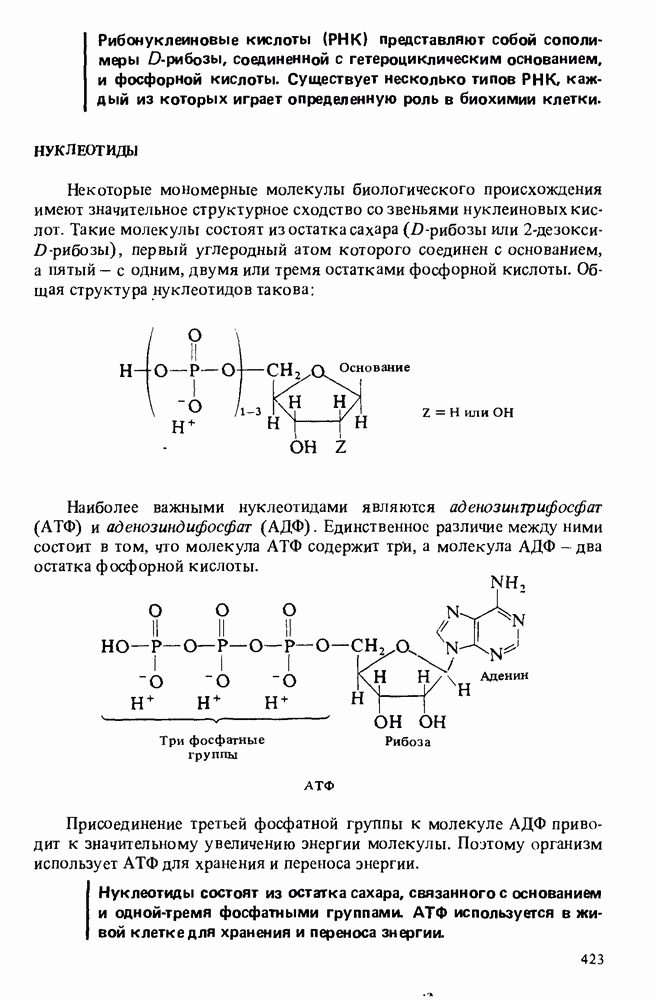
- НУКЛЕОТИДЫ
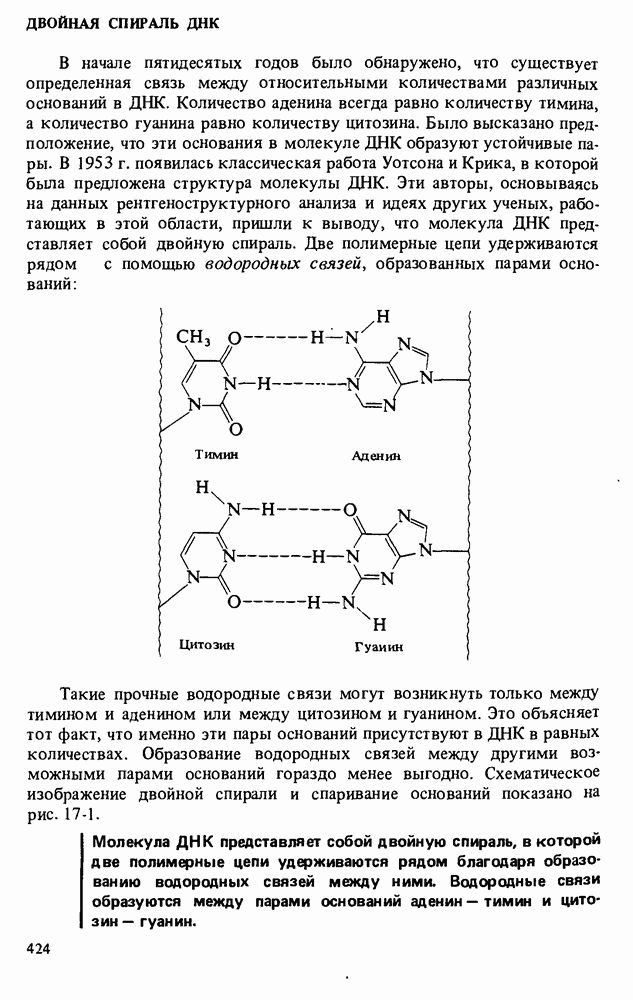
- ДВОЙНАЯ СПИРАЛЬ ДНК
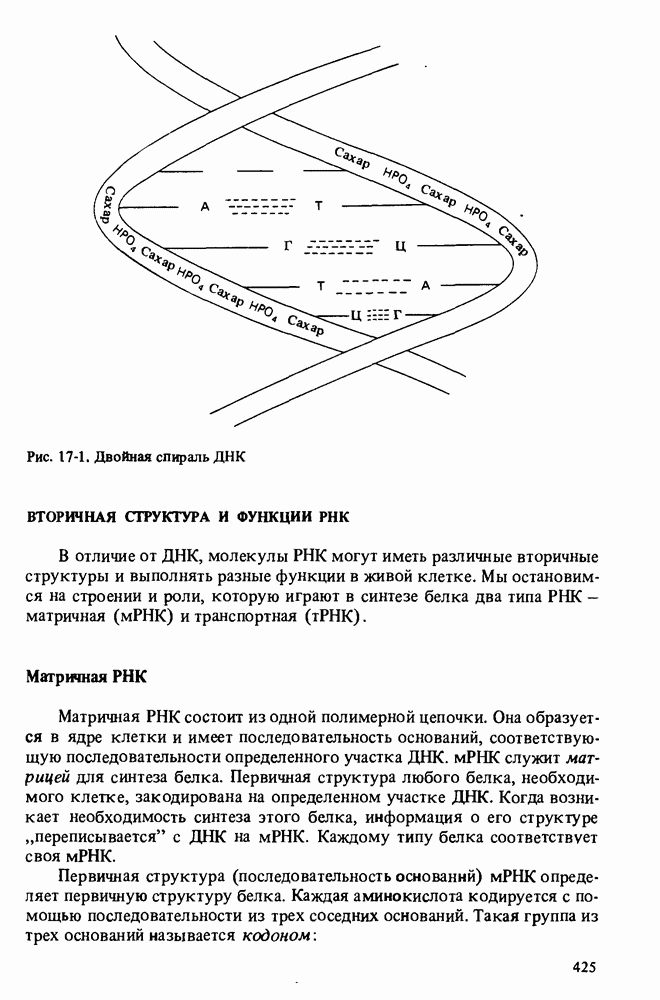
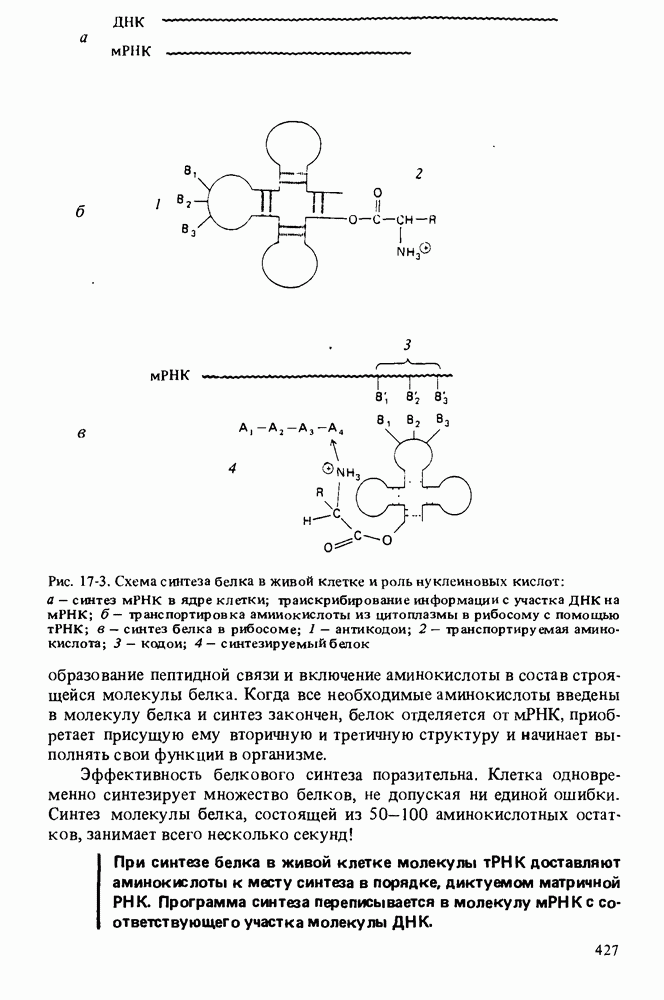
- ВТОРИЧНАЯ СТРУКТУРА И ФУНКЦИИ РНК
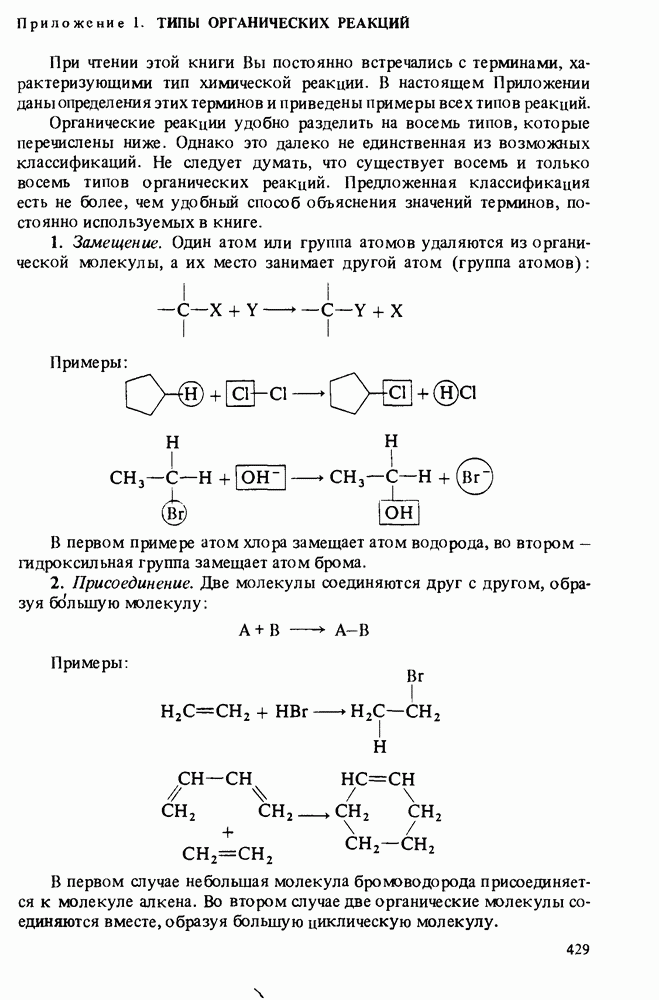
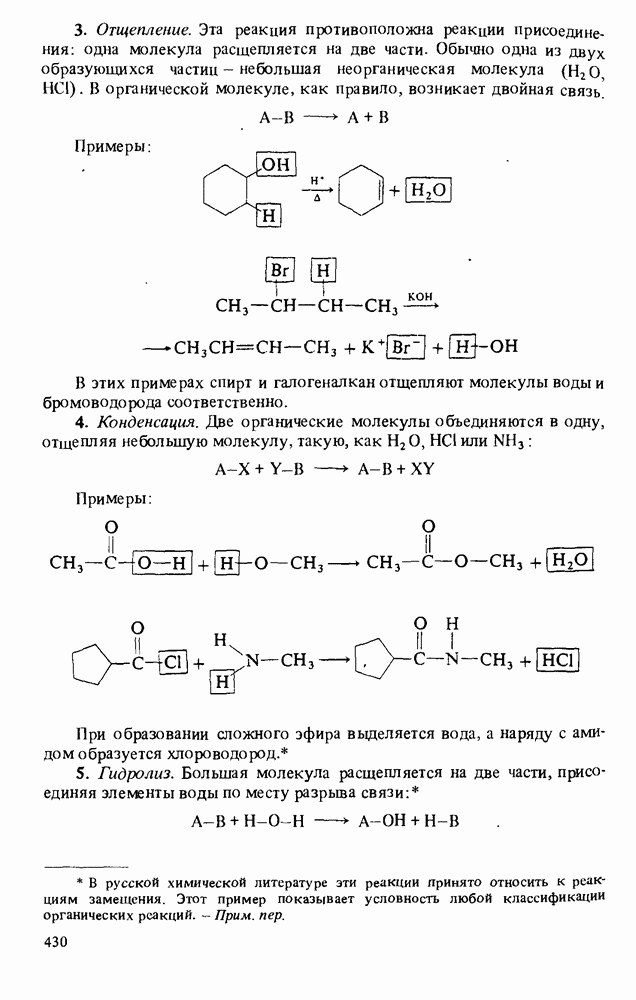
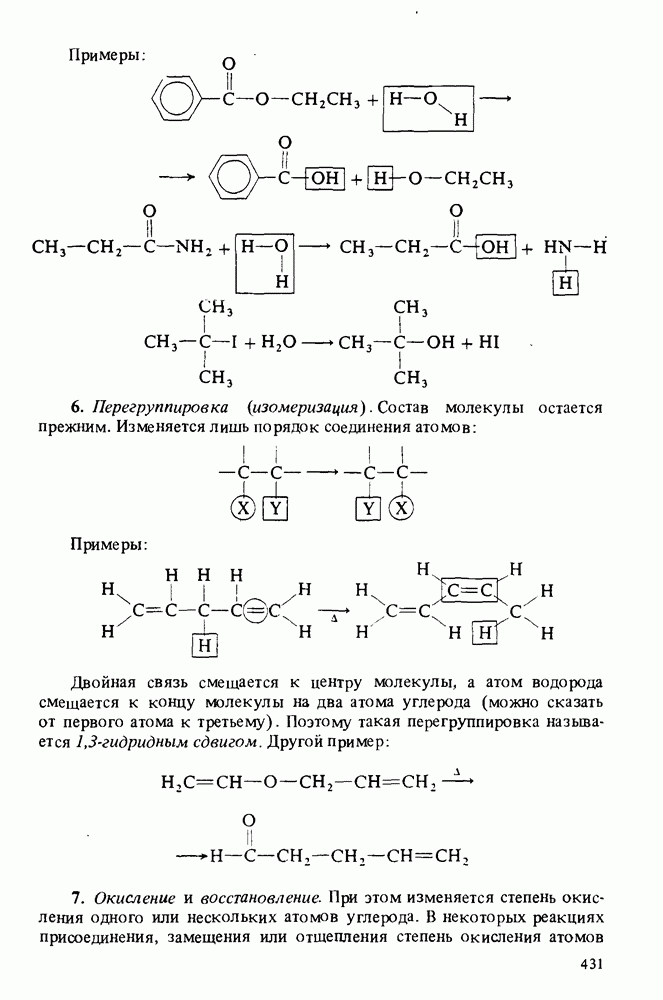
- Приложение 1. ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ
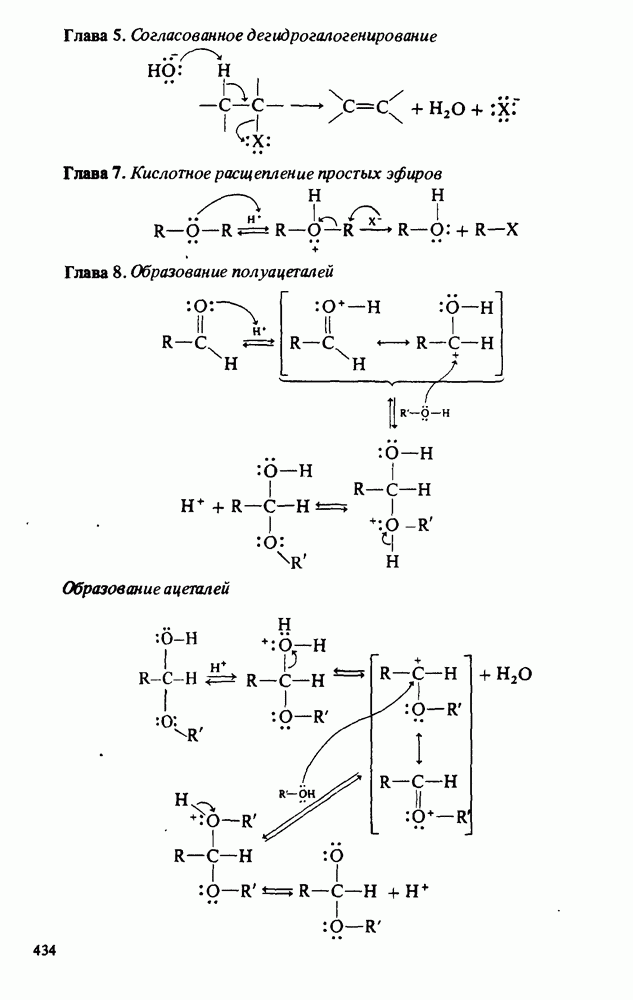
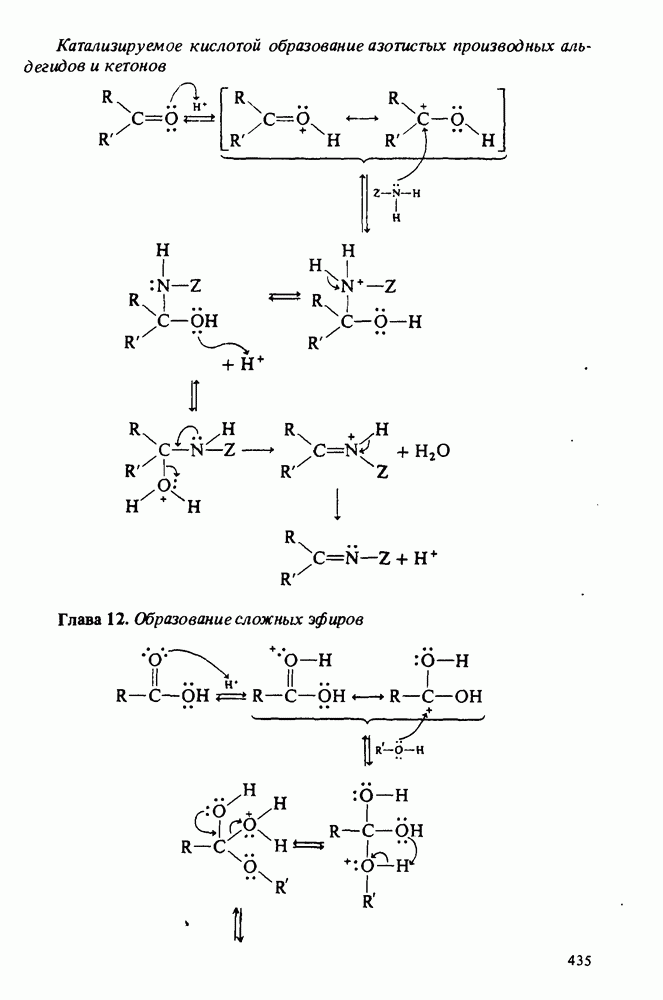
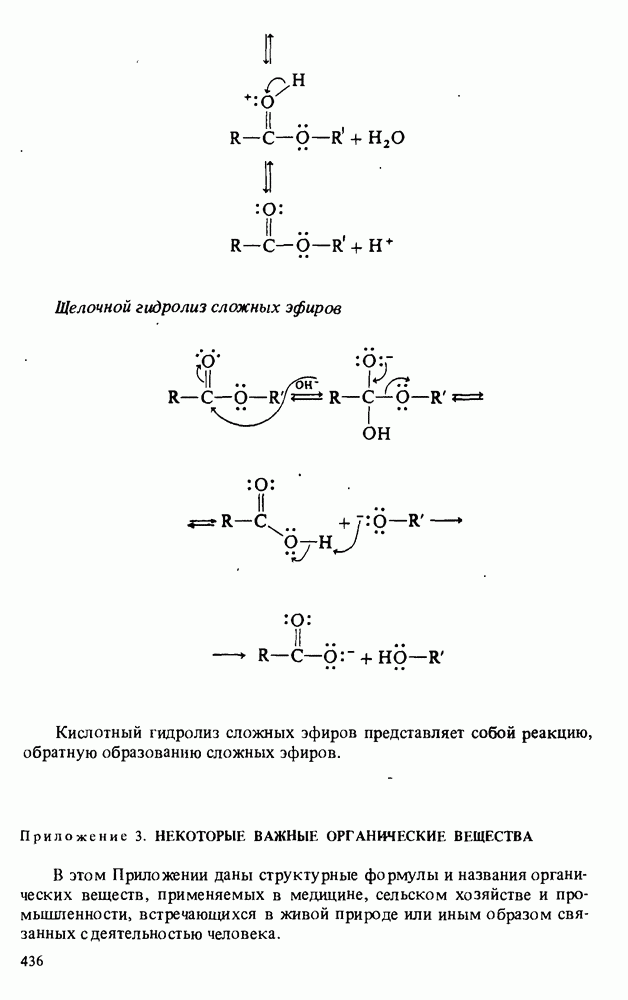
- Приложение 2. МЕХАНИЗМЫ НЕКОТОРЫХ РЕАКЦИЙ
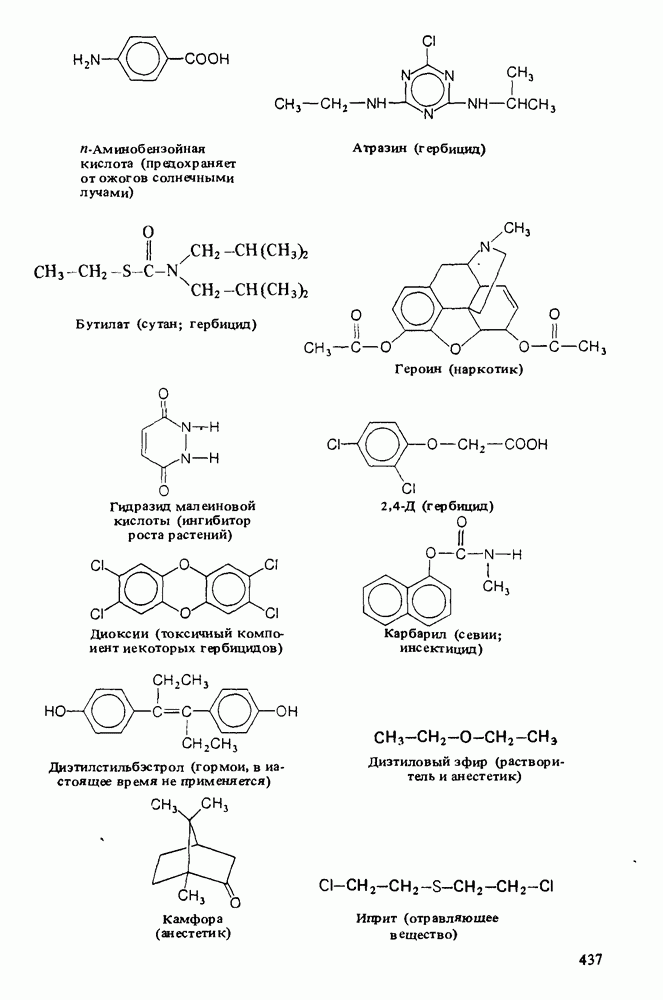
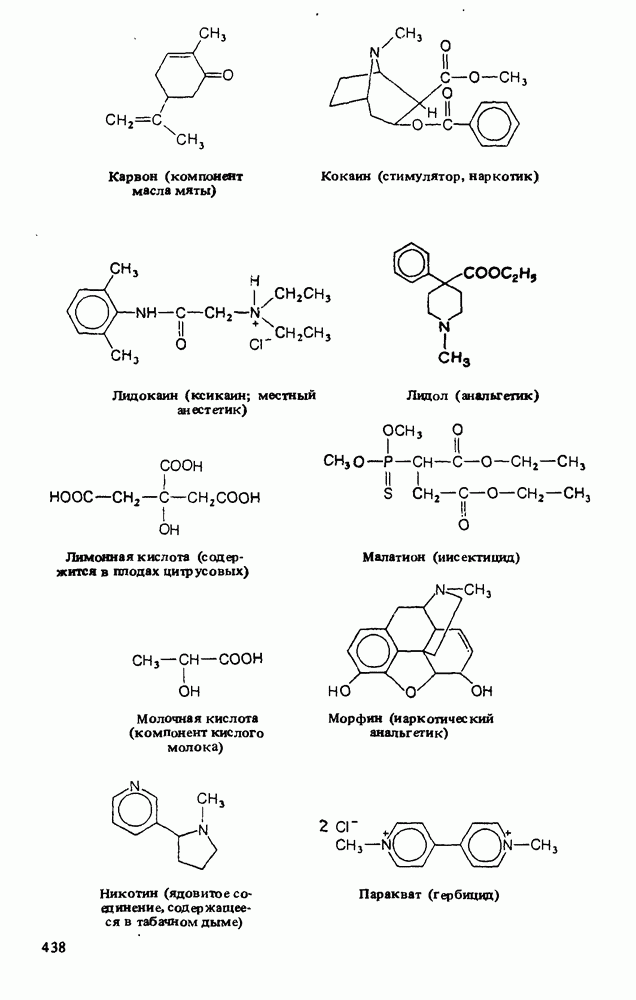
- Приложение 3. НЕКОТОРЫЕ ВАЖНЫЕ ОРГАНИЧЕСКИЕ ВЕЩЕСТВА