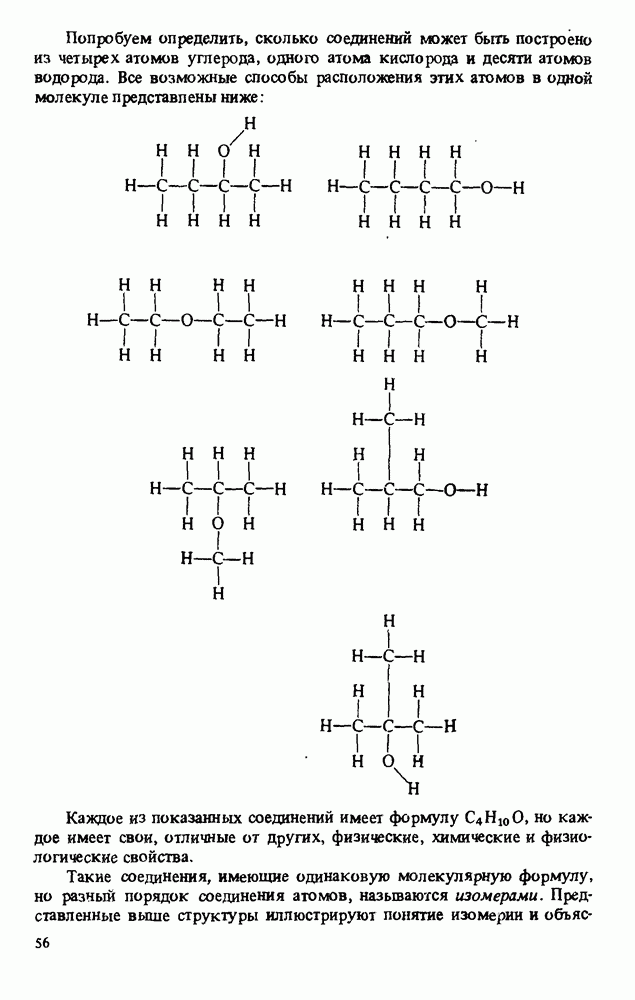| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
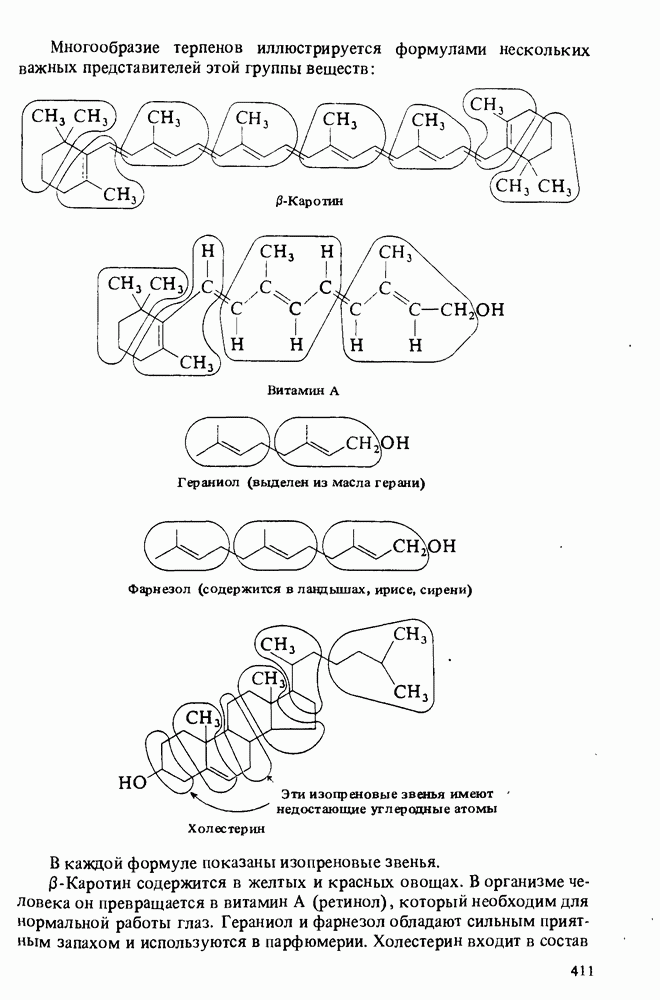
ГЕОМЕТРИЯ МОЛЕКУЛ
Под геометрией молекулы понимают пространственное расположение атомов, т. е. длины связей и углы между ними. Экспериментально форма (или геометрия) молекул изучается методами рентгенографического анализа кристаллов и дифракции электронов.
Для обсуждения вопросов пространственного строения молекул важно понимать значение следующих терминов.
Молекула  электронейтральная частица, состоящая из двух или более ковалентно связанных атомов.
электронейтральная частица, состоящая из двух или более ковалентно связанных атомов.
Карбкатион (карбениевый  -трупт ковалентно связанных атомов, содержащая положительно заряженный атом углерода, например
-трупт ковалентно связанных атомов, содержащая положительно заряженный атом углерода, например 
Карбанион — группа ковалентно связанных атомов, содержащая отрицательно заряженный атом углерода, например 
Свободный радикал — атом или группа атомов, содержащая неспаренный электрон, например  или
или 
Длина связи — среднее расстояние между ядрами ковалентно связанных атомов. Среднее значение используется потому, что атомы непрерывно осциллируют, то сближаясь, то удаляясь друг от друга.
Валентный угол — среднее значение угла между двумя ковалентными связями. Из-за колебаний атомов в молекуле величина угла в каждый данный момент может несколько отличаться от средней.
Для органической химии большое значение имеют три типа расположения атомов вокруг атома углерода:

Все валентные углы в молекуле метана  равны 109,5°. Такое расположение атомов называется тетраэдрическим и характерно для всех соединений, в которых имеются атомы углерода, связанные четырьмя простыми связями.
равны 109,5°. Такое расположение атомов называется тетраэдрическим и характерно для всех соединений, в которых имеются атомы углерода, связанные четырьмя простыми связями.
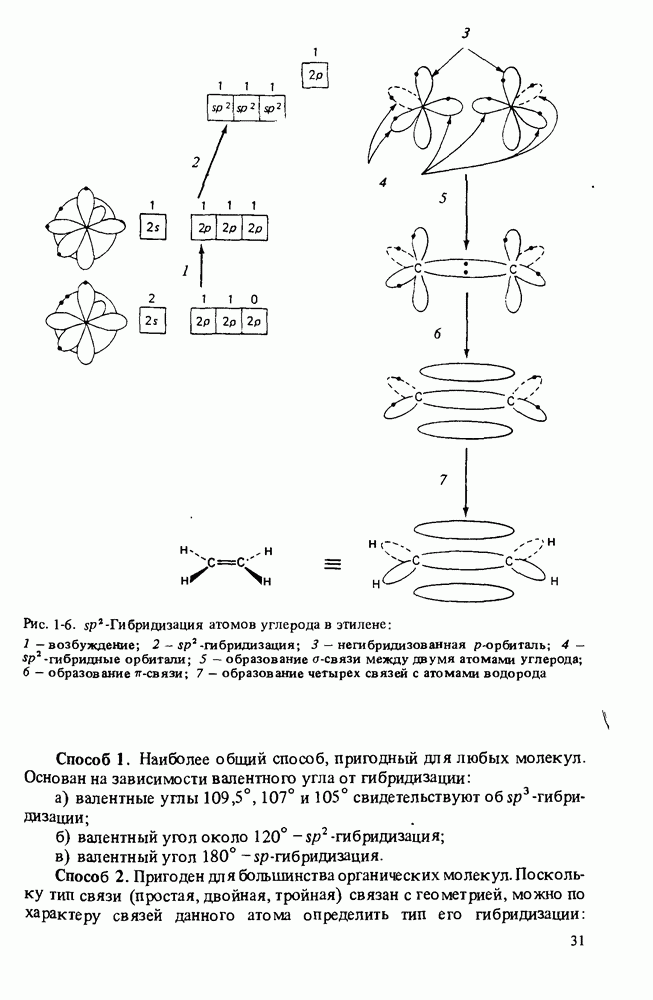
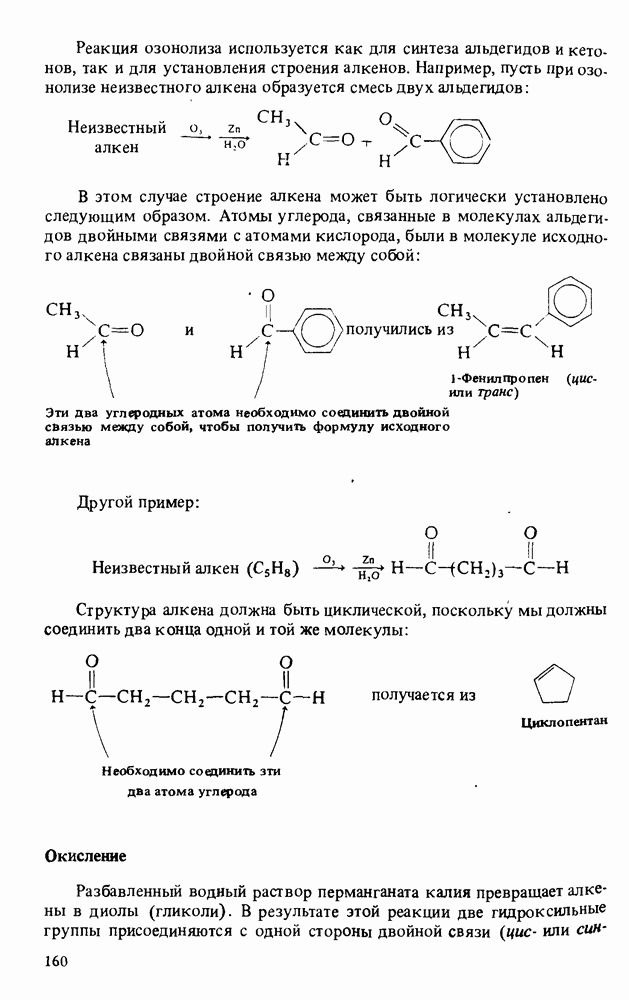
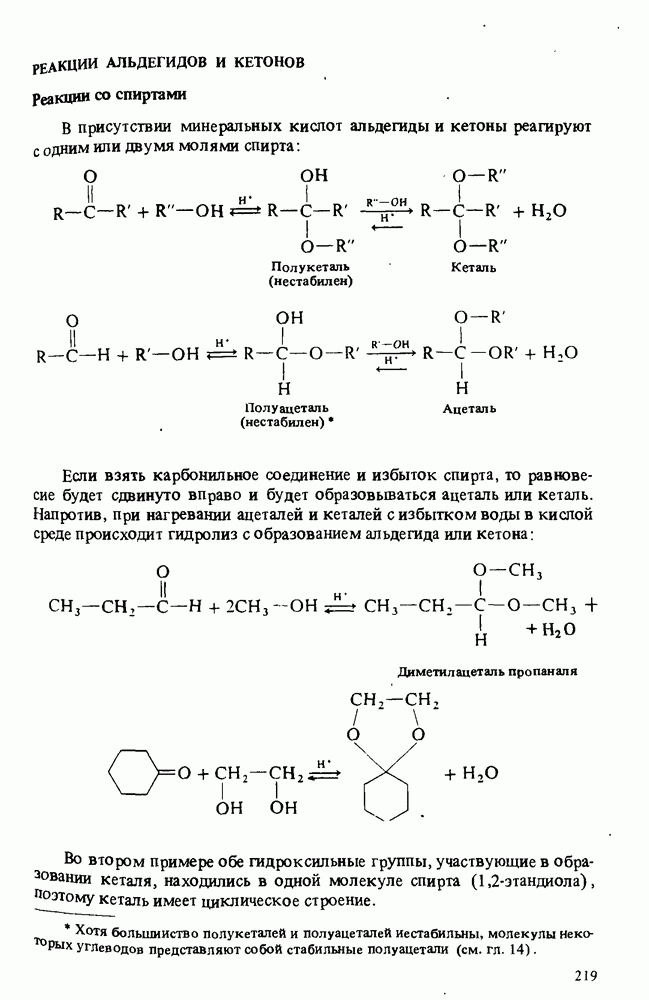
Формальдегид  - плоская молекула. Валентные углы в ней составляют по 120°. Такая геометрия свойственна всем молекулам, включающим атом углерода, связанный одной двойной и двумя простыми связями, как, например, в молекуле этилена.
- плоская молекула. Валентные углы в ней составляют по 120°. Такая геометрия свойственна всем молекулам, включающим атом углерода, связанный одной двойной и двумя простыми связями, как, например, в молекуле этилена.
Надо заметить, что величина валентных углов может в разных молекулах незначительно различаться. Эти различия определяются размерами атомов, связанных с атомом углерода. Например, в молекуле дихлорметана  валентный угол между связями
валентный угол между связями  несколько больше, чем между связями
несколько больше, чем между связями  Это объясняется большими размерами атома хлора по сравнению с атомом водорода. Тем не менее, углы близки к стандартной величине 109,5°, и тетраэдрическая конфигурация сохраняется.
Это объясняется большими размерами атома хлора по сравнению с атомом водорода. Тем не менее, углы близки к стандартной величине 109,5°, и тетраэдрическая конфигурация сохраняется.
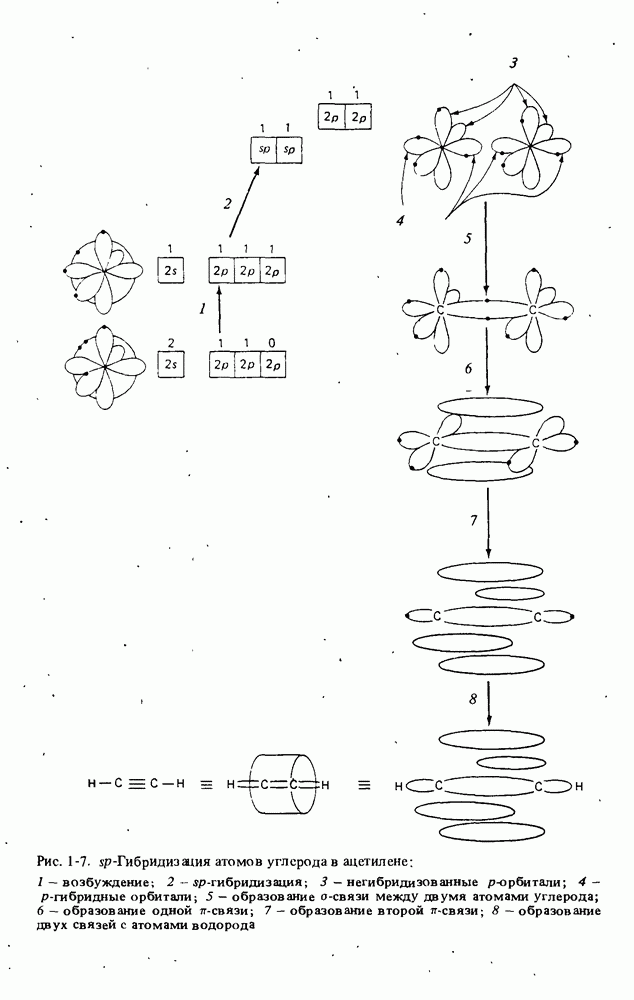
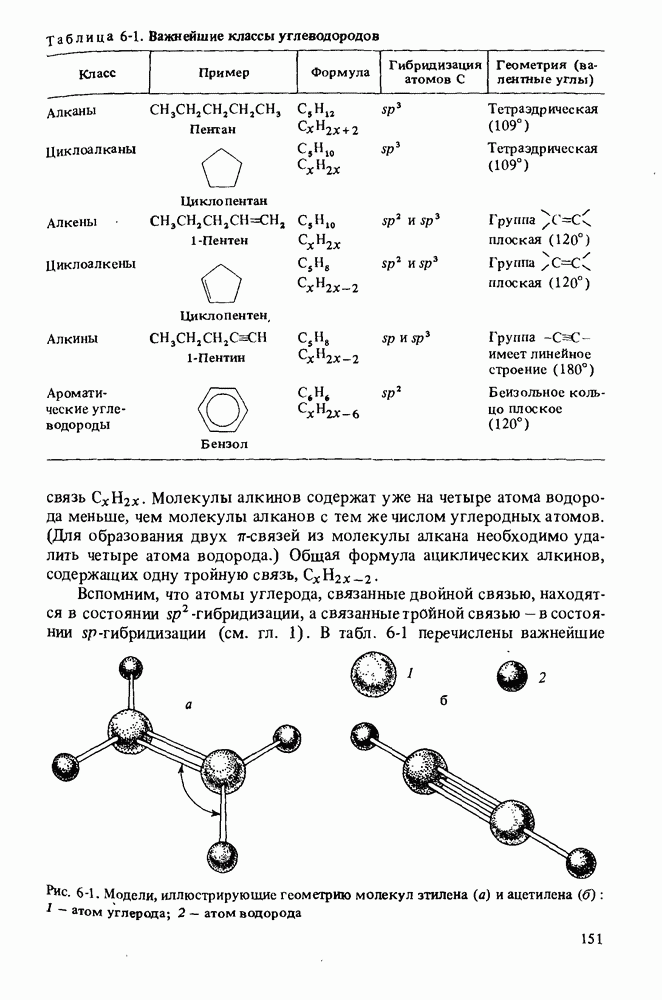
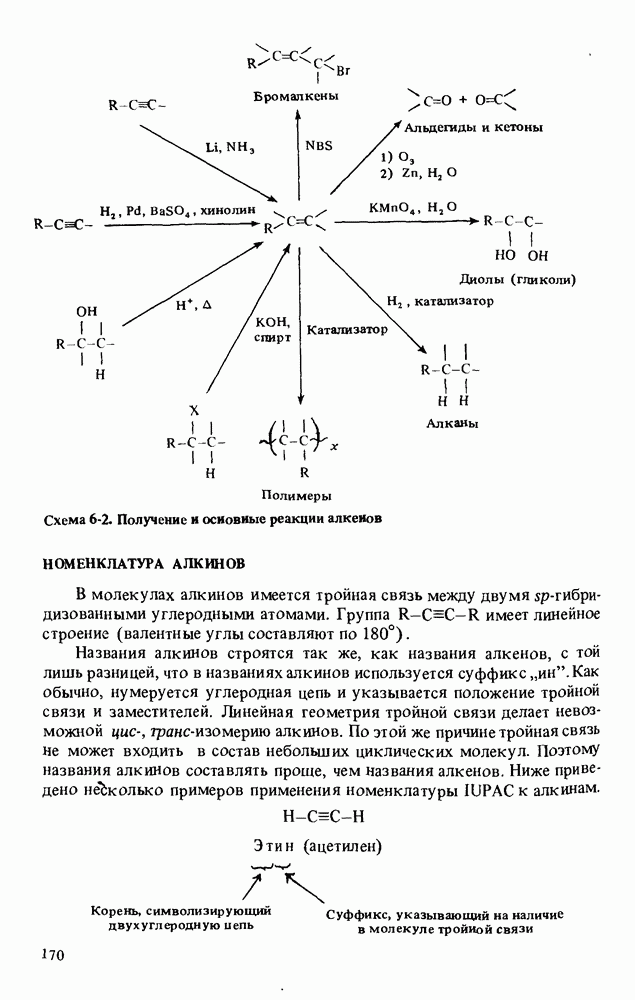
Третий тип формы молекул иллюстрируется молекулой ацетилена. Строение ацетилена линейное, а валентные углы составляют по 180°. Такая геометрия характерна для всех атомов углерода, связанных одной тройной и одной простой связью.
В органических соединениях часто встречаются атомы кислорода и азота. В этих случаях валентные углы близки к тетраэдрическим. Ниже показаны неорганические соединения кислорода и азота:

Примерно такая же геометрия сохраняется и в органических соединениях кислорода и азота, независимо от сложности структуры и
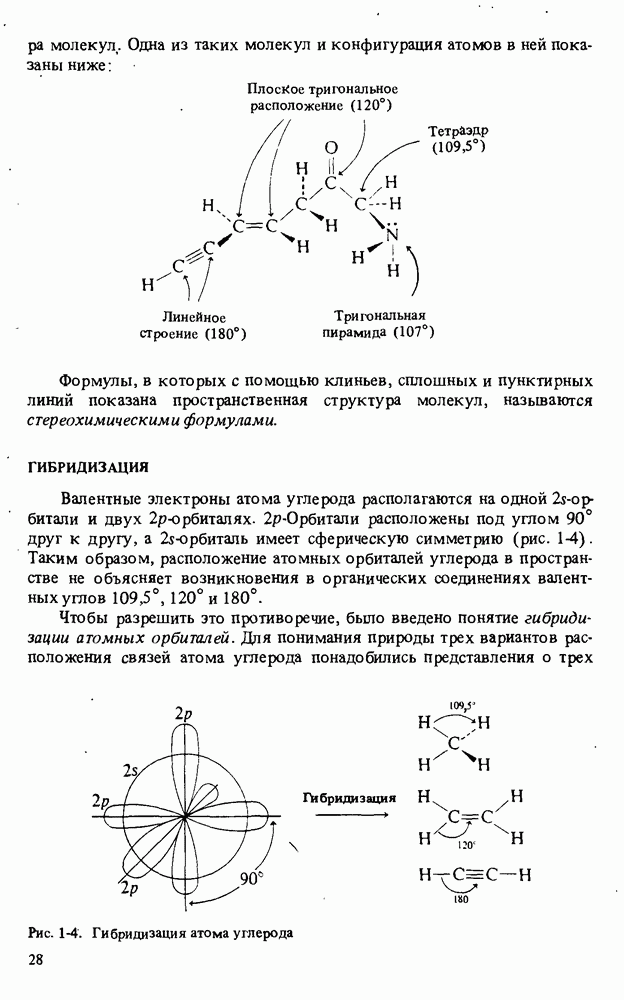
размера молекул. Одна из таких молекул и конфигурация атомов в ней показаны ниже:

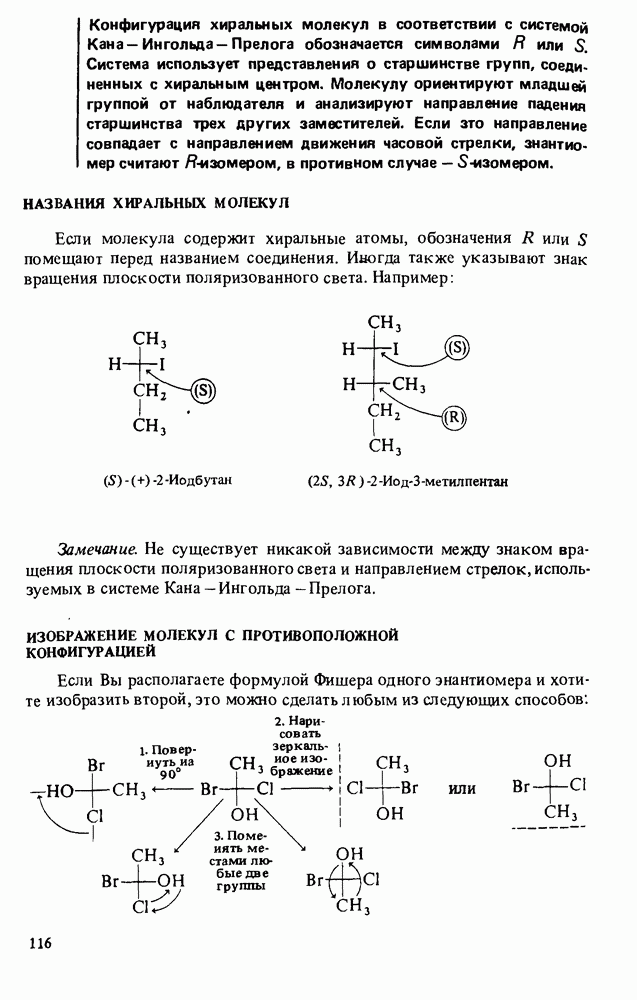
Формулы, в которых с помощью клиньев, сплошных и пунктирных линий показана пространственная структура молекул, называются стереохимыческими формулами.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ
- Глава 1. КЛЮЧЕВЫЕ ПОНЯТИЯ ХИМИИ
- АТОМНАЯ ТЕОРИЯ
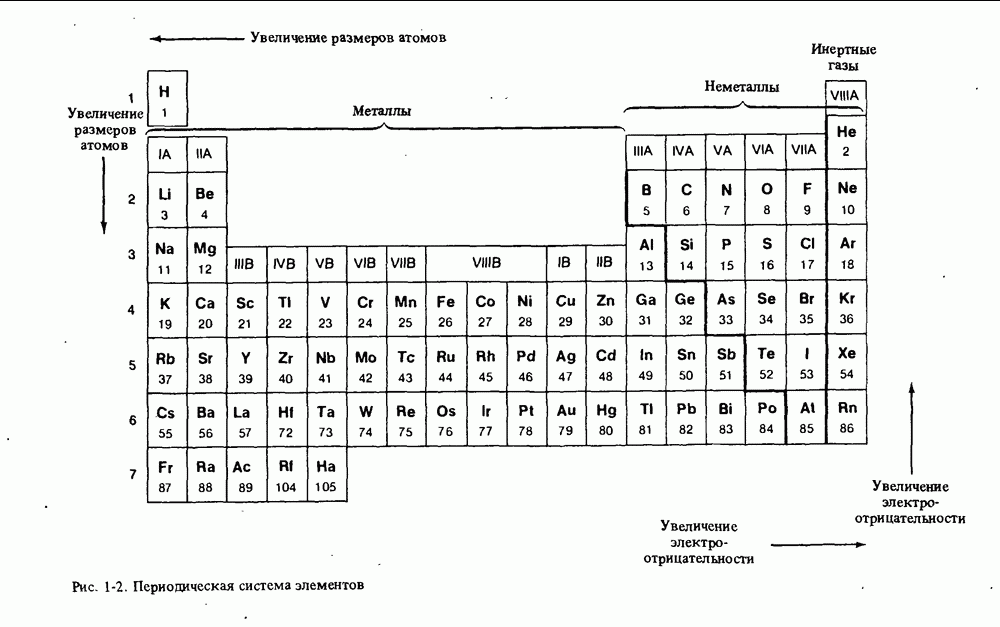
- ПЕРИОДИЧЕСКАЯ СИСТЕМА
- ХИМИЧЕСКАЯ СВЯЗЬ
- ФОРМУЛЫ ЛЬЮИСА
- ФОРМАЛЬНЫЙ ЗАРЯД
- РЕЗОНАНС
- ГЕОМЕТРИЯ МОЛЕКУЛ
- ГИБРИДИЗАЦИЯ
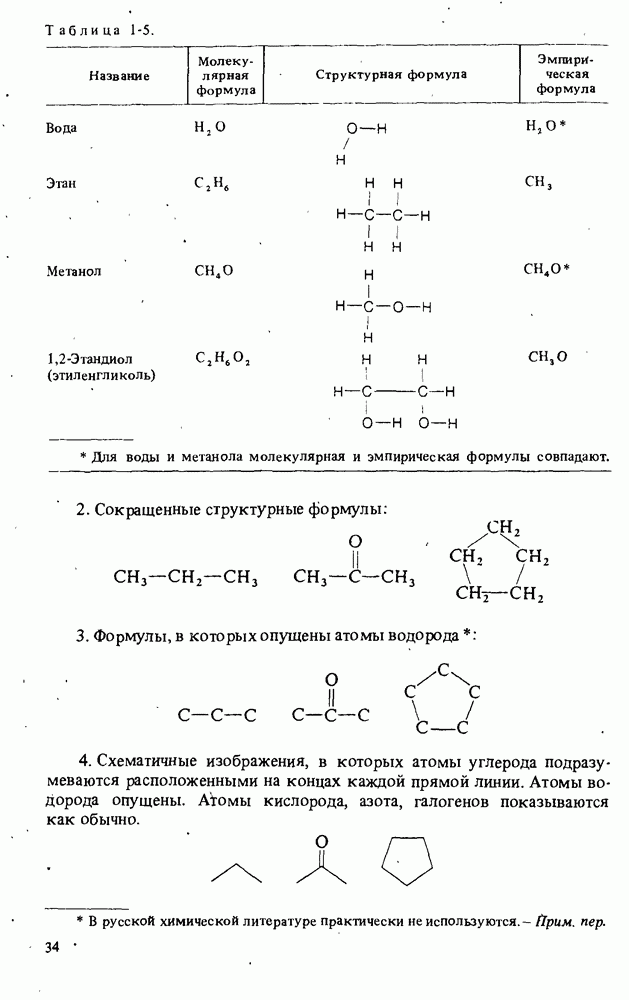
- ХИМИЧЕСКИЕ ФОРМУЛЫ
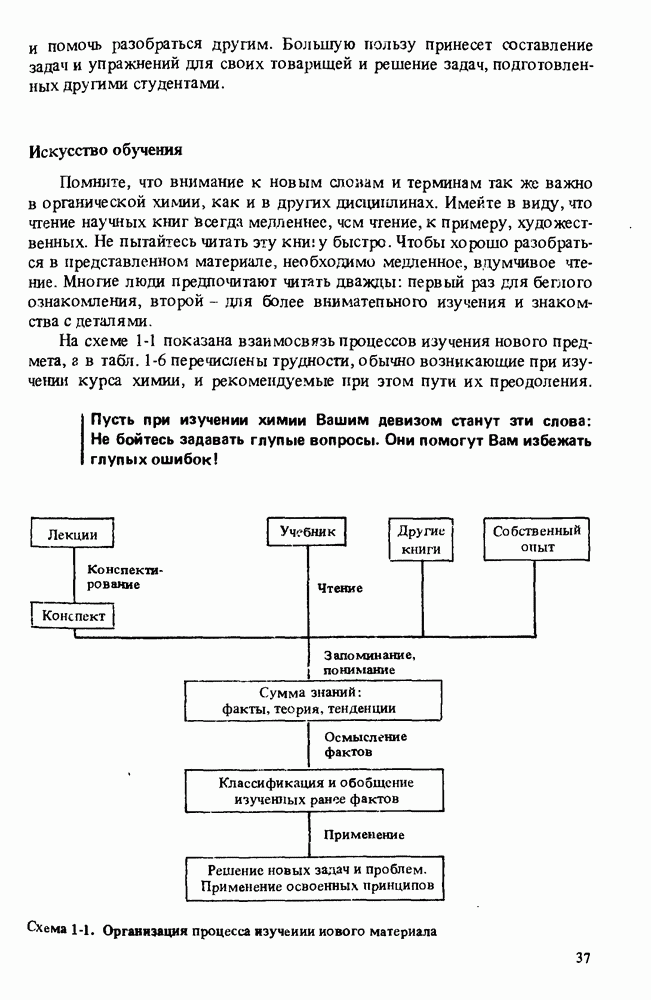
- СОВЕТЫ ИЗУЧАЮЩЕМУ ОРГАНИЧЕСКУЮ ХИМИЮ
- СВОДКА ОСНОВНЫХ ПОЛОЖЕНИЙ ГЛ. 1
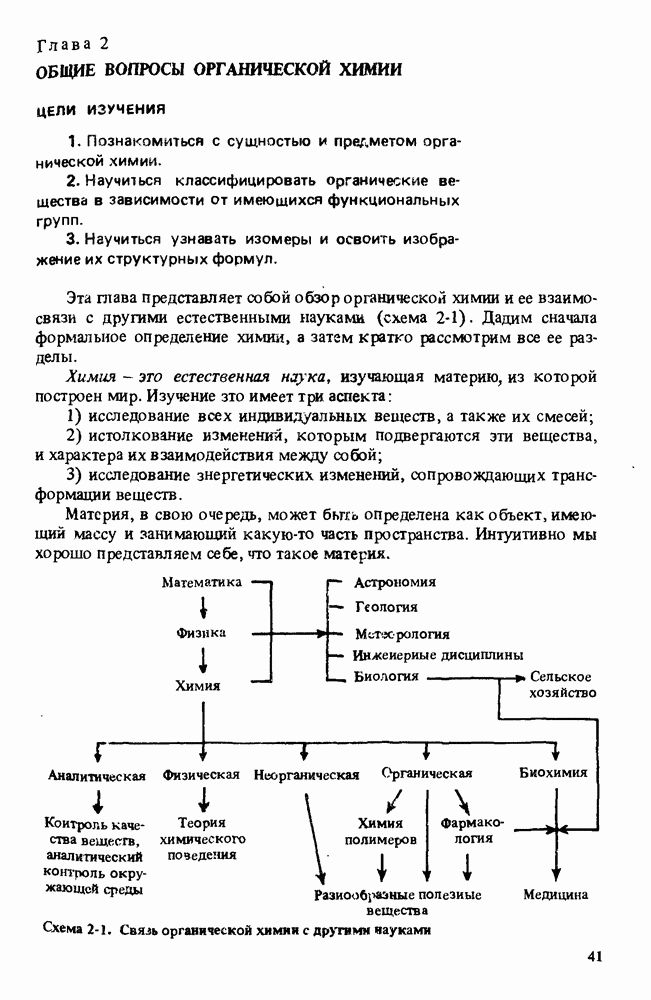
- Глава 2. ОБЩИЕ ВОПРОСЫ ОРГАНИЧЕСКОЙ ХИМИИ
- РАЗДЕЛЫ ХИМИИ
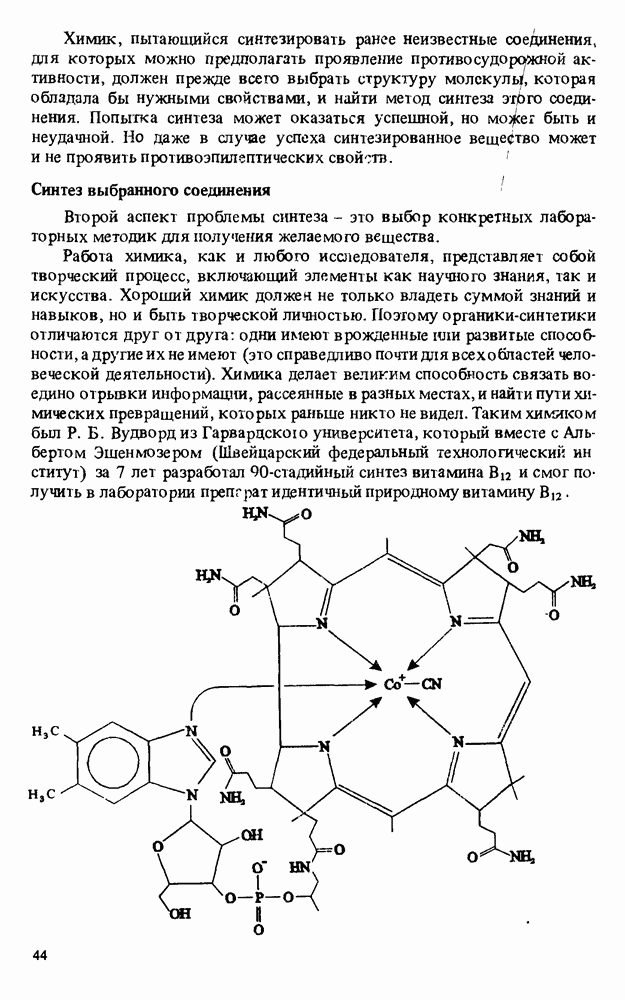
- СИНТЕТИЧЕСКАЯ ОРГАНИЧЕСКАЯ ХИМИЯ
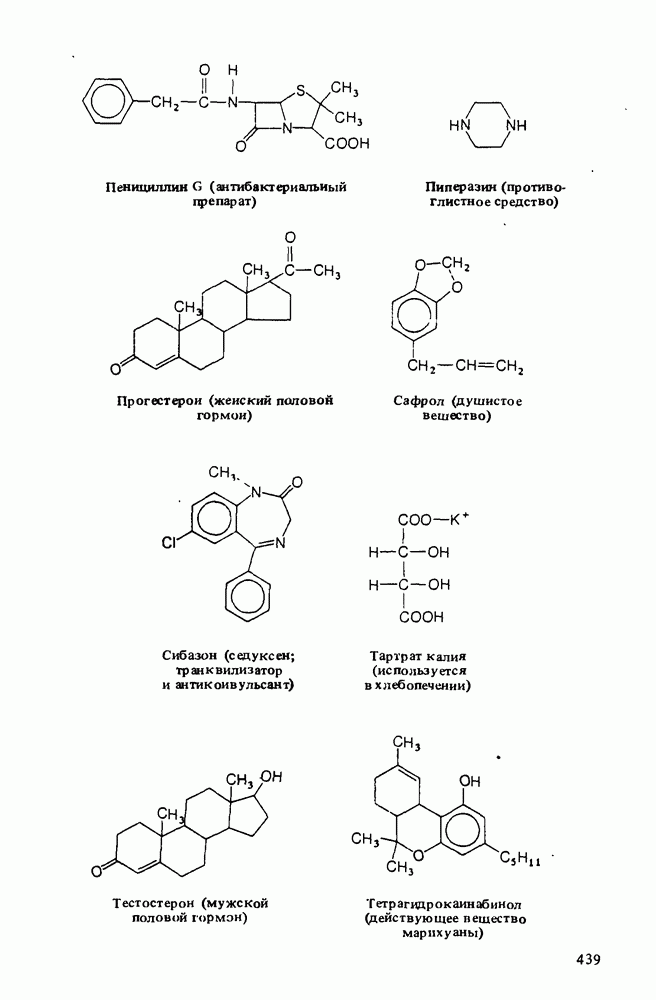
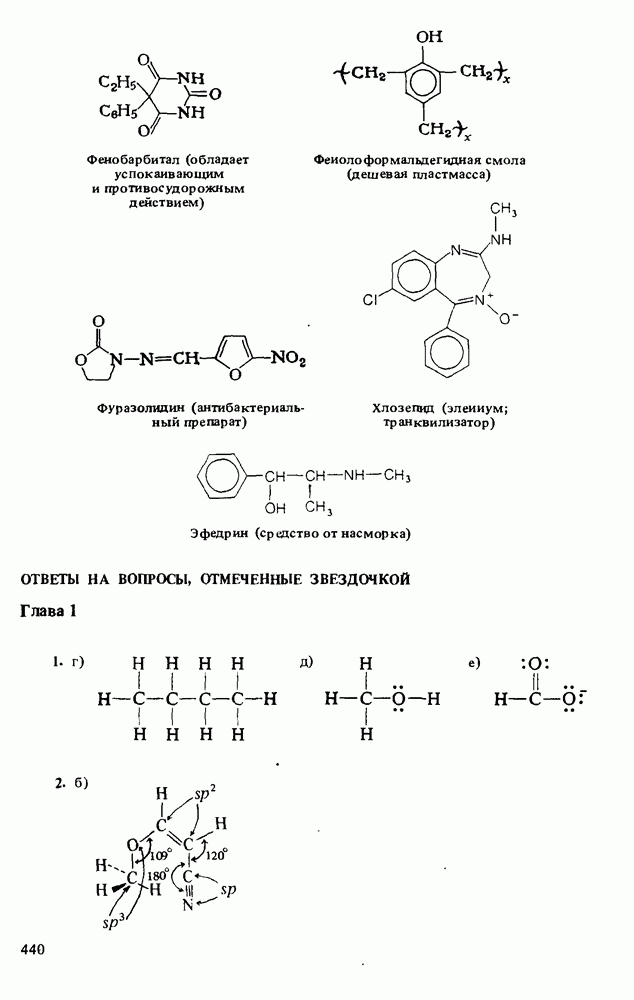
- ПОЛЕЗНЫЕ ОРГАНИЧЕСКИЕ ВЕЩЕСТВА
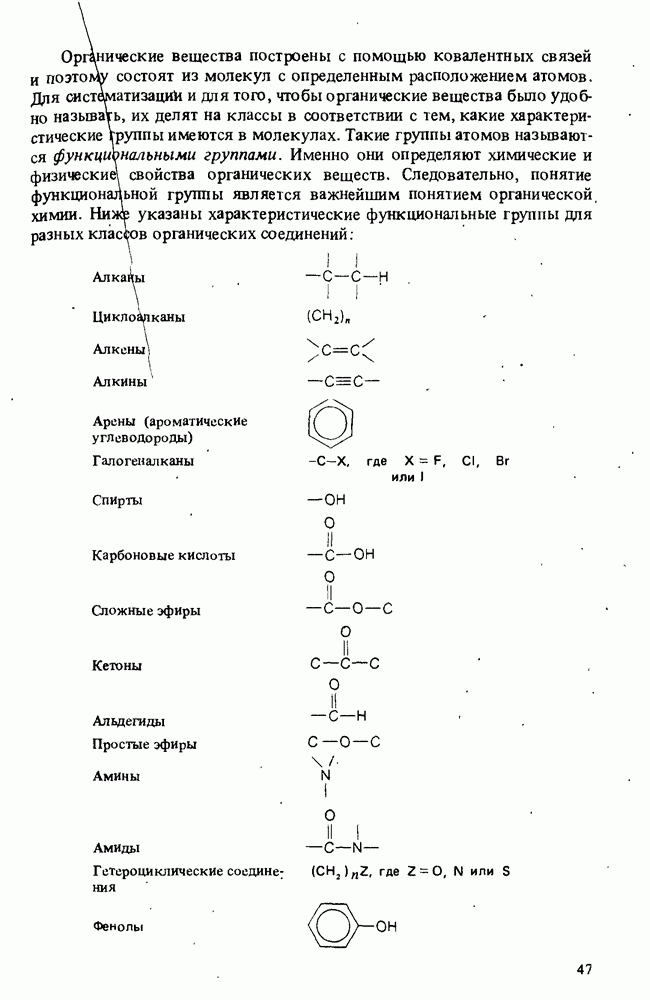
- КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ. ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
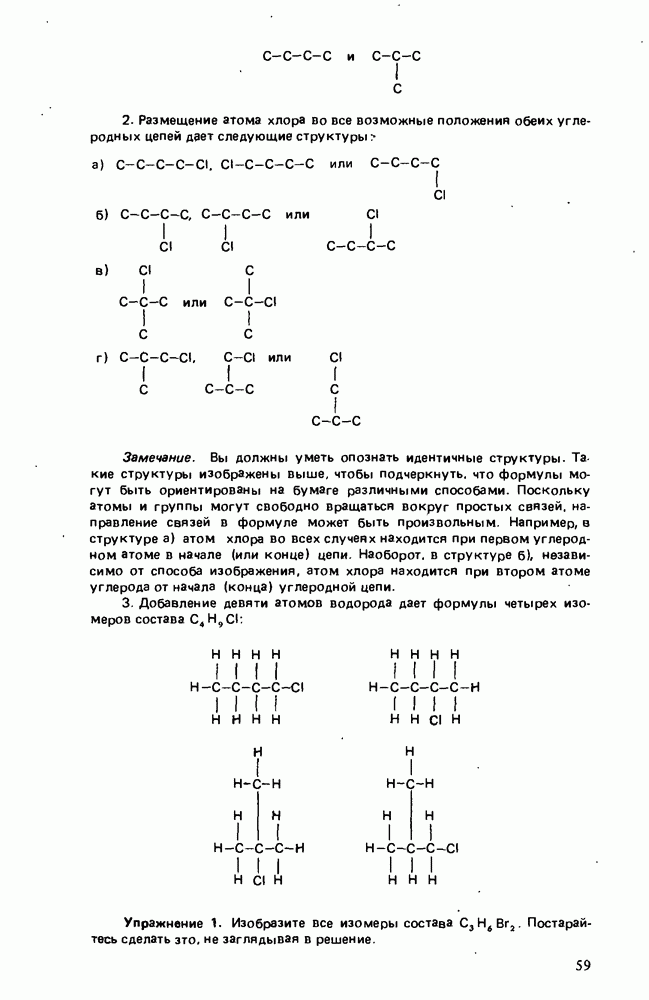
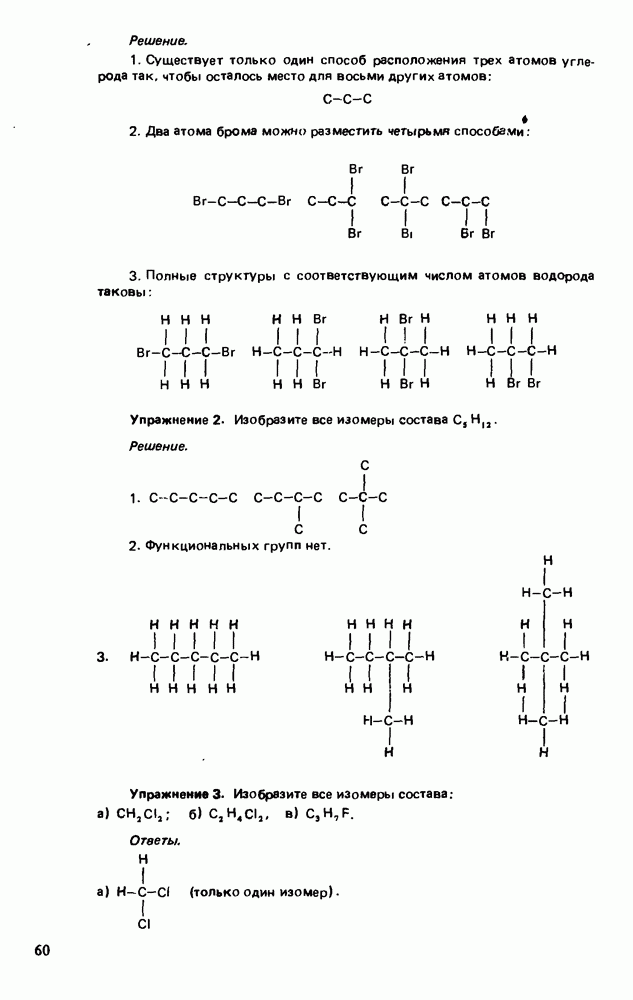
- ИЗОМЕРИЯ
- СВОДКА ОСНОВНЫХ ПОЛОЖЕНИЙ ГЛ. 2
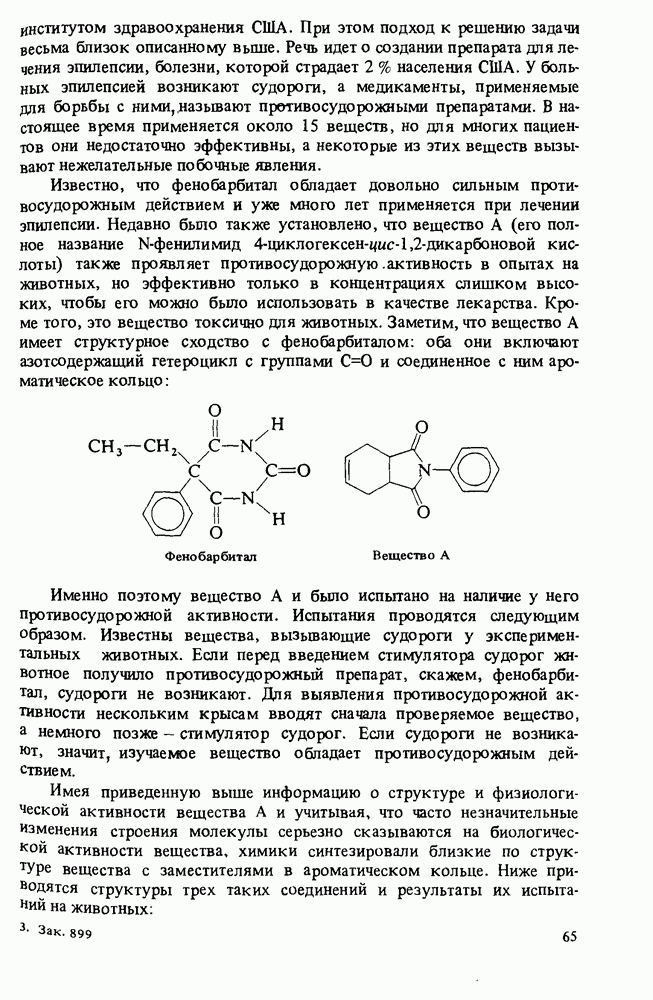
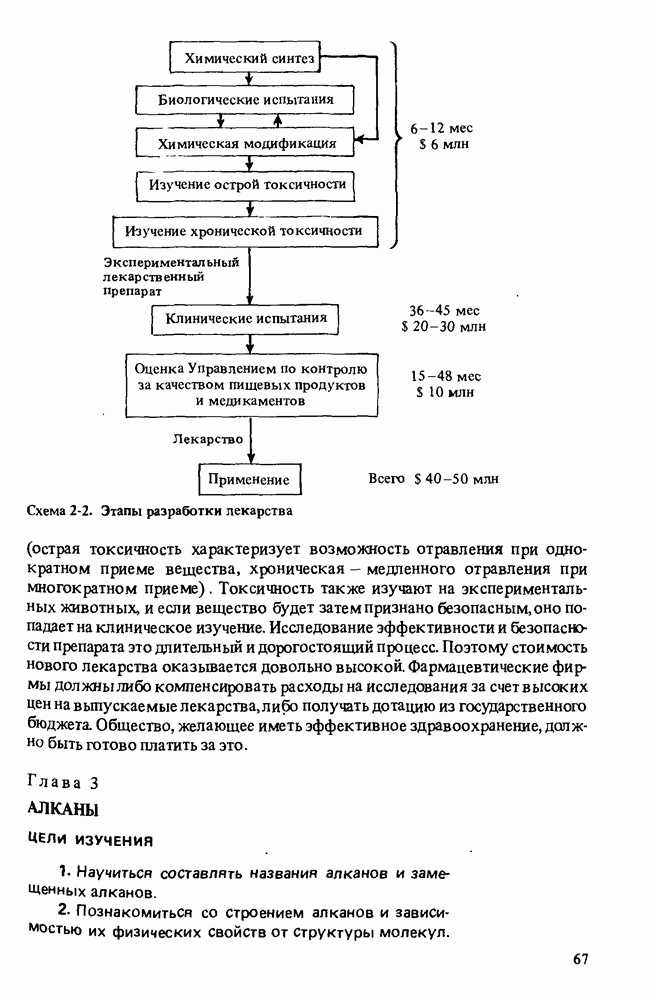
- Прикладная органическая химия: ХИМИЧЕСКИЙ СИНТЕЗ И МЕДИЦИНСКИЕ ИССЛЕДОВАНИЯ
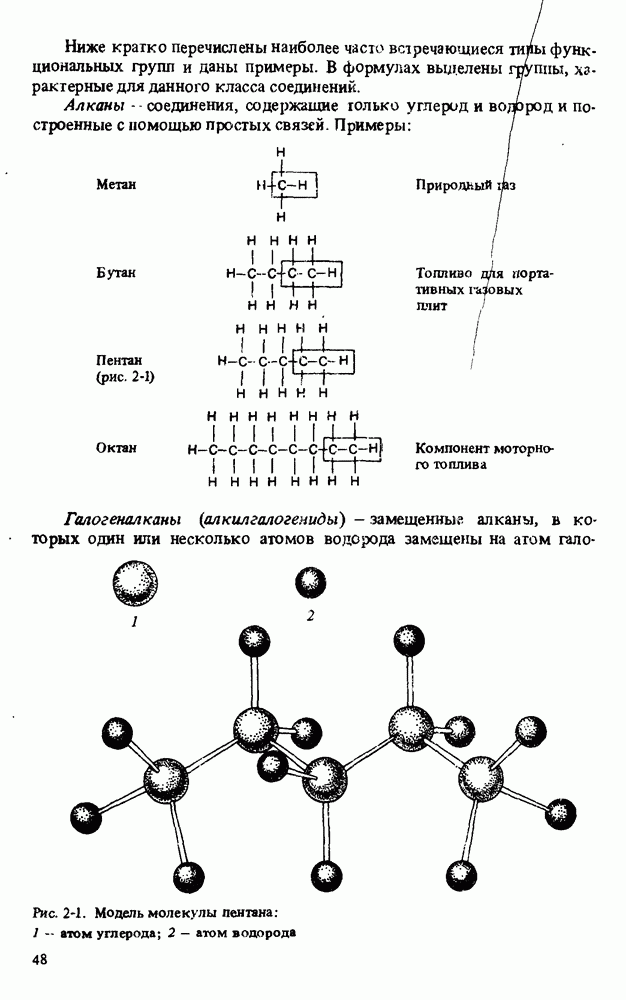
- Глава 3. АЛКАНЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА АЛКАНОВ
- СТРОЕНИЕ АЛКАНОВ
- ПОЛУЧЕНИЕ АЛКАНОВ
- РЕАКЦИИ АЛКАНОВ
- ХИМИЯ НЕФТИ
- СОВЕТЫ ИЗУЧАЮЩЕМУ ОРГАНИЧЕСКУЮ ХИМИЮ. ИЗУЧЕНИЕ РЕАКЦИЙ
- Глава 4. СТЕРЕОХИМИЯ И ОПТИЧЕСКАЯ АКТИВНОСТЬ
- СПОСОБЫ ИЗОБРАЖЕНИЯ ЭНАНТИОМЕРОВ
- ОБОЗНАЧЕНИЕ АБСОЛЮТНОЙ КОНФИГУРАЦИИ
- НАЗВАНИЯ ХИРАЛЬНЫХ МОЛЕКУЛ
- ИЗОБРАЖЕНИЕ МОЛЕКУЛ С ПРОТИВОПОЛОЖНОЙ КОНФИГУРАЦИЕЙ
- D,L-НОМЕНКЛАТУРА ЭНАНТИОМЕРОВ
- ТЕРМИНОЛОГИЯ, ПРИМЕНЯЕМАЯ В СТЕРЕОХИМИИ
- ЗНАЧЕНИЕ ОПТИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ
- Глава 5. ОРГАНИЧЕСКИЕ ГАЛОГЕНСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
- ПОЛУЧЕНИЕ ГАЛОГЕНАЛКАНОВ
- РЕАКЦИИ ГАЛОГЕНАЛКАНОВ
- ПРАКТИЧЕСКИ ВАЖНЫЕ ГАЛОГЕНАЛКАНЫ
- Прикладная органическая химия: ОРГАНИЧЕСКИЕ ПЕСТИЦИДЫ
- Глава 6. НЕНАСЫЩЕННЫЕ УГЛЕВОДОРОДЫ
- НОМЕНКЛАТУРА АЛКЕНОВ
- ПОЛУЧЕНИЕ АЛКЕНОВ
- ОСНОВНЫЕ РЕАКЦИИ АЛКЕНОВ
- ПОЛИМЕРЫ
- НОМЕНКЛАТУРА АЛКИНОВ
- ПОЛУЧЕНИЕ АЛКИНОВ
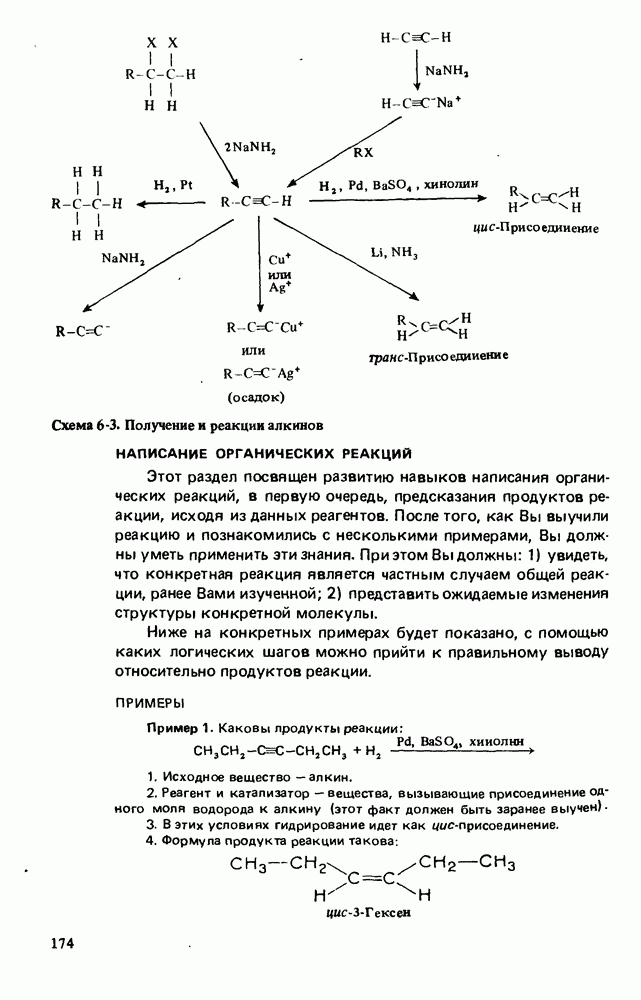
- РЕАКЦИИ АЛКИНОВ
- НАПИСАНИЕ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- Глава 7. СПИРТЫ И ПРОСТЫЕ ЭФИРЫ
- НОМЕНКЛАТУРА СПИРТОВ
- НЕКОТОРЫЕ ВАЖНЫЕ ВЕЩЕСТВА, СОДЕРЖАЩИЕ СПИРТОВУЮ ГРУППУ
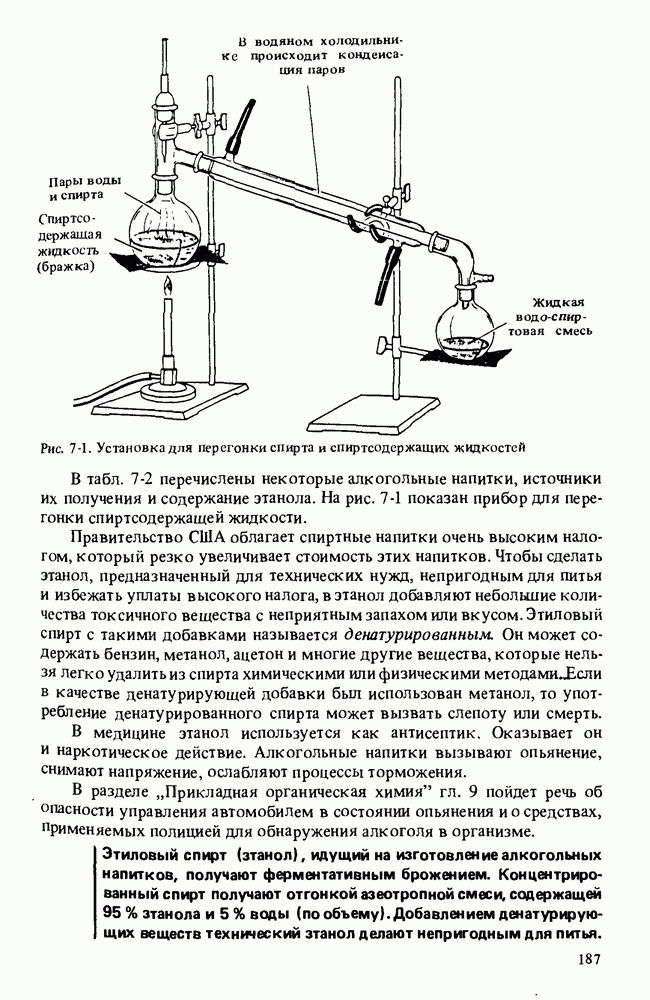
- ЭТИЛОВЫЙ СПИРТ. ПРОИЗВОДСТВО СПИРТНЫХ НАПИТКОВ
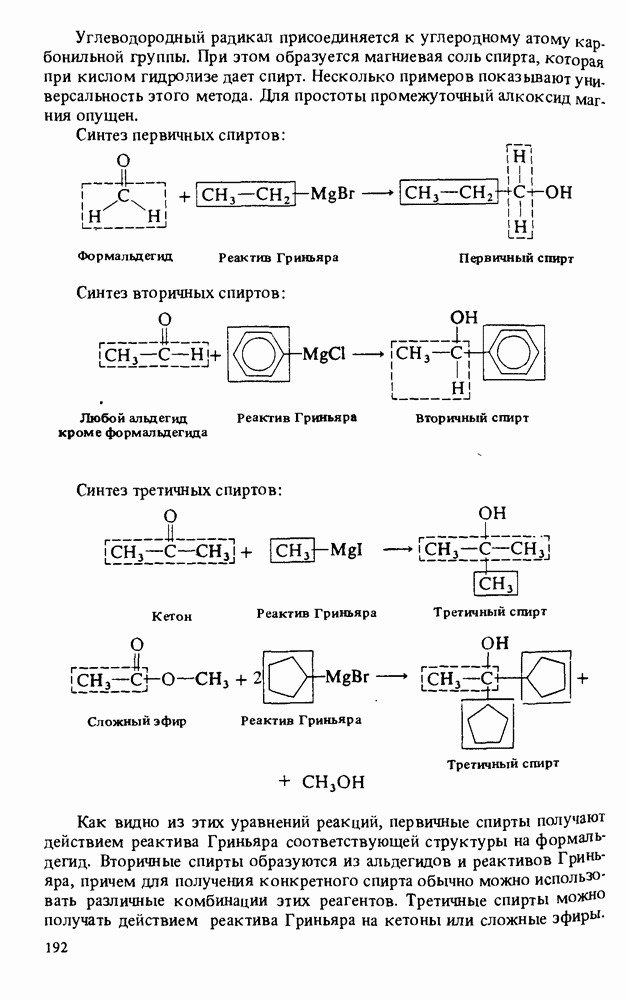
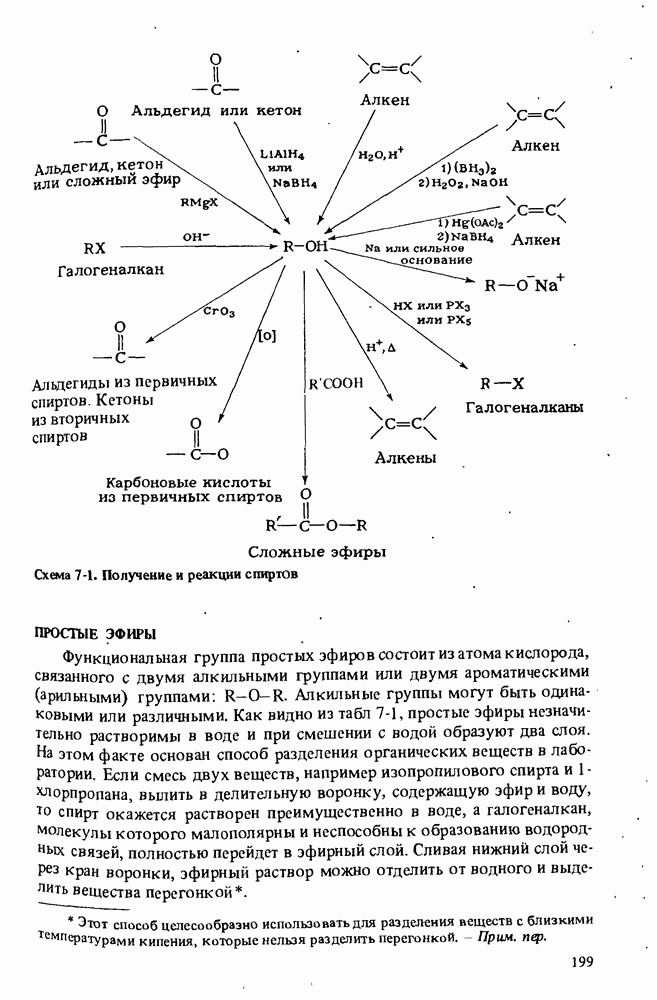
- ПОЛУЧЕНИЕ СПИРТОВ
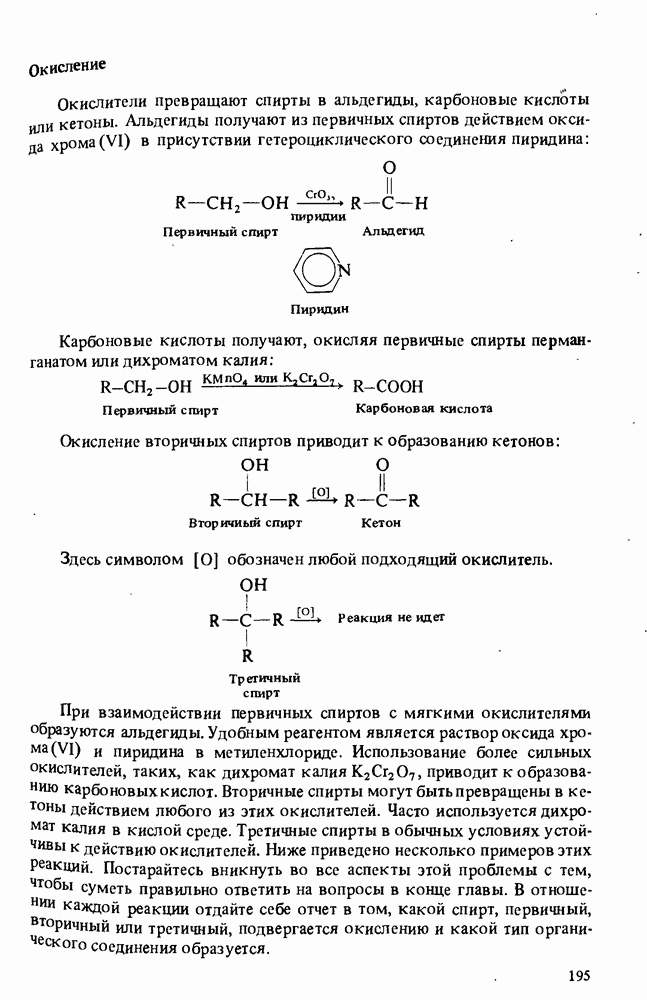
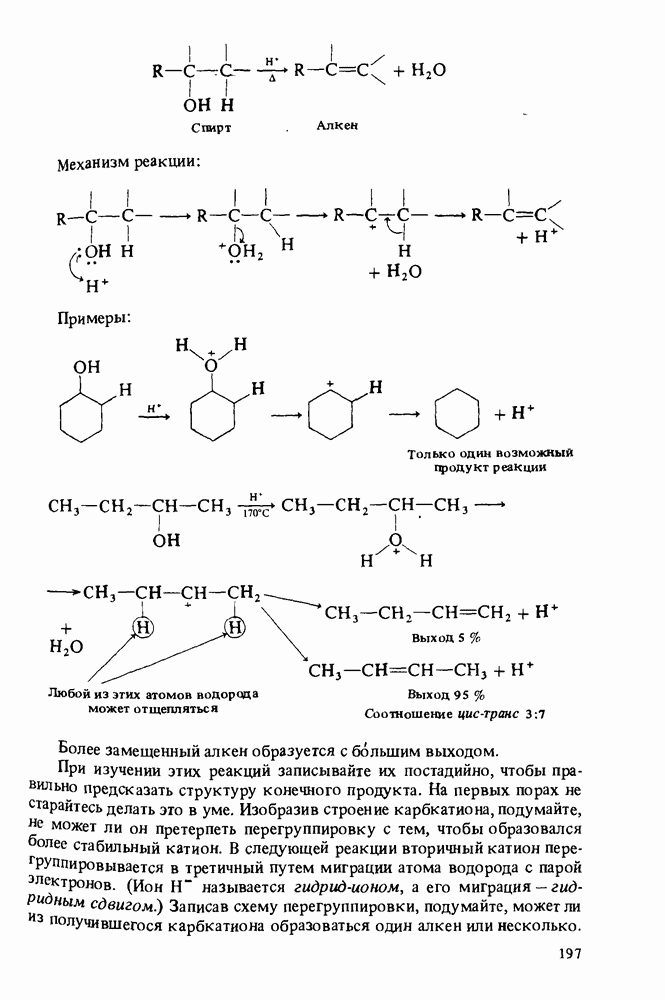
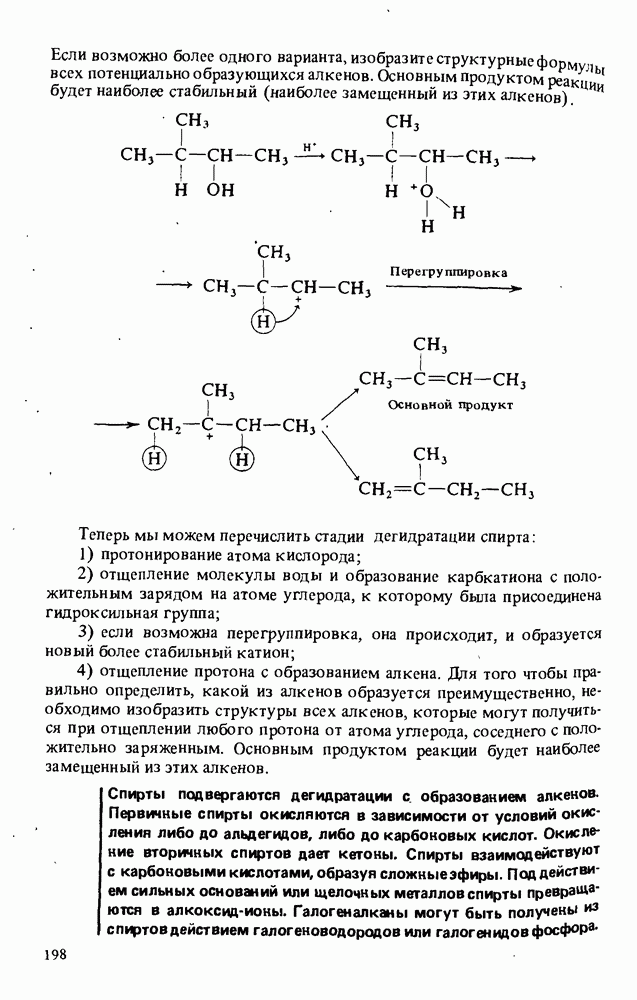
- РЕАКЦИИ СПИРТОВ
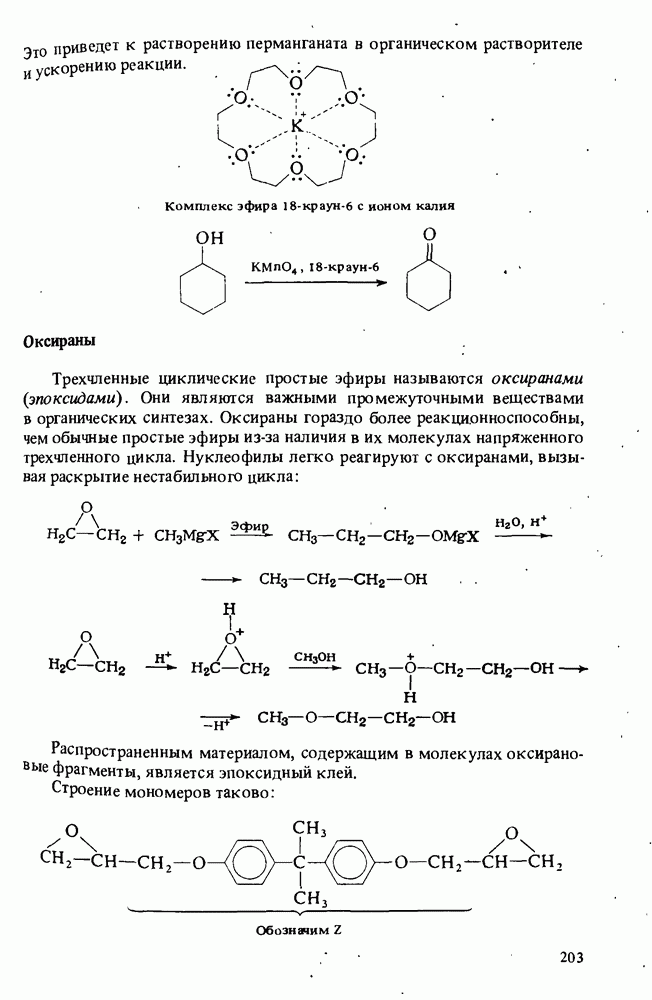
- ПРОСТЫЕ ЭФИРЫ
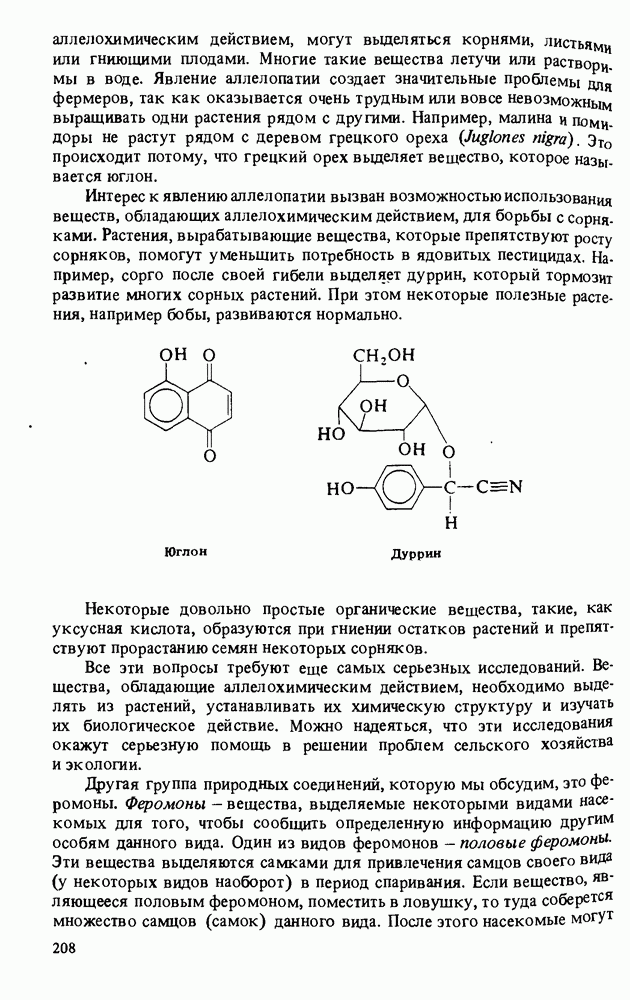
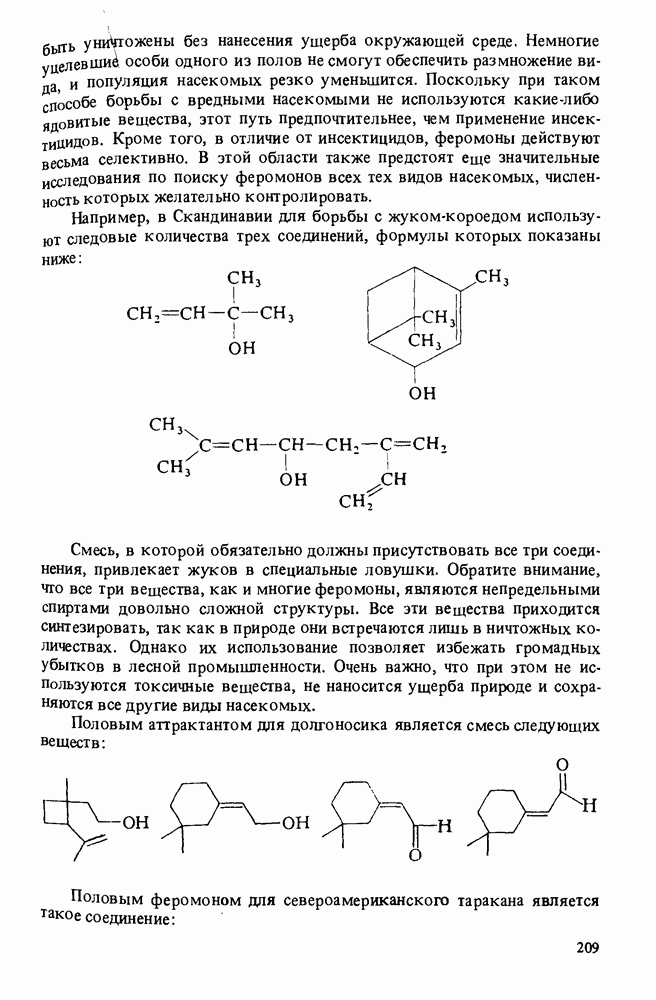
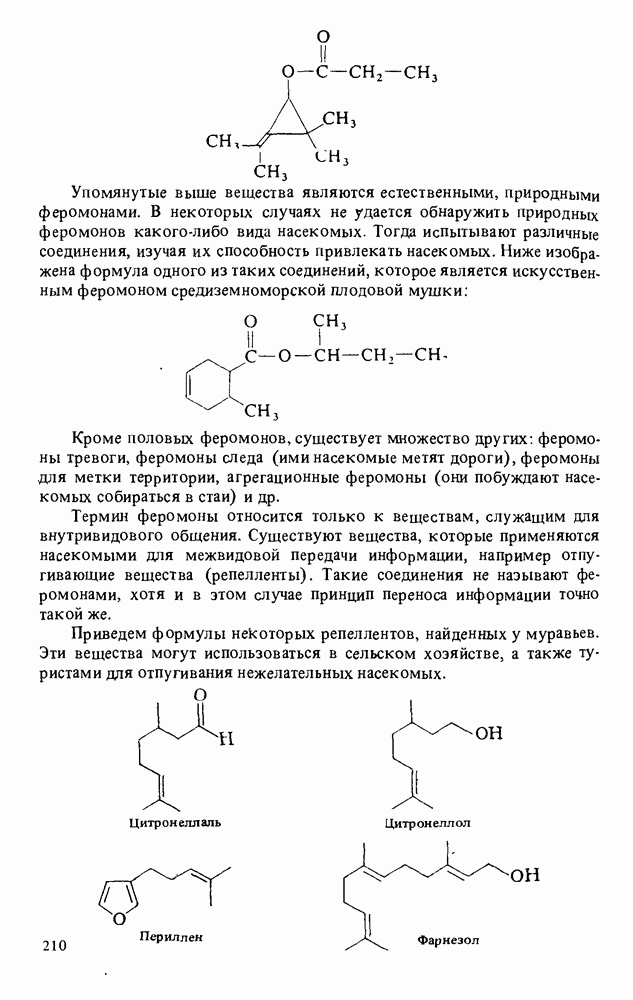
- Прикладная органическая химия: ВЕЩЕСТВА, ОБЛАДАЮЩИЕ АЛЛЕЛОХИМИЧЕСКИМ ДЕЙСТВИЕМ. ФЕРОМОНЫ
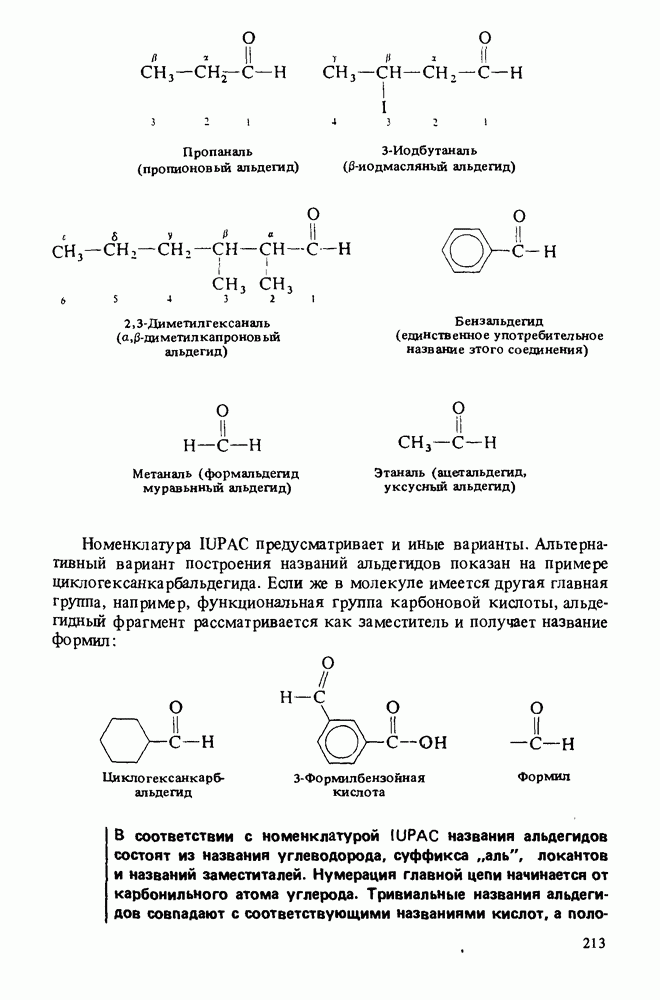
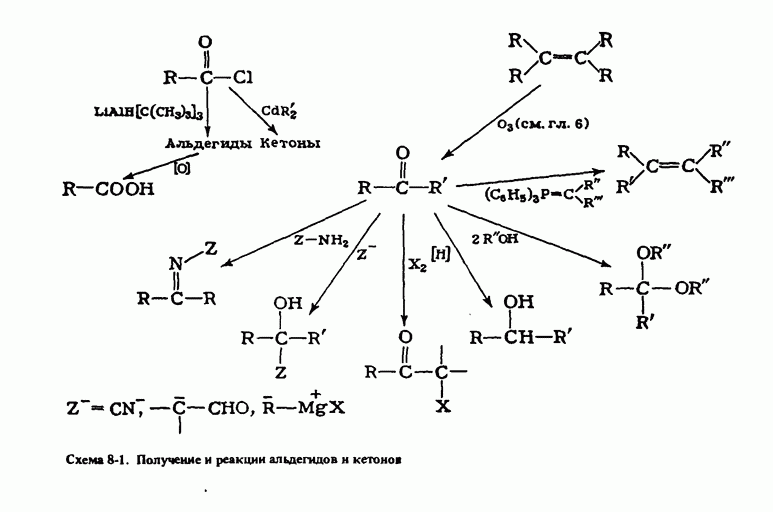
- Глава 8. АЛЬДЕГИДЫ И КЕТОНЫ
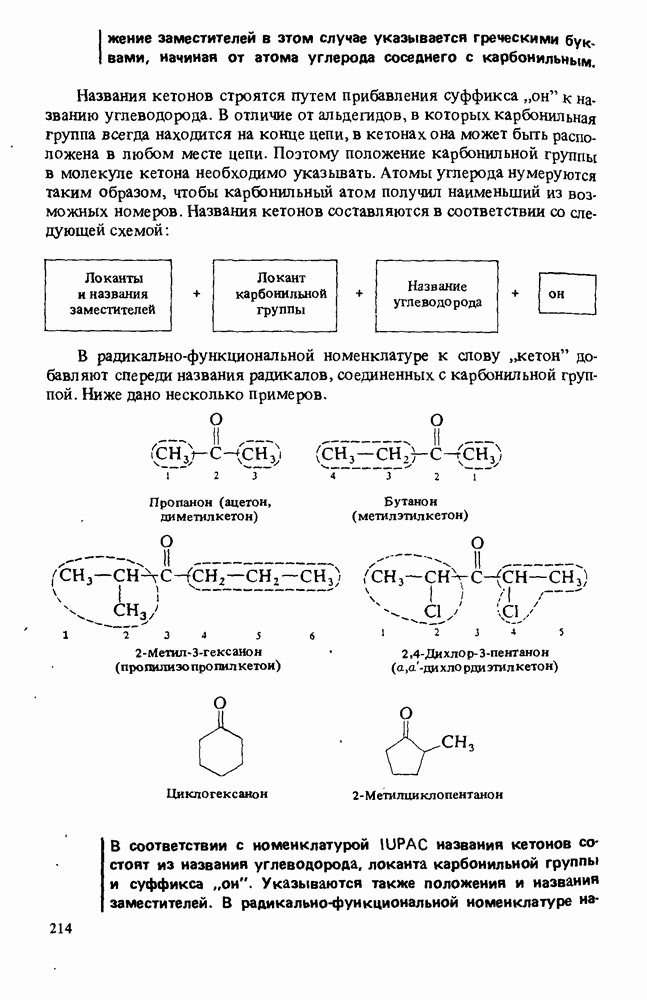
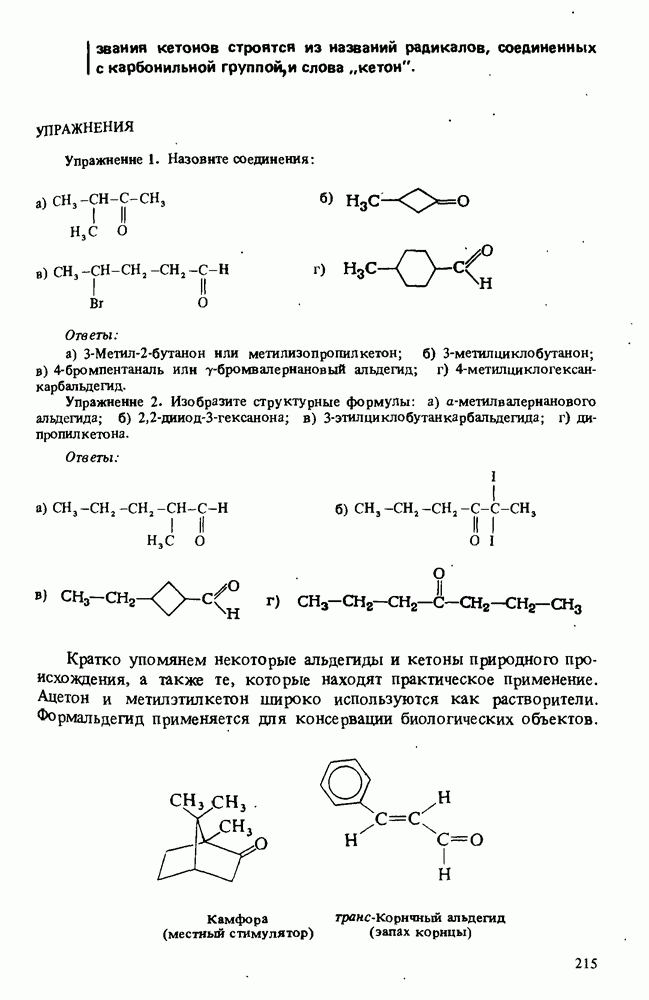
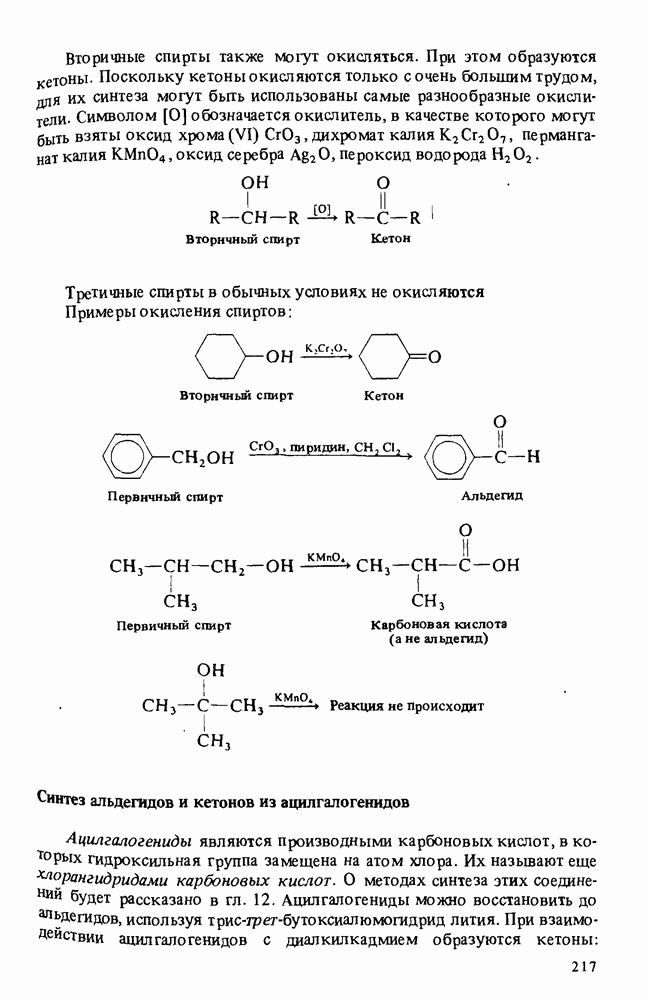
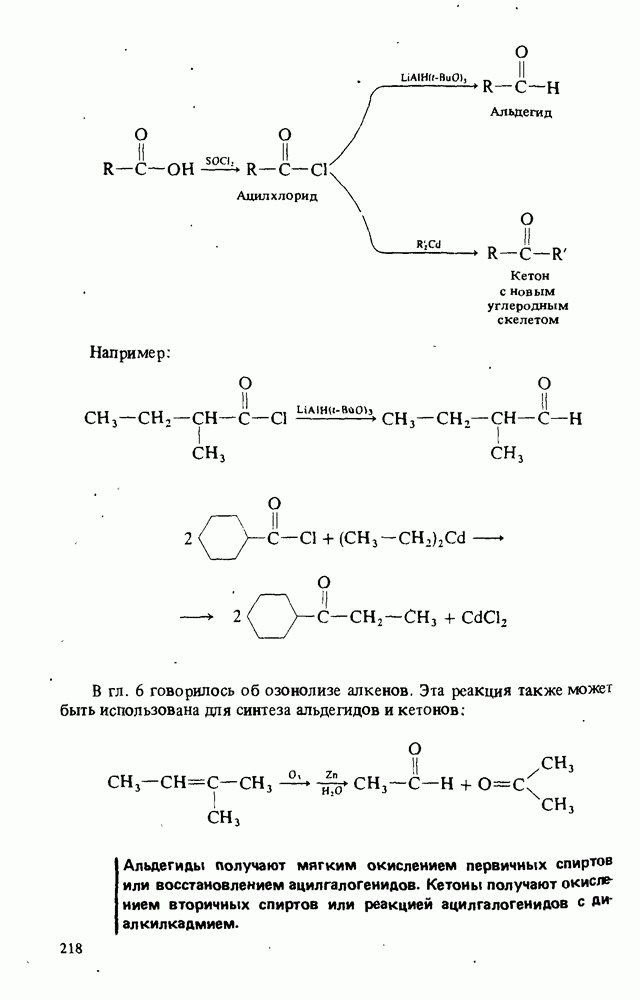
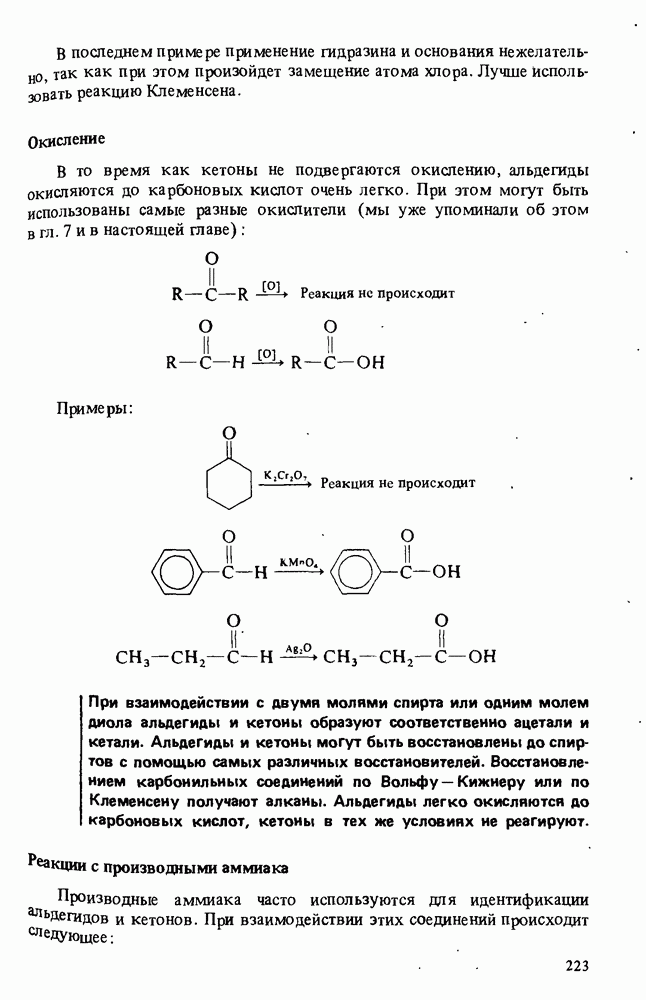
- ПОЛУЧЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ
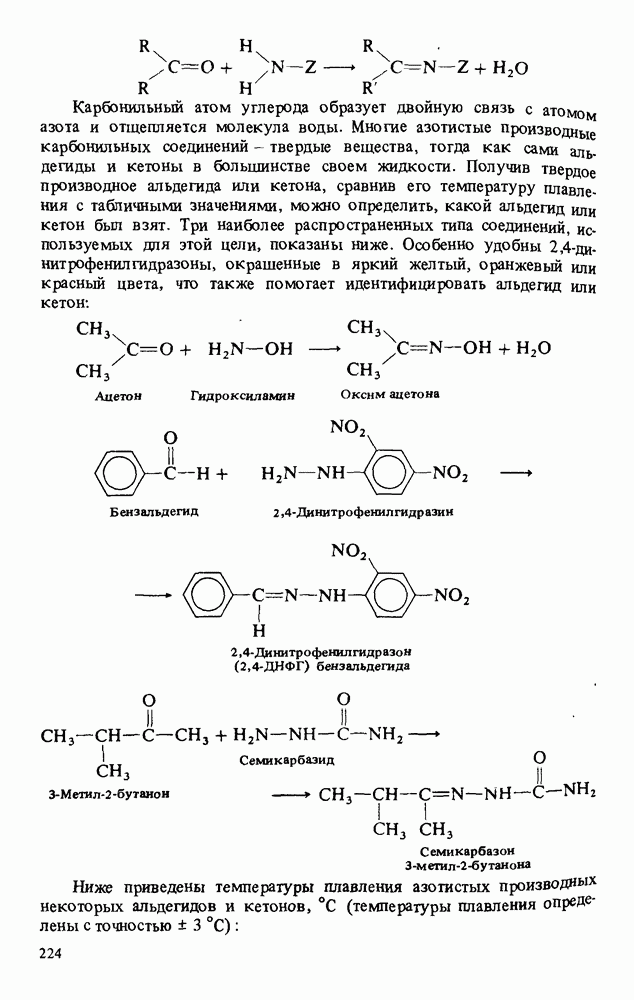
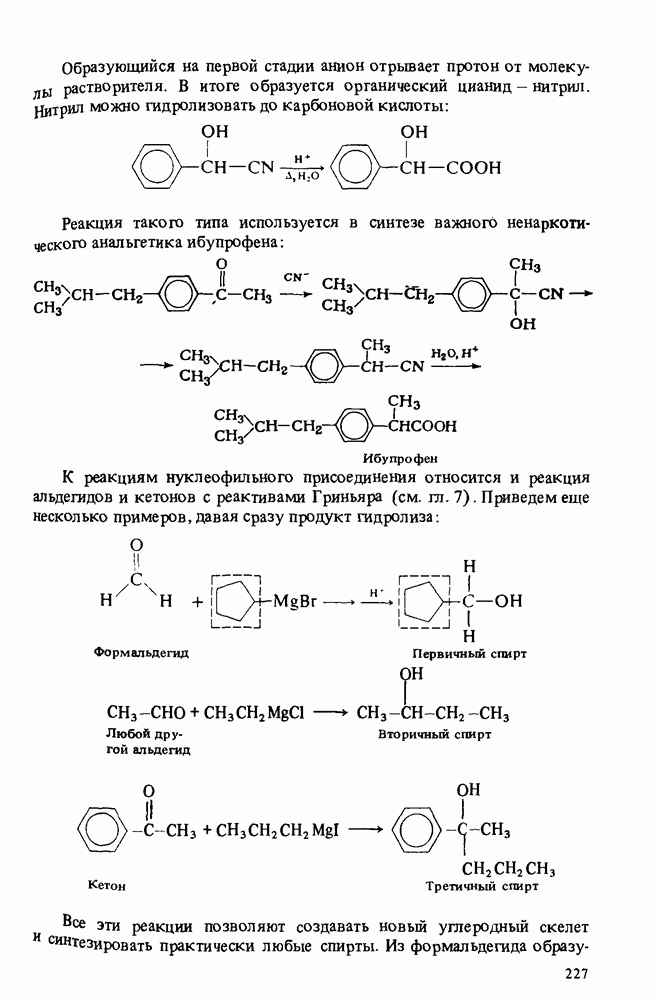
- РЕАКЦИИ АЛЬДЕГИДОВ И КЕТОНОВ
- Глава 9. АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
- НОМЕНКЛАТУРА АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ
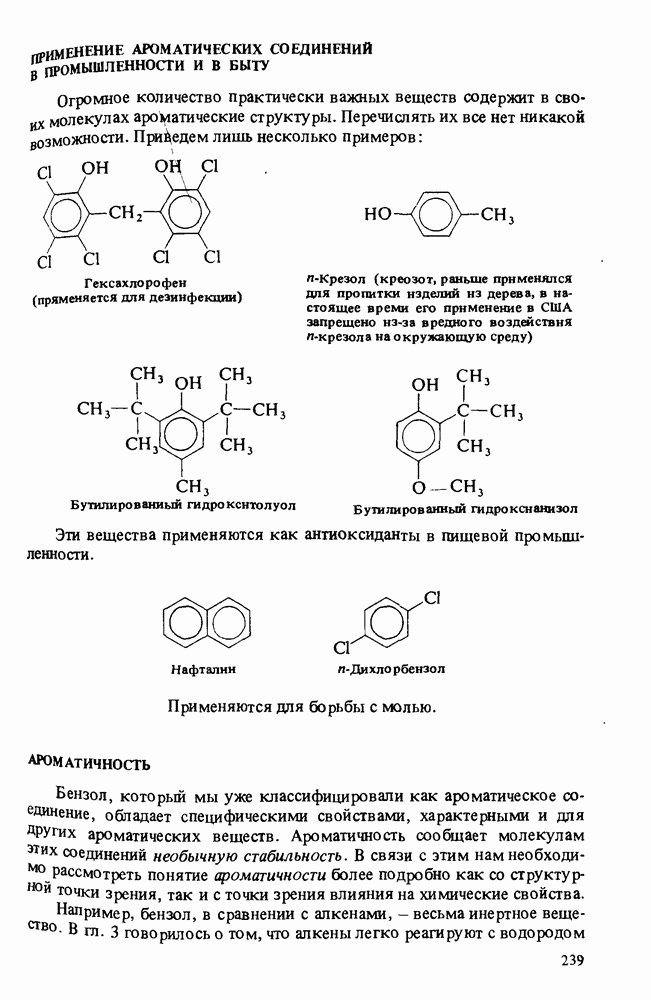
- ПРИМЕНЕНИЕ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ В ПРОМЫШЛЕННОСТИ И В БЫТУ
- АРОМАТИЧНОСТЬ
- ПОЛУЧЕНИЕ АЛКИЛЬБЕНЗОЛОВ
- РЕАКЦИИ БЕНЗОЛА И ЕГО ПРОИЗВОДНЫХ
- АРОМАТИЧЕСКОЕ ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ
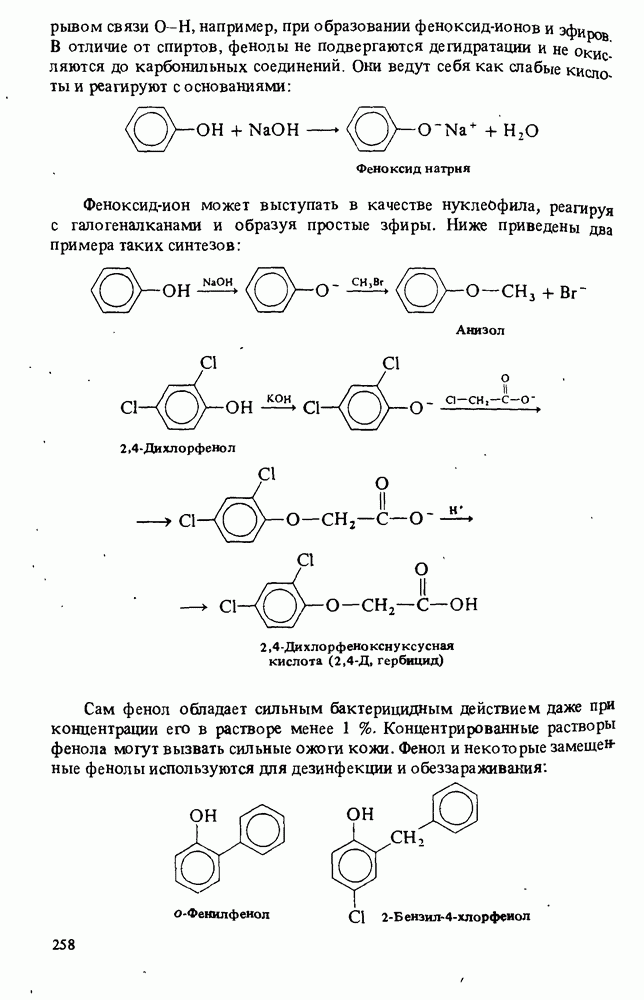
- ФЕНОЛЫ
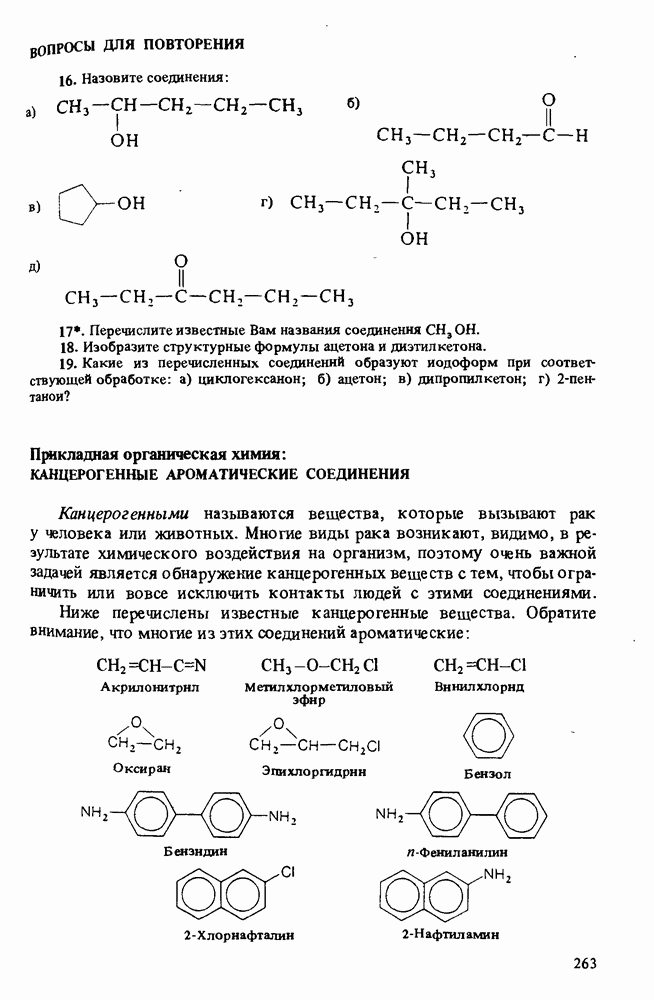
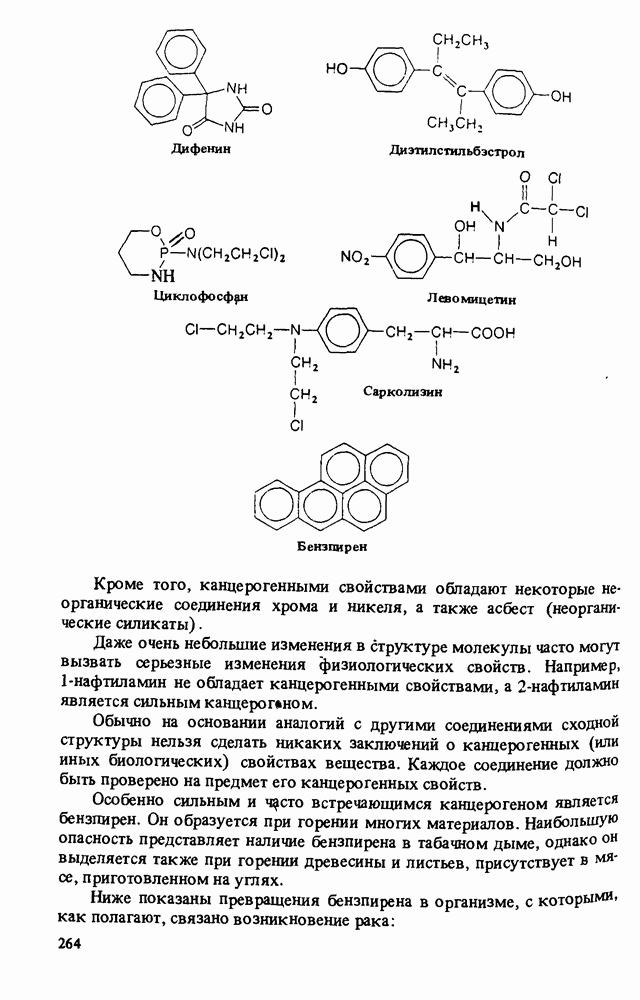
- Прикладная органическая химия: КАНЦЕРОГЕННЫЕ АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
- Глава 10. ОРГАНИЧЕСКИЙ СИНТЕЗ
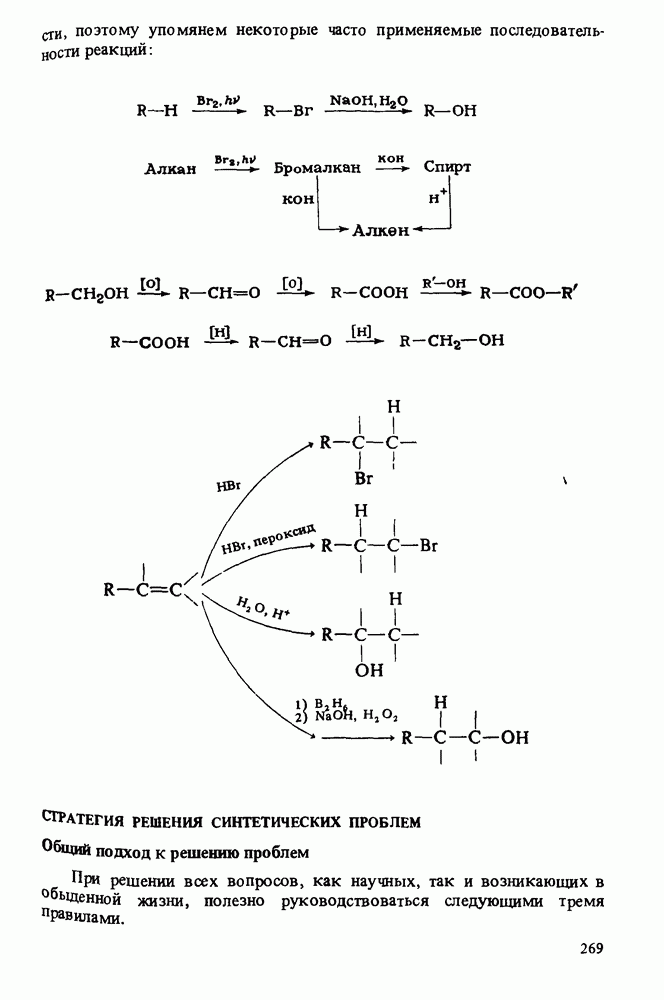
- СТРАТЕГИЯ РЕШЕНИЯ СИНТЕТИЧЕСКИХ ПРОБЛЕМ
- Глава 11. МОЛЕКУЛЯРНАЯ СПЕКТРОСКОПИЯ
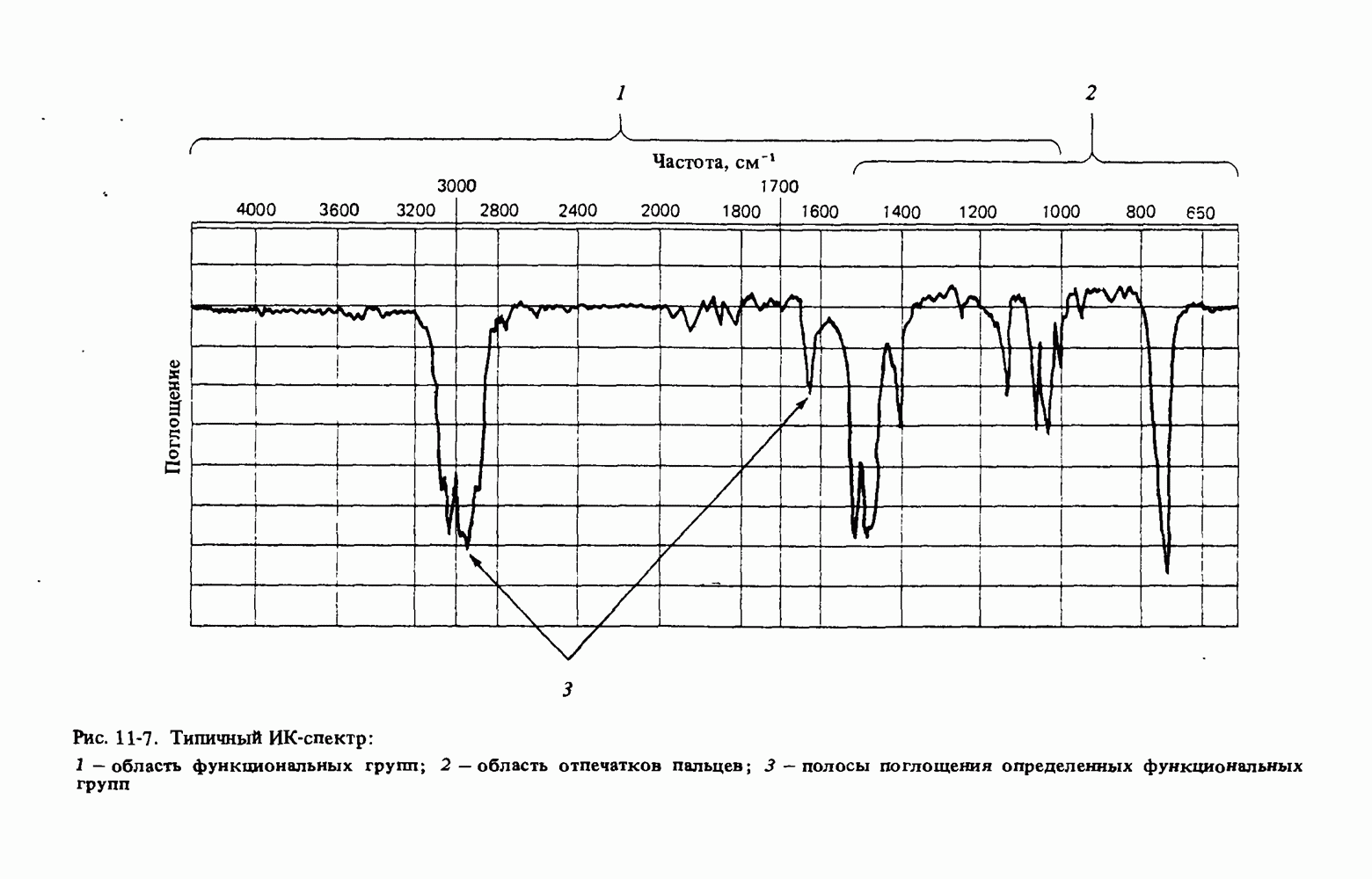
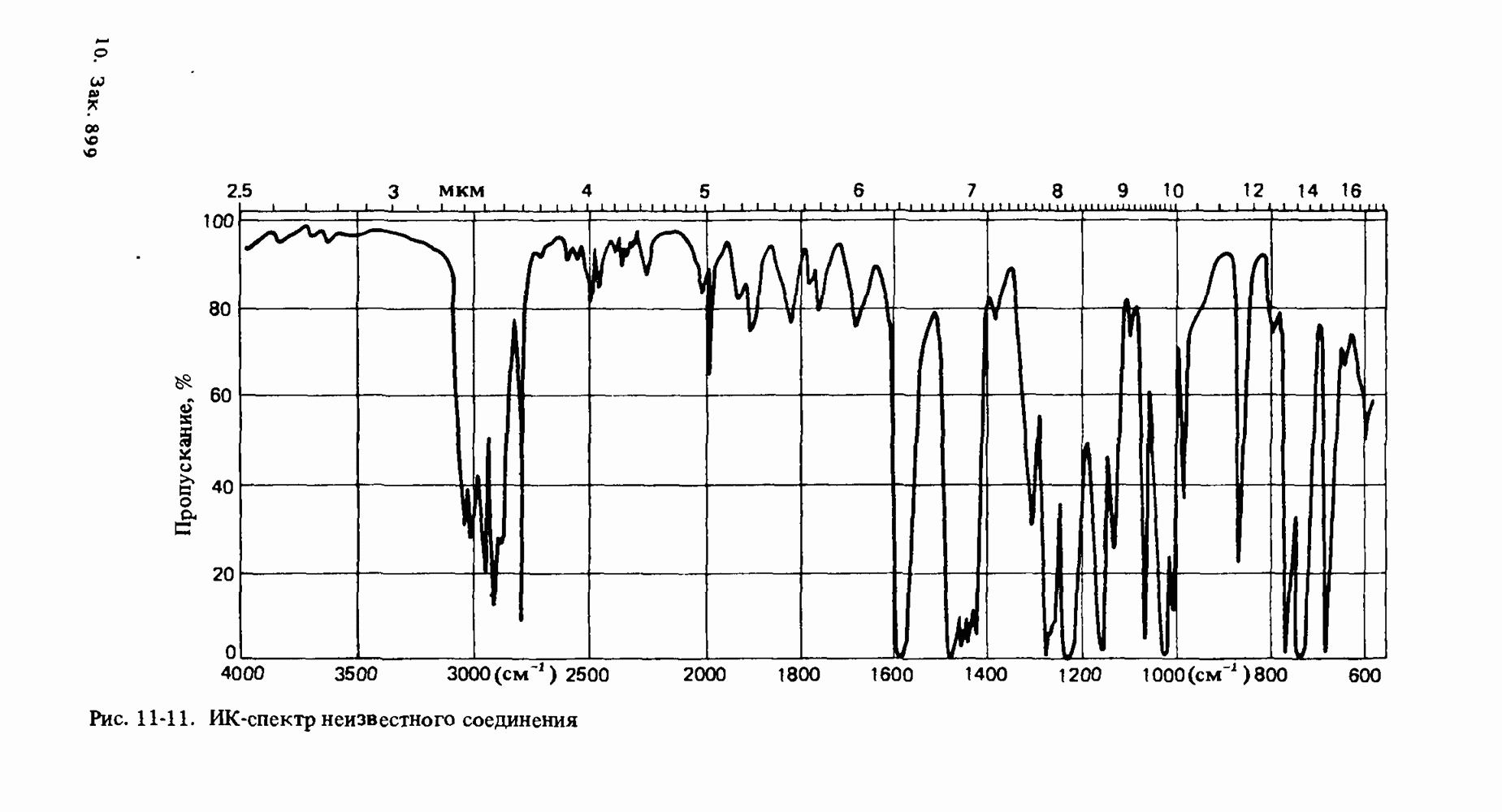
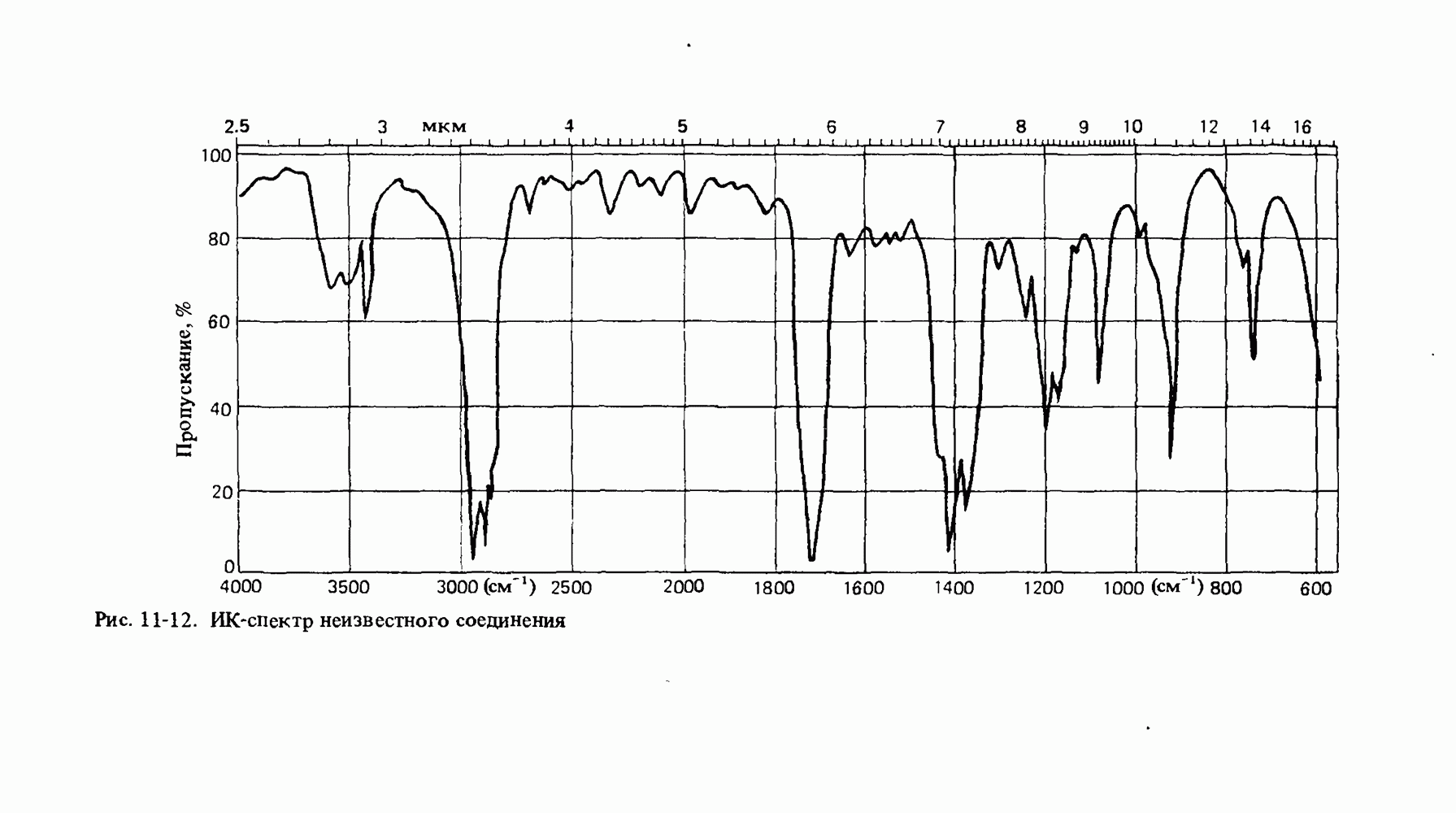
- ИНФРАКРАСНАЯ СПЕКТРОСКОПИЯ
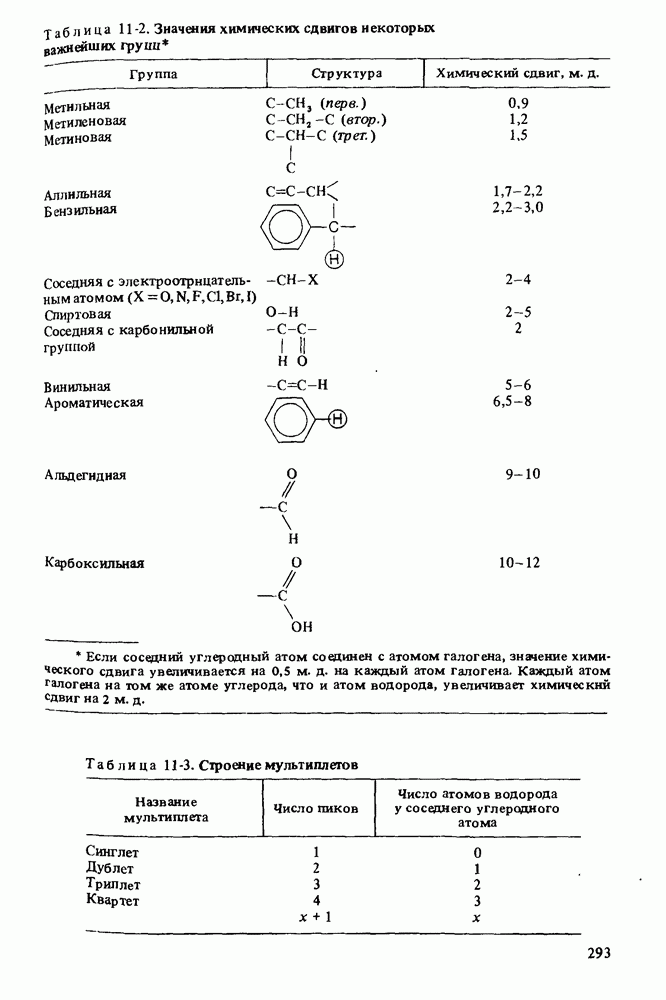
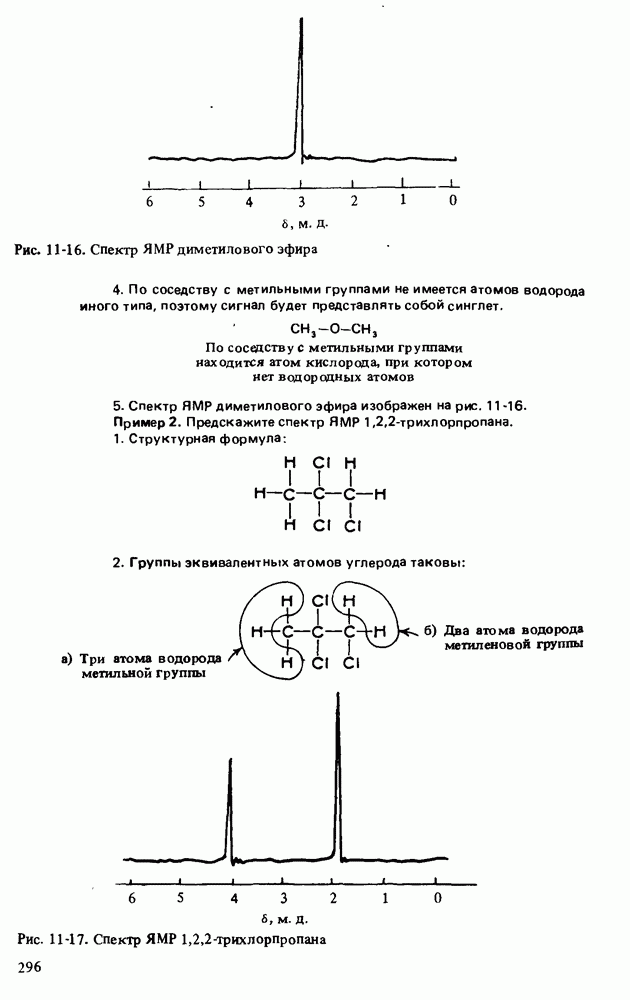
- СПЕКТРОСКОПИЯ ЯДЕРНОГО МАГНИТНОГО РЕЗОНАНСА
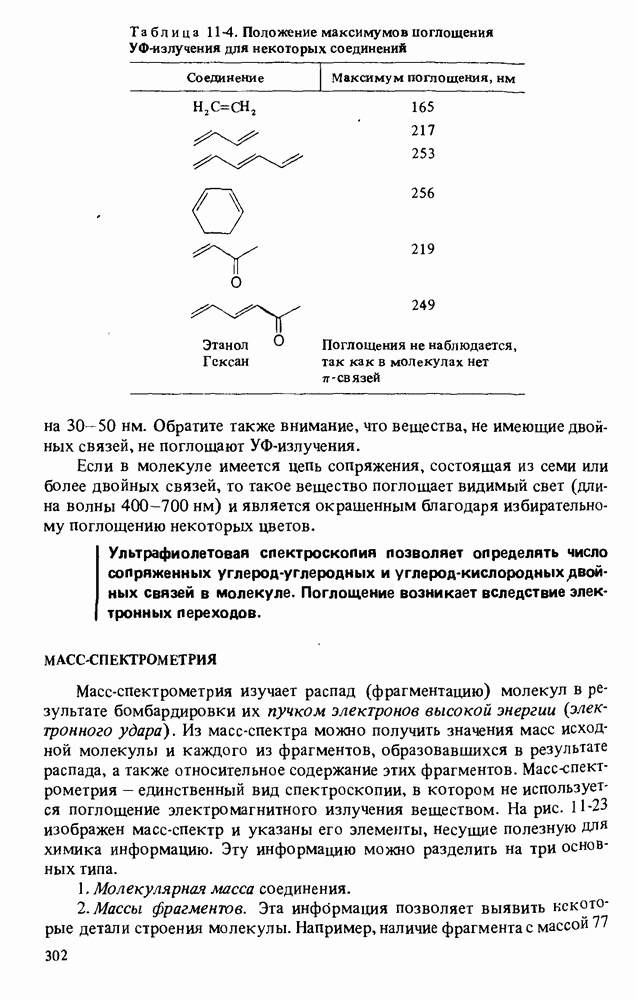
- УЛЬТРАФИОЛЕТОВАЯ СПЕКТРОСКОПИЯ
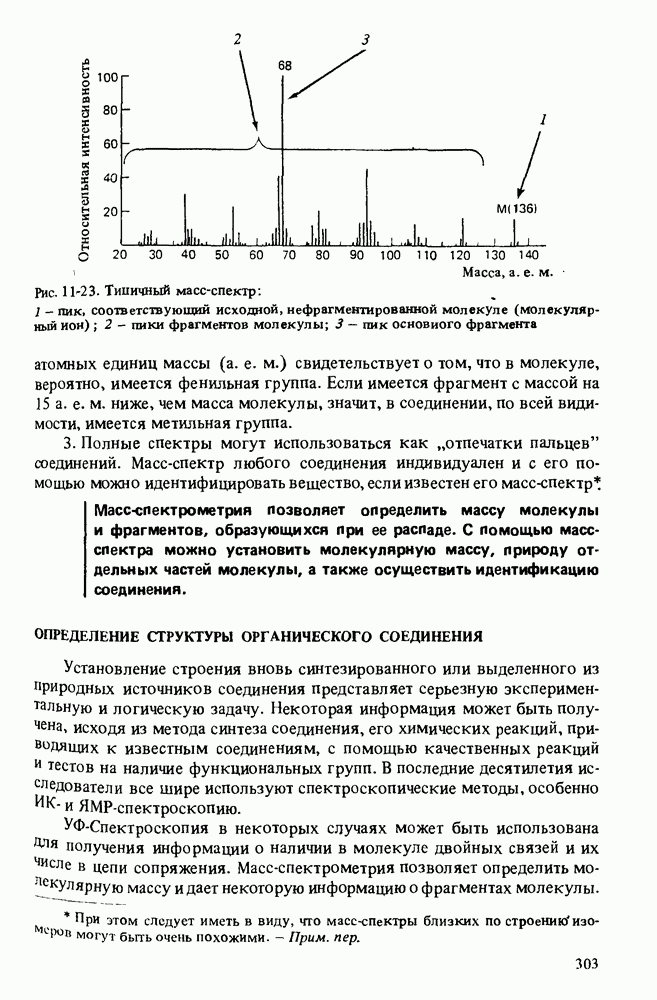
- МАСС-СПЕКТРОМЕТРИЯ
- ОПРЕДЕЛЕНИЕ СТРУКТУРЫ ОРГАНИЧЕСКОГО СОЕДИНЕНИЯ
- Прикладная органическая химия: ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ АЛКОГОЛЯ В КРОВИ
- Глава 12. КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
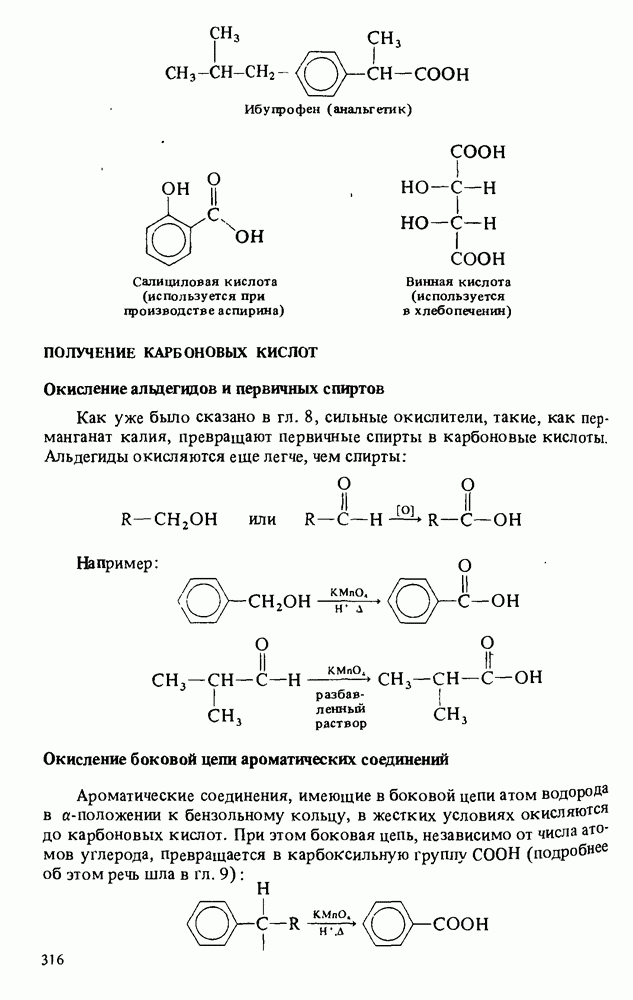
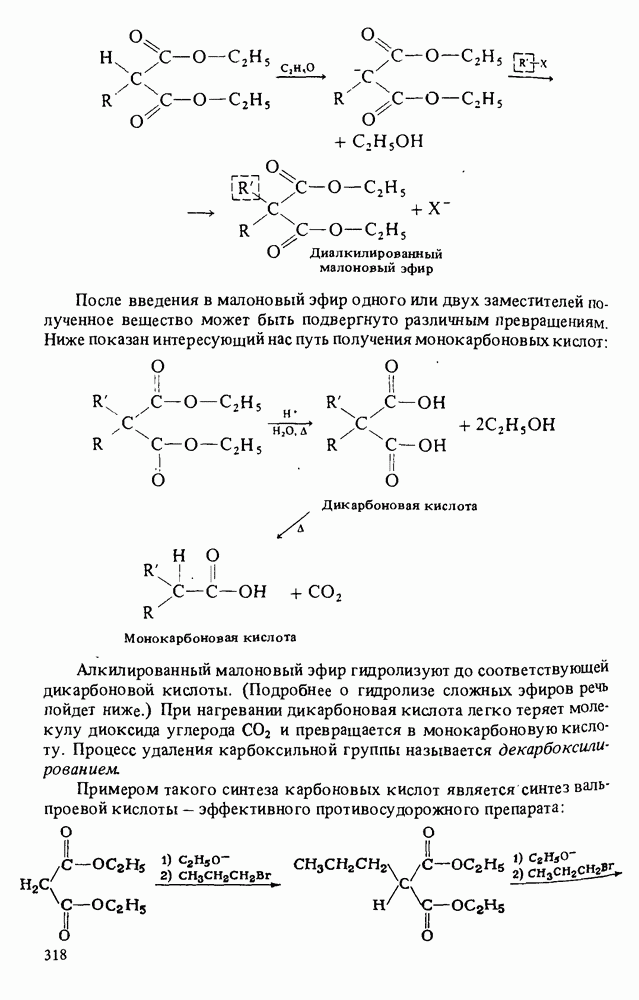
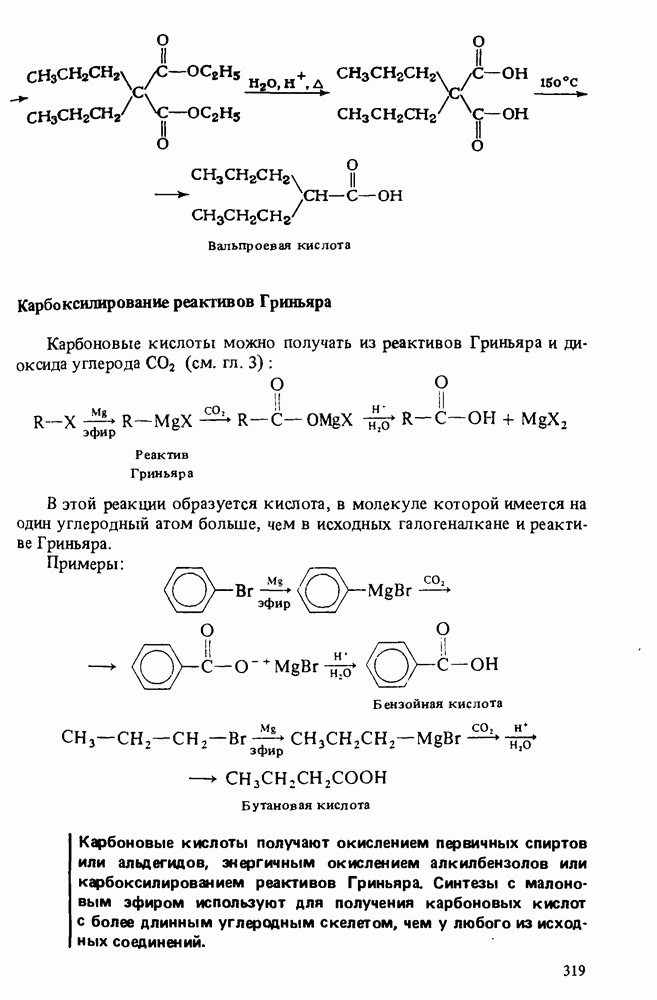
- ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ
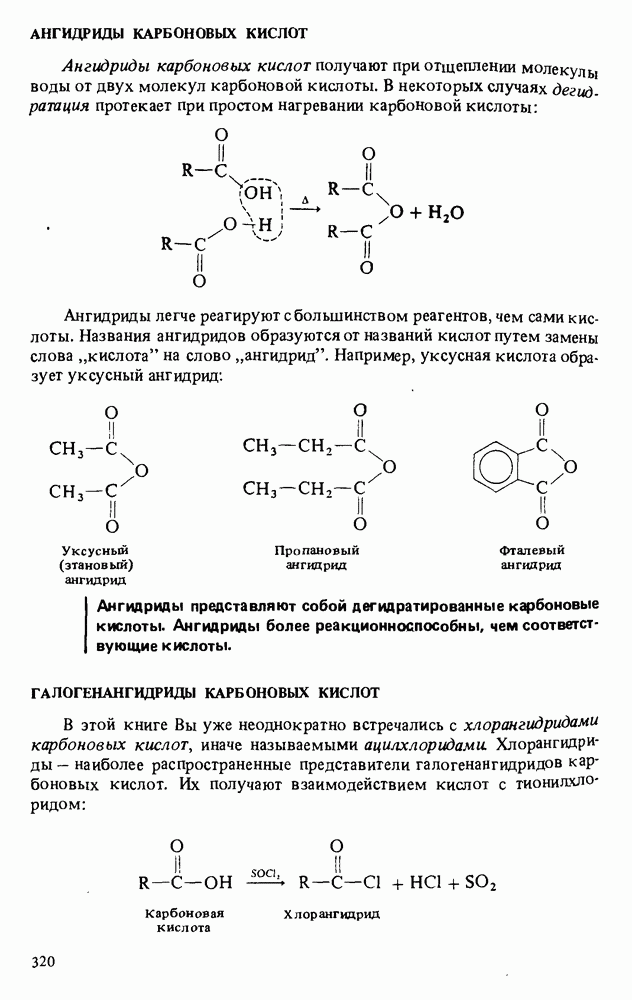
- АНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
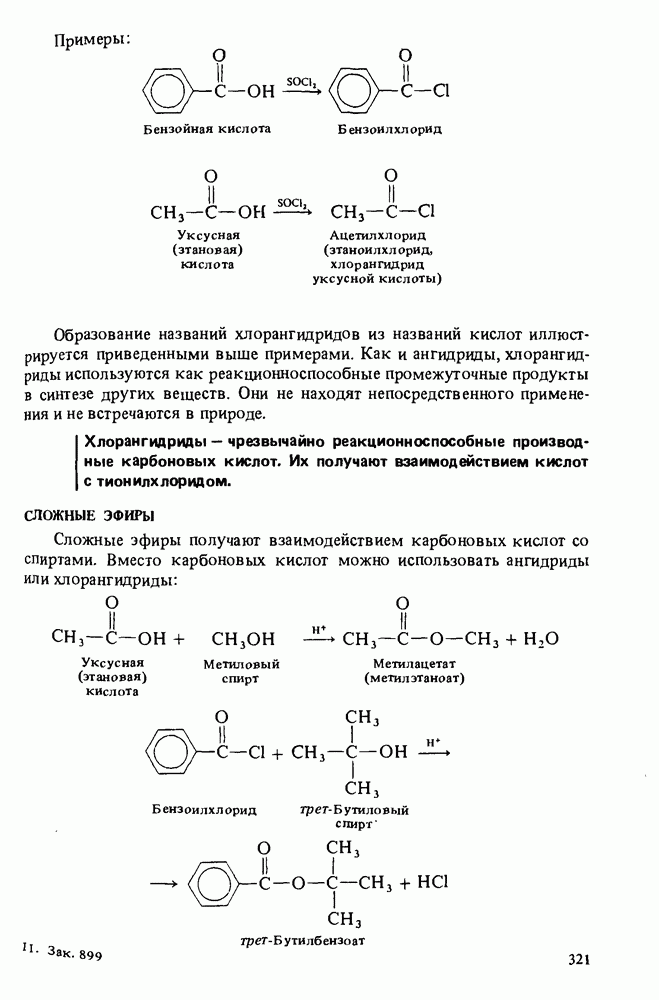
- ГАЛОГЕНАНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
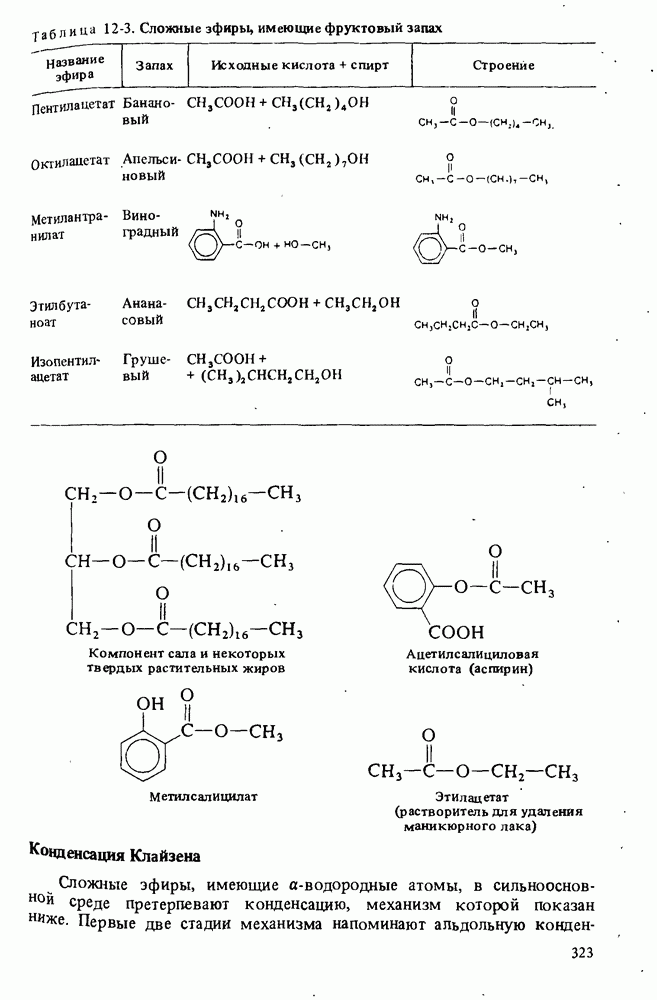
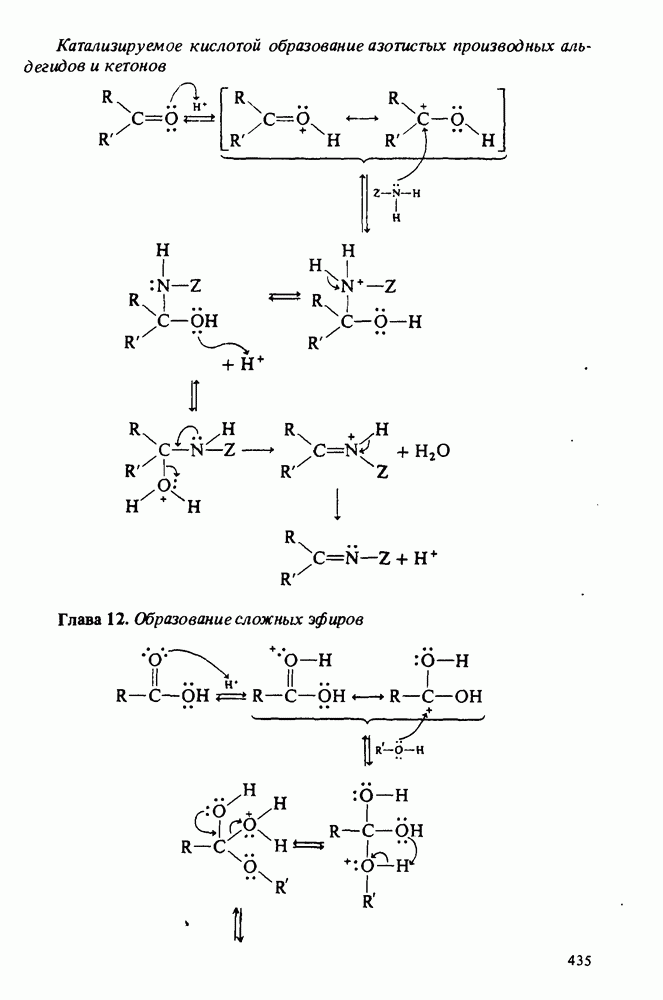
- СЛОЖНЫЕ ЭФИРЫ
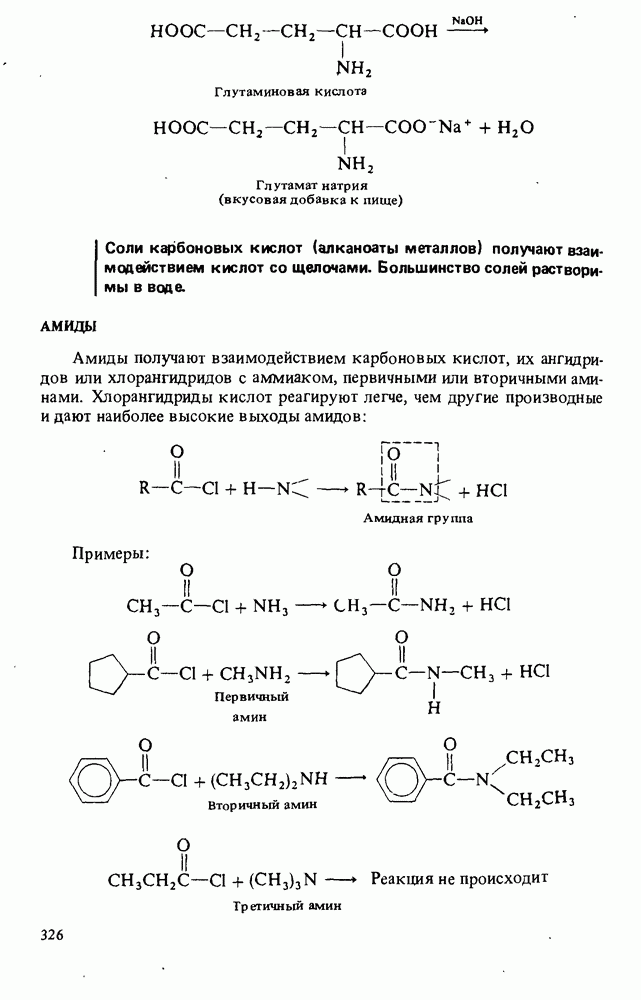
- СОЛИ
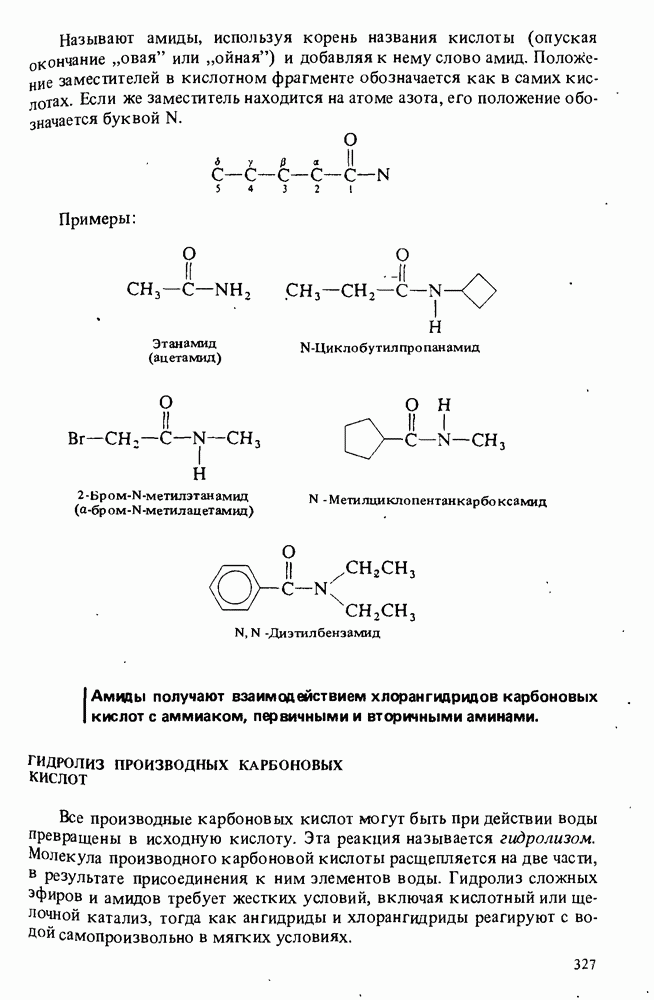
- АМИДЫ
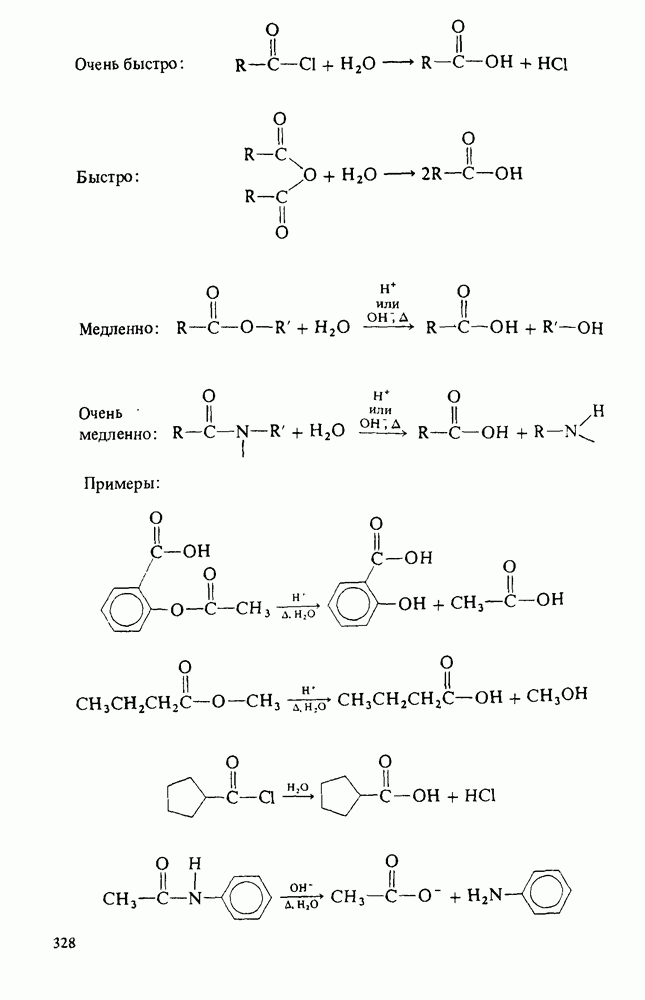
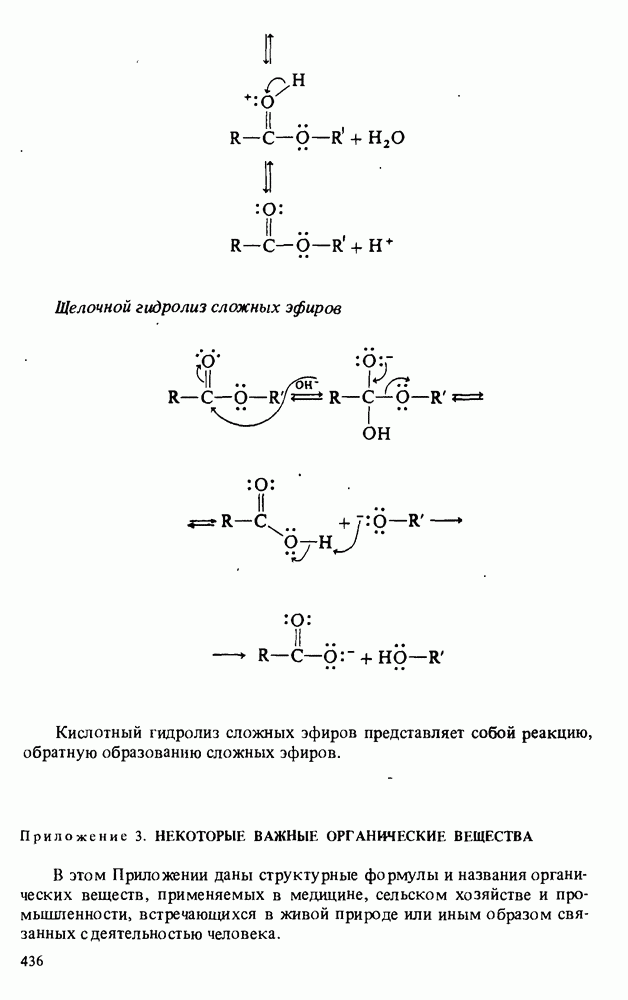
- ГИДРОЛИЗ ПРОИЗВОДНЫХ КАРБОНОВЫХ КИСЛОТ
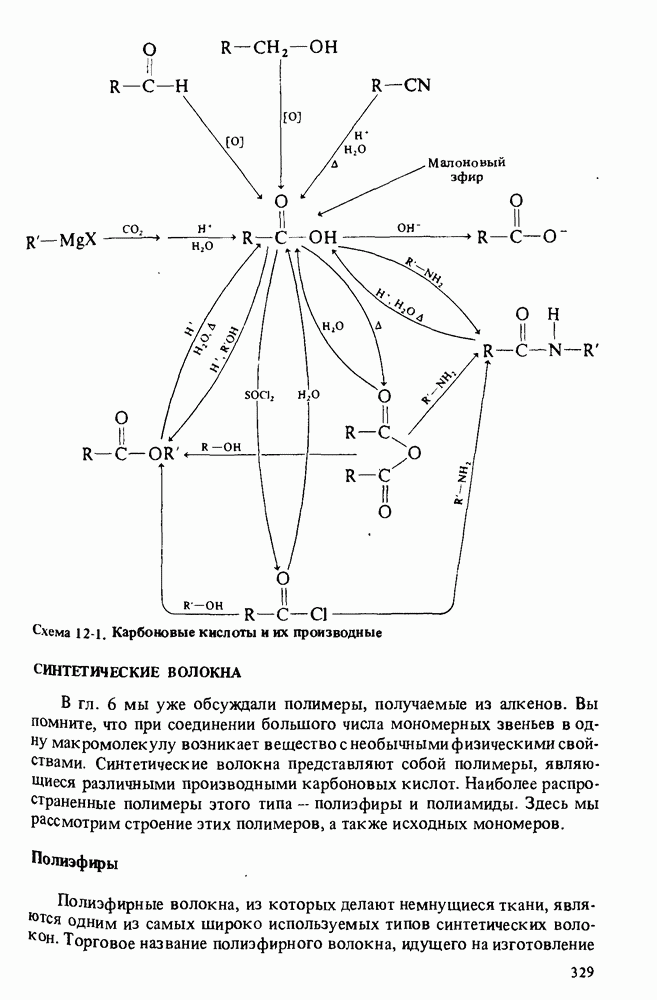
- СИНТЕТИЧЕСКИЕ ВОЛОКНА
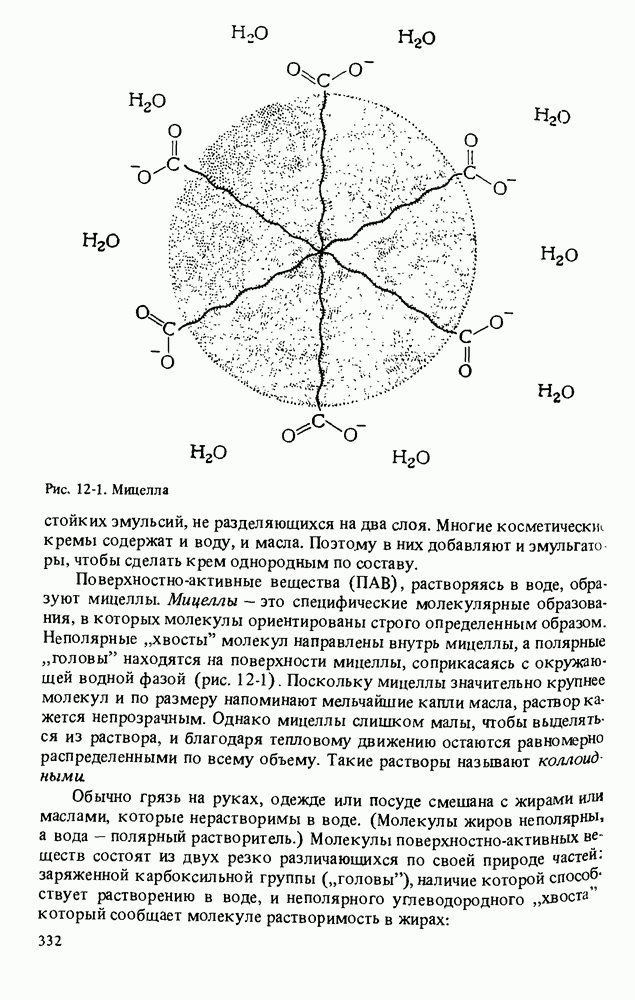
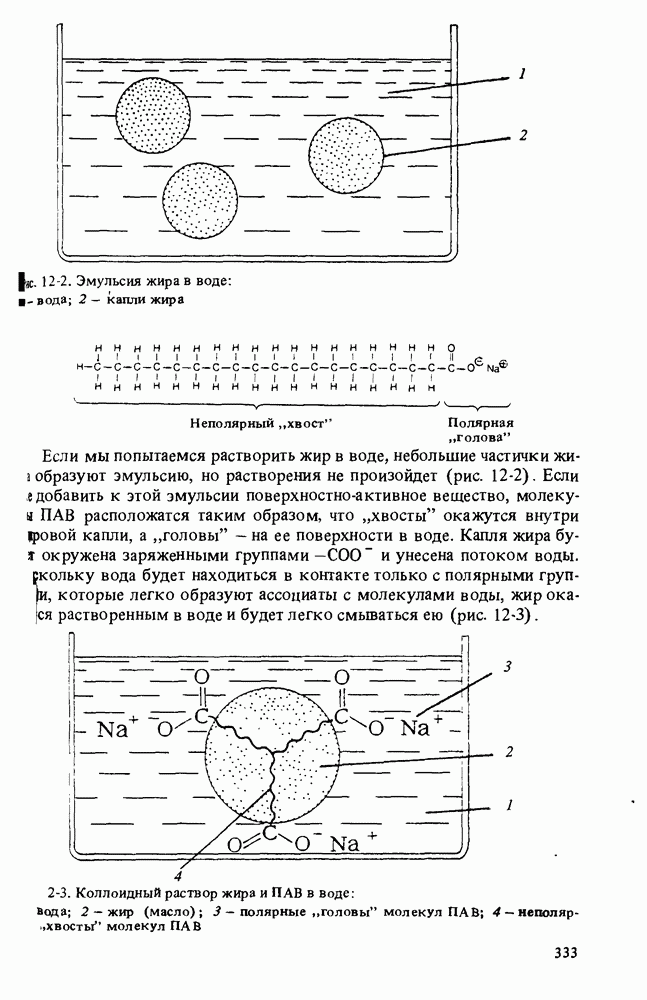
- МОЮЩИЕ СРЕДСТВА
- Прикладная органическая химия: СВОЙСТВА ВОЛОКОН
- Глава 13. АМИНЫ
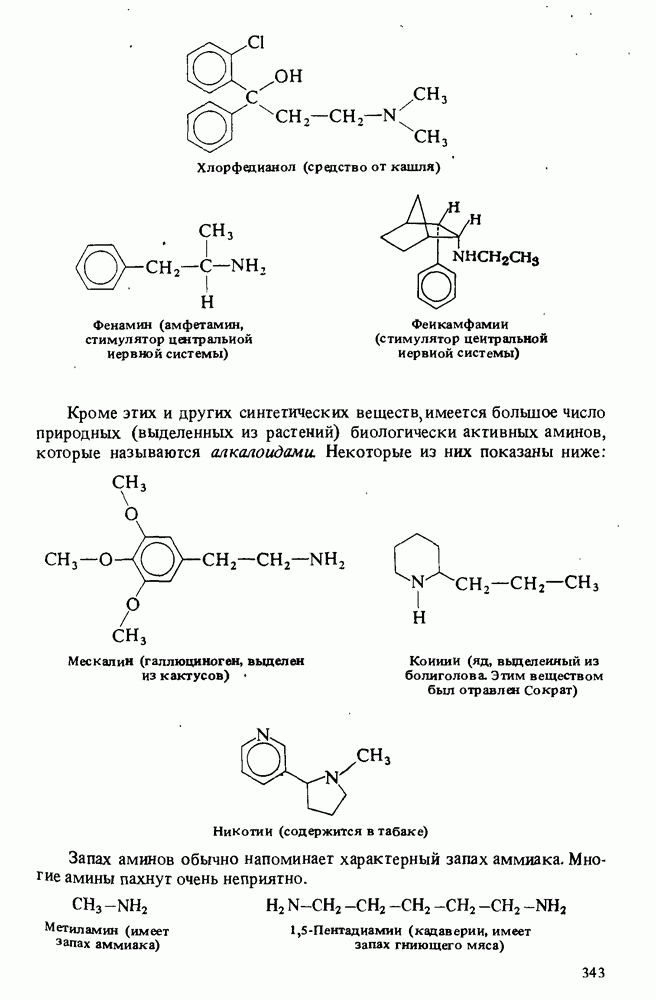
- БИОЛОГИЧЕСКИ АКТИВНЫЕ АМИНЫ
- ОСНОВНОСТЬ АМИНОВ
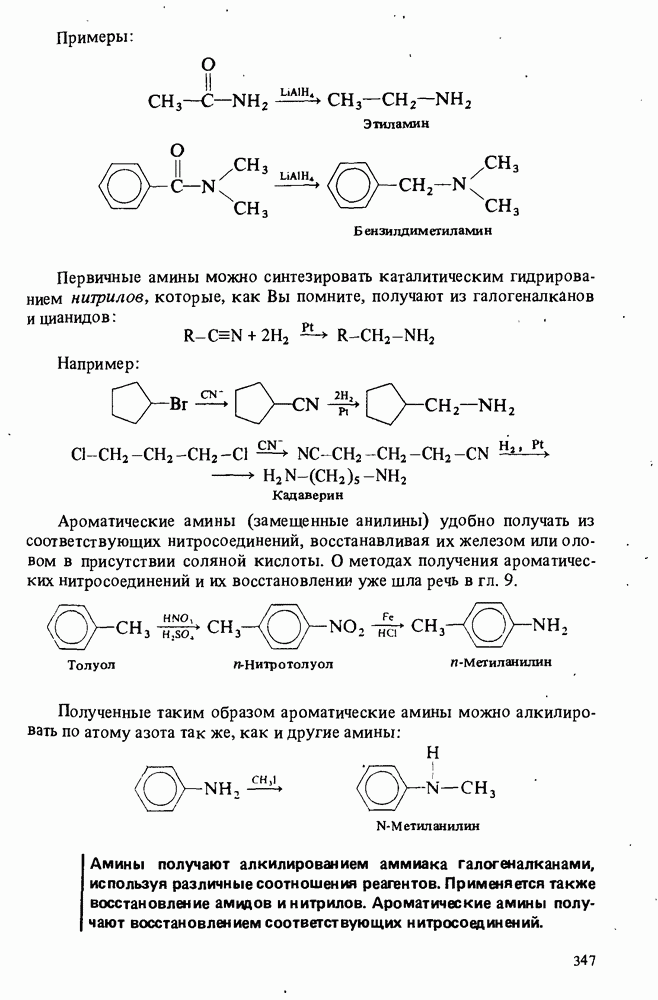
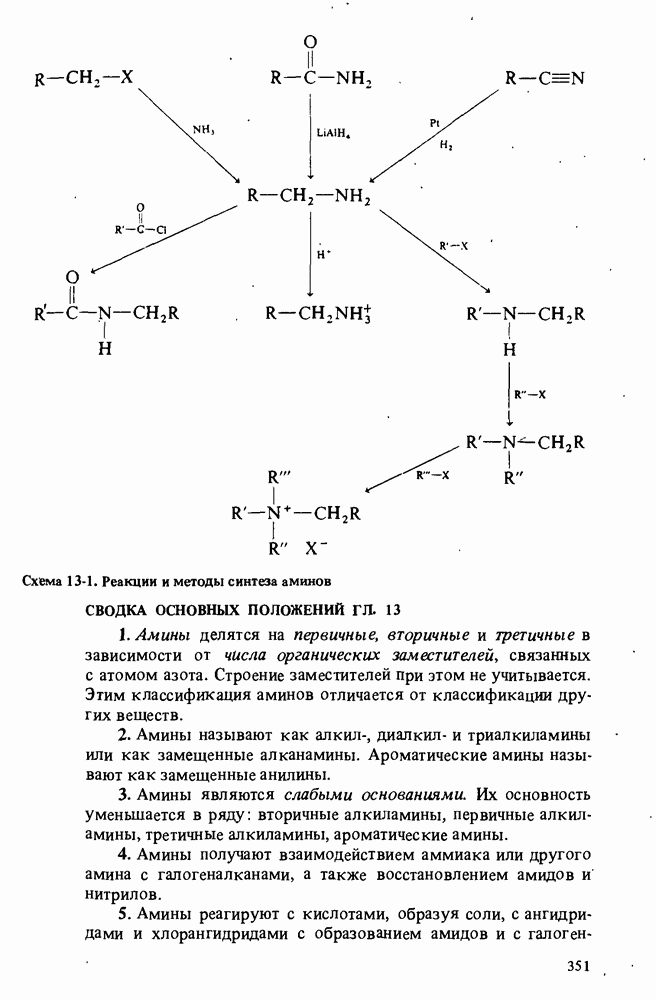
- ПОЛУЧЕНИЕ АМИНОВ
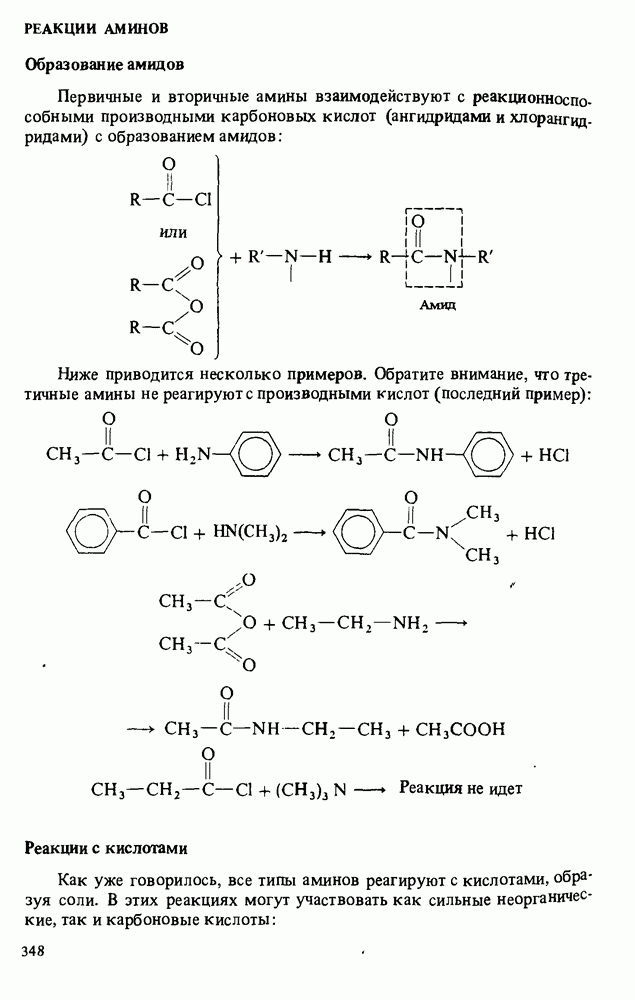
- РЕАКЦИИ АМИНОВ
- Прикладная органическая химия: ПОЛИМЕРЫ, ПОДВЕРГАЮЩИЕСЯ БИОЛОГИЧЕСКОЙ ДЕСТРУКЦИИ
- Глава 14. УГЛЕВОДЫ
- МОНОСАХАРИДЫ
- РЕАКЦИИ МОНОСАХАРИДОВ
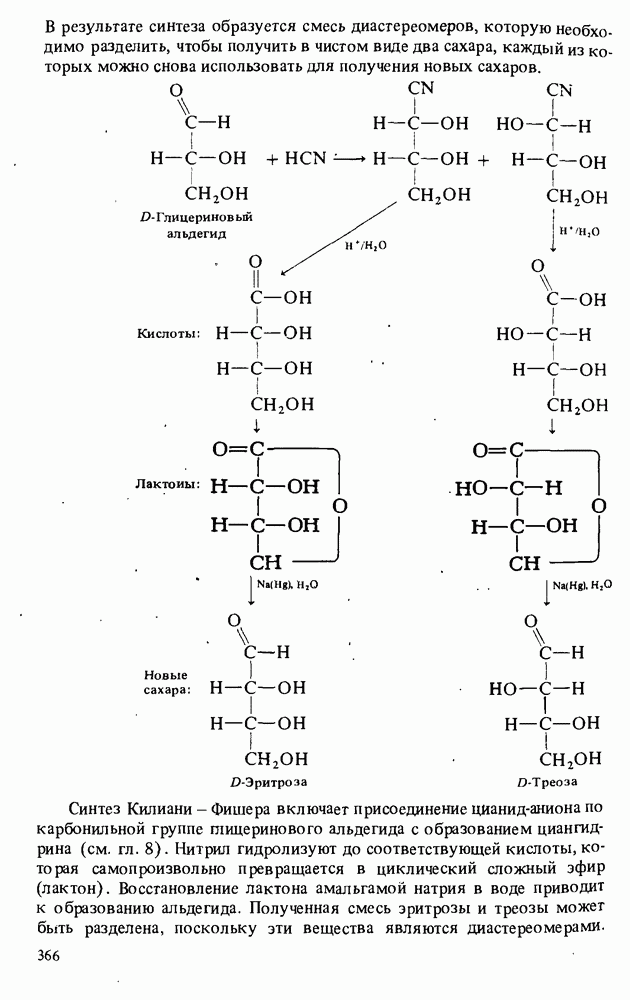
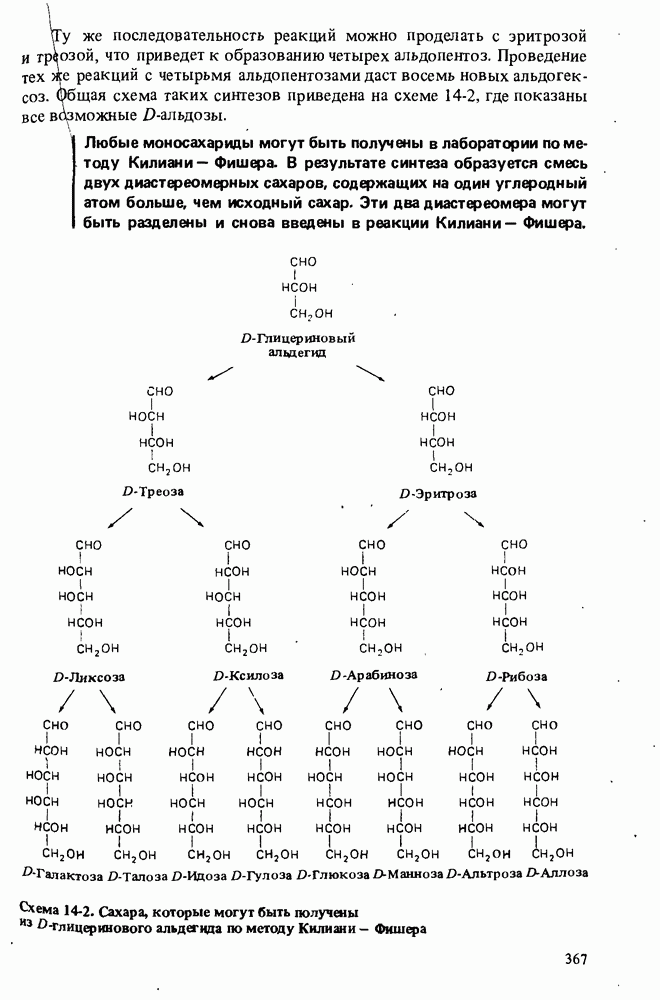
- СИНТЕЗЫ САХАРОВ
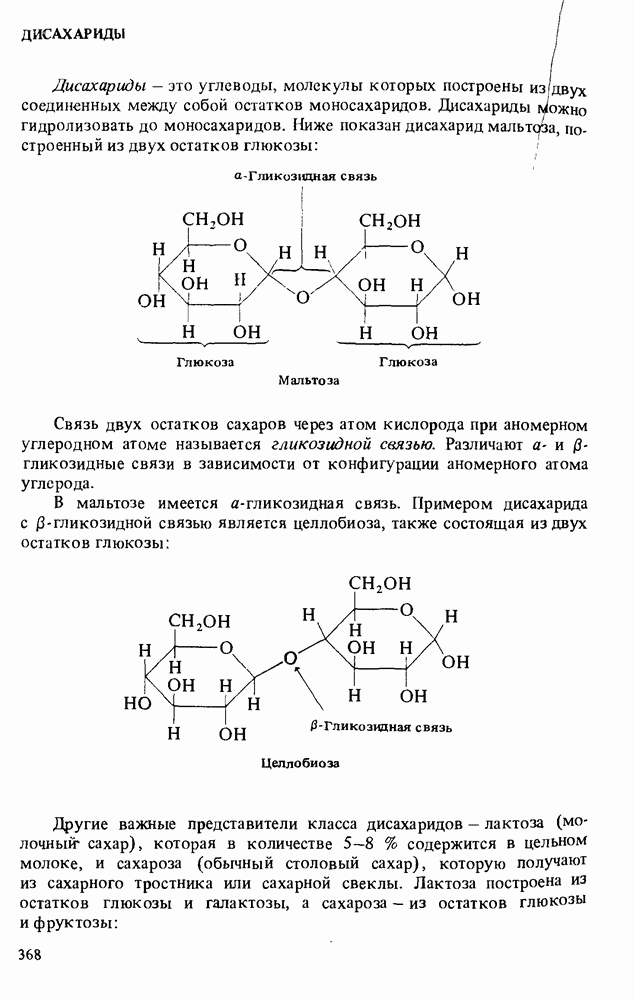
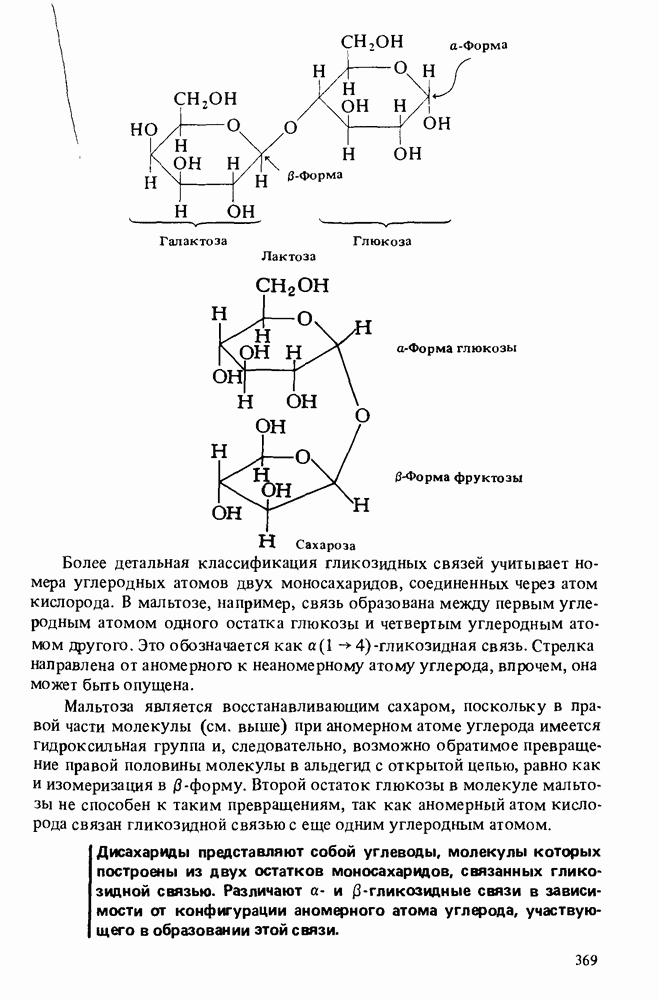
- ДИСАХАРИДЫ
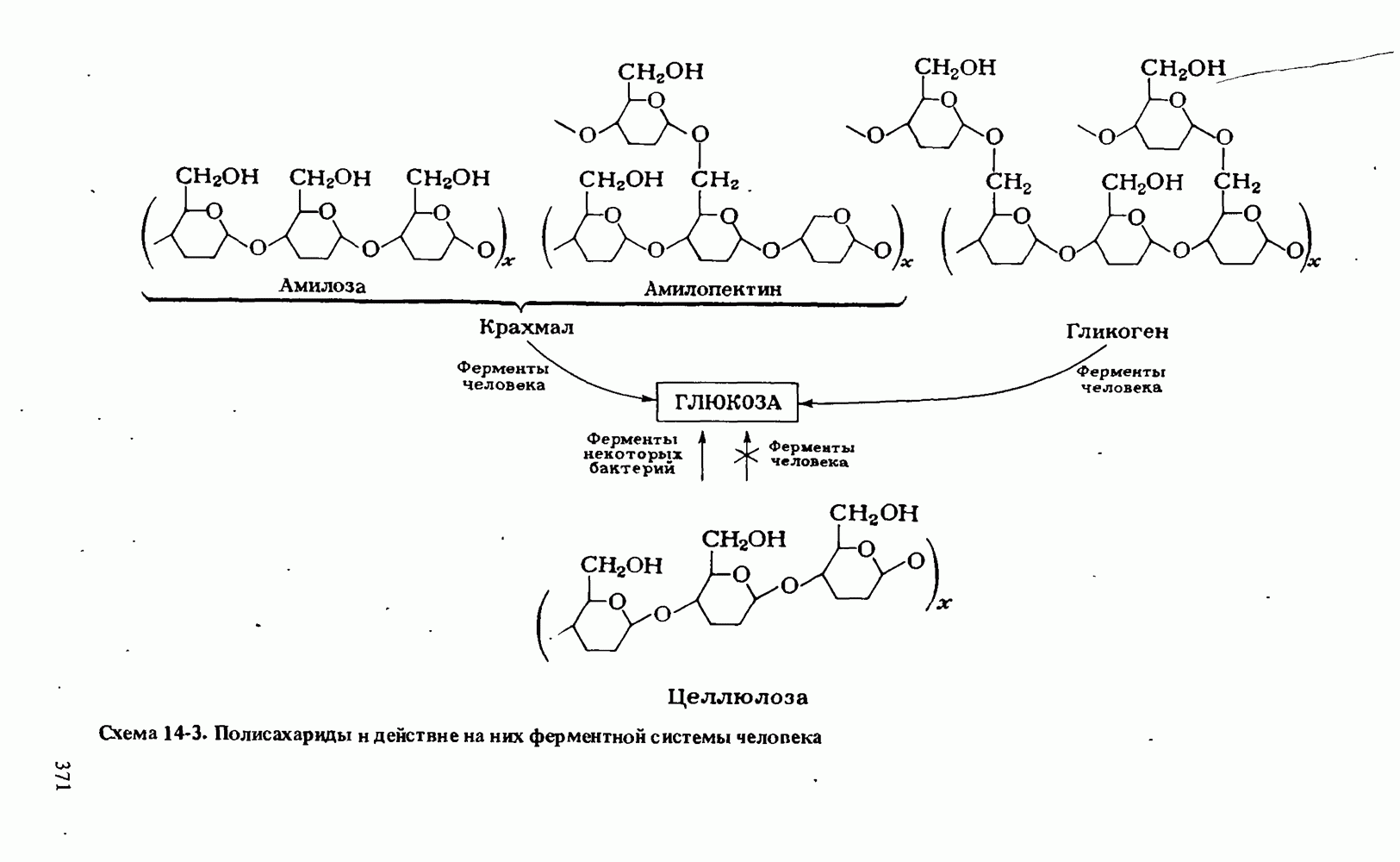
- ПОЛИСАХАРИДЫ
- Прикладная органическая химия: ПИЩЕВЫЕ СВОЙСТВА УГЛЕВОДОВ
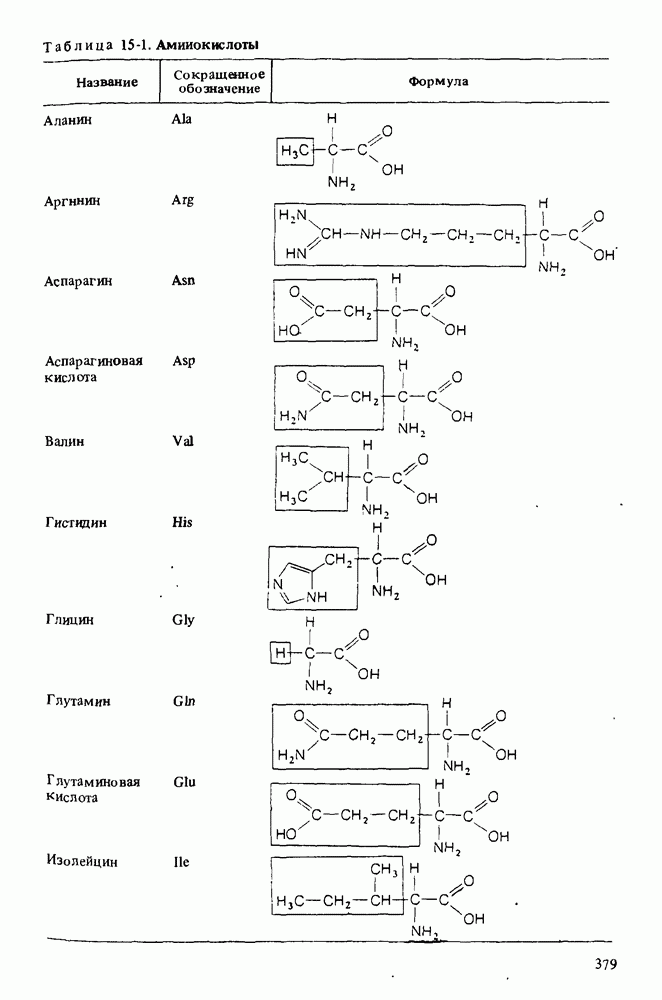
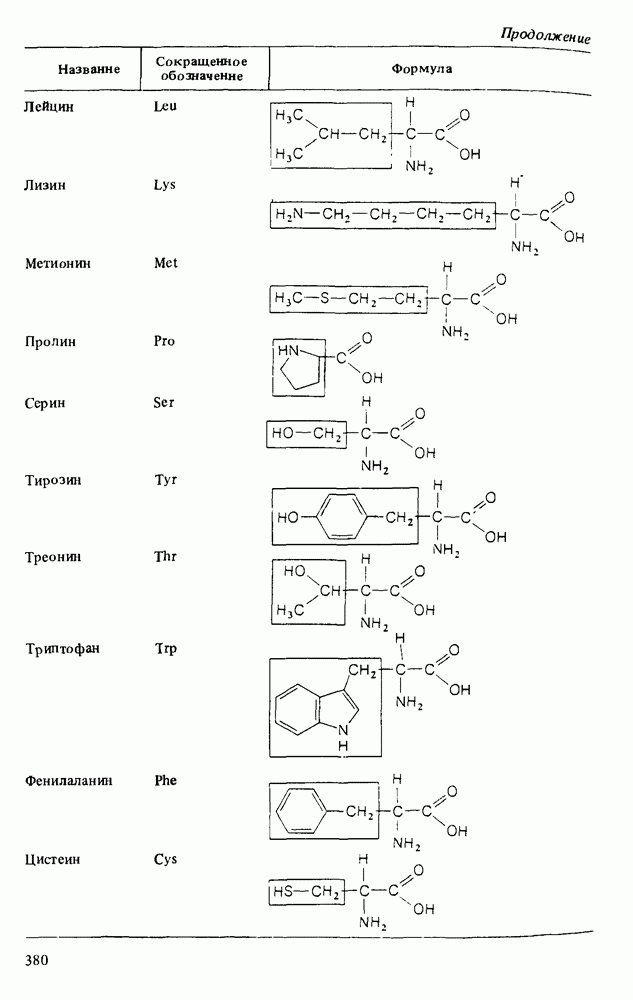
- Глава 15. АМИНОКИСЛОТЫ И БЕЛКИ
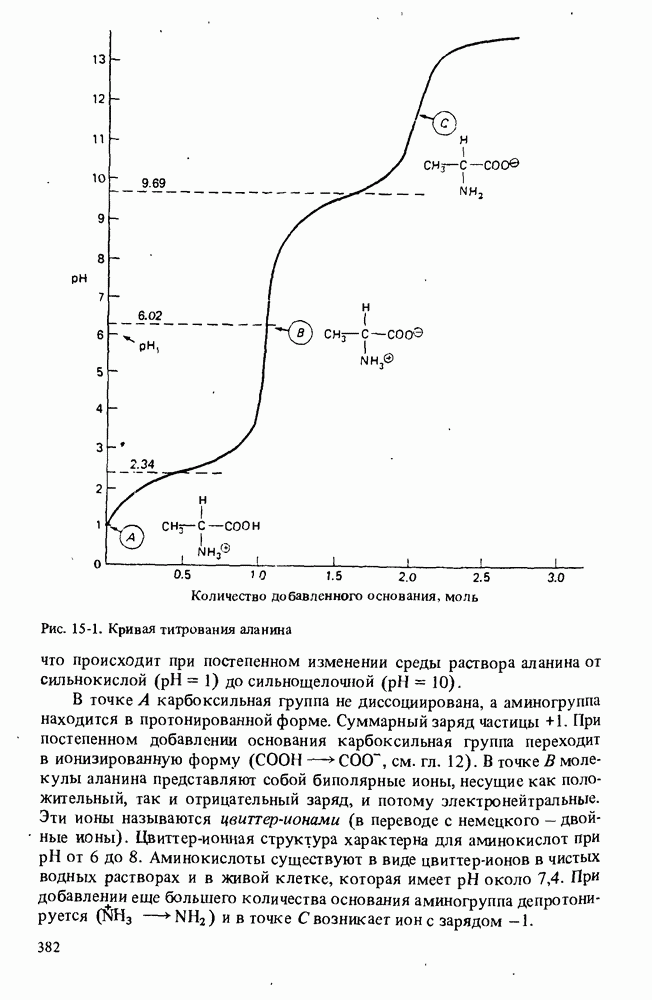
- КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА АМИНОКИСЛОТ
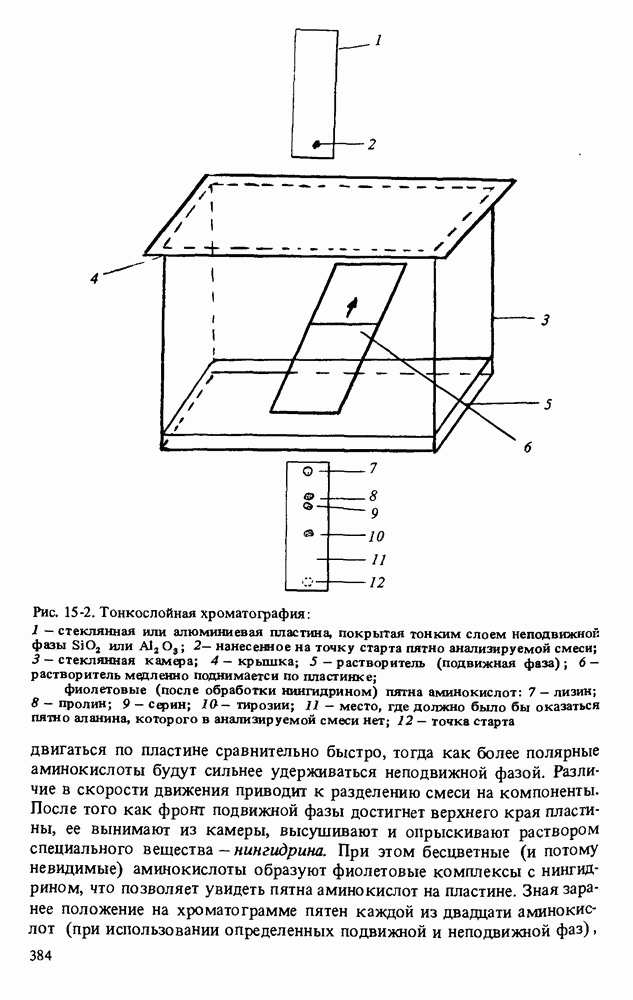
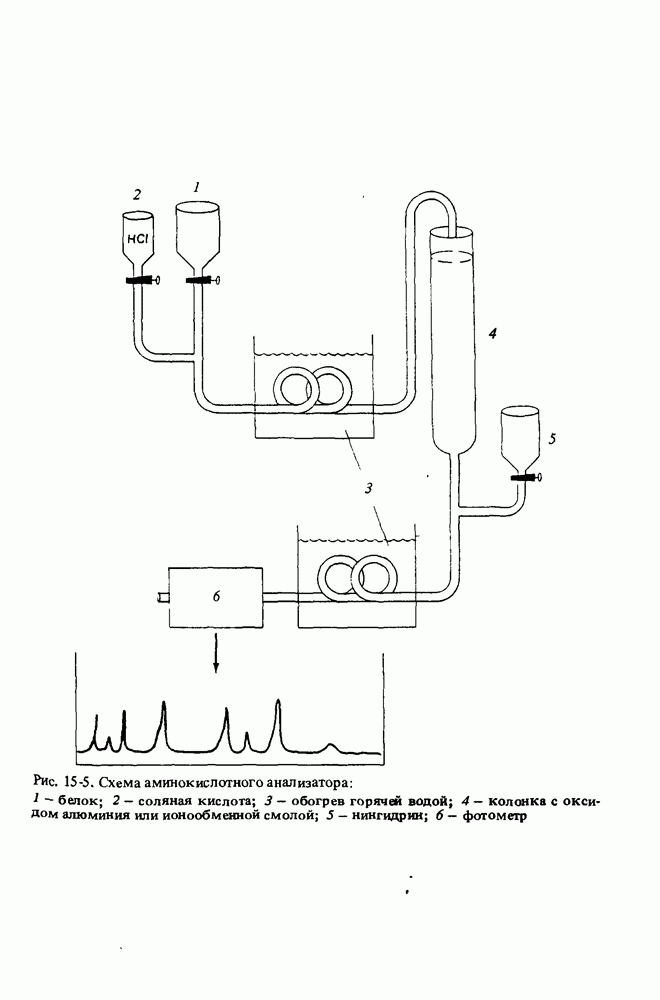
- АНАЛИЗ АМИНОКИСЛОТ
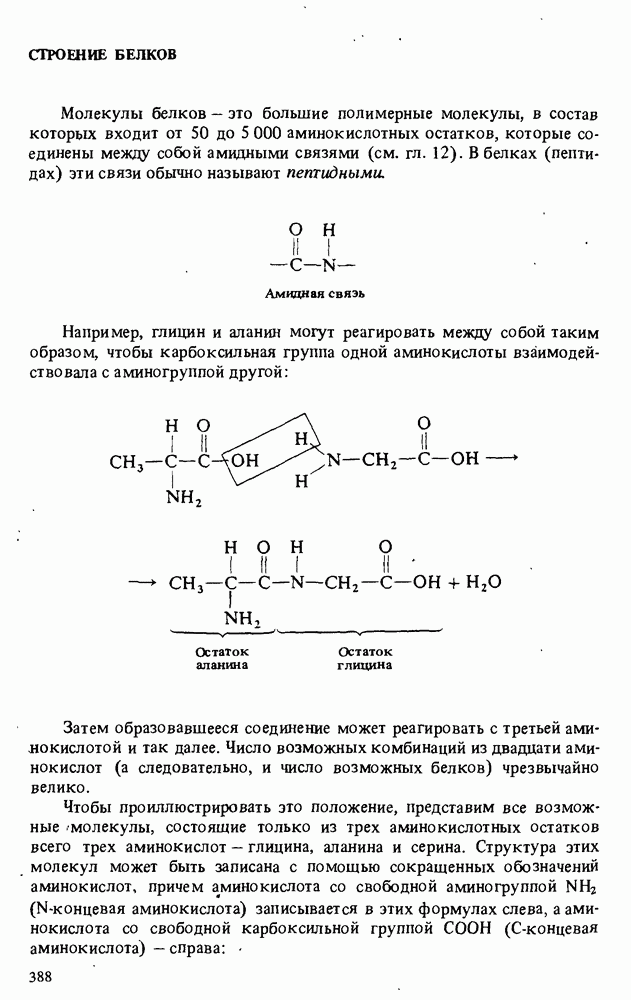
- СТРОЕНИЕ БЕЛКОВ
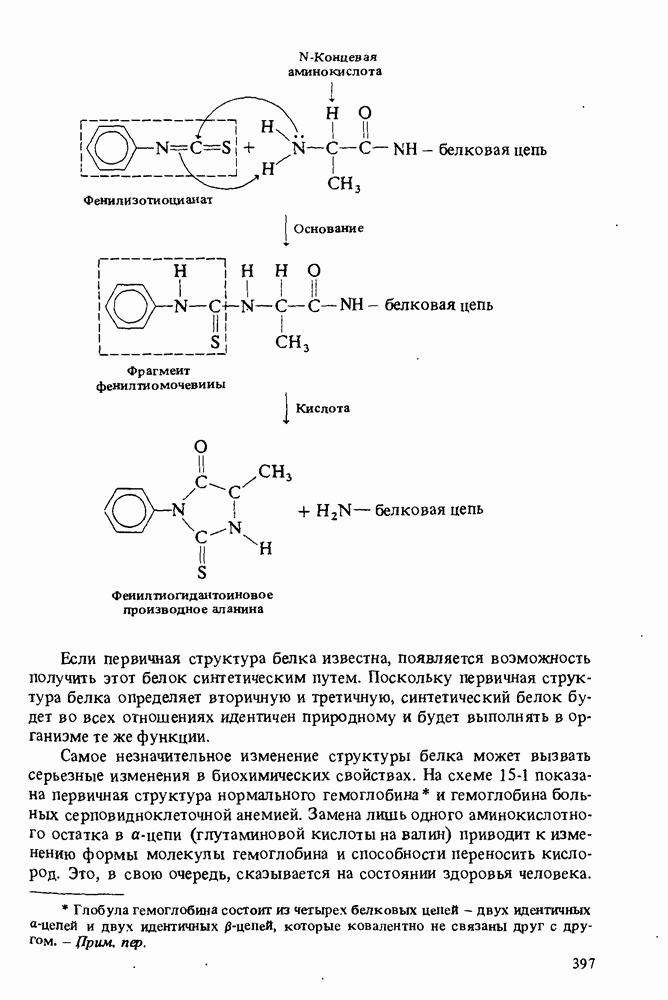
- УСТАНОВЛЕНИЕ ПЕРВИЧНОЙ СТРУКТУРЫ БЕЛКОВ
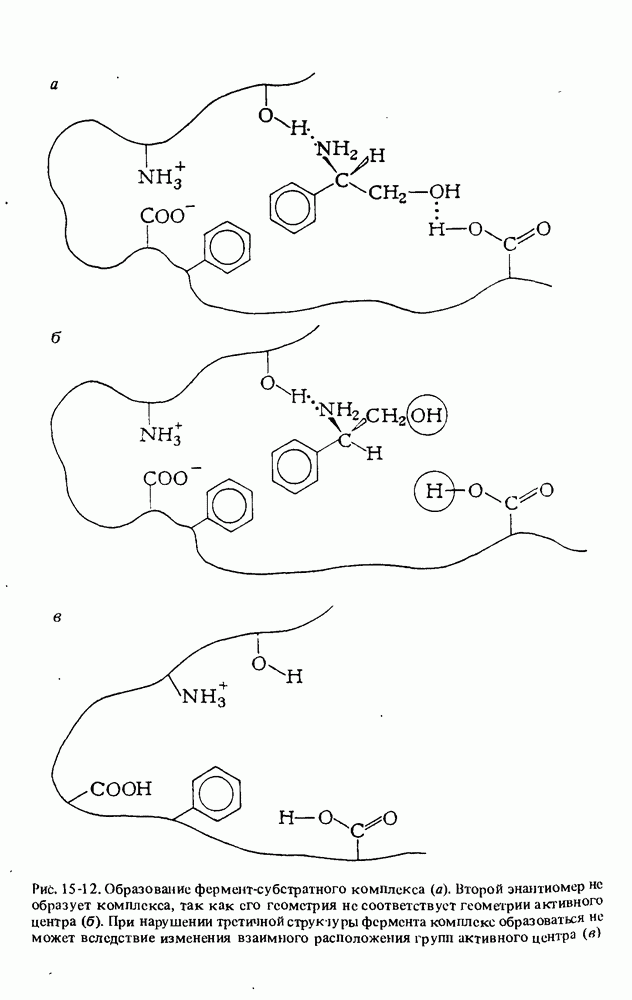
- ФЕРМЕНТЫ
- Глава 16. ЛИПИДЫ
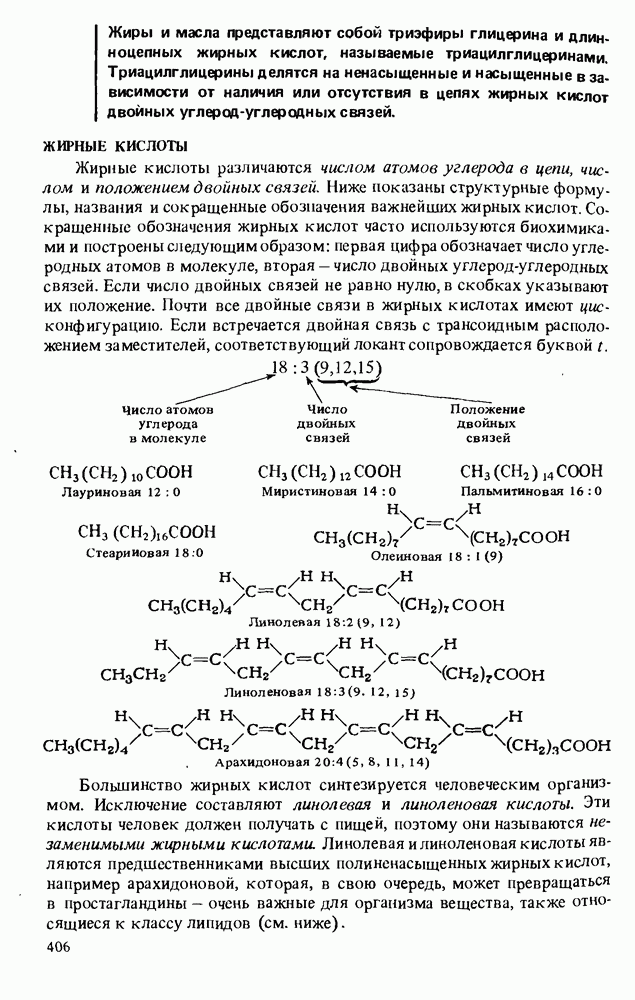
- ЖИРНЫЕ КИСЛОТЫ
- НАЗВАНИЯ ТРИАЦИЛГЛИЦЕРИНОВ
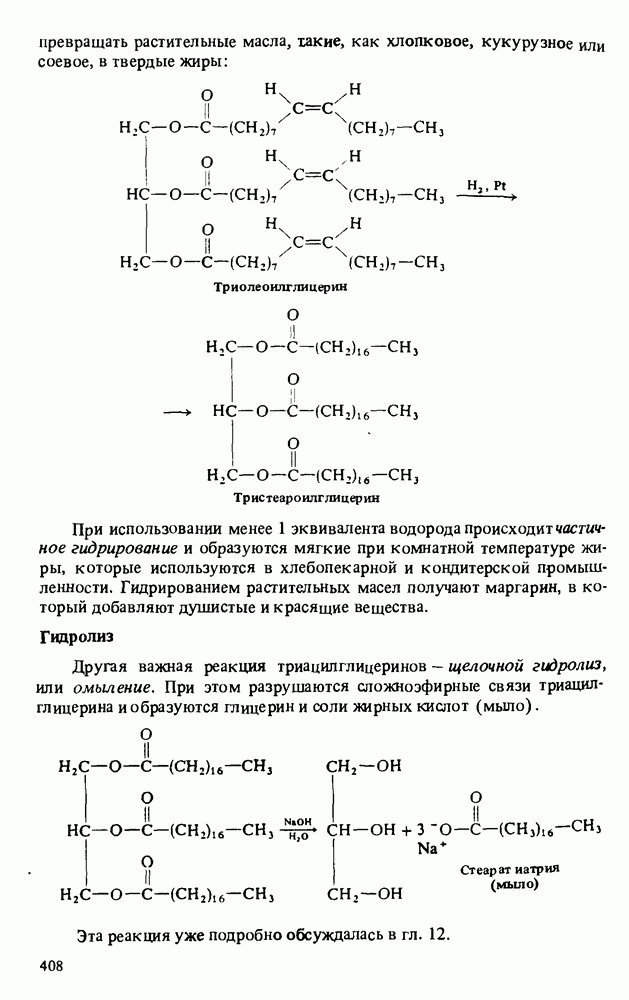
- РЕАКЦИИ ТРИАЦИЛГЛИЦЕРИНОВ
- ЛИПИДЫ, ОТЛИЧНЫЕ ОТ ТРИАЦИЛГЛИЦЕРИНОВ
- Прикладная органическая химия: ПИЩЕВЫЕ СВОЙСТВА ЛИПИДОВ
- Глава 17. НУКЛЕИНОВЫЕ КИСЛОТЫ
- РИБОНУКЛЕИНОВЫЕ КИСЛОТЫ
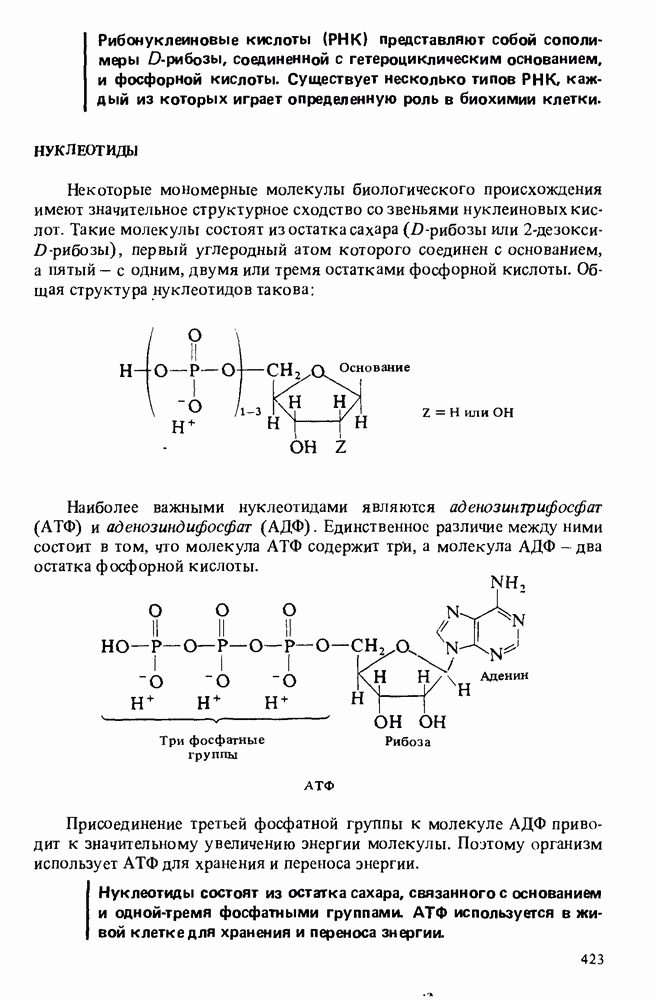
- НУКЛЕОТИДЫ
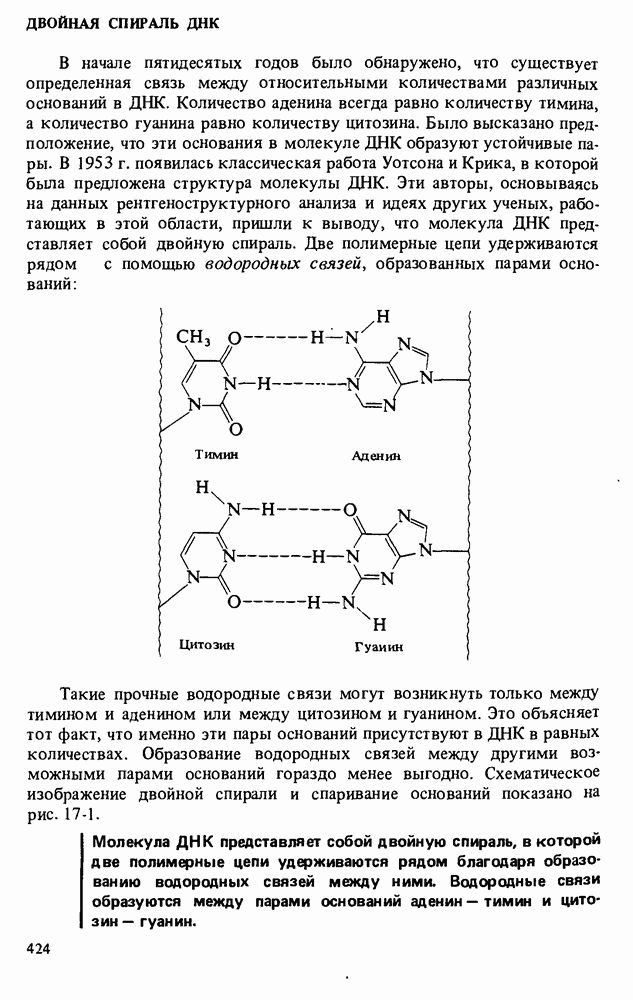
- ДВОЙНАЯ СПИРАЛЬ ДНК
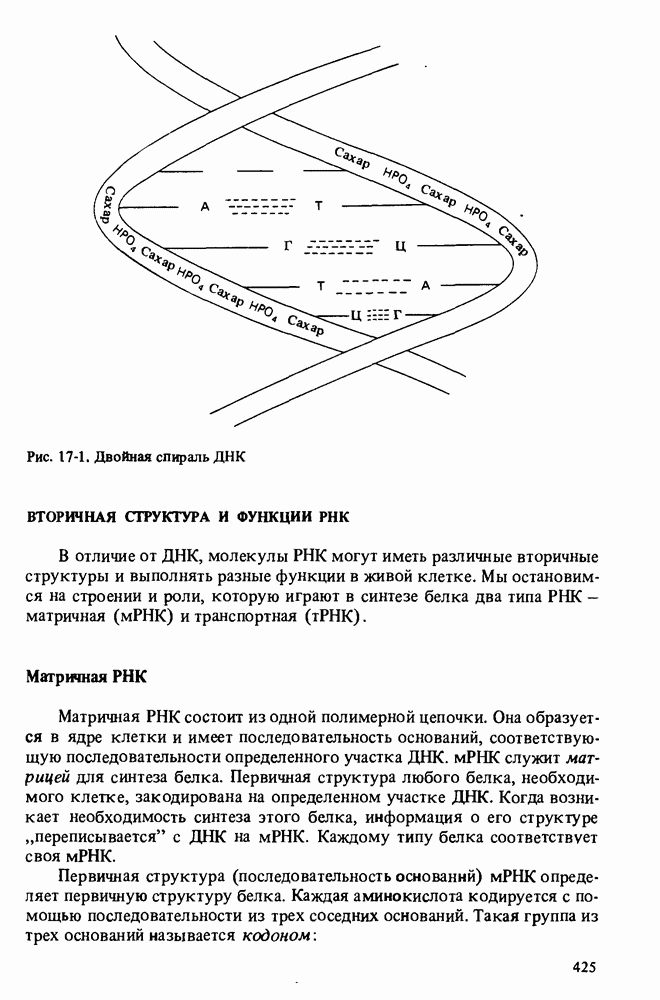
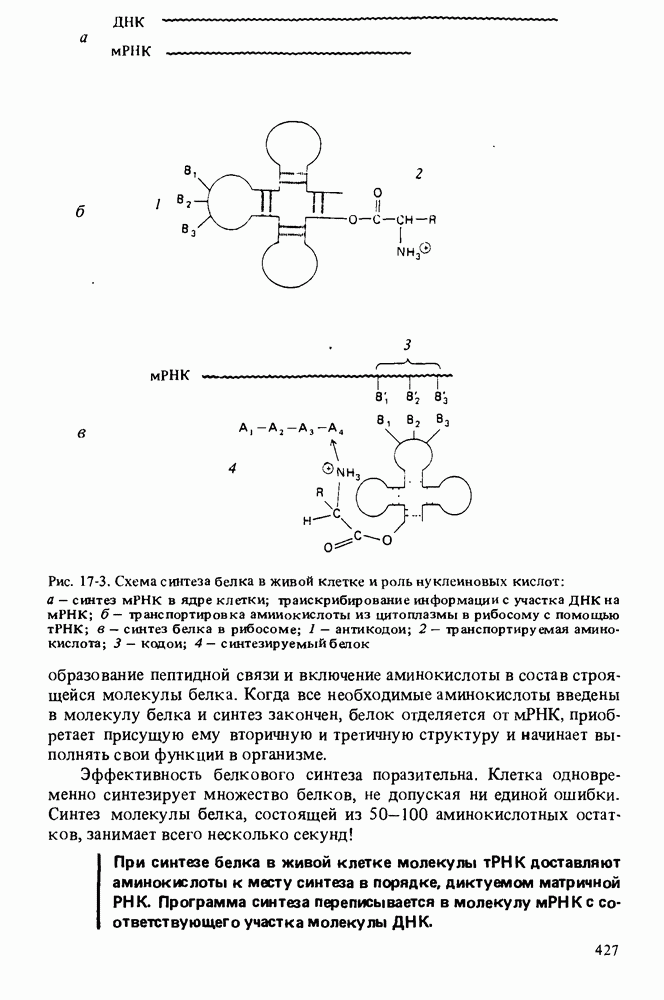
- ВТОРИЧНАЯ СТРУКТУРА И ФУНКЦИИ РНК
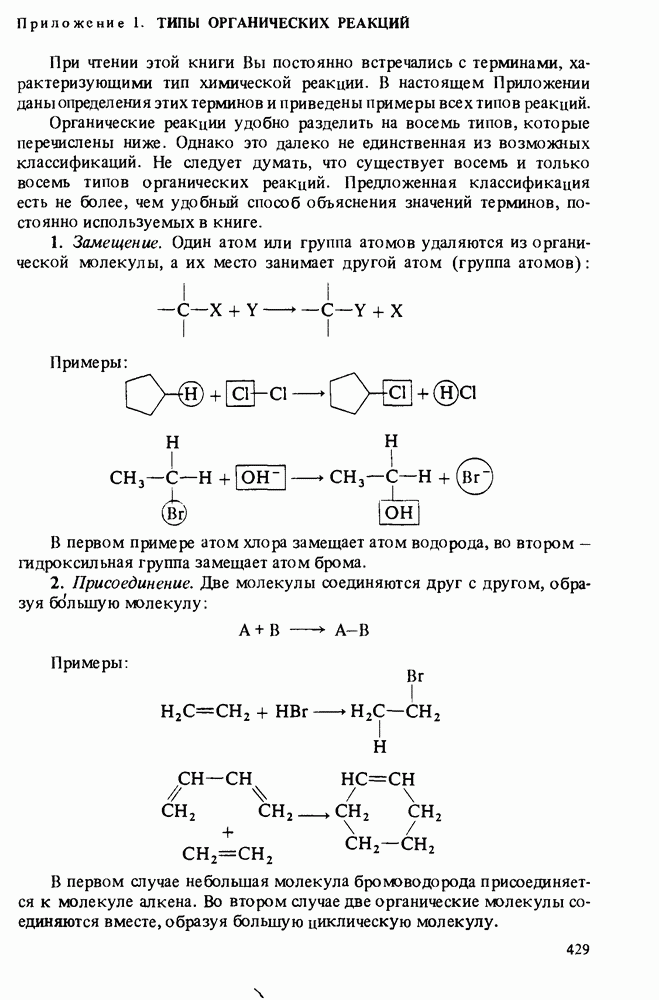
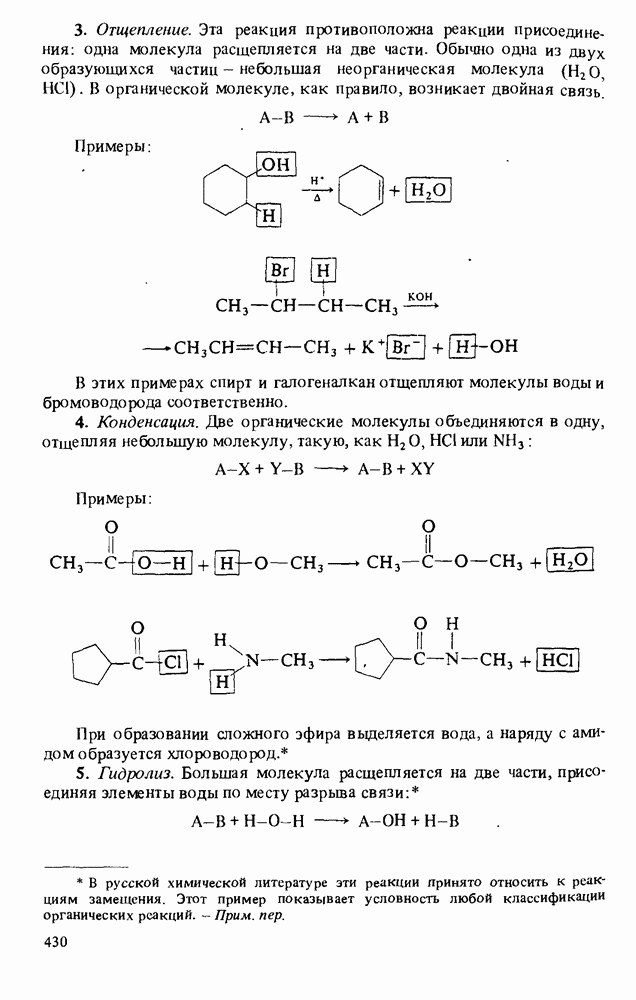
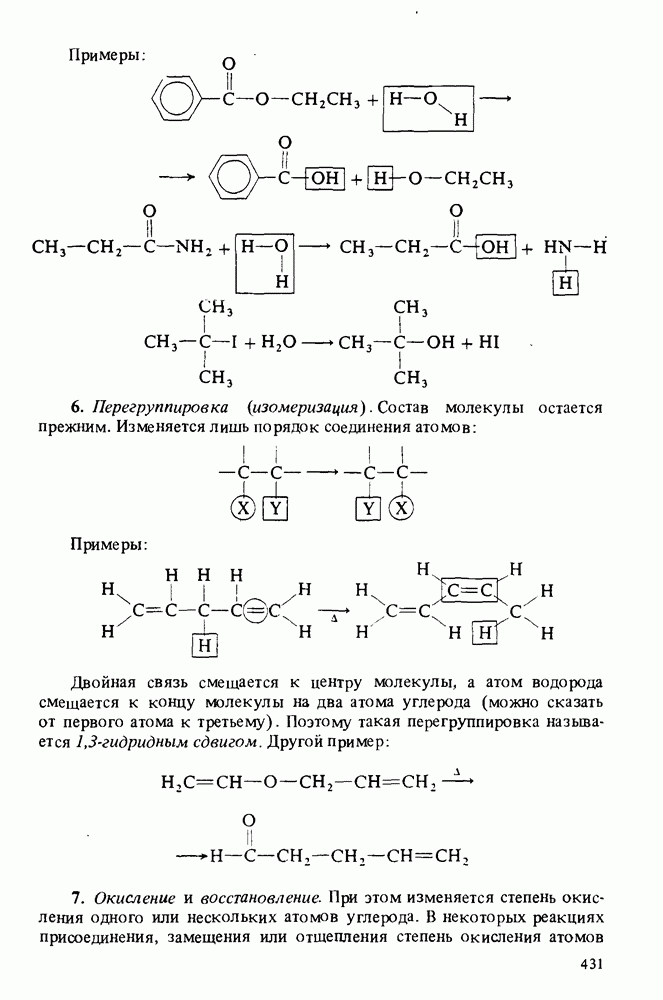
- Приложение 1. ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ
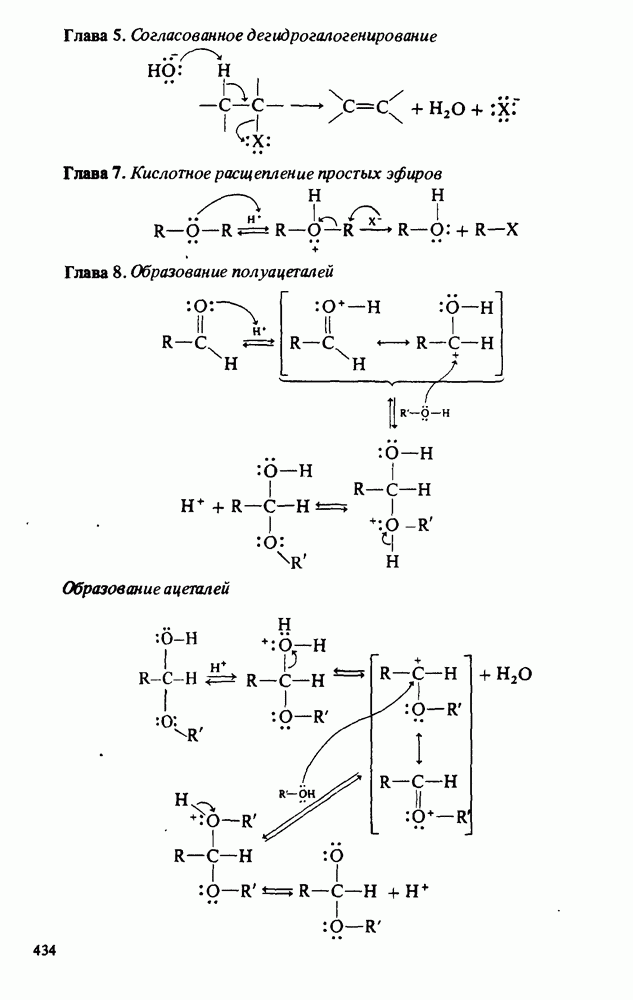
- Приложение 2. МЕХАНИЗМЫ НЕКОТОРЫХ РЕАКЦИЙ
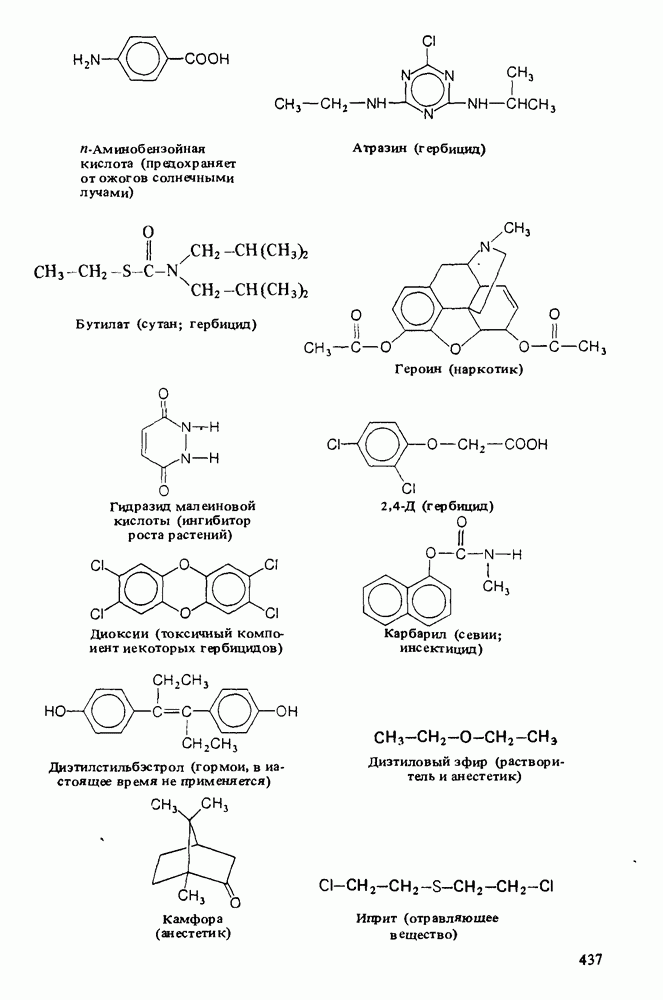
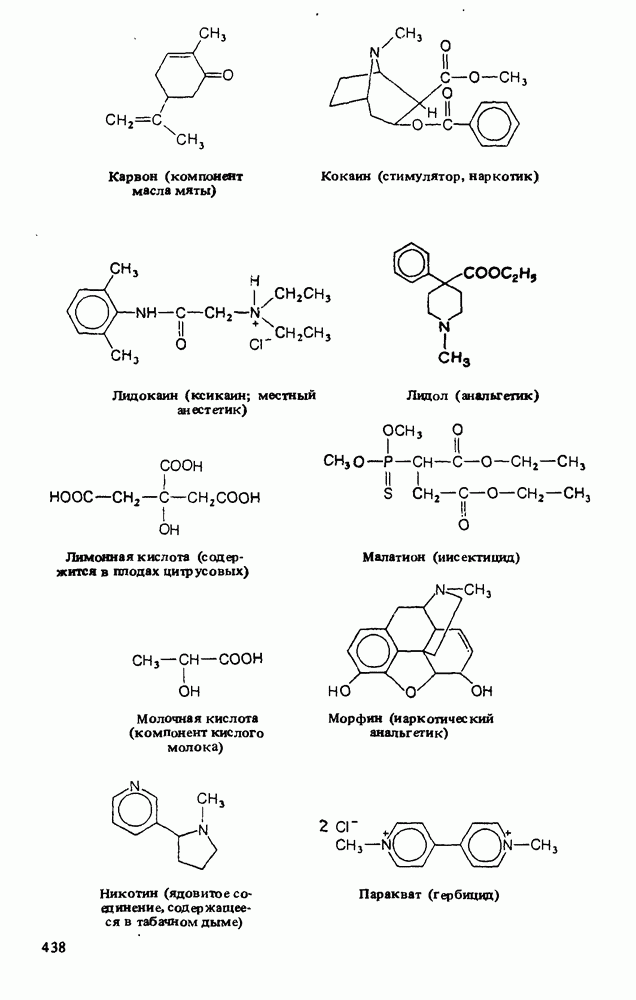
- Приложение 3. НЕКОТОРЫЕ ВАЖНЫЕ ОРГАНИЧЕСКИЕ ВЕЩЕСТВА