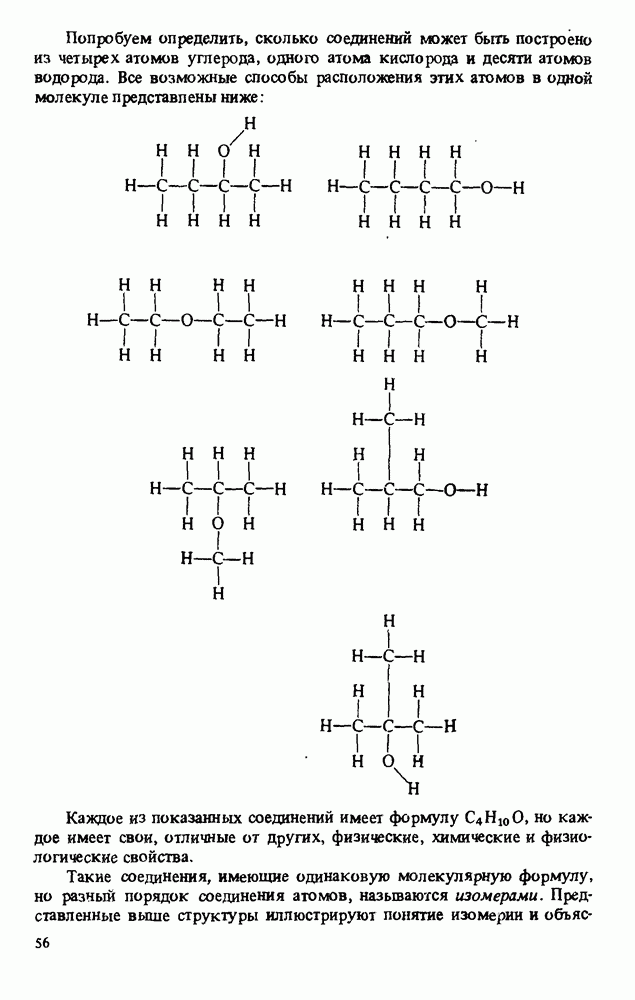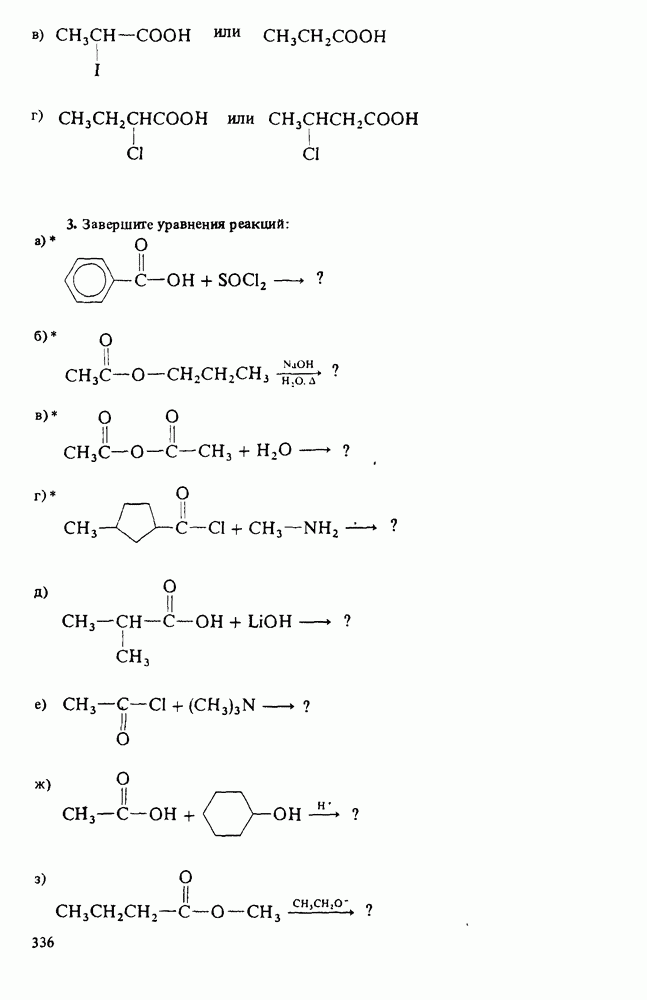| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ПРОСТЫЕ ЭФИРЫ
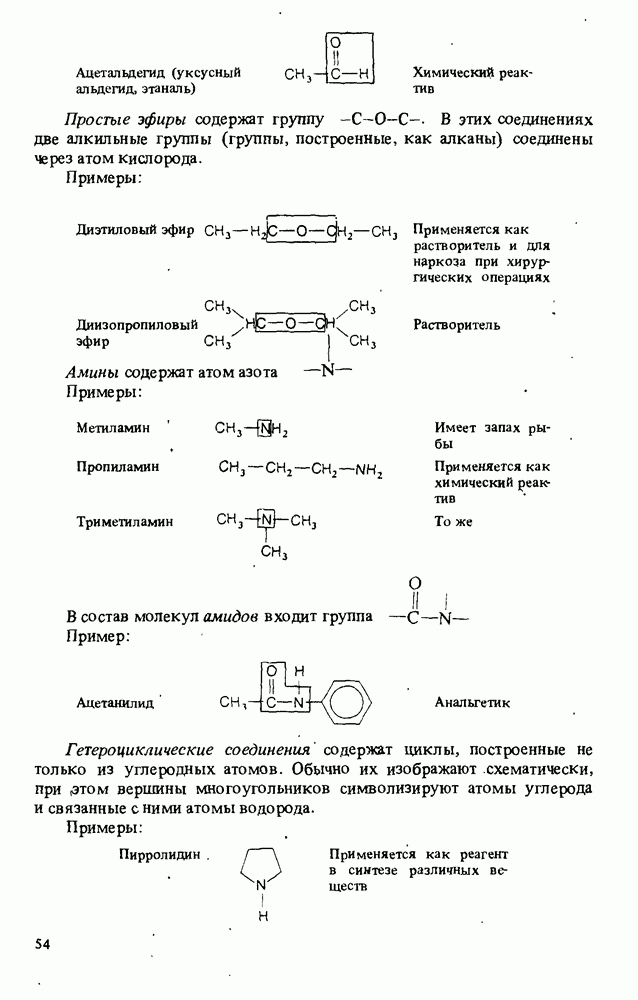
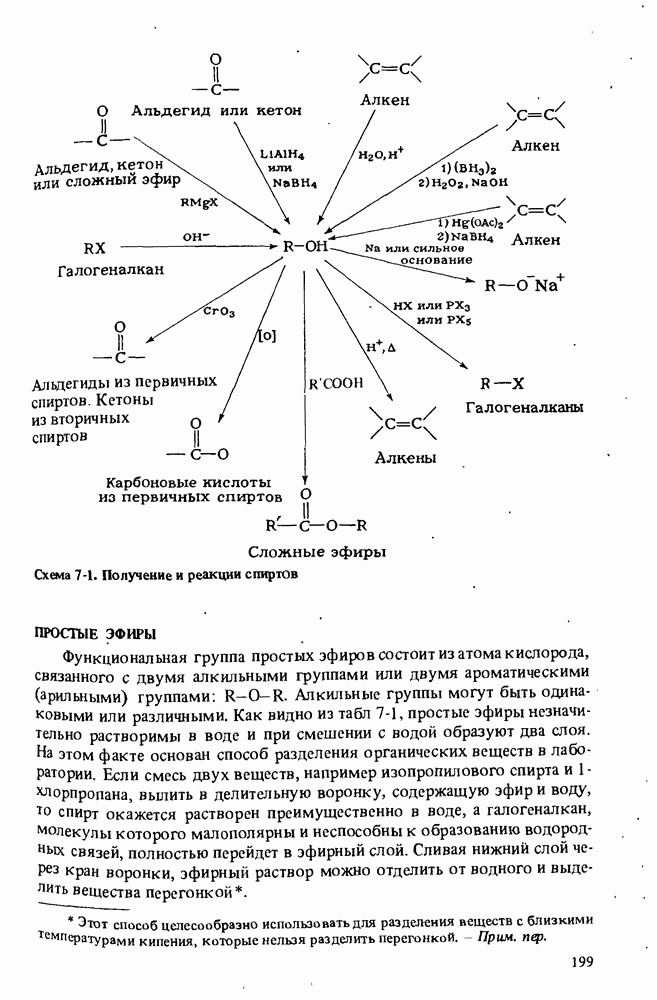
Функциональная группа простых эфиров состоит из атома кислорода, связанного с двумя алкильными группами или двумя ароматическими (арильными) группами: R-О-R. Алкильные группы могут быть одинаковыми или различными. Как видно из табл 7-1, простые эфиры незначительно растворимы в воде и при смешении с водой образуют два слоя. На этом факте основан способ разделения органических веществ в лаборатории. Если смесь двух веществ, например изопропилового спирта и 1-хлорпропана, вылить в делительную воронку, содержащую эфир и воду, то спирт окажется растворен преимущественно в воде, а галогеналкан, молекулы которого малополярны и неспособны к образованию водородных связей, полностью перейдет в эфирный слой. Сливая нижний слой через кран воронки, эфирный раствор можно отделить от водного и выделить вещества перегонкой.
Номенклатура простых эфиров
Простые эфиры называют обычно по правилам радикально-функциональной номенклатуры, добавляя к названиям двух радикалов слово "эфир":

В более сложных случаях используют номенклатуру IUPAC и рассматривают алкокси-группу как заместитель. Например, метилциклогексиловый эфир будет иметь название метоксициклогексан. Другой пример:

Получение простых эфиров
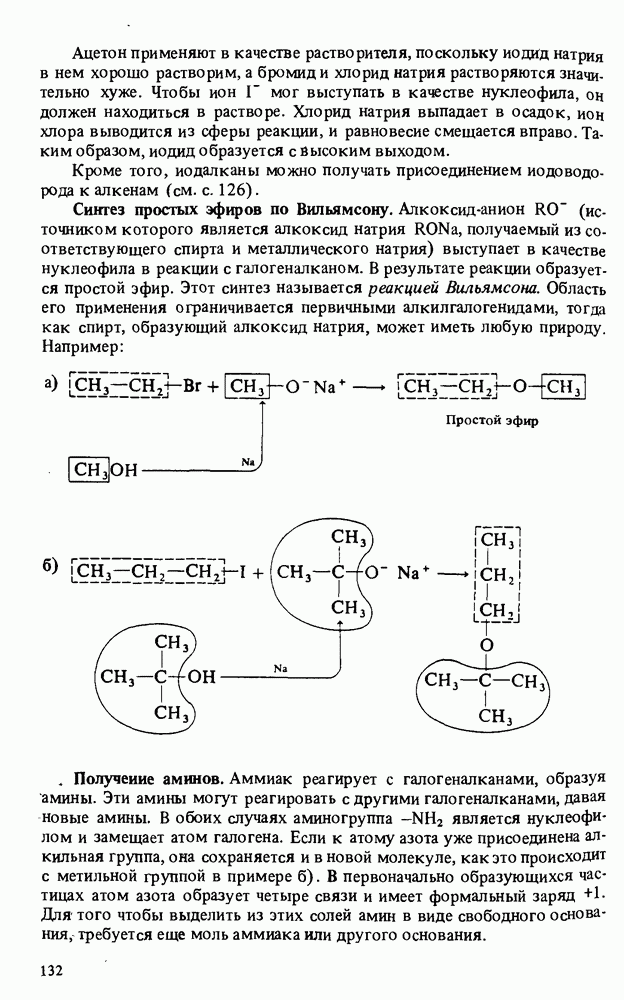
Удобным общим методом получения простых эфиров является синтез Вильямсона (см. гл. 5).

Один из двух радикалов R переходит в эфир из молекулы спирта. Второй R переходит из молекулы галогеналкана. Наилучшие выходы простого эфира достигаются, если R - первичный радикал. В этом случае реакция идет по Механизму  Например:
Например:

Симметричные простые эфиры можно получить межмолекулярнои дегидратацией первичных спиртов:

Для других спиртов с этой реакцией конкурирует образование алкенов но иногда можно подобрать условия, при которых основным продуктом реакции будет простой эфир:

Реакции простых эфиров
Простые эфиры - довольно инертные соединения. Они устойчивы к действию восстановителей, оснований и большинства кислот. Простые эфиры горят на воздухе, образуя воду и диоксид углерода. Они реагируют с бромоводо родом и иодоводородом с расщеплением  ирной связи и образованием галогеналкана и спирта. Спирт при этом тут же реагирует со второй молекулой бромоводорода, превращаясь также в галогеналкан:
ирной связи и образованием галогеналкана и спирта. Спирт при этом тут же реагирует со второй молекулой бромоводорода, превращаясь также в галогеналкан:

Например:

Инертность простых эфиров делает их удобными растворителями.
Простые эфиры обычно получают из алкокоид-анионов и первичных  стена
стена  кенов (синтез Вильямсона). Другой способ синтеза межмолекулярная дегидратация первичных спиртов. Простые эфиры довольно инертны, но расщепляются галогеноводородами.
кенов (синтез Вильямсона). Другой способ синтеза межмолекулярная дегидратация первичных спиртов. Простые эфиры довольно инертны, но расщепляются галогеноводородами.

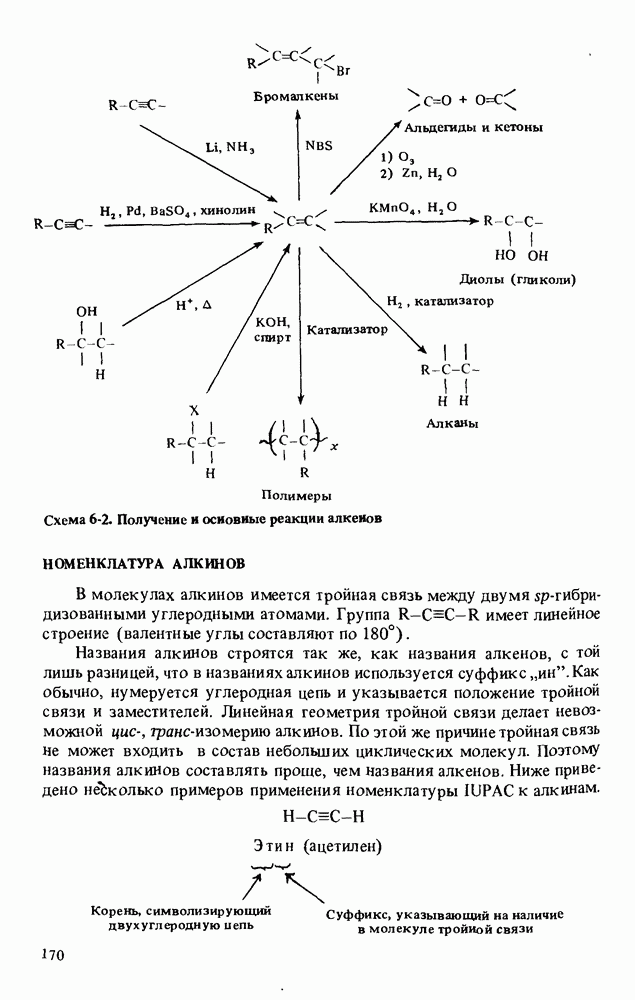
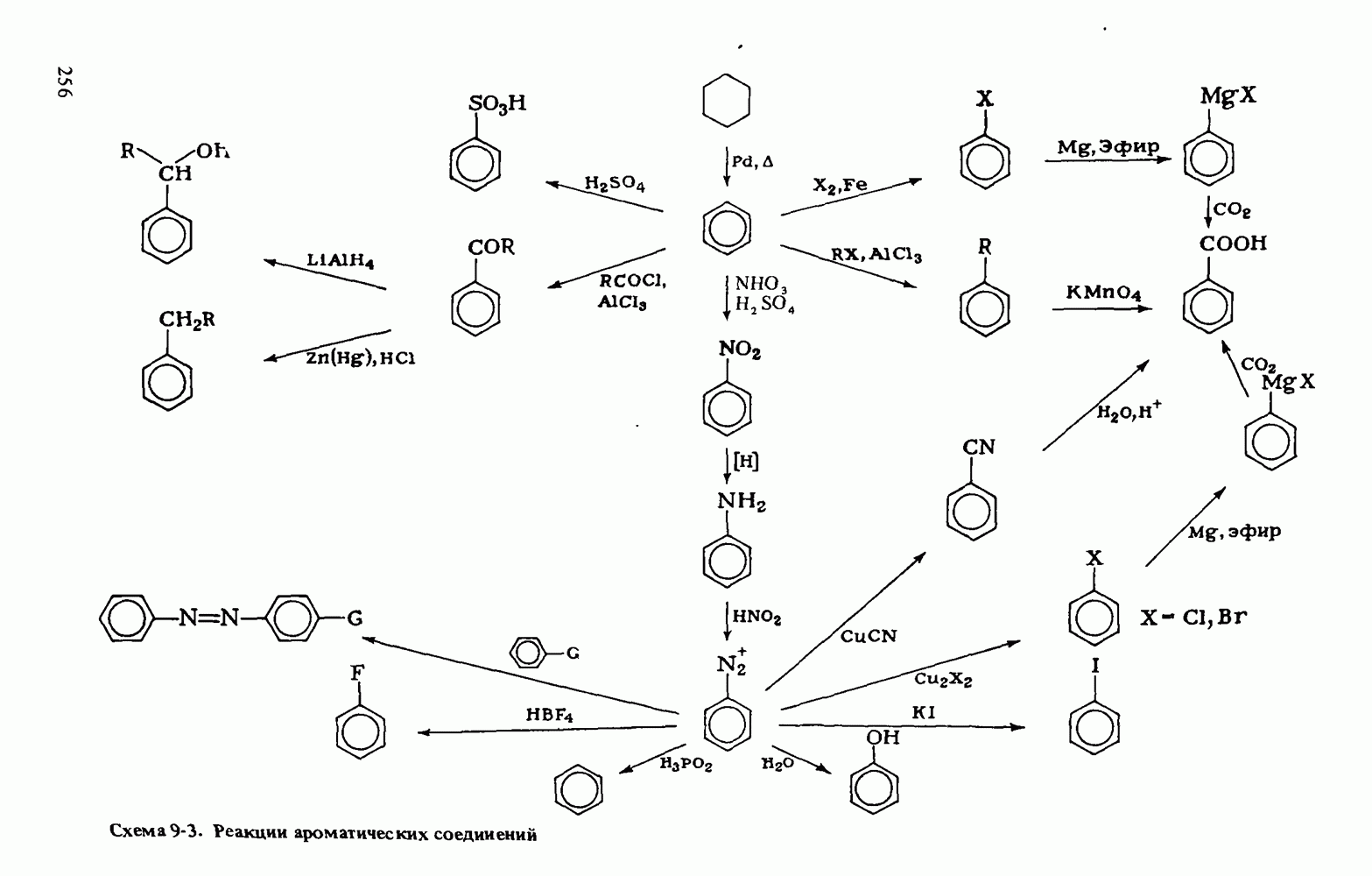
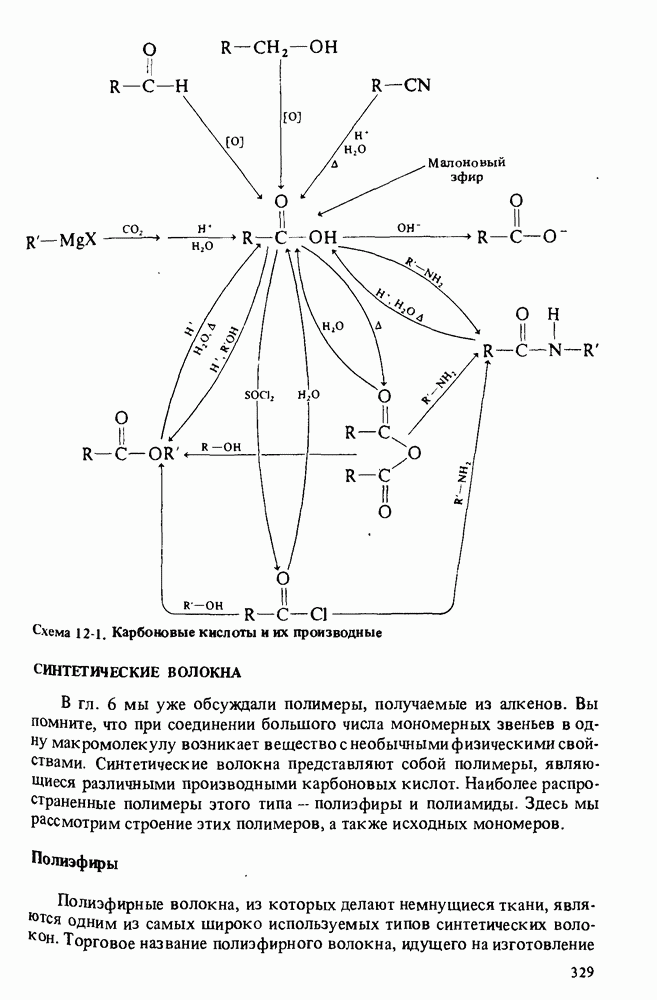
Схема 7-2. Получение и реакции простых эфиров
Практически важные простые эфиры
Диэтиловый эфир и два циклических простых эфира, которые показаны ниже, широко применяются как растворители:

Эфиры с низкой молекулярной массой, такие, как диэтиловый, весьма опасны в пожарном отношении. Они легко воспламеняются и хорошо горят. Кроме того, простые эфиры при контакте с воздухом могут образовывать взрывоопасные пероксиды.
Диизопропиловый эфир некоторое время использовался для общей анестезии, но был вытеснен более безопасными и эффективными анестетиками, такими, как циклопропан и тиопенталнатрий. Эвгенол, пахучий компонент гвоздичного масла, также имеет функциональную группу простого эфира. Простыми эфирами является и большинство неионных поверхностно-активных веществ. Формула одного из них показана ниже. Это вещество используется как добавка к косметическим кремам для создания пены из смеси воды и масел, которые не смешиваются с водой. Половой фермой непарного шелкопряда представляет собой циклический простой эфир (оксиран, см. следующий раздел):

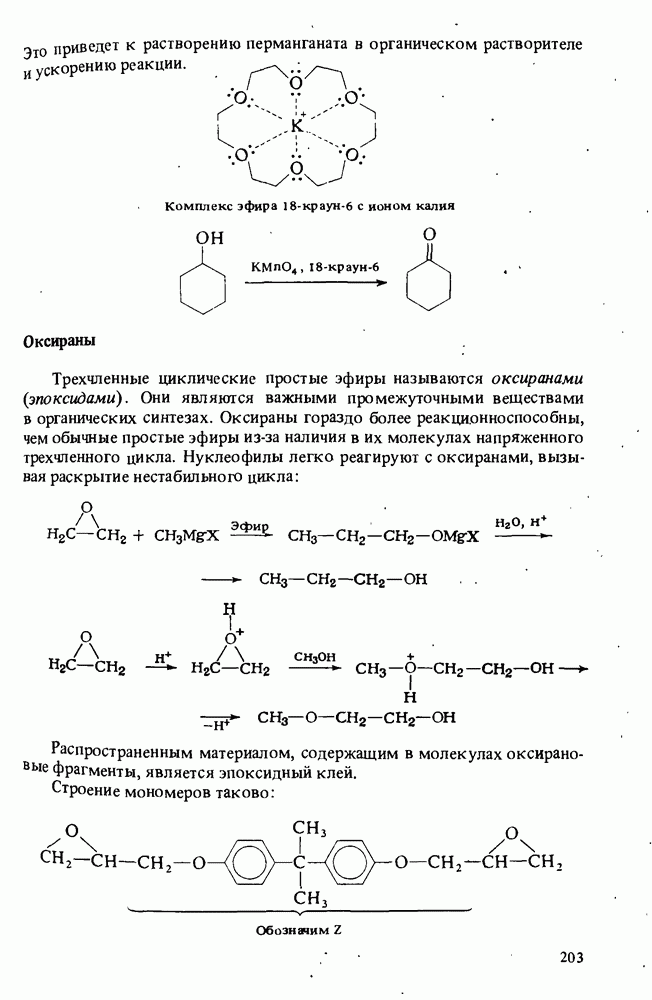
Другим интересным типом простых эфиров являются краун-эфиры. Такое название они получили потому, что их молекулы по форме напоминают корону (от английского слова crown - корона). Эфир, который показан ниже, называется 18-краун-6. Он представляет собой 18-членный цикл, в который входит 6 атомов кислорода. Замечательным свойством этого соединения является его способность координироваться с ионом калия и делать соли калия растворимыми в алканахи других неполярных растворителях, в которых соли обычно нерастворимы. Таким образом, для того чтобы окислить циклогексанол перманганатом калия, достаточно добавить к реакционной смеси небольшое количество эфира 18-краун-6
Это приведет к растворению перманганата в органическом растворителе и ускорению реакции.

Оксираны
Трехчленные циклические простые эфиры называются оксыранамы (эпоксидами). Они являются важными промежуточными веществами в органических синтезах. Оксираны гораздо более реакционно способны, чем обычные простые эфиры из-за наличия в их молекулах напряженного трехчленного цикла. Нуклеофилы легко реагируют с оксиранами, вызывая раскрытие нестабильного цикла:

Распространенным материалом, содержащим в молекулах оксирано  фрагменты, является эпоксидный клей. Строение мономеров таково:
фрагменты, является эпоксидный клей. Строение мономеров таково:


При смешении этих двух веществ начинается полимеризация и образуется прочный полимер:

СВОДКА ОСНОВНЫХ ПОЛОЖЕНИЙ ГЛ. 7
1. Физические свойства соединений определяются их строением. Значительная полярность спиртов и образование водородных связей являются причиной высоких температур кипения этих веществ и растворимости их в воде. В ряду соединений одного класса выполняется правило: чем больше молекулярная масса, тем выше температура кипения и тем ниже растворимость в воде.
2. В соответствии с правилами номенклатуры IUPAC названия спиртов состоят из названия углеводорода, к которому присоединена гидрок сильная группа, суффикса "ол", локанта гидроксильной группы, а также локантов и названий заместителей. Радикально-функциональная номенклатура предусматривает прибавление к слову "спирт" прилагательного, образованного от названия радикала, соединенного с гидрок сильной группой. Используются также тривиальные названия.
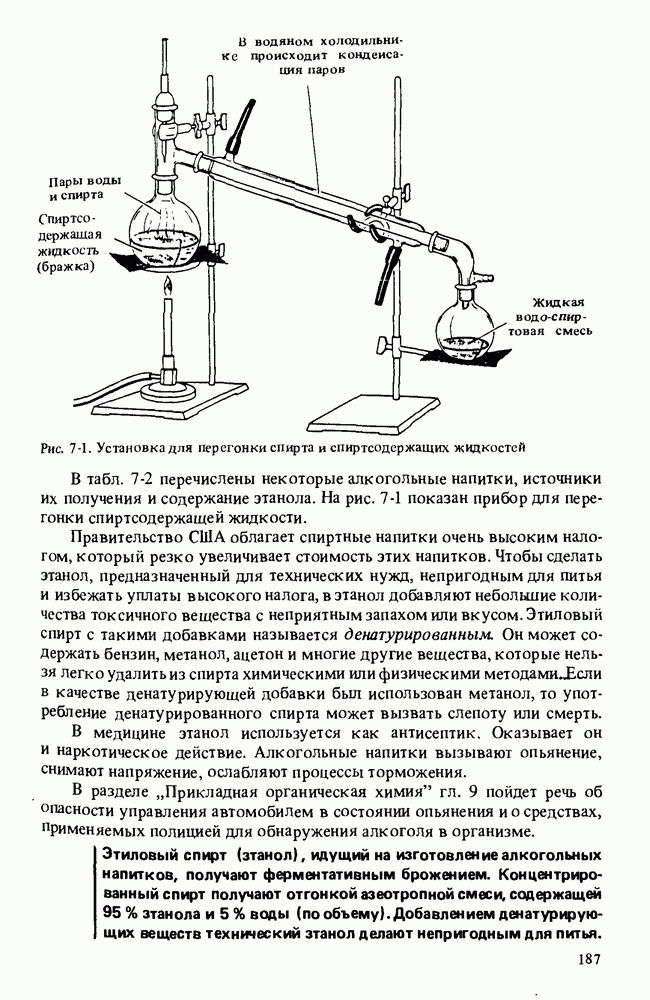
3. Этиловый спирт входит в состав алкогольных напитков. Для этих целей его получают из зерна ферментативным брожением. Крепкий спирт получают фракционной перегонкой бродильной смеси. В некоторых случаях этанол сознательно денатурируют, добавляя токсичные вещества, чтобы сделать его непригодным для питья.
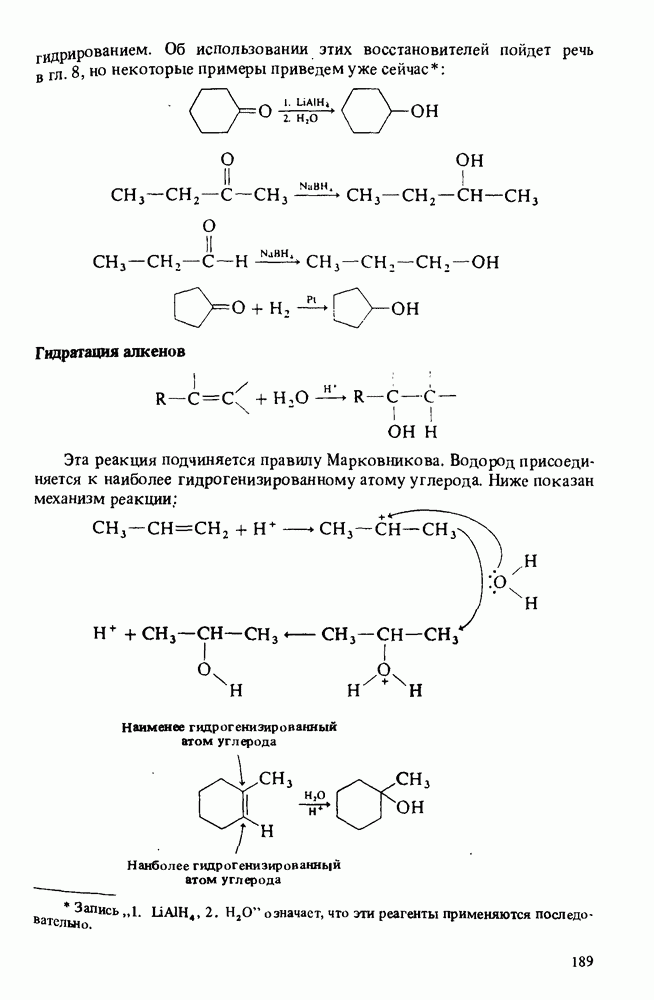
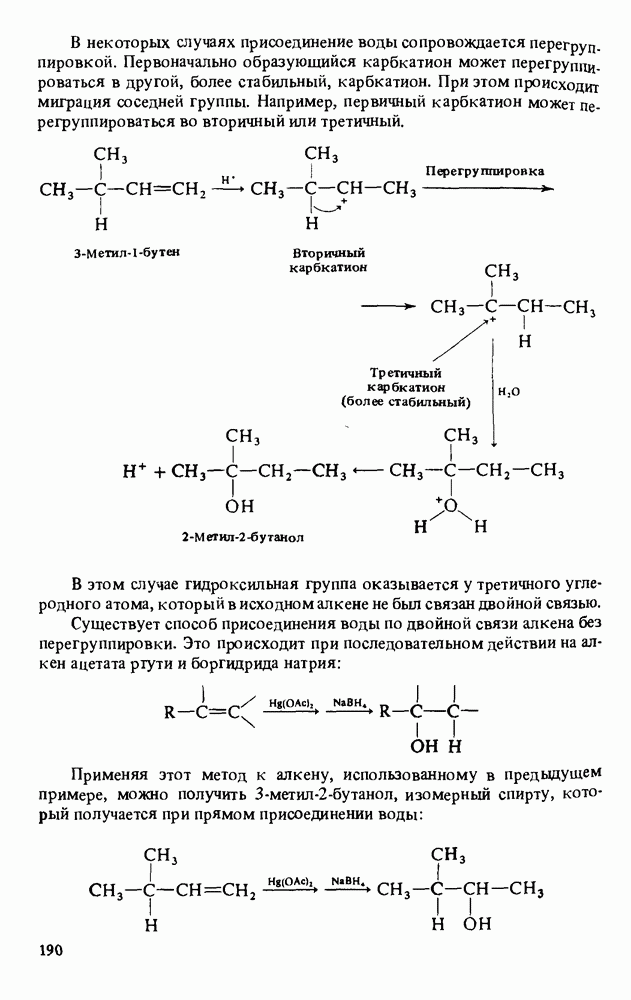
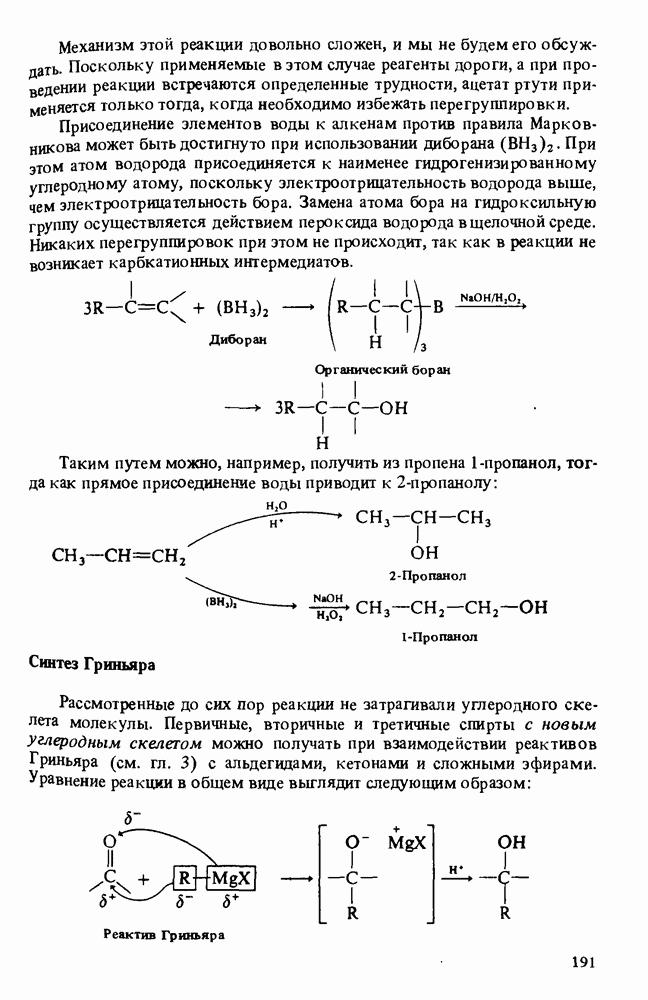
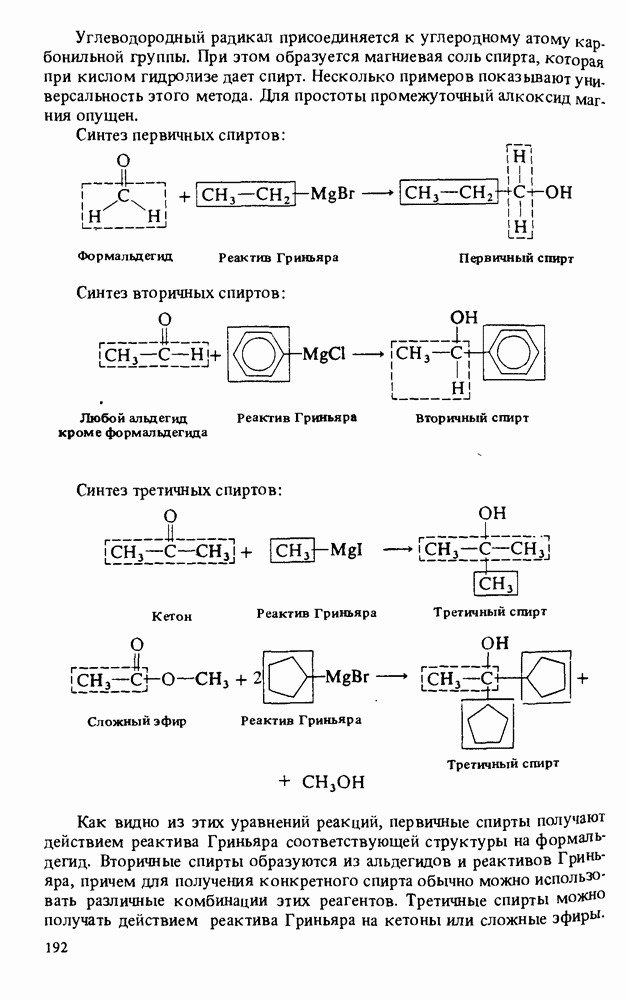
4. Многие спирты получают в промышленности гидратацией соответствующих алкенов. Метанол синтезируют взаимодействием оксида углерода и водорода. В лаборатории спирты получают восстановлением альдегидов и кетонов, гидратацией алкенов и взаимодействием реактивов Гриньяра с альдегидами, кетонами и сложными эфирами.
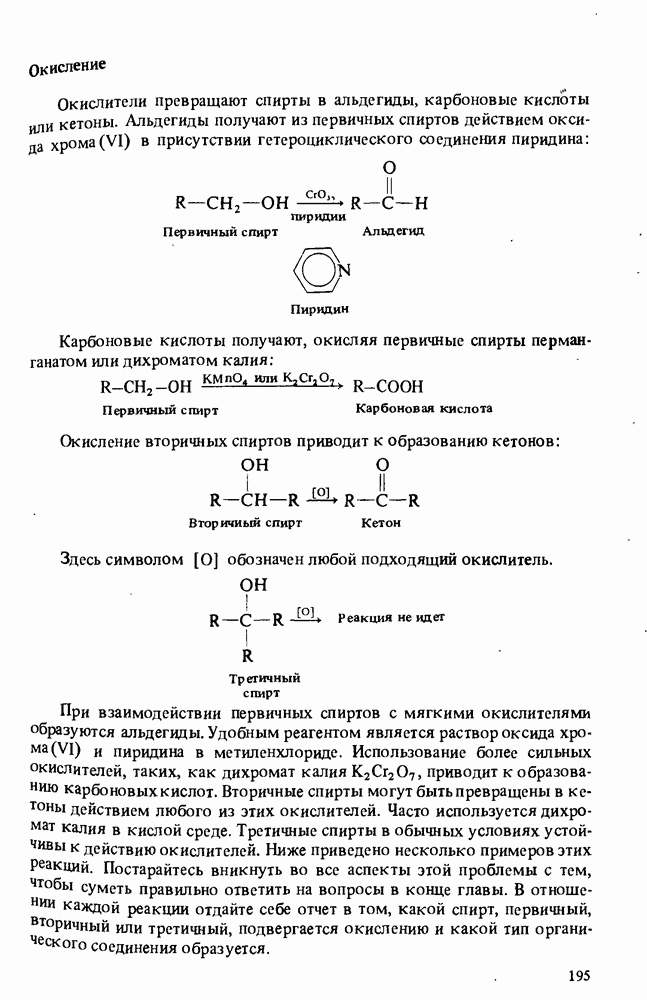
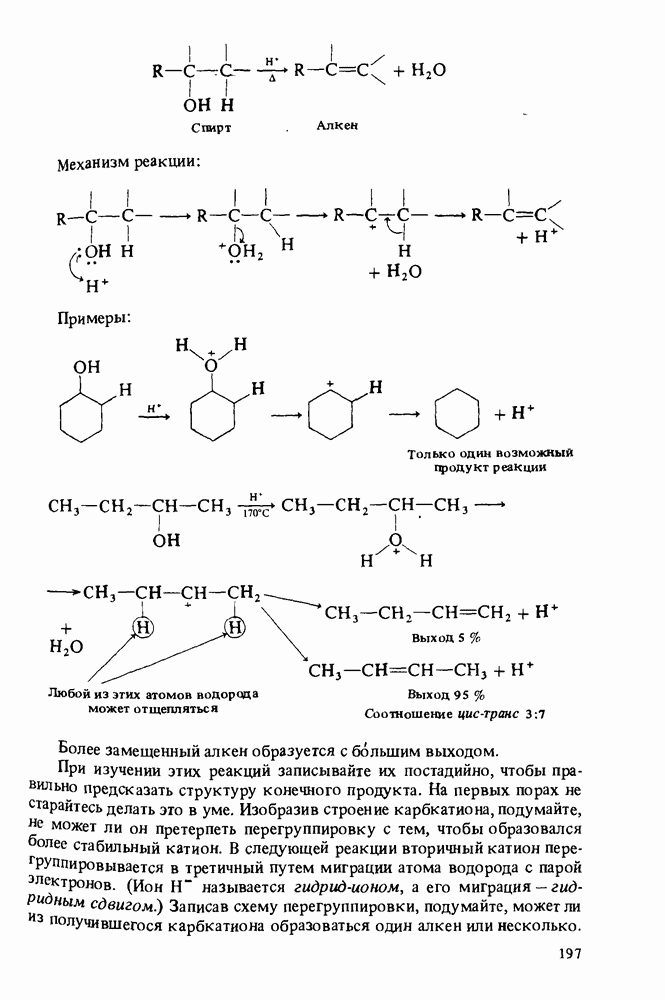
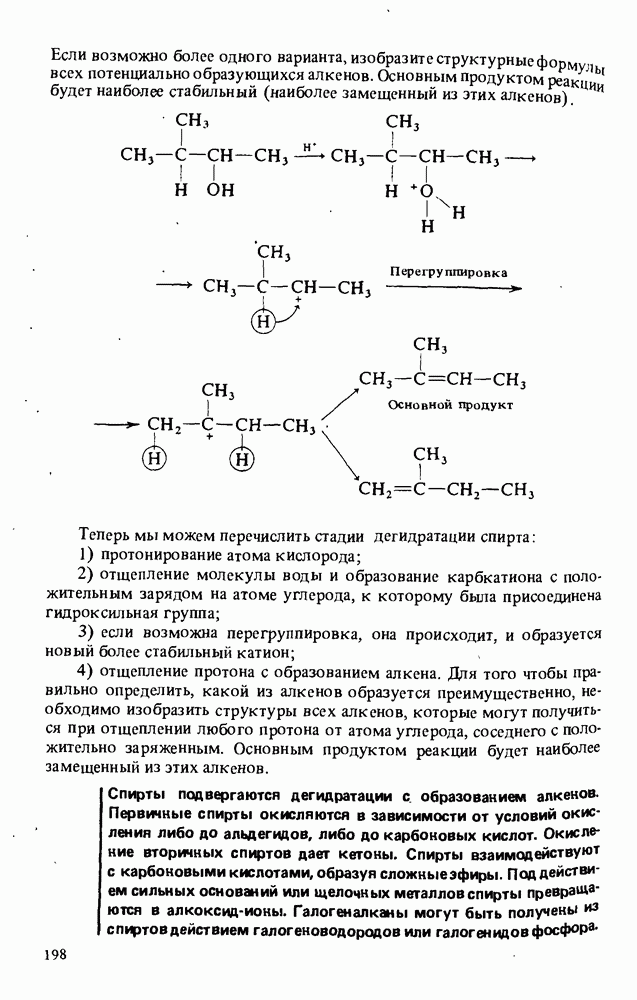
5. Спирты могут быть превращены в целый ряд других соединений, таких, как алкоксиды металлов, сложные эфиры, альдегиды, кетоны, карбоновые кислоты, алкены, галогеналканы.
6. Названия простых эфиров строятся из названий групп, соединенных с атомом кислорода, и слова "эфир". Можно также называть простые эфиры как алкоксизамещенные алканы.
7. Простые эфиры получают по реакции Вильямсона или межмолекулярной дегидратацией спиртов.
8. Простые эфиры весьма инертны, но под действием бромоводорода и иодоводорода подвергаются расщеплению.
9. Оксираны, трехчленные простые эфиры, в отличие от других простых эфиров, реагируют с различными реагентами, образуя продукты раскрытия трехчленного цикла. На основе оксиранов получают эпоксидные смолы и клеи.
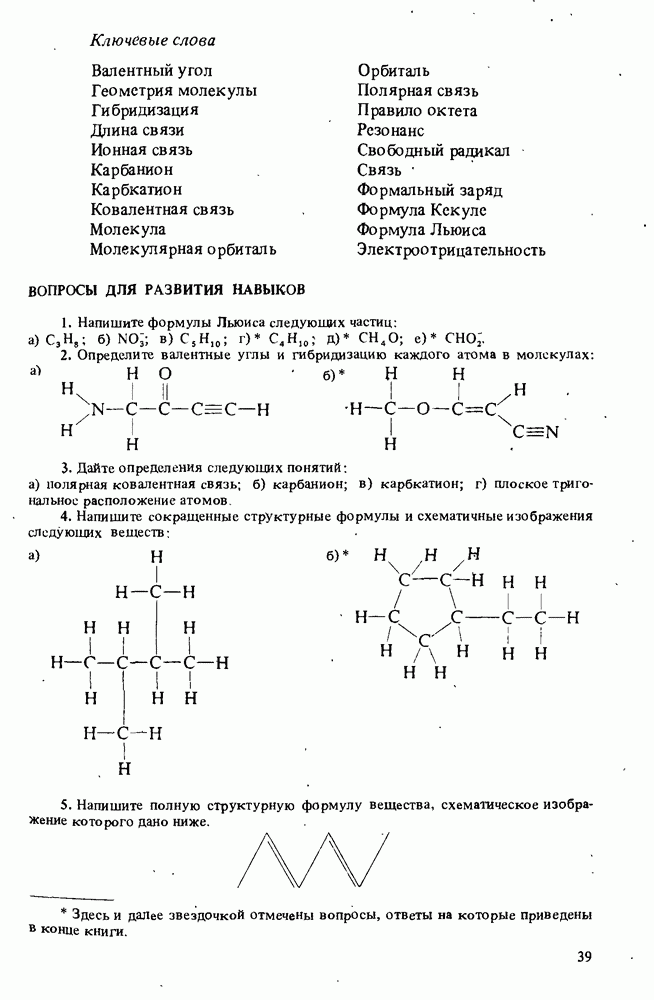
Ключевые слова
(см. скан)
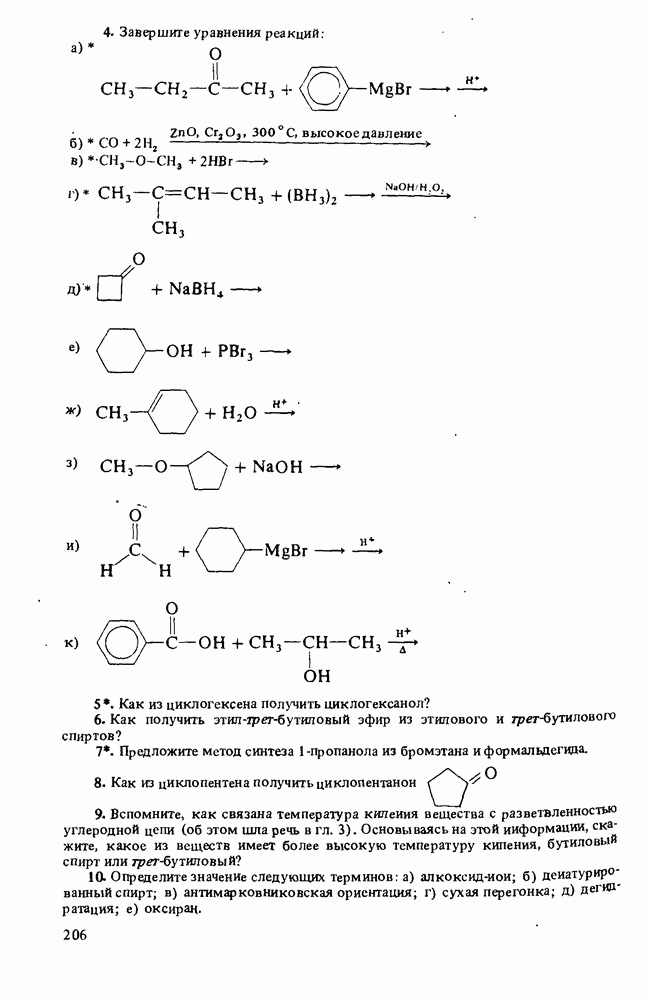
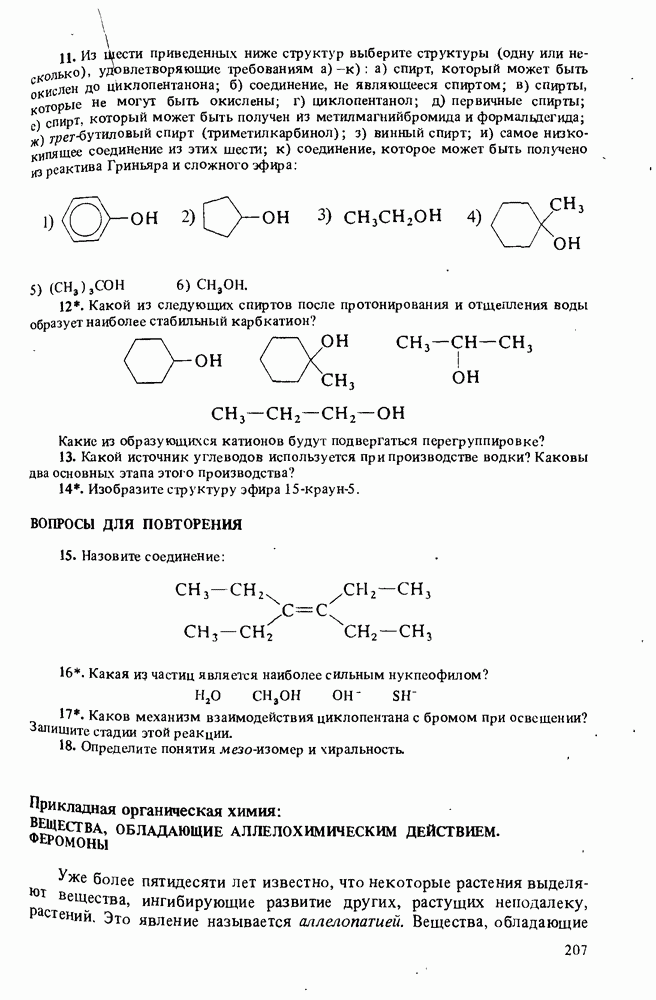
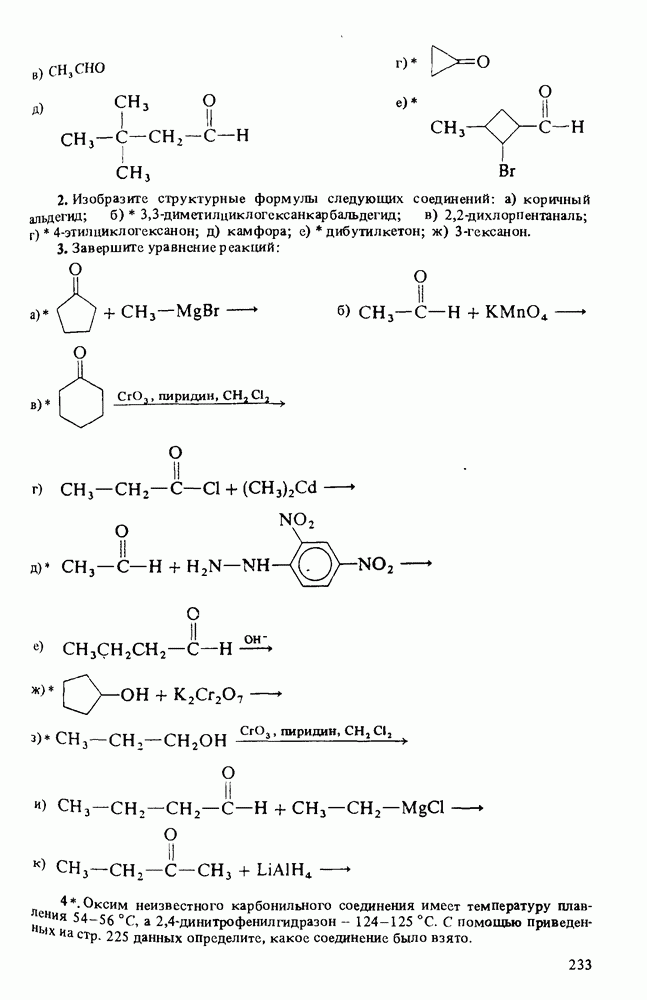
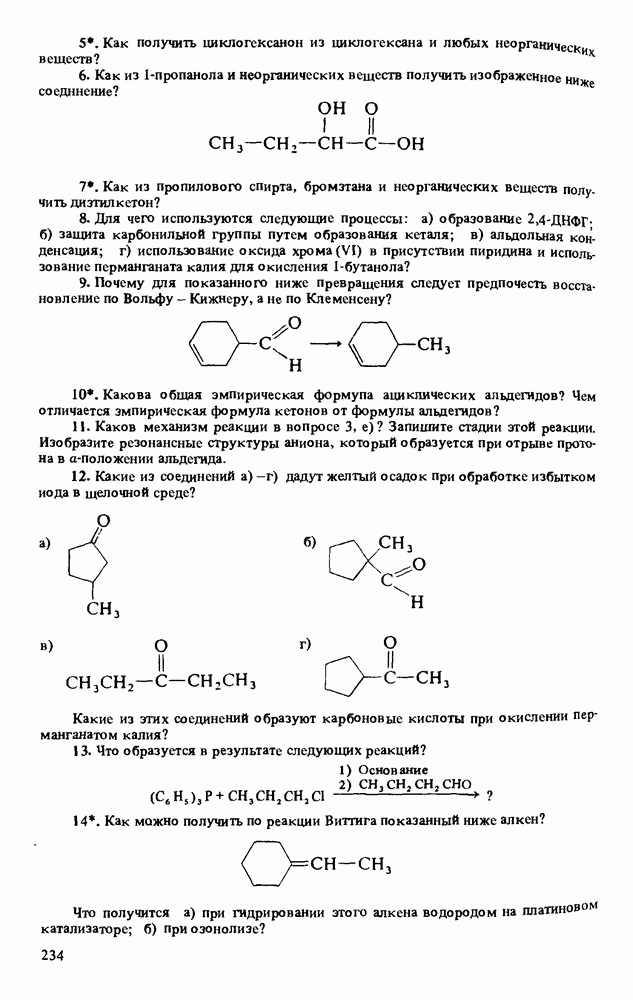
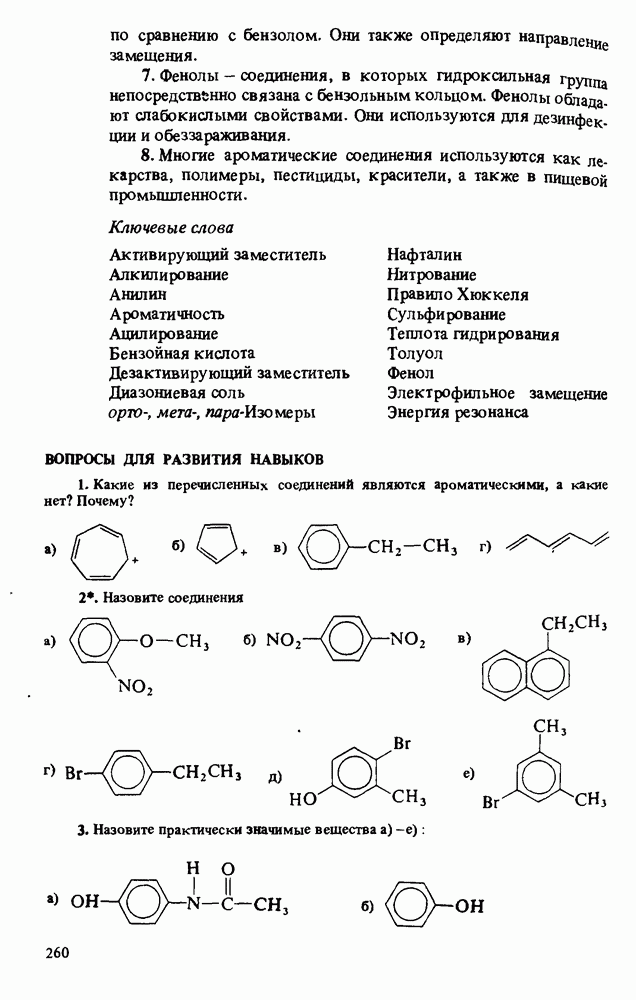
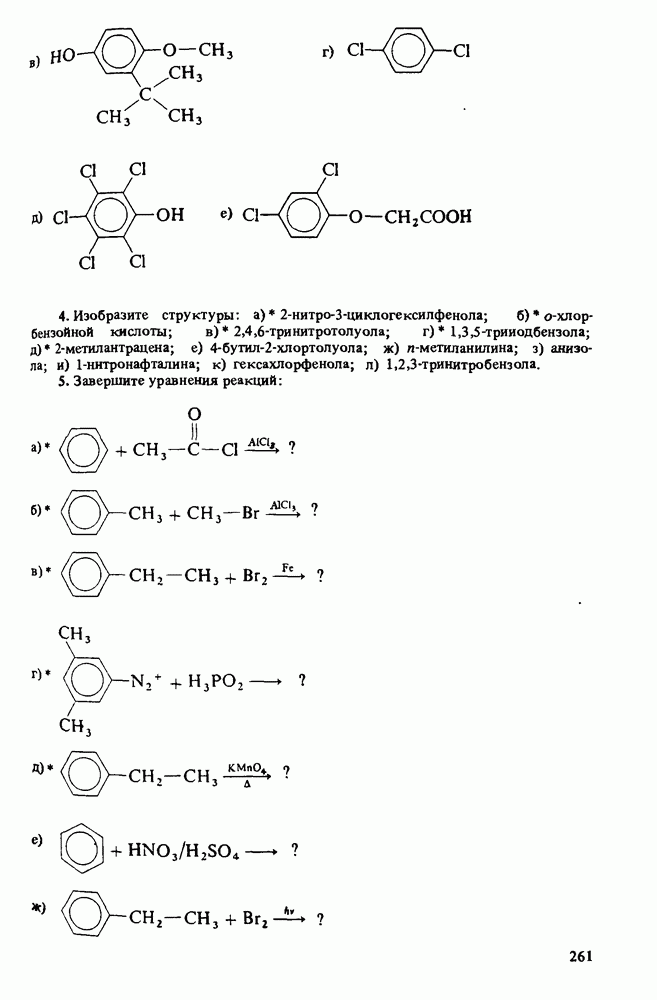
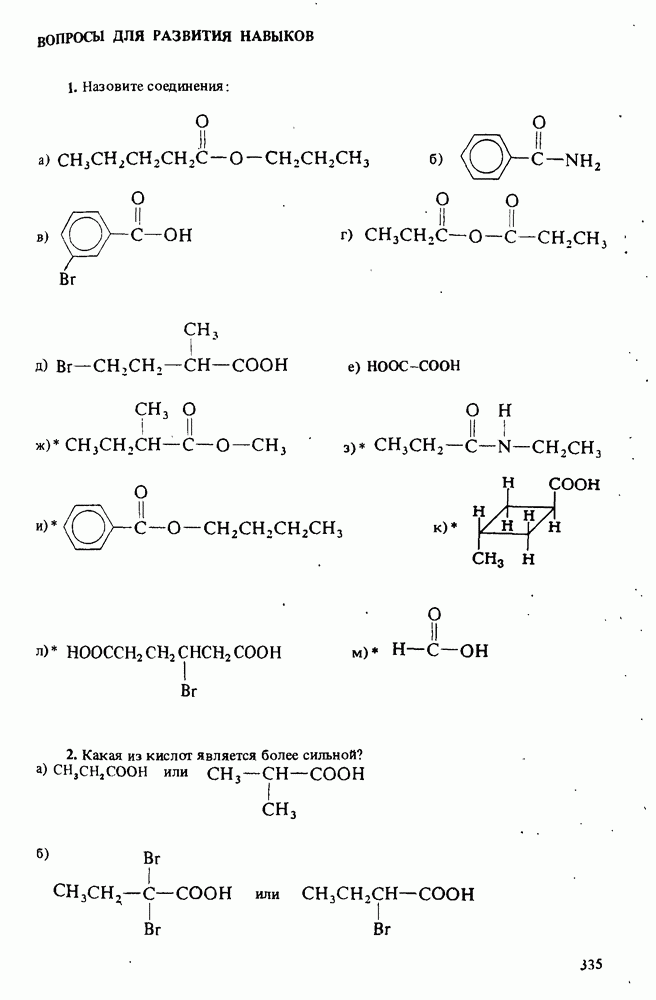
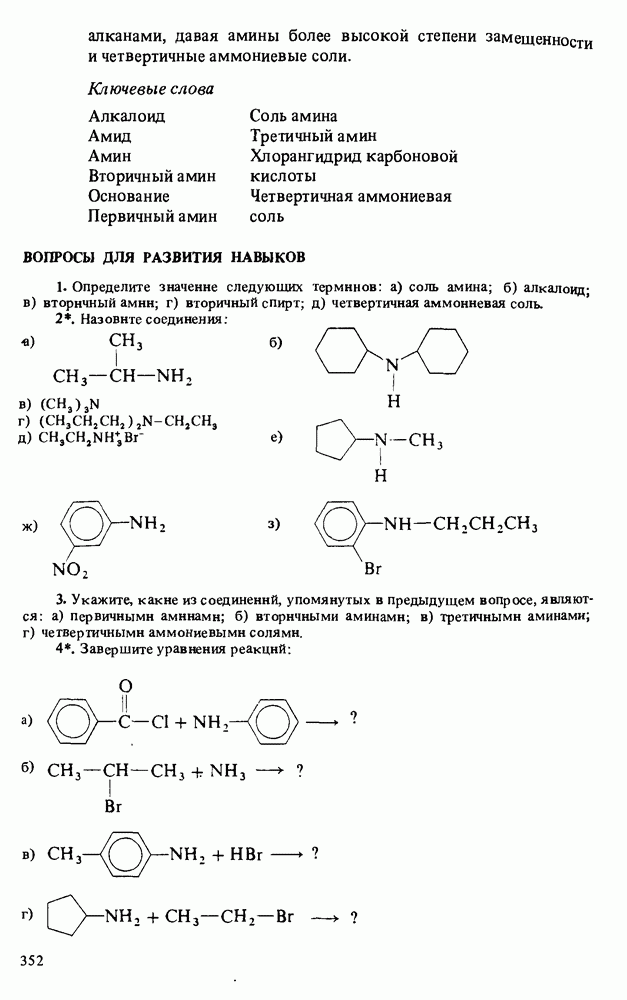
ВОПРОСЫ ДЛЯ РАЗВИТИЯ НАВЫКОВ
(см. скан)
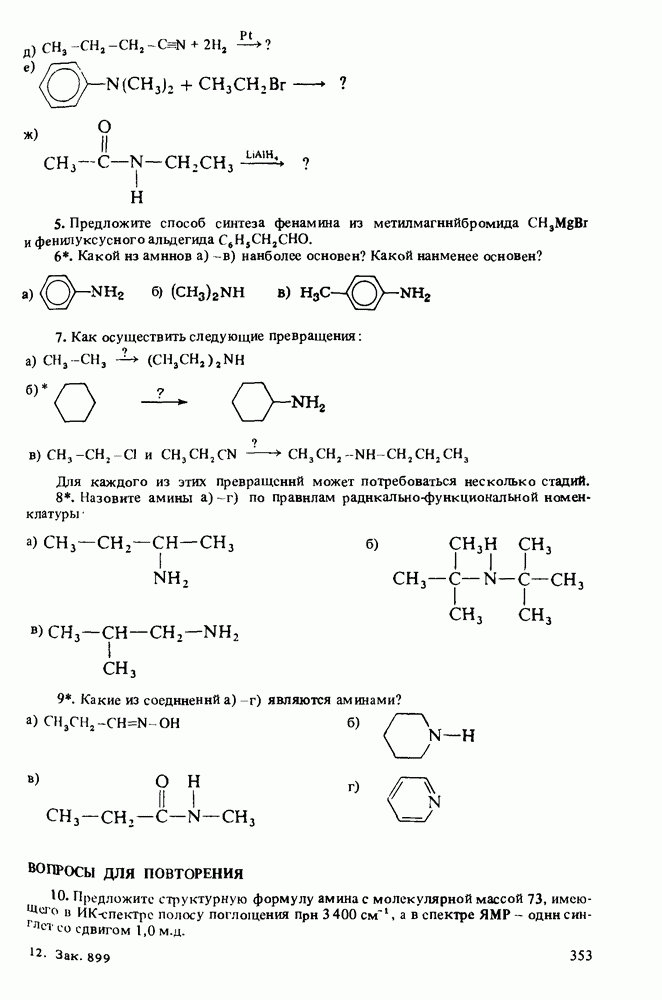
(см. скан)
(см. скан)
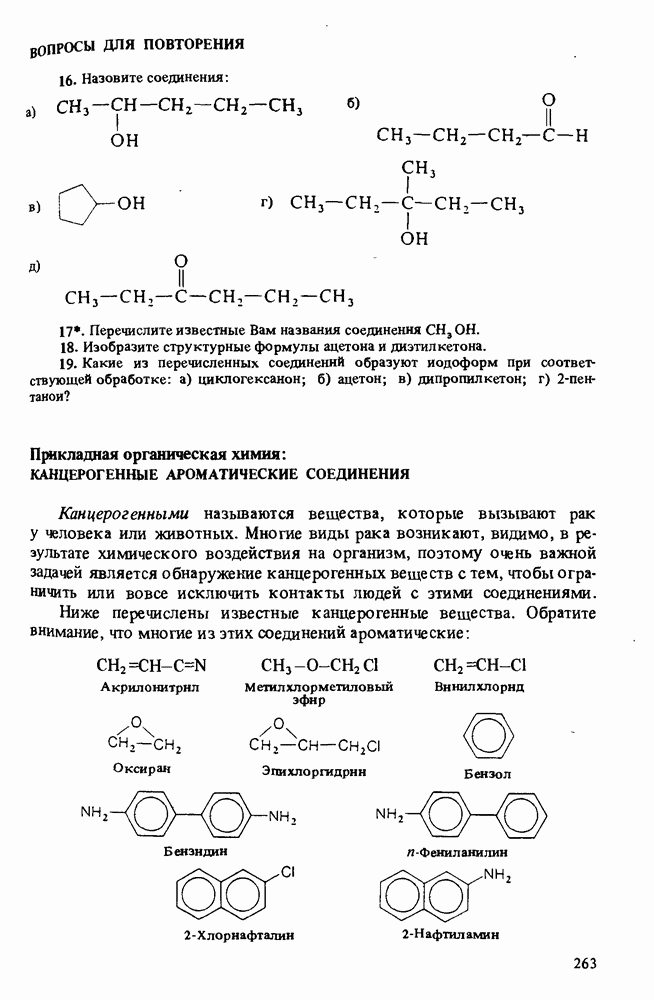
ВОПРОСЫ ДЛЯ ПОВТОРЕНИЯ
(см. скан)
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ
- Глава 1. КЛЮЧЕВЫЕ ПОНЯТИЯ ХИМИИ
- АТОМНАЯ ТЕОРИЯ
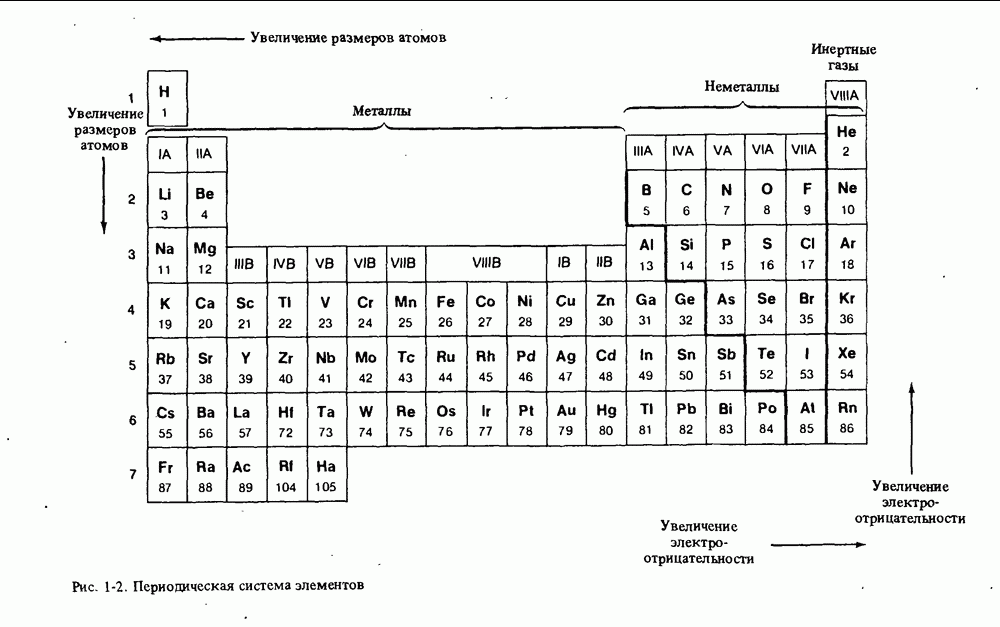
- ПЕРИОДИЧЕСКАЯ СИСТЕМА
- ХИМИЧЕСКАЯ СВЯЗЬ
- ФОРМУЛЫ ЛЬЮИСА
- ФОРМАЛЬНЫЙ ЗАРЯД
- РЕЗОНАНС
- ГЕОМЕТРИЯ МОЛЕКУЛ
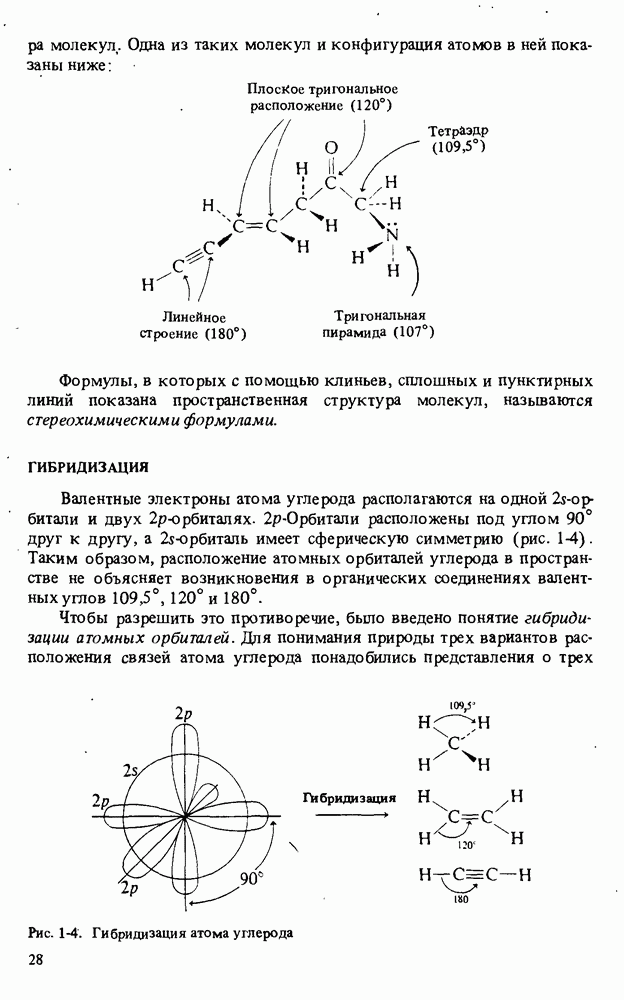
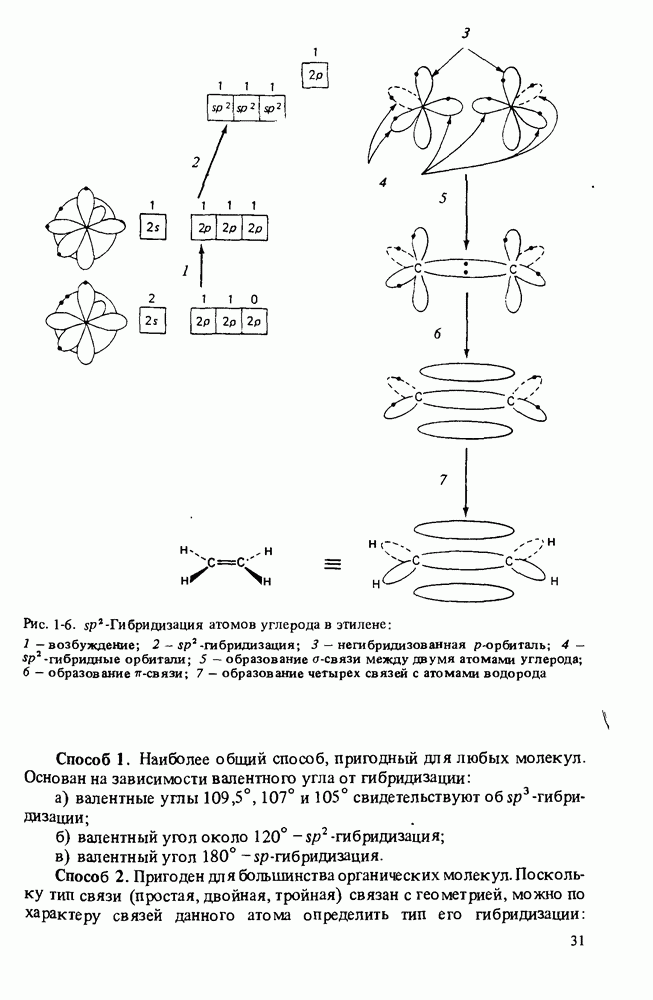
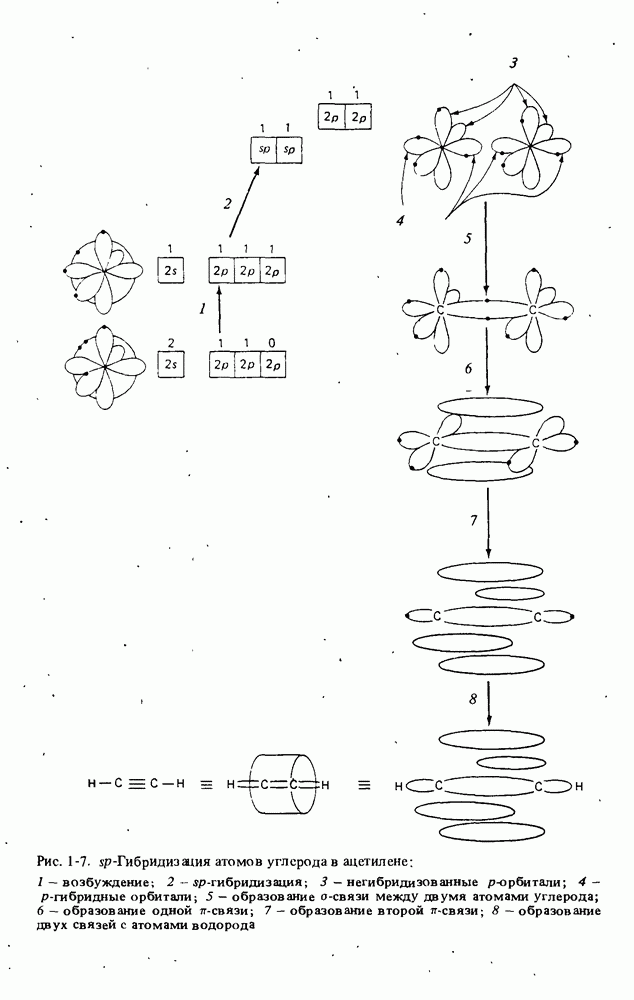
- ГИБРИДИЗАЦИЯ
- ХИМИЧЕСКИЕ ФОРМУЛЫ
- СОВЕТЫ ИЗУЧАЮЩЕМУ ОРГАНИЧЕСКУЮ ХИМИЮ
- СВОДКА ОСНОВНЫХ ПОЛОЖЕНИЙ ГЛ. 1
- Глава 2. ОБЩИЕ ВОПРОСЫ ОРГАНИЧЕСКОЙ ХИМИИ
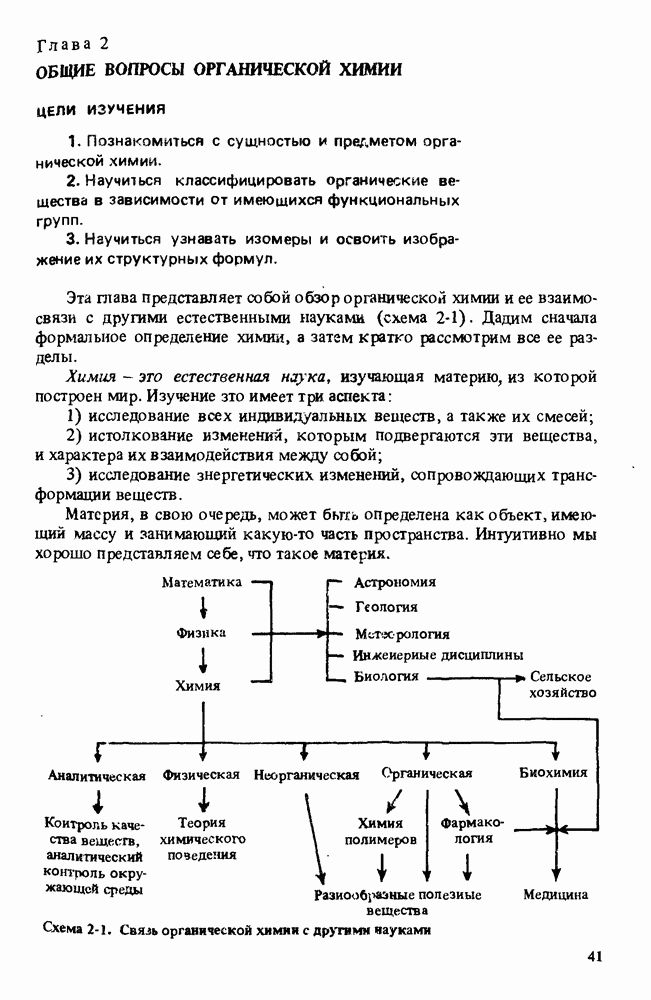
- РАЗДЕЛЫ ХИМИИ
- СИНТЕТИЧЕСКАЯ ОРГАНИЧЕСКАЯ ХИМИЯ
- ПОЛЕЗНЫЕ ОРГАНИЧЕСКИЕ ВЕЩЕСТВА
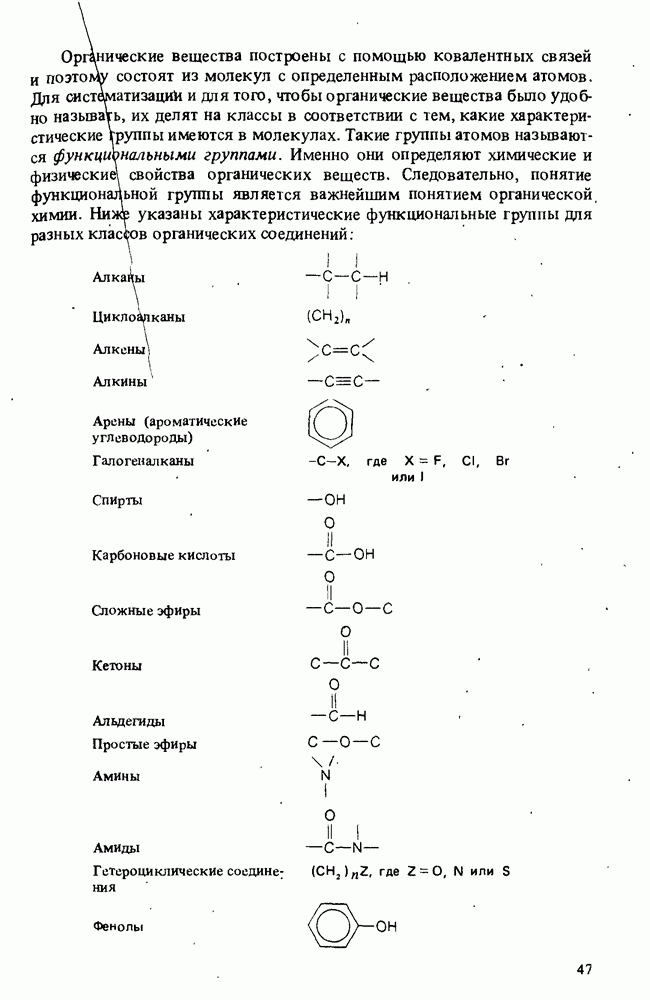
- КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ. ФУНКЦИОНАЛЬНЫЕ ГРУППЫ
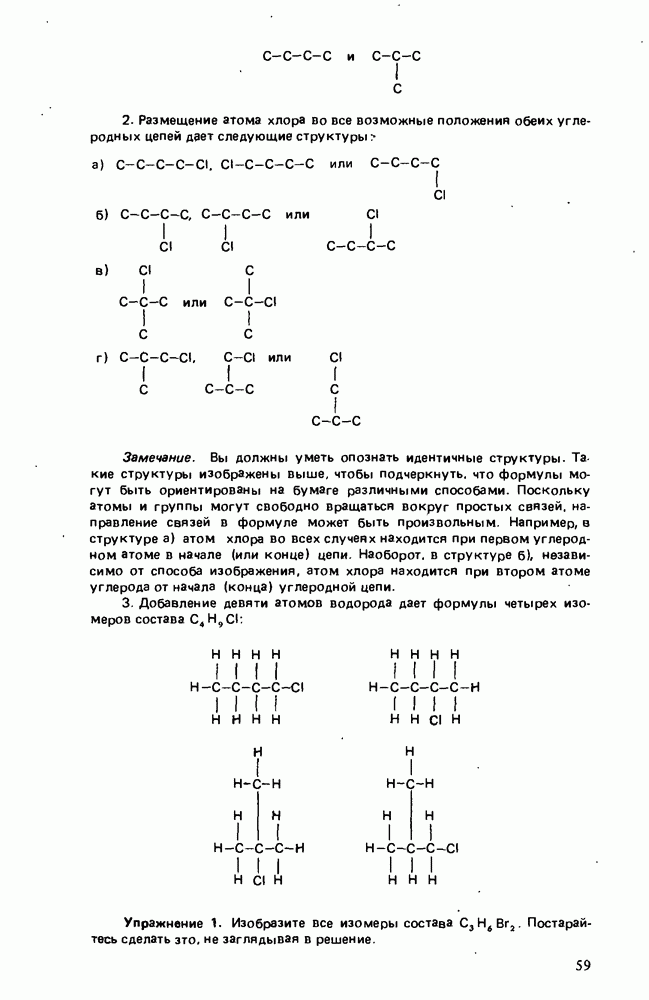
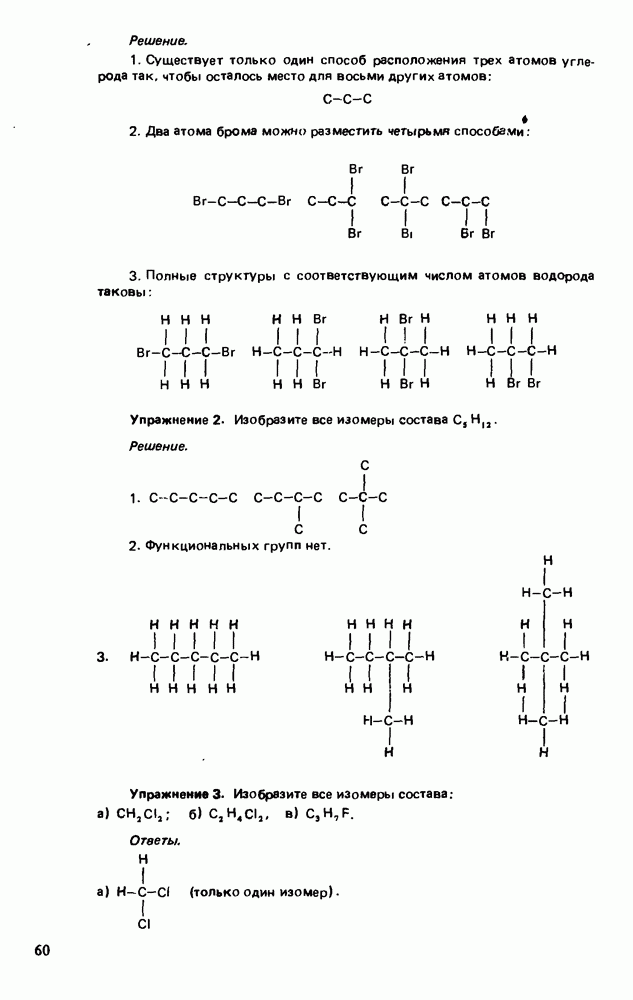
- ИЗОМЕРИЯ
- СВОДКА ОСНОВНЫХ ПОЛОЖЕНИЙ ГЛ. 2
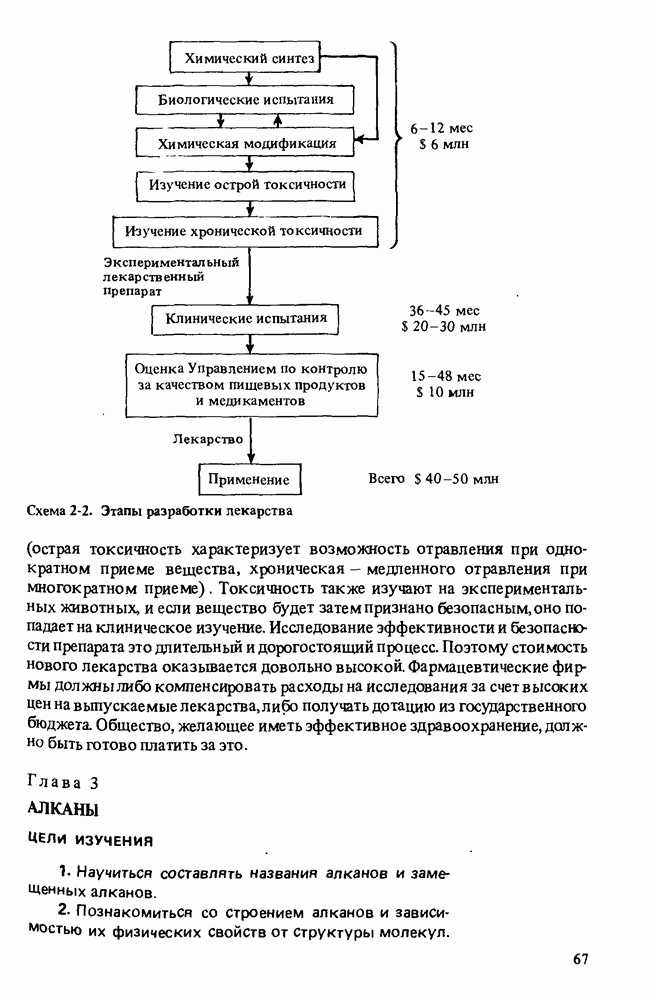
- Прикладная органическая химия: ХИМИЧЕСКИЙ СИНТЕЗ И МЕДИЦИНСКИЕ ИССЛЕДОВАНИЯ
- Глава 3. АЛКАНЫ
- ФИЗИЧЕСКИЕ СВОЙСТВА АЛКАНОВ
- СТРОЕНИЕ АЛКАНОВ
- ПОЛУЧЕНИЕ АЛКАНОВ
- РЕАКЦИИ АЛКАНОВ
- ХИМИЯ НЕФТИ
- СОВЕТЫ ИЗУЧАЮЩЕМУ ОРГАНИЧЕСКУЮ ХИМИЮ. ИЗУЧЕНИЕ РЕАКЦИЙ
- Глава 4. СТЕРЕОХИМИЯ И ОПТИЧЕСКАЯ АКТИВНОСТЬ
- СПОСОБЫ ИЗОБРАЖЕНИЯ ЭНАНТИОМЕРОВ
- ОБОЗНАЧЕНИЕ АБСОЛЮТНОЙ КОНФИГУРАЦИИ
- НАЗВАНИЯ ХИРАЛЬНЫХ МОЛЕКУЛ
- ИЗОБРАЖЕНИЕ МОЛЕКУЛ С ПРОТИВОПОЛОЖНОЙ КОНФИГУРАЦИЕЙ
- D,L-НОМЕНКЛАТУРА ЭНАНТИОМЕРОВ
- ТЕРМИНОЛОГИЯ, ПРИМЕНЯЕМАЯ В СТЕРЕОХИМИИ
- ЗНАЧЕНИЕ ОПТИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ
- Глава 5. ОРГАНИЧЕСКИЕ ГАЛОГЕНСОДЕРЖАЩИЕ СОЕДИНЕНИЯ
- ПОЛУЧЕНИЕ ГАЛОГЕНАЛКАНОВ
- РЕАКЦИИ ГАЛОГЕНАЛКАНОВ
- ПРАКТИЧЕСКИ ВАЖНЫЕ ГАЛОГЕНАЛКАНЫ
- Прикладная органическая химия: ОРГАНИЧЕСКИЕ ПЕСТИЦИДЫ
- Глава 6. НЕНАСЫЩЕННЫЕ УГЛЕВОДОРОДЫ
- НОМЕНКЛАТУРА АЛКЕНОВ
- ПОЛУЧЕНИЕ АЛКЕНОВ
- ОСНОВНЫЕ РЕАКЦИИ АЛКЕНОВ
- ПОЛИМЕРЫ
- НОМЕНКЛАТУРА АЛКИНОВ
- ПОЛУЧЕНИЕ АЛКИНОВ
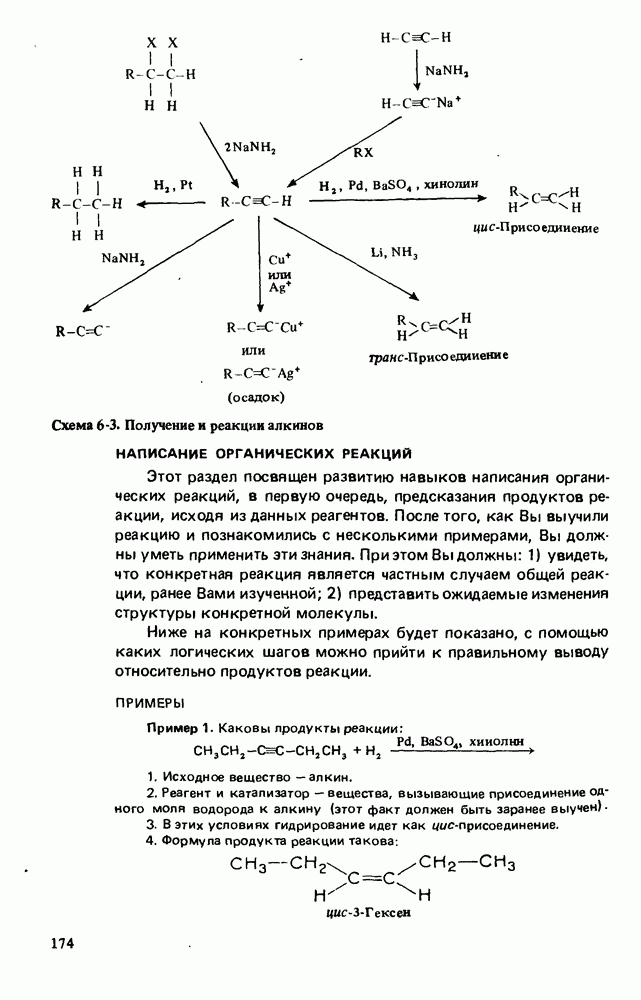
- РЕАКЦИИ АЛКИНОВ
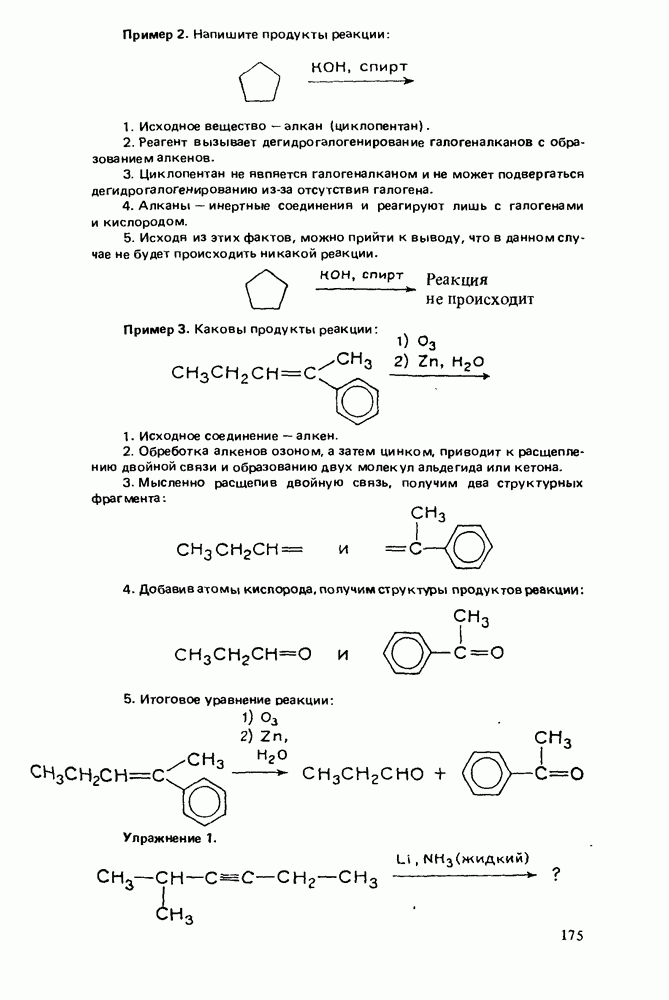
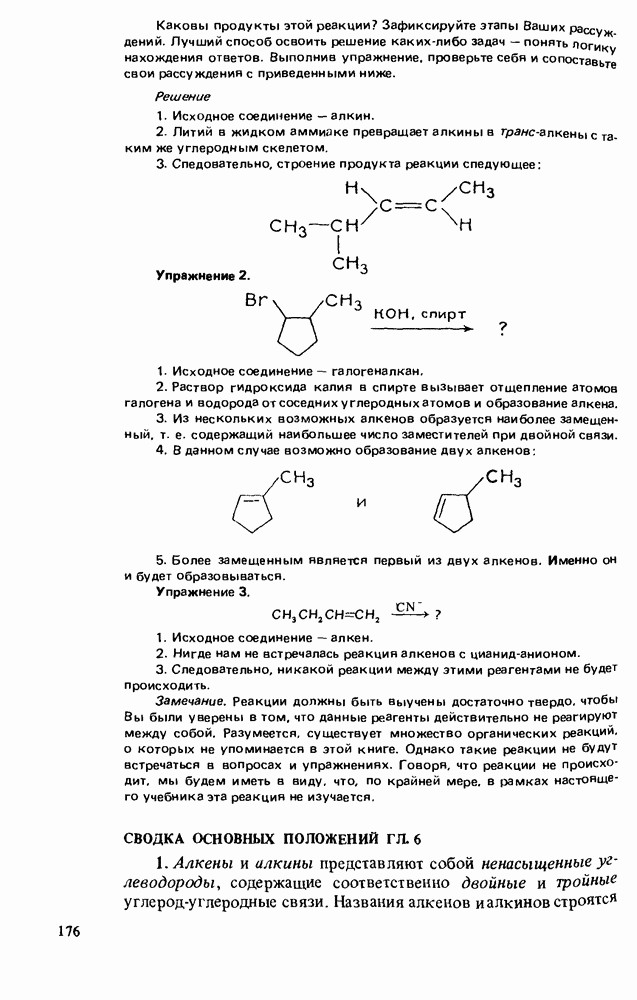
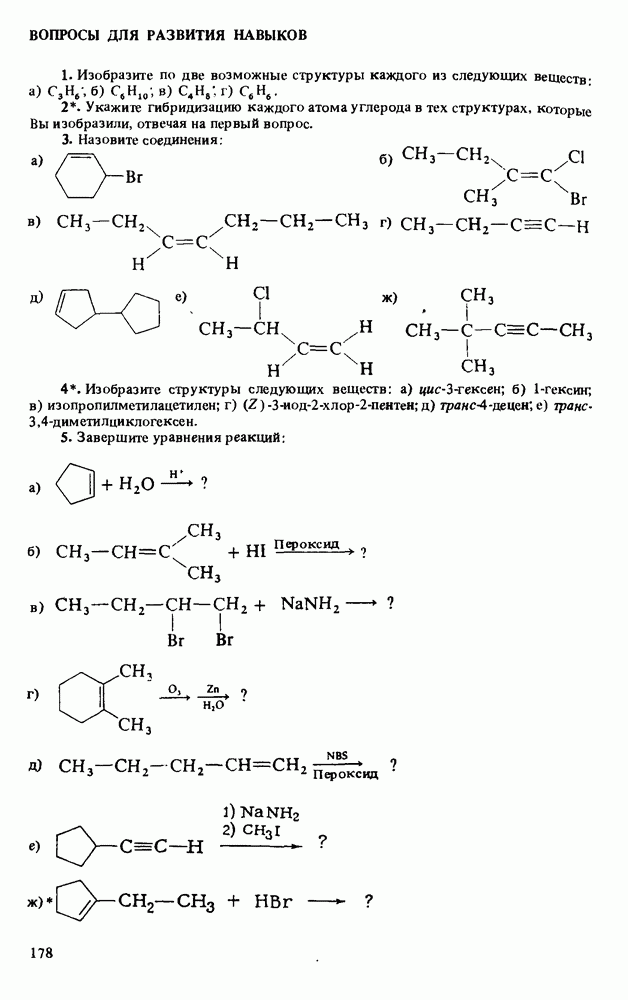
- НАПИСАНИЕ ОРГАНИЧЕСКИХ РЕАКЦИЙ
- Глава 7. СПИРТЫ И ПРОСТЫЕ ЭФИРЫ
- НОМЕНКЛАТУРА СПИРТОВ
- НЕКОТОРЫЕ ВАЖНЫЕ ВЕЩЕСТВА, СОДЕРЖАЩИЕ СПИРТОВУЮ ГРУППУ
- ЭТИЛОВЫЙ СПИРТ. ПРОИЗВОДСТВО СПИРТНЫХ НАПИТКОВ
- ПОЛУЧЕНИЕ СПИРТОВ
- РЕАКЦИИ СПИРТОВ
- ПРОСТЫЕ ЭФИРЫ
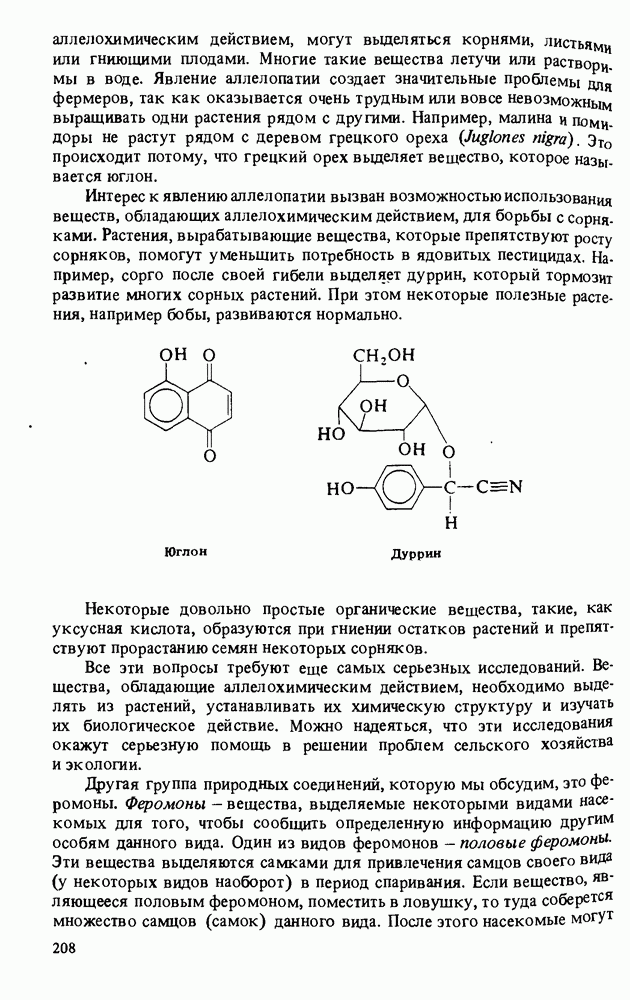
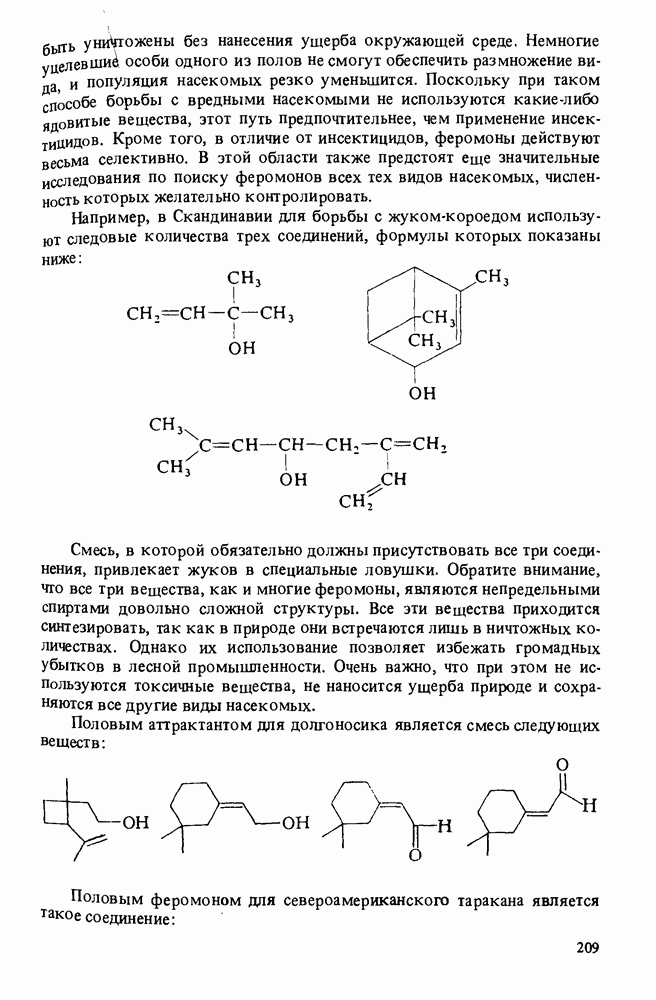
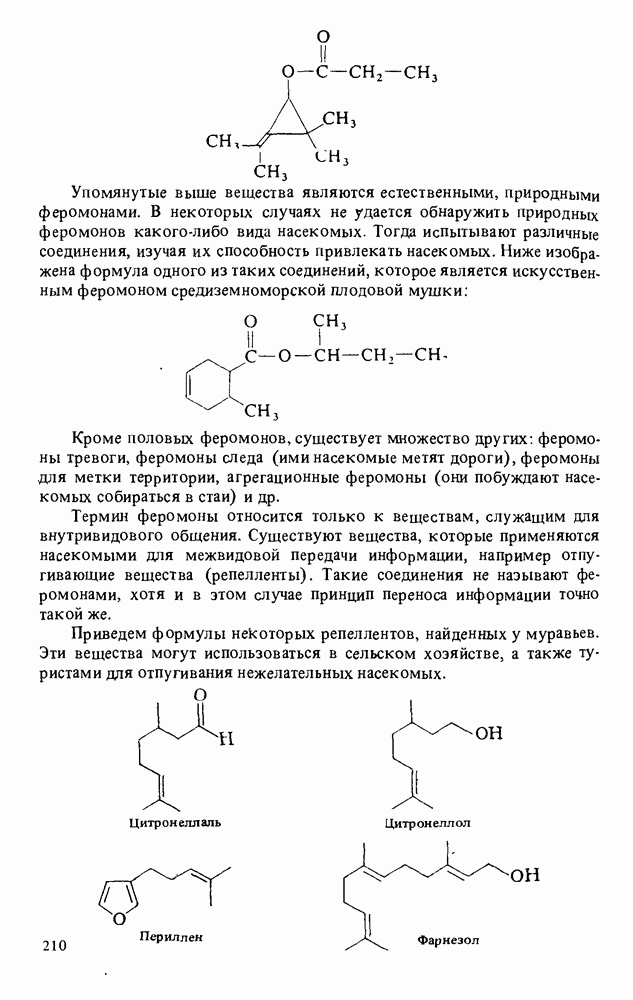
- Прикладная органическая химия: ВЕЩЕСТВА, ОБЛАДАЮЩИЕ АЛЛЕЛОХИМИЧЕСКИМ ДЕЙСТВИЕМ. ФЕРОМОНЫ
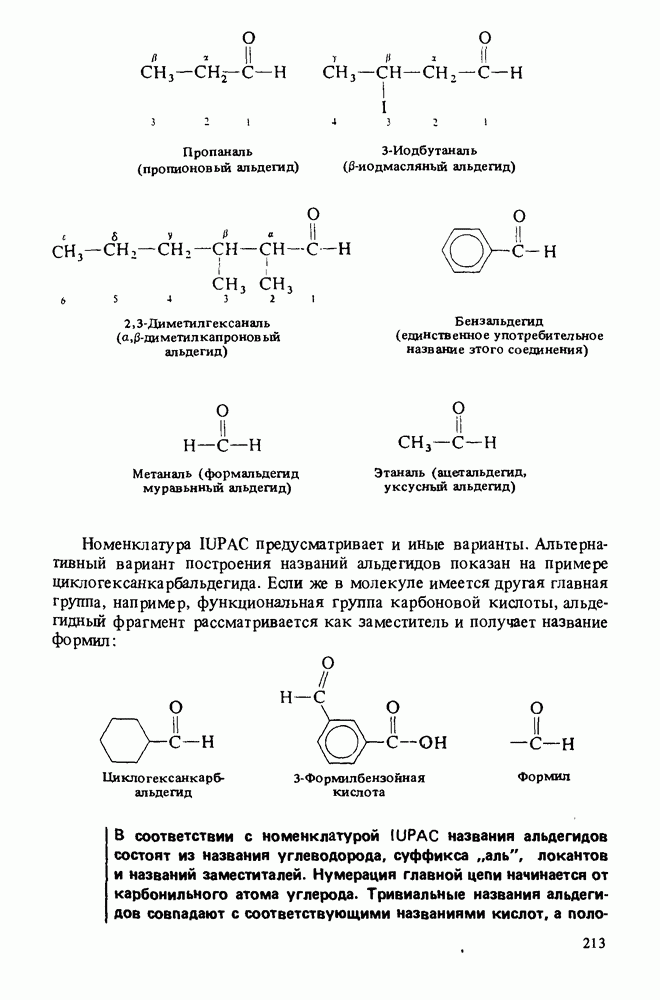
- Глава 8. АЛЬДЕГИДЫ И КЕТОНЫ
- ПОЛУЧЕНИЕ АЛЬДЕГИДОВ И КЕТОНОВ
- РЕАКЦИИ АЛЬДЕГИДОВ И КЕТОНОВ
- Глава 9. АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
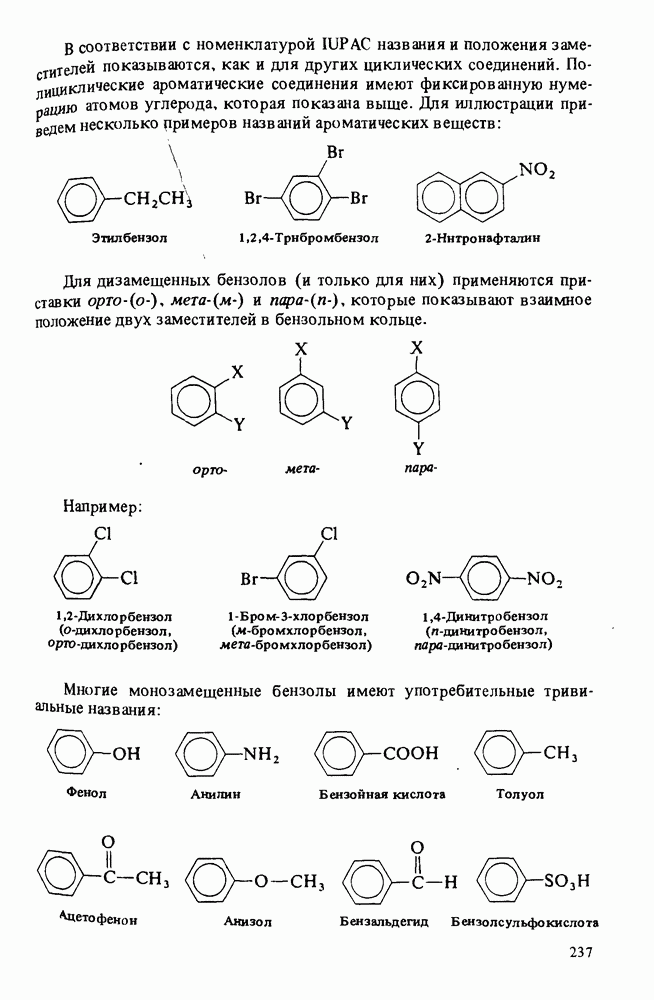
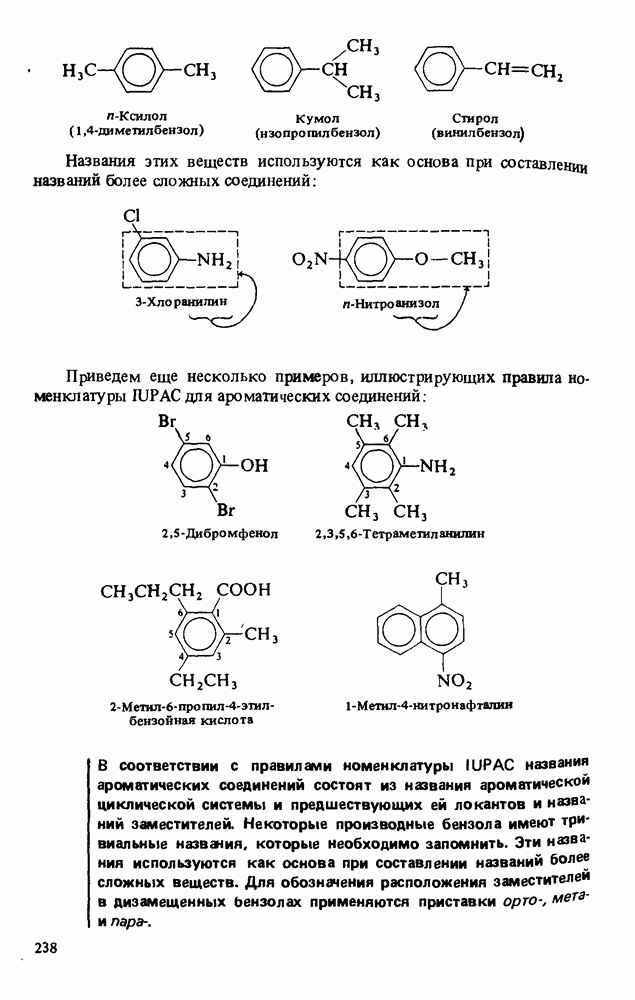
- НОМЕНКЛАТУРА АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ
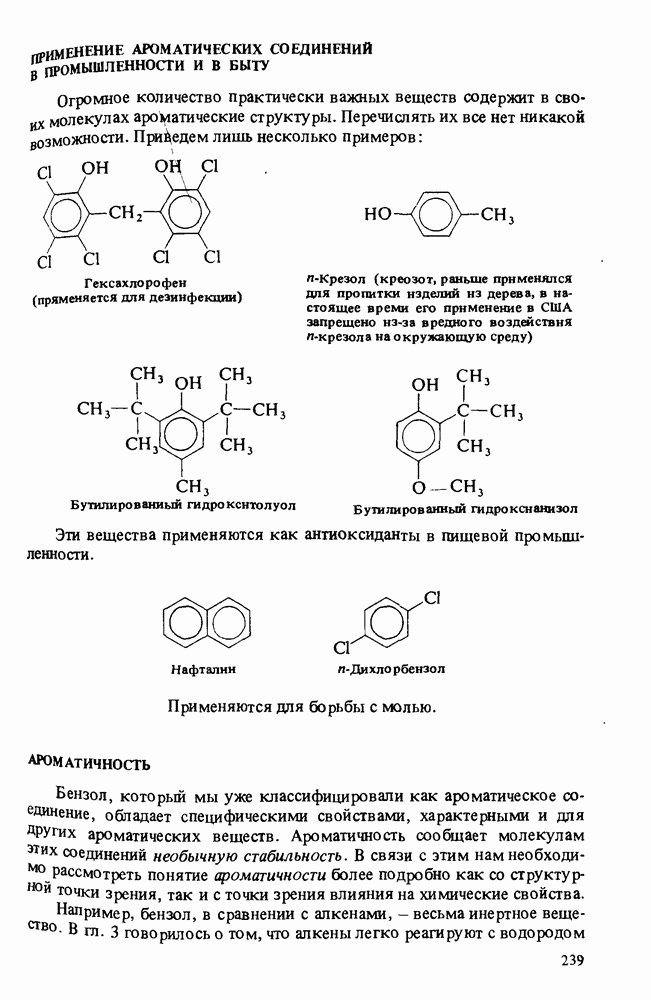
- ПРИМЕНЕНИЕ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ В ПРОМЫШЛЕННОСТИ И В БЫТУ
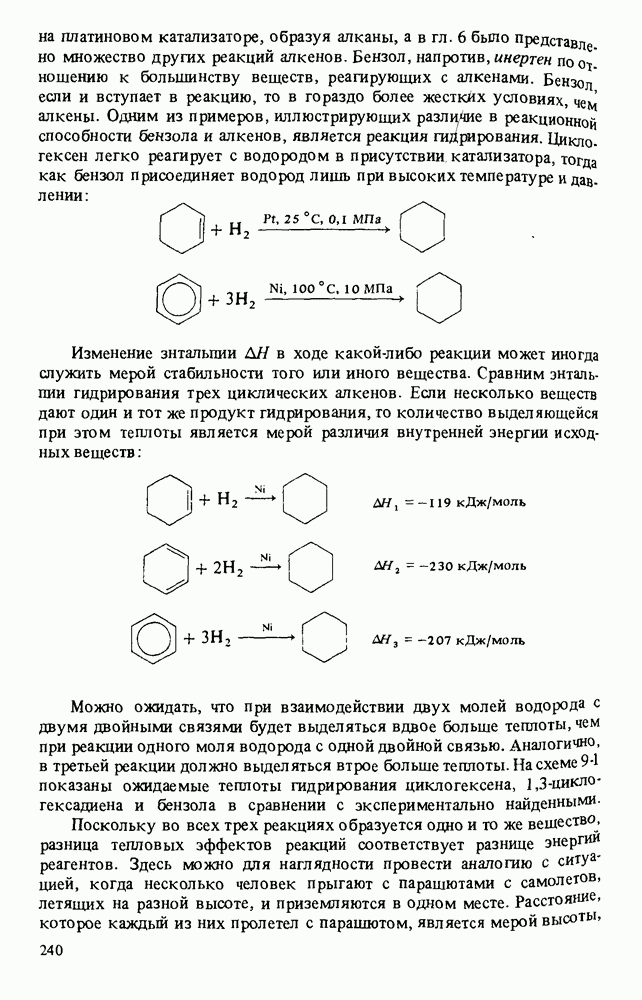
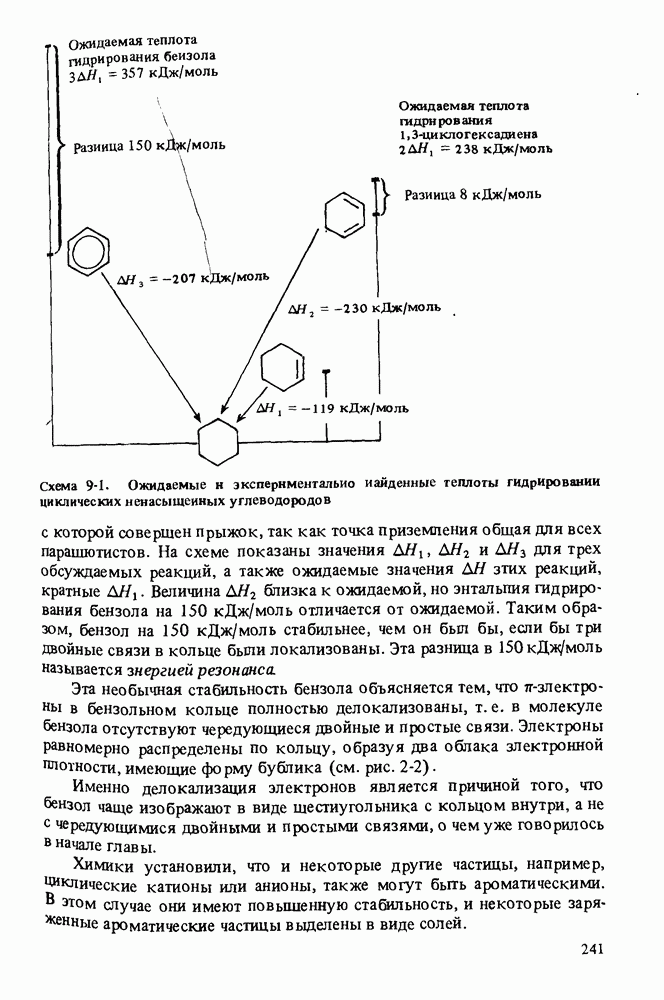
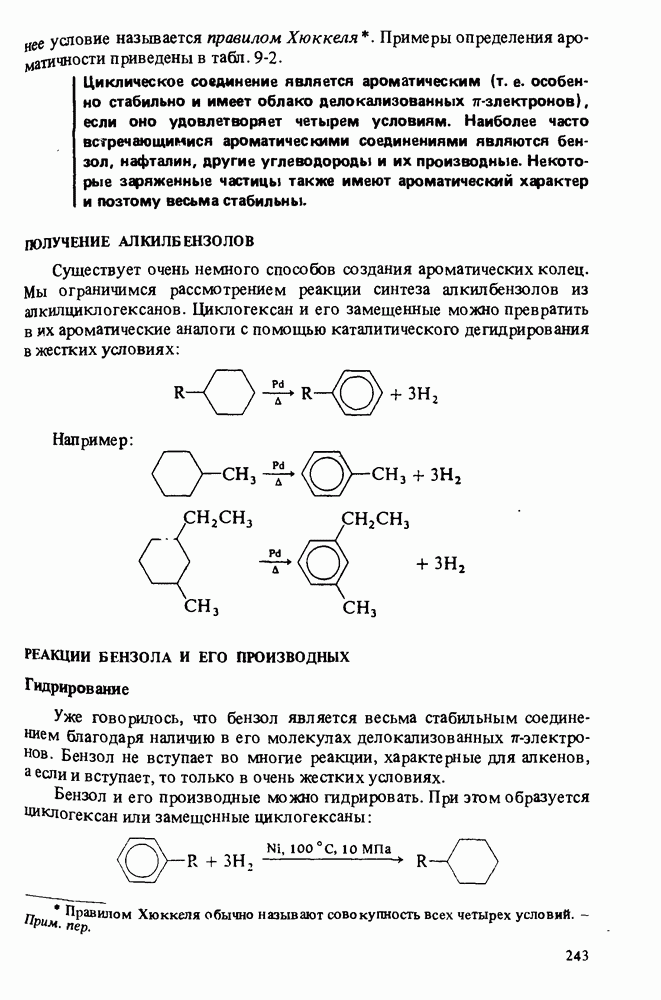
- АРОМАТИЧНОСТЬ
- ПОЛУЧЕНИЕ АЛКИЛЬБЕНЗОЛОВ
- РЕАКЦИИ БЕНЗОЛА И ЕГО ПРОИЗВОДНЫХ
- АРОМАТИЧЕСКОЕ ЭЛЕКТРОФИЛЬНОЕ ЗАМЕЩЕНИЕ
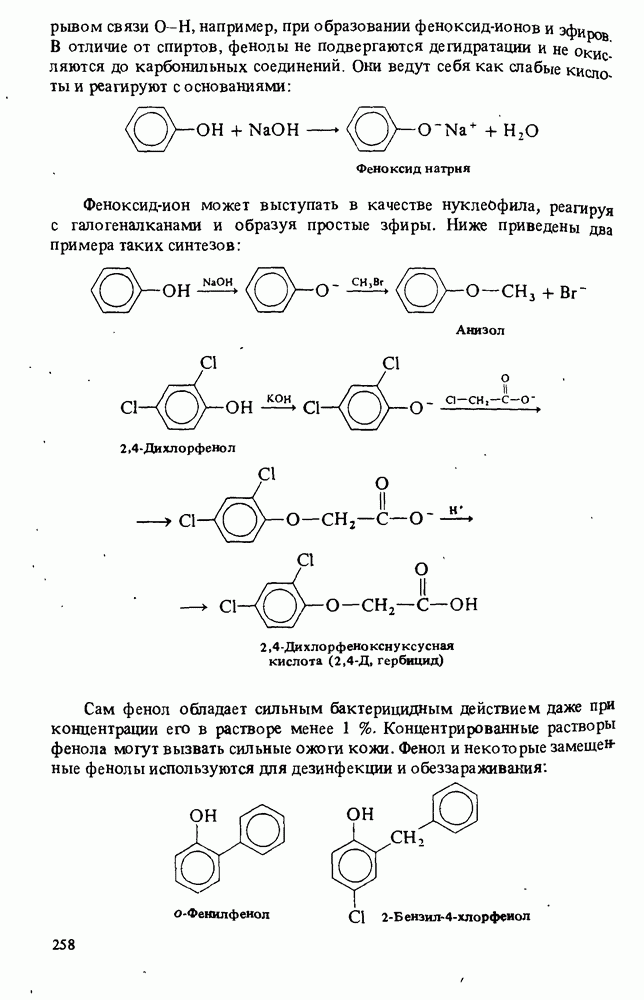
- ФЕНОЛЫ
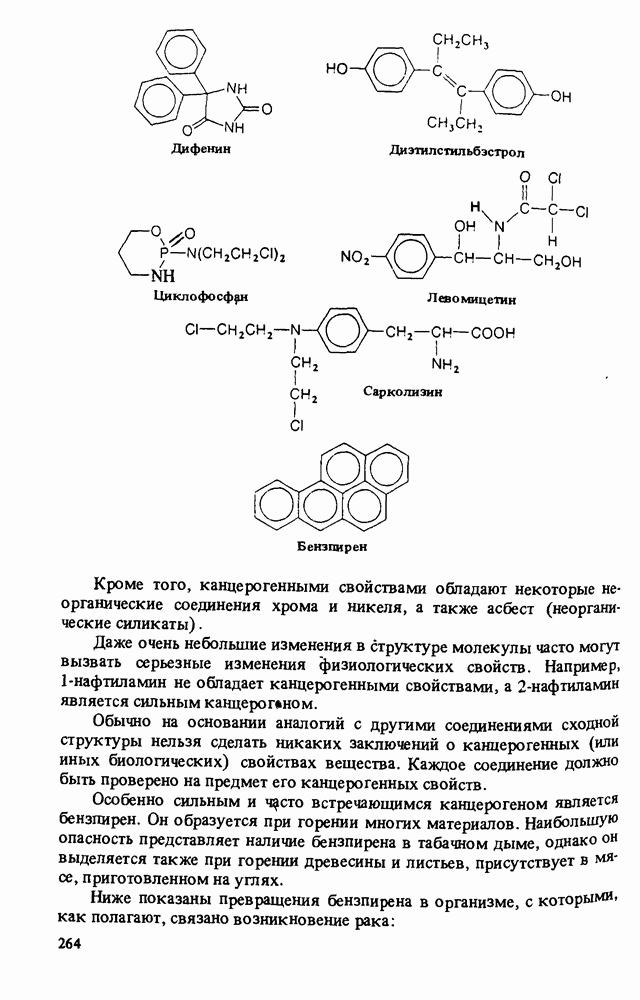
- Прикладная органическая химия: КАНЦЕРОГЕННЫЕ АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
- Глава 10. ОРГАНИЧЕСКИЙ СИНТЕЗ
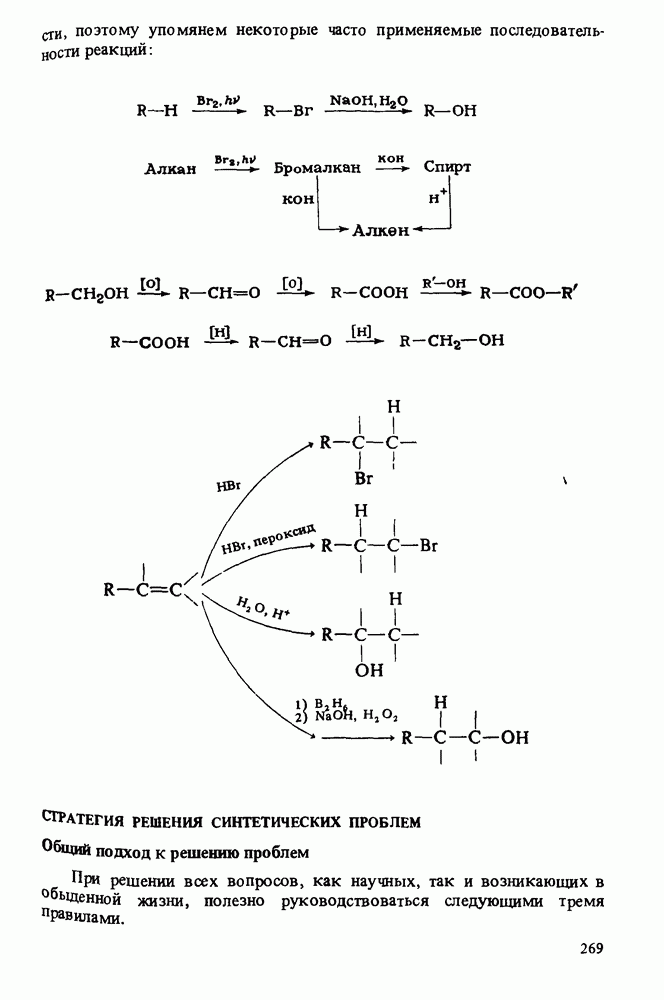
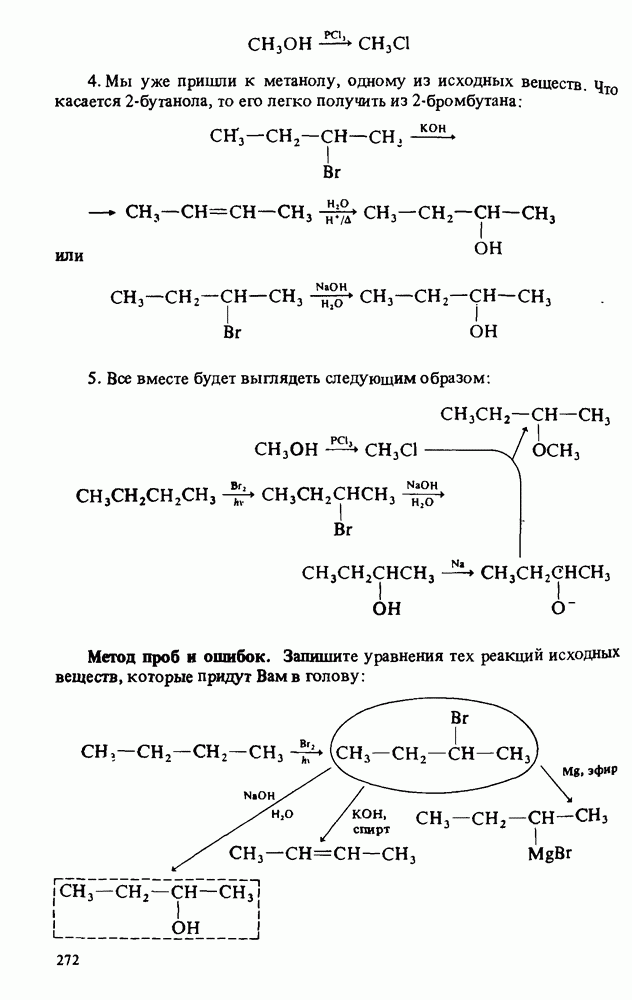
- СТРАТЕГИЯ РЕШЕНИЯ СИНТЕТИЧЕСКИХ ПРОБЛЕМ
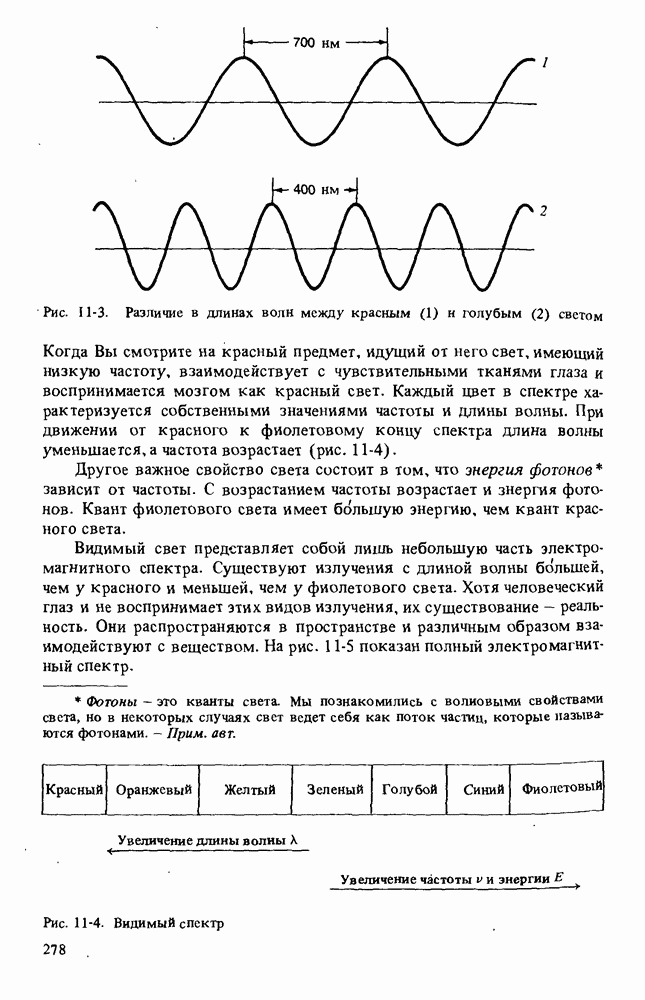
- Глава 11. МОЛЕКУЛЯРНАЯ СПЕКТРОСКОПИЯ
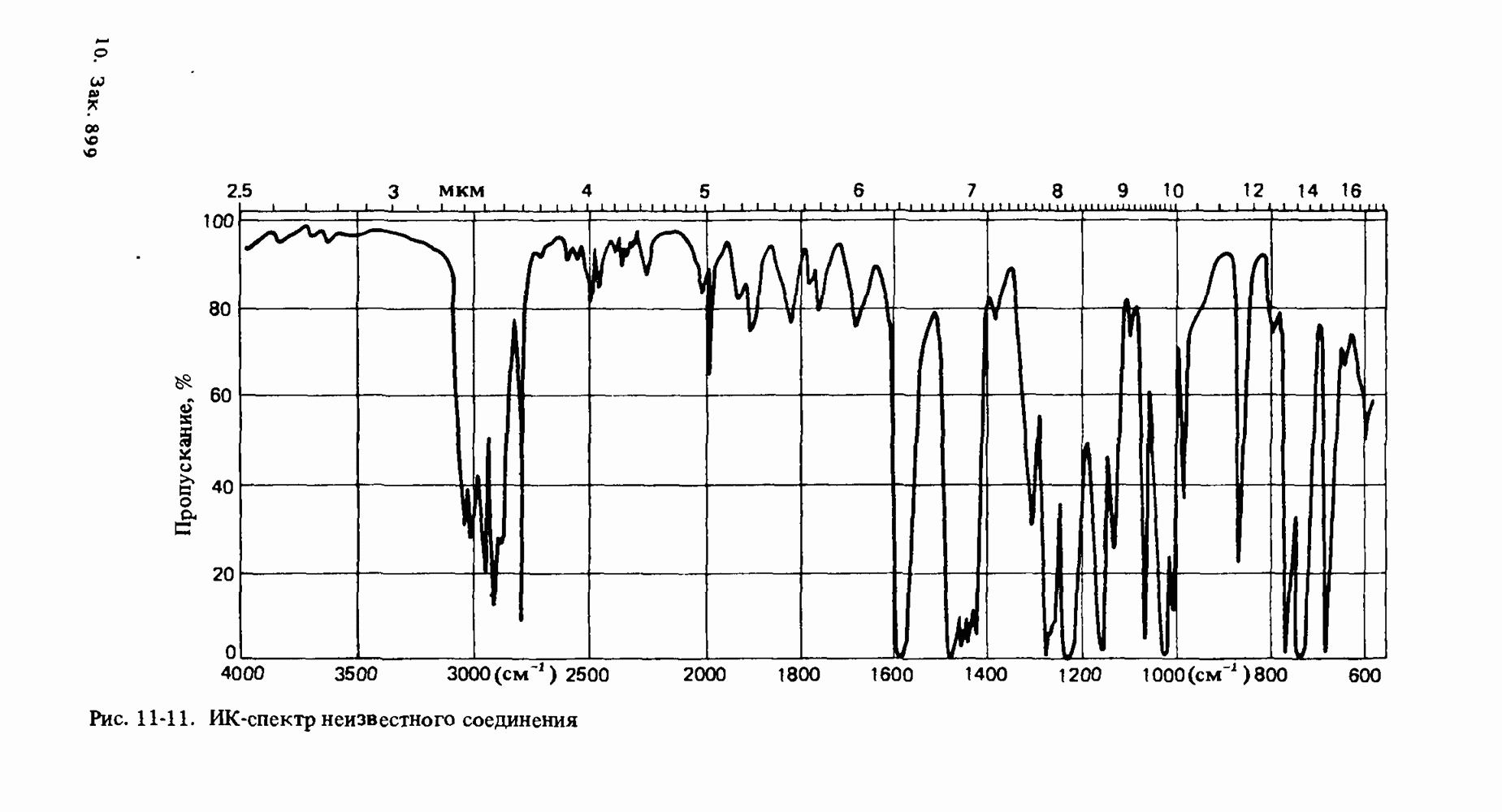
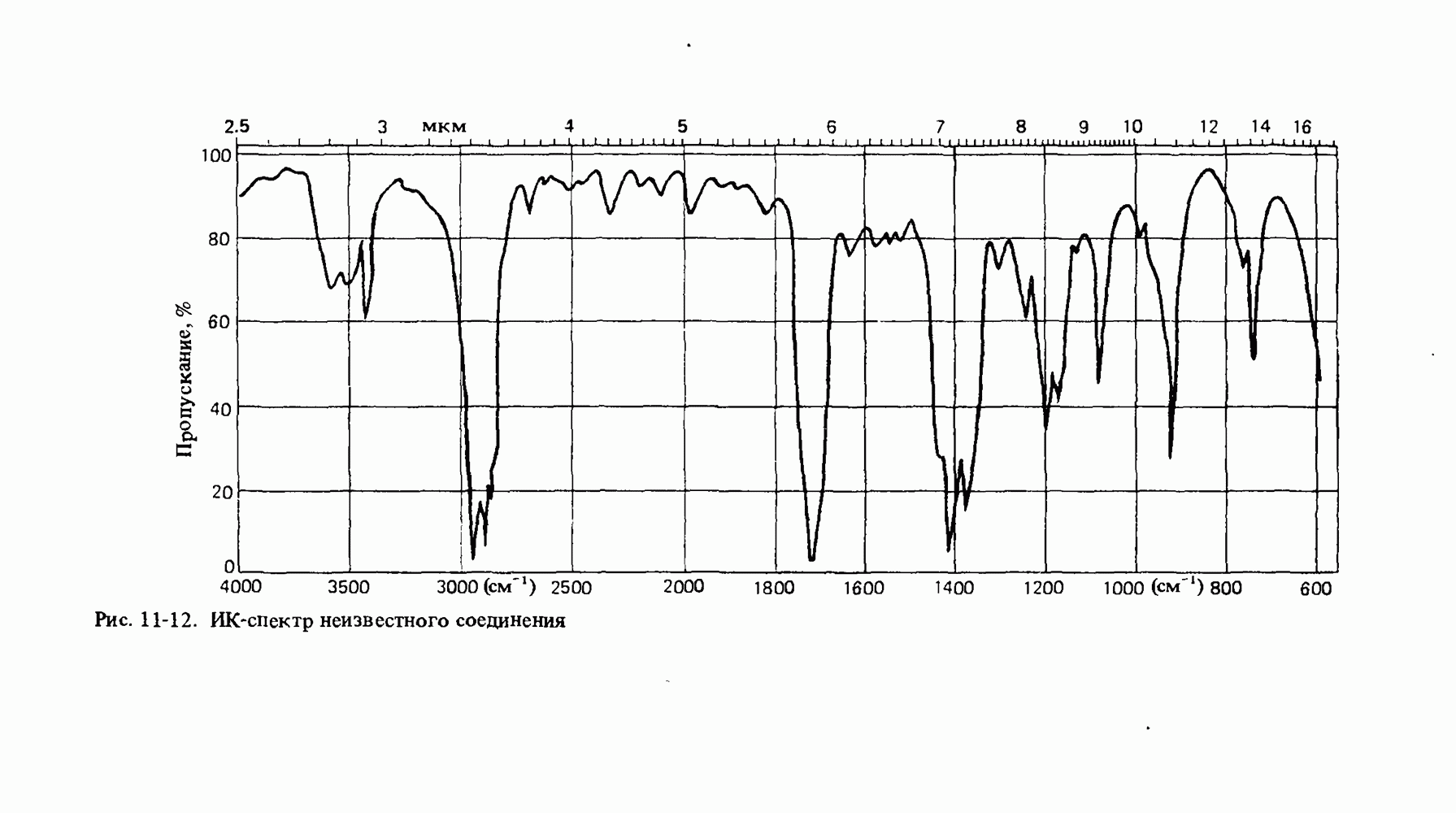
- ИНФРАКРАСНАЯ СПЕКТРОСКОПИЯ
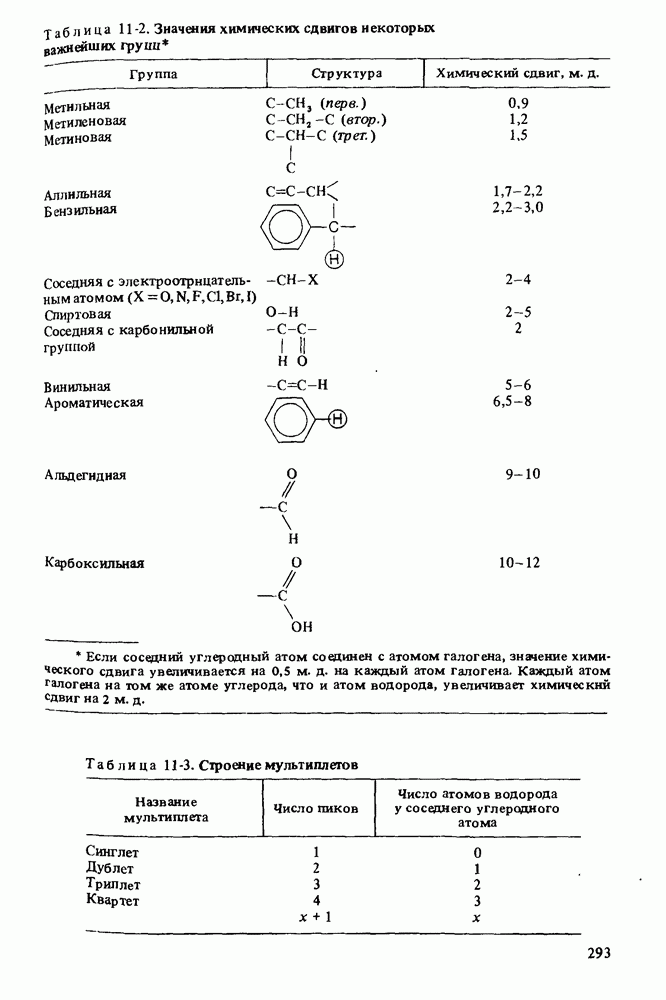
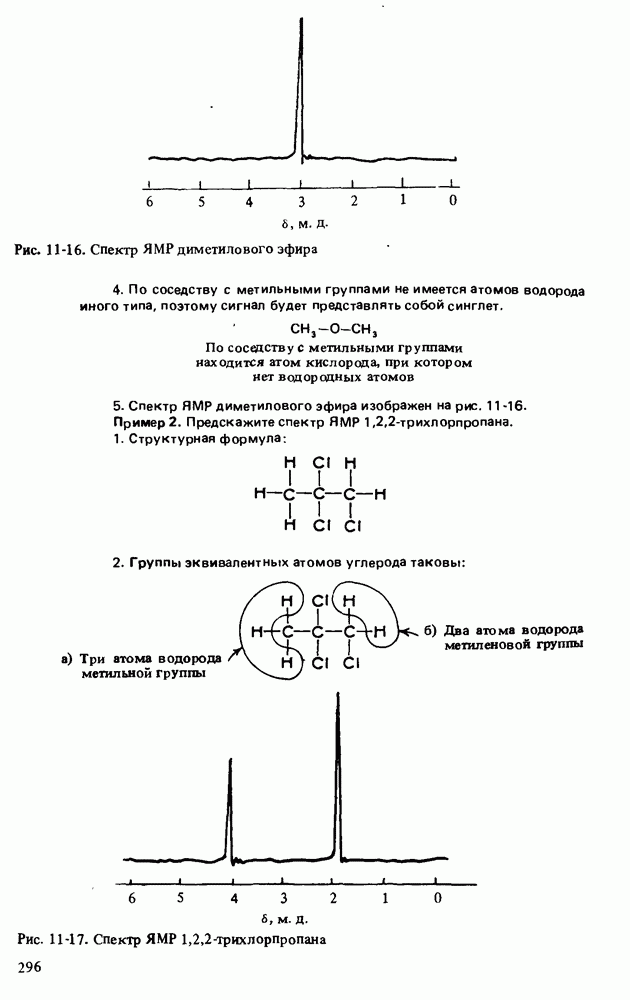
- СПЕКТРОСКОПИЯ ЯДЕРНОГО МАГНИТНОГО РЕЗОНАНСА
- УЛЬТРАФИОЛЕТОВАЯ СПЕКТРОСКОПИЯ
- МАСС-СПЕКТРОМЕТРИЯ
- ОПРЕДЕЛЕНИЕ СТРУКТУРЫ ОРГАНИЧЕСКОГО СОЕДИНЕНИЯ
- Прикладная органическая химия: ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ АЛКОГОЛЯ В КРОВИ
- Глава 12. КАРБОНОВЫЕ КИСЛОТЫ И ИХ ПРОИЗВОДНЫЕ
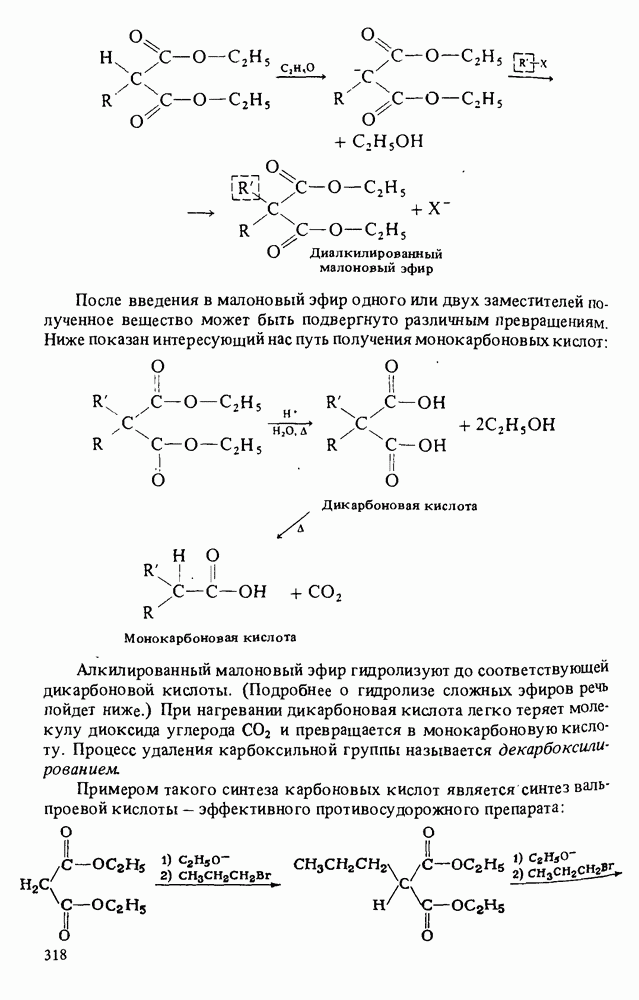
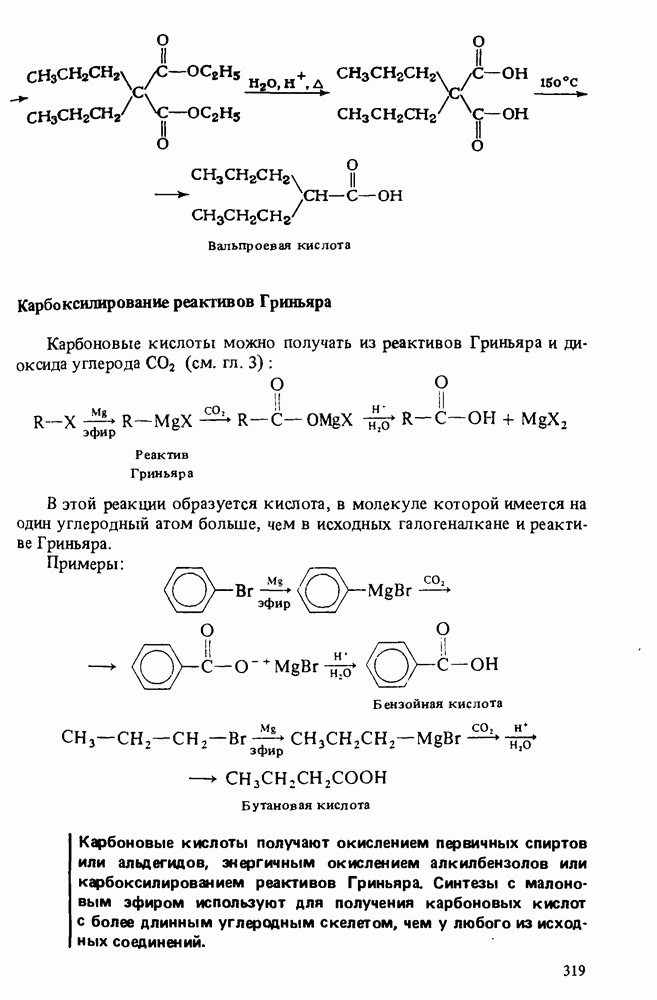
- ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ
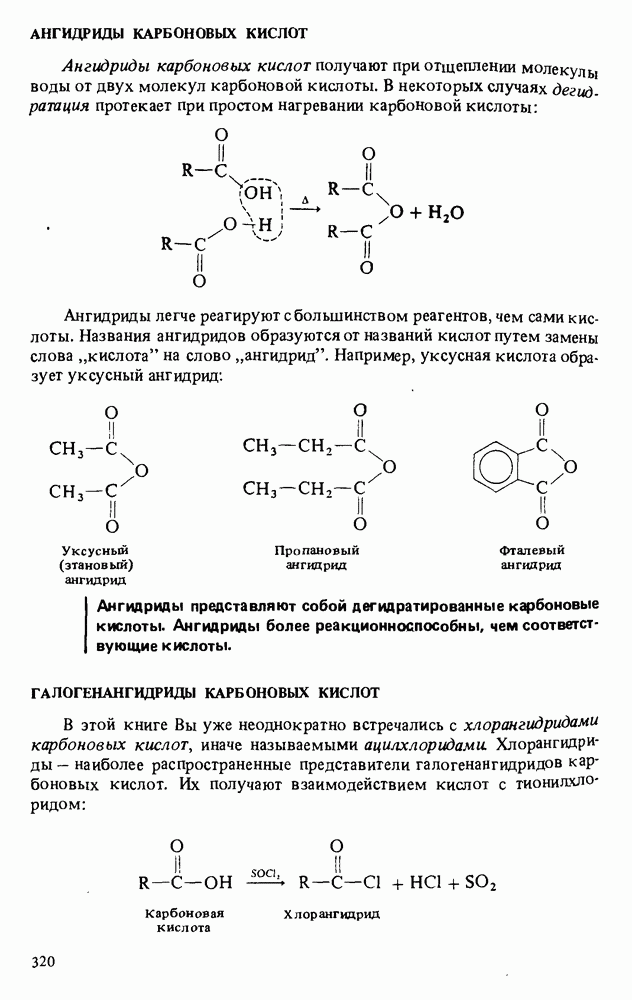
- АНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
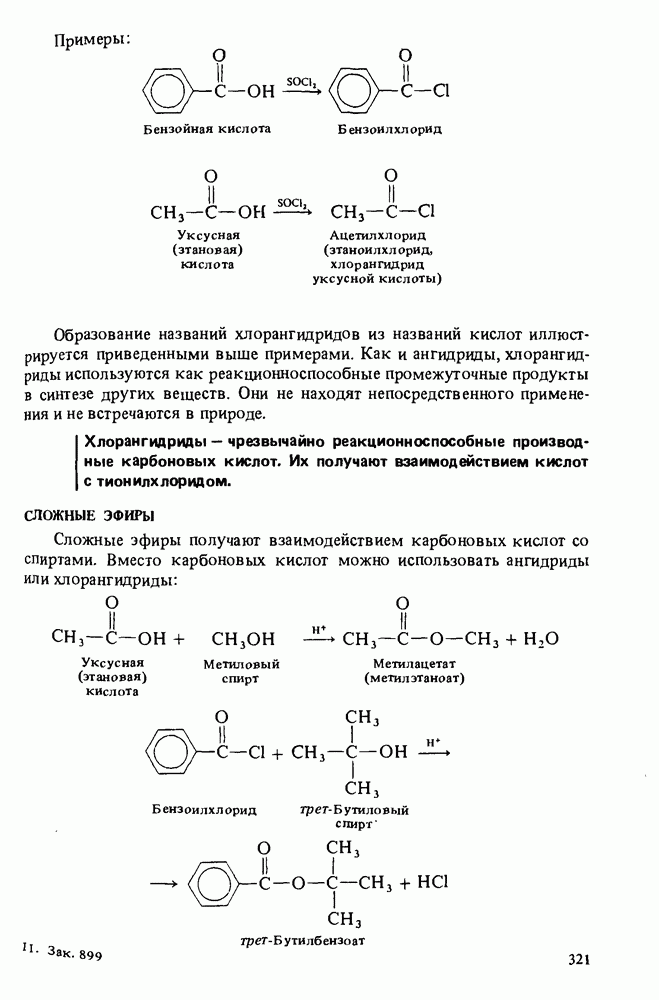
- ГАЛОГЕНАНГИДРИДЫ КАРБОНОВЫХ КИСЛОТ
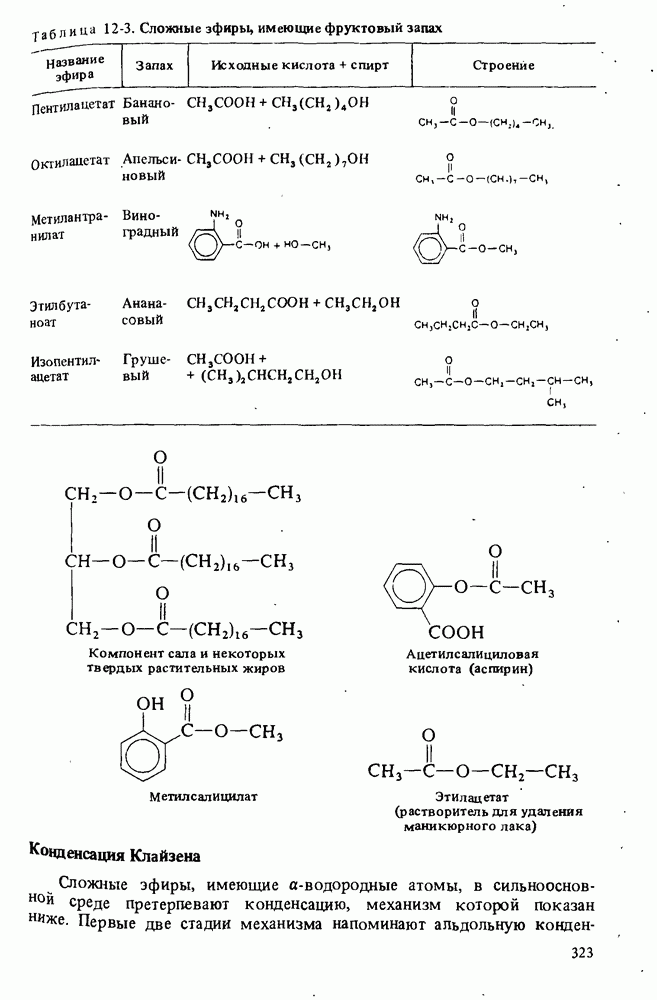
- СЛОЖНЫЕ ЭФИРЫ
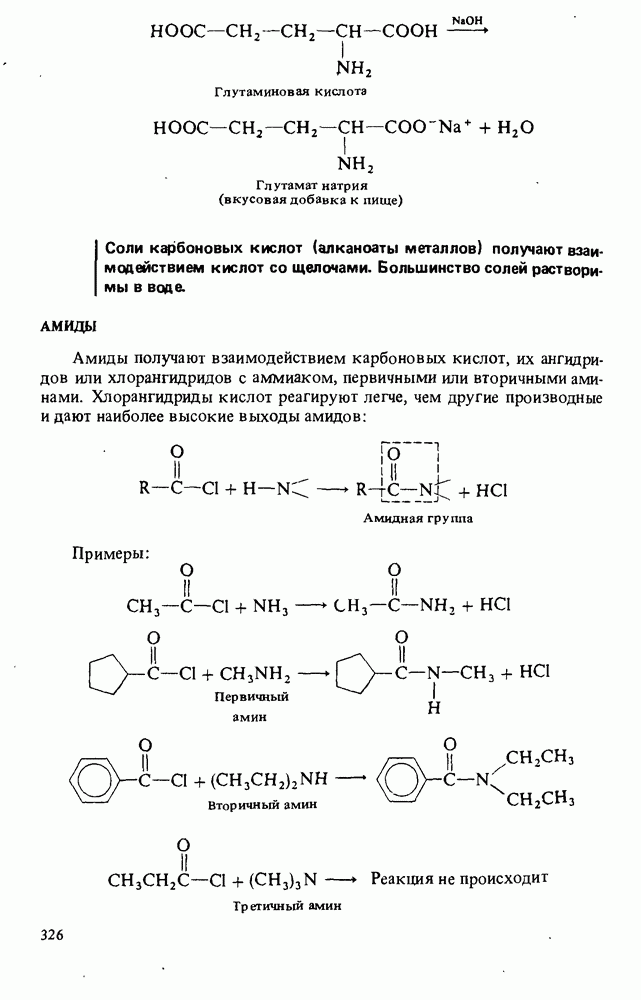
- СОЛИ
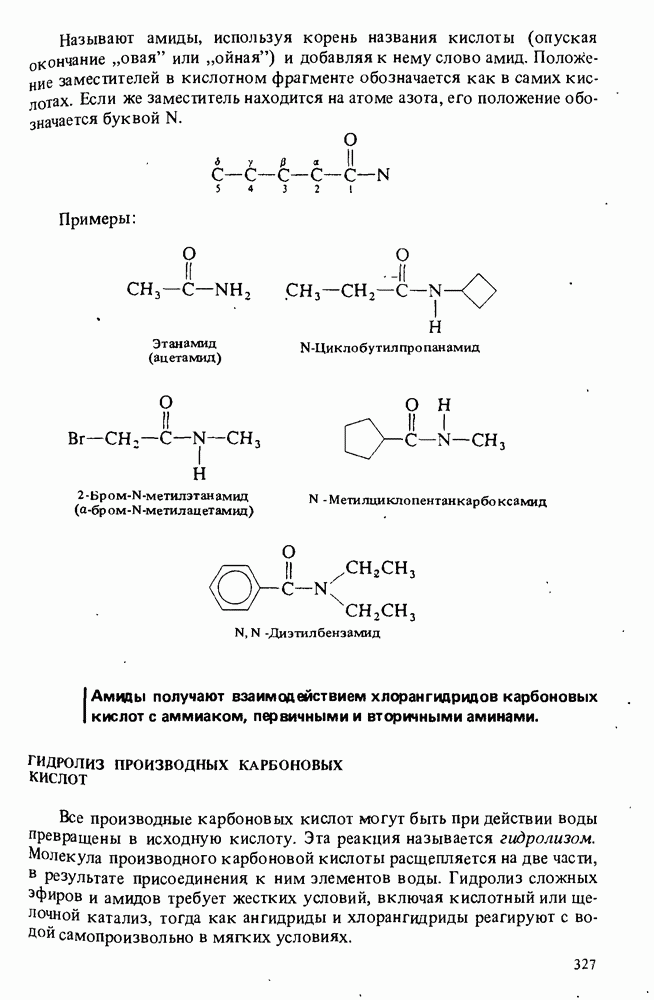
- АМИДЫ
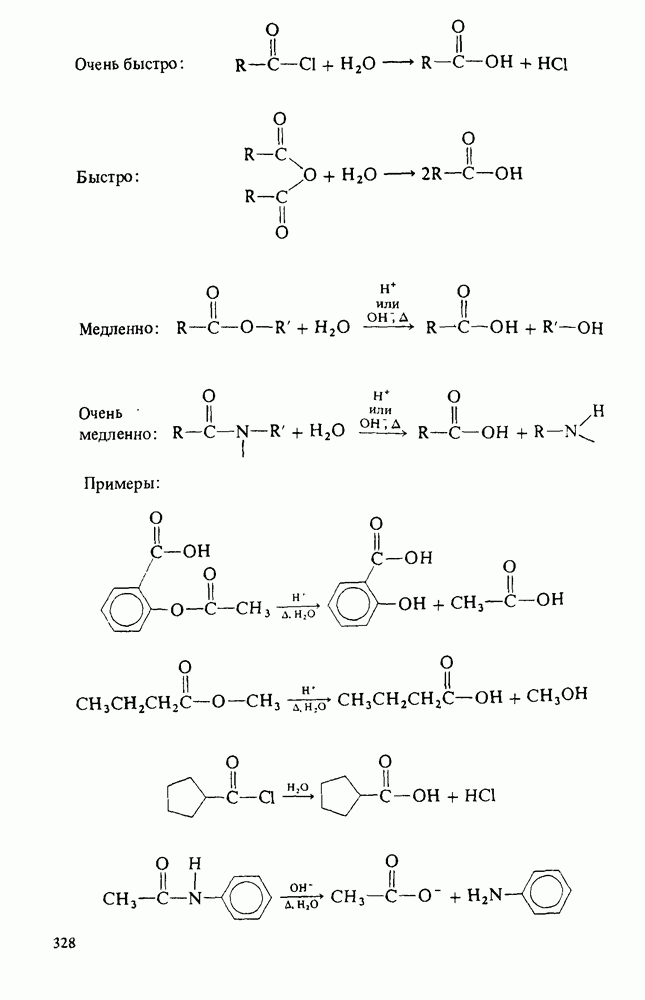
- ГИДРОЛИЗ ПРОИЗВОДНЫХ КАРБОНОВЫХ КИСЛОТ
- СИНТЕТИЧЕСКИЕ ВОЛОКНА
- МОЮЩИЕ СРЕДСТВА
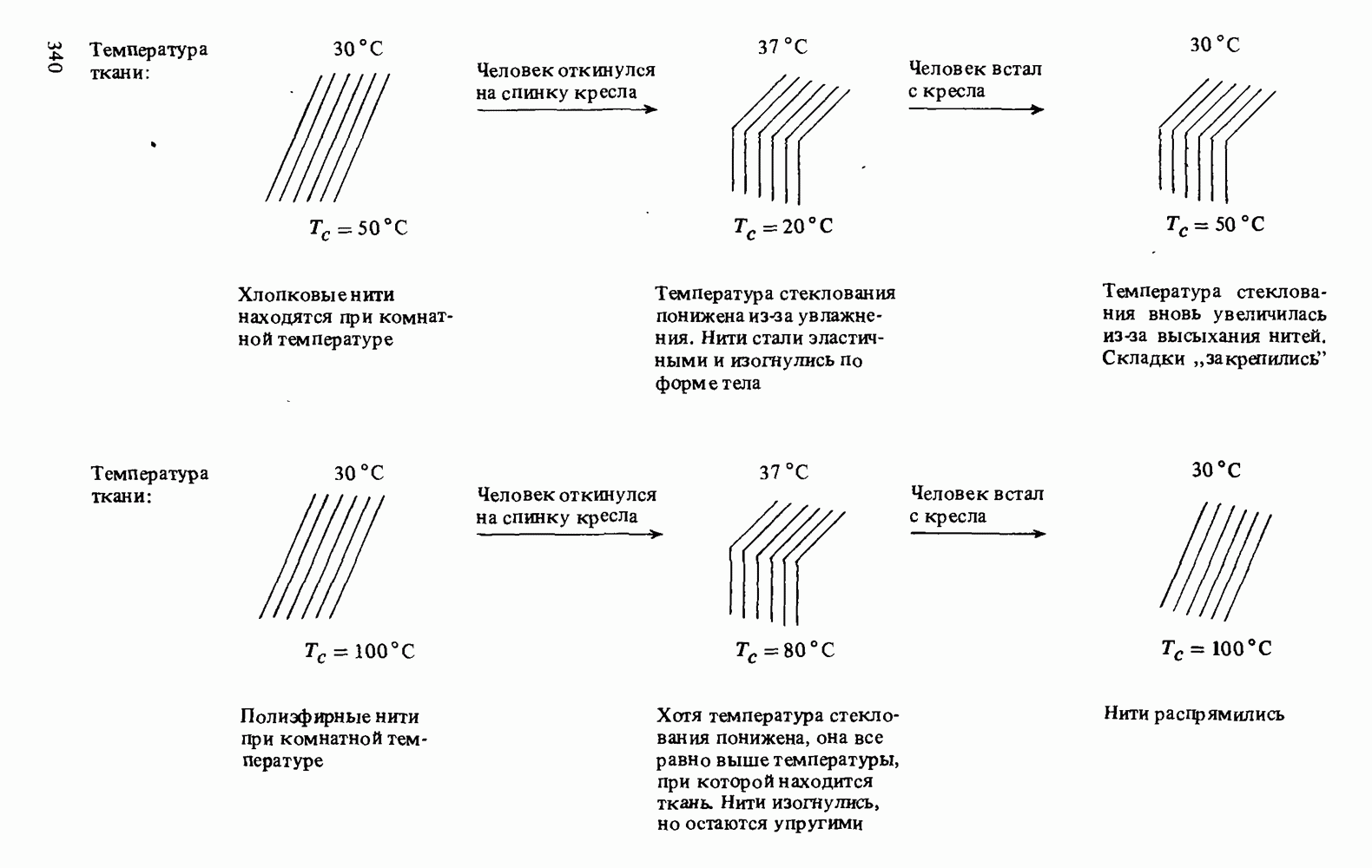
- Прикладная органическая химия: СВОЙСТВА ВОЛОКОН
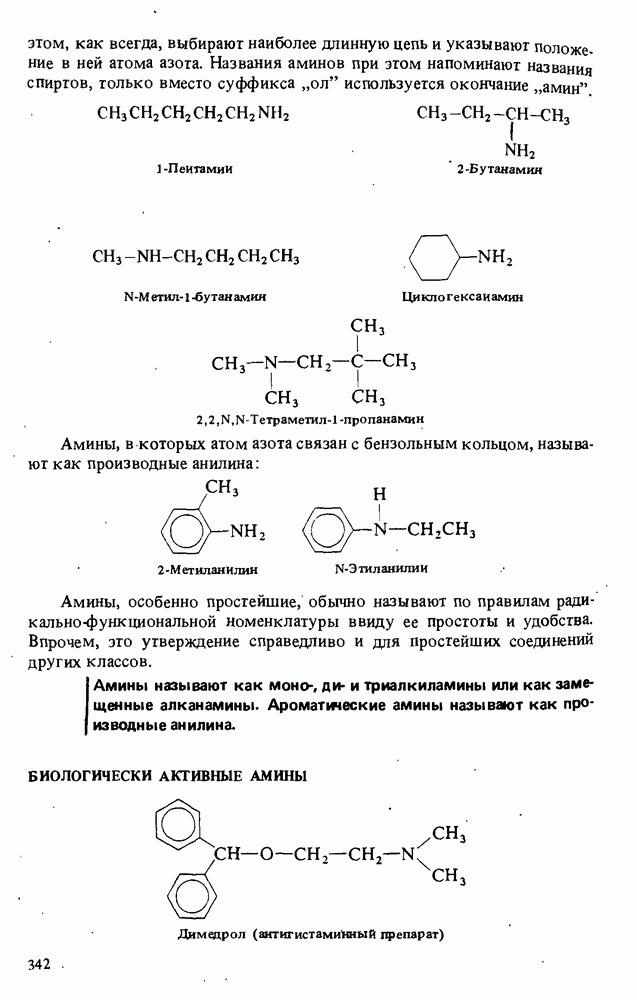
- Глава 13. АМИНЫ
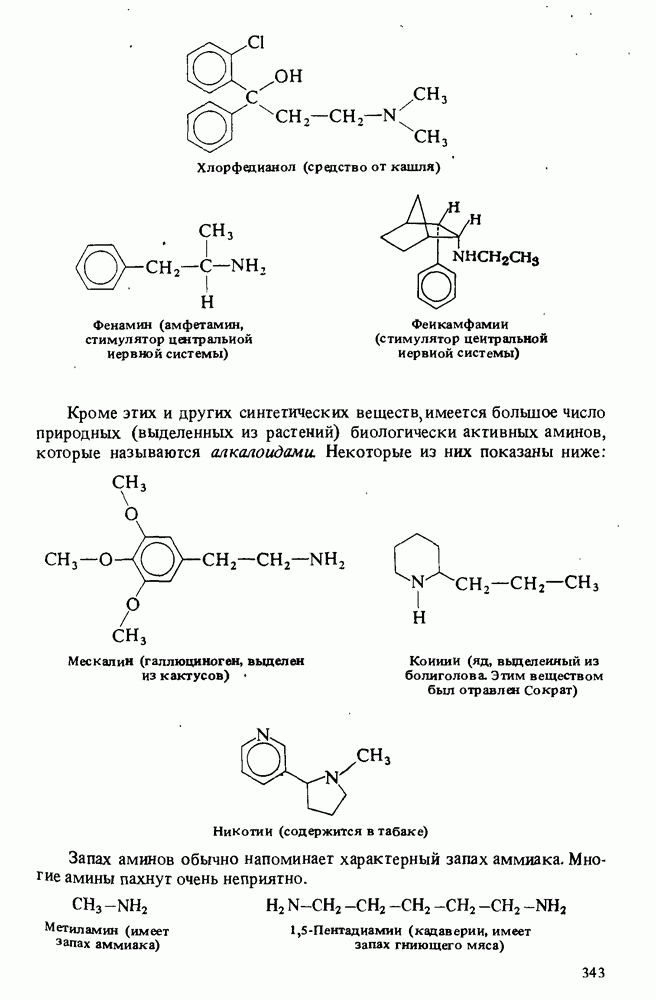
- БИОЛОГИЧЕСКИ АКТИВНЫЕ АМИНЫ
- ОСНОВНОСТЬ АМИНОВ
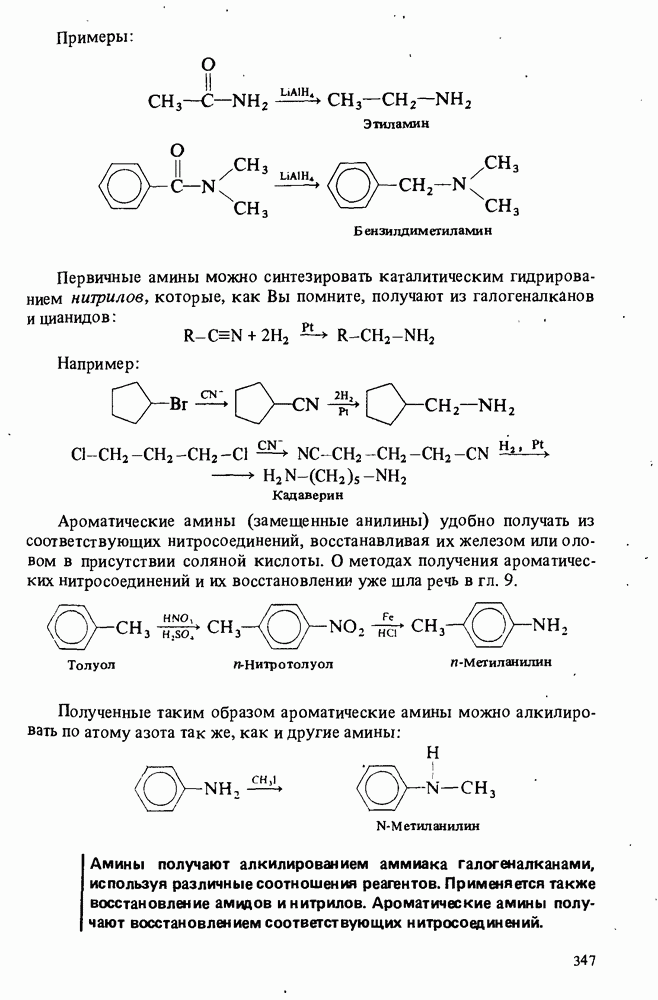
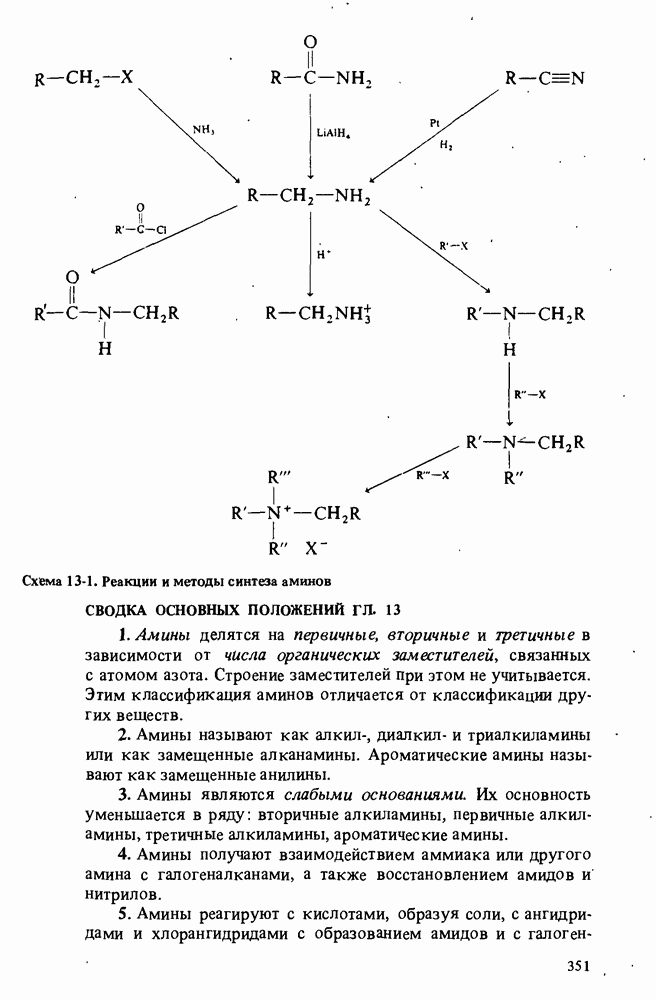
- ПОЛУЧЕНИЕ АМИНОВ
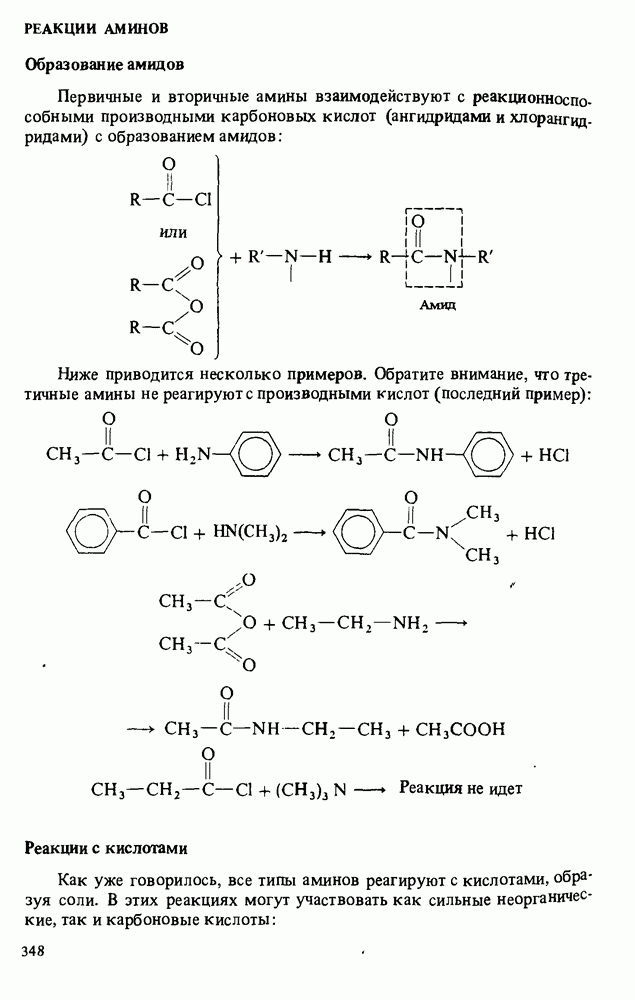
- РЕАКЦИИ АМИНОВ
- Прикладная органическая химия: ПОЛИМЕРЫ, ПОДВЕРГАЮЩИЕСЯ БИОЛОГИЧЕСКОЙ ДЕСТРУКЦИИ
- Глава 14. УГЛЕВОДЫ
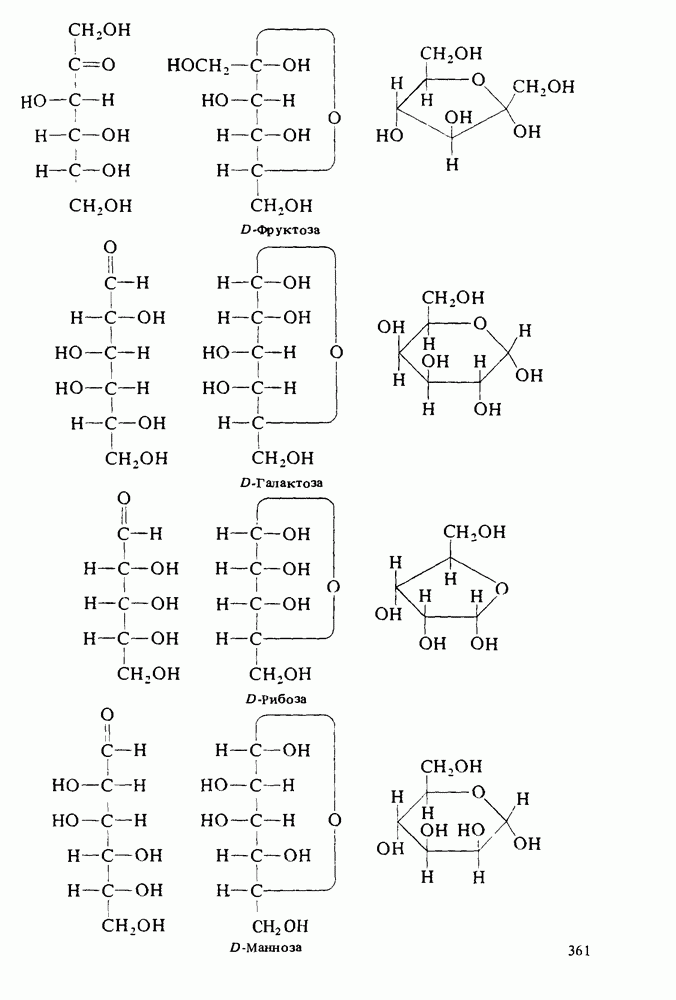
- МОНОСАХАРИДЫ
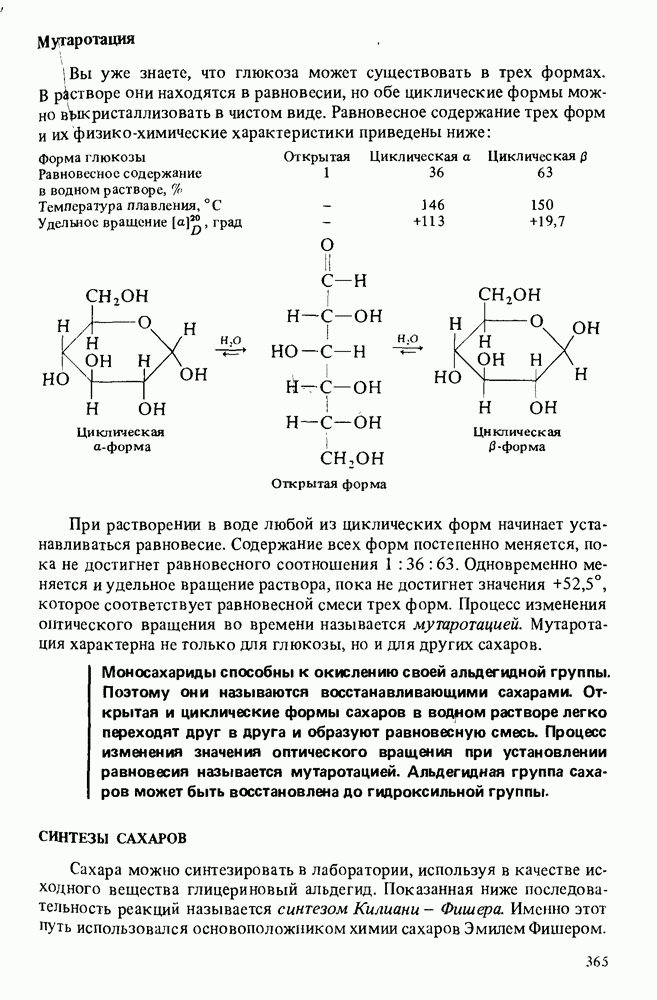
- РЕАКЦИИ МОНОСАХАРИДОВ
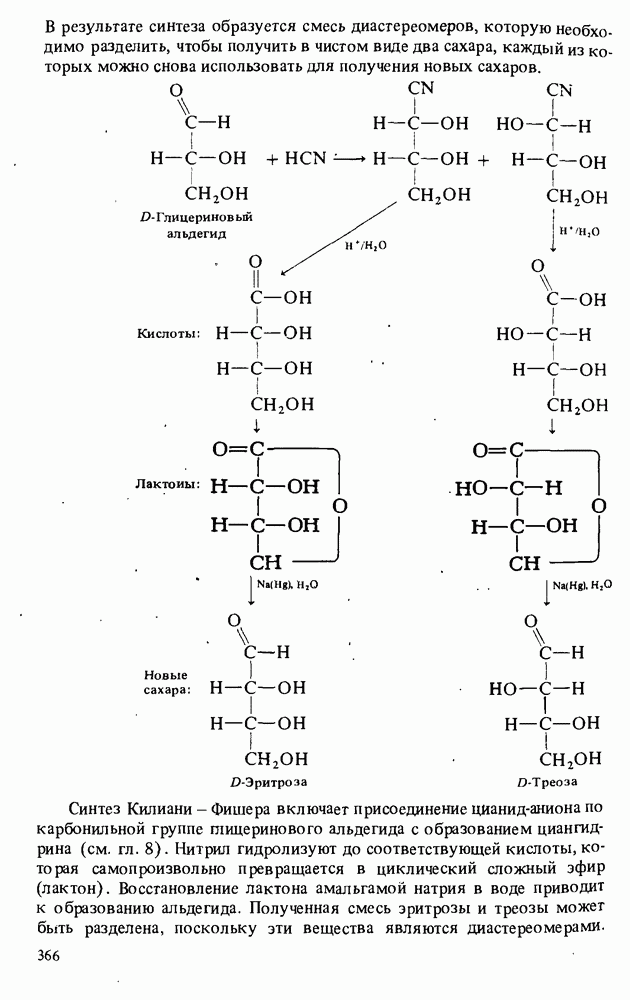
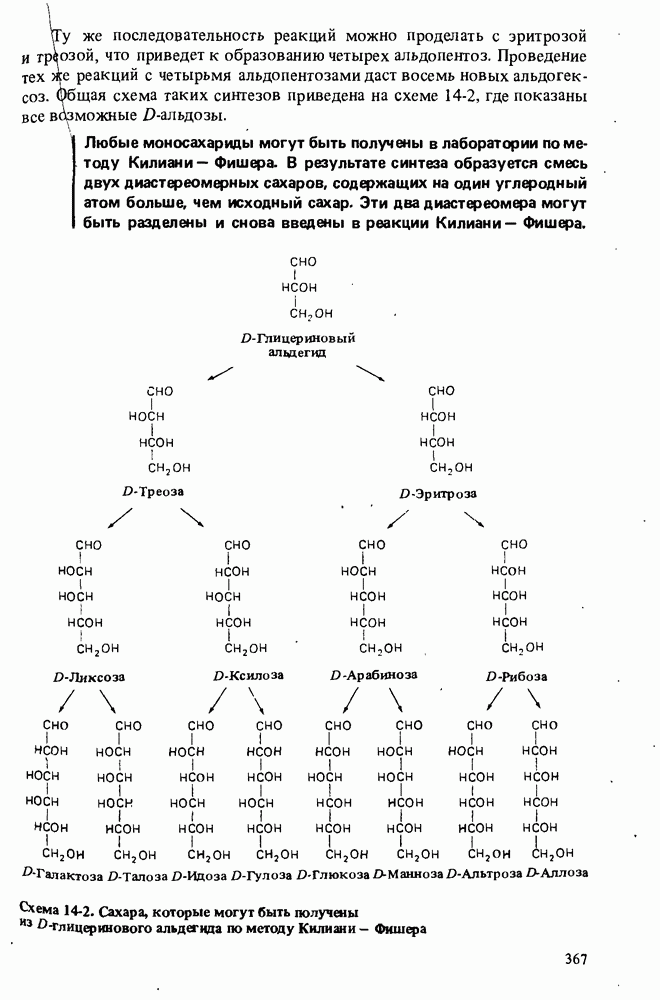
- СИНТЕЗЫ САХАРОВ
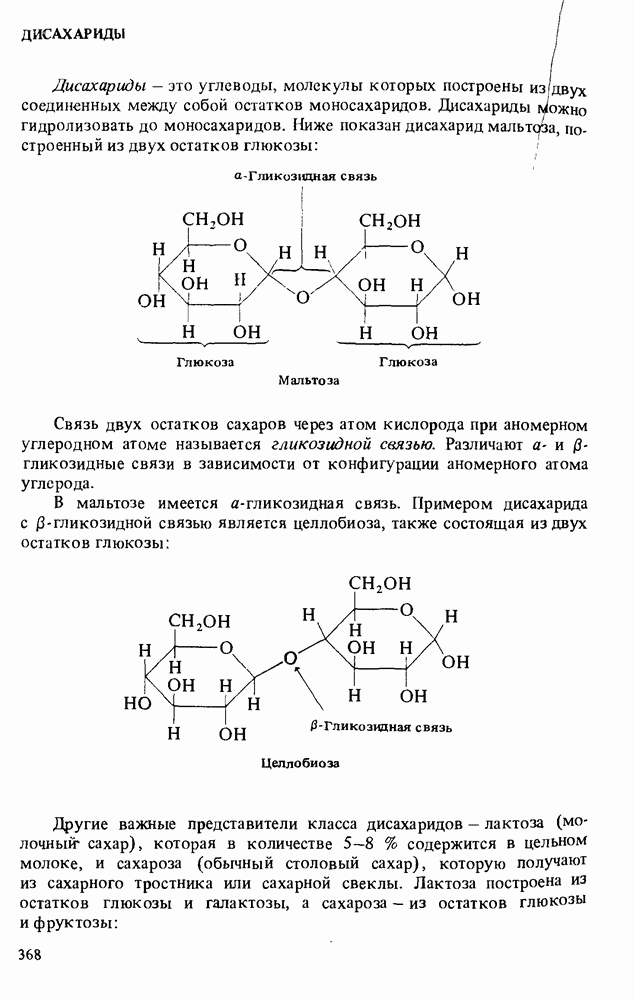
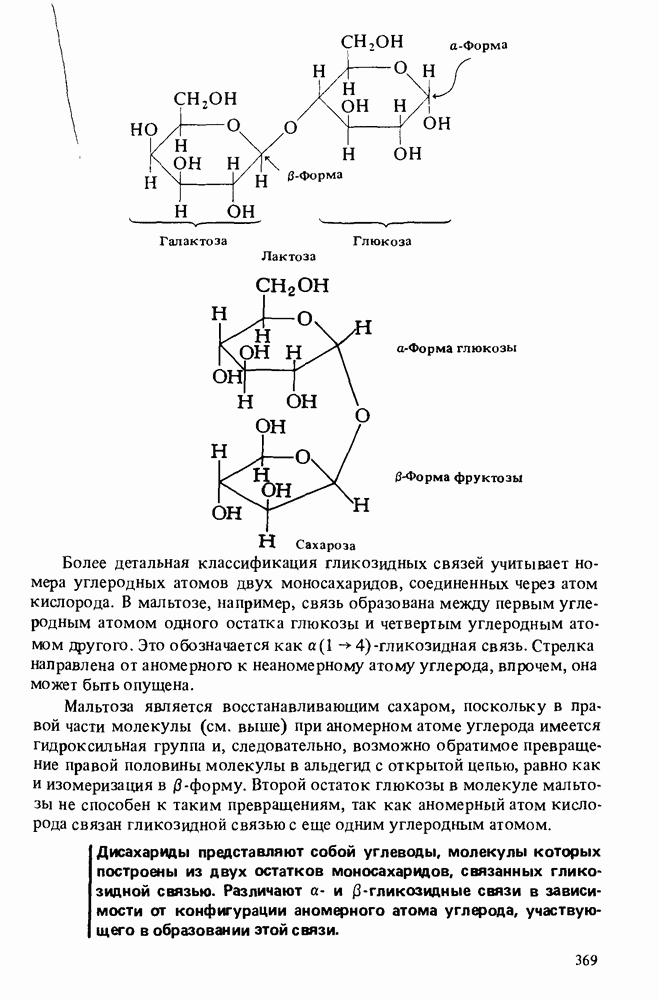
- ДИСАХАРИДЫ
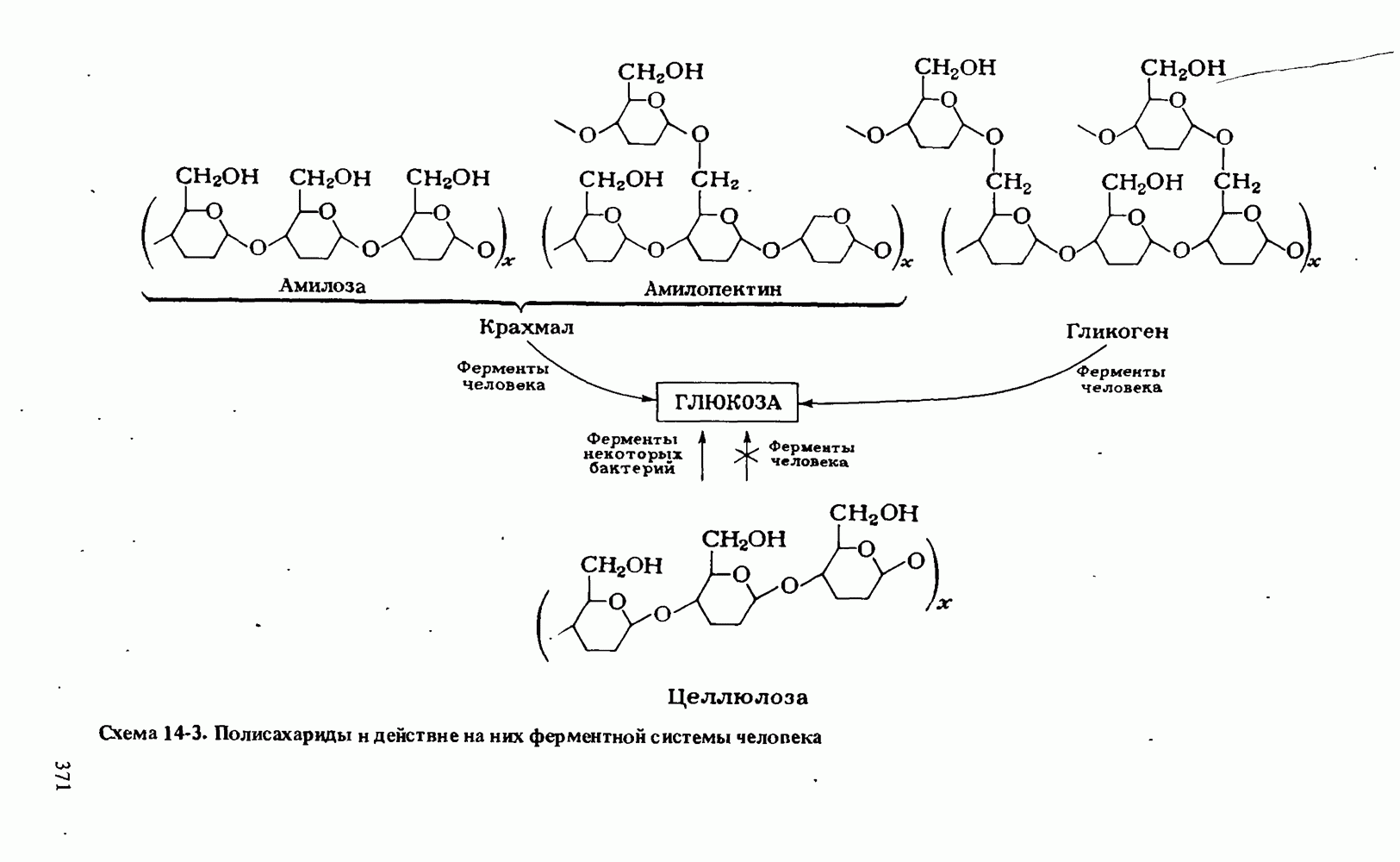
- ПОЛИСАХАРИДЫ
- Прикладная органическая химия: ПИЩЕВЫЕ СВОЙСТВА УГЛЕВОДОВ
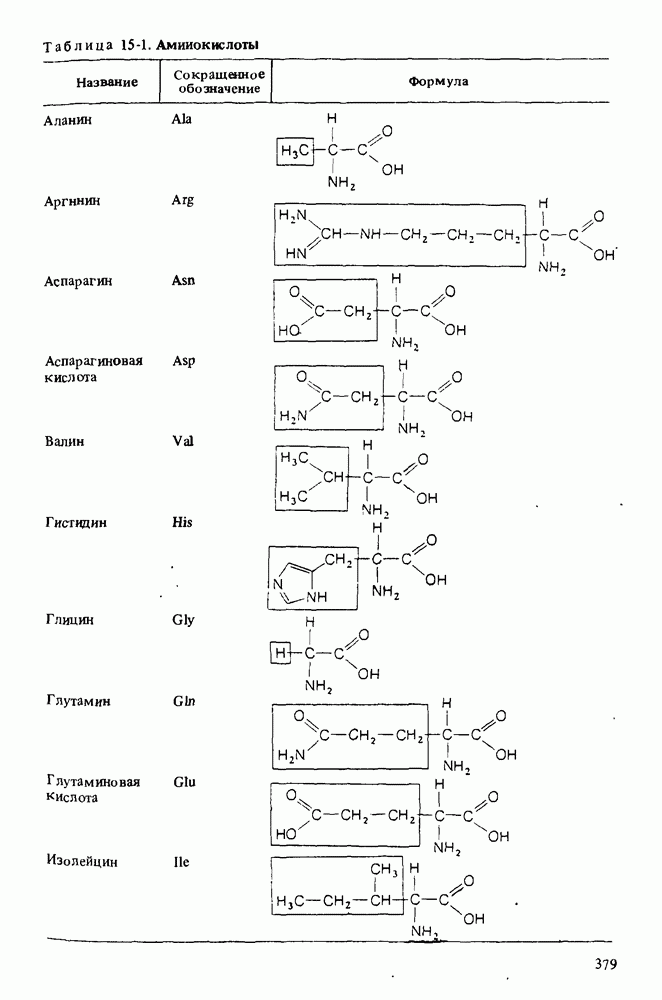
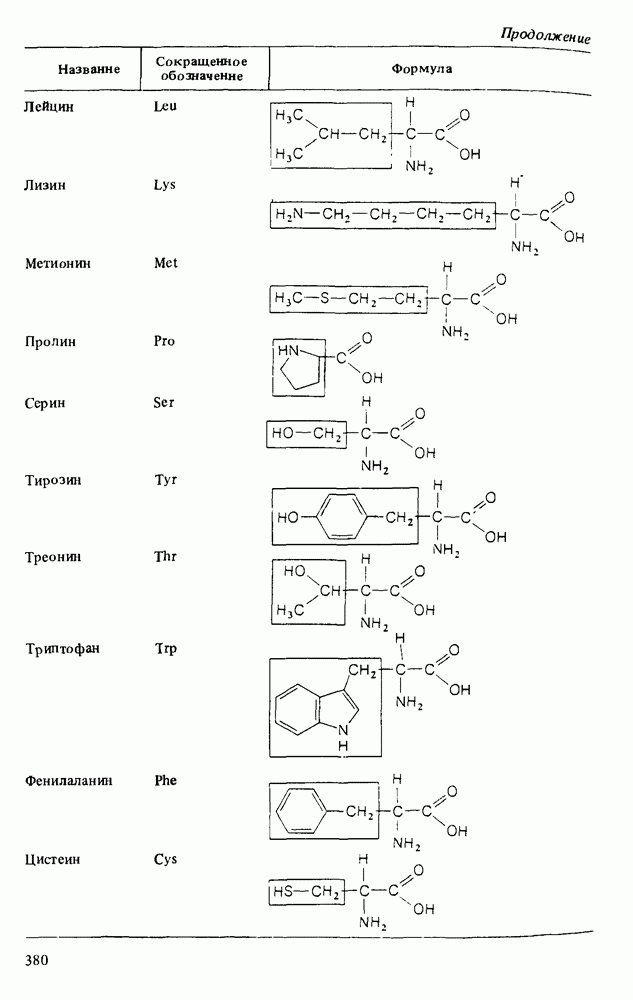
- Глава 15. АМИНОКИСЛОТЫ И БЕЛКИ
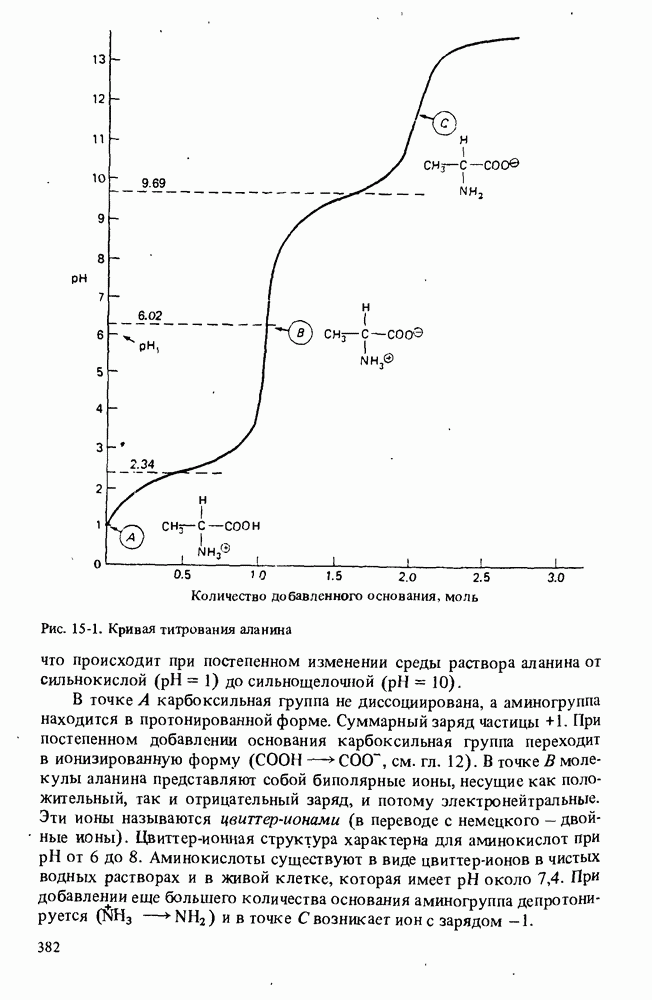
- КИСЛОТНО-ОСНОВНЫЕ СВОЙСТВА АМИНОКИСЛОТ
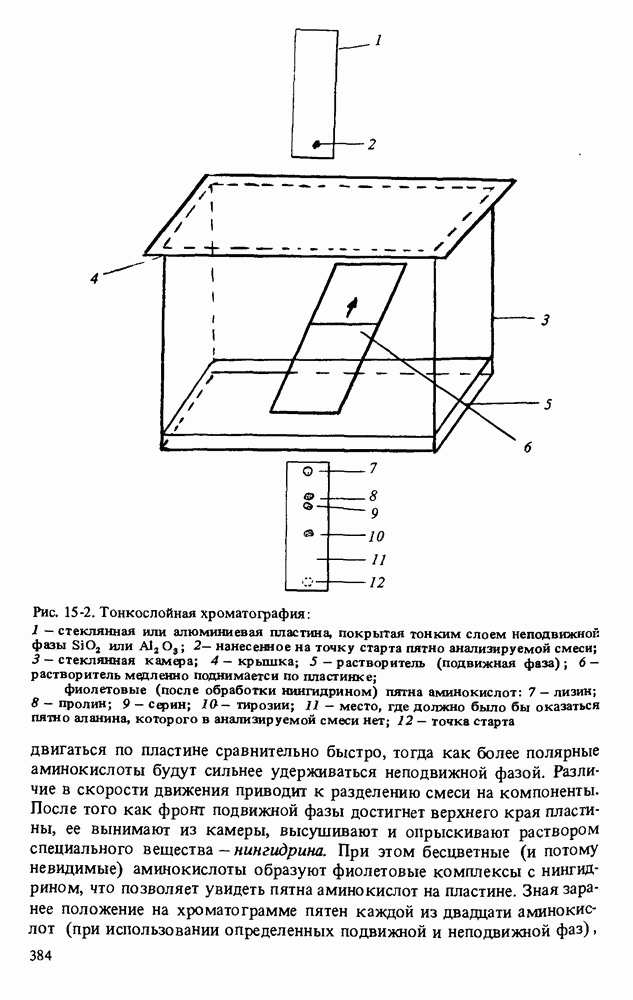
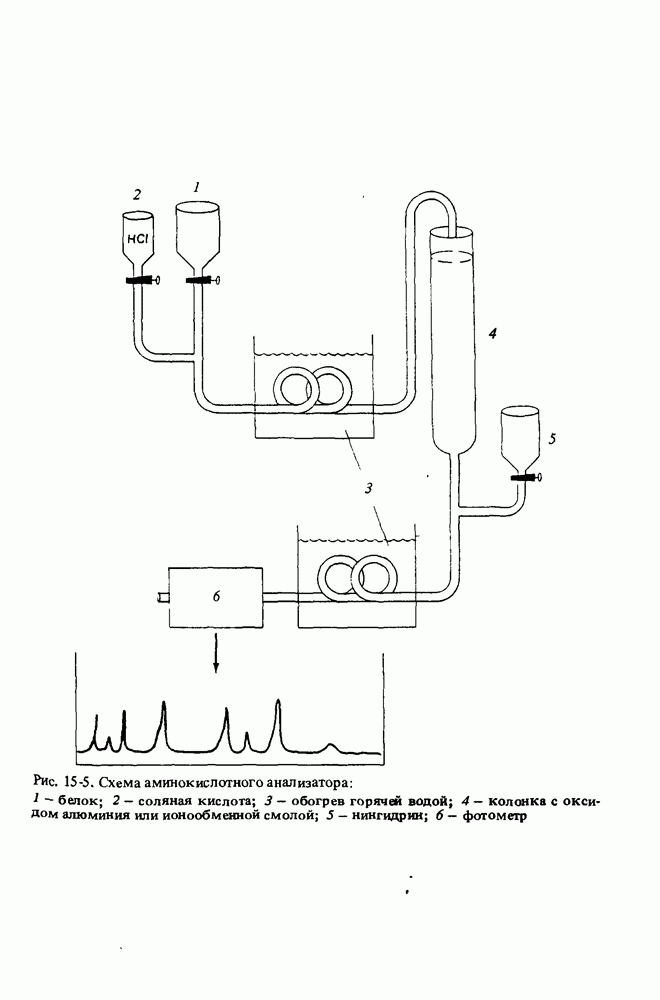
- АНАЛИЗ АМИНОКИСЛОТ
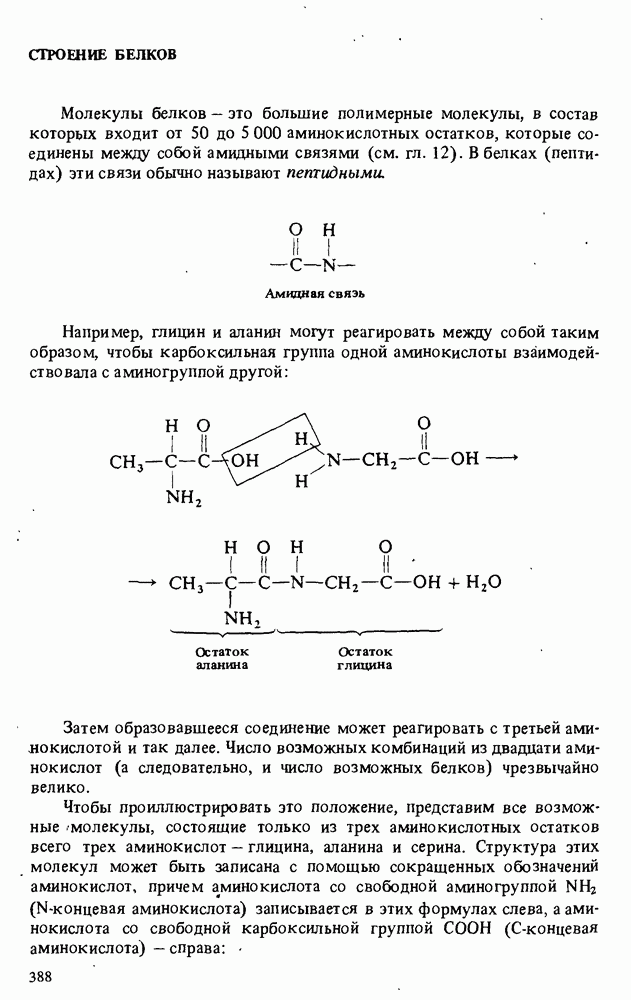
- СТРОЕНИЕ БЕЛКОВ
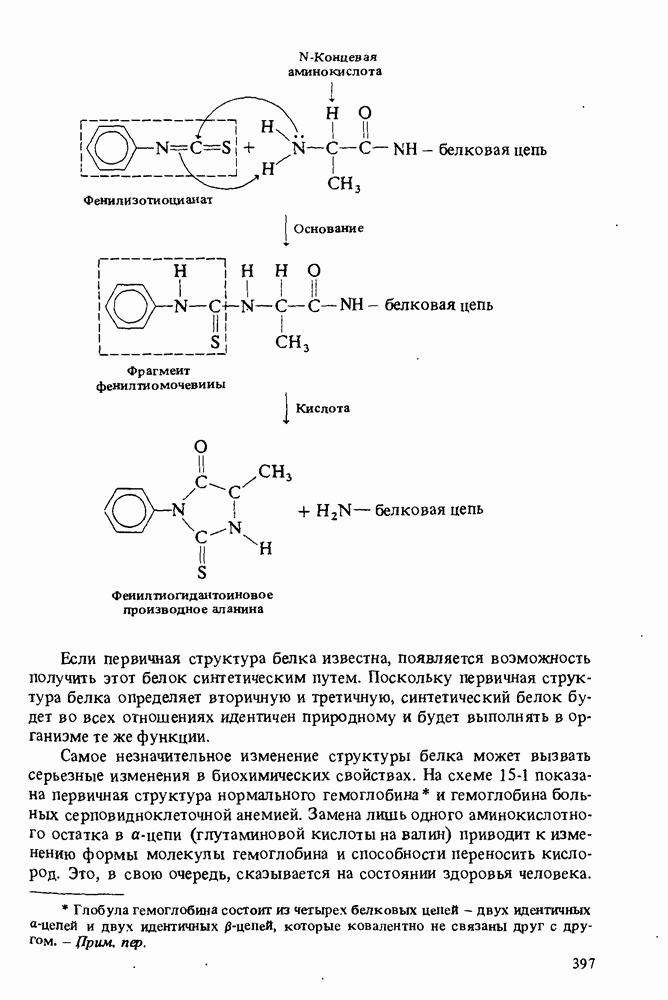
- УСТАНОВЛЕНИЕ ПЕРВИЧНОЙ СТРУКТУРЫ БЕЛКОВ
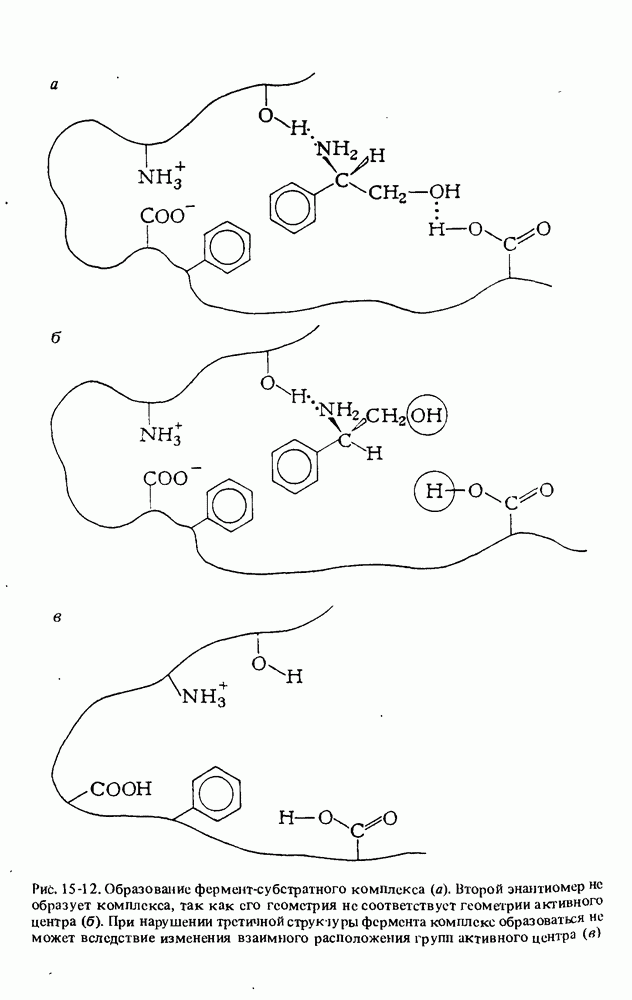
- ФЕРМЕНТЫ
- Глава 16. ЛИПИДЫ
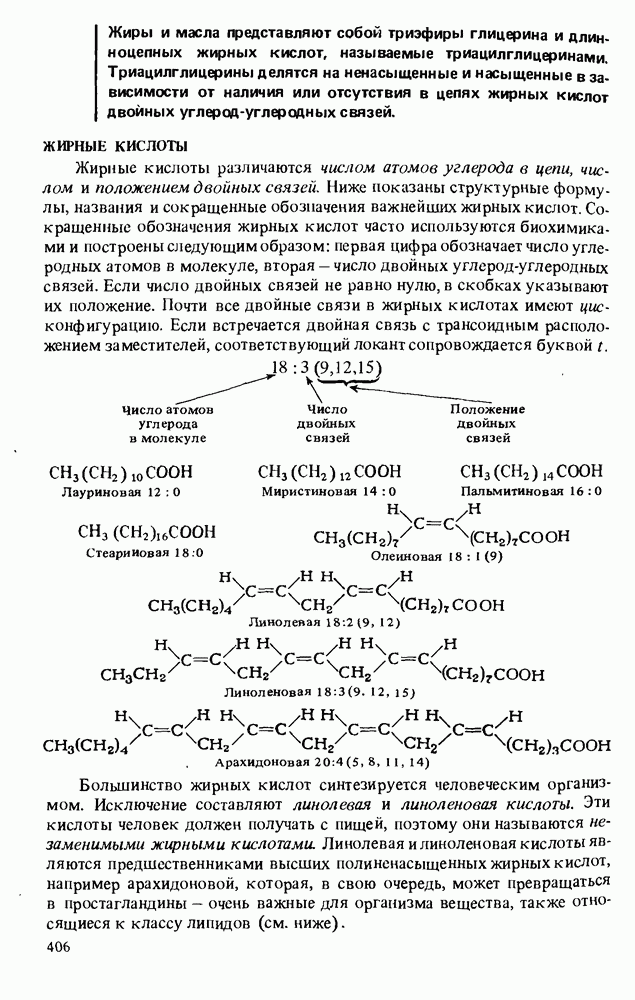
- ЖИРНЫЕ КИСЛОТЫ
- НАЗВАНИЯ ТРИАЦИЛГЛИЦЕРИНОВ
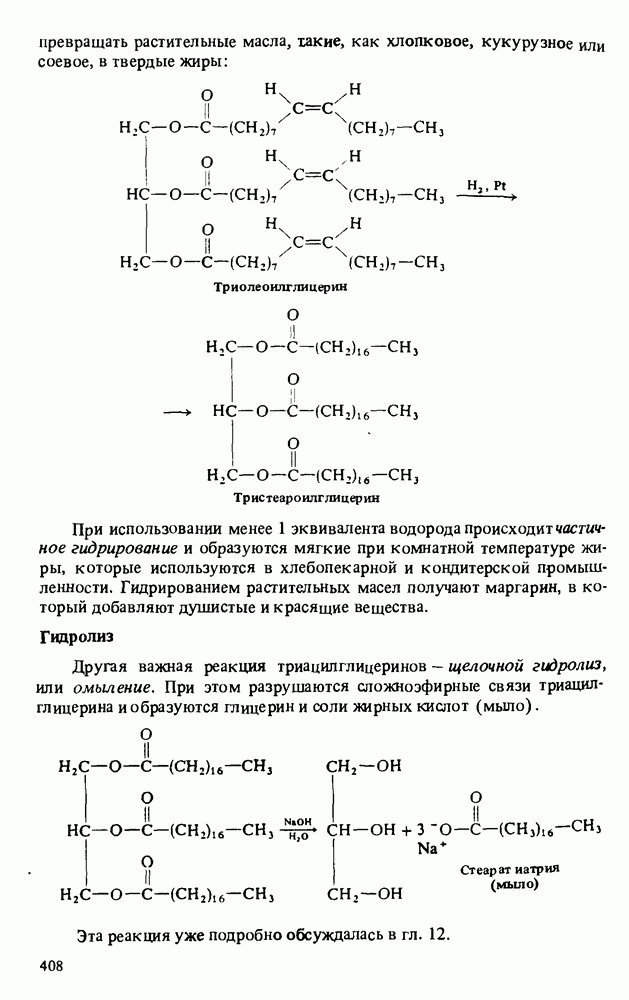
- РЕАКЦИИ ТРИАЦИЛГЛИЦЕРИНОВ
- ЛИПИДЫ, ОТЛИЧНЫЕ ОТ ТРИАЦИЛГЛИЦЕРИНОВ
- Прикладная органическая химия: ПИЩЕВЫЕ СВОЙСТВА ЛИПИДОВ
- Глава 17. НУКЛЕИНОВЫЕ КИСЛОТЫ
- РИБОНУКЛЕИНОВЫЕ КИСЛОТЫ
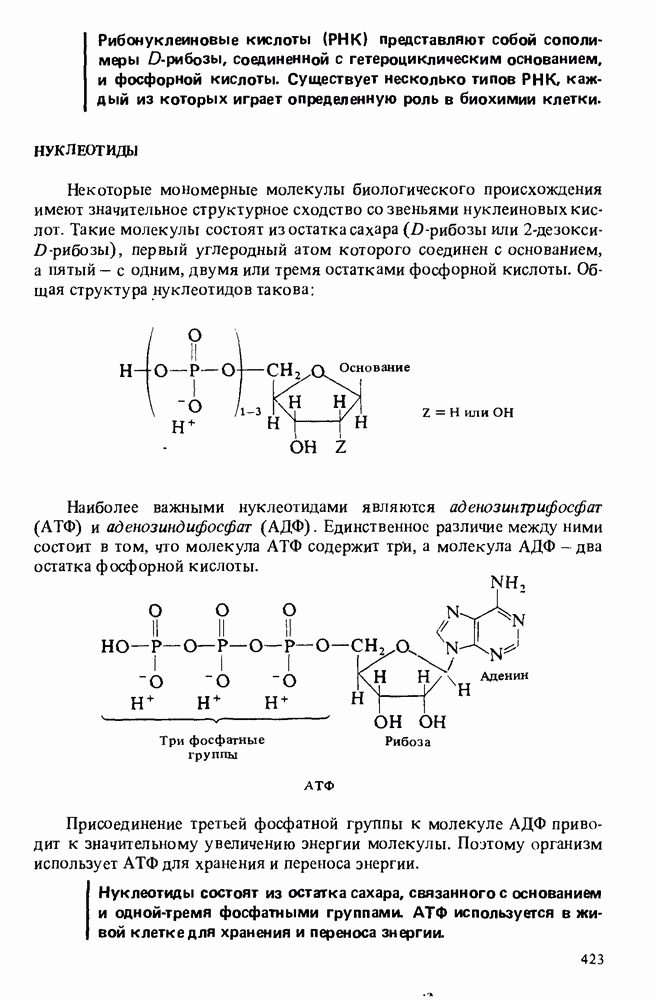
- НУКЛЕОТИДЫ
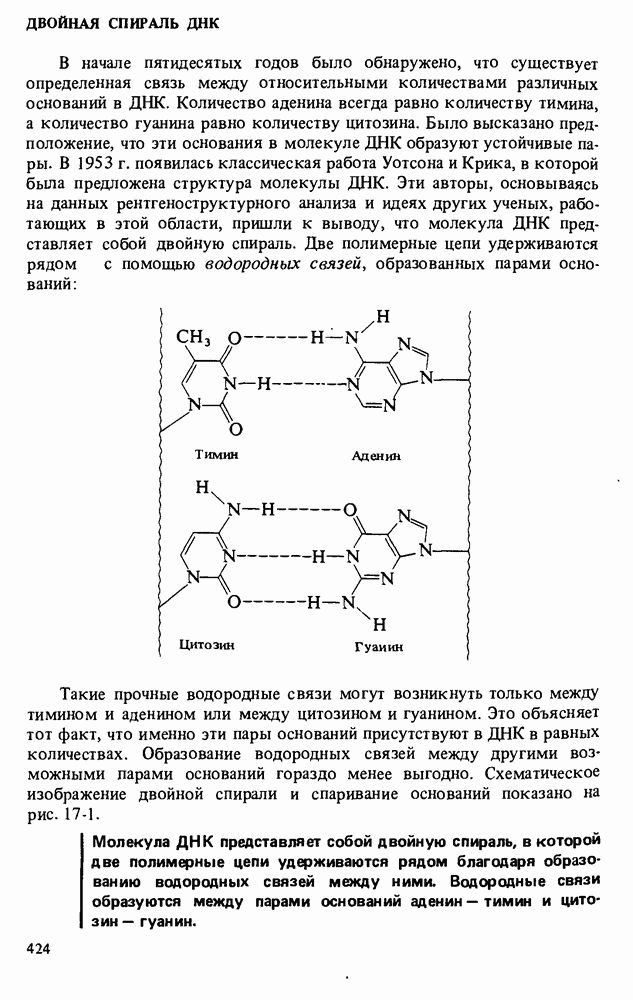
- ДВОЙНАЯ СПИРАЛЬ ДНК
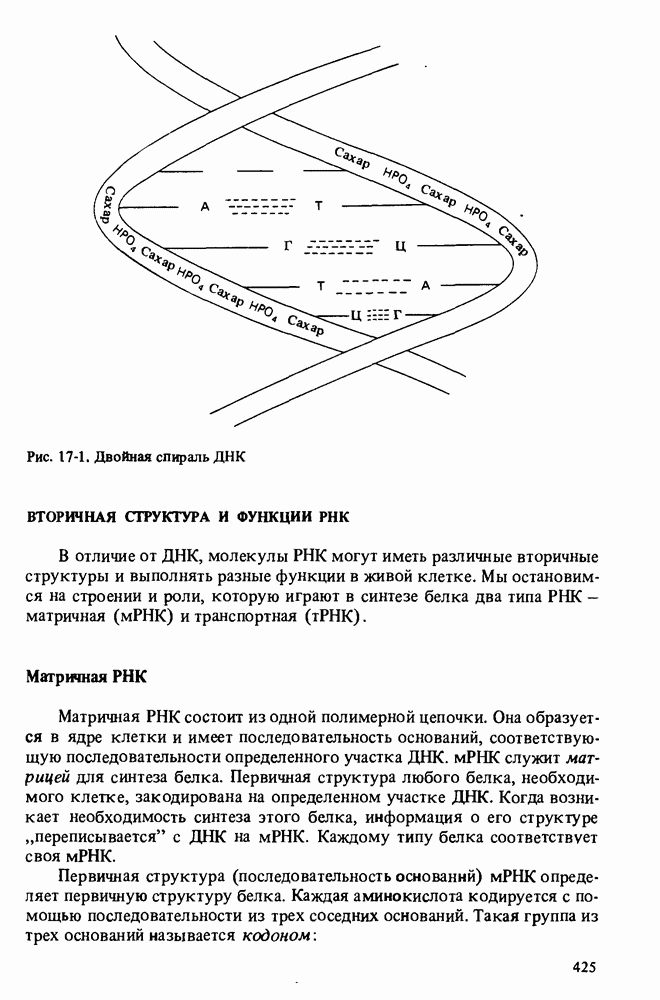
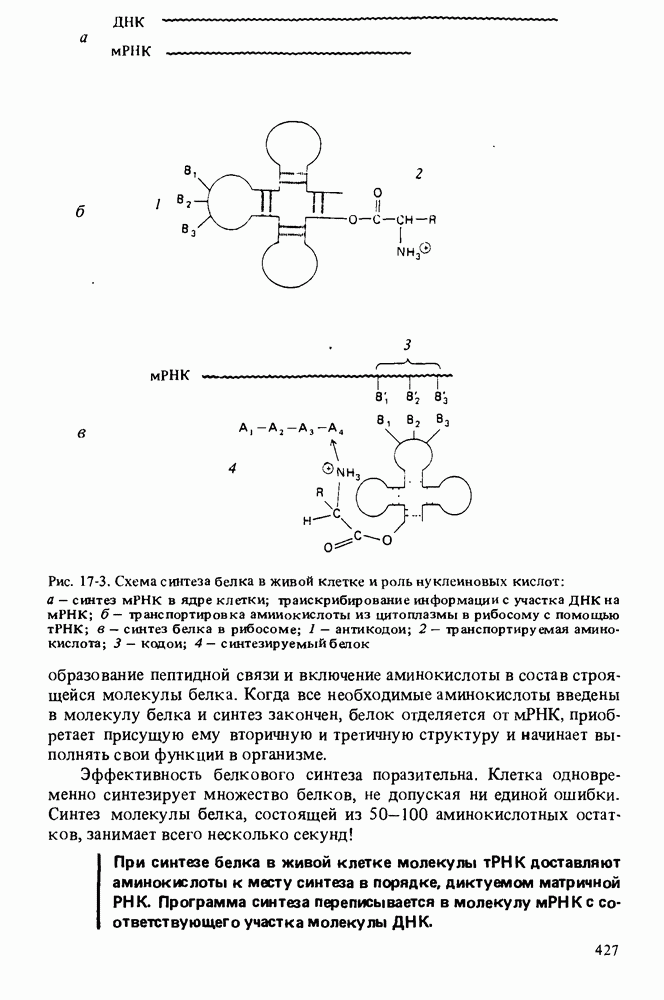
- ВТОРИЧНАЯ СТРУКТУРА И ФУНКЦИИ РНК
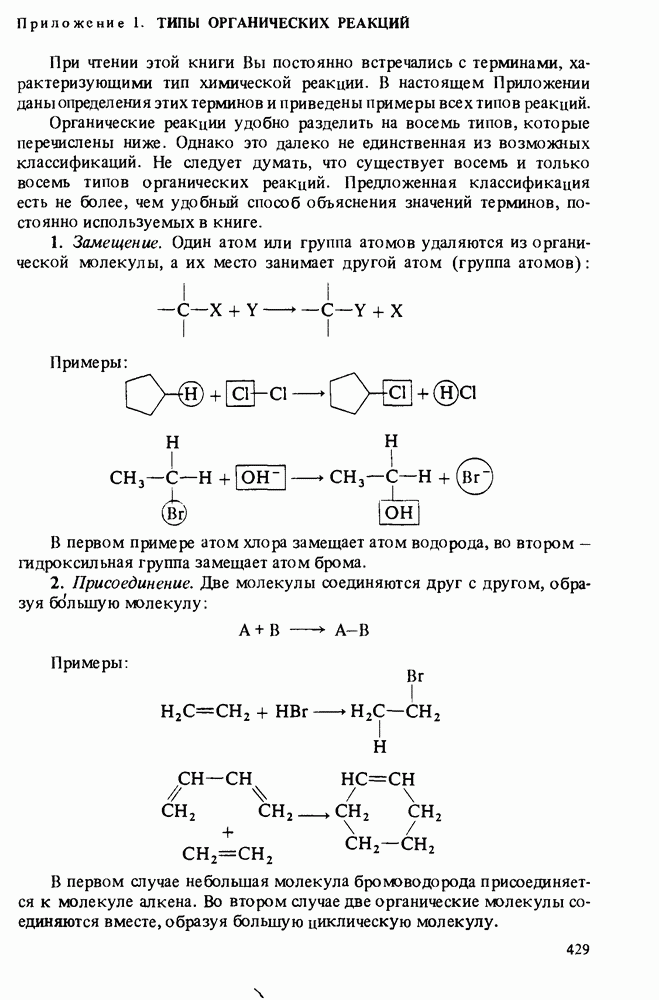
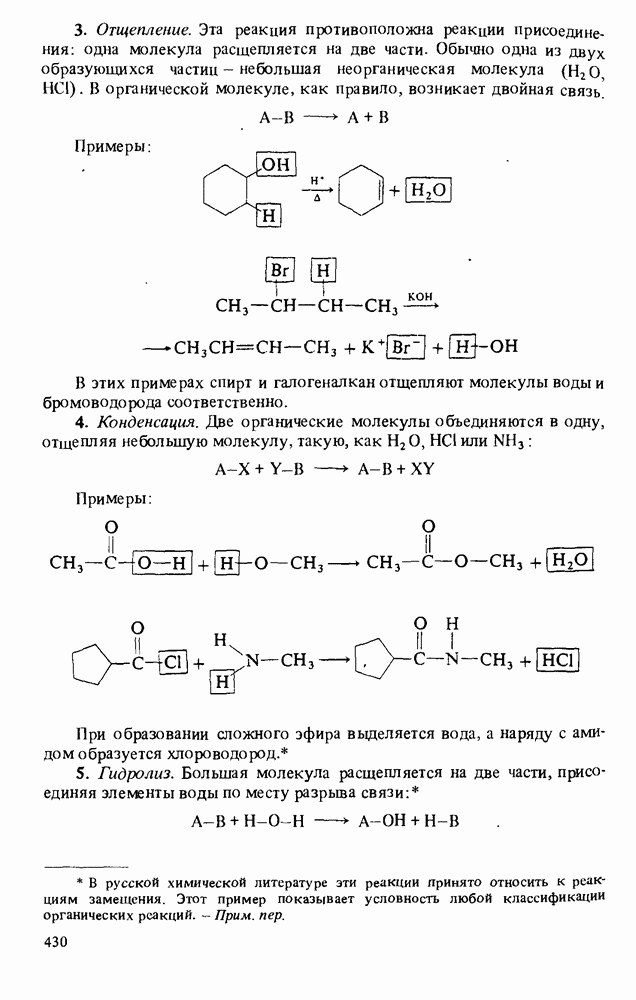
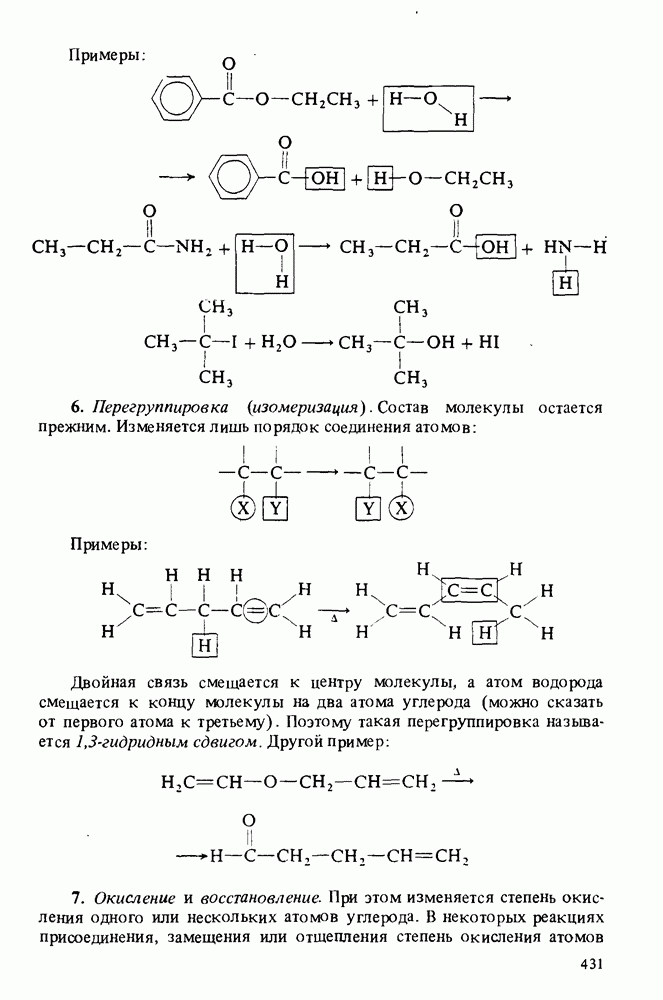
- Приложение 1. ТИПЫ ОРГАНИЧЕСКИХ РЕАКЦИЙ
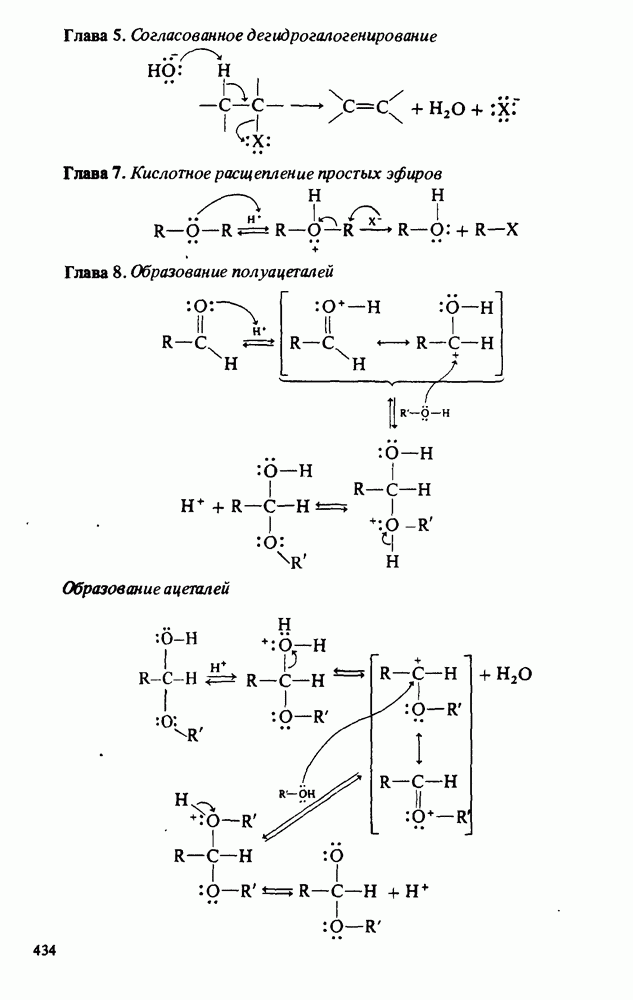
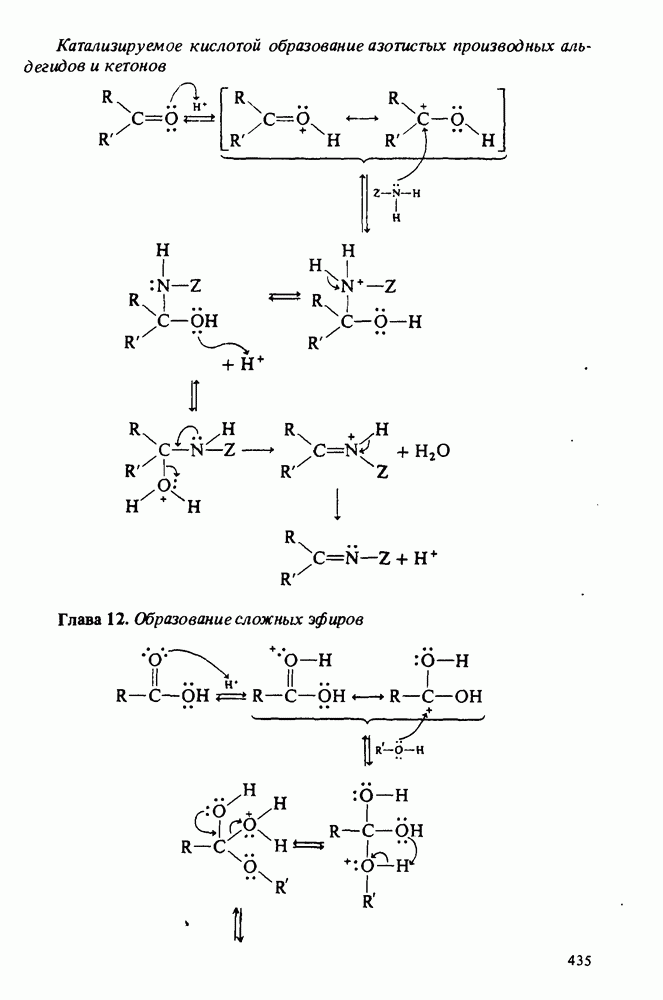
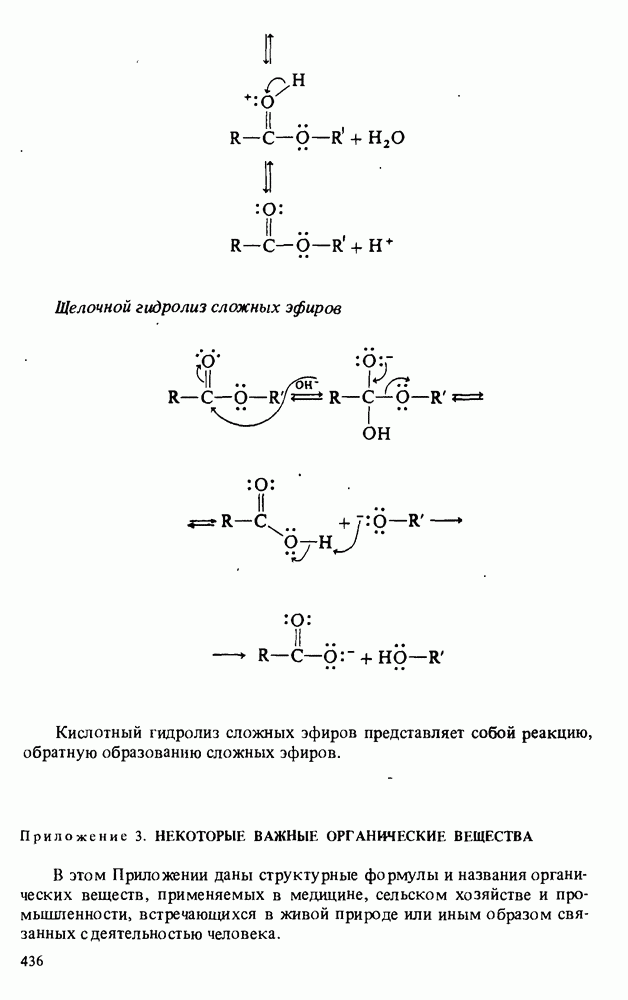
- Приложение 2. МЕХАНИЗМЫ НЕКОТОРЫХ РЕАКЦИЙ
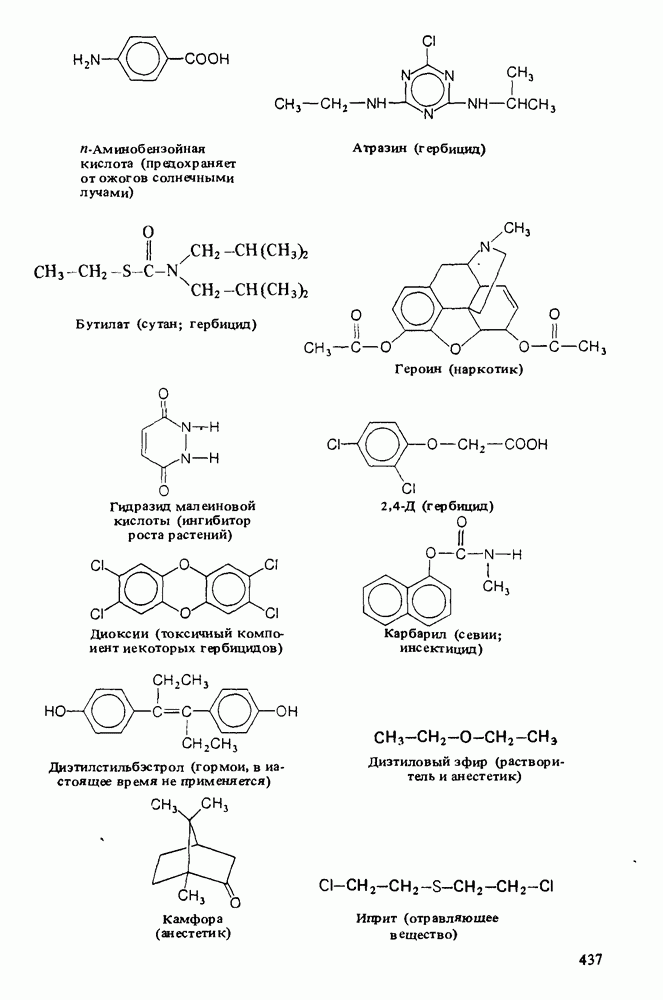
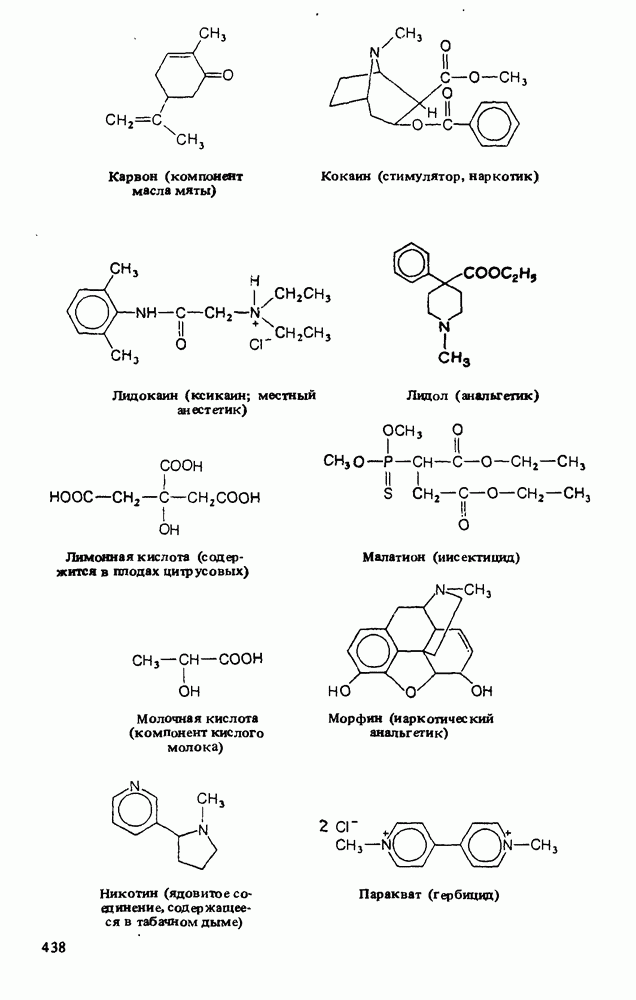
- Приложение 3. НЕКОТОРЫЕ ВАЖНЫЕ ОРГАНИЧЕСКИЕ ВЕЩЕСТВА