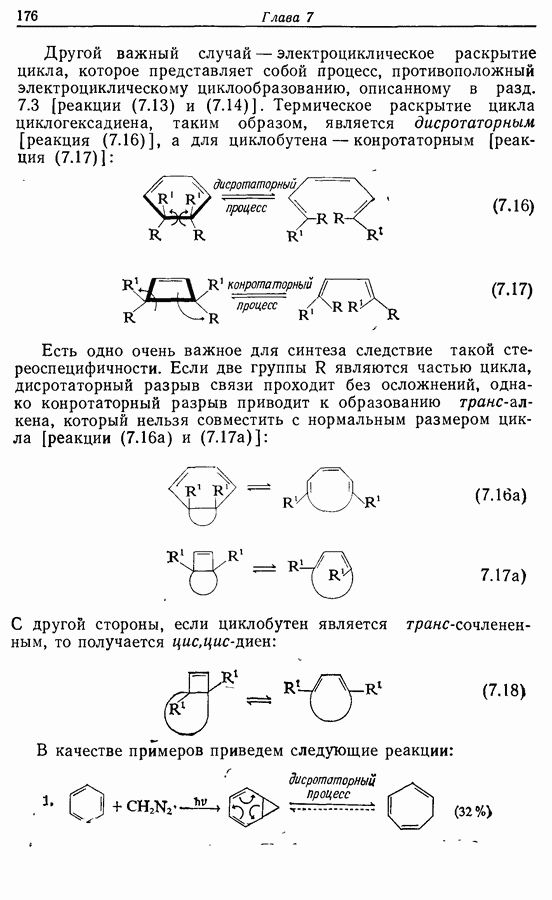
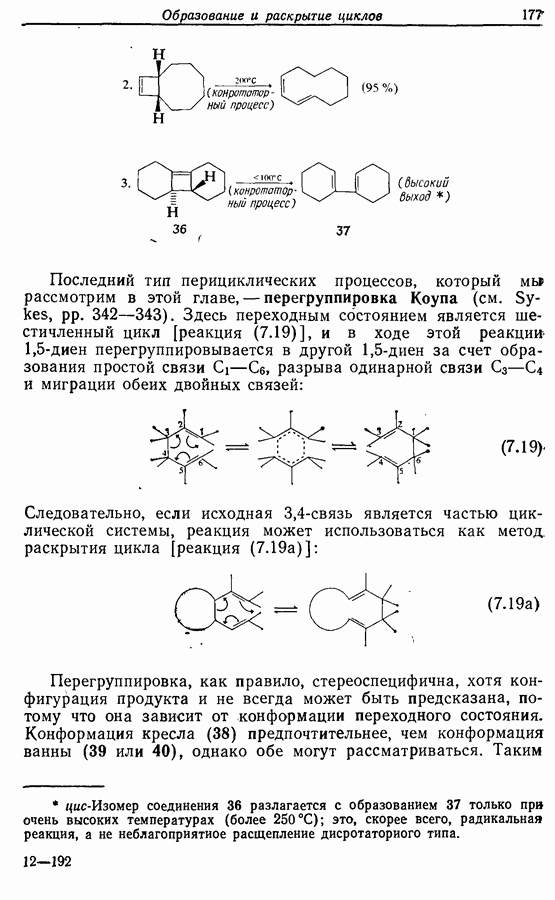
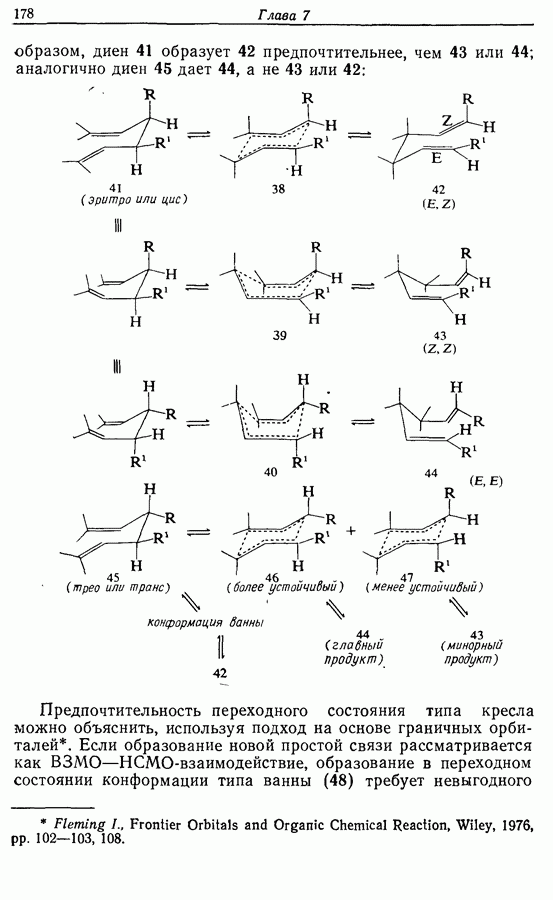
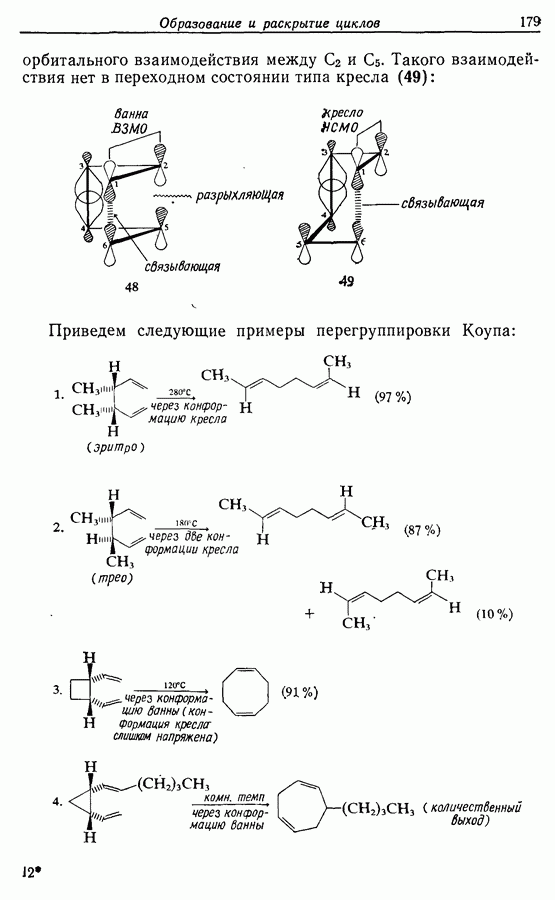
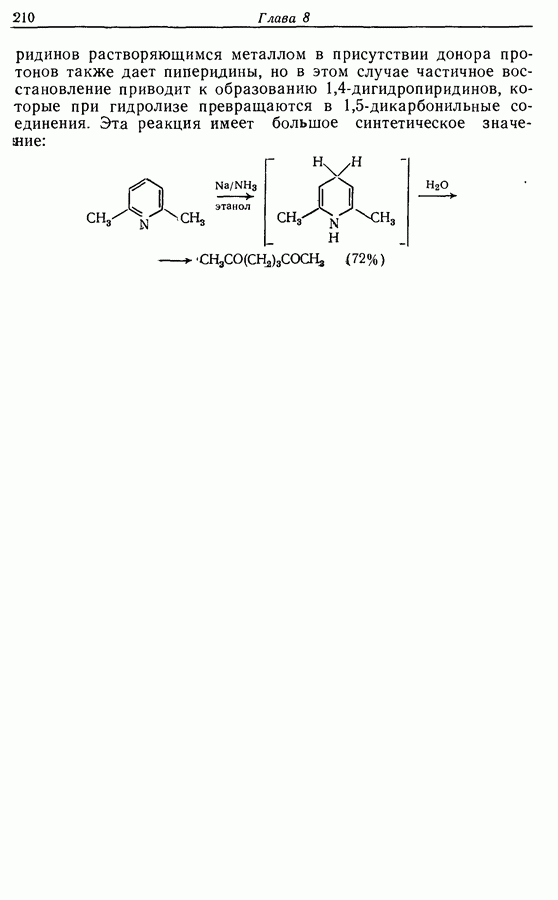
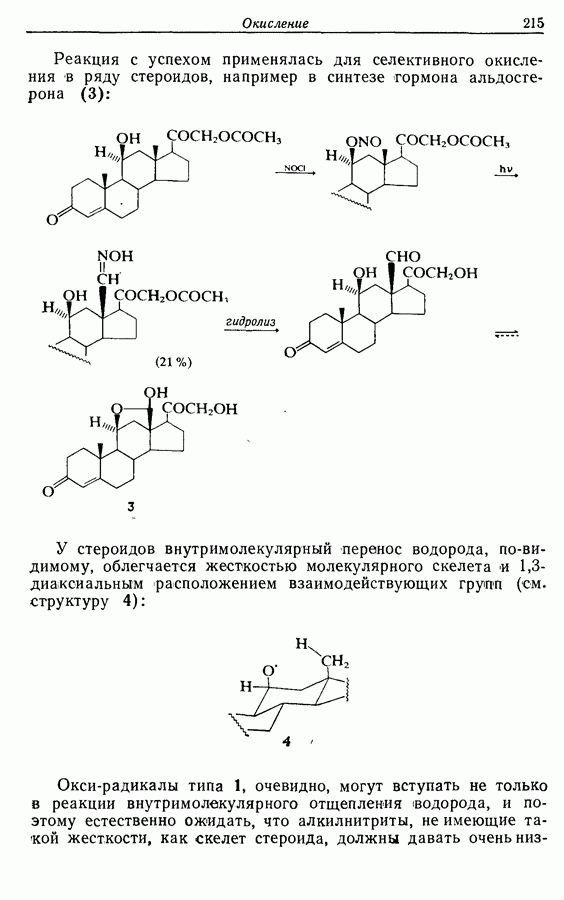
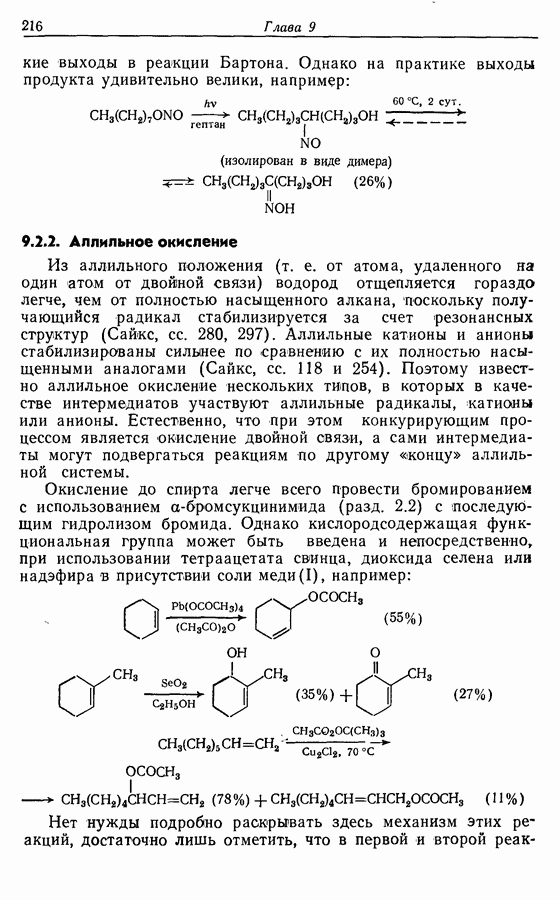
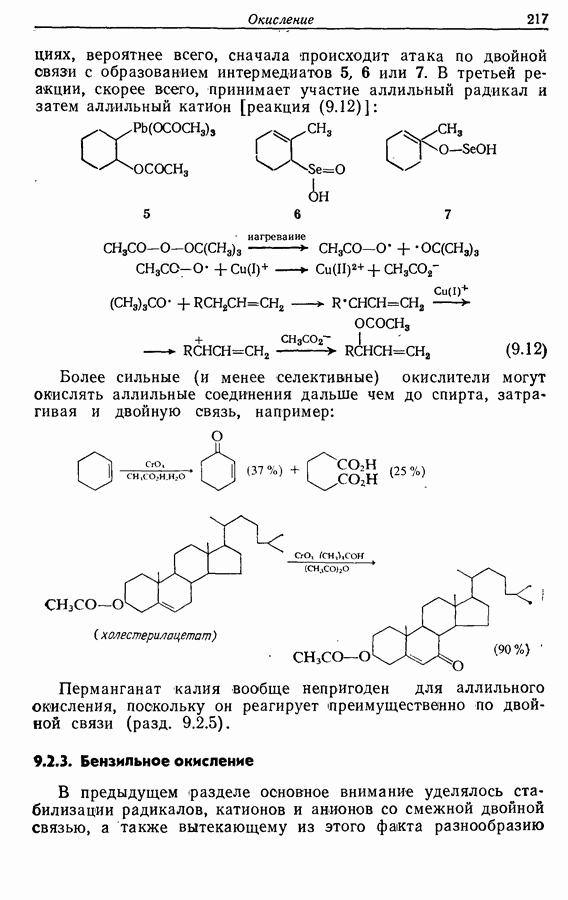
| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
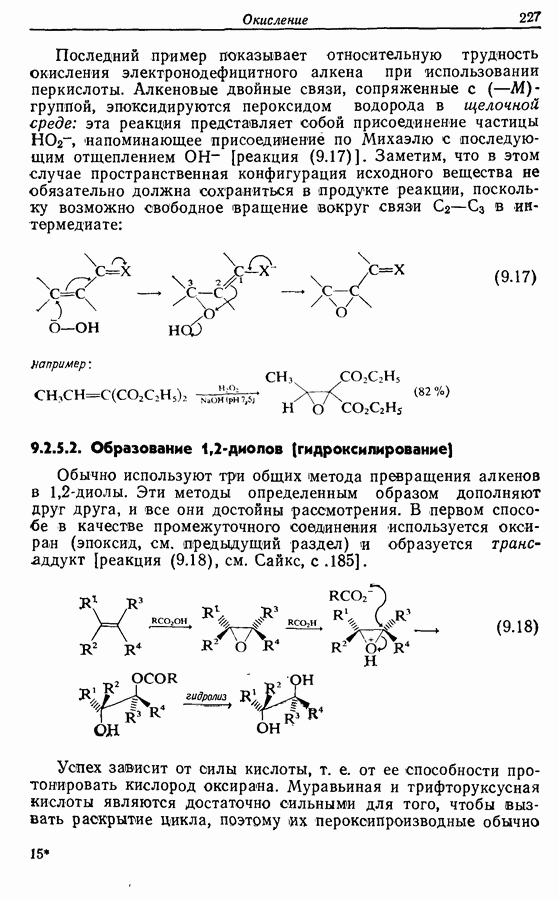
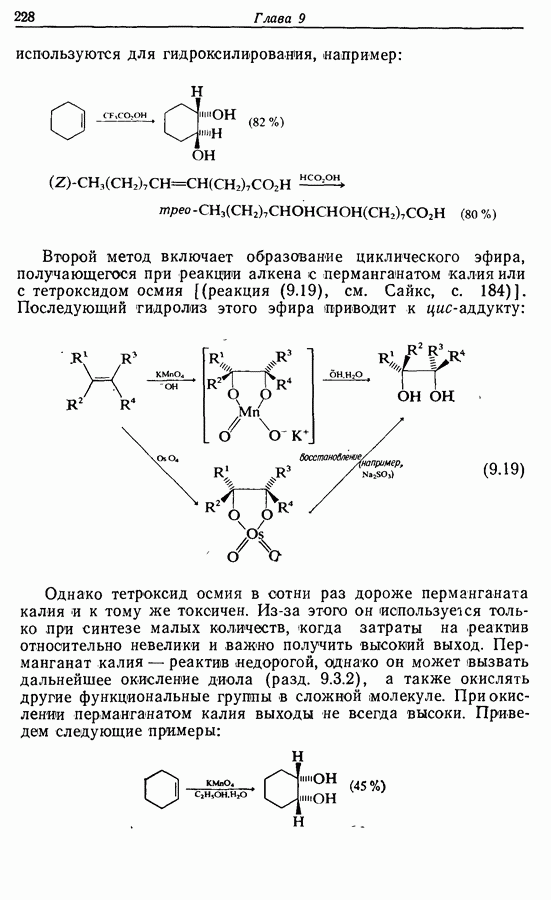
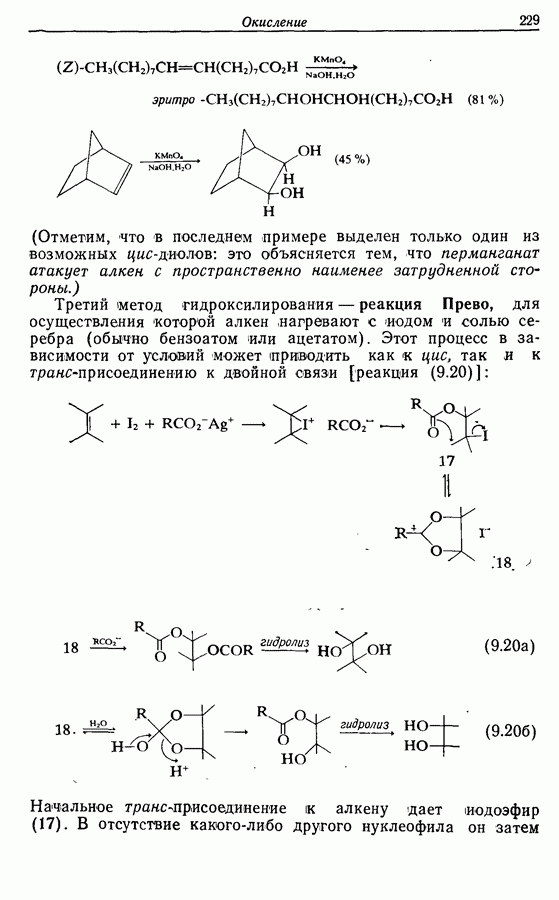
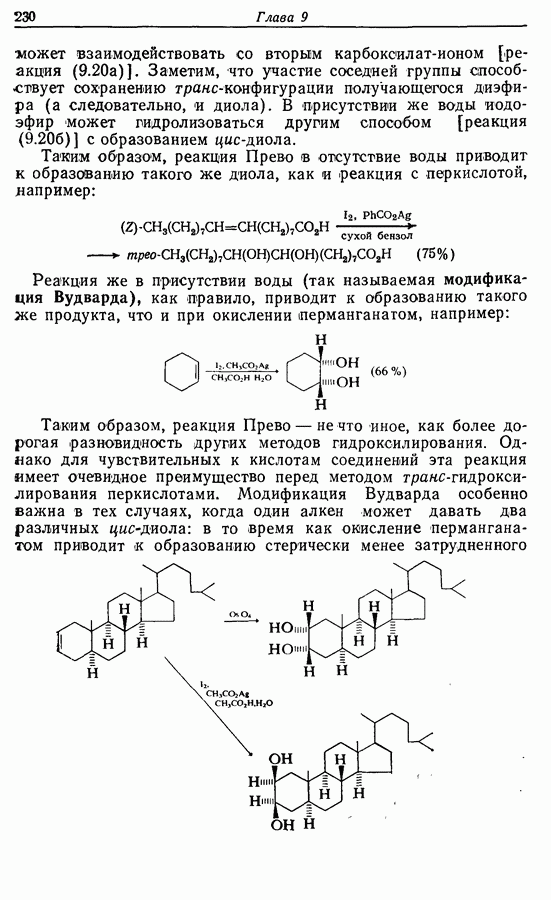
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
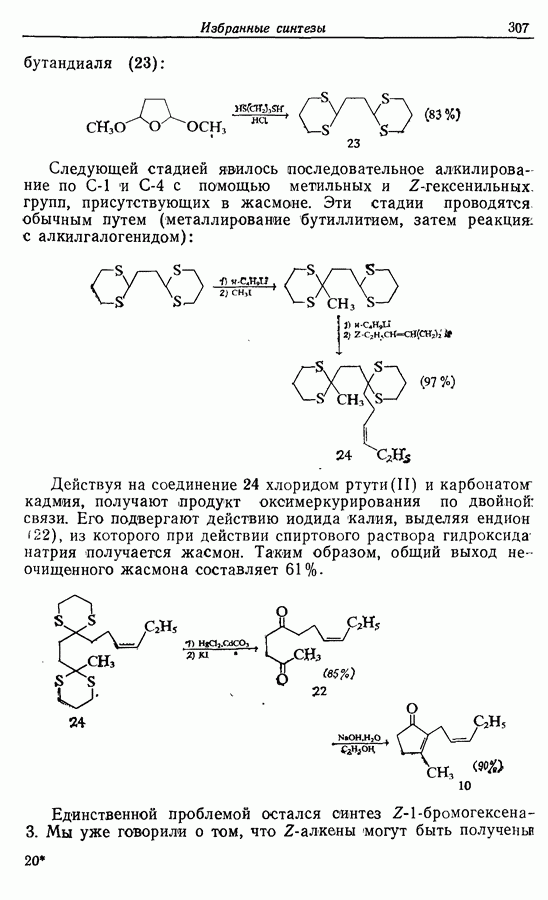
14.2. Z-Геникосен-6-он-11
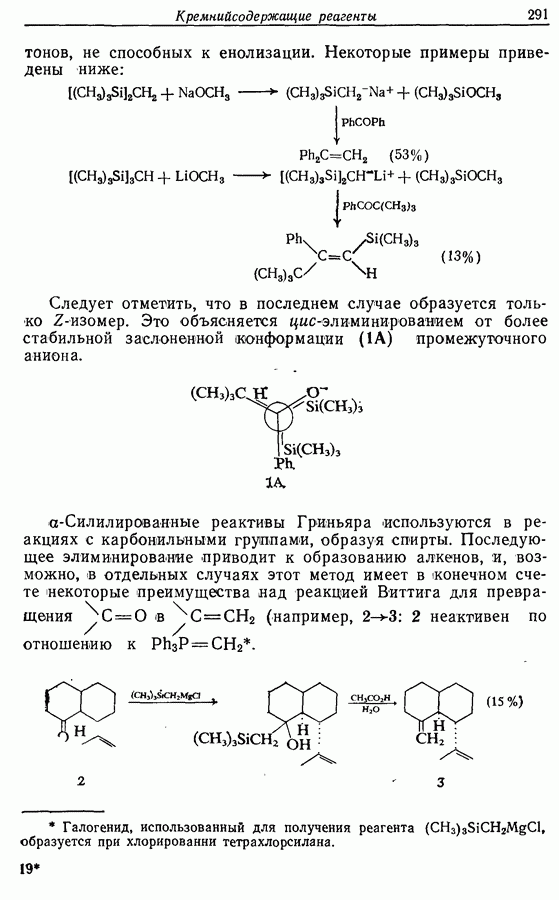
В разд. 3.1 были высказаны предположения о различных способах получения этого соединения из небольших фрагментов. Теперь рассмотрим подробнее, как этот феромон может быть синтезирован, а затем разберем три опубликованных способа синтеза.
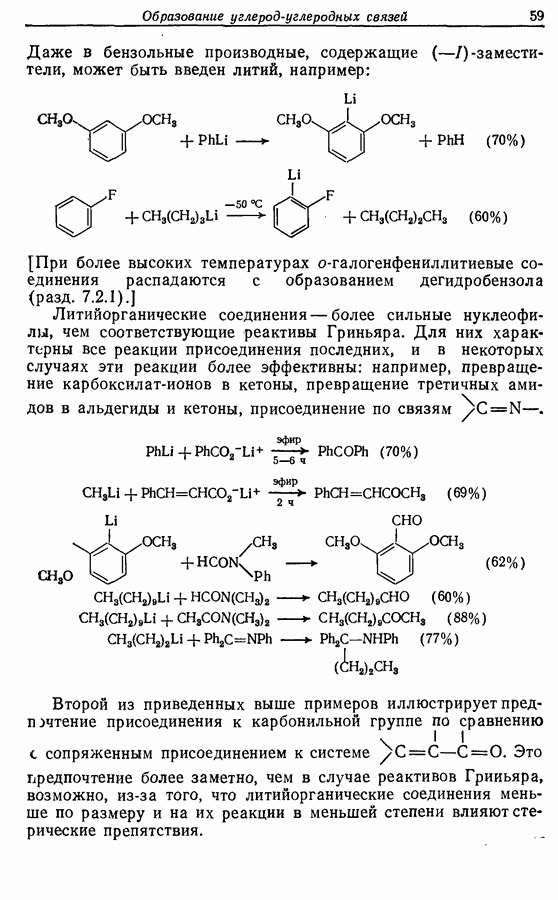
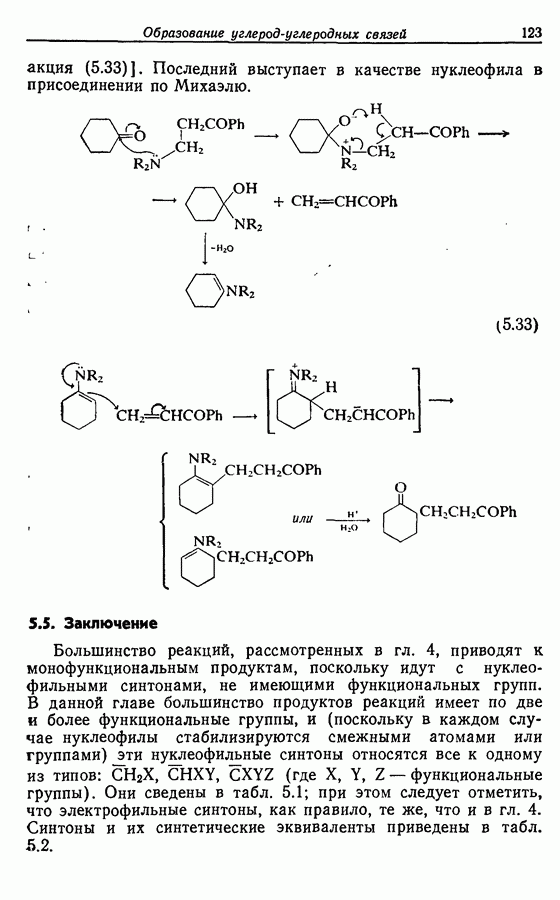
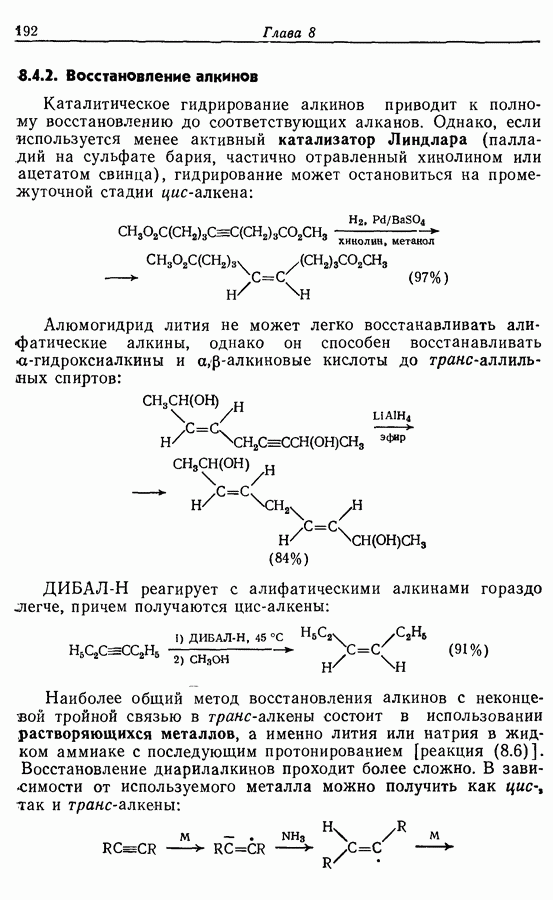
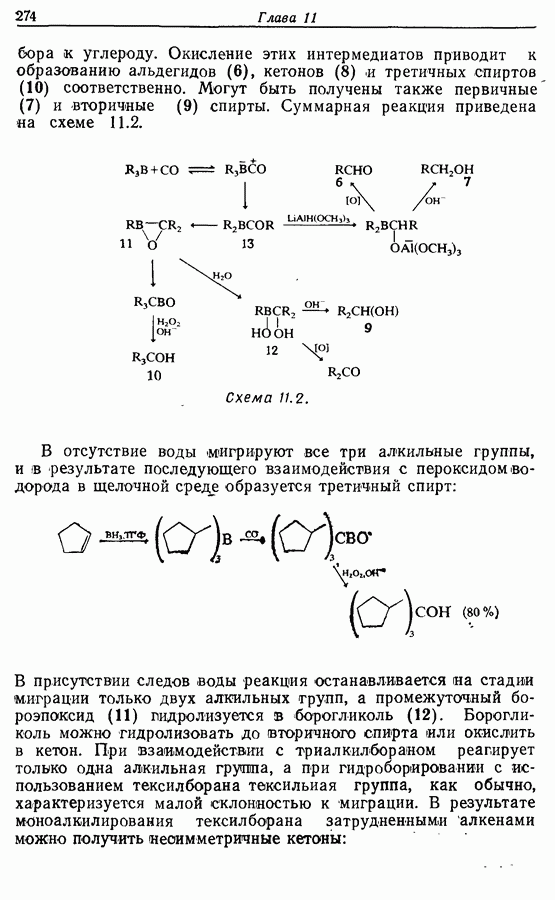
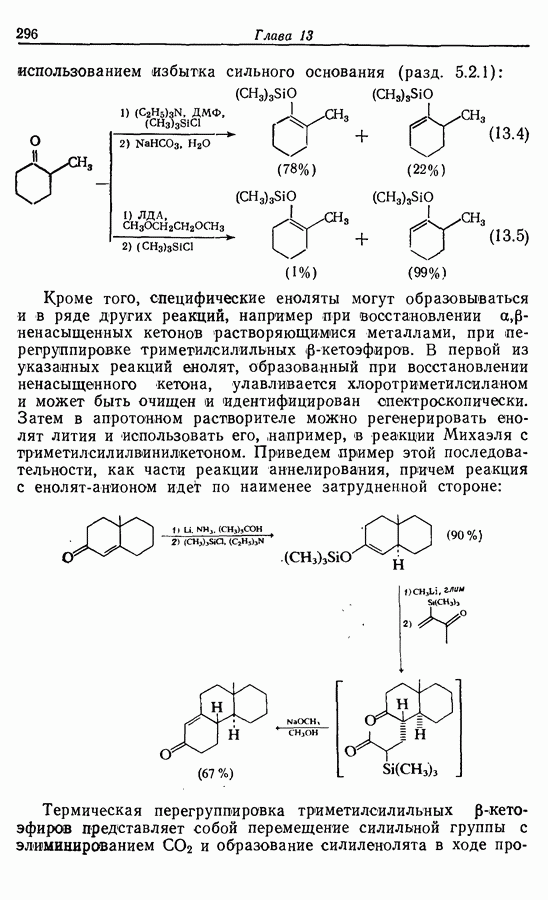
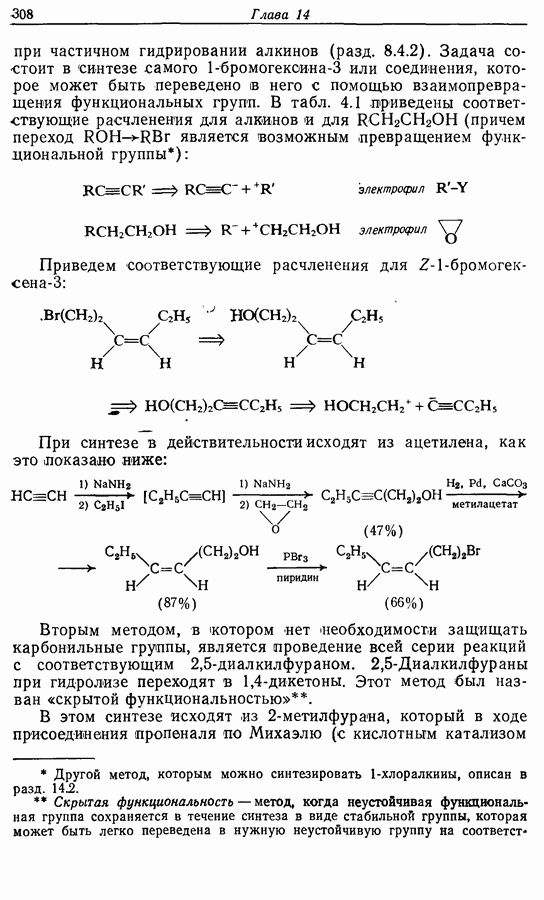
При рассмотрении возможных путей синтеза заданной молекулы следует отметить следующие основные черты. Во-первых,  -алкены чаще всего получают при частичном гидрировании алкинов (разд. 8.4.2) или при «бессолевой» реакции Виттига (разд. 5.3.1.3). Во-вторых, функциональные группы достаточно удалены друг от друга для того, чтобы предположить, что их можно рассматривать независимо друг от друга. В-третьих, в случае синтеза с участием алкинов тройная связь более устойчива, чем карбонильная группа, особенно к действию нуклеофильных реагентов, и поэтому тройную связь удобнее вводить первой.
-алкены чаще всего получают при частичном гидрировании алкинов (разд. 8.4.2) или при «бессолевой» реакции Виттига (разд. 5.3.1.3). Во-вторых, функциональные группы достаточно удалены друг от друга для того, чтобы предположить, что их можно рассматривать независимо друг от друга. В-третьих, в случае синтеза с участием алкинов тройная связь более устойчива, чем карбонильная группа, особенно к действию нуклеофильных реагентов, и поэтому тройную связь удобнее вводить первой.
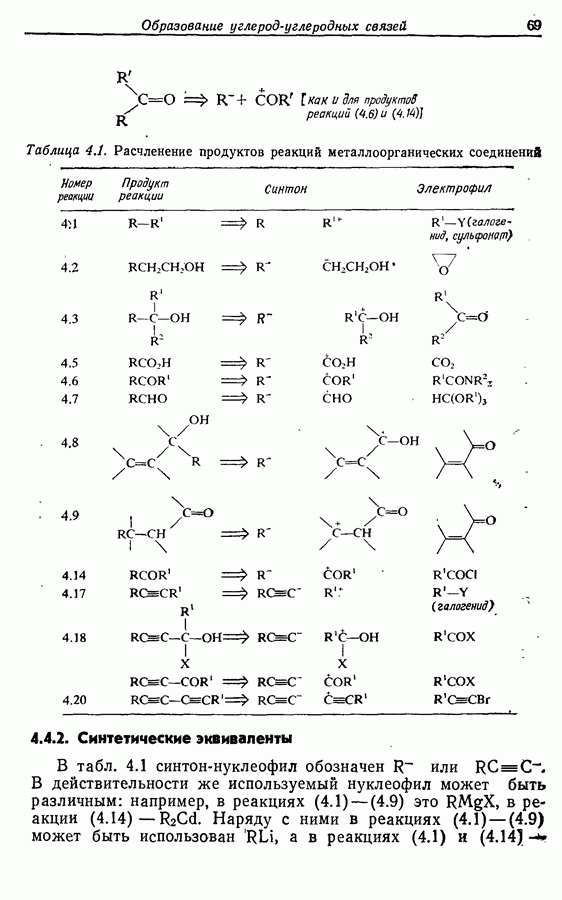
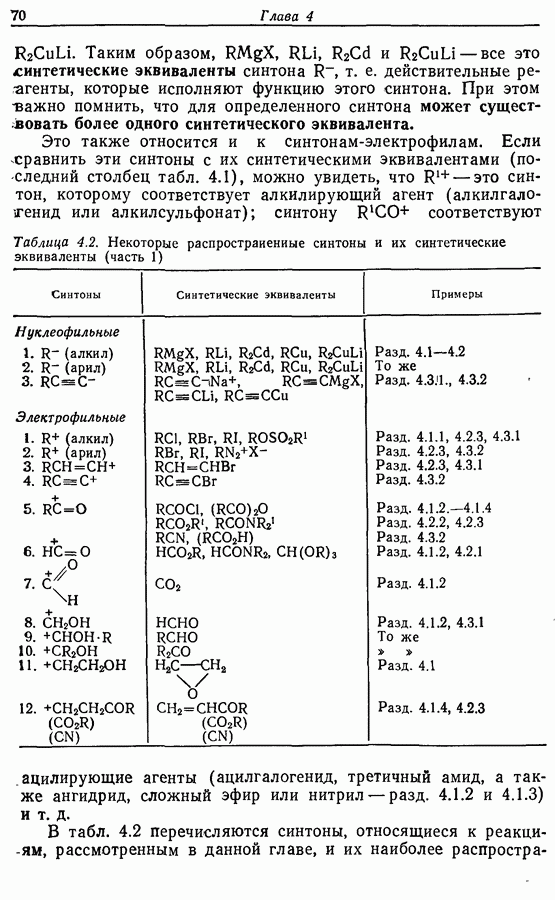
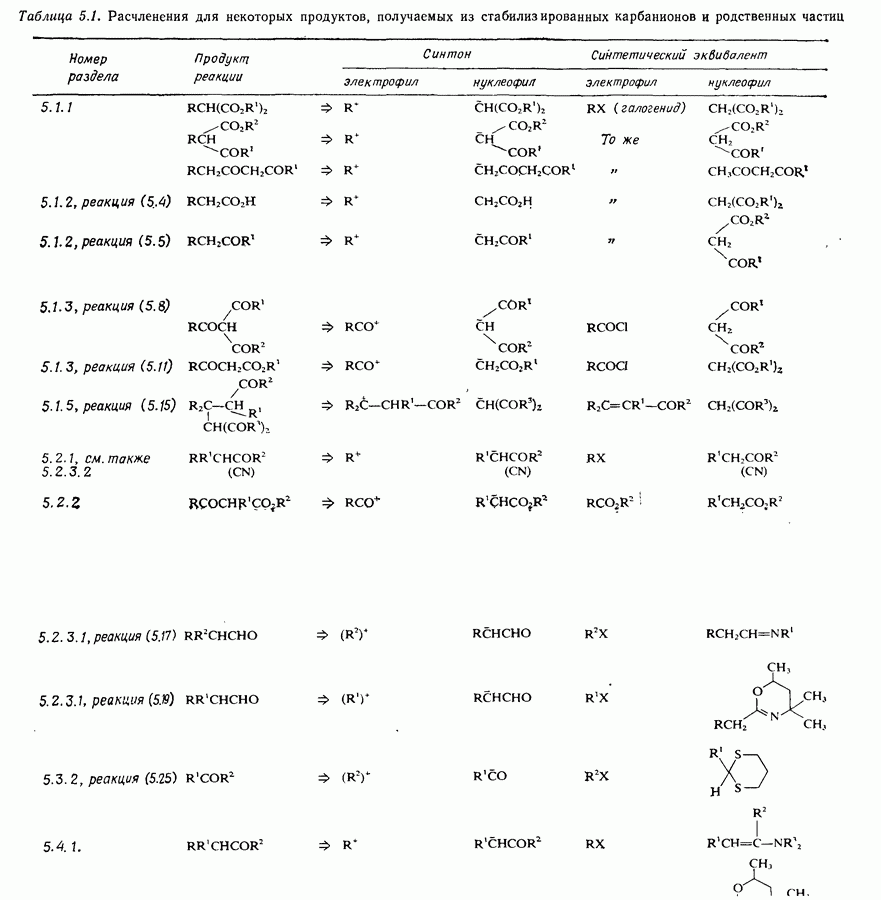
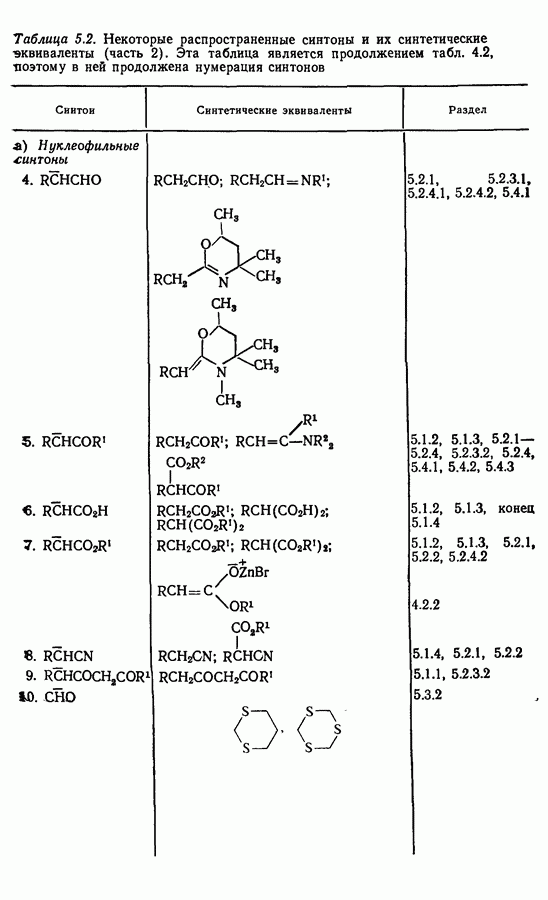
При рассмотрении возможных путей синтеза с участием алкинов следует упомянуть расчленения для алкинов, приведенные в табл. 4.1, и расчленения для кетонов, приведенные в табл. 4.1 и 5.1. Синтетические эквиваленты можно найти в табл. 4.2 и 5.2.

Посмотрим теперь на заданную молекулу и обсудим возможные пути ее синтеза (см. схему на стр. 301).
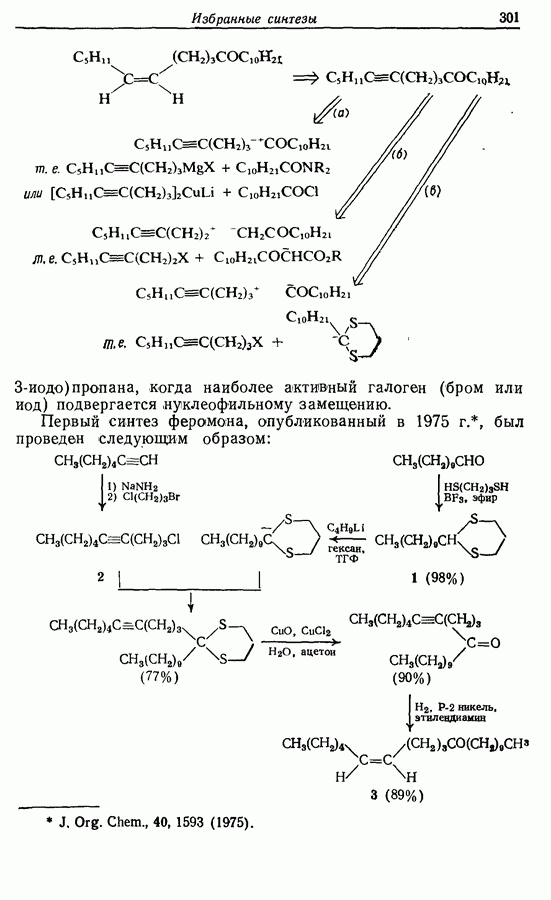
Синтетические эквиваленты децилсодержащих синтонов, получающихся при расчленении связи  легко образуются из доступного уидеканаля (синтез этого соединения приведен в <разд. 4.2.1 и 5.3.2), поэтому данный вариант расчленения, возможно, будет наиболее выгодным. Электрофильным синтетическим эквивалентом в случае (в) является 1-галогеноде-цин-4. Им может служить, например, 1-хлородецин-4, который может быть получен из аниона гептана-1 и 1-хлоро-3-бромо(или
легко образуются из доступного уидеканаля (синтез этого соединения приведен в <разд. 4.2.1 и 5.3.2), поэтому данный вариант расчленения, возможно, будет наиболее выгодным. Электрофильным синтетическим эквивалентом в случае (в) является 1-галогеноде-цин-4. Им может служить, например, 1-хлородецин-4, который может быть получен из аниона гептана-1 и 1-хлоро-3-бромо(или

3-иодо) пропана, когда наиболее активный галоген (бром или иод) подвергается нуклеофильному замещению.
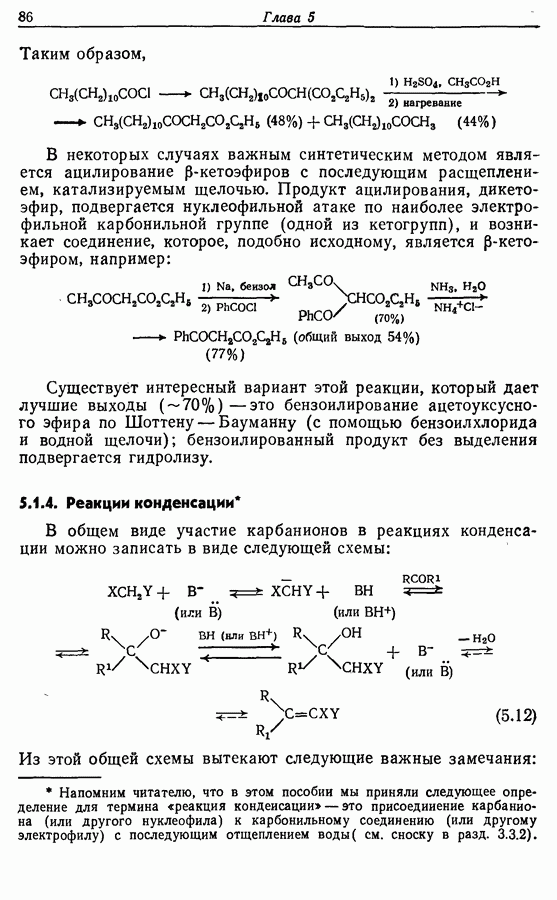
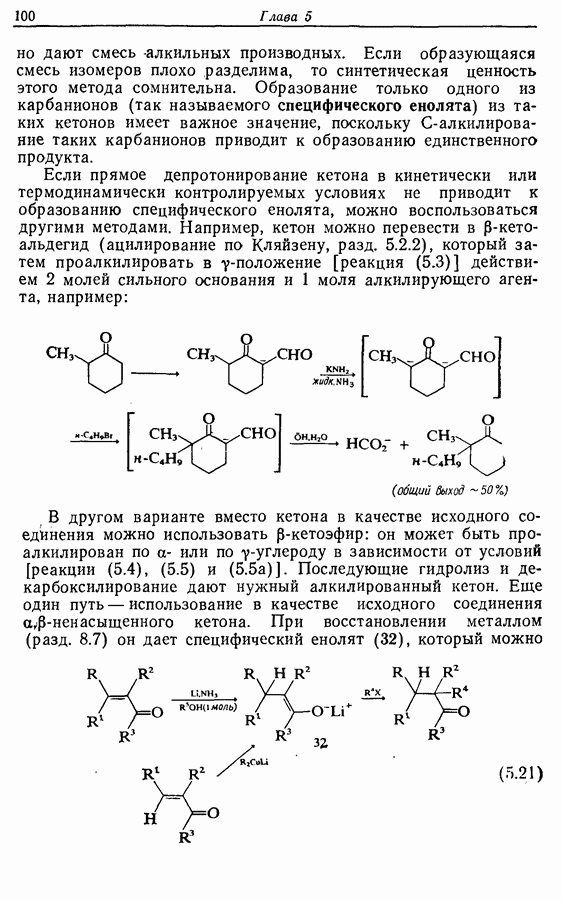
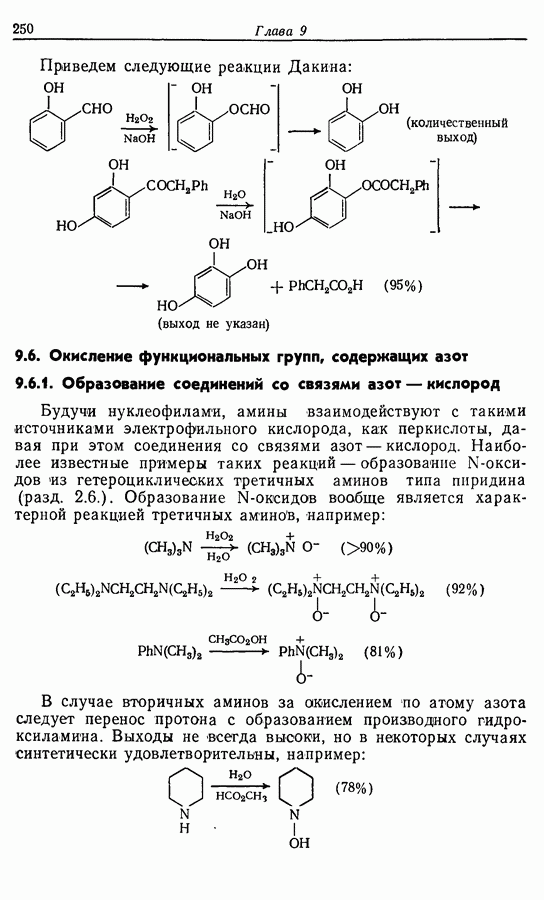
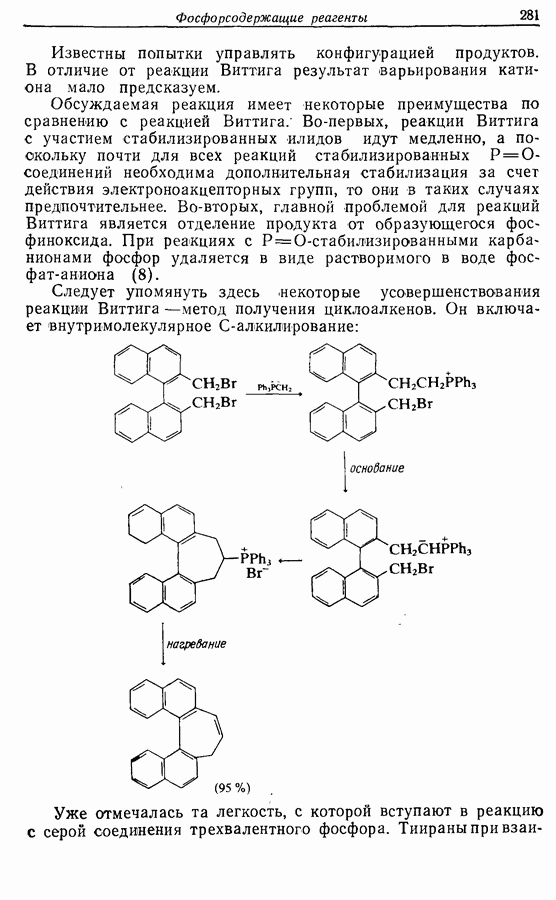
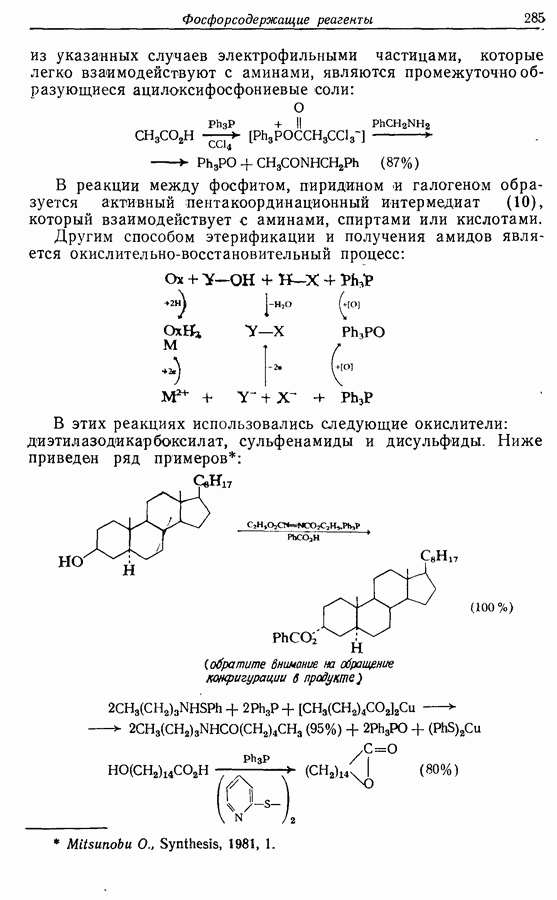
Первый синтез феромона, опубликованный в 1975 г., был проведен следующим образом:
(см. скан)
Алкильная цепь образуется при нуклеофильном замещении анионом дитиана (1), полученного из ундеканаля, хлоралкина (2), синтезированного реакцией аниона гептина-1 с 1-бромо-З-хлоропропаном. Дитиан расщепляется при действии окоида и хлорида меди (II) в водно-ацетоновом растворе, а феромон, 2-геникосен-6-он-11 (3), образуется при частичном гидрировании с никелевым катализатором в присутствии этилендиамина.
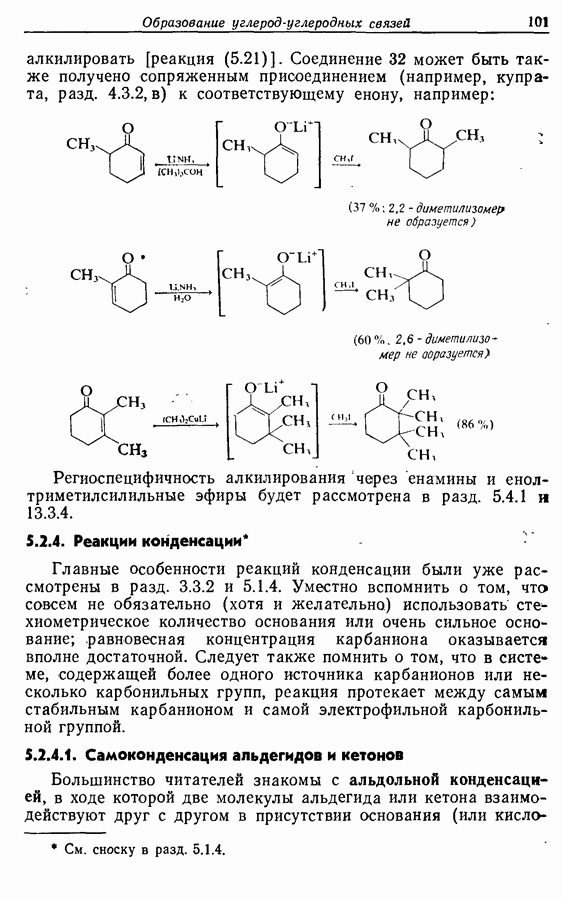
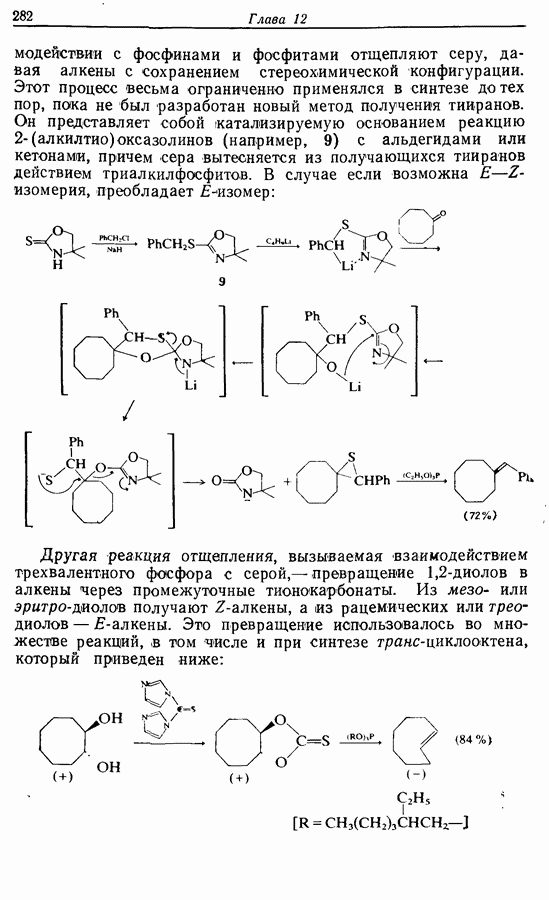
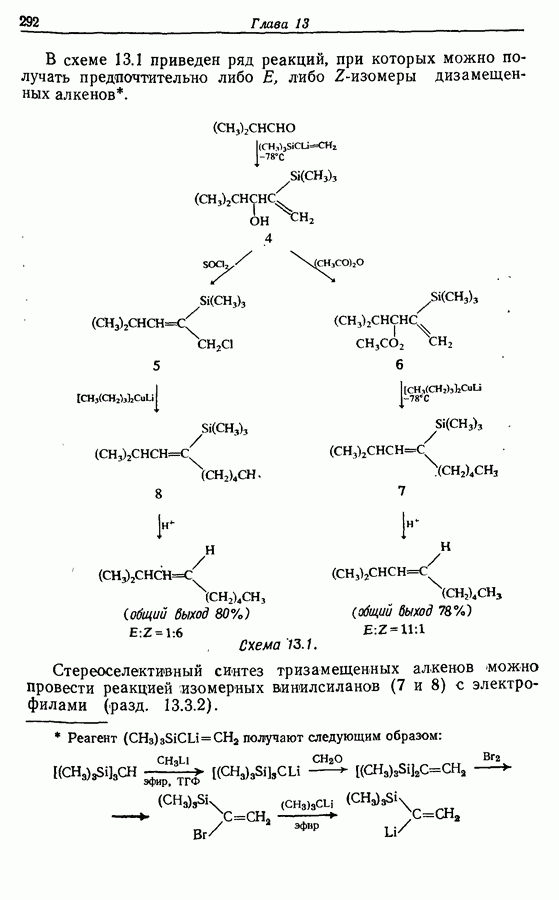
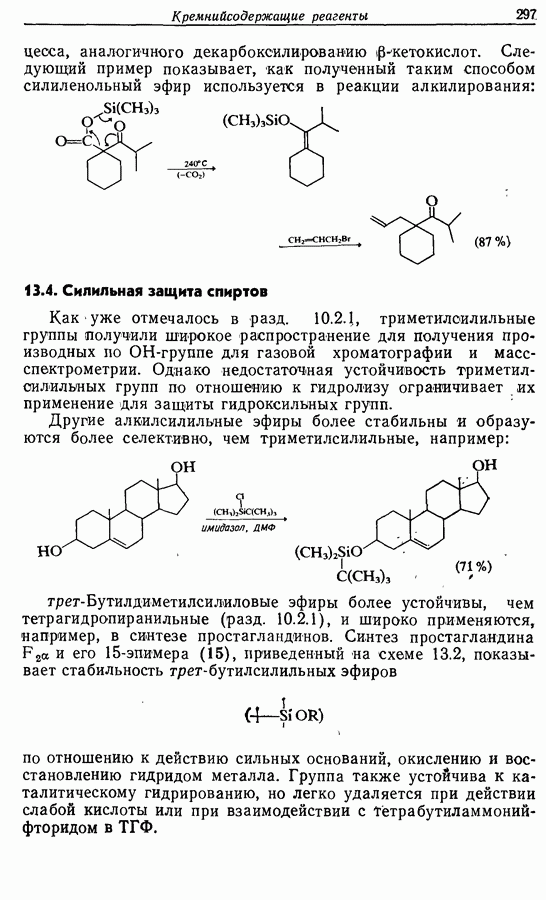
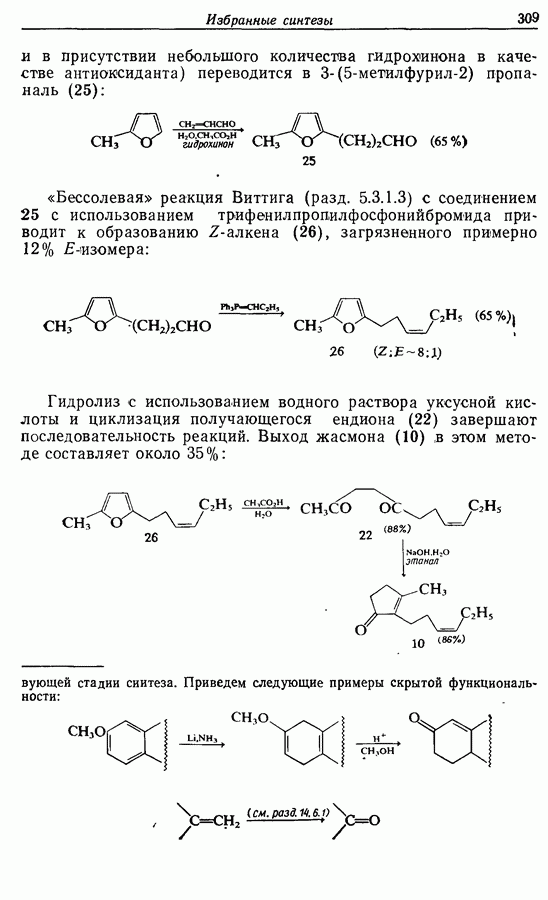
Как и предполагалось ранее,  -алкены можно получить при «бессолевой» реакции Виттига. Во втором синтезе феромона использовался именно этот метод, и
-алкены можно получить при «бессолевой» реакции Виттига. Во втором синтезе феромона использовался именно этот метод, и  -алкенная функциональная группа вводилась с самого начала. Карбонильная группа получалась через вторичный спирт. Расчленения, приводящие к этому пути, следующие:
-алкенная функциональная группа вводилась с самого начала. Карбонильная группа получалась через вторичный спирт. Расчленения, приводящие к этому пути, следующие:

Расчленения  приводят к ненасыщенным спиртам в качестве основных промежуточных соединений. Как мы увидим далее, соединение 4 получают при «бессолевой» реакции
приводят к ненасыщенным спиртам в качестве основных промежуточных соединений. Как мы увидим далее, соединение 4 получают при «бессолевой» реакции
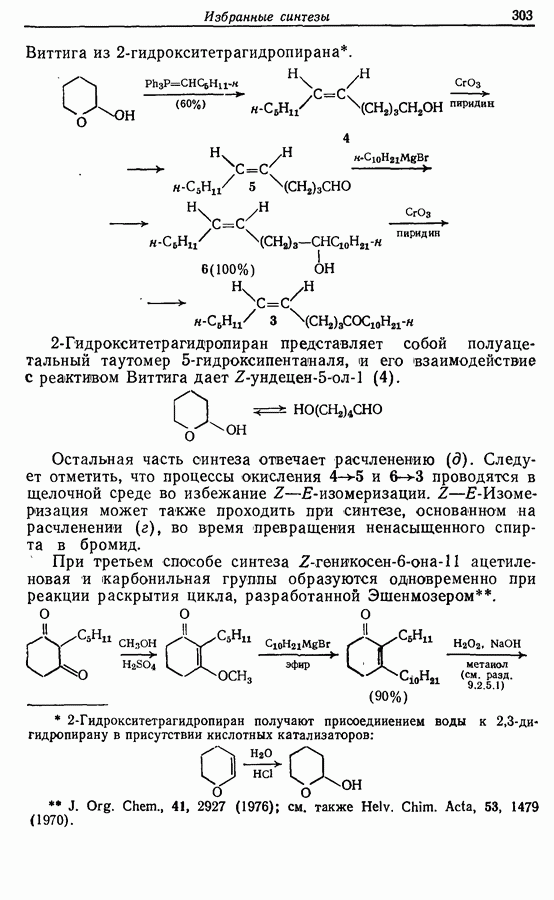
Виттига из 2-гидрокситетрагидропирана.

2-Гидрокситетрагидропиран представляет собой полуацетальный таутомер  -гидроксипентаналя, и его взаимодействие с реактивом Виттига дает
-гидроксипентаналя, и его взаимодействие с реактивом Виттига дает 

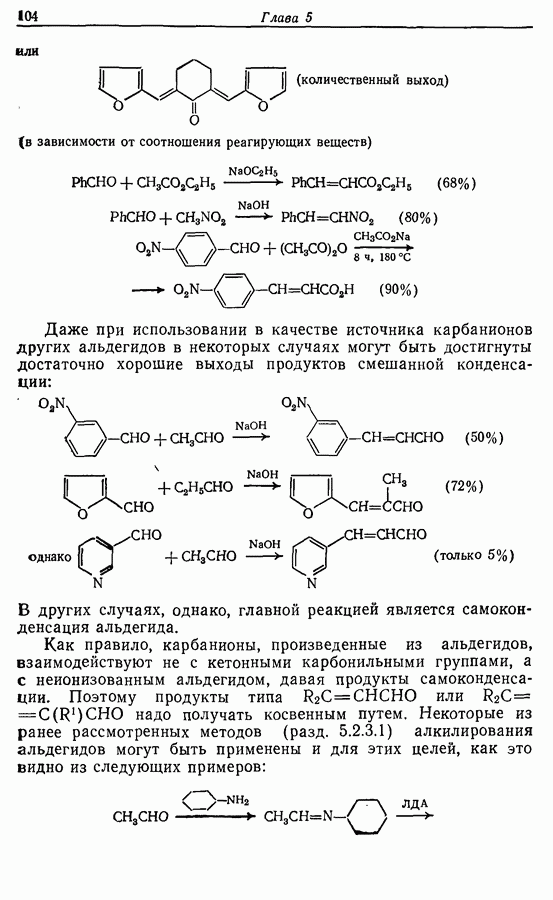
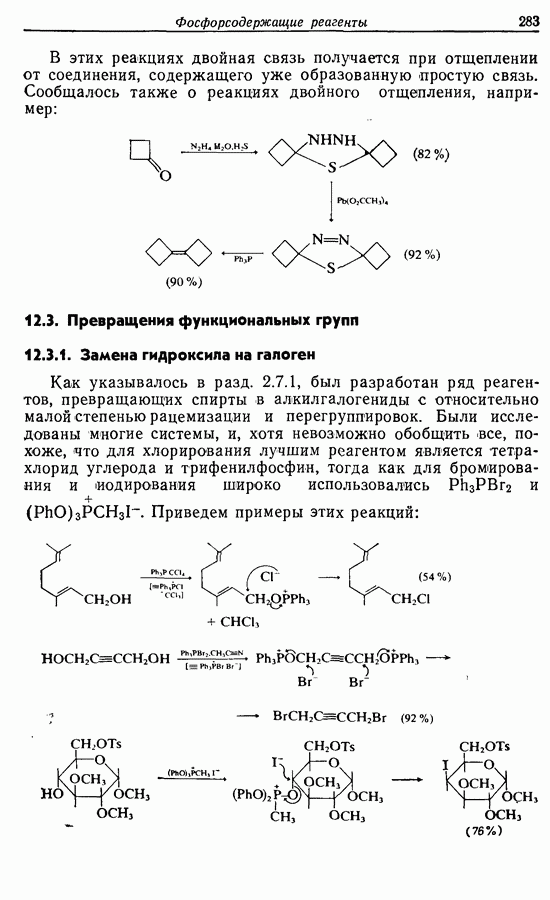
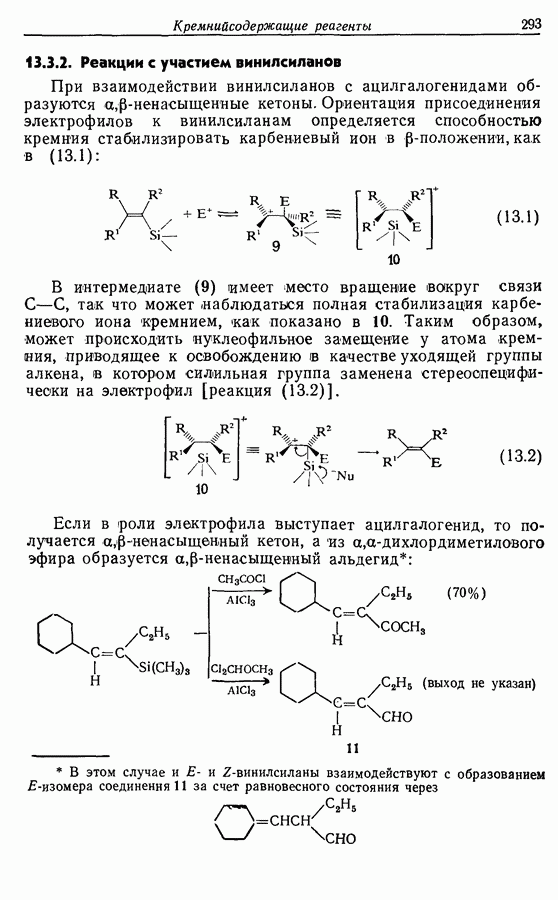
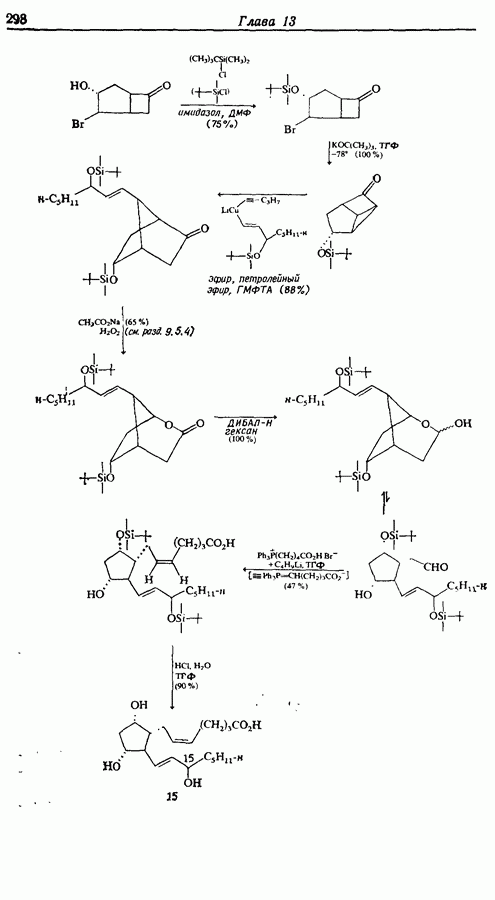
Остальная часть синтеза отвечает расчленению (5). Следует отметить, что процессы окисления  и проводятся в щелочной среде во избежание
и проводятся в щелочной среде во избежание  -изомеризации.
-изомеризации.  -Изоме-ризация может также проходить при синтезе, основанном на расчленении
-Изоме-ризация может также проходить при синтезе, основанном на расчленении  во время превращения ненасыщенного спирта в бромид.
во время превращения ненасыщенного спирта в бромид.
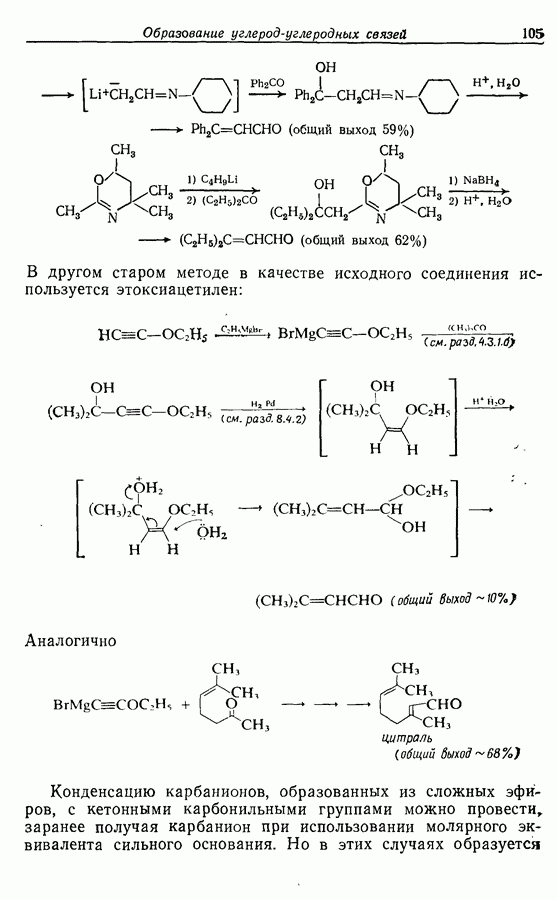
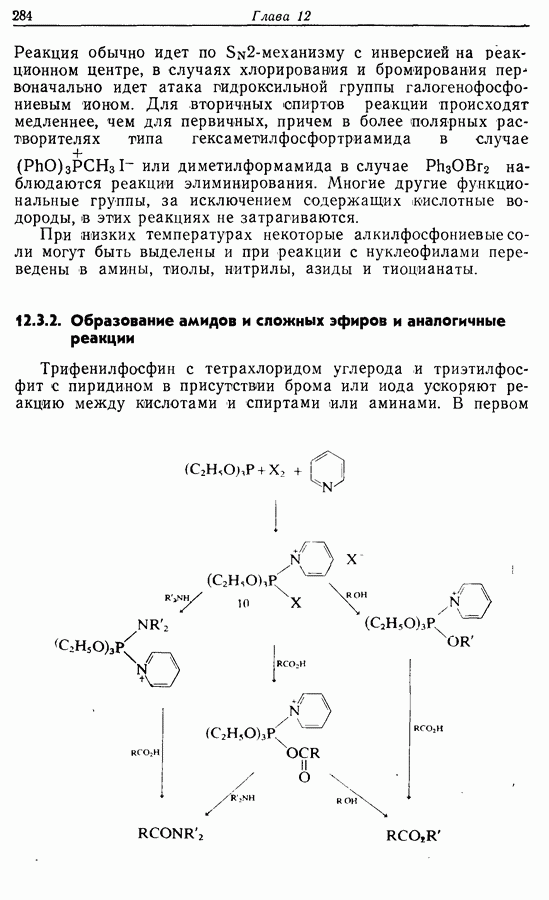
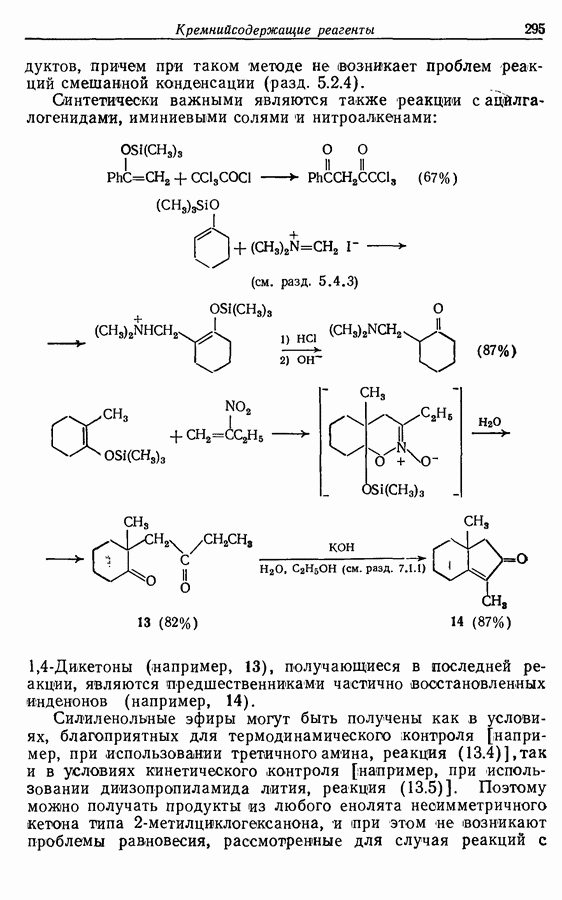
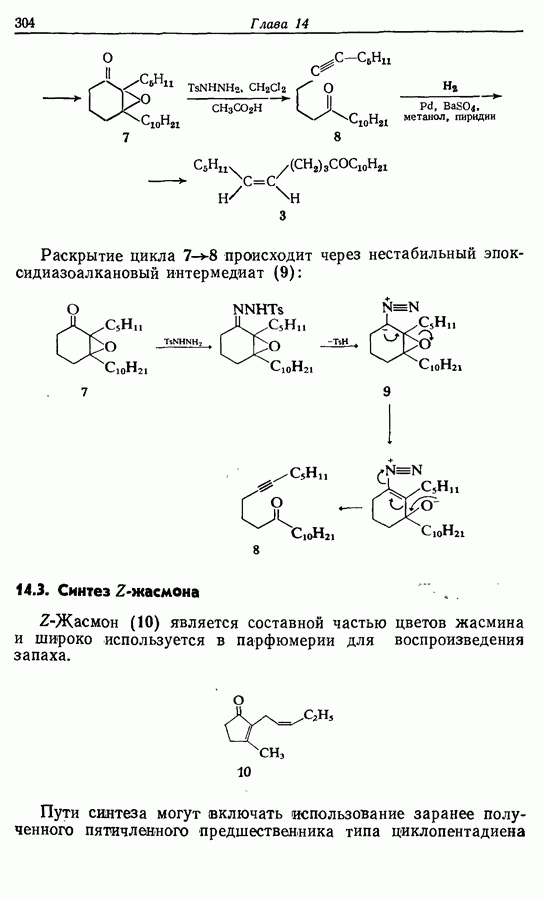
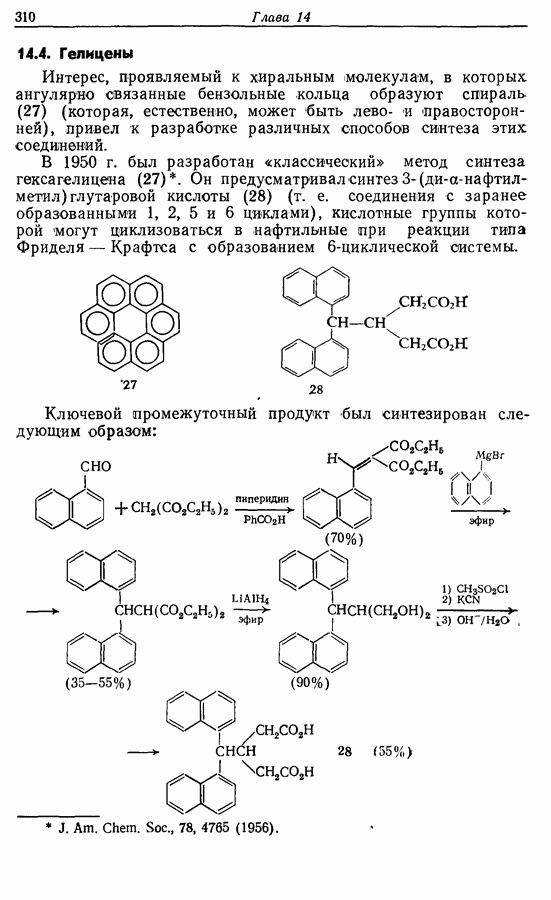
При третьем способе синтеза Z-геникосен-6-она-11 ацетиленовая и карбонильная группы образуются одновременно при реакции раскрытия цикла, разработанной Эшенмозером.

Раскрытие цикла  происходит через нестабильный эпокоидиазоалкановый интермедиат (9):
происходит через нестабильный эпокоидиазоалкановый интермедиат (9):

| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- 1. ВВЕДЕНИЕ
- 2. ВВЕДЕНИЕ И ВЗАИМОПРЕВРАЩЕНИЯ ФУНКЦИОНАЛЬНЫХ ГРУПП
- 2.1. Введение функциональных групп в апканы
- 2.2. Введение функциональных групп в алкены
- 2.3. Введение функциональных групп в апкины
- 2.4. Введение функциональных групп в ароматические углеводороды (арены)
- 2.5. Введение функциональных групп в производные бензола
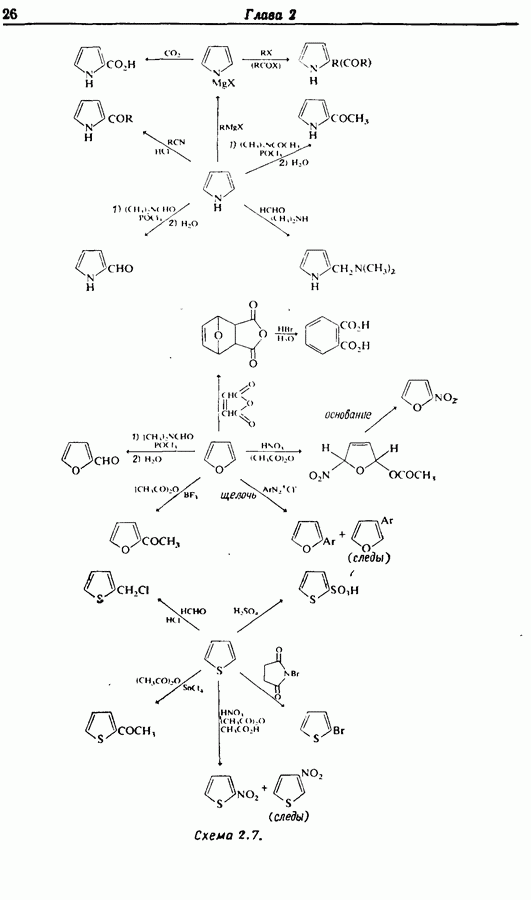
- 2.6. Введение функциональных групп в простые гетероциклические соединения
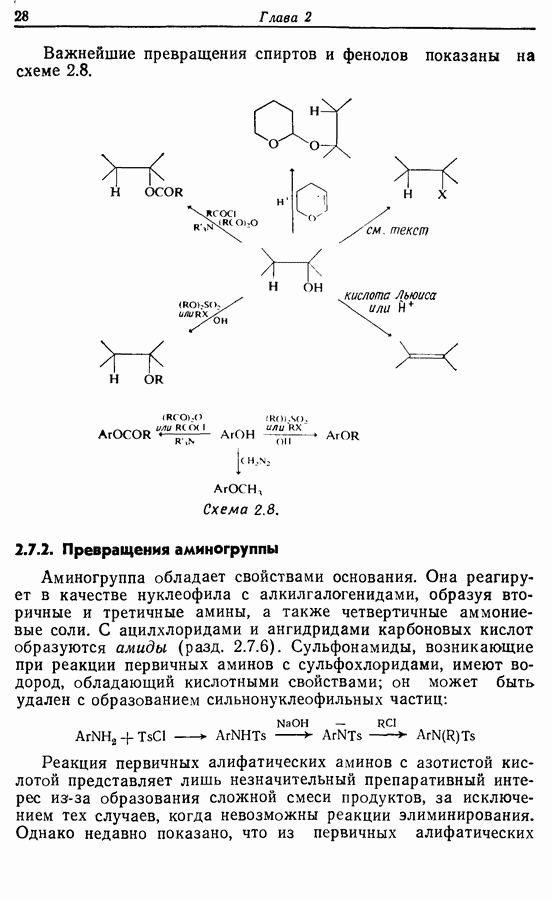
- 2.7. Взаимопревращения функциональных групп
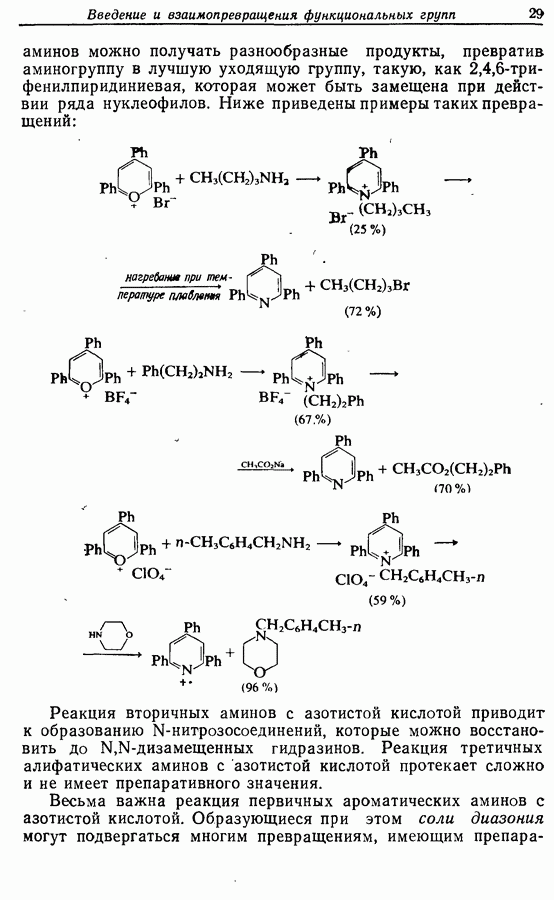
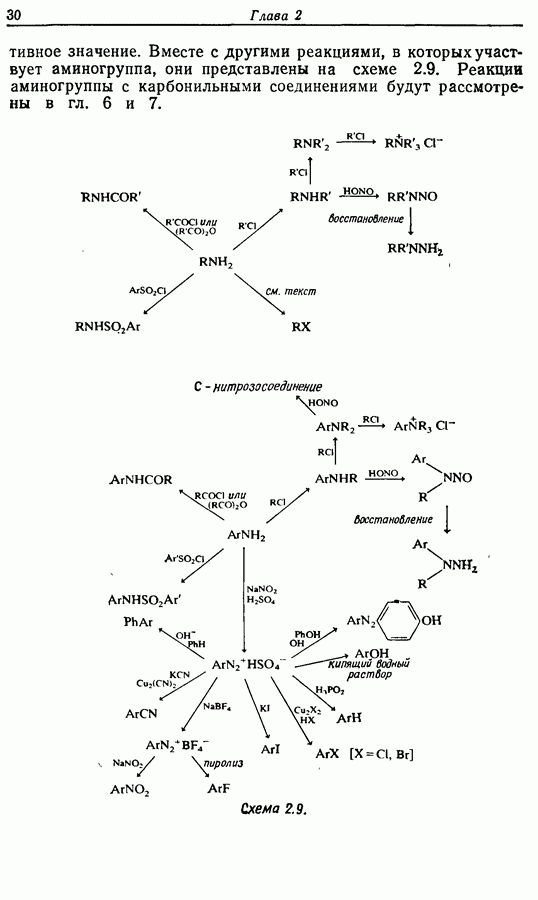
- 2.7.2. Превращения аминогруппы
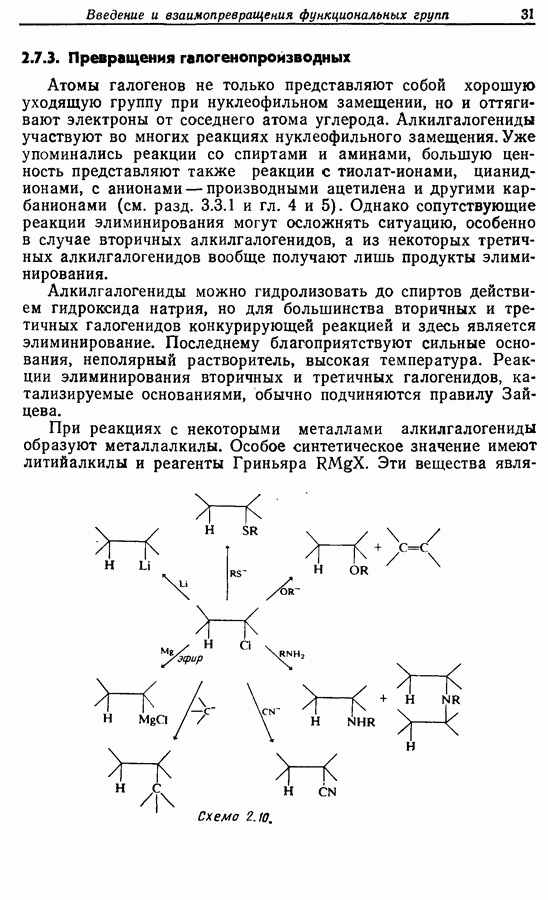
- 2.7.3. Превращения галогенопроизводных
- 2.7.4. Превращения нитросоединений
- 2.7.5. Превращения альдегидов и кетонов
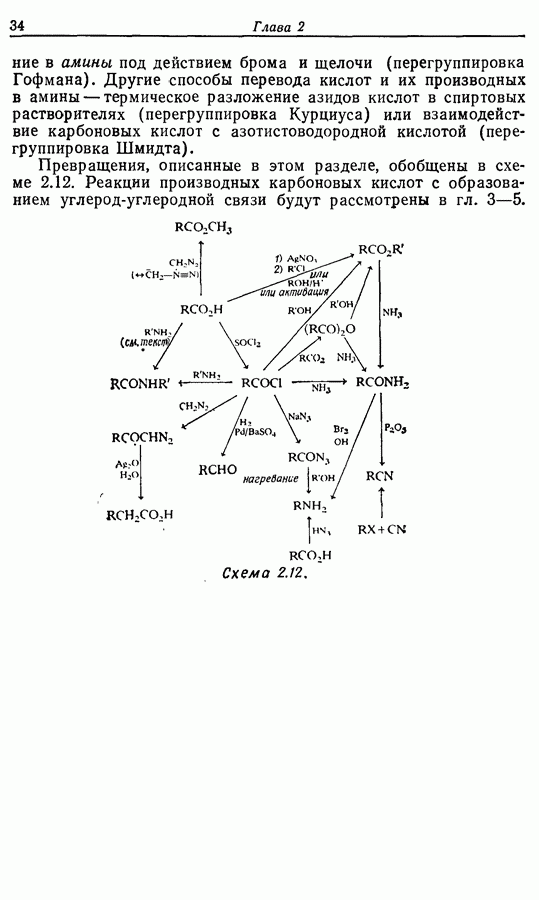
- 2.7.6. Превращения кислот и их производных
- 3. ПРИНЦИПЫ ОБРАЗОВАНИЯ УГЛЕРОД-УГЛЕРОДНОЙ СВЯЗИ
- 3.2. Расчленение и синтоны
- 3.3. Электрофильные углеродные частицы
- 3.4. Нуклеофильиые углеродные частицы
- 3.4.2. Стабилизированные карбанионы
- 3.4.3. Алкены, арены и гетероарены
- 4. ОБРАЗОВАНИЕ УГЛЕРОД-УГЛЕРОДНЫХ СВЯЗЕЙ: РЕАКЦИИ МЕТАЛЛООРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 4.1. Реактивы Гриньяра и электрофилы
- 4.2. Другие металлоорганические реактивы и электрофилы
- 4.2.2. Цинк- и кадмийорганические соединения
- 4.2.3. Органические соединения меди (I)
- 4.3. Реакции нуклеофилов, образованных из алкинов-1
- 4.3.2. Алкинильные соединения меди (I)
- 4.4. Выводы
- 4.5. Примеры
- 5. ОБРАЗОВАНИЕ УГЛЕРОД-УГЛЕРОДНЫХ СВЯЗЕЙ: ИСПОЛЬЗОВАНИЕ СТАБИЛИЗИРОВАННЫХ КАРБАНИОНОВ И РОДСТВЕННЫХ НУКЛЕОФИЛОВ
- 5.1.1. Алкилирование
- 5.1.2. Гидролиз алкинированных продуктов: путь к карбоновым кислотам и кетонам
- 5.1.3. Ацилирование
- 5.1.4. Реакции конденсации
- 5.1.5. Реакции с соединениями типа … и родственными системами: реакция Михаэля
- 5.2. Карбанионы, стабилизированные одной (-М)-группой
- 5.2.3. Косвенные пути получения a-алкилированных альдегидов и кетонов
- 5.2.4. Реакции конденсации
- 5.2.5. Реакция Михаэля
- 5.3. Карбанионы, стабилизированные соседними атомами фосфора или серы
- 5.3.2. Карбанионы, стабилизированные двумя атомами серы
- 5.4. Алкены, арены и гетероарены как нуклеофилы
- 5.4.3. Реакции присоединения и конденсации с карбонильными и родственными им соединениями
- 5.5. Заключение
- 5.6. Задачи
- 6. ОБРАЗОВАНИЕ СВЯЗЕЙ УГЛЕРОДА С ГЕТЕРОАТОМОМ: ОСНОВНЫЕ ПРИНЦИПЫ
- 6.1. Связи углерод — галоген
- 6.2. Связи углерод — кислород и углерод — сера
- 6.3. Связи углерод — азот
- 6.3.2. Электрофильный азот и нуклеофильный углерод
- 6.3.3. Нитрозосоединения, включая нитриты
- 7. ОБРАЗОВАНИЕ И РАСКРЫТИЕ ЦИКЛОВ
- 7.1. Внутримолекулярная циклизация в результате электрофильно-нуклеофильного взаимодействия
- 7.1.2. Условия внутримолекулярного циклообразования. Правила Болдуина
- 7.1.3. Присоединение по Михаэлю в процессах циклизации
- 7.1.4. Образование ароматических и гетероароматических циклов
- 7.2. Циклоприсоединение
- 7.2.2. 1,3-Диполярное циклоприсоединение
- 7.2.3. Присоединение карбенов и нитренов к алкенам
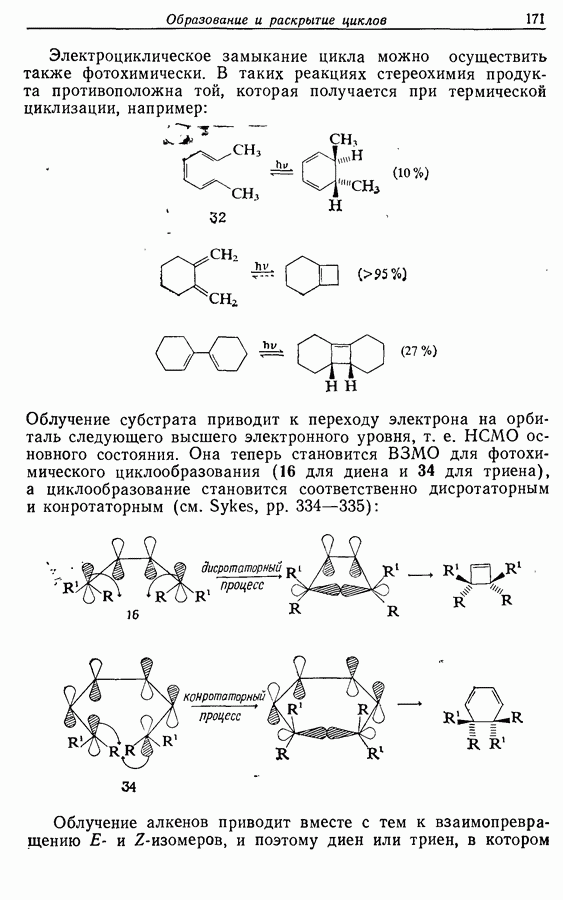
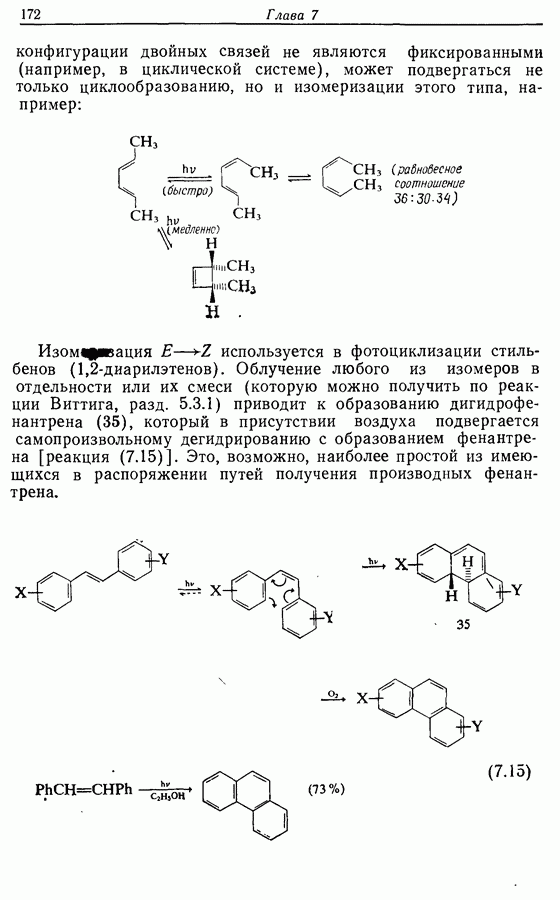
- 7.3. Электроциклическое циклообразование
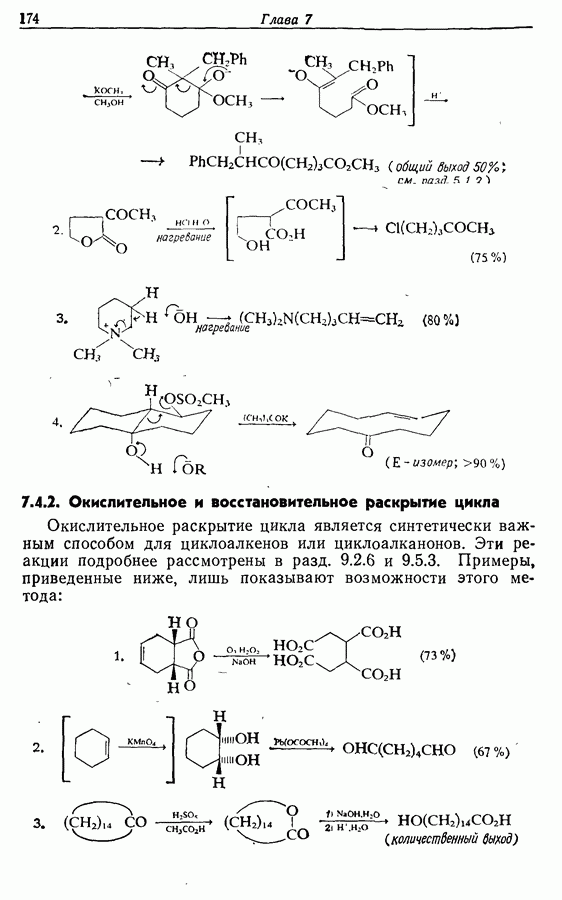
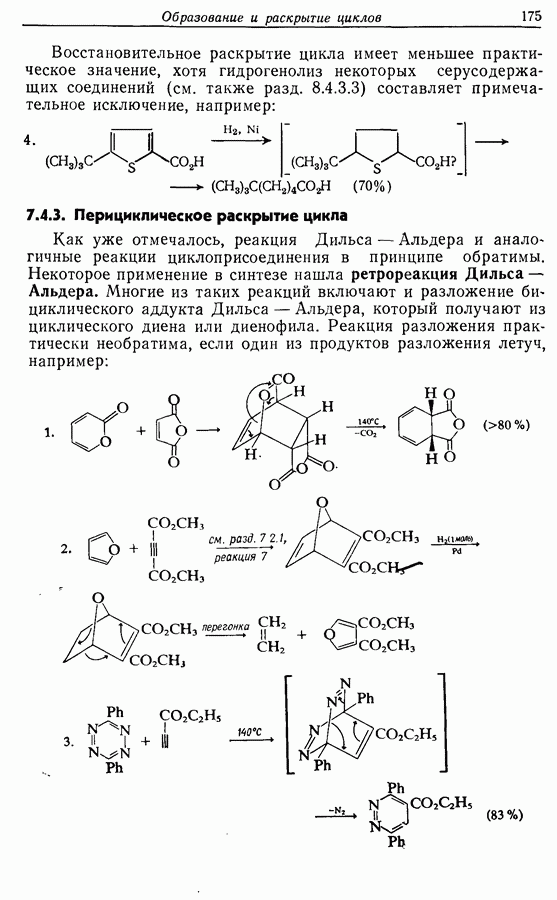
- 7.4. Раскрытие цикла
- 7.5. Выводы и задачи
- 8. ВОССТАНОВЛЕНИЕ
- 8.1. Каталитическое гидрирование
- 8.2. Восстановление гидридами металлов
- 8.3. Восстановление растворяющимися металлами
- 8.4. Восстановление определенных функциональных групп
- 8.4.2. Восстановление алкинов
- 8.4.3. Восстановление альдегидов и кетонов
- 8.4.4. Восстановление карбоновых кислот и их производных
- 8.4.5. Восстановление нитрилов
- 8.4.6. Восстановление иминов и оксимов, включая восстановительное алкилирование
- 8.5. Восстановительное расщепление связи углерод — гетероатом
- 8.6. Восстановительное раскрытие цикла в эпоксидах
- 8.7. Восстановление a,b-ненасыщенных карбонильных соединений
- 8.8. Восстановление сопряженных диенов
- 8.9. Восстановление ароматических и гетероароматических соединений
- 9. ОКИСЛЕНИЕ
- 9.2. Окисление углеводородов
- 9.2.2. Аллильное окисление
- 9.2.3. Бензильное окисление
- 9.2.4. Дегидрирование алканов, алкильных групп и алкенов
- 9.2.5. Окислительное присоединение к алкенам
- 9.2.6. Окислительная деструкция алкенов
- 9.2.7. Окисление алкинов
- 9.3. Окисление спиртов и их производных
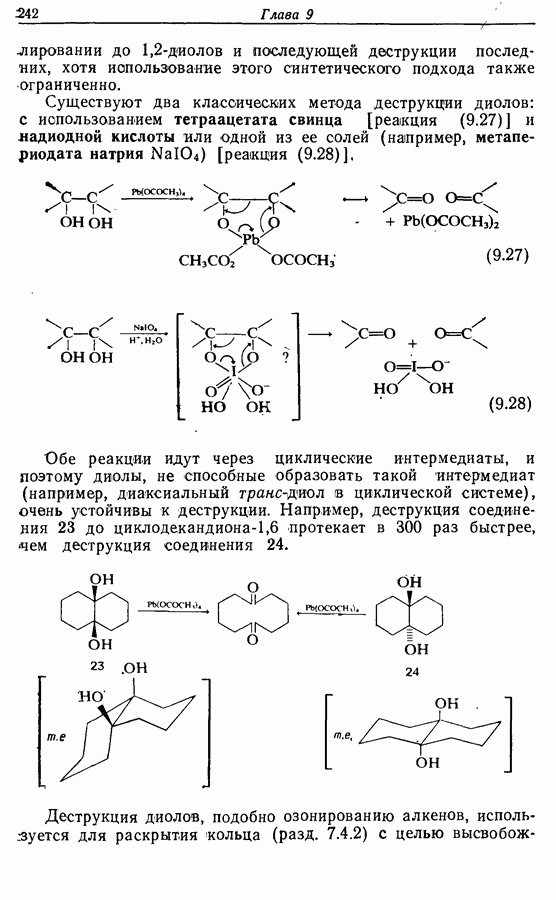
- 9.3.2. Окислительная деструкция 1,2-диолов
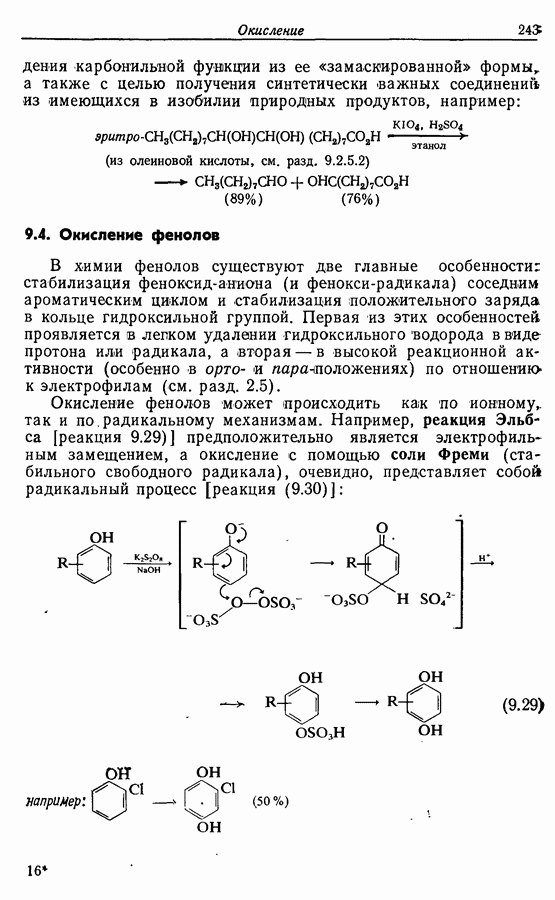
- 9.4. Окисление фенолов
- 9.5. Окисление альдегидов и кетонов
- 9.5.2. Окисление в 1,2-дикарбонильные соединения
- 9.5.3. Окисление до сложных эфиров: реакции Байера — Виллигера и Дакина
- 9.6. Окисление функциональных групп, содержащих азот
- 9.6.2. Дегидрирование соединений, содержащих азотные функциональные группы
- 9.7. Окисление серусодержащих функциональных групп
- 10. ЗАЩИТНЫЕ ГРУППЫ
- 10.2. Защита спиртов
- 10.3. Защита диолов
- 10.4. Защита карбоновых кислот
- 10.5. Защита аминогрупп
- 10.6. Защита карбонильных групп
- 11. БОРСОДЕРЖАЩИЕ РЕАГЕНТЫ
- 11.1. Гидроборирование алкенов при действии борана
- 11.2. Гидроборирование алкенов действием алкилборанов
- 11.3. Реакции борорганических соединений
- 11.4. Гидроборирование диенов
- 11.5. Гидроборирование алкинов
- 12. ФОСФОРСОДЕРЖАЩИЕ РЕАГЕНТЫ
- 12.1. Введение в химию фосфорорганических соединений
- 12.2. Образование углерод-углеродных двойных связей
- 12.3. Превращения функциональных групп
- 12.4. Реакции дезоксигенирования
- 13. КРЕМНИЙСОДЕРЖАЩИЕ РЕАГЕНТЫ
- 13.1. Введение в химию кремнийорганических соединений
- 13.2. Синтез кремнийорганических соединений
- 13.3. Реакции с образованием углерод-углеродных связей
- 13.4. Синильная защита спиртов
- 14. ИЗБРАННЫЕ СИНТЕЗЫ
- 14.2. Z-Геникосен-6-он-11
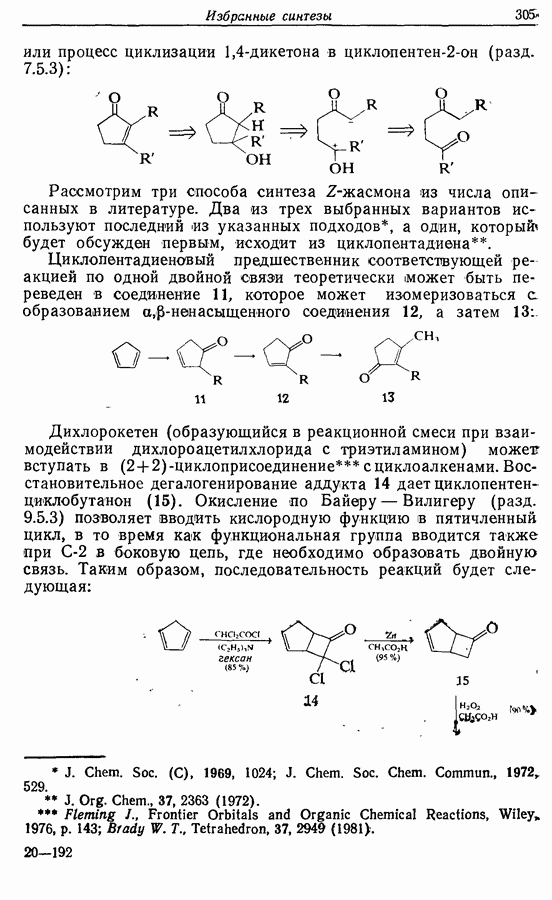
- 14.3. Синтез Z-жасмона
- 14.4. Гелицены
- 14.5. Анулены
- 14.6. Синтезы стероидов
- 14.6.2. Превращение растительных стероидов в стероидные гормоны
- 14.7. Синтез пептидов
- 14.7.2. Техника синтеза пептидов
- ЛИТЕРАТУРА