| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
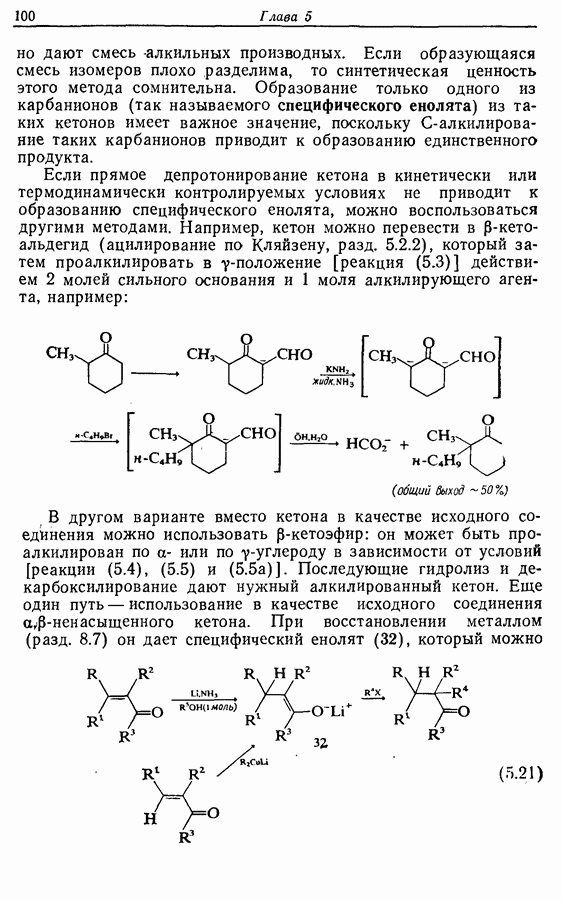
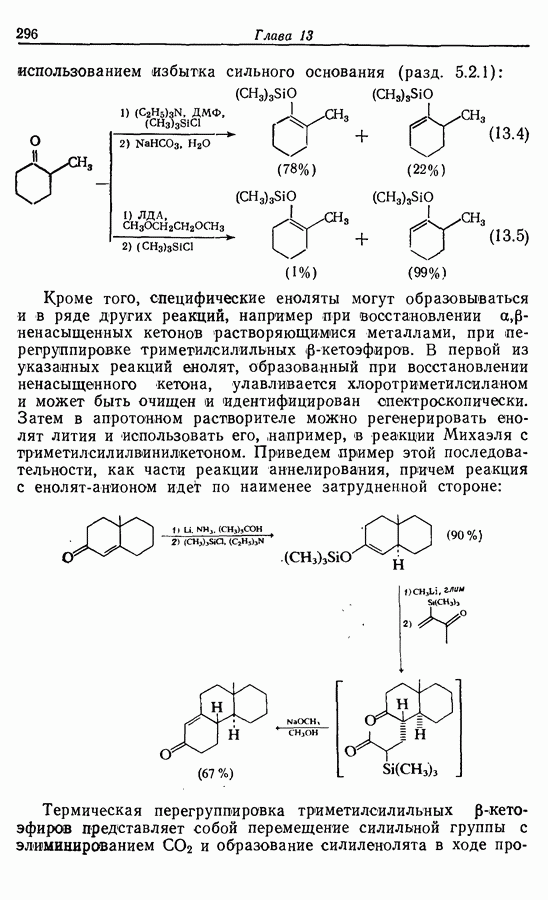
10.2. Защита спиртов
10.2.1. Образование простых эфиров
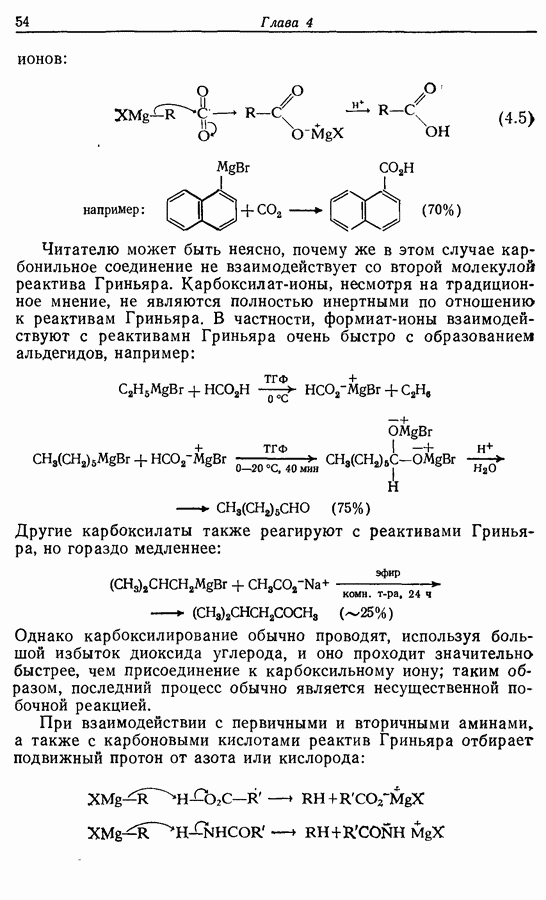
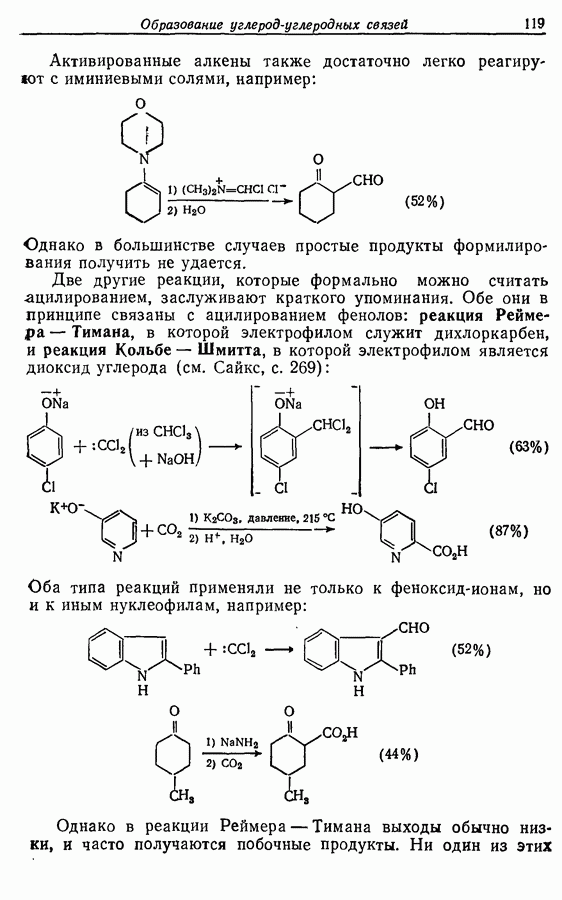
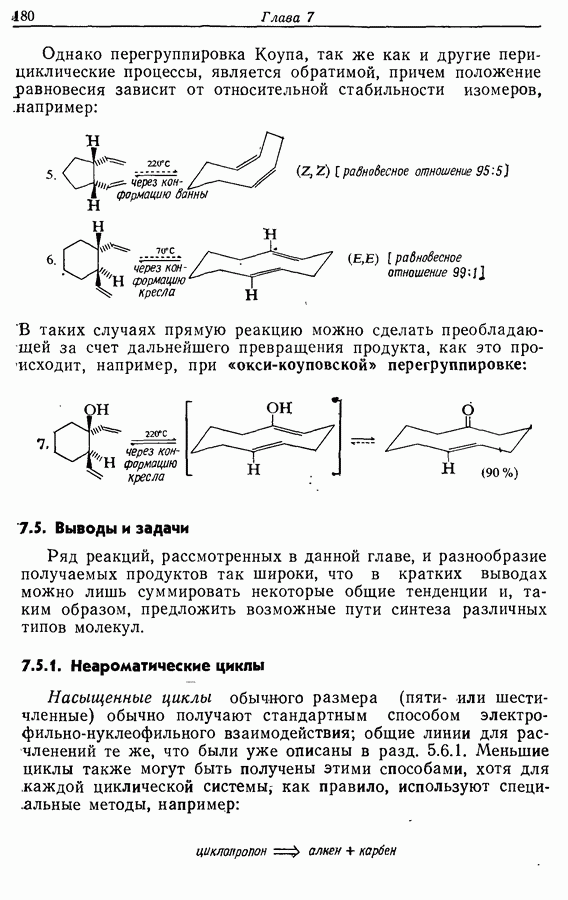
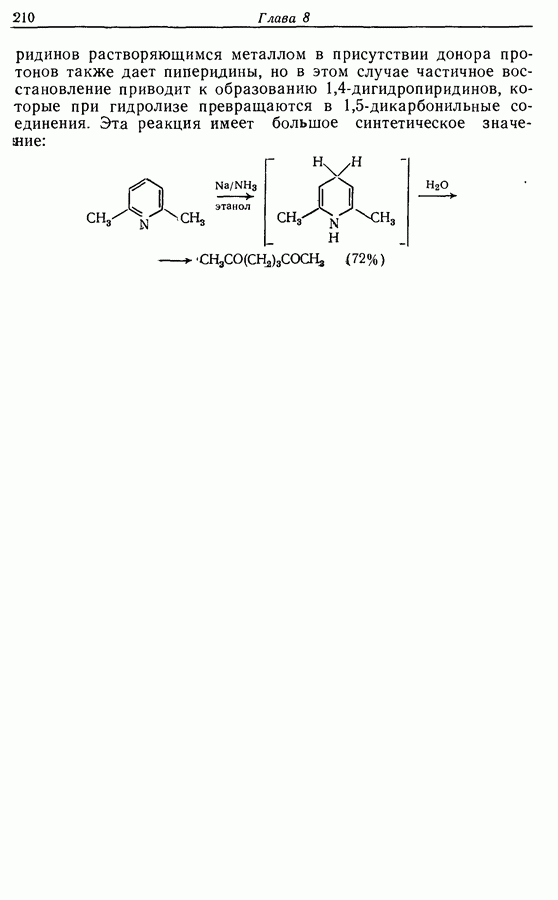
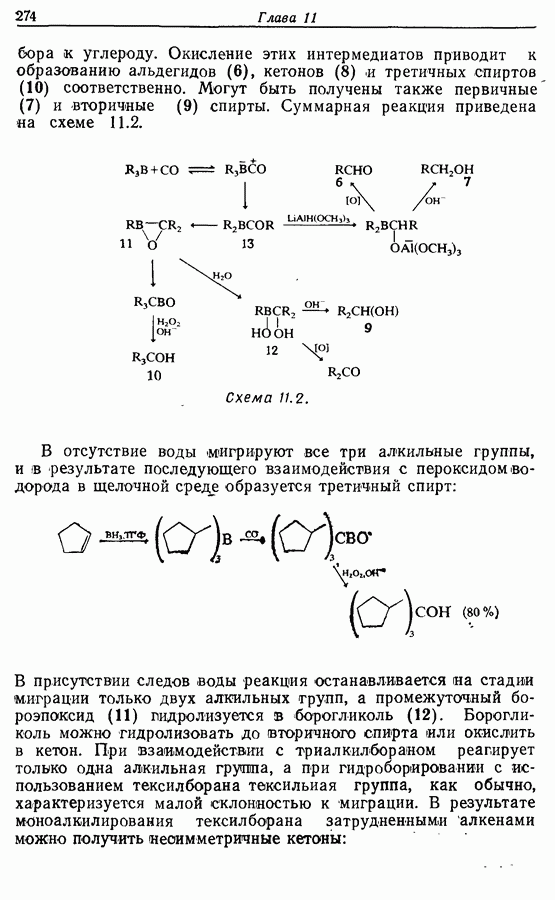
Простые эфиры в общем случае стабильны  действию большинства окислителей в нейтральных и щелочных условиях. Хотя метиловый и этиловый эфиры легко образуются (например, схема
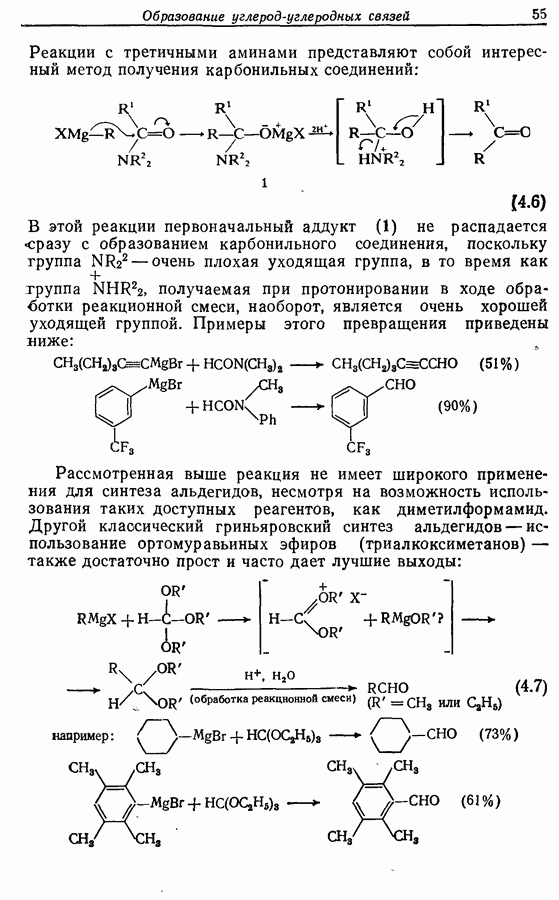
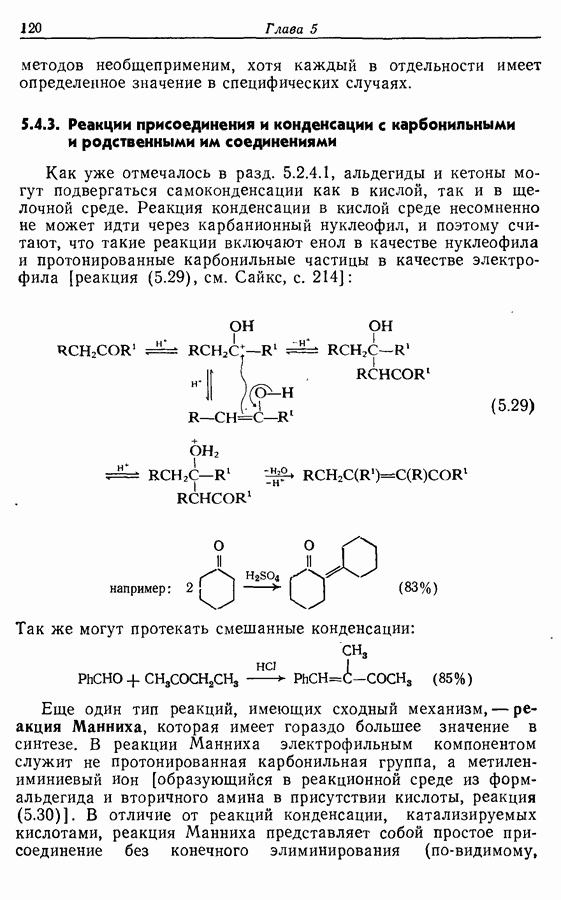
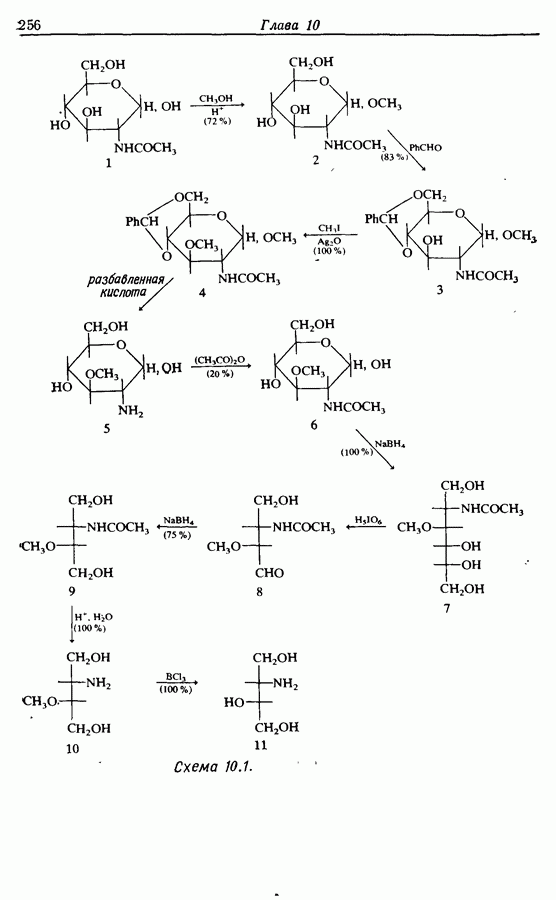
действию большинства окислителей в нейтральных и щелочных условиях. Хотя метиловый и этиловый эфиры легко образуются (например, схема  но не могут быть легко расщеплены. Исключение, впрочем, составляет химия углеводов. Метиловые эфиры по
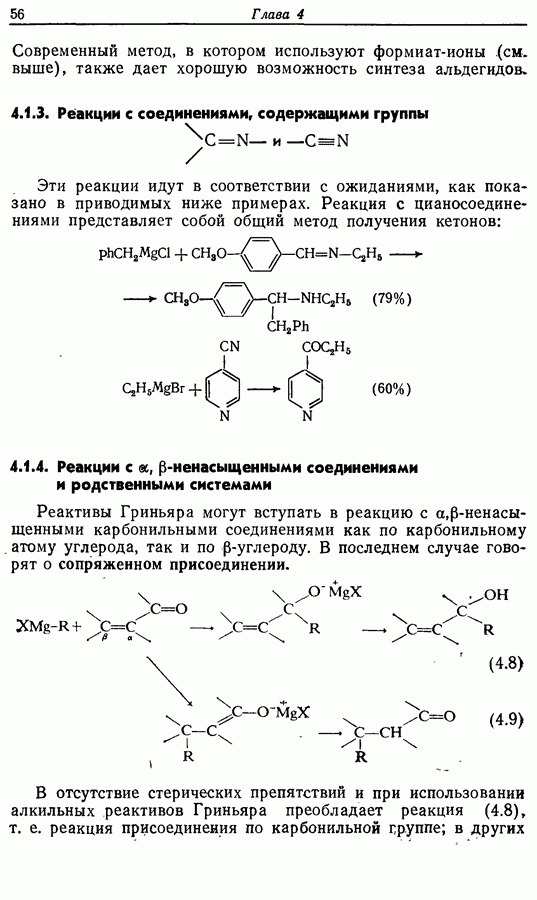
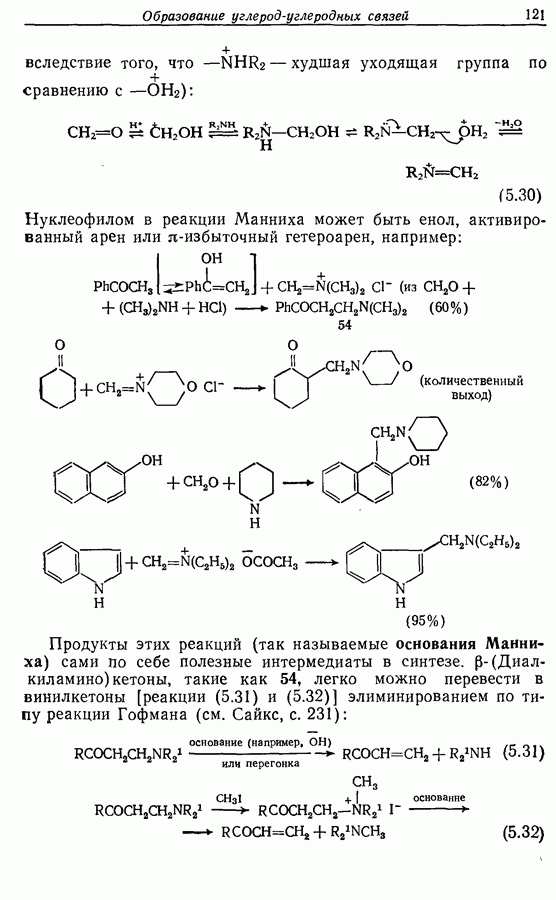
но не могут быть легко расщеплены. Исключение, впрочем, составляет химия углеводов. Метиловые эфиры по  которые в действительности являются ацеталями, легко гидролизуются (например, схема
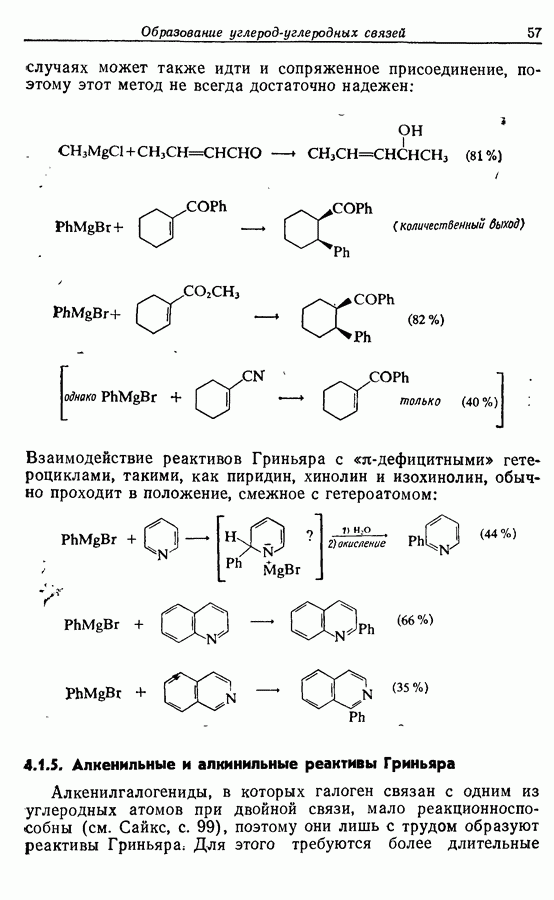
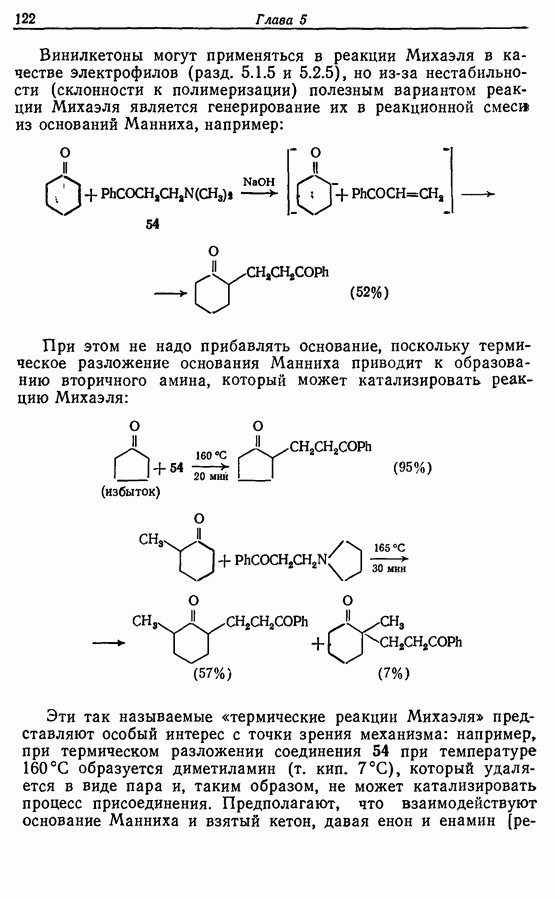
которые в действительности являются ацеталями, легко гидролизуются (например, схема  Для разложения эфиров можно использовать также кислоты Льюиса как, например, трихлорид бора (например, схема
Для разложения эфиров можно использовать также кислоты Льюиса как, например, трихлорид бора (например, схема 
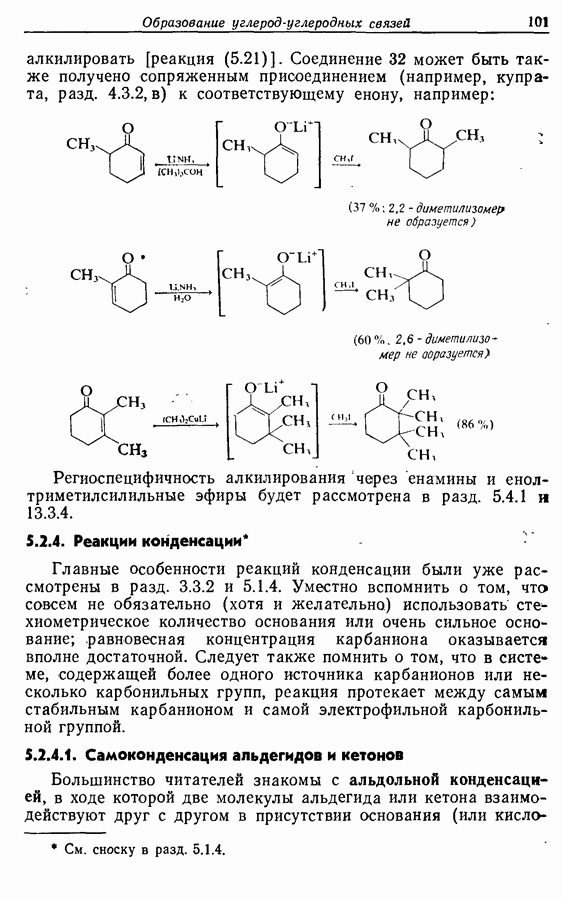
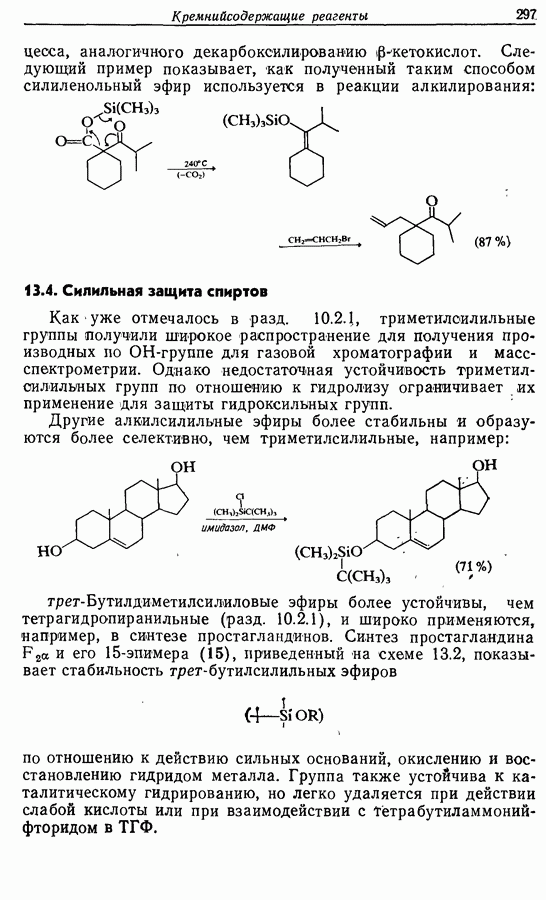
Наиболее часто используют бензильные, тритильные (три-фенилметильные), тетрагидропиранильные и триалкилсилильные эфиры. Триметилсилильные эфиры широко использовались в хроматографии массспектрометрии, однако они слишком легка гидродазуются для использования в синтетических целях. Недавно было установлено, что объемистые силильные производные типа трет-бутилдиметилоилильных несколько стабильнее триметильных производных и поэтому могут использоваться, когда необходима селективная защита (разд. 13.4).
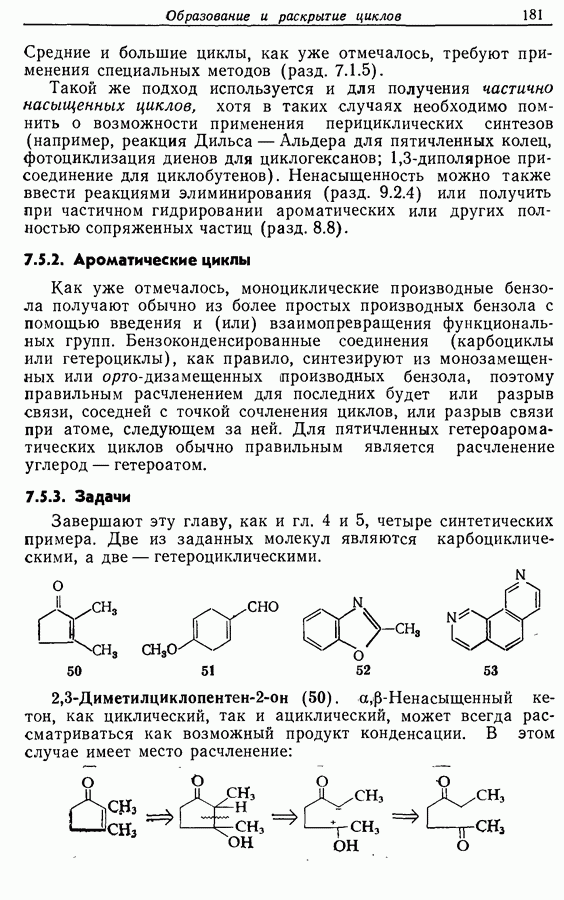
Бензильные и тритильные эфиры получаются при действии на спирт соответствующего галогенида в присутствии основания [например, схема  Гидроксильная группа может вновь регенерироваться при гидрогенолизе или, в случае тритильных эфиров, при действии слабой кислоты [например, схема
Гидроксильная группа может вновь регенерироваться при гидрогенолизе или, в случае тритильных эфиров, при действии слабой кислоты [например, схема  Тритильный остаток в пространственно затрудненные спирты вводится значительно медленнее, чем в случае первичных спиртов; это можно использовать для селективной защиты [схема
Тритильный остаток в пространственно затрудненные спирты вводится значительно медленнее, чем в случае первичных спиртов; это можно использовать для селективной защиты [схема 
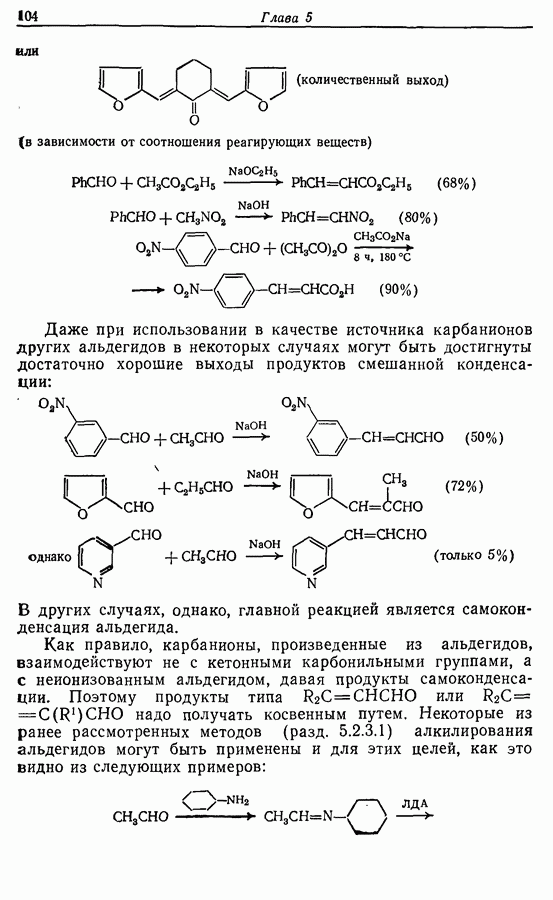
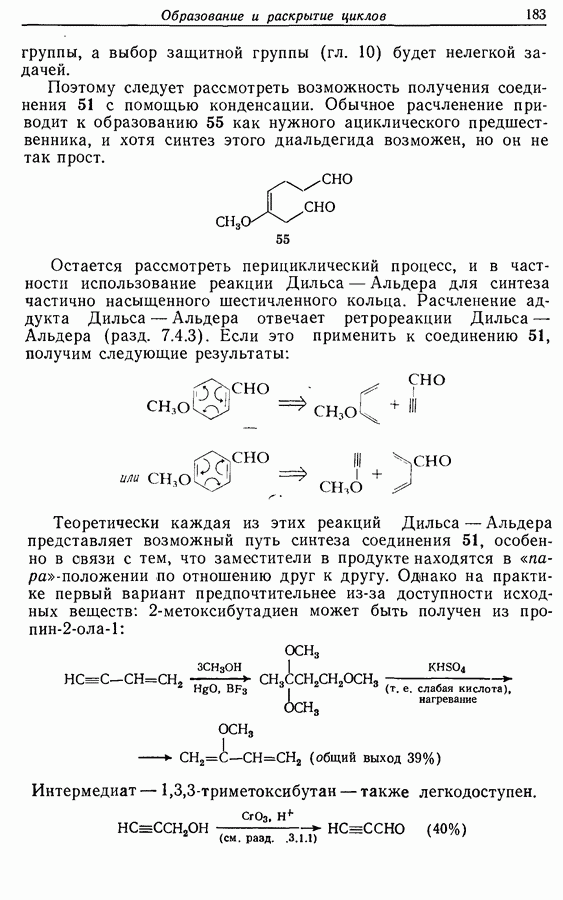
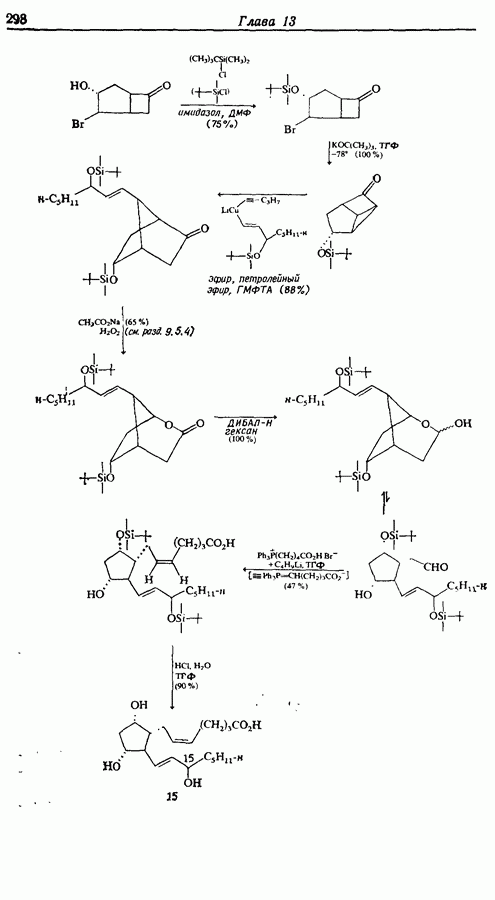
Тетрагидропиранильные эфиры образуются из спирта и  -дигидрогтирана при кислотном катализе. Спирт регенерируется три действии разбавленной серной кислоты. Спирты часто защищают таким образом для проведения реакций с металло-органическими соединениями; защитная группа часто снимается в ходе обработки реакционной смеси (схема 10.3).
-дигидрогтирана при кислотном катализе. Спирт регенерируется три действии разбавленной серной кислоты. Спирты часто защищают таким образом для проведения реакций с металло-органическими соединениями; защитная группа часто снимается в ходе обработки реакционной смеси (схема 10.3).

Схема 10.3.

(кликните для просмотра скана)
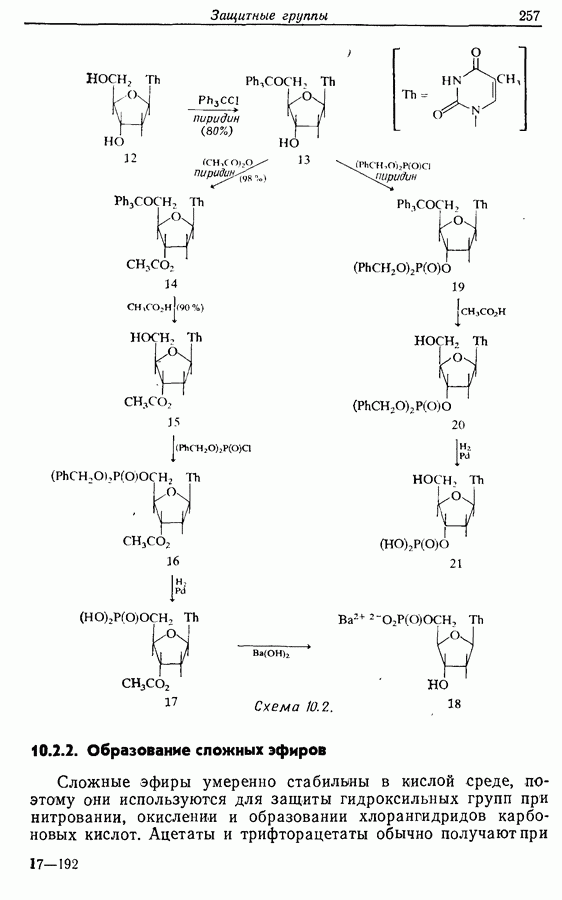
Схема 10.2. (см. скан)
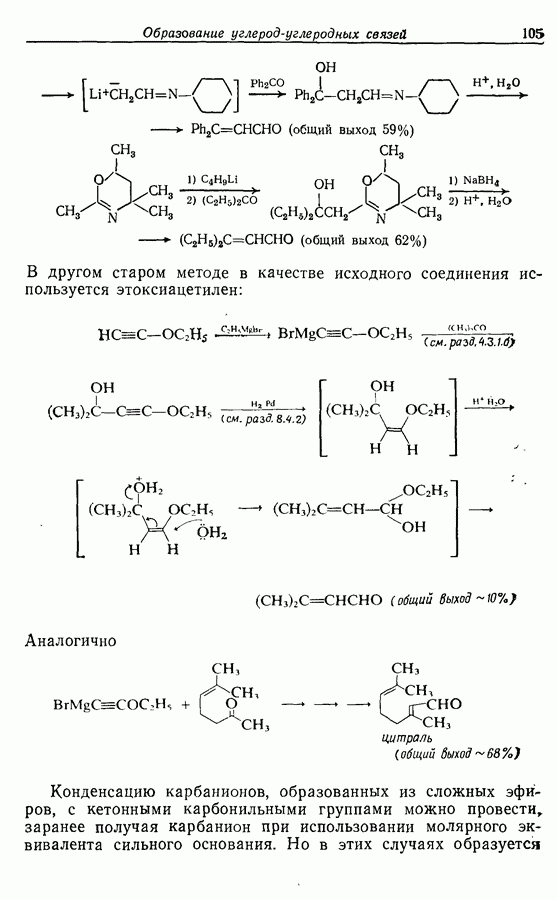
10.2.2. Образование сложных эфиров
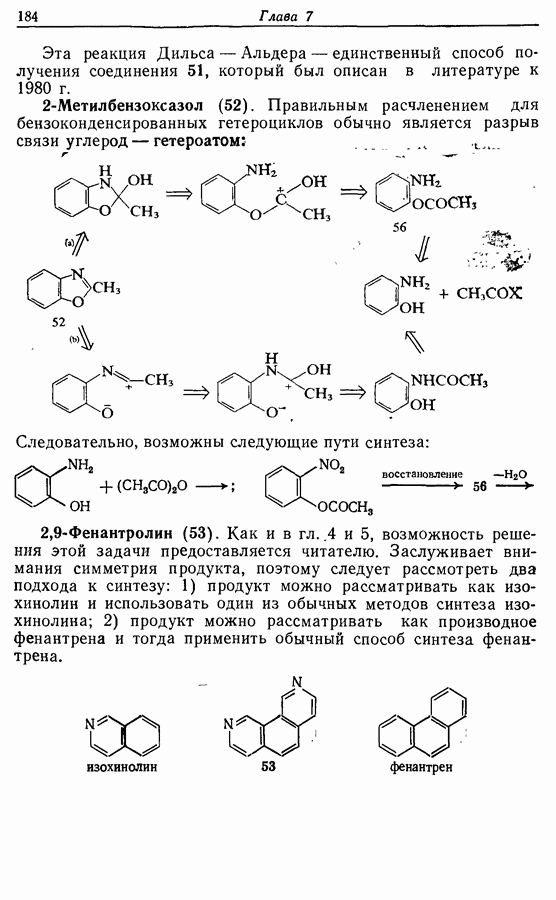
Сложные эфиры умеренно стабильны в кислой среде, поэтому они используются для защиты гидроксильных групп при нитровании, окислении и образовании хлораншдридов карбоновых кислот. Ацетаты и трифторацетаты обычно получают при
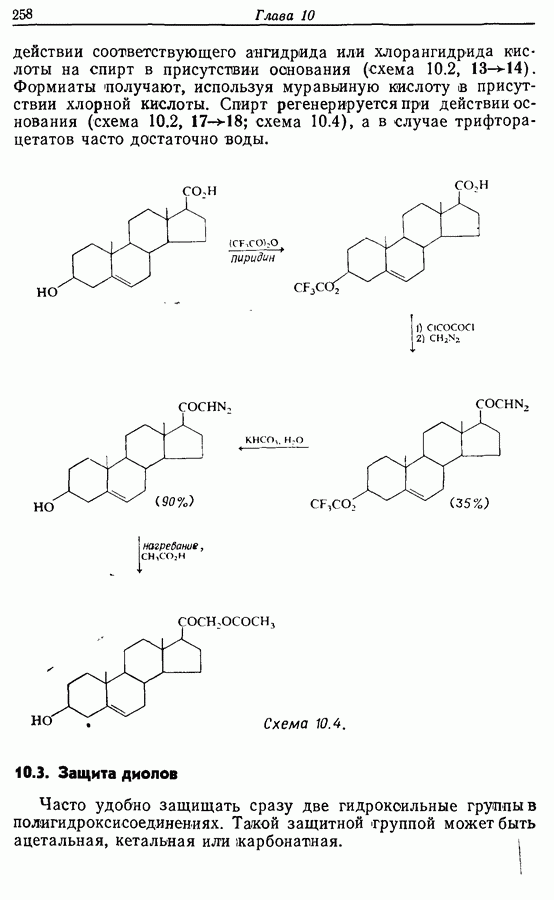
действии соответствующего ангидрида или хлорангидрида кислоты на спирт в присутствии основания (схема 10.2, 13-14). Формиаты получают, используя муравьиную кислоту в присутствии хлорной кислоты. Спирт регенерируется при действии основания (схема 10.2,  ; схема 10.4), а в случае трифторацетатов часто достаточно воды.
; схема 10.4), а в случае трифторацетатов часто достаточно воды.
Схема 10.4. (см. скан)
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- 1. ВВЕДЕНИЕ
- 2. ВВЕДЕНИЕ И ВЗАИМОПРЕВРАЩЕНИЯ ФУНКЦИОНАЛЬНЫХ ГРУПП
- 2.1. Введение функциональных групп в апканы
- 2.2. Введение функциональных групп в алкены
- 2.3. Введение функциональных групп в апкины
- 2.4. Введение функциональных групп в ароматические углеводороды (арены)
- 2.5. Введение функциональных групп в производные бензола
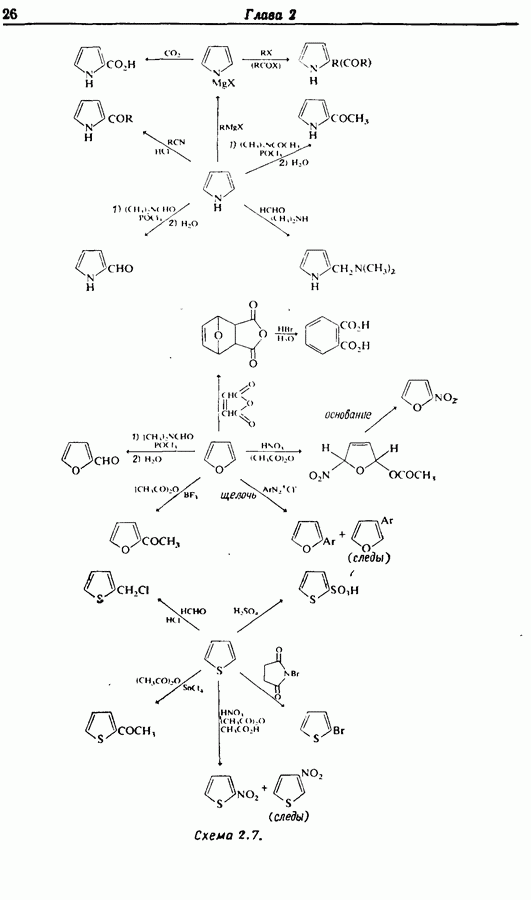
- 2.6. Введение функциональных групп в простые гетероциклические соединения
- 2.7. Взаимопревращения функциональных групп
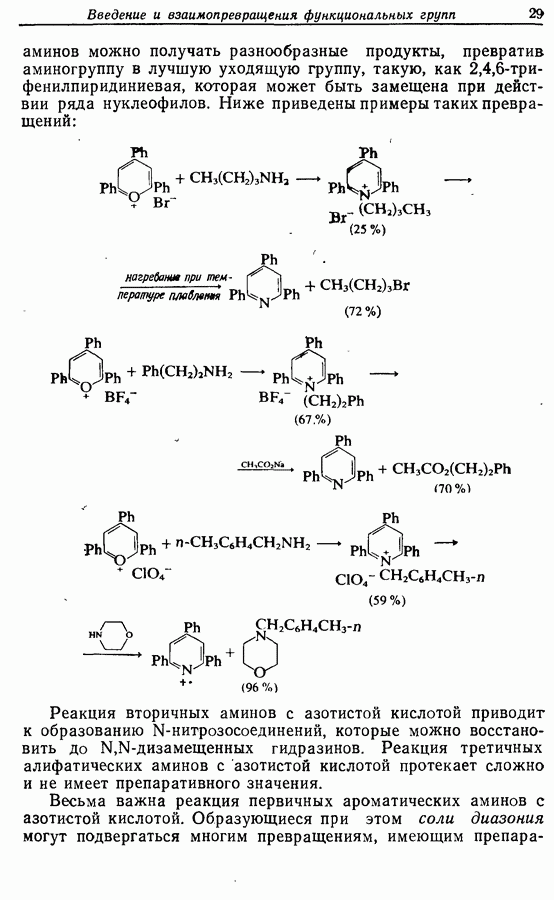
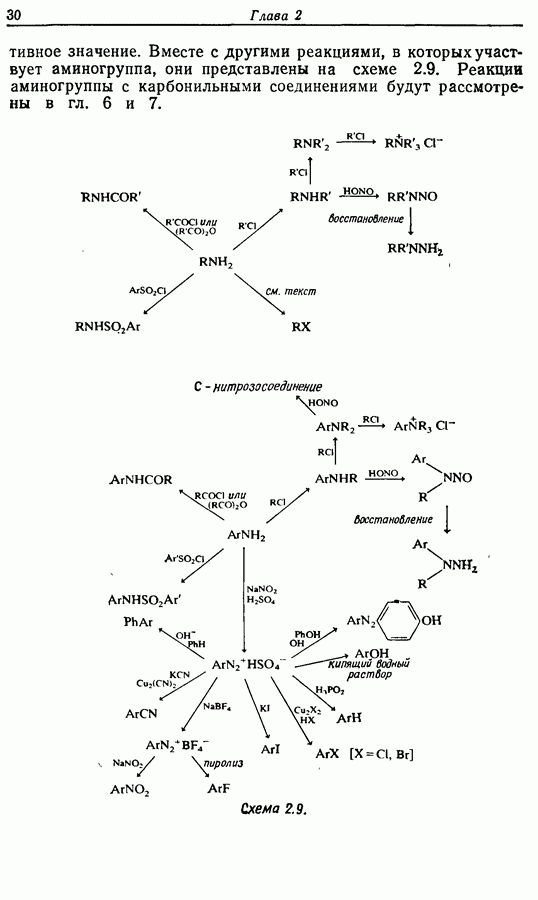
- 2.7.2. Превращения аминогруппы
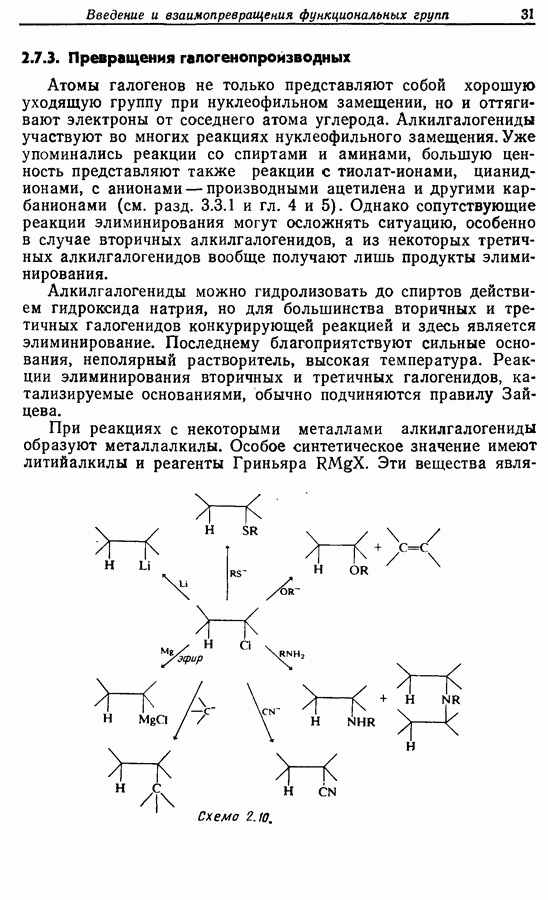
- 2.7.3. Превращения галогенопроизводных
- 2.7.4. Превращения нитросоединений
- 2.7.5. Превращения альдегидов и кетонов
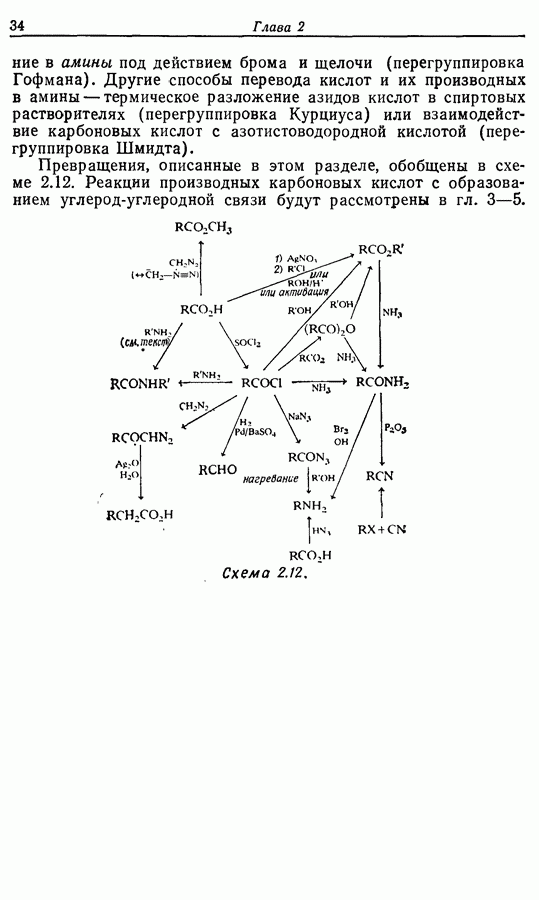
- 2.7.6. Превращения кислот и их производных
- 3. ПРИНЦИПЫ ОБРАЗОВАНИЯ УГЛЕРОД-УГЛЕРОДНОЙ СВЯЗИ
- 3.2. Расчленение и синтоны
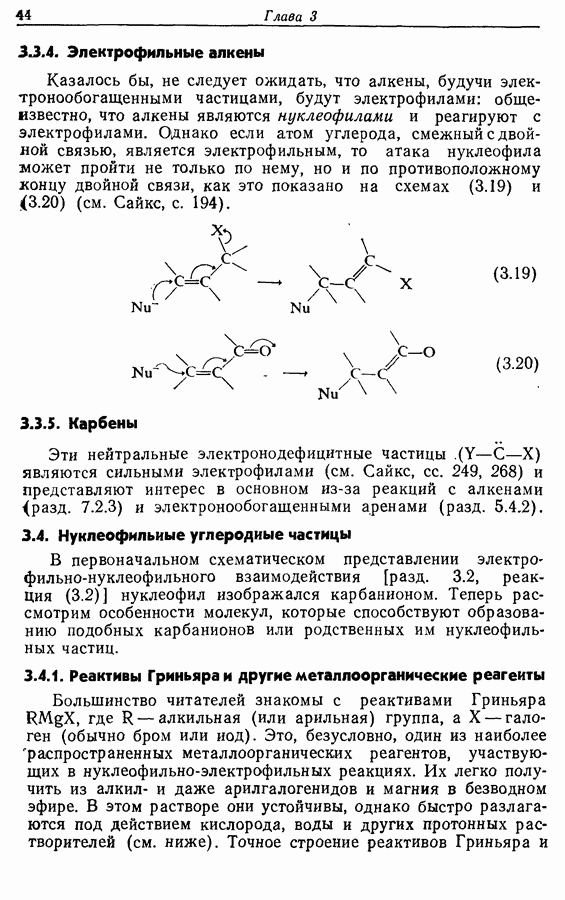
- 3.3. Электрофильные углеродные частицы
- 3.4. Нуклеофильиые углеродные частицы
- 3.4.2. Стабилизированные карбанионы
- 3.4.3. Алкены, арены и гетероарены
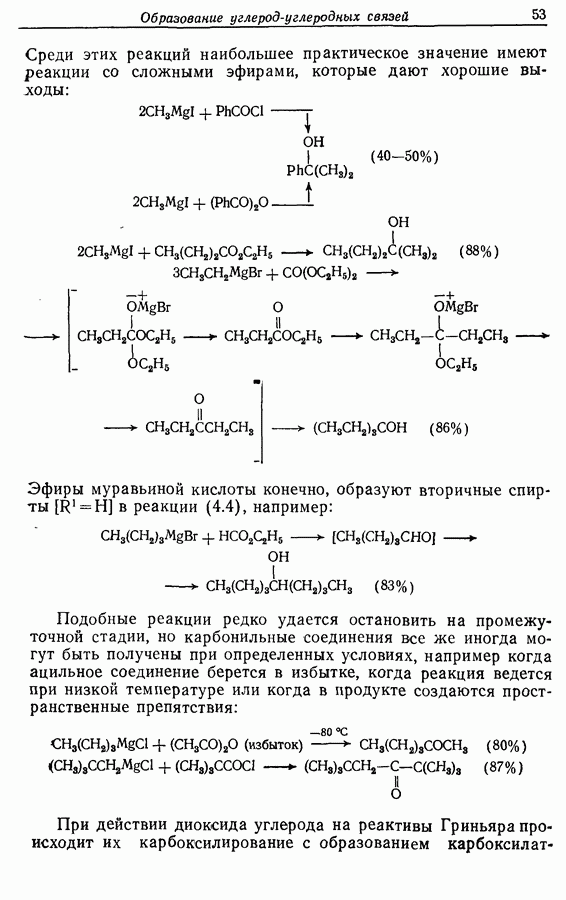
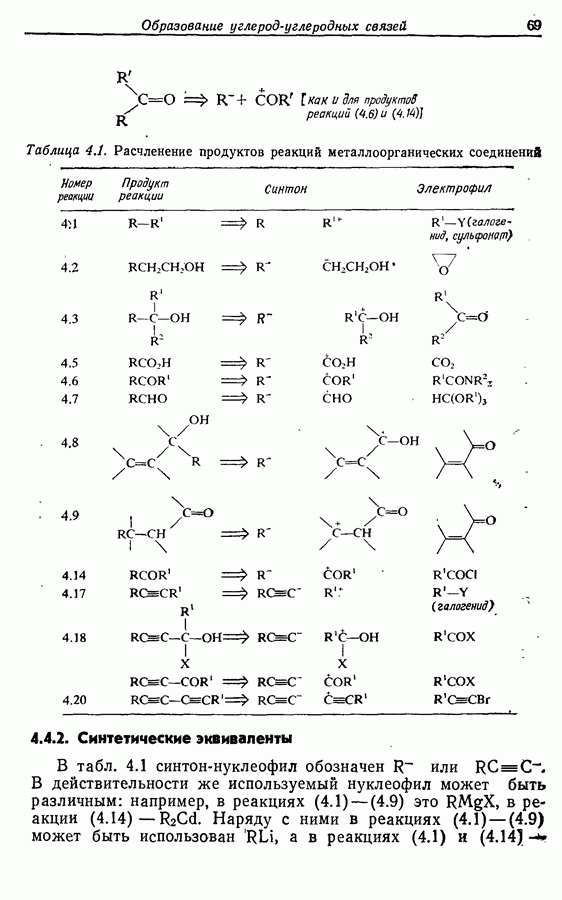
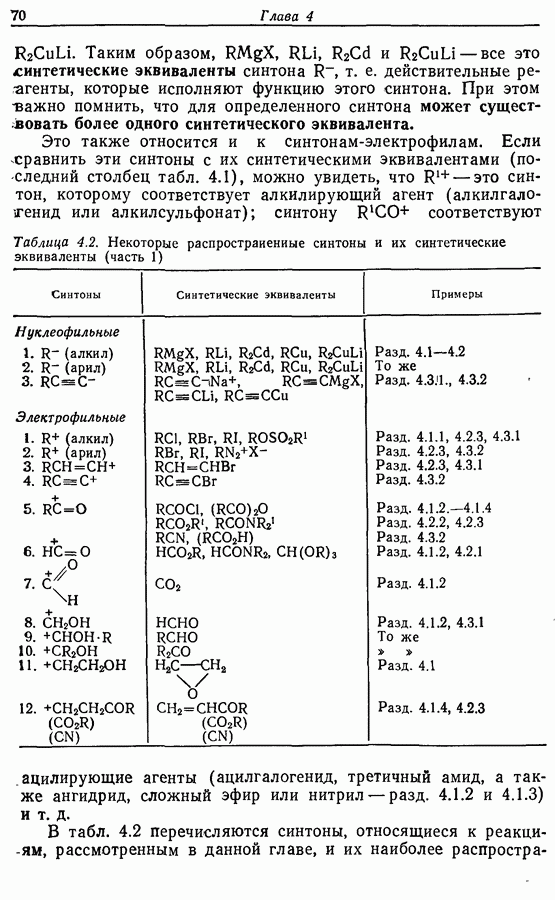
- 4. ОБРАЗОВАНИЕ УГЛЕРОД-УГЛЕРОДНЫХ СВЯЗЕЙ: РЕАКЦИИ МЕТАЛЛООРГАНИЧЕСКИХ СОЕДИНЕНИЙ
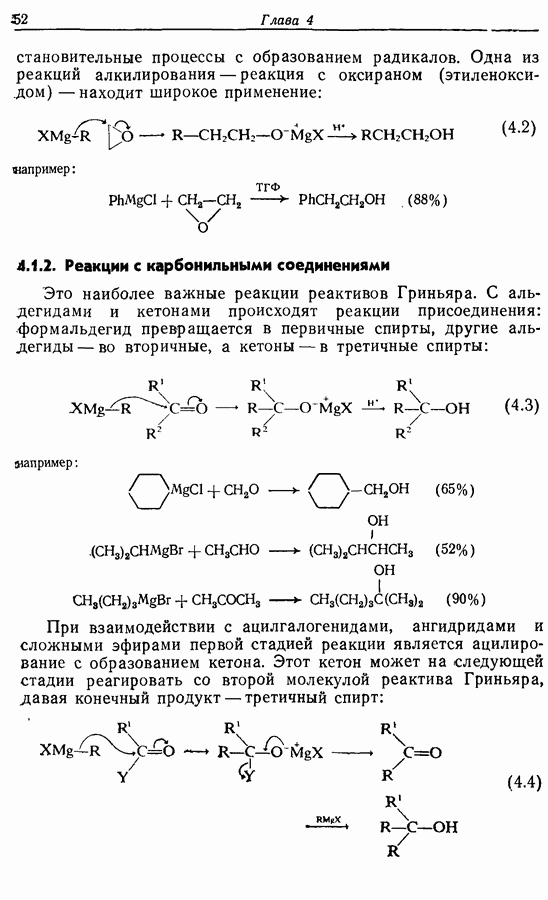
- 4.1. Реактивы Гриньяра и электрофилы
- 4.2. Другие металлоорганические реактивы и электрофилы
- 4.2.2. Цинк- и кадмийорганические соединения
- 4.2.3. Органические соединения меди (I)
- 4.3. Реакции нуклеофилов, образованных из алкинов-1
- 4.3.2. Алкинильные соединения меди (I)
- 4.4. Выводы
- 4.5. Примеры
- 5. ОБРАЗОВАНИЕ УГЛЕРОД-УГЛЕРОДНЫХ СВЯЗЕЙ: ИСПОЛЬЗОВАНИЕ СТАБИЛИЗИРОВАННЫХ КАРБАНИОНОВ И РОДСТВЕННЫХ НУКЛЕОФИЛОВ
- 5.1.1. Алкилирование
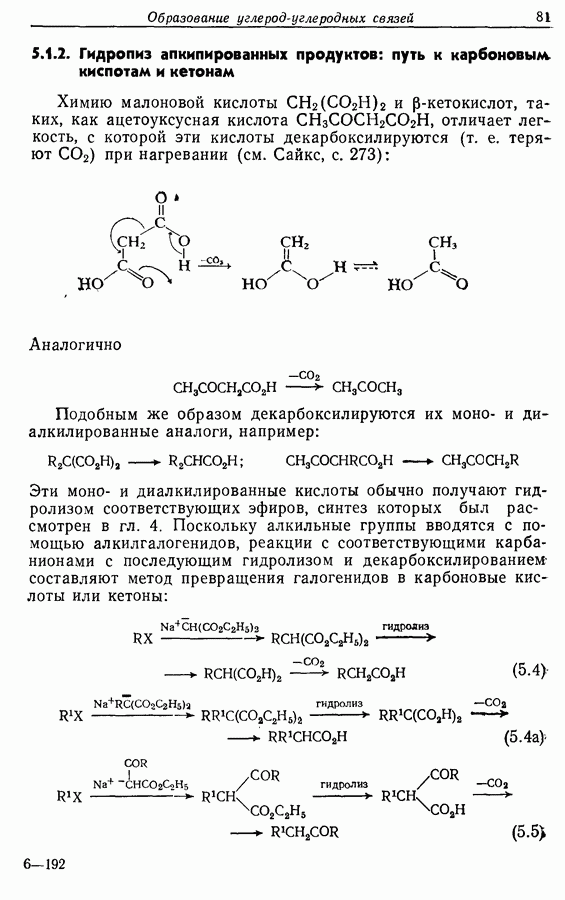
- 5.1.2. Гидролиз алкинированных продуктов: путь к карбоновым кислотам и кетонам
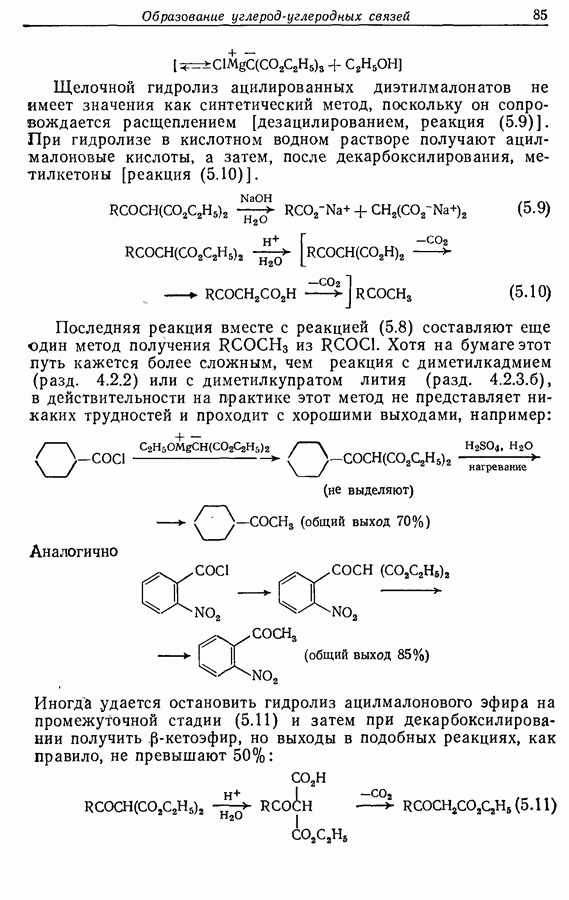
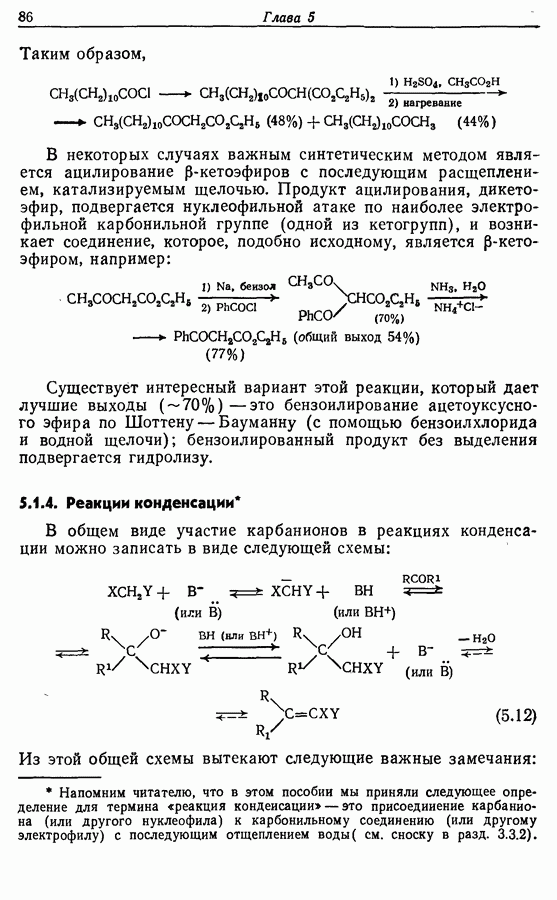
- 5.1.3. Ацилирование
- 5.1.4. Реакции конденсации
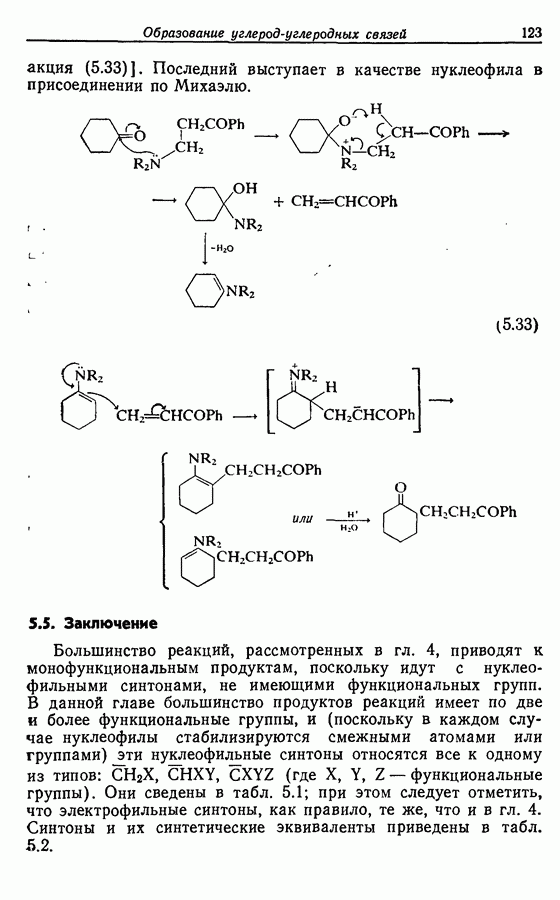
- 5.1.5. Реакции с соединениями типа … и родственными системами: реакция Михаэля
- 5.2. Карбанионы, стабилизированные одной (-М)-группой
- 5.2.3. Косвенные пути получения a-алкилированных альдегидов и кетонов
- 5.2.4. Реакции конденсации
- 5.2.5. Реакция Михаэля
- 5.3. Карбанионы, стабилизированные соседними атомами фосфора или серы
- 5.3.2. Карбанионы, стабилизированные двумя атомами серы
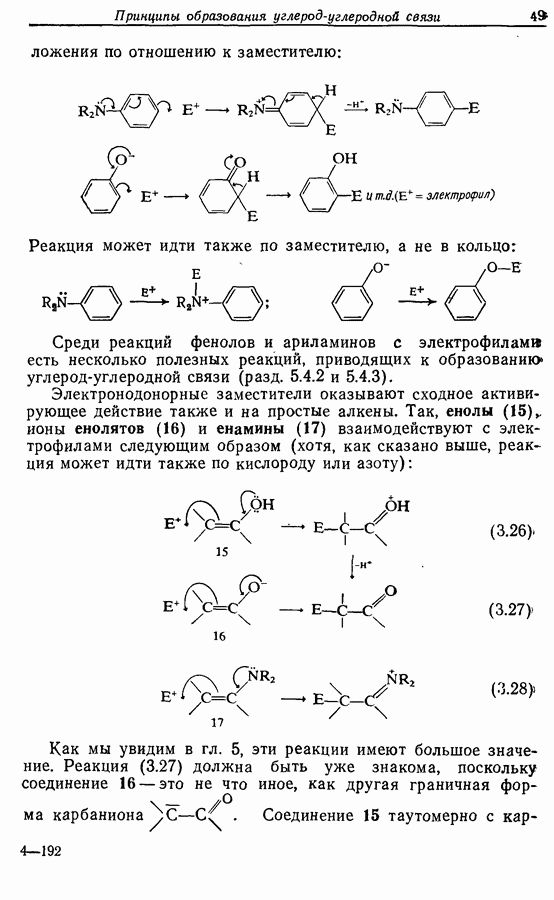
- 5.4. Алкены, арены и гетероарены как нуклеофилы
- 5.4.3. Реакции присоединения и конденсации с карбонильными и родственными им соединениями
- 5.5. Заключение
- 5.6. Задачи
- 6. ОБРАЗОВАНИЕ СВЯЗЕЙ УГЛЕРОДА С ГЕТЕРОАТОМОМ: ОСНОВНЫЕ ПРИНЦИПЫ
- 6.1. Связи углерод — галоген
- 6.2. Связи углерод — кислород и углерод — сера
- 6.3. Связи углерод — азот
- 6.3.2. Электрофильный азот и нуклеофильный углерод
- 6.3.3. Нитрозосоединения, включая нитриты
- 7. ОБРАЗОВАНИЕ И РАСКРЫТИЕ ЦИКЛОВ
- 7.1. Внутримолекулярная циклизация в результате электрофильно-нуклеофильного взаимодействия
- 7.1.2. Условия внутримолекулярного циклообразования. Правила Болдуина
- 7.1.3. Присоединение по Михаэлю в процессах циклизации
- 7.1.4. Образование ароматических и гетероароматических циклов
- 7.2. Циклоприсоединение
- 7.2.2. 1,3-Диполярное циклоприсоединение
- 7.2.3. Присоединение карбенов и нитренов к алкенам
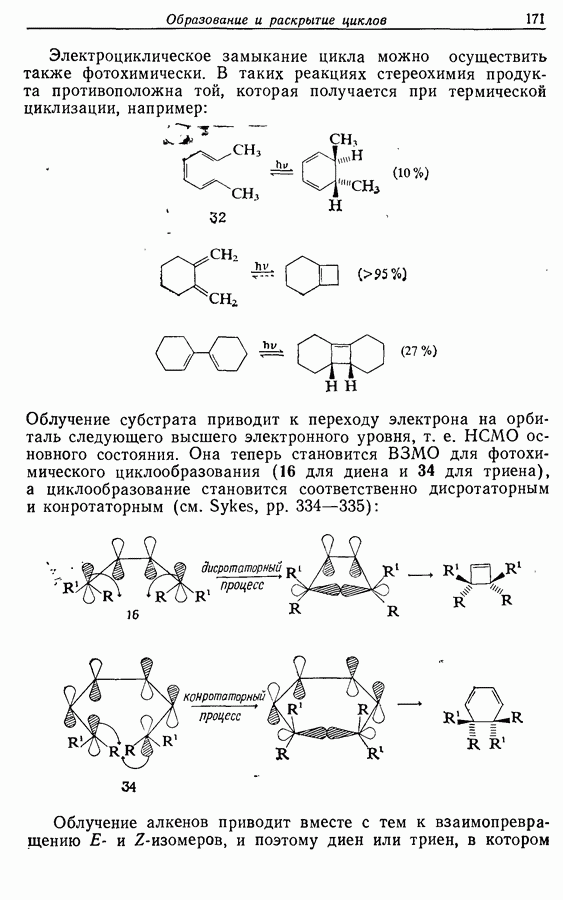
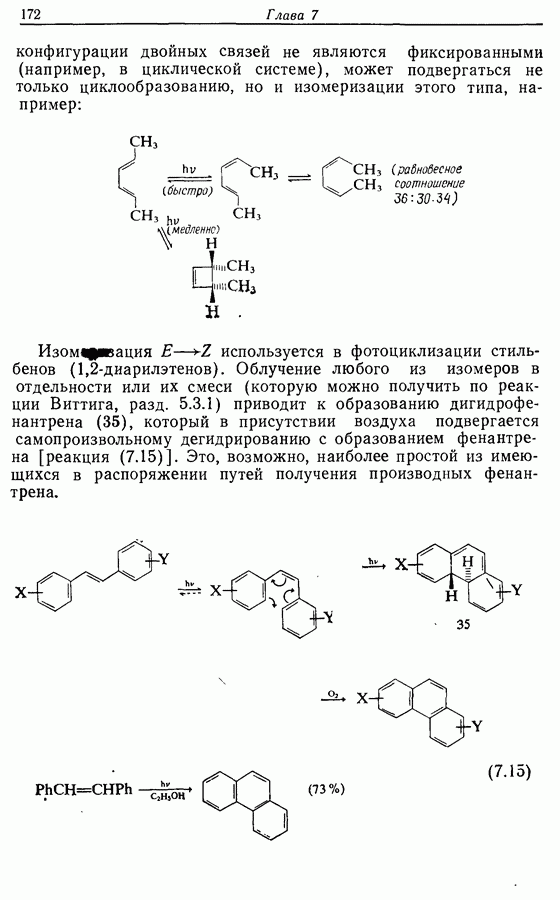
- 7.3. Электроциклическое циклообразование
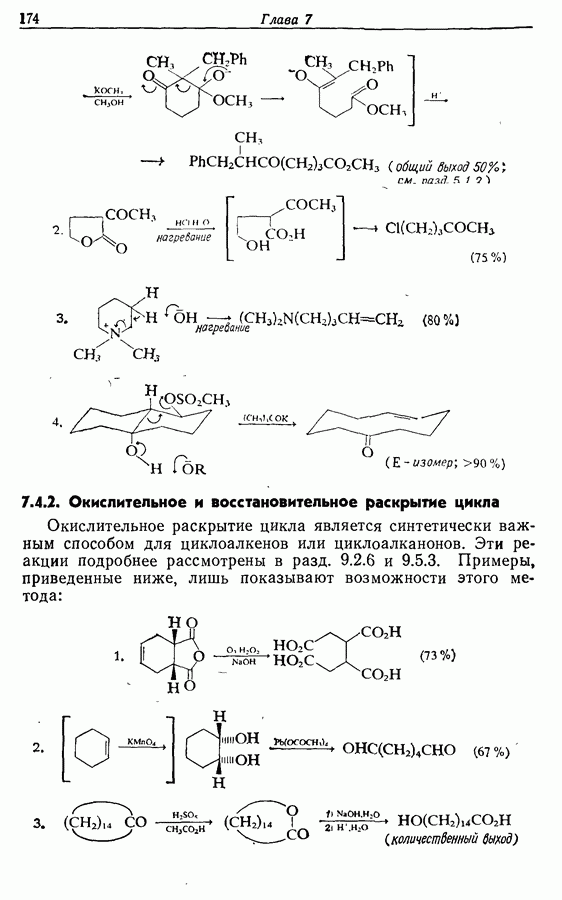
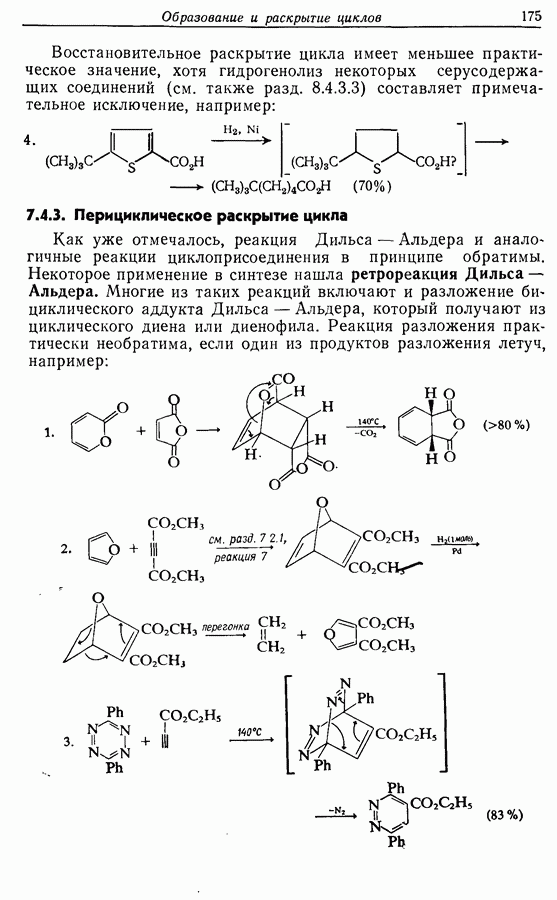
- 7.4. Раскрытие цикла
- 7.5. Выводы и задачи
- 8. ВОССТАНОВЛЕНИЕ
- 8.1. Каталитическое гидрирование
- 8.2. Восстановление гидридами металлов
- 8.3. Восстановление растворяющимися металлами
- 8.4. Восстановление определенных функциональных групп
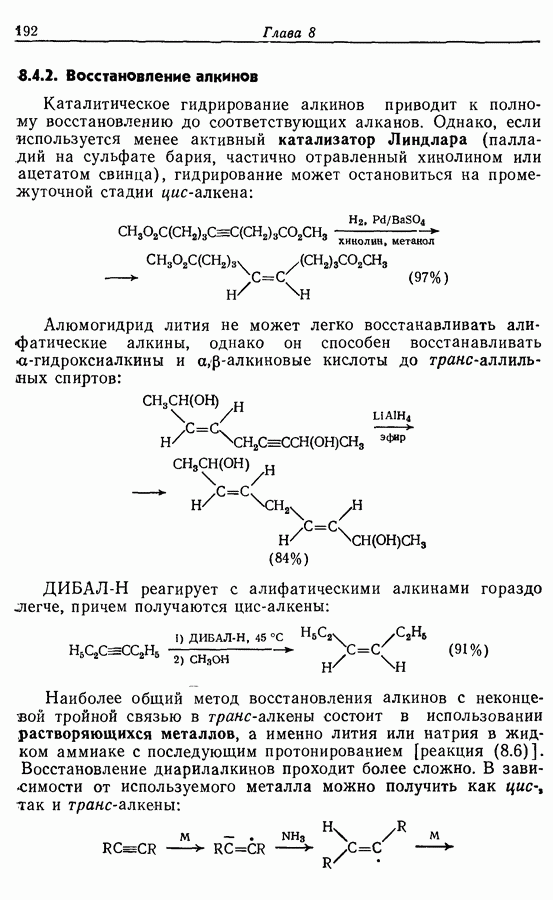
- 8.4.2. Восстановление алкинов
- 8.4.3. Восстановление альдегидов и кетонов
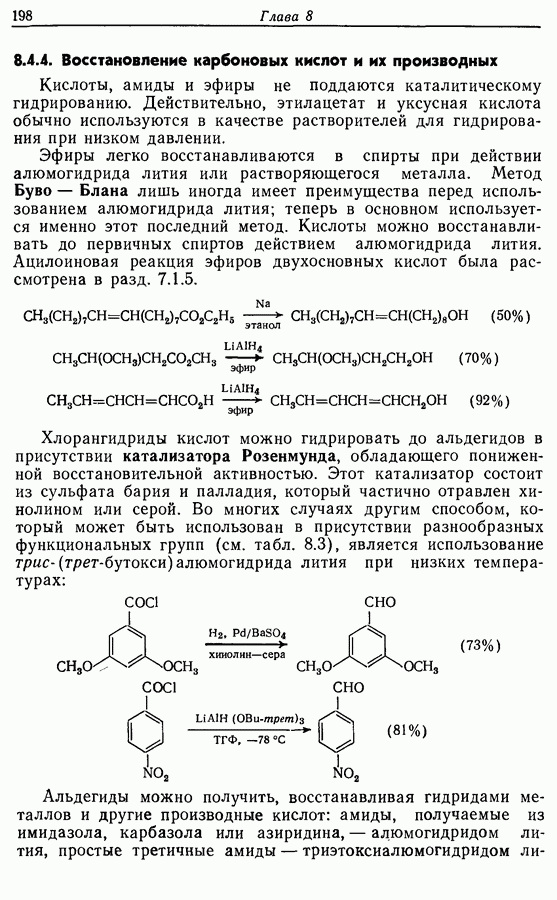
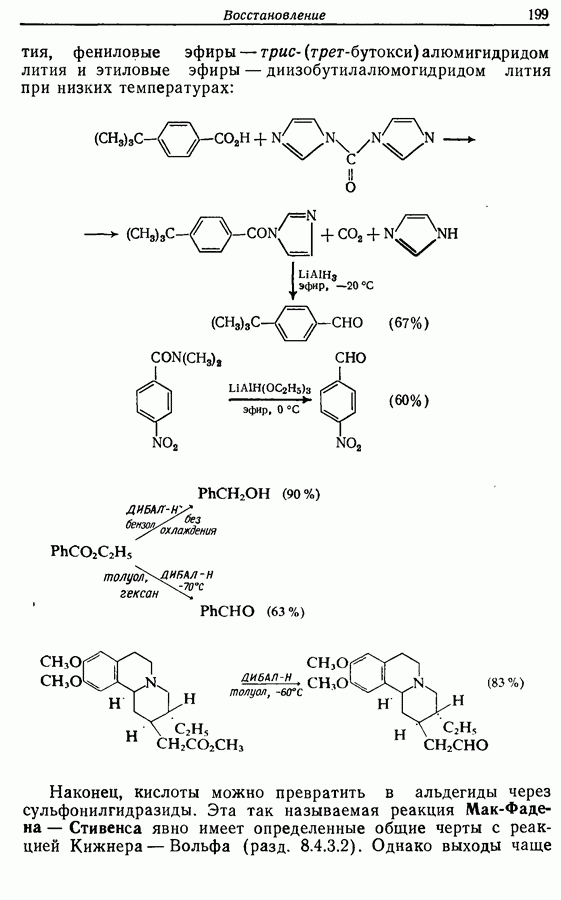
- 8.4.4. Восстановление карбоновых кислот и их производных
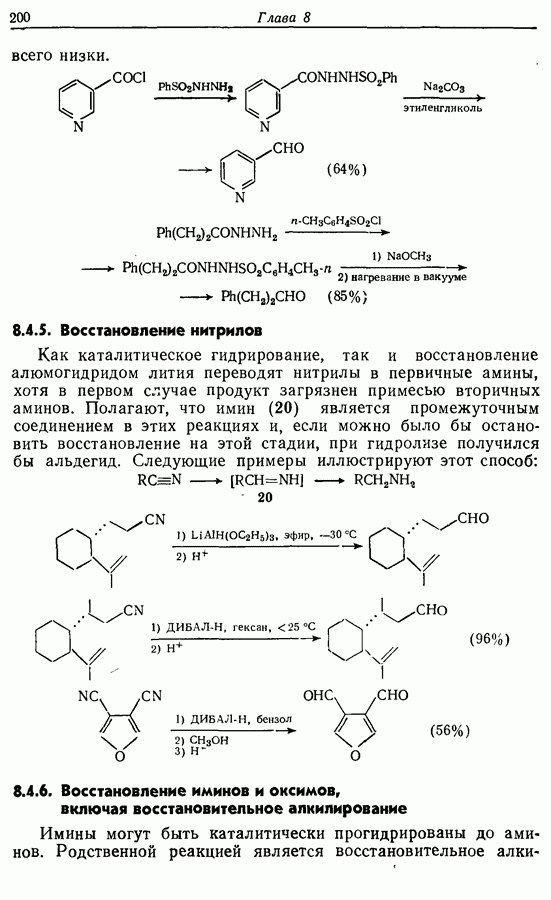
- 8.4.5. Восстановление нитрилов
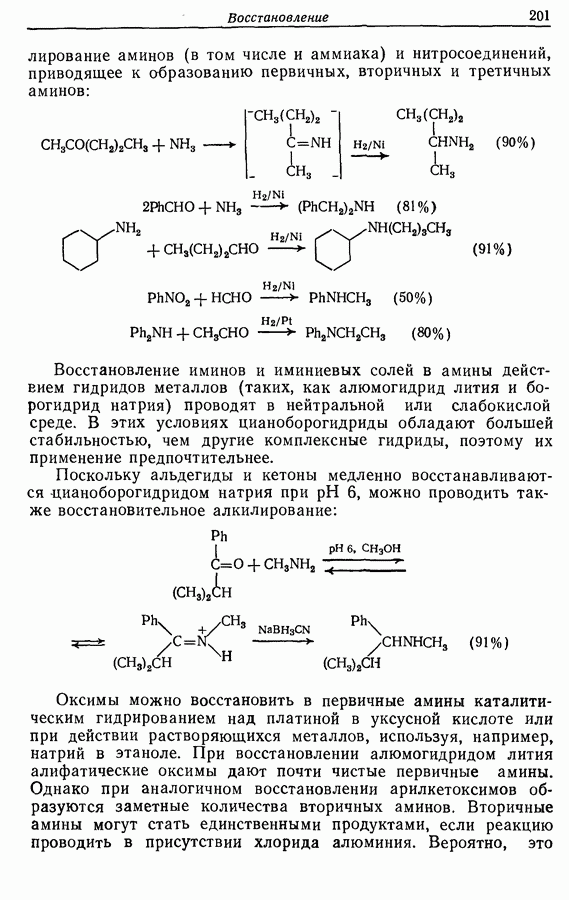
- 8.4.6. Восстановление иминов и оксимов, включая восстановительное алкилирование
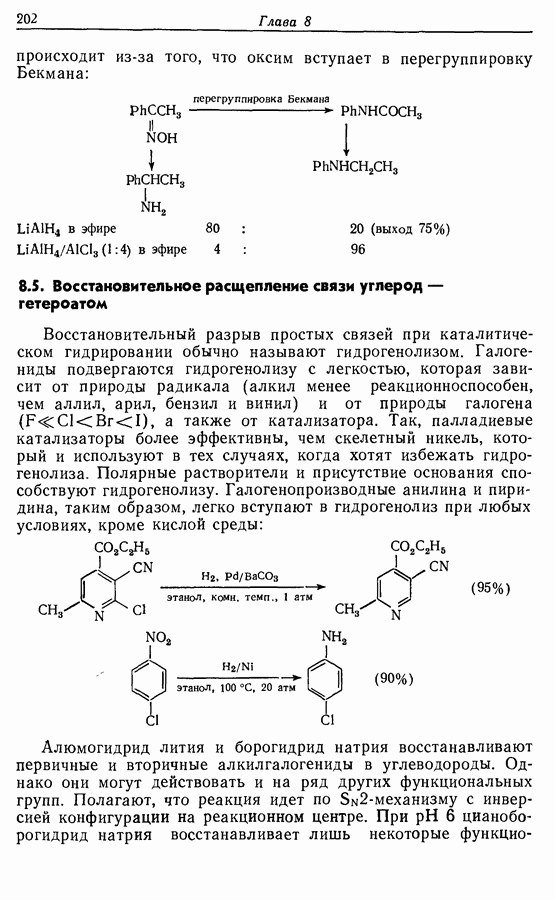
- 8.5. Восстановительное расщепление связи углерод — гетероатом
- 8.6. Восстановительное раскрытие цикла в эпоксидах
- 8.7. Восстановление a,b-ненасыщенных карбонильных соединений
- 8.8. Восстановление сопряженных диенов
- 8.9. Восстановление ароматических и гетероароматических соединений
- 9. ОКИСЛЕНИЕ
- 9.2. Окисление углеводородов
- 9.2.2. Аллильное окисление
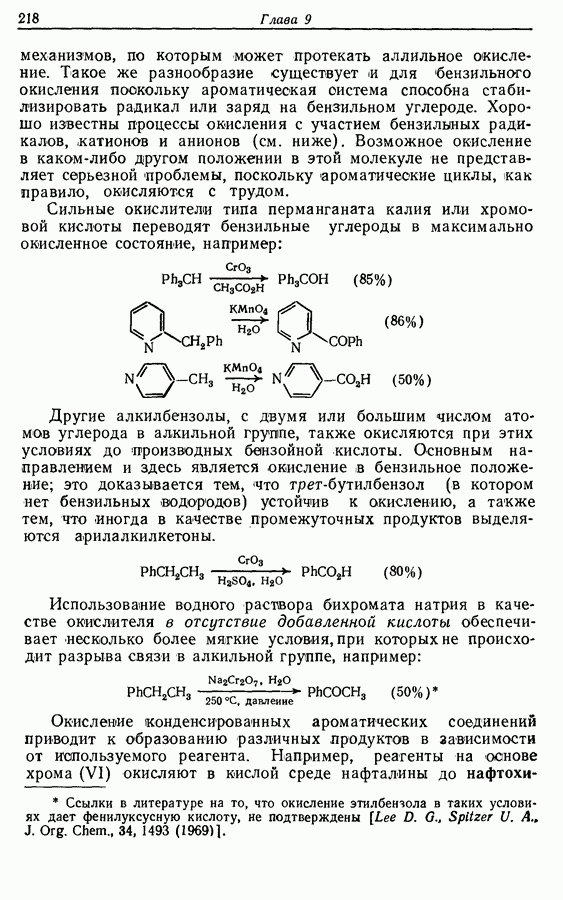
- 9.2.3. Бензильное окисление
- 9.2.4. Дегидрирование алканов, алкильных групп и алкенов
- 9.2.5. Окислительное присоединение к алкенам
- 9.2.6. Окислительная деструкция алкенов
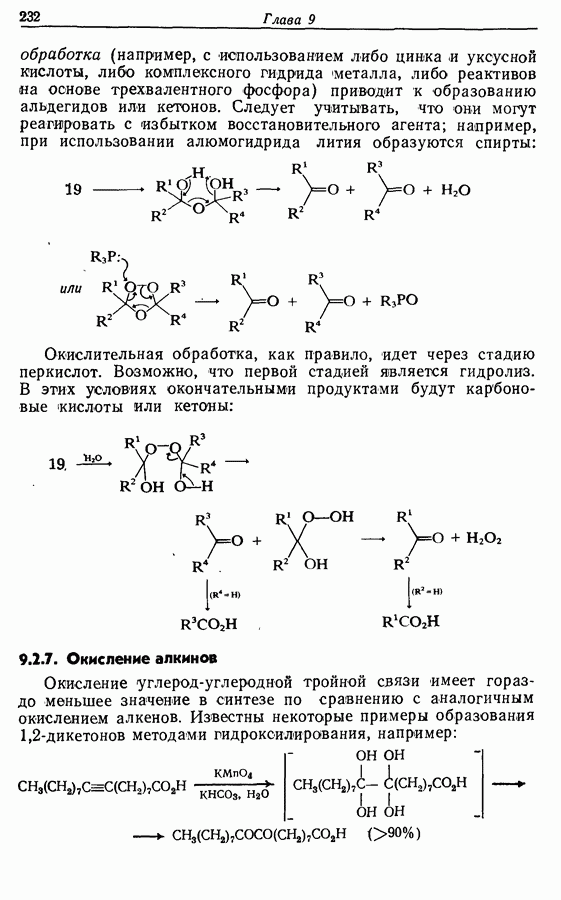
- 9.2.7. Окисление алкинов
- 9.3. Окисление спиртов и их производных
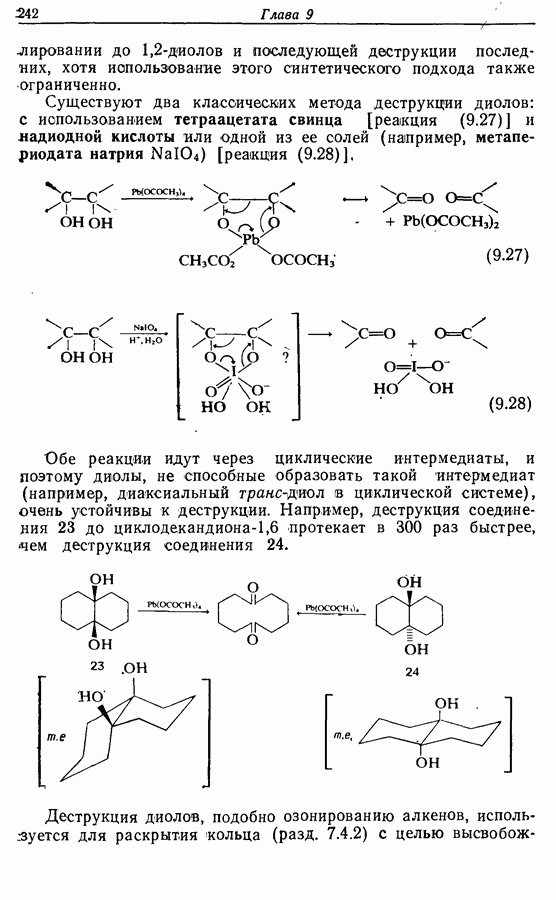
- 9.3.2. Окислительная деструкция 1,2-диолов
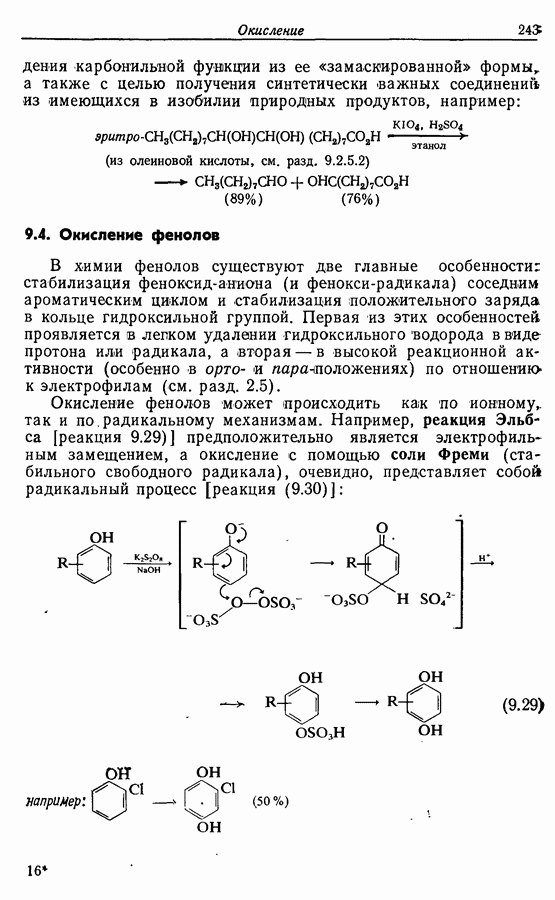
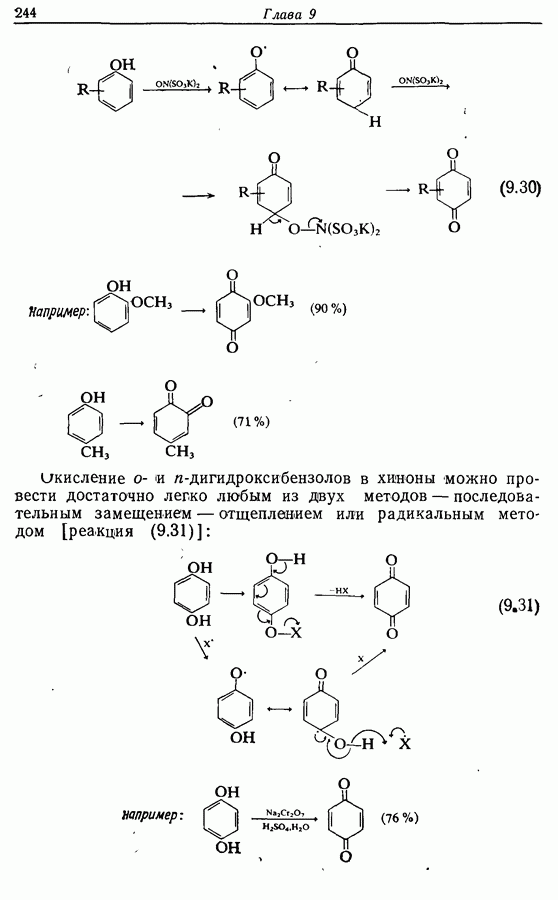
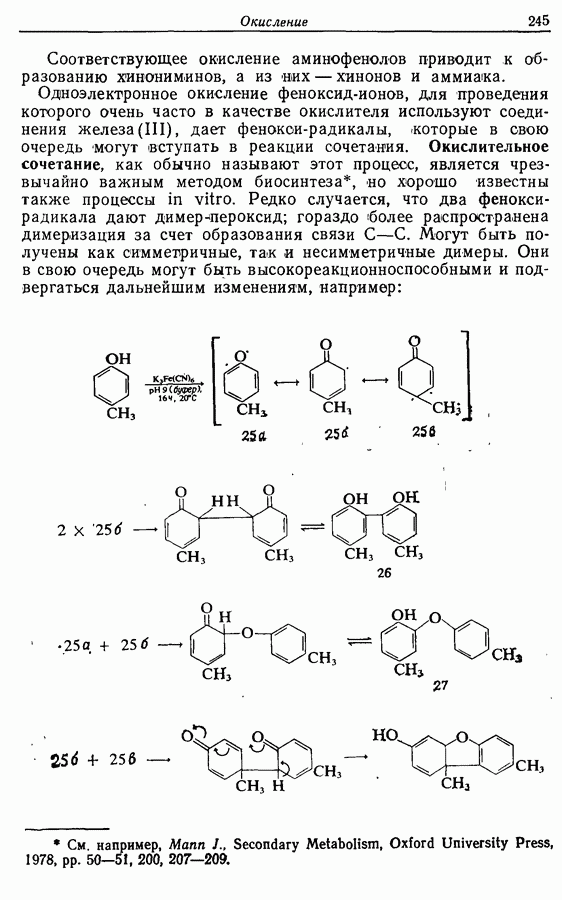
- 9.4. Окисление фенолов
- 9.5. Окисление альдегидов и кетонов
- 9.5.2. Окисление в 1,2-дикарбонильные соединения
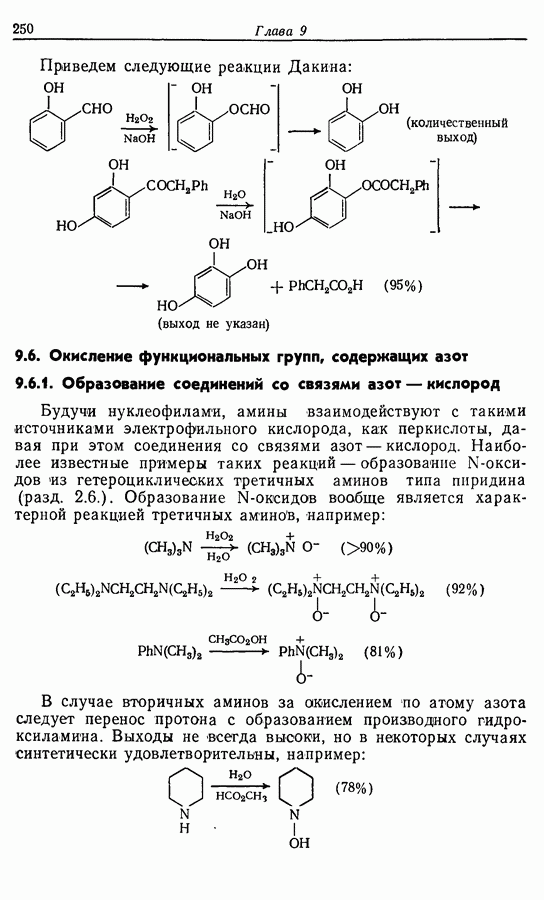
- 9.5.3. Окисление до сложных эфиров: реакции Байера — Виллигера и Дакина
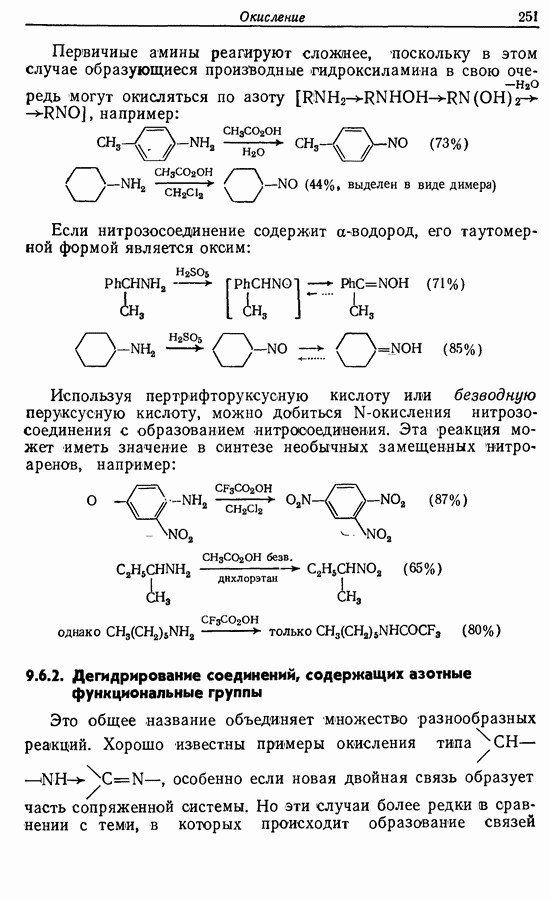
- 9.6. Окисление функциональных групп, содержащих азот
- 9.6.2. Дегидрирование соединений, содержащих азотные функциональные группы
- 9.7. Окисление серусодержащих функциональных групп
- 10. ЗАЩИТНЫЕ ГРУППЫ
- 10.2. Защита спиртов
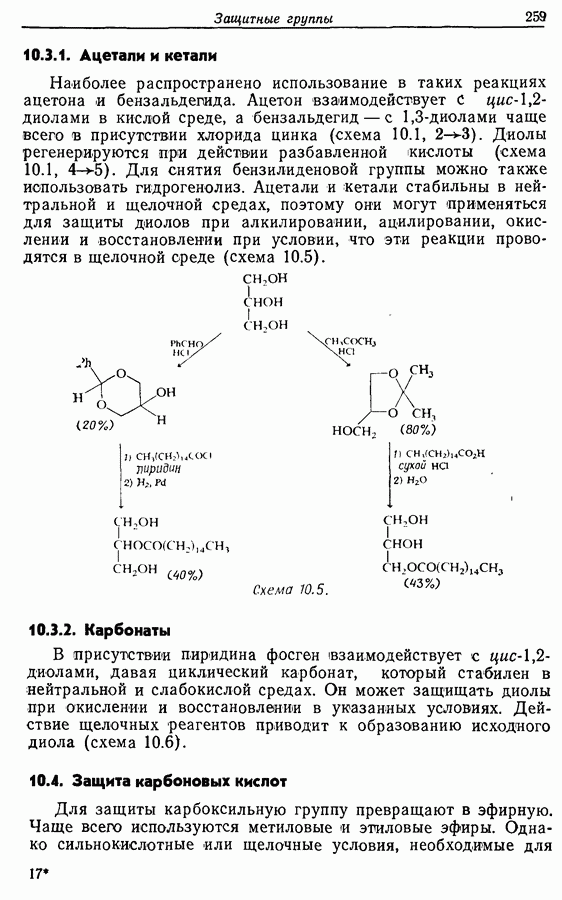
- 10.3. Защита диолов
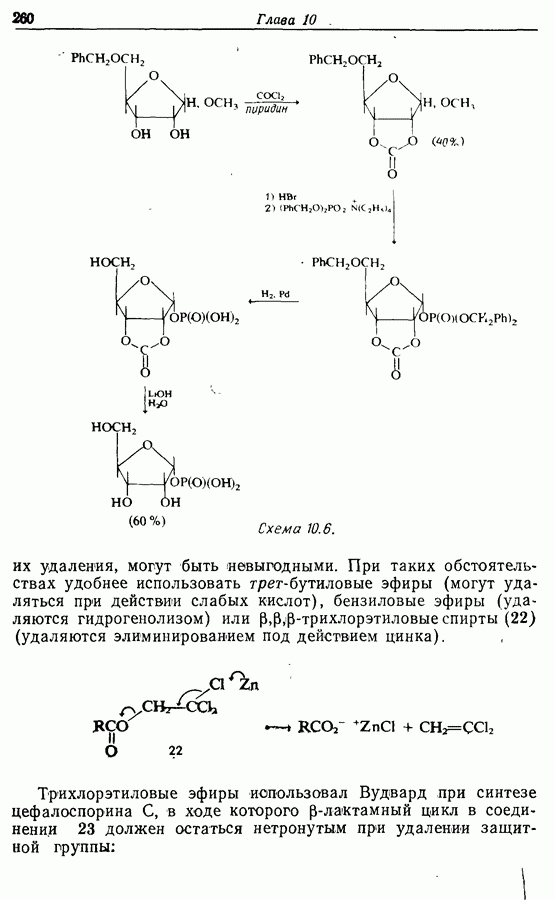
- 10.4. Защита карбоновых кислот
- 10.5. Защита аминогрупп
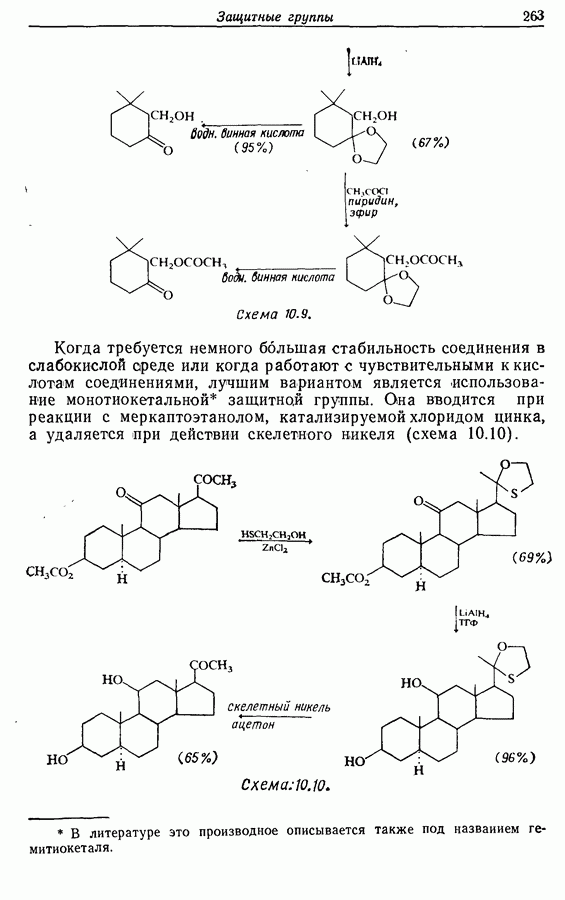
- 10.6. Защита карбонильных групп
- 11. БОРСОДЕРЖАЩИЕ РЕАГЕНТЫ
- 11.1. Гидроборирование алкенов при действии борана
- 11.2. Гидроборирование алкенов действием алкилборанов
- 11.3. Реакции борорганических соединений
- 11.4. Гидроборирование диенов
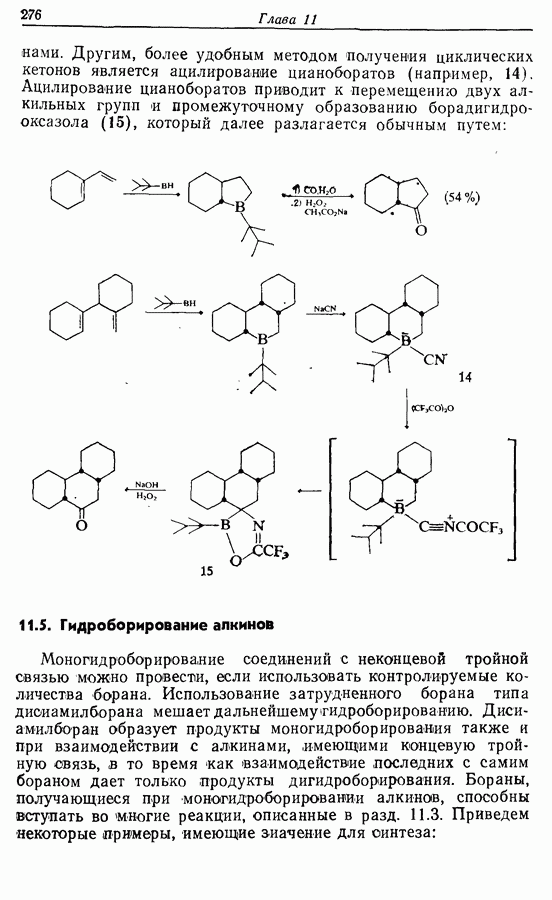
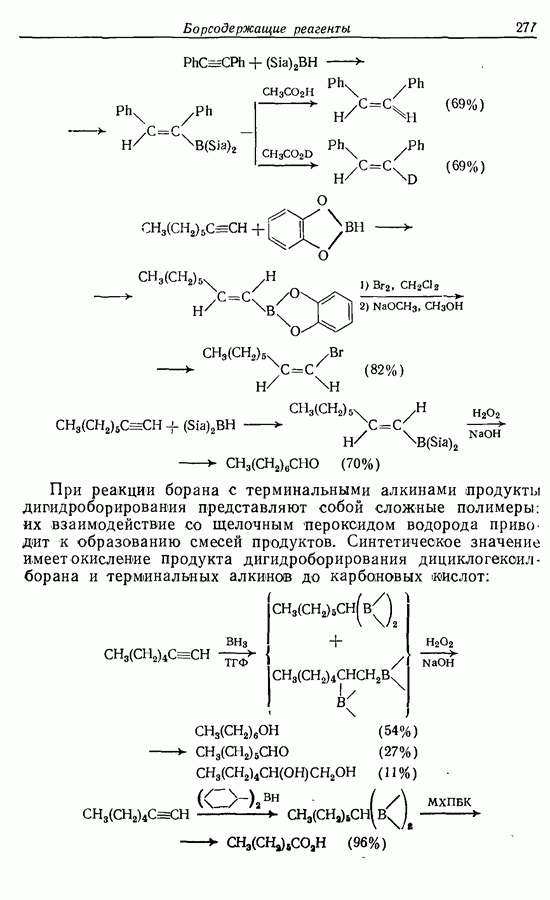
- 11.5. Гидроборирование алкинов
- 12. ФОСФОРСОДЕРЖАЩИЕ РЕАГЕНТЫ
- 12.1. Введение в химию фосфорорганических соединений
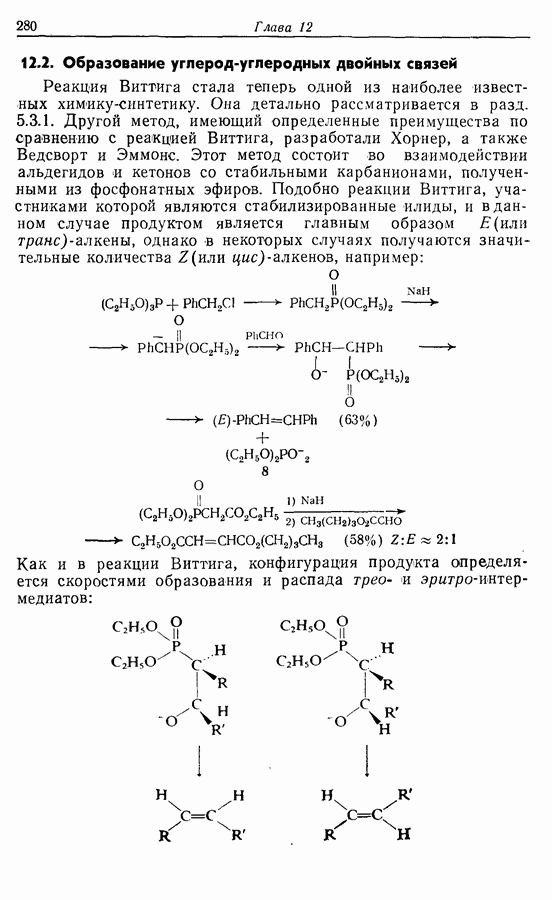
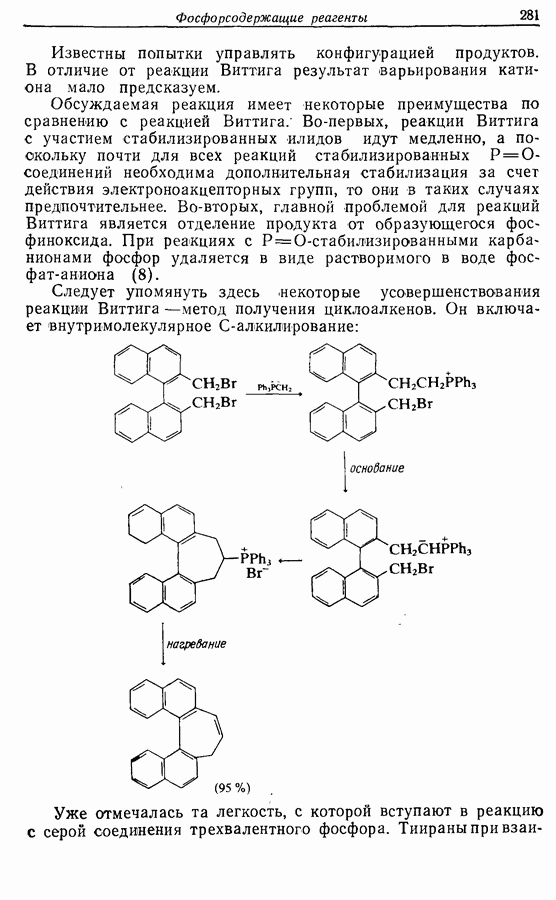
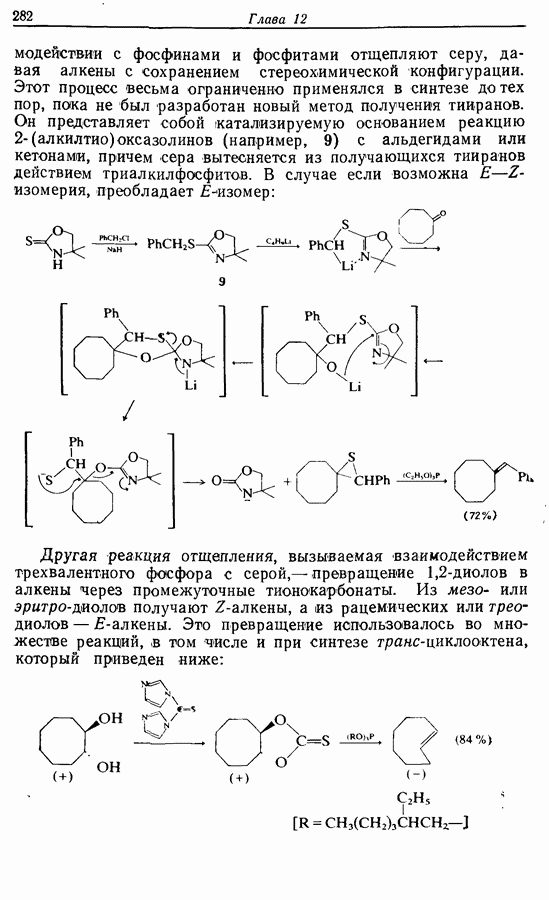
- 12.2. Образование углерод-углеродных двойных связей
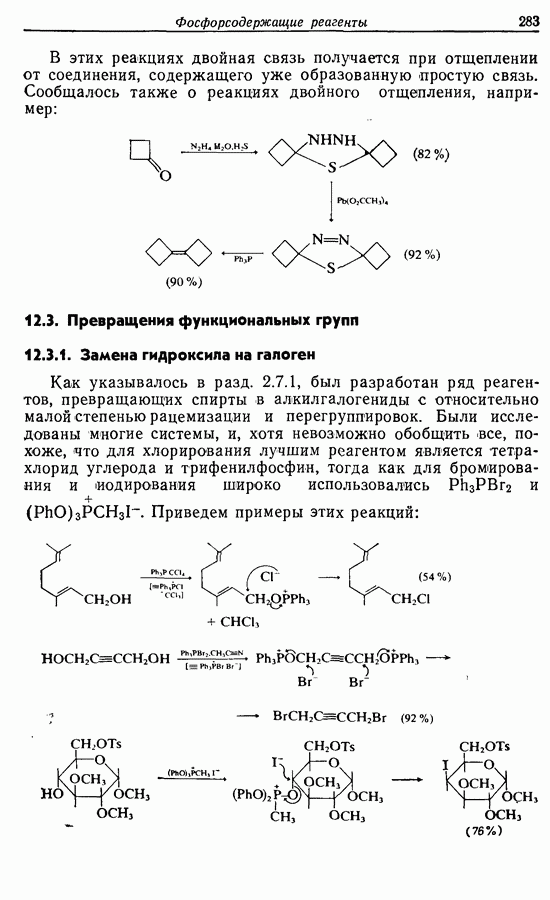
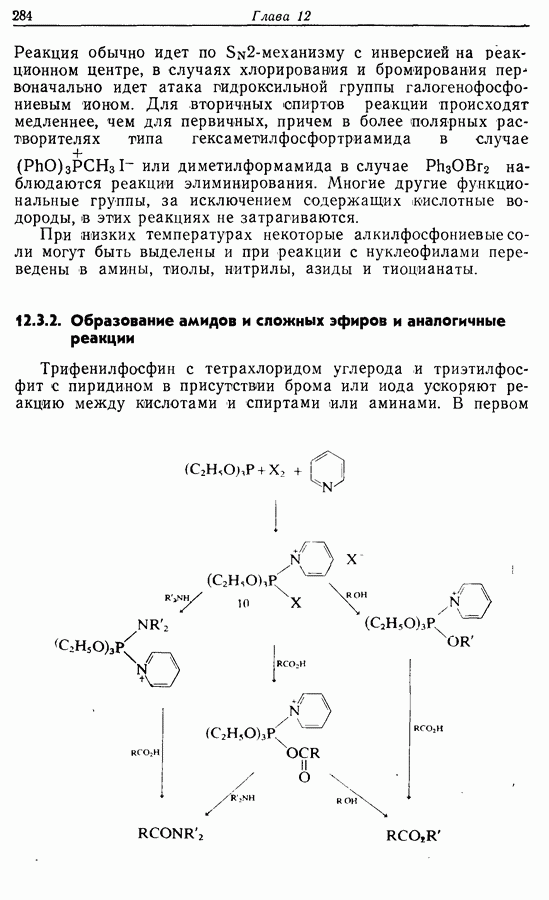
- 12.3. Превращения функциональных групп
- 12.4. Реакции дезоксигенирования
- 13. КРЕМНИЙСОДЕРЖАЩИЕ РЕАГЕНТЫ
- 13.1. Введение в химию кремнийорганических соединений
- 13.2. Синтез кремнийорганических соединений
- 13.3. Реакции с образованием углерод-углеродных связей
- 13.4. Синильная защита спиртов
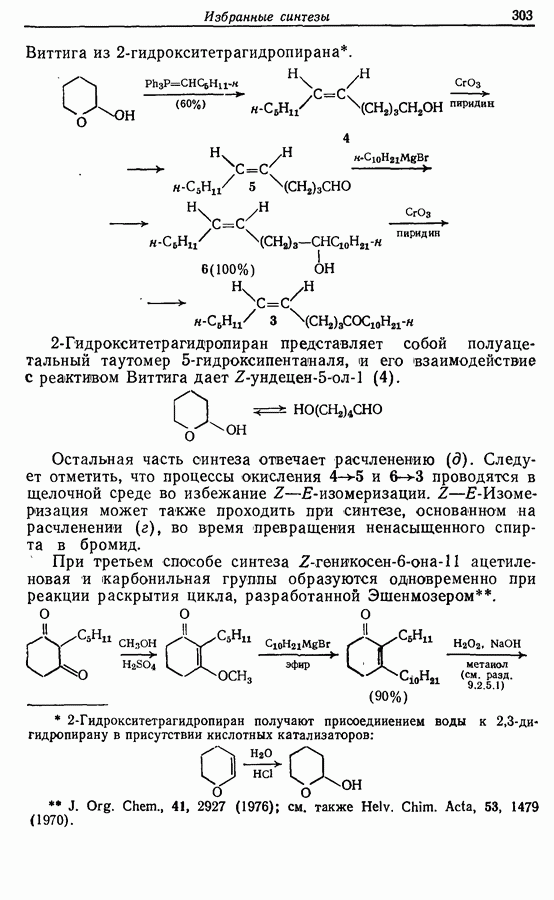
- 14. ИЗБРАННЫЕ СИНТЕЗЫ
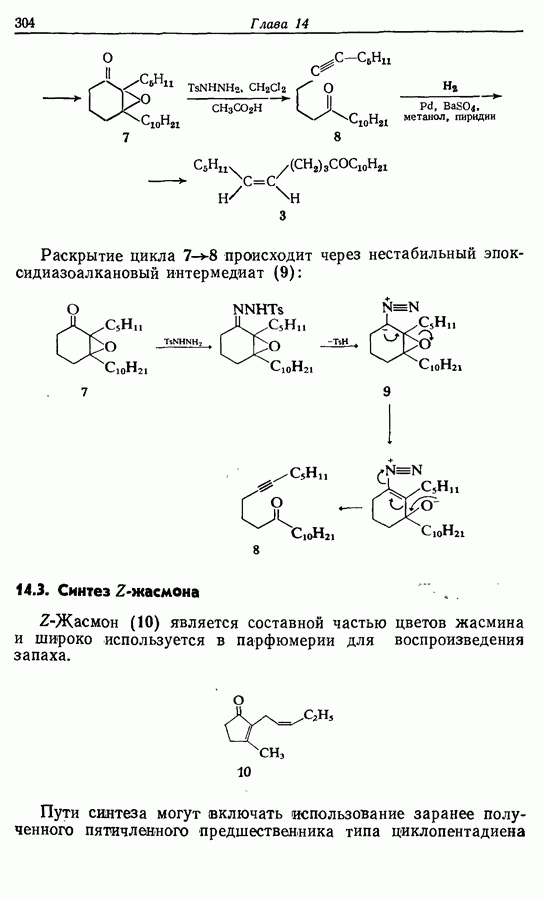
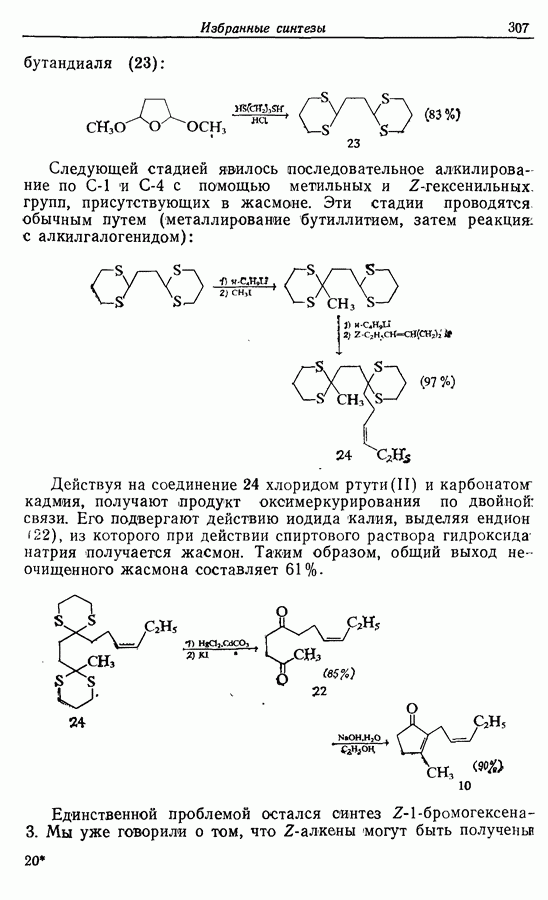
- 14.2. Z-Геникосен-6-он-11
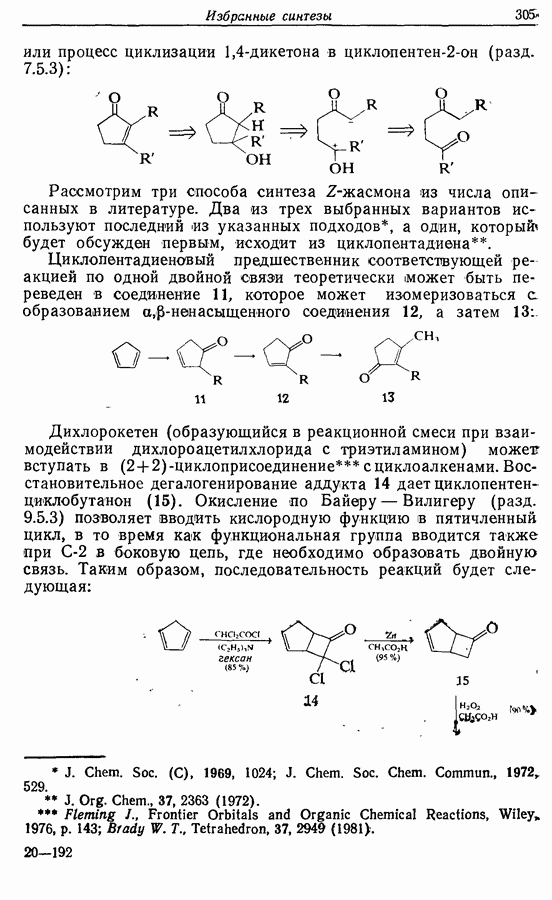
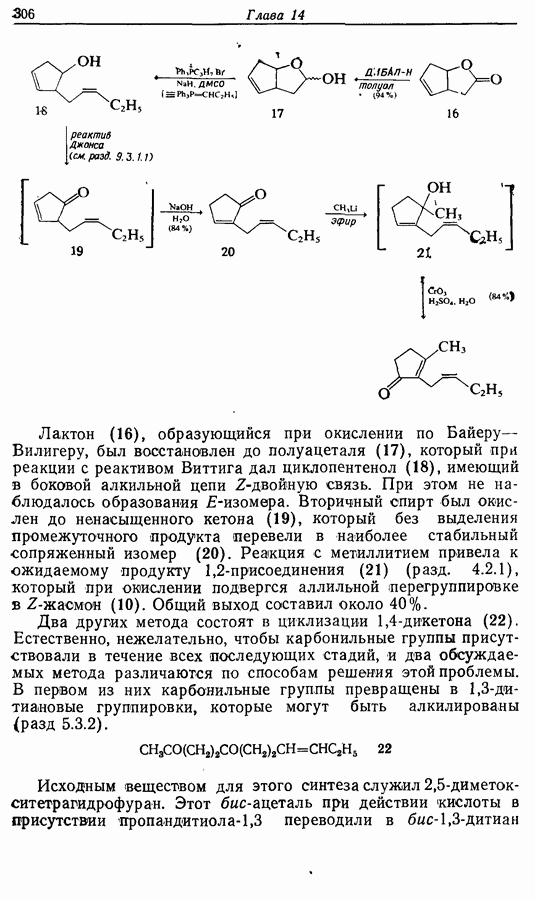
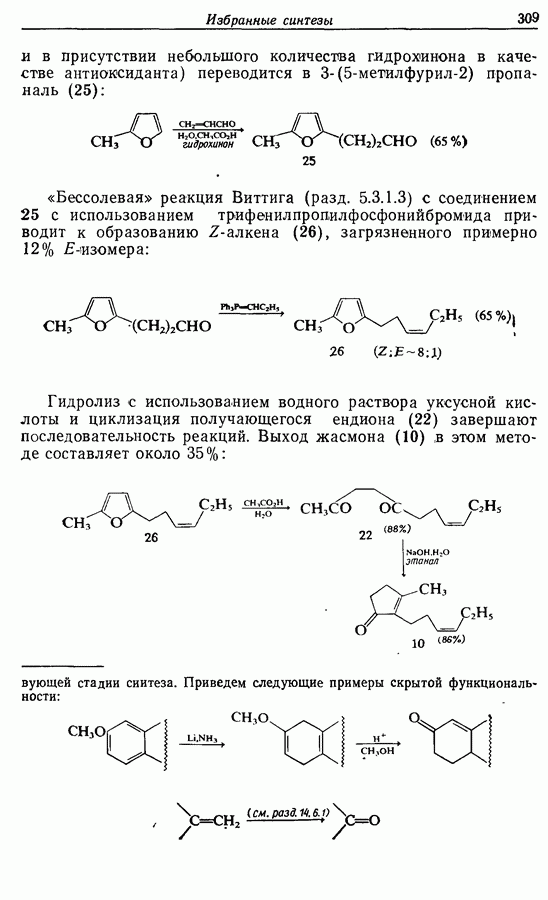
- 14.3. Синтез Z-жасмона
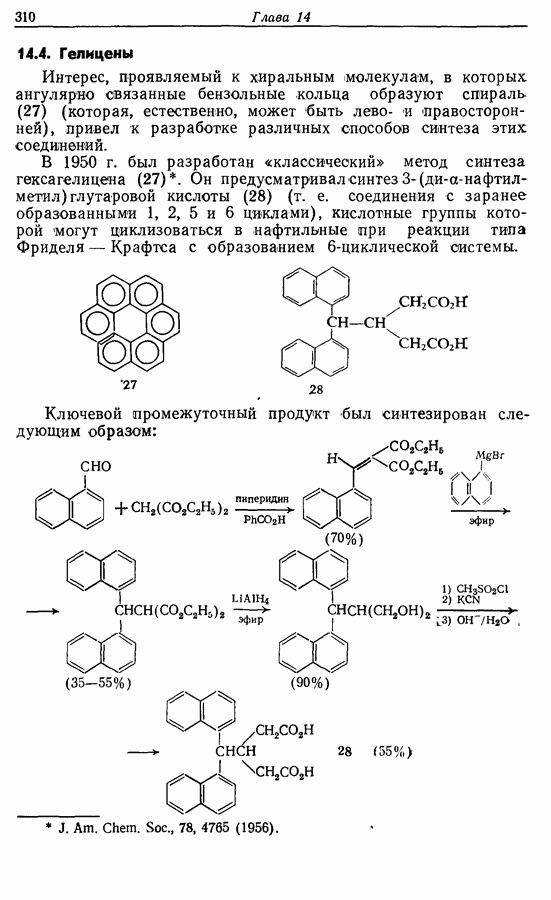
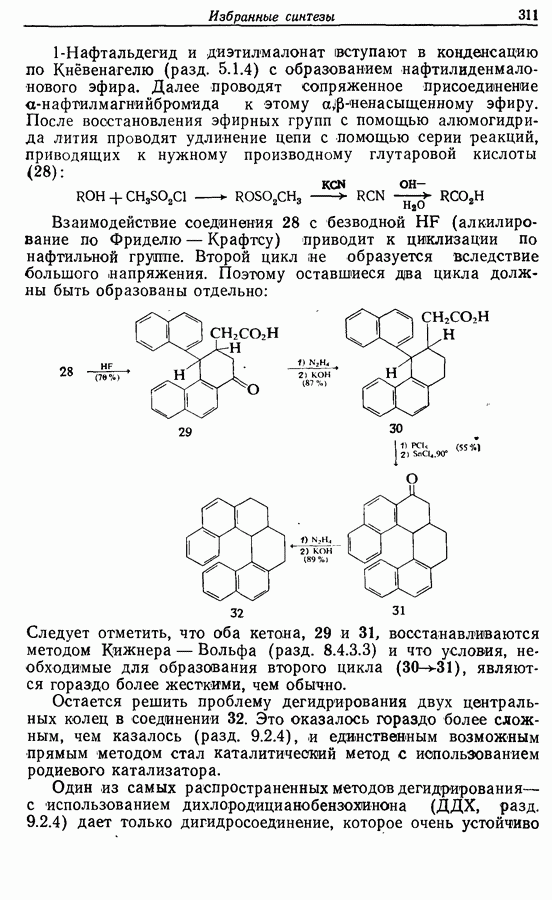
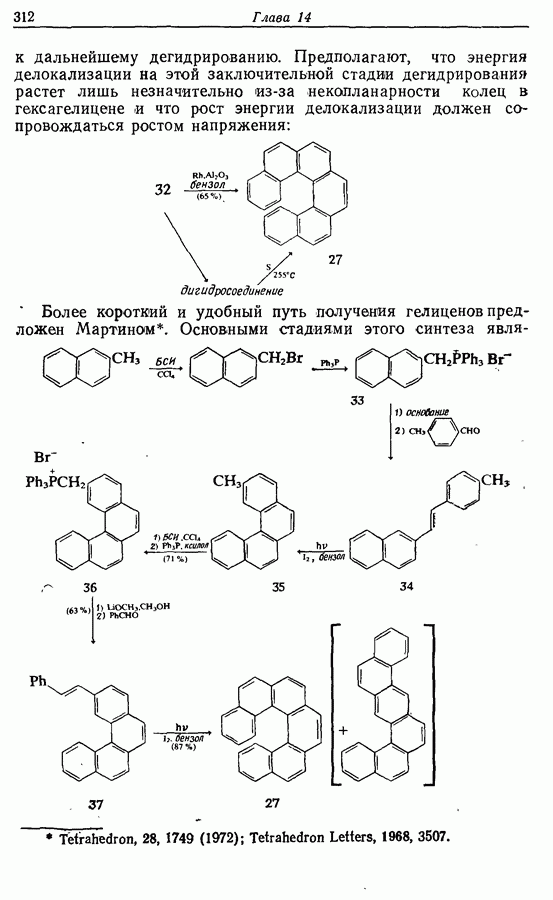
- 14.4. Гелицены
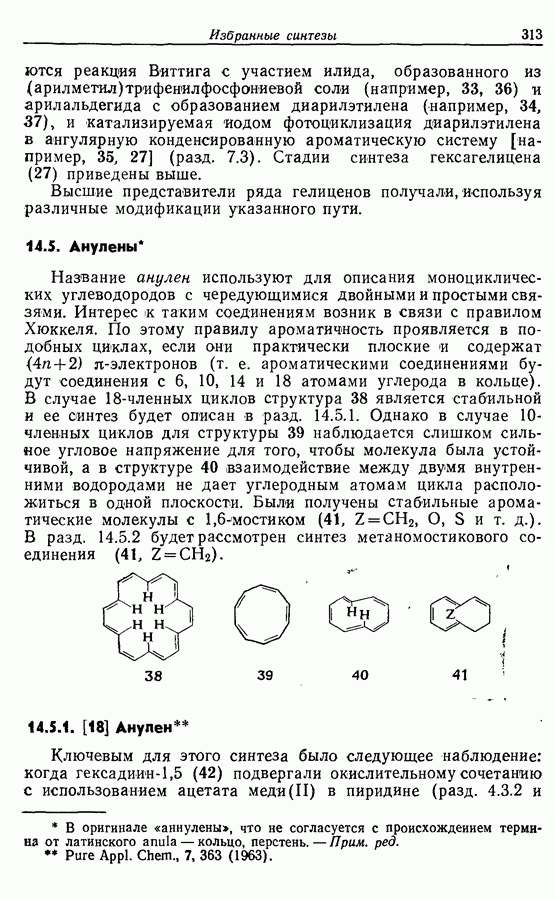
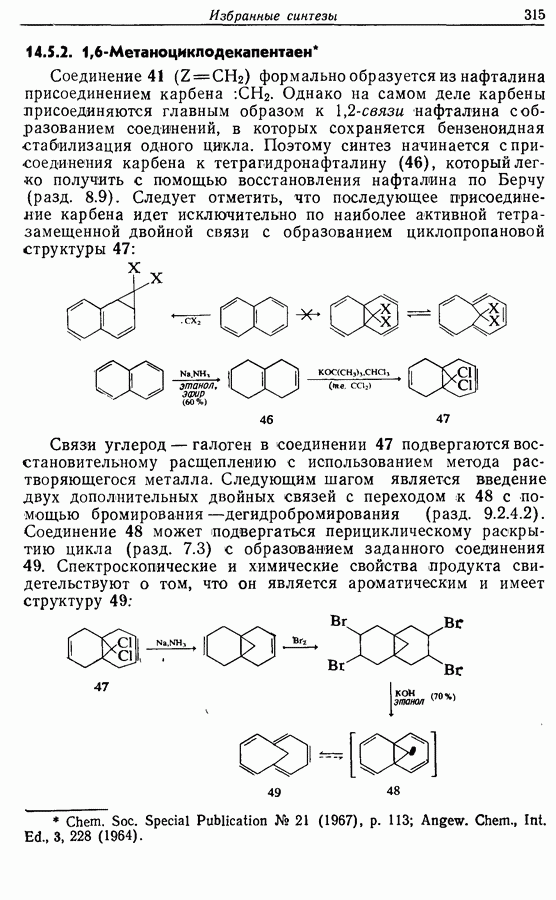
- 14.5. Анулены
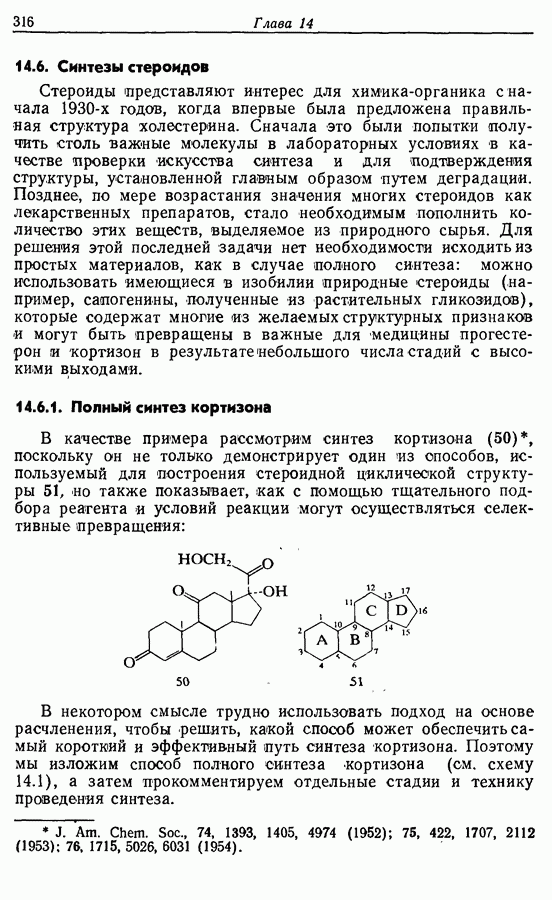
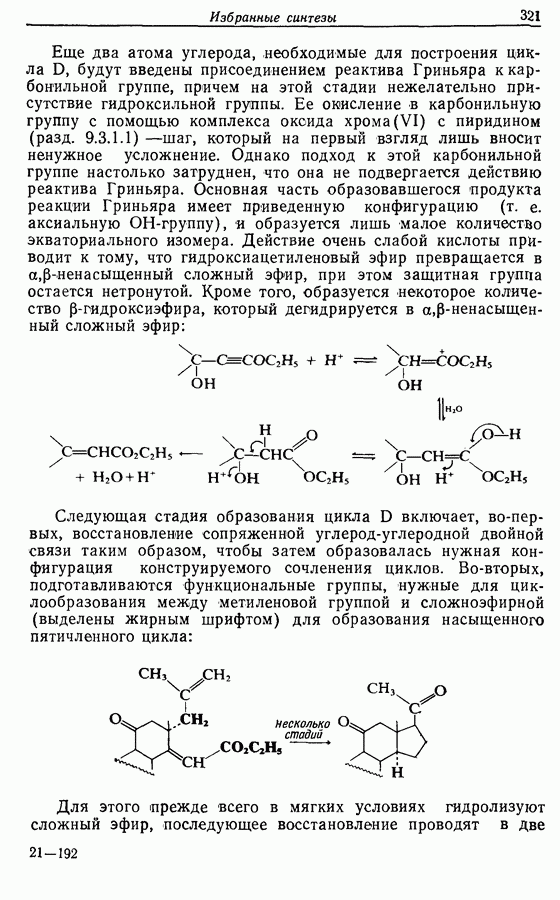
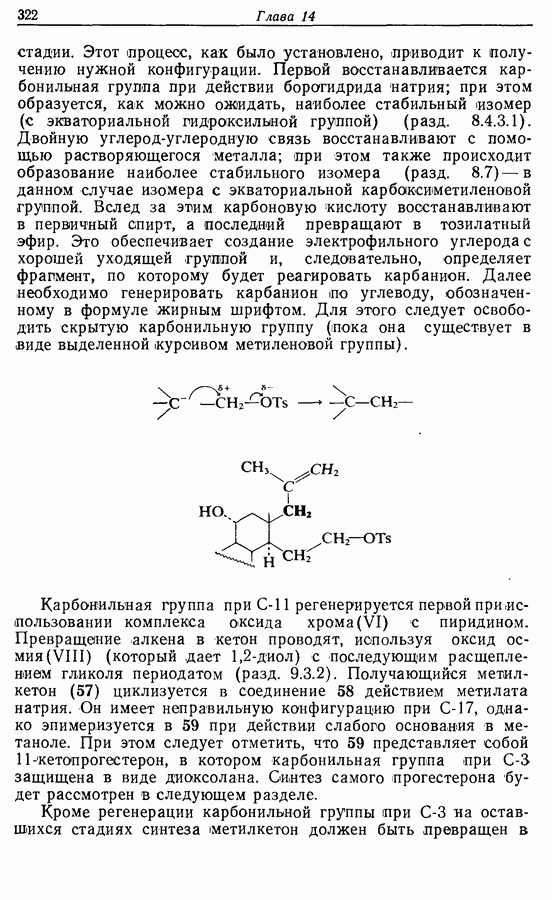
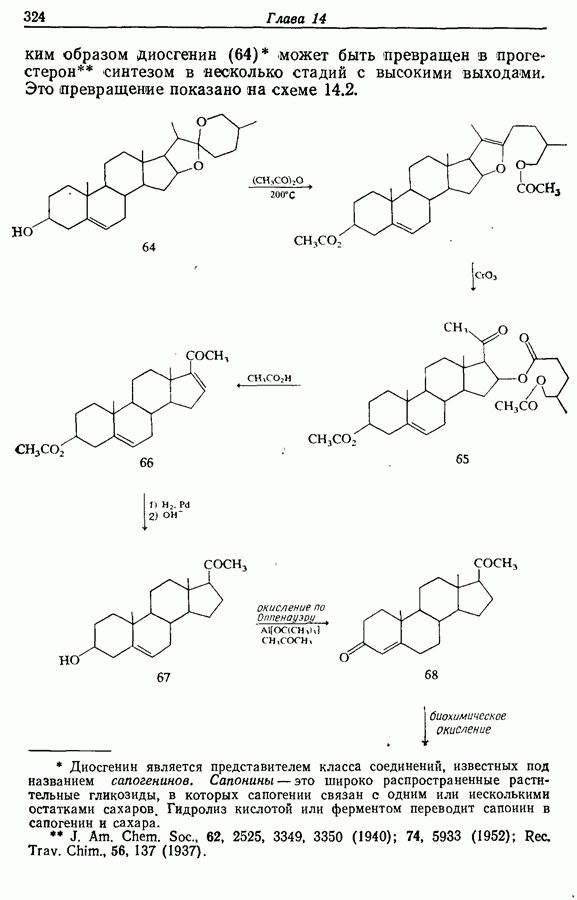
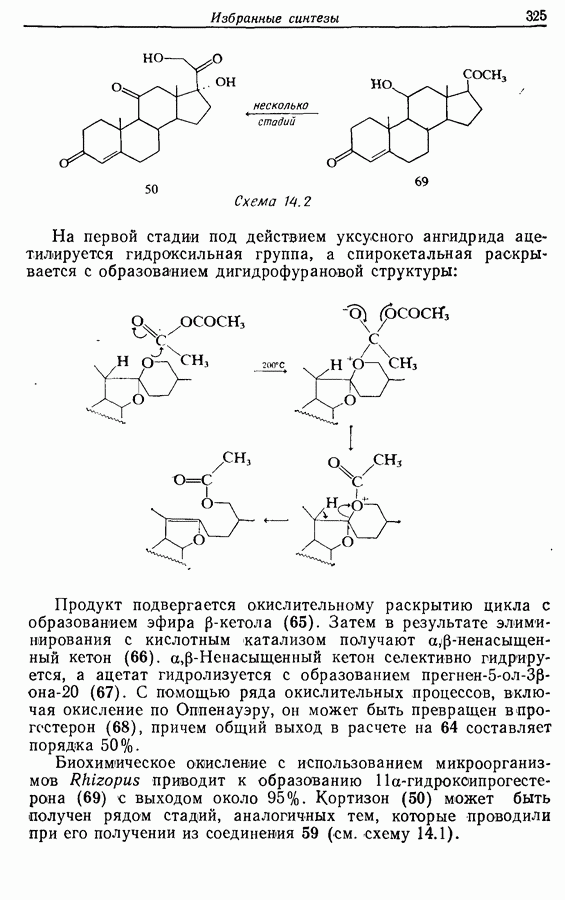
- 14.6. Синтезы стероидов
- 14.6.2. Превращение растительных стероидов в стероидные гормоны
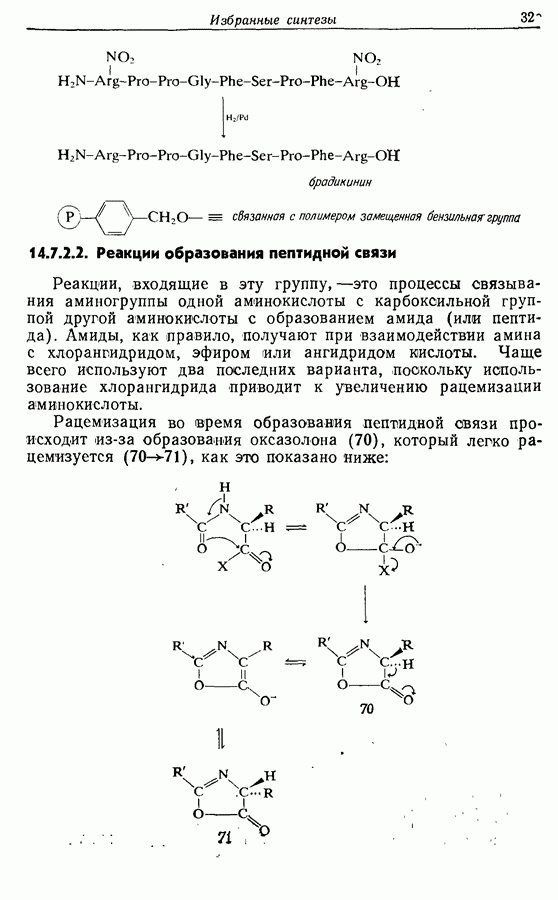
- 14.7. Синтез пептидов
- 14.7.2. Техника синтеза пептидов
- ЛИТЕРАТУРА