| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
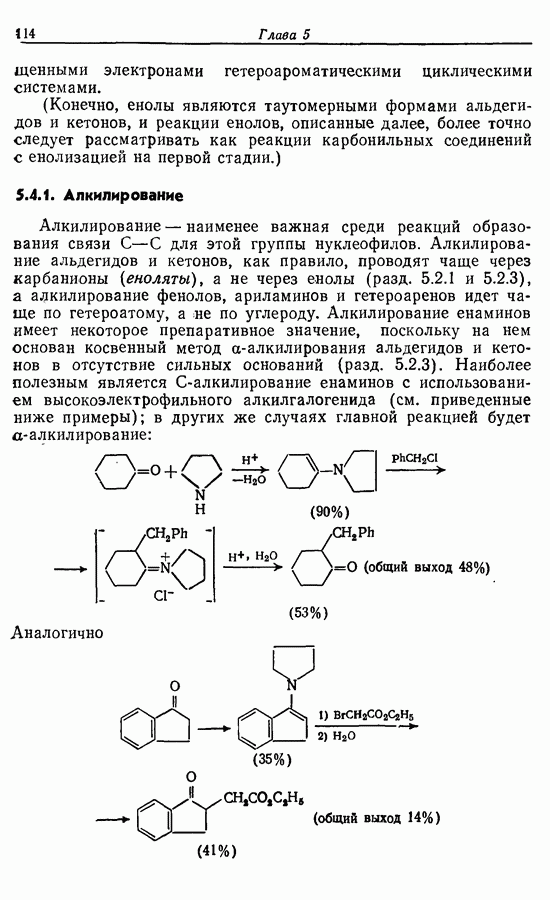
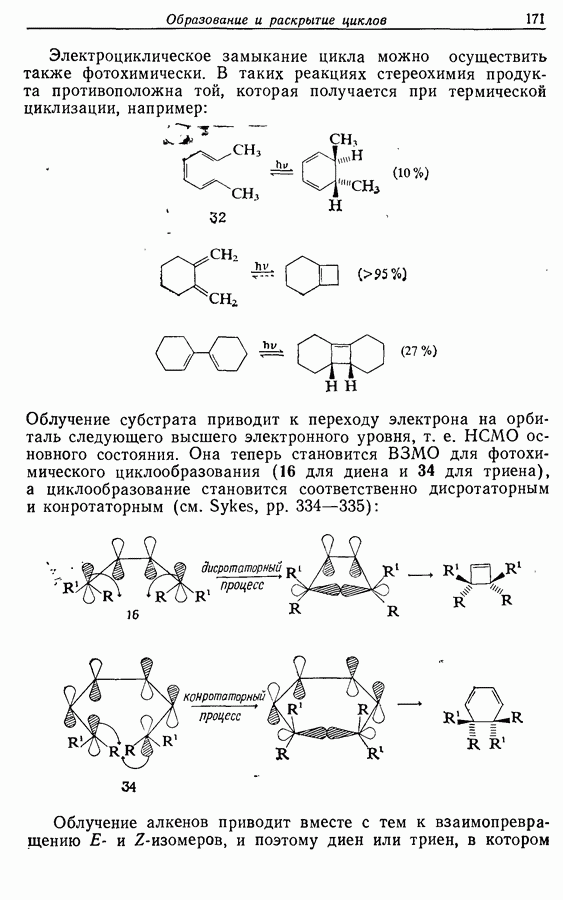
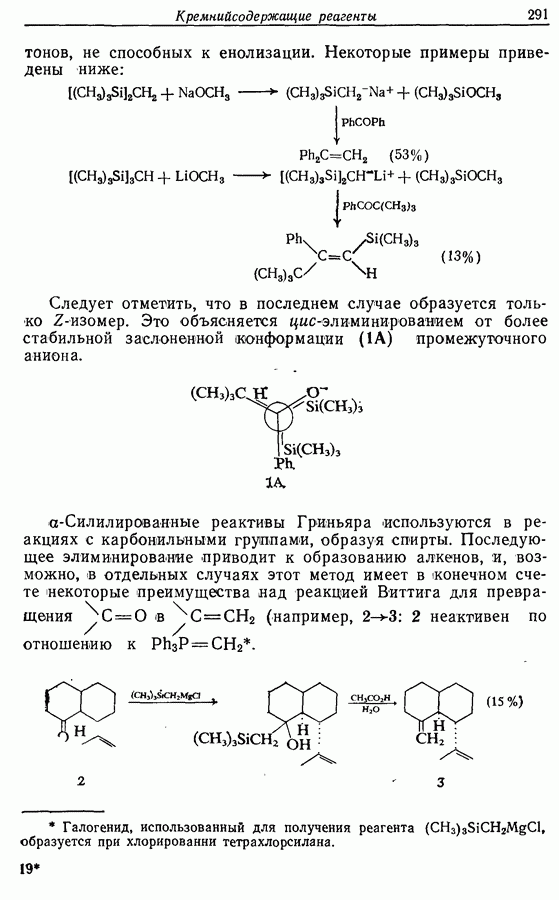
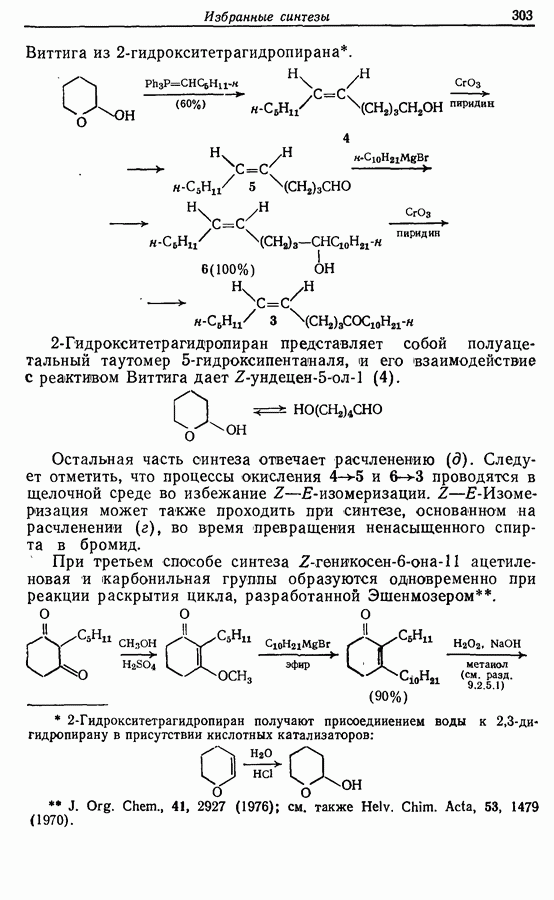
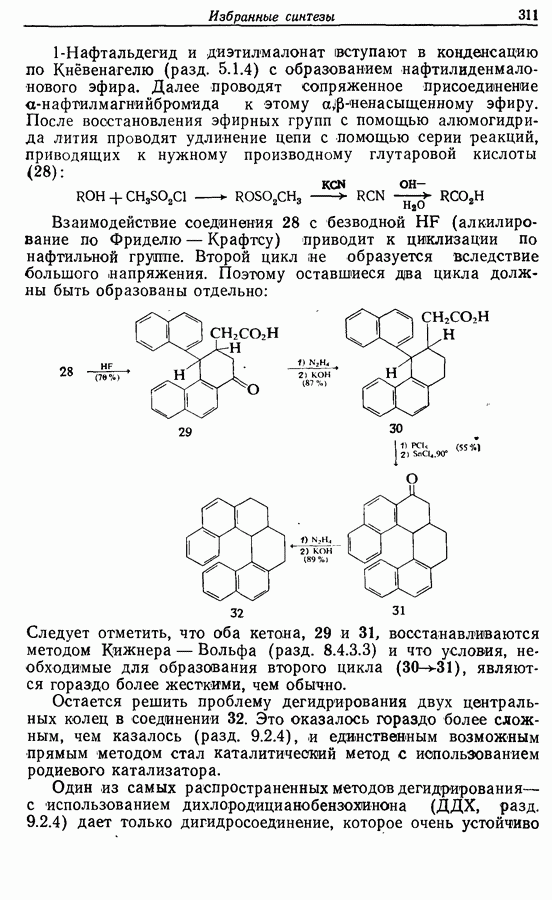
14.3. Синтез Z-жасмона
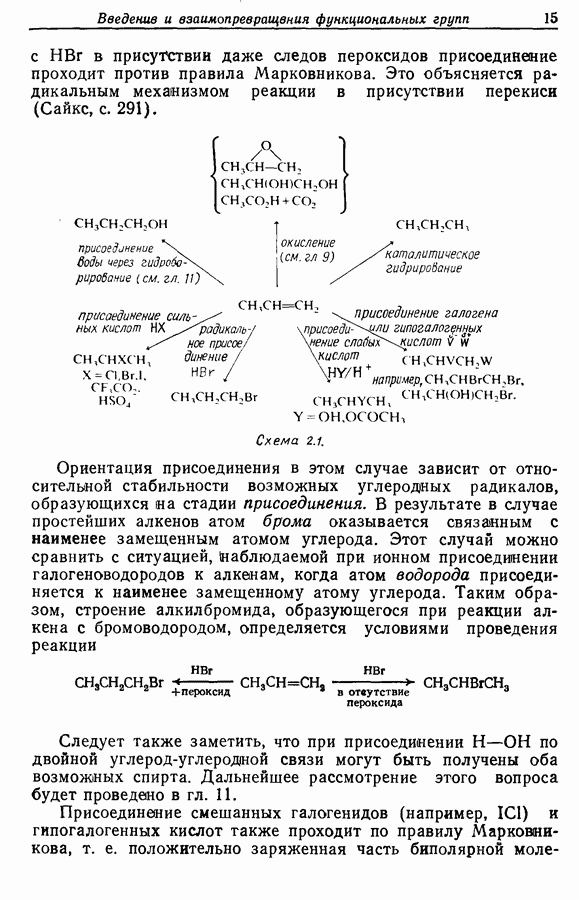
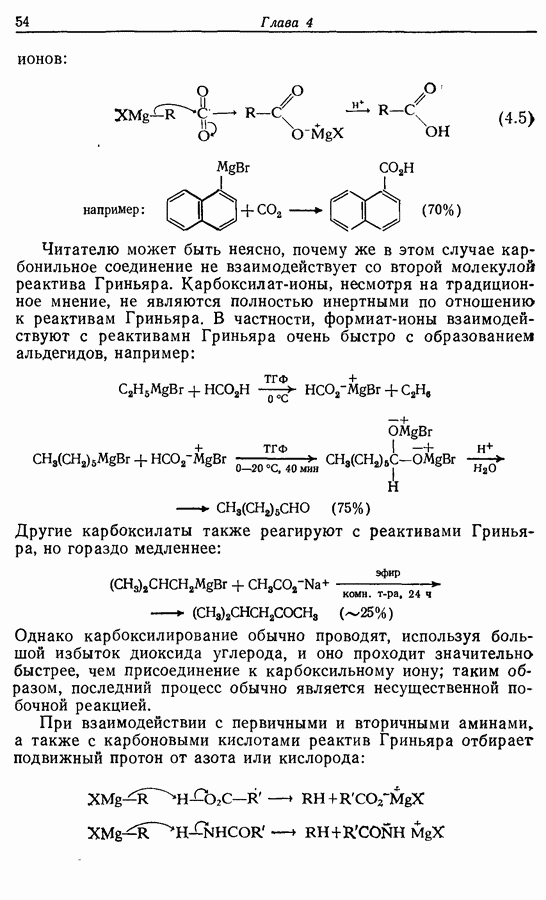
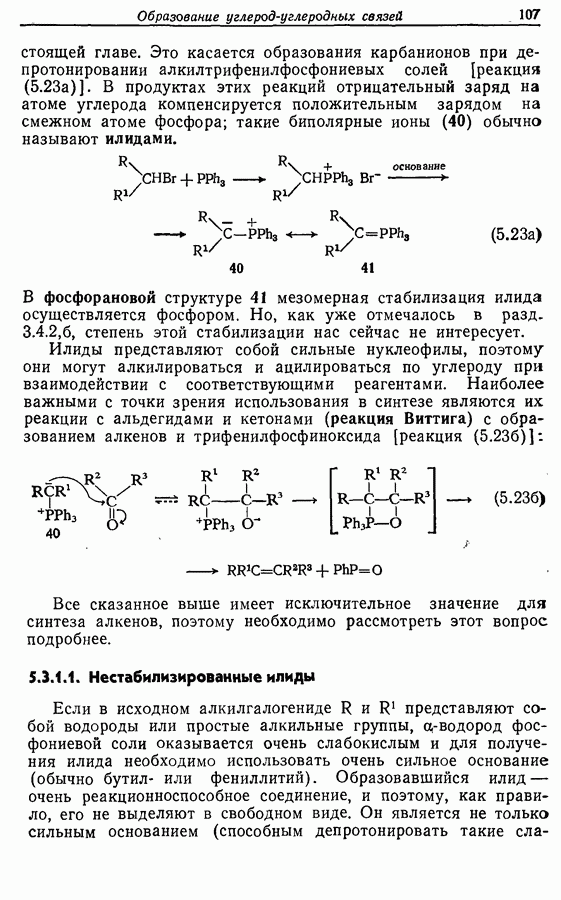
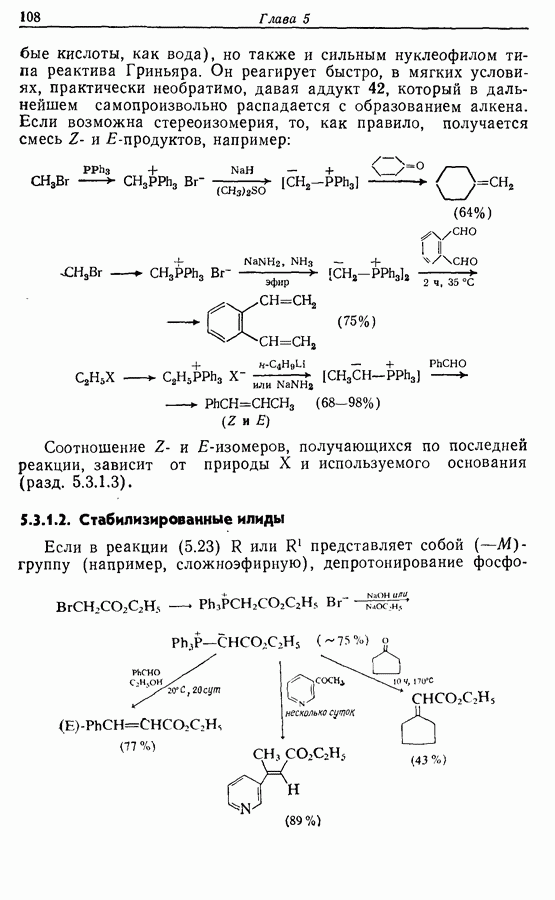
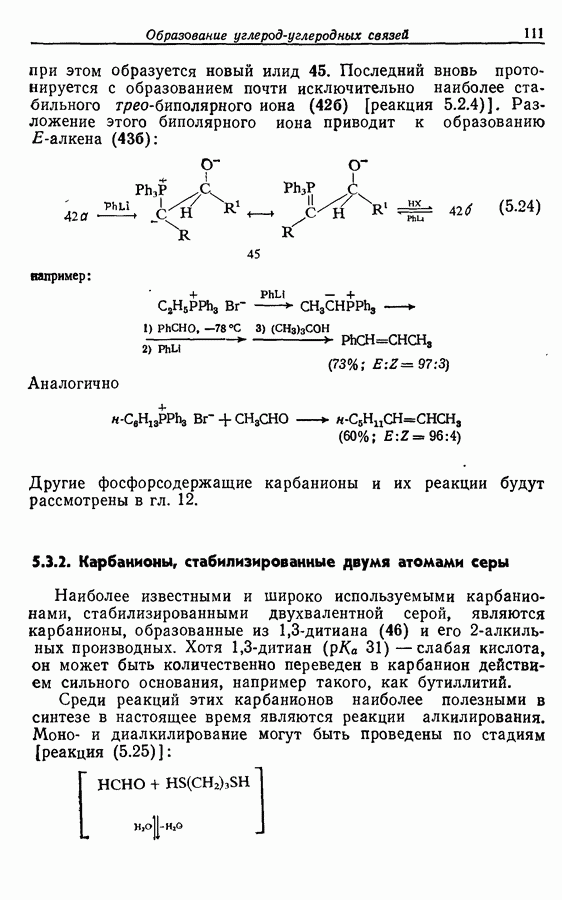
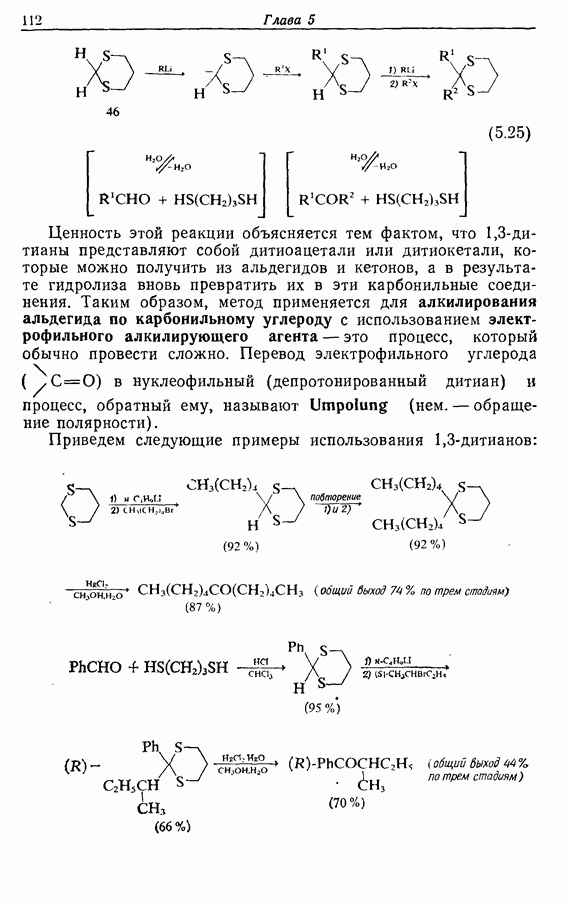
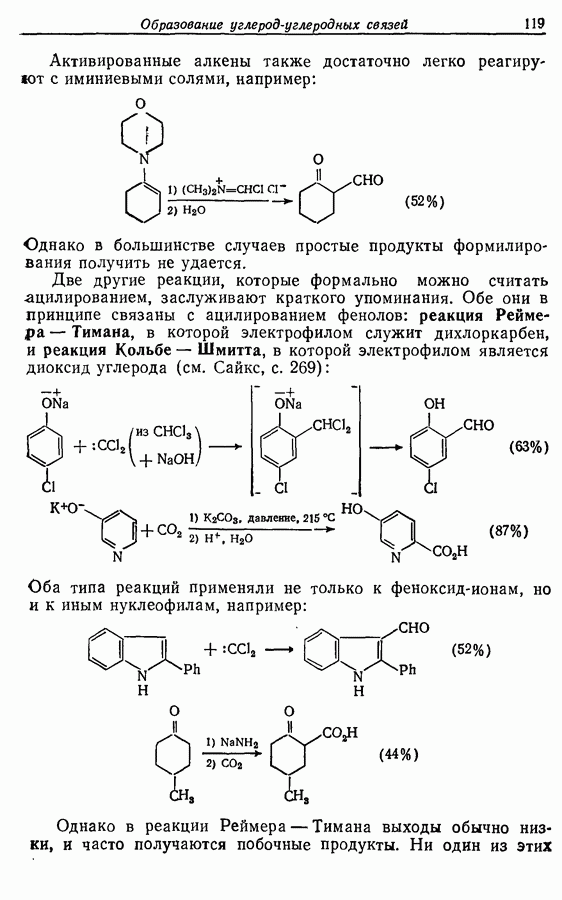
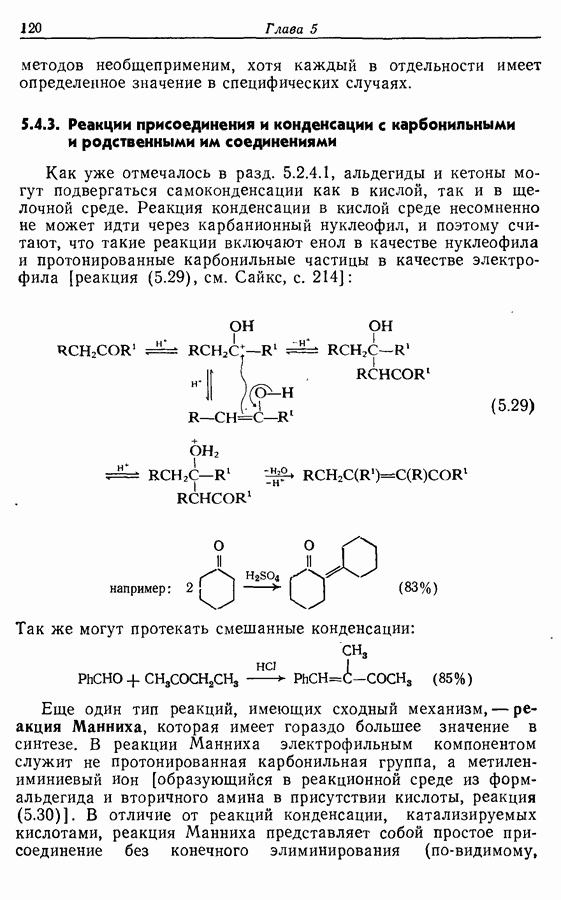
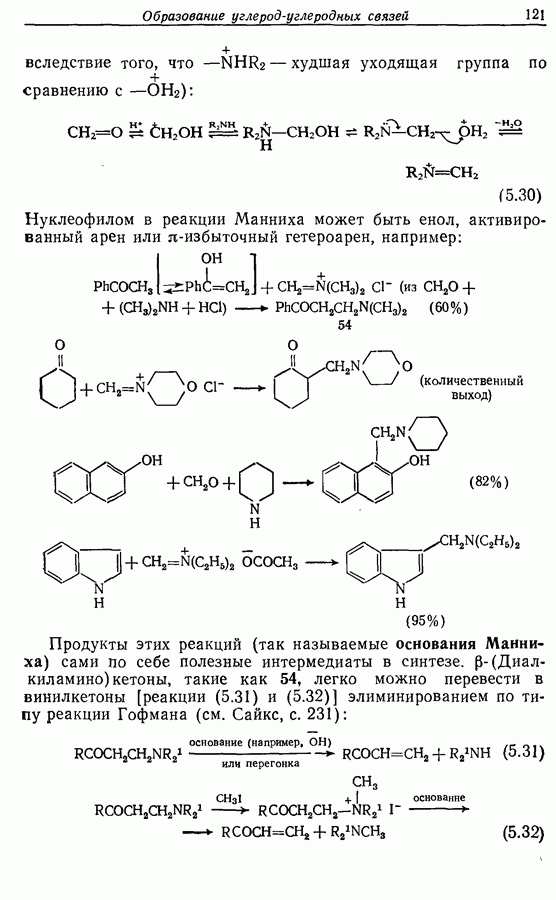
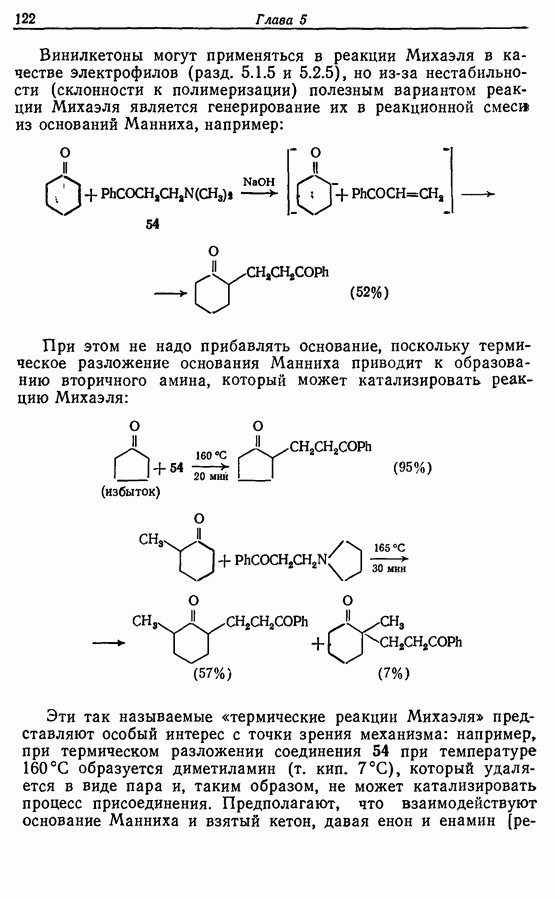
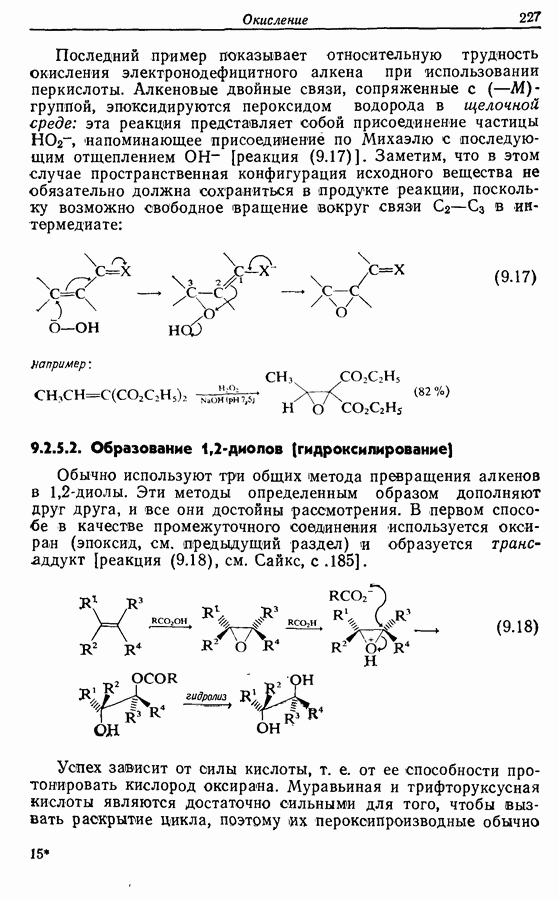
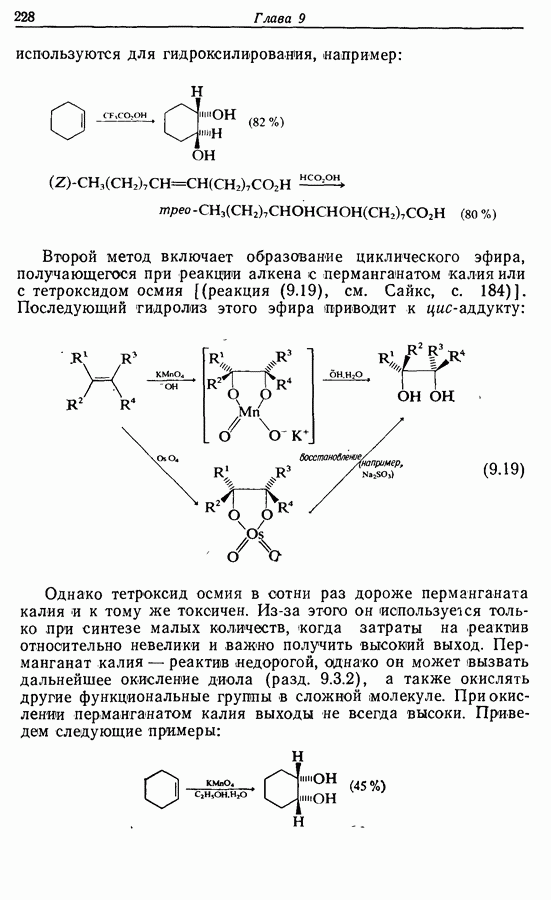
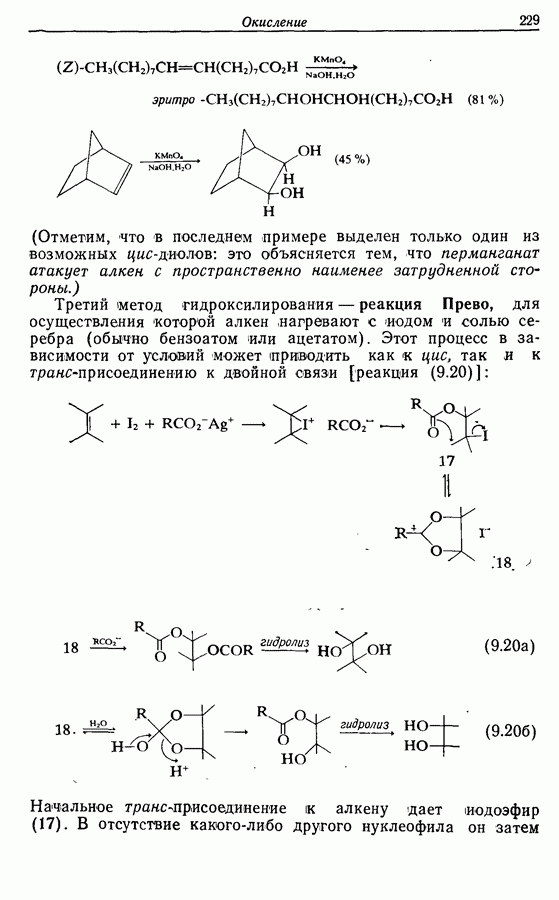
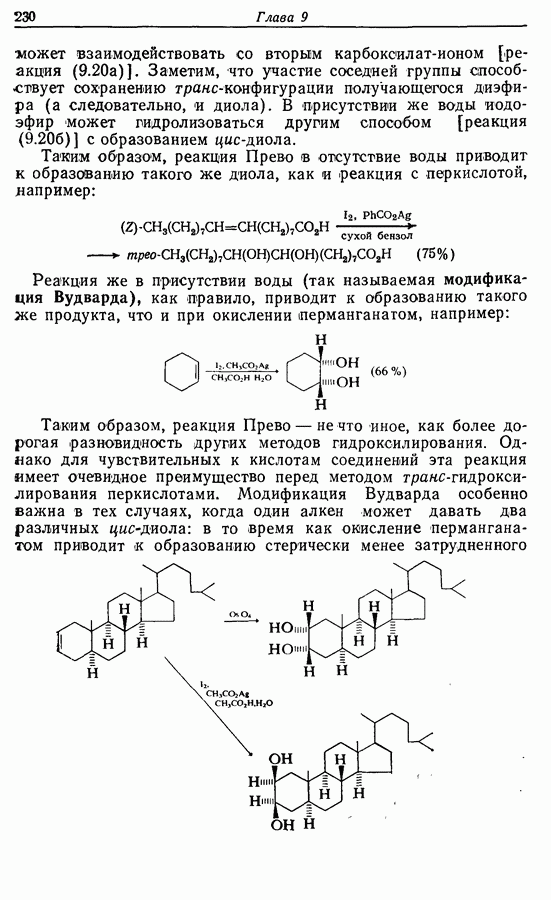
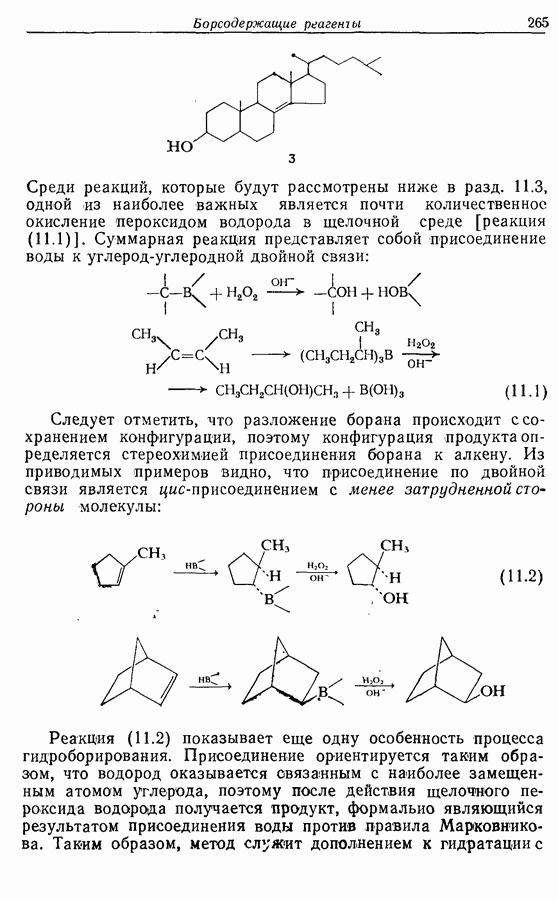
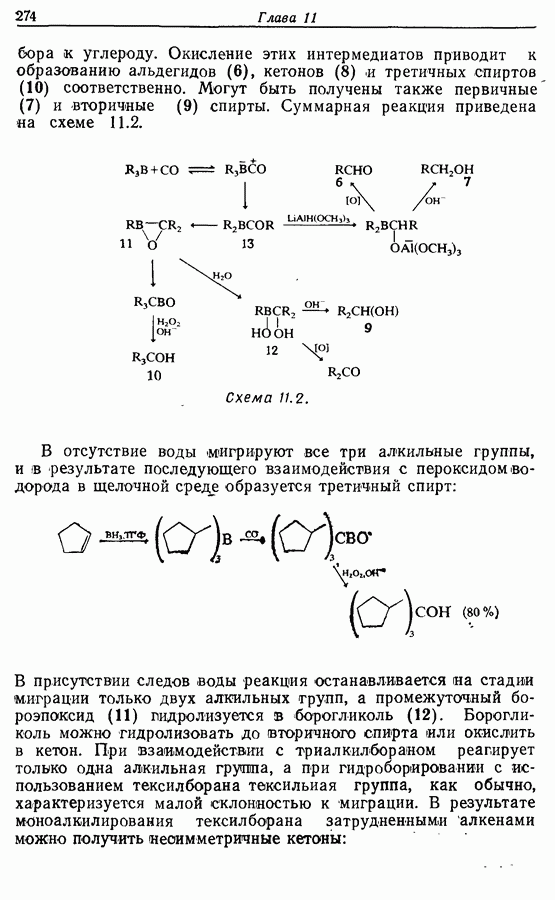
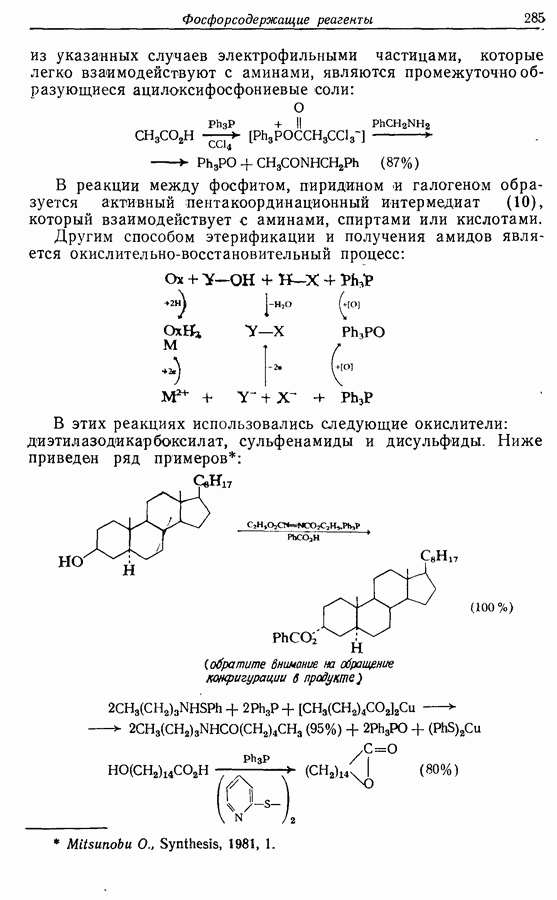
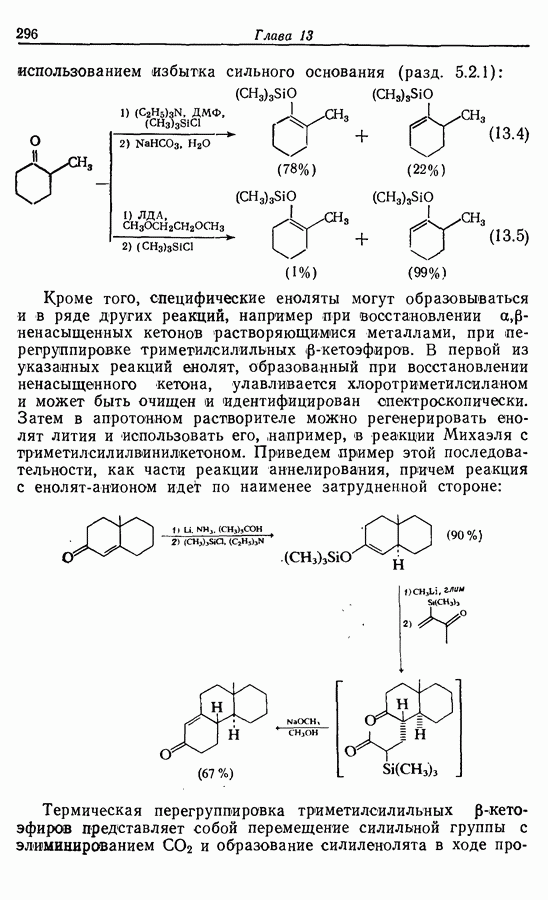
Z-Жасмон (10) является составной частью цветов жасмина и широко используется в парфюмерии для воспроизведения запаха.

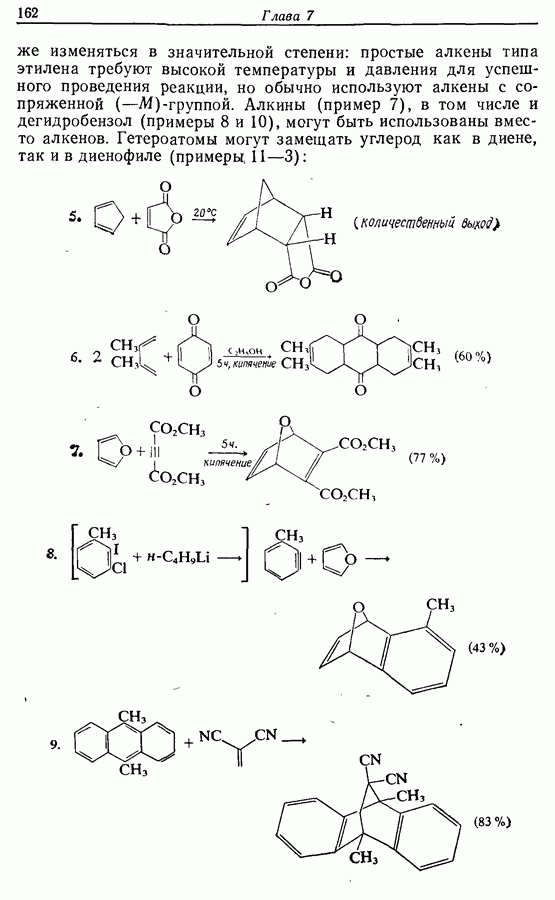
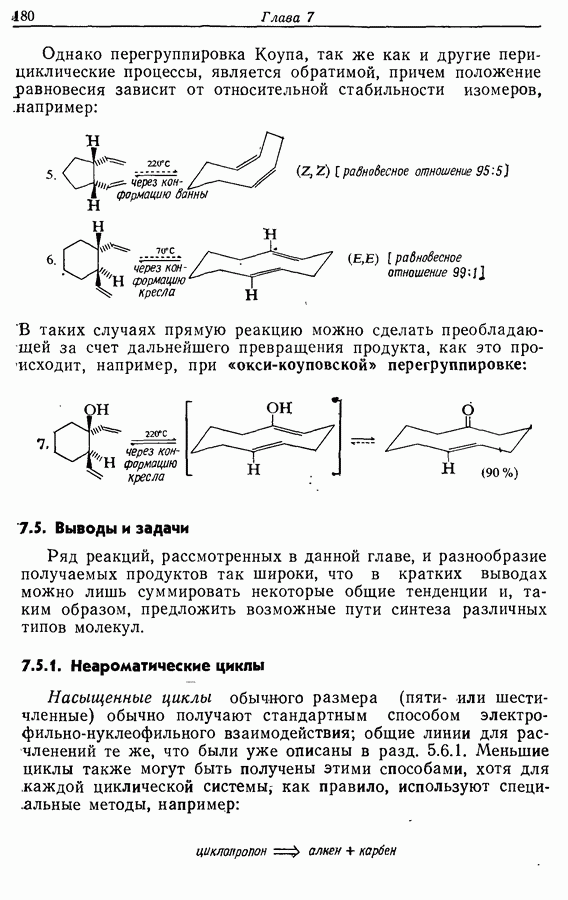
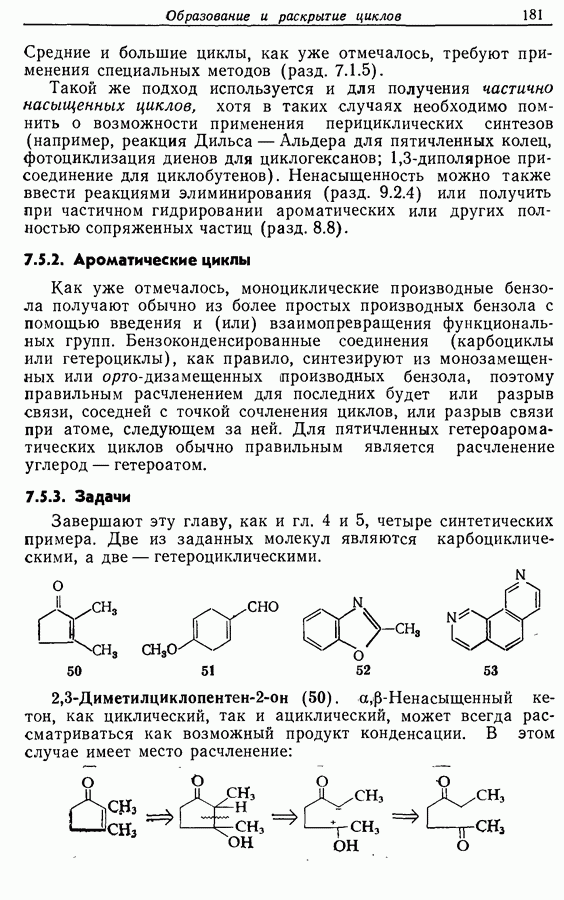
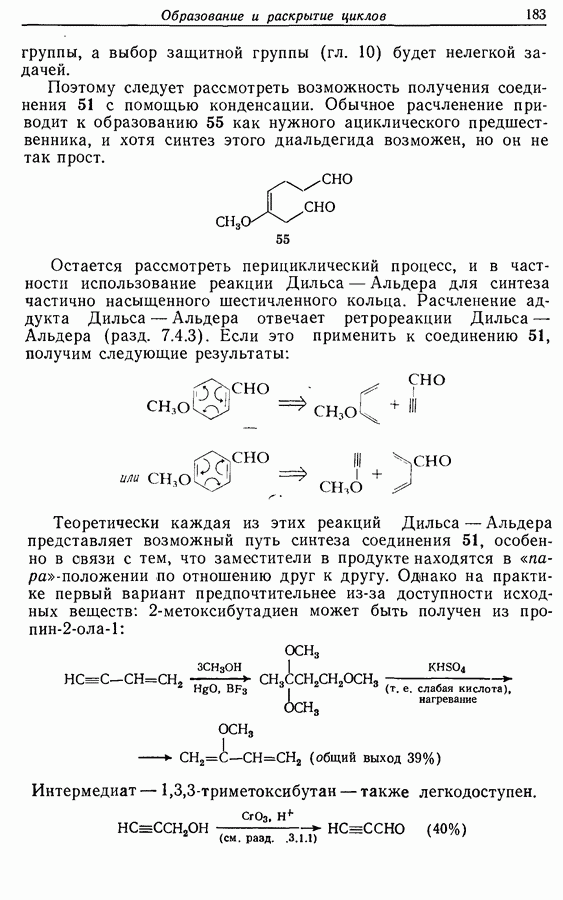
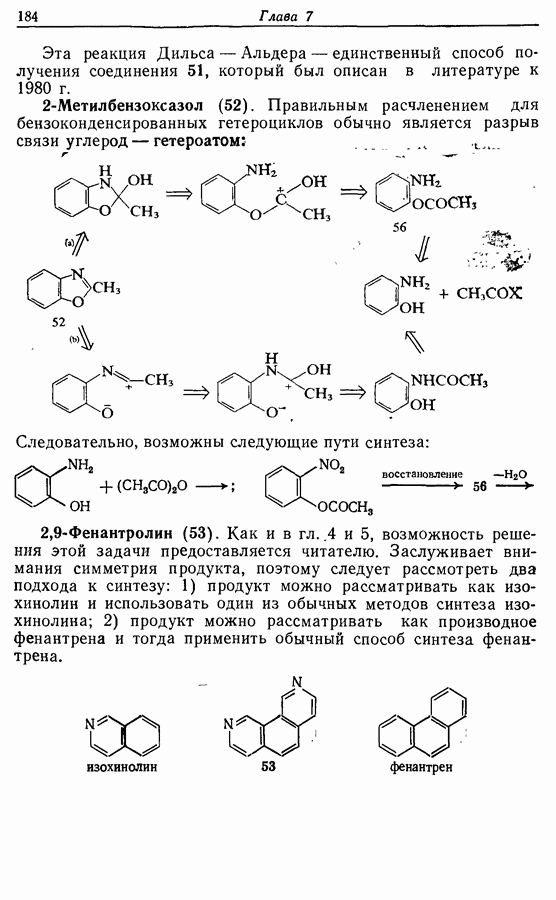
Пути синтеза могут включать использование заранее полученного пятичленного предшественника типа циклопентадиена

или процесс циклизации 1,4-дикетона в циклопентен-2-он (разд. 7.5.3):

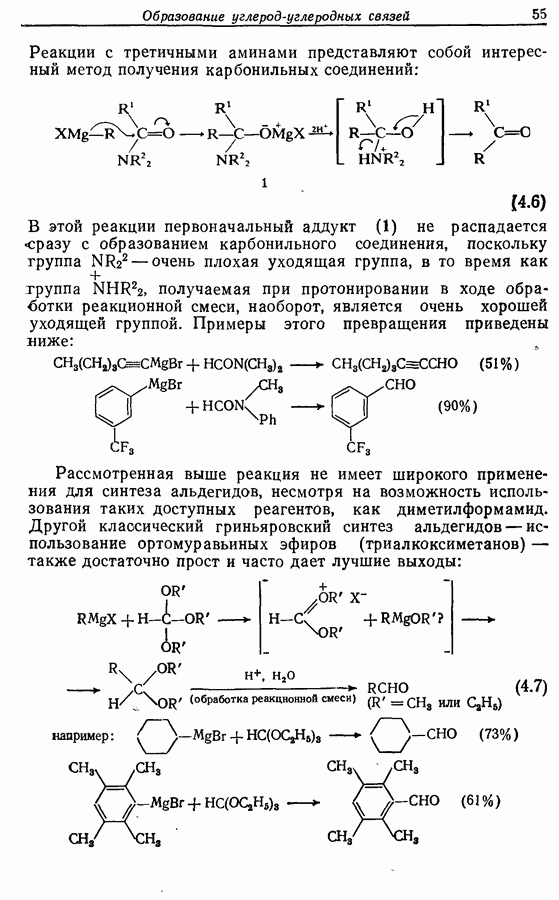
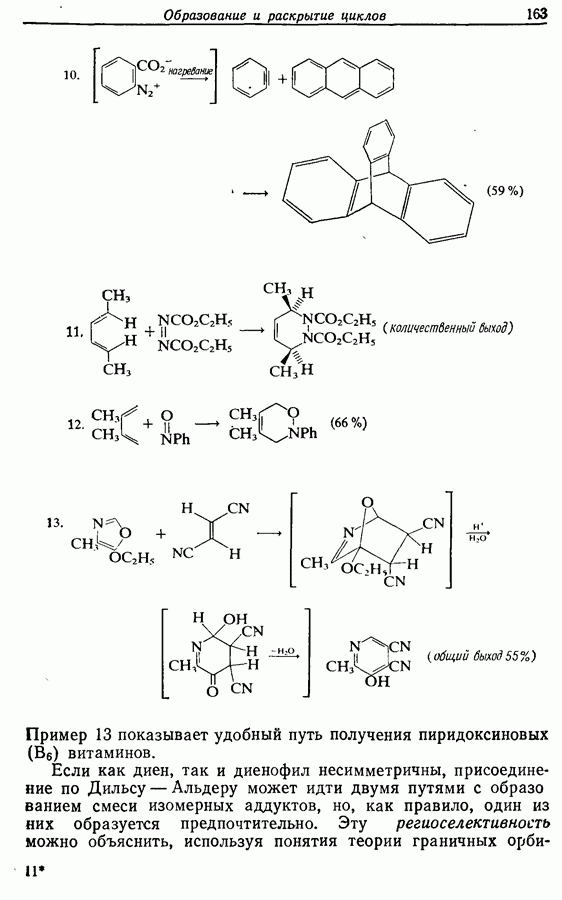
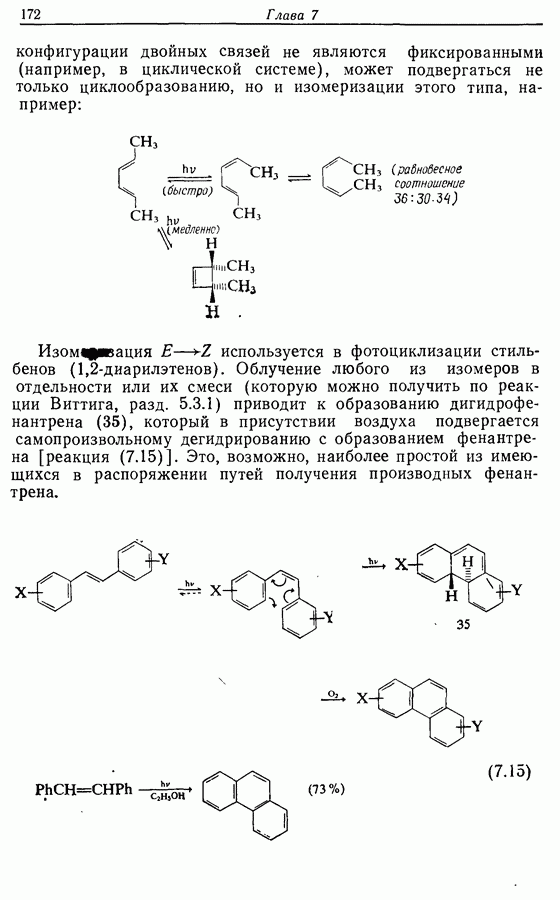
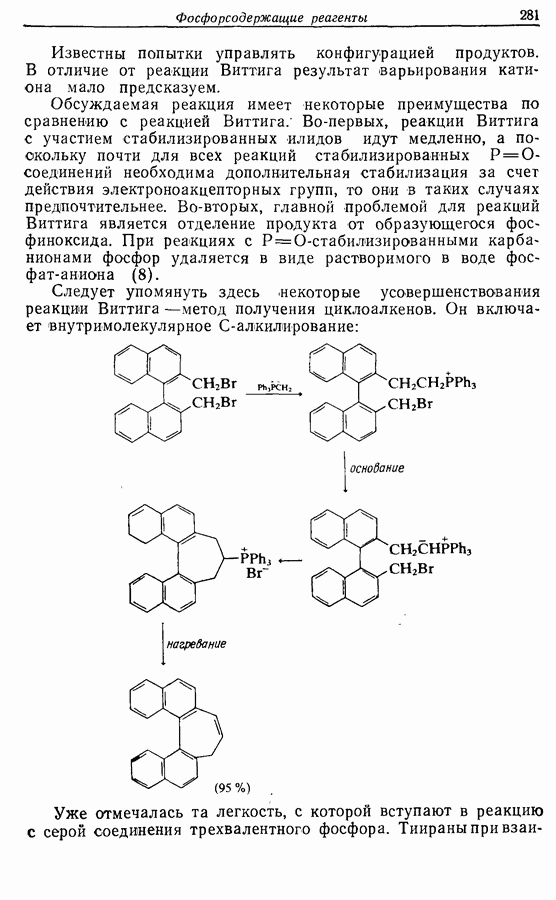
Рассмотрим три способа синтеза Z-жасмона из числа описанных в литературе. Два из трех выбранных вариантов используют последний из указанных подходов, а один, который будет обсужден первым, исходит из циклопентадиена.
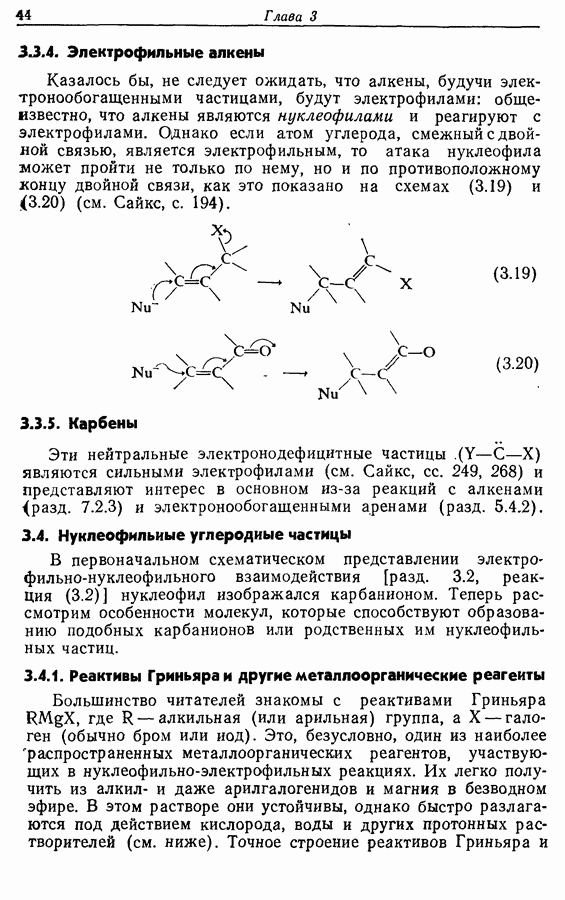
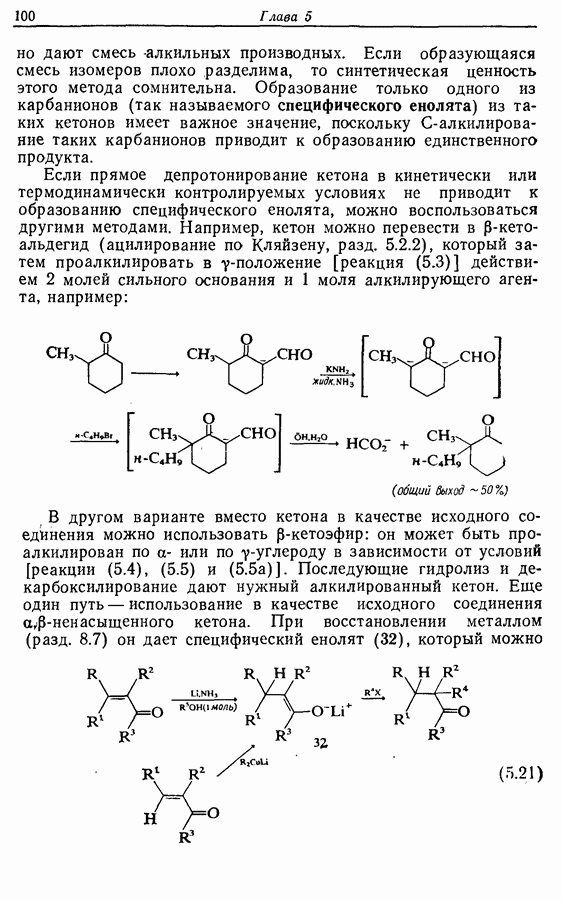
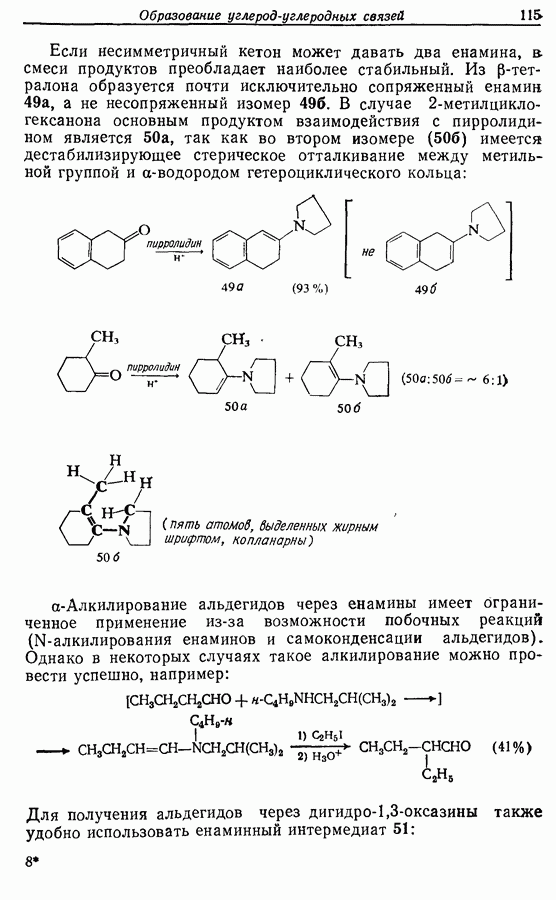
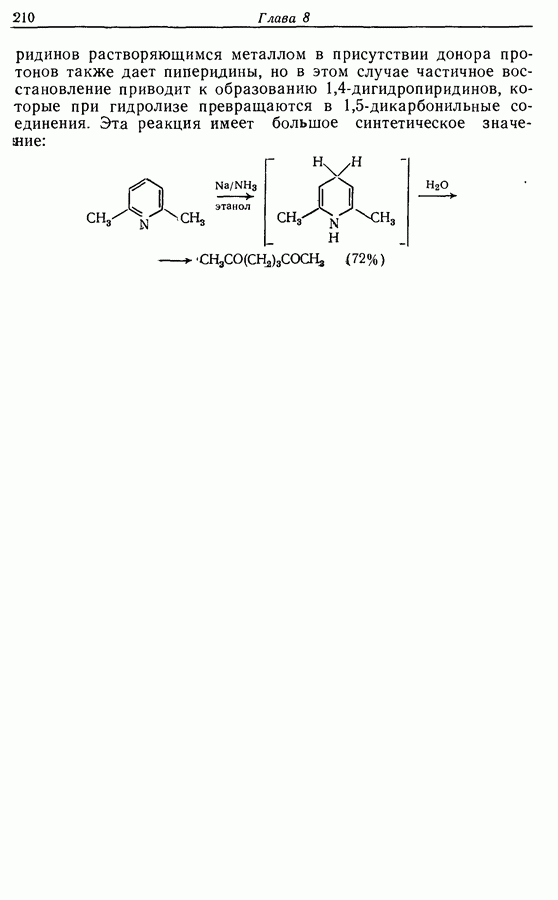
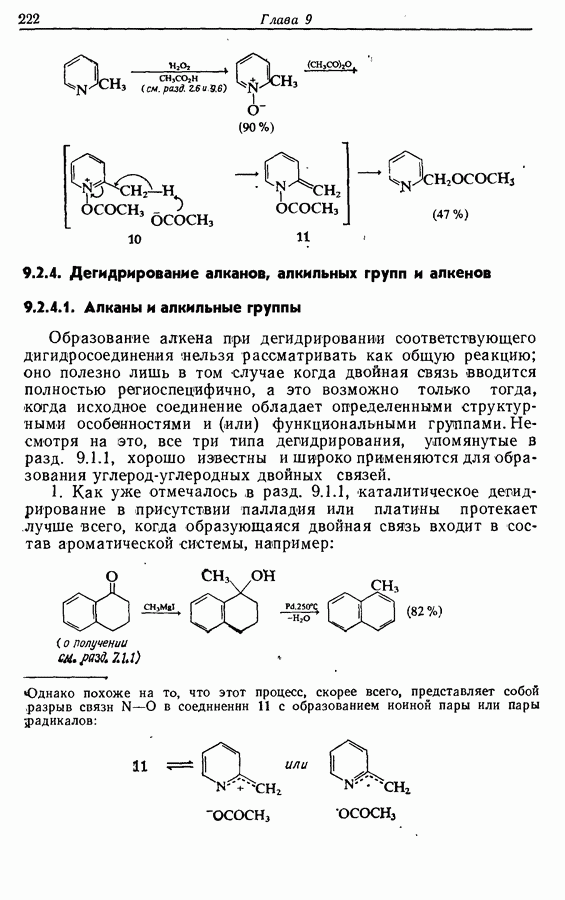
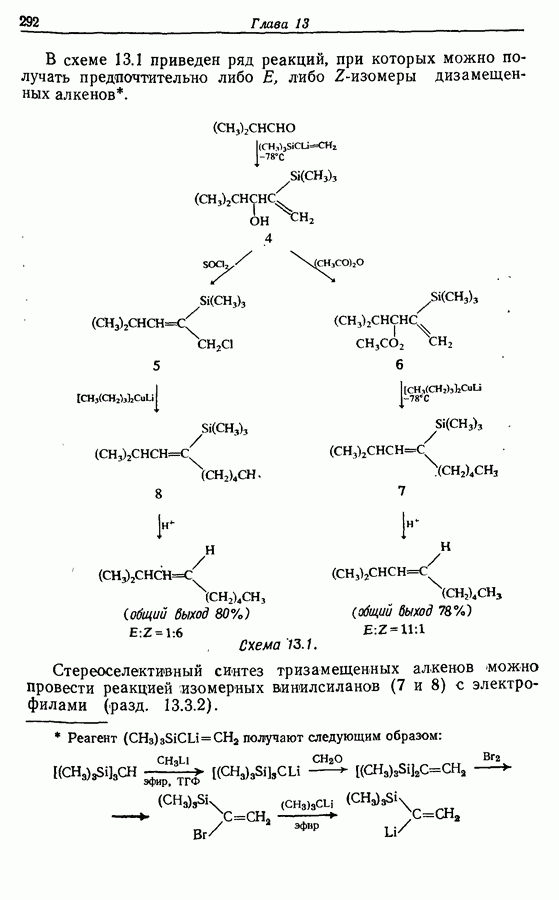
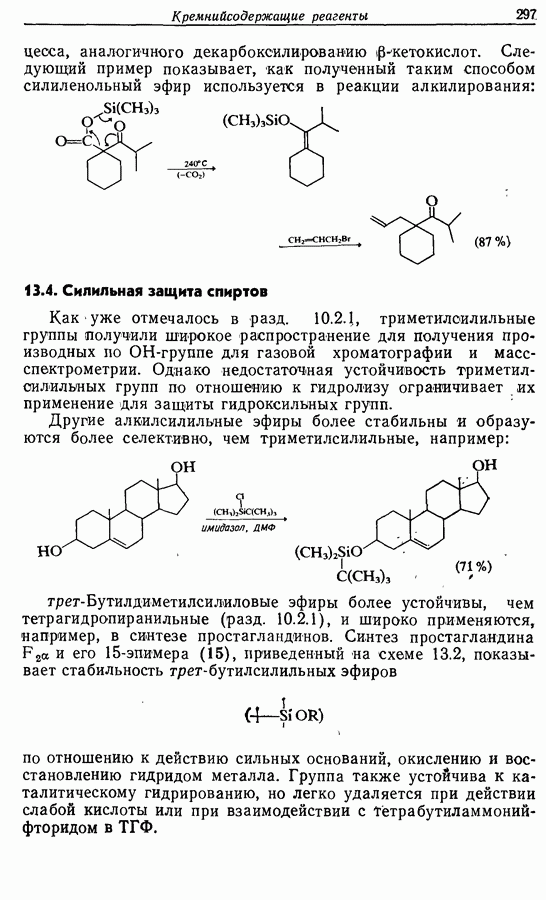
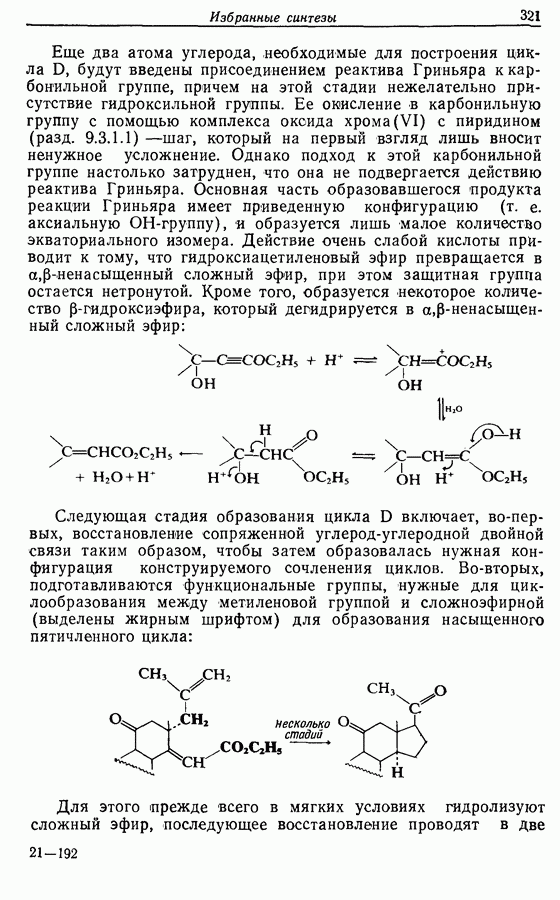
Циклопентадиеновый предшественник соответствующей реакцией по одной двойной связи теоретически ожет быть переведен в соединение 11, которое может изомеризоваться с образованием  -ненасыщенного соединения 12, а затем
-ненасыщенного соединения 12, а затем 

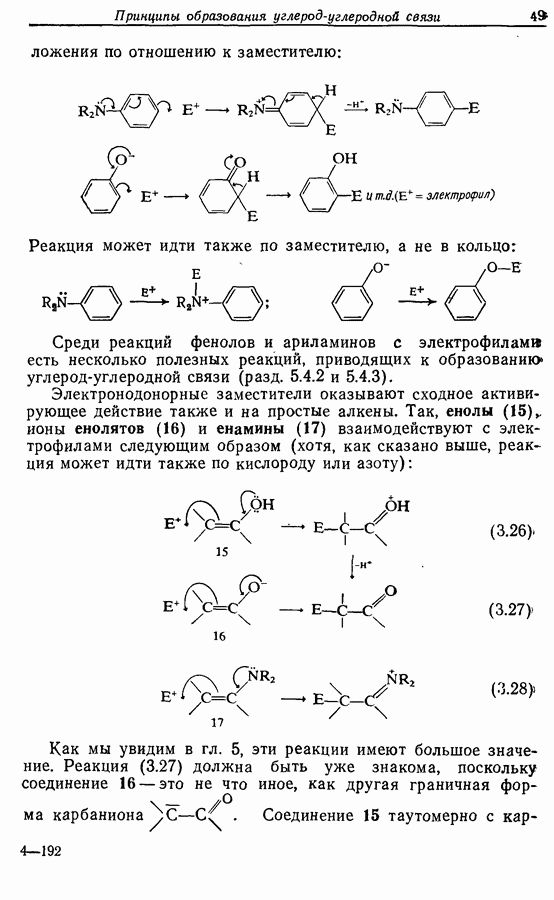
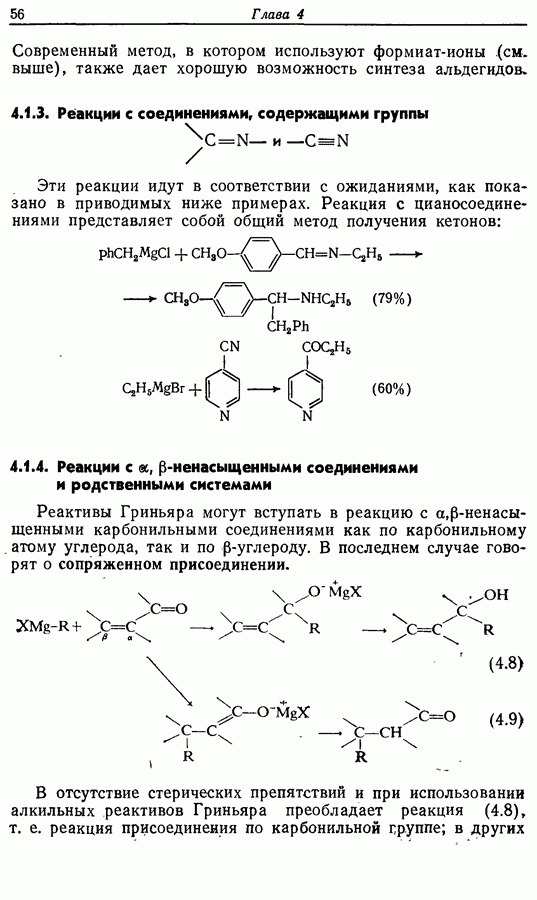
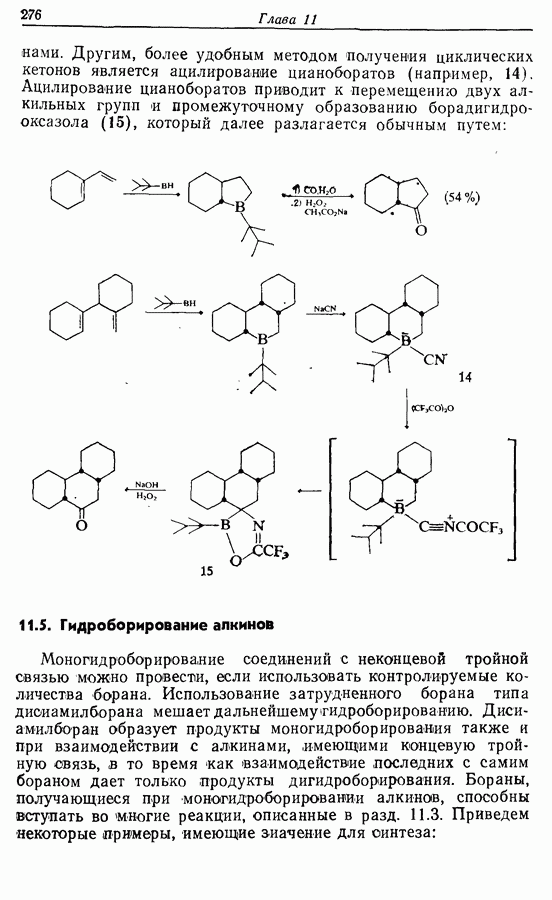
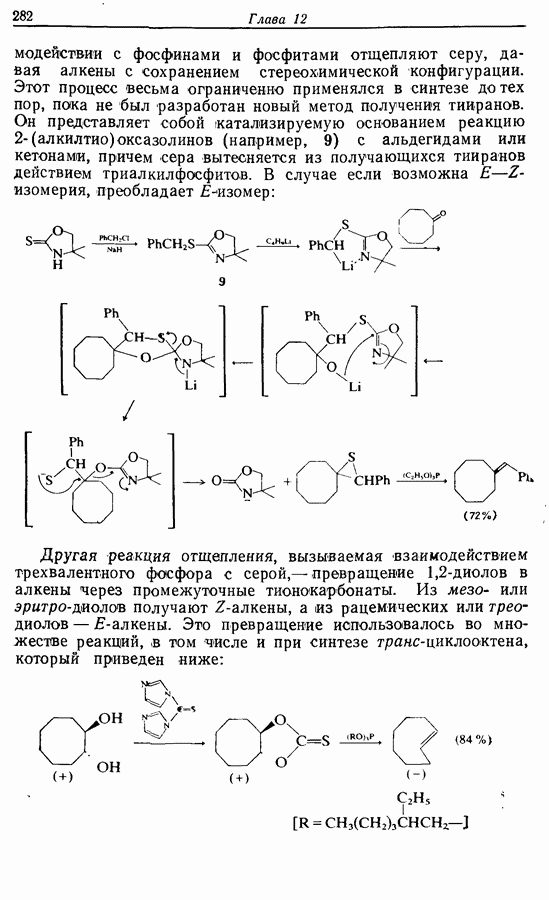
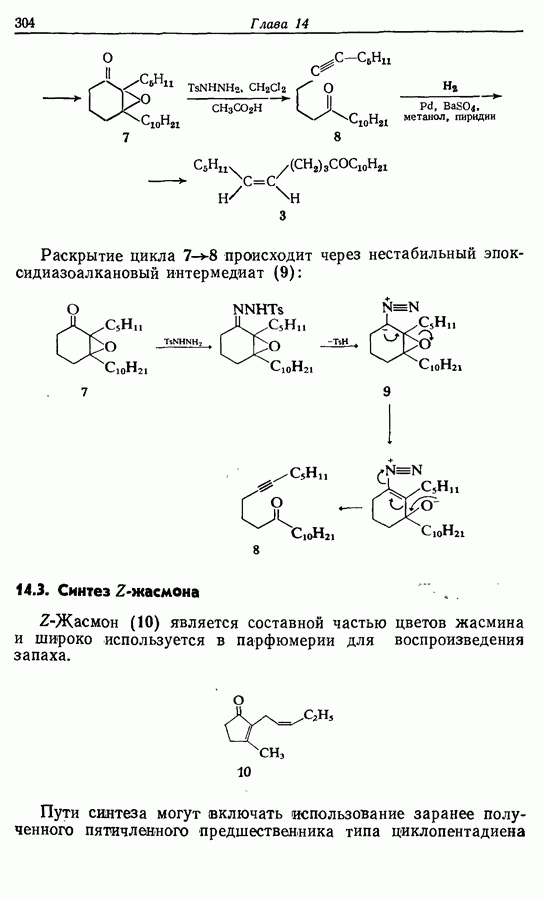
Дихлорокетен (образующийся в реакционной смеси при взаимодействии дихлороацетилхлорида с триэтиламином) можетг вступать в  -циклоприсоединение сциклоалкенами. Восстановительное дегалогенирование аддукта 14 дает циклопентен-циклобутанон (15). Окисление по Байеру — Вилигеру (разд. 9.5.3) позволяет вводить кислородную функцию
-циклоприсоединение сциклоалкенами. Восстановительное дегалогенирование аддукта 14 дает циклопентен-циклобутанон (15). Окисление по Байеру — Вилигеру (разд. 9.5.3) позволяет вводить кислородную функцию  пятичленный цикл, в то время как функциональная группа вводится также при
пятичленный цикл, в то время как функциональная группа вводится также при  в боковую цепь, где необходимо образовать двойную связь. Таким обрааом, последовательность реакций будет следующая:
в боковую цепь, где необходимо образовать двойную связь. Таким обрааом, последовательность реакций будет следующая:


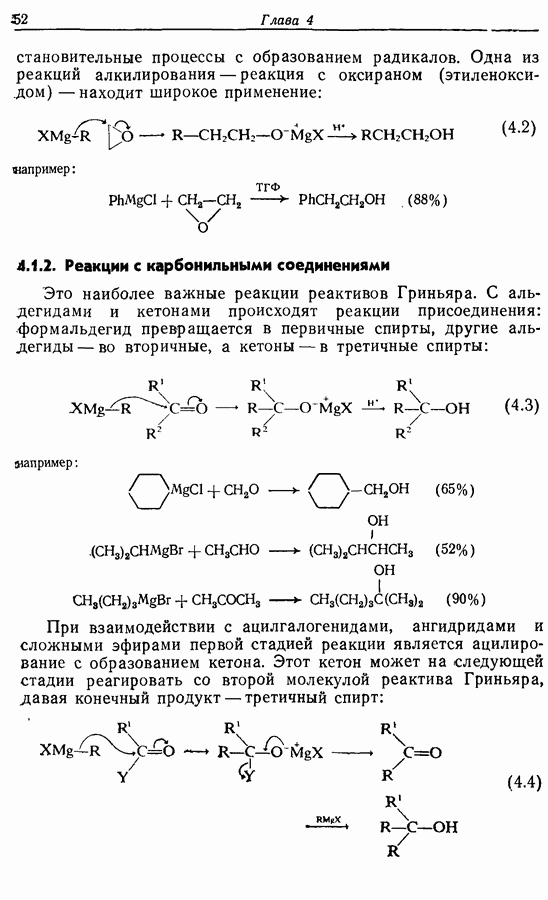
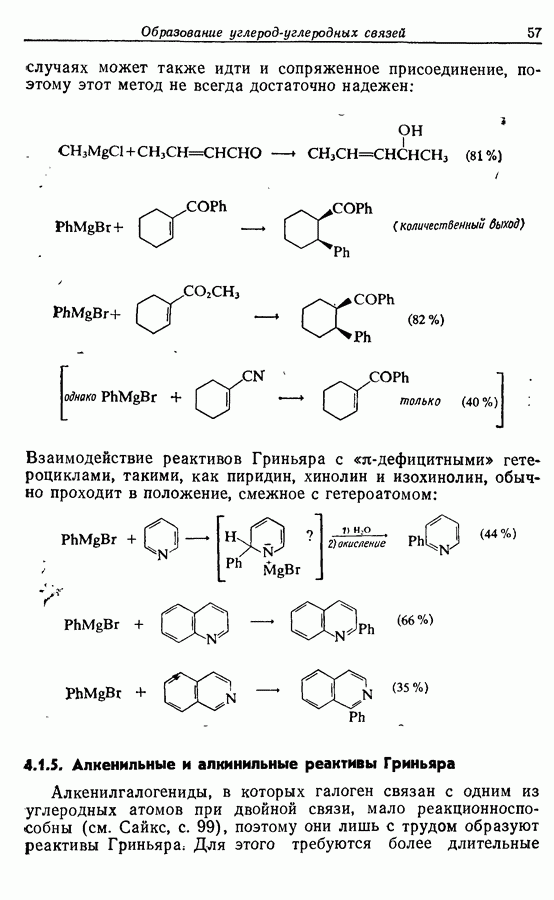
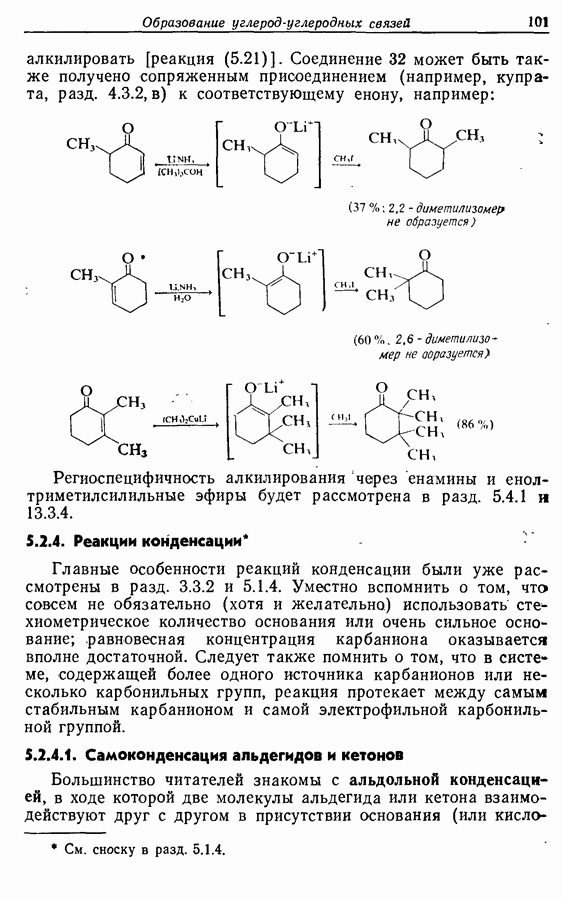
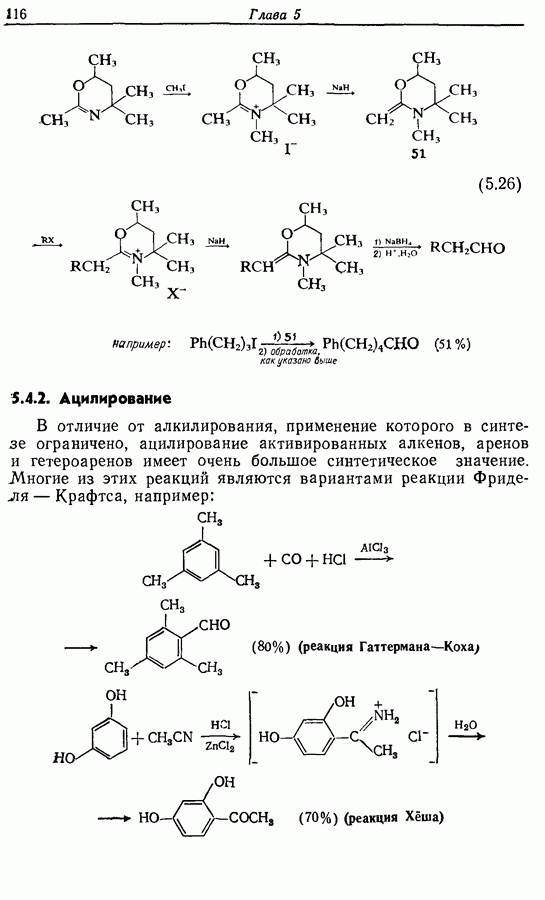
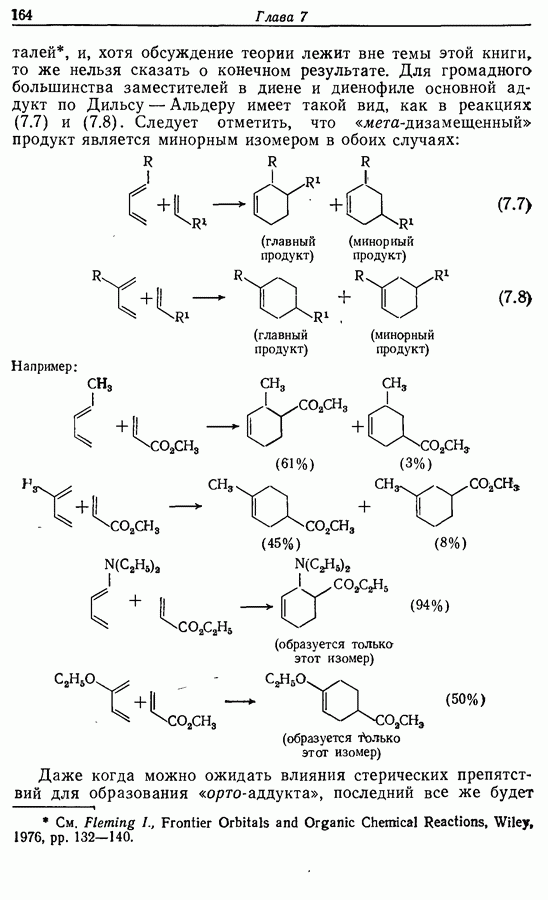
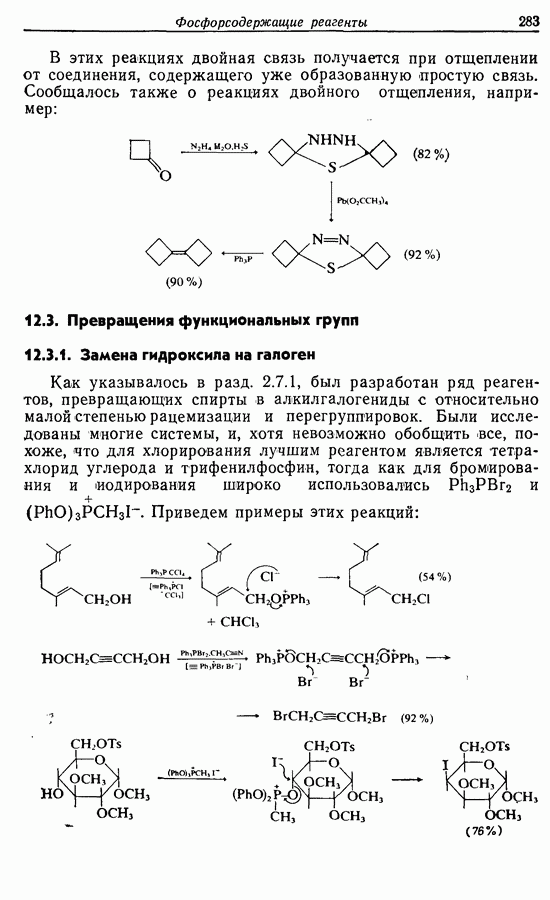
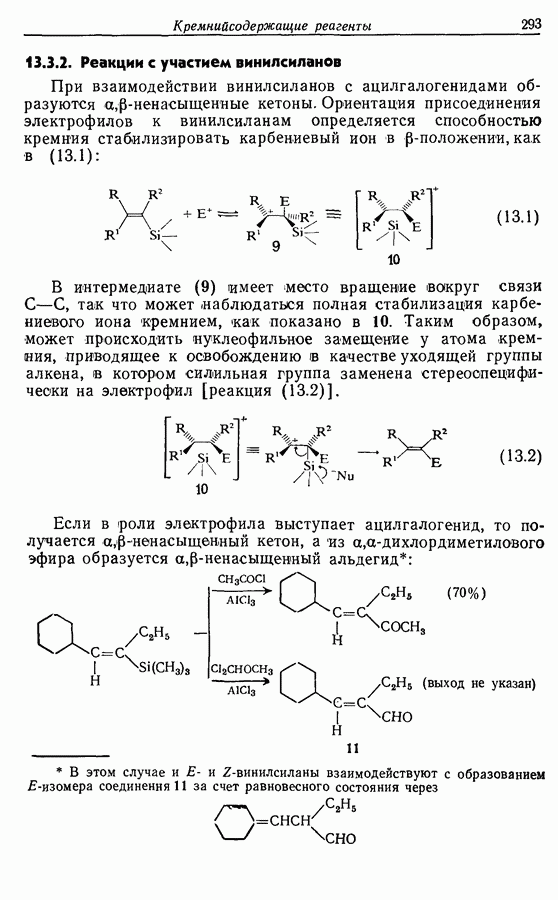
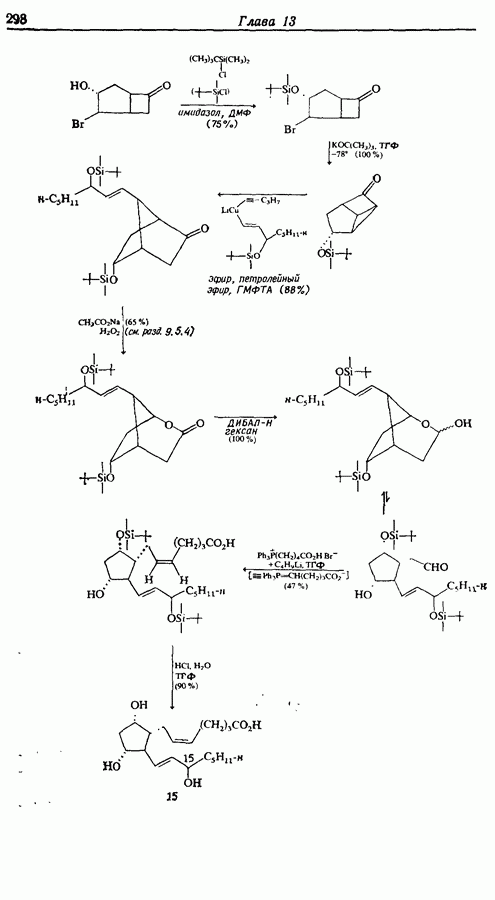
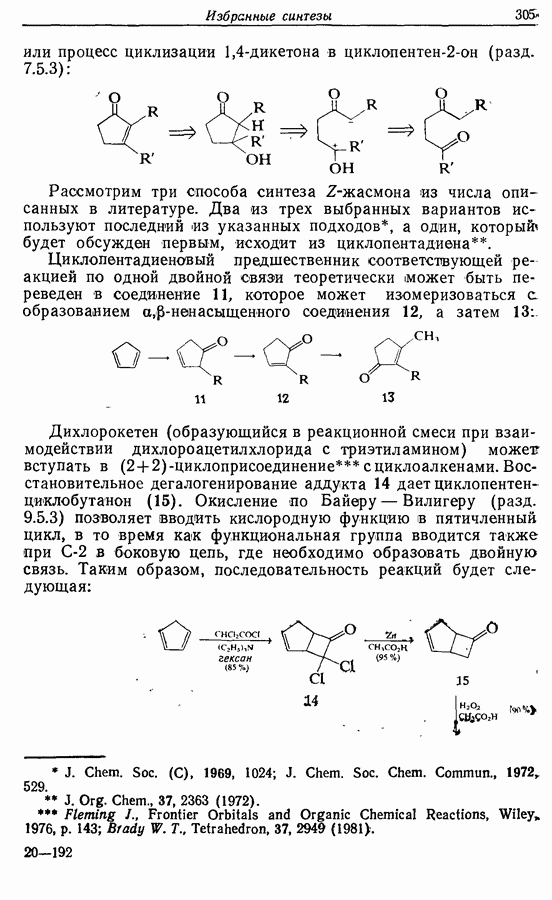
Лактон (16), образующийся при окислении по Байеру— Вилигеру, был восстановлен до полуацеталя (17), который при реакции с реактивом Виттига дал циклопентенол (18), имеющий в боковой алкильной цепи  -двойную связь. При этом не наблюдалось образования
-двойную связь. При этом не наблюдалось образования  -изомера. Вторичный спирт был окислен до ненасыщенного кетона (19), который без выделения промежуточного продукта перевели в наиболее стабильный сопряженный изомер (20). Реакция с метиллитием привела к ожидаемому продукту 1,2-присоединения (21) (разд. 4.2.1), который при окислении подвергся аллильной (перегруппировке в Z-жасмон (10). Общий выход составил около 40%.
-изомера. Вторичный спирт был окислен до ненасыщенного кетона (19), который без выделения промежуточного продукта перевели в наиболее стабильный сопряженный изомер (20). Реакция с метиллитием привела к ожидаемому продукту 1,2-присоединения (21) (разд. 4.2.1), который при окислении подвергся аллильной (перегруппировке в Z-жасмон (10). Общий выход составил около 40%.
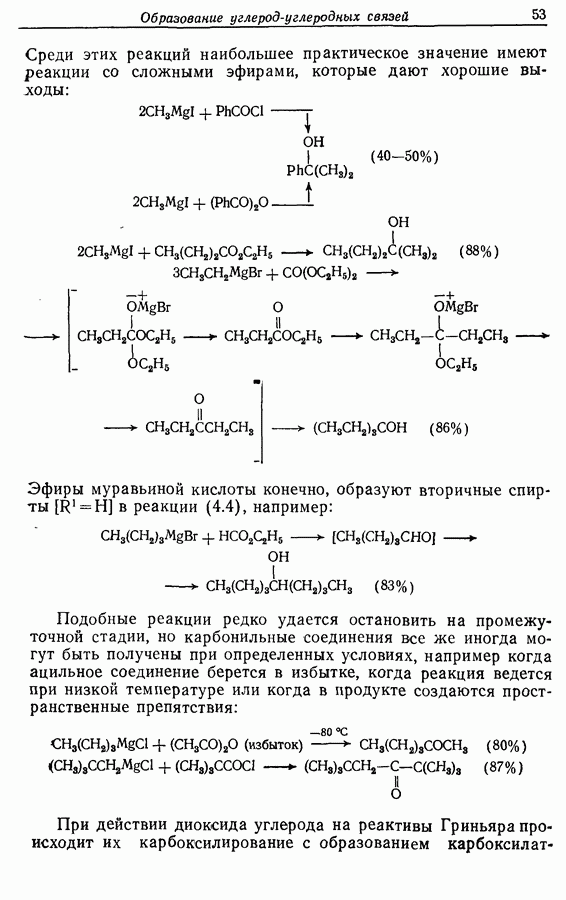
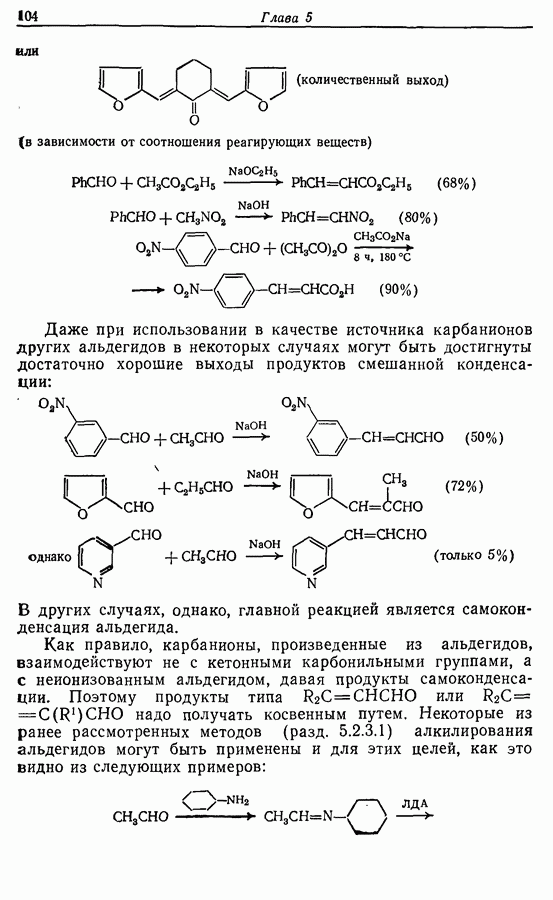
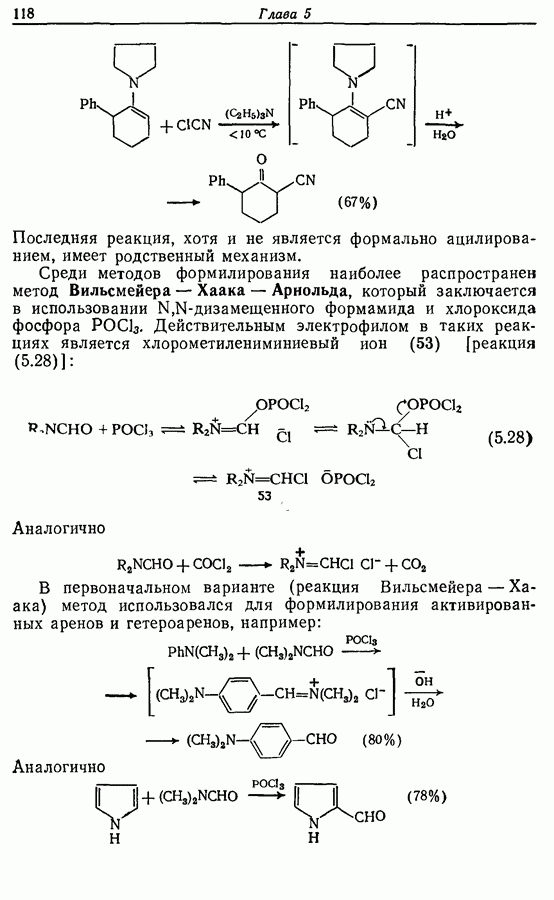
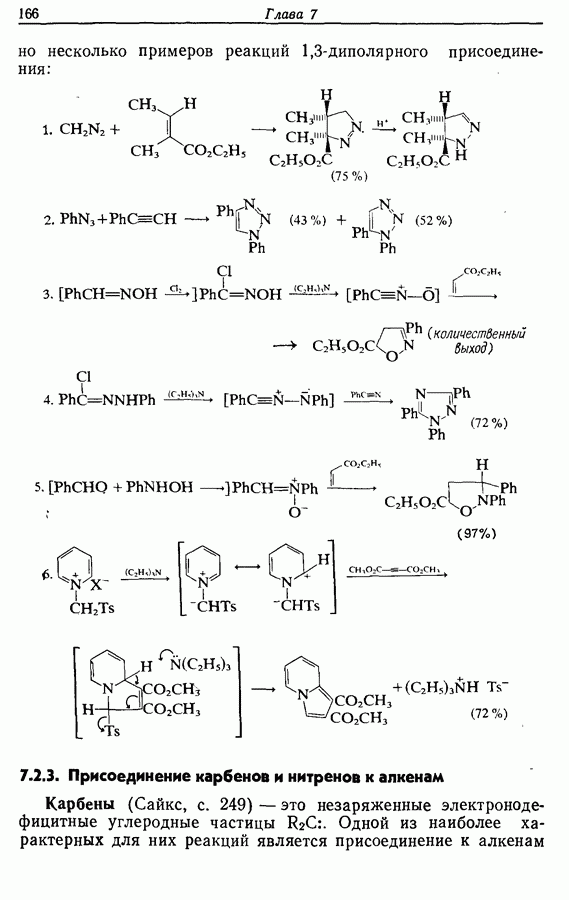
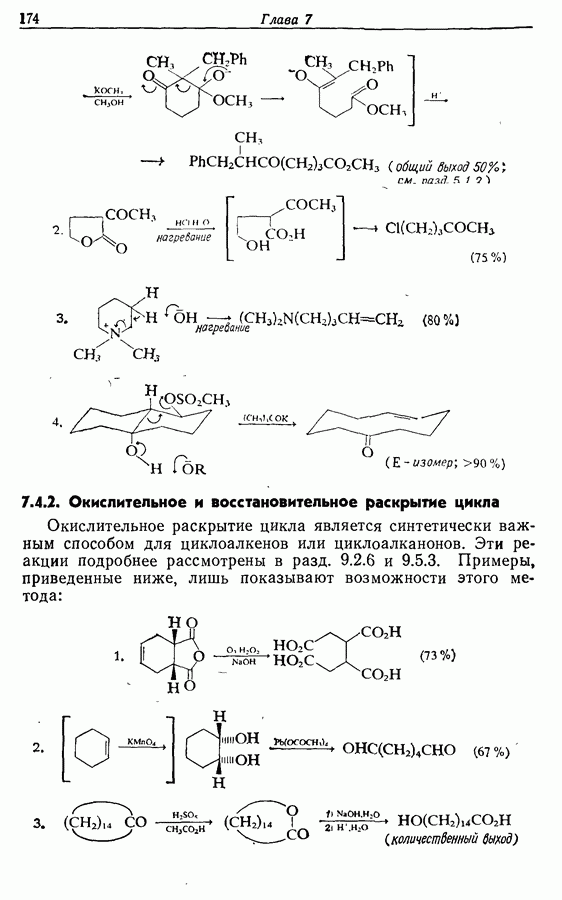
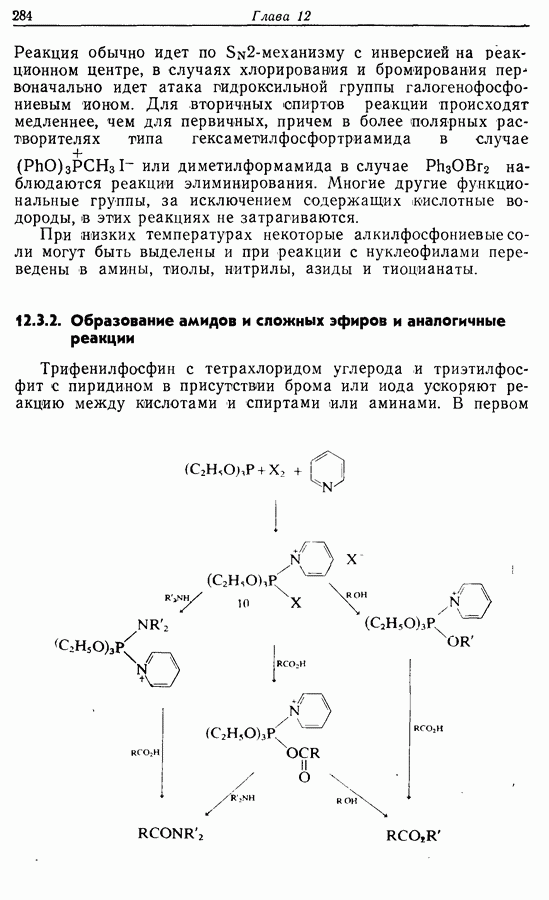
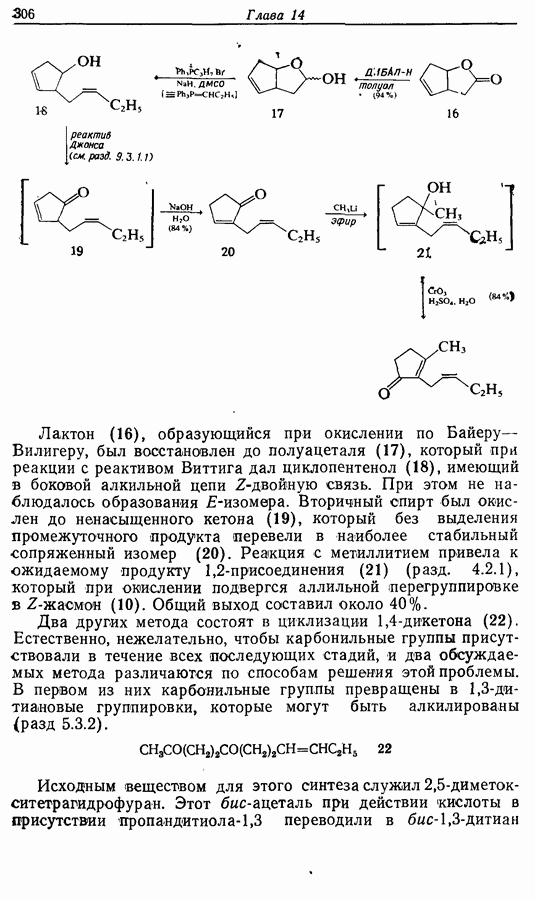
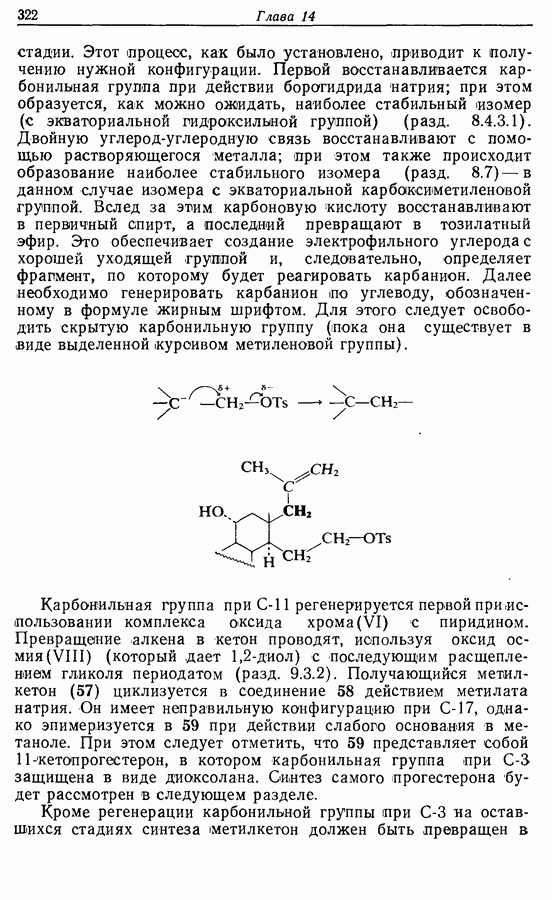
Два других метода состоят в циклизации 1,4-дикетона (22). Естественно, нежелательно, чтобы карбонильные группы присутствовали в течение всех последующих стадий, и два обсуждаемых метода различаются по способам решения этой проблемы. В первом из них карбонильные группы превращены в 1,3-дитиановые группировки, которые могут быть алкилированы <разд 5.3.2).

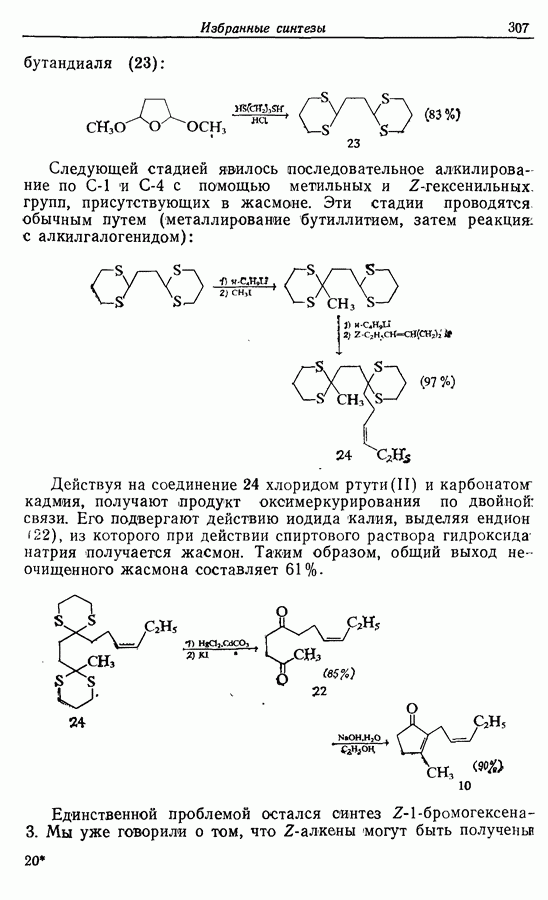
Исходным веществом для этого синтеза служил 2,5-диметокситетрагидрофуран. Этот бис-ацеталь при действии кислоты в присутствии пропандитиола-1,3 переводили в бис-1,3-дитиан
бутандиаля (23):

Следующей стадией явилось последовательное алкилирование по  с помощью метальных и Z-гексенильных групп, присутствующих в жасмопе. Эти стадии проводятся обычным путем (металлирование бутиллитием, затем реакция: с алкилгалогенидом):
с помощью метальных и Z-гексенильных групп, присутствующих в жасмопе. Эти стадии проводятся обычным путем (металлирование бутиллитием, затем реакция: с алкилгалогенидом):

Действуя на соединение 24 хлоридом ртути (II) и карбонатом кадмия, получают продукт оксимеркурирования по двойной: связи. Его подвергают действию иодида калия, выделяя ендион  из которого при действии спиртового раствора гидроксида натрия получается жасмон. Таким образом, общий выход неочищенного жасмона составляет 61%.
из которого при действии спиртового раствора гидроксида натрия получается жасмон. Таким образом, общий выход неочищенного жасмона составляет 61%.

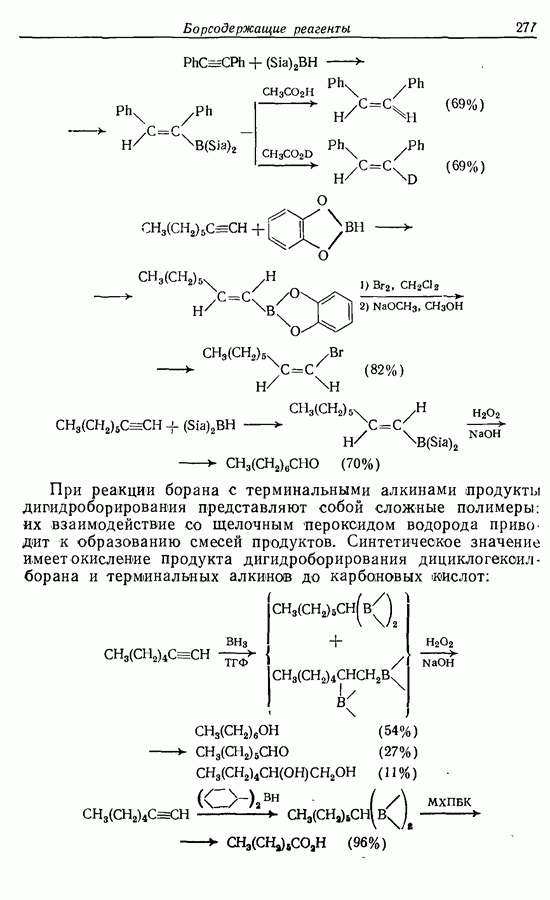
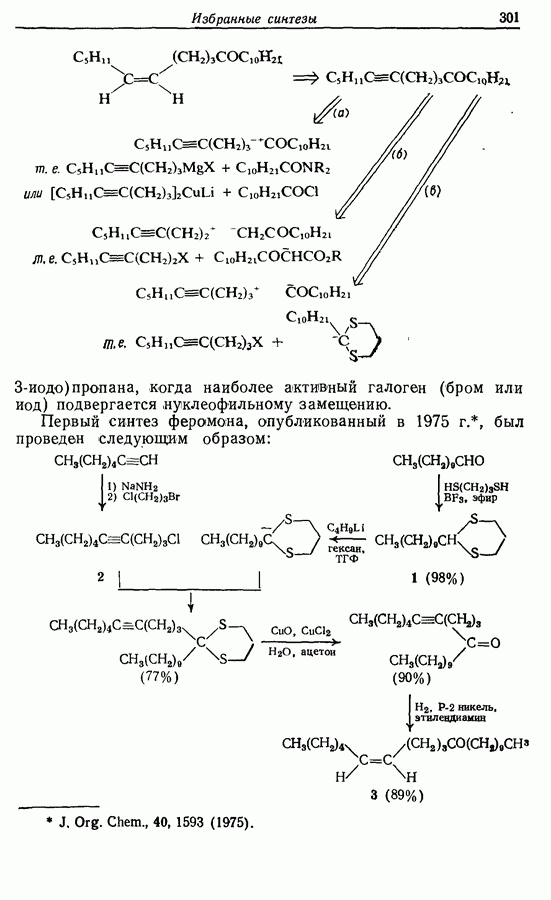
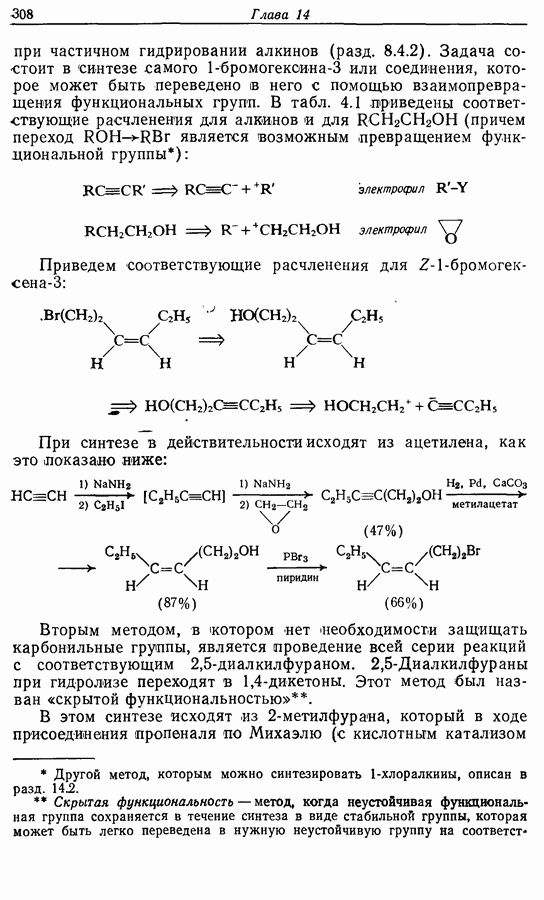
Единственной проблемой остался синтез Z-1-бромогексена-3. Мы уже говорили о том, что Z-алкены могут быть получены
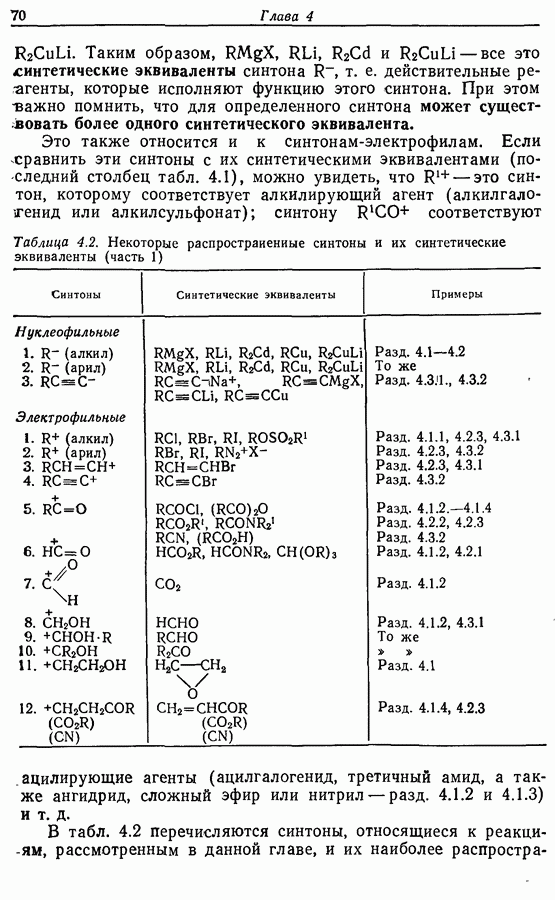
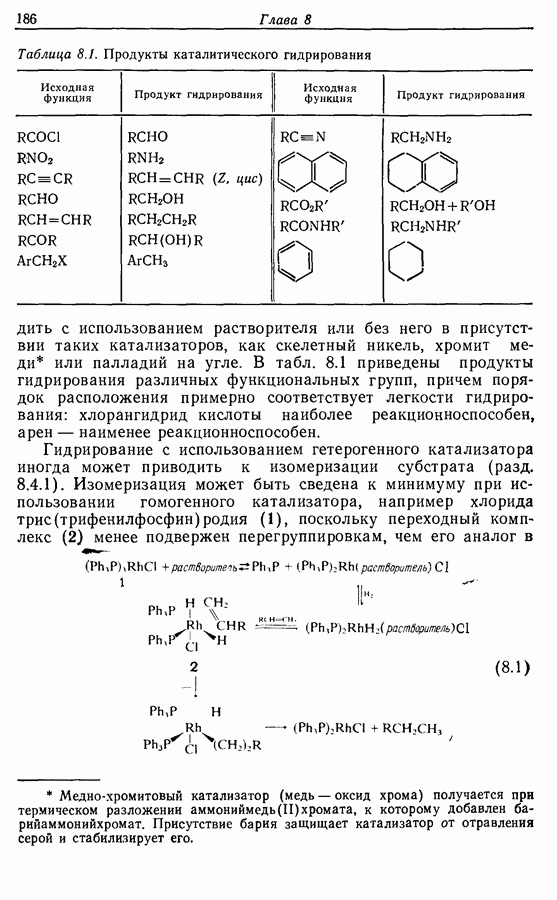
при частичном гидрировании алкинов (разд. 8.4.2). Задача состоит в синтезе самого 1-бромогекоина-3 или соединения, которое может быть переведено  него с помощью взаимопревращения функциональных групп. В табл. 4.1 приведены соответствующие расчленения для алкинов и для
него с помощью взаимопревращения функциональных групп. В табл. 4.1 приведены соответствующие расчленения для алкинов и для  (причем переход
(причем переход  является возможным превращением функциональной группы:
является возможным превращением функциональной группы:

Приведем соответствующие расчленения для Z-1-бромогексена-3:

При синтезе в действительности исходят из ацетилена, как это показано ниже:

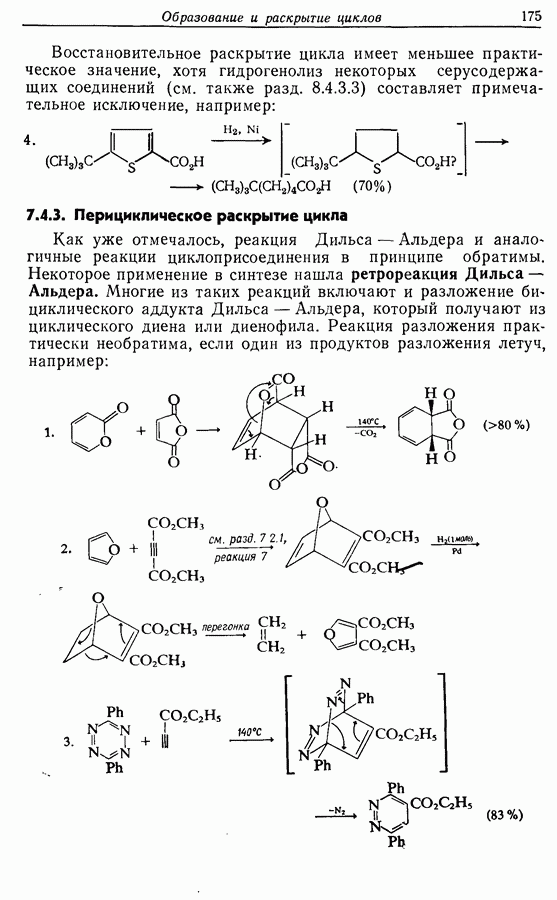
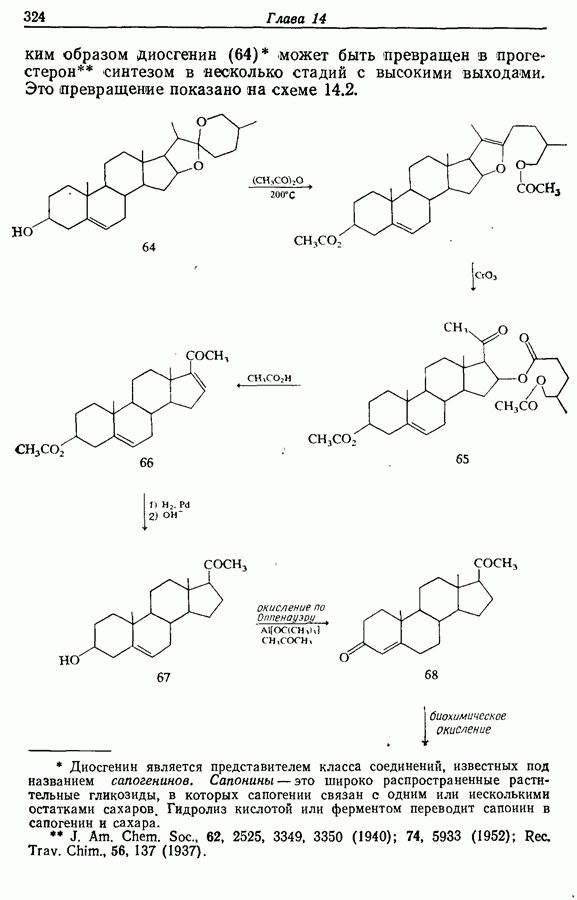
Вторым методом, в котором нет необходимости защищать карбонильные группы, является проведение всей серии реакций с соответствующим  -диалкилфураном.
-диалкилфураном.  -Диалкилфураны при гидролизе переходят в
-Диалкилфураны при гидролизе переходят в  -дикетоны. Этот метод был назван «скрытой функциональностью».
-дикетоны. Этот метод был назван «скрытой функциональностью».
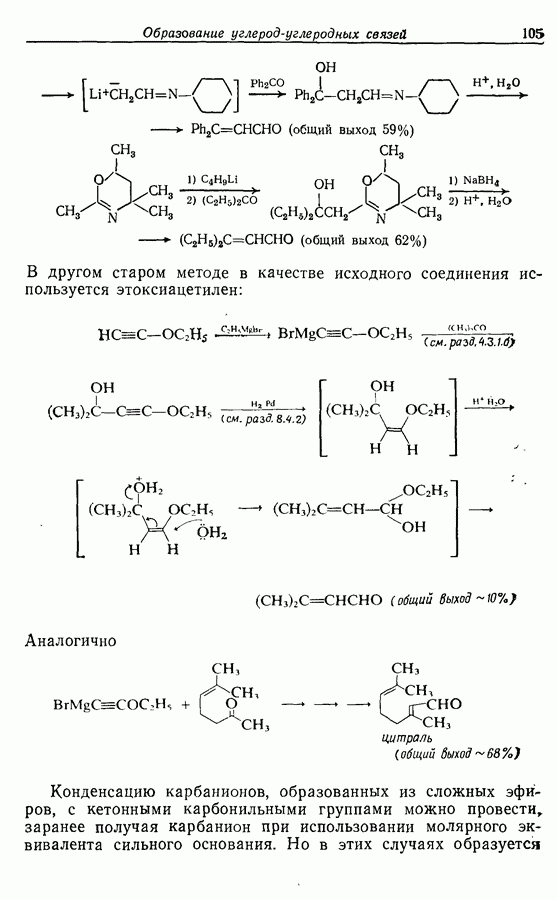
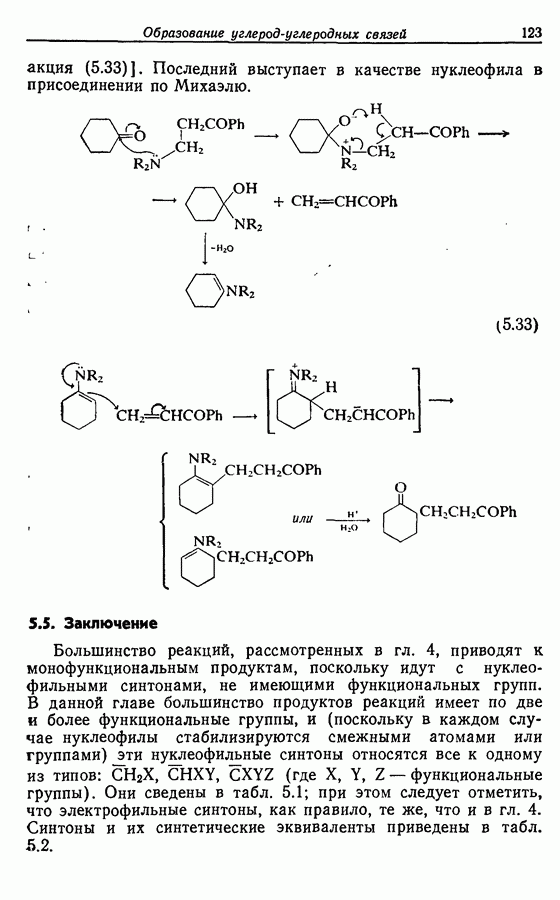
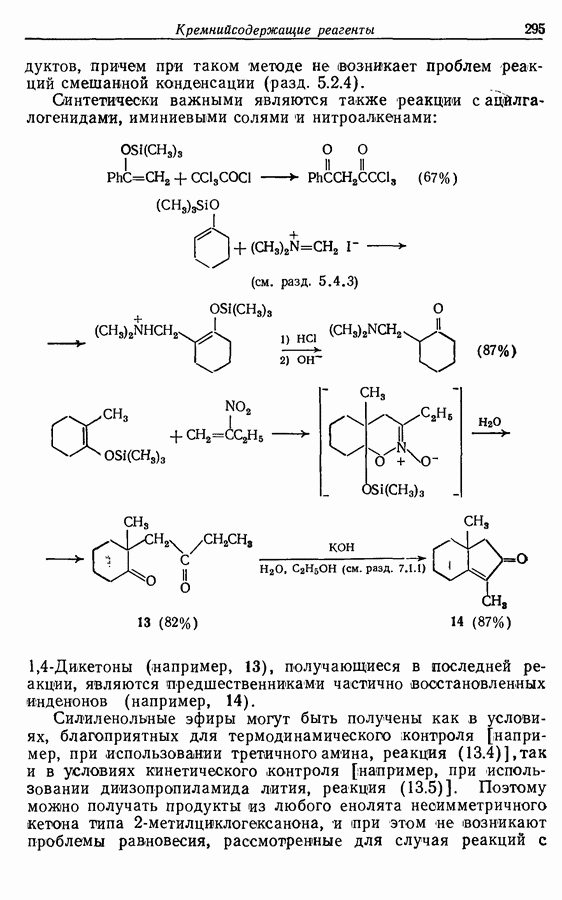
В этом синтезе исходят из  -метилфурана, который в ходе присоединения пропеналя по Михаэлю (с кислотным катализом
-метилфурана, который в ходе присоединения пропеналя по Михаэлю (с кислотным катализом
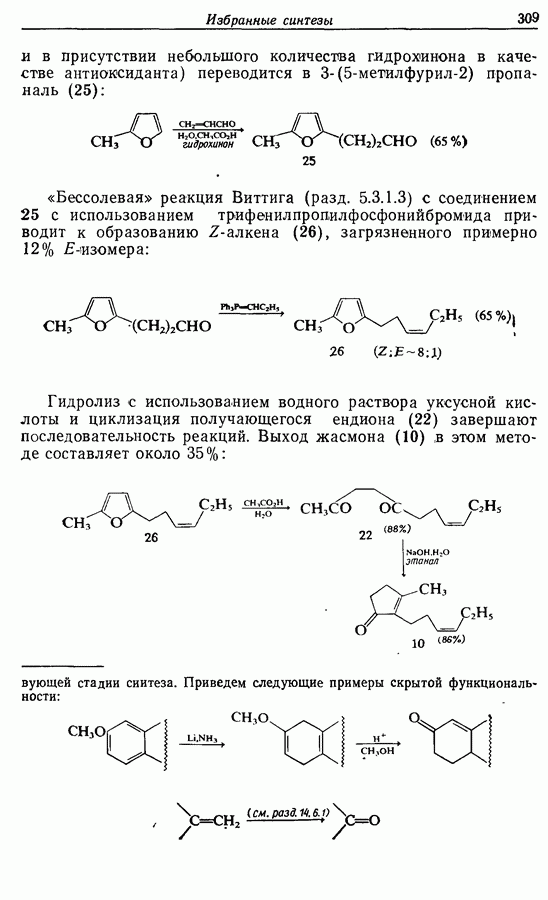
и в присутствии небольшого количества гидрохинона в качестве антиоксиданта) переводится в 3-(5-метилфурил-2) пропаналь (25):

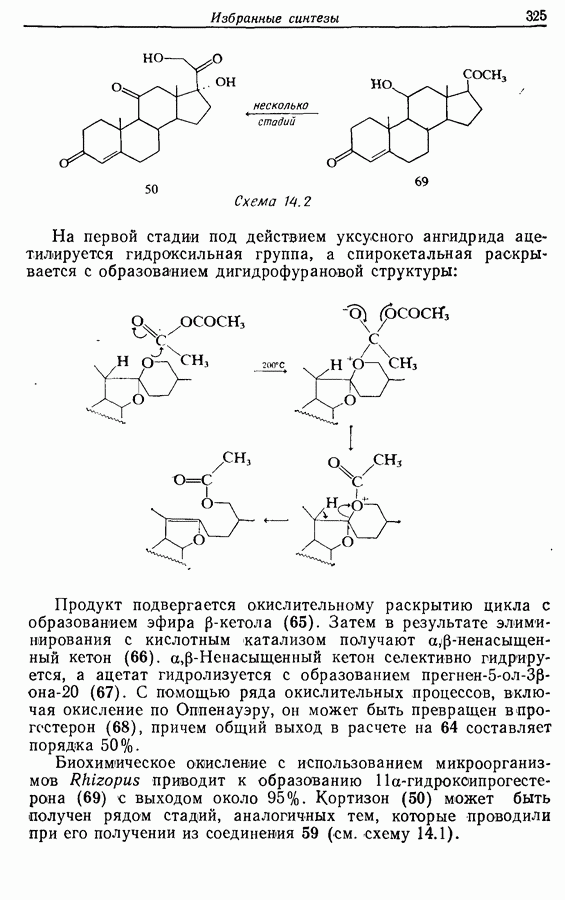
«Бессолевая» реакция Виттига (разд. 5.3.1.3) с соединением 25 с использованием трифенилпропилфосфонийбромида приводит к образованию  -алкена (26), загрязненного примерно 12%
-алкена (26), загрязненного примерно 12%  -изомера:
-изомера:

Гидролиз с использованием водного раствора уксусной кислоты и циклизация получающегося ендиона (22) завершают последовательность реакций. Выход жасмона (10) (в этом методе составляет около 35%:

| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- 1. ВВЕДЕНИЕ
- 2. ВВЕДЕНИЕ И ВЗАИМОПРЕВРАЩЕНИЯ ФУНКЦИОНАЛЬНЫХ ГРУПП
- 2.1. Введение функциональных групп в апканы
- 2.2. Введение функциональных групп в алкены
- 2.3. Введение функциональных групп в апкины
- 2.4. Введение функциональных групп в ароматические углеводороды (арены)
- 2.5. Введение функциональных групп в производные бензола
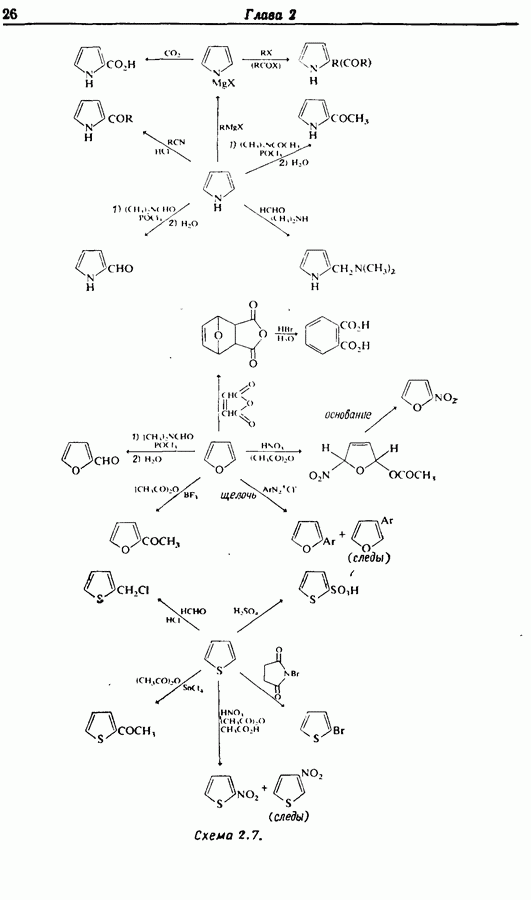
- 2.6. Введение функциональных групп в простые гетероциклические соединения
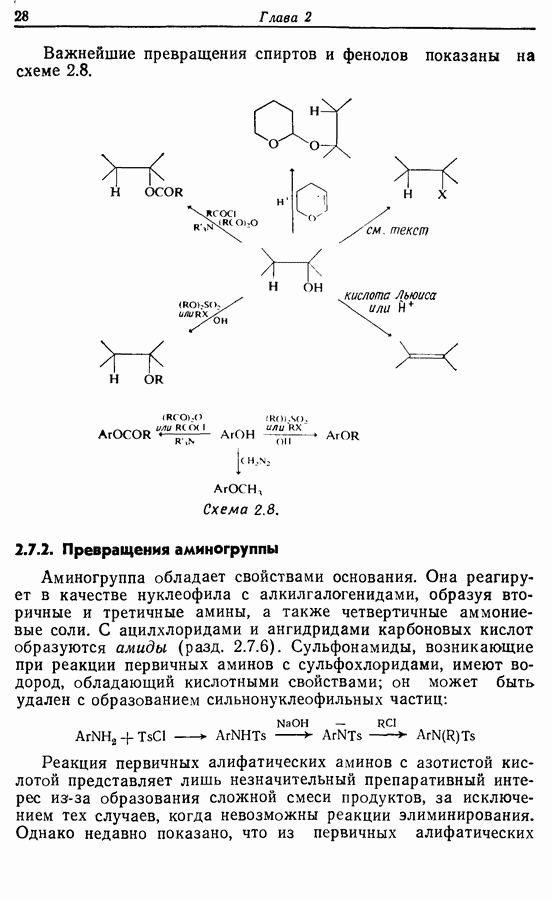
- 2.7. Взаимопревращения функциональных групп
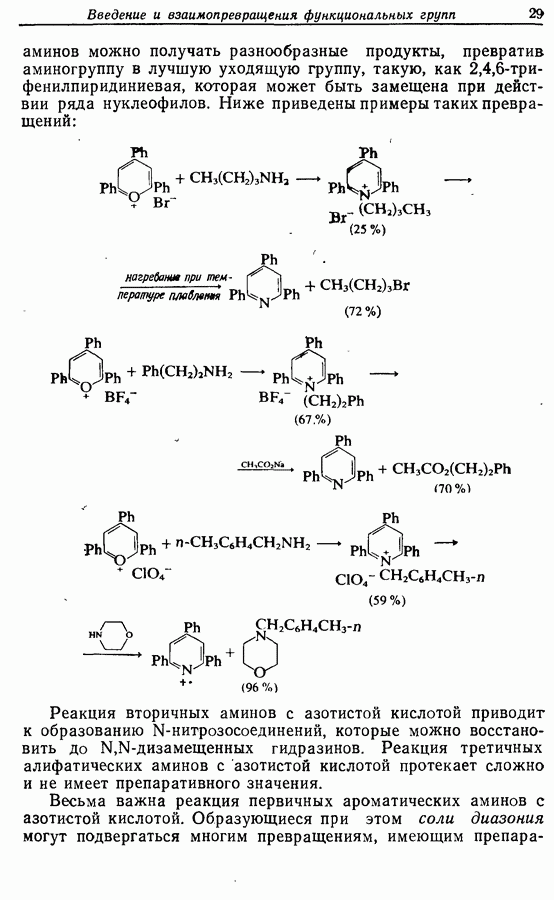
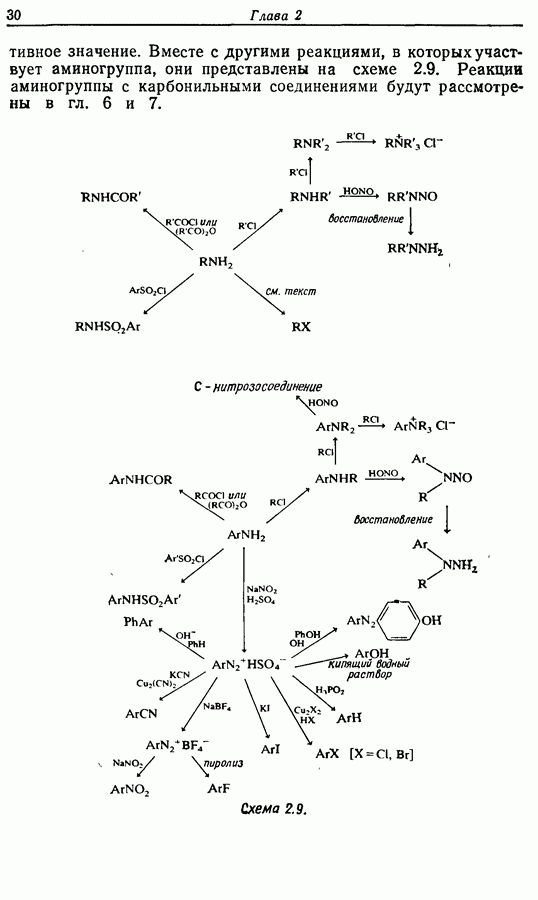
- 2.7.2. Превращения аминогруппы
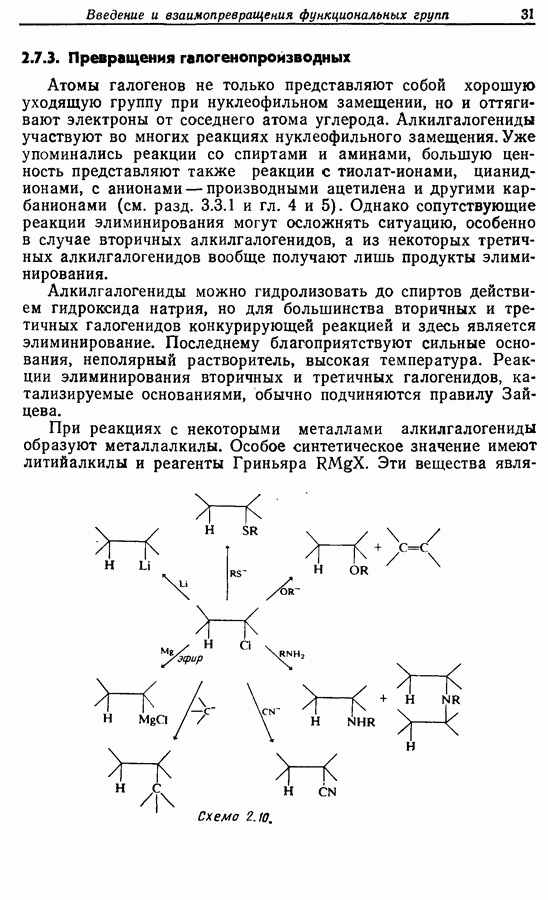
- 2.7.3. Превращения галогенопроизводных
- 2.7.4. Превращения нитросоединений
- 2.7.5. Превращения альдегидов и кетонов
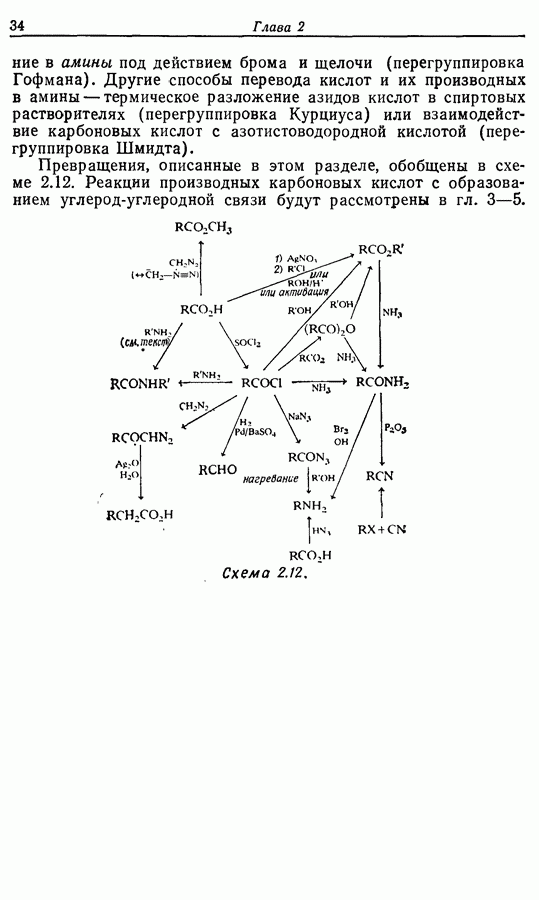
- 2.7.6. Превращения кислот и их производных
- 3. ПРИНЦИПЫ ОБРАЗОВАНИЯ УГЛЕРОД-УГЛЕРОДНОЙ СВЯЗИ
- 3.2. Расчленение и синтоны
- 3.3. Электрофильные углеродные частицы
- 3.4. Нуклеофильиые углеродные частицы
- 3.4.2. Стабилизированные карбанионы
- 3.4.3. Алкены, арены и гетероарены
- 4. ОБРАЗОВАНИЕ УГЛЕРОД-УГЛЕРОДНЫХ СВЯЗЕЙ: РЕАКЦИИ МЕТАЛЛООРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 4.1. Реактивы Гриньяра и электрофилы
- 4.2. Другие металлоорганические реактивы и электрофилы
- 4.2.2. Цинк- и кадмийорганические соединения
- 4.2.3. Органические соединения меди (I)
- 4.3. Реакции нуклеофилов, образованных из алкинов-1
- 4.3.2. Алкинильные соединения меди (I)
- 4.4. Выводы
- 4.5. Примеры
- 5. ОБРАЗОВАНИЕ УГЛЕРОД-УГЛЕРОДНЫХ СВЯЗЕЙ: ИСПОЛЬЗОВАНИЕ СТАБИЛИЗИРОВАННЫХ КАРБАНИОНОВ И РОДСТВЕННЫХ НУКЛЕОФИЛОВ
- 5.1.1. Алкилирование
- 5.1.2. Гидролиз алкинированных продуктов: путь к карбоновым кислотам и кетонам
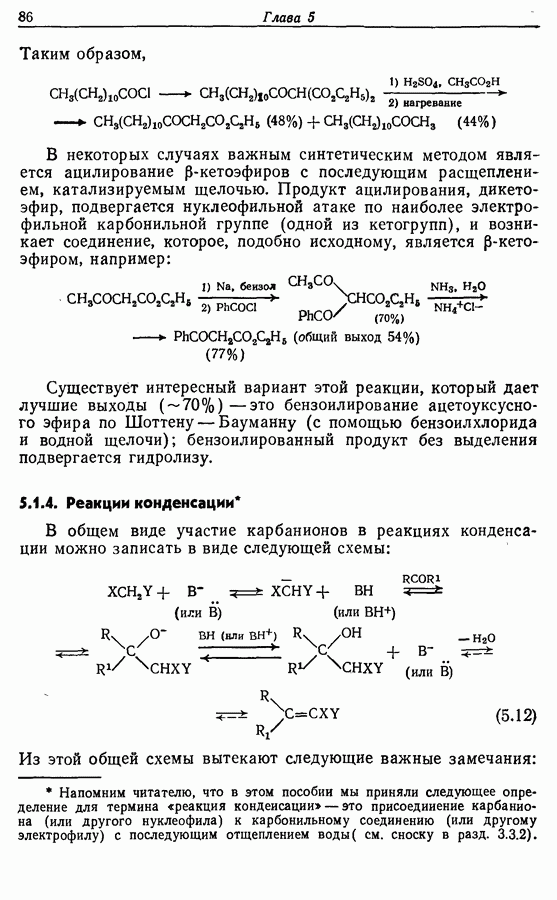
- 5.1.3. Ацилирование
- 5.1.4. Реакции конденсации
- 5.1.5. Реакции с соединениями типа … и родственными системами: реакция Михаэля
- 5.2. Карбанионы, стабилизированные одной (-М)-группой
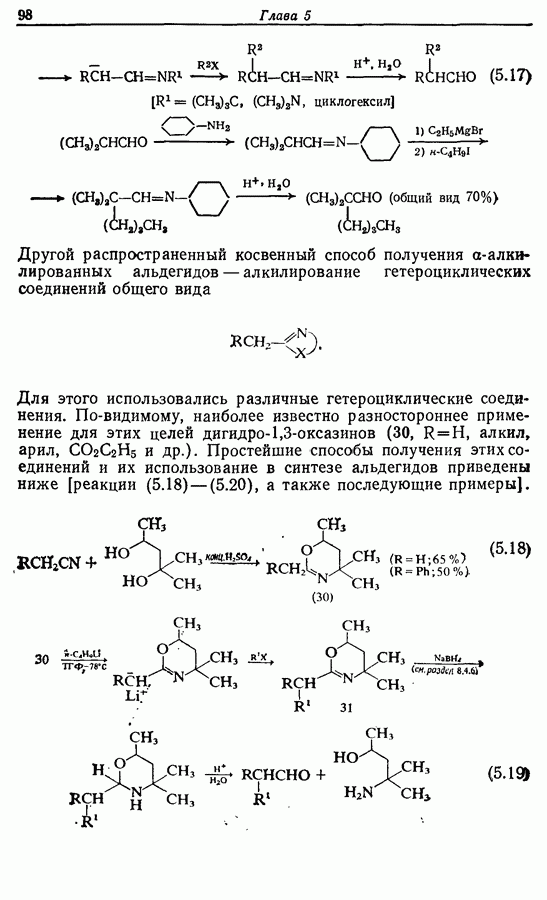
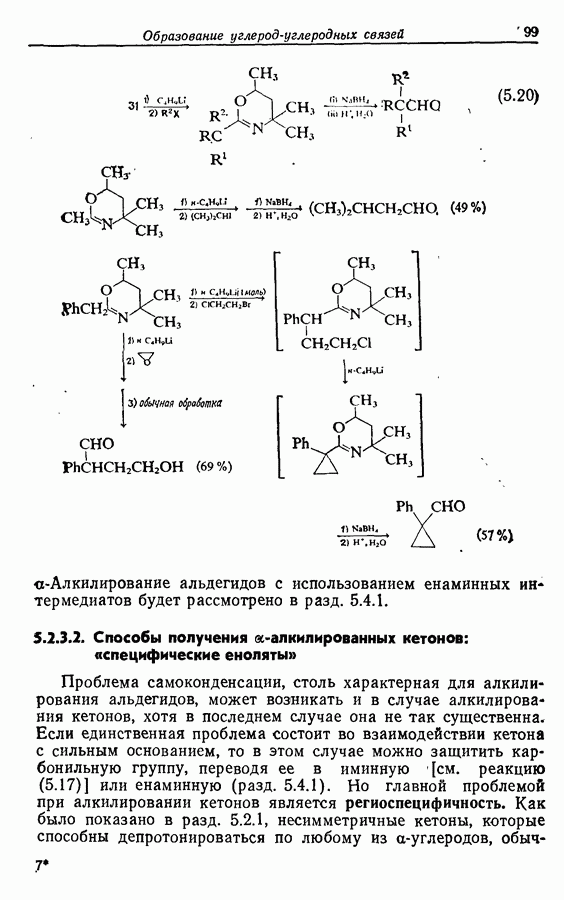
- 5.2.3. Косвенные пути получения a-алкилированных альдегидов и кетонов
- 5.2.4. Реакции конденсации
- 5.2.5. Реакция Михаэля
- 5.3. Карбанионы, стабилизированные соседними атомами фосфора или серы
- 5.3.2. Карбанионы, стабилизированные двумя атомами серы
- 5.4. Алкены, арены и гетероарены как нуклеофилы
- 5.4.3. Реакции присоединения и конденсации с карбонильными и родственными им соединениями
- 5.5. Заключение
- 5.6. Задачи
- 6. ОБРАЗОВАНИЕ СВЯЗЕЙ УГЛЕРОДА С ГЕТЕРОАТОМОМ: ОСНОВНЫЕ ПРИНЦИПЫ
- 6.1. Связи углерод — галоген
- 6.2. Связи углерод — кислород и углерод — сера
- 6.3. Связи углерод — азот
- 6.3.2. Электрофильный азот и нуклеофильный углерод
- 6.3.3. Нитрозосоединения, включая нитриты
- 7. ОБРАЗОВАНИЕ И РАСКРЫТИЕ ЦИКЛОВ
- 7.1. Внутримолекулярная циклизация в результате электрофильно-нуклеофильного взаимодействия
- 7.1.2. Условия внутримолекулярного циклообразования. Правила Болдуина
- 7.1.3. Присоединение по Михаэлю в процессах циклизации
- 7.1.4. Образование ароматических и гетероароматических циклов
- 7.2. Циклоприсоединение
- 7.2.2. 1,3-Диполярное циклоприсоединение
- 7.2.3. Присоединение карбенов и нитренов к алкенам
- 7.3. Электроциклическое циклообразование
- 7.4. Раскрытие цикла
- 7.5. Выводы и задачи
- 8. ВОССТАНОВЛЕНИЕ
- 8.1. Каталитическое гидрирование
- 8.2. Восстановление гидридами металлов
- 8.3. Восстановление растворяющимися металлами
- 8.4. Восстановление определенных функциональных групп
- 8.4.2. Восстановление алкинов
- 8.4.3. Восстановление альдегидов и кетонов
- 8.4.4. Восстановление карбоновых кислот и их производных
- 8.4.5. Восстановление нитрилов
- 8.4.6. Восстановление иминов и оксимов, включая восстановительное алкилирование
- 8.5. Восстановительное расщепление связи углерод — гетероатом
- 8.6. Восстановительное раскрытие цикла в эпоксидах
- 8.7. Восстановление a,b-ненасыщенных карбонильных соединений
- 8.8. Восстановление сопряженных диенов
- 8.9. Восстановление ароматических и гетероароматических соединений
- 9. ОКИСЛЕНИЕ
- 9.2. Окисление углеводородов
- 9.2.2. Аллильное окисление
- 9.2.3. Бензильное окисление
- 9.2.4. Дегидрирование алканов, алкильных групп и алкенов
- 9.2.5. Окислительное присоединение к алкенам
- 9.2.6. Окислительная деструкция алкенов
- 9.2.7. Окисление алкинов
- 9.3. Окисление спиртов и их производных
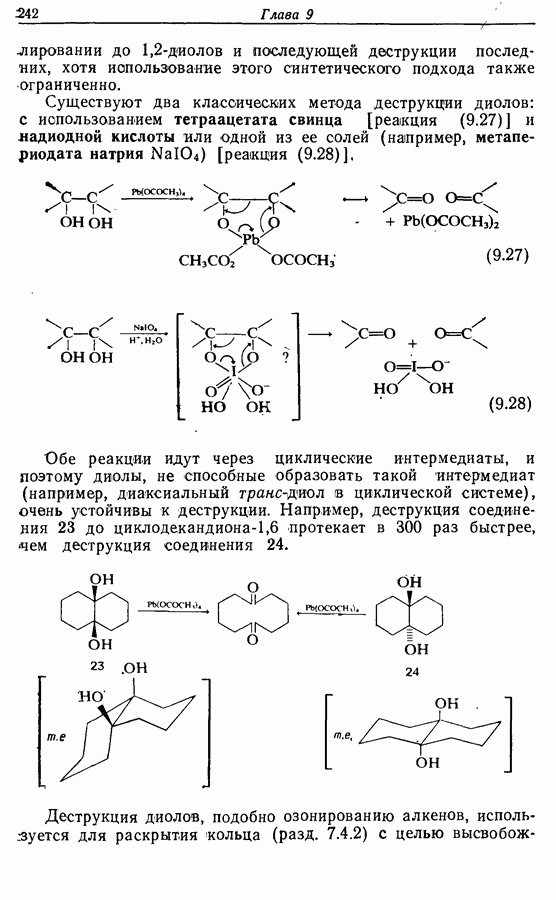
- 9.3.2. Окислительная деструкция 1,2-диолов
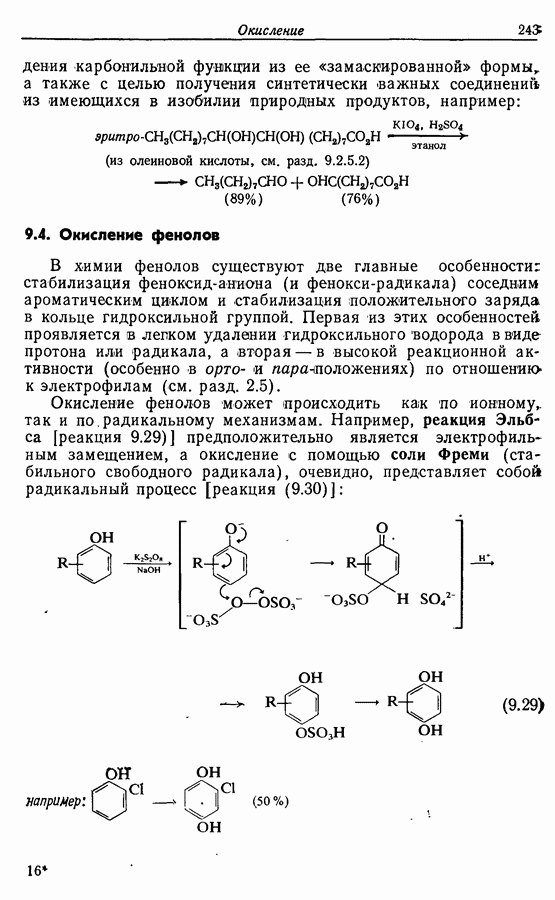
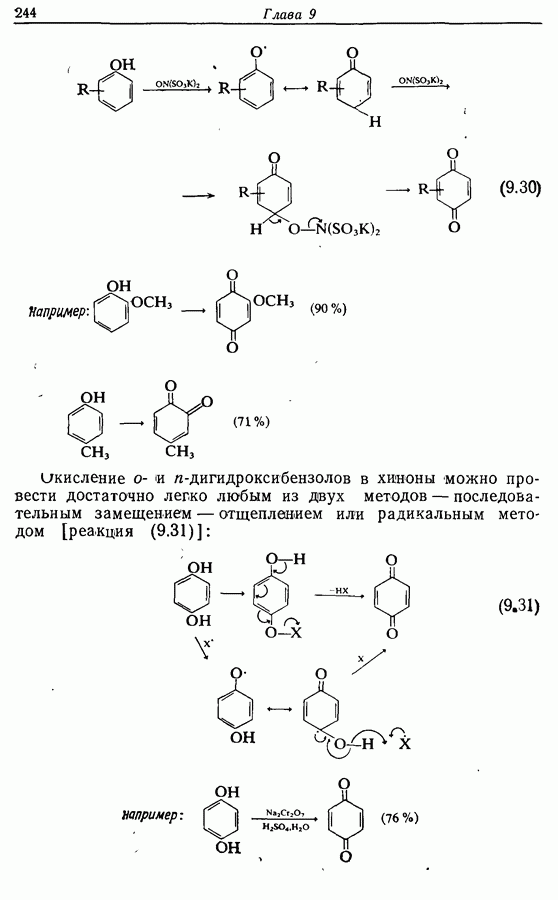
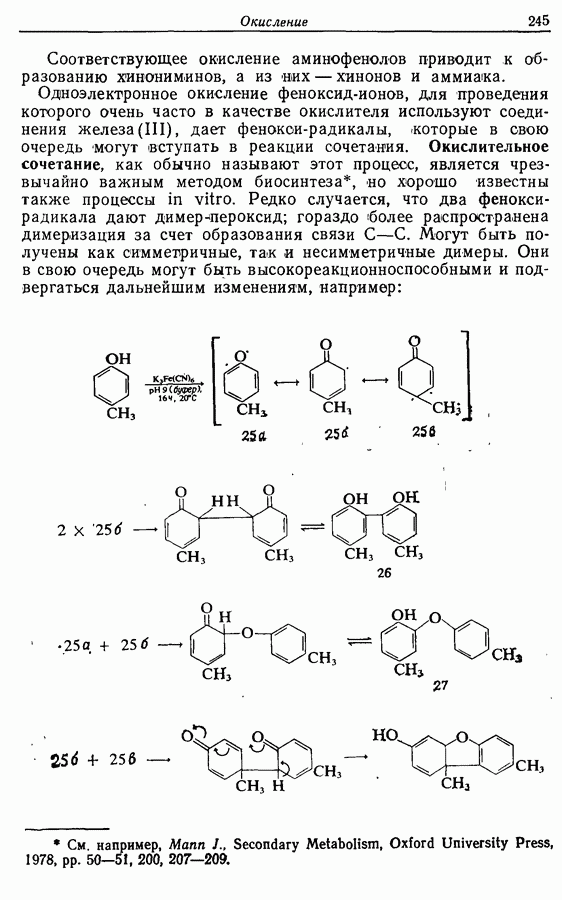
- 9.4. Окисление фенолов
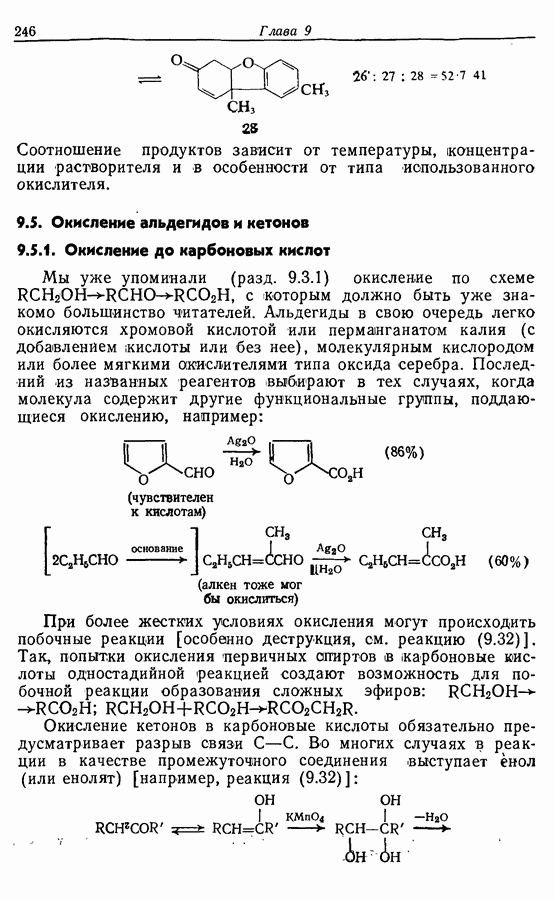
- 9.5. Окисление альдегидов и кетонов
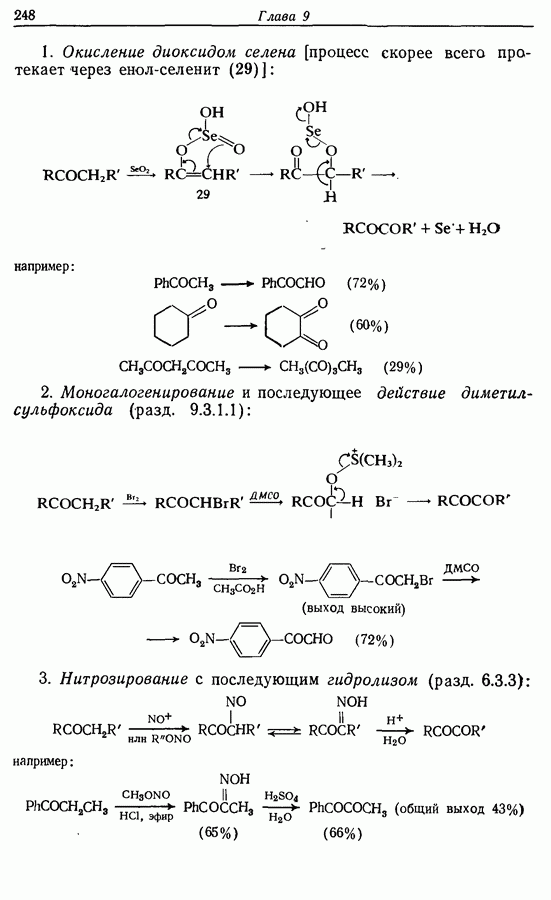
- 9.5.2. Окисление в 1,2-дикарбонильные соединения
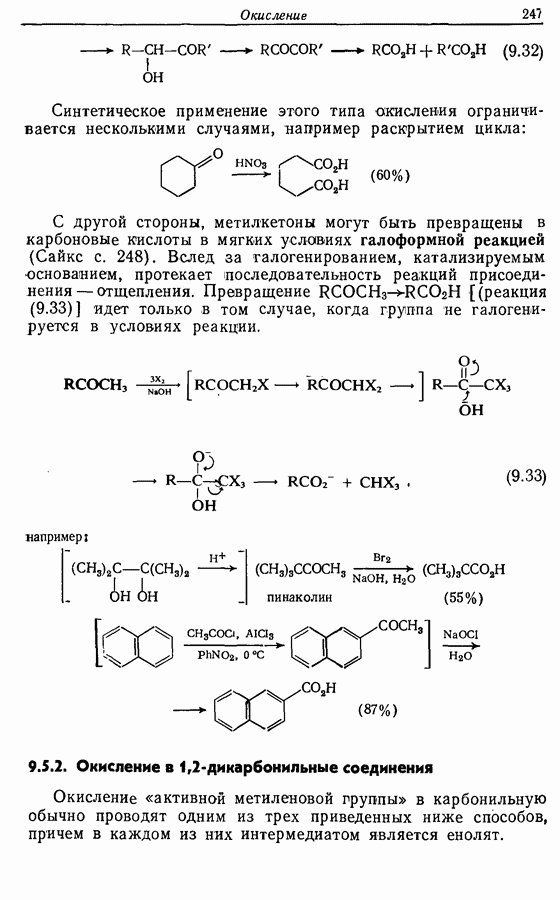
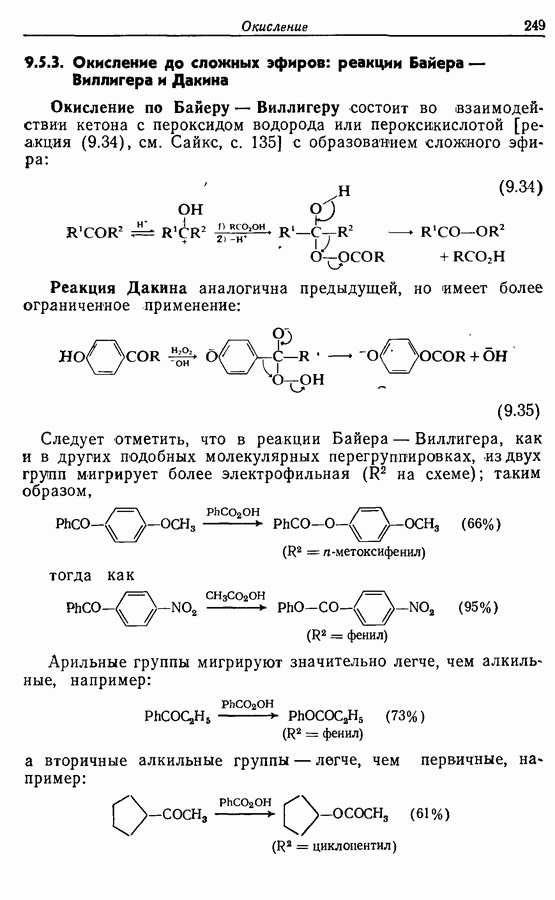
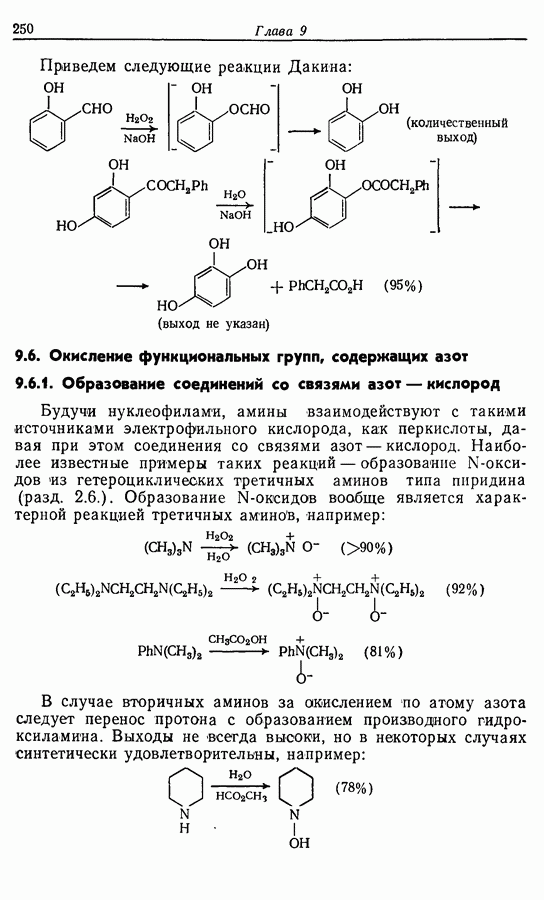
- 9.5.3. Окисление до сложных эфиров: реакции Байера — Виллигера и Дакина
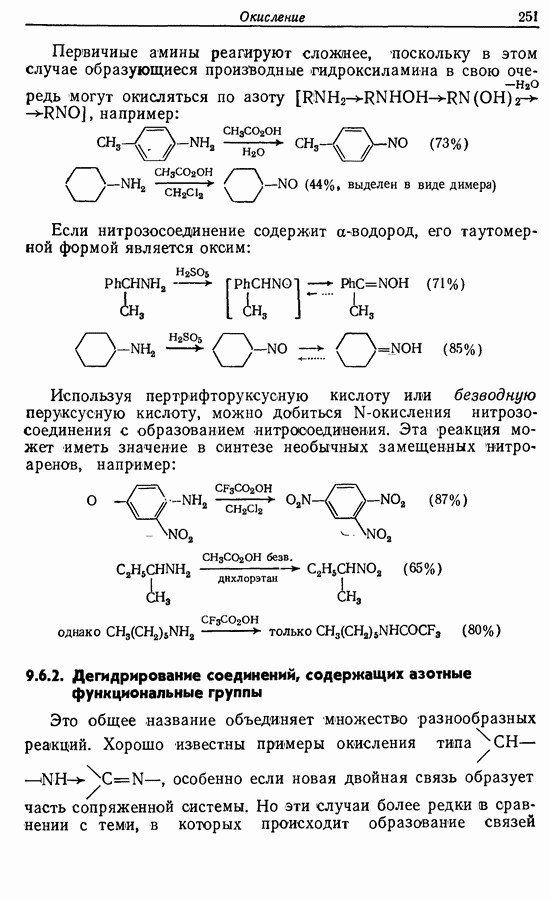
- 9.6. Окисление функциональных групп, содержащих азот
- 9.6.2. Дегидрирование соединений, содержащих азотные функциональные группы
- 9.7. Окисление серусодержащих функциональных групп
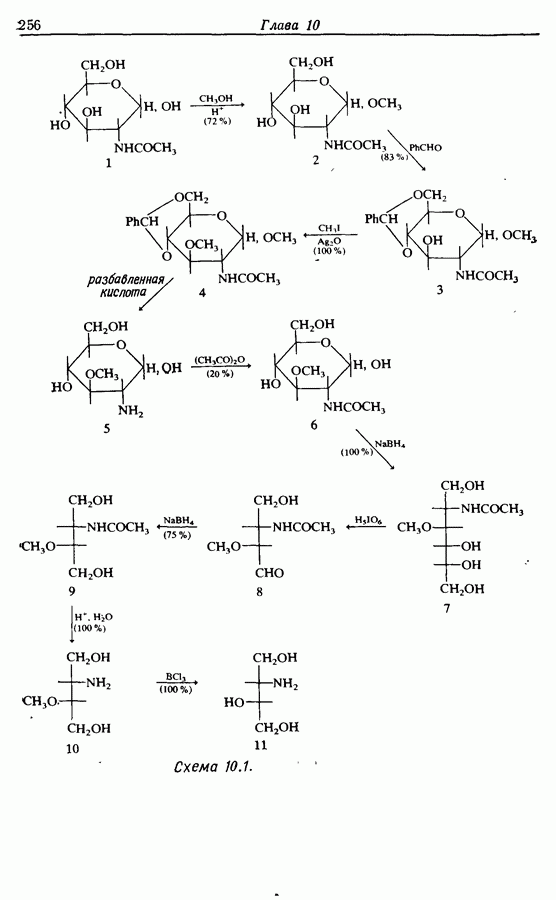
- 10. ЗАЩИТНЫЕ ГРУППЫ
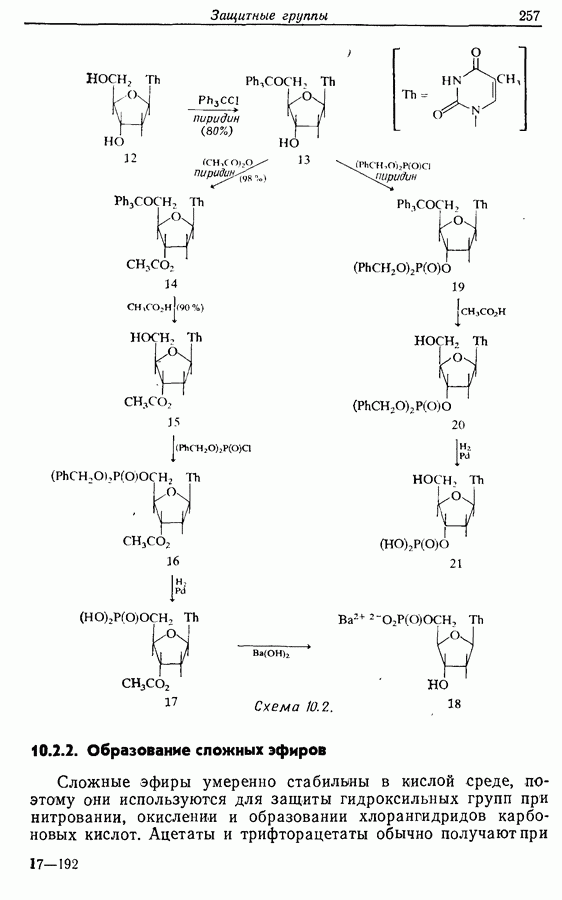
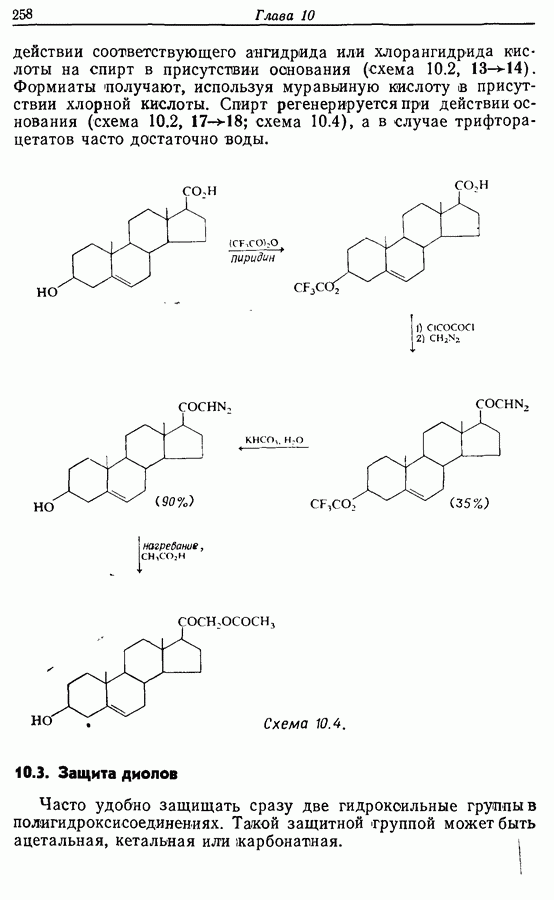
- 10.2. Защита спиртов
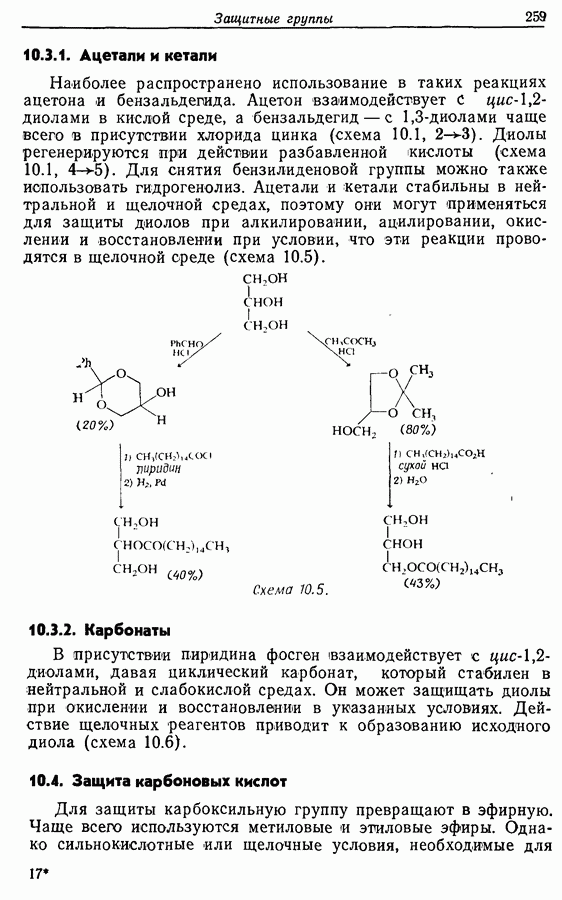
- 10.3. Защита диолов
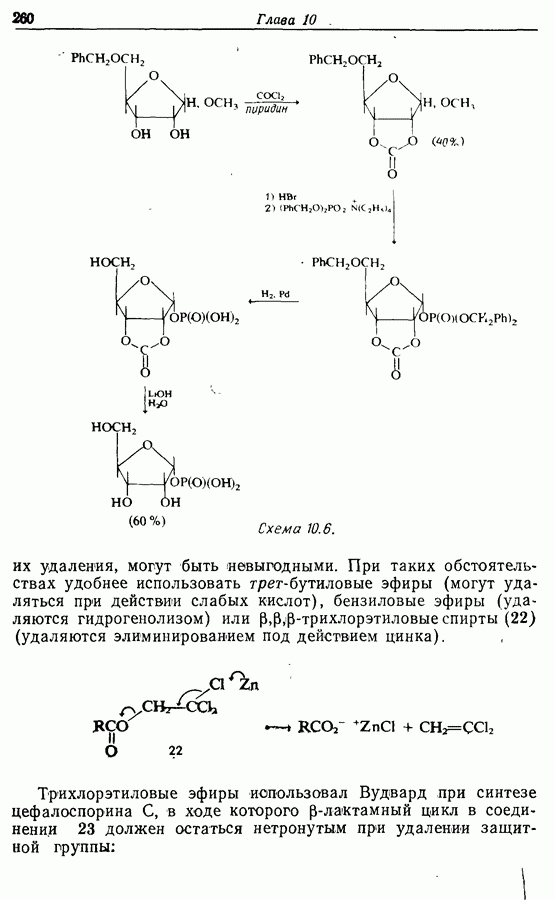
- 10.4. Защита карбоновых кислот
- 10.5. Защита аминогрупп
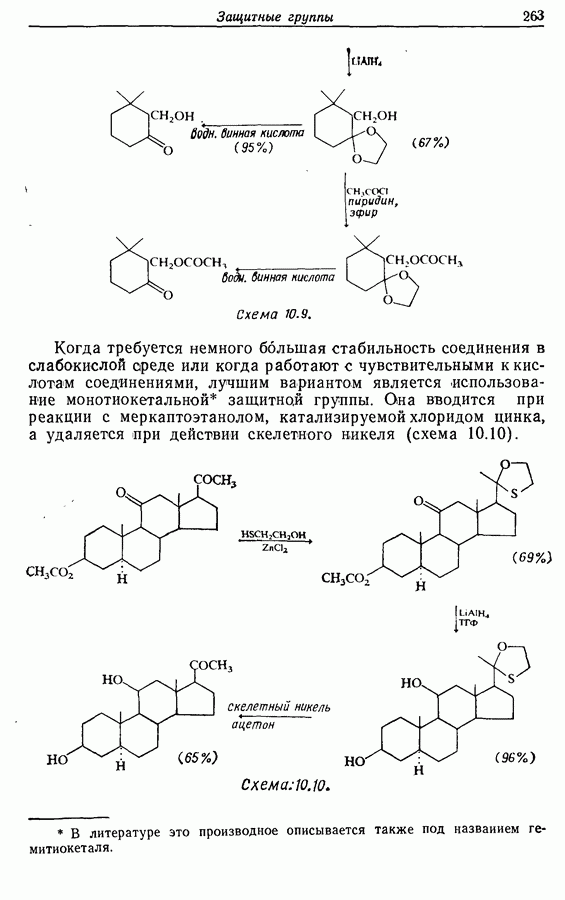
- 10.6. Защита карбонильных групп
- 11. БОРСОДЕРЖАЩИЕ РЕАГЕНТЫ
- 11.1. Гидроборирование алкенов при действии борана
- 11.2. Гидроборирование алкенов действием алкилборанов
- 11.3. Реакции борорганических соединений
- 11.4. Гидроборирование диенов
- 11.5. Гидроборирование алкинов
- 12. ФОСФОРСОДЕРЖАЩИЕ РЕАГЕНТЫ
- 12.1. Введение в химию фосфорорганических соединений
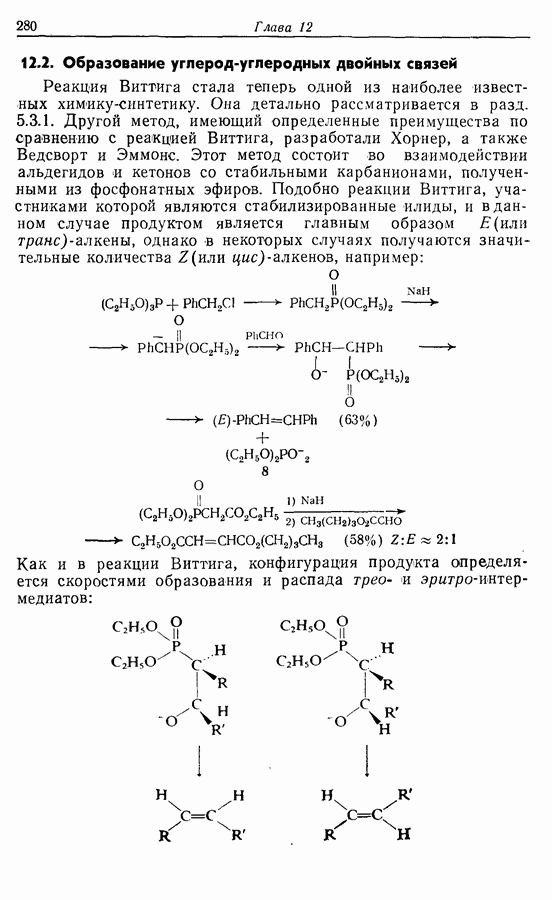
- 12.2. Образование углерод-углеродных двойных связей
- 12.3. Превращения функциональных групп
- 12.4. Реакции дезоксигенирования
- 13. КРЕМНИЙСОДЕРЖАЩИЕ РЕАГЕНТЫ
- 13.1. Введение в химию кремнийорганических соединений
- 13.2. Синтез кремнийорганических соединений
- 13.3. Реакции с образованием углерод-углеродных связей
- 13.4. Синильная защита спиртов
- 14. ИЗБРАННЫЕ СИНТЕЗЫ
- 14.2. Z-Геникосен-6-он-11
- 14.3. Синтез Z-жасмона
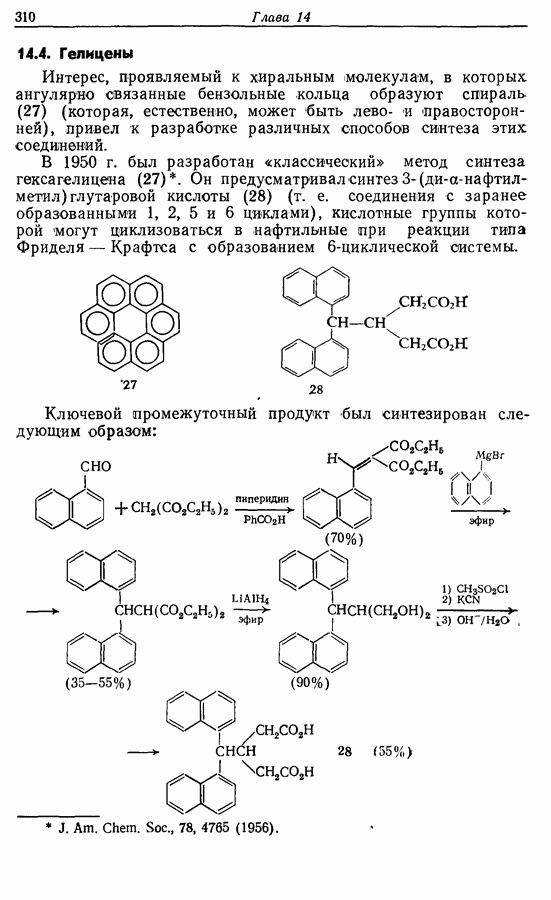
- 14.4. Гелицены
- 14.5. Анулены
- 14.6. Синтезы стероидов
- 14.6.2. Превращение растительных стероидов в стероидные гормоны
- 14.7. Синтез пептидов
- 14.7.2. Техника синтеза пептидов
- ЛИТЕРАТУРА