| << Предыдущий параграф | Следующий параграф >> |
Пред.
След.
Макеты страниц
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
ДЛЯ СТУДЕНТОВ И ШКОЛЬНИКОВ ЕСТЬ
ZADANIA.TO
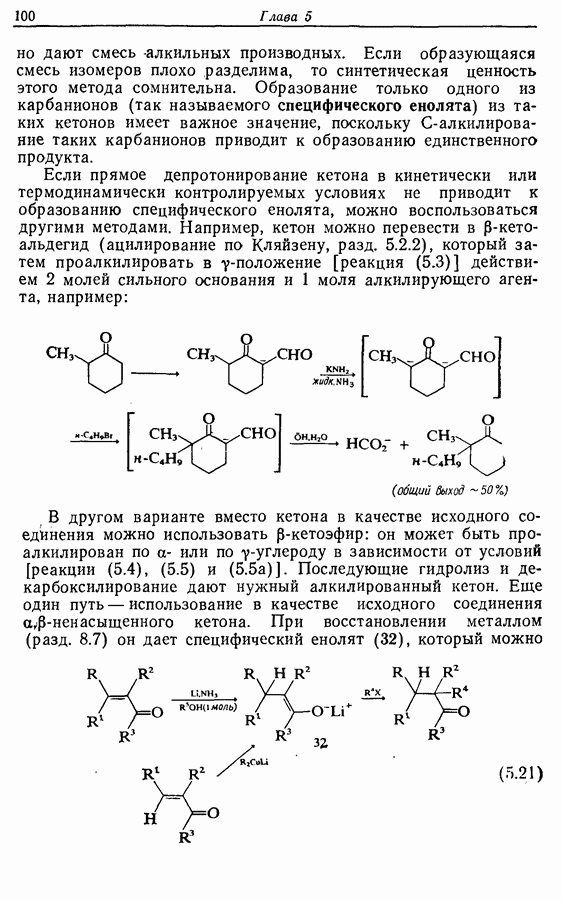
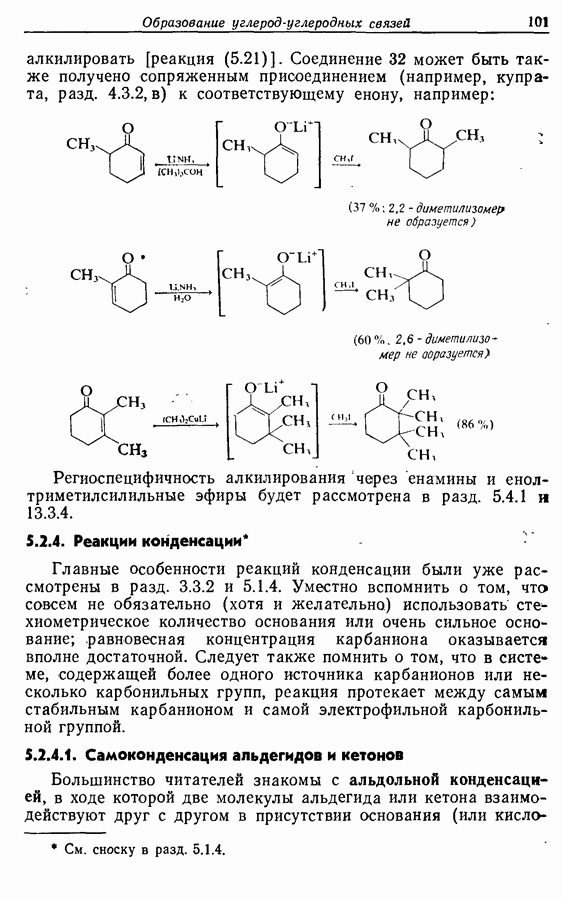
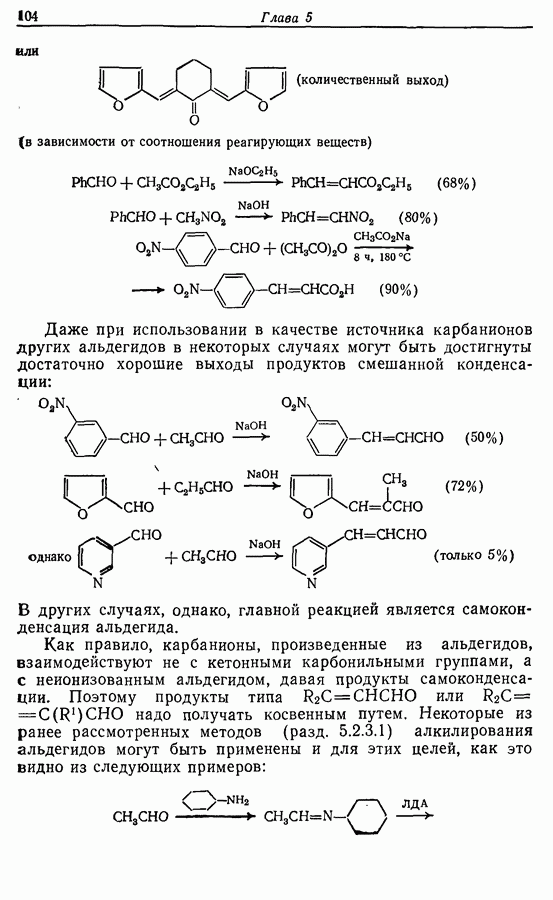
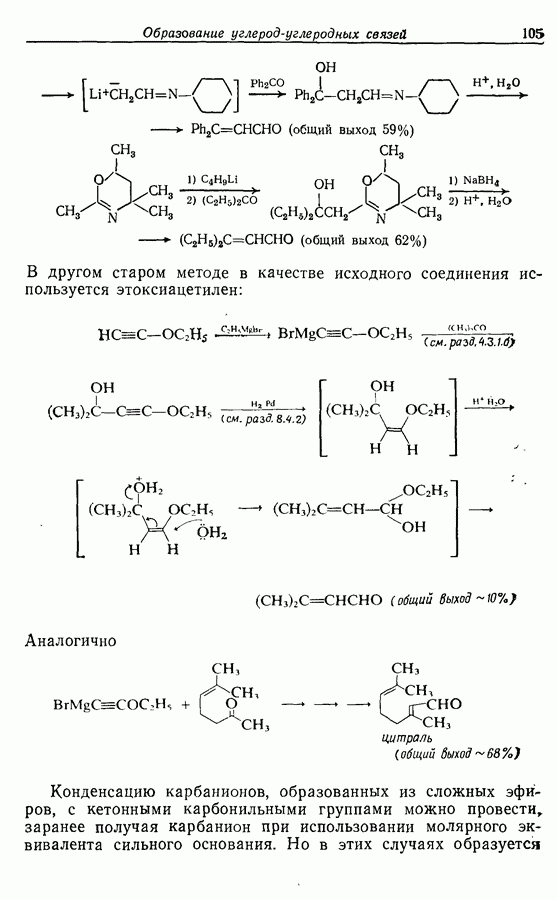
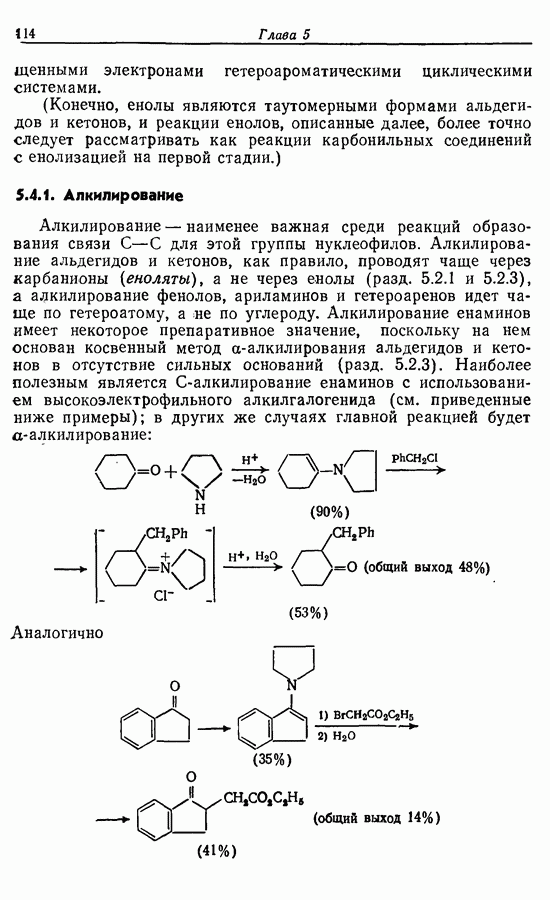
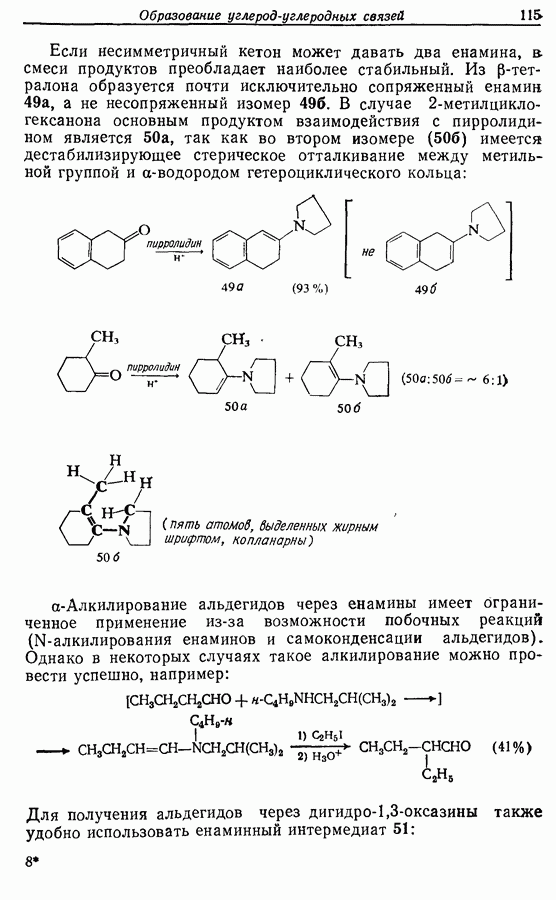
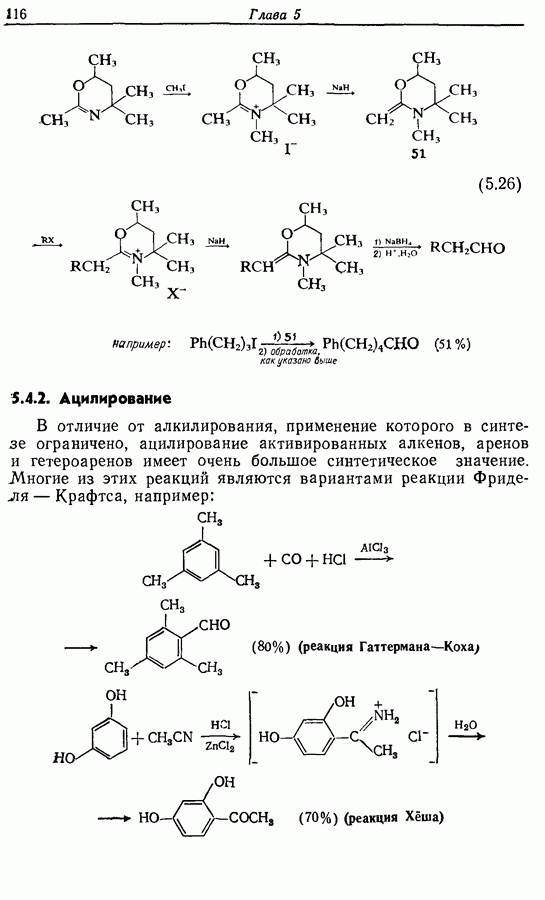
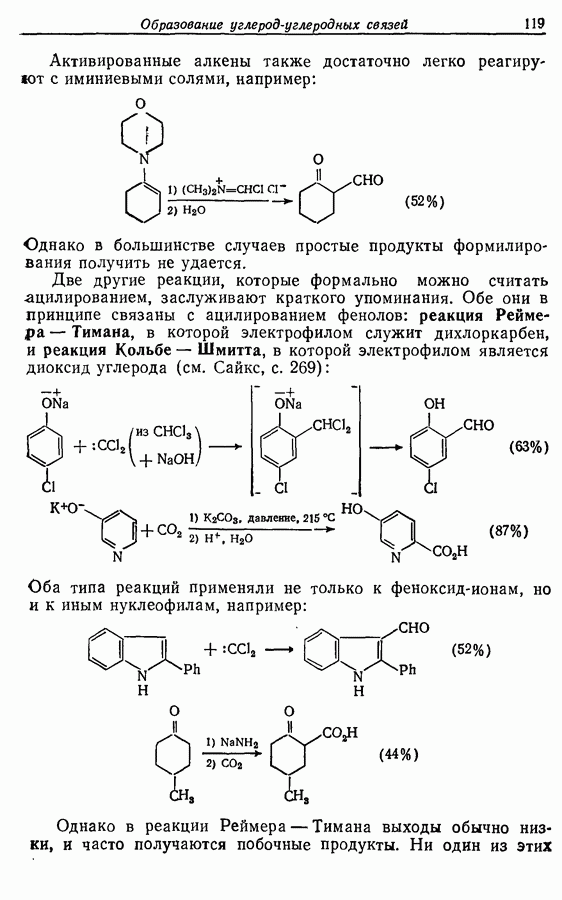
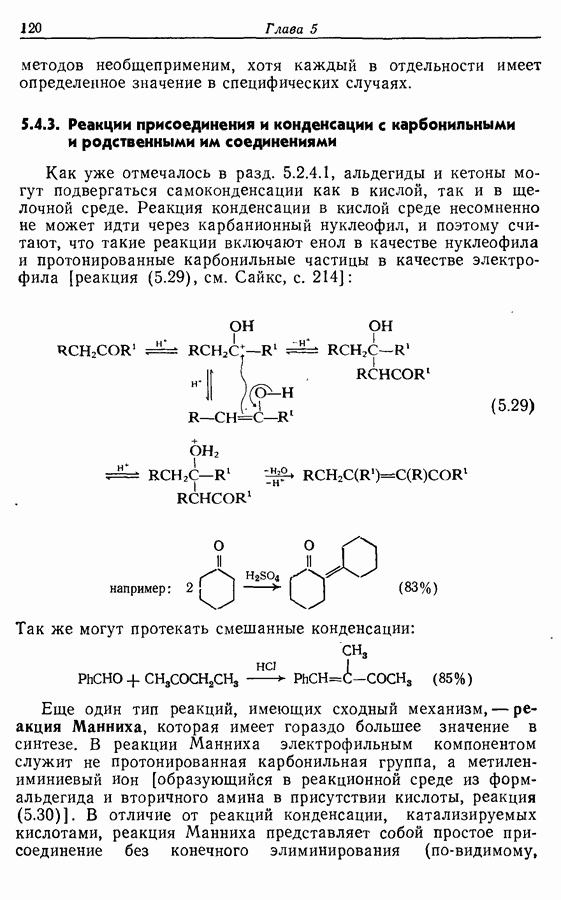
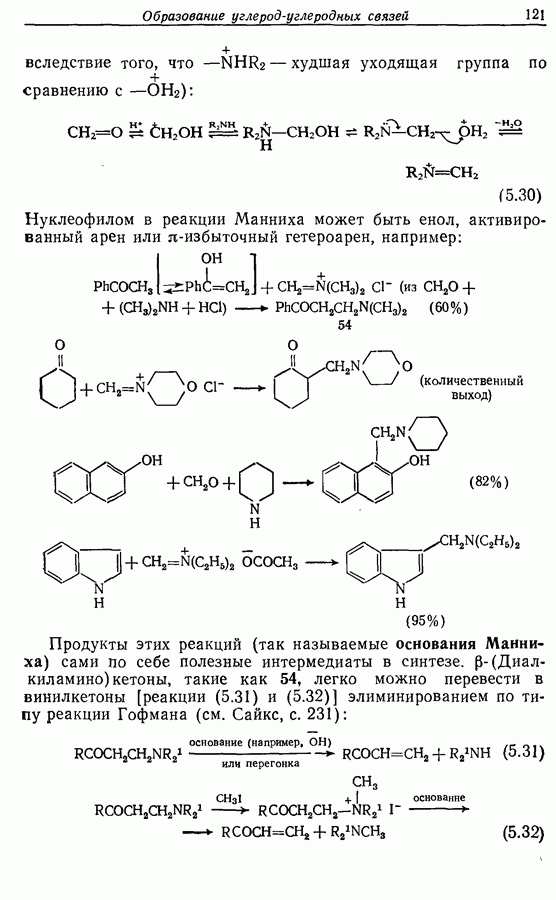
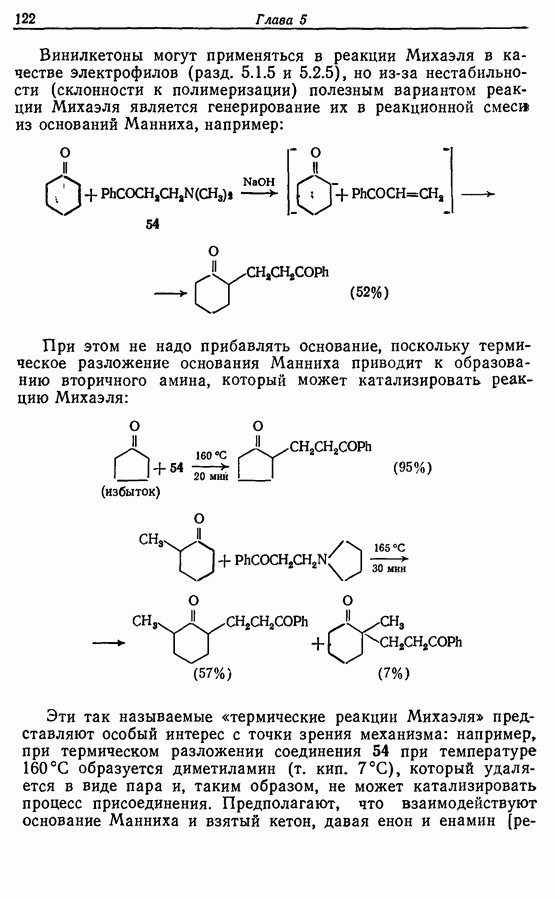
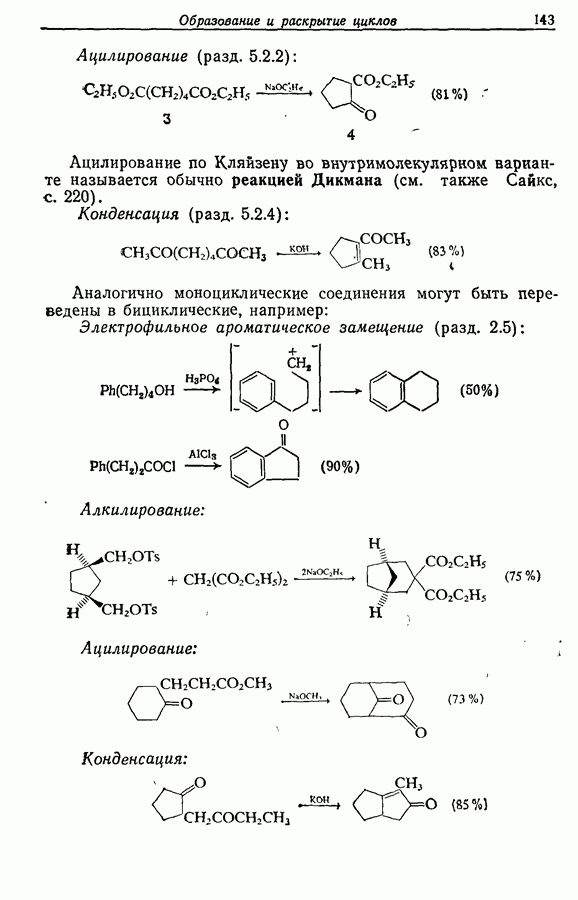
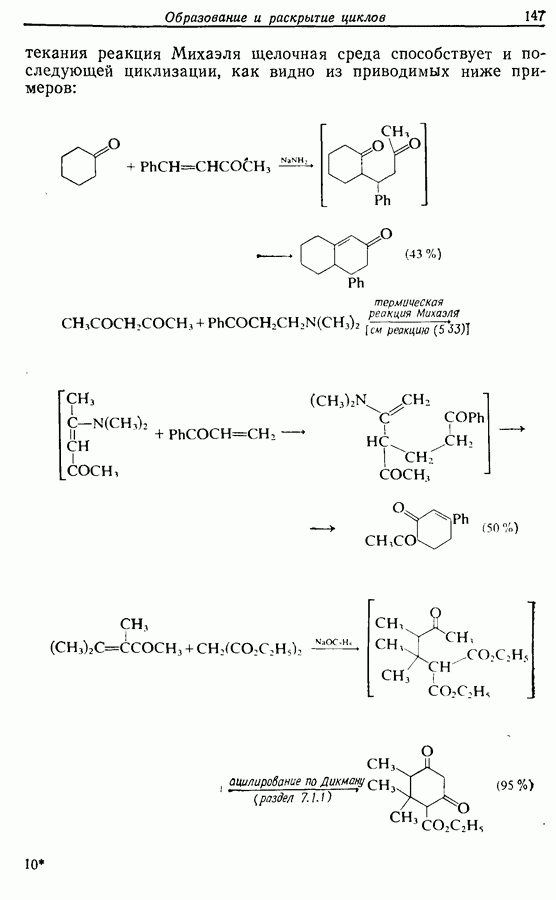
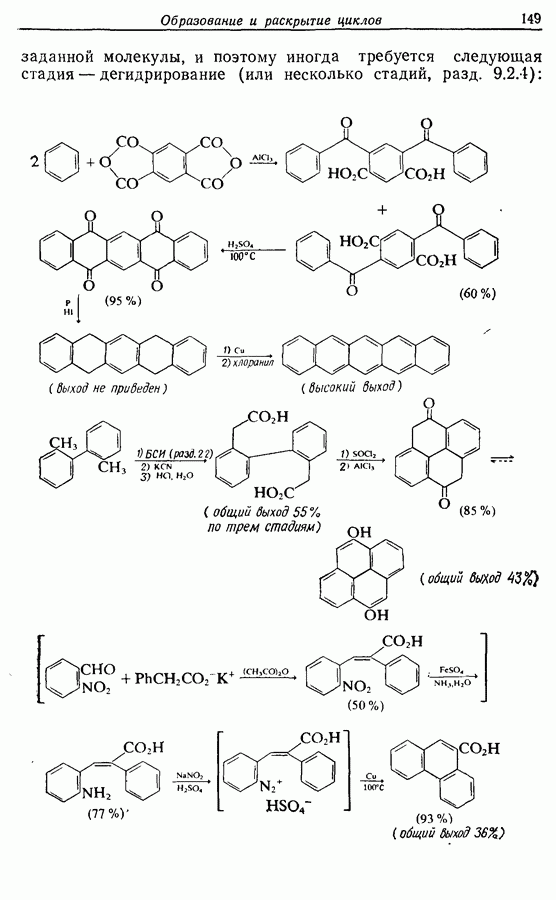
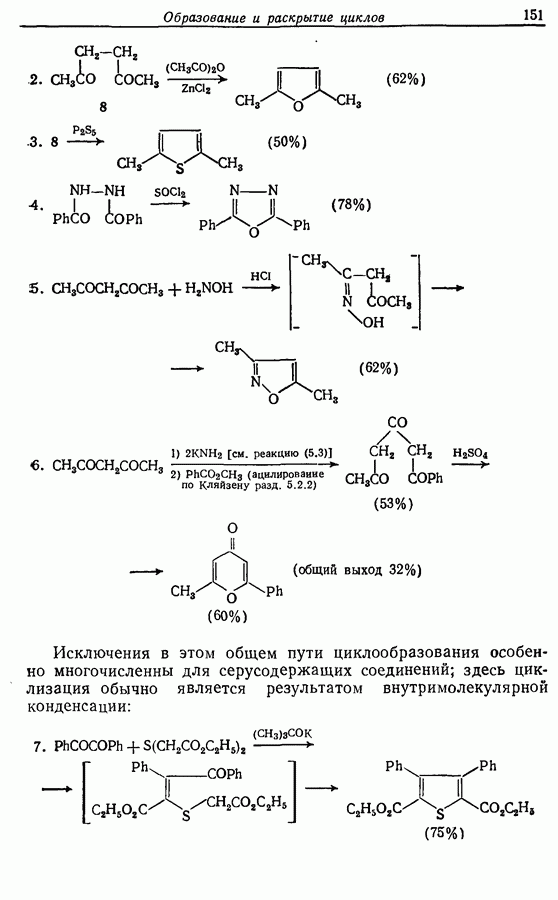
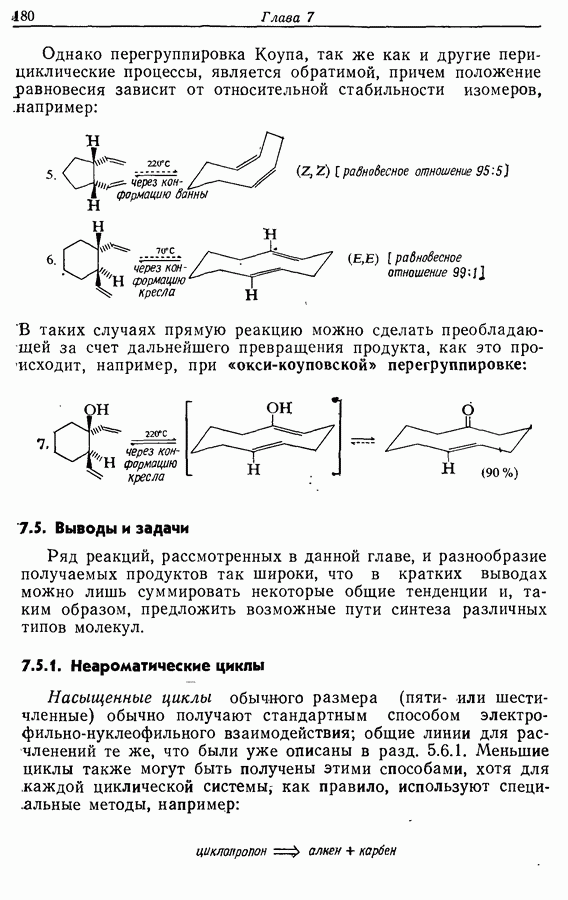
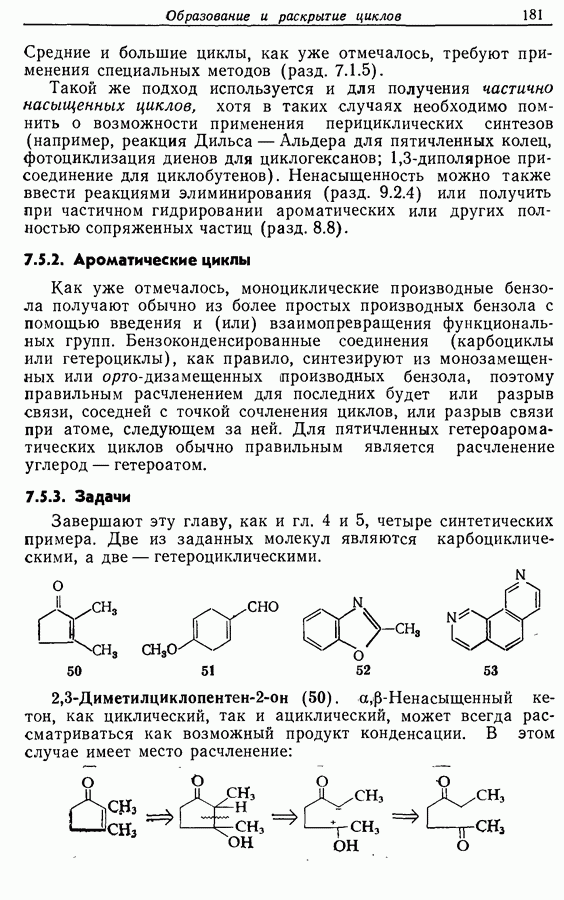
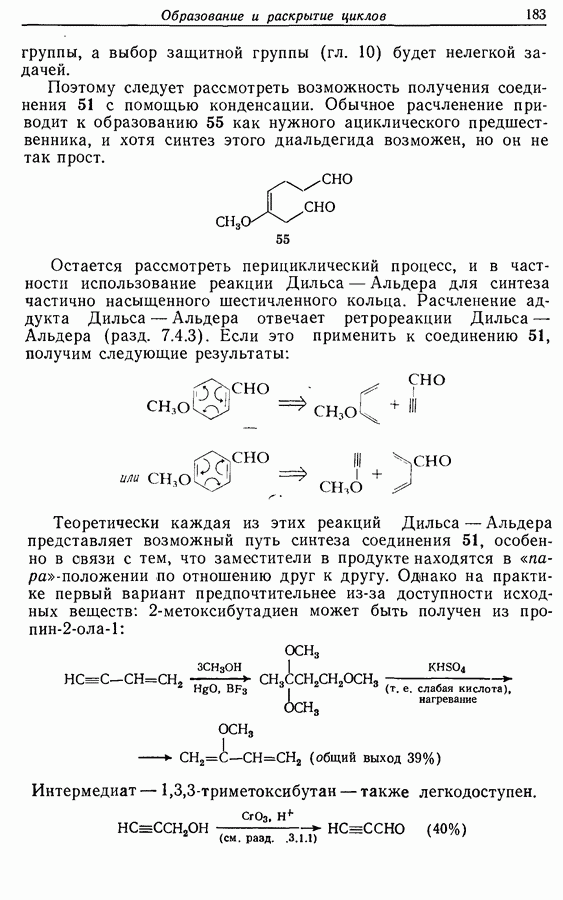
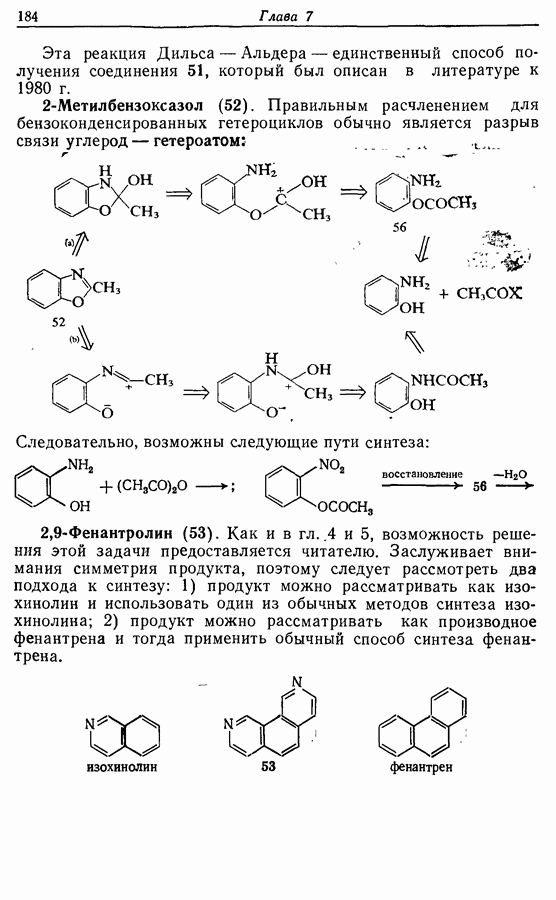
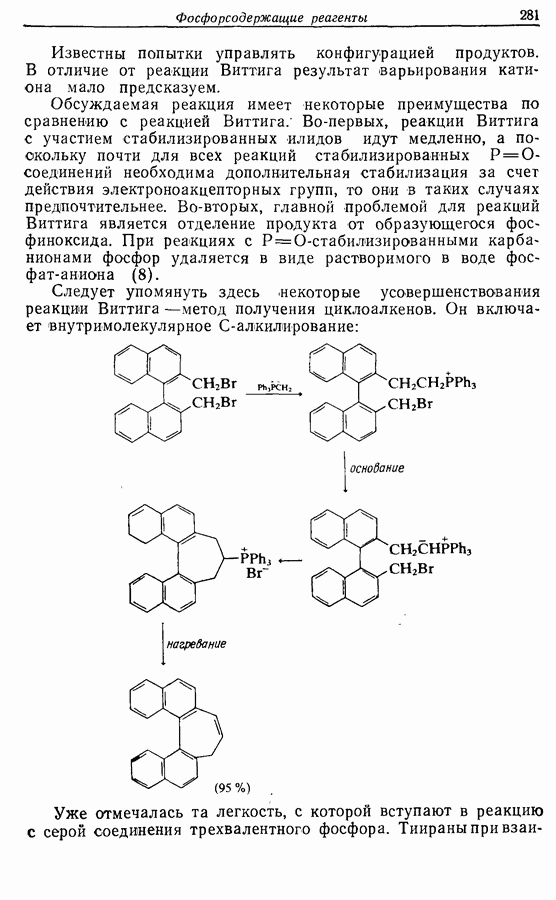
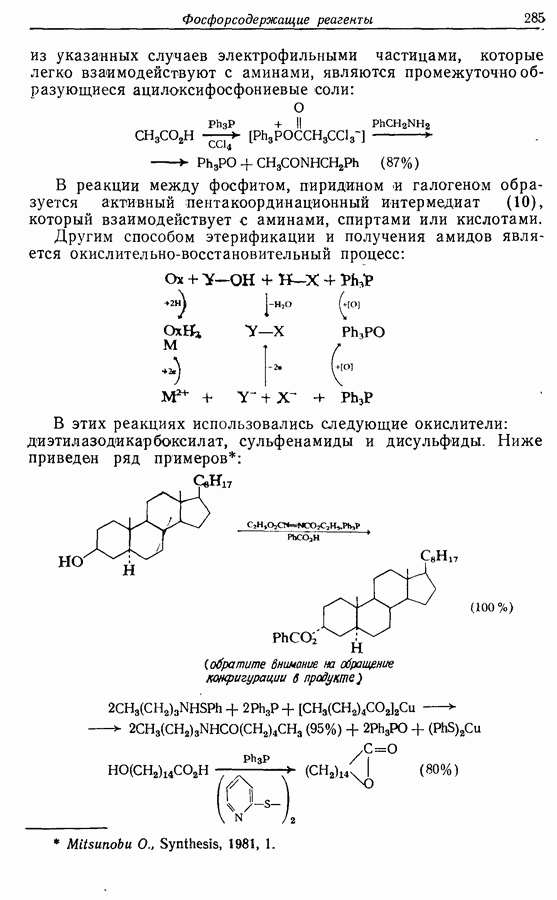
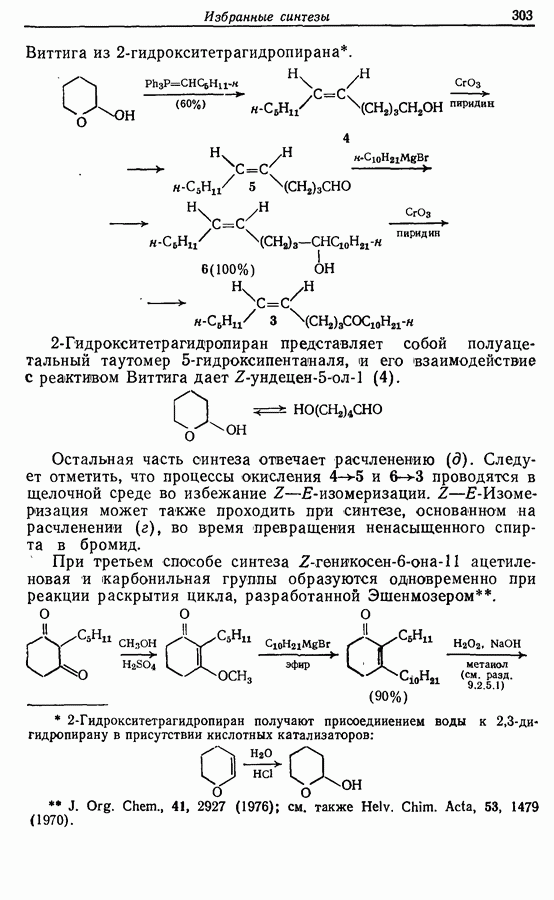
2.6. Введение функциональных групп в простые гетероциклические соединения
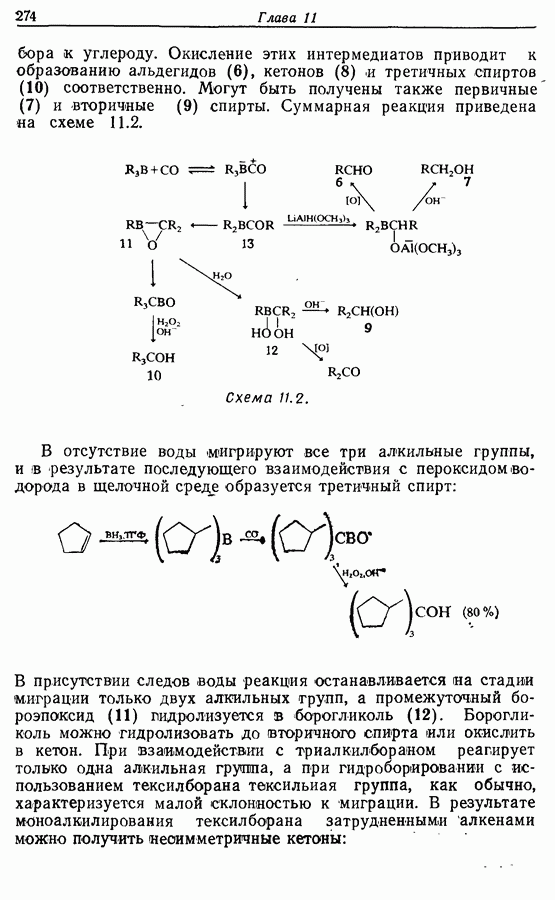
В данной книге мы можем только в общих чертах познакомить читателя с некоторыми из наиболее важных реакций простейших гетероциклических соединений. Для более подробного ознакомления с ними и с реакциями более сложных гетероциклических соединений следует обратиться к специальной литературе.
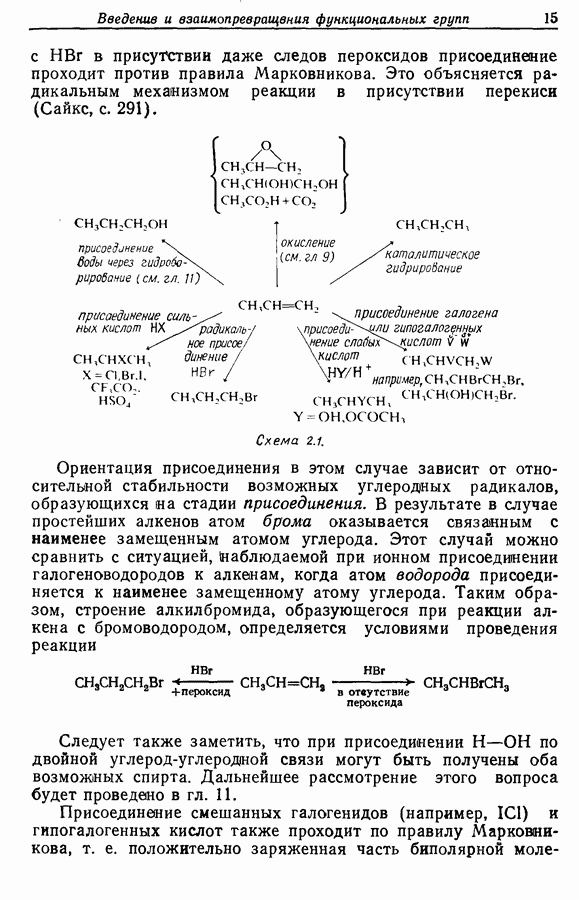
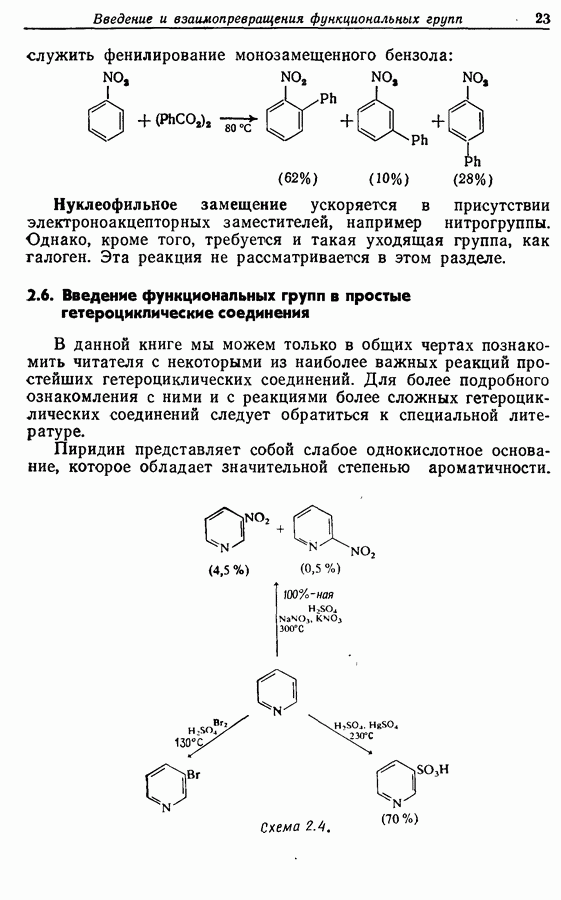
Пиридин представляет собой слабое однокислотное основание, которое обладает значительной степенью ароматичности.

Схема 2.4.
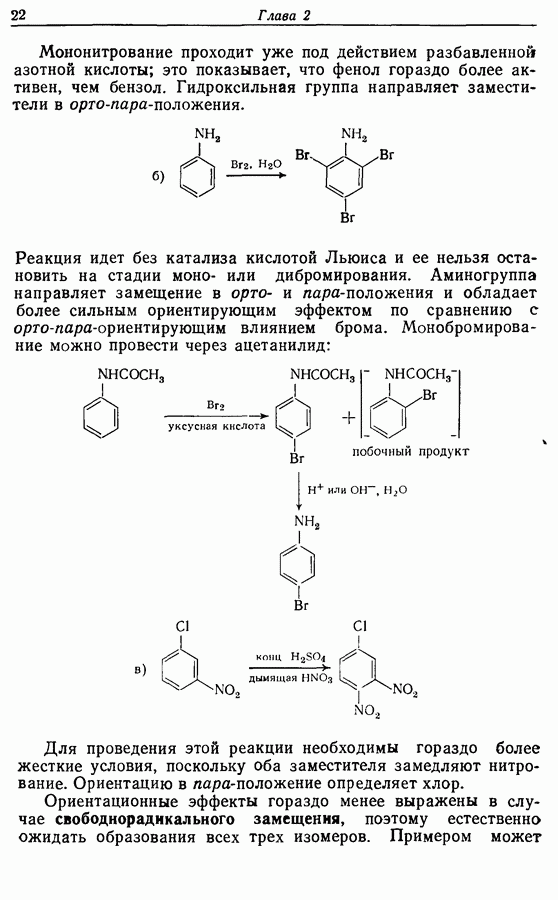
При взаимодействии с метилиодидом он образует четвертичную соль, которая при нагревании перегруппировывается в 2- и  -метилпиридинийиодиды. Расчеты по методу молекулярных орбиталей показывают, что наибольшая электронная плотность имеется на атоме
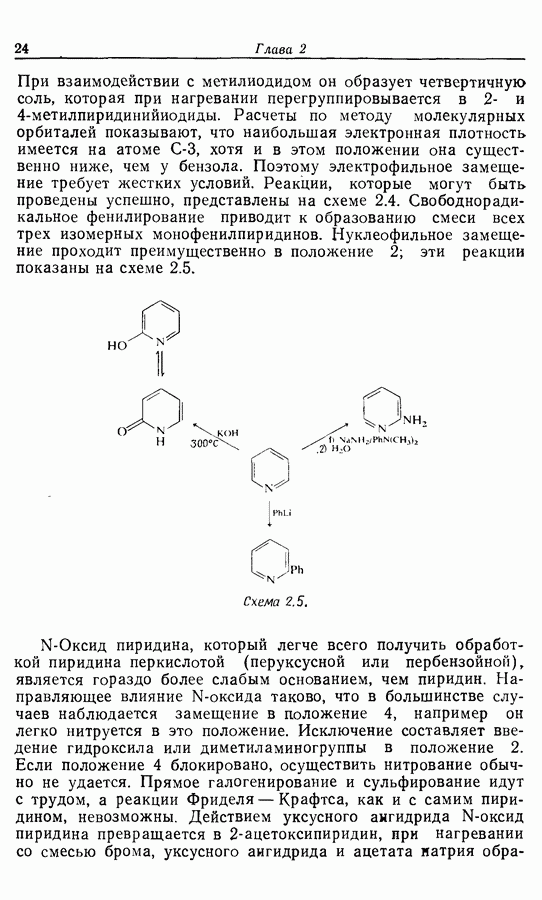
-метилпиридинийиодиды. Расчеты по методу молекулярных орбиталей показывают, что наибольшая электронная плотность имеется на атоме  хотя и в этом положении она существенно ниже, чем у бензола. Поэтому электрофильное замещение требует жестких условий. Реакции, которые могут быть проведены успешно, представлены на схеме 2.4. Свободнорадикальное фенилирование приводит к образованию смеси всех трех изомерных монофенилпиридинов. Нуклеофильное замещение проходит преимущественно в положение 2; эти реакции показаны на схеме 2.5.
хотя и в этом положении она существенно ниже, чем у бензола. Поэтому электрофильное замещение требует жестких условий. Реакции, которые могут быть проведены успешно, представлены на схеме 2.4. Свободнорадикальное фенилирование приводит к образованию смеси всех трех изомерных монофенилпиридинов. Нуклеофильное замещение проходит преимущественно в положение 2; эти реакции показаны на схеме 2.5.

Схема 2.5.
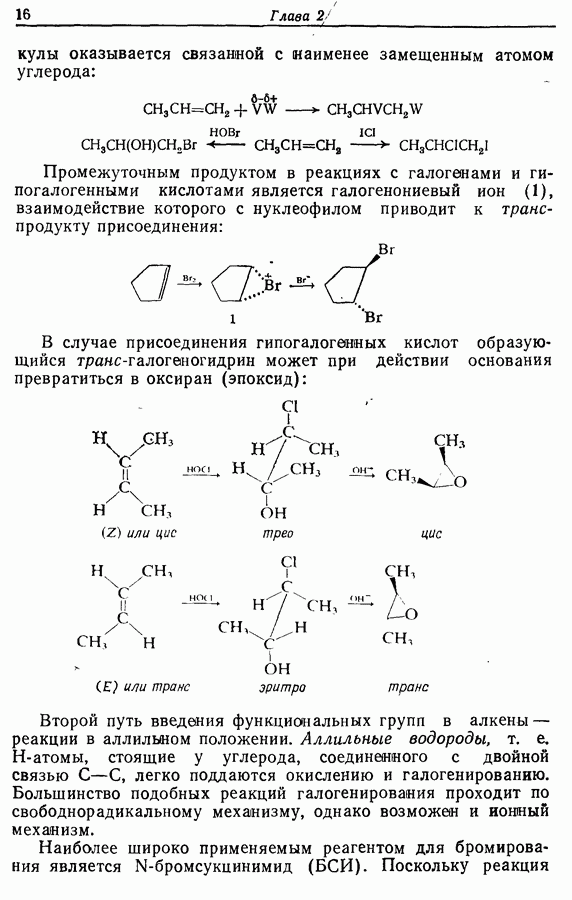
 -Оксид пиридина, который легче всего получить обработкой пиридина перкислотой (перуксусной или пербензойной), является гораздо более слабым основанием, чем пиридин. Направляющее влияние
-Оксид пиридина, который легче всего получить обработкой пиридина перкислотой (перуксусной или пербензойной), является гораздо более слабым основанием, чем пиридин. Направляющее влияние  -оксида таково, что в большинстве случаев наблюдается замещение в положение 4, например он легко нитруется в это положение. Исключение составляет введение гидроксила или диметиламиногруппы в положение 2. Если положение 4 блокировано, осуществить нитрование обычно не удается. Прямое галогенирование и сульфирование идут с трудом, а реакции Фриделя-Крафтса, как и с самим пиридином, невозможны. Действием уксусного ангидрида
-оксида таково, что в большинстве случаев наблюдается замещение в положение 4, например он легко нитруется в это положение. Исключение составляет введение гидроксила или диметиламиногруппы в положение 2. Если положение 4 блокировано, осуществить нитрование обычно не удается. Прямое галогенирование и сульфирование идут с трудом, а реакции Фриделя-Крафтса, как и с самим пиридином, невозможны. Действием уксусного ангидрида  -оксид пиридина превращается в
-оксид пиридина превращается в  -ацетоксипиридин, при нагревании со смесью брома, уксусного ангидрида и ацетата натрия
-ацетоксипиридин, при нагревании со смесью брома, уксусного ангидрида и ацетата натрия
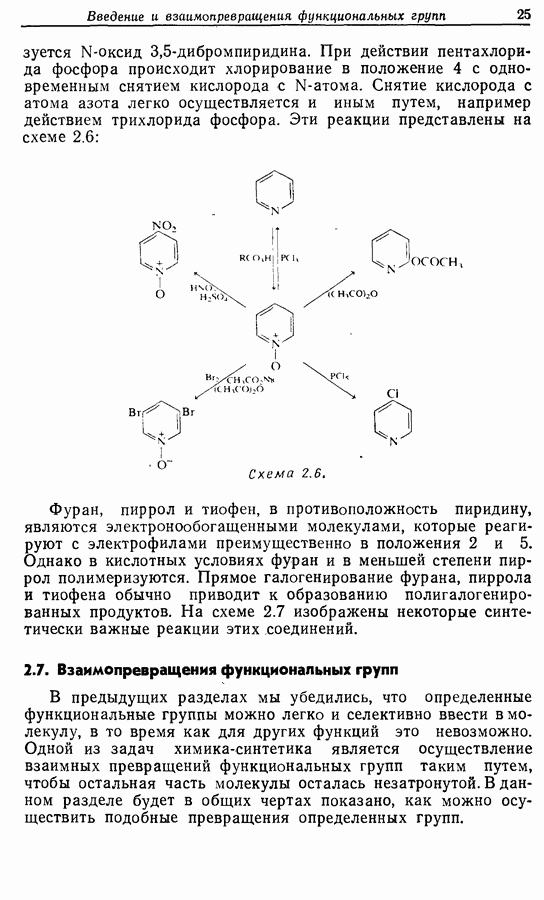
образуется N-оксид 3,5-дибромпиридина. При действии пентахлорида фосфора происходит хлорирование в положение 4 с одновременным снятием кислорода с  -атома. Снятие кислорода с атома азота легко осуществляется и иным путем, например действием трихлорида фосфора. Эти реакции представлены на схеме 2.6:
-атома. Снятие кислорода с атома азота легко осуществляется и иным путем, например действием трихлорида фосфора. Эти реакции представлены на схеме 2.6:

Схема 2.6.
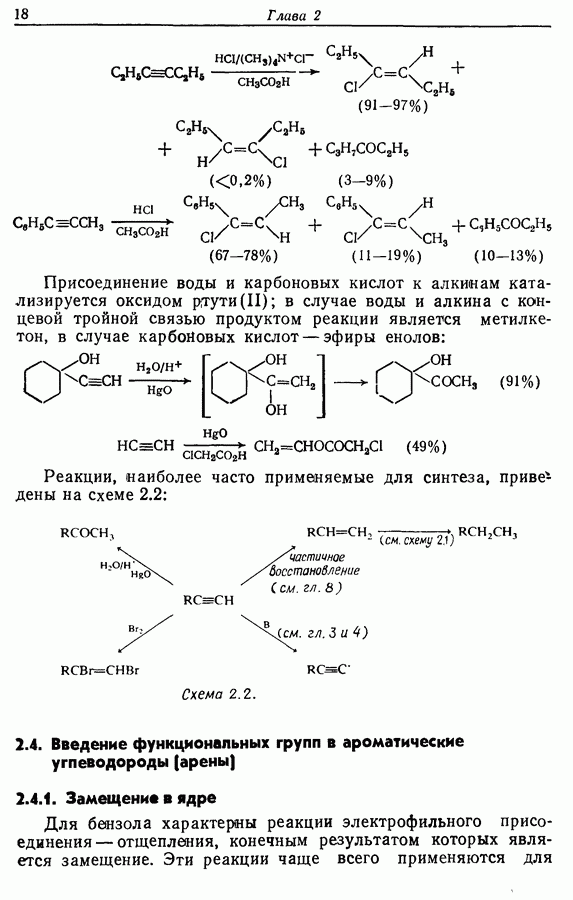
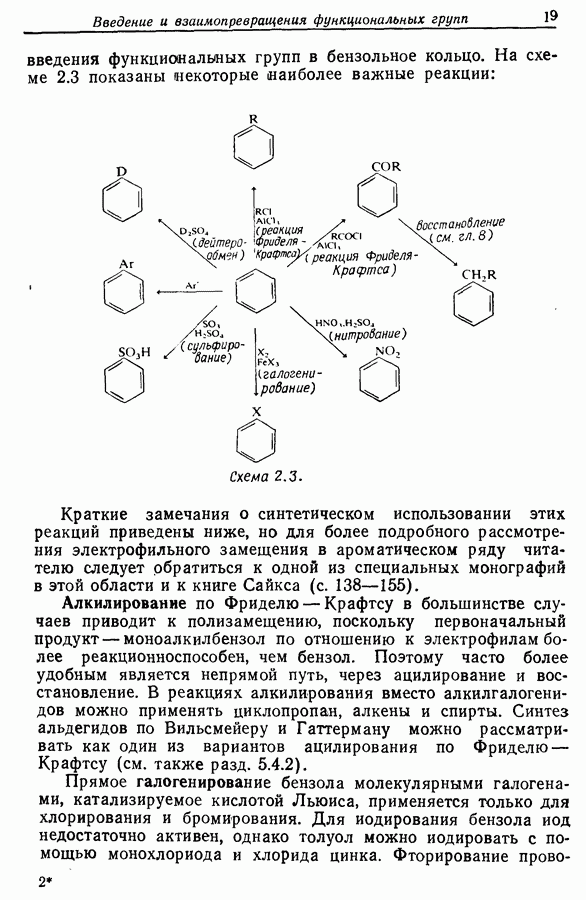
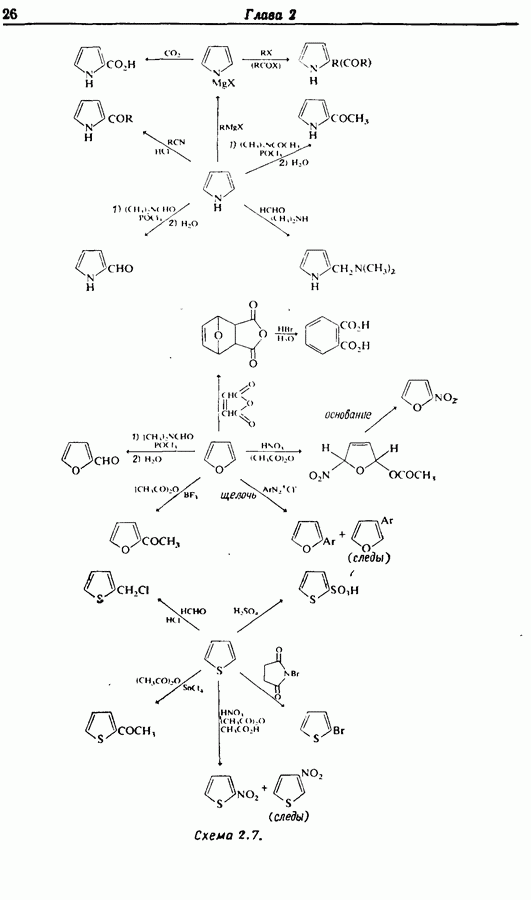
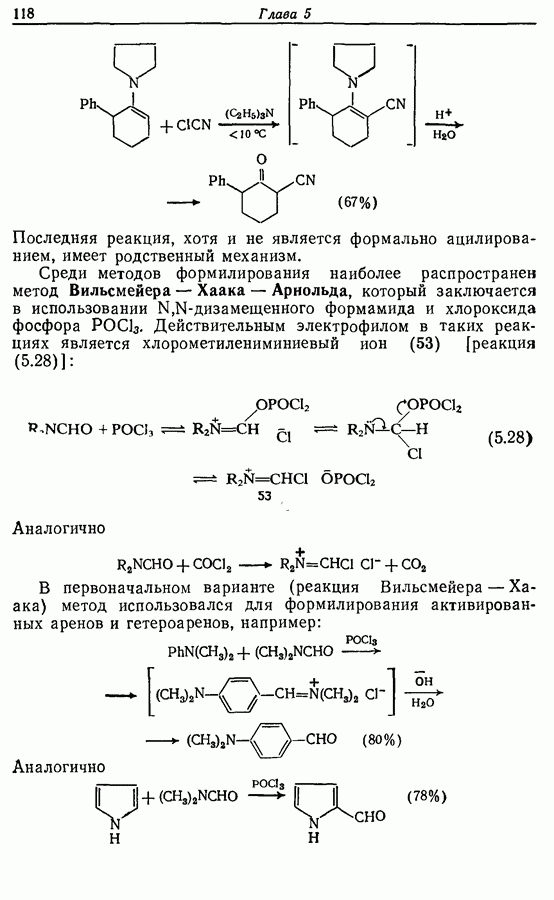
Фуран, пиррол и тиофен, в противоположность пиридину, являются электронообогащенными молекулами, которые реагируют с электрофилами преимущественно в положения 2 и 5. Однако в кислотных условиях фуран и в меньшей степени пиррол полимеризуются. Прямое галогенирование фурана, пиррола и тиофена обычно приводит к образованию полигалогенированных продуктов. На схеме 2.7 изображены некоторые синтетически важные реакции этих соединений.
| << Предыдущий параграф | Следующий параграф >> |
Оглавление
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- 1. ВВЕДЕНИЕ
- 2. ВВЕДЕНИЕ И ВЗАИМОПРЕВРАЩЕНИЯ ФУНКЦИОНАЛЬНЫХ ГРУПП
- 2.1. Введение функциональных групп в апканы
- 2.2. Введение функциональных групп в алкены
- 2.3. Введение функциональных групп в апкины
- 2.4. Введение функциональных групп в ароматические углеводороды (арены)
- 2.5. Введение функциональных групп в производные бензола
- 2.6. Введение функциональных групп в простые гетероциклические соединения
- 2.7. Взаимопревращения функциональных групп
- 2.7.2. Превращения аминогруппы
- 2.7.3. Превращения галогенопроизводных
- 2.7.4. Превращения нитросоединений
- 2.7.5. Превращения альдегидов и кетонов
- 2.7.6. Превращения кислот и их производных
- 3. ПРИНЦИПЫ ОБРАЗОВАНИЯ УГЛЕРОД-УГЛЕРОДНОЙ СВЯЗИ
- 3.2. Расчленение и синтоны
- 3.3. Электрофильные углеродные частицы
- 3.4. Нуклеофильиые углеродные частицы
- 3.4.2. Стабилизированные карбанионы
- 3.4.3. Алкены, арены и гетероарены
- 4. ОБРАЗОВАНИЕ УГЛЕРОД-УГЛЕРОДНЫХ СВЯЗЕЙ: РЕАКЦИИ МЕТАЛЛООРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 4.1. Реактивы Гриньяра и электрофилы
- 4.2. Другие металлоорганические реактивы и электрофилы
- 4.2.2. Цинк- и кадмийорганические соединения
- 4.2.3. Органические соединения меди (I)
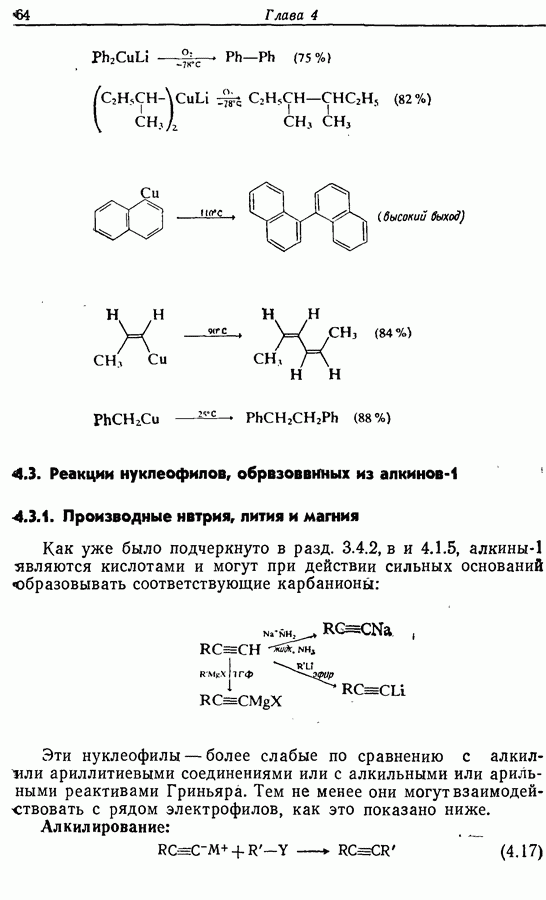
- 4.3. Реакции нуклеофилов, образованных из алкинов-1
- 4.3.2. Алкинильные соединения меди (I)
- 4.4. Выводы
- 4.5. Примеры
- 5. ОБРАЗОВАНИЕ УГЛЕРОД-УГЛЕРОДНЫХ СВЯЗЕЙ: ИСПОЛЬЗОВАНИЕ СТАБИЛИЗИРОВАННЫХ КАРБАНИОНОВ И РОДСТВЕННЫХ НУКЛЕОФИЛОВ
- 5.1.1. Алкилирование
- 5.1.2. Гидролиз алкинированных продуктов: путь к карбоновым кислотам и кетонам
- 5.1.3. Ацилирование
- 5.1.4. Реакции конденсации
- 5.1.5. Реакции с соединениями типа … и родственными системами: реакция Михаэля
- 5.2. Карбанионы, стабилизированные одной (-М)-группой
- 5.2.3. Косвенные пути получения a-алкилированных альдегидов и кетонов
- 5.2.4. Реакции конденсации
- 5.2.5. Реакция Михаэля
- 5.3. Карбанионы, стабилизированные соседними атомами фосфора или серы
- 5.3.2. Карбанионы, стабилизированные двумя атомами серы
- 5.4. Алкены, арены и гетероарены как нуклеофилы
- 5.4.3. Реакции присоединения и конденсации с карбонильными и родственными им соединениями
- 5.5. Заключение
- 5.6. Задачи
- 6. ОБРАЗОВАНИЕ СВЯЗЕЙ УГЛЕРОДА С ГЕТЕРОАТОМОМ: ОСНОВНЫЕ ПРИНЦИПЫ
- 6.1. Связи углерод — галоген
- 6.2. Связи углерод — кислород и углерод — сера
- 6.3. Связи углерод — азот
- 6.3.2. Электрофильный азот и нуклеофильный углерод
- 6.3.3. Нитрозосоединения, включая нитриты
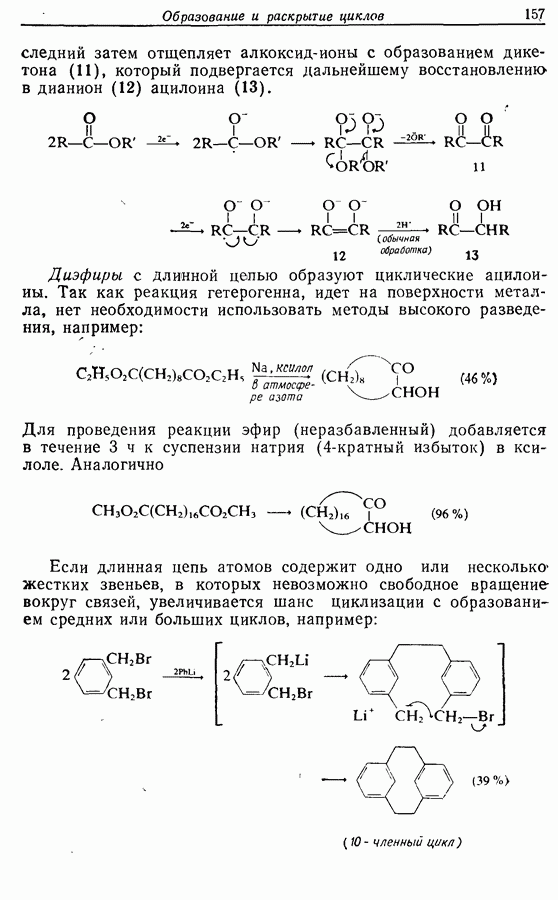
- 7. ОБРАЗОВАНИЕ И РАСКРЫТИЕ ЦИКЛОВ
- 7.1. Внутримолекулярная циклизация в результате электрофильно-нуклеофильного взаимодействия
- 7.1.2. Условия внутримолекулярного циклообразования. Правила Болдуина
- 7.1.3. Присоединение по Михаэлю в процессах циклизации
- 7.1.4. Образование ароматических и гетероароматических циклов
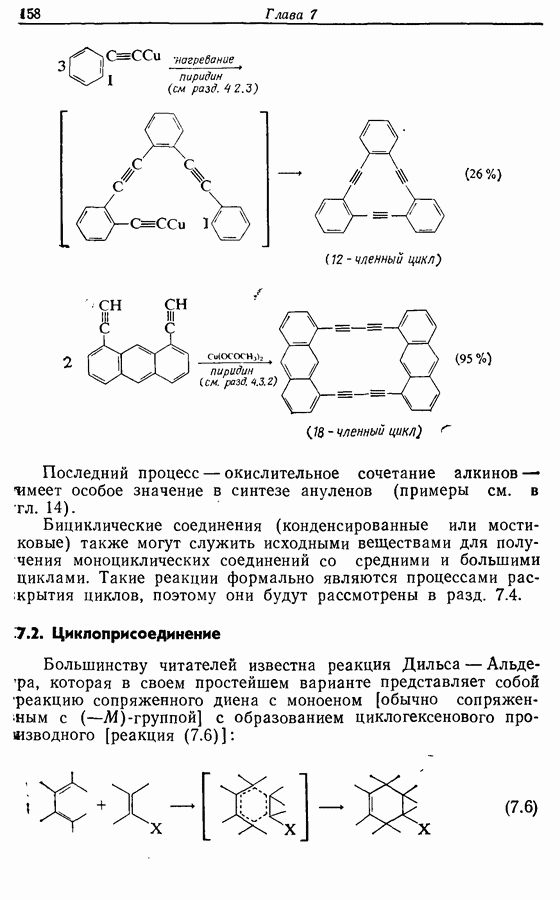
- 7.2. Циклоприсоединение
- 7.2.2. 1,3-Диполярное циклоприсоединение
- 7.2.3. Присоединение карбенов и нитренов к алкенам
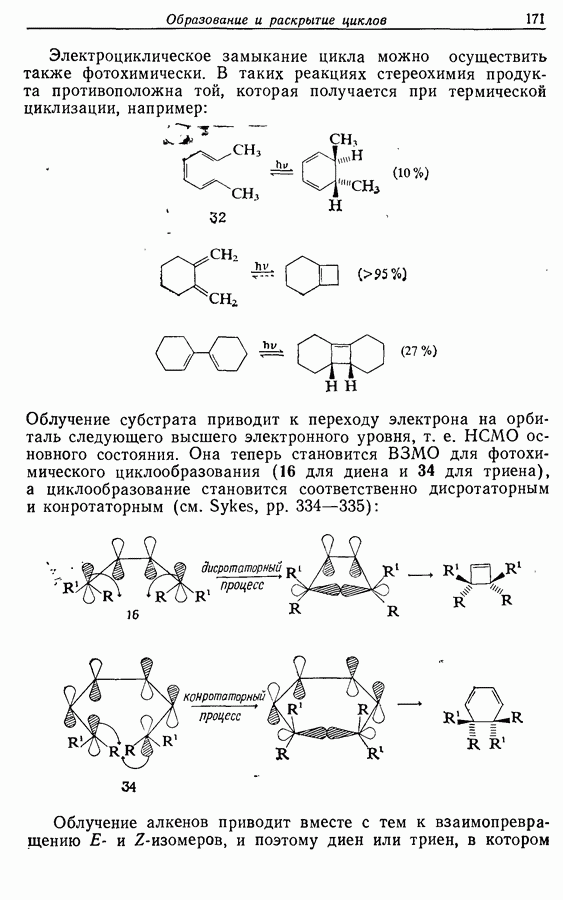
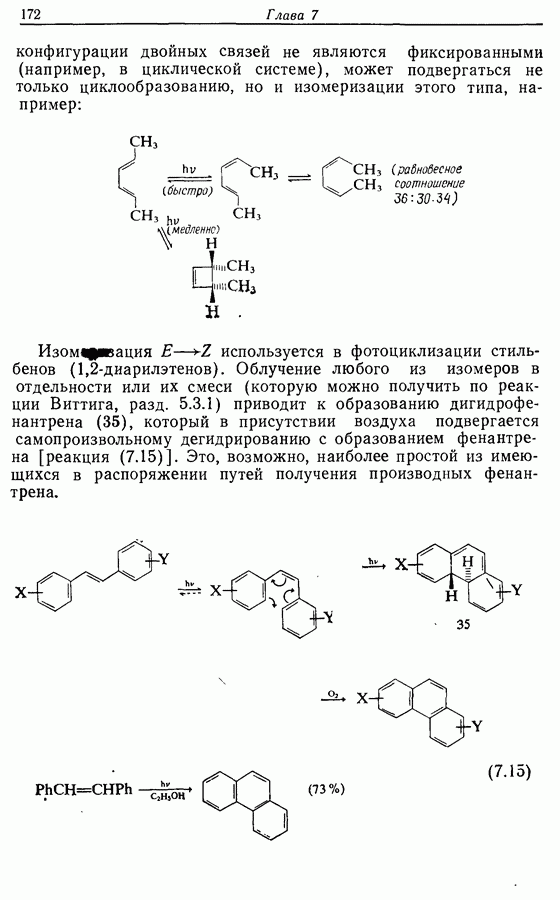
- 7.3. Электроциклическое циклообразование
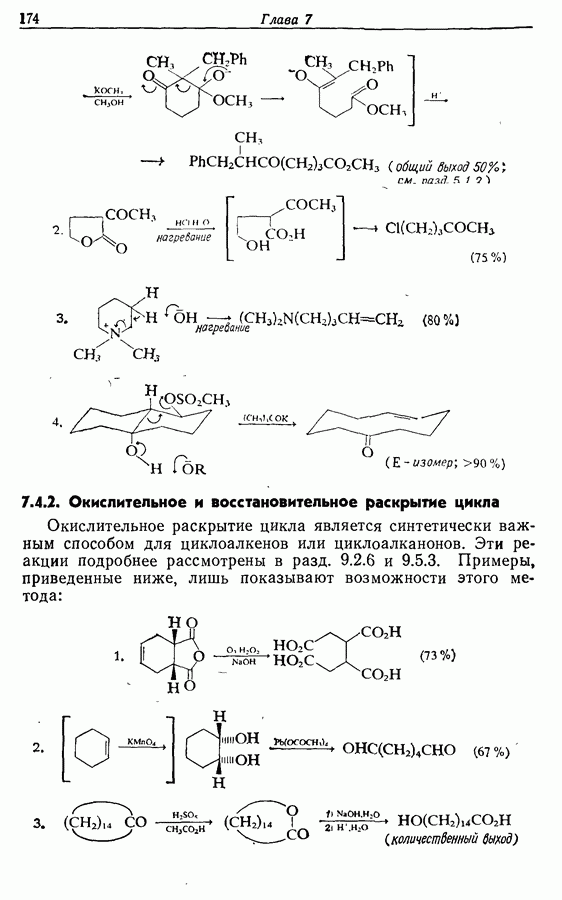
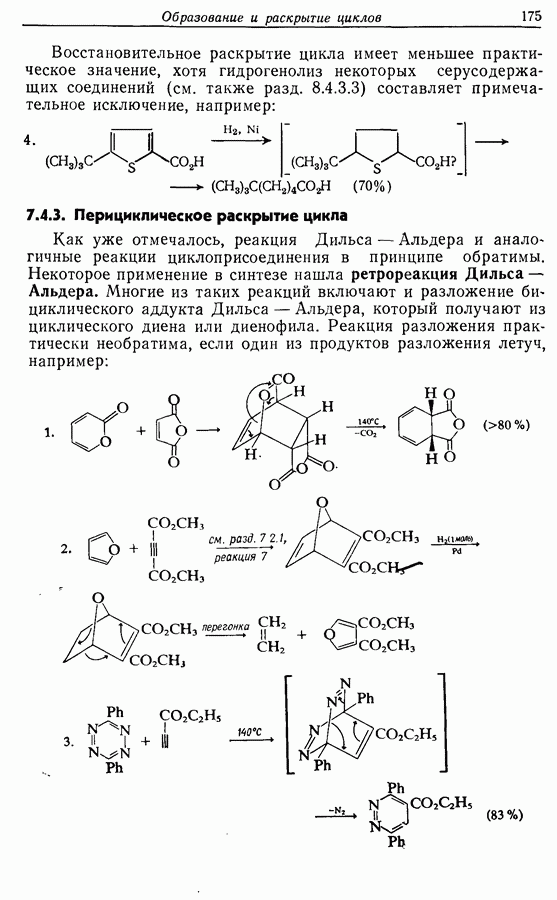
- 7.4. Раскрытие цикла
- 7.5. Выводы и задачи
- 8. ВОССТАНОВЛЕНИЕ
- 8.1. Каталитическое гидрирование
- 8.2. Восстановление гидридами металлов
- 8.3. Восстановление растворяющимися металлами
- 8.4. Восстановление определенных функциональных групп
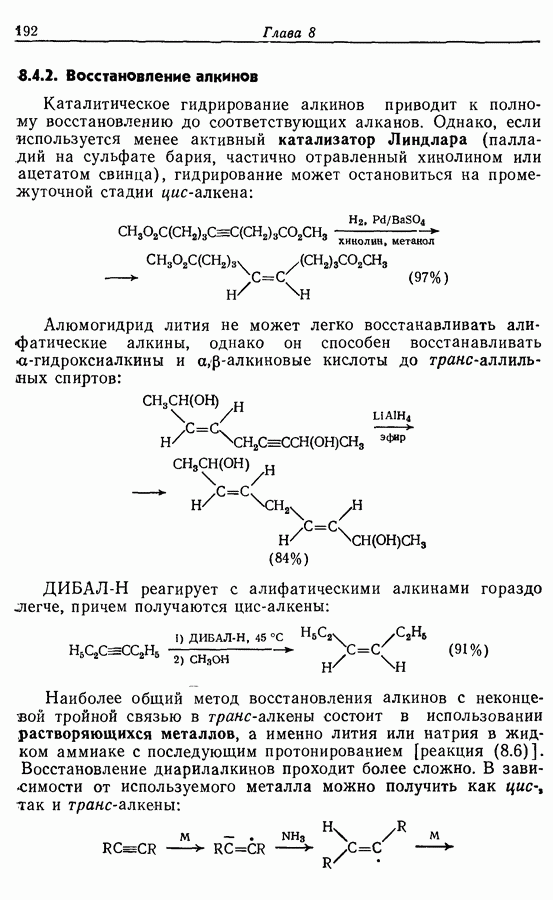
- 8.4.2. Восстановление алкинов
- 8.4.3. Восстановление альдегидов и кетонов
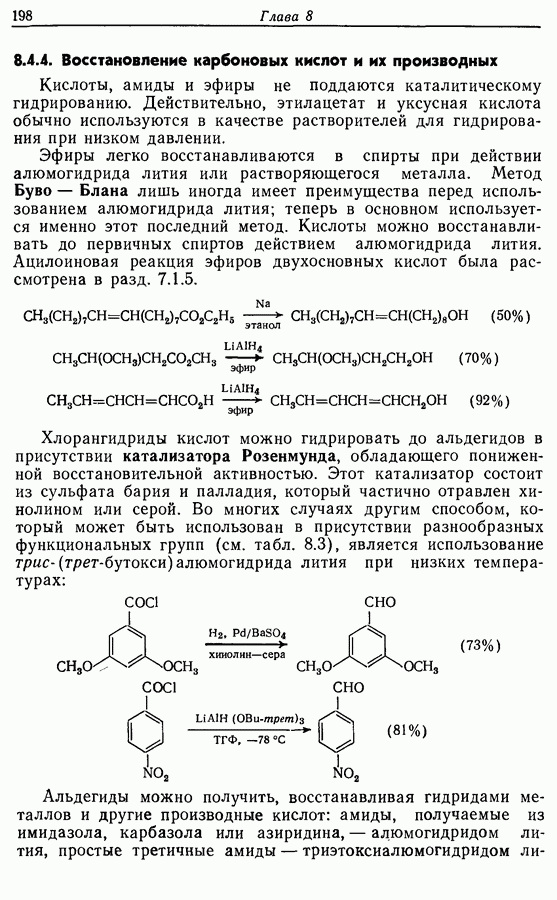
- 8.4.4. Восстановление карбоновых кислот и их производных
- 8.4.5. Восстановление нитрилов
- 8.4.6. Восстановление иминов и оксимов, включая восстановительное алкилирование
- 8.5. Восстановительное расщепление связи углерод — гетероатом
- 8.6. Восстановительное раскрытие цикла в эпоксидах
- 8.7. Восстановление a,b-ненасыщенных карбонильных соединений
- 8.8. Восстановление сопряженных диенов
- 8.9. Восстановление ароматических и гетероароматических соединений
- 9. ОКИСЛЕНИЕ
- 9.2. Окисление углеводородов
- 9.2.2. Аллильное окисление
- 9.2.3. Бензильное окисление
- 9.2.4. Дегидрирование алканов, алкильных групп и алкенов
- 9.2.5. Окислительное присоединение к алкенам
- 9.2.6. Окислительная деструкция алкенов
- 9.2.7. Окисление алкинов
- 9.3. Окисление спиртов и их производных
- 9.3.2. Окислительная деструкция 1,2-диолов
- 9.4. Окисление фенолов
- 9.5. Окисление альдегидов и кетонов
- 9.5.2. Окисление в 1,2-дикарбонильные соединения
- 9.5.3. Окисление до сложных эфиров: реакции Байера — Виллигера и Дакина
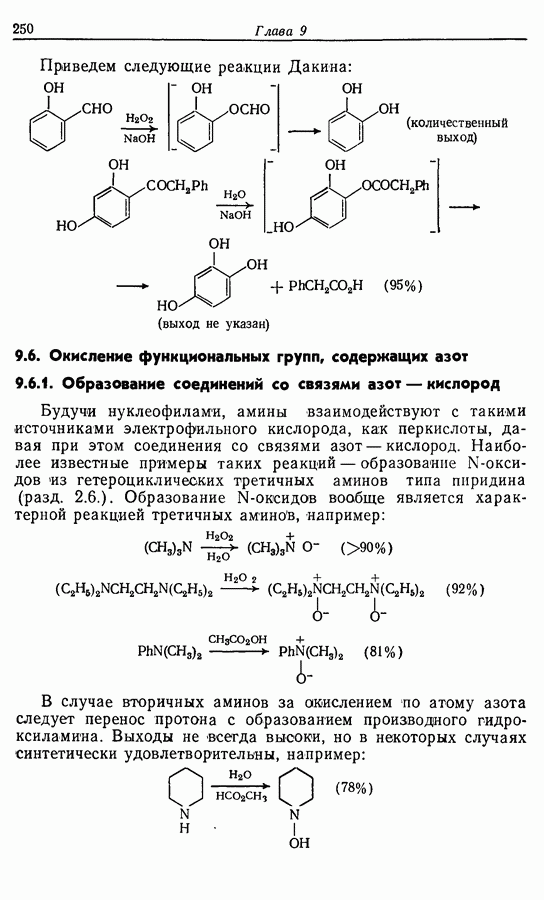
- 9.6. Окисление функциональных групп, содержащих азот
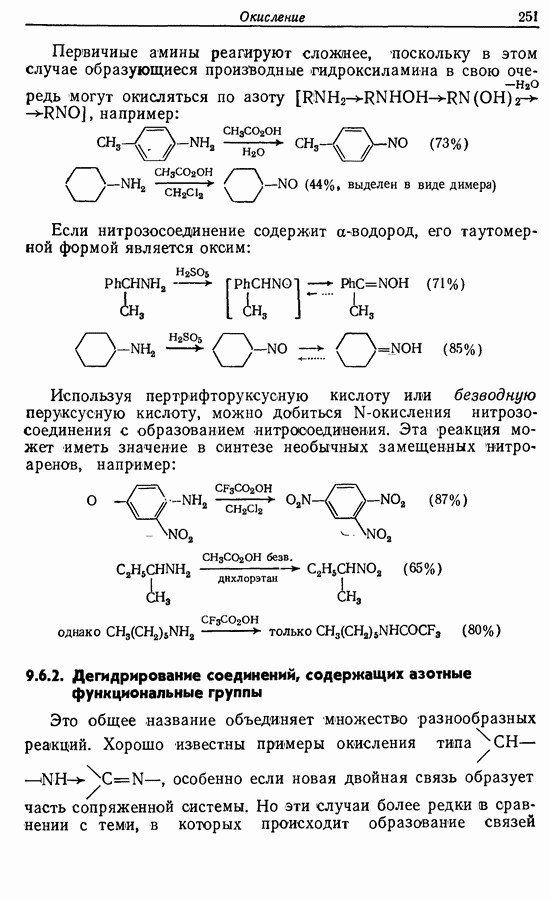
- 9.6.2. Дегидрирование соединений, содержащих азотные функциональные группы
- 9.7. Окисление серусодержащих функциональных групп
- 10. ЗАЩИТНЫЕ ГРУППЫ
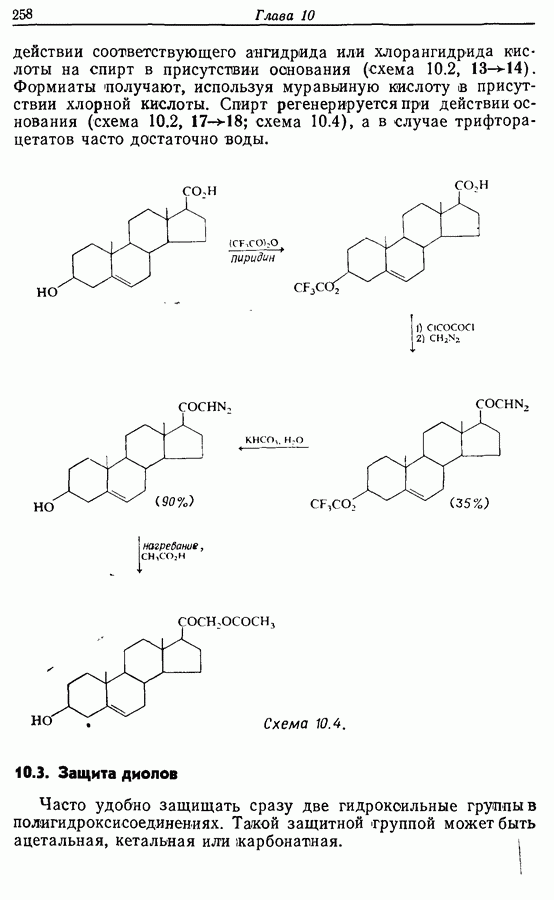
- 10.2. Защита спиртов
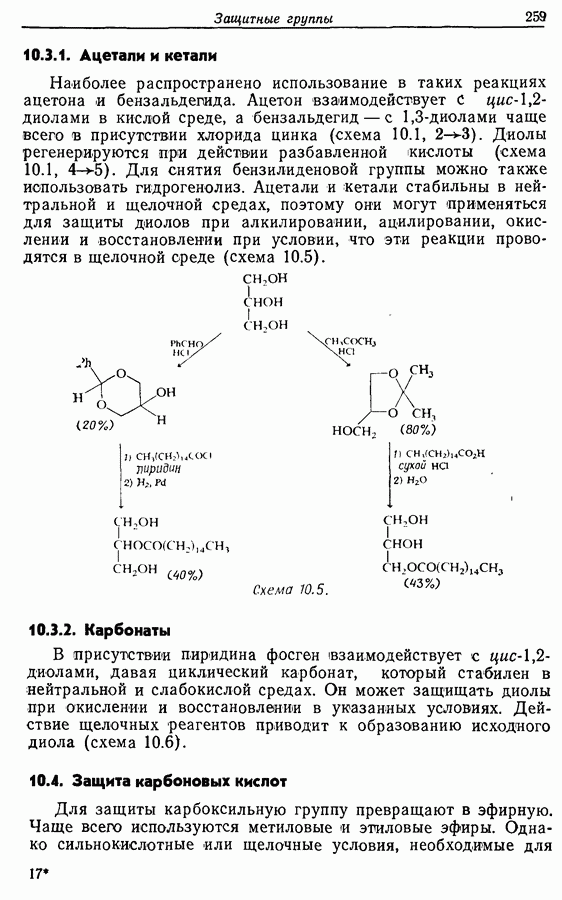
- 10.3. Защита диолов
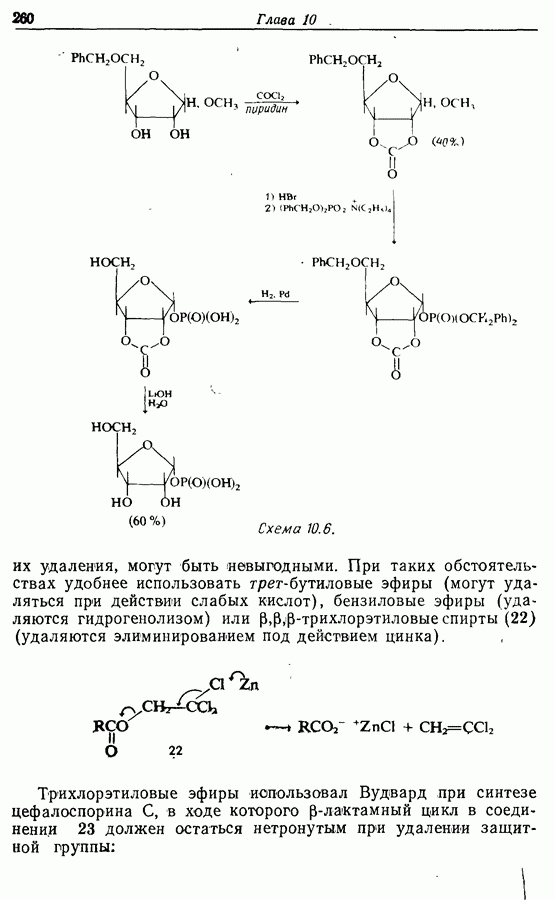
- 10.4. Защита карбоновых кислот
- 10.5. Защита аминогрупп
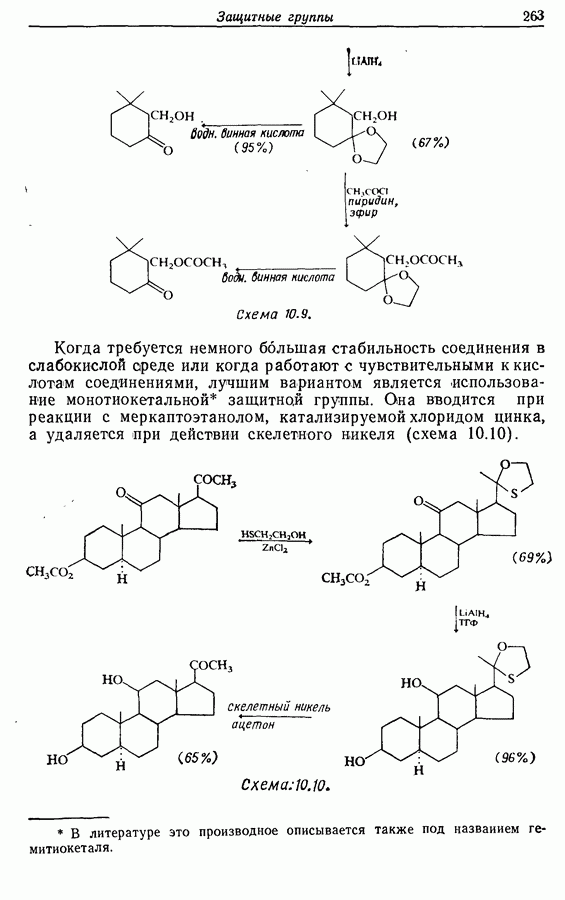
- 10.6. Защита карбонильных групп
- 11. БОРСОДЕРЖАЩИЕ РЕАГЕНТЫ
- 11.1. Гидроборирование алкенов при действии борана
- 11.2. Гидроборирование алкенов действием алкилборанов
- 11.3. Реакции борорганических соединений
- 11.4. Гидроборирование диенов
- 11.5. Гидроборирование алкинов
- 12. ФОСФОРСОДЕРЖАЩИЕ РЕАГЕНТЫ
- 12.1. Введение в химию фосфорорганических соединений
- 12.2. Образование углерод-углеродных двойных связей
- 12.3. Превращения функциональных групп
- 12.4. Реакции дезоксигенирования
- 13. КРЕМНИЙСОДЕРЖАЩИЕ РЕАГЕНТЫ
- 13.1. Введение в химию кремнийорганических соединений
- 13.2. Синтез кремнийорганических соединений
- 13.3. Реакции с образованием углерод-углеродных связей
- 13.4. Синильная защита спиртов
- 14. ИЗБРАННЫЕ СИНТЕЗЫ
- 14.2. Z-Геникосен-6-он-11
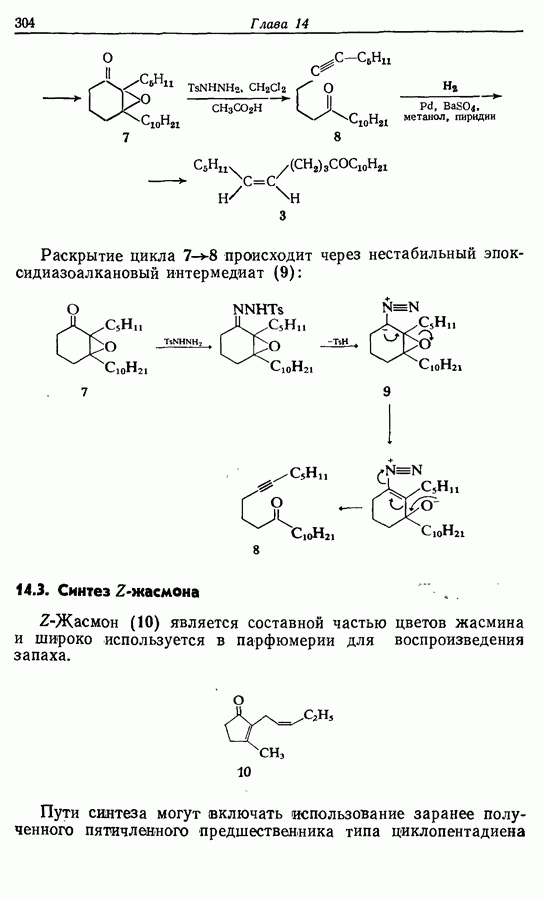
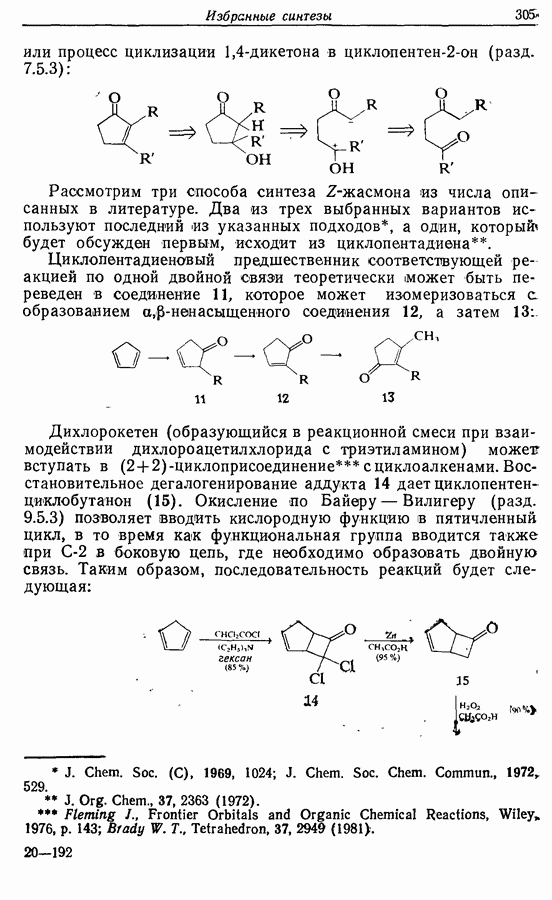
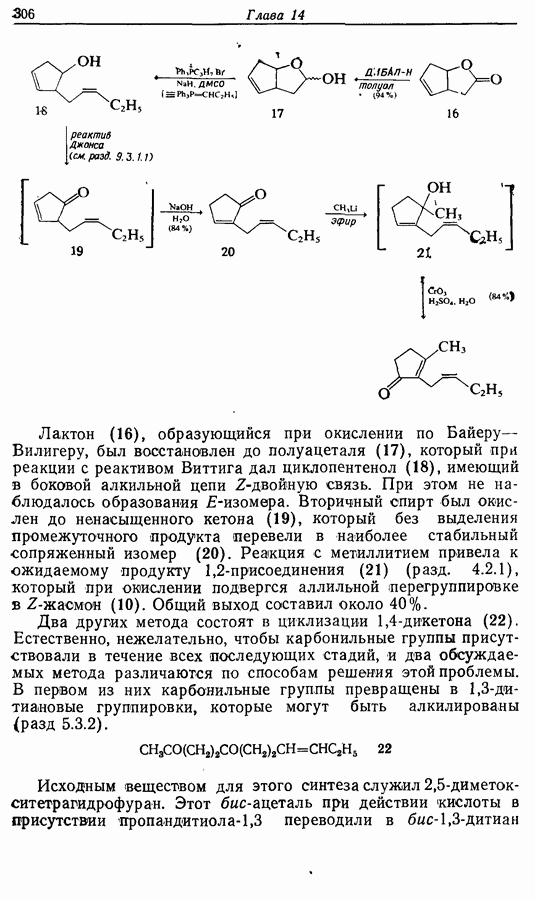
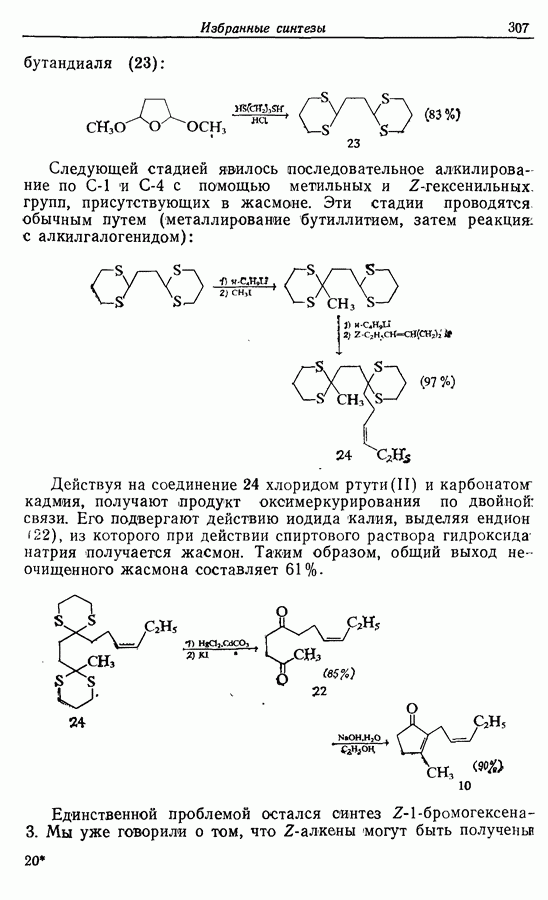
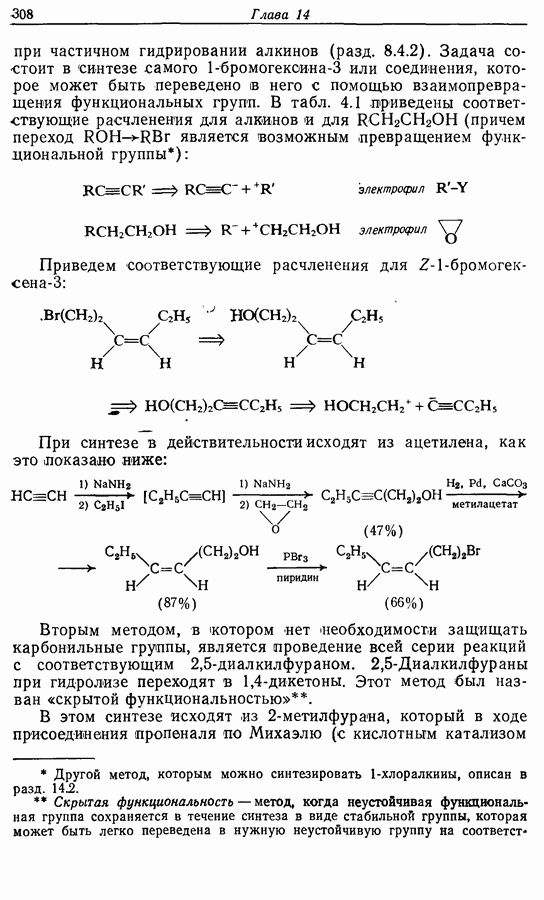
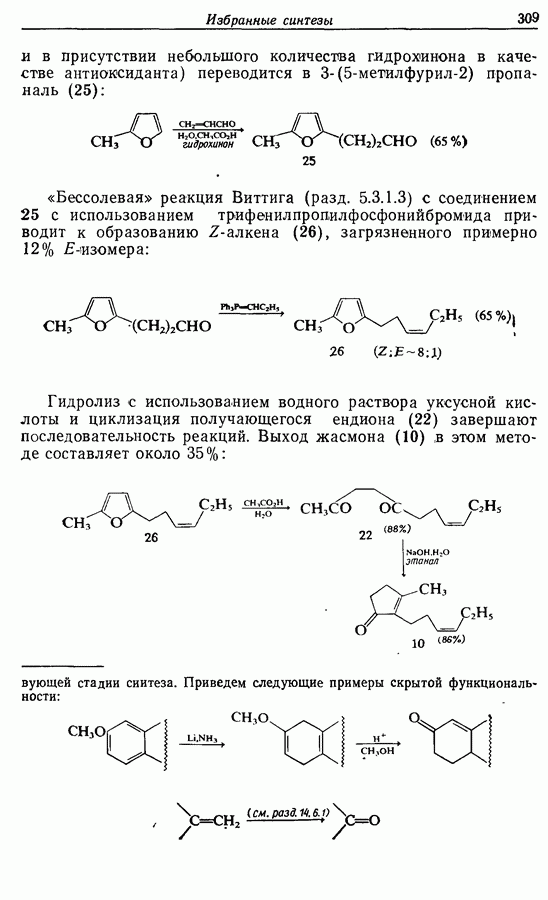
- 14.3. Синтез Z-жасмона
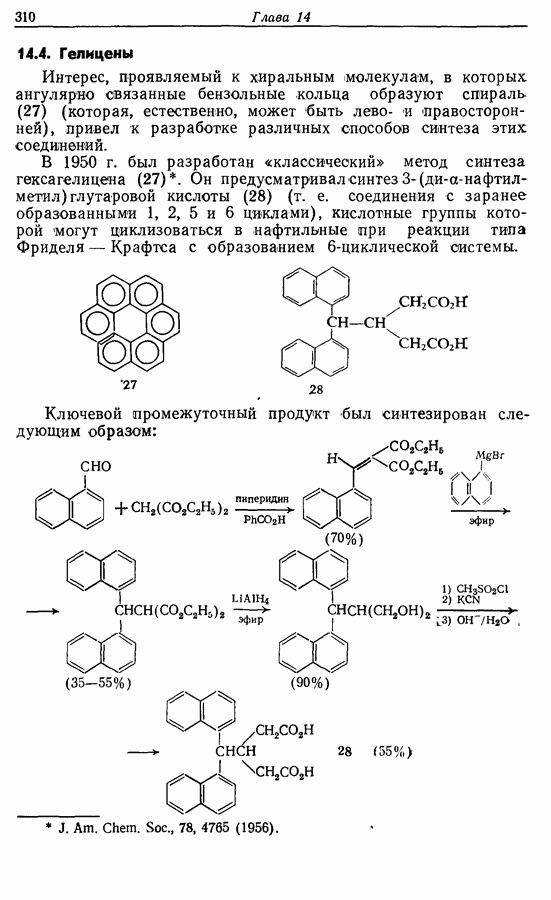
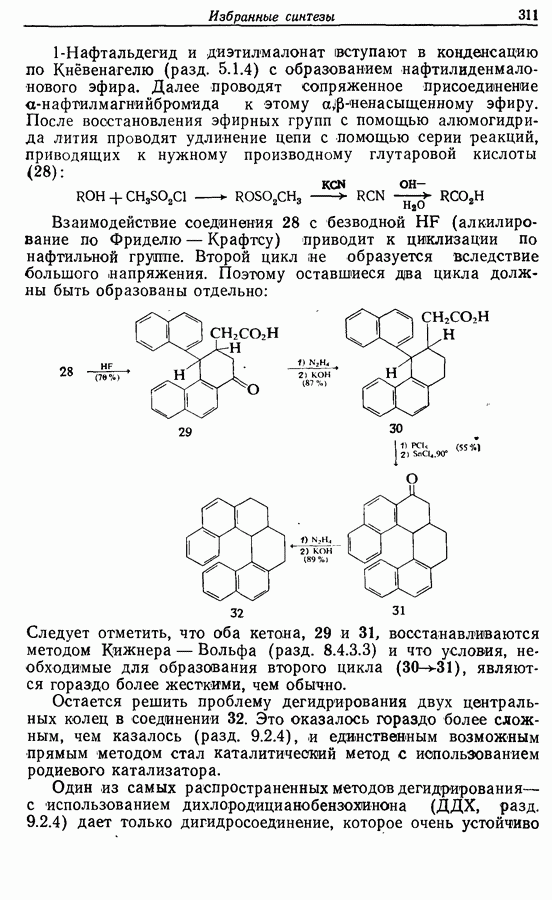
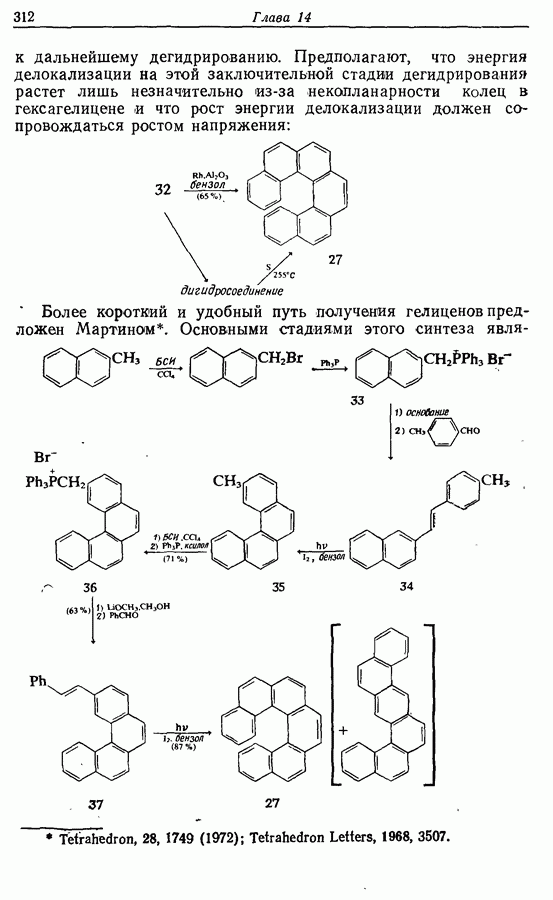
- 14.4. Гелицены
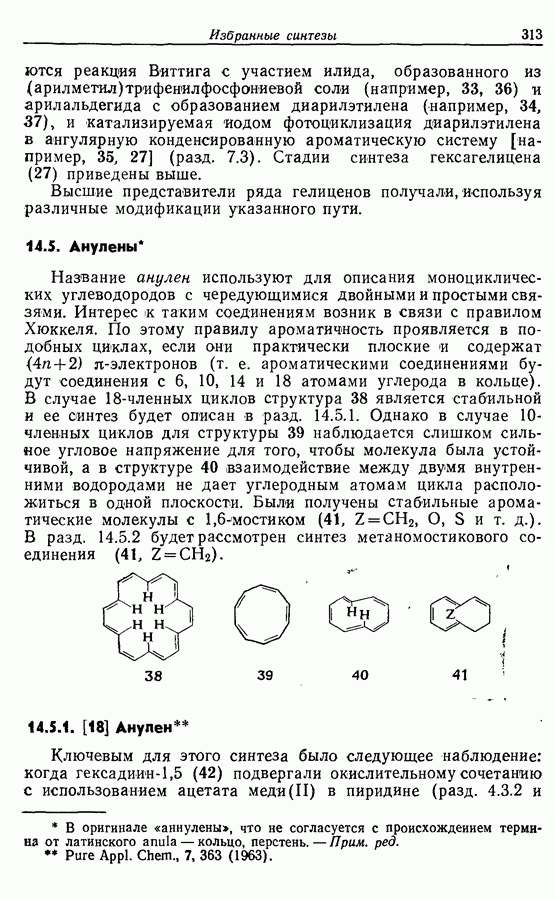
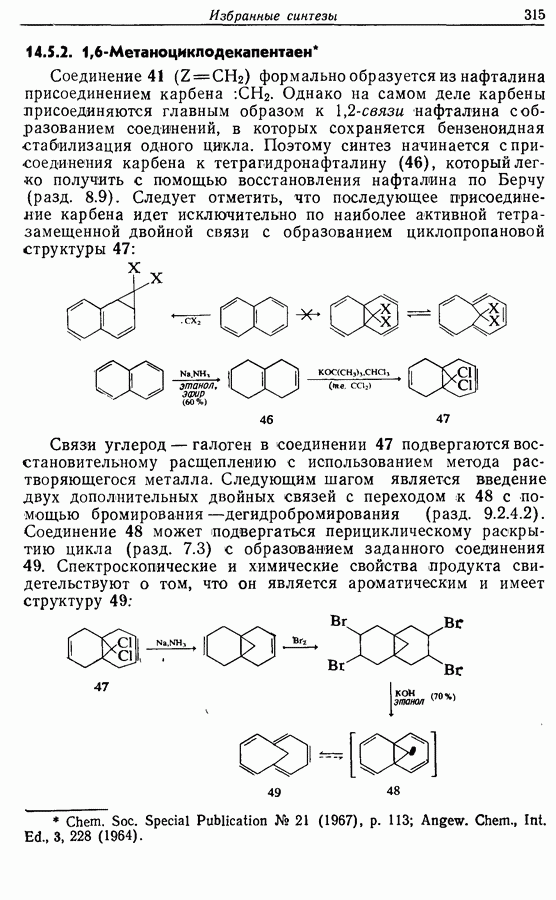
- 14.5. Анулены
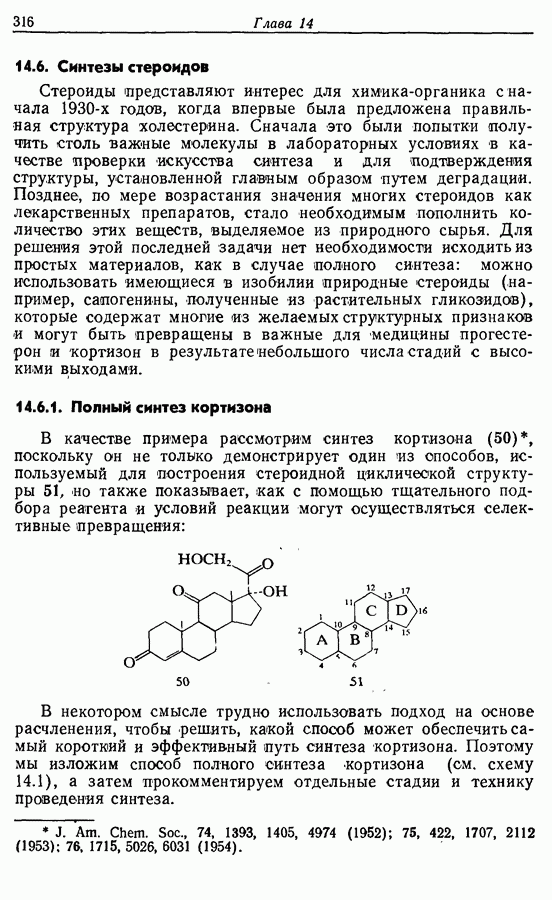
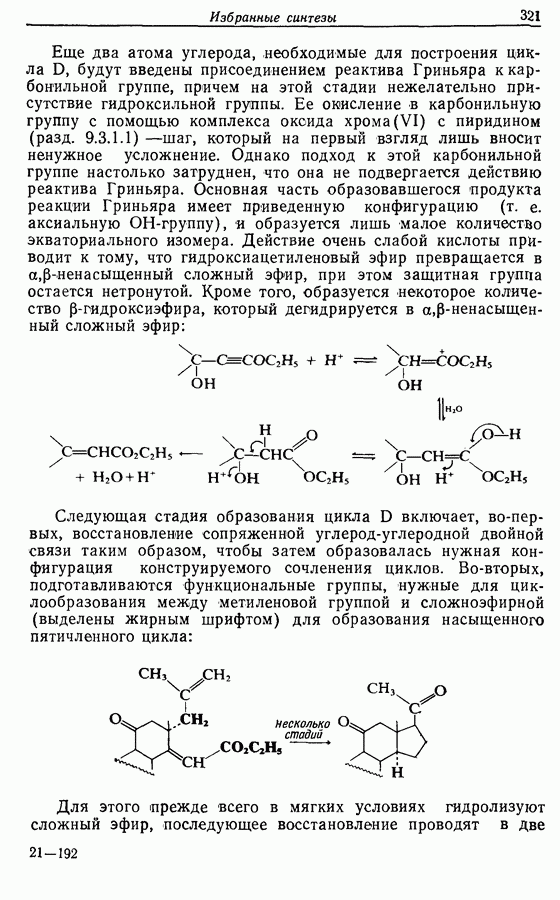
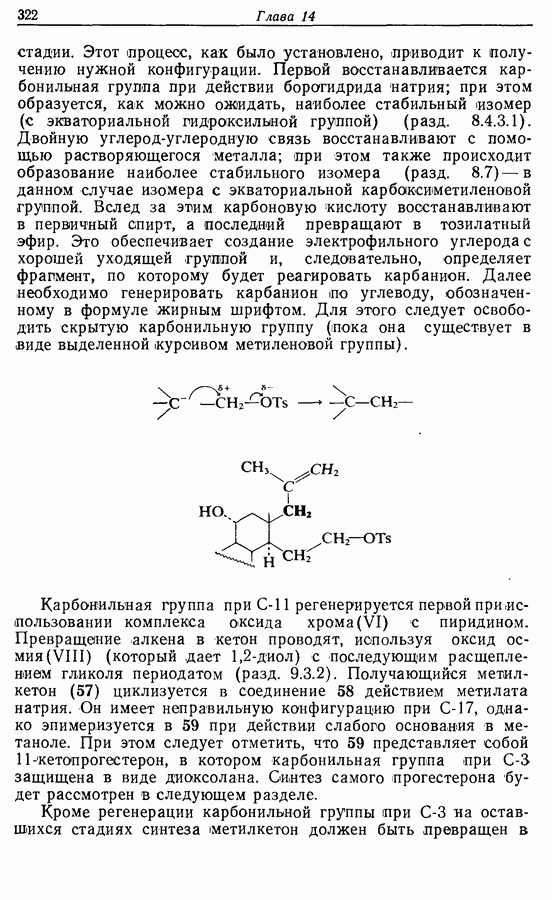
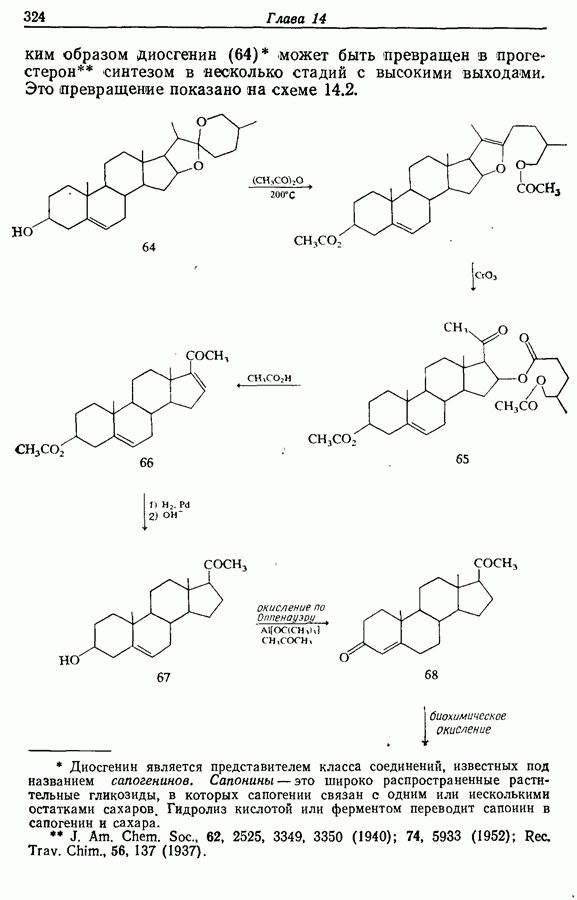
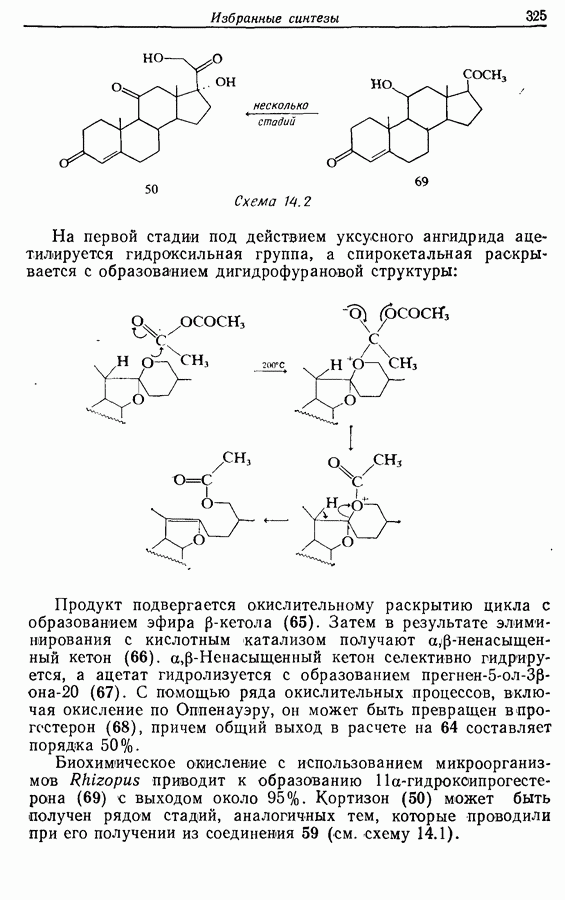
- 14.6. Синтезы стероидов
- 14.6.2. Превращение растительных стероидов в стероидные гормоны
- 14.7. Синтез пептидов
- 14.7.2. Техника синтеза пептидов
- ЛИТЕРАТУРА