| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
9.3. Окисление спиртов и их производных
9.3.1. Образование альдегидов и кетонов (дегидрирование)
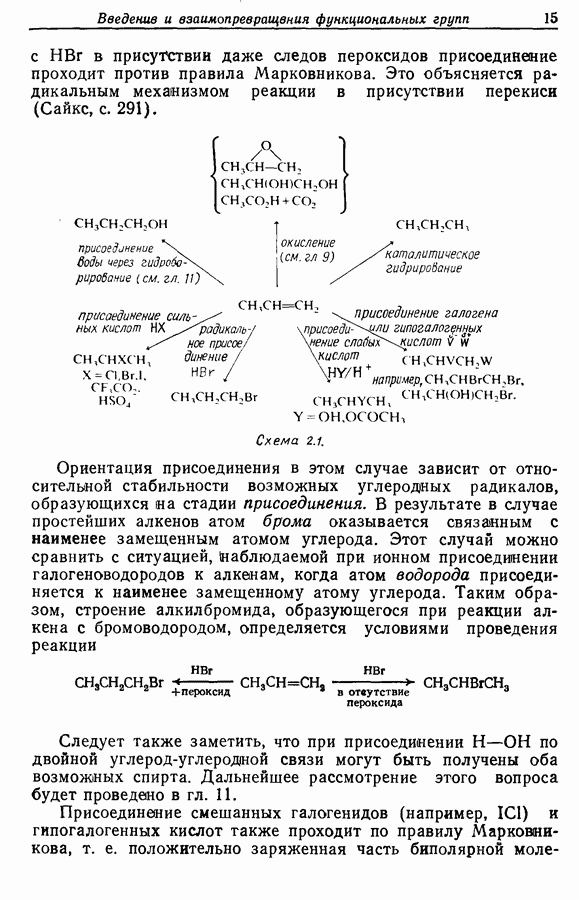
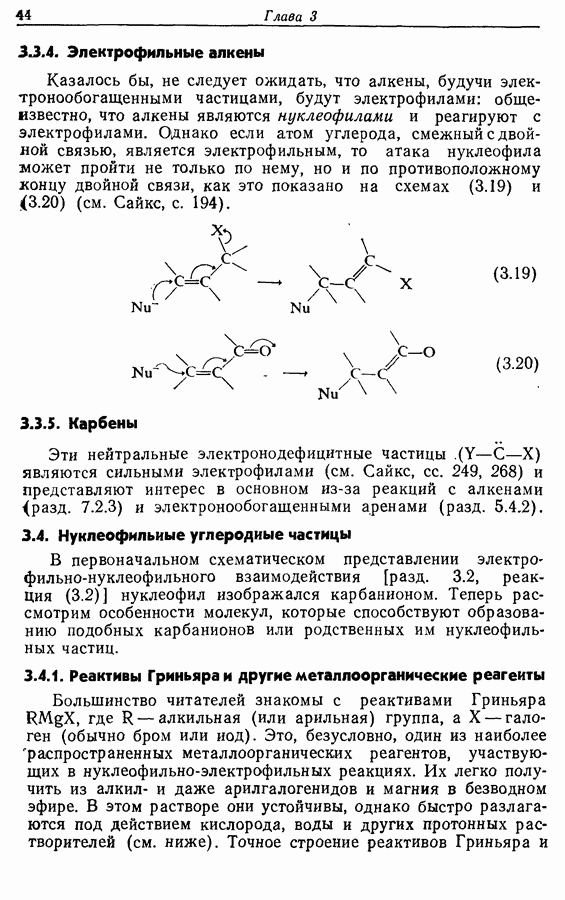
Большинство студентов в начале изучения органической химии узнают, что окисление первичных спиртов приводит к образованию альдегидов и затем карбоновых кислот; окисление вторичных спиртов дает кетоны, а третичные спирты устойчивы к окислению до тех пор, пока условия  станут достаточно жесткими для осуществления разрыва связи
станут достаточно жесткими для осуществления разрыва связи  Соответствующие реакции, приводимые как примеры в элементарных курсах, на деле неселективны, если использовать такие реагенты, как горячий подкисленный раствор перманганата калия или горячую хромовую смесь. Поэтому была проделана большая работа по созданию методов селективного окисления спиртов в карбонильные соединения.
Соответствующие реакции, приводимые как примеры в элементарных курсах, на деле неселективны, если использовать такие реагенты, как горячий подкисленный раствор перманганата калия или горячую хромовую смесь. Поэтому была проделана большая работа по созданию методов селективного окисления спиртов в карбонильные соединения.
Превращение спиртов в карбонильные соединения формально является дегидрированием, поэтому могут быть применены все три метода, описанные в разд. 9.1.1.
9.3.1.1. Метод замещения — отщепления
Этот метод наиболее распространен, по крайней мере в лабораторной практике.
Для окисления вторичных спиртов в кетоны чаще всего применяют окислители, содержащие хром (VI). Часто реакция идет через хромовый эфир, например:

Хромсодержащие частицы, получающиеся на этой, первой стадии [производное хрома (IV)], не являются конечным продуктом. Дальнейшая сложная последовательность окислительно-восстановительных стадий (детали которых нас здесь не интересуют) приводит в конце концов к образованию соли хрома (III),
а общее стехиометрическое уравнение этой реакции имеет следующий вид:

или

или

Известно много вариантов окислительных реакций такого типа. Если спирт не содержит других функциональных групп, способных окисляться, и не чувствителен к действию кислот, то наиболее подходящим окислителем является водный раствор хромовой кислоты в серной кислоте или уксусной кислоте, например:

Селективное окисление спиртов, содержащих двойную или тройную связь, можно (провести используя реагент Джонса [водный раствор оксида хрома (VI) и серной кислоты в строго стехиометрических количествах]. При этом спирт, растворенный в ацетоне, титруется реагентом при комнатной или более низкой температуре. При таких условиях селективно окисляется только спиртовая группа, например:

Аналогично

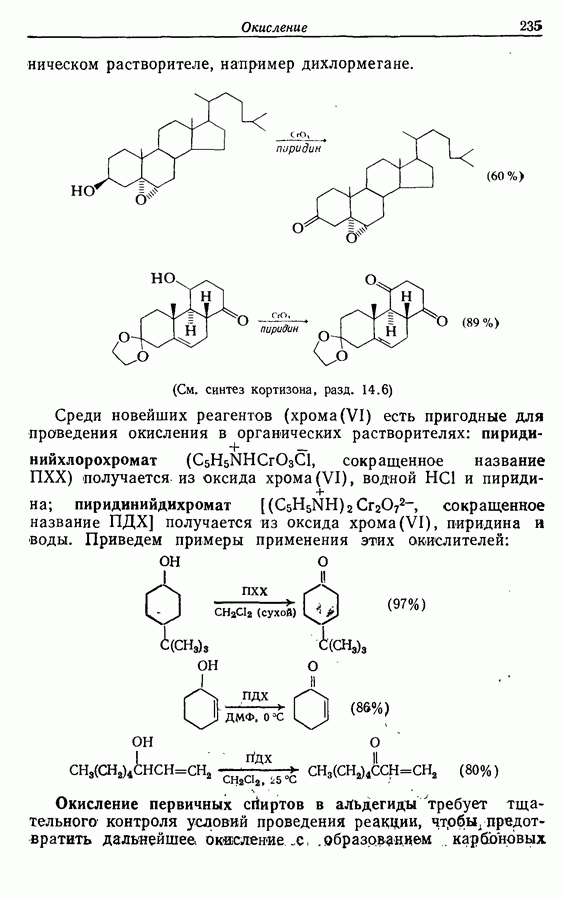
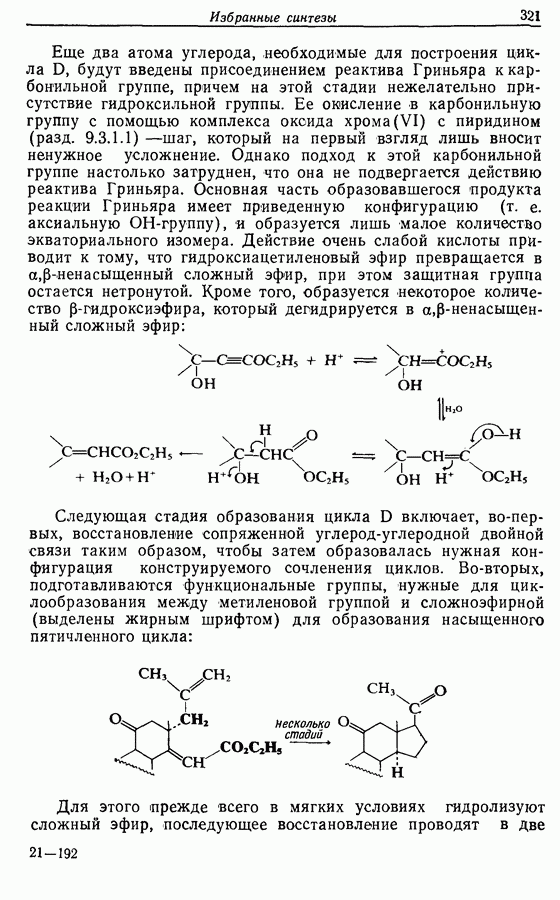
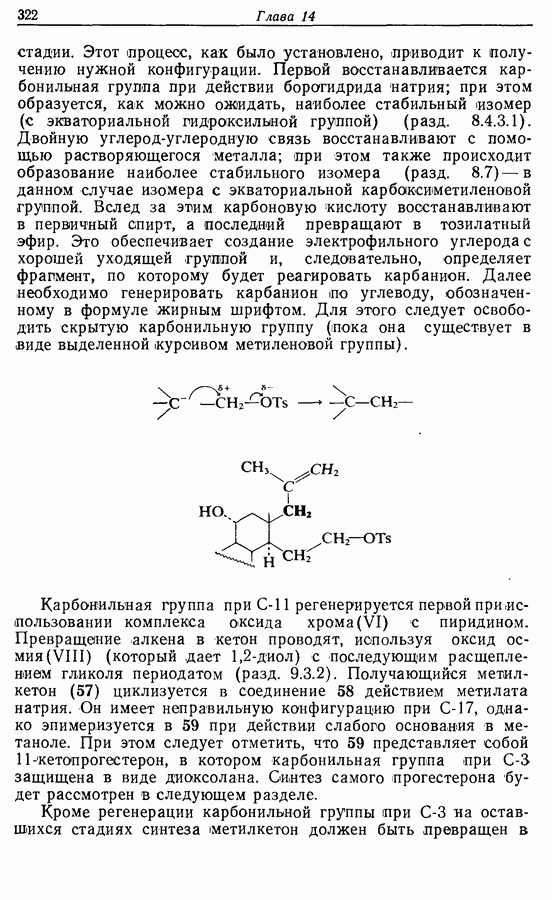
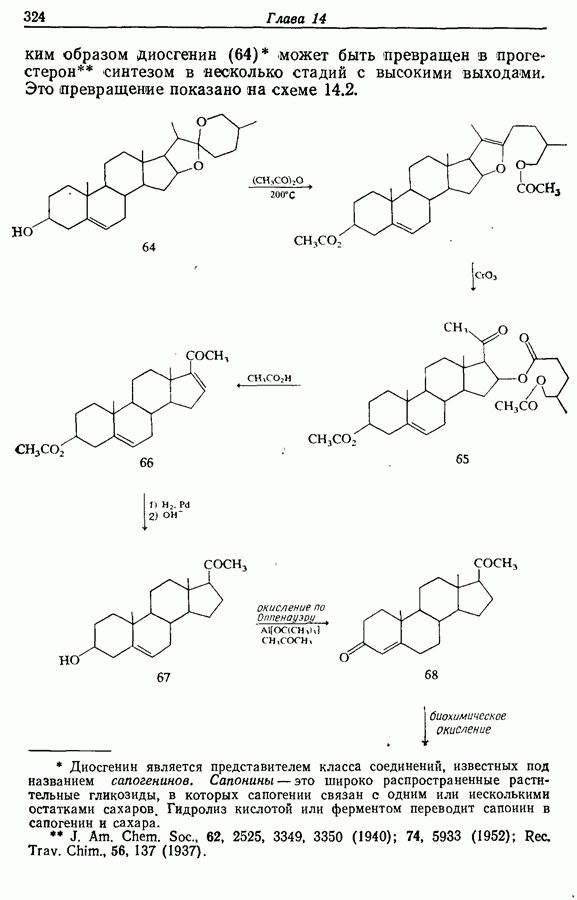
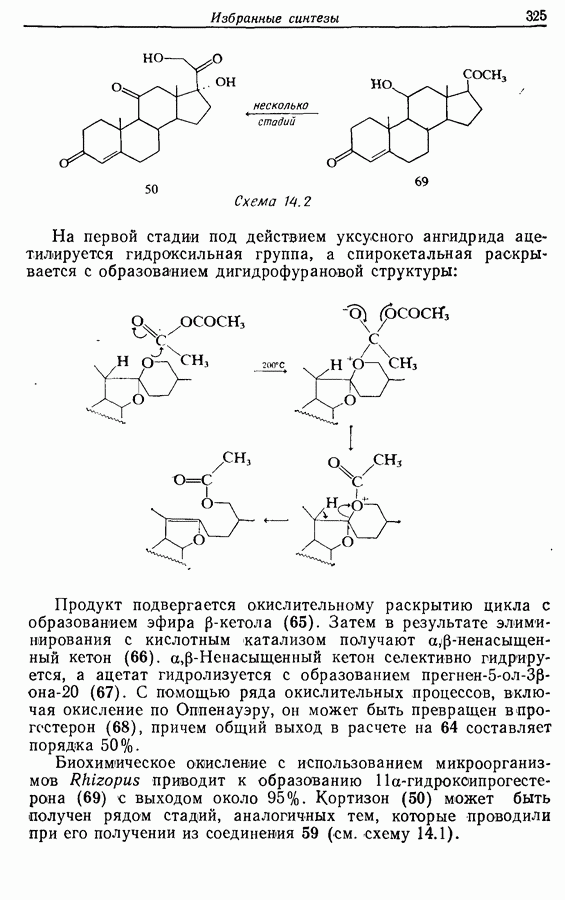
Если применение этого метода осложняется чувствительностью спирта к кислотам, в качестве окислителя может быть выбран оксид хрома (VI) в пиридине. Комплекс оксида хрома с пиридином может быть выделен и растворен в другом
органическом растворителе, например дихлормегане.

(См. синтез кортизона, разд. 14.6)
Среди новейших реагентов (хрома (VI) есть пригодные для проведения окисления в органических растворителях: пиридинийхлорохромат  сокращенное название ПХХ) получается из оксида хрома (VI), водной
сокращенное название ПХХ) получается из оксида хрома (VI), водной  и пиридина; пиридинийдихромат
и пиридина; пиридинийдихромат  сокращенное название
сокращенное название  получается из оксида хрома (VI), пиридина и воды. Приведем примеры применения этих окислителей:
получается из оксида хрома (VI), пиридина и воды. Приведем примеры применения этих окислителей:

Окисление первичных сйиртов в альдегиды требует тщательного контроля условий проведения реакции, чтобы предотвратить дальнейшее, окисление с образованием карбоновых
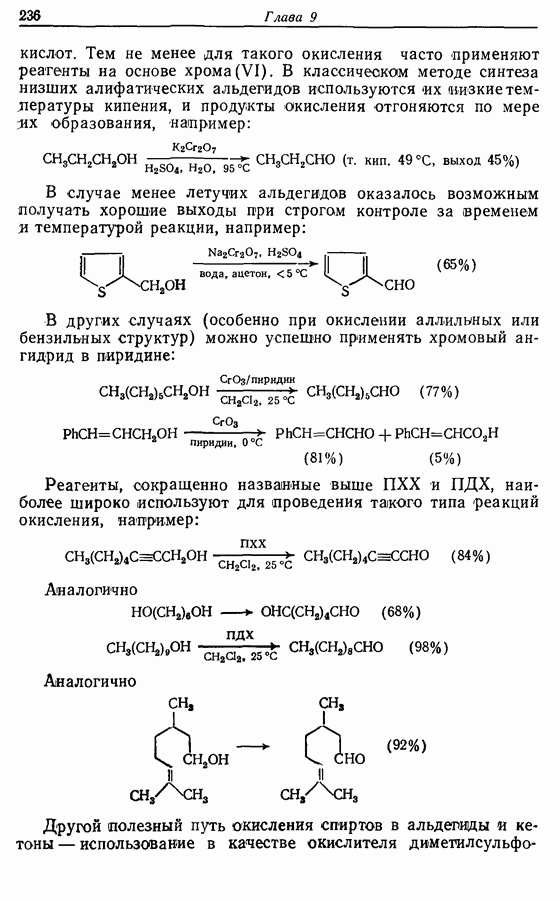
кислот. Тем не менее для такого окисления часто применяют реагенты на основе хрома (VI). В классическом методе синтеза низших алифатических альдегидов используются их мзкие температуры кипения, и продукты окисления отгоняются по мере да образования, например:

В случае менее летучих альдегидов оказалось возможным получать хорошие выходы при строгом контроле за временем и температурой реакции, например:

В других случаях (особенно при окислении аллильных или бензильных структур) можно успешно применять хромовый ангидрид в пиридине:

Реагенты, сокращенно названные выше  и
и  наиболее широко используют для проведения такого типа реакций окисления, например:
наиболее широко используют для проведения такого типа реакций окисления, например:

Аналогично

Аналогично

Другой полезный путь окисления спиртов в альдегиды и кетоны — использование в качестве окислителя
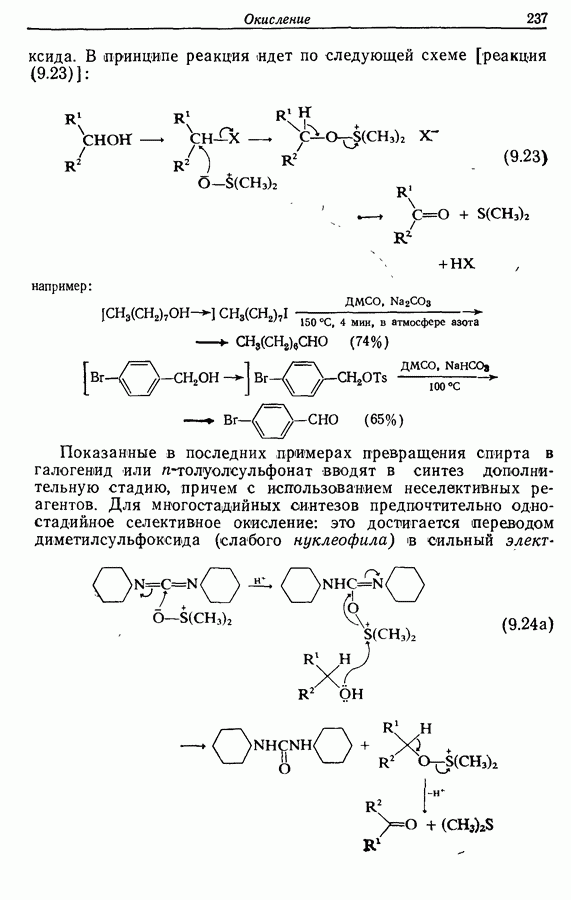
диметилсульфоксида. В принципе реакция идет по следующей схеме [реакция (9.23)]:

например:

Показанные в последних примерах превращения спирта в галогенид или  -толуолсульфонат вводят в синтез дополнительную стадию, причем с использованием неселективных реагентов. Для многостадийных синтезов предпочтительно одностадийное селективное окисление: это достигается переводом диметилсульфоксида (слабого нуклеофила) в сильный
-толуолсульфонат вводят в синтез дополнительную стадию, причем с использованием неселективных реагентов. Для многостадийных синтезов предпочтительно одностадийное селективное окисление: это достигается переводом диметилсульфоксида (слабого нуклеофила) в сильный
(см. скан)
электрофил, который может реагировать непосредственно со спиртами. Подобную активацию диметилсульфоксида чаще всего проводят с помощью  -дициклогексилкарбодиимида
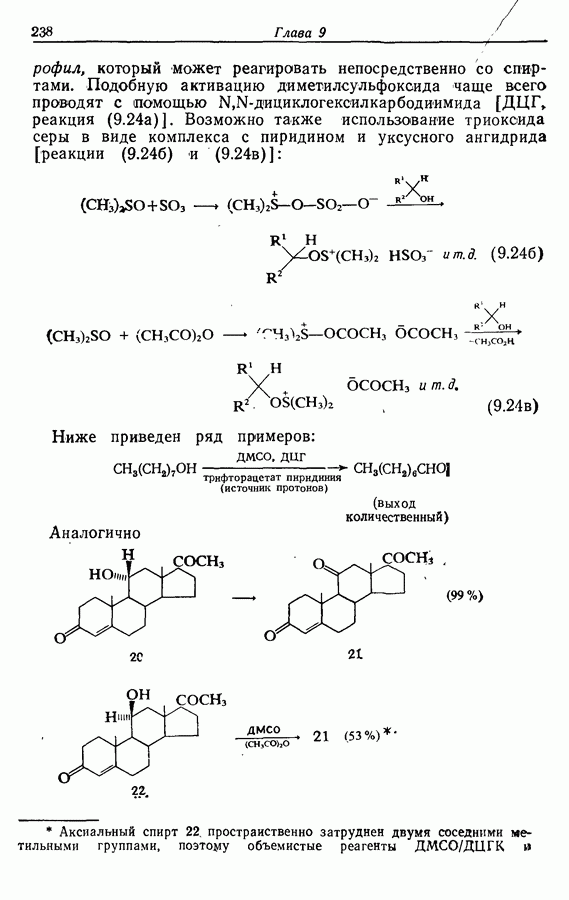
-дициклогексилкарбодиимида  реакция (9.24а)]. Возможно также использование триокоида серы в виде комплекса с пиридином и уксусного ангидрида [реакции (9.24б) и (9.24в)]:
реакция (9.24а)]. Возможно также использование триокоида серы в виде комплекса с пиридином и уксусного ангидрида [реакции (9.24б) и (9.24в)]:

Ниже приведен ряд примеров:

Аналогично


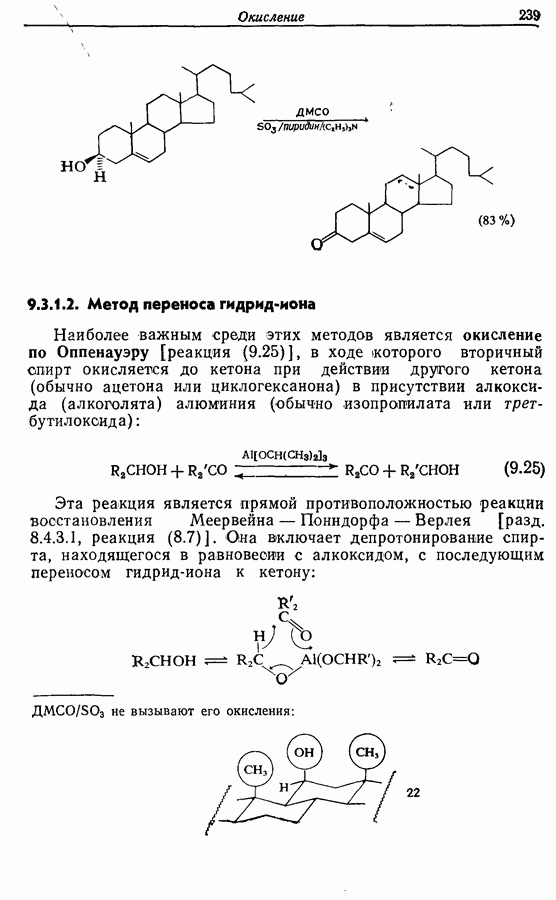
9.3.1.2. Метод переноса гидрид-иона
Наиболее важным среди этих методов является окисление по Оппенауэру [реакция (9.25)], в ходе (которого вторичный спирт окисляется до кетона при действии другого кетона (обычно ацетона или циклогексанона) в присутствии алкоксида (алкоголята) алюминия (обычно изопропилата или трет-бутилокоида):

Эта реакция является прямой противоположностью реакции восстановления Меервейна — Понндорфа — Верлея [разд. 8.4.3.1, реакция (8.7)]. Она включает депротонирование спирта, находящегося в равновесии с алкоксидом, с последующим переносом гидрид-иона к кетону:

Равновесие (9.25) обычно смещено вправо за счет использования большого избытка акцептора гидрида 
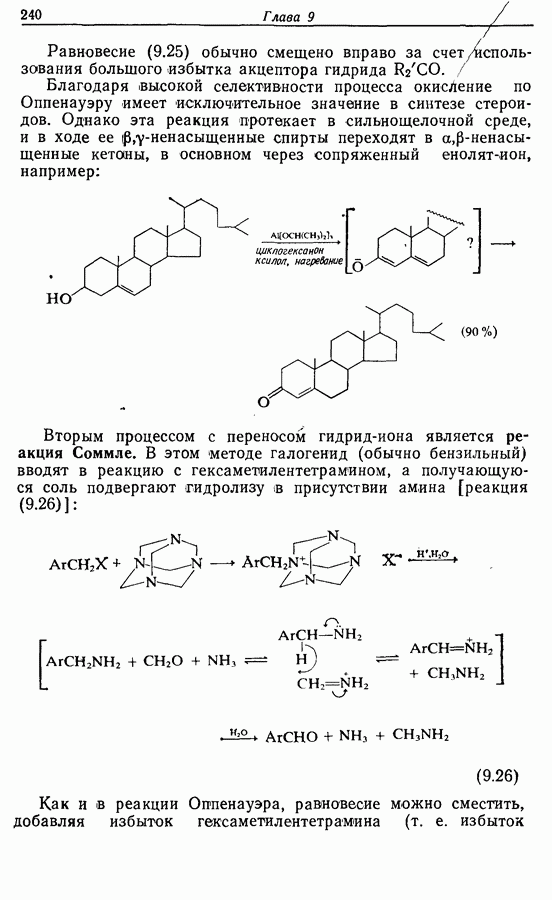
Благодаря высокой селективности процесса окисление по Оппенауэру имеет исключительное значение в синтезе стероидов. Однако эта реакция протекает в сильнощелочной среде, и в ходе ее  -ненасыщенные спирты переходят в
-ненасыщенные спирты переходят в  -ненасыщенные кетаны, в основном через сопряженный енолят-ион, например:
-ненасыщенные кетаны, в основном через сопряженный енолят-ион, например:

Вторым процессом с переносом гидрид-иона является реакция Соммле. В этом методе галогенид (обычно бензильный) вводят в реакцию с гексаметилентетрамином, а получающуюся соль подвергают гидролизу  присутствии амина [реакция (9.26)]:
присутствии амина [реакция (9.26)]:

Как и  реакции Оггпенауэра, равновесие можно сместить, добавляя избыток гексаметилентетрамина (т. е. избыток
реакции Оггпенауэра, равновесие можно сместить, добавляя избыток гексаметилентетрамина (т. е. избыток
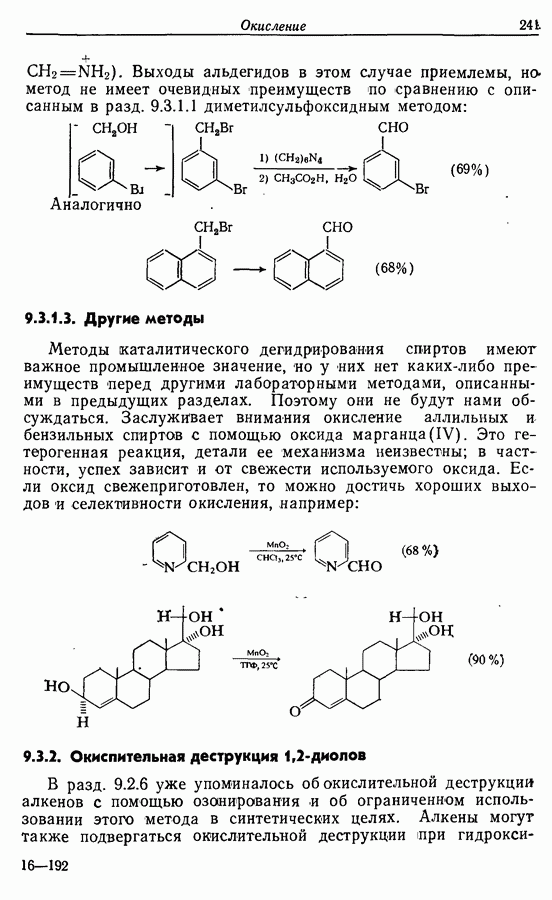
 Выходы альдегидов в этом случае приемлемы, но метод не имеет очевидных преимуществ по сравнению с описанным в разд. 9.3.1.1 диметилсульфоксидным методом:
Выходы альдегидов в этом случае приемлемы, но метод не имеет очевидных преимуществ по сравнению с описанным в разд. 9.3.1.1 диметилсульфоксидным методом:

Аналогично

9.3.1.3. Другие методы
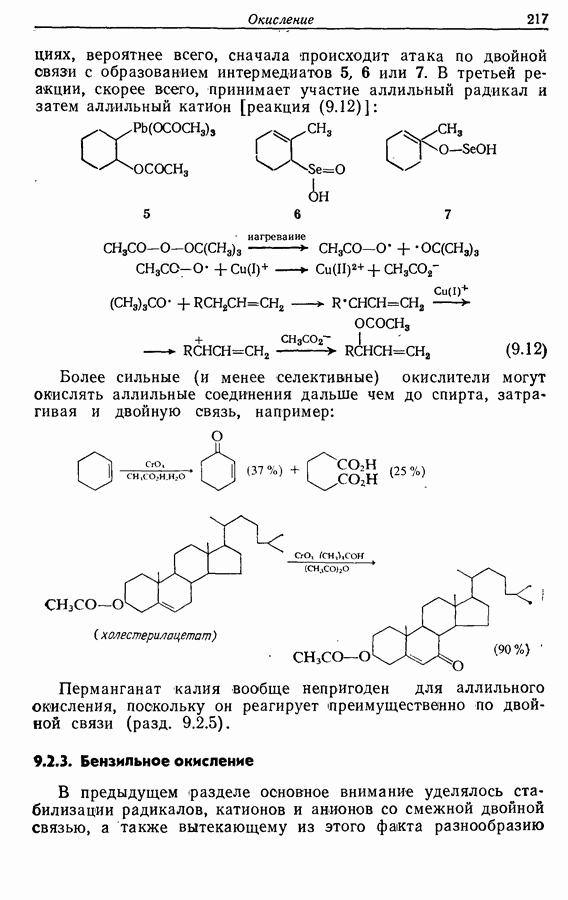
Методы каталитического дегидрирования спиртов имеют важное промышленное значение, но у них нет каких-либо преимуществ перед другими лабораторными методами, описанными в предыдущих разделах. Поэтому они не будут нами обсуждаться. Заслуживает внимания окисление аллильных и бензильных спиртов с помощью оксида марганца (IV). Это гетерогенная реакция, детали ее механизма неизвестны; в частности, успех зависит и от свежести используемого оксида. Если оксид свежеприготовлен, то можно достичь хороших выходов и селективности окисления, например:

| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА ПЕРЕВОДА
- 1. ВВЕДЕНИЕ
- 2. ВВЕДЕНИЕ И ВЗАИМОПРЕВРАЩЕНИЯ ФУНКЦИОНАЛЬНЫХ ГРУПП
- 2.1. Введение функциональных групп в апканы
- 2.2. Введение функциональных групп в алкены
- 2.3. Введение функциональных групп в апкины
- 2.4. Введение функциональных групп в ароматические углеводороды (арены)
- 2.5. Введение функциональных групп в производные бензола
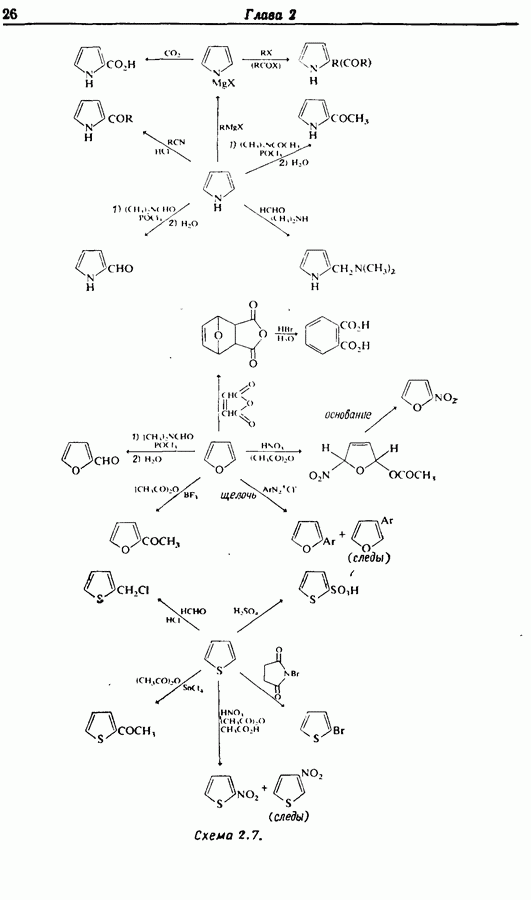
- 2.6. Введение функциональных групп в простые гетероциклические соединения
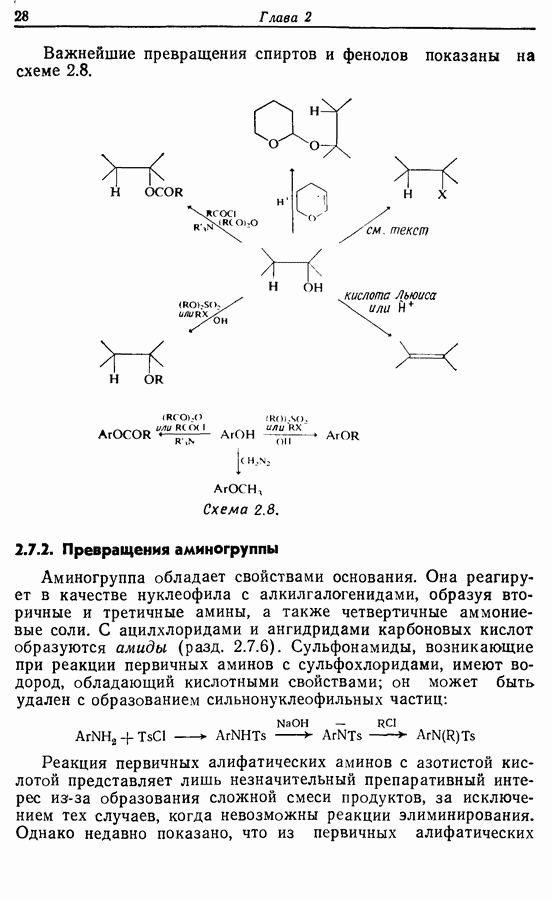
- 2.7. Взаимопревращения функциональных групп
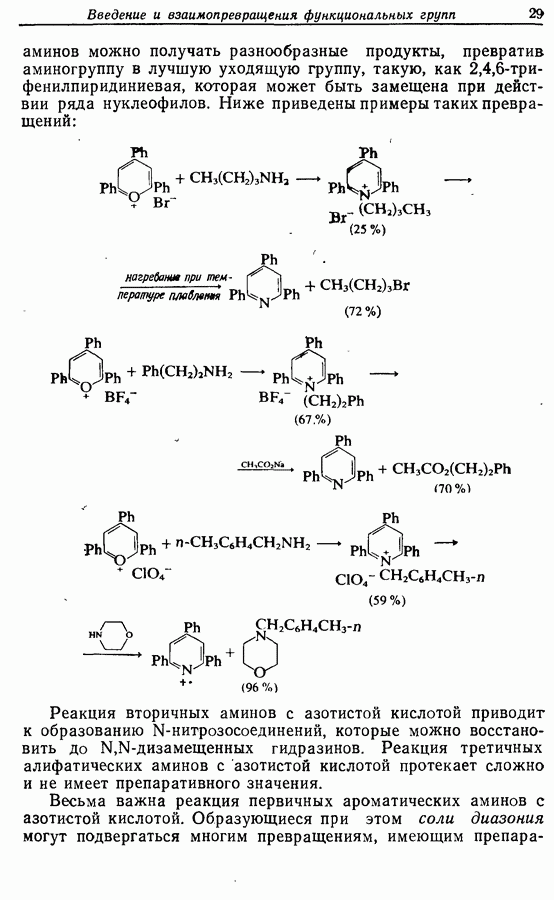
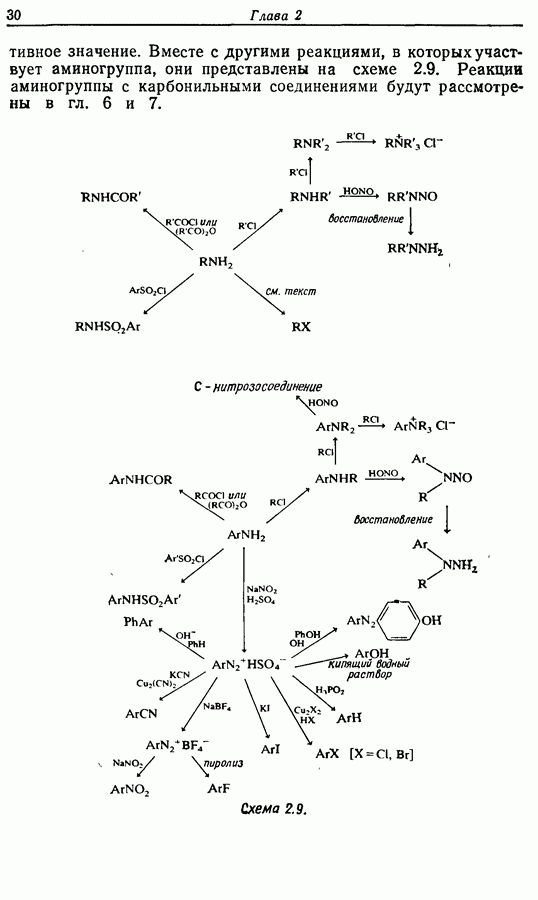
- 2.7.2. Превращения аминогруппы
- 2.7.3. Превращения галогенопроизводных
- 2.7.4. Превращения нитросоединений
- 2.7.5. Превращения альдегидов и кетонов
- 2.7.6. Превращения кислот и их производных
- 3. ПРИНЦИПЫ ОБРАЗОВАНИЯ УГЛЕРОД-УГЛЕРОДНОЙ СВЯЗИ
- 3.2. Расчленение и синтоны
- 3.3. Электрофильные углеродные частицы
- 3.4. Нуклеофильиые углеродные частицы
- 3.4.2. Стабилизированные карбанионы
- 3.4.3. Алкены, арены и гетероарены
- 4. ОБРАЗОВАНИЕ УГЛЕРОД-УГЛЕРОДНЫХ СВЯЗЕЙ: РЕАКЦИИ МЕТАЛЛООРГАНИЧЕСКИХ СОЕДИНЕНИЙ
- 4.1. Реактивы Гриньяра и электрофилы
- 4.2. Другие металлоорганические реактивы и электрофилы
- 4.2.2. Цинк- и кадмийорганические соединения
- 4.2.3. Органические соединения меди (I)
- 4.3. Реакции нуклеофилов, образованных из алкинов-1
- 4.3.2. Алкинильные соединения меди (I)
- 4.4. Выводы
- 4.5. Примеры
- 5. ОБРАЗОВАНИЕ УГЛЕРОД-УГЛЕРОДНЫХ СВЯЗЕЙ: ИСПОЛЬЗОВАНИЕ СТАБИЛИЗИРОВАННЫХ КАРБАНИОНОВ И РОДСТВЕННЫХ НУКЛЕОФИЛОВ
- 5.1.1. Алкилирование
- 5.1.2. Гидролиз алкинированных продуктов: путь к карбоновым кислотам и кетонам
- 5.1.3. Ацилирование
- 5.1.4. Реакции конденсации
- 5.1.5. Реакции с соединениями типа … и родственными системами: реакция Михаэля
- 5.2. Карбанионы, стабилизированные одной (-М)-группой
- 5.2.3. Косвенные пути получения a-алкилированных альдегидов и кетонов
- 5.2.4. Реакции конденсации
- 5.2.5. Реакция Михаэля
- 5.3. Карбанионы, стабилизированные соседними атомами фосфора или серы
- 5.3.2. Карбанионы, стабилизированные двумя атомами серы
- 5.4. Алкены, арены и гетероарены как нуклеофилы
- 5.4.3. Реакции присоединения и конденсации с карбонильными и родственными им соединениями
- 5.5. Заключение
- 5.6. Задачи
- 6. ОБРАЗОВАНИЕ СВЯЗЕЙ УГЛЕРОДА С ГЕТЕРОАТОМОМ: ОСНОВНЫЕ ПРИНЦИПЫ
- 6.1. Связи углерод — галоген
- 6.2. Связи углерод — кислород и углерод — сера
- 6.3. Связи углерод — азот
- 6.3.2. Электрофильный азот и нуклеофильный углерод
- 6.3.3. Нитрозосоединения, включая нитриты
- 7. ОБРАЗОВАНИЕ И РАСКРЫТИЕ ЦИКЛОВ
- 7.1. Внутримолекулярная циклизация в результате электрофильно-нуклеофильного взаимодействия
- 7.1.2. Условия внутримолекулярного циклообразования. Правила Болдуина
- 7.1.3. Присоединение по Михаэлю в процессах циклизации
- 7.1.4. Образование ароматических и гетероароматических циклов
- 7.2. Циклоприсоединение
- 7.2.2. 1,3-Диполярное циклоприсоединение
- 7.2.3. Присоединение карбенов и нитренов к алкенам
- 7.3. Электроциклическое циклообразование
- 7.4. Раскрытие цикла
- 7.5. Выводы и задачи
- 8. ВОССТАНОВЛЕНИЕ
- 8.1. Каталитическое гидрирование
- 8.2. Восстановление гидридами металлов
- 8.3. Восстановление растворяющимися металлами
- 8.4. Восстановление определенных функциональных групп
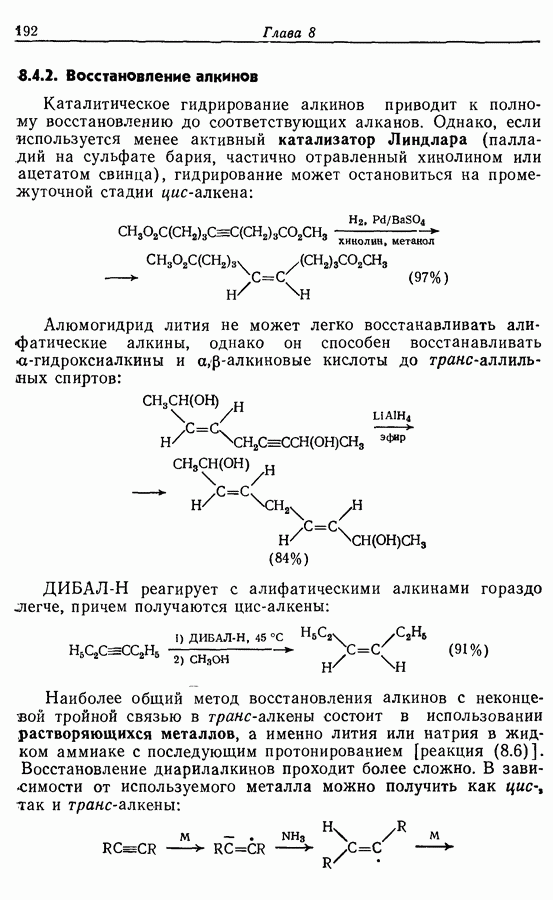
- 8.4.2. Восстановление алкинов
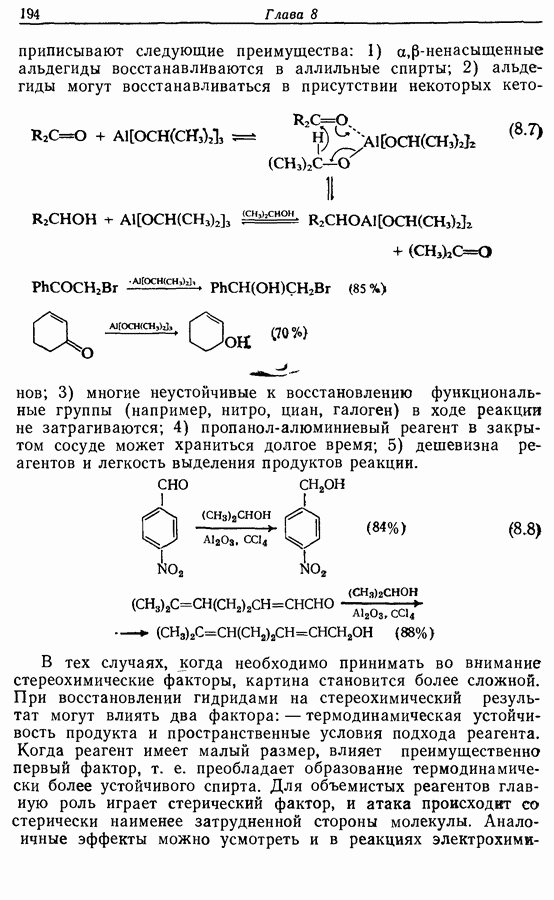
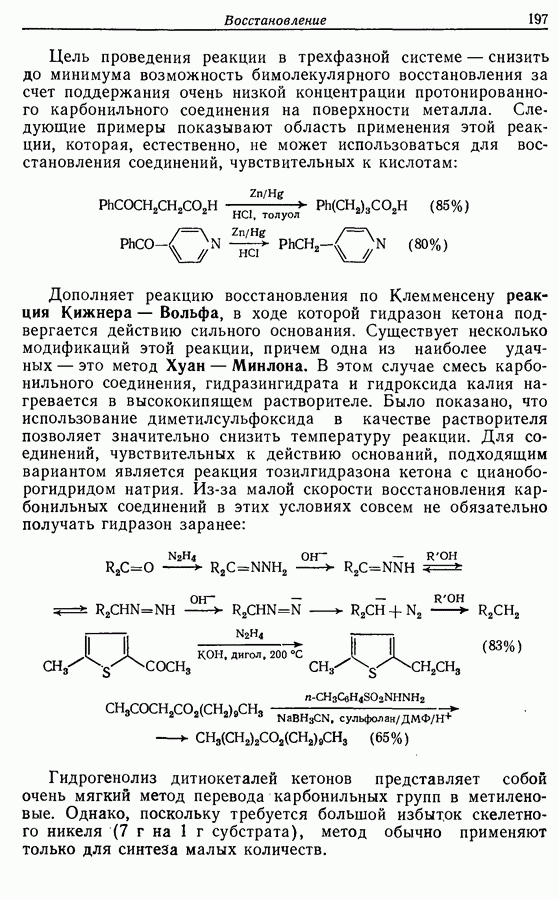
- 8.4.3. Восстановление альдегидов и кетонов
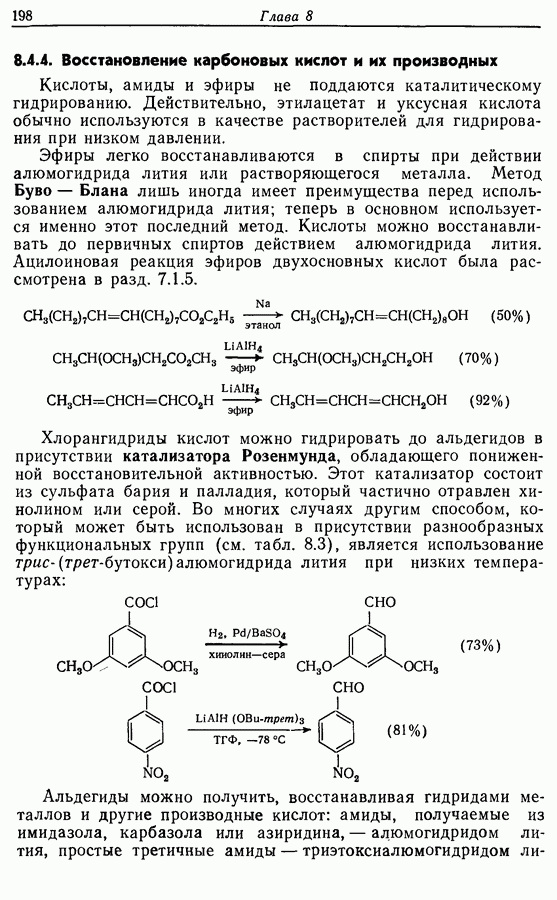
- 8.4.4. Восстановление карбоновых кислот и их производных
- 8.4.5. Восстановление нитрилов
- 8.4.6. Восстановление иминов и оксимов, включая восстановительное алкилирование
- 8.5. Восстановительное расщепление связи углерод — гетероатом
- 8.6. Восстановительное раскрытие цикла в эпоксидах
- 8.7. Восстановление a,b-ненасыщенных карбонильных соединений
- 8.8. Восстановление сопряженных диенов
- 8.9. Восстановление ароматических и гетероароматических соединений
- 9. ОКИСЛЕНИЕ
- 9.2. Окисление углеводородов
- 9.2.2. Аллильное окисление
- 9.2.3. Бензильное окисление
- 9.2.4. Дегидрирование алканов, алкильных групп и алкенов
- 9.2.5. Окислительное присоединение к алкенам
- 9.2.6. Окислительная деструкция алкенов
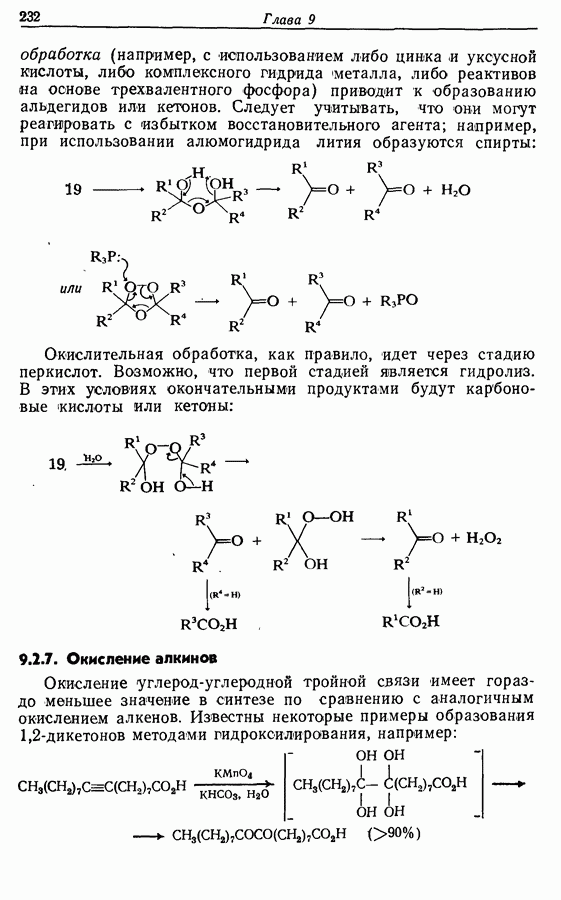
- 9.2.7. Окисление алкинов
- 9.3. Окисление спиртов и их производных
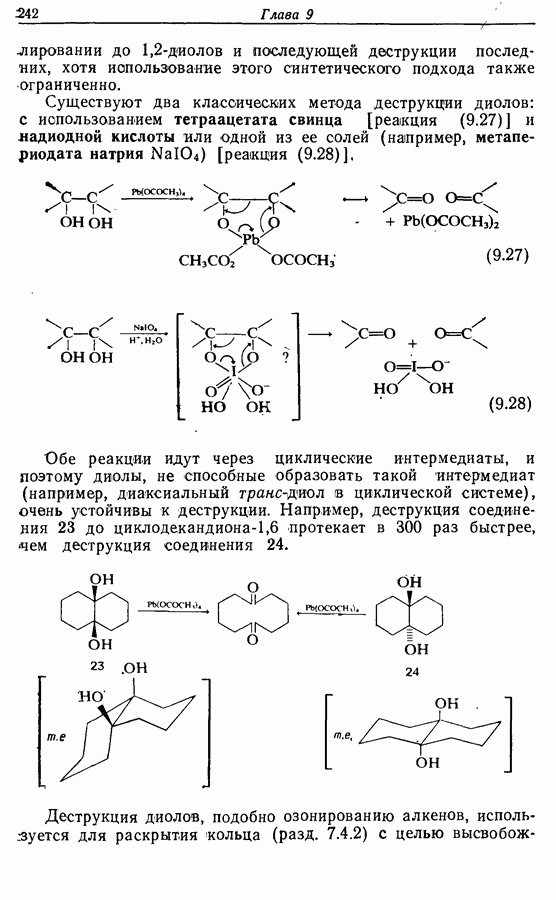
- 9.3.2. Окислительная деструкция 1,2-диолов
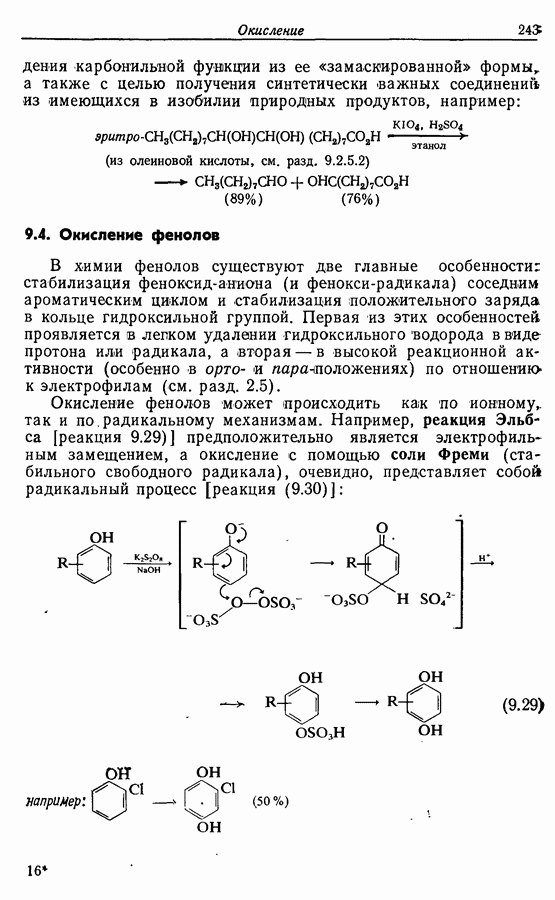
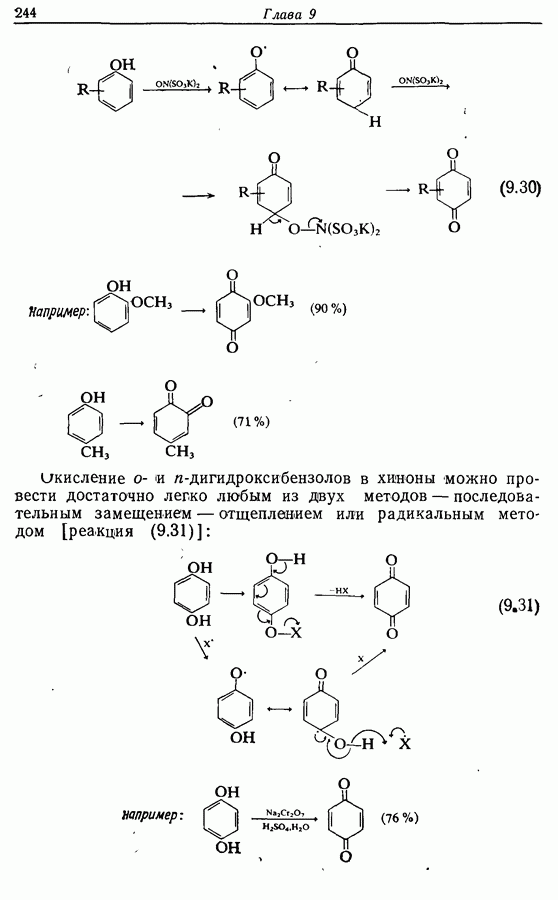
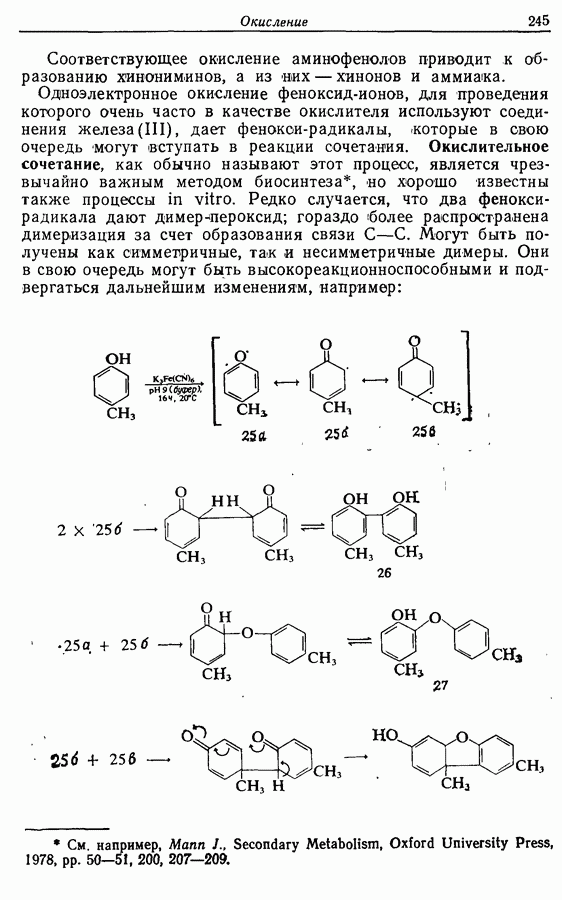
- 9.4. Окисление фенолов
- 9.5. Окисление альдегидов и кетонов
- 9.5.2. Окисление в 1,2-дикарбонильные соединения
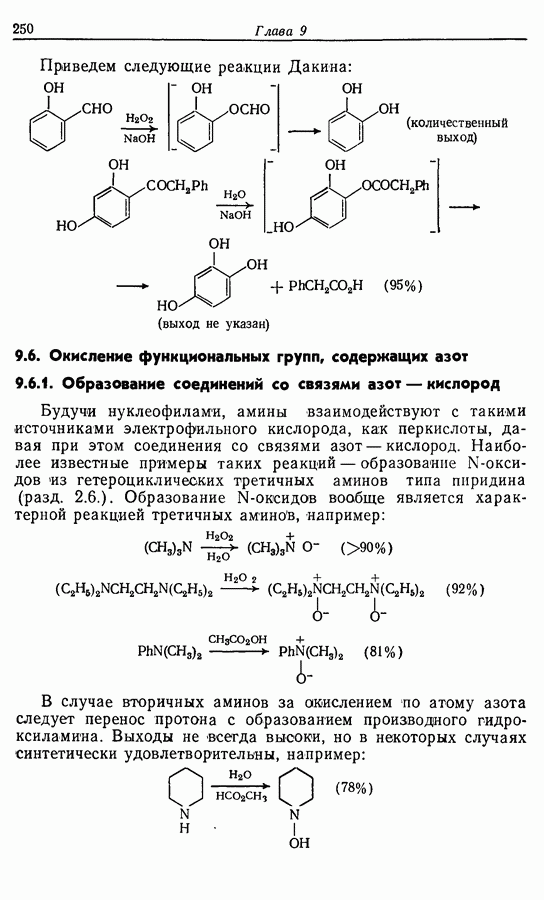
- 9.5.3. Окисление до сложных эфиров: реакции Байера — Виллигера и Дакина
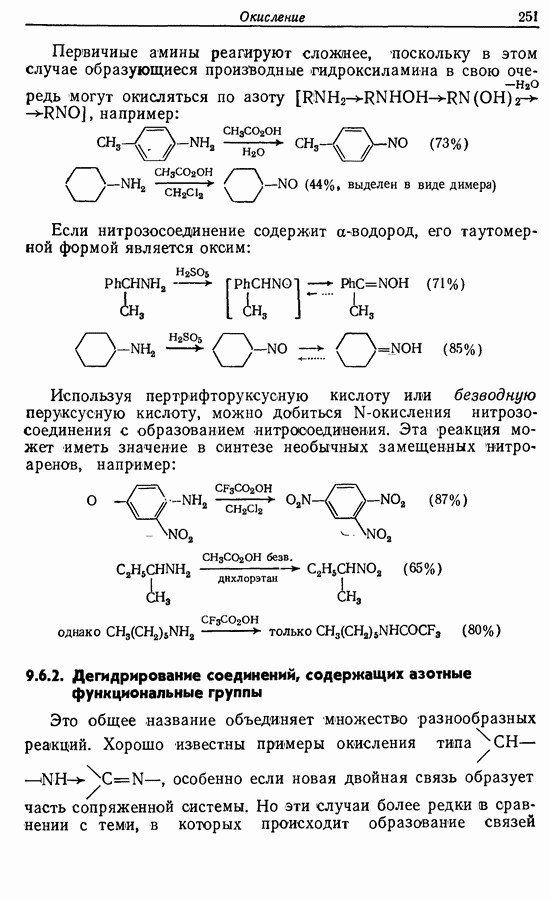
- 9.6. Окисление функциональных групп, содержащих азот
- 9.6.2. Дегидрирование соединений, содержащих азотные функциональные группы
- 9.7. Окисление серусодержащих функциональных групп
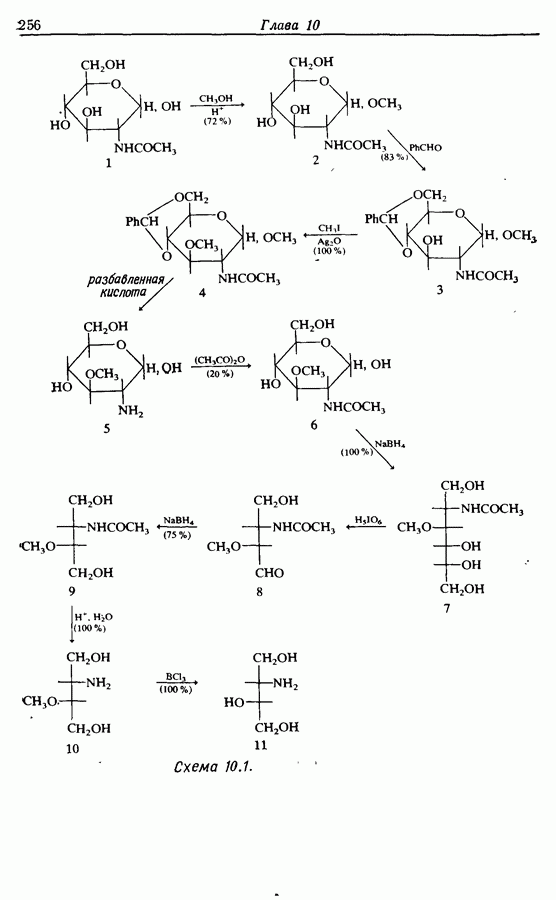
- 10. ЗАЩИТНЫЕ ГРУППЫ
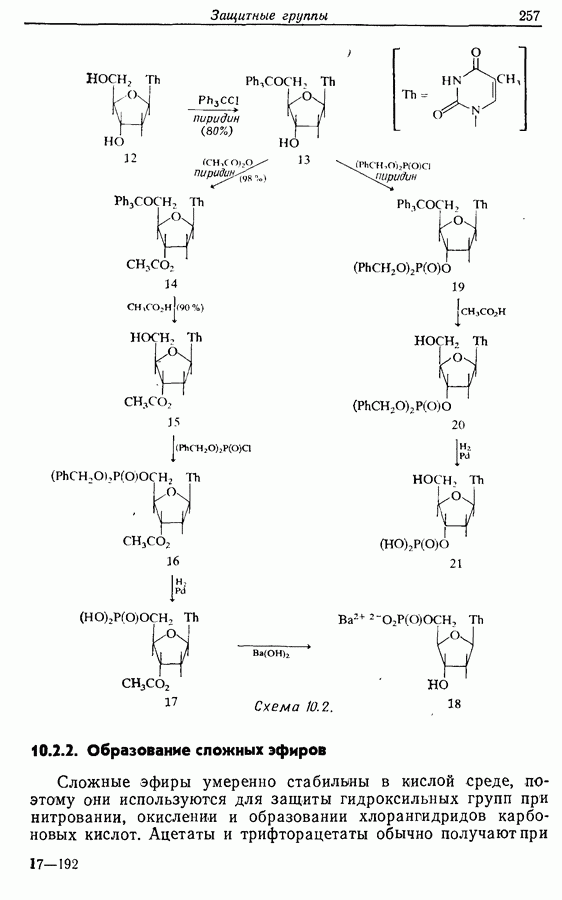
- 10.2. Защита спиртов
- 10.3. Защита диолов
- 10.4. Защита карбоновых кислот
- 10.5. Защита аминогрупп
- 10.6. Защита карбонильных групп
- 11. БОРСОДЕРЖАЩИЕ РЕАГЕНТЫ
- 11.1. Гидроборирование алкенов при действии борана
- 11.2. Гидроборирование алкенов действием алкилборанов
- 11.3. Реакции борорганических соединений
- 11.4. Гидроборирование диенов
- 11.5. Гидроборирование алкинов
- 12. ФОСФОРСОДЕРЖАЩИЕ РЕАГЕНТЫ
- 12.1. Введение в химию фосфорорганических соединений
- 12.2. Образование углерод-углеродных двойных связей
- 12.3. Превращения функциональных групп
- 12.4. Реакции дезоксигенирования
- 13. КРЕМНИЙСОДЕРЖАЩИЕ РЕАГЕНТЫ
- 13.1. Введение в химию кремнийорганических соединений
- 13.2. Синтез кремнийорганических соединений
- 13.3. Реакции с образованием углерод-углеродных связей
- 13.4. Синильная защита спиртов
- 14. ИЗБРАННЫЕ СИНТЕЗЫ
- 14.2. Z-Геникосен-6-он-11
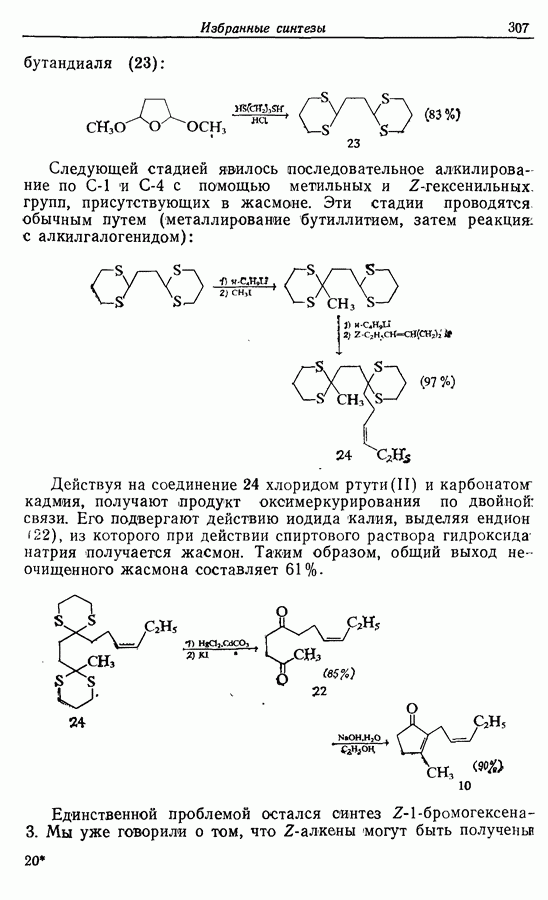
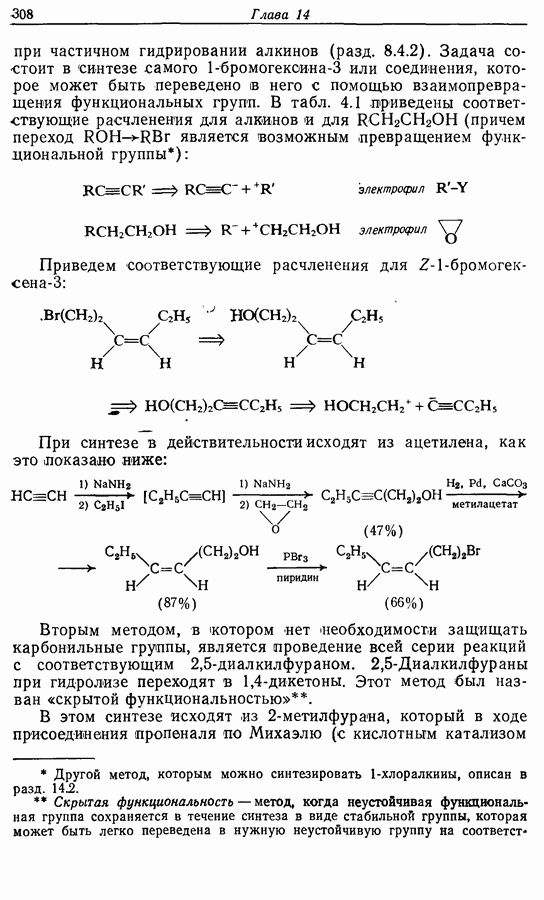
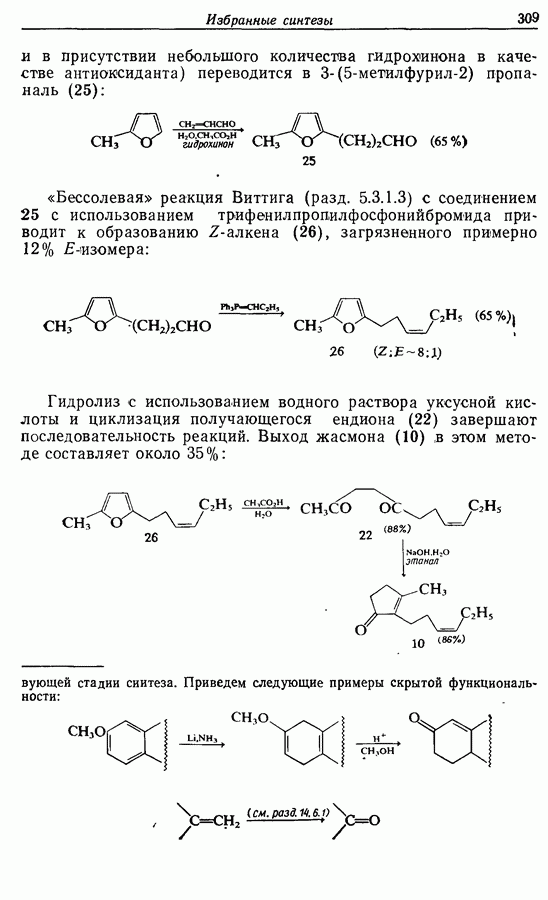
- 14.3. Синтез Z-жасмона
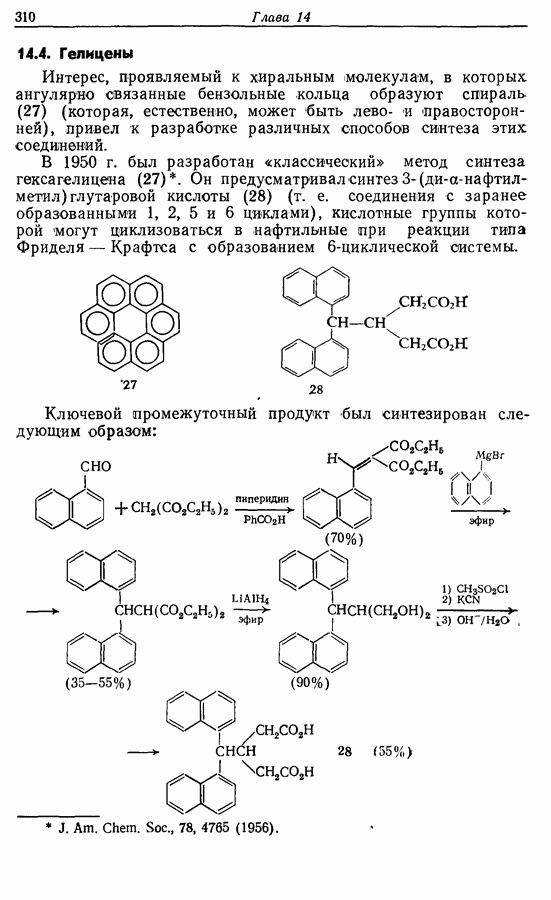
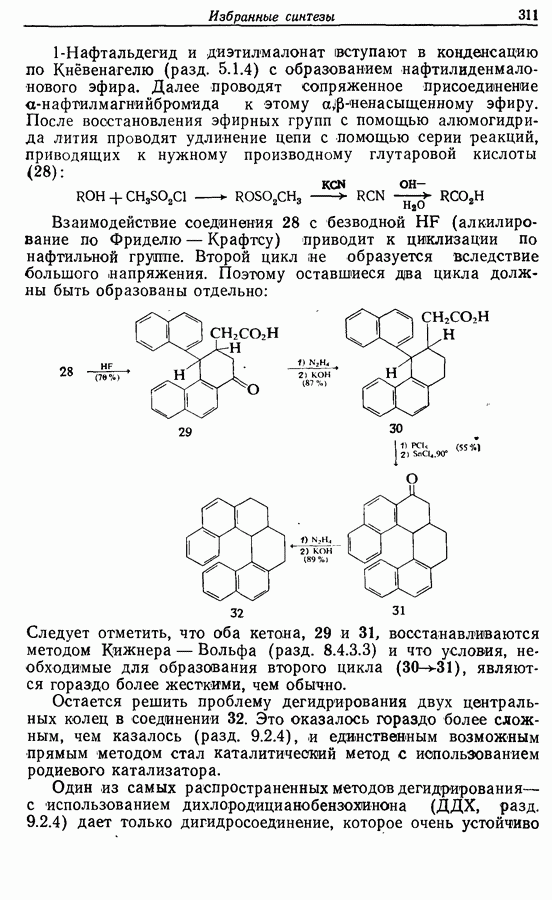
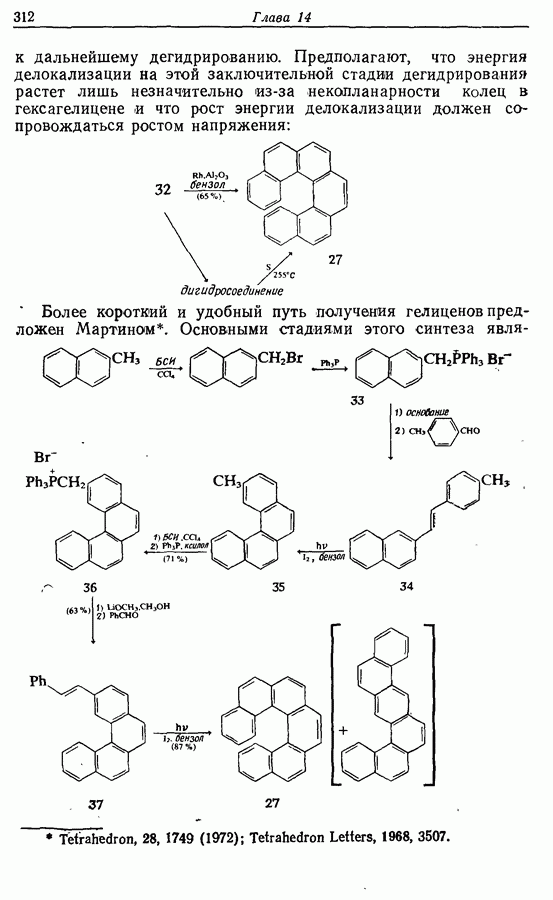
- 14.4. Гелицены
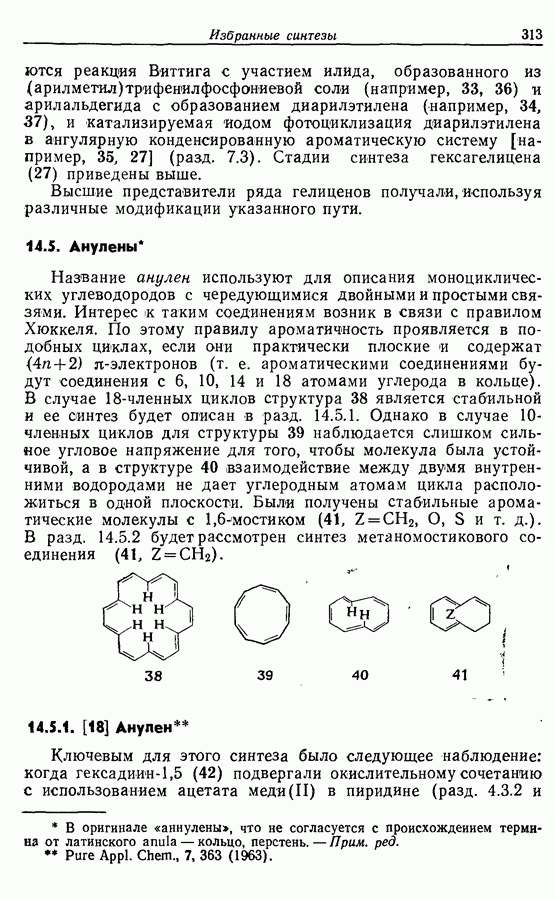
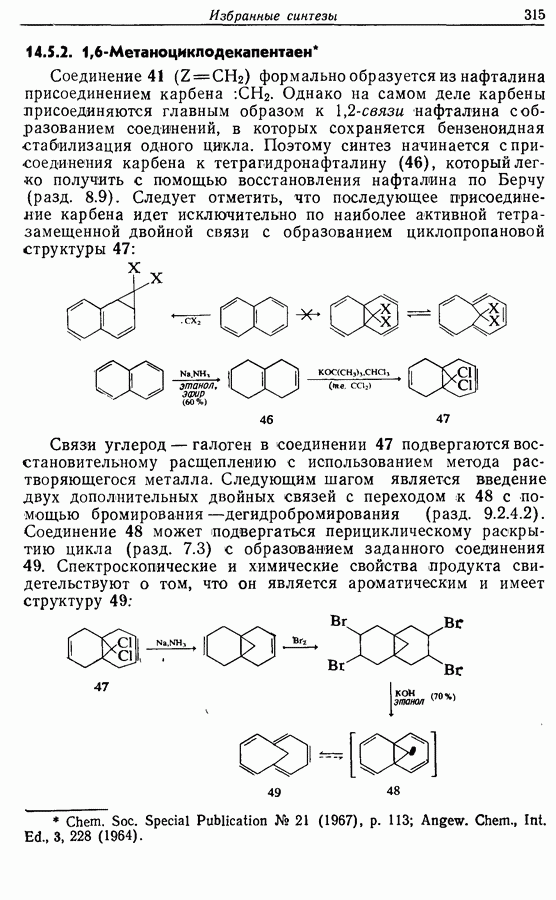
- 14.5. Анулены
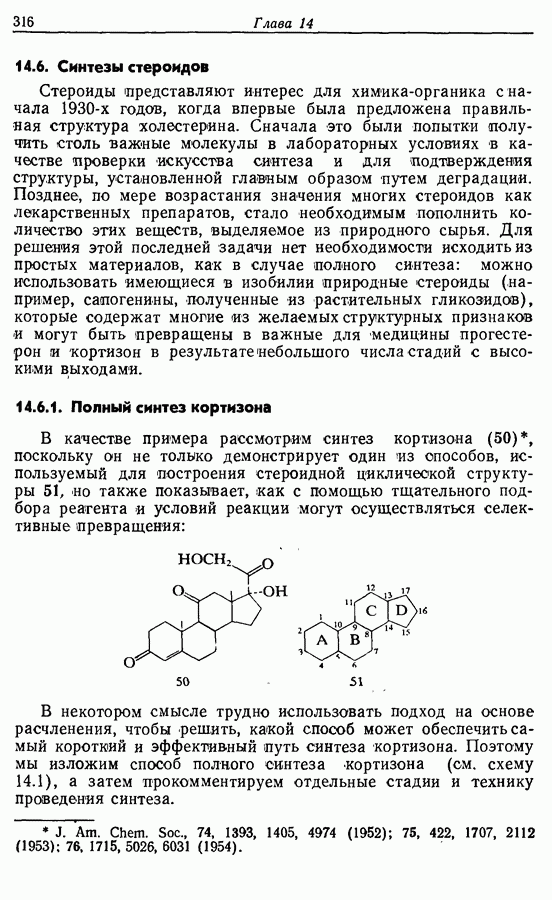
- 14.6. Синтезы стероидов
- 14.6.2. Превращение растительных стероидов в стероидные гормоны
- 14.7. Синтез пептидов
- 14.7.2. Техника синтеза пептидов
- ЛИТЕРАТУРА