| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
Глава I. ОСНОВНЫЕ ПОЛОЖЕНИЯ ТЕРМОДИНАМИКИ ГЕТЕРОГЕННЫХ РАВНОВЕСИЙ
В этой главе рассматриваются важнейшие положения термодинамики гетерогенных систем, которые составляют фундамент теории фазовых равновесий всех типов, в том числе и равновесий жидкость — пар. Мы с достаточной подробностью остановимся на формулировке принципа равновесия, на выводе и обсуждении условий равновесия и устойчивости, правиле фаз и особых случаях его применения, на некоторых других вопросах. Это представляется целесообразным, поскольку почти все прикладные проблемы теории фазовых равновесий решаются на базе термодинамики, многие инженеры и исследователи постоянно пользуются приложениями термодинамики, но значительно меньше число специалистов, хорошо знающих ее исходные, фундаментальные положения.
1.1. ПРИНЦИП РАВНОВЕСИЯ
Принцип (критерий) равновесия был сформулирован Гиббсом более 100 лет назад и опубликован в его знаменитой работе «О равновесии гетерогенных веществ» [1]. Принцип формулируется так:
система находится в состоянии равновесия, если ее энтропия при всех возможных изменениях, совместимых с условиями постоянства энергии, объема и масс всех компонентов, остается постоянной или уменьшается.
Это положение записывается следующим образом:

где символ  отвечает любым возможным изменениям энтропии первого порядка малости.
отвечает любым возможным изменениям энтропии первого порядка малости.
Условия постоянства  определяют изоляцию системы от внешней среды. Знак равенства в (1.1) соответствует протеканию обратимых (равновесных) процессов; энтропия уменьшается при необратимых процессах; в случае изолированной системы ими могут быть флуктуации плотности, концентрации и т. п.
определяют изоляцию системы от внешней среды. Знак равенства в (1.1) соответствует протеканию обратимых (равновесных) процессов; энтропия уменьшается при необратимых процессах; в случае изолированной системы ими могут быть флуктуации плотности, концентрации и т. п.
Гиббс приводит и другую, по сути, эквивалентную формулировку принципа —
система находится в состоянии равновесия, если ее энергия при всех возможных изменениях, совместимых с условиями постоянства энтропии, объема и масс всех компонентов остается постоянной или возрастает 

Принцип равновесия представляет собой самое общее выражение условий равновесия для систем любого типа — как гомогенных, так и гетерогенных. Он позволяет получить в развернутом виде условия термодинамического равновесия между фазами, определить типы равновесий и установить условия термодинамической устойчивости фаз (условия стабильности). По своему содержанию принцип равновесия близок ко второму началу термодинамики, его можно рассматривать как одну из формулировок второго начала в применении к равновесным системам.
Известно, что второе начало может быть выражено разными способами. Например, Гуггенгейм [2, стр. 15] вводит его посредством такого постулата —
существует функция состояния энтропия  которая обладает следующими свойствами: если при бесконечно малом изменении состояния системы поглощенную из окружающей среды теплоту обозначить через
которая обладает следующими свойствами: если при бесконечно малом изменении состояния системы поглощенную из окружающей среды теплоту обозначить через 

При этом естественные процессы — это те, которые происходят в действительности, самопроизвольно, приближают систему к равновесию. Неестественные процессы могут протекать только при внешних воздействиях или же быть результатом флуктуаций. Можно видеть, что соотношения (1.3) по своему содержанию очень близки к принципу равновесия.
Действительно, если система уже находится в состоянии равновесия, то для нее мыслимы только процессы, уводящие от равновесия или не нарушающие его, т. е. возможны случаи (1.36) и (1.3в); тогда

Если сопоставить (1.4) с первым началом термодинамики, выражаемом в форме

то окажется, что для системы, находящейся в состоянии равновесия, возможны только такие процессы, для которых

Из выражения (1.5), при наложении условий постоянства  или
или  сразу же получаем формулировки принципа равновесия (1.1) и (1.2).
сразу же получаем формулировки принципа равновесия (1.1) и (1.2).
Для равновесных процессов (1.5) переходит в следующее

одно из фундаментальных уравнений, которое для системы из  компонентов с переменной массой принимает вид:
компонентов с переменной массой принимает вид:

Из (1.5) и (1.6) обычным путем, используя преобразование Лежандра, получаем другие фундаментальные уравнения и формулировки принципа равновесия, выраженные через: энергию Гельмгольца —

энергию Гиббса —

Из (1.1), (1.2), (1.8) и (1.9) следует, что для системы, находящейся в состоянии равновесия, энтропия имеет условный максимум, а внутренняя энергия, энергия Гельмгольца и энергия Гиббса условный минимум. При этом условия экстремума для каждой из функций различны, они указаны при записи приведенных критериев равновесия. Так, энтропия имеет условный максимум при заданных значениях  а энергия Гиббса — условный минимум при заданных значениях
а энергия Гиббса — условный минимум при заданных значениях  .
.
Выполнение любого из критериев является необходимым и достаточным условием для утверждения, что система находится в состоянии равновесия, в этом отношении все варианты записи эквивалентны. Однако они отличаются по широте. Форма (1.1) ближе всего к выражению второго начала и из нее, или же из (1.2), как это будет показано в разд. 1.2, можно получить полные условия равновесия. Форма записи (1.9) наиболее удобна, так как закреплены переменные  , которые часто являются постоянными в эксперименте, в том числе и при изучении равновесия жидкость — пар. Но из этой формы нельзя получить условия термического и механического равновесий, они как бы уже заранее заданы закреплением
, которые часто являются постоянными в эксперименте, в том числе и при изучении равновесия жидкость — пар. Но из этой формы нельзя получить условия термического и механического равновесий, они как бы уже заранее заданы закреплением  . Полезно дать геометрическую
. Полезно дать геометрическую

Рис. 1.1. Зависимость энергии от энтропии пр» постоянном объеме системы
иллюстрацию принципа равновесия. Представим поверхность в системе координат  сечение этой поверхности при
сечение этой поверхности при  изображено на рис. 1.1. Равновесные состояния системы лежат на поверхности
изображено на рис. 1.1. Равновесные состояния системы лежат на поверхности  при заданном объеме и энтропии
при заданном объеме и энтропии  (точка пересечения штрих-линии с осью абсцисс) равновесному состоянию отвечает точка
(точка пересечения штрих-линии с осью абсцисс) равновесному состоянию отвечает точка  в ней энергия имеет условный минимум (ограничивающие условия
в ней энергия имеет условный минимум (ограничивающие условия  выше кривой расположена область неравновесных состояний; состояния, отвечающие точкам ниже кривой, не имеют физического смысла.
выше кривой расположена область неравновесных состояний; состояния, отвечающие точкам ниже кривой, не имеют физического смысла.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА
- Глава I. ОСНОВНЫЕ ПОЛОЖЕНИЯ ТЕРМОДИНАМИКИ ГЕТЕРОГЕННЫХ РАВНОВЕСИЙ
- 1.2. УСЛОВИЯ РАВНОВЕСИЯ ГЕТЕРОГЕННЫХ СИСТЕМ
- 1.3. ТИПЫ РАВНОВЕСИЙ
- 1.4. УСЛОВИЯ УСТОЙЧИВОСТИ
- 1.5. ПРАВИЛО ФАЗ
- Глава II. ОДНОКОМПОНЕНТНЫЕ СИСТЕМЫ
- II.1. ДИАГРАММЫ СОСТОЯНИЯ
- II.2. УРАВНЕНИЕ КЛАУЗИУСА—КЛАПЕЙРОНА
- II.3. ЗАВИСИМОСТЬ ДАВЛЕНИЯ ОТ ТЕМПЕРАТУРЫ. УРАВНЕНИЕ АНТУАНА
- II.4. ЗАКОН СООТВЕТСТВЕННЫХ СОСТОЯНИЙ
- II.5. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА. ДРУГИЕ АНАЛИТИЧЕСКИЕ УРАВНЕНИЯ СОСТОЯНИЯ
- II.6. ВИРИАЛЬНОЕ УРАВНЕНИЕ СОСТОЯНИЯ
- Глава III. ДВОЙНЫЕ СИСТЕМЫ
- III.1. ДИАГРАММЫ РАВНОВЕСИЯ ДЛЯ ДВОЙНЫХ СИСТЕМ
- III.2. ОБОБЩЕННОЕ ДИФФЕРЕНЦИАЛЬНОЕ УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- III.3. ЗАКОНЫ КОНОВАЛОВА
- III.4. ЗАКОНЫ ВРЕВСКОГО
- III.5. ИДЕАЛЬНЫЕ СИСТЕМЫ
- III.6. РАЗБАВЛЕННЫЕ РАСТВОРЫ
- III.7 РЕАЛЬНЫЕ СИСТЕМЫ
- III.8. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ СМЕШЕНИЯ И РАВНОВЕСИЕ ЖИДКОСТЬ—ПАР
- III.9. ОБ АЗЕОТРОПИИ В БИНАРНЫХ СИСТЕМАХ
- III.10. ТРЕХФАЗНЫЕ РАВНОВЕСИЯ ЖИДКОСТЬ—ЖИДКОСТЬ—ПАР В ДВОЙНЫХ СИСТЕМАХ
- III.11. ФАЗОВЫЕ ДИАГРАММЫ БИНАРНЫХ СИСТЕМ В ШИРОКОМ ИНТЕРВАЛЕ ТЕМПЕРАТУР И ДАВЛЕНИЙ
- Глава IV. ТРОЙНЫЕ И МНОГОКОМПОНЕНТНЫЕ СИСТЕМЫ
- IV.2. ПРОЯВЛЕНИЕ ЗАКОНОВ КОНОВАЛОВА И ВРЕВСКОГО В ТРОЙНЫХ И МНОГОКОМПОНЕНТНЫХ СИСТЕМАХ
- IV.3. ОТКРЫТЫЕ ФАЗОВЫЕ ПРОЦЕССЫ. ТЕРМОДИНАМИКО-ТОПОЛОГИЧЕСКИЕ ЗАКОНОМЕРНОСТИ
- Глава V. МЕТОДЫ ЭКСПЕРИМЕНТАЛЬНОГО ИССЛЕДОВАНИЯ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР
- V.I. ЦИРКУЛЯЦИОННЫЙ МЕТОД
- V.2. МЕТОД ОТКРЫТОГО ИСПАРЕНИЯ
- V.3. МЕТОД СТРУИ ИНЕРТНОГО ГАЗА
- V.4. СТАТИЧЕСКИЙ МЕТОД
- V.5. ИЗОПИЕСТИЧЕСКИЙ МЕТОД
- V.6. ИЗМЕРЕНИЕ ТЕМПЕРАТУРЫ КИПЕНИЯ ПРИ ПОСТОЯННОМ ДАВЛЕНИИ
- V.7. РАСЧЕТ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР ПО ЗАВИСИМОСТИ ДАВЛЕНИЯ ПАРА ОТ СОСТАВА РАСТВОРА ПРИ ПОСТОЯННОЙ ТЕМПЕРАТУРЕ
- V.8. МЕТОДЫ ИССЛЕДОВАНИЯ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР С ПОМОЩЬЮ ГАЗОВОЙ ХРОМАТОГРАФИИ
- V.9. РАВНОВЕСИЕ ЖИДКОСТЬ—ПАР ДЛЯ РАЗБАВЛЕННЫХ РАСТВОРОВ
- Глава VI. МЕТОДЫ ПРОВЕРКИ ЭКСПЕРИМЕНТАЛЬНЫХ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ-ПАР
- VI.2. ОБЩАЯ ОЦЕНКА ТЕРМОДИНАМИЧЕСКИХ МЕТОДОВ ПРОВЕРКИ И ИСПРАВЛЕНИЯ ДАННЫХ
- VI.3. ПРОВЕРКА ДАННЫХ С ПОМОЩЬЮ УРАВНЕНИЙ ГИББСА—ДЮГЕМА И ДЮГЕМА—МАРГУЛЕСА
- VI.4. МЕТОД РЕДЛИХА—КИСТЕРА
- VI.5. МЕТОД ВАН-НЕССА
- VI.6. СТАТИСТИЧЕСКИЕ МЕТОДЫ ОБРАБОТКИ ЭКСПЕРИМЕНТАЛЬНЫХ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ—ПАР
- VI.7. МЕТОДЫ ПРОВЕРКИ ТЕРМОДИНАМИЧЕСКОЙ СОГЛАСОВАННОСТИ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ—ПАР В ТРОЙНЫХ СИСТЕМАХ
- VI.8. СОПОСТАВЛЕНИЕ МЕТОДОВ РЕДЛИХА—КИСТЕРА И ВАН-НЕССА
- Глава VII. МЕТОДЫ РАСЧЕТА РАВНОВЕСИЙ ЖИДКОСТЬ—ПАР
- VII. 1. ТЕРМОДИНАМИЧЕСКИЕ ПАРАМЕТРЫ РАВНОВЕСНЫХ ЖИДКОСТИ И ПАРА
- VII.2. АЛГОРИТМЫ РАСЧЕТА ФАЗОВЫХ РАВНОВЕСИЙ
- VII.3. УЧЕТ НЕИДЕАЛЬНОСТИ ПАРОВОЙ ФАЗЫ ПРИ СРЕДНИХ И НИЗКИХ ДАВЛЕНИЯХ
- VII.4. ПОЛИНОМИАЛЬНЫЕ УРАВНЕНИЯ ДЛЯ КОЭФФИЦИЕНТОВ АКТИВНОСТИ И УРАВНЕНИЕ ВАН-ЛААРА
- VII.5. МОДЕЛИ ЛОКАЛЬНОГО СОСТАВА
- VII.6. ОЦЕНКА ПАРАМЕТРОВ МОДЕЛЕЙ ЖИДКОЙ ФАЗЫ
- VII.7. СОПОСТАВЛЕНИЕ МОДЕЛЕЙ ЖИДКОЙ ФАЗЫ ПРИ ОПИСАНИИ ФАЗОВЫХ РАВНОВЕСИЙ
- VII.8. РЕШЕТОЧНЫЕ МОДЕЛИ. МОДЕЛЬ БАРКЕРА
- Глава VIII. ГРУППОВЫЕ МОДЕЛИ РАСТВОРОВ
- VIII.1. ОСНОВНЫЕ ОСОБЕННОСТИ ГРУППОВЫХ МОДЕЛЕЙ РАСТВОРОВ
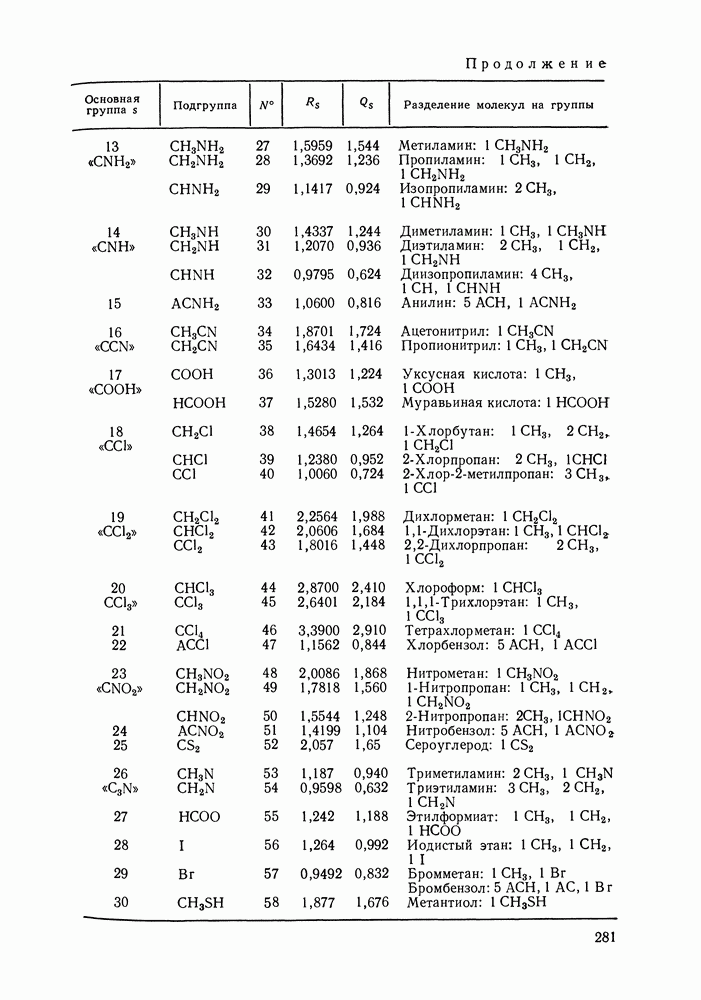
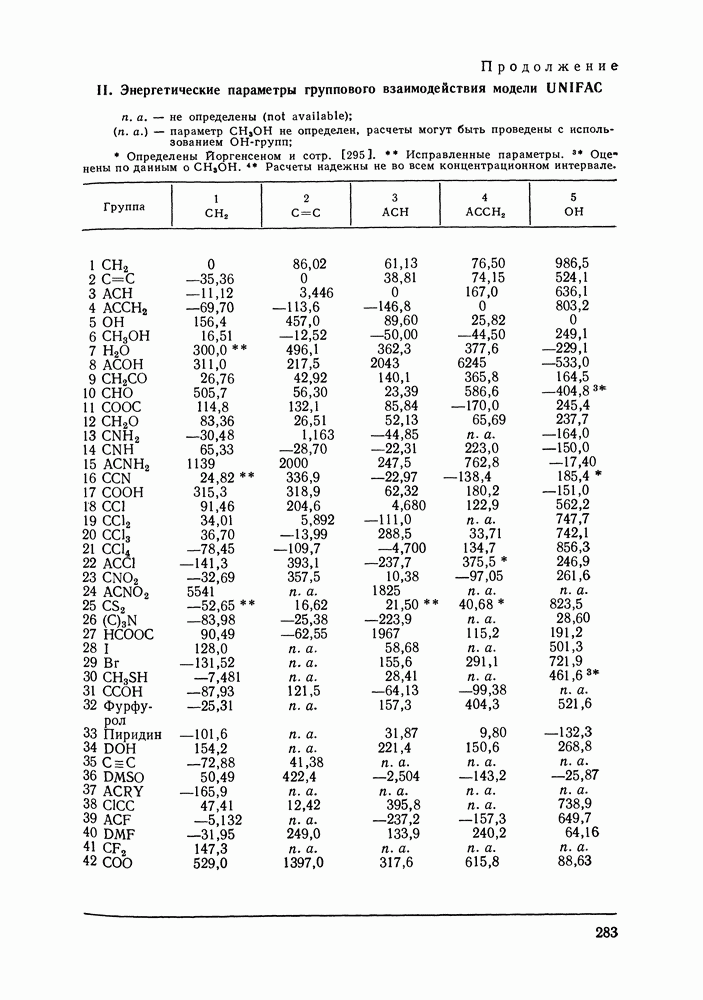
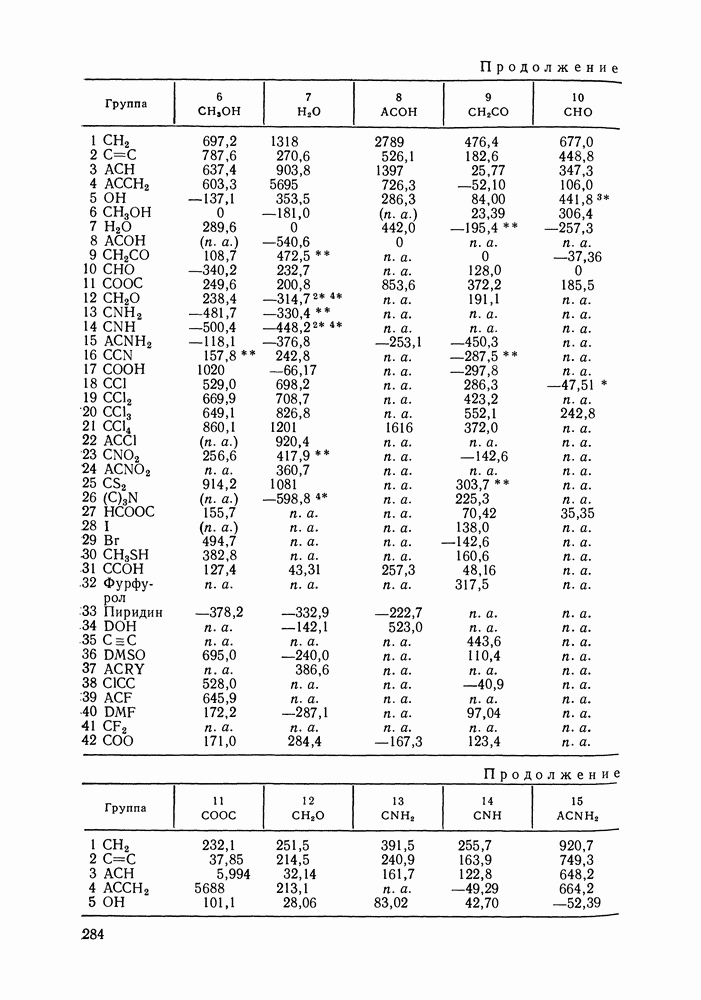
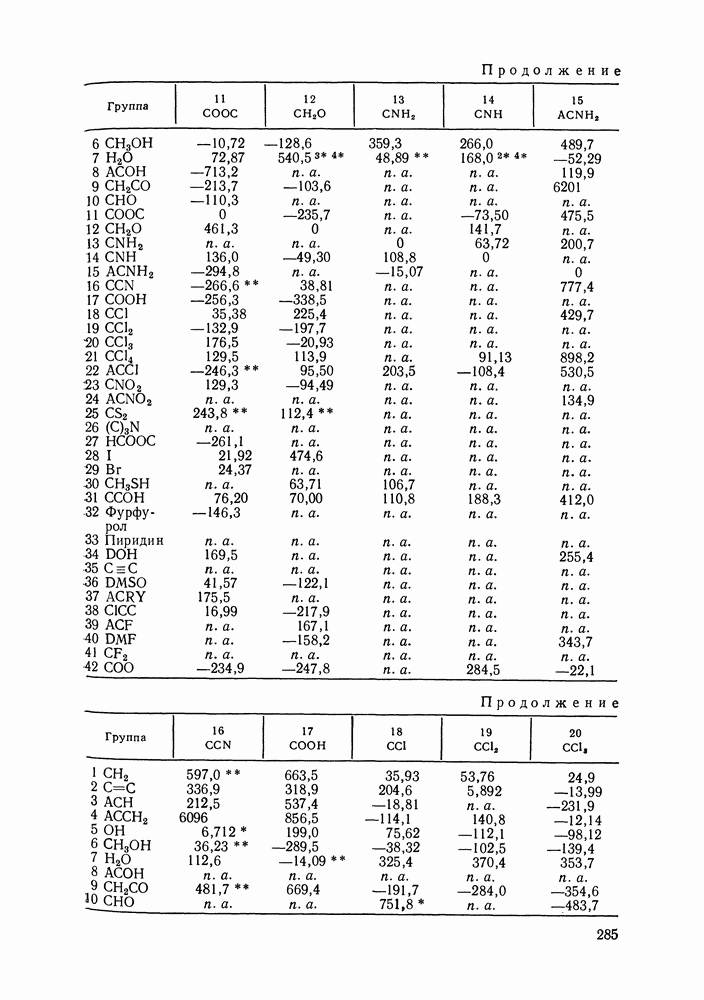
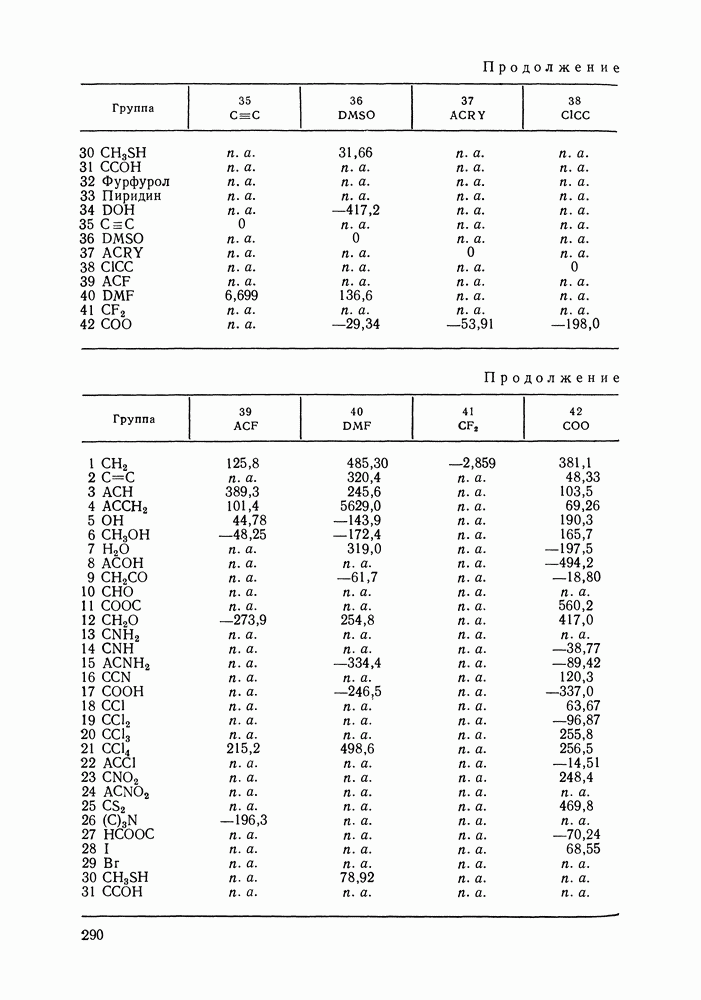
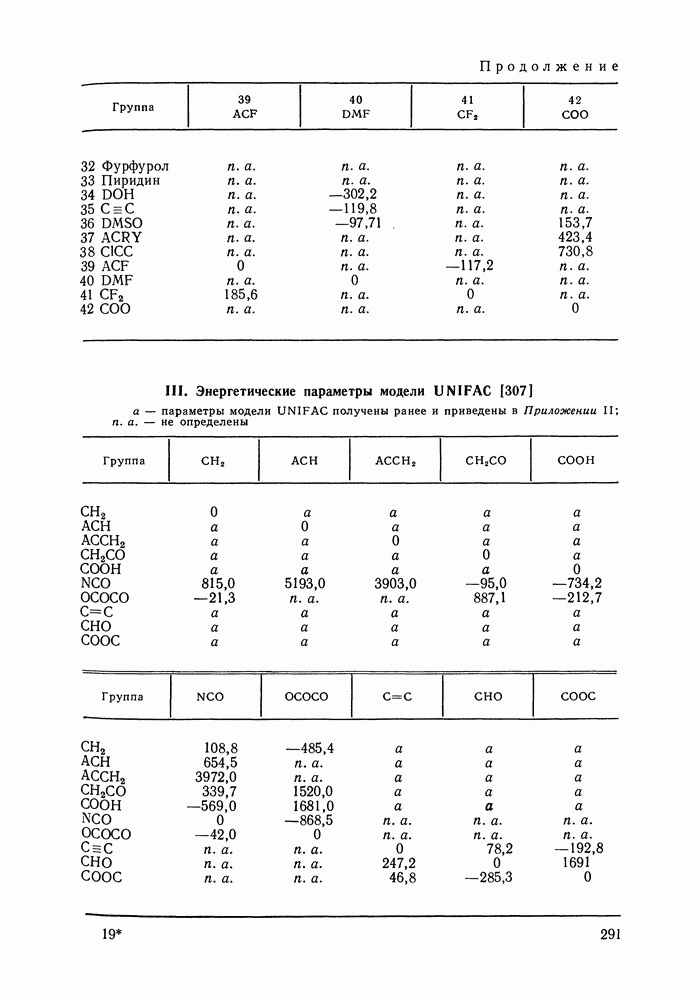
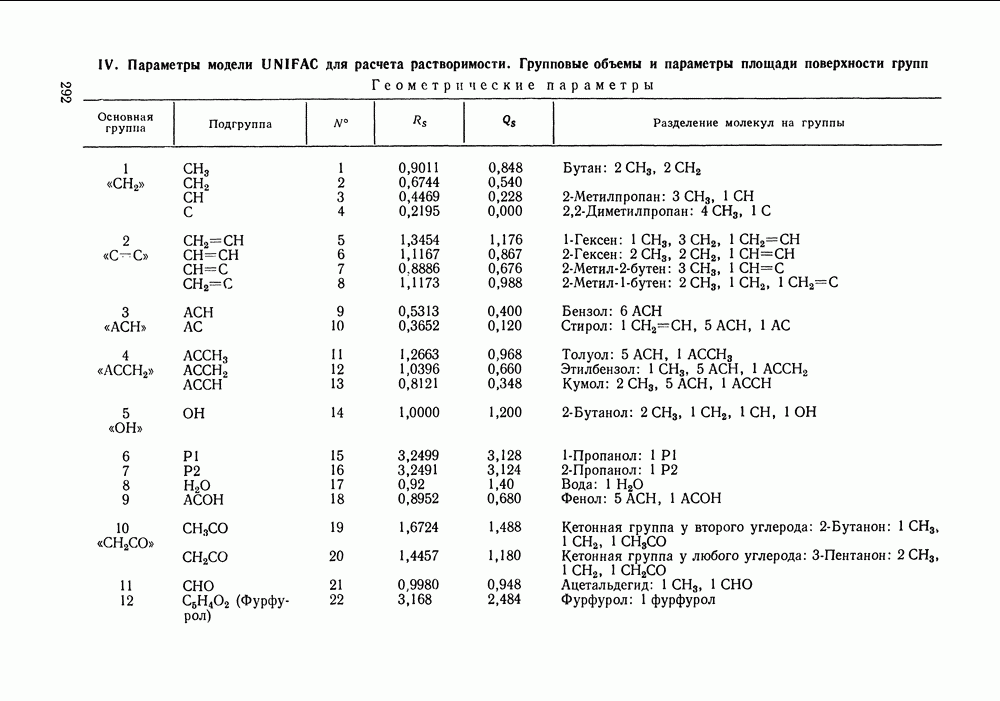
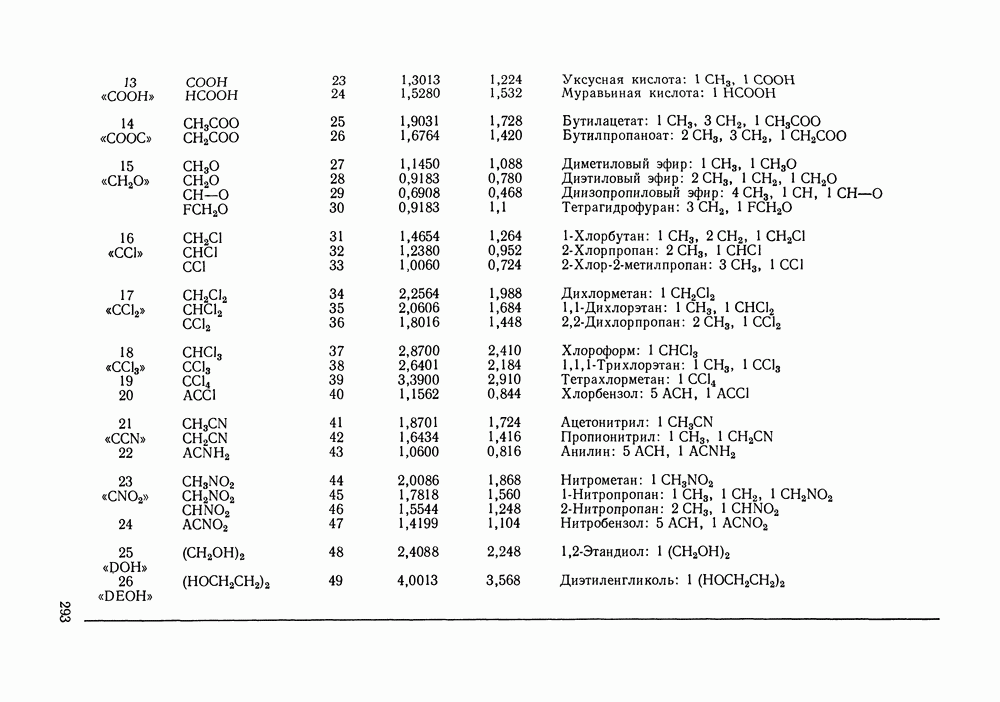
- VIII.2. МОДЕЛЬ UNIFAC
- VIII.3. КВАЗИХИМИЧЕСКИЕ ГРУППОВЫЕ МОДЕЛИ
- Глава IX. ДЫРОЧНАЯ РЕШЕТОЧНАЯ КВАЗИХИМИЧЕСКАЯ МОДЕЛЬ, ЕЕ ГРУППОВОЙ ВАРИАНТ
- IX.2. ФОРМУЛИРОВКА ДЫРОЧНОЙ КВАЗИХИМИЧЕСКОЙ МОДЕЛИ
- IX.3. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ СИСТЕМЫ
- IX.4. О МЕТОДИКЕ РАСЧЕТА
- IX.5. РЕЗУЛЬТАТЫ РАСЧЕТОВ И ВОЗМОЖНОСТИ МОДЕЛИ
- IX.6. ПРИМЕРЫ РАСЧЕТА