| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
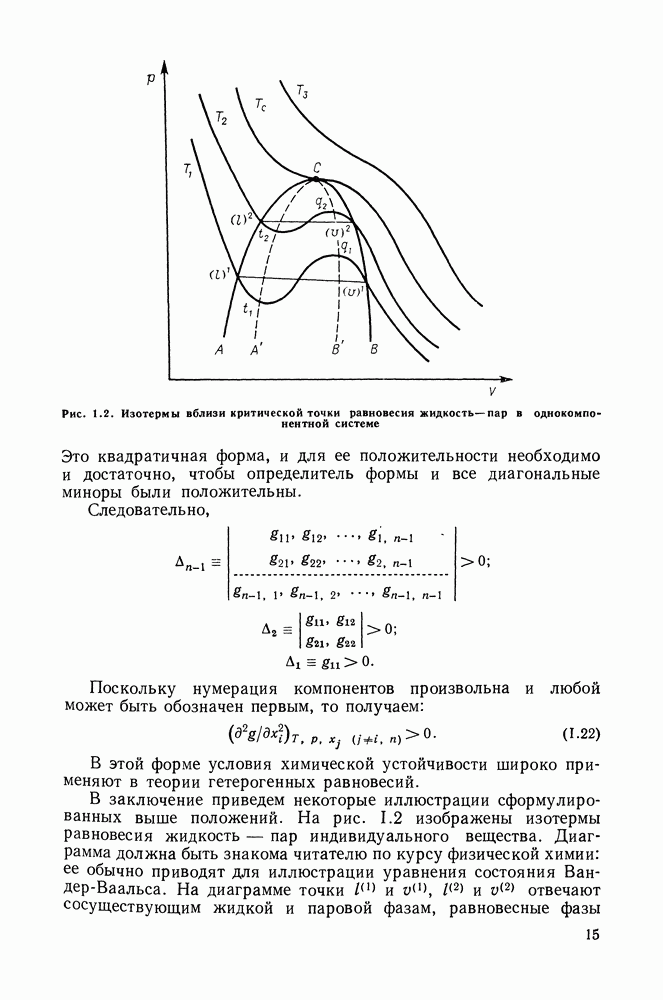
IX.4. О МЕТОДИКЕ РАСЧЕТА
Для вычислений с помощью обсуждаемой модели необходимо по тем или иным экспериментальным данным определить геометрические  и энергетические
и энергетические  параметры для
параметры для
молекул компонентов, входящих в рассматриваемую систему. Модель можно применять с индивидуальными для каждой системы параметрами и в групповом варианте: для этого достаточно предположить, что параметры группы одни и те же, независимо от того, в молекулу какого компонента эта группа входит.
Параметры  можно оценить по экспериментальным данным о термодинамических свойствах чистых компонентов, при определении энергетических параметров в ряде случаев необходимы данные для бинарных систем. Площади поверхности групп
можно оценить по экспериментальным данным о термодинамических свойствах чистых компонентов, при определении энергетических параметров в ряде случаев необходимы данные для бинарных систем. Площади поверхности групп  при известных
при известных  вычисляются по формуле
вычисляются по формуле  Значения факторов объемности выбираем с учетом размера и формы групп. Так, молекулы алканов рассматриваем как линейные цепочки
Значения факторов объемности выбираем с учетом размера и формы групп. Так, молекулы алканов рассматриваем как линейные цепочки  для молекулы в целом), и величины
для молекулы в целом), и величины  для входящих в эти молекулы функциональных групп выбираем, используя соотношение:
для входящих в эти молекулы функциональных групп выбираем, используя соотношение:

которое следует из формулы  вследствие аддитивности молекулярной поверхности
вследствие аддитивности молекулярной поверхности  и объема
и объема  Здесь
Здесь  число групп типа
число групп типа  в молекуле компонента
в молекуле компонента  Для молекулы воды
Для молекулы воды  близко к единице, поэтому принимали
близко к единице, поэтому принимали  (таким должен быть фактор объемности молекулы, занимающей одно место решетки); то же значение I взято для сероводорода.
(таким должен быть фактор объемности молекулы, занимающей одно место решетки); то же значение I взято для сероводорода.
Факторы объемности функциональных групп можно также оценивать по величинам вандерваальсовых объемов и площадей поверхности из таблиц Бонди [219] (так, например, оценивали  для гидроксильной группы спиртов). При определении геометрических параметров группы
для гидроксильной группы спиртов). При определении геометрических параметров группы  (атом водорода, способный к образованию водородной связи) учитывали, что каждая такая группа может принимать участие лишь в одной связи, т. е.
(атом водорода, способный к образованию водородной связи) учитывали, что каждая такая группа может принимать участие лишь в одной связи, т. е. 
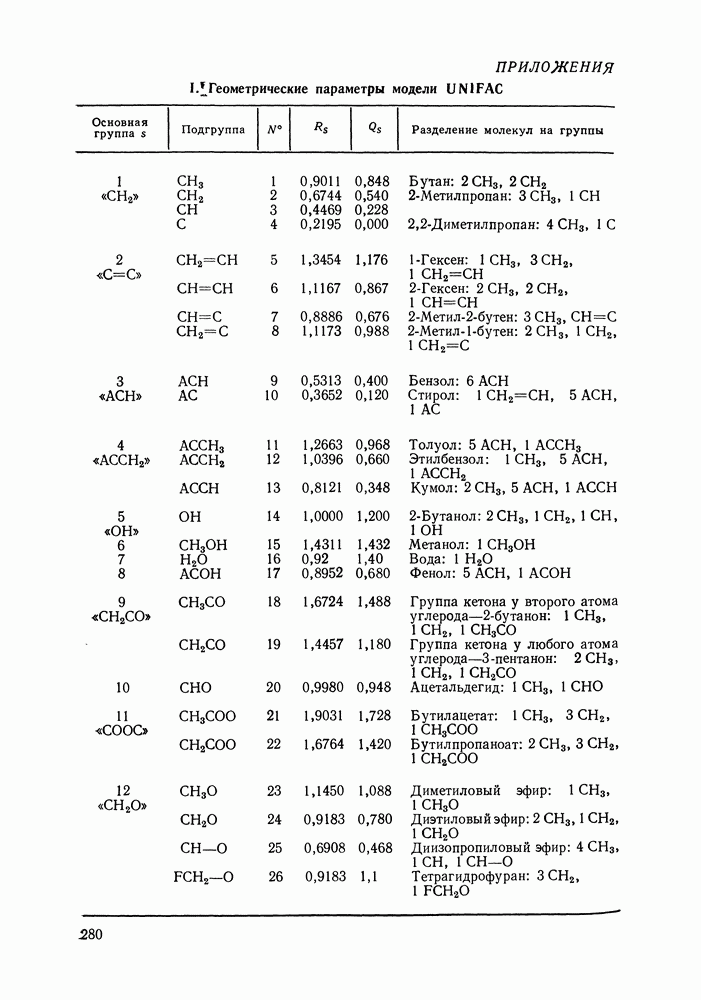
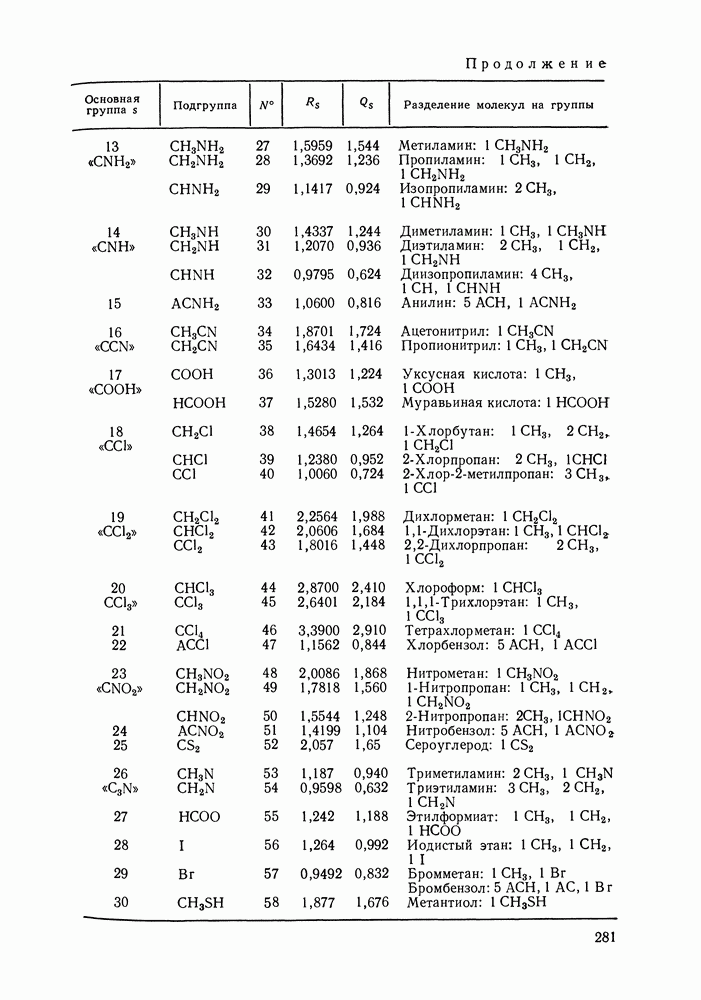
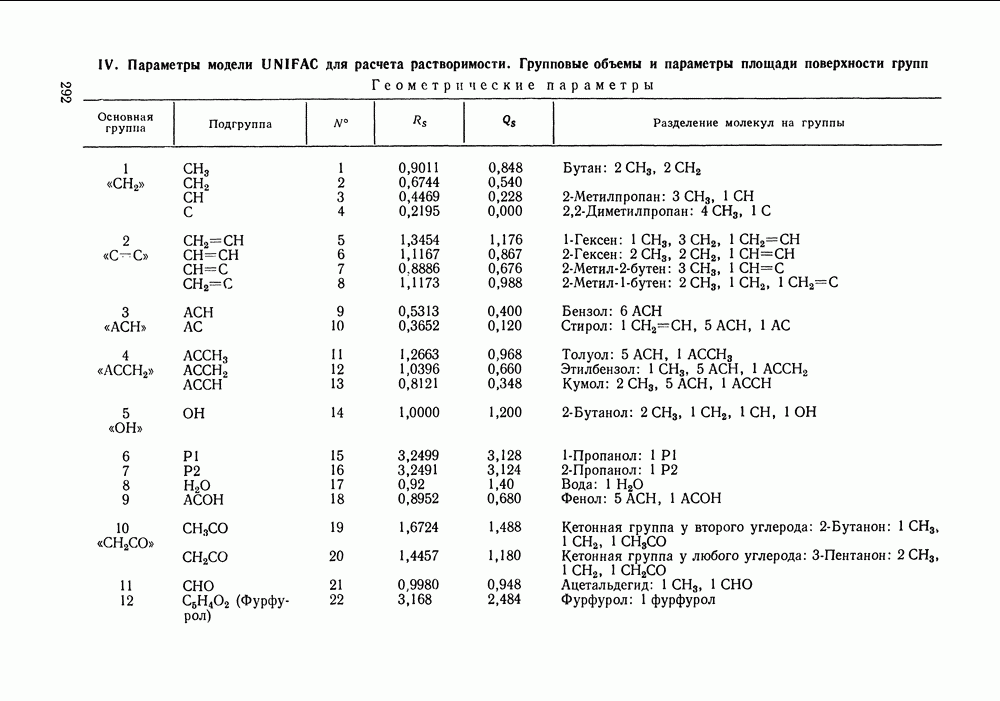
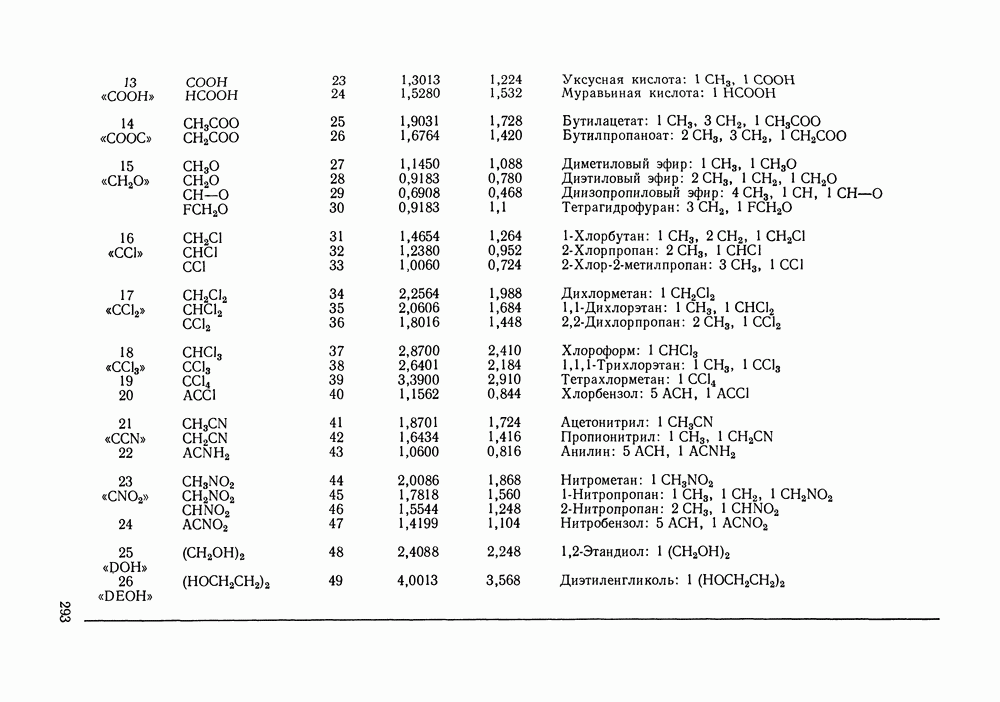
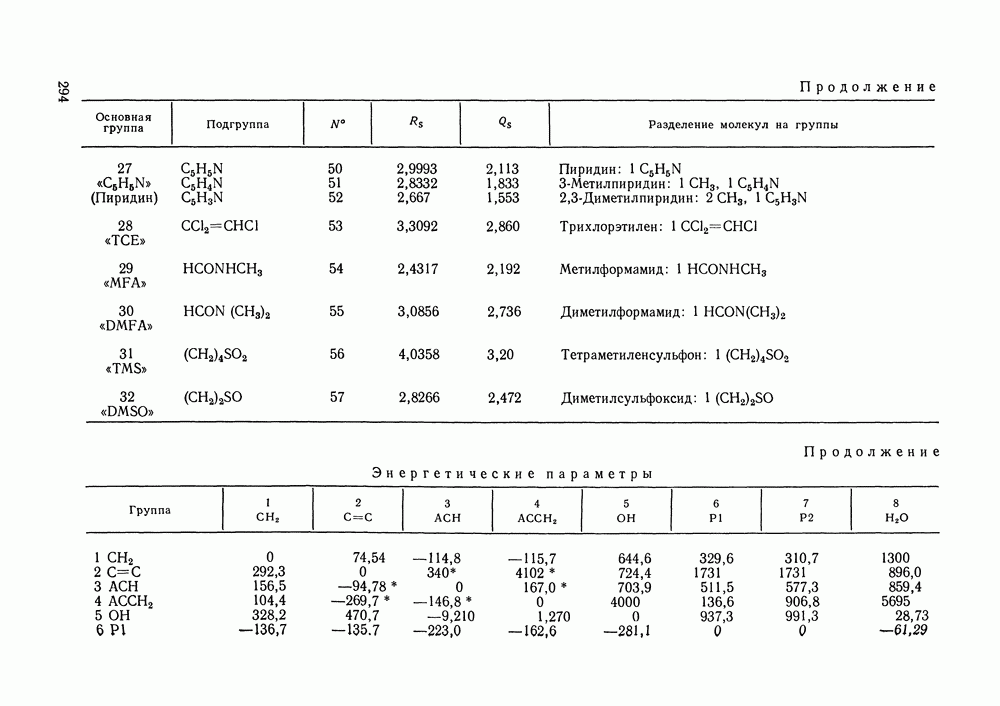
Конкретные значения геометрических параметров функциональных групп приведены в табл. IX. 1, которая, кроме того, показывает и принятый способ деления молекул на группы.
Из приведенных выше примеров следует, что используемые модели реальной структуры молекул весьма условны и способны лишь приближенно учесть молекулярную форму. Однако при расчетах комбинаторной составляющей термодинамических свойств согласно достаточно грубому приближению Ставермана более тщательное рассмотрение строения молекул вряд ли целесообразно. Описанный выше способ учета геометрии молекул аналогичен часто применяемому в решеточных моделях без вакансий. Отметим, что теоретически более последовательные методы изучения комбинаторики систем из частиц различной формы ограничены в настоящее время достаточно простыми системами: в лучшем случае удается рассмотреть смеси, моделируемые прямоугольными параллелепипедами с неодинаковыми длинами ребер [353].
Таблица IX.1 (см. скан) Геометрические параметры групп 
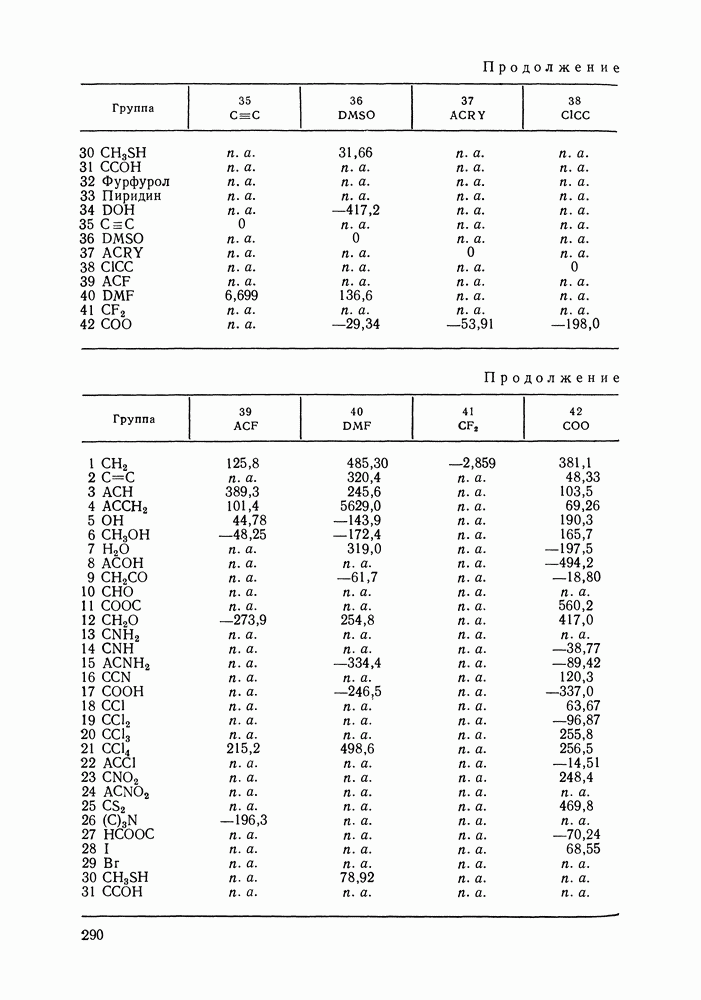
Число энергетических параметров модели (число различных энергий взаимообмена) обычно меньше числа сортов контактов между группами, поскольку вводятся усредненные параметры, относящиеся к нескольким неспецифическим типам контактов. Так, для воды взаимодействия  и
и  характеризовались одним параметром, особо выделялся параметр, отвечающий контакту
характеризовались одним параметром, особо выделялся параметр, отвечающий контакту  (водородной связи). Взаимодействие молекул воды и алкана описывали с помощью одного усредненного параметра
(водородной связи). Взаимодействие молекул воды и алкана описывали с помощью одного усредненного параметра  т. е. принимали:
т. е. принимали: 
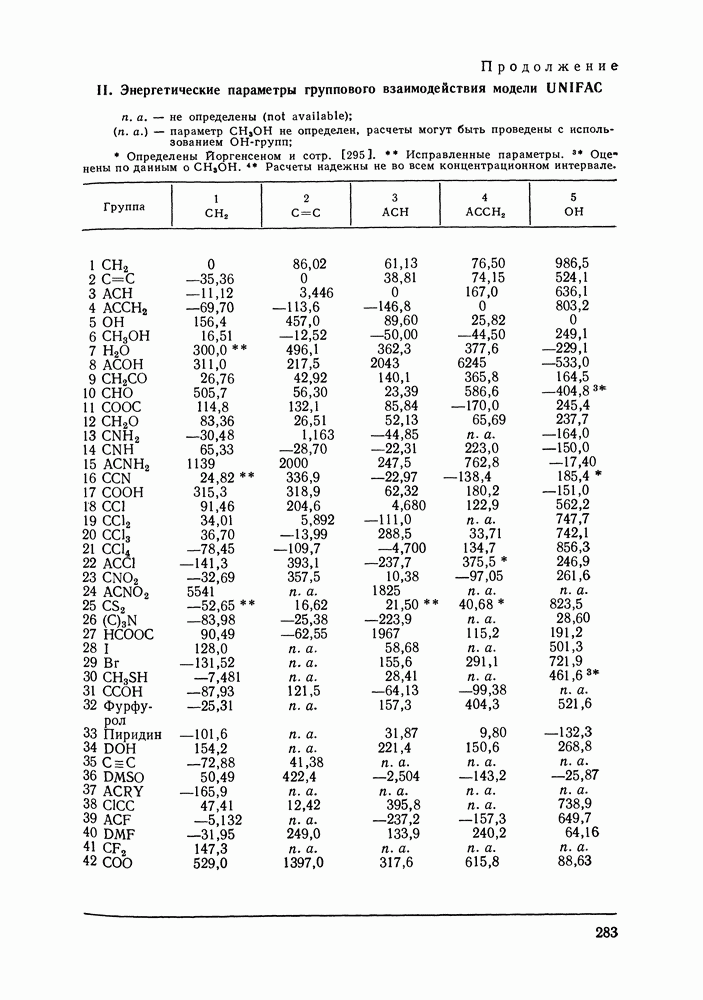
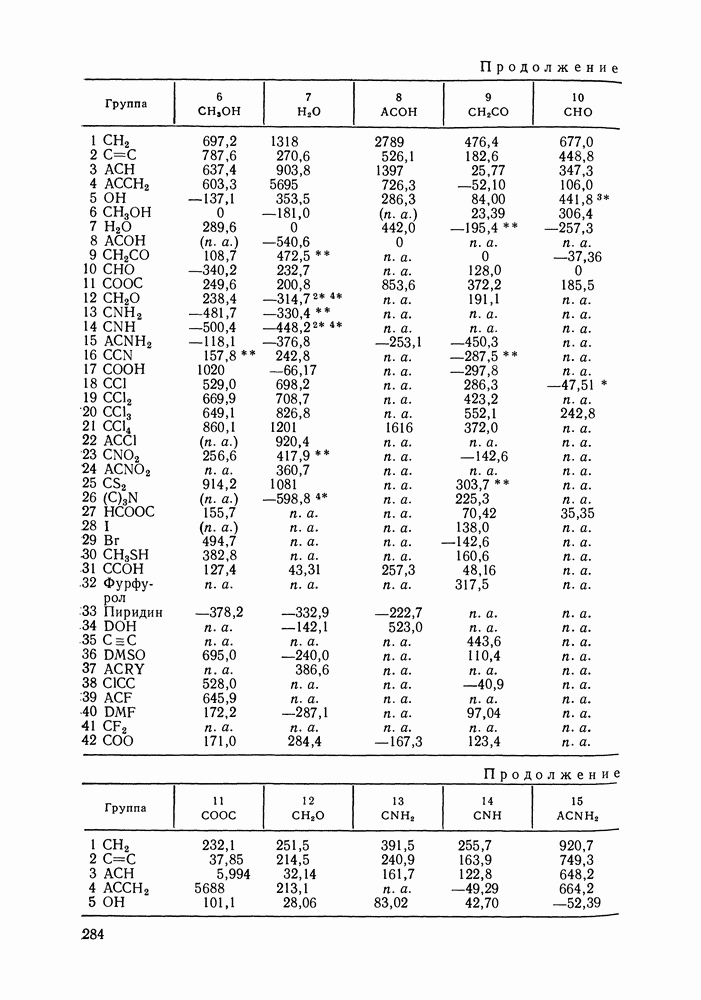
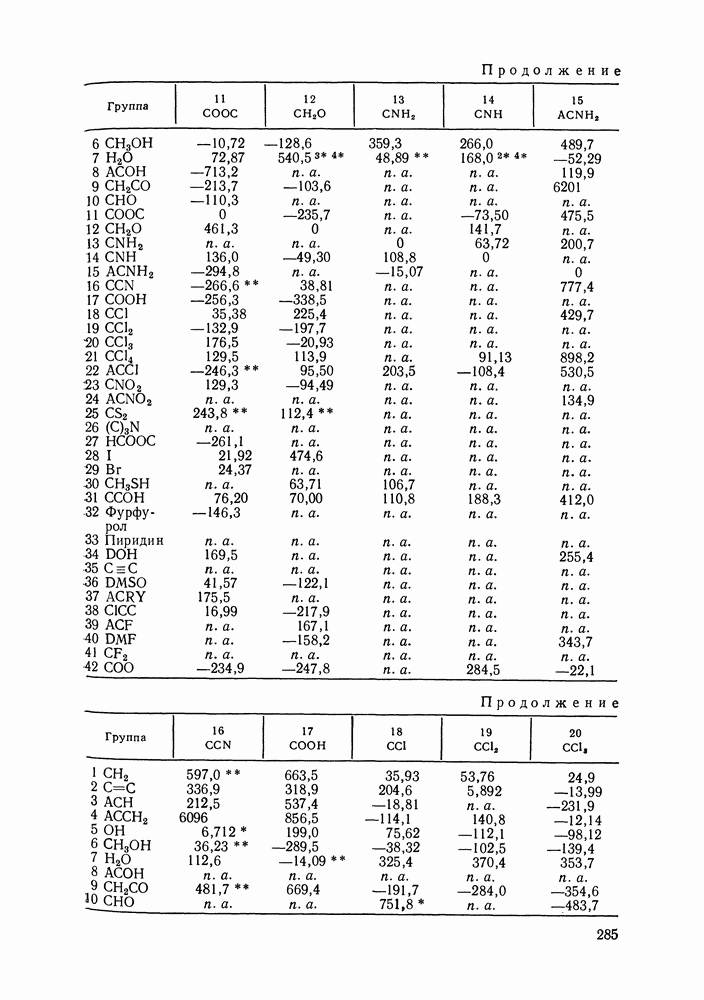
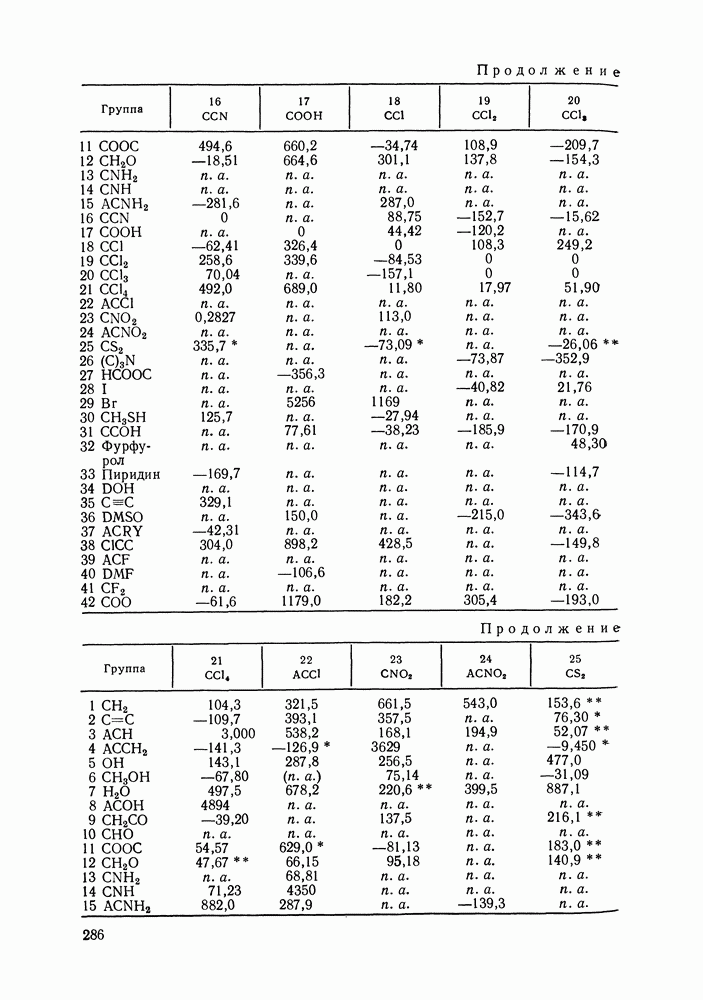
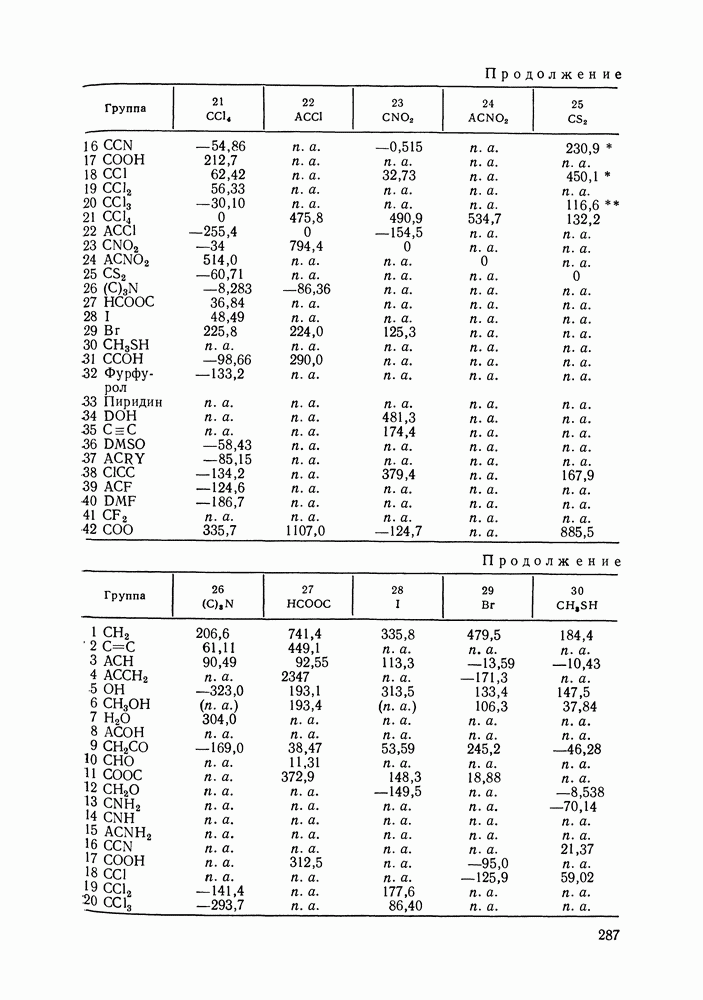
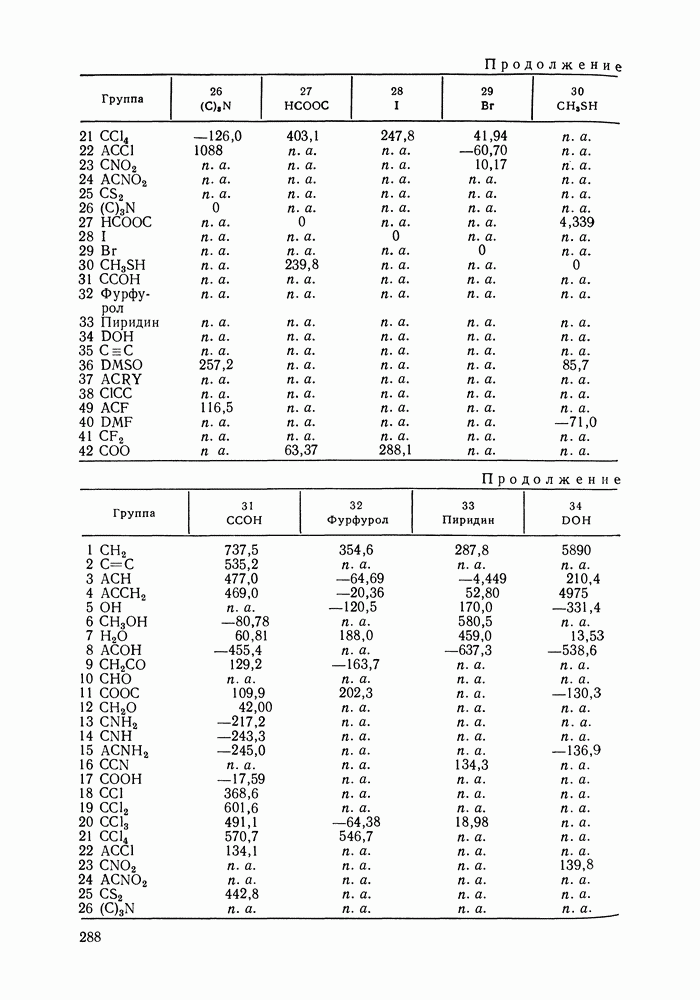
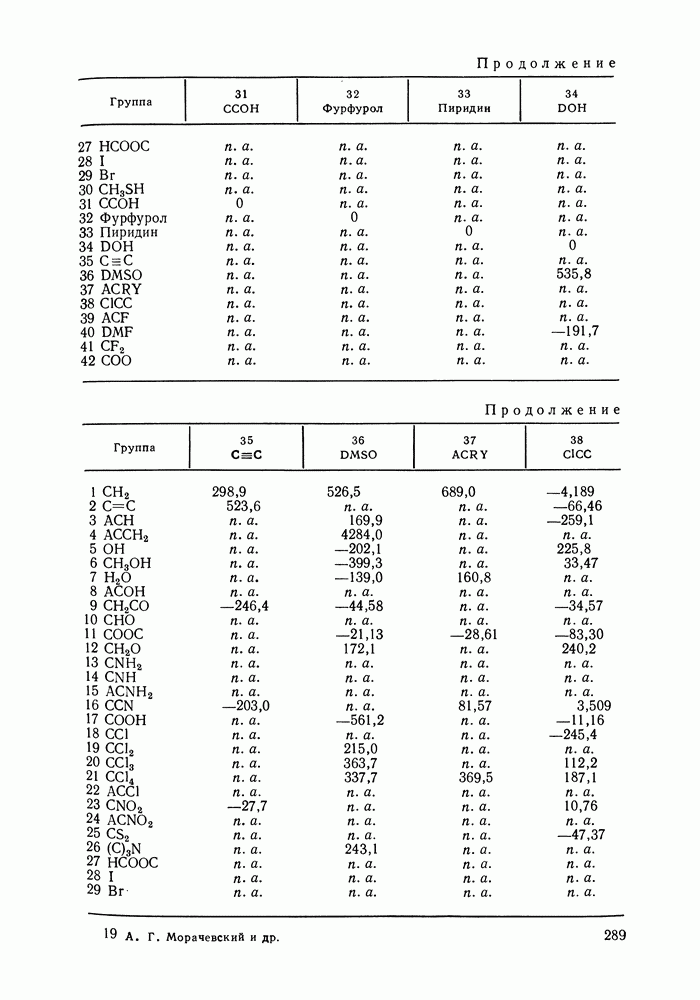
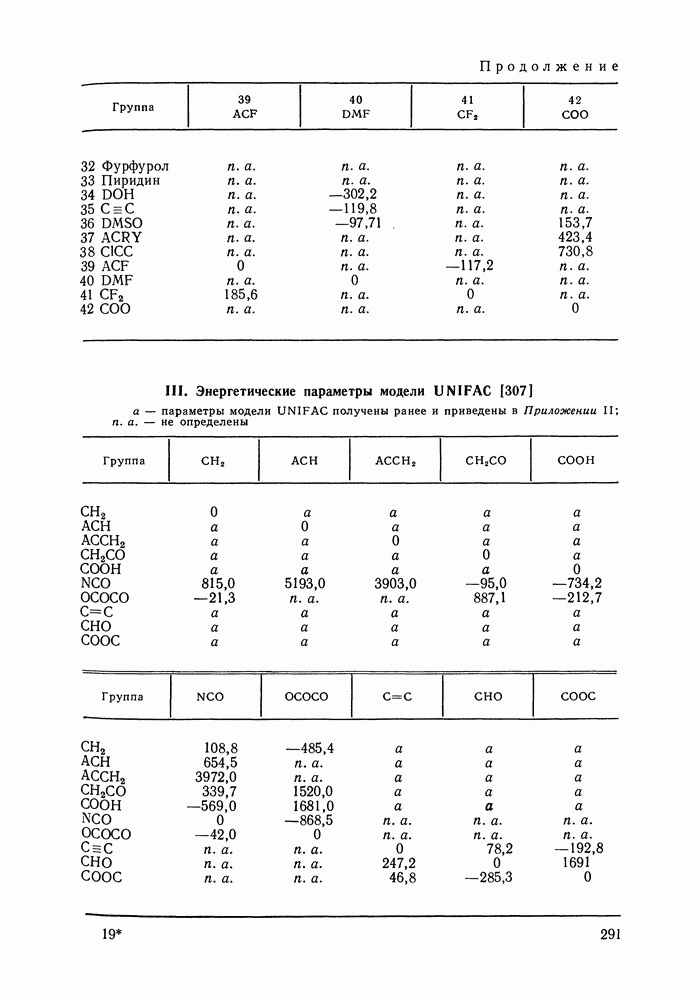
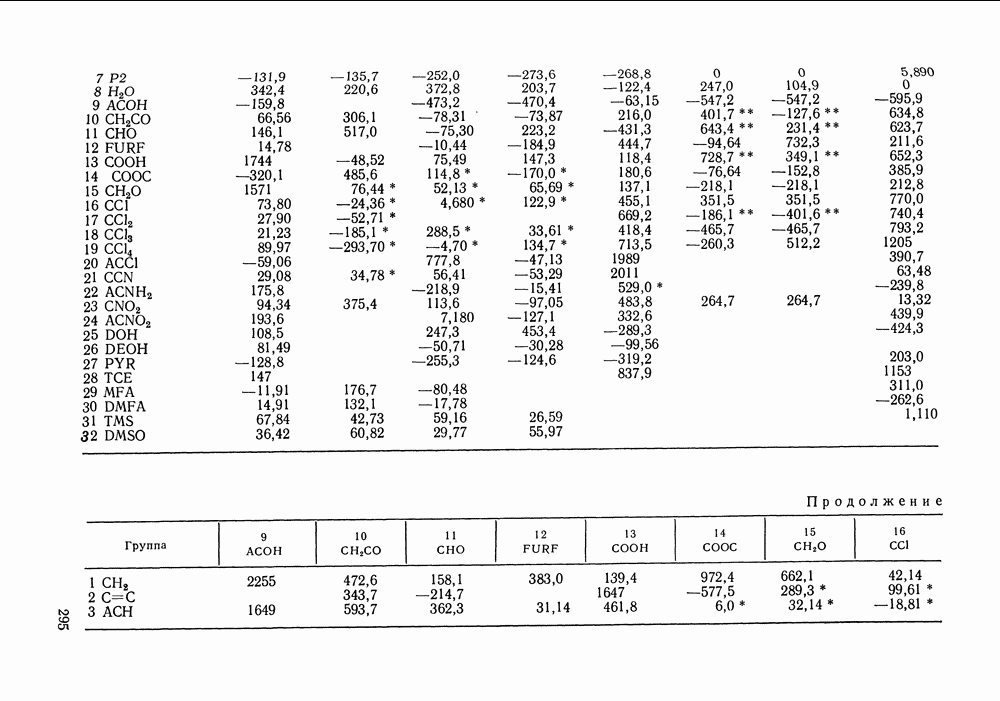
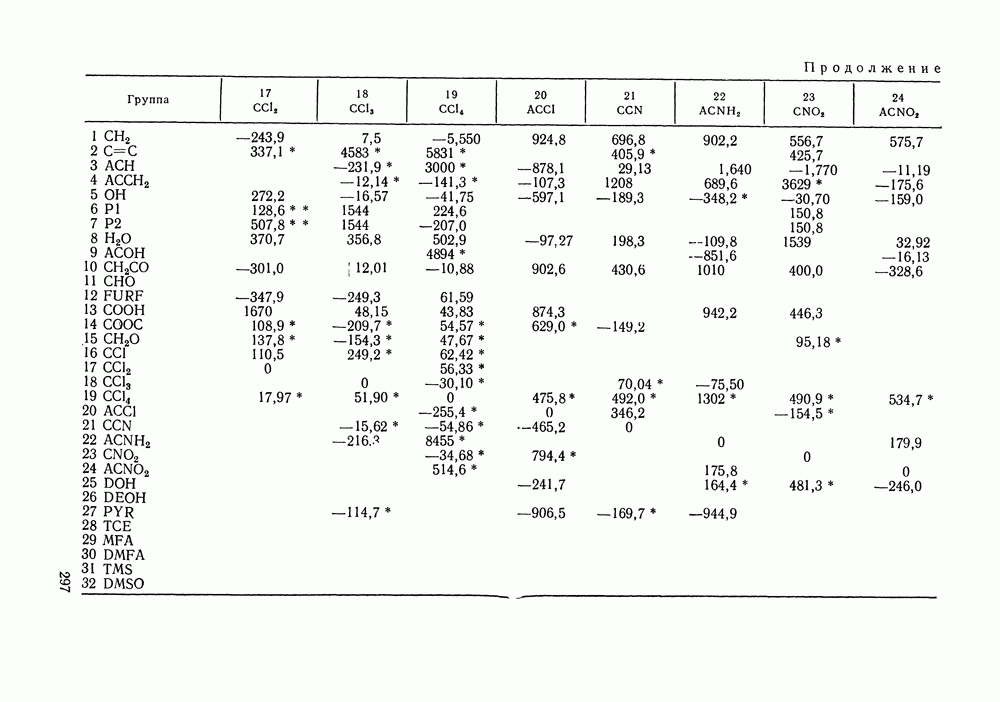
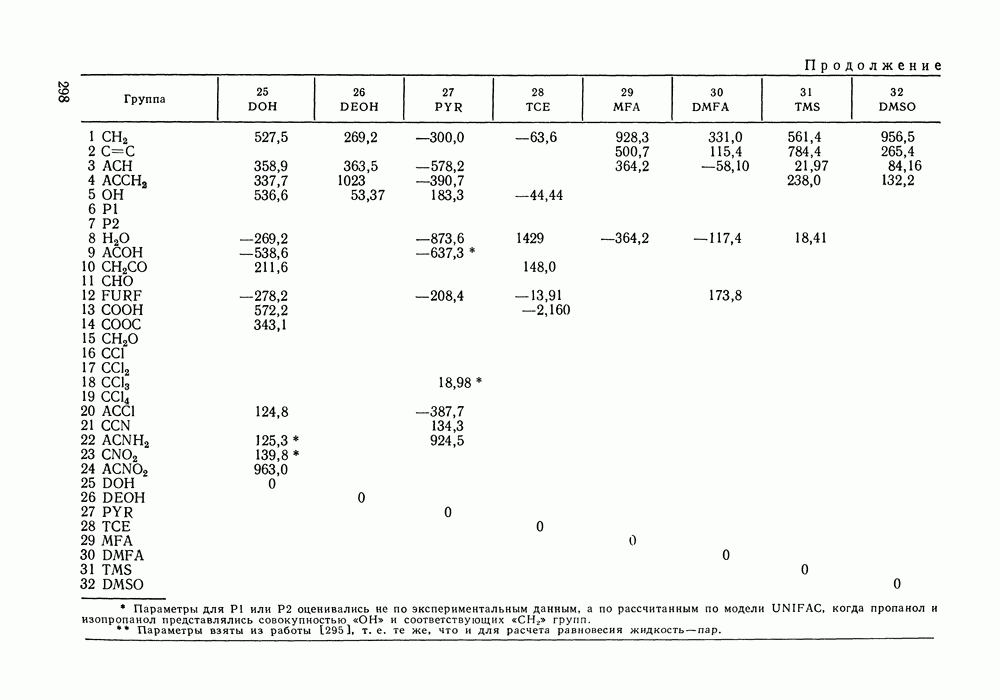
Аналогично, не детализируется описание взаимодействия гидроксильной группы алканолов с углеводородными радикалами алканолов и алканов, взаимодействия молекул сероводорода с молекулами алканов и т. д. (подробнее принятый способ описания взаимодействий указан в табл. IX.2). Предварительно выяснили чувствительность результатов, даваемых моделью, к такого рода упрощениям: специально проводились расчеты для ряда вариантов, в которых различия энергетических параметров учитывались более детально.
Термодинамические свойства системы и фазовые равновесия можно рассчитать по следующей общей схеме. Для заданной температуры равновесные составы жидкости и пара, а также концентрации дырок в обеих фазах найдем, решая систему уравнений  Уравнение
Уравнение  определяет равновесное давление. Изотермическую сжимаемость и коэффициент термического
определяет равновесное давление. Изотермическую сжимаемость и коэффициент термического
расширения вычислим с помощью  внутреннее давление — по
внутреннее давление — по  энтальпию испарения по
энтальпию испарения по  а коэффициенты активности и избыточные функции по
а коэффициенты активности и избыточные функции по  Для расчета коэффициентов активности во всем концентрационном интервале, включая предельно разбавленные растворы, формулу
Для расчета коэффициентов активности во всем концентрационном интервале, включая предельно разбавленные растворы, формулу  удобно преобразовать к виду:
удобно преобразовать к виду:

Это выражение в отличие от  не содержит неопределенностей, поскольку даже для очень плотных жидкостей
не содержит неопределенностей, поскольку даже для очень плотных жидкостей 
Остановимся теперь на методике расчета фазовых равновесий. Согласно дырочной модели жидкость и пар рассматривают как флюидные фазы, описывающиеся единым уравнением состояния. Поэтому для расчета равновесия жидкость—пар (и, конечно, жидкость—жидкость) можно пользоваться известными алгоритмами, применяемыми обычно для расчета равновесия жидкость-жидкость.
Для этих целей может быть, например, использован алгоритм из работы [144], оказавшийся особенно эффективным при расчетах равновесия жидкость—жидкость, благодаря быстрой сходимости (алгоритм основан на сочетании метода простых итераций с методом Вегстейна решения систем алгебраических уравнений). При расчетах равновесия жидкость—пар непосредственно применять
Таблица IX.2 (см. скан) Энергетические параметры групп 
названный алгоритм, в котором фиксируется брутто-состав совокупности фаз (а) и  нежелательно. В эксперименте контролируемой переменной обычно является состав жидкости
нежелательно. В эксперименте контролируемой переменной обычно является состав жидкости  задавать его гораздо удобнее (тогда легко сопоставить результаты расчета с экспериментальными данными). Если состав жидкости известен, то для расчета равновесия жидкость—пар согласна дырочной модели по существу остается определить
задавать его гораздо удобнее (тогда легко сопоставить результаты расчета с экспериментальными данными). Если состав жидкости известен, то для расчета равновесия жидкость—пар согласна дырочной модели по существу остается определить  о — долю дырок в жидкой фазе (плотность жидкости) и
о — долю дырок в жидкой фазе (плотность жидкости) и  концентрацию дырок и молекул в паре (плотность и состав пара).
концентрацию дырок и молекул в паре (плотность и состав пара).
Для рассматриваемой нами модели состав фазы (а) связан с концентрационными переменными  соотношениями:
соотношениями:

Значения переменных  известны. При фиксированной температуре из уравнений
известны. При фиксированной температуре из уравнений  (IX.35) рассчитывали
(IX.35) рассчитывали  Алгоритм из работы [144] модифицирован так, что в процессе решения системы
Алгоритм из работы [144] модифицирован так, что в процессе решения системы  состав жидкости
состав жидкости  неизменно находится на секущей, определяемой
неизменно находится на секущей, определяемой  [отношение любых двух
[отношение любых двух  при
при  постоянно и равно Это обеспечивает постоянство состава жидкости
постоянно и равно Это обеспечивает постоянство состава жидкости  в ходе решения системы
в ходе решения системы  Для чистых компонентов
Для чистых компонентов  и
и  вырождается в условие
вырождается в условие  которое не влияет на способ решения
которое не влияет на способ решения 
Геометрическую интерпретацию решения уравнений  (IX.41) дадим на примере бинарной системы. В такой системе присутствуют компонент 1, компонент 2 и дырки. Всевозможные составы системы могут быть изображены на обычном концентрационном треугольнике Гиббса (рис. IX. 1), причем вершины этого треугольника отвечают «чистым решеткам», содержащим лишь частицы одного сорта (компонент 1, компонент 2, дырки). Стороны треугольника 1—0 и 2—0 отвечают чистым компонентам 1 и 2, причем каждой точке на этих сторонах соответствует свое значение величины
(IX.41) дадим на примере бинарной системы. В такой системе присутствуют компонент 1, компонент 2 и дырки. Всевозможные составы системы могут быть изображены на обычном концентрационном треугольнике Гиббса (рис. IX. 1), причем вершины этого треугольника отвечают «чистым решеткам», содержащим лишь частицы одного сорта (компонент 1, компонент 2, дырки). Стороны треугольника 1—0 и 2—0 отвечают чистым компонентам 1 и 2, причем каждой точке на этих сторонах соответствует свое значение величины  следовательно, определенный молярный объем. Точки на стороне 1—2 представляют решетку без вакансий
следовательно, определенный молярный объем. Точки на стороне 1—2 представляют решетку без вакансий  но поскольку на этой стороне
но поскольку на этой стороне  (см. IX.41), то можно сказать, что сторона 1—2 изображает истинные (т. е. измеряемые экспериментально) составы
(см. IX.41), то можно сказать, что сторона 1—2 изображает истинные (т. е. измеряемые экспериментально) составы 
Составы равновесных жидкости и пара образуют бинодаль, аналогичную бинодали растворимости в тройных системах. Раствору заданного состава [н. равновесному с паром, отвечает согласно  (IX.41) точка пересечения бинодали (жидкая ветвь) и секущей, проведенной из вершины
(IX.41) точка пересечения бинодали (жидкая ветвь) и секущей, проведенной из вершины  в точку
в точку  на стороне 1—2. Эта точка определяет
на стороне 1—2. Эта точка определяет  Состав пара, равновесного
Состав пара, равновесного

Рис. IX. 1. Геометрическая интерпретация расчетов равновесия жидкость—пар согласно дырочной модели для бинарной системы компонент  -компонент 2
-компонент 2
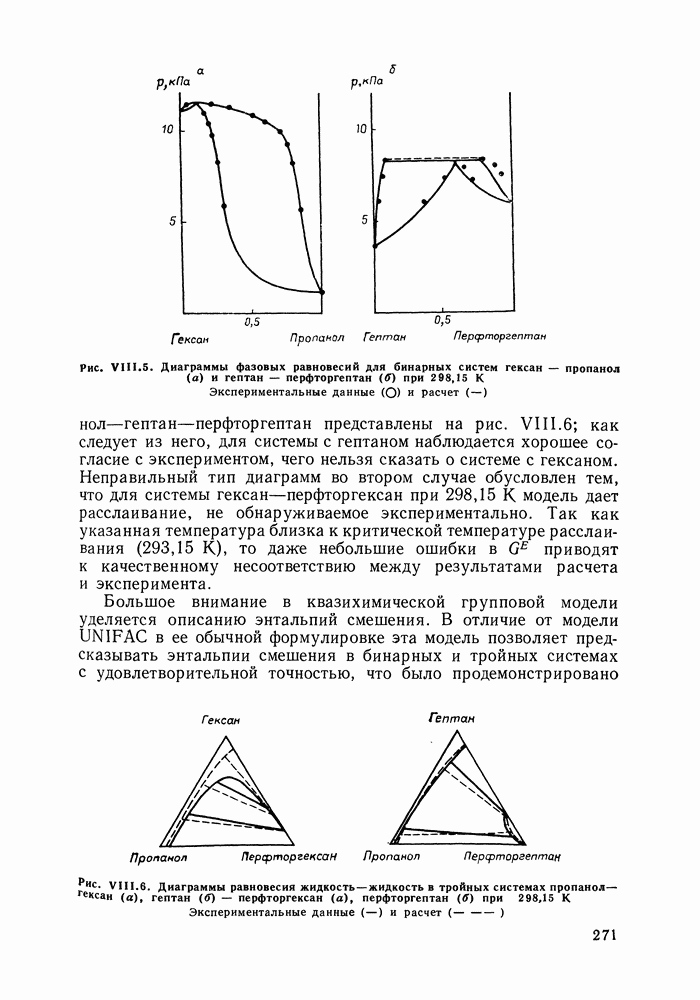
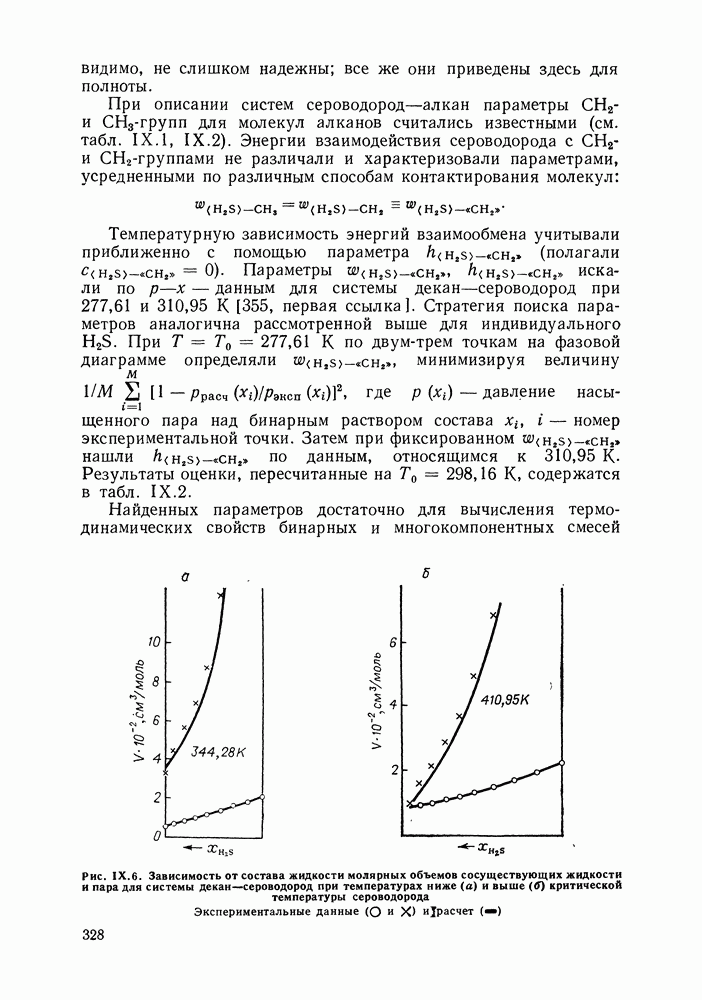
Кривые изображают проекции бинодали при температурах ниже (а) и выше (б) критической температуры компонента 2
с раствором, лежит на другой ветви бинодали и, если смесь не азеотропна, не на секущей 
При расчете равновесия жидкость—пар задаем начальные приближения для величин  при
при  т. е. точки
т. е. точки  образующие ноду начального приближения. В итерационном процессе решения системы
образующие ноду начального приближения. В итерационном процессе решения системы  точка А смещается вдоль секущей, показанной на рис. IX. 1, а, в то время как на смещения точки В не наложено подобных ограничений. Решение найдено, когда точки
точка А смещается вдоль секущей, показанной на рис. IX. 1, а, в то время как на смещения точки В не наложено подобных ограничений. Решение найдено, когда точки  оказываются на жидкой и паровой ветвях бинодали. Для систем, в которых один из компонентов находится при температуре выше критической, диаграмма равновесия жидкость—пар будет иметь вид, показанный на рис. IX.1,б.
оказываются на жидкой и паровой ветвях бинодали. Для систем, в которых один из компонентов находится при температуре выше критической, диаграмма равновесия жидкость—пар будет иметь вид, показанный на рис. IX.1,б.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА
- Глава I. ОСНОВНЫЕ ПОЛОЖЕНИЯ ТЕРМОДИНАМИКИ ГЕТЕРОГЕННЫХ РАВНОВЕСИЙ
- 1.2. УСЛОВИЯ РАВНОВЕСИЯ ГЕТЕРОГЕННЫХ СИСТЕМ
- 1.3. ТИПЫ РАВНОВЕСИЙ
- 1.4. УСЛОВИЯ УСТОЙЧИВОСТИ
- 1.5. ПРАВИЛО ФАЗ
- Глава II. ОДНОКОМПОНЕНТНЫЕ СИСТЕМЫ
- II.1. ДИАГРАММЫ СОСТОЯНИЯ
- II.2. УРАВНЕНИЕ КЛАУЗИУСА—КЛАПЕЙРОНА
- II.3. ЗАВИСИМОСТЬ ДАВЛЕНИЯ ОТ ТЕМПЕРАТУРЫ. УРАВНЕНИЕ АНТУАНА
- II.4. ЗАКОН СООТВЕТСТВЕННЫХ СОСТОЯНИЙ
- II.5. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА. ДРУГИЕ АНАЛИТИЧЕСКИЕ УРАВНЕНИЯ СОСТОЯНИЯ
- II.6. ВИРИАЛЬНОЕ УРАВНЕНИЕ СОСТОЯНИЯ
- Глава III. ДВОЙНЫЕ СИСТЕМЫ
- III.1. ДИАГРАММЫ РАВНОВЕСИЯ ДЛЯ ДВОЙНЫХ СИСТЕМ
- III.2. ОБОБЩЕННОЕ ДИФФЕРЕНЦИАЛЬНОЕ УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- III.3. ЗАКОНЫ КОНОВАЛОВА
- III.4. ЗАКОНЫ ВРЕВСКОГО
- III.5. ИДЕАЛЬНЫЕ СИСТЕМЫ
- III.6. РАЗБАВЛЕННЫЕ РАСТВОРЫ
- III.7 РЕАЛЬНЫЕ СИСТЕМЫ
- III.8. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ СМЕШЕНИЯ И РАВНОВЕСИЕ ЖИДКОСТЬ—ПАР
- III.9. ОБ АЗЕОТРОПИИ В БИНАРНЫХ СИСТЕМАХ
- III.10. ТРЕХФАЗНЫЕ РАВНОВЕСИЯ ЖИДКОСТЬ—ЖИДКОСТЬ—ПАР В ДВОЙНЫХ СИСТЕМАХ
- III.11. ФАЗОВЫЕ ДИАГРАММЫ БИНАРНЫХ СИСТЕМ В ШИРОКОМ ИНТЕРВАЛЕ ТЕМПЕРАТУР И ДАВЛЕНИЙ
- Глава IV. ТРОЙНЫЕ И МНОГОКОМПОНЕНТНЫЕ СИСТЕМЫ
- IV.2. ПРОЯВЛЕНИЕ ЗАКОНОВ КОНОВАЛОВА И ВРЕВСКОГО В ТРОЙНЫХ И МНОГОКОМПОНЕНТНЫХ СИСТЕМАХ
- IV.3. ОТКРЫТЫЕ ФАЗОВЫЕ ПРОЦЕССЫ. ТЕРМОДИНАМИКО-ТОПОЛОГИЧЕСКИЕ ЗАКОНОМЕРНОСТИ
- Глава V. МЕТОДЫ ЭКСПЕРИМЕНТАЛЬНОГО ИССЛЕДОВАНИЯ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР
- V.I. ЦИРКУЛЯЦИОННЫЙ МЕТОД
- V.2. МЕТОД ОТКРЫТОГО ИСПАРЕНИЯ
- V.3. МЕТОД СТРУИ ИНЕРТНОГО ГАЗА
- V.4. СТАТИЧЕСКИЙ МЕТОД
- V.5. ИЗОПИЕСТИЧЕСКИЙ МЕТОД
- V.6. ИЗМЕРЕНИЕ ТЕМПЕРАТУРЫ КИПЕНИЯ ПРИ ПОСТОЯННОМ ДАВЛЕНИИ
- V.7. РАСЧЕТ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР ПО ЗАВИСИМОСТИ ДАВЛЕНИЯ ПАРА ОТ СОСТАВА РАСТВОРА ПРИ ПОСТОЯННОЙ ТЕМПЕРАТУРЕ
- V.8. МЕТОДЫ ИССЛЕДОВАНИЯ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР С ПОМОЩЬЮ ГАЗОВОЙ ХРОМАТОГРАФИИ
- V.9. РАВНОВЕСИЕ ЖИДКОСТЬ—ПАР ДЛЯ РАЗБАВЛЕННЫХ РАСТВОРОВ
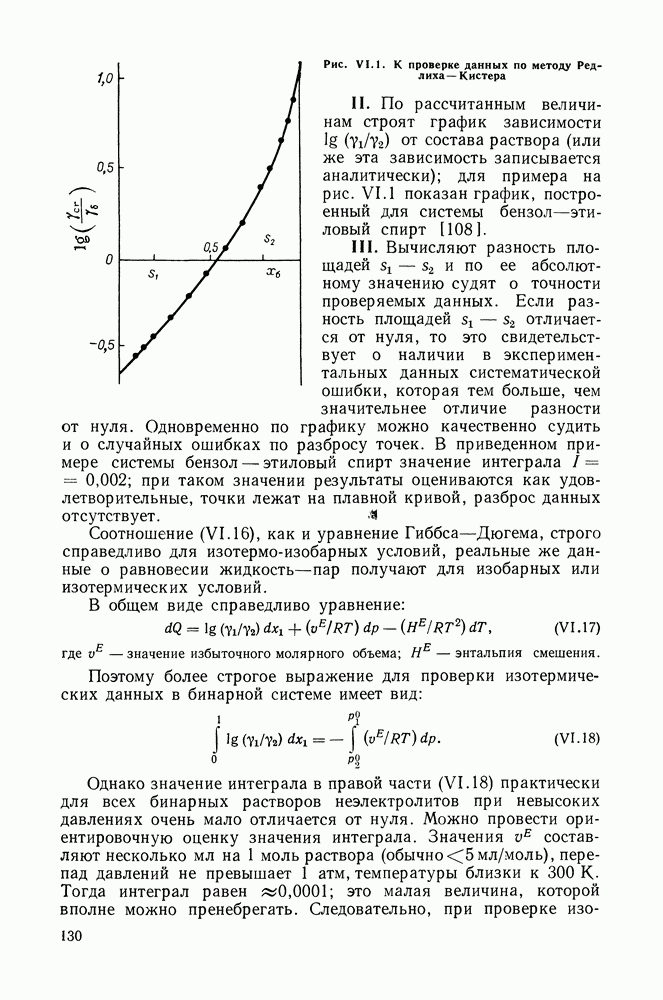
- Глава VI. МЕТОДЫ ПРОВЕРКИ ЭКСПЕРИМЕНТАЛЬНЫХ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ-ПАР
- VI.2. ОБЩАЯ ОЦЕНКА ТЕРМОДИНАМИЧЕСКИХ МЕТОДОВ ПРОВЕРКИ И ИСПРАВЛЕНИЯ ДАННЫХ
- VI.3. ПРОВЕРКА ДАННЫХ С ПОМОЩЬЮ УРАВНЕНИЙ ГИББСА—ДЮГЕМА И ДЮГЕМА—МАРГУЛЕСА
- VI.4. МЕТОД РЕДЛИХА—КИСТЕРА
- VI.5. МЕТОД ВАН-НЕССА
- VI.6. СТАТИСТИЧЕСКИЕ МЕТОДЫ ОБРАБОТКИ ЭКСПЕРИМЕНТАЛЬНЫХ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ—ПАР
- VI.7. МЕТОДЫ ПРОВЕРКИ ТЕРМОДИНАМИЧЕСКОЙ СОГЛАСОВАННОСТИ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ—ПАР В ТРОЙНЫХ СИСТЕМАХ
- VI.8. СОПОСТАВЛЕНИЕ МЕТОДОВ РЕДЛИХА—КИСТЕРА И ВАН-НЕССА
- Глава VII. МЕТОДЫ РАСЧЕТА РАВНОВЕСИЙ ЖИДКОСТЬ—ПАР
- VII. 1. ТЕРМОДИНАМИЧЕСКИЕ ПАРАМЕТРЫ РАВНОВЕСНЫХ ЖИДКОСТИ И ПАРА
- VII.2. АЛГОРИТМЫ РАСЧЕТА ФАЗОВЫХ РАВНОВЕСИЙ
- VII.3. УЧЕТ НЕИДЕАЛЬНОСТИ ПАРОВОЙ ФАЗЫ ПРИ СРЕДНИХ И НИЗКИХ ДАВЛЕНИЯХ
- VII.4. ПОЛИНОМИАЛЬНЫЕ УРАВНЕНИЯ ДЛЯ КОЭФФИЦИЕНТОВ АКТИВНОСТИ И УРАВНЕНИЕ ВАН-ЛААРА
- VII.5. МОДЕЛИ ЛОКАЛЬНОГО СОСТАВА
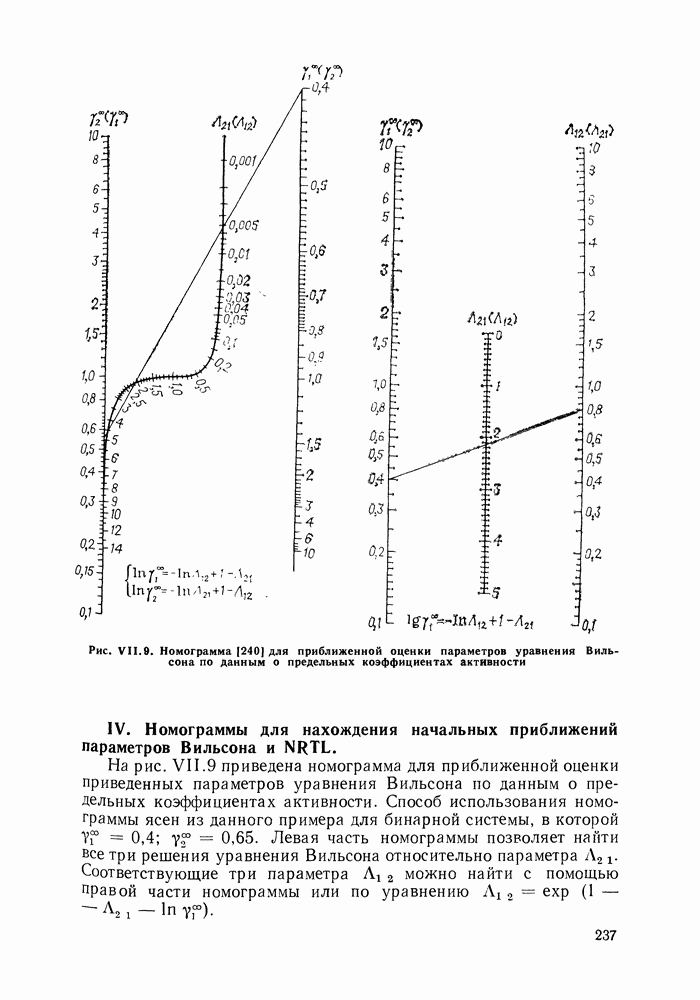
- VII.6. ОЦЕНКА ПАРАМЕТРОВ МОДЕЛЕЙ ЖИДКОЙ ФАЗЫ
- VII.7. СОПОСТАВЛЕНИЕ МОДЕЛЕЙ ЖИДКОЙ ФАЗЫ ПРИ ОПИСАНИИ ФАЗОВЫХ РАВНОВЕСИЙ
- VII.8. РЕШЕТОЧНЫЕ МОДЕЛИ. МОДЕЛЬ БАРКЕРА
- Глава VIII. ГРУППОВЫЕ МОДЕЛИ РАСТВОРОВ
- VIII.1. ОСНОВНЫЕ ОСОБЕННОСТИ ГРУППОВЫХ МОДЕЛЕЙ РАСТВОРОВ
- VIII.2. МОДЕЛЬ UNIFAC
- VIII.3. КВАЗИХИМИЧЕСКИЕ ГРУППОВЫЕ МОДЕЛИ
- Глава IX. ДЫРОЧНАЯ РЕШЕТОЧНАЯ КВАЗИХИМИЧЕСКАЯ МОДЕЛЬ, ЕЕ ГРУППОВОЙ ВАРИАНТ
- IX.2. ФОРМУЛИРОВКА ДЫРОЧНОЙ КВАЗИХИМИЧЕСКОЙ МОДЕЛИ
- IX.3. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ СИСТЕМЫ
- IX.4. О МЕТОДИКЕ РАСЧЕТА
- IX.5. РЕЗУЛЬТАТЫ РАСЧЕТОВ И ВОЗМОЖНОСТИ МОДЕЛИ
- IX.6. ПРИМЕРЫ РАСЧЕТА