| << Предыдущий параграф | Следующий параграф >> |
Распознанный текст, спецсимволы и формулы могут содержать ошибки, поэтому с корректным вариантом рекомендуем ознакомиться на отсканированных изображениях учебника выше
Также, советуем воспользоваться поиском по сайту, мы уверены, что вы сможете найти больше информации по нужной Вам тематике
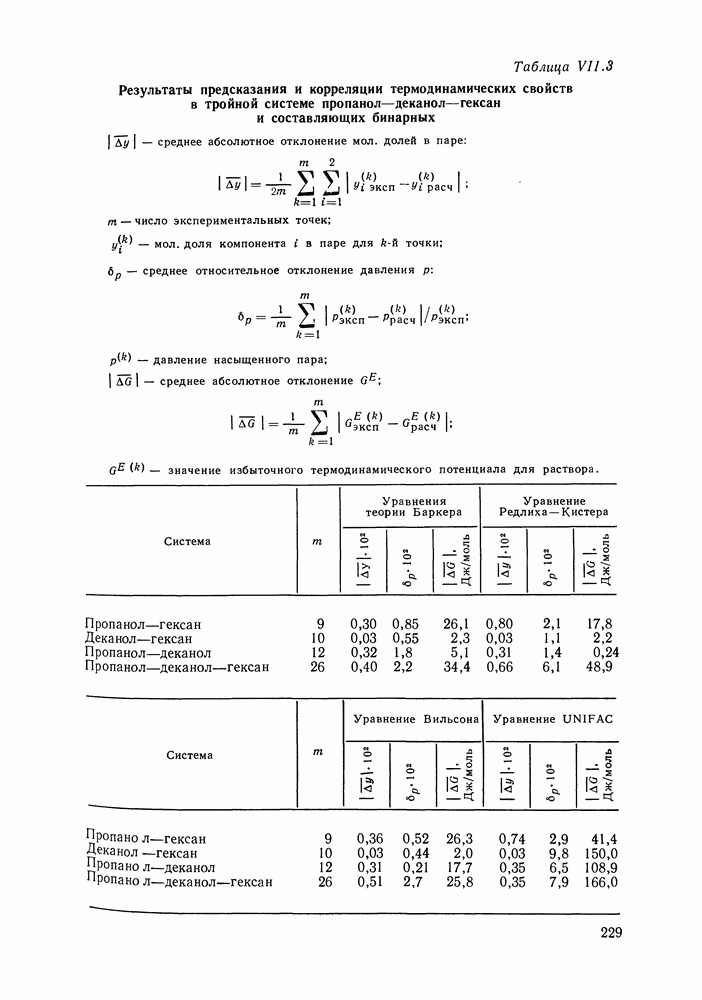
VI.7. МЕТОДЫ ПРОВЕРКИ ТЕРМОДИНАМИЧЕСКОЙ СОГЛАСОВАННОСТИ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ—ПАР В ТРОЙНЫХ СИСТЕМАХ
Работ, посвященных методам проверки данных о равновесии: жидкость—пар в тройных системах и тем более в системах с большим числом компонентов, немного. Известные работы — довольно старые, выполнены в 50-х гг. Такое положение объясняется тем, что в случае тройных систем большую долю данных получают путем расчетов на основе соответствующих бинарных систем, например, по уравнениям модели локальных составов. Такие данные всегда будут термодинамически согласованными, если их проверять каким-либо методом базирующимся на уравнении Гиббса-Дюгема.
Для той части тройных систем, которые изучены экспериментально, проверка на термодинамическую согласованность не является особо актуальной — обычно в той же серии экспериментов изучают и бинарные системы, составляющие тройную, их проверить значительно проще, а если данные для бинарных систем точны, то мало оснований предполагать ошибки в данных для тройной системы (те же реактивы, обычно та же методика постановки опыта). Отмеченные выше обстоятельства относятся к систематическим ошибкам в экспериментальных данных. Случайные ошибки, разброс данных обнаруживают и устраняют обычными приемами обработки результатов наблюдений.
Остановимся на нескольких методах, предложенных для проверки термодинамической согласованности данных о равновесии жидкость—пар в тройных системах. Разумеется, что все сказанное выше в этом параграфе не ставит под сомнение полезность таких методов.
В одной из первых работ метод Редлиха-Кистера распространен на тройные системы [138].
Применяется функция  для тройных систем:
для тройных систем:

Метод состоит в интегрировании уравнения  при изменении состава раствора по секущим концентрационного треугольника, выходящим из вершины на противоположную сторону, и по сечениям треугольника, для которых постоянна мольная доля одного из компонентов.
при изменении состава раствора по секущим концентрационного треугольника, выходящим из вершины на противоположную сторону, и по сечениям треугольника, для которых постоянна мольная доля одного из компонентов.
В работе [139] было показано, что интегрирование  можно проводить не только по секущим или сечениям, но и по линиям, отвечающим любому способу изменения состава тройного раствора. При любом способе изменения состава раствора справедливо:
можно проводить не только по секущим или сечениям, но и по линиям, отвечающим любому способу изменения состава тройного раствора. При любом способе изменения состава раствора справедливо:

где интегрирование проводится по избранной траектории составов,  и
и  значения функции
значения функции  для растворов, точки составов которых выбраны граничными условиями интегрирования.
для растворов, точки составов которых выбраны граничными условиями интегрирования.
Возможность интегрирования при любом способе изменения состава раствора повышает надежность проверки. Так, если данные подробные, и интегрирование проводится по изотермо-изобаре, то с равной (и высокой) степенью точности можно проверять и изобарные и изотермические данные (нет необходимости учитывать тепловой интеграл).
Полезны такие способы изменения состава расгвора, при которых начальная и конечная точки линии оказываются точками состава чистых компонентов или бинарных азеотропных смесей.
В этих случаях практически исключается ошибка в определении  для граничных условий. При интегрировании по замкнутому контуру сумма интегралов в
для граничных условий. При интегрировании по замкнутому контуру сумма интегралов в  должна быть равна нулю.
должна быть равна нулю.
Для случая тройных расслаивающихся растворов уравнение  справедливо при изменении состава раствора по изотерме или изобаре взаимной растворимости жидкостей и, следовательно, метод может быть применен для проверки данных о трехфазном равновесии жидкость—жидкость—пар.
справедливо при изменении состава раствора по изотерме или изобаре взаимной растворимости жидкостей и, следовательно, метод может быть применен для проверки данных о трехфазном равновесии жидкость—жидкость—пар.
Оригинальный метод анализа диаграмм равновесия жидкость— пар в тройных системах был предложен Сусаревым и Горбуновым [140]; получено уравнение:

которое является одной из форм уравнения Гиббса-Дюгема. Здесь  относительные летучести в тройной системе.
относительные летучести в тройной системе.
Уравнение  позволяет определить направление хода изотермо-изобар поверхности пара при любом составе пара, для которого известен состав равновесного раствора. Метод пригоден для качественного обнаружения как случайных, так и систематических ошибок в эксперименте. Определенные расчетом направления изотермо-изобар могут быть изображены на треугольнике составов отрезками касательных прямых. Совокупность таких отрезков должна показывать расположение изотермо-изобар пара, возможно сравнение с изотермо-изобарами, построенными на основании измерений или температур кипения или давления. Кроме того, можно обнаружить нарушения закономерности расположения указанных отрезков, что будет связано со случайными ошибками. Для иллюстрации метода приводятся диаграммы на рис. VI.5.
позволяет определить направление хода изотермо-изобар поверхности пара при любом составе пара, для которого известен состав равновесного раствора. Метод пригоден для качественного обнаружения как случайных, так и систематических ошибок в эксперименте. Определенные расчетом направления изотермо-изобар могут быть изображены на треугольнике составов отрезками касательных прямых. Совокупность таких отрезков должна показывать расположение изотермо-изобар пара, возможно сравнение с изотермо-изобарами, построенными на основании измерений или температур кипения или давления. Кроме того, можно обнаружить нарушения закономерности расположения указанных отрезков, что будет связано со случайными ошибками. Для иллюстрации метода приводятся диаграммы на рис. VI.5.
Метод Ван-Несса проверки данных в бинарных системах распространен на тройные системы [119, вторая ссылка]. В отличие от бинарных для тройных систем при описании зависимости  от состава бинарного раствора должна использоваться некоторая модель жидкой фазы; в частности, применяли модель, описываемую уравнением Маргулеса. Для аппроксимации зависимости от состава трехкомпонентного раствора использовали корреляцию 1141]:
от состава бинарного раствора должна использоваться некоторая модель жидкой фазы; в частности, применяли модель, описываемую уравнением Маргулеса. Для аппроксимации зависимости от состава трехкомпонентного раствора использовали корреляцию 1141]:

Здесь  значения
значения  для составляющих бинарных систем, когда состав бинарного раствора отвечает секущей, проведенной через точку состава тройного раствора из противоположной вершины концентрационного треугольника.
для составляющих бинарных систем, когда состав бинарного раствора отвечает секущей, проведенной через точку состава тройного раствора из противоположной вершины концентрационного треугольника.
Коэффициенты  находят в итерационном процессе путем минимизации разности квадратов отклонений между экспериментальными и рассчитанными значениями давления —
находят в итерационном процессе путем минимизации разности квадратов отклонений между экспериментальными и рассчитанными значениями давления —  Для практических расчетов обычно полагают
Для практических расчетов обычно полагают  Проверку на термодинамическую согласованность
Проверку на термодинамическую согласованность

Рис. IV.5. Иллюстрация метода, предложенного в работе [140]

Рис. VI.6. Одна из термодинамических закономерностей диаграмм жидкость—идеальный пар
проводят так же, как и в [90, р. 238], по отклонениям в составе пара  которые не должны превышать
которые не должны превышать  (мол.).
(мол.).
Для качественной проверки данных о равновесии жидкость — пар в тройных системах могут быть полезны некоторые общетермодинамические положения, вытекающие из условий равновесия и устойчивости, и не связанные непосредственно с уравнением Гиббса-Дюгема. Эти положения удобны для контроля правильности построения диаграммы равновесия жидкость — пар в тройной системе. Например, показано, что если из вершины треугольника концентраций провести секущую, касательную к изотермо-изобаре, построенной в переменных состава пара, то пар, отвечающий точке касания, должен находиться в равновесии с раствором, в котором концентрация компонента (отвечающего вершине, из которой проведена секущая) будет той же, что и в паре. Эта закономерность иллюстрируется схематически рис. VI.6, где штриховой линией изображена изотермоизобара в переменных пара, а сплошной — в переменных раствора. В точке и секущая касается изотермы-изобары пара, соответствующая нода жидкость — пар параллельна стороне I—III; в точках и и I содержание второго компонента в растворе и равновесном паре одинаково. При выводе этого положения принимается единственное допущение — подчинение паровой фазы законам идеальных газов.
| << Предыдущий параграф | Следующий параграф >> |
- ПРЕДИСЛОВИЕ РЕДАКТОРА
- Глава I. ОСНОВНЫЕ ПОЛОЖЕНИЯ ТЕРМОДИНАМИКИ ГЕТЕРОГЕННЫХ РАВНОВЕСИЙ
- 1.2. УСЛОВИЯ РАВНОВЕСИЯ ГЕТЕРОГЕННЫХ СИСТЕМ
- 1.3. ТИПЫ РАВНОВЕСИЙ
- 1.4. УСЛОВИЯ УСТОЙЧИВОСТИ
- 1.5. ПРАВИЛО ФАЗ
- Глава II. ОДНОКОМПОНЕНТНЫЕ СИСТЕМЫ
- II.1. ДИАГРАММЫ СОСТОЯНИЯ
- II.2. УРАВНЕНИЕ КЛАУЗИУСА—КЛАПЕЙРОНА
- II.3. ЗАВИСИМОСТЬ ДАВЛЕНИЯ ОТ ТЕМПЕРАТУРЫ. УРАВНЕНИЕ АНТУАНА
- II.4. ЗАКОН СООТВЕТСТВЕННЫХ СОСТОЯНИЙ
- II.5. УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА. ДРУГИЕ АНАЛИТИЧЕСКИЕ УРАВНЕНИЯ СОСТОЯНИЯ
- II.6. ВИРИАЛЬНОЕ УРАВНЕНИЕ СОСТОЯНИЯ
- Глава III. ДВОЙНЫЕ СИСТЕМЫ
- III.1. ДИАГРАММЫ РАВНОВЕСИЯ ДЛЯ ДВОЙНЫХ СИСТЕМ
- III.2. ОБОБЩЕННОЕ ДИФФЕРЕНЦИАЛЬНОЕ УРАВНЕНИЕ ВАН-ДЕР-ВААЛЬСА
- III.3. ЗАКОНЫ КОНОВАЛОВА
- III.4. ЗАКОНЫ ВРЕВСКОГО
- III.5. ИДЕАЛЬНЫЕ СИСТЕМЫ
- III.6. РАЗБАВЛЕННЫЕ РАСТВОРЫ
- III.7 РЕАЛЬНЫЕ СИСТЕМЫ
- III.8. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ СМЕШЕНИЯ И РАВНОВЕСИЕ ЖИДКОСТЬ—ПАР
- III.9. ОБ АЗЕОТРОПИИ В БИНАРНЫХ СИСТЕМАХ
- III.10. ТРЕХФАЗНЫЕ РАВНОВЕСИЯ ЖИДКОСТЬ—ЖИДКОСТЬ—ПАР В ДВОЙНЫХ СИСТЕМАХ
- III.11. ФАЗОВЫЕ ДИАГРАММЫ БИНАРНЫХ СИСТЕМ В ШИРОКОМ ИНТЕРВАЛЕ ТЕМПЕРАТУР И ДАВЛЕНИЙ
- Глава IV. ТРОЙНЫЕ И МНОГОКОМПОНЕНТНЫЕ СИСТЕМЫ
- IV.2. ПРОЯВЛЕНИЕ ЗАКОНОВ КОНОВАЛОВА И ВРЕВСКОГО В ТРОЙНЫХ И МНОГОКОМПОНЕНТНЫХ СИСТЕМАХ
- IV.3. ОТКРЫТЫЕ ФАЗОВЫЕ ПРОЦЕССЫ. ТЕРМОДИНАМИКО-ТОПОЛОГИЧЕСКИЕ ЗАКОНОМЕРНОСТИ
- Глава V. МЕТОДЫ ЭКСПЕРИМЕНТАЛЬНОГО ИССЛЕДОВАНИЯ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР
- V.I. ЦИРКУЛЯЦИОННЫЙ МЕТОД
- V.2. МЕТОД ОТКРЫТОГО ИСПАРЕНИЯ
- V.3. МЕТОД СТРУИ ИНЕРТНОГО ГАЗА
- V.4. СТАТИЧЕСКИЙ МЕТОД
- V.5. ИЗОПИЕСТИЧЕСКИЙ МЕТОД
- V.6. ИЗМЕРЕНИЕ ТЕМПЕРАТУРЫ КИПЕНИЯ ПРИ ПОСТОЯННОМ ДАВЛЕНИИ
- V.7. РАСЧЕТ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР ПО ЗАВИСИМОСТИ ДАВЛЕНИЯ ПАРА ОТ СОСТАВА РАСТВОРА ПРИ ПОСТОЯННОЙ ТЕМПЕРАТУРЕ
- V.8. МЕТОДЫ ИССЛЕДОВАНИЯ РАВНОВЕСИЯ ЖИДКОСТЬ—ПАР С ПОМОЩЬЮ ГАЗОВОЙ ХРОМАТОГРАФИИ
- V.9. РАВНОВЕСИЕ ЖИДКОСТЬ—ПАР ДЛЯ РАЗБАВЛЕННЫХ РАСТВОРОВ
- Глава VI. МЕТОДЫ ПРОВЕРКИ ЭКСПЕРИМЕНТАЛЬНЫХ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ-ПАР
- VI.2. ОБЩАЯ ОЦЕНКА ТЕРМОДИНАМИЧЕСКИХ МЕТОДОВ ПРОВЕРКИ И ИСПРАВЛЕНИЯ ДАННЫХ
- VI.3. ПРОВЕРКА ДАННЫХ С ПОМОЩЬЮ УРАВНЕНИЙ ГИББСА—ДЮГЕМА И ДЮГЕМА—МАРГУЛЕСА
- VI.4. МЕТОД РЕДЛИХА—КИСТЕРА
- VI.5. МЕТОД ВАН-НЕССА
- VI.6. СТАТИСТИЧЕСКИЕ МЕТОДЫ ОБРАБОТКИ ЭКСПЕРИМЕНТАЛЬНЫХ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ—ПАР
- VI.7. МЕТОДЫ ПРОВЕРКИ ТЕРМОДИНАМИЧЕСКОЙ СОГЛАСОВАННОСТИ ДАННЫХ О РАВНОВЕСИИ ЖИДКОСТЬ—ПАР В ТРОЙНЫХ СИСТЕМАХ
- VI.8. СОПОСТАВЛЕНИЕ МЕТОДОВ РЕДЛИХА—КИСТЕРА И ВАН-НЕССА
- Глава VII. МЕТОДЫ РАСЧЕТА РАВНОВЕСИЙ ЖИДКОСТЬ—ПАР
- VII. 1. ТЕРМОДИНАМИЧЕСКИЕ ПАРАМЕТРЫ РАВНОВЕСНЫХ ЖИДКОСТИ И ПАРА
- VII.2. АЛГОРИТМЫ РАСЧЕТА ФАЗОВЫХ РАВНОВЕСИЙ
- VII.3. УЧЕТ НЕИДЕАЛЬНОСТИ ПАРОВОЙ ФАЗЫ ПРИ СРЕДНИХ И НИЗКИХ ДАВЛЕНИЯХ
- VII.4. ПОЛИНОМИАЛЬНЫЕ УРАВНЕНИЯ ДЛЯ КОЭФФИЦИЕНТОВ АКТИВНОСТИ И УРАВНЕНИЕ ВАН-ЛААРА
- VII.5. МОДЕЛИ ЛОКАЛЬНОГО СОСТАВА
- VII.6. ОЦЕНКА ПАРАМЕТРОВ МОДЕЛЕЙ ЖИДКОЙ ФАЗЫ
- VII.7. СОПОСТАВЛЕНИЕ МОДЕЛЕЙ ЖИДКОЙ ФАЗЫ ПРИ ОПИСАНИИ ФАЗОВЫХ РАВНОВЕСИЙ
- VII.8. РЕШЕТОЧНЫЕ МОДЕЛИ. МОДЕЛЬ БАРКЕРА
- Глава VIII. ГРУППОВЫЕ МОДЕЛИ РАСТВОРОВ
- VIII.1. ОСНОВНЫЕ ОСОБЕННОСТИ ГРУППОВЫХ МОДЕЛЕЙ РАСТВОРОВ
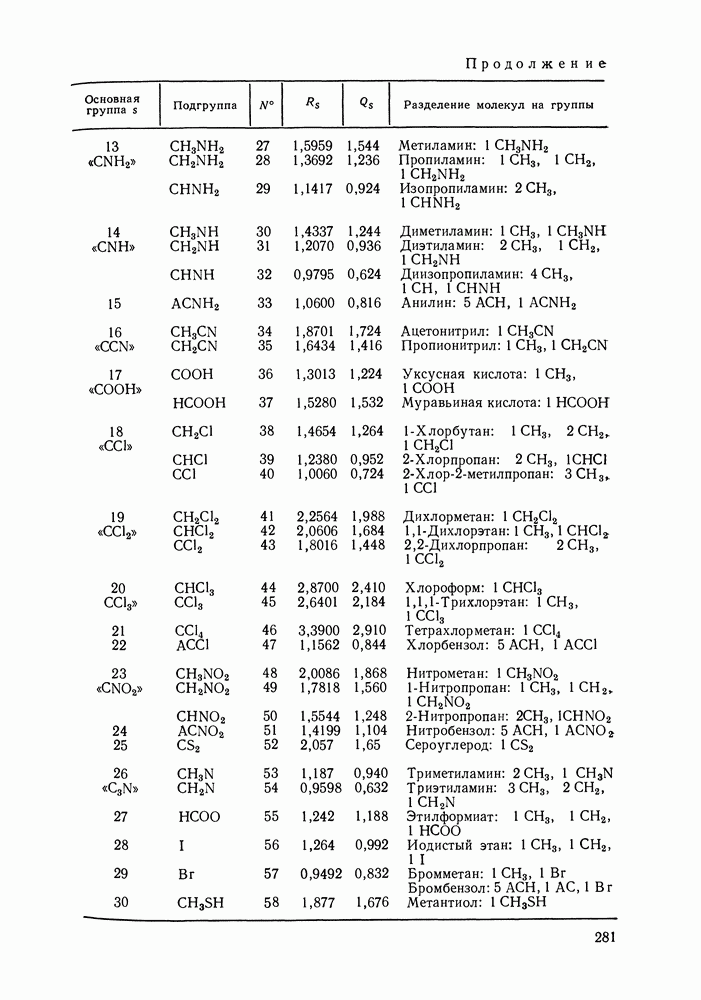
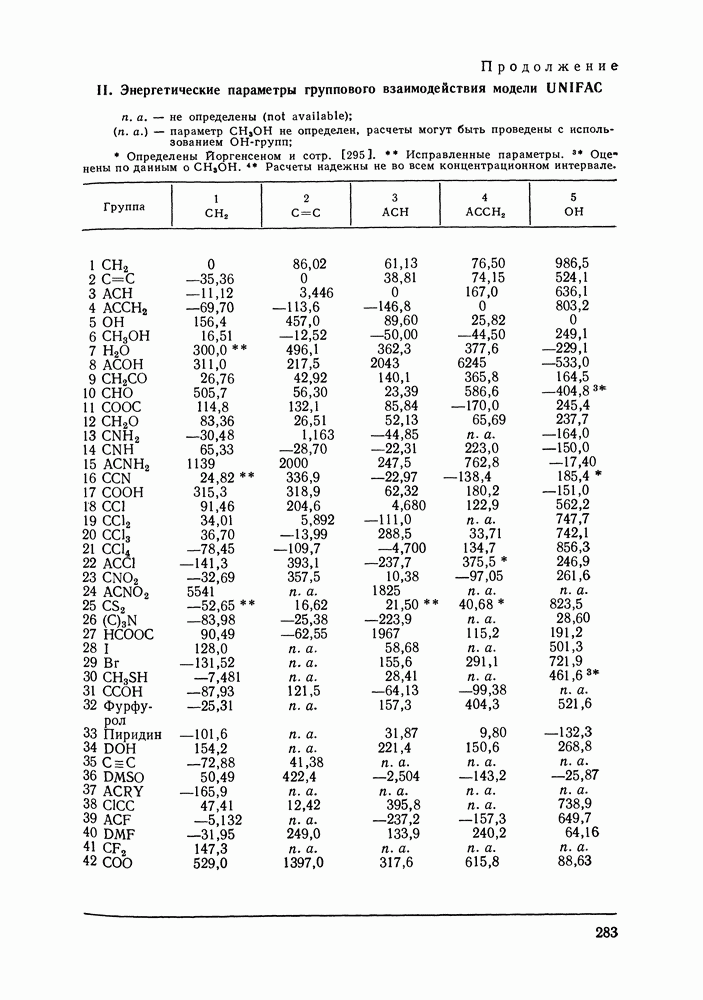
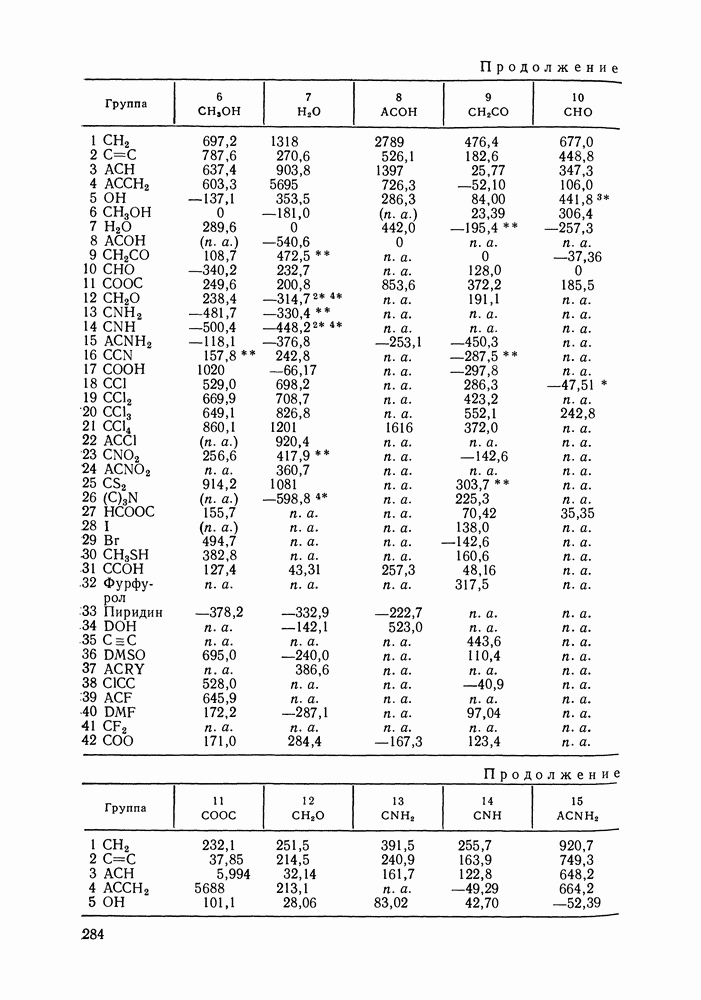
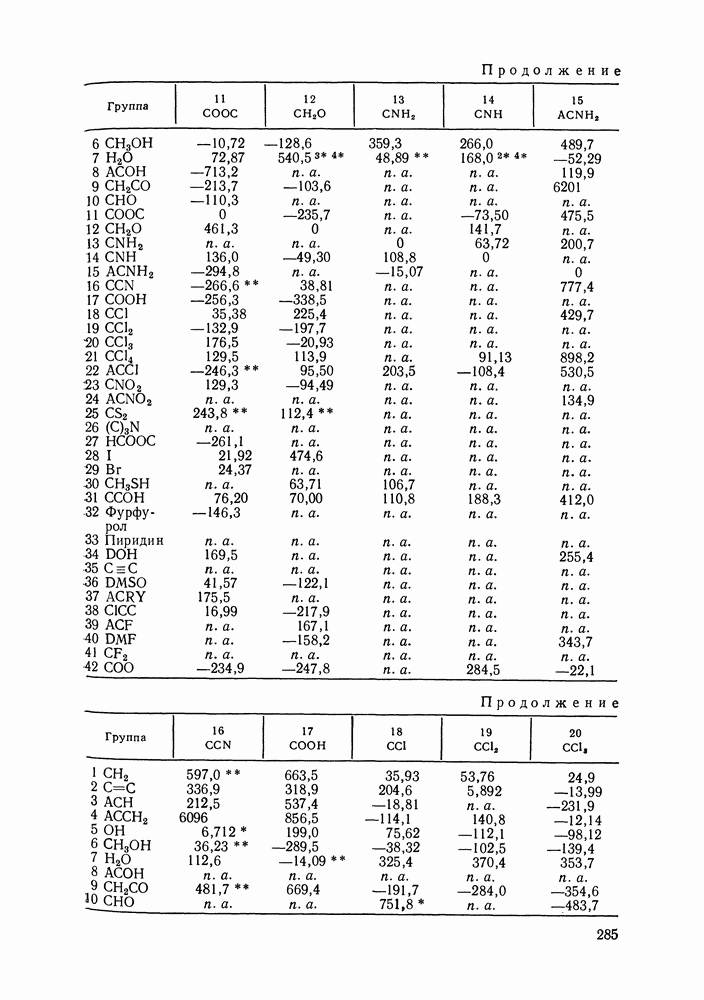
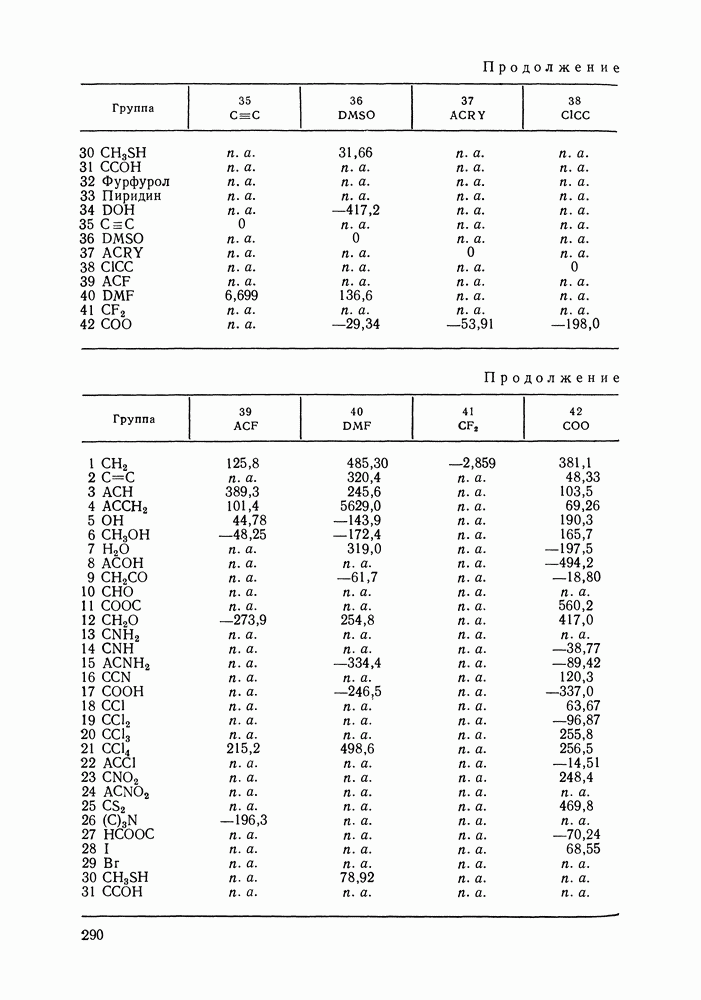
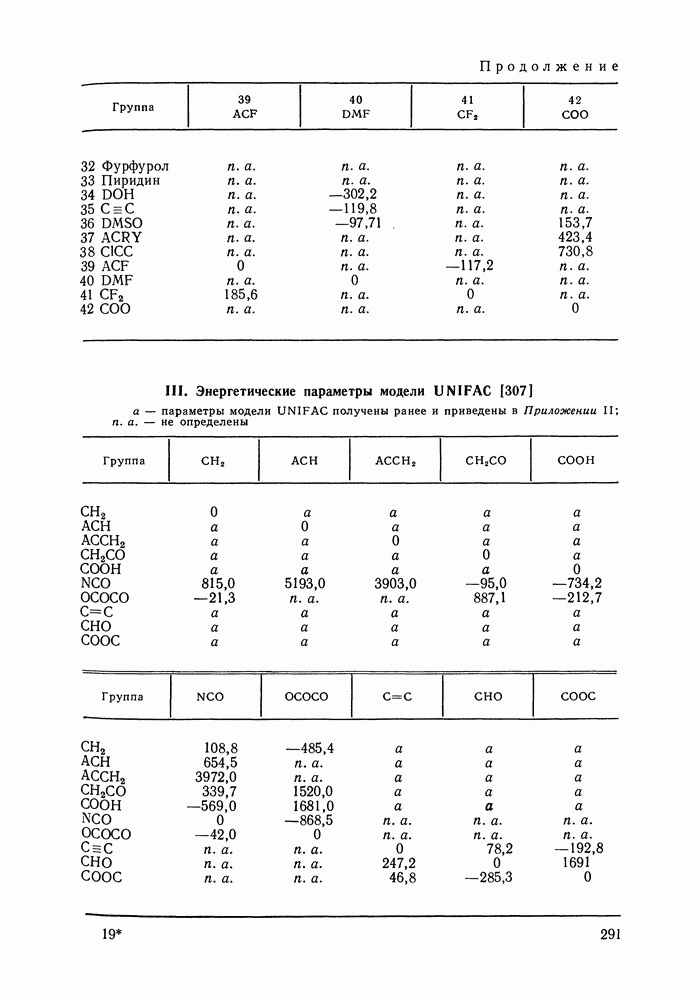
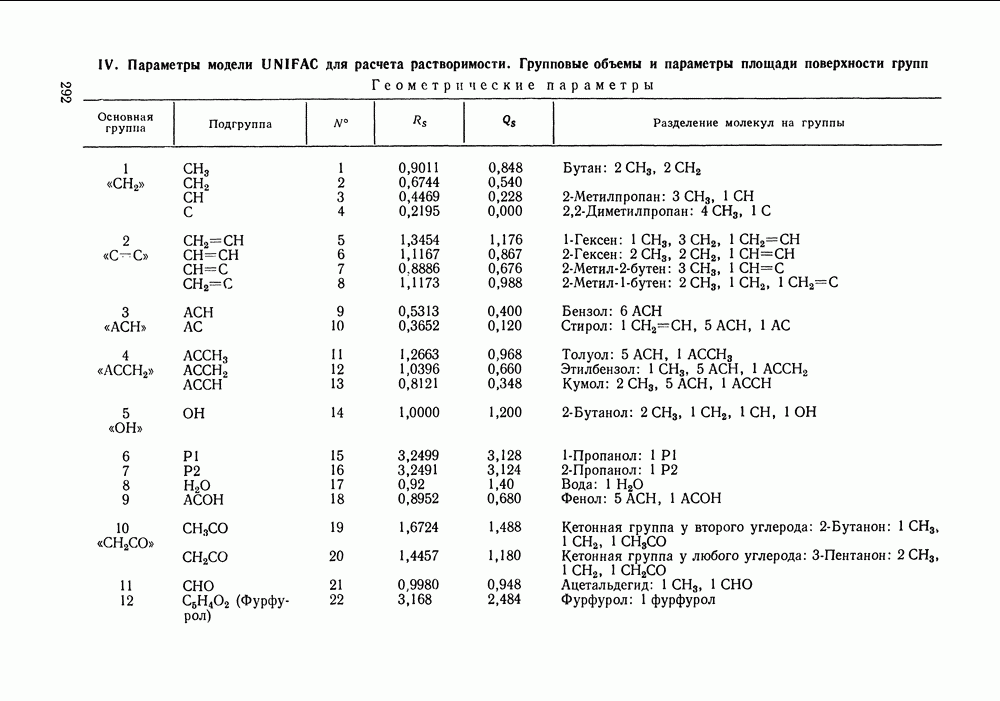
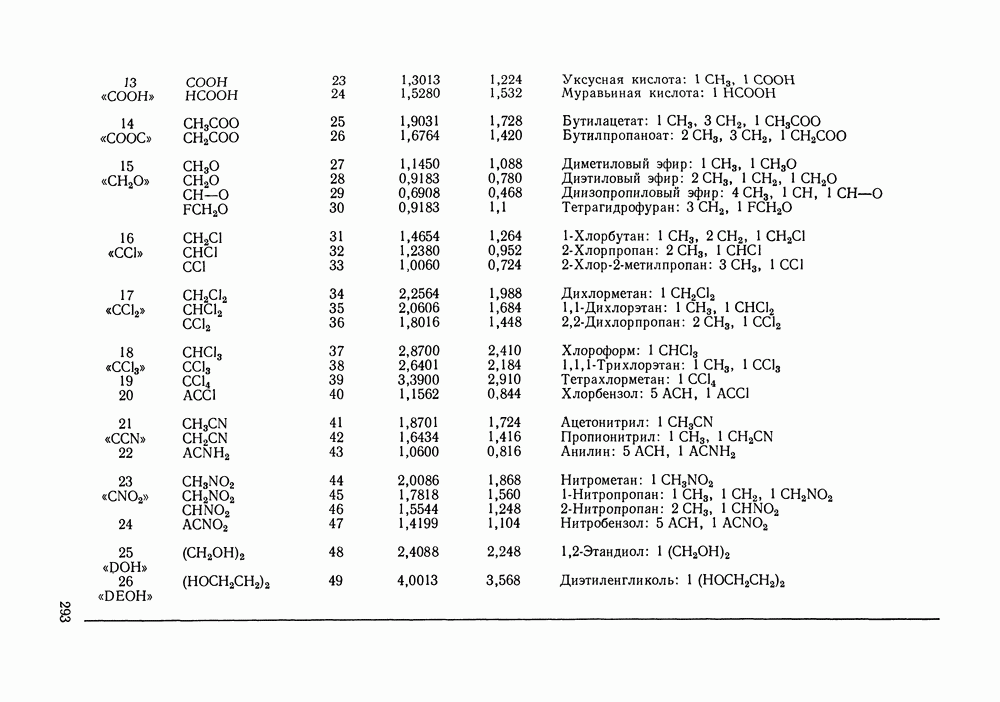
- VIII.2. МОДЕЛЬ UNIFAC
- VIII.3. КВАЗИХИМИЧЕСКИЕ ГРУППОВЫЕ МОДЕЛИ
- Глава IX. ДЫРОЧНАЯ РЕШЕТОЧНАЯ КВАЗИХИМИЧЕСКАЯ МОДЕЛЬ, ЕЕ ГРУППОВОЙ ВАРИАНТ
- IX.2. ФОРМУЛИРОВКА ДЫРОЧНОЙ КВАЗИХИМИЧЕСКОЙ МОДЕЛИ
- IX.3. ТЕРМОДИНАМИЧЕСКИЕ ФУНКЦИИ СИСТЕМЫ
- IX.4. О МЕТОДИКЕ РАСЧЕТА
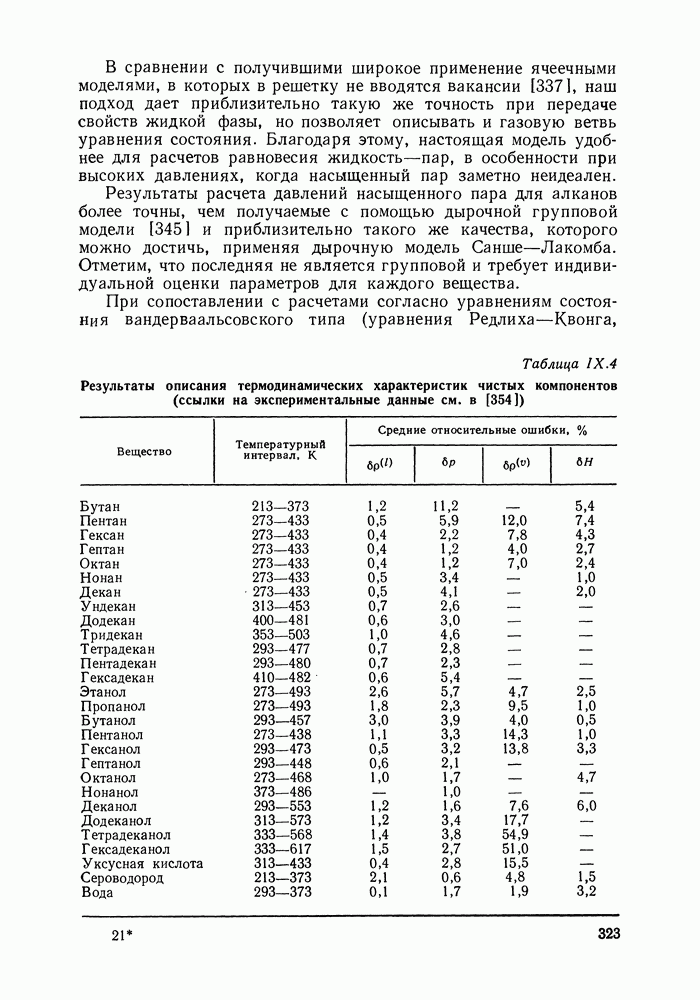
- IX.5. РЕЗУЛЬТАТЫ РАСЧЕТОВ И ВОЗМОЖНОСТИ МОДЕЛИ
- IX.6. ПРИМЕРЫ РАСЧЕТА